JP2017145268A - 遅延放出性薬物製剤 - Google Patents
遅延放出性薬物製剤 Download PDFInfo
- Publication number
- JP2017145268A JP2017145268A JP2017112044A JP2017112044A JP2017145268A JP 2017145268 A JP2017145268 A JP 2017145268A JP 2017112044 A JP2017112044 A JP 2017112044A JP 2017112044 A JP2017112044 A JP 2017112044A JP 2017145268 A JP2017145268 A JP 2017145268A
- Authority
- JP
- Japan
- Prior art keywords
- delayed release
- coating
- core
- eudragit
- layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Landscapes
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
Description
第1のポリマー材料は典型的に、好ましくは複数のグルコース単位を含有する、多糖、例えばポリグルコシドを含む。好ましい実施形態では、多糖は、デンプン、アミロース、アミロペクチン、キトサン、硫酸コンドロイチン、シクロデキストリン、デキストラン、プルラン、カラギーナン、スクレログルカン、キチン、カードラン及びレバンからなる群から選択される少なくとも1種の多糖である。多糖はデンプン、アミロース又はアミロペクチンであることがさらに好ましく、最も好ましくはデンプンである。
本発明は、pH依存性の様式で溶解する第2のポリマー材料の使用を伴う。第2の材料は、pH感受性のフィルム形成ポリマーであり、即ち、そのpH未満では水性媒体に不溶であり、そのpH以上では水性媒体に可溶である「pH閾値」を有する。したがって、周囲媒体のpHが第2のポリマー材料の溶解を誘発し、pH閾値未満では第2のポリマー材料は全く(実質的に全く)溶解しない。周囲媒体のpHが一旦pH閾値に到達する(又はそれを超える)と、第2のポリマー材料は可溶となる。
第1のポリマー材料の第2のポリマー材料に対する割合は典型的に、少なくとも1:99、例えば少なくとも10:90、及び好ましくは少なくとも25:75である。この割合は典型的には99:1以下、例えば75:25以下、及び好ましくは60:40以下である。幾つかの実施形態では、この割合は35:65以下であり得る。幾つかの好ましい実施形態では、この割合は10:90〜75:25、例えば10:90〜60:40、及び好ましくは25:75〜60:40である。幾つかの特に好ましい実施形態では、この割合は15:85〜35:65、例えば25:75〜35:65、及び好ましくは約30:70である。他の特に好ましい実施形態では、この割合は40:60〜約60:40、例えば約50:50である。
本発明による製剤はさらに、コアと外部層との間に位置する内部層を有する。内部層は、胃液に不溶であり腸液に可溶であってよい、しかし好ましくは胃液及び腸液の両方(本明細書では胃腸液という)に可溶である、第3のポリマー材料を含む。
好ましい実施形態では、内部層は少なくとも1種の塩基を含む。塩基の目的は、腸液が外部層に浸透し始めたときに、外部層の下側にアルカリ性環境を提供することである。特定の理論に拘束されるものではないが、本発明者らは、アルカリ性環境のpHが第2のポリマー材料のpH閾値よりも高いために、アルカリ性の環境が外部層の溶解、ひいては崩壊をも促進し、それによって、外部コーティングが一旦溶解及び/又は崩壊すると製剤からの薬物の放出が加速されるものと考えている。
内部コーティングは好ましくは、少なくとも1種の緩衝剤を含む。緩衝剤の目的は、腸液が外部層に浸透し始めたときに外部層の下側のpH緩衝容量を提供又は増大することである。特定の理論に拘束されるものではないが、本発明者らは、緩衝剤は、内部層を溶解する際の緩衝容量を高め、外部層中のポリマーのイオン化及び溶解を助けるものと考えている。所与のpHに対し、緩衝容量が高いほど、ポリマー溶解の速度が速いと考えられる。内部層内に塩基が存在する実施形態では、腸液が一旦外部層に浸透すると、緩衝剤が外部層下のアルカリ環境を維持するのを助ける。
緩衝剤及び/又は塩基に加えて、内部層は、可塑剤(クエン酸トリエチル等)、粘着防止剤(GMS等)、及び界面活性剤(ポリソルベート80等)から選択される添加剤を含む、従来のポリマーフィルム用添加剤を含んでもよい。
本発明の製剤は、活性コアと、内部層、及び/又は外部層をコーティングする上部コーティング層との間に追加(又は分離)層を有していてもよい。
「コア」は、内部層が適用される固形物である。コアは任意の好適な剤形、例えば、錠剤、ペレット、顆粒、微粒子、硬質若しくは軟質カプセル、又はマイクロカプセルであってよい。好ましい実施形態では、コアは錠剤又はカプセルである。
本発明の第2の態様によれば、治療によるヒト又は動物の身体の医学的処置の方法において使用するための、第1の態様による製剤が提供される。
本発明の第6の態様によれば、第1の態様による結腸に薬物を送達するための経口投与用遅延放出性薬物製剤を製造するための方法が提供される。この方法は、
薬物を含むコアを形成し、
上述した第3のポリマー材料を溶媒系中に含む内部コーティング調製品を使用して前記コアをコーティングし、内部被覆コアを形成し、
結腸細菌による攻撃を受けやすい第1のポリマー材料及び約pH6以上のpH閾値を有する第2のポリマー材料を溶媒系中に含む外部コーティング調製品で前記内部被覆コアをコーティングし、外部被覆コアを形成する
ことを含み、
前記第3のポリマー材料は非イオン性ポリマーであり、前記内部コーティング調製品は緩衝剤及び塩基からなる群から選択される少なくとも1種の添加剤を含む。
薬物を含むコアを形成し、
腸液又は胃腸液に可溶である非イオン性ポリマーを溶媒系中に含む分離層コーティング調製品、及び腸液又は胃腸液に可溶である第3のポリマー材料を溶媒系中に含む内部層コーティング調製品からなる群から選択される少なくとも1種のコーティング調製品を使用して前記コアをコーティングし、中間被覆コアを形成し、及び
結腸細菌による攻撃を受けやすい第1のポリマー材料の水性調製品を約pH6以上のpH閾値を有する第2のポリマー材料の有機調製品と組み合わせて、外部層コーティング調製品を形成し、
前記中間被覆コアを前記外部層コーティング調製品でコーティングして、外部層被覆コアを形成する
ことを含み、
前記第3のポリマー材料は、非イオン性ポリマーであり、前記内部コーティング調製品は、緩衝剤及び塩基から選択される少なくとも1種の添加剤を含む。
従来の遅延放出性剤形からの薬物放出プロファイルはしばしば、胃の状態、即ち胃が「摂食」状態か「絶食」状態かに依存する。簡単に言うと、「摂食状態」はtlag、即ち剤形からの薬物の初期放出までの時間に影響し得る胃滞留時間の増大につながる。加えて、胃を出た後のin vivo溶解が速いと、Cmax、即ち薬物のピーク血漿濃度の増大がもたらされ得る。
被覆された5ASA剤形について、アルコール誘導性の早期放出(用量のダンピング(dose dumping))が観察された(Fadda他、(2008)「Impairment of drug release from modified release formulations in the presence of alcohol(アルコールの存在下での放出改善製剤からの薬物放出の障害)」Int. J. Pharm. 360;171−176)。予備的な結果は、0.1NのHCl中40%エタノールに2時間曝露した場合、本発明による製剤は、胃の中でのアルコール誘導性の分解に対してより耐性があり、したがってアルコールの影響をあまり被らないということを示している。この予備的な結果を確かめるためにはさらなる研究が提案される。
5−アミノサリチル酸(メサラジンEP)は、Cambrex Karlskoga社(スウェーデン・カールスクーガ)から購入した。ラクトース(Tablettose80)は、Meggle(独国ハンブルク)から購入した。デンプングリコール酸ナトリウム(Explotab(商標))は、JRS Pharma(独国ローゼンベルク)から購入した。タルクは、Luzenac Deutschland社(独国デュッセルドルフ)から購入した。ポリビニルピロリドン(PVP)は、ISP Global Technologies(独国ケルン)から購入した。ステアリン酸マグネシウムは、Peter Greven社(独国バート・ミュンスターアイフェル)から購入した。Eudragit(登録商標)S100、Eudragit(登録商標)L30D−55及びEudragit(登録商標)FS30Dはすべて、Evonik社(独国ダルムシュタット)から購入した。トウモロコシデンプン(NI−460及びEurylonVI若しくは6)は、Roquette(仏国レストロン)から購入した。ポリソルベート80、ブタン−1−オール及び水酸化ナトリウムはすべて、Sigma−Aldrich(スイス・ブックス)から購入した。リン酸二水素カリウム、グリセリルモノステアレート(GMS)、クエン酸トリエチル(TEC)及びアンモニア溶液(25%)はすべて、VWR International LTD(英国プール)から購入した。
流動床造粒とそれに続くブレンディング及び圧縮によって寸法14.5×5.7mmの楕円形に成形した400mgの5ASA錠剤コアを調製した。各錠剤は76.9重量%の5ASA(400mg;薬物);14.7重量%のラクトース(充填剤);1.7重量%のPVP(バインダー);3.5重量%のデンプングリコール酸ナトリウム(崩壊剤);並びに2重量%のタルク及び1.2重量%のステアリン酸マグネシウム(潤滑剤)を含有していた。
湿式造粒によって楕円形に成形した1200mgの5ASA錠剤コア(寸法21×10mmを有する)を調製した。各錠剤は85.7重量%の5ASA(1200mg)、9.2重量%の微結晶セルロース、1.7重量%のHPMC、2.9重量%のデンプングリコール酸ナトリウム、及び0.5重量%のステアリン酸マグネシウムを含有していた。
内部層
内部コーティング層は、pHをpH8に調整したEudragit(登録商標)−S100の水性調製品を用いて適用した。内部層の組成はまた、50%のクエン酸トリエチル(乾燥ポリマー重量基準)、10%のリン酸二水素カリウム(乾燥ポリマー重量基準)、10%グリセリルモノステアレート(GMS;乾燥ポリマー重量基準)及び40%のポリソルベート80(GMS重量基準)を含んでいた。pH8が得られるまで1MのNaOHを用いてpHを調整した。リン酸二水素カリウム及びクエン酸トリエチルを蒸留水に溶解し、次いで機械撹拌下でEudragit(登録商標)−S100を分散させた。次にこの分散液のpHを1MのNaOHを用いてpH8に調整し、1時間混合を続けた。
外部コーティング層は、水性デンプン分散液と有機Eudragit(登録商標)−S100溶液との混合物から適用した。
分離層
HPMCと20%のポリエチレングリコール6000(PEG6000)(乾燥ポリマー重量基準)との混合物を含有する分離層を使用した。
内部層を、pHをpH8に調整したEudragit(登録商標)L30D−55の水性コーティング調製品から適用した。内部層の組成はまた、20%のTEC(乾燥ポリマー重量基準)、1%のリン酸二水素カリウム(乾燥ポリマー重量基準)及び50%のタルク(乾燥ポリマー重量基準)を含んでいた。pH8が得られるまで1MのNaOHを用いてpHを調整した。
外部層を、水性デンプン分散液と水性Eudragit(登録商標)S100溶液との混合物から適用した。
分離層
分離層は、HPMCと20%のポリエチレングリコール6000(PEG6000)(乾燥ポリマー重量基準)との混合物によって形成する。
内部層は、pHをpH8に調整したEudragitL30D−55の水性調製品から適用する。内部層の組成はまた、20%のTEC(乾燥ポリマー重量基準)、1%のリン酸二水素カリウム(乾燥ポリマー重量基準)、及び50%のタルク(乾燥ポリマー重量基準)を含んでいる。pH8が得られるまで1MのNaOHを用いてpHを調整する。
外部層は、Eudragit(登録商標)L30D−55とグアーガムとの混合物から適用する。
分離層
分離層はポリビニルアルコール、即ちPVA(Opadry85F)から構成される。
内部層は、ポリビニルアルコール(Opadry85F)及び20%のリン酸二水素カリウム(Opadry85F基準)から構成される。
外部層製剤は、水性デンプン分散液とEudragit(登録商標)S100及びEudragit(登録商標)FS30Dの50:50ブレンド(乾燥ポリマー基準)の水性分散液との混合物から適用する。
分離層
実施例3と同様に分離層を形成したが、コーティングパラメータは以下の通りであった:吹付け速度2.33g/min/kg錠剤コア、噴霧圧力0.7バール、給気量16.3m3/h/kg錠剤コア、及び生成物温度33℃。
内部層の組成が(50%ではなく)70%のクエン酸トリエチル(乾燥ポリマー重量基準)及び(10%ではなく)1%のリン酸二水素カリウム(乾燥ポリマー重量基準)を含み、コーティング調製品を分離層被覆した1200mgの錠剤上に、有孔パンコーティング機を用いてコーティングし、コーティングパラメータが以下の通り:吹付け速度2.9g/min/kg錠剤、噴霧圧力0.6バール、給気量16.3m3/h/kg錠剤、及び生成物温度33℃であったことを除いて、実施例1と同様にして、内部コーティング層を形成した。
13.18%のベンガラ(Eudragitポリマー重量基準)及び2.27%の黄色酸化鉄(Eudragitポリマー重量基準)を高せん断ホモジナイズ下でエタノール中に懸濁し、この懸濁液をデンプンとEudragitとの混合物に加え、これをさらに30分間混合してから、GMSを添加したことと、コーティング調製品を内部層で被覆した1200mgの5ASA錠剤上に有孔パンコーティング機を用いてコーティングしたこと、及びスプレーコーティングパラメータが以下の通り:吹付け速度3.1g/min/kg錠剤、噴霧圧力0.4バール、給気量21.7m3/h/kg錠剤、及び生成物温度34℃であったことを除いて、実施例1と同様にして外部コーティング層を形成した。
分離層
実施例3に記載した通りに、分離層を1200mgの5ASA錠剤コア上に形成した。
実施例5に記載した通りに、内部層を分離層被覆した1200mgの5ASA錠剤コア上に形成した。
トウモロコシデンプン:ブタン−1−オール:水の比率を1:1:約9.5としたこと、デンプン:EudragitSの比率を50:50としたこと、及びスプレーパラメータが以下の通り:吹付け速度7.4g/min/kg錠剤、噴霧圧力0.4バール、給気量40m3/h/kg錠剤、及び生成物温度34℃であったことを除いて、実施例5に記載した通りに、外部コーティング層を、内部層被覆5ASA錠剤コア上に形成した。
分離層
流動床スプレーコーティング機を使用し、コーティングパラメータが以下の通り:吹付け速度3.1g/min/kg錠剤、噴霧圧力0.2バール、及び給気温度40℃であったことを除いて、実施例3に記載した手順を用いて、分離層を400mgの5ASA錠剤コアに適用した。
内部層の組成が(50%ではなく)70%のクエン酸トリエチル(乾燥ポリマー重量基準)及び(10%ではなく)1%のリン酸二水素カリウム(乾燥ポリマー重量基準)を含んでいたことを除いて、実施例1に記載したのと同様にして、内部コーティング層を適用した。さらに、内部コーティング層調製品を、分離層被覆した400mgの5ASA錠剤コア上にコーティングした。
13.18%のベンガラ(Eudragitポリマー重量基準)及び2.27%の黄色酸化鉄(Eudragitポリマー重量基準)を高せん断ホモジナイズ下でエタノール中に懸濁し、この懸濁液をデンプンとEudragitとの混合物に加え、これをさらに30分間混合してからGMSを添加したこと、及び外部コーティング層調製品を内部層被覆した400mgの5ASA錠剤コア上にコーティングしたことを除いて、実施例1と同様に、外部コーティング層を形成した。コーティングパラメータは以下の通りであった:吹付け速度11ml/min/kg錠剤、噴霧圧力0.2バール、及び給気温度40℃。
Eudragit(登録商標)−S100を含有するコーティング層を有機コーティング組成物として適用した。このコーティング組成物は、20%のクエン酸トリエチル(乾燥ポリマー重量基準)、10%のグリセリルモノステアレート(乾燥ポリマー重量基準)、及び40%のポリソルベート80(GMS重量基準)を含有していた。簡単に言うと、クエン酸トリエチルを96%エタノールに溶解し、その後機械撹拌下でEudragit(登録商標)−S100を溶解し、混合を1時間続けた。
コーティング層組成物は、水性デンプン分散液と有機Eudragit(登録商標)−S100溶液との混合物を含有する。水性デンプン分散液は、トウモロコシデンプンを磁石式撹拌下で、ブタン−1−オール中に分散させ、次いで水中に分散させることによって調製した。トウモロコシデンプン:ブタン−1−オール:水の比率は1:2:22とした。得られた分散液を加熱沸騰させて、一晩撹拌下で冷却した。冷却した調製品の固形分%は、分散液の最終重量基準で計算した(加熱中の蒸発を考慮)。
内部層
内部コーティング層は、pHをpH8に調整されたEudragit(登録商標)−S100の水性調製品によって構成される。内部層の組成はまた、50%のクエン酸トリエチル(乾燥ポリマー重量基準)、10%のリン酸二水素カリウム(乾燥ポリマー重量基準)、10%のグリセリルモノステアレート(乾燥ポリマー重量基準)及び40%のポリソルベート80(GMS重量基準)を含む。1MのNaOHを用いてpH8が得られるまでpHを調整した。リン酸二水素カリウム及びクエン酸トリエチルを蒸留水に溶解し、次いで機械撹拌下でEudragit(登録商標)−S100を分散させた。1MのNaOHを用いてpHをpH8に調整し、1時間混合を続けた。
外部コーティング層はEudragit(登録商標)−S100で構成され、有機溶液として適用される。このコーティング溶液は、20%のクエン酸トリエチル(乾燥ポリマー重量基準)、10%のグリセリルモノステアレート(乾燥ポリマー重量基準)、及び40%のポリソルベート80(GMS重量基準)を含有する。簡単に言うと、クエン酸トリエチルを96%エタノールに溶解し、次いでEudragit(登録商標)−S100を機械撹拌下で溶解し、1時間混合を続けた。
分離層
分離層は、HPMCと20%のポリエチレングリコール6000(PEG6000)(乾燥ポリマー重量基準)との混合物から形成する。
内部層は、EudragitL30D−55の標準(非中和)の水性調製品から作製する。内部層の組成はまた、20%のTEC(乾燥ポリマー重量基準)及び50%のタルク(乾燥ポリマー重量基準)を含む。
外部層は、水性デンプン分散液と水性Eudragit(登録商標)S100再分散液との混合物から作製する。
分離層 分離層を、HPMCと20%のポリエチレングリコール6000(PEG6000)(乾燥ポリマー重量基準)との混合物から適用する。
内部層を、EudragitL30D−55の標準(非中和)の水性調製品から適用した。内部層の組成はまた、20%のTEC(乾燥ポリマー重量基準)及び50%のタルク(乾燥ポリマー重量基準)を含んでいた。
外部層はEudragitL30D−55とグアーガムとの混合物を含有する。
分離層
分離層はポリビニルアルコール(Opadry85F)から構成された。
外部層製剤は、水性デンプン分散液とEudragit(登録商標)S100及びEudragit(登録商標)FS30Dの50:50ブレンド(乾燥ポリマー基準)の水性分散液との混合物から適用する。
分離層
分離層被覆した1200mgの5ASA錠剤コアを、比較例4と同様に調製した。
分離層
分離層被覆した1200mgの5ASA錠剤コアを、比較例4と同様に調製した。
外部層は、水性デンプン分散液と水性EudragitS100再分散液との混合物から適用する。
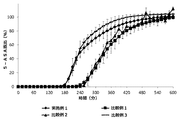
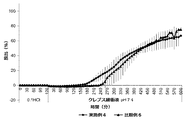
USPのII型装置により、50rpmのパドル速度及び37±0.5℃の媒体温度を用いて、in vitro溶解研究を行った。錠剤は、まず0.1MのHCl中で2時間、次いでクレブス緩衝液(pH7.4)中で8又は10時間試験した。緩衝液のpHは5%CO2/95%O2を連続注入することによって7.4±0.05で安定化させた。5分おきに、HCl中では吸光波長301nmで、及びクレブス緩衝液中では330nmで吸光度測定を行った。クレブス緩衝液1リットル当たりの組成は、0.16gのKH2PO4、6.9gのNaCl、0.35gのKCl、0.29gのMgSO4・7H2O、0.376gのCaCl2・2H2O、及び2.1gのNaHCO3である。15分間隔で取られた測定のみを図1に示す。
製剤を試験するのに用いた発酵アッセイは、Hughes他(「In vitro fermentation of oat and barley derived beta−glucans by human faecal microbiota(ヒト糞便微生物叢によるエンバク及びオオムギ由来のβ−グルカンのin vitro発酵)」、FEMS Microbiol. Ecol.;2008;64(3);pp.482−493)の方法を基本とした。
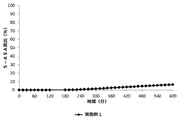
薬物放出試験#2と同様だが、糞便スラリーのpHをpH6.5に維持した。
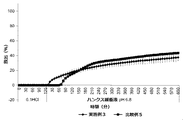
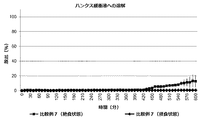
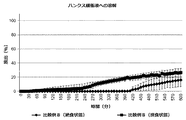
USPのII型装置により、50rpmのパドル速度及び37±0.5℃の媒体温度を用いて、in vitro溶解研究を行った。錠剤は、まず0.1MのHCl中で2時間、次いでハンクス緩衝液(pH6.8)中で8又は10時間試験した。緩衝液のpHは、5%CO2/95%O2を連続注入することによって6.8±0.05で安定化させた。5分おきに、HCl中では吸光波長301nmで、及びハンクス緩衝液pH6.8中では330nmで吸光度測定を行った。ハンクス緩衝液1リットル当たりの組成は、0.06gのKH2PO4、0.06gのNa2HPO4・2H2O、8.0gのNaCl、0.4gのKCl、0.2gのMgSO4・7H2O、0.139gのCaCl2・2H2O及び0.350gのNaHCO3である。
USPのII型装置により、50rpmのパドル速度及び37±0.5℃の媒体温度を用いて、in vitro溶解研究を行った。「絶食」状態をシミュレーションする場合は、薬物放出試験#4で記載したやり方で研究を行った。
被覆された錠剤を、崩壊装置において、0.1NのHClの水−アルコール溶液(40%エタノール)を用いて2時間試験した。2時間の終わりに、錠剤の形態を、亀裂及び/又は膨潤の存在について視覚的に評価した。
図1〜4に示した結果により、本発明による被覆錠剤は、比較例の錠剤よりも有意に優れていることが実証される。これに関して、本発明による錠剤について、比較錠剤に対して、第2のポリマー材料のpH閾値(pH7)よりも高いpH(pH7.4)及び該pH閾値よりも低いpH(pH6.8又はpH6.5)の両方で薬物放出の加速が観察される。
Claims (38)
- 薬物を患者の結腸に送達するための、経口投与用の遅延放出性薬物製剤であって、前記製剤は、
コア及びコア用コーティングを含み、該コアは薬物を含み、該コーティングは外部層、並びに、分離層及び内部層からなる群から選択される、コアと外部層との間の少なくとも1つの層を含み、
前記外部層は、結腸細菌による攻撃を受けやすい第1のポリマー材料と、約pH6以上にpH閾値を有する第2のポリマー材料との混合物を含み、
前記内部層は、腸液又は胃腸液に可溶の非イオン性ポリマーである第3のポリマー材料を含み、かつ、前記内部層に緩衝剤及び塩基から選択される少なくとも1種の添加剤を含み、
前記分離層は、腸液又は胃腸液に可溶な非イオン性ポリマーを含み、
前記外部層は、水性媒体中の前記第1のポリマー材料を有機媒体中の前記第2のポリマー材料と組み合わせることによって形成されたコーティング調製品を用いて、内部層又は分離層に直接適用される、
遅延放出性薬物製剤。 - 前記有機媒体が、C1〜C4アルコール、メチルグリコール、ブチルグリコール、アセトン、メチルグリコールアセテート、及びこれらの混合物からなる群から選択される、請求項1に記載の遅延放出性薬物製剤。
- 前記有機媒体がエタノールを含む、請求項1又は請求項2に記載の遅延放出性薬物製剤。
- 前記有機媒体が85〜98%のエタノールである、請求項1〜3のいずれかに記載の遅延放出性薬物送達製剤。
- 前記有機媒体が、約2%〜約10%のポリマー固体を含有する、先行する請求項のいずれかに記載の遅延放出性薬物送達製剤。
- 前記有機媒体が約6%のポリマー固体を含有する、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記水性媒体が、水、C1〜C6アルコール、及びこれらの混合物からなる群から選択される、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記水性媒体が、水と、C1〜C6アルコール、好ましくはブタン−1−オールとの混合物である、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記混合物中の水とアルコールとの比率が、少なくとも5:1、好ましくは約11:1である、請求項8に記載の遅延放出性薬物製剤。
- 前記外部層が、全ポリマー材料に基づいて約2mg/cm2〜約10mg/cm2の厚さを有する、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記外部層が、全ポリマー材料に基づいて約7mg/cm2の厚さを有する、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記外部層が、約3%〜約8%の総重量増加(TWG)の厚さを有する、請求項1〜9のいずれかに記載の遅延放出性薬物製剤。
- 前記外部層が、約5%のTWGの厚さを有する、請求項1〜9のいずれかに記載の遅延放出性薬物製剤。
- 前記第1のポリマー材料及び第2のポリマー材料が、約1:99〜約60:40の比率で外部層中に存在する、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記第1のポリマー材料及び第2のポリマー材料が、約25:75〜約35:65、好ましくは約30:70の比率で外部層中に存在する、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記第1のポリマー材料がデンプンである、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記第2のポリマー材料が、約125,000g/molの分子量、約1:2の酸:エステル比、及び約pH7のpH閾値を有するポリ(メタクリル酸/メチルメタクリレート)コポリマーである、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 内部層の前記非イオン性ポリマー及び分離層の前記非イオン性ポリマーが、独立して、メチルセルロース(MC)、ヒドロキシプロピルセルロース(HPC)、ヒドロキシプロピルメチルセルロース(HPMC)、ポリ(エチレンオキシド)−グラフト−ポリビニルアルコ−ル、ポリビニルピロリドン(PVP)、ポリエチレングリコール(PEG)、及びポリビニルアルコール(PVA)からなる群から選択される、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記製剤が前記分離層及び前記内部層を含む、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記第3のポリマー材料が、分離層の非イオン性ポリマーと同じ非イオン性ポリマーである、請求項19に記載の遅延放出性薬物製剤。
- 前記内部層が、少なくとも1種の緩衝剤及び少なくとも1種の塩基を含む、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記緩衝剤が、1〜16個の炭素原子を有するカルボン酸、アルカリ金属塩、アルカリ土類金属塩、アンモニウム塩、及び可溶性金属塩からなる群から選択される、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記緩衝剤がリン酸塩である、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記緩衝剤がリン酸二水素カリウムである、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記緩衝剤が、第3のポリマー材料の乾燥重量に基づいて約0.1重量%〜約20重量%の量で内部層中に存在する、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記塩基が、水酸化物塩基、アルカリ金属重炭酸塩、アルカリ金属炭酸塩、アルカリ金属リン酸塩、アルカリ金属クエン酸塩、又は生理学的に許容されるアミン類からなる群から選択される、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記塩基が水酸化物塩基である、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 前記塩基が水酸化ナトリウムである、先行する請求項のいずれかに記載の遅延放出性薬物製剤。
- 請求項1に記載の結腸に薬物を送達するための経口投与用の遅延放出性薬物製剤の製造方法であって、前記方法は、
薬物を含むコアを形成し、
腸液又は胃腸液に可溶である非イオン性ポリマーを溶媒系中に含む分離層コーティング調製品及び腸液又は胃腸液に可溶である第3のポリマー材料を溶媒系中に含む内部層コーティング調製品からなる群から選択される少なくとも1種のコーティング調製品を使用して前記コアを被覆し、中間被覆コアを形成し、
結腸細菌による攻撃を受けやすい第1のポリマー材料の水性調製品を約pH6以上のpH閾値を有する第2のポリマー材料の有機調製品と組み合わせて外部層コーティング調製品を形成し、
前記中間被覆コアを前記外部層コーティング調製品で被覆し、外部層被覆コアを形成する
ことを含み、
前記第3のポリマー材料が非イオン性ポリマーであり、かつ、前記内部コーティング調製品は緩衝剤及び塩基から選択される少なくとも1種の添加剤を含む、
方法。 - 前記分離層コーティング調製品を用いてコアを直接被覆して、前記中間被覆コアを形成する、請求項29に記載の方法。
- 前記内部層コーティング調製品を用いてコアを直接被覆して、前記中間被覆コアを形成する、請求項29に記載の方法。
- 前記分離層コーティング調製品を用いてコアを直接被覆して、分離層被覆コアを形成し、これを次に前記内部層コーティング調製品を用いて直接被覆して、前記中間被覆コアを形成する、請求項29に記載の方法。
- 前記製剤が、請求項2〜28のいずれかに定義される通りである、請求項29〜32のいずれかに記載の方法。
- 前記内部層コーティング調製品又は前記分離層コーティング調製品の溶媒系が水性である、請求項29〜33のいずれかに記載の方法。
- 前記内部コーティング調製品のpHが、約pH7.5〜約pH10、好ましくは約pH7.5〜約pH8.5、より好ましくは約pH8になるように調整される、請求項29〜34のいずれかに記載の方法。
- 前記塩基が、水酸化物塩基、アルカリ金属重炭酸塩、アルカリ金属炭酸塩、アルカリ金属リン酸塩、アルカリ金属クエン酸塩、又は生理学的に許容されるアミン類からなる群から選択される、請求項29〜35のいずれかに記載の方法。
- 前記塩基が水酸化物である、請求項29〜36のいずれかに記載の方法。
- 前記塩基が水酸化ナトリウムである、請求項29〜37のいずれかに記載の方法。
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261640217P | 2012-04-30 | 2012-04-30 | |
| EP12166110.2A EP2659881B1 (en) | 2012-04-30 | 2012-04-30 | A delayed release drug formulation |
| EP12166110.2 | 2012-04-30 | ||
| US61/640,217 | 2012-04-30 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2015509407A Division JP6621662B2 (ja) | 2012-04-30 | 2013-04-29 | 遅延放出性薬物製剤 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2017145268A true JP2017145268A (ja) | 2017-08-24 |
| JP6700220B2 JP6700220B2 (ja) | 2020-05-27 |
Family
ID=54196716
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017112044A Expired - Fee Related JP6700220B2 (ja) | 2012-04-30 | 2017-06-06 | 遅延放出性薬物製剤 |
| JP2017112035A Active JP6626470B2 (ja) | 2012-04-30 | 2017-06-06 | 遅延放出性薬物製剤 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2017112035A Active JP6626470B2 (ja) | 2012-04-30 | 2017-06-06 | 遅延放出性薬物製剤 |
Country Status (10)
| Country | Link |
|---|---|
| JP (2) | JP6700220B2 (ja) |
| CL (2) | CL2017001990A1 (ja) |
| CU (2) | CU24342B1 (ja) |
| CY (1) | CY1121470T1 (ja) |
| EC (2) | ECSP14028079A (ja) |
| HK (1) | HK1244435B (ja) |
| HR (3) | HRP20190470T1 (ja) |
| IL (2) | IL235283A (ja) |
| PH (3) | PH12017502369A1 (ja) |
| ZA (1) | ZA201407675B (ja) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3662900A1 (en) * | 2018-12-07 | 2020-06-10 | Tillotts Pharma AG | Colonic drug delivery formulation |
| ES2994844T3 (en) * | 2018-12-07 | 2025-02-03 | Tillotts Pharma Ag | Colonic drug delivery formulation |
| ES3002632T3 (en) | 2018-12-07 | 2025-03-07 | Tillotts Pharma Ag | Delayed release drug formulation comprising an outerlayer with an enzymatically degradable polymer, its composition and its method of manufacturing |
| CN113493220A (zh) * | 2020-04-02 | 2021-10-12 | 杨洋 | 中空金属氧化物微球及其制备方法和药物缓释用途 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5422121A (en) * | 1990-11-14 | 1995-06-06 | Rohm Gmbh | Oral dosage unit form |
| JP2010526110A (ja) * | 2007-05-07 | 2010-07-29 | エボニック レーム ゲゼルシャフト ミット ベシュレンクテル ハフツング | 薬剤を加速放出する腸溶コーティングを含む固体剤形 |
Family Cites Families (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DK2659881T3 (en) * | 2012-04-30 | 2018-02-05 | Tillotts Pharma Ag | Delayed release drug formulation |
-
2013
- 2013-04-29 HR HRP20190470TT patent/HRP20190470T1/hr unknown
- 2013-04-29 CU CUP2016000014A patent/CU24342B1/xx unknown
- 2013-04-29 HR HRP20192210TT patent/HRP20192210T1/hr unknown
- 2013-04-29 CU CUP2016000026A patent/CU24343B1/xx unknown
-
2014
- 2014-10-22 IL IL235283A patent/IL235283A/en active IP Right Grant
- 2014-10-22 ZA ZA2014/07675A patent/ZA201407675B/en unknown
- 2014-10-22 IL IL235282A patent/IL235282A/en active IP Right Grant
- 2014-11-25 EC ECIEPI201428079A patent/ECSP14028079A/es unknown
- 2014-11-25 EC ECIEPI201428077A patent/ECSP14028077A/es unknown
-
2015
- 2015-03-19 HK HK18103919.2A patent/HK1244435B/en not_active IP Right Cessation
-
2017
- 2017-06-06 JP JP2017112044A patent/JP6700220B2/ja not_active Expired - Fee Related
- 2017-06-06 JP JP2017112035A patent/JP6626470B2/ja active Active
- 2017-08-03 CL CL2017001990A patent/CL2017001990A1/es unknown
- 2017-08-03 CL CL2017001989A patent/CL2017001989A1/es unknown
- 2017-12-20 PH PH12017502369A patent/PH12017502369A1/en unknown
-
2018
- 2018-02-12 PH PH12018500304A patent/PH12018500304A1/en unknown
- 2018-06-19 PH PH12018501311A patent/PH12018501311A1/en unknown
-
2019
- 2019-03-15 CY CY20191100312T patent/CY1121470T1/el unknown
- 2019-04-17 HR HRP20190727TT patent/HRP20190727T1/hr unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5422121A (en) * | 1990-11-14 | 1995-06-06 | Rohm Gmbh | Oral dosage unit form |
| JP2010526110A (ja) * | 2007-05-07 | 2010-07-29 | エボニック レーム ゲゼルシャフト ミット ベシュレンクテル ハフツング | 薬剤を加速放出する腸溶コーティングを含む固体剤形 |
Non-Patent Citations (1)
| Title |
|---|
| DAN. MED. BULL., vol. 46, no. 3, JPN6016046566, 1999, pages 183 - 196, ISSN: 0003951680 * |
Also Published As
| Publication number | Publication date |
|---|---|
| IL235282A (en) | 2017-09-28 |
| CU20160026A7 (es) | 2016-05-30 |
| CL2017001990A1 (es) | 2018-03-16 |
| JP2017145267A (ja) | 2017-08-24 |
| CL2017001989A1 (es) | 2018-03-16 |
| IL235283A (en) | 2017-09-28 |
| PH12018501311A1 (en) | 2020-09-14 |
| HK1202267A1 (en) | 2015-09-25 |
| HK1202266A1 (en) | 2015-09-25 |
| HK1244435B (en) | 2019-10-25 |
| CU20160014A7 (es) | 2016-04-25 |
| CU24342B1 (es) | 2018-05-08 |
| JP6626470B2 (ja) | 2019-12-25 |
| PH12017502369A1 (en) | 2020-09-28 |
| HRP20190470T1 (hr) | 2019-05-17 |
| PH12018500304B1 (en) | 2018-09-24 |
| CY1121470T1 (el) | 2020-05-29 |
| HRP20190727T1 (hr) | 2019-06-14 |
| ECSP14028079A (es) | 2015-12-31 |
| HRP20192210T1 (hr) | 2020-02-21 |
| ECSP14028077A (es) | 2015-12-31 |
| JP6700220B2 (ja) | 2020-05-27 |
| PH12018500304A1 (en) | 2018-09-24 |
| ZA201407675B (en) | 2016-05-25 |
| CU24343B1 (es) | 2018-05-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP6621662B2 (ja) | 遅延放出性薬物製剤 | |
| JP6273356B2 (ja) | 遅延放出性薬物製剤 | |
| JP6700220B2 (ja) | 遅延放出性薬物製剤 | |
| HK1244435A (en) | A delayed release drug formulation | |
| HK1240817A (en) | A delayed release drug formulation | |
| HK1202267B (en) | A delayed release drug formulation |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20170626 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20180228 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20180521 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20180831 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20190109 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190509 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20190531 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20190702 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20190814 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20191106 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200213 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200214 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20200318 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20200327 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20200414 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20200430 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 6700220 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| LAPS | Cancellation because of no payment of annual fees |