JP2022523402A - 術後認知機能障害の予防及び治療のための化合物 - Google Patents
術後認知機能障害の予防及び治療のための化合物 Download PDFInfo
- Publication number
- JP2022523402A JP2022523402A JP2021551941A JP2021551941A JP2022523402A JP 2022523402 A JP2022523402 A JP 2022523402A JP 2021551941 A JP2021551941 A JP 2021551941A JP 2021551941 A JP2021551941 A JP 2021551941A JP 2022523402 A JP2022523402 A JP 2022523402A
- Authority
- JP
- Japan
- Prior art keywords
- surgery
- methyl
- subject
- substituted
- compound
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/15—Oximes (>C=N—O—); Hydrazines (>N—N<); Hydrazones (>N—N=) ; Imines (C—N=C)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/28—Drugs for disorders of the nervous system for treating neurodegenerative disorders of the central nervous system, e.g. nootropic agents, cognition enhancers, drugs for treating Alzheimer's disease or other forms of dementia
Landscapes
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Psychiatry (AREA)
- Hospice & Palliative Care (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
Abstract
Description
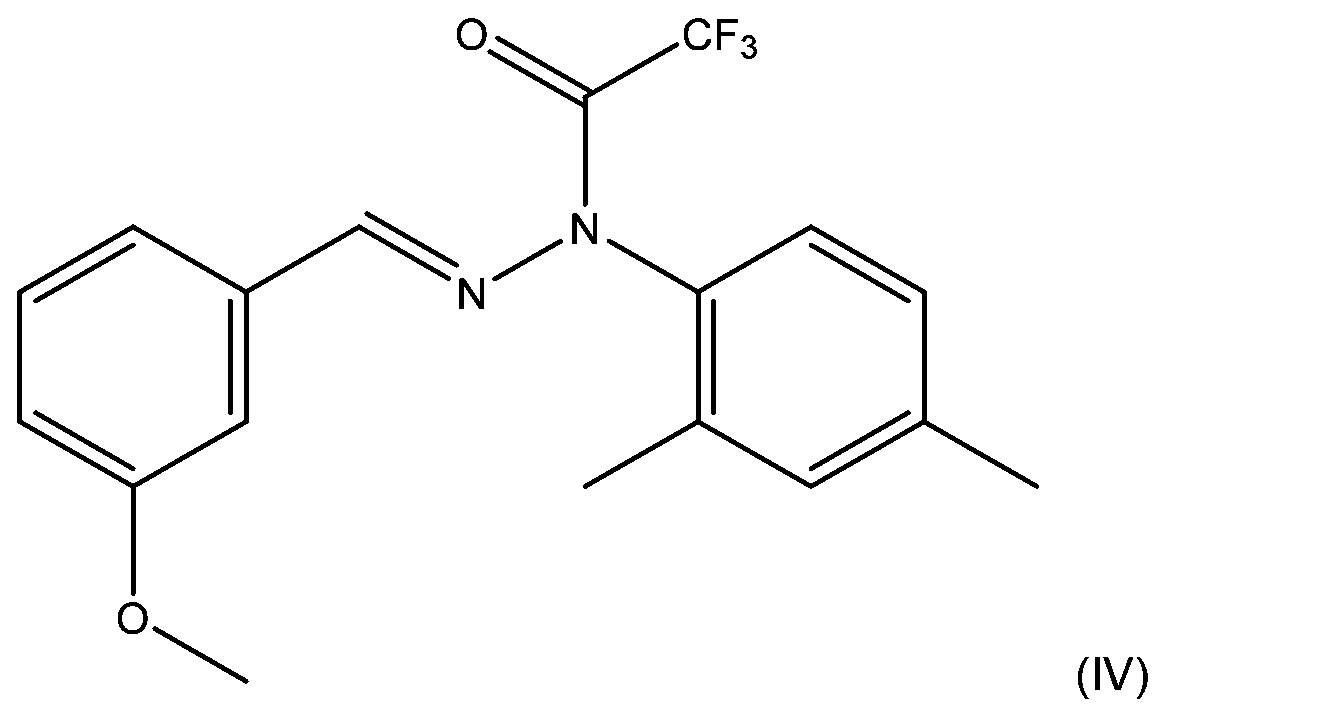
幾つかの実施形態では、POCD又はその1つ以上の症状の予防又は治療に使用するための化合物が提供される。幾つかの実施形態では、本発明の化合物は、式Iの構造:
(i)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はメチルであり、RB4はメチルであり;
(ii)RA2、RA3、RA5、及びRA6はHであり、RA4はメトキシであり、RB2はメチルであり、RB4はメチルであり;
(iii)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はHであり、RB4はHであり;
(iv)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はメチルであり、RB4はメチルであり;
(v)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はHであり、RB4はHであり;
(vi)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はHであり、RB4はメチルであり;
(vii)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はHであり、RB4はメチルであり;
(viii)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はメチルであり、RB4はHであり;
(ix)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はメチルであり、RB4はHであり;
(x)RA2、RA3、RA5、及びRA6はHであり、RA4はCOOHであり、RB2はメチルであり、RB4はメチルであり;
(xi)RA2、RA4、及びRA5はHであり、RA3及びRA6はヒドロキシルであり、RB2はメチルであり、RB4はメチルであり;
(xii)RA2、RA4、及びRA6はHであり、RA3及びRA5はヒドロキシルであり、RB2はメチルであり、RB4はメチルであり;
(xiii)RA2、RA4、及びRA5はHであり、RA3はメトキシであり、RA6はFであり、RB2はHであり、RB4はClであり;
(xiv)RA3及びRA5はHであり、RA2及びRA6はFであり、RA4はヒドロキシルであり、RA6はFであり、RB2はHであり、RB4はFであり;
(xv)RA2、RA4、及びRA6はHであり、RA3はヒドロキシルであり、RA5はFであり、RB2はHであり、RB4はFであるか;又は
(xvi)RA2、RA5、及びRA6はHであり、RA3及びRA4を合わせて-O-CH2-O-であり、RA5はFであり、RB2はHであり、RB4はFである。
術後認知機能障害(POCD)又はその1つ以上の症状を予防、軽減、遅延、及び/又は治療する方法が、本明細書に提示され、この方法は、ある特定の実施形態では、治療的有効量の本発明の化合物、又は本発明の化合物を含む医薬組成物を、対象(例えば、それを必要とする対象)に投与するステップを含む。ある特定の実施形態では、POCDは、医療処置後に発生する新しい認知障害又は認知機能の低下であり、術前及び術後の認知力検査の結果を比較することによって診断することができる。幾つかの実施形態では、POCDは、医療処置(例えば、大手術)によって誘発される認知機能の障害又は低下である。幾つかの実施形態では、POCDは、本明細書に開示される方法によって予防又は治療(例えば、軽減、遅延、及び/又は排除)することができる、認知機能の慢性の障害又は低下(すなわち、慢性POCD)である。幾つかの実施形態では、慢性POCDとは、治療がない場合に6ヶ月超、12ヶ月超、又は18ヶ月超の間持続しうる、医療処置によって誘発される認知機能の慢性障害又は認知機能の低下を指す。したがって、幾つかの実施形態では、方法は、治療的有効量の本明細書に開示される化合物を対象に投与することを含む、対象における慢性の術後認知機能障害(POCD)又はその1つ以上の症状を予防又は治療するステップを含む。幾つかの実施形態では、POCDは、本明細書に開示される方法によって予防及び/又は治療(例えば、軽減、遅延、及び/又は排除)することができる、認知機能の急性障害又は認知機能の急性低下(すなわち、急性POCD)である。幾つかの実施形態では、急性POCDは、医療処置によって誘発される認知機能の障害又は認知機能の低下であり、これは、医療処置後、最長6ヶ月、最長12ヶ月、最長20ヶ月、又は最長36ヶ月持続しうる。したがって、幾つかの実施形態では、方法は、治療的有効量の本明細書に開示される化合物を対象に投与することを含む、対象における急性術後認知機能障害(POCD)又はその1つ以上の症状を予防又は治療するステップを含む。術後認知機能障害のさらなる非限定的な例には、術後の記憶喪失、術後の集中力の喪失、術後のせん妄、術後の急性錯乱状態、術後の意識低下、及び術後の認知機能の低下が含まれ、これらはすべて、医療処置によって誘発されるか、医療処置の結果である。幾つかの実施形態では、POCDとは、医療処置によって増悪又は悪化する既存の認知状態を指す。幾つかの実施形態では、POCDとは、医療処置によって増悪及び/又は悪化する既存の(例えば、事前に診断された)神経変性疾患の急性又は慢性の増悪及び/又は悪化を指す。
「対象」という用語は、哺乳動物を指す。任意の適切な哺乳動物が、本明細書に記載される方法又は組成物によって治療されうる。哺乳動物の非限定的な例には、ヒト、非ヒト霊長類(例えば、類人猿、ギボン、チンパンジー、オランウータン、サル、マカクなど)、家畜(例えば、犬及び猫)、畜産動物(例えば、ウマ、ウシ、ヤギ、ヒツジ、ブタ)、及び実験動物(例えば、マウス、ラット、ウサギ、モルモット)が含まれる。幾つかの実施形態では、対象は、非ヒト霊長類又はヒトである。幾つかの実施形態では、対象はヒトである。対象は、任意の年齢又は発達の任意の段階(例えば、成人、十代、子供、乳児、又は子宮内の哺乳動物)でありうる。対象は、男性/オス又は女性/メスでありうる。
幾つかの実施形態では、医療処置は、小手術及び/又は大手術を含む。ある特定の実施形態では、手術は、外科的切開を伴う侵襲的な医療プロセスである。医療処置には、局所麻酔又は全身麻酔の使用が含まれうる。大手術の非限定的な例には、腹腔を開くことを含む手術、頭蓋骨の欠損を伴う手術、重度の出血のリスクを伴う手術、患者の生命が危険にさらされる手術、主要臓器(例えば、心臓、肺、腎臓、胃、腸、骨、脳、胃、膵臓、胆嚢、虫垂、結腸、及び肝臓)の完全な又は部分的な摘出、置換、又は修復を伴う手術など、及びそれらの組合せが含まれる。幾つかの実施形態では、大手術は、(例えば、最初の切開から閉鎖縫合まで測定して)少なくとも0.3時間、少なくとも0.4時間、少なくとも0.5時間、少なくとも1時間、少なくとも1.5時間、少なくとも2時間、又は少なくとも2.5時間の期間を有する外科的処置である。幾つかの実施形態では、大手術は、0.5時間から20時間、又は1時間から15時間の期間を有する外科的処置である。幾つかの実施形態では、医療処置は、少なくとも0.5時間、少なくとも1時間、少なくとも1.5時間、又は少なくとも2時間の全身麻酔を必要とする手術である。大手術のさらなる非限定的な例には、心臓手術、血管形成術、臓器移植手術、臓器又は組織の完全又は部分的除去、脳手術、骨置換又は修復手術 (例えば、膝関節置換術、又は股関節置換術など)、関節固定術、バイパス手術、ヘルニア修復、腹部手術、減量手術、顔面再建、乳房再建手術、植え替え手術、診査手術、切断、および骨盤底手術が含まれる。幾つかの実施形態では、大手術は、対象が手術中に人工呼吸器又は人工心肺装置を必要とする手術である。
幾つかの実施形態では、組成物又は医薬組成物は、本発明の化合物を含む。幾つかの実施形態では、組成物又は医薬組成物は、治療的有効量の本発明の化合物を含む。幾つかの実施形態では、組成物又は医薬組成物は、本明細書に開示される化合物を、1μgから100mg、又は10μgから100μgの範囲の量で含む。幾つかの実施形態では、POCD又はその1つ以上の症状の予防又は治療に使用するための本発明の化合物を含む医薬組成物が提供される。幾つかの実施形態では、医薬組成物は、本発明の化合物と、薬学的に許容される賦形剤、希釈剤、添加剤、又は担体とを含む。
本発明の組成物、医薬組成物、又は化合物を対象に投与する任意の適切な方法を使用することができる。本明細書に開示される本発明の化合物又は組成物の投与のために、任意の適切な製剤及び/又は投与経路を使用することができる(例えば、ここに参照することによってその全体が本明細書に組み込まれる、Fingl et al.1975, “The Pharmacological Basis of Therapeutics”を参照)。適切な製剤及び/又は投与経路は、例えば、対象のリスク、年齢、及び/又は状態を考慮して、医療専門家(例えば、医師)によって選択されうる。投与経路の非限定的な例には、局所又は局部(例えば、経皮的又は皮膚的に(例えば、皮膚又は表皮上)、眼内又は眼の上、鼻腔内、経粘膜、耳、耳内(例えば、鼓膜の後ろ))、経腸(例えば、胃腸管を介して、例えば、経口的に(例えば、錠剤、カプセル、顆粒、液体、乳化型、トローチ剤、又はそれらの組合せとして)、舌下、胃栄養チューブ、直腸などによって、送達される)、非経口投与(例えば、非経口的に、例えば、静脈内、動脈内、筋肉内、腹腔内、皮内、皮下、腔内、頭蓋内、関節内、関節腔に、心臓内、(心臓に)、海綿体内注射、病巣内(病変に)、骨内注入(骨髄に)、脊髄内(脊柱管に)、子宮内、膣内、膀胱内注入、硝子体内)によるなど、又はそれらの組合せが含まれる。
幾つかの実施形態では、本発明の化合物の量(例えば、医薬組成物中)は、治療的有効量である。ある特定の実施形態では、医薬組成物は、治療的有効量の本明細書に開示される化合物を含む。幾つかの実施形態では、治療的有効量の本発明の化合物が対象に投与される。幾つかの実施形態では、本発明の化合物の治療的有効量は、有効な治療成績を得るために必要な量である。ある特定の実施形態では、本発明の化合物の治療的有効量は、本明細書で想定されている医療処置によって誘発されたPOCD、術後のせん妄、術後の急性錯乱状態、術後の意識低下、術後の中枢性抗コリン症候群、術後の無動症、又は術後の認知機能の低下のうちの1つ以上の症状を予防、治療、その重症度を軽減、その発症を遅延、及び/又は緩和するのに十分な量である。治療的有効量の決定は、とりわけ本明細書に提供される詳細な開示に照らして、十分に当業者の能力の範囲内である。
幾つかの実施形態では、本発明の化合物又は本発明の化合物を含む医薬組成物を含むキットが提供される。幾つかの実施形態では、キットは、本発明の化合物を含む医薬組成物の1回以上の用量を含む。幾つかの実施形態では、キットは、1回以上の用量の本明細書に記載される本発明の化合物又はその医薬組成物を含むことができる、1つ以上のパック及び/又は1つ以上の分配装置を含む。パックの非限定的な例には、本明細書に記載される本発明の化合物又は組成物含む、金属、ガラス、又はプラスチックの容器、シリンジ、又はブリスターパックが含まれる。ある特定の実施形態では、キットは、本明細書に記載される本発明の化合物又は組成物を含んでも含まなくてもよい、シリンジ又は吸入器などの分配装置を含む。パック及び/又はディスペンサ装置には、投与のための説明書を添付することができる。パック又はディスペンサには、医薬品の製造、使用、又は販売を規制する政府機関によって規定された形式の容器に関連する通知を添付することもでき、この通知は、ヒト又は動物への投与用の薬物の剤形の機関による承認を反映している。このような通知は、例えば、米国食品医薬品局によって処方薬について承認されたラベル、又は承認された製品インサートでありうる。
この研究では、POCDの動物モデルにおけるJ147の効果を調査した。
オスのウィスターラット(約350g)をランダムに4つの実験群に分けた;非手術;対照腹部手術;手術+急性J147治療(7mg/ラット、強制経口投与による、手術前4~5時間);手術+慢性J147(500mg/kg食物、手術の1週間前から研究終了まで)。時限血液試料を収集した。術後9~11日目、一般的な行動(オープンフィールド:OF)及び認知能力(新規物体/新規位置認識:NOR/NLR;モリス水迷路:MWM)について試験した。14日目、ラットを殺処分にし、さらなる分析のために血液及び脳組織を収集した。(神経)炎症は、循環サイトカインレベル及び脳内のミクログリア活性化によって調査した。
合計60匹のオスのウィスターラット(Wu-Wistar、Envigo社、オランダ国所在)を5つのコホートで研究した。そのために、手術時に各群が約350gになることを確実にするように、ラットを異なる体重クラス(220~280g)の5つの群に分けて注文した。ラットは、実験開始の少なくとも2週間前に施設に到着し、逆転した明暗サイクル12:12下に置かれ、午前9時に消灯とした。ラットは、制御された条件下(温度20±2度、湿度50%±10%)で、標準的なケージに2~3匹の群で収容された。ラットに水とTeklad(Envigo社、2018年)固形飼料(chow food)を自由に与えた。手術後、ラットを個別に収容した。すべての実験の承認は、オランダの該当する動物福祉委員会によって与えられた。
各コホート内で、ラット(コホートあたりn=12)は、非手術、対照手術、手術+急性J147、及び手術+慢性J147を含む4つの実験群に均等に分けられた。非手術及び対照手術群の半分は、ビヒクルの強制経口投与を受け、急性期治療の対照としての役割を果たした。
急性経口治療のために、結晶性J147を「懸濁ベース」(Fagron社、オランダ国所在)に7mg/mlで懸濁し、均質になるまでボルテックス撹拌した。治療日に、強制経口投与の30分前に1mlの新鮮な懸濁液を調製し、柔軟な強制経口投与チューブを使用して投与した。準備中、強制経口投与容器は、J147の光感度を基準にして、アルミ箔で覆った。経口J147投与(Abrexa社)に関する薬物動態研究に従い、J147懸濁液の強制経口投与は、血漿レベルが最大値に達した、手術の4~5時間前に提供された。対照ラットは、手術時間の4~5時間前に、懸濁液の1mlベースの強制経口投与を受けた。
慢性経口治療のために、J147が500mg/kgの濃度で食餌(Teklad 2018、Envigo社)に添加された。J147はAbrexa社から提供され、Envigo社が食餌を準備した。慢性治療された動物は、手術の1週間前から殺処分まで、J147の食餌を与えられた。J147の食餌は自由に投与された。手術後、明期の最後の1時間の間に、食物摂取量を毎日測定した。J147の食餌は-20℃(暗)で保存された。対照ラットはTeklad 2018の食餌(Envigo社)を受けた。
腹部手術は、Hovensら、2014で以前に説明したように行われた。セボフルラン(空気中±2.5%/O2=2/1)を使用してラットに麻酔をし、0.01mg/kgのブプレノルフィンを皮下投与した。体温を保つために電気毛布を使用した。白線に沿って切開を行い、腸を露出させた。上腸間膜動脈を周囲の組織から隔離し、30分間クランプし、その間、脱水を防ぐために、腸と外科的創傷を生理食塩水に浸したガーゼで覆った。この間、動物には、患者の静脈ラインの挿入を模倣し、時限採血を可能にするために、留置頸静脈カテーテルを備えていた。そのために、鎖骨下領域を切開し、頸静脈を周囲の組織から解放し、カテーテルを導入して、右心房のすぐ上の大静脈へと進行させた。カテーテルの他方の端を頭の皮下に誘導し、歯科用セメントで頭蓋骨に固定した。カテーテルをヘパリン溶液に溶解したPVPで満たし、プラスチックプラグで閉じた。続いて腸間膜動脈クランプを取り外した後、腸を静かに戻し、腹壁と皮膚を別々に縫合糸で閉じた。クランプ及び再灌流は、クランプ部位の遠位の腸間膜動脈における脈動の有無によって視覚的に確認した。誘導から回復まで、手順には約60分を要する。術後、動物を回復させ、その後、個別に収容した。ラットの体重を暗期の最後の1時間に毎日測定した。手術後の最初の5日以内での最大の体重減少を、経験した手術の重症度の尺度として採用した。
行動試験は、ラットの暗(活動)期に実施した。ライトは午後9時に点灯し、午前9時に消灯した。試験には暗期の最初の1時間と最後の1時間は含まれていないため、ラットは暗期の最初の1時間に食べることが可能であった。一般的な探索行動及び不安は、オープンフィールド(OF)試験;モリス水迷路(MWM)での空間学習、空間記憶、及び認知の柔軟性;新規位置認識テスト(NL)での空間作業記憶(NL);物体認識の作業記憶についての新規物体認識テスト(NO)で試験した。
オープンフィールド試験は、探索及び不安行動を評価するために実施した。箱は、中央領域(60×60cm)、4つの側面領域(20×60cm)、及び4つの隅部領域(20×20cm)の領域に分割された正方形(100×100×40cm)で構成した。ラットは、実際の試験の少なくとも1時間前に、箱の中で5分間自由に動けるようにさせることによって、実際の行動試験の前に行動の設定に慣れさせた。試験では、各ラットは箱の中央にランダムな順序で配置され、ラットが中央領域を画成するラインの1つを横切ったときに試験が開始された。5分後、ラットを箱からそっと取り出し、ケージに戻した。各ラットの前に、箱を70%エタノールで洗浄した。ラットの動きと位置は、隅部、壁、及び中央での時間、中央の訪問数、及び歩いた距離として記録され、Ethovision(Noldus社、オランダ所在)で分析した。飼育行動はElineで分析した。探索行動は、試験中にラットが移動した距離と飼育回数によって測定され、不安は、中央領域で過ごした時間の割合及び中央の訪問数の逆数として得た。
新規物体及び新規位置認識は、空間的短期記憶及び物体記憶を評価するために、1つの手順でランダムな順序で試験した。この試験では、2つの透明な壁と2つの灰色の壁を備えた開いた正方形の箱(50×50×40cm)を使用した。試験に用いる物体は、さまざまな物体に対するラットの好みを調査するパイロット研究から選択した。試験の前日に、ラットを3分間、箱に慣れさせた。試験は4つのフェーズで構成され、各フェーズに3分を要した。各フェーズ間には、ラットが試験用の箱に留まる45秒の休憩があった。最初のフェーズは空箱で実施され、2番目のフェーズでは2つの同一の物体が箱の最も近い端の両方の隅部に配置された。このフェーズでは、ラットは両方の物体を探索することが可能であった。この探索フェーズの後、新規物体試験又は新規位置試験のいずれかを実施した。各フェーズの開始前に、両方の物体を箱から取り出し、70%エタノールで洗浄した。新規物体(NO)試験中に、慣れ親しんだ物体の1つを新規物体に置き換え、また、新規位置(NL)試験中には、慣れ親しんだ物体の1つを箱の上部に再配置した。各試験の後、次の動物を入れる前に、箱を70%エタノールで洗浄し、臭いの手がかりを取り除いた。試験は、Elineを使用して手動で分析した。ベースライン探索行動は、ラットがフェーズ2で両方の物体の探索に費やした時間で計算した。新規物体選好性及び新規位置選好性を、新規物体又は再配置された物体の探索に費やされた時間を両方の物体の探索に費やされた時間で割った商として計算した。ベースライン状態で物体の探索に費やされたた時間が3%未満のラットの結果は、以降の分析から除外した。また、位置及び物体の認識で0.00及び1.00のスコアのラットのデータも、以降の分析から除外した。
モリス水迷路は、合計6回のトレーニングセッション、2回の探索試行、及び3回の逆トレーニングセッションで構成されていた。試験は、空間学習、空間記憶、及び認知的柔軟性をそれぞれ評価するために行った。迷路は、水面下1~2cmに沈められた、目に見えないプラットフォームを備えた丸いプール(直径140cm)を必要とした。セッション中、水温は26±1度であった。視覚的な手がかりでプールを取り囲み、それを4つの仮想象限に分割した。プラットフォームは、トレーニングセッション中にターゲット象限に配置し、探索試行中にプールから取り外し、逆トレーニングセッション中に反対の象限に再配置した。
行動試験の3日後、ラットをペントバルビタール(90mg/kg)で麻酔した。心臓に穿刺し、血液試料を採取した。血液試料を1600×gで10分間遠心分離し、血漿を収集して、さらに分析するまで-80℃で保存した。ラットを、ヘパリンを含む生理食塩水による経心臓灌流によって殺処分した。CSF試料を収集した。脳の半分を、海馬、線条体、及び前頭前野に分け、液体窒素で凍結し、分子分析用に-80℃で保存した。脳のもう半分をパラホルムアルデヒド(PFA、4%)で固定し、免疫組織化学的分析用に処理した。
頸静脈カテーテルを備えたすべてのラットから血液試料を採取した。手術の1、6、24時間後(h)に血液を採取した(500μL)。慢性及び急性のJ147治療群の動物については、手術中に採血(250μL)も行った。血液試料を1600×gで10分間遠心分離し、血漿を収集して、さらに分析するまで-80℃で保存した。手術の血液試料は-20℃で保存した。
手術時のJ147の実際のレベルを測定するために、手術時に血液試料を収集した。頸静脈カテーテルから、250μlの血液を10μlの12.5%トリフルオロ酢酸(TFA)を含むK3 EDTAコーティングチューブに採取した。EDTA及びTFAとの接触を促進するためにチューブを数回反転させ、その後、遠心分離するまで氷上に置いた。採取後30分以内(4℃、10分、1600×g)に試料を遠心分離し、血漿を得た。収集した血漿を、さらに分析するまで-20℃で保存した。J147の光感度を基準に、常にバイアルをアルミ箔で包んだ。
脳を室温で36~39時間、0.1M PB中の4%PFAで後固定した。後固定した後の脳を、0.01M PBを伴った4%PFAから、室温で100rpmのシェーカーで±96時間、洗い流した。脳を、96時間以内に8回洗浄した。その後、脳を0.01M PB中、30%スクロース上に室温で一晩置いた。脳が沈んだら、ミリQ水で洗浄し、軽く撫でて乾かした。その後、脳を液体窒素で凍結し、さらに分析するまで-80℃で保存した。
脳を25μmの厚さの切片へと切断し、0.01M PBS+0.1%アジ化ナトリウム中に4℃で浮遊させて保存した。染色する前に、浮遊切片を0.3%H202で30分間、前処理した。
実験グループは次のもので構成される:1.非手術対照食餌;2.非手術対照食餌+ビヒクル強制経口投与;3.手術対照食餌;4.手術対照食餌及びビヒクル強制経口投与;5.手術対照食餌及び急性治療用のJ147強制経口投与;6.手術及び慢性治療用のJ147食餌。全体的な分析では、非手術対照としてプールした群1及び2;治療群5及び6の手術対照としてプールした群3及び4を比較する。
研究を計画通りに実施した。行動の部分は、実験群に均等に分けられた12匹のラットの5つのコホートで研究した。行動を記録し、オフラインで分析した。組織と体液を収集し、変動を制限するために、その後の処理用に同時に保存した。
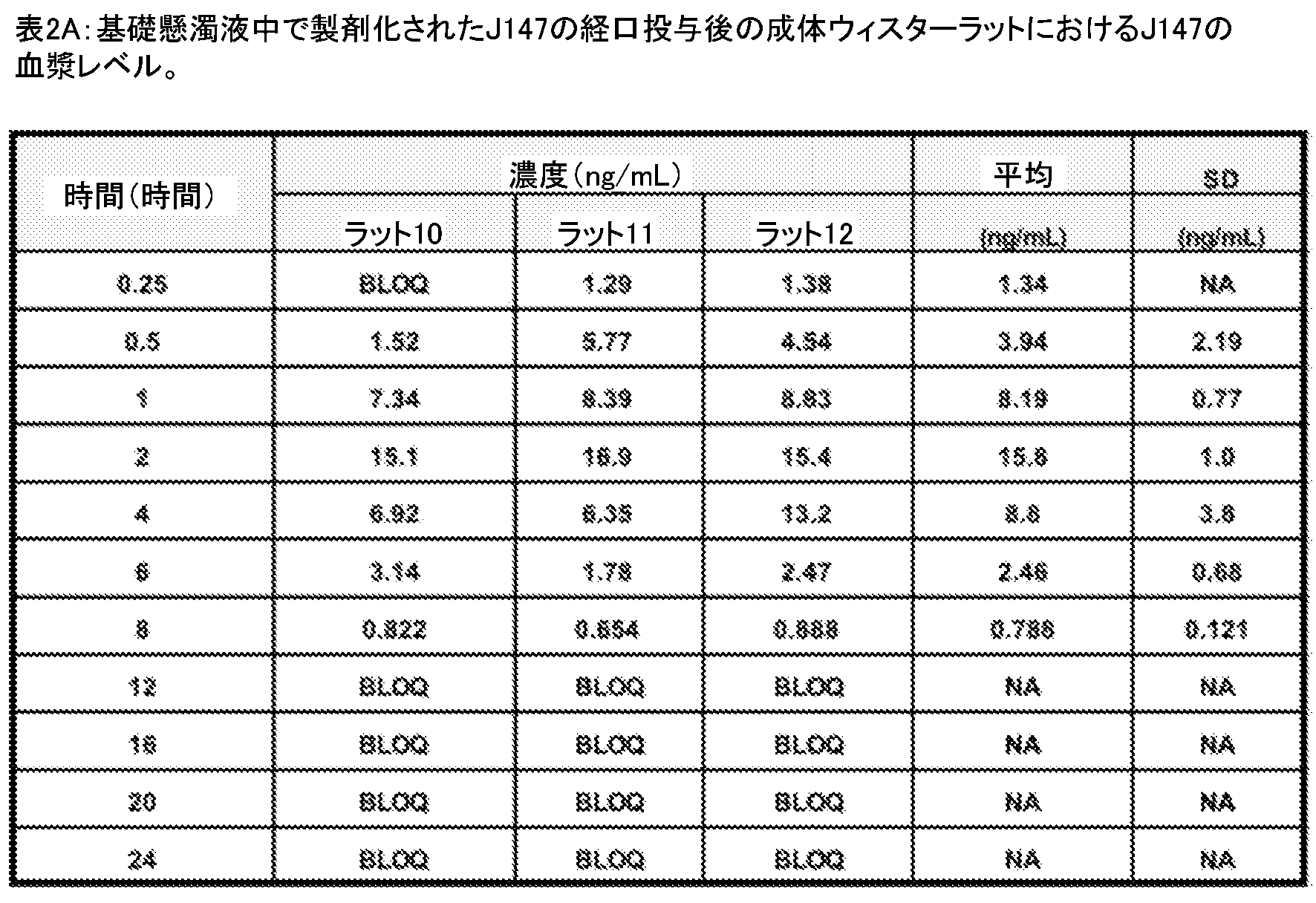
J147治療ラット及び3匹の対照ラットにおいて手術中に得られた血漿試料を、J147の循環レベルについて測定した。20mg/kgの基礎懸濁液中のJ147の経口投与後、及び5mg/kgでの血管内投与後のラットにおけるJ147の血漿及び脳レベルの両方の薬物動態学的測定の結果を以下の表2A~Cに示す。適切なピークの不存在をゼロとすると、平均濃度は対照で0ng/ml、急性治療ラットで3.103ng/ml、慢性治療ラットで0.233ng/mlである。食餌中のJ147レベルも確認した(467mg/kg)。J147食餌を与えられたラットは、食餌を与えられた最初の週に32.0±1.8g増加したが、これは、対照給餌ラットの33.5±3.0gに匹敵し、食餌に対する選好性又は嫌悪感は示唆されなかった。手術及び個別収容後の最初の10日間に、食餌を与えられたラットは平均20±1gを摂取し、これは、対照食を用いた手術での20±1g及び非手術対照での23±1gと同様であり、これにより、10mgのJ147/ラット/日の予想摂取量が確認され、食餌に対する選好性又は嫌悪感がないことをさらに裏付けている。
手術を受けた48匹のラットはすべて生存し、行動試験に供された。1匹のラットが、行動試験と殺処分との間に原因不明で死亡した。ビヒクル強制経口投与の明確な効果は観察されなかったため、対照群をプールし、行動分析のために以下の実験群を得た:非手術対照;手術対照;手術+急性J147;手術+慢性J147(n=15/群)。
オープンフィールド
一般的な探索行動及び不安を調査するために、オープンフィールド試験を使用した。図2は、中央領域にいる時間又は歩行距離に対し、手術又は治療のいずれも有意な影響がないことを示している。しかしながら、特に、J147で慢性治療された手術ラットは、他の群よりも中央で過ごす時間が長くなる傾向がある。実際、これらのラットはかなり頻繁に中央領域を訪れ、かなり多くの飼育行動を示した。
新規物体/新規位置認識(NOR/NLR)
NOR及びNLR試験の結果を表1に示す。空のケージの探索後、ラットに2つの同様の物体を提示した。全体として、群は物体に対して同様の関心を示しており、新規性に対する不安がないことを示唆した。驚いたことに、対照群のより多くのラット(平均45%)は、物体への関心が低いか、物体の一方だけに関心があったために除外する必要があったのに対し、両方の治療群では少なかった(17%)。新規又は再配置された物体に対する選好性における群間での有意差は観察されなかった。NORは群間で区別されなかった;すべての群が新規物体を認識した(手術+急性J147;p=0.083)。NLR試験では、両方の治療群が上記ランダムに実施された。
すべての群が有意な学習プロセスを示し、群間で違いはなかった(図3)。同様の空間学習能力にもかかわらず、空間記憶は、ターゲット象限で費やされた時間とラットがプラットフォームの位置を泳いだ回数からわかるように、群間で有意に異なっていた。記憶の固定化と逆転学習は群間で違いはなかった。それにもかかわらず、最後の学習セッションでの潜時と記憶の固定化との間の非常に有意な相関によって示されるように、最もよく学習したラットは、より良好な記憶の固定化を示した。
表2A~C J147の血漿及び脳レベルの薬物動態測定
表2A~2B。20mg/kgで成体ウィスターラットに経口投与された、基礎懸濁液中で製剤化されたJ147の血漿及び脳レベルの薬物動態測定。
概して、慢性治療ラットは改善を示した。これらのラットは、手術後の体重減少が大幅に減った;OFの中央領域への飼育及び訪問の大幅な増加を示した;NLRで最高のパフォーマンスを発揮し、MWMの空間記憶を大幅に改善した。NOR、空間及び逆転学習は影響を受けなかった。データは、慢性的なJ174が、パワー体重減少及びOFの行動によって示されるように、概して、手術後の状態を改善したことを示唆している。さらには、慢性的J147の投与は、手術後のすべての認知障害を予防することができた。
60歳の男性被験者が心臓バイパス手術を受ける予定であるとする。J147は、手術の24、12、3時間前に1mg/kgの用量で経口投与され、手術の翌日から開始して、手術後1~6週間にわたり、1日1回、複数回投与される。被験者は、手術の前日と1週間後に、1つ以上の適切な認知力検査を実施することによってPOCDについて評価される。手術の1週間後、被験者は認知機能の喪失がないと判断される。
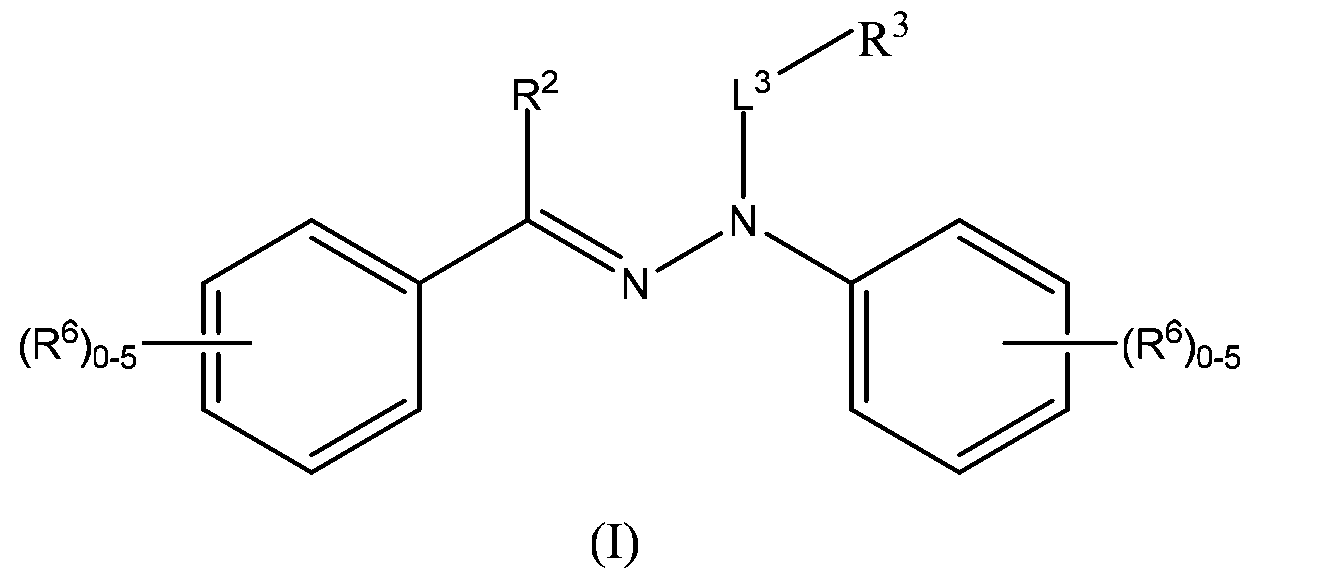
A1. それを必要とする対象における術後認知機能障害(POCD)を治療又は予防する方法であって、治療的有効量の式Iの構造を有する化合物:
[式中、
R2は、H及びメチルからなる群より選択され;
R3は、トリフルオロメチル又は他のフルオロ置換アルキルであり;
L3はカルボニルであり;かつ
R6は、存在ごとに独立して、アルキル、置換アルキル、シクロアルキル、置換シクロアルキル、ヒドロキシル、アルコキシ、置換アルコキシ、アリールオキシ、置換アリールオキシ、メルカプト、アルキルチオ、アリールチオ、カルボニル、アリール、置換アリール、置換複素環式、ハロゲン、シアノ、シアノアルキル、ニトロ、アミノ、アミジノ、カルバメート、S(O)nR7、及びC(O)R8からなる群より選択されるか、又は隣接する位置にある2つのR6が結合して、隣接するフェニル部分と融合した、任意選択的に置換されたヘテロアリール又はヘテロアルキル環を形成し;
R7は、H、R9、NH2、HNR9、又はNR9R10であり;
R8は、OH、OR9、NH2、NHR9、又はNR9R10であり;
R9及びR10は、存在ごとに独立して、任意選択的に置換されたアルキルであり;かつ
n=1又は2である]。
A2. R6が、存在ごとに、アルキル、置換アルキル、ヒドロキシル、アルコキシ、置換アルコキシ、ハロゲン、及びC(O)R8からなる群より選択される、実施形態A1に記載の方法。
A3. R6が、存在ごとに、メチル、メトキシ、ペルフルオロメチル、ペルフルオロメトキシ、ヒドロキシル、Cl、F、及びIからなる群より選択される、実施形態A2に記載の方法。
A4. 化合物が、式IIの構造:
を有する、実施形態A1に記載の方法[式中、
(i)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はメチルであり、RB4はメチルであるか;又は
(ii)RA2、RA3、RA5、及びRA6はHであり、RA4はメトキシであり、RB2はメチルであり、RB4はメチルであるか;又は
(iii)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はHであり、RB4はHであるか;又は
(iv)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はメチルであり、RB4はメチルであるか;又は
(v)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はHであり、RB4はHであるか;又は
(vi)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はHであり、RB4はメチルであるか;又は
(vii)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はHであり、RB4はメチルであるか;又は
(viii)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はメチルであり、RB4はHであるか;又は
(ix)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はメチルであり、RB4はHであるか;又は
(x)RA2、RA3、RA5、及びRA6はHであり、RA4はCOOHであり、RB2はメチルであり、RB4はメチルであるか;又は
(xi)RA2、RA4、及びRA5はHであり、RA3及びRA6はヒドロキシルであり、RB2はメチルであり、RB4はメチルであるか;又は
(xii)RA2、RA4、及びRA6はHであり、RA3及びRA5はヒドロキシルであり、RB2はメチルであり、RB4はメチルであるか;又は
(xiii)RA2、RA4、及びRA5はHであり、RA3はメトキシであり、RA6はFであり、RB2はHであり、RB4はClであるか;又は
(xiv)RA3及びRA5はHであり、RA2及びRA6はFであり、RA4はヒドロキシルであり、RA6はFであり、RB2はHであり、RB4はFであるか;又は
(xv)RA2、RA4、及びRA6はHであり、RA3はヒドロキシルであり、RA5はFであり、RB2はHであり、RB4はFであるか;又は
(xvi)RA2、RA5、及びRA6はHであり、RA3及びRA4を合わせて-O-CH2-O-であり、RA5はFであり、RB2はHであり、RB4はFである]。
を含む治療的有効量の化合物を対象に投与するステップを含む、対象における術後認知機能障害(POCD)又はその1つ以上の症状を予防又は治療する方法。
を含む、実施形態C1からC2のいずれかに記載の方法[式中、R1は、メチル、フルオロメチル、ジフルオロメチル、トリフルオロメチル、ブロモメチル、ジブロモメチル又はトリブロモメチルであり;R2は、OCH3、OCF3、又はOCBr3であり;R3及びR4は、水素、ヒドロキシル、ハロゲン(例えば、Cl、F又はBr)、メチル、メトキシ、又はアミンから独立して選択される]。
Claims (16)
- 対象における術後認知機能障害(POCD)又はその1つ以上の症状を予防、軽減、遅延、又は治療する方法であって、式Iの構造:
を含む、治療的有効量の化合物を前記対象に投与するステップを含む、方法
[式中、
R2は、H及びメチルからなる群より選択され;
R3はトリフルオロメチル又は他のフルオロ置換アルキルであり;
L3はカルボニルであり;
R6は、存在ごとに独立して、アルキル、置換アルキル、シクロアルキル、置換シクロアルキル、ヒドロキシル、アルコキシ、置換アルコキシ、アリールオキシ、置換アリールオキシ、メルカプト、アルキルチオ、アリールチオ、カルボニル、アリール、置換アリール、置換複素環式、ハロゲン、シアノ、シアノアルキル、ニトロ、アミノ、アミジノ、カルバメート、S(O)nR7、及びC(O)R8からなる群より選択されるか、あるいは、隣接する位置にある2つのR6が結合して、前記隣接するフェニル部分と融合した、任意選択的に置換されたヘテロアリール又はヘテロアルキル環を形成し;
R7は、H、R9、NH2、HNR9、又はNR9R10であり;
R8は、OH、OR9、NH2、NHR9、又はNR9R10であり;
R9及びR10は、存在ごとに独立して、任意選択的に置換されたアルキルであり;かつ
n=1又は2である]。 - 前記化合物が、式IIの構造:
を有する、請求項1に記載の方法
[式中、
(i)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はメチルであり、RB4はメチルであるか;又は
(ii)RA2、RA3、RA5、及びRA6はHであり、RA4はメトキシであり、RB2はメチルであり、RB4はメチルであるか;又は
(iii)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はHであり、RB4はHであるか;又は
(iv)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はメチルであり、RB4はメチルであるか;又は
(v)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はHであり、RB4はHであるか;又は
(vi)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はHであり、RB4はメチルであるか;又は
(vii)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はHであり、RB4はメチルであるか;又は
(viii)RA2、RA3、RA4、RA5、及びRA6はHであり、RB2はメチルであり、RB4はHであるか;又は
(ix)RA2、RA4、RA5、及びRA6はHであり、RA3はメトキシであり、RB2はメチルであり、RB4はHであるか;又は
(x)RA2、RA3、RA5、及びRA6はHであり、RA4はCOOHであり、RB2はメチルであり、RB4はメチルであるか;又は
(xi)RA2、RA4、及びRA5はHであり、RA3及びRA6はヒドロキシルであり、RB2はメチルであり、RB4はメチルであるか;又は
(xii)RA2、RA4、及びRA6はHであり、RA3及びRA5はヒドロキシルであり、RB2はメチルであり、RB4はメチルであるか;又は
(xiii)RA2、RA4、及びRA5はHであり、RA3はメトキシであり、RA6はFであり、RB2はHであり、RB4はClであるか;又は
(xiv)RA3及びRA5はHであり、RA2及びRA6はFであり、RA4はヒドロキシルであり、RA6はFであり、RB2はHであり、RB4はFであるか;又は
(xv)RA2、RA4、及びRA6はHであり、RA3はヒドロキシルであり、RA5はFであり、RB2はHであり、RB4はFであるか;又は
(xvi)RA2、RA5、及びRA6はHであり、RA3とRA4を合わせて-O-CH2-O-であり、RA5はFであり、RB2はHであり、RB4はFである]。 - 前記POCDが、医療処置によって誘発されるか、又は医療処置の結果である、請求項1から3のいずれか一項に記載の方法。
- 前記医療処置が大手術を含む、請求項4に記載の方法。
- 前記大手術が、0.5時間から20時間の期間を有する外科的処置を含む、請求項5に記載の方法。
- 前記医療処置が、心臓手術、血管形成術、臓器移植手術、臓器又は組織の完全又は部分的除去、脳手術、骨置換又は修復手術、腹部手術、顔面再建又は修復手術、及び骨盤底手術から選択される、請求項4から6のいずれか一項に記載の方法。
- 前記対象が60歳超、又は65歳超である、請求項1から7のいずれか一項に記載の方法。
- 前記対象がヒトである、請求項1から8のいずれか一項に記載の方法。
- 前記対象が、前記医療処置の前に安定した認知機能を示す、請求項4から9のいずれか一項に記載の方法。
- 前記対象が、前記医療処置の前に、以前に認知障害又は神経変性疾患と診断されていない、請求項4から9のいずれか一項に記載の方法。
- 前記対象が、前記医療処置の前に神経変性疾患と診断される、請求項4から9のいずれか一項に記載の方法。
- 前記神経変性疾患が、アルツハイマー病、パーキンソン病、ハンチントン病、筋萎縮性側索硬化症、緑内障、網膜変性症、黄斑変性症、老人性難聴、軽度の認知機能障害、認知症、進行性核上性麻痺、脊髄小脳失調症、網膜神経障害、末梢神経障害、糖尿病性神経障害、バックグラウンド神経障害、家族性アミロイド多発神経障害、老人性全身性アミロイドーシス、プリオン性疾患、スクレイピー、ウシ海綿状脳症、クロイツフェルト・ヤコブ病、ゲルストマン・シュトロイスラー・シャインカー症候群、及びアミロイド症から選択される、請求項12に記載の方法。
- 前記化合物が、前記医療処置又は手術の前、周術期、最中、又は後に投与される、請求項4から13のいずれか一項に記載の方法。
- 前記化合物が0.5mg/kgから50mg/kgの用量で投与される、請求項1から14のいずれか一項に記載の方法。
- 前記化合物が経口又は静脈内投与される、請求項1から15のいずれか一項に記載の方法。
Applications Claiming Priority (7)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962812309P | 2019-03-01 | 2019-03-01 | |
| US62/812,309 | 2019-03-01 | ||
| US201962929694P | 2019-11-01 | 2019-11-01 | |
| US62/929,694 | 2019-11-01 | ||
| US201962937653P | 2019-11-19 | 2019-11-19 | |
| US62/937,653 | 2019-11-19 | ||
| PCT/US2020/020709 WO2020180823A1 (en) | 2019-03-01 | 2020-03-02 | Compounds for prevention and treatment of post-operative cognitive dysfunction |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2022523402A true JP2022523402A (ja) | 2022-04-22 |
| JP7629678B2 JP7629678B2 (ja) | 2025-02-14 |
Family
ID=72337216
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021551941A Active JP7629678B2 (ja) | 2019-03-01 | 2020-03-02 | 術後認知機能障害の予防及び治療のための化合物 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US20220273590A1 (ja) |
| EP (1) | EP3931178B1 (ja) |
| JP (1) | JP7629678B2 (ja) |
| CN (1) | CN114174255A (ja) |
| CA (1) | CA3132291A1 (ja) |
| ES (1) | ES3036920T3 (ja) |
| WO (1) | WO2020180823A1 (ja) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2025515374A (ja) * | 2022-04-29 | 2025-05-14 | ノエティクス ファルマ エルエルシー | 術後認知機能障害(pocd)の予防と治療 |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU2018387681B2 (en) * | 2017-12-18 | 2024-08-01 | Dsm Ip Assets B.V. | Storage stable mixtures, method of improving retention of a compound and use of rice hulls and/or rice bran to enhance retention of a compound |
| US20210361598A1 (en) * | 2020-04-28 | 2021-11-25 | Abrexa Pharmaceuticals, Inc. | Compounds for prevention and treatment of post-intensive care cognitive dysfunction and cognitive dysfunction resulting from respiratory distress |
| WO2024155966A1 (en) * | 2023-01-20 | 2024-07-25 | Loma Linda University Health | Methods and compositions for treatment of niemann-pick disease type c and charcot-marie-tooth disease |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009052116A1 (en) * | 2007-10-15 | 2009-04-23 | The Salk Institute For Biological Studies | Methods for treating a variety of diseases and conditions, and compounds useful therefor |
| WO2017140684A2 (en) * | 2016-02-15 | 2017-08-24 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the treatment of post-operative cognitive dysfunction |
| JP2018502121A (ja) * | 2014-12-31 | 2018-01-25 | グゥアンヂョウ マグパイ ファーマシューティカルズ カンパニー リミテッド | トリフルオロアセトヒドラジド類化合物及びその調製方法並びに製薬における応用 |
Family Cites Families (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4017540A (en) * | 1968-03-04 | 1977-04-12 | The Upjohn Company | Method of use, composition, and compounds |
| US20100004302A1 (en) * | 2003-04-29 | 2010-01-07 | Connie Erickson-Miller | Methods for Treating Degenerative Diseases/Injuries |
| US20070238700A1 (en) * | 2006-04-10 | 2007-10-11 | Winzenberg Kevin N | N-phenyl-1,1,1-trifluoromethanesulfonamide hydrazone derivative compounds and their usage in controlling parasites |
| US20100099775A1 (en) * | 2008-10-17 | 2010-04-22 | Alpharx Inc. | Method for ameliorating of post-anesthetic recovery |
| WO2011101634A2 (en) * | 2010-02-17 | 2011-08-25 | Imperial Innovations Limited | Methods |
| WO2017112701A1 (en) * | 2015-12-22 | 2017-06-29 | Zogenix International Limited | Metabolism resistant fenfluramine analogs and methods of using the same |
-
2020
- 2020-03-02 ES ES20767071T patent/ES3036920T3/es active Active
- 2020-03-02 CN CN202080030286.1A patent/CN114174255A/zh active Pending
- 2020-03-02 US US17/435,683 patent/US20220273590A1/en active Pending
- 2020-03-02 CA CA3132291A patent/CA3132291A1/en active Pending
- 2020-03-02 WO PCT/US2020/020709 patent/WO2020180823A1/en not_active Ceased
- 2020-03-02 JP JP2021551941A patent/JP7629678B2/ja active Active
- 2020-03-02 EP EP20767071.2A patent/EP3931178B1/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009052116A1 (en) * | 2007-10-15 | 2009-04-23 | The Salk Institute For Biological Studies | Methods for treating a variety of diseases and conditions, and compounds useful therefor |
| US20100305181A1 (en) * | 2007-10-15 | 2010-12-02 | Schubert David R | Methods for treating a variety of diseases and conditions, and compounds useful therefor |
| JP2018502121A (ja) * | 2014-12-31 | 2018-01-25 | グゥアンヂョウ マグパイ ファーマシューティカルズ カンパニー リミテッド | トリフルオロアセトヒドラジド類化合物及びその調製方法並びに製薬における応用 |
| WO2017140684A2 (en) * | 2016-02-15 | 2017-08-24 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods and pharmaceutical compositions for the treatment of post-operative cognitive dysfunction |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2025515374A (ja) * | 2022-04-29 | 2025-05-14 | ノエティクス ファルマ エルエルシー | 術後認知機能障害(pocd)の予防と治療 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20220273590A1 (en) | 2022-09-01 |
| EP3931178A4 (en) | 2022-11-23 |
| CA3132291A1 (en) | 2020-09-10 |
| JP7629678B2 (ja) | 2025-02-14 |
| EP3931178A1 (en) | 2022-01-05 |
| WO2020180823A1 (en) | 2020-09-10 |
| ES3036920T3 (en) | 2025-09-25 |
| EP3931178B1 (en) | 2025-06-25 |
| CN114174255A (zh) | 2022-03-11 |
| EP3931178C0 (en) | 2025-06-25 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102014883B1 (ko) | 근위축성 측삭 경화증 치료용 신규 조성물 | |
| EP3931178B1 (en) | Compounds for prevention and treatment of post-operative cognitive dysfunction | |
| US9907787B2 (en) | Method of supplementing the diet and ameliorating oxidative stress | |
| US8426368B2 (en) | Method of ameliorating oxidative stress and supplementing the diet | |
| US10233198B2 (en) | Pro-drugs of NSAIAs with very high skin and membranes penetration rates and their new medicinal uses | |
| EA030839B1 (ru) | Ингибиторы рециклинга желчных кислот при лечении холестатических заболеваний печени у детей | |
| JP7740810B2 (ja) | 呼吸困難に起因する集中治療後の認知機能障害及び認知障害の予防及び治療のための化合物 | |
| RU2693627C2 (ru) | Комбинации эдаравона для лечения ишемических повреждений мозга | |
| JP2009539996A (ja) | 腎機能障害を持つ個体における利尿改善方法 | |
| RU2341261C2 (ru) | Композиции, содержащие эпотилоны, и их применение для лечения карциноидного синдрома | |
| KR20210148078A (ko) | 조직 관류 증가에 사용하기 위한 이노시톨 포스페이트 화합물 | |
| JPWO2017057562A1 (ja) | 末梢神経障害又は脊髄損傷の治療剤及び/又は予防剤 | |
| US12357596B2 (en) | Compounds for prevention and treatment of obesity and related disorders | |
| US20240226069A1 (en) | Vafidemstat for use in treating autism spectrum disorders | |
| CN111388471B (zh) | 一种治疗胆囊炎的药物及其应用 | |
| US20260076926A1 (en) | Compounds for use in organ preservation and organ transplantation | |
| WO2025135087A1 (ja) | 慢性移植片対宿主病における眼合併症の予防治療用医薬組成物 | |
| HK40089435A (zh) | 预防和治疗重症监护後认知功能障碍和呼吸窘迫致认知功能障碍的化合物 | |
| CN111166868A (zh) | 一种用于治疗神经疾病和障碍的组合物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230227 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240403 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240703 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240903 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241002 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250107 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250131 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7629678 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |