JP2023123760A - ムコ多糖症i型を治療するための遺伝子治療 - Google Patents
ムコ多糖症i型を治療するための遺伝子治療 Download PDFInfo
- Publication number
- JP2023123760A JP2023123760A JP2023108011A JP2023108011A JP2023123760A JP 2023123760 A JP2023123760 A JP 2023123760A JP 2023108011 A JP2023108011 A JP 2023108011A JP 2023108011 A JP2023108011 A JP 2023108011A JP 2023123760 A JP2023123760 A JP 2023123760A
- Authority
- JP
- Japan
- Prior art keywords
- vector
- hidua
- months
- human
- administration
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/43—Enzymes; Proenzymes; Derivatives thereof
- A61K38/46—Hydrolases (3)
- A61K38/47—Hydrolases (3) acting on glycosyl compounds (3.2), e.g. cellulases, lactases
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/005—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'active' part of the composition delivered, i.e. the nucleic acid delivered
- A61K48/0058—Nucleic acids adapted for tissue specific expression, e.g. having tissue specific promoters as part of a contruct
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/63—Introduction of foreign genetic material using vectors; Vectors; Use of hosts therefor; Regulation of expression
- C12N15/79—Vectors or expression systems specially adapted for eukaryotic hosts
- C12N15/85—Vectors or expression systems specially adapted for eukaryotic hosts for animal cells
- C12N15/86—Viral vectors
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/335—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin
- A61K31/34—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having five-membered rings with one oxygen as the only ring hetero atom, e.g. isosorbide
- A61K31/343—Heterocyclic compounds having oxygen as the only ring hetero atom, e.g. fungichromin having five-membered rings with one oxygen as the only ring hetero atom, e.g. isosorbide condensed with a carbocyclic ring, e.g. coumaran, bufuralol, befunolol, clobenfurol, amiodarone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/436—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a six-membered ring having oxygen as a ring hetero atom, e.g. rapamycin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/439—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom the ring forming part of a bridged ring system, e.g. quinuclidine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5377—1,4-Oxazines, e.g. morpholine not condensed and containing further heterocyclic rings, e.g. timolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/57—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone
- A61K31/573—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of two carbon atoms, e.g. pregnane or progesterone substituted in position 21, e.g. cortisone, dexamethasone, prednisone or aldosterone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/76—Viruses; Subviral particles; Bacteriophages
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N7/00—Viruses; Bacteriophages; Compositions thereof; Preparation or purification thereof
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/14—Hydrolases (3)
- C12N9/24—Hydrolases (3) acting on glycosyl compounds (3.2)
- C12N9/2402—Hydrolases (3) acting on glycosyl compounds (3.2) hydrolysing O- and S- glycosyl compounds (3.2.1)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Y—ENZYMES
- C12Y302/00—Hydrolases acting on glycosyl compounds, i.e. glycosylases (3.2)
- C12Y302/01—Glycosidases, i.e. enzymes hydrolysing O- and S-glycosyl compounds (3.2.1)
- C12Y302/01076—L-Iduronidase (3.2.1.76)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2300/00—Mixtures or combinations of active ingredients, wherein at least one active ingredient is fully defined in groups A61K31/00 - A61K41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/0083—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the administration regime
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14121—Viruses as such, e.g. new isolates, mutants or their genomic sequences
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14132—Use of virus as therapeutic agent, other than vaccine, e.g. as cytolytic agent
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2750/00—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA ssDNA viruses
- C12N2750/00011—Details
- C12N2750/14011—Parvoviridae
- C12N2750/14111—Dependovirus, e.g. adenoassociated viruses
- C12N2750/14141—Use of virus, viral particle or viral elements as a vector
- C12N2750/14143—Use of virus, viral particle or viral elements as a vector viral genome or elements thereof as genetic vector
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Medicinal Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Epidemiology (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Virology (AREA)
- Immunology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Plant Pathology (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Physics & Mathematics (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Mycology (AREA)
- Dermatology (AREA)
- Obesity (AREA)
- Diabetes (AREA)
- Hematology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
【解決手段】ヒト患者におけるα-L-イズロニダーゼ欠損症の治療に有用な治療レジメンであって、(a)AAV9カプシド、及び患者においてその発現を指令する調節性配列の制御下にあるヒトα-L-イズロニダーゼをコードする配列を含む核酸を有する組換えAAV;(b)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤から選択される、第1の免疫抑制剤;並びに(c)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤から選択される、第2の免疫抑制剤を患者に投与することを含む、レジメンとする。
【選択図】図22
Description
本出願には、米国政府からの助成金、国立衛生研究所(NIH)番号R01DK54481、P40OD010939及びP30ES013508によってある程度支援された研究が含まれている。米国政府は本発明に特定の権利を有してもよい。
本発明は、ハーラー症候群、ハーラー・シャイエ症候群及び/またはシャイエ症候群であると診断された患者を含むムコ多糖症I型(MPS I)を治療するための遺伝子治療のアプローチに関する。
-イズロニダーゼ(hIDUA)をコードする配列を含む核酸であって、ヒトhIDUAコード配列が、機能的hIDUAをコードする配列番号1のヌクレオチド配列または配列番号1と少なくとも約80%同一である配列を有する、核酸;(b)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第1の免疫抑制剤;並びに(c)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第2の免疫抑制剤を患者に投与することを含み、ここで、免疫抑制剤の少なくとも一方の投与は、AAVベクターの送達の前または同日に開始し;免疫抑制剤の少なくとも一方の投与は、ベクター投与後少なくとも8週間継続する。患者には、最初に静脈内ステロイドを投与し、続いて経口ステロイドを投与することができる。特定の実施形態では、免疫抑制剤は、1つ以上のコルチコステロイド、及び任意に、ミコフェノール酸モフェチル(MMF)、及び/または1つ以上のマクロライドである。1つ以上のマクロライドは、カルシニューリン阻害剤(たとえば、タクロリムス)、mTOR阻害剤(たとえば、シロリムス、テムシロリムス、エベロリムス、または別のラパログ)、またはそれらの組み合わせであり得る。特定の実施形態では、患者へのステロイドの投与は、ベクター投与の12週間後に中止される。特定の実施形態では、ミコフェノール酸モフェチル(MMF)及びタクロリムスは、ベクター投与前に0~15日間送達される。特定の実施形態では、免疫抑制剤は、ミコフェノール酸モフェチル(MMF)及びシロリムスである。特定の実施形態では、免疫抑制剤がタクロリムス及びシロリムスの両方を含む場合、各々の低用量を使用して、約4ng/mL~約8ng/mL、または合計約8ng/mL~約16ng/mLの血液トラフレベルを維持する。免疫補助剤がタクロリムスまたはシロリムスの一方のみを含む特定の実施形態では、総用量は約16ng/mL~約24ng/mLの範囲である。タクロリムスまたはシロリムスの一方のみが使用される特定の実施形態では、初期負荷用量は約3mg/m2である。特定
の実施形態では、免疫抑制療法は、ベクター投与前の約-14日から約-1日に開始される。特定の実施形態では、コードされたhIDUAは、(a)配列番号2(Genbank NP_000193)のアミノ酸約1~約653;及び(b)配列番号2の約27~約653の酸に融合した異種リーダー配列を含む合成ヒト酵素から選択される配列を有する。特定の実施形態では、核酸配列は、5’逆方向末端反復(ITR)配列、ニワトリβアクチンイントロン、CB7プロモータ、ポリAシグナル、及び/または3’ ITR配列をさらに含む。特定の実施形態では、rAAVは、6~9のpHを有する懸濁液中にある。特定の実施形態では、rAAVは、髄内注入を介して送達される。特定の実施形態では、hIDUA遺伝子を含むrAAVは、静脈内投与される。特定の実施形態では、治療の有効性は、任意に聴覚脳幹試験によって、聴覚能力変化を測定することによって評価される。特定の実施形態では、rAAVは(i)≧4ヶ月齢~<9ヶ月齢のヒト対象に約1.2×1012~約6.0×1012GCまたは約6.0×1012~約3.0×1013GC、(ii)≧9ヶ月齢~<18ヶ月齢のヒト対象に約2×1012~約6.0×1013または約1.0×1013~約5.0×1013GC、(iii)≧9ヶ月齢~<18ヶ月齢のヒト対象に約2.2×1012~約1.1×1013GCまたは約1.1×1013~約5.5×1013GCの総平坦用量を投与するために、ヒト対象への髄内注入用に製剤化される。
(a)≧4ヶ月齢~<9ヶ月齢のヒト対象に約1.2×1012~約6.0×1012GCもしくは約6.0×1012~約3.0×1013GC;または(b)≧9ヶ月齢~<18ヶ月齢のヒト対象に約2×1012~約6.0×1013GCもしくは約1.0×1013~約5.0×1013GC;または(c)≧9カ月齢~<18カ月齢のヒト対象に約2.2×1012~約1.1×1013GCもしくは約1.1×1013~約5.5×1013GCの総平坦用量を投与するために、それを必要とするヒト対象への髄内注入のために製剤化された、ヒトα-L-イズロニダーゼ(hIDUA)をコードする異種核酸を含む組換えAAVベクターを含む組成物が提供される。特定の実施形態では、ヒトhIDUAコード配列は、機能的hIDUAをコードする配列番号1のヌクレオチド配列、または配列番号1と少なくとも約80%同一の配列を有する。特定の実施形態では、組成物は、(i)グルココルチコ
イド、ステロイド、代謝拮抗物質、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第1の免疫抑制剤、及び(ii)それらの少なくとも1つから選択される少なくとも第2の免疫抑制剤との共療法を使用し、免疫抑制剤の投与はベクターの送達の前または同日に開始し;免疫抑制剤の少なくとも一方との投与は、ベクター投与後少なくとも8週間継続する。
の脳質量gの同等量に及ぶ。或いは、以下の治療上有効な平坦用量を指示した年齢群の患者に投与することができる。
・新生児:約1×1011~約3×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・9ヵ月~6歳:約6×1012~約3×1014GC;
・3~6歳:約1.2×1013~約6×1014GC;
・6~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
・新生児:約3.8×1012~約1.9×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・9ヵ月~36ヵ月:1013~約5×1013GC;
・6~12歳:約1.2×1013~約6×1014GC;
・3~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
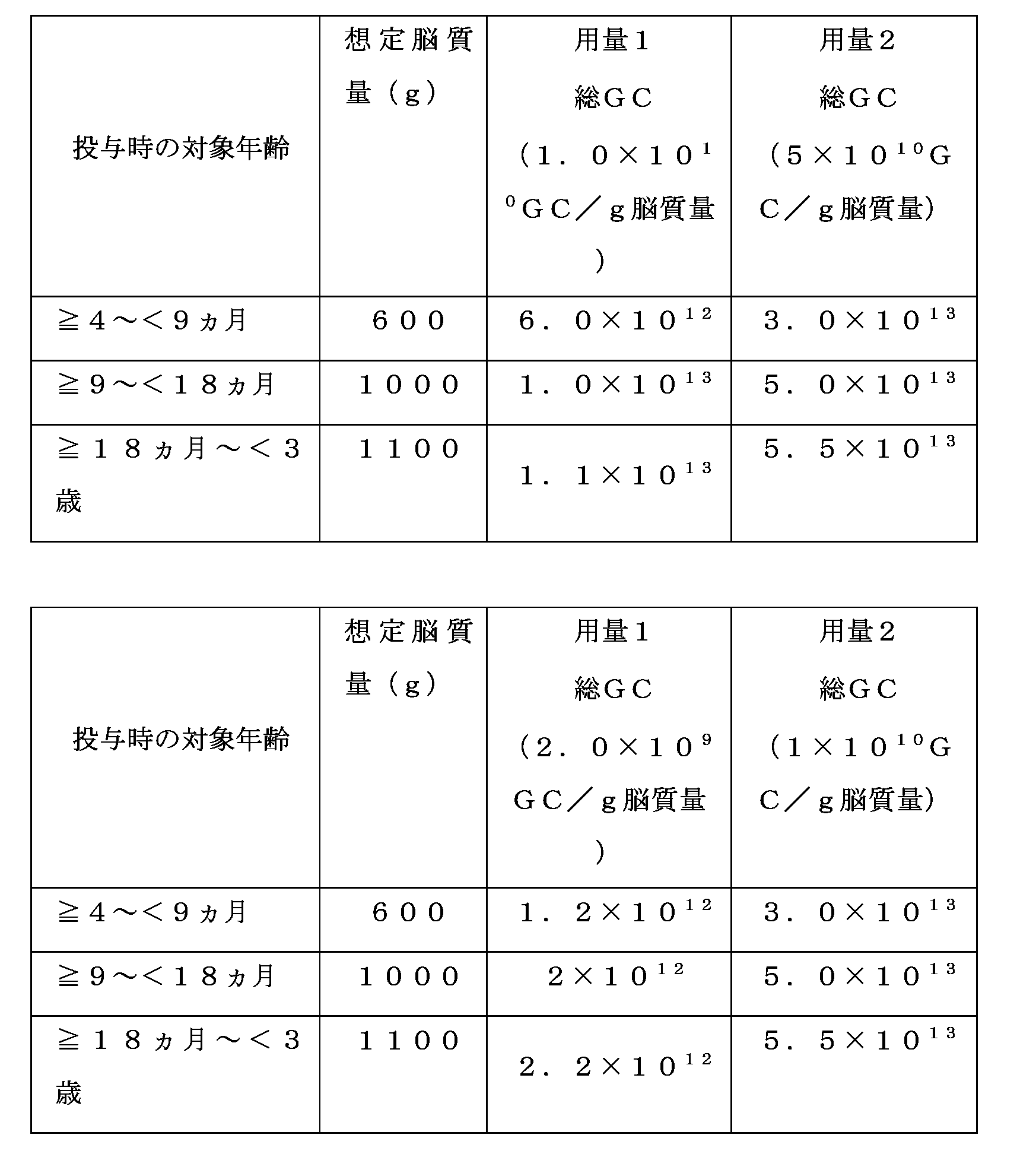
(1×1010GC/脳質量g)の用量が、(≧)4ヵ月以上~(<)9ヵ月未満の患者に投与される。特定の実施形態では、2×1012総GC(2.0×109GC/g脳質量)
または1×1013総GC(1×1010GC/g脳質量)の平坦用量が(≧)9ヵ月以上~(<)18ヵ月未満の患者に投与される。特定の実施形態では、2.2×1012総GC(2.0×109GC/g脳質量)または1.1×1013総GC(1×1010GC/g脳質
量)の平坦用量が(≧)18ヵ月以上~(<)3歳未満の患者に投与される。特定の実施形態では、6.0×1012(1.0×1010GC/g脳質量)または3×1013総ゲノムコピー(GC)(5×1010GC/g脳質量)の平坦用量が(≧)4ヵ月以上~(<)9ヵ月未満の患者に投与される。特定の実施形態では、1.0×1013(1.0×1010GC/g脳質量)または5.0×1013総GC(5×1010GC/g脳質量)の平坦用量が(≧)9ヵ月以上~(<)18ヵ月未満の患者に投与される。特定の実施形態では、1.1×1013(1.0×1010GC/g脳質量)または5.5×1013総GC(5×1010GC/g脳質量)の平坦用量が(≧)18ヵ月以上~(<)3歳未満の患者に投与される。特定の実施形態では、2.6×1012ゲノムコピー(GC)(2.0×109GC/g
脳質量)の平坦用量が6歳または6歳を超える患者に投与される。特定の実施形態では、1.3×1013(GC)(1.0×1010GC/g脳質量)の平坦用量が6歳または6歳を超える患者に投与される。一部の実施形態では、12歳以上のMPSI患者(18歳以上を含む)に投与される用量は、1.4×1013ゲノムコピー(GC)(1.1×1010GC/g脳質量)である。一部の実施形態では、12歳以上のMPS I患者(18歳以上を含む)に投与される用量は7×1013GC(5.6×1010GC/g脳質量)である。その上、さらなる実施形態では、MPS I患者に投与される用量は少なくとも約4×108GC/g脳質量~約4×1011GC/g脳質量である。特定の実施形態では、MP
S Iの新生児に投与される用量は、約1.4×1011から約1.4×1014GCまでに及び;3~9ヵ月の乳児に投与される用量は、約2.4×1011から約2.4×1014GCまでに及び;9~36カ月のMPS Iの幼児に投与される用量は、約4×1011から約4×1014GCまでに及び;3~12歳のMPS Iの小児に投与される用量は、約4.8×1011から約4.8×1014GCまでに及び;12歳以上の小児及び成人に投与される用量は、約5.6×1011から約5.6×1014GCまでに及ぶ。
がら、白質後索における両側性の軸索変性から成るCNSの病変は90日目及び180日目での脊髄にて観察された。これらの軸索の変化は後根神経節におけるニューロンに対する免疫が介在する効果に続発すると見なされる。
ムス0.5mg/m2/日、1日2回に分割、目標血中濃度4~8ng/mlで48週目
まで投与)からなるISレジメンを受容する。一部の実施形態では、最初の併用免疫抑制療法は、最初にプレドニゾンを中止し、続いてタクロリムス及び最後にシロリムスを用いて、連続的に減少される。
アクチンのプロモータ(CB7)とのハイブリッドによって制御される。特定の実施形態では、髄内、嚢内、及び全身性の投与に好適な医薬組成物が提供され、それは、生理的に適合性の水性緩衝液と界面活性剤と任意の賦形剤とを含む製剤緩衝液にてrAAV.hIDUAベクターの懸濁液を含む。rAAV懸濁液はさらに、
(i)rAAVゲノムコピー(GC)の力価が少なくとも1×109GC/mL~1×1
014GC/mL(+/-20%)であること;
(ii)SDS-PAGE解析(実施例6Dを参照のこと)によって測定されるとき、rAAVの中空粒子/完全粒子の比が0.01~0.05(95%~99%中空カプシドがない)の間である、または別の実施形態では、少なくとも約50%、少なくとも約80%、少なくとも約85%、もしくは少なくとも約90%中空カプシドがないこと;及び/または
(iii)少なくとも約4×108GC/g脳質量~約4×1011GC/g脳質量のrA
AV懸濁液の投与が効能を有すること
を特徴とする。
患者の脳質量gと等価である。或いは、以下の治療上有効な平坦用量を指示した年齢群の患者に投与することができる。
・新生児:約1×1011~約3×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・9ヵ月~6歳:約6×1012~約3×1014GC;
・3歳未満(新生児から3歳まで):約1×1011~約1.2×1013GC
・3~6歳:約1.2×1013~約6×1014GC;
・6~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
・新生児:約3.8×1012~約1.9×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・9~36ヵ月:約1013~約5×1013GC;
・3歳未満(新生児から3歳まで):約1×1011~約1.2×1013GC
・6~12歳:約1.2×1013~約6×1014GC;
・3~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
量)または6×1012総GC(1×1010GC/g脳質量)の平坦用量が(≧)4ヵ月以上~(<)9ヵ月未満の患者に投与される。特定の実施形態では、2×1012総GC(2.0×109GC/g脳質量)または1×1013総GC(1×1010GC/g脳質量)の
平坦用量が(≧)9ヵ月以上~(<)18ヵ月未満の患者に投与される。特定の実施形態では、2.2×1012総GC(2.0×109GC/g脳質量)または1.1×1013総
GC(1×1010GC/g脳質量)の平坦用量が(≧)18ヵ月以上~(<)3歳未満の患者に投与される。特定の実施形態では、6×1012(1.0×1010GC/g脳質量)または3×1013総ゲノムコピー(GC)(5×1010GC/g脳質量)の平坦用量が(≧)4ヵ月以上~(<)9ヵ月未満の患者に投与される。特定の実施形態では、1.0×1013(1.0×1010GC/g脳質量)または5.0×1013総GC(5×1010GC/g脳質量)の平坦用量が(≧)9ヵ月以上~(<)18ヵ月未満の患者に投与される。特定の実施形態では、1.1×1013(1.0×1010GC/g脳質量)または5.5×1013総GC(5×1010GC/g脳質量)の平坦用量が(≧)18ヵ月以上~(<)3歳未満の患者に投与される。特定の実施形態では、2.6×1012ゲノムコピー(GC)(2.0×109GC/g脳質量)の平坦用量が6歳または6歳を超える患者に投与され
る。特定の実施形態では、1.3×1013(GC)(1.0×1010GC/g脳質量)の平坦用量が6歳または6歳を超える患者に投与される。一部の実施形態では、12歳以上のMPS I患者(18歳以上を含む)に投与される用量は1.4×1013ゲノムコピー(GC)(1.1×1010GC/g脳質量)である。一部の実施形態では、12歳以上のMPS I患者(18歳以上を含む)に投与される用量は7×1013GC(5.6×1010GC/g脳質量)である。その上、さらなる実施形態では、MPS I患者に投与される用量は少なくとも約4×108GC/g脳質量~約4×1011GC/g脳質量である。
特定の実施形態では、MPS Iの新生児に投与される用量は約1.4×1011から約1.4×1014GCまでに及び;3~9ヵ月の乳児に投与される用量は、約2.4×1011から約2.4×1014GCまでに及び;9~36カ月の幼児に投与される用量は、約4×1011から約4×1014GCまでに及び;3~12歳の小児に投与される用量は、約4.8×1011から約4.8×1014GCまでに及び;12歳以上の小児及び成人に投与される用量は、約5.6×1011から約5.6×1014GCまでに及ぶ。
実施例6)。
Infectious Diseases,2009.199(3):p.381-390にて記載されたように測定されてもよい。
al,“Self-complementary recombinant adeno-associated virus(scAAV)vectors promote
efficient transduction independently of
DNA synthesis”,Gene Therapy,(August,2001),Vol.8,Number,16,Pages,1248-1254を参照のこと。自己相補性AAVは米国特許第6,596,535号;同第7,125,717号;及び同第7,456,683号に記載されており、そのそれぞれが全体として参照によって本明細書に組み入れられる。
(ゲノムは、人工的ゲノムの増幅及びパッケージングに必要とされるシグナルが隣接する対象とする導入遺伝子のみを含有する―「パワー不足」であるように操作することができる)が、これらの遺伝子は産生の間に供給されてもよい。従って、複製に必要とされるウイルス酵素の存在を除いて子孫ビリオンの複製及び感染は起きないので、それは遺伝子治療での使用に安全であると見なされる。
5.1.1.発現カセット
特定の実施形態では、配列番号1のヌクレオチド配列を有することを特徴とするhIDUA遺伝子を含有する発現カセットを含むAAVベクターが提供される。本発明者らによって開発されたこの配列は、配列番号2をコードするGenBankNP000194.2の公開された遺伝子コーディング配列と約83%の同一性を有する。別の実施形態では、発現カセットは配列番号1に対して少なくとも約80%同一であるヌクレオチド配列を有することを特徴とするhIDUA遺伝子を含有し、機能的なヒトα-L-イズロニダーゼをコードする。別の実施形態では、配列は配列番号1に対して少なくとも約85%同一性であり、または配列番号1に対して少なくとも約90%同一であり、機能的なヒトα-L-イズロニダーゼをコードする。一実施形態では、配列は、配列番号1に対して少なくとも約95%同一であり、配列番号1に対して少なくとも約97%同一であり、または配列番号1に対して少なくとも約99%同一であり、機能的なヒトα-L-イズロニダーゼをコードする。一実施形態では、これは、配列番号1の約1~約78に相当するヒトα-L-イズロニダーゼ(すなわち、配列番号2のアミノ酸26付近またはアミノ酸27付近からアミノ酸653付近をコードする)のリーダーペプチド配列を含む完全長のhIDUA遺伝子を包含する。別の実施形態では、hIDUA遺伝子は、機能的なヒトα-L-イズロニダーゼ酵素、すなわち、配列番号2のアミノ酸27付近~653付近または本明細書で特定されるその機能的な変異体の1つの分泌された部分に融合される異種リーダー配列を含む合成ペプチドである機能的な合成ヒトα-L-イズロニダーゼ酵素をコードする。その上さらなる発現カセットは配列番号5及び配列番号6で特定されるものを含む。それぞれでは、各発現カセットはAAV2の5’及び3’ITRが隣接する。さらに、それぞれはプロモータ、エンハンサ、hIDUA遺伝子、及びポリAを含有する。
ミノ酸配列を比較するのにALIGNプログラムを利用する場合、PAM120残基重み付け表、12のギャップ長ペナルティ及び4のギャップペナルティを使用することができ;及びFASTA(Pearson,W.R.及びLipman,D.J.,Proc.Natl.Acad.Sci.USA,85:2444-2448,1988,Wisconsin配列解析パッケージの一部として利用可能)。SeqWebソフトウエア(ウェブに基づくGCG Wisconsinパッケージへのインターフェース:Gapプログラム)。
本明細書に記載されている発現カセットはAAVの5’逆方向末端反復(ITR)及びAAVの3’ITRを利用した。しかしながら、これらの要素の他の構成が好適であってもよい。D-配列と末端分離部位(trs)を欠失させているΔITRと呼ばれる5’ITRの短縮型が記載されている。別の実施形態では、完全長のAAVの5’ITR及び/または3’ITRが使用される。偽型AAVが作製されるべきである場合、発現におけるITRはカプシドのAAV供給源とは異なる供給源から選択される。たとえば、AAV2のITRは、CNSまたはCNS内の組織もしくは細胞を標的とするのに特定の効率性を有するAAVのカプシドと共に使用するために選択されてもよい。一実施形態では、AAV2に由来するITR配列またはその欠失型(ΔITR)を都合上使用して規制当局の承認を加速する。しかしながら、他のAAV供給源に由来するITRが選択されてもよい。ITRの供給源がAAV2に由来し、AAVのカプシドが別のAAV供給源に由来する場合、得られるベクターは偽型と呼ばれてもよい。しかしながら、AAVのITRの他の供給源が利用されてもよい。
her.,7:1503-14),骨オステオカルシン(Stein,et al.,(1997),Mol.Biol.Rep.,24:185-96);骨シアロタンパク質(Chen,et al.,(1996),J.Bone Miner.Res.,11:654-64),リンパ球(CD2,Hansal,et al.,(1998),J.Immunol.,161:1063-8;免疫グロブリン重鎖;T細胞受容体鎖),ニューロン特異的なエノラーゼ(NSE)プロモータのようなニューロン性(Andersen,et al.,(1993),Cell.Mol.Neurobiol.,13:503-15),ニューロフィラメント軽鎖遺伝子(Piccioli,et al.,(1991),Proc.Natl.Acad.Sci.USA,88:5611-5),及びニューロン特異的なvgf遺伝子(Piccioli,et al.,(1995),Neuron,15:373-84)。或いは、調節できるプロモータが選択されてもよい。たとえば、参照によって本明細書に組み入れられるWO2011/126808B2を参照のこと。
特定の実施形態では、AAVカプシド、その中でパッケージされているAAV逆方向末端反復、その発現を制御する調節性配列の制御下でのヒトα-L-イズロニダーゼ(hIDUA)遺伝子を有する組換えアデノ随伴ウイルス(rAAV)粒子が提供され、その際、前記hIDUA遺伝子は配列番号1で示される配列または機能的なヒトα-L-イズロニダーゼをコードするそれと少なくとも約95%同一である配列を有する。図1の模式図も参照のこと。一実施形態では、hIDUAの発現カセットにはAAVの5’ITRとAAVの3’ITRが隣接する。別の実施形態では、AAVは一本鎖AAVであってもよい。
-A1;EP1310571]。WO2003/042397(AAV7及び他のサルAAV),米国特許7790449及び米国特許7282199(AAV8)、WO2005/033321及びUS7,906,111(AAV9)、及びWO2006/110689]、及びrh10[WO2003/042397],AAV3B;AAVdj[US2010/0047174]も参照のこと。特に望ましいrAAVの1つはAAV2/8.TBG.hIDUA.coである。
る。GC/mLで割ったPt/mLが粒子のゲノムコピーに対する比(pt/GC)を与える。Pt/mL-GC/mLは中空Pt/mLを与える。Pt/mLで割った中空Pt/mLに100を掛けて中空粒子の比率を得る。
で)でさらに短い時間(たとえば、約5~10分間)実施されてもよい。同様に、熱による不活化は一般に、約95℃で約15分間であるが、温度はさらに低下させてもよく(たとえば、約70℃~約90℃)、時間は増やしてもよい(たとえば、約20分間~約30分間)。次いで試料を希釈し(たとえば、1000倍)、標準アッセイで記載されたようなTaqMan解析に供する。
rAAV9.hIDUA製剤は、生理食塩水と界面活性剤と生理的に適合性の塩または塩の混合物とを含有する水溶液に懸濁された有効量のAAV.hIDUAベクターを含有する懸濁液である。好適には、製剤は、生理的に許容できるpHに、たとえば、pH6~8、またはpH6.5~7.5、pH7.0~7.7、またはpH7.2~7.8の範囲で調整される。脳脊髄液のpHは約7.28~約7.32なので、髄内送達のためにはこの範囲内のpHが所望であってもよいのに対して、静脈内送達については、6.8~約7.2のpHが所望であってもよい。しかしながら、最も広い範囲内及びこれら部分範囲内での他のpHが他の経路の送達のために選択されてもよい。
テル、TWEEN(ポリオキシエチレンソルビタン脂肪酸エステル)、エタノール及びポリエチレングリコールが選択されてもよい。一実施形態では、製剤はポロキサマーを含有する。これらのコポリマーは、文字「P」(ポロキサマーのための)に続く3つの数字によって共通して名付けられ、最初の2つの数字×100はポリオキシプロピレンのコアのおよその分子量を与え、最後の数字×10はポリオキシエチレン含量の比率を与える。一実施形態では、ポロキサマー188が選択される。界面活性剤は懸濁液の約0.0005%~約0.001%までの量で存在してもよい。
を含有してもよい。
ウム塩化カリウム、塩化カルシウム(たとえば、塩化カルシウム・2H2O)、リン酸ナ
トリウム(たとえば、二塩基リン酸ナトリウム)、及びそれらの混合物の1以上を含む緩衝化生理食塩水溶液を含有してもよい。製剤は、本明細書に記載されるように、たとえばデキストロース及び/またはポロキサマーも含有し得る。好適には、髄内送達については、浸透圧は脳脊髄液(たとえば、約270~約290)に適合する範囲内である。たとえば、emedicine.medscape.com/article/2093316-overview.を参照のこと。任意で、髄内送達については、市販の希釈剤を懸濁剤として、または別の懸濁剤及び他の任意の賦形剤との組み合わせで使用してもよい。たとえば、エリオットB(登録商標)[Lukare Medical]を参照のこと。
流空気流キャビネット中で実施され得る。注射器及び無針瓶アダプターを使用して、AAV9.hIDUA(予め凍結されていてもよい)を含有する予め規定された容量の懸濁液を取り出し、次いで、プラスチック針シースで覆われた滅菌ステンレス鋼鈍針で注射器をキャップする。注射器及び無針瓶アダプターを使用して、予め規定された容量の希釈剤を取り出し、次いで、プラスチック針シースで覆われた滅菌ステンレス鋼鈍針で注射器をキャップする。希釈剤、次いでAAV9.hIDUAを含有する懸濁液を、無菌技術を使用して第3の「投与」シリンジに送達し、注射器の外側の無菌性が維持されることを確実にする。チップキャップを用いて注射器をキャップし、反転によって混合する。キャップを外し、所望の送達容量にプライミングし、キャップし、レッテルを付け、滅菌バッグ中に包装し、これは6時間以内に使用するために手術室に輸送され得る。
5.2.1.標的患者集団
本明細書で提供されるのは、本明細書に記載されているような治療上有効な量の修飾されたhIDUAの発現カセットを送達することを含むI型ムコ多糖症を治療する方法である。特に、本明細書で提供されるのは、それを必要とする患者に治療上有効な量の本明細書に記載されているrAAV.hIDUAを送達することを含む、MPS Iであると診断された患者にて神経認知の低下を防ぐ、治療する及び/または改善する方法である。「治療上有効な量」の本明細書に記載されているrAAV.hIDUAベクターは以下の段落のいずれか1つで特定される症状の1以上を是正してもよい。
として使用されてもよい。特に、実際にIDUA活性のレベルを有さない、導入遺伝子の産物が「異物」として見られ得る患者では、hIDUA導入遺伝子の産物に対する有害な免疫応答の可能性を防ぐために、前もっての免疫抑制療法が望ましくてもよい。以下に記載されているマウス、イヌ及びNHPにおける非臨床試験の結果は、hIDUAに対する免疫応答及び神経炎症の発生に矛盾しない。類似の反応はヒト対象では起きないかもしれないが、予防免疫抑制療法はrAAV.hIDUAのレシピエントすべてに推奨される。
ラフレベルを維持するように調整された低用量である方がよい。特定の実施形態では、これらの薬剤の一方のみを使用する場合、タクロリムス及び/またはシロリムスについての総用量は、約16ng/mL~約24ng/mLの範囲であり得る。薬剤の一方のみが使用される場合、ラベル用量(より高い用量);たとえば、12時間毎に2分割された用量として付与される、0.15~0.20mg/kg/日のタクロリムス;及び1mg/m2/日のシロリムスを使用すべきであり;負荷用量は、3mg/m2であるべきである。MMFがレジメンに追加される場合、タクロリムス及び/またはシロリムスの用量は、作用機序が異なるため維持され得る。これら及び他の治療法は、約-14日目~-1日目に開始され(たとえば、-2日目、0日目等)、約1週間(7日間)まで,または約60日間まで、または約12週間まで、または約16週間まで、または約24週間まで、または約48週間まで、または必要に応じてそれより長く継続し得る。特定の実施形態では、タクロリムスを含まない投与計画が選択される。
・以下のいずれかを含むIC注入について禁忌を有する:
〇ベースラインMRI検査の見直しがIC注入の禁忌を示す。
〇IC注入の禁忌を生じる頭部/頸部の手術の既往。
〇CT(または造影剤)または全身麻酔に対する禁忌を有する。
〇MRI(またはガドリニウム)に対する禁忌を有する。
〇<30mL/分/1.73m2の推定糸球体濾過量(eGFR)を有する。
・MPS Iに起因しない神経認知欠損を有する、または神経精神病状態も診断を有する。
・タクロリムス、シロリムス、プレドニゾロン、メチルプレドニゾロン、またはプレドニゾロンの1以上に対する過敏性反応の既往を有する。
・免疫抑制療法について適当ではない状態(たとえば、<1.3×103/μLの好中球
の絶対数、<100×103/μLの血小板数及び<12g/dL(男)または<10g
/dL(女)のヘモグロビン)を有する。
・腰椎穿刺に対する禁忌を有する。
・HSCTを受けている。
・治療の前6ヵ月以内にIT投与を介してラロニダーゼ投与を受けていた。
・どこかの時点でラロニダーゼIT投与を受け、患者を過度のリスクに置くIT投与に関連すると見なされる重大な有害事象を経験した。
・治療の前少なくとも3ヵ月間完全寛解になっていない、リンパ腫の既往、または皮膚の有棘細胞癌もしくは基底細胞癌以外の別の癌の既往。
・患者がギルバート症候群の以前既知の既往症及び総ビリルビンの<35%の結合ビリルビンを示す分画ビリルビンを有さない限り、>3×正常の上限(ULN)のアラニンアミノトランスフェラーゼ(ALT)またはアスパラギン酸アミノトランスフェラーゼ(AST)または>1.5×ULNの総ビリルビン。
・ヒト免疫不全ウイルス(HIV)陽性検査の既往、活動型または再発性のB型肝炎またはC型肝炎、またはB型肝炎、C型肝炎またはHIVの陽性スクリーニング検査の既往。・妊娠中、出産後<6週、母乳授乳中、または妊娠を計画中(自己またはパートナー)。・治療の前1年以内のアルコールまたは薬物の乱用の既往。
・患者の安全を脅かす深刻なまたは不安定な医学的または心理学的な状態を有する。
・制御不良の発作。
象は18歳以上の成人であり得る。6歳以上の小児の登録は、この対象において、遺伝子治療後8週目に安全性の懸念が同定されない場合にのみ開始される。
1)3歳未満の男性または女性。
2)対象の法定保護者は、治験の性質が説明された後、治験に関連する手続きが行われる前に、署名付きのインフォームドコンセントを提供する意思があり、かつ提供することができる。
3)重度のMPS I-ハーラーと診断されたことが証明されている:
4)MPS I-ハーラーに適合する臨床的徴候及び症状の存在、及び/または
5)重度の表現型と排他的に関連する突然変異についてのホモ接合性もしくは複合ヘテロ接合性。
6)55以上の知能指数(IQ)スコアを有する
7)補助具の有無にかかわらず、必要なプロトコール試験を完了するのに十分な聴覚能力及び視覚能力を有し、該当する場合、試験日に補助具を着用することに従う意思がある。
8)以下のいずれかを含むIC注入には禁忌である:
a)神経放射線科医/神経外科医の判定委員会によるベースライン磁気共鳴画像法(MRI)検査のレビューは、IC注入の禁忌を示す。
b)神経放射線科医/神経外科医の判定委員会による入手可能な情報のレビューに基づき、IC注入を禁忌とした以前の頭部/頸部手術の既往歴。
c)コンピュータ断層撮影(CT)(または造影剤)または全身麻酔に禁忌である。
d)MRI(またはガドリニウム)に禁忌である。
e)推定糸球体濾過量(eGFR)<30mL/分/1.73m2である。
9)MPS Iに起因しない神経認知障害を有するか、またはPIの見解で研究結果の解釈を混乱させる可能性のある神経精神状態の診断を有する。
10)腰椎穿刺に禁忌である。
11)造血幹細胞移植(HSCT)を受けている
12)AAVベースの遺伝子治療製品による治療歴がある
13)任意の時間に髄内(IT)ラロニダーゼを投与され、PIの見解では対象を過度のリスクにさらすと考えられるIT投与に関連すると考えられる有意なAEを経験した。
14)スクリーニング前少なくとも3ヵ月間完全寛解していないリンパ腫の既往歴または皮膚の扁平上皮癌もしくは基底細胞癌以外の別の癌の既往歴がある。
15)最大の内科的治療にもかかわらず、制御されていない高血圧(収縮期血圧[BP]>180mmHg、拡張期血圧>100mmHg)。
16)血小板数<100,000/マイクロリットル(μL)である
17)対象にギルバート症候群の既往歴がない限り、スクリーニング時にアラニンアミ
ノトランスフェラーゼ(ALT)またはアスパラギン酸アミノトランスフェラーゼ(AST)>3×正常上限(ULN)または総ビリルビン>1.5×ULNを有する。
18)ヒト免疫不全ウイルス(HIV)もしくはB型肝炎もしくはC型肝炎ウイルス感染の既往歴を有し、またはB型肝炎表面抗原もしくはB型肝炎コア抗体もしくはC型肝炎もしくはHIV抗体のスクリーニング検査陽性である。
19)インフォームド・コンセントフォーム(ICF)に署名する前の30日以内または5半減期以内(いずれか長い方)に治験薬を受容した
20)治験実施に関与する医療機関の従業員もしくはその他の個人の一等家族であるか、または治験実施に関与する医療機関の従業員もしくはその他の個人である。
21)PIの見解で、対象の安全性を損なう臨床的に有意なECG異常がある。
22)PIの見解で、対象の安全性、または治験への参加もしくは治験結果の解釈の成功を損なう重篤または不安定な医学的または心理的状態を有する。
23)医療機関の神経放射線科医/神経外科医の意見において、及びメディカルモニターとの議論において、対象の投与及び適切な投与に影響を及ぼし得る(脳)室シャント。
21)タクロリムス、シロリムスまたはプレドニゾンに対する過敏症反応の既往歴;
22)原発性免疫不全(たとえば、一般的な可変性免疫不全症候群)、脾臓摘出、または対象を感染症にかかりやすくするあらゆる基礎疾患の既往歴。
23)スクリーニングの少なくとも12週間前に完全には消失しなかった帯状疱疹、サイトメガロウイルス、またはエプスタインバーウイルス(EBV)感染。
24)来診2の少なくとも8週間前に消失しなかった入院または非経口抗感染薬による治療を必要とするあらゆる感染。
25)来診2前の10日以内に経口抗感染薬(抗ウイルス薬を含む)を必要とするあらゆる活動性感染。
26)活動性結核(TB)の既往歴またはスクリーニング中のクォンティフェロンTBゴールド検査の陽性。
27)ICFに署名する前の8週間以内のあらゆる生ワクチン。
28)ICFに署名する前の8週間以内の大手術または治験期間中に計画された大手術。
29)登録後6ヵ月以内にアデノイド切除術または扁桃摘出術の必要性を予測する。アデノイド切除術または扁桃摘出術が予測される場合は、スクリーニング前に実施すべきである。
30)絶対好中球数<1.3×103/μL。
31)臨床医が免疫抑制療法に適切ではないと考える任意の状態または実験室異常。
患者への投与に好適な医薬組成物は、生理的に適合性の水性緩衝液と界面活性剤と任意の賦形剤とを含む製剤緩衝液におけるrAAV.hIDUAベクターの懸濁液を含む。特定の実施形態では、本明細書に記載されている医薬組成物は髄内に投与される。別の実施形態では、本明細書に記載されている医薬組成物は嚢内に投与される。別の実施形態では、本明細書に記載されている医薬組成物は静脈内に投与される。特定の実施形態では、医薬組成物は20分間(±5分間)にわたる点滴によって末梢静脈を介して送達される。しかしながら、この時間は必要に応じてまたは所望に応じて調整されてもよい。しかしながら、投与のさらに他の経路が選択されてもよい。代わりにまたはさらに、投与の経路は所望に応じて組み合わせてもよい。
じて)。任意で、点滴/注入を忍容するために対象の年齢及び能力を考慮して、治療上有効な量の初回用量は分割点滴/注入の期間にわたって送達されてもよい。しかしながら、完全な治療用量の反復毎週の注入は必要とされず、心地よさと治療結果の双方の点で患者に利点を提供する。
Vのゲノムコピー(GC)の力価を有する。特定の実施形態では、rAAV懸濁液におけるrAAVの中空粒子/完全粒子の比は0.01~0.05の間である(95%~99%中空カプシドはない)。一部の実施形態では、それを必要とするMPS I患者は、rAAV懸濁液の少なくとも約4×108GC/g脳質量~約4×1011GC/g脳質量の用
量を投与される。
等価)の範囲である。或いは、以下の治療上有効な平坦用量を指示した年齢群の患者に投与することができる。
・新生児:約1×1011~約3×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・4ヵ月以上~9ヵ月未満:約1.2×1012~約6×1012;
・9ヵ月以上~18ヵ月未満:約2×1012~約1.0×1013;
・18ヵ月以上~3歳未満:約2.2×1012~約1.1×1013;
・9ヵ月~6歳:約6×1012~約3×1014GC;
・3歳未満(新生児から3歳まで):約1×1011~約1.2×1013GC;
・3~6歳:約1.2×1013~約6×1014GC;
・6~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
・新生児:約3.8×1012~約1.9×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・4ヵ月以上~9ヵ月未満:約6.0×1012~約3.0×1013;
・9ヵ月以上~18ヵ月未満:約1.0×1013~約5.0×1013;
・18ヵ月以上~3歳未満:約1.1×1013~約5.5×1013;
・9~36ヵ月:約1013~約5×1013GC;
・3歳未満(新生児から3歳まで):約1×1011~約1.2×1013GC;
・6~12歳:約1.2×1013~約6×1014GC;
・3~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
量)または6×1012総GC(1×1010GC/g脳質量)の平坦用量が(≧)4ヵ月以上~(<)9ヵ月未満の患者に投与される。特定の実施形態では、2×1012総GC(2.0×109GC/g脳質量)または1×1013総GC(1×1010GC/g脳質量)の
平坦用量が(≧)9ヵ月以上~(<)18ヵ月耳案の患者に投与される。特定の実施形態では、2.2×1012総GC(2.0×109GC/g脳質量)または1.1×1013総
GC(1×1010GC/g脳質量)の平坦用量が(≧)18ヵ月以上~(<)3歳未満の患者に投与される。特定の実施形態では、6.0×1012(1.0×1010GC/g脳質
量)または3×1013総ゲノムコピー(GC)(5×1010GC/g脳質量)の平坦用量が(≧)4ヵ月以上~(<)9ヵ月未満の患者に投与される。特定の実施形態では、1.0×1013(1.0×1010GC/g脳質量)または5.0×1013総GC(5×1010GC/g脳質量)の平坦用量が(≧)9ヵ月以上~(<)18ヵ月未満の患者に投与される。特定の実施形態では、1.1×1013(1.0×1010GC/g脳質量)または5.5×1013総GC(5×1010GC/g脳質量)の平坦用量が(≧)18ヵ月以上~(<)3歳未満の患者に投与される。特定の実施形態では、2.6×1012ゲノムコピー(GC)(2.0×109GC/g脳質量)の平坦用量が6歳以上の患者に投与される。特定
の実施形態では、1.3×1013(GC)(1.0×1010GC/g脳質量)の平坦用量が6歳以上の患者に投与される。一部の実施形態では、12歳以上のMPSI患者(18歳以上を含む)に投与される用量は1.4×1013ゲノムコピー(GC)(1.1×1010GC/g脳質量)である。一部の実施形態では、12歳以上のMPSI患者(18歳以上を含む)に投与される用量は7×1013ゲノムコピー(GC)(5.6×1010GC/g脳質量)である。その上さらなる実施形態では、MPS I患者に投与される用量は約4×108GC/g脳質量~約4×1011GC/g脳質量である。特定の実施形態では、
MPS I新生児に投与される用量は約1.4×1011から約1.4×1014GCにまで及び;3~9ヵ月の乳児に投与される用量は約2.4×1011から約2.4×1014GCにまで及び;9~36カ月の幼児に投与される用量は約4×1011から約4×1014GCにまで及び;3~12歳の小児に投与される用量は約4.8×1011から約4.8×1014GCにまで及び;12歳以上の小児及び成人に投与される用量は約5.6×1011から約5.6×1014GCにまで及ぶ。
~5×1014GCを含む。別の実施形態では、用量は約3.8×1012~約1.9×1014GCを含む。さらなる実施形態では、患者はハーラー症候群を有する少なくとも約3ヵ月齢から12ヵ月齢まで、少なくとも約3ヵ月から24ヵ月まで、または少なくとも約3ヵ月から36ヵ月まで、少なくとも約3ヵ月から6歳まで、少なくとも6ヵ月から6歳まで、少なくとも12ヵ月から6歳までの乳児対象であり、用量は4×108GCのrAA
V9.hIDUA/g脳質量~3×1012GCのrAAV9.hIDUA/g脳質量の少なくとも同等物を含む。別の例では、患者はハーラー・シャイエ症候群を有する3歳までの小児であり、用量は少なくとも4×108GCのrAAV9.hIDUA/g脳質量~
5×1010GCのrAAV9.hIDUA/g脳質量の同等物を含む。別の例では、患者はハーラー・シャイエ症候群を有する少なくとも約6歳から18歳までの小児であり、用量は少なくとも4×108GCのrAAV9.hIDUA/g脳質量~3×1012GCの
rAAV9.hIDUA/g脳質量の同等物を含む。
治療法の有効性は、(a)MPS I患者における神経認知低下の予防、及び(b)疾
患の生体マーカー、たとえば、CSF、血清及び/または尿におけるGAGのレベル及び/または酵素活性の低下、及び/または肝臓及び脾臓の容量を評価することによって測定することができる。神経認知は、知能指数(IQ)を測定することによって、たとえば、ハーラーの対象についてBayleyの乳児発達スケールによって測定されるように、またはハーラー・シャイエの対象についてWechsler短縮版知能検査(WASI)によって測定されるように判定することができる。神経認知の発達及び機能の他の適当な測定、たとえば、Bayleyの乳児発達スケール(BSID-III)を用いて発達指数(DQ)を評価すること、Hopkins言語学習試験を用いて記憶を評価すること、及び/または注意変数試験(TOVA)を使用することが利用されてもよい。聴力脳幹反応(ABR)検査により測定される聴覚能力の変化。他の神経心理学的機能、たとえば、vineland適応行動尺度(たとえば、Vineland II)、視覚処理、微細運動、コミュニケーション、社会化、日常生活技能、及び情動や行動上の健康がモニターされる。容量測定の拡散テンソル画像(DTI)を取得するための脳の磁気共鳴画像診断(MRI)、及び休息状態のデータ、超音波検査による平均神経断面積、脊髄圧迫の改善、安全性、肝臓サイズ及び脾臓サイズも管理される。
ト患者から脳脊髄液または血漿の試料を得ることと、試料にてスペルミンの濃度レベルを検出することと、1ng/mLを超えるスペルミン濃度を有する患者にてMPS Iから選択されるムコ多糖症であると患者を診断することと、たとえば、本明細書に記載されているような用具を用いて本明細書で提供されるように診断された患者に有効量のヒトα-L-イズロニダーゼ(hIDUA)を送達することとが関与する。
analysis is plant samples by ion pair liquid chromatography coupled with electrospray tandem mass spectrometry,”Plant Physiology and Biochemistry,47(2009):592-598,オンラインで利用可能,2009年2月28日;MR.Hakkinen,et
al,“Analysis of underivatized polyamines by reversed phase liquid chromatography with electrospray tandem mass spectrometry”,J.Pharm.Biomec.Analysis,44(2007):625-634に記載されているアッセイ、定量的同位元素希釈液体クロマトグラフィ(LC)/質量分光分析(MS)アッセイ。他の好適なアッセイが使用されてもよい。
I患者にてCSFのグリコサミノグリカン(GAG)の神経認知との関係を評価することによって判定される。一部の実施形態では、本明細書に記載されている治療剤の有効性は、磁気共鳴画像解析(MRI)によって、たとえば、灰白質及び白質及びCFS脳室の容量分析によって測定されるようなMPS I患者におけるCNSへの物理的変化に対する治療剤の効果を評価することによって判定される。一部の実施形態では、本明細書に記載されている治療剤の有効性は、MPS I患者の脳脊髄液(CSF)、血清及び尿における生体マーカー(たとえば、GAG、HS)に対する治療剤の薬物動態効果を評価することによって判定される。一部の実施形態では、本明細書に記載されている治療剤の有効性は、MPS I患者における生活の質(QOL)に対する治療剤の影響を評価することによって判定される。一部の実施形態では、本明細書に記載されている治療剤の有効性は、MPS I患者における運動機能に対する治療剤の影響を評価することによって判定される。一部の実施形態では、本明細書に記載されている治療剤の有効性は、MPS I患者における成長及び発達の診査事項に対する治療剤の効果を評価することによって判定される。
は他の組織にて検出されるとき、少なくとも約2%の発現レベルが治療効果を提供してもよい。しかしながら、さらに高い発現レベルが達成されてもよい。そのような発現レベルは正常で機能的なヒトIDUAレベルの2%から約100%までであってもよい。特定の実施形態では、正常の発現よりも高いレベルがCSF,血清または他の組織にて検出されてもよい。
hIDUAの全身性送達を伴うCNSへのrAAV.hIDUAの遺伝子治療送達の併用は本発明の方法によって包含される。全身性送達はERT(たとえば、アルデュラザイム(登録商標)を用いて)、または肝臓に指向性を持つrAAV.hIDUA(AAV8カプシドを持つrAAV.hIDUA)を用いた追加の遺伝子治療が伴われ得る。
内であるように調整されてもよく;別の実施形態では、双方の経路によって送達される組み合わせたベクターが1×1011~1×1016の範囲内である。或いは、各ベクターは約108GC~約1012GC/ベクターの量で送達されてもよい。そのような用量が実質的
に同時に、または異なった時間に、たとえば、約1日~約12週間離して、もしくは約3日~約30日離して、もしくは他の好適な時に送達されてもよい。
に十分量のhIDUA酵素または肝臓を指向するrAAV.hIDUAを投与して導入遺伝子に特異的な寛容を誘導することと、(b)患者のCNSにrAAV9.hIDUAを投与することとを含み、rAAV.hIDUAは患者にて治療レベルのhIDUAの発現を指向する。
NP_000193)のアミノ酸約1~約653;または(b)配列番号2の約27~約653の酸に融合した異種リーダー配列を含む合成ヒト酵素から選択される配列を有す
る。
本発明は本明細書に記載されている(以下の実施例5)rAAV.hIDUA医薬組成物の製造を提供する。説明に役立つ製造プロセスは図11に提供されている。rAAV.hIDUAベクターは図11に示すフローチャートで示すように製造することができる。手短には、好適な細胞培養によって細胞を製造する(たとえば、HEK293細胞)。本明細書に記載されている遺伝子治療のベクターを製造する方法には、遺伝子治療のベクターの作製に使用されるプラスミドDNAの生成、ベクターの生成及びベクターの精製のような当該技術で周知の方法が含まれる。一部の実施形態では、遺伝子治療のベクターはA
AVベクターであり、生成されるプラスミドは、AAVゲノムと対象とする遺伝子とをコードするAAVシス-プラスミド、AAVrep及びcap遺伝子を含有するAAVトランス-プラスミド、及びアデノウイルスヘルパープラスミドである。ベクター生成のプロセスは、たとえば、細胞培養の開始、細胞の継代、細胞の播種、プラスミドDNAによる細胞への形質移入、形質移入後の無血清培地への培地交換、及びベクター含有細胞及び培養培地の回収のような方法工程を含むことができる。回収されたベクター含有細胞及び培養培地は本明細書では粗細胞回収物と呼ばれる。
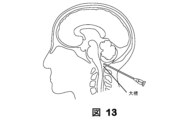
態様の1つでは、本明細書で提供されるベクターはこのセクションで提供され、実施例及び図12にてさらに記載されている方法及び/または用具を介して髄内に投与されてもよい。代わりに、他の用具及び方法が選択されてもよい。方法は、患者の大槽の中にクモ膜下穿刺針を進める工程と、クモ膜下穿刺針の近位ハブに柔軟な配管の全長を接続し、柔軟な配管の近位末端に弁の出力ポートを接続する工程と、前記進める工程と接続する工程の後、患者の脳脊髄液で配管が自給されるのを可能にした後、ある量の等張溶液を含有する第1の容器を弁の水洗入口部に接続し、その後、ある量の医薬組成物を含有する第2の容器を弁のベクター入口部に接続する工程とを含む。第1と第2の容器を弁に接続した後、流体流動のための経路は弁のベクター入口部と出口部の間で開放され、医薬組成物がクモ膜下穿刺針を介して患者に注入され、医薬組成物を注入した後、流体流動のための経路は弁の水洗入口部と出口部の間で開放され、クモ膜下穿刺針を介して等張溶液が注入され、医薬組成物を患者のなかへ洗い流す。
とが含まれる。用具にはさらに、第1の容器に相互接続される第1の入口部と、第2の容器に相互接続される第2の入口部と、クモ膜下穿刺針に相互接続される出口部と、クモ膜下穿刺針を介して医薬組成物と等張溶液の流動を制御するルアーロックとを有する弁が含まれる。
えば、腰部傍脊柱筋、骨、脳幹及び脊髄)の視覚化を可能にするコンピュータ断層撮影(CT)画像を入手してもよい。針ハブにおける脳脊髄液(CSF)の観察及び大槽内での針先端の視覚化によって正しい針の配置を確認する。その後、相対的に短い配管20を挿入されたクモ膜下穿刺針26に連結し、次いで四方活栓16を配管20の反対側の端に連結してもよい。
頚部の磁気共鳴画像診断(MRI)が得られてもよい。頭頚部のMRIに加えて、治験医師は屈曲/拡張試験を介した頸部のさらなる評価の必要性を判定してもよい。MRIプロトコールはT1、T2、DTI、FLAIR及びCINEのプロトコール画像を含んでもよい。
の詳細な評価を提供する麻酔の手術前評価も「-28日目」~「1日目」に得られてもよく、MPS対象の特定の生理的ニーズに留意する。
成人の腰椎穿刺(LP)キット(施設によって供給される);
BD(Becton Dickinson)の22または25ゲージ×3-7”のクモ膜下穿刺針(Quincke bevel);
インターベンション医師の指示で使用される同軸導入針(クモ膜下穿刺針の導入用);
旋回(回転)オスルアーロック付き四方小口径活栓;
メスルアーロックアダプター付きTコネクタ延長セット(配管)、6.7インチのおよその長さ;
髄内投与用のオムニパック180(イオヘキソール);
静脈内(IV)投与用のヨウ素化造影剤;
注入用の1%リドカイン溶液(成人LPキットで供給されなければ);
予め充填された生理食塩水(無菌)の10ccの水洗注射器;
X線不透過性マーカー(複数可);
外科用調製器具/髭剃り用かみそり刃;
挿管された対象の適正な位置決めを可能にする枕/支持体;
気管内挿管器具、一般的な麻酔器及び人工呼吸器;
手術中の神経生理学的モニタリング(IONM)器具(及び必要な人材);並びに
ベクターを含有する10ccの注射器;別個の調剤学マニュアルに従って調製され、CT/手術室(OR)の部屋に運ばれる。
神経学的な評価がプロトコールのとおりに続くであろうし、主任治験医師が病院及び研究スタッフと共同で対象の看護を監督する。
この実施例はMPS Iを有する患者のための遺伝子治療の処置に関する。この実施例では、遺伝子治療のベクターである、野生型のhIDUA酵素をコードする修飾されたhIDUA遺伝子を発現する複製欠損のアデノ随伴ウイルスベクター9であるAAV9.CB7.hIDUAがMPS I患者の中枢神経系(CNS)に投与される。AAVベクターの用量が全身麻酔下でCNSに直接注入される。本明細書に記載されているように、神経認知の発達及び/または生体マーカーを含む代理マーカーの臨床測定、たとえば、対象のCSFまたは血清における病原性GAG及び/またはヘキソサミニダーゼの濃度の低下を用いて治療の有効性を評価する。
説明に役立つ遺伝子治療のベクターであるAAV9.CB.hIDUAが実施例3に記載されている。導入遺伝子のカセットからの発現は、CMVの前初期エンハンサ(C4)とニワトリのβアクチンプロモータのハイブリッドであるCB7プロモータによって推進される一方で、このプロモータからの転写はニワトリのβアクチンのイントロン(CI)の存在によって増強される。発現カセットのためのポリAシグナルはRBGポリAである。ベクターは製剤緩衝液(エリオットB溶液、0.001%プルロニックF68)に懸濁される。製造過程は以下の実施例5にて詳細に記載されている。
6歳以上である患者は、2.6×1012GC(2.0×109GG/g脳質量)(低用
量)または1.3×1013GC(1.0×1010GC/g脳質量)(高用量)のrAAV9.CB7.hIDUAの単回の髄内/嚢内投与を受ける。ベクターの投与については、患者は全身麻酔下に置かれる。腰椎穿刺を行い、先ず5ccのCSFを取り出し、続いてITで造影剤を注入して大槽の視覚化を助ける。CT(造影剤による)を利用して針の挿入及び後頭下の空間へのrAAV9.CB7.hIDUAの投与を導く。
所見のリスクを変化させるとは予想されない。重要なことに、NHPのいずれも、組織病理学的所見に関連する臨床症状を示さなかった。5×1010GC/g脳質量のより高い用量は、MPS Iイヌにおいて毒性が観察された用量(1×1012GC/g脳質量)より約20倍低く、本明細書に記載のGLP毒性試験においてNHPにおいて試験された最高用量(1.1×1011GC/g脳質量)より約2倍低い。
・新生児:約1×1011~約3×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・9ヵ月~6歳:約6×1012~約3×1014GC;
・3~6歳:約1.2×1013~約6×1014GC;
・6~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
・新生児:約3.8×1012~約1.9×1014GC;
・3~9ヵ月:約6×1012~約3×1014GC;
・9ヵ月~36ヵ月:約1013~約5×1013GC;
・6~12歳:約1.2×1013~約6×1014GC;
・3~12歳:約1.2×1013~約6×1014GC;
・12歳以上:約1.4×1013~約7.0×1014GC;
・18歳以上(成人):約1.4×1013~約7.0×1014GC。
ベクター投与の朝(投与前1日目)に、患者は、少なくとも30分間にわたってメチルプレドニゾロン10mg/kg IV(最大500mg)を受ける。メチルプレドニゾロンは、腰椎穿刺及びrAAV9.CB7.hIDSの髄内(IC)注入の前に投与される。アセトアミノフェン及び抗ヒスタミン薬による前投与は任意である。
mg/kg/日。9~12週目:0.1mg/kg。
スの負荷用量×3用量を投与する。-1日目から:シロリムス0.5mg/m2/日を、
4~8ng/mlの標的血中濃度で1日2回投与に分割した。シロリムスは48週目の来診後に中止する。
・ベクター投与の朝(投与前1日目)に、患者は、少なくとも30分間にわたってメチルプレドニゾロン10mg/kg IV(最大500mg)を受ける。メチルプレドニゾロンは、腰椎穿刺及びrAAV9.CB7.hIDSのIC注入の前に投与される必要がある。アセトアミノフェン及び抗ヒスタミン薬による前投与は、研究者の裁量により任意である。
2日目から2週目の終わりまで:0.5mg/kg/日
3及び4週目:0.35mg/kg/日
5~8週目:0.2mg/kg/日
9~12週目:0.1mg/kg
プレドニゾンは12週後に中止する。プレドニゾンの正確な用量は、次に高い臨床的に実際的な用量に調整することができる。
・ベクター投与の2日前(-2日目):4時間毎に1mg/m2のシロリムスの負荷用
量×3用量を投与する。
・-1日目から:シロリムス0.5mg/m2/日を、1~3ng/mlの標的血中濃
度で1日2回投与に分割した。
・シロリムスは48週目の来診後に中止する。
・タクロリムスを2日目(rAAV9.CB7.hIDUA投与の翌日)に0.05mg/kgの用量で1日2回で開始し、24週間血中濃度2~4ng/mLを達成するように調整する。
・24週目の来診から、タクロリムスを8週間かけて漸減する。24週目に、用量を約50%減少させる。28週目に、用量をさらに約50%減少させる。タクロリムスは32週目に中止する。
・タクロリムス及びシロリムス血中濃度のモニタリング
好適な患者には、
血漿、線維芽細胞または白血球で測定されたとき酵素活性によって確認されたMPS
Iの文書化された診断を有するもの;
他の神経学的なまたは精神医学的な因子によって説明できなければ、以下:IQ検査の平均値を下回る2:1標準偏差のスコアもしくは神経心理学的機能(言語の理解力、記憶、注意または知覚的推論)の1ドメインにおけるスコアのいずれかとして定義されるMPS Iによる早期の神経認知欠損の文書化された証拠(カルテ)、
逐次試験における1標準偏差を上回る低下の文書化された歴史的証拠(カルテ)を有するもの;
補助具の有無にかかわらず、試験日に該当する場合、必要とされるプロトコール試験を完成させ、進んで補助具を装用することに従うのに十分な聴覚能力及び視覚能力を有するものが挙げられてもよく、
任意で、少なくとも6ヵ月間のERT(たとえば、アルデュラザイム(登録商標)[ラロニダーゼ]IV)の安定な投与計画上にある。
・以下のいずれかを含むIC注入について禁忌を有する:
ベースラインMRI検査の見直しがIC注入の禁忌を示す
IC注入の禁忌を生じる以前の頭部/頸部の手術の既往
CT(または造影剤)または全身麻酔に対する禁忌を有する
MRI(またはガドリニウム)に対する禁忌を有する
<30mL/分/1.73m2の推定糸球体濾過量(eGFR)を有する
・MPS Iに起因しない神経認知欠損または神経精神病の状態を有する
・シロリムス、MMFまたはプレドニゾロンに対する過敏性反応の既往を有する
・免疫抑制療法について適当ではない状態(たとえば、<1.3×103/μLの好中球
の絶対数、<100×103/μLの血小板数及び<12g/dL[男]または<10g
/dL[女]のヘモグロビン)を有する
・腰椎穿刺に対する禁忌を有する
・HSCTを受けている
・治療の前6ヵ月以内にIT投与を介してラロニダーゼ投与を受けていた
・どこかの時点でラロニダーゼIT投与を受け、患者を過度のリスクに置くIT投与に関連すると見なされる有意な有害事象を経験した
・治療の前少なくとも3ヵ月間完全寛解になっていない、リンパ腫の既往、または皮膚の有棘細胞癌または基底細胞癌以外の別の癌の既往
・患者がギルバート症候群の以前既知の既往症及び総ビリルビンの<35%の結合ビリルビンを示す分画ビリルビンを有さない限り、>3×正常の上限(ULN)のアラニンアミノトランスフェラーゼ(ALT)またはアスパラギン酸アミノトランスフェラーゼ(AST)または>1.5×ULNの総ビリルビン
・ヒト免疫不全ウイルス(HIV)陽性検査の既往、活動型または再発性のB型肝炎またはC型肝炎、またはB型肝炎、C型肝炎またはHIVの陽性スクリーニング検査の既往
・妊娠中、出産後<6週、母乳授乳中、または妊娠を計画中(自己またはパートナー)
・治療の前1年以内のアルコールまたは薬物の乱用の既往
・患者の安全を脅かす深刻なまたは不安定な医学的または心理学的な状態を有する。
・制御不良の発作。
・新生児;
・3~9ヵ月齢;
・4ヵ月齢以上~9ヵ月齢未満;
・9ヵ月齢以上~18ヵ月齢未満;
・9~36ヵ月齢;
・18ヵ月齢以上~3歳未満;
・3~12歳;
・12歳以上;
・18歳以上の年齢での男女の対象が挙げられる。
1)対象の法定保護者は、治験の性質が説明された後、治験に関連する手続きが行われる前に、署名付きのインフォームドコンセントを提供する意思があり、かつ提供することができる。
2)重度のMPS I-ハーラーと診断されたことが証明されている:
a)MPS I-ハーラーに適合する臨床的徴候及び症状の存在、及び/または
b)重度の表現型と排他的に関連する突然変異についてのホモ接合性もしくは複合ヘテロ接合性。
3)55以上の知能指数(IQ)スコアを有する
4)補助具の有無にかかわらず、必要なプロトコール試験を完了するのに十分な聴覚能力及び視覚能力を有し、該当する場合、試験日に補助具を着用することに従う意思がある。
5)以下のいずれかを含むIC注入には禁忌である:
a)神経放射線科医/神経外科医の判定委員会によるベースライン磁気共鳴画像法(MRI)検査のレビューは、IC注入の禁忌を示す。
b)神経放射線科医/神経外科医の判定委員会による入手可能な情報のレビューに基づき、IC注入を禁忌とした以前の頭部/頸部手術の既往歴。
c)コンピュータ断層撮影(CT)(または造影剤)または全身麻酔に禁忌である。
d)MRI(またはガドリニウム)に禁忌である。
e)推定糸球体濾過量(eGFR)<30mL/分/1.73m2である。
6)MPS Iに起因しない神経認知障害を有するか、または医師の見解で研究結果の解釈を混乱させる可能性のある神経精神状態の診断を有する。
7)腰椎穿刺に禁忌である。
8)造血幹細胞移植(HSCT)を受けている
9)AAVベースの遺伝子治療製品による治療歴がある
10)任意の時間に髄内(IT)ラロニダーゼを投与され、医師の見解では対象を過度のリスクにさらすと考えられるIT投与に関連すると考えられる有意なAEを経験した。
11)スクリーニング前少なくとも3ヵ月間完全寛解していないリンパ腫の既往歴または皮膚の扁平上皮癌もしくは基底細胞癌以外の別の癌の既往歴がある。
12)最大の内科的治療にもかかわらず、制御されていない高血圧(収縮期血圧[BP]>180mmHg、拡張期血圧>100mmHg)。
13)血小板数<100,000/マイクロリットル(μL)である
14)対象にギルバート症候群の既往歴がない限り、スクリーニング時にアラニンアミノトランスフェラーゼ(ALT)またはアスパラギン酸アミノトランスフェラーゼ(AST)>3×正常上限(ULN)または総ビリルビン>1.5×ULNを有する。
15)ヒト免疫不全ウイルス(HIV)もしくはB型肝炎もしくはC型肝炎ウイルス感染の既往歴を有し、またはB型肝炎表面抗原もしくはB型肝炎コア抗体もしくはC型肝炎もしくはHIV抗体のスクリーニング検査陽性である。
16)インフォームド・コンセントフォーム(ICF)に署名する前の30日以内また
は5半減期以内(いずれか長い方)に治験薬を受容した
17)治験実施に関与する医療機関の従業員もしくはその他の個人の一等家族であるか、または治験実施に関与する医療機関の従業員もしくはその他の個人である。
18)PIの見解で、対象の安全性を損なう臨床的に有意なECG異常がある。
19)PIの見解で、対象の安全性、または治験への参加もしくは治験結果の解釈の成功を損なう重篤または不安定な医学的または心理的状態を有する。
20)医療機関の神経放射線科医/神経外科医の意見において、及びメディカルモニターとの議論において、対象の投与及び適切な投与に影響を及ぼし得る(脳)室シャント。
21)タクロリムス、シロリムスまたはプレドニゾンに対する過敏症反応の既往歴;
22)原発性免疫不全(たとえば、一般的な可変性免疫不全症候群)、脾臓摘出、または対象を感染症にかかりやすくするあらゆる基礎疾患の既往歴。
23)スクリーニングの少なくとも12週間前に完全には消失しなかった帯状疱疹、サイトメガロウイルス、またはエプスタインバーウイルス(EBV)感染。
24)来診2の少なくとも8週間前に消失しなかった入院または非経口抗感染薬による治療を必要とするあらゆる感染。
25)来診2前の10日以内に経口抗感染薬(抗ウイルス薬を含む)を必要とするあらゆる活動性感染。
26)活動性結核(TB)の既往歴またはスクリーニング中のクォンティフェロンTBゴールド検査の陽性。
27)ICFに署名する前の8週間以内のあらゆる生ワクチン。
28)ICFに署名する前の8週間以内の大手術または治験期間中に計画された大手術。
29)登録後6ヵ月以内にアデノイド切除術または扁桃摘出術の必要性を予測する。アデノイド切除術または扁桃摘出術が予測される場合は、スクリーニング前に実施すべきである。
30)絶対好中球数<1.3×103/μL。
31)臨床医が免疫抑制療法に適切ではないと考える任意の状態または実験室異常。
主要な臨床目的には、MPSI欠損に関連する神経認知の低下を防ぐこと及び/もしくは任意で元に戻すこと、並びに/または神経発達低下を遅延もしくは停止させることが挙げられる。臨床目的は、たとえば、ハーラーの対象についてBayleyの乳児及び幼児発達スケール(Bayley Scale of Infant and Toddler Development)、第3版(Bayley III)、並びに/またはWechslerのプレスクール及びプライマリー知能スケール(Wechsler Preschool and Primary Scales of Intelligence)、第4版(WPPSI-IV)]、並びに適応行動(Vineland-2)によって測定されるような、またはハーラー・シャイエの対象についてWASIによって測定されるような、知能指数(IQ)を測定することによって判定される。神経認知の発達及び機能の他の適当な測定、たとえば、Bayleyの乳児発達スケール(BSID-III)を用いて発達指数(DQ)を評価すること、Hopkins言語学習試験を用いて、並びに/またはWASI-I及び/もしくはBayler-III、並びに/または注意変数試験(TOVA)を用いて記憶を評価することが利用される。
で、血漿をバイオマーカー(GAG及びIDUA)についてモニターする。CSFは、IDUA活性、抗IDUA抗体、ヘキソサミニダーゼ(hex)活性、及びpGAGについて評価される。ベクター(たとえば、AAV9)に対する中和抗体及びIDUAに対する結合抗体の存在はCSF及び血清にて評価されてもよく、ベクターのカプシド(たとえば、AAV9)に対するT細胞応答はELISPOTアッセイによって評価されてもよく、CSF、血清及び尿におけるIDUA発現の薬物動態と同様にベクターの濃度(AAV9のDNAに対する定量的PCR(qPCR))がモニターされてもよい。CSF、血漿及び尿中のベクター排出がモニターされてもよい。
この実施例は、イヌ及び非ヒト霊長類の双方において、新生仔におけるアデノ随伴ウイルス(AAV)ベクターを用いた肝指向型の遺伝子導入は導入遺伝子に対する免疫寛容の持続した状態を誘導し、中枢神経系(CNS)を標的とするその後のベクター投与の有効性を実質的に改善することを実証している。このアプローチは、酵素α-L-イズロニダーゼ(IDUA)の活性の欠損のための進行性のCNS疾患を特徴とするリソソーム蓄積症であるムコ多糖症I型(MPS I)のイヌモデルに適用された。1ヵ月齢のイヌにおける髄内AAV送達を用いたCNSを標的とする遺伝子導入はイヌIDUAに対する抗体の誘導を生じ、それは脳の病変の改善を部分的に減衰させた。1週齢にてイヌIDUAを発現しているベクターによって全身性に処理されたMPS Iイヌは酵素に対する抗体を発生させず、1ヵ月齢での髄内AAV送達の際、CNSにて強固な発現を示し、脳の蓄積症の完全な是正を生じた。ヒトIDUAを発現するAAVベクターで全身性に処理された新生仔アカゲザルは同様に導入遺伝子に対して寛容を発生し、劇的に高いCSFでのIDUAの発生及びその後のCNSでの遺伝子治療後の抗体誘導の非存在を生じた。これらの知見は、免疫学的な発達の決定的な期間の間に導入遺伝子に対する寛容を誘導することによって遺伝子治療の有効性及び安全性を改善する可能性を示唆している。
1.ベクターの作製
被験物質は、ニワトリβアクチンプロモータ(CB7)とキメライントロン(CI)とコドンを最適化させたイヌIDUA導入遺伝子(cIDUA)とポリアデニル化シグナル(RBG)から成る発現カセットをパッケージするAAV9のカプシドから成った。発現構築物にはAAV血清型2の逆方向末端反復が隣接した。このベクターは、AAV2/9.CB7.CI.cIDUA.RBGまたはAAV9.CB7.CI.cIDUA.RBGと名付けられる。一部の動物は新生仔のとき異なるベクターによって静脈内で処理されてイヌIDUAタンパク質に対する寛容を誘導した。このベクターは、肝臓特異的な甲状腺ホルモン結合グロブリンプロモータ(TBG)と人工イントロン(PI)とコドンを最適化させたイヌIDUA導入遺伝子(cIDUA)とポリアデニル化シグナル(RBG)
から成る発現カセットをパッケージするAAV8のカプシドから成った。発現構築物にはAAV血清型2の逆方向末端反復が隣接した。ベクターは293細胞の三重形質移入によって作製し、以前記載された[L.Wang,et al,Human gene therapy,22,1389-1401,(2011);published online EpubNov]ようなイオジキサノール勾配で精製した。
MPS Iイヌのコロニーは、研究における動物の飼育及び使用に関するNIH及びUSDAのガイドラインのもとでペンシルベニア大学獣医学部で維持された。MPS Iイヌの試験プロトコールはすべてペンシルベニア大学の施設内実験動物委員会によって承認された。新生仔MPS Iイヌにおけるベクター注入については、AAV8ベクターを0.5~1mLの無菌生理食塩水にて希釈し、頸静脈を介して注入した。AAV9ベクターの髄内注入及びCSFの回収は、以前記載された[C.Hinderer,et al,Intrathecal Gene Therapy Corrects CNS Pathology in a Feline Model of Mucopolysaccharidosis I.Molecular therapy:the journal of the American Society of Gene Therapy,(2014);published online EpubJul,16]ような後頭下のアプローチを介して行った。合計9匹のMPS Iイヌがこの研究に含まれた。遺伝子型はPCR及び血清の酵素アッセイによって出生時に確認した。6匹のイヌが、1日齢(N=3)または7日齢(N=3)でAAV血清型8ベクター(5×1012ゲノムコピー/kg[GC/kg]体重)のIV注入を投与された。1匹は出生後3日で死亡した。処理した残り5匹の動物と同様に3匹の未処理のMPS Iイヌを1ヵ月齢で髄内AAV9(1012GC/kg)によって処理した。最初の7週齢まで毎週、その後毎月、血液を末梢血管から採取した。CSF(1mL)は、髄内注入のとき(1ヵ月齢)、注入の7及び21日目、及びその後毎月採取した。ナトリウムペントバルビタール80mg/kg、IV)の投与によって安楽死を行った。5匹の動物は9ヵ月齢で安楽死させ、残りは11カ月齢で安楽死させた。未処理のMPS I及び対照は6ヵ月齢~26カ月齢の間で安楽死させた。組織を採取し、以前記載[Hinderer,et al,2014]されたように処理した。
血清や血漿を採取するために末梢血管から血液試料(約3~6mL)を出生時、次いで毎月採取した。試料採取が完了した際、デクスメデトミジンに匹敵する用量で反転アチパメゾールをIMで与えた。
1.MPS Iイヌにおける髄内AAV9が介在する遺伝子導入の後のイヌIDUAに対する抗体の誘導
MPS Iイヌモデルはヒト疾患の症状の多数を忠実に繰り返す[E.Kakkis,et al,Molecular genetics and metabolism,
83,163-174(2004);published online EpubSep-Oct;R.M.Shull,et al,Am.J.Pathol.114,487-495(1984)]。これらの動物は、IDUAの第1イントロンの保持を生じるスプライス部位の突然変異のせいで検出可能なIDUA活性を有さない[K.Menon,et al,(Genomics,14,763-768(1992)]。これらの動物には検出可能なIDUA発現がないことを考えて、これらの個体は一般に完全長ではないIDUAを産生する対立遺伝子を運び、そのタンパク質に対してそれらが免疫的に遭遇したことがないままであるので、我々はそれらが、MPS Iの重篤形態の患者で生じる髄内遺伝子治療に対する免疫応答をモデル化することを予想した[N.J.Terlato,G.F.Cox,Can mucopolysaccharidosis type
I disease severity be predicted based on a patient’s genotype? A comprehensive review of the literature.Genetics in medicine:official journal of the American College of Medical Genetics 5,286-294(2003);published online EpubJul-Aug]。MPS Iイヌの脳は、ニューロンにおけるGM3のようなガングリオシドの広範な蓄積、と同様にコレステロールとLIMP2を含むリソソームの膜タンパク質との異常な蓄積を含む、MPS
Iに関連する特徴的な病態を示す[R.M.Shull,et al,Am.J.Pathol.114,487-495(1984)]。MPS Iイヌはまた、髄膜におけるグリコサミノグリカン(GAG)の顕著な蓄積を示し、一部のMPS I患者における脊髄圧迫に寄与する過程である有意な髄膜肥厚を生じる[E.Kachur,et al,Neurosurgery,47,223-228(2000);published
online EpubJul;A.Taccone,et al,Pediatric Radiology,23,349-352(1993);published online EpubSep;S.Vijay,J.E.Wraith,Clinical presentation and follow-up of patients
with the attenuated phenotype of mucopolysaccharidosis type I.Acta Paediatrica,94,872-877(2005)]。
MPS IイヌにおいてイヌIDUAの新生仔発現がその酵素に対する免疫寛容を誘導し得るかどうかを判定するために、出生後1日目(N=3)または7日目(N=3)に肝
臓選択性のプロモータからイヌIDUAを発現するAAV血清型8ベクターのIV注入によって6匹のイヌを処理した。出生日に処理したイヌのうち1匹は処理の2日後に死亡した。生き残った新生仔のイヌは全体として未処理のMPS Iイヌについての病歴データに類似し、最初の2週齢でおよそ20%の死亡率を有する[Vite,R.et al,Molecular therapy:the journal of the American Society of Gene Therapy 15,1423-1431(2007);published online EpubAug]。MPS Iイヌにおけるこの早期の死亡率の原因は究明されていない;この処理された動物では、死体の検視はMPS Iに典型的な全身性の病変と同様に全身性の細菌感染の可能な証拠を示した。処理した動物は血清IDUAの上昇とそれに続く迅速な低下を明らかにした。これは、新生仔における肝臓遺伝子導入に非統合性のベクターを利用する以前の研究における肝細胞の分裂の間でのベクターゲノムの喪失による一時的な発現の観察に一致する[L.Wang,et al,Human gene therapy,23,533-539(2012);published online EpubMay]。
2.MPS IイヌのCNSにおける生化学的な及び組織学的な異常の是正
リソソーム酵素であるヘキソサミニダーゼ(Hex)はMPS I動物の組織で上方調節され、脳組織及びCSFの双方で上昇したHex活性はIDUA欠乏の下流で生じる異常な細胞性の過程についての有用なマーカーとして役立つ[Hinderer,et al.(2014)]。ベクターの髄内送達のとき(生後約1ヵ月)のCSFのHex活性の測定は、MPS Iイヌすべてにて異常に上昇したHex活性を示した。髄内AAV9のみで処理した動物はHex活性で中程度の低下を示し、最高の残留IDUA発現を伴う動物のみが正常範囲のHex活性に達した。新生仔で全身性の遺伝子導入によって処理され、その後ベクターの髄内投与を受けた5匹の動物はすべてCSFのHexの完全な正常化を実証した。2匹の髄内の処理のみを受けた最低のCSFのIDUAレベルの動物では効果はやや低下したが、脳組織試料におけるHex活性はCSFのHexよりも治療に大きな応答を示し、処理した動物すべてにおいて脳のHex活性の実質的な低下を伴った。
する脊髄圧迫の多数の症例に関与し、CSF再吸収の正常な経路を妨害することによって一部のMPS I患者における交通性水頭症の発症に寄与する可能性もある。処理された動物はすべて髄膜のGAG蓄積での改善の証拠を示した。寛容のイヌすべて及び非寛容のイヌ1匹において髄膜はほぼ完全に正常であると思われた一方で、CSFの最低のIDUA活性を持つ2匹の非寛容の動物は一部のGAG蓄積を保持した。
MPS Iイヌにおいて観察された免疫寛容誘導のための新生仔の時間帯が霊長類にて見いだされ得るかどうかを評価するために、新生仔アカゲザル(N=4)にて類似の研究を行った。これらの動物はIDUA欠乏ではないので、ヒトIDUA導入遺伝子を用いて、活性のある内在性遺伝子を欠いている患者にて種特異的な導入遺伝子に対して予想され得る免疫応答をモデル化した。2匹の新生仔アカゲザルに肝臓特異的なプロモータからヒトIDUAを発現するAAV8ベクターをIVで出生時投与した。双方とも血清IDUA活性の一時的な上昇を明らかにした。2匹の追加の新生仔に無関係な導入遺伝子(ヒト第IX因子)を発現するAAV8ベクターをIVで出生時投与した。4匹の動物すべてに、1ヵ月齢で髄内注入によってヒトIDUAを発現するAAV9ベクターを投与した。MPS Iイヌに類似して、IDUA未処理の動物は注入の3週間後、CSFのIDUA活性の低下を示し、投与後2ヵ月までにほぼベースラインレベルに戻った。これらの動物はまたCSFにおいて導入遺伝子特異的な抗体を発生した。出生時にIDUA遺伝子導入をIVで投与した2匹の動物はCSFにてヒトIDUAに対する抗体を発生させず、AAV9の髄内投与の2ヵ月後、正常の10倍を超える高いCSFの酵素活性を維持した。動物はすべて研究期間の間、頑丈で健康のままであり、有害事象の証拠はなく、年齢に基づいて且つ既往対照と比べて正常な成長の軌跡、及び完全な血球数(CBC)及び正常限界範囲内の生化学検査を伴った。
野生型の治療用タンパク質に対する免疫活性化は劣性疾患についての潜在的な懸念である。抗体は静脈内で送達される酵素の分布及び取り込みを妨害することができるので、タンパク質補充療法に対する抗体反応は一部のLSDについて特に難易度が高い[E.J.Langereis,et al,Molecular genetics and metabolism,(2014);published online EpubOct,29]。抗体は形質導入された細胞から分泌される酵素が介在する相互是正を妨害し得るので、抗体はこれらの疾患を標的とする遺伝子治療にとって同等に問題がある。
る現在のデータは、イヌと同様に残留IDUA活性を有さない重篤な疾患のMPS I患者についてさえ、髄内遺伝子導入の後で生じる可能性がある抗導入遺伝子抗体反応は有害な臨床事象を生じず、抗体反応にもかかわらず、実質的な有効性は保持されることを示している。しかしながら、これらのデータはまた、CNSにおけるIDUAに対する抗体反応を防ぐことがMPS Iのための髄内遺伝子治療の有効性を改善することも示唆している。
A.材料及び方法
ベクターは、ヒトのイズロニダーゼ(hIDUA)を発現する血清型9の非複製組換えアデノ随伴ウイルス(AAV)である。AAV9血清型はIC投与に続いてCNSでのhIDUA産物の効率的な発現を可能にする。
AAV-hIDUAベクターゲノムのプラスミドであるpAAV.CB7.CI.hI
DUAco.RBG(p3032)は7,165bpのサイズである。このプラスミドに由来するベクターゲノムは、hIDUA発現カセットに隣接するAAV2に由来するITRを伴った一本鎖DNAゲノムである。導入遺伝子カセットからの発現は、CMVの前初期エンハンサ(C4)とニワトリのβアクチンプロモータの間のハイブリッドであるCB7プロモータによって推進される一方で、このプロモータからの転写はニワトリのβアクチンのイントロン(CI)の存在によって増強される。発現カセットのためのポリAシグナルはRBGポリAである。プラスミドはコドンを最適化し、hIDUA配列を合成することによって構築され、得られた構築物は次いでプラスミド、pENN.AAV.CB7.CI.RBG(p1044)、CB7とCIとRBGを含有するAAV2のITRが隣接する発現カセットの発現要素にクローニングされてpAAV.CB7.CI.hIDUAco.RBG(p3032)を得た。
逆方向末端反復(ITR):AAVのITR(GenBank #NC001401)は両端で同一であるが、逆向きである配列である。AAV2のITR配列は、AAVとアデノウイルスのヘルパー機能がトランスで提供されると、双方ともベクターDNAの複製の開始点及びベクターゲノムのパッケージングシグナルとして機能する。そのようなものとして、ITR配列はベクターゲノムの複製及びパッケージングに必要とされるシス配列のみを表す。
の開始点及びベクターゲノムのパッケージングシグナルとして機能する。そのようなものとして、ITR配列はベクターゲノムの複製及びパッケージングに必要とされるシス配列のみを表す。
MPS Iイヌのコロニーは、研究における動物の飼育及び使用に関するNIH及びUSDAのガイドラインのもとでペンシルベニア大学獣医学部で維持された。試験プロトコールはすべてペンシルベニア大学の施設内実験動物委員会によって承認された。組換えヒトIDUAの点滴については、使用直前にラロニダーゼ(Genzyme)を生理食塩水で5倍に希釈した。末梢静脈のカテーテルを介して点滴は2時間にわたって行った。AAV9ベクターの髄内注入及びCSFの採取は、以前記載された[C.Hinderer,et al,(Mol.Ther.J.Am.Soc.Gene Ther.22,2018-2027(2014)]ように後頭下のアプローチを介して行った。ナトリウムペントバルビタール(80mg/kg、IV)の投与によって安楽死を行った。以前記載された[Hinderer(2014)]ように組織を採取し、処理した。
以前記載された[C.Hinderer,et al,(Mol.Ther.J.Am.Soc.Gene Ther.22,2018-2027(2014))]ように組織溶解物及びCSFにてIDUA及びHexの活性を測定した。
リン酸緩衝液pH5.8にて5μg/mLに希釈した組換えヒトIDUA(Genzyme)によって4度で一晩ポリスチレンのELISAプレートをコーティングした。プレートを洗浄し、pH5.8のリン酸緩衝液中の2%BSAでブロックした。PBSにて1:50に希釈したCSF試料と共にプレートを室温で1時間インキュベートした。プレートを洗浄し、2%BSAを伴ったリン酸緩衝液にて1:10,000に希釈したHRPを結合した抗イヌIgG(Pierce,Rockford,IL)によって結合抗体を検出した。テトラメチルベンジジン基質で15分間ELISAを発色させ、次いで2Nの硫酸で反応を止め、450nmにて吸光度を測定した。連続希釈した陽性試料の標準曲線から力価を算出した。
脳の組織学的な解析は、GM3について陽性のニューロン、コレステロール及びLIMP2の蓄積を定量するための以下の改変と共に以前記載された[C.Hinderer,2014]ように実施し;LIMP2及びフィリピンで染色した大脳皮質の切片の画像は、層I(分子層)と層IIの間の境界が画像の上縁を形成するように10×の対物レンズで撮影した。各動物から合計10枚の画像を取得した。GM3で染色した脳の切片の画像は、脳の分子層を含む大脳皮質表面に直下の領域から4×対物レンズで撮影した。各動物からの7枚の画像を解析した。画像はすべて以前記載された[M.Aldenboven,et al,Biology of Blood and Marrow Transplantation,14,485-498(2008);published online EpubMay]ように「閾値」及び「粒子を解析する」モジュールを用いてImageJソフトウエア(Rasband,W. S.,National Institutes of Health,USA;rsb.info.nih.gov/ij/)によって処理した。頸部髄膜の肥厚の定量は頸部脊髄のH&E染色した切片で実施し
た。300μm間隔でスライド当たり髄膜の全厚さの15の測定を行った。
8 Vectors.Human gene therapy,22,1389-1401,(2011);published online EpubNov]ようなTaqManPCRによってベクターゲノムを定量した。データは適宜、Kruskal-Wallisの検定、とその後のDunnの検定またはMann-Whitneyの検定を用いて評価した。p<0.05を統計的に有意と見なした。統計的解析はすべてPrism6.0(GraphPadソフトウエア)を用いて行った。
1.ヒトIDUAを発現する髄内AAV9はMPS Iイヌにて導入遺伝子に特異的な強力な免疫を引き出す。
すべての動物でリンパ球性の髄液細胞増加症も示した(図4A、未処理)。このコホートでは、上昇したCSFの抗体及び細胞数は臨床兆候及び他の臨床検査の異常とは関連せず、髄液細胞増加症は自然に解消した。注入の6ヵ月後の剖検時、組織学的な評価は脳または脊髄にて病状の証拠を示さなかった。ベクターの生体分布は広範なCNSの形質導入及びベクターゲノムの持続性を実証した。
導入遺伝子に対する誇張された免疫応答の非存在下でヒトIDUAを発現するAAV9ベクターを評価するために、我々は新生仔曝露を介してヒトタンパク質に対する免疫寛容を誘導しようと試みた。出生5日後に、肝特異的プロモータからヒトIDUAを発現するAAV血清型8ベクター(AAV8)の単回静脈内注入によって6匹のMPS Iイヌを処理した。1ヵ月齢にて、以下:1010、1011及び1012GC/kgのような3つのコホート(コホート当たりn=2の動物)においてヒトIDUAを発現する異なる用量のAAV9ベクターの大槽内への髄内注入によって動物を処理した。動物はすべて寛容化されていない動物に類似してCSFのIDUA活性の用量依存性の上昇を示した(図2A)が、このコホートではCSF酵素の発現は21日目を超えて持続し、実験が持続する間検出可能なままだった(図2B、寛容化)。CSFの抗体反応は、処理を経験したことがない(すなわち、寛容化されていない)動物が髄内ベクターを投与された場合に見られるものと比べて鈍く;寛容化されたコホートにおける2匹(I-602及びI-606)だけが検出可能な力価を示し、それは同等のベクター用量で処理した処理未経験動物よりもおよそ20倍低かった(図3)。このコホートで最高の抗体力価を持つイヌ(I-606)だけが処理未経験動物よりも低レベルにもかかわらず、21日目でCSFでの高いリンパ球を示した(図4A及び4B)。これらのコホートでは臨床的な有害事象はなかった。
新生仔遺伝子導入を介してヒトIDUAに対して寛容化した6匹のMPS IイヌをAAV9の髄内注入の6ヵ月後に屠殺した。脳の溶解物はベクターの最高用量でヘキソサミニダーゼ活性の完全な正常化を実証し、最低用量での部分的な是正を伴った(図5)。ヘキソサミニダーゼ活性はベクター用量のすべてにおいてCSFにて正常化された(図8)。MPS I患者における脊髄圧迫に寄与し得る頸部髄膜の肥厚は、すべての用量で処理
された動物にて元に戻った(図9)。脳の組織学的な評価は、hIDUAに寛容のイヌではLIMP2及びGM3の蓄積での用量依存性の低下を示した(図6A、6B)。最高のベクター用量で処理した動物は正常対照に類似するLIMP2及びGM2の染色を示し;最低用量では、一部のマーカー(LIMP2及びHex)では測定できる改善がなかったのに対してGM2の蓄積は明らかには低下しなかった。従って、1010GC/kgの低用量は最小効果用量(MED)であると思われた。
1×1010GC/g脳質量)GCに相当する。
ヒトIDUAの肝臓発現が寛容の誘導に必要であるかどうかを判定するために、我々は、1ヵ月齢でのAAV9の髄内注入の前、出生後7及び14日目に組換えヒトIDUA(
0.58mg/kg)の点滴によって2匹のMPS Iイヌ(I-663及びI-664)を処理した。ヒトIDUAを発現するベクターで新生仔として処理されたイヌに類似して、酵素処理したイヌは高レベルのCSF IDUA活性(図2A、2B)及びヒトIDUAに対する最小の抗体反応(図2)またはCSFの髄液細胞増加症(図4A-4B3)を持続して示した。双方の動物で脳のヘキソサミニダーゼ活性は低下し(図5)、蓄積病変は効果的に一掃された(図6A、6B)。
MPS Iの治療のための髄内AAV9送達の有効性を評価することは、CSFへの注入を介して達成され得るベクターの分布及び疾患特異的なマーカーに対する形質導入のその程度の影響の双方の評価を必要とした。これらの研究は、十分に類似するサイズ及び生体構造も示して臨床的な送達法及び得られるベクター分布の意味ある評価を可能にしつつ、疾患の病態生理を正確に反映し得る動物モデルの使用を必要とした。MPS Iイヌモデルはヒトの表現型を忠実に複製し、同じ生化学的な及び組織学的な病変だけでなく、同じ臨床所見も示す[KP.Menon,et al,Genomics,14:763-8(1992);RM.Shull,et al,(1984);RM.Shull,et al,(1994);C.Ciron,et al,Ann Neurol,60:204-213(2006);P.Dickson,et al,Ann.Neurol,60:204-213(2006)]。ヒトにおけるMPS Iに対する表現型の類似性のゆえに、MPS Iイヌは全身性疾患の治療のための酵素補充療法の開発で広範に使用された[RM.Shull,et al,PNAS,91:12937-12941(1994);P.Dickson,et al,J.Clin.Invest,118:2868-2876(2008)]。MPS Iイヌはまた、散発的に脊髄圧迫及び水頭症を発生する疾患のCNS所見も模倣する[P.Dickson,et al,Mol.Genet.Metab.99,S15-S15(2010);P.I.Dickson,et al,Mol.Genet.Metab.98,70-70(2009);C.H.Vite,et al,Comp.Med.63,163-173(2013)]。MPS Iイヌについて認知試験は報告されていないけれども、脳における組織学的な及び生化学的な所見は十分に特徴付けられ、その疾患の重篤な形態を持つヒトにおける知見を忠実に反復している[RM Shull(1984);C.Ciron(2006);SU Walkley,et al,Acta Neuropathol.(Berl.)75,611-620(1988)]。MPS Iイヌの脳はリソソーム膜タンパク質(LIMP2)及びガングリオシド(GM3)の蓄積並びにヘキソサミニダーゼ(Hex)のようなリソソーム酵素の上方調節を明示している。ガングリオシドの蓄積はMPS I及び他のリソソーム蓄積疾患における認知機能と相関するので、疾患の重症度及び治療転帰を評価するための重要なマーカーである[S.U.Walkley,M.T.Vanier,Secondary lipid accumulation in lysosomal disease, Biochim.Biophys.Acta BBA-Mol.Cell Res.1793,726-736(2009);G.Constantopoulos,et al,J.Neurochem.34,1399-1411(1980)]。MPS Iイヌはまた患者で特定されるものに類似するニューロンの形態における変化も示す[SU Walkley,(1988)]。これらの著しい類似性によってこれはヒトにおけるMPS IのCNS所見に対する新規の治療法としてのAAVの髄内送達の評価のための説得力のあるモデルになった。ITでのAAV9の送達のために臨床的に使用される投与の経路を反復する大型動物モデルの能力と同様に得られるベクターのCNSにおける分布はさらに、これらの研究にとってのMPS Iイヌの妥当性を支持した。
におけるヒトIDUAに対する免疫応答は患者で観察されるものよりもはるかに極端であることは明らかである。イヌ及びMPS I患者の双方におけるタンパク質の静脈内送達は抗体を誘発することが多いが、イヌでは、これらの反応はさらに強力であり、連続投与の際、低下しそうになく、それに続く点滴に対するアナフィラキシー反応に関連することが多い[RM.Shull,et al,1994);E.Kakkis,et al,Proc.Natl.Acad.Sci.UA.101,829-34(2004)]。CNSにおけるヒトIDUAに対する免疫応答の差異は一層さらに顕著であり;酵素の髄内点滴で処理されたMPS Iイヌは髄膜炎と同様にCSFで検出可能な抗体反応の証拠を示す。対照的に、タンパク質の反復IT点滴によって治療された小児及び成人のMPS
I患者双方については、類似の有害効果はなく、IDUAに対するCSF抗体について治療された5人の患者のうち、たった1人が陽性であった[C.Ciron(2006);P.Dickson,et al,(2010);P.I.Dickson,et al,Mol.Genet.Metab.98,70-70(2009);P.I.Dickson,et al,Mol.Genet.Metab.101,115-122(2010);P.I.Dickson,et al,Mol.Genet.Metab.93,247-247(2008);E.Kakkis,et al,Mol.Genet.Metab.83,163-174(2004);T.C.Lund,et al,Mol.Genet.Metab.111,S74(2);M.Vera,et al,Pediatr.Res.74,712-720(2013)]。興味深いことに、MPS
Iイヌは、ヒト酵素に対するよりも低レベルであるが、イヌIDUAに対してもCSF抗体を発生させるということは、このモデルがIDUAに対する免疫に向けた全体的に大きな傾向を有することを示唆しており、それは種特異的ではないタンパク質の使用によって悪化する。MPS Iイヌ及び患者におけるヒトIDUAの静脈内送達及び髄内送達双方の転帰におけるこれらの際立った差異は、MPS IイヌにおけるヒトIDUAに対する一貫して悪化した免疫応答を示し、この応答を防ぐことがヒトにて予想されるベクター活性を反復させるのに必要であることを示唆している。新生仔曝露を介してタンパク質に対する寛容を誘導することが、悪化した免疫応答の介入なしでこのモデルにてヒトベクターの有効性の評価を可能にした。これは、最も妥当な動物モデルにてヒト初回遺伝子治療試験の設計で必須の因子である最小有効用量の正確な決定を可能にする重要情報を提供した。さらに詳しくは、広範な投与量決定試験をMPS Iイヌにて実施した。最小有効用量は免疫寛容の動物で決定されたが、本明細書に記載されているoqPCR法によって決定されたように2×109GC/g脳質量の用量であると推定される。用量漸増安全性試
験は免疫能力のある(すなわち、IDUAにもAAVにも遭遇していない)イヌにて実施し、毒性は1012GC/gの用量で観察された。免疫介在性毒性の厳密なイヌモデルにおける1012GC/gでの用量制限毒性試験(DLT)の知見に基づいて、アカゲザルにおける公式の医薬品安全性試験実施基準(GLP)の毒性試験にて10倍低い用量を投与するであろう。公式のGLP非ヒト霊長類(NHP)毒性試験で評価される用量は1.1×1011GC/g脳質量であろう。毒性に遭遇しなければ、臨床の出発用量は1.1×1010GC/g脳質量であろう。この出発用量はイヌMPS Iモデルにおける最小有効用量(MED)よりもほぼ5倍多く、MPS Iイヌ及びネコの研究にて信頼できる組織学的反応を明示した用量とほぼ同じであるということは、この用量の臨床有効性の理に適った期待を支持している。出発用量はまたMPS Iイヌで毒性が観察された用量よりもほぼ90倍少なく、非ヒト霊長類で調べられた用量よりも10倍少ないということは、ベクターまたは導入遺伝子に関連する毒性に対してさらに大きな感受性を示すヒト対象の潜在力を説明する許容できる安全性限界を提供している。これらのデータに基づいて、出発用量は許容できる利益:リスクのプロファイルを表し、その際、用量は治療範囲内にある(従って臨床利益を提供してもよい)と予想されるが、毒性ベクター用量を下回る(従ってそれなりに安全であるはずである)と予想される。以下の計算はイヌにおける用量をヒトにおける出発用量にどのように外挿するかを示す:1ヵ月齢のイヌの脳=45グラム;処理されたことがないイヌ:MED9×1010GC合計(2×109GC/g脳質量);成人
の脳=1300グラム;ヒトの出発用量(5×イヌMED)、1.4×1013GC合計(1.1×1010GC/g脳質量)。このアプローチがなければ、唯一の選択肢は種特異的導入遺伝子によるベクターからの有効性データを外挿することであり、それは効能に重要な差異を有してもよく、またはヒトタンパク質に対してさらに免疫寛容であるあまり代表的ではない動物モデルに研究を動かし得る。新生仔寛容の誘導プロトコールが免疫抑制剤の二次的な結末を回避する明瞭な利点を有するけれども、この設定では薬理学的な免疫抑制も採用することができる。
併用することが患者の転帰を実質的に改善してもよい。認可された組換え酵素の利便性によってMPS Iがこのアプローチの最初のヒト試験での優れた候補者になる。ヒト新生児が寛容の誘導のために1~2週間の同様の時間帯を示すのであれば、上手く行く介入に十分早期の患者を特定するために新生児のスクリーニングが必須である。従って、MPS
I及び他のリソソーム蓄積疾患についての新生児スクリーニングの進行中の実施は新生児寛容の誘導プロトコールの臨床的評価に決定的に重要であろう。
A.髄内送達
この研究の目的は、6~9ヵ月齢のヒト乳児に発達上類似するモデルである1ヵ月齢のアカゲザルにてヒトIDUAを発現するAAV9ベクターであるAAV2/9.CB7.CI.hIDUAco.RBGの髄内(IT)投与の安全性を評価することだった。加えて、この研究は血清または脳脊髄液(CSF)における導入遺伝子産物に対する抗体がベクター投与の安全性及びヒトIDUAの活性に影響を及ぼすかどうかを評価した。
なかった。
この研究で使用したベクターには、rAAV9.hIDUA、rAAV8.hIDUA及び無関係な導入遺伝子(hFIX)を有するAAV8ベクターが含まれる。
4匹の1ヵ月齢のアカゲザル(M.mulatta)に3×1012GC/kgのrAAV9.hIDUAをITで投与し、ベクター投与の後1年を超えてモニターした。これらの動物のうち2匹はヒトIDUAタンパク質に対して出生時寛容化した。
ベクターは、サイトメガロウイルスのプロモータ(CMV)とキメライントロン(PI)とコドンを最適化したヒトIDUA導入遺伝子(hIDUA)とポリアデニル化シグナル(SV40)とから成る発現カセットをパッケージするAAV9カプシドから成った。発現カセットにはAAV血清型2の逆方向末端反復が隣接した。この研究ではベクターは1つ使用されたが、このベクターは、AAV2/9.CMV.PI.hIDUA.SV40、AAV2/9.CMV.PI.hIDUAco.SV40、AAV2/9.CMV.PI.hIDUAco.SV40PAまたはAAV9.CMV.PI.hIDUA.SV40のいずれかとして示される。
この研究には、2匹のメスのカニクイザル(ID06-09及び07-19)が含まれた。双方のカニクイザルは1012ゲノムコピー/kg体重(GC/kg)のAAV2/9.CMV.PI.hIDUAco.SV40PAの投与を受けた。それが臨床使用で提案された経路なので、後頭下穿刺を介した髄内(IT)投与が選択された。
2匹のメス成熟カニクイザルをCNVプロモータからヒトIDUAを発現するAAV9ベクターの髄内注入によって処理した。ベクター投与ののち研究の1、7、14、28、91、118、147、182、208、239、261、294、322、350、378、413、434、462、490、518、561、589、624、及び636日目に、体重、身体検査、及び血球数及び血清臨床検査値を評価し、その後、組織病理及びベクターの生体分布の解析のために動物を剖検した。ベクターに関連した臨床的な有害事象はなかった。1匹の動物がベクター投与の600日後に大腿動脈瘤を発症した。これは反復した採血に続発すると考えられ、処理関連でありそうにない。最終CSFパラメータを含む臨床病理パラメータに対する処理関連の影響はなかった。組織病理はCNS病変の証拠を示さず、末梢器官における明らかなベクター関連の異常を示さなかった。生体分布の解析は、例外1つを伴って末梢器官よりも1~2桁多い、双方のNHPSの脳及び脊髄におけるベクターの沈着を示した。AAV9カプシドに対する予め存在する中和抗体がない動物1匹にて有意な肝臓分布が生じ、その際、ベクターに対する血清抗体が予め存在する動物は最小限の肝臓の形質導入を示した。双方の動物からの脳切片の免疫染色はヒトIDUAの発現を明らかにした。
処理に遭遇したことがないマウスと同様に導入遺伝子産物であるヒトのイズロニダーゼ(IDUA)に対する既存の抗体を持つマウスにおいてAAV9.hIDUAの脳室内(ICV)投与に続く毒性の証拠を評価するように予備研究が設計された。
GC)にて毒性は明らかだった。
以下の非ヒト霊長類(NHP)の安全性研究は、2用量を使用する蛍光透視ガイド下後頭下注入(大槽)を含んだ。低用量(LD)は1.1×1010GC/gであり、高用量(HD)は1.1×1011GC/g(イヌ最大耐量(MTD)と同等)であった。免疫抑制を伴うHD(IS)を伴うアームについては、プロトコールは以下のようにMMF及びシロリムスの共投与を含んだ:MMFは21日目から60日目まで、及びシロリムスは-21日目から90日目まで。試験したNHPでは、臨床所見はなく、血清化学または血液学的パラメータに臨床的に有意な異常はなかった。抗AAV及び抗hIDUA免疫応答並びに免疫介在性軸索障害の証拠があった。これらのデータは、図22~23及び以下の表に提供される。
この研究は、アカゲザルにおける画像誘導の後頭下穿刺法によって投与後180日までのAAV9.CB7.hIDUAの安全性及び生体分布を評価した。成熟アカゲザル(n=9、メス6、オス3、1A、B及びC群)に画像誘導の後頭下穿刺法によって1.1×1011GC/g脳質量の用量に近似的に相当する1013GCのAAV9.CB7.hIDUAの単回用量を投与した。追加の3匹の動物(メス2、オス1、2A及びB群)に画像誘導の後頭下穿刺法によって溶媒(エリオットB(登録商標)+0.001%プルロニック(登録商標)F68)の単回用量を投与した。被験物質または対照物質の投与ののち14日目(1A及び2A群)、90日目(1B及び2B群)または180日目(1C群)に動物を安楽死させ、剖検した。毒性は、研究の0、3、7、14、21、30、45、60及び90日目に毎日の観察によって、及び身体検査、CBCや血清の化学パネル、凝固パネル、及びCSFの細胞数の解析、タンパク質やグルコースの濃度によって評価した。剖検では、病理学者が肉眼病変について組織を評価し、顕微鏡で調べた。ベクターのカプシド及び導入遺伝子産物に対するT細胞応答はELISPOTによって評価し、導入遺伝子産物に対する抗体反応はELISAによって血清及びCSFにて測定した。ベクターの生体分布はqPCRによって評価した。
させ、剖検した動物の脳及び脊髄にて同じレベルで持続した。末梢器官、特に肝臓及び脾臓(105~106GC/μgDNA)、細網内皮系組織(リンパ節及び骨髄103~104GC/μgDNA)及び心臓(103~104GC/μgDNA)への有意なベクターの分布もあった。これらのデータはベクターが末梢に広がり、ベクターの髄内送達に続いて肝
臓の形質導入が可能であることを示唆している。
AAV9.hIDUA試験ベクター(エリオットB(登録商標)+0.001%プルロニック(登録商標)F68における)を評価した。この研究には12匹のアカゲザルが含まれた。動物は無作為に5群に割り当てた。オス1及びメス2から成る試験群1A、1B及び1Cを試験ベクターで処理し、それぞれ、研究の14±2日目、90±2日目、または180±2日目に安楽死させ、剖検した。2A群及び2B群の動物は溶媒(エリオット製剤緩衝液)で処理し、それぞれ14±2日目または90±2日目に安楽死させ、剖検した。
ベクターの投与処置に関連した有害事象はなかった。AAVベクターゲノムは、AAV9.hIDUA試験ベクターで処理した動物すべての脳及び脊髄の全体にわたって測定した時点すべてにおいて検出され、レベルはこれらの組織では時間を超えて同等だった。末梢臓器、特に肝臓にて有意なベクターの分布もあり、末梢組織におけるベクターゲノムのレベルは時間を超えて同等だった。溶媒対照にも14日で安楽死させた試験ベクター動物にも臨床的な、肉眼でのまたは組織学的な知見はなかった。軽い一時的なCSFでの単核細胞増加症が5/6のAAV9.hIDUA処理動物で観察され、ピークは投与後30日前後だった。
AAV9.hIDUA試験ベクター処理動物で検出され、hIDUAペプチドに対する末梢T細胞の応答は4/6の試験ベクターで処理した90日の動物及び1/3の処理した180日の動物にて観察された。顕微鏡上では、6/6のAAV9.hIDUA試験ベクター処理動物にて、後根神経節(組織学的評価には利用できないDRG)の感覚ニューロン内での細胞体損傷を示唆する脊髄の背面感覚白質路における最小限から中程度の軸索変性症があった。上行背面感覚路における軸索変性症の解剖学的位置は、後根神経節からの感覚ニューロンの特異的な関与を示唆している。それらのニューロンはAAVの髄内投与ののち普通相当に形質導入されるという事実及びCSF抗体(21日からの)とCSFの髄液細胞増加(30日でピーク)の経時変化、及び90日での動物の大半における導入遺伝子特異的なT細胞応答の存在は、hIDUAに対する細胞介在性の細胞傷害性免疫応答が後根神経節で生じたことを示唆している。
この探索的GLP研究の目的は、1×1012GC合計(1.1×1010GC/g脳質量)及び1×1013GC合計(1.1×1011GC/g脳質量)の2用量レベルでのIC投与AAV9.hIDUA試験ベクターの安全性を評価し、高用量でのIC投与R AAV9.hIDUA試験ベクターの安全性に対する免疫抑制療法の効果を評価することであった。免疫抑制レジメンは、シロリムス(ラパマイシン)及びミコフェノール酸モフェチル(MMF)を、AAV9.hIDUA試験ベクター投与の少なくとも2週間前から開始し、60日目(MMF)及び90日目(シロリムス)まで、シロリムスについては、血漿トラフレベルを可能な限り10~15μg/Lに近く、ミコフェノール酸(MMFの活性代謝産物)については、2~3.5μg/mLに維持する用量で継続して投与することからなっていた。
損傷したDRGニューロンに属する軸索の変性(ダイバック現象)によって、最小から軽度の背柱軸索障害を導くと結論付けられた。
これらのデータは、DRGニューロンの免疫介在性破壊が軸索障害を引き起こし得ることを示す。hIDUAを発現するDRGニューロン及びニューロン死の周りに、ニューロン周囲炎症性浸潤が観察された。DRG由来の上行軸索を含む背側索で軽度から中等度の軸索障害が観察された。異常な所見を有する動物は、すべて、導入遺伝子産物に対する体液性応答及びT細胞応答の両方を有する。動物は、研究を通して臨床的に正常であった。使用した免疫抑制レジメン(MMF+シロリムス)は、導入遺伝子に対する免疫応答を減弱したが、一貫して防ぐことはなかった。軸索障害と抗AAV9応答との間に相関は見られなかった。このことから、AAV9.hIDUAを用いた最初の研究では、ニューロン細胞に対する免疫介在性損傷のリスクを最小限に抑えるために免疫抑制が必要であると結論付けられた。結論として、前臨床試験は、MPS I(AAV9.hIDUA)における神経認知症状に対処するためのIT AAV9ベースの遺伝子治療の開発を支持する。前臨床試験の結果は、免疫介在性毒性のリスクを最小限に抑えるために、AAV9.hIDUAによる治療とともに免疫抑制を含めることを必要とする。
rAAV9.CB7.hIDUAは、(i)hIDUAベクターゲノムプラスミドと、(ii)AAVのrep2とcap9の野生型遺伝子を含有するpAAV29と呼ばれるAAVヘルパープラスミドと、(iii)pAdΔF6(Kan)と呼ばれるヘルパーアデノウイルスプラスミドとのヒトHEK293MCB細胞への三重形質移入によって作製する。パッケージされたベクターゲノムのサイズは4344ntである。
AAV2/9ヘルパープラスミドpAAV29KanRRepは4つの野生型AAV2repタンパク質とAAV9に由来する3つの野生型AAV VPカプシドタンパク質をコードする。キメラパッケージ構築物を作り出すために、先ず、野生型AAV2のrep及びcap遺伝子を含有するプラスミドp5E18からAAV2のcap遺伝子を取り出し、肝臓DNAから増幅したAAV9のcap遺伝子のPCR断片で置き換えた。得られたプラスミドは識別子pAAV2-9(p0008)を与えられた。正常ではrepの発現を推進するAAVのp5プロモータがこの構築物ではrepの5’末端からcapの3’末端に動かされることに留意のこと。この配置は、プロモータとrep遺伝子(すなわち、プラスミドの主鎖)の間にスペーサーを導入し、repの発現を下方調節し、ベクターの作製を支援する能力を高めるのに役立つ。p5E18におけるプラスミドの主鎖はpBluescriptKSに由来する。AAV2/9ヘルパープラスミドpAAV29KanRRep2は4つの野生型AAV2repタンパク質と3つの野生型AAV VPカプシドタンパク質とカナマイシン耐性とをコードする。
1010個まで増やすであろう。ガンマ線照射したUSが供給源の10%ウシ胎児血清(FBS)を補完したダルベッコ改変イーグル培地(DMEM)で構成される培地にて細胞が培養されるであろう。細胞は足場依存性であり、細胞の解離は動物産物を含まない解離試薬であるTrypLE Selectを用いて達成されるであろう。細胞の播種は無菌で使い捨てのバイオプロセスバッグ及び配管セットを用いて達成されるであろう。細胞は、37℃(±2℃)で5%(±0.5%)CO2の雰囲気にて維持されるであろう。細胞培
養培地は新鮮な無血清のDMEM培地で置き換えられ、最適化されたPEIに基づく形質導入法を用いて3種の作製プラスミドで形質移入されるであろう。作製過程で使用されるプラスミドはすべてCMO品質システム並びにcGMP製造の最も際立った特徴;追跡可能性、文書管理及び材料分離を利用する基礎構造という背景において作製されるであろう。
。
的に捕捉するCapture SelectTM Poros-AAV2/9アフィニティ樹脂(Life Technologies)に適用されるであろう。これらのイオン条件下で、有意な比率の残留する細胞性のDNA及びタンパク質がカラムを通って流れる一方で、AAV粒子は効率的に捕捉される。適用に続いて、カラムを洗浄して追加の供給不純物を取り除き、その後に10分の1の容量の中和緩衝液(Bis Tris Propane,200mM,pH10.2)への回収によって即座に中和される低pH工程の溶出(400mMのNaCl、20mMのクエン酸ナトリウム、pH2.5)が続く。
血清型の同一性、中空粒子の含量及び導入遺伝子産物の同一性を含む特徴付けアッセイが行われる。アッセイの説明は以下に現れる。
ウイルスベクターのゲノムDNAを単離し、プライマーウォーキングを用いた2倍配列包括度によって配列が決定されるであろう。配列比較が行われ、予想配列と比較されるであろう。
ベクターのAAV2/9血清型の確認は、質量分光分析(MS)によるVP3カプシドタンパク質のペプチドの解析に基づいたアッセイによって達成される。方法には、SDS-PAGEゲルから切り出したVP3タンパク質のバンドの多重酵素消化(トリプシン、キモトリプシン、及びエンドプロテイナーゼGlu-C)、とその後のカプシドタンパク質の配列決定を行うためのQ-Exactive Orbitrap質量分光計におけるUPLC-MS/MSでの性状分析が関与する。宿主タンパク質生成物の差し引き及び質量スペクトルから導き出したカプシドタンパク質の配列を可能にする直列質量スペクトル(MS)法が開発された。
oqPCRに基づいたゲノムコピー力価が連続希釈の範囲にわたって決定され、同族のプラスミド標準(pAAV.CB7.CI.hIDUAco.RBG.KanR)と比較されるであろう。oqPCRはDNA分解酵素I及びプロテイナーゼKによる逐次消化とそれに続くqPCR解析を利用して、カプシドに包まれたベクターゲノムのコピーを測定する。DNAの検出は、RBGポリA領域とハイブリッド形成する蛍光でタグを付けたプローブと組み合わせたこの同じ領域を標的とする配列特異的なプライマーを用いて達成されるであろう。プラスミドDNAの標準曲線との比較はPCR後の試料の操作を必要とすることなく力価の決定を可能にする。多数の標準、検証試料及び対照(バックグランド及びDNAの混入のための)がアッセイに導入されている。このアッセイは現在制限されていないが、CMOによって制限されるであろう。アッセイは、感度、検出の限界、制限の範囲、及びアッセイ内やアッセイ間の精度を含むアッセイのパラメータを確立し、定義することによって制限されるであろう。内部AAV9参照ロットが確立され、適格性試験に使用されるであろう。我々の以前の経験は、ここに記載されている最適化されたqPCRによって得られる力価が前臨床データの生成で使用された我々の標準qPCRによって達成されたものよりも一般に2.5倍高いことを示唆していることに留意のこと。
薬剤製品の粒子総含量はSDS-PAGE解析によって決定されるであろう。イオジキサノール勾配で精製される参照ベクターの調製物は種々の方法(分析用超遠心、電子顕微鏡、及び260/280nmでの吸光度)によって解析され、調製物が>95%のゲノム含有(完全)粒子を含有することを立証する。この参照物質を既知のゲノムコピー数(従って延長上で考えると粒子数)に連続希釈し、類似の希釈系列の薬剤製品と共にSDS-PAGEゲルにて泳動する。参照物質及び薬剤製品VP3タンパク質のバンド双方のピーク領域の体積をデンシトメトリーによって測定し、参照物質の体積を粒子数に対してプロットする。薬剤物質の粒子総濃度はこの曲線からの外挿によって決定され、次いでゲノムコピー(GC)力価を差し引いて中空粒子の力価を得る。中空粒子の完全粒子に対する比は中空粒子力価に対するGC力価の比である。
感染力価(IU)を用いてRC32細胞(rep2を発現しているHeLa細胞)におけるベクターの生産的取り込み及び複製を判定する。以前公開されたものに類似する96穴終点形式が採用されている。手短には、rAAV9.CB.hIDUAの連続希釈及び各希釈でrAAVの12の複製を伴う単一希釈のAd5によってRC32細胞を同時に感染させる。感染の72時間後、細胞を溶解し、qPCRを行ってrAAVベクターの入力
に比べた増幅を検出する。TCID50算出の終点希釈(Spearman-Karber)を行ってIU/mlとして表される複製力価を決定する。「感染力」の値は細胞と接触する粒子、受容体結合、内部移行、核への輸送及びゲノム複製に左右されるので、それらは、アッセイの構造、及び使用される細胞株における適当な受容体及び結合後の経路の存在によって影響を受ける。受容体及び結合後の経路は普通、不死化された細胞株では維持されないので、感染力アッセイの力価は存在する「感染性」粒子の数の絶対測定値ではない。しかしながら、カプシドに包まれたGCの「感染性単位」に対する比(GC/IU比として記載される)はロットからロットの間での製品一貫性の測定値として使用することができる。
GC/IU比は製品一貫性の測定値である。oqPCRの力価(GC/ml)を「感染性単位」(IU/ml)で割って算出されたGC/IU比を得る。
作製過程で生じる可能性があり得る複製能力を持つAAV2/9(rcAAV)の存在について試料が解析されるであろう。細胞に基づく増幅及び継代とそれに続くリアルタイムqPCRによるrcAAVのDNAの検出(cap9標的)から成る3継代アッセイが開発されている。細胞に基づく成分は、試験試料及び野生型ヒトアデノウイルス5型(Ad5)の希釈物を伴うHEK293細胞の植菌単層(P1)から成る。1010GCのベクター生成物が調べた生成物の最大量であろう。アデノウイルスの存在のゆえに、複製能力のあるAAVは細胞培養にて複製するであろう。2日後、細胞溶解物を生成し、Ad5を熱不活化する。清澄化した溶解物を次いで2回目の細胞(P2)に入れ、(再びAd5の存在下で)感度を高める。2日後、細胞溶解物を生成し、Ad5を熱不活化する。清澄化した溶解物を次いで3回目の細胞(P3)に入れ、(再びAd5の存在下で)感度を最大化する。2日後、細胞を溶解し、DNAを遊離させ、次いでそれをqPCRに供し、AAV9 cap配列を検出する。Ad5依存性の様子でのAAV9 cap配列の増幅はrcAAVの存在を示す。AAV2rep遺伝子とAAV9cap遺伝子とを含有するAAV2/9代理陽性対照の使用は、アッセイの検出限界(LOD)が決定される(0.1、1、10及び100IU)のを可能にし、rAAV9.CB7.hIDUAベクターの連続希釈(1×1010、1×109、1×108、1×107GC)を用いて試験試料に存在
するrcAAVのおよそのレベルを定量することができる。
qPCRのGC力価を遺伝子発現に関連付けるために、既知の感染効率の細胞当たりのGCによってHuh7またはHEK293細胞に形質導入し、形質導入の72時間後IDUA活性について上清をアッセイすることによって試験管内のバイオアッセイが行われるであろう。IDUA活性は、0.1mlの水で希釈した試料を100ミリモル/Lの4MU-イズロニド0.1mlと共に37度で1~3時間インキュベートすることによって測定される。290ミリモル/Lのグリシン2ml、180ミリモル/Lのクエン酸ナトリウムpH10.9の添加によって反応を止め、4MUの標準希釈に対する蛍光を比較することによって遊離した4MUを定量する。高度に活性がある前臨床及びtoxのベクター調製物は製品活性の解釈を可能にするであろう。
ビシンコニン酸アッセイを用いたウシ血清アルブミン(BSA)の標準曲線に対する総タンパク質についてベクター試料を先ず定量する。キットで提供されているMicro-BCA試薬と等量の試料を混合することによって測定は行われる。同じ手順がBSA標準の希釈に対して適用される。混合物を60℃でインキュベートし、吸光度を562nmで測定する。4パラメータ適合を用いて既知の濃度の標準吸光度から標準曲線を生成する。4パラメータ回帰に従って未知の試料が定量される。
25、50及び100ngのタンパク質の同時に電気泳動したBSA標準と比較することによって不純物のバンドをデンシトメトリーにより定量する。これらの量はAAVの総タンパク質試料の1%、2%及び4%を表す。3つのAAV特異的なタンパク質VP1、VP2及びVP3の添加で出現する染色されたバンドはタンパク質の不純物と見なされる。不純物のバンドはすべて参照タンパク質と比較し、不純物の質量パーセントと同様におよその分子量が報告される。SDS-PAGEゲルを用いてVP1、VP2及びVP3タンパク質を定量し、その比も決定するであろう。
成熟カニクイザルに1×1012GC/kgのAAV9.CMV.hIDUAを後頭下で注入し、636日後、組織を回収し、即座に-80℃に凍結する。QIAamp DNA
Mini Kit(Qiagen,Valencia,CA,USA)を用いて細胞性の全DNAを組織から抽出する。抽出したDNAにおけるベクターゲノムの検出及び定量は、SV40ポリA内の配列を標的とするプライマー及びプローブのセットを用いたリアルタイムPCR(TaqMan Universal Master Mix, Applied Biosystems,Foster City,CA,USA)によって実施する。PCR条件は、それぞれ鋳型としての100ngの細胞性の全DNA、300nMのプライマー及び200nMのプローブで設定する。サイクルは、95.8℃で10分間、95.8℃で15秒間と60.8℃で1分とを40サイクルだった。
本研究では、MPS Iイヌに由来するCSF試料の代謝産物のプロファイリングを行ったが、それはCSFのメタボロームにおける実質的な疾患関連の変化を明らかにした。最も顕著な差異は正常対照に比較したスペルミンのレベルでの30倍の上昇だった。この知見はMPS I患者の試料と同様にMPS Iのネコモデルで確認された。スペルミンはHSに結合し、スペルミンの細胞への取り込みはこの相互作用に依存する[M.Belting,S.Persson,L.-Å.Fransson,Proteoglycan involvement in polyamine uptake.Biochemical Journal,338,317-323(1999);J.E.Welch,P.Bengtson,K.Svensson,A.Wittrup,G.J.Je
nniskens,G.B.Ten Dam,T.H.Van Kuppevelt,M. Belting,Single chain fragment anti-heparan sulfate antibody targets the polyamine transport system and attenuates polyamine-dependent cell proliferation.International journal of oncology,32,749-756(2008);published online EpubApr]。グリピカン-1のような細胞表面のプロテオグリカンはそのHS部分を介してスペルミンを結合することができ、グリピカンタンパク質のエンドサイトーシスの後、HS鎖の細胞内切断は結合したスペルミンを細胞内で遊離させる(K.Ding,S.et al,The Journal of biological chemistry,276,46779-46791,(2001);published online EpubDec,14)。従って、インタクトなHSの再生利用はスペルミンの取り込みに必須である。MPS Iでは、細胞外のスペルミンの蓄積は、不十分なHSの再生利用のゆえのこの取り込みメカニズムの阻害を介して、またはMPSで蓄積する細胞外GAGへのスペルミンの単純な結合を介して生じ、スペルミン結合の平衡をシフトさせて細胞外分布をより好む。さらなる研究はMPS IのCSFにおけるスペルミン蓄積に対するこれらのメカニズムの相対的な寄与に対処すべきである。
emergence of neuronal connectivity.Current opinion in neurobiology,16,40-51(2006);published online EpubFeb(10.1016/j.conb.2006.01.011)]。従って、スペルミンの蓄積はMPS Iにおける異常な神経突起成長を促進する幾つかの因子の1つであってもよい。
てもよく、それはこの疾患に関連する認知不全を説明してもよい。これらの知見はまた、CSFのスペルミンがMPS Iのための新規のCNS指向型の治療の薬物力学を評価するための非侵襲性の生体マーカーとして有用であってもよいことも示している。
実験設計:この研究は当初、健常対照に由来する試料に比べてMPS I患者のCSF試料にて有意に異なるレベルで存在する代謝産物を検出するように設計された。MPS IHの小児及び健常対照に由来するCSF試料の限定された利用可能性のせいで、その後ヒト試料にて候補生体マーカーを評価するつもりで、当初の評価は多数が利用できるMPS Iイヌに由来するCSF試料を用いて実施した。個々の未処理のMPS Iイヌに由来する合計15のCSF試料が分析に利用可能であり、追加の15試料は健常対照から得られた。前向き代謝産物評価におけるMPS IイヌのCSFにて上昇したスペルミンを特定した後、遺伝子治療によって処理されたMPS Iイヌ及びネコの以前の研究に由来するCSF試料と同様に患者の試料にてスペルミンを後向きに測定した。これらの分析のための各群に含まれる対象の数は試料の利用性によって限定され、統計的考慮に基づかなかったので、場合によっては数は統計的比較には不十分である。各状態について定量された細胞の数は、状態当たり>30細胞が細胞当たりの分枝長、神経突起数または神経突起分岐で20%の差異を検出するのに必要とされることを示した予備実験に基づいた。細胞をプレートに入れ、指定された薬剤で処理した後、ウェルをコード化し、細胞画像の取得及び神経突起長や分岐の手動での定量が盲検化したレビュアーによって実施された。異なる基材(チャンバースライド(SigmaS6815)ではなくポリ-L-リシン(Sigma)でコーティングされた組織培養プレート)を用いて野生型とMPSのマウスのニューロンの比較を繰り返し、類似の結果だった。双方の基材を用いて、スペルミン添加の有無で野生型ニューロンの比較を4回行い、類似の結果だった。CSF代謝産物のプロファイリング:CSF代謝産物のプロファイリングはMetabolonによって行った。
酸を含有する水とエタノールを用いて勾配溶出した。塩基性抽出物はメタノールと水を用いて、しかし、6.5mMの重炭酸アンモニウムによって同様に溶出した。第3のアリコートは、陰性イオン化とその後の10mMのギ酸アンモニウムを伴った水とアセトニトリルから成る勾配を用いたHILICカラム(Waters UPLC BEH Amide2.1×150mm,1.7μm)からの溶出を介して解析した。MS解析はMSと動的排除を用いたデータ依存性のMSn走査との間で交互に行った。走査範囲は方法間でやや変化したが、80~1000m/zを対象とした。
GC-MSによる解析に定められた試料は、ビストリメチル-シリルトリフルオロアセトアミドを用いて乾燥窒素のもとで誘導体化されるのに先立って、最低18時間真空下で乾燥させた。誘導体化した試料は、ヘリウムをキャリア気体として60℃~340℃の温度範囲で17.5分間で5%ジフェニル/95%ジメチルポリシロキサン溶融石英カラム(20m×0.18mm ID;0.18umの膜厚)にて分離した。電子衝撃イオン化(EI)を用い、単位質量分解能で操作されるThermo- Finnigan Trace DSQ高速走査シングル四重極質量分析計で試料を解析した。走査範囲は50~750m/zだった。
ose,CA)を用いて以下のパラメータ:4000Vでのスプレー電圧、270℃でのキャピラリー温度、35任意単位でのシース気体圧、2任意単位でのイオンスイープ気体圧、10任意単位での補助気体圧、200℃の気化器温度、50でのチューブレンズオフセット、35でのキャピラリーオフセット及び0でのスキマーオフセットによる陽イオンモードでMS/MSを実施した。0.002m/zの走査幅及び0.15秒の走査時間で以下の推移:203.1/112.1(スペルミン);211.1/120.1(スペルミン-d8)をモニターした。
EpubFeb(10.1016/j.conb.2006.01.011)。生ピークデータを対数変換し、正常試料の値の平均値に対して基準化した。他の統計的解析はすべてGraphPad Prism6で行った。培養したニューロンの分枝長、神経突起数、及び分岐をANOVAとその後のDunnettの検定によって比較した。CSFのスペルミン及び皮質のGAP43はKruskal-Wallisの検定とその後のDunnの検定によって比較した。
評価において検出できない値はデータセットで観察された最小値に帰属させた。生ピークデータを正常試料の値の平均値に対して基準化し、対数変換した。他の統計的解析はすべてGraphPad Prism6で行った。培養したニューロンの分枝長、神経突起数、及び分岐はANOVAとそれに続くDunnettの検定によって比較した。CSFのスペルミン及び皮質のGAP43はKruskal-Wallisの検定とその後のDunnの検定によって比較した。
1.代謝産物のプロファイリングを介した上昇したCSFスペルミンの特定
CSF代謝産物の当初の評価はMPS Iのイヌモデルを用いて行った。これらの動物はIDUA遺伝子にてスプライス部位に突然変異を持ち、酵素発現の完全な喪失及びMPS I患者のそれに類似する臨床的及び組織学的な特徴の発達を生じる(K.P.Menon,et al,Genomics,14,763-768,(1992);R.Shull,et al.,The American journal of pathology,114,487(1984))。CSF試料は15匹の正常イヌ及び15匹のMPS Iイヌから採取した。CSF試料はLC及びGC-MSによって代謝産物の相対的な量について評価した。質量分光計によってCSF試料にて合計281の代謝産物を陽性で特定することができた。これらのうち、47(17%)は対照に比べてMPS Iイヌで有意に上昇し、88(31%)は対照に比べて低下していた。群間で最も異なる50代謝産物のヒートマップを図17Aに示す。代謝産物のプロファイリングは、MPS Iイヌと正常イヌとの間でポリアミン、スフィンゴ脂質、アセチル化アミノ酸及びヌクレオチドの代謝において顕著な差異を特定した。ランダムフォレストクラスター化解析は、MPS Iイヌと正常イヌとの間における代謝産物の差異への最大の寄与因子としてポリアミンスペルミンを特定した(図21)。試料採取の時点で1ヵ月齢未満だったMPS Iイヌ1匹を除いて、MPS Iイヌでは平均でスペルミンは30倍を超えて上昇した。CSFにおけるスペルミンを定量的に測定するために安定同位元素希釈(SID)-LC-MS/MSアッセイが開発された。ハーラー症候群の6人の幼児(6~26ヵ月齢)及び2人の健常対照(36及び48ヵ月齢)に由来する試料を評価した。双方の健常対照はアッセイの定量限界(1ng/mL)を下回るCSFのスペルミンのレベルを有したのに対して、MPS I患者に由来するCSF試料は平均で定量限界を10倍上回った(図17B)。MPS IH患者におけるスペルミンの上昇は、スペルミンの結合と取り込みにおけるHSの既知の役割に矛盾しないと思われた[M.Belting,et al,Journal of Biological Chemistry,278,47181-47189(2003);M.Belting,et al,Proteoglycan
involvement in polyamine uptake.Biochemical Journal,338,317-323(1999);J.E.Welch,et al,International journal of oncology,32,749-756(2008))]。正常イヌ及びMPS Iイヌの脳試料はポリアミン合成経路における転写上調節される酵素について類似のmRNA発現レベルを有するので、上昇した合成は上昇したCSFスペルミンの原因ではありそうにないと思われた。
軸索の損傷に続いて、ニューロンはポリアミン合成を上方調節し、それは神経突起の伸長を促進する(D.Cai,et al,Neuron,35,711-719(2002);published online EpubAug,15;K.Deng,et
al,The Journal of neuroscience,:the official journal of the Society for Neuroscience,29,9545-9552(2009);published online EpubJul,29;Y.Gao,et al,Neuron,44,609-6
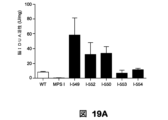
21(2004);published online EpubNov,18;R.C.Schreiber,et al.,Neuroscience,128,741-749(2004))。従って我々は、MPSのニューロンで記載されている異常な神経突起過剰成長の表現型におけるスペルミンの役割を評価した(Hocquemiller,S.,et al,Journal of neuroscience research,88,202-213(2010))。MPS Iマウスに由来するE18皮質ニューロンの培養はコロニーの野生型マウスに由来するニューロンよりも培養にて4日後、大きな神経突起数、分岐及び合計分枝長を示した(図19A~F)。スペルミン合成の阻害剤であるAPCHAによるMPSニューロンの処理は神経突起成長と分岐を有意に減らした。この効果はスペルミンを置き換えることによって反転できた(図18A~F)。同じ濃度のAPCHAは正常ニューロンの成長に影響を及ぼさなかった。生体内で特定されたものに類似する濃度で野生型ニューロンの培養にスペルミンを添加することは神経突起成長と分岐において有意な増加を生じた(図18A~F)。
生体内でのGAP43の発現及びスペルミンの蓄積に対するIDUA欠乏の効果を評価するために、我々は、未処理のMPS Iイヌと同様にCNS指向型の遺伝子治療で処理したものにてCSFのスペルミンのレベル及び脳のGAP43のレベルを測定した。我々は以前、イヌIDUA導入遺伝子を運ぶアデノ随伴ウイルス血清型9ベクターの髄内注入で処理した5匹のMPS Iイヌを記載した(C.Hinderer,et al,Molecular therapy:the journal of the American Society of Gene Therapy,23,1298-1307(2015);published online Epub Aug)。MPS Iイヌは正常なIDUA酵素に対する抗体を発生することができるので、イヌのうち2匹は新生仔として肝臓IDUA遺伝子導入で予備処理してそのタンパク質に対する免疫寛容を誘導した。寛容化されたイヌは双方とも、AAV9処理に続く正常を十分に上回る脳IDUA活性を示した。3匹の寛容化されなかったイヌは様々なレベルの発現を示し、1匹の動物は正常より大きいレベルに達し、他の2匹はほぼ正常の発現を示した(図19A~D)。CSFのスペルミン低下は脳のIDUA活性に反比例し、最低のIDUA発現の2匹のイヌでは未処理の動物に比べて3倍の低下を示し、最高の発現の動物では20倍を超える低下があった(図19A~D)。GAP43はMPS Iイヌの前頭皮質では上方調節され、発現はベクターで処理した動物すべてにおいて正常化された(図19A~19D)。
Iネコは高いCSFスペルミンを示すことを見いだした(図20A、20B)(C.Hinderer,et al,Molecular therapy:the jour
nal of the American Society of
Gene Therapy.22,2018-2027(2014);published online EpubDec(10.1038/mt.2014.135))。ネコIDUAを発現する高用量のAAV9の髄内投与はCSFスペルミンのレベルを正常化した(図20A)。
本研究で我々はMPS Iイヌに由来するCSF試料の代謝産物のプロファイリングを行い、それはCSFメタボロームにおける実質的な疾患関連の変化を明らかにした。最も顕著な差異は正常対照に比べたスペルミンのレベルでの30倍を超える上昇だった。この知見はMPS I患者と同様にMPS Iのネコモデルにて確認された。スペルミンは高親和性でHSに直接結合し、スペルミンの細胞取り込みはこの相互作用に左右される(M.Belting,S.PERSSON,L.-A.Fransson,Proteoglycan involvement in polyamine uptake. Biochemical Journal,338,317-323(1999);J.E.Welch,et al,International journal of oncology,32,749-756(2008))。グリピカン-1のような細胞表面のプロテオグリカンはそのHS部分を介してスペルミンを結合することができ、グリピカンタンパク質のエンドサイトーシスの後、HS鎖の細胞内切断は結合したスペルミンを細胞内で遊離させる(Belting,et al.上記で引用;K.Ding,S.et
al,The Journal of biological chemistry,276,46779-46791,(2001);published online EpubDec,14)。従って、インタクトなHSの再生利用はスペルミンの取り込みに必須である。IDUAの欠乏のゆえの不十分なHSの再生利用はこのスペルミンの取り込みメカニズムを阻害し、細胞外スペルミンの蓄積をもたらす。或いは、細胞外GAGがスペルミンを隔離し、平衡をシフトさせて細胞外分布に有利に働いてもよい。この研究におけるLC-MSの試料調製で採用されるメタノール脱タンパク質工程も可溶性HSを沈殿させるということは、CSFで検出されるスペルミンは結合していないので、GAGの結合ではなく取り込みの阻害が細胞外スペルミンの蓄積の原因であることを示唆している(N.Volpi,Journal of chromatography.B,Biomedical applications,685,27-34(1996);published online EpubOct,11)。神経ネットワークの形成及び維持は神経突起成長及びシナプス形成の正確な制御を必要とする。発生の間、CNSの環境は神経突起の形成に対してだんだん阻害性になっていき、ミエリン関連タンパク質が成人の脳では神経突起成長を大きく遮断している。神経突起成長の低下に向かうこの発生上のシフトはGAP43の発現と平行する(S.M.De la Monte,et al,Developmental Brain Research,46,161-168(1989);published online Epub4/1/)。MPSのニューロンが示す持続するGAP43の発現及び誇張された神経突起の伸長が阻害と成長の促進シグナルのこの正常な均衡を妨げ、その結果、異常な結合性及び損傷された認知を生じてもよい(Hocquemiller,et al,上記で引用)。HSの蓄積が神経突起成長の増加にどのようにつながるのかは解明されていない。多数の研究が神経突起の伸長にポリアミンを関与させ;軸索の損傷に続いて、スペルミン及びその前駆体であるプトレシン及びスペルミジンの合成についての律速酵素が上昇し、ミエリンからの阻害性シグナルが存在しても神経突起の伸長の増強を可能にする(Cia(2002),Deng(2009),Gao(2004)すべて上記で引用)。さらに、プトレシンによるニューロンの処理はCSFに直接注入されると神経突起成長を誘導し、効果はスペルミン合成の阻害剤によって阻止される(Deng(2009);上記で引用)。ポリアミンが神経突起成長に対して効果を発揮するメカニズムは知られていない。可能性のある標的の1つは、NMDA受容体であり、その活性化はスペルミンの結合によって強化される。(J.Le
rma,Neuron,8,343-352(1992);published online Epub2//(dx.doi.org/10.1016/0896-6273(92)90300-3))。NMDAのシグナル伝達は神経突起の伸長を誘導し、受容体のスペルミン感受性のサブユニットは発生の間、高度に発現される(D.Georgiev,et al,Experimental cell research,314,2603-2617(2008);published online EpubAug,15(10.1016/j.yexcr.2008.06.009);R.G.Kalb,Regulation of motor neuron dendrite growth by NMDA receptor activation. Development,120,3063-3071(1994);J.Zhong,et al,Journal of neurochemistry,64,531-539(1995))。とりわけ、多数の神経栄養因子はHSが修飾した受容体を介して結合し、細胞外マトリクスにおけるHSとの相互作用は神経突起成長に影響を及ぼすことができる(D.Van Vactor,et al,Current opinion in neurobiology,16,40-51(2006);published online
EpubFeb(10.1016/j.conb.2006.01.011))。従って、スペルミンの蓄積はMPS Iにおける異常な神経突起成長を促進する幾つかの因子の1つであってもよい。CSF試料が評価された15匹のMPS Iイヌのうち、1匹だけがスペルミン濃度の正常範囲内に入った。28日齢で、これは研究に含まれた最も幼若な動物だった。この研究はそれがハーラー症候群の乳児で6ヵ月齢までにすでに上昇することを実証しているが、この知見はスペルミンの蓄積が年齢依存性であってもよいことを示している。将来の研究はMPS患者にてCSFスペルミンのレベルを長期にわたって評価すべきである。ほとんどの患者は発達遅滞の発症に先立って1~2年の正常な発達を経験するので、もし、スペルミンがMPS患者の年齢と共に増加するのであれば、これは認知低下の動態を説明し得る。神経突起成長を変化させる代謝産物の蓄積を誘発する損傷されたHS代謝の可能性は、MPSにおける酵素の欠乏と異常な神経突起成長の表現型との間での新規の関係性を指し示し、それはこれらの疾患に関連する認知不全を説明してもよい。将来の研究は他のMPSにおけるスペルミンの上昇を確認すべきである。これらの知見はまた、CSFのスペルミンが、MPSのための新規のCNS指向型の治療法の薬物動態を評価するための非侵襲性の生体マーカーとして有用であることも示している。CNS指向型の治療法についての将来の試験は認知評価項目とCSFスペルミンの変化との間の相関を評価すべきである。
A.前処置スクリーニングの評価
1.プロトコール来診1:スクリーニング
治験責任医師は、対象(または指定された介護者)がインフォームドコンセントにサインする際、完全に情報が与えられるために嚢内(IC)処置、投与処置自体及び可能性のある安全性リスクすべてにつながるスクリーニング過程を記載するであろう。
適格性をよく調べる適当な時間を与えるために、最初のスクリーニング来訪と試験来訪2(0日目)前の1週間までの間の時間で以下の手順が行われるべきである。
・ガドリニウムの有無での頭部/頸部の磁気共鳴画像診断(MRI)[注:対照はガドリニウムを受け取る好適な候補者でなければならない(すなわち、eGFR>30mL/分/1.73m2)]
・頭部/頸部のMRIに加えて、治験医師は屈曲/伸長試験を介した頸部のさらなる評価の必要性を判定するであろう
・MRIプロトコールにはT1、T2、DTI、FLAIR及びCINEのプロトコール画像が含まれるであろう
・CSFの流れの適切な評価及びCSF空間の間での連絡の考えられる遮断または喪失の特定を可能にする頭部/頸部のMRA/MRV(注:硬膜内/経硬膜手術の既往を持つ対象は除外されてもよく、またはさらなる検査(たとえば、放射線ヌクレオチド大槽造影法)を必要としてもよい)
・神経放射線科医/神経外科医の対象処置評価会議:3施設からの代表者が電話会議(またはウェブ会議)を有して利用できる情報(走査、既往歴、身体検査、臨床検査等)に基づいてIC処置について各対象の適格性を議論するであろう。あらゆる試みを行って対象を損なうIC処置または評価に向かう手続きの際の合意を達成すべきである(すなわち、各メンバーは行われた決断を受け入れる準備万端であるべきである)
・麻酔術前評価、MPS患者の特定の生理的必要性に留意しながら、気道、頸部(短縮した/肥厚した)及び頭部の可動域(頸部屈曲の程度)の詳細な評価を伴った-28日目~1日目
IC処置に先立って、CT室は以下の設備及び薬物が存在することを確認するであろう:
・成人腰椎穿刺キット(施設ごとに供給される)
・BD(Becton Dickinson)22または25ゲージ×3~7”のクモ膜下穿刺針(Quincke先端部)
・インターベンション医師の裁量で使用される(クモ膜下穿刺針の導入のための)同軸導入針(たとえば、18G×3.5”)
・旋回(回転)オスルアーロック付きの四方小口径活栓
・メスルアーロックアダプター付きのTコネクタ延長セット(配管)、およそ6.7”の長さ
・オムニパック180(イオヘキソール)、クモ膜下腔内投与用
・静脈内(IV)投与用のヨウ素化造影剤
・注入用の1%リドカイン溶液(成人LPキットで供給されなければ)
・予め充填された10cc生理食塩水(無菌)の水洗注射器
・X線不透過性マーカー(複数可)
・外科用準備装備/髭剃り刃
・挿管された対象の正しい位置決めを可能にする枕/支持体
・気管内挿管の装置、全身麻酔用の機械、及び人工呼吸器
・手術中の神経生理学的なモニタリング(IONM)装置(及び必要な人材)
・別々の薬局マニュアルに従って調製され、CT/手術室(OR)の部屋に運ばれるAAV9.hIDUAを含有する10ccの注射器
・試験及び手順についてのインフォームドコンセントが確認され、カルテ及び/または試験ファイルの中で文書化されるであろう。放射線科及び麻酔科のスタッフからの手順に関する別々の合意が施設内要件によって得られるであろう。
・試験対象は施設内指針に従って適当な病院内看護ユニットにて取り付けられる静脈内アクセスを有するであろう(たとえば、2つのIVアクセス部位)。静脈内流体は麻酔科医の裁量で投与されるであろう。
・麻酔科医の裁量で及び施設内指針ごとに、試験対象は、適当な患者看護ユニット、保持区域または外科/CTの処置室に誘導され、そこで全身麻酔の投与と共に気管内挿管を受けるであろう。
・腰椎穿刺を行い、先ず5ccの脳脊髄液(CSF)を取り出し、その後髄内に造影剤(オムニパック180)を注入して大槽の視覚化を助けるであろう。患者の適当な位置決め操作を行って造影剤の大槽内への拡散を促す。
・すでにそのように行われていないのであれば、手術中神経生理学的モニタリング(IONM)装置を対象に取り付けるであろう。
・対象は腹臥位または側臥位でCTスキャナー台に載せられるであろう。
・適当と見なされれば、対象は、術前評価の間安全であると判定される程度に頸部屈曲を提供し、且つ位置決めの後文書化される正常な神経生理学的なモニターシグナルを提供する方法で位置決めされるであろう。
・以下の試験スタッフ及び治験医師(複数可)が存在することを確認し、施設内で特定されるであろう。
〇処置を行うインターベンション医師/神経外科医
〇麻酔科医及び呼吸器技師
〇看護師及び医師助手
〇CT(またはOR)技師
〇神経生理学技師
〇現場研究コーディネーター
・頭蓋底の下の患者の皮膚は適宜剃られるであろう。
・CTスカウト画像化を行い、その後、必要とみなされればインターベンション医師よる処置前計画のIV造影剤でのCTを行い標的の位置を突き止め、脈管構造を画像化するであろう。
・いったん標的部位(大槽)が特定され、針の軌道が計画されると、皮膚が用意され、施設内指針のとおりに無菌技法を用いて手術用覆布で覆われるであろう。
・インターベンション医師によって指示されたようにX線不透過性マーカーが標的皮膚の位置に置かれるであろう。
・マーカーの下の皮膚は1%リドカインの浸潤を介して麻酔されるであろう。
・同軸導入針を使用する選択肢と共に、22Gまたは25Gのクモ膜下穿刺針が大槽に向かって進められるであろう。
・針を進めた後、施設内設備を用いて実現可能な最薄のCTスライス厚さ(理想的には≦2.5mm)を用いてCT画像が得られるであろう。連続CT画像は、針及び関連する軟組織(たとえば、傍脊柱筋群、骨、脳幹及び脊髄)の適切な視覚化を可能にする可能な最低放射線量を使用すべきである。
・正しい針の配置は、針ハブにおけるCSFの観察及び大槽内での針の視覚化によって確認されるであろう。
・インターベンション医師は、ベクターを含有する注射器が滅菌野に近いが、その外側に置かれることを確認するであろう。ベクターを取り扱う、または投与することに先立って、施設は、滅菌野内での処置を支援するスタッフによって手袋、マスク及び眼の保護が行われることを確認するであろう(滅菌野の外側の他のスタッフはこれらの手順を取る必要はない)。
・短い(約6”)の延長配管を挿入されたクモ膜下穿刺針に取り付け、それを次いで四方活栓に取り付けるであろう。この装置が対象のCSFでいったん自給されると、10ccの予め充填された生理食塩水の水洗注射器が四方活栓に取り付けられるであろう。
・ベクターを含有する注射器がインターベンション医師に手渡され、四方活栓のポートに取り付けられるであろう。
・ベクターを含有する注射器に対する活栓のポートがいったん開放されると、注入の間に過剰な力がプランジャーにかからないように注意を払いながら、注射器の内容物はゆっくり(およそ1~2分間かけて)注入されるべきである。
・AAV9.hIDUA試験ベクターを含有する注射器の内容物がいったん注入されると、取り付けられた予め充填された注射器を用いて活栓と針の構築が1~2ccの生理食塩水で洗い流され得るように活栓が回されるであろう。
・準備ができると、インターベンション医師は彼/彼女が対象から装置を取り外すことをスタッフに注意喚起する。
・1回の動きで、針、延長配管、活栓及び注射器が対象からゆっくり取り外され、バイオハザード廃棄物容器または硬質容器(針用)の中に廃棄するための外科用トレイに置く。・針の挿入部位は出血またはCSFの漏出の兆候について調べ、治験医師によって指示されたように処理されるであろう。指示されたように、ガーゼ、外科用テープ及び/またはTegaderm包帯を用いて部位が手当てされるであろう。
・対象はCTスキャナーを出て、仰臥位でストレッチャーに乗るであろう。
・麻酔が中断され、麻酔後の看護についての以下の施設内指針について対象が看護されるであろう。神経生理モニターはこの研究対象から取り除かれる。
・回復の間、対象が横たわるストレッチャーの頭部をやや高くすべきである(約30度)。
・対象は、施設内指針のとおりに好適な麻酔後看護ユニットに移されるであろう。
・対象が適正に意識を回復し、安定な状態になった後、彼/彼女はプロトコールが命じる評価のために適当なフロア/ユニットに収容されるであろう。神経学的な評価がプロトコールのとおりに続き、治験責任医師は病院スタッフ及び研究スタッフと共同で対象の看護を監督する。
この研究の目的は、脳室内(ICV)注入及び腰椎穿刺を介した注入を含む、CSFへの投与のさらに日常的な方法を評価することであった。手短には、この研究では、ICVとICのAAV投与をイヌで比較した。ベクターの投与を非ヒト霊長類にて腰椎穿刺を介して評価し、一部の動物はベクターの頭蓋分布を改善することが示唆されている手順である、注入後のトレンデレンブルグ体位に置いた。イヌの研究では、ICV及びICのベクター投与は脳及び脊髄の全体を通して類似する効率的な形質導入を生じた。しかしながら、ICVコホートの動物は、明らかに導入遺伝子産物に対する重度のT細胞応答のせいで脳炎を発症した。ICVコホートのみでのこの導入遺伝子に特異的な免疫応答の発生は導入遺伝子発現の部位での注入手順に由来する局在化した炎症の存在に関連することが疑われる。NHPの研究では、腰椎槽へのベクター投与に続く形質導入効率は、極度に大きな注入容量(CSF総容量のおよそ40%)を用いることによって我々の以前の研究に比べて改善した。しかしながら、このアプローチはIC投与よりも依然として効率が悪い。注入の後トレンデレンブルグ体位に動物を置くことは追加の利益を提供しなかった。しかしながら、大きな注入容量はベクターの頭蓋分布を改善できることが見いだされた。
る有効な分布を達成することを見いだした。我々はまたNHPにおける腰椎穿刺によるベクター送達、及び注入後トレンデレンブルグ体位に動物を置くことの効果も評価した。我々は大きな注入容量がベクターの頭蓋分布を改善できることを見いだしたが、注入後の位置決めの明瞭な効果はなかった。
1.ベクターの作製:GFPベクターは、サイトメガロウイルスの前初期エンハンサを伴ったニワトリβアクチンプロモータと、人工イントロンと、増強緑色蛍光タンパク質cDNAと、ウッドチャック肝炎ウイルス転写後調節因子と、ウサギβグロビンポリアデニル化配列とを含む発現カセットを運ぶAAV血清型9のカプシドから成った。GUSBベクターは、サイトメガロウイルスの前初期エンハンサを伴ったニワトリβアクチンプロモータと、人工イントロンと、イヌGUSBのcDNAと、ウサギβグロビンポリアデニル化配列とを含む発現カセットを運ぶAAV血清型9のカプシドから成った。ベクターはHEK293細胞の三重形質移入によって作製し、以前記載された[Lock,et al,Human gene therapy.Oct,2010;21(10):1259-1271]ようにイオジキサノール勾配で精製した。
イヌはすべて、研究における動物の飼育と使用に関する国立衛生研究所とUSDAの指針のもとでペンシルベニア大学獣医学部のヒト遺伝性疾患の動物モデルのための国立委託センターで育てられた(NIH OD P40-010939)。
この研究には9歳~12歳の間の6匹のカニクイザルが含まれた。動物は1回につき4~8kgの間で注入された。注入に先立ってベクター(2×1013GC)を5mLのオムニパック(イオヘキソール)180造影剤で希釈した。腰椎穿刺を介したベクターの注入は以前記載された[Hinderer,Molecular Therapy-Methods & Clinical Development.12/10/online,2014;1]ように行った。髄内空間への正しい注入は蛍光透視法によって検証した。トレンデレンブルグ群の動物については、ベッドの頭部を注入の直後10分間30度下げた。安楽死及び組織採取は以前記載された[Hinderer,Molecular Therapy-Methods & Clinical Development.12/10/online,2014;1]ように行った。
この研究には1歳のMPS Iイヌ6匹が含まれた。ICV処理したイヌすべてにおいてベースラインMRIを行い、注入の組み合わせを計画した。嚢内注入は以前記載された[Hinderer,et al,Molecular therapy:the journal of the American Society of Gene Therapy.Aug,2015;23(8):1298-1307]ように行った。ICVの注入については、静脈内プロポフォールでイヌを麻酔し、気管内挿管し、イソフルランで麻酔下を維持し、定位固定枠に入れた。皮膚を無菌で準備し、注入部位の上で切開した。注入部位で単一の穿頭孔を開け、それを介して26ゲージの針を所定の深さに進めた。CSFの戻りで配置を確認した。ベクター(1mL中で1.8×1013GC)をゆっくり1~2分かけて注入した。安楽死及び組織採取は以前記載された[Hinderer,et al,Molecular therapy:the journal of the American Society of Gene Therapy.Aug,2015;23(8):1298-1307]ように行った。
GPFの発現の評価について記載されたように脳を処理した[Hinderer,Molecular Therapy-Methods & Clinical Development.12/10/online,2014;1]。GUSB酵素の染色及びGM3の染色は以前記載された[Gurda,et al,Molecular therapy:the journal of the American Society of Gene Therapy.Oct,8,2015.]ように行った。
剖検のとき、ベクターで処理したイヌからヘパリン処理した試験管に血液を採取した。Ficoll勾配遠心分離によって末梢血単核細胞を単離した。AAV9カプシドペプチド及びGFPペプチドに対するT細胞応答はインターフェロンガンマのELISPOTによって評価した。AAV9及びGFPのペプチドライブラリは10アミノ酸が重複した15量体として合成した(Mimotopes)。AAV9ペプチドライブラリは3つのプール:ペプチド1~50のプールA、ペプチド51~100のプールB及びペプチド101~146のプールCにグループ分けした。GFPペプチドライブラリも3つのプールにグループ分けした。ホルボール12-ミリステート13-アセテートに加えたイオノマイシン塩(PMA+ION)を陽性対照として使用した。DMSOを陰性対照として使用した。細胞をペプチドで刺激し、記載されたようにインターフェロンガンマの分泌を検出した。応答が100万個のリンパ球当たり双方とも55スポット形成単位(SFU)を超え、且つDMSO陰性対照の少なくとも3倍であった場合、応答を陽性と見なした。
剖検のとき、生体分布についての組織をドライアイスで即座に凍結した。DNAの単離及びTaqManPCRによるベクターゲノムの定量は記載された[Wang,et al,Human gene therapy.Nov,011;22(11):1389-1401]ように行った。
GUSB活性は記載された[Gurda,et al,Molecular therapy:the journal of the American Society of Gene Therapy.Oct,8,2015]ようにCSFにて測定した。
1.イヌにおける脳室内及び嚢内のベクター送達の比較
リソソーム蓄積症であるムコ多糖症I型(MPS I)のイヌモデルを用いた我々の以前の研究は、大槽へのAAV9の注入は脳及び脊髄全体を効果的に標的とすることができることを実証した[Hinderer,et al,Molecular therapy:the journal of the American Society of
Gene Therapy.Aug,2015;23(8):1298-1307]。この研究では、我々は、成熟MPS Iイヌの大槽または側脳室に投与されたGFPレポーター遺伝子を発現するAAV9ベクターの分布を比較した。ベクター(1.8×1013ゲノムコピー)の大槽への1mLの単回注入によって3匹のイヌを処理した。追加の3匹のイヌは側脳室への同じベクターの単回ベクター注入を受けた。ICV注入によって処理したイヌについてはベースラインMRIを行って注入のためのさらに大きな側脳室を選択し、目標座標を定義する。定位固定枠を用いて注入を行い、指定された脳室を正確に標的とした。
た(図14)。定量的PCRによるベクターゲノムの測定は脳の採取した領域及び脊髄すべての全体を通してベクターの沈着を明らかにした(図15)。ベクターゲノムの分布と一致して、大脳皮質のほとんどの領域と同様に脊髄全体にわたって導入遺伝子の強力な発現が検出できた。脊髄の組織学はアルファ運動ニューロンの強い形質導入について顕著であり、形質導入の勾配は胸椎及び腰椎のセグメントをより好んだ。
我々は以前、NHPの大槽または腰椎槽へのAAV9の注入を比較し、腰椎経路は脊髄を標的とするのに10倍効率が低く、脳を標的とするのに100倍効率が低いことを見いだした[C.Hinderer,et al,Molecular Therapy-Methods & Clinical Development.12/10/online,2014;1]。その後、他の研究者が、腰椎穿刺によるAAV9の投与を用いたさらに良好な形質導入を実証し、ベクターの頭蓋分布の改善は注入後、動物をトレンデレンブルグ体位に置くことによって達成された[Myer,et al,Molecular therapy:the journal of the American Society of Gene Therapy.Oct,31,2014]。このアプローチでは、ベクターは過剰容量の造影剤に希釈され、溶液の密度を高め、トレンデレンブルグにある間、重力が推進する分布を促進する。L3-4間隙にてGFPを発現するAAV9(2×1013ゲノムコピー)の単回注入で6匹の成熟カニクイザルを処理した。ベクターは最終容量5mLのイオヘキソール180造影剤に希釈した。動物のうち4匹は、注入直後の10分間、処置台の頭側を-30度の角度の状態で置いた。10分後、蛍光透視画像を捕捉してCSFにおける造影剤分布を検証した。とりわけ、この大きな注入容量(動物のCSF総容量のおよそ40%)[Reiselbach,et al,New England Journal of Medicine.1962;267(25):1273-1278]に伴って、トレンデレンブルグ体位に置かれていない動物においてでさえ造影剤は脊髄クモ膜下腔に沿って及び基底槽の中に迅速に分布した(図18)。P
CRによるベクターゲノムの分布(図19)及びGFP発現(図20)の解析は脳及び脊髄の全体にわたる形質導入を実証した。形質導入された細胞の数または分布に対する注入後位置決めの明らかな効果はなかった。以前報告されたように、髄内のAAV投与の後、末梢及び肝形質導入へのベクター逃避があった[Hinderer,et al,Molecular Therapy-Methods & Clinical Development.12/10/online,2014;1;Haurigot,et al,Journal of Clinical Investigation.Aug,2013;123(8):3254-3271]。肝臓形質導入の程度はAAV9に対する既存の中和抗体(NAb)の存在に依存する。6匹の動物のうち4匹は検出できるベースラインのAAV9のNAb(<1.5の力価)を有さず、2匹の動物(4051及び07-11)は1:40の力価でAAV9に対する検出できる既存の抗体を有した。以前の結果に一致して、既存の抗体は肝臓形質導入を阻止し、脾臓へのベクターの分布の増加を生じた[Wang,et al,Human gene therapy.Nov,2011;22(11):1389-1401,but had no impact on CNS transduction;Haurigot,et al,Journal of Clinical Investigation.Aug,2013;123(8):3254-3271]。
後頭下穿刺法は臨床現場では一般的な手順ではないので、我々は、側脳室及び腰椎槽を含むCSFアクセスのさらに日常的な部位を評価した。ここで、我々は、高い密度のベクター溶液と注入後のトレンデレンブルグ体位とを採用して腰椎領域から頭蓋へのベクターの分布を改善する方法を評価した。
り得ることを示唆している。
(配列表フリーテキスト)
以下の情報は数的識別子<223>のもとで配列を含有するフリーテキストのために提供される。
Claims (38)
- ヒト患者におけるα-L-イズロニダーゼ欠損症の治療に有用な治療レジメンであって、前記レジメンは:
(a)AAV9カプシド、及び患者においてその発現を指令する調節性配列の制御下にあるヒトα-L-イズロニダーゼ(hIDUA)をコードする配列を含む核酸であって、ヒトhIDUAコード配列が、機能的hIDUAをコードする配列番号1のヌクレオチド配列または配列番号1と少なくとも約80%同一である配列を有する、核酸を有する組換えAAV(rAAV);
(b)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第1の免疫抑制剤;並びに
(c)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第2の免疫抑制剤を患者に投与することを含み、
少なくとも1の免疫抑制剤の投与は、AAVベクターの送達の前または同日に開始し;
少なくとも1の前記免疫抑制剤の投与は、ベクター投与後少なくとも8週間継続する、レジメン。 - 前記患者は最初に静脈内ステロイド、続いて経口ステロイドが投与される、請求項1に記載のレジメン。
- 免疫抑制剤は、1つ以上のコルチコステロイド、及び任意に、ミコフェノール酸モフェチル(MMF)、及び/または1つ以上のマクロライドである、請求項1または請求項2に記載のレジメン。
- 前記1つ以上のマクロライドは、テムシロリムスまたはシロリムスを含む、請求項1~3のいずれか1項に記載のレジメン。
- ステロイドの前記患者への投与が、ベクター投与の12週間後に中止される、請求項2~4のいずれか1項に記載のレジメン。
- ミコフェノール酸モフェチル(MMF)及びタクロリムスが、ベクター投与前に0~15日間送達される、請求項1~5のいずれか1項に記載のレジメン。
- 前記免疫抑制剤がミコフェノール酸モフェチル(MMF)及びシロリムスである、請求項1~5のいずれか1項に記載のレジメン。
- 前記免疫抑制剤がタクロリムス及びシロリムスの両方を含む場合、各々の低用量を使用して、約4ng/mL~約8ng/mL、または合計約8ng/mL~約16ng/mLの血液トラフレベルを維持する、請求項1~6のいずれか1項に記載のレジメン。
- 前記免疫抑制剤がタクロリムスまたはシロリムスの一方のみを含む場合、総用量が約16ng/mL~約24ng/mLの範囲である、請求項1~7のいずれか1項に記載のレジメン。
- タクロリムスまたはシロリムスの一方のみが使用され、初期負荷用量が約3mg/m2
である、請求項1~9のいずれか1項に記載のレジメン。 - 免疫抑制療法が、ベクター投与前の約-14日目~-1日目に開始される、請求項1~
10のいずれか1項に記載のレジメン。 - 前記コードされたhIDUAが、
(a)配列番号2(Genbank NP_000193)のアミノ酸約1~約653;及び
(b)配列番号2の約アミノ酸27~約653に融合した異種リーダー配列を含む合成ヒト酵素
から選択される配列を有する、請求項1~11のいずれか1項に記載のレジメン。 - 前記核酸配列が、5’逆方向末端反復(ITR)配列、ニワトリβアクチンイントロン、CB7プロモータ、ポリAシグナル、及び/または3’ITR配列をさらに含む、請求項1~12のいずれか1項に記載のレジメン。
- 前記rAAVが6~9のpHを有する懸濁液中にある、請求項1~13のいずれか1項に記載のレジメン。
- 前記rAAVが髄内注入を介して送達される、請求項14に記載のレジメン。
- hIDUA遺伝子を含むrAAVを静脈内に共投与することをさらに含む、請求項15に記載のレジメン。
- 治療の有効性が、任意に聴覚脳幹試験によって、聴覚能力変化を測定することによって評価される、請求項1~16のいずれか1項に記載のレジメン。
- rAAVが、ヒト対象への髄内注入のために製剤化されて;
(i)≧4ヶ月齢~<9ヶ月齢のヒト対象に対する約1.2×1012~約6.0×1012GCもしくは約6.0×1012~約3.0×1013GC;
(ii)≧9ヶ月齢~<18ヶ月齢のヒト対象に対する約2×1012~約6.0×1013もしくは約1.0×1013~約5.0×1013GC;または
(iii)≧9ヶ月齢~<18ヶ月齢のヒト対象に対する約2.2×1012~約1.1×1013GCもしくは約1.1×1013~約5.5×1013GC;
の総平坦用量を投与する、請求項1~17のいずれか1項に記載のレジメン。 - ヒトα-L-イズロニダーゼ(hIDUA)をコードする異種核酸を含む組換えAAVベクターを含む組成物であって、ヒトhIDUAコード配列が、機能的hIDUAをコードする配列番号1または配列番号1と少なくとも約80%同一である配列を有し、AAVベクターが、それを必要とするヒト対象への髄内注入のために製剤化されて:
(a)≧4ヶ月齢~<9ヶ月齢のヒト対象に対する約1.2×1012~約6.0×1012GCもしくは約6.0×1012~約3.0×1013GC;
(b)≧9ヶ月齢~<18ヶ月齢のヒト対象に対する約2×1012~約6.0×1013もしくは約1.0×1013~約5.0×1013GC;または
(c)≧9ヶ月齢~<18ヶ月齢のヒト対象に対する約2.2×1012~約1.1×1013GCもしくは約1.1×1013~約5.5×1013GC;
の総平坦用量を投与する、組成物。 - (i)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第1の免疫抑制剤:及び
(ii)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第2の免疫抑制
剤、
との共療法における使用であって、
免疫抑制剤の投与は、AAVベクターの送達の前または同日に開始し;
免疫抑制剤の少なくとも一方の投与は、ベクター投与後少なくとも8週間継続する、
使用のための、請求項19に記載の組成物。 - ヒトα-L-イズロニダーゼ(hIDUA)をコードする異種核酸を含む組換えAAVベクターとの併用療法における使用のための免疫抑制剤であって、前記ヒトhIDUAコード配列が、機能的hIDUAをコードする配列番号1または配列番号1と少なくとも約80%同一である配列を有し、
前記免疫抑制剤が;(a)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第1の免疫抑制剤;及び(b)グルココルチコイド、ステロイド、代謝拮抗剤、T細胞阻害剤、マクロライド、または細胞増殖抑制剤のうちの少なくとも1つから選択される少なくとも第2の免疫抑制剤を含み、
前記免疫抑制剤の投与は、AAVベクターの送達の前または同日に開始し;前記免疫抑制剤の少なくとも一方の投与は、ベクター投与後少なくとも8週間継続する、免疫抑制剤。 - 前記AAVベクターが、それを必要とするヒト対象への髄内注入のために製剤化されて:
(i)≧4ヶ月齢~<9ヶ月齢のヒト対象に対する約1.2×1012~約6.0×1012GCもしくは約6.0×1012~約3.0×1013GC;
(ii)≧9ヶ月齢~<18ヶ月齢のヒト対象に対する約2×1012~約6.0×1013GCもしくは約1.0×1013~約5.0×1013GC;または
(iii)≧9ヶ月齢~<18ヶ月齢のヒト対象に対する約2.2×1012~約1.1×1013GCもしくは約1.1×1013~約5.5×1013GC、
の総平坦用量を投与する、請求項21に記載の免疫抑制剤。 - 前記免疫抑制剤が、ベクター送達前に患者に投与可能な静脈内ステロイドと、ベクター送達後に患者に投与可能な経口ステロイドとを含む、請求項19もしくは20に記載の組成物、または請求項21もしくは22に記載の免疫抑制剤。
- 免疫抑制剤が、1つ以上のコルチコステロイド、及び任意に、ミコフェノール酸モフェチル(MMF)及び/または1つ以上のマクロライドである、請求項20に記載の組成物、または請求項21もしくは22に記載の免疫抑制剤。
- 前記1つ以上のマクロライドがテムシロリムスまたはシロリムスを含む、請求項24に記載の組成物または請求項24に記載の免疫抑制剤。
- 前記患者へのステロイドの投与が、ベクター投与の12週間後に中止される、請求項23~25のいずれか1項に記載の組成物または免疫抑制剤。
- ミコフェノール酸モフェチル(MMF)及びタクロリムスが、ベクター投与前0~15日間送達される、請求項23~26のいずれか1項に記載の組成物または免疫抑制剤。
- 前記免疫抑制剤がミコフェノール酸モフェチル(MMF)及びシロリムスである、請求項23~26のいずれか1項に記載の組成物または免疫抑制剤。
- 前記免疫抑制剤がタクロリムス及びシロリムスの両方を含む場合、各々の低用量を使用
して、約4ng/mL~約8ng/mL、または合計約8ng/mL~約16ng/mLの血液トラフレベルを維持する、請求項23~26のいずれか一項に記載の組成物または免疫抑制剤。 - 前記免疫抑制剤がタクロリムスまたはシロリムスの一方のみを含み、総用量が約16ng/mL~約24ng/mLの範囲である、請求項20~28のいずれか1項に記載の組成物または免疫抑制剤。
- タクロリムスまたはシロリムスの一方のみが使用され、初期負荷用量が約3mg/m2
である、請求項30に記載の組成物または免疫抑制剤。 - 前記免疫抑制療法が、ベクター投与前の約-14日目~-1日目に開始される、請求項20~30のいずれか一項に記載の組成物または免疫抑制剤。
- 前記コードされたhIDUAが:
(a)配列番号2(Genbank NP_000193)のアミノ酸約1~約653;及び
(b)配列番号2の約アミノ酸27~約653に融合した異種リーダー配列を含む合成ヒト酵素
から選択される配列を有する、請求項19、20または23~31のいずれか1項に記載の組成物または請求項20~31のいずれか1項に記載の免疫抑制剤。 - 前記核酸配列が、5’逆方向末端反復(ITR)配列、ニワトリβアクチンイントロン、CB7プロモータ、ポリAシグナル、及び/または3’ITR配列をさらに含む、請求項19、20または23~31のいずれか1項に記載の組成物または請求項21~32のいずれか1項に記載の免疫抑制剤。
- 前記rAAVが6~9のpHを有する懸濁液中にある、請求項19、20または23~31のいずれか1項に記載の組成物または請求項21~32のいずれか1項に記載の免疫抑制剤。
- 前記rAAVが髄内注入を介して送達される、請求項35に記載の組成物または請求項35に記載の免疫抑制剤。
- 前記hIDUA遺伝子を含むrAAVを静脈内に共投与することをさらに含む、請求項19、20もしくは23~36のいずれか1項に記載の組成物または請求項21~36のいずれか1項に記載の免疫抑制剤。
- 治療の有効性が、任意に聴覚脳幹試験によって、聴覚能力変化を測定することによって評価される、請求項19、20もしくは23~36のいずれか1項に記載の組成物または請求項21~36のいずれか1項に記載の免疫抑制剤。
Applications Claiming Priority (8)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762529385P | 2017-07-06 | 2017-07-06 | |
| US62/529,385 | 2017-07-06 | ||
| US201762530614P | 2017-07-10 | 2017-07-10 | |
| US62/530,614 | 2017-07-10 | ||
| US201862616106P | 2018-01-11 | 2018-01-11 | |
| US62/616,106 | 2018-01-11 | ||
| PCT/US2018/040957 WO2019010335A1 (en) | 2017-07-06 | 2018-07-05 | AAV9 MEDIATED GENE THERAPY FOR TREATING MUCOPOLYSACCHARIDOSIS TYPE I |
| JP2020500131A JP2020526514A (ja) | 2017-07-06 | 2018-07-05 | ムコ多糖症i型を治療するための遺伝子治療 |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020500131A Division JP2020526514A (ja) | 2017-07-06 | 2018-07-05 | ムコ多糖症i型を治療するための遺伝子治療 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023123760A true JP2023123760A (ja) | 2023-09-05 |
| JP7670759B2 JP7670759B2 (ja) | 2025-04-30 |
Family
ID=63036365
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020500131A Pending JP2020526514A (ja) | 2017-07-06 | 2018-07-05 | ムコ多糖症i型を治療するための遺伝子治療 |
| JP2023108011A Active JP7670759B2 (ja) | 2017-07-06 | 2023-06-30 | ムコ多糖症i型を治療するための遺伝子治療 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020500131A Pending JP2020526514A (ja) | 2017-07-06 | 2018-07-05 | ムコ多糖症i型を治療するための遺伝子治療 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US11890329B2 (ja) |
| EP (1) | EP3676385A1 (ja) |
| JP (2) | JP2020526514A (ja) |
| KR (2) | KR20200053468A (ja) |
| AU (1) | AU2018298133A1 (ja) |
| BR (1) | BR112020000063A2 (ja) |
| CA (1) | CA3068328A1 (ja) |
| IL (1) | IL271780A (ja) |
| MA (1) | MA50016A (ja) |
| SG (1) | SG11201912631PA (ja) |
| WO (1) | WO2019010335A1 (ja) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SI2984166T1 (sl) | 2013-03-15 | 2020-09-30 | The Trustees Of The University Of Pennsylvania | Sestavki za zdravljenje MPSI |
| CN105377039A (zh) | 2013-05-15 | 2016-03-02 | 明尼苏达大学董事会 | 腺相关病毒介导的基因向中枢神经系统转移 |
| EP3411488A1 (en) | 2016-02-03 | 2018-12-12 | The Trustees Of The University Of Pennsylvania | Gene therapy for treating mucopolysaccharidosis type i |
| MA50016A (fr) | 2017-07-06 | 2020-07-08 | Univ Pennsylvania | Thérapie génique médiée par aav9 pour traiter la mucopolysaccharidose de type i |
| TWI835747B (zh) | 2017-09-22 | 2024-03-21 | 賓州大學委員會 | 用於治療黏多醣病 ii 型之基因治療 |
| WO2020113034A1 (en) * | 2018-11-30 | 2020-06-04 | Avexis, Inc. | Aav viral vectors and uses thereof |
| WO2021081217A1 (en) * | 2019-10-23 | 2021-04-29 | The Trustees Of The University Of Pennsylvania | Compositions for drg-specific reduction of transgene expression |
| WO2021150570A1 (en) * | 2020-01-22 | 2021-07-29 | Regenxbio Inc. | Treatment of mucopolysaccharidosis i with fully-human glycosylated human alpha-l-iduronidase (idua) |
| IL300407A (en) * | 2020-08-10 | 2023-04-01 | Prevail Therapeutics Inc | Gene therapies for lysosomal disorders |
| US20230346979A1 (en) * | 2020-08-10 | 2023-11-02 | Prevail Therapeutics, Inc. | Gene therapies for neurodegenerative disorders |
| WO2022165313A1 (en) | 2021-02-01 | 2022-08-04 | Regenxbio Inc. | Gene therapy for neuronal ceroid lipofuscinoses |
| WO2022170082A1 (en) * | 2021-02-05 | 2022-08-11 | Regents Of The University Of Minnesota | Methods for preventing cardiac or skeletal defects in diseases including mucopolysaccharidoses |
| EP4294461A4 (en) * | 2021-02-22 | 2025-06-25 | Decibel Therapeutics, Inc. | METHODS AND COMPOSITIONS FOR REDUCING NUCLEIC ACID VECTOR-INDUCED TOXICITY IN THE INNER EAR |
| WO2024205528A1 (en) * | 2023-03-31 | 2024-10-03 | Erci̇yes Üni̇versi̇tesi̇ Strateji̇ Geli̇şti̇rme Dai̇re Başkanliği | A multi-head for use in electrohydrodynamic |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015164723A1 (en) * | 2014-04-25 | 2015-10-29 | The Trustees Of The University Of Pennsylvania | Methods and compositions for treating metastatic breast cancer and other cancers in the brain |
| WO2016187017A1 (en) * | 2015-05-15 | 2016-11-24 | Mcivor R Scott | Adeno-associated for therapeutic delivery to central nervous system |
| WO2017024198A1 (en) * | 2015-08-06 | 2017-02-09 | The Trustees Of The University Of Pennsylvania | Glp-1 and use thereof in compositions for treating metabolic diseases |
| WO2017040254A1 (en) * | 2015-08-28 | 2017-03-09 | Laufer Wind Group Llc | Mitigation of small unmanned aircraft systems threats |
Family Cites Families (49)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AU649897B2 (en) | 1991-11-14 | 1994-06-02 | Women's And Children's Hospital | Synthetic alpha-L-iduronidase and genetic sequences encoding same |
| US6149909A (en) | 1995-06-23 | 2000-11-21 | Women's And Children's Hospital | Synthetic α-L-iduronidase and genetic sequences encoding same |
| US5478745A (en) | 1992-12-04 | 1995-12-26 | University Of Pittsburgh | Recombinant viral vector system |
| AU722624B2 (en) | 1996-09-06 | 2000-08-10 | Trustees Of The University Of Pennsylvania, The | An inducible method for production of recombinant adeno-associated viruses utilizing T7 polymerase |
| CA2328518A1 (en) | 1998-05-13 | 1999-11-18 | Harbor-Ucla | Recombinant (alpha)-l-iduronidase, methods for producing and purifying the same and methods for treating diseases caused by deficiencies thereof |
| PT1916258E (pt) | 1999-08-09 | 2014-07-29 | Genzyme Corp | Aumento da expressão de uma sequência nucleotídica heteróloga de cadeia simples a partir de vectores virais recombinantes por concepção da sequência de maneira que esta forme pares de bases intracadeia |
| US6426208B1 (en) | 1999-11-12 | 2002-07-30 | Harbor-Ucla Research And Education Institute | Recombinant α-L-iduronidase, methods for producing and purifying the same and methods for treating diseases caused by deficiencies thereof |
| RU2196988C2 (ru) | 2000-04-19 | 2003-01-20 | Государственный новосибирский областной клинический диагностический центр | Способ диагностики мукополисахаридозов |
| AU2001267337A1 (en) | 2000-06-30 | 2002-01-14 | Maxygen Aps | Peptide extended glycosylated polypeptides |
| NZ532635A (en) | 2001-11-13 | 2007-05-31 | Univ Pennsylvania | A method of identifying unknown adeno-associated virus (AAV) sequences and a kit for the method |
| DK2359869T3 (en) | 2001-12-17 | 2019-04-15 | Univ Pennsylvania | Sequences of adeno-associated virus (AAV) serotype 8, vectors containing these, and uses thereof |
| AU2003302724A1 (en) | 2002-08-13 | 2004-07-09 | Mcivor, Scott, R. | Methods of using vectors to treat metabolic disorders |
| US7155804B2 (en) | 2003-09-17 | 2007-01-02 | Moog Inc. | Method of forming an electric motor |
| CN1856576B (zh) | 2003-09-30 | 2011-05-04 | 宾夕法尼亚州立大学托管会 | 腺伴随病毒(aav)进化支、序列、含有这些序列的载体及它们的应用 |
| WO2006110689A2 (en) | 2005-04-07 | 2006-10-19 | The Trustees Of The University Of Pennsylvania | Method of increasing the function of an aav vector |
| EP1777906A1 (en) | 2005-06-09 | 2007-04-25 | Matsushita Electric Industrial Co., Ltd. | Amplitude error compensating apparatus and orthogonality error compensating apparatus |
| US7588772B2 (en) | 2006-03-30 | 2009-09-15 | Board Of Trustees Of The Leland Stamford Junior University | AAV capsid library and AAV capsid proteins |
| US20090062144A1 (en) | 2007-04-03 | 2009-03-05 | Nancy Lan Guo | Gene signature for prognosis and diagnosis of lung cancer |
| US9415121B2 (en) | 2008-12-19 | 2016-08-16 | Nationwide Children's Hospital | Delivery of MECP2 polynucleotide using recombinant AAV9 |
| JP2014503173A (ja) | 2009-11-05 | 2014-02-13 | プロイェクト、デ、ビオメディシナ、シーマ、ソシエダッド、リミターダ | 制御された発現系 |
| US20130023033A1 (en) | 2010-03-29 | 2013-01-24 | The Trustees Of The University Of Pennsylvania | Pharmacologically induced transgene ablation system |
| EP2826860B1 (en) | 2010-04-23 | 2018-08-22 | University of Massachusetts | CNS targeting AAV vectors and methods of use thereof |
| US8927514B2 (en) | 2010-04-30 | 2015-01-06 | City Of Hope | Recombinant adeno-associated vectors for targeted treatment |
| EP2394667A1 (en) | 2010-06-10 | 2011-12-14 | Laboratorios Del Dr. Esteve, S.A. | Vectors and sequences for the treatment of diseases |
| DK2675902T3 (da) | 2011-02-17 | 2019-06-03 | Univ Pennsylvania | Sammensætninger og fremgangsmåder til at ændre vævsspecificitet og forbedre aav9-medieret genoverførsel |
| HRP20171334T1 (hr) | 2011-04-22 | 2017-11-17 | The Regents Of The University Of California | Virioni adeno-povezanog virusa s kapsid varijantom i postupci njihove upotrebe |
| DK3444342T3 (da) | 2012-07-11 | 2020-08-24 | Sangamo Therapeutics Inc | Fremgangsmåder og sammensætninger til behandlingen af lysosomale aflejringssygdomme |
| WO2014125647A1 (ja) | 2013-02-18 | 2014-08-21 | 富士通オプティカルコンポーネンツ株式会社 | 光受信装置 |
| SI2984166T1 (sl) | 2013-03-15 | 2020-09-30 | The Trustees Of The University Of Pennsylvania | Sestavki za zdravljenje MPSI |
| CN105377039A (zh) | 2013-05-15 | 2016-03-02 | 明尼苏达大学董事会 | 腺相关病毒介导的基因向中枢神经系统转移 |
| CA2915296A1 (en) | 2013-06-11 | 2015-02-26 | Portage Pharmaceuticals Ltd. | Structure, manufacturing and uses of human-derived cell-permeable peptides conjugated with specific biologically active cargo peptides |
| US9585971B2 (en) | 2013-09-13 | 2017-03-07 | California Institute Of Technology | Recombinant AAV capsid protein |
| BR112017005892A2 (pt) | 2014-09-24 | 2017-12-12 | Hope City | variantes de vetor de vírus adeno-associado para edição de genoma de alta eficácia e métodos da mesma |
| CN107002096A (zh) | 2014-10-06 | 2017-08-01 | 阿罗根有限公司 | 基于aav的基因疗法 |
| US10604747B2 (en) * | 2015-08-06 | 2020-03-31 | Academia Sinica | Engineered enzyme for enzyme replacement therapy |
| HK1257024A1 (zh) * | 2015-08-31 | 2019-10-11 | 宾夕法尼亚大学 | 用於治疗伴侣动物的aav-epo |
| US20180236105A1 (en) * | 2015-10-23 | 2018-08-23 | University Of Iowa Research Foundation | Methods for treating neurodegenerative diseases using gene therapy to delay disease onset and progression while providing cognitive protection |
| WO2017100676A1 (en) | 2015-12-11 | 2017-06-15 | The Trustees Of The University Of Pennsylvania | Scalable purification method for aav8 |
| EP3387138B1 (en) | 2015-12-11 | 2022-01-26 | The Trustees Of The University Of Pennsylvania | Scalable purification method for aav9 |
| US11028372B2 (en) | 2015-12-11 | 2021-06-08 | The Trustees Of The University Of Pennsylvania | Scalable purification method for AAVRH10 |
| US11015173B2 (en) | 2015-12-11 | 2021-05-25 | The Trustees Of The University Of Pennsylvania | Scalable purification method for AAV1 |
| CA3010738A1 (en) * | 2016-01-15 | 2017-07-20 | Sangamo Therapeutics, Inc. | Methods and compositions for the treatment of neurologic disease |
| EP3411488A1 (en) | 2016-02-03 | 2018-12-12 | The Trustees Of The University Of Pennsylvania | Gene therapy for treating mucopolysaccharidosis type i |
| EP3541946A1 (en) | 2016-11-15 | 2019-09-25 | Regents Of The University Of Minnesota | Method for improving neurological function in mpsi and mpsii and other neurological disorders |
| CA3049915A1 (en) | 2017-01-31 | 2018-08-09 | Stephen YOO | Treatment of mucopolysaccharidosis i with fully-human glycosylated human alpha-l-iduronidase (idua) |
| MA50016A (fr) | 2017-07-06 | 2020-07-08 | Univ Pennsylvania | Thérapie génique médiée par aav9 pour traiter la mucopolysaccharidose de type i |
| IL280198B2 (en) | 2018-07-18 | 2026-01-01 | Regenxbio Inc | Treatment of mucopolysaccharidosis I with fully glycosylated human iduronidase-alpha-L (idus) |
| WO2021150570A1 (en) | 2020-01-22 | 2021-07-29 | Regenxbio Inc. | Treatment of mucopolysaccharidosis i with fully-human glycosylated human alpha-l-iduronidase (idua) |
| WO2022170082A1 (en) | 2021-02-05 | 2022-08-11 | Regents Of The University Of Minnesota | Methods for preventing cardiac or skeletal defects in diseases including mucopolysaccharidoses |
-
2018
- 2018-07-05 MA MA050016A patent/MA50016A/fr unknown
- 2018-07-05 KR KR1020207003304A patent/KR20200053468A/ko not_active Ceased
- 2018-07-05 EP EP18746390.6A patent/EP3676385A1/en active Pending
- 2018-07-05 CA CA3068328A patent/CA3068328A1/en active Pending
- 2018-07-05 SG SG11201912631PA patent/SG11201912631PA/en unknown
- 2018-07-05 US US16/624,084 patent/US11890329B2/en active Active
- 2018-07-05 AU AU2018298133A patent/AU2018298133A1/en not_active Abandoned
- 2018-07-05 BR BR112020000063-9A patent/BR112020000063A2/pt unknown
- 2018-07-05 KR KR1020247013510A patent/KR20240063170A/ko active Pending
- 2018-07-05 JP JP2020500131A patent/JP2020526514A/ja active Pending
- 2018-07-05 WO PCT/US2018/040957 patent/WO2019010335A1/en not_active Ceased
-
2019
- 2019-12-31 IL IL271780A patent/IL271780A/en unknown
-
2023
- 2023-06-30 JP JP2023108011A patent/JP7670759B2/ja active Active
- 2023-12-13 US US18/538,866 patent/US20240307511A1/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2015164723A1 (en) * | 2014-04-25 | 2015-10-29 | The Trustees Of The University Of Pennsylvania | Methods and compositions for treating metastatic breast cancer and other cancers in the brain |
| WO2016187017A1 (en) * | 2015-05-15 | 2016-11-24 | Mcivor R Scott | Adeno-associated for therapeutic delivery to central nervous system |
| WO2017024198A1 (en) * | 2015-08-06 | 2017-02-09 | The Trustees Of The University Of Pennsylvania | Glp-1 and use thereof in compositions for treating metabolic diseases |
| WO2017040254A1 (en) * | 2015-08-28 | 2017-03-09 | Laufer Wind Group Llc | Mitigation of small unmanned aircraft systems threats |
Non-Patent Citations (3)
| Title |
|---|
| ERIK ALLEN LYKKEN: "RECENT PROGRESS AND CONSIDERATIONS FOR AAV GENE THERAPIES TARGETING THE CENTRAL NERVOUS SYSTEM", JOURNAL OF NEURODEVELOPMENTAL DISORDERS, vol. VOL:10, NR:1, JPN5020008613, 18 May 2018 (2018-05-18), GB, pages 1 - 10, ISSN: 0005554448 * |
| NEUROBIOL DIS., vol. 43, no. 1, JPN6023008095, 2011, pages 123 - 133, ISSN: 0005554449 * |
| VICTORIA M VELASQZEZ: "EFFECTIVE DEPLETION OF PRE-EXISTING ANTI-AAV ANTIBODIES REQUIRES BROAD IMMUNE TARGETING", METHODS & CLINICAL DEVELOPMENT, vol. 4, JPN5020008612, 25 January 2017 (2017-01-25), pages 159 - 168, ISSN: 0005554447 * |
Also Published As
| Publication number | Publication date |
|---|---|
| SG11201912631PA (en) | 2020-01-30 |
| JP2020526514A (ja) | 2020-08-31 |
| MA50016A (fr) | 2020-07-08 |
| JP7670759B2 (ja) | 2025-04-30 |
| WO2019010335A1 (en) | 2019-01-10 |
| US11890329B2 (en) | 2024-02-06 |
| IL271780A (en) | 2020-02-27 |
| KR20200053468A (ko) | 2020-05-18 |
| CA3068328A1 (en) | 2019-01-10 |
| KR20240063170A (ko) | 2024-05-09 |
| EP3676385A1 (en) | 2020-07-08 |
| AU2018298133A1 (en) | 2020-01-23 |
| US20200147185A1 (en) | 2020-05-14 |
| US20240307511A1 (en) | 2024-09-19 |
| BR112020000063A2 (pt) | 2020-07-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US20240024510A1 (en) | Gene therapy for treating mucopolysaccharidosis type i | |
| JP7670759B2 (ja) | ムコ多糖症i型を治療するための遺伝子治療 | |
| US20220125949A1 (en) | Gene therapy for treating mucopolysaccharidosis type ii | |
| US20240016903A1 (en) | Gene therapy for treating mucopolysaccharidosis type ii |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230630 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230630 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240605 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20240905 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20241105 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20241205 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250213 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250319 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250417 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7670759 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |