JP3750010B2 - 2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体 - Google Patents
2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体 Download PDFInfo
- Publication number
- JP3750010B2 JP3750010B2 JP21468499A JP21468499A JP3750010B2 JP 3750010 B2 JP3750010 B2 JP 3750010B2 JP 21468499 A JP21468499 A JP 21468499A JP 21468499 A JP21468499 A JP 21468499A JP 3750010 B2 JP3750010 B2 JP 3750010B2
- Authority
- JP
- Japan
- Prior art keywords
- bipyridine
- metal complex
- chiral
- represented
- bis
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Images
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E10/00—Energy generation through renewable energy sources
- Y02E10/50—Photovoltaic [PV] energy
Landscapes
- Pyridine Compounds (AREA)
Description
【発明の属する技術分野】
この出願の発明は、2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体に関するものである。さらに詳しくは、この出願の発明は、光触媒、電子機能材料等として有用な2,2′−ビピリジン系配位子金属錯体の新しい製造方法とキラル金属錯体に関するものである。
【0002】
【従来の技術とその課題】
金属錯体化合物については、その光反応機能や電子移動機能、さらには生理活性機能等について注目されて数多くの合成法が報告されている。
【0003】
そして近年では、光学活性な金属錯体を合成するための不斉合成も検討されている。
しかしながら、金属錯体の不斉合成は容易ではなく、多くの場合、光学分割による方法が採用され、しかも、この光学分割すら難しい場合が少くないのが実情である。
【0004】
たとえばルテニウムトリス(ビピリジン)型錯体は、光触媒としてよく知られた化合物であり、光照射条件下、電子移動反応ならびにエネルギー移動反応を触媒する。このルテニウム錯体は8配位錯体であり、Δ体Λ体の二つの光学活性異性体をもつことが知られている。これらの光学異性体の光学分割にはこれまでに、(1)光学活性な分割剤を用いる方法、(2)光学活性カラムを用いた分割、の2つの方法が知られている(前者が歴史的に古く、今でも一般的方法である。後者は有機化合物に関してはかなり実績はあるものの、金属錯体に適用した例はまだ少なく、ごく最近、数例が報告されているにすぎない。)
このような状況において、光学活性なルテニウムトリス(ビピリジン)型錯体は不斉光触媒として重要であるが、これまではいったんラセミ体(Δ体とΛ体の等量混合物)を合成した後、上記2つの方法のいずれかで光学分割するしか方法がなかった。もう一つの可能性としては、中間体として光学活性なルテニウムビス(ビピリジン)型錯体を合成し、そこから光学活性なトリス体を誘導する方法が考えられるが、これまでにそのような報告例は全くない。その理由として、ルテニウムビス(ビピリジン)型錯体は一般的にトリス体に比べて熱的に不安定であり、光学分割した例すら極めて少数しか知られていないことがある。
【0005】
その一例として、〔Ru(bpy)2 (CO)2 〕(Br)2 (bpy=2,2′−ビピリジン)のラセミ体を合成し、分割剤を用いて光学分割した例(Inorg. Chem.1995,34,3857−3858)があるが、この化合物は熱的に安定なため光学分割が可能であったが、安定すぎるためトリス体への誘導は極めて難しく、通常のトリス体への誘導は行われていない。
【0006】
そこでこの出願の発明は、以上のとおりの従来技術の限界を克服し、簡便に、しかも選択的に2,2′−ビピリジン系配位子のトリス体の誘導を可能とする、金属錯体の新しい製造方法を提供することを課題としている。そしてまた、この出願の発明は、新しいキラルな金属錯体を提供することも課題としている。
【0007】
【課題を解決するための手段】
この出願の発明は、上記の課題を解決するものとして、第1には、次式
Mh3
(Mは遷移金属原子を、hはハロゲン原子を示す。)で表わされる金属ハライドに、2,2′−ビピリジン系配位子(A)化合物を反応させて、次式
〔MA3 〕2+
(Mは前記のものを示し、Aは、2,2′−ビピリジン系配位子を示す。)
で表わされるカチオンの錯体を製造することを特徴とする2,2′−ビピリジン系配位子金属錯体の製造方法を提供する。
【0008】
また、この出願の発明は、上記方法について、第2には、2,2′−ビピリジン系配位子(A)は、キラルな置換基を有している方法を、第3には、2,2′−ビピリジン系配位子(A)化合物は、多段階で添加反応させる方法を、第4には、2,2′−ビピリジン系配位子(A)化合物は、4,4′−位置の置換基により相違する2種(A1 ,A2 )または3種(A1 ,A2 ,A3 )のものとする方法を、第5には、2種(A1 ,A2 )または3種(A1 ,A2 ,A3 )の2,2′−ビピリジン系配位子化合物は、各々、異なる反応段階で添加反応させる方法を、第6には、2種(A1 ,A2 )または3種(A1 ,A2 ,A3 )の2,2′−ビピリジン系配位子のうちの少くとも1種のものは、4,4′−位置に、キラルな置換基を有している方法を、第7には、キラルな置換基は、アミド基またはエステル基である方法を、第8には、遷移金属原子Mは、周期律表第8族の貴金属原子である方法も提供する。そして、この出願の発明は、第9には、次式(1)(2)(3)(4);
〔M(A1 )3 〕2+ (1)
〔M(A1 )2 A2 〕2+ (2)
〔M(A1 )(A2 )2 〕2+ (3)
〔M(A1 )(A2 )(A3 )〕2+ (4)
(Mは遷移金属原子を示し、A1 ,A2 およびA3 は、置換基により各々相違する2,2′−ビピリジン系配位子を示し、少くともA1 の置換基はキラルな置換基であって、A2 およびA3 の一方もしくは両方の置換基もキラルな置換基であってもよいことを示す。)
のうちのいずれかで表われるカチオンの錯体であることを特徴とするキラル金属錯体を提供し、第10には、キラルな置換基は、アミド基またはエステル基であるキラル金属錯体を、第11には、遷移金属原子Mは、周期律表第8族の貴金属原子であるキラル金属錯体をも提供する。
【0009】
【発明の実施の形態】
この出願の発明は上記のとおりの特徴をもつものであるが、以下にその実施の形態について説明する。
【0010】
まず特徴的なことは、この出願の発明の製造方法では、中間体化合物の単離(分離)を必要とすることなしに、いわゆる「ワンポット」で2,2′−ビピリジン系配位子(A)を持つトリス体のカチオン錯体を製造することである。反応は、前記のように、Mh3 の金属ハライドと、2,2′−ビピリジン系配位子(A)化合物との反応により可能とされる。トリス体としての〔MA3 〕2+カチオンの錯体が生成されることになる。
【0011】
反応は一般ないしは多段の反応として行うことができる。そして、2,2′−ビピリジン系配位子(A)化合物としては、1種のもの(A1 )ばかりでなく、結合する置換基によって相違する2種(A1 ,A2 )あるいは3種(A1 ,A2 ,A3 )のものを用いてもよい。
【0012】
このような2,2′−ビピリジン系配位子の種類に応じて、この出願の発明では、次式
〔M(A1 )3 〕2+ (1)
〔M(A1 )2 A2 〕2+ (2)
〔M(A1 )(A2 )2 〕2+ (3)
〔M(A1 )(A2 )(A3 )〕2+ (4)
のいずれかによって表わされるトリス体のカチオン錯体が製造されることになる。複数種の配位子により構成されるカチオンの錯体の場合には、配位子の種類毎に多段となる反応とすることがより実際的である。たとえば、〔M(A1 )(A2 )(A3 )〕2+のカチオン錯体を製造する際には、たとえば次式のように、A1 の導入、A2 の導入、そしてA3 の導入の各工程を多段反応工程として構成することが考慮される。
【0013】
【化1】
【0014】
カチオンの錯体を構成する遷移金属原子Mとしては、多価金属の各種のものでよいが、なかでも周期律表第8族の貴金属原子、具体的にはRu(ルテニウム)、Rh(ロジウム)、Pd(パラジウム)、Pt(白金)が望ましいものとして例示される。なかでもRu(ルテニウム)が重要なものの一つである。
【0015】
原料化合物としての金属ハライドMh3 を構成するハロゲン原子hとしては、より実際的に好ましいのは塩素原子である。
2,2′−ビピリジン系配位子A、またはA1 ,A2 ,A3 についての「2,2′−ビピリジン系」との規定は、2,2′−ビピリジン骨格を有し、2,2′−位置の骨格構成窒素原子が配位結合を可能とする。たとえば、2,2′−ビピリジン骨格を持つもの、そして、この骨格に炭素環が縮含している1,10−フェナントロクン類などがこの発明の「ビピリジン系」となる。2,2′−ビピリジン骨格には各種の置換基を有していてもよいことを意味している。これら置換基としては、配位結合を阻害しない限り各種のものであってよく、たとえば、水素原子、アルキル基、アリール基等の炭化水素基、アルコキシ基、カルボキシル基、エステル基、アミド基、アミノ基等であってよい。なかでも、この出願の発明では、2,2′−ビピリジンの4,4′−位置に置換基を有するものが、特に、この4,4′−位置にキラルな置換基を有するものが例示される。キラル置換基を4,4′−位置に持つ2,2′−ビピリジン系配位子は、トリス体カチオン錯体の光機能性等の観点において注目されるものだからである。
【0016】
特に、この発明においては、前記の式(1)(2)(3)(4)のいずれかで表わされ、しかも、A1 ,A2 およびA3 が、置換基によって各々相違するものであって、少くともA1 の置換基はキラルな置換基であり、A2 およびA3 の一方もしくは両方の置換基もキラルな置換基であってもよい、キラル金属錯体が提供されることになる。
【0017】
この場合のキラル置換基としては、置換基の構成内にキラル中心を持つものが考慮される。そして、たとえば−CO−NH−R,−CO−O−R(Rは、キラル中心を持つ有機部位である)等のアミドやエステルの置換基がこのものとして挙げられる。
【0018】
金属ハライドMh3 との反応による2,2′−ビピリジン配位子(A)もしくは(A1 ,A2 ,A3 )の導入においては、反応温度は、30〜reflux温度の範囲程度において、アルコール、DMF、DMSO等の溶媒中において行うことが考慮される。2,2′−ビピリジン配位子(A)の化合物の使用量は、配位数に対応して当量ないしはその前後であってよい。特に限定されることはない。
【0019】
なお、この発明の方法においては、中間生成物は本質的に単離(分離)を必要としていないが、所望により単離(分離)してもよい。
また、この発明の方法において製造されるキラル金属錯体については、キラルHPLCにより光学分割することができ、高純度なジアステレオイソマーに分割することができる。
【0020】
そこで以下に実施例を示し、さらに詳しくこの出願の発明について説明する。
【0021】
【実施例】
(実施例1)
<a>RuCl3 (2mmol)を乾燥DMF(35ml)に溶解し、無水LiCl:(2.3mmol)を添加して、懸濁液を5分間70℃の温度で攪拌した。1.1当量の dmbpy(4,4′ジメチル−2,2′−ビピリジン)を加えて、90℃の温度において1.5時間、N2 雰囲気下に攪拌した。
【0022】
次いで、120℃の温度において、Rambpy(4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジン)を添加してN2 雰囲気下に反応させた。冷却後、反応混合液を濾過して未反応RuCl3 、および他の不溶成分を除去した。濾液を減圧乾燥して溶媒DMFを回収し、固形分をエーテルで洗浄した。
【0023】
固形分残渣をメタノール(100ml)に溶解し、Sestbpy (4,4′−ビス((S)−(−)−α−フェニルエチルオキシカルボニル)−2,2′−ビピリジンを加え、65℃の温度において反応させた。
【0024】
室温に冷却後、減圧下に溶媒を蒸発除去し、残渣油状物を少量のアセトンに溶解した後にジエチルエーテルをゆっくりと添加した。1時間室温で攪拌後、沈澱物を減圧濾過した。
【0025】
固形分を少量のアセトニトリルに再溶解し、CH3 CN−MeOH混合溶出液によるSephadex−LH−20−100のカラムクロマトグラフィーにより精製した。粗ラセミ体生成物として、
〔Ru(dmbpy)(Sestbpy)(Rambpy)〕2+
のカチオン錯体(化合物No.58)を得た。
<b>上記<a>と同様にして、Sestbpy に代えて、Restbpy (4,4′−ビス((R)−(+)−α−フェニルエチルオキシカルボニル)−2,2′−ビピリジン)を用い、ラセミ体の〔Ru(dmbpy)(Restbpy)(Rambpy)〕2+のカチオン錯体(化合物No.68)を得た。
【0026】
以上の<a><b>について、その反応式は次に示すことができる。
【0027】
【化2】
【0028】
<c>上記<a><b>のラセミ混合物は、キラルカラムを用いての分取HPLCによりΔ/∧ジアステレオマーに光学分割した。
その結果と、分析値を表1および表2に示した。
【0029】
表1中のX,Y,Zは、2,2′−ビピリジン配位子の4,4′−位置の置換基を示している。
また、図1および図2には、各々のCDスペクトルを示した。
【0030】
【表1】
【0031】
【表2】
【0032】
(実施例2)
次の反応式
【0033】
【化3】
【0034】
に従って、RuCl3 との反応により、XおよびRが各種の組合わせからなる以下のカチオン錯体を製造した。
〔Ru(Sambpy)2 (bpy) 〕2+ (化合物No.51)
〔Ru(Rambpy)2 (bpy) 〕2+ (化合物No.61)
〔Ru(Sambpy)2 (dmbpy) 〕2+ (化合物No.54)
〔Ru(Rambpy)2 (bpy) 〕2+ (化合物No.64)
〔Ru(Sestbpy)2 (Sambpy) 〕2+ (化合物No.57)
〔Ru(Restbpy)2(Rambpy)〕2+ (化合物No.67)
ここで、Sambpy等の表記は次のものを示している。
【0035】
Sambpy:(4,4′−ビス((S)−(−)−α−フェニルエチルアミド)−2,2′−ビピリジン)
Rambpy:(4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジン)
Sestbpy :(4,4′−ビス((S)−(−)−α−フェニルエチルオキシカルボニル−2,2′−ビピリジン)
Restbpy :(4,4′−ビス((R)−(+)−α−フェニルエチルオキシカルボニル−2,2′−ビピリジン)
bpy :(2,2′−ビピリジン)
dmbpy :4,4′ジメチル−2,2′−ビピリジン)
次いで、各々生成されたラセミ混合物を、キラルカラムによる分取HPLCで光学分割し、ジアステレオマーを得た。
【0036】
HPLCの結果と、分析値を表3および表4に示した。表3中のX,Y,Zは、表1と同様のことを意味している。
【0037】
【表3】
【0038】
【表4】
【0039】
図3、図4および図5は、各々、光学分割後のフラクション(F1,f1)(F2,f2)について、化合物No.51,61,54,64,57および67のCDスペクトルを示したものである。
【0040】
また、図6は、化合物No.51および54のカチオン錯体のUV/Visスペクトルを、図7は、化合物No.51,61,54,64のジアステレオマーのUV/Visスペクトルを示した図である。
(実施例3)
次の反応式
【0041】
【化4】
【0042】
に従って、RuCl3 に対し、3当量のSambpyおよびRambpyを反応させ、各々、ラセミ体として、〔Ru(Sambpy)3 〕2+(化合物No.53)、〔Ru(Rambpy)3 〕2+(化合物No.63)のカチオン錯体を得た。
【0043】
分取HPLCにより光学分割し、各々の錯体のジアステレオマーを得た。
HPLCの結果、分析値を表5および表6に示した。
【0044】
【表5】
【0045】
【表6】
【0046】
ジアステレオマーのCDスペクトルおよびUV/Visスペクトルを図8および図9に示した。
【0047】
【発明の効果】
以上詳しく説明したとおり、この出願の発明によって、簡便に、しかも選択的に、2,2′−ビピリジン系配位子のトリス体の誘導を可能とする。新しい金属錯体の製造法が実現される。そしてまた、この発明によって新しい金属錯体も提供される。
【図面の簡単な説明】
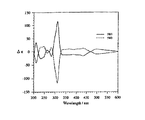
【図1】実施例1の化合物No.58についてのCDスペクトルを示した図である。
【図2】実施例1の化合物No.68についてのCDスペクトルを示した図である。
【図3】化合物No.51,61についてのCDスペクトル図である。
【図4】化合物No.54,64についてのCDスペクトル図である。
【図5】化合物No.57,67についてのCDスペクトル図である。
【図6】化合物No.51,54についてのUV/Visスペクトル図である。
【図7】化合物No.51,61,54,64についてのUV/Visスペクトル図である。
【図8】化合物No.53,63についてのCDスペクトル図である。
【図9】化合物No.53,63のUV/Visスペクトル図である。
Claims (17)
- 次式
Ruh3
(Ruはルテニウムを、hはハロゲン原子を示す。)
で表わされる金属ハライドに、アミド基またはエステル基であるキラルな置換基を有する2,2′−ビピリジン系配位子(A)化合物を反応させて、次式
〔RuA3 〕2+
(Ruは前記のものを示し、Aは、アミド基またはエステル基であるキラルな置換基を有する2,2′−ビピリジン系配位子を示す。)
で表わされるカチオンの錯体を製造することを特徴とする2,2′−ビピリジン系配位子金属錯体の製造方法。 - 2,2′−ビピリジン系配位子(A)化合物は、多段階で添加反応させる請求項1の製造方法。
- 2,2′−ビピリジン系配位子(A)化合物は、4,4′−位置の置換基により相違する2種(A1 ,A2 )または3種(A1 ,A2 ,A3)のものとする請求項1または2の製造方法。
- 2種(A1 ,A2 )または3種(A1 ,A2 ,A3 )の2,2′−ビピリジン系配位子化合物は、各々、異なる反応段階で添加反応させる請求項3の製造方法。
- 2種(A1 ,A2 )または3種(A1 ,A2 ,A3 )の2,2′−ビピリジン系配位子のうちの少くとも1種のものは、4,4′−位置に、キラルな置換基を有している請求項3または4の製造方法。
- 次式(1)(2)(3)(4);
〔Ru(A1 )3 〕2+ (1)
〔Ru(A1 )2 A2 〕2+ (2)
〔Ru(A1 )(A2 )2 〕2+ (3)
〔Ru(A1 )(A2 )(A3 )〕2+ (4)
(Ruはルテニウムを示し、A1 ,A2 およびA3 は、置換基により各々相違する2,2′−ビピリジン系配位子を示し、少くともA1 の置換基はアミド基またはエステル基であるキラルな置換基であって、A2 およびA3 の一方もしくは両方の置換基もアミド基またはエステル基であるキラルな置換基であってもよいことを示す。)のうちのいずれかで表わされるカチオンの錯体であることを特徴とするキラル金属錯体。 - 前記アミド基またはエステル基であるキラルな置換基が、2,2′−ビピリジン系配位子の4,4′−位置に置換されている、請求項6のキラル金属錯体。
- 請求項7のキラル金属錯体が次式(5)
[Ru( dmbpy )( Sestbpy )( Rambpy )] 2+ (5)
(ただし、Ruはルテニウムを、 dmbpy は4,4′−ジメチル−2,2′−ビピリジンを、 Sestbpy は4,4′−ビス((S)−(−)−α−フェニルエチルオキシカルボニル)−2,2′−ビピリジンを、 Rambpy は4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(6)
[Ru( dmbpy )( Restbpy )( Rambpy )] 2+ (6)
(ただし、Ruはルテニウムを、 dmbpy は4,4′−ジメチル−2,2′−ビピリジンを、 Restbpy は4,4′−ビス((R)−(+)−α−フェニルエチルオキシカルボニル−2,2′−ビピリジンを、 Rambpy は4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(7)
[Ru( Sambpy ) 2 ( bpy )] 2+ (7)
(ただし、Ruはルテニウムを、 Sambpy は4,4′−ビス((S)−(−)−α−フェニルエチルアミド)−2,2′−ビピリジンを、 bpy は2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(8)
[Ru( Rambpy ) 2 ( bpy )] 2+ (8)
(ただし、Ruはルテニウムを、 Rambpy は4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジンを、 bpy は2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(9)
[Ru( Sambpy ) 2 ( dmbpy )] 2+ (9)
(Ruはルテニウムを、 Sambpy は4,4′−ビス((S)−(−)−α−フェニルエチルアミド)−2,2′−ビピリジン、 dmbpy は4,4′−ジメチル−2,2′−ビリピジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(10)
[Ru( Rambpy ) 2 ( bpy )] 2+ (10)
(Ruはルテニウムを、 Rambpy は4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジンを、 bpy は2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(11)
[Ru( Sestbpy ) 2 ( Sambpy )] 2+ (11)
(Ruはルテニウムを、 Sestbpy は4,4′−ビス((S)−(−)−α−フェニルエチルオキシカルボニル)−2,2′−ビピリジンを、 Sambpy は4,4′−ビス((S)−(−)−α−フェニルエチルアミド)−2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(12)
[Ru( Restbpy ) 2 ( Rambpy )] 2+ (12)
(Ruはルテニウムを、 Restbpy は4,4′−ビス((R)−(+)−α−フェニルエチルオキシカルボニル)−2,2′−ビピリジンを、 Rambpy は4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(13)
[Ru( Sambpy ) 3 ] 2+ (13)
(Ruはルテニウムを、 Sambpy は4,4′−ビス((S)−(−)−α−フェニルエチルアミド)−2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。 - 請求項7のキラル金属錯体が次式(14)
[Ru( Rambpy ) 3 ] 2+ (14)
(ただし、Ruはルテニウムを、 Rambpy は4,4′−ビス((R)−(+)−α−フェニルエチルアミド)−2,2′−ビピリジンを示す。)
で表わされるキラル金属錯体。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP21468499A JP3750010B2 (ja) | 1999-07-29 | 1999-07-29 | 2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP21468499A JP3750010B2 (ja) | 1999-07-29 | 1999-07-29 | 2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2001039994A JP2001039994A (ja) | 2001-02-13 |
| JP3750010B2 true JP3750010B2 (ja) | 2006-03-01 |
Family
ID=16659882
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP21468499A Expired - Fee Related JP3750010B2 (ja) | 1999-07-29 | 1999-07-29 | 2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体 |
Country Status (1)
| Country | Link |
|---|---|
| JP (1) | JP3750010B2 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP5550238B2 (ja) * | 2009-01-07 | 2014-07-16 | 株式会社豊田中央研究所 | 金属錯体色素及びこれを用いた色素増感型太陽電池 |
-
1999
- 1999-07-29 JP JP21468499A patent/JP3750010B2/ja not_active Expired - Fee Related
Also Published As
| Publication number | Publication date |
|---|---|
| JP2001039994A (ja) | 2001-02-13 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US4994590A (en) | Ruthenium-phoshine complex | |
| US4845124A (en) | Platinum (IV) complexes | |
| JP5207445B2 (ja) | 2−(アミノメチル)ピリジン及びフォスフィンを有するルテニウムの複合体、その調製方法、並びに触媒としての使用 | |
| US5012002A (en) | 2,2'-bis(di-(m-tolyl)phosphino)-1,1'-binaphthyl | |
| US20100076210A1 (en) | Method for producing a ruthenium complex | |
| JP2681057B2 (ja) | 2,2’―ビス(ジフェニルホスフィノ)―5,5’,6,6’,7,7’,8,8’―オクタヒドロ―1,1’―ビナフチル及びこれを配位子とする遷移金属錯体 | |
| Sato et al. | Pd (BF4) 2 complexes of 1, 1′-bis (alkyl-or aryl-) thio]-and 1, 1′-bis (diphenylphosphino)-ferrocenes. Bond formation between the Fe and Pd atoms | |
| Yap et al. | Development of a novel chiral palladacycle and its application in asymmetric hydrophosphination reaction | |
| US4705895A (en) | 5,5'-diamino or 5,5'-diacetamido-2,2'-bis(diphenylphosphino)-1,1'-binaphthyls | |
| JP2003252884A (ja) | 新規ルテニウム錯体およびこれを触媒として用いるアルコール化合物の製造方法 | |
| JP3750010B2 (ja) | 2,2′−ビピリジン系配位子金属錯体の製造方法とキラル金属錯体 | |
| JP6923542B2 (ja) | モノカルボニルルテニウム触媒及びモノカルボニルオスミウム触媒 | |
| Matsushima et al. | Synthesis and Properties of Planar-Chiral (η 6-Benzene)(η 5-cyclopentadienyl) ruthenium (II) Complexes in an Optically Pure Form | |
| Brunner et al. | Optically active transition metal complexes. Part 117: Synthesis, crystal structure and properties of chiral (η6-arene) ruthenium complexes with N, O-and N, N-ligands | |
| CN112694489B (zh) | N-杂环卡宾铜催化剂的制备方法 | |
| US5648548A (en) | Optically active asymmetric diphosphine and process for producing optically active substance in its presence | |
| JP2003535869A (ja) | 不斉触媒用キラル配位子 | |
| JP5252921B2 (ja) | ジホスフィン配位子およびそれを用いた遷移金属錯体 | |
| US20030078416A1 (en) | Substituted phenanthrolines | |
| US5808162A (en) | Chiral unsymmetric diphosphine compound and transition metal complex containing the same as ligand | |
| JPH04120085A (ja) | ポルフイリン誘導体 | |
| JP3864297B2 (ja) | 金属錯体の製造方法 | |
| JP3750011B2 (ja) | 金属錯体の製造方法とアミノ酸修飾金属錯体 | |
| Mary et al. | Ruthenium (II) complexes of a new tetrapyrazolic macrocycle | |
| Gobetto et al. | [Os3 (H) 2 (CO) 10] derivatives containing the short bite ligands bis (diphenylphosphino) methane and 2-(diphenylphosphino) pyridine |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20050720 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20050809 |
|
| A521 | Written amendment |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20051006 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20051109 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20051121 |
|
| R150 | Certificate of patent or registration of utility model |
Free format text: JAPANESE INTERMEDIATE CODE: R150 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20091216 Year of fee payment: 4 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20101216 Year of fee payment: 5 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20111216 Year of fee payment: 6 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121216 Year of fee payment: 7 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20121216 Year of fee payment: 7 |
|
| FPAY | Renewal fee payment (event date is renewal date of database) |
Free format text: PAYMENT UNTIL: 20131216 Year of fee payment: 8 |
|
| LAPS | Cancellation because of no payment of annual fees |