JP7093473B2 - Small tablets with excellent manufacturability and elution - Google Patents
Small tablets with excellent manufacturability and elution Download PDFInfo
- Publication number
- JP7093473B2 JP7093473B2 JP2021564057A JP2021564057A JP7093473B2 JP 7093473 B2 JP7093473 B2 JP 7093473B2 JP 2021564057 A JP2021564057 A JP 2021564057A JP 2021564057 A JP2021564057 A JP 2021564057A JP 7093473 B2 JP7093473 B2 JP 7093473B2
- Authority
- JP
- Japan
- Prior art keywords
- imeglimin
- hydrochloride
- less
- tablet according
- tablet
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/53—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with three nitrogens as the only ring hetero atoms, e.g. chlorazanil, melamine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/36—Polysaccharides; Derivatives thereof, e.g. gums, starch, alginate, dextrin, hyaluronic acid, chitosan, inulin, agar or pectin
- A61K47/38—Cellulose; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/2027—Organic macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyvinyl pyrrolidone, poly(meth)acrylates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/28—Dragees; Coated pills or tablets, e.g. with film or compression coating
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Diabetes (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Endocrinology (AREA)
- Emergency Medicine (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Medicinal Preparation (AREA)
- Semiconductor Lasers (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Description
本発明は、イメグリミンまたはその薬学的に許容される塩を含む医薬品組成物であって、製造性及び溶出性に優れた小型錠剤に関する。 The present invention relates to a pharmaceutical composition containing imeglimin or a pharmaceutically acceptable salt thereof, which is a small tablet having excellent manufacturability and elution.
糖尿病は世界中で多くの患者が存在し、2017年のIDF(International Diabetes Federation/国際糖尿病連合)の発表では、現在、世界の成人の11人に1人が糖尿病患者で、2015年の総患者数より1000万人増加して4億2500万人となり、2045年までに約7億人に増加するとの予測を示した。日本では、特に、糖尿病患者はほとんど2型糖尿病患者であり、316万6000人の糖尿病患者がいるとされている。 There are many patients with diabetes all over the world, and according to the 2017 IDF (International Diabetes Federation) announcement, one in 11 adults in the world is currently diabetic, and the total number of patients in 2015. The number will increase by 10 million to 425 million, and is expected to increase to about 700 million by 2045. In Japan, in particular, most diabetic patients are type 2 diabetic patients, and it is estimated that there are 3,166,000 diabetic patients.
イメグリミンは糖尿病治療薬として広く知られており、2型糖尿病の治療に使用されているが、1日200~4000mgと多量経口投与する必要があり(特許文献1)、その経口投与の方法に課題があった。 Imeglimin is widely known as a therapeutic agent for diabetes and is used for the treatment of type 2 diabetes. However, it is necessary to orally administer a large amount of 200 to 4000 mg daily (Patent Document 1), and there is a problem in the method of oral administration thereof. was there.
特許文献1にはイメグリミンの経口投与製剤として、イメグリミン含有割合が83.4%のフィルムコーティング錠が開示されているが、その具体的な製造方法は開示されていない。また、特許文献2にはイメグリミンの経口投与製剤として、処方成分を混合・打錠する直接打錠法を用い、1kgスケールで製造された、イメグリミン含有割合が87.0%の錠剤が開示されている。しかし、直接打錠法は小スケールでの製造は容易であるが、製造スケールが上がると打錠時の粉体圧縮時間が減少し、薬物の圧縮成形性が悪い場合は、打錠障害などが発生し、打錠が困難になることがある。したがって、イメグリミンの経口錠剤を大スケールで安定的に製造できる方法は実質的に知られていなかった。 Patent Document 1 discloses a film-coated tablet having an imeglimin content of 83.4% as an orally-administered preparation of imeglimin, but does not disclose a specific production method thereof. Further, Patent Document 2 discloses a tablet having an imeglimin content of 87.0%, which is produced on a 1 kg scale by using a direct tableting method in which a prescription component is mixed and tableted as an orally administered preparation of imeglimin. There is. However, although the direct tableting method is easy to manufacture on a small scale, the powder compression time during tableting decreases as the manufacturing scale increases, and if the drug's compression moldability is poor, tableting problems may occur. It may occur and it may be difficult to lock. Therefore, a method capable of stably producing an oral tablet of imeglimin on a large scale has not been substantially known.
本発明の課題は、1日当たりの用量が非常に多いイメグリミンの投与にあたり、1錠あたりに高含量のイメグリミンを含有し、且つ溶出性に優れた小型化された錠剤、およびその安定供給可能な製造方法を提供することにある。 The subject of the present invention is a miniaturized tablet containing a high content of imeglimin per tablet and having excellent elution in the administration of imeglimin having a very large daily dose, and production thereof that can be stably supplied. To provide a method.
本発明者らは、鋭意検討を行った結果、崩壊剤を用い、更に水溶性結合剤として高割合のヒドロキシプロピルセルロース、ポリビニルアルコールまたは/およびヒドロキシプロピルメチルセルロースを用いることにより、優れた溶出性を示し、かつ非常に小型化されたイメグリミンの錠剤が安定的に生産できることを見出した。また、その製造方法として流動層造粒法を用いることを見出した。 As a result of diligent studies, the present inventors showed excellent elution by using a disintegrant and a high proportion of hydroxypropyl cellulose, polyvinyl alcohol or / and hydroxypropylmethyl cellulose as a water-soluble binder. Moreover, it was found that a very miniaturized imeglimin tablet can be stably produced. It was also found that the fluidized bed granulation method is used as the production method.
すなわち、本発明は以下の通りである。 That is, the present invention is as follows.
[項1]
(1)イメグリミンまたはその薬学的に許容される塩を84~95wt%、(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤、及び(3)崩壊剤を含有する錠剤。[Item 1]
One or more binders selected from the group consisting of (1) imeglimin or a pharmaceutically acceptable salt thereof in an amount of 84 to 95 wt%, (2) hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose, and a binder thereof. (3) Tablets containing a disintegrant.
[項2]
(1)イメグリミンまたはその薬学的に許容される塩を88~95wt%含有する、項1に記載の錠剤。
または
[項2’]
(1)イメグリミンまたはその薬学的に許容される塩を88~95wt%、(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤、及び(3)崩壊剤を含有する錠剤。[Item 2]
(1) The tablet according to Item 1, which contains 88 to 95 wt% of imeglimin or a pharmaceutically acceptable salt thereof.
Or [Item 2']
One or more binders selected from the group consisting of (1) imeglimin or a pharmaceutically acceptable salt thereof in an amount of 88 to 95 wt%, (2) hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose, and a binder thereof. (3) Tablets containing a disintegrant.
[項3]
(1)イメグリミンまたはその薬学的に許容される塩を90~95wt%含有する、項1に記載の錠剤。[Item 3]
(1) The tablet according to Item 1, which contains 90 to 95 wt% of imeglimin or a pharmaceutically acceptable salt thereof.
[項4]
(1)イメグリミンまたはその薬学的に許容される塩を90~92wt%含有する、項1または2に記載の錠剤。[Item 4]
(1) The tablet according to Item 1 or 2, which contains 90 to 92 wt% of imeglimin or a pharmaceutically acceptable salt thereof.
[項5]
(3)崩壊剤を0.2~7.5wt%含有する、項1又は2に記載の錠剤。[Item 5]
(3) The tablet according to Item 1 or 2, which contains 0.2 to 7.5 wt% of a disintegrant.
[項6]
(3)崩壊剤を0.2~5.0wt%含有する、項1~5のいずれか一項に記載の錠剤。[Item 6]
(3) The tablet according to any one of Items 1 to 5, which contains 0.2 to 5.0 wt% of a disintegrant.
[項7]
(3)崩壊剤を0.2~4.0wt%含有する、項1~6のいずれか一項に記載の錠剤。[Item 7]
(3) The tablet according to any one of Items 1 to 6, which contains 0.2 to 4.0 wt% of a disintegrant.
[項8]
(3)崩壊剤を0.2~3.0wt%含有する、項1~7のいずれか一項に記載の錠剤。[Item 8]
(3) The tablet according to any one of Items 1 to 7, which contains 0.2 to 3.0 wt% of a disintegrant.
[項9]
(3)崩壊剤を0.2~2.0wt%含有する、項1~8のいずれか一項に記載の錠剤。[Item 9]
(3) The tablet according to any one of Items 1 to 8, which contains 0.2 to 2.0 wt% of a disintegrant.
[項10]
(3)崩壊剤を0.5~7.5wt%含有する、項1又は2に記載の錠剤。[Item 10]
(3) The tablet according to Item 1 or 2, which contains 0.5 to 7.5 wt% of a disintegrant.
[項11]
(3)崩壊剤を0.5~5.0wt%含有する、項1~4、10のいずれか一項に記載の錠剤。[Item 11]
(3) The tablet according to any one of Items 1 to 4 and 10, which contains 0.5 to 5.0 wt% of a disintegrant.
[項12]
(3)崩壊剤を0.5~4.0wt%含有する、項1~4、10、11のいずれか一項に記載の錠剤。[Item 12]
(3) The tablet according to any one of Items 1 to 4, 10 and 11, which contains 0.5 to 4.0 wt% of a disintegrant.
[項13]
(3)崩壊剤を0.5~3.0wt%含有する、項1~4、10~12のいずれか一項に記載の錠剤。[Item 13]
(3) The tablet according to any one of Items 1 to 4, 10 to 12, which contains 0.5 to 3.0 wt% of a disintegrant.
[項14]
(3)崩壊剤を0.5~2.0wt%含有する、項1~4、10~13のいずれか一項に記載の錠剤。[Item 14]
(3) The tablet according to any one of Items 1 to 4, 10 to 13, which contains 0.5 to 2.0 wt% of a disintegrant.
[項15]
(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤を4.5~7.0wt%を含有する項1~14のいずれか一項に記載の錠剤。[Item 15]
(2) Any one of Items 1 to 14 containing 4.5 to 7.0 wt% of one or more binders selected from the group consisting of hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose. The tablets described in.
[項16]
(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤を4.5~6.0wt%を含有する項1~15のいずれか一項に記載の錠剤。[Item 16]
(2) Any one of Items 1 to 15 containing 4.5 to 6.0 wt% of one or more binders selected from the group consisting of hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose. The tablets described in.
[項17]
(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤を4.5~5.5wt%を含有する項1~16のいずれか一項に記載の錠剤。[Item 17]
(2) Any one of Items 1 to 16 containing 4.5 to 5.5 wt% of one or more binders selected from the group consisting of hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose. The tablets described in.
[項18]
(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤を4.8~5.5wt%を含有する項1~17のいずれか一項に記載の錠剤。[Item 18]
(2) Item 1 to Item 17 containing 4.8 to 5.5 wt% of one or more binders selected from the group consisting of hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose. The tablets described in.
[項19]
ヒドロキシプロピルセルロースの粘度が2.0~400mPa・sである項1~18のいずれか一項に記載の錠剤。[Item 19]
Item 6. The tablet according to any one of Items 1 to 18, wherein the hydroxypropyl cellulose has a viscosity of 2.0 to 400 mPa · s.
[項20]
ヒドロキシプロピルセルロースの粘度が6.0~400mPa・sである項1~19のいずれか一項に記載の錠剤。[Item 20]
Item 6. The tablet according to any one of Items 1 to 19, wherein the hydroxypropyl cellulose has a viscosity of 6.0 to 400 mPa · s.
[項21]
ポリビニルアルコールの粘度が3.4~9.2mPa・sである項1~20のいずれか一項に記載の錠剤。[Item 21]
Item 6. The tablet according to any one of Items 1 to 20, wherein the polyvinyl alcohol has a viscosity of 3.4 to 9.2 mPa · s.
[項22]
ポリビニルアルコールの粘度が4.3~5.8mPa・sである項1~21のいずれか一項に記載の錠剤。[Item 22]
Item 6. The tablet according to any one of Items 1 to 21, wherein the polyvinyl alcohol has a viscosity of 4.3 to 5.8 mPa · s.
[項23]
ヒドロキシプロピルメチルセルロースの粘度が4.0~12.0mPa・sである項1~22のいずれか一項に記載の錠剤。[Item 23]
Item 6. The tablet according to any one of Items 1 to 22, wherein the viscosity of hydroxypropylmethyl cellulose is 4.0 to 12.0 mPa · s.
[項24]
ヒドロキシプロピルメチルセルロースの粘度が4.0~6.0mPa・sである項1~23のいずれか一項に記載の錠剤。[Item 24]
Item 6. The tablet according to any one of Items 1 to 23, wherein the viscosity of hydroxypropylmethyl cellulose is 4.0 to 6.0 mPa · s.
[項25]
ヒドロキシプロピルメチルセルロースの粘度が4.5~6.0mPa・sである項1~24のいずれか一項に記載の錠剤。[Item 25]
Item 6. The tablet according to any one of Items 1 to 24, wherein the viscosity of hydroxypropylmethyl cellulose is 4.5 to 6.0 mPa · s.
[項26]
2.0~2.9mPa・sの粘度を示すヒドロキシプロピルセルロースが3.5wt%以下、および150~400mPa・sのヒドロキシプロピルセルロースが1.5wt%以下の範囲で含まれる、項1~19、21~25のいずれか一項に記載の錠剤。[Item 26]
Items 1 to 19 contain hydroxypropyl cellulose having a viscosity of 2.0 to 2.9 mPa · s in the range of 3.5 wt% or less and hydroxypropyl cellulose having a viscosity of 150 to 400 mPa · s in the range of 1.5 wt% or less. The tablet according to any one of 21 to 25.
[項27]
(2)結合剤がヒドロキシプロピルセルロース及びポリビニルアルコールからなる群から選択される1種または2種である、項1~22、26のいずれか一項に記載の錠剤。[Item 27]
(2) The tablet according to any one of Items 1 to 22, 26, wherein the binder is one or two selected from the group consisting of hydroxypropyl cellulose and polyvinyl alcohol.
[項28]
(2)結合剤がヒドロキシプロピルセルロース及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種である、項1~20、23~26のいずれかの一項に記載の錠剤。[Item 28]
(2) The tablet according to any one of Items 1 to 20 and 23 to 26, wherein the binder is one or two selected from the group consisting of hydroxypropyl cellulose and hydroxypropyl methyl cellulose.
[項29]
(2)結合剤がヒドロキシプロピルセルロースである、項1~20、26~28のいずれかの一項に記載の錠剤。[Item 29]
(2) The tablet according to any one of Items 1 to 20 and 26 to 28, wherein the binder is hydroxypropyl cellulose.
[項30]
(3)崩壊剤がクロスカルメロースナトリウム、デンプングリコール酸ナトリウム及びクロスポピドンからなる群から選択される1種または2種以上である、項1~29のいずれか一項に記載の錠剤。[Item 30]
(3) The tablet according to any one of Items 1 to 29, wherein the disintegrant is one or more selected from the group consisting of sodium croscarmellose, sodium starch glycolate and crospopidone.
[項31]
(3)崩壊剤がクロスカルメロースナトリウムである、項1~30のいずれか一項に記載の錠剤。[Item 31]
(3) The tablet according to any one of Items 1 to 30, wherein the disintegrant is croscarmellose sodium.
[項32]
流動層造粒法を用いて製造される、項1~31のいずれか一項に記載の錠剤。[Item 32]
Item 2. The tablet according to any one of Items 1 to 31, which is produced by using a fluidized bed granulation method.
[項33]
流動層造粒法を用いて製造される、項1~31のいずれか一項に記載の錠剤の製造方法。[Item 33]
Item 6. The method for producing a tablet according to any one of Items 1 to 31, which is produced by using a fluidized bed granulation method.
[項34]
流動層造粒法を用いて製造される、項1~18のいずれか一項に記載の錠剤。[Item 34]
Item 6. The tablet according to any one of Items 1 to 18, which is produced by using a fluidized bed granulation method.
[項35]
流動層造粒法を用いて製造される、項1~18のいずれか一項に記載の錠剤の製造方法。[Item 35]
Item 6. The method for producing a tablet according to any one of Items 1 to 18, which is produced by using a fluidized bed granulation method.
[項36]
(1)イメグリミンまたはその薬学的に許容される塩、(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤、及び(3)崩壊剤を含有する造粒顆粒を、流動層造粒法を用いて製造する工程を含む、項35に記載の、錠剤の製造方法。[Item 36]
(1) Imeglycin or a pharmaceutically acceptable salt thereof, (2) one or more binders selected from the group consisting of hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose, and (3) disintegrant. Item 3. The method for producing a tablet according to Item 35, which comprises a step of producing granulated granules containing the above-mentioned granules by using a fluidized bed granulation method.
[項37]
(1)イメグリミンまたはその薬学的に許容される塩及び(3)崩壊剤を含有する粉末に、(2)ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上の結合剤を添加し、流動層造粒法を用いて、製造する工程を含む、項36に記載の、錠剤の製造方法。[Item 37]
One or two selected from the group consisting of (2) hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose in a powder containing (1) imeglycin or a pharmaceutically acceptable salt thereof and (3) a disintegrant. Item 3. The method for producing a tablet according to Item 36, which comprises a step of adding the above binder and producing by using a fluidized layer granulation method.
[項38]
さらに打錠工程またはフィルムコーティング工程を含む、項36または37に記載の製造方法。[Item 38]
Item 6. The production method according to Item 36 or 37, further comprising a tableting step or a film coating step.
[項39]
流動層造粒工程、打錠工程またはフィルムコーティング工程のいずれかの工程を10kg以上の製造量で製造する、項38に記載の製造方法。[Item 39]
Item 38. The production method according to Item 38, wherein any of the fluidized bed granulation step, the tableting step, and the film coating step is manufactured with a production amount of 10 kg or more.
[項40]
流動層造粒工程、打錠工程またはフィルムコーティング工程のいずれかの工程を30kg以上の製造量で製造する、項38に記載の製造方法。[Item 40]
Item 38. The production method according to Item 38, wherein any of the fluidized bed granulation step, the tableting step, and the film coating step is manufactured with a production amount of 30 kg or more.
[項41]
流動層造粒工程、打錠工程またはフィルムコーティング工程のいずれかの工程を50kg以上の製造量で製造する、項38に記載の製造方法。[Item 41]
Item 38. The production method according to Item 38, wherein any of the fluidized bed granulation step, the tableting step, and the film coating step is manufactured with a production amount of 50 kg or more.
本発明におけるイメグリミン組成物は、崩壊剤を用い、更に結合剤としてヒドロキシプロピルセルロース、ポリビニルアルコールまたは/およびヒドロキシプロピルメチルセルロースを多く用いて、流動層造粒法で製造することにより、圧縮成形性が悪いイメグリミンの含有割合が非常に高いにもかかわらず、生産スケールでの安定供給可能な製造性を有する。また、本発明におけるイメグリミン組成物は溶出性が良好であり、生物学的利用能(Bioavailability)に優れた経口製剤を提供することが可能となる。さらに、本発明におけるイメグリミン組成物は、イメグリミンの含有割合が非常に高いことで、服薬が継続しやすい小型化された錠剤を提供することができる。 The imeglimin composition in the present invention has poor compression moldability by being produced by a fluidized bed granulation method using a disintegrant and a large amount of hydroxypropyl cellulose, polyvinyl alcohol or / and hydroxypropyl methyl cellulose as a binder. Despite the extremely high content of imeglimin, it has manufacturability that enables stable supply on a production scale. In addition, the imeglimin composition in the present invention has good dissolution property, and it is possible to provide an oral preparation having excellent bioavailability. Furthermore, the imeglimin composition in the present invention has a very high content of imeglimin, so that it is possible to provide a miniaturized tablet that can be easily taken.
以下、本発明につき、さらに詳しく説明する。 Hereinafter, the present invention will be described in more detail.
(a)錠剤
本発明の錠剤は、素錠、素錠の表面にフィルムコートを施したフィルムコート錠(本明細書において、FC錠と記載することもある)、素錠の表面に糖衣を施した糖衣錠のような形態を含み、好ましくは素錠またはフィルムコート錠である。当該素錠は、イメグリミン含有組成物を含み、さらには本発明の機能を失わない程度に、他の添加剤を任意に含んでもよい。当該イメグリミン含有組成物は、(1)イメグリミンまたはその薬学的に許容される塩、(2)水溶性高分子結合剤として、ヒドロキシプロピルセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上、(3)崩壊剤を含み、また、賦形剤および滑沢剤を任意に含んでいてもよく、さらには本発明の機能を失わない程度に他の添加剤を任意に含んでいてもよい。当該フィルムコートはフィルムコート剤を含み、さらには本発明の機能を失わない程度に他の添加剤を任意に含んでもよい。 (A) Tablets The tablets of the present invention are uncoated tablets, film-coated tablets in which the surface of the uncoated tablets is coated with a film (sometimes referred to as FC tablets in the present specification), and the surface of the uncoated tablets is coated with sugar. It contains a sugar-coated tablet-like form, and is preferably an uncoated tablet or a film-coated tablet. The uncoated tablet contains an imeglimin-containing composition, and may optionally contain other additives to the extent that the function of the present invention is not lost. The imeglimin-containing composition is selected from the group consisting of (1) imeglimin or a pharmaceutically acceptable salt thereof, and (2) hydroxypropyl cellulose, polyvinyl alcohol and hydroxypropyl methyl cellulose as a water-soluble polymer binder 1). Seeds or two or more, (3) containing disintegrants, optionally containing excipients and lubricants, and optionally other additives to the extent that they do not impair the functionality of the invention. It may be included. The film coating contains a film coating agent, and may optionally contain other additives to the extent that the function of the present invention is not lost.
(b)イメグリミン
本発明における「イメグリミン」とは、糖尿病治療薬として知られている化合物であって、化学名は(6R)-N2,N2,6-トリメチル-3,6-ジヒドロ-1,3,5-トリアジン-2,4-ジアミン(CAS登録番号:775351-65-0)であり、以下の化学構造を有する。また、「イメグリミン」は(6S)-N2,N2,6-トリメチル-3,6-ジヒドロ-1,3,5-トリアジン-2,4-ジアミン(CAS登録番号:1251468―04―8)も含む。
本発明においては、イメグリミンの全ての形態(例えば、互変異性体、非晶質、結晶性、様々な結晶多形など)を包含し、その光学異性体またはその混合物を包含する。当該混合物のR体は、好ましくは、90wt%以上、95wt%以上、97wt%以上、99wt%以上含まれる。
本発明に用いられるイメグリミンは、必要に応じ、所望の粒子径に粉砕してもよい。体積比による平均粒子径(50%粒子径,D50)としては、例えば11~274μm、好ましくは11μm~169μmの範囲が挙げられる。The present invention includes all forms of imeglimin (eg, tautomers, amorphous, crystalline, various crystalline polymorphs, etc.), including optical isomers thereof or mixtures thereof. The R-form of the mixture is preferably contained in an amount of 90 wt% or more, 95 wt% or more, 97 wt% or more, and 99 wt% or more.
The imeglimin used in the present invention may be pulverized to a desired particle size, if necessary. The average particle size (50% particle size, D50) based on the volume ratio may be, for example, in the range of 11 to 274 μm, preferably 11 μm to 169 μm.
本発明の錠剤におけるイメグリミンの構成比としては、84wt%以上、好ましくは88wt%以上、90wt%以上である。本発明におけるイメグリミンの構成比としては、好ましくは90wt%以下、92wt%以下、95wt%以下である。また、本発明の錠剤における、1錠中に含まれるイメグリミンまたはその薬学的に許容される塩の含量としては、500mgが好ましい。 The composition ratio of imeglimin in the tablet of the present invention is 84 wt% or more, preferably 88 wt% or more, and 90 wt% or more. The composition ratio of imeglimin in the present invention is preferably 90 wt% or less, 92 wt% or less, and 95 wt% or less. The content of imeglimin or a pharmaceutically acceptable salt thereof contained in one tablet of the tablet of the present invention is preferably 500 mg.
イメグリミンの薬学的に許容される塩として、酸付加塩が挙げられるがこれに限られない。酸付加塩としては、例えば、塩酸塩、臭化水素酸塩、硫酸塩、ヨウ化水素酸塩、硝酸塩、リン酸塩等の無機酸塩、又はクエン酸塩、シュウ酸塩、フタル酸塩、フマル酸塩、マレイン酸塩、コハク酸塩、リンゴ酸塩、酢酸塩、ギ酸塩、プロピオン酸塩、安息香酸塩、トリフルオロ酢酸塩、メタンスルホン酸塩、ベンゼンスルホン酸塩、para-トルエンスルホン酸塩、カンファースルホン酸塩等の有機酸塩が挙げられ、さらには酸性アミノ酸とのアミノ酸塩も挙げられる。イメグリミンの薬学的に許容される塩として、好ましくは、塩酸塩である。 Pharmaceutically acceptable salts of imeglimin include, but are not limited to, acid addition salts. Examples of the acid addition salt include inorganic acid salts such as hydrochloride, hydrobromide, sulfate, hydroiodide, nitrate and phosphate, or citrate, oxalate and phthalate. Fumarate, maleate, succinate, malate, acetate, formate, propionate, benzoate, trifluoroacetate, methanesulfonate, benzenesulfonate, para-toluenesulfonic acid Examples thereof include organic acid salts such as salts and camphor sulfonates, and further include amino acid salts with acidic amino acids. The pharmaceutically acceptable salt of imeglimin is preferably hydrochloride.
(c)ヒドロキシプロピルセルロース
本発明におけるヒドロキシプロピルセルロースの粘度は、特に限定されないが、2.0~400mPa・sを有し、好ましくは6.0~400mPa・sを有する。
また、本発明の錠剤におけるヒドロキシプロピルセルロースの構成比は、特に限定されないが、2.0~2.9mPa・sの粘度を示すヒドロキシプロピルセルロースを3.5wt%以下及び、150~400mPa・sのヒドロキシプロピルセルロースを1.5wt%以下の範囲で含むことが好ましい。
ヒドロキシプロピルセルロースは、好ましくは4.5wt%以上、4.6wt%以上、4.7wt%以上、4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ヒドロキシプロピルセルロースは、好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下、5.6wt以下%、5.7wt%以下、5.8wt%以下、5.9wt%以下、6.0wt%以下、6.1wt%以下、6.2wt%以下、6.3wt%以下、6.4wt%以下、6.5wt%以下、6.6wt%以下、6.7wt%以下、6.8wt%以下、6.9wt%以下、7.0wt%以下含まれる。
ヒドロキシプロピルセルロースは、さらに好ましくは4.6wt%以上、4.7wt%以上、4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ヒドロキシプロピルセルロースは、さらに好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下、5.6wt以下%、5.7wt%以下、5.8wt%以下、5.9wt%以下、6.0wt%以下含まれる。
ヒドロキシプロピルセルロースは、最も好ましくは4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ヒドロキシプロピルセルロースは、最も好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下含まれる。 (C) Hydroxypropyl Cellulose The viscosity of hydroxypropyl cellulose in the present invention is not particularly limited, but has 2.0 to 400 mPa · s, preferably 6.0 to 400 mPa · s.
The composition ratio of hydroxypropyl cellulose in the tablet of the present invention is not particularly limited, but hydroxypropyl cellulose having a viscosity of 2.0 to 2.9 mPa · s is 3.5 wt% or less and 150 to 400 mPa · s. It is preferable to contain hydroxypropyl cellulose in the range of 1.5 wt% or less.
Hydroxypropyl cellulose is preferably contained in an amount of 4.5 wt% or more, 4.6 wt% or more, 4.7 wt% or more, 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. Hydroxypropyl cellulose is preferably 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, 5.5 wt% or less, 5.6 wt% or less%, 5 7.7 wt% or less, 5.8 wt% or less, 5.9 wt% or less, 6.0 wt% or less, 6.1 wt% or less, 6.2 wt% or less, 6.3 wt% or less, 6.4 wt% or less, 6.5 wt % Or less, 6.6 wt% or less, 6.7 wt% or less, 6.8 wt% or less, 6.9 wt% or less, 7.0 wt% or less.
Hydroxypropyl cellulose is more preferably contained in an amount of 4.6 wt% or more, 4.7 wt% or more, 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. Hydroxypropyl cellulose is more preferably 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, 5.5 wt% or less, 5.6 wt% or less, It includes 5.7 wt% or less, 5.8 wt% or less, 5.9 wt% or less, and 6.0 wt% or less.
Hydroxypropyl cellulose is most preferably contained in an amount of 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. Hydroxypropyl cellulose is most preferably contained in an amount of 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, and 5.5 wt% or less.
(d)ポリビニルアルコール(ポリビニルアルコール系樹脂)
本発明におけるポリビニルアルコールはポリビニルアルコール系樹脂であり、ポリビニルアルコール誘導体を含む。好ましくはポリビニルアルコール(PVA)である。特に限定されるものではないが、ポリビニルアルコール(PVA)は部分けん化物を用いることが好ましい。なお。けん化度が97mol%以上を完全けん化物、けん化度が79から96mol%は部分けん化物と呼ばれる。
本発明におけるポリビニルアルコールは、特に限定されないが、3.4~9.2mPa・sを有し、好ましくは4.3~5.8mPa・s、より好ましくは4.8~5.8mPa・sを有する。
本発明の錠剤におけるポリビニルアルコールは、例えば、好ましくは4.5wt%以上、4.6wt%以上、4.7wt%以上、4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ポリビニルアルコールは、好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%、5.6wt%以下、5.7wt%以下、5.8wt%以下、5.9wt%以下、6.0wt%以下、6.1wt%以下、6.2wt%以下、6.3wt%以下、6.4wt%以下、6.5wt%以下、6.6wt%以下、6.7wt%以下、6.8wt%以下、6.9wt%以下、7.0wt%以下含まれる。
ポリビニルアルコールは、さらに好ましくは4.6wt%以上、4.7wt%以上、4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ポリビニルアルコールは、さらに好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下、5.6wt以下%、5.7wt%以下、5.8wt%以下、5.9wt%以下、6.0wt%以下含まれる。
ポリビニルアルコールは、最も好ましくは4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ポリビニルアルコールは、最も好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下含まれる。
本発明におけるポリビニルアルコール系樹脂は、例えば、ポリビニルアルコール・アクリル酸・メタクリル酸メチル共重合体、ポリビニルアルコール・ポリエチレングリコールグラフトコポリマー等も含む。 (D) Polyvinyl alcohol (polyvinyl alcohol-based resin)
The polyvinyl alcohol in the present invention is a polyvinyl alcohol-based resin and contains a polyvinyl alcohol derivative. It is preferably polyvinyl alcohol (PVA). Although not particularly limited, it is preferable to use a partially saponified product for polyvinyl alcohol (PVA). note that. A saponification degree of 97 mol% or more is called a complete saponification, and a saponification degree of 79 to 96 mol% is called a partial saponification.
The polyvinyl alcohol in the present invention is not particularly limited, but has 3.4 to 9.2 mPa · s, preferably 4.3 to 5.8 mPa · s, and more preferably 4.8 to 5.8 mPa · s. Have.
The polyvinyl alcohol in the tablet of the present invention preferably contains, for example, 4.5 wt% or more, 4.6 wt% or more, 4.7 wt% or more, 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. .. Polyvinyl alcohol is preferably 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, 5.5 wt%, 5.6 wt% or less, 5.7 wt. % Or less, 5.8 wt% or less, 5.9 wt% or less, 6.0 wt% or less, 6.1 wt% or less, 6.2 wt% or less, 6.3 wt% or less, 6.4 wt% or less, 6.5 wt% or less , 6.6 wt% or less, 6.7 wt% or less, 6.8 wt% or less, 6.9 wt% or less, 7.0 wt% or less.
Polyvinyl alcohol is more preferably contained in an amount of 4.6 wt% or more, 4.7 wt% or more, 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. Polyvinyl alcohol is more preferably 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, 5.5 wt% or less, 5.6 wt% or less%, 5 It includes 7.7 wt% or less, 5.8 wt% or less, 5.9 wt% or less, and 6.0 wt% or less.
Polyvinyl alcohol is most preferably contained in an amount of 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. Polyvinyl alcohol is most preferably contained in an amount of 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, and 5.5 wt% or less.
The polyvinyl alcohol-based resin in the present invention also includes, for example, polyvinyl alcohol / acrylic acid / methyl methacrylate copolymer, polyvinyl alcohol / polyethylene glycol graft copolymer and the like.
(e)ヒドロキシプロピルメチルセルロース
本発明におけるヒドロキシプロピルメチルセルロースの粘度は、特に限定されないが、4.0~12.0mPa・sを有し、好ましくは4.0~6.0mPa・sより好ましくは4.5~6.0mPa・sを有する。
本発明の錠剤におけるヒドロキシプロピルメチルセルロースは、好ましくは4.5wt%以上、4.6wt%以上、4.7wt%以上、4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ヒドロキシプロピルメチルセルロースは、好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下、5.6wt%以下、5.7wt%以下、5.8wt%以下、5.9wt%以下、6.0wt%以下、6.1wt%以下、6.2wt%以下、6.3wt%以下、6.4wt%以下、6.5wt%以下、6.6wt%以下、6.7wt%以下、6.8wt%以下、6.9wt%以下、7.0wt%以下含まれる。
ヒドロキシプロピルメチルセルロースは、さらに好ましくは4.6wt%以上、4.7wt%以上、4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ヒドロキシプロピルメチルセルロースは、さらに好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下、5.6wt以下%、5.7wt%以下、5.8wt%以下、5.9wt%以下、6.0wt%以下含まれる。
ヒドロキシプロピルメチルセルロースは、最も好ましくは4.8wt%以上、4.9wt%以上、5.0wt%以上含まれる。ヒドロキシプロピルメチルセルロースは、最も好ましくは5.0wt%以下、5.1wt%以下、5.2wt%以下、5.3wt%以下、5.4wt%以下、5.5wt%以下含まれる。 (E) Hydroxypropyl Methyl Cellulose The viscosity of hydroxypropylmethyl cellulose in the present invention is not particularly limited, but has 4.0 to 12.0 mPa · s, and is preferably 4.0 to 6.0 mPa · s. It has 5 to 6.0 mPa · s.
The hydroxypropylmethyl cellulose in the tablet of the present invention preferably contains 4.5 wt% or more, 4.6 wt% or more, 4.7 wt% or more, 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. The hydroxypropylmethyl cellulose is preferably 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, 5.5 wt% or less, 5.6 wt% or less, 5 7.7 wt% or less, 5.8 wt% or less, 5.9 wt% or less, 6.0 wt% or less, 6.1 wt% or less, 6.2 wt% or less, 6.3 wt% or less, 6.4 wt% or less, 6.5 wt % Or less, 6.6 wt% or less, 6.7 wt% or less, 6.8 wt% or less, 6.9 wt% or less, 7.0 wt% or less.
The hydroxypropylmethyl cellulose is more preferably contained in an amount of 4.6 wt% or more, 4.7 wt% or more, 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. The hydroxypropylmethyl cellulose is more preferably 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, 5.5 wt% or less, 5.6 wt% or less, It includes 5.7 wt% or less, 5.8 wt% or less, 5.9 wt% or less, and 6.0 wt% or less.
The hydroxypropylmethyl cellulose is most preferably contained in an amount of 4.8 wt% or more, 4.9 wt% or more, and 5.0 wt% or more. The hydroxypropylmethyl cellulose is most preferably contained in an amount of 5.0 wt% or less, 5.1 wt% or less, 5.2 wt% or less, 5.3 wt% or less, 5.4 wt% or less, and 5.5 wt% or less.
(f)崩壊剤
本発明に用いられる崩壊剤は、湿式造粒時に薬物が水分吸収し溶解または固結することを防ぎ、造粒時に製造装置内で良好な流動性を示すために必要である。錠剤の小型化を達成する為には、錠剤中の含有量が低い場合でも良好な水分吸収性、錠剤化後の崩壊性を示すことが望ましい。
本発明に用いられる崩壊剤としては、特に限定されないが、通常製剤化において用いられる崩壊剤を用いることができる。例えば、デンプン類、低置換度ヒドロキシプロピルセルロース、カルメロース、カルメロースカルシウム、カルメロースナトリウム、クロスポビドン、クロスカルメロースナトリウム、カルボキシメチルスターチナトリウム(デンプングリコール酸ナトリウムとも称される)等が挙げられる。また、崩壊剤は2種以上を用いてもよい。
好ましくはクロスポビドン、クロスカルメロースナトリウム、カルボキシメチルスターチナトリウムであり、より好ましくはクロスカルメロースナトリウムである。本発明の錠剤における崩壊剤は、好ましくは0.1wt%以上、0.2wt%以上、0.5wt%以上、1.0wt%以上、1.5wt%以上含まれる。崩壊剤は、好ましくは7.5wt%以下、7.4wt%以下、7.3wt%以下、7.2wt%以下、7.1wt%以下、7.0wt%以下、6.9wt%以下、6.8wt%以下、6.7wt%以下、6.6wt%以下、6.5wt%以下、6.4wt%以下、6.3wt%以下、6.2wt%以下、6.1wt%以下、6.0wt%以下、5.9wt%以下、5.8wt%以下、5.7wt%以下、5.6wt%以下、5.5wt%以下、5.0wt%以下、4.5wt%以下、4.0wt%以下、3.5wt%以下、3.0wt%以下、2.5wt%以下、2.0wt%以下含まれる。 (F) Disintegrant The disintegrant used in the present invention is necessary to prevent the drug from absorbing water and dissolving or solidifying during wet granulation, and to exhibit good fluidity in the manufacturing apparatus during granulation. .. In order to achieve miniaturization of tablets, it is desirable to show good water absorption and disintegration after tableting even when the content in the tablets is low.
The disintegrant used in the present invention is not particularly limited, but a disintegrant usually used in the formulation can be used. For example, starches, low-substituted hydroxypropyl cellulose, carmellose, carmellose calcium, carmellose sodium, crospovidone, croscarmellose sodium, sodium carboxymethyl starch (also referred to as sodium starch glycolate) and the like can be mentioned. Further, two or more kinds of disintegrants may be used.
It is preferably crospovidone, croscarmellose sodium, carboxymethyl starch sodium, and more preferably croscarmellose sodium. The disintegrant in the tablet of the present invention preferably contains 0.1 wt% or more, 0.2 wt% or more, 0.5 wt% or more, 1.0 wt% or more, and 1.5 wt% or more. The disintegrant is preferably 7.5 wt% or less, 7.4 wt% or less, 7.3 wt% or less, 7.2 wt% or less, 7.1 wt% or less, 7.0 wt% or less, 6.9 wt% or less, 6. 8 wt% or less, 6.7 wt% or less, 6.6 wt% or less, 6.5 wt% or less, 6.4 wt% or less, 6.3 wt% or less, 6.2 wt% or less, 6.1 wt% or less, 6.0 wt% Below, 5.9 wt% or less, 5.8 wt% or less, 5.7 wt% or less, 5.6 wt% or less, 5.5 wt% or less, 5.0 wt% or less, 4.5 wt% or less, 4.0 wt% or less, It includes 3.5 wt% or less, 3.0 wt% or less, 2.5 wt% or less, and 2.0 wt% or less.
(g)賦形剤
本発明に用いられる賦形剤としては、特に限定されないが、通常製剤化において用いられる賦形剤を用いることができる。例えば、結晶セルロース、糖または糖アルコール等が挙げられる。糖または糖アルコールとしては、例えば、マンニトール、エリスリトール、キシリトール、マルチトール、ソルビトール、乳糖、白糖、トレハロース等が挙げられる。また、賦形剤は1種または2種以上を組み合わせて使用することができる。
賦形剤の含有量としては、好ましくは0.1wt%以上、0.5wt%以上、1.0wt%以上、2.0wt%以上である。賦形剤の含有量としては、好ましくは7.5wt%以下、7.4wt%以下、7.3wt%以下、7.2wt%以下、7.1wt%以下、7.0wt%以下、6.9wt%以下、6.8wt%以下、6.7wt%以下、6.6wt%以下、6.5wt%以下、6.4wt%以下、6.3wt%以下、6.2wt%以下、6.1wt%以下、6.0wt%以下、5.9wt%以下、5.8wt%以下、5.7wt%以下、5.6wt%以下、5.5wt%以下、5.0wt%以下、4.5wt%以下、4.0wt%以下、3.5wt%以下、3.0wt%以下、2.5wt%以下、2.0wt%以下である。 (G) Excipient The excipient used in the present invention is not particularly limited, but an excipient usually used in the formulation can be used. For example, crystalline cellulose, sugar, sugar alcohol and the like can be mentioned. Examples of the sugar or sugar alcohol include mannitol, erythritol, xylitol, maltitol, sorbitol, lactose, sucrose, trehalose and the like. In addition, the excipient may be used alone or in combination of two or more.
The content of the excipient is preferably 0.1 wt% or more, 0.5 wt% or more, 1.0 wt% or more, and 2.0 wt% or more. The content of the excipient is preferably 7.5 wt% or less, 7.4 wt% or less, 7.3 wt% or less, 7.2 wt% or less, 7.1 wt% or less, 7.0 wt% or less, 6.9 wt. % Or less, 6.8 wt% or less, 6.7 wt% or less, 6.6 wt% or less, 6.5 wt% or less, 6.4 wt% or less, 6.3 wt% or less, 6.2 wt% or less, 6.1 wt% or less , 6.0 wt% or less, 5.9 wt% or less, 5.8 wt% or less, 5.7 wt% or less, 5.6 wt% or less, 5.5 wt% or less, 5.0 wt% or less, 4.5 wt% or less, 4 .0 wt% or less, 3.5 wt% or less, 3.0 wt% or less, 2.5 wt% or less, 2.0 wt% or less.
(h)滑沢剤
本発明においては、滑沢剤を添加することができる。滑沢剤は、原薬や顆粒の種類により打錠時に杵臼に原薬や顆粒が付着することを防止し、錠剤の効率的な製造が期待される。滑沢剤は、打錠前にその他の成分と混合してもよいし、打錠時に杵臼に噴霧してもよい。本発明に用いられる滑沢剤としては、特に限定されないが、例えば、ステアリン酸、ステアリン酸マグネシウム、ステアリン酸カルシウム、フマル酸ステアリルナトリウム、タルク、カルナウバロウ、ショ糖脂肪酸エステル等が挙げられる。これらの滑沢剤は1種または2種以上を組み合わせて使用することができる。本発明に用いられる滑沢剤としては、好ましくは、ステアリン酸マグネシウムである。
滑沢剤の含有量としては、好ましくは0.1wt%以上、0.2wt%以上、0.4wt%以上、0.6wt%、0.8wt%以上、1.0wt%以上である。滑沢剤の含有量としては、好ましくは4.0wt%以下、3.5wt%以下、3.0wt%以下、2.5wt%以下、2.0wt%以下、1.8wt%以下、1.6wt%以下、1.4wt%以下、1.2wt%以下、1.0wt%以下である。
滑沢剤の含有量としては、さらに好ましくは、0.4wt%以上、0.6wt%、0.8wt%以上、1.0wt%以上である。滑沢剤の含有量としては、さらに好ましくは2.0wt%以下、1.8wt%以下、1.6wt%以下、1.4wt%以下、1.2wt%以下、1.0wt%以下である。 (H) Lubricants In the present invention, a lubricant can be added. Lubricants prevent the drug substance and granules from adhering to the mortar at the time of tableting depending on the type of drug substance and granules, and are expected to efficiently produce tablets. The lubricant may be mixed with other components before tableting, or may be sprayed onto the mortar at the time of tableting. The lubricant used in the present invention is not particularly limited, and examples thereof include stearic acid, magnesium stearate, calcium stearate, sodium stearyl fumarate, talc, carnauba wax, and sucrose fatty acid ester. These lubricants can be used alone or in combination of two or more. The lubricant used in the present invention is preferably magnesium stearate.
The content of the lubricant is preferably 0.1 wt% or more, 0.2 wt% or more, 0.4 wt% or more, 0.6 wt%, 0.8 wt% or more, and 1.0 wt% or more. The content of the lubricant is preferably 4.0 wt% or less, 3.5 wt% or less, 3.0 wt% or less, 2.5 wt% or less, 2.0 wt% or less, 1.8 wt% or less, 1.6 wt. % Or less, 1.4 wt% or less, 1.2 wt% or less, 1.0 wt% or less.
The content of the lubricant is more preferably 0.4 wt% or more, 0.6 wt%, 0.8 wt% or more, and 1.0 wt% or more. The content of the lubricant is more preferably 2.0 wt% or less, 1.8 wt% or less, 1.6 wt% or less, 1.4 wt% or less, 1.2 wt% or less, and 1.0 wt% or less.
(i)他の添加剤
本発明の錠剤には、上記以外にも本発明の機能を失わない程度に他の添加剤を加えることができる。他の添加剤としては、例えば、甘味剤、矯味剤、矯臭剤、香料、流動化剤(例、アエロジル)、帯電防止剤、着色剤、可塑剤、凝集防止剤、光沢化剤(例、カルナウバロウ、タルク)等が挙げられるが、これらに限定されるものではない。 (I) Other Additives In addition to the above, other additives can be added to the tablets of the present invention to the extent that the functions of the present invention are not lost. Other additives include, for example, sweeteners, flavoring agents, flavoring agents, fragrances, fluidizing agents (eg Aerosil), antistatic agents, colorants, plasticizers, anti-aggregating agents, brightening agents (eg carnauba wax). , Talc), etc., but is not limited to these.
(j)フィルムコート剤
フィルムコートに用いるフィルムコート剤としては、例えば、ヒプロメロース、ヒドロキシプロピルセルロース、ポリビニルピロリドン、ポリビニルアルコール、ポリビニルアルコール・ポリエチレングリコール・グラフトコポリマー、メタクリル酸コポリマーL、メタクリル酸コポリマーLD、メタクリル酸コポリマーS、アミノアルキルメタクリレートコポリマーRS、アクリル酸エチル・メタクリル酸メチルコポリマー等の基材と、ポリエチレングリコール、プロピレングリコール、トリアセチン、クエン酸トリエチル、グリセリン、グリセリン脂肪酸エステル等の可塑剤を組み合わせたものが挙げられるが、これに限定されるものではない。また、酸化チタン、酸化鉄、タルク、着色剤等の添加剤を加えることもできる。好ましくは、基材としてはヒプロメロース、ヒドロキシプロピルセルロースおよびポリビニルアルコール、可塑剤としてはポリエチレングリコール、プロピレングリコールおよびクエン酸トリエチルである。 (J) Film coating agent Examples of the film coating agent used for film coating include hypromellose, hydroxypropyl cellulose, polyvinylpyrrolidone, polyvinyl alcohol, polyvinyl alcohol / polyethylene glycol graft copolymer, methacrylic acid copolymer L, methacrylic acid copolymer LD, and methacryl. A combination of a base material such as acid copolymer S, aminoalkyl methacrylate copolymer RS, ethyl acrylate / methyl methacrylate copolymer and a plasticizer such as polyethylene glycol, propylene glycol, triacetin, triethyl citrate, glycerin and glycerin fatty acid ester is However, it is not limited to this. Further, additives such as titanium oxide, iron oxide, talc, and a colorant can be added. Preferably, the base material is hypromellose, hydroxypropyl cellulose and polyvinyl alcohol, and the plasticizers are polyethylene glycol, propylene glycol and triethyl citrate.
「優れた溶出性」
優れた溶出性とは、日本薬局方溶出試験第2法に従い以下の溶出試験条件で、試作した製剤の溶出試験を実施した際に、30分時点で好ましくは80%以上、85%以上、90%以上、95%以上の溶出率を示し、60分時点で好ましくは97%以上、98%以上、99%以上の溶出率を示す。また60分時点で好ましくは、103%以下、102%以下、100%以下の溶出率を示す。
試験溶液:日本薬局方溶出試験第2液
パドル回転数:50rpm
試験液:900mL "Excellent elution"
Excellent dissolution is preferably 80% or more, 85% or more, 90 at 30 minutes when the dissolution test of the prototype formulation is carried out under the following dissolution test conditions in accordance with the second method of the Japanese Pharmacopoeia dissolution test. It shows an elution rate of% or more and 95% or more, and preferably 97% or more, 98% or more, and 99% or more elution rate at 60 minutes. Further, at 60 minutes, the elution rate is preferably 103% or less, 102% or less, and 100% or less.
Test solution: Japanese Pharmacopoeia dissolution test 2nd solution Paddle rotation speed: 50 rpm
Test solution: 900 mL
「大スケールでの製造」
本発明における大スケールでの製造とは、造粒工程、打錠工程、フィルムコーティング工程のいずれかの工程を、好ましくは10kg以上、15kg以上、20kg以上、25kg以上、30kg以上、35kg以上、40kg以上、45kg以上、50kg以上の製造量(仕込み量)で製造することである。 "Manufacturing on a large scale"
The large-scale production in the present invention means that any one of the granulation step, the tableting step, and the film coating step is preferably 10 kg or more, 15 kg or more, 20 kg or more, 25 kg or more, 30 kg or more, 35 kg or more, 40 kg. As mentioned above, it is manufactured with a production amount (charged amount) of 45 kg or more and 50 kg or more.
「粘度」
本発明における高分子の粘度は、B型粘度計を用いて、20℃の2wt%高分子水溶液を測定する場合の粘度を指す。
本発明の錠剤に含まれるイメグリミン含有組成物の製造法としては、打錠障害を防止し、適切な硬度の錠剤を得るために、圧縮成形性に優れた顆粒を製造することが出来る造粒法が望ましい。例えば、流動層造粒法が挙げられ、好ましくは、結合剤溶液を噴霧する流動層造粒法が望ましいが、結合剤を一部粉末で加える流動層造粒法を用いても良い。
本発明はこれらに限定されるわけではないが、以下に、例えば流動層造粒法で、フィルムコート錠を製造する工程例を挙げる。 "viscosity"
The viscosity of the polymer in the present invention refers to the viscosity when measuring a 2 wt% polymer aqueous solution at 20 ° C. using a B-type viscometer.
As a method for producing an imeglimin-containing composition contained in a tablet of the present invention, a granulation method capable of producing granules having excellent compression moldability in order to prevent tableting trouble and obtain a tablet having an appropriate hardness. Is desirable. For example, a fluidized bed granulation method can be mentioned, preferably a fluidized bed granulation method in which a binder solution is sprayed, but a fluidized bed granulation method in which a binder is partially added as a powder may be used.
The present invention is not limited to these, but the following is an example of a process for producing a film-coated tablet by, for example, a fluidized bed granulation method.
(1)ヒドロキシプロピルセルロース水溶液の調製
ヒドロキシプロピルセルロースを精製水に溶解する。ヒドロキシプロピルセルロースの量としては、精製水の量に対し、例えば、1~20wt%の範囲、好ましくは2~6.5wt%の範囲から選択される。(1) Preparation of Hydroxypropyl Cellulose Aqueous Solution Hydroxypropyl cellulose is dissolved in purified water. The amount of hydroxypropyl cellulose is selected from, for example, 1 to 20 wt%, preferably 2 to 6.5 wt% with respect to the amount of purified water.
(2)イメグリミン含有組成物の製造(流動層造粒工程)
イメグリミン、アエロジルおよび崩壊剤を流動層造粒機に仕込み、上記(1)の工程で調製された水溶性高分子水溶液を散布しながら造粒する。(2) Production of imeglimin-containing composition (fluidized bed granulation step)
Imeglimin, Aerosil and a disintegrant are charged in a fluidized bed granulator, and granulated while spraying the water-soluble polymer aqueous solution prepared in the above step (1).
(3)イメグリミン含有組成物の乾燥
上記造粒物を、減圧または常圧にて乾燥する。この乾燥は、赤外線水分計やハロゲン式水分計にて80℃で測定される乾燥減量値が、例えば、3wt%以内、好ましくは2wt%以内になるように行う。(3) Drying of imeglimin-containing composition The above granulated product is dried under reduced pressure or normal pressure. This drying is performed so that the drying weight loss value measured at 80 ° C. with an infrared moisture meter or a halogen type moisture meter is, for example, within 3 wt%, preferably within 2 wt%.
(4)滑沢剤の配合(混合工程)
上記(3)で乾燥したイメグリミン含有組成物に流動化剤、滑沢剤を加えて混合する。混合は、例えば、攪拌ミキサーに分類される混合機が用いられる。具体的には、タンブラーブレンダー、Vブレンダー、ダブルコーン、ビンタンブラー等が挙げられる。但し、これらに限定されるものではない。(4) Blending of lubricant (mixing process)
A fluidizing agent and a lubricant are added to the imeglimin-containing composition dried in (3) above and mixed. For mixing, for example, a mixer classified as a stirring mixer is used. Specific examples thereof include a tumbler blender, a V blender, a double cone, and a bin tumbler. However, it is not limited to these.
(5)打錠(打錠工程)
上記混合物を打錠して素錠を調製する。打錠装置としては、例えば、ロータリー式に分類される打錠機等が挙げられる。(5) Locking (locking process)
The above mixture is beaten to prepare an uncoated tablet. Examples of the locking device include a locking machine classified as a rotary type.
(6)フィルムコート(フィルムコーティング工程)
上記素錠にフィルムコートを施す。コーティング装置としては、例えばコーティングパンに分類される装置が挙げられる。好ましくは通気式コーティングシステムに分類される装置が挙げられる。(6) Film coating (film coating process)
A film coat is applied to the above-mentioned uncoated lock. Examples of the coating device include a device classified as a coating pan. Devices are preferably classified as a ventilated coating system.
(7)フィルムコート錠の乾燥
上記フィルムコート錠を乾燥する。乾燥は減圧または常圧で行い、赤外線水分計やハロゲン式水分計にて80℃で測定される乾燥減量値が、例えば、3wt%以下、好ましくは2wt%以下になるように行う。(7) Drying the film-coated lock The film-coated lock is dried. Drying is carried out under reduced pressure or normal pressure so that the drying weight loss value measured at 80 ° C. with an infrared moisture meter or a halogen type moisture meter is, for example, 3 wt% or less, preferably 2 wt% or less.
以下、実施例および試験例を挙げて、本発明をさらに具体的に説明するが、本発明はこれらに限定されるものではない。 Hereinafter, the present invention will be described in more detail with reference to Examples and Test Examples, but the present invention is not limited thereto.
本実施例および試験例に使用した薬剤および添加剤は、特に断りがない限り、以下のものを使用した。
イメグリミン塩酸塩:大日本住友製薬株式会社
結晶セルロース(セオラスTMPH-101):旭化成株式会社
軽質無水ケイ酸(AEROSILTM200):日本アエロジル株式会社
クロスカルメロースナトリウム(Ac-Di-SolTMSD-711):FMC Health and Nutrition
ヒドロキシプロピルセルロース(HPC-SSL/2.0~2.9mPa・s注1)):日本曹達株式会社
ヒドロキシプロピルセルロース(HPC-L/6.0~10.0mPa・s注1)):日本曹達株式会社
ヒドロキシプロピルセルロース(HPC-M/150~400mPa・s注1)):日本曹達株式会社
ヒプロメロース(ヒドロキシプロピルメチルセルロース)(TC-5RTM/6mPa・s注2)):信越化学工業株式会社
ポビドン(KollidonTMK30/5.5~8.5mPa・s注3)):BASF
ポリビニルアルコール(GohsenolTM EG-05P/4.8~5.8mPa・s注4)):三菱化学株式会社
ステアリン酸マグネシウム(ステアリン酸マグネシウム(植物性)):太平化学産業株式会社
OPADRYTMtm 07F28588 WHITE:日本カラコン合同会社
タルク(高級タルクMSP):日本タルク株式会社
クロスポビドン(KollidonTMCL):BASF
デンプングリコール酸ナトリウム(PrimojelTM):DFE Pharma
注1)20℃、2%溶液におけるメーカーカタログ値。
注2)20℃、2%溶液におけるメーカーカタログ値。
注3)20℃、10%溶液におけるメーカーカタログ値。
注4)20℃、4%溶液におけるメーカーカタログ値。Unless otherwise specified, the following agents and additives were used in the present examples and test examples.
Imeglycin hydrochloride: Dainippon Sumitomo Pharmaceutical Co., Ltd. Crystalline cellulose (Theoras TM PH-101): Asahi Kasei Co., Ltd. Light anhydrous silicic acid (AEROSIL TM 200): Nippon Aerosil Co., Ltd. Croscarmellose sodium (Ac-Di-Sol TM SD-) 711): FMC Health and Nutrition
Hydroxypropyl cellulose (HPC-SSL / 2.0-2.9 mPa · s Note 1) ): Nippon Soda Co., Ltd. Hydroxypropyl cellulose (HPC-L / 6.0-10.0 mPa · s Note 1 )): Nippon Soda Hydroxypropyl Cellulose Co., Ltd. (HPC-M / 150-400 mPa · s Note 1) ): Nippon Soda Co., Ltd. Hypromellose (Hydroxypropyl Methyl Cellulose) (TC-5R TM / 6 mPa · s Note 2) ): Shinetsu Chemical Industry Co., Ltd. Povidon (Kollidon TM K30 / 5.5-8.5 mPa · s Note 3) ): BASF
Polyvinyl alcohol (Gohsenol TM EG-05P / 4.8-5.8 mPa · s Note 4) ): Mitsubishi Chemical Corporation Magnesium stearate (magnesium stearate (vegetable)): Taihei Chemical Corporation OPADRY TM tm 07F28588 WHITE : Japan Talc GK (luxury talc MSP): Japan Talc Co., Ltd. Cross Povidon (Kollidon TM CL): BASF
Sodium Starch Glycolate (Primogel TM ): DFE Pharma
Note 1) Manufacturer's catalog value at 20 ° C and 2% solution.
Note 2) Manufacturer's catalog value at 20 ° C and 2% solution.
Note 3) Manufacturer's catalog value at 20 ° C and 10% solution.
Note 4) Manufacturer's catalog value at 20 ° C and 4% solution.
実施例1:イメグリミン塩酸塩を500mg含有する錠剤(1)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
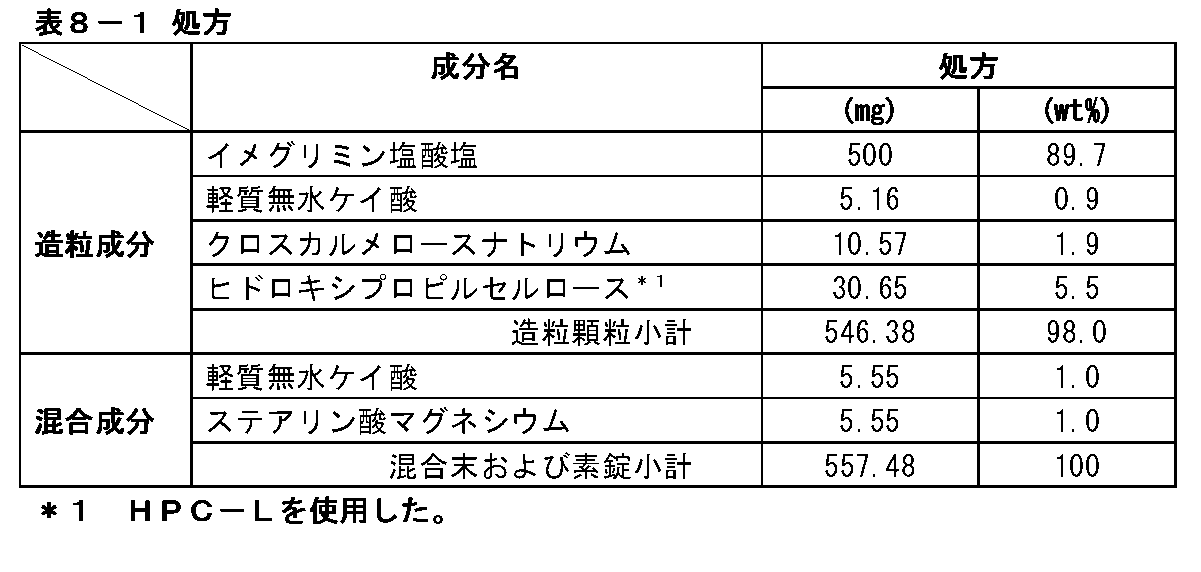
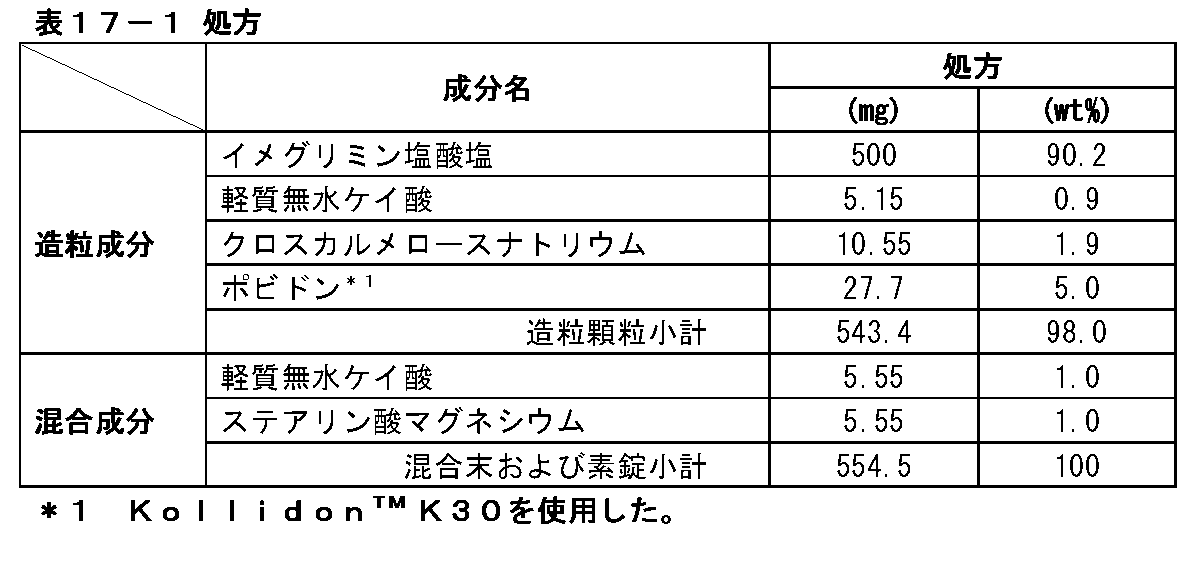
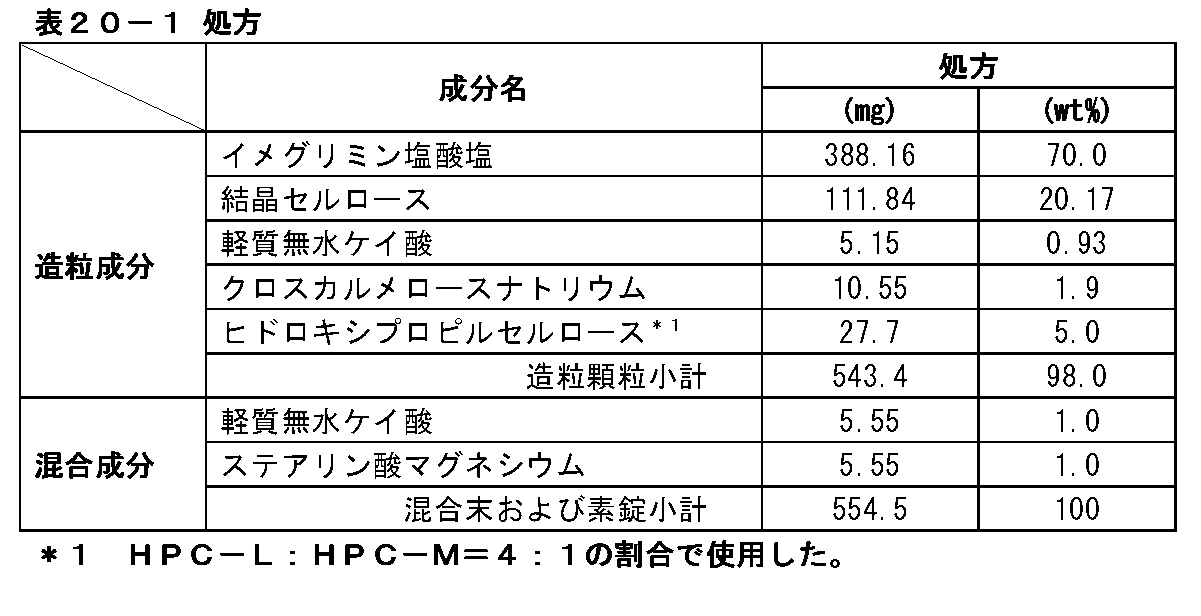
表1-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 1: Tablet containing 500 mg of imeglimin hydrochloride (1)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 1-1 were produced.
B.製造方法
(1)5wt%ヒドロキシプロピルセルロース溶液(1)の調製
1900gの精製水をSUS製のビーカーにとり、撹拌しながら100gのHPC-Lを徐々に投入し、溶解させた。一昼夜静置した後、再度撹拌し、5wt%ヒドロキシプロピルセルロース溶液(1)を調製した。B. Production Method (1) Preparation of 5 wt% Hydroxypropyl Cellulose Solution (1) 1900 g of purified water was placed in a beaker made of SUS, and 100 g of HPC-L was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 5 wt% hydroxypropyl cellulose solution (1).
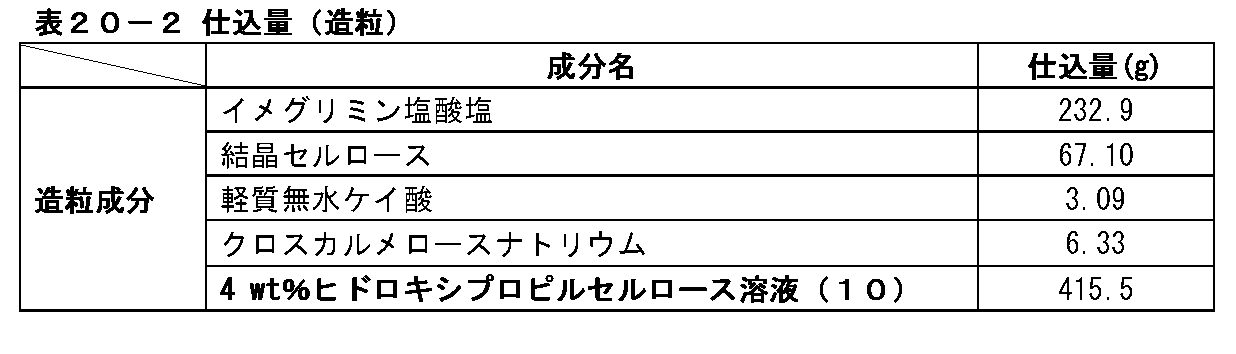
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
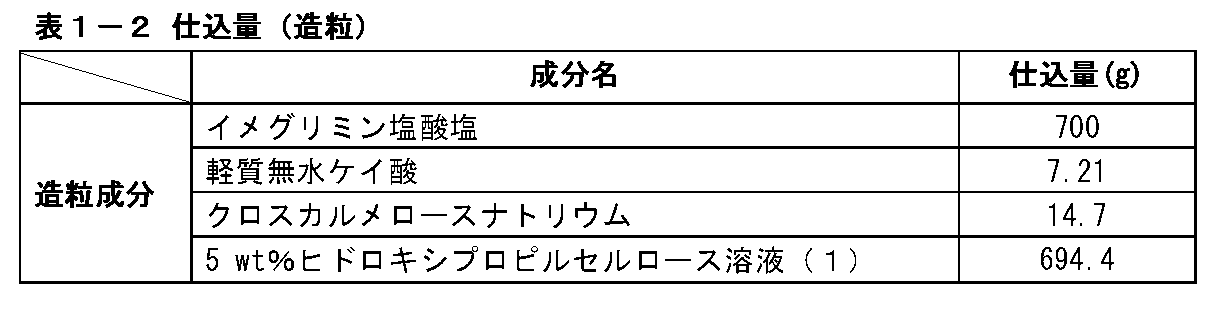
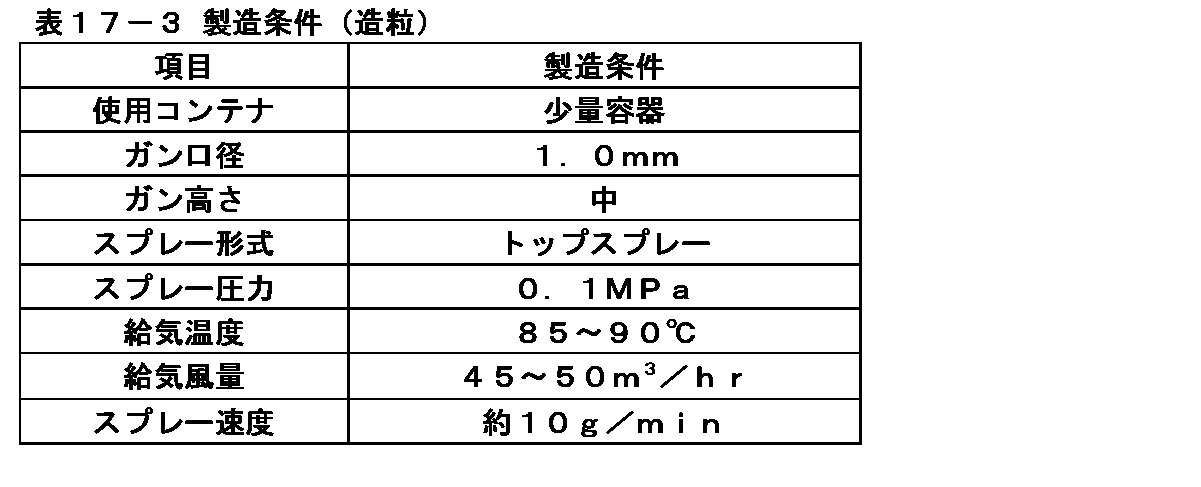
表1-2に記載の仕込量と表1-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表1-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が35℃になるまで流動させながら混合した。続いて、流動させながら表1-2記載の仕込量の5wt%ヒドロキシプロピルセルロース溶液(1)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 1-2 and the production conditions shown in Table 1-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 1-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 35 ° C. Subsequently, the 5 wt% hydroxypropyl cellulose solution (1) of the charged amount shown in Table 1-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
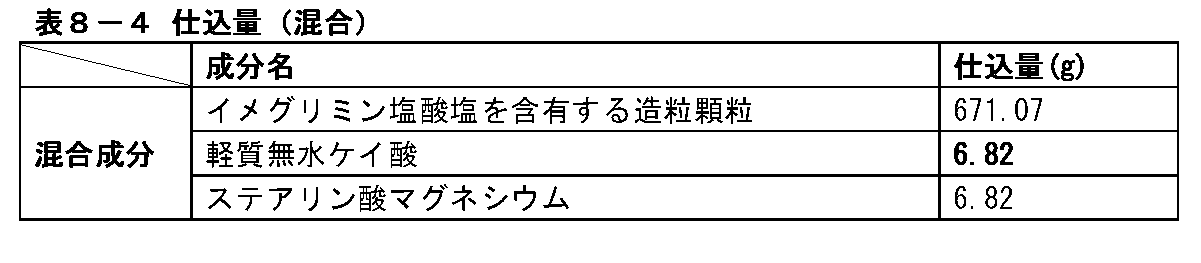
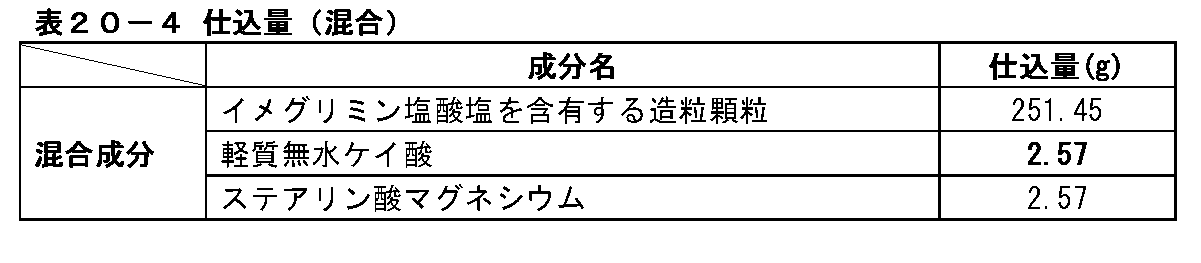
(3)イメグリミン塩酸塩を含有する混合末の製造
表1-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。V10型コンテナに、表1-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表1-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで10分間混合した。続いて、V10型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 1-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 1-4 are added to the V10 type container, and then the amount of light anhydrous silicic acid shown in Table 1-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-5 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V10 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-5 type).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
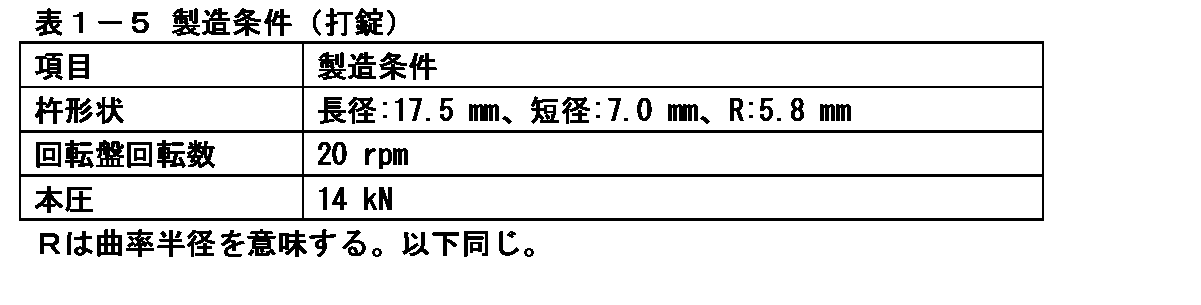
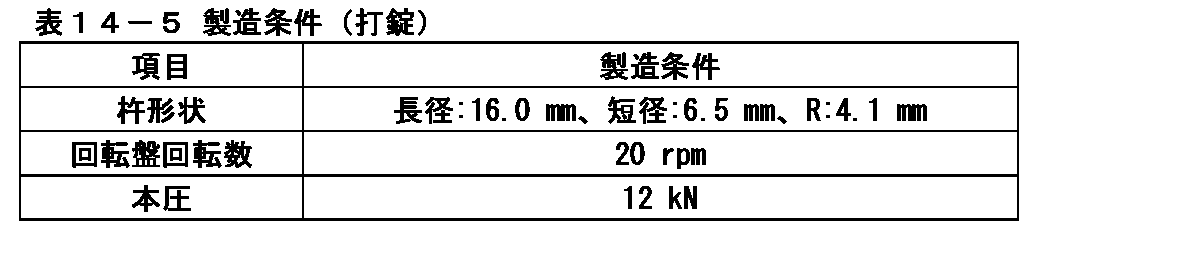
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表1-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 1-5. It was locked and an uncoated tablet was manufactured.
実施例2:イメグリミン塩酸塩を500mg含有する錠剤(2)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
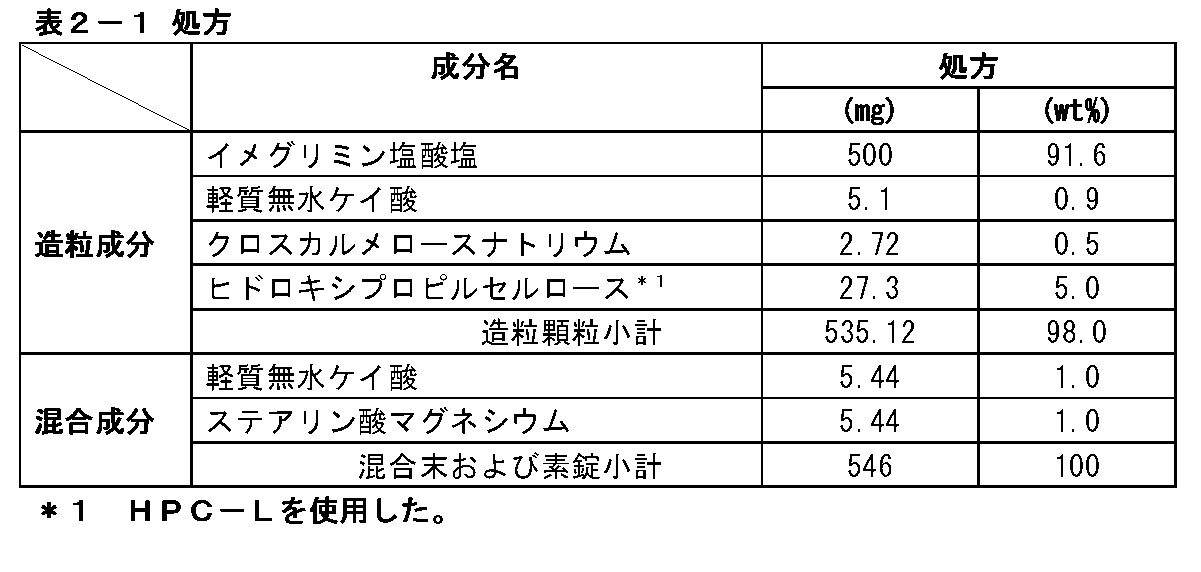
表2-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 2: Tablet containing 500 mg of imeglimin hydrochloride (2)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 2-1 were produced.
B.製造方法
(1)5wt%ヒドロキシプロピルセルロース溶液(2)の調製
1900gの精製水をSUS製のビーカーにとり、撹拌しながら100gのHPC-Lを徐々に投入し、溶解させた。一昼夜静置した後、再度撹拌し、5wt%ヒドロキシプロピルセルロース溶液(2)を調製した。B. Production Method (1) Preparation of 5 wt% Hydroxypropyl Cellulose Solution (2) 1900 g of purified water was placed in a beaker made of SUS, and 100 g of HPC-L was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 5 wt% hydroxypropyl cellulose solution (2).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表2-2に記載の仕込量と表2-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表2-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が35℃になるまで流動させながら混合した。続いて、流動させながら表2-2記載の仕込量の5wt%ヒドロキシプロピルセルロース溶液(2)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.9mm、回転数900rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 2-2 and the production conditions shown in Table 2-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 2-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 35 ° C. Subsequently, the 5 wt% hydroxypropyl cellulose solution (2) of the charged amount shown in Table 2-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.9 mm and a rotation speed of 900 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
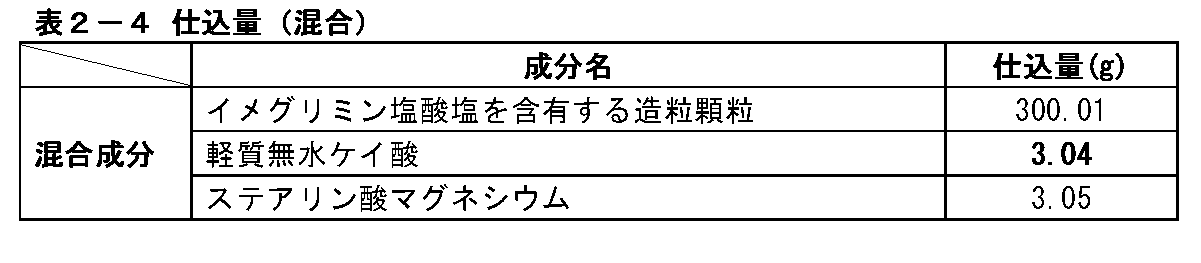
表2-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。V2型コンテナに、表2-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表2-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-3型)を用いて40rpmで10分間混合した。続いて、V2型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-3型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 2-4. Granulated granules containing the imeglimin hydrochloride in the amount shown in Table 2-4 are put into a V2 type container, and then the light anhydrous silicic acid in the amount shown in Table 2-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-3 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V2 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-3 type).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表2-5の条件で打錠し、素錠を製造した。
(4) Manufacture of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locking machine (manufactured by Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 2-5. It was locked and an uncoated tablet was manufactured.
実施例3:イメグリミン塩酸塩を500mg含有する錠剤(3)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
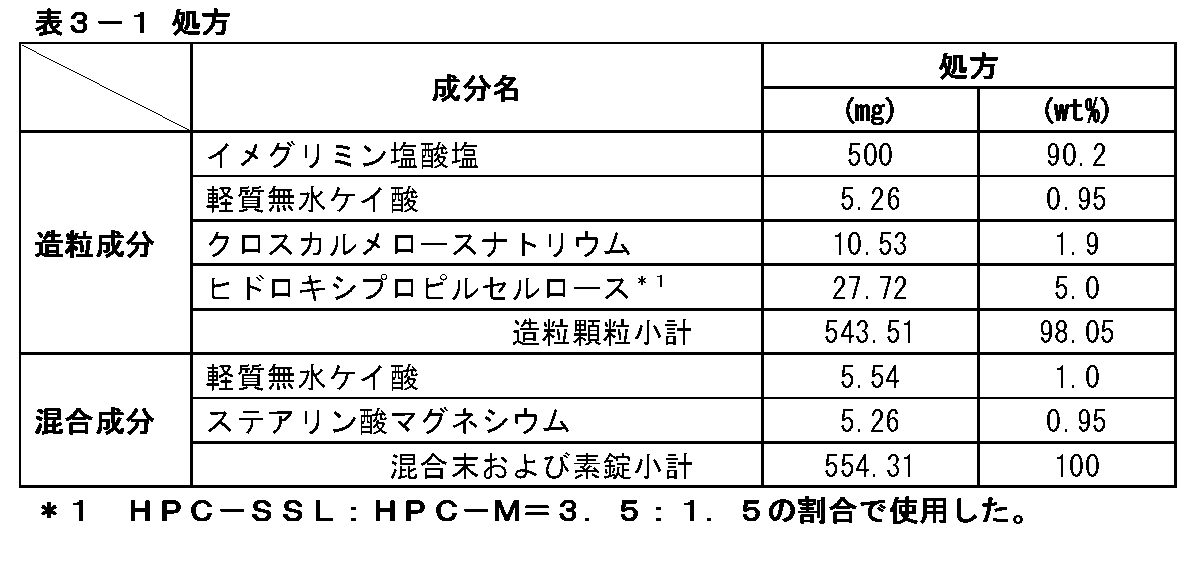
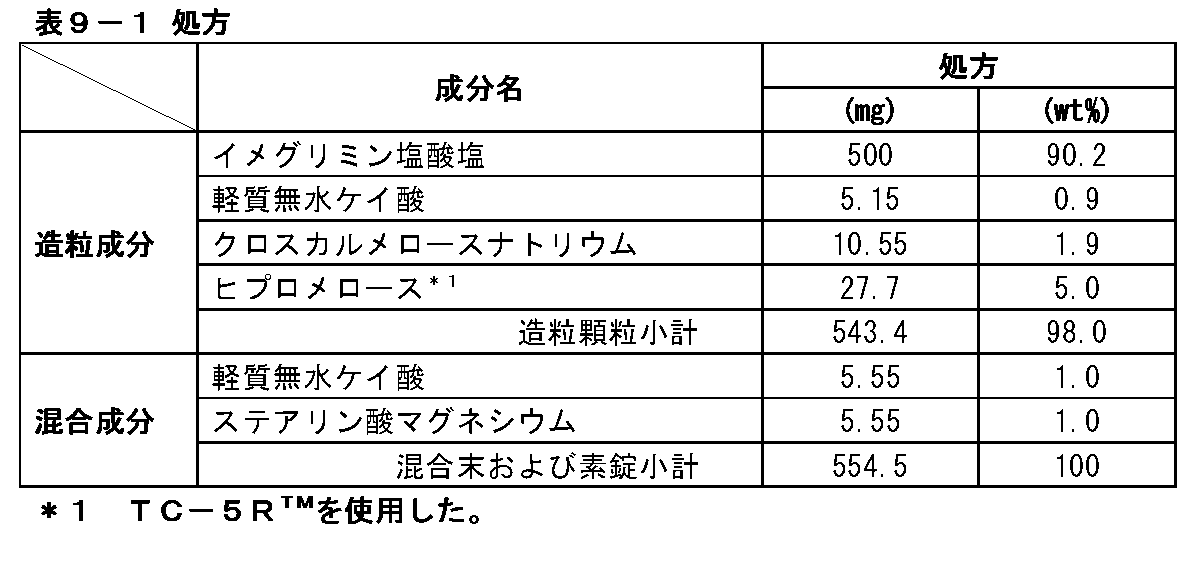
表3-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 3: Tablets containing 500 mg of imeglimin hydrochloride (3)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 3-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(1)の調製
1920gの精製水をSUS製のビーカーにとり、撹拌しながら56gのHPC-SSLを徐々に投入し、続いて24gのHPC-Mを投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(1)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (1) Take 1920 g of purified water in a beaker made of SUS, gradually add 56 g of HPC-SSL while stirring, and then add 24 g of HPC-M. And dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (1).
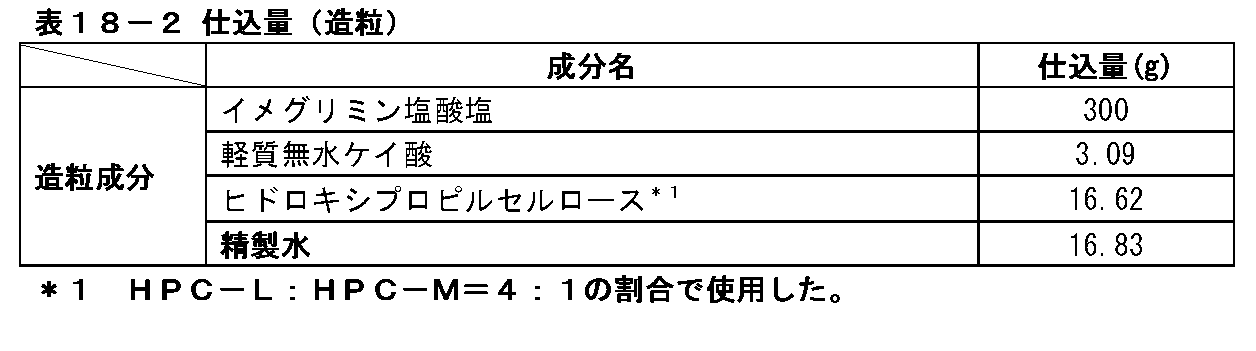
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表3-2に記載の仕込量と表3-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表3-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が35℃になるまで流動させながら混合した。続いて、流動させながら表3-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(1)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 3-2 and the production conditions shown in Table 3-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 3-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 35 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (1) of the charged amount shown in Table 3-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
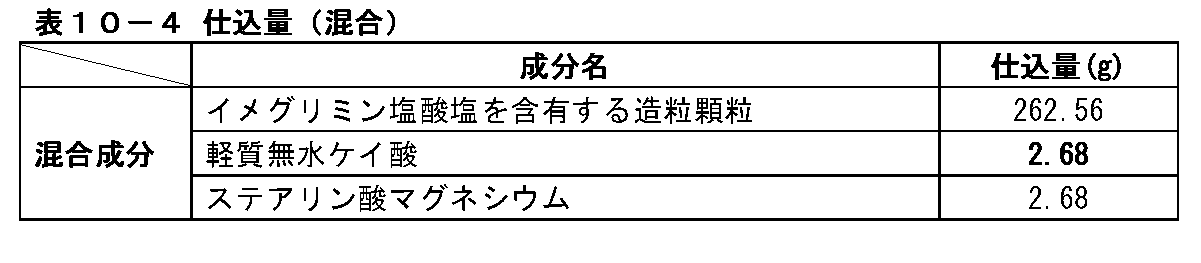
(3)イメグリミン塩酸塩を含有する混合末の製造
表3-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。V10型コンテナに、表3-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表3-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで10分間混合した。続いて、V10型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 3-4. Granulated granules containing the imeglimin hydrochloride in the amount shown in Table 3-4 are put into a V10 type container, and then the light anhydrous silicic acid in the amount shown in Table 3-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-5 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V10 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-5 type).
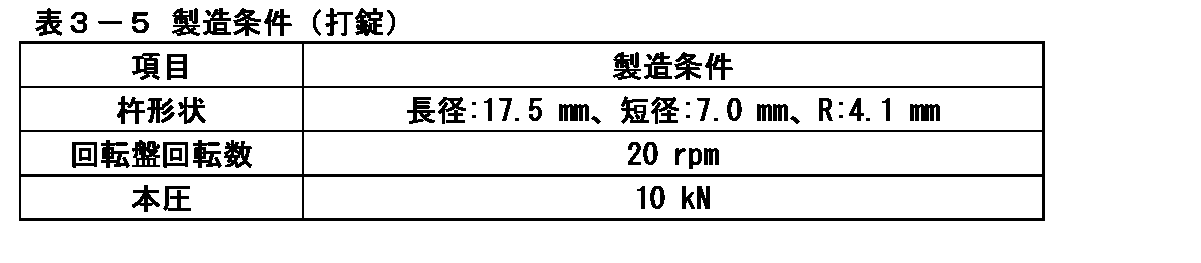
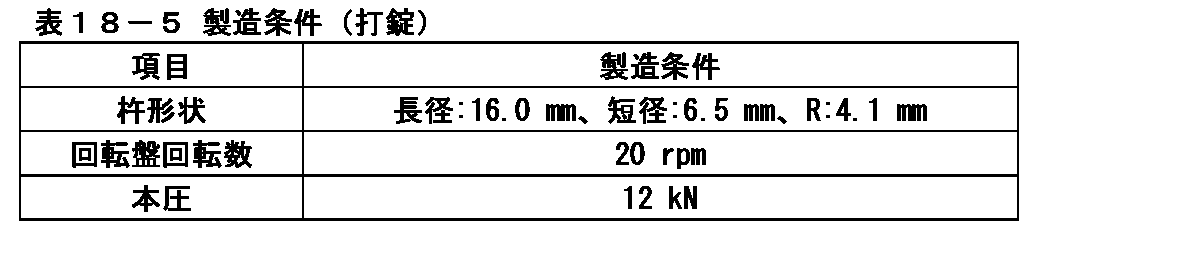
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表3-5の条件で打錠し、素錠を製造した。
(4) Manufacture of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locking machine (manufactured by Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 3-5. It was locked and an uncoated tablet was manufactured.
実施例4:イメグリミン塩酸塩を500mg含有する錠剤(4)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表4-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 4: Tablets containing 500 mg of imeglimin hydrochloride (4)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 4-1 were produced.
B.製造方法
(1)6.5wt%ヒドロキシプロピルセルロース溶液(1)の調製
1870gの精製水をSUS製のビーカーにとり、撹拌しながら130gのHPC-Lを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、6,5wt%ヒドロキシプロピルセルロース溶液(1)を調製した。B. Production Method (1) Preparation of 6.5 wt% Hydroxypropyl Cellulose Solution (1) 1870 g of purified water was placed in a beaker made of SUS, and 130 g of HPC-L was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 6.5 wt% hydroxypropyl cellulose solution (1).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表4-2に記載の仕込量と表4-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表4-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が35℃になるまで流動させながら混合した。続いて、流動させながら表4-2記載の仕込量の6.5wt%ヒドロキシプロピルセルロース溶液(1)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 4-2 and the production conditions shown in Table 4-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 4-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 35 ° C. Subsequently, the 6.5 wt% hydroxypropyl cellulose solution (1) of the charged amount shown in Table 4-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表4-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。V10型コンテナに、表4-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表4-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで10分間混合した。続いて、V10型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 4-4. Granulated granules containing the imeglimin hydrochloride in the amount shown in Table 4-4 are put into a V10 type container, and then the light anhydrous silicic acid in the amount shown in Table 4-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-5 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V10 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-5 type).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
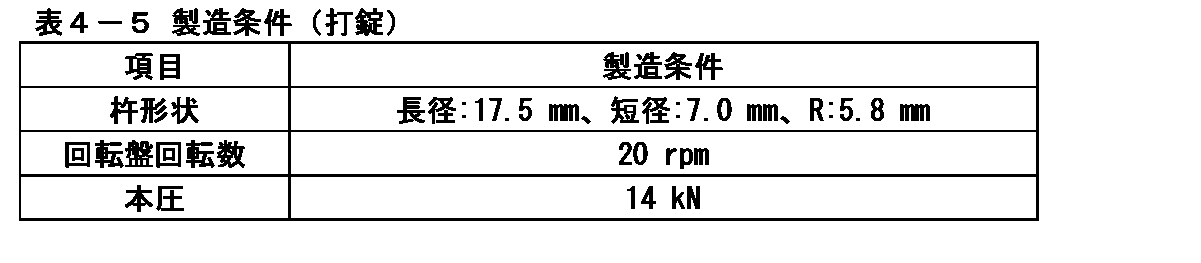
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表4-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locking machine (manufactured by Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 4-5. It was locked and an uncoated tablet was manufactured.
実施例5:イメグリミン塩酸塩を500mg含有する錠剤(5)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表5-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 5: Tablet containing 500 mg of imeglimin hydrochloride (5)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 5-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(2)の調製
64.8kgの精製水をSUS製のビーカーにとり、撹拌しながら2.43kgのHPC-Lを徐々に投入し、続いて0.27kgのHPC-Mを徐々に投入して溶解させた。この液を2つ調製し、一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(2)を合計135kg調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (2) Take 64.8 kg of purified water in a beaker made of SUS, gradually add 2.43 kg of HPC-L while stirring, and then 0.27 kg. HPC-M was gradually added and dissolved. Two of these solutions were prepared, allowed to stand for a whole day and night, and then stirred again to prepare a total of 135 kg of a 4 wt% hydroxypropyl cellulose solution (2).
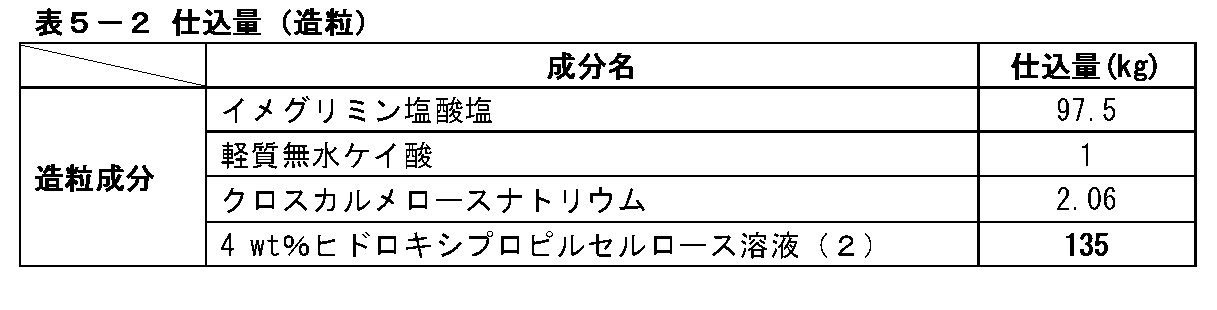
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表5-2に記載の仕込量と表5-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表5-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(フロイント産業株式会社製、NFLO-120SJC型)に投入し、排気温度が60℃になるまで流動させながら混合した。続いて、流動させながら表5-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(2)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
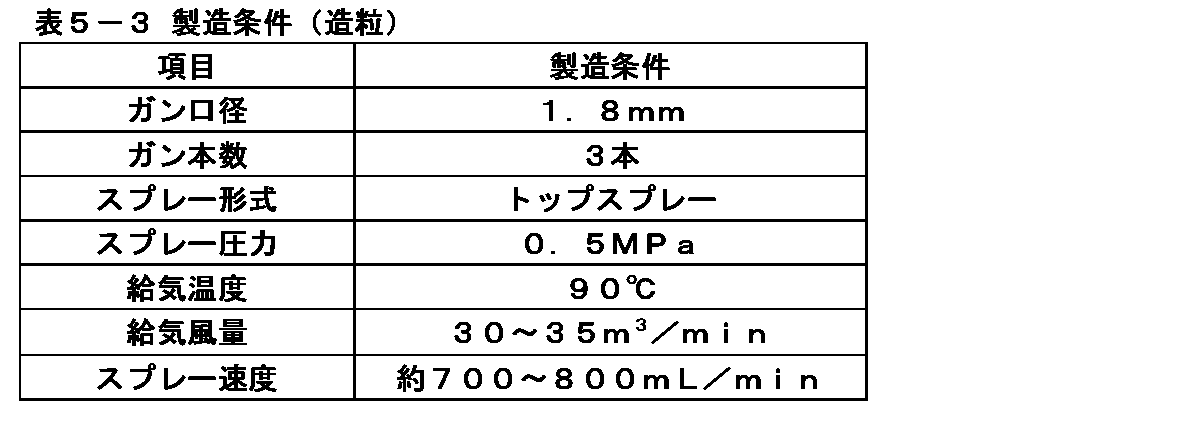
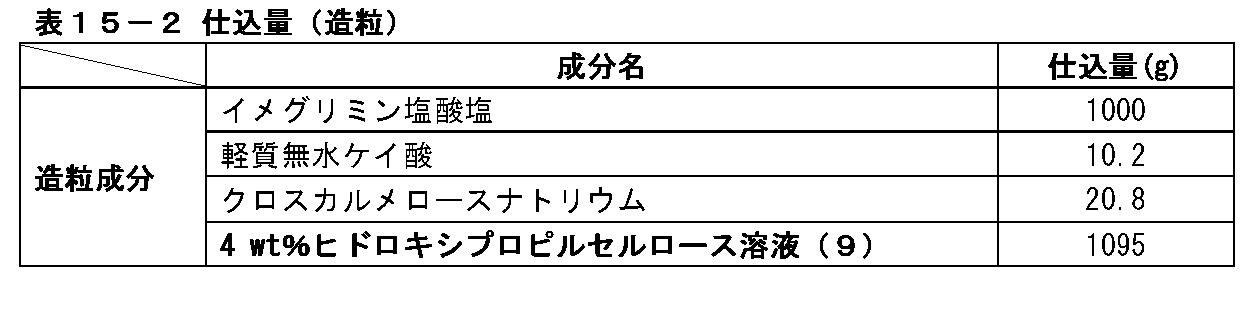
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 5-2 and the production conditions shown in Table 5-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 5-2 were put into a fluidized bed granulation dryer (NFLO-120SJC type manufactured by Freund Sangyo Co., Ltd.), and the exhaust temperature was increased. Was mixed while flowing until the temperature reached 60 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (2) of the charged amount shown in Table 5-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表5-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。800Lのコンテナに、表5-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表5-4に記載の仕込量の軽質無水ケイ酸を加え、コンテナ混合機(山崎金属機械製、タンブラーブレンダー)を用いて12rpmで5分間混合した。続いて、800Lのコンテナにステアリン酸マグネシウムを投入し、さらにコンテナ混合機(山崎金属機械製、タンブラーブレンダー)を用いて12rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 5-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 5-4 are put into an 800 L container, and then the amount of light anhydrous silicic acid shown in Table 5-4 is added to the container mixer. (Tumbler blender manufactured by Yamazaki Metal Machinery Co., Ltd.) was used to mix at 12 rpm for 5 minutes. Subsequently, magnesium stearate was put into an 800 L container, and further mixed at 12 rpm for 5 minutes using a container mixer (manufactured by Yamazaki Metal Machinery Co., Ltd., tumbler blender).
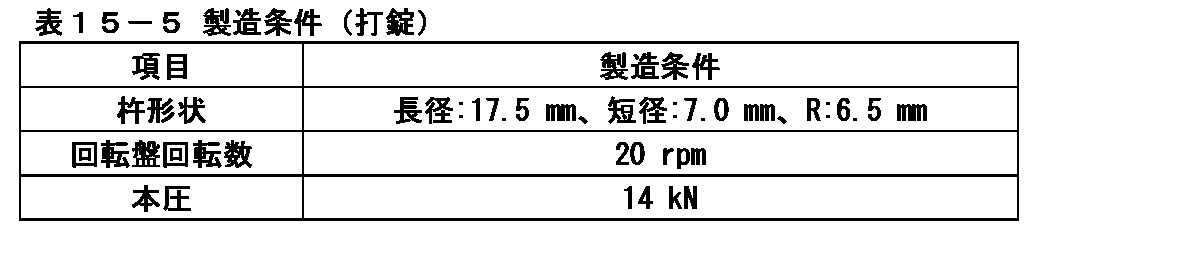
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表5-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 5-5. It was locked and an uncoated tablet was manufactured.
実施例6:イメグリミン塩酸塩を500mg含有する錠剤(6)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表6-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 6: Tablet containing 500 mg of imeglimin hydrochloride (6)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 6-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(3)の調製
64.8kgの精製水をSUS製のビーカーにとり、撹拌しながら2.16kgのHPC-Lを徐々に投入し、続いて0.54kgのHPC-Mを徐々に投入して溶解させた。この液を2つ調製し、一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(3)を合計135kg調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (3) Take 64.8 kg of purified water in a beaker made of SUS, gradually add 2.16 kg of HPC-L while stirring, and then 0.54 kg. HPC-M was gradually added and dissolved. Two of these solutions were prepared, allowed to stand for a whole day and night, and then stirred again to prepare a total of 135 kg of a 4 wt% hydroxypropyl cellulose solution (3).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
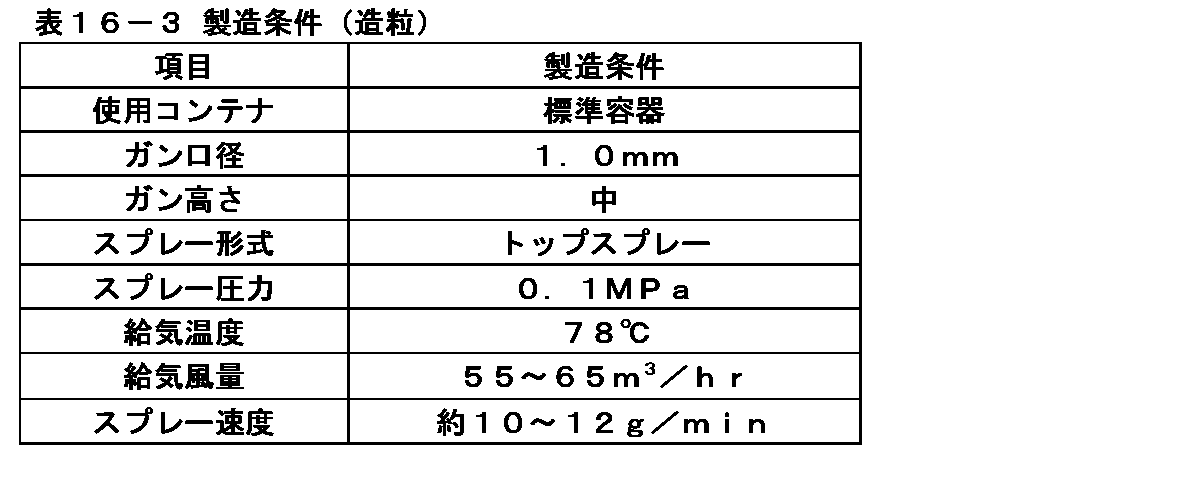
表6-2に記載の仕込量と表6-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表6-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(フロイント産業株式会社製、NFLO-120SJC型)に投入し、排気温度が55℃になるまで流動させながら混合した。続いて、流動させながら表6-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(3)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 6-2 and the production conditions shown in Table 6-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 6-2 were put into a fluidized bed granulation dryer (NFLO-120SJC type manufactured by Freund Sangyo Co., Ltd.), and the exhaust temperature was increased. Was mixed while flowing until the temperature reached 55 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (3) of the charged amount shown in Table 6-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表6-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末の製造をした。800Lのコンテナに、表6-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表6-4に記載の仕込量の軽質無水ケイ酸およびステアリン酸マグネシウムを軽く混合して加え、コンテナ混合機(山崎金属機械製、タンブラーブレンダー)を用いて12rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 6-4. In an 800 L container, put the granulated granules containing the imeglimin hydrochloride in the amount shown in Table 6-4, and then lightly add the light anhydrous silicic acid and magnesium stearate in the amount shown in Table 6-4. The mixture was added and mixed using a container mixer (manufactured by Yamazaki Metal Machinery Co., Ltd., tumbler blender) at 12 rpm for 5 minutes.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
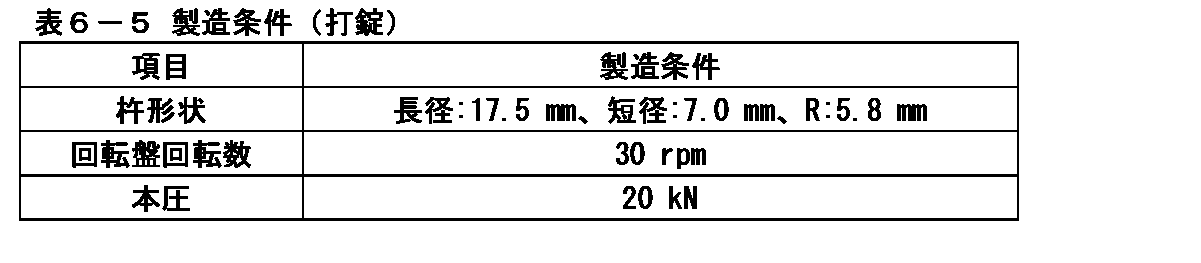
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表6-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 6-5. It was locked and an uncoated tablet was manufactured.
(5)フィルムコーティング液(1)の調製
55.2kgの精製水をSUS製のタンクにとり、撹拌しながら4.8kgのOPADRYTM tm 07F28588 WHITEを徐々に投入し、分散・溶解させた。この液を目開き106μmのスクリーンを通して、フィルムコーティング液(1)とした。(5) Preparation of film coating liquid (1) 55.2 kg of purified water was placed in a SUS tank, and 4.8 kg of OPADRY TM tm 07F28588 WHITE was gradually added while stirring to disperse and dissolve. This liquid was passed through a screen having an opening of 106 μm to obtain a film coating liquid (1).
(6)イメグリミン塩酸塩を500mg含有するフィルムコーティング錠の製造
表6-6に記載の条件でイメグリミン塩酸塩500mgを含有するフィルムコーティング錠を製造した。まず、82.5kgの素錠をコーティング機(フロイント産業株式会社製、AQC-170FS型)に投入し、コーティングパンを寸動回転させながら、表6-6の条件で排気温度が50℃になるまで加温した。続いて、コーティングパンを4rpmで回転させながら、表6-6の条件でフィルムコーティング液(1)をスプレーし、被膜量が約14mgになるまでフィルムコーティングした。その後、コーティングパンを2rpmで回転させながら排気温度が55℃になるまで乾燥し、21.38gのタルクを散布した。
(6) Production of Film-Coated Tablets Containing 500 mg of Imeglimin Hydrochloride A film-coated tablet containing 500 mg of imeglimin hydrochloride was produced under the conditions shown in Table 6-6. First, an 82.5 kg uncoated lock is put into a coating machine (AQC-170FS type manufactured by Freund Sangyo Co., Ltd.), and the exhaust temperature becomes 50 ° C. under the conditions shown in Table 6-6 while rotating the coating pan. It was warmed up to. Subsequently, while rotating the coating pan at 4 rpm, the film coating liquid (1) was sprayed under the conditions shown in Table 6-6, and the film was coated until the film amount became about 14 mg. Then, the coating pan was rotated at 2 rpm and dried until the exhaust temperature reached 55 ° C., and 21.38 g of talc was sprayed.
実施例7:イメグリミン塩酸塩を500mg含有する錠剤(7)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
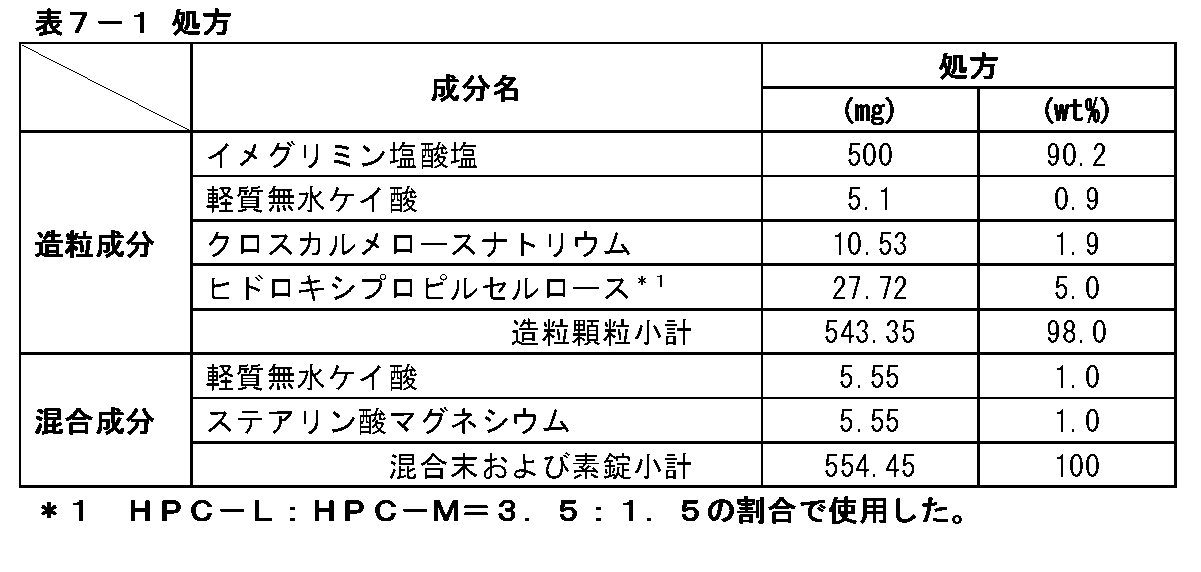
表7-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 7: Tablet containing 500 mg of imeglimin hydrochloride (7)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 7-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(4)の調製
23284.9gの精製水をSUS製のビーカーにとり、撹拌しながら679.0gのHPC-Lを徐々に投入し、続いて291.2gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(4)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (4) Take 23284.9 g of purified water in a beaker made of SUS, gradually add 679.0 g of HPC-L while stirring, and then 291.2 g. HPC-M was gradually added and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (4).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
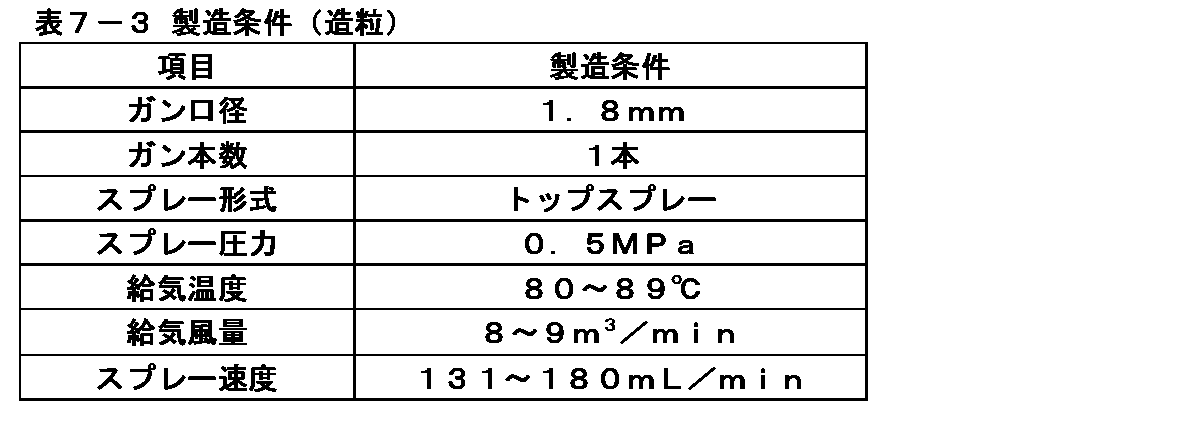
表7-2に記載の仕込量と表7-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表7-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(フロイント産業株式会社製、NFLF-30型)に投入し、排気温度が35℃になるまで流動させながら混合した。続いて、流動させながら表7-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(4)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 7-2 and the production conditions shown in Table 7-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 7-2 were put into a fluidized bed granulation dryer (NFLF-30 type manufactured by Freund Sangyo Co., Ltd.), and the exhaust temperature was increased. Was mixed while flowing until the temperature reached 35 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (4) of the charged amount shown in Table 7-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表7-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末の製造をした。110Lのコンテナに、表7-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表7-4に記載の仕込量の軽質無水ケイ酸を加え、コンテナ混合機(ピックステクニカ製、ピックスブレンダー)を用いて20rpmで10分間混合した。続いて、110Lのコンテナにステアリン酸マグネシウムを投入し、さらにコンテナ混合機(ピックステクニカ製、ピックスブレンダー)を用いて20rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 7-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 7-4 are put into a 110 L container, and then the amount of light anhydrous silicic acid shown in Table 7-4 is added to the container mixer. Mixing was performed at 20 rpm for 10 minutes using (Picks Blender, manufactured by Pickstecnica). Subsequently, magnesium stearate was put into a 110 L container, and the mixture was further mixed at 20 rpm for 5 minutes using a container mixer (Pix Blender manufactured by Pickstechnica).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表7-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 7-5. It was locked and an uncoated tablet was manufactured.
実施例8:イメグリミン塩酸塩を500mg含有する錠剤(8)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表8-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 8: Tablets containing 500 mg of imeglimin hydrochloride (8)
A. Formulation of uncoated tablets containing 500 mg of imeglimin hydrochloride Granulated granules, mixed powders and uncoated tablets having the composition shown in Table 8-1 were produced.
B.製造方法
(1)6.5wt%ヒドロキシプロピルセルロース溶液(2)の調製
1870gの精製水をSUS製のビーカーにとり、撹拌しながら130gのHPC-Lを徐々に投入し、溶解させた。一昼夜静置した後、再度撹拌し、6.5wt%ヒドロキシプロピルセルロース溶液(2)を調製した。B. Production Method (1) Preparation of 6.5 wt% Hydroxypropyl Cellulose Solution (2) 1870 g of purified water was placed in a beaker made of SUS, and 130 g of HPC-L was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 6.5 wt% hydroxypropyl cellulose solution (2).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表8-2に記載の仕込量と表8-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表8-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が36℃になるまで流動させながら混合した。続いて、流動させながら表8-2記載の仕込量の6.5wt%ヒドロキシプロピルセルロース溶液(2)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 8-2 and the production conditions shown in Table 8-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 8-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 36 ° C. Subsequently, the 6.5 wt% hydroxypropyl cellulose solution (2) of the charged amount shown in Table 8-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表8-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。V10型コンテナに、表8-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表8-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで10分間混合した。続いて、V10型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 8-4. Granulated granules containing the imeglimin hydrochloride in the amount shown in Table 8-4 are put into a V10 type container, and then the light anhydrous silicic acid in the amount shown in Table 8-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-5 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V10 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-5 type).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表8-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 8-5. It was locked and an uncoated tablet was manufactured.
実施例9:イメグリミン塩酸塩を500mg含有する錠剤(9)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表9-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 9: Tablet containing 500 mg of imeglimin hydrochloride (9)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 9-1 were produced.
B.製造方法
(1)4wt%ヒプロメロース溶液(1)の調製
1920gの精製水をSUS製のビーカーにとり、撹拌しながら80gのTC-5RTMを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒプロメロース溶液(2)を調製した。B. Production Method (1) Preparation of 4 wt% Hypromellose Solution (1) 1920 g of purified water was placed in a beaker made of SUS, and 80 g of TC- 5RTM was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hypromellose solution (2).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表9-2に記載の仕込量と表9-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表9-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、2分間流動させながら混合した。続いて、混合しながら表9-2記載の仕込量の4wt%ヒプロメロース溶液(1)をスプレーした。さらに、乾燥した後、目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 9-2 and the production conditions shown in Table 9-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 9-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type) and mixed while flowing for 2 minutes. did. Subsequently, the 4 wt% hypromellose solution (1) of the charged amount shown in Table 9-2 was sprayed while mixing. Further, after drying, granules containing imeglimin hydrochloride were prepared through a granulator (Comil 194S type manufactured by Paulek) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表9-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。表9-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒が入ったポリ袋に、表9-4に記載の仕込量の軽質無水ケイ酸を投入し、2分間振り混ぜた。その後、表9-4に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した。
(3) Production of mixed powder containing imeglimin hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 9-4. The amount of light anhydrous silicic acid shown in Table 9-4 was added to a plastic bag containing the granulated granules containing the amount of imeglimin hydrochloride shown in Table 9-4, and the mixture was shaken for 2 minutes. Then, the charged amount of magnesium stearate shown in Table 9-4 was added, and the mixture was further shaken for 1 minute to mix.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表9-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 9-5. It was locked and an uncoated tablet was manufactured.
実施例10:イメグリミン塩酸塩を500mg含有する錠剤(10)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表10-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 10: Tablets containing 500 mg of imeglimin hydrochloride (10)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 10-1 were produced.
B.製造方法
(1)4wt%ポリビニルアルコール溶液(1)の調製
1920gの精製水をSUS製のビーカーにとり、加熱し沸騰させた。加熱した精製水を撹拌しながら80gのGohsenolTM EG-05Pを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、精製水を加えて溶液が2000gになるよう補正し、4wt%ポリビニルアルコール溶液(1)を調製した。B. Production method (1) Preparation of 4 wt% polyvinyl alcohol solution (1) 1920 g of purified water was placed in a beaker made of SUS and heated to a boil. 80 g of Gohsenol TM EG-05P was gradually added and dissolved while stirring the heated purified water. After allowing to stand for a whole day and night, the mixture was stirred again, purified water was added to adjust the solution to 2000 g, and a 4 wt% polyvinyl alcohol solution (1) was prepared.
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表10-2に記載の仕込量と表10-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表10-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、3分間流動させながら混合した。続いて、混合しながら表10-2記載の仕込量の4wt%ポリビニルアルコール溶液(1)をスプレーした。さらに、乾燥した後、目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 10-2 and the production conditions shown in Table 10-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 10-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type) and mixed while flowing for 3 minutes. did. Subsequently, the 4 wt% polyvinyl alcohol solution (1) of the charged amount shown in Table 10-2 was sprayed while mixing. Further, after drying, granules containing imeglimin hydrochloride were prepared through a granulator (Comil 194S type manufactured by Paulek) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表10-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末の製造をした。表10-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒が入ったポリ袋に、表10-4に記載の仕込量の軽質無水ケイ酸を投入し、2分間振り混ぜた。その後、表10-4に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 10-4. The amount of light anhydrous silicic acid shown in Table 10-4 was added to a plastic bag containing the granulated granules containing the amount of imeglimin hydrochloride shown in Table 10-4, and the mixture was shaken for 2 minutes. Then, the amount of magnesium stearate shown in Table 10-4 was added, and the mixture was further shaken for 1 minute to mix.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表10-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 10-5. It was locked and an uncoated tablet was manufactured.
実施例11:イメグリミン塩酸塩を500mg含有する錠剤(11)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表11-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 11: Tablet containing 500 mg of imeglimin hydrochloride (11)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 11-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(5)の調製
2880gの精製水をSUS製のビーカーにとり、撹拌しながら95.99gのHPC-Lを徐々に投入し、続いて24gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(5)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (5) Take 2880 g of purified water in a beaker made of SUS, gradually add 95.99 g of HPC-L while stirring, and then add 24 g of HPC-M. Was gradually added and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (5).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表11-2に記載の仕込量と表11-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表11-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスポビドンを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が38℃になるまで流動させながら混合した。続いて、流動させながら表11-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(5)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 11-2 and the production conditions shown in Table 11-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and crospovidone shown in Table 11-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.), and the exhaust temperature was adjusted. Mixing was carried out while flowing until the temperature reached 38 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (5) of the charged amount shown in Table 11-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表11-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。ポリエチレン製袋に、表11-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表11-4に記載の仕込量の軽質無水ケイ酸を加え、2分間手混合した。続いて、ステアリン酸マグネシウムを投入し1分間手混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 11-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 11-4 are put into a polyethylene bag, and then the amount of light anhydrous silicic acid shown in Table 11-4 is added, and the hands are added for 2 minutes. Mixed. Subsequently, magnesium stearate was added and manually mixed for 1 minute.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表11-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 11-5. It was locked and an uncoated tablet was manufactured.
実施例12:イメグリミン塩酸塩を500mg含有する錠剤(12)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表12-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 12: Tablets containing 500 mg of imeglimin hydrochloride (12)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 12-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(6)の調製
2880gの精製水をSUS製のビーカーにとり、撹拌しながら95.99gのHPC-Lを徐々に投入し、続いて24gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(6)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (6) Take 2880 g of purified water in a beaker made of SUS, gradually add 95.99 g of HPC-L while stirring, and then add 24 g of HPC-M. Was gradually added and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (6).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表12-2に記載の仕込量と表12-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表12-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、デンプングリコール酸ナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が39℃になるまで流動させながら混合した。続いて、流動させながら表12-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(6)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 12-2 and the production conditions shown in Table 12-3. First, the charged amounts of imeglycin hydrochloride, light anhydrous silicic acid, and sodium starch glycolate shown in Table 12-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 39 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (6) of the charged amount shown in Table 12-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表12-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。ポリエチレン製袋に、表12-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表12-4に記載の仕込量の軽質無水ケイ酸を加え、2分間手混合した。続いて、ステアリン酸マグネシウムを投入し1分間手混合した。
(3) Production of mixed powder containing imeglimin hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 12-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 12-4 are put into a polyethylene bag, and then the amount of light anhydrous silicic acid shown in Table 12-4 is added, and the hands are added for 2 minutes. Mixed. Subsequently, magnesium stearate was added and manually mixed for 1 minute.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表12-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 12-5. It was locked and an uncoated tablet was manufactured.
実施例13:イメグリミン塩酸塩を500mg含有する錠剤(13)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表13-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Example 13: Tablets containing 500 mg of imeglimin hydrochloride (13)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 13-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(7)の調製
2880gの精製水をSUS製のビーカーにとり、撹拌しながら95.99gのHPC-Lを徐々に投入し、続いて24gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(7)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (7) Take 2880 g of purified water in a beaker made of SUS, gradually add 95.99 g of HPC-L while stirring, and then add 24 g of HPC-M. Was gradually added and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (7).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表13-2に記載の仕込量と表13-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表13-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)に投入し、排気温度が35℃になるまで流動させながら混合した。続いて、流動させながら表13-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(7)をスプレーした。その後、流動させながら排気温度が45℃になるまで乾燥した後、容器から取り出した。さらに取り出した顆粒を目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 13-2 and the production conditions shown in Table 13-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 13-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type manufactured by Paulek Co., Ltd.) and exhausted. Mixing was carried out while flowing until the temperature reached 35 ° C. Subsequently, the 4 wt% hydroxypropyl cellulose solution (7) of the charged amount shown in Table 13-2 was sprayed while flowing. Then, it was dried while flowing until the exhaust temperature reached 45 ° C., and then taken out from the container. Further, the granules taken out were made into granulated granules containing imeglimin hydrochloride through a granulator (manufactured by Paulek, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表13-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。ポリエチレン製袋に、表13-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表13-4に記載の仕込量の軽質無水ケイ酸を加え、2分間手混合した。続いて、ステアリン酸マグネシウムを投入し1分間手混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 13-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 13-4 are put into a polyethylene bag, and then the amount of light anhydrous silicic acid shown in Table 13-4 is added, and the hands are added for 2 minutes. Mixed. Subsequently, magnesium stearate was added and manually mixed for 1 minute.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表13-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 13-5. It was locked and an uncoated tablet was manufactured.
比較例1:イメグリミン塩酸塩を167mg含有する錠剤(14)
A.イメグリミン塩酸塩167mgを含有する素錠の処方
表14-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Comparative Example 1: Tablet containing 167 mg of imeglimin hydrochloride (14)
A. Formulation of Uncoated Tablets Containing 167 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 14-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(8)の調製
1920gの精製水をSUS製のビーカーにとり、撹拌しながら64gのHPC-Lを徐々に投入し、続いて16gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(8)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (8) Take 1920 g of purified water in a beaker made of SUS, gradually add 64 g of HPC-L while stirring, and then gradually add 16 g of HPC-M. It was put into the water and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (8).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表14-2に記載の仕込量と表14-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表14-2に記載の仕込量のイメグリミン塩酸塩、結晶セルロース、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、3分間流動させながら混合した。続いて、混合しながら表14-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(8)をスプレーした。さらに、乾燥した後、目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 14-2 and the production conditions shown in Table 14-3. First, the charged amounts of imeglimin hydrochloride, crystalline cellulose, light anhydrous silicic acid, and croscarmellose sodium shown in Table 14-2 were put into a fluidized bed granulator / dryer (Multiplex MP-01 type) and flowed for 3 minutes. It was mixed while letting it. Subsequently, the 4 wt% hydroxypropyl cellulose solution (8) of the charged amount shown in Table 14-2 was sprayed while mixing. Further, after drying, granules containing imeglimin hydrochloride were prepared through a granulator (Comil 194S type manufactured by Paulek) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表14-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末の製造をした。表14-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒が入ったポリ袋に、表14-4に記載の仕込量の軽質無水ケイ酸を投入し、2分間振り混ぜた。その後、表14-4に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 14-4. The amount of light anhydrous silicic acid shown in Table 14-4 was added to a plastic bag containing the granulated granules containing the amount of imeglimin hydrochloride shown in Table 14-4, and the mixture was shaken for 2 minutes. Then, the charged amount of magnesium stearate shown in Table 14-4 was added, and the mixture was further shaken for 1 minute to mix.
(4)イメグリミン塩酸塩を167mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に167mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表14-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 167 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 167 mg of imeglimin hydrochloride under the conditions shown in Table 14-5. It was locked and an uncoated tablet was manufactured.
比較例2:イメグリミン塩酸塩を500mg含有する錠剤(15)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表15-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Comparative Example 2: Tablets containing 500 mg of imeglimin hydrochloride (15)
A. Formulation of uncoated tablets containing 500 mg of imeglimin hydrochloride Granulated granules, mixed powders and uncoated tablets having the composition shown in Table 15-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(9)の調製
1152gの精製水をSUS製のビーカーにとり、撹拌しながら36gのHPC-Lを徐々に投入し、続いて12gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(9)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (9) Take 1152 g of purified water in a beaker made of SUS, gradually add 36 g of HPC-L while stirring, and then gradually add 12 g of HPC-M. It was put into the water and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (9).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表15-2に記載の仕込量と表15-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表15-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、3分間流動させながら混合した。続いて、混合しながら表15-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(9)をスプレーした。さらに、乾燥した後目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 15-2 and the production conditions shown in Table 15-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 15-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type) and mixed while flowing for 3 minutes. did. Subsequently, the 4 wt% hydroxypropyl cellulose solution (9) of the charged amount shown in Table 15-2 was sprayed while mixing. Further, after drying, granules containing imeglimin hydrochloride were obtained through a granulator (Comil 194S type manufactured by Paulec) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表15-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末の製造をした。V10型コンテナに、表15-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表15-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで10分間混合した。続いて、V10型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 15-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 15-4 are put into a V10 type container, and then the amount of light anhydrous silicic acid shown in Table 15-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-5 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V10 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-5 type).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表15-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locking machine (manufactured by Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 15-5. It was locked and an uncoated tablet was manufactured.
比較例3:イメグリミン塩酸塩を500mg含有する錠剤(16)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表16-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Comparative Example 3: Tablets containing 500 mg of imeglimin hydrochloride (16)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 16-1 were produced.
B.製造方法
(1)5wt%ヒドロキシプロピルセルロース溶液(3)の調製
1900gの精製水をSUS製のビーカーにとり、撹拌しながら100gのHPC-Lを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、5wt%ヒドロキシプロピルセルロース溶液(3)を調製した。B. Production Method (1) Preparation of 5 wt% Hydroxypropyl Cellulose Solution (3) 1900 g of purified water was placed in a beaker made of SUS, and 100 g of HPC-L was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 5 wt% hydroxypropyl cellulose solution (3).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表16-2に記載の仕込量と表16-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表16-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、排気温度が31℃になるまで混合した。続いて、混合しながら表16-2記載の仕込量の5wt%ヒドロキシプロピルセルロース溶液(3)をスプレーした。さらに、乾燥した後、目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)で整粒してイメグリミン塩酸塩を含有する造粒顆粒とした。この造粒顆粒を2つ製造した。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 16-2 and the production conditions shown in Table 16-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 16-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type), and the exhaust temperature became 31 ° C. It was mixed until it became. Subsequently, the 5 wt% hydroxypropyl cellulose solution (3) of the charged amount shown in Table 16-2 was sprayed while mixing. Further, after drying, the granules were sized by a granulator (Comil 194S type manufactured by Paulec) set to an opening of 1.4 mm and a rotation speed of 1400 rpm to obtain granulated granules containing imeglimin hydrochloride. Two of these granulated granules were produced.
(3)イメグリミン塩酸塩を含有する混合末の製造
表16-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。V10型コンテナに、表16-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒を投入し、続いて表16-4に記載の仕込量の軽質無水ケイ酸を加え、混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで10分間混合した。続いて、V10型コンテナにステアリン酸マグネシウムを投入し、さらに混合機(筒井理化学器械株式会社製、S-5型)を用いて40rpmで5分間混合した。
(3) Production of mixed powder containing imeglimin hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 16-4. Granulated granules containing the amount of imeglimin hydrochloride shown in Table 16-4 are put into a V10 type container, and then the amount of light anhydrous silicic acid shown in Table 16-4 is added to the mixer ( Using Tsutsui Rikagaku Kikai Co., Ltd., S-5 type), mixing was performed at 40 rpm for 10 minutes. Subsequently, magnesium stearate was put into a V10 type container, and further mixed at 40 rpm for 5 minutes using a mixer (manufactured by Tsutsui Rikagaku Kikai Co., Ltd., S-5 type).
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、AQUARIUS3型)を用いて表16-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (Kikusui Seisakusho, AQUARIUS type 3) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 16-5. It was locked and an uncoated tablet was manufactured.
比較例4:イメグリミン塩酸塩を500mg含有する錠剤(17)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表17-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Comparative Example 4: Tablets containing 500 mg of imeglimin hydrochloride (17)
A. Formulation of uncoated tablets containing 500 mg of imeglimin hydrochloride Granulated granules, mixed powders and uncoated tablets having the composition shown in Table 17-1 were produced.
B.製造方法
(1)4wt%ポビドン溶液(1)の調製
1920gの精製水をSUS製のビーカーにとり、撹拌しながら80gのKollidonTM K30を徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ポビドン溶液(1)を調製した。B. Production method (1) Preparation of 4 wt% povidone solution (1) 1920 g of purified water was placed in a beaker made of SUS, and 80 g of Kollidon TM K30 was gradually added and dissolved while stirring. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% povidone solution (1).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表17-2に記載の仕込量と表17-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表17-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、3分間流動させながら混合した。続いて、混合しながら表17-2記載の仕込量の4wt%ポビドン溶液(1)をスプレーした。さらに、乾燥した後、目開きが1000μmの篩を通した後、目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 17-2 and the production conditions shown in Table 17-3. First, the charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, and croscarmellose sodium shown in Table 17-2 were put into a fluidized bed granulation dryer (Multiplex MP-01 type) and mixed while flowing for 3 minutes. did. Subsequently, the 4 wt% povidone solution (1) of the charged amount shown in Table 17-2 was sprayed while mixing. Further, after drying, the granules containing imeglimin hydrochloride are passed through a sieve having an opening of 1000 μm and then through a granulator (Paulec, Comil 194S type) set to an opening of 1.4 mm and a rotation speed of 1400 rpm. And said.
(3)イメグリミン塩酸塩を含有する混合末の製造
表17-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。表17-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒が入ったポリ袋に、表17-4に記載の仕込量の軽質無水ケイ酸を投入し、2分間振り混ぜた。その後、表17-4に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 17-4. The amount of light anhydrous silicic acid shown in Table 17-4 was added to a plastic bag containing the granulated granules containing the amount of imeglimin hydrochloride shown in Table 17-4, and the mixture was shaken for 2 minutes. Then, the charged amount of magnesium stearate shown in Table 17-4 was added, and the mixture was further shaken for 1 minute to mix.
(4)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表17-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 17-5. It was locked and an uncoated tablet was manufactured.
比較例5:イメグリミン塩酸塩を500mg含有する錠剤(18)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表18-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Comparative Example 5: Tablet containing 500 mg of imeglimin hydrochloride (18)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 18-1 were produced.
B.製造方法
(1)イメグリミン塩酸塩を含有する造粒顆粒の製造
表18-1に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、ヒドロキシプロピルセルロース(3.32gのHPC-Mと13.3gのHPC-L)を高速撹拌造粒機(株式会社パウレック製、FM-VG-05型)に投入し、表18-3に記載の条件で2分間混合した。続いて、混合しながら表18-2に記載の仕込量の精製水をパウレック標準スプレーガンを用いてスプレーした後、2分間混合した。撹拌造粒機(株式会社パウレック製、FM-VG-05型)から取り出し、目開きが1000μmの篩を通した後、流動層造粒乾燥機(株式会社パウレック製、マルチプレックスMP-01型)へ投入した。表18-2に記載の条件で流動させながら乾燥を行い、目開き710μの篩を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
B. Production Method (1) Production of Granulated Granules Containing Imeglimin Hydrochloride The amount of imeglimin hydrochloride, light anhydrous silicic acid, hydroxypropyl cellulose (3.32 g HPC-M and 13.3 g) shown in Table 18-1. HPC-L) was put into a high-speed stirring granulator (FM-VG-05 type manufactured by Paulek Co., Ltd.) and mixed for 2 minutes under the conditions shown in Table 18-3. Subsequently, while mixing, the charged amounts of purified water shown in Table 18-2 were sprayed using a Paulek standard spray gun, and then mixed for 2 minutes. Take out from a stirring granulator (Maurek Co., Ltd., FM-VG-05 type), pass through a sieve with a mesh opening of 1000 μm, and then pass through a fluidized bed granulator dryer (Paurek Co., Ltd., multiplex MP-01 type). I put it in. Drying was carried out while flowing under the conditions shown in Table 18-2, and granules containing imeglimin hydrochloride were obtained through a sieve having an opening of 710 μm.
(2)イメグリミン塩酸塩を含有する混合末の製造
表18-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。表18-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒が入ったポリ袋に、表18-4に記載の仕込量の軽質無水ケイ酸、クロスカルメロースナトリウムを投入し、2分間振り混ぜた。その後、表18-4に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した。
(2) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 18-4. Put the light anhydrous silicic acid and croscarmellose sodium in the amount shown in Table 18-4 into a plastic bag containing the granulated granules containing the imeglimin hydrochloride in the amount shown in Table 18-4. Shake for minutes. Then, the charged amount of magnesium stearate shown in Table 18-4 was added, and the mixture was further shaken for 1 minute to mix.
(3)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表18-5の条件で打錠し、素錠を製造した。
(3) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 18-5. It was locked and an uncoated tablet was manufactured.
比較例6:イメグリミン塩酸塩を500mg含有する錠剤(19)
A.イメグリミン塩酸塩500mgを含有する素錠の処方
表19-1の組成からなる混合末および素錠を製造した。
Comparative Example 6: Tablet containing 500 mg of imeglimin hydrochloride (19)
A. Formulation of Uncoated Tablets Containing 500 mg of Imeglimin Hydrochloride A mixed powder and uncoated tablets having the composition shown in Table 19-1 were produced.
B.製造方法
(1)イメグリミン塩酸塩を含有する混合末の製造
表19-2に記載の仕込量でイメグリミン塩酸塩を含有する混合末を製造した。表19-2に記載の仕込量のイメグリミン塩酸塩、軽質無水ケイ酸、ヒドロキシプロピルセルロース、クロスカルメロースナトリウムをポリ袋に投入し、2分間振り混ぜた。その後、表19-2に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した。
B. Production Method (1) Production of Mixed Powder Containing Imeglimin Hydrochloride A mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 19-2. The charged amounts of imeglimin hydrochloride, light anhydrous silicic acid, hydroxypropyl cellulose, and croscarmellose sodium shown in Table 19-2 were placed in a plastic bag and shaken for 2 minutes. Then, the charged amount of magnesium stearate shown in Table 19-2 was added, and the mixture was further shaken for 1 minute to mix.
(2)イメグリミン塩酸塩を500mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に500mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表19-3の条件で打錠し、素錠を製造した。
(2) Production of uncoated tablets containing 500 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 500 mg of imeglimin hydrochloride under the conditions shown in Table 19-3. It was locked and an uncoated tablet was manufactured.
比較例7:イメグリミン塩酸塩を388mg含有する錠剤(20)
A.イメグリミン塩酸塩388mgを含有する素錠の処方
表20-1の組成からなる造粒顆粒、混合末および素錠を製造した。
Comparative Example 7: Tablet containing 388 mg of imeglimin hydrochloride (20)
A. Formulation of Uncoated Tablets Containing 388 mg of Imeglimin Hydrochloride Granulated granules, mixed powder and uncoated tablets having the composition shown in Table 20-1 were produced.
B.製造方法
(1)4wt%ヒドロキシプロピルセルロース溶液(10)の調製
1920gの精製水をSUS製のビーカーにとり、撹拌しながら64gのHPC-Lを徐々に投入し、続いて16gのHPC-Mを徐々に投入して溶解させた。一昼夜静置した後、再度撹拌し、4wt%ヒドロキシプロピルセルロース溶液(10)を調製した。B. Production method (1) Preparation of 4 wt% hydroxypropyl cellulose solution (10) Take 1920 g of purified water in a beaker made of SUS, gradually add 64 g of HPC-L while stirring, and then gradually add 16 g of HPC-M. It was put into the water and dissolved. After allowing to stand for a whole day and night, the mixture was stirred again to prepare a 4 wt% hydroxypropyl cellulose solution (10).
(2)イメグリミン塩酸塩を含有する造粒顆粒の製造
表20-2に記載の仕込量と表20-3に記載の製造条件でイメグリミン塩酸塩を含有する造粒顆粒を製造した。まず、表20-2に記載の仕込量のイメグリミン塩酸塩、結晶セルロース、軽質無水ケイ酸、クロスカルメロースナトリウムを流動層造粒乾燥機(マルチプレックスMP-01型)に投入し、3分間流動させながら混合した。続いて、混合しながら表20-2記載の仕込量の4wt%ヒドロキシプロピルセルロース溶液(10)をスプレーした。さらに、乾燥した後、目開き1.4mm、回転数1400rpmに設定した整粒機(パウレック製、コーミル194S型)を通してイメグリミン塩酸塩を含有する造粒顆粒とした。
(2) Production of Granulated Granules Containing Imeglimin Hydrochloride Granulated granules containing imeglimin hydrochloride were produced under the charging amount shown in Table 20-2 and the production conditions shown in Table 20-3. First, the charged amounts of imeglimin hydrochloride, crystalline cellulose, light anhydrous silicic acid, and croscarmellose sodium shown in Table 20-2 were put into a fluidized bed granulator / dryer (Multiplex MP-01 type) and flowed for 3 minutes. It was mixed while letting it. Subsequently, the 4 wt% hydroxypropyl cellulose solution (10) of the charged amount shown in Table 20-2 was sprayed while mixing. Further, after drying, granules containing imeglimin hydrochloride were prepared through a granulator (Comil 194S type manufactured by Paulek) set to an opening of 1.4 mm and a rotation speed of 1400 rpm.
(3)イメグリミン塩酸塩を含有する混合末の製造
表20-4に記載の仕込量でイメグリミン塩酸塩を含有する混合末の製造をした。表20-4に記載の仕込量のイメグリミン塩酸塩を含有する造粒顆粒が入ったポリ袋に、表20-4に記載の仕込量の軽質無水ケイ酸を投入し、2分間振り混ぜた。その後、表20-4に記載の仕込量のステアリン酸マグネシウムを投入し、さらに1分間振り混ぜて混合した。
(3) Production of mixed powder containing imeglimin hydrochloride The mixed powder containing imeglimin hydrochloride was produced in the amount shown in Table 20-4. The amount of light anhydrous silicic acid shown in Table 20-4 was added to a plastic bag containing the granulated granules containing the amount of imeglimin hydrochloride shown in Table 20-4, and the mixture was shaken for 2 minutes. Then, the charged amount of magnesium stearate shown in Table 20-4 was added, and the mixture was further shaken for 1 minute to mix.
(4)イメグリミン塩酸塩を388mg含有する素錠の製造
イメグリミン塩酸塩が1錠中に388mg含有するようにロータリー式打錠機(菊水製作所製、VELA2型)を用いて表20-5の条件で打錠し、素錠を製造した。
(4) Production of uncoated tablets containing 388 mg of imeglimin hydrochloride Using a rotary locker (manufactured by Kikusui Seisakusho, VELA2 type) so that one tablet contains 388 mg of imeglimin hydrochloride under the conditions shown in Table 20-5. It was locked and an uncoated tablet was manufactured.
試験例1:混合末のかさ密度
実施例1~13及び比較例1、2、4~7について混合末のかさ密度を測定した。かさ密度は25mLメスシリンダーまたは50mLメスシリンダーに約10gの混合末を緩やかに流入させ、粉面高さの目盛りを読み取り、下記式より算出した。その結果を表21に示す。
<かさ密度の計算式>
かさ密度(g/mL)=試料採取量(g)/粉面の高さの目盛り(mL)
Test Example 1: Bulk Density of Mixed Powder The bulk density of the mixed powder was measured for Examples 1 to 13 and Comparative Examples 1, 2, 4 to 7. The bulk density was calculated from the following formula by gently pouring about 10 g of mixed powder into a 25 mL graduated cylinder or a 50 mL graduated cylinder, reading the scale of the powder surface height. The results are shown in Table 21.
<Calculation formula for bulk density>
Bulk density (g / mL) = Sampling volume (g) / Powder surface height scale (mL)
試験例2:打錠性の評価と素錠の形状、硬度、摩損度の測定
実施例1~13および比較例1~7について、打錠性を評価し、素錠の厚み、硬度及び摩損度を測定した。素錠の厚みおよび硬度はERWEKA製のMultiCheck 5を使用し、5錠または10錠の平均値を記載した。また、錠剤の摩損度試験は日本薬局方に記載の試験法に従い、富山産業製のFRIABILATOR TFT-1200を使用して測定した。測定結果を表22に示す。
表22より、実施例1~13は良好な強度を示しており、医薬品として流通させるに十分にたる強度を有していることが明らかとなった。一方で、比較例2及び比較例3はキャッピング錠が発生しており、日本薬局方の錠剤の摩損度試験法の判定基準における物理的強度の指標である1.0%以下を満たすことができず、錠剤として市場に提供することが困難であることが明らかとなった。なお、比較例4~6についてはキャッピングにより打錠することができなかった。この結果から、イメグリミンは圧縮成形性が悪く、錠剤中の薬物含有割合が高くなると打錠障害(キャッピング)が発生しやすいことが分かった。また、錠剤の高薬物含量化させる際に通常選択される攪拌造粒法を用いて製造すると、キャッピングが発生しやすいことが分かった。通常、流動層造粒法は薬物含有割合が高くなると、流動層造粒機内で流動不良が起こり、造粒が難しくなるため、薬物高含有化させる際には用いられない。一方で、イメグリミンでは、処方中に崩壊剤を添加することで、高薬物含有量処方でも流動層造粒機内で流動させることが出来た。また、水溶性高分子結合剤は多量に使用すると、粗大粒が発生し、打錠性や錠剤の溶出性が悪化することが知られているが、あえて水溶性高分子結合剤であるヒドロキシプロピルセルロース、ポリビニルアルコールまたはヒドロキシプロピルメチルセルロースを比較的多量用いることにより、打錠障害が起きない小型化錠剤を製造することが出来た。 Test Example 2: Evaluation of tableting property and measurement of shape, hardness, and abrasion degree of uncoated tablet For Examples 1 to 13 and Comparative Examples 1 to 7, the tableting property was evaluated, and the thickness, hardness, and abrasion degree of the uncoated tablet were evaluated. Was measured. For the thickness and hardness of the uncoated tablets, MultiCheck 5 manufactured by ERWEKA was used, and the average value of 5 tablets or 10 tablets was described. The abrasion degree test of the tablet was measured using a FRIABILATOR TFT-1200 manufactured by Toyama Sangyo in accordance with the test method described in the Japanese Pharmacopoeia. The measurement results are shown in Table 22.
From Table 22, it was clarified that Examples 1 to 13 showed good strength and had sufficient strength to be distributed as a pharmaceutical product. On the other hand, in Comparative Example 2 and Comparative Example 3, capping tablets are generated, and can satisfy 1.0% or less, which is an index of physical strength in the judgment criteria of the tablet abrasion degree test method of the Japanese Pharmacopoeia. However, it became clear that it was difficult to provide it to the market as a tablet. In addition, Comparative Examples 4 to 6 could not be locked by capping. From this result, it was found that imeglimin has poor compression moldability, and when the drug content in the tablet is high, tableting disorder (capping) is likely to occur. It was also found that capping is likely to occur when manufactured using the stirring granulation method usually selected for increasing the drug content of tablets. Normally, the fluidized bed granulation method is not used for increasing the drug content because when the drug content ratio is high, flow failure occurs in the fluidized bed granulator and granulation becomes difficult. On the other hand, with imeglimin, by adding a disintegrant during the formulation, even a high drug content formulation could be fluidized in the fluidized bed granulator. Further, it is known that when a large amount of a water-soluble polymer binder is used, coarse particles are generated and the tableting property and the elution property of the tablet are deteriorated. However, hydroxypropyl, which is a water-soluble polymer binder, is intentionally used. By using a relatively large amount of cellulose, polyvinyl alcohol or hydroxypropylmethyl cellulose, it was possible to produce a miniaturized tablet that does not cause tableting trouble.
試験例3:想定される一日当たりの投与製剤数
想定される一日当たりの投与製剤数を表23に示す。比較例についてはキャッピングにより安定して打錠できなかったため、混合末をカプセルに充填すると仮定して以下の式から算出した。なお、算出した投与製剤数は小数点第1位を切り上げて整数で算出した。
<カプセル剤の投与製剤数の計算式>
投与製剤数 = 2000 mgに相当する混合末の質量(g)/かさ密度(g/mL)/カプセルボディの容量(mL)
<カプセルの大きさ>
1号カプセル
ボディの容積(mL):約0.50
結合時の全長(mm):約19.4
ボディの外径(mm):約6.63
2号カプセル
ボディの容積(mL):約0.37
結合時の全長(mm):約18.0
ボディの外径(mm):約6.07
表23に示されるように、本願により、明らかに一日当たりの投与製剤数を減らすことができ、これにより、生産性の向上及び服薬アドヒアランスの向上が見込まれる。 Test Example 3: Assumed number of administered preparations per day Table 23 shows the assumed number of administered preparations per day. Since the comparative example could not be locked stably due to capping, it was calculated from the following formula assuming that the mixed powder was filled in a capsule. The calculated number of pharmaceutical products was calculated by rounding up to the first decimal place.
<Calculation formula for the number of capsules to be administered>
Number of pharmaceutical products to be administered = mass of mixed powder corresponding to 2000 mg / bulk density (g / mL) / volume of capsule body (mL)
<Capsule size>
Volume 1 capsule body (mL): Approximately 0.50
Overall length (mm) at the time of bonding: Approximately 19.4
Body outer diameter (mm): Approximately 6.63
Volume 2 capsule body (mL): Approximately 0.37
Overall length (mm) at the time of bonding: Approximately 18.0
Body outer diameter (mm): Approximately 6.07
As shown in Table 23, the present application can clearly reduce the number of pharmaceutical formulations administered per day, which is expected to improve productivity and medication adherence.
試験例4:溶出試験
実施例1~実施例13および比較例7で製造した錠剤について、日本薬局方 一般試験法 溶出試験法に従い、以下の条件で溶出試験を実施した。
<溶出試験条件>
方法:日本薬局方一般試験法の溶出試験法(回転バスケット法)
回転数:100rpm
試験液量:900mL
試験液温度:37℃±0.5℃
試験液:溶出試験第2液
試験数:N=3 以上
<試料溶液の調製>
試験液900mLを入れた試験器に錠剤を入れ、試験開始30分後に10mLのシリンジ用いて試験液を5mL採取し、ミリポア社メンブレンフィルター(Millex LG 0.2μm×25mm)用いてゆっくりとろ過する。初めのろ液1mL以上を除き、これを試料溶液の検体とした。
<標準溶液の調製>
イメグリミン塩酸塩を50mL容メスフラスコに27.78mg秤量し、溶出試験第2液を用いて溶解させた。これを標準溶液の検体とした。
<高速液体クロマトグラフィー分析条件>
高速液体クロマトグラフィー 装置:島津製作所製 UFLC-XR
検出波長:240nm
カラム:Phenomenex製、Luna PFP (2) 150 mm × 4.6 mm I.D. 粒子径 3μm
移動相:水/メタノール/トリフルオロ酢酸混液(1000/250/1)
分析時間:6分
流量:1.2mL/min
カラム温度:40℃
注入量:2μL
サンプルクーラー温度:25℃
シリンジ洗浄液:メタノール/水混液(1/4) Test Example 4: Dissolution Test The tablets produced in Examples 1 to 13 and Comparative Example 7 were subjected to a dissolution test under the following conditions in accordance with the Japanese Pharmacopoeia general test method dissolution test method.
<Dissolution test conditions>
Method: Dissolution test method of the Japanese Pharmacopoeia general test method (rotary basket method)
Rotation speed: 100 rpm
Test solution volume: 900 mL
Test solution temperature: 37 ° C ± 0.5 ° C
Test solution: Dissolution test second solution
Number of tests: N = 3 or more <Preparation of sample solution>
Put the tablet in a tester containing 900 mL of the test solution, collect 5 mL of the test solution using a 10 mL syringe 30 minutes after the start of the test, and slowly filter using a Millipore membrane filter (Millex LG 0.2 μm × 25 mm). This was used as a sample of the sample solution except for 1 mL or more of the initial filtrate.
<Preparation of standard solution>
27.78 mg of imeglimin hydrochloride was weighed in a 50 mL volumetric flask and dissolved using the second solution of the dissolution test. This was used as a sample of the standard solution.
<High Performance Liquid Chromatography Analysis Conditions>
High Performance Liquid Chromatography Equipment: UFLC-XR manufactured by Shimadzu Corporation
Detection wavelength: 240nm
Column: Phenomenex, Luna PFP (2) 150 mm x 4.6 mm ID Particle size 3 μm
Mobile phase: Water / methanol / trifluoroacetic acid mixed solution (1000/250/1)
Analysis time: 6 minutes Flow rate: 1.2 mL / min
Column temperature: 40 ° C
Injection volume: 2 μL
Sample cooler temperature: 25 ° C
Syringe cleaning solution: Methanol / water mixture (1/4)
溶出試験結果を表24に示す。
表24に示したとおり、本発明の素錠またはFC錠の溶出は速やかであり、生体内での高い吸収性が見込まれる。また、フィルムコーティングの有無は溶出性に影響しなかった。水溶性高分子結合剤は多量に使用すると、粗大粒が発生し、打錠性や錠剤の溶出性が悪化することが知られているが、本発明ではあえて水溶性高分子結合剤であるヒドロキシプロピルセルロース、ポリビニルアルコールまたはヒドロキシプロピルメチルセルロースを比較的多量に用いることにより、打錠障害が起きない良好な溶出性を示す小型化錠剤を製造することが出来た。The dissolution test results are shown in Table 24.
As shown in Table 24, the uncoated tablet or FC tablet of the present invention is rapidly eluted and is expected to be highly absorbable in vivo. In addition, the presence or absence of film coating did not affect the elution property. It is known that when a large amount of a water-soluble polymer binder is used, coarse particles are generated and the tableting property and the elution property of the tablet are deteriorated. However, in the present invention, hydroxy, which is a water-soluble polymer binder, is intentionally used. By using a relatively large amount of propyl cellulose, polyvinyl alcohol or hydroxypropyl methyl cellulose, it was possible to produce a miniaturized tablet showing good dissolution without causing tableting trouble.
流動層造粒法を用いて製造し、崩壊剤と、水溶性結合剤として高割合のヒドロキシプロセルロース、ポリビニルアルコール及びヒドロキシプロピルメチルセルロースからなる群から選択される1種または2種以上を含有することを特徴とする本願発明により、小型かつ溶出性に優れたイメグリミンの錠剤を、安定生産することが可能となることを見出した。これにより、より効果的かつ、より高い服薬継続率をもたらす錠剤を安定的に提供することが可能になり、より優れた糖尿病治療が可能となる。 Manufactured using a fluidized bed granulation method and containing a disintegrant and one or more selected from the group consisting of a high proportion of hydroxyprocellulose, polyvinyl alcohol and hydroxypropylmethylcellulose as a water-soluble binder. It has been found that the present invention characterized by the above can stably produce imeglimin tablets which are small in size and have excellent elution. As a result, it becomes possible to stably provide tablets that are more effective and bring about a higher dose continuation rate, and it becomes possible to provide better treatment for diabetes.
Claims (36)
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2022097803A JP7671265B2 (en) | 2019-12-13 | 2022-06-17 | Small tablets with excellent manufacturability and dissolution properties |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2019225718 | 2019-12-13 | ||
| JP2019225718 | 2019-12-13 | ||
| PCT/JP2020/046253 WO2021117861A1 (en) | 2019-12-13 | 2020-12-11 | Small-sized tablet having excellent producibility and elution properties |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022097803A Division JP7671265B2 (en) | 2019-12-13 | 2022-06-17 | Small tablets with excellent manufacturability and dissolution properties |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JPWO2021117861A1 JPWO2021117861A1 (en) | 2021-06-17 |
| JPWO2021117861A5 JPWO2021117861A5 (en) | 2022-06-02 |
| JP7093473B2 true JP7093473B2 (en) | 2022-06-29 |
Family
ID=76330003
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2021564057A Active JP7093473B2 (en) | 2019-12-13 | 2020-12-11 | Small tablets with excellent manufacturability and elution |
| JP2022097803A Active JP7671265B2 (en) | 2019-12-13 | 2022-06-17 | Small tablets with excellent manufacturability and dissolution properties |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022097803A Active JP7671265B2 (en) | 2019-12-13 | 2022-06-17 | Small tablets with excellent manufacturability and dissolution properties |
Country Status (5)
| Country | Link |
|---|---|
| JP (2) | JP7093473B2 (en) |
| KR (1) | KR20220113942A (en) |
| CN (1) | CN114945370A (en) |
| TW (1) | TW202135826A (en) |
| WO (1) | WO2021117861A1 (en) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116440075B (en) * | 2023-06-01 | 2025-05-06 | 苏州中化药品工业有限公司 | A dry suspension and preparation method thereof |
Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009523139A (en) | 2006-01-13 | 2009-06-18 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of triazine derivative and insulin secretagogue |
| JP2009523141A (en) | 2006-01-13 | 2009-06-18 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of triazine derivative and HMG-CoA reductase inhibitor |
| JP2012511521A (en) | 2008-12-12 | 2012-05-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of insulin and triazine and its use for treating diabetes |
| WO2014038593A2 (en) | 2012-09-05 | 2014-03-13 | テイカ製薬株式会社 | Granulated material for tablet that rapidly disintegrates in mouth |
| JP2017141289A (en) | 2012-01-06 | 2017-08-17 | エルセリクス セラピューティクス インコーポレイテッド | Biguanide composition and method for treating metabolic disorder |
| WO2017170858A1 (en) | 2016-03-31 | 2017-10-05 | 大日本住友製薬株式会社 | Oral preparation having exceptional elutability |
| JP2018154586A (en) | 2017-03-17 | 2018-10-04 | ライオン株式会社 | tablet |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| TWI436768B (en) | 2010-06-09 | 2014-05-11 | Poxel | Treatment of type 2 diabetes |
| JP7266616B2 (en) * | 2018-06-14 | 2023-04-28 | ポクセル | Film-coated tablets containing triazine derivatives for use in treating diabetes |
-
2020
- 2020-12-11 JP JP2021564057A patent/JP7093473B2/en active Active
- 2020-12-11 TW TW109143784A patent/TW202135826A/en unknown
- 2020-12-11 WO PCT/JP2020/046253 patent/WO2021117861A1/en not_active Ceased
- 2020-12-11 CN CN202080085661.2A patent/CN114945370A/en active Pending
- 2020-12-11 KR KR1020227019247A patent/KR20220113942A/en not_active Withdrawn
-
2022
- 2022-06-17 JP JP2022097803A patent/JP7671265B2/en active Active
Patent Citations (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2009523139A (en) | 2006-01-13 | 2009-06-18 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of triazine derivative and insulin secretagogue |
| JP2009523141A (en) | 2006-01-13 | 2009-06-18 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of triazine derivative and HMG-CoA reductase inhibitor |
| JP2012511521A (en) | 2008-12-12 | 2012-05-24 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | Combination of insulin and triazine and its use for treating diabetes |
| JP2017141289A (en) | 2012-01-06 | 2017-08-17 | エルセリクス セラピューティクス インコーポレイテッド | Biguanide composition and method for treating metabolic disorder |
| WO2014038593A2 (en) | 2012-09-05 | 2014-03-13 | テイカ製薬株式会社 | Granulated material for tablet that rapidly disintegrates in mouth |
| WO2017170858A1 (en) | 2016-03-31 | 2017-10-05 | 大日本住友製薬株式会社 | Oral preparation having exceptional elutability |
| JP2018154586A (en) | 2017-03-17 | 2018-10-04 | ライオン株式会社 | tablet |
Also Published As
| Publication number | Publication date |
|---|---|
| KR20220113942A (en) | 2022-08-17 |
| TW202135826A (en) | 2021-10-01 |
| JPWO2021117861A1 (en) | 2021-06-17 |
| JP2022123069A (en) | 2022-08-23 |
| WO2021117861A1 (en) | 2021-06-17 |
| CN114945370A (en) | 2022-08-26 |
| JP7671265B2 (en) | 2025-05-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR100762847B1 (en) | Multiple unit type sustained release oral preparation and method for preparing same | |
| US6610326B2 (en) | Divalproex sodium tablets | |
| TWI468191B (en) | Formulations of organic compounds | |
| CN104220068B (en) | Pharmaceutical composition comprising olmesartan medoxomil and rosuvastatin or its salt | |
| WO2006070781A1 (en) | Matrix-type controlled release preparation comprising basic substance or salt thereof, and process for production of the same | |
| WO2000009133A1 (en) | Sustained release oral preparations of fasudil hydrochloride | |
| WO2001034147A1 (en) | Oral solid preparation | |
| JP2002531395A (en) | Pharmaceutical combination | |
| JP2014040475A (en) | Novel formulation | |
| CA3224531A1 (en) | A pharmaceutical composition comprising combination of sitagliptin and empagliflozin | |
| WO2013114389A1 (en) | Process for preparing solid oral formulations comprising low dose of entecavir | |
| JP7093473B2 (en) | Small tablets with excellent manufacturability and elution | |
| JP4567640B2 (en) | Miniaturized sarpogrelate hydrochloride oral dosage form | |
| WO2013061338A1 (en) | Pharmaceutical compositions of silodosin | |
| KR100780479B1 (en) | Ibudilast-containing oral preparation and preparation method thereof | |
| CA3094551C (en) | Extended release pharmaceutical composition containing fesoterodine and process for the preparation thereof | |
| HK40074201A (en) | Small-sized tablet having excellent producibility and elution properties | |
| KR20220015437A (en) | Modified release formulations of pyrimidinylamino-pyrazole compounds, and methods of treatment | |
| WO2014096983A1 (en) | Stable pharmaceutical compositions of saxagliptin or salts thereof | |
| JP5563371B2 (en) | Oral tablets containing quetiapine fumarate | |
| EP2233131A1 (en) | Pharmaceutical composition containing levodopa, entacapone and carbidopa | |
| KR102065090B1 (en) | A sustained release formulation including levetiracetam or pharmaceutically acceptable salt thereof, and Method preparing the same | |
| WO2024024865A1 (en) | Levodopa sustained release formulation | |
| EA029709B1 (en) | SOLID ORAL MEDICAL FORM, CONTAINING DECKETOPROPHEN AND TRAMADOL, AND METHOD OF ITS MANUFACTURE | |
| KR102488167B1 (en) | Solid composition of pyrrole carboxamide |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220405 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20220405 |
|
| A871 | Explanation of circumstances concerning accelerated examination |
Free format text: JAPANESE INTERMEDIATE CODE: A871 Effective date: 20220405 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20220524 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20220617 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7093473 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |