JP7355652B2 - 核酸比の決定 - Google Patents
核酸比の決定 Download PDFInfo
- Publication number
- JP7355652B2 JP7355652B2 JP2019566887A JP2019566887A JP7355652B2 JP 7355652 B2 JP7355652 B2 JP 7355652B2 JP 2019566887 A JP2019566887 A JP 2019566887A JP 2019566887 A JP2019566887 A JP 2019566887A JP 7355652 B2 JP7355652 B2 JP 7355652B2
- Authority
- JP
- Japan
- Prior art keywords
- amplification
- cell
- cells
- normalized value
- organism
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- G—PHYSICS
- G06—COMPUTING OR CALCULATING; COUNTING
- G06F—ELECTRIC DIGITAL DATA PROCESSING
- G06F1/00—Details not covered by groups G06F3/00 - G06F13/00 and G06F21/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/02—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving viable microorganisms
- C12Q1/18—Testing for antimicrobial activity of a material
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6813—Hybridisation assays
- C12Q1/6816—Hybridisation assays characterised by the detection means
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/6851—Quantitative amplification
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6844—Nucleic acid amplification reactions
- C12Q1/686—Polymerase chain reaction [PCR]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q1/00—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions
- C12Q1/68—Measuring or testing processes involving enzymes, nucleic acids or microorganisms; Compositions therefor; Processes of preparing such compositions involving nucleic acids
- C12Q1/6876—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes
- C12Q1/6888—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for detection or identification of organisms
- C12Q1/689—Nucleic acid products used in the analysis of nucleic acids, e.g. primers or probes for detection or identification of organisms for bacteria
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B20/00—ICT specially adapted for functional genomics or proteomics, e.g. genotype-phenotype associations
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B20/00—ICT specially adapted for functional genomics or proteomics, e.g. genotype-phenotype associations
- G16B20/10—Ploidy or copy number detection
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B25/00—ICT specially adapted for hybridisation; ICT specially adapted for gene or protein expression
- G16B25/10—Gene or protein expression profiling; Expression-ratio estimation or normalisation
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B25/00—ICT specially adapted for hybridisation; ICT specially adapted for gene or protein expression
- G16B25/20—Polymerase chain reaction [PCR]; Primer or probe design; Probe optimisation
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B40/00—ICT specially adapted for biostatistics; ICT specially adapted for bioinformatics-related machine learning or data mining, e.g. knowledge discovery or pattern finding
- G16B40/20—Supervised data analysis
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16B—BIOINFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR GENETIC OR PROTEIN-RELATED DATA PROCESSING IN COMPUTATIONAL MOLECULAR BIOLOGY
- G16B40/00—ICT specially adapted for biostatistics; ICT specially adapted for bioinformatics-related machine learning or data mining, e.g. knowledge discovery or pattern finding
- G16B40/30—Unsupervised data analysis
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H50/00—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics
- G16H50/20—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics for computer-aided diagnosis, e.g. based on medical expert systems
-
- G—PHYSICS
- G16—INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR SPECIFIC APPLICATION FIELDS
- G16H—HEALTHCARE INFORMATICS, i.e. INFORMATION AND COMMUNICATION TECHNOLOGY [ICT] SPECIALLY ADAPTED FOR THE HANDLING OR PROCESSING OF MEDICAL OR HEALTHCARE DATA
- G16H50/00—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics
- G16H50/50—ICT specially adapted for medical diagnosis, medical simulation or medical data mining; ICT specially adapted for detecting, monitoring or modelling epidemics or pandemics for simulation or modelling of medical disorders
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12Q—MEASURING OR TESTING PROCESSES INVOLVING ENZYMES, NUCLEIC ACIDS OR MICROORGANISMS; COMPOSITIONS OR TEST PAPERS THEREFOR; PROCESSES OF PREPARING SUCH COMPOSITIONS; CONDITION-RESPONSIVE CONTROL IN MICROBIOLOGICAL OR ENZYMOLOGICAL PROCESSES
- C12Q2600/00—Oligonucleotides characterized by their use
- C12Q2600/106—Pharmacogenomics, i.e. genetic variability in individual responses to drugs and drug metabolism
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N2800/00—Detection or diagnosis of diseases
- G01N2800/26—Infectious diseases, e.g. generalised sepsis
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- Physics & Mathematics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- General Health & Medical Sciences (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Biophysics (AREA)
- Medical Informatics (AREA)
- Analytical Chemistry (AREA)
- Molecular Biology (AREA)
- General Engineering & Computer Science (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- Immunology (AREA)
- Public Health (AREA)
- Theoretical Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Evolutionary Biology (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Bioinformatics & Computational Biology (AREA)
- Data Mining & Analysis (AREA)
- Biomedical Technology (AREA)
- Epidemiology (AREA)
- Databases & Information Systems (AREA)
- Primary Health Care (AREA)
- Pathology (AREA)
- Evolutionary Computation (AREA)
- Toxicology (AREA)
- Artificial Intelligence (AREA)
- Bioethics (AREA)
- Computer Vision & Pattern Recognition (AREA)
- Software Systems (AREA)
- Medicinal Chemistry (AREA)
Description
この出願は、2017年12月21日に出願されたオーストラリアの仮特許出願番号2017905138号から優先権を主張し、その内容全体が相互参照により本明細書に組み込まれる。
実施態様1.細胞、生物、またはウイルスからの核酸の増幅によって得られた定量的データを正規化する方法であって、前記方法が以下:
(i)
-第1の遺伝子のゲノムDNAおよび第1の遺伝子から転写されたRNAの増幅からの、および
-細胞、生物、またはウイルスの非転写DNAの配列の増幅からの、
定量的データを取得すること;ならびに
(ii)定量的データを使用して、前記増幅の前に核酸サンプル内に存在する
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
-転写されていない前記ゲノムDNA、に対する、
相対量を表す正規化値(nV)を導き出すこと、
を含む、方法。
実施態様2.定量的データがアンプリコンコピー数であって、ならびに方法が以下:
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物の増幅から生成された総アンプリコン数を表す値A(vA)、および非転写DNAの配列から生成された総アンプリコン数を表す値B(vB)を取得すること;
-式:
vA/vB=nV
またはその等価形を使用して正規化値(nV)を計算すること、
を含む、実施態様1に記載の方法。
実施態様3.定量的データがアンプリコンコピー数であり、方法が以下:
-第1の遺伝子からのゲノムDNAおよびRNA転写産物の増幅、および少なくとも1つのさらなる遺伝子からのゲノムDNAおよびRNA転写産物の増幅
から生成された総アンプリコン数を表す値X(vX)を取得すること;
-非転写DNAの配列から生成された総アンプリコン数を表す値B(vB)を取得すること、
-式:
vX/(vB x(X+1))=nV
(式中Xは前記さらなる遺伝子(複数可)の数である)またはその等価形を使用して正規化値(nV)を計算すること
を含む、
実施態様1に記載の方法。
実施態様4.増幅がデジタルポリメラーゼ連鎖反応(dPCR)である、実施態様2または実施態様3に記載の方法。
実施態様5.定量的データが閾値(Ct)であり、ならびに方法が以下:
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物の増幅からサイクル閾値CtAを取得すること、
-非転写DNAの配列の増幅からサイクル閾値CtBを取得すること;および
-式:
2CtB - CtA=nV
またはその等価形を使用して正規化値(nV)を計算すること
を含む、実施態様1に記載の方法。
実施態様6.定量的データが閾値(Ct)であり、ならびに方法が以下:
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物の増幅、および少なくとも1つのさらなる遺伝子からのゲノムDNAおよびRNA転写産物の増幅
からのサイクル閾値CtXを取得すること;
-非転写DNAの配列の増幅からサイクル閾値CtBを取得すること;および
-式:
2CtB - CtX/(X+1)=nV
(式中Xは前記さらなる遺伝子(複数可)の数である)またはその等価形を使用して正規化値(nV)を計算すること
を含む、実施態様1に記載の方法。
実施態様7.増幅が定量的ポリメラーゼ連鎖反応(qPCR)である、実施態様5または実施態様6に記載の方法。
実施態様8.非転写DNAの配列がゲノムDNAである、実施態様1~7のいずれか1つに記載の方法。
実施態様9.細胞、生物、またはウイルスからの核酸の前記増幅を実施することをさらに含む、実施態様1~8のいずれか1つに記載の方法。
実施態様10.細胞、生物、またはウイルスからの核酸が全核酸の抽出物である、実施態様1~9のいずれか1つに記載の方法。
実施態様11.前記増幅が、以下:ポリメラーゼ連鎖反応(PCR)、逆転写ポリメラーゼ連鎖反応(RT-PCR)、鎖置換増幅(SDA)、ループ介在等温増幅(LAMP)、ローリングサークル増幅(RCA)、リコンビナーゼポリメラーゼ増幅(RPA)、ヘリカーゼ依存性増幅(HDA)、鎖侵入ベース増幅(SIBA)、転写媒介増幅(TMA)、自家持続配列複製(3SR)、核酸配列ベース増幅(NASBA)、またはそれらの任意の組み合わせ:を使用して実施される、実施態様1~10のいずれか1つに記載の方法。
実施態様12.正規化値(nV)を使用して細胞、生物、またはウイルスにおける転写活性のレベルを評価することをさらに含む、実施態様1~11のいずれか1つに記載の方法。
実施態様13.以下:
-転写活性を有しないことが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された転写陰性の正規化値(nV-)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を、転写陰性の正規化値(nV-)と比較して、それにより細胞、生物、またはウイルスにおける転写活性のレベルを評価すること、
をさらに含む、実施態様1~12のいずれか1つに記載の方法。
実施態様14.転写陰性の正規化値(nV-)が、前記一連の前記正規化値(nV)から生成された平均値である、実施態様13に記載の方法。
実施態様15.以下:
-転写陰性の正規化値(nV-)が、細胞、生物またはウイルスにおける転写活性の有無を評価するための基本値として使用され;そして
-転写活性の欠如が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陰性の正規化値(nV-)以下である場合に示され;または
-転写活性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陰性の正規化値(nV-)を上回る場合に示される、
実施態様13および14に記載の方法。
実施態様16.前記転写陰性の正規化値(nV-)が、以下:
-転写活性を有しないことが知られている細胞、生物、もしくはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/または
-前記転写陰性の正規化値(nV-)が、細胞、生物もしくはウイルスにおける転写活性の有無を予測する信頼区間を伴い提供される、
実施態様13~15のいずれか1つに記載の方法。
実施態様17.信頼区間が90%を超える、または95%を超える、実施態様16に記載の方法。
実施態様18.以下:
-転写活性を有することが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された転写陽性の正規化値(nV+)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を転写陽性の正規化値(nV+)と比較して、それにより細胞、生物、またはウイルスにおける転写活性レベルを評価すること
をさらに含む、実施態様13~17のいずれか1つに記載の方法。
実施態様19.転写陽性の正規化値(nV+)は、前記一連の前記正規化値(nV)から生成された平均値である、実施態様18に記載の方法。
実施態様20.以下:
-転写陽性の正規化値(nV+)は、細胞、生物、またはウイルスにおける転写活性の基本値として使用され;および
-転写活性の欠乏(lack)もしくは欠如(absence)が、細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陽性の正規化値(nV+)を下回る場合に示され;または
-転写活性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陽性の正規化値(nV+)以上の場合に示される、
実施態様18または実施態様19に記載の方法。
実施態様21.前記転写陽性の正規化値(nV+)が、以下:
-転写活性を有することが知られている細胞、生物、もしくはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/または
-前記転写陽性の正規化値(nV+)が、細胞、生物もしくはウイルスにおける転写活性の有無を予測する信頼区間を伴い提供される、
実施態様18~20のいずれか1つに記載の方法。
実施態様22.信頼区間が90%を超える、または95%を超える、実施態様21に記載の方法。
実施態様23.以下:
-転写活性を有さないことが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された、転写陰性の正規化値(nV-)を取得すること;
-転写活性を有することが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された、転写陽性の正規化値(nV+)を取得すること;ならびに
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を、以下:
(i)転写陰性の正規化値(nV-)および転写陽性の正規化値(nV+)、または
(ii)転写陰性の正規化値(nV-)および転写陽性の正規化値(nV+)の中間にある合算された転写正規化値(nV±)、
と比較し、
それにより、細胞、生物、またはウイルスにおける転写活性のレベルを評価すること
をさらに含む、実施態様13に記載の方法。
実施態様24.合算された転写正規化値(nV±)が、
式:
(nV+)+(nV-)/2=(nV±)
またはその等価形
を使用して計算される、
実施態様23に記載の方法。
実施態様25.前記合算された転写正規化値(nV±)が、以下:
-前記一連の転写陰性の正規化値(nV-)および/または前記転写陽性の正規化値(nV+)に統計的変動を組み込む;および/または
-前記合算された転写正規化値(nV+)が、細胞、生物、またはウイルスにおける転写活性の有無を予測する信頼区間を伴い提供される
実施態様24に記載の方法。
実施態様26.信頼区間が90%を超える、または95%を超える、実施態様25に記載の方法。
実施態様27.細胞、生物、またはウイルスにおける転写活性のレベルが、以下
-試験細胞または試験生物の生存率;
-試験細胞、生物またはウイルスの生死;
-試験細胞、生物、またはウイルス内の転写の摂動
のいずれか1以上を決定する目的で評価される、実施態様12~26のいずれか1つに記載の方法。
実施態様28.正規化値(nV)を使用して細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価することをさらに含み、以下:
-前記細胞、生物、またはウイルスが、核酸の前記増幅の前に薬剤で処理されており、および
-前記正規化値(nV)が、以下:
(i)薬剤耐性;または
(ii)薬剤感受性、
であることが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成されたコントロールの正規化値(cnV)と比較され、
それにより、細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価する、
実施態様1~11のいずれか1つに記載の方法。
実施態様29.以下:
-薬剤感受性があることが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された薬剤感受性の正規化値(dsV)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を薬剤感受性の正規化値(dsV)と比較して、それにより薬剤耐性または薬剤感受性の、もしくは細胞、生物、またはウイルスにおけるレベルを評価し、細胞、生物、またはウイルスが、核酸の前記増幅の前に薬剤で処理されていること
をさらに含む、実施態様1~11または28のいずれか1つに記載の方法。
実施態様30.薬剤感受性の正規化値(dsV)が、前記一連の前記正規化値(nV)から生成された平均値である、実施態様29に記載の方法。
実施態様31.以下:
-薬剤感受性の正規化値(dsV)が、細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性の有無を評価するための基本値として使用され;および
-薬剤耐性が、細胞、生物もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤感受性の正規化値(dsV)を上回る場合に示され;または
-薬剤感受性が、細胞、生物もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤感受性の正規化値(dsV)以下である場合に示される、
実施態様29または実施態様30に記載の方法。
実施態様32.前記薬剤感受性の正規化値(dsV)が、以下:
-薬剤感受性があることが知られている細胞、生物、またはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/または
-前記薬剤感受性の正規化値(dsV)が以下:
(i)細胞、生物もしくはウイルスにおける薬剤耐性;または
(ii)細胞、生物もしくはウイルスにおける薬剤感受性
の有無を予測する信頼区間を伴い提供される、
実施態様29~31のいずれか1つに記載の方法。
実施態様33.信頼区間が90%を超える、または95%を超える、実施態様32に記載の方法。
実施態様34.以下:
-薬剤耐性があることが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された薬剤耐性の正規化値(drV)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を薬剤耐性の正規化値(drV)と比較して、それにより薬剤耐性もしくは薬剤感受性、または細胞、生物、もしくはウイルスにおけるレベルを評価し、細胞、生物、またはウイルスが核酸の前記増幅の前に薬剤で処理されていることをさらに含む、実施態様1~11または28のいずれか1つに記載の方法。
実施態様35.薬剤耐性の正規化値(drV)が、前記一連の前記正規化値(nV)から生成された平均値である、実施態様34に記載の方法。
実施態様36.以下:
-薬剤耐性の正規化値(drV)が、細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性の有無を評価するための基本値として使用され;および
-薬剤耐性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤耐性の正規化値(drV)以上である場合に示され;または
-薬剤感受性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤耐性の正規化値(drV)を下回る場合に示される、
実施態様34または実施態様35に記載の方法。
実施態様37.前記薬剤耐性の正規化値(drV)が、以下:
-薬剤耐性があることが知られている細胞、生物、またはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/あるいは
-前記薬剤耐性の正規化値(drV)が以下:
(i)細胞、生物もしくはウイルスにおける薬剤耐性;または
(ii)細胞、生物もしくはウイルスにおける薬剤感受性
の有無を予測する信頼区間を伴い提供される、
実施態様34~36のいずれか1つに記載の方法。
実施態様38.信頼区間が90%を超える、または95%を超える、実施態様37に記載の方法。
実施態様39.正規化値(nV)を使用して細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価することをさらに含み、以下:
-核酸の前記増幅の前に薬剤で処理されている前記細胞、生物、またはウイルスの第1の集団を使用して、第1の前記正規化値(nV)を生成し、
-核酸の前記増幅の前に薬剤で処理されていない前記細胞、生物、またはウイルスの第2の集団を使用して、第2の前記正規化値(nV)を生成し、
-前記第1の正規化値(nV)と前記第2の正規化値(nV)を比較して、薬剤処理の有りもしくはなしでの、細胞、生物、またはウイルスにおける転写活性のレベルを評価し、それにより細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価する、
実施態様1~11のうちの1つに記載の方法。
実施態様40.前記薬剤感受性が、前記第1の正規化値(nV)が前記第2の正規化値(nV)よりも低い場合に示される、実施態様39に記載の方法。
実施態様41.薬剤が抗菌剤である、実施態様27~40のいずれか1つに記載の方法。
実施態様42.薬剤が、アミノグリコシド、アンサマイシン、カルバセフェム、カルバペネム、セファロスポリン、グリコペプチド、マクロライドペニシリン、モノバクタム、ポリペプチド、キノロン、スルホンアミド、テトラサイクリンから選択されるクラスの抗菌剤である、実施態様27~41のいずれか1つに記載の方法。
実施態様43.薬剤が、シプロフロキサシン、アジスロマイシン、リファンピシン、またはドキシサイクリンである、実施態様27~42のいずれか1つに記載の方法。
実施態様44.第1の遺伝子が、クラミジア種(例えば、クラミジア・トラコマチス)、ゴノレア種、またはマイコプラズマ種(例えば、マイコプラズマ・ゲニトラリウム(Mycoplasma genitralium))由来の遺伝子である、実施態様27~43のいずれか1つに記載の方法。
実施態様45.第1の遺伝子からの前記ゲノムDNAおよび第1の遺伝子から転写されたRNA、ならびに前記非転写DNAの配列が、同じ反応で共増幅される、実施態様1~44のいずれか1つに記載の方法。
実施態様46.前記反応が逆転写酵素の使用を含む、実施態様45に記載の方法。
実施態様47.細胞が哺乳動物細胞、ヒト細胞、動物細胞、植物細胞、細菌細胞、ウイルスに感染した宿主細胞、または細菌に感染した宿主細胞である、実施態様1~46のいずれか1つに記載の方法。
実施態様48.生物が、哺乳動物、ヒト、植物、細菌、ウイルス、真菌、藻類、古細菌または原生動物である、実施態様1~47のいずれか1つに記載の方法。
実施態様1.細胞または生物の転写活性を評価する方法であって、
以下:
-細胞または生物からの全核酸に対して核酸増幅反応を行い、核酸増幅が以下:
全核酸サンプルを、第1の遺伝子からのゲノムDNAおよび第1の遺伝子から転写されたRNAを増幅できる1つまたは複数のプライマーと接触させること、
全核酸サンプルを、細胞または生物で転写されない非コードゲノムDNAの領域を増幅することができる1つまたは複数のプライマーと接触させること;
を含み:
-核酸増幅反応の速度論を分析して、以下:
(i)第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
(ii)非コードDNAの前記領域、に対する
比率を導き出し、
比率が、核酸増幅反応を行う前の全核酸サンプル内に存在する(i)および(ii)の相対量を表すこと;ならびに
-比率を分析して、細胞または生物の転写活性を評価し、以下:
1の比率は、細胞または生物に転写活性がないことを示し、
および
1を超える比率は、細胞もしくは生物に転写活性が存在するか、または存在し得ることを示すこと
を含む方法。
実施態様2.1.5、1.7、1.9、2、2.2、2.4、2.5、2.7、2.9または3を超える比が、細胞または生物における転写活性を示す、実施態様1に記載の方法。
実施態様3.1.5、1.4、1.3、1.2または1.1未満の比が細胞または生物における転写活性の欠如を示す、実施態様1に記載の方法。
実施態様4.細胞または生物の生存を評価する方法であって、
以下:
-細胞または生物の全核酸(total nucleic acid the cell or organism)に対して核酸増幅反応を行い、核酸増幅が以下:
全核酸サンプルを、第1の遺伝子からのゲノムDNAおよび第1の遺伝子から転写されたRNAを増幅できる1つまたは複数のプライマーと接触させること、
全核酸サンプルを、細胞または生物で転写されない非コードゲノムDNAの領域を増幅することができる1つまたは複数のプライマーと接触させること;
を含み:
-核酸増幅反応の速度論を分析して、以下:
(i)第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
(ii)非コードDNAの前記領域、に対する
比率を導き出し、
比率が、核酸増幅反応を行う前の全核酸サンプル内に存在する(i)および(ii)の相対量を表すこと;ならびに
-比率を分析して、細胞または生物の転写活性を評価し、以下:
1の比率は、細胞または生物が生存していないことを示し、および
1を超える比率は、細胞または生物が生存している、または生存し得ることを示すこと
を含む方法。
実施態様5.1.5、1.7、1.9、2、2.2、2.4、2.5、2.7、2.9または3を超える比が、細胞または生物が生存していることを示す、実施態様4に記載の方法。
実施態様6.1.5、1.4、1.3、1.2または1.1未満の比が、細胞または生物が生存していないことを示す、実施態様4に記載の方法。
実施態様7.細胞または生物が死んでいるかを決定する方法であって、
以下:
-細胞または生物からの全核酸に対して核酸増幅反応を行い、核酸増幅が以下:
全核酸サンプルを、第1の遺伝子からのゲノムDNAおよび第1の遺伝子から転写されたRNAを増幅できる1つまたは複数のプライマーと接触させること、
全核酸サンプルを、細胞または生物で転写されない非コードゲノムDNAの領域を増幅することができる1つまたは複数のプライマーと接触させること;
を含むこと:
-核酸増幅反応の速度論を分析して、以下:
(i)第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
(ii)非コードDNAの前記領域、に対する
の比率を導き出し、
比率が、核酸増幅反応を行う前の全核酸サンプル内に存在する(i)および(ii)の相対量を表すこと;ならびに
-比率を分析して、細胞または生物の転写活性を評価し、以下:
1の比率は、細胞または生物が死んでいることを示し、および
1を超える比率は、細胞または生物が生きている、または生きている可能性があることを示すこと
を含む方法。
実施態様8.1.5、1.7、1.9、2、2.2、2.4、2.5、2.7、2.9または3を超える比が、細胞または生物が生きていることを示す、実施態様7に記載の方法。
実施態様9.1.5、1.4、1.3、1.2または1.1未満の比が、細胞または生物が生きていないことを示す、実施態様7に記載の方法。
実施態様10.細胞内の転写の摂動を検出するための方法であって、
以下:
-細胞または生物からの全核酸に対して核酸増幅反応を行い、核酸増幅が以下:
全核酸サンプルを、第1の遺伝子からのゲノムDNAおよび第1の遺伝子から転写されたRNAを増幅できる1つまたは複数のプライマーと接触させること、
全核酸サンプルを、細胞または生物で転写されない非コードゲノムDNAの領域を増幅することができる1つまたは複数のプライマーと接触させること;
を含むこと:
-核酸増幅反応の速度論を分析して、以下:
(i)第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
(ii)非コードDNAの前記領域、に対する
の比率を導き出し、
比率が、核酸増幅反応を行う前の全核酸サンプル内に存在する(i)および(ii)の相対量を表すこと;ならびに
-比率を分析して、細胞または生物の転写活性を評価し、以下:
1の比率は、細胞または生物の完全な転写の摂動を示し、
および
1を超える比率は、細胞または生物における転写の摂動の欠如を示すこと
を含む方法。
実施態様11.1.5、1.7、1.9、2、2.2、2.4、2.5、2.7、2.9または3を超える比が、細胞または生物における転写の摂動の欠如を示す、実施態様10に記載の方法。
実施態様12.1.5、1.4、1.3、1.2または1.1未満の比が、細胞または生物における部分的または完全な転写の摂動を示す、実施態様10に記載の方法。
実施態様13.前記核酸増幅反応中に、以下:
(i)非コードDNAの前記領域、および
(ii)第1の遺伝子の前記ゲノムDNAとRNA転写産物;
のサイクル閾値(Ct)の値を生成すること、ならびに前記値を比較することにより比率を得ることを含む、
実施態様1~12のいずれか1つに記載の方法。
実施態様14.以下:
-第1の遺伝子の前記ゲノムDNAとRNA転写産物のサイクル閾値ctAを生成し、および、核酸増幅反応の開始後に、非コードDNAの前記領域のサイクル閾値CtBを生成すること;
-式:
2CtB-CtA=2ΔCt
を使用して、CtB値およびctA値の間の倍数変化を計算すること;ならびに
-式:
2ΔCt/TR
を使用して比率を生成し
TRが、細胞の全核酸サンプル中の非コードゲノムDNAの領域のコピーに対する第1の遺伝子のゲノムDNAのコピーの比率であること
を含む、実施態様1~13のいずれか1つに記載の方法。
実施態様15.以下:
-全核酸サンプルを、第2の遺伝子からのゲノムDNAおよび第2の遺伝子から転写されたRNAを増幅することができる1つまたは複数のプライマーと接触させることをさらに含む核酸増幅反応を行うこと、ならびに
-核酸増幅反応の速度論を分析して、以下:
(i)非コードDNAの前記領域の、
(ii)核酸増幅反応を行う前に、全核酸サンプル内に存在する第1および第2の遺伝子の前記ゲノムDNAおよびRNA転写産物に対する
相対量を表す比率を導き出すことの、
実施形態1~14のいずれか1つに記載の方法。
実施態様16.以下:
-第1および第2の遺伝子の前記ゲノムDNAおよびRNA転写産物のサイクル閾値ctAを生成し、および、核酸増幅反応の開始後に、非コードDNAの前記領域のサイクル閾値CtBを生成すること;
-式:
2CtB-CtA=2ΔCt
を使用して、CtB値およびctA値の間の倍数変化を計算すること
-式
2ΔCt/TR
を使用して比率を生成し
TRは、第1および第2の遺伝子のゲノムDNAのコピーの、細胞の全核酸サンプル中の非コードゲノムDNAの領域のコピーに対する比であること
を含む、実施態様15に記載の方法。
実施態様17.比の前記分析が、一連の陰性または陽性のコントロール細胞または生物での方法を行うことから得られた比と閾値の比を比較すること、および表現型を示す平均閾値の比の値を得ることを含む、実施態様1~16のいずれか1つに記載の方法。
実施態様18.細胞または生物の薬剤耐性または薬剤感受性を検出するための方法であって、以下:
-薬剤で処理されていない細胞または生物の第1のサンプルから得られた全核酸に対して第1の核酸増幅反応を行うこと;ならびに
-薬剤で処理されている細胞または生物の第2のサンプルから得られた全核酸に対して第2の核酸増幅反応を行い;
各前記核酸増幅反応は別々に行われ、および以下:
全核酸サンプルを、第1の遺伝子からのゲノムDNAおよび第1遺伝子から転写されたRNAを増幅できる1つまたは複数のプライマーと接触させること、
全核酸サンプルを、細胞または生物で転写されない非コードゲノムDNAの領域を増幅することができる1つまたは複数のプライマーと接触させること
を含むこと;
-以下:
(i)第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
(ii)非コードDNAの前記領域、に対する
第1および第2の比率を得るために、前記各核酸増幅反応の速度論を分析し、
比率が、核酸増幅反応を行う前の全核酸サンプルに存在する(i)および(ii)の相対量を表すこと;ならびに
-比率を比較して、細胞または生物が薬剤に耐性を有するか否かを評価し、以下:
第1と第2の比率が等しい場合、細胞または生物における完全な薬剤耐性が示され、および
第2の比率が第1の比率より低い場合、薬剤に対する細胞または生物の感受性が示されること
を含む、方法。
実施態様19.第2の比の値が、以下:1%、2%、5%、7.5%、10%、12%、15%または20%以下;第1の比率の値よりも低い場合、細胞または生物が薬剤耐性を有するとみなされる、実施態様18に記載の方法。
実施態様20.第2の比の値が、第1の比率より少なくとも:10%、20%、30%、40%または50%である場合、細胞または生物が薬剤感受性があるとみなされる、実施態様18に記載の方法。
実施態様21.増幅方法が、以下:ポリメラーゼ連鎖反応(PCR)、鎖置換増幅(SDA)、ヘリカーゼ依存性増幅(HDA)、リコンビナーゼポリメラーゼ増幅(RPA)、ループ媒介等温増幅(LAMP)、ローリングサークル増幅(RCA)、転写媒介増幅(TMA)、自立式配列複製(3SR)、核酸配列ベース増幅(NASBA)、逆転写ポリメラーゼ連鎖反応(RT-PCR)、およびその任意の組み合わせからなる群から選択される、
実施態様1~20のいずれか1つに記載の方法。
実施態様22.細胞が、哺乳動物細胞、ヒト細胞、植物細胞、細菌細胞、ウイルスに感染した宿主細胞、または細菌に感染した宿主細胞である、実施態様1~21のいずれか1つに記載の方法。
実施態様23.生物が、細菌、ウイルス、真菌、藻類、古細菌または原生動物である、実施形態1~21のいずれか1つに記載の方法。
本明細書で使用される場合、単数形「a」、「an」、および「the」には、文脈からそうでないことが明確に示されていない限り、複数の参照が含まれる。例えば、句「ポリヌクレオチド」には、複数のポリヌクレオチドも含まれる。
以下の略語は、本明細書および明細書全体で使用される:
GAT:遺伝子および転写
NED:非発現DNA
FC:倍数変化
TR:理論比
Ct:閾値サイクル/サイクル閾値
DMEM:ダルベッコ改変イーグル培地
LLE:液液抽出
MOI:感染の多重度
PI:感染後
PT:処理後
TNA:全核酸
IF:免疫蛍光
IFU:封入体形成単位
MIC:最小阻止濃度
TOC:治癒試験
NAAT:核酸増幅技術
STI:性感染症
AMR:抗菌剤耐性
EMA:エチジウムモノアジド
PMA:プロポジウムモノアジド
MNAzyme:多成分核酸酵素、または多分割核酸酵素;
パートザイム(Partzyme):オリゴヌクレオチドを含む部分酵素;
ave;平均
PCR:ポリメラーゼ連鎖反応;
gDNA:ゲノムDNA
dsDNA:二本鎖DNA
rc:逆相補体
NTC:鋳型なしコントロール
qPCR:リアルタイム定量PCR
R2;相関係数
nM;ナノモラー
mM;ミリモラー
μL;マイクロリットル
dNTP;デオキシリボヌクレオチド三リン酸
NF-H2O:ヌクレアーゼフリー水;
F:フルオロフォア;
Q:クエンチャー;
N = A、C、T、G、またはその任意の類似体;
N’= N に相補的な、またはNと塩基対となり得る任意のヌクレオチド;
W:AまたはT;
R:A、G、またはAA;
rN:任意のリボヌクレオチド塩基;
rR:AまたはG;
rY:CまたはU;
M:AまたはC;
H:A、C、またはT;
D:G、A、またはT;
JOEまたは6-JOE:6-カルボキシ-4',5'-ジクロロ-2'、7'-ジメトキシフルオレセイン;
FAMまたは6-FAM:6-カルボキシフルオレセイン。
BHQ1:ブラックホールクエンチャー1
BHQ2:ブラックホールクエンチャー2
RT-PCR:逆転写ポリメラーゼ連鎖反応
SDA:鎖置換増幅
HDA:ヘリカーゼ依存性増幅
RPA:リコンビナーゼポリメラーゼ増幅
LAMP:ループ媒介等温増幅
RCA:ローリングサークル増幅
TMA:転写媒介増幅
3SR:自家持続配列複製
NASBA:核酸配列ベース増幅
IB:アイオワブラック(登録商標)FQ
IBR:アイオワブラック(登録商標)RQ
mRNA:メッセンジャーRNA
tRNA:トランスファーRNA
rRNA:リボソームRNA
以下の詳細な説明は、当業者が本発明を実施できるように、本発明の例示的な実施態様を十分詳細に伝える。説明した様々な実施態様の特徴または限定は、必ずしも本発明の他の実施態様または本発明全体を限定するものではない。したがって、以下の詳細な説明は、本発明の範囲を限定するものではなく、それは特許請求の範囲によってのみ定義される。
この戦略には、特定の遺伝子およびそれらのRNA転写産物の増幅が含まれ、そして転写されないことが知られている特定のDNA配列に対して正規化される。RT-PCR中、特定の転写産物を標的とするプライマーは、それが転写された遺伝子も増幅する。遺伝子およびその関連転写産物の測定は、本明細書ではGAT(Gene And Transcript)と呼ばれる。さらに、RT-PCR中に、RNAに転写されないDNA領域のためにプライマーが存在する場合、このDNAのみを増幅することもできる。これはNED(Non-Expressed DNA)と呼ばれる。GATおよびNEDを同時に推定するための標的増幅プロトコルはVITA(Viable Transcript Analysis)試験と呼ばれ、したがって増幅がPCRによる場合、この方法はVITA PCRと呼ばれる。
本発明の方法は、核酸増幅反応から生じる産物の量的測定に適用することができる。標的DNAおよび/または標的RNA(例えば、mRNA)配列からアンプリコンを生成することができる任意の核酸増幅反応を使用できる。例えば、逆転写酵素PCR(RT-PCR)、定量的PCR(qPCR)、および/またはデジタルPCR(dPCR)などのポリメラーゼ連鎖反応(PCR)増幅を使用し得る。適切な増幅反応の他の非限定的な例には、鎖置換増幅(SDA)、ループ媒介等温増幅(LAMP)、ローリングサークル増幅(RCA)、リコンビナーゼポリメラーゼ増幅(RPA)、ヘリカーゼ依存性増幅(HDA)、鎖侵入ベース増幅(SIBA)、転写媒介増幅(TMA)、自家持続配列複製(3SR)、核酸配列ベース増幅(NASBA)、およびそれらの組み合わせが含まれる。
本発明の方法は、転写の程度に着目した任意の適切な対象に適用することができる(例えば、転写レベル、転写の摂動、生存、死、薬剤および他の化合物などの剤への応答、などのいずれか1以上の測定として)。
いくつかの実施態様において、本発明は、細胞、生物またはウイルス(など)における転写活性の有無を予測する、合算された転写正規化値(nV±)を決定する方法を提供する。同様の方法は、(i)薬剤に耐性があり、(ii)薬剤に感受性があることが知られている細胞、生物、またはウイルスの集団など、サンプルの2つの集団間の転写活性の差を決定するために適用され得る。
nV±は、nV +の下位検定の臨界点、および上位検定nV-の臨界点の中間点として計算でき、どちらも95%の信頼レベルである。
nV±=((nV+ - 1.645*δ+) + (nV- + 1.645*δ-)) / 2
式中:
nV+は、転写活性を有することが知られている細胞、生物、またはウイルスの集団の個々から得られたnV値の平均である。
nV-は、転写活性を有しないことが知られている細胞、生物、またはウイルスの集団の個々から得られたnV値の平均である。
δ+は、転写活性および臨界点を有することが知られている細胞、生物、またはウイルスの集団の個々から得られたnV値の標準偏差である。
δ-は、転写活性を有しないことが知られている細胞、生物、またはウイルスの集団の個々から得られた標準偏差nV値である。
これより、以下の特定の実施例を参照して本発明を説明するが、これは決して限定するものとして解釈されるべきではない。
クラミジア・トラコマチス(血清型D、実験室株UW-3/Cx)サンプルをHEp-2細胞で増殖させ、処理せず(抗生物質アジスロマイシンとインキュベートせず)、「生きた細菌」のポジティブコントロールを再現するか、または異なる濃度のアジスロマイシンとでインキュベートし、死んだ細菌をシミュレートするサンプルを作製するかのいずれかにした(アジスロマイシンはクラミジア性器感染症の第一選択治療である)。条件は次の通りであった。
感染後(PI)4時間に、DMEMを交換し、抗生物質アジスロマイシン(Sigma Aldrich)を様々な用量で添加し、回収するまで5%CO2、37℃で再度インキュベートした。使用した異なる抗生物質濃度は、i)抗生物質なし(0 μg/mL)、ii)<MIC(0.008 μg/mL)、iii)MIC(0.064 μg/mL)、およびiv)>MIC(0.512 μg/mL)であった。これらの実験のために選択された「MIC用量」は、この現在の株を使用した実験室で観察されたものよりわずかに多い;しかしながら、再現性のあるバクテリアの死滅を保証するために特に選択された。使用される用量は、文献に記載されているMIC分析とも一致する。PI44時間で、ショ糖-リン酸-グルタミン酸(SPG)緩衝液(250 mMのショ糖、10 nMのリン酸ナトリウムおよび5 mMのL-グルタミン酸)を使用して細胞を回収した。体積の半分は、免疫蛍光染色による生存率の計数のために保存され(1.2生存率/免疫蛍光染色を参照);他の半分は、TNAおよび/またはRNAの抽出用に保持された。サンプルは、さらに処理するまで-80℃で保存した。各条件でトリプリケートで培養した。
PI4時間に、DMEMを交換し、シクロヘキシミドを添加して、インキュベーションを続けた。指数関数成長期において一度、PI24時間で、処理を行った。これは、各感染のDMEMを交換し、i)抗生物質なし、またはii)アジスロマイシン(0.128 μg/mL)のMICよりも高いレベルの抗生物質を添加することで達成された。その後、SPGバッファーを使用して処理後(PT)30分、1時間、または6時間でサンプルを回収し、さらに処理するまで-80℃で保存した。
感染後、4時間の時点で培地の交換はなく、本質的に非同調的な集団が作製され、これは、in vivo条件により似ている。指数関数成長期において一度、PI20時間で、処理を行った。これは、各ウェルのDMEMを交換し、i)抗生物質なし、またはii)抗生物質(0.256 μg/mLリファンピシン)を添加することのいずれかで達成された。次に、サンプルを5%CO2、37℃でインキュベートし、PT 5分後に回収した;または室温でインキュベートし、PT 15分後に回収した。回収にはSPGバッファーを使用し、直後にTNAを抽出した。この処理プロトコルに使用された株は、1)リファンピシンに感受性の血清型D 実験室株(UW-3/Cx)、および5)リファンピシンに耐性の、血清型L2 実験室作製変異株であった。
感染後、4時間の時点で培地の交換はなかった。指数関数的増殖期において一度、PIの20時間または24時間のいずれかで、各ウェルのDMEMを交換し、望ましい量の抗生物質を添加することにより達成されるアジスロマイシンの様々な用量で細胞を処理した。感染に対して加えた抗生物質処理の用量は、i)抗生物質なし、ii)0.128 μg/mL、iii)0.192 μg/mL、iv)0.256 μg/mL、およびv)0.512 μg/mLであった。次に、サンプルを5%CO2、37℃でインキュベートし、SPGバッファーを使用してPT 1時間で回収し、さらに処理するまで-80℃で保存するか、または回収直後に抽出した。
感染後、4時間の時点で培地の交換はなかった。指数関数的増殖期において一度、PI20時間で、細胞を異なる抗生物質の単一の用量で処理した。使用した抗生物質は、i)アジスロマイシン、ii)ドキシサイクリン、およびiii)リファンピシンで、それぞれ0.256 μg/mLの用量であった。この処理プロトコルに使用された株は、株 1)血清型D 実験室株(UW-3/Cx)、株 2)血清型L2野生型実験室株(434/Bu)、株 3)血清型L2実験室作製変異株、トリメトプリム耐性、株 4)血清型L2実験室作製変異株、スペクチノマイシン耐性、および株 5)血清型L2実験室作製変異株、リファンピシン耐性、であった。すべての血清型および各抗生物質のMICは、文献に記載された標準手順を使用して、事前に決定され、以下の表にリストした。MIC分析(表1)によると、使用されたすべての株は、抗生物質アジスロマイシンおよびドキシサイクリンに感受性があった。株1、2、3、および4はリファンピシンにも感受性があり、株5はその同じ抗生物質に耐性がある。次に、サンプルを5%CO2、37℃でインキュベートし、SPGバッファーを使用して、PT 1時間で回収し、すぐに抽出した。各条件について2つの生物学的レプリケートを得た。
PI 4時間で、DMEMを交換し、シクロヘキシミド(1 μg/mL)を添加して、感染を同調させ、宿主細胞によるタンパク質の産生を停止した。この時点で、抗生物質の添加も行われ、半分の数のウェルが未処理のままにし、他の半分は高用量の抗生物質のアジスロマイシンで処理した。回収するまで、細胞を再度5%CO2、37℃でインキュベートした。使用された異なる条件は、i)「Alive CT」を表す抗生物質なし、またはii)「Dead CT」を表す-抗生物質プラス(0.512 μg/mL)であった。PI 44時間で、SPGバッファーを使用して細胞を回収し、および様々な比率で混合して、以下の表に示すように、生細胞および非生細胞の割合を変えたサンプルを作製した。体積の半分は、免疫蛍光染色による生存率のカウントのために保存され(1.2生存率/免疫蛍光染色を参照;データは含まれていない);他の半分はTNAの抽出のために保持された。これらは、次いで、さらに処理されるまで-80℃で保存された。
生存を測定するために回収したサンプルを連続希釈し、平底96ウェルプレート(Nunc(商標)、Thermo Fisher)上にある、新鮮なHEp-2単層上で培養した。感染は、28℃の温度で30分間、500 gでの遠心分離のアシストによる接種により完了し、その後5%CO2、37℃でインキュベートした。各サンプルをトリプリケートで培養した。PI 38時間で、培養物をメタノールで固定し、および顕微鏡検査のために染色した。
1.3.1 抽出プロトコルA
TNA抽出のために回収したサンプルを氷上で解凍し、細胞破片を4℃で10分間800 gでペレット化し、その後4℃で20分間14000 rpmで上清を遠心分離した。ペレットをプロテイナーゼK消化ミックス(10 mg/mL プロテイナーゼK(Ambion)、1mM Tris pH7.5、0.5M EDTA、5M NaCl、10%SDSおよびヌクレアーゼフリー水(Ambion)に再懸濁し、56℃で60分インキュベートした。消化後、フェノール:クロロホルム:イソアミル(25:24:1、pH 6.5~6.9、Sigma Aldrich)を混合物に添加し、激しくボルテックスし、最大速度で5分間遠心分離した。酢酸ナトリウム(3M、pH5.2、Sigma Aldrich)および100%エタノール(Sigma Aldrich)を添加して上相を維持した。これを再びボルテックスし、20分間(室温で10分間、-20℃で10分間)インキュベートした。次に、TNAを10分間高速(14000 rpm)でペレット化し、その後70%エタノールを使用した洗浄ステップを2回行った。次に、ペレットを15分間風乾し、その後50 μLの水で溶出した。溶出液を定量し、-80℃で保存した。
回収したサンプルを氷上で解凍した後、4℃で20分間、14000rpmで細胞をペレット化した。このステップの後、PuriSpin FireMonkey抽出キット(RevoluGen)を使用して、DNAおよびRNAを同時に抽出するために製造業者の指示に従った。
回収したサンプルを氷上で解凍した後、4℃で20分間、14000rpmで細胞をペレット化した。このステップに続いて、追加のオンカラムDNase消化を伴う、動物細胞からの全RNAの精製のための製造業者の指示に従った。抽出はRNeasy Mini Kit(Qiagen)を使用して行った。
以下の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出したTNAサンプルのDNAおよびGATのレベルを推定する。TNAは、実施例1(1.1.1処理プロトコルA)で記載したように、抗生物質とインキュベートしていない細胞(未処理、生細胞)、およびMICの8分の1(<MIC)、MIC(MIC)またはMICの8倍(>MIC)の濃度の抗生物質とインキュベートした細胞から抽出した。omp1遺伝子およびその転写産物を標的とするプライマーを使用して、クラミジアDNAおよびRNAを増幅した。GATのレベルは、omp1遺伝子およびその転写産物(DNAプラスRNA)の両方が増幅されたRT-PCRによって推定された。omp1遺伝子のみ(DNAのみ)のレベルは、逆転写酵素を含まない別個のPCRで測定した。
パートザイムは、omp1遺伝子またはomp1転写産物の両方の増幅によって生成されたアンプリコンに結合すると、活性のMNAzymeに集合するように設計された。一旦集合すると、MNAzymeはレポーター基質Sub2-FBを切断できる。パートザイムAおよびパートザイムBの配列を、5'から3'の順で、以下にリストした。太字の塩基は標的とハイブリダイズし、下線が引かれた塩基は、集合されたMNAzymeの触媒中心の一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、基質は5'末端の6-FAM部分(以下基質名の「F」で示される)および3'末端のIABkFQクエンチャー部分(以下基質名の「IB」で示される)で末端標識された。492 nm(FAM励起波長)で励起しながら、516 nm(FAM蛍光波長)で基質の切断をモニターした。この実施例のレポーター基質は、5'から3'の順で、配列が以下に示されている。小文字の塩基はRNAを表しおよび大文字の塩基はDNAを表す。
クラミジア・トラコマチスに感染した細胞から抽出されたTNA鋳型のin vitro増幅は、以下にリストされたプライマーを使用して行われた。フォワードプライマーとリバースプライマーは、PCRでomp1遺伝子内のDNAを増幅するために使用され、ならびにomp-1遺伝子および転写産物内の、DNAおよびRNAの両方をRT-PCRにより増幅するために使用された。すべての配列は5'から3'の順で記入する。
RNAおよびDNA(TNA)は、実施例1(1.1 培養および1.1.1 処理プロトコルA)にしたがってHEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、フェノール:クロロホルム:イソアミルを使用する、実施例1(1.3 全核酸(TNA)抽出、1.3.1抽出プロトコルA)にも記載されている液-液抽出(LLE)技術として行われた。
PCRおよびRT-PCRミックスの両方には、全体積20 μLに、40 nMの5'プライマー、200 nMの3'プライマー、200 nMのパートザイムA、200 nMのパートザイムB、200 nMのSub2-FB、1xSensiFASTプローブNo-ROXミックス(Bioline)、8 mM MgCl2(Bioline)、およびヌクレアーゼフリー水(Ambion)が含まれていた。さらに、RT-PCRミックスには、0.2 U/μL RiboSafe RNase 阻害剤(Bioline)と0.2 μLの逆転写酵素(Bioline)が含まれていた。反応は、BioRad(登録商標)CFX96サーモサイクラーで同じサイクリングパラメータを使用してトリプリケートで:48℃で10分間、95℃で2分間、95℃で5秒間および61℃で30秒間(サイクルあたりマイナス0.5℃)を10サイクル、および95℃で5秒間、52℃で50秒間を30サイクル、で行った。RT-PCRおよびPCRミックスは、5 μLのTNA鋳型(1/100希釈)が含まれていたか、または鋳型なし(dH2O)かのいずれかであった。
クラミジアDNAおよびRNA(GAT)、またはDNAのみ、をそれぞれRT-PCRおよびPCRにより、未処理の生細胞および、MIC未満(<MIC)、MIC(MIC)、またはMIC超(>MIC)濃度の抗生物質とインキュベートした細胞から抽出したTNAをそれぞれ使用して増幅した。表2は、各反応タイプおよびサンプルについて測定された閾値サイクル(Ct)値を示す。ΔCtは、増幅プロットから得られたPCR(DNAのみ)およびRT-PCR(GAT)のCt値間の差として計算された。次に、倍数変化(RNAプラスDNA(GAT)対DNAのみのコピー数の比で、理論的にはそれらのΔCt値につながる)は、2ΔCtと推定され、図3パネルiiiにプロットされた。次に、結果を各細胞集団の生存率と比較した(図3パネルii)。
次の実施例は、GATおよびNEDアッセイの適切な標的をスクリーニングする方法を示す。クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から核酸を抽出した。TNAおよびRNAは、PI 24時間で回収された生細胞から抽出された。次に、選択した遺伝子とその転写産物(GAT)、または非転写遺伝子のみ(NED)を標的とするプライマーペアを使用して、核酸を増幅した。各標的の適切性は、(i)遺伝子およびその転写産物の両方が検出される、全RNAでのRT-PCRによるRNAの検出と、ならびに(ii)遺伝子DNAのみが検出されるPCRによるDNAの検出の比較により決定された。これらの実験では、GATのCtが両方の反応間の違いを示すと予測されるが、NEDのCtは違いを示さないはずである。
パートザイムは、それらがomp1遺伝子またはomp1転写産物のいずれかの増幅によって生成されたアンプリコンに結合すると、活性のMNAzymeに集合するように設計された。一度集合すると、MNAzymeはレポーター基質Sub102(20)-FBを切断できる。パートザイムの2番目のペアは、infA_IGRと呼ばれる非転写DNAの領域の増幅により生成されたアンプリコンに結合すると、活性のMNAzymeに集合し、NEDの測定を提供するように設計された。一度集合すると、このMNAzymeはレポーター基質Sub72-A1Bを切断できる。各MNAzymeのパートザイムAおよびパートザイムBの配列を、5'から3'の順で以下にリストする。太字の塩基は標的とハイブリダイズし、下線が引かれた塩基は、集合されたMNAzymeの触媒中心の一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、それぞれ異なるフルオロフォアで標識された、2つの異なるレポーター基質を使用した。Sub102(20)-FBは、5'末端を6-FAMおよび3'末端をIABkFQで末端標識され、492 nmで励起しながら516 nmでその切断をモニターした。Sub72-A1Bは、5'末端をATTO(商標)Rho101および3'末端をIAbRQSpで標識され、592 nmで励起しながら609 nmでその切断をモニターした。この実施例のレポーター基質は、5'から3'の順で、配列を伴って以下に示される。小文字の塩基はRNAを表しおよび大文字の塩基はDNAを表す。
クラミジア・トラコマチスに感染した細胞から抽出されたTNAおよびRNA鋳型のin vitro増幅は、以下にリストされたプライマーを使用して行われた。フォワードおよびリバースプライマーを使用して、PCRおよびRT-PCRによりomp1遺伝子および転写産物(GAT)ならびにinfA_IGR DNA(NED)の領域を増幅した。すべての配列は5'から3'の順に記入する。
核酸は、実施例1(1.1培養)に記載されているように、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から抽出された。PI 4時間で、DMEMをシクロヘキシミドに置き換えて、感染を同調させ、宿主によるタンパク質合成を停止した。細菌の指数関数的増殖期の、感染後24時間で回収されるまで、細胞を5%CO2、37℃で再びインキュベートした。
PCRおよびRT-PCRミックスの両方には、全体積20μLに、40 nMの5'プライマー、200 nMの3'プライマー、200 nMのパートザイムA、200nMのパートザイムB、200nMのGATのSub2-FB、200nMのNEDのSub72-A1B、1x SensiFASTプローブNo-ROXミックス(Bioline)、8 mM MgCl2(Bioline)、およびヌクレアーゼフリー水(Ambion)が含まれていた。さらに、RT-PCRミックスには0.2 U/μL RiboSafe RNase阻害剤(Bioline)および0.2μLの逆転写酵素(Bioline)が含まれていた。反応は、BioRad(登録商標)CFX96サーモサイクラーで同じサイクリングパラメータを使用して行われた:48℃で10分間、95℃で2分間、95℃で5秒間および61℃で30秒間を10サイクル(サイクルあたりマイナス0.5℃)、ならびに95℃で5秒間および52℃で50秒間を30サイクル。RT-PCRおよびPCRミックスには、5μLのTNAもしくはRNA鋳型(1/100希釈)が含まれていたか、または鋳型なし(dH2O)かのいずれかであった。
クラミジアDNAおよびRNA、またはDNAのみを、PI24時間で未処理の生細胞から採取した、RNAおよびTNAサンプルでそれぞれRT-PCRおよびPCRにより増幅した。表3Aは、行われた反応のアンプリコンのタイプおよび由来を示す。表3Bは、各反応タイプおよびサンプルについて測定された閾値サイクル(Ct)値を示す。ΔCtは、増幅プロットから得られたPCR(DNAのみ)とRT-PCR(DNAおよびRNA)のCt値間の差として計算された(図4)。
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出したTNAサンプルのNEDおよびGATのレベルを推定する。TNAは、実施例1、処理プロトコルA(1.1.1)で説明されているように、抗生物質とインキュベートしていない細胞(未処理、生細胞)、およびMICの8分の1(<MIC)、MIC(MIC)またはMICの8倍(>MIC)の濃度の抗生物質とインキュベートした細胞から抽出された。クラミジアDNAおよびRNA(GAT)は、omp1遺伝子およびその転写産物を標的とするプライマーを使用したRT-PCRにより増幅された。クラミジアDNAのみ(NED)は、転写されない、infAIGRと呼ばれる、ゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRで共増幅された。GATおよびNEDのCt値が決定された。
パートザイムは、omp1遺伝子およびomp1転写産物の両方の増幅によって生成されたアンプリコンに結合すると、活性なMNAzymeに集合するように設計された。集合すると、このMNAzymeはレポーター基質Sub2-FBを切断し得る。パートザイムの2番目のペアは、infA_IGRと示される非転写領域の増幅によって生成されたアンプリコンに結合すると、活性なMNAzymeに集合するように設計された。集合すると、このMNAzymeはレポーター基質Sub72-A1Bを切断し得る。パートザイムAおよびパートザイムBの配列を、5'から3'の順で、以下にリストする。太字の塩基は標的とハイブリダイズし、下線が引かれた塩基は、集合されたMNAzymeの触媒コアの一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、それぞれ異なるフルオロフォアで標識された、2つの異なるレポーター基質を使用した。Sub2-FBは5'末端が6-FAMで末端標識され、3'末端がIABkFQであり、492 nmで励起しながら516 nmで切断をモニターした。Sub72-A1Bの5'末端にATTO(商標)Rho101、3'末端にIAbRQSpのラベルを付け、その切断A1Bを592 nmで励起しながら609 nmでモニターした。この例のレポーター基質は、5'から3'の順で、以下に配列と共に示されている。小文字の塩基はRNAを表しおよび大文字の塩基はDNAを表す。
クラミジア・トラコマチスに感染した細胞から抽出されたTNA鋳型のin vitro増幅は、以下にリストされたプライマーを使用して行われた。フォワードおよびリバースプライマーを使用して、RT-PCRでomp1 RNAおよびDNA(GAT)ならびにinf_AGR DNA(NED)を増幅した。すべての配列は5'から3'の順で記入する。
RNAおよびDNA(TNA)は、実施例1(1.1 培養、1.1.1 処理プロトコルA)の通りにHEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、フェノール:クロロホルム:イソアミルを使用する、実施例1(1.3 全核酸(TNA)抽出、1.3.1 抽出プロトコルA)にも記載されているLLE技術として行われた。
すべての反応には、全体積20 μLに、40 nMの各フォワードプライマー、200 nMの各リバースプライマー、200 nMの各パートザイム A、200 nMの各パートザイム B、200 nMの各基質、1x SensiFAST Probe No-ROXミックス(Bioline)、2 mM MgCl2(Bioline)、0.2 U/μL RiboSafe RNase 阻害剤(Bioline)、0.2 μLの逆転写酵素(Bioline)、およびヌクレアーゼフリー水(Ambion)が含まれていた。すべての反応は、BioRad(登録商標)CFX96サーモサイクラーでトリプリケートで行った。サイクリングパラメータは、48℃で10分間、95℃で2分間、95℃で5秒間および61℃で30秒間(サイクルあたり温度が0.5℃低下)を10サイクル、ならびに95℃で5秒間および52℃で50秒を30サイクルであった。反応には、5 μLのTNA鋳型(1/100希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
クラミジアDNAおよびRNA(GAT)、またはDNAのみ(NED)は、生存未処理の細胞から、およびMIC未満(<MIC)、MICまたはMIC超(>MIC)濃度の抗生物質とインキュベートした細胞から抽出されたTNAの単一のRT-PCRで共増幅した(図5パネルi)。表4は、各サンプルのGATまたはNEDについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDおよびGATシグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GATのNEDに対する比)は2ΔCtと推定され(表4)およびVITAインデックスは図5のパネルiにプロットされた。次に、結果を各細胞集団の生存率と比較した(図3パネルiおよびii)。
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出したTNAサンプルのNEDおよびGATのレベルを推定する。TNAは、抗生物質とインキュベートしていない細胞(未処理、生細胞)、およびMICの8分の1(<MIC)、MIC(MIC)またはMICの8倍(>MIC)の濃度の抗生物質とインキュベートした細胞から、実施例1、処理プロトコルA(1.2.1)に記載されたように抽出された。クラミジアDNAおよびRNA(GAT)は、omp1遺伝子およびその転写産物(GAT1/2)の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。クラミジアDNAのみ(NED)は、転写されない、infAIGR(infA遺伝子間領域)と呼ばれる、ゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRで共増幅された。GAT1/2およびNEDのCt値が得られた。
パートザイムは、omp1遺伝子またはomp1転写産物のいずれかの増幅によって生成されたアンプリコンに結合した場合に、2つの活性のMNAzymeに集合するように設計された。これらの2つのMNAzymeは、omp1の2つの別個の領域(GAT1およびGAT2領域)の増幅により誘導される2つの異なるアンプリコンに結合することができた。一度集合すると、両方のMNAzymeは、同じレポーター基質Sub2-FBを切断できる。パートザイムの3番目のペアは、infA_IGRで示される非転写DNA領域の増幅によって生成されたアンプリコンに結合する場合、活性のMNAzymeに集合し、NEDの測定を提供するように設計された。一度集合すると、このMNAzymeは、レポーター基質Sub72-A1Bを切断できる。各MNAzymeのパートザイムAおよびパートザイムBの配列は、5'から3'の順で、以下にリストする。太字の塩基は標的とハイブリダイズし、下線が引かれた塩基は、集合されたMNAzymeの触媒コアの一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、実施例4(4.2レポーター基質)のように、それぞれ異なるフルオロフォアで標識された、2つの異なるレポーター基質を使用した。
クラミジア・トラコマチスに感染した細胞から抽出されたTNA鋳型のin vitro増幅は、以下にリストされたプライマーを使用して行われた。フォワードプライマーおよびリバースプライマーを使用して、RT-PCRによりomp1遺伝子および転写産物の2つの領域(GAT1とGAT2)ならびにinfA_IGR DNA(NED)を増幅した。すべての配列は5'から3'の順で記入する。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.1 処理プロトコルA)に記載されているように、HEp-2細胞で培養して、in vitroの方法で得られているクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、フェノール:クロロホルム:イソアミルを使用する、実施例1(1.3 全核酸(TNA)抽出、1.3.1 抽出プロトコルA)にも記載されているLLE技術として行った。
すべての反応には、全体積20 μLに、40 nMの各フォワードプライマー、200 nMの各リバースプライマー、200 nMの各パートザイム A、200 nMの各パートザイム B、400 nMの各基質配列番号3および200 nMの基質配列番号11、1x SensiFAST Probe No-ROXミックス(Bioline)、2 mM MgCl2(Bioline)、0.2 U/μL RiboSafe RNase 阻害剤(Bioline)、0.2 μLの逆転写酵素(Bioline)およびヌクレアーゼフリー水(Ambion)を含んだ。BioRad(登録商標)CFX96サーモサイクラーですべての反応をトリプリケートで行った。サイクリングパラメータは、48℃で10分間、95℃で2分間、95℃で5秒間および61℃で30秒間を10サイクル(サイクルあたり温度において0.5℃の減少を伴う)、および95℃で5秒間および52℃で50秒間を30サイクルであった。反応には、5 μLのTNA鋳型(1/100希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
omp1遺伝子および転写産物内の2つの領域(GAT1およびGAT2)から、および1つのNED領域からのクラミジアDNAおよびRNAを、生存未処理の細胞およびMIC未満(<MIC)、MIC、またはMIC超(>MIC)濃度の抗生物質とインキュベートした細胞から抽出したTNAからの単一のRT-PCRで共増幅した(図5パネルii)。表5に、各サンプルで、NED、ならびにGAT1およびGAT2(GAT1/2)からの合算されたシグナルについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDおよびGAT1/2のCt値間の差として計算された。次に、それらのΔCt値に論理的に導く倍数変化(GATのNEDに対する比)は2ΔCtと推定され、および表5に示された。VITAインデックスは、FCをTRで割ることによって計算された(この場合は2)。次に結果が、各細胞集団の生存と比較された。
特定の遺伝子は、たとえば細菌の発生サイクルの特定の段階の間でのみ発現される可能性があるので、DNAおよびその関連RNA転写産物の両方を増幅できる複数のプライマーセットを組み込む能力は、実際非常に望ましい。(好ましくは異なる条件下で高レベルに)発現した複数の遺伝子を含むアッセイは、ほとんど見込みのない条件(desperate conditions)下で一貫して検出される発現を確保できる。
下記の実施例では、臨床サンプルのNEDに対するGATのレベルを推定する。尿サンプルは、第一選択の抗生物質アジスロマイシンに対して、連続して治療が失敗した、症状のある患者から得られた。サンプルからTNAを抽出し、生/生存(陽性参照)または死(陰性参照)であることが確認されたクラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出した参照の材料と一緒に試験した。GATを測定するために、omp1遺伝子とその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRにより、クラミジアDNAおよびRNAを増幅した。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルが決定され、およびVITAインデックスの計算に使用された。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイム オリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例5(それぞれ5.1、5.2および5.3)の通りであった。
臨床サンプル:
RNAとDNA(TNA)は、尿の臨床検体から共抽出され、これは、第一選択の抗生物質処理に対して、連続して治療が失敗した患者から得られている。合計8mLの尿をペレット化し、その後に核酸を抽出し、DNAおよびRNAの両方を同時に抽出するために製造元の指示にしたがって、FireMonkey PuriSpin抽出キットを使用して、実施例1(1.3 全核酸(TNA)抽出、1.3.2抽出プロトコルB)に記載されているように行った。
参照の材料:
RNAおよびDNA(TNA)は、in vitroの方法で得られた、HEp-2細胞で培養され、実施例1で記載されているように、高用量のアジスロマイシン抗生物質(0.512 μL/mL)で処理され「死」と確認されたか、または処理されず「生」と確認されたクラミジア・トラコマチス(血清型D)から共抽出された。これらの参照サンプルの生存の状態は、免疫蛍光染色によって確認された。抽出は、フェノール:クロロホルム:イソアミルを使用して、実施例1(1.3 全核酸(TNA)抽出、1.3.1抽出プロトコルA)にも記載されている液液抽出(LLE)技術として行った。
使用したRT-PCR条件は、実施例5(5.5)に記載の通りであり、以下の修正を加えた:0.1μLの逆転写酵素(Bioline)を10μLの全反応量で添加し、これには、臨床サンプルから抽出した2.5μLのTNA(原液)、または2.5μLの各参照のTNAサンプル(1/100希釈)が含まれたか、標的なし(dH2O)かのいずれかであった。
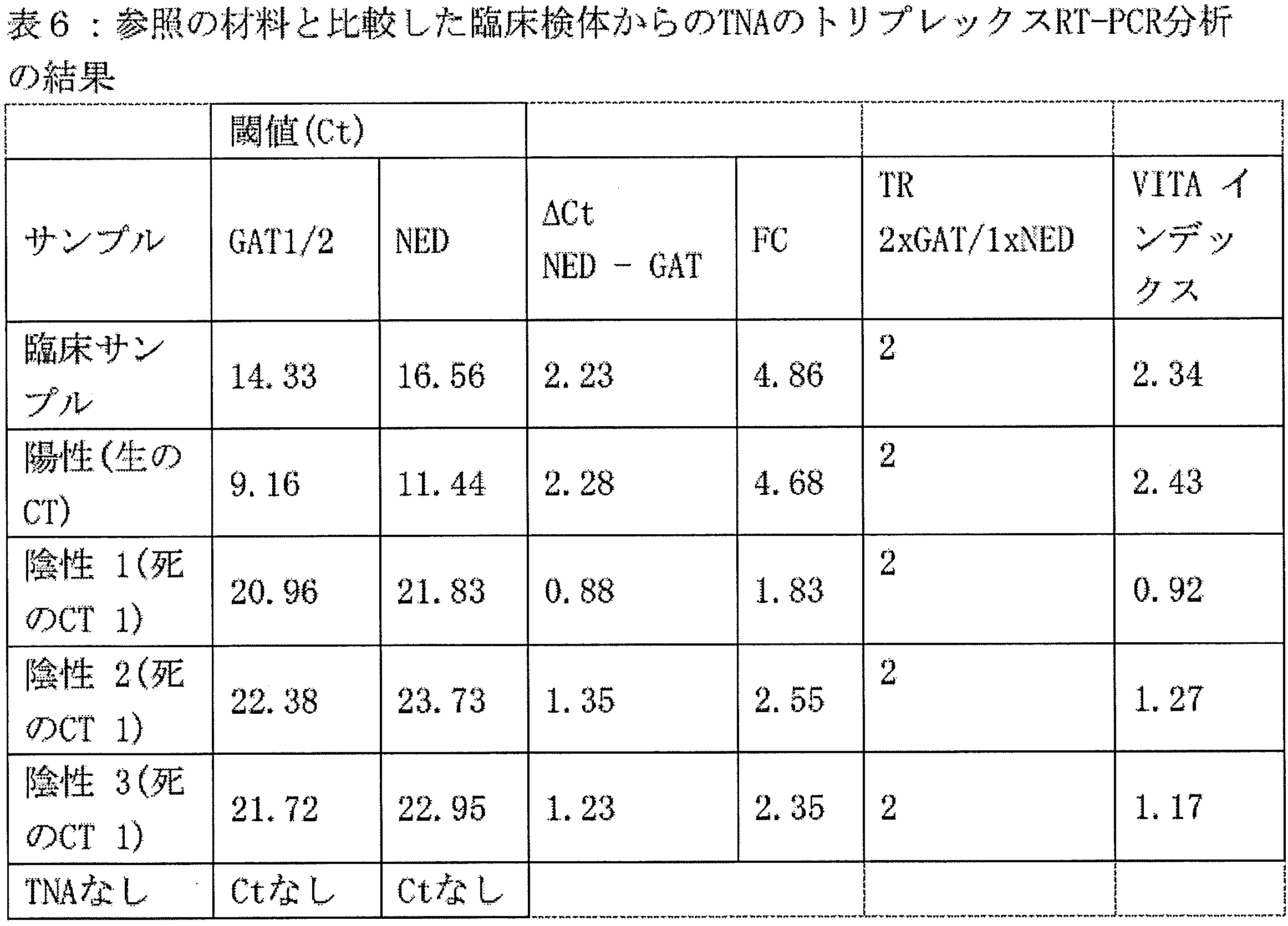
omp1遺伝子および転写産物(GAT1およびGAT2)の2つの領域、および1つのNED領域、からのクラミジアDNAおよびRNAが、共増幅され、尿の臨床サンプルから抽出されたTNAからの単一のRT-PCRで検出された(図6パネルi)。臨床サンプルの増幅は、「生の(Alive) CT」(未処理サンプル)または「死の(Dead) CT」(高用量のアジスロマイシンで処理)のいずれかの、クラミジア培養物由来の参照サンプルと比較された(図6パネルii)。ΔCtは、NEDおよびGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2およびNED間の差)は、2ΔCtと推定され、表6に示した。
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出した、TNAサンプルのGATレベルの変化を推定する。TNAを細胞から抽出し、指数関数成長期に、感染後24時間で、実施例1、処理B(1.1.2)で記載したように、MICで抗生物質で処理したか、または処理しなかった(コントロール)。omp1遺伝子とその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRにより、クラミジアDNAおよびRNAを増幅し、GATを測定した。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルを推定し、VITAインデックスの計算に使用した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイム オリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例5(それぞれ5.1、5.2および5.3)の通りであった。使用したRT-PCR反応条件は、実施例5(5.5)に記載された通りであった。これらの反応には、5μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.2処理プロトコルB)に記載された通り、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、フェノール:クロロホルム:イソアミルを使用して、下記の修正を伴い、実施例1(1.3全核酸(TNA)抽出、1.3.1抽出プロトコルA)にも記載されているLLE技術として行った;細胞片ペレット化ステップは、この実施例ではサンプルの抽出中に行われなかった。
omp1遺伝子および転写産物内の2つの領域(GAT1およびGAT2)、および1つのNED領域からのクラミジアDNAおよびRNAが共増幅され、クラミジア培養物から抽出されたTNAからの単一のRT-PCRで検出された。これらの培養物は、指数関数成長期に、抗生物質で処理または未処理のまま(コントロール)にし、処理後1および6時間で回収した(図7パネルi)。表4に、各サンプルのGAT1/2およびNEDについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDおよびGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2とNED間の差)は、2ΔCtと推定され、表7に示した。その後、各時点で、処理反応なし(コントロール)および抗生物質で処理したものとの間で結果を比較した(図7パネルii)。
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出したTNAサンプルのGATの、NEDに対するレベルの変化を推定する。TNAは、指数関数成長期の間の感染後24時間で、MICで、抗生物質で処理された細胞、または処理されなかった細胞(コントロール)から抽出された。処理は、アジスロマイシン(0.128 μg/mL)を使用した実施例1、処理B(1.1.2)に記載した通りであった。GATの測定を得るために、クラミジアDNAおよびRNAは、omp1遺伝子およびその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルを推定し、およびVITAインデックスの計算に使用した。さらに、処理サンプルおよび未処理サンプルのVITAインデックスを使用して、ΔVITA比を計算した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイムオリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例5(それぞれ5.1、5.2および5.3)の通りであった。使用したRT-PCR条件は、実施例5(5.5)で説明した通りで、そして反応には5 μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.2処理プロトコルB)に記載されているように、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、下記の修正を伴い、フェノール:クロロホルム:イソアミルを使用して、実施例1(1.3全核酸(TNA)抽出、1.3.1抽出プロトコルA)に記載されているように、LLE技術として行われた;細胞片ペレット化ステップは、この実施例ではサンプルの抽出中に行われなかった。
omp遺伝子および転写産物(GAT1とGAT2)内の2つの領域、ならびに1つのNED領域からのクラミジアDNAおよびRNAが、共増幅され、クラミジア培養物から抽出されたTNAから単一RT-PCRで検出された。これらの培養物は、指数関数成長期に抗生物質で処理または未処理のまま(コントロール)にし、0.128 μg/mLのアジスロマイシン処理後30分または1時間で回収した(図7パネルi)。表8に、各サンプルのGAT1/2およびNEDについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDおよびGAT1/2シグナルのCt値間の差として計算された。次に、それらのΔCt値に理論的につながる倍数変化(GAT1/2およびNED間の差)は2ΔCtと推定され、表8に示された。その後、処理反応なし(コントール)および各時点で抗生物質で処理したものとの間で結果を比較した(図7パネルiii)。
下記の実施例では、クラミジア・トラコマチス株1および株5(それぞれリファンピシン耐性の血清型D 実験室株および血清型L2株)に感染したHEp-2細胞から抽出したTNAサンプルのGATの、NEDに対するレベルの変化を推定する。TNAは、指数関数成長期にある感染後20時間で、濃度0.256 μg/mLの抗生物質リファンピシンで処理された細胞、または処理されなかった細胞(コントロール)のいずれかから抽出された。処理は、実施例1、処理C(1.1.3)に記載された通りであった。GATの測定を得るために、クラミジアDNAおよびRNAは、omp1遺伝子およびその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルを推定し、VITAインデックスの計算に使用した。これに対してさらに、処理サンプルおよび未処理サンプルのVITAインデックスを使用して、ΔVITA比を計算した。
パートザイムは、omp1遺伝子またはomp1転写産物のいずれか増幅によって生成されたアンプリコンに結合すると、2つの活性のあるMNAzymeに集合するように設計された。これらの2つのMNAzymeは、omp1の2つの別個の領域(GAT1およびGAT2領域)の増幅により誘導される2つの異なるアンプリコンに結合することができた。一度集合すると、両方のMNAzymeは同じレポーター基質Sub102(20)-FBを切断できる。パートザイムの3番目のペアは、infA_IGRで示される非転写DNA領域の増幅によって生成されたアンプリコンに結合すると、活性のあるMNAzymeに集合し、NEDの測定を提供するように設計された。集合すると、このMNAzymeはレポーター基質Sub72-A1Bを切断できる。各MNAzymeのパートザイムAおよびパートザイムBの配列を、5'から3'の順で以下にリストする。太字の塩基は標的とハイブリダイズし、下線が引かれた塩基は、集合したMNAzymeの触媒中心の一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、それぞれ異なるフルオロフォアで標識された、2つの異なるレポーター基質を使用した。Sub102(20)-FBは、5'末端を6-FAMおよび3'末端をIABkFQで末端標識され、492 nmで励起しながら516 nmで切断をモニターした。Sub72-A1Bは、5'末端をATTO(商標)Rho101および3'末端をIAbRQSpで標識され、592 nmで励起しながら609 nmで切断をモニターした。この実施例のレポーター基質は、5'から3'の順で、以下に示される。小文字の塩基はRNAを表しおよび大文字の塩基はDNAを表す。
クラミジア・トラコマチスに感染した細胞から抽出されたTNAテンプレートのin vitro増幅は、以下にリストされたプライマーを使用して行った。フォワードおよびリバースプライマーを使用して、RT-PCRで、omp1遺伝子および転写産物(GAT1およびGAT2)の2つの領域ならびにinfA_IGR DNA(NED)の領域を増幅した。すべての配列は5'から3'の順に書き込まれる。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.3処理プロトコルC)に記載されているように、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、FireMonkey PuriSpin抽出キットを使用して行い、実施例1(1.3 全核酸(TNA)抽出、1.3.2抽出プロトコルB)で定義されているように、またDNAおよびRNAを同時に抽出するために製造元の指示にしたがって行った。
すべての反応物は、全体積20 μLに、40 nMの各フォワードプライマー、200 nMの各リバースプライマー、200 nMの各パートザイムA、200 nMの各パートザイムB、400 nMの基質配列番号10および200 nmの基質配列番号11、1x SensiFASTプローブNo-ROXミックス(Bioline)、2 mM MgCl2(Bioline)、0.2 U/μL RiboSafe RNase 阻害剤(Bioline)、0.2 μLの逆転写酵素(Bioline)およびヌクレアーゼフリー水(Ambion)を含んだ。BioRad(登録商標)CFX96サーモサイクラーですべての反応をトリプリケートで行った。サイクリングパラメータは、48℃で10分間、95℃で2分間、95℃で5秒間および61℃で30秒間を10サイクル(サイクルあたり温度が0.5℃低下)、ならびに95℃で5秒間および52℃で50秒間を30サイクル。反応には5 μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)かのいずれかであった。
omp1遺伝子および転写産物(GAT1とGAT2)内の2つの領域、ならびに1つのNED領域からのクラミジアDNAおよびRNAが共増幅され、クラミジア培養物から抽出されたTNAからの単一のRT-PCRで検出された。これらの培養物は、指数関数成長期に抗生物質で処理されたか、または未処理のまま(コントロール)であった。それらを37℃で5分間(図7パネルiv)または室温で15分間(図7パネルv)のいずれかでインキュベートした。処理に使用された抗生物質は、リファンピシンで、濃度が0.256 μg/mLで、感受性株のMICの32倍、および耐性株のMICの32分の1と等価であった。表9に、各サンプルのGAT1/2およびNEDについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDシグナルおよびGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2およびNED間の差)は、2ΔCtと推定され、表9に示した。その後、処理反応なし(コントロール)および各時点で、抗生物質で処理したものとの間で結果を比較した(図7パネルivおよびv)。
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出した、TNAサンプルのGATの、NEDに対する変化を推定する。TNAは、未処理(コントロール)かまたは様々な用量の抗生物質(アジスロマイシン);具体的には、MICの4倍(0.128 μg/mL)、MICの6倍(0.192 μg/mL)、MICの8倍(0.256 μg/mL)の濃度で処理されたかのいずれかの細胞から抽出された。抗生物質は、実施例1、処理D(1.1.4)に記載されている通り、細胞が指数関数成長期にある感染後24時間で添加した。GATを測定するために、クラミジアDNAおよびRNAは、omp1遺伝子およびその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。NEDを測定するために、クラミジアDNAの別の領域を、転写されていないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRで共増幅した。GATおよびNEDのレベルが推定され、VITAインデックスの計算に使用された。これに対してさらに、処理サンプルおよび未処理サンプルのVITAインデックスを使用して、ΔVITA比を計算した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイムオリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例5(それぞれ5.1、5.2および5.3)の通りであった。使用したRT-PCR条件は、実施例5(5.5)に記載した通りで、反応には、5 μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)かのいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.4処理プロトコルD)に記載されている通り、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、フェノール:クロロホルム:イソアミルを使用する、下記の修正(;細胞片ペレット化ステップは、この実施例ではサンプルの抽出中に行われなかった)を伴った、実施例1(1.3 全核酸(TNA)抽出、1.3.1抽出プロトコルA)にも記載されているLLE技術として行われた。
omp1遺伝子および転写産物内の2つの領域(GAT1およびGAT2)、および1つのNED領域からのクラミジアDNAおよびRNAが共増幅され、クラミジア培養物から抽出されたTNAを使用した単一のRT-PCRで検出された。これらの培養物を、指数関数成長期に抗生物質の一連の用量で処理するか、未処理(コントロール)のままにして、1時間のインキュベーション後に回収した(図8パネルi)。表10は、各サンプルのGAT1/2およびNEDについて測定された閾値サイクル(Ct)値を示している。ΔCtは、NEDシグナルとGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2およびNED間の差)は、2ΔCtと推定され、表10に示されている。その後、処理反応なし(コントロール)および、異なる用量の抗生物質で処理したものとの間で結果を比較した(図8パネルii)
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出した、TNAサンプルのGATの、NEDに対する変化を推定する。TNAは、未処理(コントロール)かまたは抗生物質アジスロマイシンを様々な用量;具体的には、MICの4倍(0.128 μg/mL)、MICの6倍(0.192 μg/mL)、MICの8倍(0.256 μg/mL)、MICの16倍(0.512 μg/mL)の濃度で処理したかのいずれかの細胞から抽出された。抗生物質を、実施例1、処理D(1.1.4)に記載されている通り、細胞が指数関数成長期にある感染後20時間で添加した。GATを測定するために、クラミジアDNAおよびRNAは、omp1遺伝子およびその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。NEDを測定するために、クラミジアDNAの別の領域を、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRで共増幅した。GATおよびNEDのレベルを推定し、VITAインデックスの計算に使用した。これに対してさらに、処理サンプルおよび未処理サンプルのVITAインデックスを使用して、ΔVITA比を計算した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイムオリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例9(それぞれ9.1、9.2および9.3)の通りであった。使用されたRT-PCR条件は、実施例9(9.5)で記載された通りで、反応には5 μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.4処理プロトコルD)に記載されている通り、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、FireMonkey PuriSpin抽出キットを使用して行い、実施例1(1.3 全核酸(TNA)抽出、1.3.2抽出プロトコルB)で定義されているように、DNAおよびRNAの同時抽出のために製造元の指示にしたがって行った。
2つの領域(GAT1およびGAT2)、および1つのNED領域からのクラミジアDNAおよびRNAの共増幅は、クラミジア培養物から抽出されたTNAを使用した単一のRT-PCRでモニターされた。これらの培養物を、指数関数成長期に一連の用量の抗生物質で処理するか、または未処理(コントロール)のままにして、処理後1時間で回収した(図8パネルi)。表11に、各サンプルのGAT1/2およびNEDについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDシグナルおよびGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2およびNED間の差)は、2ΔCtと推定され、表11に示した。次に、処理反応なし(コントロール)および、異なる用量の抗生物質で処理したものとの間で結果を比較した(図8パネルiii)。
下記の実施例では、TNAサンプルのNEDに対するGATレベルの変化を評価することにより、ある特定の薬物に対する細菌の感受性を分析している。これらは次に、抗生物質で処理されたサンプルおよび処理されていないサンプル(コントロール)の間で比較された。サンプルは、試験されたアジスロマイシンおよびドキシサイクリンの両方の薬剤に感受性があることが知られている、異なるクラミジア・トラコマチス株に感染したHEp-2細胞から得られた。TNAは、指数関数成長期にある細胞で、感染後20時間でいずれかの抗生物質(0.256 μg/mL)の単一の用量で処理された細胞であるか、または処理されていない細胞(コントロール)のいずれかで、処理後1時間インキュベートされた細胞から抽出された。処理は、実施例1、処理E(1.1.5)に記載されている通りであった。GATの測定を得るために、クラミジアDNAおよびRNAは、omp1遺伝子およびその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルを推定し、およびVITAインデックスの計算に使用した。さらに、処理サンプルおよび未処理サンプルのVITAインデックスを使用して、ΔVITA比を計算した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイムオリゴヌクレオチド、レポーター基質およびPCRプライマーは実施例9(それぞれ9.1、9.2および9.3)の通りであった。使用したRT-PCR条件は、実施例9(9.5)で記載した通りで、反応には5 μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.5処理プロトコルE)に記載されているように、HEp-2細胞で培養された、クラミジア・トラコマチスの異なる株から共抽出された。抽出は、FireMonkey PuriSpin抽出キットを使用して行い、実施例1(1.3 全核酸(TNA)抽出、1.3.2抽出プロトコルB)で定義されているように、DNAおよびRNAを同時に抽出するために製造元の指示にしたがって行った。
2つのGAT領域および1つのNED領域からのクラミジアDNAおよびRNAが、共増幅され、クラミジア培養物から抽出されたTNAからの単一RT-PCRで検出された。これらの培養物を、指数関数成長期に抗生物質で処理するまたは未処理のまま(コントロール)にして、処理1時間後に回収した。表12aおよび12bは、各個々の株および処理に使用される抗生物質、すなわちそれぞれアジスロマイシンおよびドキシサイクリンの各サンプル(処理または未処理)の閾値サイクル(Ct)値を示している。ΔCtは、NEDシグナルおよびGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2およびNED間の差)は、2ΔCtと推定されて、表12aおよび12bに示される。次に、各株について、処理反応なし(コントロール)および抗生物質で処理したものとの間で、結果を比較した。試験した抗生物質は、アジスロマイシン(表12a、図9パネルi)およびドキシサイクリン(表12b、図9パネルii)であった。
以下の実施例では、TNAサンプルのNEDに対するGATレベルの変化を評価することにより、ある特定の薬剤に対する細菌の感受性を分析している。これらは次に、抗生物質で処理されたサンプルおよび処理されていないサンプル(コントロール)の間で比較された。サンプルは、培養において、以前に薬剤のリファンピシンに感受性がある(合計4つの株:血清型D、実験室株(株1)、血清型L2、野生タイプ実験室株(株2)、血清型L2、トリメトプリム耐性株(株3)および血清型L2、スペクチノマイシン耐性株(株4));またはリファンピシン耐性(血清型L2、リファンピシン耐性株(株5))のいずれかと特徴付けられた、異なるクラミジア・トラコマチス株に感染したHEp-2細胞から得られた。TNAは、指数関数成長期にある感染20時間後に、高い用量の抗生物質で処理された細胞であるか、または処理されなかった細胞(コントロール)のいずれかから抽出された。処理は、実施例1、処理E(1.1.5)に記載されている通りであり、単一の濃度のリファンピシン(0.256 μg/mL)を使用し、これは、感受性株のMICの32倍、および耐性株のMICの32分の1と等価である。GATの測定を得るために、クラミジアDNAおよびRNAは、omp1遺伝子およびその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRによって増幅された。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルを推定し、VITAインデックスの計算に使用した。これに対してさらに、処理サンプルおよび未処理サンプルのVITAインデックスを使用して、ΔVITAを計算した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイムオリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例9(それぞれ9.1、9.2および9.3)の通りであった。使用したRT-PCR条件は、実施例9(9.5)で説明した通りで、そして反応には5 μLのTNAテンプレート(1/1000希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.5処理プロトコルE)に記載されているように、HEp-2細胞で培養されたすべての異なるクラミジア・トラコマチス株(1、2、3、4、および5株)から共抽出された。抽出は、FireMonkey PuriSpin抽出キットを使用して行い、実施例1(1.3 全核酸(TNA)抽出、1.3.2抽出プロトコルB)で定義されているように、DNAおよびRNAを同時に抽出するために製造元の指示にしたがって行った。
2つのGAT領域および1つのNED領域からのクラミジアDNAおよびRNAが、共増幅され、クラミジア培養物から抽出されたTNAからの単一RT-PCRで検出された。これらの培養物は、指数関数成長期に抗生物質(リファンピシン)、または未処理のまま(コントロール)で処理し、そして処理後1時間で回収した。表13に、個々の株ごとの、各サンプルの成分の閾値サイクル(Ct)値を示す。ΔCtは、NEDシグナルおよびGAT1/2シグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GAT1/2およびNED間の差)は、2ΔCtと推定され、表13に示した。結果は、各株について、処理反応なし(コントロール)および抗生物質で処理したものの間で比較した(図9パネルiii);そして結果は、感受性株対耐性株で比較した。倍数変化およびVITAインデックスは、処理後1時間ですべてのサンプルについて計算された(表13)。
下記の実施例では、図10に示す過程を記載し、この過程は、性感染症およびそれらの抗生物質耐性/感受性の状態を含む、感染症の一般的なスクリーニングとして使用できる。臨床標本は、ナイセリア・ゴノレア(Neisseria gonorrhea(GC))、クラミジア・トラコマチス(CT)、またはマイコプラズマ・ゲニタリウム(MG)などの性感染症を有する疑いのある患者から採取することができる。標本をサブサンプルに分割し、一方を一切の抗生物質とインキュベートせず、もう一方を、GC、CT、およびMGの1つ以上の処理に使用される一連の抗生物質の存在下でインキュベートする。インキュベーション後、GCおよび/またはCTおよび/またはMGに特異的な、GATおよびNEDを標的とするプライマーを用いたマルチプレックスVITAPCRアッセイで全核酸を分析し得る。特定の生物に対する陽性のGATおよびNEDシグナルにより、STIの診断が可能になり得、薬剤の存在下または非存在下でのVITAインデックスの比較により、どの治療法(therapy, or therapies,)が患者の治療に使用できるのか明らかになり得る。
下記の実施例では、生存から死菌まで様々なロードのサンプルのNEDおよびGATのレベルを推定する。TNAは、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出され、それは未処理(生 CT)または抗生物質アジスロマイシンを40時間の高用量0.512 ug/mlで処理(死 CT)されたかのいずれかであった。回収時に、これらを異なる比で混合して、実施例1、処理F(1.1.6)に記載された通り、0%、0.1%、0.2%、0.5%、1%、10%、20%、50%および100%の異なる生存のロードを取得した。GATを測定するために、omp1遺伝子とその転写産物の2つの異なる位置を標的とするプライマーを使用したRT-PCRにより、クラミジアDNAおよびRNAを増幅した。NEDを測定するために、転写されないゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRでクラミジアDNAの別の領域を共増幅した。GATおよびNEDのレベルを推定し、およびVITAインデックスの計算に使用した。
GAT1、GAT2およびNEDの増幅および検出に使用されるパートザイム オリゴヌクレオチド、レポーター基質およびPCRプライマーは、実施例9(それぞれ9.1、9.2および9.3)の通りであった。この実施例では、NEDのリバースプライマー(配列番号23)を下記に置換した。
使用したRT-PCR条件は、実施例9(9.5)に記載されている通りで、反応には5 μLのTNAテンプレート(1/100希釈)が含まれていたか、または標的なし(dH2O)かのいずれかであった。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.6処理プロトコルF)に記載されている通り、HEp-2細胞で培養されたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、FireMonkey PuriSpin抽出キットを使用して行い、実施例1(1.3 全核酸(TNA)抽出、1.3.2抽出プロトコルB)で定義されているように、DNAおよびRNAを同時に抽出するために製造元の指示にしたがって行った。
クラミジアDNAおよびRNA(GAT)、またはDNAのみ(NED)は、生存クラミジアの様々なロードを生成するために、生存の未処理細胞(生 CT)、および高用量の抗生物質での処理細胞(死 CT)の混合物から抽出されたTNAからの単一のRT-PCRで共増幅された。表14に、反応でGAT1またはGAT1/2のいずれかを使用して、各生存ロードに対して測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDシグナルおよびGATシグナルのCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GATのNEDに対する比)は2ΔCtと推定され、表15にプロットされ、VITAインデックスは図11のパネルiにプロットされた。次に、結果を各混合物の生存率と比較した。
下記の実施例では、クラミジア・トラコマチス(血清型D)に感染したHEp-2細胞から抽出されたTNAサンプルのNEDおよびGATのレベルを推定する。TNAは、実施例1、処理プロトコルA(1.2.1)で記載した通り、抗生物質とインキュベートしていない細胞(未処理、生細胞)、およびMICの8分の1(<MIC)、MIC(MIC)またはMICの8倍(>MIC)の濃度の抗生物質とインキュベートした細胞から抽出された。クラミジアDNAおよびRNA(GAT)は、omp1遺伝子およびその転写産物(GAT1/2)の2つの異なる位置を標的とするプライマーを使用したRT-PCRにより増幅された。この実験で2つのomp1 GAT標的を増幅するために使用された2つのプライマーペア(セクション16.3 配列番号4および24、配列番号16および25)は、実施例5を含む前の実施例で使用された2つのGATプライマーペア(セクション5.3 配列番号4および5、配列番号16および17)を使用して生成されたアンプリコンよりも長いアンプリコンを生成した。得られたアンプリコンは、それぞれGAT1およびGAT2で、215 bpおよび311 bpの長さであった。クラミジアDNAのみ(NED)は、転写されないInfA_IGRと呼ばれるゲノムDNAの領域を標的とするプライマーを使用して、同じRT-PCRミックスで共増幅された。GAT1/2およびNEDのCt値は、すべての処理のRT-PCRで推定された。
パートザイムは、omp1遺伝子またはomp1転写産物のいずれかの増幅によって生成されたアンプリコンに結合すると、2つの活性のMNAzymeに集合するように設計された。これらの2つのMNAzymeは、omp1の2つの別々の領域(GAT1およびGAT2領域)の増幅により得られる2つの異なるアンプリコンに結合することができた。一度集合すると、両方のMNAzymeは同じレポーター基質Sub102(20)-FBを切断できる。パートザイムの3番目のペアは、infA_IGRで示される非転写DNA領域の増幅によって生成されたアンプリコンに結合する場合、活性のMNAzymeに集合し、したがってNEDの測定を提供するように設計された。一度集合すると、このMNAzymeは、レポーター基質Sub72-A1Bを切断できる。各MNAzymeについてパートザイムAおよびパートザイムBの配列を、5'から3'の順で、以下にリストする。太字の塩基は標的とハイブリダイズし、下線が引かれた塩基は、集合されたMNAzymeの触媒中心の一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、それぞれ異なるフルオロフォアで標識された、2つの異なるレポーター基質を使用した。Sub102(20)-FBは、5'末端を6-FAMおよび3'末端をIABkFQで末端標識され、その切断を492 nmで励起しながら516 nmで切断をモニターした。Sub72-A1Bは、5'末端をATTO(商標)Rho101および3'末端をIAbRQSpで標識され、その切断を592 nmで励起しながら609 nmで切断をモニターした。この実施例のレポーター基質は、5'から3'の順で、以下に配列が示される。小文字の塩基はRNAを表しおよび大文字の塩基はDNAを表す。
クラミジア・トラコマチスに感染した細胞から抽出されたTNA鋳型のin vitro増幅は、以下にリストされたプライマーを使用して行われた。フォワードプライマーおよびリバースプライマーを使用して、RT-PCRによりomp1遺伝子および転写産物の2つの領域(GAT1とGAT2)ならびにinfA_IGR DNA(NED)を増幅した。すべての配列は、5'から3'の順に記入する。
RNAおよびDNA(TNA)は、実施例1(1.1培養、1.1.1 処理プロトコルA)に記載されているように、HEp-2細胞で培養する、in vitroの方法で得られたクラミジア・トラコマチス(血清型D)から共抽出された。抽出は、フェノール:クロロホルム:イソアミルを使用する、実施例1(1.3 全核酸(TNA)抽出)にも記載されているLLE技術として行った。
全ての反応には、全体積20 μLに、40 nMの各フォワードプライマー、200 nMの各リバースプライマー、200 nMの各パートザイムA、200 nMの各パートザイムB、400 nmの基質配列番号10、200 nMの基質配列番号11、1xSensiFASTプローブNo-ROXミックスOne-Step(Bioline)、2 mM MgCl2(Bioline)、0.2 U/μL RiboSafe RNase阻害剤(Bioline)、0.2 μLの逆転写酵素(Bioline)およびヌクレアーゼフリー水(Ambion)を含んだ。すべての反応は、BioRad(登録商標)CFX96サーモサイクラーで、トリプリケートで行った。サイクリングパラメータは、48℃で10分間、95℃で2分間、95℃で5秒間および61℃で30秒間(サイクルあたり温度が0.5℃低下)を10サイクル、および95℃で5秒間、52℃で50秒間を30サイクル、であった。反応は、5 μLのTNA鋳型(1/1000希釈)が含まれていたか、または標的なし(dH2O)のいずれかであった。
omp遺伝子および転写産物(GAT1およびGAT2)内の2つの領域、および1つのNED領域からのクラミジアDNAおよびRNAを、生存未処理細胞から、およびMIC未満(<MIC)、MICと同等(MIC)またはMIC超(>MIC)濃度の抗生物質とインキュベートした細胞から、抽出されたTNAの単一のRT-PCRで共増幅した。表15に、各サンプルにおける、NED、ならびにGAT1およびGAT2(GAT1/2)からの結合シグナルについて測定された閾値サイクル(Ct)値を示す。ΔCtは、NEDおよびGAT1/2のCt値間の差として計算された。次に、理論的にそれらのΔCt値につながる倍数変化(GATのNEDに対する比)は2ΔCtと推定され、表15に示された。VITAインデックスは、FCをTRで除算して計算された。次に、結果を各細胞集団の生存率と比較した。
下記の実施例では、ナイセリア・ゴノレア(Neisseria gonorrhoeae(GC))のTOCおよびASTで、診断に使用されるGATおよびNEDを標的とするアッセイについて説明する。このアッセイは、TNAサンプルの、GATの、NEDに対する変化を推定する。GATを測定するために、遺伝子およびその転写産物または複数の遺伝子およびそれらの転写産物の位置を標的とするプライマーを使用して、RT-PCRでゴノレア(gonorrhoeae) DNAおよびRNAを増幅する。NEDを測定するために、ゴノレア(gonorrhoeae) DNAの別の領域を、転写されないゲノムDNAの領域を標的とするプライマーペアを使用して、同じRT-PCR反応で共増幅する。潜在的なGATおよびNED標的は、実施例3の通りスクリーニングできる。GATおよびNEDのレベルが推定され、およびVITAインデックスの計算に使用される。生成されたVITAインデックスにより、任意の特定のサンプル(例:尿、膣スワブ、直腸スワブまたは咽頭スワブ)の生物の生存率を決定できる。これに対してさらに、サンプルは、サンプルを分割し、ならびに所望の薬剤または複数の薬剤の存在下および非存在下でインキュベートすることにより、抗生物質感受性試験にも使用できる。GATおよびNEDのレベルが推定され、および各条件のVITAインデックスの計算に使用される。これに対してさらに、処理および未処理サンプルのVITAインデックスを使用してΔVITAを計算し、最終的に生物の感受性または耐性プロファイルを決定する。これは、療法のガイダンスに役立ち、症状を最初に示した時に最良の選択の抗生物質が与えられる。
パートザイムは、異なる遺伝子、ompAまたはcysK遺伝子または転写産物の増幅によって生成されたアンプリコンに結合すると、2つの活性のMNAzymeに集合するように設計された。これらの2つのMNAzymeは、それぞれGAT1およびGAT2を表す、2つの別々の遺伝子の増幅によって得られる2つの異なるアンプリコンに結合するように設計されている。一度集合すると、両方のMNAzymeは同じレポーター基質Sub97(20)-JBを切断できる。パートザイムの3番目のペアは、NEDの測定候補であるIGR1109で示される非転写DNA領域の増幅によって生成されたアンプリコンに結合する場合、活性のMNAzymeに集合するように設計されている。一度集合すると、このMNAzymeはレポーター基質Sub84(20)-CBを切断できる。各MNAzymeのパートザイムAおよびパートザイムBの配列を、5'から3'の順で以下にリストする。太字の塩基は、標的とハイブリダイズし、下線が引かれた塩基は、集合されたMNAzymeの触媒中心の一部を形成し、斜体の塩基は基質にハイブリダイズする配列を指す。
本実施例では、別個のフルオロフォアで標識された、2つの異なるレポーター基質は、上記にリストしたパートザイム/MNAzymeを組み込んだシステムでの検出に有用である。これらの基質は、5'末端で5-JOENで末端標識され、および3'末端でIABkFQで末端標識されたSub97(20)-JB(その切断は、529 nmで励起しながら555 nmでモニターできる)ならびに、5'末端で5Cy5で、3'末端でIAbRQSpで標識されたSub84(20)-CB(その切断は、648 nmで励起しながら668 nmでモニターできる)である。これらのレポーター基質は、5'から3'の順で、配列が以下に示され、小文字の塩基はRNAを表し、および大文字の塩基はDNAを表す。
TNAの増幅は、下記のプライマーを使用して行うことができる。フォワードおよびリバースプライマーは、2つの別個の遺伝子および転写産物で、RT-PCRによってIGR1109 DNA(NED)と同様に、ompAおよびcysK(GAT1およびGAT2)、を増幅するように設計されている。すべての配列は5'から3'の順に記入する。
porBおよびrpmBを含む追加の候補遺伝子のGATのプライマーは、実施例3で概説した方法を使用してスクリーニングできる。
下記の実施例では、特定のマルチプレックスアッセイで得られたVITAインデックスで観察される絶対値にさらに影響を与える可能性のあるパラメーターについて説明する。VITA PCR分析に含まれるGATおよびNEDアッセイの増幅効率は、理想的にはGATおよびNEDに対して高くおよび等しくなければならない。実施例5を含む、いくつかの実施例で使用された、クラミジア・トラコマチスを標的とするGAT1、GAT2、およびNEDの増幅効率は、連続的に希釈された合成標的配列を使用して推定され、およびR2>0.998で、効率が100%に近く、相互に類似することがわかった(データは示していない)。反応のすべての成分が効率的および相互に同等な場合、実施例5(図5パネルii)で証明された通り、得られたVITAインデックスは、生細胞および非生細胞間を正確に区別できることが示されている。
Claims (15)
- 細胞、生物、またはウイルスからの核酸の増幅によって得られた定量的データを正規化する方法であって、前記方法が以下:
(i)
-第1の遺伝子からのゲノムDNAおよび第1の遺伝子から転写されたRNAの増幅からの、および
-細胞、生物、またはウイルスの非転写DNAの配列の増幅からの、
定量的データを取得すること;ならびに
(ii)定量的データを使用して、前記増幅の前に核酸サンプル内に存在する
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物、の
-前記非転写DNAの配列、に対する、
相対量を表す正規化値(nV)を導き出すこと、
を含み、
第1の遺伝子からの前記ゲノムDNAおよび第1の遺伝子から転写されたRNA、ならびに前記非転写DNAの配列が、同じ反応で共増幅される、
方法。 - 定量的データがアンプリコンコピー数であって、ならびに方法が以下:
(i)
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物の増幅から生成された総アンプリコン数を表す値A(vA)、および非転写DNAの配列から生成された総アンプリコン数を表す値B(vB)を取得すること;
-式:
vA/vB=nV
を使用して正規化値(nV)を計算すること、ならびに/あるいは
(ii)
-第1の遺伝子からのゲノムDNAおよびRNA転写産物の増幅、ならびに少なくとも1つのさらなる遺伝子からのゲノムDNAおよびRNA転写産物の増幅から生成された総アンプリコン数を表す値X(vX)を取得すること;
-非転写DNAの配列から生成された総アンプリコン数を表す値B(vB)を取得すること、
-式:
vX/(vB x(X+1))=nV
(式中Xは前記さらなる遺伝子(複数可)の数である)を使用して正規化値(nV)を計算すること
を含む、請求項1に記載の方法。 - 定量的データが閾値(Ct)であり、ならびに方法が以下:
(i)
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物の増幅からサイクル閾値CtAを取得すること、
-非転写DNAの配列の増幅からサイクル閾値CtBを取得すること;および
-式:
2CtB - CtA=nV
を使用して正規化値(nV)を計算すること、ならびに/あるいは
(ii)
-第1の遺伝子の前記ゲノムDNAおよびRNA転写産物の増幅、および少なくとも1つのさらなる遺伝子からのゲノムDNAおよびRNA転写産物の増幅からのサイクル閾値CtXを取得すること;
-非転写DNAの配列の増幅からサイクル閾値CtBを取得すること;および
-式:
2CtB - CtX/(X+1)=nV
(式中Xは前記さらなる遺伝子(複数可)の数である)を使用して正規化値(nV)を計算すること
を含む、請求項1に記載の方法。 - (i)細胞、生物、またはウイルスからの核酸が全核酸の抽出物である、および/あるいは
(ii)正規化値(nV)を使用して細胞、生物、またはウイルスにおける転写活性のレベルを評価することをさらに含む、および/あるいは
(iii)任意の前記増幅が、以下:ポリメラーゼ連鎖反応(PCR)、逆転写ポリメラーゼ連鎖反応(RT-PCR)、鎖置換増幅(SDA)、ループ介在等温増幅(LAMP)、ローリングサークル増幅(RCA)、リコンビナーゼポリメラーゼ増幅(RPA)、ヘリカーゼ依存性増幅(HDA)、鎖侵入ベース増幅(SIBA)、転写媒介増幅(TMA)、自家持続配列複製(3SR)、核酸配列ベース増幅(NASBA)、定量的ポリメラーゼ連鎖反応(qPCR)、デジタルポリメラーゼ連鎖反応(dPCR)、またはそれらの任意の組み合わせ:を使用して実施される、
請求項1~3のいずれか一項に記載の方法。 - (i) 正規化値(nV)を使用して細胞、生物、またはウイルスにおける転写活性のレベルを評価すること;ならびに/あるいは
(ii)
-転写活性を有しないことが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された転写陰性の正規化値(nV-)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を、転写陰性の正規化値(nV-)と比較して、それにより細胞、生物、またはウイルスにおける転写活性のレベルを評価すること、
をさらに含む、請求項1~4のいずれか一項に記載の方法。 - 以下:
(i)
-転写陰性の正規化値(nV-)が、細胞、生物またはウイルスにおける転写活性の有無を評価するための基本値として使用され;そして
-転写活性の欠如が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陰性の正規化値(nV-)以下である場合に示され;または
-転写活性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陰性の正規化値(nV-)を上回る場合に示される、ならびに/あるいは
(ii) 前記転写陰性の正規化値(nV-)が、以下:
-転写活性を有しないことが知られている細胞、生物、もしくはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/または
-前記転写陰性の正規化値(nV-)が、細胞、生物もしくはウイルスにおける転写活性の有無を予測する信頼区間を伴い提供される、
請求項5に記載の方法。 - 以下:
-転写活性を有することが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された転写陽性の正規化値(nV+)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を転写陽性の正規化値(nV+)と比較して、それにより細胞、生物、またはウイルスにおける転写活性レベルを評価すること
をさらに含み;
好ましくは、以下:
(i)-転写陽性の正規化値(nV+)は、細胞、生物、またはウイルスにおける転写活性の基本値として使用され;および
-転写活性の欠乏(lack)もしくは欠如(absence)が、細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陽性の正規化値(nV+)を下回る場合に示され;または
-転写活性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が転写陽性の正規化値(nV+)以上の場合に示される;ならびに/あるいは
(ii) 前記転写陽性の正規化値(nV+)が、以下:
-転写活性を有することが知られている細胞、生物、もしくはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/または
-前記転写陽性の正規化値(nV+)が、細胞、生物もしくはウイルスにおける転写活性の有無を予測する信頼区間を伴い提供される、
請求項5または6のいずれか一項に記載の方法。 - 以下:
-転写活性を有さないことが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された、転写陰性の正規化値(nV-)を取得すること;
-転写活性を有することが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された、転写陽性の正規化値(nV+)を取得すること;ならびに
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を、以下:
(i)転写陰性の正規化値(nV-)および転写陽性の正規化値(nV+)、または
(ii)転写陰性の正規化値(nV-)および転写陽性の正規化値(nV+)の中間にある合算された転写正規化値(nV±)、
と比較し、
それにより、細胞、生物、またはウイルスにおける転写活性のレベルを評価することをさらに含み、好ましくは:
(i) 合算された転写正規化値(nV±)が、
式:
(nV+)+(nV-)/2=(nV± )
を使用して計算される、ならびに/または
(ii) 前記合算された転写正規化値(nV±)が、以下:
-前記一連の転写陰性の正規化値(nV-)および/または前記転写陽性の正規化値(nV+)に統計的変動を組み込む;および/または
-前記合算された転写正規化値(nV±)が、細胞、生物、またはウイルスにおける転写活性の有無を予測する信頼区間を伴い提供される、
請求項5に記載の方法。 - 細胞、生物、またはウイルスにおける転写活性のレベルが、以下
-試験細胞または試験生物の生存率;
-試験細胞、生物またはウイルスの生死;
-試験細胞、生物、またはウイルス内の転写の摂動
のいずれか1以上を決定する目的で評価される、請求項5~8のいずれか一項に記載の方法。 - (i) 正規化値(nV)を使用して細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価し、以下:
-前記細胞、生物、またはウイルスが、核酸の前記増幅の前に薬剤で処理されており、および
-前記正規化値(nV)が、以下:
(i)薬剤耐性;または
(ii)薬剤感受性、
であることが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成されたコントロールの正規化値(cnV)と比較され、それにより、細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価すること;ならびに/または
(ii) 以下:
-薬剤感受性があることが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された薬剤感受性の正規化値(dsV)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を薬剤感受性の正規化値(dsV)と比較して、それにより薬剤耐性または薬剤感受性の、もしくは細胞、生物、またはウイルスにおけるレベルを評価し、細胞、生物、またはウイルスが、核酸の前記増幅の前に薬剤で処理されていること
をさらに含む、請求項1~4のいずれか一項に記載の方法。 - 以下:
(a)-薬剤感受性の正規化値(dsV)が、細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性の有無を評価するための基本値として使用され;および
-薬剤耐性が、細胞、生物もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤感受性の正規化値(dsV)を上回る場合に示され;または
-薬剤感受性が、細胞、生物もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤感受性の正規化値(dsV)以下である場合に示される、ならびに/あるいは;
(b) 前記薬剤感受性の正規化値(dsV)が、以下:
-薬剤感受性があることが知られている細胞、生物、またはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/または
-前記薬剤感受性の正規化値(dsV)が以下:
(i)細胞、生物もしくはウイルスにおける薬剤耐性;または
(ii)細胞、生物もしくはウイルスにおける薬剤感受性
の有無を予測する信頼区間を伴い提供される、
請求項10に記載の方法。 - 以下:
-薬剤耐性があることが知られている細胞、生物、またはウイルスの集団の個々から得られた一連の前記正規化値(nV)を使用して生成された薬剤耐性の正規化値(drV)を取得すること;および
-細胞、生物、またはウイルスからの核酸の前記増幅によって得られた正規化値(nV)を薬剤耐性の正規化値(drV)と比較して、それにより薬剤耐性もしくは薬剤感受性、または細胞、生物、もしくはウイルスにおけるレベルを評価し、細胞、生物、またはウイルスが核酸の前記増幅の前に薬剤で処理されていること
をさらに含む、請求項1~4または10のいずれか一項に記載の方法。 - 以下:
(a)-薬剤耐性の正規化値(drV)が、細胞、生物、もしくはウイルスにおける薬剤耐性または薬剤感受性の有無を評価するための基本値として使用され;および
-薬剤耐性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤耐性の正規化値(drV)以上である場合に示され;または
-薬剤感受性が、細胞、生物、もしくはウイルスからの核酸の前記増幅によって得られた正規化値(nV)が薬剤耐性の正規化値(drV)を下回る場合に示される、ならびに/あるいは
(b) 前記薬剤耐性の正規化値(drV)が、以下:
-薬剤耐性があることが知られている細胞、生物、もしくはウイルスの集団の個々からの前記一連の正規化値(nV)に統計的変動を組み込む;および/あるいは
-前記薬剤耐性の正規化値(drV)が以下:
(i)細胞、生物もしくはウイルスにおける薬剤耐性;または
(ii)細胞、生物もしくはウイルスにおける薬剤感受性
の有無を予測する信頼区間を伴い提供される、
請求項12に記載の方法。 - 正規化値(nV)を使用して細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価することをさらに含み、以下:
-核酸の前記増幅の前に薬剤で処理されている前記細胞、生物、またはウイルスの第1の集団を使用して、第1の前記正規化値(nV)を生成し、
-核酸の前記増幅の前に薬剤で処理されていない前記細胞、生物、またはウイルスの第2の集団を使用して、第2の前記正規化値(nV)を生成し、
-前記第1の正規化値(nV)と前記第2の正規化値(nV)を比較して、薬剤処理の有りもしくはなしでの、細胞、生物、またはウイルスにおける転写活性のレベルを評価し、それにより細胞、生物、またはウイルスにおける薬剤耐性または薬剤感受性のレベルを評価し、場合により、前記薬剤感受性が、前記第1の正規化値(nV)が前記第2の正規化値(nV)よりも低い場合に示される、
請求項1~4の一項に記載の方法。 - (i)薬剤が、抗菌剤、好ましくはアミノグリコシド、アンサマイシン、カルバセフェム、カルバペネム、セファロスポリン、グリコペプチド、マクロライドペニシリン、モノバクタム、ポリペプチド、キノロン、スルホンアミド、テトラサイクリンから選択されるクラスの抗菌剤である;および/あるいは
(ii)薬剤が、シプロフロキサシン、アジスロマイシン、リファンピシン、またはドキシサイクリンである;および/あるいは
(iii)第1の遺伝子が、クラミジア種(例えば、クラミジア・トラコマチス)、ゴノレア種、またはマイコプラズマ種(例えば、マイコプラズマ・ゲニタリウム)由来の遺伝子である;および/あるいは
(iv)細胞が哺乳動物細胞、ヒト細胞、動物細胞、植物細胞、細菌細胞、ウイルスに感染した宿主細胞、または細菌に感染した宿主細胞である;および/あるいは
(v)生物が、哺乳動物、ヒト、植物、細菌、ウイルス、真菌、藻類、古細菌または原生動物である、
請求項10~14のいずれか一項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| AU2017905138A AU2017905138A0 (en) | 2017-12-21 | Nucleic acid ratio determination | |
| AU2017905138 | 2017-12-21 | ||
| PCT/AU2018/051406 WO2019119072A1 (en) | 2017-12-21 | 2018-12-21 | Nucleic acid ratio determination |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2021507674A JP2021507674A (ja) | 2021-02-25 |
| JP2021507674A5 JP2021507674A5 (ja) | 2021-08-12 |
| JP7355652B2 true JP7355652B2 (ja) | 2023-10-03 |
Family
ID=66992472
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019566887A Active JP7355652B2 (ja) | 2017-12-21 | 2018-12-21 | 核酸比の決定 |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US12123051B2 (ja) |
| EP (1) | EP3685385A4 (ja) |
| JP (1) | JP7355652B2 (ja) |
| KR (1) | KR102862383B1 (ja) |
| CN (1) | CN111492434B (ja) |
| AU (1) | AU2018390995B2 (ja) |
| BR (1) | BR112020000845A2 (ja) |
| CA (1) | CA3066287A1 (ja) |
| IL (1) | IL271510B2 (ja) |
| MX (1) | MX2020006590A (ja) |
| SG (1) | SG11201912883WA (ja) |
| WO (1) | WO2019119072A1 (ja) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115786549A (zh) * | 2022-10-31 | 2023-03-14 | 宁波大学 | 用于替加环素耐药基因tet(X) RPA检测的引物和探针序列及其应用 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012171997A1 (en) | 2011-06-14 | 2012-12-20 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for determining the expression level of a gene of interest including correction of rt-qpcr data for genomic dna-derived signals |
| JP2013500706A (ja) | 2009-07-31 | 2013-01-10 | キアゲン ゲーエムベーハー | Rnaの正規化した定量化方法 |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ATE335843T1 (de) * | 1996-05-02 | 2006-09-15 | Applera Corp | Quantifizierung von rna-transkripten mittels genomischer dna als internen standard der amplifizierungsreaktion |
| US6258543B1 (en) * | 1996-05-02 | 2001-07-10 | Xtrana, Inc. | Quantitation of RNA transcripts using genomic DNA as the internal amplification competitor |
| WO2005019453A2 (en) * | 2001-05-18 | 2005-03-03 | Sirna Therapeutics, Inc. | RNA INTERFERENCE MEDIATED INHIBITION OF GENE EXPRESSION USING CHEMICALLY MODIFIED SHORT INTERFERING NUCLEIC ACID (siNA) |
| EP1418241A1 (en) * | 2002-11-08 | 2004-05-12 | PrimaGen Holding B.V. | Method for quantifying a ratio between at least two nucleic acid sequences |
| DK1948822T3 (da) | 2005-10-07 | 2011-10-17 | Johnson & Johnson Res Pty Ltd | Multikomponent-nukleinsyreenzymer og fremgangsmåder til deres anvendelse |
| CN101600808B (zh) | 2006-10-06 | 2014-07-09 | 强生研究有限公司 | 分子开关及其使用方法 |
| BRPI0809964A2 (pt) | 2007-04-05 | 2014-10-07 | Johnson & Johnson Res Pty Ltd | Método para detectar a presença um pelo menos um alvo, pelo menos dois alvos ou um apluralidade de alvos, método para a detecção de um primeiro facilitador de montagem usando uma cascata, uso de um par de ácidos nucléicos isolados, enzima mna ligase e seu uso, produto de enzima mna ligase, uso de pelo menos dois olingonucleotídeos cmo substratos |
| US8021846B2 (en) * | 2008-03-12 | 2011-09-20 | Medical Diagnostic Laboratories, Llc | Method for determining azole resistance in Candida glabrata |
| US8426133B2 (en) * | 2009-05-26 | 2013-04-23 | Quest Diagnostics Investments Incorporated | Methods for detecting gene dysregulation by intragenic differential expression |
| WO2011109901A1 (en) * | 2010-03-10 | 2011-09-15 | The Governors Of The University Of Alberta | Detection and quantification of viable bacteria in a sample using rpos mrna |
| US20130095489A1 (en) * | 2010-05-04 | 2013-04-18 | Centers For Disease Control And Prevention | Process for detection of multidrug resistant tuberculosis using real-time pcr and high resolution melt analysis |
| US9694049B2 (en) * | 2011-08-11 | 2017-07-04 | Board Of Regents Of The Nevada System Of Higher Education On Behalf Of The Unitversity Of Nevada, Reno | Methods for treating muscular dystrophy |
| US20180087113A1 (en) * | 2016-09-27 | 2018-03-29 | Oncology Venture ApS | Methods for predicting drug responsiveness in cancer patients |
-
2018
- 2018-12-21 JP JP2019566887A patent/JP7355652B2/ja active Active
- 2018-12-21 CN CN201880043163.4A patent/CN111492434B/zh active Active
- 2018-12-21 WO PCT/AU2018/051406 patent/WO2019119072A1/en not_active Ceased
- 2018-12-21 IL IL271510A patent/IL271510B2/en unknown
- 2018-12-21 KR KR1020197038255A patent/KR102862383B1/ko active Active
- 2018-12-21 CA CA3066287A patent/CA3066287A1/en active Pending
- 2018-12-21 US US16/619,932 patent/US12123051B2/en active Active
- 2018-12-21 AU AU2018390995A patent/AU2018390995B2/en active Active
- 2018-12-21 EP EP18891196.0A patent/EP3685385A4/en active Pending
- 2018-12-21 SG SG11201912883WA patent/SG11201912883WA/en unknown
- 2018-12-21 BR BR112020000845-1A patent/BR112020000845A2/pt unknown
- 2018-12-21 MX MX2020006590A patent/MX2020006590A/es unknown
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2013500706A (ja) | 2009-07-31 | 2013-01-10 | キアゲン ゲーエムベーハー | Rnaの正規化した定量化方法 |
| WO2012171997A1 (en) | 2011-06-14 | 2012-12-20 | INSERM (Institut National de la Santé et de la Recherche Médicale) | Methods for determining the expression level of a gene of interest including correction of rt-qpcr data for genomic dna-derived signals |
Non-Patent Citations (1)
| Title |
|---|
| Nucleic Acids Research,2012年,Vol.40, No.7,Article No.e51 |
Also Published As
| Publication number | Publication date |
|---|---|
| EP3685385A4 (en) | 2021-09-22 |
| BR112020000845A2 (pt) | 2020-07-21 |
| CA3066287A1 (en) | 2019-06-27 |
| CN111492434B (zh) | 2024-04-19 |
| WO2019119072A1 (en) | 2019-06-27 |
| IL271510B1 (en) | 2025-03-01 |
| NZ759676A (en) | 2025-05-02 |
| CN111492434A (zh) | 2020-08-04 |
| RU2020102949A (ru) | 2022-01-21 |
| MX2020006590A (es) | 2020-09-09 |
| AU2018390995A1 (en) | 2019-12-19 |
| AU2018390995B2 (en) | 2023-11-23 |
| EP3685385A1 (en) | 2020-07-29 |
| US20200199651A1 (en) | 2020-06-25 |
| KR20200101269A (ko) | 2020-08-27 |
| KR102862383B1 (ko) | 2025-09-18 |
| SG11201912883WA (en) | 2020-01-30 |
| IL271510A (en) | 2020-02-27 |
| US12123051B2 (en) | 2024-10-22 |
| JP2021507674A (ja) | 2021-02-25 |
| IL271510B2 (en) | 2025-07-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| CA2782692C (en) | Methods for the diagnosis of bacterial vaginosis | |
| Wei et al. | Exponential amplification reaction and triplex DNA mediated aggregation of gold nanoparticles for sensitive colorimetric detection of microRNA | |
| JP2018504891A (ja) | リアルタイムPCRによる細胞溶解物からのHBV cccDNA定量化のための新規ハイスループット法 | |
| RU2650806C2 (ru) | Субстраты нуклеиновых кислот с ферментативной активностью | |
| CN101619346B (zh) | 人冠心病易感基因-脂蛋白a基因拷贝数变异检测方法和试剂盒 | |
| KR102814480B1 (ko) | 표적 핵산을 검출하기 위한 루프형 프라이머 및 루프-드-루프 방법 | |
| US20180073087A1 (en) | Qualitative and absolute quantification kit for detecting hepatitis b virus cccdna | |
| WO2023025259A1 (zh) | 检测微小rna的方法和试剂盒 | |
| JP2017525386A (ja) | 微生物の非存在の検出の方法およびキット | |
| WO2021257844A1 (en) | Saliva-based molecular testing for sars-cov-2 | |
| WO2021226278A1 (en) | An ultrasensitive rapid and portable case13d-based diagnostic assay | |
| JP7355652B2 (ja) | 核酸比の決定 | |
| JP2021534764A (ja) | 細菌の核酸を検出し、細菌性膣炎を診断するための組成物および方法 | |
| RU2803339C2 (ru) | Определение соотношения нуклеиновых кислот | |
| KR20240067091A (ko) | 다양한 내부 변형을 갖는 루프형 프라이머 및 표적 탐지를 위한 루프-디-루프 방법 | |
| US9970053B2 (en) | Washing-free template-ready PCR detection method for RNA | |
| EP4558645A1 (en) | Method for nucleic acid detection using signal-mediated amplification of rna technology and rna aptamers | |
| RU2532344C2 (ru) | Способ диагностики гиперпролиферативных состояний и оценки риска развития рака шейки матки при цервикальной интраэпителиальной неоплазии и папилломавирусном носительстве на основе определения уровней мрнк функционального комплекса генов человека | |
| EP1869218A2 (en) | Nucleic acid detection | |
| CN106916908B (zh) | HBV cccDNA的富集提取方法及检测引物组、探针和方法 | |
| Rosenbohm | Qualitative and Semiquantitative Isothermal Detection of Nucleic Acids for Point-Of-Care Testing Applications | |
| US9464321B2 (en) | Methods and reagents that specifically detect, distinguish and quantify IFN-λ2 mRNA from IFN-λ3 mRNA in humans | |
| Tang et al. | Monitoring p21 mRNA expression in living cell based on molecular beacon fluorescence increasing rate | |
| CN106661611A (zh) | 检测阴道毛滴虫的方法 | |
| HK1243137A1 (en) | A novel high-throughput method for quantification of hbv cccdna from cell lysate by real-time pcr |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A529 | Written submission of copy of amendment under article 34 pct |
Free format text: JAPANESE INTERMEDIATE CODE: A529 Effective date: 20200319 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210629 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210629 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220726 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20221020 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230126 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230418 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230705 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20230822 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20230921 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7355652 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |