JP7547554B2 - Sulfur-containing compounds and polymers and their use in electrochemical cells - Patents.com - Google Patents
Sulfur-containing compounds and polymers and their use in electrochemical cells - Patents.com Download PDFInfo
- Publication number
- JP7547554B2 JP7547554B2 JP2023080125A JP2023080125A JP7547554B2 JP 7547554 B2 JP7547554 B2 JP 7547554B2 JP 2023080125 A JP2023080125 A JP 2023080125A JP 2023080125 A JP2023080125 A JP 2023080125A JP 7547554 B2 JP7547554 B2 JP 7547554B2
- Authority
- JP
- Japan
- Prior art keywords
- electrolyte
- lithium
- sulfur
- polymer
- electrode material
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 title claims description 91
- 229920000642 polymer Polymers 0.000 title claims description 70
- 150000001875 compounds Chemical class 0.000 title claims description 38
- 229910052717 sulfur Inorganic materials 0.000 title description 58
- 239000011593 sulfur Substances 0.000 title description 58
- 239000003792 electrolyte Substances 0.000 claims description 77
- -1 alkylene glycol Chemical compound 0.000 claims description 70
- 239000007772 electrode material Substances 0.000 claims description 61
- 229920001577 copolymer Chemical group 0.000 claims description 32
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 28
- UHOVQNZJYSORNB-UHFFFAOYSA-N monobenzene Natural products C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 claims description 26
- 239000011230 binding agent Substances 0.000 claims description 25
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 claims description 22
- 229910052744 lithium Inorganic materials 0.000 claims description 22
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 claims description 20
- LYCAIKOWRPUZTN-UHFFFAOYSA-N ethylene glycol Natural products OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims description 20
- 239000000203 mixture Substances 0.000 claims description 20
- 150000003839 salts Chemical class 0.000 claims description 18
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 claims description 16
- 239000002033 PVDF binder Substances 0.000 claims description 15
- 125000003118 aryl group Chemical group 0.000 claims description 14
- 239000002904 solvent Substances 0.000 claims description 13
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 claims description 12
- 229920000459 Nitrile rubber Polymers 0.000 claims description 12
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 claims description 12
- 125000002947 alkylene group Chemical group 0.000 claims description 12
- 229910052799 carbon Inorganic materials 0.000 claims description 12
- 229910003473 lithium bis(trifluoromethanesulfonyl)imide Inorganic materials 0.000 claims description 12
- QSZMZKBZAYQGRS-UHFFFAOYSA-N lithium;bis(trifluoromethylsulfonyl)azanide Chemical compound [Li+].FC(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)F QSZMZKBZAYQGRS-UHFFFAOYSA-N 0.000 claims description 12
- 229920001451 polypropylene glycol Chemical group 0.000 claims description 12
- 239000007787 solid Substances 0.000 claims description 11
- IIPYXGDZVMZOAP-UHFFFAOYSA-N lithium nitrate Chemical compound [Li+].[O-][N+]([O-])=O IIPYXGDZVMZOAP-UHFFFAOYSA-N 0.000 claims description 10
- 229920001343 polytetrafluoroethylene Polymers 0.000 claims description 10
- 239000004810 polytetrafluoroethylene Substances 0.000 claims description 10
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 claims description 10
- 239000004020 conductor Substances 0.000 claims description 9
- YEJRWHAVMIAJKC-UHFFFAOYSA-N 4-Butyrolactone Chemical compound O=C1CCCO1 YEJRWHAVMIAJKC-UHFFFAOYSA-N 0.000 claims description 8
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 claims description 8
- 229920003171 Poly (ethylene oxide) Polymers 0.000 claims description 8
- 239000004721 Polyphenylene oxide Substances 0.000 claims description 8
- 125000005529 alkyleneoxy group Chemical group 0.000 claims description 8
- GAEKPEKOJKCEMS-UHFFFAOYSA-N gamma-valerolactone Chemical compound CC1CCC(=O)O1 GAEKPEKOJKCEMS-UHFFFAOYSA-N 0.000 claims description 8
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 claims description 8
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 8
- 229920000570 polyether Polymers 0.000 claims description 8
- 229920002134 Carboxymethyl cellulose Polymers 0.000 claims description 7
- 125000000732 arylene group Chemical group 0.000 claims description 7
- 229920002313 fluoropolymer Polymers 0.000 claims description 7
- PQXKHYXIUOZZFA-UHFFFAOYSA-M lithium fluoride Chemical compound [Li+].[F-] PQXKHYXIUOZZFA-UHFFFAOYSA-M 0.000 claims description 7
- 239000005518 polymer electrolyte Substances 0.000 claims description 7
- 229920003048 styrene butadiene rubber Polymers 0.000 claims description 7
- 125000004434 sulfur atom Chemical group 0.000 claims description 7
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 claims description 6
- 239000000654 additive Substances 0.000 claims description 6
- 239000001768 carboxy methyl cellulose Substances 0.000 claims description 6
- 235000010948 carboxy methyl cellulose Nutrition 0.000 claims description 6
- 239000008112 carboxymethyl-cellulose Substances 0.000 claims description 6
- 239000011245 gel electrolyte Substances 0.000 claims description 6
- 239000011244 liquid electrolyte Substances 0.000 claims description 6
- ACFSQHQYDZIPRL-UHFFFAOYSA-N lithium;bis(1,1,2,2,2-pentafluoroethylsulfonyl)azanide Chemical compound [Li+].FC(F)(F)C(F)(F)S(=O)(=O)[N-]S(=O)(=O)C(F)(F)C(F)(F)F ACFSQHQYDZIPRL-UHFFFAOYSA-N 0.000 claims description 6
- VDVLPSWVDYJFRW-UHFFFAOYSA-N lithium;bis(fluorosulfonyl)azanide Chemical compound [Li+].FS(=O)(=O)[N-]S(F)(=O)=O VDVLPSWVDYJFRW-UHFFFAOYSA-N 0.000 claims description 6
- WNXJIVFYUVYPPR-UHFFFAOYSA-N 1,3-dioxolane Chemical compound C1COCO1 WNXJIVFYUVYPPR-UHFFFAOYSA-N 0.000 claims description 5
- 229910013553 LiNO Inorganic materials 0.000 claims description 5
- 230000000996 additive effect Effects 0.000 claims description 5
- 229910021389 graphene Inorganic materials 0.000 claims description 5
- 125000001072 heteroaryl group Chemical group 0.000 claims description 5
- 125000002080 perylenyl group Chemical group C1(=CC=C2C=CC=C3C4=CC=CC5=CC=CC(C1=C23)=C45)* 0.000 claims description 5
- RUOJZAUFBMNUDX-UHFFFAOYSA-N propylene carbonate Chemical compound CC1COC(=O)O1 RUOJZAUFBMNUDX-UHFFFAOYSA-N 0.000 claims description 5
- VAYTZRYEBVHVLE-UHFFFAOYSA-N 1,3-dioxol-2-one Chemical compound O=C1OC=CO1 VAYTZRYEBVHVLE-UHFFFAOYSA-N 0.000 claims description 4
- DLFVBJFMPXGRIB-UHFFFAOYSA-N Acetamide Chemical compound CC(N)=O DLFVBJFMPXGRIB-UHFFFAOYSA-N 0.000 claims description 4
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 claims description 4
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 claims description 4
- 229920000049 Carbon (fiber) Polymers 0.000 claims description 4
- OIFBSDVPJOWBCH-UHFFFAOYSA-N Diethyl carbonate Chemical compound CCOC(=O)OCC OIFBSDVPJOWBCH-UHFFFAOYSA-N 0.000 claims description 4
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 claims description 4
- KMTRUDSVKNLOMY-UHFFFAOYSA-N Ethylene carbonate Chemical compound O=C1OCCO1 KMTRUDSVKNLOMY-UHFFFAOYSA-N 0.000 claims description 4
- ZHNUHDYFZUAESO-UHFFFAOYSA-N Formamide Chemical compound NC=O ZHNUHDYFZUAESO-UHFFFAOYSA-N 0.000 claims description 4
- JGFBQFKZKSSODQ-UHFFFAOYSA-N Isothiocyanatocyclopropane Chemical compound S=C=NC1CC1 JGFBQFKZKSSODQ-UHFFFAOYSA-N 0.000 claims description 4
- 239000006230 acetylene black Substances 0.000 claims description 4
- 125000006267 biphenyl group Chemical group 0.000 claims description 4
- PWLNAUNEAKQYLH-UHFFFAOYSA-N butyric acid octyl ester Natural products CCCCCCCCOC(=O)CCC PWLNAUNEAKQYLH-UHFFFAOYSA-N 0.000 claims description 4
- 239000006229 carbon black Substances 0.000 claims description 4
- 239000004917 carbon fiber Substances 0.000 claims description 4
- 239000002041 carbon nanotube Substances 0.000 claims description 4
- 229910021393 carbon nanotube Inorganic materials 0.000 claims description 4
- 125000002993 cycloalkylene group Chemical group 0.000 claims description 4
- 229920001971 elastomer Polymers 0.000 claims description 4
- 229920005558 epichlorohydrin rubber Polymers 0.000 claims description 4
- JBTWLSYIZRCDFO-UHFFFAOYSA-N ethyl methyl carbonate Chemical compound CCOC(=O)OC JBTWLSYIZRCDFO-UHFFFAOYSA-N 0.000 claims description 4
- 229910002804 graphite Inorganic materials 0.000 claims description 4
- 239000010439 graphite Substances 0.000 claims description 4
- 125000005549 heteroarylene group Chemical group 0.000 claims description 4
- 125000006588 heterocycloalkylene group Chemical group 0.000 claims description 4
- 125000005647 linker group Chemical group 0.000 claims description 4
- VNWKTOKETHGBQD-UHFFFAOYSA-N methane Chemical compound C VNWKTOKETHGBQD-UHFFFAOYSA-N 0.000 claims description 4
- UUIQMZJEGPQKFD-UHFFFAOYSA-N n-butyric acid methyl ester Natural products CCCC(=O)OC UUIQMZJEGPQKFD-UHFFFAOYSA-N 0.000 claims description 4
- CSHWQDPOILHKBI-UHFFFAOYSA-N peryrene Natural products C1=CC(C2=CC=CC=3C2=C2C=CC=3)=C3C2=CC=CC3=C1 CSHWQDPOILHKBI-UHFFFAOYSA-N 0.000 claims description 4
- 125000003367 polycyclic group Chemical group 0.000 claims description 4
- 229920001223 polyethylene glycol Chemical group 0.000 claims description 4
- 239000005060 rubber Substances 0.000 claims description 4
- LMBFAGIMSUYTBN-MPZNNTNKSA-N teixobactin Chemical compound C([C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H](CCC(N)=O)C(=O)N[C@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CO)C(=O)N[C@H]1C(N[C@@H](C)C(=O)N[C@@H](C[C@@H]2NC(=N)NC2)C(=O)N[C@H](C(=O)O[C@H]1C)[C@@H](C)CC)=O)NC)C1=CC=CC=C1 LMBFAGIMSUYTBN-MPZNNTNKSA-N 0.000 claims description 4
- PYOKUURKVVELLB-UHFFFAOYSA-N trimethyl orthoformate Chemical compound COC(OC)OC PYOKUURKVVELLB-UHFFFAOYSA-N 0.000 claims description 4
- 229910013063 LiBF 4 Inorganic materials 0.000 claims description 3
- 229910013870 LiPF 6 Inorganic materials 0.000 claims description 3
- 239000002174 Styrene-butadiene Substances 0.000 claims description 3
- 239000007788 liquid Substances 0.000 claims description 3
- BSFLBLPKMFBUKI-UHFFFAOYSA-M lithium 4,5-dicyanotriazole-4-carboxylate Chemical compound C(#N)C1(N=NN=C1C#N)C(=O)[O-].[Li+] BSFLBLPKMFBUKI-UHFFFAOYSA-M 0.000 claims description 3
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 claims description 3
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 claims description 3
- 229910001496 lithium tetrafluoroborate Inorganic materials 0.000 claims description 3
- CVVIFWCYVZRQIY-UHFFFAOYSA-N lithium;2-(trifluoromethyl)imidazol-3-ide-4,5-dicarbonitrile Chemical compound [Li+].FC(F)(F)C1=NC(C#N)=C(C#N)[N-]1 CVVIFWCYVZRQIY-UHFFFAOYSA-N 0.000 claims description 3
- MCVFFRWZNYZUIJ-UHFFFAOYSA-M lithium;trifluoromethanesulfonate Chemical compound [Li+].[O-]S(=O)(=O)C(F)(F)F MCVFFRWZNYZUIJ-UHFFFAOYSA-M 0.000 claims description 3
- LZDKZFUFMNSQCJ-UHFFFAOYSA-N 1,2-diethoxyethane Chemical compound CCOCCOCC LZDKZFUFMNSQCJ-UHFFFAOYSA-N 0.000 claims description 2
- VFRGATWKSPNXLT-UHFFFAOYSA-N 1,2-dimethoxybutane Chemical compound CCC(OC)COC VFRGATWKSPNXLT-UHFFFAOYSA-N 0.000 claims description 2
- JWUJQDFVADABEY-UHFFFAOYSA-N 2-methyltetrahydrofuran Chemical compound CC1CCCO1 JWUJQDFVADABEY-UHFFFAOYSA-N 0.000 claims description 2
- PPDFQRAASCRJAH-UHFFFAOYSA-N 2-methylthiolane 1,1-dioxide Chemical compound CC1CCCS1(=O)=O PPDFQRAASCRJAH-UHFFFAOYSA-N 0.000 claims description 2
- 229910015015 LiAsF 6 Inorganic materials 0.000 claims description 2
- IEJIGPNLZYLLBP-UHFFFAOYSA-N dimethyl carbonate Chemical compound COC(=O)OC IEJIGPNLZYLLBP-UHFFFAOYSA-N 0.000 claims description 2
- MHCFAGZWMAWTNR-UHFFFAOYSA-M lithium perchlorate Chemical compound [Li+].[O-]Cl(=O)(=O)=O MHCFAGZWMAWTNR-UHFFFAOYSA-M 0.000 claims description 2
- LYGJENNIWJXYER-UHFFFAOYSA-N nitromethane Chemical compound C[N+]([O-])=O LYGJENNIWJXYER-UHFFFAOYSA-N 0.000 claims description 2
- 239000003880 polar aprotic solvent Substances 0.000 claims description 2
- FVSKHRXBFJPNKK-UHFFFAOYSA-N propionitrile Chemical compound CCC#N FVSKHRXBFJPNKK-UHFFFAOYSA-N 0.000 claims description 2
- HXJUTPCZVOIRIF-UHFFFAOYSA-N sulfolane Chemical compound O=S1(=O)CCCC1 HXJUTPCZVOIRIF-UHFFFAOYSA-N 0.000 claims description 2
- 206010006580 Bundle branch block left Diseases 0.000 claims 1
- 229910019142 PO4 Inorganic materials 0.000 claims 1
- 125000003709 fluoroalkyl group Chemical group 0.000 claims 1
- 239000000499 gel Substances 0.000 claims 1
- 229920006168 hydrated nitrile rubber Polymers 0.000 claims 1
- 125000006340 pentafluoro ethyl group Chemical group FC(F)(F)C(F)(F)* 0.000 claims 1
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 claims 1
- 239000010452 phosphate Substances 0.000 claims 1
- 239000005077 polysulfide Substances 0.000 description 22
- 229920001021 polysulfide Polymers 0.000 description 22
- 150000008117 polysulfides Polymers 0.000 description 22
- 238000007334 copolymerization reaction Methods 0.000 description 19
- 230000015572 biosynthetic process Effects 0.000 description 18
- 239000000463 material Substances 0.000 description 18
- 238000003786 synthesis reaction Methods 0.000 description 18
- MERLDGDYUMSLAY-UHFFFAOYSA-N 4-[(4-aminophenyl)disulfanyl]aniline Chemical compound C1=CC(N)=CC=C1SSC1=CC=C(N)C=C1 MERLDGDYUMSLAY-UHFFFAOYSA-N 0.000 description 16
- VLDPXPPHXDGHEW-UHFFFAOYSA-N 1-chloro-2-dichlorophosphoryloxybenzene Chemical compound ClC1=CC=CC=C1OP(Cl)(Cl)=O VLDPXPPHXDGHEW-UHFFFAOYSA-N 0.000 description 15
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 14
- 238000000034 method Methods 0.000 description 13
- 238000004433 infrared transmission spectrum Methods 0.000 description 12
- 238000006068 polycondensation reaction Methods 0.000 description 12
- 239000004642 Polyimide Substances 0.000 description 11
- 229920001721 polyimide Polymers 0.000 description 11
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 11
- 230000008569 process Effects 0.000 description 11
- PSDYQSWHANEKRV-UHFFFAOYSA-N [S]N Chemical compound [S]N PSDYQSWHANEKRV-UHFFFAOYSA-N 0.000 description 9
- 238000003780 insertion Methods 0.000 description 9
- 230000037431 insertion Effects 0.000 description 9
- 230000014759 maintenance of location Effects 0.000 description 9
- 239000000178 monomer Substances 0.000 description 9
- 239000002134 carbon nanofiber Substances 0.000 description 8
- 238000000921 elemental analysis Methods 0.000 description 8
- 239000011149 active material Substances 0.000 description 7
- 125000000217 alkyl group Chemical group 0.000 description 7
- 238000004090 dissolution Methods 0.000 description 6
- 238000005259 measurement Methods 0.000 description 6
- 238000006116 polymerization reaction Methods 0.000 description 6
- 238000003756 stirring Methods 0.000 description 6
- 239000003232 water-soluble binding agent Substances 0.000 description 6
- 239000004743 Polypropylene Substances 0.000 description 5
- 229910003002 lithium salt Inorganic materials 0.000 description 5
- 159000000002 lithium salts Chemical group 0.000 description 5
- 229920001155 polypropylene Polymers 0.000 description 5
- 238000010438 heat treatment Methods 0.000 description 4
- YTVNOVQHSGMMOV-UHFFFAOYSA-N naphthalenetetracarboxylic dianhydride Chemical compound C1=CC(C(=O)OC2=O)=C3C2=CC=C2C(=O)OC(=O)C1=C32 YTVNOVQHSGMMOV-UHFFFAOYSA-N 0.000 description 4
- 239000002491 polymer binding agent Substances 0.000 description 4
- 239000007774 positive electrode material Substances 0.000 description 4
- BWGNESOTFCXPMA-UHFFFAOYSA-N Dihydrogen disulfide Chemical compound SS BWGNESOTFCXPMA-UHFFFAOYSA-N 0.000 description 3
- 239000004698 Polyethylene Substances 0.000 description 3
- UCKMPCXJQFINFW-UHFFFAOYSA-N Sulphide Chemical compound [S-2] UCKMPCXJQFINFW-UHFFFAOYSA-N 0.000 description 3
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 3
- 229910052782 aluminium Inorganic materials 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 125000004432 carbon atom Chemical group C* 0.000 description 3
- 239000010406 cathode material Substances 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 238000004146 energy storage Methods 0.000 description 3
- 239000010408 film Substances 0.000 description 3
- 239000007789 gas Substances 0.000 description 3
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 3
- 239000011261 inert gas Substances 0.000 description 3
- 239000003960 organic solvent Substances 0.000 description 3
- 229920000573 polyethylene Polymers 0.000 description 3
- 238000001228 spectrum Methods 0.000 description 3
- 229910001220 stainless steel Inorganic materials 0.000 description 3
- 239000010935 stainless steel Substances 0.000 description 3
- 125000001424 substituent group Chemical group 0.000 description 3
- IBVPVTPPYGGAEL-UHFFFAOYSA-N 1,3-bis(prop-1-en-2-yl)benzene Chemical compound CC(=C)C1=CC=CC(C(C)=C)=C1 IBVPVTPPYGGAEL-UHFFFAOYSA-N 0.000 description 2
- JDZCKJOXGCMJGS-UHFFFAOYSA-N [Li].[S] Chemical compound [Li].[S] JDZCKJOXGCMJGS-UHFFFAOYSA-N 0.000 description 2
- 125000003545 alkoxy group Chemical group 0.000 description 2
- 238000002484 cyclic voltammetry Methods 0.000 description 2
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 2
- 230000000694 effects Effects 0.000 description 2
- 238000000157 electrochemical-induced impedance spectroscopy Methods 0.000 description 2
- 239000011262 electrochemically active material Substances 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 230000014509 gene expression Effects 0.000 description 2
- 239000005431 greenhouse gas Substances 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 229920000767 polyaniline Polymers 0.000 description 2
- 229920005596 polymer binder Polymers 0.000 description 2
- 230000009467 reduction Effects 0.000 description 2
- 125000006273 (C1-C3) alkyl group Chemical group 0.000 description 1
- YJTKZCDBKVTVBY-UHFFFAOYSA-N 1,3-Diphenylbenzene Chemical group C1=CC=CC=C1C1=CC=CC(C=2C=CC=CC=2)=C1 YJTKZCDBKVTVBY-UHFFFAOYSA-N 0.000 description 1
- 125000004343 1-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])(*)C([H])([H])[H] 0.000 description 1
- YBYIRNPNPLQARY-UHFFFAOYSA-N 1H-indene Natural products C1=CC=C2CC=CC2=C1 YBYIRNPNPLQARY-UHFFFAOYSA-N 0.000 description 1
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 238000004566 IR spectroscopy Methods 0.000 description 1
- 229910018091 Li 2 S Inorganic materials 0.000 description 1
- 229910012424 LiSO 3 Inorganic materials 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- GJEAMHAFPYZYDE-UHFFFAOYSA-N [C].[S] Chemical class [C].[S] GJEAMHAFPYZYDE-UHFFFAOYSA-N 0.000 description 1
- GTDPSWPPOUPBNX-UHFFFAOYSA-N ac1mqpva Chemical compound CC12C(=O)OC(=O)C1(C)C1(C)C2(C)C(=O)OC1=O GTDPSWPPOUPBNX-UHFFFAOYSA-N 0.000 description 1
- 125000004054 acenaphthylenyl group Chemical group C1(=CC2=CC=CC3=CC=CC1=C23)* 0.000 description 1
- 125000004453 alkoxycarbonyl group Chemical group 0.000 description 1
- 125000003368 amide group Chemical group 0.000 description 1
- 125000002178 anthracenyl group Chemical group C1(=CC=CC2=CC3=CC=CC=C3C=C12)* 0.000 description 1
- 125000004104 aryloxy group Chemical group 0.000 description 1
- 125000004429 atom Chemical group 0.000 description 1
- 125000003828 azulenyl group Chemical group 0.000 description 1
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 1
- 230000005540 biological transmission Effects 0.000 description 1
- 235000010290 biphenyl Nutrition 0.000 description 1
- 239000004305 biphenyl Substances 0.000 description 1
- 229910052794 bromium Inorganic materials 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 150000001721 carbon Chemical group 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 229910052801 chlorine Inorganic materials 0.000 description 1
- 239000002131 composite material Substances 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 125000004093 cyano group Chemical group *C#N 0.000 description 1
- 230000001351 cycling effect Effects 0.000 description 1
- 125000000753 cycloalkyl group Chemical group 0.000 description 1
- OOTFVKOQINZBBF-UHFFFAOYSA-N cystamine Chemical compound CCSSCCN OOTFVKOQINZBBF-UHFFFAOYSA-N 0.000 description 1
- 229940099500 cystamine Drugs 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 125000006159 dianhydride group Chemical group 0.000 description 1
- 229910000071 diazene Inorganic materials 0.000 description 1
- 150000004862 dioxolanes Chemical class 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 238000002848 electrochemical method Methods 0.000 description 1
- 239000002001 electrolyte material Substances 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 1
- 125000003983 fluorenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3CC12)* 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- 239000002803 fossil fuel Substances 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 125000003187 heptyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000000592 heterocycloalkyl group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000007970 homogeneous dispersion Substances 0.000 description 1
- 150000002430 hydrocarbons Chemical group 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 125000003454 indenyl group Chemical group C1(C=CC2=CC=CC=C12)* 0.000 description 1
- 238000009830 intercalation Methods 0.000 description 1
- 230000002687 intercalation Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 230000007774 longterm Effects 0.000 description 1
- 239000011159 matrix material Substances 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 1
- 238000012986 modification Methods 0.000 description 1
- 230000004048 modification Effects 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 125000001624 naphthyl group Chemical group 0.000 description 1
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229920000620 organic polymer Polymers 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 1
- 239000013500 performance material Substances 0.000 description 1
- 238000005504 petroleum refining Methods 0.000 description 1
- 125000001792 phenanthrenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C=CC12)* 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 239000011541 reaction mixture Substances 0.000 description 1
- 238000006479 redox reaction Methods 0.000 description 1
- 238000007142 ring opening reaction Methods 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- NGDIAZZSCVVCEW-UHFFFAOYSA-M sodium;butyl sulfate Chemical compound [Na+].CCCCOS([O-])(=O)=O NGDIAZZSCVVCEW-UHFFFAOYSA-M 0.000 description 1
- 239000007784 solid electrolyte Substances 0.000 description 1
- 239000008247 solid mixture Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- BDHFUVZGWQCTTF-UHFFFAOYSA-M sulfonate Chemical compound [O-]S(=O)=O BDHFUVZGWQCTTF-UHFFFAOYSA-M 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 238000005987 sulfurization reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 239000010409 thin film Substances 0.000 description 1
- 125000003944 tolyl group Chemical group 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- 238000004073 vulcanization Methods 0.000 description 1
- 238000010792 warming Methods 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D209/00—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom
- C07D209/02—Heterocyclic compounds containing five-membered rings, condensed with other rings, with one nitrogen atom as the only ring hetero atom condensed with one carbocyclic ring
- C07D209/44—Iso-indoles; Hydrogenated iso-indoles
- C07D209/48—Iso-indoles; Hydrogenated iso-indoles with oxygen atoms in positions 1 and 3, e.g. phthalimide
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G73/00—Macromolecular compounds obtained by reactions forming a linkage containing nitrogen with or without oxygen or carbon in the main chain of the macromolecule, not provided for in groups C08G12/00 - C08G71/00
- C08G73/06—Polycondensates having nitrogen-containing heterocyclic rings in the main chain of the macromolecule
- C08G73/10—Polyimides; Polyester-imides; Polyamide-imides; Polyamide acids or similar polyimide precursors
- C08G73/1057—Polyimides containing other atoms than carbon, hydrogen, nitrogen or oxygen in the main chain
- C08G73/1064—Polyimides containing other atoms than carbon, hydrogen, nitrogen or oxygen in the main chain containing sulfur
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08G—MACROMOLECULAR COMPOUNDS OBTAINED OTHERWISE THAN BY REACTIONS ONLY INVOLVING UNSATURATED CARBON-TO-CARBON BONDS
- C08G75/00—Macromolecular compounds obtained by reactions forming a linkage containing sulfur with or without nitrogen, oxygen, or carbon in the main chain of the macromolecule
- C08G75/14—Polysulfides
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/052—Li-accumulators
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0565—Polymeric materials, e.g. gel-type or solid-type
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0567—Liquid materials characterised by the additives
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0568—Liquid materials characterised by the solutes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M10/00—Secondary cells; Manufacture thereof
- H01M10/05—Accumulators with non-aqueous electrolyte
- H01M10/056—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes
- H01M10/0564—Accumulators with non-aqueous electrolyte characterised by the materials used as electrolytes, e.g. mixed inorganic/organic electrolytes the electrolyte being constituted of organic materials only
- H01M10/0566—Liquid materials
- H01M10/0569—Liquid materials characterised by the solvents
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/13—Electrodes for accumulators with non-aqueous electrolyte, e.g. for lithium-accumulators; Processes of manufacture thereof
- H01M4/137—Electrodes based on electro-active polymers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/38—Selection of substances as active materials, active masses, active liquids of elements or alloys
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/36—Selection of substances as active materials, active masses, active liquids
- H01M4/60—Selection of substances as active materials, active masses, active liquids of organic compounds
- H01M4/602—Polymers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/621—Binders
- H01M4/622—Binders being polymers
- H01M4/623—Binders being polymers fluorinated polymers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M4/62—Selection of inactive substances as ingredients for active masses, e.g. binders, fillers
- H01M4/624—Electric conductive fillers
- H01M4/625—Carbon or graphite
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M4/00—Electrodes
- H01M4/02—Electrodes composed of, or comprising, active material
- H01M2004/026—Electrodes composed of, or comprising, active material characterised by the polarity
- H01M2004/028—Positive electrodes
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0025—Organic electrolyte
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0017—Non-aqueous electrolytes
- H01M2300/0065—Solid electrolytes
- H01M2300/0082—Organic polymers
-
- H—ELECTRICITY
- H01—ELECTRIC ELEMENTS
- H01M—PROCESSES OR MEANS, e.g. BATTERIES, FOR THE DIRECT CONVERSION OF CHEMICAL ENERGY INTO ELECTRICAL ENERGY
- H01M2300/00—Electrolytes
- H01M2300/0085—Immobilising or gelification of electrolyte
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E60/00—Enabling technologies; Technologies with a potential or indirect contribution to GHG emissions mitigation
- Y02E60/10—Energy storage using batteries
Landscapes
- Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Electrochemistry (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Manufacturing & Machinery (AREA)
- Inorganic Chemistry (AREA)
- Condensed Matter Physics & Semiconductors (AREA)
- General Physics & Mathematics (AREA)
- Physics & Mathematics (AREA)
- Medicinal Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Polymers & Plastics (AREA)
- Materials Engineering (AREA)
- Dispersion Chemistry (AREA)
- Battery Electrode And Active Subsutance (AREA)
- Secondary Cells (AREA)
- Polymers With Sulfur, Phosphorus Or Metals In The Main Chain (AREA)
- Macromolecular Compounds Obtained By Forming Nitrogen-Containing Linkages In General (AREA)
- Indole Compounds (AREA)
Description
関連出願
本願は、適用法に基づき、2017年10月2日出願のカナダ特許出願第2,981,012号の優先権を主張する。その内容は、参照によりその全文があらゆる目的で本明細書に組み込まれる。
RELATED APPLICATIONS This application claims priority under applicable law to Canadian Patent Application No. 2,981,012, filed October 2, 2017, the contents of which are incorporated herein by reference in their entirety for all purposes.
技術分野
本願は、特にリチウム電池において、正極の電気化学的活物質として、固体ポリマー電解質(SPE)として、または電解質の添加剤として使用するためのポリマーおよびオリゴマーの分野に関する。
TECHNICAL FIELD This application relates to the field of polymers and oligomers for use as electrochemically active materials in positive electrodes, as solid polymer electrolytes (SPEs) or as additives to electrolytes, especially in lithium batteries.
地球環境への意識は、温室効果ガスの問題およびその地球への影響に対する答えを見つけるために多くの科学者に影響を与えている。輸送は温室効果ガス排出において主要な役割を果たすということが分かっているので、輸送を電化することは間違いなく地球温暖化への解決策の一部である。したがって、環境により優しく、より手頃な価格で、より安全で、化石燃料の性能に近い性能(自律性および電力など)を提供する新しい電池材料を設計することが重要である。 Awareness of the global environment has inspired many scientists to find answers to the problem of greenhouse gases and their impact on the planet. As we know that transportation plays a major role in greenhouse gas emissions, electrifying transportation is definitely part of the solution to global warming. Therefore, it is important to design new battery materials that are more environmentally friendly, more affordable, safer and offer performances (such as autonomy and power) close to those of fossil fuels.
有機カソードは、エネルギー貯蔵に関する需要を満たすことができる電池の製造の最有力候補である。これらの材料の利点は、合成温度がインターカレーション材料の合成温度よりも大幅に低いことである(Armandら、Nature,2008,451,652)。さらに、それらは豊富に存在する元素で構成され、優れた電気化学性能を提供する(Le Gallら、Journal of Power Sources,2003,316-320)。一方、それらの最大の欠点は、活物質が電解質に溶出することに関連し、それは電池の安定性に大きく影響する(Chenら、ChemSusChem.,2008,1,348-355)。電気化学的に活性な有機ポリマーは、サイクル性のより高い材料を得るために、活物質の溶解を抑制または低減することを可能にすることができる(Zengら、Electrochimica Acta,2014,447-454)。 Organic cathodes are prime candidates for the production of batteries capable of meeting the demands of energy storage. The advantage of these materials is that their synthesis temperatures are significantly lower than those of intercalation materials (Armand et al., Nature, 2008, 451, 652). Moreover, they are composed of abundant elements and offer excellent electrochemical performance (Le Gall et al., Journal of Power Sources, 2003, 316-320). On the other hand, their biggest drawback is related to the dissolution of the active material into the electrolyte, which greatly affects the stability of the battery (Chen et al., ChemSusChem., 2008, 1, 348-355). Electrochemically active organic polymers can make it possible to inhibit or reduce the dissolution of the active material in order to obtain more cyclable materials (Zeng et al., Electrochimica Acta, 2014, 447-454).
硫黄元素も、高いエネルギー密度をもつ電池の製造の候補である。実際に、リチウム硫黄(Li-S)電池は、この元素によって提供される利点、すなわち1675mAh/gという大容量と非常に豊富であることを考慮すると非常に有望である。後者は、硫黄が石油精製の副産物であるという事実に起因している(Hyunら、ACS Energy Letters,2016,1,566-572)。しかし、Li-Sバッテリーには、サイクル中の硫黄の還元によって生成されるポリスルフィド(Li2Sx、x=4~8)の溶解をはじめとする数個の欠点もある。その上、ひとたび溶解すると、ポリスルフィドは、「シャトル効果」と呼ばれる、リチウム表面(アノード)を不安定化させる現象に関与する。この現象は、安定性の低下および低いクーロン効率をもたらす(Zhouら、J.Am.Chem.Soc.2013,135,16736-16743)。 Elemental sulfur is also a candidate for the production of batteries with high energy density. Indeed, lithium-sulfur (Li-S) batteries are very promising given the advantages offered by this element, namely its large capacity of 1675 mAh/g and its great abundance. The latter is attributed to the fact that sulfur is a by-product of petroleum refining (Hyun et al., ACS Energy Letters, 2016, 1, 566-572). However, Li-S batteries also have several drawbacks, including the dissolution of polysulfides (Li 2 S x , x=4-8) that are generated by the reduction of sulfur during cycling. Moreover, once dissolved, polysulfides are involved in a phenomenon called the "shuttle effect," which destabilizes the lithium surface (anode). This phenomenon leads to reduced stability and low coulombic efficiency (Zhou et al., J. Am. Chem. Soc. 2013, 135, 16736-16743).
この問題を解決するために使用される1つの戦略は、硫黄粒子のカプセル化を伴う。例えば、Zhouら(J.Am.Chem.Soc.2013,135,16736-16743)は、硫黄をポリアニリン(PANI)でコーティングして、このシェルの内部のポリスルフィドを固定化した。硫黄をカプセル化することにより、電池の安定性を高めることが可能になる。しかし、この元素の添加は、活物質中の硫黄の量をたった58重量%に制限する。つまり、この材料の42重量%は電気化学的に不活性な材料からなり、それにより電極材料の電荷密度を低下させる。この戦略により、97%を超えるクーロン効率をまだ得ることができるが、それでも長期サイクル性には限界がある。 One strategy used to solve this problem involves the encapsulation of sulfur particles. For example, Zhou et al. (J. Am. Chem. Soc. 2013, 135, 16736-16743) coated sulfur with polyaniline (PANI) to immobilize the polysulfides inside this shell. Encapsulating the sulfur makes it possible to increase the stability of the battery. However, the addition of this element limits the amount of sulfur in the active material to only 58% by weight; that is, 42% by weight of this material consists of electrochemically inactive material, thereby reducing the charge density of the electrode material. With this strategy, coulombic efficiencies of over 97% can still be obtained, but the long-term cyclability is still limited.
炭素-硫黄複合材料の合成も提示されている。例えば、Wangら(Journal of Power Sources,2011,7030-7034)は、グラフェン-硫黄複合材料を合成した。この新しい材料は、固有の導電率を高めることだけでなく、理論値とほぼ同等の初期容量を達成することも可能にする。しかし、グラフェンが存在することにより、ポリスルフィド溶解の現象を抑制することはできず、この材料は、硫黄自体と同等の容量損失を有する。 The synthesis of carbon-sulfur composites has also been presented. For example, Wang et al. (Journal of Power Sources, 2011, 7030-7034) synthesized a graphene-sulfur composite. This new material makes it possible not only to increase the specific electrical conductivity, but also to achieve an initial capacity almost equal to the theoretical value. However, the presence of graphene does not suppress the phenomenon of polysulfide dissolution, and this material has a capacity loss comparable to that of sulfur itself.
硫黄に富むポリマーを得るために、硫黄元素と1またはそれを超える有機モノマーとの共重合も調査されている。硫黄が159℃を超えて加熱されると、(S8)環の開環が起こり、それによりラジカル重合を受けることのできるジラジカルが生成される。Chungら(Nature Chemistry,2013,5,518-524)は、Li-S電池用の、硫黄に富む共重合体を開発した。硫黄元素は、逆加硫により、異なるパーセンテージの1,3-ジイソプロペニルベンゼン(DIB)と共重合された。共重合により、ポリスルフィドの溶解を制限することができるマトリックスを作製することが可能になる。それらの電気化学的結果は、優れたクーロン効率および良好な容量保持を示す。しかし、上に提示されるように、使用される有機モノマーは電気化学的に非活性であり、そのことにより、不活性な塊の存在、および結果的にエネルギー密度の低下がもたらされる。
したがって、例えば、先行する材料のいくつかの利点を組み合わせると同時に、それらの少なくとも1つの欠点を排除する、新しい電極材料の開発が必要である。
Copolymerization of elemental sulfur with one or more organic monomers has also been investigated to obtain sulfur-rich polymers. When sulfur is heated above 159° C., the (S 8 ) ring opening occurs, which generates diradicals that can undergo radical polymerization. Chung et al. (Nature Chemistry, 2013, 5, 518-524) developed sulfur-rich copolymers for Li—S batteries. Elemental sulfur was copolymerized with different percentages of 1,3-diisopropenylbenzene (DIB) by inverse vulcanization. The copolymerization makes it possible to create a matrix that can limit the dissolution of polysulfides. Their electrochemical results show excellent coulombic efficiency and good capacity retention. However, as presented above, the organic monomers used are electrochemically inactive, which leads to the presence of inactive masses and, consequently, to a reduced energy density.
Thus, for example, there is a need for the development of new electrode materials that combine some of the advantages of previous materials while eliminating at least one of their disadvantages.
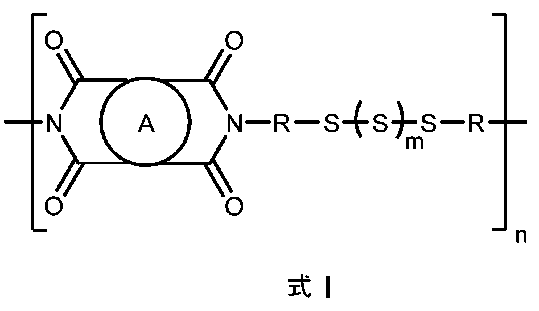
第1の態様によれば、本記載は、式Iのポリマー:
Aは、電子の非局在化を許容する不飽和基、例えば、置換または非置換のアリールおよびヘテロアリール基、ならびにそれらの縮合または非縮合多環式対応物から選択され;
Rは、直鎖または分岐鎖C2-6アルキレン、直鎖または分岐鎖C2-6アルキレンオキシ、直鎖または分岐鎖C2-6アルキレングリコール、直鎖または分岐鎖C2-6アルキレンオキシC2-6アルキレン、直線状または分岐鎖ポリ(C2-6アルキレングリコール)、C6-12アリーレン、C3-12シクロアルキレン、C5-12ヘテロアリーレン、およびC3-12ヘテロシクロアルキレンから選択される置換または非置換有機連結基であり;
mは、ポリマーリンクのジスルフィド結合に挿入された硫黄原子の平均数を表し、ゼロであり得ず、すなわち、m>0、例えば0<m≦8、または1≦m≦6、または1≦m≦4であり;かつ
nは、ポリマー中の単位の平均数を表し、例えば、nは2~500、または5~300の範囲内であり得る)
に関する。
According to a first aspect, the present disclosure relates to a polymer of formula I:
A is selected from unsaturated groups that allow for electron delocalization, such as substituted or unsubstituted aryl and heteroaryl groups, and their fused or non-fused polycyclic counterparts;
R is a substituted or unsubstituted organic linking group selected from linear or branched C 2-6 alkylene, linear or branched C 2-6 alkyleneoxy, linear or branched C 2-6 alkylene glycol, linear or branched C 2-6 alkyleneoxy C 2-6 alkylene, linear or branched poly(C 2-6 alkylene glycol), C 6-12 arylene, C 3-12 cycloalkylene, C 5-12 heteroarylene, and C 3-12 heterocycloalkylene;
m represents the average number of sulfur atoms inserted into the disulfide bonds of the polymer links and cannot be zero, i.e., m>0, e.g., 0<m≦8, or 1≦m≦6, or 1≦m≦4; and n represents the average number of units in the polymer, e.g., n can be in the range of 2 to 500, or 5 to 300.
Regarding.
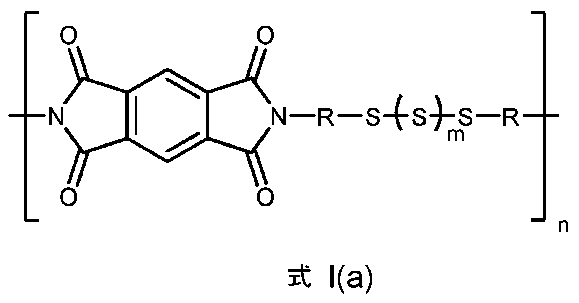
一実施形態によれば、Aは、ベンゼン、ナフタレン、ペリレンおよびビフェニル基から選択される。例えば、Aは、ベンゼン基であり、ポリマーは式I(a):
のポリマーである。
According to one embodiment, A is selected from benzene, naphthalene, perylene and biphenyl groups. For example, A is a benzene group and the polymer has formula I(a):
It is a polymer of.
別の実施形態によれば、Rは、ベンゼン、エチレン、プロピレン、ポリ(エチレングリコール)、ポリ(プロピレングリコール)、およびエチレングリコールとプロピレングリコールの共重合体の基から選択される。 According to another embodiment, R is selected from the group consisting of benzene, ethylene, propylene, poly(ethylene glycol), poly(propylene glycol), and copolymers of ethylene glycol and propylene glycol.
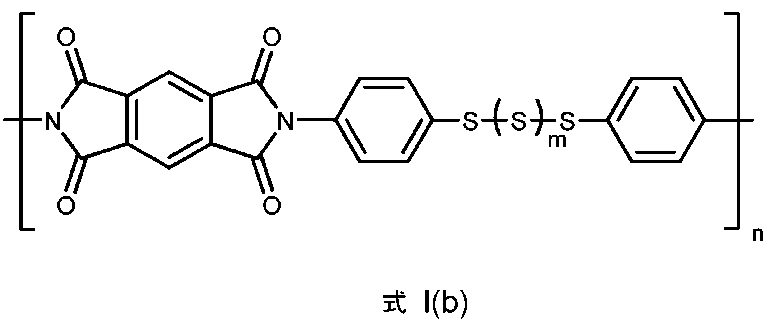
ポリマーの例は、式I(b):
によっても例示される。
An example of a polymer has formula I(b):
This is also exemplified by:
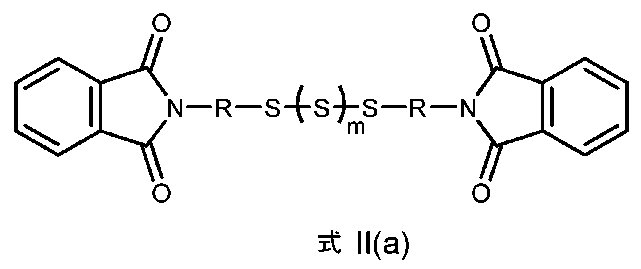
別の態様によれば、本記載は、式IIの化合物:
に関する。
According to another aspect, the present disclosure relates to a compound of formula II:
Regarding.
この化合物の一例は、式II(a):
で表される。
An example of this compound is represented by formula II(a):
It is expressed as:
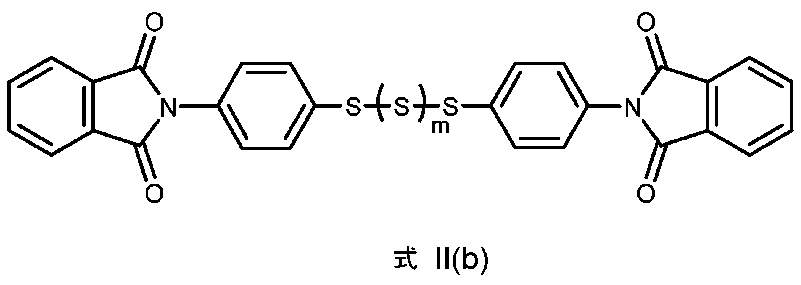
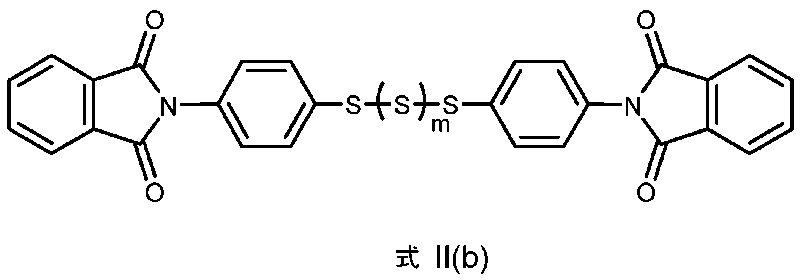
化合物の別の例は、式II(b):
によって例示される。
Another example of a compound has formula II(b):
As exemplified by:
別の態様によれば、本記載は、本明細書において定義されるポリマーまたは化合物を含む電極材料に関する。例えば、電極材料は、導電性材料、バインダー、または両方の組合せをさらに含む。電極材料は、遊離硫黄元素(Sx)を含むこともある。 According to another aspect, the present description relates to an electrode material comprising a polymer or compound as defined herein. For example, the electrode material further comprises a conductive material, a binder, or a combination of both. The electrode material may also comprise free elemental sulfur (S x ).
一実施形態によれば、導電性材料は、カーボンブラック、Ketjen(商標)カーボン、シャウィニガンカーボン、アセチレンブラック、グラファイト、グラフェン、カーボンファイバー(例えばカーボンナノファイバー(例えば、気相で形成されたVGCF)など)、カーボンナノチューブ、またはそれらの少なくとも2つの組合せから選択される。 According to one embodiment, the conductive material is selected from carbon black, Ketjen™ carbon, Shawinigan carbon, acetylene black, graphite, graphene, carbon fibers (e.g., carbon nanofibers (e.g., VGCF formed in the gas phase), etc.), carbon nanotubes, or a combination of at least two thereof.
一実施形態によれば、バインダーは、ポリエーテル型のポリマーバインダー、フッ素化ポリマー型、または水溶性バインダーである。一例によれば、ポリエーテル型のポリマーバインダーは、直線状、分岐鎖、および/または架橋したものであり、ポリ(エチレンオキシド)(PEO)、ポリ(プロピレンオキシド)(PPO)、またはこれら2つの組合せ(またはEO/PO共重合体)に基づき、架橋可能な単位を必要に応じて含む。別の例によれば、フッ素化ポリマーバインダーは、PVDF(ポリフッ化ビニリデン)またはPTFE(ポリテトラフルオロエチレン)である。最後に、水溶性バインダーの例には、SBR(スチレン-ブタジエンゴム)、NBR(アクリロニトリル-ブタジエンゴム)、HNBR(水素化NBR)、CHR(エピクロロヒドリンゴム)、またはACM(アクリレートゴム)が挙げられ、必要に応じてCMC(カルボキシメチルセルロース)を含む。 According to one embodiment, the binder is a polymeric binder of polyether type, fluorinated polymer type, or water-soluble binder. According to one example, the polymeric binder of polyether type is linear, branched, and/or crosslinked, optionally including crosslinkable units, based on poly(ethylene oxide) (PEO), poly(propylene oxide) (PPO), or a combination of the two (or EO/PO copolymers). According to another example, the fluorinated polymeric binder is PVDF (polyvinylidene fluoride) or PTFE (polytetrafluoroethylene). Finally, examples of water-soluble binders include SBR (styrene-butadiene rubber), NBR (acrylonitrile-butadiene rubber), HNBR (hydrogenated NBR), CHR (epichlorohydrin rubber), or ACM (acrylate rubber), optionally including CMC (carboxymethylcellulose).
さらなる態様によれば、本記載は、集電体に適用された、本明細書において定義される電極材料を含む正極に関する。 According to a further aspect, the present disclosure relates to a positive electrode comprising an electrode material as defined herein applied to a current collector.
さらなる態様によれば、本記載は、本明細書において定義されるポリマーまたは本明細書において定義される化合物を含む電解質にも関する。一実施形態によれば、電解質は、溶媒中の塩を含む液体電解質である。一代替形態によれば、電解質は、溶媒中の塩および必要に応じて溶媒和ポリマーを含むゲル電解質である。第2の代替形態によれば、電解質は、溶媒和ポリマー中に塩を含む固体ポリマー電解質(SPE)である。例えば、本明細書において定義されるポリマー、または本明細書において定義される化合物は添加剤である。あるいは、SPEの溶媒和ポリマーは、本明細書において定義されるポリマー、または本明細書において定義される化合物である。別の実施形態によれば、塩はリチウム塩である。一実施形態によれば、電解質は、硫黄元素、バインダー、添加剤またはそれらの少なくとも2つの組合せをさらに含む。 According to a further aspect, the present description also relates to an electrolyte comprising a polymer as defined herein or a compound as defined herein. According to one embodiment, the electrolyte is a liquid electrolyte comprising a salt in a solvent. According to one alternative, the electrolyte is a gel electrolyte comprising a salt in a solvent and optionally a solvating polymer. According to a second alternative, the electrolyte is a solid polymer electrolyte (SPE) comprising a salt in a solvating polymer. For example, the polymer as defined herein or the compound as defined herein is an additive. Alternatively, the solvating polymer of the SPE is a polymer as defined herein or a compound as defined herein. According to another embodiment, the salt is a lithium salt. According to one embodiment, the electrolyte further comprises elemental sulfur, a binder, an additive or a combination of at least two thereof.
別の態様は、カソード、電解質、およびアノードを含む電気化学セルに言及し、ここでカソードは、本明細書において定義される電極材料を含む。代替実施形態によれば、これらの電気化学セルは、本明細書において定義される、負極、電解質および正極を含む。代替実施形態によれば、これらの電気化学セルは、本明細書において定義される、カソード、アノードおよび電解質を含む。本記載は、そのような電気化学セルを含むリチウム電池にも言及する。 Another aspect refers to electrochemical cells comprising a cathode, an electrolyte, and an anode, where the cathode comprises an electrode material as defined herein. According to alternative embodiments, these electrochemical cells comprise a negative electrode, an electrolyte, and a positive electrode as defined herein. According to alternative embodiments, these electrochemical cells comprise a cathode, an anode, and an electrolyte as defined herein. The description also refers to lithium batteries comprising such electrochemical cells.
最後に、本記載は、本明細書において定義されるポリマーおよび化合物、電極材料、電解質材料、電極、電解質、およびそれらを含む電気化学セルを製造するためのプロセスに言及する。これらの電気化学セルの使用、より詳細には、携帯機器、例えば、携帯電話、カメラ、タブレットまたはラップトップでの、電気自動車またはハイブリッド車での、あるいは再生可能エネルギー貯蔵での使用も企図される。
本発明の実施形態において、例えば以下の項目が提供される。
(項目1)
式Iのポリマー:
Aは、電子の非局在化を許容する不飽和基、例えば、置換または非置換のアリールおよびヘテロアリール基、ならびにそれらの縮合または非縮合多環式等価物から選択され;
Rは、直鎖または分岐鎖C2-6アルキレン、直鎖または分岐鎖C2-6アルキレンオキシ、直鎖または分岐鎖C2-6アルキレングリコール、直鎖または分岐鎖C2-6アルキレンオキシC2-6アルキレン、直線状または分岐鎖ポリ(C2-6アルキレングリコール)、C6-12アリーレン、C3-12シクロアルキレン、C5-12ヘテロアリーレン、およびC3-12ヘテロシクロアルキレンから選択される置換または非置換有機連結基であり;
mは、ポリマーリンクのジスルフィド結合に挿入された硫黄原子の平均数を表し、ゼロであり得ず、すなわち、m>0、例えば0<m≦8、または1≦m≦6、または1≦m≦4であり;かつ
nは、ポリマー中の単位の平均数を表し、例えば、nは2~500、または5~300の範囲内であり得る]。
(項目2)
Aが、ベンゼン、ナフタレン、ペリレン、およびビフェニル基から選択される、項目1に記載のポリマー。
(項目3)
前記ポリマーが式I(a):
のポリマーである項目1または2に記載のポリマー。
(項目4)
Rが、ベンゼン、エチレン、プロピレン、ポリ(エチレングリコール)、ポリ(プロピレングリコール)、およびエチレングリコールとプロピレングリコールの共重合体の基から選択される、項目1から3のいずれか一項に記載のポリマー。
(項目5)
前記ポリマーが式I(b):
のポリマーである、項目4に記載のポリマー。
(項目6)
式IIの化合物:
(項目7)
前記化合物が式II(a):
の化合物である、項目6に記載の化合物。
(項目8)
前記化合物が式II(b):
の化合物である、項目6に記載の化合物。
(項目9)
項目1から5のいずれか一項に定義されるポリマー、または項目6から8のいずれか一項に定義される化合物を含む電極材料。
(項目10)
硫黄元素をさらに含む、項目9に記載の電極材料。
(項目11)
導電性材料、バインダー、または両方の組合せをさらに含む、項目9または10に記載の電極材料。
(項目12)
前記導電性材料が、カーボンブラック、Ketjen(商標)カーボン、シャウィニガンカーボン、アセチレンブラック、グラファイト、グラフェン、カーボンファイバー(例えばカーボンナノファイバー(例えば、気相で形成されたVGCF)など)、およびカーボンナノチューブ、またはそれらの少なくとも2つの組合せから選択される、項目11に記載の電極材料。
(項目13)
前記バインダーがポリエーテル型のポリマーバインダー、フッ素化ポリマー、または水溶性バインダーである、項目11または12に記載の電極材料。
(項目14)
前記ポリエーテル型のポリマーバインダーが直線状、分岐鎖、および/または架橋したものであり、ポリ(エチレンオキシド)(PEO)、ポリ(プロピレンオキシド)(PPO)、またはこれら2つの混合物(またはEO/PO共重合体)に基づき、架橋可能な単位を必要に応じて含む、項目13に記載の電極材料。
(項目15)
前記フッ素化ポリマーバインダーが、PVDF(ポリフッ化ビニリデン)またはPTFE(ポリテトラフルオロエチレン)である、項目13に記載の電極材料。
(項目16)
前記水溶性バインダーが、SBR(スチレン-ブタジエンゴム)、NBR(アクリロニトリル-ブタジエンゴム)、HNBR(水素化NBR)、CHR(エピクロロヒドリンゴム)、またはACM(アクリレートゴム)であり、必要に応じてCMC(カルボキシメチルセルロース)を含む、項目13に記載の電極材料。
(項目17)
集電体に適用された、項目9から16のいずれか一項に記載の電極材料を含む正極。
(項目18)
項目1から5のいずれか一項に定義されるポリマー、または項目6から8のいずれか一項に定義される化合物を含む電解質。
(項目19)
前記電解質が、溶媒中の塩を含む液体電解質である、項目18に記載の電解質。
(項目20)
前記電解質が、溶媒中の塩および必要に応じて溶媒和ポリマーを含むゲル電解質である、項目18に記載の電解質。
(項目21)
前記溶媒が、エチレンカーボネート(EC)、ジエチルカーボネート(DEC)、プロピレンカーボネート(PC)、ジメチルカーボネート(DMC)、エチルメチルカーボネート(EMC)、γ-ブチロラクトン(γ-BL)、ビニレンカーボネート(VC)、酪酸メチル(MB)、γ-バレロラクトン(γ-VL)、1,2-ジメトキシエタン(DME)、1,2-ジエトキシエタン(DEE)、2-メチルテトラヒドロフラン、ジメチルスルホキシド、ホルムアミド、アセトアミド、ジメチルホルムアミド、ジオキソラン、アセトニトリル、プロピルニトリル、ニトロメタン、エチルモノグリム、トリメトキシメタン、ジオキソラン誘導体、スルホラン、メチルスルホラン、プロピレンカーボネート誘導体、テトラヒドロフラン、およびそれらの混合物から選択される極性非プロトン性溶媒である、項目19または20に記載の電解質。
(項目22)
前記電解質が、溶媒和ポリマー中の塩を含む固体ポリマー電解質(SPE)である、項目18に記載の電解質。
(項目23)
前記ポリマーまたは前記化合物が添加剤である、項目18から22のいずれか一項に記載の電解質。
(項目24)
前記溶媒和ポリマーが、項目1から5のいずれか一項に定義される前記ポリマーまたは項目6から8のいずれか一項に定義される前記化合物である、項目22に記載の電解質。
(項目25)
前記電解質が、硫黄元素をさらに含む、項目18から24のいずれか一項に記載の電解質。
(項目26)
前記塩がリチウム塩である、項目19から25のいずれか一項に記載の電解質。
(項目27)
前記塩が、ヘキサフルオロリン酸リチウム(LiPF6)、リチウムビス(トリフルオロメタンスルホニル)イミド(LiTFSI)、リチウムビス(フルオロスルホニル)イミド(LiFSI)、リチウム2-トリフルオロメチル-4,5-ジシアノイミダゾレート(LiTDI)、リチウム4,5-ジシアノ-1,2,3-トリアゾレート(LiDCTA)、リチウムビス(ペンタフルオロエチルスルホニル)イミド(LiBETI)、テトラフルオロホウ酸リチウム(LiBF4)、リチウムビス(オキサラト)ボレート(LiBOB)、硝酸リチウム(LiNO3)、塩化リチウム(LiCl)、臭化リチウム(LiBr)、フッ化リチウム(LiF)、過塩素酸リチウム(LiClO4)、ヘキサフルオロヒ酸リチウム(LiAsF6)、トリフルオロメタンスルホン酸リチウム(LiSO3CF3)(LiTf)、フルオロアルキルリン酸リチウムLi[PF3(CF2CF3)3](LiFAP)、リチウムテトラキス(トリフルオロアセトキシ)ボレートLi[B(OCOCF3)4](LiTFAB)、リチウムビス(1,2-ベンゼンジオラト(2-)-O、O’)ボレートLi[B(C6O2)2](LBBB)およびそれらの組合せから選択される、項目26に記載の電解質。
(項目28)
前記電解質が、電解質バインダーをさらに含む、項目18から27のいずれか一項に記載の電解質。
(項目29)
前記電解質バインダーが、ポリエーテル型のポリマーバインダー、フッ素化ポリマー、または水溶性バインダーである、項目28に記載の電解質。
(項目30)
前記フッ素化ポリマーバインダーがポリフッ化ビニリデン(PVDF)である、項目29に記載の電解質。
(項目31)
カソード、電解質、およびアノードを含む電気化学セルであって、前記カソードが、項目9から16のいずれか一項に定義される電極材料を含む、電気化学セル。
(項目32)
負極、電解質および項目17に定義される正極を含む、電気化学セル。
(項目33)
カソード、アノードおよび項目18から30のいずれか一項に定義される電解質を含む電気化学セル。
(項目34)
負極、電解質および正極を含む電気化学セルであって、前記正極が項目17に定義されるものであり、前記電解質が項目18から30のいずれか一項に定義されるものである、電気化学セル。
(項目35)
項目31から34のいずれか一項に定義される電気化学セルを含むリチウム電池。
Finally, the present description refers to processes for producing the polymers and compounds defined herein, electrode materials, electrolyte materials, electrodes, electrolytes, and electrochemical cells containing them. The use of these electrochemical cells is also contemplated, more particularly in portable devices, such as mobile phones, cameras, tablets or laptops, in electric or hybrid vehicles, or in renewable energy storage.
In an embodiment of the present invention, for example, the following items are provided:
(Item 1)
Polymer of Formula I:
A is selected from unsaturated groups that allow for electron delocalization, such as substituted or unsubstituted aryl and heteroaryl groups, and fused or non-fused polycyclic equivalents thereof;
R is a substituted or unsubstituted organic linking group selected from linear or branched C 2-6 alkylene, linear or branched C 2-6 alkyleneoxy, linear or branched C 2-6 alkylene glycol, linear or branched C 2-6 alkyleneoxy C 2-6 alkylene, linear or branched poly(C 2-6 alkylene glycol), C 6-12 arylene, C 3-12 cycloalkylene, C 5-12 heteroarylene, and C 3-12 heterocycloalkylene;
m represents the average number of sulfur atoms inserted into the disulfide bonds of the polymer links and cannot be zero, i.e., m>0, e.g., 0<m≦8, or 1≦m≦6, or 1≦m≦4; and n represents the average number of units in the polymer, e.g., n can be in the range of 2 to 500, or 5 to 300.
(Item 2)
2. The polymer of
(Item 3)
The polymer has formula I(a):
3. The polymer according to
(Item 4)
4. The polymer according to any one of the preceding claims, wherein R is selected from the group consisting of benzene, ethylene, propylene, poly(ethylene glycol), poly(propylene glycol), and copolymers of ethylene glycol and propylene glycol.
(Item 5)
The polymer has formula I(b):
5. The polymer according to claim 4, which is a polymer of formula:
(Item 6)
Compound of Formula II:
(Item 7)
The compound has formula II(a):
7. The compound according to claim 6, which is a compound of formula:
(Item 8)
The compound has formula II(b):
7. The compound according to claim 6, which is a compound of formula:
(Item 9)
Electrode material comprising a polymer as defined in any one of
(Item 10)
10. The electrode material according to item 9, further comprising elemental sulfur.
(Item 11)
11. The electrode material of
(Item 12)
Item 12. The electrode material of item 11, wherein the conductive material is selected from carbon black, Ketjen™ carbon, Shawinigan carbon, acetylene black, graphite, graphene, carbon fibers (such as carbon nanofibers (e.g., VGCF formed in the gas phase)), and carbon nanotubes, or a combination of at least two thereof.
(Item 13)
13. The electrode material according to item 11 or 12, wherein the binder is a polyether type polymer binder, a fluorinated polymer, or a water-soluble binder.
(Item 14)
14. The electrode material according to item 13, wherein the polymer binder of polyether type is linear, branched and/or crosslinked and optionally comprises crosslinkable units based on poly(ethylene oxide) (PEO), poly(propylene oxide) (PPO), or a mixture of the two (or EO/PO copolymers).
(Item 15)
Item 14. The electrode material according to item 13, wherein the fluorinated polymer binder is PVDF (polyvinylidene fluoride) or PTFE (polytetrafluoroethylene).
(Item 16)
Item 14. The electrode material according to item 13, wherein the water-soluble binder is SBR (styrene-butadiene rubber), NBR (acrylonitrile-butadiene rubber), HNBR (hydrogenated NBR), CHR (epichlorohydrin rubber), or ACM (acrylate rubber), and optionally contains CMC (carboxymethyl cellulose).
(Item 17)
17. A positive electrode comprising the electrode material according to any one of items 9 to 16 applied to a current collector.
(Item 18)
9. An electrolyte comprising a polymer as defined in any one of
(Item 19)
20. The electrolyte of claim 18, wherein the electrolyte is a liquid electrolyte comprising a salt in a solvent.
(Item 20)
19. The electrolyte according to claim 18, wherein the electrolyte is a gel electrolyte comprising a salt in a solvent and optionally a solvating polymer.
(Item 21)
21. The electrolyte according to
(Item 22)
20. The electrolyte of claim 18, wherein the electrolyte is a solid polymer electrolyte (SPE) comprising a salt in a solvating polymer.
(Item 23)
23. The electrolyte of any one of claims 18 to 22, wherein the polymer or the compound is an additive.
(Item 24)
23. The electrolyte of claim 22, wherein the solvating polymer is the polymer defined in any one of
(Item 25)
25. The electrolyte of any one of claims 18 to 24, wherein the electrolyte further comprises elemental sulfur.
(Item 26)
26. The electrolyte of any one of claims 19 to 25, wherein the salt is a lithium salt.
(Item 27)
The salt may be selected from the group consisting of lithium hexafluorophosphate (LiPF 6 ), lithium bis(trifluoromethanesulfonyl)imide (LiTFSI), lithium bis(fluorosulfonyl)imide (LiFSI), lithium 2-trifluoromethyl-4,5-dicyanoimidazolate (LiTDI), lithium 4,5-dicyano-1,2,3-triazolate (LiDCTA), lithium bis(pentafluoroethylsulfonyl)imide (LiBETI), lithium tetrafluoroborate (LiBF 4 ), lithium bis(oxalato)borate (LiBOB), lithium nitrate (LiNO 3 ), lithium chloride (LiCl), lithium bromide (LiBr), lithium fluoride (LiF), lithium perchlorate (LiClO 4 ), lithium hexafluoroarsenate (LiAsF 6 ), lithium trifluoromethanesulfonate (LiSO 3 CF 3 27. The electrolyte of claim 26 , wherein the lithium fluoride is selected from lithium fluoride , ...
(Item 28)
28. The electrolyte of any one of claims 18 to 27, wherein the electrolyte further comprises an electrolyte binder.
(Item 29)
29. The electrolyte of claim 28, wherein the electrolyte binder is a polyether type polymeric binder, a fluorinated polymer, or a water-soluble binder.
(Item 30)
30. The electrolyte of claim 29, wherein the fluorinated polymer binder is polyvinylidene fluoride (PVDF).
(Item 31)
17. An electrochemical cell comprising a cathode, an electrolyte, and an anode, wherein the cathode comprises an electrode material as defined in any one of claims 9 to 16.
(Item 32)
18. An electrochemical cell comprising a negative electrode, an electrolyte and a positive electrode as defined in item 17.
(Item 33)
31. An electrochemical cell comprising a cathode, an anode and an electrolyte as defined in any one of items 18 to 30.
(Item 34)
31. An electrochemical cell comprising a negative electrode, an electrolyte and a positive electrode, wherein the positive electrode is as defined in item 17 and the electrolyte is as defined in any one of items 18 to 30.
(Item 35)
35. A lithium battery comprising an electrochemical cell as defined in any one of items 31 to 34.
本明細書で使用されるすべての技術的および科学的な用語および表現は、本技術に関連する分野の当業者によって一般に理解されるものと同じ定義を有する。それでも、使用されるいくつかの用語および表現の定義は、以下に提供される。 All technical and scientific terms and expressions used herein have the same definitions as commonly understood by a person skilled in the art related to the present technology. Nevertheless, definitions of some of the terms and expressions used are provided below.
本明細書において使用される「約」という用語は、ほぼ、その付近、およびおよそを意味する。「約」という用語が数値に関連して使用される場合、それは、例えば、公称値に対して10%の変動で数値を上下に変更する。この用語は、例えば、測定装置または丸めによる実験誤差も考慮に入れることがある。 As used herein, the term "about" means approximately, in the vicinity, and in the region of. When the term "about" is used in connection with a numerical value, it modifies the numerical value above and below with, for example, a variance of 10% from the nominal value. The term may also take into account experimental error, for example, due to a measuring device or rounding.
値の範囲が本願において言及されている場合、その範囲の下限および上限は、特に明記しない限り、常に定義に含まれる。 Whenever a range of values is mentioned in this application, the lower and upper limits of the range are always included in the definition, unless otherwise stated.
本明細書に記載される化学構造は、当分野の基準に従って描かれている。また、描かれている炭素原子などの原子に不完全な原子価が含まれているように見える場合には、たとえ水素原子が明示的に描かれていない場合でも、原子価は1またはそれを超える水素原子によって満たされていると見なされる。 The chemical structures depicted herein are drawn in accordance with standards of the art. Also, where an atom, such as a drawn carbon atom, appears to have incomplete valences, the valences are considered to be satisfied by one or more hydrogen atoms, even if no hydrogen atoms are explicitly drawn.
本明細書において使用される、用語「アルキル」または「アルキレン」とは、直鎖または分岐鎖基を含む、1~16個の炭素原子を有する飽和炭化水素基を指す。アルキル基の例としては、限定されないが、メチル、エチル、プロピル、ブチル、ペンチル、ヘキシル、ヘプチル、オクチル、ノニル、デシル、イソプロピル、tert-ブチル、sec-ブチル、イソブチルなどが挙げられる。アルキル基が2つの官能基の間に位置する場合、アルキレンという用語、例えばメチレン、エチレン、プロピレンなども使用され得る。「Ci-Ciiアルキル」および「Ci-Ciiアルキレン」という用語は、数「i」から数「ii」までの炭素原子を有するアルキルまたはアルキレン基をそれぞれ指す。 As used herein, the term "alkyl" or "alkylene" refers to a saturated hydrocarbon group having from 1 to 16 carbon atoms, including straight or branched chain groups. Examples of alkyl groups include, but are not limited to, methyl, ethyl, propyl, butyl, pentyl, hexyl, heptyl, octyl, nonyl, decyl, isopropyl, tert-butyl, sec-butyl, isobutyl, and the like. When an alkyl group is located between two functional groups, the term alkylene may also be used, such as methylene, ethylene, propylene, and the like. The terms "C i -C ii alkyl" and "C i -C ii alkylene" refer to an alkyl or alkylene group having from number "i" to number "ii" carbon atoms, respectively.
本明細書において使用される、「アリール」または「アリーレン」という用語は、共役した単環系または多環系(縮合もしくは非縮合)において、4n+2個のπ(パイ)電子(nは1~3の整数である)を有し、6~20個の環原子を有する芳香族基を指す。多環系は、少なくとも1つの芳香環を含む。この基は、直接結合されるかまたはC1-C3アルキル基を介して接続されてよい。アリール基の例としては、限定されないが、フェニル、ベンジル、フェネチル、1-フェニルエチル、トリル、ナフチル、ビフェニル、テルフェニル、インデニル、ベンゾシクロオクテニル、ベンゾシクロヘプテニル、アズレニル、アセナフチレニル、フルオレニル、フェナントレニル、アントラセニル、ペリレニルなどが挙げられる。アリール基が2つの官能基の間に位置する場合、アリーレンという用語も使用され得る。アリールまたはアリーレンという用語には、置換された基または置換されていない基が含まれる。例えば、「C6-Cnアリール」という用語は、環構造中に6個から指定された「n」個の炭素原子を有するアリール基を指す。 As used herein, the term "aryl" or "arylene" refers to an aromatic group having 4n+2 π (pi) electrons (n is an integer from 1 to 3) and 6 to 20 ring atoms in a conjugated monocyclic or polycyclic ring system (fused or non-fused). Polycyclic ring systems contain at least one aromatic ring. The group may be directly bonded or connected through a C 1 -C 3 alkyl group. Examples of aryl groups include, but are not limited to, phenyl, benzyl, phenethyl, 1-phenylethyl, tolyl, naphthyl, biphenyl, terphenyl, indenyl, benzocyclooctenyl, benzocycloheptenyl, azulenyl, acenaphthylenyl, fluorenyl, phenanthrenyl, anthracenyl, perylenyl, and the like. When an aryl group is located between two functional groups, the term arylene may also be used. The terms aryl or arylene include substituted or unsubstituted groups. For example, the term "C 6 -C n aryl" refers to an aryl group having from 6 to the designated "n" carbon atoms in the ring structure.
「置換された」という用語は、基に関連している場合、少なくとも1つの水素原子が適切な置換基で置き換えられている基を指す。置換基の限定されない例は、シアノ、ハロゲン(すなわちF、Cl、Br、またはI)、アミド、ニトロ、トリフルオロメチル、低級アルキル、シクロアルキル、ヘテロシクロアルキル、アリール、ヘテロアリール、低級アルコキシ、アリールオキシ、ベンジルオキシ、ベンジル、アルコキシカルボニル、スルホニル、スルホネート、シラン、シロキサン、ホスホナト、ホスフィナトなどを含む。これらの置換基は、許容される場合、例えば、この基がアルキル基、アルコキシ基、アリール基等を含む場合に置換されることもできる。 The term "substituted" when referring to a group refers to a group in which at least one hydrogen atom has been replaced with a suitable substituent. Non-limiting examples of substituents include cyano, halogen (i.e., F, Cl, Br, or I), amido, nitro, trifluoromethyl, lower alkyl, cycloalkyl, heterocycloalkyl, aryl, heteroaryl, lower alkoxy, aryloxy, benzyloxy, benzyl, alkoxycarbonyl, sulfonyl, sulfonate, silane, siloxane, phosphonato, phosphinato, and the like. These substituents can also be substituted where permitted, for example, when the group contains an alkyl group, an alkoxy group, an aryl group, and the like.
本記載は、硫黄元素と有機モノマーの共重合、または、硫黄と、ジスルフィド結合を含む化合物との反応に関する。例えば、本願は、硫黄と電気化学的に活性なポリイミドとの共重合の結果であるポリマーを含む。あるいは、硫黄の反応をジイミドジスルフィドと行い、それによりどちらも電気化学的に活性なスルフィドセグメントと有機セグメントを含む化合物を得る。これらの化合物およびポリマーは、溶解の問題を低減または排除することによって硫黄の電気化学的性能を改善するだけでなく、レドックス反応で同様に活性である有機セグメントの存在を考えると、容量に寄与することもあり得る。したがって、本明細書において定義されたポリマーまたは化合物を含む電極材料は、ハイブリッド有機硫黄正極材料と特徴付けることができる。 The present description relates to the copolymerization of elemental sulfur with organic monomers or the reaction of sulfur with compounds containing disulfide bonds. For example, the present application includes polymers resulting from the copolymerization of sulfur with electrochemically active polyimides. Alternatively, the reaction of sulfur with diimide disulfides results in compounds containing sulfide and organic segments, both of which are electrochemically active. These compounds and polymers not only improve the electrochemical performance of sulfur by reducing or eliminating the dissolution problem, but may also contribute to capacity, given the presence of organic segments that are similarly active in redox reactions. Thus, electrode materials containing the polymers or compounds defined herein can be characterized as hybrid organosulfur cathode materials.
例えば、このポリマーは、電気化学的に活性なポリイミドセグメントと、-S-(S)m-S-(m≧1)の形式のポリスルフィドセグメントで構成される共重合体である。ポリマーの例は、式I:
Aは、電子の非局在化を許容する不飽和基、例えば、置換または非置換のアリールおよびヘテロアリール基、ならびにそれらの縮合または非縮合多環式対応物から選択され;
Rは、直鎖または分岐鎖C2-6アルキレン、直鎖または分岐鎖C2-6アルキレンオキシ、直鎖または分岐鎖C2-6アルキレングリコール、直鎖または分岐鎖C2-6アルキレンオキシC2-6アルキレン、直線状または分岐鎖ポリ(C2-6アルキレングリコール)、C6-12アリーレン、C3-12シクロアルキレン、C5-12ヘテロアリーレン、およびC3-12ヘテロシクロアルキレンから選択される置換または非置換有機連結基であり;
mは、ポリマーリンクのジスルフィド結合に挿入された硫黄原子の平均数を表し、ゼロであり得ず、すなわち、m>0、例えば0<m≦8、または1≦m≦6、または1≦m≦4であり;かつ
nは、ポリマー中の単位の平均数を表し、例えば、nは2~500、または5~300の範囲内であり得る)
によって表される。
For example, the polymer is a copolymer composed of electrochemically active polyimide segments and polysulfide segments of the form -S-(S) m -S- (m≧1). An example of a polymer is represented by Formula I:
A is selected from unsaturated groups that allow for electron delocalization, such as substituted or unsubstituted aryl and heteroaryl groups, and their fused or non-fused polycyclic counterparts;
R is a substituted or unsubstituted organic linking group selected from linear or branched C 2-6 alkylene, linear or branched C 2-6 alkyleneoxy, linear or branched C 2-6 alkylene glycol, linear or branched C 2-6 alkyleneoxy C 2-6 alkylene, linear or branched poly(C 2-6 alkylene glycol), C 6-12 arylene, C 3-12 cycloalkylene, C 5-12 heteroarylene, and C 3-12 heterocycloalkylene;
m represents the average number of sulfur atoms inserted into the disulfide bonds of the polymer links and cannot be zero, i.e., m>0, e.g., 0<m≦8, or 1≦m≦6, or 1≦m≦4; and n represents the average number of units in the polymer, e.g., n can be in the range of 2 to 500, or 5 to 300.
It is represented by:
一例によれば、Aは、ベンゼン、ナフタレン、ペリレンおよびビフェニル基から選択されてよい。 According to one example, A may be selected from benzene, naphthalene, perylene and biphenyl groups.
例えば、Aは、ベンゼン基であり、ポリマーは、式I(a):
のポリマーである。
For example, A is a benzene group and the polymer has the formula I(a):
It is a polymer of.
別の例によれば、Rは、ベンゼン、エチレン、プロピレン、ポリ(エチレングリコール)、ポリ(プロピレングリコール)、およびエチレングリコールとプロピレングリコールの共重合体の基から選択されてよい。 By way of further example, R may be selected from the group consisting of benzene, ethylene, propylene, poly(ethylene glycol), poly(propylene glycol), and copolymers of ethylene glycol and propylene glycol.
例えば、AおよびRは、ベンゼン基であり、ポリマーは、式I(b)またはI(c):
のポリマーである。
For example, A and R are benzene groups and the polymer has the formula I(b) or I(c):
It is a polymer of.
別の例によれば、活物質はむしろ式IIの化合物:
である。
According to another example, the active material may rather be a compound of formula II:
It is.
例えば、Aは、ベンゼンであり、ポリマーは、式II(a):
のポリマーである。
For example, A is benzene and the polymer has the formula II(a):
It is a polymer of.
例えば、Rはベンゼンであり、ポリマーは、式II(b):
のポリマーである。
For example, R is benzene and the polymer has the formula II(b):
It is a polymer of.
本願はまた、硫黄元素との反応による重合および硫化のステップを含む、本明細書において定義され、有機硫化物ハイブリッドを含むポリマーの合成のためのプロセスを記載し、これらのステップは任意の順序で行われる。例えば、このプロセスは以下のステップを含む:
a)電気化学的に活性なポリイミドを形成するための、二無水物とジアミンジスルフィドとの間の重縮合による重合;および
b)電気化学的に活性なポリイミドと硫黄元素S8の共重合による、ポリスルフィドセグメント(-(S)m-の形式;m≧1)の挿入。
The present application also describes a process for the synthesis of polymers, including organic sulfide hybrids, as defined herein, which comprises the steps of polymerization and sulfurization by reaction with elemental sulfur, these steps being carried out in any order. For example, the process comprises the steps of:
a) polymerization by polycondensation between a dianhydride and a diamine disulfide to form an electrochemically active polyimide; and b) copolymerization of the electrochemically active polyimide with elemental sulfur S8 to insert a polysulfide segment (of the form -(S) m- ; m>1).
一例によれば、共重合体の有機セグメントは、ピロメリト酸二無水物(1)と4-アミノフェニルジスルフィド(2)との間の重縮合によって合成されてポリイミド(3)を形成する。例えば、重縮合は約150℃の温度で行われる。共重合体は、スキーム1に例示される重合プロセスによって調製することができる:
一例によれば、ポリスルフィドセグメント(-(S)m-の形式;m≧1)は、次にジスルフィド結合に挿入される。次に、挿入は、150℃もしくはそれを超える温度、または185℃もしくはそれを超える温度、または160℃~200℃の間の温度で、ジスルフィド結合を含む電気化学的に活性なポリイミドおよび硫黄元素S8を加熱することにより、行うことができる。加熱ステップは、硫黄元素S8環を開環させて、ポリスルフィドセグメント(-(S)m-の形式;m≧1)をジスルフィド結合に挿入し、ポリスルフィドを形成することを可能にする。ポリスルフィドセグメントの挿入は、スキーム2に例示されるプロセスによって行うことができ、このプロセスでは、ポリスルフィドセグメント(-(S)m-の形式;m≧1)の挿入が185℃でポリイミド(3)のジスルフィド結合に対して行われ、ポリイミド-co-ポリスルフィド(4)が得られる:
a)ジアミンジスルフィドと硫黄元素S8の重合によって行われる、ポリスルフィドを形成するセグメント(-(S)m-の形式;m≧1)の挿入によるアミノ-硫黄コモノマーの合成;および
b)ポリイミドを形成するためのアミノ-硫黄コモノマーと二無水物の重縮合。
According to one example, polysulfide segments (of the form -(S) m -; m≧1) are then inserted into the disulfide bonds. The insertion can then be carried out by heating the electrochemically active polyimide containing disulfide bonds and elemental sulfur S 8 at a temperature of 150° C. or higher, or at a temperature of 185° C. or higher, or between 160° C. and 200° C. The heating step opens the elemental sulfur S 8 ring, allowing the polysulfide segments (of the form -(S) m -; m≧1) to be inserted into the disulfide bonds to form polysulfides. The insertion of polysulfide segments can be carried out by the process illustrated in Scheme 2, in which the insertion of polysulfide segments (of the form -(S) m -; m≧1) is carried out into the disulfide bonds of polyimide (3) at 185° C. to obtain polyimide-co-polysulfide (4):
a) synthesis of amino-sulfur comonomers by polymerization of diamine disulfides with elemental sulfur S8 , with insertion of segments (of the form -(S) m- ; m>1) to form polysulfides; and b) polycondensation of amino-sulfur comonomers with dianhydrides to form polyimides.
一例によれば、ポリスルフィドセグメント(-(S)m-の形式;m≧1)は、ジアミンジスルフィドのジスルフィド結合に挿入される。挿入は、150℃もしくはそれを超える温度、または185℃もしくはそれを超える温度、または160℃~200℃の間の温度で、硫黄元素S8およびジスルフィド結合を含むジアミンジスルフィドを加熱することにより行うことができる。加熱ステップは、硫黄元素S8環を開環させて、ポリスルフィドセグメントをジスルフィド結合に挿入し、ポリスルフィドを形成することを可能にする。ポリスルフィドセグメントの挿入は、スキーム3に例示されるプロセスによって行うことができ、このプロセスでは、ポリスルフィドセグメントの挿入が、185℃で4-アミノフェニルジスルフィド(2)のジスルフィド結合で行われ、アミノ-硫黄コモノマー(3)が得られる:
一例によれば、次に、重合は、アミノ-硫黄コモノマー(3)とピロメリト酸二無水物(4)との間の重縮合によって行われて、ポリイミド-co-ポリスルフィド(5)を形成する。重縮合は、例えば約150℃の温度で行うことができる。ポリマーは、スキーム4に例示される重合プロセスによって調製することができる:
本願はまた、電気化学的活物質として本明細書において定義されるポリマーまたは化合物を含む正極材料を提唱する。一例によれば、正極材料は、導電性材料、バインダー、またはそれらの組合せをさらに含むことがある。電極材料は、遊離硫黄元素(Sx)を含むこともある。 The present application also proposes a positive electrode material comprising a polymer or compound defined herein as an electrochemically active material. According to an example, the positive electrode material may further comprise a conductive material, a binder, or a combination thereof. The electrode material may also comprise free elemental sulfur (S x ).
導電性材料の限定されない例は、炭素源、例えばカーボンブラック、Ketjen(商標)カーボン、シャウィニガンカーボン、アセチレンブラック、グラファイト、グラフェン、カーボンファイバー(例えばカーボンナノファイバー、例えば、気相で形成されたVGCFなど)、およびカーボンナノチューブ、またはそれらの少なくとも2つの組合せなどを含み得る。例えば、導電性材料は、VGCFとKetjen(商標)ブラックの組合せである。 Non-limiting examples of conductive materials may include carbon sources such as carbon black, Ketjen™ carbon, Shawinigan carbon, acetylene black, graphite, graphene, carbon fibers (e.g., carbon nanofibers, such as VGCF formed in the gas phase), and carbon nanotubes, or a combination of at least two thereof. For example, the conductive material is a combination of VGCF and Ketjen™ black.
バインダーの限定されない例は、直線状、分岐鎖、および/または架橋ポリエーテル型のポリマーであり、ポリ(エチレンオキシド)(PEO)、ポリ(プロピレンオキシド)(PPO)、またはこれら2つの組合せ(またはEO/PO共重合体)に基づき得、架橋可能な単位を必要に応じて含むポリマー;ポリフッ化ビニリデン(PVDF)またはポリテトラフルオロエチレン(PTFE)などのフッ素化ポリマー;あるいは、例えばスチレン-ブタジエンゴム(SBR)、アクリロニトリル-ブタジエンゴム(NBR)、水素化NBR(HNBR)、エピクロロヒドリンゴム(CHR)、またはアクリレートゴム(ACM)などの水溶性バインダーである水溶性バインダーを含み、必要に応じてカルボキシメチルセルロース(CMC)を含む。例えば、バインダーはPVDFであり、塗布のために正極材料の他の成分と混合されるときにN-メチル-2-ピロリドン(NMP)に溶解され、この溶媒はその後に除去される。 Non-limiting examples of binders include linear, branched and/or cross-linked polyether type polymers, which may be based on poly(ethylene oxide) (PEO), poly(propylene oxide) (PPO), or a combination of the two (or EO/PO copolymers), optionally including cross-linkable units; fluorinated polymers such as polyvinylidene fluoride (PVDF) or polytetrafluoroethylene (PTFE); or water-soluble binders, such as styrene-butadiene rubber (SBR), acrylonitrile-butadiene rubber (NBR), hydrogenated NBR (HNBR), epichlorohydrin rubber (CHR), or acrylate rubber (ACM), optionally including carboxymethylcellulose (CMC). For example, the binder is PVDF, which is dissolved in N-methyl-2-pyrrolidone (NMP) when mixed with the other components of the cathode material for application, and the solvent is subsequently removed.
一例によれば、正極材料は、集電体(例えば、アルミニウム、銅)に適用することができる。あるいは、正極は自立することができる。例えば、集電体はアルミニウムである。 According to one example, the positive electrode material can be applied to a current collector (e.g., aluminum, copper). Alternatively, the positive electrode can be free-standing. For example, the current collector is aluminum.
本願はまた、少なくとも、本明細書において定義される正極材料、負極および電解質を含む電気化学セルも提唱する。次に、電池のさまざまな成分とのその適合性のために電解質が選択される。任意の種類の電解質、例えば、液体、ゲルまたは固体の電解質が企図される。 The present application also proposes an electrochemical cell including at least a positive electrode material, a negative electrode, and an electrolyte as defined herein. The electrolyte is then selected for its compatibility with the various components of the battery. Any type of electrolyte is contemplated, e.g., liquid, gel, or solid electrolytes.
本願はまた、本明細書において定義されるポリマーまたは本明細書において定義される化合物を含む電解質を提唱する。 The present application also proposes an electrolyte comprising a polymer as defined herein or a compound as defined herein.
一例によれば、電解質は、溶媒中の塩を含む液体電解質である。一代替形態によれば、電解質は、溶媒中の塩および必要に応じて溶媒和ポリマーを含むゲル電解質である。別の代替形態によれば、電解質は、溶媒和ポリマー中に塩を含む固体ポリマー電解質(SPE)である。 According to one example, the electrolyte is a liquid electrolyte comprising a salt in a solvent. According to one alternative, the electrolyte is a gel electrolyte comprising a salt in a solvent and optionally a solvating polymer. According to another alternative, the electrolyte is a solid polymer electrolyte (SPE) comprising a salt in a solvating polymer.
相溶性のある電解質は、通常、少なくとも1つのリチウム塩、例えばヘキサフルオロリン酸リチウム(LiPF6)、リチウムビス(トリフルオロメタンスルホニル)イミド(LiTFSI)、リチウムビス(フルオロスルホニル)イミド(LiFSI)、リチウム2-トリフルオロメチル-4,5-ジシアノイミダゾレート(LiTDI)、リチウム4,5-ジシアノ-1,2,3-トリアゾレート(LiDCTA)、リチウムビス(ペンタフルオロエチルスルホニル)イミド(LiBETI)、テトラフルオロホウ酸リチウム(LiBF4)、リチウムビス(オキサラト)ボレート(LiBOB)、硝酸リチウム(LiNO3)、塩化リチウム(LiCl)、臭化リチウム(LiBr)、フッ化リチウム(LiF)など、および非水性溶媒(有機)または溶媒和ポリマーに溶解したそれらを含む組成物を含む。例えば、電解質は、ジメトキシエタン(DME)および1,3-ジオキソラン(DOL)(DME/DOL)に溶解したLiTFSIであり、それには硝酸リチウム(1%、LiNO3)が含まれている。 Compatible electrolytes typically include at least one lithium salt, such as lithium hexafluorophosphate (LiPF 6 ), lithium bis(trifluoromethanesulfonyl)imide (LiTFSI), lithium bis(fluorosulfonyl)imide (LiFSI), lithium 2-trifluoromethyl-4,5-dicyanoimidazolate (LiTDI), lithium 4,5-dicyano-1,2,3-triazolate (LiDCTA), lithium bis(pentafluoroethylsulfonyl)imide (LiBETI), lithium tetrafluoroborate (LiBF 4 ), lithium bis(oxalato)borate (LiBOB), lithium nitrate (LiNO 3 ), lithium chloride (LiCl), lithium bromide (LiBr), lithium fluoride (LiF), and the like, and compositions comprising the same dissolved in a non-aqueous (organic) solvent or a solvating polymer. For example, the electrolyte is LiTFSI dissolved in dimethoxyethane (DME) and 1,3-dioxolane (DOL) (DME/DOL), which contains lithium nitrate (1%, LiNO 3 ).
別の例によれば、電解質は、硫黄元素、電解質バインダー、セパレータ、添加剤またはそれらの少なくとも2つの組合せをさらに含んでよい。 According to another example, the electrolyte may further include elemental sulfur, an electrolyte binder, a separator, an additive, or a combination of at least two thereof.
例えば、電解質バインダーはPVDF(ポリフッ化ビニリデン)である。例えば、電解質は、0重量%~25重量%の間、特に0重量%~20重量%の間、より特に5重量%~15重量%の間、さらにより特に7重量%~13重量%の間、理想的には10重量%の電解質バインダーを含む(上限および下限を含む)。 For example, the electrolyte binder is PVDF (polyvinylidene fluoride). For example, the electrolyte comprises between 0% and 25% by weight, particularly between 0% and 20% by weight, more particularly between 5% and 15% by weight, even more particularly between 7% and 13% by weight, ideally 10% by weight of the electrolyte binder (upper and lower limits included).
セパレータの限定されない例には、ポリエチレン(PE)、ポリプロピレン(PP)、セルロース、ポリテトラフルオロエチレン(PTFE)、ポリフッ化ビニリデン(PVDF)およびポリプロピレン-ポリエチレン-ポリプロピレン(PP/PE/PP)膜が含まれ得る。 Non-limiting examples of separators may include polyethylene (PE), polypropylene (PP), cellulose, polytetrafluoroethylene (PTFE), polyvinylidene fluoride (PVDF) and polypropylene-polyethylene-polypropylene (PP/PE/PP) membranes.
別の例によれば、電解質は、本明細書において定義される塩を溶媒和ポリマー中に含む固体ポリマー電解質(SPE)であり、該溶媒和ポリマーは本明細書において定義されるポリマーである。例えば、SPEは、60重量%~95重量%の間、特に65重量%~90重量%の間、より特に70重量%~85重量%の間、さらにより特に75重量%~85重量%の間、理想的には80重量%の本明細書において定義されるポリマーを含む(上限および下限を含む)。例えば、SPEは、5重量%~40重量%の間、特に10重量%~35重量%の間、より特に15重量%~30重量%の間、より特に15重量%~25重量%の間、理想的には20重量%の塩を含む(上限および下限を含む)。 According to another example, the electrolyte is a solid polymer electrolyte (SPE) comprising a salt as defined herein in a solvating polymer, the solvating polymer being a polymer as defined herein. For example, the SPE comprises between 60% and 95% by weight, in particular between 65% and 90% by weight, more particularly between 70% and 85% by weight, even more particularly between 75% and 85% by weight, ideally 80% by weight of a polymer as defined herein (including upper and lower limits). For example, the SPE comprises between 5% and 40% by weight, in particular between 10% and 35% by weight, more particularly between 15% and 30% by weight, more particularly between 15% and 25% by weight, ideally 20% by weight of a salt (including upper and lower limits).
本願はまた、カソード、アノードおよび本明細書において定義される電解質を含む電気化学セルも提唱する。本願はまた、カソード、アノードおよび電解質を含む電気化学セルも企図し、ここで電解質およびカソードは本明細書において定義される通りである。 The present application also contemplates an electrochemical cell comprising a cathode, an anode and an electrolyte as defined herein. The present application also contemplates an electrochemical cell comprising a cathode, an anode and an electrolyte, where the electrolyte and the cathode are as defined herein.
別の態様によれば、本願の電気化学セルは、リチウム電池に含まれる。例えば、リチウム電池はリチウム-硫黄電池である。 According to another aspect, the electrochemical cell of the present application is included in a lithium battery. For example, the lithium battery is a lithium-sulfur battery.
別の態様によれば、本願の電気化学セルは、携帯機器、例えば、携帯電話、カメラ、タブレットまたはラップトップで、電気自動車またはハイブリッド車で、あるいは再生可能エネルギー貯蔵で使用される。 According to another aspect, the electrochemical cells of the present application are used in portable devices, such as mobile phones, cameras, tablets or laptops, in electric or hybrid vehicles, or in renewable energy storage.
以下の実施例は例示であり、記載された本発明の範囲をさらに限定するものと解釈されるべきではない。 The following examples are illustrative and should not be construed as further limiting the scope of the invention described.
実施例1-有機硫黄ハイブリッド活性電極材料の合成
a)ピロメリト酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(5重量%)の共重合
電極材料の合成を、マグネチックバーを装備した25mLフラスコ内で行った。活性電極材料を、0.085gの硫黄元素S8(0.33mmol)と0.745gの4-アミノフェニルジスルフィド(3mmol)を合わせることにより調製した。次に、フラスコを密閉し、不活性ガス(N2)流下に置いた。フラスコの空気がパージされたら、混合物を、均一な液体が得られるまで約30分間、500rpmの一定の撹拌下で185℃の温度に加熱した。次に、混合物を150℃の温度に冷却した後、密閉したキャップを取り外して、事前に有機溶媒であるN,N-ジメチルホルムアミド(DMF)に溶解させた0.654gのピロメリト酸二無水物(3mmol)を添加した。次に、混合物を含有するフラスコを覆い、撹拌下(500rpm)で26時間、150℃の温度で保持した。次に、混合物を冷却した。このようにして生成された固体を回収し、テトラヒドロフラン(THF)で洗浄し、未反応の硫黄を昇華させるために真空下で乾燥させた。最後に、生成された活性電極材料(ポリマー)中の硫黄の割合を元素分析によって測定した。この実施例の活性電極材料は、5%の硫黄を含んでいた。
Example 1 - Synthesis of Organosulfur Hybrid Active Electrode Material a) Copolymerization of Pyromellitic Dianhydride, 4-Aminophenyl Disulfide and Sulfur (5 wt%) The synthesis of the electrode material was carried out in a 25 mL flask equipped with a magnetic bar. The active electrode material was prepared by combining 0.085 g of elemental sulfur S8 (0.33 mmol) and 0.745 g of 4-aminophenyl disulfide (3 mmol). The flask was then sealed and placed under a flow of inert gas ( N2 ). Once the flask was purged of air, the mixture was heated to a temperature of 185°C under constant stirring at 500 rpm for about 30 minutes until a homogenous liquid was obtained. The mixture was then cooled to a temperature of 150°C, after which the sealed cap was removed and 0.654 g of pyromellitic dianhydride (3 mmol) previously dissolved in the organic solvent N,N-dimethylformamide (DMF) was added. The flask containing the mixture was then covered and kept at a temperature of 150° C. under stirring (500 rpm) for 26 hours. The mixture was then cooled. The solid thus produced was collected, washed with tetrahydrofuran (THF) and dried under vacuum in order to sublimate the unreacted sulfur. Finally, the percentage of sulfur in the produced active electrode material (polymer) was determined by elemental analysis. The active electrode material in this example contained 5% sulfur.
b)ピロメリト酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(25重量%)の共重合
この活性電極材料の合成を、実施例1(a)に示されるプロセスに従って行った。アミノ-硫黄コモノマーの合成のための硫黄元素S8および4-アミノフェニルジスルフィドの質量は、それぞれ0.309g(1.206mmol)および0.447g(1.8mmol)であり、重縮合のためのピロメリト酸二無水物の質量は、0.393g(1.8mmol)であった。このように生成された活性電極材料は、元素分析により測定して25重量%の硫黄を含んでいた。
b) Copolymerization of pyromellitic dianhydride, 4-aminophenyl disulfide and sulfur (25 wt%). The synthesis of this active electrode material was carried out according to the process shown in Example 1(a). The masses of elemental sulfur S 8 and 4-aminophenyl disulfide for the synthesis of the amino-sulfur comonomer were 0.309 g (1.206 mmol) and 0.447 g (1.8 mmol), respectively, and the mass of pyromellitic dianhydride for the polycondensation was 0.393 g (1.8 mmol). The active electrode material thus produced contained 25 wt% sulfur as determined by elemental analysis.
c)ピロメリト酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(35重量%)の共重合
この活性電極材料の合成を、実施例1(a)に示されるプロセスに従って行った。アミノ-硫黄コモノマーの合成のための硫黄元素S8および4-アミノフェニルジスルフィドの質量は、それぞれ1.033g(4.026mmol)および1g(4.026mmol)であり、重縮合のためのピロメリト酸二無水物の質量は、0.878g(4.026mmol)であった。このように生成された活性電極材料は、元素分析により測定して35重量%の硫黄を含んでいた。
c) Copolymerization of pyromellitic dianhydride, 4-aminophenyl disulfide and sulfur (35 wt%). The synthesis of this active electrode material was carried out according to the process shown in Example 1(a). The masses of elemental sulfur S 8 and 4-aminophenyl disulfide for the synthesis of the amino-sulfur comonomer were 1.033 g (4.026 mmol) and 1 g (4.026 mmol), respectively, and the mass of pyromellitic dianhydride for the polycondensation was 0.878 g (4.026 mmol). The active electrode material thus produced contained 35 wt% sulfur as determined by elemental analysis.
d)ピロメリト酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(63重量%)の共重合
この活性電極材料の合成を、実施例1(a)に示されるプロセスに従って行った。アミノ-硫黄コモノマーの合成のための硫黄元素S8および4-アミノフェニルジスルフィドの質量は、それぞれ2.463g(9.6mmol)および0.397g(1.6mmol)であり、重縮合のためのピロメリト酸二無水物の質量は、0.349g(1.6mmol)であった。このように得られた活性電極材料は、元素分析により測定して63重量%の硫黄を含んでいた。
d) Copolymerization of pyromellitic dianhydride, 4-aminophenyl disulfide and sulfur (63 wt%). The synthesis of this active electrode material was carried out according to the process shown in Example 1(a). The masses of elemental sulfur S 8 and 4-aminophenyl disulfide for the synthesis of the amino-sulfur comonomer were 2.463 g (9.6 mmol) and 0.397 g (1.6 mmol), respectively, and the mass of pyromellitic dianhydride for the polycondensation was 0.349 g (1.6 mmol). The active electrode material thus obtained contained 63 wt% sulfur as determined by elemental analysis.
e)ピロメリト酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(95重量%)の共重合
この活性電極材料の合成を、実施例1(a)に示されるプロセスに従って行った。アミノ-硫黄コモノマーの合成のための硫黄元素S8および4-アミノフェニルジスルフィドの質量は、それぞれ8.978g(35mmol)および0.248g(1mmol)であり、重縮合のためのピロメリト酸二無水物の質量は、0.218g(1mmol)であった。このように生成された活性電極材料は、元素分析により測定して95重量%の硫黄を含んでいた。
e) Copolymerization of pyromellitic dianhydride, 4-aminophenyl disulfide and sulfur (95 wt%). The synthesis of this active electrode material was carried out according to the process shown in Example 1(a). The masses of elemental sulfur S 8 and 4-aminophenyl disulfide for the synthesis of the amino-sulfur comonomer were 8.978 g (35 mmol) and 0.248 g (1 mmol), respectively, and the mass of pyromellitic dianhydride for the polycondensation was 0.218 g (1 mmol). The active electrode material thus produced contained 95 wt% sulfur as determined by elemental analysis.
f)1,4,5,8-ナフタレンテトラカルボン酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(20重量%)の共重合
g)1,4,5,8-ナフタレンテトラカルボン酸二無水物、4-アミノフェニルジスルフィドおよび硫黄(30重量%)の共重合
活性電極材料の合成を、実施例1(f)に示されるプロセスに従って行った。アミノ-硫黄コモノマーの合成のための硫黄元素S8および4-アミノフェニルジスルフィドの質量は、それぞれ2.052g(8mmol)および1.987g(8mmol)であり、重縮合のための1,4,5,8-ナフタレンテトラカルボン酸二無水物の質量は、2.145g(8mmol)であった。このように生成された活性電極材料は、元素分析により測定して30重量%の硫黄を含んでいた。
g) Copolymerization of 1,4,5,8-naphthalenetetracarboxylic dianhydride, 4-aminophenyl disulfide and sulfur (30 wt%). The synthesis of the active electrode material was carried out according to the process shown in Example 1(f). The masses of elemental sulfur S 8 and 4-aminophenyl disulfide for the synthesis of the amino-sulfur comonomer were 2.052 g (8 mmol) and 1.987 g (8 mmol), respectively, and the mass of 1,4,5,8-naphthalenetetracarboxylic dianhydride for the polycondensation was 2.145 g (8 mmol). The active electrode material thus produced contained 30 wt% sulfur as determined by elemental analysis.
h)重縮合とそれに続く硫黄(20重量%)の挿入によるピロメリト酸二無水物とシスタミンの共重合
共重合体の合成を、マグネチックバーを装備した100mLフラスコ内で行った。この物質は、7.614gのシスタミン二塩酸塩(0.5mol)と10.91gのピロメリト酸二無水物(0.5mol)を合わせることにより調製した。次に、混合物を撹拌下(500rpm)で26時間、150℃の温度に加熱した。次に、混合物を冷却した。このようにして生成された固体を回収し、テトラヒドロフラン(THF)で洗浄した。次に、1.204gのこの共重合体をNMPに分散させ、1.856gの硫黄元素S8(50重量%)を添加した。次に、フラスコを密閉し、不活性ガス(N2)流下に置いた。フラスコの空気がパージされたら、混合物を500rpmの一定の撹拌下で約20時間、185℃の温度に加熱した。次に、混合物を冷却した。このようにして生成された固体を回収し、テトラヒドロフラン(THF)で洗浄し、真空下で乾燥させて未反応の硫黄を昇華させた。最後に、生成された活性電極材料(ポリマー)中の硫黄の割合を元素分析によって測定した。この実施例の活性電極材料は、20%の硫黄を含んでいた。
h) Copolymerization of pyromellitic dianhydride and cystamine by polycondensation followed by insertion of sulfur (20 wt%). The synthesis of the copolymer was carried out in a 100 mL flask equipped with a magnetic bar. This material was prepared by combining 7.614 g of cystamine dihydrochloride (0.5 mol) and 10.91 g of pyromellitic dianhydride (0.5 mol). The mixture was then heated to a temperature of 150° C. under stirring (500 rpm) for 26 hours. The mixture was then cooled. The solid thus formed was collected and washed with tetrahydrofuran (THF). 1.204 g of this copolymer was then dispersed in NMP and 1.856 g of elemental sulfur S 8 (50 wt%) was added. The flask was then sealed and placed under a flow of inert gas (N 2 ). Once the flask was purged of air, the mixture was heated to a temperature of 185° C. under constant stirring at 500 rpm for about 20 hours. The mixture was then cooled. The solid thus produced was collected, washed with tetrahydrofuran (THF) and dried under vacuum to sublimate the unreacted sulfur. Finally, the percentage of sulfur in the produced active electrode material (polymer) was determined by elemental analysis. The active electrode material in this example contained 20% sulfur.
実施例2-電気化学セルの調製
a)カソード
カソード材料は、60重量%のハイブリッド有機硫化物電極材料、すなわち実施例1のポリイミド-co-ポリスルフィド、またはポリイミドジスルフィド(基準)、30重量%の導電性カーボン(15% VGCFおよび15% Ketjen(商標)600カーボン)および10重量%のバインダー、すなわちN-メチル-2-ピロリドン(NMP)に溶解したポリフッ化ビニリデン(PVDF)で構成される。集電体はアルミニウムである。溶媒は塗布後に蒸発する。
Example 2 - Preparation of electrochemical cells a) Cathode The cathode material is composed of 60 wt% hybrid organosulfide electrode material, i.e. polyimide-co-polysulfide of Example 1, or polyimide disulfide (reference), 30 wt% conductive carbon (15% VGCF and 15
b)電解質
電解質は、ジメトキシエタン(DME)と1,3-ジオキソランの混合物(DME/DOL)に溶解したリチウムビス(トリフルオロメタンスルホニル)イミド(LiTFSI)の1M溶液、および硝酸リチウム(1%、LiNO3)で構成される。
b) Electrolyte The electrolyte consists of a 1 M solution of lithium bis(trifluoromethanesulfonyl)imide (LiTFSI) dissolved in a mixture of dimethoxyethane (DME) and 1,3-dioxolane (DME/DOL), and lithium nitrate (1%, LiNO 3 ).
c)アノード
アノードは薄膜の形態の金属リチウムで構成される。
c) Anode The anode consists of metallic lithium in the form of a thin film.
d)電気化学セル
セルは、したがって次の要素で調製される:
Li/電解質/カソード/Al
d) Electrochemical Cell A cell is therefore prepared with the following components:
Li/electrolyte/cathode/Al
セル1
セル1は、実施例2(a)に示されるジスルフィドポリイミドを含む基準カソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
セル2
セル2は、実施例1(c)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 2
Cell 2 includes a cathode as shown in Example 2(a) comprising the electrode material of Example 1(c), an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
セル3
セル3は、実施例1(d)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 3
Cell 3 includes a cathode as shown in Example 2(a) containing the electrode material of Example 1(d), an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
セル4
セル4は、実施例1(e)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 4
Cell 4 includes a cathode as shown in Example 2(a) comprising the electrode material of Example 1(e), an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
セル5
セル5は、実施例1(b)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
セル6
セル6は、実施例1(f)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 6
Cell 6 includes a cathode as shown in Example 2(a) comprising the electrode material of Example 1(f), an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
セル7
セル7は、実施例1(g)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 7
Cell 7 includes a cathode as shown in Example 2(a) comprising the electrode material of Example 1(g), an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
セル8
セル8は、実施例1(h)の(硫黄を添加しない)電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 8
Cell 8 includes a cathode as shown in Example 2(a) containing the electrode material (without added sulfur) of Example 1(h), an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
セル9
セル9は、20重量%の硫黄を含有する実施例1(a)の電極材料を含む実施例2(a)に示されるカソード、実施例2(b)に示される電解質、および実施例2(c)に示される金属リチウムで構成されるアノードを含む。
Cell 9
Cell 9 includes a cathode as shown in Example 2(a) comprising the electrode material of Example 1(a) containing 20% by weight sulfur, an electrolyte as shown in Example 2(b), and an anode composed of metallic lithium as shown in Example 2(c).
実施例3-電気化学的特性
電気化学測定を、実施例2(d)の電気化学セルで実施した。図1に実証されるように、ジスルフィド結合に挿入された硫黄の存在により、改良された容量およびサイクル性を有する、より性能の高い材料を得ることが可能になる。図1(A)および1(B)はそれぞれ、セル1(基準)およびセル2のサイクル数の関数として、容量および容量保持の結果を示す。実際、提示された結果を比較することにより、容量および容量保持の割合の大幅な改善を、セル1と比較してセル2について観察することができる。
Example 3 - Electrochemical properties Electrochemical measurements were carried out on the electrochemical cell of Example 2(d). As demonstrated in Figure 1, the presence of sulfur inserted in the disulfide bonds makes it possible to obtain higher performance materials with improved capacity and cyclability. Figures 1(A) and 1(B) show the results of capacity and capacity retention as a function of cycle number for Cell 1 (reference) and Cell 2, respectively. Indeed, by comparing the presented results, a significant improvement in capacity and percentage of capacity retention can be observed for Cell 2 compared to
図2は、セル2のC/10における第1のサイクルの容量の結果を電圧の関数として示す。新しい材料の容量へのポリマーの寄与は、約2.2Vのプラトーの存在によって確認することができる。セル2は、C/10で290mAh g-1の第1の放電容量を得、C/2で100サイクル後に、65%の容量保持率を得る。 Figure 2 shows the first cycle capacity results as a function of voltage at C/10 for cell 2. The polymer contribution to the capacity of the new material can be confirmed by the presence of a plateau at about 2.2 V. Cell 2 obtains a first discharge capacity of 290 mAh g -1 at C/10 and a capacity retention of 65% after 100 cycles at C/2.
図3は、C/10におけるセル3~5の第1の充放電曲線を示す。初期容量は、活物質の性質によって異なる。セル3、セル4およびセル5で得た容量は、それぞれ407mAh g-1、570mAh g-1および277mAh g-1である。
Figure 3 shows the first charge-discharge curves of cells 3-5 at C/10. The initial capacity varies depending on the nature of the active materials. The capacities obtained for
図4は、セル6および7のC/10における第1のサイクルの容量の結果を電圧の関数として示す。新しい材料の容量への硫黄の寄与は、およそ2.05Vのプラトーの存在によって確認することができる。セル6は、C/10で305mAh g-1の第1の放電容量と、C/2で50サイクル後に91%の容量保持率を得る。セル7の場合、第1の放電の容量はC/10で443mAh g-1であり、50サイクル後の容量保持率は75%である。 Figure 4 shows the first cycle capacity results at C/10 as a function of voltage for cells 6 and 7. The sulfur contribution to the capacity of the new material can be confirmed by the presence of a plateau around 2.05 V. Cell 6 obtains a first discharge capacity of 305 mAh g -1 at C/10 and a capacity retention of 91% after 50 cycles at C/2. For cell 7, the first discharge capacity is 443 mAh g -1 at C/10 and a capacity retention of 75% after 50 cycles.
図5(a)は、セル8および9のサイクリックボルタモグラムを示す。硫黄の添加の、酸化および還元ピークの強度への影響を確認することが可能である。さらに、図5(b)で観察され得るように、硫黄を追加すると容量の増加が得られる。セル8は、C/10で138mAh g-1の初期放電容量と、C/2で100サイクル後に37%の容量保持率を得る。セル9の場合、第1の放電で得られる容量はC/10で195mAh g-1であり、100サイクル後の容量保持率は50%である。 Figure 5(a) shows the cyclic voltammograms of cells 8 and 9. It is possible to see the effect of the addition of sulfur on the intensity of the oxidation and reduction peaks. Moreover, as can be observed in Figure 5(b), an increase in capacity is obtained by adding sulfur. Cell 8 obtains an initial discharge capacity of 138 mAh g- 1 at C/10 and a capacity retention of 37% after 100 cycles at C/2. For cell 9, the capacity obtained at the first discharge is 195 mAh g -1 at C/10, with a capacity retention of 50% after 100 cycles.
実施例4-材料組成の特性評価および決定
実施例1に提示された材料の組成は、透過赤外分光スペクトルを使用して決定した。図6は、実施例1(b)、(c)、(d)に示した活性電極材料の赤外線透過スペクトルならびに共重合中に使用したモノマーのスペクトル、硫黄を添加しないイミド共重合体の赤外線透過スペクトルおよび硫黄元素の赤外線透過スペクトルを示す。
Example 4 - Characterization and Determination of Material Composition The composition of the materials presented in Example 1 was determined using transmission infrared spectroscopy. Figure 6 shows the infrared transmission spectra of the active electrode materials shown in Examples 1(b), (c), and (d) as well as the spectra of the monomers used during copolymerization, the infrared transmission spectrum of the imide copolymer without added sulfur, and the infrared transmission spectrum of elemental sulfur.
図7は、実施例1(f)および1(g)に示した活性電極材料の赤外線透過スペクトルならびに共重合で使用したモノマーのスペクトル、硫黄元素の赤外線透過スペクトルおよび硫黄を含まない共重合体の赤外線透過スペクトルを示す。 Figure 7 shows the infrared transmission spectra of the active electrode materials shown in Examples 1(f) and 1(g), as well as the spectra of the monomers used in the copolymerization, the infrared transmission spectrum of elemental sulfur, and the infrared transmission spectrum of a copolymer that does not contain sulfur.
図8は、実施例1(h)に示した活性電極材料の赤外線透過スペクトルならびに共重合で使用したモノマーのスペクトル、硫黄元素の赤外線透過スペクトルおよび硫黄を添加しない共重合体の赤外線透過スペクトルを示す。 Figure 8 shows the infrared transmission spectrum of the active electrode material shown in Example 1(h), as well as the spectrum of the monomer used in the copolymerization, the infrared transmission spectrum of elemental sulfur, and the infrared transmission spectrum of the copolymer without added sulfur.
実施例5-イオン導電率
a)実施例1(c)に示した材料のイオン導電率の測定
イオン導電率の結果を、実施例1(c)に示した共重合体について得た。これを行うために、実施例1(c)に示した共重合体を、有機溶媒(NMP)中で、リチウム塩(LiTFSI)およびバインダー(PVDF)と混合した。均一な分散液を、厚さ27μmのステンレス鋼箔に塗布した。次に、フィルムを120℃の温度で16時間乾燥させた。NMPが蒸発し、70:20:10(質量百分率)の比(共重合体:LiTFSI:PVDF)が得られた。
Example 5 - Ionic conductivity a) Measurement of the ionic conductivity of the material shown in Example 1(c) Ionic conductivity results were obtained for the copolymer shown in Example 1(c). To do this, the copolymer shown in Example 1(c) was mixed with a lithium salt (LiTFSI) and a binder (PVDF) in an organic solvent (NMP). A homogeneous dispersion was applied to a stainless steel foil with a thickness of 27 μm. The film was then dried at a temperature of 120° C. for 16 hours. The NMP evaporated and a ratio (copolymer:LiTFSI:PVDF) of 70:20:10 (by weight percentage) was obtained.
次に、得られたフィルムを2つのステンレス鋼電極の間に配置し、コインセルに組み立てて、イオン導電率を測定した。電気化学インピーダンス分光測定を、さまざまな温度(25℃、40℃、60℃および80℃)で800kHzと100Hzの間で実施した。 The resulting film was then placed between two stainless steel electrodes and assembled into a coin cell to measure the ionic conductivity. Electrochemical impedance spectroscopy measurements were performed between 800 kHz and 100 Hz at various temperatures (25°C, 40°C, 60°C and 80°C).
図9のグラフは、測定された導電率値を温度の関数として示す。3.06×10-6S・cm-1の最大値が80℃の温度で得られた。 9 graph shows the measured conductivity values as a function of temperature. A maximum value of 3.06×10 −6 S·cm −1 was obtained at a temperature of 80° C.
b)実施例1(d)に示した材料のイオン導電率の測定
実施例1(d)に示した硫黄含有共重合体の温度の関数としての導電率を、実施例5(a)に示した方法および比を使用して測定した。イオン導電率の結果を図10に示す。1.12×10-8S・cm-1の最大値が80℃の温度で得られた。
b) Measurement of the ionic conductivity of the material shown in Example 1(d) The conductivity as a function of temperature of the sulfur-containing copolymer shown in Example 1(d) was measured using the method and ratios shown in Example 5(a). The ionic conductivity results are shown in Figure 10. A maximum of 1.12 x 10-8 S cm- 1 was obtained at a temperature of 80°C.
c)実施例1(g)に示した材料のイオン導電率の測定
実施例1(g)に示した硫黄含有共重合体の温度の関数としての導電率を、実施例5(a)に示した方法および比を使用して測定した。結果を図11(A)に示す。6.43×10-9S・cm-1の最大値が80℃の温度で得られた。
c) Measurement of the ionic conductivity of the material shown in Example 1(g) The conductivity as a function of temperature of the sulfur-containing copolymer shown in Example 1(g) was measured using the method and ratios shown in Example 5(a). The results are shown in Figure 11(A). A maximum of 6.43 x 10-9 S cm- 1 was obtained at a temperature of 80°C.
d)実施例1(g)に示した材料のイオン導電率の測定
イオン導電率を、実施例1(g)に示した硫黄含有共重合体について2度目として測定した。これを行うために、実施例1(g)に示した硫黄含有共重合体を、20重量%のリチウム塩(LiTFSI)と混合した。この固体混合物を、150℃の温度で30分間、2つのステンレス鋼電極間でプレスした。次に、電気化学インピーダンス分光測定を、さまざまな温度(25℃、40℃、60℃および80℃)で800kHzと100Hzの間で測定した。結果を図11(B)に示す。1.1×10-5S・cm-1の最大イオン導電率が40℃の温度で得られた。
d) Measurement of the ionic conductivity of the material shown in Example 1(g) The ionic conductivity was measured a second time on the sulfur-containing copolymer shown in Example 1(g). To do this, the sulfur-containing copolymer shown in Example 1(g) was mixed with 20% by weight of a lithium salt (LiTFSI). This solid mixture was pressed between two stainless steel electrodes at a temperature of 150° C. for 30 minutes. Electrochemical impedance spectroscopy measurements were then performed between 800 kHz and 100 Hz at various temperatures (25° C., 40° C., 60° C. and 80° C.). The results are shown in FIG. 11(B). A maximum ionic conductivity of 1.1×10 −5 S·cm −1 was obtained at a temperature of 40° C.
企図される本発明の範囲から逸脱することなく、上記の実施形態のいずれかに多数の修正を行うことができる。本願において言及されるいずれの参考文献、特許、または科学文献の文書も、あらゆる目的においてその全文が参照により本明細書に組み込まれる。 Numerous modifications can be made to any of the above embodiments without departing from the scope of the invention as contemplated. Any reference, patent, or scientific literature documents mentioned in this application are hereby incorporated by reference in their entirety for all purposes.
Claims (19)
[式中、
Aは、置換または非置換のアリールおよびヘテロアリール基、ならびにそれらの縮合または非縮合多環式等価物から選択される電子の非局在化を許容する不飽和基であり;
Rは、非置換直鎖または分岐鎖C2-6アルキレン、置換または非置換直鎖または分岐鎖C2-6アルキレンオキシ、置換または非置換直鎖または分岐鎖C2-6アルキレングリコール、置換または非置換直鎖または分岐鎖C2-6アルキレンオキシC2-6アルキレン、置換または非置換直線状または分岐鎖ポリ(C2-6アルキレングリコール)、置換または非置換C6-12アリーレン、置換または非置換C3-12シクロアルキレン、置換または非置換C5-12ヘテロアリーレン、および置換または非置換C3-12ヘテロシクロアルキレンから選択される有機連結基であり;
mは、前記化合物のジスルフィド結合に挿入された硫黄原子の数を表し、0ではない、すなわち、m>0である]。 Compound of Formula II:
[Wherein,
A is an unsaturated group that allows for electron delocalization selected from substituted or unsubstituted aryl and heteroaryl groups, and their fused or non-fused polycyclic equivalents;
R is an organic linking group selected from unsubstituted linear or branched C 2-6 alkylene, substituted or unsubstituted linear or branched C 2-6 alkyleneoxy, substituted or unsubstituted linear or branched C 2-6 alkylene glycol, substituted or unsubstituted linear or branched C 2-6 alkyleneoxy C 2-6 alkylene, substituted or unsubstituted linear or branched poly(C 2-6 alkylene glycol), substituted or unsubstituted C 6-12 arylene, substituted or unsubstituted C 3-12 cycloalkylene , substituted or unsubstituted C 5-12 heteroarylene, and substituted or unsubstituted C 3-12 heterocycloalkylene;
m represents the number of sulfur atoms inserted into the disulfide bond of the compound and is not 0, i.e., m>0.
[式中、Rおよびmは、請求項1から3のいずれか一項に定義される通りである]
の化合物である、請求項1から4のいずれか一項に記載の化合物。 The compound has formula II(a):
wherein R and m are as defined in any one of claims 1 to 3.
5. The compound according to claim 1 ,
[式中、mは、請求項1または2に定義される通りである]
の化合物である、請求項1から4のいずれか一項に記載の化合物。 The compound has formula II(b):
wherein m is as defined in claim 1 or 2.
5. The compound according to claim 1 ,
直線状、分岐鎖、および/または架橋したものから選択され、ポリ(エチレンオキシド)(PEO)、ポリ(プロピレンオキシド)(PPO)、およびこれら2つの混合物(またはEO/PO共重合体)に基づき、架橋可能な単位を必要に応じて含むポリエーテル型のポリマーバインダーであるか;
PVDF(ポリフッ化ビニリデン)およびPTFE(ポリテトラフルオロエチレン)から選択されるフッ素化ポリマーバインダーであるか;または
SBR(スチレン-ブタジエンゴム)、NBR(アクリロニトリル-ブタジエンゴム)、HNBR(水素化NBR)、CHR(エピクロロヒドリンゴム)、およびACM(アクリレートゴム)から選択され、必要に応じてCMC(カルボキシメチルセルロース)を含む、
請求項7または8に記載の電極材料。 The binder is
a polyether type polymeric binder selected from linear , branched and/or crosslinked, based on poly(ethylene oxide) (PEO), poly(propylene oxide) (PPO), and mixtures of the two ( or EO/PO copolymers), optionally containing crosslinkable units;
PVDF (polyvinylidene fluoride) and PTFE (polytetrafluoroethylene); or
SBR (styrene-butadiene rubber), NBR (acrylonitrile-butadiene rubber), HNBR (hydrogenated NBR), CHR (epichlorohydrin rubber), and ACM (acrylate rubber), optionally containing CMC (carboxymethyl cellulose);
The electrode material according to claim 7 or 8 .
前記カソードが、請求項7から10のいずれか一項に定義される電極材料を含む:
前記カソードが、請求項11に定義される正極である;
前記電解質が、請求項12から17のいずれか一項に定義される通りである;または
前記カソードが、正極であり、請求項11に定義される通りであり、そして前記電解質が、請求項12から17のいずれか一項に定義される通りである、
電気化学セル。 An electrochemical cell comprising a cathode, an electrolyte, and an anode,
The cathode comprises an electrode material as defined in any one of claims 7 to 10:
The cathode is a positive electrode as defined in claim 11;
the electrolyte is as defined in any one of claims 12 to 17; or the cathode is a positive electrode and is as defined in claim 11 and the electrolyte is as defined in any one of claims 12 to 17.
Electrochemical cell.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CA2981012A CA2981012A1 (en) | 2017-10-02 | 2017-10-02 | Sulphur polymers and compositions and their use as an active electrode material |
| CA2,981,012 | 2017-10-02 | ||
| JP2020518728A JP7281459B2 (en) | 2017-10-02 | 2018-10-02 | Sulfur-containing compounds and polymers and their use in electrochemical cells |
Related Parent Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020518728A Division JP7281459B2 (en) | 2017-10-02 | 2018-10-02 | Sulfur-containing compounds and polymers and their use in electrochemical cells |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2023099650A JP2023099650A (en) | 2023-07-13 |
| JP7547554B2 true JP7547554B2 (en) | 2024-09-09 |
Family
ID=65992271
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020518728A Active JP7281459B2 (en) | 2017-10-02 | 2018-10-02 | Sulfur-containing compounds and polymers and their use in electrochemical cells |
| JP2023080125A Active JP7547554B2 (en) | 2017-10-02 | 2023-05-15 | Sulfur-containing compounds and polymers and their use in electrochemical cells - Patents.com |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020518728A Active JP7281459B2 (en) | 2017-10-02 | 2018-10-02 | Sulfur-containing compounds and polymers and their use in electrochemical cells |
Country Status (10)
| Country | Link |
|---|---|
| US (2) | US11469419B2 (en) |
| EP (1) | EP3692017B1 (en) |
| JP (2) | JP7281459B2 (en) |
| KR (2) | KR102763330B1 (en) |
| CN (1) | CN111164073B (en) |
| CA (1) | CA2981012A1 (en) |
| ES (1) | ES2970935T3 (en) |
| HU (1) | HUE065494T2 (en) |
| PL (1) | PL3692017T3 (en) |
| WO (1) | WO2019068182A1 (en) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2981012A1 (en) | 2017-10-02 | 2019-04-02 | Hydro-Quebec | Sulphur polymers and compositions and their use as an active electrode material |
| EP4165109A2 (en) * | 2020-06-12 | 2023-04-19 | Cytec Industries, Inc. | Sulfur-containing material and use thereof |
| JP7495155B2 (en) * | 2020-11-11 | 2024-06-04 | 国立研究開発法人物質・材料研究機構 | Optimization system, optimization method, program, electrolyte for lithium secondary battery, and lithium secondary battery |
| CN113174044B (en) * | 2021-03-19 | 2023-06-09 | 天目湖先进储能技术研究院有限公司 | Modified polyimide binder and its preparation method and application |
| CN113150277B (en) * | 2021-04-02 | 2023-01-13 | 天目湖先进储能技术研究院有限公司 | Self-healing polyimide conductive adhesive, preparation method, electrode plate and lithium battery |
| CN113381060B (en) * | 2021-06-21 | 2022-06-21 | 浙江大学 | All-solid-state composite electrolyte and preparation method and application thereof |
| CN114400323A (en) * | 2021-12-10 | 2022-04-26 | 江阴迅泰科技有限责任公司 | Preparation method of novel disulfide bond sulfur-containing polymer positive active substance |
| CN115894917B (en) * | 2022-12-02 | 2024-04-02 | 湖北大学 | A kind of polyarylene sulfide polymer and its preparation method and application |
| CN117964899B (en) * | 2024-02-23 | 2024-09-17 | 太原工业学院 | Transparent self-repairing polyimide film and preparation method and application thereof |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002512273A (en) | 1998-04-17 | 2002-04-23 | キンバリー クラーク ワールドワイド インコーポレイテッド | Novel photopolymerization initiator and its use |
| JP2005251556A (en) | 2004-03-04 | 2005-09-15 | Mitsubishi Chemicals Corp | Non-aqueous electrolyte for lithium secondary battery and lithium secondary battery using the same |
| JP2011052210A (en) | 2009-08-03 | 2011-03-17 | Yokohama Rubber Co Ltd:The | Thermoplastic elastomer composition |
| JP2012162710A (en) | 2011-01-19 | 2012-08-30 | Sekisui Chem Co Ltd | Adhesive for semiconductor |
Family Cites Families (19)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2981012A (en) | 1959-05-28 | 1961-04-25 | Cleveland Trencher Co | Mobile ditching machine |
| US4197133A (en) * | 1977-10-14 | 1980-04-08 | Ciba-Geigy Corporation | Photo-curable compositions of matter containing bis-azidophthalimidyl derivatives |
| EP0213573B1 (en) | 1985-08-30 | 1991-11-21 | General Electric Company | Crystalline polyimides containing cumulative phenylene sulfide units |
| US4716216A (en) | 1985-08-30 | 1987-12-29 | General Electric Company | Crystalline polyimides containing cumulative phenylene sulfide units |
| DE69006377T2 (en) | 1989-03-10 | 1994-09-01 | Tomoegawa Paper Mfg Co Ltd | Diamine compounds, their preparation and polyamideimide resins produced therefrom. |
| EP0449117A3 (en) | 1990-03-23 | 1992-05-06 | Matsushita Electric Industrial Co., Ltd. | Organic polymer and preparation and use thereof |
| DE4243463A1 (en) * | 1992-09-01 | 1994-03-03 | Basf Ag | Polyimide with special bonding properties to metal, esp. e.g. gold - prepd. by vapour deposition of pyromellitic dianhydride and di:amino-di:phenyl di:sulphide on a metal substrate, followed by imidisation |
| JP2000511342A (en) | 1996-05-22 | 2000-08-29 | モルテック コーポレイション | Composite cathodes, chemical cells containing novel composite cathodes, and processes for making them |
| US20030157409A1 (en) * | 2002-02-21 | 2003-08-21 | Sui-Yang Huang | Polymer lithium battery with ionic electrolyte |
| CN101704950B (en) * | 2009-11-03 | 2013-07-31 | 中国科学院宁波材料技术与工程研究所 | PASSI terpolymer and preparation method thereof |
| US20140045078A1 (en) * | 2011-04-26 | 2014-02-13 | Solvay Sa | Lithium air battery cell |
| US8796406B2 (en) * | 2011-08-12 | 2014-08-05 | Momentive Performance Materials Inc. | Siloxane copolymer and solid polymer electrolyte comprising such siloxane copolymers |
| EP2651051A1 (en) | 2012-04-13 | 2013-10-16 | Alcatel Lucent | Nonlinear Cross-Polarization Mitigation Algorithm |
| WO2014010854A1 (en) * | 2012-07-09 | 2014-01-16 | 주식회사 엘지화학 | High voltage anode active material and lithium secondary battery including same |
| KR20150036022A (en) * | 2012-07-13 | 2015-04-07 | 솔베이(소시에떼아노님) | Fluorinated carbonyl compounds comprising a triple bond, methods for their manufacture and uses thereof |
| KR101749188B1 (en) * | 2012-12-24 | 2017-06-21 | 삼성에스디아이 주식회사 | Cyclotriphosphazene compound, preparing method thereof, electrolyte for lithium secodary battery, and lithium secodary battery including the same |
| KR102006721B1 (en) * | 2015-06-22 | 2019-08-02 | 주식회사 엘지화학 | Electrode for lithium secondary battery, method for manufacturing the same, electrode assembly comprising the same, and lithium secondary battery comprising the same |
| US10683419B2 (en) * | 2016-03-23 | 2020-06-16 | The Regents Of The University Of California | Redox-active supramolecular polymer binders derived from perylene bisimide nanowires enable high-rate lithium-sulfur batteries |
| CA2981012A1 (en) | 2017-10-02 | 2019-04-02 | Hydro-Quebec | Sulphur polymers and compositions and their use as an active electrode material |
-
2017
- 2017-10-02 CA CA2981012A patent/CA2981012A1/en not_active Abandoned
-
2018
- 2018-10-02 US US16/644,714 patent/US11469419B2/en active Active
- 2018-10-02 WO PCT/CA2018/051239 patent/WO2019068182A1/en not_active Ceased
- 2018-10-02 PL PL18864901.6T patent/PL3692017T3/en unknown
- 2018-10-02 JP JP2020518728A patent/JP7281459B2/en active Active
- 2018-10-02 HU HUE18864901A patent/HUE065494T2/en unknown
- 2018-10-02 EP EP18864901.6A patent/EP3692017B1/en active Active
- 2018-10-02 ES ES18864901T patent/ES2970935T3/en active Active
- 2018-10-02 CN CN201880064264.XA patent/CN111164073B/en active Active
- 2018-10-02 KR KR1020207012837A patent/KR102763330B1/en active Active
- 2018-10-02 KR KR1020247000440A patent/KR102857996B1/en active Active
-
2022
- 2022-08-25 US US17/895,307 patent/US12431499B2/en active Active
-
2023
- 2023-05-15 JP JP2023080125A patent/JP7547554B2/en active Active
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002512273A (en) | 1998-04-17 | 2002-04-23 | キンバリー クラーク ワールドワイド インコーポレイテッド | Novel photopolymerization initiator and its use |
| JP2005251556A (en) | 2004-03-04 | 2005-09-15 | Mitsubishi Chemicals Corp | Non-aqueous electrolyte for lithium secondary battery and lithium secondary battery using the same |
| JP2011052210A (en) | 2009-08-03 | 2011-03-17 | Yokohama Rubber Co Ltd:The | Thermoplastic elastomer composition |
| JP2012162710A (en) | 2011-01-19 | 2012-08-30 | Sekisui Chem Co Ltd | Adhesive for semiconductor |
Non-Patent Citations (1)
| Title |
|---|
| GASPERT B. et al.,Optically Active Trisulphides and Tetrasulphides Related to L-Cystine,CROATICA CHEMICA ACTA,1960年,Vol. 32,p. 85-90 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102857996B1 (en) | 2025-09-12 |
| JP2023099650A (en) | 2023-07-13 |
| JP2020536147A (en) | 2020-12-10 |
| US12431499B2 (en) | 2025-09-30 |
| JP7281459B2 (en) | 2023-05-25 |
| US20230064888A1 (en) | 2023-03-02 |
| CA3075242A1 (en) | 2019-04-11 |
| ES2970935T3 (en) | 2024-05-31 |
| WO2019068182A1 (en) | 2019-04-11 |
| PL3692017T3 (en) | 2024-04-29 |
| US20200287218A1 (en) | 2020-09-10 |
| EP3692017A1 (en) | 2020-08-12 |
| US11469419B2 (en) | 2022-10-11 |
| HUE065494T2 (en) | 2024-06-28 |
| CN111164073A (en) | 2020-05-15 |
| EP3692017A4 (en) | 2021-06-23 |
| KR20200067172A (en) | 2020-06-11 |
| CN111164073B (en) | 2024-12-31 |
| KR102763330B1 (en) | 2025-02-07 |
| CA2981012A1 (en) | 2019-04-02 |
| EP3692017B1 (en) | 2023-11-29 |
| KR20240007963A (en) | 2024-01-17 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7547554B2 (en) | Sulfur-containing compounds and polymers and their use in electrochemical cells - Patents.com | |
| CN105103361B (en) | Nonaqueous electrolyte for battery, compound, polyelectrolyte and lithium secondary battery | |
| EP2541663A1 (en) | Nonaqueous electrolyte and lithium secondary battery using the same | |
| JP2020536147A5 (en) | ||
| CN105762336B (en) | Anode composite material, preparation method thereof, and lithium ion battery | |
| CN111033862A (en) | Decomposition inhibition method of silyl ester compound | |
| US20170179529A1 (en) | Safe additive, electrolyte and lithium ion battery using the same | |
| JP2024069434A (en) | Polymer additives and their use in electrode materials and electrochemical cells - Patents.com | |
| US12074271B2 (en) | Lithium secondary battery including electrolyte additive for lithium secondary battery | |
| KR102233775B1 (en) | Polymer, and Electrolyte and Lithium battery comprising polymer | |
| JP4811070B2 (en) | Non-aqueous electrolyte battery electrolyte, electrolyte and non-aqueous electrolyte battery | |
| KR100762796B1 (en) | Method for manufacturing negative active material for lithium secondary battery and lithium secondary battery having same | |
| JP5998013B2 (en) | Electric storage device and electrolyte | |
| CA3075242C (en) | Sulfur-containing compounds and polymers and the use thereof in electrochemical cells | |
| KR20250147113A (en) | Method for preparing polymer electrolyte | |
| CN105336954B (en) | Anode composite material and preparation method thereof and lithium ion battery | |
| JP2014096304A (en) | Secondary battery and method for manufacturing the same | |
| CN114695953A (en) | High-voltage high-safety polyimide gel polymer electrolyte, preparation method and application thereof, and lithium ion battery | |
| JP2019061836A (en) | Lithium ion secondary battery |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230515 |
|
| A977 | Report on retrieval |
Free format text: JAPANESE INTERMEDIATE CODE: A971007 Effective date: 20240221 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240226 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240524 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20240815 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20240828 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7547554 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |