JP7600528B2 - 粒子の製造方法 - Google Patents
粒子の製造方法 Download PDFInfo
- Publication number
- JP7600528B2 JP7600528B2 JP2020045858A JP2020045858A JP7600528B2 JP 7600528 B2 JP7600528 B2 JP 7600528B2 JP 2020045858 A JP2020045858 A JP 2020045858A JP 2020045858 A JP2020045858 A JP 2020045858A JP 7600528 B2 JP7600528 B2 JP 7600528B2
- Authority
- JP
- Japan
- Prior art keywords
- liquid
- particles
- active substance
- physiologically active
- dispersion
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5021—Organic macromolecular compounds
- A61K9/5031—Organic macromolecular compounds obtained otherwise than by reactions only involving carbon-to-carbon unsaturated bonds, e.g. polyethylene glycol, poly(lactide-co-glycolide)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5089—Processes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5192—Processes
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/42—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins
- C07K16/4208—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an idiotypic determinant on Ig
- C07K16/4241—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against immunoglobulins against an idiotypic determinant on Ig against anti-human or anti-animal Ig
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Immunology (AREA)
- Biophysics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Biochemistry (AREA)
- Genetics & Genomics (AREA)
- Physics & Mathematics (AREA)
- Biomedical Technology (AREA)
- Nanotechnology (AREA)
- Optics & Photonics (AREA)
- Medicinal Preparation (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Description
例えば、w/oエマルションを用いてPLGAにIgG抗体を含有させた溶液を、スプレードライ法で噴霧乾燥し、粒子を製造する方法などが報告されている(例えば、非特許文献1参照)。
分散液を用いて粒子を形成する造粒工程と、を含み、
前記生理活性物質が生体高分子化合物であり、
前記生体高分子化合物が抗体及びタンパク質から選択されるものであり、
前記基材が脂溶性であり、
前記分散液が、W/Oエマルションである。
従来技術では、生理活性物質を含有する「水相」に界面活性剤を溶解しており、界面活性剤による粒子の安定化(徐放性の向上)については検討されていない。また、従来技術では、生成する粒子中のIgG抗体(生理活性物質)の安定性、即ち、粒子に取り込まれた生理活性物質の生理活性を維持することができるか否かは検討されていない。
なお、本発明では、「粒子」を「マイクロカプセル」又は「マイクロ粒子」と称することもある。
本願において「粒子」といった場合、特段の記載のない限り基材及び生理活性物質を含む粒状組成物の集団を意味する。
本発明の粒子は、典型的には所望の機能を発揮する機能性粒子である。本発明の粒子は、含まれる基材を適宜選択することにより、所望の機能を有する機能性粒子となるように設計することができる。
機能性粒子としては、例えば、所望の生理的効果を発揮するために、生理活性物質を目的部位に送達する粒子、すなわちドラッグデリバリーシステムに用いられる粒子(DDS粒子)や、長期的に薬剤を放出し続ける徐放性粒子、難溶性の生理活性物質を可溶化するための可溶化粒子等が挙げられる。
分散封入体粒子は、生理活性物質が基材中に分散して封入されている形態であれば特に限定されず、基材中における生理活性物質の分散度合いが均一でなくてもよい。
また、粒子が複数種類の基材を含み、そのうちの一の基材が粒子中の所定の場所に偏って含有されている場合、生理活性物質が封入されている場所における基材の種類に応じて分散度合いが異なってもよい。
分散封入体粒子に相当する粒子としては、例えば、本発明の粒子、エマルション法を用いて製造された粒子などが挙げられる。
偏在封入体粒子は、生理活性物質が偏在して基材中に封入されている形態であり、言い換えると、粒子中の基材と生理活性物質が実質的に分離して位置することで生理活性物質が基材中に封入されている形態である。
偏在封入体粒子の形態としては、例えば、生理活性物質を含有する中心部と基材を含有し中心部を包含する外周部とを有する粒子の形態が挙げられる。偏在封入体粒子に相当する粒子としては、例えば、リポソーム、ミセル、コーティング粒子などが挙げられる。
吸着の種類としては、化学吸着と物理吸着とが挙げられる。
結合の種類としては、水素結合、共有結合、イオン結合、キレート結合等が挙げられる。
担持体粒子に相当する粒子としては、例えば、生理活性物質が多孔質状の基材表面(外部表面だけでなく内部表面も含む)に担持されている多孔質粒子などが挙げられる。
また、本形態の具体例としては、生理活性物質が表面基材側に偏って含有されている形態、及び生理活性物質が内部基材側に偏って含有されている形態等が挙げられるが、生理活性物質が内部基材側に偏って含有されている形態が好ましい。生理活性物質が内部基材側に偏って含有されていることで、生理活性物質の溶出速度が抑制された徐放性粒子を作製することができる。
確認方法の一例としては、走査型電子顕微鏡、透過型電子顕微鏡、又は走査型プローブ顕微鏡等で粒子断面を観察する方法などが挙げられる。
また、確認方法の他の一例としては、飛行時間型二次イオン質量法を用いて表面基材の成分を測定し、内部基材の成分と異なることを判断できれば上記粒子であると確認する方法が挙げられる。
さらに、他の確認方法としては、電子染色や溶解処理等の前処理を行うことも可能で、例えば、水溶性成分の基材と非水溶性成分の基材からなる上記粒子の場合は、粒子断面を水に浸漬させて、水溶性成分を完全に溶解させた断面を走査型電子顕微鏡で観察することで、粒子断面の残存部分が非水溶性成分、空隙部分に水溶性成分が分布していたと判断して、上記粒子であると判断してもよい。
本発明の粒子の製造方法は、生理活性物質が溶解した液Aと、基材及び界面活性剤が溶解した液Bと、を用いて分散液を調製する調製工程と、分散液を用いて粒子を形成する造粒工程と、を含み、更に必要に応じてその他の工程を含む。
液A及び液Bは互いに混合しない溶媒であることが好ましく、特に液Aが水、液Bがジクロロメタンであることが特に好ましい。
液A及び液Bには生理活性物質や基材以外の添加物を溶解させてもよく、W/Oエマルションを安定化させるために、液Bに前記界面活性剤を添加する。
調整工程は、液Aと、液Bと、を用いて分散液を調製する工程である。
なお、分散液とは、一の物質(分散質)が他の物質(分散媒)中に細粒として浮遊している懸濁液を意味する。本明細書においては、他の物質(分散媒)が液B、一の物質(分散質)が液Aとなる。
液Aと液Bを混合する方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、一の容器に液Bを入れた状態で、液Aを同じ容器に入れることなどが挙げられる。
液Aと液Bを撹拌する方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、撹拌子を用いた撹拌、ホモジナイザーを用いた撹拌などが挙げられる。
液Aは、生理活性物質が溶媒Aに溶解した液体であり、必要に応じてその他の成分を含有する。
ここで、溶解とは、常温常圧環境において、生理活性物質を溶媒に入れ撹拌したときに、撹拌している溶媒中において生理活性物質が目視できない状態であることを意味する。
生理活性物質は、生体内において何らかの生理活性を有するものであればいかなるものであってもよいが、好ましい一態様において、加熱、冷却、振とう、撹拌、pH変化などの化学的または物理的刺激により生理活性が変化する性質を有する。
本願において「生理活性物質」は、生体に生理的効果を発揮させるために用いられる有効成分であり、例えば、医薬化合物、食品化合物、化粧料化合物などを含む生理活性を有する低分子化合物、抗体、酵素等のタンパク質及びDNA、RNA等の核酸などの生体高分子を含む生理活性を有する高分子化合物などが挙げられる。
また、「生理的効果」とは、生理活性物質が目的部位で生理活性を発揮することにより生じる効果であり、例えば、生体、組織、細胞、タンパク質、DNA、RNA等に量的及び/又は質的な変化、影響をもたらすことである。また、「生理活性」とは、生理活性物質が目的部位(例えば、標的組織等)に作用して変化、影響を与えることである。
目的部位としては、例えば、細胞表面又は細胞内に存在する受容体等であることが好ましい。この場合は、生理活性物質が特定の受容体に結合する生理活性によって細胞にシグナルが伝わり、結果として生理的効果が発揮される。生理活性物質は、生体内の酵素により成熟型に変換された上で特定の受容体に結合し、生理的効果が発揮される物質であってもよい。この場合、本願では、成熟型に変換される前の物質も生理活性物質に含まれるものとする。
なお、生理活性物質は、生物(ヒト又はヒト以外の生物)が作り出す物質であってもよいし、人工的に合成された物質であってもよい。
本願において、生理活性を有する高分子化合物とは前記生理活性物質に包含されるもので、抗体、酵素などのタンパク質及びDNA、RNA等の核酸などの生体高分子を含む高分子化合物が挙げられる。この中でも特に抗体が有機溶媒や温度によって生理活性能が低下しやすい。
本願において「生理活性が変化する性質」としては、例えば、生理活性量が増大または低減する性質、生理活性効率が上昇または低下する性質、及び生理活性の種類が変わる性質などが挙げられるが、生理活性量が低減する性質又は生理活性効率が低下する性質であることが好ましく、生理活性量が低減する性質であることがより好ましい。また、生理活性の変化としては、可逆的な変化及び不可逆的な変化が挙げられるが、生理活性が不可逆的に変化する性質であることが好ましい。
本願において「加熱」及び「冷却」は、典型的には生理活性物質を含む液体に熱エネルギーを加えること、及び該液体から熱エネルギーを奪うことである。「加熱」または「冷却」されると、生理活性物質の分子構造や立体構造の変化などにより、生理活性が変化する場合がある。具体的には、例えば、生理活性物質がタンパク質である場合、タンパク質が熱変性すること、及びタンパク質が低温変性することなどが挙げられる。また、生理活性物質が核酸である場合は、核酸が分解することなどが挙げられる。以上のように、「生理活性物質の生理活性が変化する温度」は、選択される生理活性物質の種類によって異なるが、本明細書に接した当業者であれば、容易に当該温度を認識できる。
生理活性を有する低分子化合物としては、一般的に、分子量が数百から数千であって天然又は人工の物質が含まれる。なお、分子量としては、重量平均分子量、及び数平均分子量のどちらを用いてもよい。
また、低分子化合物としては、上記の水難溶解性物質に相当する物質、上記の水溶性物質に相当する物質などがある。
水難溶解性物質とは、JIS Z 7260-107に準拠して測定することができる水/オクタノール分配係数(logP値)が3以上である物質を意味する。
また、水溶性物質とは、JIS Z 7260-107に準拠して測定することができる水/オクタノール分配係数(logP値)が3未満である物質を意味する。
なお、低分子化合物は、生理活性物質として機能する限り、塩、水和物等のいずれの形態であってもよい。
水難溶解性物質の具体例としては、例えば、ゲフィチニブ、エルロチニブ、オシメルチニブ、ボスニチブ、バンデタニブ、アレクチニブ、ロルラチニブ、アベマシクリブ、チロホスチンAG494、ソラフェニブ、ダサチニブ、ラパチニブ、イマチニブ、モテサニブ、レスタウルチニブ、タンズチニブドルソモルヒン、アキシチニブ、4-ベンジル-2-メチル-1,2,4-チアジアゾリジン-3,5-ジオン等のキナーゼ阻害剤が挙げられる。
生理活性能を有する高分子化合物としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、生体高分子化合物などが挙げられる。生体高分子化合物としては、例えば、核酸、タンパク質を含むポリペプチド、糖質、脂質などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
核酸としては、典型的にはDNA、RNA及びその組み合わせ等が挙げられ、これらの配列の一部又は全部が化学的に修飾された化学修飾核酸に置換されていてもよい。また、PNA(peptide nucleic acid)、モルフォリノアンチセンスオリゴ(Morpholino antisense oligo)等の化学合成核酸アナログも核酸に含まれる。
また、標的遺伝子の発現を抑制することを目的とする場合、核酸としては、例えば、標的遺伝子の転写産物又はその一部に対するアンチセンス核酸、標的遺伝子の転写産物を特異的に開裂するリボザイム活性を有する核酸、標的遺伝子の発現をRNAi効果により阻害する作用を有する短鎖核酸、microRNA(miRNA)、アプタマー、オリゴヌクレオチドを改質したロックド核酸(Locked Nucleic Acid)などを挙げることができる。
ポリペプチドは、複数のアミノ酸からなる重合体を意味し、そのうち高次構造を有し、かかる高次構造に由来する機能を発揮するポリペプチドを特にタンパク質という。
ポリペプチドとしては、例えば、天然に存在する状態から修飾されていないもの、及び修飾されているものの双方が含まれる。
本発明の「抗体」は、典型的にはIgG、IgE、IgM、IgA、IgDなどのイムノグロブリン分子であるが、特定の抗原に結合し得る限り、抗原結合領域を有するそれらの抗体断片(例えばF(ab’)2断片、Fab’断片、Fab断片、Fv断片、rIgG断片、一本鎖抗体など)や抗体修飾物(標識抗体など)も含まれる。
糖質としては、例えば、単糖、二糖、オリゴ糖、及び多糖等が挙げられる。また、これら糖質がタンパク質や脂質などと共有結合した複合糖質、糖の還元基にアルコール、フェノール、サポニン、色素などのアグリコンが結合した配糖体も糖質に含まれる。
脂質としては、例えば、単純脂質、複合脂質、及び誘導脂質等が挙げられる。
0.1質量%以上20質量%以下がより好ましい。
溶媒Aとしては、生理活性物質を溶解することができれば特に制限はなく、目的に応じて適宜選択することができ、例えば、水、ヘキサフルオロ-2-プロパノール(HFIP)などが挙げられる。
その他の成分としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、緩衝液などが挙げられる。
液Bは、基材及び界面活性剤が溶媒Bに溶解した液体であり、必要に応じてその他の成分を含有する。
ここで、溶解とは、常温常圧環境において、基材及び界面活性剤を溶媒に入れ撹拌したときに、撹拌している溶媒中において固体である基材が目視できない状態であることを意味する。
本願において「基材」は、粒子に含まれる成分であり、1つ1つの粒子を構成する基となる材質である。
基材は、粒子を構成する基となる材質である。したがって常温で固体であることが好ましい。
基材としては、ともに含有される生理活性物質に悪影響を与える物質でない限り特に限定されず、低分子量の物質であってもよいし、高分子量の物質であってもよい。
本発明の粒子は好ましくは生体に適用される粒子であるため、基材は好ましくは生体に対して毒性を有しない物質である。
低分子量の物質は、重量平均分子量が15,000未満の化合物であることが好ましい。
高分子量の物質は、重量平均分子量が15,000以上の化合物であることが好ましい。
上述のとおり基材は1種のみであっても2種以上であってもよく、後述する任意の基材を組み合わせて用いてもよい。
低分子量の物質としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、脂質類、糖類、シクロデキストリン類、アミノ酸類、及び有機酸類などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
脂質類としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、中鎖又は長鎖のモノグリセリド、中鎖又は長鎖のジグリセリド、中鎖又は長鎖のトリグリセリド、リン脂質、植物油(例えば、大豆油、アボカド油、スクアレン油、ゴマ油、オリーブ油、トウモロコシ油、ナタネ油、サフラワー油、ヒマワリ油等)、魚油、調味油、水不溶性ビタミン、脂肪酸、これらの混合物、及びこれらの誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
糖類としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、グルコース、マンノース、イドース、ガラクトース、フコース、リボース、キシロース、ラクトース、スクロース、マルトース、トレハロース、ツラノース、ラフィノース、マルトトリオース、アカルボース、シクロデキストリン類、アミロース(デンプン)、セルロースなどの単糖類や多糖類の他、グリセリン、ソルビトール、ラクチトール、マルチトール、マンニトール、キシリトール、エリスリトールなどの糖アルコール(ポリオール)、並びにこれらの誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
シクロデキストリン類としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ヒドロキシプロピル-β-シクロデキストリン、β-シクロデキストリン、γ-シクロデキストリン、α-シクロデキストリン、及びシクロデキストリン誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
アミノ酸類としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、バリン、リジン、ロイシン、スレオニン、イソロイシン、アスパラギン、グルタミン、フェニルアラニン、アスパラギン酸、セリン、グルタミン酸、メチオニン、アルギニン、グリシン、アラニン、チロシン、プロリン、ヒスチジン、システイン、トリプトファン、及びこれらの誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
有機酸類としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、アジピン酸、アスコルビン酸、クエン酸、フマル酸、没食子酸、グルタル酸、乳酸、リンゴ酸、マイレン酸、コハク酸、酒石酸、及びこれらの誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
高分子量の物質としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、水溶性セルロース、ポリアルキレングリコール、ポリ(メタ)アクリルアミド、ポリ(メタ)アクリル酸、ポリ(メタ)アクリル酸エステル、ポリアリルアミン、ポリビニルピロリドン、ポリビニルアルコール、ポリ酢酸ビニル、生分解性樹脂、ポリグリコール酸、ポリアミノ酸、ゼラチン、フィブリンなどのタンパク質、多糖類及びこれらの誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
水溶性セルロースとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、メチルセルロース、エチルセルロース等のアルキルセルロース;ヒドロキシエチルセルロース、ヒドロキシプロピルセルロース等のヒドロキシアルキルセルロース;及びヒドロキシエチルメチルセルロース、ヒドロキシプロピルメチルセルロース等のヒドロキシアルキルアルキルセルロースなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。これらの中でも、生体適合性が高く、かつ粒子を製造する際に用いる溶媒に対する溶解度が高い点から、ヒドロキシプロピルセルロース、及びヒドロキシプロピルメチルセルロースが好ましく、ヒドロキシプロピルセルロースがより好ましい。
ヒドロキシプロピルセルロースは、粘度が異なる種々の製品が各社から市販されており、いずれも本発明の基材に使用することができる。ヒドロキシプロピルセルロースの2質量%水溶液(20℃)粘度としては、特に制限はなく、目的に応じて適宜選択することができるが、2.0mPa・s(センチポイズ、cps)以上4,000mPa・s(センチポイズ、cps)以下が好ましい。
また、ヒドロキシプロピルセルロースの粘度は、ヒドロキシプロピルセルロースの重量平均分子量、置換度、及び分子量に依存すると考えられる。
ヒドロキシプロピルセルロースの重量平均分子量としては、特に制限はなく、目的に応じて適宜選択することができるが、15,000以上400,000以下が好ましい。なお、重量平均分子量は、例えば、ゲル浸透クロマトグラフィー(GPC)を用いて測定することができる。
ヒドロキシプロピルセルロースの市販品としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、分子量15,000以上30,000以下、かつ粘度2.0mPa・s以上2.9mPa・s以下のHPC-SSL等、分子量30,000以上50,000以下、かつ粘度3.0mPa・s以上5.9mPa・s以下のHPC-SL等、分子量55,000以上70,000以下、かつ粘度6.0mPa・s以上10.0mPa・s以下のHPC-L等、分子量110,000以上150,000以下、かつ粘度150mPa・s以上400mPa・s以下のHPC-M等、及び分子量250,000以上400,000以下、かつ粘度1,000mPa・s以上4,000mPa・s以下のHPC-H等(以上、日本曹達株式会社製)などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。これらの中でも、分子量15,000以上30,000以下、かつ粘度2.0mPa・s以上2.9mPa・s以下のHPC-SSLが好ましい。なお、上記市販品において、分子量はゲル浸透クロマトグラフィー(GPC)を用いて測定され、粘度は2質量%水溶液(20℃)を用いて測定される。
ポリアルキレングリコールとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ポリエチレングリコール(PEG)、ポリプロピレングリコール、ポリブチレングリコール、及びこれらの共重合体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリ(メタ)アクリルアミドとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、N-メチル(メタ)アクリルアミド、N-エチル(メタ)アクリルアミド、N-プロピル(メタ)アクリルアミド、N-ブチル(メタ)アクリルアミド、N-ベンジル(メタ)アクリルアミド、N-ヒドロキシエチル(メタ)アクリルアミド、N-フェニル(メタ)アクリルアミド、N-トリル(メタ)アクリルアミド、N-(ヒドロキシフェニル)(メタ)アクリルアミド、N-(スルファモイルフェニル)(メタ)アクリルアミド、N-(フェニルスルホニル)(メタ)アクリルアミド、N-(トリルスルホニル)(メタ)アクリルアミド、N,N-ジメチル(メタ)アクリルアミド、N-メチル-N-フェニル(メタ)アクリルアミド、及びN-ヒドロキシエチル-N-メチル(メタ)アクリルアミドなどのモノマーの重合体が挙げられる。これらモノマーは、1種単独で重合されてもよいし、2種以上を併用し重合されてもよい。また、これら重合体は、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリ(メタ)アクリル酸としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ポリアクリル酸、ポリメタクリル酸等のホモポリマー、アクリル酸-メタクリル酸共重合体等のコポリマーなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリ(メタ)アクリル酸エステルとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、エチレングリコールジ(メタ)アクリレート、ジエチレングリコールジ(メタ)アクリレート、プロピレングリコールジ(メタ)アクリレート、グリセロールポリ(メタ)アクリレート、ポリエチレングリコール(メタ)アクリレート、トリメチロールプロパントリ(メタ)アクリレート、ペンタエリスリトールテトラ(メタ)アクリレート、1,3-ブチレングリコールジ(メタ)アクリレートなどのモノマーの重合体が挙げられる。これらモノマーは、1種単独で重合されてもよいし、2種以上を併用し重合されてもよい。また、これら重合体は、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリアリルアミンとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ジアリルアミン、トリアリルアミンなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリビニルピロリドンとしては、市販品を用いることができる。ポリビニルピロリドンの市販品としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、プラスドンC-15(ISP TECHNOLOGIES社製)、コリドンVA64、コリドンK-30、コリドンCL-M(以上、KAWARLAL社製)、コリコートIR(BASF社製)などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリビニルアルコールとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、シラノール変性ポリビニルアルコール、カルボキシル変性ポリビニルアルコール、アセトアセチル変性ポリビニルアルコールなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ポリ酢酸ビニルとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、酢酸ビニル-クロトン酸コポリマー、酢酸ビニル-イタコン酸コポリマーなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
生分解性樹脂としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、生分解性ポリエステルなどが挙げられる。生分解性ポリエステルとしては、例えば、ポリ乳酸;ポリ-ε-カプロラクトン;ポリエチレンサクシネート、ポリブチレンサクシネート、ポリブチレンサクシネートアジペートなどのサクシネート系重合体(ポリ乳酸グリコール酸共重合体);ポリヒドロキシプロピオネート、ポリヒドロキシブチレート、ポリヒドロキシパリレートなどのポリヒドロキシアルカノエート、ポリグリコール酸等が挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。これらの中でも、生体適合性が高く、含有する生理活性物質を徐放的に溶出させることができる点からポリ乳酸が好ましい。
ポリ乳酸の重量平均分子量としては、特に制限はなく、目的に応じて適宜選択することができるが、5,000以上100,000以下が好ましく、10,000以上70,000以下がより好ましく、10,000以上50,000以下が更に好ましく、10,000以上30,000以下が特に好ましい。
ポリ乳酸の含有量は特に制限はなく、目的に応じて適宜選択することができるが、基材の質量に対して50質量%以上が好ましく、50質量%以上99質量%以下がより好ましく、75質量%以上99質量%以下が更に好ましく、80質量%以上99質量%以下が特に好ましい。
ポリグリコール酸としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、乳酸に由来する構成単位とグリコール酸に由来する構成単位とを有する共重合体である乳酸・グリコール酸共重合体、グリコール酸に由来する構成単位とカプロラクトンに由来する構成単位とを有する共重合体であるグリコール酸・カプロラクトン共重合体、グリコール酸に由来する構成単位と炭酸トリメチレンに由来する構成単位とを有する共重合体であるグリコール酸・炭酸トリメチレン共重合体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。これらの中でも、生体適合性が高く、含有する生理活性物質を徐放的に溶出させることができ、かつ含有する生理活性物質を長期的に保存することができる点から乳酸・グリコール酸共重合体が好ましい。
乳酸・グリコール酸共重合体の重量平均分子量としては、特に制限はなく、目的に応じて適宜選択することができるが、2,000~250,000が好ましく、2,000~100,000がより好ましく、3,000~50,000が更に好ましく、5,000~10,000が特に好ましい。
乳酸・グリコール酸共重合体における、乳酸に由来する構成単位(L)とグリコール酸に由来する構成単位(G)とのモル比率(L:G)としては、特に制限はなく、目的に応じて適宜選択することができるが、1:99~99:1が好ましく、25:75~99:1がより好ましく、30:70~90:10が更に好ましく、50:50~85:15が特に好ましい。
乳酸・グリコール酸共重合体の含有量は特に制限はなく、目的に応じて適宜選択することができるが、基材の質量に対して50質量%以上が好ましく、50質量%以上99質量%以下がより好ましく、75質量%以上99質量%以下が更に好ましく、80質量%以上99質量%以下が特に好ましい。
ポリアミノ酸としては、特に制限はなく、目的に応じて適宜選択することができる。ポリアミノ酸は、上記アミノ酸の項目において例示したアミノ酸を任意に組み合わせてポリマー化したものであってよいが、好ましくは単一のアミノ酸がポリマー化したものである。好ましいポリアミノ酸としては、例えば、ポリ-α-グルタミン酸、ポリ-γ-グルタミン酸、ポリアスパラギン酸、ポリリジン、ポリアルギニン、ポリオルニチン、ポリセリン等のアミノ酸単独重合体、又はこれらの共重合体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ゼラチンとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、石灰処理ゼラチン、酸処理ゼラチン、ゼラチン加水分解物、ゼラチン酵素分散物、又はこれらの誘導体などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ゼラチン誘導体に利用される天然分散剤ポリマーとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、タンパク質、多糖類、核酸などが挙げられる。これらの中には、天然分散剤ポリマー、又は合成分散剤ポリマーからなる共重合体も含まれる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
ゼラチン誘導体とは、ゼラチン分子に疎水性基を共有結合させて誘導体化したゼラチンを意味する。疎水性基としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ポリ乳酸、ポリグリコール酸、ポリ-ε-カプロラクトン等のポリエステル類;コレステロール、ホスファチジルエタノールアミン等の脂質;アルキル基、ベンゼン環を含む芳香族基;複素芳香族基、又はこれらの混合物などが挙げられる。
タンパク質としては、生理活性物質の生理活性に悪影響を及ぼさない限り特に制限はなく、目的に応じて適宜選択することができ、例えば、コラーゲン、フィブリン、アルブミンなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
多糖類としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、キチン、キトサン、ヒアルロン酸、アルギン酸、デンプン、ペクチンなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
基材は、基材を含有する粒子を医薬製剤、機能性食品、及び機能性化粧品等に含有させることができる物質であることが好ましいため、上記材料の中でも、生体毒性を有しない物質、特に生分解性ポリマーなどの生分解性を有する物質であることが好ましい。
界面活性剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、塩化ベンザルコニウム、レシチン、ソルビタン脂肪酸エステル、ポリオキシエチレン硬化ひまし油、ポリオキシエチレンポリオキシプロピレングリコール、ポリオキシエチレンソルビタンモノオレエート、ポリビニルアルコール、モノオレイン酸ソルビタン、モノステアリン酸グリセリン、セスキオレイン酸ソルビタン、モノステアリン酸ソルビタン、モノステアリン酸グリセリル、ポリグリセリン脂肪酸エステル、ポリソルベート80等のポリソルベート;ポリオキシエチレン・ポリオキシプロピレン共重合体;ラウリル硫酸ナトリウムなどが挙げられる。
界面活性剤の指標として、親水親油バランスがあるが、本発明においては、親水親油バランスが1以上8以下であることが好ましく、3以上6以下であることがさらに好ましい。その中でも、セスキオレイン酸ソルビタン(親水親油バランス:4)が特に好ましい。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
溶媒Bとしては、基材を溶解することができれば特に制限はなく、目的に応じて適宜選択することができ、例えば、ジクロロメタン、酢酸メチル、ヘキサフルオロ―2-プロパノールなどが挙げられる。
その他の成分としては、特に制限はなく、目的に応じて適宜選択することができる。
また、分散液の表面張力としては、特に制限はなく、目的に応じて適宜選択することができるが、10mN/m以上60mN/m以下が好ましく、20mN/m以上50mN/m以下がより好ましい。なお、表面張力は、例えば、ハンディ表面張力計(装置名:PocketDyne、KRUSS社製)を用いて、最大泡圧法により25℃、ライフタイム1,000msの条件により測定できる。分散液の表面張力が、0.5mPa・s以上15.0mPa・s以下であることで、液滴を吐出する手段を用いる場合において、好適な吐出を行うことができるため好ましい。
造粒工程は、調製した分散液を用いて粒子を形成する工程である。
調製した分散液を液滴化する工程は、分散液を液滴化する工程である。調製した分散液を液滴化する工程としては、分散液を液滴化することができれば特に制限はなく、目的に応じて適宜選択することができ、例えば、分散液を気体中に噴霧する方法、分散液を液滴吐出手段により吐出して液滴を形成する方法などが挙げられる。
(a)振動を用いて液体収容部の容積を変化させる容積変化手段を用いた方法
(b)液体収容部に振動を加えながら液体収容部に設けた複数の吐出孔より液体を放出し、液体を柱状から括れ状態を経て液滴化させる括れ発生手段を用いた方法
(c)ノズルが形成された薄膜を振動させるノズル振動手段を用いた方法
容積変化手段としては、液体収容部の容積を変化させることができれば特に制限はなく、目的に応じて適宜選択することができ、例えば、電圧を加えると伸縮する圧電素子(「ピエゾ素子」と称することもある)などが挙げられる。
振動を発生させる手段としては、圧電素子を用いることが一般的である。圧電素子としては、特に制限はなく、形状、大きさ、及び材質を適宜選択することができ、例えば、従来のインクジェット吐出方式に用いられている圧電素子を好適に使用することができる。
圧電素子の形状、及び大きさとしては、特に制限はなく、吐出孔の形状などにあわせて適宜選択することができる。
圧電素子の材質としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、チタン酸ジルコン酸鉛(PZT)等の圧電セラミックス、ポリフッ化ビニリデン(PVDF)等の圧電ポリマー、水晶、LiNbO3、LiTaO3、KNbO3等の単結晶などが挙げられる。
吐出孔の断面形状、及び大きさについては適宜選択することができる。
吐出孔の断面形状としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、(1):内部(液体収容部側)から外部(液体が吐出される側)に向かって開口径が小さくなるようなテーパー形状、(2):内部(液体収容部側)から外部(液体が吐出される側)に向かってラウンド形状を持ちながら開口径が狭くなるような形状、(3):内部(液体収容部側)から外部(液体が吐出される側)に向かって一定のノズル角度を持って開口径が狭くなるような形状、(4):(1)の形状及び(2)の形状の組合せなどが挙げられる。これらの中でも、吐出孔において液にかかる圧力が最大となる点から、(3)の形状が好ましい。
(3)の形状におけるノズル角度としては、特に制限はなく、目的に応じて適宜選択することができるが、60°以上90°以下が好ましい。ノズル角度が、60°以上90°以下であると液滴吐出を安定化することができる。
吐出孔の大きさとしては、特に制限はなく、目的に応じて適宜選択することができ、例えば、直径が1,000μm未満であることが好ましく、1.0μm以上1,000μm未満であることがより好ましく、1.0μm以上500μm以下であることが更に好ましく、1.0μm以上50μm以下であることが特に好ましい。なお、吐出孔の形状が真円でない場合は、吐出孔の面積と同等の面積を有する真円における直径を採用する。
液滴化した分散液を乾燥する工程は、液滴から溶媒を気化させて液滴に含まれていた溶媒を除去する工程である。液滴化した分散液を乾燥する工程としては、液滴化した分散液を乾燥することができれば特に制限はなく、目的に応じて適宜選択することができ、例えば、分散液を液滴化する工程において、気体中に放出された液滴を気体中に飛行させることにより行う方法などが挙げられる。
搬送気流を用いて液滴から溶媒を気化させる方法としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、搬送気流の搬送方向を、液滴を吐出する方向に対して略垂直方向とする方法などが好ましい。
また、搬送気流は、温度、蒸気圧、気体の種類などを適宜調整することが好ましい。なお、搬送気流の温度を調整するために加熱手段を設けてもよいが、上記の通り、造粒工程では液滴同士の合着が抑制された吐出がなされる。そのため、搬送気流によって溶媒の乾燥が促進されるため、加熱手段による加熱の程度を抑制することができ、具体的には、生理活性物質の生理活性が変化しない程度の加熱にすることができる。
また、捕集された粒子が固体状態を維持していれば、溶媒が完全に気化していなくてもよく、回収後に別工程で乾燥工程を追加で設けてもよい。また、温度変化や化学変化などの適用により、液滴から溶媒を気化させる方法を用いてもよい。
その他の工程としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、粒子捕集工程などが挙げられる。
粒子捕集工程は、製造した粒子を捕集する工程であり、粒子捕集手段により好適に実施することができる。粒子捕集手段としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、サイクロン捕集、バックフィルターなどが挙げられる。
本発明の粒子の製造方法に係る粒子の製造装置としては、生理活性物質が溶解した液Aと、基材及び界面活性剤が溶解した液Bと、を用いて分散液を調製する調製手段と、分散液を気体中に吐出して粒子を形成する造粒手段と、を有し、液体収容容器などを有し、更に必要に応じてその他の手段を有する。
調製手段については、本発明の粒子の製造方法において説明した各工程を行うための手段と同様のものである。
造粒手段としては、調製した分散液を液滴化する液滴形成手段と、液滴化した分散液を乾燥する乾燥手段とを有する。
液滴形成手段としては、分散液を液滴化することができれば特に制限はなく、目的に応じて適宜選択することができ、例えば、液滴吐出手段などが挙げられる。
液滴吐出手段は、基材、生理活性物質及び溶媒を含有する分散液を気体中に吐出して液滴を形成する手段である。スプレーノズルやディスクを用いた液滴吐出手段はあるが、好ましい態様において、液滴吐出手段は、振動により分散液を吐出して液滴を形成するものである。
まず、粒子の製造装置を構成する一手段である液柱共鳴液滴吐出手段について具体的に説明する。
図1は、液柱共鳴液滴吐出手段の一例を示す概略断面図である。液柱共鳴液滴吐出手段11は、液共通供給路17及び液柱共鳴液室18を有する。液柱共鳴液室18は、長手方向の両端の壁面のうち一方の壁面に設けられた液共通供給路17と連通されている。また、液柱共鳴液室18は、両端の壁面と連結する壁面のうち一つの壁面に液滴21を吐出する吐出孔19と、吐出孔19と対向する壁面に設けられ、かつ液柱共鳴定在波を形成するために高周波振動を発生する振動発生手段20とを有する。なお、振動発生手段20には、高周波電源が接続されている。また、液柱共鳴吐出手段11から吐出された液滴21を搬送する気流を供給する気流通路が設けられていてもよい。
基材、生理活性物質、及び良溶媒を含有する液体14は、液循環ポンプにより液供給管を通って、液柱共鳴液滴吐出手段11の液共通供給路17内に流入し、液柱共鳴液室18に供給される。そして、液体14が充填されている液柱共鳴液室18内には、振動発生手段20によって発生する液柱共鳴定在波により圧力分布が形成される。そして、液柱共鳴定在波において振幅の大きな部分であって圧力変動が大きい、定在波の腹となる領域に配置されている吐出孔19から液滴21が吐出される。この液柱共鳴による定在波の腹となる領域は、定在波の節以外の領域であり、定在波の圧力変動が液を吐出するのに十分な大きさの振幅を有する領域が好ましく、圧力定在波の振幅が極大になる位置(速度定在波としての節)から極小になる位置に向かって±1/4波長の領域がより好ましい。
定在波の腹になる領域であれば、吐出孔が複数で開口されていても、それぞれからほぼ均一な液滴を形成することができ、更には効率的に液滴の吐出を行うことができ、吐出孔の詰まりも生じ難くなる。なお、液共通供給路17を通過した液体14は液戻り管により循環される。液滴21の吐出によって液柱共鳴液室18内の液体14の量が減少すると液柱共鳴液室18内の液柱共鳴定在波の作用による吸引力が作用し、液共通供給路17から供給される液体14の流量が増加する。そして、液柱共鳴液室18内に液体14が補充される。そして、液柱共鳴液室18内に液体14が補充されると、液共通供給路17を通過する液体14の流量が元に戻る。
液柱共鳴液滴吐出手段11における液柱共鳴液室18は、金属、セラミックス、シリコーンなどの駆動周波数において液体の共鳴周波数に影響を与えない程度の高い剛性を持つ材質により形成されるフレームがそれぞれ接合されて形成されている。また、図1に示すように、液柱共鳴液室18の長手方向の両端の壁面間の長さLは、液柱共鳴原理に基づいて決定される。更に、液柱共鳴液室18は、生産性を飛躍的に向上させるために1つの液滴形成ユニットに対して複数配置されていることが好ましい。液柱共鳴液室18の数としては、特に制限はなく、1個以上2,000個以下が好ましい。また、液柱共鳴液室毎に、液供給のための流路が液共通供給路17から連通接続されており、液共通供給路17には複数の液柱共鳴液室18と連通している。
また、液柱共鳴液滴吐出手段11における振動発生手段20は所定の周波数で駆動できるものであれば特に制限はないが、圧電体を弾性板9に貼りあわせた形態が好ましい。周波数としては、生産性の点から、150kHz以上がより好ましく、300kHz以上500kHz以下がさらに好ましい。弾性板は、圧電体が接液しないように液柱共鳴液室の壁の一部を構成している。圧電体は、例えば、チタン酸ジルコン酸鉛(PZT)等の圧電セラミックスなどが挙げられ、一般に変位量が小さいため積層して使用されることが多い。この他にも、ポリフッ化ビニリデン(PVDF)等の圧電ポリマーや、水晶、LiNbO3、LiTaO3、KNbO3等の単結晶などが挙げられる。更に、振動発生手段20は、1つの液柱共鳴液室毎に個別に制御できるように配置されていることが好ましい。また、上記の1つの材質のブロック状の振動部材を液柱共鳴液室の配置にあわせて、一部切断し、弾性板を介してそれぞれの液柱共鳴液室を個別制御できるような構成が好ましい。
さらに、吐出孔19の開口を多数設けることができ、生産効率が高くなる点から、吐出孔19を液柱共鳴液室18内の幅方向に設ける構成を採用することが好ましい。また、吐出孔19の開口配置によって液柱共鳴周波数が変動するため、液柱共鳴周波数は液滴の吐出を確認して適宜決定することが望ましい。
乾燥手段は、液滴から溶媒を気化させて液滴に含まれていた溶媒を除去することで粒子を造粒する手段である。
乾燥手段としては、例えば、液滴から溶媒を気化させるための空間を形成する部材などが挙げられる。
乾燥手段としては、搬送気流を形成する搬送気流形成手段を有していることが好ましい。
次に、実施形態の具体例について、図2~4を用いて説明する。
図2は、粒子の製造装置の一例を示す概略図である。図3は、粒子の製造装置に用いられる液滴吐出手段の一例を示す概略断面図である。図4は、粒子の製造装置に用いられる液滴吐出手段の他の一例を示す概略断面図である。
図2に示す粒子の製造装置300は、液滴吐出手段302、乾燥捕集ユニット360、搬送気流排出口365、及び粒子貯留部363を有する。液滴吐出手段302には、液体314を収容する液体収容器313と、液体収容器313に収容されている液体314を、液供給管316を通して液滴吐出手段302に供給し、更に液戻り管322を通って液体収容器313に戻すために液供給管316内の液体314を圧送する液循環ポンプ315とが連結されており、随時、液体314を液滴吐出手段302に供給できる。液供給管316にはP1、乾燥捕集ユニットにはP2の圧力測定器が設けられており、液滴吐出手段302への送液圧力及び、乾燥捕集ユニット内の圧力は圧力計P1、P2によって管理される。このときに、P1の圧力測定値がP2の圧力測定値よりも大きい場合には、液体314が吐出孔から染み出すおそれがあり、P1の圧力測定値がP2の圧力測定値よりも小さい場合には、液滴吐出手段302に気体が入り、吐出が停止する恐れがあるため、P1の圧力測定値とP2の圧力測定値とがほぼ同じあることが好ましい。
チャンバー361内では、搬送気流導入口364から作られる下降気流(搬送気流)301が形成されている。液滴吐出手段302から吐出された液滴321は、重力よってのみではなく、搬送気流301によっても下方に向けて搬送され、搬送気流排出口365を通り、粒子捕集手段362によって捕集され、粒子貯留部363に貯留される。
なお、液滴吐出工程において、吐出した液滴同士が乾燥前に接触すると、液滴同士が合着することがある。粒度分布が狭い粒子を得るためには、吐出した液滴同士の距離が保たれていることが好ましい。しかしながら、吐出された液滴は一定の初速度を持っているが空気抵抗により、やがて失速する。失速した液滴に対し、後から吐出された液滴が追いついた場合であって、液滴の乾燥が不十分であるとき、液滴同士が合着し得る。合着を防ぐためには液滴の速度低下を抑制し、液滴同士を接触させないように搬送気流301によって合着を抑制しながら、液滴を乾燥させつつ搬送することが好ましい。そのため、搬送気流301は、液滴吐出手段302の近傍において液滴吐出方向と同一方向に配置することが好ましい。なお、液滴同士が接触する場合であっても、接触時までに十分に乾燥していれば合着しないため、そのような場合は搬送気流301を用いなくてもよい。
図3は、図2における粒子の製造装置の液滴吐出手段の拡大図である。図3に示すように、液滴吐出手段302は、容積変化手段320、弾性板309、及び液体収容部319を有する。液滴吐出手段302は、容積変化手段320に電圧が印加されると変形し、液体収容部319の容積を減少させるため、液体収容部319に貯留している液体を吐出孔から液滴321として吐出する。
図4は、粒子の製造装置の液滴吐出手段の他の態様を示す図である。図4に示すように、気流通路312において、搬送気流301は、吐出方向に対して略垂直方向であってもよい。なお、搬送気流301は、角度を持っていてもよく、液滴吐出手段302より液滴が離れるような角度を持っていることが好ましい。図4のように、容積変化手段320により弾性板309を介して液体収容部319の容積を変化させて、液滴321を吐出し、吐出した液滴321に対して略垂直方向から合着防止の搬送気流301を与える場合は、吐出孔から合着防止の搬送気流301によって液滴321が搬送された際に液滴が通る軌跡が重ならないように吐出孔を配置することが好ましい。
なお搬送気流301によって合着を防いだ後に、別の気流によって粒子捕集手段まで粒子を運んでもよい。
また、搬送気流には、液滴の乾燥を促進させるような化学物質を混入してもよい。搬送気流の状態は、限定されることはなく、層流や旋回流や乱流であってもよい。
搬送気流を構成する気体の種類は、特に制限はなく、目的に応じて適宜選択することができ、空気を用いても、窒素等の不燃性気体を用いてもよい。
また、搬送気流の温度は、適宜調整可能であるが、気流の温度により、液滴に含まれる生理活性物質の生理活性が変化しない温度である。
図2で示された粒子捕集手段362によって得られた粒子に含まれる残留溶媒量が多い場合は、これを低減するために、必要に応じて、二次乾燥を行うことが好ましい。二次乾燥としては、流動床乾燥や真空乾燥のような一般的な公知の乾燥手段を用いることができる。
液体収容容器は、基材、生理活性物質、及び溶媒を含有する液体を収容した容器である。
液体収容容器は、可とう性があってもよいし、可とう性がなくてもよい。液体収容容器の材質は、特に制限はなく、目的に応じて適宜選択することができ、例えば、樹脂製であってもよいし、金属製であってもよい。液体収容容器の構造としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、密閉構造であってもよいし、非密閉構造であってもよい。
本発明の粒子の特徴的な物性としては、例えば、生理活性率、粒度分布、粒径等が挙げられる。
本願において「生理活性率」は、粒子の製造に用いられた材料における生理活性の量に対する、当該材料により製造された粒子における生理活性の量の割合({粒子製造後の生理活性の量/粒子製造前の生理活性の量}×100)を表す。
また、「生理活性の量」とは、生理活性物質の生理活性を定量的に測定したときに得られる測定値を表す。ここで、「定量的に測定」とは、生理活性の量そのものを定量的に測定する直接的な方法に限られず、例えば、生理活性の量を所定の基準と比較して測定する相対的な定量的測定方法であってもよい。
本発明の粒子の製造方法により製造される粒子は、生理活性率が高い性質を有することが好ましい。具体的には、生理活性率は、40%以上であることが好ましく、50%以上であることがより好ましく、60%以上であることが更に好ましく、70%以上であることが特に好ましい。
生理活性維持率とは、粒子の製造工程を経て維持される生理活性物質における生理活性の割合を表す。生理活性物質は、加熱、冷却、又は外部応力により生理活性が変化する場合があるため、粒子の製造工程において、加熱、冷却、振とう、撹拌等を伴う処理が実行されると生理活性維持率が低下し、結果として生理活性率も低下する。
また、生理活性物質保持率とは、粒子の製造工程を経て粒子中に保持される生理活性物質の割合を表す。例えば、粒子の製造工程において、生理活性物質が分解または流出などにより失われ、結果として粒子内に保持される生理活性物質の総量が減ってしまう場合がある。このような場合に生理活性物質保持率が低下し、結果として生理活性率も低下する。
生理活性率が高い性質を有する粒子を作製する方法としては、例えば、加熱、冷却、及び/又は外部応力等による活性の低下を伴わない粒子の製造方法を実行すること、生理活性物質そのものの損失量が低減された粒子の製造方法を実行すること等が挙げられる。
本発明の粒子は、粒度分布が狭い性質を有することが好ましい。かかる粒度分布の狭さを表す指標としては、具体的には、例えば、Relative Span Factor(R.S.F)や体積平均粒径(Dv)/個数平均粒径(Dn)などが挙げられ、例えばR.S.F.が0<(R.S.F)≦1.2であること、体積平均粒径(Dv)/個数平均粒径(Dn)が1.00以上1.50以下であることが好ましい。粒度分布が上記範囲内であることで、目的とする粒径から見て粗大粒子に相当する粒子の割合が低下する。これにより、粒子を医薬組成物に含有させる場合等、ろ過滅菌してから用いなければならないときであっても、ろ過滅菌フィルターを詰まらせることなく、簡便かつ効率的にろ過滅菌を行うことができる。また、粒子の大きさが均一になることで、各粒子における生理活性物質及び基材の含有量や、各粒子の表面積が均一になる。これにより、各粒子から溶出する生理活性物質の量が均等になり、生理活性物質の高度な徐放性制御が可能な粒子を提供することができる。また、粒子の大きさが均一になることで、基材に含有されていない生理活性物質単体からなる小粒径粒子の発生を抑制することができ、初期バーストが抑制された徐放性を有する粒子を提供することができる。
本願において「Relative Span Factor(R.S.F)」は、(D90-D10)/D50で定義される。D90は累積粒度分布の小粒子側からの累積90体積%を表し、D50は累積粒度分布の小粒子側からの累積50体積%を表し、D10は累積粒度分布の小粒子側からの累積10体積%を表す。(R.S.F)は、0<(R.S.F)≦1.2であることが好ましく、0<(R.S.F)≦1.0であることがより好ましく、0<(R.S.F)≦0.6であることが更に好ましい。
(R.S.F)の測定方法としては、例えば、動的光散乱法による濃厚系アナライザー(「FPAR-1000」、大塚電子株式会社製)を用いて測定する方法等が挙げられる。
体積平均粒径(Dv)/個数平均粒径(Dn)は、体積平均粒径(Dv)を個数平均粒径(Dn)で除した値である。体積平均粒径(Dv)/個数平均粒径(Dn)は、1.00以上1.50以下であることが好ましく、1.00以上1.20以下であることがより好ましい。
体積平均粒径(Dv)、及び個数平均粒径(Dn)の測定方法としては、例えば、レーザー回折・散乱式粒度分布測定装置(装置名:マイクロトラックMT3000II、マイクロトラック・ベル株式会社製)を用いて測定する方法等が挙げられる。
粒子の体積平均粒径(Dv)が1μm以上100μm以下である場合、十分な量の生理活性物質を保持することができ、例えば、生理活性物質を長期に渡って徐放可能な粒子を製造することができる。なお、体積平均粒径(Dv)は、1μm以上50μm以下であることがより好ましく、1μm以上30μm以下であることが更に好ましく、10μm以上30μm以下であることが特に好ましい。
粒子の体積平均粒径(Dv)の測定方法としては、例えば、動的光散乱法による濃厚系アナライザー(「FPAR-1000」、大塚電子株式会社製)を用いて測定する方法、及びレーザー回折・散乱式粒度分布測定装置(装置名:マイクロトラックMT3000II、マイクロトラック・ベル株式会社製)を用いて測定する方法等が挙げられる。
本発明の粒子は、必要に応じて、分散剤、添加剤等のその他成分を組み合わせることで、例えば、医薬組成物、機能性食品、及び機能性化粧品等に用いることができる。また、粒子は、各種用途に応じて機能性粒子としてもよい。機能性微粒子としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、即時放出性粒子、徐放性粒子、pH依存放出性粒子、pH非依存放出性粒子、腸溶性コーティング粒子、放出制御コーティング粒子、ナノ結晶含有粒子などが挙げられる。
医薬組成物は、本発明の粒子を含み、必要に応じて、製剤用等の添加物質を含む。添加物質としては、特に制限はなく、目的に応じて適宜選択することができる。添加物質としては、例えば、賦形剤、矯味剤、崩壊剤、流動化剤、吸着剤、滑沢剤、矯臭剤、界面活性剤、香料、着色剤、抗酸化剤、隠蔽剤、静電気防止剤、湿潤剤、分散安定剤などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
賦形剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、乳糖、ショ糖、マンニトール、ブドウ糖、果糖、麦芽糖、エリスリトール、マルチトール、キシリトール、パラチノース、トレハロース、ソルビトール、結晶セルロース、タルク、無水ケイ酸、無水リン酸カルシウム、沈降炭酸カルシウム、ケイ酸カルシウムなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
矯味剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、L-メントール、白糖、D-ソルビトール、キシリトール、クエン酸、アスコルビン酸、酒石酸、リンゴ酸、アスパルテーム、アセスルファムカリウム、ソーマチン、サッカリンナトリウム、グリチルリチン二カリウム、グルタミン酸ナトリウム、5’-イノシン酸ナトリウム、5’-グアニル酸ナトリウムなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
崩壊剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、低置換度ヒドロキシプロピルセルロース、カルメロース、カルメロースカルシウム、カルボキシメチルスターチナトリウム、クロスカルメロースナトリウム、クロスポビドン、ヒドロキシプロピルスターチ、トウモロコシデンプンなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
流動化剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、軽質無水ケイ酸、含水二酸化ケイ素、タルクなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
軽質無水ケイ酸としては、市販品を用いることができる。軽質無水ケイ酸の市販品としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、アドソリダー101(フロイント産業株式会社製:平均細孔径:21nm)などが挙げられる。
吸着剤としては、市販品を用いることができる。吸着剤の市販品としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、商品名:カープレックス(成分名:合成シリカ、DSL.ジャパン株式会社の登録商標)、商品名:アエロジル(日本アエロジル株式会社の登録商標)200(成分名:親水性フュームドシリカ)、商品名:サイリシア(成分名:非晶質二酸化ケイ素、富士シリシア化学株式会社の登録商標)、商品名:アルカマック(成分名:合成ヒドロタルサイト、協和化学株式会社の登録商標)などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
滑沢剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ステアリン酸マグネシウム、ステアリン酸カルシウム、ショ糖脂肪酸エステル、フマル酸ステアリルナトリウム、ステアリン酸、ポリエチレングリコール、タルクなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
矯臭剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、トレハロース、リンゴ酸、マルトース、グルコン酸カリウム、アニス精油、バニラ精油、カルダモン精油などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
界面活性剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、塩化ベンザルコニウム、レシチン、ソルビタン脂肪酸エステル、ポリオキシエチレン硬化ひまし油、ポリオキシエチレンポリオキシプロピレングリコール、ポリオキシエチレンソルビタンモノオレエート、ポリビニルアルコール、モノオレイン酸ソルビタン、モノステアリン酸グリセリン、セスキオレイン酸ソルビタン、モノステアリン酸ソルビタン、モノステアリン酸グリセリル、ポリグリセリン脂肪酸エステル、ポリソルベート80等のポリソルベート;ポリオキシエチレン・ポリオキシプロピレン共重合体;ラウリル硫酸ナトリウムなどが挙げられる。界面活性剤の指標として、親水親油バランスがあるが、本発明においては、親水親油バランスが1以上8以下であることが好ましく、3以上6以下であることがさらに好ましい。その中でも、セスキオレイン酸ソルビタン(親水親油バランス:4)が特に好ましい。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
香料としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、レモン油、オレンジ油、はっか油などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
着色剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、酸化チタン、食用黄色5号、食用青色2号、三二酸化鉄、黄色三二酸化鉄などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
抗酸化剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、アスコルビン酸ナトリウム、L-システイン、亜硫酸ナトリウム、ビタミンEなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
隠蔽剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、酸化チタンなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
静電気防止剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、タルク、酸化チタンなどが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
湿潤剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、ポリソルベート80、ラウリル硫酸ナトリウム、ショ糖脂肪酸エステル、マクロゴール、ヒドロキシプロピルセルロース(HPC)などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
医薬組成物の製剤としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、大腸デリバリー製剤、リピッドマイクロスフェア製剤、ドライエマルション製剤、自己乳化型製剤、ドライシロップ、経鼻投与用粉末製剤、経肺投与用粉末製剤、ワックスマトリックス製剤、ハイドロゲル製剤、高分子ミセル製剤、粘膜付着型製剤、胃内浮遊製剤、リポソーム製剤、固体分散体製剤などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
分散安定剤としては、特に制限は無く、目的に応じて適宜選択することができ、例えば、ポリビニルアルコール、ポリビニルピロリドン、アルギン酸ナトリウム、カルボキシビニルポリマー、結晶セルロース、カルメロースナトリウム、グアガム、ゼラチン、キサンタンガム、デキストリン、ペクチンやステアリン酸などの脂肪酸などが挙げられる。これらは、1種単独で使用してもよいし、2種以上を併用してもよい。
医薬組成物の剤形としては、例えば、錠剤、カプセル剤、坐剤、他の固形の剤形等;鼻内用乃至肺投与用のエアロゾル等;注射用剤、眼内用剤、耳内用剤、経口用剤等の液剤などが挙げられる。
医薬組成物の投与経路としては、特に制限はなく、目的に応じて適宜選択することができ、例えば、経口投与、鼻腔投与、直腸投与、膣投与、皮下投与、静脈内投与、肺投与などが挙げられる。これらの中でも、経口投与が好ましい。
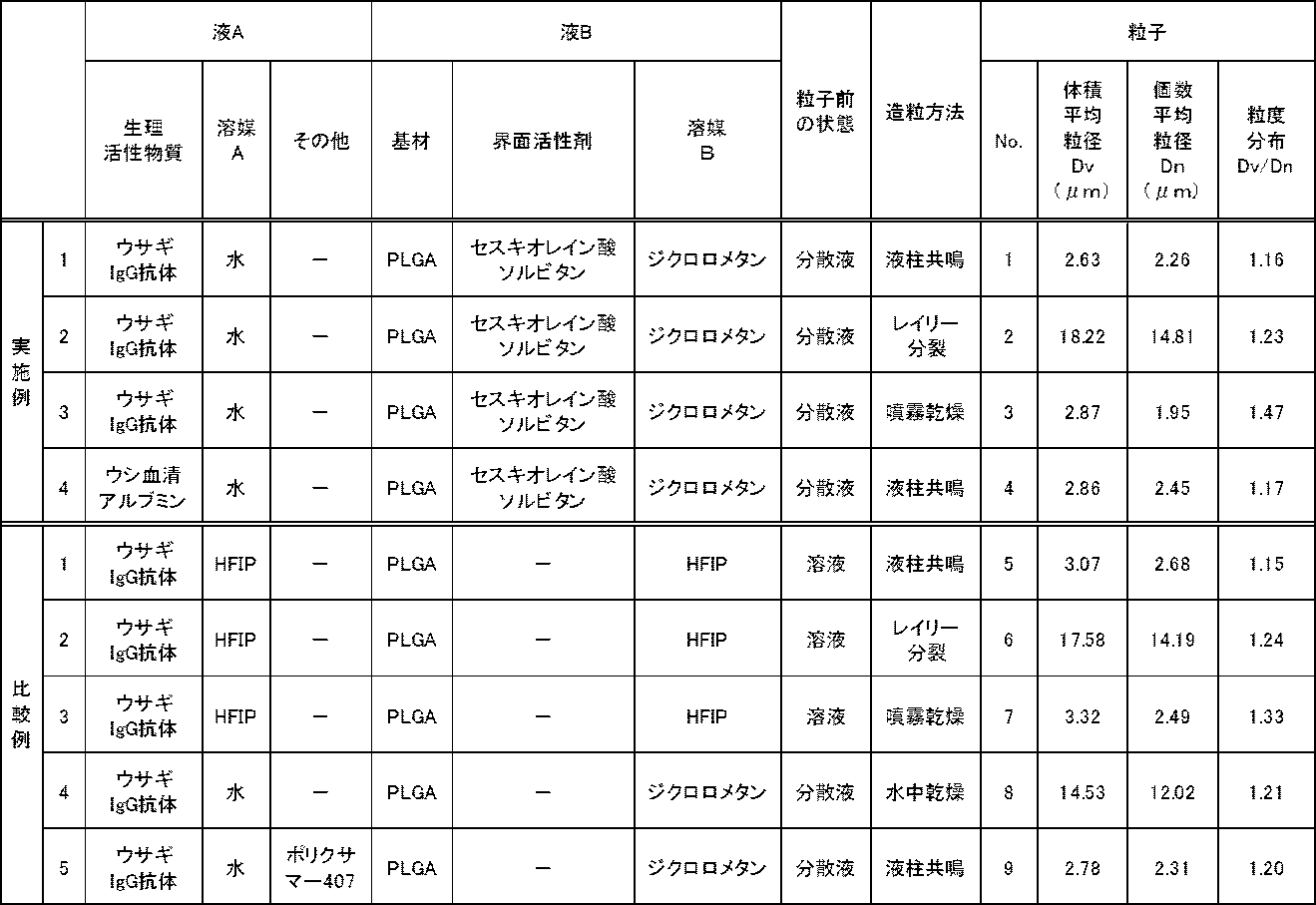
-分散液1の調製-
生理活性物質としてウサギIgG抗体(メルク株式会社製)を、溶媒Aとしての純水に添加し、液A1を調製した。なお、液A1の全量に対する生理活性物質の含有量を1.2mg/mLとなるように調製した。
また、基材としてポリ乳酸グリコール酸(PLGA5050、富士フイルム和光純薬株式会社製)と、界面活性剤としてセスキオレイン酸ソルビタン(SPAN83、東京化成工業株式会社製)とを、溶媒Bとしてのジクロロメタン(富士フイルム和光純薬株式会社製)に添加し、液B1を調製した。なお、液B1の全量に対するポリ乳酸グリコール酸の含有量を12.0mg/mL、セスキオレイン酸ソルビタンの含有量を0.5vol%となるように調製した。
次に、液A1と液B1を、質量比で液A1:液B1=1:9となるように混合し、混合した溶液をホモジナイザー(装置名:sonicstar85、アズワン株式会社製)により、出力90%、10分間ホモジナイズして分散液1(W/Oエマルション)を調製した。
図2の粒子の製造装置において、吐出口の数を液柱共鳴室1つ当たり1つとした図4に示す液滴吐出手段を用いて、得られた分散液1を吐出して液滴を形成し、液滴から溶媒を除去することで、粒子1を造粒した。
得られた粒子1の体積平均粒子径は(Dv)は2.63μm、個数平均粒径(Dn)は2.26μm、粒度分布(Dv/Dn)は1.16であった。なお、これらは、レーザー回折・散乱式粒度分布測定装置(装置名:マイクロトラックMT3000II、マイクロトラック・ベル株式会社製)を用いて測定した。以下同様にして体積平均粒径、個数平均粒径、粒度分布を測定した。測定解析条件、粒子の製造条件は下記の通りである。
[粒度分布の測定条件]
・測定モード:透過モード
・粒子屈折率:1.40
・Set Zero時間:10秒
・測定時間:10秒
[粒子の製造条件]
・吐出口の形状:真円
・吐出口の直径:8μm
・乾燥気流量:乾燥窒素 50L/分
-粒子2の造粒(レイリー分裂)-
実施例1において、使用する液滴吐出手段を特許第4647506号公報に記載のレイリー分裂タイプの吐出手段に変更した以外は、実施例1と同様にして粒子2を造粒した。
得られた粒子2の体積平均粒子径は(Dv)は18.22μm、個数平均粒径(Dn)は14.81μm、粒度分布(Dv/Dn)は1.23であった。なお、粒子製造条件は下記の通りである。
[粒子の製造条件]
・吐出口の形状:真円
・吐出口の直径:30μm
・分散液押し出し圧力:0.15MPa
-粒子3の造粒(噴霧乾燥)-
実施例1において噴霧乾燥法による粒子の製造装置(装置名:有機溶媒用スプレードライヤー、製品型番:GS310、4流体ノズル、藤崎電機株式会社製)を用いた以外は、実施例1と同様にして粒子3を造粒した。
得られた粒子3の体積平均粒子径は(Dv)は2.87μm、個数平均粒径(Dn)は1.95μm、粒度分布(Dv/Dn)は1.47であった。なお、噴霧乾燥条件は下記の通りである。
―噴霧乾燥条件―
・ノズルに対する分散液1の送り量:10mL/分
・乾燥気流量:乾燥窒素:30L/分
・オリフィス圧:1.3kPa
・温度(Inlet):50℃
・温度(Outlet):40℃
実施例1において、生理活性物質をウサギIgG抗体からアルブミン(商品名:アルブミン・ウシ結成由来、製造会社名:富士フイルム和光純薬工業株式会社製)に変更した以外は、実施例1と同様にして、粒子4を造粒した。
得られた粒子4の体積平均粒子径は(Dv)は2.86μm、個数平均粒径(Dn)は2.45μm、粒度分布(Dv/Dn)は1.17であった。
-液C1の調製-
生理活性物質としてウサギIgG抗体(メルク株式会社製)と、基材としてポリ乳酸グリコール酸(PLGA5050、富士フイルム和光純薬株式会社製)をヘキサフルオロ―2-プロパノール(1,1,1,3,3,3-ヘキサフロオロ―2-プロパノール、HFIP、富士フイルム和光純薬工業株式会社製)20mLに添加し、液C1を調製した。なお、液C1の全量に対する生理活性物質の含有量を1.2mg/mL、ポリ乳酸グリコール酸の含有量を12.0mg/mLとなるように調製した。
実施例1において、分散液1を液C1に変更した以外は、実施例1と同様にして粒子5を造粒した。
得られた粒子5の体積平均粒子径は(Dv)は3.07μm、個数平均粒径(Dn)は2.677μm、粒度分布(Dv/Dn)は1.15であった。
実施例2において、分散液1を液C1に変更した以外は、実施例2と同様にして粒子6を造粒した。
得られた粒子6の体積平均粒子径は(Dv)は17.58μm、個数平均粒径(Dn)は14.19μm、粒度分布(Dv/Dn)は1.24であった。
実施例3において、分散液1を液C1に変更した以外は、実施例3と同様にして粒子7を造粒した。
得られた粒子7の体積平均粒子径は(Dv)は3.32μm、個数平均粒径(Dn)は2.49μm、粒度分布(Dv/Dn)は1.33であった。
-分散液2の調製-
生理活性物質としてウサギIgG抗体(メルク株式会社製)を、溶媒Aとしての純水1.0mLに添加し、液A2を調製した。なお、液A2の全量に対する生理活性物質の含有量を1.2mg/mLとなるように調製した。
また、基材としてポリ乳酸グリコール酸(PLGA5050、富士フイルム和光純薬株式会社製)を、溶媒Bとしてのジクロロメタン(富士フイルム和光純薬株式会社製)5.0mLに添加し、液B2を調製した。なお、液B2の全量に対するポリ乳酸グリコール酸の含有量を30.0mg/mLとなるように調製した。
次に、液A1と液B1を、質量比で液A1:液B1=1:5となるように混合し、混合した溶液をホモジナイザー(装置名:ポリトロン、KINEMATICA社製)により、出力90%、10分間ホモジナイズして分散液2(W/Oエマルション)を調製した。
次に、調製した分散液2 10mLを0.4%PVA水溶液100mL中に混合してW/O/Wエマルションを得た。その後、マグネティックスターラーを用いて300rpmの攪拌速度で攪拌することによりジクロロメタンを乾燥させ、固形粒子の生成を目視で確認した後、凍結乾燥させ粒子8を造粒した。
得られた粒子8の体積平均粒子径は(Dv)は14.53μm、個数平均粒径(Dn)は12.02μm、粒度分布(Dv/Dn)は1.21であった。
-分散液3の調製-
生理活性物質としてウサギIgG抗体(メルク株式会社製)と、界面活性剤としてポリクサマー407(プルロニックF-127、シグマアルドリッチ社製)とを、溶媒Aとしての純水に添加し、液A1を調製した。なお、液A1の全量に対する生理活性物質の含有量を1.2mg/mL、ポリクサマー407の含有量を0.5vol%となるように調製した。
また、基材としてポリ乳酸グリコール酸(PLGA5050、富士フイルム和光純薬株式会社製)を、溶媒Bとしてのジクロロメタン(富士フイルム和光純薬株式会社製)に添加し、液B1を調製した。なお、液B1の全量に対するポリ乳酸グリコール酸の含有量を12.0mg/mLとなるように調製した。
次に、液A1と液B1を、質量比で液A1:液B1=1:9となるように混合し、混合した溶液をホモジナイザー(装置名:sonicstar85、アズワン株式会社製)により、出力90%、10分間ホモジナイズして分散液3(W/Oエマルション)を調製した。
実施例1において、分散液1を分散液3に変更した以外は、実施例1と同様にして粒子9を造粒した。
得られた粒子9の体積平均粒子径は(Dv)は2.78μm、個数平均粒径(Dn)は2.31μm、粒度分布(Dv/Dn)は1.20であった。
溶出試験は以下の手順で行った。粒子(粒子1~9)毎に、1.5mLマイクロチューブ内に粒子を3mg、水1mlを入れ、遠心分離(5、000rpm)を10分間行い、上澄み液500μLを回収し、0日目液とした。なお、遠心分離機はMicrofuge16, BeckmanCoulter社製を使用した。
次に、上記の操作後のマイクロチューブに水を500μL加えて、100回/分で1日間、2日間、連続で振とう(デジタルシェーカー、フロントラボ社製)させた。1日間、2日間振とうさせた後、それぞれの溶液を回収し、1日目液、2日目液とした。
製造した粒子1.0mgを0.1molに調製した水酸化ナトリウム水溶液1.0mLに入れて、1日静置させ、粒子を完全に溶解させる。溶解液を用いて、粒子中のIgGの封入率(%)を総タンパク質定量キット(micro-BCA、カタログ番号KY-2020、アプロサイエンス社製)によるBCA法により測定した。測定方法は取扱説明書に記載の通り実施した。封入率(%)は以下の数式に基づき算出した。結果を下記表1に示す。
封入率=(粒子中に存在したIgG量/IgGの仕込み量)×100(%)
前記溶出試験で得られた0日目液、1日目液と2日目液とを前記BCA法を用いて、生理活性物質の経時における溶出量を測定した。
経時における溶出率は以下の数式に基づき算出した。
溶出率(%)=(各日での溶液中のIgG量/粒子中に存在したIgG量)×100(%)
IgGは分子量が約15kDaのタンパク質であり、機能の発現には構造を保持していることが必要である。有機溶媒や界面活性剤との接触、乾燥、溶出試験中の経時変化により、構造が失われている恐れがあるので、IgGの構造を認識して検出できる手法として、ELISAを用いた。
<<手順>>
以下のバッファーを作製した
・固相化buffer:NaHCO3/Na2CO3 0.1 M/0.1 M pH 9.6
・Wash buffer:PBS(-)に0.05% tween20を溶かしたもの
・Blocking buffer:PBS(-)に0.05% Tween20, 5% BSAを溶かしたもの
-一日目-
・Anit-rabbit goat IgG(メルク社製)を固相化 bufferで10μg/mLに希釈し
・各wellに入れて冷蔵庫内で一晩静置した。
-二日目-
・wash buffer 200μLで各wellをで3回洗浄した
・Blocking bufferを各wellに50 μL入れて1時間静置した。
・wash buffer 200μLで各wellをで3回洗浄した
・測定試料と希釈系列を入れて1時間静置した。
・wash buffer 200μLで各wellをで3回洗浄した
・HRP-anti rabbit antibody(メルク社製)300ng/mLを各wellに50μL入れて1時間静置した。
・wash buffer 200μLで各wellをで3回洗浄した
・発色基質/過酸化水素溶液を入れた
・発色過程を652nmの波長でモニターし、適切なところで、反応停止剤のH2SO4溶液を加えた。
・450 nmの吸光度を測定した。
結果を下記表1に示す。表1に示す活性の数値は、溶出試験に用いた粒子中の抗体量における活性試験(ポジティブコントロール)の活性量を100%とした時の、各粒子における0日目液、1日目液、及び2日目液の液中の抗体活性率である。
なお、比較例4において、活性率(%)が実施例よりも明らかに大きくなっているのは、封入率(%)が低く、溶出率(%)が高いことから、粒子中の生理活性物質(抗体)が0日目の時点で大量に溶解し、抗体を徐放できていないことを示唆している。
<1> 生理活性物質が溶解した液Aと、基材及び界面活性剤が溶解した液Bと、を用いて分散液を調製する調製工程と、
分散液を気体中に吐出して粒子を形成する造粒工程と、を含むことを特徴とする粒子の製造方法である。
<2> 前記分散液が、W/Oエマルションである、前記<1>に記載の粒子の製造方法である。
<3> 前記界面活性剤の親水親油バランスが、1以上8以下である、前記<1>から<2>のいずれかに記載の粒子の製造方法である。
<4> 前記界面活性剤の親水親油バランスが、3以上6以下である、前記<1>から<3>のいずれかに記載の粒子の製造方法である。
<5> 前記界面活性剤が、セスキオレイン酸ソルビタンである、前記<4>に記載の粒子の製造方法である。
<6> 前記粒子が、徐放性粒子である、前記<1>から<5>のいずれかに記載の粒子の製造方法である。
<7> 前記基材が、生分解性樹脂を含む、前記<1>から<6>のいずれかに記載の粒子の製造方法である。
<8> 前記生分解性樹脂が、ポリ乳酸、及びポリ乳酸グリコール酸共重合体の少なくともいずれかを含む、前記<7>に記載の粒子の製造方法である。
<9> 前記生理活性物質が、生体高分子化合物である、前記<1>から<8>のいずれかに記載の粒子の製造方法である。
<10> 前記生体高分子化合物が、抗体である、前記<9>に記載の粒子の製造方法である。
<11> 生理活性物質が溶解した液Aと、基材及び界面活性剤が溶解した液Bと、を用いて分散液を調製する調製手段と、
分散液を気体中に吐出して粒子を形成する造粒手段と、を有することを特徴とする粒子の製造装置である。
Claims (9)
- 生理活性物質が溶解した液Aと、基材及び界面活性剤が溶解した液Bと、を用いて分散液を調製する調製工程と、
分散液を用いて粒子を形成する造粒工程と、を含み、
前記生理活性物質が生体高分子化合物であり、
前記生体高分子化合物が抗体及びタンパク質から選択されるものであり、
前記基材が脂溶性であり、
前記分散液が、W/Oエマルションであることを特徴とする粒子の製造方法。 - 前記界面活性剤の親水親油バランスが、1以上8以下である、請求項1に記載の粒子の製造方法。
- 前記界面活性剤の親水親油バランスが、3以上6以下である、請求項2に記載の粒子の製造方法。
- 前記界面活性剤が、セスキオレイン酸ソルビタンである、請求項1から3のいずれかに記載の粒子の製造方法。
- 前記粒子が、徐放性粒子である、請求項1から4のいずれかに記載の粒子の製造方法。
- 前記基材が、生分解性樹脂を含む、請求項1から5のいずれかに記載の粒子の製造方法。
- 前記生分解性樹脂が、ポリ乳酸、及びポリ乳酸グリコール酸共重合体の少なくともいずれかを含む、請求項6に記載の粒子の製造方法。
- 前記造粒工程は、前記分散液を液滴化する工程と、前記液滴化した分散液を乾燥する工程とを含み、
前記造粒工程で、液滴を搬送気流中に吐出することで前記液滴から溶媒を気化させて前記粒子を造粒する、請求項1から7のいずれかに記載の粒子の製造方法。 - 振動により前記分散液を吐出して前記液滴を形成する、請求項8に記載の粒子の製造方法。
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020045858A JP7600528B2 (ja) | 2020-03-16 | 2020-03-16 | 粒子の製造方法 |
| EP21714702.4A EP4121015B1 (en) | 2020-03-16 | 2021-03-11 | Method for producing particles |
| US17/906,326 US12453704B2 (en) | 2020-03-16 | 2021-03-11 | Method for producing particles |
| CN202180020709.6A CN115297849A (zh) | 2020-03-16 | 2021-03-11 | 用于生产颗粒的方法 |
| PCT/JP2021/009698 WO2021187289A1 (en) | 2020-03-16 | 2021-03-11 | Method for producing particles |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2020045858A JP7600528B2 (ja) | 2020-03-16 | 2020-03-16 | 粒子の製造方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| JP2021147329A JP2021147329A (ja) | 2021-09-27 |
| JP7600528B2 true JP7600528B2 (ja) | 2024-12-17 |
Family
ID=75252786
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2020045858A Active JP7600528B2 (ja) | 2020-03-16 | 2020-03-16 | 粒子の製造方法 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US12453704B2 (ja) |
| EP (1) | EP4121015B1 (ja) |
| JP (1) | JP7600528B2 (ja) |
| CN (1) | CN115297849A (ja) |
| WO (1) | WO2021187289A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN115666535B (zh) | 2020-05-20 | 2024-06-18 | 株式会社理光 | 含有脂质纳米颗粒的颗粒及其生产方法 |
| JP2023040388A (ja) * | 2021-09-10 | 2023-03-23 | 株式会社三洋物産 | 遊技機 |
| JP7815659B2 (ja) * | 2021-09-10 | 2026-02-18 | 株式会社三洋物産 | 遊技機 |
| JP2023040390A (ja) * | 2021-09-10 | 2023-03-23 | 株式会社三洋物産 | 遊技機 |
| JP2023040389A (ja) * | 2021-09-10 | 2023-03-23 | 株式会社三洋物産 | 遊技機 |
| JP7497718B2 (ja) * | 2021-12-16 | 2024-06-11 | 株式会社三洋物産 | 遊技機 |
| JP7497719B2 (ja) * | 2021-12-16 | 2024-06-11 | 株式会社三洋物産 | 遊技機 |
| JP7497720B2 (ja) * | 2021-12-16 | 2024-06-11 | 株式会社三洋物産 | 遊技機 |
| CN114767633B (zh) * | 2022-04-07 | 2023-03-31 | 郑州大学第一附属医院 | 含抗乳腺癌药物他莫昔芬的固体分散体、制备方法及制剂 |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004083575A (ja) | 2002-06-25 | 2004-03-18 | Takeda Chem Ind Ltd | 徐放性組成物の製造方法 |
| WO2015172149A1 (en) | 2014-05-09 | 2015-11-12 | Yale University | Hyperbranched polyglycerol-coated particles and methods of making and using thereof |
| WO2016183209A1 (en) | 2015-05-11 | 2016-11-17 | Yale University | Topical formulation of hyperbranched polymer-coated particles |
| JP2019521979A (ja) | 2016-06-13 | 2019-08-08 | アセンディア ファーマシューティカルズ,エルエルシー | カルベジロール分散系の非経口徐放送達 |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH10511957A (ja) * | 1995-01-05 | 1998-11-17 | ザ ボード オブ リージェンツ オブ ザ ユニヴァーシティ オブ ミシガン | 表面改質ナノ微粒子並びにその製造及び使用方法 |
| ATE272394T1 (de) * | 1996-10-31 | 2004-08-15 | Takeda Chemical Industries Ltd | Zubereitung mit verzögerter freisetzung |
| PT1532985T (pt) * | 2002-06-25 | 2017-01-20 | Takeda Pharmaceuticals Co | Processo de produção de uma composição de libertação sustentada |
| JP4647506B2 (ja) | 2006-01-27 | 2011-03-09 | 株式会社リコー | 粒子特にトナー粒子の製造方法、トナー粒子の製造装置及びトナー |
| KR100722607B1 (ko) * | 2006-05-11 | 2007-05-28 | 주식회사 펩트론 | 분산성 및 주사 투여능이 향상된 서방성 미립구의 제조방법 |
| JP5055154B2 (ja) | 2007-03-20 | 2012-10-24 | 株式会社リコー | トナーの製造方法、トナーの製造装置及びトナー |
| JP2013538855A (ja) * | 2010-09-30 | 2013-10-17 | エボニック コーポレイション | 低い残留有機溶剤の微粒子を製造するためのエマルション法 |
| EP3125871B1 (en) * | 2014-03-31 | 2020-10-21 | Pharmathen S.A. | Preparation of peptide loaded plga microspheres with controlled release characteristics |
| US11918695B2 (en) | 2014-05-09 | 2024-03-05 | Yale University | Topical formulation of hyperbranched polymer-coated particles |
| JP6582283B2 (ja) * | 2015-01-26 | 2019-10-02 | 宮崎県 | 油中ナノ粒子分散体の製造方法 |
| JP6971043B2 (ja) | 2016-03-04 | 2021-11-24 | 株式会社リコー | 微粒子の製造方法 |
| JP7546344B2 (ja) | 2018-02-09 | 2024-09-06 | 株式会社リコー | 粒子の製造方法、粒子の製造装置、及び粒子 |
| CN110123634A (zh) | 2018-02-09 | 2019-08-16 | 株式会社理光 | 颗粒的制造方法,颗粒的制造装置,以及颗粒 |
| JP7092974B2 (ja) | 2018-03-26 | 2022-06-29 | 株式会社リコー | 樹脂微粒子の製造方法、及び樹脂微粒子の製造装置 |
| JP7192232B2 (ja) | 2018-03-30 | 2022-12-20 | 株式会社リコー | 医薬品用粒子の製造装置、及び医薬品用粒子の製造方法 |
| US20220409539A1 (en) * | 2019-12-30 | 2022-12-29 | Fraunhofer Usa Inc. | Particles for multi-dose delivery |
-
2020
- 2020-03-16 JP JP2020045858A patent/JP7600528B2/ja active Active
-
2021
- 2021-03-11 WO PCT/JP2021/009698 patent/WO2021187289A1/en not_active Ceased
- 2021-03-11 US US17/906,326 patent/US12453704B2/en active Active
- 2021-03-11 EP EP21714702.4A patent/EP4121015B1/en active Active
- 2021-03-11 CN CN202180020709.6A patent/CN115297849A/zh active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2004083575A (ja) | 2002-06-25 | 2004-03-18 | Takeda Chem Ind Ltd | 徐放性組成物の製造方法 |
| WO2015172149A1 (en) | 2014-05-09 | 2015-11-12 | Yale University | Hyperbranched polyglycerol-coated particles and methods of making and using thereof |
| WO2016183209A1 (en) | 2015-05-11 | 2016-11-17 | Yale University | Topical formulation of hyperbranched polymer-coated particles |
| JP2019521979A (ja) | 2016-06-13 | 2019-08-08 | アセンディア ファーマシューティカルズ,エルエルシー | カルベジロール分散系の非経口徐放送達 |
Also Published As
| Publication number | Publication date |
|---|---|
| US20230106801A1 (en) | 2023-04-06 |
| JP2021147329A (ja) | 2021-09-27 |
| EP4121015B1 (en) | 2025-09-24 |
| WO2021187289A1 (en) | 2021-09-23 |
| EP4121015A1 (en) | 2023-01-25 |
| CN115297849A (zh) | 2022-11-04 |
| US12453704B2 (en) | 2025-10-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7600528B2 (ja) | 粒子の製造方法 | |
| US20210283057A1 (en) | Sustained-release particles and production method thereof | |
| EP3423039B1 (en) | Method for producing particles | |
| EP3524233B1 (en) | Particle-producing method and particle-producing apparatus | |
| EP4335435A1 (en) | Sustained releasing particle and method of producing sustained releasing particle | |
| KR102755855B1 (ko) | 입자의 제조 방법, 및 이 방법에 의해 제조된 입자 및 의약 | |
| JP7546344B2 (ja) | 粒子の製造方法、粒子の製造装置、及び粒子 | |
| JP7503781B2 (ja) | 粒子の製造方法、並びに、それにより製造された粒子及び医薬 | |
| US20220273575A1 (en) | Particles, pharmaceutical composition, and method for producing particles | |
| CN115666535B (zh) | 含有脂质纳米颗粒的颗粒及其生产方法 | |
| US20260076911A1 (en) | Particles, method for producing particles, and pharmaceutical composition | |
| JP2024039591A (ja) | 徐放性粒子及びその製造方法 | |
| JP2026055749A (ja) | 粒子及びその製造方法、並びに医薬組成物 | |
| JP2025173238A (ja) | 粒子、試薬、医薬組成物、粉末吸入剤及び粒子の製造方法 | |
| KR102694684B1 (ko) | 미립자의 제조 장치 및 미립자의 제조 방법 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| RD03 | Notification of appointment of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7423 Effective date: 20220601 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20230116 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20231003 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231129 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240213 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240411 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20240716 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240816 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241105 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241118 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7600528 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |