JP7601362B2 - 純粋な駆虫組成物および関連する方法 - Google Patents
純粋な駆虫組成物および関連する方法 Download PDFInfo
- Publication number
- JP7601362B2 JP7601362B2 JP2019564903A JP2019564903A JP7601362B2 JP 7601362 B2 JP7601362 B2 JP 7601362B2 JP 2019564903 A JP2019564903 A JP 2019564903A JP 2019564903 A JP2019564903 A JP 2019564903A JP 7601362 B2 JP7601362 B2 JP 7601362B2
- Authority
- JP
- Japan
- Prior art keywords
- nematicidal
- crystals
- item
- cry5b
- crystal protein
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
- A61K35/741—Probiotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/66—Microorganisms or materials therefrom
- A61K35/74—Bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/164—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/10—Anthelmintics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/32—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Bacillus (G)
- C07K14/325—Bacillus thuringiensis crystal peptides, i.e. delta-endotoxins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Veterinary Medicine (AREA)
- General Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Molecular Biology (AREA)
- Gastroenterology & Hepatology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Biochemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
Description
本発明は、米国保健福祉省(HHS)国立衛生研究所(NIH)により与えられたグラント番号NIAID 5R01AI056189-13、および米国農務省(USDA)国立食品農業研究所(NIFA)により与えられたグラント番号NIFA 2016-67015-24861の下、政府の助成を受けてなされた。政府は本発明において一定の権利を有する。
本願は、その内容が引用により本書の一部とされる2017年5月23日出願の米国仮特許出願第62/510081号の優先権を主張する。
(a)単一種の殺線虫結晶タンパク質を発現するように組換えられた芽胞不形成形態の宿主細菌を増殖させること;ここで、該芽胞不形成宿主細菌は、単一種の殺線虫結晶タンパク質から形成される天然の生物活性殺線虫結晶を産生し、該宿主細菌は増殖培地中で増殖され、場合により、該芽胞不形成宿主細菌は該天然の生物活性殺線虫結晶を該増殖培地中に放出する;
および
(b)該天然の生物活性殺線虫結晶を単離および濃縮して、単離された天然の生物活性殺線虫結晶を形成すること
を含む、医薬組成物の製造方法を提供する。
(a)単一種の殺線虫結晶タンパク質を発現するように組換えられた芽胞不形成形態の宿主細菌を増殖させること;ここで、該芽胞不形成宿主細菌は、単一種の殺線虫結晶タンパク質から形成される天然の生物活性殺線虫結晶を産生する;
(b)該増殖した芽胞不形成宿主細菌を、抗菌化合物への暴露により不活化すること;
(c)該不活化した芽胞不形成宿主細菌をホモジナイズして、細菌溶解物を形成すること;および
(d)該細菌溶解物中の天然の生物活性殺線虫結晶を濃縮して、単離された天然の生物活性殺線虫結晶を形成すること
を含む、医薬組成物の製造方法を提供する。
本発明の実施形態をさらに記載する:
[項1]
単一種の殺線虫結晶タンパク質から形成された、単離された天然の生物活性殺線虫結晶を含む医薬組成物において、該結晶タンパク質は芽胞不形成形態の宿主細菌によって産生され、該医薬組成物は、細菌芽胞、または結晶の形態の殺線虫結晶タンパク質以外の宿主細菌タンパク質を実質的に含まない、医薬組成物。
[項2]
ヒト対象への経口投与のために適当な賦形剤をさらに含む、上記項1に記載の医薬組成物。
[項3]
宿主細菌がBacillus種である、上記項1に記載の医薬組成物。
[項4]
宿主細菌がBacillus thuringiensis(Bt)である、上記項1に記載の医薬組成物。
[項5]
宿主細菌がE. coliまたはP. fluorescens種である、上記項1に記載の医薬組成物。
[項6]
芽胞不形成宿主細菌が、前記天然の生物活性殺線虫結晶が該細菌のサイトゾル中に捕らえられるように、芽胞形成の欠失をもたらす遺伝子変異を持つよう遺伝子組換えされている、上記項1に記載の医薬組成物。
[項7]
芽胞形成の欠失をもたらす遺伝子変異が、下記のものからなる群から選択される1つまたはそれ以上の遺伝子の欠失または不活性化である、上記項6に記載の医薬組成物:kinA、kinB、spo0A、spo0B、spo0E、spo0F、spo0J、spo0M spoIIB、spoIID、spoIIE、spoIIF、spoIIG、spoIIL、spoIIM、spoIIIA、spoIIIB、spoIIIE、spoIVA、spoIVC、spoIVD、spoVG、spoVK、spoVL、spoVM、spoVN、spoVP、spoVQ、spoVID、σH、σF、σE、σG、およびσK。
[項8]
芽胞形成の欠失をもたらす遺伝子変異が、spo0A遺伝子の欠失または不活性化である、上記項6に記載の医薬組成物。
[項9]
宿主細菌が、前記単一種の殺線虫結晶タンパク質を芽胞不形成特異的プロモーターの制御下に発現するように遺伝子組換えされている、上記項1に記載の医薬組成物。
[項10]
芽胞不形成特異的プロモーターが、Cry3A、GerA、GNAT、またはTadAプロモーターである、上記項9に記載の医薬組成物。
[項11]
単一種の殺線虫結晶タンパク質が、Cry5B、Cry5C、Cry5D、Cry6A、Cry13A、Cry14A、Cry21A、Cry21B、Cry55B、ならびにそれらのバリアントおよびトランケーションからなる群から選択される、上記項1に記載の医薬組成物。
[項12]
殺線虫結晶タンパク質が、Cry5Bまたはそのバリアントもしくはフラグメントである、上記項11に記載の医薬組成物。
[項13]
殺線虫結晶タンパク質が、Cry5BバリアントSer407Cysである、上記項12に記載の医薬組成物。
[項14]
単離された天然の生物活性殺線虫結晶の形態の第2の結晶タンパク質をさらに含み、該結晶は該第2の結晶タンパク質のみから形成される、上記項1に記載の医薬組成物。
[項15]
医薬組成物が、単離された天然の生物活性殺線虫結晶を少なくとも95%の含量で含む、上記項1~14のいずれかに記載の医薬組成物。
[項16]
単離された天然の生物活性殺線虫結晶が、経口投与で利用可能な投与形態にある、上記項1~15のいずれかに記載の医薬組成物。
[項17]
医薬組成物が、乾燥粉末形態であり、医薬用カプセルに封入されている、上記項1~16のいずれかに記載の医薬組成物。
[項18]
(a)単一種の殺線虫結晶タンパク質を発現するように遺伝子組換えされた芽胞不形成形態の宿主細菌を増殖させること;ここで、該芽胞不形成宿主細菌は、単一種の殺線虫結晶タンパク質から形成される天然の生物活性殺線虫結晶を産生し、該宿主細菌は増殖培地中で増殖され、場合により、該芽胞不形成宿主細菌は該天然の生物活性殺線虫結晶を該増殖培地中に放出する;
および
(b)該天然の生物活性殺線虫結晶を単離および濃縮して、単離された天然の生物活性殺線虫結晶を形成すること
を含む、医薬組成物の製造方法。
[項19]
宿主細菌がBacillus種である、上記項18に記載の方法。
[項20]
宿主細菌がBacillus thuringiensis(Bt)である、上記項18に記載の方法。
[項21]
宿主細菌がE. coliまたはP. fluorescens種である、上記項18に記載の方法。
[項22]
芽胞不形成宿主細菌が、前記天然の生物活性殺線虫結晶が該細菌のサイトゾル中に捕らえられるように、芽胞形成の欠失をもたらす遺伝子変異を持つよう遺伝子組換えされている、上記項18に記載の方法。
[項23]
芽胞形成の欠失をもたらす遺伝子変異が、下記のものからなる群から選択される1つまたはそれ以上の遺伝子の欠失または不活性化である、上記項22に記載の方法:kinA、kinB、spo0A、spo0B、spo0E、spo0F、spo0J、spo0M spoIIB、spoIID、spoIIE、spoIIF、spoIIG、spoIIL、spoIIM、spoIIIA、spoIIIB、spoIIIE、spoIVA、spoIVC、spoIVD、spoVG、spoVK、spoVL、spoVM、spoVN、spoVP、spoVQ、spoVID、σH、σF、σE、σG、およびσK。
[項24]
芽胞形成の欠失をもたらす遺伝子変異が、spo0A遺伝子の欠失または不活性化である、上記項22に記載の方法。
[項25]
宿主細菌が、単一種の殺線虫結晶タンパク質を芽胞不形成特異的プロモーターの制御下に発現するように遺伝子組換えされている、上記項18に記載の方法。
[項26]
芽胞不形成特異的プロモーターが、Cry3A、GerA、GNAT、またはTadAプロモーターである、上記項25に記載の方法。
[項27]
単一種の殺線虫結晶タンパク質が、Cry5B、Cry5C、Cry5D、Cry6A、Cry13A、Cry14A、Cry21A、Cry21B、Cry55B、ならびにそれらのバリアントおよびトランケーションからなる群から選択される、上記項18に記載の方法。
[項28]
殺線虫結晶タンパク質が、Cry5Bまたはそのバリアントもしくはフラグメントである、上記項27に記載の方法。
[項29]
殺線虫結晶タンパク質が、Cry5BバリアントSer407Cysである、上記項28に記載の方法。
[項30]
前記芽胞不形成宿主細菌を、該宿主細菌を不活化するために抗菌化合物に暴露するステップをさらに含む、上記項18に記載の方法。
[項31]
抗菌化合物が沃素である、上記項30に記載の方法。
[項32]
抗菌化合物が抗生物質医薬である、上記項30に記載の方法。
[項33]
抗菌化合物がβ-ラクタム抗生物質である、上記項30に記載の方法。
[項34]
抗菌化合物が、テルペン、ヘキサンおよびホルムアルデヒドからなる群から選択される有機溶媒である、上記項30に記載の方法。
[項35]
抗菌化合物がテルペンである、上記項34に記載の方法。
[項36]
テルペンが、チモール、オイゲノール、ゲラニオール、カルバクロールおよびシトラールまたはそれらの組み合わせからなる群から選択される、上記項35に記載の方法。
[項37]
テルペンがカルバクロールである、上記項36に記載の方法。
[項38]
抗菌化合物がヘキサンである、上記項34に記載の方法。
[項39]
前記殺線虫結晶タンパク質から前記抗菌化合物、可溶性細胞成分、脂質および細胞壁デブリを抽出するために、前記不活化された宿主細菌に食用油を加えるステップをさらに含む、上記項30に記載の方法。
[項40]
食用油がトウモロコシ油である、上記項39に記載の方法。
[項41]
前記殺線虫結晶タンパク質から前記抗菌化合物を抽出するために、前記不活化された宿主細菌に有機溶媒を加えるステップをさらに含む、上記項30に記載の方法。
[項42]
有機溶媒がヘキサンである、上記項41に記載の方法。
[項43]
ヘキサンが、不活化宿主細菌に50% v/vまで加えられる、上記項42に記載の方法。
[項44]
有機溶媒と不活化宿主細菌の混合物を遠心分離して前記殺線虫結晶タンパク質をペレット化するステップをさらに含む、上記項43に記載の方法。
[項45]
前記不活化された宿主細菌をホモジナイズして、天然の生物活性殺線虫結晶を含む細菌溶解物を形成するステップをさらに含む、上記項30に記載の方法。
[項46]
前記細菌溶解物を濃縮するステップをさらに含む、上記項45に記載の方法。
[項47]
細菌溶解物を濃縮するステップが、遠心分離、限外濾過および透析からなる群から選択される、上記項46に記載の方法。
[項48]
前記単離された天然の生物活性殺線虫結晶を、経口的に利用可能な投与形態に製剤化するステップをさらに含む、上記項18に記載の方法。
[項49]
製剤化ステップが、単離された天然の生物活性殺線虫結晶を凍結乾燥または噴霧乾燥することを含む、上記項48に記載の方法。
[項50]
製剤化ステップが、単離された天然の生物活性殺線虫結晶を医薬用カプセルに充填することを含む、上記項48に記載の方法。
[項51]
(a)単一種の殺線虫結晶タンパク質を発現するように組換えられた芽胞不形成形態の宿主細菌を増殖させること;ここで、該芽胞不形成宿主細菌は、単一種の殺線虫結晶タンパク質から形成される天然の生物活性殺線虫結晶を産生する;
(b)該増殖した芽胞不形成宿主細菌を、抗菌化合物への暴露により不活化すること;
(c)該不活化した芽胞不形成宿主細菌をホモジナイズして、細菌溶解物を形成すること;および
(d)該細菌溶解物中の天然の生物活性殺線虫結晶を濃縮して、単離された天然の生物活性殺線虫結晶を形成すること
を含む、医薬組成物の製造方法。
[項52]
前記増殖した芽胞不形成宿主細菌を不活化の前に濃縮するステップをさらに含む、上記項51に記載の方法。
[項53]
宿主細菌がBacillus種である、上記項51に記載の方法。
[項54]
宿主細菌がBacillus thuringiensis(Bt)である、上記項51に記載の方法。
[項55]
宿主細菌がE. coliまたはP. fluorescens種である、上記項51に記載の方法。
[項56]
芽胞不形成宿主細菌が、前記天然の生物活性殺線虫結晶が該細菌のサイトゾル中に捕らえられるように、芽胞形成の欠失をもたらす遺伝子変異を持つよう遺伝子組換えされている、上記項51に記載の方法。
[項57]
芽胞形成の欠失をもたらす遺伝子変異が、下記のものからなる群から選択される1つまたはそれ以上の遺伝子の欠失または不活性化である、上記項56に記載の方法:kinA、kinB、spo0A、spo0B、spo0E、spo0F、spo0J、spo0M spoIIB、spoIID、spoIIE、spoIIF、spoIIG、spoIIL、spoIIM、spoIIIA、spoIIIB、spoIIIE、spoIVA、spoIVC、spoIVD、spoVG、spoVK、spoVL、spoVM、spoVN、spoVP、spoVQ、spoVID、σH、σF、σE、σG、およびσK。
[項58]
芽胞形成の欠失をもたらす遺伝子変異が、spo0A遺伝子の欠失または不活性化である、上記項56に記載の方法。
[項59]
宿主細菌が、前記単一種の殺線虫結晶タンパク質を芽胞不形成特異的プロモーターの制御下に発現するように遺伝子組換えされている、上記項56に記載の方法。
[項60]
芽胞不形成特異的プロモーターが、Cry3A、GerA、GNAT、またはTadAプロモーターである、上記項59に記載の方法。
[項61]
単一種の細胞質結晶タンパク質が、Cry5B、Cry6A、Cry5C、Cry5D、Cry13A、Cry14A、Cry21A、Cry21B、Cry55B、ならびにそれらのバリアントおよびトランケーションからなる群から選択される、上記項51に記載の方法。
[項62]
殺線虫結晶タンパク質が、Cry5Bまたはそのバリアントもしくはフラグメントである、上記項61に記載の方法。
[項63]
殺線虫結晶タンパク質が、Cry5BバリアントSer407Cysである、上記項62に記載の方法。
[項64]
抗菌化合物が沃素である、上記項51に記載の方法。
[項65]
抗菌化合物が抗生物質医薬である、上記項51に記載の方法。
[項66]
抗菌化合物がβ-ラクタム抗生物質である、上記項51に記載の方法。
[項67]
抗菌化合物が、テルペン、ヘキサンおよびホルムアルデヒドからなる群から選択される有機溶媒である、上記項51に記載の方法。
[項68]
抗菌化合物がテルペンである、上記項67に記載の方法。
[項69]
テルペンが、チモール、オイゲノール、ゲラニオール、カルバクロールおよびシトラールまたはそれらの組み合わせからなる群から選択される、上記項68に記載の方法。
[項70]
テルペンがカルバクロールである、上記項69に記載の方法。
[項71]
抗菌化合物がヘキサンである、上記項70に記載の方法。
[項72]
前記不活化された宿主細菌から前記抗菌化合物および細胞壁デブリを抽出するステップをさらに含む、上記項51に記載の方法。
[項73]
前記殺線虫結晶タンパク質から前記不活化剤を抽出するために、前記不活化された宿主細菌に食用油を加えるステップをさらに含む、上記項51に記載の方法。
[項74]
食用油がトウモロコシ油である、上記項73に記載の方法。
[項75]
前記殺線虫結晶タンパク質から前記抗菌化合物、可溶性細胞成分、脂質および細胞壁デブリを抽出するために、前記不活化された宿主細菌に有機溶媒を加えるステップをさらに含む、上記項51に記載の方法。
[項76]
有機溶媒がヘキサンである、上記項75に記載の方法。
[項77]
ヘキサンが、不活化宿主細菌に50% v/vまで加えられる、上記項76に記載の方法。
[項78]
有機溶媒と不活化宿主細菌の混合物を遠心分離して前記殺線虫結晶タンパク質をペレット化するステップをさらに含む、上記項75に記載の方法。
[項79]
前記単離された天然の生物活性殺線虫結晶を、経口的に利用可能な投与形態に製剤化するステップをさらに含む、上記項51~78のいずれかに記載の方法。
[項80]
製剤化ステップが、前記単離された天然の生物活性殺線虫結晶を凍結乾燥または噴霧乾燥することを含む、上記項79に記載の方法。
[項81]
製剤化ステップが、前記単離され精製された天然の生物活性殺線虫結晶を医薬用カプセルに充填するステップことを含む、上記項79に記載の方法。
[項82]
対象において寄生虫または蠕虫感染を処置するための方法であって、
単一種の殺線虫結晶タンパク質から形成される、単離された天然の生物活性殺線虫結晶を含む医薬組成物を処置有効量で対象に投与することを含み、ここで、該医薬組成物は、細菌芽胞、または結晶の形態の殺線虫結晶タンパク質以外の宿主細菌タンパク質を実質的に含まない、方法。
[項83]
殺線虫結晶タンパク質が、Cry5B、Cry5C、Cry5D、Cry6A、Cry13A、Cry14A、Cry21A、Cry21B、Cry55B、ならびにそれらのバリアントおよびトランケーションからなる群から選択される、上記項82に記載の方法。
[項84]
殺線虫結晶タンパク質がCry5Bである、上記項82に記載の方法。
[項85]
殺線虫結晶タンパク質が、Cry5BバリアントSer407Cysである、上記項82に記載の方法。
[項86]
医薬組成物が、単離された天然の生物活性殺線虫結晶の形態の第2の結晶タンパク質をさらに含み、該結晶は該第2の結晶タンパク質のみから形成される、上記項82に記載の方法。
[項87]
医薬組成物が、単離された天然の生物活性殺線虫結晶を少なくとも約95%の含量で含む、上記項82に記載の方法。
[項88]
医薬組成物が、乾燥粉末形態であり、医薬用カプセルに封入されている、上記項82に記載の方法。
いくつかの態様において、本開示の細菌は、芽胞不形成細菌である。本書において、用語「芽胞不形成細菌」は、芽胞形成能力のない野生型細菌(例えばある種のグラム陰性細菌)、および芽胞形成を欠くように組換えられた芽胞形成細菌の遺伝的バリアント(例えばある種のグラム陽性細菌)を包含する。本書において、「芽胞形成の欠失をもたらす変異」または「芽胞形成の欠失をもたらす遺伝子変異」とは、芽胞形成経路の構成員の欠失をもたらす任意の遺伝子変異、および/または生存能力のある芽胞の形成を阻止する任意の遺伝子変異をさす。例えば、芽胞不形成細菌およびその作製は、国際特許出願番号PCT/US2017/013436に記載されており、それを参照により本書の一部とする。
本書において、「殺線虫タンパク質」とは、文脈から異義であることが明らかでない限り、線虫または蠕虫に対し毒性活性を示す任意のタンパク質をいう。殺線虫タンパク質の例には、蠕虫(例えば回虫)に感染した脊椎動物の消化管への経口投与(経口摂取物、飲料、食物、ピル、カプセル、粉末等)による送達のための、細菌の駆虫Cryタンパク質(例えばCrickmore et al., 1998 Microbiology and Molecular Biology Reviews 62(3): 807-813; Schnepf et al., 1998 Microbiology and Molecular Biology Reviews 62(3): 775-806; B. thuringiensis Cryタンパク質Cry5B(例えば配列番号1)およびそのサブバリアント、Cry13A(例えば配列番号2)およびそのサブバリアント、Cry14A(例えば配列番号3)およびそのサブバリアント、Cry21A(例えば配列番号4~5)およびそのサブバリアント、ならびにCry6Aおよびそのサブバリアント(例えば配列番号6)を包含するが、それに限定されない)のような結晶タンパク質が含まれる。Cryタンパク質は、細菌のサイトゾル中に発現され、結晶を形成し、該駆虫タンパク質へのアクセスは、細菌の溶解または開放によって可能となる。殺線虫結晶タンパク質(例えばCryタンパク質)から形成される殺線虫結晶は蠕虫において毒性を誘導するが、これは、可溶化または脱結晶化によって個々の殺線虫結晶タンパク質を放出し、それによって結晶タンパク質が蠕虫に直接作用できるようになることによる。
結晶タンパク質は、その有効性向上のためにトランケートされうる。STH防除のためのBt毒素(例えば結晶タンパク質)の有用性は、STHが摂取可能なタンパク質サイズによって制限されうる。いくつかの寄生回虫は、約40kDaよりも大きいタンパク質を摂取し難い。したがって、任意の特定のBt毒の有効性は、STHが取り込むタンパク質のサイズ排除によって制限され得、したがって、STH腸に容易に吸収されるように、毒性活性を維持しながら、十分小さいものであるべきである。トランケートされた毒素は、細菌における発現がより容易でありうる。トランケートされた毒素を製造することにより、標的STHが、全長プロトキシン(不活性)のトランケートされた活性毒素形態への正しいプロセシングのための適正なプロテアーゼを有しなければならないという要件も緩和される。したがって、トランケートされた毒素は、STH標的において適正なプロテアーゼプロセシング酵素が存在するか否かに関わらず、直ちに中毒のために利用可能である。また、トランケートされた毒素は、それを発現する細胞内において可溶性であり、不溶性封入体(該細胞に対し毒性でありうるか、または毒素の誤った折り畳みをもたらしうる)を形成する可能性がより低いので、トランケートされた毒素は微生物中で、より高いレベルで発現しうる。したがって、トランケートされたBt毒素フラグメント(例えば結晶タンパク質フラグメント)を製造することが望ましい。「トランケートされた」とは、Bt毒素タンパク質(結晶タンパク質)に関して言うとき、全長ではないが、対応する全長Bt毒素タンパク質の毒素活性を少なくとも5%、10%、20%、30%、40%、50%、60%、70%、80%、もしくは90%またはそれ以上維持するBt毒素タンパク質のことをいう。
異種Cryタンパク質発現および生物活性を所望の細菌において確認したら、該組換え細菌を、治療型および予防型の駆虫実験に使用しうる。
本開示の方法は、Bacillus由来の結晶タンパク質およびその誘導体を使用する、寄生虫、例えば線虫および扁形動物の防除に関する。本発明の範囲に含まれる寄生虫は、以下に属するものを包含するが、それに限定されない:Class Adenophorea、例えばOrder Mononchida、Family Plectidae、およびOrder Stichosomida、Family MermithidaeおよびTetradonematidae;Class Secernentea、例えばOrder Rhabditida、Family Carabonematidae、Cephalobidae、Chambersiellidae、Heterorhabditidae、Oxyuridae、Panagrolaimidae、Rhabditidae、Steinernematidae、Syrphonematidae、Syrphonematidae、またはThelastomatidae;Order Spirurida、Family Filariidae、Onchocercidae、Physalopteridae、Syngamidae、Spiruridae、Subuluridae、またはThelaziidae;Order Diplogasterida、Family Diplogasteridae;およびOrder Tylenchida、Family Allantonematidae、Aphelenchidae、Aphelenchoididae、Entaphelenchidae、Fergusobiidae、Phaenopsitylenchidae、Sphaerulariidae、Anguinidae、Dolichodoridae、Belonolaimidae、Pratylenchidae、Hoplolamidae、Heteroderidae、Criconematidae、Tylenchulidae、またはTylenehidae。一態様において、寄生虫は、Class Secernentea、Order Ascaridida、Family Ascarididae;Class Adenophorea、Order Trichurida、Family Trichuridae;Class Secernentea、Order Strongylida、Family Ancylostomatidae(ancylostomidae)またはTrichostrongylidae;またはClass Secernentea、Order Spirurida、Family Dracunculidae、Filariidae、またはOnchocercidaeに属するものである。
いくつかの態様において、本発明の医薬組成物は、少なくとも1つのさらなる処置剤との組み合わせとして投与される。さらなる処置剤は、例えば、小分子またはポリペプチド(抗体およびその断片を包含する)でありうる。さらなる態様において、さらなる処置剤は、ニコチン性アセチルコリン受容体アゴニストである。いくつかの態様において、さらなる処置剤は、本発明の医薬組成物と同時に投与される。いくつかの態様において、さらなる処置剤は、本発明の医薬組成物と(順序は問わず)前後して投与される。いくつかの態様において、前記ニコチン性アセチルコリン受容体アゴニストは、レバミソールファミリーのニコチン性アセチルコリン受容体アゴニストから選択される。いくつかの態様において、ニコチン性アセチルコリン受容体アゴニストはレバミソールである。いくつかの態様において、レバミソールが、約0.1mg/kg~約5.0mg/kgの量で投与される。いくつかの態様において、ニコチン性アセチルコリン受容体アゴニストはピランテルまたはトリベンジミジン(tribendimidine)である。いくつかの態様において、ピランテルが、約1.0mg/kg~約15.0mg/kgの量で投与される。いくつかの態様において、トリベンジミジンが、約0.25mg/kg~約10mg/kgの量で投与される。
本発明は、対象の消化管への純粋な結晶タンパク質の投与を企図する。したがって、本発明の医薬組成物は、経口投与用に製剤化されうる。経口投与は好ましくは、水性懸濁液、エマルジョン、粉末または固体として行われる。本発明の組成物は、食物中に組み込まれるか、または使用者によって消費前に食物に添加されうる。消化管への投与は、(例えばゲルまたは半固形製剤である)肛門坐剤の形態であってもよい。そのような調製物はいずれも、標準的な方法を用いて調製される。
本発明の方法は、対象において寄生蠕虫感染を処置するためのものであり、単一種の殺線虫結晶タンパク質から形成される単離された天然の生物活性殺線虫結晶を含む組成物を処置有効量で対象に投与することを含む。本発明の医薬組成物は、細菌芽胞、または結晶の形態の殺線虫結晶タンパク質以外の宿主細菌タンパク質を実質的に含まない。
本書において、文脈から異義であることが明らかでない限り、用語「処置」、および同様の用語、例えば「処置される」、「処置する」等は、有益な、または所望の結果(これは、臨床的に望ましい結果を包含し、好ましくは臨床的に望ましい結果である)を得るためのアプローチをさす。処置は、任意に、疾患の症状もしくは状態の改善、または疾患もしくは状態の進行の遅延を伴いうる。
芽胞形成欠失細胞においてCry5Bを製造するため、B. thuringiensis(Bt)株4D8;この株は、結晶タンパク質発現を欠き(Identification of Bacillus thuringiensis subsp. kurstaki strain HD1-Like bacteria from environmental and human samples after aerial spraying of Victoria, British Columbia, Canada, with Foray 48B. Appl Environ Microbiol. 2001 Mar;67(3):1035-43)、この株において、芽胞形成のマスターspo0Aレギュレーター(spo0A-)が相同組換えにより欠失された。本組成はさらに、Cry5B-BaCC(サイトゾルに結晶を含むBacillus(Bacillus with Cytosolic Crystal))と称される
図6に、IBaCCからCry5B結晶タンパク質を精製するために用いる方法のフローチャートを示す。大量のCry5Bタンパク質をIBaCCから精製するために、10Lの培養物の採取を行った(図6、ステップ610)。10LのBaCCを、250~350OD/mLとなるまで増殖させた。次いで、そのBaCCを遠心分離(8000×g、30分間)により0.5L~1Lに濃縮し、その後、1mL/Lカルバクロールを加えて室温で15分間撹拌することにより不活化して(ステップ612)、IBaCCを得た。不活化ステップの前のBaCCの濃縮を、他の方法、例えば限外濾過または透析によって行ってもよい。
いくつかのBaCC株、例えば4D8株は、成長サイクルの最後に自己溶解する。この自己溶解により、抗菌化合物による不活化後にホモジナイズを行うステップが必要無くなるか、またはその必要性が低減されうる。したがって、図6の精製フローチャートにおいて、自己溶解する細菌株を使用する場合は、ホモジナイズステップ614を省略するか、またはパス回数を少なくしうる。そのような態様において、自己溶解BaCCの10L培養物の採取を行いうる(図6、ステップ610)。10LのBaCCを、250~350OD/mLとなるまで増殖させうる。次いで、BaCCを遠心分離により0.5L~1Lに濃縮し、その後、1mL/Lカルバクロールを加えて室温で15分間撹拌することにより不活化して(ステップ612)、IBaCCを得ることができる。不活化の前および/または後にIBaCCは自己溶解しているので、ホモジナイズの必要は無かった。不活化ステップ前のBaCCの濃縮は、他の方法、例えば限外濾過または透析によって行ってもよい。
インビトロで、実施例2に記載のように製造したPCCで処理した後の鞭虫の運動性を調べた。鞭虫を各ウェルに、抗生物質を含むRPMI培地中、3匹ずつ入れた。PCC(Cry5B)の用量は20、100および500μg/mLで、各用量につき4つのウェルを使用した。図9Aに、示されている時点で測定した鞭虫運動性に対するPCC(Cry5B)の用量応答効果のグラフを示す。データは、ウェル毎に平均運動性指数として表され、ここで、3=運動性が高い、2=運動性が緩徐、1=触れても不動、である。
PCCが鞭虫量を低減する能力をハムスターにおいて調べた。マウスを鞭虫Trichuris murisに感染させた。マウスを2群に分け(各群4匹)、水、および実施例2に記載のように製造したCry5B約500mg/kgのPCC油洗浄物で処置した。両群に、水およびPCC油洗浄物を、0.5mlの体積で単回投与として、強制経口投与した。感染後34日目に、処置前の糞便中の卵数を測定し、マウスを、等しい糞便中の卵数で2群に分けた。感染後35日目に、強制経口投与による処置をマウスに行った。感染後41日目(処置から6日後)に、処置後の評価を、すべてのマウスを切開して総鞭虫数(盲腸)を測定して行った。鞭虫量の45%の低下が見られた(水の場合、平均5.5の鞭虫数;PCCの場合、平均3の鞭虫数)(p=0.02)。
インビトロで鉤虫(Necator americanus)の運動性を、実施例2に記載のように製造したPCCによる処理後に調べた。各ウェルに3匹の鉤虫を入れ、各用量につき4つのウェルを用い、用量は250μg/mLとした。図10Aは、Cry5B PCCへのインビトロ暴露後の鉤虫運動性の経時変化を示すグラフである。PCCは、鉤虫中毒に対し用量依存的効果を示した。データは、ウェル毎に平均運動性指数として表され、ここで、3=運動性が高い、2=運動性が緩徐である、1=触れられなければ動かない、0=触れられても動かない、である。
PCCを10mg/kgの用量で用いて、鉤虫Nector americanusに感染させたハムスターを処置した。6匹のハムスターをN. americanusに感染させ、該寄生虫の駆除を防ぐために本実験の期間にわたって免疫抑制レジメン(デキサメタゾンを飲料水に含め、かつ、週2回注射した)に付した。鉤虫を与えた後(約60日後)に、3匹のハムスターを経口PCC 10mg/kgの単回用量で処置し、3匹のハムスターを対照としての水で処置した。処置前に糞便中の卵数測定値を得て虫が棲み付いたことを確認し、処置前の糞便中卵数が等しくなるようにハムスターを2群に分けた。処置後5日目に動物を殺し、腸内鉤虫量を調べた。
図12は、Ancyclostoma ceylanicum鉤虫の卵から幼虫への成長に対する、さまざまな濃度のCry5B PCC(3つの調製物)の毒性を、Cry5B IBaCCと比較して示すヒストグラムである。一部のCry5B PCCはリゾチームの添加により処理したが、これはCry5B PCCの毒性に影響を及ぼさないようであった。A. ceylanicumの卵(卵約65個/ウェル、複数ウェル/用量)を大腸菌食物源と共に緩衝液に入れ、25℃で7日間成長させた。7日目に、孵化して第3幼虫感染段階まで成長した卵の数を調べる。PCCは低濃度でも、IBaCCよりも高い活性で、該鉤虫の成長を阻止することができる(IC50が約15ng/mL)。
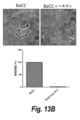
Cry5Bを発現するB. thuringiensisを、実施例1に記載のように、すなわち、(BaCC)10Lの規模で培養した(ステップ631)(図13A)。遠心分離(4500rpm、4℃で60分間)により細胞を10倍濃縮した後(ステップ632)、洗ったBaCCを水500mL(最終体積)中に懸濁し、ヘキサンを最終濃度10% v/vで加え、密閉容器内で室温で1時間混合して、IBaCCを調製した(ステップ633)。図13Bに、BaCCからのIBaCCの調製を示す顕微鏡画像を示す。左の顕微鏡画像はBaCCを示し、右の顕微鏡画像では、ロッド状の構造が破壊されており、BaCCに対するヘキサンの効果が示される。図13Bの棒グラフは、BaCC(100%細胞増殖)、および10%ヘキサンで処理されたBaCC(0%細胞増殖、完全な不活化)の細胞増殖パーセンテージの値を示す。図13Cに、BaCC出発材料、および図13Aのフローチャートに示す方法に付した後の最終的な精製PCC産物の、SDS-PAGEゲルの画像を示す。ヘキサンの代わりに他の細胞不活化手段、例えば界面活性剤、抗菌剤、殺生物剤等を使用することができる。
もう1つの実施例において、実施例9の方法を、実施例9のヘキサン相分配法と組み合わせた。図14は、細菌の不活化のために10%ヘキサンを、他の細菌汚染物を除去するために50%ヘキサンを用いてBaCCから調製したPCC(PCC-Hex/Hex)の生物活性を示すグラフである。グラフには、未凍結乾燥PCCを菱形で、凍結乾燥PCCを四角形で示す。表示の値は、幼虫段階L4で出発した単一のC. elegansの、3日後の繁殖サイズの平均値である(条件毎にn=3)。PCCの効力は、10μg/mLで繁殖サイズの出現を完全に抑制するので、優れている。これに対し、文献に記載されるデータによると、この用量での抑制率は平均70%である(Hu, Y, et al., Proc Natl Acad Sci USA 107: 5955-60 (2010))。これらデータから、PCC Hex/Hex法は凍結乾燥との適合性が十分であることが示される。
図15に、細菌の不活化(IBaCC)のためにカルバクロールを、他の細菌汚染物を除去するために50%ヘキサン相分配を用いてBaCCから調製したPCC(PCC-Carv&Hex)の生物活性を示す。表示の値は、7日目の、成熟した感染性幼虫段階に達した鉤虫A. ceylanicum卵のパーセントである。バーが低いほど、鉤虫成長の阻害が大きいことを示す。対照は、培地中のヘキサンのみであり、終濃度をPCCサンプルにおけるのと同じとしたものである。データは、ヘキサン単独では寄生虫に対し効果がないことを示している。
Claims (4)
- 単離された天然の生物活性殺線虫結晶を含む医薬組成物を製造する方法であって、
(a)単一種の殺線虫結晶タンパク質を発現するように遺伝子組換えされた芽胞不形成形態の宿主細菌を増殖させること;ここで、前記芽胞不形成宿主細菌は、単一種の殺線虫結晶タンパク質から形成される天然の生物活性殺線虫結晶を産生し、前記宿主細菌は増殖培地中で増殖される;
(b)前記芽胞不形成宿主細菌を濃縮すること;
(c)前記濃縮した芽胞不形成宿主細菌を、それを不活化するために、テルペン、ヘキサンまたはホルムアルデヒドを含む抗菌化合物に暴露すること;および
(d)前記殺線虫結晶から、前記抗菌化合物、可溶性の細胞成分、脂質および細胞壁デブリを抽出するために、前記不活化された芽胞不形成宿主細菌に食用油を加えること
を含み、
前記宿主細菌が、前記天然の生物活性殺線虫結晶が前記細菌のサイトゾル中に捕らえられるように、芽胞形成の欠失をもたらす遺伝子変異を持つよう遺伝子組換えされたバチルス・チューリンゲンシス(Bacillus thuringiensis)であり、ここで、芽胞形成の欠失をもたらす前記遺伝子変異が、spo0A遺伝子の欠失または不活性化である、
方法。 - 前記宿主細菌が、前記単一種の殺線虫結晶タンパク質を芽胞不形成特異的プロモーターの制御下に発現するように遺伝子組換えされており、ここで、
前記単一種の殺線虫結晶タンパク質が、Cry5B、または配列番号1との配列同一性が少なくとも90%、少なくとも95%もしくは少なくとも98%であるアミノ酸配列を有するそのバリアントもしくはトランケーションであるか、またはCry5BバリアントSer407Cys、または配列番号7との配列同一性が少なくとも90%、少なくとも95%もしくは少なくとも98%であるアミノ酸配列を有するそのバリアントもしくはトランケーションであり、
前記芽胞不形成特異的プロモーターが、Cry3A、GerA、GNATまたはTadAプロモーターである、
請求項1に記載の方法。 - 前記不活化された宿主細菌をホモジナイズして、前記天然の生物活性殺線虫結晶を含む細菌溶解物を形成するステップをさらに含む、請求項1または2に記載の方法。
- 前記単離された天然の生物活性殺線虫結晶を、経口投与で利用可能な投与形態に製剤化するステップをさらに含む、請求項1~3のいずれかに記載の方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2024127610A JP2024150746A (ja) | 2017-05-23 | 2024-08-02 | 純粋な駆虫組成物および関連する方法 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201762510081P | 2017-05-23 | 2017-05-23 | |
| US62/510,081 | 2017-05-23 | ||
| PCT/US2018/033962 WO2018217807A1 (en) | 2017-05-23 | 2018-05-22 | Purified anthelmintic compositions and related methods |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024127610A Division JP2024150746A (ja) | 2017-05-23 | 2024-08-02 | 純粋な駆虫組成物および関連する方法 |
Publications (3)
| Publication Number | Publication Date |
|---|---|
| JP2020521744A JP2020521744A (ja) | 2020-07-27 |
| JP2020521744A5 JP2020521744A5 (ja) | 2021-07-26 |
| JP7601362B2 true JP7601362B2 (ja) | 2024-12-17 |
Family
ID=64397008
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2019564903A Active JP7601362B2 (ja) | 2017-05-23 | 2018-05-22 | 純粋な駆虫組成物および関連する方法 |
| JP2024127610A Pending JP2024150746A (ja) | 2017-05-23 | 2024-08-02 | 純粋な駆虫組成物および関連する方法 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2024127610A Pending JP2024150746A (ja) | 2017-05-23 | 2024-08-02 | 純粋な駆虫組成物および関連する方法 |
Country Status (7)
| Country | Link |
|---|---|
| US (4) | US11844815B2 (ja) |
| EP (1) | EP3630150B1 (ja) |
| JP (2) | JP7601362B2 (ja) |
| CN (2) | CN117752694A (ja) |
| AU (2) | AU2018271878B2 (ja) |
| CA (1) | CA3062638A1 (ja) |
| WO (1) | WO2018217807A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10940170B2 (en) | 2014-07-07 | 2021-03-09 | University Of Massachusetts | Anthelmintic probiotic compositions and methods |
| US11484568B2 (en) | 2016-01-15 | 2022-11-01 | University Of Massachusetts | Anthelmintic compositions and methods |
| JP7601362B2 (ja) | 2017-05-23 | 2024-12-17 | ユニバーシティー オブ マサチューセッツ | 純粋な駆虫組成物および関連する方法 |
| WO2020113365A1 (zh) * | 2018-12-03 | 2020-06-11 | 清华大学 | 一种高产脂肽的基因工程菌及其应用 |
| CN111387226B (zh) * | 2020-04-13 | 2021-04-13 | 山西省农业科学院植物保护研究所 | 一种用于防治山楂叶螨的生物农药组合物及其制备方法和应用 |
| CN115057915B (zh) * | 2021-12-28 | 2024-04-26 | 四川农业大学 | 一种大肠杆菌表达蛋白Cry5B在制备抗大熊猫蛔虫成虫和L4期幼虫活性药物中的应用 |
| FR3135093B1 (fr) * | 2022-05-02 | 2026-01-02 | Institut National De Rech Pour Lagriculture Lalimentation Et Lenvironnement | Production de protéines d’intérêt dans une souche bactérienne non-sporulante |
| US20240269199A1 (en) * | 2023-01-18 | 2024-08-15 | University Of Massachusetts | Compositions for control of human and animal parasitic nematodes and methods of use |
| CN119081942B (zh) * | 2024-09-11 | 2025-04-15 | 中国农业科学院植物保护研究所 | 一株具有提高Cry蛋白杀虫活性的非靶标肠道乳植杆菌菌株及应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007062064A2 (en) | 2005-11-23 | 2007-05-31 | Regents Of The University Of California, San Diego | Methods and compositions for controlling parasitic infections with bt crystal proteins |
Family Cites Families (20)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4865981A (en) | 1985-08-16 | 1989-09-12 | Mycogen Corporation | Cloning and expression of Bacillus Thuringiensis toxin gene toxic to bettles of the order coleoptera |
| US5753492A (en) | 1987-08-12 | 1998-05-19 | Mycogen Corporation | Genes encoding nematode-active toxins from Bacillus thuringiensis strains |
| IL89307A0 (en) * | 1988-02-19 | 1989-09-10 | Ecogen Inc | Bacillus thuringiensis var.israelensis cryd toxin gene,protein and related insecticide compositions |
| US5596071A (en) | 1991-05-22 | 1997-01-21 | Mycogen Corporation | Bacillus thuringiensis toxins active against hymenopteran pests |
| JPH07504815A (ja) | 1992-02-27 | 1995-06-01 | マイクロバイアル テクニクス リミティド | 乳酸菌における異種遺伝子の発現およびその発現産物 |
| DK0603992T4 (da) | 1992-12-22 | 2001-03-05 | Univ Cincinnati | Oral indgivelse af immunologisk aktive biomolekyler og andre terapeutiske proteiner |
| FR2704860B1 (fr) | 1993-05-05 | 1995-07-13 | Pasteur Institut | Sequences de nucleotides du locus cryiiia pour le controle de l'expression de sequences d'adn dans un hote cellulaire. |
| US6060594A (en) | 1997-12-18 | 2000-05-09 | Ecogen, Inc. | Nucleic acid segments encoding modified bacillus thuringiensis coleopteran-toxic crystal proteins |
| US7351881B2 (en) | 2003-02-20 | 2008-04-01 | Athenix Corporation | AXMI-008, a delta-endotoxin gene and methods for its use |
| CN1244530C (zh) | 2003-09-08 | 2006-03-08 | 中国农业科学院饲料研究所 | 饲用抗菌剂香芹酚的绿色合成工艺 |
| WO2006123157A2 (en) | 2005-05-18 | 2006-11-23 | University Of Bath | Nematistatic protein |
| NZ594744A (en) | 2006-06-14 | 2013-03-28 | Athenix Corp | Axmi-031, axmi-039, axmi-040 and axmi-049, a family of delta-endotoxin genes and methods for their use |
| WO2009002580A2 (en) * | 2007-04-02 | 2008-12-31 | Boston Medical Center Corporation | Method for bacterial lysis |
| WO2010053517A2 (en) | 2008-10-29 | 2010-05-14 | Aroian Raffi V | Combination therapy to combat helminth resistance |
| AU2014321319B2 (en) * | 2013-09-19 | 2019-12-19 | The Gilla Company, Inc. | Antimicrobial compositions |
| WO2016007355A1 (en) | 2014-07-07 | 2016-01-14 | Aroian Raffi Van | Anthelmintic probiotic compositions and methods |
| US10940170B2 (en) | 2014-07-07 | 2021-03-09 | University Of Massachusetts | Anthelmintic probiotic compositions and methods |
| US20170369537A1 (en) | 2014-12-19 | 2017-12-28 | Danisco Us Inc. | Enhanced protein expression |
| US11484568B2 (en) | 2016-01-15 | 2022-11-01 | University Of Massachusetts | Anthelmintic compositions and methods |
| JP7601362B2 (ja) | 2017-05-23 | 2024-12-17 | ユニバーシティー オブ マサチューセッツ | 純粋な駆虫組成物および関連する方法 |
-
2018
- 2018-05-22 JP JP2019564903A patent/JP7601362B2/ja active Active
- 2018-05-22 EP EP18805734.3A patent/EP3630150B1/en active Active
- 2018-05-22 WO PCT/US2018/033962 patent/WO2018217807A1/en not_active Ceased
- 2018-05-22 CN CN202311600934.4A patent/CN117752694A/zh active Pending
- 2018-05-22 AU AU2018271878A patent/AU2018271878B2/en active Active
- 2018-05-22 CN CN201880041884.1A patent/CN111148524A/zh active Pending
- 2018-05-22 US US16/607,677 patent/US11844815B2/en active Active
- 2018-05-22 CA CA3062638A patent/CA3062638A1/en active Pending
-
2022
- 2022-04-26 US US17/729,785 patent/US11826389B2/en active Active
-
2023
- 2023-10-12 US US18/485,796 patent/US12290539B2/en active Active
-
2024
- 2024-08-02 JP JP2024127610A patent/JP2024150746A/ja active Pending
-
2025
- 2025-01-16 US US19/024,549 patent/US20250161373A1/en active Pending
- 2025-07-08 AU AU2025205222A patent/AU2025205222A1/en active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2007062064A2 (en) | 2005-11-23 | 2007-05-31 | Regents Of The University Of California, San Diego | Methods and compositions for controlling parasitic infections with bt crystal proteins |
Non-Patent Citations (2)
| Title |
|---|
| BIO/TECHNOLOGY,1995年,Vol.13,pp.67-71 |
| EVELYN DURMAZ,INTRACELLULAR AND EXTRACELLULAR EXPRESSION OF BACILLUS THURINGIENSIS CRYSTAL PROTEIN 以下備考,APPLIED AND ENVIRONMENTAL MICROBIOLOGY,2016年02月,VOL:82, NR:4,PAGE(S):1286-1294,https://aem.asm.org/content/aem/82/4/1286.full.pdf,CRY5B IN LACTOCOCCUS LACTIS FOR USE AS AN ANTHELMINTHIC |
Also Published As
| Publication number | Publication date |
|---|---|
| WO2018217807A1 (en) | 2018-11-29 |
| US20200188452A1 (en) | 2020-06-18 |
| US12290539B2 (en) | 2025-05-06 |
| US20220354905A1 (en) | 2022-11-10 |
| US11844815B2 (en) | 2023-12-19 |
| AU2025205222A1 (en) | 2025-07-31 |
| CA3062638A1 (en) | 2018-11-29 |
| CN111148524A (zh) | 2020-05-12 |
| JP2020521744A (ja) | 2020-07-27 |
| US11826389B2 (en) | 2023-11-28 |
| US20250161373A1 (en) | 2025-05-22 |
| JP2024150746A (ja) | 2024-10-23 |
| AU2018271878B2 (en) | 2025-04-17 |
| US20240148800A1 (en) | 2024-05-09 |
| CN117752694A (zh) | 2024-03-26 |
| AU2018271878A1 (en) | 2019-11-28 |
| EP3630150A1 (en) | 2020-04-08 |
| EP3630150A4 (en) | 2021-04-28 |
| EP3630150B1 (en) | 2024-09-11 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7601362B2 (ja) | 純粋な駆虫組成物および関連する方法 | |
| US12576129B2 (en) | Anthelmintic compositions and methods | |
| US7713726B2 (en) | Inhibition of pathogens by probiotic bacteria | |
| US20230132133A1 (en) | Methods and compositions for the treatment of c. difficile | |
| AU785159B2 (en) | Inhibition of pathogens by bacillus coagulans strains | |
| US20210268045A1 (en) | Anthelmintic probiotic compositions and methods | |
| WO2019162652A1 (en) | Pathogenic bacteria | |
| US20240269199A1 (en) | Compositions for control of human and animal parasitic nematodes and methods of use | |
| US10940170B2 (en) | Anthelmintic probiotic compositions and methods | |
| WO2025245028A2 (en) | Novel anthelmintic cry proteins and uses thereof | |
| US20210052679A1 (en) | Probiotic delivery of guided antimicrobial peptides | |
| BR122022016032B1 (pt) | Composição de cepa bacteriana | |
| OA20578A (en) | Probiotic delivery of guided antimicrobial peptides. |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20210514 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20210514 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20220531 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220831 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230110 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20230328 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20230609 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20230912 |
|
| A601 | Written request for extension of time |
Free format text: JAPANESE INTERMEDIATE CODE: A601 Effective date: 20231129 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240129 |
|
| A02 | Decision of refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A02 Effective date: 20240402 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20240802 |
|
| A911 | Transfer to examiner for re-examination before appeal (zenchi) |
Free format text: JAPANESE INTERMEDIATE CODE: A911 Effective date: 20240919 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20241105 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20241128 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7601362 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |