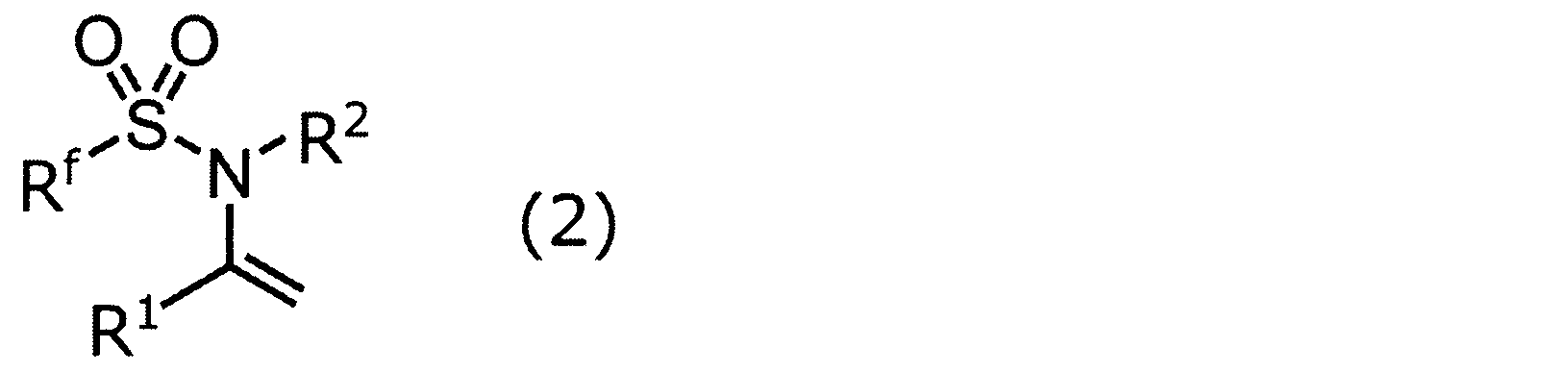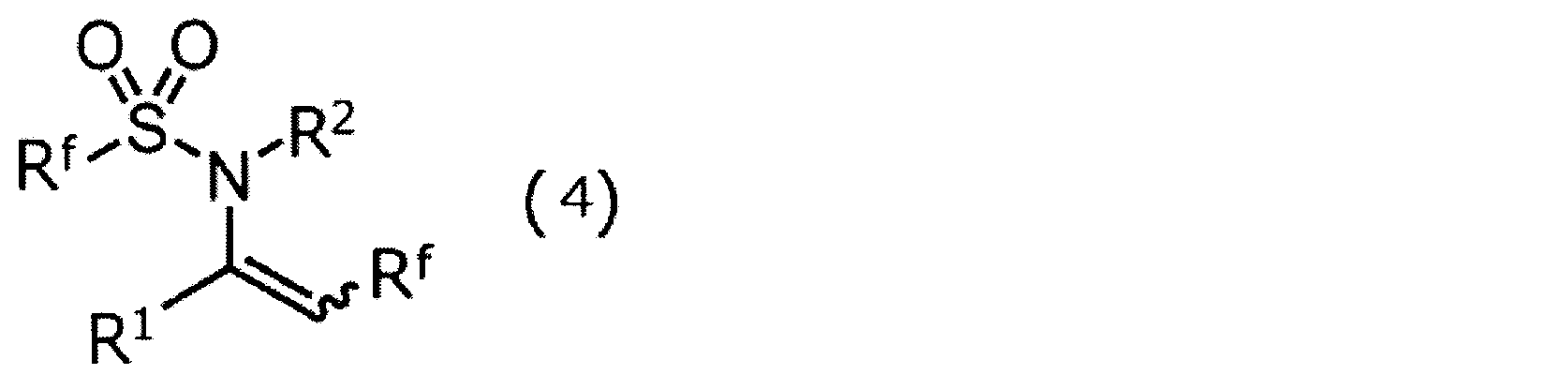本発明のフルオロアルキル置換ビニルフルオロアルカンスルホニルアミドの製造方法は、イミン又はN-フルオロアルキルスルホニルエナミン、前記イミン又はN-フルオロアルキルスルホニルエナミンに対して1モル当量を超えるフルオロアルキルスルホン酸無水物、及び前記イミン又はN-フルオロアルキルスルホニルエナミンに対して1モル当量を超える塩基の存在下で、ラジカル開始剤を作用させる方法である。ここで、上記イミンは、以下の構造を含む化合物であれば特に制限されない(下記式中、R、R’、R”はアルキル基を表す。)。
また、上記N-フルオロアルキルスルホニルエナミンは、以下の構造を含む化合物であれば特に制限されない(下記式中、R、R’、R”はアルキル基、Rfはフルオロアルキル基を表す。)。
本発明におけるイミンとして、具体的には、以下の式(1)で表される化合物等を例示することができる。
(式中、R
1は、置換基を有していてもよい鎖状炭化水素基、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよい複素環基、-OR
3、-NR
4R
5、又は、置換基を有していてもよい鎖状炭化水素基と、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基及び置換基を有していてもよい複素環基からなる群から選択される少なくとも一つの基とが複合した基を表し、
R2は、水素原子、置換基を有していてもよい鎖状炭化水素基、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよい複素環基、又は、置換基を有していてもよい鎖状炭化水素基と、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基及び置換基を有していてもよい複素環基からなる群から選択される少なくとも一つの基とが複合した基を表し、
R3は、水素原子、置換基を有していてもよい鎖状炭化水素基、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよい複素環基、又は、置換基を有していてもよい鎖状炭化水素基と、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基及び置換基を有していてもよい複素環基からなる群から選択される少なくとも一つの基とが複合した基を表し、
R4及びR5は、同一でも異なっていてもよく、水素原子、置換基を有していてもよい鎖状炭化水素基、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基、置換基を有していてもよい複素環基、又は、置換基を有していてもよい鎖状炭化水素基と、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基及び置換基を有していてもよい複素環基からなる群から選択される少なくとも一つの基とが複合した基を表す。)
式(1)中、「置換基を有していてもよい鎖状炭化水素基」における「鎖状炭化水素基」として、具体的には、アルキル基、アルケニル基、アルキニル基等を例示することができ、また、アルカジエニル基、アルカトリエニル基等のように、アルキル基における炭素-炭素結合の2ないし3個が二重結合に変換された基であってもよい。
上記アルキル基としては、直鎖状でも分枝状でもよく、具体的には、メチル基、エチル基、n-プロピル基、イソプロピル基、n-ブチル基、イソブチル基、sec-ブチル基、tert-ブチル基、n-ペンチル基、イソペンチル基、ネオペンチル基、n-へキシル基、n-ヘプチル基、n-オクチル基、n-ノニル基、n-デシル基等のC1~10のアルキル基等を例示することができる。
なお、「C1~10」の用語は、母核となる基の炭素原子数が1~10個であることを表している。この炭素原子数には、置換基の中に在る炭素原子の数を含まない。例えば、置換基としてエトキシ基を有するブチル基は、C2アルコキシC4アルキル基に分類する。以下、本明細書において、同じ意味で用いる。
上記アルケニル基としては、直鎖状でも分岐状でもよく、具体的には、ビニル基、1-プロペニル基、2-プロペニル基、1-ブテニル基、2-ブテニル基、3-ブテニル基、1-ペンテニル基、1-ヘキセニル基、1-ヘプテニル基、1-オクテニル基、1-ノネニル基、1-デセニル基等のC2~10のアルケニル基等を例示することができる。
上記アルキニル基としては、直鎖状でも分岐状であってもよく、具体的には、エチニル基、1-プロピニル基、1-ブチニル基、1-ペンチニル基、1-ヘキサニル基、1-ヘプチニル基、1-オクチニル基、1-ノニル基等のC2~10のアルキニル基等を例示することができる。
アルキル基における炭素-炭素結合の2~3個が二重結合に変換された基として、具体的には、上記炭素数1~10のアルキル基における炭素-炭素結合の2~3個が二重結合に変換された基である、1,3-ブタジエニル等の炭素数4~6のアルカジエニル基、1,3,5-ヘキサトリエニル等のアルカトリエニル基を例示することができる。
式(1)中、「置換基を有していてもよい環状脂肪族炭化水素基」における「環状脂肪族炭化水素基」として、具体的には、員数3~10の単環脂肪族炭化水素基又は縮合環脂肪族炭化水素基等を例示することができる。単環脂肪族炭化水素基として、具体的には、飽和または不飽和の環状脂肪族炭化水素基である、シクロアルキル基、シクロアルケニル基、シクロアルカジエニル基等を例示することができる。
上記シクロアルキル基として、具体的には、シクロプロピル基、シクロブチル基、シクロペンチル基、シクロへキシル基、シクロヘプチル基、シクロオクチル基、シクロノニル基、シクロデシル基等を例示することができる。
上記シクロアルケニル基として、具体的には、1-シクロペンテニル基、2-シクロペンテニル基、1-シクロヘキセニル基、1-シクロブテニル基、1-シクロヘプテニル基等を例示することができる。
上記シクロアルカジエニル基として、具体的には、2,4-シクロペンタジエニル基、2,4-シクロヘキサジエニル基、2,5-シクロヘキサジエニル基等を例示することができる。
上記縮合環脂肪族炭化水素基としては、上記単環脂肪族炭化水素基と置換基を有していてもよい芳香族炭化水素が縮合したものも包含され、具体的には、1-インダニル基、2-インダニル基、1,2,3,4-テトラヒドロナフタレン-1-イル基、1,2,3,4,5,6,7,8,9,10-デカヒドロナフタレン-1-イル基、1-ヒドリンダニル基、exo-又はendo-トリシクロ[5.2.1.0]デカン-4-イル基、2-ボルネン-5-イル基、2-ノルボルネン-5-イル基、exo-又はendo-トリシクロ[5.2.1.0]デカ-3-エン-8-イル基、1,2,3,4,5,6,7,8-オクタヒドロナフタレン-1-イル基、トリシクロ[6.2.1.0]ウンデカ-4-エン-8-イル基、テトラシクロ[6.2.1.1.0]ドデカ-4-エン-9-イル基、ビシクロ[2.2.1]ヘプタ-2,5-ジエン-3-イル基、3a,4,7,7a-テトラヒドロインデン-3-イル基等を例示することができる。
式(1)中、「置換基を有していてもよい芳香族炭化水素基」における「芳香族炭化水素基」としては、単環式でも縮合多環式でもよく、具体的には、フェニル基、1-ナフチル基、2-ナフチル基、1-アズレニル基、3-インデニル基、1-インダニル基、5-テトラリニル基等を例示することができる。
式(1)中、「置換基を有していてもよい複素環基」における「複素環基」として、具体的には、窒素原子、酸素原子及び硫黄原子からなる群より選択される少なくとも1個のヘテロ原子を含む員数5~10の単環複素環基又は員数5~10の単環芳香族複素環基若しくは縮合芳香族複素環等を例示することができ、縮合芳香族複素環基には、ベンゼン環と窒素原子、酸素原子及び硫黄原子からなる群より選択される少なくとも1個のヘテロ原子を含む単環複素環が縮合したものが包含される。
前記複素環基として、具体的には、1-ピペリジニル基、1-モルホリニル基、2-ピロリル基、2-イミダゾリル基、2-ベンゾイミダゾリル基、3-ピラゾリル基、2-チアゾリル基、3-イソチアゾリル基、2-オキサゾリル基、3-イソオキサゾリル基、4-フラザニル基、2-ピリジニル基、2-ピラジニル基、2-ピリミジニル基、3-ピリダジニル基、2-フラニル基、2-ピラニル基、2-チエニル基、2-ベンゾチオフェニル基、2-チオピラニル基、1-イソチオクロメニル基、2-チオクロメニル基、9-チオキサンテニル基、1-チアントレニル基、1-フェノキサチインニル基、1-ピロリジニル基、5H-1-ピリンジン-5-イル基、インドリジン-1-イル基、1-イソインドリル基、1-インドリル基、1-インダゾリニル基、2-プリニル基、1-キノリジニル基、1-イソキノリニル基、2-キノリニル基、2,6-ナフチリジン-1-イル基、2,7-ナフチリジン-1-イル基、1-フタラジニル基、2-キノキサリニル基、2-キナゾリニル基、3-シンノリニル基、2-プテリジニル基、9-カルバゾリル基、9-β-カルボリニル基、10-フェナントリジニル基、9-アクリジニル基、2-ペリミジニル基、1,10-フェナントロリン-2-イル基、1-フェナジニル基、1-フェノチアジニル基、1-フェノキサジニル基、2-アンチリジニル基、1-イソベンゾフラニル基、2-ベンゾフラニル基、1-イソクロメニル基、2-クロメニル基、9-キサンテニル基、パラチアジニル基、1,2,4-トリアゾール-3-イル基、1,2,3-トリアゾール-1-イル基、5-テトラゾリル基等を例示することができる。
式(1)中、「置換基を有していてもよい鎖状炭化水素基と、置換基を有していてもよい環状脂肪族炭化水素基、置換基を有していてもよい芳香族炭化水素基及び置換基を有していてもよい複素環基からなる群から選択される少なくとも一つの基とが複合した基」とは、前記置換基を有していてもよい鎖状炭化水素基と、前記置換基を有していてもよい環状脂肪族炭化水素基、前記置換基を有していてもよい芳香族炭化水素基及び前記置換基を有していてもよい複素環基からなる群から選択される少なくとも一つの基とが複合した基であり、具体的には、前記置換基を有していてもよい鎖状炭化水素基と前記置換基を有していてもよい環状脂肪族炭化水素基とが複合した基、前記置換基を有していてもよい鎖状炭化水素基と前記置換基を有していてもよい芳香族炭化水素基とが複合した基、前記置換基を有していてもよい鎖状炭化水素基と前記置換基を有していてもよい複素環基とが複合した基を好適に例示することができる。
上記「置換基を有していてもよい鎖状炭化水素基と前記置換基を有していてもよい環状脂肪族炭化水素基とが複合した基」として、具体的には、シクロプロピルメチル基、シクロブチルメチル基、シクロペンチルメチル基、シクロへキシルメチル基、シクロヘプチルメチル基、シクロオクチルメチル基、シクロノニルメチル基、シクロデシルメチル基等のシクロアルキルアルキル基等を例示することができる。
上記「置換基を有していてもよい鎖状炭化水素基と前記置換基を有していてもよい芳香族炭化水素基とが複合した基」として、具体的には、ベンジル基、フェネチル基、ナフチルメチル基等を例示することができる。
上記「置換基を有していてもよい鎖状炭化水素基と前記置換基を有していてもよい複素環基とが複合した基」として、具体的には、2-ピペリジニルメチル基、1-モルホリニルメチル基、2-ピロリルメチル基、2-イミダゾリルメチル基、2-イミダゾリジニルメチル基、2-ベンゾイミダゾリルメチル基、3-ピラゾリルメチル基、2-チアゾリルメチル基等を例示することができる。
式(1)中、「置換基を有していてもよい鎖状炭化水素基」、「置換基を有していてもよい環状脂肪族炭化水素基」、「置換基を有していてもよい芳香族炭化水素基」、「置換基を有していてもよい複素環基」における「置換基」は化学的に許容され、本発明の効果を有する限りにおいて特に制限されない。
具体的には、
メチル基、エチル基、n-プロピル基、i-プロピル基、n-ブチル基、s-ブチル基、i-ブチル基、t-ブチル基、n-ペンチル基、n-ヘキシル基、n-ヘプチル基、n-オクチル基、n-ノニル基若しくはn-デシル基等のC1~10アルキル基;
ビニル基、1-プロペニル基、2-プロペニル基(アリル基)、1-ブテニル基、2-ブテニル基、3-ブテニル基、1-メチル-2-プロペニル基若しくは2-メチル-2-プロペニル基等のC2~6アルケニル基;
エチニル基、1-プロピニル基、2-プロピニル基、1-ブチニル基、2-ブチニル基、3-ブチニル基若しくは1-メチル-2-プロピニル基等のC2~6アルキニル基;
シクロプロピル基、シクロブチル基、シクロペンチル基、シクロヘキシル基若しくはキュバニル基等のC3~8シクロアルキル基;
フェニル基若しくは1-ナフチル基等のC6~10アリール基;
ベンジル基若しくはフェネチル基等のC6~10アリールC1~6アルキル基;
3~6員ヘテロシクリル基;
3~6員へテロシクリルC1~6アルキル基;
水酸基;
メトキシ基、エトキシ基、n-プロポキシ基、i-プロポキシ基、n-ブトキシ基、s-ブトキシ基、i-ブトキシ基若しくはt-ブトキシ基等のC1~6アルコキシ基;
ビニルオキシ基、アリルオキシ基、プロペニルオキシ基若しくはブテニルオキシ基等のC2~6アルケニルオキシ基;
エチニルオキシ基若しくはプロパルギルオキシ基等のC2~6アルキニルオキシ基;
フェノキシ基若しくは1-ナフトキシ基等のC6~10アリールオキシ基;
ベンジルオキシ基若しくはフェネチルオキシ基等のC6~10アリールC1~6アルコキシ基;
2-チアゾリルオキシ基若しくは2-ピリジルオキシ基等の5~6員ヘテロアリールオキシ基;
2-チアゾリルメチルオキシ基若しくは2-ピリジルメチルオキシ基等の5~6員ヘテロアリールC1~6アルキルオキシ基;
ホルミル基;
アセチル基若しくはプロピオニル基等のC1~6アルキルカルボニル基;
ホルミルオキシ基;
アセチルオキシ基、プロピオニルオキシ基等のC1~6アルキルカルボニルオキシ基;
ベンゾイル基等のC6~10アリールカルボニル基;
ベンゾイルオキシ基等のC6~10アリールカルボニルオキシ基;
メトキシカルボニル基、エトキシカルボニル基、n-プロポキシカルボニル基、i-プロポキシカルボニル基、n-ブトキシカルボニル基若しくはt-ブトキシカルボニル基等のC1~6アルコキシカルボニル基;
メトキシカルボニルオキシ基、エトキシカルボニルオキシ基、n-プロポキシカルボニルオキシ基、i-プロポキシカルボニルオキシ基、n-ブトキシカルボニルオキシ基、若しくはt-ブトキシカルボニルオキシ基等のC1~6アルコキシカルボニルオキシ基;
カルボキシル基;
フルオロ基、クロロ基、ブロモ基若しくはアイオド基等のハロゲノ基;
クロロメチル基、クロロエチル基、トリフルオロメチル基、1,2-ジクロロ-n-プロピル基、1-フルオロ-n-ブチル基若しくはパーフルオロ-n-ペンチル基等のC1~6ハロアルキル基;
2-クロロ-1-プロペニル基若しくは2-フルオロ-1-ブテニル基等のC2~6ハロアルケニル基;
4,4-ジクロロ-1-ブチニル基、4-フルオロ-1-ペンチニル基若しくは5-ブロモ-2-ペンチニル基等のC2~6ハロアルキニル基;
トリフルオロメトキシ基、2-クロロ-n-プロポキシ基若しくは2,3-ジクロロブトキシ基等のC1~6ハロアルコキシ基;
2-クロロプロペニルオキシ基若しくは3-ブロモブテニルオキシ基等のC2~6ハロアルケニルオキシ基;
クロロアセチル基、トリフルオロアセチル基若しくはトリクロロアセチル基等のC1~6ハロアルキルカルボニル基;
アミノ基;
メチルアミノ基、ジメチルアミノ基若しくはジエチルアミノ基等のC1~6アルキル置換アミノ基;
アニリノ基若しくは1-ナフチルアミノ基等のC6~10アリールアミノ基;
ベンジルアミノ基若しくはフェネチルアミノ基等のC6~10アリールC1~6アルキルアミノ基;
ホルミルアミノ基;
アセチルアミノ基、プロパノイルアミノ基、ブチリルアミノ基若しくはi-プロピルカルボニルアミノ基等のC1~6アルキルカルボニルアミノ基;
ベンゾイルアミノ基等のC6~10アリールカルボニルアミノ基;
メトキシカルボニルアミノ基、エトキシカルボニルアミノ基、n-プロポキシカルボニルアミノ基若しくはi-プロポキシカルボニルアミノ基等のC1~6アルコキシカルボニルアミノ基;
アミノカルボニル基、ジメチルアミノカルボニル基、フェニルアミノカルボニル基若しくはN-フェニル-N-メチルアミノカルボニル基等の無置換若しくは置換基を有するアミノカルボニル基;
イミノメチル基、1-イミノエチル基若しくは1-イミノ-n-プロピル基等のイミノC1~6アルキル基;
N-ヒドロキシ-イミノメチル基、1-(N-ヒドロキシイミノ)エチル基、1-(N-ヒドロキシイミノ)-n-プロピル基、N-メトキシイミノメチル基若しくは1-(N-メトキシイミノ)エチル基等の無置換若しくは置換基を有するN-ヒドロキシイミノC1~6アルキル基;
アミノカルボニルオキシ基;
エチルアミノカルボニルオキシ基若しくはジメチルアミノカルボニルオキシ基等のC1~6アルキル置換アミノカルボニルオキシ基;
メルカプト基;
メチルチオ基、エチルチオ基、n-プロピルチオ基、i-プロピルチオ基、n-ブチルチオ基、i-ブチルチオ基、s-ブチルチオ基若しくはt-ブチルチオ基等のC1~6アルキルチオ基;
トリフルオロメチルチオ基若しくは2,2,2-トリフルオロエチルチオ基等のC1~6ハロアルキルチオ基;
フェニルチオ基若しくは1-ナフチルチオ基等のC6~10アリールチオ基;
2-チアゾリルチオ基若しくは2-ピリジルチオ基等の5~6員ヘテロアリールチオ基;
メチルスルフィニル基、エチルスルフィニル基若しくはt-ブチルスルフィニル基等のC1~6アルキルスルフィニル基;
トリフルオロメチルスルフィニル基若しくは2,2,2-トリフルオロエチルスルフィニル基等のC1~6ハロアルキルスルフィニル基;
フェニルスルフィニル基若しくは1-ナフチルスルフィニル基等のC6~10アリールスルフィニル基;
2-チアゾリルスルフィニル基若しくは2-ピリジルスルフィニル基等の5~6員ヘテロアリールスルフィニル基;
メチルスルホニル基、エチルスルホニル基若しくはt-ブチルスルホニル基等のC1~6アルキルスルホニル基;
トリフルオロメチルスルホニル基若しくは2,2,2-トリフルオロエチルスルホニル基等のC1~6ハロアルキルスルホニル基;
フェニルスルホニル基若しくは1-ナフチルスルホニル基等のC6~10アリールスルホニル基;
2-チアゾリルスルホニル基若しくは2-ピリジルスルホニル基等の5~6員ヘテロアリールスルホニル基;
メチルスルホニルオキシ基、エチルスルホニルオキシ基若しくはt-ブチルスルホニルオキシ基等のC1~6アルキルスルホニルオキシ基;
トリフルオロメチルスルホニルオキシ基若しくは2,2,2-トリフルオロエチルスルホニルオキシ基等のC1~6ハロアルキルスルホニルオキシ基;
トリメチルシリル基、トリエチルシリル基若しくはt-ブチルジメチルシリル基等のトリC1~6アルキル置換シリル基;
トリメチルシリルオキシ基、トリエチルシリルオキシ基若しくはt-ブチルジメチルシリルオキシ基等のトリC1~6アルキル置換シリルオキシ基;
トリフェニルシリル基等のトリC6~10アリール置換シリル基;
トリフェニルシリルオキシ基等のトリC6~10アリール置換シリルオキシ基;
シアノ基又はニトロ基等を例示することができる。
また、これらの「置換基」は、当該置換基中のいずれかの水素原子が、異なる構造の基で置換されていてもよい。その場合の「置換基」として、具体的には、C1~6アルキル基、C1~6ハロアルキル基、C1~6アルコキシ基、C1~6ハロアルコキシ基、ハロゲノ基、シアノ基又はニトロ基等を例示することができる。
また、上記の「3~6員ヘテロシクリル基」とは、窒素原子、酸素原子及び硫黄原子からなる群から選ばれる1~4個のヘテロ原子を環の構成原子として含むものである。ヘテロシクリル基は、単環及び多環のいずれであってもよい。多環ヘテロシクリル基は、少なくとも一つの環がヘテロ環であれば、残りの環が飽和脂環、不飽和脂環または芳香環のいずれであってもよい。「3~6員ヘテロシクリル基」として、具体的には、3~6員飽和ヘテロシクリル基、5~6員ヘテロアリール基、5~6員部分不飽和ヘテロシクリル基等を例示することができる。
3~6員飽和ヘテロシクリル基として、具体的には、2-アジリジニル基、2-エポキシ基、2-ピロリジニル基、2-テトラヒドロフラニル基、2-チアゾリジニル基、2-ピペリジル基、2-ピペラジニル基、1-モルホリニル基、2-ジオキソラニル基若しくは2-ジオキサニル基等を例示することができる。
5員ヘテロアリール基として、具体的には、2-ピロリル基、2-フリル基、2-チエニル基、2-イミダゾリル基、3-ピラゾリル基、2-オキサゾリル基、3-イソオキサゾリル基、2-チアゾリル基、3-イソチアゾリル基、1,2,4-トリアゾール-3-イル基、1,2,4-オキサジアゾール-3-イル基、1,2,4-チアジアゾ-ル-3-イル基、5-テトラゾリル基等を例示することができる。
6員ヘテロアリール基として、具体的には、2-ピリジル基、3-ピラジニル基、2-ピリミジニル基、2-ピリダジニル基、1,3,5-トリアジン-2-イル基等を例示することができる。
5~6員部分不飽和ヘテロシクリル基とし、具体的には、2-オキサゾリニル基若しくは3-イソオキサゾリニル基等を例示することができる。
3~6員へテロシクリルC1~6アルキル基として、具体的には、2-アジリジニルメチル基、グリシジル基、2-ピロリジルメチル基、2-テトラヒドロフラニルメチル基、2-チアゾリジニルメチル基、2-ピロリルメチル基、2-フリルメチル基、2-イミダゾリルメチル基、2-ピリジルメチル基又は4-ピリジルメチル基等を例示することができる。
式(1)のR1中、「-OR3」のR3として、具体的には、R1の官能基として例示されたものと同じ官能基を例示することができる。「-OR3」として、具体的には、メトキシ基、エトキシ基、n-プロポキシ基、i-プロポキシ基、n-ブトキシ基、s-ブトキシ基、i-ブトキシ基若しくはt-ブトキシ基等のC1~6アルコキシ基、ビニルオキシ基、アリルオキシ基、プロペニルオキシ基若しくはブテニルオキシ基等のC2~6アルケニルオキシ基、エチニルオキシ基若しくはプロパルギルオキシ基等のC2~6アルキニルオキシ基、フェノキシ基若しくは1-ナフトキシ基等のC6~10アリールオキシ基、ベンジルオキシ基若しくはフェネチルオキシ基等のC6~10アリールC1~6アルコキシ基、2-チアゾリルオキシ基若しくは2-ピリジルオキシ基などの5~6員ヘテロアリールオキシ基又はチアゾリルメチルオキシ基若しくはピリジルメチルオキシ基等の5~6員ヘテロアリールC1~6アルキルオキシ基等を例示することができる。
式(1)のR1中、「-NR4R5」のR4及びR5として、具体的には、R1の官能基として例示されたものと同じ官能基を例示することができる。「-NR4R5」として、具体的には、メチルアミノ基、ジメチルアミノ基若しくはジエチルアミノ基等のC1~6アルキル置換アミノ基、アニリノ基若しくは1-ナフチルアミノ基等のC6~10アリールアミノ基又はベンジルアミノ基若しくはフェネチルアミノ基等のC6~10アリールC1~6アルキルアミノ基等を例示することができる。
本発明におけるN-フルオロアルキルスルホニルエナミンとして、具体的には、以下の式(2)で表される化合物等を例示することができる。
式(2)中、R1及びR2は、式(1)におけるR1及びR2と同じ定義であり、RfはC1~C10フルオロアルキル基を示す。
式(2)中、Rfの「C1~C10フルオロアルキル基」は、水素原子の全てがフッ素原子により置換されたアルキル基(ペルフルオロアルキル基)であっても、水素原子の一部がフッ素原子により置換されたアルキル基であってもよく、具体的には、CF3、C2F5、C3F7、C4F9、C5F11、C6F13、C7F15又はC8F17等のペルフルオロアルキル基、CF2H、CFH2、CF2CF2H、CH2CF3、CH2CH2CF3、CH2C2F5、CH2CH2C2F5、CH2C3F7、CH2CH2C3F7、CH2C4F9又はCH2CH2C4F9等の部分フッ素置換アルキル基等を例示することができる。中でも、アルキル基中の水素原子の60%以上がフッ素原子で置換されているフルオロアルキル基が好ましく、70%以上、80%以上、90%以上がさらに好ましい。さらに、その中でもC1~C6のフルオロアルキル基が好ましく、さらにはC1~C3のフルオロアルキル基が好ましく、中でもCF3、CF2CF2H、CF2CF3が好ましい。
本発明におけるフルオロアルキルスルホン酸無水物としては、具体的には、以下の式(3)で表される化合物等を例示することができる。
(RfSO2)2O (3)
(式中、Rfは、式(2)におけるRfと同じ定義である。)
本発明において、出発物質としてN-フルオロアルキルスルホニルエナミンを用いる場合、N-フルオロアルキルスルホニルエナミンとフルオロアルキルスルホン酸無水物のフルオロアルキル基を異なるものにすることにより、2つのフルオロアルキル基がそれぞれ異なるフルオロアルキル置換ビニルフルオロアルカンスルホニルアミドを製造してもよい。ここで、N-フルオロアルキルスルホニルエナミンは、イミンとフルオロアルキルスルホン酸無水物とを、前記イミンに対して1モル当量を超える塩基の存在下で反応させることにより合成してもよい。
本発明の製造方法において、反応は無溶媒又は有機溶媒中で行うことができる。ここで、用いる有機溶媒として、具体的には、クロロホルム、ジクロロメタン、1,2-ジクロロエタン、1,1,2,2-テトラクロロエタン、クロロベンゼン、o-ジクロロベンゼン、1,3,5-トリクロロベンゼン、ブロモベンゼン、ヨードベンゼン、トリフルオロメチルベンゼン、フルオロベンゼン、若しくはジフルオロベンゼン等の有機ハロゲン系溶媒;ベンゼン、トルエン、キシレン若しくはメシチレン等の芳香族炭化水素;ジメチルホルムアミド(DMF)、ジメチルスルホキシド(DMSO)、ジエチルエーテル、ジイソプロピルエーテル、ジ(n-ブチル)エーテル、モノグライム、ジグライム、トリグライム、テトラヒドロフラン、1,4-ジオキサン、アニソール、ベラトロール、ジエチルスルフィド、ジ(n-ブチル)スルフィド、アセトニトリル、プロピオニトリル若しくはベンゾニトリル等非プロトン性極性溶媒;ペンタン、ヘキサン、シクロペンタン若しくはシクロヘキサン等の脂肪族炭化水素等を例示することができるが、中でも、有機ハロゲン系溶媒が好ましく、さらに、ジクロロメタン又は1,2-ジクロロエタン、より好ましくは脱水ジクロロメタン又は脱水1,2-ジクロロエタンを好適に使用することができる。
これら有機溶媒の使用量は、特に限定されないが、イミン又はN-フルオロアルキルスルホニルエナミンに対して、重量比で0.5倍~20倍の範囲が好ましい。
本発明の製造方法におけるイミン又はN-フルオロアルキルスルホニルエナミンに対するフルオロアルキルスルホン酸無水物の使用量は、1モル当量を超える量であればよく、例えば1.1モル当量以上、1.5モル当量以上、2モル当量以上、3モル当量以上を挙げることができ、上限は特に限定されないが、例えば5モル当量以下を挙げることができる。
本発明における塩基としては、具体的には、トリエチルアミン、ジイソプロピルエチルアミン、ピリジン、2,6-ルチジン、2,6-ジクロロピリジン、2,4,6-トリメチルピリジン、2,4,6-トリ-tert-ブチルピリジン、2,6-ジ-tert-ブチル-4-メチルピリジン、2,6-ジ-tert-ブチルピリジン若しくは2,4,6-トリ-tert-ブチルピリミジン等の有機塩基又は炭酸カリウム若しくは炭酸ナトリウム等の無機塩基等を例示することができるが、中でも嵩高い塩基である2,4,6-トリ-tert-ブチルピリジン、2,6-ジ-tert-ブチル-4-メチルピリジン、2,6-ジ-tert-ブチルピリジン、2,4,6-トリ-tert-ブチルピリミジンが好ましい。
本発明の製造方法におけるイミン又はN-フルオロアルキルスルホニルエナミンに対する塩基の使用量は、1モル当量を超える量であればよく、例えば2モル当量以上、3モル当量以上、4モル当量以上、5モル当量以上を挙げることができ、上限は特に限定されないが、例えば10モル当量以下を挙げることができる。
本発明の製造方法におけるラジカル開始剤は、出発物からラジカルを発生させるものであれば特に限定されるものではないが、具体的には、トリエチルボラン若しくはトリブチルボラン等のトリアルキルボラン化合物と分子状酸素、ジエチル亜鉛等のジアルキル亜鉛と分子状酸素、アゾビスイソブチロニトリルや2,2’-アゾビス(イソ酪酸)ジメチル等のアゾ化合物又はジ(t-ブチル)パーオキサイド等のパーオキサイド化合物等を例示することができる。これらのうち、トリアルキルボラン化合物と分子状酸素の組み合わせや、アゾビスイソブチロニトリル、2,2’-アゾビス(イソ酪酸)ジメチルが好ましく、トリアルキルボラン化合物としては、トリエチルボランが好ましい。
本発明の製造方法におけるイミン又はN-フルオロアルキルスルホニルエナミンに対するラジカル開始剤の使用量は、モル比で0.1~1.0当量の範囲が好ましい。分子状酸素は、微量存在していれば十分である。また、出発物からラジカルを発生させる方法としては、アゾ化合物を添加し光を照射する条件や、過酸化物を添加し光を照射する条件も用いることができる。
本発明の製造方法における反応温度は、特に限定されないが、通常、-100℃~150℃であり、好ましくは0℃~100℃であり、より好ましくは10℃~50℃であり、さらに好ましくは15℃~30℃である。反応は、室温で行うこともできる。反応圧力は、常圧又は加圧下にて実施することができるが、常圧下が好ましい。反応時間は通常1分~200時間であり、好ましくは1時間~10時間であり、より好ましくは1時間~5時間であり、さらに好ましくは1時間~3時間である。なお、反応は十分な攪拌下にて行うことが望ましい。反応後は酢酸や塩酸等の酸あるいは水を添加し、反応試剤を失活させ、不溶物を除去した後、公知の蒸留法、抽出、晶出、再結晶、クロマトグラフィー等の精製によりフルオロアルキル置換ビニルフルオロアルカンスルホニルアミドを単離することができる。
本発明の製造方法により得られるフルオロアルキル置換ビニルフルオロアルカンスルホニルアミドとは、上記イミンとフルオロアルキルスルホン酸無水物との反応生成物であって、具体的には、以下の式(4)で表される化合物等を例示することができる。
式(4)中、R1、R2及びRfは、式(1)におけるR1及びR2、並びに式(2)におけるRfと同じ定義である。なお、出発物質としてN-フルオロアルキルスルホニルエナミンを用いる場合、2つのRfは同じでも異なっていてもよい。
上記式(4)で表される化合物は、1又は2以上の不斉炭素原子を有する場合があり、また、幾何異性や軸性キラリティを生じることがあるので、複数の立体異性体として存在することがある。これらの立体異性体、それらの混合物及びラセミ体は、式(4)で表される化合物に包含される。本発明の製造方法により得られるフルオロアルキル置換ビニルフルオロアルカンスルホニルアミドは、医薬品や農薬の合成中間体として好適に使用することができる。
本発明の製造方法は、イミン及びフルオロアルキルスルホン酸無水物を出発物質として用い、イミンのNに対するフルオロアルキルスルホン酸付加によるN-フルオロアルキルスルホニルエナミン中間体にラジカル開始剤が作用し、さらにフルオロアルキル基が付加されるという三段階の反応をワンポットで行うことができる点で、非常に簡便且つ特徴的な方法である。もしくはN-フルオロアルキルスルホニルエナミンを出発物質として用い、ラジカル開始剤が作用し、さらにフルオロアルキル基が付加されるという二段階の反応をワンポットで行うことができる点で、非常に簡便且つ特徴的な方法である。したがって、医薬品や農薬合成に汎用されることが期待される。
以下、実施例を用いて本発明をより詳細に説明するが、本発明の技術的範囲は、これらに限定されるものではない。
[実施例1]~[実施例9]
本発明の製造方法により、以下の表1に記載のとおりフルオロアルキル置換ビニルフルオロアルカンスルホニルアミド(表1中、2の化合物)の製造を行った。詳細手順は後述のとおりである。
実施例1 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-メトキシフェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-メトキシフェニル)-N-フェニルエタン-1-イミンを62.7mg(0.28mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を217.9mg(0.88mmol,3.1equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を11.2mg(0.05mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,2.8equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを15.9mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-メトキシフェニル)-1-プロペン-1-イル)メタンスルホンアミド(72%)及び中間体1,1,1-トリフルオロ-N-(1-(4-メトキシフェニル)ビニル)-N-フェニルメタンスルホンアミド(19%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が70.0mg(0.16mmol,59%)及び中間体が26.6mg(0.07mmol,27%)得られた。
1H-NMR(500MHz,CDCl3)δ7.29(q,J=2.5Hz,3H),7.18-7.21(m,4H),6.80(dt,J=9.2,2.4Hz,2H),6.25(q,J=7.1Hz,1H),3.78(s,3H)
実施例2 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-フルオロフェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-フルオロフェニル)-N-フェニルエタン-1-イミンを53.7mg(0.25mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を215.3mg(0.87mmol,3.5equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を12.1mg(0.05mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.1equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを14.4mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-フルオロフェニル)-1-プロペン-1-イル)メタンスルホンアミド(60%)及び中間体1,1,1-トリフルオロ-N-(1-(4-フルオロフェニル)ビニル)-N-フェニルメタンスルホンアミド(26%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が48.0mg(0.12mmol,46%)及び中間体が20.8mg(0.06mmol,21%)得られた。
1H-NMR(500MHz,CDCl3)δ7.33-7.28(m,3H),7.22-7.16(m,4H),6.98(tt,J=9.0,2.4Hz,2H),6.32(q,J=7.3Hz,1H);13C-NMR(126MHz,CDCl3)δ163.54(d,JC-F=252Hz),147.28(q,JC-F=4.8Hz),135.70,131.21(d,JC-F=8.4Hz),129.81,129.58,129.48,128.16(d,JC-F=3.6Hz),121.74(q,JC-F=271Hz),119.97(q,JC-F=324Hz),117.97(q,JC-F=36Hz),115.54(d,JC-F=22Hz);19F-NMR(471MHz,CDCl3)δ-56.21(d,J=6.8Hz,3F),-72.51(s,3F),-109.13(tt,J=8.2,5.5Hz,1F);HRMS(ESI-TOF)calcdforC16H9NO2F7S([M-1]-)412.0242,found412.0242
実施例3 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-クロロフェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-クロロフェニル)-N-フェニルエタン-1-イミンを58.8mg(0.26mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を216.4mg(0.87mmol,3.4equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を13.0mg(0.06mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.0equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを13.3mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-クロロフェニル)-1-プロペン-1-イル)メタンスルホンアミド(77%)及び中間体1,1,1-トリフルオロ-N-(1-(4-クロロフェニル)ビニル)-N-フェニルメタンスルホンアミド(20%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が55.0mg(0.13mmol,50%)及び中間体が13.9mg(0.04mmol,15%)得られた。
1H-NMR(500MHz,CDCl3)δ7.34-7.25(m,5H),7.19-7.14(m,4H),6.33(q,J=7.3Hz,1H);13C-NMR(126MHz,CDCl3)δ147.12(q,JC-F=6Hz),136.51,135.60,130.58,130.41,129.88,129.64,129.45,128.62,121.69(q,JC-F=271Hz),119.64(q,JC-F=321Hz),118.21(q,JC-F=36Hz);19F-NMR(471MHz,CDCl3)δ-56.21(d,J=6.8Hz,3F),-72.51(s,3F);HRMS(ESI-TOF)calcdforC16H9NO2F6S35Cl([M-1]-)427.9947,found427.9947
実施例4 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-ブロモフェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-ブロモフェニル)-N-フェニルエタン-1-イミンを69.3mg(0.25mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を216.3mg(0.87mmol,3.5equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を14.2mg(0.06mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.1equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを14.8mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-ブロモフェニル)-1-プロペン-1-イル)メタンスルホンアミド(70%)及び中間体1,1,1-トリフルオロ-N-(1-(4-ブロモフェニル)ビニル)-N-フェニルメタンスルホンアミド(17%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が60.7mg(0.13mmol,51%)及び中間体が34.4mg(0.08mmol,34%)得られた。
13C-NMR(126MHz,CDCl3)δ147.14(q,JC-F=6Hz),135.57,131.58,131.06,130.58,129.89,129.65,129.44,124.85,121.67(q,JC-F=271Hz),119.94(q,JC-F=324Hz),118.22(q,JC-F=34Hz);19F-NMR(471MHz,CDCl3)δ-56.20(d,J=8.2Hz,3F),-72.52(s,3F);HRMS(ESI-TOF)calcdforC16H9NO2F6S79Br([M-1]-)471.9442,found471.9440
実施例5 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-ヨードフェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-ヨードフェニル)-N-フェニルエタン-1-イミンを80.8mg(0.25mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を220.3mg(0.89mmol,3.5equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を11.7mg(0.05mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.1equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを15.0mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-ヨードフェニル)-1-プロペン-1-イル)メタンスルホンアミド(72%)及び中間体1,1,1-トリフルオロ-N-(1-(4-ヨードフェニル)ビニル)-N-フェニルメタンスルホンアミド(26%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が68.1mg(0.13mmol,52%)及び中間体が29.2mg(0.06mmol,22%)得られた。
1H-NMR(500MHz,CDCl3)δ7.63(dt,J=8.6,2.0Hz,2H),7.33-7.29(m,3H),7.16(dd,J=8.0,1.7Hz,2H),6.93(dt,J=8.8,2.1Hz,2H),6.31(q,J=7.3Hz,1H);13C-NMR(126MHz,CDCl3)δ147.25(q,JC-F=6Hz),137.50,135.56,131.64,130.57,129.89,129.65,129.43,121.66(q,JC-F=271Hz),119.93(q,JC-F=325Hz),118.20(q,JC-F=36Hz),96.93;19F-NMR(471MHz,CDCl3)δ-56.17(d,J=8.2Hz,3F),-72.47(s,3F);HRMS(ESI-TOF)calcdforC16H9NO2F6SI([M-1]-)519.9303,found519.9303
実施例6 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-(メチルスルホニル)フェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-(メチルスルホニル)フェニル)-N-フェニルエタン-1-イミンを52.3mg(0.19mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を219.5mg(0.88mmol,4.7equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を14.0mg(0.06mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,4.1equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを10.8mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-(メチルスルホニル)フェニル)-1-プロペン-1-イル)メタンスルホンアミド(61%)及び中間体1,1,1-トリフルオロ-N-(1-(4-(メチルスルホニル)フェニル)ビニル)-N-フェニルメタンスルホンアミド(39%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が42.0mg(0.09mmol,46%)及び中間体が24.7mg(0.06mmol,18%)得られた。
1H-NMR(500MHz,CDCl3)δ7.87(d,J=8.0Hz,2H),7.41(d,J=8.6Hz,2H),7.30-7.35(m,3H),7.16(d,J=6.9Hz,2H),6.41(q,J=7.3Hz,1H),3.04(s,3H);19F-NMR(471MHz,CDCl3)δ-56.14(d,J=8.2Hz,3F),-72.43(s,3F)
実施例7 4-(3,3,3-トリフルオロ-1-((1,1,1-トリフルオロ-N-フェニルメチル)スルホンアミド)-1-プロペン-1-イル)安息香酸メチルの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-4-(1-(フェニルイミノ)エチル)安息香酸メチルを63.1mg(0.25mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を217.1mg(0.87mmol,3.5equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を12.8mg(0.06mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.1equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを21.3mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物4-(3,3,3-トリフルオロ-1-((1,1,1-トリフルオロ-N-フェニルメチル)スルホンアミド)-1-プロペン-1-イル)安息香酸メチル(71%)及び中間体4-(1-((1,1,1-トリフルオロ-N-フェニルメチル)スルホンアミド)ビニル)安息香酸メチル(24%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が59.2mg(0.13mmol,52%)及び中間体が17.9mg(0.05mmol,17%)得られた。
1H-NMR(500MHz,CDCl3)δ7.95(dt,J=8.4,1.9Hz,2H),7.32-7.27(m,5H),7.16(dt,J=6.3,1.9Hz,2H),6.37(q,J=7.3Hz,1H),3.90(s,3H);13C-NMR(126MHz,CDCl3)δ166.08,147.12(q,JC-F=6Hz),136.46,135.47,131.61,129.91,129.62,129.51,129.37,129.16,121.61(q,JC-F=271Hz),119.93(q,JC-F=324Hz),118.25(q,JC-F=35Hz),52.34;19F-NMR(471MHz,CDCl3)δ-56.21(d,J=6.8Hz,3F),-72.53(s,3F);HRMS(ESI-TOF)calcdforC18H12NO4F6S([M-1]-)452.0391,found452.0392
実施例8 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-シアノフェニル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(4-シアノフェニル)-N-フェニルエタン-1-イミンを54.4mg(0.25mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を215.4mg(0.87mmol,3.5equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を13.6mg(0.06mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.1equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを10.1mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-シアノフェニル)-1-プロペン-1-イル)メタンスルホンアミド(58%)及び中間体1,1,1-トリフルオロ-N-(1-(4-シアノフェニル)ビニル)-N-フェニルメタンスルホンアミド(26%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が45.6mg(0.11mmol,44%)及び中間体が20.7mg(0.06mmol,25%)得られた。
1H-NMR(500MHz,CDCl3)δ7.58(d,J=8.0Hz,2H),7.31-7.36(m,5H),7.15-7.16(m,2H),6.39(q,J=7.3Hz,1H);19F-NMR(471MHz,CDCl3)δ-56.20(d,J=8.2Hz,3F),-72.47(d,J=2.7Hz,3F)
実施例9 1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(ナフタレン-1-イル)-1-プロペン-1-イル)メタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ(E)-1-(ナフタレン-1-イル)-N-フェニルエタン-1-イミンを63.3mg(0.26mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を218.4mg(0.88mmol,3.4equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を11.0mg(0.05mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.13mL(0.77mmol,3.0equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを13.4mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(ナフタレン-1-イル)-1-プロペン-1-イル)メタンスルホンアミド(9%)及び中間体1,1,1-トリフルオロ-N-(1-(ナフタレン-1-イル)ビニル)-N-フェニルメタンスルホンアミド(79%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が8.5mg(0.02mmol,7%)及び中間体が61.1mg(0.16mmol,52%)得られた。
1H-NMR(500MHz,CDCl3)δ7.80(d,J=8.0Hz,1H),7.77(d,J=8.6Hz,1H),7.77(d,J=8.0Hz,1H),7.67(s,1H),7.54-7.47(m,2H),7.35(dd,J=8.6,1.7Hz,1H),7.25-7.19(m,5H),6.39(q,J=7.3Hz,1H);13C-NMR(126MHz,CDCl3)δ148.28(q,JC-F=6Hz),135.78,133.61,132.27,129.79,129.68,129.47,129.38,128.50,128.16,127.71,127.55,126.75,125.24,121.88(q,JC-F=270Hz),120.04(q,JC-F=325Hz),117.93(q,JC-F=35Hz);19F-NMR(471MHz,CDCl3)δ-56.05(d,J=8.2Hz,3F),-72.38(s,3F);HRMS(ESI-TOF)calcdforC20H12NO2F6S([M-1]-)444.0493,found444.0493
[実施例10]
1,1,1-トリフルオロ-N-(3,3,4,4,5,5,6,6,6-ノナフルオロ-1-(4-メトキシフェニル)-1-ヘキセン-1-イル)-N-フェニルメタンスルホンアミドの合成
10mL2口ナスフラスコに撹拌子を加えてフレームドライした。そこへ1,1,2,2,3,3,4,4,4-ノナフルオロ-N-(1-(4-メトキシフェニル)ビニル)-N-フェニルブタン-1-スルホンアミドを118.0mg(0.233mmol)、2,4,6-トリ-tert-ブチルピリミジン(TTBP)を145.5mg(0.586mmol,2.5equiv)、2,2’-アゾビス(イソ酪酸)ジメチル(V-601)を11.8mg(0.05mmol)加えて窒素置換した。次に1,2-ジクロロエタンを2mL、Tf2Oを0.08mL(0.47mmol,2.0equiv)加えて80℃で加熱しながら3時間攪拌した。室温まで攪拌後、1M塩酸を10mL加えて30分間攪拌した。その後ジクロロメタンで抽出して、硫酸ナトリウムで脱水した。これを1口ナスフラスコに移して濃縮した。内部標準として1,1,2,2-テトラクロロエタンを10.1mg(0.09mmol)加えてNMR測定を行った。得られた積分比から収率を算出し、目的生成物1,1,1-トリフルオロ-N-(3,3,4,4,5,5,6,6,6-ノナフルオロ-1-(4-メトキシフェニル)-1-ヘキセン-1-イル)-N-フェニルメタンスルホンアミド(71%)及び原料1,1,2,2,3,3,4,4,4-ノナフルオロ-N-(1-(4-メトキシフェニル)ビニル)-N-フェニルブタン-1-スルホンアミド(22%)がそれぞれ得られた。シリカゲルカラムクロマトグラフィーで単離精製を実施し、目的物が71.1mg(0.124mmol,53%)及び原料が23.8mg(0.05mmol,20%)得られた。
1H-NMR(500MHz,CDCl3)δ7.27-7.31(m,3H),7.15-7.19(m,4H),6.78(d,J=9.4Hz,2H),6.26(t,J=13.2Hz,1H),5.29(s,1H),3.77(s,3H),1.25-1.33(m,6H),0.89(t,J=6.9Hz,4H);19F-NMR(471MHz,CDCl3)δ-72.73--72.69(m,3F), -81.02--80.97(m,3F),-104.97--104.97(m,2F),-123.89--123.87(m,2F),-125.74--125.69(m,2F)
[実施例11]
当量数の検討
イミンに対するTf2Oの当量数を、表2のとおり検討した。Tf2O及び2,4,6-トリ-tert-ブチルピリミジン(TTBP)の使用量以外は、実施例1と同様の手順により反応を行った。
ここでの結果より、イミンに対するTf2Oが1.1モル当量以上のときに、目的物である1,1,1-トリフルオロ-N-フェニル-N-3,3,3-トリフルオロ-1-(4-メトキシフェニル)-1-プロペン-1-イル)メタンスルホンアミド(表2中、2の化合物)を確認することができた。