JP7674354B2 - 肝線維症および線維症に関連する他の疾患に対するエキソソームベースの療法 - Google Patents
肝線維症および線維症に関連する他の疾患に対するエキソソームベースの療法 Download PDFInfo
- Publication number
- JP7674354B2 JP7674354B2 JP2022533626A JP2022533626A JP7674354B2 JP 7674354 B2 JP7674354 B2 JP 7674354B2 JP 2022533626 A JP2022533626 A JP 2022533626A JP 2022533626 A JP2022533626 A JP 2022533626A JP 7674354 B2 JP7674354 B2 JP 7674354B2
- Authority
- JP
- Japan
- Prior art keywords
- fibrosis
- stat3
- pharmaceutical composition
- exosomes
- liver
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/51—Nanocapsules; Nanoparticles
- A61K9/5107—Excipients; Inactive ingredients
- A61K9/5176—Compounds of unknown constitution, e.g. material from plants or animals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/10—Dispersions; Emulsions
- A61K9/127—Synthetic bilayered vehicles, e.g. liposomes or liposomes with cholesterol as the only non-phosphatidyl surfactant
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/047—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates having two or more hydroxy groups, e.g. sorbitol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/05—Phenols
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/045—Hydroxy compounds, e.g. alcohols; Salts thereof, e.g. alcoholates
- A61K31/05—Phenols
- A61K31/055—Phenols the aromatic ring being substituted by halogen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/14—Quaternary ammonium compounds, e.g. edrophonium, choline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/13—Amines
- A61K31/155—Amidines (), e.g. guanidine (H2N—C(=NH)—NH2), isourea (N=C(OH)—NH2), isothiourea (—N=C(SH)—NH2)
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/28—Compounds containing heavy metals
- A61K31/305—Mercury compounds
- A61K31/31—Mercury compounds containing nitrogen
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4178—1,3-Diazoles not condensed 1,3-diazoles and containing further heterocyclic rings, e.g. pilocarpine, nitrofurantoin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4425—Pyridinium derivatives, e.g. pralidoxime, pyridostigmine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/7105—Natural ribonucleic acids, i.e. containing only riboses attached to adenine, guanine, cytosine or uracil and having 3'-5' phosphodiester links
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7088—Compounds having three or more nucleosides or nucleotides
- A61K31/713—Double-stranded nucleic acids or oligonucleotides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K48/00—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy
- A61K48/0008—Medicinal preparations containing genetic material which is inserted into cells of the living body to treat genetic diseases; Gene therapy characterised by an aspect of the 'non-active' part of the composition delivered, e.g. wherein such 'non-active' part is not delivered simultaneously with the 'active' part of the composition
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/50—Microcapsules having a gas, liquid or semi-solid filling; Solid microparticles or pellets surrounded by a distinct coating layer, e.g. coated microspheres, coated drug crystals
- A61K9/5005—Wall or coating material
- A61K9/5063—Compounds of unknown constitution, e.g. material from plants or animals
- A61K9/5068—Cell membranes or bacterial membranes enclosing drugs
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/113—Non-coding nucleic acids modulating the expression of genes, e.g. antisense oligonucleotides; Antisense DNA or RNA; Triplex- forming oligonucleotides; Catalytic nucleic acids, e.g. ribozymes; Nucleic acids used in co-suppression or gene silencing
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/11—Antisense
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2310/00—Structure or type of the nucleic acid
- C12N2310/10—Type of nucleic acid
- C12N2310/14—Type of nucleic acid interfering nucleic acids [NA]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/31—Combination therapy
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2320/00—Applications; Uses
- C12N2320/30—Special therapeutic applications
- C12N2320/32—Special delivery means, e.g. tissue-specific
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Epidemiology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Molecular Biology (AREA)
- Genetics & Genomics (AREA)
- Organic Chemistry (AREA)
- Biomedical Technology (AREA)
- Zoology (AREA)
- Biochemistry (AREA)
- Biotechnology (AREA)
- Wood Science & Technology (AREA)
- General Engineering & Computer Science (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Physics & Mathematics (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Dermatology (AREA)
- Botany (AREA)
- Plant Pathology (AREA)
- Microbiology (AREA)
- Nanotechnology (AREA)
- Optics & Photonics (AREA)
- Dispersion Chemistry (AREA)
- Cell Biology (AREA)
- Virology (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Description
本願は、2019年12月5日に出願された米国特許仮出願第62/943,943号の優先権の恩典を主張する。米国特許仮出願第62/943,943号は、その全体が参照により本明細書に組み入れられる。
本発明は全体として医学分野に関する。さらに具体的には、本発明は、線維症および線維症に関連する疾患を処置するための組成物および方法に関する。
肝線維症は肝臓における過剰な細胞外マトリックス(ECM)沈着を特徴とし、この沈着は機能的な実質に取って代わり、世界中で健康に重大な影響を及ぼしている(Hernandez-Gea et al., 2001)。現在のところ、継続した肝臓損傷の軽減または肝臓移植を除いて有効な抗線維症療法はない(Bataller et al., 2005)。肝線維症に対する有効な処置は革新的な新手法を緊急に必要としている。重要な肝線維症制御因子中でシグナル伝達性転写因子3(STAT3)シグナル伝達経路は中心で関係しており、線維芽細胞と肝臓星状細胞(HSC)の活性化と、これらの細胞の筋線維芽細胞様表現型への変換を引き起こす(Chakraborty et al., 2017; Xiang et al., 2018; Pechkovsky et al., 2012)。STAT3は、サイトカイン活性化に応答してヤヌスチロシンキナーゼ(JAK)によってリン酸化される転写因子である。リン酸化STAT3は活性化されると二量体化し、核に移動してサイトカイン応答性下流遺伝子の転写を活性化する(Chakraborty et al., 2017)。STAT3を活性化するサイトカインには、TGFβ1(Meng et al., 2016)、サイトカインのIL-6ファミリー、および成長ホルモン(GH)が含まれる。STAT3活性化は、患者とマウスモデルにおいて観察される線維症肝臓において報告されており(Xiang et al., 2018; Choi et al., 2019)、ソラフェニブまたは他の阻害物質を用いたSTAT3阻害はマウスのCCl4誘導性肝線維症を部分的に寛解させる(Choi et al., 2019; Su et al., 2015)。STAT3は肝線維症の重要な弱点として現れたが、STAT3特異的阻害物質が無いために、STAT3を治療標的とすることは依然として難題である(Bartneck et al., 2014)。従って、特異的な抗線維症療法を開発するためにSTAT3シグナル伝達を阻害する新たな手段が必要とされている。
本開示の態様は、ナノ粒子、組成物、薬学的組成物、核酸、阻害RNA分子、治療用組成物を調製するための方法、エキソソームを単離するための方法、脂質ベースナノ粒子を調製するための方法、および対象を処置するための方法を含む。本開示の組成物は、以下の成分:リポソーム、エキソソーム、阻害RNA、siRNA、shRNA、miRNA、増殖因子、非修飾アンチセンスオリゴヌクレオチド、修飾アンチセンスオリゴヌクレオチド、および抗菌剤のうちの少なくとも1つ、2つ、3つ、4つ、5つ、またはそれ以上を含んでもよい。一部の態様では、これらの成分のいずれか1つまたはそれ以上が本開示の組成物から除外され得る。本開示の方法は、以下の工程:薬学的組成物を投与する工程、エキソソームを投与する工程、リポソームを投与する工程、阻害RNAを投与する工程、リポソームを作製する工程、対象からエキソソームを得る工程、間葉系細胞からエキソソームを精製する工程、阻害RNAを作製する工程、siRNAを合成する工程、脂質ナノ粒子を調製する工程、阻害RNAを脂質ベースナノ粒子に導入する工程、阻害RNAをナノ粒子にカプセル化する工程、線維症を有すると対象を診断する工程、および対象の線維症を処置する工程のうちの少なくとも1つ、2つ、3つ、4つ、またはそれ以上を含んでもよい。一部の態様では、これらの工程のいずれか1つまたは複数が本開示の方法から除外され得ることが意図される。
STAT3ポリヌクレオチドにハイブリダイズする阻害RNAを含有する脂質ベースナノ粒子を含む、組成物。
[本発明1002]
前記脂質ベースナノ粒子がその表面にCD47を含む、本発明1001の組成物。
[本発明1003]
前記脂質ベースナノ粒子がその表面に増殖因子を含む、本発明1001または1002の組成物。
[本発明1004]
前記脂質ベースナノ粒子がリポソームまたはエキソソームである、本発明1001~1003のいずれかの組成物。
[本発明1005]
前記阻害RNAが、siRNA、shRNA、アンチセンスオリゴヌクレオチド、miRNA、またはプレmiRNAである、本発明1001~1004のいずれかの組成物。
[本発明1006]
前記阻害RNAがアンチセンスオリゴヌクレオチドであり、かつ前記アンチセンスオリゴヌクレオチドが修飾されている、本発明1005の組成物。
[本発明1007]
前記阻害RNAがSTAT3タンパク質の発現をノックダウンする、本発明1001~1006のいずれかの組成物。
[本発明1008]
前記阻害RNAのサイズが18~30ヌクレオチドである、本発明1001~1007のいずれかの組成物。
[本発明1009]
前記阻害RNAがSEQ ID NO:1を含む、本発明1001~1008のいずれかの組成物。
[本発明1010]
前記阻害RNAがSEQ ID NO:2を含む、本発明1001~1008のいずれかの組成物。
[本発明1011]
前記阻害RNAがSEQ ID NO:3を含む、本発明1001~1008のいずれかの組成物。
[本発明1012]
前記阻害RNAがSEQ ID NO:4を含む、本発明1001~1008のいずれかの組成物。
[本発明1013]
前記阻害RNAがSEQ ID NO:5を含む、本発明1001~1008のいずれかの組成物。
[本発明1014]
本発明1001~1013のいずれかの組成物と賦形剤とを含む、薬学的組成物。
[本発明1015]
非経口投与用に製剤化されている、本発明1014の薬学的組成物。
[本発明1016]
静脈内注射、筋肉内注射、皮下注射、または腹腔内注射用に製剤化されている、本発明1015の薬学的組成物。
[本発明1017]
抗菌剤をさらに含む、本発明1014~1016のいずれかの薬学的組成物。
[本発明1018]
前記抗菌剤が、塩化ベンザルコニウム、塩化ベンゼトニウム、ベンジルアルコール、ブロノポール、セントリミド(centrimide)、塩化セチルピリジニウム、クロルヘキシジン、クロロブタノール、クロロクレゾール、クロロキシレノール、クレゾール、エチルアルコール、グリセリン、エキセチジン(exetidine)、イミド尿素、フェノール、フェノキシエタノール、フェニルエチルアルコール、硝酸フェニル水銀、プロピレングリコール、またはチメロサールである、本発明1017の薬学的組成物。
[本発明1019]
その必要がある患者において線維症または線維症に関連する状態を処置する方法であって、本発明1014~1018のいずれかの薬学的組成物を前記患者に投与する工程を含む、前記方法。
[本発明1020]
前記薬学的組成物を投与する工程が、前記患者における細胞への前記阻害RNAの送達をもたらす、本発明1019の方法。
[本発明1021]
前記線維症が、肝線維症、肺線維症、肺性線維症、嚢胞性線維症、特発性肺線維症(IPF)、または放射線誘発性肺損傷である、本発明1019または1020の方法。
[本発明1022]
前記線維症が肝線維症である、本発明1021の方法。
[本発明1023]
前記薬学的組成物が全身投与によって投与される、本発明1019~1021のいずれかの方法。
[本発明1024]
前記全身投与が静脈内投与である、本発明1023の方法。
[本発明1025]
少なくとも第2の療法を前記患者に実施する工程をさらに含む、本発明1019~1024のいずれかの方法。
[本発明1026]
前記患者がヒトである、本発明1019~1025のいずれかの方法。
[本発明1027]
前記脂質ベースナノ粒子がエキソソームであり、前記エキソソームが前記患者にとって自己由来である、本発明1026の方法。
[本発明1028]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるCol1a1発現を低減させる、本発明1019~1027のいずれかの方法。
[本発明1029]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるActa2発現を低減させる、本発明1019~1027のいずれかの方法。
[本発明1030]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるCol1a2発現を低減させる、本発明1019~1027のいずれかの方法。
[本発明1031]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるVim発現を低減させる、本発明1019~1027のいずれかの方法。
[本発明1032]
前記肝細胞が肝臓星状細胞である、本発明1019~1031のいずれかの方法。
[本発明1033]
前記肝臓星状細胞が活性化肝臓星状細胞である、本発明1019~1031のいずれかの方法。
[本発明1034]
STAT3ポリヌクレオチドにハイブリダイズする阻害RNAを含有する脂質ベースナノ粒子を含む、組成物。
[本発明1035]
前記脂質ベースナノ粒子がその表面にCD47を含む、本発明1034の組成物。
[本発明1036]
前記脂質ベースナノ粒子がその表面に増殖因子を含む、本発明1034の組成物。
[本発明1037]
前記脂質ベースナノ粒子がリポソームまたはエキソソームである、本発明1034の組成物。
[本発明1038]
前記阻害RNAが、siRNA、shRNA、アンチセンスオリゴヌクレオチド、miRNA、またはプレmiRNAである、本発明1034の組成物。
[本発明1039]
前記阻害RNAがアンチセンスオリゴヌクレオチドであり、かつ前記アンチセンスオリゴヌクレオチドが修飾されている、本発明1038の組成物。
[本発明1040]
前記阻害RNAがSTAT3タンパク質の発現をノックダウンする、本発明1034の組成物。
[本発明1041]
前記阻害RNAのサイズが18~30ヌクレオチドである、本発明1034の組成物。
[本発明1042]
前記阻害RNAがSEQ ID NO:1を含む、本発明1034の組成物。
[本発明1043]
前記阻害RNAがSEQ ID NO:2を含む、本発明1034の組成物。
[本発明1044]
前記阻害RNAがSEQ ID NO:3を含む、本発明1034の組成物。
[本発明1045]
前記阻害RNAがSEQ ID NO:4を含む、本発明1034の組成物。
[本発明1046]
前記阻害RNAがSEQ ID NO:5を含む、本発明1034の組成物。
[本発明1047]
本発明1034~1046のいずれかの組成物と賦形剤とを含む、薬学的組成物。
[本発明1048]
非経口投与用に製剤化されている、本発明1047の薬学的組成物。
[本発明1049]
静脈内注射、筋肉内注射、皮下注射、または腹腔内注射用に製剤化されている、本発明1048の薬学的組成物。
[本発明1050]
抗菌剤をさらに含む、本発明1048の薬学的組成物。
[本発明1051]
前記抗菌剤が、塩化ベンザルコニウム、塩化ベンゼトニウム、ベンジルアルコール、ブロノポール、セントリミド、塩化セチルピリジニウム、クロルヘキシジン、クロロブタノール、クロロクレゾール、クロロキシレノール、クレゾール、エチルアルコール、グリセリン、エキセチジン、イミド尿素、フェノール、フェノキシエタノール、フェニルエチルアルコール、硝酸フェニル水銀、プロピレングリコール、またはチメロサールである、本発明1050の薬学的組成物。
[本発明1052]
その必要がある患者において線維症または線維症に関連する状態を処置する方法であって、本発明1047~1051のいずれかの薬学的組成物を前記患者に投与する工程を含む、前記方法。
[本発明1053]
前記薬学的組成物を投与する工程が、前記患者における細胞への前記阻害RNAの送達をもたらす、本発明1052の方法。
[本発明1054]
前記線維症が、肝線維症、肺線維症、肺性線維症、嚢胞性線維症、特発性肺線維症(IPF)、または放射線誘発性肺損傷である、本発明1052の方法。
[本発明1055]
前記線維症が肝線維症である、本発明1054の方法。
[本発明1056]
前記薬学的組成物が全身投与によって投与される、本発明1052の方法。
[本発明1057]
前記全身投与が静脈内投与である、本発明1056の方法。
[本発明1058]
少なくとも第2の療法を前記患者に実施する工程をさらに含む、本発明1052の方法。
[本発明1059]
前記患者がヒトである、本発明1052の方法。
[本発明1060]
前記脂質ベースナノ粒子がエキソソームであり、前記エキソソームが前記患者にとって自己由来である、本発明1059の方法。
[本発明1061]
前記エキソソームが、前記患者から得られる体液試料から得られる、本発明1060の方法。
[本発明1062]
前記体液試料が、血液、リンパ液、唾液、尿、脳脊髄液、骨髄吸引液、眼滲出物/涙、または血清である、本発明1061の方法。
[本発明1063]
前記エキソソームが間葉系細胞から得られる、本発明1060の方法。
[本発明1064]
前記組成物が1回より多く投与される、本発明1052の方法。
[本発明1065]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるCol1a1発現を低減させる、本発明1052の方法。
[本発明1066]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるActa2発現を低減させる、本発明1052の方法。
[本発明1067]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるCol1a2発現を低減させる、本発明1052の方法。
[本発明1068]
前記薬学的組成物を投与する工程が、前記患者の肝細胞におけるVim発現を低減させる、本発明1052の方法。
[本発明1069]
前記肝細胞が肝臓星状細胞である、本発明1052の方法。
[本発明1070]
前記肝臓星状細胞が活性化肝臓星状細胞である、本発明1052の方法。
[本発明1071]
STAT3ポリヌクレオチドにハイブリダイズする阻害RNAを脂質ベースナノ粒子に導入する工程を含む、治療用組成物を調製する方法。
[本発明1072]
前記脂質ベースナノ粒子がその表面にCD47を含む、本発明1071の方法。
[本発明1073]
前記脂質ベースナノ粒子がその表面に増殖因子を含む、本発明1071または1072の方法。
[本発明1074]
前記脂質ベースナノ粒子がリポソームまたはエキソソームである、本発明1071~1073のいずれかの方法。
[本発明1075]
前記阻害RNAが、siRNA、shRNA、アンチセンスオリゴヌクレオチド、miRNA、またはプレmiRNAである、本発明1071~1074のいずれかの方法。
[本発明1076]
前記阻害RNAがアンチセンスオリゴヌクレオチドであり、かつ前記アンチセンスオリゴヌクレオチドが修飾されている、本発明1075の方法。
[本発明1077]
前記阻害RNAがSTAT3タンパク質の発現をノックダウンする、本発明1071~1076のいずれかの方法。
[本発明1078]
前記阻害RNAのサイズが18~30ヌクレオチドである、本発明1071~1077のいずれかの方法。
[本発明1079]
前記阻害RNAがSEQ ID NO:1を含む、本発明1071~1078のいずれかの方法。
[本発明1080]
前記阻害RNAがSEQ ID NO:2を含む、本発明1071~1078のいずれかの方法。
[本発明1081]
前記阻害RNAがSEQ ID NO:3を含む、本発明1071~1078のいずれかの方法。
[本発明1082]
前記阻害RNAがSEQ ID NO:4を含む、本発明1071~1078のいずれかの方法。
[本発明1083]
前記阻害RNAがSEQ ID NO:5を含む、本発明1071~1078のいずれかの方法。
本発明の他の目的、特徴、および利点は以下の詳細な説明から明らかになる。しかしながら、詳細な説明および具体的な実施例は、本発明の、ある特定の態様を示しているが、この詳細な説明から本発明の精神および範囲の中で様々な修正および変更が当業者に明らかになるので例示にすぎないことが理解されるはずである。
肝線維症および肺線維症を含む臓器線維症のメディエーターであるSTAT3を標的とする、アンチセンスオリゴヌクレオチド(ASO)およびsiRNAを含む阻害RNA分子を運搬するように操作されたエキソソームが本明細書において提供される。これらの操作されたエキソソームは、肝線維症および肺線維症を含む線維症を処置するのに使用することができる。間葉系幹細胞から得られたエキソソームは肺と肝臓に非常に多く分布するので、ASOまたはsiRNAの送達は効率的になる。
脂質ベースナノ粒子は、リポソーム、エキソソーム、脂質調製物、または別の脂質ベースナノ粒子、例えば、脂質ベース小胞(例えば、DOTAP:コレステロール小胞)である。脂質ベースナノ粒子は正に荷電してもよく、負に荷電していてもよく、中性でもよい。脂質ベースナノ粒子は、転写および翻訳、シグナル伝達、走化性、または他の細胞機能を可能にする必要な成分を含んでもよい。一態様では、これらの項目のうちの1つまたは複数が除外され得ることが意図される。
「リポソーム」は、閉じた脂質二重層または凝集物を生じることで形成される様々な単一膜および多重膜の脂質ビヒクルを含む総称的な用語である。リポソームは、一般的にリン脂質を含む二重層膜を有する小胞構造と、一般的に水性組成物を含む内部媒体を有すると特徴付けられることがある。本明細書において提供されるリポソームには、単層リポソーム、多重膜リポソーム、および多胞体リポソーム(multivesicular liposome)が含まれる。本明細書において提供されるリポソームは正に荷電してもよく、負に荷電していてもよく、中性に荷電していてもよい。ある特定の態様では、リポソームは電荷が中性である。
本明細書で使用する「マイクロベシクル」および「エキソソーム」という用語は、直径(または粒子がスフェロイドでない場合は最大の寸法)が約10nm~約5000nm、より典型的には30nm~1000nm、最も典型的には約50nm~750nmであり、エキソソームの膜の少なくとも一部が細胞から直接得られている膜状粒子を指す。本開示のエキソソームの直径は、少なくとも10nm、20nm、30nm、40nm、50nm、60nm、70nm、80nm、90nm、100nm、200nm、300nm、400nm、500nm、600nm、700nm、800nm、900nm、1000nm、2000nm、3000nm、4000nm、もしくは5000nm、またはその中で導き出せる任意の範囲、多くても10nm、20nm、30nm、40nm、50nm、60nm、70nm、80nm、90nm、100nm、200nm、300nm、400nm、500nm、600nm、700nm、800nm、900nm、1000nm、2000nm、3000nm、4000nm、もしくは5000nm、またはその中で導き出せる任意の範囲、または、約10nm、20nm、30nm、40nm、50nm、60nm、70nm、80nm、90nm、100nm、200nm、300nm、400nm、500nm、600nm、700nm、800nm、900nm、1000nm、2000nm、3000nm、4000nm、もしくは5000nm、またはその中で導き出せる任意の範囲でもよい。最も一般的には、エキソソームのサイズ(平均直径)はドナー細胞のサイズの5%までである。従って、特に意図されるエキソソームには、細胞から脱落したエキソソームが含まれる。
翌日に細胞が約70%コンフルエントになるように、1日目に、10%FBSを含有する培地が入っているT225フラスコに、十分な数の細胞(例えば、約500万個の細胞)を播種する。2日目に、細胞の表面にある培地を吸引し、細胞をPBSで2回洗浄し、次いで、25~30mLの基本培地(すなわち、PenStrepもFBSも無い)を細胞に添加する。細胞を24~48時間インキュベートする。48時間のインキュベーションが好ましいが、細胞株の中には無血清培地に対して感受性が高いものもあり、そのため、インキュベーション時間を24時間に短縮しなければならない。FBSは、NanoSight結果を強くゆがめるエキソソームを含有することに留意のこと。
最初に、血清試料を氷上で解凍する。次いで、250μLの無細胞血清試料を11mLのPBSで希釈する。0.2μm孔フィルターで濾過する。希釈した試料を150,000×gで4℃で一晩超遠心分離する。翌日、上清を注意深く捨て、11mL PBSでエキソソームペレットを洗浄する。150,000×gで4℃で2時間、2回目の超遠心分離を行う。最後に、上清を注意深く捨て、分析のために100μL PBSにエキソソームペレットを再懸濁する。
1×108個のエキソソーム(NanoSight分析によって測定した)または100nmリポソーム(例えば、Encapsula Nano Sciencesから購入した)と、1μgのsiRNA(Qiagen)またはshRNAを400μLのエレクトロポレーション緩衝液(1.15mMリン酸カリウム, pH7.2、25mM塩化カリウム、21%Optiprep)に入れて混合する。4mmキュベットを用いてエキソソームまたはリポソームを電気穿孔する(例えば、Alvarez-Erviti et al., 2011; El-Andaloussi et al., 2012を参照されたい)。エレクトロポレーション後に、エキソソームまたはリポソームをプロテアーゼフリーRNaseで処理し、その後に10×濃縮RNAse阻害物質を添加する。最後に、前記のように超遠心分離法下でエキソソームまたはリポソームをPBSで洗浄する。
A.アンチセンスオリゴヌクレオチド
アンチセンスオリゴヌクレオチド(ASO)治療用物質は、典型的に長さが約16~30ヌクレオチドの一本鎖核酸治療剤であり、培養状態の標的細胞中または生物における標的細胞中の標的核酸配列に対して相補的である。
ある特定の態様では、本開示のASOは修飾されてもよい。「修飾ASO」とは、核酸成分、すなわち、糖、塩基、およびリン酸部分のうちの1つまたは複数が天然で生じるものとは異なる分子、例えば、ヒトの体内で生じるものとは異なる分子を指す。ASOに対する、いくつかの修飾が当技術分野において説明される。これらの修飾は、標的mRNAに対する特異性を維持しながら、ASO特性、例えば、ヌクレアーゼに対する耐性、生体膜を横断する透過性、可溶性、安定性、または薬物動態学的特性および薬物動力学的特性の調整を改善することを目的とする。例えば、ヌクレオチド上の修飾には、LNA、HNA、CeNA、2'-メトキシエチル、2'-O-アルキル、2'-O-アリル、2'-C-アリル、2'-フルオロ、2'-デオキシ、2'-ヒドロキシル、およびその組み合わせが含まれ得るが、これに限定されない。一態様では、これらの修飾のうちの1つまたは複数が除外され得ると意図される。
治療用核酸は、天然塩基(すなわち、A、G、U、C、またはT)を含んでもよく、修飾塩基(例えば、7-デアザグアノシン、イノシンなど)を含んでもよい。塩基の修飾は、リボ核酸(すなわち、A、C、G、およびU)ならびにデオキシリボ核酸(すなわち、A、C、G、およびT)において生じる標準的な塩基、糖、および/またはリン酸バックボーン化学構造のバリエーションである修飾塩基(または修飾ヌクレオシドもしくは修飾ヌクレオチド)の組み込みを含む。この範囲に含まれるものは、例えば、Gm(2'-メトキシグアニル酸)、Am(2'-メトキシアデニル酸)、Cf(2'-フルオロシチジル酸)、Uf(2'-フルオロウリジル酸)、Ar(リボアデニル酸)である。アプタマーはまた、シトシン、または5-メチルシトシン、4-アセチルシトシン、3-メチルシトシン、5-ヒドロキシメチルシトシン、2-チオシトシン、5-ハロシトシン(例えば、5-フルオロシトシン、5-ブロモシトシン、5-クロロシトシン、および5-ヨードシトシン)、5-プロピニルシトシン、6-アゾシトシン、5-トリフルオロメチルシトシン、N4,N4-エタノシトシン、フェノキサジンシチジン、フェノチアジンシチジン、カルバゾールシチジン、もしくはピリドインドールシチジンを含む任意のシトシン関連塩基も含んでもよい。アプタマーは、グアニン、または6-メチルグアニン、1-メチルグアニン、2,2-ジメチルグアニン、2-メチルグアニン、7-メチルグアニン、2-プロピルグアニン、6-プロピルグアニン、8-ハログアニン(例えば、8-フルオログアニン、8-ブロモグアニン、8-クロログアニン、および8-ヨードグアニン)、8-アミノグアニン、8-スルフヒドリルグアニン、8-チオアルキルグアニン、8-ヒドロキシグアニン、7-メチルグアニン、8-アザグアニン、7-デアザグアニン、もしくは3-デアザグアニンを含む任意のグアニン関連塩基をさらに含んでもよい。アプタマーは、アデニン、または6-メチルアデニン、N6-イソペンテニルアデニン、N6-メチルアデニン、1-メチルアデニン、2-メチルアデニン、2-メチルチオ-N6-イソペンテニルアデニン、8-ハロアデニン(例えば、8-フルオロアデニン、8-ブロモアデニン、8-クロロアデニン、および8-ヨードアデニン)、8-アミノアデニン、8-スルフヒドリルアデニン、8-チオアルキルアデニン、8-ヒドロキシアデニン、7-メチルアデニン、2-ハロアデニン(例えば、2-フルオロアデニン、2-ブロモアデニン、2-クロロアデニン、および2-ヨードアデニン)、2-アミノアデニン、8-アザアデニン、7-デアザアデニン、もしくは3-デアザアデニンを含む任意のアデニン関連塩基をさらに含んでもよい。ウラシル、または5-ハロウラシル(例えば、5-フルオロウラシル、5-ブロモウラシル、5-クロロウラシル、5-ヨードウラシル)、5-(カルボキシヒドロキシメチル)ウラシル、5-カルボキシメチルアミノメチル-2-チオウラシル、5-カルボキシメチルアミノメチルウラシル、ジヒドロウラシル、1-メチルプソイドウラシル、5-メトキシアミノメチル-2-チオウラシル、5'-メトキシカルボニルメチルウラシル、5-メトキシウラシル、5-メチル-2-チオウラシル、2-チオウラシル、4-チオウラシル、5-メチルウラシル、ウラシル-5-オキシ酢酸メチルエステル、ウラシル-5-オキシ酢酸、プソイドウラシル、5-メチル-2-チオウラシル、2-チオウラシル、3-(3-アミノ-3-N-2-カルボキシプロピル)ウラシル、5-メチルアミノメチルウラシル、5-プロピニルウラシル、6-アゾウラシル、または4-チオウラシルを含む任意のウラシル関連塩基も含まれる。
ASOにおいて使用するための修飾糖部分は当技術分野において周知であり、例えば、その全体が参照により本明細書に組み入れられる米国特許第9,045,754号で説明されている。修飾糖は、ASO標的に対するASOの親和性を変える、典型的には高める、および/またはヌクレアーゼ耐性を高めるのに使用することができる。例えば、一部の態様では、ASO標的に対するASOの結合親和性は、ASOのヌクレオシドサブユニットに置換基を組み込むことによって高めることができる。一部の態様では、置換基は、ASOのヌクレオシドサブユニットのペントフラノシル糖部分の2'位置に位置する置換基であるT置換基である。置換基には、フルオロ、アルコキシ、アミノ-アルコキシ、アリルオキシ、イミダゾリルアルコキシ、およびポリエチレングリコールが含まれるが、これに限定されない。アルコキシおよびアミノアルコキシ基は、一般的に、低級アルキル基、特に、C1~C9アルキルを含む。特定の態様では、2'置換基は2'-O-メチルである。ポリエチレングリコールは、構造(O-CH2-CH2)n-O-アルキルのものである。特定の態様では、置換基は、式(-O-CH2-CH2)n-O-アルキルのポリエチレングリコール置換基であり、n=1およびアルキル=CH3である。この修飾は、オリゴヌクレオチド標的に対するオリゴヌクレオチドの親和性とオリゴヌクレオチドのヌクレアーゼ耐性を高めることが示されている。上記で引用された米国特許第7,629,321号を参照されたい。結合親和性を高めるためのさらなる特に有用な2'-置換基は2'-フルオロ基である。
核酸治療剤は少なくとも1つのホスホロチオエートまたはメチルホスホネートヌクレオチド間結合をさらに含んでもよい。ホスホロチオエートまたはメチルホスホネートヌクレオチド間結合修飾は、センス鎖もしくはアンチセンス鎖または(センス鎖を含む核酸治療剤中の)その両方の鎖の任意の位置にある任意のヌクレオチド上にあってもよい。例えば、ヌクレオチド間結合修飾は、センス鎖上またはアンチセンス鎖上にある、あらゆるヌクレオチドにあってもよい。それぞれのヌクレオチド間結合修飾は、センス鎖上またはアンチセンス鎖上にある互い違いのパターンであってもよい。または、センス鎖またはアンチセンス鎖は互い違いのパターンでヌクレオチド間結合修飾を含有してもよい。センス鎖上にあるヌクレオチド間結合修飾の互い違いのパターンはアンチセンス鎖と同じでも、異なってもよく、センス鎖上にあるヌクレオチド間結合修飾の互い違いのパターンには、アンチセンス鎖上にあるヌクレオチド間結合修飾の互い違いのパターンと比べて変化があってもよい。
siRNA(例えば、siNA)は当技術分野において周知である。例えば、siRNAおよび二本鎖RNAは米国特許第6,506,559号および同第6,573,099号、ならびに米国特許出願第2003/0051263号、同第2003/0055020号、同第2004/0265839号、同第2002/0168707号、同第2003/0159161号、および同第2004/0064842号で記載されている。これらは全て、その全体が参照により本明細書に組み入れられる。
ヒトを含む哺乳動物の多数の重篤な疾患が線維症と関連する。本明細書で使用する「線維症」とは、(このような形成が望ましいものでも、望ましいものでなくても)線維組織の形成を伴う任意の状態を含む。このような状態には、結合組織炎症、線維腫形成(線維腫症)、線維症(肺線維症および肝線維症を含む)、線維弾性症(心内膜線維)、フィブロミオパシー(fibromyopathy)形成、子宮筋腫形成、フィブロイドーマ(fibroidoma)形成、線維粘液腫形成、およびフィブロシストーシス(fibrocystitis)(嚢胞性線維症を含む)が含まれるが、これに限定されない。
治療用物質を発現するかまたは治療用物質を含むエキソソームを全身投与または局所投与して、テロメラーゼ活性を高めることができると意図される。治療用物質を発現するかまたは治療用物質を含むエキソソームは静脈内投与、くも膜下腔内投与、および/または腹腔内投与することができる。治療用物質を発現するかまたは治療用物質を含むエキソソームは単独で投与されてもよく、第2の薬物と組み合わせて投与されてもよい。
本開示の様々な局面では、エキソソームを体液または組織培養培地から精製するための必要な成分を含むキットが想定される。他の局面では、エキソソームを単離し、治療用核酸、治療用タンパク質、または阻害RNAでトランスフェクトするための必要な成分を含むキットが想定される。キットは、このような任意の成分を含む1つまたは複数の密封したバイアルを含んでもよい。一部の態様では、キットはまた、キットの成分と反応しない容器である適切な容器手段、例えば、エッペンドルフチューブ、アッセイプレート、注射器、瓶、またはチューブも備えてよい。容器は、プラスチックまたはガラスなどの滅菌可能な材料から作られてもよい。キットは、本明細書において説明される方法の手順工程を概説する指示書をさらに備えてもよく、本明細書に記載のものと実質的に同じ手順に従うか、または当業者に公知である。指示書の情報は、コンピュータを用いて実行された時に、試料からエキソソームを精製し、エキソソームを治療用カーゴでトランスフェクトする現実または仮想の手順を表示する機械可読指示書を備えるコンピュータ可読媒体の中にあってもよい。
以下の実施例は、本発明のある特定の態様を証明するために含まれる。以下の実施例に開示される技法は、本発明者が発見した技法が本発明の実施において十分に機能することを示し、従って、本発明を実施するための好ましい態様を構成すると考えられると当業者に理解されるはずである。しかしながら、本開示を考慮すれば、本発明の精神および範囲から逸脱することなく、開示された特定の態様において多くの変更を加えることができ、それでもなお、類似または同様の結果を得ることができると当業者に理解されるはずである。
Balb/c成獣マウスにCC14を6週間、隔週でi.p.注射することによって肝線維症を誘導した。肝線維症を有するマウスと肝線維症を有さないマウスに両方とも109個の色素標識エキソソームまたは色素のみを静脈内投与した。投与して3時間後にマウスを安楽死させた。マウスに与えたDiR標識エキソソームはIVISイメージングを用いてアッセイした(図1)。マウスに与えたPHK67標識エキソソームは共焦点顕微鏡観察を用いてアッセイした。エキソソームは健常マウスおよび線維症マウスの両方の肝臓に局在化した。しかしながら、健常マウスと比べて線維症マウスでは局在化レベルが増加した。
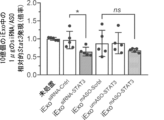
C57Bl6成獣マウスにCC14を6週間、隔週でi.p.注射することによって肝線維症を誘導した。次いで、MSC由来エキソソーム(1回の注射あたり、1用量につき1.5μgのsiRNAまたはASOを含む15億個のエキソソーム)を48時間ごとに投与した。エキソソームは、スクランブルドsiRNA、STAT3 siRNA、非修飾STAT3アンチセンスオリゴヌクレオチド、修飾スクランブルドアンチセンスオリゴヌクレオチド、または修飾STAT3アンチセンスオリゴヌクレオチドを含有した。処置後にマウスを安楽死させ、その肝臓を切片化し、ヘマトキシリンおよびエオシン(H&E)染色のために処理し、染色切片を画像化した(図2A)。線維症レベルを定量した(図2B)。結果から、STAT3 siRNA、非修飾STAT3アンチセンスオリゴヌクレオチド、および修飾STAT3アンチセンスオリゴヌクレオチドは線維症レベルを低減したことが分かる。
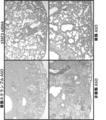
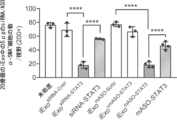
マウスにブレオマイシンを用いて肺線維症を誘導した。次いで、MSC由来エキソソーム(1回の注射あたり、1用量につき5μgのsiRNAまたはASOを含む20億個のエキソソーム)を48時間ごとに投与した。エキソソームは、STAT3 siRNA、非修飾STAT3アンチセンスオリゴヌクレオチド、修飾スクランブルドアンチセンスオリゴヌクレオチド、または修飾STAT3アンチセンスオリゴヌクレオチドを含有した。処置後にマウスを安楽死させ、その肺を切片化し、ヘマトキシリンおよびエオシン(H&E)染色のために処理し、染色切片を画像化した(図3A)。線維症レベルを定量した(図3B)。結果から、STAT3 siRNAは線維症レベルを最も大きく減少させたことが分かる。
結果
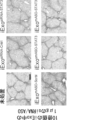
STAT3を標的とするsiRNAまたはASOをロードしたiExosome(核酸ペイロードを送達するように操作されたエキソソーム)の効率を確かめるために、野生型(WT)マウスから単離した初代肝臓星状細胞(HSC)を7日間培養した。これによりHSCは自発的に活性化した(図4A)(Zhai et al., 2019; Lu et al., 2014; Mederacke et al., 2013)。HSCの活性化はα-平滑筋アクチン(α-SMA)の発現を特徴とする(図4B)。iExosiRNA-STAT3またはiExomASO-STAT3処理によってHSCにおけるStat3 mRNAレベル(図4Cおよび4D)は脂質ベーストランスフェクション試薬(図5Aおよび5B)と比較して同様の効率で低減した。
HSC単離およびα-SMA染色
以前に説明された方法(Vinas et al., 2003)に従ってマウス初代HSCを8週齢の雌Balb/cマウスから単離した。マウス初代HSCを、20%FBS(Gemini)を含有する高グルコースダルベッコ変法イーグル培地(DMEM, Gibco)の中で培養した。培養によって活性化された初代HSC(7日目)をCy3-α-SMA抗体(Sigma, C6198, 1:200)で一晩免疫染色した。200×倍率の代表的な画像をAxiovert 200およびAxiocam HRcカメラ(Zeiss)によって撮影した。
TRIzol(商標)(Invitrogen, 15596018)を用いて全RNAを肝臓組織から単離し、High-Capacity cDNA Reverse Transcriptase Kit(Life Technology)によって製造業者の説明書に従ってcDNAを作製した。定量RT-PCRをSYBR Green PCR Master Mixを用いて行った。全量の標的遺伝子mRNAをGAPDH発現に対して標準化した。以下のプライマー配列:
を使用した。分散の統計解析はΔCtで行った。変化倍率を示し、対照比較群を1に設定して対照群に対して標準化した。
テキサス大学MD Anderson Cancer CenterのCell Therapy Laboratoryから入手し、20%FBS、1%ペニシリン-ストレプトマイシン(Corning)、1%L-グルタミン(Corning)、および1%非必須アミノ酸(NEAA, Gibco)を加えたαMEM(Corning)の中で骨髄由来MSCを培養した。エキソソーム収集には継代4~6のMSCを使用した。本発明者らの確立したプロトコール(Mendt et al., 2018; Kamerkar et al., 2017)に従ってエキソソームを分画遠心分離プロセスによって精製した。簡単に言うと、細胞を70~80%コンフルエンシーまで増殖させ、1×PBS(Corning)で洗浄し、無血清培地(1%ペニシリン-ストレプトマイシン、1%L-グルタミン、および1%NEAAを含むαMEM)の中で48時間培養した。上清を収集し、800×gで5分間、その後に2,000×gで10分間遠心分離し、0.2μmフィルター(Thermo Fisher)で濾過した。濾過した上清をSW 32 Tiローター(Beckman)に入れて100,000×gで4℃で3時間遠心分離した。上清を吸引し、ペレットを100μLの1×PBSに再懸濁した。エキソソームの濃度およびサイズをナノ粒子トラッキング解析(NTA, NanoSight LM10, Malvern)によって検証した。100億個のエキソソームのアリコートを使用前に-80℃で保管した。低用量混合物は、100μlのPlasmaLyte(Medline, BHL2B2544XH)の中に、NTAに従う10億個の全エキソソームと1μgのsiRNAまたはアンチセンスオリゴ(ASO)を含有した。これに対して、高用量混合物は、100μlのPlasmaLyteの中に20億個の全エキソソームと5μgのsiRNAまたはASOを含有した。400μlのRNAi-エキソソーム混合物をキュベットにロードし、次いで、400V、125μF、および∞オームで電気穿孔した。すぐにキュベットを氷に移した。siSTAT3配列:センス鎖
、アンチセンス
(Sigma-Aldrich)。mASO Scrbl配列は、
であった。umASO STAT3配列は、
であった。mASO STAT3配列は、
であった。「m」は2’O-メトキシ-エチル塩基を示す。*はホスホロチオエート結合を示す。siCntrlはSigma-Aldrich(SIC001, Sigma-Aldrich)から入手した。ASOはIntegrated DNA Technologies, Incによって合成された。マウスSTAT3とヒトSTAT3を標的とするように、等しい潜在的な効力をもつsiRNAを設計した。ASOもマウスSTAT3とヒトSTAT3を標的とするように設計したが、マウス配列と3つのヌクレオチドミスマッチがあるために、マウスSTAT3に対する効力が潜在的に低かった。
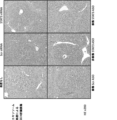
肝線維症を誘導するために(下記で詳述するように)マウスをCCl4で処置した。MSC由来エキソソームの生体内分布については、以前に述べられたように(Mendt et al., 2018)、XenoLight DiR(ヨウ化1,1'-ジオクタデシルテトラメチルヨードトリカルボシアニン, Perkin Elmer,カタログ125964)で標識した8×109個の精製エキソソームを健常マウス(シャム)および線維症Balb/cマウスにi.p(100μl)注射した。希釈したDiR(100μl)を対照として注射した。注射して6時間後にマウスを安楽死させ、様々な組織(腎臓、脾臓、肝臓、膵臓、および腸)を収集し、すぐに画像化した。簡単に言うと、5×109個のMSC由来エキソソームごとに1μM DiRで標識し、次いで、37℃で1時間、4℃で15分間インキュベートし、次いで、10mlの1×PBSに溶解して40,000gの超遠心分離によって4℃で3時間洗浄した(Mendt et al., 2018)。標識エキソソーム(8×109個)を100μlの1×PBSに再懸濁した。対照群については、上記と同じ手順に従って3時間超遠心分離することで1μlのDiRを11mlの1×PBSで希釈した。対照試料(DiRのみ)を100μlの1×PBSに再懸濁した。変種臓器の蛍光強度を画像化し、780nmのEmフィルターと、710nmのExフィルターが付いたIVIS 200小動物イメージングシステム(small animal imaging system)(PerkinElmer)を用いて定量した。
(下記で詳述するように)マウスをCCl4で処置して肝線維症を誘導した。注射前に、MSC由来エキソソームをAF647タグ化siRNAおよびmASOと共に電気穿孔した。次いで、これらのAF647標識iExosomeおよびAF647タグ化裸のsiRNAまたはmASOをWT Balb/cマウスおよび線維症マウスにi.p.注射した。切片化した肝臓標本をDAPIで染色し、次いでマウントした。画像を共焦点レーザースキャニング顕微鏡(Zeiss LSM800)によって入手し、次いで、AF647陽性細胞の核の数を計数し、その数を核の総数で割ることによって定量した。1つの臓器につき3つのランダムな視野を取り込んだ(200×)。
肝線維症をBalb/cマウス(Jackson laboratoryから購入した8週齢の雌)において誘導した。CCl4(Sigma, 56-23-5)を100μlのオリーブ油に溶解して10%の投与量で37日間にわたって週2回、i.p.注射することで肝臓損傷を誘導した。対照マウスには、CCl4がないオリーブ油を投与した(図5D)。9日後に、マウスを無作為に13の群に割り付けた。マウスには、100μl体積のPlasmaLyte(Medline)に溶解した1μg siRNA/ASOの10億個の操作されたエキソソームもしくは5μg siRNA/ASOの20億個の操作されたエキソソームまたはsiRNA-STAT3/mASO-STAT3のみも1日おきにi.p.投与した。最後のiExosome注射の24時間以内にマウスを安楽死させた。全てのプロトコールと手順がMDACCの動物実験委員会(Institute for Animal Care and Use Committee)によって承認された。
肝臓を10%中性緩衝ホルマリンで固定し、パラフィン包埋した。シリウスレッド染色のために5μm厚のパラフィン切片を使用した。3回リンスし、ヴァイゲルトヘマトキシリンで8分間染色した後に、スライドをピクロシリウスレッドで1時間、対比染色した。肝線維症を定量するために、カウンティンググリッドを用いて、各マウスから3つの独立したシリウスレッド染色切片を分析した。以前に述べられたように(Whittaker et al., 1994)、肝線維症のパーセント領域を計算した。
組織を10%ホルマリンで一晩固定し、脱水し、およびパラフィン包埋した。次いで、5μm切片を分析のために処理した。1mM EDTA-TE(pH9.0)中で1時間の熱媒介性抗原賦活化を行った。一次抗体と一晩インキュベーションする1時間前に、コラーゲンI(Southern Biotech, 1310-01, 1:200)染色のために切片を、TBSに溶解した4%CWFSゼラチン(Aurion)でブロックした。ビオチン化抗ヤギ(Vector Laboratories, BA9500, 1:400)とインキュベートした後に、切片をABCと30分反応させ、次いで、製造業者のプロトコールに従ってDABによって発色させた。
マウス血液を後眼窩叢(retro-orbital plexus)から収集した。次いで、すぐに血清を6,000rpm、4℃で10分間の遠心分離によって単離し、使用前に-80℃で保管した。血清のALTおよびAST含有率の測定はMDACCの獣医病理学部門によって行われた。
肝臓組織試料を10%緩衝ホルマリンで固定し、パラフィン包埋した。厚さが5μmの組織切片をヘマトキシリン・エオシン(H&E)で染色した。各スライドについて5つの別々の200×視野を無作為に選択し、壊死した肝細胞および変性した肝細胞の数を、Adobe Photoshop 7.0のカウンティングツールを用いて手作業で計数した。肝細胞は、細胞質が凝集しており、濃く染色されていることと、核が無いことで壊死していると定義された(Krishna et al., 2017)。肝細胞変性は、特に以前に報告されたように(Lackner et al., 2008)、細胞の膨張と拡大が発見されることで確かめられた。
TRIzol(商標)(Invitrogen, 15596018)を用いて全RNAを肝臓から抽出し、製造業者の説明書に従って精製した。RNA完全性は、MDACC SequencingとncRNA ProgramコアによるRNA 6000 Nanoアッセイを用いて確かめた。肝臓RNA配列決定は、Illumina TrueSeq stranded mRNAseq MDACC SequencingとncRNA Programコアを用いて行った。ゲノムマッピングは、TopHatソフトウェア(v2.0.9; ワールドワイドウェブ上でccb.jhu.edu/software/tophat/index.shtmlから入手可能)を用いて行った。本発明者らはRNA-Seqデータから転写物を特定するためにCufflinksアルゴリズムを使用し、遺伝子発現プロファイリングのために、DESeq2(ワールドワイドウェブ上でbioconductor.org/packages/release/bioc/html/DESeq2.htmlから入手可能)を用いて、異なって発現した遺伝子を決定した。偽発見率(FDR)は、複数の試験のp値の有意性閾値を決定するために行った。有意な発現遺伝子は0.05未満のFDRによって決定した。ジーンセットエンリッチメントアナリシス(Gene Set Enrichment Analysis)(GSEA)および遺伝子アノテーションは、WebGestalt 2019(ワールドワイドウェブ上でwebgestalt.org/から入手可能)(He et al., 2019)によって行った。STAT-ECM遺伝子相互作用調節ネットワークは、NetworkAnalyst 3.0(ワールドワイドウェブ上でnetworkanalyst.ca/から入手可能)(Zhou et al., 2019)を用いて作成した。
使用した統計解析を図面の簡単な説明において詳述した。データを平均±平均の標準誤差で表した。p<0.05が統計的に有意だとみなした。GraphPad Prism(GraphPad Software)を使用して、一元配置ANOVAまたは独立両側スチューデントt検定とウエルチの補正を用いて統計的有意性を証明した。統計検定の有意性を以下のようにグラフ中で報告した:****(p<0.0001)、***(p<0.001)、**(p<0.01)、*(p<0.05)、n.s.(p>0.05)。
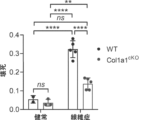
活性化肝臓星状細胞またはαSMA+筋線維芽細胞にCol1a1遺伝子のノックアウト変異(Col1a1cKO)を有するマウスを作製した。あるマウス群にCCl4をi.p.注射することによって肝線維症を誘導した。これに対して、対照群にはCCl4を与えなかった。線維症群と対照(「健常」)群を両方とも屠殺および分析した。野生型(WT)と比較して、Col1a1cKOマウスではコラーゲンIと肝線維症の有意な低減が観察された(図10A~F)。WTと比較して、肝線維症を有するCol1a1cKOマウスでは肝線維症と関連するグローバル発現パターンの多くが有意に改善した(図10Gおよび10H)。
Claims (22)
- その必要がある患者において線維症または線維症に関連する状態の処置に使用するための、STAT3ポリヌクレオチドにハイブリダイズするSTAT3阻害RNAを含有する脂質ベースナノ粒子を含む、薬学的組成物であって、前記阻害RNAが、SEQ ID NO:1、SEQ ID NO:2、SEQ ID NO:3、SEQ ID NO:4、またはSEQ ID NO:5を含む、前記薬学的組成物。
- 前記脂質ベースナノ粒子がその表面にCD47及び/または増殖因子を含む、請求項1記載の薬学的組成物。
- 前記脂質ベースナノ粒子がエキソソームまたはリポソームである、請求項1または2記載の薬学的組成物。
- 前記阻害RNAがSTAT3タンパク質の発現をノックダウンする、請求項1~3のいずれか一項記載の薬学的組成物。
- 賦形剤をさらに含む、請求項1~4のいずれか一項記載の薬学的組成物。
- 非経口投与用に製剤化されている、請求項1~5のいずれか一項記載の薬学的組成物。
- 抗菌剤をさらに含む、請求項1~6のいずれか一項に記載の薬学的組成物であって、前記抗菌剤が、塩化ベンザルコニウム、塩化ベンゼトニウム、ベンジルアルコール、ブロノポール、セントリミド(centrimide)、塩化セチルピリジニウム、クロルヘキシジン、クロロブタノール、クロロクレゾール、クロロキシレノール、クレゾール、エチルアルコール、グリセリン、エキセチジン(exetidine)、イミド尿素、フェノール、フェノキシエタノール、フェニルエチルアルコール、硝酸フェニル水銀、プロピレングリコール、またはチメロサールである、前記薬学的組成物。
- 前記薬学的組成物の投与が、前記患者における細胞への前記阻害RNAの送達をもたらす、請求項1~7のいずれか一項記載の薬学的組成物。
- 前記線維症が、肝線維症、肺線維症、肺性線維症、嚢胞性線維症、特発性肺線維症(IPF)、または放射線誘発性肺損傷である、請求項1~8のいずれか一項記載の薬学的組成物。
- 前記線維症が肝線維症である、請求項1~8のいずれか一項に載の薬学的組成物。
- 全身投与によって投与され、かつ/または1回より多く投与される、請求項1~10のいずれか一項記載の薬学的組成物。
- 少なくとも第2の療法を前記患者に実施する工程をさらに含む、請求項1~11のいずれか一項記載の薬学的組成物。
- 前記患者がヒトである、請求項1~12のいずれか一項記載の薬学的組成物。
- 前記脂質ベースナノ粒子がエキソソームであり、かつ前記エキソソームが前記患者にとって自己由来である、請求項13記載の薬学的組成物。
- 前記脂質ベースナノ粒子がエキソソームであり、かつ前記エキソソームが間葉系細胞から得られる、請求項13または14記載の薬学的組成物。
- 前記脂質ベースナノ粒子がエキソソームであり、かつ前記エキソソームが、患者由来の血液、リンパ液、唾液、尿、脳脊髄液、骨髄吸引液、眼滲出物/涙、または血清からのものである、請求項13~15のいずれか一項記載の薬学的組成物。
- 前記薬学的組成物の投与が、前記患者の肝細胞におけるCol1a1, Acta2, Col1a2, またはVim発現を低減させる、請求項1~16のいずれか一項記載の薬学的組成物。
- 前記肝細胞が、肝臓星状細胞または活性化肝臓星状細胞である、請求項17記載の薬学的組成物。
- STAT3ポリヌクレオチドにハイブリダイズするSTAT3阻害RNAを脂質ベースナノ粒子に導入する工程を含む、治療用組成物を調製する方法であって、前記阻害RNAがSEQ ID NO:1, SEQ ID NO:2, SEQ ID NO:3, SEQ ID NO:4,または SEQ ID NO:5を含む、前記方法。
- 前記脂質ベースナノ粒子がその表面にCD47及び/または増殖因子を含む、請求項19記載の方法。
- 前記脂質ベースナノ粒子がエキソソームまたはリポソームである、請求項19または20記載の方法。
- 前記阻害RNAがSTAT3タンパク質の発現をノックダウンする、請求項19~21のいずれか一項に記載の方法。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962943943P | 2019-12-05 | 2019-12-05 | |
| US62/943,943 | 2019-12-05 | ||
| PCT/US2020/063475 WO2021113761A1 (en) | 2019-12-05 | 2020-12-04 | Exosomes-based therapy for liver fibrosis and other diseases associated with fibrosis |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| JP2023505273A JP2023505273A (ja) | 2023-02-08 |
| JPWO2021113761A5 JPWO2021113761A5 (ja) | 2023-12-12 |
| JP2023505273A5 JP2023505273A5 (ja) | 2023-12-12 |
| JP7674354B2 true JP7674354B2 (ja) | 2025-05-09 |
Family
ID=76222148
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| JP2022533626A Active JP7674354B2 (ja) | 2019-12-05 | 2020-12-04 | 肝線維症および線維症に関連する他の疾患に対するエキソソームベースの療法 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20230013636A1 (ja) |
| EP (1) | EP4069205A4 (ja) |
| JP (1) | JP7674354B2 (ja) |
| KR (1) | KR20220124170A (ja) |
| CN (1) | CN115297850A (ja) |
| AU (1) | AU2020398177A1 (ja) |
| CA (1) | CA3164248A1 (ja) |
| WO (1) | WO2021113761A1 (ja) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3775258A4 (en) | 2018-03-28 | 2022-01-26 | Board of Regents, The University of Texas System | IDENTIFICATION OF EPIGENETIC ALTERATIONS IN DNA ISOLATED FROM EXOSOMES |
| JP2021526556A (ja) | 2018-05-30 | 2021-10-07 | ダイレクト バイオロジクス エルエルシー | 成長因子および細胞外小胞を凍結または粉状にした、間葉系幹細胞(msc)の調製物を含む助剤、ならびにその使用方法 |
| BR112021015549A2 (pt) | 2019-02-07 | 2021-10-26 | Direct Biologics Llc | Método para tratar osteoartrite com uma combinação de exossomos de células tronco mesenquimais, células tronco mesenquimais sinoviais e andaimes |
| CA3146433A1 (en) | 2019-07-18 | 2021-01-21 | Direct Biologics Llc | Preparations comprising mesenchymal stem cells and cannabinoids and methods of their use |
| CA3147366A1 (en) * | 2019-08-14 | 2021-02-18 | Adam T. BOUTIN | Extracellular vesicles with stat3-antisense oligonucleotides |
| CA3171143A1 (en) * | 2020-03-13 | 2021-09-16 | Codiak Biosciences, Inc. | Targeted delivery of extracellular vesicles |
| US12590310B2 (en) | 2020-04-22 | 2026-03-31 | Direct Biologics, Llc | Methods and compositions for treating inflammatory conditions associated with infectious disease |
| CN117757792A (zh) * | 2023-12-26 | 2024-03-26 | 圣诺生物医药技术(苏州)有限公司 | 一种用于治疗肝损伤的核酸干扰药物 |
| US12502407B2 (en) | 2024-04-25 | 2025-12-23 | Direct Biologics, Llc | Treatment of fistula with bone marrow mesenchymal stem cell derived extracellular vesicles |
Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007523074A (ja) | 2004-02-06 | 2007-08-16 | アイシス・ファーマシューティカルズ・インコーポレイテッド | アンチセンスオリゴヌクレドチドによるstat3発現の調節 |
| JP2010538660A (ja) | 2007-09-17 | 2010-12-16 | イントラドイグム コーポレーション | STAT3siRNA含有組成物及びそれらの使用法 |
| JP2011511807A (ja) | 2008-02-07 | 2011-04-14 | テラピオ コーポレイション | 薬物タンパク質および/または遺伝物質などの積荷の送達のための組成物 |
| WO2019157535A1 (en) | 2018-02-12 | 2019-08-15 | Codiak Biosciences, Inc. | Methods and compositions for macrophage polarization |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP3050566B1 (en) * | 2007-09-10 | 2018-11-28 | Boston Biomedical, Inc. | A novel group of stat3 pathway inhibitors and cancer stem cell pathway inhibitors |
| US8591905B2 (en) * | 2008-10-12 | 2013-11-26 | The Brigham And Women's Hospital, Inc. | Nicotine immunonanotherapeutics |
| CN102378766A (zh) * | 2009-03-23 | 2012-03-14 | 夸克医药公司 | 治疗癌症和纤维化疾病的化合物组合物和方法 |
| JP5943993B2 (ja) * | 2011-04-01 | 2016-07-05 | アイオーニス ファーマシューティカルズ, インコーポレーテッドIonis Pharmaceuticals,Inc. | 転写のシグナル伝達及び活性化因子3(stat3)発現の調節 |
| DK3209778T3 (da) * | 2014-10-24 | 2019-05-27 | Astrazeneca | Kombination |
| US20180177727A1 (en) * | 2015-06-10 | 2018-06-28 | Board Of Regents, The University Of Texas System | Use of exosomes for the treatment of disease |
| EP3319976B1 (en) * | 2015-07-09 | 2021-09-01 | Insmed Incorporated | Compositions and methods for treating lung diseases and lung injury |
| HK1256704A1 (zh) * | 2015-08-21 | 2019-10-04 | 辉瑞公司 | 包含治疗剂的治疗性纳米粒及其制备和使用方法 |
| JP7813099B2 (ja) * | 2018-03-28 | 2026-02-12 | ボード オブ リージェンツ,ザ ユニバーシティ オブ テキサス システム | 治療用物質を標的送達するためのエキソソームの使用法 |
-
2020
- 2020-12-04 JP JP2022533626A patent/JP7674354B2/ja active Active
- 2020-12-04 AU AU2020398177A patent/AU2020398177A1/en active Pending
- 2020-12-04 CN CN202080094331.XA patent/CN115297850A/zh active Pending
- 2020-12-04 WO PCT/US2020/063475 patent/WO2021113761A1/en not_active Ceased
- 2020-12-04 US US17/782,976 patent/US20230013636A1/en active Pending
- 2020-12-04 KR KR1020227022785A patent/KR20220124170A/ko active Pending
- 2020-12-04 CA CA3164248A patent/CA3164248A1/en active Pending
- 2020-12-04 EP EP20897141.6A patent/EP4069205A4/en active Pending
Patent Citations (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2007523074A (ja) | 2004-02-06 | 2007-08-16 | アイシス・ファーマシューティカルズ・インコーポレイテッド | アンチセンスオリゴヌクレドチドによるstat3発現の調節 |
| JP2010538660A (ja) | 2007-09-17 | 2010-12-16 | イントラドイグム コーポレーション | STAT3siRNA含有組成物及びそれらの使用法 |
| JP2011511807A (ja) | 2008-02-07 | 2011-04-14 | テラピオ コーポレイション | 薬物タンパク質および/または遺伝物質などの積荷の送達のための組成物 |
| WO2019157535A1 (en) | 2018-02-12 | 2019-08-15 | Codiak Biosciences, Inc. | Methods and compositions for macrophage polarization |
Non-Patent Citations (5)
| Title |
|---|
| Ruenn Chai LAI et al.,"Exosomes for drug delivery - a novel application for the mesenchymal stem cell",Biotechnology Advances,2013年09月,Vol. 31, No. 5,p.543-551,DOI: 10.1016/j.biotechadv.2012.08.008 |
| Sushrut KAMERKAR et al.,"Exosomes facilitate therapeutic targeting of oncogenic KRAS in pancreatic cancer",Nature,2017年06月,Vol. 546, No. 7659,p.498-503,DOI: 10.1038/nature22341 |
| Takeshi KATSUDA et al.,"Potential application of mesenchymal stem cell-derived exosomes as a novel therapeutic drug",Drug Delivery System,2014年,Vol. 29, No. 2,p.140-151,DOI: 10.2745/dds.29.140 |
| Xiaoli RONG et al.,"Human bone marrow mesenchymal stem cells-derived exosomes alleviate liver fibrosis through the Wnt/β-catenin pathway",Stem Cell Research & Therapy,2019年03月18日,Vol. 10, No. 1,DOI: 10.1186/s13287-019-1204-2 |
| Yu FUJITA et al.,"Clinical Application of Mesenchymal Stem Cell-Derived Extracellular Vesicle-Based Therapeutics for Inflammatory Lung Diseases",Journal of Clinical Medicine,2018年10月14日,Vol. 7, No. 10,p.355,DOI: 10.3390/jcm7100355 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3164248A1 (en) | 2021-06-10 |
| KR20220124170A (ko) | 2022-09-13 |
| US20230013636A1 (en) | 2023-01-19 |
| WO2021113761A1 (en) | 2021-06-10 |
| AU2020398177A1 (en) | 2022-07-07 |
| EP4069205A1 (en) | 2022-10-12 |
| CN115297850A (zh) | 2022-11-04 |
| JP2023505273A (ja) | 2023-02-08 |
| EP4069205A4 (en) | 2024-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7674354B2 (ja) | 肝線維症および線維症に関連する他の疾患に対するエキソソームベースの療法 | |
| CN107980062B (zh) | 用于靶向亨廷汀mRNA的寡核苷酸化合物 | |
| JP6023126B2 (ja) | 標的遺伝子の発現を抑制する組成物 | |
| JP2024023853A (ja) | 疾患の処置のためのエキソソームの使用 | |
| Yoon et al. | Self-assembled micelle interfering RNA for effective and safe targeting of dysregulated genes in pulmonary fibrosis | |
| JP2018100284A (ja) | 線維症および炎症状態を処置するための多標的調整 | |
| JP2011502118A (ja) | 筋障害を相殺するための手段と方法 | |
| AU2014359716A1 (en) | Means for lung specific delivery | |
| HK1199215A1 (en) | Compositions and methods for efficacious and safe delivery of sirna using specific chitosan-based nanocomplexes | |
| WO2023051822A1 (zh) | 用于治疗与pcsk9相关疾病的靶向寡核苷酸 | |
| Sun et al. | MicroRNA biogenesis is enhanced by liposome-encapsulated Pin1 inhibitor in hepatocellular carcinoma | |
| Yao et al. | Nucleic acid nanomaterials-based therapy for osteoarthritis: Progress and prospects | |
| CN105555279B (zh) | 用于治疗脓毒症的MicroRNA抑制 | |
| JP7599698B2 (ja) | エキソソームを用いたがん遺伝子に対する治療的な標的指向化の方法 | |
| JP7481694B2 (ja) | 核酸送達複合体 | |
| US20220267769A1 (en) | Medical uses, methods and uses | |
| Momin et al. | The Challenges and Opportunities in the Development of MicroRNA Therapeutics: A Multidisciplinary Viewpoint. Cells 2021, 10, 3097 | |
| Soleimani et al. | CD73 Downregulation by EGFR-Targeted Liposomal CD73 siRNA Potentiates Antitumor Effect of Liposomal Doxorubicin (Doxil) in 4T1 Tumor-Bearing Mice | |
| Suri | Lipid Nanoparticle Mediated Oral Delivery of RNA for Inflammatory Bowel Disease | |
| JP2025078002A (ja) | 線維化を伴う肝疾患を予防又は治療するための医薬組成物 | |
| Wang | Fabrication and Characterization of a Targeted, Coated Cationic Liposome for Delivery of Double-Stranded miRNA-146a Mimic to Diseased Endothelial Cells in Atherosclerosis | |
| SHOBAKI | Targeting macrophages in the tumor-microenvironment to enhance their anti-tumorous functions by gene silencing using optimized siRNA-loaded lipid nanoparticles | |
| HK40042570A (en) | Oligonucleotide compounds for targeting huntingtin mrna |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20220815 |
|
| RD04 | Notification of resignation of power of attorney |
Free format text: JAPANESE INTERMEDIATE CODE: A7424 Effective date: 20230623 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20231201 |
|
| A621 | Written request for application examination |
Free format text: JAPANESE INTERMEDIATE CODE: A621 Effective date: 20231201 |
|
| A131 | Notification of reasons for refusal |
Free format text: JAPANESE INTERMEDIATE CODE: A131 Effective date: 20241212 |
|
| A521 | Request for written amendment filed |
Free format text: JAPANESE INTERMEDIATE CODE: A523 Effective date: 20250311 |
|
| TRDD | Decision of grant or rejection written | ||
| A01 | Written decision to grant a patent or to grant a registration (utility model) |
Free format text: JAPANESE INTERMEDIATE CODE: A01 Effective date: 20250331 |
|
| A61 | First payment of annual fees (during grant procedure) |
Free format text: JAPANESE INTERMEDIATE CODE: A61 Effective date: 20250424 |
|
| R150 | Certificate of patent or registration of utility model |
Ref document number: 7674354 Country of ref document: JP Free format text: JAPANESE INTERMEDIATE CODE: R150 |