KR20100109902A - 대규모 미생물 배양 방법 - Google Patents
대규모 미생물 배양 방법 Download PDFInfo
- Publication number
- KR20100109902A KR20100109902A KR1020107013061A KR20107013061A KR20100109902A KR 20100109902 A KR20100109902 A KR 20100109902A KR 1020107013061 A KR1020107013061 A KR 1020107013061A KR 20107013061 A KR20107013061 A KR 20107013061A KR 20100109902 A KR20100109902 A KR 20100109902A
- Authority
- KR
- South Korea
- Prior art keywords
- oxygen
- culture medium
- microorganism
- conditions
- succinic acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/40—Preparation of oxygen-containing organic compounds containing a carboxyl group including Peroxycarboxylic acids
- C12P7/44—Polycarboxylic acids
- C12P7/46—Dicarboxylic acids having four or less carbon atoms, e.g. fumaric acid, maleic acid
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N1/00—Microorganisms; Compositions thereof; Processes of propagating, maintaining or preserving microorganisms or compositions thereof; Processes of preparing or isolating a composition containing a microorganism; Culture media therefor
- C12N1/20—Bacteria; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
- C12P7/06—Ethanol, i.e. non-beverage
- C12P7/065—Ethanol, i.e. non-beverage with microorganisms other than yeasts
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
- C12P7/16—Butanols
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/02—Preparation of oxygen-containing organic compounds containing a hydroxy group
- C12P7/04—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic
- C12P7/18—Preparation of oxygen-containing organic compounds containing a hydroxy group acyclic polyhydric
- C12P7/20—Glycerol
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P7/00—Preparation of oxygen-containing organic compounds
- C12P7/40—Preparation of oxygen-containing organic compounds containing a carboxyl group including Peroxycarboxylic acids
- C12P7/56—Lactic acid
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02E—REDUCTION OF GREENHOUSE GAS [GHG] EMISSIONS, RELATED TO ENERGY GENERATION, TRANSMISSION OR DISTRIBUTION
- Y02E50/00—Technologies for the production of fuel of non-fossil origin
- Y02E50/10—Biofuels, e.g. bio-diesel
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Life Sciences & Earth Sciences (AREA)
- Zoology (AREA)
- Wood Science & Technology (AREA)
- Health & Medical Sciences (AREA)
- Genetics & Genomics (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Tropical Medicine & Parasitology (AREA)
- Virology (AREA)
- Biomedical Technology (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
Description
도 2는 실시예 3의 조건에 따라 산소가 풍부한 단계에서의 교반이 바이오매스의 생산 성능(CO2 하에 18 시간 동안 배양시킨 후 측정됨)에 미치는 영향을 나타내는 도면.
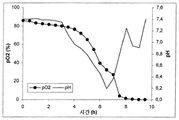
도 3은 산소가 풍부한 단계와 산소가 결핍된 단계 동안, 산소 분압(pO2), pH 및 실시예 4의 조건에 따라 배양배지에 첨가된 NaOH의 양의 변화추이를 각각 나타내는 그래프.
Claims (16)
- 대사 물질을 생산하는 미생물을 단일 반응기에서 배양하는 방법으로,
a) 대사 물질을 생산할 수 있는 미생물과 배양배지를 반응기에서 접종하는 단계와,
b) 상기 배지의 pH를 조절하거나 하지 않아도 되되, 바람직하게는 상기 배지의 pH를 조절하여, 상기 미생물을, 상기 반응기 내, 산소가 풍부한 조건 하에 배양하는 단계와,
c) 상기 미생물을, 상기 반응기 내, 5% 미만의 산소를 함유하는 산소 희박 조건에 적응시키는 단계와,
d) C02 또는 불활성 기체와 혼합된 CO2로 퍼징함으로써 상기 반응기 내부를 산소 결핍 조건으로 변경하는 단계와,
e) 상기 대사 물질을 생산하기에 충분한 기간 동안 상기 미생물을 상기 산소 결핍 조건 하에 배양하는 단계
를 포함하는 방법. - 제1항에 있어서, 상기 대사 물질은 숙신산, 말산(malic acid), 푸마르산(fumaric acid), 젖산, 글리세롤, 에탄올, 이소프로판올, 부탄올로 구성된 군에서 선택되되, 바람직하게는 숙신산인 것을 특징으로 하는 방법.
- 제1항에 있어서, 상기 미생물은 Escherichia 또는 Escherichia coli 중에서 선택되는 것을 특징으로 하는 방법.
- 제2항에 있어서, 상기 미생물은 동일한 가용량의 NADH에 대해 야생형 균주보다 더 많은 숙신산염을 생산하도록 유전자적으로 변형된 재조합 Escherichia coli인 것을 특징으로 하는 방법.
- 제4항에 있어서, 상기 미생물은 비활성화된 adhE , ldhA , ack - pta 및/또는 iclR 유전자를 함유하며, 과잉발현된 pyc 유전자를 가진 것을 특징으로 하는 방법.
- 제4항에 있어서, 미생물은 유전자형 ΔadhE ΔldhA ΔiclR Δackpta PYC 또는 ΔadhE ΔldhA ΔiclR Δack PYC 또는 ΔadhE ΔldhA ΔiclR Δpta PYC를 가지는 것을 특징으로 하는 방법.
- 제4항에 있어서, 미생물은 SBS550MG-pHL413인 것을 특징으로 하는 방법.
- 제5항에 있어서, 배양배지는 무기질 배양배지인 것을 특징으로 하는 방법.
- 제8항에 있어서, 단계 c) 또는 단계 e) 동안에 적어도 1회 이상 추가의 탄소를 첨가하는 단계를 포함하는 것을 특징으로 하는 방법.
- 제9항에 있어서, 추가의 탄소는, 배양배지의 pH가 상기 적응 단계 동안에 약 7 미만의 값으로 저하되는 경우에 첨가되는 것을 특징으로 하는 방법.
- 제10항에 있어서, 단계 d)는 배양배지의 pH가 약 7.2로 증가된 경우에 수행되는 것을 특징으로 하는 방법.
- 제10항에 있어서, 단계 d)는 상기 배양배지가 2시간 이상 동안 산소 희박 조건 하에 놓여진 경우에 수행되는 것을 특징으로 하는 방법.
- 제1항에 있어서, 단계 c)는, t=0에 배양배지에 도입된 탄소 공급원의 대부분이 상기 미생물에 의해 단계 b) 동안에 소비된 후에 수행되는 것을 특징으로 하는 방법.
- 제1항에 있어서, 상기 적응 단계는, 상기 미생물이 600nm 에서의 흡광도가 15를 초과하는 경우에 시작되는 것을 특징으로 하는 방법.
- 제1항에 있어서, 단계 a) 내지 단계 e)는 발효기 내에서 수행되는 것을 특징으로 하는 방법.
- 제1항에 있어서, 단계 e)가 끝난 후 배양배지에 존재하는 숙신산염 이온을 숙신산으로 전환시키기 위한 산화반응 단계 f)를 더 포함하는 것을 특징으로 하는 방법.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/IB2007/055409 WO2009083756A1 (en) | 2007-12-28 | 2007-12-28 | Large scale microbial culture method |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20100109902A true KR20100109902A (ko) | 2010-10-11 |
Family
ID=39869967
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020107013061A Ceased KR20100109902A (ko) | 2007-12-28 | 2007-12-28 | 대규모 미생물 배양 방법 |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US8486686B2 (ko) |
| EP (1) | EP2225383A1 (ko) |
| JP (1) | JP2011507541A (ko) |
| KR (1) | KR20100109902A (ko) |
| CN (1) | CN101918574A (ko) |
| BR (1) | BRPI0722315A2 (ko) |
| CA (1) | CA2709515A1 (ko) |
| WO (1) | WO2009083756A1 (ko) |
Families Citing this family (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011064151A1 (en) | 2009-11-24 | 2011-06-03 | Dsm Ip Assets B.V. | Process for the crystallization of succinic acid |
| EP2371802A1 (en) | 2010-03-30 | 2011-10-05 | DSM IP Assets B.V. | Process for the crystallization of succinic acid |
| US20130171704A1 (en) * | 2010-09-24 | 2013-07-04 | Roquette Freres Sa | Dicarboxylic acid production process |
| CN102653779B (zh) * | 2011-03-04 | 2014-02-19 | 北京科润三联生物技术有限责任公司 | 一种新型重组抗菌多肽药物的制备方法 |
| EP2964687A2 (en) | 2013-03-08 | 2016-01-13 | DSM IP Assets B.V. | Polyester |
| FR3028864B1 (fr) | 2014-11-26 | 2018-05-18 | Roquette Freres | Procede de recuperation de cristaux d'acide succinique avec mise en œuvre de tensioactifs au cours de la cristallisation, cristaux obtenus et leurs utilisations |
| PL3227256T3 (pl) | 2014-12-02 | 2019-09-30 | Roquette Frères | Sposób wytwarzania kwasu bursztynowego z bulionu fermentacyjnego z zastosowaniem nanoflltracji do oczyszczania zawracanego do obiegu ługu macierzystego |
| WO2016137897A1 (en) | 2015-02-24 | 2016-09-01 | William Marsh Rice University | Kasiii-free fa synthesis |
| EP3067378A1 (en) | 2015-03-11 | 2016-09-14 | DSM IP Assets B.V. | Polyester |
| WO2017177071A1 (en) | 2016-04-08 | 2017-10-12 | William Marsh Rice University | Improved galactose utilization |
| WO2017192925A1 (en) * | 2016-05-05 | 2017-11-09 | William Marsh Rice University | Improved microbial production of fats |
Family Cites Families (11)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5034105A (en) * | 1989-07-27 | 1991-07-23 | Michigan Biotechnology Institute | Carboxylic acid purification and crystallization process |
| US5869301A (en) | 1995-11-02 | 1999-02-09 | Lockhead Martin Energy Research Corporation | Method for the production of dicarboxylic acids |
| KR19990013007A (ko) * | 1997-07-31 | 1999-02-25 | 박원훈 | 형질전환된 대장균 ss373(kctc 8818p)과 이를 이용한숙신산의 생산방법 |
| WO2003040690A2 (en) * | 2001-11-02 | 2003-05-15 | Rice University | Recycling system for manipulation of intracellular nadh availability |
| US7927859B2 (en) | 2003-08-22 | 2011-04-19 | Rice University | High molar succinate yield bacteria by increasing the intracellular NADH availability |
| US7262046B2 (en) * | 2004-08-09 | 2007-08-28 | Rice University | Aerobic succinate production in bacteria |
| CN101044245B (zh) * | 2004-08-27 | 2012-05-02 | 莱斯大学 | 具有增加的琥珀酸产量的突变大肠杆菌菌株 |
| WO2007030830A2 (en) * | 2005-09-09 | 2007-03-15 | Genomatica, Inc. | Methods and organisms for the growth-coupled production of succinate |
| CN101029316B (zh) * | 2006-12-13 | 2010-06-09 | 华东理工大学 | 大肠杆菌生产琥珀酸的方法 |
| JP5034630B2 (ja) * | 2007-04-12 | 2012-09-26 | 三菱化学株式会社 | 有機酸生産微生物の菌体の調製法及び有機酸の製造法 |
| FR2925068B1 (fr) * | 2007-12-13 | 2010-01-08 | Roquette Freres | Procedes de production d'acide succinique |
-
2007
- 2007-12-28 WO PCT/IB2007/055409 patent/WO2009083756A1/en not_active Ceased
- 2007-12-28 KR KR1020107013061A patent/KR20100109902A/ko not_active Ceased
- 2007-12-28 CN CN2007801019569A patent/CN101918574A/zh active Pending
- 2007-12-28 US US12/747,979 patent/US8486686B2/en not_active Expired - Fee Related
- 2007-12-28 JP JP2010540180A patent/JP2011507541A/ja active Pending
- 2007-12-28 EP EP07870493A patent/EP2225383A1/en not_active Ceased
- 2007-12-28 CA CA2709515A patent/CA2709515A1/en not_active Abandoned
- 2007-12-28 BR BRPI0722315-3A2A patent/BRPI0722315A2/pt not_active Application Discontinuation
Also Published As
| Publication number | Publication date |
|---|---|
| JP2011507541A (ja) | 2011-03-10 |
| CN101918574A (zh) | 2010-12-15 |
| EP2225383A1 (en) | 2010-09-08 |
| US20100317086A1 (en) | 2010-12-16 |
| WO2009083756A1 (en) | 2009-07-09 |
| US8486686B2 (en) | 2013-07-16 |
| BRPI0722315A2 (pt) | 2014-06-10 |
| CA2709515A1 (en) | 2009-07-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20100109902A (ko) | 대규모 미생물 배양 방법 | |
| US7244610B2 (en) | Aerobic succinate production in bacteria | |
| US20060073577A1 (en) | High succinate producing bacteria | |
| EP1781797B1 (en) | Mutant e. coli strain with increased succinic acid production | |
| US20100297715A1 (en) | Method for producing succinic acid | |
| CN104762336B (zh) | 1,5-戊二胺的制备方法 | |
| US20060040368A1 (en) | Aerobic succinate production in bacteria | |
| HU227509B1 (en) | A method for the production of dicarboxylic acids | |
| Goel et al. | Suppressed acid formation by cofeeding of glucose and citrate in Bacillus cultures: emergence of pyruvate kinase as a potential metabolic engineering site | |
| CN102154339A (zh) | 一种产丁二酸大肠杆菌基因工程菌株的构建方法 | |
| CN102618478B (zh) | 一株产d-乳酸动态调控重组菌及用其制备d-乳酸的方法 | |
| CN113046283A (zh) | 一株通过还原tca途径生产己二酸的工程菌株及其构建方法 | |
| WO2005033324A1 (ja) | D−乳酸菌生産用生体触媒 | |
| Huang et al. | Redirecting carbon flux in Torulopsis glabrata from pyruvate to α-ketoglutaric acid by changing metabolic co-factors | |
| WO2009048202A1 (en) | Method for preparing succinic acid using glycerol as carbon source | |
| CN101654666B (zh) | 用于生产d-乳酸的生物催化剂 | |
| CN117866866A (zh) | 一种利用富马酸生产依克多因的重组大肠杆菌及其构建方法和应用 | |
| CN106884001B (zh) | 一种重组嗜碱芽孢杆菌及其制备方法和应用以及制备d-乳酸的方法 | |
| JPWO2011013721A1 (ja) | 乳酸製造方法 | |
| CN106337064B (zh) | 一种l-苹果酸的生产方法 | |
| CN119709808B (zh) | 一种以蔗糖为原料合成乳酸单体的方法 | |
| Zhao et al. | Improving glutarate production in Escherichia coli by enhancing the CoA precursors | |
| CN121610431A (zh) | 一种高效合成乙醇酸的大肠杆菌的构建方法 | |
| CN121801790A (zh) | 一株高效利用混合碳源从头高效合成γ-氨基丁酸的基因工程菌、方法和应用 | |
| CN121271919A (zh) | 一种协同利用co2产苹果酸大肠杆菌基因工程菌的构建方法与应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20100614 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| A201 | Request for examination | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20121221 Comment text: Request for Examination of Application |
|
| N231 | Notification of change of applicant | ||
| PN2301 | Change of applicant |
Patent event date: 20130124 Comment text: Notification of Change of Applicant Patent event code: PN23011R01D |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20140411 Patent event code: PE09021S01D |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20140820 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20140411 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |