KR20130122902A - 종양 치료용 면역원성 조성물 및 방법 - Google Patents
종양 치료용 면역원성 조성물 및 방법 Download PDFInfo
- Publication number
- KR20130122902A KR20130122902A KR1020127031065A KR20127031065A KR20130122902A KR 20130122902 A KR20130122902 A KR 20130122902A KR 1020127031065 A KR1020127031065 A KR 1020127031065A KR 20127031065 A KR20127031065 A KR 20127031065A KR 20130122902 A KR20130122902 A KR 20130122902A
- Authority
- KR
- South Korea
- Prior art keywords
- tumor
- cells
- cancer
- patient
- immunogenic composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/7024—Esters of saccharides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/739—Lipopolysaccharides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/36—Skin; Hair; Nails; Sebaceous glands; Cerumen; Epidermis; Epithelial cells; Keratinocytes; Langerhans cells; Ectodermal cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/37—Digestive system
- A61K35/38—Stomach; Intestine; Goblet cells; Oral mucosa; Saliva
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/37—Digestive system
- A61K35/39—Pancreas; Islets of Langerhans
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/55—Glands not provided for in groups A61K35/22 - A61K35/545, e.g. thyroids, parathyroids or pineal glands
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/193—Colony stimulating factors [CSF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/0005—Vertebrate antigens
- A61K39/0011—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/04—Antineoplastic agents specific for metastasis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
- A61P37/04—Immunostimulants
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/52—Cytokines; Lymphokines; Interferons
- C07K14/53—Colony-stimulating factor [CSF]
- C07K14/535—Granulocyte CSF; Granulocyte-macrophage CSF
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5152—Tumor cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/51—Medicinal preparations containing antigens or antibodies comprising whole cells, viruses or DNA/RNA
- A61K2039/515—Animal cells
- A61K2039/5156—Animal cells expressing foreign proteins
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55522—Cytokines; Lymphokines; Interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/555—Medicinal preparations containing antigens or antibodies characterised by a specific combination antigen/adjuvant
- A61K2039/55511—Organic adjuvants
- A61K2039/55572—Lipopolysaccharides; Lipid A; Monophosphoryl lipid A
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Epidemiology (AREA)
- Immunology (AREA)
- Cell Biology (AREA)
- Engineering & Computer Science (AREA)
- Zoology (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Virology (AREA)
- Developmental Biology & Embryology (AREA)
- Gastroenterology & Hepatology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Organic Chemistry (AREA)
- Molecular Biology (AREA)
- Oncology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Endocrinology (AREA)
- Dermatology (AREA)
- Biochemistry (AREA)
- Toxicology (AREA)
- Hematology (AREA)
- Biophysics (AREA)
- Genetics & Genomics (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
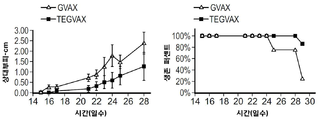
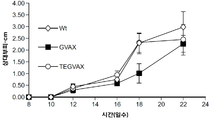
도 2A, 2B 및 2C는 TEGVAX가 생체 내에서 종양 억제 반응을 유도할 수 있음을 도시한다. B16 접종된 C57BL/6(도 2A), SCCFVII/SF 접종된 C3H(도 2B), 및 CT26 접종된 Balb/c(도 2C) 마우스를 전형적으로 종양 주사 후 3 내지 5일째에 종양 주변에 적합한 PBS, GVAX 또는 TEGVAX로 처리하였다. 연구된 모든 쥐 모델 중 TEGVAX 그룹에서 생체 내 종양 진행은 GVAX 그룹에서의 경우보다 통계학적으로 더 느렸다. B16 및 SCCFVII/SF 모델의 경우, GVAX 처리된 그룹과 PBS 처리된 그룹 간에 차이는 없었다. CT26 모델에서, TEGVAX 그룹의 마우스의 40 내지 60%가 18일까지 그들의 촉진 가능한 종양의 검출할 수 없는 수준으로의 회귀를 경험하였다. 293T 세포 내로 제형화된 동몰의 LPS가 또한 대조용의 처리된 마우스에 비해 성장 속도의 차이를 보이지 않았다. 종양의 회귀를 나타낸 마우스를 CT26 종양(2 x 106)으로 재접종하였으며 종양 성장이 기록되지 않았다. 3 개의 쥐 모델 모두에서, 감소된 종양 성장 속도는 GVAX 그룹에서의 경우에 비해 TEGVAX 그룹에서 마우스의 증대된 생존과 상관이 있었다.
도 3은 TEGVAX에 대해 기록된 개선된 생체 내 종양 억제 반응이 MyD88 의존성임을 도시한다. B16 모델을 사용하여, 상기 생체 내 종양 성장 속도를 종양 접종 후 3 내지 5일째에 종양 내로 수행된 백신 처리와 함께 MyD88 빈 마우스로 수행하였다. TEGVAX 처리된 그룹에서 종양 억제 반응은 MyD88 빈 마우스에서 없어진다.
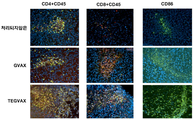
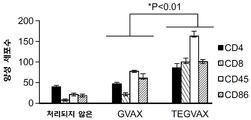
도 4A 및 4B는 TEGVAX 처리가 종양 미세환경 내로의 림프구 및 항원 제공 세포 침투를 증가시킴을 도시한다. 도 4A는 대조군, GVAX 또는 TEGVAX로 처리된 CT26 종양에서 CD4+, CD8+, CD86+ 및 CD45+ 세포의 면역조직화학 염색의 일련의 현미경 사진이다. 황색 세포는 첫 번째 2 개의 패널 중 CD4 또는 CD8과 CD45의 공-국소화된 염색을 나타낸다. 세 번째 패널은 단독의 CD86 접합체 염색을 나타낸다. 이들 세포를 40X 배율로 슬라이스당 10 개의 무작위로 선택된 시야에서 정식으로 정량분석하였다. 도 4B는 면역조직화학에 의해 획득된 정량분석된 데이터의 그래프 표현이다. GVAX 또는 TEGVAX로 처리된 종양 내에서, 상기 두 그룹 간에 각각의 정량분석된 CD4, CD8, CD86 및 CD45 세포에서 통계학적 차이가 존재하였다(P<0.01).
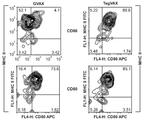
도 5는 TEGVAX 처리가 배액 림프절(DLN)에서 활성화된 수지상 세포(DC)를 증가시킴을 도시한다. CT26 종양 함유 Balb/c 마우스를 종양 주사 후 3일째에 PBS(도시 안 됨), GVAX 또는 TEGVAX로 종양 주변에 처리하였다. DC를 처리 후 5 내지 7일째에 상기 DLN으로부터 단리하였다. B220+CD11c+세포를 거르고 CD86, MHCCII 및 CD80 염색을 도시된 바와 같이 분석하였다. TEGVAX는 GVAX 처리된 그룹에 비해 DLN에서 CD80+MHCII+CD뿐만 아니라 CD86+MHCII+의 증가된 수를 가졌다.
도 6A 및 6B는 TEGVAX 처리가 종양 특이성 CD8+ T-세포의 수를 증가시킴을 도시한다. CT26 함유 Balb/c 마우스를 3일째에 PBS, GVAX, 또는 TEGVAX로 종양 주변에 처리하고, 5일 후에 CD8+ 세포를 비장 및 림프절로부터 단리 및 정제하였다. ELISPOT 분석을 APC로서 4T1 세포 및 AH1 펩타이드를 사용하여 수행하고 IFN-수준을 측정하였다. 도 6A는 비장 및 배액 LN 모두에서 GVAX 그룹에 비해 TEGVAX 그룹에서 AH1 특이성 IFN-생산 T-세포의 수가 통계학적으로 더 크다는 그래프이다(P<0.01). 도 6B는 AH1 특이성 CTL 살해의 그래프이다. 생체 내 CTL 분석을 사용하여 TEGVAX로 처리된 또는 상기 없이 처리된 CT26 종양 함유 마우스에서 AH1 특이성 CTL의 살해 퍼센트를 측정하였다. -gal CFSE 표지된 저 세포 및 AH1 CFSE 표지된 고 세포를 고유, 종양 함유 또는 TEGVAX 처리된 종양 함유 그룹들에 동시 주사하였다. 평균적인 평균 특이성 종양 용해는 처리되지 않은 그룹에 비해 TEGVAX 그룹에서 더 높았다(P<0.07).
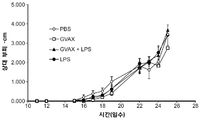
도 7은 제형 없이 별도로 주사된 동 몰의 PLS와 병용된 GVAX가 종양 억제 반응을 유도하지 않음을 도시한다. B16 함유 마우스를 GVAX, LPS, 또는 LPS와 GVAX의 혼합물로, 리포솜 제형 없이 종양 주변에 처리하였다. 도 2에 사용된 바와 같은 동 몰 량의 LPS를 이들 실험에서 종양 주변에 주사하였다.
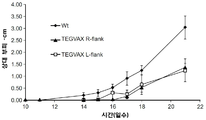
도 8은 TEGVAX가 전신적인 종양 억제 반응을 또한 유도할 수 있음을 도시한다. B16 종양 모델을 사용하여, 마우스를 TEGVAX로 종양 주변에 처리하거나 또는 TEGVAX를 종양 접종 부위로부터 대측성 사지 내로 주사하여 처리하였다. TEGVAX 그룹은 모두 유사한 생체 내 종양 성장 속도를 나타내었다.
도 9는 GVAX, R848 및 GLA의 조합이 흑색종 종양 세포 성장을 방지함을 도시하는 그래프이다. GVAX 및 다양한 TLR 작용물질과의 그의 제형을 B16 종양 접종 후 3일째에 주사하였다. 상기 종양은 백신 처리 시에 촉진할 수 없었다. 상기 종양의 상대적인 성장 속도를 각각의 그룹에 대해 추적하였다. GVAX, GLA 및 R848로 처리된 B16 종양의 경우, 상기 종양 성장은 처음에 다른 그룹들보다 적은 것으로 기록되었으며, 이들 마우스 중 일부에서 상기 종양은 회귀하였다.
도 10은 TLR 작용물질 증대된 GVAX가 확립된 B16 종양에 대해 종양 성장 속도를 감소시킴을 도시하는 그래프이다. B16 종양 세포를 발바닥에 주사하였으며, 일단 종양이 촉진되었으면, 상기 마우스를 도면에서 지시하는 바와 같이 백신 제형으로 처리하였다. 상기 백신을 대측성 사지에 주사하였다.
도 11은 GVAX/GLA/R848로 처리된 마우스가 가장 많은 수의 p15E-특이성 T-세포를 가지며 이러한 결과는 생체 내 종양 성장 속도와 상관이 있음을 도시하는 ELISPOT 분석 및 생체 내 CTL 분석의 결과를 도시하는 여러 개의 패널을 제공한다. 상기 백신 제형으로 처리된 마우스를 처리 후 1 내지 2주째에 수확하고, 그의 비장을 종양 특이성 T-세포에 대해 분석하였다. 이에 관하여 도 11A, 11B 및 11C로 제공한다.
도 12는 GVAX/GLA/R848로 처리된 마우스가 활성화된 수지상 세포를 현저하게 증대시켰음을 도시하는 2 개의 패널을 제공한다.
도 13은 GVAX/GLA/R848로 처리된 마우스가 Il-12를 발현하는 CD11c+ 세포의 수를 통계학적 유의수준으로 가짐을 도시하는 FACS 분석을 제공한다.
도 14는 확립된 B16 종양에 대한 GVAX/GLA/R848의 다양한 제형들의 효과를 도시하는 그래프이다. IDC-1005는 포스파티딜콜린을 함유하는 안정한 스쿠알렌 수중 유적형 유화액을 포함하는 비히클 존재 하의 GLA/R848이다.
Claims (43)
- 재조합 면역 자극 사이토킨(cytokine)을 발현하고 하나 이상의 톨형 수용체(toll-like receptor, TLR) 작용물질(agonist)을 포함하는 하나 이상의 증식-무능(proliferation-incompetent) 유전자 변형된 종양 세포(neoplastic cells)를 포함하는 면역원성 조성물.
- 제 1 항에 있어서,
사이토킨이 과립구-대식세포 콜로니-자극 인자(GM-CSF)인 면역원성 조성물. - 제 1 항에 있어서,
세포가 필적할만한 양의 하나 이상의 TLR 작용물질 및 GM-CSF를 포함하는 면역원성 조성물. - 제 1 항에 있어서,
TLR 작용물질이 TLR4, TLR5, TLR6, TLR7 또는 TLR8, TLR9 작용물질인 면역원성 조성물. - 제 1 항에 있어서,
TLR4 작용물질 및 TLR7/8 작용물질을 포함하는 면역원성 조성물. - 제 5 항에 있어서,
TLR4 작용물질이 LPS, LPS 단편, 또는 합성 글리코피라노실(glycopyranosyl) 지질 A 유사체(analogue)이고, TLR7/8 동족체(analog)가 R848인 면역원성 조성물. - 제 1 항에 있어서,
세포가 조사(irradiation)에 의해 증식 무능으로 되는 면역원성 조성물. - 제 1 항에 있어서,
종양 세포가 백혈병, 만성 골수성 백혈병, 전립선암, 두경부, 편평 세포 암종, 설암, 후두암, 편도선암, 하인두암, 비인두암, 유방암, 결장암, 폐암, 흑색종, 췌장암, 교모세포종 및 뇌암으로 이루어진 그룹 중에서 선택되는 면역원성 조성물. - 제 1 항에 있어서,
적어도 약 1 ng의 TLR4 작용물질/1 x 105 세포 내지 10 ng의 TLR4 작용물질/1 x 105 세포를 포함하는 면역원성 조성물. - 제 1 항에 있어서,
적어도 약 3 내지 5 ng/5 x 105 세포를 포함하는 면역원성 조성물. - 제 1 항에 있어서,
세포가 리포펙타민(lipofectamine) 또는 다른 리포솜 벡터(liposomal vector)와 함께 TLR 작용물질을 포함하는 면역원성 조성물. - 제 11 항에 있어서,
세포가 LPS/리포솜 미셀(micelle)을 포함하는 면역원성 조성물. - 제 1 항에 있어서,
하나 이상의 종양 항원을 발현하는 세포를 더욱 포함하는 면역원성 조성물. - 제 1 항 내지 제 13 항 중 어느 한 항에 있어서,
세포가 자기조직 또는 동종이계인 면역원성 조성물. - 환자에게서 종양을 개선하기 위한 백신으로서, 약학적으로 허용 가능한 부형제 내에, 재조합 면역 자극 사이토킨을 발현하고 유효량의 외부 톨형 수용체(TLR)를 포함하는 유효량의 증식-무능 종양 세포를 포함하는 백신.
- 제 15 항에 있어서,
세포가 GM-CSF를 발현하도록 유전자 변형된 백신. - 제 15 항에 있어서,
조성물이 TLR4 작용물질 및 TLR7/8 작용물질을 포함하는 백신. - 제 17 항에 있어서,
TLR4 작용물질이 LPS, LPS 단편, 또는 합성 글루코피라노실 지질 A 유사체이고, TLR7/8 동족체가 R848인 백신. - 제 15 항에 있어서,
세포가 LPS/리포솜 미셀을 포함하는 백신. - 제 12 항에 있어서,
하나 이상의 종양 항원을 발현하는 세포를 더욱 포함하는 백신. - 제 12 항 내지 제 20 항 중 어느 한 항에 있어서,
세포가 자기조직 또는 동종이계인 백신. - 종양이 있거나 또는 종양이 발병할 소인이 있는 환자에게서 종양 세포 항원-특이성 면역 반응을 유도하는 방법으로서, 상기 환자에게서 종양 세포 항원-특이성 면역 반응을 유도하기에 충분한 양으로, 상기 환자에게 유효량의, 재조합 면역 자극 사이토킨을 발현하고 외부 톨형 수용체(TLR) 작용물질을 포함하는 하나 이상의 증식-무능 종양 세포를 포함하는 면역원성 조성물을 투여함을 포함하는 방법.
- 종양이 있거나 또는 종양이 발병할 소인이 있는 환자에게서 종양을 치료하거나 예방하는 방법으로서, 상기 환자에게서 종양 세포 항원-특이성 면역 반응을 유도하기에 충분한 양으로, 상기 환자에게 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여하여, 상기 환자를 치료함을 포함하는 방법.
- 종양이 있는 환자에게서 종양 진행 또는 전이를 치료하거나 예방하는 방법으로서, 상기 환자에게 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여하여, 상기 환자에게서 종양 진행 또는 전이를 치료하거나 예방함을 포함하는 방법.
- 환자에게서 확립된 종양(established tumor)을 치료하거나 또는 종양 형성을 예방하는 방법으로서, 상기 환자에게 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여하여, 상기 환자에게서 확립된 종양을 치료하거나 종양 형성을 예방함을 포함하는 방법.
- 미소 전이(micrometastasis) 또는 후유증이 있는 환자에게서 상기 미소 전이 또는 후유증을 치료하는 방법으로서, 상기 환자에게 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여하여, 상기 환자에게서 미소 전이 또는 후유증을 치료함을 포함하는 방법.
- 환자의 면역 방법으로서, 상기 환자에게 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여함을 포함하는 방법.
- 제 14 항 내지 제 27 항 중 어느 한 항에 있어서,
종양 세포가 암 세포주로부터 유래하거나 또는 종양으로부터 유래하는 방법. - 제 17 항에 있어서,
암 세포주 또는 종양이 백혈병, 만성 골수성 백혈병, 전립선암, 두경부, 편평 세포 암종, 설암, 후두암, 편도선암, 하인두암, 비인두암, 유방암, 결장암, 폐암, 흑색종, 췌장암, 교모세포종 및 뇌암으로 이루어진 그룹 중에서 선택되는 방법. - 제 14 항 내지 제 16 항 중 어느 한 항에 있어서,
면역원성 조성물을 전신으로 또는 국소로 투여하는 방법. - 제 19 항에 있어서,
면역원성 조성물을 근육 내 주사, 정맥 내 주사, 종양 내 주사, 또는 종양 주변 주사에 의해 투여하는 방법. - 제 8 항 또는 제 9 항에 있어서,
환자에게 유효량의 하나 이상의 화학요법제를 투여함을 또한 포함하는 방법. - 제 12 항에 있어서,
하나 이상의 화학요법제가 아비라테론 아세테이트, 알트레타민, 무수빈블라스틴, 아우리스타틴, 벡사로텐, 바이칼류타미드, BMS184476, 2,3,4,5,6-펜타플루오로-N-(3-플루오로-4-메톡시페닐)벤젠 설폰아미드, 블레오마이신, N,N-다이메틸-L-발릴-L-발릴-N-메틸-L-발릴-L-프롤릴-L-프롤린-t-부틸아미드, 카켁틴, 세마도틴, 클로람부실, 사이클로포스파미드, 3',4'-다이데하이드로-4'-데옥시-8'-노르빈-칼류코블라스틴, 도세탁솔, 도세탁셀, 사이클로포스파미드, 카보플라틴, 칼머스틴(BCNU), 시스플라틴, 크립토피신, 사이클로포스파미드, 시타라빈, 다카바진(DTIC), 닥티노마이신, 다우노루비신, 데시타빈 돌라스타틴, 독소루비신(아드리아마이신), 에토포시드, 5-플루오로유라실, 피나스테라이드, 플루타미드, 하이드록시유레아 및 하이드록시유레아탁산, 이포스파미드, 리아로졸, 로니다민, 로머스틴(CCNU), MDV3100, 메클로레타민(질소 머스타드), 멜팔란, 미보뷸린 이세티오네이트, 리족신, 세르테네프, 스트렙토조신, 미토마이신, 메토트렉세이트, 탁산, 닐루타미드, 오나프리스톤, 패클리탁셀, 프레드니머스틴, 프로카바진, RPR109881, 스트라머스틴 포스페이트, 타목시펜, 타소네르민, 탁솔, 트레티노인, 빈블라스틴, 빈크리스틴, 빈데신 설페이트, 및 빈플루닌으로 이루어진 그룹으로부터 선택되는 방법. - 제 12 항 내지 제 31 항 중 어느 한 항에 있어서,
GVAX 단독 사용에 비해 수지상 세포의 활성화를 증대시키고/시키거나 AH1-특이성 세포독성 T-세포 또는 p15E-특이성 세포독성 T-세포의 수를 증가시키는 방법. - 제 12 항 내지 제 31 항 중 어느 한 항에 있어서,
GVAX 단독 사용에 비해 종양 세포 증식, 종양 성장, 또는 환자 생존을 감소시키거나 안정화시키는 방법. - GM-CSF를 암호화하는 발현 벡터 및 하나 이상의 TLR 작용물질을 포함하는 증식-무능 종양 세포.
- 제 34 항에 있어서,
백혈병, 만성 골수성 백혈병, 전립선암, 두경부, 편평 세포 암종, 설암, 후두암, 편도선암, 하인두암, 비인두암, 유방암, 결장암, 폐암, 흑색종, 췌장암, 교모세포종 및 뇌암, 또는 이들의 세포주로부터 유래하는 종양 세포. - 제 34 항에 있어서,
TLR4 및 TLR7/8 작용물질을 포함하는 종양 세포. - 제 34 항에 있어서,
TLR 작용물질이 리포솜 벡터와 함께 존재하는 종양 세포. - 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신 및 약학적으로 허용 가능한 부형제를 포함하는 종양 치료용 약학 조성물.
- 종양 치료용 키트로서, 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신 및 제 22 항 내지 제 33 항 중 어느 한 항의 방법에서 상기 키트를 사용하기 위한 설명서를 포함하는 키트.
- 환자에게서 경부 암을 치료하거나 예방하는 방법으로서, 상기 환자에게 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여하여, 상기 환자에게서 경부 암을 치료하거나 예방함을 포함하는 방법.
- 환자에게서 다형성 TLR 결핍증을 치료하는 방법으로서, 상기 환자에게 유효량의 제 1 항 내지 제 21 항 중 어느 한 항의 면역원성 조성물 또는 백신을 투여하여, 상기 환자에게서 상기 다형성 TLR 결핍증을 치료함을 포함하는 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US32847110P | 2010-04-27 | 2010-04-27 | |
| US61/328,471 | 2010-04-27 | ||
| PCT/US2011/034139 WO2011139769A2 (en) | 2010-04-27 | 2011-04-27 | Immunogenic compositions and methods for treating neoplasia |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20130122902A true KR20130122902A (ko) | 2013-11-11 |
Family
ID=44861853
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020127031065A Ceased KR20130122902A (ko) | 2010-04-27 | 2011-04-27 | 종양 치료용 면역원성 조성물 및 방법 |
Country Status (11)
| Country | Link |
|---|---|
| US (2) | US9248170B2 (ko) |
| EP (1) | EP2563384B1 (ko) |
| JP (2) | JP6042802B2 (ko) |
| KR (1) | KR20130122902A (ko) |
| CN (1) | CN103118697A (ko) |
| AU (1) | AU2011248583B2 (ko) |
| BR (2) | BR112012027745A2 (ko) |
| CA (2) | CA2798074A1 (ko) |
| EA (1) | EA030337B1 (ko) |
| NZ (1) | NZ603786A (ko) |
| WO (2) | WO2011136828A1 (ko) |
Families Citing this family (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP6042802B2 (ja) * | 2010-04-27 | 2016-12-14 | ザ・ジョンズ・ホプキンス・ユニバーシティ | 新生物(腫瘍)を治療するための免疫原性組成物及び方法。 |
| EP2758080B1 (en) * | 2011-09-19 | 2018-03-07 | The Johns Hopkins University | Cancer immunotherapy |
| EP2780363B1 (en) | 2011-11-17 | 2019-07-03 | Glia SP Z.O.O. | Compositions and methods for treating glioma |
| SG11201401471PA (en) * | 2011-11-30 | 2014-08-28 | Astrazeneca Ab | Combination treatment of cancer |
| CN104507538B (zh) * | 2012-06-08 | 2018-04-06 | 艾杜罗生物科技公司 | 癌症免疫疗法的组合物和方法 |
| SI2931738T1 (sl) | 2012-12-13 | 2019-05-31 | Aduro Biotech, Inc. | Sestave, ki vsebujejo ciklične purin dinukleotide z definirano stereokemijo, ter metode za njihovo pripravo in uporabo |
| SG11201508165VA (en) | 2013-04-29 | 2015-11-27 | Sloan Kettering Inst Cancer | Compositions and methods for altering second messenger signaling |
| JP2016518140A (ja) | 2013-05-03 | 2016-06-23 | ザ リージェンツ オブ ザ ユニバーシティ オブ カリフォルニア | I型インターフェロンの環状ジヌクレオチド誘導法 |
| US9549944B2 (en) | 2013-05-18 | 2017-01-24 | Aduro Biotech, Inc. | Compositions and methods for inhibiting “stimulator of interferon gene”—dependent signalling |
| JP6453855B2 (ja) | 2013-05-18 | 2019-01-16 | アドゥロ バイオテック,インク. | 「インターフェロン遺伝子の刺激因子」依存性シグナル伝達を活性化するための組成物及び方法 |
| US9463198B2 (en) * | 2013-06-04 | 2016-10-11 | Infectious Disease Research Institute | Compositions and methods for reducing or preventing metastasis |
| CA2919268C (en) | 2013-07-25 | 2023-09-05 | Exicure, Inc. | Spherical nucleic acid-based constructs as immunostimulatory agents for prophylactic and therapeutic use |
| WO2015017652A1 (en) | 2013-07-31 | 2015-02-05 | Memorial Sloan-Kettering Cancer Center | Sting crystals and modulators |
| US20150086592A1 (en) | 2013-09-25 | 2015-03-26 | Sequoia Sciences, Inc | Compositions of vaccines and adjuvants and methods for the treatment of urinary tract infections |
| US9149522B2 (en) | 2013-09-25 | 2015-10-06 | Sequoia Sciences, Inc. | Compositions of vaccines and adjuvants and methods for the treatment of urinary tract infections |
| US9504743B2 (en) | 2013-09-25 | 2016-11-29 | Sequoia Sciences, Inc | Compositions of vaccines and adjuvants and methods for the treatment of urinary tract infections |
| US9149521B2 (en) | 2013-09-25 | 2015-10-06 | Sequoia Sciences, Inc. | Compositions of vaccines and adjuvants and methods for the treatment of urinary tract infections |
| EP3508198A1 (en) | 2014-06-04 | 2019-07-10 | Exicure, Inc. | Multivalent delivery of immune modulators by liposomal spherical nucleic acids for prophylactic or therapeutic applications |
| EP4681782A2 (en) | 2015-01-12 | 2026-01-21 | Children's Medical Center Corporation | Pro-inflammatory and adjuvant functions of toll-like receptor 4 antagonists |
| ES2761861T3 (es) | 2015-01-21 | 2020-05-21 | Univ Leland Stanford Junior | Uso de agonistas de TLR y agente anti-CD47 para mejorar la fagocitosis de las células cancerosas |
| EP3824908A1 (en) | 2015-04-10 | 2021-05-26 | Capsugel Belgium NV | Abiraterone acetate lipid formulations |
| CN108289858A (zh) * | 2015-06-30 | 2018-07-17 | 宾夕法尼亚州立大学托管会 | 用于治疗肿瘤性皮肤疾病的瑞喹莫特局部可注射组合物 |
| PT3386500T (pt) | 2015-12-09 | 2023-01-06 | Univ Illinois | Supressores seletivos do recetor de estrogénio à base de benzotiofeno |
| US11697851B2 (en) | 2016-05-24 | 2023-07-11 | The Regents Of The University Of California | Early ovarian cancer detection diagnostic test based on mRNA isoforms |
| WO2018039629A2 (en) | 2016-08-25 | 2018-03-01 | Northwestern University | Micellar spherical nucleic acids from thermoresponsive, traceless templates |
| WO2018081168A2 (en) | 2016-10-24 | 2018-05-03 | The Board Of Trustees Of The University Of Illinois | Benzothiophene-based selective mixed estrogen receptor downregulators |
| CA3048057A1 (en) | 2017-01-06 | 2018-07-12 | G1 Therapeutics, Inc. | Combination therapy for the treatment of cancer |
| FR3072880A1 (fr) * | 2017-10-30 | 2019-05-03 | Institut National De La Sante Et De La Recherche Medicale (Inserm) | Formulation liposomale et son utilisation en therapie anti-tumorale |
| JP7287708B2 (ja) * | 2019-02-08 | 2023-06-06 | プロジェニア インコーポレイテッド | Toll-like受容体7または8アゴニストとコレステロールの結合体およびその用途 |
| CN114401738B (zh) * | 2019-03-14 | 2025-02-07 | 加利福尼亚大学董事会 | 作为疫苗佐剂的tlr4和tlr7配体制剂 |
| CN111773381A (zh) * | 2020-07-06 | 2020-10-16 | 贵阳市第二人民医院 | 一种靶向tem-1基因疫苗及其构建与应用 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5637483A (en) * | 1991-10-04 | 1997-06-10 | Whitehead Institute For Biomedical Research | Irradiated tumor cell vaccine engineered to express GM-CSF |
| US5904920A (en) | 1991-10-04 | 1999-05-18 | Whitehead Institute For Biomedical Research | Regulation of systemic immune responses utilizing cytokines and antigens |
| US6033674A (en) | 1995-12-28 | 2000-03-07 | Johns Hopkins University School Of Medicine | Method of treating cancer with a tumor cell line having modified cytokine expression |
| US6277368B1 (en) | 1996-07-25 | 2001-08-21 | The Regents Of The University Of California | Cancer immunotherapy using autologous tumor cells combined with cells expressing a membrane cytokine |
| ES2218994T3 (es) | 1998-02-02 | 2004-11-16 | The Johns Hopkins University School Of Medicine | Linea celular inmunomoduladora universal que expresa citocinas y composiciones relacionadas y procedimientos de fabricacion y uso. |
| WO2000072686A1 (en) | 1999-06-02 | 2000-12-07 | Cell Genesys, Inc. | Regulation of systemic immune responses utilizing cytokines and antigens |
| US20030044393A1 (en) * | 2001-07-06 | 2003-03-06 | Annie-Chen Tran | Method for increasing tumor cell immunogenicity using heat shock protein |
| US20040197312A1 (en) * | 2003-04-02 | 2004-10-07 | Marina Moskalenko | Cytokine-expressing cellular vaccine combinations |
| US20050013812A1 (en) * | 2003-07-14 | 2005-01-20 | Dow Steven W. | Vaccines using pattern recognition receptor-ligand:lipid complexes |
| GB0321615D0 (en) * | 2003-09-15 | 2003-10-15 | Glaxo Group Ltd | Improvements in vaccination |
| US20060057127A1 (en) | 2004-09-10 | 2006-03-16 | Pocheng Liu | Cytokine-expressing cellular vaccines for treatment of prostate cancer |
| CN101355928B (zh) | 2005-04-26 | 2013-05-22 | 卫材R&D管理株式会社 | 用于癌症免疫疗法的组合物和方法 |
| US20090081157A1 (en) * | 2006-01-09 | 2009-03-26 | Richard Syd Kornbluth | Immunostimulatory Combinations for Vaccine Adjuvants |
| EP3403667B1 (en) | 2006-09-26 | 2020-07-22 | Infectious Disease Research Institute | Vaccine composition containing synthetic adjuvant |
| US8840881B2 (en) | 2008-08-28 | 2014-09-23 | Aduro Gvax Inc. | Methods and compositions for treating prostate cancer or inducing a humoral immune response against prostate cancer |
| JP5816627B2 (ja) * | 2009-10-27 | 2015-11-18 | イミュニカム・エイビイ | 抗原特異的t細胞の増殖のための方法 |
| JP6042802B2 (ja) * | 2010-04-27 | 2016-12-14 | ザ・ジョンズ・ホプキンス・ユニバーシティ | 新生物(腫瘍)を治療するための免疫原性組成物及び方法。 |
| EP2758080B1 (en) * | 2011-09-19 | 2018-03-07 | The Johns Hopkins University | Cancer immunotherapy |
-
2010
- 2010-10-15 JP JP2013507935A patent/JP6042802B2/ja not_active Expired - Fee Related
- 2010-10-15 WO PCT/US2010/052889 patent/WO2011136828A1/en not_active Ceased
- 2010-10-15 CA CA2798074A patent/CA2798074A1/en not_active Abandoned
- 2010-10-15 BR BR112012027745A patent/BR112012027745A2/pt not_active IP Right Cessation
-
2011
- 2011-04-27 AU AU2011248583A patent/AU2011248583B2/en not_active Ceased
- 2011-04-27 EP EP11777959.5A patent/EP2563384B1/en not_active Not-in-force
- 2011-04-27 NZ NZ603786A patent/NZ603786A/en not_active IP Right Cessation
- 2011-04-27 EA EA201291117A patent/EA030337B1/ru not_active IP Right Cessation
- 2011-04-27 CN CN2011800318714A patent/CN103118697A/zh active Pending
- 2011-04-27 WO PCT/US2011/034139 patent/WO2011139769A2/en not_active Ceased
- 2011-04-27 CA CA2797842A patent/CA2797842A1/en not_active Abandoned
- 2011-04-27 KR KR1020127031065A patent/KR20130122902A/ko not_active Ceased
- 2011-04-27 JP JP2013508211A patent/JP6095227B2/ja not_active Expired - Fee Related
- 2011-04-27 BR BR112012027747A patent/BR112012027747A2/pt not_active IP Right Cessation
-
2012
- 2012-10-29 US US13/663,045 patent/US9248170B2/en not_active Expired - Fee Related
-
2015
- 2015-12-17 US US14/972,865 patent/US20160193313A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| JP6095227B2 (ja) | 2017-03-15 |
| EP2563384B1 (en) | 2018-04-25 |
| AU2011248583B2 (en) | 2017-01-19 |
| CA2798074A1 (en) | 2011-11-03 |
| JP6042802B2 (ja) | 2016-12-14 |
| US20160193313A1 (en) | 2016-07-07 |
| JP2013529192A (ja) | 2013-07-18 |
| CA2797842A1 (en) | 2011-11-10 |
| WO2011139769A3 (en) | 2012-04-05 |
| WO2011136828A1 (en) | 2011-11-03 |
| EA201291117A1 (ru) | 2013-04-30 |
| EP2563384A2 (en) | 2013-03-06 |
| WO2011139769A2 (en) | 2011-11-10 |
| US20130177625A1 (en) | 2013-07-11 |
| EP2563384A4 (en) | 2014-03-12 |
| NZ603786A (en) | 2015-07-31 |
| EA030337B1 (ru) | 2018-07-31 |
| AU2011248583A1 (en) | 2012-12-13 |
| JP2013525450A (ja) | 2013-06-20 |
| CN103118697A (zh) | 2013-05-22 |
| US9248170B2 (en) | 2016-02-02 |
| BR112012027745A2 (pt) | 2017-01-10 |
| BR112012027747A2 (pt) | 2017-01-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR20130122902A (ko) | 종양 치료용 면역원성 조성물 및 방법 | |
| KR101205064B1 (ko) | 암 면역요법을 위한 조성물과 방법 | |
| US9770467B2 (en) | Compositions and methods for cancer immunotherapy | |
| AU2010248761B2 (en) | Vaccine immunotherapy | |
| JP2018021047A (ja) | 癌免疫療法 | |
| US20170202949A1 (en) | Defective ribosomal products in blebs (dribbles) and methods of use to stimulate an immune response | |
| Li et al. | The in vivo immunomodulatory and synergistic anti-tumor activity of thymosin α1–thymopentin fusion peptide and its binding to TLR2 | |
| WO2009052561A1 (en) | Compositions and methods for manipulating an immune response | |
| AU2013203561B2 (en) | Vaccine immunotherapy | |
| EP3000471A1 (en) | Novel immunostimulatory molecules |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
Patent event date: 20121127 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PG1501 | Laying open of application | ||
| PA0201 | Request for examination |
Patent event code: PA02012R01D Patent event date: 20160426 Comment text: Request for Examination of Application |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20170703 Patent event code: PE09021S01D |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20180423 Patent event code: PE09021S01D |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20181224 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20180423 Comment text: Notification of reason for refusal Patent event code: PE06011S01I Patent event date: 20170703 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |