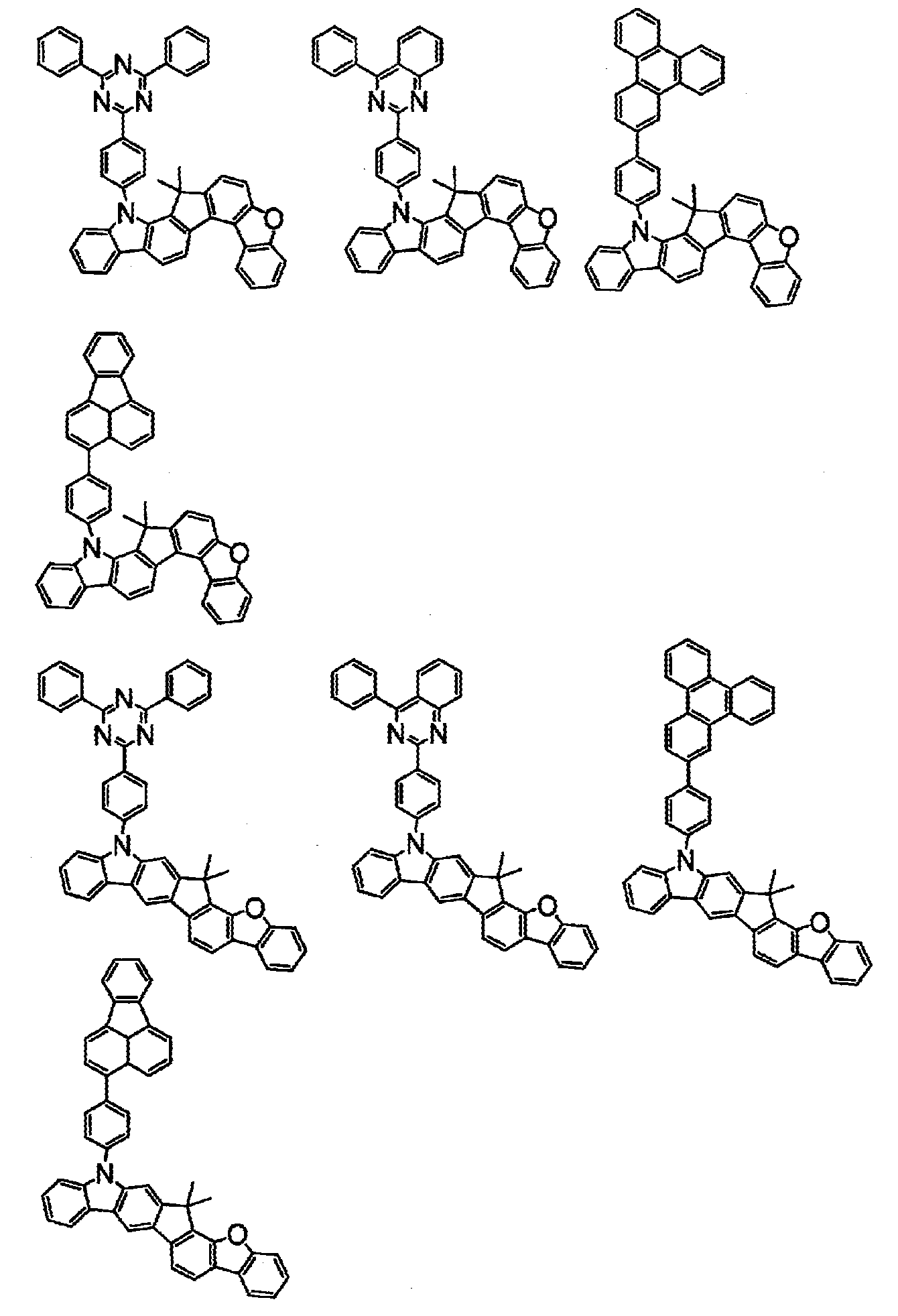KR20170052521A - 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 - Google Patents
화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 Download PDFInfo
- Publication number
- KR20170052521A KR20170052521A KR1020167002885A KR20167002885A KR20170052521A KR 20170052521 A KR20170052521 A KR 20170052521A KR 1020167002885 A KR1020167002885 A KR 1020167002885A KR 20167002885 A KR20167002885 A KR 20167002885A KR 20170052521 A KR20170052521 A KR 20170052521A
- Authority
- KR
- South Korea
- Prior art keywords
- group
- ring
- synthesis
- bonded
- carbon atoms
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 Cc1c(Cc2c-3c(*)c(*)c(*)c2*)c-3c(*)c-2c1C(*)(*)c1c(*)c([n](*)c3c(*)c(*)*(C)c(*)c33)c3c(*)c-21 Chemical compound Cc1c(Cc2c-3c(*)c(*)c(*)c2*)c-3c(*)c-2c1C(*)(*)c1c(*)c([n](*)c3c(*)c(*)*(C)c(*)c33)c3c(*)c-21 0.000 description 56
- GRJXDJKMXAWCHI-UHFFFAOYSA-N C=CC(c1ccc2[nH]c3ccccc3c2c1)=C Chemical compound C=CC(c1ccc2[nH]c3ccccc3c2c1)=C GRJXDJKMXAWCHI-UHFFFAOYSA-N 0.000 description 1
- RKDDRHJBLWLLFV-UHFFFAOYSA-N CC(C)(C(C=Cc1c2c3ccccc3[o]1)=CC2c1ccc2c3ccccc33)c1c2[n]3-c(cc1)ccc1-c1[n+](Cc2ccccc2)[N-](C)c(-c2ccccc2)n1 Chemical compound CC(C)(C(C=Cc1c2c3ccccc3[o]1)=CC2c1ccc2c3ccccc33)c1c2[n]3-c(cc1)ccc1-c1[n+](Cc2ccccc2)[N-](C)c(-c2ccccc2)n1 RKDDRHJBLWLLFV-UHFFFAOYSA-N 0.000 description 1
- XPAYCFWSYQKIRZ-UHFFFAOYSA-N CC(C)(C12)c(cc3[o]c(cccc4)c4c3c3)c3C1=CCc1ccccc1N2c(cc1)ccc1-c(cc1)ccc1[Si](C)(C)C Chemical compound CC(C)(C12)c(cc3[o]c(cccc4)c4c3c3)c3C1=CCc1ccccc1N2c(cc1)ccc1-c(cc1)ccc1[Si](C)(C)C XPAYCFWSYQKIRZ-UHFFFAOYSA-N 0.000 description 1
- YWWZDZCSBHRFDQ-UHFFFAOYSA-N CC(C)(C1=CC23)c(c4c(cc5)c(cccc6)c6[o]4)c5C1=CC2c1ccccc1N3c(cc1)ccc1-c1nc(-c2ccccc2)c(cccc2)c2n1 Chemical compound CC(C)(C1=CC23)c(c4c(cc5)c(cccc6)c6[o]4)c5C1=CC2c1ccccc1N3c(cc1)ccc1-c1nc(-c2ccccc2)c(cccc2)c2n1 YWWZDZCSBHRFDQ-UHFFFAOYSA-N 0.000 description 1
- QUYJEDLETCKHKB-UHFFFAOYSA-N CC(C)(C1=CC23)c(c4c(cc5)c6ccccc6[o]4)c5C1=CC2C1=CCCC=C1N3c(cc1)ccc1-c(cc1)cc2c1c(cccc1)c1c1c2cccc1 Chemical compound CC(C)(C1=CC23)c(c4c(cc5)c6ccccc6[o]4)c5C1=CC2C1=CCCC=C1N3c(cc1)ccc1-c(cc1)cc2c1c(cccc1)c1c1c2cccc1 QUYJEDLETCKHKB-UHFFFAOYSA-N 0.000 description 1
- JHKJZYZHELFNQD-PUZJPNBESA-N CC(C)(C1C=C2Oc(ccc(C(C3)=NC(c4ccccc4)=NC3[C@@H]3C=CC=CC3)c3)c3C2=CC1C1=CC2c3ccccc33)C1=CC[N]23c1ccccc1 Chemical compound CC(C)(C1C=C2Oc(ccc(C(C3)=NC(c4ccccc4)=NC3[C@@H]3C=CC=CC3)c3)c3C2=CC1C1=CC2c3ccccc33)C1=CC[N]23c1ccccc1 JHKJZYZHELFNQD-PUZJPNBESA-N 0.000 description 1
- OKDPRPWRTDCGEY-UHFFFAOYSA-N CC(C)(c(c(-c1c2)c3)cc4c3C(CCC=C3)=C3C4=C)c1cc1c2C2=CCCC=C2N1c(cc1)ccc1-c1cccc2c1cccc2 Chemical compound CC(C)(c(c(-c1c2)c3)cc4c3C(CCC=C3)=C3C4=C)c1cc1c2C2=CCCC=C2N1c(cc1)ccc1-c1cccc2c1cccc2 OKDPRPWRTDCGEY-UHFFFAOYSA-N 0.000 description 1
- JJALIQFTLOALED-UHFFFAOYSA-N CC(C)(c(c(-c1c2)c3)cc4c3c(cccc3)c3[n]4-c(cc3)ccc3-c3cc4ccccc4cc3)c1cc1c2c(cccc2)c2[o]1 Chemical compound CC(C)(c(c(-c1c2)c3)cc4c3c(cccc3)c3[n]4-c(cc3)ccc3-c3cc4ccccc4cc3)c1cc1c2c(cccc2)c2[o]1 JJALIQFTLOALED-UHFFFAOYSA-N 0.000 description 1
- CMTVWJBMAIKNSG-UHFFFAOYSA-N CC(C)(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccc(C4=CC=C5c6ccccc6C6=CC=CC4C56)c4c3cccc4)c1cc1c2c(cccc2)c2[o]1 Chemical compound CC(C)(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccc(C4=CC=C5c6ccccc6C6=CC=CC4C56)c4c3cccc4)c1cc1c2c(cccc2)c2[o]1 CMTVWJBMAIKNSG-UHFFFAOYSA-N 0.000 description 1
- NKJAAYWCEQDGQE-UHFFFAOYSA-N CC(C)(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccccc3)c1cc1c2c(cc(C(C2)C=Cc3c2c(cccc2)c2[n]3-c2ccccc2)cc2)c2[o]1 Chemical compound CC(C)(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccccc3)c1cc1c2c(cc(C(C2)C=Cc3c2c(cccc2)c2[n]3-c2ccccc2)cc2)c2[o]1 NKJAAYWCEQDGQE-UHFFFAOYSA-N 0.000 description 1
- PCUCQTRFKAPAEP-UHFFFAOYSA-N CC(C)(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccccc3)c1cc1c2c2cc(-c(cc3)ccc3-c3nc(C4=CCCC=C4)[n+](Cc4ccccc4)[n-]3)ccc2[o]1 Chemical compound CC(C)(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccccc3)c1cc1c2c2cc(-c(cc3)ccc3-c3nc(C4=CCCC=C4)[n+](Cc4ccccc4)[n-]3)ccc2[o]1 PCUCQTRFKAPAEP-UHFFFAOYSA-N 0.000 description 1
- VKPIPQWVVNTZGD-UHFFFAOYSA-N CC(C)(c(c(C1=CC2C(C3)C4=CC=C3c(cc3c5c6cccc5)ccc3[n]6-c3ccccc3)c3)cc(OC5)c3-c3c5cccc3)C1=CC2N4c1ccccc1 Chemical compound CC(C)(c(c(C1=CC2C(C3)C4=CC=C3c(cc3c5c6cccc5)ccc3[n]6-c3ccccc3)c3)cc(OC5)c3-c3c5cccc3)C1=CC2N4c1ccccc1 VKPIPQWVVNTZGD-UHFFFAOYSA-N 0.000 description 1
- MAQYLVAGLUGDGR-UHFFFAOYSA-N CC(C)(c(cc(c(c1ccccc11)c2)[n]1-c1nc(C3=CC=C4C(C=CCC5)=C5C5=CC=CC3C45)ccc1)c2-c1c2)c1cc1c2c2ccccc2[o]1 Chemical compound CC(C)(c(cc(c(c1ccccc11)c2)[n]1-c1nc(C3=CC=C4C(C=CCC5)=C5C5=CC=CC3C45)ccc1)c2-c1c2)c1cc1c2c2ccccc2[o]1 MAQYLVAGLUGDGR-UHFFFAOYSA-N 0.000 description 1
- RBEMESPSOQBXNL-UHFFFAOYSA-N CC(C)(c(cc1[o]c2ccccc2c1c1)c1C1=CC2c3ccccc33)C1=CC2N3c(c1c2cccc1)ccc2-c1nc(-c2ccccc2)c(cccc2)c2n1 Chemical compound CC(C)(c(cc1[o]c2ccccc2c1c1)c1C1=CC2c3ccccc33)C1=CC2N3c(c1c2cccc1)ccc2-c1nc(-c2ccccc2)c(cccc2)c2n1 RBEMESPSOQBXNL-UHFFFAOYSA-N 0.000 description 1
- JNKYZUYFRXPMTH-UHFFFAOYSA-N CC(C)(c(ccc-1c2Cc3c-1cccc3)c2-c1c2)c1cc(c1ccccc11)c2[n]1-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CC=CC1C23 Chemical compound CC(C)(c(ccc-1c2Cc3c-1cccc3)c2-c1c2)c1cc(c1ccccc11)c2[n]1-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CC=CC1C23 JNKYZUYFRXPMTH-UHFFFAOYSA-N 0.000 description 1
- WVMLJYQIYZYNME-UHFFFAOYSA-N CC(C)(c(ccc1c2C3C=CC=CC3O1)c2-c1ccc2c3ccccc33)c1c2[n]3-c(cc1)ccc1-c1nc(cccc2)c2c(-c2ccccc2)n1 Chemical compound CC(C)(c(ccc1c2C3C=CC=CC3O1)c2-c1ccc2c3ccccc33)c1c2[n]3-c(cc1)ccc1-c1nc(cccc2)c2c(-c2ccccc2)n1 WVMLJYQIYZYNME-UHFFFAOYSA-N 0.000 description 1
- ANHQEDFQPSGMAX-UHFFFAOYSA-N CC(C)(c1c(-c2ccc3c4ccccc44)c(C(CCC=C5)=C5OCC5)c5cc1)c2c3[n]4-c(cc1)ccc1C(C=C1)=CCc2c1c(cccc1)c1c1c2cccc1 Chemical compound CC(C)(c1c(-c2ccc3c4ccccc44)c(C(CCC=C5)=C5OCC5)c5cc1)c2c3[n]4-c(cc1)ccc1C(C=C1)=CCc2c1c(cccc1)c1c1c2cccc1 ANHQEDFQPSGMAX-UHFFFAOYSA-N 0.000 description 1
- GYHCOFCGQOODMC-UHFFFAOYSA-N CC(C)(c1c2)c(c3c(cc4)c(cccc5)c5[o]3)c4-c1cc1c2c2ccccc2[n]1-c1ccc-2c3c1cccc3-c1ccccc-21 Chemical compound CC(C)(c1c2)c(c3c(cc4)c(cccc5)c5[o]3)c4-c1cc1c2c2ccccc2[n]1-c1ccc-2c3c1cccc3-c1ccccc-21 GYHCOFCGQOODMC-UHFFFAOYSA-N 0.000 description 1
- NCPWENAVNKSJOE-VHXPQNKSSA-N CC(C)(c1c2)c(c3c(cc4)c5ccccc5[o]3)c4-c1cc(c1ccccc11)c2[n]1-c(cc1)ccc1C1=CC=C2C(C)=C(/C=C\O)C3=CC=CC1C23 Chemical compound CC(C)(c1c2)c(c3c(cc4)c5ccccc5[o]3)c4-c1cc(c1ccccc11)c2[n]1-c(cc1)ccc1C1=CC=C2C(C)=C(/C=C\O)C3=CC=CC1C23 NCPWENAVNKSJOE-VHXPQNKSSA-N 0.000 description 1
- JVUWRZOLBUSKPR-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1c3cccc1)c2[n]3-c1cccc(-c2cc(-c3ccccc3)nc(-c3ccccc3)n2)n1 Chemical compound CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1c3cccc1)c2[n]3-c1cccc(-c2cc(-c3ccccc3)nc(-c3ccccc3)n2)n1 JVUWRZOLBUSKPR-UHFFFAOYSA-N 0.000 description 1
- YLWTZKPPPJQUIF-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1c3cccc1)c2[n]3-c1nc(-c2[n+](Cc3ccccc3)[n-]c(-c3ccccc3)n2)ccc1 Chemical compound CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1c3cccc1)c2[n]3-c1nc(-c2[n+](Cc3ccccc3)[n-]c(-c3ccccc3)n2)ccc1 YLWTZKPPPJQUIF-UHFFFAOYSA-N 0.000 description 1
- BXFKFMGLHDOUFB-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1c3cccc1)c2[n]3-c1nc(C2=NC(c3ccccc3)=C3C=CC=CC3N2)ccc1 Chemical compound CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1c3cccc1)c2[n]3-c1nc(C2=NC(c3ccccc3)=C3C=CC=CC3N2)ccc1 BXFKFMGLHDOUFB-UHFFFAOYSA-N 0.000 description 1
- QZDUISRILMHIJH-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1ccccc11)c2[n]1-c1ccc(-c2cc3c(cccc4)c4c(cccc4)c4c3cc2)c2c1cccc2 Chemical compound CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1ccccc11)c2[n]1-c1ccc(-c2cc3c(cccc4)c4c(cccc4)c4c3cc2)c2c1cccc2 QZDUISRILMHIJH-UHFFFAOYSA-N 0.000 description 1
- JBBFYSYKUIMPJE-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1ccccc11)c2[n]1-c1nc(-c2nc(-c3ccccc3)cc(-c3ccccc3)n2)ccc1 Chemical compound CC(C)(c1c2)c(cc3[o]c(cccc4)c4c3c3)c3-c1cc(c1ccccc11)c2[n]1-c1nc(-c2nc(-c3ccccc3)cc(-c3ccccc3)n2)ccc1 JBBFYSYKUIMPJE-UHFFFAOYSA-N 0.000 description 1
- HEQZNHDCKQPPAM-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c4ccccc4c3c3)c3-c1cc(C1=C=CCC=C11)c2N1c1nc(-c(cc2)cc3c2c(cccc2)c2c2c3cccc2)ccc1 Chemical compound CC(C)(c1c2)c(cc3[o]c4ccccc4c3c3)c3-c1cc(C1=C=CCC=C11)c2N1c1nc(-c(cc2)cc3c2c(cccc2)c2c2c3cccc2)ccc1 HEQZNHDCKQPPAM-UHFFFAOYSA-N 0.000 description 1
- UIEWARYDVFLXGZ-UHFFFAOYSA-N CC(C)(c1c2)c(cc3[o]c4ccccc4c3c3)c3-c1cc(c1c3ccc(-c4ccc5[o]c(CCC=C6)c6c5c4)c1)c2[n]3-c1ccccc1 Chemical compound CC(C)(c1c2)c(cc3[o]c4ccccc4c3c3)c3-c1cc(c1c3ccc(-c4ccc5[o]c(CCC=C6)c6c5c4)c1)c2[n]3-c1ccccc1 UIEWARYDVFLXGZ-UHFFFAOYSA-N 0.000 description 1
- BCNWYXLNSYRHIN-UHFFFAOYSA-N CC(C)(c1c2c3ccccc33)c(c4c(cc5)c(cccc6)c6[o]4)c5-c1ccc2[n]3-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CC=CC1C23 Chemical compound CC(C)(c1c2c3ccccc33)c(c4c(cc5)c(cccc6)c6[o]4)c5-c1ccc2[n]3-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CC=CC1C23 BCNWYXLNSYRHIN-UHFFFAOYSA-N 0.000 description 1
- UPRNWWGOTHXFQU-UHFFFAOYSA-N CC(C)(c1c2c3ccccc33)c(c4c(cc5)c6ccccc6[o]4)c5-c1ccc2[n]3-c(cc1)ccc1-c1nc(-c2ccccc2)c(cccc2)c2n1 Chemical compound CC(C)(c1c2c3ccccc33)c(c4c(cc5)c6ccccc6[o]4)c5-c1ccc2[n]3-c(cc1)ccc1-c1nc(-c2ccccc2)c(cccc2)c2n1 UPRNWWGOTHXFQU-UHFFFAOYSA-N 0.000 description 1
- ISQFMQAHUNLCQK-UHFFFAOYSA-N CC(C)(c1c2c3ccccc33)c(c4c(cc5)c6ccccc6[o]4)c5-c1ccc2[n]3-c(cc1)ccc1C1=NC(c2ccccc2)=CC=C(C)C(c2ccccc2)=N1 Chemical compound CC(C)(c1c2c3ccccc33)c(c4c(cc5)c6ccccc6[o]4)c5-c1ccc2[n]3-c(cc1)ccc1C1=NC(c2ccccc2)=CC=C(C)C(c2ccccc2)=N1 ISQFMQAHUNLCQK-UHFFFAOYSA-N 0.000 description 1
- HLVGCBZMHNNJNC-UHFFFAOYSA-N CC1(C)C(C=CC(C2c3c4cccc3)N4c3cc(cccc4)c4c4c3cccc4)=C2c2c1cc1[o]c(cccc3)c3c1c2 Chemical compound CC1(C)C(C=CC(C2c3c4cccc3)N4c3cc(cccc4)c4c4c3cccc4)=C2c2c1cc1[o]c(cccc3)c3c1c2 HLVGCBZMHNNJNC-UHFFFAOYSA-N 0.000 description 1
- SVVDPXKSIXSGBG-UHFFFAOYSA-N CC1(C)C(c2c(CC3)c(CCC=C4)c4[o]2)=C3c(cc2)c1c1c2C2=CCCC=C2N1c(cc1)ccc1-c1cc2c(cccc3)c3c(cccc3)c3c2cc1 Chemical compound CC1(C)C(c2c(CC3)c(CCC=C4)c4[o]2)=C3c(cc2)c1c1c2C2=CCCC=C2N1c(cc1)ccc1-c1cc2c(cccc3)c3c(cccc3)c3c2cc1 SVVDPXKSIXSGBG-UHFFFAOYSA-N 0.000 description 1
- UCMRALZQZKMPCF-UHFFFAOYSA-N CC1(C)c(c(c2c3cccc2)c(cc2)[n]3-c3cc4c(cccc5)c5c(cccc5)c5c4cc3)c2-c2c1ccc1c2[o]c2c1cccc2 Chemical compound CC1(C)c(c(c2c3cccc2)c(cc2)[n]3-c3cc4c(cccc5)c5c(cccc5)c5c4cc3)c2-c2c1ccc1c2[o]c2c1cccc2 UCMRALZQZKMPCF-UHFFFAOYSA-N 0.000 description 1
- XTNZPDFNTCXGGC-UHFFFAOYSA-N CC1(C)c(c(c2ccccc22)c(cc3)[n]2C2=CCC4c5ccccc5C5=CC=CC2C45)c3-c2c1ccc1c2[o]c2c1cccc2 Chemical compound CC1(C)c(c(c2ccccc22)c(cc3)[n]2C2=CCC4c5ccccc5C5=CC=CC2C45)c3-c2c1ccc1c2[o]c2c1cccc2 XTNZPDFNTCXGGC-UHFFFAOYSA-N 0.000 description 1
- WNZKKTIAPIJVPW-UHFFFAOYSA-N CC1(C)c(c2c(cc3)c(cccc4)c4[o]2)c3-c(cc2)c1c1c2c(cccc2)c2[n]1-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CCCC1C23 Chemical compound CC1(C)c(c2c(cc3)c(cccc4)c4[o]2)c3-c(cc2)c1c1c2c(cccc2)c2[n]1-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CCCC1C23 WNZKKTIAPIJVPW-UHFFFAOYSA-N 0.000 description 1
- FOVKBRGBYCGEAD-UHFFFAOYSA-N CC1(C)c(c2c(cc3)c4ccccc4[o]2)c3-c2ccc3[n](C4N=C(c5ccccc5)c(cccc5)c5N4)c4ccccc4c3c12 Chemical compound CC1(C)c(c2c(cc3)c4ccccc4[o]2)c3-c2ccc3[n](C4N=C(c5ccccc5)c(cccc5)c5N4)c4ccccc4c3c12 FOVKBRGBYCGEAD-UHFFFAOYSA-N 0.000 description 1
- LYHXNHFIATYMND-UHFFFAOYSA-N CC1(C)c(cc(c2ccccc2[n]2-c(cc3)ccc3-c(cc3)cc4c3c3ccccc3c3ccccc43)c2c2)c2-c2c1ccc1c2[o]c2c1cccc2 Chemical compound CC1(C)c(cc(c2ccccc2[n]2-c(cc3)ccc3-c(cc3)cc4c3c3ccccc3c3ccccc43)c2c2)c2-c2c1ccc1c2[o]c2c1cccc2 LYHXNHFIATYMND-UHFFFAOYSA-N 0.000 description 1
- LFEDQFPLQKEAGR-UHFFFAOYSA-N CC1(C)c2c(c(cccc3)c3[o]3)c3ccc2C(C23)=C1C=CC2c(cccc1)c1N3c1ccc2[o]c3ccccc3c2c1 Chemical compound CC1(C)c2c(c(cccc3)c3[o]3)c3ccc2C(C23)=C1C=CC2c(cccc1)c1N3c1ccc2[o]c3ccccc3c2c1 LFEDQFPLQKEAGR-UHFFFAOYSA-N 0.000 description 1
- KSQONIREZGFSRC-UHFFFAOYSA-N CC1(C)c2c(c3ccccc3[n]3-c(cc4)ccc4C4=CC=C5c6ccccc6C6=CC=CC4C56)c3ccc2C2=C1C=CC1C(CCC=C3)=C3OC21 Chemical compound CC1(C)c2c(c3ccccc3[n]3-c(cc4)ccc4C4=CC=C5c6ccccc6C6=CC=CC4C56)c3ccc2C2=C1C=CC1C(CCC=C3)=C3OC21 KSQONIREZGFSRC-UHFFFAOYSA-N 0.000 description 1
- CDGSZMHKJUUUNO-UHFFFAOYSA-N CC1(C)c2c(c3ccccc3[n]3-c4nc(-c5ccccc5)c(cccc5)c5n4)c3ccc2-c2c3OC4C=CC=CC4c3ccc12 Chemical compound CC1(C)c2c(c3ccccc3[n]3-c4nc(-c5ccccc5)c(cccc5)c5n4)c3ccc2-c2c3OC4C=CC=CC4c3ccc12 CDGSZMHKJUUUNO-UHFFFAOYSA-N 0.000 description 1
- ARSHODZYKNSWKD-UHFFFAOYSA-N CC1(C)c2c(c3ccccc3[n]3-c4nc(C5C=CC=CC5)cc(-c5ccccc5)n4)c3ccc2-c2c3OC4C=CC=CC4c3ccc12 Chemical compound CC1(C)c2c(c3ccccc3[n]3-c4nc(C5C=CC=CC5)cc(-c5ccccc5)n4)c3ccc2-c2c3OC4C=CC=CC4c3ccc12 ARSHODZYKNSWKD-UHFFFAOYSA-N 0.000 description 1
- UUGORQSVHOUPGQ-UHFFFAOYSA-N CC1(C)c2c3[o]c4ccccc4c3ccc2-c2c(c3ccccc3[n]3C4=CCCC(C(CC5)=Cc6c5[o]c5c6cccc5)=C4)c3ccc12 Chemical compound CC1(C)c2c3[o]c4ccccc4c3ccc2-c2c(c3ccccc3[n]3C4=CCCC(C(CC5)=Cc6c5[o]c5c6cccc5)=C4)c3ccc12 UUGORQSVHOUPGQ-UHFFFAOYSA-N 0.000 description 1
- NTFRALMCCCTJME-UHFFFAOYSA-N CC1(C)c2c3[o]c4ccccc4c3ccc2C(C2)C1=Cc(c1ccccc11)c2[n]1-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CC=CC1C23 Chemical compound CC1(C)c2c3[o]c4ccccc4c3ccc2C(C2)C1=Cc(c1ccccc11)c2[n]1-c(cc1)ccc1C1=CC=C2c3ccccc3C3=CC=CC1C23 NTFRALMCCCTJME-UHFFFAOYSA-N 0.000 description 1
- WSNIFRUYXMZSNW-UHFFFAOYSA-N CC1(C)c2cc(Br)ccc2C2C=CC(I)=CC12 Chemical compound CC1(C)c2cc(Br)ccc2C2C=CC(I)=CC12 WSNIFRUYXMZSNW-UHFFFAOYSA-N 0.000 description 1
- APVDYBDINCIMLR-UHFFFAOYSA-N CC1(C)c2ccc(c(cccc3)c3[o]3)c3c2-c2c1ccc(c1c3cccc1)c2[n]3-c1ccccc1 Chemical compound CC1(C)c2ccc(c(cccc3)c3[o]3)c3c2-c2c1ccc(c1c3cccc1)c2[n]3-c1ccccc1 APVDYBDINCIMLR-UHFFFAOYSA-N 0.000 description 1
- OBDGUQGKHBZNSX-UHFFFAOYSA-N C[Si](C)(C)C(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccccc3)(c1cc1c2c2ccccc2[o]1)[Si+](C)(C)Cc1ccc(c2cc(-c3c(C4(C#N)C#N)cc5[o]c6ccccc6c5c3)c4cc2[n]2-c3ccccc3)c2c1 Chemical compound C[Si](C)(C)C(c(c(-c1c2)c3)cc4c3c3ccccc3[n]4-c3ccccc3)(c1cc1c2c2ccccc2[o]1)[Si+](C)(C)Cc1ccc(c2cc(-c3c(C4(C#N)C#N)cc5[o]c6ccccc6c5c3)c4cc2[n]2-c3ccccc3)c2c1 OBDGUQGKHBZNSX-UHFFFAOYSA-N 0.000 description 1
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D491/00—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00
- C07D491/02—Heterocyclic compounds containing in the condensed ring system both one or more rings having oxygen atoms as the only ring hetero atoms and one or more rings having nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D451/00 - C07D459/00, C07D463/00, C07D477/00 or C07D489/00 in which the condensed system contains two hetero rings
- C07D491/04—Ortho-condensed systems
- C07D491/044—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring
- C07D491/048—Ortho-condensed systems with only one oxygen atom as ring hetero atom in the oxygen-containing ring the oxygen-containing ring being five-membered
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D495/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms
- C07D495/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having sulfur atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D495/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/02—Use of particular materials as binders, particle coatings or suspension media therefor
- C09K11/025—Use of particular materials as binders, particle coatings or suspension media therefor non-luminescent particle coatings or suspension media
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- H01L51/0054—
-
- H01L51/0071—
-
- H01L51/0085—
-
- H01L51/5016—
-
- H01L51/5056—
-
- H01L51/5072—
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/11—OLEDs or polymer light-emitting diodes [PLED] characterised by the electroluminescent [EL] layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/15—Hole transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K50/00—Organic light-emitting devices
- H10K50/10—OLEDs or polymer light-emitting diodes [PLED]
- H10K50/14—Carrier transporting layers
- H10K50/16—Electron transporting layers
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/30—Coordination compounds
- H10K85/341—Transition metal complexes, e.g. Ru(II)polypyridine complexes
- H10K85/342—Transition metal complexes, e.g. Ru(II)polypyridine complexes comprising iridium
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/615—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene
- H10K85/622—Polycyclic condensed aromatic hydrocarbons, e.g. anthracene containing four rings, e.g. pyrene
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6572—Polycyclic condensed heteroaromatic hydrocarbons comprising only nitrogen in the heteroaromatic polycondensed ring system, e.g. phenanthroline or carbazole
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6574—Polycyclic condensed heteroaromatic hydrocarbons comprising only oxygen in the heteroaromatic polycondensed ring system, e.g. cumarine dyes
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/657—Polycyclic condensed heteroaromatic hydrocarbons
- H10K85/6576—Polycyclic condensed heteroaromatic hydrocarbons comprising only sulfur in the heteroaromatic polycondensed ring system, e.g. benzothiophene
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1007—Non-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/18—Metal complexes
- C09K2211/185—Metal complexes of the platinum group, i.e. Os, Ir, Pt, Ru, Rh or Pd
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K2101/00—Properties of the organic materials covered by group H10K85/00
- H10K2101/10—Triplet emission
-
- H—ELECTRICITY
- H10—SEMICONDUCTOR DEVICES; ELECTRIC SOLID-STATE DEVICES NOT OTHERWISE PROVIDED FOR
- H10K—ORGANIC ELECTRIC SOLID-STATE DEVICES
- H10K85/00—Organic materials used in the body or electrodes of devices covered by this subclass
- H10K85/60—Organic compounds having low molecular weight
- H10K85/649—Aromatic compounds comprising a hetero atom
- H10K85/654—Aromatic compounds comprising a hetero atom comprising only nitrogen as heteroatom
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Physics & Mathematics (AREA)
- Spectroscopy & Molecular Physics (AREA)
- Optics & Photonics (AREA)
- Crystallography & Structural Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Electroluminescent Light Sources (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
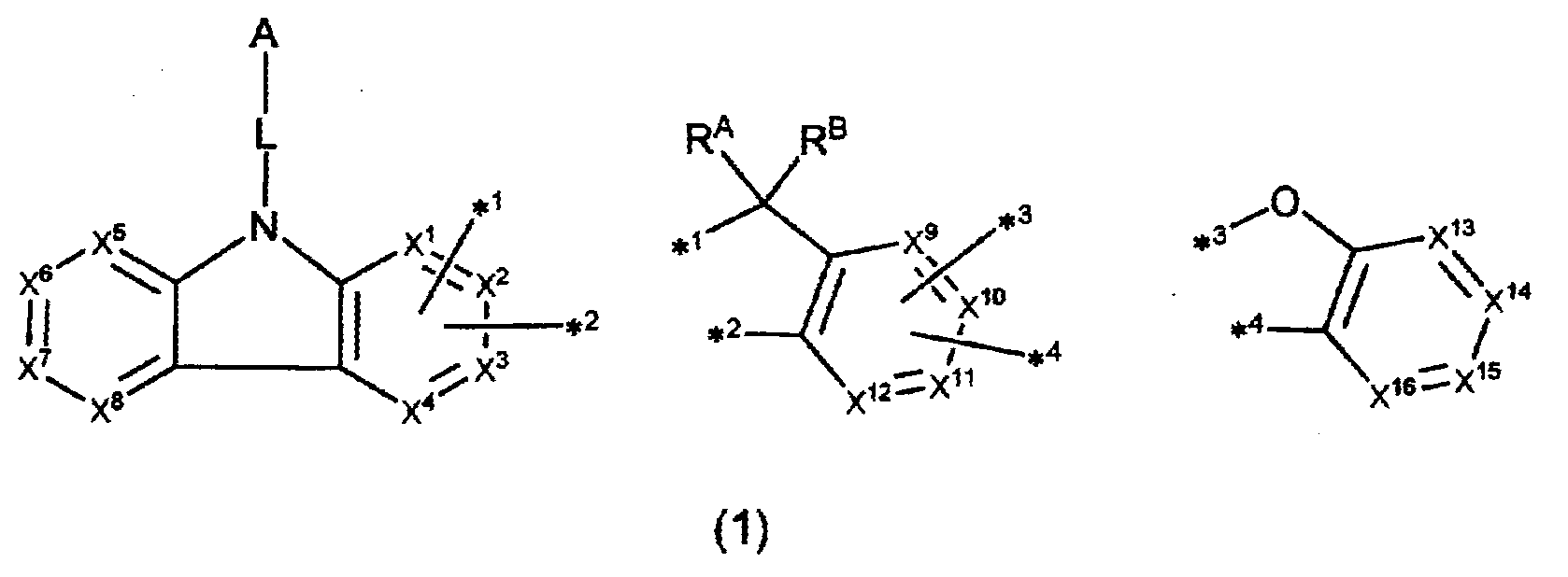
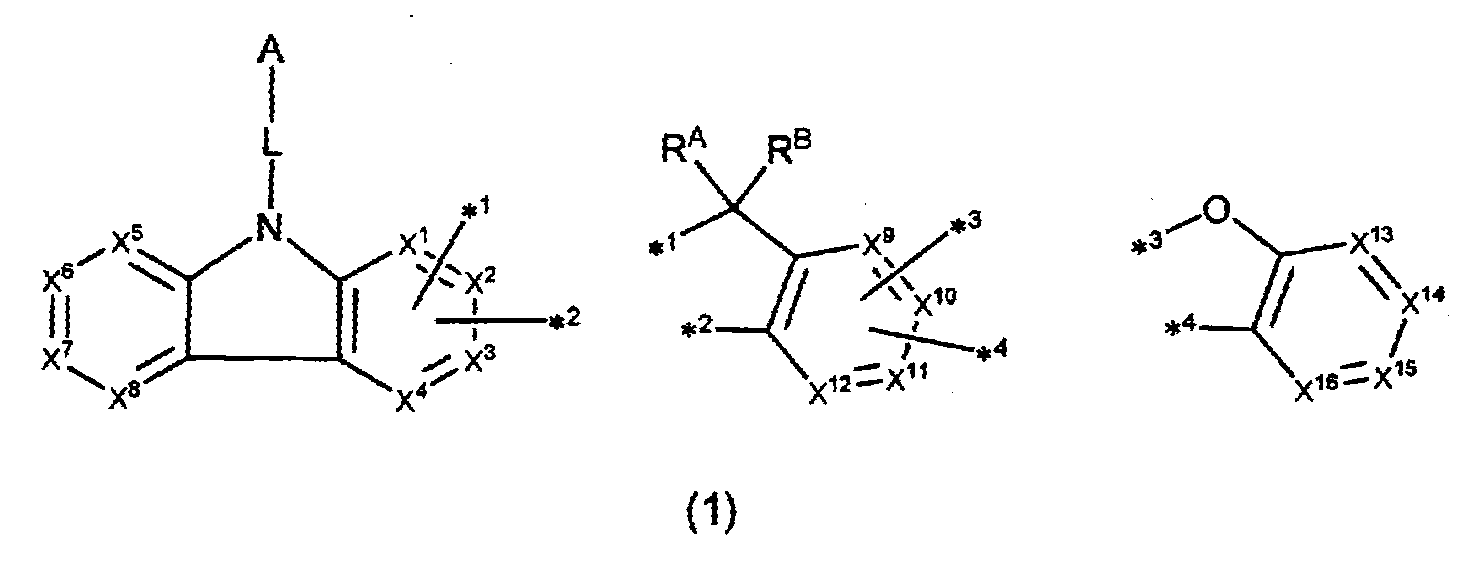
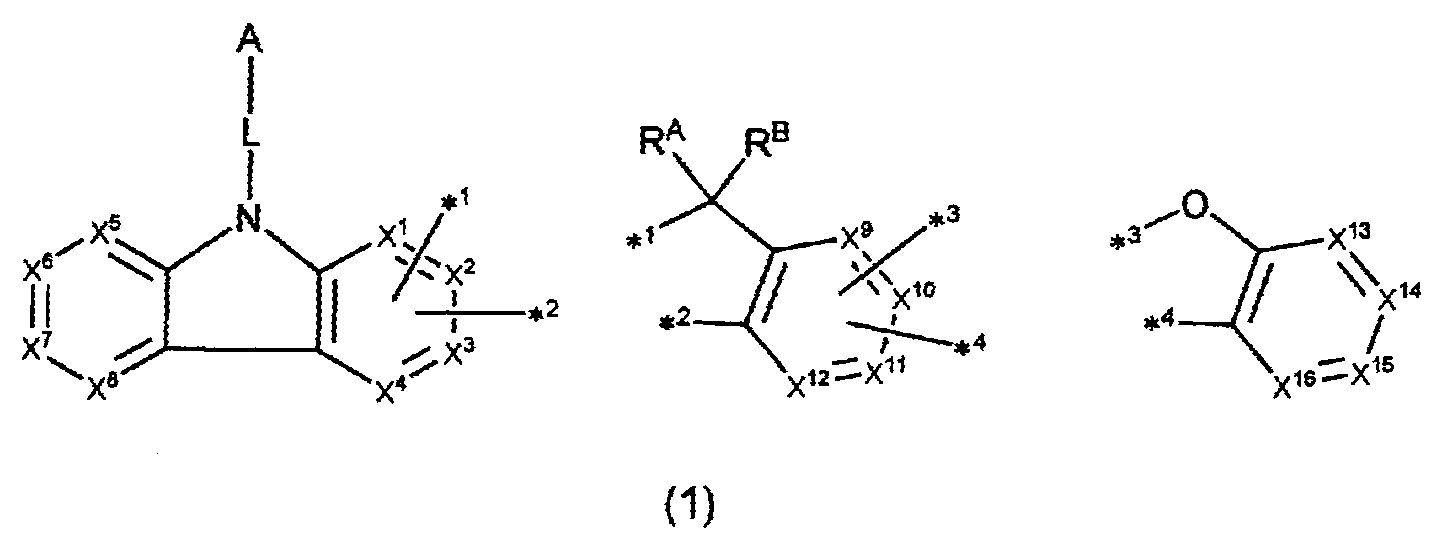
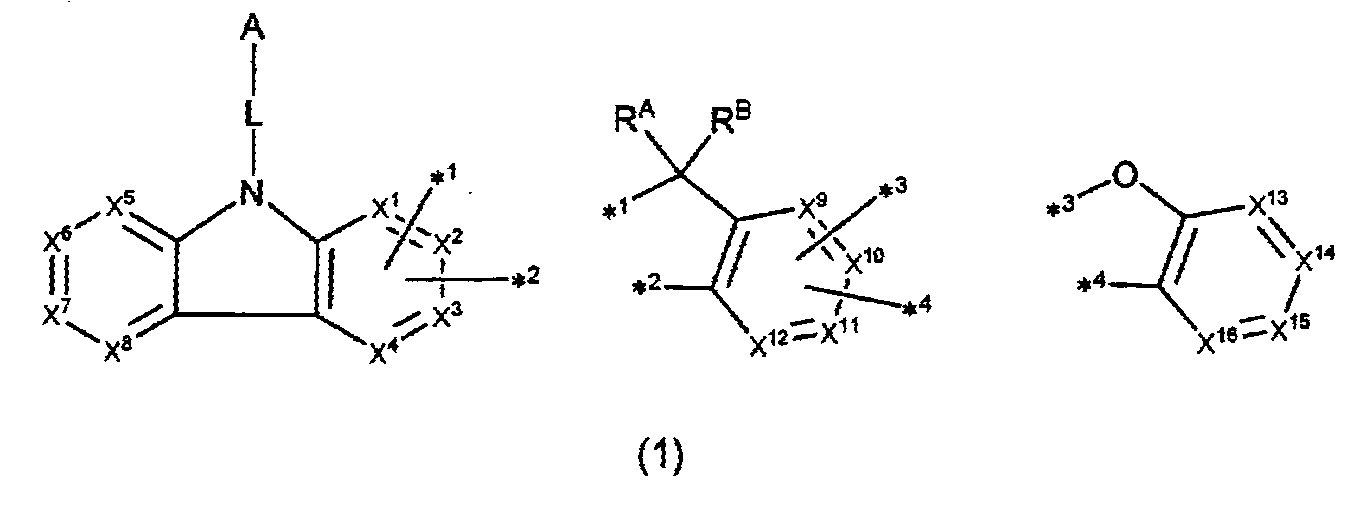
〔상기 식(1) 중, A, L, X1∼X16, R, RA 및 RB는 명세서 중에서 정의한 대로이다.〕
Description
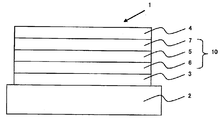
2: 기판
3: 양극
4: 음극
5: 발광층
6: 양극측 유기 박막층
7: 음극측 유기 박막층
10: 발광 유닛
Claims (26)
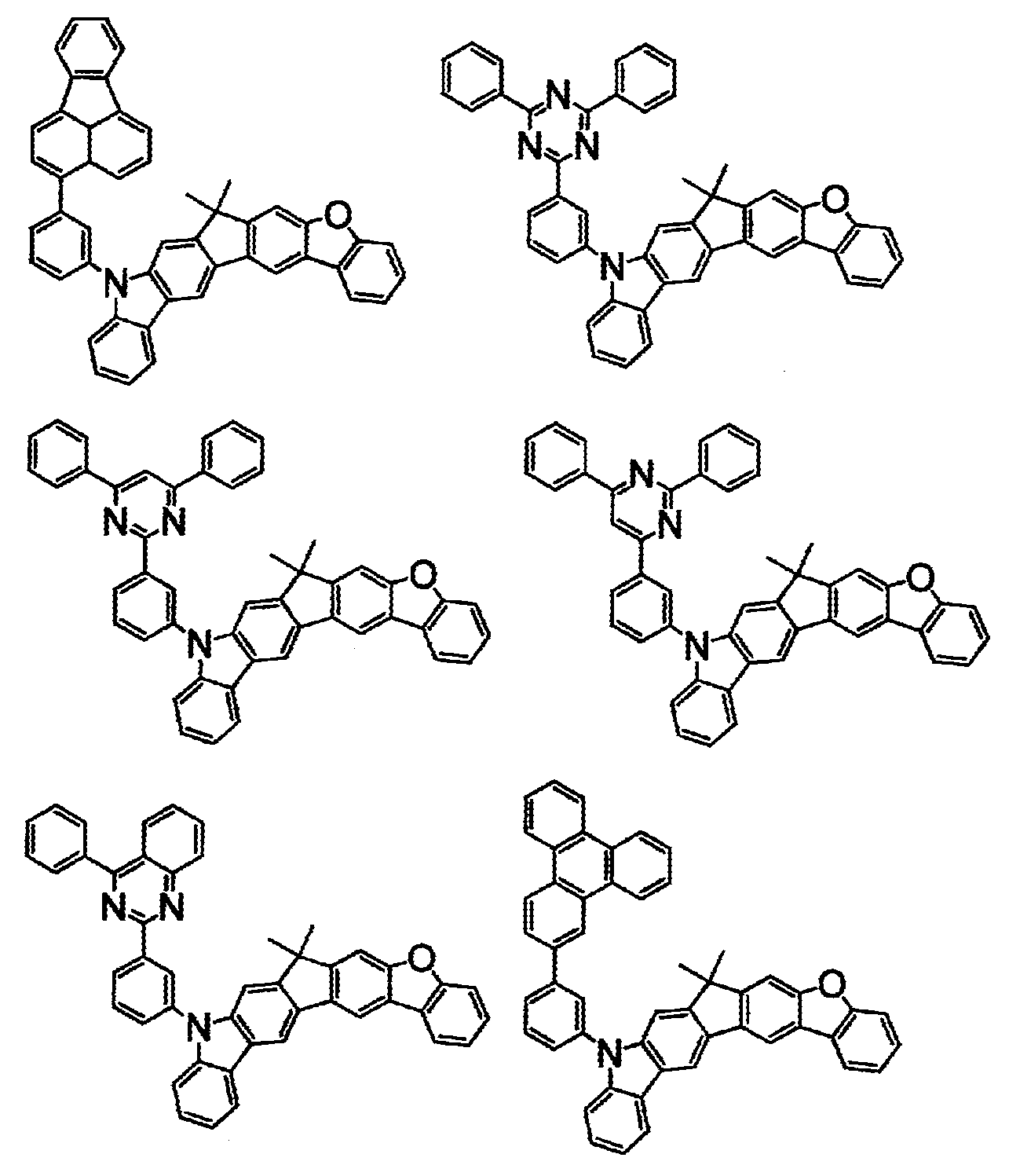
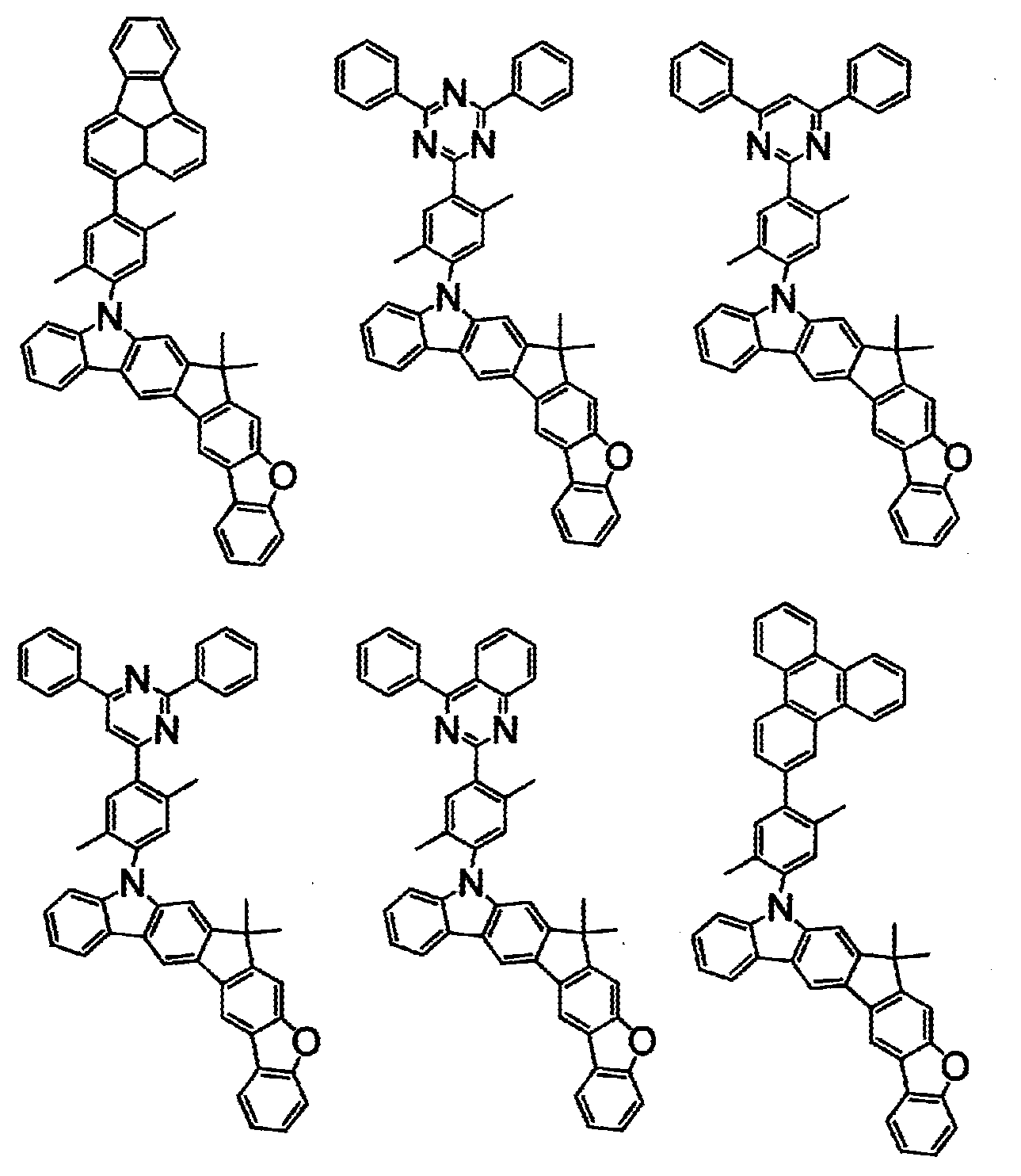
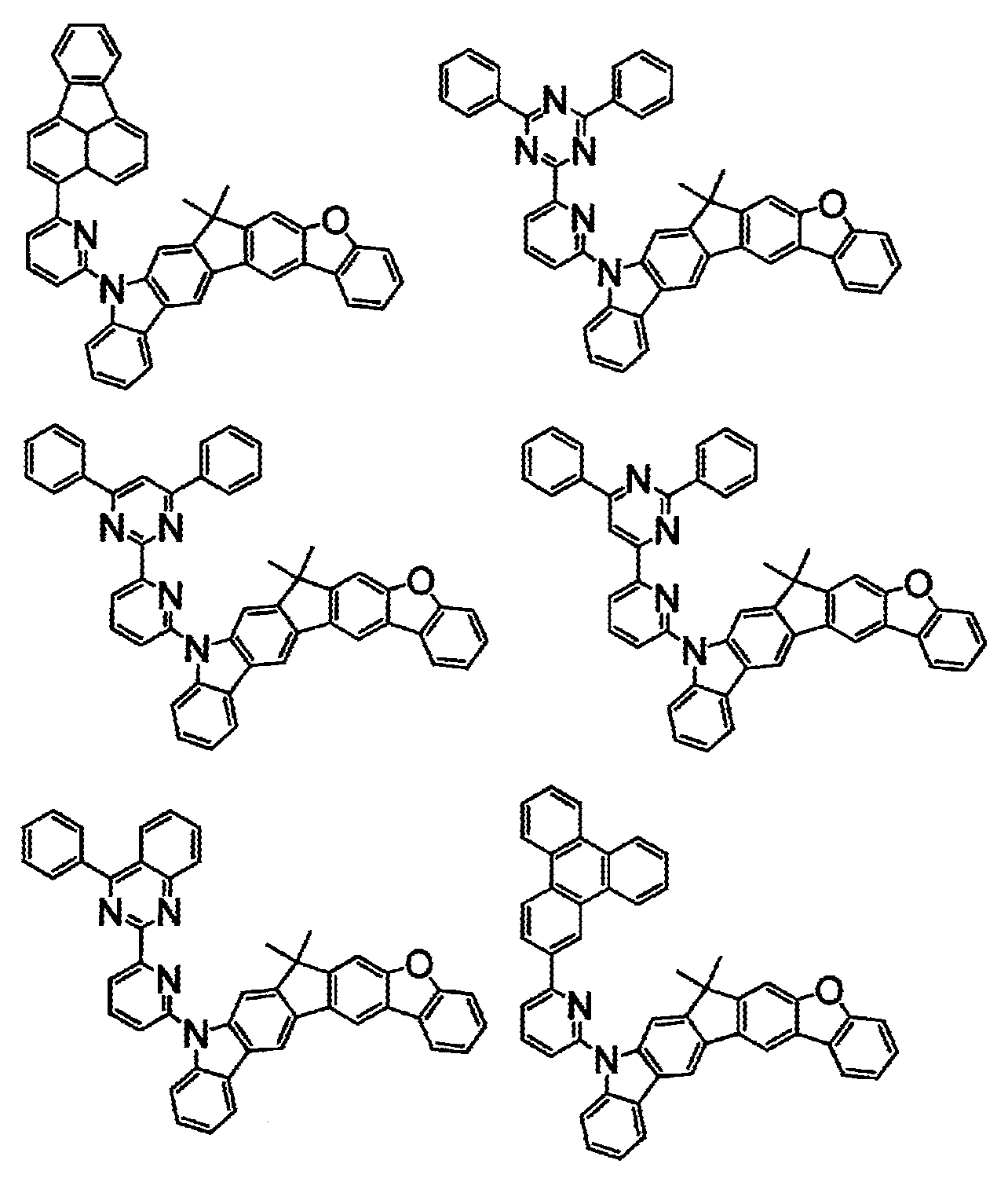
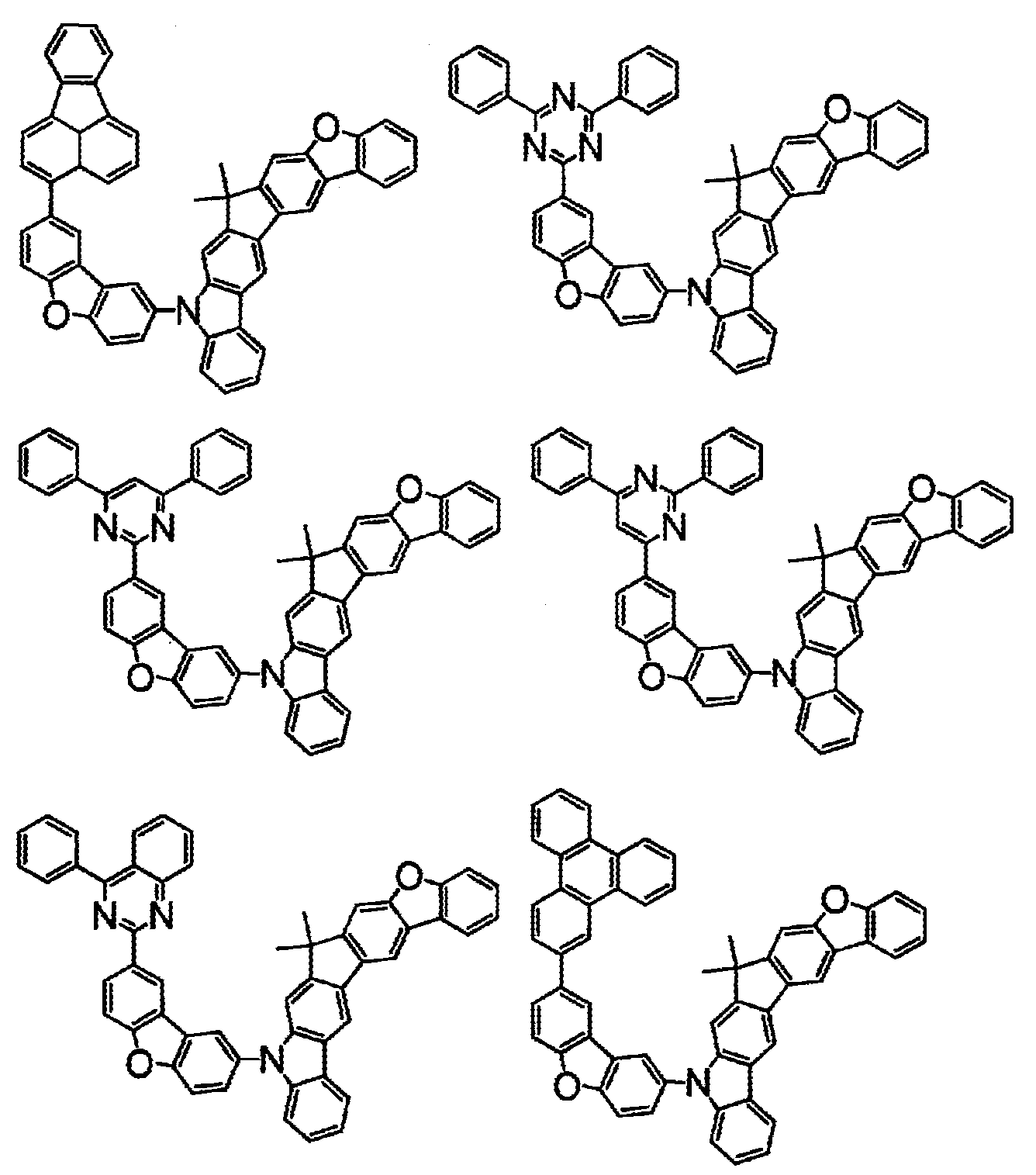
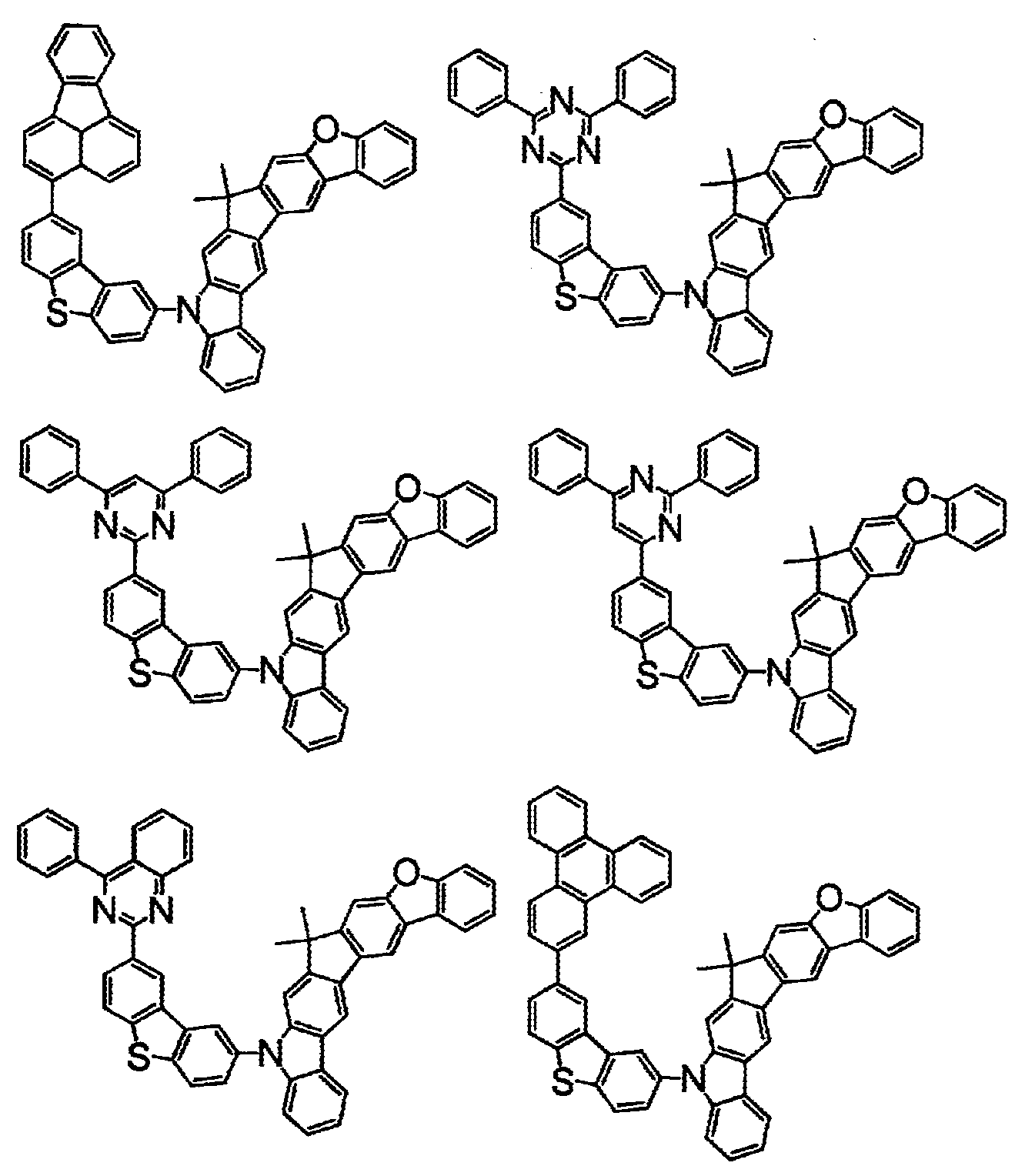
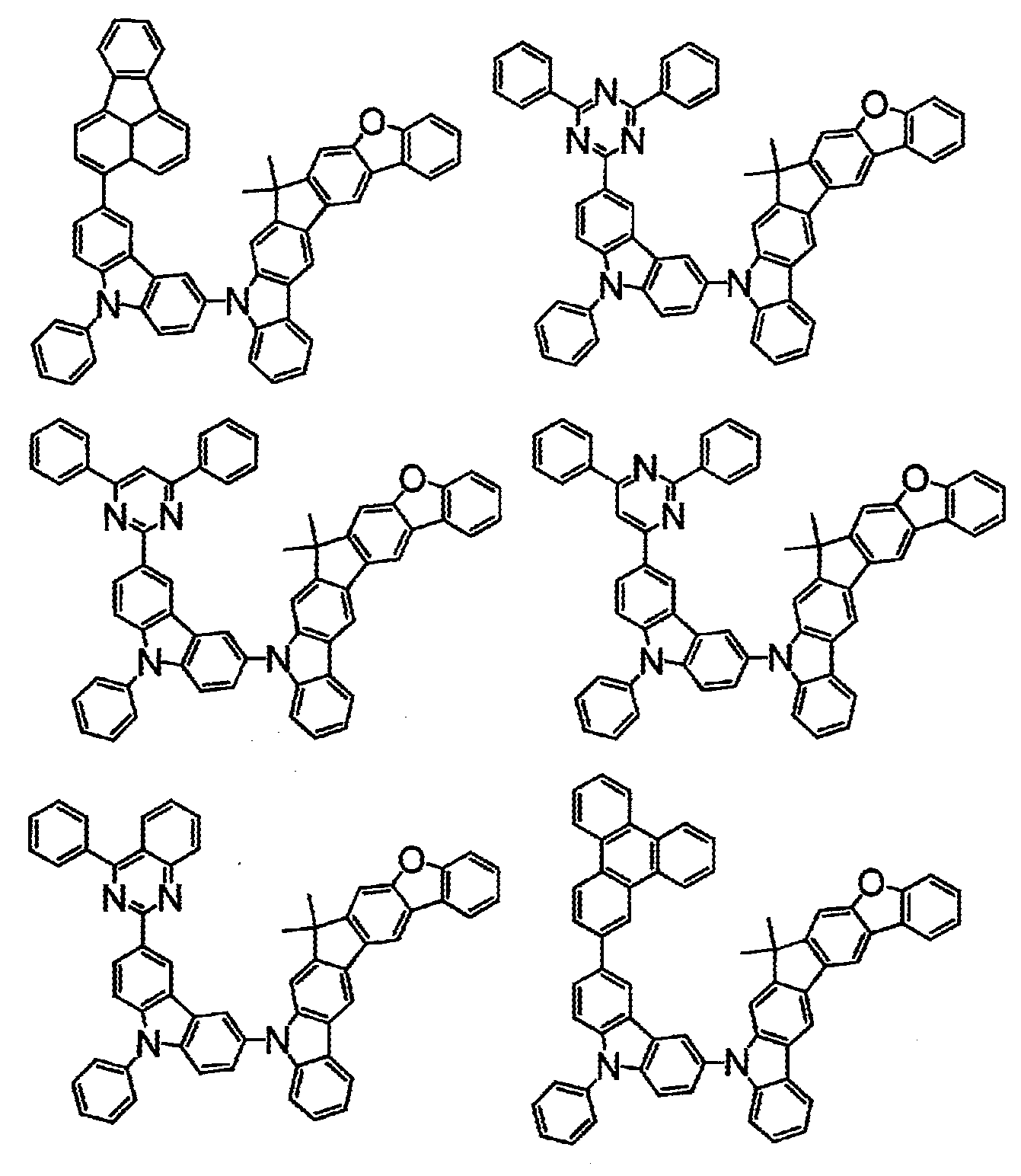
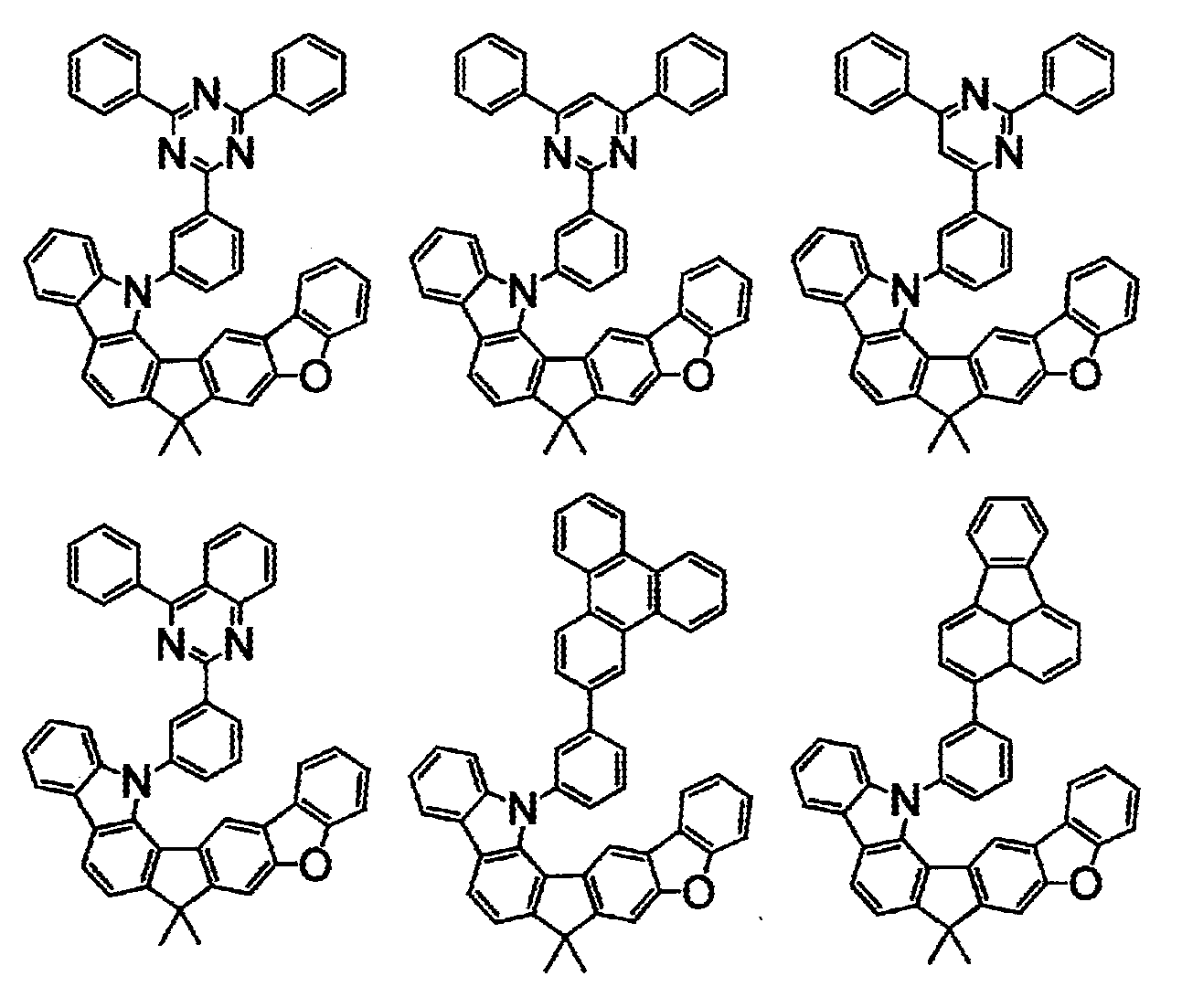
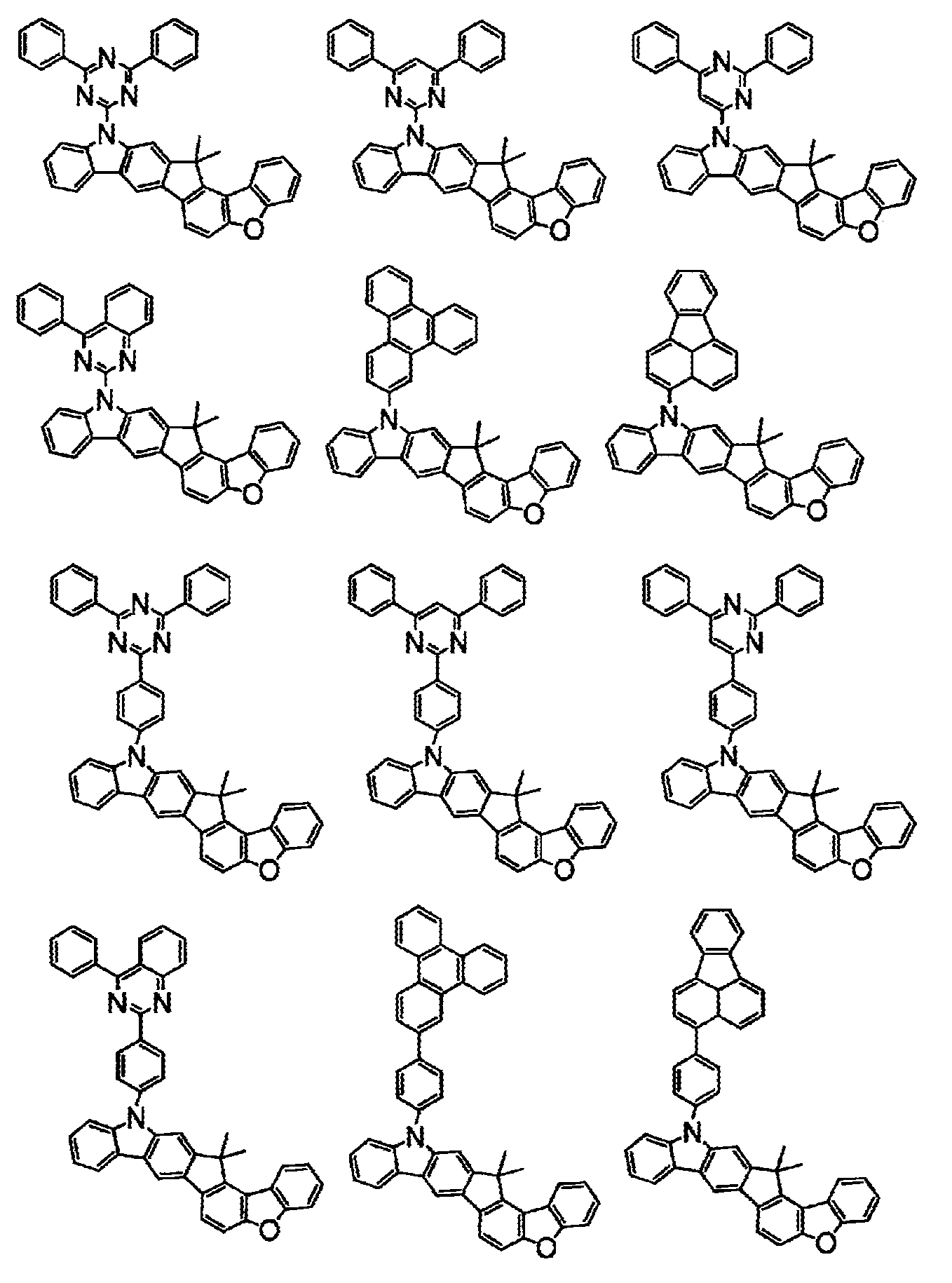
- 하기 화학식(1)로 표시되는 화합물.
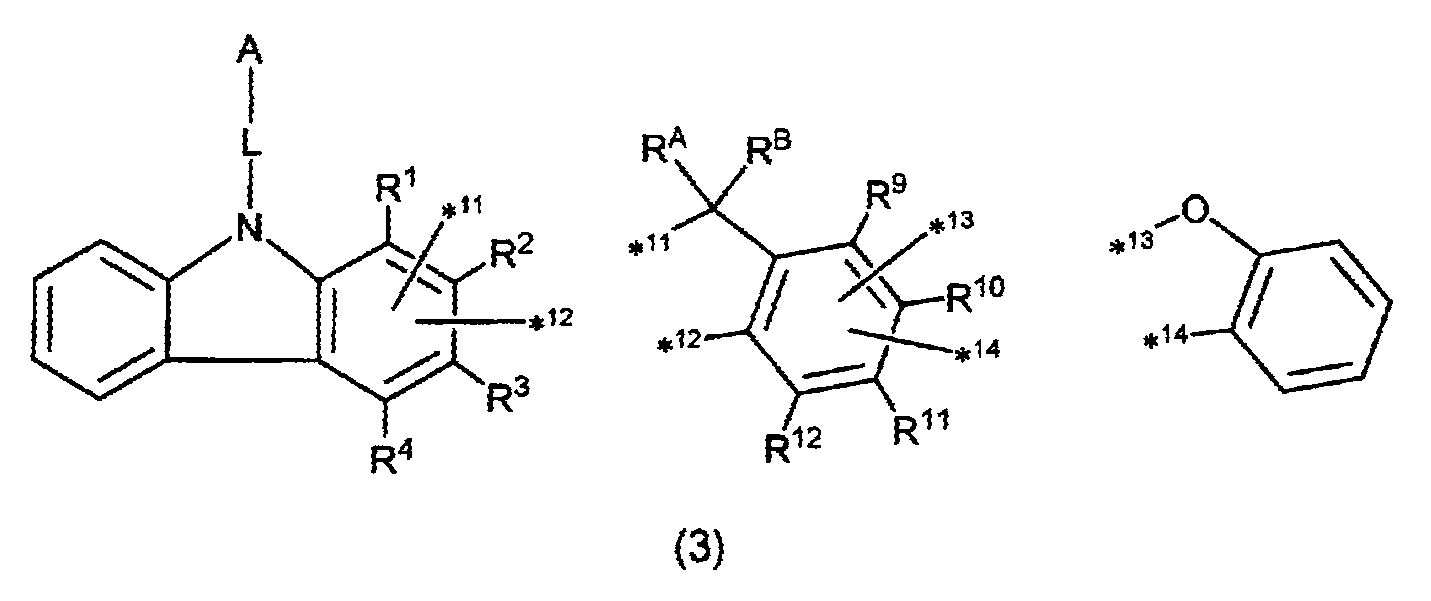
〔상기 화학식(1) 중, A는, 치환 또는 비치환된 환형성 탄소수 6∼50의 아릴기, 또는 치환 또는 비치환된 환형성 원자수 3∼50의 헤테로아릴기이다.
L은, 단일결합, 치환 또는 비치환된 환형성 탄소수 6∼60의 아릴렌기, 또는 치환 또는 비치환된 환형성 원자수 3∼50의 헤테로아릴렌기이다.
X1∼X4로부터 선택되는 2개는, 각각 *1 또는 *2와 결합하는 탄소 원자이며, 그 이외의 X1∼X4 중 2개는, 각각 독립적으로, C(R) 또는 질소 원자이다.
X9∼X12로부터 선택되는 2개는, 각각 *3 또는 *4와 결합하는 탄소 원자이며, 그 이외의 X9∼X12 중 2개는, 각각 독립적으로, C(R) 또는 질소 원자이다.
X5∼X8 및 X13∼X16은, 각각 독립적으로, C(R) 또는 질소 원자이다.
R은, 각각 독립적으로, 수소 원자 또는 치환기이고, 복수 존재하는 R은 각각 동일해도 되고, 상이해도 된다. 또한, 복수 존재하는 R로부터 선택되는 2개는 서로 결합하여 환을 형성하고 있어도 된다.
RA 및 RB는, 각각 독립적으로, 수소 원자, 치환 또는 비치환된 탄소수 1∼20의 알킬기, 치환 또는 비치환된 환형성 탄소수 6∼50의 아릴기, 치환 또는 비치환된 환형성 원자수 3∼50의 헤테로아릴기, 할로젠 원자, 탄소수 1∼50의 알킬기 및 환형성 탄소수 6∼50의 아릴기로부터 선택되는 치환기를 갖는 모노치환, 다이치환 또는 트라이치환 실릴기, 치환 또는 비치환된 탄소수 1∼20의 알콕시기, 치환 또는 비치환된 환형성 탄소수 6∼50의 아릴옥시기, 또는 사이아노기이다. RA 및 RB는 서로 동일해도 되고, 상이해도 된다. 또한, RA 및 RB는 서로 결합하여 환을 형성하고 있어도 된다.〕 - 제 1 항에 있어서,
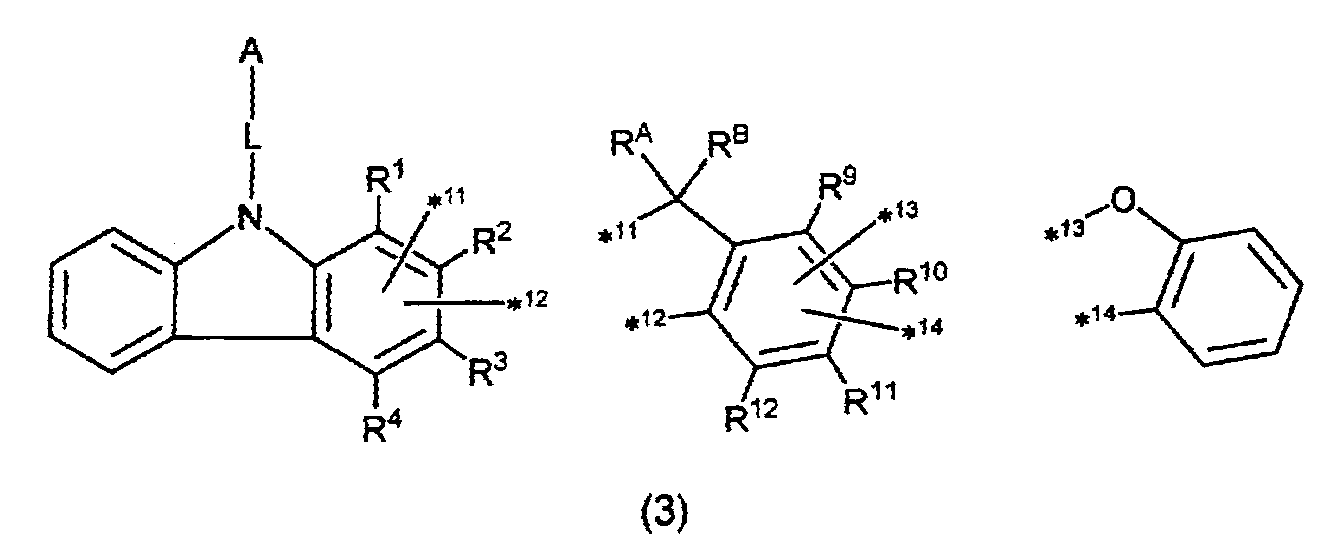
하기 화학식(2)로 표시되는 화합물.
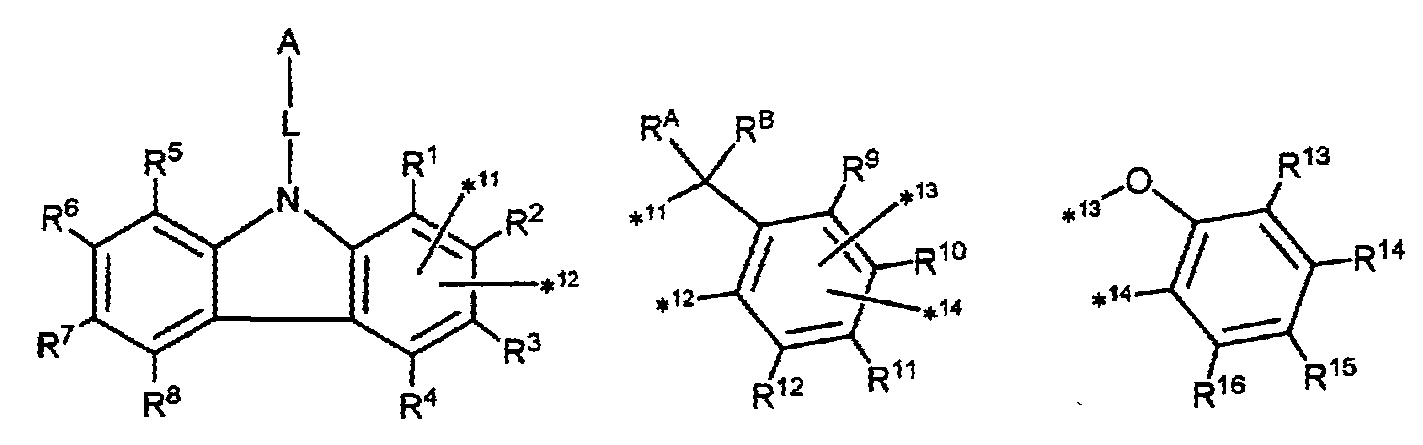
〔상기 화학식(2) 중, A, L, RA 및 RB는 제 1 항의 상기 화학식(1)에 관한 기재와 동일하다.
R1∼R4로부터 선택되는 2개의 기는, 탈리되어, 당해 기와 결합해 있던 탄소 원자가 *11 또는 *12와 결합하고, 그 이외의 R1∼R4 중 2개는, 각각 독립적으로, 수소 원자 또는 치환기이다.
R9∼R12로부터 선택되는 2개의 기는, 탈리되어, 당해 기와 결합해 있던 탄소 원자가 *13 또는 *14와 결합하고, 그 이외의 R9∼R12 중 2개는, 각각 독립적으로, 수소 원자 또는 치환기이다.
R5∼R8 및 R13∼R16은, 각각 독립적으로, 수소 원자 또는 치환기이며, 각각 동일해도 되고, 상이해도 된다.
한편, *11∼*14와의 결합에 관여하지 않는 R1∼R16으로부터 선택되는 2개는 서로 결합하여 환을 형성하고 있어도 된다.〕 - 제 2 항 또는 제 3 항에 있어서,
상기 화학식(2) 또는 (3) 중의, R1과 R2, R2와 R3, 및 R3과 R4로부터 선택되는 2개의 기가, 탈리되어, 당해 기와 결합해 있던 탄소 원자가 *11 또는 *12와 결합하고, R9와 R10, R10과 R11, 및 R11과 R12로부터 선택되는 2개의 기가, 탈리되어, 당해 기와 결합해 있던 산소 원자가 *3 또는 *4와 결합하는 화합물. - 제 5 항에 있어서,
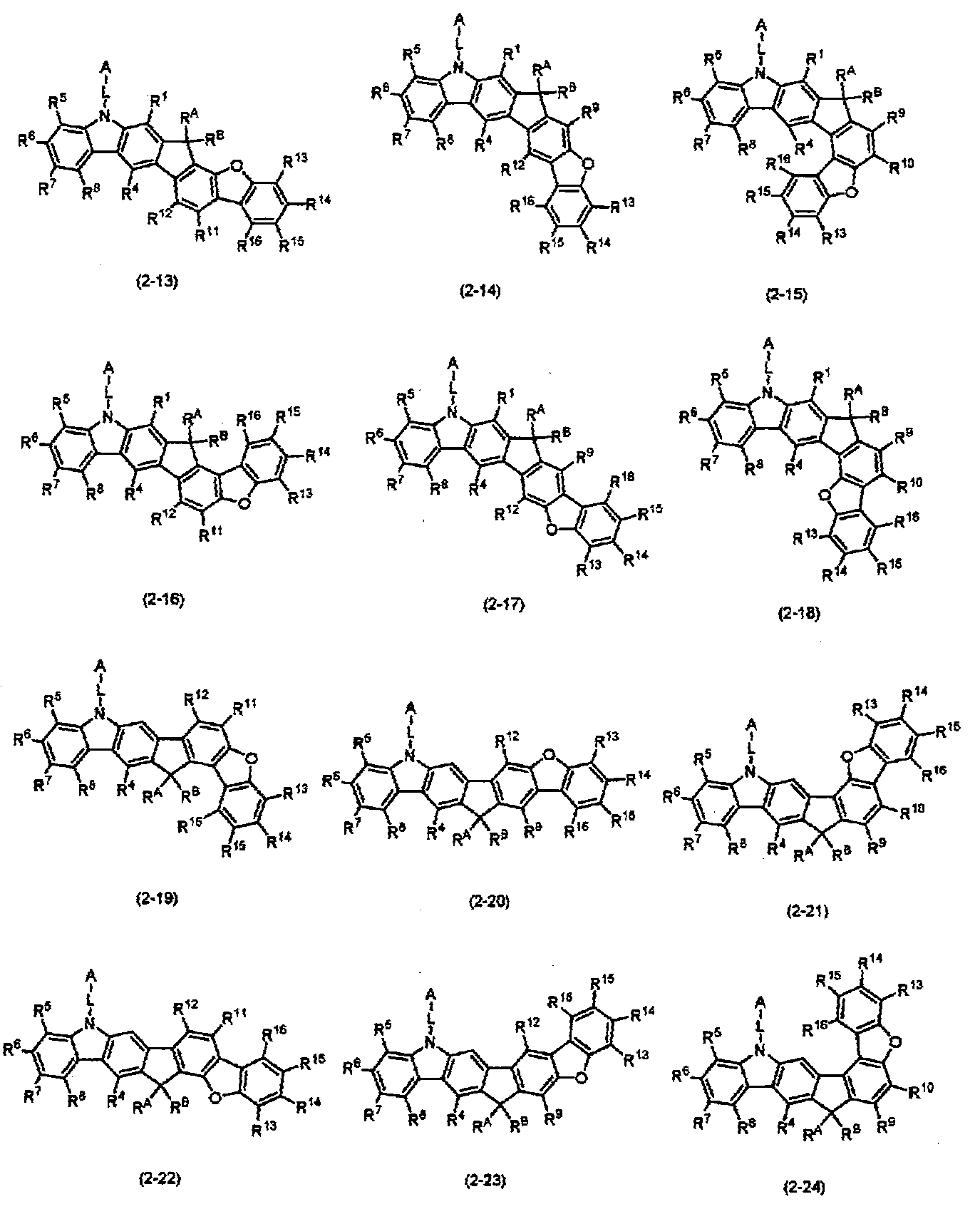
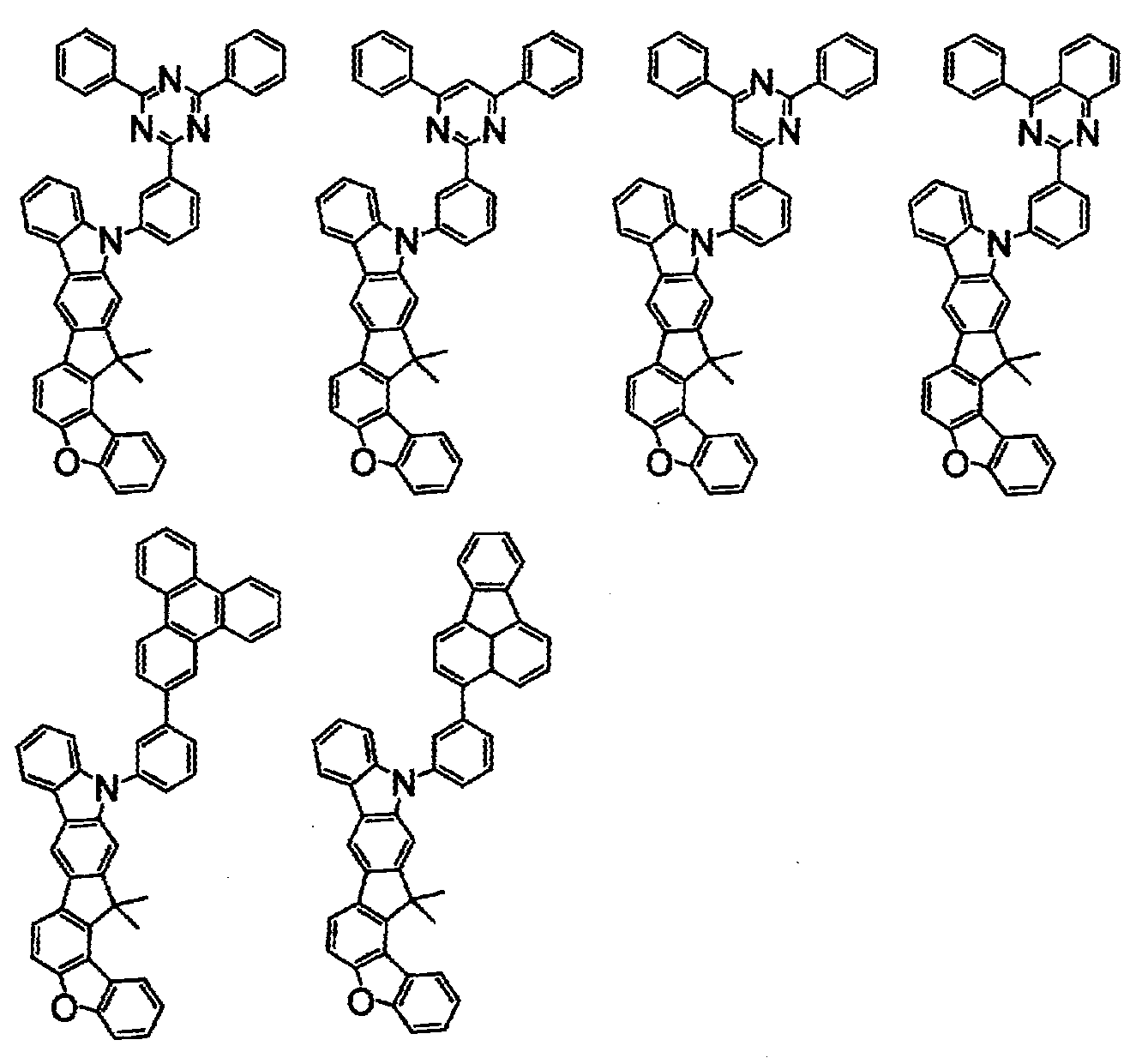
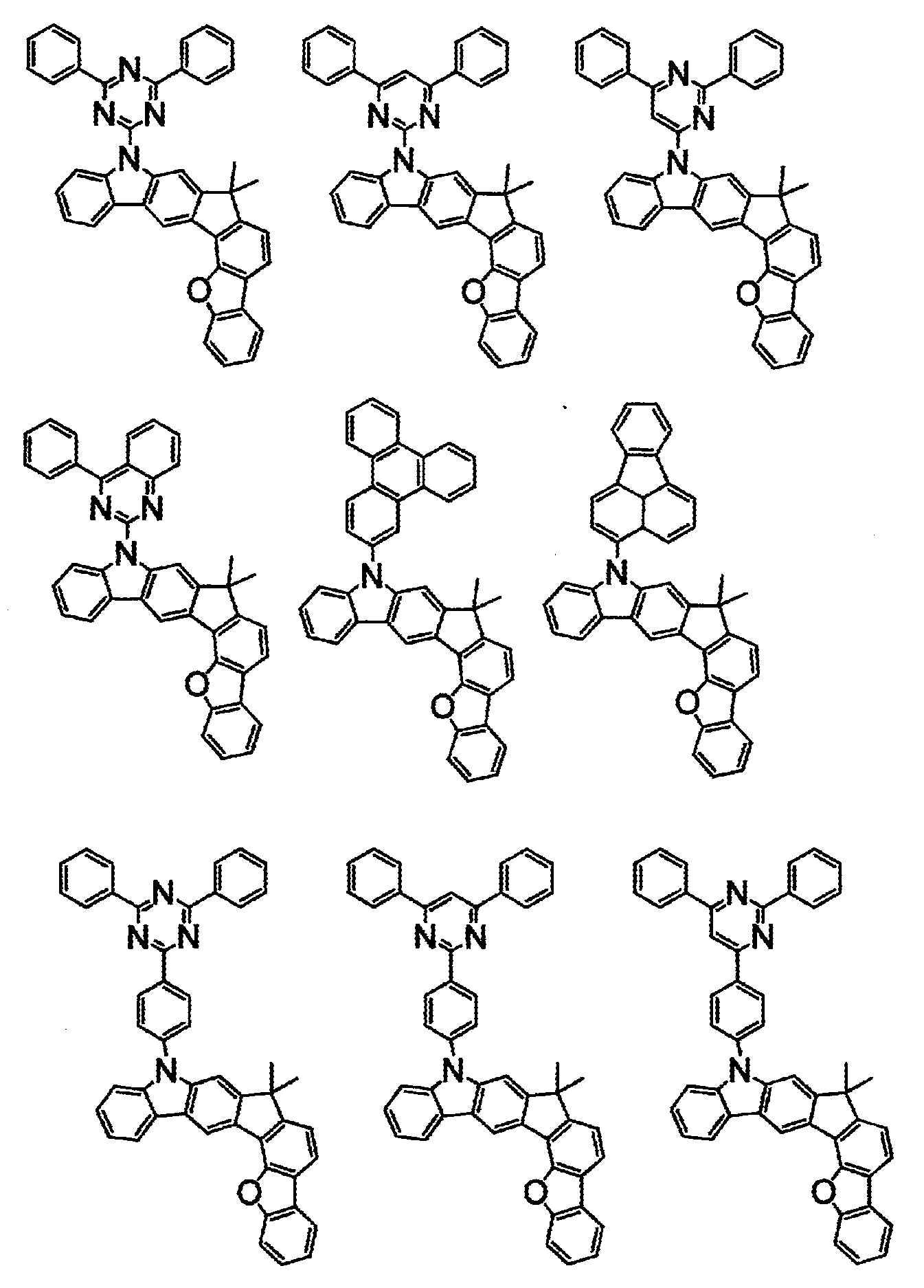
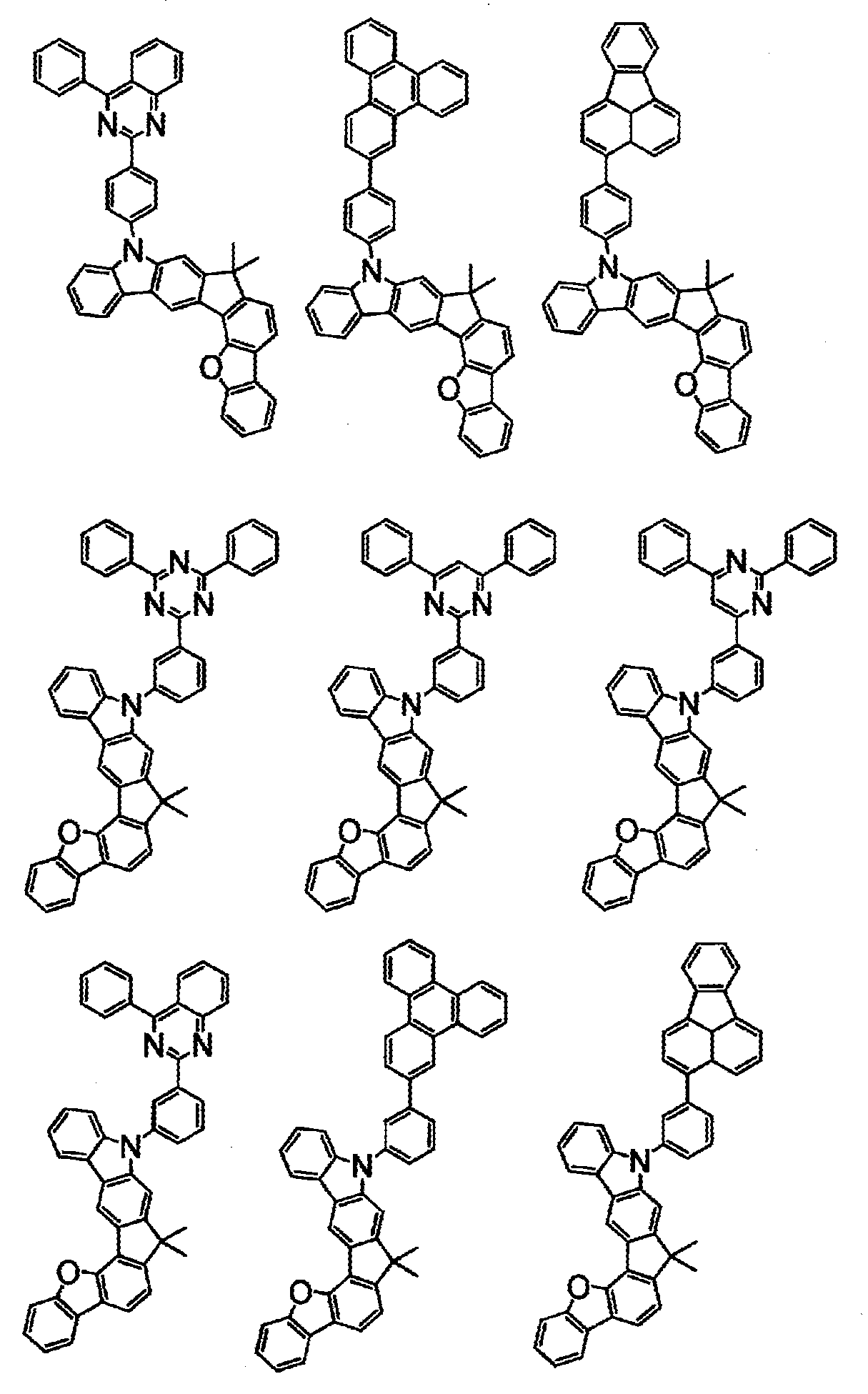
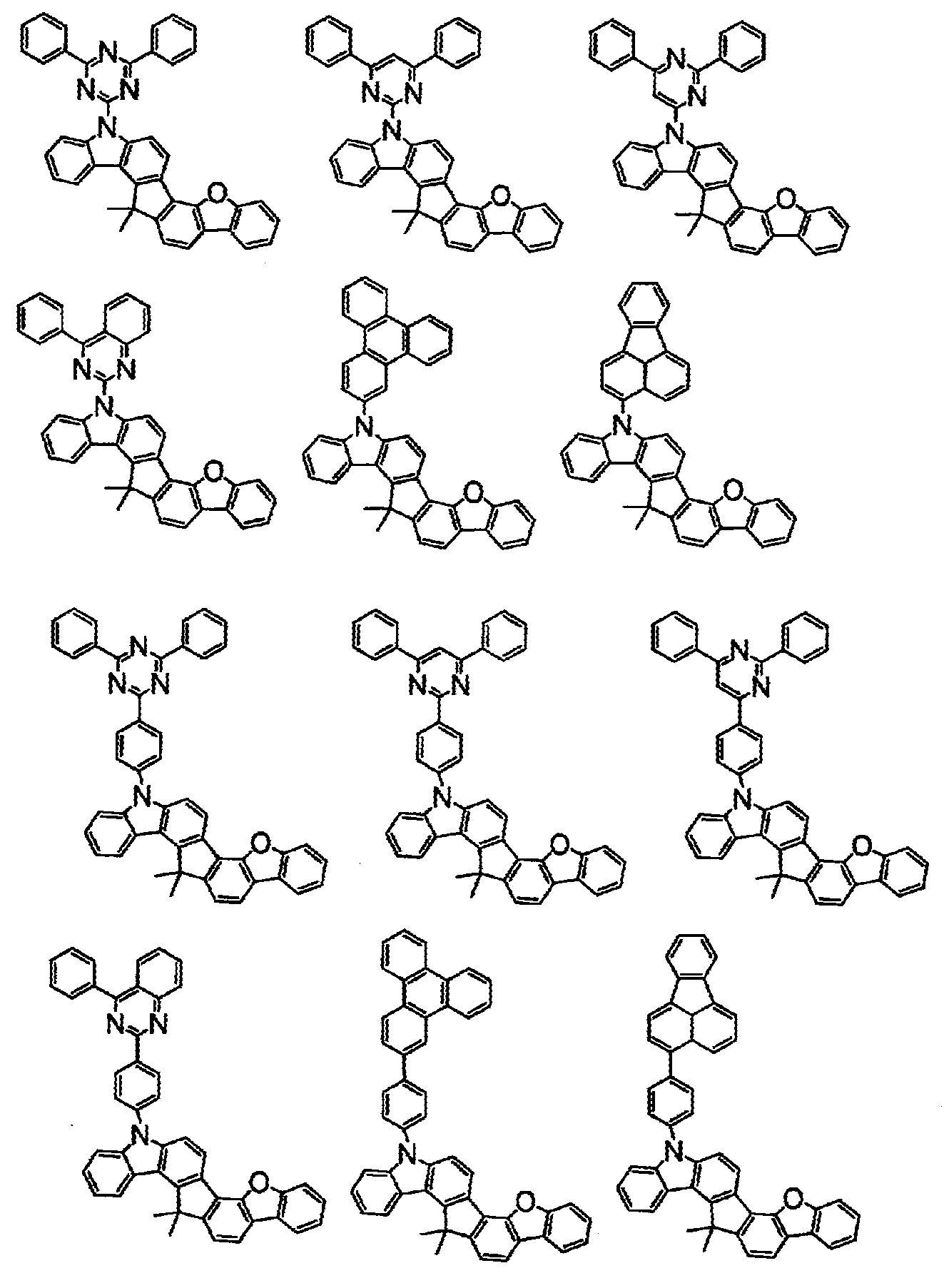
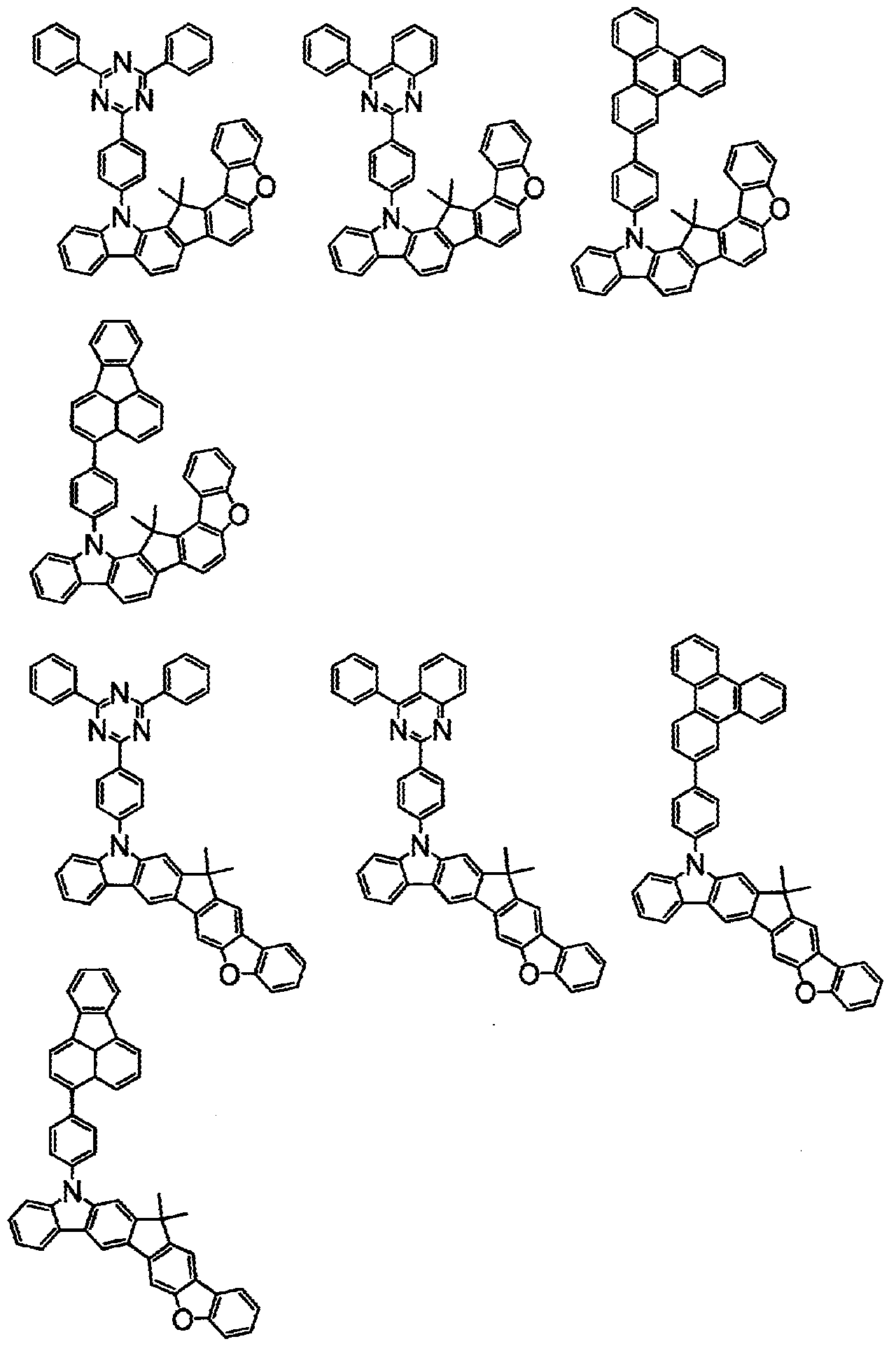
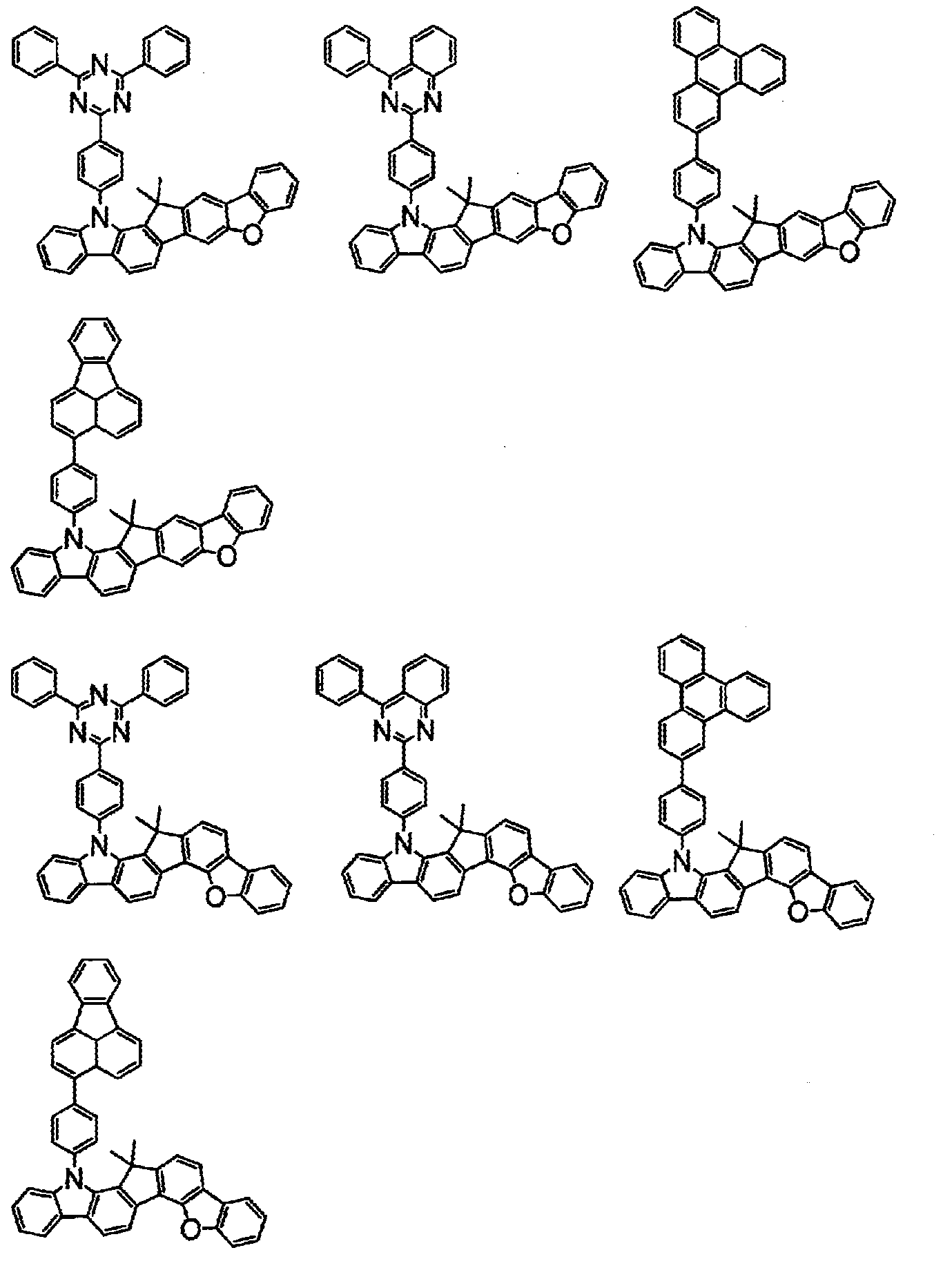
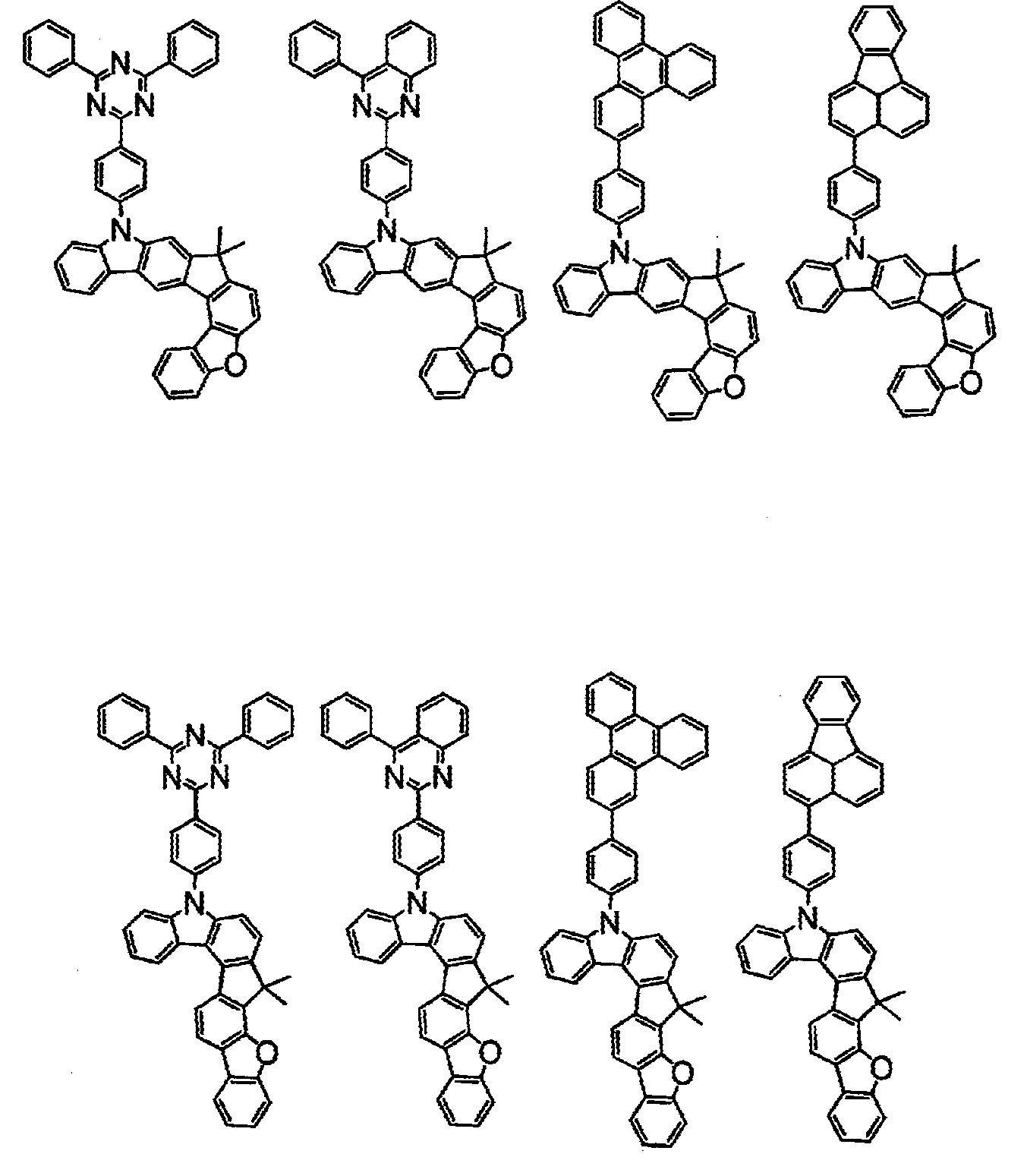
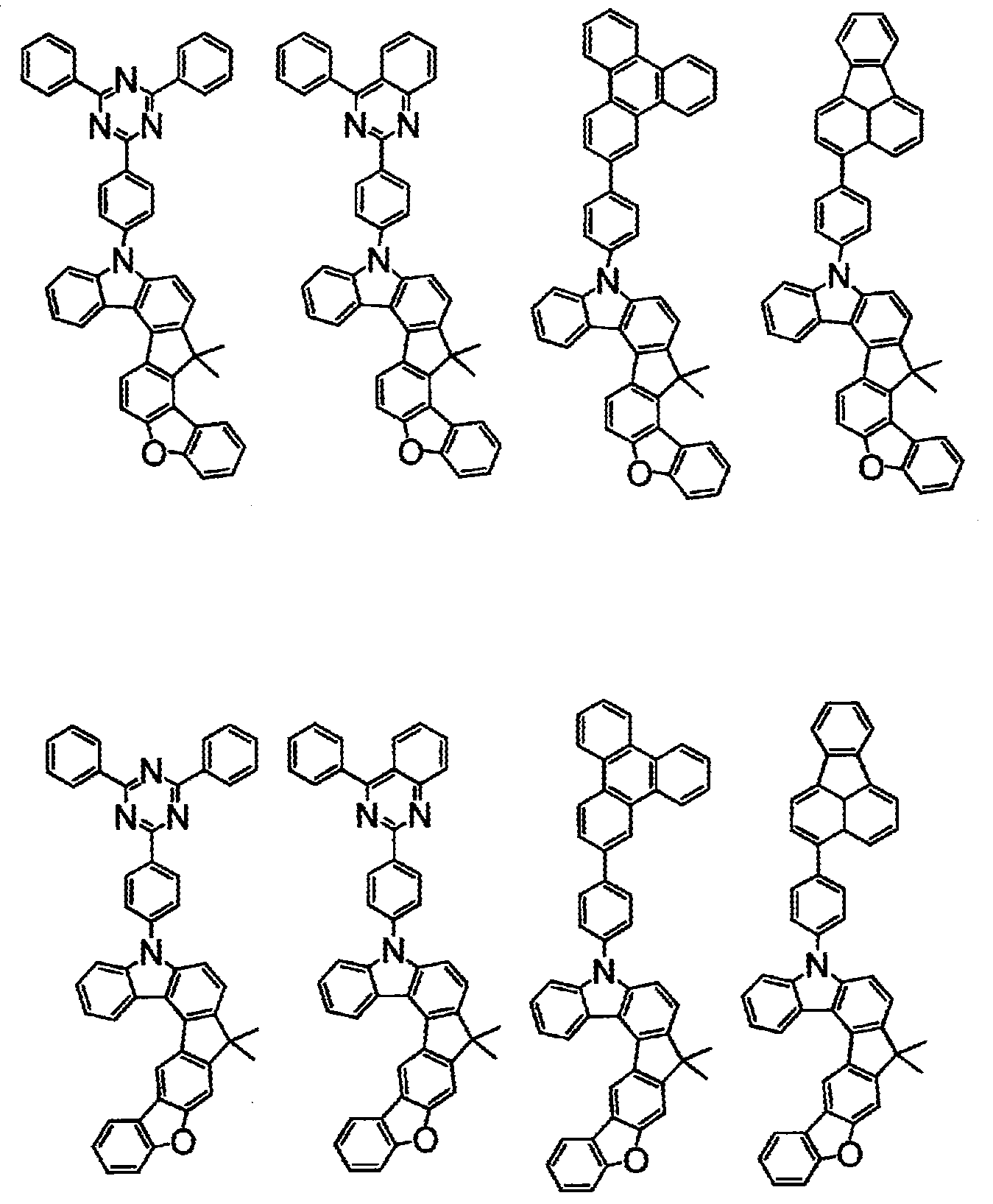
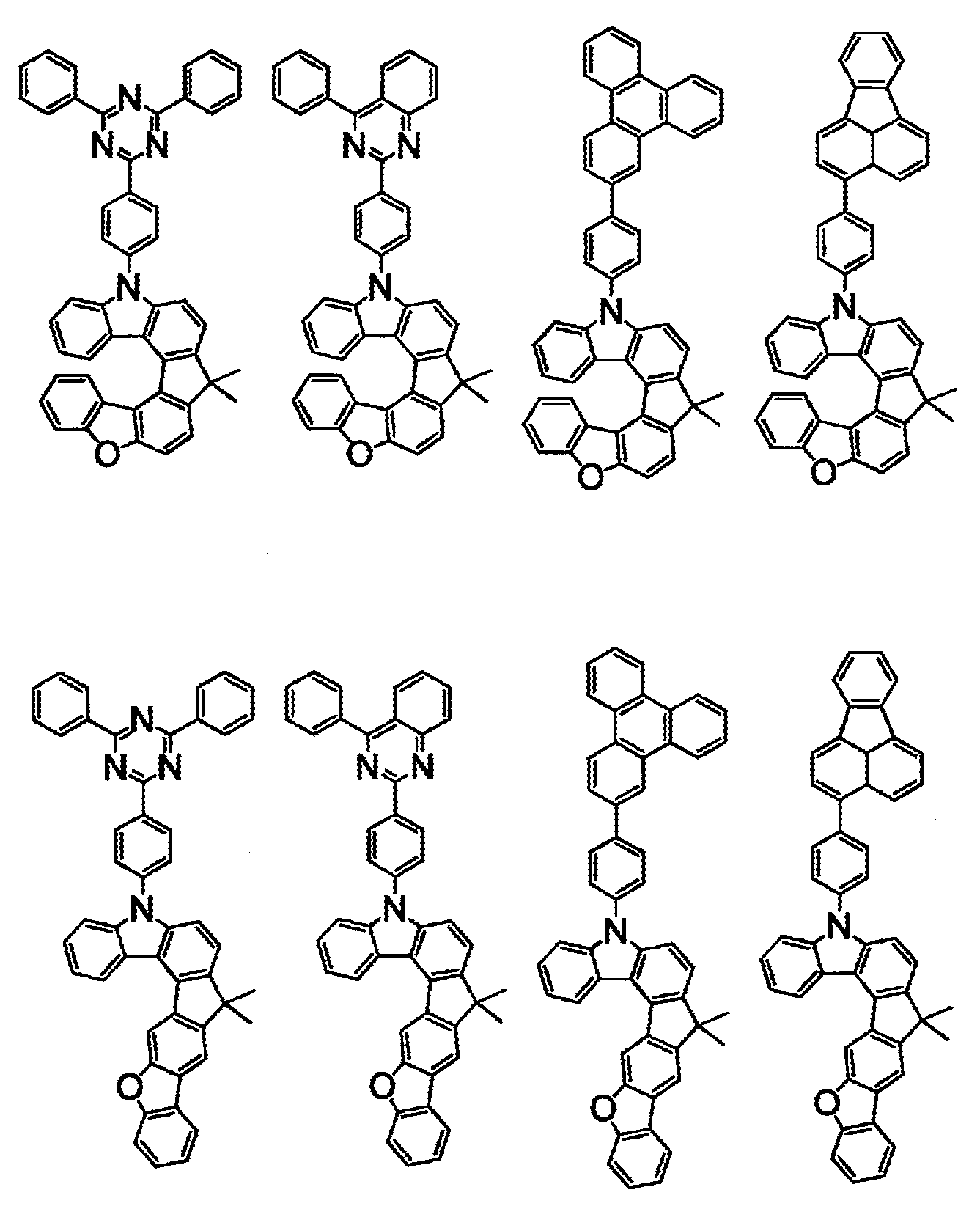
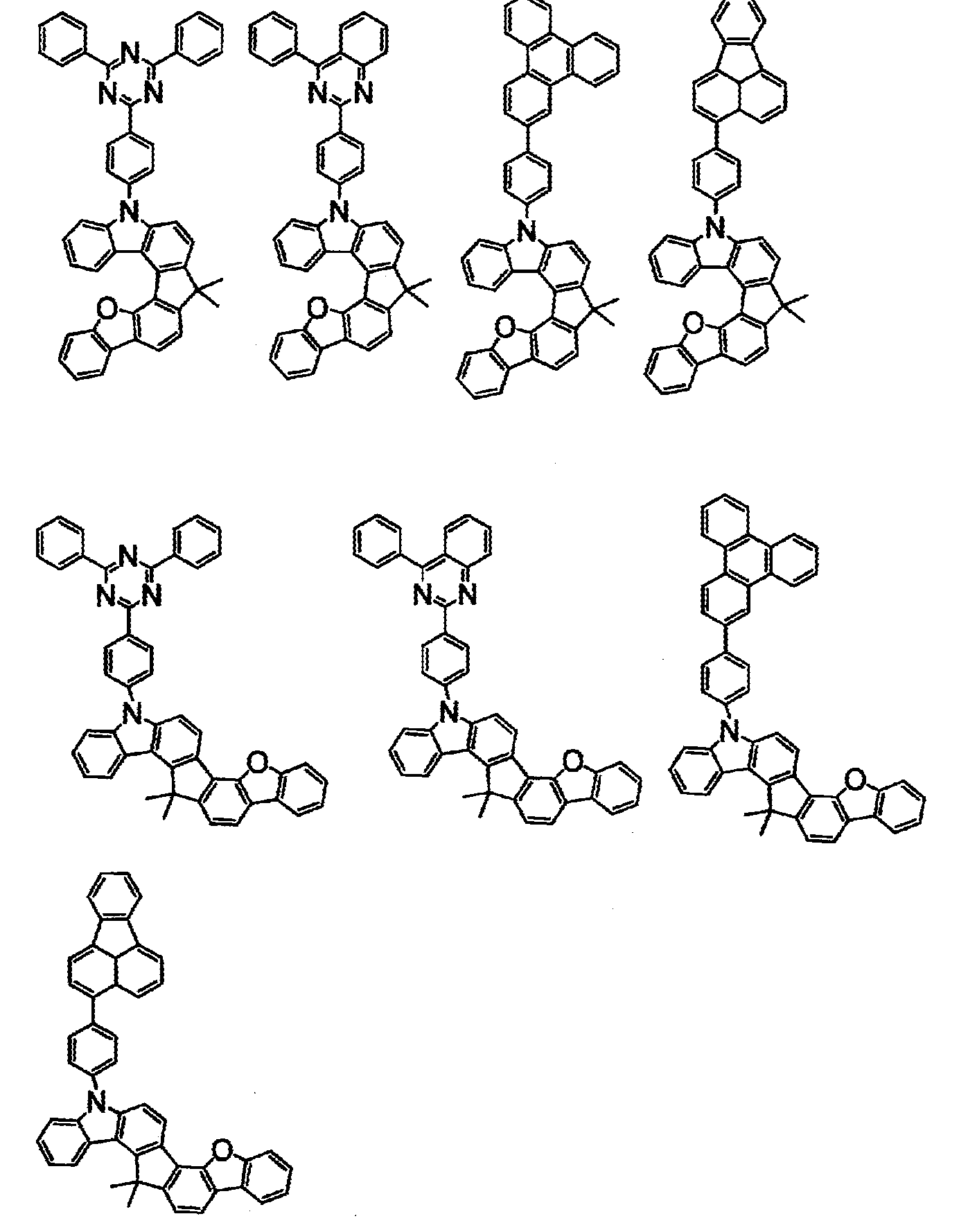
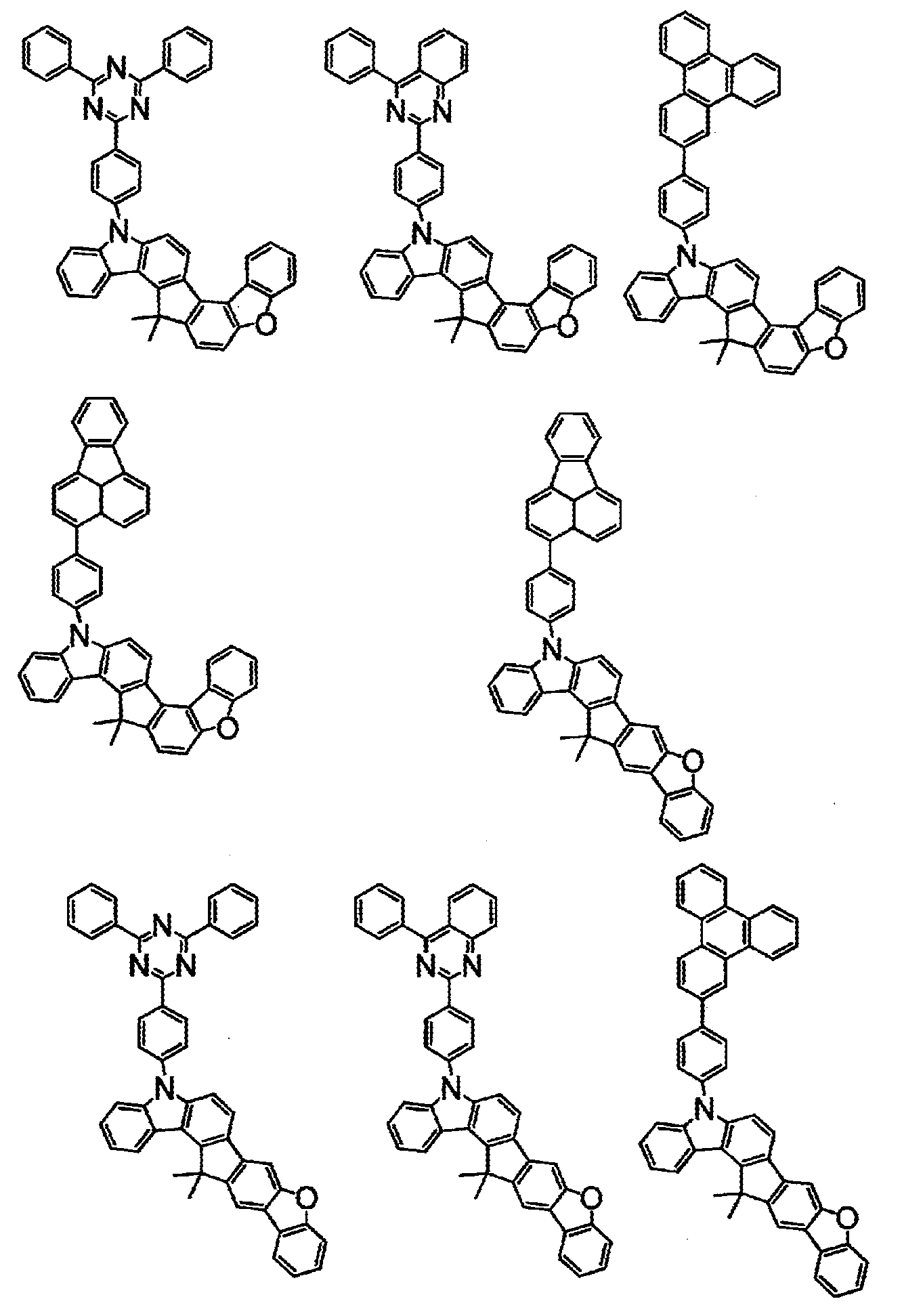
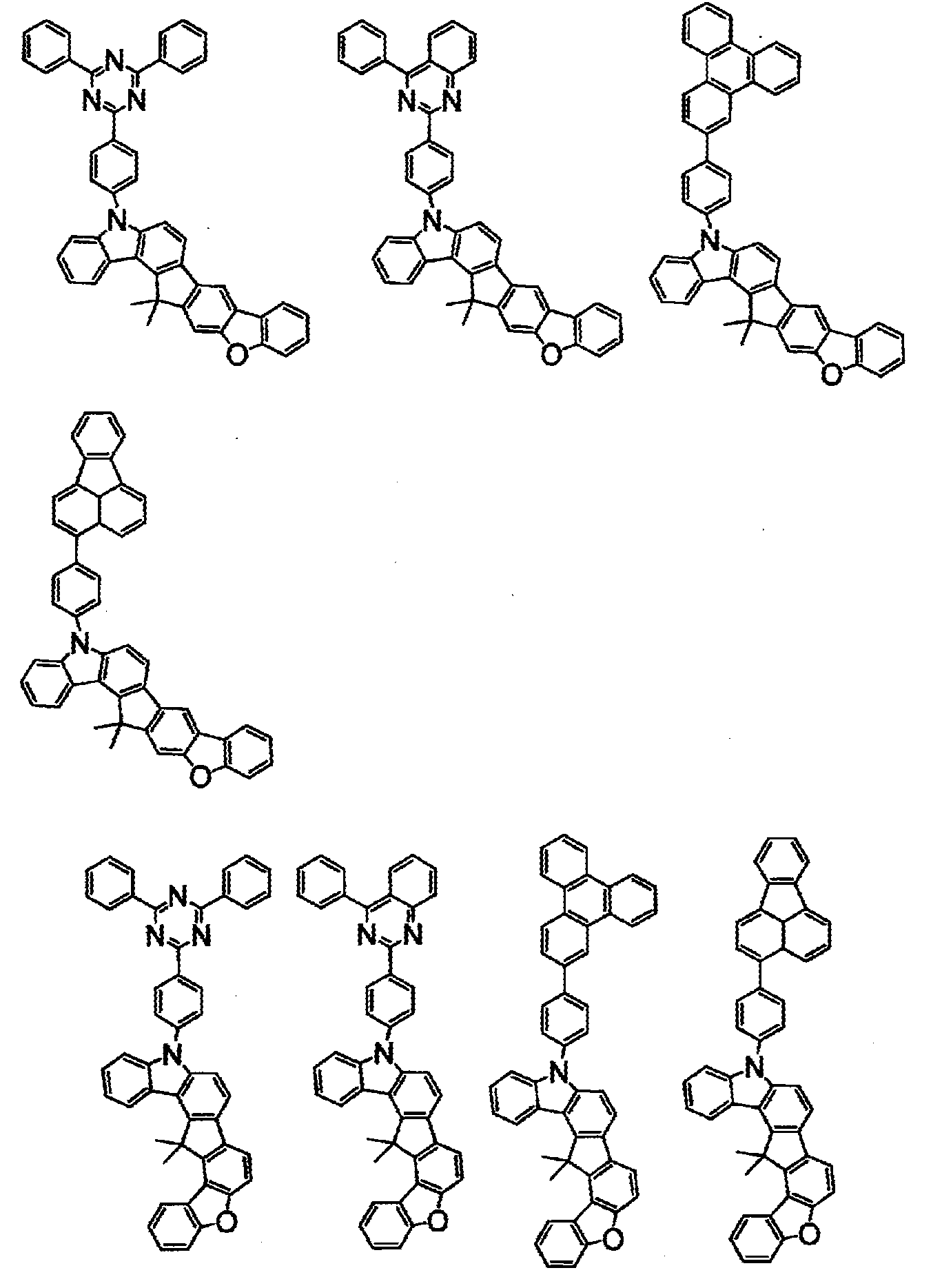
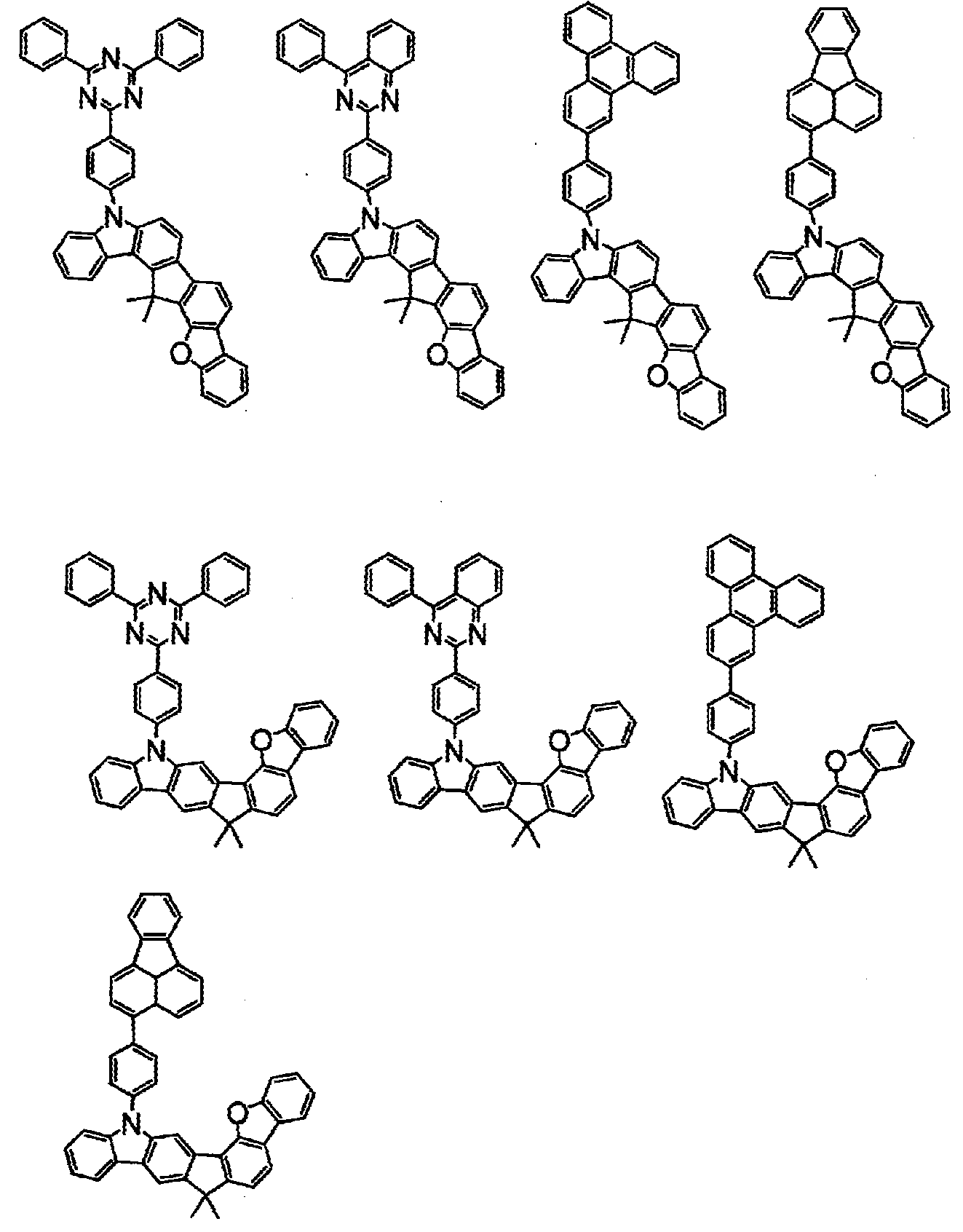
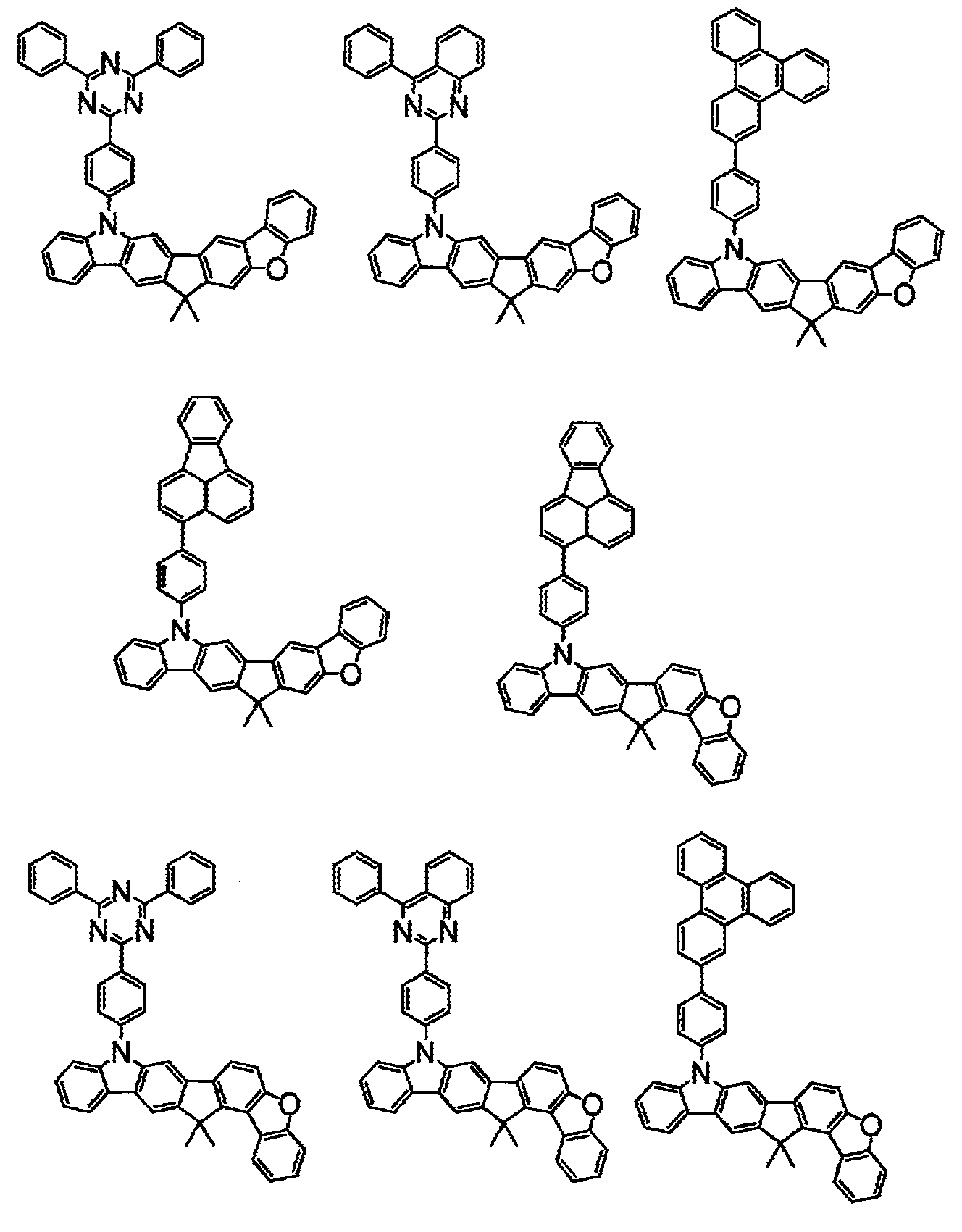
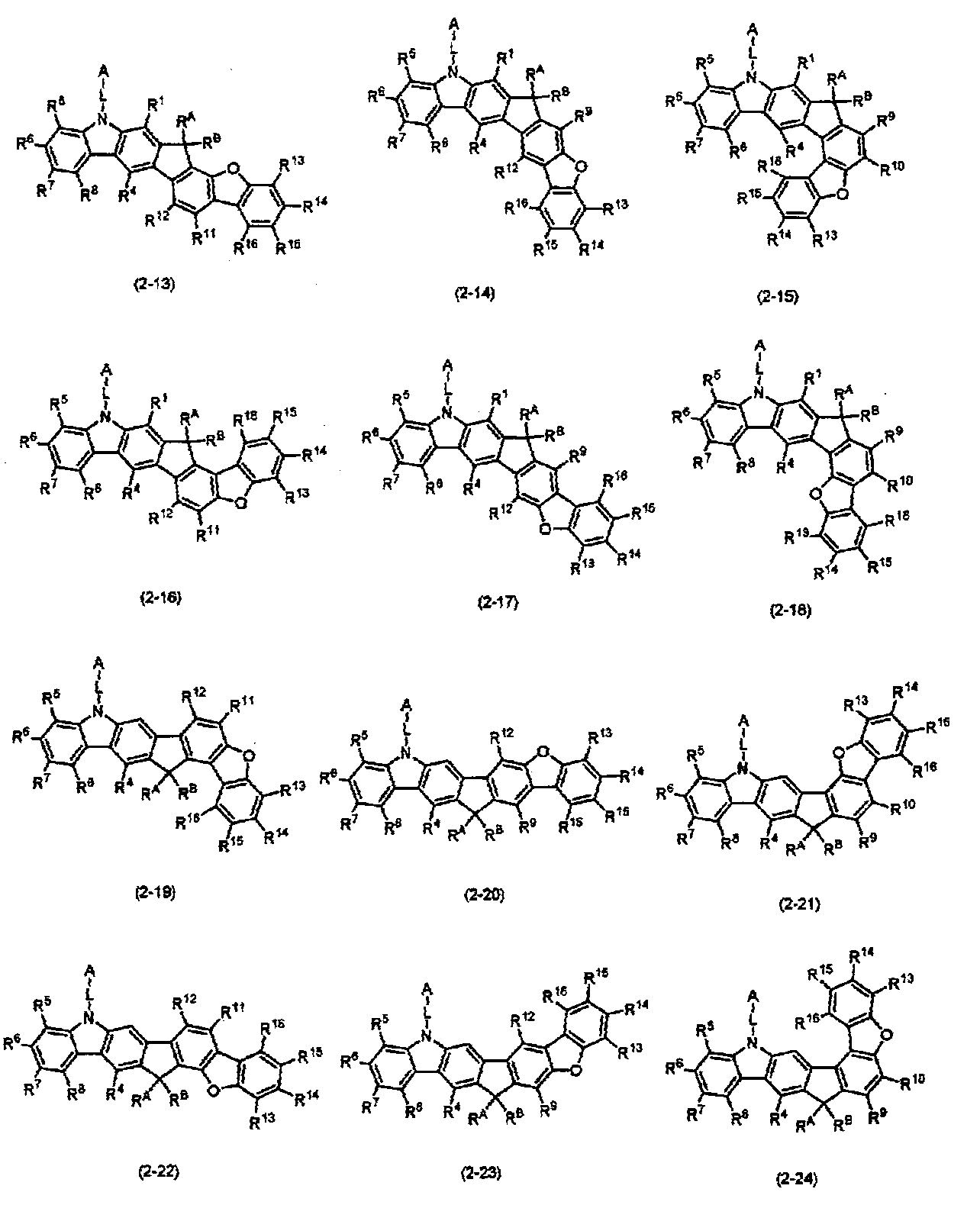
상기 화학식(2-2), (2-3), (2-4), (2-6), (2-7), (2-8), (2-9), (2-10), (2-11), (2-12), (2-13), (2-14), (2-15), (2-16), (2-17), (2-18), (2-19), (2-21), (2-23), (2-24), (2-25), (2-26), (2-27), (2-28), (2-29), (2-30), (2-31), (2-32), (2-33), (2-34), (2-35) 및 (2-36) 중 어느 하나로 표시되는 화합물. - 제 5 항에 있어서,
상기 화학식(2-7), (2-9), (2-11), (2-12), (2-14), (2-15), (2-16), (2-18), (2-26), (2-27), (2-28), (2-30), (2-31), (2-33), (2-35) 및 (2-36) 중 어느 하나로 표시되는 화합물. - 제 1 항 내지 제 7 항 중 어느 한 항에 있어서,
A가, 치환 또는 비치환된 환형성 탄소수 6∼24의 아릴기, 또는 치환 또는 비치환된 환형성 원자수 3∼24의 질소 원자, 산소 원자 또는 황 원자 함유 헤테로아릴기인 화합물. - 제 1 항 내지 제 8 항 중 어느 한 항에 있어서,
A가 치환 또는 비치환된 축합 아릴기인 화합물. - 제 9 항에 있어서,
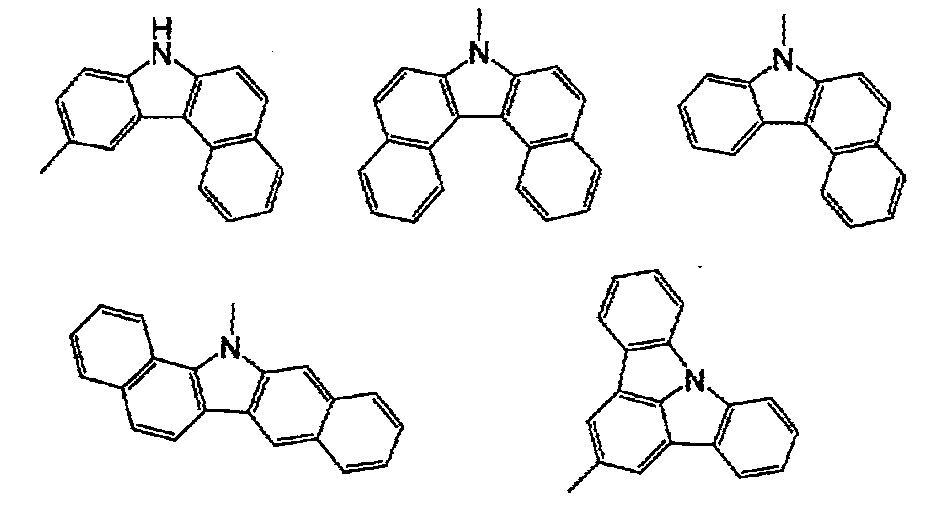
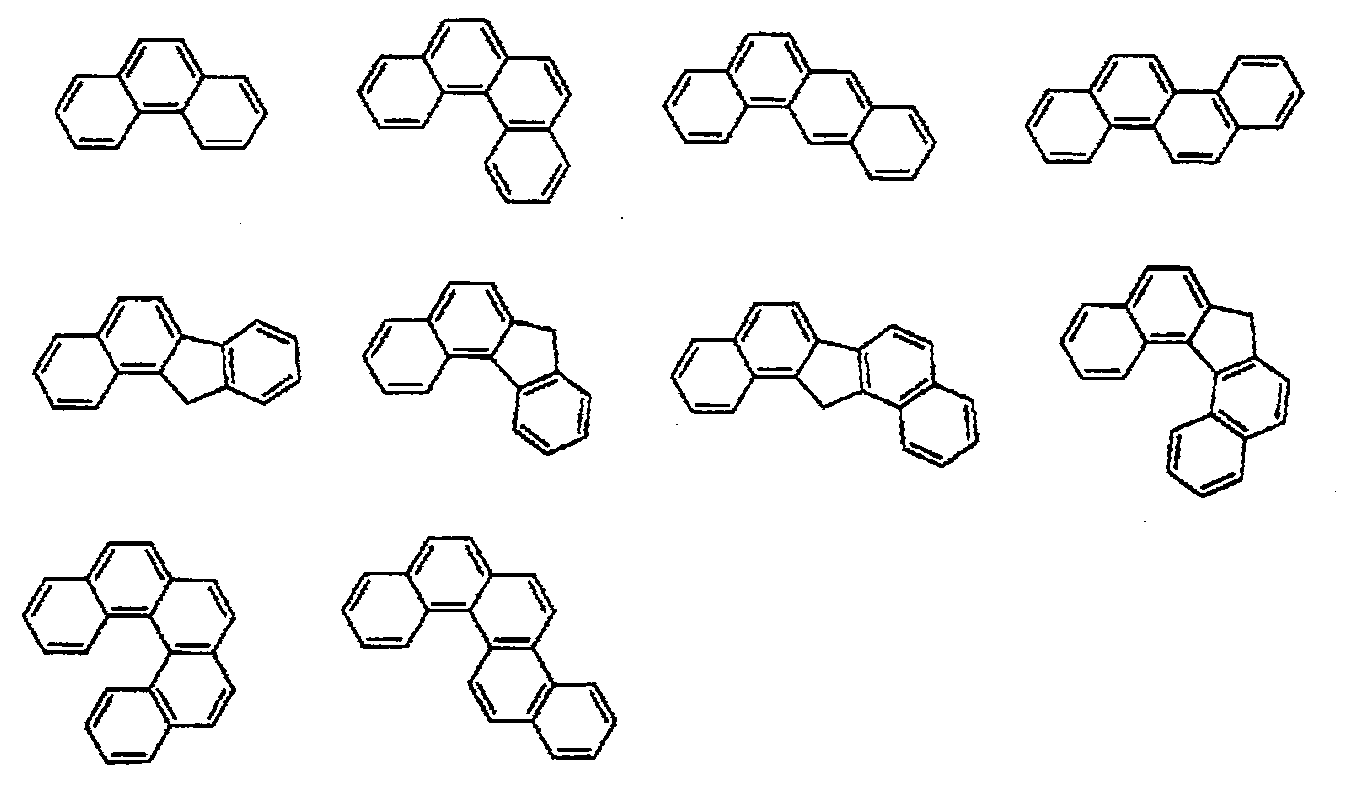
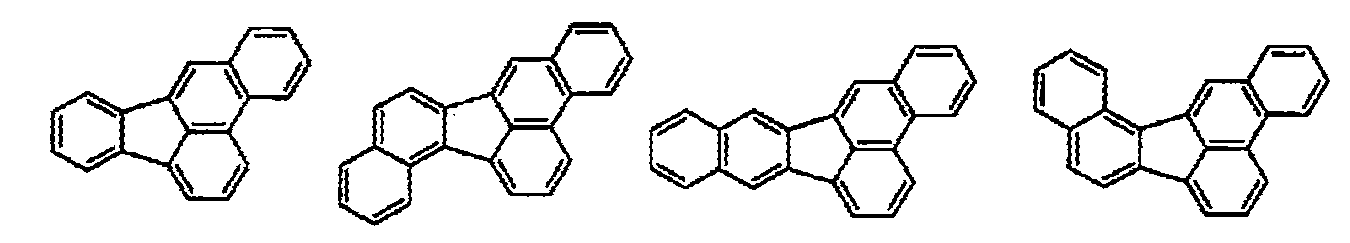
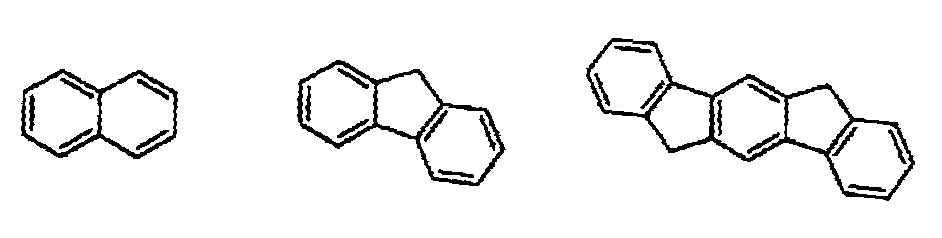
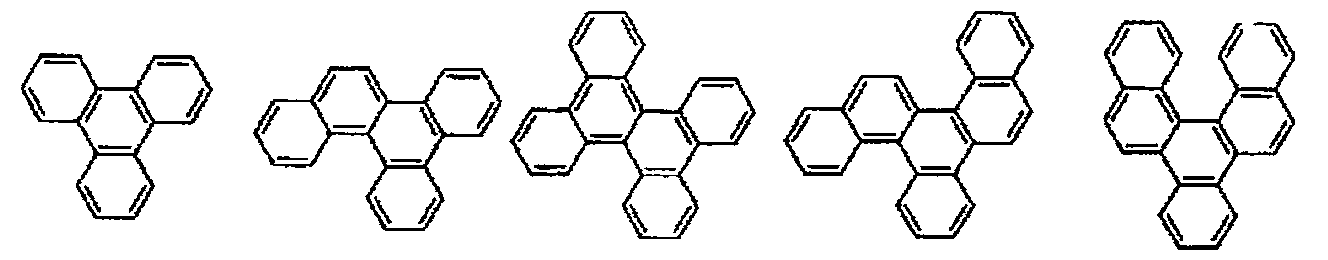
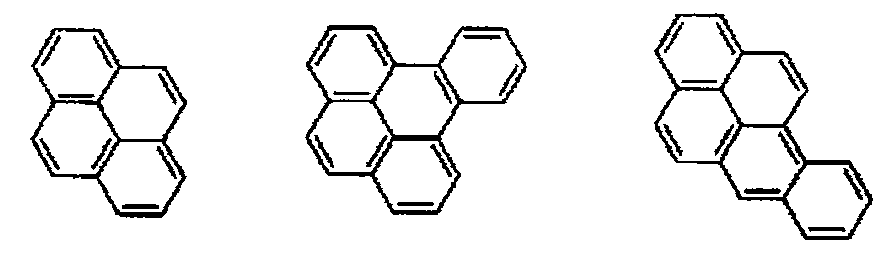
상기 축합 아릴기가 하기 화학식(a1-1)∼(a1-6) 중 어느 하나로 표시되는 화합물의 1가의 잔기인 화합물.
〔상기 화학식(a1-1)∼(a1-5)에 있어서, Ar1∼Ar7은, 각각 독립적으로, 각 식 중의 a 및 b 또는 c 및 d로 표시되는 2개의 탄소 원자와 함께, 환형성 탄소수 6∼18의 환구조를 형성한다.
또한, 상기 화학식(a1-6)에 있어서, Ar8은, 당해 식 중의 a, b 및 c로 표시되는 3개의 탄소 원자와 함께, 환형성 탄소수 6∼18의 환구조를 형성하고, Ar9는, 당해 식 중의 b, c, d 및 e로 표시되는 4개의 탄소 원자와 함께, 환형성 탄소수 6∼18의 환구조를 형성한다.
한편, 상기 화학식(a1-1)∼(a1-6) 중의 수소 원자와 결합해 있는 탄소 원자는, 당해 수소 원자 대신에, 전술한 치환기에 의해서 치환되어 있어도 된다.〕 - 제 1 항 내지 제 8 항 중 어느 한 항에 있어서,
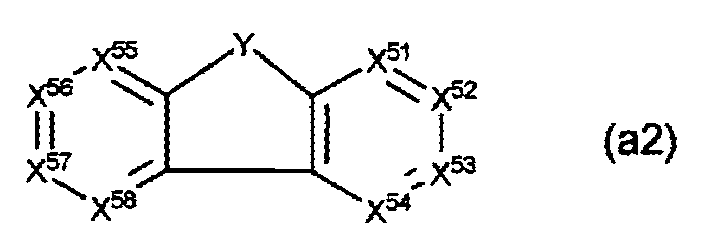
A가, 하기 화학식(a2)로 표시되는 화합물의 1가의 잔기인 화합물.
〔상기 화학식(a2) 중, X51∼X58은, 각각 독립적으로, C(R) 또는 질소 원자이다. R은, 각각 독립적으로, 수소 원자 또는 치환기이고, 복수 존재하는 R로부터 선택되는 2개는 서로 결합하여 환을 형성해도 된다.
Y는 산소 원자, 황 원자, -NRc, 또는 -C(Rd)(Re)-이다. Rc, Rd 및 Re는, 각각 독립적으로, 수소 원자 또는 치환기이고, Rd 및 Re는 서로 결합하여 환을 형성해도 된다.〕 - 제 13 항에 있어서,
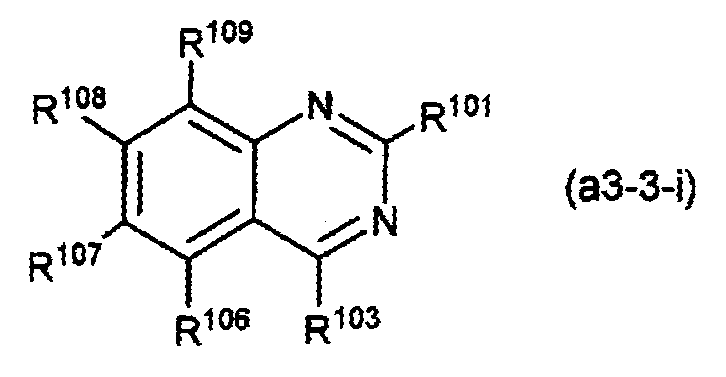
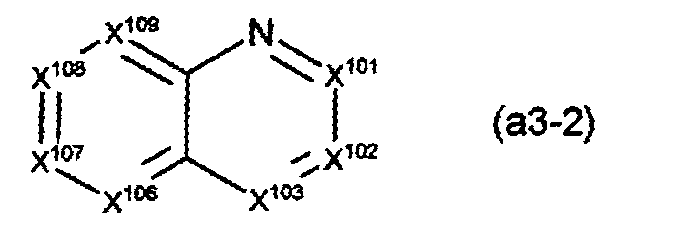
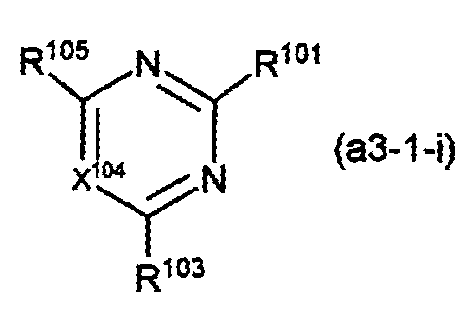
A가, 하기 화학식(a3-1-i) 또는 (a3-3-i)로 표시되는 화합물의 1가의 잔기인 화합물.
〔상기 화학식(a3-1-i) 중, X104는, C(R104) 또는 질소 원자를 나타낸다. R101 및 R103∼R105는, 각각 독립적으로, 수소 원자 또는 치환기이며, R103∼R105로부터 선택되는 2개는 서로 결합하여 환을 형성하고 있어도 된다.〕
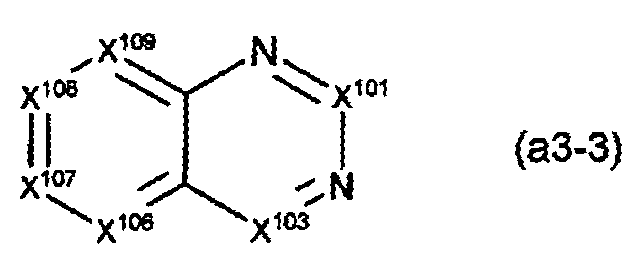
〔상기 화학식(a3-3-i) 중, R101, R103 및 R106∼R109는, 각각 독립적으로, 수소 원자 또는 치환기이며, R103 및 R106∼R109로부터 선택되는 2개는 서로 결합하여 환을 형성하고 있어도 된다.〕 - 제 2 항에 있어서,
하기 화학식(4)로 표시되는 화합물.
〔상기 화학식(4) 중, L, RA 및 RB는 제 1 항의 상기 화학식(1)에 관한 기재와 동일하고, R1∼R16 및 *11∼*14는 제 2 항의 상기 화학식(2)에 관한 기재와 동일하다.
X101∼X105는, 각각 독립적으로, *a와 결합하는 탄소 원자, C(RY), 또는 질소 원자를 나타낸다. RY는 수소 원자 또는 치환기이고, 복수 존재하는 RY는 각각 동일해도 되고, 상이해도 된다. 또한, 복수 존재하는 RY로부터 선택되는 2개는 서로 결합하여 환을 형성하고 있어도 된다.〕 - 제 1 항 내지 제 17 항 중 어느 한 항에 있어서,
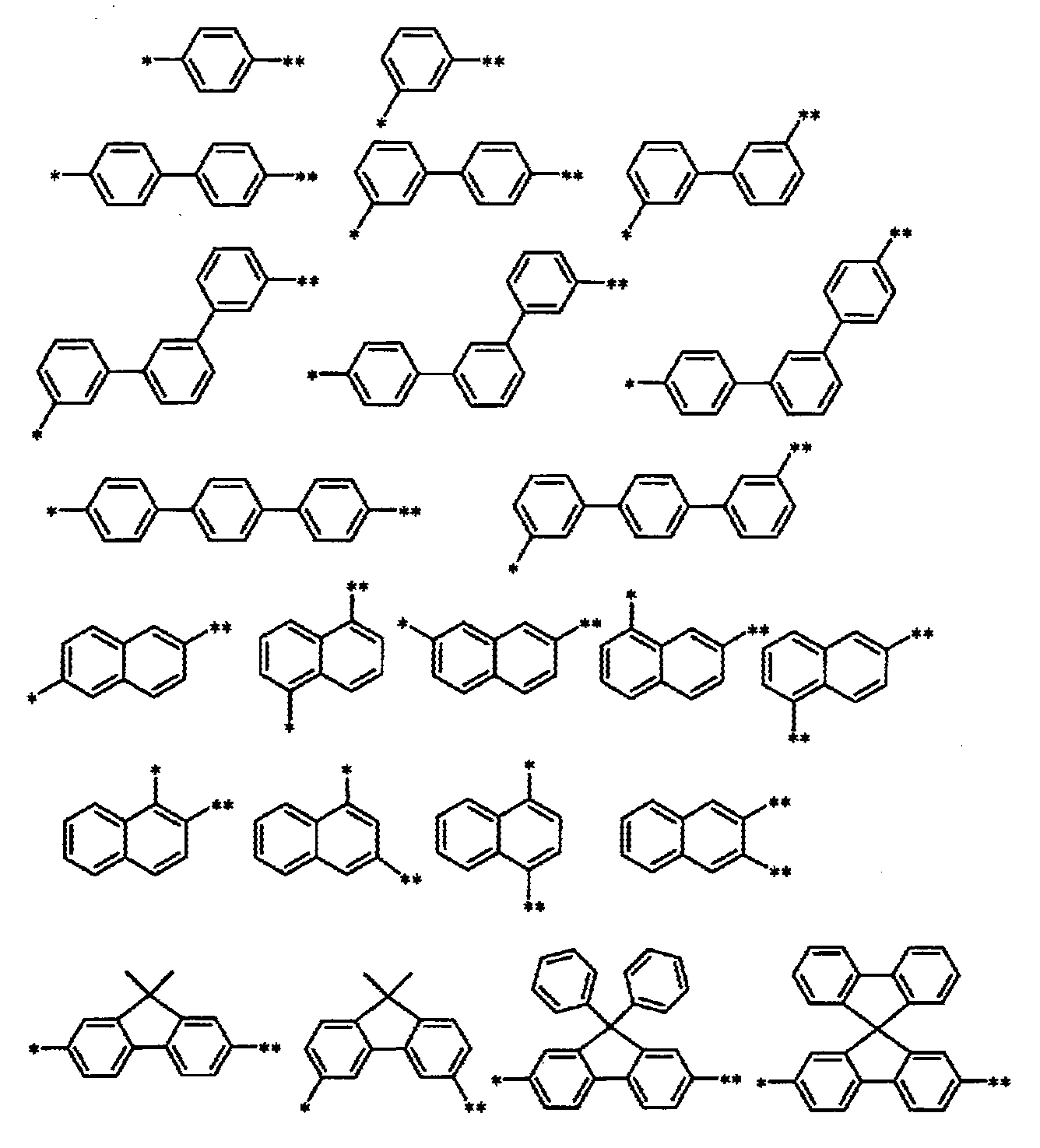
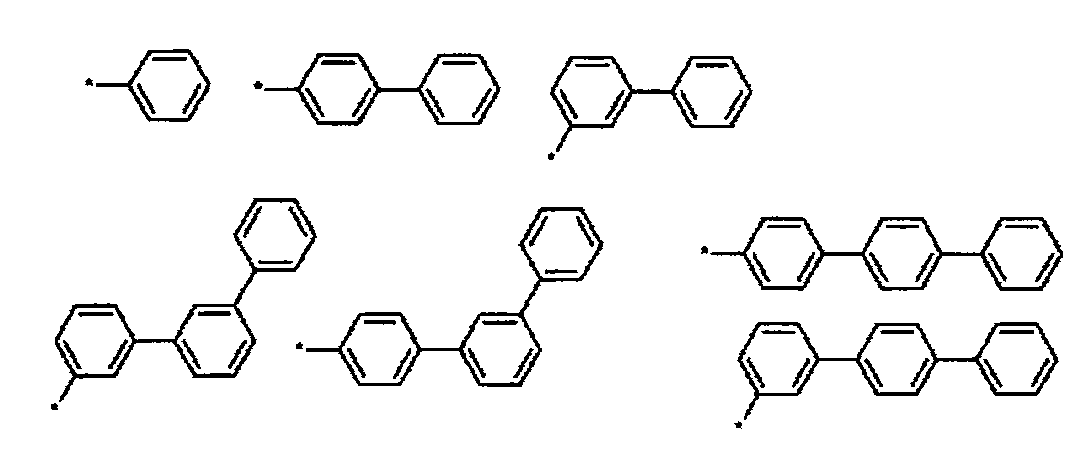
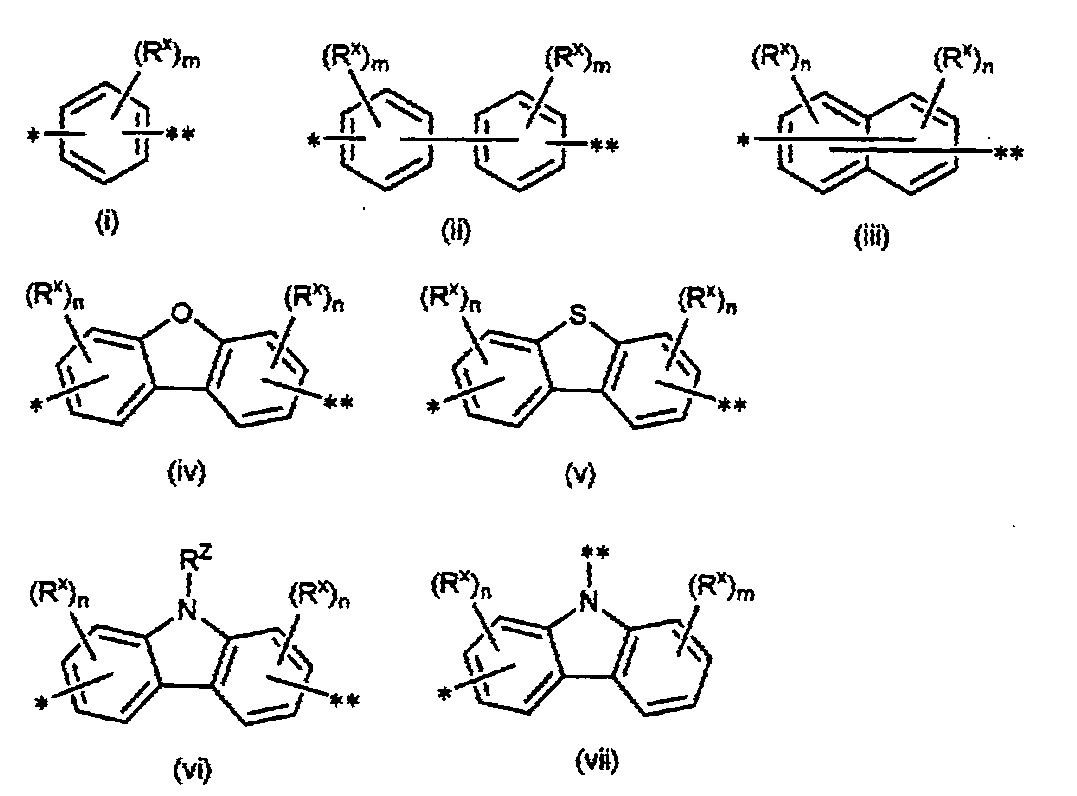
L이, 단일결합, 또는 하기 화학식(i)∼(vii) 중 어느 하나로 표시되는 기인 화합물.
〔식 중, RX는, 각각 독립적으로, 수소 원자 또는 치환기이며, RX를 복수 갖는 경우, 해당 복수의 RX는 서로 동일해도 상이해도 되고, 복수의 RX로부터 선택되는 2개가 서로 결합하여 환구조를 형성해도 된다. 상기 식(vi) 중, RZ는 수소 원자 또는 치환기이다. m은, 각각 독립적으로, 0∼4의 정수이며, n은, 각각 독립적으로, 0∼3의 정수이다. * 및 **는 상기 화학식(1) 중의 질소 원자 또는 A와의 결합 위치를 나타낸다.〕 - 제 1 항 내지 제 18 항 중 어느 한 항에 있어서,
상기 치환기, 또는 「치환 또는 비치환」이라는 기재에 있어서의 치환기가, 모두, 탄소수 1∼50의 알킬기, 환형성 탄소수 3∼50 사이클로알킬기, 환형성 탄소수 6∼50의 아릴기, 환형성 탄소수 6∼50의 아릴기를 갖는 탄소수 7∼51의 아르알킬기, 아미노기, 탄소수 1∼50의 알킬기 및 환형성 탄소수 6∼50의 아릴기로부터 선택되는 치환기를 갖는 모노치환 또는 다이치환 아미노기, 탄소수 1∼50의 알킬기를 갖는 알콕시기, 환형성 탄소수 6∼50의 아릴기를 갖는 아릴옥시기, 탄소수 1∼50의 알킬기 및 환형성 탄소수 6∼50의 아릴기로부터 선택되는 치환기를 갖는 모노치환, 다이치환 또는 트라이치환 실릴기, 환형성 원자수 5∼50의 헤테로아릴기, 탄소수 1∼50의 할로알킬기, 할로젠 원자, 사이아노기, 나이트로기, 탄소수 1∼50의 알킬기 및 환형성 탄소수 6∼50의 아릴기로부터 선택되는 치환기를 갖는 설폰일기, 탄소수 1∼50의 알킬기 및 환형성 탄소수 6∼50의 아릴기로부터 선택되는 치환기를 갖는 다이치환 포스포릴기, 알킬설폰일옥시기, 아릴설폰일옥시기, 알킬카보닐옥시기, 아릴카보닐옥시기, 붕소 함유기, 아연 함유기, 주석 함유기, 규소 함유기, 마그네슘 함유기, 리튬 함유기, 하이드록시기, 알킬 치환 또는 아릴 치환 카보닐기, 카복실기, 바이닐기, (메트)아크릴로일기, 에폭시기, 및 옥세탄일기로 이루어지는 군으로부터 선택되는 기인 화합물. - 제 1 항 내지 제 19 항 중 어느 한 항에 기재된 화합물로 이루어지는 유기 전기발광 소자용 재료.
- 음극, 양극, 및 해당 음극과 해당 양극 사이에 일층 이상의 유기 박막층을 갖는 유기 전기발광 소자로서,
상기 일층 이상의 유기 박막층이 발광층을 포함하고, 상기 일층 이상의 유기 박막층의 적어도 1층이 제 1 항 내지 제 19 항 중 어느 한 항에 기재된 화합물을 포함하는 층인 유기 전기발광 소자. - 제 20 항에 있어서,
상기 발광층이 제 1 항 내지 제 19 항 중 어느 한 항에 기재된 화합물을 포함하는 유기 전기발광 소자. - 제 21 항 또는 제 22 항에 있어서,
상기 발광층이 추가로 형광 발광 재료 및 인광 발광 재료로부터 선택되는 1종 이상을 함유하는 유기 전기발광 소자. - 제 21 항 내지 제 23 항 중 어느 한 항에 있어서,
상기 일층 이상의 유기 박막층이 추가로 정공 수송층을 포함하는 유기 전기발광 소자. - 제 21 항 내지 제 24 항 중 어느 한 항에 있어서,
상기 일층 이상의 유기 박막층이 추가로 전자 수송층을 포함하는 유기 전기발광 소자. - 제 21 항 내지 제 25 항 중 어느 한 항에 기재된 유기 전기발광 소자를 탑재한 전자 기기.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JPJP-P-2014-165453 | 2014-08-15 | ||
| JP2014165453 | 2014-08-15 | ||
| PCT/JP2015/072975 WO2016024637A1 (ja) | 2014-08-15 | 2015-08-14 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、及び電子機器 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20170052521A true KR20170052521A (ko) | 2017-05-12 |
| KR102449305B1 KR102449305B1 (ko) | 2022-09-29 |
Family
ID=55304263
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020167002885A Active KR102449305B1 (ko) | 2014-08-15 | 2015-08-14 | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 |
Country Status (5)
| Country | Link |
|---|---|
| US (1) | US20170005274A1 (ko) |
| JP (1) | JP6431032B2 (ko) |
| KR (1) | KR102449305B1 (ko) |
| CN (1) | CN105531278B (ko) |
| WO (1) | WO2016024637A1 (ko) |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPWO2017038728A1 (ja) | 2015-08-28 | 2018-06-14 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、及び電子機器 |
| KR102438615B1 (ko) * | 2016-07-27 | 2022-08-31 | 에스에프씨 주식회사 | 유기발광 화합물 및 이를 포함하는 유기발광소자 |
| US10957865B2 (en) | 2016-07-27 | 2021-03-23 | Sfc Co., Ltd. | Organic light emitting compound and organic light emitting diode including the same |
| CA3298593A1 (en) | 2016-12-02 | 2026-03-02 | The Research Foundation For The State University Of New York | Fabrication method for fused multi-layer amorphous selenium sensor |
| EP3617210A1 (en) * | 2018-08-31 | 2020-03-04 | Idemitsu Kosan Co., Ltd. | Polycyclic compound, and an organic electroluminescence device comprising the polycyclic compound |
| JP2022053547A (ja) | 2018-12-03 | 2022-04-06 | 出光興産株式会社 | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、及び電子機器 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010136109A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012069121A1 (de) * | 2010-11-24 | 2012-05-31 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20130052485A (ko) | 2011-11-11 | 2013-05-22 | (주)씨에스엘쏠라 | 유기발광화합물 및 이를 이용한 유기 광소자 |
| KR20140056215A (ko) * | 2011-07-15 | 2014-05-09 | 이데미쓰 고산 가부시키가이샤 | 질소 함유 방향족 복소환 유도체 및 그것을 이용한 유기 전기발광 소자 |
| KR20150095186A (ko) * | 2014-02-12 | 2015-08-20 | 삼성전자주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US6503905B1 (en) * | 1998-12-29 | 2003-01-07 | Pfizer Inc | 3,3-biarylpiperidine and 2,2-biarylmorpholine derivatives |
| US8278828B1 (en) * | 2001-10-23 | 2012-10-02 | Imaging Systems Technology | Large area organic LED display |
| KR101511072B1 (ko) * | 2009-03-20 | 2015-04-10 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 발광 화합물 및 이를 포함하는 유기 전계 발광소자 |
| KR101531904B1 (ko) * | 2010-10-13 | 2015-06-29 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전자재료용 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| US20140217378A1 (en) * | 2011-06-24 | 2014-08-07 | Idemitsu Kosan Co., Ltd. | Organic electroluminescent element |
| KR102048688B1 (ko) * | 2011-09-09 | 2019-11-26 | 이데미쓰 고산 가부시키가이샤 | 질소 함유 헤테로 방향족환 화합물 |
| KR101380335B1 (ko) * | 2011-10-10 | 2014-04-10 | 삼성디스플레이 주식회사 | 헤테로시클릭 화합물, 이를 포함하는 유기 발광 소자 및 평판 표시 장치 |
| KR101950474B1 (ko) * | 2012-08-22 | 2019-02-21 | 삼성디스플레이 주식회사 | 유기 발광 소자 |
| EP2907815B1 (en) * | 2014-02-12 | 2023-12-06 | Samsung Electronics Co., Ltd. | Condensed cyclic compound and organic light-emitting device including the same |
-
2015
- 2015-08-14 KR KR1020167002885A patent/KR102449305B1/ko active Active
- 2015-08-14 US US15/107,300 patent/US20170005274A1/en not_active Abandoned
- 2015-08-14 JP JP2016502135A patent/JP6431032B2/ja not_active Expired - Fee Related
- 2015-08-14 CN CN201580001556.5A patent/CN105531278B/zh not_active Expired - Fee Related
- 2015-08-14 WO PCT/JP2015/072975 patent/WO2016024637A1/ja not_active Ceased
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2010136109A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2012069121A1 (de) * | 2010-11-24 | 2012-05-31 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| KR20140056215A (ko) * | 2011-07-15 | 2014-05-09 | 이데미쓰 고산 가부시키가이샤 | 질소 함유 방향족 복소환 유도체 및 그것을 이용한 유기 전기발광 소자 |
| KR20130052485A (ko) | 2011-11-11 | 2013-05-22 | (주)씨에스엘쏠라 | 유기발광화합물 및 이를 이용한 유기 광소자 |
| KR20150095186A (ko) * | 2014-02-12 | 2015-08-20 | 삼성전자주식회사 | 축합환 화합물 및 이를 포함한 유기 발광 소자 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN105531278A (zh) | 2016-04-27 |
| JPWO2016024637A1 (ja) | 2017-06-01 |
| JP6431032B2 (ja) | 2018-11-28 |
| CN105531278B (zh) | 2021-01-26 |
| KR102449305B1 (ko) | 2022-09-29 |
| WO2016024637A1 (ja) | 2016-02-18 |
| US20170005274A1 (en) | 2017-01-05 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102088180B1 (ko) | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 | |
| KR102193512B1 (ko) | 화합물 | |
| JP5856671B2 (ja) | 化合物 | |
| CN105658620B (zh) | 化合物、有机电致发光元件用材料、有机电致发光元件和电子设备 | |
| CN111712493B (zh) | 化合物和使用了其的有机电致发光元件 | |
| JP2019112419A (ja) | 有機ホウ素化合物 | |
| KR20170027691A (ko) | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 | |
| WO2019146781A1 (ja) | 化合物及びそれを用いた有機エレクトロルミネッセンス素子 | |
| CN110800122B (zh) | 有机电致发光器件 | |
| KR102404303B1 (ko) | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자 및 전자 기기 | |
| KR102449305B1 (ko) | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 | |
| CN119080760A (zh) | 化合物和使用了其的有机电致发光元件 | |
| CN113631543A (zh) | 有机电致发光元件和使用其的电子设备 | |
| JP2018108939A (ja) | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、及び電子機器 | |
| JP2018108941A (ja) | 化合物、これを用いた有機エレクトロルミネッセンス素子用材料、及びこれを用いた有機エレクトロルミネッセンス素子並びに電子機器 | |
| KR20180016328A (ko) | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자 및 전자 기기 | |
| WO2016056640A1 (ja) | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、及び電子機器 | |
| WO2016163372A1 (ja) | 化合物、これを用いた有機エレクトロルミネッセンス素子用材料、及びこれを用いた有機エレクトロルミネッセンス素子並びに電子機器 | |
| JP2015019018A (ja) | 有機エレクトロルミネッセンス素子 | |
| JP6367061B2 (ja) | 化合物、有機エレクトロルミネッセンス素子用材料、有機エレクトロルミネッセンス素子、及び電子機器 | |
| CN119183450A (zh) | 化合物、有机电致发光元件用材料、有机电致发光元件和电子设备 | |
| KR20250007515A (ko) | 화합물, 유기 전기발광 소자용 재료, 유기 전기발광 소자, 및 전자 기기 | |
| CN117083261A (zh) | 化合物、有机电致发光元件用材料、有机电致发光元件和电子设备 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| A201 | Request for examination | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-3-3-R10-R18-oth-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U12-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 4 |