KR20180096609A - 섬유증 질병의 치료 및/또는 예방을 위한 아미노나프토퀴논 화합물 - Google Patents
섬유증 질병의 치료 및/또는 예방을 위한 아미노나프토퀴논 화합물 Download PDFInfo
- Publication number
- KR20180096609A KR20180096609A KR1020187016101A KR20187016101A KR20180096609A KR 20180096609 A KR20180096609 A KR 20180096609A KR 1020187016101 A KR1020187016101 A KR 1020187016101A KR 20187016101 A KR20187016101 A KR 20187016101A KR 20180096609 A KR20180096609 A KR 20180096609A
- Authority
- KR
- South Korea
- Prior art keywords
- methyl
- alkyl
- dioxo
- benzamide
- chloro
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4409—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 4, e.g. isoniazid, iproniazid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/16—Amides, e.g. hydroxamic acids
- A61K31/165—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide
- A61K31/166—Amides, e.g. hydroxamic acids having aromatic rings, e.g. colchicine, atenolol, progabide having the carbon of a carboxamide group directly attached to the aromatic ring, e.g. procainamide, procarbazine, metoclopramide, labetalol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/12—Ketones
- A61K31/122—Ketones having the oxygen directly attached to a ring, e.g. quinones, vitamin K1, anthralin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
- A61K31/403—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil condensed with carbocyclic rings, e.g. carbazole
- A61K31/404—Indoles, e.g. pindolol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/415—1,2-Diazoles
- A61K31/416—1,2-Diazoles condensed with carbocyclic ring systems, e.g. indazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/4164—1,3-Diazoles
- A61K31/4184—1,3-Diazoles condensed with carbocyclic rings, e.g. benzimidazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/41—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with two or more ring hetero atoms, at least one of which being nitrogen, e.g. tetrazole
- A61K31/425—Thiazoles
- A61K31/426—1,3-Thiazoles
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/4353—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems
- A61K31/437—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom ortho- or peri-condensed with heterocyclic ring systems the heterocyclic ring system containing a five-membered ring having nitrogen as a ring hetero atom, e.g. indolizine, beta-carboline
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4402—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 2, e.g. pheniramine, bisacodyl
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4406—Non condensed pyridines; Hydrogenated derivatives thereof only substituted in position 3, e.g. zimeldine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
- A61K31/4453—Non condensed piperidines, e.g. piperocaine only substituted in position 1, e.g. propipocaine, diperodon
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4706—4-Aminoquinolines; 8-Aminoquinolines, e.g. chloroquine, primaquine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/4965—Non-condensed pyrazines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/519—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim ortho- or peri-condensed with heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K45/00—Medicinal preparations containing active ingredients not provided for in groups A61K31/00 - A61K41/00
- A61K45/06—Mixtures of active ingredients without chemical characterisation, e.g. antiphlogistics and cardiaca
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C15/00—Cyclic hydrocarbons containing only six-membered aromatic rings as cyclic parts
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0019—Injectable compositions; Intramuscular, intravenous, arterial, subcutaneous administration; Compositions to be administered through the skin in an invasive manner
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Organic Chemistry (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pulmonology (AREA)
- Heart & Thoracic Surgery (AREA)
- Cardiology (AREA)
- Urology & Nephrology (AREA)
- Gastroenterology & Hepatology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
Description
도 2a 및 도 2b는 WI-38 세포에서 ET-1-유도 CTGF 발현에 대한 L056의 효과를 도시한 것이다. WI-38 폐 섬유아세포를 ET-1(10 nM)과 함께 2시간 동안 인큐베이션하기 전 30분 동안 및 인큐베이션 동안 상이한 농도의 L056(0.3, 1, 3 또는 10 μM)과 함께 인큐베이션하였다. L056은 농도-의존 방식으로 WI-38 폐 섬유아세포로부터의 ET-1-유도 CTGF 생산을 유의미하게 억제하였다. 도 2a, 웨스턴 블롯 플롯; 도 2b, 웨스턴 블롯의 정량적 검정.
도 3a 및 도 3b는 WI-38 세포에서 트롬빈-1-유도 CTGF 발현에 대한 L056의 효과를 도시한 것이다. WI-38 폐 섬유아세포를 트롬빈(1 U/ml)과 함께 2시간 동안 인큐베이션하기 전 30분 동안 및 인큐베이션 동안 상이한 농도의 L056(0.3, 1, 3 또는 10 μM)과 함께 인큐베이션하였다. L056은 농도-의존 방식으로 WI-38 폐 섬유아세포로부터의 트롬빈-유도 CTGF 생산을 유의미하게 억제하였다. 도 3a, 웨스턴 블롯 플롯; 도 3b, 웨스턴 블롯의 정량적 검정.
도 4a, 도 4b, 및 도 4c는 WI-38 세포에서 TGF-β-유도 콜라겐 발현에 대한 L056의 효과를 도시한 것이다. WI-38 폐 섬유아세포를 TGF-β(10 ng/mL)와 함께 2시간 동안 인큐베이션하기 전 30분 동안 및 인큐베이션 동안 상이한 농도의 L056(0.3, 1, 3 또는 10 μM)과 함께 인큐베이션하였다. L056은 농도-의존 방식으로 WI-38 폐 섬유아세포로부터의 TGF-β-유도 콜라겐 생산을 유의미하게 억제하였다. 도 4a, 웨스턴 블롯 플롯; 도 4b, 웨스턴 블롯의 정량적 검정; 도 4c, 면역형광 플롯.
도 5a 및 도 5b는 WI-38 세포에서 TGF-β-유도 α-SMA 발현에 대한 L056의 효과를 도시한 것이다. WI-38 폐 섬유아세포를 TGF-β(10 ng/mL)와 함께 2시간 동안 인큐베이션하기 전 30분 동안 및 인큐베이션 동안 상이한 농도의 L056(0.3, 1, 3 또는 10 μM)과 함께 인큐베이션하였다. L056은 농도-의존 방식으로 WI-38 폐 섬유아세포로부터의 TGF-β-유도 α-SMA 생산을 유의미하게 억제하였다. 도 5a, 웨스턴 블롯 플롯; 도 5b, 웨스턴 블롯의 정량적 검정
도 6a, 도 6b 및 도 6c는 WI-38 세포에서 TGF-β-유도 피브로넥틴 발현에 대한 L056의 효과를 도시한 것이다. WI-38 폐 섬유아세포를 TGF-β(10 ng/mL)와 함께 2시간 동안 인큐베이션하기 전 및 동안에 30분 동안 상이한 농도의 L056(0.3, 1, 3 또는 10 μM)과 함께 인큐베이션하였다. L056은 농도-의존 방식으로 WI-38 폐 섬유아세포로부터의 TGF-β-유도 피브로넥틴 생산을 유의미하게 억제하였다. 도 6a, 웨스턴 블롯 플롯; 도 6b, 웨스턴 블롯의 정량적 검정; 도 6c, 면역형광 플롯.
도 7은 WI38 세포에서 세포 생존력에 대한 L056의 효과를 도시한 것이다.
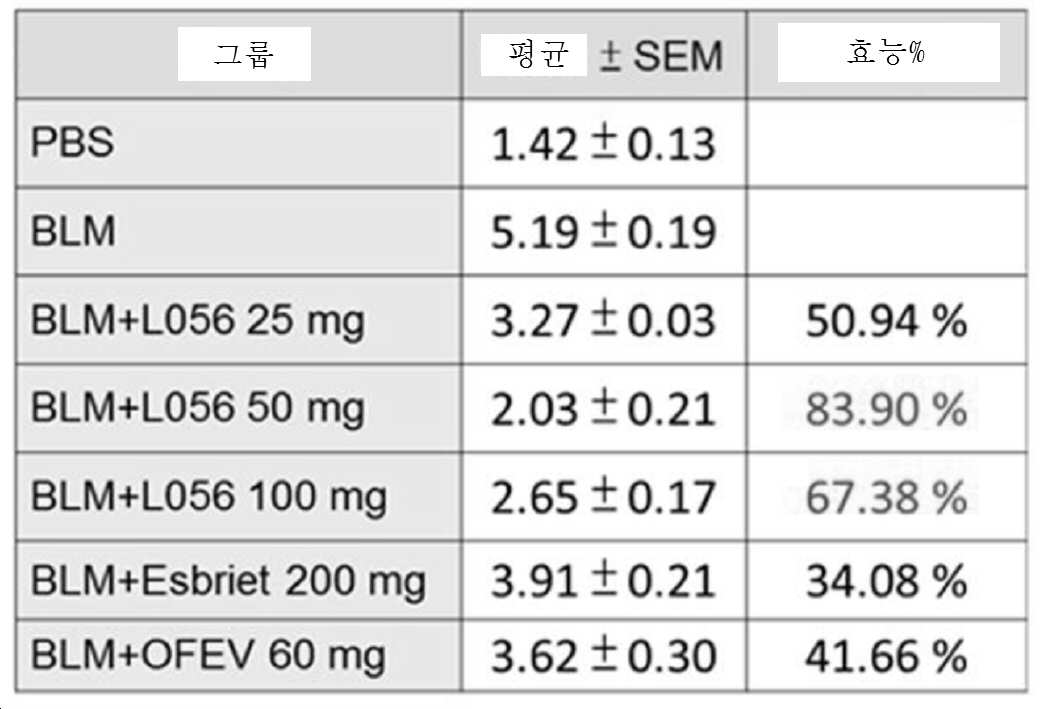
도 8a 및 도 8b는 마우스에서 BLM-유도 폐섬유증의 섬유증 스코어에 대한 L056 효과의 효과를 도시한 것이다. C57BL/6 마우스(8주)를 기관내 투여에 의해 블레오마이신(BLM, 0.05 U/50 ㎕) 또는 PBS(50 ㎕)로 치료하였다. L056(25, 50, 100 mg/kg/일, q.d.), 닌테다닙(OFEV)(200 mg/kg/일, q.d.) 또는 에스브리에트(즉, 피르페니돈)(200 mg/kg/일, q.d.)를 BLM 치료 후 10 내지 38일 동안 블레오마이신-치료된 마우스에 경구 투여하였다. 39일 째에, 마우스를 희생시키고, 폐 조직의 조직학적 분석을 헤마톡실린-에오신(H&E) 염색에 의해 수행하였다(초기 배율, x100). 조직학의 반정량적 분석은, 블레오마이신 투여가 폐에서 상승된 조직학 섬유증 스코어를 야기시킴을 나타내었다. 도 8a, 조직학 섬유증 스코어 플롯; 도 8b, H&E 염색 플롯.
도 9a 내지 도 9d는 전-섬유조직 발생 및 증식 매개체, 콜라겐, CTGF, 피브로넥틴 및 α-SMA 각각에 대한 억제 효과를 도시한 것이다. 도 9a, 콜라겐에 대한 H&E 염색 플롯; 도 9b, CTGF에 대한 H&E 염색 플롯; 도 9c, 피브로넥틴에 대한 H&E 염색 플롯; 도 9d, α-SMA에 대한 H&E 염색 플롯.
도 10a 및 도 10b는 마우스에서 CCl4-유도 간 섬유증에 대한 L056의 효과를 도시한 것이다(치료 모델). 도 10a, 시리우스 레드 염색; 도 10b, CCl4-유도 간 섬유증에 대한 MPT0L056의 억제.
도 11은 마우스에서 CCl4-유도 α-SMA 발현에 대한 L056의 효과를 도시한 것이다(치료 모델).
Claims (28)
- 대상체에 활성 성분으로서 유효량의 하기 화학식 (I)의 화합물 또는 이의 약제학적으로 허용되는 염, 용매화물 또는 전구약물을 투여하는 것을 포함하여, 이를 필요로 하는 대상체에서 섬유증 질병(fibrosis disease)을 예방 및/또는 치료하는 방법:
상기 식에서,
R1은 할로겐, C1- 10알킬, C2- 10알케닐, C2- 10알키닐, NH2, NO2, OH 또는 CN이며;
각 R2는 동일하거나 상이하고, H, C1- 10알킬, C2- 10알케닐, C2- 10알키닐, NH2, NO2, C1- 10알킬옥시, C1- 10알킬티오, C1- 10알킬아미노, C1- 10알킬옥시C1 - 10알킬, OH 또는 CN, C6- 10아릴 또는 N, O 및 S로 이루어진 군으로부터 선택된 1 내지 3개의 헤테로원자를 갖는 C5-7헤테로시클릭을 나타내며;
R3은 H, C1- 10알킬, C2- 10알케닐, C2- 10알키닐, NH2, NO2, OH 또는 CN이며;
R4는 H, C1- 10알킬, C2- 10알케닐, C2- 10알키닐, NH2, NO2, OH 또는 CN이며;
R5는 부재, OH, C3- 10시클로알킬, C6- 10아릴, O, N 및 S로부터 선택된 0 내지 3개의 헤테로원자를 갖는 C5- 7헤테로시클릭 고리 또는 O, N 및 S로부터 선택된 0 내지 3개의 헤테로원자를 갖는 C10-12 융합된 헤테로시클릭 고리이며, 시클로알킬, 아릴, 헤테로시클릭 고리 및 융합된 헤테로시클릭 고리 각각은 OH; 할로겐; NH2; NO2, CN, C1-10알킬; C2- 10알케닐; C2- 10알키닐; C1- 10알킬옥시; N, O 및 S로 이루어진 군으로부터 선택된 1 내지 3개의 헤테로원자를 가지고 C1- 10알킬, C2- 10알케닐, C2- 10알키닐, OH, 할로겐, CN, NH2 또는 NO2로 치환되거나 비치환된 C5- 10헤테로아릴; -S(O)2-페닐 (여기서, 페닐은 할로겐, OH, CN, NH2, NO2, C1- 10알킬, C2- 10알케닐, C2- 10알키닐 또는 C1-10알킬옥시로 치환되거나 비치환됨); -C(O)NHOH; -C(O)NH2; -C(O)-페닐 (여기서, 페닐은 OH, 할로겐, CN, NH2, NO2, C1- 10알킬, C2- 10알케닐, C2- 10알키닐 또는 C1- 10알킬옥시로 이루어진 군으로부터 선택된 1 내지 5개의 동일하거나 상이한 치환체로 치환되거나 비치환됨); -C(O)NRaRb; NHS(O)2페닐 (여기서, 페닐은 OH, 할로겐, CN, NH2, NO2, C1-10알킬, C2- 10알케닐, C2- 10알키닐 또는 C1- 10알킬옥시로 선택적으로 치환됨); C1- 10알킬렌-헤테로아릴; -S(O)2-헤테로아릴; -S(O)2-헤테로시클릭 고리; -S(O)2N(H)-헤테로아릴; -알킬렌-N(H)-헤테로아릴; C1- 10알킬로 치환되거나 비치환된 헤테로시클릭 고리 중 1 내지 3개로 치환되거나 비치환되며;
Ra 및 Rb는 동일하거나 상이하고, 독립적으로, H; OH; 알킬; 알케닐; 알키닐; 알킬옥시; 시클로알킬; 헤테로시클릴; 알킬렌아미노; 알킬렌-N-(알킬)2; OH, 할로겐, CN, NH2, NO2, 알킬, 알케닐, 알키닐, 알킬옥시 또는 헤테로아릴로 치환되거나 비치환된 아릴; OH, 할로겐, CN, NH2, NO2, 알킬, 알케닐, 알키닐 또는 알킬옥시로 치환되거나 비치환된 헤테로아릴; 알킬렌-헤테로아릴; 또는 알킬로 치환되거나 비치환된 알킬렌-헤테로시클릴을 나타내며;
X는 -C(O), -S(O)2 또는 -NH-C(O)-이며;
Y는 -C- 또는 -N-이며;
m은 0 내지 3의 정수이며;
n은 0 내지 7의 정수이다. - 제1항에 있어서, m이 0이며; R1이 할로겐이며; n이 1 내지 4의 임의의 정수이며; R3이 H이며; X가 -C(O)-이며; R4가 H이며; R5가 OH; C3- 8시클로알킬; OH, CN, 할로겐, NH2 또는 C1- 4알킬피페라지닐로부터 선택된 1 내지 3개의 동일하거나 상이한 치환체로 치환되거나 비치환된 페닐; C1- 6알킬피페라지닐; C1- 6알킬피리디닐; C1- 6알킬피롤리디닐; 피리디닐; 피리미디닐; 피라지닐; 피페라지닐; 피롤리디닐; 티아졸릴; 벤즈이미다졸릴; 피라졸릴; 인다졸릴; 피라졸릴; 퀴놀리닐; 인돌릴; C1- 4인돌릴; 인다졸릴; 아자인돌릴; 아자인다졸릴; 데아자푸리닐; 인다닐; 모르폴리노일 또는 C1- 4알킬모르폴리노일이며, 이들 각각이 OH, CN, 할로겐 또는 NH2로부터 선택된 1, 2 또는 3개의 기로 치환되거나 비치환된 방법.
- 제1항에 있어서, m이 0이며; R1이 할로겐이며; n이 1 내지 2의 임의의 정수이며; R3이 H이며; X가 -C(O)이며; R4가 H이며; R5가 OH; C3- 8시클로알킬; 피리디닐; 1 내지 3개의 NH2, 할로겐, OH, CN 또는 C1- 4알킬피페라지닐에 의해 치환된 페닐; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 피리니디닐; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 피라지닐; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 티아졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 벤즈이미다졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 피라졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 인다졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 티아졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 퀴놀리닐; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 인돌릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 인다졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 아자인다졸릴; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 데아자푸리닐; NO2, NH2 또는 C1- 4알킬에 의해 치환되거나 비치환된 인다닐; 또는 NO2, NH2 또는 C1-4알킬에 의해 치환되거나 비치환된 모르폴리노일인 방법.
- 제1항에 있어서, m이 0이며; n이 O이며; X가 -C(O)이며; Y가 -N-이며; R1이 할로겐 또는 C1- 4알킬이며; R3이 H이며; R4가 H 또는 C1- 4알킬이며; R5가 피리디닐, 피라지닐, 또는 피리미디닐인 방법.
- 제1항에 있어서, m이 0이며; n이 0이며; X가 -C(O)이며; Y가 -N-이며; R1이 할로겐이며; R3이 H이며; R4가 H이며; R5가 피리디닐, 피라지닐, 또는 피리미디닐인 방법.
- 제1항에 있어서, m이 0이며; n이 0이며; X가 S(O)2이며; Y가 -N-이며; R1이 할로겐 또는 C1- 4알킬이며; R3이 H이며; R4로부터 결합된 질소 원자와 함께 R4 및 R5가 비시클릭 고리를 형성하며, 바람직하게, 융합된 비시클릭 고리가 인돌릴 또는 아자인돌릴인 방법.
- 제1항에 있어서, m이 0이며; R1이 할로겐이며; n이 1 내지 4의 임의의 정수이며; R3이 H이며; X가 C(O)이며; R4가 H이며; R5가 알킬렌-R6이며, 여기서, R6이 NRaRb, O, N 및 S로부터 선택된 0 내지 3개의 헤테로원자를 갖는 C5- 7헤테로시클릭 고리; 또는 O, N 및 S로부터 선택된 0 내지 3개의 헤테로원자를 갖는 C10-12 융합된 헤테로시클릭 고리이며; Ra 및 Rb가 알킬인 방법.
- 제1항에 있어서, m이 0이며; R1이 할로겐이며; n이 1 내지 2의 임의의 정수이며; R3이 H이며; X가 C(O)이며; R4가 H이며; R5가 (CH2)1- 4R6이며, 여기서, R6이 비치환되거나 치환된 피롤리디닐, 옥솔라닐, 티올라닐, 피롤릴, 푸라닐, 티오페닐, 피페리디닐, 옥사닐, 티아닐, 모르폴리노일, 피리디닐, 피페리디닐, 피페라지닐, 티오피라닐, 피라지닐, 피리미디닐, 피리다지닐, 티아졸릴; 벤즈이미다졸릴; 피라졸릴; 인다졸릴; 피라졸릴; 퀴놀리닐; 인돌릴; 인다졸릴; 아자인돌릴; 아자인다졸릴; 데아자푸리닐; 또는 인다닐인 방법.
- 제1항에 있어서, m이 0이며; R1이 할로겐이며; n이 1 내지 2의 임의의 정수이며; R3이 H이며; X가 C(O)이며; R4가 H이며; R5가 (CH2)1- 4R6이며, 여기서, R6이 비치환되거나 치환된 피롤리디닐, 모르폴리노일, 피리디닐, 피페리디닐, 피페라지닐, 또는 인돌릴인 방법.
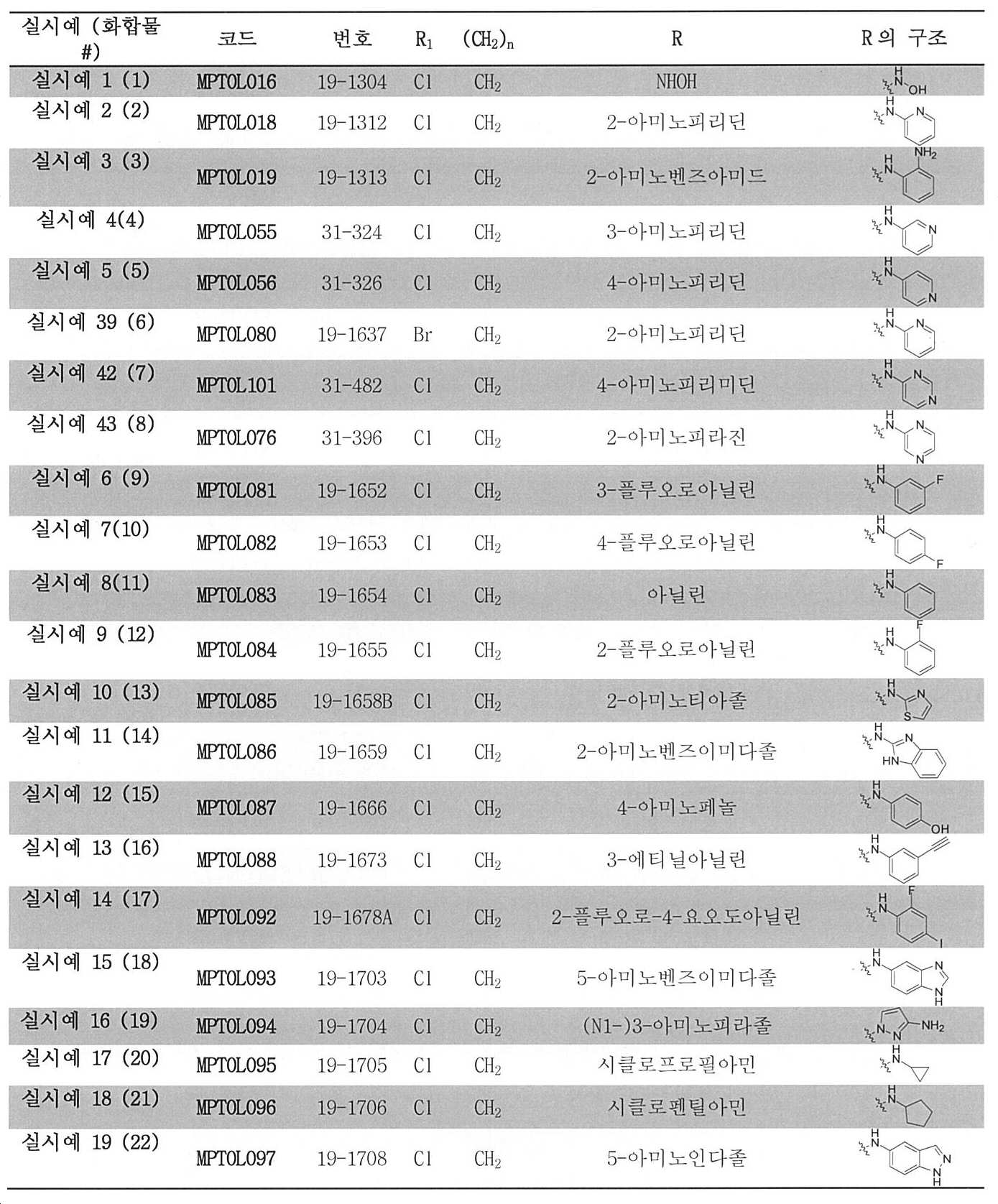
- 제1항에 있어서, 화합물이
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-히드록시벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(피리딘-2-일)벤즈아미드;
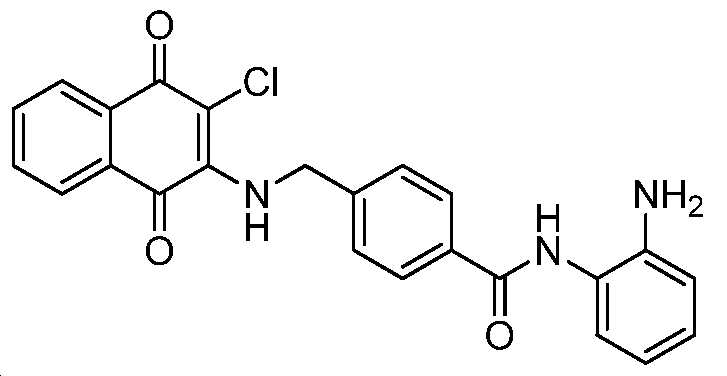
N-(2-아미노페닐)-4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(피리딘-3-일)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(피리딘-3-일)벤즈아미드;
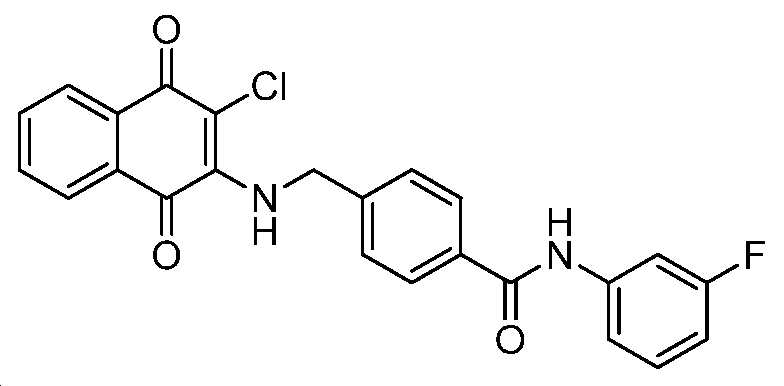
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(3-플루오로페닐)벤즈아미드;
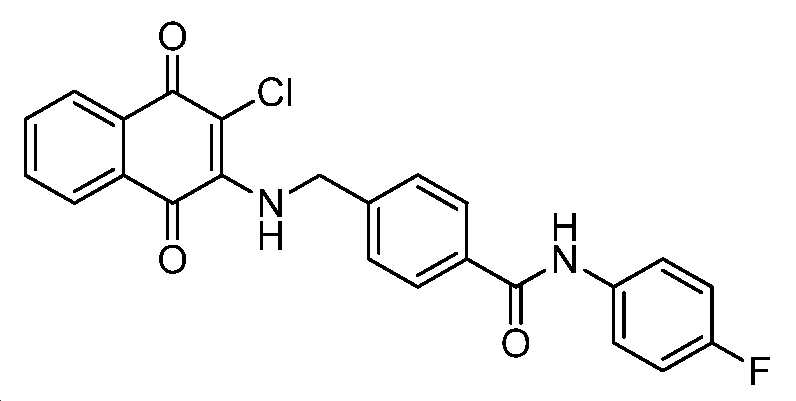
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(4-플루오로페닐)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-페닐벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-플루오로페닐)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(티아졸-2-일)벤즈아미드;
N-(1H-벤조[d]이미다졸-2-일)-4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)벤즈아미드;
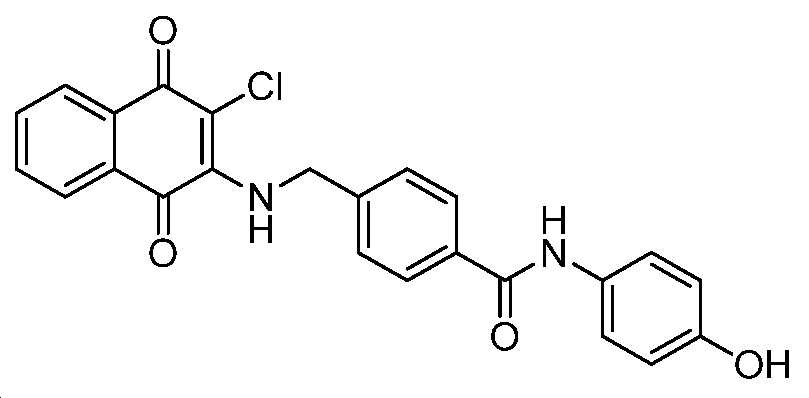
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(4-히드록시페닐)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(3-에티닐페닐)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-플루오로-4-요오도페닐)벤즈아미드;
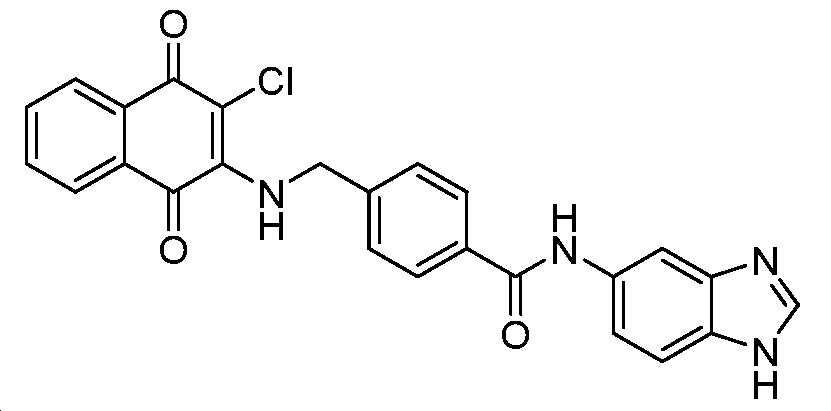
N-(1H-벤조[d]이미다졸-5-일)-4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)벤즈아미드;
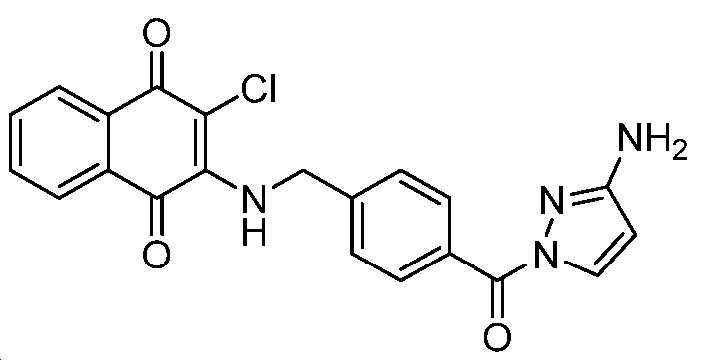
2-(4-(3-아미노-1H-피라졸-1-카르보닐)벤질아미노)-3-클로로나프탈렌-1,4-디온;
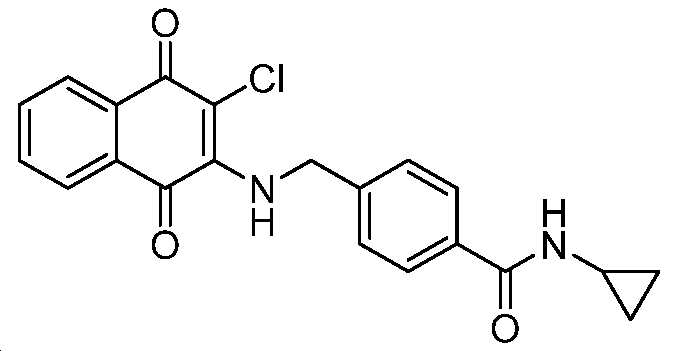
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-시클로프로필벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-시클로펜틸벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-인다졸-5-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(5-메틸티아졸-2-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(5-메틸-3H-피라졸-3-일)벤즈아미드;
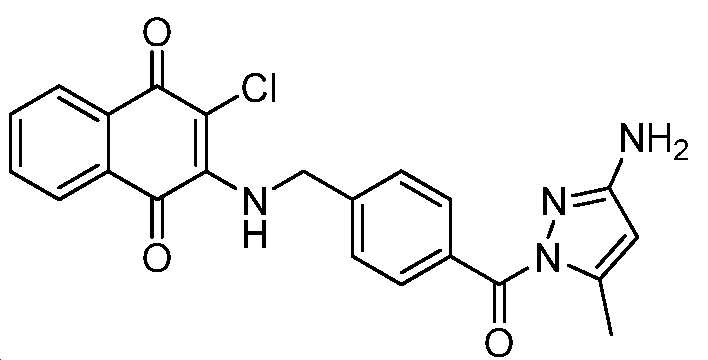
2-(4-(3-아미노-5-메틸-1H-피라졸-1-카르보닐)벤질아미노)-3-클로로나프탈렌-1,4-디온;
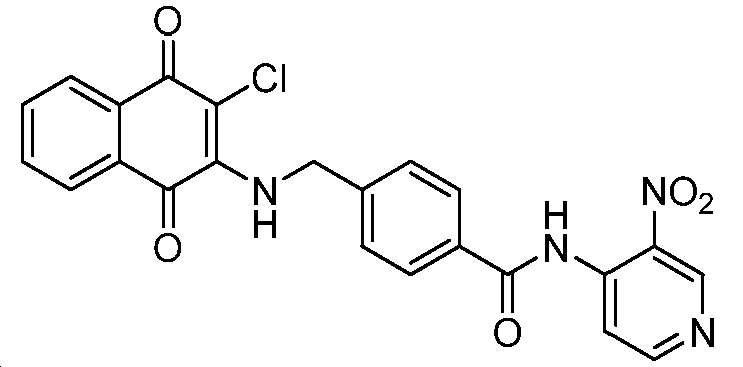
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(3-니트로피리딘-4-일)벤즈아미드;
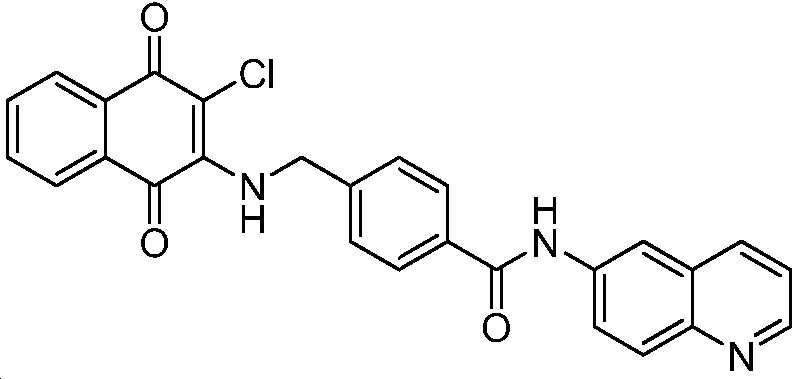
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(퀴놀린-6-일)벤즈아미드;
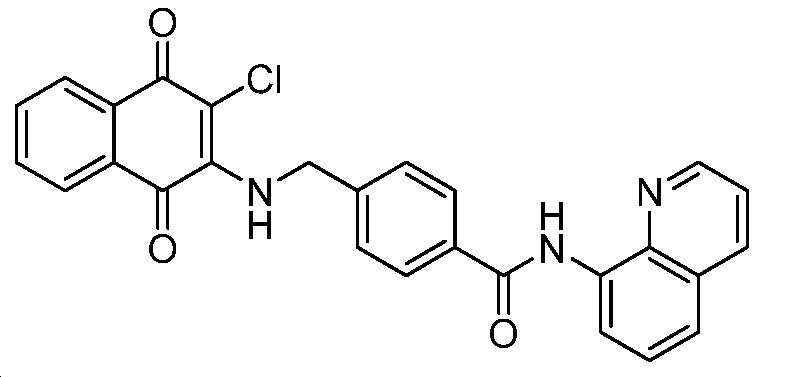
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(퀴놀린-8-일)벤즈아미드;
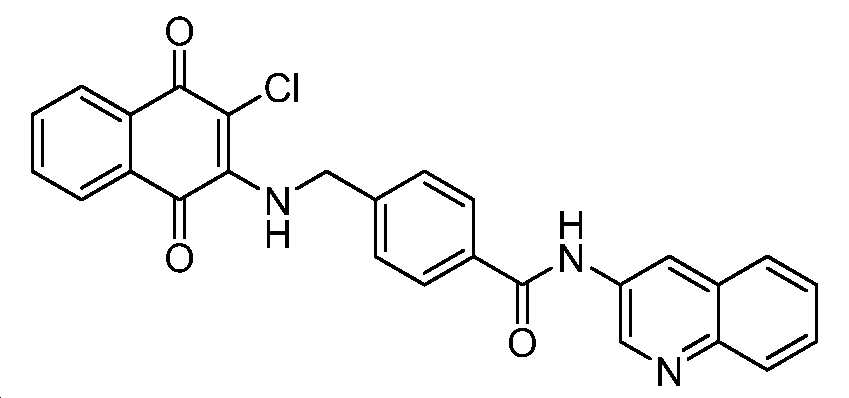
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(퀴놀린-3-일)벤즈아미드;
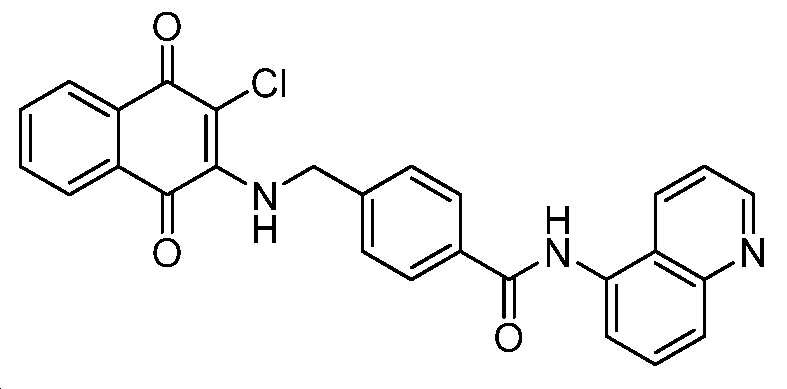
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(퀴놀린-5-일)벤즈아미드;
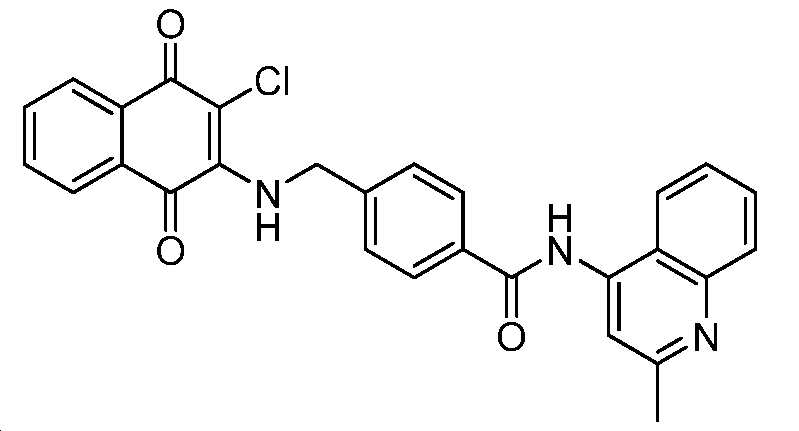
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(2-메틸퀴놀린-4-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-인돌-5-일)벤즈아미드;
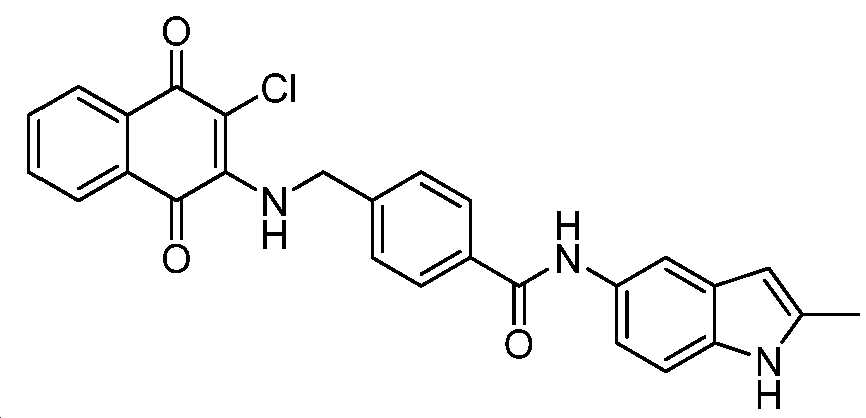
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(2-메틸-1H-인돌-5-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-인돌-5-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-인돌-4-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(4-(4-에틸피페라진-1-일)페닐)벤즈아미드;
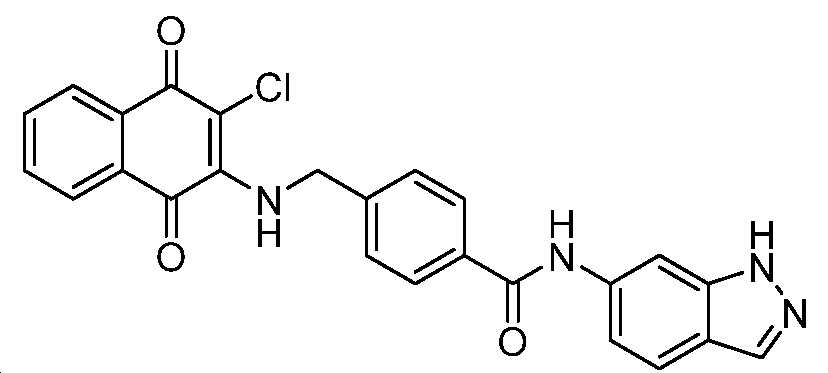
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-인다졸-6-일)벤즈아미드;
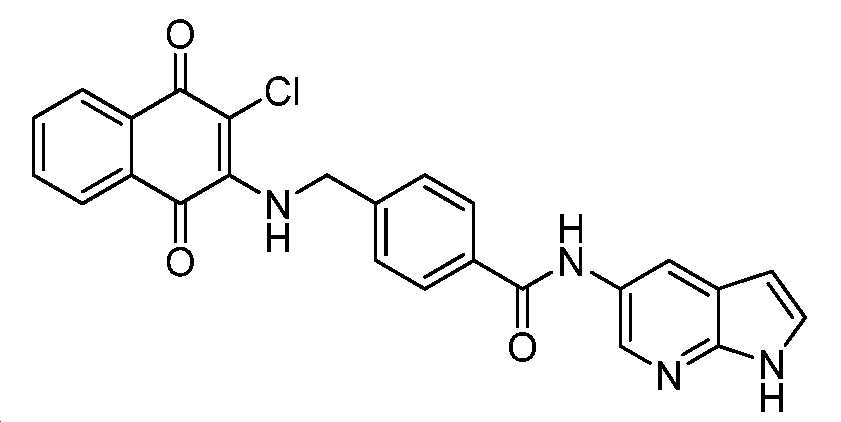
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-피롤로[2,3-b]피리딘-5-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(1H-피라졸로[3,4-b]피리딘-5-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(7-메틸-7H-피롤로[2,3-d]피리미딘-4-일)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(2,3-디히드로-1H-인덴-4-일)벤즈아미드;
4-(((3-브로모-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(피리딘-2-일)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(피리미딘-4-일)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(피라진-2-일)벤즈아미드;
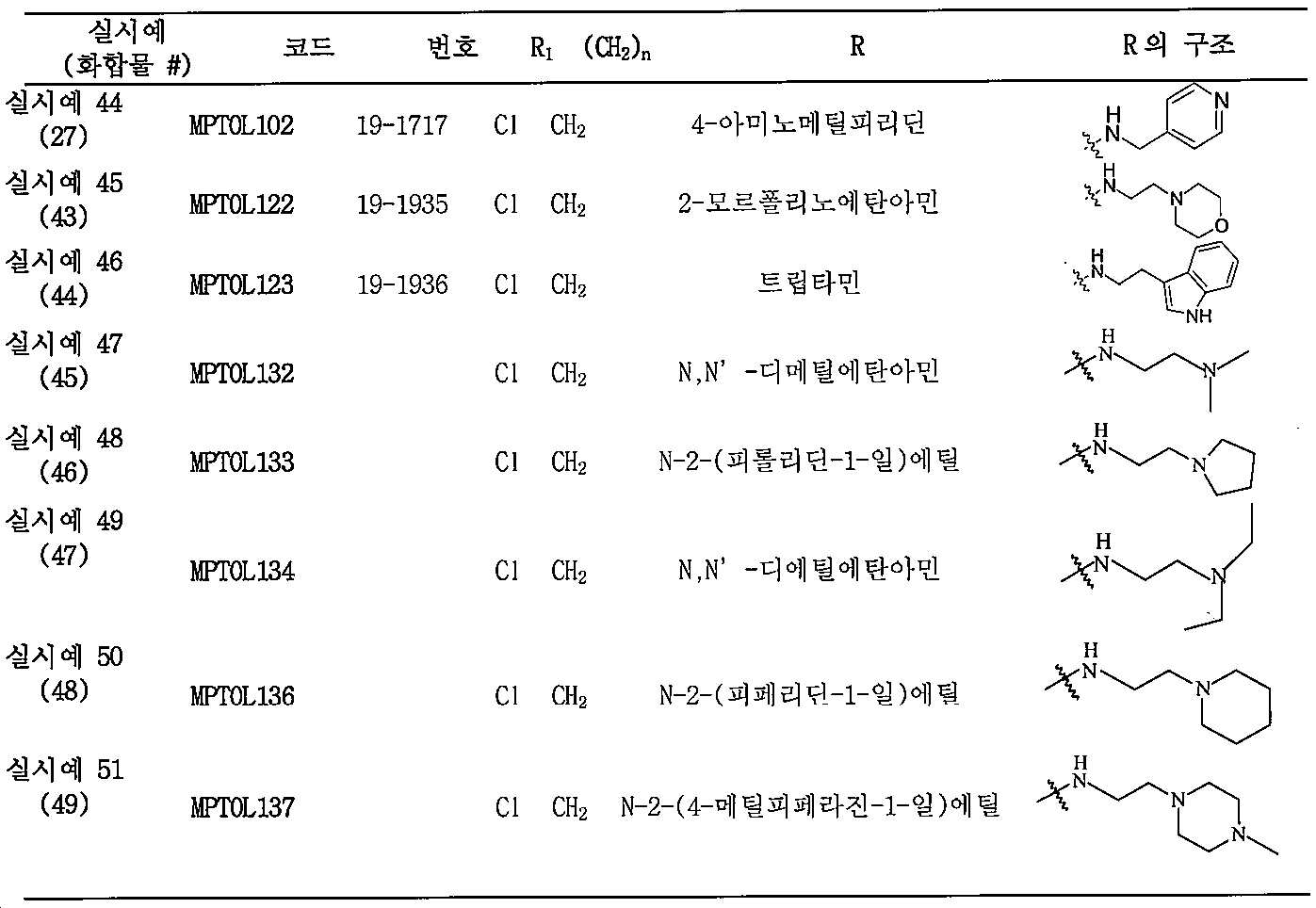
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(피리딘-4-일메틸)벤즈아미드;
4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)-N-(2-모르폴리노에틸)벤즈아미드;
N-(2-(1H-인돌-3-일)에틸)-4-((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일아미노)메틸)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-(디메틸아미노)에틸)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-(피롤리딘-1-일)에틸)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-(디에틸아미노)에틸)벤즈아미드;
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-(피페리딘-1-일)에틸)벤즈아미드; 및
4-(((3-클로로-1,4-디옥소-1,4-디히드로나프탈렌-2-일)아미노)메틸)-N-(2-(4-메틸피페라진-1-일)에틸)벤즈아미드로부터 선택된 방법. - 제1항에 있어서, 본 발명의 방법에서 사용되는 활성 성분의 유효량이 약 1.5 mg/kg/일 내지 약 20 mg/kg/일의 범위인 방법.
- 제1항에 있어서, 치료를 위한 유효량이 약 5.0 mg/kg/일 내지 약 15 mg/kg/일인 방법.
- 제1항에 있어서, 치료를 위한 유효량이 약 1.5 mg/kg/일 내지 약 8 mg/kg/일인 방법.
- 제1항에 있어서, 활성 성분이 제2 항-섬유증 제제(second anti-fibrosis agent)와 함께 추가로 공동-투여되는 방법.
- 제15항에 있어서, 제2 항-섬유증 제제가 피르페니돈, 닌테다닙, LOXL2 항체, 심투주맙, IL-13 항체, 레브리키주맙, αVβ6 항체, STX-100, CTGF 항체, FG-3019, 티펠루카스트, MN-001, 에어로졸 피르페니돈 또는 GP-101인 방법.
- 제15항에 있어서, 공동-투여가 동시, 개별 또는 순차적 투여인 방법.
- 제1항에 있어서, 섬유증 질병이 피부 섬유증, 폐섬유증, 신장 섬유증, 간 섬유증, 장 섬유증, 낭포성 섬유증, 심장 섬유증, 자궁근종 또는 샘근육증인 방법.
- 제18항에 있어서, 폐섬유증이 특발성 폐섬유증인 방법.
- 제18항에 있어서, 폐섬유증 또는 특발성 폐섬유증의 치료가 폐 이식, 고압 산소 요법(hyperbaric oxygen therapy, HBOT) 또는 호흡 재활(pulmonary rehabilitation)과의 동시-투여 요법을 추가로 포함하는 방법.
- 하나 이상의 단위 투약 형태에 활성 성분으로서 약 일일 용량의 제1항에서 정의된 바와 같은 화학식 (I)의 화합물, 또는 약제학적으로 허용되는 염, 용매화물 또는 전구약물을 포함하는 약제 조성물.
- 제21항에 있어서, 화합물이 약 100 mg 내지 약 1,400 mg의 범위인 약제 조성물.
- 제21항에 있어서, 하나 이상의 캡슐 형태 또는 정제 형태인 약제 조성물.
- 제21항에 있어서, 하나 이상의 단위 투약 형태에 약 140 mg 내지 약 1,050 mg의 활성 성분을 포함하는 약제 조성물.
- 제21항에 있어서, 단일 정제에 약 100 mg 내지 약 300 mg의 활성 성분을 포함하는 약제 조성물.
- 제21항에 있어서, 단일 캡슐에 약 100 mg 내지 약 500 mg의 활성 성분을 포함하는 약제 조성물.
- 제21항에 있어서, 제2 항-섬유증 제제를 추가로 포함하는 약제 조성물.
- 제27항에 있어서, 제2 항-섬유증 제제가 피르페니돈, 닌테다닙, LOXL2 항체, 심투주맙, IL-13 항체, 레브리키주맙, αVβ6 항체, STX-100, CTGF 항체, FG-3019, 티펠루카스트, MN-001, 에어로졸 피르페니돈 또는 GP-101인 약제 조성물.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201562256516P | 2015-11-17 | 2015-11-17 | |
| US62/256,516 | 2015-11-17 | ||
| PCT/US2016/062568 WO2017087695A1 (en) | 2015-11-17 | 2016-11-17 | Aminonaphthoquinone compounds for treatment and/or prevention of fibrosis diseases |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20180096609A true KR20180096609A (ko) | 2018-08-29 |
Family
ID=58717862
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020187016101A Ceased KR20180096609A (ko) | 2015-11-17 | 2016-11-17 | 섬유증 질병의 치료 및/또는 예방을 위한 아미노나프토퀴논 화합물 |
Country Status (8)
| Country | Link |
|---|---|
| US (2) | US11833122B2 (ko) |
| EP (1) | EP3377062B1 (ko) |
| JP (2) | JP7085994B2 (ko) |
| KR (1) | KR20180096609A (ko) |
| CN (2) | CN120204220A (ko) |
| ES (1) | ES2955665T3 (ko) |
| TW (1) | TWI673049B (ko) |
| WO (1) | WO2017087695A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024225820A1 (ko) * | 2023-04-28 | 2024-10-31 | 한국원자력의학원 | 폐섬유화 예방 또는 치료를 위한 다코미티닙 및 닌테다닙의 병용 요법 |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MD3762368T2 (ro) | 2018-03-08 | 2022-07-31 | Incyte Corp | Compuși diol aminopirazină ca inhibitori ai PI3K-Y |
| WO2020010003A1 (en) | 2018-07-02 | 2020-01-09 | Incyte Corporation | AMINOPYRAZINE DERIVATIVES AS PI3K-γ INHIBITORS |
Family Cites Families (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20040167189A1 (en) * | 2002-03-22 | 2004-08-26 | The Government Of The U.S.A., As Represented By The Secretary, Dept. Of Health And Human Services | Materials and methods for inhibiting Wip1 |
| ATE392212T1 (de) | 2002-07-25 | 2008-05-15 | Charite Universitaetsmedizin | Verwendung eines proteasom-inhibitors zur behandlung fibrotischer erkrankungen |
| ES2510840T3 (es) | 2004-05-10 | 2014-10-21 | Onyx Therapeutics, Inc. | Compuestos para la inhibición enzimática del proteosoma |
| DE602005026556D1 (de) * | 2004-12-07 | 2011-04-07 | Proteolix Inc | Zusammensetzung zur proteasomhemmung |
| WO2010005534A2 (en) * | 2008-06-30 | 2010-01-14 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Proteasome inhibitors for selectively inducing apoptosis in cancer cells |
| CA2992981C (en) | 2015-07-23 | 2023-10-17 | Taipei Medical University | Aminonaphthoquinone compounds and pharmaceutical composition for blocking ubiquitination-proteasome system in diseases |
| ES2825348T3 (es) | 2015-07-30 | 2021-05-17 | Calgent Biotechnology Co Ltd | Compuestos y composición farmacéutica asociados al sistema ubiquitinación-proteasoma |
-
2016
- 2016-11-17 KR KR1020187016101A patent/KR20180096609A/ko not_active Ceased
- 2016-11-17 EP EP16867152.7A patent/EP3377062B1/en active Active
- 2016-11-17 CN CN202510406652.3A patent/CN120204220A/zh active Pending
- 2016-11-17 TW TW105137577A patent/TWI673049B/zh active
- 2016-11-17 WO PCT/US2016/062568 patent/WO2017087695A1/en not_active Ceased
- 2016-11-17 US US15/776,698 patent/US11833122B2/en active Active
- 2016-11-17 JP JP2018525670A patent/JP7085994B2/ja active Active
- 2016-11-17 CN CN201680067312.1A patent/CN108697697A/zh active Pending
- 2016-11-17 ES ES16867152T patent/ES2955665T3/es active Active
-
2022
- 2022-06-07 JP JP2022092059A patent/JP7667764B2/ja active Active
-
2023
- 2023-10-23 US US18/492,627 patent/US12453708B2/en active Active
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2024225820A1 (ko) * | 2023-04-28 | 2024-10-31 | 한국원자력의학원 | 폐섬유화 예방 또는 치료를 위한 다코미티닙 및 닌테다닙의 병용 요법 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA3005614A1 (en) | 2017-05-26 |
| JP2022116328A (ja) | 2022-08-09 |
| US20180325845A1 (en) | 2018-11-15 |
| EP3377062C0 (en) | 2023-09-06 |
| CN120204220A (zh) | 2025-06-27 |
| TWI673049B (zh) | 2019-10-01 |
| EP3377062A4 (en) | 2019-07-03 |
| JP2019501126A (ja) | 2019-01-17 |
| JP7667764B2 (ja) | 2025-04-23 |
| US11833122B2 (en) | 2023-12-05 |
| EP3377062B1 (en) | 2023-09-06 |
| US20240130984A1 (en) | 2024-04-25 |
| WO2017087695A1 (en) | 2017-05-26 |
| EP3377062A1 (en) | 2018-09-26 |
| JP7085994B2 (ja) | 2022-06-17 |
| TW201720433A (zh) | 2017-06-16 |
| US12453708B2 (en) | 2025-10-28 |
| ES2955665T3 (es) | 2023-12-05 |
| CN108697697A (zh) | 2018-10-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US8822478B2 (en) | Indazole inhibitors of the WNT signal pathway and therapeutic uses thereof | |
| CN1795195B (zh) | 新颖的吡啶并吡嗪及其作为激酶调节剂的用途 | |
| CN105120862A (zh) | Wnt信号途径的3-(苯并咪唑-2-基)-吲唑抑制剂及其治疗应用 | |
| WO2010021381A1 (ja) | 縮合複素環誘導体およびその用途 | |
| US12453708B2 (en) | Aminonaphthoquinone compounds for treatment and/or prevention of fibrosis diseases | |
| EP3080125A1 (en) | Novel azaindole derivatives as selective histone deacetylase (hdac) inhibitors and pharmaceutical compositions comprising the same | |
| TWI783205B (zh) | 鹵代烯丙基胺類化合物及其用途 | |
| CA3005614C (en) | Aminonaphthoquinone compounds for treatment and/or prevention of fibrosis diseases | |
| HK1224176B (en) | Indazole inhibitors of the wnt signal pathway and therapeutic uses thereof |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
St.27 status event code: N-2-6-B10-B15-exm-PE0601 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T13-X000 | Administrative time limit extension granted |
St.27 status event code: U-3-3-T10-T13-oth-X000 |
|
| T11-X000 | Administrative time limit extension requested |
St.27 status event code: U-3-3-T10-T11-oth-X000 |
|
| T13-X000 | Administrative time limit extension granted |
St.27 status event code: U-3-3-T10-T13-oth-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| D21 | Rejection of application intended |
Free format text: ST27 STATUS EVENT CODE: A-1-2-D10-D21-EXM-PE0902 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |