KR20200027251A - 혈구 분석 장치, 이를 이용한 혈구 분석 방법 - Google Patents
혈구 분석 장치, 이를 이용한 혈구 분석 방법 Download PDFInfo
- Publication number
- KR20200027251A KR20200027251A KR1020180105326A KR20180105326A KR20200027251A KR 20200027251 A KR20200027251 A KR 20200027251A KR 1020180105326 A KR1020180105326 A KR 1020180105326A KR 20180105326 A KR20180105326 A KR 20180105326A KR 20200027251 A KR20200027251 A KR 20200027251A
- Authority
- KR
- South Korea
- Prior art keywords
- laser
- path
- scattered light
- blood cell
- irradiated
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/17—Systems in which incident light is modified in accordance with the properties of the material investigated
- G01N21/47—Scattering, i.e. diffuse reflection
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/6486—Measuring fluorescence of biological material, e.g. DNA, RNA, cells
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/483—Physical analysis of biological material
- G01N33/487—Physical analysis of biological material of liquid biological material
- G01N33/49—Blood
-
- G—PHYSICS
- G02—OPTICS
- G02B—OPTICAL ELEMENTS, SYSTEMS OR APPARATUS
- G02B27/00—Optical systems or apparatus not provided for by any of the groups G02B1/00 - G02B26/00, G02B30/00
- G02B27/09—Beam shaping, e.g. changing the cross-sectional area, not otherwise provided for
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N21/00—Investigating or analysing materials by the use of optical means, i.e. using sub-millimetre waves, infrared, visible or ultraviolet light
- G01N21/62—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light
- G01N21/63—Systems in which the material investigated is excited whereby it emits light or causes a change in wavelength of the incident light optically excited
- G01N21/64—Fluorescence; Phosphorescence
- G01N21/645—Specially adapted constructive features of fluorimeters
- G01N2021/6463—Optics
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Physics & Mathematics (AREA)
- Engineering & Computer Science (AREA)
- General Physics & Mathematics (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Analytical Chemistry (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Pathology (AREA)
- Hematology (AREA)
- Molecular Biology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Medicinal Chemistry (AREA)
- Food Science & Technology (AREA)
- Urology & Nephrology (AREA)
- Biophysics (AREA)
- Ecology (AREA)
- Optics & Photonics (AREA)
- Investigating Or Analysing Materials By Optical Means (AREA)
- Investigating Or Analysing Biological Materials (AREA)
Abstract
Description
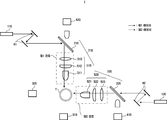
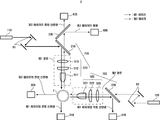
도 2는 본 발명의 일 실시예에 따른 혈구 분석 장치의 구성들이 도시된 도면이다.
도 3은 도 2의 혈구 분석 장치에 의해 조사된 제1 레이저 및 제2 레이저에 대한 산란광들의 이동 경로가 표시된 도면이다.
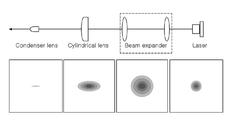
도 4는 빔 쉐이퍼에 의해 레이저의 단면 형상이 변화되는 일 예가 도시된 도면이다.
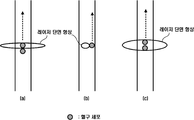
도 5는 미세관으로 조사되는 레이저 단면 형상에 따른 검출 결과가 변화되는 일 예가 도시된 도면이다.
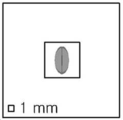
도 6은 측방 광 검출기로 입사되는 측방 산란광의 단면 형상의 일 예가 도시된 도면이다.
도 7은 본 발명의 다른 실시예에 따른 혈구 분석 장치의 구성들이 도시된 도면이다.
도 8은 본 발명의 일 실시예에 따른 혈구 분석 방법의 개략적인 흐름이 도시된 순서도이다.
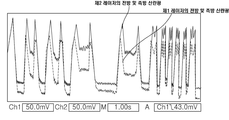
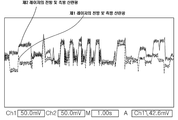
도 9 및 도 10은 본 발명에 따른 본 발명에 따른 혈구 분석 장치를 이용한 혈구 분석을 위한 신호 측정 결과를 나타내는 그래프이다.
110: 제1 레이저 발생 장치
120: 제2 레이저 발생 장치
210: 제1 색 선별 거울
220: 제2 색 선별 거울
230: 제3 색 선별 거울
310: 제1 전방 광 검출기
320: 제2 전방 광 검출기
410: 제1 측방 광 검출기
420: 제2 측방 광 검출기
510: 제1 빔 쉐이퍼
520: 제2 빔 쉐이퍼
600: 형광 검출기
Claims (15)
- 혈액 세포가 이동하는 미세관에 레이저를 조사하여 혈액 세포에 의해 산란되는 광을 측정하는 혈구 분석 장치에 있어서,
제1 레이저 발생 장치에 의해 생성된 제1 레이저가 상기 미세관에 제1 경로를 따라 조사되도록, 제1 레이저 발생 장치로부터 입사되는 상기 제1 레이저를 제1 경로로 반사시키는 제1 색 선별 거울과, 반사된 상기 제1 레이저가 미리 정해진 단면 형상으로 상기 미세관에 조사되도록, 상기 제1 경로를 따라 배열되는 제1 빔 쉐이퍼로 구성된 제1 광학계; 및
제2 레이저 발생 장치에 의해 생성되며, 상기 제1 레이저의 파장보다 높은 파장을 갖는 제2 레이저가 상기 미세관에 제2 경로를 따라 조사되도록, 상기 제2 레이저 발생 장치로부터 입사되는 상기 제2 레이저를 제2 경로로 투과시키면서, 상기 혈액 세포에 조사된 상기 제1 레이저에 대한 측방 산란광 중 상기 제2 경로로 진행하는 측방 산란광을 반사시키는 제2 색 선별 거울과, 투과된 상기 제2 레이저 및 상기 제2 경로로 진행하는 상기 제1 레이저의 측반 산란광이 미리 정해진 단면 형상을 갖도록, 상기 제2 경로를 따라 배열되는 제2 빔 쉐이퍼로 구성된 제2 광학계를 포함하는, 혈구 분석 장치.
- 제1항에 있어서,
상기 제1 빔 쉐이퍼 및 상기 제2 빔 쉐이퍼는,
빔 익스펜더(beam expander), 실린더 렌즈(cylinder lens) 및 집속 렌즈(condenser lens)를 포함하되,
상기 미세관으로부터 상기 제1 경로 또는 상기 제2 경로를 따라 상기 빔 익스펜더, 상기 실린더 렌즈 및 상기 집속 렌즈가 순차적으로 배열된 광학계인, 혈구 분석 장치.
- 제2항에 있어서,
상기 제1 색 선별 거울은 상기 제1 빔 쉐이퍼의 집속 렌즈로부터 상기 제1 경로 상의 후단에 배치되고,
상기 제2 색 선별 거울은 상기 제2 빔 쉐이퍼의 집속 렌즈로부터 상기 제2 경로 상의 후단에 배치되는, 혈구 분석 장치.
- 제2항에 있어서,
상기 미리 정해진 단면 형상은 장축이 상기 미세관의 직경보다 크고, 단축이 상기 혈액 세포의 크기보다 작은 타원형인, 혈구 분석 장치.
- 제1항에 있어서,
상기 제1 색선별 거울은,
상기 제1 경로 상에서 중첩된 상기 제1 레이저 및 상기 제2 레이저에 대한 측방 산란광을 분리시키도록, 상기 제1 레이저 발생 장치로부터 입사되는 상기 제1 레이저를 상기 제1 경로로 반사시키면서, 상기 제1 경로를 따라 입사되는 상기 제2 레이저에 대한 측방 산란광은 투과시키는, 혈구 분석 장치.
- 제1항에 있어서,
상기 제2 색선별 거울은,
상기 제2 경로 상에서 중첩된 상기 제2 레이저 및 상기 제1 레이저에 대한 측방 산란광을 분리시키도록, 상기 제2 레이저 발생 장치로부터 상기 제2 경로를 따라 입사되는 상기 제2 레이저를 투과시키면서, 상기 제2 경로를 따라 입사되는 상기 제1 레이저에 대한 측방 산란광은 반사시키는, 혈구 분석 장치.
- 제1항에 있어서,
상기 제1 경로로부터 연장되는 직선 상에 배치되어, 상기 혈액 세포에 조사된 상기 제1 레이저에 대한 전방 산란광을 측정하는 제1 전방 광 검출기; 상기 제2 경로로부터 연장되는 직선 상에 배치되어, 상기 혈액 세포에 조사된 상기 제2 레이저에 대한 전방 산란광을 측정하는 제2 전방 광 검출기;
상기 혈액 세포에 조사된 상기 제1 레이저에 대한 측방 산란광 중 상기 제2 경로로 진행하는 측방 산란광을 측정하는 제1 측방 광 검출기; 및
상기 제1 경로로부터 연장되는 직선 상에 배치되어, 상기 혈액 세포에 조사된 상기 제2 레이저에 대한 측방 산란광 중 상기 제1 경로로 진행하는 측방 산란광을 측정하는 제2 측방 광 검출기를 더 포함하는, 혈구 분석 장치.
- 제7항에 있어서,
상기 제1 측방 광 검출기 및 상기 제2 측방 광 검출기는 광전자 증폭 튜브(Photo-Multiplier Tube, PMT)이고,
상기 제1 전방 광 검출기 및 상기 제2 전방 광 검출기는 광전 다이오드(Photo-diode, PD)인, 혈구 분석 장치.
- 제1항에 있어서,
상기 제1 색 선별 거울과 상기 제2 측방 광 검출기 사이에 배치되어, 상기 혈액 세포에 조사된 상기 제2 레이저에 대한 형광 중 상기 제1 경로로 진행하는 형광을 반사시키는 제3 색 선별 거울; 및
상기 제3 색 선별 거울에 의해 반사된 형광을 측정하는 형광 검출기를 더 포함하는, 혈구 분석 장치.
- 제9항에 있어서,
상기 제3 색 선별 거울은,
상기 제1 경로를 따라 입사되는 상기 제2 레이저에 대한 측방 산란광은 투과시키면서, 상기 제1 경로를 따라 입사되는 상기 제2 레이저에 대한 형광은 반사시키는, 혈구 분석 장치.
- 제9항에 있어서,
상기 형광 검출기는 광전자 증폭 튜브(Photo-Multiplier Tube, PMT)인, 혈구 분석 장치.
- 제1항에 있어서,
상기 제1 경로와 상기 제2 경로는 동일한 2차원 평면 상에서 직교하는 경로인, 혈구 분석 장치.
- 제1항에 있어서,
상기 제1 레이저 발생 장치와 상기 제1 색 선별 거울 사이에 배치되어, 상기 제1 레이저 발생 장치에 의해 생성된 상기 제1 레이저를 반사시켜 상기 제1 색 선별 거울로 입사되도록 하는 적어도 하나의 제1 반사 미러; 및
상기 제2 레이저 발생 장치와 상기 제2 색 선별 거울 사이에 배치되어, 상기 제2 레이저 발생 장치에 의해 생성된 상기 제2 레이저를 반사시켜 상기 제2 색 선별 거울로 입사되도록 하는 적어도 하나의 제2 반사 미러를 더 포함하는, 혈구 분석 장치.
- 제1항에 기재된 혈구 분석 장치를 이용한 혈구 분석 방법에 있어서,
혈액 세포가 이동하는 미세관에 서로 다른 입사 각도를 갖는 제1 레이저 및 제2 레이저를 조사하고,
제1 경로를 따라 조사된 상기 제1 레이저에 대한 전방 산란광 및 측방 산란광을 측정하고, 상기 제1 레이저에 대한 측방 산란광 중 제2 경로를 따라 진행하는 측방 산란광과 동일한 경로를 따라 상기 미세관에 조사되는 상기 제2 레이저에 대한 전방 산란광 및 측방 산란광을 측정하며,
측정된 상기 제1 경로로부터 연장되는 방향으로 진행되는 상기 제1 레이저에 대한 전방 산란광, 상기 제2 경로를 따라 진행되는 상기 제1 레이저에 대한 측방 산란광, 상기 제2 경로로부터 연장되는 방향으로 진행되는 상기 제2 레이저에 대한 전방 산란광 및 상기 제1 경로를 따라 진행되는 상기 제2 레이저에 대한 측방 산란광에 기반하여 상기 혈액 세포의 종류를 분석하는, 혈구 분석 방법.
- 제14항에 있어서,
상기 혈액 세포로 조사된 상기 제2 레이저에 대한 형광 중 상기 제1 경로를 따라 진행하는 형광을 측정하는 것을 더 포함하고,
상기 혈액 세포의 종류를 분석하는 것은,
측정된 상기 제1 레이저에 대한 전방 산란광, 상기 제1 레이저에 대한 측방 산란광, 상기 제2 레이저에 대한 전방 산란광, 상기 제2 레이저에 대한 측방 산란광 및 상기 제2 레이저에 대한 형광 각각의 전압 크기를 기초로 상기 혈액 세포의 종류를 분석하는, 혈구 분석 방법.
Priority Applications (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020180105326A KR102122020B1 (ko) | 2018-09-04 | 2018-09-04 | 혈구 분석 장치, 이를 이용한 혈구 분석 방법 |
| PCT/KR2019/008725 WO2020050488A1 (ko) | 2018-09-04 | 2019-07-16 | 혈구 분석 장치, 이를 이용한 혈구 분석 방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020180105326A KR102122020B1 (ko) | 2018-09-04 | 2018-09-04 | 혈구 분석 장치, 이를 이용한 혈구 분석 방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20200027251A true KR20200027251A (ko) | 2020-03-12 |
| KR102122020B1 KR102122020B1 (ko) | 2020-06-12 |
Family
ID=69722019
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020180105326A Active KR102122020B1 (ko) | 2018-09-04 | 2018-09-04 | 혈구 분석 장치, 이를 이용한 혈구 분석 방법 |
Country Status (2)
| Country | Link |
|---|---|
| KR (1) | KR102122020B1 (ko) |
| WO (1) | WO2020050488A1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102861152B1 (ko) * | 2025-01-15 | 2025-09-18 | 신희원 | 바이오칩의 광 투과도 측정장치 및 측정방법 |
Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20080007473A (ko) * | 2005-04-21 | 2008-01-21 | 호리바 에이비엑스 에스.에이.에스 | 미시적 요소들의 다중매개변수 분석을 위한 기기 및 방법 |
| KR20140118864A (ko) * | 2013-03-29 | 2014-10-08 | 시스멕스 가부시키가이샤 | 입자측정장치 |
| KR101681422B1 (ko) | 2015-07-31 | 2016-11-30 | 가톨릭대학교 산학협력단 | 다수의 레이저를 사용하는 세포 분석 장치 |
| WO2017199511A1 (ja) * | 2016-05-19 | 2017-11-23 | 富士電機株式会社 | 水質分析計 |
| KR20180032080A (ko) * | 2016-09-21 | 2018-03-29 | (주)뉴옵틱스 | 혈구 분석 시스템 및 분석방법 |
| KR20180051844A (ko) | 2016-11-09 | 2018-05-17 | (주)뉴옵틱스 | 혈구 분석 시스템 및 분석방법 |
-
2018
- 2018-09-04 KR KR1020180105326A patent/KR102122020B1/ko active Active
-
2019
- 2019-07-16 WO PCT/KR2019/008725 patent/WO2020050488A1/ko not_active Ceased
Patent Citations (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20080007473A (ko) * | 2005-04-21 | 2008-01-21 | 호리바 에이비엑스 에스.에이.에스 | 미시적 요소들의 다중매개변수 분석을 위한 기기 및 방법 |
| KR20140118864A (ko) * | 2013-03-29 | 2014-10-08 | 시스멕스 가부시키가이샤 | 입자측정장치 |
| KR101681422B1 (ko) | 2015-07-31 | 2016-11-30 | 가톨릭대학교 산학협력단 | 다수의 레이저를 사용하는 세포 분석 장치 |
| WO2017199511A1 (ja) * | 2016-05-19 | 2017-11-23 | 富士電機株式会社 | 水質分析計 |
| KR20180032080A (ko) * | 2016-09-21 | 2018-03-29 | (주)뉴옵틱스 | 혈구 분석 시스템 및 분석방법 |
| KR20180051844A (ko) | 2016-11-09 | 2018-05-17 | (주)뉴옵틱스 | 혈구 분석 시스템 및 분석방법 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102861152B1 (ko) * | 2025-01-15 | 2025-09-18 | 신희원 | 바이오칩의 광 투과도 측정장치 및 측정방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102122020B1 (ko) | 2020-06-12 |
| WO2020050488A1 (ko) | 2020-03-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP5381741B2 (ja) | 光学的測定装置及び光学的測定方法 | |
| US8018592B2 (en) | Optical system for a particle analyzer and particle analyzer using same | |
| US7477363B2 (en) | Flow cytometer | |
| US20140339446A1 (en) | Scanning image flow cytometer | |
| US20230012588A1 (en) | Observation device | |
| KR101681422B1 (ko) | 다수의 레이저를 사용하는 세포 분석 장치 | |
| JP5828440B1 (ja) | 微小粒子測定装置 | |
| KR20060096982A (ko) | 입자 분류 시스템용 광학 검출기 | |
| JPWO2009098868A1 (ja) | 蛍光検出装置及び蛍光検出方法 | |
| CN111133291B (zh) | 用于落射荧光测量的光学流式细胞仪 | |
| CN115244379B (zh) | 辨别系统、辨别方法及检测系统 | |
| US9086377B2 (en) | Optical system for fluorescence detection and fine particle analyzing apparatus | |
| KR102122020B1 (ko) | 혈구 분석 장치, 이를 이용한 혈구 분석 방법 | |
| JP6129014B2 (ja) | 蛍光検出装置および蛍光検出方法 | |
| JP2003004625A (ja) | フローサイトメータ | |
| KR20230053730A (ko) | 유체 기둥 내 물체로부터의 집광 | |
| KR100860933B1 (ko) | 플로우 셀 및 이를 이용한 입자측정장치 | |
| JPS6244649A (ja) | 粒子解析装置 | |
| EP4332557B1 (en) | A system for optical inspection of a substrate using same or different wavelengths | |
| JPS62245942A (ja) | 粒子解析装置 | |
| JP2026507735A (ja) | 単一の非コヒーレント光源から発せられるビームを分割することによって蛍光及び散乱を測定する光学フローサイトメータ | |
| CN119183528A (zh) | 用于流式细胞仪的抑制元件 | |
| CN112683758A (zh) | 一种颗粒分析方法、装置及颗粒分选设备 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| A201 | Request for examination | ||
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| N231 | Notification of change of applicant | ||
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| R15-X000 | Change to inventor requested |
St.27 status event code: A-3-3-R10-R15-oth-X000 |
|
| R16-X000 | Change to inventor recorded |
St.27 status event code: A-3-3-R10-R16-oth-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-5-5-R10-R13-asn-PN2301 St.27 status event code: A-5-5-R10-R11-asn-PN2301 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 6 |
|
| R18 | Changes to party contact information recorded |
Free format text: ST27 STATUS EVENT CODE: A-5-5-R10-R18-OTH-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |