KR20200029559A - 사용된 강황 - 이의 방법 및 조성물 - Google Patents
사용된 강황 - 이의 방법 및 조성물 Download PDFInfo
- Publication number
- KR20200029559A KR20200029559A KR1020207004552A KR20207004552A KR20200029559A KR 20200029559 A KR20200029559 A KR 20200029559A KR 1020207004552 A KR1020207004552 A KR 1020207004552A KR 20207004552 A KR20207004552 A KR 20207004552A KR 20200029559 A KR20200029559 A KR 20200029559A
- Authority
- KR
- South Korea
- Prior art keywords
- turmeric
- protein
- water
- hours
- concentrate
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K36/00—Medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicines
- A61K36/18—Magnoliophyta (angiosperms)
- A61K36/88—Liliopsida (monocotyledons)
- A61K36/906—Zingiberaceae (Ginger family)
- A61K36/9066—Curcuma, e.g. common turmeric, East Indian arrowroot or mango ginger
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/185—Acids; Anhydrides, halides or salts thereof, e.g. sulfur acids, imidic, hydrazonic or hydroximic acids
- A61K31/19—Carboxylic acids, e.g. valproic acid
- A61K31/195—Carboxylic acids, e.g. valproic acid having an amino group
- A61K31/197—Carboxylic acids, e.g. valproic acid having an amino group the amino and the carboxyl groups being attached to the same acyclic carbon chain, e.g. gamma-aminobutyric acid [GABA], beta-alanine, epsilon-aminocaproic acid or pantothenic acid
- A61K31/198—Alpha-amino acids, e.g. alanine or edetic acid [EDTA]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/70—Carbohydrates; Sugars; Derivatives thereof
- A61K31/715—Polysaccharides, i.e. having more than five saccharide radicals attached to each other by glycosidic linkages; Derivatives thereof, e.g. ethers, esters
- A61K31/716—Glucans
- A61K31/718—Starch or degraded starch, e.g. amylose, amylopectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/415—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from plants
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08B—POLYSACCHARIDES; DERIVATIVES THEREOF
- C08B30/00—Preparation of starch, degraded or non-chemically modified starch, amylose, or amylopectin
- C08B30/20—Amylose or amylopectin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/30—Extraction of the material
- A61K2236/33—Extraction of the material involving extraction with hydrophilic solvents, e.g. lower alcohols, esters or ketones
- A61K2236/331—Extraction of the material involving extraction with hydrophilic solvents, e.g. lower alcohols, esters or ketones using water, e.g. cold water, infusion, tea, steam distillation or decoction
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/30—Extraction of the material
- A61K2236/39—Complex extraction schemes, e.g. fractionation or repeated extraction steps
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/50—Methods involving additional extraction steps
- A61K2236/51—Concentration or drying of the extract, e.g. Lyophilisation, freeze-drying or spray-drying
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2236/00—Isolation or extraction methods of medicinal preparations of undetermined constitution containing material from algae, lichens, fungi or plants, or derivatives thereof, e.g. traditional herbal medicine
- A61K2236/50—Methods involving additional extraction steps
- A61K2236/53—Liquid-solid separation, e.g. centrifugation, sedimentation or crystallization
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Natural Medicines & Medicinal Plants (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Rheumatology (AREA)
- General Chemical & Material Sciences (AREA)
- Botany (AREA)
- Molecular Biology (AREA)
- Biotechnology (AREA)
- Mycology (AREA)
- Microbiology (AREA)
- Medical Informatics (AREA)
- Alternative & Traditional Medicine (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Immunology (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Pain & Pain Management (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Genetics & Genomics (AREA)
- Gastroenterology & Hepatology (AREA)
- Polymers & Plastics (AREA)
- Materials Engineering (AREA)
- Biophysics (AREA)
- Medicines Containing Plant Substances (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Medicinal Preparation (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
Abstract
Description
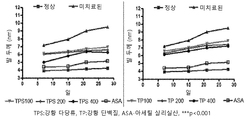
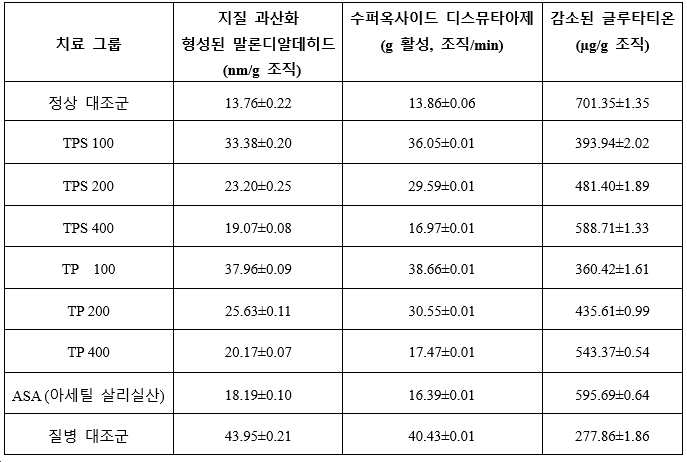
도 2는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 두께의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 3은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 부종의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 4는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여함으로써 유도된 (발 두께 및 부종의 감소에 의해 측정된) 쥐의 발의 염증을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
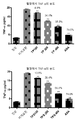
도 5는 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여한 후 혈청 염증 마커 IL-6을 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
도 6은 결핵균(Mycobacterium tuberculosis)(쥐에서 보강제 유도된 류마티스 관절염)을 함유하는 완전 보강제를 투여한 후 혈청 염증 마커 TNF-α를 감소시키는 28일 치료 후의 사용된 강황 다당류와 사용된 강황 당단백질의 유효 농도(100 mg/kg 체중, 200mg/kg 체중 및 400mg/kg 체중)의 비교적인 능력을 그래프로 도시한다.
Claims (12)
- 사용된 강황(spent turmeric)의 물 추출(water extraction) 방법으로서,
상기 방법은,
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(total dissolved solid, TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화(powdering) 및 체질(sieving)하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질(hydrophobic protein)과 함께 발생하는 것인, 단계;
를 포함하는 것인, 사용된 강황의 물 추출 방법.
- 사용된 강황의 물 추출 방법으로서,
상기 방법은,
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린(decanting) 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적(soaking volume)의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드(curcuminoid) 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계;
를 포함하는 것인, 사용된 강황의 물 추출 방법.
- 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 포유류의 염증을 치료하여 염증 감소 효과를 발생시키는 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 포유류의 류마티스 관절염을 치료하여, 통증, 종창, 부종을 포함하는 포유류의 류마티스 관절염 증상을 감소시키고, IL-6 및 TNF-α의 혈청 마커를 감소시키는 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 포유류의 류마티스 관절염을 치료하여, 통증, 종창, 부종을 포함하는 포유류의 류마티스 관절염 증상을 감소시키고, IL-6 및 TNF-α의 혈청 마커를 감소시키는 효과를 발생시키는 방법으로서,
상기 방법은 사용된 강황 단백질 또는 사용된 강황 전분의 유효량을 상기 포유류에 투여하는 단계를 포함하고, 상기 단백질 및 전분은 하기 단계를 포함하는 공정에 의해 수득되는 것인, 방법:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 사용된 강황 재료로부터 수득된 단백질 조성물로서,
상기 단백질 조성물은 하기 단계를 포함하는 사용된 강황의 물 추출에 의해 수득되는 것인, 단백질 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계; 및
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계.
- 사용된 강황 재료로부터 수득된 단백질 조성물로서,
상기 단백질 조성물은 하기 단계를 포함하는 사용된 강황의 물 추출에 의해 수득되는 것인, 단백질 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계; 및
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계.
- 소수성 단백질을 갖는 다당류를 포함하는 다당류 조성물로서,
상기 조성물은 하기 단계를 포함하는 공정을 통해 사용된 강황으로부터 수득되는 것인, 다당류 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계; 및
c) 고진공 하에서 20%의 총 용존 고형물(TDS)로 단계 b)의 여과액을 농축시킨 후, 100 L/hour의 유속으로 120 ℃에서 분무 건조하여 단백질(당단백질) 분말을 수득하는 단계; 및
d) 단계 c)의 단백질이 없는 단계 a)의 사용된 강황 재료-2를 24시간 동안 120 ℃에서 건조시킨 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 소수성 단백질을 갖는 다당류를 포함하는 다당류 조성물로서,
상기 조성물은 하기 단계를 포함하는 공정을 통해 사용된 강황으로부터 수득되는 것인, 다당류 조성물:
a) 6시간 동안 온도 65 ℃에서 가끔 교반하면서, 사용된 강황과 물의 비율이 약 1:10 내지 약 1:50이고, 가장 바람직한 비율이 1:10이 되도록 사용된 강황을 물로 추출하여, 사용된 강황과 사용된 강황 재료-2의 물 추출물을 수득하는 단계;
b) 단계 a)의 물 추출물을 원심분리하여, 모래 또는 먼지 입자를 포획하여 투명한 여과액을 수득하는 단계;
c) 고진공 하에서 60 ℃에서 단계 b)의 여과액을 농축시켜 농축물을 수득하고, 상기 농축물을 추가로 냉각하는 단계;
d) 유기 용매와 농축물, 바람직한 양태에서 아세톤과 농축물의 비율이 1:2가 되도록 단계 c)의 농축물에 유기 용매, 바람직한 양태에서 아세톤을 첨가한 후, 가끔 교반하면서 4시간 동안 실온에서 배양하여, 아세톤 침전된 단백질을 형성하고, 단백질 침전물을 그 위에 상청액이 있도록 완전히 침강시키는 단계;
e) 상기 단백질 침전물을 파괴하지 않으면서 단계 d)의 상청액을 따라 버린 후, 여과하고, 침전물을 아세톤으로 세척하여 수분을 제거하고, 다시 여과하는 단계;
f) 고진공 하에서 60 ℃에서 즉시 단계 e)의 단백질 침전물을 건조시켜 미세한 단백질(당단백질) 분말을 수득하는 단계;
g) 단계 f)의 단백질이 없는 단계 a)의 사용된 강황 재료-2에 각각 46 ℃ 및 30 ℃에서 4시간 동안 담금 체적의 아세톤 및 메탄올로 세척하여, 미량의 커큐미노이드 및 옥살산 함량을 제거하여 세척된 사용된 강황 재료-2를 형성하는 단계; 및
h) 24시간 동안 단계 g)의 세척된 사용된 강황 재료-2를 건조시켜 잔여 용매를 제거한 후, 분말화 및 체질하여 강황 전분(다당류)을 수득하는 단계로, 상기 다당류는 소수성 단백질과 함께 발생하는 것인, 단계.
- 식물 단백질 조성물로서,
상기 단백질 조성물은 사용된 강황으로부터 수득되고,
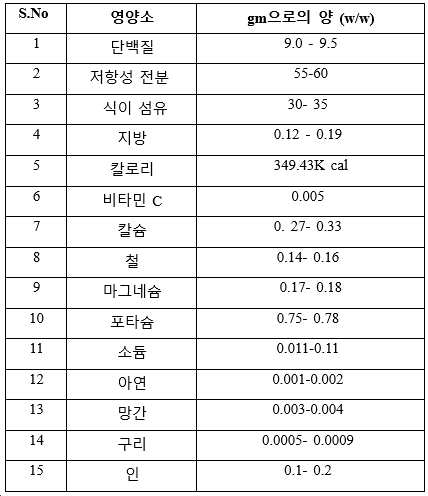
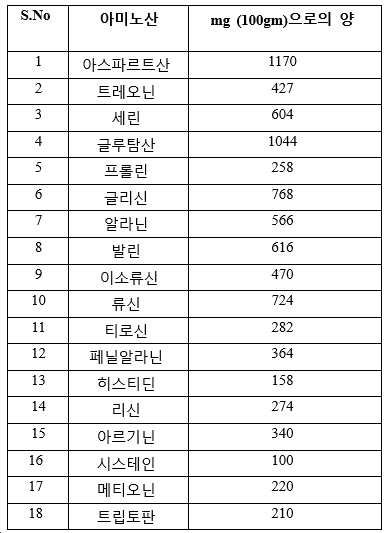
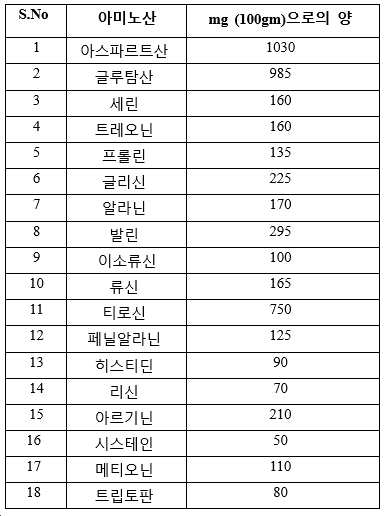
상기 단백질 조성물은 속도 제한 아미노산(rate limiting aminoacid) 시스테인 및 메티오닌을 포함하는 것을 특징으로 하는 것인, 식물 단백질 조성물.
- 식물 다당류 조성물(전분)으로서,
상기 다당류 조성물은 사용된 강황으로부터 수득되고,
α, 1-4 결합(아밀로오스) 및 α, 1-6 결합(아밀로펙틴)에 의해 연결된 90%의 글루코오스 잔기를 갖는 저항성 전분(resistant starch)으로서 소수성 당단백질과 함께 발생하는 것을 특징으로 하는 것인, 식물 다당류 조성물.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020227009200A KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN201741026215 | 2017-07-24 | ||
| IN201741026215 | 2017-07-24 | ||
| PCT/US2018/042390 WO2019022991A1 (en) | 2017-07-24 | 2018-07-17 | CURCUMA RESIDUES - METHODS AND COMPOSITIONS THEREOF |
Related Child Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227009200A Division KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20200029559A true KR20200029559A (ko) | 2020-03-18 |
Family
ID=65039792
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020207004552A Ceased KR20200029559A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
| KR1020227009200A Ceased KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227009200A Ceased KR20220041945A (ko) | 2017-07-24 | 2018-07-17 | 사용된 강황 - 이의 방법 및 조성물 |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US11298395B2 (ko) |
| EP (1) | EP3658161A4 (ko) |
| JP (1) | JP7209691B2 (ko) |
| KR (2) | KR20200029559A (ko) |
| AU (1) | AU2018307222B2 (ko) |
| CA (1) | CA3071190C (ko) |
| WO (1) | WO2019022991A1 (ko) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102237450B1 (ko) * | 2019-08-30 | 2021-04-06 | 한국식품연구원 | 강황잎 추출물을 유효성분으로 포함하는 장기능 개선용 조성물 |
| WO2021124246A1 (en) * | 2019-12-19 | 2021-06-24 | Arjuna Natural Private Limited | Resistant starch composition from natural sources and their preparation |
| CN116606385B (zh) * | 2023-04-28 | 2024-04-16 | 广州工程技术职业学院 | 莪术多糖及其制备方法和应用 |
Family Cites Families (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPS6067428A (ja) * | 1983-09-22 | 1985-04-17 | Takuo Kosuge | 蛋白結合多糖体,その製造法,及び該蛋白結合多糖体を有効成分とする抗腫瘍剤 |
| WO1996003999A1 (es) * | 1994-08-03 | 1996-02-15 | A.S.A.C. Pharmaceutical International, A.I.E. | Procedimiento para la obtencion de extractos apolares y polares de curcuma y aplicaciones de los mismos |
| US20020018787A1 (en) | 1999-05-21 | 2002-02-14 | Roger V. Kendall | Methods and compositions for modulating immune response and for the treatment of inflammatory disease |
| ES2154610B1 (es) | 1999-09-23 | 2001-11-16 | Asac Compania De Biotecnologia | Nuevas actividades farmacologicas de los extractos de curcuma longa. |
| JPWO2004104036A1 (ja) | 2003-05-21 | 2006-10-26 | 不二製油株式会社 | 大豆ホエー蛋白及び大豆ホエー蛋白分解物の製造法 |
| US7205011B2 (en) * | 2003-11-14 | 2007-04-17 | Board Of Regents, Acting For And On Behalf Of, University Of Arizona | Anti-inflammatory activity of a specific turmeric extract |
| US7070816B2 (en) * | 2003-12-05 | 2006-07-04 | New Chapter, Inc. | Methods for treating prostatic intraepithelial neoplasia with herbal compositions |
| US20170042833A1 (en) * | 2014-03-12 | 2017-02-16 | Benny Antony | Formulation of Curcuminoids with Enhanced Bioavailability of Curcumin, Demethoxycurcumin, Bisdemethoxycurcumin and method of preparation and uses thereof |
| AU2007227397A1 (en) | 2006-03-17 | 2007-09-27 | Herbalscience Singapore Pte. Ltd. | Extracts and methods comprising curcuma species |
| TWI320714B (en) | 2006-09-15 | 2010-02-21 | Dev Center Biotechnology | Plant extracts for the treatment of rheumatoid arthritis |
| TWI504394B (zh) | 2011-04-29 | 2015-10-21 | Ind Tech Res Inst | 安托芬之製備方法 |
| US9345258B2 (en) | 2011-08-25 | 2016-05-24 | Natural Remedies Pvt Ltd. | Synergistic phytochemical composition and a process for preparation thereof |
| US20140010903A1 (en) * | 2012-07-04 | 2014-01-09 | Akay Flavours & Aromatics Pvt Ltd. | Curcuminoid composition with enhanced bioavailability and a process for its preparation |
| KR101495991B1 (ko) * | 2013-03-22 | 2015-02-26 | 한규호 | 울금의 커큐민을 제거한 울금 잔사를 포함하는 식욕억제 및 비만의 예방 또는 치료용 조성물 |
| EP3035947A4 (en) * | 2013-08-19 | 2018-09-26 | Aurea Biolabs Private Limited | A novel composition of curcumin with enhanced bioavailability |
| US10323227B2 (en) * | 2014-08-29 | 2019-06-18 | Sami Labs Limited | Process for enhancing the viable counts of lactic acid bacteria and useful compositions thereof |
| US20160256513A1 (en) * | 2015-03-04 | 2016-09-08 | The Synergy Company of Utah, LLC d/b/a Synergy Production Laboratories | Synergized turmeric |
| WO2017195220A1 (en) * | 2016-05-11 | 2017-11-16 | Deshpande Rajendra Sham | Process for extraction of curcuminoids |
-
2018
- 2018-07-17 KR KR1020207004552A patent/KR20200029559A/ko not_active Ceased
- 2018-07-17 KR KR1020227009200A patent/KR20220041945A/ko not_active Ceased
- 2018-07-17 CA CA3071190A patent/CA3071190C/en active Active
- 2018-07-17 WO PCT/US2018/042390 patent/WO2019022991A1/en not_active Ceased
- 2018-07-17 EP EP18838837.5A patent/EP3658161A4/en active Pending
- 2018-07-17 JP JP2020503985A patent/JP7209691B2/ja active Active
- 2018-07-17 US US16/632,953 patent/US11298395B2/en active Active
- 2018-07-17 AU AU2018307222A patent/AU2018307222B2/en not_active Ceased
Also Published As
| Publication number | Publication date |
|---|---|
| CA3071190A1 (en) | 2019-01-31 |
| EP3658161A1 (en) | 2020-06-03 |
| WO2019022991A1 (en) | 2019-01-31 |
| EP3658161A4 (en) | 2021-04-21 |
| AU2018307222B2 (en) | 2022-02-24 |
| KR20220041945A (ko) | 2022-04-01 |
| JP7209691B2 (ja) | 2023-01-20 |
| JP2021509660A (ja) | 2021-04-01 |
| AU2018307222A1 (en) | 2020-03-05 |
| US11298395B2 (en) | 2022-04-12 |
| CA3071190C (en) | 2023-02-14 |
| US20200164019A1 (en) | 2020-05-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Chen et al. | Preparation, characterization and anti-diabetic activity of polysaccharides from adlay seed | |
| Ravikumar et al. | Hepatoprotective and antioxidant activity of a mangrove plant Lumnitzera racemosa | |
| Wen et al. | Advantages of the polysaccharides from Gracilaria lemaneiformis over metformin in antidiabetic effects on streptozotocin-induced diabetic mice | |
| Samal et al. | Isolation, preliminary characterization and hepatoprotective activity of polysaccharides from Tamarindus indica L. | |
| KR20200029559A (ko) | 사용된 강황 - 이의 방법 및 조성물 | |
| Zhang et al. | Recent developments in stigma maydis polysaccharides: Isolation, structural characteristics, biological activities and industrial application | |
| Savych et al. | Antioxidant activity in vitro of antidiabetic herbal mixtures | |
| AU2012338742B2 (en) | Composition comprising chicory extract | |
| CN111671765A (zh) | 一种褐藻膳食纤维在制备治疗或预防代谢综合症的药品、食品和/或保健品中的应用 | |
| Chowdhury et al. | The potential role of mushrooms in the prevention and treatment of diabetes: a review | |
| CN104689251B (zh) | 一种缓解化学性肝损伤的中药组合物、其制备方法及中药制剂 | |
| Shailajan et al. | Effect of Asteracantha longifolia Nees. against CCl4 induced liver dysfunction in rat | |
| Peng et al. | Extraction, characterization, and antioxidant activity of Eucommia ulmoides polysaccharides | |
| Chien et al. | Dihydromyricetin-rich herbal mixture extracts as a potential prescription for treatment of metabolic syndrome in rats fed a high-fat diet and subacute toxicity assessment in rats | |
| JP2965490B2 (ja) | 霊芝エキスの抽出法 | |
| Huang et al. | Antidiabetic effect of a new peptide from Squalus mitsukurii liver (S‐8300) in streptozocin‐induced diabetic mice | |
| JP2005068112A (ja) | マイタケ由来の抽出物およびグリコプロテイン並びにその製造方法 | |
| Kavishankar et al. | Hepatoprotective and antioxidant activity of N-Trisaccharide in different experimental rats | |
| CA2515607A1 (en) | Use of lupinus albus conglutin gamma for the treatment of type ii diabetes | |
| Ojo et al. | Ameliorative potentials of Saponins from Helianthus annuus roots on hepatoprotective and some kidney function indices of alloxan-induced diabetic rats | |
| El-Batal et al. | Ameliorating effect of yeast Glucan with zinc Bisglycinate in Histological and Biochemical changes in γ-irradiated rats | |
| Gara et al. | Inhibition of key digestive enzymes related to diabetes and protection of β-cell and liver-kidney functions by Hypnea spinella sulfated polysaccharide in diabetic rats | |
| CN113880962A (zh) | 一种无花果多糖及其提取方法和应用 | |
| CN111758830A (zh) | 降血脂抗氧化压片糖果 | |
| JP2009126856A (ja) | 血中中性脂肪上昇抑制剤 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| AMND | Amendment | ||
| PA0105 | International application |
Patent event date: 20200217 Patent event code: PA01051R01D Comment text: International Patent Application |
|
| PA0201 | Request for examination | ||
| PG1501 | Laying open of application | ||
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
Comment text: Notification of reason for refusal Patent event date: 20210621 Patent event code: PE09021S01D |
|
| AMND | Amendment | ||
| E601 | Decision to refuse application | ||
| PE0601 | Decision on rejection of patent |
Patent event date: 20220106 Comment text: Decision to Refuse Application Patent event code: PE06012S01D Patent event date: 20210621 Comment text: Notification of reason for refusal Patent event code: PE06011S01I |
|
| X091 | Application refused [patent] | ||
| AMND | Amendment | ||
| PX0901 | Re-examination |
Patent event code: PX09011S01I Patent event date: 20220106 Comment text: Decision to Refuse Application Patent event code: PX09012R01I Patent event date: 20210923 Comment text: Amendment to Specification, etc. Patent event code: PX09012R01I Patent event date: 20200217 Comment text: Amendment to Specification, etc. |
|
| PX0601 | Decision of rejection after re-examination |
Comment text: Decision to Refuse Application Patent event code: PX06014S01D Patent event date: 20220215 Comment text: Amendment to Specification, etc. Patent event code: PX06012R01I Patent event date: 20220207 Comment text: Decision to Refuse Application Patent event code: PX06011S01I Patent event date: 20220106 Comment text: Amendment to Specification, etc. Patent event code: PX06012R01I Patent event date: 20210923 Comment text: Notification of reason for refusal Patent event code: PX06013S01I Patent event date: 20210621 Comment text: Amendment to Specification, etc. Patent event code: PX06012R01I Patent event date: 20200217 |
|
| X601 | Decision of rejection after re-examination | ||
| PA0104 | Divisional application for international application |
Comment text: Divisional Application for International Patent Patent event code: PA01041R01D Patent event date: 20220318 |