본 명세서에서 사용하는 「절대적」이라는 용어는, 「상대적」의 반대어로서 사용되는 용어로서, 측정 조건에 따라 값이 좌우되기 어렵다는 것을 의미한다. 또한, 측정 조건이 변화되어도 값이 전혀 변화되지 않는다는 것을 의미하는 것이 아니라, 측정 조건이 변화되었다 하더라도 본 발명의 목적을 달성하기에는 충분한 정밀도의 값을 얻을 수 있다는 것을 의미한다.
[어레이]
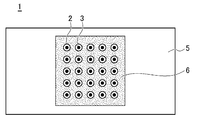
본 발명의 어레이에 대하여, 도 1, 2를 이용하여 설명한다.
도 1에 나타낸 바와 같이, 본 발명의 어레이(1)는, 기판(5)과, 기판(5)상의 소수성 피막(6)을 포함한다. 소수성 피막(6)에는, 관통공(2)이 복수 설치되어 있고, 관통공(2)은, 기판(5)에 달하여 있다.
여기서, 기판(5)은, 후술하는 핵산의 탑재, 진핵세포의 탑재, 리간드의 적용, 리간드에 대한 활성화도의 측정에서, 핸들링할 수 있는 정도의 강도를 가진 재료, 예를 들면 25℃에서의 영률이 0.01GPa 이상 1000GPa 이하의 재료를 사용할 수 있고, 메커니컬 핸드(로봇 핸드)가 취급하기 쉬운 1 이상 500GPa 이하의 재료를 바람직하게 사용할 수 있다.
또한 기판(5)은, 후술하는 핵산의 탑재, 진핵세포의 탑재, 리간드의 적용에 있어서, 화학적, 생물학적으로 저해 작용을 나타내지 않는 것이 바람직하며, 석영 유리, 붕규산 유리, 소다알루미노실리케이트 유리(화학강화유리를 포함한다), 바륨붕규산 유리, 소다석회 유리로 예시되는 유리나 세라믹, 폴리카보네이트, 폴리메틸메타크릴레이트, 폴리스티렌, 지환식 폴리올레핀, 폴리메틸펜텐 등의 각종 합성수지를 예시할 수 있다. 이 중, 합성 수지에 관해서는, 상술한 화학적, 생물학적 저해 작용을 나타내지 않도록 유의하면, 예를 들면 첨가제의 작용에 유의하면, 열가소성 수지, 열경화성 수지, 방사선 경화 수지(자외선, 전자선의 예를 포함함)도 사용하는 것이 가능하다. 일례로서는, 붕규산 유리를 사용한 슬라이드 글래스가 있다.
기판(5)은, 플라스마 처리, 오존 처리, 이온 처리, 방사선 처리 등의 표면 활성화 처리에 의해, 기판(5) 표면을 친수화 할 수 있다.
기판(5)의 크기에 제한은 없으나, 전형적으로는 100mm각(角) 이하이면, 사람에 의한 조작, 기계 조작 모두 취급이 쉬워, 바람직하다. 또한, 기판(5)의 두께에 제한은 없으나, 전형적으로는 0mm를 넘고 10mm 이하이면, 사람에 의한 조작, 기계 조작 모두 취급하기 쉬워, 바람직하다.
소수성 피막(6)은, 후술하는 진핵세포 탑재시에, 진핵세포를 적당히 밀어내, 진핵세포를 소수성 피막(6) 내의 관통공(2)에 수납되기 쉽게 하는 작용을 갖는다. 즉, 소수성 피막(6)은, 적당한 소수성을 갖고 있으며, 이러한 소수성은, 소수성 피막(6)의 관통공(2) 이외의 평면 부분에서의 접촉각(°)으로 정의할 수 있다.
소수성 피막(6)의 접촉각은, 23℃의 물을 사용한 경우에, 70° 이상 175° 이하가 바람직하다. 즉 발수성, 초발수성이라 불리는 접촉각을 나타내는 피막도 포함된다. 본 발명의 소수성 피막(6)의 접촉각은, 전형적으로는, 75° 이상, 80° 이상, 90° 이상, 100° 이상, 110° 이상, 120° 이상, 130° 이상, 135° 이상, 140° 이상, 145° 이상, 150° 이상, 155° 이상, 160° 이상, 165° 이상, 170° 이상이다. 또한, 전형적으로는, 170° 이하, 165° 이하, 160° 이하, 155° 이하, 150° 이하, 145° 이하, 140° 이하, 135° 이하, 130° 이하, 120° 이하, 110° 이하, 100° 이하, 90° 이하, 80° 이하이다.
본 발명의 일 실시형태에 있어서, 소수성 피막(6)의 접촉각은, 23℃의 물을 사용한 경우에, 130° 이상 165° 이하이다.
이러한 접촉각을 갖는 소수성 피막(6)의 구체적인 예로서는, 실리콘계 수지, 불소계 수지, 실리콘-불소계 수지를 사용할 수 있다. 또한, 폴리에틸렌글리콜(PEG) 등의 지방족 탄화수소, 또는 방향족 탄화수소에 대하여, 소수성기를 도입한 유도체도 사용할 수 있다.
또한, 열가소성 수지, 열경화성 수지, 방사선 경화 수지(자외선, 전자선의 예를 포함함)에 대하여, 실리콘계 실란 커플링제나 불소계 실란 커플링제를 작용시킨 수지도 사용할 수 있다(작용이란, 공중합이나, 표면 석출, 표면 코팅을 포함한다). 소수성 피막(6)은, 후술하는 핵산의 탑재, 진핵세포의 탑재, 리간드 적용에 있어서, 화학적, 생물학적으로 저해 작용을 나타내지 않는 것이 바람직하게 사용된다.
소수성 피막(6)의 두께에 제한은 없으나, 후술하는 핵산, 및 진핵세포의 탑재를 양호하게 실시할 수 있다는 점에서, 1㎛ 이상 200㎛ 이하인 것이 바람직하다. 특히 탑재한 진핵세포가, 외부 환경의 진동에 의해 탈리되지 않도록, 10㎛ 이상 200㎛ 이하가 바람직하다. 또한 탑재한 진핵세포가, 외부 환경의 진동이나 온도 변화 등의 외란에 의해, 관통공(2) 밖으로 이동되지 않도록, 25㎛ 이상 200㎛ 이하가 바람직하다. 전형적으로는, 30㎛ 이상, 35㎛ 이상, 40㎛ 이상, 45㎛ 이상, 50㎛ 이상, 55㎛ 이상, 60㎛ 이상이다. 또한, 전형적으로는, 180㎛ 이하, 160㎛ 이하, 140㎛ 이하, 120㎛ 이하, 100㎛ 이하, 80㎛ 이하이다.
소수성 피막(6)은, 오프셋 인쇄, 패드 인쇄, 스크린 인쇄, 잉크젯 프린트 등의 소수성 피막(6)의 도막과, 관통공(2)을 동시에 작성하는 방법으로 작성할 수 있고, 소수성 피막(6)을 전체면에 도포한 후에, 관통공(2)을, 리소그래피 수법으로 작성할 수도 있다. 오프셋 인쇄, 패드 인쇄의 경우에는, 1㎛ 이상 10㎛ 이하의 두께, 스크린 인쇄의 경우에는, 20㎛ 이상 70㎛ 이하의 두께를 작성하는데 적합하다.
소수성 피막(6)이 기판(5)을 피복하는 범위는, 모든 관통공(2)이 배치된 영역을 덮을 수 있는 범위 이상이면 특별히 제한되지 않으며, 어레이(1)에서, 기판(5)의 전체면을 피복하는 것일 수도 있다. 예를 들면, 도 1에 나타낸 바와 같이, 관통공(2) 모두를 덮으면서, 어레이(1)의 주연부(周緣部)는 기판(5)이 노출되도록 형성할 수 있다.
어레이(1)의 관통공(2)에는, 소정의 수용체를 형성할 수 있는 핵산(3)이, 기판(5)에 접해 탑재되어 있다. 여기서, 핵산(3)은, 소정의 수용체를 코드하는 유전자를 포함하는 핵산을 포함하고 있다. 어레이(1)에 탑재되어, 기판(5)에 접하는 핵산(3)은 복수이고, 어레이(1)의 관통공(2) 각각에 핵산(3)이 탑재되어 있다. 예를 들면 소정의 수용체를 코드하는 유전자를 포함하는 핵산(3)이, 관통공(2)마다, 각각 다른 종류의 핵산(3)이 탑재되어 있을 수 있다.
여기서, 수용체란, 이른바 막관통형 수용체를 가리키며, 대사형 수용체, 이온 채널형 수용체를 포함한다.
대사형 수용체의 예로서는, G단백질 공역형 수용체, 티로신 키나아제 수용체, 구아닐산 고리화효소(guanylate cyclase) 수용체가 있다.
G단백질 공역형 수용체의 예로서는, 후각 수용체, 무스카린성 아세틸콜린 수용체, 아데노신 수용체, 아드레날린 수용체, GABA 수용체(B형), 앤지오텐신 수용체, 칸나비노이드 수용체, 콜레키스토키닌 수용체, 도파민 수용체, 글루카곤 수용체, 히스타민 수용체, 오피오이드 수용체, 세크레틴 수용체, 세로토닌 수용체, 가스트린 수용체, P2Y 수용체, 로돕신이 있다.
티로신 키나아제 수용체의 예로서는, 인슐린 수용체, 세포증식인자의 수용체, 사이토카인의 수용체가 있다.
구아닐산 고리화효소 수용체의 예로서는, GC-A, GC-B, GC-C가 있다.
이온 채널형 수용체의 예로서는, 니코틴성 아세틸콜린 수용체, 글리신 수용체, GABA 수용체(A형, C형), 글루타민산 수용체, 세로토닌 수용체 3형, 이노시톨트리스인산(IP3) 수용체, 리아노딘 수용체, P2X 수용체가 있다.
상술한 핵산에 포함되는 유전자에 의해 코드되는 수용체의 유래는, 본 발명의 효과를 발휘하는 범위에 한해서 특별히 한정되지 않는다. 예를 들면, 동물 유래, 포유류 유래, 마우스 유래, 영장류 유래, 또는 인간 유래를 들 수 있다.
본 발명의 어레이(1)의 관통공(2)에 탑재되는 핵산(3)은, 본 발명의 효과를 발휘하는 범위에 한해서 특별히 한정되지 않는다. 구체적으로는, DNA, RNA, PNA 등을 예시할 수 있다.
핵산(3)은, 진핵세포에 핵산(3)을 도입하기 위해 사용되는 지질, 폴리머, 바이러스 또는 자기입자(磁氣粒子)를 더 포함할 수 있다. 예를 들면, 후술하는 플라스미드, 유전자 도입 시약을 포함할 수 있다. 또한, 진핵세포와 기판(5)과의 접착성을 높이기 위한, 세포 접착을 촉진하는 화합물을 포함할 수 있다.
본 발명의 어레이(1)의 관통공(2) 내부에 탑재되는 핵산(3)은, 예를 들면, 인간 유래의 후각 수용체라면, 다음에 나타내는 NCBI의 액세션 번호로 특정되는 404개의 유전자를 들 수 있다.
KP290534.1, NG_002151.2, NG_004125, NG_004272.4, NG_004652.2, NM_001001656, NM_001001657, NM_001001658, NM_001001659, NM_001001667, NM_001001674, NM_001001821, NM_001001824, NM_001001827.1, NM_001001912.2, NM_001001913, NM_001001914, NM_001001915, NM_001001916.2, NM_001001917.2, NM_001001918, NM_001001919, NM_001001920, NM_001001921, NM_001001922.2, NM_001001923, NM_001001952, NM_001001953.1, NM_001001954, NM_001001955.2, NM_001001956, NM_001001957, NM_001001957.2, NM_001001958.1, NM_001001959, NM_001001960.1, NM_001001961, NM_001001963.1, NM_001001964.1, NM_001001965, NM_001001966, NM_001001967, NM_001001968, NM_001002905.1, NM_001002907.1, NM_001002917.1, NM_001002918.1, NM_001002925, NM_001003443.2, NM_001003745.1, NM_001003750.1, NM_001004052.1, NM_001004058.2, NM_001004059.2, NM_001004063.2, NM_001004064.1, NM_001004124.2, NM_001004134.1, NM_001004135, NM_001004136.1, NM_001004137, NM_001004195.2, NM_001004297.2, NM_001004450, NM_001004451.1, NM_001004452.1, NM_001004453.2, NM_001004454.1, NM_001004456.1, NM_001004457, NM_001004458.1, NM_001004459.1, NM_001004460.1, NM_001004461, NM_001004461.1, NM_001004462, NM_001004462.1, NM_001004463.1, NM_001004464.1, NM_001004465, NM_001004466, NM_001004467.1, NM_001004469, NM_001004471.2, NM_001004472, NM_001004473, NM_001004474, NM_001004475, NM_001004476, NM_001004477, NM_001004478, NM_001004479, NM_001004480, NM_001004481, NM_001004482, NM_001004483, NM_001004484, NM_001004484, NM_001004485, NM_001004486, NM_001004487, NM_001004488, NM_001004489.2, NM_001004490, NM_001004491, NM_001004491.1, NM_001004492, NM_001004684, NM_001004685, NM_001004686, NM_001004686.2, NM_001004687, NM_001004688, NM_001004689, NM_001004690, NM_001004691, NM_001004692, NM_001004693, NM_001004694.2, NM_001004695, NM_001004696, NM_001004697, NM_001004698.2, NM_001004699.2, NM_001004700.2, NM_001004701.2, NM_001004702.1, NM_001004703.1, NM_001004704.1, NM_001004705, NM_001004706.1, NM_001004707.3, NM_001004708, NM_001004711, NM_001004712, NM_001004713.1, NM_001004714, NM_001004715, NM_001004717, NM_001004719, NM_001004723.2, NM_001004724, NM_001004725, NM_001004726, NM_001004727.1, NM_001004728, NM_001004729, NM_001004730.1, NM_001004731, NM_001004733.2, NM_001004734, NM_001004735, NM_001004736.3, NM_001004737, NM_001004738.1, NM_001004739, NM_001004740, NM_001004741.1, NM_001004742.2, NM_001004743, NM_001004744.1, NM_001004745.1, NM_001004746.1, NM_001004747.1, NM_001004748.1, NM_001004749.1, NM_001004750.1, NM_001004751, NM_001004752.1, NM_001004753, NM_001004754.0, NM_001004755.1, NM_001004756.2, NM_001004757.2, NM_001004758.1, NM_001004759.1, NM_001004760, NM_001005160, NM_001005161.3, NM_001005162.2, NM_001005163, NM_001005164.2, NM_001005165, NM_001005167, NM_001005168, NM_001005169, NM_001005170.2, NM_001005171.2, NM_001005172.2, NM_001005173.3, NM_001005174, NM_001005175.3, NM_001005177.3, NM_001005178, NM_001005179.2, NM_001005180.2, NM_001005181, NM_001005181.2, NM_001005182, NM_001005182, NM_001005183, NM_001005184, NM_001005185, NM_001005186.2, NM_001005187, NM_001005188, NM_001005189, NM_001005190.1, NM_001005191.2, NM_001005192.2, NM_001005193, NM_001005194.1, NM_001005195.1, NM_001005196.1, NM_001005197.1, NM_001005198.1, NM_001005199.1, NM_001005200.1, NM_001005201.1, NM_001005202.1, NM_001005203.2, NM_001005204, NM_001005205.2, NM_001005211, NM_001005212.3, NM_001005213, NM_001005216.3, NM_001005218.1, NM_001005222, NM_001005222.2, NM_001005224, NM_001005226.2, NM_001005234.1, NM_001005235, NM_001005236.3, NM_001005237.1, NM_001005238, NM_001005239, NM_001005240, NM_001005241.3, NM_001005243, NM_001005245, NM_001005270.4, NM_001005272.3, NM_001005274.1, NM_001005275.1, NM_001005276, NM_001005278, NM_001005279, NM_001005280.1, NM_001005281, NM_001005282, NM_001005283.2, NM_001005284, NM_001005285, NM_001005286, NM_001005287, NM_001005288, NM_001005288.2, NM_001005289, NM_001005323, NM_001005324, NM_001005325, NM_001005326, NM_001005327.2, NM_001005328, NM_001005329, NM_001005329.1, NM_001005334, NM_001005338, NM_001005465.1, NM_001005466.2, NM_001005467.1, NM_001005468.1, NM_001005469, NM_001005470.1, NM_001005471, NM_001005479.1, NM_001005480.2, NM_001005482, NM_001005483, NM_001005484, NM_001005484, NM_001005486, NM_001005487.1, NM_001005489, NM_001005489, NM_001005490, NM_001005490.1, NM_001005491.1, NM_001005492, NM_001005493, NM_001005494, NM_001005495, NM_001005496, NM_001005497, NM_001005499, NM_001005500, NM_001005501, NM_001005503, NM_001005504, NM_001005504, NM_001005512.2, NM_001005513.1, NM_001005514, NM_001005515, NM_001005516, NM_001005517, NM_001005518, NM_001005519.2, NM_001005522, NM_001005566.2, NM_001005567, NM_001005853, NM_001013355.1, NM_001013356.2, NM_001013357.1, NM_001013358.2, NM_001079935, NM_001146033.1, NM_001160325, NM_001197287, NM_001258283, NM_001258284, NM_001258285, NM_001291438.1, NM_001317107.1, NM_001348224.1, NM_001348266.1, NM_001348271.1, NM_001348273.1, NM_001348286.1, NM_002548.2, NM_002550.2, NM_002551.3, NM_003552.3, NM_003553.2, NM_003554.2, NM_003555, NM_003696.2, NM_003697, NM_003700, NM_006637, NM_007160.3, NM_012351.2, NM_012352.2, NM_012353., NM_012360, NM_012363.1, NM_012363.1., NM_012364.1, NM_012365, NM_012367, NM_012368.2, NM_012369.2, NM_012373.2, NM_012374, NM_012375, NM_012377, NM_012378.1, NM_013936.3, NM_013937.3, NM_013938, NM_013939.2, NM_013940.2, NM_013941., NM_014565.2, NM_014566, NM_01750, NM_017506.1, NM_019897.2, NM_030774.3, NM_030876.5, NM_030883.4, NM_030901.1, NM_030903.3, NM_030904, NM_030905.2, NM_030908.2, NM_030946, NM_030959.2, NM_033057.2, NM_033179.2, NM_033180.4, NM_054104, NM_054105, NM_054106, NM_054107.1, NM_080859.1, NM_152430.3, NM_153444, NM_153445, NM_172194, NM_173351, NM_175883.2, NM_175911.3, NM_178168.1, NM_198074.4, NM_198944.1, NM_205859, NM_206880, NM_206899, NM_207186.2 또는 NM_207374.3.
본 발명의 어레이(1)에 탑재되는 핵산(3)의 형태는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다.
구체적으로 상기의 핵산(3)을, 관통공(2) 내의 기판(5)상에 배치시키는 방법은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 도트 형태로 핵산(3)을 프린트하는 방법을 들 수 있다. 이와 같이 프린트할 때에는, 하기의 실시예에서 예로 든 것과 같은, 프린트시에 용액의 변성을 받기 어려운 피에조 소자(MEMS를 포함함)를 구비하는 공지된 기기 또는 그 동등품, 예를 들면 잉크젯 타입의 프린터를 사용할 수 있다.
관통공(2) 내의 핵산(3)은, 전형적으로는 직경 10㎛ 이상 300㎛ 이하의 크기로 설치된다.
본 발명의 어레이(1)는, 세포와 접촉시킴으로써, 해당 세포 내에 수용체를 코드하는 유전자를 도입할 수 있다. 이로 인해, 상기 세포 내에 수용체를 발현시킬 수 있다. 일례로서 동물 유래, 포유류 유래, 또는 인간 유래의 후각 수용체를 발현시킬 수 있다.
본 발명의 어레이(1)에 대하여, 어레이(1)가 구비하는 기본적인 구성에 대하여 설명하였으나, 여러가지 응용이 가능하다. 예를 들면, 어레이(1)는, 기판(5)의 소수성 피막(6)에 덮이지 않은 영역, 또는 소수성 피막(6)의 관통공(2) 이외의 영역을 이용하여, 식별 번호를 기재하는 영역을 설치할 수 있다. 구체적으로는, 1차원 바코드, 2차원 바코드(QR코드(등록상표)를 포함함)와 같이 미리 정한 영숫자를, 광학적, 자기적, 전자적으로 읽어낼 수 있는 형태로 기재할 수 있다.
코드는, 어레이(1)마다 다른 유니크한 코드일 수 있고, 어레이(1)마다 동일한 고정 코드일 수도 있다. 또한, 식별 번호는, 어레이(1)에서의 핵산(3)의 배치 정보를 포함할 수 있다. 예를 들면, 핵산(3)에 관해서, 핵산(3)의 어레이(1)에서의 X 좌표, Y 좌표, 및 그 위치에 놓인 핵산의 구성(배열)에 관한 정보를, 행렬 형태로 코드화하여 기록한 것일 수 있다.
또한, 식별 번호를 기재하는 영역은, 자필이나 레이저 가공에 의해 묘화가 가능한 블랭크 영역(예를 들면, 조면화(粗面化)한 영역, 레이저광을 받아 착색되는 재료를 도포한 영역)일 수도 있다.
또한, 어레이(1)는, 진핵세포(4)를 탑재하기까지의 대기 시간 중, 안정적으로 보존하기 위하여, 폴리에틸렌, 폴리프로필렌 등의 합성 수지의 필름 봉투, 또는 폴리스티렌, 유리 등의 용기 안에 수납될 수 있다. 수납에 있어서는, 봉투 또는 용기 안은, 진공, 감압대기, 질소, 아르곤 등의 불활성 가스로 봉입할 수도 있다.
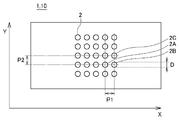
다음으로, 관통공(2)의 형상, 및 그 배치에 대하여, 도 2를 이용하여 설명한다. 도 2는, 어레이(1)에서의 관통공(2)의 배치를 나타내는, 매크로적인 평면도이다. 이의 설명에 있어서, 상술한 기판(5), 소수성 피막(6), 및 핵산(3)은, 도시하지 않았다. 구체적으로는, 도 2는, 어레이(1)가 직방체인 경우의 평면도이며, 어레이(1)의 긴 방향을 X축, 직교 방향(X축에 대하여 수직 방향)을 Y 축으로 하고 있다.
관통공(2)은 어레이(1)에 있어서, 복수 설치되어 있고, 그 형상은 임의이나, 삼각, 사각 등의 다각형이나 원을 이용할 수 있다. 원은 타원일 수도 있다. 관통공(2)의 형상은, 원, 특히 진원(眞圓)인 것이 가장 바람직하다. 도 2는, 관통공(2)이 진원이고, 어레이(1)에 25개 배치된 예를 도시하고 있다.
관통공(2)의 크기는, 그 단면적 평균치가, 1개당 0.125mm2 이상인 것이 바람직하다. 여기서 단면적 평균치란, 관통공(2)의 중심축 방향에 대하여 수직인 방향에 대한 면적을, 관통공(2)의 높이 방향(깊이 방향)에 대하여 모두 산출하여 평균화한 것이다.
즉, 관통공(2)의 형상이, 부감도에서 진원인 경우에는, 그 직경(도 2에서, 관통공(2B)의 직경(D)에 대응)은 0.4mm 이상이나, 이것으로 한정되는 것은 아니다. 관통공(2)의 크기가, 그 단면적 평균치가 0.125mm2 이상인 경우에는, 관통공(2) 1개에 대하여, 400개 이상의 진핵세포를 접촉시킬 수 있고, 후술하는 진핵세포의 형질 전환에 개체 차가 있다 하더라도, 계측에 적합한 세포수를 확보하기 쉽다. 예를 들면, 단면적 평균치가 0.125mm2 미만의 관통공(2)인 경우에는, 관통공(2) 내의 세포수가 적어지기 때문에, 충분한 형질 전환된 세포수를 확보할 수 없거나, 혹은, 수용체의 활성화도를 통계 처리하기에 충분한 세포수를 확보할 수 없는 등 부적합하다. 소정의 수용체가 후각 수용체인 경우에는, 관통공(2) 1개에 대하여, 400개 이상의 2.5% 정도에 상당하는 10개 이상의 진핵세포가 발현하게 되어, 수용체의 활성화도를 통계 처리하기에 필요한 세포수가 얻어진다.
1개의 어레이(1)에는, 소정의 수용체를 코드하는 핵산(3)이 모두 배치되어 있는 것이 바람직하다. 즉, 복수의 핵산(3)에 의해, 각각의 핵산(3)마다 대응되는 수용체가 발현하는 경우, 각각의 핵산(3)이 1개씩, 어레이(1)의 관통공(2) 내에 배치되는 것이 바람직하다. 바꾸어 말하면, 각 관통공(2)마다, 다른 소정의 수용체를 코드하는 유전자를 포함하는 핵산(3)이 설치되어 있다.
일례로서 수용체가 인간의 후각 수용체인 경우, 수용체의 종류는 약 400종류에 달한다. 이 때, 냄새의 감지능은, 온도, 풍량, 대기 분포(기류에 의해 발생되는 대기 중의 분자의 농도 분포)라고 하는 환경 요소에 의해 좌우되기 때문에, 1개 어레이에 대하여, 수용체의 1세트에 상당하는 약 400개의 서로 다른 핵산(3)을 배치하여, 1회 측정으로 1세트 모든 수용체에 대하여 일괄하여 측정을 하는 것이 가장 바람직하다. 이 때, 어레이(1)는, 약 400개의 관통공(2)을 갖는다.
후술하는 측정방법에서, 활성화도의 측정을 리얼타임으로 실시하는, 특히 초단위로 연속해서 측정하기 위해서는, 수백 개(예를 들면 200개 이상)의 관통공(2)을 동시에 측정하는 것이 필요하다.
특히, 형광을 이용하여 측정을 하기 위해서는, 형광 측정에 이용되는 광학계(예를 들면 광학 현미경)의 대물렌즈의 관찰 시야가 유한하다는 이유에서, 관통공(2)의 크기, 관통공(2)끼리의 중심 간격(피치)이 제한을 받게 된다.
예를 들면 300개 이상, 특히 400개 전후의 관통공(2)을 동시에 측정하기 위해서는, 전형적으로는, 관통공(2)의 단면적 평균치는 0.283mm2 이하인 것이 바람직하다. 관통공(2)의 형상이, 진원인 경우에는, 그 직경(도 2에서, 관통공(2B)의 직경(D)에 상당)은 0.6mm 이하이다. 또한, 각 스팟의 중심 간격(도 2에서, 관통공(2B)와 관통공(2A)가 이루는 X축상의 피치(P1), 또는 관통공(2B)와 관통공(2C)가 이루는 Y축상의 피치(P2))는, 0.6mm 이상 0.8mm 이하가 바람직하다. 또한, 피치(P1)=피치(P2)인 것이 바람직하다. 피치(P1)=피치(P2)=0.6mm 이상 0.8mm 이하인 것이 가장 바람직하다.
즉, 형광치를 측정에 이용하는 경우, 예를 들면 관통공(2)이 진원인 경우, 직경(D)은, 0.4mm 이상 0.6mm 이하가 바람직하고, 평균 피치(P1) 및 평균 피치(P2)는, 0.6mm 이상 0.8mm 이하가 바람직하다.
여기서, 직경(D)는, 0.42mm 이상, 0.44mm 이상, 0.46mm 이상, 0.48mm 이상, 0.50mm 이상일 수 있고, 0.58mm 이하, 0.56mm 이하, 0.54mm 이하, 0.52mm 이하일 수 있다.
또한, 평균 피치(P1), 및 (P2)는, 각각 독립적으로, 0.64mm 이상, 0.68mm 이상, 0.72mm 이상, 0.76mm 이상일 수 있고, 0.76mm 이하, 0.72mm 이하, 0.68mm 이하일 수 있다.
일 실시형태에 있어서, 관통공(2)은 진원이고, 그 직경(D)은, 0.5mm이고, 평균 피치(P1)= 평균 피치(P2)=0.7mm이다. 이들 수치를 이용하여, X축에 22개, Y축에 18개, 합계 396개의 관통공(2)을 갖는 어레이(1)는, 각 관통공의 중심은, 15.58mm×12.82mm의 범위 내에 밀집하여 배치되게 된다.
[진핵세포를 수납하고 있는 어레이]
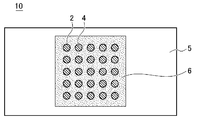
본 발명의 진핵세포를 수납하고 있는 어레이(이후, 진핵세포 어레이(10)라고 하기도 한다)에 대하여, 도 3, 도 2, 및 도 4를 이용하여 설명한다. 도 3에 나타낸 바와 같이, 본 발명의 진핵세포를 수납하고 있는 어레이(10)는, 어레이(1)를 베이스로 하고 있으며, 기판(5)과, 기판(5)상의 소수성 피막(6)과, 핵산(3), 을 포함한다. 소수성 피막(6)에는, 관통공(2)이 복수 설치되어 있고, 관통공(2)의 형상 및 배치는, 어레이(1)와 동일하다(도 2에 도시). 그리고 관통공(2)에는, 진핵세포영역(4)이 설치되어 있다.
도 4는, 관통공(2) 하나를 확대한 모식적인 평면도로서, 소수성 피막(6)에 대하여, 관통공(2A), 진핵세포영역(4A)이 설치되어 있다. 그리고 진핵세포영역(4A) 안에는, 기판(5)상에 탑재된 핵산(3)과 겹치도록, 복수개의 진핵세포가 설치되어 있다(도 4에서, 모식적으로 5개의 진핵세포(4A1)~(4A5)를 도시하고, 핵산(3)은 도시하지 않음).
도 4에서, 1개의 관통공(2)에 대하여, 진핵세포수를 5개로 예시하였으나, 2개 이상, 5개 이상, 10개 이상, 50개 이상, 100개 이상, 200개 이상, 300개 이상, 400개 이상, 500개 이상, 600개 이상, 700개 이상, 800개 이상, 1000개 이상, 2000개 이상, 일 수 있다.
또한, 10000개 이하, 9000개 이하, 8000개 이하, 7000 이하, 6000개 이하, 5000개 이하, 4000개 이하, 3000개 이하, 2000개 이하, 1000개 이하, 일 수 있다. 진핵세포는, 예를 들면, 동물 유래, 포유류 유래, 영장류 유래, 인간 유래의 진핵세포일 수 있다.
일 실시형태에서, 진핵세포는 인간 유래의 진핵세포이고, 400개 이상 1000개 이하이다.
이와 같이 관통공(2) 내의 핵산(3) 1개에 대하여, 진핵세포를 복수개 탑재함으로써, 핵산(3)을 근원으로 한 진핵세포 내의 수용체 발현에 있어서, 발현한다, 발현하지 않는다, 라는 편차가 있다 하더라도, 특정의 핵산(3)에 대하여, 측정할 수 없다고 하는 리스크를 줄일 수 있다. 예를 들면, 일 실시형태에서, 핵산(3)이 후각 수용체이고, 진핵세포가 인간 유래의 진핵세포이며, 1개의 관통공(2)(1개의 핵산(3))에 대하여, 진핵세포를 400개 배치한 경우, 약 1할에 상당하는 40개 정도의 진핵세포가, 측정 가능한 상태로 발현한다. 그리고, 40개의 진핵세포의 하나 하나를 개별로 인식하여, 정보로서 취급함으로써, 인간의 후각 수용체 약 400종류의 전체에 대하여, 피험물질에 대한 활성화도를 측정하는 측정계를 수립할 수 있다.
그런데, 수용체를 디바이스화하는 경우, 세포에서의 수용체의 발현에는, 세포의 유전자를 변환시키는 안정발현(안정적 트랜스펙션)과, 세포 내에 플라스미드를 도입하여 실시하는 일과성 발현(일과성 트랜스펙션)의 2개의 방법이 있다.
안정발현의 경우에는, 세포 내 유전자의 정보가 변환되기 때문에, 영속적으로 사용할 수 있는 한편, 유전자 발현의 수율이 나쁘기 때문에, 소정의 수용체에 대하여, 세포 배양한 것으로부터 선별하여, 디바이스에 탑재하게 된다. 따라서, 안정발현한 수용체, 예를 들면 수백 개의 수용체를, 1개의 디바이스에 탑재하기 위해서는, 방대한 노력과 코스트가 든다.
한편, 일과성 발현은, 단기간, 전형적으로는 1주간 전후밖에, 발현한 세포를 지속해서 사용할 수 없으나, 작성은 비교적 용이하여, 1개의 디바이스에 탑재하는 것은 가능하다. 작성은 비교적 용이하나, 발현 정도에는 편차가 있다.
본 발명의 진핵세포 어레이(10)는, 이러한 일과성 발현에 의해 수용체를 작성하는 수법과의 적합성이 우수하다. 즉, 관통공(2) 내의 핵산(3)에 대하여, 일례로서 진핵세포를 400개 배치(예를 들면, 관통공(2A) 내에 진핵세포를 400개 수납)할 수 있기 때문에, 일과성 발현에 의한 발현의 편차가 있더라도, 10개 정도의 진핵세포는, 측정 가능한 수용체를 발현한다. 이러한 약 10개의 수용체는, 활성화도의 측정에 있어서 서로 성능차를 갖지만, 측정계에 있어서, 10개의 진핵세포의 하나 하나를 개별로 인식하여, 각각의 세포에 대하여, 후술하는 활성화도의 산출방법(A), 또는 산출방법(B)을 따라, 정규화된 활성화도를 측정, 산출한다면, 각각의 수용체에 대하여, 적절하게 활성화도의 정보를 제공할 수 있다.
포유류 유래의 수용체를 발현시키는 진핵세포를 입수하는 방법은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 마우스 유래의 후세포를 포함하는 초대 배양 세포를 이용할 수 있다. 또한, 후술하는 본 발명의 세포를 이용할 수도 있다.
상기의 발현량을 확인하는 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 웨스턴블롯 등의 공지 기술에 근거하는 수단을 들 수 있다.
상기한 진핵세포에서 발현되는 수용체의 종류는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 1개의 세포에 대하여 1종류의 후각 수용체를 발현하는 것으로 할 수도 있고, 복수 종류의 후각 수용체가 발현하는 것으로 할 수도 있다. 1개의 세포에 1종류의 후각 수용체를 발현하는 것이 바람직하다.
예를 들면, 동정(同定)되어 있는 포유류 유래의 후각 수용체가 α, β, γ 및 δ의 4종류였을 때, α와 β가 진핵세포A에 발현되고, β와 γ가 진핵세포B에 발현되고, 그리고 δ가 진핵세포C에 발현되는 한편, 진핵세포A, B 및 C에서 발현되는 α, β, γ 및 δ의 총량이 동일하며, 진핵세포A, B 및 C가 동일계 내에서 발현되고 있는 것을 바람직한 형태로 들 수 있다.
진핵세포에서 발현하는 수용체는, 후술하는 본 발명의 산출방법(A) 또는 산출방법(B)를 실시하기 전에 동정할 수도 있고, 실시한 후에 동정할 수도 있다. 실시하기 전에 동정하는 것이라면, 이미 동정된 포유류 유래의 후각 수용체를 발현시키는 유전자를, 상기의 진핵세포에 도입할 수 있고, 실시한 후에 동정하는 것이라면, 후술하는 활성화도의 산출방법(A) 또는 산출방법(B)에 따라 활성화도를 측정한 후의 세포에 대하여, 공지의 유전자 해석에 관한 기술을 조합함으로써, 용이하게 세포에 포함되는 후각 수용체를 동정할 수 있다.
본 발명의 진핵세포 어레이(10)에 대하여, 진핵세포 어레이(10)가 구비하는 기본적인 구성에 대하여 설명하였으나, 여러가지 응용이 가능하다. 예를 들면 진핵세포 어레이(10)는, 기판(5)의 소수성 피막(6)으로 덮여 있지 않은 영역, 또는 소수성 피막(6)의 관통공(2) 이외의 영역을 이용하여, 식별 번호를 기재하는 영역을 설치할 수 있다. 구체적으로는, 1차원 바코드, 2차원 바코드(QR코드(등록상표)를 포함함)와 같이 미리 정한 영숫자를, 광학적, 자기적, 전자적으로 읽어낼 수 있는 형태로 기재할 수 있다.
코드는, 진핵세포 어레이(10)마다 다른 유니크한 코드일 수 있고, 진핵세포 어레이(10)마다 동일한 고정된 코드일 수도 있다. 또한, 식별 번호는, 어레이(1)에 있어서의 핵산(3)의 배치 정보를 포함할 수 있다. 예를 들면, 핵산(3)에 관하여, 핵산(3)의 어레이(1)에 있어서의 X좌표, Y좌표, 및 그 위치에 놓인 핵산의 구성(배열)에 관한 정보를, 행렬 형태로 코드화하여 기록한 것일 수도 있다.
또한, 식별 번호를 기재하는 영역은, 자필이나 레이저 가공에 의해 묘화가 가능한 블랭크 영역(예를 들면, 조면화한 영역, 레이저광을 받아 착색되는 재료를 도포한 영역)일 수 있다.
또한, 진핵세포 어레이(10)는, 안정적으로 보존하기 위하여, 폴리에틸렌, 폴리프로필렌 등의 합성 수지의 필름봉투, 또는 폴리스티렌, 유리 등의 용기 안에, 수납될 수 있다. 수납에 있어서는, 봉투 또는 용기 안은, 진공, 감압 대기, 질소, 아르곤 등의 불활성 가스 봉입으로 할 수도 있다.
[진핵세포]
본 발명의 진핵세포(예를 들면 도 4에서의 진핵세포(4A1)~(4A5))는, 소정의 수용체가 후각 수용체일 때, 외래 유전자로서 CNGA2 및 GNAL을 발현하는 진핵세포이다. 진핵세포로는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 효모 세포, 동물 세포, 곤충 세포, 포유류 세포, 영장류 세포 등을 들 수 있다. 상기한 진핵세포 중에서도 포유류 세포가 바람직하고, 특히 취급이 용이한 불사화된 HEK293 세포, CHO 세포, 또는 HeLa 세포 등으로 대표되는 라인 세포가 바람직하다. 또한, 래트 후각 신경세포 유래의 Rolf Ba. T 세포(Glia 16:247(1996))도 이용할 수 있다.
CNGA2란, Cyclic Nucleotide Gated Channel Alpha 2라 불리는 세포막에 존재하는 단백질을 코드하는 유전자로, 이것은 cAMP에 의존하여 칼슘 이온 채널로서 작용한다.
상기한 CNGA2의 유래는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 포유류 유래로 하는 것을 예시할 수 있다. 그 중에서도, 마우스 유래, 인간 유래를 들 수 있다.
CNGA2가 코드하는 단백질의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 1로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
또한, 서열 번호 1로 나타내는 염기 서열이 코드하는 아미노산 서열은, 이것이 칼슘 이온 채널로서 작용할 수 있는 한에는, 그 변이체도 상기의 CNGA2에 포함될 수 있다. 예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실(缺失), 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
상기의 CNGA2가 코드하는 단백질의 변이체 중에서도, 칼슘 이온 채널로서 보다 효율적으로 작용한다는 관점에서, 서열 번호 1로 나타내는 염기 서열이 코드하는 인간 유래 CNGA2의 아미노산 서열의 342번째의 글루타민산을 글리신으로, 460번째의 시스테인을 트립토판으로, 그리고 583번째의 글루타민산을 메티오닌으로 한 변이체가 바람직하다.
본 발명의 세포에서 발현하는 GNAL이란, Guanine nucleotide-binding protein G subunit alpha L이라 불리는 단백질을 코드하는 유전자로, 이것은 후신경 세포 중에서 후각 수용체를 발현하는 세포에 있어서, 후각 수용체에의 자극에 따라 야기되는 시그널 전달을 담당하는 저분자량 G단백질이다.
상기의 GNAL의 유래는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 포유류 유래로 하는 것을 예시할 수 있다. 이 중에서도, 마우스 유래, 인간 유래를 들 수 있다.
GNAL의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 2로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다. 또한, 서열 번호 2로 나타내는 염기 서열이 코드하는 아미노산 서열은, 후신경 세포 중에서 후각 수용체를 발현하는 세포에 있어서, 후각 수용체에의 자극에 따라 야기되는 시그널 전달을 담당할 수 있는 한, 그 변이체도 상기의 GNAL에 포함될 수 있다. 예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실, 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
본 발명의 세포는, 상기의 유전자가 코드하는 단백질 이외에, 아데닐산 고리화효소와 저분자량 G단백질의 β도메인 및 γ도메인을 갖고 있다.
상기의 본 발명의 세포는, 또한, 외래 유전자로서, CNGA4 및/또는 CNGB1b를 발현하는 세포로 하는 것이 바람직하다.
CNGA4란, Cyclic Nucleotide Gated Channel Alpha 4라 불리는 세포막에 존재하는 단백질을 코드하는 유전자로, 이것도 상기의 CNGA2가 코드하는 단백질과 마찬가지로 칼슘 이온 채널로서 작용한다.
상기의 CNGA4의 유래는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 포유류 유래로 하는 것을 예시할 수 있다. 그 중에서도, 마우스 유래, 인간 유래를 들 수 있다.
CNGA4가 코드하는 단백질의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 3으로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
또한, 서열 번호 3으로 나타내는 염기 서열이 코드하는 아미노산 서열은, 칼슘 이온 채널로서 작용할 수 있는 한, 그 변이체도 상기의 CNGA4에 포함될 수 있다.
예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실, 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
CNGB1b란, Cyclic Nucleotide Gated Channel Beta 1b라 불리는 세포막에 존재하는 단백질을 코드하는 유전자로, 이것도 상기의 CNGA2 및 CNGA4가 코드하는 단백질과 마찬가지로, 칼슘 이온 채널로서 작용한다.
상기의 CNGB1b의 유래는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 포유류 유래로 하는 것을 예시할 수 있다. 그 중에서도, 마우스 유래, 인간 유래를 들 수 있다.
CNGB1b가 코드하는 단백질의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 4로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
또한, 서열 번호 4로 나타내는 염기 서열이 코드하는 아미노산 서열은, 칼슘 이온 채널로서 작용할 수 있는 한, 그 변이체도 상기의 CNGB1b에 포함될 수 있다. 예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실, 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
본 발명의 세포에서 CNGA2, CNGA4 및 CNGB1b가 발현될 때, 이들 3자가 각각 2:1:1로 발현하는 것이, 후각 수용체에 대한 자극에 의해 야기되는 세포 내의 시그널 전달로 상승되는 cAMP에 대한 감도가 상승하므로 바람직하다.
상기의 본 발명의 세포는, 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 단백질을 코드하는 유전자를 발현하는 세포로 하는 것이 바람직하다.
상기의 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 단백질이란, 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, RTP1, RTP2, REEP1 등의 단백질을 들 수 있다.
RTP1의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 5로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
또한, 서열 번호 5로 나타내는 염기 서열이 코드하는 아미노산 서열은, 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 한, 그 변이체도 상기의 RTP1에 포함될 수 있다. 예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실, 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
상기의 RTP1의 스플라이스 변이체는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면 RTP1L, RTP1S 등을 들 수 있다. 이 중에서도, RTP1S라고 하면, 서열 번호 6으로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
RTP2의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 7로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
또한, 서열 번호 7로 나타내는 염기 서열이 코드하는 아미노산 서열은, 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 한, 그 변이체도 상기의 RTP2에 포함될 수 있다. 예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실, 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
REEP1의 아미노산 서열은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 서열 번호 8로 나타내는 염기 서열이 코드하는 아미노산 서열을 들 수 있다.
또한, 서열 번호 8로 나타내는 염기 서열이 코드하는 아미노산 서열은, 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 한, 그 변이체도 상기의 REEP1에 포함될 수 있다. 예를 들면, 변이 전후의 아미노산의 상동성이, 80% 이상, 바람직하게는 85% 이상, 바람직하게는 90% 이상, 바람직하게는 91% 이상, 더욱 바람직하게는 95% 이상이다. 이러한 변이에는, 치환, 결실, 삽입 등의 형태가 포함된다. 따라서, 상기의 변이체에는 스플라이스 변이체도 포함될 수 있다.
상기의 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 단백질을 코드하는 유전자의 상류에는, 이들 유전자에 대하여 후성적(epigenetic) 영향을 미치지 않는 프로모터가 배치되어 있는 것이 바람직하다.
이러한 프로모터는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, Elongation Factor-1α(EF-1α)를 들 수 있다.
상기의 후성적 영향을 미치지 않는 프로모터의 유래는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 마우스 유래 또는 인간 유래를 들 수 있다.
본 발명의 진핵세포는, CNGA2 및 GNAL를 갖는 벡터 (본 명세서에서, 이것을 「벡터A」라 부르기도 한다)를 진핵세포에 도입함으로써 제조할 수 있다. 또한, 이와 같이 하여 제조한 세포에, CNGA4 및/또는 CNGB1b를 갖는 벡터 (본 명세서에서, 이것을 「벡터B」라고 부르기도 한다)를 도입할 수 있다. 그리고, 세포 내에서 발현하는 후각 수용체를 소포체막으로부터 세포막으로 이행시켜, 해당 후각 수용체의 해당 세포 표면으로의 제시 효율을 상승시킬 수 있는 단백질을 코드하는 유전자를 갖는 벡터(본 명세서에서, 이것을 「벡터C」라고 부르기도 한다)를 도입할 수 있다.
본 발명의 벡터는, 상기의 벡터A, B 및 C의 어느 하나이다. 이들 벡터를 도입하여, 각각이 갖는 유전자를 발현시킬 수 있는 진핵세포는 특별히 한정되지 않는다. 예를 들면, 효모 세포, 포유류 세포, 곤충 세포를 들 수 있다. 이 중에서도, 포유류 세포가 바람직하다. 상기에 의해 구축된 벡터는, 공지된 바이러스를 이용하여, 재조합 바이러스를 제작할 수 있고, 이러한 재조합 바이러스는, 진핵세포에 대하여, 일과성 발현을 유도할 수 있다. 공지된 바이러스란, 예를 들면, 아데노바이러스, 레트로바이러스, 아데노 수반 바이러스, 바큘로바이러스를 들 수 있다.
상기의 벡터A, B, 및 C는, 조건을 조절하면, 안정발현을 유도하는 것도 가능하다. 예를 들면, 본 발명의 세포의 염색체상에, 후각 수용체를 코드하는 유전자가 배치되는 영역을 일정 개수 이상 설치함으로써, 안정발현이 달성된다. 상기의 영역은, 상술한 염색체상의 소정의 위치에 설치된 재조합효소(recombinase)에 반응하는 영역이다.
이러한 재조합효소는 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, Flp, Cre 등을 들 수 있다. 이들 재조합효소에 반응하는 영역으로는, 각각 Frt 및 LoxP를 들 수 있다.
상기한 바와 같이, 본 발명의 세포의 염색체에, 후각 수용체를 코드하는 유전자가 편입되는 영역을 일정 개수 이상 갖고 있기 때문에, 이 영역에만 후각 수용체를 코드하는 유전자를 편입할 수 있다. 예를 들면, 상기 영역의 개수에 따라서 후각 수용체를 코드하는 유전자가 편입되는 개수도 조절할 수 있으므로, 상기 세포에서 발현하는 후각 수용체의 양을 조절할 수도 있다.
상기의 본 발명의 세포에 의하면, 후신경세포에서 실시되는 후각 수용체의 자극에 의해 야기되는 시그널 전달을 실현할 수 있다. 따라서, 본 발명의 세포를 이용함으로써, 후술하는 본 발명의 활성화도의 산출방법(A), (B)를 호적하게 실시할 수 있다.
상기의 후각 수용체에는, 이들이 세포막상에 정확한 토폴로지로 발현하도록 하기 위하여, Rhodopsin 분자 N 말단 20 아미노산 잔기인 서열 번호 9로 나타내는 아미노산(MNGTEGPNFYVPFSNKTGVV)을, 이것에 융합한 상태로 본 발명의 세포에 편입되어 함께 발현되는 것이 바람직하다.
[활성화 정도의 산출방법]
본 발명의 피험물질(본 명세서에서, 이것을 리간드라고 부르기도 한다)에 의한 수용체에 대한 활성화 정도를 산출하는 방법(이하, 명세서에서, 이것을 「산출방법」이라고 부르기도 한다)은, 산출방법(A)와, 산출방법(B)가 있다.
[활성화 정도의 산출방법(A)]
활성화 정도의 산출방법(A)은, 이하의 공정1~3을 포함하는 방법이다.
(공정1)
수용체를 발현하는 진핵세포에 대하여 피험물질을 접촉시켰을 때, 해당 세포 내로 수용되는 이온량을 측정하는 공정.
(공정2)
상기 공정1에서 측정에 사용한 세포와 동일한 세포를 탈분극 했을 때의 해당 세포 내의 이온량을 측정하는 공정.
(공정3)
상기 공정1에서 측정한 수치와 상기 공정2에서 측정한 수치와의 비를 산출하는 공정.
상기 공정1 및 공정2는, 공정3 이전에 실시할 수 있고, 상기 공정1과 공정2를 실시하는 순서는, 본 발명의 산출방법에 의해 얻어지는 효과에 영향을 미치지 않는 범위에서, 특별히 한정되지 않는다. 본 발명의 산출방법에 의해 얻는 수치의 신뢰도를 감안하면, 공정1 이후에 공정2를 실시하는 것이 바람직하다.
상기의 피험물질이란, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 일반적으로 인간 등의 동물에 의해 인식되지 않는 냄새 성분을 함유하는 물질도, 본 발명의 산출방법에 있어서의 피험물질에 포함할 수도 있다.
상기의 피험물질의 카테고리는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 순물질로 할 수도 있고, 혼합물로 할 수도 있다. 또한 순물질이, 단체(單體)이거나, 화합물이거나, 특별히 한정되지 않는다.
상기의 피험물질의 형상도, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 기체, 고체, 또는 액체의 어느 하나의 형상일 수 있다.
상기의 수용체는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 상술한 어레이(1)가 갖는 핵산(3)이 속하는 소정의 수용체일 수 있고, 이른바 막관통형 수용체를 가리켜, 예를 들면, 대사형 수용체, 이온 채널형 수용체를 포함할 수 있다.
대사형 수용체의 예로는, G단백질 공역형 수용체, 티로신 키나아제 수용체, 구아닐산 고리화효소 수용체가 있다.
G단백질 공역형 수용체의 예로는, 후각 수용체, 무스카린성 아세틸콜린 수용체, 아데노신 수용체, 아드레날린 수용체, GABA 수용체(B형), 앤지오텐신 수용체, 칸나비노이드 수용체, 콜레키스토키닌 수용체, 도파민 수용체, 글루카곤 수용체, 히스타민 수용체, 오피오이드 수용체, 세크레틴 수용체, 세로토닌 수용체, 가스트린 수용체, P2Y 수용체, 로돕신이 있다.
티로신 키나아제 수용체의 예로는, 인슐린 수용체, 세포증식인자의 수용체, 사이토카인의 수용체가 있다.
구아닐산 고리화효소 수용체의 예로는, GC-A, GC-B, GC-C가 있다.
이온 채널형 수용체의 예로는, 니코틴성 아세틸콜린 수용체, 글리신 수용체, GABA 수용체(A형, C형), 글루타민산 수용체, 세로토닌 수용체 3형, 이노시톨트리스인산(IP3) 수용체, 리아노딘 수용체, P2X 수용체가 있다.
상기 공정1 및 공정2에서의 세포 내의 이온량을 측정하는 공정이 대상으로 하는 이온 종류는, 상기 수용체의 종류에 따라 다르다. 예를 들면 수용체가 후각 수용체인 경우에는, 칼슘 이온을 예시할 수 있고, 니코틴성 아세틸콜린 수용체의 경우에는, 나트륨 이온을 예시할 수 있고, 글리신 수용체의 경우에는, 염화물 이온을 예시할 수 있다.
수용체가 후각 수용체이고, 피험물질을 접촉시키는 방법에 대하여, 다음에 설명한다. 피험물질이 고체인 경우에는, 그것에 함유되는 냄새 성분을 용출할 수 있는 공지된 용매를 이용하여 얻은 용액을, 진핵세포에 적용함으로써, 당해 피험물질을 진핵세포에 접촉시킬 수 있다. 또한, 피험물질이 기체인 경우에도, 그것에 함유되는 냄새 성분을 흡수할 수 있는 공지된 용매를 이용하여 얻은 용액을, 진핵세포에 적용함으로써, 당해 피험물질을 진핵세포에 접촉시킬 수 있다.
상기의 공지된 용매란, 본 발명의 방법에 의해 포유류 유래의 후각 수용체에 응답하지 않는 용매인 한, 특별히 한정되지 않는다. 예를 들면, 물, 완충액, DMSO, 메탄올, 에탄올, 배지(培地), 링거 용액 등을 들 수 있다.
이하에, 본 발명의 산출방법에 있어서의 각 공정에 대하여 상세히 기술한다.
[공정1에 대하여]
본 발명의 산출방법의 공정1은, 수용체를 발현하는 진핵세포에 대하여, 상기 피험물질을 접촉시켰을 때, 해당 세포 내로 수용되는 이온량을 측정하는 공정이다.
이후, 수용체를, 포유류 유래의 후각 수용체로 하고, 세포 내로 수용되는 이온이, 칼슘 이온인 예를 대표로, 이하에 설명한다.
공정1에서, 포유류 유래의 후각 수용체를 발현하는 진핵세포를 유지하기 위한 배지, 배양 조건 등은, 공정1 및 공정2에서의 진핵세포 내로 수용되는 칼슘 이온량의 측정에 영향을 주지 않는 범위에서, 특별히 한정되지 않는다. 예를 들면, 통상, 포유류에 유래하는 세포를 배양할 수 있는 배지, 온도, 이산화탄소 농도를 들 수 있다.
공정1에서 포유류 유래의 후각 수용체를 발현하는 진핵세포로 수용되는 칼슘 이온량을 측정하는 장소는, 상기의 배지, 및 배양 환경을 유지할 수 있는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 디시상, 플레이트상, 멀티웰 플레이트상, 챔버상, 어레이상 등의 세포 배양에 적합한 장소를 예시할 수 있다. 본 발명의 산출방법을 하이스루풋으로 실시한다는 관점에서, 멀티웰상, 멀티웰이 설치된 챔버상, 및 어레이상에서 측정하는 것이 바람직하다. 이 때, 각 웰에 격납되는 세포가 발현하는 포유류 유래의 후각 수용체는, 각각 다른 후각 수용체인 것이 바람직하다.
공정1에서의 포유류 유래의 후각 수용체를 발현하는 진핵세포 내로 수용되는 칼슘 이온량을 측정하는 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 색소를 이용하는 수단, 칼슘 결합 단백질을 이용하는 수단 등을 들 수 있다.
상기의 수단에 이용되는 색소는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, Fluo-4, Rhod-3, Fluo-3, Fura-2, Indo-1, Quin-2, Rhod-2, 또는 Fluo-8 등으로 대표되는 형광 색소를 들 수 있다. 이들 형광 색소는 세포막 투과성을 높이는 AM유도체(아세톡시메틸기에 의한 보호)인 것이 바람직하다.
AM체는 수중에서 과립이 될 수 있기 때문에, 이것을 세포에 수용시키는 것을 목적으로, Pluronic F-127, 또는 Cremophor EL 등의 계면활성제를 이용할 수 있다. 상기 색소 중에서도, 세포 내로 수용되는 칼슘 이온량의 시간 경과에 따른 측정이 가능하다는 것, 효율적으로 측정할 수 있다는 것, 현미경 B 여기(勵起) 부근의 범용성이 높은, 단일 파장 여기, 단일 파장 형광의 특성을 갖는다는 것, Ca 착체 해리정수(Kd)가 1nmol/ml 이하라는 것 등의 관점에서, Fluo-3, Fluo-4, Quin-2 등을 이용하는 것이 바람직하다. 이들 색소를 이용하여 세포 내로 수용되는 칼슘 이온량을 측정하는 구체적인 방법은, 특별히 한정되지 않는다. 구체적으로는, 이들 색소와 칼슘 이온을 접촉시켜, 서로 결합된 상태에 수반되어 해당 색소에 의해 나타나는 형광치를 측정하는 방법을 들 수 있다.
상기의 수단에 이용되는 칼슘 결합 단백질은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, G-Geco, B-Geco, R-Geco, GEX-Geco, GEM-Geco 등의 Geco; Case 12, CEPIA, Aequorin, Cameleon, Pericam 또는 GcaMP 등으로 대표되는 칼슘에 결합하는 형광 단백질을 들 수 있다. 이들 칼슘 결합 단백질을 이용하여 세포 내로 수용되는 칼슘 이온량을 측정하는 구체적인 방법은, 특별히 한정되지 않는다. 구체적으로는, 이들 칼슘 결합 단백질과 칼슘 이온을 접촉시켜, 서로가 결합한 상태에 수반되어 해당 칼슘 결합 단백질에 의해 나타나는 형광치를 측정하는 방법을 들 수 있다.
공정1에서 칼슘 이온량을 측정하는 방법은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 칼슘 이온량을 측정하는 수단이 색소를 이용하는 수단인 경우, 세포를 자극하지 않은 상태의 수치(형광치)를 기준으로 하여, 세포에 피험물질을 접촉시킨 후에 얻어지는 수치를 그대로 칼슘 이온량으로서 측정할 수 있다.
구체적으로 상기의 수치를 구하는 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 상기의 색소를 이용하여 칼슘 이온량을 측정하는 것이라면, 세포를 자극하지 않은 상태에서 측정되는 형광치(본 명세서에서, 이것을 「백그라운드치 」라 부르기도 한다)와, 자극 후에 측정되는 형광치와의 일차원 수치의 차를, 공정1에서 구하는 수치로 할 수 있다.
또한, 세포를 자극하지 않은 상태에서 측정되는 형광치(백그라운드치)와, 자극 후에 측정되는 형광치와의 이차원 수치의 차를 기초로, 공정1의 수치를 구할 수도 있다.
[공정2에 대하여]
본 발명의 산출방법의 공정1은, 상기 공정1에서 측정에 사용한 세포와 동일한 세포를 탈분극 했을 때의 칼슘 이온량을 측정하는 공정이다.
공정2에 있어서, 공정1에서 측정에 사용한 세포와 동일한 세포를 탈분극 하는 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 칼륨 화합물, 또는 이오노포어를 상기의 세포에 접촉시키는 수단을 들 수 있다.
상기의 칼륨 화합물은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 염화칼륨, 브롬화칼륨, 수산화칼륨, 칼륨아미드, 불화칼륨, 질산칼륨, 아질산칼륨, 황산칼륨, 아황산칼륨, 탄산칼륨, 탄산수소칼륨, 제1인산칼륨, 제2인산칼륨, 제3인산칼륨, 크롬산칼륨, 중크롬산칼륨, 피로인산칼륨, 메타인산칼륨, 염소산칼륨, 과염소산칼륨, 망간산칼륨, 과망간산칼륨, 산화칼륨, 과산화칼륨, 규산칼륨, 브롬산칼륨, 요오드산칼륨 등으로 대표되는 무기 칼륨 화합물; 포름산칼륨, 아세트산칼륨, 구연산칼륨, 옥살산칼륨, 푸마르산칼륨, 낙산칼륨, 젖산칼륨, 주석산칼륨, 숙신산칼륨, 올레산칼륨, 팔미트산칼륨, 아스파르트산칼륨, 글루타민산칼륨 등으로 대표되는 유기 칼륨 화합물을 들 수 있다.
이들 칼륨 화합물 중에서도, 배지 중에서의 용해성과 세포 독성의 관점에서 무기 칼륨 화합물이 바람직하며, 염화칼륨이 가장 바람직하다.
상기의 칼륨 화합물의 사용량은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 사용되는 칼륨 화합물이 염화칼륨인 경우, 통상은 10~500mM 정도이고, 바람직하게는 50~200mM 정도의 사용량으로 할 수 있다.
상기의 이오노포어는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, Ionomycin, A23187(Calcimycin) 및 4-Bromo-A23187 등을 들 수 있다.
상기의 이오노포어의 사용량도, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 상기의 Ionomycin이라면 통상은 1μM 정도로 할 수 있다.
공정2에서의 포유류 유래의 후각 수용체를 발현하는 진핵세포를 유지하기 위한 배지, 배양 조건 등; 포유류 유래의 후각 수용체를 발현하는 진핵세포로 수용되는 칼슘 이온량을 측정하는 장소; 및 포유류 유래의 후각 수용체를 발현하는 진핵세포 내로 수용되는 칼슘 이온량을 측정하는 수단은, 상기의 공정1에서 설명한 것과 동일하게 할 수 있다.
[공정3에 대하여]
본 발명의 산출방법의 공정3은, 상기 공정1에서 측정한 수치와 상기 공정2에서 측정한 수치와의 비를 산출하는 공정이다. 공정3에서 산출되는 비(비율)는, 공정1에서 측정한 수치를 공정2에서 산출되는 수치로 나누어 얻어지는 수치일 수 있다.
공정1 및 공정2에서 산출하는 방법이 상기의 형광치를 이용하는 경우에, 상기 공정3 전에 공정1 및 공정2에서 산출한 계내(系內)에 소정의 농도의 킬레이트제(예를 들면, EDTA 또는 EGTA 등)를 이용하여 얻어지는 형광치를 백그라운드치로 보정함으로써, 공정3에서 산출되는 수치를 보다 정밀한 것으로 할 수 있다.
공정2에서 얻어지는 수치가 후각 수용체를 발현하는 세포에서 후각 자극에 반응하여 야기되는 시그널 캐스케이드의 최종 이벤트에 상당한다. 또한, 공정2에서 세포를 탈분극 한다는 공정은, 본 발명의 산출방법에서 측정 대상으로 하는 후각 수용체를 발현하는 세포의 최종 이벤트의 포지티브 컨트롤이 되는 공정에 상당하므로, 이로 인해 얻어지는 구체적인 수치는 실험 조건 등에 영향을 받기 어렵고, 어느 정도의 절대적인 값을 나타낸다고 이해된다.
그러나, 공정1에서 얻어지는 수치는, 측정 조건 등에 의해 얻어지는 수치가 일정하지 않아, 어떤 기준치에 대한 상대적인 값으로서 얻는 것이 바람직하다.
그래서, 공정2에서 얻어지는 절대적인 수치를 기준으로 하여 공정1에서 얻어지는 수치를 산출함으로써, 특정의 피험물질에 대한 특정의 후각 수용체를 발현하는 세포에 대한 활성화 정도를, 어느 정도 절대적인 수치로서 산출하는 것이 가능해진다.
[활성화 정도의 산출방법(B)]
본 발명의 피험물질에 의한 수용체에 대한 활성화 정도를 산출하는 제2의 방법에 대하여, 설명한다. 구체적으로는, 이하의 공정1~3을 포함하는 방법이다.
(공정1)
수용체를 발현하는 진핵세포에 대하여, 피험물질을 접촉시키기 전부터 형광 측정을 개시하고, 접촉 전의 제1 소정 시간에서의 형광의 평균치를 Fbase로 하는 공정.
(공정2)
수용체를 발현하는 진핵세포에 대하여, 피험물질을 접촉시키고, 피험물질의 접촉 후의 제2 소정 시간에서의 형광의 최대치를 Fmax로 하는 공정.
(공정3)
Fmax/Fbase를 산출하여, 활성화도로 하는 공정.
본 활성화 정도의 산출방법(B)에서는, 공정1, 공정2, 공정3의 순서로 실시할 수 있다.
반복 측정하는 경우에도, 예를 들면 2회째의 측정도, 공정1, 공정2, 공정3의 순서로 실시할 수 있다.
상기의 피험물질이란, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 일반적으로 인간 등의 동물의 감각 기관에 의해 인식되지 않는 성분을 함유하는 물질도, 본 발명의 산출방법에 있어서의 피험물질에 포함될 수 있다.
상기의 피험물질의 카테고리는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 순물질로 할 수도 있고 혼합물로 할 수도 있다. 또한 순물질이, 단체(單體)이거나, 화합물이거나도, 특별히 한정되지 않는다.
상기의 피험물질의 형상도, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 기체, 고체, 또는 액체의 어느 하나의 형상일 수 있다.
상기의 수용체는, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 상술한 어레이(1)가 갖는 핵산(3)이 속하는 소정의 수용체일 수 있고, 이른바 막관통형 수용체를 나타내는, 예를 들면, 대사형 수용체, 이온 채널형 수용체를 포함할 수 있다.
대사형 수용체의 예로서는, G단백질 공역형 수용체, 티로신 키나아제 수용체, 구아닐산 고리화효소 수용체가 있다.
G단백질 공역형 수용체의 예로서는, 후각 수용체, 무스카린성 아세틸콜린 수용체, 아데노신 수용체, 아드레날린 수용체, GABA 수용체(B형), 앤지오텐신 수용체, 칸나비노이드 수용체, 콜레키스토키닌 수용체, 도파민 수용체, 글루카곤 수용체, 히스타민 수용체, 오피오이드 수용체, 세크레틴 수용체, 세로토닌 수용체, 가스트린 수용체, P2Y 수용체, 로돕신이 있다.
티로신 키나아제 수용체의 예로서는, 인슐린 수용체, 세포증식인자의 수용체, 사이토카인의 수용체가 있다.
구아닐산 고리화효소 수용체의 예로서는, GC-A, GC-B, GC-C가 있다.
이온 채널형 수용체의 예로서는, 니코틴성 아세틸콜린 수용체, 글리신 수용체, GABA 수용체(A형, C형), 글루타민산 수용체, 세로토닌 수용체 3형, 이노시톨트리스인산(IP3) 수용체, 리아노딘 수용체, P2X 수용체가 있다.
이들 수용체의 활성화도에 따라서, 세포 내로 수용된다고 이미 알려진 물질을, 측정 대상으로 할 수 있다. 예를 들면 수용체가 후각 수용체인 경우에는, 세포 내의 물질로서, 칼슘을 예시할 수 있다.
수용체가 후각 수용체이며, 피험물질을 접촉시키는 방법에 대하여, 다음에 설명한다. 피험물질이 고체인 경우에는, 그것에 함유되는 냄새 성분을 용출시킬 수 있는 공지된 용매를 이용하여 얻어지는 용액을, 진핵세포에 적용함으로써, 당해 피험물질을 진핵세포에 접촉시킬 수 있다. 또한, 피험물질이 기체인 경우에도, 그것에 함유되는 냄새 성분을 흡수할 수 있는 공지된 용매를 이용하여 얻어지는 용액을, 진핵세포에 적용함으로써, 당해 피험물질을 진핵세포에 접촉시킬 수 있다.
상기의 공지된 용매란, 본 발명의 방법에 따라 포유류 유래의 후각 수용체에 응답하지 않는 용매인 한, 특별히 한정되지 않는다. 예를 들면, 물, 완충액, DMSO, 메탄올, 에탄올, 배지, 링거 용액 등을 들 수 있다.
[공정1에 대하여]
본 발명의 산출방법의 공정1은, 수용체를 발현하는 진핵세포에 대하여, 상기 피험물질을 접촉시켰을 때, 해당 세포 내로 수용되는 물질을 측정하는 공정이다. 이후, 수용체를, 포유류 유래의 후각 수용체로 하여, 세포 내로 수용되는 물질이, 칼슘인 계로 대표시켜, 이하에 설명한다.
공정1에서, 포유류 유래의 후각 수용체를 발현하는 진핵세포를 유지하기 위한 배지, 배양 조건 등은, 공정1 및 공정2에서의 진핵세포 내로 수용되는 칼슘량의 측정에 영향을 주지 않는 범위에서, 특별히 한정되지 않는다. 예를 들면, 통상, 포유류에 유래하는 세포를 배양할 수 있는 배지, 온도, 이산화탄소 농도를 들 수 있다.
공정1에서 포유류 유래의 후각 수용체를 발현하는 진핵세포로 수용되는 칼슘을 측정하는 장소는, 상기의 배지, 및 배양 환경을 유지할 수 있는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 디시상, 플레이트상, 멀티웰 플레이트상, 챔버상, 어레이상 등의 세포 배양에 적합한 장소를 예시할 수 있다. 본 발명의 산출방법을 하이스루풋으로 실시한다는 관점에서, 멀티웰상, 멀티웰이 설치된 챔버상, 및 어레이상에서 측정하는 것이 바람직하다. 이 때, 각 웰에 격납되는 세포가 발현하는 포유류 유래의 후각 수용체는, 각각 다른 후각 수용체인 것이 바람직하다.
공정1에서의 포유류 유래의 후각 수용체를 발현하는 진핵세포 내로 수용되는 칼슘을 측정하는 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 칼슘용 형광 지시약을 이용하는 수단 등을 들 수 있다. 칼슘용 형광 지시약은, 칼슘의 양에 따라서, 형광 강도가 변화하는 작용을 갖고 있다.
상기의 수단에 이용되는 형광 지시약은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 세포 내 칼슘을 측정하기 위한 이른바 칼슘 지시약을 이용할 수 있다. 예를 들면, Calbryte520, Calbryte590, Calbryte630를 이용하여 세포 내의 칼슘 농도의 변화를, 형광으로서 정색(呈色) 하는 지시약을 이용할 수 있다. 이들 형광 지시약은, 세포막 투과성을 높이는 AM유도체(아세톡시메틸기에 의한 보호)인 것이 바람직하다.
AM체는 수중에서 과립이 될 수 있기 때문에, 이것을 세포로 수용시키는 것을 목적으로 하여, Pluronic F-127, 또는 Cremophor EL 등의 계면활성제를 이용할 수 있다.
상기의 지시약 중에서도, 세포 내로 수용되는 칼슘량의 시간 경과에 따른 측정이 가능하다는 것, 효율적으로 측정할 수 있다는 것, 현미경 G여기 부근의 범용성이 높은, 단일 파장 여기, 단일 파장 형광의 특성을 갖는다는 것 등의 관점에서, Calbryte520AM을 이용하는 것이 바람직하다. 이러한 색소를 이용하여 세포 내로 수용되는 칼슘량을 측정하는 구체적인 방법은, 특별히 한정되지 않는다. 구체적으로는, 지시약과 세포 내 칼슘을 접촉시켜, 서로 결합된 상태에 수반되어 해당 지시약에 의해 나타나는 형광치를 측정하는 방법을 들 수 있다.
(공정1)은, 수용체를 발현한 진핵세포에 대하여, 피험물질을 접촉시키기 전부터 형광 측정을 개시하여, 접촉 전의 제1 소정 시간에서의 형광의 평균치를 Fbase로 하는 공정이다. 여기서, 접촉 전의 제1 소정 시간이란, 피험물질을 접촉시키기 전의, 진핵세포 어레이(10) 및 측정계가, 열적 안정, 화학적 안정의 상태를 계측하기 위한 시간이다.
따라서, 제1 소정 시간의 개시시각은, 진핵세포 어레이(10)를 측정계에 설치하여, 열적으로 평형에 달하는 시간에 의해 설정된다. 또한, 제1 소정 시간의 종료시각은, 환경과의 화학적인 평형 상태가 무너지는 타이밍, 즉 진핵세포 어레이(10)에 피험물질을 접촉시키는 타이밍을 포함하지 않는다. 진핵세포 어레이(10)는 유한의 크기를 가지므로, 진핵세포 어레이(10)의 양단에서는 피험물질의 접촉에 시간차가 발생하는 것도 고려하여, 제1 소정 시간의 종료시각은, 피험물질을 접촉시키는 타이밍보다 전으로 설정하는 것이 바람직하다.
예를 들면, 제1 소정 시간은, 측정 개시부터 피험물질 접촉 전 1분전까지의 시간으로, 전형적으로는, 피험물질 접촉 6분전~1분전의 5분간의 시간이다.
본 발명의 효과를 발휘하는 범위에 한하여, 제1 소정 시간의 개시시각은, 피험물질 접촉의 30분전, 20분전, 10분전, 9분전, 8분전, 7분전, 5분전일 수 있고, 제1 소정 시간의 종료시각은, 3분전, 2분 30초전, 2분전, 1분 30초전, 50초전, 40초전, 30초전, 20초전, 10초전일 수 있다.
(공정2)는, 수용체를 발현한 진핵세포에 대하여, 피험물질을 접촉시켰을 때쯤부터 형광 측정을 개시하여, 접촉 후의 제2 소정 시간에서의 형광의 최대치를 Fmax로 하는 공정이다. 따라서, 제2 소정 시간은, Fmax를 넘어서, 형광이 저하되는 경향이 지속되는 것을 확인할 수 있는 추가 시간(경과 관찰 시간)을 포함하여 설정하는 것이 필요하다.
여기서, 수용체에 대한 피험물질의 응답 속도는, 극히 빠르다는 점에서, 제2 소정 시간의 개시시각은, 피험물질을 접촉시킨 시각과 동일하게 하는 것이 바람직하다.
한편, 형광의 최대치 Fmax에 관해서는, 수용체의 종류, 피험물질에 따라 피크로부터 저하로 전환되는 시각이나, 하강 곡선의 형태에 편차가 있기 때문에, 추가 시간(경과 관찰 시간)은 비교적 길게 할 필요가 있다. 많은 수용체의 종류, 피험물질을 검토한 결과, 하나의 판단 기준으로는, 형광 강도가 피크치에서 하강으로 전환된 후, 200초간 이상, 하강 경향이 지속된 경우에, 피크치를 Fmax로 판단할 수 있다. 또한, 다른 판단 기준으로는, 형광 강도가 피크치에서 하강으로 전환된 후, 제2 소정 시간의 개시시각으로부터 피크치까지의 경과시간의 0.3배 이상의 추가 시간에 걸쳐, 하강 경향이 지속된 경우에, 피크치를 Fmax로 판단할 수 있다.
예를 들면, 제2 소정 시간은, 피험물질 접촉 후 0~20분후까지의 시간으로, 전형적으로는, 피험물질 접촉 후 0~10분후의 10분간의 시간이다.
본 발명의 효과를 발휘하는 범위에 한하여, 제2 소정 시간의 개시시각은, 피험물질 접촉의 3초 후, 5초 후, 10초 후, 20초 후, 30초후 일수 있고, 제2 소정 시간의 종료시각은, 12 분후, 15분후, 25분후, 30분후일 수 있다.
이와 같이 하여 구한 Fbase, Fmax에 근거하여, Fmax/Fbase를 산출함으로써, 수용체의 활성화도를 구할 수 있다.
도 5는, 산출방법(B)에 따른 형광 측정의 예를 나타내는 도이다. 횡축은 시간(초)이고, 종축이 형광 강도(임의 단위)로 되어 있다. 횡축의 시간은 측정 개시를 0초로 한 것이고, 측정 개시 360초(도 5에서, T360이라고 표시)에 있어서, 수용체를 발현하는 진핵세포에 피험물질을 접촉시키고 있다. 도 5의 예에서, 제1 소정 시간은, T0~T300으로, 즉 피험물질 접촉 6분전~1분전의 5분간의 시간이다. 또한, 제2 소정 시간은, T360~T900으로, 즉 피험물질 접촉 0분후~10분후의 10분간의 시간이다.
도 5가 나타낸 바와 같이, 제1 소정 시간에서의 형광은 안정되어 있고, 그 평균치는 베이스 라인으로서 적당하다. 또한 제2 소정 시간에서의 형광은, 예리한 피크를 가지므로, 최대치의 검출은 용이하게 이루어질 수 있다. 따라서, Fmax를 Fbase로 나누는 것은, 활성화도를 효과적으로 나타내는 지표가 될 수 있다.
도 5의 예에서는, Fbase=656이고, Fmax=949이므로, 이들 수치에 근거하여, 활성화도는, Fmax/Fbase=1.4로 산출된다.
산출방법(B)의 이점으로는, 산출방법(A)와 비교하여, 탈분극의 공정, 양성대조물질을 접촉시키는 공정을 반드시 필요로 하는 것은 아니라는 높은 측정 재현성에 있다.
도 6은, 일과성 발현시킨 각종 후각 수용체에 대하여, 피험물질을 접촉시켰을 때의, 형광 강도의 시간 응답성을 측정한 것이다(측정 개시로부터 360초에서, 피험물질을 접촉시키고 있다). 도 6의 [A]는, 후각 수용체 중, 전형적인 5예에 대한 시간 응답성을 조사한 결과이다. 도 6의 [A]가 나타내는 바와 같이, 측정 개시부터 400~450초에서 형광 강도는 최대치를 나타내고, 이후 감쇠하고 있다.
그러나, 수용체 OR8U1(도 6의 [D])에 대해서는, 측정 개시로부터 500초 부근에서 형광의 최대치를 나타내고, 이후 감쇠하고 있다.
또한, 수용체 OR2G2(도 6의 [B]), 수용체 OR4C11(도 6의 [C])에 대해서는, 측정 개시로부터 600초 부근에서 형광은 최대치를 나타내고, 600~900초의, 거의 플랫이라고 부를 수 있는 기간을 경과한 후, 감쇠로 전환되고 있다.
이와 같이 수용체에 따라, 시간 응답성이 다르고, 일부 수용체에서는, 피험물질 접촉의 영향을 길게 받는 것이 있다.
또한, 측정 개시전의 시간에 있어서의 형광 강도에 대해서도, 수용체 마다 경향이 다르다.
이러한 점에서, 제1 소정 시간보다 제2 소정 시간을 길게 설정하는 것이 바람직하고, 이와 같이 시간 설정을 하는 한, 측정치 Fmax/Fbase는, 활성화도의 지표로서 높은 신뢰성을 갖는다. 이러한 측정방법을 채용하는 한, 양성대조물질을 접촉시키지 않고, 피험물질을 반복 접촉시켜, 활성화도를 반복 측정할 수 있다.
전형적으로는, 제1 소정 시간은, 피험물질 접촉 6분전~1분전의 5분간의 시간이고, 제2 소정 시간은, 피험물질 접촉 0분후~10분후의 10분간의 시간이다.
산출방법(B)는, 품질관리의 수법을 병용하여, 더욱 신뢰성 향상을 도모할 수도 있다. 예를 들면, 원인은 불분명하나, 측정계 전체에 외란이 혼입되어, 측정 신호(형광 강도)에 노이즈가 중첩될 수 있다. 또한 측정계 전체적으로, 형광 강도가 낮아질 수도 있다. 이러한 경우의 측정에 있어서도, 신뢰성을 확보하는 방법으로서, 제1 소정 시간 중의 형광 강도의 표준편차(SD)를 측정하여, 활성화도로서 채용할 것인지 아닌지를 판정하는 파라미터로서 이용한다. 구체적으로는, Fbase+5SD를 산출하여, 상술한 측정치 Fmax와 비교한다. 측정치 Fmax가 Fbase+5SD 이상일 때는 활성화도로서 채용하고, 측정치 Fmax가 Fbase+5SD 미만일 때는 활성화도로서 채용하지 않는다. 이와 같이 측정치에 대하여, 통계적인 판정을 실시함으로써, 측정치 Fmax/Fbase를 활성화도로서 취급할 때 신뢰성은 더욱 향상된다.
예를 들면, 도 5의 예에서는, 제1 소정 시간 중의 형광 강도의 표준편차(SD)는, SD=9이고, 상술한 바와 같이, Fbase=656, Fmax=949이므로, Fbase+5SD=701로 산출된다. 이 때, Fmax는 Fbase+5SD 이상이며, 활성화도로서 충분히 채용할 수 있는 활성화도이다.
상술한 바와 같이, 측정치 Fmax/Fbase는, 활성화도의 지표로서, 본래, 높은 신뢰성을 갖는다는 점에서, 양성대조물질을 접촉시키지 않고, 피험물질을 반복 접촉시켜, 활성화도를 반복 측정할 수 있다.
이러한 반복 측정에 있어서, 측정치에 높은 신뢰성이 요구되는 경우에는, 1회째의 측정 다음의 2회째의 측정은, 2회째의 측정에 있어서의 Fbase(이후, Fbase2라고 적기도 한다)가, 상술한 Fbase+5SD를 밑도는 시간까지 방치됨(예를 들면 링거액을 관류(灌流)함)으로써, 2회째의 측정은, 1회째 측정의 영향을 받지 않고 실시할 수 있다. Fbase2<Fbase+5SD가 되는 시간(완화 시간)은, 수용체나 피험물질에도 의하나, 전형적으로는 20분 이상이다. 마찬가지로 3회째 이후의 측정도, 이러한 방법을 이용하여 실시할 수 있다.
한편, 수용체를 복수 배치한 어레이에 있어서, 반복 측정을 실시하는 경우에는, 수용체 마다 완화 시간이 다르기 때문에, 모든 수용체가 Fbase2<Fbase+5SD의 조건을 만족하는 시간까지 방치하면 막대한 시간을 필요로 할 수 있다. 따라서, 측정의 시간 효율을 우선하는 경우에는, Fbase2≥Fbase+5SD인 타이밍에서도, 2회째의 측정을 실시할 수 있다. 즉, 2회째 측정 개시 전에, Fbase2를 구하는 공정1을 실시하고 있음으로써, 계속적으로 2회째의 측정을 실시할 수 있다. 마찬가지로, 3회째 이후의 측정도 실시할 수 있다.
이상, 본 발명의 활성화도의 산출방법(B)에 대하여, 피험물질과의 접촉에 의해, 진핵세포 내로 수용되는 물질을 형광 지시약에 의해 검출하는 계를 대표로 설명하였으나, 산출방법(B)은, 이것으로 한정되지 않고, 폭넓은 응용이 가능하다, 예를 들면, 피험물질과의 접촉에 의해, 진핵세포 내로 수용되는 이온을, 이온 측정용의 형광 색소, 또는 형광성 결합 단백질에 의해 검출하는 계에 대해서도, 동일하게 적용할 수 있다.
또한, 본 발명의 활성화도의 산출방법(A), 및 본 발명의 활성화도의 산출방법(B)는, 본 발명의 진핵세포 어레이(10), 특히 수용체를 발현한 진핵세포 어레이(본 명세서에서, 수용체 어레이(10r)라고 하기도 한다)에도 적용할 수 있다.
활성화도는, Fmax/Fbase를 기본으로 한 수치계산에 의해, 다른 수치 표현도 가능하다. 예를 들면, 수용체가 갖는 최대 활성화도를 100%로 하고, 그에 대한 비율(%)로 표현할 수 있다. 구체적으로는, 피험물질 대신에, 예를 들면 칼슘 이오노포어(세포 내의 칼슘 농도를 100%로 높이는 시약)나 dbcAMP(칼슘 채널의 CNG를 100% 활성화하는 시약) 등의 양성대조시약으로 처리함으로써, 수용체가 갖는 최대 활성화도를 구할 수 있다. 상기의 도 5의 예에서는, 최대 활성화도에 있어서의 Fmax/Fbase는 2.2라는 것을 미리 알고 있으므로, 도 5의 Fmax/Fbase=1.4의 측정치에 있어서의 피험물질에 의한 활성화는, 1.4/2.2=0.64, 즉 그 수용체가 갖는 최대 활성화도에 대하여, 64%가 발휘되었다, 고 표현할 수도 있다.
[수용체 어레이의 측정방법]
본 발명의 수용체 어레이(10r)에 대하여, 각 수용체에 대한 활성화도를 측정하는 방법은, 전형적으로는, 이하와 같다. 여기에서는, 활성화도의 산출방법(B)을 이용한 예를 이용하여 설명한다.
수용체 어레이(10r)에, 측정용 형광 물질, 측정용 형광 색소, 또는 형광성 결합 단백질을 작용시켜, 피험물질의 접촉에 근거하는 활성화도를 형광으로 치환되는 반응계를 수립한다.
계속하여, 수용체 어레이(10r)의 관통공(2)의 전체를 포함하는 영역을, 동시에 일괄하여 화상 데이터로서 취득하는 측정계를 수립한다. 여기서, 측정계는, 수용체 어레이(10r)의 관통공(2)(관통공(2A) 등)을 개별로 인식할 뿐만 아니라, 관통공(2) 내부의 각 진핵세포(진핵세포(4A1), (4A2), (4A3), (4A4), (4A5) 등)를 개별로 인식할 수 있도록, 수광(受光) 광학계를 설정한다.
계속해서, 피험물질을, 반응계를 수립한 수용체 어레이(10r)에 대하여 접촉시킨다.
여기서, 측정계는, 피험물질을 접촉시키기 전부터 동작시켜, 제1 소정 시간 동안, 화상 데이터를 취득한다.
또한, 측정계는, 피험물질을 접촉시킬 때 부근에서부터 동작시켜, 제 2 소정 시간 동안, 화상 데이터를 취득한다.
제2 소정 시간 경과 후, 진핵세포 각각의 형광을 수치화하고, 각 세포 단위로 수치를 연산함으로써 활성화도를 산출한다.
이 때, 각 세포 단위의 형광의 수치는, 슬라이스 레벨(형광 강도의 고정치)을 설정하는 수법에 의해, 품질관리를 실시하고, 소정치 이상의 데이터만을 채용하여, 각 세포 단위로 수치를 연산함으로써 활성화도를 산출하는 것도 허용된다.
또한, 각 세포 단위의 활성화도는, Fbase+5SD에 의한 판정에 의해, 품질관리를 실시하여, 신뢰성 높은 데이터를 채용하고, 출력하는 것도 허용된다.
또한, 각 세포 단위의 활성화도는, 공지된 통계 수법에 의해, 품질관리를 실시하여, 각 수용체마다, 1개의 데이터를 산출하고, 출력하는 것도 허용된다. 그 결과, 예를 들면, 400개의 수용체에 대하여, 400개의 활성화도의 수치를 출력하는 것이 허용된다.
본 발명의 방법에 따라 산출되는 수치는, 예를 들면, 이러한 수치의 산출 대상으로 한 수용체, 및 해당 수용체에 작용시킨 피험물질의 농도 등과 함께, 일군의 정보로서 이용할 수 있다.
따라서, 수용체가 후각 수용체인 경우에는, 본 발명에 의해 산출되는 수치를 포함하는 일군의 정보는, 이것을 데이타베이스로서 이용함으로써, 후술하는 본 발명의 냄새를 구성하는 방법, 또는 냄새가 구성된 조성물의 제조방법 등에 유용하다.
본 발명의 산출방법에 의해 얻어지는 수치는, 다음과 같은 다양한 용도에 사용할 수 있다.
예를 들면, 어떤 물질의 냄새를, 그 외의 2개 이상의 물질의 냄새를 조합함으로써, 재현하는 방법을 제공할 수 있다. 이에 대하여, 본 발명의 냄새를 구성하는 방법에서 상세하게 후술한다. 그리고, 어떤 물질의 냄새가 구성된 조성물을, 그 외의 2개 이상의 물질을 조합하여 재현하는 방법도 제공할 수 있다. 이에 대하여, 냄새가 구성된 조성물의 제조방법에서 상세하게 후술한다.
[냄새를 구성하는 방법]
본 발명의 목표물질의 냄새를 구성하는 방법(이하, 본 명세서에서, 이것을 「구성방법」이라고 방법 부르기도 한다.)은, 2개 이상의 표준물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도를 기준으로, 목표물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도가 구성되도록, 해당 2개 이상의 표준물질을 조합하여, 해당 목표물질의 냄새를 구성하는 방법이다.
상기의 2개 이상의 표준물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도의 입수 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 본 발명의 산출방법(A) 및/또는 산출방법(B)에 의해 얻어지는 수치를 이용할 수 있다.
상기의 목표물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도의 입수 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 본 발명의 산출방법(A) 및/또는 산출방법(B)에 의해 얻어지는 수치를 이용할 수 있다.
구체적으로 조합하는 방법에 대하여, 도 7에 나타낸 모식도를 기본으로 설명한다. 도 7의 모식도에서, 목표물질에 의한 냄새를 구성하는, 즉 목적물질에 의한 포유류 유래의 후각 수용체(예를 들면 α, β, γ, δ 및 ε)에의 활성화 정도를 나타낸다.
여기서, 표준물질로서, 예를 들면 a, b, c, d 및 e 중에서, a, c 및 e를 조합함으로써, 목표물질에 의한 포유류 유래의 후각 수용체의 활성화 정도를 구성할 수 있음을 도 7의 모식도에 나타내고 있다. 즉, 조합하는 방법은, 패턴 매칭법으로, 목표물질에 대한 후각 수용체 α, β, γ, δ 및 ε 에 있어서의 각각 활성화도와, 각 표준물질의 후각 수용체 α, β, γ, δ 및 ε 에 있어서의 각각 활성화도를 비교하여, 가장 가까운 것을 선발하는 방법이다. 대부분의 경우, 목표물질의 구성이, 1개의 표준물질에 의해 달성되지는 않기 때문에, 이러한 패턴 매칭법은, 복수회 실시된다. 예를 들면 도 7의 경우, 최초의 패턴 매칭법에 의해, 표준물질a가 선발되었다고 하면, 수용체 α, β, 및 γ에 대해서는 목표가 달성된 것이 되므로, 2회째의 패턴 매칭법에서는, 수용체 δ 및 ε에만 주목하여 실시된다. 그 결과, 표준물질 c가 선발되고, 동일하게 3회째의 패턴 매칭이 수용체 ε에만 주목하여 실시된 결과, 표준물질 e가 선발된다.
상기의 표준물질에 의한 포유류 유래의 후각 수용체의 활성화 정도에 대하여, 표준물질에 의한 포유류 유래의 후각 수용체에 대한 자극 농도(피험물질 농도)와, 그에 따라 반응할 때 나타나는 포유류 유래의 후각 수용체에 대한 활성화 정도와의 사이에, 선형성이 인정되지 않는 경우에는, 특정 농도의 표준물질에 의한 포유류 유래의 후각 수용체에 대한 활성화 정도를 기본으로 하여, 목표물질에 의한 포유류 유래의 후각 수용체에 대한 활성화 정도가 구성되도록 조합할 수 있다.
후각 수용체에 대한 자극 농도(피험물질 농도)와, 후각 수용체의 활성화도와의 사이는, 비선형인 경우가 많고, 또한 양자의 관계를, 함수로 나타낼 수 없는 경우도 있다. 이러한 경우에는, 복수 농도의 표준물질에 대하여, 각종 후각 수용체의 활성화도 데이터를 수집하고, 이러한 작업을 또한 복수의 표준물질에 대하여 실시하여, 수치화(데이터화)하는 것을 생각할 수 있다. 이와 같이 하여 얻은 데이터(이후, 제1 데이터라고 하기도 한다)는, 표준물질(복수), 농도(복수), 수용체(복수)의 삼차원 행렬로 나타낼 수 있다.
또한, 목표물질에 대하여 동일한 수치화를 실시하여, 제2 데이터를 얻을 수 있고, 일차원 행렬로 나타낼 수 있다.
따라서, 제1 데이터에 대하여, 제2 데이터를 이용하여 소정의 연산을 함으로써, 복수의 표준물질 후보와, 복수의 농도 후보와의 조합에 있어서, 목표물질에 가장 가까운 최적해를 얻을 수 있다. 또한, 연산 과정에 있어서, 복수의 표준물질을 이용하여 구성한 가상 물질(계산기상의 버추얼의 구성물질)에 대하여, 목표물질과의 차분을 구하여 검정하는 검정(檢定) 공정을 설치할 수도 있다.
[냄새가 구성된 조성물의 제조방법]
본 발명의 목표물질의 냄새가 구성된 조성물의 제조방법은, 2개 이상의 표준물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도를 기준으로, 목표물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도가 구성되도록, 해당 2개 이상의 표준물질을 조합하여, 해당 목표물질의 냄새가 구성된 조성물의 제조방법이다.
상기의 2개 이상의 표준물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도의 입수 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 본 발명의 산출방법에 의해 얻어지는 수치를 이용할 수 있다.
상기의 목표물질에 의한 포유류 유래의 각 후각 수용체에 대한 활성화 정도의 입수 수단은, 본 발명의 효과를 발휘하는 범위에 한하여, 특별히 한정되지 않는다. 예를 들면, 본 발명의 산출방법에 의해 얻어지는 수치를 이용할 수 있다.
구체적으로 조합하는 방법에 대해서는, 상기의 냄새를 구성하는 방법에서 설명하는 바와 같이, 도 7에 나타내는 모식도를 기본으로 설명할 수 있다. 즉, 도 7의 예에서는, 표준물질 a, c 및 e를 등량씩 혼합함으로써, 목표물질을 구성할 수 있다.
본 발명의 제조방법에 따라 제조되는 조성물은, 목표물질이 비싸더라도, 이것과 동등한 냄새를 구성하는 조성물을 저렴하게 작성할 수도 있다는 효과를 나타낸다.
[시료의 냄새를, 목적하는 냄새로 수정하기 위한 물질의 스크리닝 방법]
상술한 냄새의 구성 방법을 응용하여, 냄새의 수정을 실시할 수 있다. 즉, 수정하고자 하는 시료의 냄새와, 목표하는 냄새의 양방에 대하여, 후각 수용체(예를 들면 α, β, γ, δ 및 ε)에의 활성화도를 측정한다. 여기서, 활성화도의 평가는, 예를 들면 상술한 산출방법(A) 및/또는 산출방법(B)을 이용할 수 있다.
여기서, 목표로 하는 냄새와 수정하고자 하는 시료의 냄새 비교를, 각 수용체 마다 실시한다. 그 다음에, 특정 수용체에 대하여(예를 들면 수용체 α에 대하여), 표준물질로서 무엇을, 어느 정도 가하면 목표로 하는 수용체 α가 검지(檢知)하는 냄새에 가까워질까를 검토하여, 가산(加算)하는 후보 물질을, 복수의 표준물질에서 선발한다. 이 때, 수정하고자 하는 냄새와 선발한 표준물질을 가산한 냄새에 대하여, 수용체의 활성화도가, 목표로 하는 냄새의 수용체 α의 활성화도에 가까워졌는지의 여부를 판단 기준으로 하여, 선발을 실시한다.
냄새의 가산은, 실제로 표준물질의 혼합·구성일 수 있고, 계산기상의 버추얼 구성일 수도 있다. 목표로 하는 냄새에 가까워졌는지의 여부 판단은, 혼합·구성한 물질의 수용체 α에 대하여 구하는 활성화도를 기준으로 하여 실시한다. 이러한 조작을 수용체 α에 대하여 반복 실시하여, 가장 가까워졌을 때, 후보 물질의 선발을 실시할 수 있다.
이상은, 설명의 간단화를 위하여, 수용체 α에 대하여 주목하였으나, 복수의 수용체에 대하여, 이러한 조작을 동시에 실시하는 것도 가능하다. 예를 들면 수용체의 종류가 n종류인 경우에는, n차원 공간에서의 유클리드 거리가 최소가 되도록, 후보 물질을 선발할 수 있다.
또한, 표준물질에 의한 각 수용체의 활성화도에 관한 이미 알려진 정보를 데이타베이스에 수납해 두고, 데이타베이스의 정보와의 비교에 의해, 수용체의 활성화도가, 목표로 하는 냄새의 활성화도에 가까워졌는지 여부를 판단 기준으로 하여 선발을 실시할 수도 있다. 또한 데이타베이스는, 대표적인 냄새를 발하는 물질의 데이타베이스로서 상기 설명을 실시하였으나, 이것 이외에, 대표적인 냄새를 소거(消去)하는 물질의 데이터베이스일 수도 있다.
시료의 냄새를, 목적하는 냄새로 수정하는 방법은, 환경(공간)의 냄새를 쾌적한 것으로 수정하는 것으로 응용할 수 있는 외에, 환경(공간)의 냄새를 소거하여(소취하여), 쾌적한 것으로 수정하는 것에도 응용할 수 있다. 또한, 본 스크리닝 방법의 한층 더한 응용으로서 데오도런트 물질을 제공할 수도 있다.
[실시예]
이하에, 본 발명을 보다 상세하게 설명하기 위한 실시예를 나타낸다. 그러나 본 발명이 이하에 나타내는 실시예로 한정되지 않는다는 것은 말할 필요도 없다.
1) 마우스 후각 수용체의 단리(單離)
일본 SLC로부터 3-5주령의 C57/BL6J(암컷)를 구입하였다. 3mL의 Urethane solution(300mg/mL; U2500, Sigma-Aldrich)으로 정맥 마취한 후, 마우스를 단두하고, 빙상에서 후상피를 적출하였다. 적출한 후상피는 1mM의 Cystein을 함유하는 Ca2+ ringer solution(pH7.2; NaCl 140mM, KCl 5mM, CaCl2 1mM, MgCl2 1mM, HEPES 10mM, glucose 10mM, 및 피루브산나트륨 1mM)에 분산시키고, 1 units/mL의 papain, 또는 0.25mg/mL의 trypsin으로 처리하였다. 여기에, 0.1mg/mL의 DNase I, 0.1mg/mL의 BSA, 및 500μM의 leupeptin(trypsin의 경우는 0.025mg/mL의 trypsin inhibitor)을 함유하는 Ca2+ ringer solution을 등량 가하여, 효소 반응을 정지시킨 후, 셀 스트레이너에 2회 통과시켜, 큰 조직편을 제거하였다.
제거 후의 샘플에 대하여 원심분리 처리를 실시하고, 이것을 한번 세정하여, 후상피 유래 세포 용액을 얻었다.
2) 원셀 시스템의 이용 및 이를 이용한 해석 수단
상기에서 얻은 후상피 유래 세포 용액을 1000rpm, 5분간 원심분리(2420, KUBOTA Co.)를 실시하여 상청을 제거한 후, 여기에 250μL의 5μM Fluo 4-AM(F312, Dojindo), 0.02wt% Pluronic F-127(P6867, Molecular Probes)을 함유하는 Ca2+ ringer solution을 가하였다. As OneCell Picking 시스템(애즈원; 전자동 1세포 해석 단리장치[온도조절장치, 타임 랩스 장치, 관류장치부착]; 요시모토 외, Scientific Reports Vol. 3(2013) 1191; 이하, 본 명세서에서, 이것을 「원셀 시스템」이라 부르기도 한다.)용의 직경 10㎛ 나노 챔버를 약 40만개 갖는 폴리스티렌제 슬라이드를 2%의 PVP(폴리비닐피롤리돈(나카라이))에 담근 후, 원셀 시스템용의 관류지그에 설치하고, 상기 처리를 실시한 후상피 유래 세포 용액을 가하여, 가볍게 원심(7xg, 1분간, 3회)을 실시하여, 나노 챔버 내에 후상피 유래 세포를 격납하였다.
그 다음에, 원셀 시스템의 소정 위치에 설치하여, Ca2+ ringer solution을 순환시킨 상태로 유지하고, 4배 대물렌즈를 통하여, 나노 챔버에 포함되는 각 후상피 유래 세포의 Fluo-4 유래의 형광상(螢光像)의 확인을 실시하여, 형광 강도의 시간 변화를 기록하였다.
후상피 유래 세포에의 자극은 다음과 같이 실시하였다. 상기의 후상피 유래 세포가 격납된 슬라이드에 대하여, Ca2+ ringer solution을 2분간 환류(250μL/min)시킨 후, 100μL의 high K+ ringer solution(pH7.2; NaCl 40mM, KCl 100mM, CaCl2 1mM, MgCl2 1mM, HEPES 10mM, glucose 10mM, 피루브산나트륨 1mM)을 20초간 환류시켜, 일과성의 Fluo-4 유래의 형광의 증강에 의해, 후상피 유래 세포에 포함되는 후신경세포의 위치를 확인하였다. 그 결과, 슬라이드에 격납된 후상피 유래 세포 중, 후신경세포 개수는 약 1만개였다.
3) 후각 유전자의 동정
상기의 조건에서, 후상피 유래 세포에 대하여 냄새 분자인 2-펜타논(30μM)으로 10초간, 2-펜타논(3mM)으로 10초간 자극을 실시하고, 그 다음에 high K+ ringer solution에 의해 후상피 유래 세포에 포함되는 후신경세포를 동정하였다. 그 결과, 약 1만개의 후신경세포 중 약 100개가 2-펜타논에 반응하였기 때문에, 이들 후신경세포 중 임의의 2세포(세포 번호로 HI28-03, 및 HI25-18이라 한다)를, 원셀 시스템에 부속되는 유리 캐필러리로 1세포 단위로 회수하여(용량 50nL), 4.5μL Cell lysis solution(Cell Amp Whole Transcriptome Amplification Kit Ver.2; Takara)을 포함하는 PCR 튜브로 이동시켰다. 그 다음에, 즉시 동일 키트의 지시에 따라서, 역전사 반응을 실시하였다.
다음으로, 역전사 반응의 산물을 마우스 후각 수용체의 3번째의 막관통 도메인에 대한 포워드 프라이머(서열 번호 10)와, 7번째의 막관통 도메인에 대한 리버스 프라이머인 (서열 번호 11) 또는 (서열 번호 12)에 의해 PCR를 실시하였다.
PCR용의 효소는 LA-Taq(Takara) 그리고 PCR 버퍼는 GC buffer I(Takara)를 사용하여, 94℃ 1 min의 1 cycle 반응 후에, 94℃ 0.5 min, 40℃ 0.5 min, 72℃ 2 min의 35 cycles의 반응을 실시하고, 마지막으로 72℃ 5min의 1 cycle 반응을 실시하였다. 이와 같이 하여 얻은 DNA 단편(斷片)을 pMD20 플라스미드(Takara)에 서브클로닝하여, 2-펜타논에 반응한 세포(HI28-03 및 HI25-18)에서 발현하는 후각 수용체의 염기 서열을 결정하였다.
그 결과, HI28-03은 Olfr168(mOR271-1; GenBank accession number: AY317252)로, 그리고 HI25-18은 Olfr205(mOR182-11P; GenBank accession number: BC150839)로, 각각 동정되었다.
상기의 수법으로, 후상피 유래 세포에 포함되는 후신경세포 중에서, 냄새 분자로서 피리딘에 응답하는 2개의 후신경세포(각각, 세포번호 IG04-13과 HG28-24로 한다.)를 얻었다. 이들 세포에서 발현하는 후각 수용체를, 상기의 방법으로 동정한 결과, IG04-13은 Olfr45(mOR253-2; GenBank accession number: AY317653), 또한 HG28-24는 Olfr166(mOR270-1; GenBank accession number: AY317250)로 동정되었다.
그리고, 상기의 수법으로 후상피 유래 세포에 포함되는 후신경세포 중에서, 냄새 분자로서 2-부탄온에 응답하는 후신경세포(세포번호 HE22-23)를 얻었다. 이 세포에서 발현하는 후각 수용체를, 상기의 방법으로 동정한 결과, 후각 수용체 Olfr1258(mOR232-3; GenBank accession number: AY318460)인 것을 동정하였다.
4) 동정한 후각 유전자에 대한 활성화 정도의 산출방법(산출방법(A))
상기의 후신경세포 중, 2-펜타논에 의한 자극에 응답한 HI28-03 세포 및 HI25-18 세포에 대하여, 재차 2-펜타논에 의한 자극을 실시하고, 이들 세포 내에 대한 자극 후에 Ca2+ 이온이 수용된 양을, Fluo-4에 유래하는 형광 강도의 상승량으로서 측정하였다.
구체적으로는, 원셀 장치에 세팅한 후상피 유래 세포를 격납한 슬라이드 글래스에 상기의 Ca2+ ringer solution을 환류시키고, 2분 간격으로 후기하는 3mM의 2-펜타논을 함유하는 Ca2+ ringer solution 용액을 20초간 가하고, 각각의 후신경세포에 대한 일과성의 Fluo-4에 유래하는 형광 강도의 증강 정도를 5회 반복하여 측정하였다(도 8).
그 결과, HI28-03 세포에서는 형광 강도가 46±12로 증강되었다는 수치를 나타내고, HI25-18 세포에서는 38±10로 증강되었다는 수치를 나타내었다. 그러나, 이들 수치에 대한 CV치는, 모두 26%로 불안정한 측정이 되어 버렸다.
그래서, 상기의 high K+ ringer solution에 의해 2-펜타논에 응답한 HI28-03 세포 및 HI25-18 세포의 CNG 채널을 탈분극 시킨 경우에 얻어지는 Fluo-4에 유래하는 형광 강도의 상승치를 100%로 하고, 이 수치에 대한 각종 농도의 2-펜타논에 의한 자극 후의 양쪽 후신경세포의 Fluo-4에 유래하는 형광 강도의 상승치를 상대치로 표현한 경우(5회 각각 독립적으로 실험을 실시하였다), HI28-03 세포에서는 74±3, 그리고 HI25-18 세포에서 67±4가 되고, 그 CV치는 각각 4% 및 6%로 현저하게 안정되었다.
또한, 상기의 후신경세포 중, 피리딘에 의한 자극에 응답한 IG04-13 세포 및 HG28-24 세포에 대하여, 재차 피리딘에 의한 자극을 실시하여, 이들 세포 내에 대한 자극 후에 Ca2+ 이온이 수용된 양을, Fluo-4에 유래하는 형광 강도의 상승량으로서 측정하였다(도 9).
그 결과, IG04-13 세포에서는 형광 강도가 195±70으로 증강되고, 그리고 HG28-24 세포에서는 153±47로 증강되었다는 수치를 나타내었다. 그러나, 이들 수치에 대한 CV치는, 각각 36% 및 31%로 매우 불안정한 측정이 되어 버렸다.
그래서, 상기의 high K+ ringer solution에 의해 피리딘에 응답한 IG04-13 세포 및 HG28-24 세포의 CNG 채널을 탈분극 시킨 경우에 얻어지는 Fluo-4에 유래하는 형광 강도의 상승치를 100%로 하고, 이 수치에 대한 각종 농도의 피리딘에 의한 자극 후의 양쪽 후신경세포의 Fluo-4에 유래하는 형광 강도의 상승치를 상대치로 표현한 경우(5회 각각 독립적으로 실험을 실시하였다), IG04-13 세포에서는 120±6, 그리고 HG28-24 세포에서 132±5가 되어, 그 CV치는 각각 5% 및 4%로 현저하게 안정되었다.
상기 측정계의 고도의 정량성은, Fluo-4에 유래하는 형광 강도의 변화량이 그 피크의 높이에 근거하여 측정될 뿐만 아니라, 피크의 면적에 근거한 측정에서도, 유지되고 있다는 것도 확인되었다. 그리고, 후각 수용체를 발현하는 후신경세포에 존재하는 CNG 채널의 탈분극을 일으키는 약제는, high K+ ringer solution 뿐만 아니라, 이미 알려진 이오노포어에서도 동일하게 사용 가능하다는 것이 확인되었다.
5) 재구성 실험
상기의 3) 및 4)에서 얻어진 마우스 유래 후각 수용체가, 확실하게 스크리닝에 사용한 냄새 분자에 응답하는지 확인하기 위하여, HEK293 세포 내에, 후각 수용체로부터, Gαolf를 포함하는 헤테로 삼량체 G단백질을 거쳐, 아데닐산 고리화효소를 활성화시켜 ATP로부터 cAMP를 축적시키고, 세포 내 cAMP 농도 의존적으로 루시페레이스 발현을 유도하는 계를 재구성하였다.
구체적으로는, 마우스 유래 후각 수용체 유전자인 Olfr168, Olfr205, Olfr45 및 Olfr166와 서열 번호 9로 나타내는 아미노산 서열을 코드하는 DNA를 각각 융합시킨 유전자를, SRα 프로모터의 하류에 편입시킨 pME18S 플라스미드, Gαolf를 발현시키는 서열 번호 2로 나타내는 아미노산 서열을 코드하는 염기 서열을 갖는 플라스미드, 후각 수용체를 골지체로부터 세포 표층에의 제시 효율을 상승시키는 인자인 서열 번호 6에 기재되는 염기 서열을 갖는 Receptor-transporting protein 1S(RTP 1S)를 발현시키는 플라스미드 및 cAMP 응답성 루시페레이스 발현 플라스미드 pGlosensor-22(프로메가)를 Lipofectamine 2000(Life Technologies)에 의해 HEK293T 세포에 도입하여, 일과성 발현시켰다.
이로 인해, 마우스 유래 후각 수용체 유전자인 Olfr168을 발현시킨 경우, 단계적으로 희석한 냄새 분자 2-펜타논으로 자극하여 유도된 루시페레이스 활성을 측정한 바, 2-펜타논에 대하여 농도 의존적으로 루시페레이스 활성이 상승하여, EC50치가 2.1±0.6mM로 산출되었다. 이것은, Olfr168을 발현하는 후신경세포(도 8)와 유사한 2-펜타논에 대한 응답성이고, Olfr168을 활성화 가능한 냄새 분자의 하나는 2-펜타논이라는 것을 나타내고 있다. 또한, Olfr205를 발현하는 HEK293 세포의 EC50치(약 4mM)는 Olfr205를 발현하는 후신경세포와 유사한 2-펜타논에 대한 응답성을 나타내었기 때문에, Olfr205를 활성화 가능한 냄새 분자의 하나는 2-펜타논이라는 것을 나타내고 있다. 다음으로, Olfr45 또는 Olfr166을 발현하는 HEK293 세포의 EC50치(약 5mM)는 Olfr45 또는 Olfr166를 발현하는 후신경세포와 유사한 피리딘에 대한 응답성을 나타내었기 때문에, Olfr45 또는 Olfr166을 활성화 가능한 냄새 분자의 하나는 피리딘이라는 것을 나타내고 있다. 더욱이 Olfr1258를 발현하는 HEK293 세포의 EC50치(약 1.5mM)은 Olfr1258을 발현하는 후신경세포와 유사한 2-부탄온에 대한 응답성을 나타내었기 때문에, Olfr1258를 활성화 가능한 냄새 분자의 하나는 2-부탄온이라는 것을 나타내고 있다.
이상으로부터, 상기의 3)에 기재된 방법에 의하면, 임의의 냄새 분자에 대응되는 후각 수용체군을 발현하는 각 후신경세포를 단리(單離)하는 것이 가능하다는 것이 판명되었다.
6) 인간 후각 수용체 발현용 플라스미드의 제작
인간 유래 후각 수용체 유전자군에서 선발된 인간 유래 후각 수용체 유전자 404종류를, 각각 발현하는 플라스미드를 합성 DNA에 의해 구축한다. 서열 번호 X9로 나타내는 아미노산을 코드하는 유전자를, 상기의 각 인간 유래 후각 수용체 DNA와 융합시키고, 이들을 SRα 프로모터에 의해 발현시키도록 한다.
더욱이 1세포당의 인간 유래 후각 수용체의 발현량을 일정하게 하기 위하여, HEK293 세포 및 CHO 세포의 염색체상의 정해진 위치에게만 유전자가 삽입되는 Flp-In system(Invitrogen사) 대응의 플라스미드(pcDNA5/FRT)를 채용한다.
7) 인간 후각 수용체 발현을 서포트하는 인자군의 발현 플라스미드의 제작
인간 유래 후각 수용체 유전자를 포유류 세포에서 효율적으로 기능을 유지한 채로 발현시키기 위하여, 인간 유래 후각 수용체를 골지체로부터 세포 표층으로의 제시 효율을 상승시키는 인자라고 생각되고 있는 Receptor-transporting protein 1(RTP1)을 코드하는 DNA(서열 번호 5) 또는 그의 트랜스클립트 베리언트인 RTP1S(서열 번호 6), Receptor-transporting protein 2(RTP2)를 코드하는 DNA(서열 번호 7) 및 REEP1을 코드하는 DNA(서열 번호 8)를 포함하는 포유류 세포 발현용 플라스미드를 제작한다.
구체적으로는, pUC18 플라스미드의 멀티클로닝사이트에, 후성적 영향을 받기 어렵다고 여겨지는 Human Elongation Factor-1α(EF-1α) promoter와 Human T-Cell Leukemia Virus 1(HTLV1) 유래 LTR에 유래하는 the R segment and part of the U5 sequence(R-U5')와의 하이브리드 프로모터 및 SV40 유래 polyA 사이트 사이에 Kozak 규칙에 따라서 상기의 각 DNA(RTP1, RTP2, REEP1 및 약제 선택 마커인 블라스티사이딘 내성(Bsr) 유전자)를 텐덤에 삽입하고, Construct 1이라 명명하는 포유류 세포 발현용 플라스미드를 제작한다.
8) 인간 유래 후각 수용체 발현 세포에의 Gαolf 및 CNG 발현 플라스미드 제작
상기의 5) 재구성 실험에 기재된 방법에서는, 이소적(異所的)으로 세포에서 포유류 유래 후각 수용체를 발현시켜도, 그 냄새 분자에 의한 활성화를 측정할 때는 세포 내 cAMP 농도의 상승이 지표로서 사용되어 왔으나, 이러한 방법은 엔드포인트어세이로, 인간 유래 후각 수용체를 발현하는 세포군의 망라적이면서 동시에 하이스루풋의 해석을 가능하게 하는 리얼타임어세이는 아니다.
현재, cAMP 농도 의존적으로 형광 강도가 변화하는 Flamindo2 등의 형광 단백질은 몇 개 정도 존재하나, 그 대부분이 응답 가능한 cAMP 농도의 다이내믹 레인지가 좁거나, cAMP 농도 상승에 동반하여 형광이 감쇠하기 때문에 수많은 세포군에서 cAMP 농도가 상승한 세포를 순간적으로 선택하기에는 부적당하거나, 신속한 측정에 적합한 1파장 여기를 1파장의 형광으로 관찰하는 것이 없기 때문에, 세포 내 cAMP를 리얼타임으로 동시에 고감도로 측정할 수 있는 형광 검출계는 존재하지 않는다. 따라서, 인간 유래 후각 수용체를 발현하는 세포군의 리얼타임 해석을 실현하기 위하여, cyclic nucleotide gated ion-channel(CNG)을 동시에 발현할 필요가 있다.
그래서, CNG를 구성하는 3종류의 유전자(CNGA2 서브유닛, CNGA4 서브유닛, CNGB1b 서브유닛)의 발현을 시도한다. 사용되는 DNA는, CNGA2 서브유닛은 서열 번호 1, CNGA4 서브유닛은 서열 번호 3, CNGB1b 서브유닛은 서열 번호 4로 나타내는 염기 서열을 포함하는 DNA이다.
구체적으로는, 네오마이신 내성 유전자를 갖는 pcDNA3.1+/C-(K) DYK 플라스미드의 CMV 프로모터와 SV40 polyA 사이트 사이의 멀티클로닝사이트에, Kozak 규칙에 따른 CNGA2 서브유닛 유전자, SV40 polyA 사이트, hEF1-HTLV 프로모터, Kozak 규칙에 따른 Gαolf 유전자로 구성되는 합성 DNA를 텐덤에 삽입하고 이것을 Construct 2라 명명한다.
다음으로, 탈감작되기 어려운 CNGA2 서브유닛 3 아미노산 잔기(서열 번호 1로 나타내는 염기 서열이 코드하는 아미노산 서열의 342번째의 글루타민산, 460번째의 시스테인, 그리고 583번째의 글루타민산)의 변이체(E342G/C460W/E583M)를 사용하면, 세포 내 Ca2+ 농도의 감쇠가 억제되기 때문에, 엔드포인트어세이였다 하더라도, 인간 유래 후각 수용체의 활성화 효율이 약한 경우에 호적하다.
구체적으로는 발현 플라스미드는 CNGA2 서브유닛에 상기의 변이를 실시하여, Construct 2와 동일하게 제작한다(이것을 Construct M2라고 명명한다).
실제 측정에 세포 내 Ca2+ 농도의 상승을 측정하기 위해서는, CNG 서브유닛에 관해서 말하면 CNGA2 서브유닛만으로도 가능하고, Construct 2 및 Construct M2로 충분한 감도를 얻을 수 있으나, CNG가 갖는 활성을 더욱 충분히 발휘시키기 위해서는, CNGA4 서브유닛 및 CNGB1b 서브유닛도 발현시킬 수 있다.
그래서, pUC18 플라스미드의 멀티클로닝사이트에 hEF1-HTLV 프로모터와 SV40 유래 polyA 사이트 사이에 Kozak 규칙에 따라서 각 유전자(CNGA4 서브유닛 유전자와 CNGB1b 서브유닛 유전자 및 약제 선택 마커인 퓨로마이신 내성(Puro) 유전자)를 텐덤에 삽입하고, 이것을 Construct 3이라 명명한다.
9) HEK293 세포 및 CHO 세포에의 편입
HEK293 세포 또는 CHO 세포에, 상법(常法)에 따라서 Construct 1을 형질 전환시키고, 블라스티사이딘 선발을 실시하여, 블라스티사이딘 내성의 Construct 1을 안정적으로 유지하여 RTP1, RTP2, REEP1을 발현하는 세포를 얻는다. 다음으로, 상기의 형질 전환된 세포에 대하여, Construct 2를 형질 전환시키고, 네오마이신 선발을 실시하여, 네오마이신·블라스티사이딘 내성의 Construct 1과 2를 안정적으로 유지하고, RTP1, RTP2, REEP1에 가하여, CNGA2 서브유닛과 Gαolf를 발현하는 세포를 얻고, 각각 HEK293-C1/2주(株) 및 CHO-C1/2주라 명명한다.
또한, 양쪽 주에 대하여, Construct 3을 형질 전환하고, 퓨로마이신 선발을 실시하여, 네오마이신, 블라스티사이딘, 퓨로마이신 내성의 Construct 1, 2 및 3을 안정적으로 유지하여 RTP1, RTP2, REEP1, CNGA2 서브유닛, Gαolf, CNGA4 서브유닛, 및 CNGB1b 서브유닛을 발현하는 세포를 얻고, 각각 HEK293-C1/2/3주 및 CHO-C1/2/3주라 명명한다.
여기서, 인간 유래 후각 수용체를 발현하는 벡터가, 도입하는 세포의 염색체상의 정해진 위치에 편입되는 것을 목적으로 하여, 상기의 HEK293 세포 또는 CHO 세포 대신에, Flp-In-293 세포 및 Flp-In-CHO 세포(양쪽 세포 모두 Invitrogen사)를 이용하여, 상기의 Construct 1과 2, 및 Construct 1, 2 및 3을 안정적으로 유지하는 발현주의 제작도 동일하게 실시한다. 이들을, 각각 F293-C1/2; FCHO-C1/2; F293-C1/2/3; FCHO-C1/2/3이라 명명한다.
10) 임의의 냄새에 응답하는 인간 후각 수용체의 단리
상기의 HEK293-C1/2주에 대하여, 상기 6)에서 제작되는 인간 유래 후각 수용체 발현 플라스미드 404종류를 형질 전환하고, 2)의 방법으로 원셀 머신에 탑재하고, 3)의 방법으로 임의의 냄새 분자(바닐린) 10mM로 자극을 실시하면, 몇개의 세포에서 형광 강도의 증가가 관찰될 것이 기대되므로, 이들 세포 회수(回收)를 실시하고, pME18S에 삽입된 인간 유래 후각 수용체 유전자부분을 증폭하는 PCR을 실시한다. 증폭된 염기 서열을 해석하면 OR10G4일 가능성이 있고, 기보(旣報)의 것과 일치한다(Mainland JD 외, Nature Neuroscience 17, 114-120(2014)).
또한, 5)의 방법으로 세포 내 Ca2+ 농도 변화에 근거하는 형광 강도를 다른 세포에서 반복 정량한 바, CV치 5% 전후로 극히 안정될 것이 기대된다.
동일한 결과는, 다른 냄새 분자인 1mM 쿠마린과 1mM 캐러멜 퓨라논에서, 각각 기보의 OR5P3(쿠마린 응답성 인간 유래 후각 수용체: Saito H 외, Science Signaling 2, ra9(2009))과 OR8D1(캐러멜 퓨라논 응답성 인간 유래 후각 수용체: Mainland JD외, Nature Neuroscience 17, 114-120(2014))으로 동정되므로, 본 방법을 이용하면, 임의의 냄새 분자에 대응되는 인간 유래 후각 수용체의 단리가 가능해질 것이라 기대된다.
또한, 마찬가지로 상기 6)에서 제작되는 인간 유래 후각 수용체 발현 플라스미드 404종류와 pOF44 플라스미드(Invitrogen)를 F293-C1/2주로 형질 전환하고, 히그로마이신 내성·제오신 감수성의 세포를 선발하여, 상기와 동일한 어세이를 실시하면, 바닐린에 응답하는 인간 유래 후각 수용체로서 OR10G4가 동일하게 단리될 것이 기대된다.
11) 인간 후각 수용체 발현 세포 어레이의 작성법
상기 6)에서 제작되는 404종류의 인간 유래 후각 수용체 발현 플라스미드의 pcDNA5/FRT-Rhod-KP290534.1 1μL(DNA량: 500ng)를, 유전자 도입 시약인 Lipofectamine2000(Invitrogen) 1μL와 혼합하고, 이것을 기판상에서 어레이 형태가 되도록 100pL씩 도트 프린트를 실시한다. 사용된 기판은 슬라이드 글래스(마츠나미가라스) 표층을 플라스마 처리 장치(야마토과학 PM100)로 플라스마 처리하여 친수성을 높인 것이다. 도트 프린트에 사용한 기계는, MicroJet사의 LaboJet-500을 이용한다. 여기서, 기판에 고착시키는 플라스미드 및 유전자 도입 시약을 포함하는 복합체는, 직경 50㎛ 정도가 되도록 배치한다.
12) 인간 후각 수용체 발현 세포 어레이를 이용하여 임의의 냄새에 응답하는 인간 후각 수용체의 단리
상기 11)의 방법으로, 어레이용 슬라이드 글래스의 404 개소에 각각 상기의 인간 유래 후각 수용체의 발현 플라스미드를 고정화하고, 각각의 고정화된 부위의 상부로부터 HEK293-C1/2주를 각각 등량이 되도록 적하하고, 특정의 배양 조건에서 정치(靜置)하여 2일 후에 관찰한 바, 플라스미드를 고정화하고 있는 개소에, 적하된 HEK293-C1/2주가 증식하여 콜로니를 형성할 것이 기대된다.
동시에, EGFP(녹색 형광 단백질) 발현 플라스미드를, 동일하게 고정화한 어레이용 슬라이드 글래스도 대조로서 검토한 바, 모든 고정화 부위에 콜로니가 형성되어, EGFP의 발현을 확인할 수 있다고 기대된다.
그 다음에, 2)에 나타낸 방법으로 상기의 원셀 시스템에 콜로니가 형성된 기판을 탑재하고, 3)에 나타낸 방법으로 임의의 냄새 분자인 바닐린을 이용하여, 이것을 10mM의 농도로 자극을 실시한 바, 몇 개의 세포에서 형광 강도의 증가가 관찰되었다.
그 중에는, 상술한 OR10G4 발현 플라스미드를 고정화한 장소에 콜로니화하여 생육하는 HEK293-C1/2주가 존재할 것이 기대된다. 5)에 나타낸 방법으로 세포 내 Ca2+ 농도 변화에 근거하는 형광 강도를 다른 세포로 반복 정량한 바, CV치 5% 전후로 극히 안정된다고 기대된다.
마찬가지로, 1mM 쿠마린과 1mM 캐러멜 퓨라논으로도 실시한 바, 각각 상술한 OR5P3과 OR8D1 발현 플라스미드를 고정화한 장소에 콜로니화하여 생육하는 HEK293-C1/2주가 존재한다고 기대된다.
이상과 같이, 본 방법을 이용하면, 임의의 냄새 분자에 대응되는 인간 유래 후각 수용체의 단리가, 세포 회수를 하지 않아도 실시할 수 있다는 것이 기대된다.
13) 인간 후각 수용체 발현 세포 어레이의 작성, 및 산출방법(B)에 의한 활성화도의 측정
상기 11), 12)의 인간 후각 수용체 발현 세포 어레이의 작성법을, 본 발명의 어레이(1), 수용체 어레이(10r)에 적용한 실시예를 다음에 나타낸다.
이용된 기판(5)은, 슬라이드 글래스(마츠나미가라스)를, 플라스마 처리하여 친수성을 높인 것이다. 또한, 소수성 피막(6)은, 불소계 수지로, 스크린 인쇄에 의해, 관통공(2)을 복수 가진 소수성 피막(6)을, 기판(5)상에 형성하였다. 여기서, 소수성 피막(6)의 23℃에서의 물을 이용한 접촉각은, 150°였다.
상기 6)에서 제작되는 404종류의 인간 유래 후각 수용체 발현 플라스미드의 pcDNA5/FRT-Rhod-KP290534.1 1μL(DNA량: 500ng)를, 유전자 도입 시약인 Lipofectamine2000(Invitrogen) 1μL와 혼합하고, 이것을 각 관통공(2)에 대하여, 100pL씩 도트 프린트를 실시하였다. 여기서, 기판(5)에 고착시키는 플라스미드 및 유전자 도입 시약을 포함하는 복합체는, 직경 50㎛ 정도가 되도록 프린트 되어 있다. 이와 같이 하여 어레이(1)를 완성시켰다.
이어서, 어레이(1)의 각 관통공(2)에 대하여, HEK293-C1/2주를 각각 등량이 되도록 적하하고, 1개의 관통공(2)에 대하여 복수의 진핵세포가 수용되어, 진핵세포 어레이(10)를 완성시켰다.
계속해서, 특정의 배양 조건에서, 2일간 인큐베이션 하였다. HEK293-C1/2주는 증식하여, 각 관통공(2)의 내부에서, 복수의 세포에 일과성 발현이 유도되고, 복수의 수용체가 형성되었다. 이와 같이 하여 수용체 어레이(10r)를 완성시켰다.
수용체 어레이(10r)에 대하여, 피험물질로서 라텍스·링거액을 접촉시키고, 산출방법(B)에 의한 활성화도 측정을 실시하였다. 여기서, 라텍스·링거액이란, 라텍스를 250℃로 가열하고, 발생한 가스를 링거액에 포집한 용액이다. 활성화도의 측정에 있어서는, 칼슘용 형광 지시약인 Calbryte 520AM 용액을 이용하여, 세포 내의 칼슘 농도의 변화를, 형광 강도로서 관찰하였다.
여기서, Calbryte 520AM 용액은, Calbryte 520AM과, 계면활성제 Pluronic F-127을 포함하고, 링거액을 용매로 하는 용액이다.
또한, 형광 강도 측정의 제1 소정 시간은, 피험물질 접촉 6분전~1분전의 5분간의 시간(T0~T300초)이고, 제2 소정 시간은, 피험물질 접촉 0분후~10분후의 10분간의 시간(T360~T900초)이다.
수용체 OR5A1에 대하여, 수용체 OR5A1을 발현한 5개의 진핵세포에 대하여 측정한 형광 강도를, 도 10에 나타낸다. 도 10은, 횡축에 시간(초), 종축에 형광 강도를 나타낸 것이다. 5개의 곡선이, 각각 5개의 세포(Cell 1~Cell 5)를 나타내고 있다. 각각의 세포는, 피험물질에 대한 응답 특성이 각각 다르나, 경향은 매우 유사하다는 것을 알 수 있다(도 10에서, Fbase를 0으로 하는 원점 보정을 실시하였다).
이들 5개의 세포에 대하여, 각각 활성화도(Fmax/Fbase)를 산출하고, 5개의 평균치, 표준편차, 변동 계수를 구하였다. 평균치는 1.5, 표준편차는 0.08, CV치(변동 계수)는 5%로 매우 높은 재현성으로 측정되었다는 것을 확인할 수 있었다.
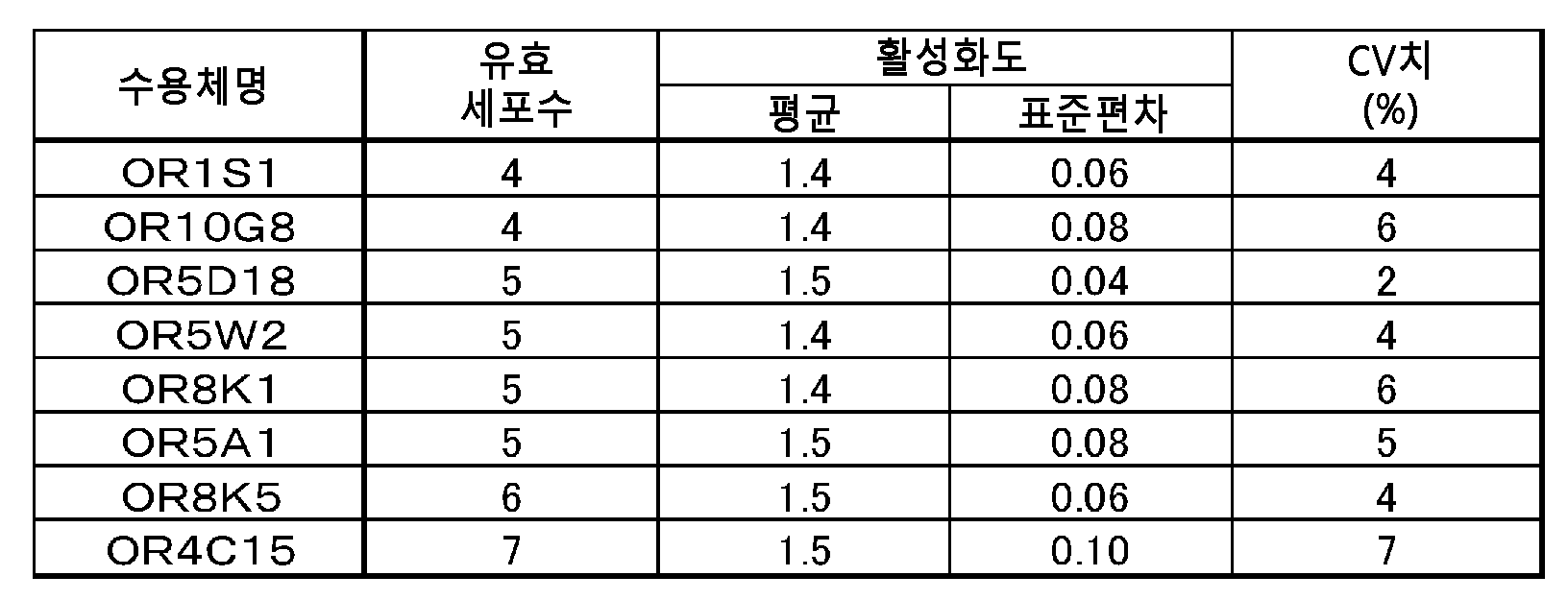
또한, 동일한 수법으로, 7개의 다른 수용체에 대하여, 각 수용체당 4개 이상의 세포수의 활성화도 측정을 실시하여, 데이터 검증을 실시하였다. 결과를 표 1에 나타낸다(표 1은, 수용체 OR5A1의 측정치도 포함한다). 모든 수용체에서, CV치(변동 계수)는 7%이하로, 높은 재현성으로 측정할 수 있다는 것을 확인할 수 있었다.
14) 화상 데이터 처리
본 발명의 활성화도 측정방법은, 관통공(2) 전체를 포함하는 영역을, 동시에 화상 데이터로서 일괄 취득하고, 관통공(2) 내의 진핵세포를 개별로 인식하여, 각 진핵세포의 각각의 형광을 수치화하는 공정을 포함하고 있다. 이러한 세포 하나 하나에 대한 개별 인식이나, 개별 데이터 처리, 연산 처리는, 공지된 화상 처리 소프트웨어를 이용하여 가능하다.
도 11은, 수용체 어레이(10r)에 대하여, 화상 데이터를 일괄 취득하고, 세포 단위의 개별 인식을 실시한 예를 나타낸다.
도 11의 [1]은, 화상 처리의 일례로서, 피험물질을 접촉시키기 1분전의 화상과, 피험물질을 접촉시킨 1분후의 화상의 차분 화상이다(Step 1). 소수성 피막(6) 안에 설치된 관통공(2) 99개를 일괄하여 눈으로 확인할 수 있다. 또한 각 관통공(2) 안에, 복수의 세포가 수용되어 있는 것을 알 수 있다.
도 11의 [2]는, 개별 데이터 처리의 일례로서, Step 1의 화상 데이터에 대하여, 형광 강도 200(슬라이스 레벨) 이상의 강도를 갖는 세포를, 1세포 단위로 인식하여, 세포 단위로 라벨화한 화상이다. 이러한 화상 샘플에서는, 1개의 관통공(2)에 대하여, 최대 2개의 세포가 형광 강도 200 이상을 나타내고 있는 것을 일괄하여 눈으로 확인할 수 있다.
도 11의 [3]은, 연산 처리의 일례로서, 피험물질을 접촉시키기 전후의 화상으로부터 세포 단위로 연산을 실시하고, Fmax≥Fbase+5SD Step이 되는 세포를, 1세포 단위로 판정하여, 세포 단위로 라벨화한 화상이다. 이러한 화상 샘플에서는, 전체 영역에 대하여, 3개의 세포가 판정 결과, 채용되고 있다.
이와 같이, 관통공(2)에 복수의 진핵세포가 수용되어 있는 경우라도, 세포 하나 하나를 개별로 인식하는 것은 가능하며, 세포 단위로 소정의 연산 처리를 실시하는 것은 충분히 가능하다.
15) 냄새의 구성(1)
멜론 냄새를 목표물질로 하고, 표준물질(오이 냄새, 바나나 냄새, 마요네즈 냄새)로 목표물질을 구성한다.
<샘플 조제>
시료(멜론, 오이, 바나나, 마요네즈) 각 3입방센티미터를, 30mL 바이알의 저부에 설치하고, 그 상부에 시료에 접촉시키지 않고, 실리카 모노리스 포집제(Mono Trap RGPS TD(GL사이언스사제))를 설치하였다. 실온에서 24시간 경과후, 실리카 모노리스 포집제를 꺼내고, 신속하게 포터블 서멀 디솔버 Handy TD TD265(GL사이언스사제)로 옮겨, 1초 30℃의 속도로 350℃까지 승온시키고, 링거 용액에 배출되는 냄새 성분을 버블링하여, 트랩하였다. 링거액의 조성은, 이하와 같고, pH7.2의 혼합액을, 4℃로 보존한 것이다:
NaCl 140mM
KCl 5mM
CaCl2 1mM
MgCl2 1mM
HEPES 10mM
D-글루코오스 10mM
피루브산나트륨 1mM
얻은 시료 유래의 냄새 성분을 포함하는 링거 용액은, 즉시 인간 후각 수용체 발현 세포 어레이(수용체 어레이(10r))를 이용하는 망라적 냄새 분석, 즉 냄새 성분을 포함하는 링거 용액을 피험물질로서 제공하여, 각 수용체에 대한 활성화도를 측정하였다. 측정방법은, 13)에 기재된 활성화도 측정과 동일하다.
분석:
각 시료 유래의 냄새에 의한 인간 후각 수용체의 활성화 정도를, 냄새 매트릭스에 의해, 시각화하였다. 냄새 매트릭스란, 매트릭스의 각 격자점이, 인간 후각 수용체 각각에 대응되는 개념이다. 구체적으로는, 인간 후각 수용체(396종류), 음성 대조 수용체(후각 수용체가 아닌 GPCR를 발현) 2종류, 수용체를 발현하지 않은 세포 2종류의 합계 400종류를, 20Х20의 격자점으로 표현하였다.
목표물질인 멜론 냄새를 도 12에 나타낸다. 또한, 표준물질A인 오이 냄새를 도 13의 [A], 표준물질 B인 바나나 냄새를 도 13의 [B], 표준물질 C인 마요네즈 냄새를 도 13의 [C]에 나타낸다. 이들 냄새 매트릭스의 데이터로부터, 목표물질인 멜론을 구성하려면, 오이 냄새를 베이스로, 바나나 냄새와 마요네즈 냄새를 혼합하면 되고, 구체적으로는, 표준물질 A(농도 a%)는 a=70%, 표준물질 B(농도 b%)는 b=20%, 표준물질 C(농도 c%)는 c=10%, 를 혼합하는 것이 최적이라고 판단되었다. 이들 비율에 따라 계산기적으로 구성한 냄새 매트릭스를, 도 13의 [D]에 나타낸다. 목표물질(도 12)과, 계산상의 구성물질(도 13의 [D])은, 서로 상사형을 나타낸다.
그 다음에 각 냄새 성분을 포함하는 링거 용액을, 상기 혼합비로 혼합하여, 구성 멜론 냄새로 하였다.
관능 시험:
상기 구성 멜론 냄새의 관능 시험을, 이마무라 미호 「화학과 생물」(Vol. 50, No.11, 2012)에 기재되어 있는 QDA법(정량적 묘사분석법)에 따라서 실시하였다.
사용한 샘플은, 상기의 방법으로 작성한 구성 멜론 냄새, 오이 냄새, 바나나 냄새, 마요네즈 냄새, 멜론 냄새를 각각 포함하는 링거 용액 1mL, 그리고 유사 냄새로서 수박 냄새, 호박 냄새, 복숭아 냄새, 멜론 소다 냄새를 각각 포함하는 링거 용액 1mL를 준비하였다.
볼런티어의 관능 시험원 20명이, 상기 샘플(전체 9종류)을 평가하였는데, 20명 중 18명이, 구성 멜론 냄새와 목표물질인 멜론 냄새(오리지널 멜론 냄새)가, 가장 공통된 특징적 향조(香調)를 갖고 있다고 판단하였다. 한편, 구성 멜론 냄새와 목표물질인 멜론 냄새 이외의 샘플이, 가장 공통된 특징적 향조를 갖고 있다, 고 판단한 사람은 없었다.
16) 냄새의 구성(2)
15)와 동일한 방법으로, 우유 유래 냄새 성분을 포함하는 링거 용액, 단무지 유래 냄새 성분을 포함하는 링거 용액, 콘스프 유래 냄새 성분을 포함하는 링거 용액을 준비하였다.
콘스프 냄새의 냄새 매트릭스를 구성하기 위해서는, 우유 냄새의 냄새 매트릭스와, 단무지 냄새의 냄새 매트릭스로부터, 우유 유래 냄새 성분을 포함하는 링거 용액과, 단무지 유래 냄새 성분을 포함하는 링거 용액을 등량 혼합하는 것이 적합하다고 판단되었다.
그래서 얻어진 구성 콘스프 냄새와, 목표물질인 콘스프 냄새(오리지널 콘스프 냄새), 그리고 동일하게 제작된 생크림 냄새, 클램 차우더 냄새, 콩소메 냄새를, 15)와 동일한 관능 시험에 의해 평가한 바, 구성 콘스프 냄새와, 목표물질인 콘스프 냄새(오리지널 콘스프 냄새)가 가장 공통된 특징적 향조를 갖고 있다고, 볼런티어의 관능 시험원 20명 중 17명이 판단하였다. 한편, 구성 콘스프 냄새와, 목표물질인 콘스프 냄새 이외의 샘플이 가장 공통된 특징적 향조를 갖고 있다고 판단한 사람은 없었다.