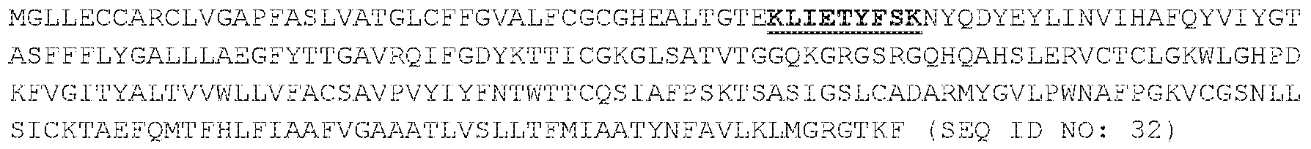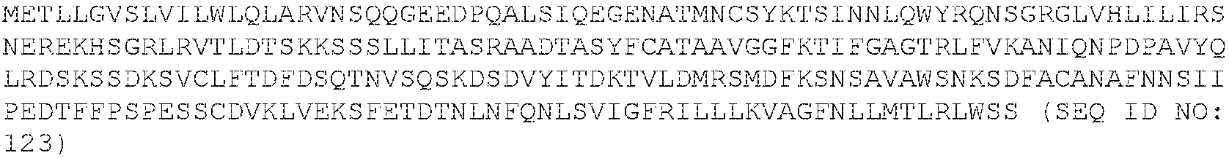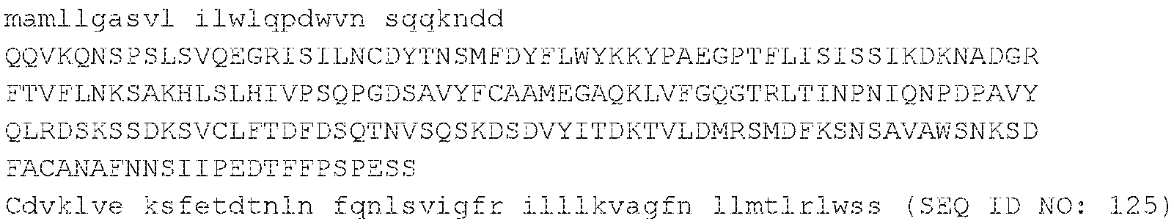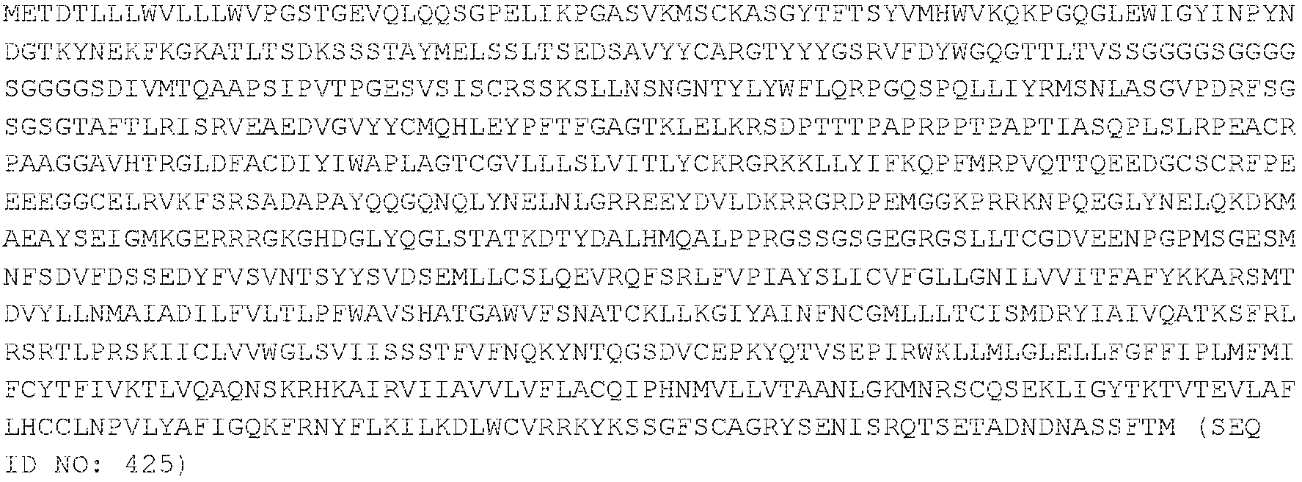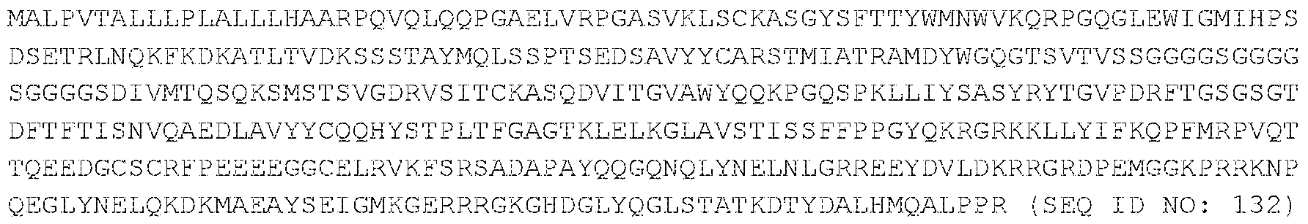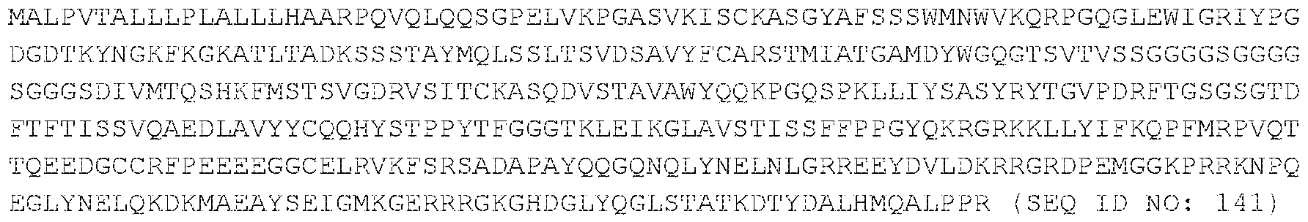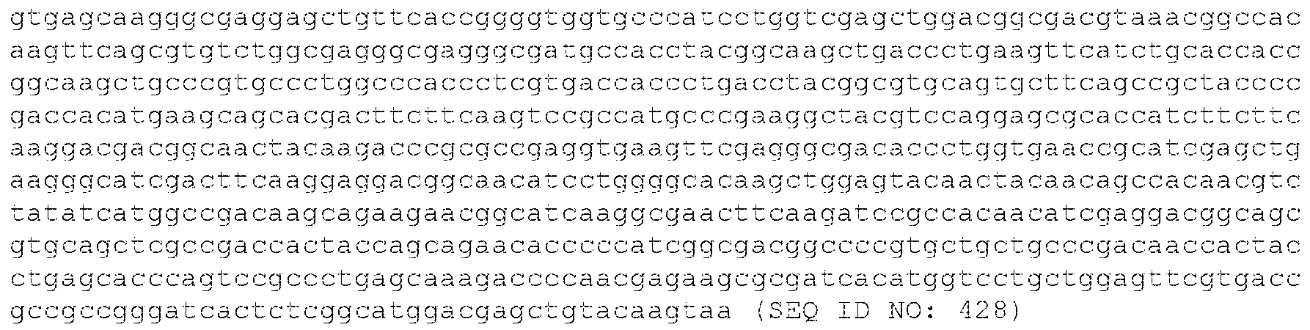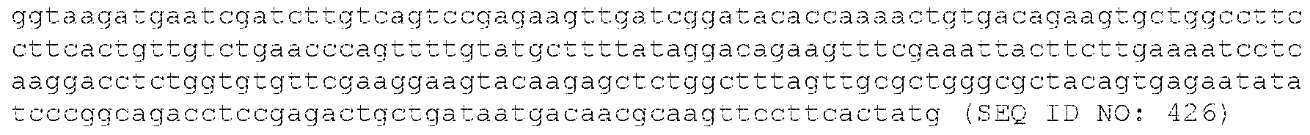자가반응성 T 세포(예를 들어, 다발성 경화증에 관여하는 미엘린 구성성분에 대한 것들)는 정상적인 개체에서 존재한다. 질병 유도의 대부분의 결정요인은, 이들 자가반응성 T 세포가 자가면역 환자에서(예를 들어, MS 환자에서) 촉발되는 경우 발생하는 면역 반응의 클래스에 존재한다. 병적 자가반응성 T 세포의 발생은 특이적인 주 조직적합성 복합체(MHC)와 비-MHC 유전자 둘 모두에 의해 선호되며, 이들은 개체가 반응하는 단백질 서열 및 면역 반응의 클래스를 결정한다.
일단, 면역 공격이 초기 자가항원(예를 들어, MS에서 미엘린 항원) 상에서 시작하면, 다른 자가항원에 대한 반응성의 확산이 존재하며; 즉, T 세포가 하나의 자가항원(예를 들어, MS에서 뇌 단백질)을 공격한다면, 다른 구조가 손상되고 이들은 추가의 T 세포가, 모든 자가면역 장애에 의해 공유되고 일반적으로 질병 반응에 보편적인 과정인 "에피토프-확산"이라고 하는 과정에서 다른 표적을 공격하도록 감작시킬 수 있다.
B 세포는 또한, 초기 자가반응성 공격에 의해 유발되는 초기 질병 병변, 예를 들어, 활성 MS 병변에서 면역 반응의 통상적인 구성성분이다. B 세포 축적은 패킹된 응집물 또는 이소성(ectopic) B 세포 여포(follicle)로서 발생한다. 문헌[Serafini et al., Brain Pathol. 14: 164-144 (2004); Wekerle, Autoimmunity, 50:1, 57-60 (2017); 및 Probstel, et al., International journal of molecular sciences, 16(7), pp.16576-16592 (2015)]. MS에서, B 세포는 RR-병기, SP-병기 및 P-병기 MS 환자의 뇌 및 척수에서 발견되는 것으로 보고되었다. B 세포를 직접적으로 또는 간접적으로 표적화하는 치료적 치료는 자가면역 질병, 예컨대 MS의 치료에 유익한 것으로 입증되었다. Wekerle, 2017.
CD4+ 세포와 CD8+ T 세포 둘 모두는 MS 병변에 존재하고, 질병 발달에 있어서 중심적인 역할을 하는 것으로 여겨진다. 미엘린-반응성(MBP, PLP 및 MOG) CD4 및 CD8 세포의 증가된 빈도는 건강한 대조군과 비교하여 MS 환자에서 발견된다. 문헌[Cao, et al., Sci. Transl. Med. 7 (287), 287ra74 (2014); Martin, et al., J. Exp. Med. 173 (Jan 1, 1991); Ota, et al., Nature 346, 183 (Jul 12, 1990); Pette, et al., Neurology 40, 1770 (1990); 및 Raddassi, et al., J. Immunol. 187, 1039 (2011)].
IFN-감마를 생성하는 Th1 세포 및 Th17 세포는 독특하게 병원성이다. Th1 세포의 발달을 촉진하는 인자는 MS 환자에서 상승되고, 또한 바이러스 감염에 의해 촉발되며: 감마 인터페론; IL-12 - 는 면역계에 영향을 주고 MS를 돕는 대체로 모든 치료에서, 대체로 모두 Th1 반응을 저하시키고 Th2 및 TH3 반응을 증가시킨다. Th17 세포는 조직 염증 부위에 존재하고, 자가면역 만성 염증성 질환에 연루되어 있다. Th17을 생성하는 CD4 및 CD8 세포는 환자의 병변, 혈액 및 CSF에서 증가된다. 문헌[Tzartos 2008; Matusevicius 1999; Bruchlacher-Waldert 2009]. Th17 세포 상에서 CCR6 및 CD161은 염증형성(inflamed) 조직으로 분자를 귀소시키는 것으로 가정된다[Cosmi, 2008].
Th17 세포는 또한, 많은 다른 자가면역 질병, 예컨대 전신 홍반성 루푸스, 류마티스성 관절염, 소아 특발성 관절염(소아 특발성 관절염으로도 알려져 있음), 쇼그렌 증후군, 전신성 경화증, 강직성 척추염, 1형 당뇨병, 자가면역 갑상선 질병(그레이브스 및 하시모토), 중증 근무력증, 염증성 장 질병(크론 또는 궤양성 대장염), 및 건선에 연루된다. 문헌[Tabarkiewicz et al., Archivum immunologiae et therapiae experimentalis, 63(6):435-449 (2015)].
자가면역 질병에 대한 임의의 치료의 궁극적인 목표는 병태(pathology)의 완전한 억제이다. 다발성 경화증 및 다른 자가면역 장애의 경우, 병적 림프구(B 세포와 T 세포 둘 모두, 및 필요하다면 매우 중증 경우의 경우 혈장 세포)는 질병 전개(course)를 중단시키기 위해 없어지거나 제어되어야 하는 것으로 예상되고, 질병 진행의 상이한 병기에서의 개입은 상이한 세포성 표적, 및 따라서 치료적 세포를 필요로 한다.
자가반응성 면역 세포, 예컨대 자가반응성 T 세포를 표적화하기 위한 주 조직적합성 복합체(MHC)-기반 키메라 수용체(MHC-CAR)가 본원에 개시된다. 본원에 기재된 바와 같은 MHC-CAR은 하나 이상의 MHC 폴리펩타이드 또는 이의 세포외 도메인 및 하나 이상의 세포 신호화 도메인, 예를 들어, 세포질 신호화 도메인(예를 들어, CD3ζ로부터의 것), 적어도 하나의 공동-자극 도메인(예를 들어, 4-1BB 또는 CD28로부터의 것), 또는 둘 모두를 포함한다. MHC-CAR은 자가항원 또는 자가면역 반응을 유발하는 데 있어서 자가항원을 모방하는 외래 항원으로부터의 항원성 펩타이드를 추가로 포함할 수 있다. 또한, MHC-CAR을 인코딩하는 핵산, 이를 운반하는 벡터, 및 MHC-CAR을 발현하는 유전적으로 조작된 면역 세포, 예컨대 T 세포 및 자연 살해(NK) 세포가 본원에 존재한다. 이러한 유전적으로 조작된 면역 세포는 자가반응성 면역 세포를 표적화함으로써 상기 자가반응성 면역 세포를 수반하는 자가면역 질병의 치료를 유익하게 하는 데 사용될 수 있다.
또한, 본원에 개시된 바와 같은 MHC-기반 키메라 수용체를 발현하는 유전적으로 변형된 조절 T(Treg) 세포가 본원에 개시된다. 이러한 Treg 세포는, T 세포 및/또는 B 세포 표면 마커를 표적화하는 키메라 수용체(들), 뿐만 아니라 예를 들어, 특이적인 조직 부위(예를 들어, 림프절 또는 염증 부위)를 표적화하거나 면역 반응(예를 들어, 체크포인트 조정)을 조정하기 위한 추가의 유전적 조작으로 추가로 변형될 수 있다. 유전적으로 변형된 Treg 세포는, 표적 질병의 초기-병기에서 병원성을 저해하거나, 상기 질병의 중간-병기(예를 들어, 재발형 또는 완화형 MS)에서 질병 진행을 제어하거나, 예를 들어 상기 질병의 말기-병기(예를 들어, 만성 진행형 MS)에서 병적 CD8+ T 세포의 세포독성의 유도를 통해 병태를 억제시키기 위해 사용될 수 있다.
I. 주 조직적합성 복합체(MHC)-기반 키메라 수용체(MHC-CAR)
본원에 기재된 MHC 기반 키메라 수용체(MHC-CAR)는 항원성 펩타이드(예를 들어, 잘못 접혀진 것)에 컨쥬게이션된 MHC 모이어티, 및 세포질 신호화 도메인(예를 들어, CD3ζ의 것)일 수 있는 적어도 하나의 세포 신호화 모이어티, 하나 이상의 공동-자극 도메인(예를 들어, 4-1BB 또는 CD28의 것), 또는 이들의 조합을 포함한다. 일부 경우, 항원성 펩타이드는 MHC-CAR의 융합 폴리펩타이드의 파트일 수 있다. 다른 경우에, 항원성 펩타이드는 MHC-CAR과 함께 융합 폴리펩타이드를 형성하지 않지만, MHC-CAR과 함께 복합체를 형성한다. 본원에 사용된 바와 같이, 용어 "컨쥬게이션된"은, 적어도 2개의 구성성분이 공유 결합을 통해 또는 비-공유 상호작용을 통해 물리적으로 연관됨을 의미한다.
일부 예에서, MHC-CAR은 MHC 모이어티, 항원성 펩타이드, 및 적어도 하나의 세포 신호화 모이어티를 함유하는 단일 융합 폴리펩타이드일 수 있다. 이러한 단일 융합 폴리펩타이드는 적합한 면역 세포에서 발현되는 경우 내인성 세포막 단백질(예를 들어, β-마이크로글로불린)과 함께 복합체를 형성할 수 있다.
다른 예에서, 본원에 기재된 MHC-CAR은 항원성 펩타이드를 포함하는 하나의 폴리펩타이드를 포함하는 다중-사슬 단백질 복합체, 예를 들어, 헤테로이량체(aheterodimer)일 수 있다. 일부 경우, 항원성 펩타이드 또는 폴리펩타이드는 별도의 폴리펩타이드로서 발현될 수 있으며, 이는 MHC 구성성분과 함께 복합체(예를 들어, 삼량체)를 형성할 수 있다. 항원성 폴리펩타이드는 MHC에 결합하는 잘못 접혀진 항원성 단백질일 수 있다. 선택적으로, MHC-CAR은, 항원성 펩타이드 및/또는 MHC 모이어티에 인접해 있을 수 있는 힌지 도메인, N-말단에 신호 펩타이드, 및/또는 하나 이상의 태깅 부위, 예를 들어, 히스티딘 단백질 태그 및/또는 추가로 사멸화-스위치 부위(kill-switch)로서 작용하는 RQR 도메인을 추가로 포함할 수 있다.
(i) MHC-CAR의 구성성분
(a) MHC 모이어티
본원에 개시된 MHC-CAR 구축물은 하나 이상의 MHC 폴리펩타이드 또는 이의 세포외 도메인을 포함할 수 있는 MHC 모이어티를 포함한다. MHC 모이어티는 적합한 공급원, 예를 들어, 인간 또는 비-인간 포유류(예를 들어, 원숭이, 마우스, 래트, 토끼, 돼지 등)으로부터 유래될 수 있다. 일부 경우, MHC 모이어티는 인간 MHC 분자(HLA로도 알려져 있음)로부터 유래된다. 일부 경우, 다른 세포로부터의 분자(TCR 또는 BCR)와 상호작용하는 도메인은 인간 MHC 분자로부터 유래된다. MHC 분자에는 주로 2개 클래스, MHC 클래스 I 분자 및 MHC 클래스 II 분자가 존재하며, 이들 둘 모두는 본원에 기재된 MHC-CAR을 구축하는 데 사용될 수 있다. 다양한 종(예를 들어, 인간, 비-인간 영장류, 개과(canid), 어류, 오비드(ovid), 소, 돼지, 수이드(suid), 쥐과(murid) 및 갈루스(gallus))의 MHC 클래스 I 및 클래스 II 분자의 서열은 공공 유전자 데이터세트, 예를 들어, EMBL-EBI에 의해 제공되는 IPD-MHC 데이터베이스 및 IMGT/HLA 데이터베이스 및 미국 국립 생물공학 정보 센터(NCBI)로부터 제공되는 dbMHC 데이터베이스로부터 입수 가능하다.
MHC 클래스 I 분자는 알파 사슬 및 β-마이크로글로불린을 함유하는 헤테로이량체이다. 알파 사슬의 세포외 도메인은 3개의 하위도메인, α1, α2 및 α3를 포함한다. 일부 구현예에서, MHC 모이어티는 MHC 클래스 I 분자의 알파 사슬 또는 이의 세포외 도메인, 예를 들어, α1 도메인, α2 도메인, α3 도메인, 또는 이들의 조합을 포함할 수 있다. MHC 클래스 I 분자는 인간 HLA-A 분자, 인간 HLA-B 분자 또는 인간 HLA-C 분자일 수 있다. 일부 경우, MHC 클래스 I 분자의 알파 사슬은 β-마이크로글로불린과 융합되어, 단일 사슬 융합 단백질을 생성할 수 있다. 일부 예에서, MHC 클래스 I 모이어티는 HLA A3로부터 유래되며, 이는 PLP 펩타이드와 함께 공동-사용될 수 있다. 문헌[Honma et al., J. Neuroimmunol. 73:7-14 (1997)]. 다른 예에서, MHC 클래스 I은 HLA A2로부터 유래되며, 이는 동일한 PLP 펩타이드와 함께 사용되고 바이러스 펩타이드, 예컨대 TAX를 제시할 수 있다. TAX는 인간 뉴런 단백질의 분자 모방체인 단백질 tax 또는 p40(Genbank 기탁 번호 BAB20130.1)으로부터 그리고 질병, 예컨대 류마티스성 관절염, 전신 홍반성 루푸스 및 쇼그렌 증후군에 연루된 HTLV-1 바이러스로부터 유래된다. 문헌[Garboczi, et al. The Journal of Immunology, 157(12):5403-5410, 1996. Quaresma, et al., 2015. Viruses, 8(1):5 2015]. 클래스 I 단백질 및 펩타이드는, 보다 강력한 펩타이드 적재(loading)가 중쇄의 위치 84에서 불변(invariant) 티로신을 알라닌으로 대체할 수 있도록 변형을 추가로 함유할 수 있거나; 대안적으로 펩타이드-β2m 링커의 제2 위치와 같이 위치 84 티로신은 시스테인으로 대체되어 이황화 트랩을 생성할 수 있다. 문헌[Hansen et al. Trends in immunology, 31(10):363 (2010)].
MHC 클래스 I 분자와 같이, MHC 클래스 II 분자 또한, 2개의 상동성 펩타이드, α-사슬 및 β-사슬로 구성된 헤테로이량체이다. α-사슬 및 β-사슬 각각의 세포외 도메인은 2개의 하위도메인 α1/α2, 및 β1/β2를 함유한다. MHC 클래스 II 분자가 MHC-CAR의 구축에 사용되는 경우, MHC 모이어티는 2개의 하위단위를 포함할 수 있고, 하나의 하위단위는 α-사슬 또는 이의 일부, 예를 들어, 이의 세포외 도메인(예를 들어, α1, α2, 또는 둘 모두)을 포함하고, 다른 하위단위는 b-사슬 또는 이의 일부, 예를 들어, 이의 세포외 도메인(예를 들어, β1, β2, 또는 둘 모두)을 포함할 수 있다. 다른 세포 유형과 상호작용하는 영역만 사용되는 경우(즉, α1 및 β1), 미니-MHC의 접힘(folding)을 증강시키기 위해서는 특이적인 아미노산 변형이 필요할 수 있으며, 음영 영역의 미니-서열 및 Birnbaum 등을 참조한다. MHC 클래스 II 분자는 인간 HLA DP 분자, 인간 HLA DM 분자, 인간 HLA DOA 분자, 인간 HLA DOB 분자, 인간 HLA DQ 분자 또는 인간 HLA DR 분자일 수 있다. 일부 예에서, MHC 클래스 II 분자는 인간 HLA DR 분자, 예를 들어, HLA DR*1501이다.
(b) 항원성 펩타이드
본원에 기재된 MHC-CAR의 항원성 펩타이드는 자가면역 질병에 관여하는 병원성 면역 세포(예를 들어, 자가반응성 T 세포 또는 B 세포)에 의해 인지 가능한 항원성 펩타이드이다. 적합한 MHC 분자에 의해 제시되는 경우, 이러한 항원성 펩타이드는 병원성 T 세포의 항원-특이적 T 세포 수용체와 상호작용하여, 다운스트림 면역 반응을 야기할 것이다.
일부 경우, 특이적인 항원성 펩타이드는 당업계에 알려진 방법을 사용하여 특이적인 자가면역 질병 환자, 예컨대 MS 환자에 대해 설계될 수 있다. NetMHC와 같은 프로그램은 환자의 MHC에 특이적인 항원성 펩타이드의 개인화된 설계를 가능하게 하고, 개인화된 암 백신을 개발하는 데 사용되어 왔다. 문헌[Hacohen et al., Cancer immunology research, 1(1): 11-15 (2013)]. 또한, 본 개시내용의 범위 내에는 자가면역 장애에 대한 개인화된 CAR T 및 Treg 치료법이 포함된다. 매우 강한 MHC 연관성을 갖는 장애(예컨대 MS)에 대해, 개인화된 치료법은 질병의 상이한 병기에서 대규모(large) 환자 클래스를 치료하는 데 이용될 수 있다. 최근의 연구는 또한, 자가면역 장애에 연루된 클래스 II MHC 및 특이적으로 HLA가 막 가공된 펩타이드보다 전체 항원성 단백질을 제시할 수 있음을 실증하였다. 문헌[Jiang et al., International immunology, 25(4):235-246, (2013)] 이들 MHC -단백질 복합체는, 특이적인 자가면역 장애를 갖는 것들에 특이적인 자가항체뿐만 아니라 적절하게 접힌 단백질에 결합하지 않는 항체를 포함하여 자가면역 장애에서 자가항체 생성을 유도하는 것으로 보인다. 본 발명자들은, MHC-CAR에서 항원성 단백질의 제시가 자가면역 특이적 B 세포, 예컨대 단백질에 대한 이의 특이성이 많은 철저한 시도에도 불구하고 밝혀지지 않은 올리고클로날 밴드를 생성하는 MS에서의 것들을 제거하거나 탈활성화시키기 위해 특이적인 경로를 제공할 수 있다고 생각한다. 문헌[Owens et al., Annals of neurology, 65(60):639-649, 2009; Chastre et al., New England Journal of Medicine, 374(15): 1495-1496, 2016; Housley et al., Clinical Immunology, 161(1):51-58, 2015; Larman et al., 2013. Journal of autoimmunity, 43: 1-9, 2013]. 항원성 단백질이 MHC에 결합하지 않는 경우, 해당 특이적인 MHC-CAR은 발현되지 않을 것이지만, Treg 또는 CTL로서 이는 여전히, 이의 다른 특징에 따라 그리고 상이한 특이성을 갖는 MHC-CAR T 및 Treg 세포의 환자 특이적 집단의 일부로서 면역 반응을 변형시키는 데 있어서 방관자 역할을 할 수 있다.
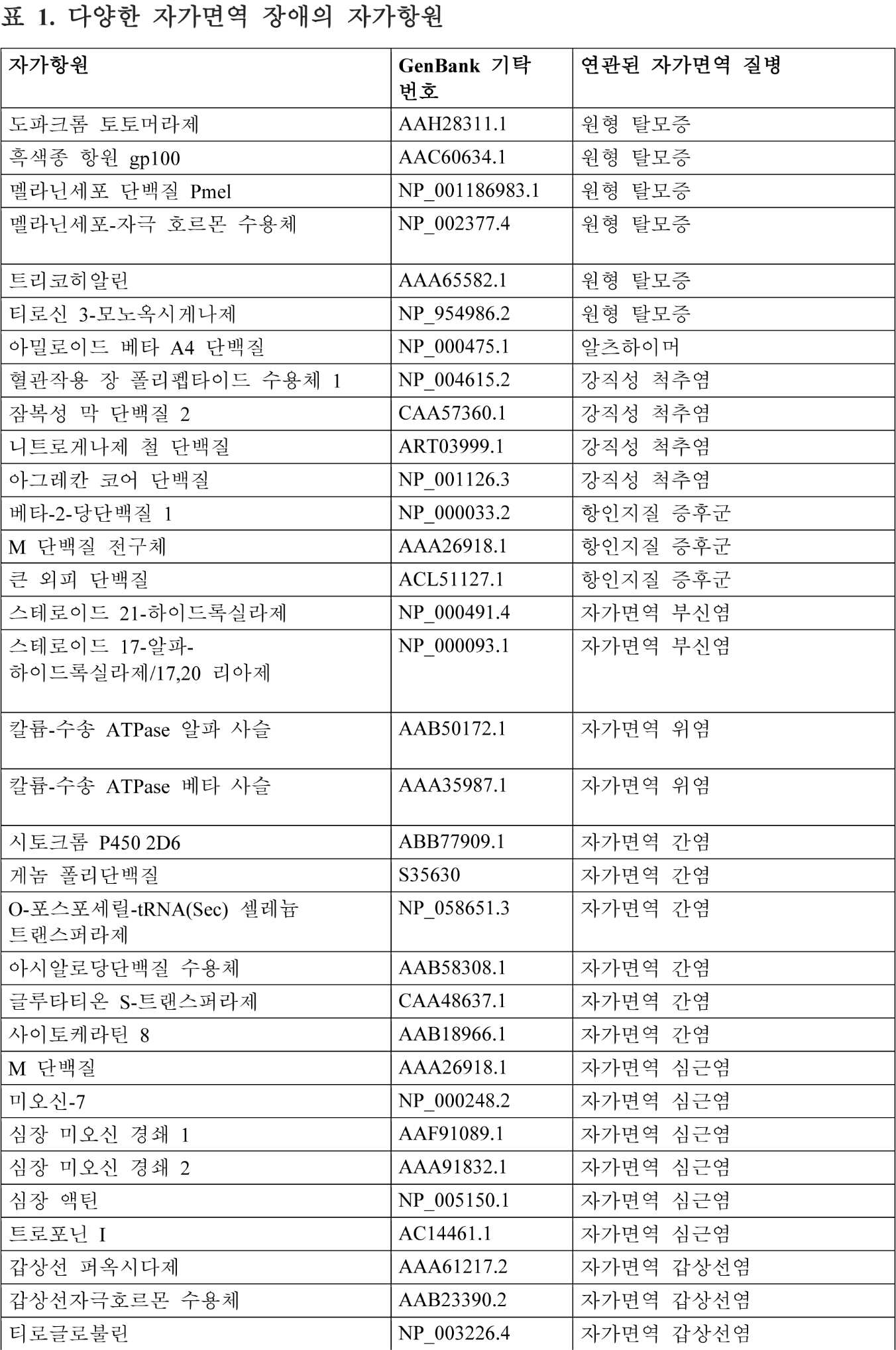
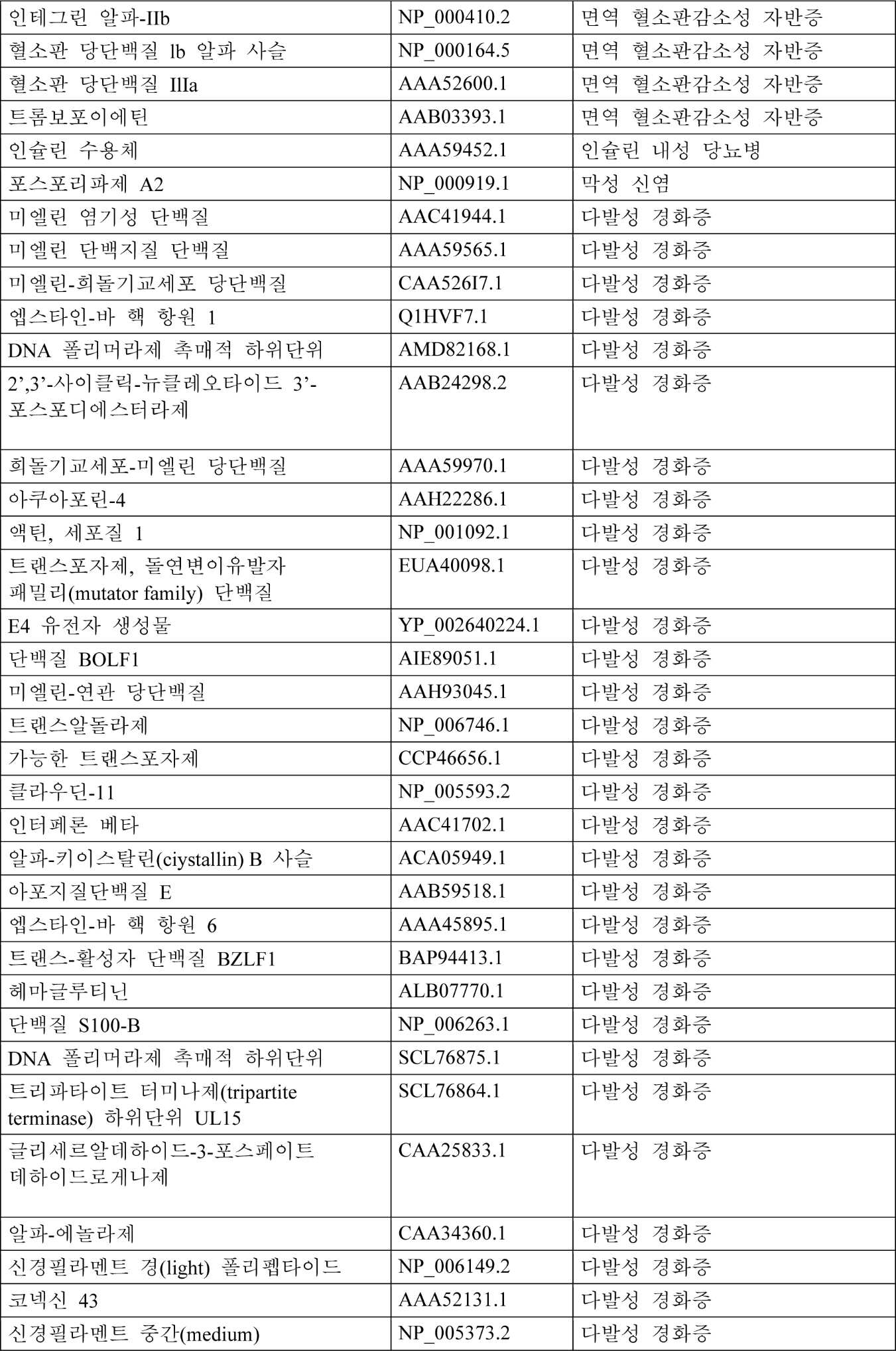
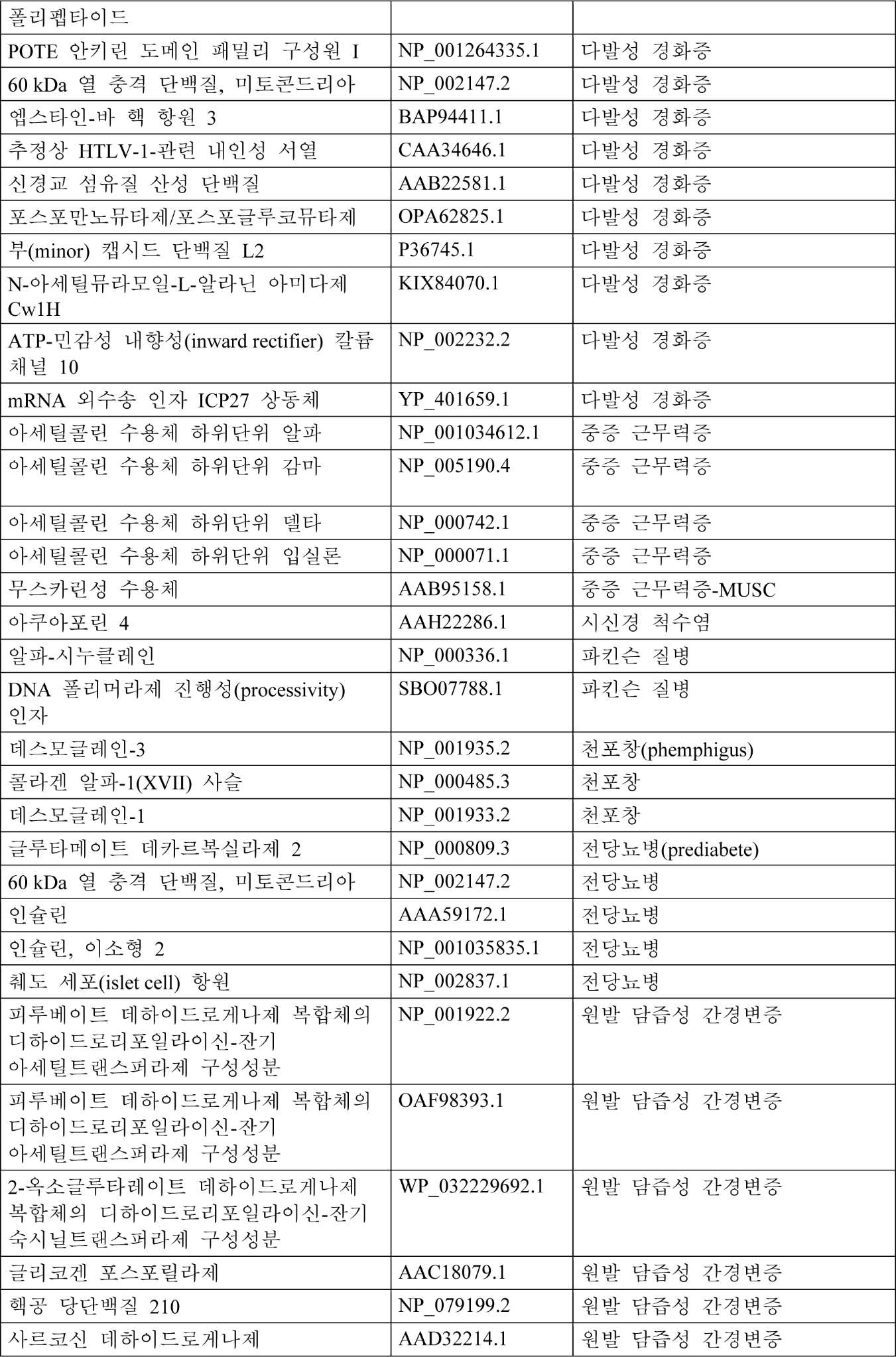
본원에 사용되는 항원성 펩타이드는 자가면역 질병에 관여하는 자가항원, 예를 들어, 다발성 경화증에 관여하는 미엘린 염기성 단백질(MBP), 미엘린 희돌기교세포 당단백질(MOG), 및 단백지질 단백질(PLP), I형 당뇨병에 관여하는 인슐린 및 글루타메이트 데카르복실라제(GAD), 류마티스성 관절염(RA)에 관여하는 트립타제, 및 하기 표 1에 포함된 단백질의 단편일 수 있다. 대안적으로, 항원성 펩타이드는 자가면역 질병에 관여하는 자가-항원에 고도로 상동성인 병원체 단백질, 예컨대 바이러스 또는 박테리아 단백질의 단편일 수 있다. 이러한 항원성 펩타이드는 또한, 표적 병원성 T 세포일 수 있다. 필요하다면, 항원성 펩타이드는, 개별적으로 발현될 수 있고 본원에 기재된 MHC-CAR의 MHC 모이어티에 직접적으로 결합하는 (전형적으로 잘못 접혀진) 항원성 단백질 또는 단백질 단편일 수 있다. 이들의 천연 상태(MHC-CAR의 MHC 모이어티보다는 MHC에 부착됨)에서, 이러한 항원성 단백질/MHC 복합체는 병원성 B 세포가 자가항체를 생성하도록 자극한다. 단백질, 예컨대 류마티스성 관절염에서 IgGH 또는 류마티스 인자(문헌[Jin et al., Proceedings of the National Academy of Sciences, 111(10):3787-3792, 2014]), 항인지질 증후군(문헌[Tanimura et al., Blood, 125(18):2835-2844, 2015]) 및 습관성 유산에서 β2-당단백질 I(문헌[Tanimura et al., Placenta, 46:108, 2016]), 자가면역 폐포 단백질증(pulmonary alveolar proteinosis)에서 GM-CSF(문헌[Hamano et al., ALVEOLAR MACROPHAGE BIOLOGY B32:A3147-A3147, 2016]), 백반에서 티로시나제(문헌[Arase et al. Journal of Dermatological Science, 84(1):e87, 2016]), 및 현미경 다발혈관염(microscopic polyangiitis)에서 미엘로퍼옥시다제(문헌[Hiwa et al., Arthritis & Rheumatology, 69(10):2069-2080, 2017])의 경우, HLA 매개 표면 제시 및 일부 경우, 잘못 접혀진 변이체/HLA 복합체의 자가항체 결합이 발생할 수 있다.
본원에 기재된 MHC-CAR에서 사용하기 위한 항원성 펩타이드는 20개 이하의 아미노산 잔기, 항원성 단백질의 세포외 도메인, 또는 전장 항원성 단백질을 함유할 수 있다. MHC 클래스 I 모이어티와 함께 공동-사용되는 경우, 항원성 펩타이드는 8 내지 10개 아미노산-길이일 수 있다. 이러한 항원성 펩타이드는 MHC 클래스 I 분자의 펩타이드 결합 부위 내로 잘 맞춰질(fit) 것이다. MHC 클래스 II 모이어티와 함께 공동-사용되는 항원성 펩타이드는 더 길 수 있으며, 예를 들어, 15 내지 24개의 아미노산 잔기 또는 항원성 단백질의 전장 이하를 함유할 수 있는데, 왜냐하면 MHC 클래스 II 분자의 항원-결합 그루브(groove)가 양쪽 말단에서 열려 있는 한편, 클래스 I 분자 상의 상응하는 항원-결합 그루브는 통상 각각의 말단에서 닫혀 있기 때문이다. 자가면역 장애에 연루된 MHC 클래스 II 분자의 열린 항원-결합 그루브는 또한, 온전한(예를 들어, 아직 잘못 접혀진) 항원성 단백질 또는 스플라이스(splice) 변이체를 빈번하게 제시할 수 있다. 문헌[Jiang et al., International immunology, 25(4):235-246, 2013].
일부 예에서, 인간 MBP의 단편은 본원에 기재된 MHC-CAR의 구축에 사용된다. 인간 MBP의 예시적인 아미노산 서열은 하기에 제공된다:
예시적인 MBP 항원성 펩타이드는 하기를 포함하지만 이들로 한정되는 것은 아니다:
SEQ ID NO: 15의 MBP 항원성 펩타이드를 인코딩하는 핵산 서열이 일례는 하기에 제공된다:
구체적인 예는 MBP13-32, MBP89-101, MBP83-99, MBP111-129 또는 MBP146-170을 포함한다.
인간 미엘린 희돌기교세포 당단백질, 단백지질 단백질 및 미엘린 연관 당단백질에 대한 예시적인 아미노산 서열은 하기에 제공된다:
>CAA52617.1 미엘린 희돌기교세포 당단백질[호모 사피엔스]
예시적인 MOG 항원성 펩타이드는 MOG1-20 또는 MOG35-55를 포함한다.
>AAA60117.1 단백지질 단백질 [호모 사피엔스]
PLP의 예시적인 항원성 단편은 밑줄표시 및 볼드체로 표시되어 있다. 다른 예는 PLP139-151(4) 또는 PLP178-191을 포함한다.
>AAH93045.1 미엘린 연관 당단백질 [호모 사피엔스]
하기 표 1은 다른 자가면역 질병과 연관된 추가의 예시적인 자가항원을 제공한다.
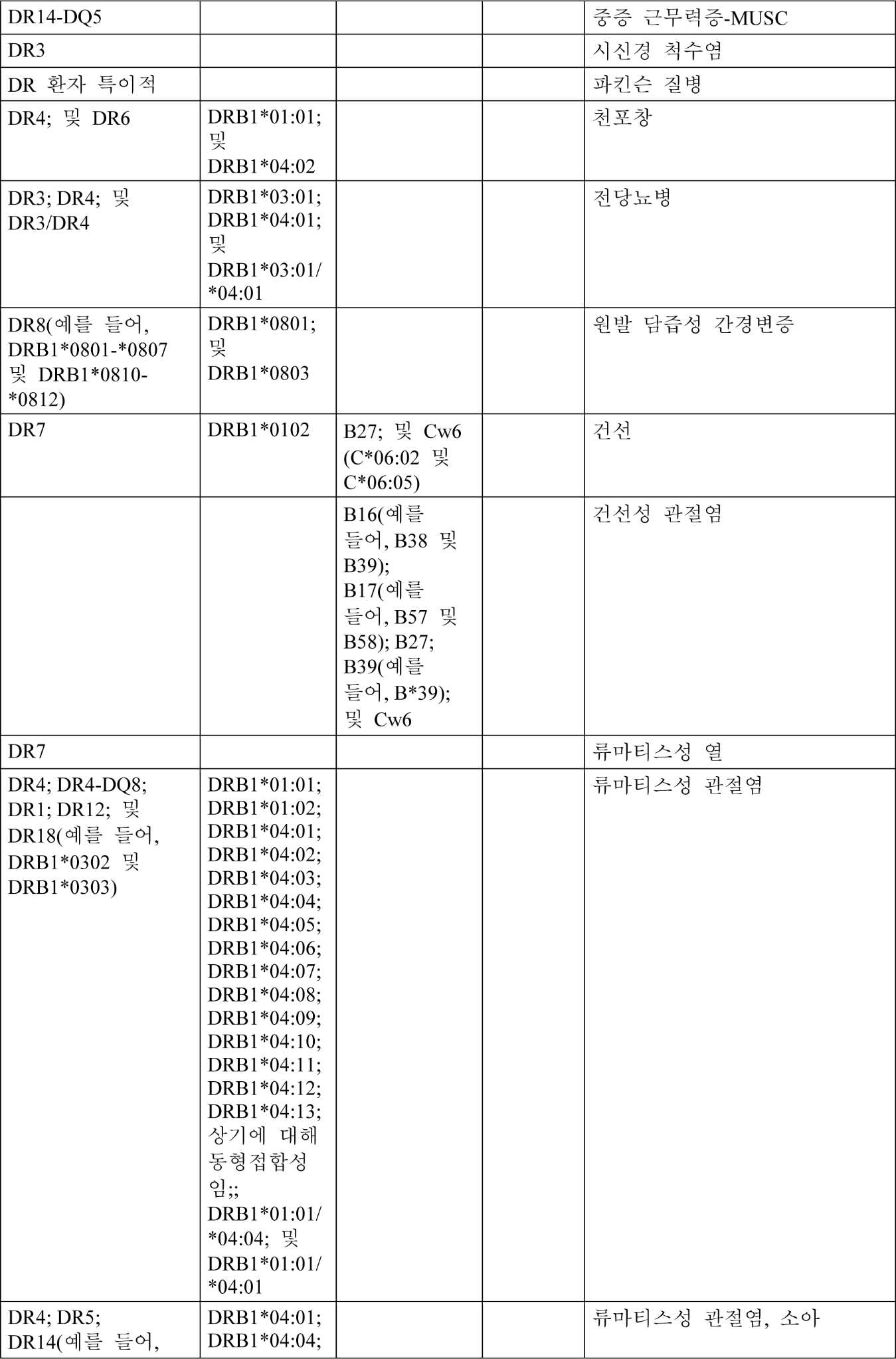
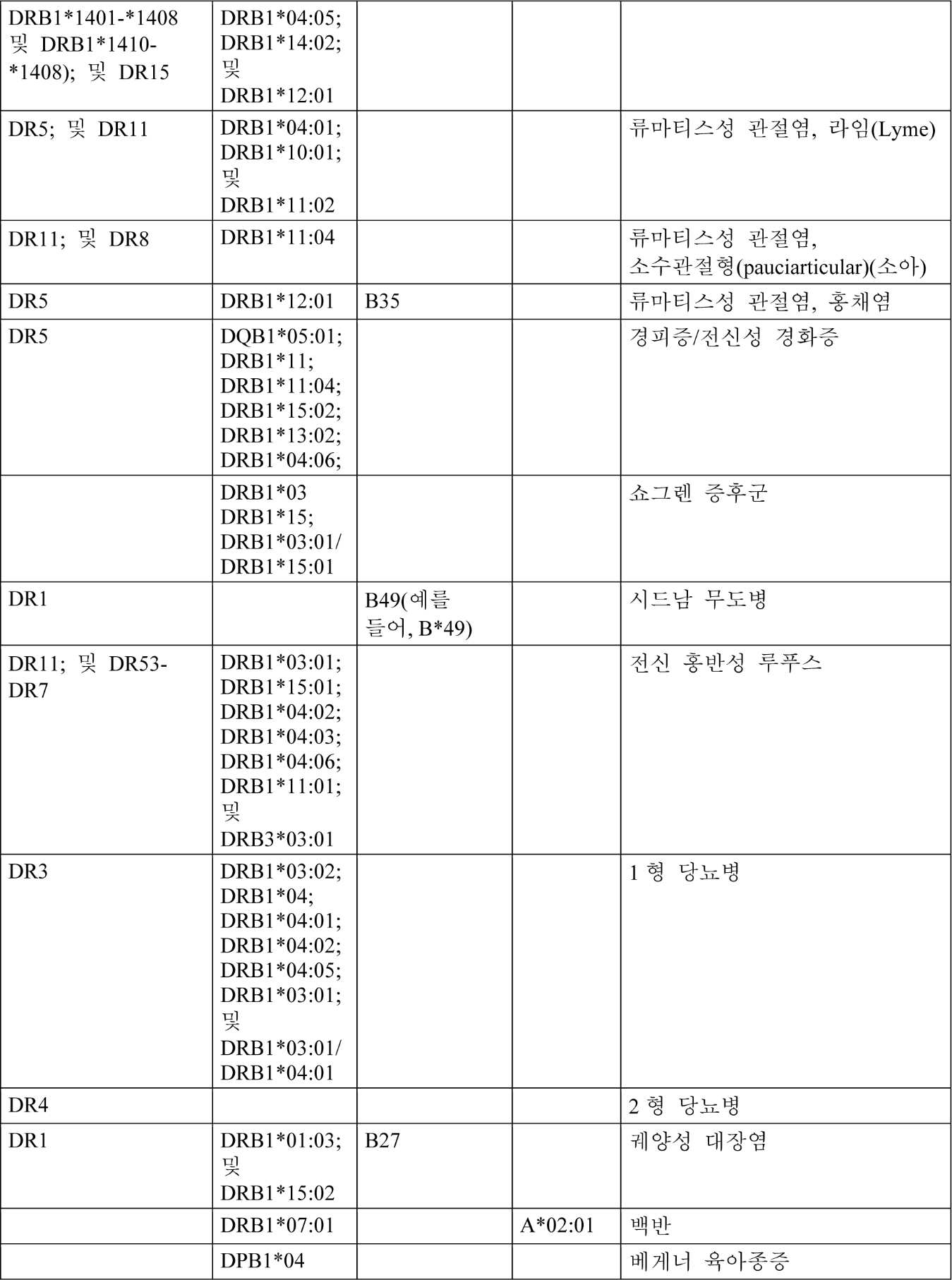
하기 표 2는 자가면역 장애와 공통으로 연관된 HLA 및 클래스를 제공하지만, 예시적인 경우 HLA 또는 이러한 HLA의 일부는 환자 특이적이고, 장애 또는 혈청학적 등가물을 앓고 있는 환자의 고분해능 서열로부터 유래될 것이다.
일부 구현예에서, 본원에 사용되는 항원 펩타이드는 HLA-DR*1501, 예를 들어, GAD 펩타이드 TYEIAPVFVLLFYVTLKKMR(SEQ ID NO: 34)(I형 당뇨병에 관여함), 상기 열거된 MBP 펩타이드, 하기 MPP 펩타이드(MS에 관여함) LLECCARCLVGAPFASLVATGLCFFGVALFC(SEQ ID NO: 35), LVGAPFASLVATGLCFFGVA(SEQ ID NO: 36), FGVALFCGCEVEALTGTEKLIETYFSKNYQD(SEQ ID NO: 37), LFCGCGHEALTGTEKLIETY(SEQ ID NO: 38), TGTEKLIETYFSKNYQDYEY(SEQ ID NO: 39), TGTEKLIETYFSKNYQDYEYL(SEQ ID NO: 40), YFSKNYQDYEYLINVIHAFQYVIYGTASFFFL(SEQ ID NO: 41), GTASFFFLYGALLLAYGFYTTGAVRQIFGDYK(SEQ ID NO: 42), LYGALLLAEGFYTTGAVRQI(SEQ ID NO: 43), FYYTTGAVRQIFGDYKTTICG(SEQ ID NO: 44), AVRQIFGDYKTTICGKGLSATV(SEQ ID NO: 45), RQIFGDYKTTCGKGLSATVTGGQKGRGSRGQ(SEQ ID NO: 46), KGLSATVTGGQKGRGYRGQH(SEQ ID NO: 47), QKGRGSRGQHQAHSLERVCH(SEQ ID NO: 48), KGRGSRGQHQAHSLERVCHCLGCWLGHPDKFV(SEQ ID NO: 49), LGHPDKFVGITYALTVVWLLVFACSAVPVYIY(SEQ ID NO: 50), SAVPVYIYFNTWTTCQSIAAPCKTSASIGTLC(SEQ ID NO: 51), AYPVYIYFNTWTTCQSIAFP(SEQ ID NO: 52), WTTCQSIAFPSKTSASIGSL(SEQ ID NO: 53), SASIGTLCADARMYGVLPWNAFFGKVCGSNLL(SEQ ID NO: 54), KVCGSNLLSICKTAEFQMTFHLFIAAFVGAAA(SEQ ID NO: 55), AAFVGAAATLVSLLTFMIAATYNFAVLKLMGR(SEQ ID NO: 56), MIAATYNFAVLKLMGRGTKF(SEQ ID NO: 57), 및 MAATYNFAVLKLMGRFTKF(SEQ ID NO: 58)와 연관이 있다.
일부 구현예에서, 항원성 펩타이드 또는 항원성 폴리펩타이드는 환자 특이적이고, 환자의 MHC에 대해 설계된다. 예를 들어, 의사는 자가면역 장애를 갖는 환자를 진단하고 질병의 중증도를 결정할 수 있다. 환자의 클래스 I(HLA-A, B 및 C) 및 클래스 II(HLA-DR, DQ, DP) 영역은 유형화(type)될 수 있으며, 이러한 유형화는 현재 DNA 시퀀싱을 사용하고 기준 데이터베이스(www.ebi.ac.uk/ipd/imgt/hla/)와 비교하여 고분해능(high resolution)으로 수행될 수 있다. 자가면역 관여의 가장 강한 증거를 갖는 환자의 클래스 I 및 II MHC는 장애에 대해 식별될 수 있다. 특정 자가면역 장애와 연관된 것으로 알려진 것들은 기준으로서 사용될 수 있다. 예를 들어, 표 1 및 표 2를 참조한다. 가장 강한 증거를 기반으로 한 항원은 장애(iedb.org/) 및 표 1에 대해 식별된다. 환자의 자가면역 연관 MHC에 결합하는 것으로 예상되는 개인화된 펩타이드(cbs.dtu.dk/services/NetMHC/ 또는 cbs.dtu.dk/services/NetMHCII/) 또는 단백질 표적(클래스 II에 대해)의 세트가 식별될 수 있다.
개인화된 MHC-CAR 렌티바이러스 또는 mRNA는 환자에 대해 병원성 면역 세포를 표적화할 수 있도록 제조될 수 있다. 개인화된 렌티바이러스는, 추가의 치료제와의 공동-치료, 병원성 세포와의 요망되는 상호작용, 요망되는 장소로의 전송(병원성 염증 세포 또는 염증 발생 세포와의 상호작용을 위해), 또는 사이토카인의 분비(염증을 감소시키기 위해)를 가능하게 하기 위해 수용체 또는 세포성 변형과 조합될 수 있는 자가 또는 동종이계 T 세포(CTL 및/또는 Treg)를 제조하는 데 사용될 수 있다.
(c) 공동-자극 신호화 도메인
많은 면역 세포는 세포의 효과기 기능을 활성화할 뿐만 아니라 세포 증식, 분화 및 생존을 촉진하기 위해 항원-특이적 신호의 자극 외에도 공동-자극을 필요로 한다. 본원에 기재된 MHC-CAR은 하나 이상의 공동-자극 신호화 도메인을 포함할 수 있다. 본원에 사용된 바와 같이, 용어 "공동-자극 신호화 도메인"은 면역 반응, 예컨대 효과기 기능을 유도하기 위해 세포 내에서 신호 전달을 매개하는 단백질의 적어도 일부를 지칭한다. 본원에 기재된 MHC-CAR의 공동-자극 신호화 도메인은 신호를 전달하고 면역 세포, 예컨대 T 세포, NK 세포, 대식세포, 호중구 또는 호산구에 의해 매개되는 반응을 조정하는, 공동-자극 단백질로부터의 세포질 신호화 도메인일 수 있다.
숙주 세포(예를 들어, 면역 세포)에서 공동-자극 신호화 도메인의 활성화는 사이토카인의 생성과 분비, 포식작용 특성, 증식, 분화, 생존, 및/또는 세포독성을 증가시키거나 저하시키기 위해 세포를 유도할 수 있다. 임의의 공동-자극 분자의 공동-자극 신호화 도메인은 본원에 기재된 MHC-CAR에 사용하기 위해 융화성(compatible)일 수 있다. 키메라 수용체에 사용하기 위한 공동-자극 신호화 도메인의 예는, 공동-자극이 특정 약물 분자(그러나 본원에서 독특한 헤테로이량체성 MHC-CAR과 연관됨)의 존재 하에서만 유도되게 하는, 비제한적으로 B7/CD28 패밀리의 구성원(예를 들어, B7-1/CD80, B7-2/CD86, B7-H1/PD-L1, B7-H2, CD28, CTLA-4, ICOS/CD278, 또는 PD-1); TNF 슈퍼패밀리의 구성원(예를 들어, 4-1BB/TNFSF9/CD137, 4-1BB 리간드/TNFSF9, CD40/TNFRSF5, CD40 리간드/TNFSF5, DR3/TNFRSF25, OX40/TNFRSF4, OX40 리간드/TNFSF4, 또는 TNF-알파); 및 다른 분자, 예컨대 FRB, 및 FKBF를 포함한 공동-자극 단백질의 세포질 신호화 도메인일 수 있다. 문헌[Wu et al., Science, 350(6258):aab4077, 2015]. 일부 구현예에서, 공동-자극 단백질의 임의의 세포질 신호화 도메인은 불활성 방관자 B 세포(예를 들어, CD19 또는 CD20-CAR이 있음) 또는 혈장 세포(예를 들어, CSl-CAR 및/또는 CS1 녹아웃이 있음)를 표적화하는 수용체에서 사용될 수 있다.
일부 경우, MHC-CAR은 조합(예를 들어, 2 또는 3) 공동-자극 도메인을 포함할 수 있고, 이는 동일한 공동-자극 수용체로부터 또는 상이한 공동-자극 수용체로부터 유래될 수 있다. 그 예는 하기를 포함한다: CD28+4-1BB, CD28+FRB, CD28+FKBF, 또는 4-1BB+FRB. 또한, 도 9를 참조한다. 일부 예에서, MHC-CAR은 CD28로부터의 공동-자극 도메인, 4-1BB로부터의 공동-자극 도메인, 또는 둘 모두를 포함한다. 일부 구현예에서, 공동-자극 도메인 전에 짧은 링커가 존재한다. 예를 들어, 클래스 II MHC-CAR에 대해, 짧은 링커는 TS(즉, MHC 내재(internal) 링커)일 수 있으며; 클래스 I MHC-CAR에 대해, 짧은 링커는 PG일 수 있다.
일부 경우, 본원에 기재된 MHC-CAR 구축물은 공동-자극 도메인을 포함할 수 있다. 대안적으로, 상기 구축물은 비-번역 요소, 예컨대 TALEN 뉴클레아제, 활성자, 또는 억제자를 함유할 수 있으며, 이는 현재 보고된 또는 비-반복체 함유 TAL 도메인을 사용하여 임상적으로 적용 가능한 렌티바이러스 형태로 실시될 수 있고 노치(Notch)로부터 유래되는 막 도메인을 통해 단일 사슬 MHC-CAR에 연결될 것이다.
본원에 기재된 MHC-CAR에 사용하기 위한 예시적인 공동-자극 도메인은 하기를 포함하지만 이들로 한정되는 것은 아니다:
(d) 세포질 신호화 도메인
면역수용체 티로신-기반 활성화 모티프(ITAM)를 포함하는 임의의 세포질 신호화 도메인은 본원에 기재된 키메라 수용체를 구축하는 데 사용될 수 있다. 본원에 사용된 바와 같이, "ITAM"은 많은 면역 세포에서 발현되는 신호화 분자의 꼬리 부분에서 일반적으로 존재하는 보존된 단백질 모티프이다. 모티프는 6 내지 8개의 아미노산에 의해 분리되는 아미노산 서열 YxxL/I의 2개 반복체를 포함하여, 보존된 모티프 YxxL/Ix(6-8)YxxL/I를 생성할 수 있으며, 여기서, 각각의 x는 독립적으로 임의의 아미노산이다. 일부 예에서, ITAM을 포함하는 세포질 신호화 도메인은 CD3ζ이다. 일부 예에서, MHC-CAR은 공동-자극 도메인을 포함하지 않고, 세포질 신호화 도메인 전에 짧은 링커가 존재한다. 예를 들어, 클래스 II MHC-CAR의 경우, 짧은 링커는 TS(즉, MHC 내재 링커)일 수 있다. 예를 들어, 클래스 I MHC-CAR의 경우, 짧은 링커는 PG일 수 있다. 일부 경우, 예컨대 공동-자극 도메인이 신호화 도메인 전에 발생하는 경우 소정의 상황에서, 링커는 AHA이거나 부재할 수 있다.
일부 구현예에서, MHC-CAR은 세포질 신호화 도메인을 포함하지 않을 수 있으며, 예를 들어, CD3ζ의 것을 포함하지 않을 수 있다. 이러한 CD3ζ-무함유 MHC-CAR은 표적 세포에 대해 억제 효과를 갖거나 표적 세포 사멸을 유도할 것이다. 문헌[Moisini, et al., The Journal of Immunology, 180(5), pp.3601-3611].
CD3ζ로부터의 예시적인 세포질 신호화 도메인이 하기에 제공된다:
CD3ζ로부터의 세포질 신호화 도메인을 인코딩하는 예시적인 핵산 서열이 하기에 제공된다:
(e) 추가의 구성성분
본원에 기재된 MHC-CAR은 선택적으로, 하기 구성성분 중 하나 이상을 추가로 포함할 수 있다: 힌지 도메인, 막관통 도메인, 신호(리더) 펩타이드, 및 펩타이드 링커.
일부 경우, 항원성 펩타이드는 생성된 MHC-CAR의 면역 표적화 활성을 증강시키고/시키거나 MHC-TCR 복합체에 대한 표적 세포에 의한 항체 반응을 감소시키기 위해 힌지 펩타이드에 연결될 수 있다. 일부 예에서, 힌지 펩타이드를 함유하는 MHC-CAR은 세포질 도메인을 포함하지 않을 수 있다(예를 들어, CD3ζ 도메인이 없음). 힌지 펩타이드를 함유하는 MHC-CAR 구축물은 또한, MHC 클래스 I 모이어티를 포함할 수 있다. 힌지 도메인은 약 10 내지 100개 아미노산, 예를 들어, 15 내지 75개 아미노산, 20 내지 50개 아미노산, 또는 30 내지 60개 아미노산을 함유할 수 있다. 일부 구현예에서, 힌지 도메인은 10, 11, 12, 13, 14,15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 35, 40, 45, 50, 55, 60, 65, 70, 또는 75개 아미노산 길이일 수 있다.
일부 예에서, 하기 펩타이드 링커가 클래스 I MHC-CAR에 사용될 수 있다:
클래스 II MHC-CAR에 대한 예시적인 펩타이드 링커는 GSGSGSGS(MHCII 링커1; SEQ ID NO: 72), GGGGSGGGGSGGGGS(MHC II 링커ll; SEQ ID NO: 68), GGGGSGGGGSGGS(SEQ ID NO: 400), 또는 본원에서 MHCI 링커(즉, MHCI 링커 1-4)로서 기재된 것들일 수 있다. 클래스 II MHC-CAR에 대한 예시적인 프리-펩타이드 링커는 AS 또는 GS, 또는 AS 또는 GS의 1 또는 2개 복사체일 수 있다.
SEQ ID NO: 400에 의해 제공되는 펩타이드 링커를 인코딩하는 핵산 서열의 일례는 하기에 제공된다.
GGGGGAGGCGGATCTGGCGGAGGCGGGAGTGGAGGCTCA(SEQ ID NO: 401)
본원에 기재된 MHC-CAR에 사용하기 위한 힌지 펩타이드는 천연-발생 수용체로부터 유래될 수 있다. 힌지 도메인을 포함하는 것으로 당업계에서 알려진 임의의 단백질의 힌지 도메인은 본원에 기재된 키메라 수용체에서 사용하기에 융화성이다. 일부 구현예에서, 힌지 도메인은 CD8α의 힌지 도메인, 예를 들어, CD8α의 힌지 도메인의 적어도 15개(예를 들어, 20, 25, 30, 35 또는 40개) 연속 아미노산을 함유하는 단편이다. 대안적으로, 힌지 도메인은 합성 펩타이드일 수 있다.
예시적인 힌지 도메인은 하기를 포함한다:
, 및
. 추가의 예는 하기에 제공된다:
DRA*0101 힌지를 인코딩하는 핵산 서열 예는 하기에 제공된다.
GAGTTCGACGCCCCATCACCGCTTCCAGAAACGACTGAA(SEQ ID NO: 417)
DRB1*1501 힌지를 인코딩하는 핵산 서열의 일례는 하기에 제공된다.
일부 구현예에서, 본원에 기재된 MHC-CAR 구축물은 막관통 도메인을 추가로 포함한다. MHC-CAR에서 사용하기 위한 임의의 막관통 도메인은 당업계에 알려진 임의의 형태일 수 있다. 본원에 사용된 바와 같이, "막관통 도메인"은 세포막, 바람직하게는 진핵 세포막에서 열역학적으로 안정한 임의의 단백질 구조를 지칭한다. 본원에서 사용되는 키메라 수용체에 사용하기에 융화성인 막관통 도메인은 천연-발생 단백질로부터 수득될 수 있다. 대안적으로, 막관통 도메인은 합성, 비-천연 발생 단백질 분절(segment), 예를 들어, 세포막에서 열역학적으로 안정한 소수성 단백질 분절이다.
막관통 도메인은 상기 막관통 도메인의 3 차원 구조를 기반으로 분류된다. 예를 들어, 막관통 도메인은 세포의 인지질 이중층을 경유(spanning)할 수 있는 알파 나선, 1개 초과의 알파 나선의 복합체, 베타-병풍, 또는 임의의 다른 안정한 구조를 형성할 수 있다. 더욱이, 막관통 도메인은 또한 또는 대안적으로, 상기 막관통 도메인이 막을 가로지르게 하는 통과(pass)의 수 및 단백질의 배향을 포함한 막관통 도메인 위상 배치(topology)를 기반으로 분류될 수 있다. 예를 들어, 단일-통과 막 단백질은 세포막을 1회 가로지르고, 다중-통과 막 단백질은 세포막을 적어도 2회(예를 들어, 2, 3, 4, 5, 6, 7회 이상) 가로지른다.
막 단백질은 세포의 내부 및 외부에 비하여 이들의 말단 및 막-통과 분절(들)의 위상 배치에 따라 I형, II형 또는 III형으로서 정의될 수 있다. I형 막 단백질은 단일 막-경유 영역을 갖고, 상기 단백질의 N-말단이 세포의 지질 이중층의 세포외 측(side)에 존재하고 상기 단백질의 C-말단이 세포질 측에 존재하도록 배향된다. II형 막 단백질 또한, 단일-막 경유 영역을 갖지만, 상기 단백질의 C-말단이 세포의 지질 이중층의 세포외 측에 존재하고 상기 단백질의 N-말단이 세포질 측에 존재하도록 배향된다. III형 막 단백질은 다수의 막-경유 분절을 갖고, 막관통 분절의 수 및 N-말단과 C-말단의 위치를 기반으로 추가로 하위-분류될 수 있다.
일부 구현예에서, 본원에 기재된 MHC-CAR의 막관통 도메인은 I형 단일-통과 막 단백질, 예를 들어, CD8α, CD8β, 4-1BB/CD137 또는 CD28로부터 유래된다. 다중-통과 막 단백질로부터의 막관통 도메인은 또한, 본원에 기재된 키메라 수용체에 사용하기에 융화성일 수 있다. 다중-통과 막 단백질은 복잡한(적어도 2, 3, 4, 5, 6, 7개 이상의) 알파 나선 또는 베타 병풍 구조를 포함할 수 있다. 바람직하게는, 다중-통과 막 단백질의 N-말단 및 C-말단은 지질 이중층의 반대되는 측에 존재하며, 예를 들어, 상기 단백질의 N-말단은 지질 이중층의 세포질 측에 존재하고 상기 단백질의 C-말단은 세포외 측에 존재한다. 다중-통과 막 단백질로부터의 1회 또는 다중 나선 통과는 본원에 기재된 키메라 수용체를 구축하는 데 사용될 수 있다.
본원에 기재된 MHC-CAR 구축물을 구축하는 데 사용하기 위한 예시적인 막관통 도메인은 하기에 제공된다:
DR*1501e 막관통 도메인을 인코딩하는 핵산 서열 예는 하기에 제공된다:
DRA*0101e 막관통 도메인을 인코딩하는 핵산 서열 예는 하기에 제공된다:
노치(Notch) 막관통 도메인:
노치 2 막관통 도메인:
일부 구현예에서, MHC-CAR은 또한, 폴리펩타이드의 N-말단에서 신호 펩타이드(신호 서열 또는 리더 펩타이드로도 알려져 있음)를 포함할 수 있다. 일반적으로, 신호 서열은 세포에서 폴리펩타이드를 요망되는 부위로 표적화하는 펩타이드 서열이다. 일부 구현예에서, 신호 서열은 MHC-CAR을 세포의 분비 경로로 표적화하고, 지질 이중층 내로의 MHC-CAR의 통합 및 앵커링을 가능하게 할 것이다. 본원에 기재된 키메라 수용체에 사용하기에 융화성인, 천연 발생 단백질의 신호 서열 또는 합성, 비-천연 발생 신호 서열을 포함한 신호 서열은 당업자에게 명백할 것이다. 일부 구현예에서, 신호 서열은 CD8α로부터 유래된다. 일부 구현예에서, 신호 서열은 CD28(예를 들어, MLRLLLALNLFPSIQVTG(SEQ ID NO: 97))로부터 유래된다.
예시적인 신호 펩타이드는 베타-2-마이크로글로불린 신호 펩타이드(예를 들어, MSRSVALAVLALLSLSGLEA(SEQ ID NO: 98)), HLA A3 신호 펩타이드(예를 들어, MAVMAPRTLLLLLSGALALTQTWA(SEQ ID NO: 99) 또는), DRA*0101 신호 펩타이드(예를 들어, MAISGVPVLGFFIIAVLMSAQESWA(SEQ ID NO: 100)), DRB1*1501 신호 펩타이드(예를 들어, MVCLKLPGGSCMTALTVTLMVLSSPLAL(SEQ ID NO: 101)), 및 DRB5 신호 펩타이드(예를 들어, MVCLKLPGGSYMAKLTVTLMVLSSPLALA(SEQ ID NO: 102))를 포함하지만 이들로 한정되는 것은 아니다. 예시적인 신호 펩타이드에 뒤이어 가요성(flexible) 프리-펩타이드 링커, 예컨대 AS, GS, ASAS, GSGS가 존재할 수 있다. 일부 구현예에서, 가요성 프리-펩타이드 링커는, 신호 펩타이드가 클래스 II이고 뒤이어 도입된 펩타이드가 존재하는 경우 사용된다. 본원에 기재된 MHC-CAR을 인코딩하는 임의의 구축물은 상기 임의의 프리-펩타이드 링커를 인코딩하는 핵산 서열을 포함할 수 있으며, 예를 들어, AS는 핵산 서열 GCATCT에 의해 인코딩될 수 있고, TS는 핵산 서열 ACAAGT에 의해 인코딩될 수 있다.
베타-2-마이크로글로불린 신호 펩타이드를 인코딩하는 핵산 서열 예는 하기에 제공된다:
일부 구현예에서, 본원에 기재된 MHC-CAR은 본원에 기재된 바와 같은 다른 구성성분들 사이에 하나 이상의 펩타이드 링커를 포함할 수 있다. 그 예는 (GlyxSer)n 링커를 포함하며, 여기서, x 및 n은 독립적으로, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12 이상을 포함하여 3 내지 12의 정수일 수 있다. 일부 예에서, 펩타이드 링커는 (Gly4Ser)n(SEQ ID NO: 103)일 수 있으며, 여기서, n은 3 내지 20의 정수일 수 있다. 구체적인 예는 (Gly4Ser)3(SEQ ID NO: 68), (Gly4Ser)6(SEQ ID NO: 69), (Gly4Ser)9(SEQ ID NO: 76), (Gly4Ser)12(SEQ ID NO: 105), 및 (Gly4Ser)15(SEQ ID NO: 106)를 포함한다.
(ii) MHC-CAR의 입체배열(configuration)
본원에 기재된 하나 이상의 구성성분을 포함하는 본원에 개시된 MHC-CAR 구축물은 임의의 적합한 포맷으로 입체배열될 수 있다. 예시적인 MHC 클래스 I 구축물 및 MHC 클래스 II 구축물은 도 7 및 도 8에 제공된다.
본원에 기재된 바와 같은 MHC 클래스 I 모이어티를 포함하는 MHC-CAR 구축물은 MHC 클래스 I 모이어티, 항원성 펩타이드, 및 신호화 도메인(예를 들어, 공동-자극 도메인, 세포질 신호화 도메인, 또는 이들의 조합), 및 선택적으로 하나 이상의 본원에 기재된 추가의 구성성분을 포함하는 단일 융합 폴리펩타이드일 수 있다. 예를 들어, 도 8을 참조한다. 일부 예에서, MHC 클래스 I CAR 구축물은 항원성 펩타이드에 인접한 힌지 도메인을 함유한다. MHC 클래스 I CAR은 β2-마이크로글로불린(b2m)을 함유하지 않을 수 있다. 세포 표면 상에서 발현되는 경우, 이러한 MHC-CAR은 내인성 b2m과 함께 헤테로이량체를 형성할 수 있다. 대안적으로, MHC 클래스 I CAR은 또한, b2m을 포함할 수 있으며, 이는 알파 사슬과 함께 융합되어 단일 폴리펩타이드를 생성할 수 있다. 일부 경우, MHC 클래스 I CAR은 2개의 하위단위를 함유할 수 있으며, 하나의 하위단위는 알파 사슬 또는 이의 일부(예를 들어, 세포외 도메인)를 포함하고, 다른 하위단위는 b2m 또는 이의 일부(예를 들어, 세포외 도메인)를 포함한다. 일부 예에서, 항원성 펩타이드는 알파 사슬에 융합될 수 있다. 다른 예에서, 항원성 펩타이드는 b2m에 융합될 수 있다. 선택적으로, MHC 클래스 I CAR은 2개의 구성성분 사이에 펩타이드 링커를 함유할 수 있다. 일례는 도 8b에 제공된다.
일부 예에서, MHC-CAR은 클래스 I 분자 또는 이의 일부, 예를 들어, HLA A3 또는 HLA A2, 및 클래스 I 분자에 의한 제시에 적합한 항원성 펩타이드(예를 들어, PLP 단편 KLIETYFSK(SEQ ID NO: 107) 또는 TAX 단편 LLFGYPVYV(SEQ ID NO: 108))를 포함한다. 선택적으로, MHC-CAR은 b2m을 추가로 포함할 수 있다. 대안적으로, b2m 분자는 클래스 I MHC-CAR로부터 별도로 발현될 수 있다. 클래스 I 분자 및 b2m 서열의 예는 하기에 제공된다:
HLA A2:
HLA A3:
상기에 대한 미세확장(microextension):
H-2Kb 알파3 도메인을 갖는 HLA A2(밑줄표시/이탤릭체)
H-2Kb 알파3 도메인을 갖는 HLA A3(밑줄표시/이탤릭체)
상기에 대한 미세확장(microextension):
베타-2-마이크로글로불린(인간):
베타-2-마이크로글로불린(마우스):
도 7은 MHC 클래스 II CAR 구축물의 많은 예시적인 설계를 제공한다. 전형적으로, MHC 클래스 II CAR 구축물은 2개의 하위단위를 함유하고, 하나의 하위단위는 알파 사슬 또는 이의 일부(예를 들어, 세포외 도메인)를 포함하고, 다른 하위단위는 베타 사슬 또는 이의 일부(예를 들어, 세포외 도메인)를 포함한다. 항원성 펩타이드는 알파 사슬 또는 베타 사슬에 융합될 수 있다. 일부 경우, MHC 클래스 II CAR은 또한, 신호 융합 폴리펩타이드 포맷으로 존재할 수 있으며, 상기 포맷에서 알파 사슬 및 베타 사슬은 융합되어 단일 폴리펩타이드를 형성한다. MHC 클래스 II CAR의 알파 사슬 및 베타 사슬은 동일한 MHC 클래스 II 분자로부터 유래될 수 있다. 대안적으로, 이들 사슬은 상이한 MHC 클래스 II 분자로부터 유래될 수 있다. 예를 들어, MHC 클래스 II CAR은 HLA DRA*1010으로부터의 알파 사슬 및 HLA DRB1*1501로부터의 베타 사슬을 함유할 수 있고, 이는 항원성 펩타이드, 예컨대 MBP 펩타이드와 융합될 수 있다.
일부 예에서, MHC-CAR은 클래스 II 분자 또는 이의 일부, 예를 들어, DRB1*1501 또는 DRA*0101, 및 클래스 II 분자에 의한 제시에 적합한 항원성 펩타이드(예를 들어, MBP 단편 DENPVVHFFKNIVTPRTPP(SEQ ID NO: 15))를 포함한다. 클래스 II 분자 서열의 예는 하기에 제공된다;
DRB1*1501:
DRA*0101
DRB1*1501 인간/IA-D베타 마우스(돌연변이화된 잔기는 볼드체 및 밑줄표시되어 있음)
DRA*0101 인간/IA-D알파 마우스(돌연변이화된 잔기는 볼드체 및 밑줄표시되어 있음)
DR-2베타 미니(돌연변이화된 잔기는 볼드체 및 밑줄표시되어 있음)
DR-2알파 미니
DRB1*1501을 인코딩하는 핵산 서열 예는 하기에 제공된다:
DRA*0101을 인코딩하는 핵산 서열 예는 하기에 제공된다:
본원에 기재된 임의의 MHC 클래스 I 및 MHC 클래스 II 구축물은 하나 이상의 신호화 도메인 및 선택적으로 하나 이상의 추가의 구성성분에 추가로 융합될 수 있다. 일부 경우, 본원에 기재된 MHC-CAR 구축물은 신호화 도메인이 없다.
바람직하게는, 본원에 기재된 바와 같은 MHC-CAR은 매칭된(matched) MHC 모이어티 및 항원성 펩타이드, 예를 들어, 천연 상태에서 항원성 펩타이드 또는 상동성 유사체에 존재할 MHC 분자를 함유한다. 일부 경우, 본원에 기재된 MHC-CAR은 HLA DRB1*1501로부터의 알파 사슬 또는 베타 사슬 및 이러한 HLA 대립유전자(allele)와 연관된 항원성 펩타이드, 예를 들어, 본원에 기재된 MBP 펩타이드 및 또한 다른 것들을 함유할 수 있다. 자가면역 질병에 관여하는 항원성 펩타이드와 특이적인 HLA 대립유전자 사이의 연관성은 당업계에 잘 알려져 있거나 일상적인 실행, 예를 들어, 라이브러리 스크리닝을 통해 식별될 수 있다.
하나의 예시적인 MHC-CAR은 하기 식을 가질 수 있다(+/-는 특정 구성성분이 선택적임을 의미함):
단일 사슬 (MHC 클래스 I 또는 II + 펩타이드) (+/-힌지) + 단일 사슬 CD28/4-1BB (+/-디류신 모티프) (+/-cd3제타)). (추가의 짧은 펩타이드 링커는 이전에 기재된 바와 같이 구성성분들 사이에 첨가될 수 있음).
다른 예시적인 MHC-CAR 설계(단일 사슬 및 다중-사슬)는 도 10에 예시되어 있다. 다중-사슬 구축물의 경우, 하나 이상의 짧은 힌지가 사용되어, MHC-CAR의 성공적인 발현을 증강시킬 수 있다. 나아가, 교차-반응성을 방지하기 위해, 구조 중 일부를 마우스 도메인으로부터의 보존된 도메인으로 대체하는 것이 바람직할 수 있다. 일부 경우, 내재 도메인만 사슬 중 하나에 부착될 수 있음을 주지한다.
MHC-CAR 결합(MBP를 나타냄) TCR의 아미노산 서열은 하기에 제공된다:
TCR 알파 MBP:
TCR 베타 MBP
TCR 알파 클래스 1
TCR 베타 클래스 I:
예시적인 CD19 표적화 CAR 구축물의 아미노산 서열은 하기에 제공된다(이들 설계가 cd28 도메인으로 대체될 수 있는 4-1BB 도메인을 함유함을 주지함):
4G7-CAR 버전 1:
4G7-CAR 버전 2:
예시적인 CD19 표적화 CAR 구축물의 핵산 서열은 하기에 제공된다.
4G7-CAR 버전 2:
MHC-CAR1 파트 B(MHC-DRB CAR)- HLA DRB1*1501(신호 펩타이드), MBP 펩타이드, HLA DRB1*1501(외부, 힌지, 막관통) CD3ζ(세포질 신호화 도메인)를 함유하는 MHC-CAR1은 하기에 제공된다:
MHC-CAR1 파트 B(MHC-DRB CAR)- HLA DRB1*1501(신호 펩타이드), MBP 펩타이드, HLA DRB1*1501(외부, 힌지, 막관통) CD3ζ(세포질 신호화 도메인)를 함유하는 MHC_CAR1을 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
MHC-CAR1 파트 A(MHC-DRA CAR) HLA-DRA*1010(신호 펩타이드, 외부, 힌지, 막관통), CD3ζ(세포질 신호화 도메인)를 함유하는 MHC-CAR은 하기에 제공된다:
MHC-CAR1 파트 A(MHC-DRA CAR) HLA-DRA*1010(신호 펩타이드, 외부, 힌지, 막관통), CD3ζ(세포질 신호화 도메인)를 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
구축물 1(CD19 CAR 및 CCR6 영역)은 하기에 제공된다:
구축물 1(CD19 CAR, CCR6, GFP 영역)은 하기에 제공된다:
구축물 1(CD19 CAR, CCR6, GFP 영역)을 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
구축물 2 MHC CAR 영역(MHC-CAR1 파트 B, MHC-CAR1 파트 A 영역)은 하기에 제공된다:
구축물 2 MHC CAR 영역(MHC-CAR1 파트 B, MHC-CAR1 파트 A)을 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
구축물 2 사멸화 스위치 및 MHC CAR 영역(RQR8, MHC-CAR1 파트 B, MHC-CAR1 파트 A 영역)은 하기에 제공된다:
구축물 2 사멸화 스위치 및 MHC CAR 영역(RQR8, MHC-CAR1 파트 B, MHC-CAR1 파트 A 영역)을 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
구축물 2(RQR8, MHC-CAR1 파트 B, MHC-CAR1 파트 A, GFP 영역)은 하기에 제공된다.
구축물 2(RQR8, MHC-CAR1 파트 B, MHC-CAR1 파트 A, GFP 영역)를 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
예시적인 CS-1 표적화 CAR 구축물의 아미노산 서열은 하기에 제공된다(이들 설계는 CD28 도메인으로 대체될 수 있는 4-1BB 도메인을 함유함을 주지함):
항-CS1-CAR-v1 (Luc63-V1 CAR):
항-CS1-CAR-v2 (Luc63-V2 CAR):
항-CS1-CAR-v3 (Luc63-V3 CAR):
항-CS1-CAR-v4 (Luc90-V1 CAR):
항-CS1-CAR-v5 (Luc90-V2 CAR):
항-CS1-CAR-v6 (Luc90-V3 CAR):
항-CS1-CAR-v7 (Luc34-V1 CAR):
항-CS1-CAR-v8 (Luc34-V2 CAR):
항-CS1-CAR-v9 (Luc34-V3 CAR):
항-CS1-CAR-v10 (LucX1-V1 CAR):
항-CS1-CAR-v11 (LucX1-V2 CAR):
항-CS1-CAR-v12 (LucX1-V3 CAR):
항-CS1-CAR-v13 (LucX2-V1 CAR):
항-CS1-CAR-v14 (LucX2-V2 CAR):
항-CS1-CAR-v15 (LucX2-V3 CAR):
(iii) MHC-CAR의 제조
본원에 기재된 임의의 MHC-CAR 구축물은 일상적인 방법, 예컨대 재조합 기술에 의해 제조될 수 있다. 본원에서 키메라 수용체를 제조하는 방법은 MHC-CAR 구축물(단일 폴리펩타이드 또는 2개의 하위단위를 포함함)을 인코딩하거나 종합하여 인코딩하는 핵산 또는 핵산 세트의 발생을 수반한다. 일부 구현예에서, 핵산은 또한, MHC-CAR의 2개의 하위단위에 대한 코딩 서열들 사이에서 또는 MHC-CAR에 대한 코딩 서열과 숙주 세포에서 MHC-CAR과 함께 공동-발현되는 다른 유전자에 대한 코딩 서열 사이에서 자가-절단형 펩타이드(예를 들어, P2A, T2A 또는 E2A 펩타이드)를 인코딩한다(하기 고찰 참조).
MHC-CAR의 각각의 구성성분의 서열은 일상적인 기술, 예를 들어, 당업계에 알려진 여러 가지 공급원들 중 임의의 하나로부터의 PCR 증폭을 통해 수득될 수 있다. 일부 구현예에서, MHC-CAR의 하나 이상의 구성성분의 서열은 인간 세포로부터 수득된다. 대안적으로, MHC-CAR의 하나 이상의 구성성분의 서열은 합성될 수 있다. 각각의 구성성분(예를 들어, 도메인)의 서열은 PCR 증폭 또는 결찰(ligation)과 같은 방법을 사용하여 직접적으로 또는 간접적으로(예를 들어, 펩타이드 링커를 인코딩하는 핵산 서열을 사용하여) 접합되어, MHC-CAR을 인코딩하는 핵산 서열을 형성할 수 있다. 대안적으로, MHC-CAR을 인코딩하는 핵산이 합성될 수 있다. 일부 구현예에서, 핵산은 DNA이다. 다른 구현예에서, 핵산은 RNA이다.
모두 본 개시내용의 범위 내에 포함되는 MHC-CAR 단백질, 이러한 단백질을 인코딩하는 핵산, 및 이러한 핵산을 운반하는 발현 벡터 중 임의의 것은, 약제학적으로 허용 가능한 담체와 혼합되어, 약제학적 조성물을 형성할 수 있으며, 이러한 약제학적 조성물 또한 본 개시내용의 범위 내에 포함된다. "허용 가능한"은, 담체가 조성물의 활성 성분(예를 들어, 핵산, 벡터, 세포, 또는 치료적 항체)과 융화성이고 상기 조성물(들)이 투여되는 대상체에게 부정적인 영향을 주지 않음을 의미한다. 본 방법에 사용되는 임의의 약제학적 조성물은 동결건조된 제제 또는 수용액의 형태에서 약제학적으로 허용 가능한 담체, 부형제 또는 안정화제를 포함할 수 있다.
완충제를 포함하여 약제학적으로 허용 가능한 담체는 당업계에 잘 알려져 있고, 포스페이트, 시트레이트 및 다른 유기산; 아스코르브산 및 메티오닌을 포함한 항산화제; 보존제; 저분자량 폴리펩타이드; 단백질, 예컨대 혈청 알부민, 젤라틴 또는 면역글로불린; 아미노산; 소수성 중합체; 단당류; 이당류; 및 기타 탄수화물; 금속 복합체; 및/또는 비-이온성 계면활성제를 포함할 수 있다. 예를 들어, 문헌[Remington: The Science and Practice of Pharmacy 20th Ed. (2000) Lippincott Williams and Wilkins, Ed. K E. Hoover]을 참조한다.
II. MHC-CAR을 발현하는 유전적으로 조작된 면역 세포
(i) MHC-CAR-발현 면역 세포
본원에 기재된 MHC-CAR을 발현하는 면역 세포는, 자가면역 질병에 관여하는 병원성 세포(예를 들어, 자가반응성 T 세포)를 MHC/펩타이드-TCR 연동을 통해 인지할 수 있는 세포의 특이적인 집단을 제공한다. 병원성 세포 상에서 MHC-CAR의 MHC-펩타이드 부분과 동족(cognate) TCR 사이의 상호작용은 MHC-CAR(선택적으로 면역 세포의 세포막 신호화 분자를 동원(recruit)함으로써)의 신호화 도메인(들)을 통해 MHC-CAR-발현 면역 세포를 활성화시켜, MHC-CAR-발현 면역 세포의 증식 및/또는 효과기 기능을 야기할 것이며, 이는 다시 병원성 세포를 제거한다. 면역 세포는 T 세포, NK 세포, 대식세포, 호중구, 호산구, 또는 이들의 임의의 조합일 수 있다. 일부 구현예에서, 면역 세포는 T 세포이다. 일부 구현예에서, 면역 세포는 NK 세포이다. 구체적인 예는 하기 실시예에서 제공된다.
면역 세포의 집단은 임의의 공급원, 예컨대 말초 혈액 단핵 세포(PBMC), 골수, 조직, 예컨대 비장, 림프절, 흉선, 종양 조직, 또는 확립된 세포주로부터 수득될 수 있다. 요망되는 유형의 면역 세포를 수득하는 데 적합한 공급원은 당업자에게 명백할 것이다. 일부 구현예에서, 면역 세포 집단은 PBMC로부터 유래된다. 요망되는 유형의 면역 세포(예를 들어, T 세포, NK 세포, 대식세포, 호중구, 호산구, 또는 이들의 임의의 조합)는, 상기 세포를 자극 분자와 함께 공동-인큐베이션함으로써 수득되는 세포 집단 내에서 확장(expand)될 수 있으며, 예를 들어, 항-CD3 및 항-CD28 항체는 T 세포의 확장에 사용될 수 있다.
본원에 기재된 임의의 MHC-CAR 구축물을 발현하는 면역 세포를 구축하기 위해, 키메라 수용체 구축물의 안정한 발현 또는 일시적인 발현을 위한 발현 벡터가 본원에 기재된 바와 같은 종래의 방법을 통해 구축되고 면역 숙주 세포 내로 도입될 수 있다. 예를 들어, MHC-CAR을 인코딩하는 핵산은 적합한 프로모터에 작동적으로 연결되어 적합한 발현 벡터, 예컨대 바이러스 벡터(예를 들어, 렌티바이러스 벡터) 내로 클로닝될 수 있다. 핵산 및 벡터는 적합한 조건 하에 제한 효소와 접촉되어, 각각의 분자 상에서 상보적인 말단을 생성할 수 있으며, 이들은 서로 짝을 이루고 리가제에 의해 접합될 수 있다. 대안적으로, 합성 핵산 링커는 키메라 수용체를 인코딩하는 핵산의 말단에 결찰될 수 있다. 합성 링커는 벡터 내의 특정 제한 부위에 상응하는 핵산 서열을 함유할 수 있다. 발현 벡터/플라스미드/바이러스 벡터의 선택은 키메라 수용체의 발현을 위한 숙주 세포의 유형에 따라 다를 것이지만, 진핵 세포에서의 통합 및 복제에 적합해야 한다.
비제한적으로 사이토메갈로바이러스(CMV) 즉각적인 초기(immediate early) 프로모터, 바이러스 LTR, 예컨대 라우스 육종(Rous sarcoma) 바이러스 LTR, HIV-LTR, HTLV-1 LTR, 시미안(simian) 바이러스 40 (SV40) 초기 프로모터, 단순 포진 tk 바이러스 프로모터를 포함한 여러 가지 프로모터가 본원에 기재된 MHC-CAR 구축물의 발현에 사용될 수 있다. 키메라 수용체의 발현을 위한 추가의 프로모터는 면역 세포에서 임의의 구성적으로 활성인 프로모터를 포함한다. 대안적으로, 임의의 조절형 프로모터가 사용될 수 있어서, 이의 발현은 면역 세포 내에서 조정될 수 있다.
추가로, 벡터는 예를 들어, 하기 중 일부 또는 모두를 함유할 수 있다: 선별 마커 유전자, 예컨대 숙주 세포에서 안정한 또는 일시적인 형질감염체의 선별을 위한 네오마이신 유전자; 높은 수준의 전사를 위한 인간 CMV의 즉각적인 초기 유전자로부터의 인핸서/프로모터 서열; mRNA 안정성을 위한 SV40으로부터의 전사 종결 및 RNA 프로세싱 신호; 적절한 에피솜 복제를 위한 복제의 SV40 폴리오마(polyoma) 기원 및 ColE1; 내재 리보솜 결합 부위(IRESes), 다재다능 다중 클로닝 부위; 센스 RNA 및 안티센스 RNA의 시험관내 전사를 위한 T7 및 SP6 RNA 프로모터; 촉발된 경우, 벡터를 운반하는 세포가 사멸하도록 유발하는 "자살 스위치(suicide switch)" 또는 "자살 유전자"(예를 들어, HSV 티미딘 키나제, 유도성 카스파제, 예컨대 iCasp9), 및 MHC-CAR의 발현을 평가하기 위한 리포터 유전자.
일부 구현예에서, 본 개시내용에 사용하기 위한 마커/소팅/자살 분자는 리툭시맙과 함께 사멸화에 및/또는 QBEND와 함께 소팅에 사용될 수 있다. (문헌[Philip et al., Blood 124(8): 1277-87; 2014]). 일례는 리툭시맙 미모토프(mimotope) 및 QBEND-10 에피토프를 함유하는 RQR8이다. 예시적인 서열은 하기에 제공된다:
RQR8을 인코딩하는 예시적인 핵산 서열은 하기에 제공된다.
또 다른 예에서, 하기 예시적인 RQR 서열 태그는 본원에 개시된 바와 같은 MHC-CAR 구축물에 부착될 수 있다:
볼드체 단편은 리툭시맙 미노토프(minotope)이고, 밑줄표시/이탤릭체 단편은 QBEND-10 에피토프이다.
적합한 벡터 및 이식유전자를 함유하는 벡터를 생성하는 방법은 당업계에 잘 알려져 있고 입수 가능하다. 본원에 기재된 MHC-CAR 구축물을 인코딩하는 핵산 서열을 포함하는 임의의 벡터 또한, 본 개시내용의 범위 내에 포함된다. 이러한 벡터는 적합한 방법에 의해 숙주 면역 세포 내로 전달될 수 있다. 벡터를 면역 세포에 전달하는 방법은 당업계에 잘 알려져 있고, DNA 전기천공, RNA 전기천공, 형질감염 시약, 예컨대 리포솜, 또는 바이러스 전달을 포함할 수 있다. 일부 구현예에서, MHC-CAR의 발현을 위한 벡터는 바이러스 전달에 의해 숙주 세포로 전달된다. 전달을 위한 예시적인 바이러스 방법은 재조합 레트로바이러스(예를 들어, PCT 공개 WO 90/07936; WO 94/03622; WO 93/25698; WO 93/25234; WO 93/11230; WO 93/10218; WO 91/02805; 미국 특허 5,219,740 및 4,777,127; 영국 특허 2,200,651; 및 유럽 특허 0 345 242 참조), 알파바이러스-기반 벡터, 및 아데노-연관 바이러스(AAV) 벡터(예를 들어, PCT 공개 WO 94/12649, WO 93/03769; WO 93/19191; WO 94/28938; WO 95/11984 및 WO 95/00655 참조)를 포함하지만 이들로 한정되는 것은 아니다. 일부 구현예에서, 키메라 수용체의 발현을 위한 벡터는 레트로바이러스이다. 일부 구현예에서, 키메라 수용체의 발현을 위한 벡터는 렌티바이러스이다.
키메라 수용체를 인코딩하는 벡터가 바이러스 벡터를 사용하여 숙주 세포로 도입되는 예에서, 면역 세포를 감염시킬 수 있고 벡터를 운반하는 바이러스 입자는 당업계에 알려진 임의의 방법에 의해 생성될 수 있고, 예를 들어, PCT 출원 WO 1991/002805 A2, WO 1998/009271 A1 및 미국 특허 6,194,191에서 찾을 수 있다. 바이러스 입자는 세포 배양 상층액으로부터 수합되고, 단리 및/또는 정제된 후 상기 바이러스 입자는 면역 세포와 접촉된다.
본원에 제공된 임의의 MHC-CAR을 인코딩하는 벡터를 숙주 세포 내로 도입한 후, 상기 세포는 키메라 수용체의 발현을 가능하게 하는 조건 하에 배양된다. MHC-CAR을 인코딩하는 핵산이 조절형 프로모터에 의해 조절되는 예에서, 숙주 세포는 상기 조절형 프로모터가 활성화되는 조건에서 배양된다. 일부 구현예에서, 프로모터는 유도성 프로모터이고, 면역 세포는 유도(inducing) 분자의 존재 하에 또는 유도 분자가 생성되는 조건 하에 배양된다. MHC-CAR이 발현되는지 결정하는 것은 당업자에게 명백할 것이고, 임의의 기지의(known) 방법, 예를 들어, 정량적 리버스 트랜스크립타제 PCR(qRT-PCR)에 의한 키메라 수용체-인코딩 mRNA의 검출 또는 웨스턴 블로팅, 형광 현미경 및 유세포분석을 포함한 방법에 의한 키메라 수용체 단백질의 검출에 의해 평가될 수 있다. 또한, 하기 실시예를 참조한다. 대안적으로, MHC-CAR의 발현은, 면역 세포가 대상체에게 투여된 후 생체내에서 일어날 수 있다.
대안적으로, 본원에 개시된 임의의 면역 세포에서 MHC-CAR 구축물의 발현은, 상기 MHC-CAR 구축물을 인코딩하는 RNA 분자를 도입함으로써 달성될 수 있다. 이러한 RNA 분자는 시험관내 전사에 의해 또는 화학적 합성에 의해 제조될 수 있다. 그 후에, RNA 분자는 적합한 숙주 세포, 예컨대 면역 세포(예를 들어, T 세포, NK 세포, 대식세포, 호중구, 호산구, 또는 이들의 임의의 조합) 내로 예를 들어, 전기천공에 의해 도입될 수 있다. 예를 들어, RNA 분자는 문헌[Rabinovich et al., Human Gene Therapy, 17:1027-1035] 및 WO WO2013/040557에 기재된 방법에 따라 합성되고 숙주 면역 세포 내로 도입될 수 있다.
본원에 기재된 임의의 MHC-CAR을 발현하는 숙주 면역 세포를 제조하는 방법은 생체외에서 숙주 면역 세포를 확장시키는 단계를 포함할 수 있다. 숙주 면역 세포를 확장시키는 것은, MHC-CAR을 발현하는 세포의 수의 증가를 초래하는, 예를 들어, 숙주 세포가 증식할 수 있게 하거나 숙주 세포가 증식하도록 자극하는 임의의 방법을 수반할 수 있다. 숙주 세포의 확장을 자극하는 방법은 키메라 수용체의 발현에 사용되는 숙주 세포의 유형에 따라 다를 것이고, 당업자에게 명백할 것이다. 일부 구현예에서, 본원에 기재된 임의의 MHC-CAR을 발현하는 숙주 면역 세포는 생체외에서 확장된 후, 대상체에게 투여될 수 있다.
(ii) 추가의 유전적 변형
하나 이상의 추가의 유전적 변형은 MHC-CAR 구축의 형질감염 이전에, 이와 동시에 또는 이후에 숙주 면역 세포 내로 도입될 수 있다. 예를 들어, 하나 이상의 마커 및/또는 자살 유전자는 숙주 면역 세포 내로 도입될 수 있다. 그 예는 그린 형광 단백질(GFP), 증강된 블루 형광 단백질(eBFP), 및 RQR 유전자, 예컨대 RQR8을 포함한다(CD34 및 CD20로부터의 표적 에피토프를 조합하는 T 세포에 대한 컴팩트 마커/자살 유전자. (문헌[Philip et al., Blood 124(8): 1277-87; 2014]). 이러한 마커/자살 유전자는 MHC-CAR 구성성분과 함께 하나의 발현 카세트에서 구축될 수 있다.
GFP의 아미노산 서열의 일례는 하기에 제공된다:
GFP를 인코딩하는 핵산 서열의 일례는 하기에 제공된다:
일부 경우, 내인성 TCR(알파 사슬, 베타 사슬, 또는 둘 모두)은, 숙주 면역 세포가 내인성 TCR을 발현하지 않도록 교란될 수 있다. 내인성 TCR에서의 결핍은 요망되지 않는 T 세포 활성화를 피할 수 있을 것이다. 대안적으로 또는 이에 더하여, 소정의 세포 표면 수용체는 녹아웃될 수 있다. 이러한 표면 수용체는 질병 치료를 위한 표적 수용체, 예를 들어, MS 치료에 대한 표적인 CD52일 수 있다. MHC-CAR 면역 세포로부터 이러한 표적 수용체의 녹아웃은 MHC-CAR 면역 세포, 및 표적 수용체에 특이적인 치료제(예를 들어, 항-CD52 항체, 예컨대 알렘투주맙(alemtuzumab))의 공동-사용을 가능하게 한다.
일부 구현예에서, 숙주 면역 세포는 특이적인 기관 또는 조직에서, 예를 들어, 림프절에서, 3차 림프 기관에서, 또는 염증 부위에서 상기 숙주 면역 세포의 체류를 증강시키기 위해 합성 표면 단백질로 변형될 수 있다. 이렇게 함으로써, 변형된 면역 세포는 표적 병원성 세포에 접근할 수 있는 한편, 혈액 뇌 장벽의 침투로 인한 치명적인 표적-외(off-target) 효과 또는 말초 혈액을 통한 면역 세포의 자유 이동을 최소화할 것이다. T 세포 분화 경로에서 초기의 세포(예를 들어, 미접촉, 줄기세포 기억, 및 중심 기억 T 세포)는 림프절로 자유롭게 이동한다. 분화가 진행됨에 따라, 대부분의 효과기 T 세포는 림프절을 떠난다. 병적 면역 세포는 또한, 염증 부위로 이동하여 이 부위에서 축적될 수 있다. 활성화된 CAR-T 세포에 의한 치료는 이들 세포가 요망되지 않는 표적과 반응하는 경우 많은 바람직하지 못한 효과를 가진다. 심장 조직과의 상호작용은 심장 단백질에 치명적일 수 있고, 뇌의 침투는 치명적인 뇌부종을 야기할 수 있다. 최근의 진전은 CD19 CAR T 치료법을 사용한 암에 대한 전신 치료에서보다 더 낮은 용량의 CAR T 치료법을 사용한 뇌암 신경교종의 치료에서 이루어져 왔다. 문헌[Brown et al., New England Journal of Medicine, 375(26):2561-2569, 2016]. 염증의 해소는 병적 환경을 보호적 환경으로 변환시키는 잠재성을 가진다. 문헌[Gagliani et al., Nature, 523(7559):221-225, 2015].
하나 이상의 림프절 체류 단백질을 면역 세포 내로 도입하는 것은 림프절에서 면역 세포의 체류를 증강시킬 수 있으며, 여기서, 면역 세포는 표적 병원성 세포로의 접근성을 여전히 갖고 있는 한편, 상기 주지된 바와 같은 요망되지 않는 효과는 유의하게 감소될 수 있다. 미접촉 림프구는 고 내피 세정맥(HEV; high endothelial venule)을 통해 림프절에 진입한다. 따라서, HEV 앵커링 및/또는 진입에 관여하는 단백질을 발현하거나 과발현하는 것은 면역 세포가 림프절 내로 진입하는 것을 용이하게 할 수 있다. 예시적인 림프절 체류 단백질은 CCR7(케모카인 수용체), MECA79(말초 림프절 어드레신(addressin)), 혈관 접착 단백질-1(VAP-1) 및 CD62(셀렉틴, 세포 접착 분자의 패밀리)를 포함하지만 이들로 한정되는 것은 아니다. 문헌[Azzi et al., Blood 124(4): 476-477, 2016; Streeter et al., J. Cell. Biol. 107:1853-186; 1988; Michie et al., Amer, J. Path. 143:1688-1698; 1993; Berg et al., J. Cell. Biol. 114:343-349; 1991; Berg et al., Nature 366:695-698; 1993; 및 Hemmerich et al., J. Exp. Med. 180:2219-2226; 1994]. 대안적으로, 흉선 및 림프 기관으로부터 림프구 유출(egress)에 관여하는 단백질(예를 들어, 스핑고신-1-포스페이트 수용체-1 또는 SIP)을 인코딩하는 유전자는 면역 세포로부터 녹아웃될 수 있다.
염증 부위로의 수송을 촉진하는 케모카인 수용체 및 접착 수용체는 또한, 면역 질병을 전파하는 병원성 세포와 MHC-CAR 면역 세포가 접촉할 수 있게 한다(문헌[Barreiro et al., Cardiovascular research, 86(2): 174-182, 2010]). 표 3 및 표 4를 참조한다. 염증을 전파하는 면역 세포를 동원하는 데 관여하는 수용체는, 3차 림프 기관(여기서, CXCL13, CCL19, CCL20, CCL21이 발현됨)으로 동원되는 수용체(즉, CXCR5, CCR7, CCR6)를 포함한다.
다른 기관/조직, 예를 들어, 뇌/CNS, 골수, 췌장, 장, 간, 폐, 비장 및/또는 흉선을 표적화하는 데 관여하는 단백질을 인코딩하는 하나 이상의 유전자가 또한, 면역 세포 내로 도입되거나 면역 세포로부터 녹아웃될 수 있다.
치료적 세포에서 바이러스 유도성 또는 일시적인 RNA 매개 발현(가능하게는 내인성 유전자의 녹아웃과 조합됨)에 의해 유전자(표 3 및 표 4에서)는 Treg 또는 CTL 세포를 요망되는 장소에 안내하거나(route) 또는 요망되는 세포를 치료 제거하는 데 사용될 수 있다. 문헌[Barreiro, et al. Cardiovascular research, 86(2):174-182, 2010]. mRNA 형질감염이 이용된다면, 이는 케모카인 또는 접착 수용체의 발현을 1주일 동안 가능하게 할 수 있다. 문헌[Wang and Riviere. Molecular Therapy-Oncolytics, 3:16015 2016].
AAC51124.1에 의해 제공된 CCR6의 아미노산 서열은 하기에 제시된다:
CCR6의 핵산 서열의 예는 하기에 제시된다:
대안적으로 또는 이에 더하여, 면역 세포 기능, 예를 들어, 증식, 세포독성 등을 증강시킬 수 있는 유전자가 또한, 면역 세포 내로 도입되거나 면역 세포로부터 녹아웃될 수 있다. 그 예는 TNF/TNFR2 과발현(수명이 짧지만 더 효과적인 CD8 T 세포의 경우), gld(FasL 돌연변이체; 림프구증식(lymphoproliferation)을 위해; CTL은 Fas-FasL 경로를 통해 사멸화시키지 않음); lpr(Fas 돌연변이체; FasL의 상향조절을 위해 - FasL-매개 세포자멸사에 대해 내성인 표적 세포); 그랜자임 B* 결핍(표적 세포에서 지연된 핵 세포자멸사 변화); 그랜자임 A & B* 결핍(표적 세포에서 지연된 핵 세포자멸사 변화); 퍼포린 결핍(과립-매개 세포자멸사의 완전한 부재); 퍼포린 및 FasL 결핍(결함성 과립-매개 및 Fas-매개 세포자멸사); 카텝신(Cathepsin) C(디펩티딜-펩티다제 I) 결핍(활성 그랜자임 및 일부 조혈 세린 프로테아제를 생성하는 데 실패함); FAS(CD95) 과소발현(underexpression); 및/또는 FASL 과발현을 포함한다.
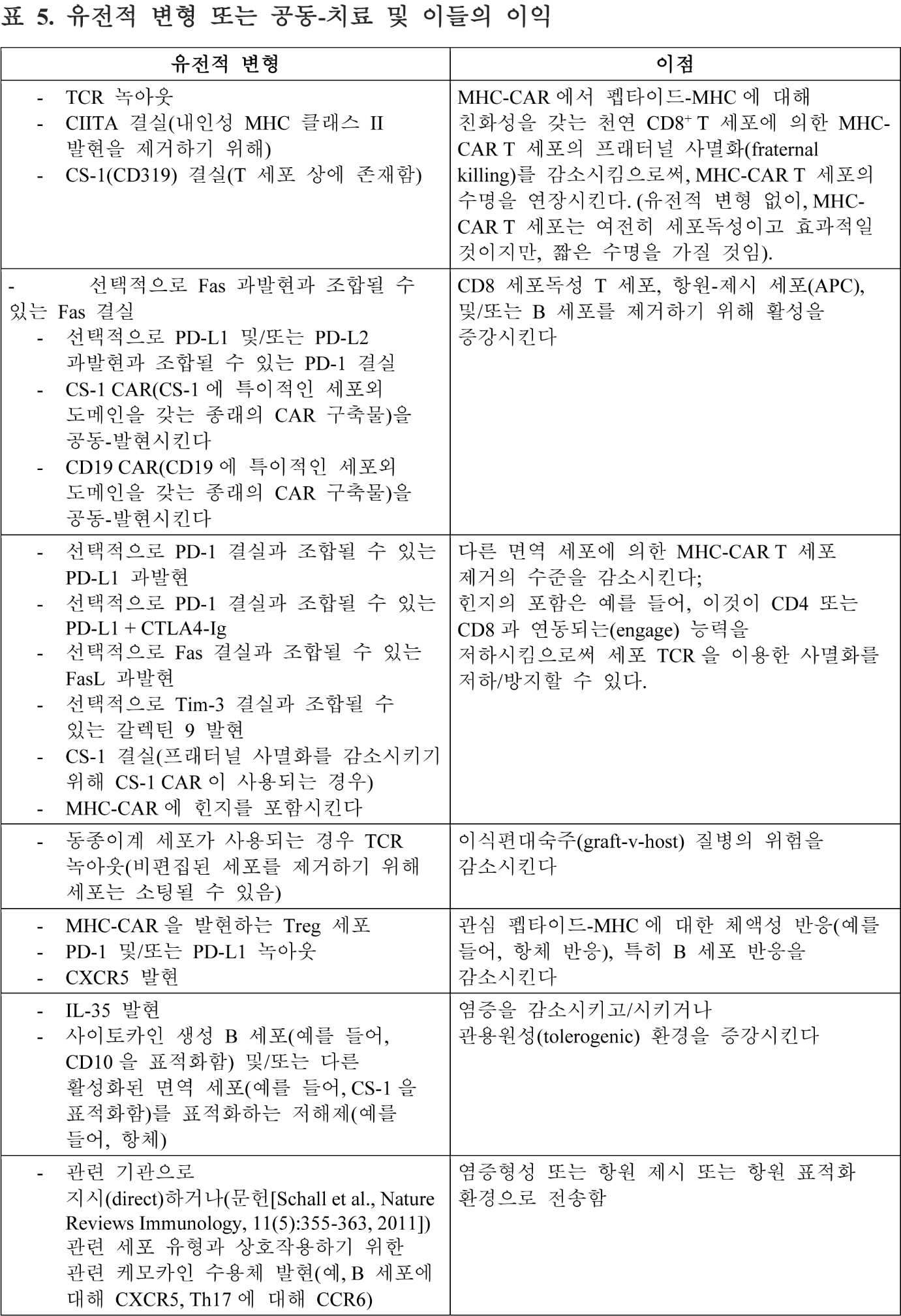
하기 표 5는 본원에 기재된 MHC-CAR T 세포의 추가의 유전적 변형 또는 공동-치료 및 이로부터 발생하는 동반 이점을 열거한다.
일부 구현예에서, PD 차단을 야기하는 유전적 변형은 본원에 기재된 바와 같이 MHC-CAR을 발현하는 면역 세포 내로 도입될 수 있다. 이러한 변형은 PD-1 녹아웃, PD-L1 또는 PD-L2 과발현, 또는 PD-L1 녹아웃 중 하나 이상을 포함한다. PD 차단은 면역-저해제(예를 들어, CTLA-4, TIM-3, LAG3, TIGIT, IDO, 또는 아르기나제의 녹아웃 또는 CTLA-4Ig 분비), 면역자극자(예를 들어, 항-OX40, 항-CD137, IL-2, TLR 리간드, 또는 STING), 및/또는 키나제 저해제(예를 들어, Braf 저해제 또는 MEK 저해제)와 조합될 수 있다
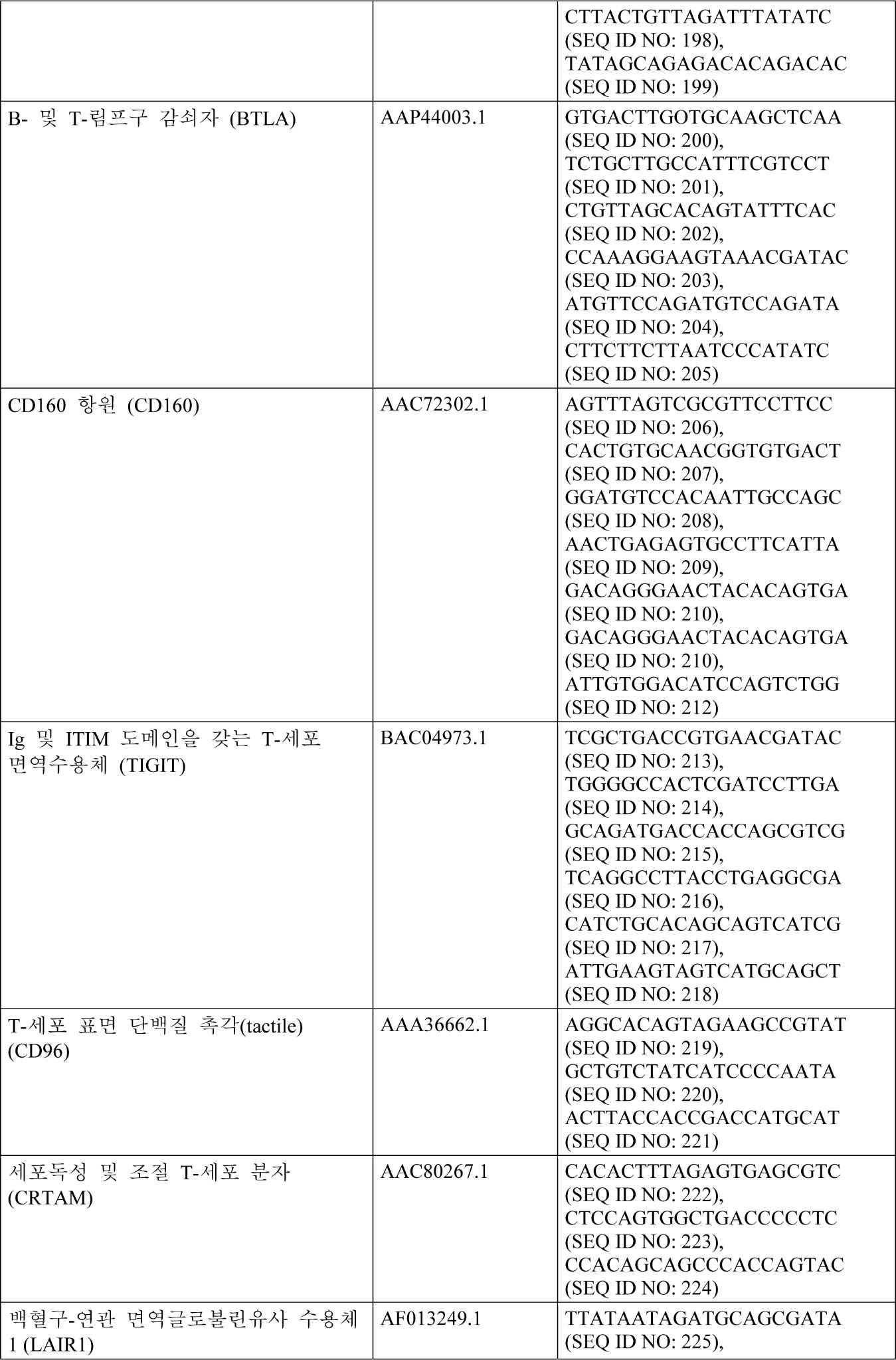
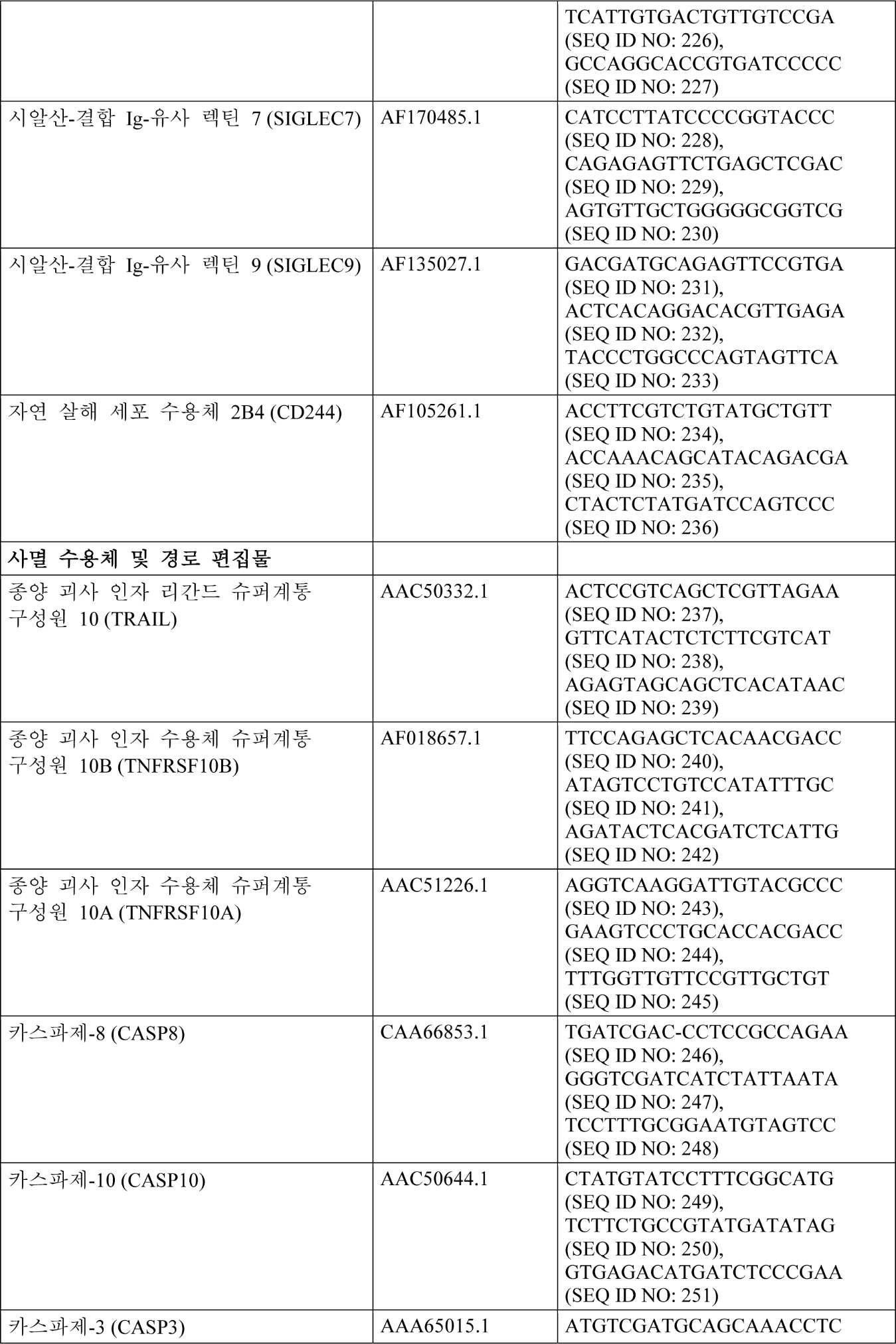
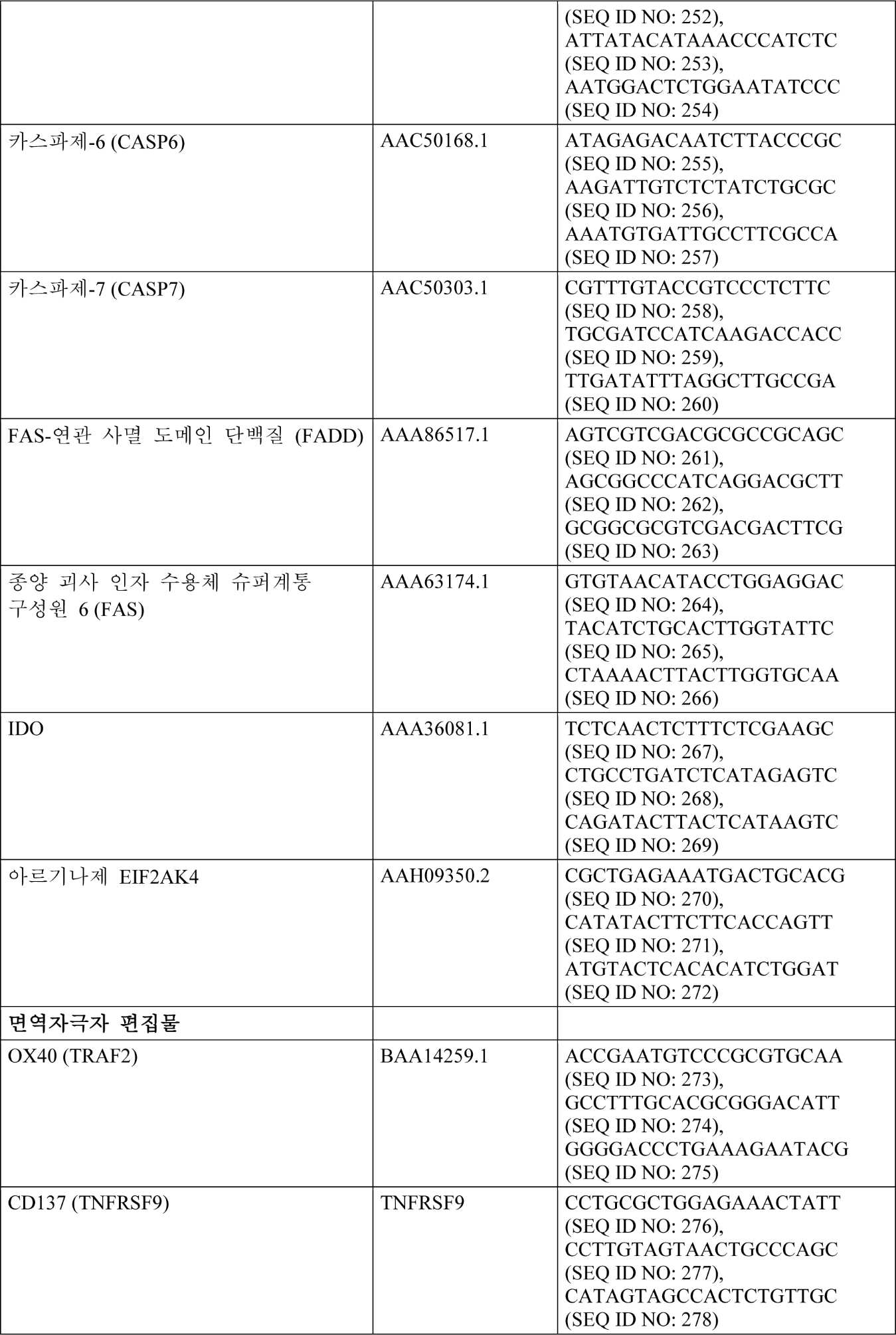
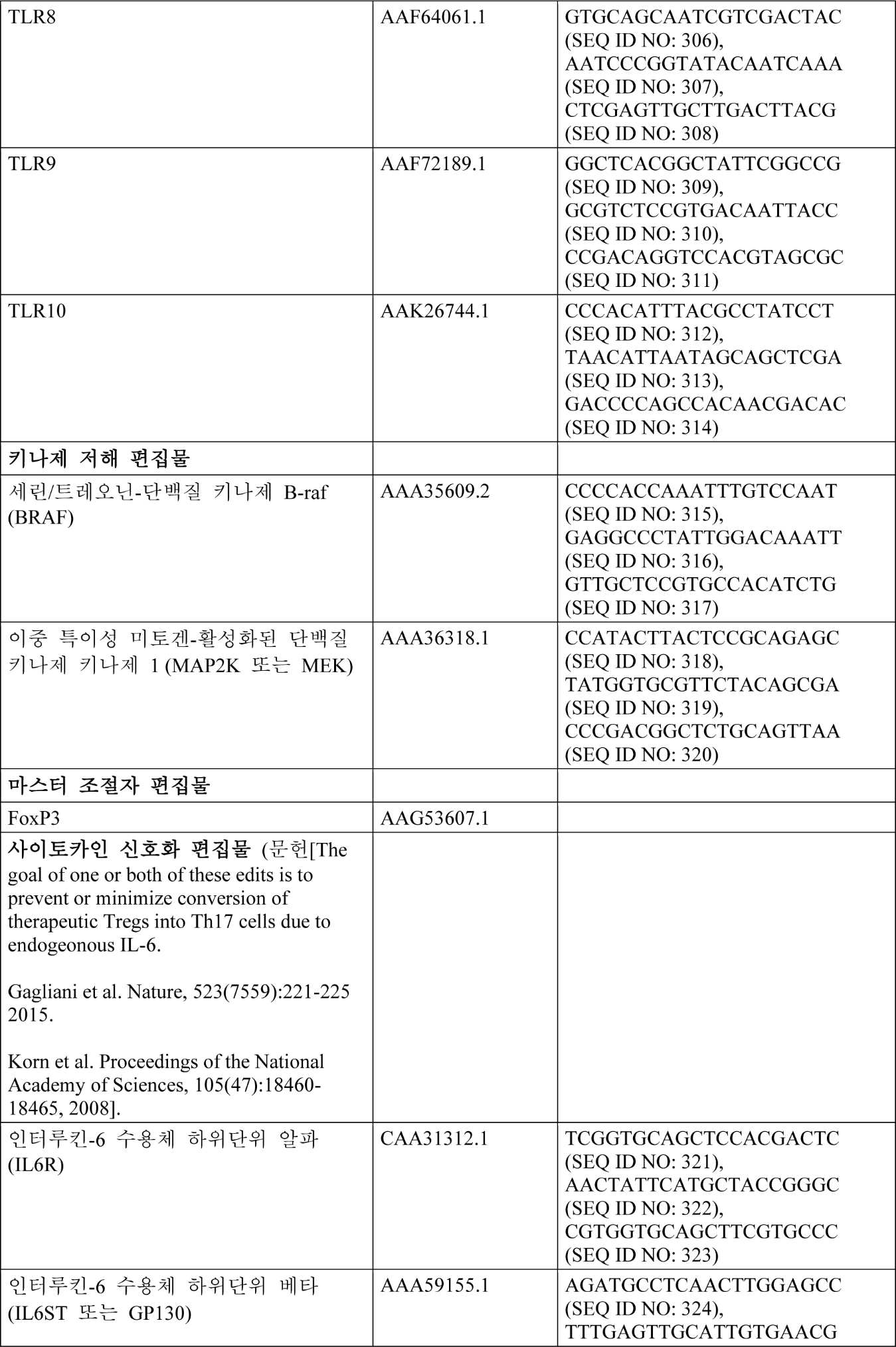
하기 표 6은 PD 차단, 면역 저해제, 사멸 수용체, 면역자극자, 톨(toll)-유사 수용체, 키나제 저해, 마스터 조절자, 사이토카인 신호화, 세포 상호작용 감소, 및 약물 상호작용 관련 편집물을 위한 예시적인 유전적 변형을 제공한다. 상기 표는 또한, 발현/과발현에 사용될 수 있는 서열에 대한 Genbank 기탁 번호뿐만 아니라 T 세포에서 Cas9을 사용하는 가이드 RNA에 대한 표적 서열을 제공한다. gRNA를 사용한 게놈 편집은 요망되는 gRNA 및 스트렙토콕커스 피오게네스(Streptococcus pyogenes) Cas9 뉴클레아제를 함유하는 렌티바이러스(lentiCRISPRv2)의 형질도입을 통해 수행된다. 이는 프로토콜에서 TALEN RNA의 전달에 대한 대안으로서 수행될 수 있다. 문헌[Sanjana, et al. Nature Methods (2014) 11(8):783-784].
하기 표는 TALEN 편집물에 대한 표적 서열, 뿐만 아니라 단백질 서열을 제공한다.
(iii) 예시적인 유전적 변형 접근법
종래의 유전적 변형 접근법은 면역 세포를 본원에 기재된 바와 같은 방식으로 유전적으로 변형시키는 데 사용될 수 있다. 일부 구현예에서, 유전적 변형은 게놈 편집을 사용하여 수행된다. "게놈 편집"은 표적 유전자의 발현을 녹아웃시키기 위해 유기체의 임의의 단백질-코딩 또는 비-코딩 뉴클레오타이드 서열을 포함한 게놈을 변형시키는 방법을 지칭한다. 일반적으로, 게놈 편집 방법은, 예를 들어, 표적화된 뉴클레오타이드 서열에서 게놈의 핵산을 절단할 수 있는 엔도뉴클레아제의 사용을 수반한다. 게놈에서 이중-가닥 절단부의 수선은 돌연변이를 도입하여 수선될 수 있고/있거나 외인성 핵산은 표적화된 부위 내로 삽입될 수 있다.
게놈 편집 방법은 일반적으로, 표적 핵산에서 이중-가닥 절단부를 발생시키는 데 관여하는 엔도뉴클레아제의 유형을 기반으로 분류된다. 이들 방법은 아연 핑거 뉴클레아제(ZFN), 전사 활성자-유사 효과기-기반 뉴클레아제(TALEN), 메가뉴클레아제, 및 CRISPR/Cas 시스템의 사용을 수반한다.
일부 경우, 본원에 기재된 바와 같은 면역 세포의 유전적 변형은, TALEN이 요망되는 표적 DNA 분자에 특이적으로 결합하여 절단할 수 있는 조작된 제하 효소인 당업계에 알려진 TALEN 기술을 사용하여 수행된다. TALEN은 전형적으로, DNA 절단 도메인에 융합된 전사 활성자-유사 효과기(TALE) DNA-결합 도메인을 함유한다. DNA 결합 도메인은 위치 12 및 13에서 분기형(divergent) 2개의 아미노산 RVD(반복체 가변 디펩타이드 모티프)를 갖는 고도로 보존된 33 내지 34개 아미노산 서열을 함유할 수 있다. RVD 모티프는 핵산 서열에 대한 결합 특이성을 결정하고, 요망되는 DNA 서열에 특이적으로 결합하기 위해 당업자에게 알려진 방법에 따라 조작될 수 있다(예를 들어, 문헌[Juillerat, et al. (January 2015). Scientific reports, 5; Miller et.al. (February 2011). Nature Biotechnology 29 (2): 143-8; Zhang et.al. (February 2011). Nature Biotechnology 29 (2): 149-53; Geiβler, et al., Boch, (2011), PLoS ONE 6 (5): e19509; Boch (February 2011). Nature Biotechnology 29 (2): 135-6; Boch, et.al. (December 2009). Science 326 (5959): 1509-12; 및 Moscou et al, (December 2009). Science 326 (5959): 1501] 참조). DNA 절단 도메인은 많은 상이한 세포 유형에서 활성인 Fokl 엔도뉴클레아제로부터 유래될 수 있다. Fokl 도메인은 이량체로서 작용하여, 표적 게놈 내 부위에 대해 적절한 배향 및 간격으로 독특한 DNA 결합 도메인을 갖는 2개의 구축물을 필요로 한다. TALE DNA 결합 도메인과 Fokl 절단 도메인 사이의 아미노산 잔기의 수와 2개의 개별 TALEN 결합 부위들 사이의 염기의 수는 높은 수준의 활성을 달성하기 위한 중요한 매개변수인 것으로 보인다. 문헌[Miller et al. (2011) Nature Biotech. 29: 143-8].
관심 표적 유전자(예를 들어, TCR, CD52, MHC, 및 본원에 기재된 다른 것들) 내의 서열에 특이적인 TALEN은 모듈형(modular) 구성성분을 사용하는 다양한 반응식을 포함하여 당업계에 알려진 임의의 방법을 사용하여 구축될 수 있다. 문헌[Zhang et al. (2011) Nature Biotech. 29: 149-53; Geibler et al. (2011) PLoS ONE 6: e19509].
관심 표적 유전자에 특이적인 TALEN은 세포 내부에서 사용되어 이중-가닥 절단부(DSB)를 생성할 수 있다. 돌연변이는, 수선 기전이 비-상동성 말단 접합을 통해 절단부를 부적절하게 수선한다면 절단부 부위에 도입될 수 있다. 예를 들어, 부적절한 수선은 프레임 시프트(frame shift) 돌연변이를 도입할 수 있다. 대안적으로, 요망되는 서열을 갖는 외래 DNA 분자는 TALEN과 함께 세포 내로 도입될 수 있다. 외래 DNA의 서열 및 염색체 서열에 따라, 이러한 과정은 결함을 교정(correct)하거나 DNA 단편을 관심 표적 유전자 내로 도입하거나, 이러한 결함을 내인성 유전자 내로 도입하여, 표적 유전자의 발현을 저하시키는 데 사용될 수 있다.
일부 경우, 본원에 기재된 바와 같은 면역 세포의 유전적 변형은 당업계에 알려진 바와 같이 CRISPR 기술(CRISPR/Cas 시스템)을 사용하여 수행된다. 이러한 변형은 결실을 포함할 수 있거나 관심 표적 유전자 내 서열의 돌연변이는 CRISPR-Cas 시스템을 사용하여 구축될 수 있으며, 이때, 일정한 간격을 두고 주기적으로 분포하는 짧은 회문 반복서열(CRISPR; Clustered Regularly Interspaced Short Palindromic Repeats)-Cas 시스템은 조작된, 비-천연 발생 CRISPR-Cas 시스템이다. 본 개시내용은 관심 표적 유전자 내의 표적 서열과 혼성화하는 CRISPR/Cas 시스템을 이용하며, 이때, CRISPR Cas 시스템은 Cas 엔도뉴클레아제 및 조작된 crRNA/tracrRNA(또는 단일 가이드 RNA("sgRNA")를 포함한다. 일부 구현예에서, CRISPR/Cas 시스템은 crRNA를 포함하고 tracrRNA 서열을 포함하지 않는다. CRISPR/Cas 복합체는 계통 특이적인 단백질 폴리뉴클레오타이드에 결합하고 단백질 폴리뉴클레오타이드의 절단을 가능하게 하여, 폴리뉴클레오타이드를 변형시킬 수 있다.
본 개시내용의 CRISPR Cas 시스템은 관심 표적 유전자 내의, 상기 유전자 내의 또는 이에 인접한 관심 영역, 예컨대 리더 서열, 트레일러(trailer) 서열 또는 인트론, 또는 코딩 영역의 업스트림 또는 다운스트림의 비-전사된 영역 내의 관심 영역에 결합하고/하거나 이를 절단할 수 있다. 본 개시내용에 사용되는 가이드 RNA(gRNA)는, gRNA가 게놈 내 예정된 절단 부위(표적 부위)로의 Cas 효소-gRNA 복합체의 결합을 지향(direct)하도록 설계될 수 있다. 절단 부위는, 미지의(unknown) 서열의 영역, 또는 SNP, 뉴클레오타이드 삽입, 뉴클레오타이드 결실, 재배열 등을 함유하는 영역을 함유하는 단편을 방출하도록 선택될 수 있다. 유전자 영역의 절단은 표적 서열의 장소에서 Cas 효소에 의해 1 또는 2개의 가닥을 절단하는 단계를 포함할 수 있다. 일 구현예에서, 이러한 절단은 표적 유전자의 저하된 전사를 초래할 수 있다. 또 다른 구현예에서, 절단은 절단된 표적 폴리뉴클레오타이드를 외인성 주형 폴리뉴클레오타이드와의 상동성 재조합에 의해 수선하는 단계를 추가로 포함할 수 있으며, 여기서, 상기 수선은 표적 폴리뉴클레오타이드의 하나 이상의 뉴클레오타이드의 삽입, 결실 또는 치환을 초래한다.
용어 "gRNA," "가이드 RNA" 및 "CRISPR 가이드 서열"은 전체에서 상호교환적으로 사용될 수 있고, CRISPR/Cas 시스템의 Cas DNA 결합 단백질의 특이성을 결정하는 서열을 포함하는 핵산을 지칭한다. gRNA는 숙주 세포의 게놈 내 표적 핵산 서열에 (이에 상보적으로, 부분적으로 또는 완전히) 혼성화한다. 표적 핵산에 혼성화하는 gRNA 또는 이의 일부는 15 내지 25개 뉴클레오타이드, 18 내지 22개 뉴클레오타이드, 또는 19 내지 21개 뉴클레오타이드 길이일 수 있다. 일부 구현예에서, 표적 핵산에 혼성화하는 gRNA 서열은 15, 16, 17, 18, 19, 20, 21, 22, 23, 24 또는 25개 뉴클레오타이드 길이이다. 일부 구현예에서, 표적 핵산에 혼성화하는 gRNA 서열은 10 내지 30개, 또는 15 내지 25개 뉴클레오타이드 길이이다.
표적 핵산에 결합하는 서열 외에도, 일부 구현예에서, gRNA는 또한, 스캐폴드(scaffold) 서열을 포함한다. 표적 핵산에 상보적인 서열과 스캐폴드 서열 둘 모두를 인코딩하는 gRNA의 발현은 표적 핵산에의 결합(혼성화)과 표적 핵산으로의 엔도뉴클레아제의 동원 둘 모두의 이중 기능을 가지며, 이는 부위-특이적 CRISPR 활성을 초래할 수 있다. 일부 구현예에서, 이러한 키메라 gRNA는 단일 가이드 RNA(sgRNA)로 지칭될 수 있다.
본원에 사용된 바와 같이, tracrRNA로도 지칭되는 "스캐폴드 서열"은, 상보적인 gRNA 서열에 결합된(혼성화된) 표적 핵산으로 Cas 엔도뉴클레아제를 동원하는 핵산 서열을 지칭한다. 적어도 하나의 스템(stem) 루프 구조를 포함하고 엔도뉴클레아제를 동원하는 임의의 스캐폴드 서열은 본원에 기재된 유전적 요소 및 벡터에서 사용될 수 있다. 예시적인 스캐폴드 서열은 당업자에게 분명할 것이고, 예를 들어, 문헌[Jinek, et al. Science (2012) 337(6096):816-821, Ran, et al. Nature Protocols (2013) 8:2281-2308], PCT 출원 WO2014/093694 및 PCT 출원 WO2013/176772에서 찾을 수 있다. 일부 구현예에서, CRISPR-Cas 시스템은 tracrRNA 서열을 포함하지 않는다.
일부 구현예에서, gRNA 서열은 스캐폴드 서열을 포함하지 않고, 스캐폴드 서열은 별도의 전사체로서 발현된다. 이러한 구현예에서, gRNA 서열은, 스캐폴드 서열의 일부에 상보적이고 스캐폴드 서열에 결합하고(혼성화하고) 엔도뉴클레아제를 표적 핵산으로 동원하는 역할을 하는 추가의 서열을 추가로 포함한다.
일부 구현예에서, gRNA 서열은 표적 핵산에 적어도 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% 또는 적어도 100% 상보적이다(또한 미국 특허 8,697,359를 참조하며, 이는 gRNA 서열과 표적 폴리뉴클레오타이드 서열의 상보성의 이의 교시에 대해 참조로서 포함되어 있음). 표적 핵산의 3' 부근에서 CRISPR 가이드 서열과 표적 핵산 사이의 미스매치는 뉴클레아제 절단 활성을 무효화할 수 있는 것으로 실증되었다(문헌[Upadhyay, et al. Genes Genome Genetics (2013) 3(12):2233-2238]). 일부 구현예에서, gRNA 서열은 표적 핵산의 3' 말단(예를 들어, 표적 핵산의 3' 말단의 마지막 5, 6, 7, 8, 9 또는 10개의 뉴클레오타이드)과 적어도 50%, 55%, 60%, 65%, 70%, 75%, 80%, 85%, 90%, 95%, 96%, 97%, 98%, 99% 또는 적어도 100% 상보적이다.
T 세포 수용체 알파 불변(TRAC) 유전자를 표적화하는 변형된 sgRNA와 비변형된 sgRNA 둘 모두를 포함하는 sgRN A 서열의 예는 본원에 제공된다. 당업자에게 분명하게 될 바와 같이, sgRNA 서열의 선별은 예측된 표적-상(on-target) 결합 부위 및/또는 표적-외 결합 부위의 수와 같은 인자에 따라 다를 수 있다. 일부 구현예에서, sgRNA 서열은 잠재적인 표적-상 부위를 최대화하고 잠재적인 표적-외 부위를 최소화하도록 선택된다.
일부 구현예에서, Cas 엔도뉴클레아제는 Cas9 뉴클레아제(또는 이의 변이체) 또는 Cpf1 뉴클레아제(또는 이의 변이체)이다. Cas9 엔도뉴클레아제는 표적 핵산의 이중-가닥 DNA를 절단하여 평활(blunt) 말단을 초래하는 반면, Cpf1 뉴클레아제를 이용한 절단은 핵산의 점착(staggered) 말단을 초래한다.
일반적으로, 표적 핵산은 3' 측(side) 또는 5' 측에서 프로토스페이서 인접 모티프(PAM; protospacer adjacent motif)의 측면에 존재하며, 이러한 PAM은 엔도뉴클레아제와 상호작용하고 엔도뉴클레아제 활성을 표적 핵산으로 표적화하는 데 추가로 관여할 수 있다. 일반적으로, 표적 핵산의 측면에 존재하는 PAM 서열은 엔도뉴클레아제 및 상기 엔도뉴클레아제가 유래되는 공급원에 따라 다른 것으로 생각된다. 예를 들어, 스트렙토콕커스 피오게네스로부터 유래되는 Cas9 엔도뉴클레아제에 대해, PAM 서열은 NGG이지만, PAM 서열 NAG 및 NGA는 더 낮은 효율로 인지될 수 있다. 스타필로콕커스 아우레우스(Staphylococcus aureus)로부터 유래되는 Cas9 엔도뉴클레아제에 대해, PAM 서열은 NNGRRT이다. 네이쎄리아 메닌지티디스(Neisseria meningitidis)로부터 유래되는 Cas9 엔도뉴클레아제에 대해, PAM 서열은 NNNNGATT이다. 스트렙토콕커스 테르모필루스(Streptococcus thermophilus)로부터 유래되는 Cas9 엔도뉴클레아제, St1Cas9 및 dSt3Cas9에 대해, PAM 서열은 각각 NNAGAAW 및 NGGNG이다. 트레포네마 덴티콜라(Treponema denticola)로부터 유래되는 Cas9 엔도뉴클레아제에 대해, PAM 서열은 NAAAAC이다. 일부 구현예에서, Cas 엔도뉴클레아제는 Cpf1 뉴클레아제이다. Cas9 엔도뉴클레아제와는 대조적으로, Cpf1 엔도뉴클레아제는 일반적으로, tracrRNA 서열을 필요로 하지 않고, 표적 핵산의 5' 말단에 위치한 PAM 서열을 인지한다. Cpf1 뉴클레아제에 대해, PAM 서열은 TTTN이다. 일부 구현예에서, Cas 엔도뉴클레아제는 MAD7(유박테리움 렉탈레(Eubacterium rectale)로부터의 Cpf1 뉴클레아제로도 지칭됨)이고, PAM 서열은 YTTTN이다.
일부 구현예에서, 세포를 유전적으로 조작하는 것은 또한, Cas 엔도뉴클레아제, 또는 이를 인코딩하는 핵산 서열(예를 들어, Cas 엔도뉴클레아제를 인코딩하는 mRNA)을 세포 내로 도입하는 단계를 포함한다. 일부 구현예에서, Cas 엔도뉴클레아제, 및 gRNA를 인코딩하는 핵산은 동일한 핵산(예를 들어, 벡터) 상에 제공된다. 일부 구현예에서, Cas 엔도뉴클레아제, 및 gRNA를 인코딩하는 핵산은 상이한 핵산(예를 들어, 상이한 벡터) 상에 제공된다. 일부 구현예에서, Cas 엔도뉴클레아제는 Cas 엔도뉴클레아제를 인코딩하는 mRNA로서 제공되고, gRNA는 변형된 gRNA 분자로서 제공된다. 대안적으로 또는 이에 더하여, Cas 엔도뉴클레아제는 단백질 형태로 세포 내로 제공되거나 도입될 수 있다.
일부 구현예에서, Cas 엔도뉴클레아제는 Cas9 효소 또는 이의 변이체이다. 일부 구현예에서, Cas9 엔도뉴클레아제는 스트렙토콕커스 피오게네스, 스타필로콕커스 아우레우스, 네이쎄리아 메닌지티디스, 스트렙토콕커스 테르모필루스 또는 트레포네마 덴티콜라로부터 유래된다. 일부 구현예에서, Cas 엔도뉴클레아제를 인코딩하는 뉴클레오타이드 서열은 숙주 세포에서 발현을 위해 코돈 최적화될 수 있다. 일부 구현예에서, 엔도뉴클레아제는 Cas9 상동체 또는 이종상동체(ortholog)이다.
일부 구현예에서, Cas9 엔도뉴클레아제를 인코딩하는 뉴클레오타이드 서열은 단백질의 활성을 변경시키기 위해 추가로 변형된다. 일부 구현예에서, Cas9 엔도뉴클레아제는 엔도뉴클레아제의 하나 이상의 촉매적 잔기를 불활성화시키기 위해 변형되었다. 일부 구현예에서, Cas9 엔도뉴클레아제는 "닉카제(nickase)" 또는 "Cas9n"으로 지칭되는 엔도뉴클레아제의 촉매적 잔기 중 하나를 불활성화시키기 위해 변형되었다. Cas9 닉카제 엔도뉴클레아제는 표적 핵산의 하나의 DNA 가닥을 절단한다. 일부 구현예에서, 본원에 기재된 방법은 2개의 별개의 절단 반응을 수반하며, 여기서, 하나의 Cas9 닉카제는 표적 핵산의 하나의 DNA 가닥을 절단하도록 지향되고 Cas9 닉카제는 표적 핵산의 제2 DNA 가닥을 절단하도록 지향된다.
(iv) MHC-CAR 조절 T 세포(Treg)
본원에 개시된 임의의 MHC-CAR-발현 T 세포는 여포 조절 세포의 면역 조정 활성을 모방할 수 있는 조절 T 세포(Treg)일 수 있다. 본원에 사용된 바와 같이, 억제자 T 세포로도 알려진 조절 T 세포 또는 Treg 세포는 면역계를 조정하며, 자가-항원에 대한 관용을 유지하며, 및/또는 자가면역 질병을 예방하는 T 세포의 하위집단을 지칭한다. Treg 세포는 자가면역 질병에 관여하는 효과기 T 세포, 예컨대 병적 CD4+ 및/또는 CD8+ 세포의 유도 및/또는 증식을 억제시키거나 하향조절하기 위해 면역억제자로서 작용한다.
본원에 개시된 유전적으로 변형된 Treg 세포는 자연상에서 Treg 세포와 연관된 하나 이상의 바이오마커, 예를 들어, CD4, FOXP3, CD25, CD45R(예를 들어, CD45RA 또는 CD45RO), 또는 이들의 조합을 발현한다. Treg 세포는 적합한 공여자(예를 들어, 치료를 받는 인간 환자)로부터 단리된 말초 혈액 단핵 세포(PBMC)를 사용하여 제조될 수 있다(이로부터 유래될 수 있음). PBMC로부터 Treg 세포의 하위집단을 단리하는 방법, 예를 들어, 세포 소팅은 당업계에 알려져 있다. 적합한 MHC-CAR 구축물에 대한 발현 벡터, 뿐만 아니라 다른 유전적 변형(예를 들어, 본원에 기재된 것들)은 본원에 기재된 바와 같은 방법 또는 당업계에 알려진 다른 방법을 통해 Treg 하위집단 내로 도입될 수 있다. 대안적으로, 유전적으로 변형된 Treg 세포는, CD25를 코딩하는 이식유전자 및/또는 다른 Treg 세포 마커를 적합한 T 세포 내로 도입함으로써 제조될 수 있으며, 이는 MHC-CAR에 대한 발현 카세트 및 선택적으로 본원에 기재된 바와 같은 다른 유전적 변형을 도입하도록 추가로 변형될 수 있다.
일부 구현예에서, 유전적으로 변형된 Treg 세포는 특이적인 유형의 병적 세포(예를 들어, CD4+ 세포 또는 CD8+ 세포)를 표적화하는 분자를 제시(예를 들어, 표면 발현 또는 표면 부착)하고/하거나 특이적인 조직 부위(예를 들어, 림프절 또는 염증 부위)를 표적화하는 분자를 제시하도록 추가로 변형될 수 있다.
일부 예에서, 유전적으로 변형된 Treg 세포는 세포외 도메인, 예컨대 B 세포 표면 마커, 예를 들어, CD19에 특이적인 단일-사슬 항체(scFv)를 포함하는 키메라 수용체(CAR)를 추가로 발현한다. 대안적으로 또는 이에 더하여, Treg 세포는 T 세포 표면 마커, 예를 들어, CS-1에 특이적인 세포외 도메인(예를 들어, scFv)을 포함하는 키메라 수용체(CAR)를 추가로 발현할 수 있다. 이러한 키메라 수용체는 단일 단백질 상에서 함께 천연적으로 확인되지 않는 조합으로 세포외 도메인, 막관통 도메인, 및 세포질 도메인(예를 들어, 공동-자극 도메인, 세포질 신호화 도메인, 예컨대 CD3ζ, 또는 이들의 조합을 포함함)을 포함하는 세포-표면 수용체일 수 있다.
Treg 세포는 추가로, 림프절 및/또는 배중심(germinal center)을 표적화하는 분자, 예를 들어, CXCR5를 제시하고/하거나 염증 부위를 표적화하는 분자, 예를 들어, CCR6를 제시할 수 있다. 배중심 B 세포(GC B 세포)를 표적화하는 것은 적어도 부분적으로는, 특수화된 헬퍼 T 세포 하위세트, CXCR5highPD-1high T 여포 헬퍼(TFH) 세포에 의해 매개될 수 있다. Foxp3+ Treg는 Bcl6의 발현 및 B 세포와의 SAP-매개 상호작용을 통해 TFH 억제자가 되도록 전환(divert)될 수 있다. 생성된 여포 조절 T 세포(TFR)는 생체내에서 TFH 세포와 Treg 세포 둘 모두의 특징을 공유하며, 배중심으로 국재화되고(localize), TFH 세포 집단 및 배중심의 크기를 조절하는 것으로 예상된다.
나아가, 본원에 개시된 Treg 세포는 본원에 기재된 바와 같은 하나 이상의 추가의 유전적 변형, 예를 들어, 체크포인트 분자 녹아웃을 포함할 수 있다.
B-세포 또는 T-세포 특이적 CAR을 발현하는 Treg 세포는 자가면역 질병에 관여하는 병적 B 세포 및/또는 T 세포를 표적화할 수 있다. 예를 들어, 본원에 기재된 바와 같은 유전적으로 변형된 Treg 세포는 여포 조절 세포와 유사한 기능, 예를 들어, B 세포, T 세포, 및/또는 수지상 세포의 표적화를 나타내어, 이로써 예를 들어, B 세포 자극을 하향조절하며, 배중심의 활성화를 저해할 수 있는 억제성 사이토카인(GCB 세포(예컨대 Il-10 및 TGF-베타)을 분비하며, Tfh(MHC CAR을 통해) 및 GCB(예를 들어, CD19 CAR을 통해)의 세포용해를 유도하며, 및/또는 GC B 세포로의 또는 T 여포 헬퍼(Tfh) 세포로의 신호화 전달을 기계적으로 교란(예를 들어, GC B 및 MHC-펩타이드 Tfh에의 결합을 통해)시키는 것으로 예상될 것이다. 대안적으로 또는 이에 더하여, Treg 세포는 헬퍼 T 세포, B 세포, 및/또는 항원 제시 세포 둘 모두와 잠재적으로 연동할 수 있거나, 일부 경우, 이러한 연동을 물리적으로 차단할 수 있다.
III. 면역치료법에서 MHC-CAR을 발현하는 면역 세포의 적용
본원에 기재된 MHC-CAR(인코딩 핵산 또는 이를 포함하는 벡터)을 발현하는 숙주 면역 세포는 자가면역 질병, 예컨대 MS, I형 당뇨병, 루푸스, 류마티스성 관절염 등에 관여하는 병원성 세포를 표적화하고 제거하는 데 유용하다. 일부 구현예에서, 대상체는 포유류, 예컨대 인간, 원숭이, 마우스, 토끼 또는 가축 포유류이다. 일부 구현예에서, 대상체는 인간, 예를 들어, 자가면역 질병(예를 들어, MS)을 갖고 있거나 갖고 있는 것으로 의심되거나 가질 위험이 있는 인간 환자이다.
MHC-CAR-발현 면역 세포는 약제학적으로 허용 가능한 담체와 혼합되어 약제학적 조성물을 형성할 수 있으며, 이러한 약제학적 조성물 또한 본 개시내용의 범위 내에 포함된다. 본원에 기재된 방법을 수행하기 위해, 유효량의, 본원에 기재된 임의의 MHC-CAR 구축물을 발현하는 면역 세포는 치료를 필요로 하는 대상체에게 투여될 수 있다. 면역 세포는 대상체에게 자가일 수 있으며, 즉, 면역 세포는 치료를 필요로 하는 대상체로부터 수득되며, MHC-CAR 구축물의 발현을 위해 유전적으로 조작되고, 선택적으로 본원에 기재된 바와 같은 하나 이상의 추가의 유전적 변형을 함유하며, 그 후에 동일한 대상체에게 투여된다. 대상체에게 자가 세포의 투여는 비-자가 세포의 투여와 비교하여 면역 세포의 감소된 거부를 초래할 수 있다. 대안적으로, 면역 세포는 동종이계 세포이며, 즉, 세포는 제1 대상체로부터 수득되며, MHC-CAR 구축물의 발현을 위해 유전적으로 조작되고, 제1 대상체와 상이하지만 동일한 종의 제2 대상체에게 투여된다. 예를 들어, 동종이계 면역 세포는 인간 공여자로부터 유래되고, 상기 공여자와 상이한 인간 수혜자에게 투여될 수 있다.
일부 구현예에서, 면역 세포는 표적 면역 질병에 대한 치료제, 예를 들어, MS 치료를 위한 알렘투주맙과 함께 공동-사용된다. 이러한 면역치료법은, 상기 면역치료법이 대상체에서 유용한 것으로 여겨지는 표적 면역 질병을 치료하거나, 경감시키거나 이의 증상을 감소시키는 데 사용된다.
MHC-CAR 면역치료법의 효능은 당업계에 알려진 임의의 방법에 의해 평가될 수 있고, 숙련된 의료 전문가에게 분명할 것이다. 예를 들어, 면역치료법의 효능은 대상체의 생존율 및/또는 대상체에서 질병 증상의 감소에 의해 평가될 수 있다.
일부 구현예에서, 본원에 개시된 임의의 MHC-CAR을 발현하는 면역 세포는, 자가면역 질병에 대한 치료제로 치료를 받았거나 치료받고 있는 대상체에게 투여된다. 본원에 개시된 임의의 하나의 MHC-CAR을 발현하는 면역 세포는 치료제와 함께 공동-투여될 수 있다. 예를 들어, 면역 세포는 인간 대상체에게 치료제와 함께 동시에 투여될 수 있다. 대안적으로, 면역 세포는 치료제를 수반하는 치료의 전개 동안 인간 대상체에게 투여될 수 있다. 일부 예에서, 면역 세포 및 치료제는 인간 대상체에게 적어도 4시간 간격을 두고, 예를 들어, 적어도 12시간 간격을 두고, 적어도 1일 간격을 두고, 적어도 3일 간격을 두고, 적어도 1주 간격을 두고, 적어도 2주 간격을 두고, 또는 적어도 1개월 간격을 두고 투여될 수 있다.
본원에 개시된 방법을 실시하기 위해, 유효량의, MHC-CAR을 발현하는 면역 세포 또는 이의 조성물은 치료를 필요로 하는 대상체(예를 들어, 인간 MS 환자)에게 적합한 경로, 예컨대 정맥내 투여를 통해 투여될 수 있다. 임의의 MHC-CAR을 발현하는 면역 세포 또는 이의 조성물은 유효량으로 대상체에게 투여될 수 있다. 본원에 사용된 바와 같이, 유효량은, 투여 시 대상체에게 치료 효과를 부여하는 각각의 작용제(예를 들어, MHC-CAR을 발현하는 면역 세포 또는 이의 조성물)의 양을 지칭한다. 본원에 기재된 세포 또는 조성물의 양이 치료 효과를 달성하였는지 여부의 결정은 당업자에게 분명할 것이다. 유효량은 당업자에 의해 인지되는 바와 같이, 건강 요원의 지식 및 전문성 내에서, 치료되는 특정 질환, 상기 질환의 중증도, 연령, 신체적 상태, 크기, 성별 및 체중을 포함한 개별적인 환자 매개변수, 치료 기간, 공존 치료법(있다면)의 성질, 구체적인 투여 경로 및 유사한 인자에 따라 다양하다. 일부 구현예에서, 유효량은 대상체에서 임의의 질병 또는 장애를 경감시키거나, 덜어주거나(relieve), 완화하거나, 개선하거나, 감소시키거나 상기 질병 또는 장애의 진행을 지연시킨다. 일부 구현예에서, 대상체는 인간이다. 일부 구현예에서, 대상체는 인간 암 환자이다.
일부 구현예에서, 대상체는, 정상적인 신체 부분을 공격하는 비정상적인 면역 반응을 특징으로 하는 자가면역 질병을 앓고 있는 인간 환자이다. 자가면역 질병의 예는 다발성 경화증, 전신 홍반성 루푸스, 류마티스성 관절염, 소아 특발성 관절염(소아 특발성 관절염으로도 알려져 있음), 쇼그렌 증후군, 전신성 경화증, 강직성 척추염, 1형 당뇨병, 자가면역 갑상선 질병(그레이브스 및 하시모토), 다발성 경화증 중증 근무력증, 염증성 장 질병(크론 또는 궤양성 대장염), 건선, 또는 표 1에서 언급된 질병을 포함한다.
일반적으로 자가면역 질병이 영향을 받을 수 있는 면역 캐스케이드에서 수많은 병기가 존재한다. 본원에 개시된 방법이 포함하는 편집물들의 조합에 의해 가능하게 이루어지는 개입의 연속체(continuum)가 존재한다. 예를 들어, MHC-CAR 외에도 별개의 표면 분자 세트를 제시하는 Treg 세포는 상이한 병기에서 자가면역 질병을 치료하는 데 사용될 수 있다.
MS를 포함한 많은 면역 장애의 초기 병기에서, 조절 기전에서 설명되지 않는 결핍(unexplained deficit)이 존재하고/하거나 관용 유도가 MS가 존재하고 T 세포에 의한 신경계 상에서의 반복된 공격이 시작된다. 적합한 MHC-CAR 및 항-CD19 CAR(선택적으로 본원에 기재된 바와 같은 다른 유전적 변형과 함께)을 발현하는 Treg 세포는 개입에 사용될 수 있다.
자가반응성 Treg 세포의 이점은 "방관자" 억제자로서 작용하여, 영향을 받는 조직에 의해 국소적으로 발현되는 동족 항원에 반응하여 부위-특이적 방식으로 염증을 약화시키는(dampen) 이들 자가반응성 Treg 세포의 능력이다. 조절 T 세포의 (자가항원에 의한) 유도는, 심지어 여러 가지 자가항원이 존재하는 경우(또는 초기/1차) 자가항원이 알려져 있지 않은 경우에도 질병 진행을 억제시킬 수 있다. Treg는 상대적으로 자유롭게 이동할 수 있고, T 세포 및 B 세포를 저해할 수 있고, 염증 환경으로 복귀하는 것을 방지할 수 있다. 이들 자가반응성 Treg는 방관자 억제자로서 작용하고 영향을 받는 조직에 의해 국소적으로 발현되는 동족 항원에 반응하여 부위-특이적 방식으로 염증을 약화시키는 이들 자가반응성 Treg의 능력에서 유리하다.
따라서, 유전적으로 변형된 Treg 세포는 자가반응성 Treg 세포의 억제자 기능을 모방하도록 설계될 수 있다. 이러한 Treg 세포는 예를 들어, PD-L1/PD-1 녹아웃을 갖도록, 염증 부위로 안내하기 위해 CCR6 및/또는 MOG 표적화 scFv를 제시하도록, 적합한 MHC-CAR 및/또는 항-CD19-CAR을 발현하도록 변형될 수 있다. 대안적으로, Treg 세포는 예를 들어, PD-L1/PD-1 녹아웃을 갖도록, 배중심 및/또는 이소성 림프절로 안내하기 위해 CXCR5를 제시하도록, 적합한 MHC-CAR 및/또는 항-CD19-CAR을 발현하도록 변형될 수 있다. 이들 유형의 Treg 세포는 염증 부위에서 병원성 세포와 상호작용하며, 병원성 상호작용을 차단하며, 및/또는 염증 환경을 진정시킬 수 있다. 이들은 초기 질병 병기에서(병원성을 저해하기 위해) 또는 세포독성치료법 후에(염증 환경으로의 복귀를 방지하기 위해) 사용될 수 있다.
재발-완화형 MS(중기-병기)는 천연적으로 그 자체를 조절하고, 이들 천연 조절 기전을 증대시키는 치료는 질병 과정을 제어하는 것을 도울 것이다. 성공적인 질병 치료에서, Th1 세포로부터 Th2 and Th3 세포로의 시프트, 및 다른 조절 세포의 출현이 존재한다. 이 병기에서, 치료 표적은 병원성 B 세포와 병원성 T 세포 둘 모두를 포함할 것이다. 이러한 중기-병기 질병을 치료하기 위한 Treg 세포는 본원에 기재된 바와 같은 적합한 MHC-CAR, 및 추가의 CAR 표적화 B 세포(예를 들어, 항-CD19 CAR) 또는 표적화 T 세포, 예컨대 CD8+ 세포를 발현할 수 있다. Treg 세포는 CXCR5를 추가로 제시하거나 CXCR5 표적화가 없을 수 있다. 항-CD19 CAR을 발현하는 Treg 세포는 배중심에서 B 세포를 제거하는 데 사용될 수 있다.
MS가 재발완화형으로부터 만성 진행형 형태(말기-병기)로 변하는 경우, T 세포는 만성 활성화 상태로 진입하고, 퇴행성 과정이 발생한다. 세포독성 CD8+ T 세포에 대한 공격적인 치료는, 충분히 세포독성인 CAR 증대를 필요로 한다. 이때, 치료는 Treg 세포에 의해 주로 구동되는 치료로부터 MHC-CAR CD8+ T 세포 및 심지어 MHC-CAR CS-1 세포에 의해 구동되는 치료로 시프트될 수 있다. 궁극적인 목표: 방관자 효과에 의해 증강되는 세포독성을 통해 병태를 억제시키는 것은 동일하게 남아 있다. 이 질병 병기에 사용하기 위한 유전적으로 조작된 T 세포는 적합한 MHC-CAR, 및 질병의 말기-병기에 관여하는 병적 T 세포, 예를 들어, CD8+ T 세포를 표적화하는 추가의 CAR을 발현할 수 있다. 일부 예에서, 추가의 CAR은 CD8+ T 세포 상에서 발현되는 당단백질인 CS-1(SLAMF7로도 알려져 있음)을 표적화할 수 있다. CS1은 CD8+ T 세포 및 혈장 세포를 표적화하고 사멸화하는 데 사용될 수 있는 유망한 항원이다. CS1-CAR T 세포는 IL-2뿐만 아니라 더 많은 IFN-감마를 분비하여, 더 높은 수준의 활성화 마커 CD69를 발현하며, 탈과립화의 더 높은 용량, 및 증강된 세포독성을 제시한다. 항-CS1 CAR은 CD8+ T-세포를 표적화할 것이다. 유전적으로 변형된 T 세포는 혈장 세포의 골수 표적화를 위한 분자, 예컨대 CXCR4, 및 CXCR3와 함께 염증형성 조직으로의 이들의 표적화를 추가로 제시할 수 있다.
문헌[Hiepe et al., Nature Reviews Rheumatology, 7(3):170-178, 2011]. 그 예는 루푸스에서 혈장 세포의 표적화를 포함한다.
IV.
치료 용도의 키트
본 개시내용은 또한, 병원성 면역 세포, 예컨대 자가면역에서 자가반응성 T 세포를 억제시키는 데 사용하기 위한 MHC-CAR-발현 면역 세포의 사용 키트를 제공한다. 이러한 키트는 MAR-CAR을 발현하는 면역 세포, 예컨대 본원에 기재된 것들, 및 약제학적으로 허용 가능한 담체를 포함하는 조성물을 포함하는 하나 이상의 용기를 포함할 수 있다.
일부 구현예에서, 키트는 본원에 기재된 임의의 방법에서 사용하기 위한 설명서를 포함할 수 있다. 포함된 설명서는 치료를 필요로 하는 대상체, 예를 들어, MS 환자에게의 MHC-CAR-발현 면역 세포의 투여에 대한 설명을 포함할 수 있다. 상기 키트는, 대상체가 치료를 필요로 하는지의 여부를 식별하는 것을 기반으로 치료에 적합한 대상체의 선택에 대한 설명을 추가로 포함할 수 있다. 일부 구현예에서, 설명서는 치료를 필요로 하는 대상체에게 면역 세포를 투여하는 설명을 포함한다.
본원에 기재된 MHC-CAR을 발현하는 면역 세포의 용도에 관한 설명서는 일반적으로, 의도된 치료를 위한 투여의 투약량, 투약 스케쥴, 및 투여 경로에 관한 정보를 포함한다. 상기 용기는 단위 용량, 벌크 패키지(예를 들어, 다중-용량 패키지) 또는 하위-단위 용량일 수 있다. 본 개시내용의 키트에 공급된 설명서는 전형적으로, 라벨 또는 패키지 인서트 상에 작성된 설명서이다. 상기 라벨 또는 패키지 인서트는, 약제학적 조성물이 대상체에서 질병 또는 장애를 치료하며, 개시를 지연시키며, 및/또는 경감시키기 위해 사용됨을 나타낸다.
본원에 제공된 키트는 적합한 포장재에 존재한다. 적합한 포장재는 바이얼, 병, 단지(jar), 가요성 포장재 등을 포함하지만 이들로 한정되는 것은 아니다. 또한, 특정 장치와 조합되어 사용되기 위한 패키지가 고려된다. 키트는 멸균 접근 포트를 가질 수 있다(예를 들어, 용기는 피부밑 주사 바늘에 의해 관통 가능한 스토퍼(stopper)를 가진 정맥내 용액 백 또는 바이얼일 수 있음). 상기 용기는 또한, 멸균 접근 포트를 가질 수 있다. 약제학적 조성물 내의 적어도 하나의 활성제는 본원에 기재된 바와 같은 MHC-CAR을 발현하는 면역 세포이다.
키트는 선택적으로, 추가의 구성성분, 예컨대 완충제 및 해석 가능한 정보를 제공할 수 있다. 정상적으로, 상기 키트는 용기, 및 상기 용기 상의 또는 상기 용기와 연관되어 있는 라벨 또는 패키지 인서트(들)를 포함한다. 일부 구현예에서, 본 개시내용은 상기 기재된 키트의 내용물을 포함하는 제조 물품을 제공한다.
추가의 정교화(elaboration) 없이, 당업자는 상기 설명을 기반으로, 본 발명을 이의 최대 정도까지 이용하는 것으로 여겨진다. 따라서, 하기 구체적인 구현예는 단순히 예시적인 것으로 간주되고, 본 개시내용의 나머지를 임의의 방식으로 제한하려는 것이 아니다. 본원에서 인용된 모든 공개문헌은 본원에서 참조된 목적 또는 주제를 위해 참조에 의해 포함된다.
실시예
본 실시예는 MS에 연루된 미엘린 염기성 단백질(MBP)-특이적 T 림프구에 대해 치료적 T 세포를 선택적으로 재지향(redirect)시키기 위해 키메라 수용체를 이용하는 세포성 면역치료법의 개발에 초점을 맞춘다[16]. 이 프로그램의 결과는 병적, 자가-특이적 T 림프구와 반작용할 수 있는 재지향된 치료적 T 세포의 추가의 개발을 지지하고, 인간화된 MBP-DR2-키메라 수용체를 MS에서 치료적 표적으로서 구체적으로 확증할 수 있다[29].
실시예 1: 미엘린 염기성 단백질에 특이적인 변형된 T-세포의 구축
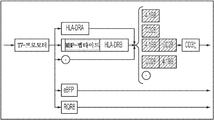
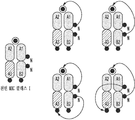
MBP-적재된 주 조직적합성 복합체-키메라 항원 수용체(MHC-CAR)를 표적화하는 항원-특이적 T-세포 수용체(TCR)에 대한 구축물은 검정법을 위해 TCR 녹아웃된 세포 내로 재도입되도록 설계된다. TCR 구축물의 설계는 공개된 구조를 갖는 항원-특이적 TCR 및 인간 세포주에서 확증된 TCR 발현 구축물을 기반으로 한다[17, 46, 51, 52]. 그린 형광 단백질(eGFP) 또는 루시퍼라제는 표지화를 위해 유전적으로 인코딩된다[28]. TCR 구축물을 포함하고 유전자를 보고하는 예시적인 렌티바이러스 발현 벡터는 도 1에 제공된다.
Jurkat E6-1(TCR을 발현하는 대조군 균주), Jurkat J.RT3-T3.5(TCRb가 결여된 균주), SupT1(손상된 TCRa를 갖는 균주) 및 1차 인간 T 세포(TCR 클론유형(clonotype)의 다양한 집단을 함유함)를 포함한 몇몇 세포주는 TCR 발현 및 활성을 시험하기 위해 선택된다.
Jurkat E6-1 세포는 말초 혈액으로부터 확립된 인간 T 림프구 세포주이다. 이는 TCR을 발현하는 대조군 세포주로서 사용된다[15, 18].
Jurkat RT3-T3.5는 TCRβ 사슬의 발현을 배제하는 돌연변이로 인해 TCRβ가 결여된다. 이는 또한, 표면 CD3를 발현하거나 T-세포 수용체 α,β 헤테로이량체를 생성하는 데 실패한다. 따라서, 이는 T-세포 수용체 유전자 전이(transfer)를 확증하는 데 사용된다[1, 6, 21, 49].
SupT1은 다수의 T 계통 마커를 발현하는 인간 림프아세포주이고, 이것이 비-기능성 수용체를 인코딩하고 TCRα를 발현하는 데 실패하기 때문에 사용된다[49].
PMBC-유래 1차 인간 T 세포는 TCR 클론유형의 다양한 레퍼토리를 함유한다.
도 1에 예시된 바와 같은 항원-특이적 TCR을 함유하는 렌티바이러스 벡터는 적어도 하나의 TCR 사슬이 결여된 암세포주를 형질도입하는 데 사용되고, 후속적으로 형광-활성화된 세포 소팅(FACS)을 사용하여 발현에 대해 평가된다. 항원-특이적 TCR을 함유하는 암세포주에서, 루시퍼라제는 마우스 연구에서 이의 사용을 가능하게 하기 위해 성공적인 안정한 발현 후 세포주에 첨가된다.
mRNA, 멀티시스트론성 mRNA, 및 렌티바이러스 전달을 위한 TCR 구축물은 간단하게, 유전적으로 인코딩된 eGFP를 기반으로 한 스크린 및 항-TCR 또는 항-CD3 항체를 이용한 표지화를 통해 진행된다[3, 19].
실시예 2: MHC-기반 키메라 수용체(MHC-CAR) 및 이를 발현하는 T-세포의 구축
(i) MHC-CAR 구축물의 설계
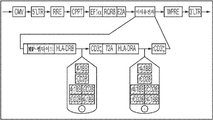
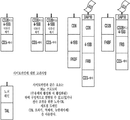
MBP 84-102 에피토프를 인간 백혈구 항원 HLADR2에 유전적으로 연결짓는 입양(adoptive) 세포 치료법을 위한 수용체가 발생되고, 키메라 세포내 신호화 도메인을 혼입하거나 결여된다[29]. 항원-주 조직적합성 복합체(Ag-MHC) 도메인은 수용체로서 역할을 하여, MBP-특이적 표적 세포의 TCR에 결합한다. Ag-MHC-CAR은, [9, 25]에서 제공된 방법에 따라, 선택적으로 추가의 공동-자극 신호화 도메인(즉, 제2 세대 또는 제3 세대 신호화 도메인)과 조합될 수 있는 CD3-ζ(즉, 제1 세대 신호화 도메인)을 갖는 전임상 마우스 모델에서 인간에서의 효능에 대해 확증되었다. MHC-CAR의 다양한 설계의 도식도는 도 2에 제공된다.
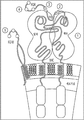
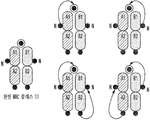
MHC-CAR은 HLA-DR의 구조를 기반으로 하여 설계되고, 여러 가지 내재 세포질 공동자극성 도메인과 함께 조합된다. MHC-CAR은 2개의 하위단위를 가진다: (i) 리더 서열, DRA*1010 도메인 및 세포질 도메인을 함유하는 α-사슬; 및 (ii) 리더 서열(HLA-DRB1*1501로부터), 펩타이드(미엘린 염기성 단백질로부터의 DENPVVHFFKNIVTPRTPP(SEQ ID NO: 15)), 도메인( HLA-DRB1*1501로부터), 및 세포질 신호 도메인, 예를 들어, CD3z를 함유하는 β-사슬[29]. 도 3. mRNA를 생성하는 데 사용되는 DNA는 단일 사슬(도 4에서 하나의 구현예로서 나타냄)을 함유하거나, 도 5에 예시된 바와 같이 멀티시스트론성이고 오르토고날 2A 서열에 의해 분리된다. 유전적으로 인코딩된 eBFP 또는 RQR8은 세포-표지화를 위해 또는 결실 기전을 제공하기 위해 세포 내로 도입된다[4, 5, 37, 40]. 도 3 및 도 5.
도 6에 예시된 바와 같이, 설계된 MHC-CAR은 태깅을 위한 많은 부위를 가진다. 부위 1은 본태(native) HLA-DR이 CIITA 편집으로 인해 발현되지 않는 경우에 대한 HLA-DR 항체 결합 부위이다[26, 38]. 부위 2 및 3은 폴리히스티딘-태그 모티프에 대한 잠재적인 삽입 부위이다[24]. 부위 4 및 5는 RQR 및 RQR8을 각각 나타낸다[37]. 다발성 경화증은 혈액 뇌 장벽 침투성에 영향을 주는 것으로 나타나 있어서, 치료적 MHC-CAR의 안전성을 증강시키기 위해서는, 유전적으로 인코딩된 RQR이 중증 MS의 치료에서 오프라벨(offlabel) 사용되는 키메라 모노클로날 항체 치료인 리툭시맙의 투여 시 MHC-CAR T 세포의 신속한 결실을 가능하게 할 것이다[42].
(ii) MHC-CAR을 발현하는 T 세포주의 구축
하기에서 고찰되는 많은 세포주는 MHC-CAR 구축물을 시험하기 위해 선택된 것이다. 그 후에, 임상적으로 번역 가능한 프로토콜을 확립하기 위해 검정법이 인간 T 세포에서 계속된다.
K56 세포는 클래스 I 및 클래스 II MHC가 결여되어 있어서, 항체를 사용한 HLA-DR 발현의 태그리스(tagless) 입증을 가능하게 한다(HLA-DR은 MHC-CAR의 구성성분임)[45]. 발현 검정법은 유세포분석을 사용하여 RQR8 발현에 비한 MHC-CAR 발현의 평가를 가능하게 할 것이고, 그 후에 동일한 렌티바이러스 구축물이 PMBC-유래 T 세포에서 사용된다[23].
KM-H2는 HLA-DR 양성 대조군 주(line)로서 사용될 수 있는 인간 호지킨 림프종 주이다[34, 44]. 상기 주지된 바와 같이 Jurkat E6-1은 CIITA의 전달 시 HLA-DR을 조건적으로 발현하고, CIITA 녹아웃이 사용된다면 CIITA TALEN을 평가하는 데 사용될 수 있다[33].
또한, 1차 인간 T 세포가 사용될 수 있다. PMBC-유래 1차 인간 T 세포는 전혈로부터 정제 및 농화(enrich)된 다음, 활성화된다. 농화 후에 전달된다. 세포는 재조합 인간 인터루킨-2(및/또는 IL-7 및/또는 IL-15)와 함께 인큐베이션된다[7, 12, 43]. 전임상 연구 및 기대하던 치료적 전개를 기반으로, 요망되는 세포 유형은, 줄기세포 기억 TSCM, 중심 기억 TCM, 및 미접촉 세포 TN의 분자적 및 기능적 특징을 갖는 CD8+ T 세포이다[11, 22, 32, 35]. 항체 염색은 세포 면역표현형(immunotyping)을 가능하게 한다[27].
신호화 도메인(CD3z, 41BB, CD28)의 과다돌연변이(permutation)를 포함하는 초기 구축물은 K562 세포에서 mRNA, 멀티시스트론성 mRNA 및 렌티바이러스 전략을 사용하여 발현된다. 세포주의 MHC 클래스 I 및 II의 결여는 성공적으로 이용되는 전략에 따라 HLA-DR 항체를 사용한 MHC-CAR 발현의 태그리스 입증을 가능하게 한다[29]. 치료적 T 세포를 포함하여 보다 임상적으로 관련된 세포주에서 발현 효능의 정량화는 구축물에 따라 다르고, RQR 부위, 폴리히스티딘-(HlS)-태그, 또는 MHCCAR(CIITA가 TALEN을 사용하여 불활성화된다면, HLA-DR 항체를 이용함)의 유전적으로 인코딩된 형광 리포터(BFP) 또는 형광 염색을 사용하여 측정될 것이다. 표지화 부위는 도 6에 나타나 있다. 잠재적인 치료적 벡터로서 MHC-CAR 전달 속도를 시험하기 위해, BFP는 구축물로부터 제거되는 한편, RQR은 보유되어 결실 대조군을 제공한다. 임상적으로 관련된 구축물의 발현율은 항체 염색 포스트-편집을 사용하여 측정된다.
전사 활성자-유사 효과기 기술(TALEN)은 또한, MHC-CAR을 발현하는 T 세포를 제조하는 데 사용될 수 있다. 인간 T 세포주는 활성화되며, TALEN으로 형질감염되고, MHC-CAR로 형질감염되거나 형질도입된다. 그 후에, 이들 세포주는 염색되고, 유세포분석에 의해 분석되어, TALEN 유전자 불활성화 및 MHC-CAR 발현을 평가한다. 요망되는 세포주에서 구축물 발현의 입증 시, 인간 T 세포주 내로의 TALEN 전달(하기에서 고찰된 바와 같이 TCRa 및 CD52 또는 CIITA)이 수행된다. TALEN은 활성화된 인간 T 세포주 내로 도입되고, 후속해서 MHC-CAR이 평가를 위해 동일한 T 세포주 내로 도입된다. 인간 T 세포의 변형은 이러한 순서로 수행되어, 본태 TCR로 인한 MHC 변형된 세포의 우연적인 프래트리시덜(fratricidal) 사멸화를 방지할 수 있다[10]. TALEN-편집된 MHC-CAR T-세포의 활성은 확증되어야 한다.
(iii) 전사 활성자-유사 효과기(TALEN)를 통한 MHC-CAR-발현 T 세포의 변형
인간 T 세포는 TALEN에 의한 TCRa, 및 CD52 또는 CIITA 유전자의 불활성화를 확증하고, 뒤이어 MHC-CAR과 조합되어 TALEN을 사용한 평가를 위해 선택된다. 전사 활성자-유사 효과기(TALEN)는 DNA에 서열-특이적 방식으로 결합한다. DNA 결합 도메인은, 특이적인 뉴클레오타이드 인자를 부여하는 분기 2 아미노산 RVD(반복체 가변 디펩타이드 모티프)를 갖는 고도로 보존된 33 내지 34개 아미노산 서열을 함유한다[23, 31].
TCR의 α 또는 β 사슬의 돌연변이는 표면 TCR 발현의 교란에 충분하다[15, 36]. TALEN은, 바람직하지 못한 전좌를 통해 증식 이점을 도입하지 않으면서 치료적 세포에서 2개의 유전자의 발현을 저해하는 데 사용된다[39] [47]. TCR 발현은, 이식편대숙주 질병(GvHD)을 예방하고 동종이계 치료법의 생성을 가능하게 하기 위해 TRAC-표적화된 TALEN을 통해 저해된다[15, 39, 47].
CD52 결실은 알렘투주맙 융화성을 위해 이루어질 수 있다. 알렘투주맙은 순환하는 T 림프구 및 B 림프구를 표적화하고 결실시키는 인간화된 항-CD52 IgG1 모노클로날 항체이다[41]. 알렘투주맙은 중증-개시 MS에서 구제(rescue) 치료법으로서 또는 제1 선(first line) 약물로서 사용될 수 있고[50], 인간 환자 집단에서 공동-투여될 것이다. TALEN 녹아웃은 환자에서 MHC-CAR을 공존 치료와 융화성으로 되게 할 것이다[14, 39]. 나아가, CIITA 결실은, HLA 클래스 II 프로모터의 전사 활성에 필수적인 유전자를 코딩하는 단백질인 MHC-CAR CIITA에서 HLA-DR의 특징화를 위해 이루어질 수 있다[26]. 녹아웃은 MHC-CAR 발현의 특징화를 위해 항체를 사용하여 HLA-DR의 직접적인 측정을 가능하게 할 것이다[38, 53]. CD52 발현의 저해는 다발성 경화증에 대한 FDA-승인 치료인 렘트라다(Lemtrada) R(알렘투주맙)을 이용한 공존 치료를 가능하게 한다[42]. 알렘투주맙은 또한, CAR T 치료법의 접목(engraftment)을 돕는 림프구-결실/림프구-억제성 작용제로서 사용된다[39]. TRAC-표적화된 및 CD52-표적화된 TALEN으로 변형된 CAR T-세포 치료법은 현재, 임상 시험에서 시험중에 있다[38, 40, 43].
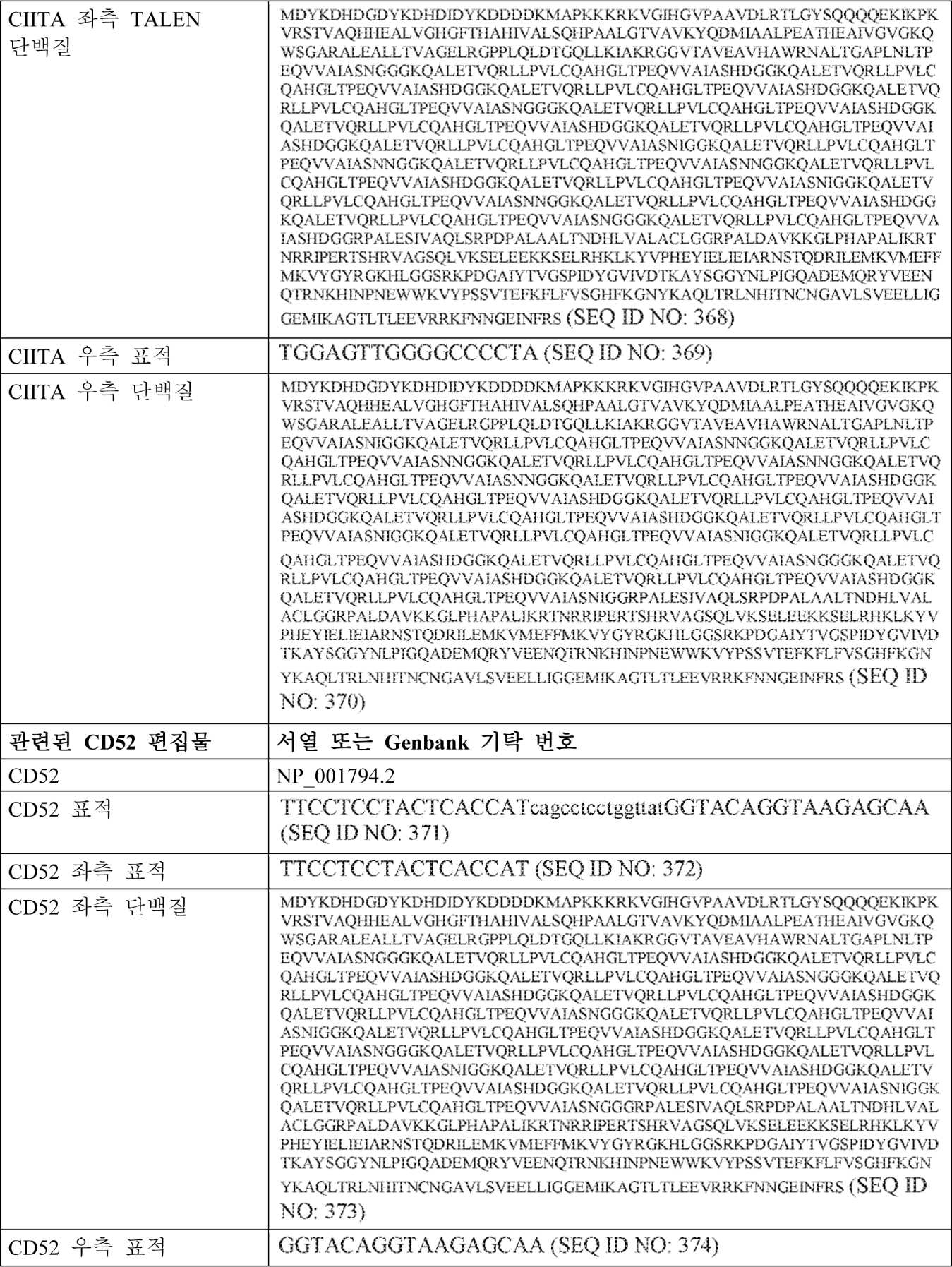
CIITA의 불활성화로서, CD52 대신에 MHC 클래스 II 트랜스활성자(transactivator)(CIITA)를 불활성화시키기 위해 TALEN은 HLA-DR 발현을 저해하여[26] [38], HLA-DR 항체 염색에 의한 MHC-CAR-함유 세포의 직접적인 식별을 가능하게 하는 것으로 예상된다. 확증된 TALEN(TRAC: TTGTCCCACAGATATCCagaaccctgaccctgCCGTGTACCAGCTGAGA(SEQ ID NO: 376), CD52:TTCCTCCTACTCACCATcagcctcctggttatGGTACAGGTAAGAGCAA(SEQ ID NO: 371), CIITA: TTCCCTCCCAGGCAGCTCacagtgtgccaccaTGGAGTTGGGGCCCCTA(SEQ ID NO: 366))은 Cellectis로부터 입수되거나 이전에 확증된 부위를 표적화하도록 설계된다[38, 43].
인간 T 세포는 활성화되고, 3개의 상이한 TALEN의 변이체를 인코딩하는 mRNA로 전기천공된다: TCR-알파 불변 사슬, CD52, 및 CIITA. 세포는 항-CD3 또는 항-TCR(TCR-알파 불변 사슬), 항-CD52(CD52), 또는 항-HLA-DR(CIITA)로 표면 염색된 다음, 유세포분석에 의해 분석된다.
TALEN 발현 검정법에서, 표적 유전자를 불활성화시키는 이전에 확증된 TALEN의 능력이 재-확증된다[39]. 전좌 연구 및 표적-외 연구는 재수행되고, 몇몇 전체-게놈 서열은 결과를 확증한다. 가이드-seq는 전체 게놈 시퀀싱에 대한 대안으로서 사용되어, 표적-상 및 표적-외 편집을 확증시킬 수 있다[8].
하나 이상의 하기 내인성 유전자가 다른 세포와의 상호작용을 감소시키도록 편집되어야 한다: TCR(TCR 알파 또는 베타 사슬을 통해; 요망되지 않는 세포로의 표적화를 감소시키기 위해), CIITA(MHC 클래스 II 유전자의 발현을 조절함; 테이스터(taster) 결실을 위한 표적 세포), B7-1(CD80) 및/또는 B7-2(CD86) 녹아웃, 및 NKG2D 리간드 또는 UL18과 함께 b2m(MHC 클래스 I 유전자의 발현을 조절함).
나아가, 하나 이상의 하기 유전자가 상호작용 세포의 기능을 변형시키기 위해 편집될 수 있다: PD-L1 +/- CTLA4-Ig 과발현; PD-L1/2 과발현 +/- PD-1 녹아웃; FasL 과발현 +/- Fas 녹아웃; 갈렉틴 9 과발현 +/- TIM3 녹아웃; 및/또는 PVT/CD155 과발현 +/- TIGIT 녹아웃. PD-1, Fas, TIm3, TIGIT에서의 결함은 환자를 자가면역에 취약하게 만든다. 일부 약물은 기능을 복구시킬 수 있다(예를 들어: Tim3, 글라티라머(glatiramer) 아세테이트 및 IFN-베타). 자가면역 질병을 앓고 있는 환자로부터의 자가 세포가 이용된다면, 이들 자가 세포는 CTL 및 Treg 기능에 영향을 주는 결함성 유전자의 환자 특이적 교정을 필요로 할 수 있다. 이들의 개인적 돌연변이 세트는 또한, CTL 또는 Treg 세포가 가장 치료적으로 관련있을 것인지, 그리고 자가 또는 동종이계 세포가 사용된다면 일부 세포 변형이 효과적일 것인지 결정할 수 있다.
나아가, 하기 편집물은 세포의 장소 및/또는 기능을 변형시킬 수 있다(예를 들어, 이를 여포 조절 세포와 더 유사하게 만들기 위해):
-
MHC-CAR-(FOX3P)-(CS1 또는 CD19 CAR)/(CS-1 CAR에 필요한 CS-1 녹아웃)
-
MHC-CAR-(FOX3P)-(CCR7 또는 CXCR5)
더욱이, 하기 편집물은 자가면역 질병을 위한 병용 치료법을 가능하게 할 수 있다(예를 들어, MS 특이적 치료제)
-
RQR 태그: 조작된 T 세포는 리툭시맙을 이용하여 제거될 수 있다(사멸화 스위치). 새로 승인된 항-CD20 항체 오크레부스(Ocrevus)에 대한 태그가 발생될 수 있었다.
-
라파마이신 스위치 : 환자가 라파마이신(타크롤리무스(tacrolimus))로 치료되는 경우에 CAR은 단지 불활성/활성화된다
-
CD52 녹아웃: 존재하는 면역 세포의 수를 저하시키기 위해 렘트라다(알렘투주맙)를 이용한 전치료(pretreament)를 가능하게 한다
-
VLA-4 녹아웃: 티사브리(tysabri)로 치료되어 병원성 면역 세포를 말초로 이동시킬 수 있으나, 조작된 세포는 그곳에서 강제로 머무르게 된다(뇌 척수에서 정체된(stuck) 세포로서 확립된 MS 환자에서는 이상적이지 않을 수 있으나; VLA-4의 동시적인 mRNA 발현은 이들 장소로의 일시적인 접근을 제공할 수 있음)
-
조작된 T 세포로부터의 IL-6 항체(토클리주맙(Toclizumab)) 분비: 조작된 T 세포가 뇌 및 척수에 접근해야 할 때 유용하지만, 이 약물은 BBB로 인해 이들 장소로 접근할 수 없다.
실시예 3: MHC-CAR 활성의 연구
(i) MHC-CAR을 발현하는 1차 T 세포의 제조
1차 T 세포는 하기와 같이 제조될 수 있다. T 세포는 말초 혈액 단핵 세포(EasySep 인간 T 세포 농화 키트, Stemcell Technologies)로부터 단리되고, (X-Vivo 15 배지, Lonza; 20 mg/ml Il-2, Miltenyi; 5% 인간 AB 혈청, Seralab)로 활성화된다(Dynabeads 인간 T-활성자 CD3/CD28, Life Technologies). MBP 항원성 펩타이드를 함유하는 적합한 MHC-CAR 구축물은 종래의 방법을 사용하여 1차 T 세포 내로 도입된다. MHC-CAR 구축물의 표면 발현은 FACS 및 항체 염색에 의해 확증된다.
(ii) 시험관내에서 MHC-CAR 활성 시험
구축물 수송 및 발현의 입증 시(mRNA, 멀티시스트론성 mRNA, 렌티바이러스와 함께), 활성 시험은 시험관내에서 수행된다. 모든 시험은 상이한 효과기 대 표적(effectontarget)(E:F) 세포 농도에서 수행된다. 시험관내 시험은 MHC-CAR 신호화 도메인 및 T 세포 하위세트의 초기 평가를 제공한다.
(iii) IL-2 생성에 의한 신호화 도메인 평가
전기천공 후 24시간째에, MHC-CAR로 일시적으로 조작된 인간 T 세포는 플레이트-결합된 HLA-DR 항체로 자극되어, MHC-CAR(다양한 신호화 도메인을 함유함)이 기능성인지 결정한다. H-2 생성은 24시간 이후에 Stemcell IL-2 ELISA 키트를 사용하여 측정된다. 이 시험은 변이체가 재조작되어야 하는지 또는 폐기되어야 하는지에 관하여 신속 검정법을 제공한다[29].
(iv) 증식 검정법을 통한 MHC-CAR 세포와 병원성 TCR 세포의 상호작용
TCR을 일시적으로 발현하는 표적 세포주는 전기천공 후 24시간째에 TCR 발현에 대해 자기적으로 소팅되고 조사(irradiate)되어, MHC-CAR과 항원-특이적 TCR의 연동이 MHC-CAR 함유 T 세포의 증식을 자극하는지 시험한다. 대안적으로, TCR을 안정하게 발현하는 표적 세포주는 조사된다. (+/-항원-특이적) TCR을 제시하는 조사된 세포는 CFSE-표지된 MHC CAR 세포와 함께 인큐베이션되고, 상이한 T:E 비에서 배양 후 측정된다[30].
(v) 탈과립화 검정법
CAR T-세포는 T 세포 마커 대신에 RQR(이는 사용되는 표적 세포 상에서 발현되지 않고 있음) 상의 에피토프 또는 eBFP를 통해 표지된다. 이 검정법은 일시적인 발현 또는 안정한 발현을 갖는 세포주에 대해 수행된다(일시적인 발현에 대한 실시예가 기재됨). 전기천공-후 24시간째에, RQR8 또는 BFP를 갖는 MHC-CAR 인간 T-세포는 표적(항원-특이적 TCR SupT1 또는 Jurkat) 또는 대조군(+/- TCR Jurkat 또는 TCR- SupT1) 세포와 함께 6시간 동안 공동-배양된다. 일시적으로 발현되는(및 이후에 안정하게 발현하는) 표적 세포는 항원-특이적 TCR로 전기천공되고, 전기천공-후 CD3 자기 비드로 소팅된다. RQR+ 또는 BFP+ MHC-CAR T-세포(항-리툭시맙 항체, QBEnd10 항체로 식별되는 바와 같음)는 유세포분석에 의해 분석되어, 이들의 표면 상에서 탈과립화 마커 CD107a의 발현을 검출한다[2].
(vi) 사이토카인 분비 검정법
이 검정법은 일시적인 발현 또는 안정한 발현(일시적인 발현이 기재됨)을 갖는 세포주에 대해 수행된다. MHC-CAR을 일시적으로 발현하는 인간 T 세포는 전기천공 후 24시간째에 표적 세포와 공동-배양 후 사이토카인 분비에 대해 평가된다. MHC-CAR을 일시적으로 발현하는 인간 T 세포는 표적(항원-특이적 TCR 함유Jurkat 또는 SupT1 세포) 또는 대조군(+/- 비-항원-특이적 Jurkat 또는 SupT1) 세포와 함께 24시간 동안 공동-배양된다. 그 후에, 항원-특이적 TCR은 검정법 전에 조사에 의해 사멸화된다. 상층액은 수합되고, TH1/TH2 사이토카인 유세포분석 비드 어레이 키트를 사용하여 분석되어, T 세포에 의해 생성되는 사이토카인을 정량화한다[13]. MHC-CAR T-세포는, 대조군 세포와의 공동-배양에서가 아니라 항원-특이적 TCR 발현 표적 세포와의 공동-배양에서 IFN 및 다른 사이토카인을 생성한다.
(vii) IFNγ 방출 검정법
다양한 수준의 MHC-CAR 발현 세포는, 형질감염 후 24시간째에 조사된 TCR T-세포와 함께 인큐베이션된다. 공동-배양은 24시간 동안 유지된다. 인큐베이션 및 원심분리 후, 상층액은 ELISA에 의해 IFNγ 검출로 시험된다.
(viii) 세포독성 검정법
TCR T-세포는 대조군 세포뿐만 아니라 치료적 MHC-CAR과 함께 인큐베이션된다. 표적 세포 및 대조군 세포는 형광 세포내 염료(CFSE 또는 셀 트레이스 바이올렛(Cell Trace Violet))로 표지된 후, MHC-CAR T-세포와 함께 공동-배양된다. 공동-배양물은 4시간 동안 인큐베이션된다. 이 인큐베이션 기간 후, 세포는 고정형 생존능 염료로 표지되고, 유세포분석에 의해 분석된다. 각각의 세포 집단(표적 또는 음성 대조군)의 생존능이 결정되고, 특이적인 세포 용해의 백본율이 계산된다. 세포독성 검정법은 전달 후 48시간째에 수행된다.
(ix) 저해 검정법
PBMC는, MHC-CAR 구축물을 발현하는 조사된 또는 미토마이신-처리된 조작된 T 세포와 함께 공동-배양된다. 대조군으로서, PBMC는, MHC-CAR 구축물을 발현하지 않는 조사된 또는 미토마이신-처리된 조작된 T 세포와 함께 공동-배양된다. 7일 후, 인간 환자 공여자 A로부터의 세포 증식은 XTT 비색 검정법에 의해 도는 CFSE 희석(FACS 분석)에 의해 측정된다. 세포 증식이 대조군에서 관찰될 것이긴 하지만, 조작된 T 세포가 분비된 FP를 발현하는 경우 어떠한 세포 증식도 예상되지 않거나 제한된 세포 증식이 예상된다. 이 실험으로부터의 결과는, MHC-CAR 발현 T 세포가 FP를 발현하는 경우 동종반응성(alloreactive) T 세포 증식이 저해됨을 보여주는 것을 목적으로 한다.
(x) 증식
MHC-CAR과 항원-특이적 TCR의 연동이 MHC-CAR 함유 T 세포의 증식을 자극하는지 시험하기 위해, TCR을 일시적으로 발현하는 표적 세포주는, 전기천공 후 24시간째에 TCR 발현에 대해 자기적으로 소팅되고 조사된다. 대안적으로, TCR을 안정하게 발현하는 표적 세포주는 조사된다. (+/-항원-특이적) TCR을 제시하는 조사된 세포는 CFSE-표지된 MHC-CAR 세포와 함께 인큐베이션되고, 증식은 상이한 T:E 비에서 배양 후 측정된다.
(xi) 생체내 시험
마우스 T 세포에서 MHC-CAR(마우스 MHC 및 인간 MHC를 가짐)은 다발성 경화증에 대한 마우스 모델인 실험적 알레르기성 뇌척수염(experimental allergic encephalomyelitis)에서 치료 효능을 이전에 보여주었다[25, 29]. 여기서, 본 발명자들은, 선행 CAR T 전임상 연구에서와 유사한 생체내 마우스 모델을 사용하여 인간 세포에서 MHC-CAR이 인간 T 세포주에서 인간 TCR을 표적화할 수 있는지 시험한다[39]. 생체내 시험은 MHC-CAR 신호화 도메인 및 T 세포 하위세트의 추가의 평가를 가능하게 한다.
MHC-CAR T-세포의 생체내 활성은 도 7에 예시된 바와 같이 마우스 이종이식 모델에서 확증될 수 있다.
면역결핍 NOG 마우스에게, MS 이종이식 마우스 모델로서 항원-특이적 TCR-루시퍼라제 발현 T-세포가 정맥내 주사된다. 그 후에, 마우스는 종양 세포주의 주사-후 2일째 또는 7일째에 상이한 용량에서 시험되는 MHC-CAR T-세포의 정맥내 용량을 받는다. CAR 렌티바이러스 벡터로 형질도입되지 않은 T-세포의 정맥내 주사는 대조군의 역할을 한다. 생물발광 신호는 상이한 동물에서 TCR-루시퍼라제 발현 세포의 확장을 따르기 위해 T-세포 주사일(D0)에, T-세포 주사 후 D7, 14, 21, 28 및 40에 결정된다[39].
본원에 나타낸 것과 유사한 백그라운드 변형(본태 TCR을 불활성화시키고 이식편 대 숙주를 최소화하기 위해 TALEN, CD52를 불활성화시키고 알렘투주맙을 이용한 동시적인 치료를 가능하게 하기 위해 TALEN, 및 결실을 가능하게 하기 위해 RQR8)을 갖는 CAR T-세포는 마우스 모델에서 이전에 확증되었고 현재 UCART19 임상 시험에 사용된다[39].
(xii) 사멸화-스위치 입증
형질도입된 T 세포는 약제학적 보체(리툭시맙, 티사브리 또는 알렘투주맙)의 포함과 함께 또는 없이 25% 아기-토끼 보체(AbD Serotec)에 4시간 동안 노출되어, 보체-의존적 세포독성(CDC)-매개 감작성을 검사한다. Miltenyi CD34 자기 비드-선택-형질도입된 RQR8 T-세포는 Q8-형질도입된 T 세포의 유사하게 처리된 집단에 대해 비교되어, CDC-매개 결실의 특이성을 실증한다. CDC 검정법 매개변수의 추가의 검사는 12.5, 25, 50 및 100 mg/mL에서 약제학적 보체와 함께 인큐베이션된 RQR8-형질도입된 T 세포를 사용하는 시간-전개/용량-적정 검정법 및 1분 내지 120분 범위의 시점 평가를 통해 달성되었다.
실시예 4: MHC-CAR을 발현하는 조절 T 세포(Treg)
항원이 다발성 경화증 및 다른 자가면역 질병에 책임이 있는 병적 T 림프구를 특이적으로 표적화하는 치료법은 항원-비특이적 치료법과 비교하여 치료 지수를 개선한 것으로 예상된다. 이 실시예는, MS에 연루된 미엘린 염기성 단백질-특이적 T 림프구에 대해 치료적 T 세포를 선택적으로 재지향하기 위해 키메라 항원 수용체를 사용하는 예시적인 세포성 면역치료법을 제공한다.
Treg 세포 소팅, 전달 및 확장
CD4+ T 세포는 RosetteSep(STEMCELL Technologies)을 통해 PBMC로부터 단리되고 CD25+ 세포(Miltenyi Biotec)에 대해 농화된 후, 살아 있는 CD4+CD45RO-CD45RA+CD25+ Treg 및 CD4+CD45RO-CD45RA+CD25- 대조군 T 세포로 FACS에 의해 소팅된다. 소팅된 T 세포는 Treg 또는 비-reg 대조군 T 각각에 대해 1,000 U/ml 또는 100 U/ml의 IL-2 중 αCD3 mAb가 적재된 인공 APC(aAPC)로 자극된다. 1일 후, 세포는 렌티바이러스로 형질도입된다. 7일째에, NGFR+ 세포는 자기 선별(Miltenyi Biotec)에 의해 정제된 다음, 상기와 같이 aAPC로 재-자극되고, 6 내지 7일 동안 확장된다.
유세포분석:
표현형 분석을 위해, 세포는 고정형 생존능 염료(FVD)(65-0865-14 및 65-0866-14, eBioscience)로 염색되고, FOXP3/전사 인자 염색 완충제 세트(eBioscience)로 고정/영속화(perm)하기 전에 표면 마커에 대해 염색된 후, 세포내 단백질에 대해 염색되었다. 사이토카인 생성의 분석을 위해, 세포는 브레펠딘(brefeldin) A(10 g ml)의 존재 하에 10 ng/ml PMA 및 500 ng/ml 이오노마이신(ionomycin)으로 4시간 동안 자극되었다(모두 Sigma-Aldrich). 시료는 유세포분석에 의해 분석되었다.
현미경조사:
PBMC는 PKH26 또는 PKH67(Sigma-Aldrich, PKH26GL-1KT 및 PKH67GL-1KT)로 표지되고, Treg는 세포 증식 염료(CPD) eFluor450(eBiosciences, 65-0842-85)로 표지된 다음, 제조업체의 일반적인 3D 겔 프로토콜에 따라 1 x DMEM 및 10% FCS로 이루어진 1.5% 래트 꼬리 콜라겐 I형(Ibidi)의 3D 겔에 현탁된다. 세포 현탁액은 μ-슬라이드 Chemotaxis3D 내로 피펫팅되고, Leica TCS SP8 공초점 현미경 상에서 습윤 인큐베이터 내에서 35℃ 및 5% C02(Tokai Hit)에서 30분 동안 중합하도록 된다. 외부 챔버는 1 x DMEM으로 충전되고, 이미지는 3시간 동안 2분마다 x10/0.30 대물렌즈를 사용하여 기록된다. eFluor450, PKH67 및 PKH26은 405 nm, 488 nm, 및 561 nm에서 여기되었고, 형광 방출은 415 내지 470 nm, 495 내지 525 nm, 및 570 내지 650 nm에서 각각 수합된다. CAR-Treg와 표적 또는 대조군 세포 사이의 상호작용의 수는 20분마다 정량화된다. 이동하지 않는 세포는 분석으로부터 배제되었다. 시야 당 각각의 표지된 세포 유형의 총 수는 ImageJ(imagej.nih.gov/ij/)에서 분석 입자 함수를 사용하여 계수될 수 있다.
트리(tree)-특이적 탈메틸화된 영역(TSDR) 분석
안정한 Foxp3의 Treg 안정한 발현은 Foxp3 유전자좌(locus) 내에서 TSDR의 선택적 탈메틸화와 연관이 있다. 안정한 발현을 시험하기 위해, 냉동된 T 세포 펠렛으로부터의 DMA는 DNeasy 혈액 및 조직 키트(QIAGEN)를 이용하여 단리되고/되었고, 비설파이트는 EZ Direct 키트(Zymo Research)로 전환되었다. BisDNA의 PCR은 인간 FOXP3 키트(Epigen DX)로 수행되었고, PyroMark 완충제 (QIAGEN)를 사용하여 피로시퀀싱(pyrosequencing)에 대해 제조된 다음, Biotage PyroMark Q96 MD 피로시퀀서(QIAGEN) 상에서 검정되었다. 결과는 Pyro Q-CpG 소프트웨어(Biotage)를 이용하여 계산되었다.
사이토카인 생성
사이토카인 생성을 측정하기 위해, T 세포주는 K562 세포(1 K562:2 T 세포)로 48시간 동안 자극된다. 상층액은 수합되고, 사이토카인 농도는 인간 Th1/Th2/Th17 사이토카인 키트(BD Biosciences)에 의해 결정되고 분석되었다.
MHC CAR-특이적 증식의 억제
표적에 특이적인 Treg가 또한, CD4+ T 세포 증식을 억제시킬 수 있었는지 시험하기 위해, MHC CAR-특이적 CD4+ T 클론이 단리된다. 엡스타인 바(Epstein Barr) 바이러스-형질전환된 B 림파블라스토이드(lymphablastoid) 세포주는 렌티바이러스를 사용하여 MHC-CAR로 형질도입되었다. EBV 세포주는 밤새 성장되었으며, 150 Gy에서 조사되고, CAR-발현 Treg 또는 종래의 T 세포의 부재 또는 존재 하에 CPD-표지된 MHC CAR-특이적 CD4+ T 클론과 함께 공동배양되었다. 증식은 4일 후에 결정되고, MHC CAR-특이적 클론의 억제의 백분율은 하기와 같이 증식의 백분율을 사용하여 계산된다: (100 - [(% 증식된 MHC CAR + 시험)/(% 증식된 MHC CAR 단독)] x 100).
구축물 수송 및 발현(mRNA, 멀티시스트론성 mRNA, 및/또는 렌티바이러스와 함께)의 입증 시, 활성 시험은 시험관내에서 시작될 것이다. 모든 시험은 상이한 효과기 대 표적(effectontarget)(E:F) 세포 농도에서 수행된다. 시험관내 시험은 MHC-CAR 신호화 도메인 및 T 세포 하위세트의 초기 평가를 제공하는 것으로 예상된다.
T 세포에서 케모카인 및 접착 수용체의 일시적인 또는 렌티바이러스 발현
수용체는 모노/폴리시스트론성 mRNA 또는 렌티바이러스 전달의 전기천공 후 인간 T 세포에서 발현된다. 수용체의 발현은 유세포분석을 사용하여 분석된다. 요약에서: 항 CD3/CD28 코팅된 비드 및 IL2와 함께 수일(3 내지 5일) 예비활성화된 5 x106개의 T 세포는 세포천공(cytoporation) 완충제 T에서 재현탁되었고, 45 ug의 mRNA로 전기천공되었다. 전기천공 후 24시간째에, 다중-사슬 CAR을 인코딩하는 폴리시스트론성 mRNA를 사용하여 조작된 인간 T 세포는 고정형 생존능 염료 eFluor-780 및 특이적인 PE-컨쥬게이션된 염소 항-마우스 IgG F(ab')2 단편으로 표지되었고, 유세포분석에 의해 분석되었다. 대안적으로, 수용체는 렌티바이러스에서 벡터화되며, 발현되고, 유사하게 분석되었다.
시험관내 화학주성 검정법
형질도입된 T 세포는 이전에 기재된 바와 같이 화학주성 검정법에 사용되었다[Burkle et al., Blood, 110(9):3316-3325, 2007; Wu and Hwang, Journal of immunology, 168(10):5096, 2002.; Singh et al, Journal of immunology, 180(1):214-221, 2008.; Ryu et al., Molecules and Cells, 39.12:898-908, 2016.]. 세포(배지 중 약 20,000개 세포, 1 백만 개 세포, 5 x 106/mL)는 5-μm 공극 크기 필터의 상부 상에 2벌 중복으로 놓인 반면, 케모카인이 있는 배지 및 케모카인이 없는 배지는 더 낮은 챔버 내로 놓였다. 37℃에서 30분, 1시간, 3시간, 5시간, 24시간 후, 플레이트의 하단까지 낙하되었던 이동된 세포는 하기의 세포였다:
A. 4x 대물렌즈를 사용하여 촬영되었다. 2개 웰 각각으로부터의 3개의 랜덤 뷰는 Image Pro Plus(Media Cybernetics, 미국 메릴랜드주 실버스프링 소재)를 사용하여 계수되었다. 3개의 독립적인 실험이 수행되었고, 유사한 결과가 존재하였다.
B. 400 μL의 세포 현탁액은 포스페이트-완충 식염수(PBS) 중 4 x 10-7 M FITC-표지된 팔로이딘, 0.5 mg/mL 1-알파-리소포스파티딜콜린(둘 모두는 Sigma, 미국 미주리주 세인트루이스 소재), 및 7% 포름알데하이드를 함유하는 100 μL의 용액에 첨가되었다. 고정된 세포는 FACSCalibur 상에서 유세포분석에 의해 분석되었고, 모든 시점은 케모카인의 첨가 전에 시료의 평균 상대 형광에 비해 플롯화된다.
C. 더 낮은 챔버 내의 세포는 Countess II FL(Thermo Fisher Scientific, USA)을 사용하여 계수되었거나 450 nm에서의 O.D. 값은 Versamax 마이크로플레이트 판독기(Molecular Devices)를 사용하여 측정되었다.
실시예 5: HEK293 세포에서 MHC-기반 키메라 수용체(MHC-CAR)의 발현
MHC-CAR을 인코딩하는 구축물은 실시예 2에서 고찰된 바와 같이 구축되었고, HEK293 세포에서 발현에 대해 평가되었다. 간략하게는, 구축물 1은 EF1알파 짧은 프로모터, CD19 CAR(4G7-CAR), CCR6, 및 GFP(SEQ ID NO: 426에 의해 제공됨)를 포함하고; 구축물 2는 EFl알파 짧은 프로모터, RQR8, MHC-CAR1 파트 B MHC-CAR1 파트 A, 및 GFP(SEQ ID NO: 409에 의해 제공됨)를 포함한다.
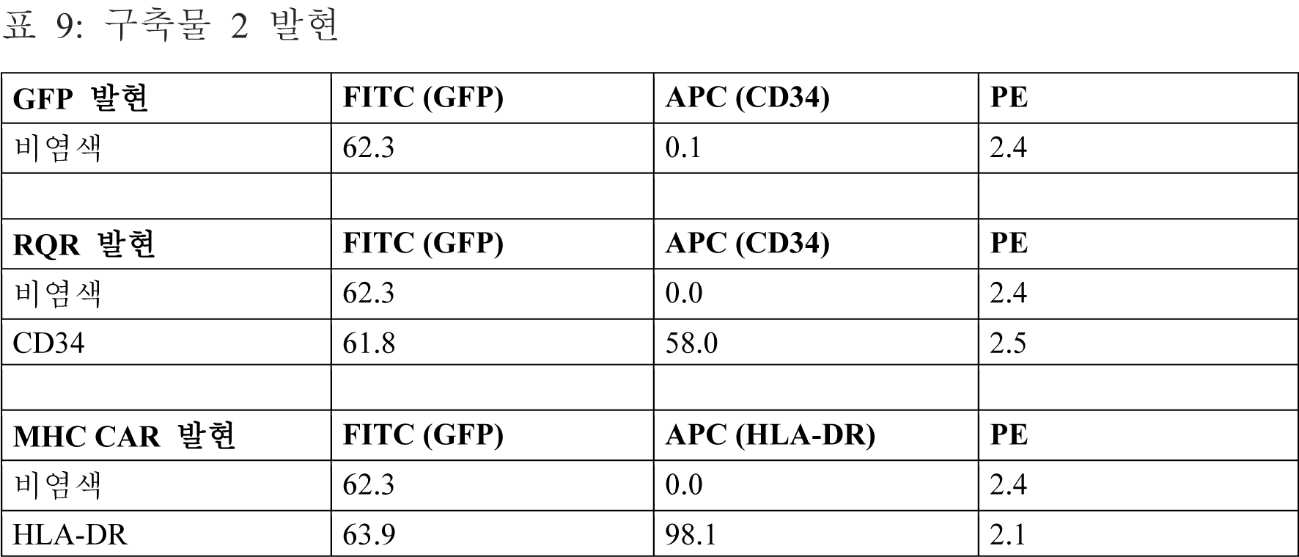
구축물 1, 2, 또는 배지 대조군(비-형질감염됨)은 HEK293 세포 내로 형질감염되고, 배양되었다. 세포는 GFP 발현을 기반으로 현미경에 의해 발현에 대해 평가되었다. GF-양성 세포의 집단은, 구축물 1 또는 구축물 2로 형질감염된 그룹에서 관찰되었다. 세포는 또한, 구축물에 의해 인코딩된 구성성분의 발현에 대해 유세포분석에 의해 평가되었다. 표 8 및 표 9.
구축물 1 발현
CCR6의 검출을 위해, 세포는 APC에 컨쥬게이션된 항-CCR6 모노클로날 항체(17-1969-42, eBioscience)와 함께 인큐베이션되었고; CD19의 검출을 위해, 세포는 비오틴화된 CD19(Acro CD9 - H8259, Acro Bio시스템), 뒤이어 스트렙타비딘-PE(405203, BioLegend®)와 함께 인큐베이션되었다.
구축물 2 발현
RQR8에 포함된 에피토프로부터의 CD34 발현의 검출을 위해, 세포를 항-CD34 APC-컨쥬게이션된 모노클로날 항체와 함께 인큐베이션하였고; MHC-CAR 발현의 검출을 위해, 세포를 항-HLA-DR 항체와 함께 인큐베이션하였다.
구축물 1의 핵산 서열(SEQ ID NO: 426)
구축물 2의 핵산 서열(SEQ ID NO: 409)
실시예 6: CD3의 발현
CD3의 발현을 평가하여, T 세포 수용체 알파 불변(TRAC) 유전자를 표적화하는 CRISPR 방법의 효능을 결정하였다. 간략하게는, 포워드 프라이머(5'-AGCGCTCTCGTACAGAGTTGG-3'(SEQ ID NO: 385)) 및 리버스 프라이머(5'-AAAAAAAGCACCGACTCGGTGCC-3'(SEQ ID NO: 386))를 사용하여 표적 부위를 증폭시킴으로써, TRAC 유전자를 표적화하는 sgRNA를 발생시켰다.
비변형된 sgRNA는 하기 핵산 서열에 의해 제공된다:
변형된 sgRNA는 하기 핵산 서열에 의해 제공된다:
1차 인간 자극된 CD3+ T-세포를, Cas9을 인코딩하는 mRNA(Cas9 단독) 또는 Cas9을 인코딩하는 mRNA와 TRAC 유전자를 표적화하는 sgRNA 둘 모두로 형질감염시켰다. 형질감염-후 7일 후, CD3의 발현을 유세포분석에 의해 평가하였다. 세포를 1:100 희석의 항-CD3-APC 항체(클론 OKT3; BioLegend® 카탈로그 번호 317318)와 함께 인큐베이션하였다. 도 11에 나타낸 바와 같이, Cas9을 인코딩하는 mRNA 및 TRAC 유전자를 표적화하는 sgRNA의 형질감염은 CD3 발현에서 실질적인 감소를 초래하였다.
실시예 7: 사멸화 스위치 입증
실시예 구축물 2에서 인코딩되는 RQR8 사멸화 스위치의 효능을 세포 생존능 검정법을 사용하여 평가하였다. 간략하게는, HEK 세포를 배지 단독, 구축물 1(SEQ ID NO: X), 구축물 2(리툭시맙-매개 RQR8 사멸화 스위치를 인코딩함, SEQ ID NO: X), 또는 구축물 1과 구축물 2 둘 모두로 형질감염시켰다. 형질감염된 HEK293 세포를 수합하고, 계수하고, 1x10^6개 세포/mL로 재현탁시켰다. 300 uL의 세포 현탁액을 48-웰 조직 배양 플레이트의 4개 웰 각각 내로 옮겼다. 100 uL의 완전 배지 및 4 uL의 리툭시맙을 제2 웰에 첨가하고, 100 uL의 새로 제조된 아기 토끼 보체 및 4 uL의 리툭시맙을 제4 웰에 첨가하였다. 상기 플레이트를 2, 4 또는 24시간 동안 인큐베이션하였다. 1 uL의 냉각된 Annexin V 완충제(150 mM NaCl, 10 mM HEPES, 10 mM CaCl)를 첨가함으로써 검정법을 종료시킨 후, 시료를 3 mL의 Annexin V 완충제를 함유하는 사전-제조된 유세포분석 튜브 내로 옮겼다.
시료를 원심분리에 의해 수합하고, 임의의 잔여 완충제를 페이퍼 타월로 블로팅(blot)하였다. 그 후에, 시료를 1 uL의 Annexin V APC로 염색하고, 보텍싱(vortex)하고, 부드러운 조명에서 15분 동안 놔두었다. 그 후에, 상기 시료를 Annexin V 완충제로 세척하고, 5 uL의 프로피듐 요오다이드/mL 완충제를 보충하고, 최종 현탁 직후에 수행되는 아이스 펜딩(ice pending) 유세포분석 상에 놓았다.
GFP-양성 세포의 백분율을 정량화하여, RQR8 사멸화 스위치에 의해 유도되는 사멸화를 정량화하였다. 도 12에 나타낸 바와 같이, 보체 단독과의 인큐베이션은 일부 세포 사멸을 초래하였으나, 생존능에서 이러한 감소는 모든 그룹의 세포에서 관찰되었다. 세포 사멸은, 리툭시맙과 보체의 조합의 존재 하에 구축물 2 또는 구축물 1과 구축물 2 둘 모두를 발현한 세포에서 관찰되었고, 이는 특이적인 RQR8-매개 세포 사멸을 나타낸다.
참고문헌
[I]
Corlien et al., International journal of cancer, 99(1):7-13, 2002.
[2]
Betts et la, Methods in cell biology, 75:497-512, 2004.
[3]
Birnbaum et al. Proceedings of the National Academy of Sciences of the United States of America, 111(49):17576, 2014.
[4]
Boissel et al., Nucleic acids research, 42(4):2591-2601, 2014.
[5]
Cai et al., Blood, 128(22):4039, 2016.
[6]
Chung et al., Proceedings of the National Academy of Sciences, 92(9):3712-3716, 1995.
[7]
Cieri et al., Blood, 121(4):573-584, 2013.
[8]
Corrigan-Curay et al., Molecular Therapy, 23(5):796-806, 2015.
[9]
Dotti et al., Immunological reviews, 257(1):107-126, 2014.
[10]
WO2015121454
[I I]
Farber et al., Nature Reviews Immunology, 14(1):24-35, 2014.
[12]
US20170183413
[13]
Galetto. Publication No. EP3137498 A1, 2017.
[14]
US20140120905
[15]
Galetto et al., Molecular Therapy-Methods & Clinical Development, 1:14021, 2014.
[16]
Goebels et a., Brain, 123(3):508-518, 2000.
[17]
Hahn et al., Nature immunology, 6(5):490-496, 2005.
[18]
Hall et al., International Immunology, 3(4):359-368, 1991.
[19]
Hart et al., Gene Therapy, 15:625-631, 2008.
[20]
Hohlfeld et al., Proceedings of the National Academy of Sciences, 101(suppl 2): 14599-14606, 2004.
[21]
Holst et al., Nature Protocols Electronic Edition, 1(1):406, 2006.
[22]
Jensen et al., Immunological reviews, 257(1):127-144, 2014.
[23]
Juillerat et al., Scientific reports, 5:8150, 2015.
[24]
Justesen et al., Immunome research, 5(1):2, 2009.
[25]
Jyothi et al., Nature biotechnology, 20(12): 1215-1220, 2002.
[26]
Mach et al., Immunological reviews, 138(1):207-221, 1994.
[27]
Maecker et al., Nature Reviews Immunology, 12(3):191-200, 2012.
[28]
Mamonkin et al., Blood, 126(8):983-992, 2015.
[29]
Moisini et al., The Journal of Immunology, 180(5):3601-3611, 2008.
[30]
Morris et al., Science translational medicine, 7(272):272ra10-272ra10, 2015.
[31]
Moscou et al., Science, 326(5959):1501-1501, 2009.
[32]
Mueller et al., Nature reviews Immunology, 16(2):79-89, 2016.
[33]
Nagarajan et al., The Journal of Immunology, 168(4): 1780-1786, 2002.
[34]
Nagy et al. , Nature medicine, 8(8):801-807, 2002.
[35]
Ophir et al., Blood, 121(7):1220-1228, 2013.
[36]
Osborn et al., Molecular therapy, 24(3):570-581, 2016.
[37]
Philip et al., Blood, 124(8):1277-1287, 2014.
[38]
US20170016025
[39]
Poirot et al., Cancer research, 75(18):3853-3864, 2015.
[40]
Qasim et al., Science translational medicine, 9(374):eaaj2013, 2017.
[41]
Ruck et al., International journal of molecular sciences, 16(7):16414-16439, 2015.
[42]
Salzer et al., Neurology, 87(20):2074-2081, 2016.
[43]
Smith et al., US Patent App. 14/018,021, 2013.
[44]
Steidl et al., Nature, 471(7338):377-381, 2011.
[45]
Suhoski et al., Molecular Therapy, 15(5):981-988, 2007.
[46]
Taylor et al., Cell, 169(1):108-119, 2017.
[47]
Valton et al., Molecular Therapy, 23(9):1507-1518, 2015.
[48]
Vanderlugt et al., Nature Reviews Immunology, 2(2):85-95, 2002.
[49]
Walchli et al., PloS one, 6(11):e27930, 2011.
[50]
Wingerchuk et al., Mayo Clinic Proceedings, 89:225-240, 2014.
[51]
Yang et al., Gene Therapy, 15(21):1411-1423, 2008.
[52]
Yang, Journal of Immunotherapy, 31 (9):830, 2008.
[53]
Zhou et al., Immunology, 122(4):476-485, 2007.
Jiang et al., International immunology, 25(4):235-246, 2013.
Busch et al., The EMBO journal, 15(2):418, 1996.
Akalin et al., Molecular Therapy, 17:S25, 2009.
Jin et al., Proceedings of the National Academy of Sciences, 111(10):3787-3792, 2014.
Tanimura et al., Blood, 125(18):2835-2844, 2015.
Hamano et al., Alveolar Macrophage Biology B32:A3147-A3147, 2016.
Arase et al., Journal of Dermatological Science, 84(1):e87, 2016.
Tanimura et al., Placenta, 46:108, 2016.
Hiwa et al., Arthritis & Rheumatology, 69(10):2069-2080, 2017.
Hansen et al. Trends in immunology, 31(10):363, 2010.
Hacohen et al., Cancer immunology research, 1(1):11-15, 2013.
Owens et al., Annals of neurology, 65(60):639-649, 2009.
Chastre et al., New England Journal of Medicine, 374(15):1495-1496, 2016.
Housley et al., Clinical Immunology, 161(1):51-58, 2015.
Larman et al., 2013. Journal of autoimmunity, 43:1-9, 2013.
Wu et al., Science, 350(6258):aab4077, 2015
Tran et al. Scientific reports, 6:31730, 2016
Schall et al., Nature Reviews Immunology, 11(5): 355-363, 2011.
Tabarkiewicz et al., Archivum immunologiae et therapiae experimentalis, 63(6):435-449, 2015.
문헌[Brown et al., New England Journal of Medicine, 375(26):2561-2569, 2016].
Gagliani et al., Nature, 523(7559):221-225, 2015.
Barreiro, et al. Cardiovascular research, 86(2):174-182, 2010
Wang and Riviere. Molecular Therapy-Oncolytics, 3:16015 2016.
Burkle et al., Blood, 110(9):3316-3325, 2007.
Wu and Hwang, Journal of immunology, 168(10):5096, 2002.
Singh et al., Journal of immunology, 180(1):214-221, 2008.
Ryu et al., Molecules and Cells, 39.12:898-908, 2016.
Hiepe et al., Nature Reviews Rheumatology, 7(3):170-178, 2011
Garboczi, et al. The Journal of Immunology, 157(12):5403-5410, 1996.
Quaresma, et al., 2015. Viruses, 8(1):5 2015.
Sanjana, et al. Nature methods, 11(8):783-784, 2014.
Korn et al. Proceedings of the National Academy of Sciences, 105(47):18460-18465, 2008.
다른 구현예
본 명세서에서 개시된 모든 특징은 임의의 조합으로 조합될 수 있다. 본 명세서에서 개시된 각각의 특징은 동일한, 등가의 또는 유사한 목적의 역할을 하는 대안적인 특징에 의해 대체될 수 있다. 따라서, 분명하게 다르게 언급되지 않는 한, 개시된 각각의 특징은 등가의 또는 유사한 특징의 포괄적인 시리즈의 일례일 뿐이다.
상기 설명으로부터, 당업자는 본 발명의 필수적인 특징을 쉽게 알아낼 수 있고, 이의 사상 및 범위로부터 벗어나지 않으면서 본 발명을 다양한 용법 및 조건에 적응시키기 위해 본 발명의 다양한 변화 및 변형을 이룰 수 있다. 따라서, 다른 구현예 또한, 청구항 내에 포함된다.