KR20200092080A - 키틴을 이용한 세슘 흡착용 조성물의 제조방법 - Google Patents
키틴을 이용한 세슘 흡착용 조성물의 제조방법 Download PDFInfo
- Publication number
- KR20200092080A KR20200092080A KR1020190009185A KR20190009185A KR20200092080A KR 20200092080 A KR20200092080 A KR 20200092080A KR 1020190009185 A KR1020190009185 A KR 1020190009185A KR 20190009185 A KR20190009185 A KR 20190009185A KR 20200092080 A KR20200092080 A KR 20200092080A
- Authority
- KR
- South Korea
- Prior art keywords
- chitin
- adsorption
- cesium
- composition
- solids
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/30—Processes for preparing, regenerating, or reactivating
- B01J20/3085—Chemical treatments not covered by groups B01J20/3007 - B01J20/3078
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/02—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material
- B01J20/0203—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising compounds of metals not provided for in B01J20/04
- B01J20/0225—Compounds of Fe, Ru, Os, Co, Rh, Ir, Ni, Pd, Pt
- B01J20/0229—Compounds of Fe
-
- B—PERFORMING OPERATIONS; TRANSPORTING
- B01—PHYSICAL OR CHEMICAL PROCESSES OR APPARATUS IN GENERAL
- B01J—CHEMICAL OR PHYSICAL PROCESSES, e.g. CATALYSIS OR COLLOID CHEMISTRY; THEIR RELEVANT APPARATUS
- B01J20/00—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof
- B01J20/02—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material
- B01J20/0203—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising compounds of metals not provided for in B01J20/04
- B01J20/0274—Solid sorbent compositions or filter aid compositions; Sorbents for chromatography; Processes for preparing, regenerating or reactivating thereof comprising inorganic material comprising compounds of metals not provided for in B01J20/04 characterised by the type of anion
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F1/00—Treatment of water, waste water, or sewage
- C02F1/28—Treatment of water, waste water, or sewage by sorption
- C02F1/281—Treatment of water, waste water, or sewage by sorption using inorganic sorbents
-
- C—CHEMISTRY; METALLURGY
- C02—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F—TREATMENT OF WATER, WASTE WATER, SEWAGE, OR SLUDGE
- C02F2101/00—Nature of the contaminant
- C02F2101/006—Radioactive compounds
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Inorganic Chemistry (AREA)
- Analytical Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Life Sciences & Earth Sciences (AREA)
- Hydrology & Water Resources (AREA)
- Engineering & Computer Science (AREA)
- Environmental & Geological Engineering (AREA)
- Water Supply & Treatment (AREA)
- Solid-Sorbent Or Filter-Aiding Compositions (AREA)
Abstract
상기의 과정을 통해 제조되는 세슘 흡착용 조성물은 수중에 함유된 세슘이온에 대해 우수한 흡착력을 나타낸다.
Description
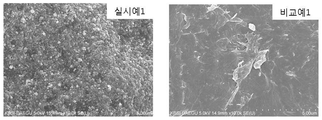
도 2는 개시된 실시예 1 및 비교예 1의 세슘 흡착용 조성물의 표면 변화를 알아보기 위해 주사전자 현미경을 촬영하여 나타낸 사진이다.
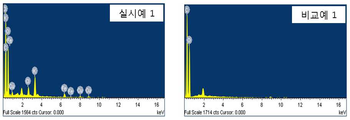
도 3은 개시된 실시예 1의 키틴을 이용한 세슘 흡착용 조성물과 비교예 1을 통해 제조된 세슘 흡착용 조성물의 합성여부를 확인하기 위해 EDX분석을 실시하여 나타낸 그래프이다.
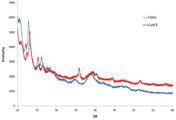
도 4는 개시된 실시예 1 및 비교예 1을 통해 제조된 세슘 흡착용 조성물을 XRD분석하여 그 결과를 나타낸 그래프이다.
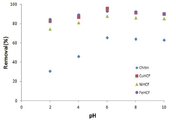
도 5는 개시된 실시예 1 내지 3 및 비교예 1을 통해 제조된 세슘 흡착용 조성물의 pH에 따른 Cs(I) 흡착률을 측정하여 나타낸 그래프이다.
도 6은 개시된 실시예 1 및 비교예 1을 통해 제조된 세슘 흡착용 조성물의 시간에 따른 Cs(I) 흡착속도를 측정하여 나타낸 그래프이다.
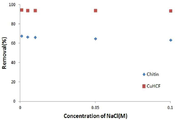
도 7은 개시된 실시예 1의 키틴을 이용한 세슘 흡착용 조성물과 비교예 1을 통해 제조된 세슘 흡착용 조성물의 이온강도에 따른 흡착력을 측정하여 나타낸 그래프이다.
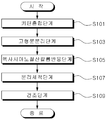
S103 ; 고형분분리단계
S105 ; 헥사시아노철산칼륨반응단계
S107 ; 분리세척단계
S109 ; 건조단계
Claims (5)
- 금속염화물 수용액에 키틴을 혼합하고 교반하는 키틴혼합단계;
상기 키틴혼합단계를 통해 제조된 고형분을 분리하는 고형분분리단계;
상기 고형분분리단계를 통해 분리된 고형분을 헥사시아노철산칼륨 수용액에 투입하는 헥사시아노철산칼륨반응단계;
상기 헥사시아노철산칼륨반응단계를 거친 고형분을 분리하고 세척하는 분리세척단계; 및
상기 분리세척단계를 통해 세척된 고형분을 건조하는 건조단계;로 이루어지는 것을 특징으로 하는 키틴을 이용한 세슘 흡착용 조성물의 제조방법.
- 청구항 1에 있어서,
상기 키틴혼합단계는 금속염화물 수용액 100 중량부에 키틴 0.5 내지 1.5 중량부를 혼합하여 이루어지는 것을 특징으로 하는 키틴을 이용한 세슘 흡착용 조성물의 제조방법.
- 청구항 1 또는 2에 있어서,
상기 금속염화물 수용액은 농도가 0.05 내지 0.15 mol/L이며,
상기 금속염화물은 염화구리, 염화니켈 및 염화철로 이루어진 그룹에서 선택된 하나로 이루어지는 것을 특징으로 하는 키틴을 이용한 세슘 흡착용 조성물의 제조방법.
- 청구항 1에 있어서,
상기 헥사시아노철산칼륨반응단계 25 내지 35℃의 온도에서 10 내지 15시간 동안 이루어지는 것을 특징으로 하는 키틴을 이용한 세슘 흡착용 조성물의 제조방법.
- 청구항 1에 있어서,
상기 헥사시아노철산칼륨 수용액은 농도가 0.05 내지 0.15 mol/L인 것을 특징으로 하는 키틴을 이용한 세슘 흡착용 조성물의 제조방법.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190009185A KR102225373B1 (ko) | 2019-01-24 | 2019-01-24 | 키틴을 이용한 세슘 흡착용 조성물의 제조방법 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR1020190009185A KR102225373B1 (ko) | 2019-01-24 | 2019-01-24 | 키틴을 이용한 세슘 흡착용 조성물의 제조방법 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20200092080A true KR20200092080A (ko) | 2020-08-03 |
| KR102225373B1 KR102225373B1 (ko) | 2021-03-09 |
Family
ID=72042978
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020190009185A Active KR102225373B1 (ko) | 2019-01-24 | 2019-01-24 | 키틴을 이용한 세슘 흡착용 조성물의 제조방법 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102225373B1 (ko) |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20230127039A (ko) * | 2022-02-24 | 2023-08-31 | 세종대학교산학협력단 | 금속 이온 흡착용 조성물 및 그 제조방법 |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR102587342B1 (ko) * | 2021-09-30 | 2023-10-12 | 나재운 | 키토산을 이용한 탄진수 응집제 |
Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002506979A (ja) * | 1998-03-10 | 2002-03-05 | ニューケム・ニュークレア・ゲーエムベーハー | 放射性核種用の吸着剤 |
| JP2013011599A (ja) * | 2011-06-02 | 2013-01-17 | Kankyo Joka Kenkyusho:Kk | 放射性物質除去材料およびその製造方法 |
| KR101589905B1 (ko) | 2014-01-29 | 2016-01-29 | 가톨릭관동대학교산학협력단 | 액상 견운모 용액 및 이것을 이용한 세슘 제거방법 |
| KR20160044404A (ko) * | 2014-10-14 | 2016-04-25 | 경북대학교 산학협력단 | 세슘 또는 스트론튬에 대한 선택적 흡착특성을 갖는 페로시안화 금속이 고정된 탄소나노튜브 흡착제의 제조방법, 이로부터 제조된 흡착제 및 상기 흡착제를 사용한 세슘 또는 스트론튬의 분리방법 |
| KR101708708B1 (ko) | 2015-09-03 | 2017-02-21 | 한국원자력연구원 | 방사성 세슘 흡착제 및 이의 제조방법 |
-
2019
- 2019-01-24 KR KR1020190009185A patent/KR102225373B1/ko active Active
Patent Citations (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2002506979A (ja) * | 1998-03-10 | 2002-03-05 | ニューケム・ニュークレア・ゲーエムベーハー | 放射性核種用の吸着剤 |
| JP2013011599A (ja) * | 2011-06-02 | 2013-01-17 | Kankyo Joka Kenkyusho:Kk | 放射性物質除去材料およびその製造方法 |
| KR101589905B1 (ko) | 2014-01-29 | 2016-01-29 | 가톨릭관동대학교산학협력단 | 액상 견운모 용액 및 이것을 이용한 세슘 제거방법 |
| KR20160044404A (ko) * | 2014-10-14 | 2016-04-25 | 경북대학교 산학협력단 | 세슘 또는 스트론튬에 대한 선택적 흡착특성을 갖는 페로시안화 금속이 고정된 탄소나노튜브 흡착제의 제조방법, 이로부터 제조된 흡착제 및 상기 흡착제를 사용한 세슘 또는 스트론튬의 분리방법 |
| KR101708708B1 (ko) | 2015-09-03 | 2017-02-21 | 한국원자력연구원 | 방사성 세슘 흡착제 및 이의 제조방법 |
Cited By (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20230127039A (ko) * | 2022-02-24 | 2023-08-31 | 세종대학교산학협력단 | 금속 이온 흡착용 조성물 및 그 제조방법 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102225373B1 (ko) | 2021-03-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Kong et al. | Needle-like Mg-La bimetal oxide nanocomposites derived from periclase and lanthanum for cost-effective phosphate and fluoride removal: characterization, performance and mechanism | |
| Tang et al. | Graphene oxide/chitosan/potassium copper hexacyanoferrate (II) composite aerogel for efficient removal of cesium | |
| Saha et al. | Keratin and chitosan biosorbents for wastewater treatment: a review | |
| Banu et al. | Removal of nitrate and phosphate ions from aqueous solution using zirconium encapsulated chitosan quaternized beads: preparation, characterization and mechanistic performance | |
| Lito et al. | Removal of anionic pollutants from waters and wastewaters and materials perspective for their selective sorption | |
| JP3749941B2 (ja) | セシウム分離材の製造方法 | |
| Gomase et al. | Sequential modifications of chitosan biopolymer for enhanced confiscation of Cr (VI) | |
| Liang et al. | Polyamine-co-2, 6-diaminopyridine covalently bonded on chitosan for the adsorptive removal of Hg (II) ions from aqueous solution | |
| Kalkan | Experimental study to remediate acid fuchsin dye using laccase-modified zeolite from aqueous solutions | |
| Adhikari et al. | Recovery of precious metals by using chemically modified waste paper | |
| KR102346593B1 (ko) | 프러시안 블루 및 그 제조방법 | |
| KR102225373B1 (ko) | 키틴을 이용한 세슘 흡착용 조성물의 제조방법 | |
| JP5336932B2 (ja) | 水質浄化材料、水質浄化方法、リン酸肥料前駆体及びリン酸肥料前駆体の製造方法 | |
| Nguyen et al. | Ionic liquid-entrapped MIL-101 (Cr)-NH2 frameworks with improved phosphate control efficiency in aqueous media | |
| CN113559820A (zh) | 一种磷霉素制药废水除磷吸附剂的制备及其应用回收方法 | |
| Deng et al. | Peroxymonosulfate activation by tin (IV) phosphate supported cobalt composite for acetaminophen degradation: Performance and mechanism | |
| CN110280227B (zh) | MnO2/PEI/TA双功能复合材料的制备及其应用 | |
| US8133838B2 (en) | Water purification material | |
| KR101946447B1 (ko) | 세슘 흡착 하이드로젤 필름의 제조방법 | |
| Ahmad et al. | Treatment methods for cadmium removal from wastewater | |
| RU2021009C1 (ru) | Способ получения композитных сорбентов и композитный сорбент | |
| CN103359789B (zh) | 碱式碳酸铋的制备方法 | |
| M Mohamed et al. | Removal of cadmium from aqueous solution using modified magnetic glycine modified cross-linked chitosan resin | |
| KR101927288B1 (ko) | 표면이 개질된 활성탄의 제조방법 및 그 방법에 의해 제조된 표면이 개질된 활성탄 | |
| JP2004298738A (ja) | ホウ素含有水の処理方法 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| E13-X000 | Pre-grant limitation requested |
St.27 status event code: A-2-3-E10-E13-lim-X000 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| GRNT | Written decision to grant | ||
| PR0701 | Registration of establishment |
St.27 status event code: A-2-4-F10-F11-exm-PR0701 |
|
| PR1002 | Payment of registration fee |
St.27 status event code: A-2-2-U10-U11-oth-PR1002 Fee payment year number: 1 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 4 |
|
| P14 | Amendment of ip right document requested |
Free format text: ST27 STATUS EVENT CODE: A-5-5-P10-P14-NAP-X000 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| P14-X000 | Amendment of ip right document requested |
St.27 status event code: A-5-5-P10-P14-nap-X000 |
|
| PR1001 | Payment of annual fee |
St.27 status event code: A-4-4-U10-U11-oth-PR1001 Fee payment year number: 5 |
|
| U11 | Full renewal or maintenance fee paid |
Free format text: ST27 STATUS EVENT CODE: A-4-4-U10-U11-OTH-PR1001 (AS PROVIDED BY THE NATIONAL OFFICE) Year of fee payment: 5 |