KR20220119065A - 불면증 치료를 위한 렘보렉산트의 용도 - Google Patents
불면증 치료를 위한 렘보렉산트의 용도 Download PDFInfo
- Publication number
- KR20220119065A KR20220119065A KR1020227023903A KR20227023903A KR20220119065A KR 20220119065 A KR20220119065 A KR 20220119065A KR 1020227023903 A KR1020227023903 A KR 1020227023903A KR 20227023903 A KR20227023903 A KR 20227023903A KR 20220119065 A KR20220119065 A KR 20220119065A
- Authority
- KR
- South Korea
- Prior art keywords
- lemborexant
- child
- acceptable salt
- patient
- pharmaceutically acceptable
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/495—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with two or more nitrogen atoms as the only ring heteroatoms, e.g. piperazine or tetrazines
- A61K31/505—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim
- A61K31/506—Pyrimidines; Hydrogenated pyrimidines, e.g. trimethoprim not condensed and containing further heterocyclic rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/20—Hypnotics; Sedatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/0012—Galenical forms characterised by the site of application
- A61K9/0053—Mouth and digestive tract, i.e. intraoral and peroral administration
Landscapes
- Health & Medical Sciences (AREA)
- Medicinal Chemistry (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Neurosurgery (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Neurology (AREA)
- Biomedical Technology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Anesthesiology (AREA)
- Nutrition Science (AREA)
- Physiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
불면증을 치료하는 방법으로서, 렘보렉산트(lemborexant) 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 렘보렉산트 5 mg 내지 10 mg 범위의 단회 일일 용량으로 또는 이의 약제학적으로 허용되는 염의 등가 용량으로 경구 투여하는 단계를 포함하고, 단, 환자가 차일드-푸 분류(Child-Pugh Classification) 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 개시된다.
Description
본 출원은 본원에 참고로 포함된 2020년 12월 20일에 출원된 미국 가출원 번호 62/951,638에 대한 우선권의 이익을 주장한다.
본 개시는 불면증을 치료하는 방법에 관한 것이다.
뇌의 시상하부에 국한된 뉴런에서 발현되는 2개의 신경 펩타이드, 오렉신(orexin)-A(OX-A, 33개의 아미노산으로 구성된 펩타이드)와 오렉신-B(OX-B, 28개의 아미노산으로 구성된 펩타이드)는 주로 뇌에 존재하는 G 단백질-결합 수용체, 즉 오렉신 수용체에 대한 내인성 리간드로 밝혀졌다(WO1996/34877, 일본 공개 특허 공보 H10-327888, H10-327889, H11-178588, 및 H10-229887, WO2016/063995, 및 Sakurai T. et al., Cell, 1998, 92, 573-585.). 오렉신 수용체는 2개의 아형, 즉 아형 1로서 OX1 수용체(OX1) 및 아형 2로서 OX2 수용체(OX2)를 포함한다. OX1은 OX-B가 아니라 OX-A에 선택적으로 결합하고, OX2는 OX-B 뿐만 아니라 OX-A에도 결합한다. 오렉신은 래트의 식량 소비를 자극하는 것으로 결정되었으며, 이는 섭식 행동을 조절하기 위한 중심 피드백 매커니즘에서 매개체로서 이러한 펩타이드의 생리적 기능을 시사한다(Sakurai T. et al., Cell, 1998, 92, 573-585).
오렉신은 또한 수면-각성 상태를 조절하는 것으로 관찰되었으며, 그에 따라 기면증, 뿐만 아니라 불면증 및 기타 수면 장애(sleep disorder)를 치료할 수 있다(Chemelli R. M. et al., Cell, 1999, 98, 437-451). 또한, 약물 중독 및 니코틴 중독과 관련된 신경 가소성에 있어서 복측 피개 영역에서의 오렉신 신호가 생체 내에서 중요한 역할을 하는 것으로 시사되었다(S. L. Borgland et al., Neuron, 2006, 49, 589-601 및 C. J. Winrow et al., Neuropharmacology, 2010, 58, 185-194). 래트를 이용한 실험에서 OX2를 선택적으로 저해함으로써 에탄올 중독을 감소시키는 것도 보고되었다(J. R. Shoblock et al., Psychopharmacology, 2010, 215: 191-203). 나아가, 래트에서 우울증 및 불안 장애와 관련된 코르티코트로핀 방출 인자(CRF)가 오렉신 유도 행동과 관련이 있으며, 오렉신이 스트레스 반응에 중요한 역할을 할 수 있다는 것도 보고되었다(T. Ida et al., Biochemical and Biophysical Research Communications, 2000, 270, 318-323).
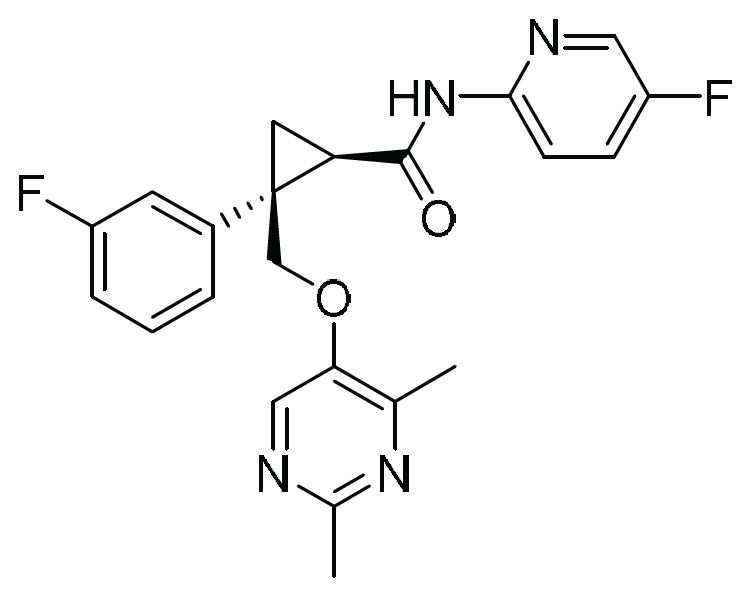
한편, 렘보렉산트(lemborexant)(화합물명: (1R,2S)-2-(((2,4-디메틸피리미딘-5-일)옥시)메틸)-2-(3-플루오로페닐)-N-(5-플루오로피리딘-2-일)시클로프로판카르복사미드)는 오렉신 수용체 길항 작용을 갖는 화합물로 알려져 있으며, 불면증과 같은 수면 장애(sleep disorder)를 치료할 수 있다(T. Ida et al., Biochemical and Biophysical Research Communications, 2000, 270, 318-323).
E2006으로도 알려진 렘보렉산트는 임상 시험에서 연구되었으며, 유리한 특성, 예를 들어 수면 개시 후 각성, 수면 개시 잠복기의 감소 및/또는 수면 효율의 개선을 지닌 것으로 알려져 있다(예를 들어, US 8,268,848 B2 및 PCT 국제 출원 번호 PCT/US2019/039333을 참조, 이들 둘 모두의 전문은 본원에 참고로 포함된다.)
CYP3A-매개 대사는 렘보렉산트에 대한 주요 제거 경로이기 때문에, 간 손상을 갖는 대상체는 렘보렉산트 대사에 문제가 있을 수 있으며, 이는 렘보렉산트의 PK에 영향을 미치고 금기로 이어질 것이다. 그러나, 차일드-푸 분류(Child-Pugh Classification) 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자를 치료하는 방법이 필요하다. 본 개시의 목적은 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에게 렘보렉산트가 투여되더라도 효과적이고 안전한 불면증 치료 방법을 제공하는 것이다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 렘보렉산트 5 mg 내지 10 mg 범위의 단회 일일 용량으로 또는 이의 약제학적으로 허용되는 염의 등가 용량으로 경구 투여하는 단계를 포함하고, 단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다. 일부 구현예에서, 환자는 차일드-푸 분류 하에서 차일드-푸 클래스 C로 분류된 중증 간 손상을 갖지 않는다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 경구 투여하는 단계를 포함하고, 5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고, 용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고, 단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다. 일부 구현예에서, 환자는 차일드-푸 분류 하에서 차일드-푸 클래스 C로 분류된 중증 간 손상을 갖지 않는다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에게 경구 투여하는 단계를 포함하고, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다.
일부 구현예에서, 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에서 불면증을 치료하는 방법으로서, 5 mg의 렘보렉산트 또는 등가량의 이의 약제학적으로 허용되는 염을 포함하는 투여형을 1일 1회 경구 투여하는 단계를 포함하는, 방법이 본원에 개시된다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 환자에서 차일드-푸 분류 하에서 환자의 간 손상 수준을 결정하는 단계; 및 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 환자에게 경구 투여하는 단계를 포함하며, 5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고, 환자가 간 손상을 갖지 않거나 차일드-푸 분류 하에서 차일드-푸 클래스 A로 분류된 경등도 간 손상을 갖는 경우, 용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다.
본 개시에 따르면, 불면증 치료는 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류되는 중등도 간 손상을 갖는 환자에게 효과적이고 안전할 수 있다.
도 1은 12시간에 걸쳐 10 mg 렘보렉산트를 정상 간 기능을 갖는 건강한 대조군 대상체, 경등도 간 손상을 갖는 환자, 및 중등도 간 손상을 갖는 환자에게 투여한 후의 평균(±SD) 혈장 렘보렉산트 농도-시간 프로파일을 도시한다.
도 2는 312시간에 걸쳐 10 mg 렘보렉산트를 정상 간 기능을 갖는 건강한 대조군 대상체, 경등도 간 손상을 갖는 환자, 및 중등도 간 손상을 갖는 환자에게 투여한 후의 평균(±SD) 혈장 렘보렉산트 농도-시간 프로파일을 도시한다.
도 3은 정상 간 기능을 갖는 건강한 대조군 대상체 대비, 경등도 또는 중등도 간 손상을 갖는 환자에 대한 기하 평균 비율(90% 신뢰 구간)을 도시한다.
도 2는 312시간에 걸쳐 10 mg 렘보렉산트를 정상 간 기능을 갖는 건강한 대조군 대상체, 경등도 간 손상을 갖는 환자, 및 중등도 간 손상을 갖는 환자에게 투여한 후의 평균(±SD) 혈장 렘보렉산트 농도-시간 프로파일을 도시한다.
도 3은 정상 간 기능을 갖는 건강한 대조군 대상체 대비, 경등도 또는 중등도 간 손상을 갖는 환자에 대한 기하 평균 비율(90% 신뢰 구간)을 도시한다.
본원에서 사용된 바와 같이, 달리 명시되지 않는 한 다음 정의가 적용될 것이다.
본원에서 사용된 바와 같이, 단수형은 하나 이상을 지칭한다.
본원에서 사용된 바와 같이, 용어 "렘보렉산트"는 (1R,2S)-2-(((2,4-디메틸피리미딘-5-일)옥시)메틸)-2-(3-플루오로페닐)-N-(5-플루오로피리딘-2-일)시클로프로판카르복사미드 또는 (1R,2S)-2-(((2,4-디메틸피리미딘-5-일)옥시)메틸)-2-(3-플루오로페닐)-N-(5-플루오로피리딘-2-일)시클로프로판-1-카르복사미드로도 알려진, 다음 구조를 갖는 화합물을 지칭한다:
렘보렉산트 또는 이의 약제학적으로 허용되는 염은, 예를 들어 WO2012/039371 및 WO2013/123240에 기재된 방법에 의해 제조될 수 있다.
본원에서 사용된 바와 같이, 용어 "약제학적으로 허용되는 염"은 모 화합물의 요망되는 생물학적 활성을 유지하고, 요망되지 않는 독물학적 영향을 부여하지 않는 염이다. 이러한 염의 예에는, (a) 무기산으로 형성된 산 부가염, 예를 들어 염산, 브롬화수소산, 황산, 인산, 질산 등; 및 유기산으로 형성된 염, 예를 들어 아세트산, 옥살산, 타르타르산, 숙신산, 말레산, 푸마르산, 글루콘산, 시트르산, 말산, 아스코르브산, 벤조산, 탄닌산, 팔미트산, 알긴산, 폴리글루탐산, 나프탈렌설폰산, 메탄설폰산, p-톨루엔설폰산, 나프탈렌디설폰산, 폴리갈락투론산 등; 및 (b) 염소, 브롬, 및 요오드와 같은 원소 음이온으로부터 형성된 염이 포함되지만 이에 제한되지는 않는다. 예를 들어 본원에 참고로 포함된 문헌[Haynes, et al., J. Pharm. Sci., 2005, 94, 10; 및 Berge, et al., J. Pharm. Sci., 1977, 66, 1]을 참조하라.
일부 구현예에서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염은 투여형으로 투여된다. 일부 구현예에서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염은 예를 들어, 캡슐, 과립, 로젠지, 펠렛, 환제, 분말, 현탁액 및 정제와 같은 고체 투여형이다.
일부 구현예에서, 투여형은 적어도 하나의 추가의 약제학적으로 허용되는 성분을 추가로 포함한다. 일부 구현예에서, 적어도 하나의 추가의 약제학적으로 허용되는 성분은 약제학적으로 허용되는 담체, 약제학적으로 허용되는 비히클, 및 약제학적으로 허용되는 부형제로부터 선택된다.
본 개시에 따른 투여형은 불면증이 있는 환자에게 경구 투여되고, 5 mg 내지 10 mg 범위의 용량의 렘보렉산트 또는 등가 용량의 렘보렉산트의 약제학적으로 허용되는 염을 포함한다. 일부 구현예에서, 투여형은 5 mg의 렘보렉산트를 포함한다. 일부 구현예에서, 투여형은 5 mg 렘보렉산트와 등가인 용량으로 렘보렉산트의 약제학적으로 허용되는 염을 포함한다. 일부 구현예에서, 투여형은 10 mg의 렘보렉산트를 포함한다. 일부 구현예에서, 투여형은 10 mg 렘보렉산트와 등가인 용량으로 렘보렉산트의 약제학적으로 허용되는 염을 포함한다.
본원에서 사용된 바와 같이, 용어 "약제학적으로 허용되는"은 담체, 희석제, 부형제 또는 비히클이 조성물의 다른 성분과 상용성이고 대상체에게 무독성 무독성임을 의미한다.
본원에서 사용된 바와 같이, 용어 "약제학적으로 허용되는 부형제"는 비히클로서 사용되는 비활성 성분(예를 들어, 물, 캡슐 껍질 등), 희석제, 또는, 투여형을 구성할 성분 또는 치료제와 같은 약물을 포함하는 약제학적 조성물을 의미한다. 용어는 또한 조성물에 응집 기능을 부여하는 비활성 성분(예를 들어, 결합제), 붕괴 기능을 부여하는 비활성 성분(예를 들어, 붕괴제), 윤활 기능을 부여하는 비활성 성분(예를 들어, 윤활제) 및/또는 다른 기능을 부여하는 비활성 성분(예를 들어, 용매, 계면활성제 등)을 포괄한다.
본원에서 사용된 바와 같이, 용어 "환자"는 포유동물 대상체와 같은 동물 대상체, 예를 들어 인간을 의미한다. 본원에서 사용된 바와 같이, 대상체는 임의의 연령일 수 있다. 일부 구현예에서, 대상체는 18세 이상일 수 있다.
본원에서 사용된 바와 같이, 용어 "치료" 및 "치료하는"은 치료적 이점 및/또는 예방적 이점을 포함하지만 이에 제한되지는 않는 유익하거나 요망되는 결과를 얻기 위한 접근법을 지칭한다.
본원에서 사용된 바와 같이, 용어 "불면증"은 다음 진단 기준을 갖는 정신 장애 진단 및 통계 편람 제5판(2013; "DSM-V")에 의해 정의된 장애를 의미한다:
A. 대상체의 주된 불만은 다음 증상 중 하나(또는 그 이상)와 관련된 수면의 양 또는 질에 대한 불만임:
1. 수면 시작의 어려움(어린이의 경우, 이는 보호자(caregiver)의 개입 없이 수면을 시작하기 어려운 것으로 나타날 수 있음).
2. 잦은 기상, 또는 기상한 후 다시 잠드는 데 있어서의 문제를 특징으로 하는, 수면 유지의 어려움(어린이의 경우, 이는 보호자의 개입 없이 다시 잠들기 어려운 것으로 나타날 수 있음).
3. 다시 잠들 수 없는 이른-아침 기상.
B. 수면 장애(sleep disturbance)가, 사회적, 직업적, 교육적, 학업적, 행동적 또는 다른 중요한 기능 영역에서 임상적으로 유의한 고통 또는 손상을 유발함.
C. 수면 곤란(sleep difficulty)이 일주일에 적어도 3번 발생함.
D. 수면 곤란이 적어도 3개월 동안 존재함.
E. 적절한 수면 기회에도 불구하고 수면 곤란이 발생함.
F. 불면증이 다른 수면-각성 장애(예를 들어, 기면증, 호흡 관련 수면 장애(sleep disorder), 일주기 리듬 수면-각성 장애, 사건수면)로는 보다 잘 설명되지 않고, 그 과정 동안에만 발생하는 것은 아님.
G. 불면증이 물질(예를 들어, 남용 약물, 약제)의 생리적 영향으로 인한 것이 아님.
H. 공존하는 정신 장애와 의학적 질환이, 불면증에 관한 주된 불만을 적절하게 설명하지 못함.
용어 "불면증"은 또한 잠들기 어려움, 수면 지속의 어려움, 간헐적 각성 및/또는 너무 일찍 일어나는 것을 포함하나 이에 제한되지는 않는 증상을 특징으로 하는 수면 장애(sleep disorder)를 의미한다. 용어는 졸음, 불안, 집중력 손상, 기억력 손상 및 과민성과 같은 주간 증상도 포괄한다. 렘보렉산트 또는 이의 약제학적으로 허용되는 염으로 치료하기에 적합한 유형의 불면증은 단기 불면증 및 만성 불면증을 포함한다.
본원에서 사용된 바와 같이, "불면증을 치료하는 것"은 치료적 이점 및/또는 예방적 이점을 포함하지만 이에 제한되지는 않는 유익하거나 요망되는 결과를 얻는 것을 지칭한다.
본원에서 사용된 바와 같이, 용어 "Cmax"는 혈장 내에서의 최대 농도를 나타낸다.
본원에서 사용된 바와 같이, 용어 "AUC(0 - inf)"는 제제 투여 직후(시간 0)부터 무한대까지의 혈장 농도-시간 곡선 아래의 면적을 나타낸다.
"차일드-푸 분류" 점수는 본원에서 간 손상 정도의 마커로 사용되며, 표 1의 기준에 따라 평가된다.
[표 1]
차일드-푸 분류를 위한 기준
cps = 초당 사이클, INR = 국제 표준화 비율(International normalized ratio), PT = 프로트롬빈 시간.
a: 총점 5 내지 6점은 차일드-푸 클래스 A로, 그리고 총점 7 내지 9점은 차일드-푸 클래스로 평가되었다.
b: 뇌병증 등급은 이상 반응에 대한 공통 용어 기준(common terminology criteria for adverse events, CTCAE)에 따라 평가되었다: 0등급: 정상적인 의식, 성격, 신경학적 검사 및/또는 뇌파도; 1등급: 안절부절, 수면 장애(sleep disturbed), 과민/초조, 진전, 필기 장애 및 5 cps 파동; 2등급: 무기력, 시간-방향 감각 상실, 부적절, 자세고정못함증, 운동 실조, 느린 삼상파; 3등급: 졸음, 혼미, 장소-방향 감각 상실, 과잉 반사, 경직, 보다 느린 파동; 4등급: 각성할 수 없는 혼수상태, 성격/행동 없음, 제뇌자, 느린 2 내지 3 cps 델타 활동.
일부 구현예에서, 불면증을 치료하는 방법으로서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 렘보렉산트 5 mg 내지 10 mg 범위의 단회 일일 용량으로 또는 이의 약제학적으로 허용되는 염의 등가 용량으로 경구 투여하는 단계를 포함하고, 단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다. 일부 구현예에서, 환자는 차일드-푸 분류 하에서 차일드-푸 클래스 C로 분류된 중증 간 손상을 갖지 않는다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 경구 투여하는 단계를 포함하고, 5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고, 용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고, 단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다. 일부 구현예에서, 환자는 차일드-푸 분류 하에서 차일드-푸 클래스 C로 분류된 중증 간 손상을 갖지 않는다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에게 경구 투여하는 단계를 포함하고, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다.
일부 구현예에서, 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에서 불면증을 치료하는 방법으로서, 5 mg의 렘보렉산트 또는 등가량의 이의 약제학적으로 허용되는 염을 포함하는 투여형을 1일 1회 경구 투여하는 단계를 포함하는, 방법이 본원에 개시된다.
일부 구현예에서, 불면증을 치료하는 방법으로서, 환자에서 차일드-푸 분류 하에서 환자의 간 손상 수준을 결정하는 단계; 및 렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 환자에게 경구 투여하는 단계를 포함하며, 5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고, 환자가 간 손상을 갖지 않거나 차일드-푸 분류 하에서 차일드-푸 클래스 A로 분류된 경등도 간 손상을 갖는 경우, 용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법이 본원에 개시된다.
본 개시의 비제한적인 구현예는 다음을 포함하지 않는다:
구현예 1: 불면증을 치료하는 방법으로서,
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 렘보렉산트 5 mg 내지 10 mg 범위의 단회 일일 용량으로 또는 이의 약제학적으로 허용되는 염의 등가 용량으로 경구 투여하는 단계를 포함하고,
단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법.
구현예 2: 불면증을 치료하는 방법으로서,
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 경구 투여하는 단계를 포함하고,
5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고,
용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고, 단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법.
구현예 3: 구현예 1 또는 2에 있어서, 환자는 차일드-푸 분류 하에서 차일드-푸 클래스 C로 분류된 중증 간 손상을 갖지 않는, 방법.
구현예 4: 불면증을 치료하는 방법으로서,
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에게 경구 투여하는 단계를 포함하고,
최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법.
구현예 5: 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에서 불면증을 치료하는 방법으로서,
5 mg의 렘보렉산트 또는 등가량의 이의 약제학적으로 허용되는 염을 포함하는 투여형을 1일 1회 경구 투여하는 단계를 포함하는, 방법.
구현예 6: 불면증을 치료하는 방법으로서,
환자에서 차일드-푸 분류 하에서 환자의 간 손상 수준을 결정하는 단계; 및
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 환자에게 경구 투여하는 단계를 포함하며,
5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고,
환자가 간 손상을 갖지 않거나 차일드-푸 분류 하에서 차일드-푸 클래스 A로 분류된 경등도 간 손상을 갖는 경우, 용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고,
환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법.
실시예
다음 실시예는 본 개시의 다양한 양태를 예시하는 것이고, 본 개시의 범위를 제한하는 것으로 해석되어서는 안 된다.
경등도 또는 중등도 간 손상을 갖는 대상체, 및 대조군으로서 일치하는 건강한 대상체(나이[±10세], 성별 및 체질량지수[BMI, ±20%] 관련)에서의, 다기관, 단회-용량, 공개-라벨, 병렬-그룹 연구를 수행하였다.
연구의 1차 목적은 단회-용량 투여 후 렘보렉산트의 PK에 대한 경등도 및 중등도 간 손상의 영향을 평가하는 것이었다.
연구의 2차 목적은 렘보렉산트 대사산물 M4, M9 및 M10의 PK에 대한 간 손상의 영향을 평가하는 것; 렘보렉산트 및 그 대사산물의 PK 매개변수와 차일드-푸 분류 점수, 혈청 알부민, 총 빌리루빈 및 PT 사이의 관계를 평가하는 것; 및 경등도 또는 중등도 간 손상을 갖는 대상체 및 건강한 대조군 대상체에서 단회-용량 투여 후 렘보렉산트의 안전성 및 내약성을 평가하는 것이었다.
연구 단계
연구는 다음 2개의 단계로 구성하였다: 사전 치료 및 치료.
사전 치료 단계에는 2개의 연구 기간을 포함시켰다: 스크리닝 및 기준선(-1일차). 대상체는 -1일차에 임상 시설에 입원하고, 8일차까지 클리닉에 감금되었고, 그 다음 14일차까지 외래 환자로서 추가 PK 샘플링을 위해 임상 시설로 되돌아왔다. 대상체의 조기 중단의 경우, 차일드 푸 클래스 A 및 B를 갖는 대상체(코호트 A 및 B) 및 일치하는 건강한 대조군(코호트 C)이 대체되는 것을 허용하였다.
치료 단계는 14일의 1개의 연구 기간으로 구성하였다.
1일차에, 대상체는 밤새 금식한 후 아침에 대략 240 mL의 물과 함께 10 mg 용량의 렘보렉산트를 경구로 단회 투여받았다. 투여 후 적어도 4시간 동안은 음식을 허용하지 않았다. 물은 약물 투여 전후 1시간을 제외하고 원하는 대로 허용하였다.
PK 평가를 위한 혈액 샘플은 용량 투여 후(postdose administration) 최대 312시간까지 사전 지정된 간격으로 수집하였다. 또한, 렘보렉산트의 혈장 단백질 결합 평가를 위한 혈액 샘플을 2개의 시점; 투여 후 대략 1시간 및 24시간째에 각 대상체로부터 수집하였다. 대상체는 연구 14일차에 퇴원하였다. 연구의 종료는 마지막 대상체의 마지막 연구 방문 날짜였다.
대상체
대상체는 다음을 포함하여, 모든 포함 기준을 충족하고 제외 기준을 충족하지 않는 경우 연구에 참여할 자격이 있었다:
1. 사전 동의 당시 18 내지 79세의 남성 또는 여성 대상체.
2. 스크리닝 시 18 내지 40 kg/m2의 BMI.
3. 비흡연자 또는 하루 20개비 이하의 담배를 피우는 흡연자.
4. 코호트 A 및 B의 경우: 각각 차일드-푸 분류 A 또는 B에 부합하고(표 1 참조), 병력 및 신체 검사에 의해 문서화된 안정적인(연구 스크리닝 전 적어도 60일 동안 질병 상태의 변화가 없음) 간 손상.
5. 코호트 C의 경우: 연령(±10세), 성별 및 BMI(±20%)와 관련하여 간 손상을 갖는 대상체와 일치하고, 병력, 신체 검사, ECG 및 임상 실험실 결정에서 정상으로부터 임상적으로 유의한 편차가 없는 것에 의해 결정된 건강한 대조군 대상체.
모든 대상체는 CYP3A 효소 또는 수송체에 영향을 미치는 음식, 음료 또는 보충제(예를 들어, St. John's wort)를 섭취하는 것을 금지당했다(예를 들어, 자몽-함유 식품, 겨자과의 채소).
총 28명의 대상체가 등록되었다; 24명의 대상체가 스크리닝을 통과하고, 투여받았고, 완료되었다. 등록되고 투여받은 모든 24명의 대상체(코호트당 8명의 대상체)를 안전성 및 PK 분석 세트에 포함시켰다.
코호트 A - 차일드 푸 클래스 A: 2명의 여성 및 6명의 남성 대상체가 있었다. 평균 연령은 57.0세였다.
코호트 B - 차일드 푸 클래스 B: 2명의 여성 및 6명의 남성 대상체가 있었다. 평균 연령은 61.4세였다.
코호트 C - 건강한 대조군 대상체: 3명의 여성 및 5명의 남성 대상체가 있었다. 평균 연령은 56.8세였다.
평가
약동학
렘보렉산트 및 그 대사산물(M4, M9 및 M10)의 PK 평가를 위한 혈액 샘플(각각 4 mL)을 투여 전(0시간), 투여 0.5, 1, 1.5, 2, 3, 4, 6, 8, 12, 24, 48, 72, 96, 120, 144, 168, 216, 264, 및 312시간 후에 수집하였다. 또한, 렘보렉산트 및 그 대사산물(M4, M9 및 M10)의 단백질 결합에 대한 혈액 샘플(시점 당 12 mL)을 해당 시점의 PK 샘플 수집과 일치하는 투여 후 1시간 및 24시간째에 수집하였다.
렘보렉산트 및 렘보렉산트 대사산물(M4, M9 및 M10)의 총 평균 혈장 농도는 탠덤 질량 분석법(LC-MS/MS)을 이용하여, 검증된 액체 크로마토그래피에 의해 측정하였다. 렘보렉산트, M4, M9 및 M10의 결합되지 않은 렘보렉산트 농도도 평형 투석 후 유사한 검증된 LC-MS/MS 방법을 사용하여 측정하였다.
안전성 평가
안전성은 일시적 이상 반응(treat-emergent adverse event, TEAE), ECG, 활력 징후, 체중, 신체 검사 및 임상 실험실 테스트(소변 검사, 혈액학 및 혈액 화학)를 모니터링하고 문서화하여 평가하였다.
결과
경등도 간 손상은 건강한 간 기능과 비교하여 렘보렉산트 Cmax 및 AUC(0-inf) 값을 각각 58% 및 25% 증가시켰고; 렘보렉산트 PK에 대한 중등도 간 손상의 영향도 유사하였다. 렘보렉산트 Cmax 및 AUC(0-inf) 값은 건강한 대상체와 비교하여, 중등도 간 손상을 갖는 대상체에서 각각 22% 및 54% 증가하였다(도 3). 렘보렉산트의 전신 제거율(total body clearance)은 건강한 대상체와 비교하여, 경등도 및 중등도 간 손상을 갖는 대상체에서 각각 20% 및 35% 감소하였다. 따라서 간 손상을 갖는 대상체에 대한 10-mg 렘보렉산트의 투여는 건강한 대상체에 대한 10-mg 렘보렉산트의 투여와 비교하여 렘보렉산트 노출의 증가를 초래하였다.
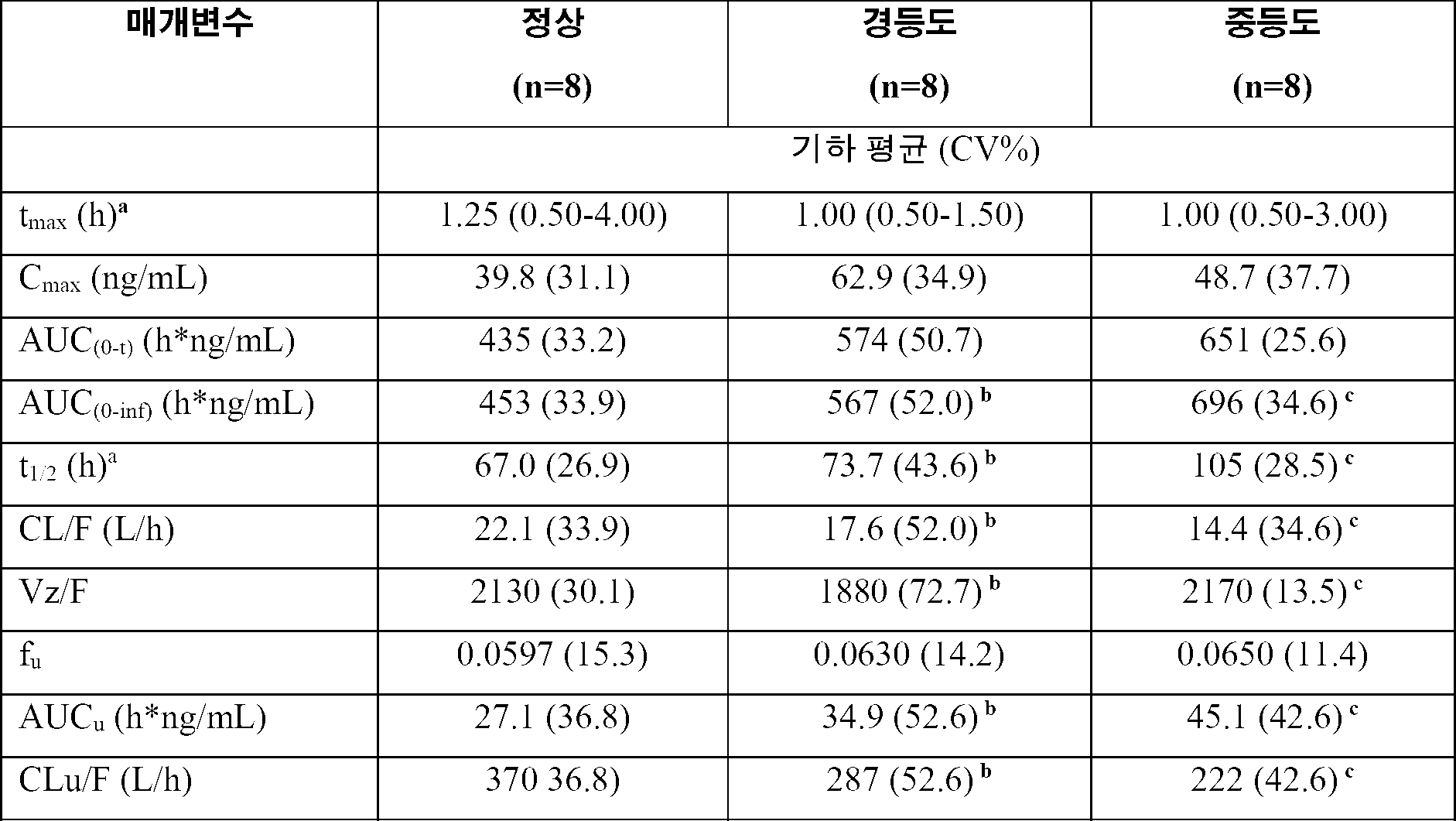
[표 2]
렘보렉산트 10 mg을 정상 간 기능, 경등도 간 손상, 또는 중등도 간 손상을 갖는 대상체에게 투여한 후의 렘보렉산트의 약동학적 매개변수의 기하 평균(CV%)
a: 중앙값(범위)으로 제시된 tmax;
b: n=7, 1명의 대상체에 대해 말기 속도 상수(terminal rate constant)를 추정할 수 없었음; 그리고
c: n=6, 2명의 대상체에 대해 말기 속도 상수를 추정할 수 없었음.
렘보렉산트 10-mg 정제의 단회-용량 후 렘보렉산트 노출(기하 평균 Cmax, AUC(0-t) 및 AUC(0-inf) 기반)은 건강한 대조군 대상체와 비교하여 경등도 또는 중등도 간 손상을 갖는 대상체에서 더 높았다. 중앙값 렘보렉산트 tmax은 1.00 내지 1.25시간 범위로 코호트 전반에 걸쳐 유사하였다. 기하 평균 CL/F는 간 손상이 증가함에 따라 감소하였으며(경등도 손상을 갖는 대상체의 경우 17.6 L/h, 중등도 간 손상을 갖는 대상체의 경우 14.4 L/h), 건강한 대조군 대상체에서 관찰된 것(22.1 L/h)보다 낮았다. 더 긴 기하 평균 반감기를 건강한 대조군 대상체(67.0 시간)와 비교하여 간 손상을 갖는 대상체에서 관찰하였다(경등도 간 손상을 갖는 대상체의 경우 73.7시간, 중등도 간 손상을 갖는 대상체의 경우 105 시간). 경등도 및 중등도 간 손상을 갖는 대상체에서 기하 평균 렘보렉산트 fu 값은 각각 0.0630 및 0.0650이었고, 건강한 대조군 대상체(0.0597)와 비슷하였다. 경등도 또는 중등도 간 손상을 갖는 더 높은 AUCu 및 더 낮은 CLu/F에 대한 경향은 AUC(0-inf) 및 CL/F에 대한 관찰과 일치하였다.
[표 3]
렘보렉산트의 자연로그-변환 전신 노출 매개변수(Systemic Exposure Parameter)의 통계적 분석(경등도 또는 중등도 간 손상 대 정상 간 기능)
a: 로그 변환 매개변수 값의 최소 제곱 평균을 기반으로 한 테스트 및 참조에 대한 기하 평균;
b: 비율(%) = 기하 평균(테스트) / 기하 평균(참조); 및
c: 90% CI.
렘보렉산트 Cmax 및 AUC(0-inf)는 건강한 대조군 대상체와 비교하여, 경등도 간 손상을 갖는 대상체에서 각각 58% 및 25% 더 높았고, 중등도 간 손상을 갖는 대상체에서 각각 22% 및 54% 더 높았다.
렘보렉산트는 M4, M9 및 M10 대사산물로 광범위하게 대사되었다. 간 손상은 M4, M9 및 M10에 대한 대사산물 대 모 노출 비율에 영향을 미치지 않는다. 또한, M4, M9 및 M10 대사산물의 t1/2는 건강한 대상체와 비교하여 경등도 간 손상을 갖는 대상체에서 변하지 않았고 중등도 간 손상 대상체를 갖는 대상체에서 1.5 내지 2.1배만큼 약간 증가하였다.
[표 4]
렘보렉산트 10-mg을 정상 간 기능, 경등도 간 손상, 또는 중등도 간 손상을 갖는 대상체에게 투여한 후의 M4, M9, 및 M10의 약동학적 매개변수의 기하 평균(CV%)
a: 중앙값(범위)으로 제시된 tmax;
b: n=7, 1명의 대상체에 대해 말기 속도 상수를 추정할 수 없었음;
c: n=6, 2명의 대상체에 대해 말기 속도 상수를 추정할 수 없었음; 그리고
d: n=5, 3명의 대상체에 대해 말기 속도 상수를 추정할 수 없었음.
렘보렉산트 대사산물(M4, M9 및 M10)의 경우, 각각의 기하 평균 Cmax는 건강한 대조군 대상체와 비교하여 경등도 또는 중등도 간 손상을 갖는 대상체에서 더 낮았고; 코호트 전반에 걸쳐 각 대사산물의 중앙값 tmax의 명백한 차이는 관찰되지 않았다. 일반적으로, M4, M9 및 M10의 AUC를 기반으로 한 노출은 코호트 전반에 걸쳐 비슷했으며, 간 손상을 동반한 대사산물 노출의 변화에 대해서는 일관된 경향이 관찰되지 않았다. 경등도 또는 중등도 간 손상을 갖는 대상체에서의 더 높은 렘보렉산트 노출(AUC(0-inf))을 반영하면, AUC(0-inf)의 기하 평균 대사산물-대-모 비율(metabolite-to-parent ratio, MPR)은 건강한 대조군 대상체에 비해 간 손상과 함께 감소하였다.
렘보렉산트 및 그 대사산물의 PK 매개변수와 차일드-푸 분류 점수, 혈청 알부민, 총 빌리루빈, MELD 점수 및 PT 사이의 관계를 산점도 및 선형 회귀를 통해 탐구하였고, 렘보렉산트에 대한 경등도 및 중등도 간 손상의 영향이 작고 유사하였음을 보여주었다. 렘보렉산트 PK와 간 기능 사이의 관계에 대한 일관된 증거는 관찰되지 않았다.
안전성은 경등도, 중등도 및 건강한 대상체 전반에 걸쳐 유사하였다. SAE는 보고되지 않았다. 총 20명(83.3%)의 대상체가 연구 동안 TEAE를 경험하였다: 클래스 A, 클래스 B, 및 건강한 대조군에서 각각 7(87.5%), 6(75.0%), 및 7(87.5%)명의 대상체. 연구 동안 모든 TEAE의 심각도는 경미하였으며, 어느 TEAE도 대상체 중단을 야기하지 않았다. 어느 TEAE도 실험실 테스트, ECG, 활력 징후 또는 신체 검사에서 임상적으로 유의한 이상과 관련되지 않았다. 탈력발작과 잠재적으로 관련된 TEAE는 없었다.
Claims (6)
- 불면증을 치료하는 방법으로서,
렘보렉산트(lemborexant) 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 렘보렉산트 5 mg 내지 10 mg 범위의 단회 일일 용량으로 또는 이의 약제학적으로 허용되는 염의 등가 용량으로 경구 투여하는 단계를 포함하고,
단, 환자가 차일드-푸 분류(Child-Pugh Classification) 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법. - 불면증을 치료하는 방법으로서,
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 이를 필요로 하는 환자에게 경구 투여하는 단계를 포함하고,
5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고,
용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고, 단, 환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법. - 제1항 또는 제2항에 있어서, 환자는 차일드-푸 분류 하에서 차일드-푸 클래스 C로 분류된 중증 간 손상을 갖지 않는, 방법.
- 불면증을 치료하는 방법으로서,
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에게 경구 투여하는 단계를 포함하고,
최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법. - 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 환자에서 불면증을 치료하는 방법으로서,
5 mg의 렘보렉산트 또는 등가량의 이의 약제학적으로 허용되는 염을 포함하는 투여형을 1일 1회 경구 투여하는 단계를 포함하는, 방법. - 불면증을 치료하는 방법으로서,
환자에서 차일드-푸 분류 하에서 환자의 간 손상 수준을 결정하는 단계; 및
렘보렉산트 또는 이의 약제학적으로 허용되는 염을 포함하는 투여형을 환자에게 경구 투여하는 단계를 포함하며,
5 mg 용량의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염은 계획된 기상 시간까지 적어도 7시간을 남겨둔 상태에서 취침 직전에 하룻밤 당 1회 이하로 환자에게 경구 투여되고,
환자가 간 손상을 갖지 않거나 차일드-푸 분류 하에서 차일드-푸 클래스 A로 분류된 경등도 간 손상을 갖는 경우, 용량은 임상 반응 및 내약성에 기초하여 10 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염으로 증가될 수 있고,
환자가 차일드-푸 분류 하에서 차일드-푸 클래스 B로 분류된 중등도 간 손상을 갖는 경우, 최대 용량은 1일 1회 5 mg의 렘보렉산트 또는 등가 용량의 이의 약제학적으로 허용되는 염인, 방법.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201962951638P | 2019-12-20 | 2019-12-20 | |
| US62/951,638 | 2019-12-20 | ||
| PCT/US2020/065891 WO2021127359A1 (en) | 2019-12-20 | 2020-12-18 | Use of lemborexant for treating insomnia |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220119065A true KR20220119065A (ko) | 2022-08-26 |
Family
ID=74191874
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227023903A Pending KR20220119065A (ko) | 2019-12-20 | 2020-12-18 | 불면증 치료를 위한 렘보렉산트의 용도 |
Country Status (11)
| Country | Link |
|---|---|
| US (1) | US20230051268A1 (ko) |
| EP (1) | EP4076463A1 (ko) |
| JP (2) | JP2023508011A (ko) |
| KR (1) | KR20220119065A (ko) |
| CN (1) | CN115003305A (ko) |
| AU (1) | AU2020408557A1 (ko) |
| BR (1) | BR112022012246A2 (ko) |
| CA (1) | CA3165481A1 (ko) |
| MX (1) | MX2022007304A (ko) |
| TW (1) | TW202137986A (ko) |
| WO (1) | WO2021127359A1 (ko) |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| KR20260029363A (ko) * | 2023-06-29 | 2026-03-04 | 얀센 파마슈티카 엔브이 | 셀토렉산트를 이용한 우울증 치료 방법 |
Family Cites Families (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0828751A4 (en) | 1995-05-05 | 1999-01-20 | Human Genome Sciences Inc | HUMAN NEUROPEPTIDE RECEPTOR |
| US6309854B1 (en) | 1996-12-17 | 2001-10-30 | Smithkline Beecham Corporation | Polynucleotides encoding ligands of the neuropeptide receptor HFGAN72 |
| US5935814A (en) | 1997-04-30 | 1999-08-10 | Smithkline Beecham Corporation | Polynucleotides encoding HFGAN72Y receptor |
| US6020157A (en) | 1997-04-30 | 2000-02-01 | Smithkline Beecham Corporation | Polynucleotides encoding HFGAN72X receptor |
| US6166193A (en) | 1997-07-25 | 2000-12-26 | Board Of Regents, University Of Texas System | Polynucleotides encoding MY1 receptor |
| SI2626350T1 (sl) | 2010-09-22 | 2015-09-30 | Eisai R&D Management Co., Ltd. | Spojina ciklopropana |
| RU2617696C2 (ru) | 2012-02-17 | 2017-04-26 | ЭЙСАЙ Ар ЭНД Ди МЕНЕДЖМЕНТ КО., ЛТД | Способы и соединения, которые можно использовать для синтеза антагонистов рецепторов орексина-2 |
| US10188652B2 (en) | 2014-10-23 | 2019-01-29 | Eisai R&D Management Co., Ltd. | Compositions and methods for treating insomnia |
| US20200093808A1 (en) * | 2017-01-27 | 2020-03-26 | Neurocrine Biosciences, Inc. | Methods for the Administration of Certain VMAT2 Inhibitors |
-
2020
- 2020-12-18 BR BR112022012246A patent/BR112022012246A2/pt unknown
- 2020-12-18 EP EP20842786.4A patent/EP4076463A1/en active Pending
- 2020-12-18 AU AU2020408557A patent/AU2020408557A1/en active Pending
- 2020-12-18 TW TW109145085A patent/TW202137986A/zh unknown
- 2020-12-18 JP JP2022537669A patent/JP2023508011A/ja active Pending
- 2020-12-18 CN CN202080094379.0A patent/CN115003305A/zh active Pending
- 2020-12-18 US US17/757,672 patent/US20230051268A1/en active Pending
- 2020-12-18 MX MX2022007304A patent/MX2022007304A/es unknown
- 2020-12-18 KR KR1020227023903A patent/KR20220119065A/ko active Pending
- 2020-12-18 WO PCT/US2020/065891 patent/WO2021127359A1/en not_active Ceased
- 2020-12-18 CA CA3165481A patent/CA3165481A1/en active Pending
-
2025
- 2025-08-06 JP JP2025131238A patent/JP2025160480A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| US20230051268A1 (en) | 2023-02-16 |
| JP2025160480A (ja) | 2025-10-22 |
| WO2021127359A1 (en) | 2021-06-24 |
| CN115003305A (zh) | 2022-09-02 |
| TW202137986A (zh) | 2021-10-16 |
| AU2020408557A1 (en) | 2022-08-11 |
| EP4076463A1 (en) | 2022-10-26 |
| CA3165481A1 (en) | 2021-06-24 |
| BR112022012246A2 (pt) | 2022-08-30 |
| JP2023508011A (ja) | 2023-02-28 |
| MX2022007304A (es) | 2022-08-22 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU2012328388B2 (en) | Treatment protocol of diabetes type 2 | |
| RU2703297C2 (ru) | Композиции и способы для лечения бессонницы | |
| RS61598B1 (sr) | Režimi doziranja za tretman pompeove bolesti | |
| JP2015537009A (ja) | 痛風の治療におけるブシラミンの使用 | |
| KR102165434B1 (ko) | 2형 당뇨병 및 다른 장애의 치료를 위한 glp1r 작용제 및 메트포민의 조합 및 이것들의 사용법 | |
| JP2024523945A (ja) | 血糖値の管理方法ならびに糖尿病及び関連状態の治療 | |
| CA3156436A1 (en) | Methods of treatment using an mtorc1 modulator | |
| JP2025160480A (ja) | 不眠症を治療するためのレンボレキサントの使用 | |
| AU2026201519A1 (en) | Lemborexant for treating sleep issues | |
| CN101584700A (zh) | 一种药物组合物 | |
| CN110305206A (zh) | 一类双靶点多肽化合物及其在制备治疗糖尿病和以其为特征的病症的药物中的应用 | |
| CN106619624A (zh) | 依帕司他在制备治疗高尿酸血症和痛风药物中的应用 | |
| US20160000738A1 (en) | Use of bucillamine in the treatment of gout | |
| CN104582701A (zh) | 减轻体重的方法 | |
| JPH01261331A (ja) | 急性及びアルコール中毒の治療に有用なフラクトース−1,6−二燐酸塩含有薬剤組成物 | |
| KR20230143978A (ko) | 시클로-히스프로를 유효성분으로 포함하는 당뇨병 예방 또는 치료용 약제학적 제제 | |
| CA2666846C (en) | Method of restoring the incretin effect | |
| Roy | Administration of once-daily canagliflozin to a non-diabetic patient in addition to standard aerobic exercise: a case report | |
| Sharma | Diabetes mellitus: an overview | |
| RU2304439C1 (ru) | Лекарственное средство и способ лечения сахарного диабета | |
| RU2844395C2 (ru) | Лемборексант для лечения проблем со сном | |
| WO2025189151A1 (en) | Methods and compositions for treating disorders associated with low c-peptide | |
| Islam | A review on synthesis, characterization, and pharmacological evaluation of second-line antidiabetic drugs | |
| JP6694216B2 (ja) | グレリンを有効成分として含有するレット症候群(rtt)の予防・治療剤 | |
| ELGHERDAWI et al. | EFFICACY AND SAFTEY OF METFORMIN AND COMBINATION THERAPY OF INSULIN AND METFORMIN IN TYPE 2 DIABETIC PATIENTS |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| D21 | Rejection of application intended |
Free format text: ST27 STATUS EVENT CODE: A-1-2-D10-D21-EXM-PE0902 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |