KR20220119080A - 치료용 종양-침윤 림프구들 배양을 위한 개선된 방법 - Google Patents
치료용 종양-침윤 림프구들 배양을 위한 개선된 방법 Download PDFInfo
- Publication number
- KR20220119080A KR20220119080A KR1020227024481A KR20227024481A KR20220119080A KR 20220119080 A KR20220119080 A KR 20220119080A KR 1020227024481 A KR1020227024481 A KR 1020227024481A KR 20227024481 A KR20227024481 A KR 20227024481A KR 20220119080 A KR20220119080 A KR 20220119080A
- Authority
- KR
- South Korea
- Prior art keywords
- cells
- tils
- population
- group
- cancer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
- C12N5/0638—Cytotoxic T lymphocytes [CTL] or lymphokine activated killer cells [LAK]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0634—Cells from the blood or the immune system
- C12N5/0636—T lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/14—Blood; Artificial blood
- A61K35/17—Lymphocytes; B-cells; T-cells; Natural killer cells; Interferon-activated or cytokine-activated lymphocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/10—Cellular immunotherapy characterised by the cell type used
- A61K40/11—T-cells, e.g. tumour infiltrating lymphocytes [TIL] or regulatory T [Treg] cells; Lymphokine-activated killer [LAK] cells
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K40/00—Cellular immunotherapy
- A61K40/40—Cellular immunotherapy characterised by antigens that are targeted or presented by cells of the immune system
- A61K40/41—Vertebrate antigens
- A61K40/42—Cancer antigens
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/18—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans
- C07K16/28—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants
- C07K16/2803—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily
- C07K16/2809—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from animals or humans against receptors, cell surface antigens or cell surface determinants against the immunoglobulin superfamily against the T-cell receptor (TcR)-CD3 complex
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K2239/00—Indexing codes associated with cellular immunotherapy of group A61K40/00
- A61K2239/46—Indexing codes associated with cellular immunotherapy of group A61K40/00 characterised by the cancer treated
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2302—Interleukin-2 (IL-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/231—Interleukin-10 (IL-10)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/23—Interleukins [IL]
- C12N2501/2315—Interleukin-15 (IL-15)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/20—Cytokines; Chemokines
- C12N2501/24—Interferons [IFN]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/50—Cell markers; Cell surface determinants
- C12N2501/515—CD3, T-cell receptor complex
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/998—Proteins not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/11—Coculture with; Conditioned medium produced by blood or immune system cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/11—Coculture with; Conditioned medium produced by blood or immune system cells
- C12N2502/1121—Dendritic cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2502/00—Coculture with; Conditioned medium produced by
- C12N2502/30—Coculture with; Conditioned medium produced by tumour cells
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Immunology (AREA)
- Chemical & Material Sciences (AREA)
- Engineering & Computer Science (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Biomedical Technology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Medicinal Chemistry (AREA)
- Epidemiology (AREA)
- Hematology (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Virology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Molecular Biology (AREA)
- Biophysics (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Developmental Biology & Embryology (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Peptides Or Proteins (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
Abstract
본 발명은 절제된(excised) TIL 함유(containing) 종양 단편들을 체크포인트 억제제들과 함께 공동-배양함으로써, T 세포 고갈을 되돌리는 것(revert)으로 알려진 다른 인터루킨들로 TIL들을 자극함으로써, 및/또는 조절되는 T 세포들 분비(secreted) 인자들 (예를 들어 IL-10)의 효과를 억제함으로써, 생체 외에서(in vitro) 소진된 종양 침윤 림프구들 (TIL들)을 활성화시켜, 이것에 의해 소진된(exhausted) T-세포들이 현재 확립된 TIL 확장 프로토콜들보다 더 빠르고 더 많은 수로 확장할 수 있는 유리한(favorable) 종양 미세환경(TME)을 생성하는 것을 목표로 한다.
Description
본 발명은 면역 체크포인트 억제제(Immune Checkpoint Inhibitors) (ICI들)와 같은, 종양 미세환경(Microenvironment)(TME) 자극제들와 함께 종양 단편들(fragments)을 포함하는 절제된(excised) TIL을 공동-배양함으로써 생체 외에서(in vitro) 고갈된(exhausted) 종양 침윤 림프구들 (TIL들)을 재활성화하고(reinvigorating), T 세포 고갈을 되돌리는(revert) 것으로 알려진 다른 인터루킨들(interleukins)로 TIL들을 자극하고, 및/또는 조절되는(regulatory) T 세포들 분비된(secreted) 인자들(factors) (IL-10 억제와 같은)의 효과를 억제하는 것을 목표로 하며, 따라서 고갈된(exhausted) T-세포들이 현재 확립된(established) TIL 확장 프로토콜들(protocols) 보다 더 빠르고 더 많은 수들로 확장할 수 있는 유리한(favorable) 종양 미세환경을 만든다.
종양 침윤 림프구들은 CTLA-4 및 PD-1/PD-L1에 대한(against) 면역 체크포인트 억제제(ICI들)의 사용(use)과 같은 면역요법(immunotherapy)을 겪는 암 환자들에서 개선된 예후(prognosis) 및 무진행 생존(progression free survival)과 관련이 있다.
그러나, 많은 다른 인자들이 면역 반응의 하향 조절에서 종양 미세환경과 관련된 것으로 보이기 때문에 여전히 일부(fraction) 환자들만이 이러한 치료법들(therapies)에 대해 지속적인 장기 반응(durable long-term response)을 갖는다. 주요 인자들 중 하나는 항원 특이적인 T-세포들의 물리적 제거 및/또는 기능장애(dysfunction)를 초래하는 T-세포들의 고갈인 것으로 보인다. 이러한 고갈 현상(phenomenon)과 관련된 인자들은 종양 미세환경(TME)에서 조절되는 T-세포들 및 NK 세포들로부터 분비된 종양 세포들, 림프(lymphoid) 및 단핵(mononuclear) 세포들 및 가용성(soluble) 분자들 상에서 발현되는 표면 마커들을 포함한다. 그러나, 인터페론 감마(interferon gamma) 및 IL-2와 같은 자극적인 인자들의 부족(lack)은 또한 TME에서 분명하다.
T-세포 고갈의 역전(Reversal)은 단일 요법으로 또는 이미 확립된 요법들과 조합하여 ICI들의 새로운 종류들(classes)의 개발에서 핵심 목표이다. 그러나, 이러한 표적들(targets)은 종종 자가면역 반응들(autoimmune responses)을 피하는 면역 관용(immune tolerance)을 유도하는 역할을 또한 하기 때문에, 억제제들의 전신(systemic) 투여는 심각한 부작용들을 일으킬 수 있다. 게다가, IL-2와 같은 T-세포 자극성(stimulatory) 분자들을 투여하는 것도 심각할 수 있고 그리고 때때로 치명적인 부작용들을 일으킬 수 있으며 따라서 숙련된 임상의들에 의해 관리될 필요가 있다. 약물 후보들을 종양에 국소적으로 투여하고 그러므로 전신 부작용들을 피하는 것이 가능하도록 몇몇 접근법들이 취해졌다. 그러나, 많은 전이성(metastatic) 환자들에서 암 세포들이 전신에 분포되어 있기 때문에, 이러한 상황들에서 이 접근법이 성공할 가능성은 의문시될 수 있다.
종양 침윤 림프구 (TIL) 요법의 사용은 전이성 흑색종, 두경부암 및 자궁 경부암과 같은 다양한 악성종양(malignancies) 환자들의 최대 55%의 객관적인(objective) 반응률과 최대 20%의 완전한(complete) 반응들로 상당한 임상적 이점을 보여주었다. 간단히 말해서, 이러한 종류의 치료법은 IL-2, 항-CD3 항체들 및 피더(feeder) 세포들로 절제된 종양으로부터 단편들을 초기에 자극함으로써 자가의(autologous) T 림프구들의 생체 외 확장을 활용하고(leverages) 그리고 따라서 종양의 퇴행 후 촉진되는 림프구제거 요법을 받은 환자들에게 T 세포들을 다시(back) 재-투여하기 전에 이들 세포들을 수십억으로 성장시킨다.
상기 TIL 요법은 비용이 많이 들고 시간이 걸린다. 따라서 현재 방법들을 최적화하는 것, 및 TIL들의 확장 기간을 단축하고, 확장 속도를 증가시키며, 그리고 또한 보다 유리한 표현형들(phenotypes)을 달성하는 방법들을 식별하는 것이 유리할 것이다.
본 발명은 TIL들의 치료적 집단으로 종양 침윤 림프구들 (TIL들) 확장함으로써 포유동물에서 암의 퇴행을 촉진하는 방법에 관한 것이며 다음을 포함한다: (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단(first population)을 획득함으로써 자가의 T 세포들을 배양하는 단계, (b) TIL들의 제2집단(second population)을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체들, 및 항원 제시 세포들 (APC들)을 보충함(supplementing)으로써 제2확장을 수행하는 단계, 여기서 상기 TIL들의 제3집단은 치료적 집단이고; 및 (d) 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서 상기 T 세포들은 포유동물에 투여되고, 그래서 포유동물에서 암의 퇴행이 촉진된다.
본 발명의 추가 측면은 다음을 포함하며 확장된 종양 침윤 림프구들 (TIL들)을 투여하는 것을 포함하는 암에 걸린 대상을 치료하는 방법에 관한 것이다: (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계, (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체들, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 상기 TIL들의 제3집단은 치료적 집단이고; 및 (d) 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되고, 그래서 포유동물에서 암의 퇴행이 촉진된다.
본 발명이 또 다른 측면은 다음을 포함하며 종양 침윤 림프구들 (TIL들)을 TIL들의 치료적 집단으로 확장하는 방법에 관한 것이다: (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계 (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; 및 (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체들, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 상기 TIL들의 제3집단은 치료적 집단이다.
하나 이상의 실시예들에서, 하나 이상의 TME 자극제들은 다음으로 구성되는 그룹들로부터 선택된다: T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들 (또는 그들의 리간드들) 상에 발현된 수용체들을 길항하는 것(antagonizing) 및/또는 억제하는 것(inhibiting)을 할 수 있는 물질들, T-세포 상향조절, 활성화, 및/또는 재활성화(reinvigoration)를 유발하는 것으로 알려진 T-세포들 상에 발현된 수용체들을 작용(작동)시키는 것(agonizing) 및/또는 자극하는 것(stimulating)을 할 수 있는 물질들, T-세포 하향조절, 비활성화, 및/또는 고갈(exhaustion)을 유발하는 것으로 알려진 가용성(soluble) 분자들 및 시토킨들(cytokines) 및 그들의 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들, 및 조절성(regulator) T-세포들을 하향조절하는 것(downregulating) 및/또는 감소시키는 것(depleting)을 할 수 있고 이에 따라 탈체(ex-vivo) T-세포 확장을 촉진할 수 있는(favoring) 물질들.
하나 이상의 실시예들에서, 하나 이상의 TME 자극제들은 하나 이상의 체크포인트 억제제들(checkpoint inhibitors) 또는 그들의 리간드들의 억제제들 예를 들어 항-PD1, 항-PD-L1, 항-PD-L2, 항-CTLA-4, 항-LAG3, 항-A2AR, 항-B7-H3, 항 B7-H4, 항-BTLA, 항-IDO, 항-HVEM, 항-IDO, 항-TDO, 항-KIR, 항-NOX2 , 항-TIM3, 항-갈랙틴(galectin)-9, 항-VISTA, 항-SIGLEC7/9이고, 그리고 여기서 하나 이상의 체크포인트 억제제들 또는 그들의 리간드들의 억제제들이 선택적으로 또한 제2확장에 첨가된다.
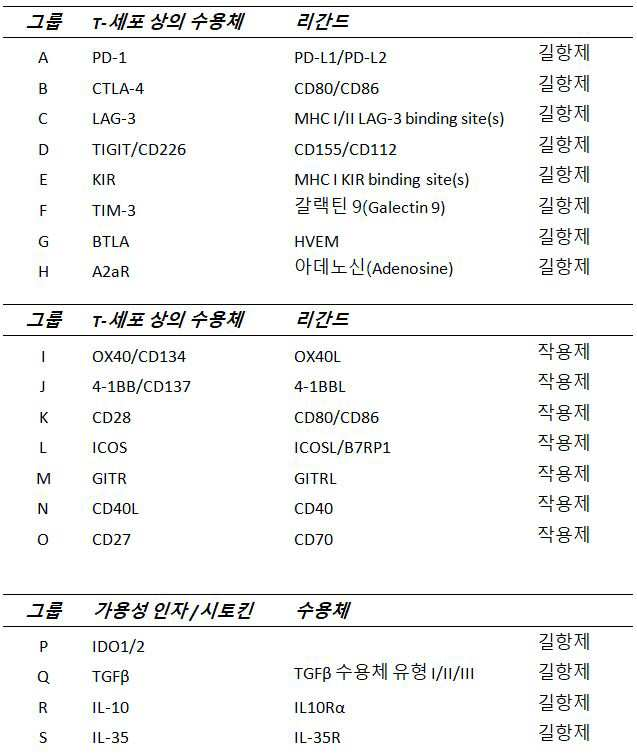
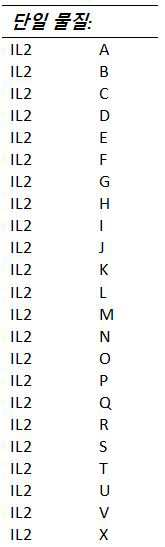
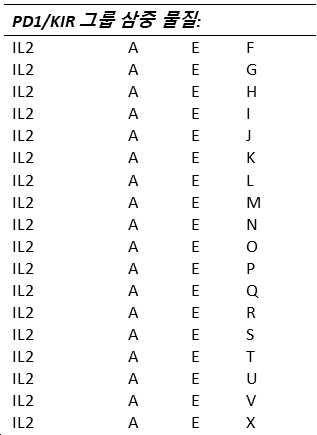
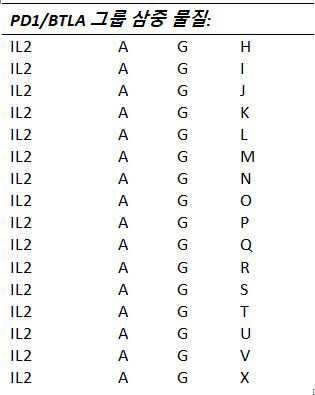
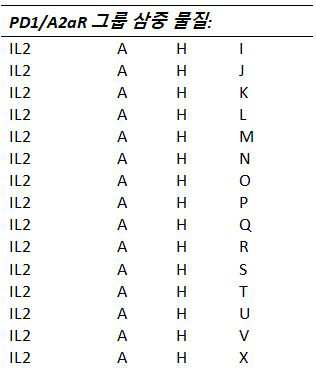
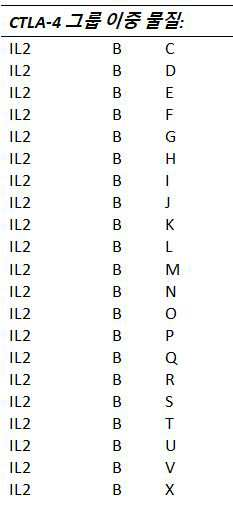
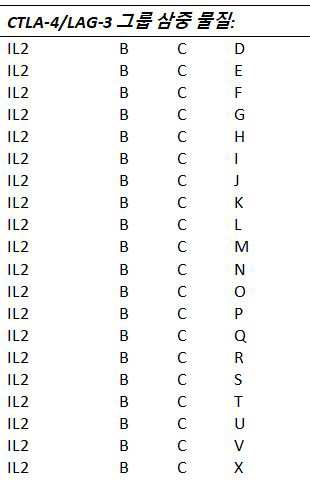
하나 이상의 실시예들에서, T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들 (또는 그들의 리간드들) 상에 발현된 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들이 다음으로 구성되는 그룹들로부터 선택된다: A: T-세포들 상의 PD-1 수용체(receptor)를 통해 작용하는(act) 물질들(substances), B: T-세포들 상의 CTLA-4 수용체를 통해 작용하는 물질들, C: T-세포들 상의 LAG-3 수용체를 통해 작용하는 물질들, D: T-세포들 상의 TIGIT/CD226 수용체를 통해 작용하는 물질들, E: T-세포들 상의 KIR 수용체를 통해 작용하는 물질들, F: T-세포들 상의 TIM-3 수용체를 통해 작용하는 물질들, G: T-세포들 상의 BTLA 수용체를 통해 작용하는 물질들, 및 H: T-세포들 상의 A2aR 수용체를 통해 작용하는 물질들.
하나 이상의 실시예들에서, 그룹 A의 물질은 펨브롤리주맙(pembrolizumab), 니볼루맙(nivolumab), 세미플리맙(cemiplimab), sym021, 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 및 더발루맙(durvalumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다.
하나 이상의 실시예들에서, 그룹 B의 물질은 이필리무맙(ipilimumab) 및 트레멜리무맙(tremelimumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 C의 물질은 렐라틀리맙(relatlimab), 에프틸라기모 알파(eftilagimo alpha), 및 sym022로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 D의 물질은 티라고루맙(tiragolumab)이다. 하나 이상의 실시예들에서, 그룹 E의 물질은 리릴루맙(lirilumab)이다. 하나 이상의 실시예들에서, 그룹 F의 물질은 sym023이다. 하나 이상의 실시예들에서, 그룹 G의 물질은 40E4 및 PJ196이다.
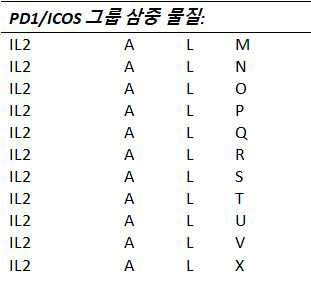
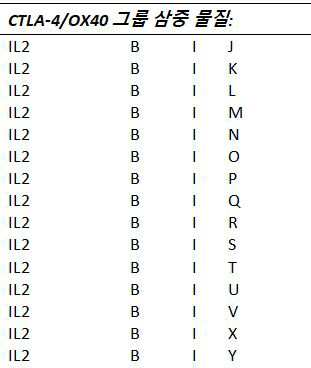
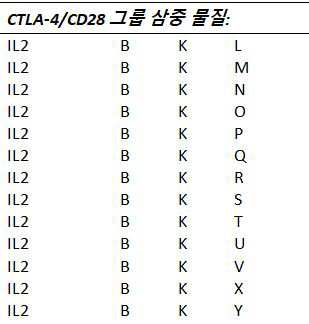
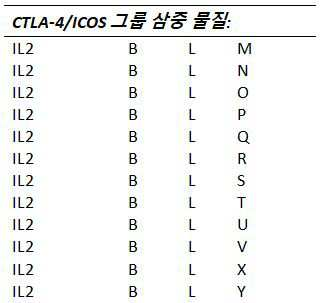
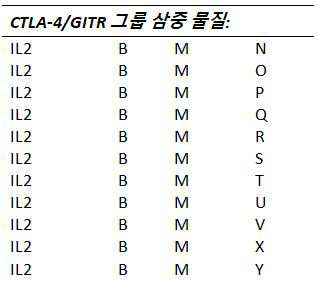
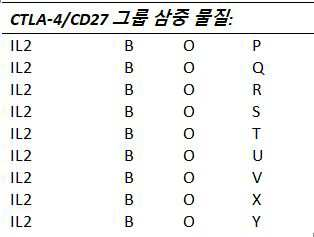
하나 이상의 실시예들에서, T-세포 상향조절, 활성화, 및/또는 재활성화(reinvigoration)를 유발하는 것으로 알려진 T-세포들 상에서 발현된 수용체들을 작용시키는 것(agonizing) 및/또는 자극하는 것을 할 수 있는 물질들은 다음으로 구성되는 그룹들로부터 선택된다: I: T-세포들 상의 OX40/CD134 수용체를 통해 작용하는 물질들, J: T-세포들 상의 4-1BB/CD137 수용체를 통해 작용하는 물질들, K: T-세포들 상의 CD28 수용체를 통해 작용하는 물질들, L: T-세포들 상의 ICOS 수용체를 통해 작용하는 물질들, M: T-세포들 상의 GITR 수용체를 통해 작용하는 물질들, N: T-세포들 상의 CD40L 수용체를 통해 작용하는 물질들, 및 O: T-세포들 상의 CD27 수용체를 통해 작용하는 물질들.
하나 이상의 실시예들에서, 그룹 J의 물질은 우렐루맙(urelumab) 및 유토밀루맙(utomilumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 K의 물질은 테랄루지맙(theraluzimab)이다. 하나 이상의 실시예들에서, 그룹 O의 물질은 발릴루맙(valilumab)이다.
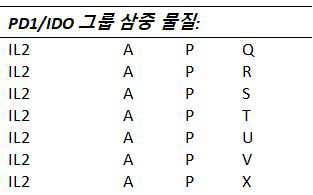
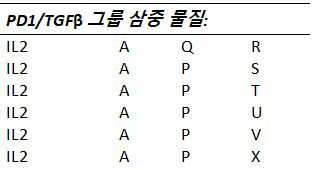
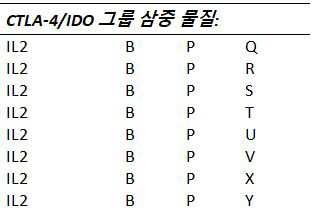
하나 이상의 실시예들에서, T-세포 하향조절, 비활성화, 및/또는 고갈을 유발하는 것으로 알려진 가용성 분자들 및 시토킨들 및 그들의 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 다음으로 구성되는 그룹들로부터 선택된다: P: T-세포들 상의 IDO1/2 수용체를 통해 작용하는 물질들, Q: T-세포들 상의 TGFβ 수용체를 통해 작용하는 물질들, R: T-세포들 상의 IL-10 수용체를 통해 작용하는 물질들, 및 S: T-세포들 상의 IL-35 수용체를 통해 작용하는 물질들.
하나 이상의 실시예들에서, 그룹 P의 물질은 에파세도스타트(epacedostat)이다. 하나 이상의 실시예들에서, 그룹 Q의 물질은 린로도스타트(linrodostat)이다. 하나 이상의 실시예들에서, 그룹 R의 물질은 갈루니서팁(galunisertib)이다.
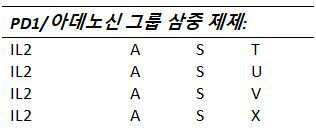
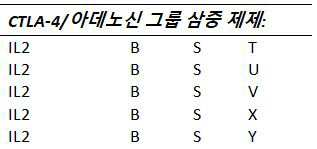
하나 이상의 실시예들에서, 조절되는 T-세포들을 하향조절하는 것(downregulating) 및/또는 감소시키는 것(depleting)을 할 수 있고 이에 따라(thereby) 탈체(ex-vivo) T-세포 확장을 촉진할 수 있는(favoring) 물질들은 다음으로 구성되는 그룹들로부터 선택된다: T: 시클로포스파미드들(cyclophosphamides), U: TKI들, V: αCD25를 통해 작용하는 물질들, 및 X: IL2/디프테리아(Diphteria) 독소(toxin) 융합들(fusions).
하나 이상의 실시예들에서, 그룹 U의 물질은 수니티닙(sunitinib)이다. 하나 이상의 실시예들에서, 그룹 V의 물질은 소라페닙(sorafenib), 이매티닙(imatinib) 및 다클리주맙(daclizumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 X의 물질은 데닐류킨 디피톡스(dinileukin diftitox)이다.
하나 이상의 실시예들에서, 물질의 농도는 0.1 g/mL 내지 300 g/mL, 예를 들어 1 g/mL 내지 100 g/mL, 예를 들어 10 g/mL 내지 100 g/mL, 예를 들어 1 g/mL 내지 10 g/mL이다.
하나 이상의 실시예들에서, T 세포들의 치료적 집단은 다음으로 구성되는 그룹들로부터 선택된 암 유형을 치료하는데 사용된다: 1: 고형(solid) 종양들, 2: ICI 나이브() 종양들, 3: MSI-H 종양들, 4: 혈액의(Hematological) 종양들, 바이러스-유발(virus-induced) 종양들, 및 5: 과-돌연변이(Hyper-mutated) 종양들 (POL-E 및 POL-D 돌연변이(mutated) 종양들과 같은).
하나 이상의 실시예들에서, T 세포들의 치료적 집단은 유방암, 신장 세포암, 방광암, 흑색종, 자궁 경부암, 위암, 결장암, 폐암, 두경부암, 난소암, 호지킨 림프종, 췌장암, 간암, 및 육종으로 구성되는 그룹들로부터 선택되는 암 유형을 치료하는데 사용된다.
하나 이상의 실시예들에서, T 세포들의 치료적 집단은 유방암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 신장 세포암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 방광암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 흑색종을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 자궁 경부암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 위암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 결장암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 폐암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 두경부암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 난소암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 호지킨 림프종을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 췌장암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 간암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 육종을 치료하는데 사용된다.
하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 20일 내지 약45일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 20일 내지 약 40일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 25일 내지 약 40일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 30일 내지 약 40일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (b)는 약 10일 내지 약 28일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (b)는 약 10일 내지 약 20일의 기간 내에 수행된다.
하나 이상의 실시예들에서, 단계 (c)는 약 12일 내지 약 18일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (c)는 약 10일 내지 약 28일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (c)는 약 10일 내지 약 20일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (c)는 약 12일 내지 약 18일의 기간 내에 수행된다.
하나 이상의 실시예들에서, 단계 (b)는 1 x 106 내지 1x 107 세포들, 예를 들어 2 x 106 내지 5x 106 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (b)는 5 x 106 내지 1x 107 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (b)는 1 x 106 내지 5x 107 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (b)는 1 x 107 내지 5x 107 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 to 1x 1012 세포들, 예를 들어 1 x 108 내지 5x 109 세포들, 예를 들어 1 x 109 내지 5x 109 세포들, 예를 들어 1 x 108 내지 5x 1010 세포들, 예를 들어 1 x 109 내지 5x 1011 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 1010 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 109 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 108 세포들을 생성한다.
하나 이상의 실시예들에서, APC는 인공의(artificial) APC들 (aAPC들) 또는 동종이계의(allogeneic) 피더 세포들이다.
하나 이상의 실시예들에서, TIL들의 치료적 집단은 환자에게 주입된다(infused).
하나 이상의 실시예들에서, 세포들은 단계 (c)를 수행하기 전에 세포 배양(cell culture)으로부터 제거되고 그리고 저장 배지(storage medium)에서 동결보존된다(cryopreserved).
하나 이상의 실시예들에서, 상기 방법은 T-세포 신호전달(signaling) 분자의 적어도 하나의 엔도도메인(endodomain)과 융합된(fused) 단일 사슬(single chain) 가변 단편(variable fragment) 항체를 포함하는 키메라(chimeric) 항원 수용체(receptor) (CAR)를 인코딩(encoding)하는 핵산(nucleic acid)을 포함하는 발현 벡터(expression vector)로 TIL들의 제1집단을 형질도입하는(transducing) 단계를 추가로 포함한다.
하나 이상의 실시예들에서, 단계 (c)는 세포 배양 배지로부터 세포들을 제거하는(removing) 단계를 추가로 포함한다.
하나 이상의 실시예들에서, 단계 (a)는 절제된 종양을 다중(multiple) 종양 단편들, 예를 들어 4 내지 50 단편들, 예를 들어 20 내지 30 단편들로 처리하는 것(processing)을 추가로 포함한다.
하나 이상의 실시예들에서, 단편들은 약 5 내지 50 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 50 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 0.1 내지 10 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 0.1 내지 1 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 0.5 내지 5 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 1 내지 10 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 1 내지 3 mm3의 크기를 갖는다.
하나 이상의 실시예들에서, 포유동물은 인간이다.
하나 이상의 실시예들에서, 세포 배양 배지는 G-Rex 용기(container) 및 Xuri 셀백(cellbag)으로 구성되는 그룹으로부터 선택된 용기에 제공된다.
한 측면은 이전 청구항들 중 어느 한 항에 따른 방법에 의해 획득할 수 있는 종양 침윤 림프구들 (TIL들)의 집단에 관한 것이다.
추가 측면은 암에 걸린 대상을 치료하는데 사용하기 위한 확장된 종양 침윤 림프구들 (TIL들)에 관한 것으로, 상기 치료는 다음 단계들을 포함한다: TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계; TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이고; 및 비골수제거 림프구제거 화학요법을 투여한 후, T 세포들의 치료적 집단을 포유동물에 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되고, 그래서 포유동물에서 암의 퇴행이 촉진된다.
추가 측면은 다음을 포함하는 방법에 의해 획득할 수 있는 종양 침윤 림프구들 (TIL들)의 집단에 관한 것이다: TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계; 및 TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3, 및 항원 제시(presenting) 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이다.
추가 측면은 IL-2 및 하나 이상의 TME 자극제들을 포함하는 TIL들의 치료적 집단에 관한 것이다.
추가 측면은 IL-2, 하나 이상의 TME 자극제들, IL-2, 항-CD3, 및 항원 제시 세포들 (APC들)을 포함하는 TIL들의 치료적 집단에 관한 것이다.
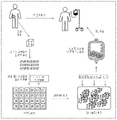
도 1은 포유동물로부터 절제된 종양 침윤 림프구들 (TIL들)을 포함하는 종양을 더 작은 단편들로 절단하고 그리고 하나 이상의 다중-웰(multi-well) 세포 배양 플레이트들(plates)에 넣는 것을 보여준다. 여기서 단편들은 TIL들의 제2집단을 생성하기 위해 제1확장 동안 인터루킨(interleukin) 2 (IL-2) 및 종양 미세환경(microenvironment)(TME) 자극제들을 포함하는 세포 배양 배지에서 배양된다(incubated). 이후, TIL들의 제2집단은 피더 세포들, 항-CD3 항체 및 IL-2를 포함하는 세포 배양 배지에서 제2(종종 급속(rapid)이라고 함)확장에서 추가로 확장된다. 제2확장은 프로토콜에 따라 달라질 수 있으며 그리고 세포 배양 장비(cell culture equipment)는 추가 하위-단계들(sub-steps)에서 하나 이상의 용기들을 사용하여 하나 이상의 단계들에서 수행되지만 단순함을 위해 도면에서 한 단계로만 설명되는 이유이다. 마지막으로, 세번째 및 TIL들의 치료적 집단을 생성하기 위해 TIL들이 수확되고 그리고 최종 TIL 생성물에 재현탁되며(resuspended), 이는 포유동물에게 다시 주입되어 암의 퇴행을 촉진한다.
도 2는 IL-2, 더발루맙 (Durva), 아벨루맙 (Avelu), 렐라틀리맙 (Relatli), 티라고루맙 (Tira), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi), 테랄리주맙(Thera), 니볼루맙 (Nivo), 또는 우렐루맙 /OKT3 (Ure)을 사용한 성공적인 세포 확장들(> 50,000 세포들/단편)의 백분율(percentage)을 보여준다.
도 3은 IL-2, 더발루맙 (Durva), 아벨루맙 (Avelu), 렐라틀리맙 (Relatli), 티라고루맙 (Tira), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi), 테랄리주맙 (Thera), 니볼루맙 (Nivo), 또는 우렐루맙 /OKT3 (Ure)을 사용한 성공적인(검은색) 세포 확장들 및 성공적이지 않은(흰색) 세포 확장들(> 50,000 세포들/단편)의 백분율(percentage)을 보여준다.
도 4는 IL-2 +/- TME-S를 사용한 성공적인 세포 확장들(> 50,000 세포들/단편)의 백분율을 보여준다. 각 그룹의 특정(specific) 자극제는 표 43을 참조한다.
도 5는 IL-2 +/- TME-S을 사용한 성공적인(검은색) 세포 확장들 및 성공적이지 않은(흰색) 세포 확장들(> 50,000 세포들/단편)의 백분율을 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다.
도 6은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 세포 배양들에 대한 총 세포 수와 확장 시간을 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 단순함(simplicity)을 위해 시각적 성장 표시 라인들(Visual growth indication lines)이 수동으로 추가되었다.
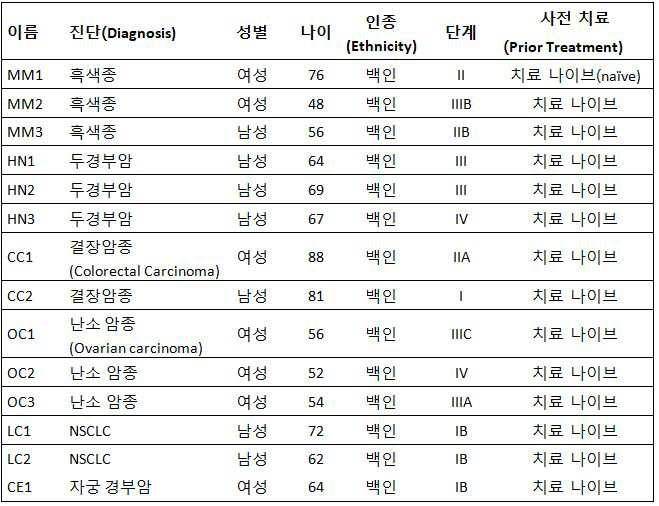
도 7은 낮은 (1 ㎍/ml), 중간(medium) (5 ㎍/ml) 및 높은 (25 ㎍/ml) 농도에서 항-CTLA-4 (이필리무맙)을 사용한 두경부암 (HN), 전이성(metastatic) 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 8은 낮은 (1 ㎍/ml), 중간 (5 ㎍/ml) 및 높은(25 ㎍/ml) 농도에서 항-PD1 (펨브롤리주맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 9는 낮은 (2 ㎍/ml) 및 중간 (10 ㎍/ml) 농도에서 OKT3 (30 ng/ml)와 함께 항-4-1BB (우렐루맙)를 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 10은 낮은 (0.02 ㎍/ml) 중간 (0.1 ㎍/ml), 높은 (2 ㎍/ml), 및 매우 높은 (2 ㎍/ml) 농도에서 항-CD28 (테랄리주맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 11은 낮은 (2 ㎍/ml), 중간 (10 ㎍/ml) 및 높은 (50 ㎍/ml) 농도에서 항-PD-L1 (아벨루맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 12는 낮은 (2 ㎍/ml), 중간 (10 ㎍/ml) 및 높은 (50 ㎍/ml) 농도에서 항-PD-1 (니볼루맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
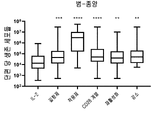
도 13은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양(incubation) 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(controls) (IL-2)과 비교하는 양측(two-tailed) Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것(non-significant)으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 14는 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들 (IL-2)과 비교하는 양측 Mann-Whitney U테스트에 의해 수행된 통계들(Statistics)이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
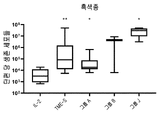
도 15는 IL-2 +/- TME-S를 포함하는G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
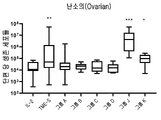
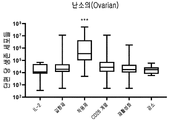
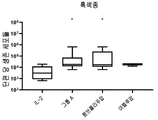
도 16은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
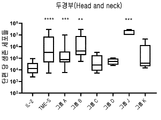
도 17은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
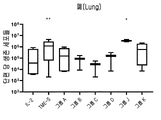
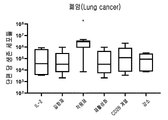
도 18은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 폐암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
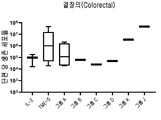
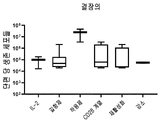
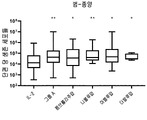
도 19는 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 결장암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 20은 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 21은 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 22는 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001 이다.
도 23은 IL-2 +/- 길항제, 작용제, CD28계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 폐암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 24는 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것 또는 감소시키는 것을 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 25는 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것 또는 감소시키는 것을 포함하는 G-Rex 플라스크에서 결장암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 26은 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것 또는 감소시키는 것을 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
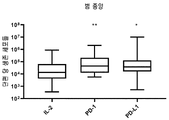
도 27은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 28은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 29는 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 30은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 폐암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
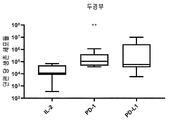
도 31은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
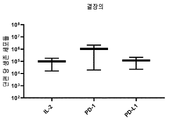
도 32는 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 결장암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
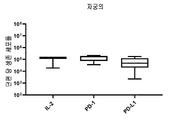
도 33은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 34는 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 35는 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 36은 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 37은 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 38은 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 39는 IL-2 +/- 그룹 A, 그룹 B, 또는 그룹 A+B를 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 40은 IL-2 +/- 우렐루맙/OKT3, 이필리무맙 (ipi), 펨브롤리주맙 (pembro)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹을 대조군들 (우렐루맙 /OKT3)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 41은 시간 지연이 있거나 없는 IL-2 +/- 우렐루맙 /OKT3, 이필리무맙 (ipi), 펨브롤리주맙 (pembro)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 42는 IL-2 + 테랄리주맙(theralizumab) 또는 IL-2 + 테랄리주맙(theralizumab), 이필리무맙(ipilimumab) (ipi) 및 펨브롤리주맙(pembrolizumab) (pembro)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 43은 IL-2 +/- TME-S를 사용하는 모든 암 유형들에 대한 성공적인 세포 확장들(> 50,000 세포들/단편)의 백분율을 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다.
도 44는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 T 세포들 (CD3+)의 빈도(frequency)를 보여준다. 사용된 자극제들은 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
도 45는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 T 세포들 (CD3+)의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 46은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 종양 단편 당 생존 T 세포들 (CD3+)의 수를 보여준다. 사용된 자극제들은 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001이다.
도 47은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 종양 단편 당 생존 T 세포들 (CD3+)의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 48은 IL-2 +/- TME-S를 사용한 CD4+ (왼쪽) 및 CD8+ (오른쪽) T 세포들의 모든 암 유형들에 대한 반응기 메모리(effector memory) T 세포들 (TEM)의 빈도를 보여준다. 사용된 자극제들은 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05이다.
도 49는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD8+ T 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 50은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 종양 단편 당 생존 CD8+ T 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 51은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD4+ T 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 52는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 NK 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 53은 OKT3 (30 ng/mL)와 함께 낮은 (2 ㎍/ml) IL-2 +/- 우렐루맙 (Ure), OKT3 (30 ng/ml)와 함께 우렐루맙 중간(medium) (10 ㎍/ml), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi)을 사용한 두경부암에 대한 T 세포들 (CD3+) 및 NK (CD3- CD56+) 세포들의 빈도들을 보여준다.
도 54는 OKT3 (30 ng/ml)와 함께 낮은 (2 ㎍/ml) IL-2 +/- 우렐루맙 (Ure), OKT3 (30 ng/ml)와 함께 우렐루맙 중간 (10 ㎍/ml), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi)을 사용한 두경부암에 대한CD8+ T 세포들의 빈도를 보여준다.
도 55는 시간 지연이 없는(흰색 막대들(bars)) 및 시간 지연이 있는(검은색 막대들) IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD3+ 세포들, NK 세포들, CD8+ 세포들, 및 CD4+ 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
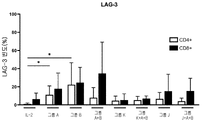
도 56은 IL-2 +/- TME-S를 사용하는 모든 암 유형들에 대한 CD4+ 세포들 (흰색 막대들) 또는 CD8+ 세포들 (검은색 막대들) 상의 LAG-3의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05이다.
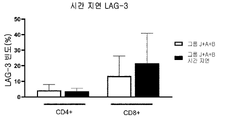
도 57은 시간 지연이 없는(흰색 막대들) 및 시간 지연이 있는(검은색 막대들) IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD4+ 세포들 또는 CD8+ 세포들 상의 LAG-3의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
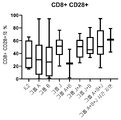
도 58은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD8+ 세포들 상의 CD28의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
도 2는 IL-2, 더발루맙 (Durva), 아벨루맙 (Avelu), 렐라틀리맙 (Relatli), 티라고루맙 (Tira), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi), 테랄리주맙(Thera), 니볼루맙 (Nivo), 또는 우렐루맙 /OKT3 (Ure)을 사용한 성공적인 세포 확장들(> 50,000 세포들/단편)의 백분율(percentage)을 보여준다.
도 3은 IL-2, 더발루맙 (Durva), 아벨루맙 (Avelu), 렐라틀리맙 (Relatli), 티라고루맙 (Tira), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi), 테랄리주맙 (Thera), 니볼루맙 (Nivo), 또는 우렐루맙 /OKT3 (Ure)을 사용한 성공적인(검은색) 세포 확장들 및 성공적이지 않은(흰색) 세포 확장들(> 50,000 세포들/단편)의 백분율(percentage)을 보여준다.
도 4는 IL-2 +/- TME-S를 사용한 성공적인 세포 확장들(> 50,000 세포들/단편)의 백분율을 보여준다. 각 그룹의 특정(specific) 자극제는 표 43을 참조한다.
도 5는 IL-2 +/- TME-S을 사용한 성공적인(검은색) 세포 확장들 및 성공적이지 않은(흰색) 세포 확장들(> 50,000 세포들/단편)의 백분율을 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다.
도 6은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 세포 배양들에 대한 총 세포 수와 확장 시간을 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 단순함(simplicity)을 위해 시각적 성장 표시 라인들(Visual growth indication lines)이 수동으로 추가되었다.
도 7은 낮은 (1 ㎍/ml), 중간(medium) (5 ㎍/ml) 및 높은 (25 ㎍/ml) 농도에서 항-CTLA-4 (이필리무맙)을 사용한 두경부암 (HN), 전이성(metastatic) 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 8은 낮은 (1 ㎍/ml), 중간 (5 ㎍/ml) 및 높은(25 ㎍/ml) 농도에서 항-PD1 (펨브롤리주맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 9는 낮은 (2 ㎍/ml) 및 중간 (10 ㎍/ml) 농도에서 OKT3 (30 ng/ml)와 함께 항-4-1BB (우렐루맙)를 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 10은 낮은 (0.02 ㎍/ml) 중간 (0.1 ㎍/ml), 높은 (2 ㎍/ml), 및 매우 높은 (2 ㎍/ml) 농도에서 항-CD28 (테랄리주맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 11은 낮은 (2 ㎍/ml), 중간 (10 ㎍/ml) 및 높은 (50 ㎍/ml) 농도에서 항-PD-L1 (아벨루맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 12는 낮은 (2 ㎍/ml), 중간 (10 ㎍/ml) 및 높은 (50 ㎍/ml) 농도에서 항-PD-1 (니볼루맙)을 사용한 두경부암 (HN), 전이성 흑색종 (MM) 및 난소암 (OC)으로부터 세포 확장에 대한 총 세포 수를 보여준다.
도 13은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양(incubation) 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(controls) (IL-2)과 비교하는 양측(two-tailed) Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것(non-significant)으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 14는 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들 (IL-2)과 비교하는 양측 Mann-Whitney U테스트에 의해 수행된 통계들(Statistics)이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 15는 IL-2 +/- TME-S를 포함하는G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 16은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 17은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 18은 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 폐암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 19는 IL-2 +/- TME-S를 포함하는 G-Rex 플라스크에서 결장암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 20은 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 21은 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 22는 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001 이다.
도 23은 IL-2 +/- 길항제, 작용제, CD28계열, 치료를 재활성화하는 것(reinvigorating) 또는 감소시키는 것(depleting)을 포함하는 G-Rex 플라스크에서 폐암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 24는 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것 또는 감소시키는 것을 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 25는 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것 또는 감소시키는 것을 포함하는 G-Rex 플라스크에서 결장암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 26은 IL-2 +/- 길항제, 작용제, CD28 계열, 치료를 재활성화하는 것 또는 감소시키는 것을 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 44를 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 27은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 28은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 29는 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 30은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 폐암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 31은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 32는 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 결장암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 33은 IL-2 +/- PD-1, PD-L1을 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 34는 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 35는 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 난소암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 36은 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 흑색종으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 37은 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 두경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 38은 IL-2 +/- 그룹 A, 펨브롤리주맙, 니볼루맙, 더발루맙, 아벨루맙을 포함하는 G-Rex 플라스크에서 자궁 경부암으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 39는 IL-2 +/- 그룹 A, 그룹 B, 또는 그룹 A+B를 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 각 그룹을 대조군들(IL-2)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 40은 IL-2 +/- 우렐루맙/OKT3, 이필리무맙 (ipi), 펨브롤리주맙 (pembro)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 각 그룹을 대조군들 (우렐루맙 /OKT3)과 비교하는 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 41은 시간 지연이 있거나 없는 IL-2 +/- 우렐루맙 /OKT3, 이필리무맙 (ipi), 펨브롤리주맙 (pembro)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 42는 IL-2 + 테랄리주맙(theralizumab) 또는 IL-2 + 테랄리주맙(theralizumab), 이필리무맙(ipilimumab) (ipi) 및 펨브롤리주맙(pembrolizumab) (pembro)을 포함하는 G-Rex 플라스크에서 임의의 암 유형으로부터 종양 조직의 배양 후 단편 당 생존 세포들의 수를 보여준다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 43은 IL-2 +/- TME-S를 사용하는 모든 암 유형들에 대한 성공적인 세포 확장들(> 50,000 세포들/단편)의 백분율을 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다.
도 44는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 T 세포들 (CD3+)의 빈도(frequency)를 보여준다. 사용된 자극제들은 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
도 45는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 T 세포들 (CD3+)의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 46은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 종양 단편 당 생존 T 세포들 (CD3+)의 수를 보여준다. 사용된 자극제들은 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001이다.
도 47은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 종양 단편 당 생존 T 세포들 (CD3+)의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 48은 IL-2 +/- TME-S를 사용한 CD4+ (왼쪽) 및 CD8+ (오른쪽) T 세포들의 모든 암 유형들에 대한 반응기 메모리(effector memory) T 세포들 (TEM)의 빈도를 보여준다. 사용된 자극제들은 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05이다.
도 49는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD8+ T 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 50은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 종양 단편 당 생존 CD8+ T 세포들의 수를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01, ***p<0.001, ****p<0.0001이다.
도 51은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD4+ T 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 52는 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 NK 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05, **p<0.01이다.
도 53은 OKT3 (30 ng/mL)와 함께 낮은 (2 ㎍/ml) IL-2 +/- 우렐루맙 (Ure), OKT3 (30 ng/ml)와 함께 우렐루맙 중간(medium) (10 ㎍/ml), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi)을 사용한 두경부암에 대한 T 세포들 (CD3+) 및 NK (CD3- CD56+) 세포들의 빈도들을 보여준다.
도 54는 OKT3 (30 ng/ml)와 함께 낮은 (2 ㎍/ml) IL-2 +/- 우렐루맙 (Ure), OKT3 (30 ng/ml)와 함께 우렐루맙 중간 (10 ㎍/ml), 펨브롤리주맙 (Pembro), 이필리무맙 (Ipi)을 사용한 두경부암에 대한CD8+ T 세포들의 빈도를 보여준다.
도 55는 시간 지연이 없는(흰색 막대들(bars)) 및 시간 지연이 있는(검은색 막대들) IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD3+ 세포들, NK 세포들, CD8+ 세포들, 및 CD4+ 세포들의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
도 56은 IL-2 +/- TME-S를 사용하는 모든 암 유형들에 대한 CD4+ 세포들 (흰색 막대들) 또는 CD8+ 세포들 (검은색 막대들) 상의 LAG-3의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었으며, *p<0.05이다.
도 57은 시간 지연이 없는(흰색 막대들) 및 시간 지연이 있는(검은색 막대들) IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD4+ 세포들 또는 CD8+ 세포들 상의 LAG-3의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
도 58은 IL-2 +/- TME-S를 사용한 모든 암 유형들에 대한 CD8+ 세포들 상의 CD28의 빈도를 보여준다. 각 그룹의 특정 자극제는 표 43을 참조한다. 양측 Mann-Whitney U 테스트에 의해 수행된 통계들이다. p>0.05 는 의미-없는 것으로 간주되었다.
본 발명은 예를 들어 체크포인트 억제제들과 함께 종양 단편들을 포함하는 절제된(excised) TIL을 공동-배양함으로써, T 세포 고갈을 되돌리는 것으로 알려진 다른 인터루킨들로 TIL들을 자극함으로써, 및/또는 조절되는 T 세포들 분비된(secreted) 인자들(예를 들어 IL-10)의 효과를 억제함으로써생체 외에서(in vitro)에서 고갈된 종양 침윤 림프구들 (TIL들)을 재활성화하고, 이에 따라 고갈된 T-세포들이 현재 확립된 TIL 확장 프로토콜들보다 더 빠르고 더 많은 수들로 확장할 수 있는 유리한(favorable) TME를 만드는 것을 목표로 한다.
이 접근법은 생체 외에서의 자극이 생체 내에서(in vivo) 허용되는 것보다 훨씬 높은 용량(dose) 수준들(levels)을 사용하여 수행될 수 있기 때문에 전신적으로 투여된 용법들에 유리할 수 있다. 예를 들어, 현재 TIL 프로토콜들은 3-6,000 IU 당(per) mL의 농도에서 IL-2을 사용하며(utilizes), 이는 전신의 권장 용량보다 5-10배 더 높다.
또한, 종양 항원들에 대한 친화도(affinity)가 높은 T 세포들은 고갈되는데(exhausted) 증가하는 경향이 있을 수 있으며, 표적화된(targeted) 인-비트로 재활성화는 친화력이 더 높은 T 세포 클론들을 확장하는데 도움이 될 수 있으며, 상기 클론들은 그들이 존재하는(residing) 종양을 더욱 공격적으로 표적화(target)할 수 있으며 이에 따라 결국 TIL 요법에 대한 이 새로운 접근의 개선된 임상 결과(clinical outcome)로 이어질 수 있다.
따라서, 본 발명은 종양 침윤 림프구들 (TIL들)을 TIL들의 치료적 집단으로 확장함으로써 포유동물에서 암의 퇴행을 촉진하는 방법에 관한 것이며, 다음을 포함한다: (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계, (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, TIL들의 제3집단은 치료적 집단이며; 및 (d) 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, T 세포들이 포유동물에 투여되고, 그래서 포유동물에서 암의 퇴행이 촉진된다.
본 발명에서 "종양 침윤 림프구들" 또는 "TIL들"은 대상(subject)의 혈류(bloodstream)를 떠나 종양으로 이동한(migrated) 백혈구들(white blood cells)로서 원래 얻어진 세포들의 집단을 의미한다. TIL들은 CD8+ 세포독소(cytotoxic) T 세포들 (림프구들), Th1 및 Th17 CD4+ T 세포들 (CD4+ 보조(helper) 세포들), 자연 살해(natural killer) 세포들, 수상(dendritic) 세포들 및 Ml 대식세포들(macrophages)을 포함하지만, 이에 제한되는 것은 아니다. TIL들 기본적인(primary) 및 이차적인(secondary) TIL들을 모두 포함한다. "기본적인 TIL들"은 본 발명에 개략된 바와 같은 환자 조직 샘플들로부터 얻은 것들이고(때때로 “신선하게 수확된(freshly harvested)"르로 지칭됨), 그리고 "이차적인 TIL들"은 본 발명에 논의된 바와 같이 확장되거나 급증된(proliferated) 임의의 TIL 세포 집단들이다. TIL들은 일반적으로 세포 표면 마커들(cell surface markers)을 사용하여, 생화학적으로 정의될 수 있거나, 종양들에 침윤하여(infiltrate) 치료에 영향을 미치는 그들의 능력에 의해, 기능적으로 정의될 수 있다. TIL들은 일반적으로 다음 바이오마커들(biomarkers) 중에서 하나 이상을 발현하여 분류될 (categorized) 수 있다: CD4, CD8, TCR ab, CD27, CD28, CD56, CCR7, CD45Ra, CD95, PD-1, 및 CD25. 추가적으로, 및 대안적으로(alternatively), TIL들은 환자에게 재도입(reintroduction) 시 고형 종양들을 침윤하는 그들의 능력에 의해 기능적으로 정의될 수 있다. TIL들은 추가로 효능(potency)에 의해 특성화될 수 있고-예를 들어, TIL들은 강력한(potent) 것으로 간주될 수 있으며, 예를 들어, 인터페론 (IFN) 방출(release)은 약 50 pg/mL 초과, 약100 pg/mL 초과, 약 150 pg/mL 초과, 또는 약 200 pg/mL 초과인 경우이다.
본 발명의 추가 측면은 다음을 포함하는 확장된 종양 침윤 림프구들 (TIL들)을 투여하는 것을 포함하는 암에 걸린 대상을 치료하는 방법에 관한 것이다: (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계, (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이고; 및 (d) 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서T 세포들은 포유동물에 투여되며, 그래서 포유동물에서 암의 퇴행이 촉진된다.
용어들 "치료(treatment)", "치료하는(treating)", "치료하다(treat)" 등은 원하는 약리학적(pharmacologic) 및/또는 생리학적(physiologic) 효과를 얻는 것을 의미한다. 상기 효과는 질병 또는 이의 증상을 완전히 또는 부분적으로 예방하는 점에서 예방적일(prophylactic) 수 있고, 및/또는 질병 및/또는 질병에 기인하는 부작용의 부분적 또는 완전한 치료의 관점에서 치료적(therapeutic)일 수 있다. 본 발명에 사용된 "치료(Treatment)"는, 포유동물, 특히 인간의 일병의 모든 치료를 포괄하며(covers), 다음을 포함한다: (a) 질병에 걸리기 쉬우나(predisposed) 아직 진단되지 않은 대상에서 발생하는 질병을 예방하는 단계; (b) 질병을 억제하는 단계, 예를 들어, 그것의 발달 또는 진행(progression)을 막는 것(arresting); 및 (c) 질병을 완화시키는 단계(relieving), 예를 들어, 질병의 퇴행을 유발하거나 및/또는 하나 이상의 질병 증상을 완화시키는 것. "치료"는 또한 질병 또는 상태(condition)가 없는 경우에도, 약리학적 효과를 제공하기 위해 제제(agent)의 전달을 포함하는(encompass) 것을 의미한다. 예를 들어, "치료"는 예를 들어, 백신의 경우와 같이, 질병 상태의 부재 하에 면역 반응을 유도하거나(elicit) 또는 면역을 부여할(confer immunity) 수 있는 조성물의 전달을 포함한다(encompasses).
용어 "항-CD3 항체"는 항체 또는 그의 변이체(variant), 예를 들어, 단일클론(monoclonal) 항체 및 성숙(mature) T 세포들의 T 세포 항원 수용체에서 CD3 수용체에 대해(against) 지시되는 인간, 인간화(humanized), 키메라(chimeric) 또는 뮤린(murine) 항체들을 포함하는 항체를 지칭한다. 항-CD3 항체들은 무로모나브(muromonab)로도 알려진, OKT3을 포함한다. 항-CD3 항체들은 또한 T3 및 CD3e으로도 알려진, UHCT1 클론(clone)을 포함한다. 다른 항-CD3 항체들은 예를 들어, 오텔릭시주마브(otelixizumab), 테플리주맙(teplizumab), 및 비실리주맙(visilizumab)을 포함한다. 실시예에서, 세포 배양 배지는 OKT3 항체를 포함한다. 일부 실시예들에서, 세포 배양 배지는 약 30 ng/mL의 OKT3 항체를 포함한다.
실시예에서, 세포 배양 배지는 약 0.1 ng/mL, 약 0.5 ng/mL, 약 1 ng/mL, 약 2.5 ng/mL, 약 5 ng/mL, 약 7.5 ng/mL, 약 10 ng/mL, 약 15 ng/mL, 약 20 ng/mL, 약 25 ng/mL, 약 30 ng/mL, 약 35 ng/mL, 약 40 ng/mL, 약 50 ng/mL, 약 60 ng/mL, 약 70 ng/mL, 약 80 ng/mL, 약 90 ng/mL, 약 100 ng/mL, 약 200 ng/mL, 약 500 ng/mL, 및 약 1 pg/mL의 OKT3 항체를 포함한다. 실시예에서, 세포 배양 배지는 0.1 ng/mL 내지 1 ng/mL, 1 ng/mL 내지 5 ng/mL, 5 ng/mL 내지 10 ng/mL, 10 ng/mL 내지 20 ng/mL, 20 ng/mL 내지 30 ng/mL, 30 ng/mL 내지 40 ng/mL, 40 ng/mL 내지 50 ng/mL, 및 50 ng/mL 내지 100 ng/mL의 OKT3 항체를 포함한다. 일부 실시예들에서, 세포 배양 배지는 OKT3 항체를 포함하지 않는다.
용어 "IL-2"(본 발명에서 "IL2"라고도 함)는 인터루킨-2(interleukin-2)로 알려진 T세포 성장 인자를 지칭하며, 인간 및 포유동물 형태들(mammalian forms), 보존적 아미노산 치환들(conservative amino acid substitutions), 당사슬들(glycoforms), 바이오시밀러들(biosimilars), 및 이의 변이체들을 포함하는 IL-2의 모든 형태들을 포함한다.
종양 단편들의 제조(preparation) 후, 생성된 세포들 (즉, 단편들)은 종양 및 다른 세포들에 비해(over) TIL들의 성장을 선호하는(favor) 조건들 하에 IL-2를 포함하는 배지(media)에서 배양된다. 일부 실시예들에서, 종양 소화물들(digests)은 IL-2의 6000 IU/mL 와 함께 비활성화된 인간 AB 혈청(serum)(또는, 일부 경우에, 본 발명에 요약된 바와 같이, aAPC 세포 집단의 존재 하에)을 포함하는 배지에서 2 mL 웰들(wells)에서 배양된다(incubated). 이 기본적인(primary) 세포 집단은 일반적으로 6 내지 14일의 기간 동안 배양되어, 벌크 TIL 집단, 일반적으로 약 1 x 106 내지 1 x 108 벌크 TIL 세포들을 생성한다. 일부 실시예들에서, 제1확장 동안의 성장 배지는 IL-2 또는 그의 변이체를 포함한다. 일부 실시예들에서, IL은 재조합(recombinant) 인간 IL-2 (rhIL-2)이다. 일부 실시예들에서 IL-2 원액(stock solution)은1mg 바이알에 대해20-30 x 106 IU/mg의 비활성(specific activity)을 갖는다. 일부 실시예들에서 IL-2 원액은 1mg 바이알에 대해 20 x 106 IU/mg의 비활성을 갖는다. 일부 실시예들에서 IL-2 원액은1mg 바이알에 대해 25 x 106 IU/mg의 비활성을 갖는다. 일부 실시예들에서 IL-2 원액은1mg 바이알에 대해 30x 106 IU/mg의 비활성을 갖는다. 일부 실시예들에서, IL- 2 원액은 IL-2의 4-8 x 106 IU/mg의 최종 농도를 갖는다. 일부 실시예들에서, IL- 2 원액은 IL-2의 5-7x 106 IU/mg의 최종 농도를 갖는다. 일부 실시예들에서, IL- 2 원액은 IL-2의 6 x 106 IU/mg의 최종 농도를 갖는다. 일부 실시예들에서, IL-2 원액은 실시예들에 기재된 바와 같이 제조된다. 일부 실시예들에서, 제1확장 배양 배지는 약 10,000 IU/mL의 IL-2, 약 9,000 IU/mL의 IL-2, 약 8,000 IU/mL의 IL-2, 약 7,000 IU/mL의 IL-2, 약 6000 IU/mL의 IL-2 또는 약 5,000 IU/mL의 IL-2를 포함한다. 일부 실시예들에서, 제1확장 배양 배지는 약 9,000 IU/mL의 IL-2 내지 약 5,000 IU/mL의 IL-2를 포함한다. 일부 실시예들에서, 제1확장 배양 배지는 약 8,000 IU/mL의 IL-2 내지 약 6,000 IU/mL의 IL-2를 포함한다. 일부 실시예들에서, 제1확장 배양 배지는 약 7,000 IU/mL의 IL-2 내지 약 6,000 IU/mL의 IL-2를 포함한다. 일부 실시예들에서, 제1확장 배양 배지는 약 6,000 IU/mL의 IL-2를 포함한다. 실시예에서, 세포 배양 배지는 추가로 IL-2를 포함한다. 일부 실시예들에서, 세포 배양 배지는 약 3000 IU/mL의 IL-2를 포함한다. 실시예에서, 세포 배양 배지는 추가로 IL-2를 포함한다. 바람직한 실시예에서, 세포 배양 배지는 약 3000 IU/mL의 IL-2를 포함한다. 실시예에서, 세포 배양 배지는 약 1000 IU/mL, 약 1500 IU/mL, 약 2000 IU/mL, 약 2500 IU/mL, 약 3000 IU/mL, 약 3500 IU/mL, 약 4000 IU/mL, 약 4500 IU/mL, 약 5000 IU/mL, 약 5500 IU/mL, 약 6000 IU/mL, 약 6500 IU/mL, 약 7000 IU/mL, 약 7500 IU/mL, 또는 약 8000 IU/mL의 IL-2를 포함한다. 실시예에서, 세포 배양 배지는 comprises 1000 내지 2000 IU/mL, 2000 내지 3000 IU/mL, 3000 내지 4000 IU/mL, 4000 내지 5000 IU/mL, 5000 내지 6000 IU/mL, 6000 내지 7000 IU/mL, 7000 내지 8000 IU/mL, 또는 약 8000 IU/mL의 IL-2를 포함한다.
IL-4, IL-7, IL-15 및/또는 IL-21은 또한 본 방법들의 단계 (b) 및/또는 (c)에 추가될 수 있다. 용어 "IL-4"(본 발명에서 "IL4"라고도 지칭됨)는 Th2 T 세포들에 의해 생성되고, 그리고 호산구들(eosinophils), 호염기구들(basophils), 및 비만(mast) 세포들에 의해 생성되는, 인터루킨 4로 알려진 시토킨(cytokine)을 지칭한다. IL-4는 순진한 헬퍼(naive helper) T 세포들 (ThO 세포들)의 Th2 T 세포들로의 분화(differentiation)를 조절한다(regulates). 용어 "IL-7"(본 발명에서 "IL7"라고도 지칭됨)은 기질의(stromal) 및 상피의(epithelial) 세포들뿐만 아니라, 수상(dendritic) 세포들로부터 획득될 수 있는 인터루킨 7로 알려진 글리코실화된(glycosylated) 조직-유래 시토킨을 지칭한다. 용어 "IL-15"(본 발명에서 "IL15"라고도 함)는 인터루킨-15로 알려진 T 세포 성장 인자를 지칭하며, 인간 및 포유동물 형태들, 보존적 아미노산 치환들, 당사슬들(glycoforms), 바이오시밀러들(biosimilars), 및 이의 변이체들을 포함하는 IL-2의 모든 형태들을 포함한다. 용어 "IL-21"(본 발명에서 "IL21"라고도 함)은 인터루킨-21로 알려진 다면 발현성의(pleiotropic) 시토킨 단백질을 지칭하며, 그리고 인간 및 포유동물 형태들, 보존적 아미노산 치환들, 당사슬들(glycoforms), 바이오시밀러들(biosimilars), 및 이의 변이체들을 포함하는 IL-21의 모든 형태들을 포함한다.
본 발명의 또 다른 측면은 다음을 포함하는 종양 침윤 림프구들 (TIL들)을 TIL들의 치료적 집단으로 확장하는 방법에 관한 것이다: (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계 (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; 및 (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서TIL들의 제3집단은 치료적 집단이다.
실험적인 결과는, 림프구제거(lymphodepletion) 종양-특이적(specific) T 림프구들의 입양 이전(adoptive transfer) 전 림프구제거(lymphodepletion)는 조절되는(regulatory) T 세포들 및 면역 시스템의 경쟁 요소들(competing elements) ("시토킨 싱크들(cytokine sinks)"을 제거함으로써 치료 효능을 강화하는데 중요한 역할을 한다는 것을 나타낸다. 따라서, 본 발명의 일부 실시예들은 본 발명의 TIL들의 도입(introduction) 전에 환자에 대한 림프구제거 단계(때때로 "면역억제성의 조건(immunosuppressive conditioning)"으로 지칭됨)를 이용한다.
단계 (a) 내지 단계 (c)로부터, 본 발명의 방법들은 폐쇄형(closed) 시스템에서 수행될 수 있다. 용어 "폐쇄형 시스템"은 외부 환경에 대해 폐쇄된 시스템을 의미한다. 세포 배양 방법들에 대한 적합한 폐쇄형 시스템은 본 발명의 방법들과 함께 사용될 수 있다. 폐쇄형 시스템은 예를 들어, 폐쇄형(closed) G-용기들(G-containers)을 포함하지만, 이에 제한되는 것은 아니다. 일단 종양 세그먼트(segment)가 폐쇄형 시스템에 추가되면, TIL들이 환자에게 투여될 준비가 될 때까지 시스템은 외부 환경에 개방되지 않는다.
용어 "TME 자극제들(stimulators)"은 고갈된(exhausted) T-세포들은 여러 배 확장하고(many fold) 그리고 그들의 항-종양을 기능적으로 회복하기 위해 재활성화될 수 있는(reinvigorated) 종양 내에서 유리한(favorable) 미세환경을 생성하는 능력을 갖는 물질들(또는 제제들(agents))에 관한 것이다. 따라서, 하나 이상의 실시예들에서, 하나 이상의 TME 자극제들은 다음으로 구성되는 그룹들로부터 선택된다: (x) T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들 (또는 그들의 리간드들) 상에서 발현되는 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 하나 이상의 물질들, (y) T-세포 상향조절, 활성화, 및/또는 재활성화를 유발하는 것으로 알려진 T-세포들 상에서 발현되는 수용체들을 작용시키는 것(agonizing) 및/또는 자극하는 것을 할 수 있는 하나 이상의 물질들, (z) T-세포 하향조절, 비활성화, 및/또는 고갈을 유발하는 것으로 알려진 그들의 수용체들 및 가용성(soluble) 분자들 및 시토킨들(cytokines)을 길항하는 것 및/또는 억제하는 것을 할 수 있는 하나 이상의 물질들, 및 (v) 조절성(regulatory) T-세포들을 하향조절하는 것 및/또는 감소시키는 것(depleting)을 할 수 있고 이에 따라 탈체(ex-vivo) 반응기(effector) T-세포 확장을 촉진할(favoring) 수 있는 하나 이상의 물질들, 및 (w) 그룹들 (x), (y), (z) 및/또는 (v)로부터 하나 이상의 물질들. 그룹 (w)는 (x), (y), (z) 및/또는 (v)로부터 물질들 중 1개, 2개 또는 3개일 수 있다. 하나 이상의 실시예들에서, (w)는 (x)로부터 물질들 중 1개 또는 2개이다. 하나 이상의 실시예들에서, (w)는 (y)로부터 물질들 중 1개 또는 2개이다. 하나 이상의 실시예들에서, (w)는 (z)로부터 물질들 중 1개 또는 2개이다. 하나 이상의 실시예들에서, (w)는 (v)로부터 물질들 중 1개 또는 2개이다. (w)는 표들 2-41 및 43-44에 나열된 표 1의 물질들 중 임의의 조합들일 수 있다.
이들은 본 방법들의 단계 (b) 및/또는 단계 (c)에 추가될 수 있으며, 그들이 초기 확장에만 필요한 경우 2, 4, 6 또는 그 이상 일(more days) 후에 확장 중에 제거될 수 있다. 그들은 세포 배양을 세척하여 제거될 수 있다. 개별(individual) TME 자극제들은 함께 추가되거나 또는 시간 경과에 따라(in time lapse), 즉, 하루 간격으로, 또는 예를 들어 2, 3, 4, 5, 6 또는 7 일 간격으로 추가될 수 있다.
하나 이상의 실시예들에서, 하나 이상의 TME 자극제들은 하나 이상의 체크포인트 억제제들 또는 그들의 리간드들 예를 들어 항-PD1, 항-PD-L1, 항-PD-L2, 항-CTLA-4, 항-LAG3, 항-A2AR, 항-B7-H3, 항 B7-H4, 항-BTLA, 항-IDO, 항-HVEM, 항-IDO, 항-TDO, 항-KIR, 항-NOX2, 항-TIM3, 항-갈랙틴(galectin)-9, 항-VISTA, 항-SIGLEC7/9의 억제제들이며, 그리고 하나 이상의 체크포인트 억제제들 또는 그들의 리간드들의 억제제들은 선택적으로 또한 제2확장에 추가된다.
하나 이상의 실시예들에서, T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들 (또는 그들의 리간드들) 상에 발현된 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 다음으로 구성되는 그룹들로부터 선택된다: A: T-세포들 상의 PD-1 수용체를 통해 작용하는 물질들, B: T-세포들 상의 CTLA-4 수용체를 통해 작용하는 물질들, C: T-세포들 상의 LAG-3 수용체를 통해 작용하는 물질들, D: T-세포들 상의 TIGIT/CD226 수용체를 통해 작용하는 물질들, E: T-세포들 상의 KIR 수용체를 통해 작용하는 물질들, F: T-세포들 상의 TIM-3 수용체를 통해 작용하는 물질들, G: T-세포들 상의 BTLA 수용체를 통해 작용하는 물질들, 및 H: T-세포들 상의 A2aR 수용체를 통해 작용하는 물질들. 주어진 수용체를 통해 작용하는 물질들의 정의는 또한 동일한 수용체들 리간드를 포함할 수 있음을 이해해야 한다. 이것은 예를 들어, PD-1 수용체의 경우 PD-L1 또는 PD-L2를 표적으로 하는 물질들도 포함할(covered) 수 있음을 의미한다. 따라서 그룹 A는 T-세포들 상의 PD-1 수용체뿐만 아니라 그것의 리간드(들)을 통해 작용하는 물질들을 포함할 수 있다.
하나 이상의 실시예들에서, 그룹 A의 물질은 펨브롤리주맙(pembrolizumab), 니볼루맙(nivolumab), 세미플리맙(cemiplimab), sym021, 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 및 더발루맙(durvalumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 A의 물질은 펨브롤리주맙이다. 하나 이상의 실시예들에서, 그룹 A의 물질은 니볼루맙이다. 하나 이상의 실시예들에서, 그룹 A의 물질은 세미플리맙이다. 하나 이상의 실시예들에서, 그룹 A의 물질은 sym021이다. 하나 이상의 실시예들에서, 그룹 A의 물질은 아테졸리주맙이다. 하나 이상의 실시예들에서, 그룹 A의 물질은 아벨루맙이다. 하나 이상의 실시예들에서, 그룹 A의 물질은 더발루맙이다.
하나 이상의 실시예들에서, 그룹 B의 물질은 이필리무맙(ipilimumab) 및 트레멜리무맙(tremelimumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 B의 물질은 이필리무맙이다. 하나 이상의 실시예들에서, 그룹 B의 물질은 트레멜리무맙이다. 하나 이상의 실시예들에서, 그룹 C의 물질은 렐라틀리맙(relatlimab), 에프틸라기모 알파(eftilagimo alpha), 및 sym022로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 D의 물질은 티라고루맙(tiragolumab)이다. 하나 이상의 실시예들에서, 그룹 E의 물질은 리릴루맙(lirilumab)이다. 하나 이상의 실시예들에서, 그룹 F의 물질은 sym023이다. 하나 이상의 실시예들에서, 그룹 G의 물질은 40E4 및 PJ196이다.
하나 이상의 실시예들에서, T-세포 상향조절, 활성화, 및/또는 재활성화를 유발하는 것으로 알려진 T-세포들 상에 발현되는 수용체들을 작용시키는 것 및/또는 자극하는 것을 할 수 있는 물질들은 다음으로 구성되는 그룹들로부터 선택된다: I: T-세포들 상의 OX40/CD137 수용체를 통해 작용하는 물질들, J: T-세포들 상의 4-1BB/CD137 수용체를 통해 작용하는 물질들, K: T-세포들 상의 CD28 수용체를 통해 작용하는 물질들, L: T-세포들 상의 ICOS 수용체를 통해 작용하는 물질들, M: T-세포들 상의 GITR 수용체를 통해 작용하는 물질들, N: T-세포들 상의 CD40L 수용체를 통해 작용하는 물질들, 및 O: T-세포들 상의 CD27 수용체를 통해 작용하는 물질들.
하나 이상의 실시예들에서, 그룹 J의 물질은 우렐루맙(urelumab) 및 유토밀루맙(utomilumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 J의 물질은 우렐루맙이다. 하나 이상의 실시예들에서, 그룹 J의 물질은 유토밀루맙이다. 그룹 J의 물질들은 OKT-3와 같은 항-CD3 물질과 조합하여 사용될 수 있다. 그러므로 하나의 조합은 우렐루맙 및 OKT-3 (우렐루맙/OKT-3)일 수 있다. 또 다른 조합은 유토밀루맙 및 OKT-3 (유토밀루맙 /OKT-3)일 수 있다. 하나 이상의 실시예들에서, 그룹 K의 물질은 테랄리주맙(theralizumab). 하나 이상의 실시예들에서, 그룹 O의 물질 발릴루맙(valilumab)이다.
하나 이상의 실시예들에서, 그룹 A의 물질들 중 하나 이상은 그룹 B의 물질들 중 하나 이상과 조합될 수 있다. 하나 이상의 실시예들에서, 그룹 A의 물질들 중 하나 이상은 그룹 B의 물질들 중 하나 이상, 및 그룹 J의 물질들 중 하나 이상과 조합될 수 있다. 이러한 조합들은 본 발명의 실시예들에서 효과적인 것으로 나타났다. 이것은 펨브롤리주맙, 니볼루맙, 세미플리맙, sym021, 아테졸리주맙, 아벨루맙으로 구성된 그룹으로부터 하나 이상으로부터 선택된 그룹 A의 하나 이상의 물질들은 이필리무맙 및 트레멜리무맙으로 구성된 그룹으로부터 하나 이상으로부터 선택된 그룹 B의 물질들 중 하나 이상과 조합될 수 있다는 것을 의미한다. 그런 다음 이들은 우렐루맙 및 유토밀루맙으로 구성된 그룹으로부터 하나 이상으로부터 선택된 그룹 J의 하나 이상의 물질들과 조합될 수 있다. 그룹 J 물질들은 OKT-3와 같은 항-CD3 물질과 조합되어 사용될 수 있다. 따라서 하나의 조합은 그룹 B로부터 이필리무맙 및 그룹 J로부터 우렐루맙과 조합된 아벨루맙, 펨브롤리주맙, 니볼루맙, 세미플리맙, sym021, 아테졸리주맙으로 구성된 그룹으로부터 하나 이상으로부터 선택된 그룹 A의 하나 이상의 물질들일 수 있다. 특정 선택(specific selection)은 OKT-3과 같은 항-CD3 물질이 있거나 또는 없는, 그룹 B로부터 이필리무맙 및 그룹 J 로부터 우렐루맙과 조합된 펨브롤리주맙일 수 있다.
하나 이상의 실시예들에서, T-세포 하향조절, 비활성화, 및/또는 고갈을 유발하는 것으로 알려진 그들의 수용체들 및 가용성 분자들 및 시토킨들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 다음으로 구성되는 그룹들로부터 선택된다: P: T-세포들 상의 IDO1/2 수용체를 통해 작용하는 물질들, Q: T-세포들 상의 TGFβ 수용체를 통해 작용하는 물질들, R: T-세포들 상의 IL-10 수용체를 통해 작용하는 물질들, 및 S: T-세포들 상의 IL-35 수용체를 통해 작용하는 물질들.
하나 이상의 실시예들에서, 그룹 P의 물질은 에파세도스타트(epacedostat)이다. 하나 이상의 실시예들에서, 그룹 Q의 물질은 린로도스타트(linrodostat)이다. 하나 이상의 실시예들에서, 그룹 R의 물질은 갈루니서팁(galunisertib)이다.
하나 이상의 실시예들에서, 조절되는(regulatory) T-세포들을 하향조절하거나 및/또는 감소시켜(depleting) 이에 따라 탈체(ex-vivo) 반응기(effector) T-세포 확장을 촉진할(favoring) 수 있는 물질들은 다음으로 구성되는 그룹들로부터 선택된다: T: 시클로포스파미드들(cyclophosphamides), U: TKI들, V: αCD25를 통해 작용하는 물질들, 및 X: IL2/디프테리아(Diphteria) 독소(toxin) 융합들(fusions).
표1에 나열된 그룹 A-X 는 표들 2-44에서 볼 수 있듯이 결합되어(combined) 여러 물질들로 사용될 수 있다. 따라서, 하나 이상의 실시예들에서 IL2는 제1확장에서 임의의 물질들(표 1 참조)과의 임의의 조합, 즉, 본 표들 2-44에 나열된 임의의 조합들에서 본 발명의 방법들의 단계 (b)에 사용된다.
하나 이상의 실시예들에서, 그룹 U의 물질은 수니티닙(sunitinib)이다. 하나 이상의 실시예들에서, 그룹 V의 물질은 소라페닙(sorafenib), 이매티닙(imatinib) 및 다클리주맙(daclizumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택된다. 하나 이상의 실시예들에서, 그룹 X의 물질은 데닐류킨 디피톡스(dinileukin diftitox)이다.
실시예 4는 TIL 배양들이 실시예 2에 기재된 바와 같이 개시될 때 TME 자극제들이 배양 배지에 첨가되었을 때, TIL 확장 탈체(ex vivo)의 성공률이 증가되었음을 입증하였다. 실시예 5는 TIL 배양들이 개시되었을 때, 실시예 2에서 수행된 바와 같이 TME 자극제들이 배양 배지에 첨가되었을 때, TIL 수율(yield)이 증가하고 TIL들의 배양 시간이 감소되었음을 입증하였다. 실시예 2에 기재된 바와 같이 수행된 실시예 6은 다양한 종양 유형들로부터 TIL 배양들이 개시되었을 때, TME 자극제들이 상이한 농도들로 배양 배지에 첨가되었을 때, TIL 수율이 증가되었음을 입증하였다.
도 27에 예시된 실시예 9는 실시예 2에서 수행된 바와 같이 표준의 어린(standard young) TIL 제조(manufacturing) 프로토콜에 TME 자극제들을 첨가하는 것이 TIL 성장을 상당히 향상시킴을 입증하였고, TIL 성장은 T-세포들(이 경우 PD-1) 상에 발현된 수용체, 또는 종양 세포들 및 종양 미세환경의 다른 세포 상에서 발현된 그것의 리간드(PD-1)를 길항함으로써 종양 단편 당 더 많은 수의 생존(viable) 세포들을 생성한다. 도 28-33에서, 표준(standard) TIL 제조 프로토콜에 PD-1 그룹 또는 PD-L1 그룹으로부터 초기 TIL 배양들에 TME 자극제들을 추가한 효과는 난소의(ovarian), 흑색종, 폐의(lung), 두경부(head and neck), 결장의(colorectal), 및 자궁 경부암, 각각에서 설명되었다. 모든 조건들(conditions)에서 중요하지는 않지만, 그 효과는 도 27에서 범-종양(pan-tumor) PD-1/PD-L1와 같이 암들 사이의 유사한 패턴을 보여준다. 이 실시예는 수용체 PD-1 또는 그것의 리간드 PD-L1을 표적으로 하는 것이 상호교환가능하고(interchangeable) 유사한 효과를 생성할 수 있음을 보여주었다.
도 35-38에서, 초기 TIL 배양들에 다른 제조업체들의 그룹 A의 억제제들을 추가하는 효과는 난소의(ovarian), 흑색종, 두경부(head and neck), 및 자궁 경부암, 각각에 설명되었다. 그 효과는 도 34에서 범-종양 실시예와 같이 암들 사이의 유사한 패턴을 보여주고 그리고 다른 제조업체들의 TME 자극제들이 유사한 효과를 얻기 위해 사용되었음을 보여주었다.
도 39는 그룹 A (PD-1 억제제 또는 그것의 리간드들), 그룹 B (CTLA-4 억제제 또는 그것의 리간드)로부터 TME 자극제들을 추가할 때, 또는 표준의 어린 TIL 제조 프로토콜과 비교하여 그룹 A 및 B 모두를 추가할 때, TIL 확장이 크게 증가했음을 보여준다. 그룹 A 와 B로부터 TME 자극제들을 함께-추가하는 것(co-adding)은 TIL 성장률을 더욱 향상시키는 경향이 있다. 도 40은 4-1BB 작용제(agonist) 및 항-CD3, 우렐루맙(urelumab)/OKT3 (그룹 J)이 단독으로, 또는 CTLA-4 억제제, 이필리무맙(ipilimumab) (그룹 B)과 조합하여, 또는 PD-1 억제제, 펨브롤리주맙(pembrolizumab) (그룹 A)과 조합하여, 또는 이필리무맙(ipilimumab) 및 펨브롤리주맙 모두 삼중 조합하여, 다양한 암들로부터 종양 단편 당 생존 세포들에서 매우 강력한 TIL 성장을 보여주었음을 보여준다. 따라서, 본 발명의 일 실시예는 본 발명의 방법들을 위한 그룹 A로부터 하나 이상의 TME 자극제들의 용도(use)에 관한 것이다. 본 발명의 일 실시예는 본 발명의 방법들을 위한 그룹 B로부터 하나 이상의 TME 자극제들의 용도에 관한 것이다. 본 발명의 일 실시예는 본 발명의 방법들을 위한 그룹 J로부터 하나 이상의 TME 자극제들의 용도에 관한 것이다. 본 발명의 추가 실시예는 그룹 A와 B로부터 하나 이상의 물질들이 TME 자극제들로서 함께 사용되는 조합에 관한 것이다. 본 발명의 추가 실시예는 그룹 A, B 및 J로부터 하나 이상의 물질들이 TME 자극제들로서 함께 사용되는 조합에 관한 것이다.
도 41에서 어린(young) TIL 배양의 제조 공정에 우렐루맙(urelumab)/OKT3을 첨가하는 동안 시간-지연의 효과를 조사하였다. 여기서, 0일 째 초기 어린 TIL 배양에 추가된 우렐루맙(urelumab)/OKT3, 이필리무맙 및 펨브롤리주맙의 삼중 조합(도면의 왼쪽)은 이필리무맙과 펨브롤리주맙을 추가하는 것과 비교되었고 그리고 시간-지연에서 우렐루맙/OKT3을 추가하기 위해 2일을 기다리는 것과 비교되었다(도면의 오른쪽). 두 조건들 사이에는 큰 차이가 없었고 두 조건들 모두 매우 강한 TIL 성장을 보였다. 도 42에서, 초기 어린(young) TIL 배양에 테랄리주맙 (theralizumab) 단독 (도면의 왼쪽) 또는 이필리무맙과 펨브롤리주맙과 조합하여 추가하는 효과를 조사하였다. 유의미하지는 않지만, 삼중 조합은 테랄리주맙 단독과 비교하여 어린 TIL들에서 더 빠른 성장률을 유도하는 경향이 있었다.
실시예 12는 TME 자극제들이 단독 또는 조합하여 배양 배지에 첨가되었을 때 TIL 배양들이 개시되었을 때(initiated), TIL 확장 탈체의 성곡률이 증가되었음을 예시한다. 따라서, 본 발명의 일 실시예는 하나 이상의 TME 자극제들의 사용 없이와 비교하여 증가된 탈체 확장을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도(use)에 관한 것이다. 본 발명의 방법들은 탈체이며 신체 위(on)에서 또는 체내에서 수행되지 않는다. 그들은 실험실에서 환자 세포들의 확장을 나타내므로 생산에 의사가 필요하지 않는다.
실시예 13은 어린 TIL 처리(processing) 단계에 TME 자극제들을 추가하면 T 세포들의 증가된 빈도와, 생존 T 세포들의 증가된 수를 포함하는 TIL 생성물(product)의 생성을 허용하는 기존의 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 T세포들의 증가된 빈도와 생존 T 세포들의 증가된 수를 포함하는 TIL 생성물(product)의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 14는 어린 TIL 제조 단계에 TME 자극제들을 추가하면 반응기 메모리(effector memory) T 세포들의 비슷한 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 반응기 메모리 T 세포들의 비슷한 빈도를 포함하는 TIL 생성물의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 15는 어린 TIL 제조 단계에 TME 자극제들을 단독 그리고 조합하여 추가하는 것이 CD8+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 따라서, 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 CD8+ T 세포들의 증가된 빈도와 함께 TIL 생성물의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 16은 어린 TIL 제조 단계에 TME 자극제들을 추가하는 것이 CD4+ T 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 CD4+ T 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 17은 어린 TIL 제조 단계에 TME 자극제들을 추가하는 것이 NK 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 따라서, 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 NK 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 18은 어린 TIL 처리(processing) 단계에 TME 자극제들을 추가하는 것이 NK 세포들의 감소된 빈도 그러나 CD8+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 따라서, 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 NK 세포들의 감소된 빈도 그러나 CD8+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 19는 어린 TIL 처리(processing) 단계에 시간 지연을 갖는 TME 자극제들을 추가하는 것이 총 T 세포들의 증가된 빈도, CD8+ T 세포들 및 NK 세포들 및 CD4+ T 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 총 T 세포들의 증가된 빈도, CD8+ T 세포들 및 NK 세포들 및 CD4+ T 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 20은 어린 TIL 제조 단계에 TME 자극제들을 추가하는 것이 종양-특이적(specific) LAG-3+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. LAG-3는 T-세포 고갈의 마커(marker)로 알려져 있으며, 종양 항원들에 대한 친화도가 높은 T 세포들은 일반적으로 고갈되는(exhausted) 경향이 증가하며, CD8+ LAG-3+ T 세포 클론들의 확장은 종양-반응성(reactive) T-세포들의 더 높은 비율(proportion)을 유도할 수 있어 TIL 요법에 대한 이 새로운 접근법의 개선된 임상 결과를 초래할 수 있다. 따라서, 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 종양-특이적 LAG-3+ T 세포들의 증가된 빈도를 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
실시예 21은 어린 TIL 제조 단계에 TME 자극제들을 추가하는 것이 CD28을 발현하는 어린 표현형(younger phenotype)을 가진 CD8+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존의 표준 TIL 프로토콜에 대한 새로운 개선을 제공했음을 예시한다. 본 발명의 일 실시예는 하나 이상의 TME 자극제들을 사용하지 않는 것에 비해 CD28을 발현하는 어린 표현형을 가진 CD8+ T 세포들의 증가된 빈도를 초래하는 본 발명에 따른 방법들에서 TME 자극제들의 용도에 관한 것이다.
여기서 제시된 접근법들을 사용하면 생체 내에서(in vivo) 허용되는(tolerated) 것보다 훨씬 높은 용량(dose) 수준들(levels)을 허용한다. 그러므로 농도들은 생체 내에서 허용되는 최대 허용 용량의 적어도 2배일 수 있다. 농도는 생체 내에서 허용되는 최대 허용 용량만큼 높은 5-10처럼 훨씬 더 높을 수 있다. 따라서, 하나 이상의 실시예들에서, 물질의 농도는 0.1 ㎍/mL 내지 300 ㎍/mL이다. 농도는 또한 1 ㎍/mL 내지 100 ㎍/mL일 수 있다. 농도는 또한 10 ㎍/mL 내지 100 ㎍/mL일 수 있다. 농도는 또한 1 ㎍/mL 내지 10 ㎍/mL일 수 있다.
하나 이상의 실시예들에서, T 세포들의 치료적 집단은 다음으로 구성되는 그룹들로부터 선택된 암 유형을 치료하는데 사용된다: 1: 고형(solid) 종양들, 2: ICI 나이브() 종양들, 3: MSI-H 종양들, 4: 혈액의(Hematological) 종양들, 5: 과-돌연변이(Hyper-mutated) 종양들 (POL-E 및 POL-D 돌연변이 종양들), 및 6: 바이러스-유발(virus-induced) 종양들.
하나 이상의 실시예들에서, T 세포들의 치료적 집단은 유방암, 신장 세포암, 방광암, 흑색종, 자궁 경부암, 위암, 결장암, 폐암, 두경부암, 난소암, 호지킨 림프종, 췌장암, 간암, 및 육종으로 구성되는 그룹들로부터 선택된 암 유형을 치료하는데 사용된다.
하나 이상의 실시예들에서, T 세포들의 치료적 집단은 유방암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 신장 세포암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 방광암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 흑색종을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 자궁 경부암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 위암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 결장암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 폐암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 두경부암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 난소암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 호지킨 림프종을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 췌장암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 간암을 치료하는데 사용된다. 하나 이상의 실시예들에서, T 세포들의 치료적 집단은 육종을 치료하는데 사용된다.
하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 20 일 내지 약 45 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 20 일 내지 약 40 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 25 일 내지 약 40일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (c) 또는 (d)는 약 30 일 내지 약 40 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (b)는 약 10 일 내지 약 28 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계들 (a) 내지 (b)는 약 10 일 내지 약 20 일의 기간 내에 수행된다.
일부 실시예들에서, 제1 TIL 확장 (단계 (a))은 1 일, 2 일, 3 일, 4 일, 5 일, 6 일, 7 일, 8 일, 9 일, 10 일, 11 일, 12 일, 13 일, 또는 14 일 동안 진행할(proceed) 수 있다. 일부 실시예들에서, 제1 TIL 확장은 1 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 2 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 3 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 4 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 5 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 6 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 7 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 8 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 9 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 10 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 11 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 12 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 13 일 내지 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 1 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 2 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 3 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 4 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 5 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 6 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 7 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 8 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 9 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 10 일 내지 11 일 동안 진행할 수 있다. 일부 실시예들에서, 제1 TIL 확장은 11 일 동안 진행할 수 있다.
하나 이상의 실시예들에서, 단계 (b)는 약 6 일 내지 약 18 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (b)는 약 7 일 내지 약 14 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (b)는 약 7 일 내지 약 10 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (b)는 약 6 일 내지 약 12 일의 기간 내에 수행된다.
하나 이상의 실시예들에서, 단계 (c)는 약 12 일 내지 약18 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (c)는 약 10 일 내지 약28 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (c)는 약 10 일 내지 약 20 일의 기간 내에 수행된다. 하나 이상의 실시예들에서, 단계 (c)는 약 12 일 내지 약 18 일의 기간 내에 수행된다.
일부 실시예들에서, 제1확장에서 제2확장으로의 전환(transition)은 단편화(fragmentation)가 발생한 날로부터 1 일, 2 일, 3 일, 4 일, 5 일, 6 일, 7 일, 8 일, 9 일, 10 일, 11 일, 12 일, 13 일, 또는 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화(fragmentation)가 발생한 날로부터 1 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1 TIL 확장은 for 2 일 내지14 일 동안 진행할 수 있다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 3 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 4 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 5 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 6 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 7 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 8 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 9 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 10 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 11 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 12 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 13 일 내지 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 14 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 1 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 2 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 3 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 4 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 5 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 6 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 7 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 8 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 9 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 10 일 내지 11 일에 발생한다. 일부 실시예들에서, 제1확장에서 제2확장으로의 전환은 단편화가 발생한 날로부터 11 일에 발생한다.
주요 발견들(key findings) 중 하나는 더 많은 TIL들이 더 빨리 도달할 수 있다는 것이다. 이것은 의학적 치료와 관련이 있기 위해서는 일정량(certain amount)의 세포들이 필요하기 때문에 높은 가치를 지닌다. 더 많은(More) 세포들이 더 빨라지면(faster) 생산 비용이 낮아질 것이고 또한 환자에게 더빨리 치료를 제공할 수 있다. 하나 이상의 실시예들에서, 단계 (b)는 1 x 106 내지 1x 107 세포들, 예를 들어 2 x 106 내지 5x 106 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (b)는 5 x 106 내지 1x 107 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (b)는 1 x 106 내지 5x 107 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (b)는 1 x 107 내지 5x 107 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 1012 세포들, 예를 들어 1 x 108 내지 5x 109 세포들, 예를 들어1 x 109 내지 5x 109 세포들, 예를 들어 1 x 108 내지 5x 1010 세포들, 예를 들어 1 x 109 내지 5x 1011 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 단계 (b)에서 확장 후 세포들의 수와 비교하여 적어도 104 배 증가, 예를 들어 적어도 103 배 증가, 예를 들어 적어도 102 배 증가, 예를 들어 적어도 10 배 증가를 초래한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 1010 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 109 세포들을 생성한다. 하나 이상의 실시예들에서, 단계 (c)는 1 x 107 내지 1x 108 세포들을 생성한다.
도 13에 예시된 실시예 7은 실시예 2에 기재된 바와 같이 수행된 표준의 어린 TIL 제조 프로토콜에 TME-자극제들을 첨가하는 것이 TIL 성장을 유의하게 향상시켜 종양 단편 당 더 많은 수의 생존 세포들을 초래한다는 것을 입증하였다. 도 20에 예시된 실시예 8은 T-세포들 (또는 그들의 리간드들) 상에 발현된 수용체들을 길항하거나(antagonizing), T-세포들 (또는 그들의 리간드들) 상에 발현된 수용체들을 작용시키거나(agonizing), 고갈된(exhausted) T-세포들 (또는 그들의 리간드들)을 재활성화하거나(reinvigorating), 조절되는(regulatory) T-세포들을 감소시키거나(depleting) 및/또는 CD28 계열(family) (또는 단백질들의 B7 계열에서 유래하는 그들의 리간드들)에서 유래한 T-세포들 상에 발현되는 수용체들을 표적화하는(targeting) TME 자극제들을 어린 TIL 처리 단계에 첨가하는 것은 더 빠른 TIL 요법(therapy) 제조 프로토콜을 허용하는 기존의 표준 TIL 프로토콜에 대해 새로운 개선을 제공했음을 입증한다. 일부 실시예들에서, 항원-제시 피더(feeder) 세포들 (APC들) 은 PBMC들이다. 일부 실시예들에서, 항원-제시 피더 세포들 (APC들)은 동종이계의(allogeneic) 피더 세포들이다. 일부 실시예들에서, 항원-제시 피더 세포들은 인공의(artificial) 항원-제시 피더 세포들이다. 실시예에서, 제2확장에서 TIL들 대(to) 항원-제시 피더 세포들의 비율(ratio)은 약 1 내지 25, 약 1 내지 50, 약 1 내지 100, 약 1 내지 125, 약 1 내지 150, 약 1 내지 175, 약 1 내지 200, 약 1 내지 225, 약 1 내지 250, 약 1 내지 275, 약 1 내지 300, 약 1 내지 325, 약 1 내지 350, 약 1 내지 375, 약 1 내지 400, 또는 약 1 내지 500이다. 실시예에서, 제2확장에서 TIL들 대 항원-제시 피더 세포들의 비율은 1 내지(to) 50 그리고(and) 1 내지(to) 300 사이이다. 실시예에서, 제2확장에서 TIL들 대 항원-제시 피더 세포들의 비율은 1 내지 100 그리고 1 내지 200 사이이다. 하나 이상의 실시예들에서, APC들은 인공의 APC들 (aAPC들)이다.
실시예에서, 본 개시의 APC들을 사용하여 확장된 TIL들은 약학적(pharmaceutical) 조성물로서 환자에게 투여된다. 실시예에서, 약학적 조성물은 멸균(sterile) 완충액(buffer)에서 TIL들의 현탁액이다. 본 개시의 PBMC들을 사용하여 확장된 TIL들은 당업계에 공지된 임의의 적합한(suitable) 경로(route)에 의해 투여될 수 있다. 일부 실시예들에서, T-세포들은 바람직하게 대략 30분 내지 60분 지속되는 단일 동맥 내의(intra-arterial) 또는 정맥으로 들어가는(intravenous) 주입(infusion)으로 투여된다. 투여의 다른 적절한 경로들은 복강내의(intraperitoneal), 척추 강내의(intrathecal), 및 림프내(intralymphatic)를 포함한다. 하나 이상의 실시예들에서, TIL들의 치료적 집단은 환자에게 주입된다(infused).
하나 이상의 실시예들에서, 세포들은 세포 배양으로부터 제거되고 그리고 단계 (c)를 수행하기 전에 저장 배지(storage medium)에서 동결보존된다(cryopreserved).
하나 이상의 실시예들에서, 상기 방법은 T-세포 신호전달(signaling) 분자의 적어도 하나의 엔도도메인(endodomain)과 융합된 단일 사슬(single chain) 가변 단편(variable fragment) 항체를 포함하는 키메라(chimeric) 항원 수용체(receptor) (CAR)를 인코딩(encoding)하는 핵산(nucleic acid)을 포함하는 발현 벡터(expression vector)로 TIL들의 제1집단을 형질도입하는(transducing) 단계를 추가로 포함한다.
하나 이상의 실시예들에서, 단계 (c)는 세포 배양 배지로부터 세포들을 제거하는 단계를 추가로 포함한다.
하나 이상의 실시예들에서, 단계 (a)는 절제된 종양을 다중(multiple) 종양 단편들(fragments), 예를 들어 4 내지 50 단편들, 예를 들어 20 내지 30 단편들로 처리하는 단계를 추가로 포함한다. 하나 이상의 실시예들에서, 단편들은 약 1 내지 50 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 5 내지 50 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 0.1 내지 10 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 0.1 내지 1 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 0.5 내지 5 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 1 내지 10 mm3의 크기를 갖는다. 하나 이상의 실시예들에서, 단편들은 약 1 내지 3 mm3의 크기를 갖는다. 종양을 파괴하기(disrupting) 위한 과정을 설명하기 위해 본 명세서에 사용되는, 용어들 "단편화하는(fragmenting)", "단편(fragment)", 및 "단편화된(fragmented)"은, 종양 조직(tissue as)의 분쇄(crushing), 슬라이스(slicing), 분할(dividing), 및 세절절개술(morcellating)과 같은 기계적 단편화(fragmentation) 방법들뿐만 아니라 종양 조직의 물리적 구조를 파괴하는(disrupting) 임의의 다른 방법을 포함한다.
하나 이상의 실시예들에서, 포유동물(mammal)은 인간이다. 일부 실시예들에서, TIL들은 종양 단편들로부터 획득된다. 일부 실시예들에서, 종양 단편은 날카로운 절개(sharp dissection)에 의해 얻어진다. 일부 실시예들에서, 종양 단편은 약 0.1 mm3 내지 10 mm3이다. 일부 실시예들에서, 종양 단편은 약 1 mm3 내지 10 mm3이다. 일부 실시예들에서, 종양 단편은 약 1 mm3 내지 8 mm3이다. 일부 실시예들에서, 종양 단편은 약 1 mm3이다. 일부 실시예들에서, 종양 단편은 약 2 mm3이다. 일부 실시예들에서, 종양 단편은 약 3 mm3이다. 일부 실시예들에서, 종양 단편은 약 4 mm3이다. 일부 실시예들에서, 종양 단편은 약 5 mm3이다. 일부 실시예들에서, 종양 단편은 약 6 mm3이다. 일부 실시예들에서, 종양 단편은 약 7 mm3이다. 일부 실시예들에서, 종양 단편은 약 8 mm3이다. 일부 실시예들에서, 종양 단편은 약 9 mm3이다. 일부 실시예들에서, 종양 단편은 약 10 mm3이다. 일부 실시예들에서, 종양들은 1-4 mm x 1-4 mm x 1-4 mm이다. 일부 실시예들에서, 종양들은 1 mm x 1 mm x 1 mm이다. 일부 실시예들에서, 종양들은 2 mm x 2 mm x 2 mm이다. 일부 실시예들에서, 종양들은 3 mm x 3 mm x 3 mm이다. 일부 실시예들에서, 종양들은 4 mm x 4 mm x 4 mm이다. 현재 상당히(fairly) 큰 단편 크기들이 필요하다(5 mm3 이상). 본 발명은 세포들이 치료에 필요한 세포 수에 더 빨리 도달하는 최적화된 방식으로 성장하기 때문에 더 작은 단편들의 사용(use)을 허용한다. 더 작은 단편들을 사용하는 것은 예를 들어, 그들의 종양이 너무 작거나 또는 작은 종양 샘플을 얻는 것이 오직 가능했기 때문에, 지금까지 치료할 수 없었던 환자들을 이제는 치료할 수 있음을 의미한다. 따라서, 본 발명의 방법들에서 사용된 단편들의 크기는 중요할 수 있다.
일부 실시예들에서, 종양 단편화(fragmentation)는 종양 내부 구조를 유지하기 위해 수행된다. 일부 실시예들에서, 종양 단편화는 매스(scapel)로 톱질 동작(sawing motion)을 수행하는 것 없이 수행된다. 일부 실시예들에서, TIL들은 종양 종양 소화물들(digests)로부터 얻어진다. 일부 실시예들에서, 종양 소화물들은 효소 배지(enzyme media), 예를 들어 이에 제한되는 것은 아니지만 RPMI 1640, 2 mM GlutaMAX,10 mg/mL 겐타마이신(gentamicin), 30 U/mL DNase, 및 1.0 mg/mL 교원질 분해효소(collagenase)에서 배양(incubation)에 의해, 이어서 기계적 해리(mechanical dissociation) (GentleMACS, Miltenyi Biotec, Auburn, CA)에 의해 생성되었다. 종양을 효소 배지에 넣은 후, 종양은 약 1분 동안 기계적으로 해리될 수 있다. 그런 다음 용액을 37℃, 5% CO2에서 30분 동안 배양한(incubated) 다음, 약 1분 동안 그것을 다시 기계적으로 파괴한다(disrupted). 37 ℃, 5% CO2에서 30분 동안 다시 배양한 후, 종양은 약 1분 동안 세 번(third time) 기계적으로 파괴될 수 있다. 일부 실시예들에서, 조직의 큰 조각들(pieces)이 존재하는 경우 세 번 기계적 파괴(disruption) 후, 37℃, 5% CO2에서 30분의 추가 배양 유무에 관계없이, 샘플에 1 또는 2 개의 추가의 기계적 해리들이 적용되었다. 일부 실시예들에서, 세포 현탁액이 많은 수의 적혈구(red blood) 세포들 또는 죽은 세포들을 포함하는 경우 최종 배양이 끝날 때, 피콜(Ficoll)을 사용한 밀도 구배 분리(density gradient separation)는 이러한 세포들을 제거하기 위해 수행될 수 있다.
하나 이상의 실시예들에서, 세포 배양 배지는 G-Rex 용기(container) 및 Xuri 셀백(cellbag)으로 구성되는 그룹으로부터 선택된 컨테이너에 제공된다.
한 측면은 이전 청구항 중 어느 한 항의 방법에 의해 획득할 수 있는 종양 침윤 림프구들 (TIL들)의 집단에 관한 것이다.
추가 측면은 암에 걸린 대상을 치료하는데 사용하기 위한 확장된 종양 침윤 림프구들 (TIL들)에 관한 것이며, 치료는 다음 단계들을 포함한다: TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들 배양하는 단계; TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이고; 및 비골수제거 림프구제거 화학요법을 투여한 후, T 세포들의 치료적 집단을 포유동물에 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되면, 그래서 포유동물에서 암의 퇴행이 촉진된다.
실시예에서, 본 발명은 TIL들의 집단으로 암을 치료하는 방법, 또는 암을 치료하기 위한 TIL들의 용도를 포함하고, 여기서 환자는 본 개시내용에 따른 TIL들의 주입 전에 비-골수제거(non-myeloablative) 화학요법으로 사전-치료된다. 실시예에서, 비-골수제거 화학요법은 2 일 동안 (TIL 주입(infusion) 전 7일 및 2일) 시클로포스파미드(cyclophosphamide) 60 mg/kg/d 이고 그리고 5 일 동안 (TIL 주입 전 5일 내지 1일) 플루다라빈(fludarabine) 25 mg/m2/d이다. 실시예에서, 본 개시내용에 따른 비-골수제거 화학요법 및 TIL 주입 (0일 째) 후, 환자는 생리학적 내성(physiologic tolerance)까지 매 8시간마다 720,000 IU/kg으로 IL-2 정맥안으로(intravenously)의 정맥 내의(intravenous) 주입을 받는다.
일부 실시예들에서, 본 개시내용은 (a) 환자로부터 절제된 종양으로부터 TIL들의 제1집단을 얻는 단계; (b) TIL들의 제2집단을 생성하기 위해 제1세포 배양 배지에 TIL들의 제1집단의 초기 확장을 수행하는 단계, 여기서 TIL들의 제2집단은 TIL들의 제1집단보다 수가 적어도 5-배 많고, 그리고 제1세포 배양 배지는 IL-2 및 하나 이상의 TME 자극제들을 포함하며; (c) TIL들의 제3집단을 얻기 위해, 제2세포 배양 배지에서 골수성 인공(myeloid artificial) 항원 제시 세포들 (골수성(myeloid) aAPC들)의 집단을 사용하여 TIL들의 제2집단의 빠른(rapid) 확산을 수행하는 단계, 여기서 TIL들의 제3집단은 빠른 확산의 시작으로부터 7일 후 TIL들의 제2집단보다 수가 적어도 50-배 많으며; 및 제2 세포 배양 배지는 IL-2 및 항-CD3을 포함하며; (d) TIL들의 제3집단의 치료학적으로 유효한 부분(effective portion)을 암을 가진 환자에게 투여하는 단계의 단계들을 포함하는 종양 침윤 림프구들 (TIL들) 의 집단으로 암을 치료하는 방법을 제공한다. 일부 실시예들에서, 본 개시내용은 암을 치료하는데 사용하기 위한 종양 침윤 림프구들 (TIL들)의 집단으로서, TIL들의 집단은 (b) TIL들의 제2집단을 생성하기 위해 제1세포 배양 배지에서 환자로부터 절제된 종양으로부터 획득된 TIL들의 제1집단의 초기 확장을 수행하는 단계, 여기서 TIL들의 제2집단은 TIL들의 제1집단보다 수가 적어도 5-배 많으며, 그리고 여기서 제1세포 배양 배지는 IL-2를 포함하며; (c) TIL들의 제3집단을 생성하기 위해 제2세포 배양 배지에서 골수성 인공 항원 제시 세포들 (골수성 aAPC들)의 집단을 사용하여 TIL들의 제2집단의 빠른 확산을 수행하는 단계, 여기서 TIL들의 제3집단은 빠른 확산의 시작으로부터 7일 후 TIL들의 제2집단보다 수가 적어도 50-배 많으며 ; 그리고 제2세포 배양 배지는 IL-2 및 항-CD3을 포함하며; (d) TIL들의 제3집단의 치료학적으로 유효한 부분을 암을 가진 환자에게 투여하는 단계의 단계들을 포함하는 방법에 의해 얻을 수 있다. 일부 실시예들에서, 상기 방법은 환자로부터 절제된 종양으로부터 TIL들의 제1집단을 획득하는 제1단계 (a)를 포함한다. 일부 실시예들에서, IL-2는 약 3000 IU/mL의 초기 농도로 존재하고 그리고 항-CD3항체는 제2세포 배양 배지에서 약 30 ng/mL의 초기 농도로 존재한다. 일부 실시예들에서, 제1확장은 14일 이하의 기간에 걸쳐 수행된다. 일부 실시예들에서 제1확장은 기체 투과성 용기(gas permeable container)를 사용하여 수행된다. 일부 실시예들에서, 제2확장은 기체 투과성 용기를 사용하여 수행된다. 일부 실시예들에서, 빠른 확장(rapid expansion)에서 TIL들의 제2집단 대 aAPC들의 집단의 비율은 1 내지 80 그리고 1 내지 400 사이이다. 일부 실시예들에서, 빠른 확장에서 TIL들의 제2집단 대 aAPC들의 집단의 비율은 약 1 내지 300이다.
추가 측면은 다음을 포함하는 방법에 의해 얻을 수 있는 종양 침윤 림프구들 (TIL들)의 집단에 관한 것이다: TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계; 및 TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이다.
추가 측면은 IL-2 및 하나 이상의 TME 자극제들을 포함하는 TIL들의 치료적 집단에 관한 것이다.
추가 측면은 IL-2, 하나 이상의 TME 자극제들, IL-2, 항-CD3, 및 항원 제시 세포들 (APC들)을 포함하는 TIL들의 치료적 집단에 관한 것이다.
하기 도면들 및 실시예들은 본 발명을 예시하기 위해 하기에 제공된다. 그것들은 예시를 위한 것이며 어느 방식으로든 제한되는 것으로 해석되어서는 안 된다.
표들
표 1
표 2
표 3
표 4
표 5
표 6
표 7
표 8
표 9
표 10
표 11
표 12
표 13
표 14
표 15
표 16
표 17
표 18
표 19
표 20
표 21
표 22
표 23
표 24
표 25
표 26
표 27
표 28
표 29
표 30
표 31
표 32
표 33
표 34
표 35
표 37
표 38
표 39
표 40
표 41
표 42
표 43
표 44
표 45
실시예들
실시예 1 - 하나 이상의 면역(immune) 조절제들(modulators)은 탈체(ex vivo) 고갈된(exhausted) T-세포들을 재활성화한다(reinvigorate)
단계 1.1: 단일 면역 조절제들의 효과
a. 다양한 환자들로부터 절제된 TIL-함유 종양 조직을 cm3 조직 당 30-50개의 종양 단편들을 절개하고(dissected) 그리고 24-웰 세포 배양 플레이트들로 옮겼다. 6000 IU/mL IL-2 및 표 1에 내열된 각각의 면역-조절제들의 없거나(기준선(baseline)) 또는 낮거나, 중간이거나, 또는 높은 농도를 포함하는 세포 배양 배지의2 mL.
b. 세포 배양 플레이트들은 세포 배양 배지가 자주 교체되는 37℃, 5% CO2 에서 배양된다. 세포 배양들은 웰(well) 당 1.5 x 106 세포들을 증가시키지 않아야 하며 그리고 새로운 웰들로 분할해야 한다.
c. 며칠 후, 세포들이 수확되고, 세포들은 양을 결정하기 위해 계산되고(counted), 그리고 유동세포분석법(flowcytometry) 생존력(viability) 및 표현형(phenotype)에 의해 분석된다
단계 1.2 PD1 동시-차단(co-blockade) 및/또는 차단/자극(stimulation)의 효과
a. PD1 차단(blockade)이 고갈된(exhausted) T-세포들을 재활성화시키는 핵심 경로(key pathway)로 명확하게 확인됨에 따라, IL-2, 최적 농도의 PD1 및 표 1에 나열된 나머지(remaining) 면역 조절제들, 및 표들 2-21에 나열된 IL-2 와의 특정 조합들을 포함하는 새로운 실험이 위와 같이 설정되고(setup) 수행된다.
단계 1.3 CTLA4 동시-차단 및/또는 차단/자극의 효과
a. CTLA4 차단이 고갈된 T-세포들을 재활성화시키는 핵심 경로들로 명확하게 확인됨에 따라, IL-2, 최적 농도의 PD1 및 표 1에 나열된 나머지 면역 조절제들, 및 표들 22-41에 나열된 IL-2와의 특정 조합들을 포함하는 새로운 실험이 위와 같이 설정되고 수행된다.
단계 2: 면역 조절제들의 농도를 추가로 미세조정하다(finetune)
단계 3: 조합의(combinatorial) 효과들의 이해
a. 새로운 실험은 위에서 설명한 것과 동일한 판독(readout)과 동시에 여러 면역 조절제들을 추가함으로써 가능한 시너지(synergistic) 효과들을 결정하기 위해 조합의 접근 방식의 첫 번째 실험에서 최적 농도에서 가장 잘 수행되는 면역 조절제들을 사용하여 유사한 방식으로 설정된다.
b. 위의 내용은 여러 번 반복(iterations)되어 결과적으로 단축된 시간, 더 높은 확장 속도 및/또는 개선된 표현형과의 조합들을 나타낸다.
단계 4: 표준 TIL 제조 프로토콜과 비교하여 환자들의 최적 조합의 검증(validation)
a. 초기 TIL 배양 확장은 실제 환자 환경(setting)에 대한 효과들을 검증하기 위해 여러 TIL 치료(therapy) 적격 환자들에서 병행하여 실행된다(run in parallel)
실시예 2 - TME 자극제들을 가진 "어린(Young)" 종양-침윤 림프구들 (TIL들)
이 실시예는 TME 자극제들을 갖는 "어린" 종양-침윤 림프구들 (TIL들)을 생성하기 위한 제조 공정을 보여준다.
다양한 조직학(various histologies)의 종양 물질(material)은 상업적 출처들(sources)로부터 얻어진다. 14명의 독립적인 환자 종양들 또는 종양 소화물들(digests)이 얻어졌다 (3명 난소암, 3명 전이성 흑색종, 3명 두경부암, 2명 폐암, 2명 결장암, 1명 자궁 경부암; 표 42). 동결보존되거나(Cryopreserved) 또는 신선한(fresh) 종양 물질(material)은 멸균 동결(sterile freezing) 또는 수송 배지(transport medium)에서 Cbio A/S로 배송되었다. 종양 물질은 멸균 상태들을 유지하기 위해 클린벤치(laminar flow hood)에서 처리되었다(handled).
TIL들은 이전에 표준 TIL 제조 프로토콜에 자세히 기재된 바와 같이 준비되었다(Friese, C. et al., CTLA-4 blockade boosts the expansion of tumor-reactive CD8+ tumor-infiltrating lymphocytes in ovarian cancer. Sci Rep 10, 3914 (2020); Jin, J. et al., Simplified Method of the Growth of Human Tumor Infiltrating Lymphocytes in Gas-permeable Flasks to Numbers Needed for Patient Treatment, Journal of Immunotherapy, 35 - Issue 3 (2012)). 간단히 말해서, TIL 배양들은 종양 단편들 또는 종양 소화물(digest)을 사용하여 설정되었다. 종양들은 1-3 mm3 단편들로 분할되었고 그리고 5% CO2의 가습된(humidified) 37℃ 인큐베이터에서, 표 43에 나열된 항-CD3 (그룹 J) 및 CD28 작용제 (그룹 K)와 함께 PD-1/PD-L1 길항제들 (그룹 A), CTLA-4 길항제 (그룹 B), LAG-3 길항제 (그룹 C), TIGIT 길항제 (그룹 D), 4-1BB 작용제 각각의 낮은, 중간의, 높은, 또는 매우 높은 농도들의 TME 자극제들과 조합을 포함하거나 또는 6000 IU/mL IL-2 (6000 IU/ml, 클리니젠(Clinigen)) 단독(기준선)을 포함하는 10ml 완전한(complete) 배지 (CM)를 갖는 G-Rex 6-웰 플레이트에 놓였다 (WilsonWolf; 웰 당 5개 단편들). CM은 총 부피가 40 ml에 도달할 때까지 4-5일마다 첨가되었다. 이어서, 배지의 절반을 제거하고 그리고 4-5일 마다 CM 및 IL-2로 교체하였다. 종양 소화물로부터 TIL 배양들은 250 μ및 IL-2 (6000 IU/ml, 클리니젠(Clinigen))의 평평한 바닥 96-웰 플레이트들에서 밤새 효소 분해(digestion)에 의해 얻은 단일-세포 현탁액들(5x105/ml)을 5% CO2가 있는 가습된 37℃ 인큐베이터에서 배양함으로써 시작되었다. 배지의 절반을 제거하고 그리고 2-3일마다 CM을 교체하였다.
CM은 GlutaMAX, 25 mM HEPES pH 7.2 (Gibco), 10% 열-비활성화된 인간(heat-inactivated) AB 혈청 (시그마-알드리치), 100 U/mL 페니실린(penicillin), 100 ㎍/mL 스트렙토마이신(streptomycin) (Gibco), 및 1.25㎍/ml 훈기존(Fungizone) (Bristol-Myers Squibb)이 포함된 RPMI1640으로 구성된다.
이 실시예는 10-28일의 나이(age)를 갖는 TME 자극제들을 갖는 "어린(young)" 종양-침윤 림프구들 (TIL들)의 생성(generation)을 보여준다.
실시예 3 -TME 자극제들을 갖는 “어린” TIL 배양들(cultures)의 표현형 분석
이 실시예는 실시예 2에 기재된 바와 같이 수행된 TME 자극제들을 갖는 "어린" TIL 배양들의 표현형 분석을 보여준다.
어린 TIL 생성(generation)을 위해 지정된(designated) 배양들이 수확되었을 때, 그들의 표현형은 유동 세포분석법(flow cytometry)에 의해 평가되었다.
TIL 표현형은 빈도 및 절대 세포 수(absolute cell count) 모두에서 생존력(viability) 및 CD3+ 부분집합, CD3+CD8+ 부분집합(subset), CD3+CD4+ 부분집합 및 NK 부분집합의 평가에 의해 결정되었다. 추가적으로, 분화 상태(differentiation status), 활성화 상태, 고갈 마커들의 발현 및 TIL들의 노화(senescence)가 평가되었다. 유동 세포분석법은 다음 마커들을 사용하여 수행되었다:
TIL 패널(Panel) 1: CD3, CD4, CD8, CD45RA, CD56, CCR7, FVS780, BTLA, LAG-3, PD-1, TIM-3
TIL 패널 2: CD3, CD4, CD8, CD45RA, CD56, CCR7, FVS780, CD-27, CD28, CD57, CD69
간단히 말해서, 패널 당 약 0.5x106 어린 TIL들은 세척되었고 그런 다음 적정(titrated) 항체들 (BD 생명화학, 표 45) 및 Brilliant Stain Buffer (BD 생명과학)와 함께 4℃에서 30분 동안 배양시켰다(incubated). 세포들은 PBS로 2회 세척되었고 그리고 유동 세포분석법 (CytoFLEX, Beckman Coulter)에 의해 직접 분석되었다.
이 실시예는 TME 자극제들을 갖는 "어린" TIL 배양들의 표현형 분석을 보여준다.
실시예 4 -탈체(ex vivo) TIL 확장의 성공률을 증가시킨 TME-자극제들
이 실시예는 실시예 2에서 기재된 바와 같이 TIL 배양들이 시작되어 수행될 때 TME 자극제들이 배양 배지에 첨가되었을 때, 탈체 TIL 확장의 성공률이 증가되었음을 입증했다.
TIL 배양들을 수확할 때 종양 단편 당 세포 수를 결정함으로써 TIL 확장의 성공률이 조사되었다. 5x104 TIL들/단편은 성공적인 TIL 배양을 위한 임계값(threshold)으로서 설정되었다.
TIL 확장의 성공률을 결정하는 것은, TME 자극제들이 "어린" TIL 배양들 (아벨루맙 68%, 렐라틀리맙(relatlimab) 70%, 티라고루맙 (tiragolumab) 76.5%, 펨브롤리주맙 82.1%, 이필리무맙 88.5%, 테랄리주맙 (theralizumab) 90.9%, 니볼루맙(nivolumab) 92.3%, 및 우렐루맙/OKT3 100%)에 추가되었을 때 TIL 배양들의 성공률은 도 2 및 3에 예시된, 기준선(baseline) 배양들 61.5%과 비교하여 증가했음을 입증했다.
그들의 표적들(targets)을 따라 TME 자극제들을 분류하면(Grouping), 실시예는 또한 그룹 C (70%, LAG-3 억제제들), 그룹 A (76.3%, PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 D (76.5%, TIGIT 억제제들), 그룹 B (88.5%, CTLA-4 및 리간드의 억제제들), 그룹 K (90.9%, CD28 작용제) 및 그룹 J (96.3%, 4-1BB 작용제는 항-CD3와 함께)로부터 억제제들을 추가하면 도 4 및 5에 예시된 것처럼, 기준선 배양들 61.5%과 비교하여 TIL 배양들의 성공률이 증가했음을 입증했다.
이 실시예는 표준 TIL 제조 프로토콜과 비교하여 TIL 배양들이 개시될 때 TME 자극제들이 배양 배지에 첨가되었을 때, TIL 확장 탈체의 성공률이 증가되었음을 입증한다.
실시예 5 -TIL 수율을 증가시키고 TIL들의 배양 시간을 감소시킨 동시-자극(co-stimulation) 또는 체크포인트(Checkpoint) 차단(blockade)
이 실시예는 실시예 2에 기재된 바와 같이, TIL 배양들이 개시되고 수행될 때 TME 자극제들이 배양 배지에 첨가되었을 때, TIL 수율이 증가하고 TIL들의 배양 시간이 감소되는 것을 입증했다.
TIL 배양들을 수확할 때 TIL 수율 및 TIL들의 배양 시간이 조사되었다. 이 분석은 IL-2 단독으로 배양된 TIL들과 비교하여 TIL 배양들이 개시되었을 때 TME 자극제들이 배양 배지에 첨가되었을 때, TIL 수율이 증가하고, 배양 시간이 감소했음을 입증했다(도 6). 여기서 그것은 그룹들 K 및 J로부터 TME 자극제들은 어린 TIL 배양 시간만 가속화했지만 -그룹들 A, B 및 C로부터 자극제들은 표준 어린 TIL 프로토콜과 비교하여 유사한 방식으로 더 빠른 성장 속도들을 유도했음을 보여주었다. 특히, 그룹 J로부터 자극제들을 A 및/또는 B와 이중 또는 삼중 조합들로 결합하는 것은 성장 속도를 더욱 가속화시켰다.
이 실시예는 TME 자극제들이 배양 배지에 첨가되었을 때, 표준 TIL 제조 프로토콜과 비교하여 TIL 배양들이 개시되었을 때, TIL 수율이 증가하고 TIL들의 배양 시간이 감소되었음을 입증하였다.
실시예 6 - 탈체(ex vivo) TIL 확장을 유도한 TME 자극제들의 다른 농도들
실시예 2에 기재된 바와 같이 수행된 이 실시예는, TME 자극제들이 다른 농도들의 배양 배지에 첨가되었을 때, 다양한 종양 유형들로부터 TIL 배양들이 개시되었을 때, TIL 수율이 증가되었음을 입증했다.
TIL 배양들을 수확할 때 TIL 수율 확장은 조사되었다. 도 7의 첫 번째 분석은 저농도, 중간 농도 또는 고농도의 CTLA-4 길항제인, 이필리무맙 (그룹 B)이 배양 배지에 첨가되었을 때, TIL 배양들이 개시되었을 때, IL-2 단독에 비해 TIL 확장은 1.15-배, 1.85-배, 및 1.53-배 증가했음을 입증했다. 이 실시예는 CTLA-4 길항제 (그룹 B)가 배양 배지에 첨가되었을 때 TIL 배양들이 용량-의존적 방식(dose-dependent manner)으로 개시되었을 때, TIL 수율이 증가되었음을 입증했다. 사용된 CTLA-4 길항제(이필리무맙)가 또한 항체-의존적(dependent) 세포의(cellular) 세포독성(cytotoxicity) (ADCC)에 의해 CTLA-4 발현 T 세포들을 감소시키는 것(deplete)으로 알려져 있음에도 불구하고, 이 새로운 발견은 T 세포들의 특정 부분집합들(subsets)을 감소시키는 것(depleting)이 다른 T 세포들의 더 빠른 성장률을 가능하게 하여 이에 따라 전체 TIL 수율을 향상시키는 방법을 제안했다.
도 8에서, 저농도, 중간 농도 또는 고농도의 PD-1 길항제, 펨브롤리주맙(그룹 A)을 배양 배지에 첨가했을 때 TIL 배양들이 시작되었을 때, TIL 수율이 표준 어린 TIL 프로토콜에 비해 용량-의존적으로 증가하는 경향을 보였음이 입증되었다.
도 9-12에서 표준 어린 TIL 프로토콜과 비교하여 TIL 수율에서 유사한 용량-의존적 효과는 각각 항-CD3 (OKT3) (그룹 J), CD28 작용제, 테랄리주맙 (그룹 K), PD-L1 억제제, 아벨루맙 (그룹 A - PD-1에 대한 리간드), 및 또 다른 PD-1 억제제, 니볼루맙 (그룹 A)과 함께, 4-1BB 작용제인 우렐루맙에 대해 설명된다.
실시예 6은 다른 농도들의 TME 자극제들이 용량 의존적 방식으로 TIL 성장에 어떻게 영향을 미쳤는지를 입증한다.
실시예 7 - 전체적으로 그리고 다른 그룹들(groupings)로부터 TIL 성장을 향상시키는 TME-자극제들
도 13에 예시된 실시예 7은 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 TME-자극제들을 첨가하는 것은 종양 단편 당 더 많은 수의 생존 세포들을 초래하는 TIL 성장을 상당히 향상시켰음을 입증했다. 이것은 난소의(ovarian), 두경부(head and neck), 결장의(colorectal), 흑색종, 자궁의(cervical), 결장의(colorectal), 및 폐암을 포함하는 다양한 고형 암들(solid cancers)로부터 대표적인 수의 종양 단편들을 사용하여 설명되었다.
TME 자극제들을 기본(underlying) 하위그룹들(subgroupings)로 나누면(Breaking), 실시예는 또한 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4의 억제제들), 그룹 J (항-CD3과 함께 4-1BB 작용제) 및 그룹 K (CD28 작용제)로부터 억제제들을 추가하면 TIL 성장도 상당히 증가했음을 입증했다. 이 실시예에서는 중요하지는 않지만 그룹들 C (LAG-3 억제제들) 및 D (TIGIT 억제제들)로부터 TME 자극제들을 첨가하면 TIL 성장도 개선되는(improved) 경향이 있었다.
도 14-19에서, 위와 동일한 그룹들(groupings)의 초기 TIL 배양들에 TME 자극제들을 추가하는 효과는 각각의 자궁의(cervical), 흑색종, 난소의(ovarian), 두경부(head and neck), 폐(lung), 및 결장암에서 설명되었다. 모든 조건들에서 중요하지는 않지만, 도 13에서 범(pan)-종양 실시예와 같이 암들 사이에서 유사한 패턴을 보여준다-비록 다른 암들에서 개별(individual) 자극제들의 효과 및 크기(magnitude)는 다양했지만 말이다.
이 실시예를 요약하면, 어린 TIL 처리(processing) 단계에 TME 자극제들을 첨가하면 기존의 표준 TIL 프로토콜에 비해 새로운 개선이 제공되어 더 빠른 TIL 치료(therapy) 제조 프로토콜이 가능해졌다.
실시예 8: TIL 성장률을 상당히 증가시킨 CD28 계열 기원(family origin)의 자극제들, 및 TIL 자극제 작용제들(agonists), 길항제들(antagonists), T-세포 감소(depleting), T-세포 재활성화(reinvigorating)
도 20에 예시된 실시예 8은, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 TME-자극제들을 첨가하는 것은 종양 단편 당 더 많은 수의 생존 세포들을 초래하는 TIL 성장을 상당히 향상시켰음을 입증한다. 이것은 난소의, 두경부, 결장의, 흑색종, 자궁의(cervical) 및 폐암을 포함하는 다양한 고형 암들로부터 대표적인 수의 종양 단편들을 사용하여 설명되었다.
TME 자극제들을 그들의 기능에 따라 하위그룹들로 나누면, 실시예는 또한 T-세포 길항제들, 작용제들, 재활성화하는것(reinvigorating), 감소시키는 것(depleting) 및 수용체들의 CD28 계열의 구성원들(members) 모두가 TIL 성장에 상당한 영향을 미치는 것을 입증했다. 2 개의 상이한 PD-1 억제제들 (펨브롤리주맙 및 니볼루맙), 2 개의 상이한 PD-L1 억제제들 (아벨루맙 및 더발루맙), CTLA-4 억제제 (이필리무맙), TIGIT 억제제(티라고루맙(tiragolumab))을 포함하여 여기에 예시된 다른 TME 길항제들의 대표적인 양이, 표준 어린 TIL 처리(process)에 비해 3-5-배 증가를 나타낸 반면, 여기서 4-1BB (항-CD3 (OKT3)과 함께 우렐루맙) 및 CD28 (테랄리주맙(theralizumab))을 표적으로 하는 자극제들에 의해 예시된 TME 작용제들은 성장을 더욱 가속화하는 것으로 보인다.
TME 길항제들을, 그들이 이필리무맙과 티라고루맙과 같은 항체-의존적 세포의(cellular) 유독성(toxicity) (ADCC)을 통해 조절되는(regulatory) T 세포들의 감소(depletion)를 허용하는지 또는 체크포인트 억제를 통해 T-세포 재활성화만을 허용하는지로 추가 분할하는 것은 또한 도 20에 예시된 바와 같이 표준 어린 TIL 프로토콜 조건들에 비해 TIL 성장률에서 상당한 개선을 입증했다.
PD-1, CTLA-4 및 CD28의 억제제들에 의해 여기서 예시된 단백질들의 CD28 계열에서 유래한 TME 자극제들 또는 PD-L1의 두 가지 다른 억제제들에 의해 여기서 예시된 단백질들의 B7-계열에서 유래한 그들의 리간드들에 대해 구체적으로 살펴보면, 표준 어린TIL 프로토콜과 비교하여 TIL 성장을 크게 향상시키는 것이 입증되었다. 여기에 표시되지 않았지만, BTLA 및 ICOS와 같은 CD28 단백질 계열에서 유래한 T 세포들 상에서 발현된 다른 수용체들은 어린 TIL 배양들에 대해 유사한 성장 자극 효과를 가질 수 있다.
도 21-26에서, 이 실시예에서 위와 동일한 그룹들의 초기 TIL 배양들에 TME 자극제들을 추가하는 효과는 흑색종, 난소의(ovarian), 폐(lung), 자궁의(cervical), 결장의(colorectal), 및 두경부암들, 각각에서 설명되었다. 모든 조건들에서 유의미한 것은 아니지만, 효과는 도 20의 범-종양 실시예와 같이 암들 사이에서 유사한 패턴을 보여주었다 - 비록 다른 암들에서 개별 자극제들의 효과와 크기는 다양하지만 말이다.
이 실시예를 요약하면, T 세포들 (또는 그들의 리간드들) 상에 발현된 수용체들을 길항하거나(antagonizing), T-세포들 상에 발현된 수용체들을 작용시키거나(agonizing), 고갈된 T-세포들 (또는 그들의 리간드들)을 재활성화하거나(reinvigorating), 조절되는(regulatory) T-세포들을 감소시키거나(depleting) 및/또는 T 세포들 CD28 계열 (또는 단백질들의 B7 계열에서 유래한 그들의 리간드들)에서 유래한 T 세포들 상에 발현된 수용체들을 표적화하는 TME 자극제들을 어린 TIL 처리(processing) 단계에 추가하는 것은 더 빠른 TIL 치료 제조 프로토콜을 허용하는 기존 표준 TIL 프로토콜에 대한 새로운 개선을 제공했다.
실시예 9 -T 세포들 또는 그들의 리간드들 상에 발현된 수용체들을 표적으로 하는 TME 자극제 길항제들은 유사한 TIL 성장 자극 효과를 입증했다
도 27에서 예시된 실시예 9는, 실시예 2에서 수행된 표준 어린 TIL 프로토콜에 TME 자극제들을 추가하면 T 세포들 (이 경우 PD-1) 상에 발현된 수용체를 자극함으로써 또는 종양 세포들 및 종양 미세환경에서 다른 세포들 상에 발현된 그것의 리간드(PD-L1)를 자극함으로써 종양 단편 당 더 많은 수의 생존 세포들을 초래하는 TIL 성장이 상당히 향상되었음을 입증했다. 난소의(ovarian), 두경부(head and neck), 결장의(colorectal), 흑색종, 자궁의(cervical) 및 폐암을 포함하는 다양한 고형 암의 대표적인 종양 단편들의 수를 사용하여 설명되었다. 이것은 T-세포 활성을 하향조절하는 것으로 알려진 T-세포들 상에 발현된 수용체들을 억제하는 방법(how)이 그들의 리간드들을 억제하는 것과 유사한 효과를 갖는 것을 보여주는 예이며, 그리고 이것은 고갈된 T 세포들을 재활성하고 어린 TIL 성장을 증가시키는 것 모두가 TIL 성장에 유사한 효과를 생성할 수 있다는 것을 보여주는 예이다. 이에 따라 PD1/PD-L1 실시예는 CTLA-4, LAG-3, TIGIT, KIR, TIM-3, BTLA 및 그들의 리간드들과 같은 T 세포들 상에 발현된 다른 수용체들에 대한 수용체/리간드 억제에 대한 보다 일반적인 경향을 예시했다.
도 28-33에서, 표준 TIL 제조 프로토콜, PD-1 그룹 또는 PD-L1 그룹의 초기 TIL 배양들에 TME 자극제들을 추가하는 효과는 각각 난소의, 흑색종, 폐, 두경부, 결장의, 및 자궁 경부암에서 설명되었다. 모든 조건들에서 중요하지는 않지만, 그 효과는 도 27의 범-종양 PD-1/PD-L1 실시예와 같이 암들 사이의 유사한 패턴을 보여주었다.
실시예 10 - 다른 제조업체들의 TME 자극제들은 유사한 TIL 성장 자극 효과를 나타냈다
도 34에 예시된 실시예 10은, 다른 제조업체들의 TME 자극제들을 첨가하는 것이 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 추가될 때 유사한 효과를 가졌으며, 이는 TIL 성장을 상당히 향상시키고 제조 기원(origin)과 무관하게 종양 단편 당 생존 세포들의 더 많은 수를 생성하였음(resulted in)을 입증한다. 이것은 난소의, 흑색종, 두경부, 및 자궁 경부암을 포함하는 다양한 고형 암들의 대표적인 수의 종양 단편들을 사용하여 설명되었다.
2개 PD-1 억제제들 (펨브롤리주맙, Merck Sharp Dome 및 니볼루맙, Bristol Myers Squibb) 및 2개 PD-L1 억제제들 (아벨루맙, Merck KgaA 및 더발루맙, AstraZeneca)은 이 실시예에서 테스트되었다. 모든 다른 TME 자극제들(stimulators)은 TIL 성장을 가속화하는 능력에서 표준 어린 TIL 프로토콜에 비해 상당한 개선을 보였다. 4개의 다른 항체들이 개별 억제제들 간에는 물론 그룹 A와 비교하여 유사한 효과들을 나타내는 경향이 있었다.
이것은 일반적으로 다양한 제조업체들의 TME 자극제들이 어떻게 상호교환가능하고 그리고 어린 TIL 제조 처리(process)를 최적화하는데 사용될 수 있는지에 대한 실시예였다.
도 35-38에서, 초기 TIL 배양들에 다른 제조업체들의 그룹 A의 억제제들을 추가하는 효과는 난소의(ovarian), 흑색종, 두경부, 및 자궁 경부암 각각에서 설명되었다. 모든 조건들에서 중요하지는 않지만, 효과는 도 34의 범-종양 실시예와 같이 암들 사이의 유사한 패턴을 보였다.
실시예 11 - 어린 TIL 성장을 더욱 향상시킨 TME 자극제들의 조합들
실시예 2에 기재된 바와 같이 수행된 이 실시예는, 다양한 조합들의 TME 자극제들이 배양 배지에 첨가되었을 때, 다양한 종양 유형들로부터 TIL 배양들이 개시되었을 때, TIL 수율이 표준 TIL 제조 프로토콜과 비교하여 증가되었음을 입증하였다.
TIL 배양들을 수확할 때 TIL 수율이 조사되었다. 그룹 A (PD-1 억제제또는 그것의 리간드들), 그룹 B (CTLA-4 억제제)의 TME 자극제들을 추가할 때, 또는 표준 어린 TIL 프로토콜과 비교하여 그룹 A 및 B 모두를 추가할 때, TIL 확장은 상당히 증가했음을, 도 39에 설명된 첫 번째 분석이 입증했다. 중요하지는 않지만 그룹 A 및 B의 TME 자극제들을 함께-첨가하는 것은 TIL 성장률을 더욱 개선시키는 경향이 있었다.
도 40에 예시된 또 다른 분석에서, 4-1BB 작용제인, 우렐루맙과 함께 항-CD3 (OKT3) (그룹 J) 단독, 또는 CTLA-4 억제제인, 이필리무맙 (그룹 B) 조합에서, 또는 PD-1 억제제인, 펨브롤리주맙 (그룹 A) 조합에서, 또는 이필리무맙 및 펨브롤리주맙 모두의 삼중 조합에서 모두 다양한 암들의 종양 단편 당 생존 세포들에서 매우 강한 TIL 성장을 보였다.
도 41에서 어린 TIL 배양에 우렐루맙/OKT3을 추가하기 위한 시간-지연 효과가 조사되었다. 여기서, 0일에 초기 어린 TIL 배양에 첨가된 우렐루맙/OKT3, 이필리무맙 및 펨브롤리주맙의 삼중 조합은(도면의 왼쪽) 이필리무맙과 펨브롤리주맙을 추가하는 것과 비교되었고 그리고 시간-지연으로 우렐루맙/OKT3을 추가하기 위해 2일 기다리는 것과 비교되었다(도면의 오른쪽). 두 조건들 사이에는 큰 차이가 없었고 그리고 두 조건들 모두 매우 강한 TIL 성장을 보였다.
도 42에서, 초기 어린 TIL 배양에 테랄리주맙 단독 (도면의 왼쪽) 또는 이필리무맙과 펨브롤리주맙 둘다 조합하여 첨가하는 효과가 조사되었다. 중요하지는 않지만, 삼중 조합이 테랄리주맙 단독에 비해 어린 TIL들에서 더 빠른 성장률을 유도하는 경향이 있었다.
실시예 12 - TME-자극제들 단독 또는 조합으로 탈체(ex vivo)TIL 확장의 증가된 성공률
이 실시예는 실시예 2에 기재된 바와 같이 수행된 TIL 배양 개시(initiation) 동안 TME 자극제들이 배양 배지에 첨가되었을 때, 탈체 TIL 확장의 성공률이 증가되었음을 입증하였다.
TIL 배양들을 수확할 때 종양 단편 당 세포 수를 결정함으로써 TIL 확장의 성공률이 조사되었다. 5x104 TIL들/단편은 성공적인 TIL 배양을 위한 임계값(threshold)으로 설정되었다.
TIL 확장의 성공률을 결정한 결과, 도 43에 예시된, 기준선(baseline) 배양들 61.5%와 비교하여, 다른 그룹들의 TME 자극제들이 "어린" TIL 배양들에 단독으로 또는 조합하여 추가되었을 때 TIL 배양들의 성공률이 증가되었음을 입증했다(그룹 A 76.3%, 그룹 B 88.5%, 그룹 J 100.0%, 그룹 A+B 83.3%, 그룹 B+J 100.0%, 그룹 A+J 100.0%, 및 그룹 A+B+J 삼중 콤보(triple combo) 96.0%).
이 실시예는 TME 자극제들이 단독 또는 조합하여 배양 배지에 첨가될 때 TIL 배양들이 표준 TIL 제조 프로토콜과 비교하여 시작될 때, TIL 확장 탈체의 성공률이 증가했음을 입증했다.
실시예 13 -TME-자극제들 전체로서, 다른 그룹들로부터 및 조합하여, T 세포들의 빈도와 수를 향상시킨다
도 44-47에 예시된 실시예 13은, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 TME-자극제들을 추가하는 것 및 실시예 3에 기재된 바와 같이 항-CD3 유동 세포분석법(flow cytometry) 항체를 사용하여 T 세포들을 염색하는 것(staining)은 TIL 성장을 상당히 향상시켰으며, TIL 성장은 IL-2 단독과 비교하여 T 세포들의 증가된 빈도 (도 44) 및 T 세포들 종양 단편 당 더 많은 수의 생존 T 세포들(도 46)을 초래하였음을 입증했다. 이것은 난소의, 두경부, 결장의, 흑색종, 자궁의, 결장의, 및 폐암을 포함하는 다양한 고형 암들로부터 종양 단편들의 대표적인 수를 사용하여 설명되었다.
TME 자극제들을 기본(underlying) 하위그룹들(subgroupings)로 나누면(Breaking), 실시예는 또한 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함) 또는 그룹 B (CTLA-4 및 리간드의 억제제들)의 억제제들을 추가하면, T 세포들을 재활성화함으로써 IL-2 단독과 비교하여 T 세포들의 빈도도 상당히 증가했음(도 45) 을 입증했다. 종양 항원들에 대한 친화도가 더 높은 T 세포들이 고갈되는 경향이 증가할 수 있기 때문에, 이것은 더 많은 종양-반응성 T 세포들의 확장으로 이어질 수 있다. 게다가, 실시예는 또한, 그룹 B의 TME 자극제들을 추가하면 그룹 J (항-CD3와 함께 4-1BB 작용제) 또는 그룹 J, A 및 B의 조합에 비해 T 세포들의 빈도도 상당히 증가했음을 입증했다 (도 45).
TME 자극제들을 기본 하위그룹들로 나누면, 실시예는 또한 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4 및 리간드의 억제제들), 그룹 K (CD28 작용제들) 및 그룹 J (항-CD3과 함께 4-1BB 작용제)의 억제제들을 추가하면 또한 IL-2 단독과 비교하여 종양 단편 당 생존 T 세포들의 수가 상당히 증가했음을 입증했다(도 47). 게다가, 실시예는 또한 그룹 J, A 및 B의 TME 자극제들의 조합들을 추가하면 그룹 A, 그룹 B 또는 그룹 A 와 B의 조합과 비교하여 종양 단편 당 생존 T 세포들의 수도 상당히 증가했음을 입증했다(도 47). 게다가, 그룹 J의 TME 자극제들만 단독 추가하는 것과 비교하여 그룹 J, A 및 B의 TME 자극제들의 조합을 추가할 때 단편 당 더 생존 가능한 T 세포들이 있는 경향이 있다 (도 47).
이 실시예를 요약하면, 어린 TIL 제조 단계에 TME 자극제들을 추가하는 것은 T 세포들의 증가된 빈도와, 생존 T 세포들의 증가된 수를 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 프로토콜에 비해(over) 새로운 개선을 제공했다.
실시예 14 -TME-자극제들 전체로서, 다른 그룹들로부터 및 조합하여 반응기(effector)-메모리 T 세포들의 빈도를 유지한다
도 48에 예시된 실시예 14는, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 제조 프로토콜에 TME-자극제들을 첨가하는 것 그리고 실시예 3에 기재된 바와 같이 항-CD3, 항-CD45RA 및 항-CCR7 유동 세포분석법(flow cytometry) 항체들을 사용하여 T 세포들을 염색하는 것(staining)은 IL-2 단독에 비해 CD4+ T 세포들에서 반응기-메모리 T 세포들의 빈도를 상당히 증가시켰고 그리고 CD8+ T 세포들에서 반응기 메모리 T 세포들의 빈도를 약간 증가시켰음을 입증했다. 이것은 난소의(ovarian), 두경부(head and neck), 결장의(colorectal), 흑색종, 자궁의(cervical), 결장의(colorectal), 및 폐암을 포함하는 다양한 고형 암들의 종양 단편들의 대표적인 수를 사용하여 설명되었다.
이 실시예를 요약하면, 어린 TIL 제조 단계에 TME 자극제들을 추가하는 것은 유사한 빈도의 반응기 메모리 T 세포들을 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 프로토콜에 대한(over) 새로운 개선을 제공했다.
실시예 15 - TME-자극제들 조합하여 CD8+ T 세포들의 빈도와 수를 향상시킨다
도 49-50에 예시된 실시예 15는, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 제조 프로토콜에 그룹 J (항-CD3과 함께 4-1BB 작용제), 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함) 및 그룹 B (CTLA-4 및 리간드의 억제제들)의 TME 자극제들의 조합을 추가하는 것 및 실시예 3에 기재된 바와 같이 항-CD3 및 항-CD8 유동 세포분석법 항체들을 사용하여 T 세포들을 염색하는 것은 IL-2 단독과 비교하여 CD8+ T 세포들의 빈도(도 49) 및 수(도 50)를 상당히 증가시키는 CD8+ T-세포 성장을 상당히 향상시켰음을 입증했다. 이것은 난소의, 두경부, 결장의, 흑색종, 자궁의, 결장의, 및 폐암을 포함하는 다양한 고형 암들의 종양 단편들의 대표적인 수를 사용하여 설명되었다.
실시예는 또한 그룹 J (항-CD3와 함께 4-1BB 작용제), 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함) 및 그룹 B (CTLA-4의 억제제들)의 TME 자극제들의 조합을 표준 어린 TIL에 추가하는 것이 그룹 A, 그룹 B 또는 그룹 J 단독의 TME 자극제들을 추가하는 것과 비교하여 CD8+ T 세포들 성장을 향상시키는 경향을 보여주었다는 것을 입증했다(도 49). 또한, 실시예는 또한 그룹 J, 그룹 A 및 그룹 B의 TME 자극제들의 조합을 추가하면 그룹 A 또는 그룹 B 단독과 비교하여 생존 CD8+ T 세포들의 수가 상당히 증가하였고 그리고 그룹 J 단독과 비교하여 생존 CD8+ T 세포들의 수가 증가하는 경향을 보였음을 입증했다 (도 50).
TIL 주입 생성물에서 CD8+ T 세포들의 증가된 빈도는 이전에 전이성 흑색종을 갖는 환자에서 TIL 치료의 유익한 임상 결과와 관련이 있었다 (Radvanyi, L. G. et al., Specific lymphocyte subsets predict response to adoptive cell therapy using expanded autologous tumor-infiltrating lymphocytes in metastatic melanoma patients. Clin. Cancer Res. 18, 6758-6770 (2012)). 따라서, CD8+ T-세포 빈도를 증가시키는 방법들은 표준 TIL 프로토콜을 사용하여 제조된 TIL들에 반응하지 않는 암 환자들에서 임상 반응들을 유도할 수 있었다.
이 실시예를 요약하면, TME 자극제들 단독 그리고 어린 TIL 처리(processing) 단계에 조합하여 추가하는 것은 CD8+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했다.
실시예 16 - TME-자극제들 조합하여 CD4+ T 세포들의 빈도를 감소시킨다
도 51에 예시된 실시예 16은 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 그룹 J (항-CD3와 함께 4-1BB 작용제), 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함) 및 그룹 B (CTLA-4의 억제제들)의 TME 자극제들의 조합을 추가하는 것 그리고 실시예 3에 기재된 바와 같이 항-CD3 및 항-CD4 유동 세포분석법 항체들을 사용하여 T 세포들을 염색하는 것은 CD4+ T-세포 성장을 상당히 감소시켰고, 이는 IL-2 단독과 비교하여 CD4+ T 세포들의 빈도를 상당히 감소시켰음을 입증했다(도 51). 이것은 난소의, 두경부, 결장의(colorectal), 흑색종, 자궁의(cervical), 결장의(colorectal), 및 폐암을 포함하는 다양한 고형 암들의 대표적인 수의 종양 단편들을 사용하여 설명되었다.
이 실시예를 요약하면, 어린(young) TIL 처리(processing) 단계에 TME 자극제들을 추가하는 것은 CD4+ T 세포들의 빈도가 감소된 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했다.
실시예 17 - 다른 그룹들의 TME-자극제들은 NK 세포들의 빈도를 감소시킨다
도 52에 예시된 실시예 17은, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함) 또는 그룹 B (CTLA-4의 억제제들)의 TME 자극제들을 추가하는 것 및 실시예 3에 기재된 바와 같이 항-CD3 및 항-CD56 유동 세포분석법 항체들을 사용하여 NK 세포들을 염색하는 것은 IL-2 단독에 비해 NK 세포들의 빈도를 감소시키는 T 세포들을 상당히 재활성화시켰음(reinvigorated)을 입증했다. 이것은 더 많은 종양-반응성 T 세포들의 확장으로 이어질 수 있다. 이것은 난소의, 두경부, 결장의, 흑색종, 결장의, 결장의, 및 폐암을 포함하는 다양한 고형 암들의 대표적인 수의 종양 단편들을 사용하여 설명되었다.
또한, 실시예는 그룹 B의 TME 자극제들을 추가하는 것이 그룹 J (항-CD3와 함께 4-1BB 작용제) 및 그룹 K (CD28 작용제들)와 비교하여 감소된 NK 세포 빈도에 대한 경향을 보였음을 입증했다.
이 실시예를 요약하면, 어린 TIL 처리(processing) 단계에 TME 자극제들을 첨가하는 것은 NK 세포들의 감소된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했다.
실시예 18 - 다른 그룹들로부터 또는 조합하여 TME-자극제들은 NK 및 T 세포들 전체 및 특히 CD8+ T 세포들의 빈도에 영향을 미친다
도 53 및 도 54에 예시된 실시예 18은, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 우렐루맙/OKT3 (그룹 J) 단독으로 또는 펨브롤리주맙 (그룹 A) 또는 이필리무맙 및 펨브롤리주맙과 조합하여(그룹 B+A) 첨가하는 것 그리고 실시예 3에 기재된 바와 같이 항-CD3, 항-CD56 및 항-CD8 유동 세포분석법 항체들을 사용하여 NK 세포들 및 T 세포들을 염색하는 것은 하나의 두경부암 샘플에서 IL-2 단독과 비교하여 NK 세포들의 증가된 빈도와 T 세포들의 감소된 빈도를 초래하는 NK 세포들을 재활성화시켰음을 입증했다(도 53). NK 세포들의 이 재활성화(reinvigoration)는, 표준 어린 TIL 제조 프로토콜에 우렐루맙 /OKT3 (그룹 J) 단독 또는 펨브롤리주맙 (그룹 A) 또는 이필리무맙 및 펨브롤리주맙(그룹 B+A)과 조합하여 추가하는 것과 비교하여 NK 세포들의 감소된 빈도와 T 세포들의 증가된 빈도를 초래하는, T 세포들을 재활성화하는 TIL 배양에 우렐루맙/OKT3에 더하여 이필리무맙을 첨가함으로써 억제되었다. 이것은 두경부암의 대표적인 샘플을 사용하여 설명되었다.
또한, 실시예는 우렐루맙/OKT3 (그룹 J) 및 이필리무맙(그룹 B)을 추가하면 우렐루맙/OKT3 단독, 우렐루맙/OKT3 및 펨브롤리주맙(그룹 A) 및 우렐루맙/OKT3, 이필리무맙 및 펨브롤리주맙과 비교하여 CD8+ T 세포 빈도가 감소했음을 입증했다(도 54).
따라서, 실시예는 우렐루맙/OKT3 (그룹 J), 이필리무맙 (그룹 B) 및 펨브롤리주맙(그룹 A)을 추가하는 것은 우렐루맙/OKT3 및 이필리무맙 단독과 비교하여 유리할(favorable) 수 있음을 입증했다.
이 실시예를 요약하면, 어린 TIL 처리(processing) 단계에 TME 자극제들을 추가하는 것은, NK 세포들의 빈도는 감소하지만 CD8+ T 세포들의 빈도는 증가하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 비해 새로운 개선을 제공했다.
실시예 19 - 시간 지연과 함께 추가된 TME-자극제들을 조합하여 CD3+ 및 CD8+ T 세포들의 빈도를 향상시키고 그리고 NK 세포들 및 CD4+ T 세포들의 빈도를 감소시킨다
도 55에 예시된 실시예 19는 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 0일에 그룹 A (PD1 및 그것이 리간드 PD-L1의 억제제들을 포함) 및 그룹 B (CTLA-4의 억제제들)의 TME 자극제들 및 2일 째 그룹 J (항-CD3와 함께 4-1BB 작용제) 의 TME 자극제의 조합을 추가하는 것 그리고 실시예 3에 기재된 바와 같이 항-CD3, 항-CD56, 항-CD8 및 항-CD4 유동 세포분석법 항체들을 사용하여 T 세포들을 염색하는 것은, 0일에 같은 그룹의 TME 자극제들의 첨가 (A, B 및 J)와 비교하여 총 T 세포들(CD3+) 및 CD8+ T 세포들(도 55) 의 증가된 빈도 및 감소된 NK 세포 및 CD4+ T 세포 빈도를 초래하는, T 세포 및 CD8+ T-세포 성장을 향상시켰음을 입증했다. 난소의, 두경부, 결장의, 흑색종, 자궁의, 결장의, 및 폐암을 포함하는 다양한 고형 암들의 대표적인 수의 종양 단편들을 사용하여 설명되었다. 시간 지연은 그룹 J 작용제들을 추가하기 전에 조절되는 CD-4+ T-세포들을 감소시키고 그리고 CD-8+ T-세포들을 재활성화하는 그룹 A 및 B 길항제들의 더 강력한 효과를 허용하는 것으로 보였다.
이 실시예를 요약하면, 어린 TIL 처리(processing) 단계에 시간 지연이 있는 TME 자극제들을 추가하는 것은 전체적으로 증가된 빈도의 T 세포들, CD8+ T 세포들 및 감소된 빈도의 NK 세포들 및 CD4+ T 세포들을 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 대해 새로운 개선을 제공했다.
실시예 20 - TME-자극제들 단독 또는 조합하여 LAG3+ T 세포들의 빈도를 향상시킨다
도 56 및 도 57에 예시된 실시예 20은, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4의 억제제들), 그룹 K (CD28 작용제들) 또는 그룹 J (항-CD3와 함께4-1BB 작용제)의 TME 자극제들 단독 또는 조합하여 첨가하는 것 그리고 실시예 3에 기재된 바와 같이 항-CD3, 항-CD8, 항-CD4 및 항-LAG-3 유동 세포분석법 항체들을 사용하여 T 세포들을 염색하는 것은 IL-2 단독에 비해 CD4+ 및 CD8+ T 세포들 모두에서 LAG-3+ T 세포들의 증가된 빈도를 초래하는 종양-특이적 T 세포들의 재활성화를 강화시켰음을 입증했다(도 56). 특히 CD4+ LAG-3+ T 세포들의 빈도는 그룹 A 및 B의 TME 자극제들을 추가할 때 상당히 더 높았다. 이것은 난소의, 두경부, 결장의, 흑색종, 자궁의, 결장의, 및 폐암을 포함하는 다양한 고형 암들의 대표적인 수의 종양 단편들을 사용하여 설명되었다.
또한, 실시예는 그룹 A, B 및 J의 TME 자극제들을 조합하여 추가하는 것과 비교하여 실시예 19에 기재된 바와 같이 시간 지연에서 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4의 억제제들), 또는 그룹 J (항-CD3와 함께 4-1BB 작용제)의 TME 자극제들의 조합을 추가하는 것은 CD8+ LAG-3+ T 세포들의 증가된 빈도를 초래하는 종양-특이적 CD8+ T 세포들의 증가된 재활성화에 대한 경향을 보였음을 입증했다(도 57).
이 실시예를 요약하면, 어린 TIL 처리(processing) 단계에 TME 자극제들을 추가하는 것은 종양-특이적 LAG-3+ T 세포들의 증가된 빈도를 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 대해 새로운 개선을 제공했다. As LAG-3은 T-세포 고갈의 마커(marker)로 알려져 있고 그리고 종양 항원들에 대한 친화도가 높은 T 세포들은 일반적으로 고갈되는 경향이 증가하기 때문에, CD8+ LAG-3+ T 세포 클론들(clones)의 확장은 종양-반응성 T-세포들의 더 높은 비율을 유도할 수 있어 TIL 요법에 대한 이 새로운 접근법의 개선된 임상 결과를 초래할 수 있다.
실시예 21 -CD28+인 더 어린(younger) 표현형을 갖는 CD8 T-세포들의 빈도를 증가시킨TME-자극제들
도 58에 예시된 실시예 21은, 실시예 2에 기재된 바와 같이 수행된 표준 어린 TIL 프로토콜에 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4의 억제제들), 그룹 K (CD28 작용제들) 또는 그룹 J (항-CD3와 함께 4-1BB 작용제)로부터 TME 자극제들 단독 또는 조합하여 첨가하는 것 그리고 실시예 3에 기재된 바와 같이 항-CD3, 항-CD8 및 항-CD28 유동 세포분석법 항체들을 사용하여 T 세포들을 염색하는 것은 IL-2 단독과 비교하여 CD8+ CD28+ T 세포들의 증가된 빈도를 초래는 더 어린 표현형을 갖는 T 세포들의 확장을 향상시켰음을 입증했다(도 58). 이것은 난소의, 두경부(head and neck), 결장의(colorectal), 흑색종, 자궁의(cervical), 결장의(colorectal), 및 폐암을 포함하는 다양한 고형 암들로부터 대표적인 수의 종양 단편들을 사용하여 설명되었다.
또한, 실시예는 그룹 A 또는 그룹 B 단독으로부터 TME 자극제들을 추가하는 것과 비교하여 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4의 억제제들), 또는 그룹 J (항-CD3과 함께 4-1BB 작용제)로부터 TME 자극제들의 조합을 추가하는 것(adding)은 CD8+ CD28+ T 세포들의 증가된 빈도를 초래하는 더 어린 표현형을 갖는 T 세포들의 증가된 확장에 대한 경향을 보였음을 입증했다(도 58).
또한, 실시예는, 그룹 A 또는 그룹 B 단독으로부터 TME 자극제들 또는 시간 지연 없이 그룹 A, 그룹 B 및 그룹 J 로부터 TME 자극제들의 조합하여 첨가하는 것(adding)과 비교하여, 실시예 19에 기재된 바와 같이 시간 지연을 갖고 그룹 A (PD1 및 그것의 리간드 PD-L1의 억제제들을 포함), 그룹 B (CTLA-4의 억제제들) 및 그룹 J (항-CD3과 함께 4-1BB 작용제)로부터 TME 자극제들의 조합을 첨가하는 것은 CD8+ CD28+ T 세포들의 증가된 빈도를 초래하는 더 어린 표현형을 갖는 T 세포들의 증가된 확장에 대한 경향을 보였음을 입증한다(도 58).
이 실시예를 요약하면, TME 자극제들을 어린 TIL 처리 단계에 추가하는 것은 CD28을 발현하는 더 어린 표현형을 갖는 증가된 빈도의 CD8+ T 세포들을 포함하는 TIL 생성물의 생성을 허용하는 기존 표준 TIL 제조 프로토콜에 대한 새로운 개선을 제공했다 .
항목들(items)
1. 다음을 포함하며, 종양 침윤 림프구들 (TIL들)을 TIL들의 치료적 집단으로 확장함으로써 포유동물에서 암의 퇴행을 촉진하는 방법으로서:
- (a) 포유동물의 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계
- (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계;
- (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, TIL들의 제3집단은 치료적 집단이며; 및
- (d) 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되고, 그래서 포유동물에서 암의 퇴행이 촉진된다.
2. 다음을 포함하며, 확장된 종양 침윤 림프구들 (TIL들)을 투여하는 것을 포함하는 암을 갖는 대상을 치료하는 방법으로서:
- (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계,
- (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계;
- (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이고; 및
- (d) 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되고, 그래서 포유동물에서 암의 퇴행이 촉진된다.
3. 다음을 포함하며 종양 침윤 림프구들 (TIL들)을 TIL들의 치료적 집단으로 확장하기 위한 방법으로서:
- (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계
- (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; 및
- (c) TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단이다.
4. 1항 내지 3항 중 어느 한 항에 있어서, 하나 이상의 TME 자극제들은 하기로 구성되는 그룹들로부터 선택되는 방법:
- (x) T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들 (또는 그들의 리간드들) 상에서 발현되는 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 하나 이상의 물질들,
- (y) T-세포 상향조절, 활성화, 및/또는 재활성화를 유발하는 것으로 알려진 T-세포들 상에서 발현되는 수용체들을 작용시키는 것(agonizing) 및/또는 자극하는 것을 할 수 있는 하나 이상의 물질들,
- (z) T-세포 하향조절, 비활성화, 및/또는 고갈을 유발하는 것으로 알려진 가용성(soluble) 분자들 및 시토킨들 및 그들의 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 하나 이상의 물질들, 및
- (v) 하나 이상의 물질들 조절되는(regulatory) T-세포들을 하향조절하는 것 및/또는 감소시키는 것을 할 수 있고 이에 따라 탈체(ex-vivo) 반응기(effector) T-세포 확장을 촉진할(favoring) 수 있는 하나 이상의 물질들, 및
- (w) 표 2-41에 나열된 것처럼 그룹들 (x), (y), (z) 및/또는 (v)로부터 하나 이상의 물질들의 특정 조합들.
5. 1항 내지 4항 중 어느 한 항에 있어서, 하나 이상의 TME 자극제들은 하나 이상의 체크포인트 억제제들 또는 그들의 리간드들의 억제제들 예를 들어 항-PD1, 항-PD-L1, 항-PD-L2, 항-CTLA-4, 항-LAG3, 항-A2AR, 항-B7-H3, 항 B7-H4, 항-BTLA, 항-IDO, 항-HVEM, 항-IDO, 항-TDO, 항-KIR, 항-NOX2, 항-TIM3, 항-갈랙틴(galectin)-9, 항-VISTA, 항-SIGLEC7/9이고, 및 하나 이상의 체크포인트 억제제들 또는 그들의 리간드들의 억제제들은 선택적으로 제2확장에도 추가되는 방법.
6. 1항 내지 5항 중 어느 한 항에 있어서, T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들(또는 그들의 리간드들) 상에 발현된 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 하기로 구성되는 그룹들로부터 선택되는 방법:
- A: T-세포들 상의 PD-1 수용체를 통해 작용하는 물질들,
- B: T-세포들 상의 CTLA-4 수용체를 통해 작용하는 물질들,
- C: T-세포들 상의 LAG-3 수용체를 통해 작용하는 물질들,
- D: T-세포들 상의 TIGIT/CD226 수용체를 통해 작용하는 물질들,
- E: T-세포들 상의 KIR 수용체를 통해 작용하는 물질들,
- F: T-세포들 상의 TIM-3 수용체를 통해 작용하는 물질들,
- G: T-세포들 상의 BTLA 수용체를 통해 작용하는 물질들, 및
- H: T-세포들 상의 A2aR 수용체를 통해 작용하는 물질들.
7. 6항에 있어서, 그룹 A의 물질은 펨브롤리주맙, 니볼루맙, 세미플리맙(cemiplimab), sym021, 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 및 더발루맙(durvalumab)으로 구성되는 그룹으로부터 하나 이상이 선택되는 방법.
8. 6-7항에 있어서, 그룹 B의 물질은 이필리무맙(ipilimumab) 및 트레멜리무맙(tremelimumab)으로 구성되는 그룹으로부터 하나 이상이 선택되는 방법.
9. 6-8항에 있어서, 그룹 C의 물질은 렐라틀리맙(relatlimab), 에프틸라기모 알파(eftilagimo alpha), 및 sym022으로 구성되는 그룹으로부터 하나 이상이 선택되는 방법.
10. 6-9항에 있어서, 그룹 D의 물질은 티라고루맙(tiragolumab)인 방법.
11. 6-10항에 있어서, 그룹 E의 물질은 리릴루맙(lirilumab)인 방법.
12. 6-11항에 있어서, 그룹 F의 물질은 sym023인 방법.
13. 6-12항에 있어서, 그룹 G의 물질은 40E4 및 PJ196인 방법.
14. 1항 내지 13항 중 어느 한 항에 있어서, T-세포 상향조절, 활성화, 및/또는 재활성화를 유발하는 것으로 알려진 T-세포들 상에 발현된 수용체들을 작용시키는 것(agonizing) 및/또는 자극하는 것을 할 수 있는 물질들은 하기로 구성되는 그룹들로부터 선택되는 방법:
- I: T-세포들 상의(on) OX40/CD134 수용체를 통해 작용하는 물질들,
- J: T-세포들 상의4-1BB/CD137 수용체를 통해 작용하는 물질들,
- K: T-세포들 상의 CD28 수용체를 통해 작용하는 물질들,
- L: T-세포들 상의 ICOS 수용체를 통해 작용하는 물질들,
- M: T-세포들 상의 GITR 수용체를 통해 작용하는 물질들,
- N: T-세포들 상의 CD40L 수용체를 통해 작용하는 물질들, 및
- O: T-세포들 상의 CD27 수용체를 통해 작용하는 물질들.
15. 14항에 있어서, 그룹 J의 물질은 우렐루맙 및 유토밀루맙으로 구성되는 그룹으로부터 하나 이상이 선택되는 방법.
16. 14항에 있어서, 그룹 K의 물질은 테랄루지맙(theraluzimab)인 방법.
17. 14항에 있어서, 그룹 O의 물질은 발릴루맙(valilumab)인 방법.
18. 1항 내지 17항 중 어느 한 항에 있어서, T-세포 하향조절, 비활성화, 및/또는 고갈을 유발하는 것으로 알려진 가용성 분자들 및 시토킨들 및 그들의 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 하기로 구성되는 그룹들로부터 선택되는 방법:
- P: T-세포들 상의 IDO1/2 수용체를 통해 작용하는 물질들,
- Q: T-세포들 상의 TGFβ 수용체를 통해 작용하는 물질들,
- R: T-세포들 상의 IL-10 수용체를 통해 작용하는 물질들, 및
- S: T-세포들 상의 IL-35 수용체를 통해 작용하는 물질들.
19. 14항에 있어서, 그룹 P의 물질은 에파세도스타트(epacedostat)인 방법.
20. 14항에 있어서, 그룹 Q의 물질은 린로도스타트(linrodostat)인 방법.
21. 14항에 있어서, 그룹 R의 물질은 갈루니서팁(galunisertib)인 방법.
22. 1항 내지 21중 어느 한 항에 있어서, 조절되는 T-세포들을 하향조절하는 것 및/또는 감소시키는 것을 할 수 있고 이에 따라 탈체(ex-vivo) 반응기(effector) T-세포 확장을 촉진할(favoring) 수 있는 물질들은 하기로 구성되는 그룹들로부터 선택되는 방법:
- T: 시클로포스파미드들(cyclophosphamides),
- U: TKI들,
- V: αCD25를 통해 작용(act)하는 물질들, 및
- X: IL2/디프테리아(Diphteria) 독소(toxin) 융합들(fusions).
23. 20항에 있어서, 그룹 U의 물질은 수니티닙(sunitinib)인 방법.
24. 20항에 있어서, 그룹 V의 물질은 소라페닙(sorafenib), 이매티닙(imatinib) 및 다클리주맙(daclizumab)으로 구성되는 그룹으로부터 하나 이상이 선택되는 방법.
25. 20항에 있어서, 그룹 X의 물질은 데닐류킨 디피톡스(dinileukin diftitox)인 방법.
26. 1항 내지 25항 중 어느 한 항에 있어서, 물질의 농도는 0.1㎍/mL 내지 300㎍/mL, 예를 들어 1㎍/mL 내지 100㎍/mL, 예를 들어 10㎍/mL 내지 100㎍/mL, 예를 들어1㎍/mL 내지 10㎍/mL인 방법.
27. 1항 내지 26항 중 어느 한 항에 있어서, T 세포들의 치료적 집단은 하기로 구성되는 그룹들로부터 선택되는 암 유형을 치료하는데 사용되는 방법:
- 1: 고형(solid) 종양들,
- 3: MSI-H 종양들,
- 4: 혈액의(Hematological) 종양들, 및
- 5: 과-돌연변이(Hyper-mutated) 종양들.
28. 1항 내지 27항 중 어느 한 항에 있어서, T 세포들의 치료적 집단은 유방암, 신장 세포암, 방광암, 흑색종, 자궁 경부암, 위암, 결장암, 폐암, 두경부암, 난소암, 호지킨 림프종, 췌장암, 간암, 및 육종으로 구성되는 그룹들로부터 선택되는 암 유형을 치료하는데 사용되는 방법.
29. 1항 내지 28항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 유방암을 치료하는데 사용되는 방법.
30. 1항 내지 29항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 신장 세포암을 치료하는데 사용되는 방법.
31. 1항 내지 30항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 방광암을 치료하는데 사용되는 방법.
32. 1항 내지 31항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 흑색종을 치료하는데 사용되는 방법.
33. 1항 내지 32항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 자궁 경부암을 치료하는데 사용되는 방법.
34. 1항 내지 33항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 위암을 치료하는데 사용되는 방법.
35. 1항 내지 34항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 결장암을 치료하는데 사용되는 방법.
36. 1항 내지 35항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 폐암을 치료하는데 사용되는 방법.
37. 1항 내지 36항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 두경부암을 치료하는데 사용되는 방법.
38. 1항 내지 37항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 난소암을 치료하는데 사용되는 방법.
39. 1항 내지 38항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 호지킨 림프종을 치료하는데 사용되는 방법.
40. 1항 내지 39항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 췌장암을 치료하는데 사용되는 방법.
41. 1항 내지 40항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 간암을 치료하는데 사용되는 방법.
42. 1항 내지 41항 중 어느 한 항에 있어서, T세포들의 치료적 집단은 육종을 치료하는데 사용되는 방법.
43. 1항 내지 42항 중 어느 한 항에 있어서, 단계들 (a) 내지 (c) 또는 (d)는 약 20 일 내지 약 45 일의 기간 내에 수행되는 방법.
44. 1항 내지 43항 중 어느 한 항에 있어서, 단계들 (a) 내지 (c) 또는 (d)는 약 20 일 내지 약 40 일의 기간 내에 수행되는 방법.
45. 1항 내지 44항 중 어느 한 항에 있어서, 단계들 (a) 내지 (c) 또는 (d)는 약 25 일 내지 약 40 일의 기간 내에 수행되는 방법.
46. 1항 내지 45항 중 어느 한 항에 있어서, 단계들 (a) 내지 (c) 또는 (d)는 약 30 일 내지 약 40 일의 기간 내에 수행되는 방법.
47. 1항 내지 46항 중 어느 한 항에 있어서, 단계들 (a) 내지 (b)는 약 10 일 내지 약 28 일의 기간 내에 수행되는 방법.
48. 1항 내지 47항 중 어느 한 항에 있어서, 단계들 (a) 내지 (b)는 약 10 일 내지 약 20 일의 기간 내에 수행되는 방법.
49. 1항 내지 48항 중 어느 한 항에 있어서, 단계 (c)는 약 12 일 내지 약 18 일의 기간 내에 수행되는 방법.
50. 1항 내지 49항 중 어느 한 항에 있어서, 단계 (c)는 약 10 일 내지 약 28 일의 기간 내에 수행되는 방법.
51. 1항 내지 50항 중 어느 한 항에 있어서, 단계 (c)는 약 10 일 내지 약 20 일의 기간 내에 수행되는 방법.
52. 1항 내지 51항 중 어느 한 항에 있어서, 단계 (c)는 약 12 일 내지 약 18 일의 기간 내에 수행되는 방법.
53. 1항 내지 52항 중 어느 한 항에 있어서, 단계 (b)는 1 x 106 내지 1x 107 세포들, 예를 들어 2 x 106 내지 5x 106 세포들을 생성하는(results in) 방법.
54. 1항 내지 53항 중 어느 한 항에 있어서, 단계 (c)는 1 x 107 내지 1x 1012 세포들, 예를 들어 1 x 108 내지 5x 109 세포들, 예를 들어 1 x 109 내지 5x 109 세포들, 예를 들어 1 x 108 내지 5x 1010 세포들, 예를 들어 1 x 109 내지 5x 1011 세포들을 생성하는 방법.
55. 1항 내지 54항 중 어느 한 항에 있어서, APC들은 인공의 APC들 (aAPC들) 또는 동종이계의(allogeneic) 피더(feeder) 세포들인 방법.
56. 1항 내지 55항 중 어느 한 항에 있어서, TIL들의 치료적 집단은 환자에게 주입되는(infused) 방법.
57. 1항 내지 56항 중 어느 한 항에 있어서, 세포들은 단계 (c)를 수행하기 전에 세포 배양(cell culture)으로부터 제거되고 저장 배지(storage medium)에서 동결보존되는 방법 .
58. 1항 내지 57항 중 어느 한 항에 있어서, T-세포 신호전달(signaling) 분자의 적어도 하나의 엔도도메인(endodomain)과 융합된(fused) 단일 사슬(single chain) 가변 단편(variable fragment) 항체를 포함하는 키메라(chimeric) 항원 수용체(receptor) (CAR)를 인코딩(encoding)하는 핵산(nucleic acid)을 포함하는 발현 벡터(expression vector)로 TIL들의 제1집단을 형질도입하는(transducing) 단계를 추가로 포함하는 방법.
59. 1항 내지 58항 중 어느 한 항에 있어서, 단계 (c)는 세포 배양 배지로부터 세포들을 제거하는 단계를 추가로 포함하는 방법.
60. 1항 내지 59항 중 어느 한 항에 있어서, 단계 (a)는 절제된 종양을 다중 종양 단편들, 예를 들어 4 내지 50 단편들, 예를 들어 20 내지 30 단편들로 처리하는 것을 추가로 포함하는 방법.
61. 60항에 있어서, 단편들은 약 5 내지 50 mm3, 20 내지 50 mm3의 크기를 갖는 방법.
62. 1항 내지 61항 중 어느 한 항에 있어서, 포유동물은 인간인 방법.
63. 1항 내지 62항 중 어느 한 항에 있어서, 세포 배양 배지는 G-Rex 용기(container) 및 Xuri 셀백(cellbag)으로 구성되는 그룹으로부터 선택된 용기에 제공되는 방법.
64. 1항 내지 63항 중 어느 한 항에 있어서, 항-CD3 항체는 OKT3인 방법.
65. 1항 내지 63항 중 어느 한 항에 따른 방법에 의해 얻을 수 있는 종양 침윤 림프구들 (TIL들)의 집단.
66. 암에 걸린 대상을 치료하는데 사용하기 위한 확장된 종양 침윤 림프구들 (TIL들)로서, 다음 단계들을 포함하는 치료:
- 포유동물의 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계
- IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에서 TIL들의 제1집단을 배양함으로써 제1확장을 수행하여 TIL들의 제2집단을 생성하는 단계;
- TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, TIL들의 제3집단은 치료적 집단이며; 및
- 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에게 T 세포들의 치료적 집단을 투여하는 단계, T 세포들은 포유동물에 투여되고, 이것에 의해 포유동물의 암의 퇴행이 촉진된다.
67. 다음을 포함하는 방법에 의해 얻을 수 있는 종양 침윤 림프구들 (TIL들)의 집단:
포유동물의 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계
TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들을 포함하는 세포 배양 배지에 TIL들의 제1집단을 배양함으로써 제1확장을 수행하는 단계; 및
TIL들의 제3집단을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체, 및 항원 제시 세포들 (APC들)을 보충함으로써 제2확장을 수행하는 단계, TIL들의 제3집단은 치료적 집단이다.
68. IL-2 및 하나 이상의 TME 자극제들을 포함하는 TIL들의 치료적 집단.
69. IL-2, 하나 이상의 TME 자극제들, IL-2, 항-CD3 항체, 및 항원 제시(presenting) 세포들 (APC들)을 포함하는 TIL들의 치료적 집단.
Claims (20)
- 암에 걸린 대상(subject)을 치료하는데 사용하기 위한 확장된 종양 침윤 림프구들(Expanded tumor infiltrating lymphocytes)(TIL들)로서, 상기 치료는 다음 단계들을 포함한다:
- 포유동물로부터 절제된(resected) 종양(tumor)으로부터 TIL들의 제1집단(first population)을 획득(obtaining)함으로써 자가의(autologous) T 세포들을 배양하는(culturing) 단계
- TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들(stimulators)을 포함하는 세포 배양 배지(cell culture medium)에서 TIL들의 제1집단을 배양함으로써 제1확장(first expansion)을 수행하는 단계;
- TIL들의 제3집단(third population)을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체(anti-CD3 antibody), 및 항원 제시 세포들(antigen presenting cells)(APC들)을 보충함으로써 제2확장(second expansion)을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단(therapeutic population)이고; 및
- 비골수제거(nonmyeloablative) 림프구제거(lymphodepleting) 화학요법(chemotherapy)을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되고, 그래서(whereupon) 포유동물에서 암의 퇴행(regression)이 촉진된다(promoted).
- 암에 걸린 대상(subject)에서 암의 퇴행(regression)을 촉진하는데 사용하기 위한 확장된 종양 침윤 림프구들(Expanded tumor infiltrating lymphocytes)(TIL들)로서, 상기 퇴행은 다음 단계들을 포함한다:
- 포유동물로부터 절제된(resected) 종양(tumor)으로부터 TIL들의 제1집단(first population)을 획득(obtaining)함으로써 자가의(autologous) T 세포들을 배양하는(culturing) 단계
- TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들(stimulators)을 포함하는 세포 배양 배지(cell culture medium)에서 TIL들의 제1집단을 배양함으로써 제1확장(first expansion)을 수행하는 단계;
- TIL들의 제3집단(third population)을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체(anti-CD3 antibody), 및 항원 제시 세포들(antigen presenting cells)(APC들)을 보충함으로써 제2확장(second expansion)을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단(therapeutic population)이고; 및
- 비골수제거 림프구제거 화학요법을 투여한 후, 포유동물에 T 세포들의 치료적 집단을 투여하는 단계, 여기서 T 세포들은 포유동물에 투여되고, 그래서(whereupon) 포유동물에서 암의 퇴행이 촉진된다.
- 종양 침윤 림프구들(TIL들)을 TIL들의 치료적 집단으로 확장하는 방법으로서:
- (a) 포유동물로부터 절제된 종양으로부터 TIL들의 제1집단을 획득함으로써 자가의 T 세포들을 배양하는 단계
- (b) TIL들의 제2집단을 생성하기 위해 IL-2 및 하나 이상의 TME 자극제들(stimulators)을 포함하는 세포 배양 배지(cell culture medium)에서 TIL들의 제1집단을 배양함으로써 제1확장(first expansion)을 수행하는 단계; 및
- (c) TIL들의 제3집단(third population)을 생성하기 위해, TIL들의 제2집단의 세포 배양 배지에 추가의 IL-2, 항-CD3 항체(anti-CD3 antibody), 및 항원 제시 세포들(antigen presenting cells)(APC들)을 보충함으로써 제2확장(second expansion)을 수행하는 단계, 여기서 TIL들의 제3집단은 치료적 집단(therapeutic population)인 것을 포함하는 방법.
- 제1항 내지 제3항 중 어느 한 항에 있어서,
하나 이상의 TME 자극제들은 T-세포 하향조절(downregulation), 비활성화(deactivation) 및/또는 고갈(exhaustion)을 유발하는 것으로 알려진 T-세포들(또는 그들의 리간드들(ligands)) 상에서 발현되는(expressed) 수용체들(receptors)을 길항하는(antagonizing) 것 및/또는 억제하는 것을 할 수 있는 하나 이상의 물질들(substances)로 정의되는 용도들 및 방법들.
- 제4항에 있어서,
T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들(또는 그들의 리간드들) 상에서 발현되는 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 다음으로부터 선택되는 용도들 및 방법들:
- A: T-세포들 상의 PD-1 수용체를 통해 작용하는(act) 물질들,
- 제5항에 있어서,
T-세포 하향조절, 비활성화 및/또는 고갈을 유발하는 것으로 알려진 T-세포들(또는 그들의 리간드들) 상에서 발현되는 수용체들을 길항하는 것 및/또는 억제하는 것을 할 수 있는 물질들은 다음으로 구성되는 그룹들의 각각으로부터 적어도 하나로부터 선택되는 용도들 및 방법들:
- A: T-세포들(또는 리간드) 상의 PD-1 수용체를 통해 작용하는 물질들, 및
- B: T-세포들(또는 리간드) 상의 CTLA-4 수용체를 통해 작용하는 물질들.
- 제5항 또는 제6항에 있어서,
T-세포 상향조절(upregulation), 활성화(activation), 및/또는 재활성화(reinvigoration)를 유발하는 것으로 알려진 T-세포들 상에서 발현되는 수용체들을 작용시키는 것(agonizing) 및/또는 자극하는 것(stimulating)을 할 수 있는 하나 이상의 물질들을 추가로 포함하고, 다음으로 구성되는 그룹으로부터 선택되는 용도들 및 방법들:
- J: T-세포들 상의 4-1BB/CD137 수용체를 통해 작용하는 물질들,
- 제5항 내지 7항 중 어느 한 항에 있어서,
그룹 A의 물질은 펨브롤리주맙(pembrolizumab), 니볼루맙(nivolumab), 세미플리맙(cemiplimab), sym021, 아테졸리주맙(atezolizumab), 아벨루맙(avelumab), 및 더발루맙(durvalumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택되는 용도들 및 방법들.
- 제5항 내지 제8항 중 어느 한 항에 있어서,
그룹 B의 물질은 이필리무맙(ipilimumab) 및 트레멜리무맙(tremelimumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택되는 용도들 및 방법들.
- 제5항 내지 제9항 중 어느 한 항에 있어서,
그룹 J의 물질은 우렐루맙(urelumab) 및 유토밀루맙(utomilumab)으로 구성되는 그룹으로부터 하나 이상으로부터 선택되는 용도들 및 방법들.
- 제5항 내지 제10항 중 어느 한 항에 있어서,
물질의 농도(concentration)는 0.1㎍/mL 내지 300㎍/mL, 예를 들어 1㎍/mL 내지 100㎍/mL, 예를 들어 10㎍/mL 내지 100㎍/mL, 예를 들어 1㎍/mL 내지 10㎍/mL, 예를 들어 2-20㎍/mL인 용도들 및 방법들.
- 제5항 내지 제11항 중 어느 한 항에 있어서,
단계들 (a) 내지 (b)는 약 7일 내지 약 28일의 기간 내에 수행되는 용도들 및 방법들.
- 제5항 내지 제12항 중 어느 한 항에 있어서,
단계 (c)는 약 7일 내지 약 21일의 기간 내에 수행되는 용도들 및 방법들.
- 제5항 내지 제13항 중 어느 한 항에 있어서,
T 세포들의 치료적 집단은 유방암(breast cancer), 신장 세포암(renal cell cancer), 방광암(bladder cancer), 흑색종(melanoma), 자궁 경부암(cervical cancer), 위암(gastric cancer), 결장암(colorectal cancer), 폐암(lung cancer), 두경부암(head and neck cancer), 난소암(ovarian cancer), 호지킨 림프종(Hodgkin lymphoma), 췌장암(pancreatic cancer), 간암(liver cancer), 및 육종(sarcomas)으로 구성되는 그룹들로부터 선택된 암 유형을 치료하는데 사용되는 용도들 및 방법들.
- 제5항 내지 제14항 중 어느 한 한에 있어서,
단계 (c)는 1 x 107 내지 1x 1012 세포들, 예를 들어 1 x 108 내지 5x 109 세포들, 예를 들어 1 x 109 내지 5x 109 세포들, 예를 들어 1 x 108 내지 5x 1010 세포들, 예를 들어 1 x 109 내지 5x 1011 세포들을 생성하는 용도들 및 방법들.
- 제1항 내지 제15항 중 어느 한 항에 있어서,
상기 항- CD3 항체는 OKT3인 용도들 및 방법들.
- 제1항 내지 제16항 중 어느 한 항에 따른 방법에 의해 획득할 수 있는 종양 침윤 림프구들(TIL들)의 집단.
- IL-2 및 하나 이상의 TME 자극제들을 포함하는 TIL들의 치료적 집단.
- 제18항에 있어서, 상기 하나 이상의 TME 자극제들은 다음으로 구성되는 그룹으로부터 선택되는 적어도 하나를 포함하는 TIL들의 치료적 집단.
- A: T-세포들 상의 PD-1 수용체를 통해 작용하는 물질들, 및
- B: T-세포들 상의 CTLA-4 수용체를 통해 작용하는 물질들.
- 제18항에 있어서, 다음으로 구성되는 그룹으로부터 선택되는 적어도 하나를 추가로 포함하는 TIL들의 치료적 집단.
J: T-세포들 상의 4-1BB/CD137 수용체를 통해 작용하는 물질들,
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19217356.5 | 2019-12-18 | ||
| EP19217356 | 2019-12-18 | ||
| PCT/EP2020/087151 WO2021123255A1 (en) | 2019-12-18 | 2020-12-18 | Improved process for culturing tumor-infiltrating lymphocytes for therapeutic use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| KR20220119080A true KR20220119080A (ko) | 2022-08-26 |
Family
ID=68944537
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020227024481A Pending KR20220119080A (ko) | 2019-12-18 | 2020-12-18 | 치료용 종양-침윤 림프구들 배양을 위한 개선된 방법 |
Country Status (14)
| Country | Link |
|---|---|
| US (1) | US20230018646A1 (ko) |
| EP (1) | EP4077640B1 (ko) |
| JP (2) | JP2023509388A (ko) |
| KR (1) | KR20220119080A (ko) |
| CN (1) | CN114929861A (ko) |
| AU (1) | AU2020408201A1 (ko) |
| BR (1) | BR112022011702A2 (ko) |
| CA (1) | CA3161510A1 (ko) |
| DK (1) | DK4077640T3 (ko) |
| ES (1) | ES2984777T3 (ko) |
| IL (1) | IL293874B2 (ko) |
| MX (1) | MX2022007416A (ko) |
| PH (1) | PH12022551495A1 (ko) |
| WO (1) | WO2021123255A1 (ko) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2021222479A1 (en) | 2020-04-28 | 2021-11-04 | Lyell Immunopharma, Inc. | Methods for culturing cells |
| CN116421720A (zh) * | 2023-04-26 | 2023-07-14 | 乔国梁 | 抗肿瘤联用细胞产品和抗肿瘤细胞产品 |
| CN118853565A (zh) * | 2024-09-14 | 2024-10-29 | 青岛华赛伯曼医学细胞生物有限公司 | 一种肿瘤浸润淋巴细胞的培养工艺 |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103374548A (zh) * | 2012-04-27 | 2013-10-30 | 上海诺昊亚医学诊断技术有限公司 | 一种肿瘤浸润淋巴细胞的高效扩增培养液 |
| EP3154350B1 (en) * | 2014-04-10 | 2024-03-27 | H. Lee Moffitt Cancer Center And Research Institute, Inc. | Enhanced expansion of tumor-infiltrating lymphocytes for adoptive cell therapy |
| EP4338799A3 (en) * | 2016-10-18 | 2024-06-05 | Regents of the University of Minnesota | Tumor infiltrating lymphocytes and methods of therapy |
| WO2018094167A1 (en) * | 2016-11-17 | 2018-05-24 | Iovance Biotherapeutics, Inc. | Remnant tumor infiltrating lymphocytes and methods of preparing and using the same |
| CN111801415A (zh) * | 2017-11-06 | 2020-10-20 | 路德维格癌症研究院 | 扩增淋巴细胞的方法 |
-
2020
- 2020-12-18 JP JP2022538307A patent/JP2023509388A/ja active Pending
- 2020-12-18 EP EP20838028.7A patent/EP4077640B1/en active Active
- 2020-12-18 BR BR112022011702A patent/BR112022011702A2/pt unknown
- 2020-12-18 WO PCT/EP2020/087151 patent/WO2021123255A1/en not_active Ceased
- 2020-12-18 DK DK20838028.7T patent/DK4077640T3/da active
- 2020-12-18 KR KR1020227024481A patent/KR20220119080A/ko active Pending
- 2020-12-18 CN CN202080087408.0A patent/CN114929861A/zh active Pending
- 2020-12-18 AU AU2020408201A patent/AU2020408201A1/en active Pending
- 2020-12-18 IL IL293874A patent/IL293874B2/en unknown
- 2020-12-18 MX MX2022007416A patent/MX2022007416A/es unknown
- 2020-12-18 US US17/756,814 patent/US20230018646A1/en active Pending
- 2020-12-18 CA CA3161510A patent/CA3161510A1/en active Pending
- 2020-12-18 ES ES20838028T patent/ES2984777T3/es active Active
- 2020-12-18 PH PH1/2022/551495A patent/PH12022551495A1/en unknown
-
2024
- 2024-09-27 JP JP2024168495A patent/JP2024175144A/ja active Pending
Also Published As
| Publication number | Publication date |
|---|---|
| CA3161510A1 (en) | 2021-06-24 |
| MX2022007416A (es) | 2022-09-19 |
| DK4077640T3 (da) | 2024-07-29 |
| CN114929861A (zh) | 2022-08-19 |
| EP4077640A1 (en) | 2022-10-26 |
| EP4077640B1 (en) | 2024-05-08 |
| IL293874A (en) | 2022-08-01 |
| JP2023509388A (ja) | 2023-03-08 |
| BR112022011702A2 (pt) | 2022-09-06 |
| IL293874B2 (en) | 2024-03-01 |
| US20230018646A1 (en) | 2023-01-19 |
| AU2020408201A1 (en) | 2022-07-14 |
| PH12022551495A1 (en) | 2023-11-13 |
| WO2021123255A1 (en) | 2021-06-24 |
| JP2024175144A (ja) | 2024-12-17 |
| IL293874B1 (en) | 2023-11-01 |
| ES2984777T3 (es) | 2024-10-31 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| JP7698672B2 (ja) | ガンマデルタt細胞の増幅、組成物およびその使用 | |
| US9585914B2 (en) | Expanded NK cells | |
| US20240374728A1 (en) | T Cell Modification | |
| KR20200133370A (ko) | 입양 주입된 t 세포의 지속성 강화 방법 | |
| KR20220068228A (ko) | 면역 세포의 확장을 위한 cbl 억제제 및 조성물 | |
| WO2018229163A1 (en) | Methods of activating v delta 2 negative gamma delta t cells | |
| Rivoltini et al. | Phenotypic and functional analysis of lymphocytes infiltrating paediatric tumours, with a characterization of the tumour phenotype | |
| JP2024175144A (ja) | 治療用途の腫瘍浸潤性リンパ球を培養するための改善プロセス | |
| CN113785048B (zh) | 用于扩增和分化在过继转移疗法中的t淋巴细胞和nk细胞的方法 | |
| KR20240107147A (ko) | Nk 세포 및 다중특이적 인게이저를 이용한 암의 치료 | |
| US20140255368A1 (en) | Method of generating tumor-specific t cells | |
| US20250090581A1 (en) | Multistep process for culturing tumor-infiltrating lymphocytes for therapeutic use | |
| WO2024126827A1 (en) | Methods for the production of lymphocytes | |
| HK40082871B (en) | Improved process for culturing tumor-infiltrating lymphocytes for therapeutic use | |
| HK40082871A (en) | Improved process for culturing tumor-infiltrating lymphocytes for therapeutic use | |
| EP3941487B1 (en) | Cd28 t cell cultures, compositions, and methods of using thereof | |
| US12589151B2 (en) | T cell modification | |
| WO2026055433A1 (en) | Expansion of tumor-reactive t cells using anti-cd28 antibodies | |
| HK40117446A (en) | T cell modification | |
| EA046613B1 (ru) | Способ размножения и дифференцировки т-лимфоцитов и nk-клеток в методах лечения с адоптивным переносом | |
| Chacon et al. | Clinical Success of Adoptive Cell Transfer Therapy Using Tumor Infiltrating Lymphocytes |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0105 | International application |
St.27 status event code: A-0-1-A10-A15-nap-PA0105 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| D21 | Rejection of application intended |
Free format text: ST27 STATUS EVENT CODE: A-1-2-D10-D21-EXM-PE0902 (AS PROVIDED BY THE NATIONAL OFFICE) |
|
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |