KR20220122467A - 사스-코로나바이러스-2에 특이적으로 결합하는 항체 및 그의 용도 - Google Patents
사스-코로나바이러스-2에 특이적으로 결합하는 항체 및 그의 용도 Download PDFInfo
- Publication number
- KR20220122467A KR20220122467A KR1020210156064A KR20210156064A KR20220122467A KR 20220122467 A KR20220122467 A KR 20220122467A KR 1020210156064 A KR1020210156064 A KR 1020210156064A KR 20210156064 A KR20210156064 A KR 20210156064A KR 20220122467 A KR20220122467 A KR 20220122467A
- Authority
- KR
- South Korea
- Prior art keywords
- antibody
- amino acid
- seq
- sars
- antigen
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—RNA viruses
- C07K16/102—Coronaviridae (F)
- C07K16/104—Severe acute respiratory syndrome coronavirus 2 [SARS‐CoV‐2]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K16/00—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies
- C07K16/08—Immunoglobulins [IG], e.g. monoclonal or polyclonal antibodies against material from viruses
- C07K16/10—RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/12—Viral antigens
- A61K39/215—Coronaviridae, e.g. avian infectious bronchitis virus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/395—Antibodies; Immunoglobulins; Immune serum, e.g. antilymphocytic serum
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K2039/505—Medicinal preparations containing antigens or antibodies comprising antibodies
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/50—Immunoglobulins specific features characterized by immunoglobulin fragments
- C07K2317/56—Immunoglobulins specific features characterized by immunoglobulin fragments variable (Fv) region, i.e. VH and/or VL
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/70—Immunoglobulins specific features characterized by effect upon binding to a cell or to an antigen
- C07K2317/76—Antagonist effect on antigen, e.g. neutralization or inhibition of binding
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K2317/00—Immunoglobulins specific features
- C07K2317/90—Immunoglobulins specific features characterized by (pharmaco)kinetic aspects or by stability of the immunoglobulin
- C07K2317/92—Affinity (KD), association rate (Ka), dissociation rate (Kd) or EC50 value
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Virology (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Immunology (AREA)
- Molecular Biology (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Communicable Diseases (AREA)
- Epidemiology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Genetics & Genomics (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biophysics (AREA)
- Oncology (AREA)
- Microbiology (AREA)
- Mycology (AREA)
- Pulmonology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Medicines Containing Antibodies Or Antigens For Use As Internal Diagnostic Agents (AREA)
- Peptides Or Proteins (AREA)
Abstract
Description
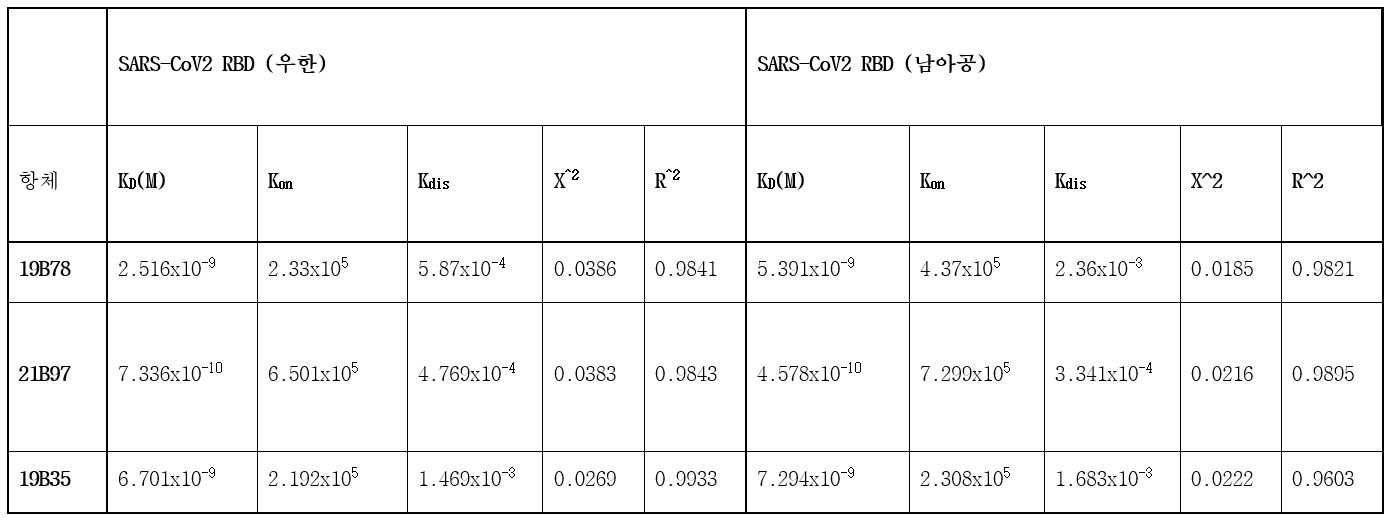
도 2는 인간 키메릭 재조합 항체의 우한 SARS-CoV-2 및 남아공 변이주 RBD에 대한 결합능력을 SARS-CoV-2 의 표면 플라즈몬 공명 분석을 통해 평형 해리상수(KD), 결합속도(Kon) 및 해리속도(Kdis) 상수를 확인한 도이다.
|
COVID-19
양성 환자 혈청 |
SARS-CoV-2 VNT | RBD-ACE2 sVNT | ||
|
RBD
(기존, 우한) |
RBD
(영국 변이주) |
RBD
(남아공 변이주) |
||
| Titer | PI value | PI value | PI value | |
| 9184 | 1:8(50%) | 41.9 | 35.8 | 5.2 |
| 9185 | 1:32 | 66.6 | 63.3 | 35.0 |
| 9768 | 1:32(50%) | 53.4 | 53.5 | 3.4 |
| 9769 | 1:16 | 38.1 | 39.2 | 10.3 |
| 9772 | 1:8 | 23.9 | 31.3 | 16.0 |
| 19777 | 1:8 | 25.4 | 32.0 | -1.0 |
| 20691 | 1:16 | 53.4 | 57.5 | 5.9 |
| 6886 | 1:16(50%) | 74.3 | 68.8 | 21.9 |
| 6887 | 1:64 | 64.0 | 63.3 | 25.0 |
| 6888 | 1:64 | 70.1 | 70.3 | 11.2 |
| NHS(Normal human serum) | -1.0 | 2.8 | -5.3 | |
| 병원음성1 | 4.3 | -4.8 | 12.2 | |
| 병원음성2 | -8.7 | -4.7 | 6.5 | |
| 병원음성3 | 11.4 | -1.7 | 7.4 | |
| 병원음성4 | 10.3 | -0.4 | 2.8 | |
| 병원음성5 | 6.6 | -0.7 | 4.5 | |
| 병원음성6 | 4.3 | -5.9 | 4.5 | |
| 병원음성7 | 14.9 | 4.7 | 9.2 | |
| 병원음성8 | 4.9 | -4.1 | 15.4 | |
| 병원음성9 | 11.8 | -1.1 | -5.2 | |
| 병원음성10 | -0.7 | -1.2 | -1.3 | |
| 클론 명 |
VNT 테스트
(한국 분리종, 스파이크 비변이주) |
|
| 19B | 7 | 1:40 |
| 10 | 1:640 | |
| 15 | 1:640(50%) | |
| 35 | 1:1280 | |
| 37 | 1:1280 | |
| 39 | 1:640 | |
| 50 | 1:160 | |
| 78 | 1:1280(50%) | |
| 90 | 1:160 | |
| 103 | 1:1280(50%) | |
| 104 | 1:160 | |
| 125 | 1:1280(50%) | |
| 141 | 1:1280 | |
| 143 | 1:1280 | |
| 21B | 12 | 1:20480 |
| 24 | 1:640 | |
| 31 | 1:10240 | |
| 38 | 1:160 | |
| 58 | 1:40960 | |
| 64 | 1:640 | |
| 97 | 1:81920(50%) | |
| 100 | 1:2560(50%) | |
| 101 | 1:163840(50%) | |
| 109 | 1:10240 | |
| 130 | 1:20480(50%) | |
| 135 | 1:2560 | |
| 138 | 1:20 | |
| 22B | 1 | 1:5120 |
| 7 | 1:2560(50%) | |
| 10 | 1:40960(50%) | |
| 17 | 1:10240(50%) | |
| RBD-ACE2 대리 바이러스 중화 테스트(sVNT) | |||
| 항체 클론 No. |
RBD
(기존, 우한) |
RBD
(영국 변이주) |
RBD
(남아공 변이주) |
| PI value | PI value | PI value | |
| 19B5 | -3.4 | -0.5 | 4.4 |
| 19B7 | 9.6 | 0.1 | 8.2 |
| 19B10 | 3.7 | 11.4 | 1.3 |
| 19B15 | 25.0 | 15.1 | 21.3 |
| 19B35 | 59.2 | 43.1 | 34.7 |
| 19B37 | 46.3 | 51.4 | 1.2 |
| 19B37-4 | 50.2 | 54.5 | 0.7 |
| 19B39 | 13.5 | 21.8 | 2.8 |
| 19B50 | 9.7 | 5.9 | 0.0 |
| 19B68 | -1.6 | 6.1 | -7.3 |
| 19B78 | 71.3 | 62.3 | 44.3 |
| 19B90 | 12.1 | 6.4 | 0.0 |
| 19B103 | 27.5 | 24.2 | -3.8 |
| 19B104 | 13.9 | 16.9 | -4.7 |
| 19B116 | -1.0 | 1.8 | -5.4 |
| 19B121 | -1.4 | -0.5 | -7.9 |
| 19B125 | 5.2 | 5.6 | 1.8 |
| 19B135 | 53.4 | 51.5 | -1.3 |
| 19B141 | 52.0 | 42.3 | -4.4 |
| 19B143 | 27.0 | 14.3 | -11.5 |
| 21B12 | 43.4 | 38.0 | 31.6 |
| 21B24 | 4.8 | -0.7 | 4.8 |
| 21B31 | -0.4 | 0.9 | 0.3 |
| 21B38 | -5.7 | 1.3 | -11.8 |
| 21B58 | 39.6 | -0.9 | 0.7 |
| 21B64 | -11.6 | 6.1 | -0.2 |
| 21B97 | 63.9 | 56.0 | 48.1 |
| 21B100 | -2.7 | 0.1 | 2.7 |
| 21B101 | -4.4 | -3.7 | -5.4 |
| 21B109 | -3.9 | -1.8 | -10.0 |
| 21B130 | -1.6 | -9.8 | 0.1 |
| 21B135 | -0.1 | 6.2 | -0.5 |
| 21B138 | -1.8 | 1.6 | -28.4 |
| 22B1 | 59.3 | 48.8 | 43.1 |
| 22B7 | 40.0 | 32.8 | 18.1 |
| 22B10 | 48.8 | 39.1 | 44.5 |
| 22B17 | 55.4 | 40.2 | 56.4 |
| RBD-ACE2 sVNT |
VNT test
(한국분리종, 스파이크 비변이주) |
|||
| 항체 클론 |
RBD
(기존, 우한) |
RBD
(영국 변이주) |
RBD
(남아공 변이주) |
|
| PI value | PI value | PI value | ||
| 19B-35-7 | 59.2 | 43.1 | 34.7 | 1:1280 |
| 19B-78-9 | 71.3 | 62.3 | 44.3 | 1:1280(50%) |
| 21B-97-3 | 63.9 | 56.0 | 48.1 | 1:81920(50%) |
Claims (20)
- 사스-코로나바이러스-2(SARS-CoV-2) 스파이크 단백질(Spike protein, S protein)의 RBD(Receptor binding domain) 에 특이적으로 결합하는 항체 또는 그의 항원 결합 단편으로서,
하기 조합 a), b) 및 c) 중 하나의 중쇄 상보성 결정영역(Heavy chain complementarity determining region: HCDR) 및 경쇄 상보성 결정영역(Light chain complementarity determining region, LCDR)을 포함하는 항체 또는 그의 항원 결합 단편:
a) 서열번호 1의 아미노산 서열로 이루어지는 HCDR1, 서열번호 2의 아미노산 서열로 이루어지는 HCDR2 및 서열번호 3의 아미노산 서열로 이루어지는 HCDR3을 포함하는 중쇄 가변영역(VH); 및 서열번호 10의 아미노산 서열로 이루어지는 LCDR1, 서열번호 11 의 아미노산 서열로 이루어지는 LCDR2, 및 서열번호 12 의 아미노산 서열로 이루어지는 LCDR3을 포함하는 경쇄 가변영역(VL);
b) 서열번호 4의 아미노산 서열로 이루어지는 HCDR1, 서열번호 5의 아미노산 서열로 이루어지는 HCDR2, 및 서열번호 6의 아미노산 서열로 이루어지는 HCDR3을 포함하는 중쇄 가변영역(VH); 및 서열번호 13의 아미노산 서열로 이루어지는 LCDR1, 서열번호 14의 아미노산 서열로 이루어지는 LCDR2, 및 서열번호 15의 아미노산 서열로 이루어지는 LCDR3을 포함하는 경쇄 가변영역(VL); 및
c) 서열번호 7의 아미노산 서열로 이루어지는 HCDR1, 서열번호 8의 아미노산 서열로 이루어지는 HCDR2, 및 서열번호 9의 아미노산 서열로 이루어지는 HCDR3을 포함하는 중쇄 가변영역(VH); 및 서열번호 16의 아미노산 서열로 이루어지는 LCDR1, 서열번호 17의 아미노산 서열로 이루어지는 LCDR2, 및 서열번호 18의 아미노산 서열로 이루어지는 LCDR3을 포함하는 경쇄 가변영역(VL). - 청구항 1에 있어서, 상기 하기 조합 중 선택된 하나의 중쇄 가변 영역 및 경쇄 가변 영역을 포함하는 항체 또는 그의 항원 결합 단편:
상기 중쇄 가변 영역은 서열번호 19로 이루어진 아미노산 및 상기 경쇄 가변 영역은 서열번호 20으로 이루어진 아미노산;
상기 중쇄 가변 영역은 서열번호 21 로 이루어진 아미노산 및 상기 경쇄 가변 영역은 서열번호 22로 이루어진 아미노산; 및
상기 중쇄 가변 영역은 서열번호 23으로 이루어진 아미노산을 포함하고, 상기 경쇄 가변 영역은 서열번호 24로 이루어진 아미노산. - 청구항 1에 있어서, 상기 RBD(Receptor binding domain) 은 서열번호 25로 이루어진 아미노산 서열의 N말단으로부터 319 내지 541번째 아미노산으로 이루어진 것인 항체 또는 그의 항원 결합 단편.
- 청구항 3에 있어서, 사스-코로나바이러스-2(SARS-CoV-2) 스파이크 단백질의 RBD(Receptor binding domain) 에 바이러스 중화능을 나타내는 것인 항체 또는 그의 항원 결합 단편.
- 청구항 1에 있어서, 서열번호 25로 이루어진 아미노산 서열의 501번째 아미노산이 아스파라긴(Asparagine, N) 에서 티로신(Tyrosine, Y)으로 치환된 사스-코로나바이러스-2(SARS-CoV-2) 스파이크 변이 단백질에 바이러스 중화능을 나타내는 것인 항체 또는 그의 항원 결합 단편.
- 청구항 1에 있어서, 서열번호 25로 이루어진 아미노산 서열의
417번째 아미노산이 라이신(Lysine, K)에서 아스파라긴(Asparagine, N)로 치환된 것;
484번째 아미노산이 글루타메이트(Glutamate, E)에서 라이신(Lysine, K)로 치환된 것; 및
501번째 아미노산이 아스파라긴(Asparagine, N) 에서 티로신(Tyrosine, Y)으로 치환된 것으로 이루어진 군으로부터 1종 이상의 변이를 포함하는 사스-코로나바이러스-2(SARS-CoV-2) 스파이크 변이 단백질에 바이러스 중화능을 나타내는 것인 항체 또는 그의 항원 결합 단편. - 청구항 1에 있어서, 상기 항체 또는 그의 항원 결합 단편은 단일클론 항체, 다특이적 항체, 인간 항체, 인간화 항체, 마우스 항체, 키메라 항체, 단쇄 Fvs(scFV), 단쇄 항체, Fab 단편, F(ab') 단편, 디설파이드-결합 Fvs(sdFV), scFv 단편, scFv-Fc 단편, Fv 단편, 디아바디(diabody), 트리아바디, 및 테트라바디로 이루어진 군으로부터 선택된 것인 항체 또는 그의 항원 결합 단편.
- 청구항 1에 있어서, 상기 항체 또는 그의 항원 결합 단편은 하이브리도마 세포로부터 생산되는 것인, 항체 또는 이의 항원 결합 단편.
- 하기 조합 중 선택된 하나의 중쇄 가변 영역 및 경쇄 가변 영역을 포함하는 아미노산 서열을 코딩하는 단리된 핵산을 포함하는 사스-코로나바이러스-2(SARS-CoV-2) 스파이크 단백질(Spike protein, S protein)의 RBD(Receptor binding domain) 에 특이적으로 결합하는 항체 또는 그의 항원 결합 단편 생산용 재조합 발현 벡터 :
상기 중쇄 가변 영역은 서열번호 19로 이루어진 아미노산 및 상기 경쇄 가변 영역은 서열번호 20으로 이루어진 아미노산;
상기 중쇄 가변 영역은 서열번호 21 로 이루어진 아미노산 및 상기 경쇄 가변 영역은 서열번호 22로 이루어진 아미노산; 및
상기 중쇄 가변 영역은 서열번호 23으로 이루어진 아미노산을 포함하고, 상기 경쇄 가변 영역은 서열번호 24로 이루어진 아미노산. - 청구항 9의 재조합 발현 벡터로 시험관(in vitro) 내 형질전환된 숙주세포.
- 청구항 10에 있어서, 상기 숙주세포는 박테리아, 효모, HEK 세포, CHO 세포, F2N 세포, HEK293 세포, HEK93T세포, COS 세포 및 항체 생산 하이브리도마 세포로 이루어지는 군으로부터 선택된 어느 하나인 것을 특징으로 하는 숙주세포.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 생산하는 하이브리도마 세포주.
- 청구항 9의 발현 벡터를 이용하여 시험관(in vitro) 내에서 숙주세포에 감염시키는 단계를 포함하는, 사스-코로나바이러스-2 스파이크 단백질의 RBD 에 결합하는 항체 또는 그의 항원 결합 단편의 생산방법.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 포함하는 사스-코로나바이러스 감염증(COVID-19)의 예방 또는 치료용 약학적 조성물.
- 청구항 14에 있어서, 주사제, 동결건조(lyophilized) 제형, 사전 충전식 주사(pre-filled syringe) 제형, 경구형 제형, 외용제, 및 좌제로 이루어진 군으로부터 선택된 제형인 것인 약학적 조성물.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 포함하는 사스-코로나바이러스 감염증(COVID-19)의 진단용 조성물.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 포함하는 사스-코로나바이러스-2에 대한 중화 항체 검출용 조성물.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 포함하는 사스-코로나바이러스 감염증(COVID-19)의 진단용 키트.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 포함하는 사스-코로나바이러스-2에 대한 중화 항체 검출용 키트.
- 청구항 1 내지 8 중 어느 한 항의 항체 또는 그의 항원 결합 단편을 개체로부터 분리된 생물학적 시료와 접촉시키는 단계; 및
상기 시료와 항체 또는 그의 항원 결합 단편의 결합에 의해 형성된 복합체를 검출하는 단계를 포함하는 사스-코로나바이러스-2를 검출하는 방법.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20210026717 | 2021-02-26 | ||
| KR1020210026717 | 2021-02-26 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| KR20220122467A true KR20220122467A (ko) | 2022-09-02 |
| KR102748987B1 KR102748987B1 (ko) | 2025-01-02 |
Family
ID=83280834
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| KR1020210156064A Active KR102748987B1 (ko) | 2021-02-26 | 2021-11-12 | 사스-코로나바이러스-2에 특이적으로 결합하는 항체 및 그의 용도 |
Country Status (1)
| Country | Link |
|---|---|
| KR (1) | KR102748987B1 (ko) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116496391A (zh) * | 2022-09-30 | 2023-07-28 | 武汉科源安博生物技术有限公司 | 针对新型冠状病毒2019-nCoV株RBD蛋白的单克隆抗体及免疫检测试剂 |
| CN118373905A (zh) * | 2024-05-22 | 2024-07-23 | 广州海关技术中心 | 结合冠状病毒SARS-CoV-2和SARS-CoV刺突蛋白RBD的中和抗体ZJ-5及其应用 |
| KR102714027B1 (ko) | 2024-03-13 | 2024-10-15 | 국방과학연구소 | 사스-코로나바이러스-2 델타 감염증 치료용 항체 mRNA 및 이를 포함한 조성물 |
| KR102714014B1 (ko) | 2024-03-13 | 2024-10-15 | 국방과학연구소 | 사스-코로나바이러스-2 델타 감염증 치료용 항체 mRNA 및 이를 포함한 조성물 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10822379B1 (en) * | 2020-03-12 | 2020-11-03 | University of Pittsburgh—of the Commonwealth System of Higher Education | Molecules that bind to SARS-CoV-2 |
| CN111999492A (zh) * | 2020-07-30 | 2020-11-27 | 山东莱博生物科技有限公司 | 一种联合检验covid-19n抗原和s蛋白抗体的胶体金免疫层析检测卡 |
| WO2022022445A1 (zh) * | 2020-07-28 | 2022-02-03 | 上海市公共卫生临床中心 | 一种特异性结合冠状病毒的抗体或其抗原结合片段 |
-
2021
- 2021-11-12 KR KR1020210156064A patent/KR102748987B1/ko active Active
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US10822379B1 (en) * | 2020-03-12 | 2020-11-03 | University of Pittsburgh—of the Commonwealth System of Higher Education | Molecules that bind to SARS-CoV-2 |
| WO2022022445A1 (zh) * | 2020-07-28 | 2022-02-03 | 上海市公共卫生临床中心 | 一种特异性结合冠状病毒的抗体或其抗原结合片段 |
| CN111999492A (zh) * | 2020-07-30 | 2020-11-27 | 山东莱博生物科技有限公司 | 一种联合检验covid-19n抗原和s蛋白抗体的胶体金免疫层析检测卡 |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN116496391A (zh) * | 2022-09-30 | 2023-07-28 | 武汉科源安博生物技术有限公司 | 针对新型冠状病毒2019-nCoV株RBD蛋白的单克隆抗体及免疫检测试剂 |
| KR102714027B1 (ko) | 2024-03-13 | 2024-10-15 | 국방과학연구소 | 사스-코로나바이러스-2 델타 감염증 치료용 항체 mRNA 및 이를 포함한 조성물 |
| KR102714014B1 (ko) | 2024-03-13 | 2024-10-15 | 국방과학연구소 | 사스-코로나바이러스-2 델타 감염증 치료용 항체 mRNA 및 이를 포함한 조성물 |
| CN118373905A (zh) * | 2024-05-22 | 2024-07-23 | 广州海关技术中心 | 结合冠状病毒SARS-CoV-2和SARS-CoV刺突蛋白RBD的中和抗体ZJ-5及其应用 |
| CN118373905B (zh) * | 2024-05-22 | 2024-12-03 | 广州海关技术中心 | 结合冠状病毒SARS-CoV-2和SARS-CoV刺突蛋白RBD的中和抗体ZJ-5及其应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| KR102748987B1 (ko) | 2025-01-02 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| KR102748987B1 (ko) | 사스-코로나바이러스-2에 특이적으로 결합하는 항체 및 그의 용도 | |
| JP5576072B2 (ja) | チロトロフィン(tsh)受容体の抗原決定領域、その使用およびその抗体 | |
| KR20230023664A (ko) | 항-클라우딘18.2 항체 및 이의 용도 | |
| WO2021218947A1 (zh) | 一种抗新型冠状病毒的单克隆抗体及其应用 | |
| MX2011001363A (es) | Anticuerpos selectivos de anti-hepcidina-25 y usos de los mismos. | |
| JP2023534923A (ja) | SARS-CoV-2を標的にする抗原結合分子 | |
| JP2010536043A (ja) | 尿ゲルゾリンの検出および定量化 | |
| AU2020351274A1 (en) | Single-domain antibodies directed against LILRB2 | |
| US20230348568A1 (en) | Epstein-barr virus monoclonal antibodies and uses thereof | |
| TWI734279B (zh) | 抗α-突觸核蛋白抗體及其用途 | |
| US20230242623A1 (en) | Compositions and methods for the diagnosis and treatment of sars-cov-2 virus infection | |
| CN121358774A (zh) | 与nkg2a结合的抗体或抗原结合片段及其用途 | |
| WO2022132904A1 (en) | Human monoclonal antibodies targeting sars-cov-2 | |
| CN113999303B (zh) | 用于体外诊断的新型冠状病毒核衣壳蛋白抗体 | |
| KR101627020B1 (ko) | 적 백혈병 세포에서 발현되는 icama4를 인지하는 항체 및 이의 용도 | |
| WO2022179535A1 (zh) | 抗SARS-CoV-2核衣壳蛋白的单克隆抗体及其制备方法和用途 | |
| CN112574297B (zh) | 抗神经氨酸酶的单克隆抗体及其应用 | |
| JP2025542128A (ja) | メタニューモウイルス融合(f)タンパク質に対する抗体及びその使用 | |
| CN107286237B (zh) | 一种抗丙型肝炎病毒抗体的获取以及应用 | |
| WO2022068895A1 (zh) | 抗SARS-CoV-2刺突蛋白膜外区的单克隆抗体及其应用 | |
| US20260092100A1 (en) | Antibodies against metapneumovirus fusion (f) protein and uses thereof | |
| CN113999302B (zh) | 用于体外诊断的新型冠状病毒核衣壳蛋白抗体 | |
| CN120665199B (zh) | 抗human IgG的抗体、其制备方法及用途 | |
| WO2012101125A1 (en) | Specific antibodies against human cxcl4 and uses thereof | |
| CN115925906B (zh) | 抗新型冠状病毒核蛋白的单克隆抗体及其应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PA0109 | Patent application |
St.27 status event code: A-0-1-A10-A12-nap-PA0109 |
|
| PA0201 | Request for examination |
St.27 status event code: A-1-2-D10-D11-exm-PA0201 |
|
| PN2301 | Change of applicant |
St.27 status event code: A-3-3-R10-R13-asn-PN2301 St.27 status event code: A-3-3-R10-R11-asn-PN2301 |
|
| PG1501 | Laying open of application |
St.27 status event code: A-1-1-Q10-Q12-nap-PG1501 |
|
| D13-X000 | Search requested |
St.27 status event code: A-1-2-D10-D13-srh-X000 |
|
| D14-X000 | Search report completed |
St.27 status event code: A-1-2-D10-D14-srh-X000 |
|
| E902 | Notification of reason for refusal | ||
| PE0902 | Notice of grounds for rejection |
St.27 status event code: A-1-2-D10-D21-exm-PE0902 |
|
| P11-X000 | Amendment of application requested |
St.27 status event code: A-2-2-P10-P11-nap-X000 |
|
| P13-X000 | Application amended |
St.27 status event code: A-2-2-P10-P13-nap-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-2-2-P10-P22-nap-X000 |
|
| E701 | Decision to grant or registration of patent right | ||
| PE0701 | Decision of registration |
St.27 status event code: A-1-2-D10-D22-exm-PE0701 |
|
| PG1601 | Publication of registration |
St.27 status event code: A-4-4-Q10-Q13-nap-PG1601 |
|
| R18-X000 | Changes to party contact information recorded |
St.27 status event code: A-5-5-R10-R18-oth-X000 |
|
| P22-X000 | Classification modified |
St.27 status event code: A-4-4-P10-P22-nap-X000 |