TW202128706A - 新型雜環化合物 - Google Patents
新型雜環化合物 Download PDFInfo
- Publication number
- TW202128706A TW202128706A TW109131236A TW109131236A TW202128706A TW 202128706 A TW202128706 A TW 202128706A TW 109131236 A TW109131236 A TW 109131236A TW 109131236 A TW109131236 A TW 109131236A TW 202128706 A TW202128706 A TW 202128706A
- Authority
- TW
- Taiwan
- Prior art keywords
- carbonyl
- hexahydropyridine
- phenyl
- compound
- formula
- Prior art date
Links
- 150000002391 heterocyclic compounds Chemical class 0.000 title abstract 2
- 150000001875 compounds Chemical class 0.000 claims abstract description 258
- 238000000034 method Methods 0.000 claims abstract description 119
- 238000004519 manufacturing process Methods 0.000 claims abstract description 9
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 claims description 174
- 150000003839 salts Chemical class 0.000 claims description 126
- -1 cyano, hydroxyl Chemical group 0.000 claims description 111
- 239000001257 hydrogen Substances 0.000 claims description 83
- 229910052739 hydrogen Inorganic materials 0.000 claims description 83
- 241000124008 Mammalia Species 0.000 claims description 55
- JUJWROOIHBZHMG-UHFFFAOYSA-N pyridine Substances C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 claims description 54
- 208000002193 Pain Diseases 0.000 claims description 46
- 229910052736 halogen Inorganic materials 0.000 claims description 42
- 150000002367 halogens Chemical class 0.000 claims description 42
- 150000002431 hydrogen Chemical class 0.000 claims description 42
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 39
- 238000011282 treatment Methods 0.000 claims description 39
- 230000002265 prevention Effects 0.000 claims description 37
- 230000036407 pain Effects 0.000 claims description 31
- 125000001072 heteroaryl group Chemical group 0.000 claims description 27
- 238000002360 preparation method Methods 0.000 claims description 26
- 230000004770 neurodegeneration Effects 0.000 claims description 23
- 201000006417 multiple sclerosis Diseases 0.000 claims description 21
- 208000015122 neurodegenerative disease Diseases 0.000 claims description 21
- JFDZBHWFFUWGJE-UHFFFAOYSA-N benzonitrile Chemical compound N#CC1=CC=CC=C1 JFDZBHWFFUWGJE-UHFFFAOYSA-N 0.000 claims description 20
- 239000003814 drug Substances 0.000 claims description 20
- 125000004076 pyridyl group Chemical group 0.000 claims description 20
- 206010028980 Neoplasm Diseases 0.000 claims description 19
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 claims description 19
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims description 19
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 17
- 208000004998 Abdominal Pain Diseases 0.000 claims description 16
- 208000018737 Parkinson disease Diseases 0.000 claims description 16
- 201000011510 cancer Diseases 0.000 claims description 16
- 125000004093 cyano group Chemical group *C#N 0.000 claims description 16
- NQRYJNQNLNOLGT-UHFFFAOYSA-N tetrahydropyridine hydrochloride Natural products C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 claims description 16
- 208000022559 Inflammatory bowel disease Diseases 0.000 claims description 15
- 201000010099 disease Diseases 0.000 claims description 15
- 125000001153 fluoro group Chemical group F* 0.000 claims description 15
- 208000030886 Traumatic Brain injury Diseases 0.000 claims description 14
- 229940079593 drug Drugs 0.000 claims description 14
- 208000020016 psychiatric disease Diseases 0.000 claims description 14
- 208000024827 Alzheimer disease Diseases 0.000 claims description 13
- 230000009529 traumatic brain injury Effects 0.000 claims description 13
- 206010029240 Neuritis Diseases 0.000 claims description 12
- 206010029350 Neurotoxicity Diseases 0.000 claims description 12
- 206010044221 Toxic encephalopathy Diseases 0.000 claims description 12
- 230000007135 neurotoxicity Effects 0.000 claims description 12
- 231100000228 neurotoxicity Toxicity 0.000 claims description 12
- 125000004289 pyrazol-3-yl group Chemical group [H]N1N=C(*)C([H])=C1[H] 0.000 claims description 12
- 125000006376 (C3-C10) cycloalkyl group Chemical group 0.000 claims description 11
- 208000019901 Anxiety disease Diseases 0.000 claims description 10
- 206010002026 amyotrophic lateral sclerosis Diseases 0.000 claims description 10
- 230000036506 anxiety Effects 0.000 claims description 10
- 239000004202 carbamide Substances 0.000 claims description 10
- 208000004296 neuralgia Diseases 0.000 claims description 10
- 208000021722 neuropathic pain Diseases 0.000 claims description 10
- 208000019695 Migraine disease Diseases 0.000 claims description 9
- 208000006011 Stroke Diseases 0.000 claims description 9
- 206010015037 epilepsy Diseases 0.000 claims description 9
- 206010027599 migraine Diseases 0.000 claims description 9
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 9
- 201000001119 neuropathy Diseases 0.000 claims description 9
- 230000007823 neuropathy Effects 0.000 claims description 9
- 208000033808 peripheral neuropathy Diseases 0.000 claims description 9
- 125000000951 phenoxy group Chemical group [H]C1=C([H])C([H])=C(O*)C([H])=C1[H] 0.000 claims description 9
- 125000004739 (C1-C6) alkylsulfonyl group Chemical group 0.000 claims description 8
- 208000000094 Chronic Pain Diseases 0.000 claims description 8
- 206010009944 Colon cancer Diseases 0.000 claims description 8
- 206010033128 Ovarian cancer Diseases 0.000 claims description 8
- 206010061535 Ovarian neoplasm Diseases 0.000 claims description 8
- 230000036952 cancer formation Effects 0.000 claims description 8
- 208000029742 colonic neoplasm Diseases 0.000 claims description 8
- 125000002720 diazolyl group Chemical group 0.000 claims description 8
- 206010073071 hepatocellular carcinoma Diseases 0.000 claims description 8
- 231100000844 hepatocellular carcinoma Toxicity 0.000 claims description 8
- 208000002551 irritable bowel syndrome Diseases 0.000 claims description 8
- 125000000335 thiazolyl group Chemical group 0.000 claims description 8
- 208000007101 Muscle Cramp Diseases 0.000 claims description 7
- 208000005298 acute pain Diseases 0.000 claims description 7
- 238000002512 chemotherapy Methods 0.000 claims description 7
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 7
- 239000008194 pharmaceutical composition Substances 0.000 claims description 7
- 208000009935 visceral pain Diseases 0.000 claims description 7
- 206010061218 Inflammation Diseases 0.000 claims description 6
- 102000004882 Lipase Human genes 0.000 claims description 6
- 108090001060 Lipase Proteins 0.000 claims description 6
- 239000004367 Lipase Substances 0.000 claims description 6
- 230000004054 inflammatory process Effects 0.000 claims description 6
- 235000019421 lipase Nutrition 0.000 claims description 6
- 125000005915 C6-C14 aryl group Chemical group 0.000 claims description 4
- 239000013543 active substance Substances 0.000 claims description 3
- 239000003795 chemical substances by application Substances 0.000 claims description 3
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 claims description 3
- 125000001424 substituent group Chemical group 0.000 claims description 3
- 230000001225 therapeutic effect Effects 0.000 claims description 3
- 125000000623 heterocyclic group Chemical group 0.000 claims description 2
- 210000005036 nerve Anatomy 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 79
- 230000008569 process Effects 0.000 abstract description 41
- 239000013067 intermediate product Substances 0.000 description 88
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 66
- 238000006243 chemical reaction Methods 0.000 description 63
- 239000007787 solid Substances 0.000 description 49
- 239000000243 solution Substances 0.000 description 44
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Chemical compound CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 42
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 41
- 239000002904 solvent Substances 0.000 description 36
- JGFZNNIVVJXRND-UHFFFAOYSA-N N,N-Diisopropylethylamine (DIPEA) Chemical compound CCN(C(C)C)C(C)C JGFZNNIVVJXRND-UHFFFAOYSA-N 0.000 description 33
- 235000019439 ethyl acetate Nutrition 0.000 description 31
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 30
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 29
- 125000006239 protecting group Chemical group 0.000 description 28
- 239000011541 reaction mixture Substances 0.000 description 26
- 239000011734 sodium Substances 0.000 description 25
- VKOBVWXKNCXXDE-UHFFFAOYSA-N icosanoic acid Chemical compound CCCCCCCCCCCCCCCCCCCC(O)=O VKOBVWXKNCXXDE-UHFFFAOYSA-N 0.000 description 24
- 125000003545 alkoxy group Chemical group 0.000 description 23
- 229910052794 bromium Inorganic materials 0.000 description 23
- 239000000460 chlorine Substances 0.000 description 23
- 239000000047 product Substances 0.000 description 23
- GDTBXPJZTBHREO-UHFFFAOYSA-N bromine Substances BrBr GDTBXPJZTBHREO-UHFFFAOYSA-N 0.000 description 22
- WKBOTKDWSSQWDR-UHFFFAOYSA-N Bromine atom Chemical compound [Br] WKBOTKDWSSQWDR-UHFFFAOYSA-N 0.000 description 21
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 21
- 239000003921 oil Substances 0.000 description 21
- 235000019198 oils Nutrition 0.000 description 21
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 21
- 150000002148 esters Chemical class 0.000 description 20
- 238000003786 synthesis reaction Methods 0.000 description 20
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 19
- KDLHZDBZIXYQEI-UHFFFAOYSA-N Palladium on carbon Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 19
- 239000002585 base Substances 0.000 description 19
- YMWUJEATGCHHMB-UHFFFAOYSA-N dichloromethane Natural products ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 19
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 18
- 230000015572 biosynthetic process Effects 0.000 description 18
- 230000000670 limiting effect Effects 0.000 description 18
- 239000012044 organic layer Substances 0.000 description 17
- 125000000217 alkyl group Chemical group 0.000 description 16
- 239000003153 chemical reaction reagent Substances 0.000 description 16
- 125000004435 hydrogen atom Chemical group [H]* 0.000 description 16
- 239000012267 brine Substances 0.000 description 15
- 125000004432 carbon atom Chemical group C* 0.000 description 15
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 15
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 14
- 239000000543 intermediate Substances 0.000 description 13
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 12
- 210000004027 cell Anatomy 0.000 description 12
- 230000000694 effects Effects 0.000 description 12
- 239000000706 filtrate Substances 0.000 description 12
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 11
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 11
- 210000004556 brain Anatomy 0.000 description 11
- 229910052801 chlorine Inorganic materials 0.000 description 11
- 239000011737 fluorine Substances 0.000 description 11
- 229910052731 fluorine Inorganic materials 0.000 description 11
- 230000002401 inhibitory effect Effects 0.000 description 11
- 125000000636 p-nitrophenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)[N+]([O-])=O 0.000 description 11
- 238000002953 preparative HPLC Methods 0.000 description 11
- 230000002829 reductive effect Effects 0.000 description 11
- 238000003756 stirring Methods 0.000 description 11
- 239000000126 substance Substances 0.000 description 11
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 11
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 11
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 10
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 10
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 10
- 125000003118 aryl group Chemical group 0.000 description 10
- 125000000753 cycloalkyl group Chemical group 0.000 description 10
- PXGOKWXKJXAPGV-UHFFFAOYSA-N Fluorine Chemical compound FF PXGOKWXKJXAPGV-UHFFFAOYSA-N 0.000 description 9
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 description 9
- DTQVDTLACAAQTR-UHFFFAOYSA-M Trifluoroacetate Chemical compound [O-]C(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-M 0.000 description 9
- 125000001584 benzyloxycarbonyl group Chemical group C(=O)(OCC1=CC=CC=C1)* 0.000 description 9
- 238000009835 boiling Methods 0.000 description 9
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 9
- TXNLQUKVUJITMX-UHFFFAOYSA-N 4-tert-butyl-2-(4-tert-butylpyridin-2-yl)pyridine Chemical group CC(C)(C)C1=CC=NC(C=2N=CC=C(C=2)C(C)(C)C)=C1 TXNLQUKVUJITMX-UHFFFAOYSA-N 0.000 description 8
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 8
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 8
- 241000699670 Mus sp. Species 0.000 description 8
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 8
- 208000036110 Neuroinflammatory disease Diseases 0.000 description 8
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Natural products OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 8
- 230000004913 activation Effects 0.000 description 8
- 238000004458 analytical method Methods 0.000 description 8
- 239000003054 catalyst Substances 0.000 description 8
- 125000005843 halogen group Chemical group 0.000 description 8
- 230000003959 neuroinflammation Effects 0.000 description 8
- RYHBNJHYFVUHQT-UHFFFAOYSA-N 1,4-Dioxane Chemical compound C1COCCO1 RYHBNJHYFVUHQT-UHFFFAOYSA-N 0.000 description 7
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 7
- 239000002253 acid Substances 0.000 description 7
- 150000001412 amines Chemical class 0.000 description 7
- 238000006880 cross-coupling reaction Methods 0.000 description 7
- 238000003818 flash chromatography Methods 0.000 description 7
- PNDPGZBMCMUPRI-UHFFFAOYSA-N iodine Chemical compound II PNDPGZBMCMUPRI-UHFFFAOYSA-N 0.000 description 7
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 7
- 239000007858 starting material Substances 0.000 description 7
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 6
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical compound CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 6
- 102100036214 Cannabinoid receptor 2 Human genes 0.000 description 6
- 101710187022 Cannabinoid receptor 2 Proteins 0.000 description 6
- 150000001200 N-acyl ethanolamides Chemical class 0.000 description 6
- KWYUFKZDYYNOTN-UHFFFAOYSA-M Potassium hydroxide Chemical compound [OH-].[K+] KWYUFKZDYYNOTN-UHFFFAOYSA-M 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 239000002671 adjuvant Substances 0.000 description 6
- PFKFTWBEEFSNDU-UHFFFAOYSA-N carbonyldiimidazole Chemical compound C1=CN=CN1C(=O)N1C=CN=C1 PFKFTWBEEFSNDU-UHFFFAOYSA-N 0.000 description 6
- 125000005112 cycloalkylalkoxy group Chemical group 0.000 description 6
- 239000002621 endocannabinoid Substances 0.000 description 6
- 239000003112 inhibitor Substances 0.000 description 6
- 229910052760 oxygen Inorganic materials 0.000 description 6
- 239000012071 phase Substances 0.000 description 6
- 238000000746 purification Methods 0.000 description 6
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 6
- 238000004808 supercritical fluid chromatography Methods 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 102100033868 Cannabinoid receptor 1 Human genes 0.000 description 5
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 5
- 210000003169 central nervous system Anatomy 0.000 description 5
- 239000013078 crystal Substances 0.000 description 5
- OCMNCWNTDDVHFK-UHFFFAOYSA-L dichloronickel;1,2-dimethoxyethane Chemical compound Cl[Ni]Cl.COCCOC OCMNCWNTDDVHFK-UHFFFAOYSA-L 0.000 description 5
- 239000002158 endotoxin Substances 0.000 description 5
- 239000006260 foam Substances 0.000 description 5
- 229920006008 lipopolysaccharide Polymers 0.000 description 5
- 125000002950 monocyclic group Chemical group 0.000 description 5
- 210000000653 nervous system Anatomy 0.000 description 5
- KJIFKLIQANRMOU-UHFFFAOYSA-N oxidanium;4-methylbenzenesulfonate Chemical compound O.CC1=CC=C(S(O)(=O)=O)C=C1 KJIFKLIQANRMOU-UHFFFAOYSA-N 0.000 description 5
- 229910052763 palladium Inorganic materials 0.000 description 5
- 239000011877 solvent mixture Substances 0.000 description 5
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 5
- 210000001519 tissue Anatomy 0.000 description 5
- RXBYRTSOWREATF-UHFFFAOYSA-N 1,2,3,4-tetrahydroacridine Chemical compound C1=CC=C2C=C(CCCC3)C3=NC2=C1 RXBYRTSOWREATF-UHFFFAOYSA-N 0.000 description 4
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 4
- BMIBJCFFZPYJHF-UHFFFAOYSA-N 2-methoxy-5-methyl-3-(4,4,5,5-tetramethyl-1,3,2-dioxaborolan-2-yl)pyridine Chemical compound COC1=NC=C(C)C=C1B1OC(C)(C)C(C)(C)O1 BMIBJCFFZPYJHF-UHFFFAOYSA-N 0.000 description 4
- VHYFNPMBLIVWCW-UHFFFAOYSA-N 4-Dimethylaminopyridine Chemical compound CN(C)C1=CC=NC=C1 VHYFNPMBLIVWCW-UHFFFAOYSA-N 0.000 description 4
- 241000208340 Araliaceae Species 0.000 description 4
- XKRFYHLGVUSROY-UHFFFAOYSA-N Argon Chemical compound [Ar] XKRFYHLGVUSROY-UHFFFAOYSA-N 0.000 description 4
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 4
- 102000018208 Cannabinoid Receptor Human genes 0.000 description 4
- 108050007331 Cannabinoid receptor Proteins 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- 241000282412 Homo Species 0.000 description 4
- WTDHULULXKLSOZ-UHFFFAOYSA-N Hydroxylamine hydrochloride Chemical compound Cl.ON WTDHULULXKLSOZ-UHFFFAOYSA-N 0.000 description 4
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 4
- PCLIMKBDDGJMGD-UHFFFAOYSA-N N-bromosuccinimide Chemical compound BrN1C(=O)CCC1=O PCLIMKBDDGJMGD-UHFFFAOYSA-N 0.000 description 4
- 235000005035 Panax pseudoginseng ssp. pseudoginseng Nutrition 0.000 description 4
- 235000003140 Panax quinquefolius Nutrition 0.000 description 4
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 4
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- 239000004480 active ingredient Substances 0.000 description 4
- YZXBAPSDXZZRGB-DOFZRALJSA-N arachidonic acid Chemical compound CCCCC\C=C/C\C=C/C\C=C/C\C=C/CCCC(O)=O YZXBAPSDXZZRGB-DOFZRALJSA-N 0.000 description 4
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 4
- 125000002619 bicyclic group Chemical group 0.000 description 4
- 239000004327 boric acid Substances 0.000 description 4
- ZADPBFCGQRWHPN-UHFFFAOYSA-N boronic acid Chemical compound OBO ZADPBFCGQRWHPN-UHFFFAOYSA-N 0.000 description 4
- 238000002425 crystallisation Methods 0.000 description 4
- 230000008025 crystallization Effects 0.000 description 4
- GPAYUJZHTULNBE-UHFFFAOYSA-N diphenylphosphine Chemical compound C=1C=CC=CC=1PC1=CC=CC=C1 GPAYUJZHTULNBE-UHFFFAOYSA-N 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 150000002066 eicosanoids Chemical class 0.000 description 4
- 239000007903 gelatin capsule Substances 0.000 description 4
- 235000008434 ginseng Nutrition 0.000 description 4
- 238000010438 heat treatment Methods 0.000 description 4
- 150000002430 hydrocarbons Chemical group 0.000 description 4
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 4
- 230000005764 inhibitory process Effects 0.000 description 4
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 4
- 239000002808 molecular sieve Substances 0.000 description 4
- 229910052757 nitrogen Inorganic materials 0.000 description 4
- 239000012299 nitrogen atmosphere Substances 0.000 description 4
- QWVGKYWNOKOFNN-UHFFFAOYSA-N o-cresol Chemical compound CC1=CC=CC=C1O QWVGKYWNOKOFNN-UHFFFAOYSA-N 0.000 description 4
- 239000012074 organic phase Substances 0.000 description 4
- 239000001301 oxygen Substances 0.000 description 4
- 229920005862 polyol Polymers 0.000 description 4
- 150000003077 polyols Chemical class 0.000 description 4
- NLKNQRATVPKPDG-UHFFFAOYSA-M potassium iodide Substances [K+].[I-] NLKNQRATVPKPDG-UHFFFAOYSA-M 0.000 description 4
- 238000011160 research Methods 0.000 description 4
- 229920006395 saturated elastomer Polymers 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 238000010898 silica gel chromatography Methods 0.000 description 4
- URGAHOPLAPQHLN-UHFFFAOYSA-N sodium aluminosilicate Chemical compound [Na+].[Al+3].[O-][Si]([O-])=O.[O-][Si]([O-])=O URGAHOPLAPQHLN-UHFFFAOYSA-N 0.000 description 4
- 229910000029 sodium carbonate Inorganic materials 0.000 description 4
- 235000017550 sodium carbonate Nutrition 0.000 description 4
- 229910000104 sodium hydride Inorganic materials 0.000 description 4
- 229910052938 sodium sulfate Inorganic materials 0.000 description 4
- 235000011152 sodium sulphate Nutrition 0.000 description 4
- 208000024891 symptom Diseases 0.000 description 4
- 239000003826 tablet Substances 0.000 description 4
- RUPAXCPQAAOIPB-UHFFFAOYSA-N tert-butyl formate Chemical group CC(C)(C)OC=O RUPAXCPQAAOIPB-UHFFFAOYSA-N 0.000 description 4
- ZVGUNGATIFIZOL-UHFFFAOYSA-N trimethyl(silyl)silane Chemical compound C[Si](C)(C)[SiH3] ZVGUNGATIFIZOL-UHFFFAOYSA-N 0.000 description 4
- RIOQSEWOXXDEQQ-UHFFFAOYSA-N triphenylphosphine Chemical compound C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 RIOQSEWOXXDEQQ-UHFFFAOYSA-N 0.000 description 4
- UCPYLLCMEDAXFR-UHFFFAOYSA-N triphosgene Chemical compound ClC(Cl)(Cl)OC(=O)OC(Cl)(Cl)Cl UCPYLLCMEDAXFR-UHFFFAOYSA-N 0.000 description 4
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 4
- GQHTUMJGOHRCHB-UHFFFAOYSA-N 2,3,4,6,7,8,9,10-octahydropyrimido[1,2-a]azepine Chemical compound C1CCCCN2CCCN=C21 GQHTUMJGOHRCHB-UHFFFAOYSA-N 0.000 description 3
- GOHBBINNYAWQGO-UHFFFAOYSA-N 2-bromo-3-chloropyridine Chemical compound ClC1=CC=CN=C1Br GOHBBINNYAWQGO-UHFFFAOYSA-N 0.000 description 3
- FZRBTBCCMVNZBD-UHFFFAOYSA-N 2-chloro-4-(trifluoromethyl)pyrimidine Chemical compound FC(F)(F)C1=CC=NC(Cl)=N1 FZRBTBCCMVNZBD-UHFFFAOYSA-N 0.000 description 3
- QILQSGMEWRSKHW-UHFFFAOYSA-N 2-chloro-4-cyclopropylpyrimidine Chemical compound ClC1=NC=CC(C2CC2)=N1 QILQSGMEWRSKHW-UHFFFAOYSA-N 0.000 description 3
- BDXYNMVQMBCTDB-UHFFFAOYSA-N 2-chloro-4-methoxypyrimidine Chemical compound COC1=CC=NC(Cl)=N1 BDXYNMVQMBCTDB-UHFFFAOYSA-N 0.000 description 3
- BHAKRVSCGILCEW-UHFFFAOYSA-N 2-chloro-4-methylpyrimidine Chemical compound CC1=CC=NC(Cl)=N1 BHAKRVSCGILCEW-UHFFFAOYSA-N 0.000 description 3
- UNCQVRBWJWWJBF-UHFFFAOYSA-N 2-chloropyrimidine Chemical compound ClC1=NC=CC=N1 UNCQVRBWJWWJBF-UHFFFAOYSA-N 0.000 description 3
- 125000003349 3-pyridyl group Chemical group N1=C([H])C([*])=C([H])C([H])=C1[H] 0.000 description 3
- FBEBVAQOMVWORE-UHFFFAOYSA-N 4-bromo-2-chloropyrimidine Chemical compound ClC1=NC=CC(Br)=N1 FBEBVAQOMVWORE-UHFFFAOYSA-N 0.000 description 3
- GZFGOTFRPZRKDS-UHFFFAOYSA-N 4-bromophenol Chemical compound OC1=CC=C(Br)C=C1 GZFGOTFRPZRKDS-UHFFFAOYSA-N 0.000 description 3
- BWVZLXTZQHILRC-UHFFFAOYSA-N 4-chloro-2-methylsulfonylpyrimidine Chemical compound CS(=O)(=O)C1=NC=CC(Cl)=N1 BWVZLXTZQHILRC-UHFFFAOYSA-N 0.000 description 3
- BEQUUSCRAKEKQM-UHFFFAOYSA-N 4-chloro-3-fluoropyridine Chemical compound FC1=CN=CC=C1Cl BEQUUSCRAKEKQM-UHFFFAOYSA-N 0.000 description 3
- ZHWYKDRRKPFHJK-UHFFFAOYSA-N 5-bromo-2-(2-chlorophenoxy)pyridine Chemical compound ClC1=CC=CC=C1OC1=CC=C(Br)C=N1 ZHWYKDRRKPFHJK-UHFFFAOYSA-N 0.000 description 3
- NLXLAEXVIDQMFP-UHFFFAOYSA-N Ammonia chloride Chemical compound [NH4+].[Cl-] NLXLAEXVIDQMFP-UHFFFAOYSA-N 0.000 description 3
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 3
- 229920002261 Corn starch Polymers 0.000 description 3
- 238000003820 Medium-pressure liquid chromatography Methods 0.000 description 3
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 3
- IMNFDUFMRHMDMM-UHFFFAOYSA-N N-Heptane Chemical compound CCCCCCC IMNFDUFMRHMDMM-UHFFFAOYSA-N 0.000 description 3
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 3
- 101150003085 Pdcl gene Proteins 0.000 description 3
- YGYAWVDWMABLBF-UHFFFAOYSA-N Phosgene Chemical compound ClC(Cl)=O YGYAWVDWMABLBF-UHFFFAOYSA-N 0.000 description 3
- OFOBLEOULBTSOW-UHFFFAOYSA-N Propanedioic acid Natural products OC(=O)CC(O)=O OFOBLEOULBTSOW-UHFFFAOYSA-N 0.000 description 3
- KEAYESYHFKHZAL-UHFFFAOYSA-N Sodium Chemical compound [Na] KEAYESYHFKHZAL-UHFFFAOYSA-N 0.000 description 3
- 125000002431 aminoalkoxy group Chemical group 0.000 description 3
- 125000004429 atom Chemical group 0.000 description 3
- SRSXLGNVWSONIS-UHFFFAOYSA-M benzenesulfonate Chemical compound [O-]S(=O)(=O)C1=CC=CC=C1 SRSXLGNVWSONIS-UHFFFAOYSA-M 0.000 description 3
- 229940077388 benzenesulfonate Drugs 0.000 description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 description 3
- 238000007664 blowing Methods 0.000 description 3
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 3
- FJDQFPXHSGXQBY-UHFFFAOYSA-L caesium carbonate Chemical compound [Cs+].[Cs+].[O-]C([O-])=O FJDQFPXHSGXQBY-UHFFFAOYSA-L 0.000 description 3
- 229910000024 caesium carbonate Inorganic materials 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000012230 colorless oil Substances 0.000 description 3
- 238000004440 column chromatography Methods 0.000 description 3
- 238000004891 communication Methods 0.000 description 3
- 229940125890 compound Ia Drugs 0.000 description 3
- 238000001816 cooling Methods 0.000 description 3
- 239000008120 corn starch Substances 0.000 description 3
- 239000012043 crude product Substances 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- HCUYBXPSSCRKRF-UHFFFAOYSA-N diphosgene Chemical compound ClC(=O)OC(Cl)(Cl)Cl HCUYBXPSSCRKRF-UHFFFAOYSA-N 0.000 description 3
- 239000008298 dragée Substances 0.000 description 3
- KTWOOEGAPBSYNW-UHFFFAOYSA-N ferrocene Chemical compound [Fe+2].C=1C=C[CH-]C=1.C=1C=C[CH-]C=1 KTWOOEGAPBSYNW-UHFFFAOYSA-N 0.000 description 3
- 210000001035 gastrointestinal tract Anatomy 0.000 description 3
- 125000004438 haloalkoxy group Chemical group 0.000 description 3
- 125000001188 haloalkyl group Chemical group 0.000 description 3
- 125000005842 heteroatom Chemical group 0.000 description 3
- OAKJQQAXSVQMHS-UHFFFAOYSA-N hydrazine Substances NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 3
- IXCSERBJSXMMFS-UHFFFAOYSA-N hydrogen chloride Substances Cl.Cl IXCSERBJSXMMFS-UHFFFAOYSA-N 0.000 description 3
- 229910000041 hydrogen chloride Inorganic materials 0.000 description 3
- 238000002347 injection Methods 0.000 description 3
- 239000007924 injection Substances 0.000 description 3
- 230000000968 intestinal effect Effects 0.000 description 3
- 239000010410 layer Substances 0.000 description 3
- 150000002617 leukotrienes Chemical class 0.000 description 3
- 239000007788 liquid Substances 0.000 description 3
- 239000007937 lozenge Substances 0.000 description 3
- IUYHWZFSGMZEOG-UHFFFAOYSA-M magnesium;propane;chloride Chemical compound [Mg+2].[Cl-].C[CH-]C IUYHWZFSGMZEOG-UHFFFAOYSA-M 0.000 description 3
- 210000000274 microglia Anatomy 0.000 description 3
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 3
- 229910052759 nickel Inorganic materials 0.000 description 3
- LXNAVEXFUKBNMK-UHFFFAOYSA-N palladium(II) acetate Substances [Pd].CC(O)=O.CC(O)=O LXNAVEXFUKBNMK-UHFFFAOYSA-N 0.000 description 3
- UQPUONNXJVWHRM-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 UQPUONNXJVWHRM-UHFFFAOYSA-N 0.000 description 3
- 239000003208 petroleum Substances 0.000 description 3
- 239000000825 pharmaceutical preparation Substances 0.000 description 3
- 229910000027 potassium carbonate Inorganic materials 0.000 description 3
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 3
- 230000000770 proinflammatory effect Effects 0.000 description 3
- 150000003180 prostaglandins Chemical class 0.000 description 3
- 230000004224 protection Effects 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 230000009257 reactivity Effects 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 239000012312 sodium hydride Substances 0.000 description 3
- 229910052717 sulfur Inorganic materials 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 239000000454 talc Substances 0.000 description 3
- 229910052623 talc Inorganic materials 0.000 description 3
- 238000002560 therapeutic procedure Methods 0.000 description 3
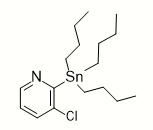
- UPSIWQDIUJUACS-UHFFFAOYSA-N tributyl-(3-chloropyridin-2-yl)stannane Chemical compound CCCC[Sn](CCCC)(CCCC)C1=NC=CC=C1Cl UPSIWQDIUJUACS-UHFFFAOYSA-N 0.000 description 3
- WUDMJZRGWGQBQH-UHFFFAOYSA-N (1-methylpyrazol-3-yl)boronic acid Chemical compound CN1C=CC(B(O)O)=N1 WUDMJZRGWGQBQH-UHFFFAOYSA-N 0.000 description 2
- WXGBZJJAGLSBPR-UHFFFAOYSA-N (2-fluoropyridin-4-yl)boronic acid Chemical compound OB(O)C1=CC=NC(F)=C1 WXGBZJJAGLSBPR-UHFFFAOYSA-N 0.000 description 2
- QBLFZIBJXUQVRF-UHFFFAOYSA-N (4-bromophenyl)boronic acid Chemical compound OB(O)C1=CC=C(Br)C=C1 QBLFZIBJXUQVRF-UHFFFAOYSA-N 0.000 description 2
- NRESDXFFSNBDGP-UHFFFAOYSA-N (4-bromophenyl)hydrazine Chemical compound NNC1=CC=C(Br)C=C1 NRESDXFFSNBDGP-UHFFFAOYSA-N 0.000 description 2
- LOVPHSMOAVXQIH-UHFFFAOYSA-M (4-nitrophenyl) carbonate Chemical compound [O-]C(=O)OC1=CC=C([N+]([O-])=O)C=C1 LOVPHSMOAVXQIH-UHFFFAOYSA-M 0.000 description 2
- YZXBAPSDXZZRGB-PNXWREOESA-N (5z,8z,11z,14z)-2,2,3,3,4,4,5,6-octadeuterioicosa-5,8,11,14-tetraenoic acid Chemical compound OC(=O)C([2H])([2H])C([2H])([2H])C([2H])([2H])C(/[2H])=C(/[2H])C\C=C/C\C=C/C\C=C/CCCCC YZXBAPSDXZZRGB-PNXWREOESA-N 0.000 description 2
- OJBYZWHAPXIJID-UHFFFAOYSA-N (6-fluoropyridin-3-yl)boronic acid Chemical compound OB(O)C1=CC=C(F)N=C1 OJBYZWHAPXIJID-UHFFFAOYSA-N 0.000 description 2
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 2
- IGZLESKZUATMSD-BQYQJAHWSA-N (e)-1-(4-bromophenyl)-3-(dimethylamino)prop-2-en-1-one Chemical compound CN(C)\C=C\C(=O)C1=CC=C(Br)C=C1 IGZLESKZUATMSD-BQYQJAHWSA-N 0.000 description 2
- 125000003088 (fluoren-9-ylmethoxy)carbonyl group Chemical group 0.000 description 2
- 125000001766 1,2,4-oxadiazol-3-yl group Chemical group [H]C1=NC(*)=NO1 0.000 description 2
- ATCMNDCOEJOOSF-UHFFFAOYSA-N 1-(4-bromophenyl)-3,5-dimethylpyrazole Chemical compound N1=C(C)C=C(C)N1C1=CC=C(Br)C=C1 ATCMNDCOEJOOSF-UHFFFAOYSA-N 0.000 description 2
- WYECURVXVYPVAT-UHFFFAOYSA-N 1-(4-bromophenyl)ethanone Chemical compound CC(=O)C1=CC=C(Br)C=C1 WYECURVXVYPVAT-UHFFFAOYSA-N 0.000 description 2
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 2
- PAQZWJGSJMLPMG-UHFFFAOYSA-N 2,4,6-tripropyl-1,3,5,2$l^{5},4$l^{5},6$l^{5}-trioxatriphosphinane 2,4,6-trioxide Chemical compound CCCP1(=O)OP(=O)(CCC)OP(=O)(CCC)O1 PAQZWJGSJMLPMG-UHFFFAOYSA-N 0.000 description 2
- NVWVWEWVLBKPSM-UHFFFAOYSA-N 2,4-difluorophenol Chemical compound OC1=CC=C(F)C=C1F NVWVWEWVLBKPSM-UHFFFAOYSA-N 0.000 description 2
- DWUJDNHHQKEOPR-UHFFFAOYSA-N 2-(2-piperidin-4-ylethyl)pyridine Chemical compound C1CNCCC1CCC1=CC=CC=N1 DWUJDNHHQKEOPR-UHFFFAOYSA-N 0.000 description 2
- BSSJQAJRTVASQD-UHFFFAOYSA-N 2-(4-bromophenyl)-5-(2,2-dimethylpropyl)-1,3,4-oxadiazole Chemical compound CC(C)(C)CC1=NN=C(O1)C1=CC=C(Br)C=C1 BSSJQAJRTVASQD-UHFFFAOYSA-N 0.000 description 2
- PQMCFTMVQORYJC-UHFFFAOYSA-N 2-aminocyclohexan-1-ol Chemical compound NC1CCCCC1O PQMCFTMVQORYJC-UHFFFAOYSA-N 0.000 description 2
- ISPYQTSUDJAMAB-UHFFFAOYSA-N 2-chlorophenol Chemical compound OC1=CC=CC=C1Cl ISPYQTSUDJAMAB-UHFFFAOYSA-N 0.000 description 2
- UDMNVTJFUISBFD-UHFFFAOYSA-N 2-fluoro-6-methylpyridine Chemical compound CC1=CC=CC(F)=N1 UDMNVTJFUISBFD-UHFFFAOYSA-N 0.000 description 2
- GDHXJNRAJRCGMX-UHFFFAOYSA-N 2-fluorobenzonitrile Chemical compound FC1=CC=CC=C1C#N GDHXJNRAJRCGMX-UHFFFAOYSA-N 0.000 description 2
- AZCCTQYOEYFRAK-UHFFFAOYSA-N 2-fluoroethylhydrazine Chemical compound NNCCF AZCCTQYOEYFRAK-UHFFFAOYSA-N 0.000 description 2
- HFHFGHLXUCOHLN-UHFFFAOYSA-N 2-fluorophenol Chemical compound OC1=CC=CC=C1F HFHFGHLXUCOHLN-UHFFFAOYSA-N 0.000 description 2
- UGEJOEBBMPOJMT-UHFFFAOYSA-N 3-(trifluoromethyl)phenol Chemical compound OC1=CC=CC(C(F)(F)F)=C1 UGEJOEBBMPOJMT-UHFFFAOYSA-N 0.000 description 2
- LTILYPOSFJLPSK-UHFFFAOYSA-N 3-chloro-5-fluoropyridine Chemical compound FC1=CN=CC(Cl)=C1 LTILYPOSFJLPSK-UHFFFAOYSA-N 0.000 description 2
- NHQDETIJWKXCTC-UHFFFAOYSA-N 3-chloroperbenzoic acid Chemical compound OOC(=O)C1=CC=CC(Cl)=C1 NHQDETIJWKXCTC-UHFFFAOYSA-N 0.000 description 2
- HORNXRXVQWOLPJ-UHFFFAOYSA-N 3-chlorophenol Chemical compound OC1=CC=CC(Cl)=C1 HORNXRXVQWOLPJ-UHFFFAOYSA-N 0.000 description 2
- SJTBRFHBXDZMPS-UHFFFAOYSA-N 3-fluorophenol Chemical compound OC1=CC=CC(F)=C1 SJTBRFHBXDZMPS-UHFFFAOYSA-N 0.000 description 2
- CELKOWQJPVJKIL-UHFFFAOYSA-N 3-fluoropyridine Chemical compound FC1=CC=CN=C1 CELKOWQJPVJKIL-UHFFFAOYSA-N 0.000 description 2
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 2
- HQSCPPCMBMFJJN-UHFFFAOYSA-N 4-bromobenzonitrile Chemical compound BrC1=CC=C(C#N)C=C1 HQSCPPCMBMFJJN-UHFFFAOYSA-N 0.000 description 2
- WXNZTHHGJRFXKQ-UHFFFAOYSA-N 4-chlorophenol Chemical compound OC1=CC=C(Cl)C=C1 WXNZTHHGJRFXKQ-UHFFFAOYSA-N 0.000 description 2
- RHMPLDJJXGPMEX-UHFFFAOYSA-N 4-fluorophenol Chemical compound OC1=CC=C(F)C=C1 RHMPLDJJXGPMEX-UHFFFAOYSA-N 0.000 description 2
- BJZWAZIZGZLNHA-UHFFFAOYSA-N 5-bromo-2-(4-chlorophenoxy)pyridine Chemical compound C1=CC(Cl)=CC=C1OC1=CC=C(Br)C=N1 BJZWAZIZGZLNHA-UHFFFAOYSA-N 0.000 description 2
- RXMSTPNZKYVUHZ-UHFFFAOYSA-N 5-bromo-2-[4-(trifluoromethoxy)phenoxy]pyridine Chemical compound C1=CC(OC(F)(F)F)=CC=C1OC1=CC=C(Br)C=N1 RXMSTPNZKYVUHZ-UHFFFAOYSA-N 0.000 description 2
- ZCYVEMRRCGMTRW-UHFFFAOYSA-N 7553-56-2 Chemical compound [I] ZCYVEMRRCGMTRW-UHFFFAOYSA-N 0.000 description 2
- KWOLFJPFCHCOCG-UHFFFAOYSA-N Acetophenone Chemical compound CC(=O)C1=CC=CC=C1 KWOLFJPFCHCOCG-UHFFFAOYSA-N 0.000 description 2
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 description 2
- USFZMSVCRYTOJT-UHFFFAOYSA-N Ammonium acetate Chemical compound N.CC(O)=O USFZMSVCRYTOJT-UHFFFAOYSA-N 0.000 description 2
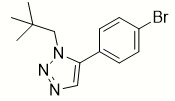
- URGKFDKKAMRIGI-UHFFFAOYSA-N BrC1=CC=C(C=C1)C1=CN=NN1CC(C)(C)C Chemical compound BrC1=CC=C(C=C1)C1=CN=NN1CC(C)(C)C URGKFDKKAMRIGI-UHFFFAOYSA-N 0.000 description 2
- 125000001313 C5-C10 heteroaryl group Chemical group 0.000 description 2
- 102000009132 CB1 Cannabinoid Receptor Human genes 0.000 description 2
- 108010073366 CB1 Cannabinoid Receptor Proteins 0.000 description 2
- 102000009135 CB2 Cannabinoid Receptor Human genes 0.000 description 2
- 108010073376 CB2 Cannabinoid Receptor Proteins 0.000 description 2
- HYKBRLYDGXRZMT-UHFFFAOYSA-N CC(C)(C)OC(N(C1)C=CCCC1Br)=O Chemical compound CC(C)(C)OC(N(C1)C=CCCC1Br)=O HYKBRLYDGXRZMT-UHFFFAOYSA-N 0.000 description 2
- JKMLXKXGNZLFBG-UHFFFAOYSA-N CC(C)(C)OC(N(C1)C=CCCC1C(C=N1)=CC=C1OC1=CC(Cl)=CC=C1)=O Chemical compound CC(C)(C)OC(N(C1)C=CCCC1C(C=N1)=CC=C1OC1=CC(Cl)=CC=C1)=O JKMLXKXGNZLFBG-UHFFFAOYSA-N 0.000 description 2
- 229940126639 Compound 33 Drugs 0.000 description 2
- 108090000695 Cytokines Proteins 0.000 description 2
- 102000004127 Cytokines Human genes 0.000 description 2
- MHZGKXUYDGKKIU-UHFFFAOYSA-N Decylamine Chemical compound CCCCCCCCCCN MHZGKXUYDGKKIU-UHFFFAOYSA-N 0.000 description 2
- 244000166102 Eucalyptus leucoxylon Species 0.000 description 2
- 235000004694 Eucalyptus leucoxylon Nutrition 0.000 description 2
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- AEMRFAOFKBGASW-UHFFFAOYSA-N Glycolic acid Chemical compound OCC(O)=O AEMRFAOFKBGASW-UHFFFAOYSA-N 0.000 description 2
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 2
- 102000017055 Lipoprotein Lipase Human genes 0.000 description 2
- 108010013563 Lipoprotein Lipase Proteins 0.000 description 2
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 2
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 241000872931 Myoporum sandwicense Species 0.000 description 2
- KWYHDKDOAIKMQN-UHFFFAOYSA-N N,N,N',N'-tetramethylethylenediamine Chemical compound CN(C)CCN(C)C KWYHDKDOAIKMQN-UHFFFAOYSA-N 0.000 description 2
- 239000007832 Na2SO4 Substances 0.000 description 2
- 229910021588 Nickel(II) iodide Inorganic materials 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-N Phosphoric acid Chemical compound OP(O)(O)=O NBIIXXVUZAFLBC-UHFFFAOYSA-N 0.000 description 2
- 239000004743 Polypropylene Substances 0.000 description 2
- 102000004005 Prostaglandin-endoperoxide synthases Human genes 0.000 description 2
- 108090000459 Prostaglandin-endoperoxide synthases Proteins 0.000 description 2
- WTKZEGDFNFYCGP-UHFFFAOYSA-N Pyrazole Chemical compound C=1C=NNC=1 WTKZEGDFNFYCGP-UHFFFAOYSA-N 0.000 description 2
- LCTONWCANYUPML-UHFFFAOYSA-N Pyruvic acid Chemical compound CC(=O)C(O)=O LCTONWCANYUPML-UHFFFAOYSA-N 0.000 description 2
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 2
- 238000006069 Suzuki reaction reaction Methods 0.000 description 2
- XNRNNGPBEPRNAR-UHFFFAOYSA-N Thromboxane B2 Natural products CCCCCC(O)C=CC1OC(O)CC(O)C1CC=CCCCC(O)=O XNRNNGPBEPRNAR-UHFFFAOYSA-N 0.000 description 2
- GCTFWCDSFPMHHS-UHFFFAOYSA-M Tributyltin chloride Chemical compound CCCC[Sn](Cl)(CCCC)CCCC GCTFWCDSFPMHHS-UHFFFAOYSA-M 0.000 description 2
- 150000007513 acids Chemical class 0.000 description 2
- 125000003277 amino group Chemical group 0.000 description 2
- 230000003110 anti-inflammatory effect Effects 0.000 description 2
- 229940114079 arachidonic acid Drugs 0.000 description 2
- 235000021342 arachidonic acid Nutrition 0.000 description 2
- 229910052786 argon Inorganic materials 0.000 description 2
- 239000012300 argon atmosphere Substances 0.000 description 2
- 150000001543 aryl boronic acids Chemical class 0.000 description 2
- 239000012131 assay buffer Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- YHNUDLCUIKMNSN-UHFFFAOYSA-N bis(1,2,4-triazol-1-yl)methanone Chemical compound C1=NC=NN1C(=O)N1C=NC=N1 YHNUDLCUIKMNSN-UHFFFAOYSA-N 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 125000001246 bromo group Chemical group Br* 0.000 description 2
- 239000002775 capsule Substances 0.000 description 2
- 229940044683 chemotherapy drug Drugs 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 229940125877 compound 31 Drugs 0.000 description 2
- DOBRDRYODQBAMW-UHFFFAOYSA-N copper(i) cyanide Chemical compound [Cu+].N#[C-] DOBRDRYODQBAMW-UHFFFAOYSA-N 0.000 description 2
- SXTLQDJHRPXDSB-UHFFFAOYSA-N copper;dinitrate;trihydrate Chemical compound O.O.O.[Cu+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O SXTLQDJHRPXDSB-UHFFFAOYSA-N 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- 238000011161 development Methods 0.000 description 2
- 230000018109 developmental process Effects 0.000 description 2
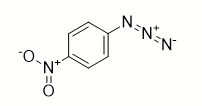
- CZZVSJPFJBUBDK-UHFFFAOYSA-N diazonio-(4-nitrophenyl)azanide Chemical compound [O-][N+](=O)C1=CC=C([N-][N+]#N)C=C1 CZZVSJPFJBUBDK-UHFFFAOYSA-N 0.000 description 2
- ZOCHARZZJNPSEU-UHFFFAOYSA-N diboron Chemical compound B#B ZOCHARZZJNPSEU-UHFFFAOYSA-N 0.000 description 2
- 125000003963 dichloro group Chemical group Cl* 0.000 description 2
- FAMRKDQNMBBFBR-BQYQJAHWSA-N diethyl azodicarboxylate Substances CCOC(=O)\N=N\C(=O)OCC FAMRKDQNMBBFBR-BQYQJAHWSA-N 0.000 description 2
- CSJLBAMHHLJAAS-UHFFFAOYSA-N diethylaminosulfur trifluoride Chemical compound CCN(CC)S(F)(F)F CSJLBAMHHLJAAS-UHFFFAOYSA-N 0.000 description 2
- 238000010790 dilution Methods 0.000 description 2
- 239000012895 dilution Substances 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- XEYBRNLFEZDVAW-ARSRFYASSA-N dinoprostone Chemical compound CCCCC[C@H](O)\C=C\[C@H]1[C@H](O)CC(=O)[C@@H]1C\C=C/CCCC(O)=O XEYBRNLFEZDVAW-ARSRFYASSA-N 0.000 description 2
- 239000012039 electrophile Substances 0.000 description 2
- 238000003821 enantio-separation Methods 0.000 description 2
- 210000000105 enteric nervous system Anatomy 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 238000000605 extraction Methods 0.000 description 2
- 239000003925 fat Substances 0.000 description 2
- 235000019197 fats Nutrition 0.000 description 2
- QEWYKACRFQMRMB-UHFFFAOYSA-N fluoroacetic acid Chemical compound OC(=O)CF QEWYKACRFQMRMB-UHFFFAOYSA-N 0.000 description 2
- 235000019253 formic acid Nutrition 0.000 description 2
- 230000006870 function Effects 0.000 description 2
- 125000000524 functional group Chemical group 0.000 description 2
- 239000003292 glue Substances 0.000 description 2
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 2
- VAMFXQBUQXONLZ-UHFFFAOYSA-N icos-1-ene Chemical compound CCCCCCCCCCCCCCCCCCC=C VAMFXQBUQXONLZ-UHFFFAOYSA-N 0.000 description 2
- 210000002865 immune cell Anatomy 0.000 description 2
- 238000001727 in vivo Methods 0.000 description 2
- 150000007529 inorganic bases Chemical class 0.000 description 2
- 229910052740 iodine Inorganic materials 0.000 description 2
- 239000011630 iodine Substances 0.000 description 2
- 150000002500 ions Chemical class 0.000 description 2
- MILUBEOXRNEUHS-UHFFFAOYSA-N iridium(3+) Chemical compound [Ir+3] MILUBEOXRNEUHS-UHFFFAOYSA-N 0.000 description 2
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 2
- 239000008101 lactose Substances 0.000 description 2
- 230000037356 lipid metabolism Effects 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- 229910052744 lithium Inorganic materials 0.000 description 2
- YNESATAKKCNGOF-UHFFFAOYSA-N lithium bis(trimethylsilyl)amide Chemical compound [Li+].C[Si](C)(C)[N-][Si](C)(C)C YNESATAKKCNGOF-UHFFFAOYSA-N 0.000 description 2
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical group [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 2
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Substances [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 238000004949 mass spectrometry Methods 0.000 description 2
- 230000003340 mental effect Effects 0.000 description 2
- KVKFRMCSXWQSNT-UHFFFAOYSA-N n,n'-dimethylethane-1,2-diamine Chemical compound CNCCNC KVKFRMCSXWQSNT-UHFFFAOYSA-N 0.000 description 2
- 239000006225 natural substrate Substances 0.000 description 2
- 210000000944 nerve tissue Anatomy 0.000 description 2
- 210000004498 neuroglial cell Anatomy 0.000 description 2
- 210000002569 neuron Anatomy 0.000 description 2
- BFSQJYRFLQUZKX-UHFFFAOYSA-L nickel(ii) iodide Chemical compound I[Ni]I BFSQJYRFLQUZKX-UHFFFAOYSA-L 0.000 description 2
- 150000007530 organic bases Chemical class 0.000 description 2
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 2
- PIBWKRNGBLPSSY-UHFFFAOYSA-L palladium(II) chloride Chemical compound Cl[Pd]Cl PIBWKRNGBLPSSY-UHFFFAOYSA-L 0.000 description 2
- YJVFFLUZDVXJQI-UHFFFAOYSA-L palladium(ii) acetate Chemical compound [Pd+2].CC([O-])=O.CC([O-])=O YJVFFLUZDVXJQI-UHFFFAOYSA-L 0.000 description 2
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 2
- 210000001428 peripheral nervous system Anatomy 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- 230000009038 pharmacological inhibition Effects 0.000 description 2
- HXITXNWTGFUOAU-UHFFFAOYSA-N phenylboronic acid Chemical compound OB(O)C1=CC=CC=C1 HXITXNWTGFUOAU-UHFFFAOYSA-N 0.000 description 2
- UYWQUFXKFGHYNT-UHFFFAOYSA-N phenylmethyl ester of formic acid Natural products O=COCC1=CC=CC=C1 UYWQUFXKFGHYNT-UHFFFAOYSA-N 0.000 description 2
- 239000011941 photocatalyst Substances 0.000 description 2
- IVDFJHOHABJVEH-UHFFFAOYSA-N pinacol Chemical compound CC(C)(O)C(C)(C)O IVDFJHOHABJVEH-UHFFFAOYSA-N 0.000 description 2
- SCVFZCLFOSHCOH-UHFFFAOYSA-M potassium acetate Chemical compound [K+].CC([O-])=O SCVFZCLFOSHCOH-UHFFFAOYSA-M 0.000 description 2
- 239000000843 powder Substances 0.000 description 2
- 239000002243 precursor Substances 0.000 description 2
- 125000004353 pyrazol-1-yl group Chemical group [H]C1=NN(*)C([H])=C1[H] 0.000 description 2
- YGSDEFSMJLZEOE-UHFFFAOYSA-N salicylic acid Chemical compound OC(=O)C1=CC=CC=C1O YGSDEFSMJLZEOE-UHFFFAOYSA-N 0.000 description 2
- DCKVNWZUADLDEH-UHFFFAOYSA-N sec-butyl acetate Chemical group CCC(C)OC(C)=O DCKVNWZUADLDEH-UHFFFAOYSA-N 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 2
- 125000003003 spiro group Chemical group 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 210000004500 stellate cell Anatomy 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- IOGXOCVLYRDXLW-UHFFFAOYSA-N tert-butyl nitrite Chemical compound CC(C)(C)ON=O IOGXOCVLYRDXLW-UHFFFAOYSA-N 0.000 description 2
- 239000012414 tert-butyl nitrite Substances 0.000 description 2
- DPKBAXPHAYBPRL-UHFFFAOYSA-M tetrabutylazanium;iodide Chemical compound [I-].CCCC[N+](CCCC)(CCCC)CCCC DPKBAXPHAYBPRL-UHFFFAOYSA-M 0.000 description 2
- 125000004495 thiazol-4-yl group Chemical group S1C=NC(=C1)* 0.000 description 2
- XNRNNGPBEPRNAR-JQBLCGNGSA-N thromboxane B2 Chemical compound CCCCC[C@H](O)\C=C\[C@H]1OC(O)C[C@H](O)[C@@H]1C\C=C/CCCC(O)=O XNRNNGPBEPRNAR-JQBLCGNGSA-N 0.000 description 2
- 230000000451 tissue damage Effects 0.000 description 2
- 231100000827 tissue damage Toxicity 0.000 description 2
- JOXIMZWYDAKGHI-UHFFFAOYSA-M toluene-4-sulfonate Chemical compound CC1=CC=C(S([O-])(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-M 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- ITMCEJHCFYSIIV-UHFFFAOYSA-M triflate Chemical compound [O-]S(=O)(=O)C(F)(F)F ITMCEJHCFYSIIV-UHFFFAOYSA-M 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 235000015112 vegetable and seed oil Nutrition 0.000 description 2
- 239000008158 vegetable oil Substances 0.000 description 2
- 239000001993 wax Substances 0.000 description 2
- RYGOBSYXIIUFOR-UHFFFAOYSA-N (1-methylpyrazol-4-yl)boronic acid Chemical compound CN1C=C(B(O)O)C=N1 RYGOBSYXIIUFOR-UHFFFAOYSA-N 0.000 description 1
- QBYIENPQHBMVBV-HFEGYEGKSA-N (2R)-2-hydroxy-2-phenylacetic acid Chemical compound O[C@@H](C(O)=O)c1ccccc1.O[C@@H](C(O)=O)c1ccccc1 QBYIENPQHBMVBV-HFEGYEGKSA-N 0.000 description 1
- ZFYIQPIHXRFFCZ-QMMMGPOBSA-N (2s)-2-(cyclohexylamino)butanedioic acid Chemical compound OC(=O)C[C@@H](C(O)=O)NC1CCCCC1 ZFYIQPIHXRFFCZ-QMMMGPOBSA-N 0.000 description 1
- SABLROJJEJTWTE-UHFFFAOYSA-N (4-bromophenyl)methylhydrazine Chemical compound NNCC1=CC=C(Br)C=C1 SABLROJJEJTWTE-UHFFFAOYSA-N 0.000 description 1
- NXLNNXIXOYSCMB-UHFFFAOYSA-N (4-nitrophenyl) carbonochloridate Chemical compound [O-][N+](=O)C1=CC=C(OC(Cl)=O)C=C1 NXLNNXIXOYSCMB-UHFFFAOYSA-N 0.000 description 1
- LOVPHSMOAVXQIH-UHFFFAOYSA-N (4-nitrophenyl) hydrogen carbonate Chemical compound OC(=O)OC1=CC=C([N+]([O-])=O)C=C1 LOVPHSMOAVXQIH-UHFFFAOYSA-N 0.000 description 1
- 125000004191 (C1-C6) alkoxy group Chemical group 0.000 description 1
- WBYWAXJHAXSJNI-VOTSOKGWSA-M .beta-Phenylacrylic acid Natural products [O-]C(=O)\C=C\C1=CC=CC=C1 WBYWAXJHAXSJNI-VOTSOKGWSA-M 0.000 description 1
- SPEUIVXLLWOEMJ-UHFFFAOYSA-N 1,1-dimethoxyethane Chemical compound COC(C)OC SPEUIVXLLWOEMJ-UHFFFAOYSA-N 0.000 description 1
- BNZOPSKVNVDPRH-UHFFFAOYSA-N 1,5-difluoro-2H-pyrimidine Chemical compound C1N=CC(=CN1F)F BNZOPSKVNVDPRH-UHFFFAOYSA-N 0.000 description 1
- IBXMKLPFLZYRQZ-UHFFFAOYSA-N 1,5-diphenylpenta-1,4-dien-3-one;palladium Chemical compound [Pd].[Pd].C=1C=CC=CC=1C=CC(=O)C=CC1=CC=CC=C1 IBXMKLPFLZYRQZ-UHFFFAOYSA-N 0.000 description 1
- NTMSIZVRQWWUQG-UHFFFAOYSA-N 1,6-dichloro-2H-pyrimidine Chemical compound ClN1CN=CC=C1Cl NTMSIZVRQWWUQG-UHFFFAOYSA-N 0.000 description 1
- XKCBZOLQCZMTCC-UHFFFAOYSA-N 1-(2,2-dimethylpropyl)pyrazole Chemical compound CC(C)(C)CN1C=CC=N1 XKCBZOLQCZMTCC-UHFFFAOYSA-N 0.000 description 1
- ASOKPJOREAFHNY-UHFFFAOYSA-N 1-Hydroxybenzotriazole Chemical group C1=CC=C2N(O)N=NC2=C1 ASOKPJOREAFHNY-UHFFFAOYSA-N 0.000 description 1
- CQWYAXCOVZKLHY-UHFFFAOYSA-N 1-bromo-2,2-dimethylpropane Chemical compound CC(C)(C)CBr CQWYAXCOVZKLHY-UHFFFAOYSA-N 0.000 description 1
- YVZFJUGPSAESPP-UHFFFAOYSA-N 1-chloro-2h-pyrimidine Chemical compound ClN1CN=CC=C1 YVZFJUGPSAESPP-UHFFFAOYSA-N 0.000 description 1
- XDIAMRVROCPPBK-UHFFFAOYSA-N 2,2-dimethylpropan-1-amine Chemical compound CC(C)(C)CN XDIAMRVROCPPBK-UHFFFAOYSA-N 0.000 description 1
- ZIIUUSVHCHPIQD-UHFFFAOYSA-N 2,4,6-trimethyl-N-[3-(trifluoromethyl)phenyl]benzenesulfonamide Chemical compound CC1=CC(C)=CC(C)=C1S(=O)(=O)NC1=CC=CC(C(F)(F)F)=C1 ZIIUUSVHCHPIQD-UHFFFAOYSA-N 0.000 description 1
- NHJVRSWLHSJWIN-UHFFFAOYSA-N 2,4,6-trinitrobenzenesulfonic acid Chemical compound OS(=O)(=O)C1=C([N+]([O-])=O)C=C([N+]([O-])=O)C=C1[N+]([O-])=O NHJVRSWLHSJWIN-UHFFFAOYSA-N 0.000 description 1
- LBLYYCQCTBFVLH-UHFFFAOYSA-N 2-Methylbenzenesulfonic acid Chemical compound CC1=CC=CC=C1S(O)(=O)=O LBLYYCQCTBFVLH-UHFFFAOYSA-N 0.000 description 1
- IQHSSYROJYPFDV-UHFFFAOYSA-N 2-bromo-1,3-dichloro-5-(trifluoromethyl)benzene Chemical group FC(F)(F)C1=CC(Cl)=C(Br)C(Cl)=C1 IQHSSYROJYPFDV-UHFFFAOYSA-N 0.000 description 1
- BPJJWAVDPVBHHL-UHFFFAOYSA-N 2-bromo-3,5-dimethyl-1H-pyrrole Chemical compound CC1=CC(C)=C(Br)N1 BPJJWAVDPVBHHL-UHFFFAOYSA-N 0.000 description 1
- 125000000954 2-hydroxyethyl group Chemical group [H]C([*])([H])C([H])([H])O[H] 0.000 description 1
- 125000004105 2-pyridyl group Chemical group N1=C([*])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- WRXAZPPGFLETFR-UHFFFAOYSA-N 3,5-difluoropyridine Chemical compound FC1=CN=CC(F)=C1 WRXAZPPGFLETFR-UHFFFAOYSA-N 0.000 description 1
- FPQQSJJWHUJYPU-UHFFFAOYSA-N 3-(dimethylamino)propyliminomethylidene-ethylazanium;chloride Chemical compound Cl.CCN=C=NCCCN(C)C FPQQSJJWHUJYPU-UHFFFAOYSA-N 0.000 description 1
- PSSWASGEGXCINO-UHFFFAOYSA-N 3-aminopiperidin-4-ol Chemical class NC1CNCCC1O PSSWASGEGXCINO-UHFFFAOYSA-N 0.000 description 1
- BMYNFMYTOJXKLE-UHFFFAOYSA-N 3-azaniumyl-2-hydroxypropanoate Chemical compound NCC(O)C(O)=O BMYNFMYTOJXKLE-UHFFFAOYSA-N 0.000 description 1
- ZFXJNYKHLITMJY-UHFFFAOYSA-N 3-bromo-2-fluoro-6-methylpyridine Chemical compound CC1=CC=C(Br)C(F)=N1 ZFXJNYKHLITMJY-UHFFFAOYSA-N 0.000 description 1
- IRIHSZDBTACXCT-UHFFFAOYSA-N 3-fluoro-2-methylpyridine Chemical compound CC1=NC=CC=C1F IRIHSZDBTACXCT-UHFFFAOYSA-N 0.000 description 1
- WZMOEPZZTTWDIA-UHFFFAOYSA-N 3-fluoro-4-methylpyridine Chemical compound CC1=CC=NC=C1F WZMOEPZZTTWDIA-UHFFFAOYSA-N 0.000 description 1
- ACCVPUIPSOKHJO-UHFFFAOYSA-N 4-(4-phenoxyphenyl)piperidine;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.C1CNCCC1C(C=C1)=CC=C1OC1=CC=CC=C1 ACCVPUIPSOKHJO-UHFFFAOYSA-N 0.000 description 1
- BAJQRLZAPXASRD-UHFFFAOYSA-N 4-Nitrobiphenyl Chemical group C1=CC([N+](=O)[O-])=CC=C1C1=CC=CC=C1 BAJQRLZAPXASRD-UHFFFAOYSA-N 0.000 description 1
- SXEMQFDLWOWACF-UHFFFAOYSA-N 4-[4-(4-fluorophenoxy)phenyl]piperidine Chemical compound C1=CC(F)=CC=C1OC1=CC=C(C2CCNCC2)C=C1 SXEMQFDLWOWACF-UHFFFAOYSA-N 0.000 description 1
- ZRWNRAJCPNLYAK-UHFFFAOYSA-N 4-bromobenzamide Chemical compound NC(=O)C1=CC=C(Br)C=C1 ZRWNRAJCPNLYAK-UHFFFAOYSA-N 0.000 description 1
- UYIMBYKIIMYFPS-UHFFFAOYSA-N 4-bromobenzohydrazide Chemical compound NNC(=O)C1=CC=C(Br)C=C1 UYIMBYKIIMYFPS-UHFFFAOYSA-N 0.000 description 1
- PKEAPXXPQSPHFU-UHFFFAOYSA-N 4-chloro-2,5-dimethylpyridine Chemical compound CC1=CC(Cl)=C(C)C=N1 PKEAPXXPQSPHFU-UHFFFAOYSA-N 0.000 description 1
- 229960000549 4-dimethylaminophenol Drugs 0.000 description 1
- TYMLOMAKGOJONV-UHFFFAOYSA-N 4-nitroaniline Chemical compound NC1=CC=C([N+]([O-])=O)C=C1 TYMLOMAKGOJONV-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- AFXQXKTVNKCKCE-UHFFFAOYSA-N 5-(2-fluoroethyl)-1H-pyrazole Chemical compound FCCC1=CC=NN1 AFXQXKTVNKCKCE-UHFFFAOYSA-N 0.000 description 1
- NZBVVPHFPDZGMW-UHFFFAOYSA-N 5-bromo-2-(3-chlorophenoxy)pyridine Chemical compound ClC1=CC=CC(OC=2N=CC(Br)=CC=2)=C1 NZBVVPHFPDZGMW-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- QGZKDVFQNNGYKY-UHFFFAOYSA-O Ammonium Chemical compound [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 1
- VHUUQVKOLVNVRT-UHFFFAOYSA-N Ammonium hydroxide Chemical compound [NH4+].[OH-] VHUUQVKOLVNVRT-UHFFFAOYSA-N 0.000 description 1
- 102000001381 Arachidonate 5-Lipoxygenase Human genes 0.000 description 1
- 108010093579 Arachidonate 5-lipoxygenase Proteins 0.000 description 1
- 239000004475 Arginine Substances 0.000 description 1
- 241000283690 Bos taurus Species 0.000 description 1
- UEEGOWARQSLXOM-UHFFFAOYSA-N BrC1=CC=C(C=C1)C1=CC=NN1CCF Chemical compound BrC1=CC=C(C=C1)C1=CC=NN1CCF UEEGOWARQSLXOM-UHFFFAOYSA-N 0.000 description 1
- RGAZOZIWKKSUOD-UHFFFAOYSA-N BrC1CC2=NC3=CC=CC=C3C=C2CC1 Chemical compound BrC1CC2=NC3=CC=CC=C3C=C2CC1 RGAZOZIWKKSUOD-UHFFFAOYSA-N 0.000 description 1
- 208000014644 Brain disease Diseases 0.000 description 1
- 238000006443 Buchwald-Hartwig cross coupling reaction Methods 0.000 description 1
- CNMQQSGBYQPUCO-UHFFFAOYSA-N C(C)(C)C1=C(C(=CC(=C1)C(C)C)C(C)C)C1=CC=CC=C1.C(CCC)P Chemical group C(C)(C)C1=C(C(=CC(=C1)C(C)C)C(C)C)C1=CC=CC=C1.C(CCC)P CNMQQSGBYQPUCO-UHFFFAOYSA-N 0.000 description 1
- UUBFAOJZJHSNMH-UHFFFAOYSA-N CC(C)(C)OC(N(C1)C=CCCC1C(C=N1)=CC=C1OC(C=CC=C1)=C1Cl)=O Chemical compound CC(C)(C)OC(N(C1)C=CCCC1C(C=N1)=CC=C1OC(C=CC=C1)=C1Cl)=O UUBFAOJZJHSNMH-UHFFFAOYSA-N 0.000 description 1
- CKVAIEXOEDACQW-UHFFFAOYSA-N CC1=CC=NCN1F Chemical compound CC1=CC=NCN1F CKVAIEXOEDACQW-UHFFFAOYSA-N 0.000 description 1
- GFETXEHMVSYAQE-UHFFFAOYSA-N CCCCOC(N(C1)C=CCCC1Br)=O Chemical group CCCCOC(N(C1)C=CCCC1Br)=O GFETXEHMVSYAQE-UHFFFAOYSA-N 0.000 description 1
- NRSKLCCINAQQQL-UHFFFAOYSA-N CCN(CC)S.F.F.F Chemical group CCN(CC)S.F.F.F NRSKLCCINAQQQL-UHFFFAOYSA-N 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- DCERHCFNWRGHLK-UHFFFAOYSA-N C[Si](C)C Chemical compound C[Si](C)C DCERHCFNWRGHLK-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 241000282472 Canis lupus familiaris Species 0.000 description 1
- UGFAIRIUMAVXCW-UHFFFAOYSA-N Carbon monoxide Chemical compound [O+]#[C-] UGFAIRIUMAVXCW-UHFFFAOYSA-N 0.000 description 1
- OKTJSMMVPCPJKN-NJFSPNSNSA-N Carbon-14 Chemical compound [14C] OKTJSMMVPCPJKN-NJFSPNSNSA-N 0.000 description 1
- 238000006964 Chan-Lam coupling reaction Methods 0.000 description 1
- WBYWAXJHAXSJNI-SREVYHEPSA-N Cinnamic acid Chemical compound OC(=O)\C=C/C1=CC=CC=C1 WBYWAXJHAXSJNI-SREVYHEPSA-N 0.000 description 1
- MPONAPFARZGDTH-UHFFFAOYSA-N Cl.OS(O)=O Chemical compound Cl.OS(O)=O MPONAPFARZGDTH-UHFFFAOYSA-N 0.000 description 1
- 229910021591 Copper(I) chloride Inorganic materials 0.000 description 1
- YZCKVEUIGOORGS-OUBTZVSYSA-N Deuterium Chemical compound [2H] YZCKVEUIGOORGS-OUBTZVSYSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- 206010013654 Drug abuse Diseases 0.000 description 1
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 1
- 241000283086 Equidae Species 0.000 description 1
- OTMSDBZUPAUEDD-UHFFFAOYSA-N Ethane Chemical compound CC OTMSDBZUPAUEDD-UHFFFAOYSA-N 0.000 description 1
- 241000282326 Felis catus Species 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000007821 HATU Substances 0.000 description 1
- 208000004547 Hallucinations Diseases 0.000 description 1
- 101000929834 Homo sapiens Monoacylglycerol lipase ABHD6 Proteins 0.000 description 1
- 102000004157 Hydrolases Human genes 0.000 description 1
- 108090000604 Hydrolases Proteins 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 108090001005 Interleukin-6 Proteins 0.000 description 1
- PWKSKIMOESPYIA-BYPYZUCNSA-N L-N-acetyl-Cysteine Chemical compound CC(=O)N[C@@H](CS)C(O)=O PWKSKIMOESPYIA-BYPYZUCNSA-N 0.000 description 1
- ODKSFYDXXFIFQN-BYPYZUCNSA-P L-argininium(2+) Chemical compound NC(=[NH2+])NCCC[C@H]([NH3+])C(O)=O ODKSFYDXXFIFQN-BYPYZUCNSA-P 0.000 description 1
- KDXKERNSBIXSRK-YFKPBYRVSA-N L-lysine Chemical compound NCCCC[C@H](N)C(O)=O KDXKERNSBIXSRK-YFKPBYRVSA-N 0.000 description 1
- 229910010082 LiAlH Inorganic materials 0.000 description 1
- KDXKERNSBIXSRK-UHFFFAOYSA-N Lysine Natural products NCCCCC(N)C(O)=O KDXKERNSBIXSRK-UHFFFAOYSA-N 0.000 description 1
- 239000004472 Lysine Substances 0.000 description 1
- 229920000168 Microcrystalline cellulose Polymers 0.000 description 1
- 102100035912 Monoacylglycerol lipase ABHD6 Human genes 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 102000006386 Myelin Proteins Human genes 0.000 description 1
- 108010083674 Myelin Proteins Proteins 0.000 description 1
- HTLZVHNRZJPSMI-UHFFFAOYSA-N N-ethylpiperidine Chemical compound CCN1CCCCC1 HTLZVHNRZJPSMI-UHFFFAOYSA-N 0.000 description 1
- 101100030361 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pph-3 gene Proteins 0.000 description 1
- GRYLNZFGIOXLOG-UHFFFAOYSA-N Nitric acid Chemical compound O[N+]([O-])=O GRYLNZFGIOXLOG-UHFFFAOYSA-N 0.000 description 1
- 208000001294 Nociceptive Pain Diseases 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 108010064785 Phospholipases Proteins 0.000 description 1
- 102000015439 Phospholipases Human genes 0.000 description 1
- OAICVXFJPJFONN-UHFFFAOYSA-N Phosphorus Chemical compound [P] OAICVXFJPJFONN-UHFFFAOYSA-N 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 206010053395 Progressive multiple sclerosis Diseases 0.000 description 1
- 208000028017 Psychotic disease Diseases 0.000 description 1
- IWYDHOAUDWTVEP-UHFFFAOYSA-N R-2-phenyl-2-hydroxyacetic acid Natural products OC(=O)C(O)C1=CC=CC=C1 IWYDHOAUDWTVEP-UHFFFAOYSA-N 0.000 description 1
- VMHLLURERBWHNL-UHFFFAOYSA-M Sodium acetate Chemical compound [Na+].CC([O-])=O VMHLLURERBWHNL-UHFFFAOYSA-M 0.000 description 1
- UIIMBOGNXHQVGW-DEQYMQKBSA-M Sodium bicarbonate-14C Chemical compound [Na+].O[14C]([O-])=O UIIMBOGNXHQVGW-DEQYMQKBSA-M 0.000 description 1
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 1
- 108091027076 Spiegelmer Proteins 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- PJANXHGTPQOBST-VAWYXSNFSA-N Stilbene Natural products C=1C=CC=CC=1/C=C/C1=CC=CC=C1 PJANXHGTPQOBST-VAWYXSNFSA-N 0.000 description 1
- 238000006619 Stille reaction Methods 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 1
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 1
- 229930006000 Sucrose Natural products 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- 238000006161 Suzuki-Miyaura coupling reaction Methods 0.000 description 1
- FEWJPZIEWOKRBE-UHFFFAOYSA-N Tartaric acid Natural products [H+].[H+].[O-]C(=O)C(O)C(O)C([O-])=O FEWJPZIEWOKRBE-UHFFFAOYSA-N 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- 241000009298 Trigla lyra Species 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- YZCKVEUIGOORGS-NJFSPNSNSA-N Tritium Chemical compound [3H] YZCKVEUIGOORGS-NJFSPNSNSA-N 0.000 description 1
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 1
- 102100040247 Tumor necrosis factor Human genes 0.000 description 1
- 206010054094 Tumour necrosis Diseases 0.000 description 1
- MUCRYNWJQNHDJH-OADIDDRXSA-N Ursonic acid Chemical compound C1CC(=O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C(O)=O)CC[C@@H](C)[C@H](C)[C@H]5C4=CC[C@@H]3[C@]21C MUCRYNWJQNHDJH-OADIDDRXSA-N 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- WJEIYVAPNMUNIU-UHFFFAOYSA-N [Na].OC(O)=O Chemical compound [Na].OC(O)=O WJEIYVAPNMUNIU-UHFFFAOYSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000001133 acceleration Effects 0.000 description 1
- 229960004308 acetylcysteine Drugs 0.000 description 1
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 208000038016 acute inflammation Diseases 0.000 description 1
- 230000006022 acute inflammation Effects 0.000 description 1
- 150000001263 acyl chlorides Chemical class 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 239000003463 adsorbent Substances 0.000 description 1
- 150000001335 aliphatic alkanes Chemical class 0.000 description 1
- 125000004390 alkyl sulfonyl group Chemical group 0.000 description 1
- 239000002168 alkylating agent Substances 0.000 description 1
- 229940100198 alkylating agent Drugs 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 229910000147 aluminium phosphate Inorganic materials 0.000 description 1
- 125000006242 amine protecting group Chemical group 0.000 description 1
- 125000004202 aminomethyl group Chemical group [H]N([H])C([H])([H])* 0.000 description 1
- 229910021529 ammonia Inorganic materials 0.000 description 1
- 235000019270 ammonium chloride Nutrition 0.000 description 1
- 235000011114 ammonium hydroxide Nutrition 0.000 description 1
- NEHMKBQYUWJMIP-UHFFFAOYSA-N anhydrous methyl chloride Natural products ClC NEHMKBQYUWJMIP-UHFFFAOYSA-N 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 230000003474 anti-emetic effect Effects 0.000 description 1
- 229940124599 anti-inflammatory drug Drugs 0.000 description 1
- 230000002001 anti-metastasis Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 230000000259 anti-tumor effect Effects 0.000 description 1
- 239000002111 antiemetic agent Substances 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- 239000008346 aqueous phase Substances 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- ODKSFYDXXFIFQN-UHFFFAOYSA-N arginine Natural products OC(=O)C(N)CCCNC(N)=N ODKSFYDXXFIFQN-UHFFFAOYSA-N 0.000 description 1
- 150000001499 aryl bromides Chemical class 0.000 description 1
- 239000012298 atmosphere Substances 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 150000008359 benzonitriles Chemical class 0.000 description 1
- 239000012964 benzotriazole Substances 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- XGIUDIMNNMKGDE-UHFFFAOYSA-N bis(trimethylsilyl)azanide Chemical compound C[Si](C)(C)[N-][Si](C)(C)C XGIUDIMNNMKGDE-UHFFFAOYSA-N 0.000 description 1
- SQMFULTZZQBFBM-UHFFFAOYSA-N bis(trimethylsilyl)silyl-trimethylsilane Chemical compound C[Si](C)(C)[SiH]([Si](C)(C)C)[Si](C)(C)C SQMFULTZZQBFBM-UHFFFAOYSA-N 0.000 description 1
- 210000004204 blood vessel Anatomy 0.000 description 1
- 125000005620 boronic acid group Chemical group 0.000 description 1
- 210000004958 brain cell Anatomy 0.000 description 1
- 230000006931 brain damage Effects 0.000 description 1
- 231100000874 brain damage Toxicity 0.000 description 1
- 208000025698 brain inflammatory disease Diseases 0.000 description 1
- 208000029028 brain injury Diseases 0.000 description 1
- 230000005587 bubbling Effects 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 1
- 125000004106 butoxy group Chemical group [*]OC([H])([H])C([H])([H])C(C([H])([H])[H])([H])[H] 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 229930003827 cannabinoid Natural products 0.000 description 1
- 239000003557 cannabinoid Substances 0.000 description 1
- 229940065144 cannabinoids Drugs 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 229910002091 carbon monoxide Inorganic materials 0.000 description 1
- QNEFNFIKZWUAEQ-UHFFFAOYSA-N carbonic acid;potassium Chemical compound [K].OC(O)=O QNEFNFIKZWUAEQ-UHFFFAOYSA-N 0.000 description 1
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 1
- 210000001175 cerebrospinal fluid Anatomy 0.000 description 1
- 239000003610 charcoal Substances 0.000 description 1
- 238000004296 chiral HPLC Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 208000037976 chronic inflammation Diseases 0.000 description 1
- 230000006020 chronic inflammation Effects 0.000 description 1
- 230000037326 chronic stress Effects 0.000 description 1
- 229930016911 cinnamic acid Natural products 0.000 description 1
- 235000013985 cinnamic acid Nutrition 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000003776 cleavage reaction Methods 0.000 description 1
- 206010009887 colitis Diseases 0.000 description 1
- 239000003086 colorant Substances 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000010276 construction Methods 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- OXBLHERUFWYNTN-UHFFFAOYSA-M copper(I) chloride Chemical compound [Cu]Cl OXBLHERUFWYNTN-UHFFFAOYSA-M 0.000 description 1
- ORTQZVOHEJQUHG-UHFFFAOYSA-L copper(II) chloride Chemical compound Cl[Cu]Cl ORTQZVOHEJQUHG-UHFFFAOYSA-L 0.000 description 1
- XTVVROIMIGLXTD-UHFFFAOYSA-N copper(II) nitrate trihydrate Substances [Cu+2].[O-][N+]([O-])=O.[O-][N+]([O-])=O XTVVROIMIGLXTD-UHFFFAOYSA-N 0.000 description 1
- OPQARKPSCNTWTJ-UHFFFAOYSA-L copper(ii) acetate Chemical compound [Cu+2].CC([O-])=O.CC([O-])=O OPQARKPSCNTWTJ-UHFFFAOYSA-L 0.000 description 1
- GBRBMTNGQBKBQE-UHFFFAOYSA-L copper;diiodide Chemical compound I[Cu]I GBRBMTNGQBKBQE-UHFFFAOYSA-L 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 239000013058 crude material Substances 0.000 description 1
- 125000004122 cyclic group Chemical group 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- NXQGGXCHGDYOHB-UHFFFAOYSA-L cyclopenta-1,4-dien-1-yl(diphenyl)phosphane;dichloropalladium;iron(2+) Chemical compound [Fe+2].Cl[Pd]Cl.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1.[CH-]1C=CC(P(C=2C=CC=CC=2)C=2C=CC=CC=2)=C1 NXQGGXCHGDYOHB-UHFFFAOYSA-L 0.000 description 1
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 230000002950 deficient Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 229910052805 deuterium Inorganic materials 0.000 description 1
- BSHICDXRSZQYBP-UHFFFAOYSA-N dichloromethane;palladium(2+) Chemical compound [Pd+2].ClCCl BSHICDXRSZQYBP-UHFFFAOYSA-N 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 230000004069 differentiation Effects 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- 125000002147 dimethylamino group Chemical group [H]C([H])([H])N(*)C([H])([H])[H] 0.000 description 1
- 229960002986 dinoprostone Drugs 0.000 description 1
- USIUVYZYUHIAEV-UHFFFAOYSA-N diphenyl ether Natural products C=1C=CC=CC=1OC1=CC=CC=C1 USIUVYZYUHIAEV-UHFFFAOYSA-N 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- GVLGDGJKSOERIG-UHFFFAOYSA-N disilanyl(trimethyl)silane Chemical compound C[Si](C)(C)[SiH2][SiH3] GVLGDGJKSOERIG-UHFFFAOYSA-N 0.000 description 1
- 238000009826 distribution Methods 0.000 description 1
- 238000002651 drug therapy Methods 0.000 description 1
- 238000000132 electrospray ionisation Methods 0.000 description 1
- 230000002996 emotional effect Effects 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 239000000839 emulsion Substances 0.000 description 1
- 206010014599 encephalitis Diseases 0.000 description 1
- 239000006274 endogenous ligand Substances 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 210000002919 epithelial cell Anatomy 0.000 description 1
- 210000005081 epithelial layer Anatomy 0.000 description 1
- CCIVGXIOQKPBKL-UHFFFAOYSA-M ethanesulfonate Chemical compound CCS([O-])(=O)=O CCIVGXIOQKPBKL-UHFFFAOYSA-M 0.000 description 1
- FAMRKDQNMBBFBR-UHFFFAOYSA-N ethyl n-ethoxycarbonyliminocarbamate Chemical compound CCOC(=O)N=NC(=O)OCC FAMRKDQNMBBFBR-UHFFFAOYSA-N 0.000 description 1
- 231100000318 excitotoxic Toxicity 0.000 description 1
- 230000003492 excitotoxic effect Effects 0.000 description 1
- 239000002360 explosive Substances 0.000 description 1
- 230000004136 fatty acid synthesis Effects 0.000 description 1
- 239000012467 final product Substances 0.000 description 1
- 239000000796 flavoring agent Substances 0.000 description 1
- 125000003709 fluoroalkyl group Chemical group 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 235000013373 food additive Nutrition 0.000 description 1
- 239000002778 food additive Substances 0.000 description 1
- 235000013355 food flavoring agent Nutrition 0.000 description 1
- 235000003599 food sweetener Nutrition 0.000 description 1
- 239000012458 free base Substances 0.000 description 1
- 235000021588 free fatty acids Nutrition 0.000 description 1
- 239000001530 fumaric acid Substances 0.000 description 1
- 239000007789 gas Substances 0.000 description 1
- 230000014509 gene expression Effects 0.000 description 1
- 208000005017 glioblastoma Diseases 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 238000004128 high performance liquid chromatography Methods 0.000 description 1
- 150000002429 hydrazines Chemical class 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- FUKUFMFMCZIRNT-UHFFFAOYSA-N hydron;methanol;chloride Chemical compound Cl.OC FUKUFMFMCZIRNT-UHFFFAOYSA-N 0.000 description 1
- NPZTUJOABDZTLV-UHFFFAOYSA-N hydroxybenzotriazole Substances O=C1C=CC=C2NNN=C12 NPZTUJOABDZTLV-UHFFFAOYSA-N 0.000 description 1
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 1
- 125000002962 imidazol-1-yl group Chemical group [*]N1C([H])=NC([H])=C1[H] 0.000 description 1
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 1
- 125000002140 imidazol-4-yl group Chemical group [H]N1C([H])=NC([*])=C1[H] 0.000 description 1
- 125000000336 imidazol-5-yl group Chemical group [H]N1C([H])=NC([H])=C1[*] 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 125000000593 indol-1-yl group Chemical group [H]C1=C([H])C([H])=C2N([*])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000002249 indol-2-yl group Chemical group [H]C1=C([H])C([H])=C2N([H])C([*])=C([H])C2=C1[H] 0.000 description 1
- 125000000814 indol-3-yl group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C([*])C2=C1[H] 0.000 description 1
- 125000004531 indol-5-yl group Chemical group [H]N1C([H])=C([H])C2=C([H])C(*)=C([H])C([H])=C12 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000002757 inflammatory effect Effects 0.000 description 1
- 208000014674 injury Diseases 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 208000028774 intestinal disease Diseases 0.000 description 1
- 230000003870 intestinal permeability Effects 0.000 description 1
- 229960004903 invert sugar Drugs 0.000 description 1
- 239000003456 ion exchange resin Substances 0.000 description 1
- 229920003303 ion-exchange polymer Polymers 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-N isopropylamine Chemical compound CC(C)N JJWLVOIRVHMVIS-UHFFFAOYSA-N 0.000 description 1
- 238000004895 liquid chromatography mass spectrometry Methods 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 159000000003 magnesium salts Chemical class 0.000 description 1
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- 238000009115 maintenance therapy Methods 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 239000011976 maleic acid Substances 0.000 description 1
- 229960002510 mandelic acid Drugs 0.000 description 1
- 230000000873 masking effect Effects 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 210000004379 membrane Anatomy 0.000 description 1
- 239000012528 membrane Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 125000000956 methoxy group Chemical group [H]C([H])([H])O* 0.000 description 1
- 229940050176 methyl chloride Drugs 0.000 description 1
- WBYWAXJHAXSJNI-UHFFFAOYSA-N methyl p-hydroxycinnamate Natural products OC(=O)C=CC1=CC=CC=C1 WBYWAXJHAXSJNI-UHFFFAOYSA-N 0.000 description 1
- KTMKRRPZPWUYKK-UHFFFAOYSA-N methylboronic acid Chemical compound CB(O)O KTMKRRPZPWUYKK-UHFFFAOYSA-N 0.000 description 1
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 1
- 235000019813 microcrystalline cellulose Nutrition 0.000 description 1
- 239000008108 microcrystalline cellulose Substances 0.000 description 1
- 229940016286 microcrystalline cellulose Drugs 0.000 description 1
- 230000002025 microglial effect Effects 0.000 description 1
- 235000010755 mineral Nutrition 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 150000007522 mineralic acids Chemical class 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 210000005012 myelin Anatomy 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000007922 nasal spray Substances 0.000 description 1
- CRSOQBOWXPBRES-UHFFFAOYSA-N neopentylidene Natural products CC(C)(C)C CRSOQBOWXPBRES-UHFFFAOYSA-N 0.000 description 1
- 230000000626 neurodegenerative effect Effects 0.000 description 1
- 230000016273 neuron death Effects 0.000 description 1
- 230000004112 neuroprotection Effects 0.000 description 1
- 230000000324 neuroprotective effect Effects 0.000 description 1
- 239000002581 neurotoxin Substances 0.000 description 1
- 231100000618 neurotoxin Toxicity 0.000 description 1
- 229910017604 nitric acid Inorganic materials 0.000 description 1
- 150000002825 nitriles Chemical group 0.000 description 1
- 231100000989 no adverse effect Toxicity 0.000 description 1
- 238000010534 nucleophilic substitution reaction Methods 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 235000005985 organic acids Nutrition 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 230000003204 osmotic effect Effects 0.000 description 1
- 235000006408 oxalic acid Nutrition 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 230000004783 oxidative metabolism Effects 0.000 description 1
- 125000004430 oxygen atom Chemical group O* 0.000 description 1
- 150000002927 oxygen compounds Chemical class 0.000 description 1
- NXJCBFBQEVOTOW-UHFFFAOYSA-L palladium(2+);dihydroxide Chemical compound O[Pd]O NXJCBFBQEVOTOW-UHFFFAOYSA-L 0.000 description 1
- FJKROLUGYXJWQN-UHFFFAOYSA-N papa-hydroxy-benzoic acid Natural products OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 230000007170 pathology Effects 0.000 description 1
- 230000037361 pathway Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 210000000578 peripheral nerve Anatomy 0.000 description 1
- 230000002085 persistent effect Effects 0.000 description 1
- 239000000575 pesticide Substances 0.000 description 1
- 239000002831 pharmacologic agent Substances 0.000 description 1
- OXDLBBKNAAFZNI-UHFFFAOYSA-N phenol;2,2,2-trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F.OC1=CC=CC=C1 OXDLBBKNAAFZNI-UHFFFAOYSA-N 0.000 description 1
- 239000010452 phosphate Substances 0.000 description 1
- 150000003904 phospholipids Chemical class 0.000 description 1
- 229910052698 phosphorus Inorganic materials 0.000 description 1
- 239000011574 phosphorus Substances 0.000 description 1
- 230000035790 physiological processes and functions Effects 0.000 description 1
- 210000004180 plasmocyte Anatomy 0.000 description 1
- 231100000614 poison Toxicity 0.000 description 1
- 229920000728 polyester Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 238000002600 positron emission tomography Methods 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 229910000160 potassium phosphate Inorganic materials 0.000 description 1
- 235000011009 potassium phosphates Nutrition 0.000 description 1
- LPNYRYFBWFDTMA-UHFFFAOYSA-N potassium tert-butoxide Chemical compound [K+].CC(C)(C)[O-] LPNYRYFBWFDTMA-UHFFFAOYSA-N 0.000 description 1
- 239000002244 precipitate Substances 0.000 description 1
- 238000012746 preparative thin layer chromatography Methods 0.000 description 1
- 239000003755 preservative agent Substances 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 230000000750 progressive effect Effects 0.000 description 1
- VVWRJUBEIPHGQF-MDZDMXLPSA-N propan-2-yl (ne)-n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)\N=N\C(=O)OC(C)C VVWRJUBEIPHGQF-MDZDMXLPSA-N 0.000 description 1
- VVWRJUBEIPHGQF-UHFFFAOYSA-N propan-2-yl n-propan-2-yloxycarbonyliminocarbamate Chemical compound CC(C)OC(=O)N=NC(=O)OC(C)C VVWRJUBEIPHGQF-UHFFFAOYSA-N 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- XEYBRNLFEZDVAW-UHFFFAOYSA-N prostaglandin E2 Natural products CCCCCC(O)C=CC1C(O)CC(=O)C1CC=CCCCC(O)=O XEYBRNLFEZDVAW-UHFFFAOYSA-N 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 125000004497 pyrazol-5-yl group Chemical class N1N=CC=C1* 0.000 description 1
- ZDYVRSLAEXCVBX-UHFFFAOYSA-N pyridinium p-toluenesulfonate Chemical compound C1=CC=[NH+]C=C1.CC1=CC=C(S([O-])(=O)=O)C=C1 ZDYVRSLAEXCVBX-UHFFFAOYSA-N 0.000 description 1
- 229940107700 pyruvic acid Drugs 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 102000005962 receptors Human genes 0.000 description 1
- 108020003175 receptors Proteins 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 238000002271 resection Methods 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229960004889 salicylic acid Drugs 0.000 description 1
- 229930195734 saturated hydrocarbon Natural products 0.000 description 1
- 230000007017 scission Effects 0.000 description 1
- 150000003335 secondary amines Chemical class 0.000 description 1
- 230000035807 sensation Effects 0.000 description 1
- 210000000329 smooth muscle myocyte Anatomy 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 239000001632 sodium acetate Substances 0.000 description 1
- 235000017281 sodium acetate Nutrition 0.000 description 1
- WRIKHQLVHPKCJU-UHFFFAOYSA-N sodium bis(trimethylsilyl)amide Chemical compound C[Si](C)(C)N([Na])[Si](C)(C)C WRIKHQLVHPKCJU-UHFFFAOYSA-N 0.000 description 1
- 239000012279 sodium borohydride Substances 0.000 description 1
- 229910000033 sodium borohydride Inorganic materials 0.000 description 1
- MNWBNISUBARLIT-UHFFFAOYSA-N sodium cyanide Chemical compound [Na+].N#[C-] MNWBNISUBARLIT-UHFFFAOYSA-N 0.000 description 1
- 235000010288 sodium nitrite Nutrition 0.000 description 1
- KKCBUQHMOMHUOY-UHFFFAOYSA-N sodium oxide Chemical compound [O-2].[Na+].[Na+] KKCBUQHMOMHUOY-UHFFFAOYSA-N 0.000 description 1
- 229910001948 sodium oxide Inorganic materials 0.000 description 1
- AKHNMLFCWUSKQB-UHFFFAOYSA-L sodium thiosulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=S AKHNMLFCWUSKQB-UHFFFAOYSA-L 0.000 description 1
- 235000019345 sodium thiosulphate Nutrition 0.000 description 1
- 239000012321 sodium triacetoxyborohydride Substances 0.000 description 1
- 230000003238 somatosensory effect Effects 0.000 description 1
- VNFWTIYUKDMAOP-UHFFFAOYSA-N sphos Chemical compound COC1=CC=CC(OC)=C1C1=CC=CC=C1P(C1CCCCC1)C1CCCCC1 VNFWTIYUKDMAOP-UHFFFAOYSA-N 0.000 description 1
- 210000000278 spinal cord Anatomy 0.000 description 1
- 230000002269 spontaneous effect Effects 0.000 description 1
- 239000003381 stabilizer Substances 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 235000021286 stilbenes Nutrition 0.000 description 1
- 238000005728 strengthening Methods 0.000 description 1
- 208000011117 substance-related disease Diseases 0.000 description 1
- 238000006467 substitution reaction Methods 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 239000005720 sucrose Substances 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- 239000003765 sweetening agent Substances 0.000 description 1
- 239000006188 syrup Substances 0.000 description 1
- 235000020357 syrup Nutrition 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 239000011975 tartaric acid Substances 0.000 description 1
- 235000002906 tartaric acid Nutrition 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 1
- 125000004496 thiazol-5-yl group Chemical group S1C=NC=C1* 0.000 description 1
- 230000036962 time dependent Effects 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 239000003440 toxic substance Substances 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 238000000844 transformation Methods 0.000 description 1
- 230000014616 translation Effects 0.000 description 1
- 238000002054 transplantation Methods 0.000 description 1
- 238000011269 treatment regimen Methods 0.000 description 1
- 150000003852 triazoles Chemical class 0.000 description 1
- PIILXFBHQILWPS-UHFFFAOYSA-N tributyltin Chemical group CCCC[Sn](CCCC)CCCC PIILXFBHQILWPS-UHFFFAOYSA-N 0.000 description 1
- 125000004205 trifluoroethyl group Chemical group [H]C([H])(*)C(F)(F)F 0.000 description 1
- 125000000876 trifluoromethoxy group Chemical group FC(F)(F)O* 0.000 description 1
- 125000002023 trifluoromethyl group Chemical group FC(F)(F)* 0.000 description 1
- SEDZOYHHAIAQIW-UHFFFAOYSA-N trimethylsilyl azide Chemical compound C[Si](C)(C)N=[N+]=[N-] SEDZOYHHAIAQIW-UHFFFAOYSA-N 0.000 description 1
- 229910000404 tripotassium phosphate Inorganic materials 0.000 description 1
- 235000019798 tripotassium phosphate Nutrition 0.000 description 1
- YFTHZRPMJXBUME-UHFFFAOYSA-N tripropylamine Chemical compound CCCN(CCC)CCC YFTHZRPMJXBUME-UHFFFAOYSA-N 0.000 description 1
- 229910052722 tritium Inorganic materials 0.000 description 1
- 230000005748 tumor development Effects 0.000 description 1
- 238000002604 ultrasonography Methods 0.000 description 1
- 230000004222 uncontrolled growth Effects 0.000 description 1
- 150000003672 ureas Chemical class 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains two hetero rings
- C07D498/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2009—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/535—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with at least one nitrogen and one oxygen as the ring hetero atoms, e.g. 1,2-oxazines
- A61K31/5375—1,4-Oxazines, e.g. morpholine
- A61K31/5383—1,4-Oxazines, e.g. morpholine ortho- or peri-condensed with heterocyclic ring systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2054—Cellulose; Cellulose derivatives, e.g. hydroxypropyl methylcellulose
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/20—Pills, tablets, discs, rods
- A61K9/2004—Excipients; Inactive ingredients
- A61K9/2022—Organic macromolecular compounds
- A61K9/205—Polysaccharides, e.g. alginate, gums; Cyclodextrin
- A61K9/2059—Starch, including chemically or physically modified derivatives; Amylose; Amylopectin; Dextrin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/485—Inorganic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4858—Organic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/48—Preparations in capsules, e.g. of gelatin, of chocolate
- A61K9/4841—Filling excipients; Inactive ingredients
- A61K9/4866—Organic macromolecular compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/18—Antipsychotics, i.e. neuroleptics; Drugs for mania or schizophrenia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D265/00—Heterocyclic compounds containing six-membered rings having one nitrogen atom and one oxygen atom as the only ring hetero atoms
- C07D265/28—1,4-Oxazines; Hydrogenated 1,4-oxazines
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D413/00—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D413/02—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings
- C07D413/12—Heterocyclic compounds containing two or more hetero rings, at least one ring having nitrogen and oxygen atoms as the only ring hetero atoms containing two hetero rings linked by a chain containing hetero atoms as chain links
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Epidemiology (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Inorganic Chemistry (AREA)
- Biomedical Technology (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Rheumatology (AREA)
- Psychiatry (AREA)
- Pain & Pain Management (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Description
本發明涉及可用於哺乳動物療法或預防法之有機化合物,特別是涉及用於下列的哺乳動物療法或預防法之單醯基甘油脂肪酶 (MAGL) 抑制劑:神經發炎、神經退化性疾病、疼痛、癌症、精神障礙、多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、發炎性腸病、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛。
內源性大麻素 (EC) 是藉由與大麻素受體 (CBR) CB1 和 CB2 交互作用發揮其生物學作用的傳訊脂質。它們調節多種生理過程,包括神經發炎、神經退化及組織再生(Iannotti, F.A. 等人,Progress in lipid research 2016, 62, 107-28)。在腦中,主要的內源性大麻素是 2-花生四烯酸甘油酯 (2-AG),其由二醯基甘油脂酶 (DAGL) 產生,並由單醯基甘油脂肪酶 MAGL 水解。MAGL 水解 85% 的 2-AG;其餘的 15% 被 ABHD6 和 ABDH12 水解(Nomura, D.K. 等人,Science 2011, 334, 809)。MAGL 在整個腦中且在大部分腦細胞類型,包括神經元、星狀細胞、寡樹突膠細胞及微膠細胞中表現(Chanda, P.K. 等人,Molecular pharmacology 2010, 78, 996;Viader, A. 等人,Cell reports 2015, 12, 798)。2-AG 水解會形成花生油酸 (AA),其為前列腺素 (PG) 及白三烯素 (LT) 前驅物。AA 之氧化代謝在發炎組織中提高。涉及發炎過程之花生油酸氧化存在兩個主要酶路徑,產生 PG 之環氧化酶及產生 LT 之 5-脂肪加氧酶。在發炎期間形成之各種環氧化酶產物中,PGE2 為最重要的一個。在發炎部位處,例如在罹患神經退化性病症之患者之腦脊髓液中已偵測到此等產物,且咸信導致發炎反應及疾病進展。不具有 MAGL 之小鼠 (Mgll-/-) 在神經系統中展現顯著降低的 2-AG 水解酶活性及提高的 2-AG 量,而其他含有花生四烯醯基之磷脂質及神經脂質物質(包括花生四烯乙醇胺 (AEA))以及其他游離脂肪酸不變。相反地,AA 及 AA 衍生之前列腺素及其他類花生酸,包括前列腺素 E2 (PGE2)、D2 (PGD2)、F2 (PGF2) 及凝血脂素 B2 (TXB2) 之含量明顯降低。磷脂酶 A2
(PLA2
) 酶已被視為 AA 之主要來源,但 cPLA2
缺失型小鼠在其腦中具有不變的 AA 含量,強化了腦中之 MAGL 用於 AA 生產及調節大腦發炎過程之關鍵作用。
神經發炎為腦疾病之常見病理性變化特徵,其包括但不限於神經退化性疾病(例如多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇及精神障礙,諸如焦慮及偏頭痛)。在腦中,類花生酸及前列腺素之生產控制神經發炎過程。促發炎劑脂多醣 (LPS) 產生大腦類花生酸之穩固的、時間依賴性增加,此在 Mgll-/- 小鼠中顯著鈍化。LPS 治療亦誘導促發炎細胞介素之普遍升高,包括介白素-1-a (IL-1-a)、IL-1b、IL-6、及腫瘤壞死因子-a (TNF-a),此在 Mgll-/- 小鼠是受制止的。
神經發炎之特徵在於中樞神經系統之先天性免疫細胞、即微膠細胞及星狀細胞之活化。據報導,抗發炎藥可壓制臨床前模型中之神經膠細胞之活化及包括阿滋海默症及多發性硬化症之疾病進展 (Lleo A., Cell Mol Life Sci. 2007, 64, 1403)。重要的是,MAGL 活性之基因及/或藥理學破壞亦阻斷腦中之微膠細胞之 LPS 誘發活化(Nomura, D.K. 等人,Science 2011, 334, 809)。
另外,MAGL 活性之基因及/或藥理學破壞在若干神經退化動物模型(包括但不限於阿滋海默症、帕金森病及多發性硬化症)中顯示為保護性的。例如,不可逆 MAGL 抑制劑已廣泛用於神經發炎及神經退化之臨床前模型(Long, J.Z. 等人,Nature chemical biology 2009, 5, 37)。此類抑制劑之全身性注射重現腦中之 Mgll-/- 小鼠表型,包括 LPS 誘發神經發炎之後的 2-AG 含量之提高、AA 含量及相關類花生酸製造之降低、以及細胞介素製造及微膠細胞活化之預防(Nomura, D.K. 等人,Science 2011, 334, 809)一起確證 MAGL 為可藥物治療的目標。
隨著 MAGL 活性之基因及/或藥理學破壞,腦中之 MAGL 天然受質 2-AG 之內源水平提高。據報導,2-AG 對疼痛具有有益的作用,例如對小鼠具有抗傷害作用(Ignatowska-Jankowska B. 等人,J. Pharmacol. Exp. Ther. 2015, 353, 424),對精神障礙,諸如慢性壓力模型中的抑鬱也具有抑制作用(Zhong P. 等人,Neuropsychopharmacology 2014, 39, 1763)。
此外,寡樹突膠細胞 (OL) 為中樞神經系統之髓鞘形成細胞,其前驅者 (OPC) 在其膜上表現大麻素受體 2 (CB2)。2-AG 為 CB1 及 CB2 受體之內源性配體。據報導,大麻素及 MAGL 藥理學抑制均減弱 OL 及 OPC 對興奮性毒化損害的脆弱性,且因此可為神經保護性的(Bernal-Chico, A. 等人,Glia 2015, 63, 163)。另外,MAGL 之藥理學抑制增加小鼠的腦中之髓鞘形成 OL 之數目,表明 MAGL 抑制可促進活體內髓鞘形成 OL 中之 OPC 分化(Alpar, A.等人,Nature communications 2014, 5, 4421)。在進展性多發性硬化症之小鼠模型中,MAGL 的抑制作用亦可促進髓鞘再生與功能恢復(Feliu A. 等人,Journal of Neuroscience 2017, 37 (35), 8385)。
此外,近年來,代謝在癌症研究中為非常重要的,尤其脂質代謝。研究人員相信,從頭脂肪酸合成在腫瘤發展方面扮演重要作用。多個研究說明,內源性大麻素具有抗腫瘤形成作用,包括抗增生、細胞凋亡誘導及抗轉移性效果。MAGL 作為脂質代謝及內源性大麻素系統兩者之重要分解酶,另外作為基因表現標誌的一部分,導致不同態樣之腫瘤形成,包括神經膠母細胞瘤(Qin, H. 等人,Cell Biochem. Biophys. 2014, 70, 33;Nomura DK 等人,Cell 2009, 140(1), 49-61;Nomura DK 等人,Chem. Biol. 2011, 18(7), 846-856;Jinlong Yin 等人,Nature Communications 2020, 11, 2978)。
內源性大麻素系統也參與許多胃腸道的生理和生理病理作用(Marquez, Suarez et al. 2009)。所有這些效果主要是經由大麻素受體 (CBR) CB1 和 CB2 所驅動。CB1 受體係廣泛存在於動物及健康人類之胃腸道中,尤其是腸神經系統 (ENS) 及上皮層以及腸壁內血管之平滑肌細胞中 (Wright, Rooney et al. 2005) 及(Duncan, Davison et al. 2005)。CB1 的活化產生止吐、抗腸蠕動、和抗發炎效果,並有助於調節疼痛(Perisetti, Rimu et al. 2020)。CB2 受體在免疫細胞(如漿細胞和巨噬細胞)、胃腸 (GI) 道固有層中表現(Wright, Rooney et al. 2005)、以及主要在與發炎性腸病 (IBD) 相關的人結腸組織的上皮細胞中表現。CB2 的活化藉由減少促發炎細胞介素發揮抗發炎效果。UC 患者結腸組織中 MAGL 表現升高,(Marquez, Suarez et al. 2009)且 IBD 患者血漿中 2-AG 量升高(Grill, Hogenauer et al. 2019)。幾項動物研究闡明,MAGL 抑制劑具有對症治療 IBD 的潛力。MAGL 抑制可防止 TNBS 誘導的小鼠結腸炎,並經由 CB1/CB2 MoA 降低局部和循環發炎標記(Marquez, Suarez et al. 2009)。此外,MAGL 抑制經由 CB1 驅動的 MoA 改善腸壁的完整性和腸通透性(Wang, Zhang et al. 2020)。
總之,壓制 MAGL 的作用及/或活化是用於治療或預防神經退化性疾病、疼痛、癌症、精神障礙、發炎性腸病、腹痛及與腸躁症候群相關的腹痛之有前景的新治療策略。此外,抑制 MAGL 的作用及/或活化是用於提供神經保護和髓鞘質再生之有前景的新治療策略。因此,對於新型 MAGL 抑制劑存在高度未滿足的醫學需求。
在一進一步方面中,本發明提供了一種製造如本文中所述的式 (I) 化合物或其藥學上可接受的鹽類之程序,其包含:
令 4a,5,6,7,8,8a-六氫-4H-吡啶幷[4,3-b][1,4]㗁𠯤-3-酮1
(其中,R1
及 R2
係如本文中定義)
與雜環狀胺2
(其中,A、B、L1
、X、m、n 及 R3
至 R7
係如本文中定義)
於鹼及脲形成試劑之存在下反應,
以形成所述式 (I) 化合物或其藥學上可接受之鹽類。
在一進一步方面中,本發明提供當根據本文所揭示之製程製造時的如本文中所揭示之式 (I) 化合物或其藥學上可接受之鹽類。
在一進一步方面中,本發明提供一種如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用以作為治療活性物質。
在一進一步方面中,本發明提供一種醫藥組成物,其係包含如本文中所揭示之式 (I) 化合物或其藥學上可接受之鹽類以及治療上惰性之載劑。
在一進一步方面中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於抑制哺乳動物單醯基甘油脂肪酶之方法。
在一進一步方面中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物之神經炎症、神經退化性疾病、疼痛、癌症及/或精神障礙。
在一進一步方面中,本發明提供一種如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於製備供治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛及/或與疼痛相關的痙攣的藥物。
定義
結合本發明之特定方面、具體實施方式或實施例描述之特徵、整體、特性、化合物、化學部分或基團應理解為適用於本文所描述之任何其他方面、具體實施方式或實施例,除非與之不相容。本說明書中所揭示之所有特徵(包括任何隨附申請專利範圍、摘要及圖式)及/或如此揭示之任何方法或程序之所有步驟可以任何組合形式組合,惟此類特徵及/或步驟中之至少一些相互排斥之組合除外。本發明不限於任何前述具體實施方式之細節。本發明擴展至本說明書(包括任何隨附申請專利範圍、摘要及圖式)中所揭示之特徵之任何新穎特徵或任何新穎組合或擴展至如此揭示之任何方法或程序之步驟的任何新穎步驟或任何新穎組合。
術語“烷基”係指代具有 1 至 12 個碳原子之單價或多價,例如單價或雙價直鏈或支鏈飽和烴基。在一些較佳具體實施方式中,烷基係含有 1 至 6 個碳原子(“C1-6-烷基”),例如 1、2、3、4、5 或 6 個碳原子。在其他具體實施方式中,烷基含有 1 至 3 個碳原子,例如 1、2 或 3 個碳原子。烷基的一些非限制實施例包括甲基、乙基、丙基、2-丙基(異丙基)、正丁基、異丁基、二級丁基、三級丁基、及 2,2-二甲基丙基。烷基之特佳但非限制性實施例係甲基及 2,2-二甲基丙基。
術語“烷氧基”是指經由氧原子接附至母分子部分之如先前所定義之烷基。除非另外說明,否則烷氧基係含有 1 至 12 個碳原子。在一些較佳具體實施方式中,烷氧基係含有 1 至 6 個碳原子(“C1-6-烷氧基”)。在其他具體實施方式中,烷氧基含有 1 至 4 個碳原子。又在其他具體實施方式中,烷氧基含有 1 至 3 個碳原子。烷氧基之一些非限制性實施例包括甲氧基、乙氧基、正丙氧基、異丙氧基、正丁氧基、異丁氧基及三級丁氧基。烷氧基的特別優選但非限制性的實施例是甲氧基。
術語“鹵素”或“鹵代”是指氟 (F)、氯 (Cl)、溴 (Br)、或碘 (I)。較佳的是,術語“鹵素”或“鹵代”是指氟 (F)、氯 (Cl) 或溴 (Br)。“鹵素”或“鹵代”之特別優選但非限制性的實施例是氟 (F) 和氯 (Cl)。
如本文中所用,術語“環烷基”係指代具有 3 至 10 個環碳原子之飽和或部分不飽和單環或雙環烴基(“C3-10-環烷基”)。在一些較佳具體實施方式中,環烷基為具有 3 至 8 個環碳原子之飽和單環烴基。“雙環之環烷基”係指代由具有兩個共有碳原子之兩個飽和碳環組成的環烷基部分,亦即,分離兩個環之橋或係單鍵或係一個或兩個環原子之鏈;亦指代螺環部分,亦即,兩個環係經由一個共有環原子連結。較佳的是,環烷基為具有 3 至 6 個環碳原子,例如具有 3、4、5 或 6 個碳原子之飽和單環烴基。環烷基之一些非限制性實施例包括環丙基、環丁基、環戊基、環己基和環庚基。環烷基的特別優選但非限制性的實施例是環丙基。
術語“芳基”是指具有總共 6 至 14 個環成員(“C6-C14-芳基”)、較佳 6 至 12 個環成員、且更佳 6 至 10 個環成員之單環、雙環、或三環碳環系統,且其中,該系統中之至少一個環是芳族的。芳基之一些非限制性實施例係包括苯基及 9H-茀基(例如,9H-茀-9-基)。芳基的特別優選但非限制性的實施例是苯基。
術語“雜芳基”是指具有總共 5 至 14 個環成員、較佳 5 至 12 個環成員、且更佳 5 至 10 個環成員之單價或多價、單環、雙環、較佳的是雙環環系統,其中,該系統中之至少一個環是芳族的,且該系統中之至少一個環含有一或多個雜原子。較佳地,“雜芳基”係指代包含 1、2、3 或 4 個獨立地選自 O、S 及 N 之雜原子的 5 至 10 員雜芳基。更佳地,“雜芳基”係指代包含 1 至 2 個獨立地選自 O、S 及 N 之雜原子的 5 至 10 員雜芳基。雜芳基之一些非限制性實施例係包括螺[環丙-1,3'-吲哚啉](例如,螺[環丙-1,3'-吲哚啉]-1'-基)、2-吡啶基、3-吡啶基、4-吡啶基、吲哚-1-基、1H-吲哚-2-基、1H-吲哚-3-基、1H-吲哚-4-基、1H-吲哚-5-基、1H-吲哚-6-基、1H-吲哚-7-基、1,2-苯幷㗁唑-3-基、1,2-苯幷㗁唑-4-基、1,2-苯幷㗁唑-5-基、1,2-苯幷㗁唑-6-基、1,2-苯幷㗁唑-7-基、1H-吲唑-3-基、1H-吲唑-4-基、1H-吲唑-5-基、1H-吲唑-6-基、1H-吲唑-7-基、吡唑-1-基、1H-吡唑-3-基、1H-吡唑-4-基、1H-吡唑-5-基、咪唑-1-基、1H-咪唑-2-基、1H-咪唑-4-基、1H-咪唑-5-基、㗁唑-2-基、㗁唑-4-基、㗁唑-5-基、1,2,4-㗁二唑-3-基、1,2,4-㗁二唑-3-基、噻唑-2-基、噻唑-4-基、噻唑-5-基、嗒𠯤-3-基及嗒𠯤-4-基。雜芳基之特佳但非限制性實施例係㗁二唑基、嗒𠯤基、吡啶基及噻唑基。
術語“羥基”是指 −OH 基團。
術語“氰基”是指 −CN(腈)基團。
術語“胺基”係指代 –NH2
基團。
術語“烷基磺醯基”係指代基團烷基-SO2
–。
術語“烷基甲醯基”係指代基團 H2
N-C(O)–。
術語“環烷基烷氧基”係指代烷氧基,其中,該烷氧基之氫原子中的至少一者業經藉由環烷基替代。較佳地,“環烷基烷氧基”係指代烷氧基,其中,該烷氧基之 1、2 或 3 個氫原子,最佳 1 個氫原子業經藉由環烷基替代。環烷基烷氧基之特佳但非限制性實施例係環丙基甲氧基。
術語“鹵烷基”所指的烷基,是其中,烷基的至少一個氫原子已被鹵素原子、較佳的是被氟替代。較佳的是,“鹵烷基”所指的烷基,是其中,烷基的 1、2 或 3 個氫原子已被鹵素原子替代、最佳的是被氟替代。鹵烷基之特佳但非限制性實施例係三氟甲基及三氟乙基。
術語“鹵烷氧基”所指的烷氧基,是其中,烷氧基的至少一個氫原子已被鹵素原子、較佳的是被氟替代。較佳的是,“鹵烷氧基”所指的烷氧基,是其中,烷氧基的 1、2 或 3 個氫原子已被鹵素原子、最佳的是被氟替代。鹵烷氧基的特別優選但非限制性的實施例是三氟甲氧基 (−OCF3
)。
術語“環烷基烷氧基”係指代烷氧基,其中,該烷氧基之氫原子中的至少一者業經藉由環烷基替代。較佳地,“環烷基烷氧基”係指代烷氧基,其中,該烷氧基之 1、2 或 3 個氫原子,最佳 1 個氫原子業經藉由環烷基替代。環烷基烷氧基之特佳但非限制性實施例係環丙基甲氧基。
術語“羥基烷基”係指代烷基,其中,該烷基之氫原子中的至少一者業經藉由羥基替代。較佳地,“羥基烷基”係指代烷基,其中,該烷基之 1、2 或 3 個氫原子,最佳 1 個氫原子業經藉由羥基替代。羥基烷基之特佳但非限制性實施例係羥甲基及羥乙基(例如,2-羥基乙基)。羥基烷基之特佳但非限制性實施例係羥甲基。
術語“胺基烷氧基”係指代烷氧基,其中,該烷氧基之氫原子中的至少一者業經藉由胺基替代。較佳地,“胺基烷氧基”係指代烷氧基,其中,該烷氧基之 1、2 或 3 個氫原子,最佳 1 個氫原子業經藉由胺基替代。胺基烷氧基之特佳但非限制性實施例係胺基甲氧基及胺基乙氧基(例如,2-胺基乙氧基)。
術語“藥學上可接受之鹽類”意指保有自由鹼或自由酸的生物有效性及特性,且並非在生物上或在其他方面有不利之處的鹽類。該鹽類是與諸如鹽酸、氫溴酸、硫酸、硝酸、磷酸及類似者、特別是鹽酸的無機酸形成,和諸如乙酸、丙酸、乙醇酸、丙酮酸、草酸、馬來酸、丙二酸、琥珀酸、延胡索酸、酒石酸、檸檬酸、苄酸、肉桂酸、苦杏仁酸、甲磺酸、乙磺酸、對甲苯磺酸、水楊酸、N-乙醯半胱胺酸及類似者之有機酸形成。另外,這些鹽類可藉由將無機鹼或有機鹼加到游離酸中來製備。衍生自無機鹼的鹽類包括但不限於鈉、鉀、鋰、銨、鈣、鎂鹽及類似者。衍生自有機鹼的鹽類包括但不限於一級胺、二級胺、和三級胺的鹽、取代胺,包括天然存在的取代胺、環胺和鹼性離子交換樹脂,諸如異丙胺、三甲胺、二乙胺、三乙胺、三丙胺、乙醇胺、離胺酸、精胺酸、N-乙基哌啶、哌啶、聚亞胺樹脂及類似者。式 (I) 化合物的特定藥學上可接受的鹽類是鹽酸鹽。
術語“保護基”(PG) 在合成化學中慣常與其相關之含義中表示選擇性阻斷多官能化合物中之反應位點以使得化學反應可在另一未保護反應位點處選擇性進行的基團。保護基可在適當時間移除。例示性保護基為胺基保護基、羧基保護基或羥基保護基。特定保護基為三級丁氧基羰基 (Boc)、苄氧羰基 (Cbz)、茀基甲氧基羰基 (Fmoc) 及苄基 (Bn)。進一步之特定保護基為三級丁氧基羰基 (Boc) 及茀基甲氧基羰基 (Fmoc)。更特定的保護基是三級丁氧羰基 (Boc)。例示性保護基及其在有機合成中之應用描述於例如“Protective Groups in Organic Chemistry”中,由 T. W. Greene 及 P. G. M. Wutts 著, 第 5 版, 2014, John Wiley & Sons, N.Y.。
術語“尿素成型試劑”是指能夠使第一胺成為將與第二胺反應從而形成尿素衍生物的物質的化合物。脲形成試劑之非限制性實施例包括碳酸雙(三氯甲基)酯、光氣、氯甲酸三氯甲酯、碳酸(4-硝基苯基)酯、1,1′-羰基-二-(1,2,4-三唑) 及 1,1’-羰基二咪唑。在 G. Sartori 等人,Green Chemistry 2000, 2, 140 中描述的尿素成型試劑是以引用方式併入本文中。
本文所述的式 (I) 化合物可包含數個非對稱中心,且其形式可為純鏡像異構物、鏡像異構物的混合物、例如像是外消旋物、光學純非鏡像異構物、非鏡像異構物的混合物、非鏡像異構外消旋物或非鏡像異構外消旋物的混合物。
依據 Cahn-Ingold-Prelog 序列法則,非對稱碳原子可為“R”或“S”組態。
縮寫“MAGL”是指單醯基甘油脂肪酶。術語“MAGL”和“單醯基甘油脂肪酶”在本文中可互換使用。
如本文中所使用的術語“治療”包括:(1) 抑制病狀、病症或病況(例如在維持治療之情況下,遏制、減少或延緩疾病的至少一個臨床或亞臨床症狀之發展或其復發);及/或 (2) 緩解病況(亦即使病狀、病症或病況或其臨床或亞臨床症狀中之至少一者消退)。對待治療的患者的益處在統計學上是顯著的,或者至少對於患者或醫師是可察覺的。然而,應瞭解的是,當將藥物投予於患者以治療疾病時,結果可能未必總是有效的治療方法。
如本文中所使用,術語“預防(法)(prophylaxis)”包括:預防或延緩哺乳動物(尤其是人)發展之病狀、病症或病況的臨床症狀之出現,該哺乳動物(尤其是人)可能罹患或易患病狀、病症或病況但又尚未經歷或呈現病狀、病症或病況之臨床或亞臨床症狀。
如本文所用,術語“神經發炎”涉及神經組織(其為神經系統之兩個部分之主要組織組分);中樞神經系統 (CNS) 之腦及脊髓;及周邊神經系統 (PNS) 之分支周邊神經之急性及慢性發炎。慢性神經發炎與神經退化性疾病(諸如阿滋海默症、帕金森氏病和多發性硬化症)有關。急性神經發炎通常緊接著在中樞神經系統損傷之後,例如由於外傷性腦損傷 (TBI)。
術語“外傷性腦損傷”(“TBI”,又稱“顱內損傷”)涉及由外部機械力產生之大腦損傷,諸如快速加速或減速、撞擊、爆炸波、或射彈之穿透。
術語“神經退化性疾病”涉及與神經元之結構或功能之進展性缺失(包括神經元死亡)相關的疾病。神經退化性疾病之實施例包括但不限於多發性硬化症、阿滋海默症、帕金森病及肌肉萎縮性側索硬化症。
術語“精神障礙 (mental disorder)”(亦稱為精神疾病或精神病症)涉及可造成痛苦或生活機能不佳之行為或精神模式。此等特徵可為持續性、復發性及緩解性的,或以單次發作形式發生。精神障礙之實施例包括但不限於焦慮及抑鬱。
術語“疼痛”涉及與實際或潛在組織損傷相關之不適感覺及情緒經歷。疼痛之實施例包括但不限於感受傷害性疼痛、慢性疼痛(包括自發性疼痛)、神經病性疼痛(包括化學療法誘導之神經病變)、幻覺痛及精神性疼痛。疼痛之特定實施例為神經病性疼痛,其由影響涉及身體感覺之神經系統(亦即體感覺系統)之任何部分的損傷或疾病引起。在一具體實施方式中,“疼痛”是由切除術或開胸術產生之神經病性疼痛。在一具體實施方式中,“疼痛”是化學療法誘導之神經病變。
術語“神經毒性”涉及神經系統中之毒性。其在曝露於天然或人造有毒物質(神經毒素)時出現,以造成神經組織損傷之方式改變神經系統之正常活性。神經毒性之實施例包括但不限於由曝露於化學療法、放射治療、藥物療法、藥物濫用、及器官移植中所使用之物質以及曝露於重金屬、某些食品及食品添加劑、農藥、工業及/或清潔溶劑、化妝品及一些天然存在之物質而產生的神經毒性。
術語“癌症”是指一種疾病,其特徵為由細胞(此等細胞為“癌細胞”)之異常不受控制生長產生的贅瘤或腫瘤之存在。如本文所用的術語癌症明確地包括但不限於肝細胞癌、結腸癌症形成及卵巢癌。
如本文所用的術語“哺乳動物”包括人及非人,且包括但不限於人、非人靈長類、犬、貓、鼠、牛、馬、及豬。在一特佳具體實施方式中,“哺乳動物”是指人。
本發明之化合物
在第一方面 (A1) 中,本發明提供式 (I) 化合物(I)
或其藥學上可接受之鹽類,其中:
A 係選自 C6
-C14
-芳基、5 至 14 員雜芳基以及 3 至 14 員雜環基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
m 係 0,n 係 0 或 1,以及,X 係 CR8
;或
m 係 1,n 係 1 或 2,以及,X 係 CR8
或 N;
R1
、R2
及 R3
係各自獨立地選自氫及 C1-6
-烷基;
R4
、R5
、R6
及 R7
係獨立地選自氫、鹵素、氰基、羥基、C1-6
-烷氧基、鹵-C1-6
-烷氧基、胺基-C1-6
-烷氧基、C1-6
-烷基、鹵-C1-6
-烷基、羥基-C1-6
-烷基、C1-6
-烷基磺醯基、SF5
、胺基甲醯基、C3-10
-環烷基-C1-6
-烷氧基–、C1-6
-烷基-NH-C(O)–、C1-6
-烷基-C(O)-NH– 及 C3-10
-環烷基,其中,每個 C3-10
-環烷基係視需要經選自 C1-6
-烷基及鹵-C1-6
-烷基之 1 至 2 個取代基取代;以及
R8
係選自氫、鹵素、羥基、鹵-C1-6
-烷基及 C1-6
-烷基。
本發明亦提供下列本發明的第一方面 (A1) 的列舉具體實施方式 (E):
E1. 根據 A1 之式 (I) 化合物或其藥學上可接受之鹽類,其中,A 係 C6
-C14
-芳基或 5 至 14 員雜芳基。
E2. 根據 A1 之式 (I) 化合物或其藥學上可接受之鹽類,其中,A 係苯基或吡啶基。
E3. 根據 A1 之式 (I) 化合物或其藥學上可接受之鹽類,其中,A 係 C6
-C14
-芳基。
E4. 根據 A1 之式 (I) 化合物或其藥學上可接受之鹽類,其中,A 係苯基。
E5. 根據 A1 及 E1 至 E4 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
B 係
(i) 苯基;以及,L1
係 –O–;或
(ii) 選自㗁二唑基、嗒𠯤基、吡啶基及噻唑基;以及,L1
係共價鍵或 –O–。
E6. 根據 A1 及 E1 至 E5 中任一項之式 (I) 化合物,其中:
m 係 0,n 係 0,以及,X 係 CR8
;或
m 係 1,n 係 1,以及,X 係 CR8
或 N。
E7. 根據 A1 及 E1 至 E5 中任一項之式 (I) 化合物,其中:m 係 0,n 係 0,以及,X 係 CR8
。
E8. 根據 A1 及 E1 至 E7 中任一項之式 (I) 化合物,其中,R1
係氫。
E9. 根據 A1 及 E1 至 E8 中任一項之式 (I) 化合物,其中,R2
係氫。
E10. 根據 A1 及 E1 至 E9 中任一項之式 (I) 化合物,其中,R3
係氫。
E11. 根據 A1 及 E1 至 E10 中任一項之式 (I) 化合物,其中,R4
係氫。
E12. 根據 A1 及 E1 至 E11 中任一項之式 (I) 化合物,其中,R5
係氫。
E13. 根據 A1 及 E1 至 E12 中任一項之式 (I) 化合物,其中,R6
係選自氫、鹵素、氰基、C1-6
-烷基、C1-6
-烷氧基、鹵-C1-6
-烷基、C3-10
-環烷基及 C1-6
-烷基磺醯基。
E14. 根據 A1 及 E1 至 E12 中任一項之式 (I) 化合物,其中,R6
係選自氫、鹵素、氰基及 C1-6
-烷基。
E15. 根據 A1 及 E1 至 E12 中任一項之式 (I) 化合物,其中,R6
係選自氫、氟基、氯基、氰基、甲基及 2,2-二甲基丙基。
E16. 根據 A1 及 E1 至 E15 中任一項之式 (I) 化合物,其中,R7
係選自氫、鹵素及 C1-6
-烷基。
E17. 根據 A1 及 E1 至 E15 中任一項之式 (I) 化合物,其中,R7
係選自氫、氟基及甲基。
E18. 根據 A1 及 E1 至 E15 中任一項之式 (I) 化合物,其中,R7
係氫或鹵素。
E19. 根據 A1 及 E1 至 E15 中任一項之式 (I) 化合物,其中,R7
係氫或氟基。
E20. 根據 A1 及 E1 至 E19 中任一項之式 (I) 化合物,其中,R8
係氫或羥基。
E21. 根據 A1 及 E1 至 E19 中任一項之式 (I) 化合物,其中,R8
係氫。
E22. 根據 A1 之式 (I) 化合物,其中,該式 (I) 化合物係式 (II) 化合物或其藥學上可接受之鹽類,(II)
其中:
A 係 C6
-C14
-芳基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、鹵素、氰基、C1-6
-烷基、C1-6
-烷氧基、鹵-C1-6
-烷基、C3-10
-環烷基及 C1-6
-烷基磺醯基;以及
R7
係選自氫、鹵素及 C1-6
-烷基。
E23. 根據 A1 之式 (I) 化合物,其中,該式 (I) 化合物係式 (II) 化合物或其藥學上可接受之鹽類,(II)
其中:
A 係 C6
-C14
-芳基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、鹵素、氰基及 C1
-6
-烷基;以及
R7
選自氫及鹵素。
E24. 根據 A1 之式 (I) 化合物,其中,該式 (I) 化合物係式 (III) 化合物或其藥學上可接受之鹽類,(III)
其中:
B 係
(i) 苯基;以及,L1
係 –O–;或
(ii) 選自㗁二唑基、嗒𠯤基、吡啶基及噻唑基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、氟基、氯基、氰基、甲基及 2,2-二甲基丙基;以及
R7
係選自氫及氟。
E25. 根據 A1 之式 (I) 化合物,其中,該式 (I) 化合物係式 (IIa) 化合物或其藥學上可接受之鹽類,(IIa)
其中:
A 係 C6
-C14
-芳基或 5 至 14 員雜芳基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
m 係 0,n 係 0,以及 X 係 CR8
;或
m 係 1,n 係 1,以及,X 係 CR8
或 N;
R6
係選自氫、鹵素、氰基、C1-6
-烷基、C1-6
-烷氧基、鹵-C1-6
-烷基、C3-10
-環烷基及 C1-6
-烷基磺醯基;
R7
係選自氫、鹵素及 C1-6
-烷基;以及
R8
係選自氫及羥基。
E26. 根據 A1 之式 (I) 化合物,其中,該式 (I) 化合物係式 (IIb) 化合物或其藥學上可接受之鹽類,(IIb)
其中:
A 係 C6
-C14
-芳基或 5 至 14 員雜芳基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、鹵素、氰基及 C1-6
-烷基;
R7
係選自氫、C1-6
-烷基及鹵素;以及
R8
係選自氫及羥基。
E27. 根據 A1 之式 (I) 化合物,其中,該式 (I) 化合物係式 (IIb) 化合物或其藥學上可接受之鹽類,(IIb)
其中:
A 係苯基或吡啶基;
B 係
(i) 苯基;以及,L1
係 –O–;或
(ii) 選自㗁二唑基、嗒𠯤基、吡啶基及噻唑基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、氟基、氯基、氰基、甲基及 2,2-二甲基丙基;
R7
係選自氫、甲基及氟基;以及
R8
係選自氫及羥基。
E28. 根據 A1 及 E1 至 E21 中任一項之式 (I) 化合物或其藥學上可接受之鹽類,其中,R1
、R2
及 R3
皆為氫。
E29. 根據 A1 及 E1 至 E21 中任一項之式 (I) 化合物或其藥學上可接受之鹽類,其中,A 係 C6
-C14
-芳基,以及,R4
及 R5
皆為氫。
E30. 根據 A1 及 E1 至 E21 中任一項之式 (I) 化合物或其藥學上可接受之鹽類,其中,A 係苯基,以及,R4
及 R5
皆為氫。
E31. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、鹵素、氰基、C1-6
-烷基、C1-6
-烷氧基、鹵-C1-6
-烷基、C3-10
-環烷基及 C1-6
-烷基磺醯基;以及
R7
係選自氫、鹵素及 C1-6
-烷基。
E32. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、鹵素、氰基及 C1-6
-烷基;以及
R7
選自氫及鹵素。
E33. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
B 係
(i) 苯基;以及,L1
係 –O–;或
(ii) 係㗁二唑基、嗒𠯤基、吡啶基及噻唑基;以及,L1
係共價鍵或 –O–;
R6
係選自氫、氟基、氯基、氰基、甲基及 2,2-二甲基丙基;以及
R7
係選自氫及氟基。
E34. 根據 A1 及 E1 至 E33 中任一項之式 (I) 化合物或其藥學上可接受之鹽類,係選自:
(4aR,8aS)-6-(3-(4-苯氧基苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-[3-[4-(2-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-(4-嘧啶-2-基氧苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(2-甲基-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-甲基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-(4-嗒𠯤-3-基氧苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(4-甲基-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(5-氟-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(5-氯-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3-吡啶氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-甲基嗒𠯤-3-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3-氯嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-甲氧嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[4-(三氟甲基)嘧啶-2-基]氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2,4-二氟苯氧)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2-氟苯氧)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2-甲基苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[3-(三氟甲基)苯氧基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
2-[4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯氧基]苯甲腈;
(4aR,8aS)-6-[3-[4-(2-氯嘧啶-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(+)-(4aR,8aS)-6-[3-[4-(4-環丙基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(6-甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(4-氯-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(3-氟-4-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(+)-(4aR,8aS)-6-[3-[4-(2-甲基磺醯基嘧啶-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[(3,6-二甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(1H-吡唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[2-(2,2-二甲基丙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[1-(2,2-二甲基丙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3-氯-2-吡啶基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2,4-二甲基㗁唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3,5-二甲基吡唑-1-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[3-(2,2-二甲基丙基)三唑-4-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,3,4-㗁二唑-2-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[2-(2-氟乙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[1-(2-氟乙基)吡唑-4-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-甲基-1,3-噻唑-2-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(1-甲基吡唑-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(6-氟吡啶-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2-氟吡啶-4-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(1-甲基吡唑-4-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2-甲基吡唑-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[5-(4-氟苯氧)-2-吡啶基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-(3-(6-(4-氟苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-(3-(6-(4-(三氟甲氧基)苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-(3-(6-(4-氯苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-[3-[4-(3,6-二甲基嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-(3-(6-(2-氯苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-(3-(6-(3-氯苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-[4-[4-(4-氟苯氧)苯基]哌啶-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-羥基-3-(4-苯氧基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-羥基-3-(5-苯氧-2-吡啶基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[4-(4-苯氧基苯基)哌啶-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;以及
(4aR,8aS)-6-[4-(4-苯氧基苯基)哌𠯤-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮。
E35. 根據 E34 之式 (I) 化合物或其藥學上可接受之鹽類,係選自:
(4aR,8aS)-6-(3-(4-苯氧基苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;
(4aR,8aS)-6-[3-[4-(3-氯嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2,4-二氟苯氧)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(2-氟苯氧)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
2-[4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯氧基]苯甲腈;
(4aR,8aS)-6-[3-[4-(3-氯-2-吡啶基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(4-甲基-1,3-噻唑-2-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[5-(4-氟苯氧)-2-吡啶基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[4-(3,6-二甲基嗒𠯤4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;
(4aR,8aS)-6-[3-[6-(2-氯苯氧)-3-吡啶]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;以及
(4aR,8aS)-6-[3-羥基-3-(4-苯氧基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮。
E36. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中,R1
及 R2
均是氫。
E37. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
R3
係氫;
m 係 0,n 係 0,以及,X 係 CR8
;或
m 係 1,n 係 1,以及,X 係 CR8
或 N;以及
R8
係氫或羥基。
E38. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
R3
係氫;
m 係 0,n 係 0,以及,X 係 CR8
;以及
R8
係氫或羥基。
E39. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
A 係 C6
-C14
-芳基或 5 至 14 員雜芳基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R4
及 R5
皆為氫;
R6
係選自氫、鹵素、氰基、C1-6
-烷基、C1-6
-烷氧基、鹵-C1-6
-烷基、C3-10
-環烷基及 C1-6
-烷基磺醯基;以及
R7
係選自氫、鹵素及 C1-6
-烷基。
E40. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
A 係 C6
-C14
-芳基或 5 至 14 員雜芳基;
B 係
(i) C6
-C14
-芳基;以及,L1
係 –O–;或
(ii) 5 至 14 員雜芳基;以及,L1
係共價鍵或 –O–;
R4
及 R5
皆為氫;
R6
係選自氫、鹵素、氰基及 C1-6
-烷基;以及
R7
係選自氫、鹵素及 C1-6
-烷基。
E41. 根據 A1 及 E1 至 E21 中任一項所述之式 (I) 化合物或其藥學上可接受之鹽類,其中:
A 係苯基或吡啶基;
B 係
(i) 苯基;以及,L1
係 –O–;或
(ii) 選自㗁二唑基、嗒𠯤基、吡啶基及噻唑基;以及,L1
係共價鍵或 –O–;
R4
及 R5
皆為氫;
R6
係選自氫、氟基、氯基、氰基、甲基及 2,2-二甲基丙基;以及
R7
係選自氫、鹵素及甲基。
在一具體具體實施方式中,本發明提供根據本文所述的式 (I) 之化合物的藥學上可接受之鹽類,特別是鹽酸鹽。在一進一步特定具體實施方式中,本發明提供如本文所述的根據式 (I) 之化合物作為游離鹼。
在一些具體實施方式中,式 (I) 化合物由其中,一或多個原子經具有不同原子質量或質量數之原子置換的同位素標記。此等經同位素標記(即放射性標記)之式 (I) 化合物被視為在本揭露之範圍內。可併入至式 (I) 化合物中之同位素之實施例包括氫、碳、氮、氧、磷、硫、氟、氯、及碘之同位素,諸如但不限於分別為2
H、3
H、11
C、13
C、14
C、13
N、15
N、15
O、17
O、18
O、31
P、32
P、35
S、18
F、36
Cl、123
I、及125
I。某些經同位素標記之式 (I) 化合物(例如併有放射性同位素者)適用於藥物及/或受質組織分佈研究。放射性同位素氚(即3
H)及碳-14(即14
C)由於其容易併入及現成偵測手段而尤其適用於此目的。例如,式 (I) 化合物可富集 1、2、5、10、25、50、75、90、95 或 99 百分比之給定同位素。
用諸如氘(即2
H)之較重同位素取代可得到某些由更大代謝穩定性產生之治療優勢,例如延長之活體內半衰期或降低之劑量需求。
用正電子發射同位素(諸如11
C、18
F、15
O 及13
N)取代可適用於正電子發射斷層攝影術 (PET) 研究,以用於檢查受質受體佔有率。經同位素標記之式 (I) 化合物通常可藉由該發明所屬技術領域具有通常知識者已知之習知技術或藉由類似於如下文所闡述之實施例中所描述之方法的方法,使用適當之經同位素標記之試劑替代先前所採用的未經標記之試劑來製備。
製造程序
本發明的式 (I) 化合物的製備可依序或收斂性合成途徑進行。以下通用方案中展示本發明之合成。進行所得產物之反應及純化所需之技能為該發明所屬技術領域具有通常知識者所知。除非有相反指示,否則用於以下方法之描述的取代基及指數具有本文中所給出之意義。
若起始物質、中間產物或式 (I) 化合物中之一者含有在一或多個反應步驟之反應條件下不穩定或具反應性之一或多個官能基,則可在施加此項技術中熟知之方法的關鍵步驟之前引入適當之保護基(如 T.W.Greene 及 P.G.M.Wutts 之“Protective Groups in Organic Chemistry”第 5 版, 2014, John Wiley & Sons, N.Y. 中所描述)。可使用文獻中所描述之標準方法在合成後期移除此等保護基。
若起始物質或中間產物含有立構中心,則式 (I) 化合物可以非鏡像異構物或鏡像異構物之混合物之形式獲得,其可藉由此項技術中熟知之方法,例如手性 HPLC、手性 SFC 或手性結晶來分離。外消旋化合物可例如經由非鏡像異構物鹽藉由用光學純酸結晶或藉由鏡像異構體分離,藉由特定層析方法,使用手性吸附劑或手性沖提液而分離成其鏡像異構體。同樣,有可能分離含有立構中心之起始物質及中間產物,以獲得非鏡像異構物/鏡像異構物富集起始物質及中間產物。在式 (I) 化合物之合成中使用此等非鏡像異構性/鏡像異構物富集起始物質及中間產物將通常產生相應的式 (I) 之非鏡像異構物/鏡像異構物富集化合物。
該發明所屬技術領域具有通常知識者將認識到,在合成式 (I) 化合物中-如果不希望如此-將採用“正交保護基策略 (orthogonal protection group strategy)”,其允許一次裂解幾個保護基而不影響分子中的其他保護基。正交保護原理係該技術中習知者且亦揭示於文獻(例如,Barany and R. B. Merrifield, J. Am. Chem. Soc. 1977, 99, 7363;H. Waldmann 等人,Angew. Chem. Int. Ed. Engl. 1996, 35, 2056)中。
該發明所屬技術領域具有通常知識者將認識到,反應順序可視中間產物之反應性及性質而變化。
更詳細地,式 (I) 化合物可藉由下文所給出之方法、藉由實施例中所給出之方法或藉由類似方法來製造。個別反應步驟之適當的反應條件為該發明所屬技術領域具有通常知識者已知。此外,對於文獻中所描述之影響所描述反應的反應條件,參見例如:Comprehensive Organic Transformations: A Guide to Functional Group Preparations, 2nd Edition, Richard C. Larock. John Wiley & Sons, New York, NY. 1999。發現在存在或不存在溶劑之情況下適宜進行反應。對於待採用之溶劑的性質無特定限制,惟該溶劑對所涉及之反應或試劑無不良影響且其至少在一定程度上可溶解試劑。所描述之反應可在廣泛範圍之溫度內進行且精確的反應溫度對於本發明並非關鍵。便利的是在 -78℃ 至回流之間的溫度範圍內進行所描述之反應。反應所需之時間亦可取決於許多因素(尤其反應溫度及試劑之性質)而有很大變化。然而,0.5 小時至若干天之時間段通常將足以得到所描述之中間產物及化合物。反應順序不限於方案中所呈現之順序,然而,視起始物質及其相應反應性而定,反應步驟之順序可自由改變。
若起始物質或中間產物非商業上可獲得或其合成未描述於文獻中,則其可以類似於用於相近類似物之現有程序之方式或如實驗部分中所概述來製備。
本文中使用以下縮寫:
AcOH = 乙酸,ACN = 乙腈,Bn = 苄基,Boc = 三級丁氧基羰基,CAS RN = 化學文摘註冊號,Cbz = 苄氧基羰基,Cs2
CO3
= 碳酸銫,CO = 一氧化碳,CuCl = 氯化銅(I),CuCN = 氰化銅(I),CuI = 碘化銅(I),DAST = 三氟化(二乙基胺基)硫,DBU = 1,8-二氮雙環[5,4,0]十一-7-烯,DEAD = 偶氮二甲酸二乙酯,DIAD = 偶氮二甲酸二異丙酯,DMAP = 4-二甲基胺基吡啶,DME = 二甲氧基乙烷,DMEDA = N,N'-二甲基伸乙基二胺,DMF = N,N-二甲基甲醯胺,DIPEA = N,N-二異丙基乙基胺,dppf = 1,1雙(二苯基膦基)二茂鐵,EDC.HCl = N-(3-二甲基胺基丙基)-N'-乙基碳化二亞胺鹽酸鹽,EI = 電子撞擊,ESI = 電灑離子化,EtOAc = 乙酸乙酯,EtOH = 乙醇,h = 小時,FA = 蟻酸,H2
O = 水,H2
SO4
= 硫酸,HATU = 1-[雙(二甲基胺基)亞甲基]-1H-1,2,3-三唑并[4,5-b]吡啶鎓-3-氧化物六氟磷酸鹽,HBTU = O-苯并三唑-N,N,N',N'-四甲基-尿素鎓-六氟-磷酸鹽,HCl = 氯化氫,HOBt = 1-羥基-1H-苯并三唑;HPLC = 高效液相層析,iPrMgCl = 氯化異丙基鎂,I2
= 碘,IPA = 2-丙醇,ISP = 離子噴霧陽性(模式),ISN = 離子噴霧陰性(模式),K2
CO3
= 碳酸鉀,KHCO3
= 碳酸氫鉀,KI = 碘化鉀,KOH = 氫氧化鉀,K3
PO4
= 磷酸三鉀,LiAlH4
或 LAH = 鋁氫化鋰,LiHMDS = 雙(三甲基矽基)醯胺鋰,LiOH = 氫氧化鋰,mCPBA = 间氯过氧苯甲酸,MgSO4
= 硫酸鎂,min = 分鐘,mL = 毫升,MPLC = 中壓液相層析,MS = 質譜,nBuLi = 正丁基鋰,NaBH3
CN = 氰基硼氫化鈉,NaH = 氫化鈉,NaHCO3
= 碳酸氫鈉,NaNO2
= 亞硝酸鈉,NaBH(OAc)3
= 三乙醯氧基硼氫化鈉,NaOH = 氫氧化鈉,Na2
CO3
= 碳酸鈉,Na2
SO4
= 硫酸鈉,Na2
S2
O3
= 硫代硫酸鈉,NBS = N-溴琥珀醯亞胺,nBuLi = 正丁基鋰,NEt3
= 三乙基胺 (TEA),NH4
Cl = 氯化銨,NMP = N-甲基-2-吡咯啶酮,OAc = 乙醯氧基,T3
P = 丙基膦酸酐,PE = 石油醚,PG = 保護基,Pd-C = 鈀/活性碳,PdCl2
(dppf)-CH2
Cl2
= 1,1'-雙(二苯基膦基)二茂鐵-二氯化鈀(II)二氯甲烷錯合物,Pd2
(dba)3
= 參(二亞苄丙酮)二鈀(0),Pd(OAc)2
= 乙酸鈀(II),Pd(OH)2
= 氫氧化鈀,Pd(PPh3
)4
= 肆(三苯基膦)鈀(0),PTSA = 對甲苯磺酸,R = 任何基團,RT = 室溫,SFC = 超臨界流體層析法,S-PHOS = 2-二環己基膦基-2',6'-二甲氧基二苯基,TBAI = 碘化四丁基銨,TEA = 三乙基胺,TFA = 三氟乙酸,THF = 四氫呋喃,TMEDA = N,N,N',N'-四甲基乙二胺,ZnCl2
= 氯化鋅,Hal = 鹵素。
方案
1
因此,在尿素成型試劑(諸如碳酸雙(三氯甲基)酯)存在下,使用適合之鹼及溶劑(例如碳酸氫鈉/DCM)使 4a,5,6,7,8,8a-六氫-4H-吡啶[4,3-b][1,4]㗁𠯤-3-酮 1 與中間產物 2 反應以得到式 I 化合物(步驟 a
)。其他脲形成試劑包括但不限於光氣、氯甲酸三氯甲酯、碳酸(4-硝基苯基)酯或 1,1’-羰基二咪唑。此類型之反應及此等試劑之用途廣泛描述於文獻(例如 G. Sartori 等人,Green Chemistry 2000, 2, 140)中。該發明所屬技術領域具有通常知識者將認識到,由於中間形成之胺甲醯氯之反應性及穩定性以及為了避免形成非所需對稱尿素副產物,試劑添加次序在此類型反應中可為重要的。
方案
1a
類比於方案 1 製備之中間產物 2a 可與芳基硼酸或雜芳基硼酸 7a (Y = B(OH)2
) 或硼酸酯(Y = 例如 4,4,5,5-四甲基-2-苯基-1,3,2-二㗁環戊硼烷 (頻哪醇) 酯,其或可商購獲得或使用如例如揭示於 Dennis G. Hall 編撰之“硼酸—製備與有機合成及醫學中之應用(第一版)”(“Boronic Acids - Preparation and Applications in Organic Synthesis and Medicine” 1st Ed., 2005, John Wiley & Sons, New York)中之文獻過程製備)反應,該反應係使用合適之觸媒(例如,二氯[1,1`-雙(二苯基膦)-二茂鐵]鈀(II) 二氯甲烷加成物、肆(三苯基膦)鈀(0) 或醋酸鈀(II)與三苯基膦)於適宜之溶劑(例如,二㗁烷、二甲氧基乙烷、水、甲苯、DMF 或其混合物)中以及合適之鹼(例如,Na2
CO3
、NaHCO3
、KF、K2
CO3
或 TEA)於介於室溫及該溶劑或溶劑混合物之沸點之間的溫度下進行,以獲得化合物 IA(步驟 a
)。這一類型之鈴木反應 (Suzuki reaction) 係廣泛揭示於文獻(例如,A. Suzuki, Pure Appl. Chem. 1991, 63, 419-422;A. Suzuki, N. Miyaura, Chem. Rev. 1995, 95, 2457-2483;A. Suzuki, J. Organomet.Chem. 1999, 576, 147-168;V. Polshettiwar 等人,Chem. Sus.Chem. 2010, 3, 502-522)中且係為該發明所屬技術領域具有通常知識者所習知。另選地,芳基或雜芳基-三氟硼酸酯(7a,其中,Y = BF3
)可用於交叉偶合反應中,該反應係應用鈀觸媒諸如,例如,肆(三苯基膦)鈀(0)、醋酸鈀(II) 或二氯[1,1`-雙(二苯基膦)二茂鐵]-鈀(II) 二氯甲烷加成物於合適之鹼諸如碳酸銫或磷酸鉀之存在下於溶劑諸如甲苯、THF、二㗁烷、水或其混合物中在介於室溫與該溶劑或溶劑混合物之沸點之間的溫度下進行(步驟 a
)。
另選地,中間產物 2a 中之溴或碘可使用例如步驟 a) 下揭示之方法交換為硼酸或硼酸酯基團,以給出中間產物 2c(步驟 b
)。
然後,中間產物 2c 可與中間產物 7b(其中,FG 係例如溴,其係或可商購獲得或類比於文獻方法製備)反應,該反應係應用此前所揭示之反應條件進行,以獲得最終之化合物 IA(步驟 c
)。
此外,可令其中,Y 較佳係溴之中間產物 7b 與中間產物 2a(其中,FG 較佳為溴,類比於方案 1 製備)進行親電體交叉偶合,該反應係在以 420 nm 藍光燈照射下使用適宜之光觸媒諸如 [Ir{dF(CF3
)ppy}2
(dtbpy)]PF6
([4,4′-雙(1,1-二甲基乙基)-2,2′-聯吡啶-N1,N1′]雙[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基-N]苯基-C]銥(III) 六氟磷酸鹽)、鎳觸媒如 NiCl2
glyme(二氯(二甲氧基乙烷)鎳)、4,4′-二-第三丁基-2,2′-二吡啶基與參(三甲基矽基)矽烷於合適之鹼諸如無水碳酸鈉之存在下於溶劑如 DME 中進行。這一類型之反應係揭示於文獻例如J. Am. Chem. Soc. 2016, 138, 8084 中。(步驟 a
)。
方案
1b
據此,藉由應用芳香族親核取代反應,中間產物 2b(可例如藉由方案 3
中詳述之通常過程獲得)可轉換為化合物 IB。使用合適之雜芳基化合物 7b(其中,Y 係合適之鹵素諸如氟、氯或溴,較佳係氟或氯,其中,R6
及 R7
係揭示於本文中,諸如 2-氯嘧啶、2-氯-4-甲基嘧啶、3-氯嗒𠯤、3,4-二氯嗒𠯤、2-氯-4-甲氧嘧啶、2-氯-4-(三氟甲基)嘧啶、3-氟-4-甲基嘧啶、3,5-二氟嘧啶、3-氯-5-氟吡啶、3-氟吡啶、2-氟苯甲腈、2-氟-6-甲基吡啶、4-溴-2-氯嘧啶、2-氯-4-環丙基嘧啶、4-氯-3-氟吡啶及 4-氯-2-(甲基磺醯基)嘧啶)處理羥基中間產物2b
,該反應係使用合適之鹼諸如 K2
CO3
或
Cs2
CO3
於適宜之溶劑諸如 DMSO、DMF 或 NMP 於從 0℃ 至最高 200℃ 範圍內的溫度下施加微波加熱而進行,獲得式IB
化合物(步驟 a
)。
方案
1c
據此,2a 類型之中間產物(可例如藉由方案 4
中詳述之通常過程獲得),其中,FG 係合適之鹵素諸如氯或溴,較佳係溴,可藉由應用 Buchwald-Hartwig 交叉偶合反應轉換為化合物 IB。使用合適之酚化合物 8(其中,R6
及 R7
係揭示於本文中,諸如苯酚)處理中間產物 2a,該反應係使用合適之觸媒系統諸如 Pd(OAc)2
與 2-二-第三丁基膦-2′,4′,6′-三異丙基聯苯於鹼諸如 K3
PO4
之存在下於適宜之溶劑諸如甲苯中在從室溫至最高該溶劑沸點範圍內的溫度下視需要施加微波加熱而進行,獲得式 IB 化合物(步驟 a
)。
另選地,中間產物 2a 中之溴可交換為硼酸基團以給出中間產物 2d(可例如藉由方案 4 中詳述之通常過程獲得)(步驟 b
)。
然後,藉由應用 Chan-Lam 交叉偶合反應,中間產物 2d 可轉換為化合物 IB。使用合適之酚化合物 8(其中,R6
及 R7
係揭示於本文中,諸如 2-氟苯酚、3-氟苯酚、4-氟苯酚、2,4-二氟苯酚、2-氯苯酚、3-氯苯酚、4-氯苯酚、2-甲基苯酚及 3-三氟甲基苯酚)處理硼酸中間產物 2d,該反應係於 TEA、Cu(OAc)2
及分子篩之存在下於溶劑如 DCM、DCE 或 CH3CN 中於室溫下進行,獲得式 IB 化合物(步驟 c
)。
方案
2
由此,3-胺基哌啶-4-醇衍生物 3(其中,“PG” 表示諸如 Cbz 或 Boc 保護基之適合保護基)可例如用醯基氯化物 4(其中,R1 如本文所定義,且“LG”表示適合之脫離基(例如 Cl 或 Br))醯化,其於合適溶劑(諸如 THF、水、丙酮或其混合物)中、使用適合之鹼(諸如碳酸鈉或碳酸鉀、氫氧化鈉或乙酸鈉)以得到中間產物 5(步驟 a)。中間產物 4 為商業上可獲得或可根據文獻方法以非手性 (R1 = H)、外消旋(R1 非 H)或單一鏡像化合物形式(R1 非 H)製備。
可使用此項技術中熟知之方法將中間產物 5 環化成中間產物 6,例如藉由用氫化鈉/THF 或叔丁醇鉀/IPA 及水處理 5(步驟 b
)。該類型的反應在文獻中有所描述(例如 Z. Rafinski 等人,J. Org.Chem. 2015, 80, 7468;S. Dugar 等人,Synthesis 2015, 47(5), 712;WO2005/066187)。
應用此項技術中已知之方法移除中間產物 6 中之保護基(例如在 0℃ 與室溫之間的溫度下使用 TFA/DCM 移除 Boc 基團,在於適合之溶劑(諸如 MeOH、EtOH、EtOAc 或其混合物)中的適合催化劑(諸如 Pd 或 Pd(OH)2
/炭)存在下使用氫移除 Cbz 基團,及如例如下列中所描述:“Protective Groups in Organic Chemistry”,T.W. Greene 及 P.G.M.Wuts,第 4 版, 2006, Wiley N.Y.),提供中間產物 1(步驟 c
)。
中間產物 1 可分別以非鏡像異構物及鏡像異構物之混合物形式或以單一立體異構物形式獲得,這取決於其合成中是否採用順式或反式-3-胺基哌啶-4-醇衍生物 3 之外消旋混合物或單一鏡像化合物形式。中間產物 3 係可商購獲得並且其合成亦業經揭示於文獻(例如,WO2005/066187;WO2011/0059118;WO2016/185279)中。光學純順式組態中間產物 1B 及 1C 可例如根據方案 3
藉由可商購獲得的外消旋-(4aR,8aS)-4a,5,6,7,8,8a-六氫-4H-吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (1A)(視需要呈例如鹽酸鹽之鹽形式)之手性分離、使用該領域中已知之方法(例如藉由非鏡像異構鹽結晶或藉由手性層析)獲得(步驟 a
)。
在一些具體實施方式中,中間產物 2 係 2b 類型之中間產物。中間產物 2b(其中,A 係芳基,m = n = 0,R1
、R2
、R3
、R4
、R5
及 R8
係如本文中揭示)可藉由該發明所屬技術領域具有通常知識者所習知並且如方案 3
中詳述之通常合成過程示例之方法製備之。
方案
3
可令經保護之胺 10(或可商購獲得或藉由該領域中已知方法製備,其中,LG 係合適之離去基團諸如溴或碘,較佳係溴,m、n 及 R3
係如本文中揭示,以及,PG 係合適之保護基諸如例如 Boc、Cbz 或 Bn)與芳基溴 11(其中,X 係溴,R4
及 R5
係如本文中揭示,諸如 4-溴苯酚)進行親電體交叉偶合,該反應係於使用 420 藍光燈照射下使用適宜之光觸媒諸如 [Ir{dF(CF3
)ppy}2
(dtbpy)]PF6
([4,4′-雙(1,1-二甲基乙基)-2,2′-聯吡啶-N1,N1′]雙[3,5-二氟-2-[5-(三氟甲基)-2-吡啶基-N]苯基-C]銥(III) 六氟磷酸鹽)、鎳觸媒如 NiCl2 glyme(二氯(二甲氧基乙烷)鎳)、4,4′-二-第三丁基-2,2′-二吡啶基及參(三甲基矽基)矽烷於合適之鹼諸如無水碳酸鈉之存在下於溶劑如 DME 中進行。這一類型之反應係揭示於文獻例如J. Am. Chem. Soc. 2016, 138, 8084 中。(步驟 a
)。應用該領域中習知之方法以及如方案 2 步驟 c下所揭示,從中間產物 12 上去除保護基,得到中間產物 13(步驟 b
)。然後,應用例如方案 1 步驟 a 中詳述之條件,使胺 13 與中間產物 1 偶合,以給出中間產物 2b(步驟 c
)。
在一些具體實施方式中,中間產物 2 係 2a、2c 或 2d 類型之中間產物。中間產物 2a、2c 及 2d(其中,A 係芳基,m = n = 0,R1
、R2
、R3
、R4
、R5
及 R8
係如本文中揭示)可藉由該發明所屬技術領域具有通常知識者所習知並且如方案 4
中詳述之通常合成過程示例之方法製備之。
方案
4
可令經保護之胺 10(或可商購獲得或藉由該領域中已知方法製備,其中,LG 係合適之離去基團諸如溴或碘,較佳係碘,m、n 及 R3
係如本文中揭示,以及,PG 係合適之保護基諸如例如 Boc、Cbz 或 Bn)與芳基硼酸 14 諸如 4-溴苯硼酸進行 Suzuki-Miyaura 交叉偶合反應,該反應係使用合適之鎳觸媒諸如碘化鎳(II) 於外消旋-(1R,2R)-2-胺基環己-1-醇及合適之鹼諸如雙(三甲基矽基)醯胺化鈉之存在下於適宜之溶劑如 iPrOH、二㗁烷、THF 或 DME(較佳地,iPrOH)中於介於室溫與該溶劑沸點之間的溫度下視需要施加微波加熱而進行,以獲得中間產物 15。這一類型之反應係揭示於文獻例如 ChemistrySelect.2017, 2, 8841 中(步驟 a
)。應用該領域中習知之方法以及如方案 2 步驟 c下所揭示,從中間產物 15 上去除保護基,得到中間產物 16(步驟 b
)。然後,應用例如方案 1 步驟 a 中詳述之條件,使胺 16 與中間產物 1 偶合,以給出中間產物 2a,其中,FG 係溴(步驟 c
)。根據如例如揭示於 Dennis G. Hall 編撰之“硼酸—製備與有機合成及醫學中之應用(第一版)”(“Boronic Acids - Preparation and Applications in Organic Synthesis and Medicine” 1st Ed., 2005, John Wiley & Sons, New York) 中之文獻過程,可將中間產物 2a 中之溴取代基轉化為硼酸或硼酸酯(例如,頻哪醇酯),該反應係使用合適之觸媒諸如 PdCl2
(dppf).CH2
Cl2
於雙(頻哪醇酯合)二硼及合適之鹼諸如 Na2
CO3
、NaHCO3
、KF、KOAc 或 TEA 之存在下於適宜之溶劑如二㗁烷、THF、DME、水或 DMF 或其混合物(較佳地,二㗁烷)中於介於室溫與該溶劑或其混合物之沸點之間的溫度下視需要施加微波加熱而減小,以獲得中間產物 2c(步驟 d
)。最後,中間產物 2c 中頻哪醇酯之水解可藉由文獻(例如,Tetrahedron letters 2005, 46, 7899)中已知之方法或使用 NaIO4
於 NH4
OAc 之存在下於水與丙酮之混合物中於大約室溫下達成,以給出中間產物 2d(步驟 e
)。
化合物 31、32a 及 32b(其中,R1
至 R7
、R8
、m 及 n 係如本文中揭示,R6a
係 C1-6
-烷基,L1
係共價鍵,A 係苯基,以及,B 係 1-(C1-6
-烷基)-取代之吡唑-3-基或吡唑-5-基)可藉由該發明所屬技術領域具有通常知識者習知並且如方案 5
中詳述之通常合成過程示例之方法製備之。
方案
5
應用如方案 1a 步驟 a 下揭示之反應條件,可令可商購獲得之硼酸酯中間產物 9 與例如根據方案 3 製備之中間產物 2a 進行 Suzuki 偶合反應,以提供化合物 31(步驟 a
)。
化合物31
可使用 R6a
LG 類型之烷基化劑(LG 係合適之離去基團諸如氯、溴、碘、OSO2
烷基(例如,mesylate(甲磺酸根))、OSO2
氟烷基(例如,triflate(三氟甲磺酸根))或 OSO2
芳基(例如,tosylate(對甲苯磺酸根)))烷基化,該反應係使用合適之鹼於適宜之溶劑中(例如,氫化鈉於 DMF 中或碳酸銫於 DMF 中)於介於 0℃ 與該溶劑沸騰溫度之間的溫度下進行,以提供可例如藉由管柱層析分離之位置異構化合物32a
及32b
(步驟 b
)。
化合物 33(其中,R1
至 R8
、m 及 n 係如本文中揭示,L1
係共價鍵,A 係苯基,以及,B 係視需要進一步經取代之吡啶)可藉由該發明所屬技術領域具有通常知識者所習知並且如方案 6
中詳述之通常合成步驟示例之方法製備之。
方案
6
可商購獲得之 2-溴-3-氯吡啶 17 中之溴可藉由該領域中已知之方法轉化為三正丁基錫基團,例如,藉由首先在合適之溶劑諸如甲苯中於一溫度範圍例如 -78℃ 至室溫下與 n-BuLi 進行溴鋰交換反應,並且令該中間產物鋰物質與氯化三正丁基錫反應以提供中間產物 18(步驟 a
)。
可使用合適之觸媒及溶劑諸如肆(三苯基膦)-鈀(0) 於 DMF 中於介於室溫與該溶劑或溶劑混合物之沸點之間的溫度下,令中間產物 18 與中間產物 2a 反應以提供化合物 33(步驟 a
)。該類型之 Stille 反應係該領域中習知者並且揭示於文獻例如 Org.React.1997, 50, 1-652、ACS Catal.2015, 5, 3040−3053 中。
在一些具體實施方式中,中間產物 2 係 2e 類型之中間產物。2e 類型之中間產物(其中,R3
、R4
、R5
、R8
、m 及 n 係如本文中定義,R6a
係 C1-6
-烷基,L1
係共價鍵,A 係苯基,以及,B 係 1-烷基取代之三唑-5-基)可藉由該發明所屬技術領域具有通常知識者所習知並且如方案 7
中詳述之通常合成過程示例之方法製備之。
方案
7
藉由該領域中已知之方法,例如,使用亞硝酸第三丁酯及偶氮三甲基矽於適宜之溶劑諸如 ACN 中,可將可商購獲得之 4-硝基苯胺轉化為中間產物20(步驟 a
)。
於合適之酸及溶劑系統諸如甲苯中之 AcOH 中,視需要使用分子篩,較佳地於高溫下,令中間產物 20 與苯乙酮(例如,4'-溴苯乙酮)及 R6b
-NH2
類型之胺反應,得到三唑中間產物 21,其中,LG 係合適之離去基團例如鹵素,特別是溴(步驟 b
)。這一類型之反應係揭示於文獻例如 Chem. Commun., 2016, 52, 2885 中。
應用例如在方案 1a 步驟 a 下所揭示之反應方案,可令中間產物 21 與可商購獲得之中間產物 10(其中,LG 係合適之離去基團諸如溴或碘,特別是溴,m、n 及 R3
係如本文中揭示,以及,PG 係合適之保護基諸如 Boc)進行親電體交叉偶合反應,以提供中間產物 22(步驟 c
)。
例如 TFA 於 DCM 中於介於 0℃ 與室溫之間的溫度下取出該保護基,獲得中間產物 2e(步驟 d
)。
在一些具體實施方式中,中間產物 2 係 2f 類型之中間產物。2f 類型之中間產物(其中,R3
、R4
、R5
、R8
、m 及 n 係如本文中定義,R6a
係 C1-6
-烷基或鹵-C1-6
-烷基,R6b
係氫、C1-6
-烷基或鹵-C1-6
-烷基,L1
係共價鍵,A 係苯基,以及,B 係吡唑-1-基)可藉由該發明所屬技術領域具有通常知識者所習知並且如方案 8 中詳述之通常合成過程示例之方法製備之。
方案
8
中間產物 23 可例如藉由 1,3-二羰基化合物與可商購獲得且視需要經取代之肼(例如,(4-溴苯基)肼)於三水合硝酸銅(II) 之存在下於合適之溶劑諸如 ACN 中進行成環縮合而製備之(步驟 a
)。
應用例如在方案 1a 步驟 a 下揭示之反應條件,可令中間產物 23 與 10 類型之中間產物(其中,PG 表示合適之保護基諸如 Cbz 或 Boc,以及,LG 係指代合適之離去基團諸如鹵素,特別是溴)進行親電體交叉偶合反應,以提供中間產物 24(步驟 b
)。
應用所印行之過程並且如方案 7 步驟 d 下揭示者去除該保護基,得到中間產物 2f(步驟 c
)。
在一些具體實施方式中,中間產物2
係2g
類型之中間產物。2g
類型之中間產物(其中,R3
、R4
、R5
、R8
、m 及 n 係如本文中定義,R6a
係 C1-6
-烷基,L1
係共價鍵,A 係苯基,以及,B 係 5取代-1,3,4-㗁二唑-2-基)可藉由該發明所屬技術領域具有通常知識者所知並且如方案 9
中詳述之通常合成過程示例之方法製備之。
方案
9
可商購獲得之醯肼(例如,4-溴苯甲醯肼)可與醯氯 R6a
C(O)Cl 於合適之鹼的存在下於適宜之溶劑中諸如 DIPEA 於 DCM 中反應以獲得中間產物 25(步驟 a
)。
例如使用 pTsOH 於甲苯中,較佳地於最高為該溶劑之沸點的高溫下,可將中間產物 25(其中,LG 係指代合適之離去基團,諸如鹵素,特別是溴)脫水以提供中間產物 26(步驟 b
)。
應用例如方案 1a 步驟 a 下揭示之反應條件,可令中間產物 26 與 10 類型之中間產物進行親電體交叉偶合反應,以提供中間產物 27(步驟 c
)。
應用所印行之過程並且如方案 7 步驟 d 下揭示者去除該保護基,得到中間產物 2g(步驟 d
)。
在一些具體實施方式中,中間產物 2 係 2h 類型之中間產物。2h 類型之中間產物(其中,R3
、R4
、R5
、R8
、m 及 n 係如本文中定義,R6a
係 C1-6
-烷基,L1
係共價鍵,A 係苯基,以及,B 係 5取代-1,2,4-㗁二唑-3-基)可藉由該發明所屬技術領域具有通常知識者所習知並且如方案 10
中詳述之通常合成過程示例之方法製備之。
方案
10
應用例如方案 1a 步驟 a 下揭示之反應條件,可商購獲得或藉由該領域中習知方法製備之視需要經取代的苯甲腈(例如,4-溴苯甲腈)可與 10 類型之中間產物進行親電體交叉偶合反應,以提供中間產物 28(步驟 a
)。
中間產物 28 與鹽酸羥胺於合適之溶劑或溶劑混合物中並且使用適宜之鹼諸如 Na2
CO3
於 EtOH 及水中,較佳於高溫下進行反應,給出苯基醯胺肟中間產物 29(步驟 b
)。
然後,中間產物 29 可與醯氯 R6a
C(O)Cl 於適宜之鹼及溶劑諸如 DIPEA 於甲苯中之存在下於從室溫至該溶劑或溶劑混合物之沸點範圍內的溫度下反應,以提供中間產物 30(步驟 c
)。
應用所印行之過程並且如方案 7 步驟 d 下揭示者去除該保護基,得到中間產物 2h(步驟 d
)。
在一方面中,本發明係提供製造如本文所揭示之式 (I) 之製程,該製程係包含:
令 4a,5,6,7,8,8a-六氫-4H-吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 1(其中,R1 及 R2 係如本文中定義)
與雜環狀胺 2(其中,A、B、L1
、X、m、n 及 R3
至 R7
係如本文中定義)
於鹼及脲形成試劑之存在下反應,
以形成所示式 (I) 化合物。
在一具體實施方式中,所提供者是根據本發明之方法,其中,該鹼是碳酸氫鈉。
在一具體實施方式中,所提供者是根據本發明之方法,其中,該尿素成型試劑是選自碳酸雙(三氯甲基)酯、光氣、氯甲酸三氯甲酯、碳酸(4-硝基苯基)酯和 1,1’-羰基二咪唑,較佳的是其中,該尿素成型試劑是碳酸雙(三氯甲基)酯。
在一方面中,本發明提供當根據本文所述的任一程序製造時的如本文中所述的式 (I) 化合物。
MAGL
抑制活性
本發明之化合物是 MAGL 抑制劑。因此,在一方面中,本發明提供如本文所述的式 (I) 化合物用於在哺乳動物中抑制 MAGL 之用途。
在一進一步方面中,本發明提供如本文所揭示之式 (I) 化合物,其用於抑制哺乳動物 MAGL 之方法。
在一進一步方面,本發明提供如本文中所述之式 (I) 化合物之用途,其用於製備用於抑制哺乳動物 MAGL 的藥物。
在一進一步方面,本發明提供了用於在哺乳動物中抑制 MAGL 之方法,該方法包含將有效量的如本文所述的式 (I) 化合物投予哺乳動物。
藉由在天然受質 2-花生四烯酸甘油酯 (2-AG) 水解產生花生四烯酸之後測定酶活性,接著可進行質譜,來描繪式 (I) 化合物之 MAGL 抑制活性。此分析在下文簡稱為“2-AG 分析法”。
在 384 孔分析盤 (PP, Greiner Cat# 784201) 中以 20 µL 之總體積進行 2-AG 分析。在 100% DMSO (VWR Chemicals 23500.297) 中在聚丙烯盤中以 3 倍稀釋步驟製得化合物稀釋液,得到 12.5 µM 至 0.8 pM 之分析中之最終濃度範圍。將 0.25 µL 化合物稀釋液 (100% DMSO) 添加至 9 µL 於分析緩衝液 (50 mM TRIS (GIBCO, 15567-027)、1 mM EDTA (Fluka, 03690-100 mL)、0.01% (v/v) Tween) 中之 MAGL 中。震盪後,將培養盤在室溫下培育 15 min。為了開始反應,添加含 10 µL 於分析緩衝液中之 2-花生四烯酸甘油酯。分析中之最終濃度為 50 pM MAGL 及 8 µM 2-花生四烯酸甘油酯。在震盪且在室溫下培育 30 min 之後,藉由添加 40 µL 含有 4 µM d8-花生油酸之 ACN 來淬滅反應物。藉由耦接至三重四極質譜儀 (Agilent 6460) 之聯機 SPE 系統 (Agilent Rapidfire) 追蹤花生油酸之量。在 ACN/水液體設定中使用 C18 SPE 管匣 (G9205A)。以負電噴霧模式操作質譜儀,遵循以下質量轉移:花生四烯酸 303.1 à 259.1,且 d8-花生四烯酸 311.1 à 267.0。基於強度比[花生油酸 / d8-花生油酸]計算化合物之活性。
表 1
| 實施例 | IC50 MAGL [nM] |
| 1 | 0.2 |
| 2 | 0.02 |
| 3 | 75.4 |
| 4 | 2.5 |
| 5 | 23.8 |
| 6 | 132.8 |
| 7 | 0.5 |
| 8 | 4.3 |
| 9 | 0.9 |
| 10 | 2.3 |
| 11 | 42.9 |
| 12 | 23.5 |
| 13 | 12.7 |
| 14 | 13.4 |
| 15 | 0.11 |
| 16 | 0.05 |
| 17 | 0.10 |
| 18 | 0.05 |
| 19 | 0.01 |
| 20 | 0.06 |
| 21 | 0.03 |
| 22 | 0.06 |
| 23 | 0.2 |
| 24 | 0.04 |
| 25 | 4.2 |
| 26 | 3.9 |
| 27 | 0.3 |
| 28 | 6.3 |
| 29 | 90.9 |
| 30 | 0.7 |
| 31 | 91.9 |
| 32a | 0.2 |
| 32b | 6.5 |
| 33 | 2.7 |
| 34 | 22.9 |
| 35 | 17.4 |
| 36 | 0.9 |
| 37 | 2.4 |
| 38 | 8.5 |
| 39 | 6.7 |
| 40 | 73.1 |
| 41 | 24.6 |
| 42 | 153.2 |
| 43 | 19.3 |
| 44 | 67.7 |
| 45 | 133.7 |
| 46 | 17.5 |
| 47 | 1.4 |
| 48 | 31.5 |
| 49 | 2.4 |
| 50 | 4.3 |
| 51 | 123.8 |
| 52 | 1.3 |
| 53 | 12.9 |
| 54 | 10.4 |
| 55 | 10.3 |
| 56 | 15.5 |
| 57 | 17.8 |
| 58 | 1096.3 |
在一方面中,本發明提供如本文所揭示之式 (I) 化合物及其藥學上可接受之鹽類或酯類,其中,該等式 (I) 化合物及其藥學上可接受之鹽類或酯類具有低於 25 µM,較佳低於 10 µM,更佳低於 5 µM 之 MAGL 抑制之 IC50
,其如本文所述之 MAGL 分析中所量測。
在一具體實施方式中,如本文所揭示之式 (I) 化合物及其藥學上可接受之鹽類或酯類具有 0.000001 µM 與 25 µM 之間的 IC50
(MAGL抑制)值,特定化合物具有 0.000005 µM 與 10 µM 之間的 IC50
值,其他特定化合物具有 0.00005 µM 與 5 µM 之間的 IC50
值,如本文所述之 MAGL 分析中所量測。
使用本發明之化合物
在一方面中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用以作為治療活性物質。
在一進一步方面中,本發明提供如本文中所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物神經發炎、神經退化性疾病、疼痛、癌症、精神障礙、及/或發炎性腸病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物神經發炎及/或神經退化性疾病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物神經退化性疾病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物癌症。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物發炎性腸病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物疼痛。
在一方面中,本發明提供一種如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛、與疼痛相關的痙攣、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛的藥物。
在一較佳具體實施方式中,本發明提供一種如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物之多發性硬化症、阿滋海默症及/或帕金森病。
在一特佳具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於治療或預防哺乳動物多發性硬化症。
在一方面中,本發明提供如本文中所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物神經發炎、神經退化性疾病、疼痛、癌症、精神障礙、及/或發炎性腸病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物神經發炎及/或神經退化性疾病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物癌症。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物神經退化性疾病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物發炎性腸病。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物疼痛。
在一方面中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於製備供治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛、與疼痛相關的痙攣、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛的藥物。
在一較佳具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物之多發性硬化症、阿滋海默症及/或帕金森病。
在一特佳具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類,其用於治療或預防哺乳動物多發性硬化症。
在一方面中,本發明提供如本文中所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物神經發炎、神經退化性疾病、疼痛、癌症、精神障礙、及/或發炎性腸病的藥物。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物神經發炎及/或神經退化性疾病的藥物。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物神經退化性疾病的藥物。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物癌症的藥物。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物發炎性腸病的藥物。
在一具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物疼痛的藥物。
在一進一步方面中,本發明提供一種如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛、與疼痛相關的痙攣、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛的藥物。
在一較佳具體實施方式中,本發明提供一種如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備治療或預防哺乳動物之多發性硬化症、阿滋海默症及/或帕金森病的藥物。
在一特佳具體實施方式中,本發明提供如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類的用途,其用於製備供治療或預防哺乳動物多發性硬化症的藥物。
在一方面中,本發明提供一種用於治療或預防哺乳動物神經發炎、神經退化性疾病、疼痛、癌症、精神障礙、及/或發炎性腸病之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一具體實施方式中,本發明提供一種用於治療或預防哺乳動物神經發炎及/或神經退化性疾病之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一具體實施方式中,本發明提供一種用於治療或預防哺乳動物神經退化性疾病之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一具體實施方式中,本發明提供一種用於治療或預防哺乳動物癌症之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一具體實施方式中,本發明提供一種用於治療或預防哺乳動物發炎性腸病之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一具體實施方式中,本發明提供一種用於治療或預防哺乳動物疼痛之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一進一步方面中,本發明提供一種用於治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛、與疼痛相關的痙攣、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一較佳具體實施方式中,本發明提供一種用於治療或預防哺乳動物多發性硬化症、阿滋海默症及/或帕金森病之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
在一特佳具體實施方式中,本發明提供一種用於治療或預防哺乳動物多發性硬化症之方法,該方法包含將有效量之如本文所揭示之式 (I) 化合物或其藥學上可接受之鹽類投予該哺乳動物。
醫藥組成物及投予
在一方面中,本發明提供了一種醫藥組成物,其包含如本文中所述之式 (I) 化合物和治療上惰性之載劑。
在一具體實施方式中,係提供根據實施例 47 或 48 之醫藥組成物。
式 (I) 化合物及其藥學上可接受的鹽類和酯類可用以作為藥物(例如以藥物製劑的形式)。藥物製劑可以內部投予,諸如口服(例如以錠劑、包衣錠、糖衣錠、硬和軟明膠膠囊、溶液、乳劑或懸浮液的形式)、鼻內(例如以鼻噴霧劑的形式)或直腸(例如以栓劑的形式)。但是,投予亦可以腸胃外進行,諸如肌肉內或靜脈內(例如以注射溶液的形式)。
式 (I) 化合物及其藥學上可接受的鹽類和酯類可與藥學上惰性、無機或有機佐劑加工以製造錠劑、包衣錠、糖衣錠、及硬明膠膠囊。可例如使用乳糖、玉米澱粉或其衍生物、滑石、硬脂酸或其鹽等作為錠劑、糖衣錠及硬明膠膠囊之此等佐劑。
軟明膠膠囊之適合佐劑為例如植物油、蠟、脂肪、半固體物質及液體多元醇等。
用於產生溶液及糖漿之適合佐劑為例如水、多元醇、蔗糖、轉化糖、葡萄糖等。
注射溶液之適合佐劑為例如水、醇、多元醇、甘油、植物油等。
栓劑之適合佐劑為例如天然或硬化油、蠟、脂肪、半固體或液體多元醇等。
此外,藥物製劑可含有防腐劑、增溶劑、增黏物質、穩定劑、濕潤劑、乳化劑、甜味劑、著色劑、調味劑、用於改變滲透壓之鹽類、緩衝劑、掩蔽劑或抗氧化劑。其亦可還含有其他治療上有價值之物質。
劑量可在較寬界限內改變且當然將適合各特定情況下之個別要求。一般而言,在口服投予之情況下,分成較佳 1 至 3 個獨立劑量(其可由例如相同量組成)的約 0.1 mg 至 20 mg/kg 體重,較佳約 0.5 mg 至 4 mg/kg 體重(例如約 300 mg/個體)之每日劑量應為適當的。然而,應清楚,當顯示有所指示時,可超出本文中給出之上限。
實施例
藉由參照以下實施例將更充分地理解本發明。然而,申請專利範圍不應被解釋為限於實施例的範圍。
如果製備例為鏡像異構物的混合物,則純鏡像異構物可藉由本文所述方法或該發明所屬技術領域具有通常知識者已知的方法分離,諸如手性層析法(例如,手性 SFC)或結晶。
如果沒有另外說明,所有反應實施例和中間產物均在氬氣氣氛下製備。
方法
A1
實施例 1
(4aR,8aS)-6-(3-(4-苯氧基苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
於密封之試管內,將 (4aR,8aS)-6-[3-(4-溴苯基)四氫吖唉-1-羰基l]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]𠯤-3-酮(BB4 步驟 c,0.04 g,0.110 mmol)、苯酚 (0.014, 0.152 mmol)、Pd(OAc)2
(0.004 g, 0.016 mmol)、2-二-第三丁基膦-2′,4′,6′-三異丙基聯苯 (0.01 g, 0.024 mmol) 及 K3
PO4
(0.043 g, 0.203 mmol) 於甲苯 (0.68 mL) 中混合。該反應混合物於 100℃ 加熱過夜。該混合物以 EtOAc 稀釋,傾入水中,並使用 EtOAc 萃取水性層。有機層以鹽水(或稱滷水)洗滌,用 Na2
SO4
乾燥,過濾並蒸發。殘質藉由製備型 HPLC 純化以給出作為灰白色泡沫之標題化合物 (0.008, 17%)。MS (ESI): m/z = 408.2 [M+H]+
。
方法
A2
實施例 2
(4aR,8aS)-6-[3-[4-(2-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 [4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯基]硼酸(BB4,0.025 g,0.07 mmol)、2-氯苯酚 (0.027 g, 0.21 mmol) 及 TEA (0.043 mL, 0.42 mmol) 於 MeCN (2 mL) 中之溶液中加入 4A 分子篩 (0.03 g) 及無水醋酸銅 (0.038 g, 0.21 mmol)。反應混合物在 30℃ 於含氧大氣下攪拌 16 小時。混合物以 NH4OH (0.3 mL) 及 H2
O (2 mL) 淬滅,並使用 EtOAc (3 x 2 mL) 萃取。將合併之有機層蒸發至乾燥,殘質藉由製備型 HPLC 純化以獲得作為灰白色固體之標題產物 (0.007 g, 23%)。MS (ESI): m/z = 442.1 [M+H]+
。
方法
A3
實施例 3
(4aR,8aS)-6-[3-(4-嘧啶-2-基氧苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
於密封之試管內,將 (4aR,8aS)-6-[3-(4-羥基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (BB3, 0.05 g, 0.150 mmol)、2-氯-嘧啶 (0.026 g, 0.230 mmol, CAS RN 1722-12-9) 及碳酸鉀 (0.062 g, 0.450 mmol, CAS RN 584-08-7) 於 DMSO (2.5 mL) 中混合。然後將反應混合物於 80℃ 加熱 12 小時。該混合物以 EtOAc 稀釋,傾入水中,並使用 EtOAc 萃取水性層。有機層以鹽水(或稱滷水)洗滌,用 Na2
SO4
乾燥,過濾並蒸發。殘質藉由製備型 HPLC 純化以獲得作為白色固體之標題產物 (0.039 g, 63%)。MS (ESI): m/z = 410.4 [M+H]+
。
方法
A4
實施例 4
(4aR,8aS)-6-[3-[4-[(2-甲基-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
於密封之試管內,將 (4aR,8aS)-6-[3-(4-羥基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (BB3, 0.050 g, 0.150 mmol)、3-氟-2-甲基吡啶 (0.046 g, 0.410 mmol) 及Cs2
CO3
(0.197 g, 0.6 mmol) 於NMP (2 mL) 中混合。然後,將反應混合物在微波輻射下於 200℃ 加熱 1 小時。該混合物以 EtOAc 稀釋,傾入水中,並使用 EtOAc 萃取水性層。有機層以鹽水(或稱滷水)洗滌,用 Na2SO4 乾燥,過濾並蒸發。殘質藉由製備型 HPLC 純化以給出作為白色固體之所欲產物 (0.007 g, 11%)。MS (ESI): m/z = 423.1 [M+H]+
。
方法
B1
實施例 30
(4aR,8aS)-6-[3-[4-[(3,6-二甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向甲基硼酸 (0.014 g, 0.24 mmol)、K2
CO3
(0.066 g, 0.48 mmol) 及 (4aR,8aS)-6-[3-[4-[(3-溴-6-甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (0.06 g, 0.12 mmol) 於二㗁烷 (2 mL) 及水 (0.5 mL) 中之溶液加入 Pd(dppf)Cl2
(0.008 g, 0.01 mmol),並將反應混合物於 100℃ 加熱 12 小時。過濾該混合物,濾液用水 (10 mL) 稀釋並使用 EtOAc (3 x 5 mL) 萃取。合併之有機相以鹽水洗滌,用 Na2
SO4
乾燥,過濾並蒸發至乾燥。殘質藉由製備型 HPLC 純化以給出作為灰白色固體之標題產物 (0.009 g, 16%)。MS (ESI): m/z = 437.2 [M+H]+
。
步驟 a) (4aR,8aS)-6-[3-[4-[(3-溴-6-甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 (4aR,8aS)-6-[3-(4-羥基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (BB3, 0.1g, 0.3 mmol)、Cs2
CO3
(0.394 g, 1.21 mmol) 於 DMSO (5 mL) 中之溶液加入 3-溴-2-氟-6-甲基吡啶 (0.086 g, 0.45 mmol),並將反應混合物於 50℃ 加熱 12 小時。過濾該混合物,濾液藉由製備型 HPLC 純化以給出作為無色泡沫之標題產物 (0.08 g, 53%)。MS (ESI): m/z = 503.2 [M+2+H]+
。
表 2 中列述之下列實施例係類比於本文中揭示之方法藉由使用所指示之中間產物及商業化合物製備
表 2
| 實施例 | 系統名 / 結構 | 建構單元 (Building Block) | MS, m/z | 方法 |
| 5 | (+)-(4aR,8aS)-6-[3-[4-(4-甲基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 2-氯-4-甲基嘧啶 CAS RN 13036-57-2 | 424.4 [M+H]+ | A3 |
| 6 | (+)-(4aR,8aS)-6-[3-(4-嗒𠯤-3-基氧苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 鹽酸3-氯嗒𠯤 CAS RN 1120-95-2 | 410.1 [M+H]+ | A3 |
| 7 | (+)-(4aR,8aS)-6-[3-[4-[(4-甲基-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 3-氟-4-甲基吡啶 | 423.1 [M+H]+ | A4 |
| 8 | (+)-(4aR,8aS)-6-[3-[4-[(5-氟-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 3,5-二氟吡啶 | 427.1 [M+H]+ | A4 |
| 9 | (+)-(4aR,8aS)-6-[3-[4-[(5-氯-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 3-氯-5-氟吡啶 | 443.1 [M+H]+ | A4 |
| 10 | (+)-(4aR,8aS)-6-[3-[4-(3-吡啶氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 3-氟吡啶 | 409.1 [M+H]+ | A4 |
| 11 | (+)-(4aR,8aS)-6-[3-[4-(4-甲基嗒𠯤-3-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 3-氯-4-甲基嗒𠯤 CAS RN 68206-04-2 | 424.5 [M+H]+ | A3* * 加熱至 130℃ |
| 12 | (+)-(4aR,8aS)-6-[3-[4-(3-氯嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 3,4-二氯嗒𠯤 CAS RN 1677-80-1 | 444.4 [M+H]+ | A3 |
| 13 | (+)-(4aR,8aS)-6-[3-[4-(4-甲氧嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 2-氯-4-甲氧嘧啶 CAS RN 22536-63-6 | 440.4 [M+H]+ | A3 |
| 14 | (+)-(4aR,8aS)-6-[3-[4-[4-(三氟甲基)嘧啶-2-基]氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 2-氯-4-(三氟甲基)嘧啶 CAS RN 33034-67-2 | 478.3 [M+H]+ | A3 |
| 15 | (+)-(4aR,8aS)-6-[3-[4-(3-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 3-氟苯酚 | 426.2 [M+H]+ | A2 |
| 16 | (+)-(4aR,8aS)-6-[3-[4-(4-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 4-氟苯酚 | 426.1 [M+H]+ | A2 |
| 17 | (+)-(4aR,8aS)-6-[3-[4-(2,4-二氟苯氧)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 2,4-二氟苯酚 | 444.1 [M+H]+ | A2 |
| 18 | (+)-(4aR,8aS)-6-[3-[4-(2-氟苯氧)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 2-氟苯酚 | 442.1 [M+H]+ | A2 |
| 19 | (+)-(4aR,8aS)-6-[3-[4-(4-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 4-氯苯酚 | 426.1 [M+H]+ | A2 |
| 20 | (+)-(4aR,8aS)-6-[3-[4-(3-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 3-氯苯酚 | 442.1 [M+H]+ | A2 |
| 21 | (+)-(4aR,8aS)-6-[3-[4-(2-甲基苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 2-甲基苯酚 | 422.2 [M+H]+ | A2 |
| 22 | (+)-(4aR,8aS)-6-[3-[4-[3-(三氟甲基)苯氧基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB4 和 3-三氟甲基苯酚 | 476.2 [M+H]+ | A2 |
| 23 | (+)-2-[4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯氧基]苯甲腈 | BB3 和 2-氟苯甲腈 | 433.2 [M+H]+ | A4* * 於 25℃ 攪拌 無微波 |
| 24 | (+)-(4aR,8aS)-6-[3-[4-(2-氯嘧啶-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 4-溴-2-氯嘧啶 CAS RN 885702-34-1 | 444.2 [M+H]+ | A3* * 於 25℃ 在 DMF 中攪拌 |
| 25 | (+)-(4aR,8aS)-6-[3-[4-(4-環丙基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 2-氯-4-環丙基嘧啶 CAS RN 954237-31-1 | 450.4 [M+H]+ | A3* * 於 50℃ 在 DMF 中加熱 |
| 26 | (+)-(4aR,8aS)-6-[3-[4-[(6-甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 2-氟-6-甲基吡啶 | 423.2 [M+H]+ | B1 步驟 a) |
| 27 | (+)-(4aR,8aS)-6-[3-[4-[(4-氯-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 4-氯-3-氟吡啶 | 443.1 [M+H]+ | A4* * 加熱至 100°C |
| 28 | (+)-(4aR,8aS)-6-[3-[4-[(3-氟-4-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 4-氯-3-氟吡啶 | 427.1 [M+H]+ | A4* * 加熱至 100°C |
| 29 | (+)-(4aR,8aS)-6-[3-[4-(2-甲基磺醯基嘧啶-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 | BB3 和 4-氯-2-(甲基磺醯基)嘧啶 CAS RN 97229-11-3 | 488.1 [M+H]+ | A3* * 於 0°C 在 DMF 中攪拌 |
實施例 31
(4aR,8aS)-6-[3-[4-(1H-吡唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 3-(4,4,5,5-四甲基-1,3,2-二㗁環戊硼烷-2-基)-1H-吡唑 (147.7 mg, 0.760 mmol; CAS RN 269410-08-4)、(4aR,8aS)-6-[3-(4-溴苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮(BB4 步驟 c,200.0 mg,0.510 mmol)及 K2
CO3
(140.22 mg, 1.01 mmol) 於 1,4-二㗁烷 (10 mL) 及水 (2 mL) 中之溶液加入 Pd(dppf)Cl2
(66.12 mg, 0.100 mmol, CAS RN 12150-46-8),並將該混合物於 90℃ 攪拌 12 h。過濾該混合物並蒸發濾液。殘質藉由製備型 HPLC(0.225% v/v FA 於水及 ACN 中)以給出作為灰白色固體之所欲產物 (6.5 mg, 0.020 mmol, 3.3%)。MS (ESI): m/z = 382.4 [M+H]+
。
實施例 32a 及 32b
(4aR,8aS)-6-[3-[4-[2-(2,2-二甲基丙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮,以及
(4aR,8aS)-6-[3-[4-[1-(2,2-二甲基丙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
將 (4aR,8aS)-6-[3-[4-(1H-吡唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮(實施例 31,140.0 mg,0.370 mmol)、1-溴-2,2-二甲基丙烷 (110.88 mg, 0.730 mmol) 及 Cs2
CO3
(239.18 mg, 0.730 mmol) 於 DMF (2.6 mL) 中之溶液於 80℃ 攪拌 12 h。該混合物以水稀釋,並使用 EtOAc 萃取三次(每次 10 mL)。合併之有機層用 Na2
SO4
乾燥,過濾並蒸發。殘質藉由製備型 HPLC(0.225% v/v FA 於水及 ACN 中)純化以及位置異構物分離,以給出各自作為淺黃色固體之實施例HR1 (2.5 mg, 0.010 mmol, 2.6%) 及實施例HR2 (31.4 mg, 0.070 mmol, 32.5%)。對於兩種位置異構物,MS (ESI): m/z =452.3 [M+H]+
。
實施例 33
(4aR,8aS)-6-[3-[4-(3-氯-2-吡啶基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向三丁基-(3-氯-2-吡啶基)錫烷 (122.5 mg, 0.300 mmol, CAS RN 206357-78-0) 及 (4aR,8aS)-6-[3-(4-溴苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮(BB4 步驟 c,100.0 mg,0.250 mmol)於 DMF (5 mL) 中之溶液加入 Pd(PPh3
)4
(58.64 mg, 0.050 mmol),並將該混合物於 100℃ 於 N2
氣氛下攪拌 12 h。將該混合物傾入水 (20 mL) 中,並使用 EtOAc 萃取三次(每次 5 mL)。合併之有機層以鹽水洗滌,用 Na2
SO4
乾燥,過濾並蒸發濾液。殘質先後經反相快速管柱層析(0.1% v/v FA 於水及 ACN 中)及製備型 HPLC(0.225% v/v FA 於水及 ACN 中)純化以獲得作為白色固體之所欲化合物(2.8 mg,99.4% 純度,2.6%)。MS (ESI): m/z = 427.2 [M+H]+
。
步驟 a) 三丁基-(3-氯-2-吡啶基)錫烷
於 N2
下,於 -78℃ 向 2-溴-3-氯吡啶 (576.0 mg, 2.99 mmol, CAS RN 96424-68-9) 於甲苯 (20 mL) 中之溶液逐滴加入 n-BuLi 於己烷中之溶液 (2.5M, 1.32 mL, 3.29 mmol)。將該反應混合物於 -78℃ 攪拌 2 h,之後加入氯化三丁基錫 (1071.73 mg, 3.29 mmol)。將反應混合物於 -78℃ 再攪拌 2 h,然後升溫至室溫,並再攪拌 12h。反應用飽和 NH4
C1 水溶液 (50 mL) 淬滅。混合物用 EtOAc 萃取三次(每次 30 mL),合併之有機層用鹽水洗滌,用 Na2
SO4
乾燥,並過濾。濾液經真空濃縮以得到作為淺黃色油之所欲產物 (1100 mg, 2.73 mmol, 91.3%),其係不經進一步純化而用於下一步驟。MS (ESI): m/z = 404.1 [M+H]+
。
實施例 34
(4aR,8aS)-6-[3-[4-(2,4-二甲基㗁唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 (4aR,8aS)-6-[3-[4-(4,4,5,5-四甲基-1,3,2-二㗁環戊硼烷-2-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮(BB4 步驟 d,80.0 mg,0.180 mmol)、Na2
CO3
(38.42 mg, 0.360 mmol) 及 5-溴-2,4-二甲基㗁唑 (31.91 mg, 0.180 mmol, CAS RN 187399-73-1) 於 1,4-二㗁烷 (4 mL) 及水 (1 mL) 中之溶液加入 [1,1'-雙(二苯基膦)二茂鐵]二氯鈀(II) (13.3 mg, 0.020 mmol),並將該混合物在 100℃ 於氮氣氛下攪拌 12 h。將該混合物傾入水 (20 mL) 中,並使用 EtOAc 萃取三次(每次 10 mL)。合併之有機層以鹽水洗滌,用 Na2
SO4
乾燥,過濾並濃縮濾液。殘質藉由製備型 HPLC(0.5% 氨於水及 ACN 中)純化以得到作為粉色固體之所欲化合物 (23.7 mg, 0.060 mmol, 30.6%)。MS (ESI): m/z = 411.2 [M+H]+
。
實施例 35
(4aR,8aS)-6-[3-[4-(3,5-二甲基吡唑-1-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 1-[4-(四氫吖唉-3-基)苯基]-3,5-二甲基吡唑 (三氟乙酸鹽) (150.0 mg, 0.440 mmol) 於 ACN (5 mL) 中之溶液先後加入 DIPEA (340.14 mg, 2.64 mmol) 及 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (169.43 mg, 0.530 mmol, BB2a),並將該反應混合物於 80℃ 攪拌 12 h。濃縮該溶液,殘質藉由製備型 HPLC(0.225% v/v TFA 於水及 ACN 中)以給出作為淺黃色固體之所欲產物(53.9 mg,0.130 mmol,27.7%,純度 92.4%)。MS (ESI): m/z = 410.0 [M+H]+
。
步驟 a) 1-(4-溴苯基)-3,5-二甲基吡唑
將 (4-溴苯基)肼 (500.0 mg, 2.67 mmol, CAS RN 41931-18-4) 及乙醯丙酮 (294.41 mg, 2.94 mmol, CAS RN 123-54-6)、三水合硝酸銅(II) (128.31 mg, 0.530 mmol, CAS RN 10031-43-3) 於 ACN (12 mL) 中之溶液於 20℃ 攪拌 2 h。該混合物以 EtOAc (20 mL) 稀釋並先後以水及鹽水洗滌,有機相用 Na2
SO4
乾燥並濃縮。殘質藉由矽膠管柱層析 (PE : EtOAc = 20 : 1) 純化以給出作為淺黃色油之所欲產物 (400 mg, 1.59 mmol, 71.2%)。MS (ESI): m/z = 251.0 [M+H]+
。
步驟 b) 3-[4-(3,5-二甲基吡唑-1-基)苯基]四氫吖唉-1-甲酸第三丁酯
向配備攪拌棒之 40 mL 小瓶內加入 3-溴四氫吖唉-1-甲酸第三丁酯 (329.08 mg, 1.39 mmol, CAS RN 1064194-10-0)、1-(4-溴苯基)-3,5-二甲基吡唑 (350.0 mg, 1.39 mmol, CAS RN 62546-27-4)、Ir[dF(CF3
)ppy]2
(dtbbpy)PF6
(7.81 mg, 0.010 mmol)、NiCl2
·glyme (1.84 mg, 0.010 mmol)、4-第三丁基-2-(4-第三丁基-2-吡啶基)吡啶 (2.24 mg, 0.010 mmol)、雙(三甲基矽基)矽基-三甲基-矽烷 (346.57 mg, 1.39 mmol)、Na2
CO3
(295.45 mg, 2.79 mmol) 以及然後之 DME (10 mL)。將小瓶密封並置於氮氣下。攪拌該反應混合物並使用 34 W 藍光 LED 燈(7 cm 距離)照射,同時吹冷風扇以將該反應溫度保持在 25℃,持續 14 h。過濾該混合物並濃縮濾液。殘質藉由反相快速管柱層析(0.1% v/v FA 於水及 ACN 中)純化以給出作為黃色油之所欲產物 (300 mg, 0.920 mmol, 65.7%)。MS (ESI): m/z = 328.1 [M+H]+。
步驟 c) 1-[4-(四氫吖唉-3-基)苯基]-3,5-二甲基吡唑,三氟乙酸鹽
向 3-[4-(3,5-二甲基吡唑-1-基)苯基]四氫吖唉-1-甲酸第三丁酯 (150.0 mg, 0.460 mmol) 於 DCM (5 mL) 中之溶液加入 TFA (1.0 mL)。混合物於 20℃ 攪拌 3 h,然後濃縮以給出作為黃色油之粗製所欲產物 (150 mg, 0.440 mmol, 95.9%)。MS (ESI): m/z = 228.1 [M+H]+
。
實施例 36
(4aR,8aS)-6-[3-[4-[3-(2,2-二甲基丙基)三唑-4-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
將 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (66.2 mg, 0.210 mmol, BB2a)、DIPEA (241.9 mg, 1.87 mmol) 及 5-[4-(四氫吖唉-3-基)苯基]-1-(2,2-二甲基丙基)三唑三氟乙酸鹽 (72.0 mg, 0.190 mmol) 於 ACN (3 mL) 中之混合物於 80℃ 攪拌 12 h。將該混合物於減壓下濃縮,殘質藉由製備型 HPLC(0.025 % FA 於水及 ACN 中)純化以給出作為淺黃色油之所欲化合物 (18 mg, 0.040 mmol, 20.5%)。MS (ESI): m/z = 453.0 [M+H]+
。
步驟 a) 1-疊氮基-4-硝基苯
將 4-硝基苯胺 (2000.0 mg, 14.48 mmol) 溶解於 ACN (20 mL),將該混合物於冰鹽浴中冷卻至 0℃。於攪拌下向該溶液加入亞硝酸第三丁酯 (1791.8 mg, 17.38 mmol),並將該混合物攪拌 10 min。然後逐滴加入疊氮基三甲基矽烷 (2.88 mL, 21.72 mmol),將所得褐色溶液於 25℃ 攪拌 2 h。將反應混合物傾入水 (100 mL) 中,使用 EtOAc 萃取三次(每次 100 mL),並在減壓下蒸發有機層。殘質藉由矽膠管柱層析 (100% PE) 純化以給出作為黃色固體之 1-疊氮基-4-硝基苯 (2100 mg, 12.64 mmol, 87.3)。
步驟 b) 5-(4-溴苯基)-1-(2,2-二甲基丙基)三唑
向 4'-溴苯乙酮 (1940.4 mg, 9.75 mmol)、新戊基胺 (1104.6 mg, 12.67 mmol)、1-疊氮基-4-硝基苯 (1600.0 mg, 9.75 mmol)、AcOH (175.6 mg, 2.92 mmol) 於甲苯 (64 mL) 中之溶液加入分子篩 (4Å, 500 mg),並將該反應於 100℃ 攪拌 16 h。過濾該反應混合物,並於減壓下蒸發濾液。殘質藉由管柱層析 (PE : EA = 3 : 1) 純化以給出作為黃色膠之所欲化合物 (997 mg, 3.39 mmol, 34.8%)。
步驟 c) 3-[4-[3-(2, 2-二甲基丙基)三唑-4-基]苯基]四氫吖唉-1-甲酸第三丁酯
類比於實施例 35 步驟 b),從 5-(4-溴苯基)-1-(2,2-二甲基丙基)三唑及 3-溴四氫吖唉-1-甲酸第三丁酯製備標題化合物。黃色膠 (75.9%)。MS (ESI): m/z = 371.0 [M+H]+
。
步驟 c) 5-[4-(四氫吖唉-3-基)苯基]-1-(2, 2-二甲基丙基)三唑三氟乙酸鹽
向 3-[4-[3-(2,2-二甲基丙基)三唑-4-基]苯基]四氫吖唉-1-甲酸第三丁酯 (70.0 mg, 0.190 mmol) 於 DCM (2 mL) 中之溶液加入 TFA (0.5 mL)。將該混合物於 20℃ 攪拌 12 h,然後於減壓下蒸發以給出作為黃色油之粗製所欲化合物 (72 mg, 0.190 mmol, 99.1%)。MS (ESI): m/z = 270.9 [M+H]+
。
實施例 37
(4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 3-[4-(四氫吖唉-3-基)苯基]-5-(2,2-二甲基丙基)-1,2,4-㗁二唑三氟乙酸鹽 (150.0 mg, 0.390 mmol) 於 ACN (4 mL) 中之溶液加入 DIPEA (301.3 mg, 2.34 mmol) 及 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (150.07 mg, 0.470 mmol, BB2a),並將該反應於 80℃ 攪拌 12 h。蒸發該反應混合物,殘質藉由製備型 HPLC(0.225% v/v FA 於水及 ACN 中)純化以給出作為淺黃色固體之所欲產物 (54.4 mg, 0.120 mmol, 30.4%)。MS (ESI): m/z = 454.4 [M+H]+
。
步驟 a) 3-(4-氰基苯基)四氫吖唉-1-甲酸第三丁酯
類比於實施例 35 步驟 b),從 4-溴苯甲腈及 3-溴四氫吖唉-1-甲酸第三丁酯製備標題化合物。淺褐色油 (1976 mg, 7.65 mmol, 69.6%)。MS (ESI): m/z = 203.6 [M-56+H]+
。
步驟 b) 3-[4-(N-羥基胺基亞胺醯基)苯基]四氫吖唉-1-甲酸第三丁酯
向鹽酸羥胺e (349.7 mg, 5.03 mmol) 於 EtOH (8 mL) 中之溶液加入 Na2CO3 (266.7 mg, 2.52 mmol) 於水 (2 mL) 中之溶液,並將混合物於 20℃ 攪拌 25 min。然後加入 3-(4-氰基苯基)四氫吖唉-1-甲酸第三丁酯 (1000.0 mg, 3.87 mmol),並將混合物於 95℃ 攪拌 12 h。混合物以水稀釋,於真空下濃縮以去除 EtOH,殘質於 EtOAc (100 mL) 與水 (100 mL) 之間分割,並使用水萃取三次。有機層用飽和 NaCl 溶液 (50 mL) 洗滌,用 Na2
SO4
乾燥,並蒸發以給出作為淺黃色油之所欲產物 (773 mg, 2.65 mmol, 68.5%)。MS (ESI): m/z = 292.5 [M+H]+
。
步驟 c) 3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-甲酸第三丁酯
於 0℃ 向 3-[4-(N-羥基胺基亞胺醯基)苯基]四氫吖唉-1-甲酸第三丁酯 (770.0 mg, 2.64 mmol) 及 DIPEA (1.41 mL, 7.93 mmol) 於甲苯 (6 mL) 中之溶液加入 3,3-二甲基丁醯氯 (426.9 mg, 3.17 mmol),將混合物於 25℃ 攪拌 10 min,然後升溫至 80℃ 並攪拌 12 h。蒸發該混合物,殘質藉由矽膠管柱層析 (PE : EA = 10 : 1) 純化以給出作為淺褐色油之所欲產物 (620 mg, 1.67 mmol, 63.2%)。MS (ESI): m/z =316.5 [M-56+H]+
。
步驟 c) 3-[4-(四氫吖唉-3-基)苯基]-5-(2,2-二甲基丙基)-1,2,4-㗁二唑(三氟乙酸鹽)
向 3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-甲酸第三丁酯 (300.0 mg, 0.810 mmol) 於 DCM (3 mL) 中之溶液加入 TFA (0.6 mL, 7.79 mmol),將混合物於 20℃ 攪拌 12 h。蒸發該混合物以獲得作為淺黃色油之粗製所欲產物 (300 mg, 0.780 mmol, 96.4%)。MS (ESI): m/z = 272.6 [M+H]+
。
實施例 38
(4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,3,4-㗁二唑-2-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 2-[4-(四氫吖唉-3-基)苯基]-5-(2,2-二甲基丙基)-1,3,4-㗁二唑三氟乙酸鹽 (100.0 mg, 0.260 mmol) 於 ACN (2.5 mL) 中之溶液加入 DIPEA (200.8 mg, 1.56 mmol) 及 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (100.04 mg, 0.310 mmol, BB2a),並將該反應於 80℃ 攪拌 12 h。蒸發縮該溶液,殘質藉由製備型 HPLC(0.225% v/v FA 於水及 ACN 中)以給出作為淺黃色固體之所欲產物 (48.3 mg, 0.110 mmol, 40.6%)。MS (ESI): m/z = 454.3 [M+H]+
。
步驟 a) 4-溴-N'-(3,3-二甲基丁醯基)苯甲醯肼
於 0℃ 向 4-溴苯甲醯肼 (5.0 g, 23.25 mmol, CAS RN 5933-32-4) 及 DIPEA (12.4 mL, 69.75 mmol, CAS RN 7087-68-5) 於 DCM (50 mL) 中之溶液加入 3,3-二甲基丁醯氯 (3.76 g, 27.9 mmol, CAS RN 122-94-1),令該混合物升溫至 20℃。於攪拌 12 h 後,該混合物以水稀釋,使用 EtOAc 萃取三次(每次 200 mL),合併之有機層用水洗滌三次(每次 100 mL)。合併之有機層用 Na2
SO4
乾燥,過濾並蒸發以給出作為淺黃色油之所欲產物 (7 g, 22.4 mmol, 96.1%)。MS (ESI): m/z = 315.4 [M+H]+
。
步驟 b) 2-(4-溴苯基)-5-(2,2-二甲基丙基)-1,3,4-㗁二唑
向 4-溴-N'-(3,3-二甲基丁醯基)苯甲醯肼 (5000.0 mg, 16.0 mmol) 於甲苯 (102 mL) 中之溶液加入 TsOH (5498.3 mg, 31.9 mmol),將混合物於 110℃ 攪拌 12 h。將該混合物濃縮,殘質藉由以 PE : EtOAc (10 : 1) 洗脫之矽膠管柱層析純化以給出作為淺黃色固體之所欲產物 (1000 mg, 3.4 mmol, 21.2%)。MS (ESI): m/z = 295.4 [M+H]+
。
步驟 c) 3-[4-[5-(2,2-二甲基丙基)-1,3,4-㗁二唑-2-基]苯基]四氫吖唉-1-甲酸第三丁酯
類比於實施例 35 步驟 b),從 2-(4-溴苯基)-5-(2,2-二甲基丙基)-1,3,4-㗁二唑及 3-溴四氫吖唉-1-甲酸第三丁酯製備標題化合物。淺褐色油。MS (ESI): m/z = 372.5 [M+H]+
。
步驟 c) 2-[4-(四氫吖唉-3-基)苯基]-5-(2,2-二甲基丙基)-1,3,4-㗁二唑(三氟乙酸鹽)
向 3-[4-[5-(2,2-二甲基丙基)-1,3,4-㗁二唑-2-基]苯基]四氫吖唉-1-甲酸第三丁酯 (200.0 mg, 0.540 mmol) 於 DCM (2 mL) 中之溶液加入 TFA (0.4 mL),將混合物於 20℃ 攪拌 12 h。蒸發該混合物以給出作為淺褐色油之粗製所欲產物 (201 mg, 0.520 mmol, 96.9%)。MS (ESI): m/z = 272.6 [M+H]+
。
實施例 39
(4aR,8aS)-6-[3-[4-[2-(2-氟乙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
於攪拌下,於 60℃ 向 5-[4-(四氫吖唉-3-基)苯基]-1-(2-氟乙基)吡唑 (110 mg, 0.380 mmol) 及 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (124 mg, 0.390 mmol, BB2a) 於 MeCN (6 mL) 中之溶液加入 N,N-二異丙基乙胺 (0.2 mL, 1.15 mmol)。將溶液於 60℃ 攪拌 16 h。於真空下濃縮該溶液以給出殘質,殘質藉由 HPLC(TFA 條件)純化以給出作為白色固體之 (4aR,8aS)-6-[3-[4-[2-(2-氟乙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (80 mg, 45%)。MS (ESI): m/z = 428.4 [M+H]+
。
步驟 a) 5-(4-溴苯基)-1-(2-氟乙基)吡唑
於攪拌下,於 20℃ 向 2-氟乙基聯胺 (330 mg, 4.23 mmol, CAS RN 126889-84-7) 於 DMF (20 mL) 中之溶液加入 (E)-1-(4-溴苯基)-3-(二甲基胺基)丙-2-烯-1-酮 (752 mg, 2.96 mmol, CAS RN 849619-11-0)。所得混合物於 25℃ 攪拌 1 h,然後於 70℃ 攪拌 5 h。於真空下濃縮該溶液以給出殘質,殘質藉由快速管柱層析(石油醚 : EtOAc 3:1)純化以給出作為白色固體之 5-(4-溴苯基)-1-(2-氟乙基)吡唑 (450 mg, 39%)。MS (ESI): m/z = 269.0/271.0 [M+H]+
。
步驟 b) 3-[4-(2-(2-氟乙基)吡唑-3-基)苯基]四氫吖唉-1-甲酸第三丁酯
將 3-溴四氫吖唉-1-甲酸第三丁酯 (395 mg, 1.67 mmol, CAS RN 1064194-10-0)、 5-(4-溴苯基)-1-(2-氟乙基)吡唑 (450 mg, 1.67 mmol)、[Ir{dF(CF3
)ppy}2
(dtbpy)]PF6
(19 mg, 0.020 mmol, CAS RN 870987-63-6)、二氯鎳 1,2-二甲氧基乙烷 (2.0 mg, 0.010 mmol)、4-第三丁基-2-(4-第三丁基-2-吡啶基)吡啶 (3.0 mg, 0.010 mmol)、雙(三甲基矽基)矽基三甲基-矽烷 (416 mg, 1.67 mmol) 及碳酸鈉 (355 mg, 3.35 mmol) 混合於 DME (15 mL) 中。攪拌該反應混合物並使用 34 W 藍光 LED 燈(7 cm 遠)照射,同時吹冷風扇以將該反應溫度保持在 25℃,持續 14 h。將該溶液傾入鹽水 (30 mL) 中並使用 EtOAc (20 mL) 萃取。於真空下濃縮有機層以給出殘質,殘質藉由製備型 TLC(石油醚 : EtOAc 1:1)純化以給出作為淺黃色油之 3-[4-[2-(2-氟乙基)吡唑-3-基]苯基]四氫吖唉-1-甲酸第三丁酯 (450 mg, 69%)。MS (ESI): m/z = 346.1 [M+H]+
。
步驟 c) 5-[4-(四氫吖唉-3-基)苯基]-1-(2-氟乙基)吡唑
將 3-[4-[2-(2-氟乙基)吡唑-3-基]苯基]四氫吖唉-1-甲酸第三丁酯 (160 mg, 0.410 mmol) 於 MeOH 中 HCl (4.0 mL, 16 mmol) 中之溶液於 25℃ 攪拌 4 h。於真空下濃縮該溶液以給出作為淺黃色油之 5-[4-(四氫吖唉-3-基)苯基]-1-(2-氟乙基)吡唑 (110 mg, 92%),其係不經進一步純化而用於下一步驟中。MS (ESI): m/z = 246.1 [M+H]+
。
實施例 40
(4aR,8aS)-6-[3-[4-[1-(2-氟乙基)吡唑-4-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
於氮氣氛下,將 1-(2-氟乙基)-4-(4,4,5,5-四甲基-1,3,2-二㗁環戊硼烷-2-基)吡唑 (58 mg, 0.24 mmol, CAS RN 1049730-39-3)、(4aR,8aS)-6-(3-(4-溴苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮(BB4 步驟 c,80 mg,0.20 mmol)、K2
CO3
(2.0 mg, 0.02 mmol)、Cs2
CO3
(198 mg, 0.610 mmol) 及 [1,1'-雙(二苯基膦)二茂鐵]二氯鈀(II) (15 mg, 0.02 mmol) 於 DMSO (4 mL) 及 H2
O (0.5 mL) 中之混合物於 80℃ 攪拌 16 h。過濾該混合物,然後藉由製備型 HPLC(鹼性條件)純化以給出作為灰色固體之標題化合物 (41 mg, 44%)。LC-MS:428.2 [M+H]+
。
實施例 41
(4aR,8aS)-6-[3-[4-(4-甲基-1,3-噻唑-2-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 31 中間產物,從 (4aR,8aS)-3-側氧基六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-6(5H)-甲酸4-硝基苯酯及 2-(4-(四氫吖唉-3-基)苯基)-4-甲基噻唑 4-甲基苯磺酸鹽製備標題化合物。無色泡沫 (37%)。MS (ESI): m/z = 413.3 [M+H]+
。
步驟 a) 3-(4-(4-甲基噻唑-2-基)苯基)四氫吖唉-1-甲酸第三丁酯
類比於 BB4 步驟 a),從 4-甲基-2-(4-(4,4,5,5-四甲基-1,3,2-二㗁環戊硼烷-2-基)苯基)噻唑 (Maybridge) 及 3-碘四氫吖唉-1-甲酸第三丁酯 (CAS RN 254454-54-1) 製備標題化合物。無色油,其係不經進一步純化而用於下一步驟中。MS (ESI): m/z = 331.2 [M+H]+
。
步驟 b) 2-[4-(四氫吖唉-3-基)苯基]-4-甲基噻唑;4-甲基苯磺酸
於回流下,將 3-(4-(4-甲基噻唑-2-基)苯基)四氫吖唉-1-甲酸第三丁酯 (28 mg, 84.7 µmol) 及 4-甲苯磺酸水合物 (19.3 mg, 102 µmol) 於 EtOAc (0.3 mL) 中之懸浮液攪拌 2 h。將混合物完全蒸發以提供所欲化合物,其係不經進一步純化而用於下一步驟中。MS (ESI): m/z = 231.1 [M+H]+
。
實施例 42
(4aR,8aS)-6-[3-[4-(1-甲基吡唑-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
將 (4aR,8aS)-6-(3-(4-溴苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮(16 mg,40.6 µmol,BB4,步驟 c)及 (1-甲基-1H-吡唑-3-基)硼酸 (5.11 mg, 40.6 µmol, CAS RN 869973-96-6)、以及肆(三苯基膦)鈀(0) (2.34 mg, 2.03 µmol) 溶解於 THF (600 µL) 及水 (60 µl) 中,並將該反應於 80℃ 攪拌過夜。反應混合物以 EtOAc 及 H2
O 萃取,有機層用 Na2
SO 乾燥並蒸發。粗產物藉由製備型 HPLC 純化以給出作為白色固體之化合物。MS (ESI): m/z = 396.2 [M+H]+
。
實施例 43
(4aR,8aS)-6-[3-[4-(6-氟吡啶-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 42,從下述者製備標題化合物:(4aR,8aS)-6-(3-(4-溴苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮(BB4,步驟 c)及 2-氟吡啶-5-硼酸 (CAS RN: 351019-18-6)。白色固體。MS (ESI): m/z = 411.2 [M+H]+
。
實施例 44
(4aR,8aS)-6-[3-[4-(2-氟吡啶-4-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 42,從下述者製備標題化合物:(4aR,8aS)-6-(3-(4-溴苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮(BB4, 步驟 c)及(2-氟吡啶-4-基)硼酸 (CAS RN: 401815-98-3)。黃色粉末 (84%)。MS (ESI): m/z = 411.2 [M+H]+
。
實施例 45
(4aR,8aS)-6-[3-[4-(1-甲基吡唑-4-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 42,從下述者製備標題化合物:(4aR,8aS)-6-(3-(4-溴苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮(BB4,步驟 c)及 1-甲基-1H-吡唑-4-硼酸 (CAS RN: 763120-58-7)。淺黃色粉末 (57%)。MS (ESI): m/z = 396.2 [M+H]+
。
實施例 46
(4aR,8aS)-6-[3-[4-(2-甲基吡唑-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 31 中間產物,從 (4aR,8aS)-3-側氧基六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-6(5H)-甲酸4-硝基苯酯及 5-(4-(四氫吖唉-3-基)苯基)-1-甲基-1H-吡唑 4-甲基苯磺酸鹽製備標題化合物。無色固體 (25%)。MS (ESI): m/z = 396.2 [M+H]+
。
步驟 a) 3-[4-(2-甲基吡唑-3-基)苯基]四氫吖唉-1-甲酸第三丁酯
類比於實施例 BB4 步驟 a,從 3-碘四氫吖唉-1-甲酸第三丁酯 (CAS RN 254454-54-1) 及 (4-(1-甲基-1H-吡唑-5-基)苯基)硼酸(恆橋產業股份有限公司 (ChemBridge Corp.))製備標題化合物。無色油,其係不經進一步純化而用於下一步驟中。MS (ESI): m/z = 314.3 [M+H]+
。
步驟 b) 5-[4-(四氫吖唉-3-基)苯基]-1-甲基吡唑;4-甲基苯磺酸
類比於實施例 41 步驟 b,從 3-[4-(2-甲基吡唑-3-基)苯基]四氫吖唉-1-甲酸第三丁酯製備標題化合物。淺褐色膠。MS (ESI): m/z = 214.1 [M+H]+
。
實施例 47
(4aR,8aS)-6-[3-[5-(4-氟苯氧)-2-吡啶基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
於 25℃ 向 2-(四氫吖唉-3-基)-5-(4-氟苯氧基)吡啶 (50 mg, 0.17 mmol) 及 DIPEA (0.17 mL, 1.04 mmol) 於 ACN (2 mL) 中之溶液加入 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (67 mg, 0.21 mmol, BB2a)。將混合物於 90℃ 攪拌 12 h,於減壓下濃縮,藉由製備型 HPLC (0.225% TFA) 純化並凍乾以給出作為淺黃色固體之標題化合物(22.1 mg, 0.050 mmol, 28.5% 產率)。MS (ESI): m/z = 427.2 [M+H]+
。
步驟 a) 3-[5-(4-氟苯氧基)-2-吡啶基]-3-羥基四氫吖唉-1-甲酸第三丁酯
將 2-溴-5-(4-氟苯氧基)吡啶 (350 mg, 1.31 mmol, CAS RN 1643917-85-4) 溶解於甲苯 (15 mL) 中並冷卻至 -78℃。逐滴加入 nBuLi 於己烷中之溶液 (0.57 mL, 1.44 mmol),將該混合物於 N2 氣氛下於 -78℃ 攪拌 30 分鐘。加入 1-Boc-3-四氫吖唉酮 (246 mg, 1.44 mmol, CAS RN 398489-26-4) 於甲苯 (2 mL) 中。將反應混合物於 0℃ 攪拌 4 h,以飽和 NH4Cl (20 mL) 淬滅並使用 EtOAc (2 x 15 mL) 萃取。合併之萃取物以鹽水 (20 mL) 洗滌,用 Na2SO4 乾燥,於真空下濃縮,並藉由反相快速層析純化以給出作為白色固體之標題化合物(171 mg, 0.470 mmol, 36.3% 產率)。MS (ESI): m/z = 361.2 [M+H]+
。
步驟 b) 3-氯-3-[5-(4-氟苯氧基)-2-吡啶基]四氫吖唉-1-甲酸第三丁酯
於 0℃ 向 3-[5-(4-氟苯氧基)-2-吡啶基]-3-羥基-四氫吖唉-1-甲酸第三丁酯 (500 mg, 1.39 mmol) 於 DCM (15 mL) 中之溶液加入亞硫醯氯 (990 mg, 8.32 mmol)。將混合物於 20℃ 攪拌 12 h,傾入飽和 Na2
CO3
(15 mL) 中,並使用 DCM (3 x 10 mL) 萃取。合併之有機層以鹽水 (20 mL) 洗滌,用 Na2
SO4
乾燥,於真空下濃縮,並藉由反相快速層析 (0.05% TFA) 純化以給出作為淺黃色油之標題化合物(230 mg, 0.610 mmol, 43.8% 產率)。MS (ESI): m/z = 322.8 [M-C4H8+H]+
。
步驟 c) 2-(四氫吖唉-3-基)-5-(4-氟苯氧基)吡啶
向 3-氯-3-[5-(4-氟苯氧基)-2-吡啶]四氫吖唉-1-甲酸第三丁酯 (200 mg, 0.530 mmol) 及甲酸 (121 mg, 2.64 mmol) 於乙醇 (12 mL) 中之溶液加入濕 Pd/C (100 mg, 0.530 mmol)。將混合物於 50℃ 攪拌 12 h 並過濾。於真空下蒸發濾液以給出黃色殘質,殘質藉由反相快速層析 (0.05% TFA) 純化以給出作為無色油之標題化合物(50 mg, 0.200 mmol, 38.8% 產率)以及作為淺褐色油之 3-[5-(4-氟苯氧基)-2-吡啶基]四氫吖唉-1-甲酸第三丁酯(54 mg, 0.160 mmol, 29.7% 產率)。MS (ESI): m/z = 245.2 [M+H]+
。
實施例 48
(4aR,8aS)-6-(3-(6-(4-氟苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
將 (4aR,8aS)-六氫-2H-吡啶基[4,3-b][1,4]㗁𠯤-3(4H)-酮 (2S,3S)-2,3-雙((4-甲基苯甲醯基)氧)琥珀酸鹽 (54.3 mg, 100 µmol) 及二(1H-1,2,4-三唑-1-基)甲酮 (16 mg, 100 µmol) 於 ACN (2 mL) 及 TEA (73 mg, 100 µL, 717 µmol) 中之溶液於室溫振蕩 90 min。加入 5-(四氫吖唉-3-基)-2-(4-氟苯氧基)吡啶 4-甲基苯磺酸鹽 (42 mg, 0.1 mmol),將混合物於室溫振蕩 30 min,之後於 60℃振蕩 90 min。透過 Hypersep Amino SPE 管柱(1 g,零件編號:60108-432)過濾該澄清溶液。該管柱用 ACN(總計 6 mL)洗滌,於減壓下去除溶劑,殘質藉由製備型 HPLC 純化以給出作為無色蠟狀固體之標題化合物(15 mg, 35.4 µmol, 35.4 % 產率)。MS (ESI): m/z = 427.2 [M+H]+
。
步驟 a) 3-(6-苯氧基吡啶-3-基)四氫吖唉-1-甲酸第三丁酯
將 DME (6 mL) 加至 5-溴-2-(4-氟苯氧基)吡啶 (686 mg, 2.56 mmol, CAS RN 936343-65-6)、3-溴四氫吖唉-1-甲酸第三丁酯 (604 mg, 2.56 mmol, CAS RN 1064194-10-0)、(Ir[dF(CF3)ppy]2(dtbpy))PF6 (29 mg, 25.6 µmol, CAS RN 870987-63-6)、參(三甲基矽基)矽烷 (636 mg, 789 µL, 2.56 mmol) 及無水碳酸鈉 (407 mg, 3.84 mmol) 之混合物中。於氬氣鼓泡透過該懸浮液下,將混合物攪拌 5 min。將反應容器密封。向另一小瓶充填氯化鎳(II) 乙二醇二甲醚錯合物 (2.8 mg, 12.8 µmol, CAS RN 29046-78-4) 及 4,4'-二-第三丁基-2,2'-聯吡啶 (3.4 mg, 12.8 µmol)。加入 DME (616 µL)。將該小瓶密封,以氬氣吹掃,超音波處理 5 min,然後傾入該反應容器中。於氬氣氛下,將該反應混合物在以 420 nm 燈照射下攪拌 3 小時。濾除固體,以乙酸乙酯洗滌,並蒸發濾液。粗產物用 isolute HM-N 吸附,乾燥,並藉由快速層析純化以給出作為淺黃色蠟狀固體之標題化合物(296 mg, 774 µmol, 30.2 % 處理)。MS (ESI): m/z = 361.2 [M+H]+
。
步驟 b) 5-(四氫吖唉-3-基)-2-(4-氟苯氧基)吡啶 4-甲基苯磺酸鹽
向 3-[4-(6-苯氧基吡啶-3-基)苯基]四氫吖唉-1-甲酸第三丁酯 (296 mg, 907 µmol) 於乙酸乙酯 (7 mL) 中之溶液加入 4-甲基苯磺酸水合物 (77 mg, 407 µmol)。於回流條件下將混合物加熱 18 h,冷卻至室溫,以 3 mL 乙醚稀釋,攪拌 1 h 並過濾。固體用乙醚 (3 x 1 mL) 洗滌並於真空下乾燥以獲得作為白色晶體之標題化合物(285 mg, 684 µmol, 75.4 % 產率)。MS (ESI): m/z = 245.1 [M+H]+
。
實施例 49
(4aR,8aS)-6-(3-(6-(4-(三氟甲氧基)苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
類比於實施例 48 中揭示之過程,令 (4aR,8aS)-六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮 (2S,3S)-2,3-雙((4-甲基苯甲醯基)氧)琥珀酸鹽與 5-(四氫吖唉-3-基)-2-(4-(三氟甲氧基)苯氧基)吡啶 4-甲基苯磺酸鹽反應以獲得作為白色泡沫之標題化合物。MS (ESI): m/z = 493.2 [M+H]+
。
步驟 a) 3-(6-(4-(t三氟甲氧基)苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯
類比於實施例 48 a 中揭示之過程,令 5-溴-2-(4-(三氟甲氧基)苯氧基)吡啶 (CAS RN 909849-01-0) 與 3-溴四氫吖唉-1-甲酸第三丁酯反應以給出作為淺黃色蠟狀固體之標題化合物。MS (ESI): m/z = 411.2 [M+H]+
。
步驟 b) 5-(四氫吖唉-3-基)-2-(4-(三氟甲氧基)苯氧基)吡啶 4-甲基苯磺酸鹽
類比於實施例 48 b 中揭示之過程,令 3-(6-(4-(三氟甲氧基)苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯與 4-甲基苯磺酸水合物反應以獲得作為白色晶體之標題化合物。MS (ESI): m/z = 311.1 [M+H]+
。
實施例 50
(4aR,8aS)-6-(3-(6-(4-氯苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
類比於實施例 48 中揭示之過程,令 (4aR,8aS)-六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮 (2S,3S)-2,3-雙((4-甲基苯甲醯基)氧)琥珀酸鹽與 5-(四氫吖唉-3-基)-2-(4-氯苯氧基)吡啶 4-甲基苯磺酸鹽反應以獲得作為白色泡沫之標題化合物。MS (ESI): m/z = 443.2 [M+H]+
。
步驟 a) 3-(6-(4-氯苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯
類比於實施例 48 a 中揭示之過程,令 5-溴-2-(4-氯苯氧基)吡啶 (CAS RN 28231-69-8) 與 3-溴四氫吖唉-1-甲酸第三丁酯反應以給出作為灰白色固體之標題化合物。MS (ESI): m/z = 361.2 [M+H]+
。
步驟 b) 5-(四氫吖唉-3-基)-2-(4-氯苯氧基)吡啶 4-甲基苯磺酸鹽
類比於實施例 48 b 中揭示之過程,令 3-(6-(4-氯苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯與 4-甲基苯磺酸水合物反應以獲得作為白色晶體之標題化合物。MS (ESI): m/z = 261.1 [M+H]+
。
實施例 51
(4aR,8aS)-6-[3-[4-(3,6-二甲基嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
於環境溫度下,將 (4aR,8aS)-6-(3-(4-羥基苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮 (50 mg, 151 µmol, BB3)、4-氯-3,6-二甲基嗒𠯤 (23.7 mg, 166 µmol, CAS RN 68206-05-3) 及 K2
CO3
(41.7 mg, 302 µmol) 於 DMSO (0.5 mL) 中之混合物於密封試管中攪拌 14 h,並藉由反相快速層析純化以給出作為灰白色固體之標題化合物 (20 mg, 30%)。MS (ESI): m/z = 438.3 [M+H]+
。
實施例 52
(4aR,8aS)-6-(3-(6-(2-氯苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
類比於實施例 48 中揭示之過程,令 (4aR,8aS)-六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮 (2S,3S)-2,3-雙((4-甲基苯甲醯基)氧)琥珀酸鹽與 5-(四氫吖唉-3-基)-2-(2-氯苯氧基)吡啶 4-甲基苯磺酸鹽反應以獲得作為灰白色固體之標題化合物。MS (ESI): m/z = 443.3 [M+H]+
。
步驟 a) 3-(6-(2-氯苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯
類比於實施例 48 a 中揭示之過程,令 5-溴-2-(2-氯苯氧基)吡啶 (CAS RN 1240670-82-9) 與 3-溴四氫吖唉-1-甲酸第三丁酯反應以給出作為黃色油之標題化合物。MS (ESI): m/z = 361.2 [M+H]+
。
步驟 b) 5-(四氫吖唉-3-基)-2-(2-氯苯氧基)吡啶 4-甲基苯磺酸鹽
類比於實施例 48 b 中揭示之過程,令 3-(6-(2-氯苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯與 4-甲基苯磺酸水合物反應以獲得作為白色晶體之標題化合物。MS (ESI): m/z = 261.1 [M+H]+
。
實施例 53
(4aR,8aS)-6-(3-(6-(3-氯苯氧)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
類比於實施例 48 中揭示之過程,令 (4aR,8aS)-六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮 (2S,3S)-2,3-雙((4-甲基苯甲醯基)氧)琥珀酸鹽與 5-(四氫吖唉-3-基)-2-(3-氯苯氧基)吡啶 4-甲基苯磺酸鹽反應以獲得作為灰白色固體之標題化合物。MS (ESI): m/z = 443.3 [M+H]+
。
步驟 a) 3-(6-(3-氯苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯
類比於實施例 48 a 中揭示之過程,令 5-溴-2-(3-氯苯氧基)吡啶 (CAS RN 1240670-82-9) 與 3-溴四氫吖唉-1-甲酸第三丁酯反應以給出作為灰白色固體之標題化合物。MS (ESI): m/z = 361.2 [M+H]+
。
步驟 b) 5-(四氫吖唉-3-基)-2-(3-氯苯氧基)吡啶 4-甲基苯磺酸鹽
類比於實施例 48 b 中揭示之過程,令 3-(6-(3-氯苯氧基)吡啶-3-基)四氫吖唉-1-甲酸第三丁酯與 4-甲基苯磺酸水合物反應以獲得作為白色晶體之標題化合物。MS (ESI): m/z = 261.2 [M+H]+
。
實施例 54
(4aR,8aS)-6-[4-[4-(4-氟苯氧)苯基]哌啶-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
將 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (90.1 mg, 0.280 mmol, BB2a)、DIPEA (362.1 mg, 2.8 mmol) 及 4-[4-(4-氟苯氧基)苯基]哌啶;2,2,2-三氟乙酸 (50 mg, 0.130 mmol, CAS RN 224449-70-1 之 TFA 鹽) 於 ACN (1 mL) 中之混合物於 80℃ 攪拌 12 h。於減壓下將反應混合物帶至乾燥。殘質藉由製備型 HPLC (0.225% TFA) 純化並凍乾以給出作為黃色固體之標題化合物(19.6 mg, 0.040 mmol, 32.5% 產率)。MS (ESI): m/z = 454.4 [M+H]+
。
實施例 55
(4aR,8aS)-6-[3-羥基-3-(4-苯氧基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 47 中揭示之過程,令 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯與 3-(4-苯氧基苯基)四氫吖唉-3-醇;2,2,2-三氟乙酸(CAS RN 2229540-84-3 之 TFA 鹽)反應以給出作為白色固體之標題化合物。MS (ESI): m/z = 424.1 [M+H]+
。
實施例 56
(4aR,8aS)-6-[3-羥基-3-(5-苯氧-2-吡啶基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 47 中揭示之過程,令 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯與 3-(5-苯氧基-2-吡啶基)四氫吖唉-3-醇;2,2,2-三氟乙酸(CAS RN 2355937-31-2 之 TFA 鹽)反應以給出作為淺黃色固體之標題化合物。MS (ESI): m/z = 425.3 [M+H]+
。
實施例 57
(4aR,8aS)-6-[4-(4-苯氧苯基)哌啶-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 47 中揭示之過程,令 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯與 4-(4-苯氧基苯基)哌啶;2,2,2-三氟乙酸 (CAS RN 1247029-36-2) 反應以給出作為白色固體之標題化合物。MS (ESI): m/z = 436.1 [M+H]+
。
實施例 58
(4aR,8aS)-6-[4-(4-苯氧基苯基)哌𠯤-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
類比於實施例 47 中揭示之過程,令 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯與 1-(4-苯氧基苯基)哌𠯤;2,2,2-三氟乙酸(CAS RN 62755-61-7 之 TFA 鹽)反應以給出作為淺紅色固體之標題化合物。MS (ESI): m/z = 437.3 [M+H]+
。
合成建構單元
BB1a & BB1b
(+)-順式-4a,5,6,7,8,8a-六氫-4H-吡啶[4,3-b][1,4]㗁𠯤-3-酮
和
(-)-順式-4a,5,6,7,8,8a-六氫-4H-吡啶[4,3-b][1,4]㗁𠯤-3-酮
外消旋-(4aR,8aS)-六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮鹽酸鹽 (BB1, 500 mg, 2.18 mmol, ChemBridge Corporation) 之鏡像異構物藉由製備型手性 HPLC(ReprosilChiral NR 管柱)分離,使用 EtOH(含有 0.05% 之 NH4OAc):正庚烷 (30 : 70)。
第一沖提鏡像異構物:(+)-順式-4a,5,6,7,8,8a-六氫-4H-吡啶[4,3-b][1,4]㗁𠯤-3-酮 (BB1a)。黃色固體(0.150 g;44.0%)。MS (ESI): m/z = 157.1 [M+H]+
。
第二沖提鏡像異構物:(-)-順式-4a,5,6,7,8,8a-六氫-4H-吡啶[4,3-b][1,4]㗁𠯤-3-酮。(BB1b)。黃色固體(0.152 g;44.6%)。MS (ESI): m/z = 157.1 [M+H]+
。
BB2a 及 BB2b
(4aR,8aS)-3-側氧基六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-6(5H)-甲酸4-硝基苯酯 (BB2a)
和
(4aS,8aR)-3-側氧基六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-6(5H)-甲酸4-硝基苯酯 (BB2b)
於 0℃ 向外消旋-(4aR,8aS)-六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮;二鹽酸鹽 (4.5 g, 19.6 mmol, BB1) 於乾燥 DCM (125 mL) 中之溶液先後加入 DIPEA (6.35 g, 8.58 mL, 49.1 mmol) 及氯甲酸4-硝基苯酯 (4.35 g, 21.6 mmol)。將反應混合物於 0℃ 攪拌 10 min,並於室溫攪拌 2 小時。粗反應物用 DCM 稀釋,轉移至分液漏斗中,用飽和 Na2
CO3
水溶液萃取。收集有機相,且水相用 DCM 反萃取。合併之有機相用 Na2
SO4
乾燥,並蒸發至乾以得到 6.62 g 作為黃色固體之外消旋粗產物 (BB7)。對粗製材料直接進行手性 SFC 分離以得到作為黃色固體之鏡像異構物 BB2b(2.72 g,第二洗出鏡像異構物)以及作為淺米黃色固體但為 BB2b 所污染之鏡像異構物 BB2a(3.25 g,第一洗出鏡像異構物)。進行進一步 SFC 手性分離以得到 2.71 g 之 BB2a。對於兩種鏡像異構物,MS (ESI): m/z = 322.2 [M+H]+
。
BB3
(4aR,8aS)-6-[3-(4-羥基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (BB2a, 1.22 g, 3.8 mmol) 及 4-(四氫吖唉-3-基)苯酚三氟乙酸鹽 (1 g, 3.8 mmol) 於 ACN (10 mL) 中之溶液加入 DIPEA (4.91 g, 37.99 mmol),並將反應混合物於 80℃ 加熱 12 小時。將該溶液蒸發至乾,並於 ACN (20 mL) 中吸收殘質。過濾所得固體沈澱,以 ACN 洗滌,並進一步乾燥以給出作為灰白色固體之標題化合物 (0.65 g, 51.6%)。MS (ESI): m/z = 332.1 [M+H]+
。
步驟 a) 3-(4-羥基苯基)四氫吖唉-1-甲酸第三丁酯
向 4-溴苯酚 (3.6 g, 21.18 mmol, CAS RN 106-41-2)、3-溴四氫吖唉-1-甲酸第三丁酯 (5 g, 21.18 mmol, CAS RN 1064194-10-0)、Ir[dF(CF3)ppy]2(dtbbpy)PF6 (0.237 g, 0.210 mmol)、NiCl2glyme (0.023 g, 0.110 mmol)、4-第三丁基-2-(4-第三丁基-2-吡啶基)吡啶 (0.034 g, 0.130 mmol)、雙(三甲基矽基)矽基-三甲基-矽烷 (5.26 g, 21.18 mmol) 及 Na2CO3 (4.49 g, 42.35 mmol) 於 DME (100 mL) 中之溶液。 攪拌該反應混合物並使用 34 W 藍光 LED 燈(7 cm 遠)照射,同時吹冷風扇以將該反應溫度保持在 25℃,持續 14 小時。過濾該反應物,蒸發濾液,並藉由製備型 HPLC 純化以給出作為淺黃色固體之標題化合物 (1.8 g, 34%)。MS (ESI): m/z =194.0 [M+H-56]+
。
步驟 b) 4-(四氫吖唉-3-基)苯酚;三氟乙酸鹽
向 3-(4-羥基苯基)四氫吖唉-1-甲酸第三丁酯 (1 g, 4.01 mmol) 於 DCM (30 mL) 中之溶液加入 TFA (5.0 mL),將反應混合物於室溫攪拌 12 小時。真空蒸發該混合物以給出作為黃色油之粗製標題化合物(1 g, 94.7% 產率)。MS (ESI): m/z = 150.1 [M+H]+
。
BB4
[4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯基]硼酸
於室溫向 (4aR,8aS)-6-(3-(4-(4,4,5,5-四甲基-1,3,2-二㗁環戊硼烷-2-基)苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮 (0.2 g, 0.453 mmol) 於 H2
O (1.2 mL) 及丙酮 (2.4 mL) 中之溶液加入 NaIO4
(0.29 g, 1.36 mmol) 及 NH4OAc (0.21 g, 2.72 mmol)。然後,將反應混合物於 30℃ 攪拌 16 小時。混合物用 EtOAc (3 x 10 mL) 萃取,合併之有機層用 Na2
SO4
乾燥,過濾並真空濃縮以給出作為白色固體之粗製標題化合物 (0.176 g)。MS (ESI): m/z = 360.2 [M+H]+
。
步驟 a) 3-(4-溴苯基)四氫吖唉-1-甲酸第三丁酯
於室溫向 3-碘四氫吖唉-1-甲酸第三丁酯 (3.0 g, 10.6 mmol, CAS RN 254454-54-1) 於 2-丙醇 (30 mL) 中之溶液加入 4-溴苯基硼酸 (4.26 g, 21.19 mmol, CAS RN 5467-74-3) 於 2-丙醇 (15 mL) 中之溶液。然後,將外消旋-(1R,2R)-2-胺基環己-1-醇 (73.18 mg, 0.640 mmol)、雙(三甲基矽基)醯胺於 THF (21.19 mL, 21.19 mmol) 中之 1M 溶液以及碘化鎳(II) (198.69 mg, 0.640 mmol) 加至該混合物中,於室溫攪拌 30 min。將混合物轉移至 10 個密封之試管內,於微波輻射下在 80℃ 加熱 30 min。合併混合物,以水 (100 mL) 稀釋,並使用乙酸乙酯 (3 x 40 mL) 萃取。合併之有機層用鹽水洗滌,用硫酸鈉乾燥,過濾並真空濃縮。殘質藉由 MPLC 純化以得到作為黃色油之標題化合物 (2.8 g, 84.6%)。MS (ESI): m/z =256.0 [M+H-56]+
。
步驟 b) 3-(4-溴苯基)四氫吖唉;三氟乙酸鹽
向 3-(4-溴苯基)四氫吖唉-1-甲酸第三丁酯 (2.7 g, 8.65 mmol) 於 DCM (50 mL) 中之溶液加入 TFA (8.0 mL),將反應混合物於室溫攪拌 12 小時。將該混合物蒸發至乾以給出作為黃色油之粗製標題化合物 (2.8 g, 99.3%)。MS (ESI): m/z = 214.0 [M+H]+
。
步驟 c) (4aR,8aS)-6-[3-(4-溴苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮
向 (4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-甲酸(4-硝基苯基)酯 (BB2a, 2.36 g, 7.36 mmol) 及 3-(4-溴苯基)四氫吖唉三氟乙酸鹽 (2 g, 6.13 mmol) 於 ACN (20 mL) 中之溶液加入 DIPEA (7.92 g, 61.33 mmol),並將反應混合物於 80℃ 加熱 12 小時。將該混合物蒸發至乾,殘質藉由製備型 HPLC 純化以給出作為黃色膠之標題化合物 (1.1 g, 45.5%)。MS (ESI): m/z = 396.1 [M+2+H]+
。
步驟 d) (4aR,8aS)-6-(3-(4-(4,4,5,5-四甲基-1,3,2-二㗁環戊硼烷-2-基)苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮
於密封之試管中,將雙(頻哪醇酯合)二硼 (0.97 g, 3.8 mmol)、KOAc (0.747 g, 7.61 mmol) 及 (4aR,8aS)-6-[3-(4-溴苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮 (1 g, 2.54 mmol) 混合於二㗁烷 (20 mL) 中。然後,加入 PdCl2
(dppf).CH2
Cl2
(0.207 g, 0.250 mmol),反應混合物以 N2 吹掃,並於 90℃ 加熱 12 小時。過濾該混合物,蒸發濾液,殘質藉由製備型 HPLC 純化以得到作為淺褐色固體之硼酸/硼酸酯 3/2 混合物形式的標題化合物 (0.65 g, 58%)。MS (ESI): m/z = 442.1 [M+H]+
。
實施例 59
式 (I) 化合物本身可用已知方式作為製造下列組成物的錠劑之活性成分:每錠劑
活性成分 200 mg
微晶型纖維素 155 mg
玉米澱粉 25 mg
滑石 25 mg
羥丙基甲基纖維素20 mg
425 mg
實施例 60
式 (I) 化合物本身可用已知方式作為製造下列組成物的膠囊之活性成分:每個膠囊
活性成分 100.0 mg
玉米澱粉 20.0 mg
乳糖 95.0 mg
滑石 4.5 mg
硬脂酸鎂0.5 mg
220.0 mg
Claims (31)
- 一種式 (I) 化合物(I) 或其藥學上可接受之鹽類,其中: A 是選自 C6 -C14 -芳基、5 至 14 員雜芳基以及 3 至 14 員雜環基; B 是 (i) C6 -C14 -芳基;以及,L1 是 –O–;或 (ii) 5 至 14 員雜芳基;以及,L1 是共價鍵或 –O–; m 是 0,n 是 0 或 1,以及 X 是 CR8 ;或 m 是 1,n 是 1 或 2,以及 X 是 CR8 或 N; R1 、R2 及 R3 係各自獨立地選自氫及 C1-6 -烷基; R4 、R5 、R6 及 R7 是獨立地選自氫、鹵素、氰基、羥基、C1-6 -烷氧基、鹵-C1-6 -烷氧基、胺基-C1-6 -烷氧基、C1-6 -烷基、鹵-C1-6 -烷基、羥基-C1-6 -烷基、C1-6 -烷基磺醯基、SF5 、胺基甲醯基、C3-10 -環烷基-C1-6 -烷氧基–、C1-6 -烷基-NH-C(O)–、C1-6 -烷基-C(O)-NH– 及 C3-10 -環烷基,其中,每個 C3-10 -環烷基係視需要經選自 C1-6 -烷基及鹵-C1-6 -烷基之 1 至 2 個取代基取代;以及 R8 係選自氫、鹵素、羥基、鹵-C1-6 -烷基及 C1-6 -烷基。
- 如請求項1之式 (I) 化合物、或其藥學上可接受之鹽類,其中,A 是 C6 -C14 -芳基或 5 至 14 員雜芳基。
- 如請求項1之式 (I) 化合物、或其藥學上可接受之鹽類,其中,A 是苯基或吡啶基。
- 如請求項1至3中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,B 是 (i) 苯基;以及,L1 是 –O–;或 (ii) 選自㗁二唑基、嗒𠯤基、吡啶基及噻唑基;以及,L1 是共價鍵或 –O–。
- 如請求項1至3中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中: m 是 0,n 是 0,以及 X 是 CR8 ;或 m 是 1,n 是 1,以及 X 是 CR8 或 N。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,m 係 0,n 係 0 及 X 係 CR8 。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R1 是氫。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R2 是氫。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R3 是氫。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R4 是氫。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R5 是氫。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R6 是選自氫、鹵素、氰基、C1-6 -烷基、C1-6 -烷氧基、鹵-C1-6 -烷基、C3-10 -環烷基及 C1-6 -烷基磺醯基。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R6 是選自氫、鹵素、氰基及 C1-6 -烷基。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R6 是選自氫、氟基、氯基、氰基、甲基及 2,2-二甲基丙基。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R7 是選自氫、鹵素及 C1-6 -烷基。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R7 是選自氫、氟基及甲基。
- 如請求項1至 3 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,R8 是氫或羥基。
- 如請求項1之式 (I) 化合物、或其藥學上可接受之鹽類,其中,該式 (I) 化合物是式 (IIa) 化合物或其藥學上可接受之鹽類,(IIa) 其中: A 是 C6 -C14 -芳基或 5 至 14 員雜芳基; B 是 (i) C6 -C14 -芳基;以及,L1 係 –O–;或 (ii) 5 至 14 員雜芳基;以及,L1 係共價鍵或 –O–; m 是 0,n 係 0,以及 X 是 CR8 ;或 m 是 1,n 係 1,以及 X 是 CR8 或 N; R6 是選自氫、鹵素、氰基、C1-6 -烷基、C1-6 -烷氧基、鹵-C1-6 -烷基、C3-10 -環烷基以及 C1-6 -烷基磺醯基; R7 是選自氫、鹵素及 C1-6 -烷基;以及 R8 是選自氫及羥基。
- 如請求項1至 3及18至 20 中任一項之式 (I) 化合物或其藥學上可接受之鹽類,其選自: (4aR,8aS)-6-(3-(4-苯氧基苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-[3-[4-(2-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-(4-嘧啶-2-基氧苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(2-甲基-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-甲基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-(4-嗒𠯤-3-基氧苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(4-甲基-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(5-氟-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(5-氯-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3-吡啶氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-甲基嗒𠯤-3-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3-氯嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-甲氧基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[4-(三氟甲基)嘧啶-2-基]氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2,4-二氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3-氯苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2-甲基苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[3-(三氟甲基)苯氧基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; 2-[4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯氧基]苯甲腈; (4aR,8aS)-6-[3-[4-(2-氯嘧啶-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (+)-(4aR,8aS)-6-[3-[4-(4-環丙基嘧啶-2-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(6-甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(4-氯-3-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(3-氟-4-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (+)-(4aR,8aS)-6-[3-[4-(2-甲基磺醯基嘧啶-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[(3,6-二甲基-2-吡啶基)氧]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(1H-吡唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[2-(2,2-二甲基丙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[1-(2,2-二甲基丙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3-氯-2-吡啶基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2,4-二甲基㗁唑-5-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3,5-二甲基吡唑-1-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[3-(2,2-二甲基丙基)三唑-4-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,3,4-㗁二唑-2-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[2-(2-氟乙基)吡唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[1-(2-氟乙基)吡唑-4-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-甲基-1,3-噻唑-2-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(1-甲基吡唑-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(6-氟吡啶-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2-氟吡啶-4-基) 氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(1-甲基吡唑-4-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2-甲基吡唑-3-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[5-(4-氟苯氧基)-2-吡啶基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-(3-(6-(4-氟苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-(3-(6-(4-(三氟甲氧基)苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-(3-(6-(4-氯苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-[3-[4-(3,6-二甲基嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-(3-(6-(2-氯苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-(3-(6-(3-氯苯氧基)吡啶-3-基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-[4-[4-(4-氟苯氧基)苯基]哌啶-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-羥基-3-(4-苯氧基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-羥基-3-(5-苯氧基-2-吡啶基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[4-(4-苯氧基苯基)哌啶-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;以及 (4aR,8aS)-6-[4-(4-苯氧基苯基)哌𠯤-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮。
- 如請求項1至 3及18至 20 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其選自: (4aR,8aS)-6-(3-(4-苯氧基苯基)四氫吖唉-1-羰基)六氫-2H-吡啶幷[4,3-b][1,4]㗁𠯤-3(4H)-酮; (4aR,8aS)-6-[3-[4-(3-氯嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2,4-二氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(2-氟苯氧基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; 2-[4-[1-[(4aR,8aS)-3-側氧-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-6-羰基]四氫吖唉-3-基]苯氧基]苯甲腈; (4aR,8aS)-6-[3-[4-(3-氯-2-吡啶基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-[5-(2,2-二甲基丙基)-1,2,4-㗁二唑-3-基]苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(4-甲基-1,3-噻唑-2-基)苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[5-(4-氟苯氧基)-2-吡啶基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[4-(3,6-二甲基嗒𠯤-4-基)氧苯基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮; (4aR,8aS)-6-[3-[6-(2-氯苯氧基)-3-吡啶基]四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮;以及 (4aR,8aS)-6-[3-羥基-3-(4-苯氧基苯基)四氫吖唉-1-羰基]-4,4a,5,7,8,8a-六氫吡啶幷[4,3-b][1,4]㗁𠯤-3-酮。
- 如請求項1至 3及18至 20 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其是根據如請求項23之方法製造的。
- 如請求項1至3及18至 20 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其中,所述式 (I) 化合物或其藥學上可接受之鹽類具有對單醯基甘油脂肪酶之 IC50 低於 10 µM。
- 如請求項1至 3及18至 20 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,其用於作為治療的活性物質。
- 一種醫藥組成物,其包含如請求項1至22、 24及25 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類,及治療上惰性之載劑。
- 如請求項1至 3及18至 20 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類、或如請求項27之醫藥組成物,用於治療或預防哺乳動物之神經發炎、神經退化性疾病、疼痛、癌症、精神障礙及/或發炎性腸病。
- 如請求項1至 3及18至 20 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類、或如請求項27之醫藥組成物,其用於治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛、與疼痛相關的痙攣、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛。
- 一種如請求項1至 22 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類之用途、其用於製備供治療或預防哺乳動物之神經發炎、神經退化性疾病、疼痛、癌症、精神障礙及/或發炎性腸病的藥物。
- 一種如請求項1至 22 中任一項之式 (I) 化合物、或其藥學上可接受之鹽類之用途、其用於製備供治療或預防哺乳動物之多發性硬化症、阿滋海默症、帕金森病、肌肉萎縮性側索硬化症、外傷性腦損傷、神經毒性、中風、癲癇、焦慮、偏頭痛、抑鬱、肝細胞癌、結腸癌症形成、卵巢癌、神經病性疼痛、化學療法引起的神經病變、急性疼痛、慢性疼痛、與疼痛相關的痙攣、腹痛、與腸躁症候群相關的腹痛及/或內臟疼痛。
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP19196879.1 | 2019-09-12 | ||
| EP19196879 | 2019-09-12 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| TW202128706A true TW202128706A (zh) | 2021-08-01 |
Family
ID=67953598
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| TW109131236A TW202128706A (zh) | 2019-09-12 | 2020-09-11 | 新型雜環化合物 |
Country Status (18)
| Country | Link |
|---|---|
| US (1) | US11814375B2 (zh) |
| EP (1) | EP4028403B1 (zh) |
| JP (1) | JP7609854B2 (zh) |
| KR (1) | KR20220062515A (zh) |
| CN (1) | CN114269755A (zh) |
| AR (1) | AR119943A1 (zh) |
| AU (1) | AU2020346350A1 (zh) |
| BR (1) | BR112022002375A2 (zh) |
| CA (1) | CA3151516A1 (zh) |
| CL (1) | CL2022000556A1 (zh) |
| CO (1) | CO2022001879A2 (zh) |
| CR (1) | CR20220104A (zh) |
| IL (1) | IL289186A (zh) |
| MX (1) | MX2022002311A (zh) |
| PE (1) | PE20220565A1 (zh) |
| PH (1) | PH12022550339A1 (zh) |
| TW (1) | TW202128706A (zh) |
| WO (1) | WO2021048242A1 (zh) |
Families Citing this family (14)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2018165520A1 (en) | 2017-03-10 | 2018-09-13 | Vps-3, Inc. | Metalloenzyme inhibitor compounds |
| AR114136A1 (es) | 2017-10-10 | 2020-07-29 | Hoffmann La Roche | Compuestos heterocíclicos |
| CN111386269A (zh) | 2017-11-28 | 2020-07-07 | 豪夫迈·罗氏有限公司 | 新型杂环化合物 |
| EP3737680A1 (en) | 2018-01-08 | 2020-11-18 | F. Hoffmann-La Roche AG | Octahydropyrido[1,2-alpha]pyrazines as magl inhibitors |
| FI3837263T3 (fi) | 2018-08-13 | 2024-09-03 | Hoffmann La Roche | Uusia heterosyklisiä yhdisteitä monoasyyliglyserolilipaasin estäjinä |
| JP7444882B2 (ja) | 2018-11-22 | 2024-03-06 | エフ. ホフマン-ラ ロシュ アーゲー | 新規の複素環化合物 |
| CA3149096A1 (en) | 2019-07-30 | 2021-02-04 | Eikonizo Therapapeutics, Inc. | Hdac6 inhibitors and uses thereof |
| PE20220565A1 (es) | 2019-09-12 | 2022-04-13 | Hoffmann La Roche | Compuestos de 4,4a,5,7,8,8a-hexapirido[4,3-b][1,4]oxazin-3-ona como inhibidores de magl |
| PH12022551475A1 (en) | 2019-12-20 | 2023-11-29 | Tenaya Therapeutics Inc | Fluoroalkyl-oxadiazoles and uses thereof |
| AU2021338497A1 (en) | 2020-09-03 | 2023-02-09 | F. Hoffmann-La Roche Ag | Heterocyclic compounds |
| CA3216768A1 (en) | 2021-05-04 | 2022-11-10 | Jin Yang | 2-fluoroalkyl-1,3,4-oxadiazol-5-yl-thiazol, hdac6 inhibitors for use in the treatment of metabolic disease and hfpef |
| AU2022426844A1 (en) | 2021-12-29 | 2024-07-04 | Psy Therapeutics, Inc. | Inhibiting monoacylglycerol lipase (magl) |
| CN116410483A (zh) * | 2023-04-14 | 2023-07-11 | 沈阳工业大学 | 一种羰基联氮杂环超分子鎓盐及其制备方法与应用 |
| CN120040415A (zh) * | 2023-11-24 | 2025-05-27 | 中国药科大学 | 一种含喹啉酮骨架的化合物及其应用 |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5214038A (en) | 1991-04-15 | 1993-05-25 | Hoechst-Roussel Pharmaceuticals Inc. | 1-(pyrido[3,4-b]-1,4-oxazinyl-4-yl)-1H-indoles and intermediates for the preparation thereof |
| US7160888B2 (en) | 2003-08-22 | 2007-01-09 | Warner Lambert Company Llc | [1,8]naphthyridin-2-ones and related compounds for the treatment of schizophrenia |
| US7579495B2 (en) | 2003-12-19 | 2009-08-25 | Momentive Performance Materials Inc. | Active-releasing cyclic siloxanes |
| EP1896453B1 (en) | 2005-06-20 | 2009-12-02 | Schering Corporation | Carbon-linked substituted piperidines and derivatives thereof useful as histamine h3 antagonists |
| JP5116687B2 (ja) | 2005-11-02 | 2013-01-09 | バイエル・ファルマ・アクチェンゲゼルシャフト | がんおよび他の過剰増殖性疾患の処置のためのピロロ[2,1−f][1,2,4]トリアジン−4−イルアミンIGF−1Rキナーゼ阻害剤 |
| AU2007217040A1 (en) | 2006-02-17 | 2007-08-30 | Memory Pharmaceuticals Corporation | Compounds having 5-HT6 receptor affinity |
| WO2007117557A2 (en) | 2006-04-05 | 2007-10-18 | Vitae Pharmaceuticals, Inc. | Diaminopropanol renin inhibitors |
| FR2915199B1 (fr) * | 2007-04-18 | 2010-01-22 | Sanofi Aventis | Derives de triazolopyridine-carboxamides et triazolopyrimidine-carboxamides, leur preparation et leur application en therapeutique. |
| TW200942537A (en) | 2008-02-01 | 2009-10-16 | Irm Llc | Compounds and compositions as kinase inhibitors |
| US8309734B2 (en) | 2008-10-29 | 2012-11-13 | Hoffmann-La Roche Inc. | Substituted pyridines as GPBAR1 agonists |
| WO2011059118A1 (ko) | 2009-11-10 | 2011-05-19 | Kim Hyun Jeen | 후각인지능력 검사 시스템 |
| US9051296B2 (en) | 2009-11-16 | 2015-06-09 | Raqualia Pharma Inc. | Aryl carboxamide derivatives as TTX-S blockers |
| US8420661B2 (en) | 2010-04-13 | 2013-04-16 | Hoffmann-La Roche Inc. | Arylethynyl derivatives |
| CN103261189B (zh) * | 2010-10-22 | 2015-01-28 | 詹森药业有限公司 | 作为单酰基甘油脂肪酶抑制剂的氨基-吡咯烷-氮杂环丁烷二酰胺 |
| AU2012255690B2 (en) | 2011-05-16 | 2015-06-11 | Bionomics Limited | Amine derivatives as potassium channel blockers |
| WO2013059118A1 (en) | 2011-10-19 | 2013-04-25 | The Trustees Of Columbia University In The City Of New York | Cyclopropenimine catalyst compositions and processes |
| WO2013080156A1 (en) | 2011-11-30 | 2013-06-06 | Actelion Pharmaceuticals Ltd | 3,7-disubstituted octahydro-2h-pyrido[4,3-e][1,3]oxazin-2-one antibiotics |
| PL2794600T3 (pl) | 2011-12-22 | 2018-06-29 | Novartis Ag | Pochodne 2,3-dihydro-benzo[1,4]oksazyny i powiązane związki jako inhibitory kinazy fosfoinozytydu-3 (PI3K) do leczenia np. reumatoidalnego zapalenia stawów |
| SI2800565T1 (sl) | 2012-01-06 | 2020-10-30 | Lundbeck La Jolla Research Center, Inc. | Karbamatne spojine in metode izdelave in uporabe le-teh |
| GB201209587D0 (en) | 2012-05-30 | 2012-07-11 | Takeda Pharmaceutical | Therapeutic compounds |
| TW201422625A (zh) | 2012-11-26 | 2014-06-16 | Novartis Ag | 二氫-吡啶并-□衍生物之固體形式 |
| BR112015026261A8 (pt) | 2013-04-16 | 2017-12-26 | Actelion Pharmaceuticals Ltd | Derivados biaromáticos antibacterianos |
| WO2016109501A1 (en) | 2014-12-30 | 2016-07-07 | Karos Pharmaceuticals, Inc. | Amide compounds as tryptophan hydroxylase inhibitors |
| WO2016158956A1 (ja) * | 2015-03-30 | 2016-10-06 | 武田薬品工業株式会社 | 複素環化合物 |
| EP3294729A1 (en) | 2015-05-13 | 2018-03-21 | Selvita S.A. | Substituted quinoxaline derivatives |
| MX387321B (es) | 2015-05-21 | 2025-03-11 | Glaxosmithkline Ip Dev Ltd | Derivados de benzoimidazol como inhibidores de peptidil arginina deiminasa 4 (pad4). |
| WO2016205590A1 (en) | 2015-06-18 | 2016-12-22 | Cephalon, Inc. | Substituted 4-benzyl and 4-benzoyl piperidine derivatives |
| WO2017087863A1 (en) | 2015-11-20 | 2017-05-26 | Abide Therapeutics, Inc. | Pyrazole compounds and methods of making and using same |
| WO2017087858A1 (en) * | 2015-11-20 | 2017-05-26 | Abide Therapeutics, Inc. | Pyrazole compounds and methods of making and using same |
| US10323026B2 (en) | 2016-03-31 | 2019-06-18 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| EP3438109B1 (en) | 2016-03-31 | 2021-08-25 | Takeda Pharmaceutical Company Limited | Heterocyclic compound |
| WO2018228934A1 (en) | 2017-06-12 | 2018-12-20 | Boehringer Ingelheim International Gmbh | Heteroaromatic compounds as vanin inhibitors |
| MX2020007318A (es) | 2017-09-29 | 2020-08-24 | Takeda Pharmaceuticals Co | Compuesto heterociclico. |
| AR114136A1 (es) | 2017-10-10 | 2020-07-29 | Hoffmann La Roche | Compuestos heterocíclicos |
| CN111386269A (zh) | 2017-11-28 | 2020-07-07 | 豪夫迈·罗氏有限公司 | 新型杂环化合物 |
| TW201930300A (zh) * | 2017-12-15 | 2019-08-01 | 瑞士商赫孚孟拉羅股份公司 | 新雜環化合物 |
| EP3737680A1 (en) | 2018-01-08 | 2020-11-18 | F. Hoffmann-La Roche AG | Octahydropyrido[1,2-alpha]pyrazines as magl inhibitors |
| WO2019180185A1 (en) | 2018-03-22 | 2019-09-26 | F. Hoffmann-La Roche Ag | Oxazine monoacylglycerol lipase (magl) inhibitors |
| FI3837263T3 (fi) | 2018-08-13 | 2024-09-03 | Hoffmann La Roche | Uusia heterosyklisiä yhdisteitä monoasyyliglyserolilipaasin estäjinä |
| CN112469724A (zh) | 2018-08-13 | 2021-03-09 | 豪夫迈·罗氏有限公司 | 作为单酰基甘油脂肪酶抑制剂的新型杂环化合物 |
| MA54555A (fr) | 2018-11-22 | 2021-09-29 | Qilu Regor Therapeutics Inc | Agonistes de glp-1r et leurs utilisations |
| JP7444882B2 (ja) * | 2018-11-22 | 2024-03-06 | エフ. ホフマン-ラ ロシュ アーゲー | 新規の複素環化合物 |
| JP7707073B2 (ja) | 2019-04-09 | 2025-07-14 | エフ. ホフマン-ラ ロシュ アーゲー | モノアシルグリセロールリパーゼ(magl)の阻害剤としての複素環式化合物 |
| BR112021026820A2 (pt) | 2019-07-03 | 2022-02-22 | Hoffmann La Roche | Inibidores heterocíclicos de monoacilglicerol lipase (magl) |
| PH12021553249A1 (en) | 2019-07-09 | 2023-02-27 | Hoffmann La Roche | New heterocyclic compounds |
| US20210094971A1 (en) | 2019-09-09 | 2021-04-01 | Hoffmann-La Roche Inc. | Heterocyclic compounds |
| JP2022548018A (ja) | 2019-09-12 | 2022-11-16 | エフ.ホフマン-ラ ロシュ アーゲー | 放射性標識化合物 |
| PE20220565A1 (es) | 2019-09-12 | 2022-04-13 | Hoffmann La Roche | Compuestos de 4,4a,5,7,8,8a-hexapirido[4,3-b][1,4]oxazin-3-ona como inhibidores de magl |
| CA3155161A1 (en) | 2019-09-23 | 2021-04-01 | F. Hoffmann-La Roche Ag | Heterocyclic compounds |
| CA3152213A1 (en) | 2019-09-24 | 2021-04-01 | F. Hoffmann-La Roche Ag | New heterocyclic monoacylglycerol lipase (magl) inhibitors |
| EP4034602A1 (en) | 2019-09-24 | 2022-08-03 | F. Hoffmann-La Roche AG | Fluorescent probes for monoacylglycerol lipase (magl) |
| US20210094972A1 (en) * | 2019-09-24 | 2021-04-01 | Hoffmann-La Roche Inc. | Heterocyclic compounds |
| AU2021338497A1 (en) | 2020-09-03 | 2023-02-09 | F. Hoffmann-La Roche Ag | Heterocyclic compounds |
-
2020
- 2020-09-10 PE PE2022000245A patent/PE20220565A1/es unknown
- 2020-09-10 US US17/017,200 patent/US11814375B2/en active Active
- 2020-09-10 EP EP20774901.1A patent/EP4028403B1/en active Active
- 2020-09-10 AU AU2020346350A patent/AU2020346350A1/en not_active Abandoned
- 2020-09-10 MX MX2022002311A patent/MX2022002311A/es unknown
- 2020-09-10 BR BR112022002375A patent/BR112022002375A2/pt not_active Application Discontinuation
- 2020-09-10 CA CA3151516A patent/CA3151516A1/en active Pending
- 2020-09-10 WO PCT/EP2020/075260 patent/WO2021048242A1/en not_active Ceased
- 2020-09-10 PH PH1/2022/550339A patent/PH12022550339A1/en unknown
- 2020-09-10 CN CN202080059190.8A patent/CN114269755A/zh active Pending
- 2020-09-10 KR KR1020227007925A patent/KR20220062515A/ko not_active Ceased
- 2020-09-10 JP JP2022516054A patent/JP7609854B2/ja active Active
- 2020-09-10 CR CR20220104A patent/CR20220104A/es unknown
- 2020-09-11 AR ARP200102527A patent/AR119943A1/es not_active Application Discontinuation
- 2020-09-11 TW TW109131236A patent/TW202128706A/zh unknown
-
2021
- 2021-12-20 IL IL289186A patent/IL289186A/en unknown
-
2022
- 2022-02-22 CO CONC2022/0001879A patent/CO2022001879A2/es unknown
- 2022-03-07 CL CL2022000556A patent/CL2022000556A1/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| WO2021048242A1 (en) | 2021-03-18 |
| EP4028403A1 (en) | 2022-07-20 |
| MX2022002311A (es) | 2022-03-25 |
| CA3151516A1 (en) | 2021-03-18 |
| IL289186A (en) | 2022-02-01 |
| KR20220062515A (ko) | 2022-05-17 |
| JP7609854B2 (ja) | 2025-01-07 |
| AU2020346350A1 (en) | 2022-02-17 |
| US20210094943A1 (en) | 2021-04-01 |
| CN114269755A (zh) | 2022-04-01 |
| EP4028403C0 (en) | 2023-11-22 |
| CR20220104A (es) | 2022-04-20 |
| PE20220565A1 (es) | 2022-04-13 |
| EP4028403B1 (en) | 2023-11-22 |
| BR112022002375A2 (pt) | 2022-07-19 |
| US11814375B2 (en) | 2023-11-14 |
| AR119943A1 (es) | 2022-01-19 |
| JP2022548028A (ja) | 2022-11-16 |
| CL2022000556A1 (es) | 2022-10-21 |
| PH12022550339A1 (en) | 2023-03-13 |
| CO2022001879A2 (es) | 2022-03-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| TW202128706A (zh) | 新型雜環化合物 | |
| US11066414B2 (en) | Cot modulators and methods of use thereof | |
| TWI818967B (zh) | 新穎雜環化合物 | |
| JP6204975B2 (ja) | Abl1、abl2およびbcr−abl1の活性を阻害するためのベンズアミド誘導体 | |
| US9018205B2 (en) | Substituted pyrimidinyl-amines as protein kinase inhibitors | |
| JP2021533093A (ja) | モノアシルグリセロールリパーゼ阻害剤としての新規複素環化合物 | |
| US20240400518A1 (en) | Sos1 inhibitor and use thereof | |
| JP2021534139A (ja) | モノアシルグリセロールリパーゼ阻害剤としての新規の複素環化合物 | |
| CA3085561A1 (en) | Cyclohexyl acid triazole azines as lpa antagonists | |
| JP2022527590A (ja) | モノアシルグリセロールリパーゼ(magl)の阻害剤としての複素環式化合物 | |
| TW202126663A (zh) | 新穎雜環化合物 | |
| US9815818B2 (en) | Cot modulators and methods of use thereof | |
| TW201922728A (zh) | 新穎雜環化合物 | |
| KR20140041583A (ko) | Lrrk2 키나제 활성의 억제제 | |
| TW202227415A (zh) | 新穎雜環化合物 | |
| TW202124392A (zh) | 新穎雜環化合物 | |
| TW202116781A (zh) | 新穎雜環化合物 | |
| JP2022544700A (ja) | 筋萎縮性側索硬化症および関連障害の治療のためにtdp-43に結合する分子 | |
| HK40062310A (zh) | 作为magl抑制剂的4,4a,5,7,8,8a-六吡啶并[4,3-b][1,4]恶嗪-3-酮化合物 | |
| RU2801190C2 (ru) | Новые гетероциклические соединения в качестве ингибиторов моноацилглицеринлипазы | |
| WO2024121779A1 (en) | Papain-like protease (plpro) inhibitors | |
| HK40110578A (zh) | 用作单酰基甘油脂肪酶抑制剂的双环杂环化合物 | |
| HK40035599A (zh) | 恶嗪单醯甘油脂肪酶(magl)抑制剂 |