WO2006100330A2 - Antibióticos polienos, composiciones que los contengan, procedimiento y microorganismos para su obtención y sus aplicaciones - Google Patents
Antibióticos polienos, composiciones que los contengan, procedimiento y microorganismos para su obtención y sus aplicaciones Download PDFInfo
- Publication number
- WO2006100330A2 WO2006100330A2 PCT/ES2006/000142 ES2006000142W WO2006100330A2 WO 2006100330 A2 WO2006100330 A2 WO 2006100330A2 ES 2006000142 W ES2006000142 W ES 2006000142W WO 2006100330 A2 WO2006100330 A2 WO 2006100330A2
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- compound
- formula
- rimocidine
- gene
- vector
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- SBGDOJWIQWHLIY-SOMWKGOZSA-N CCC[C@H](C/C=C/C=C/C=C/C=C/[C@@H](CC([C@H](C)C(C1)O)O[C@@]1(C[C@H](CCCC(C[C@H]([C@@H]1C)O)=O)O)O)OC(C(C2N)O)OC(C)C2O)OC1=O Chemical compound CCC[C@H](C/C=C/C=C/C=C/C=C/[C@@H](CC([C@H](C)C(C1)O)O[C@@]1(C[C@H](CCCC(C[C@H]([C@@H]1C)O)=O)O)O)OC(C(C2N)O)OC(C)C2O)OC1=O SBGDOJWIQWHLIY-SOMWKGOZSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H17/00—Compounds containing heterocyclic radicals directly attached to hetero atoms of saccharide radicals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K39/00—Medicinal preparations containing antigens or antibodies
- A61K39/02—Bacterial antigens
- A61K39/05—Actinobacteria, e.g. Actinomyces, Streptomyces, Nocardia, Bifidobacterium, Gardnerella, Corynebacterium; Propionibacterium
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07H—SUGARS; DERIVATIVES THEREOF; NUCLEOSIDES; NUCLEOTIDES; NUCLEIC ACIDS
- C07H17/00—Compounds containing heterocyclic radicals directly attached to hetero atoms of saccharide radicals
- C07H17/04—Heterocyclic radicals containing only oxygen as ring hetero atoms
- C07H17/08—Hetero rings containing eight or more ring members, e.g. erythromycins
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/195—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria
- C07K14/36—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from bacteria from Actinomyces; from Streptomyces (G)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N15/00—Mutation or genetic engineering; DNA or RNA concerning genetic engineering, vectors, e.g. plasmids, or their isolation, preparation or purification; Use of hosts therefor
- C12N15/09—Recombinant DNA-technology
- C12N15/11—DNA or RNA fragments; Modified forms thereof; Non-coding nucleic acids having a biological activity
- C12N15/52—Genes encoding for enzymes or proenzymes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/0004—Oxidoreductases (1.)
- C12N9/0071—Oxidoreductases (1.) acting on paired donors with incorporation of molecular oxygen (1.14)
- C12N9/0077—Oxidoreductases (1.) acting on paired donors with incorporation of molecular oxygen (1.14) with a reduced iron-sulfur protein as one donor (1.14.15)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N9/00—Enzymes; Proenzymes; Compositions thereof; Processes for preparing, activating, inhibiting, separating or purifying enzymes
- C12N9/10—Transferases (2.)
- C12N9/1003—Transferases (2.) transferring one-carbon groups (2.1)
- C12N9/1007—Methyltransferases (general) (2.1.1.)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12P—FERMENTATION OR ENZYME-USING PROCESSES TO SYNTHESISE A DESIRED CHEMICAL COMPOUND OR COMPOSITION OR TO SEPARATE OPTICAL ISOMERS FROM A RACEMIC MIXTURE
- C12P19/00—Preparation of compounds containing saccharide radicals
- C12P19/44—Preparation of O-glycosides, e.g. glucosides
- C12P19/60—Preparation of O-glycosides, e.g. glucosides having an oxygen of the saccharide radical directly bound to a non-saccharide heterocyclic ring or a condensed ring system containing a non-saccharide heterocyclic ring, e.g. coumermycin, novobiocin
- C12P19/62—Preparation of O-glycosides, e.g. glucosides having an oxygen of the saccharide radical directly bound to a non-saccharide heterocyclic ring or a condensed ring system containing a non-saccharide heterocyclic ring, e.g. coumermycin, novobiocin the hetero ring having eight or more ring members and only oxygen as ring hetero atoms, e.g. erythromycin, spiramycin, nystatin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Definitions
- the invention relates to new knotted and methylated polyenes, the process for obtaining them, characterization of biological activities and applications, for example, therapeutic, agricultural and agri-food.
- the invention also relates to: (a) methylated derivatives of other polyenes obtained in the same manner in their respective producing organisms; (b) recombinant microorganisms producing amidated polyenes as well as (c) with vectors useful for obtaining said microorganisms and (d) a procedure for obtaining aminated polyenes using acellular extracts or protein fractions obtained from producers of aminated polyenes macrolides.
- antifungal drugs Despite the need for antifungal drugs, the number of these pharmaceutical products on the market to treat systemic infections is dangerously low. Most of them, such as azoles and polyenes, which include amphotericin B, have the structural integrity of fungal membranes as a target, although, in recent years, antifungal drugs (echinocandins) have been developed that they target specific components of the cellular wall.
- Polyenes are a group of very interesting polytonic macrolides due to their antifungal activity. These compounds contain a macrolactone ring with numerous conjugated double bonds, forming chromophores with a characteristic spectrum in the ultraviolet / visible area; These characteristics are responsible for their physical and chemical properties (high light absorption, photolability and poor water solubility). Despite the importance of some examples such as amphotericin B as antifungal drugs, its precise mechanism of action is not yet well understood; however, the antifungal activity seems to be due to interactions between polyene molecules and sterol-containing membranes. This interaction provides an ion channel and the membranes become permeable causing the destruction of electrochemical gradients and the consequent cell death.
- the inventors of the invention have found that by genetic manipulation of Streptomyces diastaticus var. 108, a strain producing the polymic macrolide antibiotics rimocidine (lia) and CE-108 (Hb) (Pérez-Z ⁇ fiiga et al, (2004), J. Antibiot.
- the inventors of the invention have found that by genetic manipulation of Streptomyces diastaticus var. 108, a strain producing the polymic macrolide antibiotics rimocidine (lia) and CE-108 (Hb) (Pérez-Z ⁇ fiiga et al, (2004), J. Antibiot.
- the biosynthetic mechanism for the formation of these aforementioned rimocidine B (I-la) and CE-108B (I-Ib) polyenes is elucidated, as well as the obtention of two new rimocidine C (Illa polyenes) ) and CE-108C (HIb) (methylated polyenes, Example 2) by genetic manipulation of the cluster involved in the biosynthesis of the two macrolide antibiotics polymos rimocidine (lia) and CE-108 (Hb) (Seco et al., 2004, Chem Biol. 11: 357-366).
- the new methylated polyenes, as well as the amidated ones, have clearly improved pharmacological properties compared to native tetraenes.
- module 7 of the polyketide synthetase ( PKS) methylmalonamil-CoA is incorporated as an elongation unit, which is responsible for the presence of a methyl group in the macrocyclic ring which, subsequently, by a site-specific post-PKS modification would be oxidized to give rise to the free carboxyl group present in rimocidine (lia) and CE-108 (Hb).
- cytochrome P450 monooxygenase is involved in this oxidation, and is encoded in the biosynthetic clusters of polyenes described so far (Aparicio et al., 2003, Appl Microbiol Biotechnol 61: 179-188).
- RimG be the cytochrome P450 monooxygenase involved in the oxidation of the methyl group to originate the carboxyl group (Seco et al., 2004, Chem. Biol. 11: 357-366).
- the invention relates to two amidated polyenes identified later in this description as rimocidine B (I-la) and CE-108B (I-lb) and two methylated polyenes identified later as rimocidine C (Illa) and CE-108C (HIb ); their obtaining and applications constitute additional aspects of this invention.
- Such compounds have biocidal activity, which, in particular, is more selective against organisms that have ergosterol-containing cell membranes, either fungi or parasites.
- Biocidal compositions for example, pharmaceutical compositions and / or antifungal compositions for agricultural or agri-food use containing said aminated or methylated polyenes, constitute a further aspect of this invention.
- the use of said polyenes, whether aminated or methylated, in pharmaceutical compositions for sanitary purposes for human or animal use and / or antifungal compositions for agricultural or agri-food use constitutes another aspect of this invention.
- the invention relates to the applications of polyene AB-400 (IVb), the corresponding pimaricin amide (IVa) (Ca ⁇ edo LM et al., 2000, J. Antibiot. (Tokyo) 53: 623-626) , based on the test results of this compound, isolated from Streptomyces sp. RGU5.3 and revealed in this invention.
- IVb polyene AB-400
- IVa pimaricin amide
- the invention relates to the use of vectors derived from SCP2 * that contain at least the erythromycin resistance (ermE) gene, such as pSM784 or pSM743B, identified below.
- ermE erythromycin resistance
- the invention relates, in another aspect, to a process for the production of said amidated polyenes which comprises culturing a recombinant microorganism producing said compounds under conditions that allow the production of said polyenes, whether aminated or methylated, and, if desired. , isolate and purify said compounds.
- recombinant microorganisms include Streptomyces diastaticus var. 108/784, Streptomyces d ⁇ astaticus var. 108 / 743B and Streptomyces diastaticus var.
- the invention relates to the elucidation of the mechanism for the formation of the amide group of the aminated polyenes for which, an interruption or deletion of the rimG gene in order to block the formation of the carboxyl group was crucial.
- the formation of the carboxyl group is blocked, if the formation of the amide group takes place during the assembly of the polytonic chain, by transforming the disrupting strain with a plasmid inducing the biosynthesis of the amidated tetraenes, these should be detected in the fermentation broth . If not, it would be concluded that the formation of the amide group takes place by means of an amidotransferase activity on the free carboxyl group, once it has been formed.
- Inactivating gene disruption was chosen as an alternative to mutagenize the rimG gene. However, under these first conditions, and unexpectedly the disruption in the rimG gene performed as indicated above, generates a recombinant incapable of producing polyenes. This was interpreted to mean that the promoter used for the disruption was unable to prevent polar effects probably on the rimA gene located after the insertion point.
- the invention also relates to a methylated polyene of formula (III), hereinafter composed of the invention, useful as an antifungal and antiparasitic, and as particular objects said polyene describes the following methylated polyenes identified later in this description. as rimocidine C (Illa) and CE-108C (HIb).
- the invention relates, in another aspect, to a process for the production of said methylated polyenes of formula III which comprises culturing the disrupting microorganism producing said compounds under conditions that allow the production of said methylated polyenes, and, if desired, isolating and purify said compounds.
- the invention also relates to the use of gene disruption involved in the same chemical modification proposed for RimG (some of which have already been described) in other biosynthetic clusters of polyenes in order to produce the corresponding methylated derivatives .
- rimocidine C (Illa) and CE-108C (IHb) is based on a greater selective toxicity towards membranes containing ergosterol, either fungi or parasites, than towards human cell membranes, which significantly reduces their toxicity.
- Biocidal compositions for example, pharmaceutical compositions and / or antifungal compositions for sanitary, agricultural or agri-food use containing said methylated polyenes, constitute a further aspect of this invention.
- Another additional object of the invention is the use of a biocidal composition containing the compound of the invention for the treatment of infectious diseases in the human and animal, agricultural and food sanitary field.
- a biocidal composition containing the compound of the invention for the treatment of infectious diseases in the human and animal, agricultural and food sanitary field.
- amidotransferase activity present in the acellular extracts of the genetic recombinants of S. diastaticus var. 108 has a relaxed specificity towards the substrate being able to modify not only the native substrates rimocidine (lia) and CE-108 (Hb) in their corresponding amides rimocidine B (I-la) and CE-108B (I-lb), but which is also able to recognize heterologous substrates such as pimaricin (IVa). This did not occur for the amidotransferase activity of Streptomyces sp. RGU5.3, being only able to recognize pimaricin (IVa) as a substrate under the conditions tested.
- the invention provides an enzymatic process, hereafter enzymatic process of the invention, to convert carboxylated polyenes into the corresponding amidates, using acellular extracts of the producers or components selected either directly or immobilized in suitable supports following the technology of the field of immobilized systems from a substrate and under conditions of certain cultivation.
- the invention relates to acellular extracts of producers of amidated polyenes, carriers of an amidotransferase activity, capable of converting "in vitro" carboxylated polyenes into their corresponding amides necessary for the implementation of the enzymatic process of the invention.
- the invention relates to the acellular extracts of microorganisms S. diastaticus var. 108 / 743B, S. diastaticus var.
- Figure 1 shows a schematic representation of the physical maps of the recombinant plasmids pSM743B (rimA gene introduced in pIJ922) [ Figure IA] and pSM784 (ermE gene introduced in pIJ941) [ Figure IB].
- xysAp xysA promoter
- rimA Type I PKS involved in the biosynthetic pathway of CE-108 and rimocidine
- Ti methylenomycin resistance gene terminator
- ermE, tsr and hyg genes for resistance to erythromycin, thiostrepton and hygromycin, respectively
- riml * ⁇ riml truncated on your N-terminal Figure IC shows the chromatographic profile (HPLC) of the fermentation broth of the genetically modified strain Streptomyces diastaticus var. 108 / 743B.
- the numbers 1-4 represent 1: CE-108B (Mb); 2: CE-108 (Hb); 3: rimocidine B (Ila); and 4: rimocidine (lia).
- Figure 2 shows the antifungal activity of the four tetraenes produced by S. diastaticus var. 108 / 743B.
- the numbers that appear on each of the antibiograms refer to the applied amounts of each of the polyenes expressed in nanomoles.
- the target organisms were: P. chrysogenum, C. krusei, A. niger, C. albicans and C. neoformans (see Table 1, Exemplol).
- Figure 3 shows the biological activities of the pimaricin (IVa) and AB-400 (IVb) polyenes isolated from Streptomyces sp. RGU5.3.
- HPLC analyzes chromatograms of fermentation broths from Sti-eptomyces sp. RGU5.3 grown in medium with acetate ( Figure 3 A) or glucose ( Figure 3B) as carbon source respectively.
- Figure 3C illustrates the antifungal activity of pimaricin (IVa) and AB-400 (IVb) against P. chrysogenum; the samples of applied polyenes were (1): commercial pimaricin (Calbiochem 5279962), (2): total extract of the fermentation broth of S. sp.
- FIG. 3D shows the hemolytic activity for pimaricin (Calbiochem 527962, 98.8% purity) and AB-400 (purified by HPLC as indicated in the Experimental Procedures); the values of each polyene are expressed in nanomoles (left column) and the corresponding hemolytic activities are provided as a percentage of total hemolysis (see text for experimental procedures).
- Figure 4 shows, in panel A, a scheme of the transcription of the genes in this particular region of the chromosome deduced by endonuclease Sl protection tests carried out with different DNA fragments (Seco et al, 2004, Chem. Biol 11: 357-366).
- the transcripts are represented by dashed arrows corresponding to the polycistron of the rimE, rimF, rimG, rimH and ritnA genes.
- Deducted transcripts are represented by dashed arrows.
- the DNA fragments used for inactivating insertions of the rimG and rimE genes are indicated with a gray line; the numbers in brackets correspond to the DNA sequence deposited under the accession number AY442225.
- Panel B of this figure shows the chromatogram corresponding to the fermentation broth of S. diastaticus var. 108 :: PMl-768 / 743B, where a and b correspond to CE-108C (HIb) and rimocidine C (Illa) respectively.
- Figure 5 shows, on the left panel, the chromatogram of the fermentation broth of the S. diastaticus var. 108 :: PMl-702B / 743B.
- To the right of the chromatogram is the chemical structure deduced from the compounds detected in the chromatography. The chemical structure was deduced based on the analysis of mass spectrometry.
- Figure 6 shows the HPLC analyzes of the in vitro amidotransferase activity assays carried out with acellular extracts of S. diastaticus var.
- the chromatograms of the left and right columns show the reaction at incubation times of 0 and 60 minutes, respectively.
- the peaks are: a. CE-108B; b. CE-108; C. rimocidine B; d. rimocidine; and. pimaricin; F. AB-400
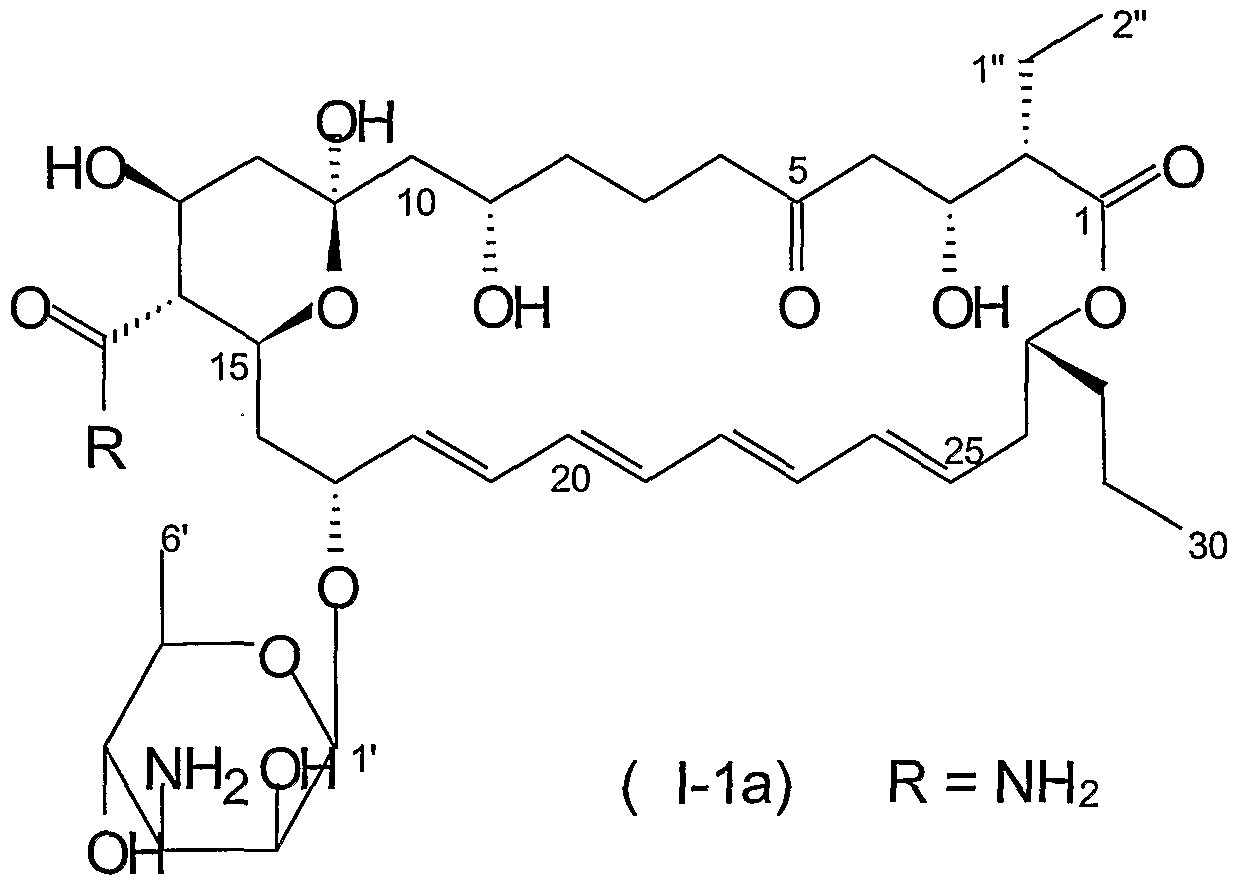
- the present invention describes a new polyethylene macrolide compound characterized by the formula (I):
- R 1 is C 1 -C 3 alkyl
- R2 is a functional group chosen from CH 3 - or CONH 2 - (methyl or primary amide), its isomers, salts, prodrugs or solvates.
- the compounds of the present invention represented by the formula (I) described above may include isomers, depending on the presence of multiple bonds (eg, Z, E), including optical isomers or enantiomers, depending on the presence of chiral centers.
- the individual isomers, enantiomers or diastereoisomers and mixtures thereof fall within the scope of the present invention.
- the individual enantiomers or diastereoisomers, as well as mixtures thereof, can be separated by conventional techniques.
- salt includes both pharmaceutically acceptable salts, that is, salts of the compound of formula (I) that can be used in the manufacture of a medicament, as pharmaceutically unacceptable salts since these may be useful. in the preparation of pharmaceutically acceptable salts.
- the nature of the pharmaceutically acceptable salt is not critical as long as it is pharmaceutically acceptable.
- pharmaceutically acceptable salts of the compounds of formula (I) are acid addition salts, which can be obtained from acids, organic or inorganic, by conventional methods well known to those skilled in the art by reacting the acid appropriate with the compound of formula (I) in the appropriate stoichiometric amount.
- prodrugs of the compounds of formula (I) are also be used to obtain said salts of Acid addition.
- prodrug includes any compound derived from a compound of formula (I), for example, esters, including carboxylic acid esters, amino acid esters, phosphate esters, metal salt sulphonate esters, etc., carbamates, amides, etc., which, when administered to an individual, is capable of providing, directly or indirectly, said compound of formula (I) in said individual.
- said derivative is a compound that increases the bioavailability of the compound of formula (I) when administered to an individual or that enhances the release of the compound of formula (I) in a biological compartment.
- the nature of said derivative is not critical as long as it can be administered to an individual and provides the compound of formula (I) in a biological compartment of an individual.
- the preparation of said prodrug can be carried out by conventional methods known to those skilled in the art.
- solvate includes both pharmaceutically acceptable solvates, that is, solvates of the compound of formula (I) that can be used in the manufacture of a medicament, as pharmaceutically acceptable solvates, which may be useful in the preparation of pharmaceutically acceptable solvates or salts.
- pharmaceutically acceptable solvate is not critical as long as it is pharmaceutically acceptable.
- the solvate is a hydrate. Solvates can be obtained by conventional solvation methods well known to those skilled in the art.
- the compounds of formula (I), their isomers, salts, prodrugs or solvates will preferably be found in a pharmaceutically acceptable or substantially pure form, that is, having a pharmaceutically acceptable level of purity excluding normal pharmaceutical additives such as diluents and carriers, and not including material considered toxic at normal dosage levels.
- the purity levels for the active ingredient are preferably greater than 50%, more preferably greater than 70%, more preferably greater than 90%. In a preferred embodiment, they are greater than 95% of the compound of formula (I), or of its salts, solvates or prodrugs.
- the compounds of the invention also include compounds that differ only in the presence of one or more isotopically enriched atoms.
- compounds having said structure, except for the replacement of a hydrogen with a deuterium or tritium, or the replacement of a carbon with a carbon enriched in 13 C or 14 C or a nitrogen enriched in 15 N are within of the scope of this invention.
- the invention relates to a compound of formula (1-1), amidated derivative of the polyene of the invention of formula (I):
- R is NH 2 ;
- R 1 is C 1 -C 3 alkyl, or an isomer, salt, prodrug or solvate thereof.
- said compound of formula (I-1) is selected from the group consisting of the compounds identified in this description as "rimocidine B", of formula (I-la), and "CE-108B", of formula ( Mb):
- the invention also relates to a compound of formula (III), methylated derivative of the polyene of the invention of formula (I):
- R is C 1 -C 3 alkyl , or an isomer, salt, prodrug or solvate thereof.
- said compound of formula (III) is selected from the group consisting of the compounds identified in this description as "rimocidine C", of formula (Illa), and "CE-108C”, of formula (HIb).
- rimocidine C Illa
- CE-108C HIb
- the chemical structure of these compounds has been characterized by various techniques as well as their biological activity (for example, mass spectrometry, NMR, antibiograms, hemolytic activity, etc.).
- the antifungal activity unlike the amidated polyenes, does not increase with respect to the parental compounds rimocidine and CE-108; however, the toxicity measured in hemolytic terms is more reduced than that of the compounds rimocidine and CE-108, which also implies an increase in the selective toxicity towards fungal membranes compared to native polyenes (Example 2).
- the compounds of formula (I), and among them the compounds of formula (Il) and (III) have, in general, biocidal activity, and, in particular, biocidal activity against organisms that possess an ergosterol-containing cell membrane, by what are potentially useful as biocides.
- a "biocide” is a chemical that stops growth or kills different types of living things.
- organisms that possess an ergosterol-containing cell membrane includes any organism provided with an ergosterol-containing cell membrane, for example, fungi, parasites, etc.
- fungi include Trypanosoma, Leishmania, etc. parasites, as well as fungi such as Fusarium oxysporium, Botrytis cinerea (phytopathogens), Candida albicans, Candida cruzei, Aspergillus niger, Criptococcus neoformans (human pathogens), among others .
- said compounds of formula (I), and among them the compounds of formula (I-1) and (III), and in particular, the compounds rimocidine B (I-la), CE-108B (I-Ib) , rimocidine C (Illa) and CE-108C (HIb) are potentially useful as biocides against such organisms that possess an ergosterol-containing cell membrane.
- said compounds are more useful as antiparasitic agents or as antifungal agents than the corresponding non-amidated polyenes.
- antifungal includes both fungicides and fungistatics.
- the invention relates to a biocidal composition
- a biocidal composition comprising a compound of formula (I), and among them compounds of formula (1-1) and (III), together with an inert carrier.
- said compound of formula (I) is selected from the group of formula (I-1), and preferably by rimocidine B (I-la), CE-108B (I-Ib) and mixtures thereof;
- said compound of formula (III) is selected from the group of formula (III), and preferably by rimocidine C (Illa), CE-108C (IHb) and mixtures thereof.
- Said biocidal composition is particularly useful against organisms that possess ergosterol-containing cell membranes.
- said biocidal composition is an antifungal composition
- a compound of formula (I) such as a compound selected from the compounds rimocidine B (Ila), CE-108B (I-Ib), rimocidine C (Illa ), CE-108C (HIb) and mixtures thereof, together with, optionally, one or more vehicles inert
- inert means that said vehicle does not have a significant biocidal activity.
- said biocidal composition may contain, in addition, other biocides, natural, recombinant or synthetic, which, if necessary, enhance the biocidal action of said compound of formula (I), for example, of the rimocidine compounds B (Ila) ) and / or CE-108B (Mb), rimocidine C (Illa), CE-108C (IHb) and their mixtures or that increase their spectrum of action.
- biocides natural, recombinant or synthetic
- the invention provides a pharmaceutical composition comprising a compound of formula (I), and among them a compound of formula (I-1) or (III) or mixtures thereof, together with, optionally, one or more pharmaceutically acceptable excipients.
- said compound of formula (I) is selected from the compounds rimocidine B (I-la), CE-108B (I-lb) and mixtures thereof, as well as the compounds of formula (III) are selected from rimocidine C (Illa), CE-108C (HIb) compounds and mixtures thereof.
- pharmaceutically acceptable excipient refers to those substances, or combination of substances, known in the pharmaceutical sector, used in the preparation of pharmaceutical administration forms and includes adjuvants, solids or liquids, solvents , surfactants, etc.
- said pharmaceutical composition may also contain one or more therapeutic agents that, if necessary, enhance the therapeutic action of said compounds of formula (I), for example, of the compounds rimocidine B, CE -108B, rimocidine C, CE -108C or increase their spectrum of action.
- Said pharmaceutical composition can be used to prevent and / or treat infections caused by pathogenic organisms of humans or animals that possess ergosterol-containing cell membranes, for example, parasites and pathogenic fungi of humans or animals.
- said pharmaceutical composition is an antiparasitic composition and can be used in the prevention and / or treatment of infections caused by parasites whose cell membranes contain ergosterol, for example, Trypanosoma, Leishmania, etc.
- said antiparasitic composition may also contain one or more antiparasitic agents that, if necessary, enhance the therapeutic action of compounds of formulas (I), for example, of the compounds rimocidine B, CE-108B, rimocidine C, CE -108C or increase their spectrum of action.
- said pharmaceutical composition is an antifungal composition and can be used in the prevention and / or treatment of fungal infections (whose cell membranes contain ergosterol).
- said antifungal composition may also contain one or more antifungal agents that, if necessary, potentiate the antifungal action of compounds of formulas (I), for example, rimocidine B, CE -108B, rimocidine C, CE-108C, or that increase their spectrum of action.
- antifungal agents include polyenes, such as amphotericin B, nystatin, AB-400, allylamines (e.g., terbinafine, naphthifine, etc.), amorolfia, tolnaphthalate, etc .; azoles, such as clotrimazole, miconazole, ketoconazole, fluconazole, itraconazole, etc .; benzof ⁇ ranos, for example, griseofulvin, etc .; pyrimidines, for example, fluocytosine, etc.
- polyenes such as amphotericin B, nystatin, AB-400, allylamines (e.g., terbinafine, naphthifine, etc.), amorolfia, tolnaphthalate, etc .
- azoles such as clotrimazole, miconazole, ketoconazole, fluconazole, itraconazole, etc
- the pharmaceutical composition provided by this invention contains between 0.01% and 99.99% by weight of a compound of formula (I), such as a compound selected from the compounds rimocidine B (I-la) , CE-108B (I-lb), rimocidine C (Illa), CE-108C (HIb) and mixtures thereof, and may be presented in any appropriate pharmaceutical form of administration depending on the route of administration chosen, for example, oral, parenteral or topical.
- a compound of formula (I) such as a compound selected from the compounds rimocidine B (I-la) , CE-108B (I-lb), rimocidine C (Illa), CE-108C (HIb) and mixtures thereof, and may be presented in any appropriate pharmaceutical form of administration depending on the route of administration chosen, for example, oral, parenteral or topical.
- the invention also relates to the use of a compound of formula (I) and / or (III) in the preparation of a medicament for the prevention and / or treatment of infection caused by pathogenic organisms of humans or animals whose cell membranes contain ergosterol, for example, human parasites or animals or human or animal pathogenic fungi.
- said compound of formula (I) and / or (III) is selected from rimocidine B (Ila), CE-108B (T-Ib), rimocidine C (Illa), CE-108C (HIb) and their mixtures.
- the invention also provides a method for preventing and / or treating infections caused by pathogenic organisms of humans or animals whose cell membranes contain ergosterol, for example, parasites of humans or animals or pathogenic fungi of humans or animals, which comprises the step of administering to an animal or a human being, in need of treatment, a therapeutically effective amount of a pharmaceutical composition provided by this invention.
- the invention provides an antifungal composition useful for controlling infection caused by phytopathogenic fungi (such as Botrytis cinerea, Fusarium oxysporum, Rhizoctonia solana, Rhizoctonia meloni, Ustilago mayan, among others) whose cell membranes contain ergosterol, which comprises a compound of formula (I) and / or (III), such as a compound selected from the compounds rimocidine B (I-la), CE-108B (Mb), rimocidine C (Illa), CE-108C (HIb) and mixtures thereof , together with, optionally, one or more agriculturally acceptable inert vehicles.
- phytopathogenic fungi such as Botrytis cinerea, Fusarium oxysporum, Rhizoctonia solana, Rhizoctonia meloni, Ustilago mayan, among others
- ergosterol which comprises a compound of formula (I) and / or (III), such as a compound selected from the compounds
- control includes the inhibition, reduction or paralysis of spore germination and / or fungal mycelium growth that may result in the removal of such fungi or in the reduction of damage caused for these.
- agriculturally acceptable inert vehicle refers to those substances, or combination of substances, known in the agricultural sector, used to vehicle compounds of interest, and includes adjuvants, solids or liquids, diluents, solvents, surfactants , etc.
- said antifungal composition further comprises of said compound of formula (I) and / or (III), for example, a compound selected from rimocidine B (I-la), CE-108B (I-lb), rimocidine C (Illa), CE-108C (HIb ) and mixtures thereof, one or more compounds with antifungal activity, for example, one or more compounds that alter the fungal cell membrane, or one or more compounds that inhibit ergosterol synthesis, such as the compounds mentioned above, or one or more compounds with enzymatic activities required for the modification or degradation of cell walls, for example, one or more lithic enzymes capable of modifying or degrading fungal cell walls, such as enzymes with cellulolytic, mannanolytic, chitinolytic or proteolytic activity (eg, cellulases, ⁇ - (l, 3) -glucanases, ⁇ - (l, 6) -glucanases, ⁇ - (l, 3) -glucanases,
- the antifungal composition useful for controlling phytopathogenic fungi contains between 0.01% and 100% by weight of said compound of formula (I) and / or (III), for example, of said compounds rimocidine B (I-la), CE-108B (I-lb), rimocidine C (Illa), CE-108C (IHb).
- Said composition may be prepared by conventional methods and may be presented in liquid or solid form, for example, in the form of a granulate. Additionally, said composition may contain additives, for example, preservatives and stabilizers that prolong the preservation and stability thereof.
- Said antifungal composition can be used, for example, to control infections caused by phytopathogenic fungi in plants and / or fruits. Therefore, the invention provides a method for controlling infection caused by a phytopathogenic fungus in a plant, in particular, a phytopathogenic fungus whose cellular membrane contains ergosterol, which comprises applying to said plant, or to the surrounding environment, said composition for control said phytopathogenic fungus.
- said method comprises the application of said composition, in a suitable amount, on the aerial parts of the plant in order to prevent and / or treat a fungal infection caused by a phytopathogenic fungus.
- the invention also provides a method for controlling infection caused by phytopathogenic fungi in a fruit, in particular, a phytopathogenic fungus whose cell membrane contains ergosterol, which comprises applying said fruit to said fruit.
- composition to control phytopathogenic fungi.
- the application of said composition, in an effective amount, on the fruit is carried out prior to its collection (pre-harvest) while in another alternative embodiment the application of the composition is carried out on the fruit already collected (post-harvest).
- the invention provides an antifungal composition useful for the control of fungi that can eventually be developed on food preparations, for example, on the surface of food preparations, such as dairy derivatives, for example, cheeses, etc., comprising a compound of formula (I) such as a compound selected from the compounds rimocidine B (Ila), CE-108B (I-lb), rimocidine C (Illa), CE-108C (IHb) and mixtures thereof, together with, optionally, one or more inert vehicles acceptable from the agri-food point of view, such as liposomal suspensions, in water, etc., among others.
- a compound of formula (I) such as a compound selected from the compounds rimocidine B (Ila), CE-108B (I-lb), rimocidine C (Illa), CE-108C (IHb) and mixtures thereof, together with, optionally, one or more inert vehicles acceptable from the agri-food point of view, such as liposomal
- control includes the inhibition, reduction or paralysis of spore germination and / or fungal mycelium growth that may result in a marked decrease in the damage caused by them; in this way the food spoil caused by the growth of fungi can be prevented or treated.
- inert agri-food vehicle refers to those substances, or combination of substances, known in the agri-food sector, used to vehicle compounds of interest, and includes adjuvants, solids or liquids, diluents, solvents, surfactants , etc.
- said antifungal composition comprises, in addition to said compound of formula (I) for example, a compound selected from rimocidine B (I-la), CE-108B (I-lb), rimocidine C (Illa), CE -108C (HIb) and mixtures thereof, one or more compounds with antifungal activity, for example, one or more compounds that alter the fungal cell membrane, or one or more compounds that inhibit ergosterol synthesis, such as the compounds mentioned previously, or one or more compounds with enzymatic activities required for the modification or degradation of cell walls, for example, one or more lytic enzymes capable of modify or degrade fungal cell walls, such as enzymes with cellulolytic, mannanolytic, chitinolytic or proteolytic activity (eg, cellulases, ⁇ - (1, 3) -glucanases, ⁇ - (l, 6) -glucanases, ⁇ - (l, 3) -glucanases, mannanas, endo-
- the compound of formula (I) will be present in said antifungal composition in an effective antifungal amount, that is, in an appropriate amount to control the infection caused by fungi susceptible to developing on food preparations.
- said antifungal composition useful for controlling fungi capable of developing on food preparations provided by this invention contains between 0.01% and 100% in weight of said compound of formula (I), for example, of said compounds rimocidine B (I-la), CE -108B (I-lb), rimocidine C (Illa), CE-108C (HIb).
- Such composition can be prepared by conventional methods and it can be presented in liquid or solid form, for example, in the form of a granulate. Additionally, said composition may contain additives, for example, preservatives and stabilizers that prolong the preservation and stability thereof.
- Said antifungal composition can be used to control infections caused by fungi that can develop in food preparations, for example, on the surface of food preparations. Therefore, the invention also provides a method of controlling infection caused by a fungus capable of developing in a food preparation, in particular, a fungus capable of developing in a food preparation whose cell membrane contains ergosterol, which comprises applying to said food preparation. , or to the surrounding environment, said antifungal composition to control said fungus capable of developing in a food preparation.
- said method comprises the application of said composition, in a suitable amount, on the surface of the food preparation in order to prevent and / or treat the food spoil due to physical growth.
- Said antifungal composition is applied externally on the surface of the food preparation.
- Plasmid pSM743B (Table 1, Example 1) ( Figure IA) is derived from plasmid pIJ922 and comprises the rimA gene and the erythromycin resistance (ermE) gene. Plasmid pSM784 (Table 1, Example 1) ( Figure IB) is derived from plasmid pIJ941 and contains the erythromycin resistance gene (ermE).
- Such plasmids pIJ922 and ⁇ IJ941 are vectors derived from the SCP2 * replicon, a low copy plasmid from Str-eptomyces coelicolor.
- the invention relates to a process for the production of a compound of formula (I-1), which comprises culturing a microorganism selected from Streptomyces diastaticus var. 108/784, Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var. 108 :: PMl-500 / 743B and combinations thereof, under conditions that allow the production of compounds of formula (I), and, if desired, isolate and purify said compounds.
- the compounds of formula (I) are selected from rimocidine B (I-la), CE-108B (I-lb) and mixtures thereof.
- the formation of the amide group in polyenes is due to an "adornment" activity due to an amidotransferase.
- an amidotransferase activity ATP / Mg dependent and capable of using glutamine as a donor of amide groups see Example 2, section B.
- amidotransferase activity present in the acellular extracts of the genetic recombinants of S. diastaticus var. 108 has a relaxed specificity towards the substrate being able to modify not only the native substrates rimocidine (lia) and CE-108 (Hb) in their corresponding amides rimocidine B (I-la) and CE-108B (I-Ib), but which is also able to recognize heterologous substrates such as pimaricin (IVa). This did not occur for the amidotransferase activity of Streptomyces sp. RGU5.3, being only able to recognize pimaricin (IVa) as a substrate under the conditions tested.
- the free carboxyl group is fairly conserved in most typical polyenes, such as amphotericin B, nystatin, pimaricin (IVa), candicidine, etc.
- the substitution of these carboxylic groups with amide groups would probably also result in knotted polyenes with improved pharmacological properties, such as higher water solubility, higher antifungal activity, and lower hemolytic activity. In short, the compounds would have greater selective toxicity against fungi.
- the invention provides an enzymatic process, hereinafter enzymatic method of the invention, to obtain a polyene amidated from polyenes with free carboxylic groups in the macrolactone ring using acellular extracts of strains producing polyenes knotted by the following steps: a) fine-tuning a mixture with a substrate consisting of a polyene with free carboxylic groups or mixtures of several of them, purified or not, and a protein extract from a strain or strains producing amidated polyenes, and b ) reaction of the mixture of a) under conditions: of dependence on ATP / Mg and capable of using glutamine as a donor of amide groups, and c) purification of the aminated polyenes.
- a particular object of the invention is the enzymatic process of The invention in which the aminated polyene to be obtained is CE-108B (I-lb), rimocidine B (I-Ia) or mixtures thereof, the substrate polyene of a) is CE-108 (Hb), rimocidine (lia) or their mixtures, purified or not, and in which the extract of a) is obtained from the following strains: S. diastaticus var. 108/784 and S. diastaticus var. 108 / 743B.
- Another particular object of the invention is the enzymatic process of the invention in which the aminated polyene to be obtained is AB-400 (IVb), the substrate polyene of a) is pimaricin (IVa), purified or not, and in which the extract of a) is obtained from the following strains: S. diastaticus var. 108/784 and & diastaticus var. 108 / 743B.
- Another particular object of the invention is the enzymatic process of the invention in which the aminated polyene to be obtained is AB-400 (IVb), the substrate polyene of a) is pimaricin (IVa), purified or not, and in which the extract of a) is obtained from the strain Streptomyces sp. RGU5.3.
- the invention relates to acellular extracts from producers of amidated polyenes, carriers of an amidotransferase activity, capable of converting or in vitro "carboxylated polyenes into their corresponding amides necessary for the implementation of the enzymatic process of the invention.
- Acellular extracts are those extracts from the homogenization of cells by various mechanical procedures (usually applicable in the field of protein manipulation) and subsequent fractionation either by filtration or differential centrifugation, to have clarified containing most of the cellular components either in suspension or in solution.
- the invention relates to the acellular extracts of microorganisms S. diastaticus var. 108 / 743B, S. diastaticus var. 108/784 (DSM 17187) - both producers of the aminated polyenes CE-108B (I-lb) and rimocidine B (I-la) - carriers of an amidotransferase activity capable of converting rimocidine (lia) and CE-108 (Hb ) in addition to other heterologous substrates in their corresponding amides; and the acellular extract of the microorganism Streptomyces sp. RGU5.3 (producer of the aminated polyene AB-400 (IVb)), capable of converting at least pimaricin (IVa) into its corresponding amide AB-400 (IVb) under the conditions tested.
- DSM 17187 both producers of the aminated polyenes CE-108B (I-lb) and rimocidine B (
- the enzymatic process of the present invention can be performed using conventional methods of immobilized enzyme systems (acellular extract of the invention) on solid supports by flowing the components of the reaction with the corresponding mobile phases, following the technology of the field of immobilized systems known by an average technician in the sector.
- immobilized enzyme systems acellular extract of the invention
- CE-108C CE-108C (HIb) are present in the fermentation broth of the microorganism identified in this description as Streptomyces diastaticus var. 108 :: PMl-768 / 743B, obtained by disruption of the rimG gene by homologous recombination with the recombinant phage PMl -768 (see Table 1, Example 2) and by transfer of plasmid pSM743B by conjugation from the Streptomyces diastaticus var. 108 / 743B as shown in Table 1, Example 1.
- Both the fragment to generate the disruption of the rimG gene, and the fragment containing the complete rimA gene to avoid polar effects can easily be obtained by people with some ability in the field, by conventional techniques of amplification of deoxyribonucleic acid (DNA).
- DNA deoxyribonucleic acid
- the strain deposited in Deutsch Sammlung von Mikroorganismen und Zellkulturen GMBH (DSMS), Braunschweig, Germany (accession number DSM 17187) can be used.
- the corresponding vectors can be introduced by conventional techniques (transformation, transfection, conjugation, etc.) into strain DSM 17187 indicated above.
- the recombinant phage PMl -768 was obtained from the phage
- Said compounds rimocidin C (Illa) and CE-108C (HIb) can be obtained directly from the fermentation broth of the microorganism Streptomyces diastaticus var. 108 :: PMl-768 / 743B and easily purified by relatively simple conventional procedures, for example, by using hydrophobic or reverse phase interaction columns.
- the invention relates to a process for the production of a compound of formula (III), which comprises the following steps: culture of the microorganism Streptomyces diastaticus var. 1O8 :: PM1-768 / 743B under conditions that allow the production of compounds of formula (III), obtaining the fermentation broth and, if desired, the isolation and purification of said compounds of formula (III).
- the process is carried out to obtain the compounds of formula (III) that are selected from rimocidine C (Illa), CE-108C QEb) and mixtures thereof.
- the culture medium of said recombinant microorganism comprises, in general, one or more carbon sources, one or more nitrogen sources, one or more inorganic salts assimilable by the microorganism, and, if necessary, one or more organic nutrients, such as vitamins and amino acids, dissolved in an aqueous medium.
- Said means, as well as the appropriate conditions are known to those skilled in the art.
- Illustrative, non-limiting examples of the means and conditions for growing said recombinant microorganism are mentioned in Example 2 of the invention (section "Experimental procedures").
- the fermentation broth of said recombinant microorganisms Streptomyces diastaticus and ⁇ X.
- SUS functional equivalents comprises a compound selected from a compound of formula (III), for example, rimocidine C (Illa), CE-108C (HIb) and mixtures thereof, and can be used as such or It may well be subsequently treated to separate the compound of interest, which can be isolated by conventional methods.
- the cell culture is centrifuged to separate the supernatant and the cell extract and the supernatant is used to isolate and, if desired, purify, the polyene, amidated or non-amidated, of interest.
- the study of the physical-chemical characteristics of said compounds allows a technician to design a procedure for purification from the supernatant.
- the invention relates to a microorganism selected from Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var. 108/784 and Streptomyces diastaticus var. 108 :: PMl-500 / 743B 5 and provides a culture of a microorganism selected from Streptomyces diastaticus var.
- the invention relates to the use of a microorganism selected from Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var. 108/784, Streptomyces diastaticus var. 108 :: PMl-500 / 743B and combinations thereof, or of said culture of microorganisms selected from Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var.
- the compound of formula (I-1) is selected from rimocidine B (I-Ia), CE-108B (I-Ib) and mixtures thereof.
- the tests carried out by the inventors showed that the fermentation broth of said recombinant microorganisms Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var. 108/784 and Streptomyces diastaticus var. 108 :: PMl-500 / 743B also contains, in addition to the knotted polyamines rimocidine B (I-la) and / or CE-108B (I-lb), the non-knotted polyenes rimocidine (lia) and / or CE-108 ( Hb), which contain a free carboxyl group.
- the invention relates to a process for the production of a compound selected from a compound of formula (I), rimocidine (lia), CE-108 (Hb) and mixtures thereof, which comprises culturing a microorganism. selected from Streptomyces diastaticus var. 108 / 743B, Streptomyces diastaticus var. 108/784, Streptomyces diastaticus var. 108 :: PMl-500 / 743B and combinations thereof, under conditions that allow the production of a compound selected from a compound of formula (I), rimocidine (lia), CE-108 (Hb) and mixtures thereof, and, if desired, isolate and purify said compound.
- the compound of formula (I) is selected from rimocidine B (Ila), CE-108B (I-lb) and mixtures thereof.
- the compound of formula (I) is selected from rimocidine B (Ila), CE-108B (I-Ib) and mixtures thereof.
- the culture medium of said recombinant microorganisms comprises, in general, one or more carbon sources, one or more nitrogen sources, one or more inorganic salts assimilable by the microorganism, and, if necessary, one or more organic nutrients, such as vitamins and amino acids, dissolved in an aqueous medium.
- Said means, as well as the appropriate conditions are known to those skilled in the art.
- Illustrative, non-limiting examples of the means and conditions for growing said recombinant microorganisms are mentioned in the Example (section "Experimental procedures").
- the fermentation broth of said recombinant microorganisms selected from Streptomyces diastaticus var.
- 108 / 743B Streptomyces diastaticus var. 108/784, Streptomyces diastaticus var. 108 :: PMl-500 / 743B and combinations thereof, comprises a compound selected from a compound of formula (I), for example, rimocidine B (I-la), CE-108B (I-Ib), rimocidine (lia ), CE-108 (Hb) and mixtures thereof, and can be used as such or it can be subsequently treated to separate the compound or compounds of interest, which can be isolated by conventional methods.
- a compound of formula (I) for example, rimocidine B (I-la), CE-108B (I-Ib), rimocidine (lia ), CE-108 (Hb) and mixtures thereof, and can be used as such or it can be subsequently treated to separate the compound or compounds of interest, which can be isolated by conventional methods.
- the cell culture is centrifuged to separate the supernatant and the cell extract and the supernatant is used to isolate and, if desired, purify, the polyene, amidated or non-amidated, of interest.
- the study of the physicochemical characteristics of said compounds allows to design a procedure for purification from the supernatant.
- the microorganism Streptomyces diastaticus var. 108 :: PMl-768 / 743B, or any other functional equivalent are part of the present invention. Therefore, in another aspect, the invention relates to the microorganism Streptomyces diastaticus var. 108 :: PMl-768 / 743B or functional equivalents useful for carrying out the procedure for obtaining the compounds of formula (III) and providing a culture of these microorganisms.
- a particular embodiment of the invention is the Streptomyces diastaticus var.
- the term "functional equivalent” refers to an element - be it a microorganism, vector, genetic construct, or fragment of a gene, method of disruption of a gene, of genetic transformation of a cell or microorganism, as the case may be - that can be developed by an average technician in the field with the different existing alternatives and that has identical or homologous characteristics to the original element referred to.
- “functional equivalent / s” means those recombinant microorganisms that can be obtained either by chromosomal deletion of the rimG gene, rather than inactivating insertion or with any other technique; said deletion can be easily made by using conventional vectors either non-replicative plasmids or being replicative with thermosensitive origin of replication. These deletions or insertions can be made by a technician with some experience in the field.
- the invention relates to the use of the microorganisms Streptomyces diastaticus var. 108 :: PMl-768 / 743B or its functional equivalents for obtaining a compound of formula (III).
- the compound of formula (III) is selected from rimocidine C (Illa), CE-108C (IHb) and mixtures thereof.
- the fermentation broth thus obtained with the process of the invention can be used directly for the preparation of certain biocidal solutions, without the need to purify the compounds of the present invention.
- the fermentation broth of the microorganisms Streptomyces diastaticus var. 108 :: PMl-768 / 743B or its functional equivalents indicated above, which comprises a compound of formula (III) may be potentially useful as a biocide and constitutes an additional aspect of this invention.
- Plasmid pSM784 derived from vector pIJ941 on which the erythromycin resistance gene has been cloned, when introduced into S. diastaticus var. 108, gives place to a strain (S. diastaticus var. 108/784) producing the new rimocidine B (I-la) and CE-108B (I-lb) amidated polyenes, in addition to rimocidine (lia) and CE-108 (Hb) .
- plasmid pSM743B derived from an SCP2 * vector plus the ermE and carrier gene, in addition to a fragment of the rim cluster (comprising the rim ⁇ gene) expressed under a promoter, endogenous or exogenous, such as the xysA promoter
- the invention relates to a vector, hereinafter vector of the invention, selected from: a) a vector derived from the vector SCP2 *, or a fragment thereof, which comprises the origin of replication of SCP2 * and the erythromycin resistance gene (ermE); b) a vector comprising (i) the origin of replication of the vector SCP2 *, (ii) the ermE gene, and (iii) a fragment of the vector SCP2 *; c) a vector comprising (i) an origin of replication, (ii) the ermE gene, and (iii) a fragment of the vector SCP2 *, wherein said origin of replication is different from the origin of replication of the vector SCP2 *; d) a vector that has no origin of replication and comprises the ermE gene and a fragment of the vector SCP2 *; e) a vector derived from the vector SCP2 * comprising (i) an origin of replication, (ii) the ermE gene
- Virtually any vector derived from the vector SCP2 * can be used, for example, pIJ922, pIJ941, etc.
- the ermE gene is a known gene (Uchiyama et al.,
- the term "SCP2 * vector fragment” refers to a nucleic acid comprising one or more SCP2 * fragments sufficient to induce the formation of knotted polyenes. Tests carried out by the inventors have shown that a nucleic acid comprising one or more fragments of the SCP2 * vector, together with the ermE gene, is necessary and sufficient for the aminated polyenes to be generated in recombinant microorganisms.
- the vector of the invention is a replicative vector derived from SCP2 *, which contains the origin of SCP2 * replication, and is also a carrier of the ermE gene, for example, pSM784.
- Said plasmid may be introduced by conventional methods (eg, transformation, electroporation, conjugation, etc.) into microorganisms producing polyane macrolides containing a free carboxyl group (eg, amphotericin B, nystatin, rimocidine, pimaricin, candicidine, etc.), in order to produce the corresponding aminated polyenes.
- microorganisms include S. noursei, S. albidus, S. rimosus, S. nodosus, S. natalensis, S. chattanoogensis, S.griseus, etc.
- the vector of the invention is a replicative vector comprising the origin of replication of the vector SCP2 *, the ermE gene and a fragment of the vector SCP2 *.
- the vector of the invention is a replicative vector comprising an origin of replication different from the origin of replication of SCP2 *, the ermE gene and a fragment of the vector SCP2 *.
- the vector of the invention is an integrative or non-replicative vector that has no origin of replication and comprises the ermE gene and a fragment of the vector SCP2 *.
- the vector of the invention is a replicative vector. comprising 'a replication origin equal to or different from the replication origin of SCP2 * vector, the gene ermE and the entire biosynthetic cluster of a polyene or a fragment of said cluster.
- the vector of the invention is a replicative vector comprising an origin of replication equal to or different from the origin of replication of the vector SCP2 *, the ermE gene, a fragment of the vector SCP2 * and the entire biosynthetic cluster of a polyene or a fragment of said cluster.
- the vector of the invention is an integrative or non-replicative vector that has no origin of replication and comprises the ermE gene and the entire biosynthetic cluster of a polyene or a fragment of said cluster.
- the vector of the invention is an integrative or non-replicative vector that lacks origin of replication and comprises the ermE gene, a fragment of the vector SCP2 * and the entire biosynthetic cluster of a polyene or a fragment of said cluster .
- vectors of the invention comprising the entire biosynthetic cluster of a polyene or a fragment thereof are used to transform polyene producing microorganisms with free carboxyl groups, the production of knotted polyenes and / or an increase in the total production of both amidated polyenes such as non-amidated polyenes, whereby said vectors can be used to increase the total production of polyenes with free carboxylic groups and / or aminated polyenes in polyene producing organisms.
- any biosynthetic cluster of a polyene or fragment thereof can be present in the vector of the invention; however, in a particular embodiment said vector comprises the entire rim cluster, rimocidine biosynthetic, or a fragment thereof (Seco E.M., et al., 2004, Chem. Biol. 11: 357-366). Although any fragment of the rim cluster can be used, in a specific embodiment, said fragment of the rim cluster comprises the rimA gene of the rim cluster.
- Said biosynthetic cluster of a polyene or fragment thereof may, optionally, be under the control of a promoter (ie, operatively linked to said promoter so as to direct the expression of the gene it controls).
- Said promoter can be endogenous or exogenous.
- said exogenous promoter is a functional promoter in Streptomyces sp., such as the xysA (xysAp) promoter of the Streptomyces halstedü JM8 xylanase gene (Ruiz-Arribas A., et al., 1997, Appl. Environ.
- Plasmid pSM743B is an illustrative example of this type of vectors of the invention.
- the vectors of the invention can be obtained by conventional methods known to those skilled in the art (Sambrook et al., Molecular Cloning. A Laboratory Manual, CoId Spring Harbor, NY, 1989).
- the vectors of the invention can be used to generate amidated or non-amidated polyenes in polyene producing microorganisms containing a free carboxyl group.
- combinations of vectors containing, on the one hand, (i) a vector comprising a biosynthetic cluster of a polyene, such as the rim cluster, or a fragment thereof, and, on the other hand, (ii) a derived vector of SCP2 * comprising the ermE gene, or a vector comprising an origin of replication different from that of SCP2 *, the ermE gene and a fragment of the vector SCP2 *, can be introduced into microorganisms producing polyane macrolides having carboxyl groups, to generate aminated or non-amidated polyenes in said microorganisms.
- the invention relates to the use of a vector of the invention to be introduced, by conventional methods, into microorganisms producing polyethylene macrolides containing free carboxyl groups (eg, amphotericin B, nystatin, rimocidine, pimaricin , candicidine, etc.), in order to produce the corresponding amidated polyenes from the corresponding recombinant microorganisms generated.
- a vector of the invention to be introduced, by conventional methods, into microorganisms producing polyethylene macrolides containing free carboxyl groups (eg, amphotericin B, nystatin, rimocidine, pimaricin , candicidine, etc.), in order to produce the corresponding amidated polyenes from the corresponding recombinant microorganisms generated.
- free carboxyl groups eg, amphotericin B, nystatin, rimocidine, pimaricin , candicidine, etc.
- Microorganisms likely to be used as hosts of the vectors of the invention include polyene-producing microorganisms that have a free carboxyl group such as Streptomyces nodosus, a natural producer of amphotericin B; Streptomyces rimosus, producer of rimocidine; Streptomyces griseus, producer of candicidine; Streptomyces natalensis, producer of pimaricin; Streptomyces noursei, nystatin producer, etc.
- polyene-producing microorganisms that have a free carboxyl group such as Streptomyces nodosus, a natural producer of amphotericin B; Streptomyces rimosus, producer of rimocidine; Streptomyces griseus, producer of candicidine; Streptomyces natalensis, producer of pimaricin; Streptomyces noursei, nystatin producer, etc.
- the invention in another aspect, relates to a process for obtaining recombinant microorganisms producing polyethylene macrolides containing an amide group comprising introducing a vector of the invention into microorganisms producing polyethylene macrolides containing free carboxyl groups.
- said recombinant microorganisms producing macrolides polyenes containing an amide group can be obtained by introducing into polysaccharide producing microorganisms polyenes containing free carboxyl groups combinations of vectors containing, on the one hand, (i) a vector comprising a biosynthetic cluster of a polyene, such as the rim cluster, or a fragment thereof, and, on the other hand, (ii) a vector derived from SCP2 * comprising the ermE gene, or a vector comprising an origin of replication different from that of SCP2 *, the ermE gene and a fragment of the SCP2 * vector, can be introduced into microorganisms producing polyane macrolides that have carboxyl groups, to generate knotted or non-knotted polyenes in said microorganisms.
- microorganisms of the invention or combinations of vectors into said microorganisms can be carried out by conventional techniques known to those skilled in the art, eg, transformation, electroporation, conjugation, etc.
- Illustrative, non-limiting examples of microorganisms producing polyane macrolides containing free carboxyl groups include various species of Streptomyces, for example, S. noursei, S. rimosus, S. nodosus, S. natalensis, S. griseus, etc.
- Recombinant microorganisms obtained as previously indicated, hereinafter recombinant microorganisms of the invention, form part of the present invention and constitute an additional aspect of this invention.
- the invention in another aspect, relates to a process for producing a polyene macrolide comprising culturing a recombinant microorganism of the invention under conditions that allow the production of said polyene macrolide, and, if desired, isolating and purifying said compound.
- said polyene macrolide is selected from a polyene macrolide containing a free carboxyl group, a polyene macrolide containing an amide group and mixtures thereof.
- polyene macrolides containing an amide group are compound AB-400 (IVb) and compounds of formula (1-1), for example, rimocidine compounds B (I-la), CE-108B (I-lb ) and their mixtures.
- formula (I) for example, compounds selected from pimaricin (IVa), AB-400 (IVb), rimocidine (lia), rimocidine B (I-la), CE-108 (Hb), CE-108B (I-lb) and mixtures thereof.
- Said recombinant microorganisms will be grown in any medium suitable for the fermentation of said microorganisms and will contain, in general, one or more carbon sources, one or more nitrogen sources, one or more inorganic salts assimilable by the microorganism, and, if necessary, one or more organic nutrients, such as vitamins and amino acids, dissolved in an aqueous medium, and the appropriate conditions (aeration / agitation, temperature and fermentation time, stages, etc.) for the growth of microorganisms and the production of polyane macrolides.
- the polyene macrolides obtained are secreted to the culture medium from where they can be recovered by conventional procedures, for example, by the use of chromatographic methods, optionally after removal of the cell extract.
- the polyene / s amidated / s of interest can be separated based on their physical-chemical characteristics, which allows to design a procedure for purification from the culture medium after the fermentation process.
- the invention also relates to the use of recombinant phage PM1-768B, derived from actinophage PMl (Malpartida and Hopwood (1986) Mol. Gen. Genet. 205: 66-73) on which a fragment of DNA internal to the rimG gene has been cloned together with the ermEp promoter; the promoter in front of the fragment internal to the gene avoids possible polar effects on the genes located next to the insertion point.
- a DNA fragment containing another functional promoter activity for Streptomyces can be used, cloned in front of any fragment internal to the rimG gene or obtained by amplification of the chromosomal DNA of the producer of rimocidine (lia) and CE-108 (Hb); the resulting construct can be cloned interchangeably in the PMl vector or in another non-replicative vector in Streptomyces (or being replicative subject to culture conditions where the vector does not replicate, such as thermosensitive replication plasmids), according to the methodology used in the field to which any operator with experience in the field has access.
- 108 / PM 1-768) (or other functionally equivalent that could be generated by the procedures indicated above) should be a producer of intermediates of the biosynthetic pathway of rimocidine (lia) and CE-108 (Hb), since the insertion inactivating, it would only affect the ability of the recombinant to complete the oxidation of the methyl side group introduced by module 7 of the polyketide synthetase rimocidine (lia) and CE-108 (Hb) (Seco et al 2004, Chem Biol., Cited supra). However, under these first conditions, and unexpectedly the disruption in the rimG gene generated generated a recombinant unable to produce polyenes.
- the disrupter must be supplemented with plasmid pSM743B or another functionally equivalent vector, capable of complementing a disruption of the rimA gene on the chromosome.
- the genetic recombinant thus obtained would contain an additional copy of the rimA gene in plasmid pSM743B (or another functionally equivalent vector) in addition to the chromosome located following the disruption of the rimG gene.
- Plasmid pSM743B (or another functionally equivalent vector, as indicated above) can be transferred by any technique usually available for Streptomyces manipulation (transformation of protoplasts, infection, conjugation, etc.). Once the constructs were confirmed, HPLC analyzes of the fermentation broth of the resulting strain (Streptomyces diastaticus var.
- rimocidine C Illa
- CE -108C IHb
- CE-108 Ub
- the rimG gene mutation can be performed by deletion of an internal fragment to the rimG gene, following conventional techniques for use for manipulation from Streptomyces.
- the present invention relates to a method of obtaining the strain of the invention producing methylated polyenes S. diastaticus var. 108 :: PMl-768 / 743B or its equivalents in which the resulting strain is exclusively affected in the expression of the rimG gene and because it comprises the following steps: a) Obtaining a mutant in the rimG gene of the S. diastaticus var. 108 or its functional equivalents by disruption or deletion of said gene, unable to produce polyenes, and b) its subsequent transformation with a vector, preferably a plasmid, capable of complementing the disruption of the rimA gene on the chromosome in said mutant.
- a vector preferably a plasmid
- the invention relates to a method of obtaining the microorganism of the invention in which the mutant of step a) is obtained by using the recombinant phage PMl-768 or any other inactivating system that is functionally equivalent to generate disruption or deletion of the rimG gene of the S. diastaticus var. 108 and in which step b) is performed with plasmid pSM743B (or functionally equivalent vector as indicated above) to complement the possible polar effect of the rimA gene on the recombinant chromosome.
- the invention relates, in another aspect, to the disruption of the rimG gene on the chromosome of Sfreptomyces diastaticus var. 108 by any conventional method and using any appropriate vector.
- Such interruption may be carried out using a strong promoter to avoid a polar effect such as the ermEp promoter (Kieser et al. (2000) Practical Streptomyces
- the invention relates in another aspect to the disruption in other polyene producers of the gene coding for the cytochrome P450 monooxygenase involved in this same oxidation (formation of the carboxyl group from the methyl group of the corresponding polyenes) in order to obtain derivatives methylated thereof. It is described that a cytochrome P450 monooxygenase is involved in this oxidation, and is encoded in the biosynthetic clusters of polyenes described so far (Aparicio et al., 2003, Appl Microbiol Biotechnol 61: 179-188). Some genes involved in this oxidation have already been described, including the genespimG (Aparicio et al, 2000, Chem. Biol.
- the invention relates to a method for obtaining microorganisms producing methylated polyethylene macrolides which comprises interrupting the gene coding for the cytochrome P450 monooxygenase involved in the formation of the free carboxyl group - gene homologous to the described gene.
- HmG in other strains - in microorganisms producing polyene macrolides containing free carboxyl groups, using for this purpose any conventional method (transformation, conjugation, electroporation, infection, etc.).
- the invention relates to the use of any vector to carry out a disruption of the gene coding for the cytochrome P450 monooxygenase involved in the formation of the free carboxyl group in microorganisms producing polyane macrolides containing free carboxyl groups, belonging among others, by way of illustration and without limiting the scope of the invention, to the following group: amphotericin B, nystatin, rimocidine, pimaricin and candicidine in order to produce the corresponding methylated polyenes.
- Streptomyces nodosus natural producer of amphotericin B
- Streptomyces rimosus producer of rimocidine
- Streptomyces griseus producer of candicidine
- Streptomyces natalensis producer of pimaricin
- Streptomyces noursei nystatin producer.
- the invention relates to the adequate expression of genes that could have been affected by a polar effect when disruption of the corresponding gene is carried out, using any vector as a vehicle (replicative plasmids, integrative plasmids, actinophages, etc.) and being introduced by any of the conventional methods (transformation, conjugation, electroporation, infection, etc.).
- vectors for example, S. noursei, S. rimosus, S. nodosus, S. natalensis and S. griseus.
- the invention in another aspect, relates to a process for producing a methylated polyene macrolide comprising culturing a genetically engineered microorganism of the invention under conditions that allow the production of said methylated polyene, and, if desired, isolating and purifying said compound which It is by way of illustration and without limiting the scope of the invention, to the following group: methylated amphotericin B, methylated nystatin, methylated pimaricin and methylated candicidine.
- Another additional object of the present invention is any of these new methylated polyenes, methylated amphoteric B, methylated nystatin, methylated pimaricin and methylated candicidine, which can be used for the preparation of biocidal and pharmacological compositions as in the case of rimocidin C and CE-180C.
- Said genetically engineered microorganisms will be grown in any medium suitable for the fermentation of said microorganisms and will contain, in general, one or more carbon sources, one or more nitrogen sources, one or more inorganic salts assimilable by the microorganism, and, if it is necessary, one or more organic nutrients, such as vitamins and amino acids, dissolved in an aqueous medium, and appropriate conditions (aeration / agitation, temperature and fermentation time, stages, etc.) will be applied for the growth of microorganisms and production of polyene macrolides.
- the polyene macrolides obtained are secreted to the culture medium from where they can be recovered by conventional procedures, for example, by the use of chromatographic methods, optionally after removal of the cell extract.
- the methylated polyene / s of interest can be separated based on their physical-chemical characteristics, which allows to design a procedure for purification from the culture medium after the fermentation process.
- Compound AB -400 (IVb), the amide corresponding to pimaricin (I Va), is a known natural product from Streptomyces costae (Ca ⁇ edo LM et al, 2000, J. Antibiot. (Tokyo) 53: 623-626) .
- amidated polyenes are significantly more soluble in water than non-amidated homologs. This characteristic together with the pharmacological properties described above make this compound susceptible to being used clinically, for topical or systemic treatment of mycosis or parasitosis; and, in the agri-food industry.
- the invention relates to a pharmaceutical composition
- a pharmaceutical composition comprising the compound AB-400 (IVb) together with, optionally, one or more pharmaceutically acceptable excipients.
- said pharmaceutical composition may also contain one or more therapeutic agents that, if necessary, enhance the therapeutic action of said compound AB -400 (IVb), or increase its spectrum of action.
- Said pharmaceutical composition can be used to prevent and / or treat infections caused by pathogenic organisms of humans or animals that possess ergosterol-containing cell membranes, for example, parasites and pathogenic fungi of humans or animals.
- said pharmaceutical composition is an antiparasitic composition and can be used in the prevention and / or treatment of infections caused by parasites whose cell membranes contain ergosterol, for example, Trypanosoma, Leishmania, etc.
- said antiparasitic composition may also contain one or more antiparasitic agents that, eventually, enhance the therapeutic action of said compound AB-400 (IVb) or increase its spectrum of action.
- said pharmaceutical composition is an antifungal composition and can be used in the prevention and / or treatment of fungal infections (whose cell membranes contain ergosterol).
- said antifungal composition may also contain one or more antifungal agents that, if necessary, potentiate the antifungal action of said compound AB -400 (IVb), or increase its spectrum of action.
- antifungal agents include polyenes, such as amphotericin B, nystatin, AB-400 (IVb), allylamines (eg 5 terbinafma, naphthifine, etc.), amorolfia, tolnaphthalate, etc .; azoles, such as clotrimazole, miconazole, ketoconazole, fluconazole, itxaconazole, etc .; benzofurans, for example, griseo ⁇ ilvina, etc .; pyrimidines, for example, fluocytosine, etc .;
- Compound AB-400 (IVb) will be present in said pharmaceutical composition in a therapeutically effective amount, that is, in an amount appropriate to exert its therapeutic effect.
- the pharmaceutical composition provided by this invention contains between 0.01% and 99.99% by weight of compound AB -400 (IVb), and can be presented in any pharmaceutical form of appropriate administration depending on the route of chosen administration, for example, oral, parenteral or topical.
- a review of the different pharmaceutical forms for drug administration and their preparation methods can be found, for example, in the Tratado de Farmacia Galenica, C. Fauli i Trillo, I Edition, 1993, Luzan 5, SA de Ediations.
- the invention also relates to the use of AB -400 (IVb) in the preparation of a medicament for the prevention and / or treatment of infection caused by pathogenic organisms of humans or animals whose cell membranes contain ergosterol, by for example, parasites of humans or animals or pathogenic fungi of humans or animals.
- the invention also provides a method for preventing and / or treating infections caused by pathogenic organisms of humans or animals whose cell membranes contain ergosterol, for example, parasites of humans or animals or pathogenic fungi of humans or animals, which comprises the step of administering to an animal or a human being, in need of treatment, a therapeutically effective amount of a pharmaceutical composition provided by this invention comprising the compound AB-400 (IVb).
- Streptomyces diastaticus var. 108 and its derivatives by genetic modification were routinely grown in liquid and solid medium SYM2 (Atlas R.M.,
- Streptomyces lividans TK21 was used as a general cloning host and grown in a solid R5 medium and YEME liquid medium as described in field manuals (Kieser T. et al, 2000, Practical Streptomyces Genetics, Norwich).
- E. coli strains were grown on Luria-Bertani agar (LB) or in LB broths as described in the specialized literature (Maniatis T. et al., 1982, Molecular Cloning: A Laboratory Manual, CoId Spring Harbor Laboratory Press, CoId Spring Harbor, NY).
- This invention with plasmid pSM743B; Producer of CE-108, rimocidine, CE-108B and rimocidine B
- This invention plasmid pSM784; Producer of CE-108, rimocidine,
- This invention replicates pHisl Vector in E, coli transporting the promoter
- This invention pSM784 1.8 kb SspI-EcoRV fragment of pGAe-1 (gene of this invention ermE resistance) cloned into the EcoRV site of pIJ941 (see Figure 1) Ap, ampicillin; Km, Kanamycin; ermE, tsr and hyg: genes for resistance to erythromycin, thioestreptone and hygromycin B
- Tests for the production of tetraenes The production of tetraenes was analyzed by extracting all of an aliquot from the culture with methanol as previously described (Seco E.M. et al., 2004, cited supra). The extracts were filtered and subjected to HPLC analysis with a Waters 600S Controller, equipped with Waters 996 PDA; The quantitative determination and chromatographic conditions were the same as those previously described (Pérez-Z ⁇ fiiga F.J., et al., 2004, cited above).
- HPLC-MS assays Mass spectra were determined on an HPLC 1100MSD equipment connected to an Agilent Technology Detector quadrupole detector, using electrospray as a source and a positive ionization mode. The chromatographic conditions were the same as previously described (Pérez-Z ⁇ iga FJ., Et al., 2004, cited supra).
- Streptomyces diastaticus var. 108/784, or possibly modified microorganisms with constructs capable of producing the amidated polyenes (as indicated above) were grown or cultivated either in SYM2 medium, solid or liquid (Pérez-Z ⁇ iga FJ, et al., 2004, cited supra ). After six days, the complete solid medium where the microorganisms were grown, was fragmented by shear by passing it through a 50 mL syringe; The solid medium thus fragmented was extracted with four volumes of methanol, previously acidified with 25 mM formic acid. The cultures from liquid medium were lyophilized before performing similar extractions with methanol.
- the aqueous suspension was stirred for 1 hour and centrifuged at 5,000 g for 20 minutes to remove the solid particles in suspension.
- the transparent supernatant was concentrated by broken-evaporation at 10-20 X 10 6 units per microliter ( ⁇ L) measured at a wavelength of 304 nanometers (nm).
- the sample was subsequently stored in 80% methanol / water until it was used. Two hundred milliliters of the liquid cell culture or a plate (24 x 24 cm) whose culture was previously extracted with 5 volumes of methanol, resulted in a production of up to 40 mg of the amidated tetraenes mixture. Samples extracted in methanol were taken to 20% methanol with water and filtered to remove precipitated material.
- the filtrate was slowly applied to an Omnifit column (250 x 25 mm, Supelco Cat No. 56010) previously filled with an ion exchange resin, such as SP-Sepharose, Phast Flow (Pharmacia) that was previously equilibrated with the same solution.
- an ion exchange resin such as SP-Sepharose, Phast Flow (Pharmacia) that was previously equilibrated with the same solution.
- rimocidine and compound CE-108 eluted with the front not attached to the column filler, as well as pigments from the culture; the corresponding rimocidine B (Ila) and CE-108B (I-Ib) amidated polyenes were completely retained.
- the column, containing the compounds of interest retained in the solid phase was washed thoroughly with the same solution to remove those compounds that do not interact with the SP Sepharosa filler.
- rimocidine B (I-la) and CE-108B (I-lb) aminated polyenes retained by column interaction, are eluted with 300 mM ammonium acetate pH 5 in 20% methanol collecting fractions at regular time intervals. From the eluted fractions, those containing mixtures of the amides of interest were selected; they got together and underwent a physical desalination process, using Sep-Pak (Waters) cartridges. Finally the desalinated fractions were dissolved in 20% methanol.
- the chromatographic parameters and the mobile phases controlled with an automatic gradient controller (Waters Automated Gradient Controller), were: 12 minutes with 100% B (20 mM ammonium acetate pH 5, 20% ethanol), 43 minutes of a binary gradient up to 50% of A (methanol) and 50% of B (curve 6 specified in Waters chromatographic controllers); 35 minutes of a binary gradient up to 100% of A (curve 8, of the same controllers mentioned above), and a constant flow of 5 mL / min.
- the fractions were collected at regular intervals (5 mL per fraction) and those carrying purified isolated compounds were pooled and subjected to an additional desalination stage, as described above and, finally, lyophilized twice.
- AB-400 (Ca ⁇ edo LM et al., 2000, J. Antibiot. (Tokyo) 53: 623-626) was also purified, from the liquid cultures of Sfreptomyces sp. RGU5.3, as described above.
- the HmA gene (Seco EM et al., 2004, Chem. Biol. 11: 357-366), encoded within a polycistronic mRNA, was cloned under the control of the xysA (xys Ap) promoter of the Streptomyces halstedii xylanase gene JM8 (Ruiz-Arribas A., 1997, Appl. Environ. Microbiol. 63: 2983-2988).
- the xys Ap promoter was rescued from pHisl as a 547 base pair BgRl / Smal fragment which also carries the terminator of the methyleneomycin resistance gene (Tl: Adham SA et al., 2001, Arch. Microbiol. 177: 91-97) located in position prior to the xys Ap promoter.
- the DNA fragment containing the rimA gene and the 3 'end of the HmI gene was merged with xys Ap in the appropriate orientation that allowed to express the HmA under the promoter xys Ap (recombinant rimA).
- the pNAe-1 ermE gene (Table 1) was rescued by digestion with the flanking enzymes and the resulting DNA fragment was cloned, in intermediate stages, following the "rimA recombinant" gene to generate, in the final construction, a DNA fragment containing (see Figure IA), from left to right: the rimA gene under the control of the xysAp promoter, the truncated riml gene fragment and finally the complete ermE gene.
- the resulting DNA fragment was cloned, via blunt ends, according to the usual technique in Molecular Biology, at the unique EcoKV restriction site, located within the thioestreptone resistance gene, of the Streptomyces pIJ922 vector.
- the resulting plasmid (pSM743B, Figure IA) confers resistance to erythromycin but not thioestreptone by having the corresponding thioestreptone resistance gene interrupted by insertion of the DNA fragment described above.
- 108 mutant with the previously unbroken rimA gene is capable of producing the native polienic macrolides (rimocidine and CE-108), as well as the new amidated macrolides ( rimocidine B and CE-108B).
- the plasmid pSM743B introduced into the silves ⁇ re strain also induced the production of the four tetraenes (amidated and carboxylated) but with an increase in the io ⁇ al production of polyenes probably due to the expression of biosin ⁇ icos genes of the clus ⁇ er Hm.
- plasmid pSM784 was considered.
- the errriE gene was cloned, following the usual technology in Molecular Biology and, in successive eiapas, in suitable vectors of Escherichia coli to obtain the complete ermE gene capable of being rescued as a fragment of blunt-end DNA.
- the DNA fragment containing the ermE gene in a DNA fragment with blunt ends was cloned into the unique EcoRV restriction site of vector pIJ941.
- the resulting vector confers resistance to erythromycin and hygromycin B although it is sensitive to thioestreptone by interrupting the resistance gene to it by inactivating insertion of the ermE gene fragment (see Figure IB).
- the resulting recombinant microorganism is capable of producing, in addition to the macrolides rimocidine (lia) and CE-108 (Hb), the new amidated polyenes CE-108B (I-lb) and rimocidine B (I-la).
- the genetic modified Streptomyces diastaticus var. 108 containing the vector pSM743B or the vector pSM784 produce both the original polyenes (rimocidine and CE-108) as well as the new aminated polyenes (CE-108B and rimocidine B), with a chromatographic profile, analyzed in HPLC, similar, as indicated in Figure 1 C. Although qualitatively both genetic recombinants produce the same polyenes, their production is significantly higher in those recombinants that contain the rimA gene and the erythromycin gene (plasmid pSM743B).
- Two interchangeable protons appeared at ⁇ 7.30 and 6.83 as wide singles.
- the rimocidine B (Ila) powder was dissolved in DMSO.
- the mass spectrum (+) - ESI MS set the molecular weight of rimocidine B (Ila) as 766, which corresponds, by high resolution, to the molecular formula C 39 H 6 2N 2 O 13 (found 767.43254, calculated 767.43301 for [M + N] + ).
- the 1 H-NMR spectrum was similar to that of CE-108B (I-lb) and showed two interchangeable H / D protons at ⁇ 7.30 and 6.83, two doublet doublets and one multiplet in the ⁇ 6 range , 40-5.80.
- the antifungal activity of the new amidated tetraenes [rimocidin B (Ila) and CE-108B (I-lb)] was tested against several fungi: Penicillium chrysogenum, Candida albicans, Aspergillus niger, Candida h'usei and Cryptococcus neoformans. Increasing amounts of the different tetraenes, dissolved in methanol, were applied on paper discs (9 mm in diameter); after application, the discs were dried and placed on the bioassay plates in which the corresponding control fungi had previously been extended.
- the hemolytic activity of the new compounds was evaluated (see the section on Experimental Procedures) against rimocidine and EC-108; Amphotericin B and nystatin A were also included. As shown in Table 2, the hemolytic activity of the amidated tetraenes [rimocidine B (Ila) and CE-108B (1-Ib)] was not significantly different from that of the corresponding tetraenes from which they came, while their antifungal activity was clearly higher.
- Streptomyces diastaticus var, 108 a producer of two natural tetraenes (rimocidine and CE-108), acquires the ability to produce, in a natural way and as main compounds, the corresponding amides (rimocidine B and CE-108B) if properly modified by genetic manipulation.
- the conversion of the free carboxylic group into an amide group entails a clear improvement in some of its pharmacological properties (substantial increase in antifungal activity but not in hemolytic activities), thus providing a significant advantage, as antifungal agents, against native tetraenes.
- amides would be the result of an amidotransferase activity subsequent to the assembly of the polytonic chain of aglycone (activity of "adornment” or post-modification) PKS), which under the experimental conditions described in this invention could be activated, or (b) a malonamil-CoA transferase activity would incorporate, by means of the condensation module 7 of the corresponding PKS (Dry EM et al, 2004, Chem. Biol.
- the product of the ermE gene (a methylase) can act on another intermediate gene, encoded within the DNA of the plasmids derived from SCP2 * (pIJ922 or pIJ941) whose final result would be the activation of a chromosomal gene responsible for the amidation of natural polyenes of Streptomyces diastaticus var. 108 (rhinocidine and CE-108).
- the present invention provides a system for generating new polyenes amidated by biotransformation by a genetically modified strain. This process, applied satisfactorily to the biosynthetic route of commercial polyenes, would undoubtedly be a simple process for the production of improved pharmaceutical compounds. Given the complexity of the polynolic structures referred to in this invention, the biotransformation proposed in this invention to generate amidated polynolic compounds constitutes an undoubtedly more efficient process than those described so far by organic synthesis to generate some semisynthetic structures.
- Bacterial strains, cloning vectors and growth conditions Bacterial strains, cloning vectors and growth conditions
- Bacterial strains and plasmids are described in Table 1. Sti'eptomyces diastaticus var. 108 and its derivatives were grown in medium
- Streptomyces lividans TK21 was used for phage propagation and as a host strain, and was grown in a solid R5 medium and YEME liquid medium as described in field manuals (Kieser T., et al., 2000, Practical Streptomyces Genetics , Norwich).
- E. coli strain JM101 was grown in Luria-Bertani medium (LB) or in LB broth as described in the specialized literature (Maniatis T. et al., 1982, Molecular Cloning Protocol
- Penicillium chrysogenum ATCC 10003 was used to test antifungal activity and was grown in MPDA medium (composition: 2% malt extract, 2% glucose, 0.1% Bactopeptone).
- Table 1 Bacterial strains and vectors used in the invention
- S. diastaticus var. Derivatives of S. diastaticus var. 108 wild This 108 :: PMl-768 with the rimG gene interrupted by insertion invention of phage PMl -768
- S. diastaticus var. Derived from S. diastaticus var. 108 wild d 108 / PM1-500 with the rim A gene interrupted by phage integration PMl -500
- invention pHJL401 Vector for cloning contains the replicon e SCP2 * and pUC19; It contains the thiostrepton resistance gene.
- Bi Shencional E. coli / Streptomyces ⁇ EL-1 EcoRI-HMIII DNA fragment of pIJ4090 This corresponds to the ermEp promoter (ref. Invention b) cloned into the EcoRI-HmdlII site of the pHJL401 vector
- PMl Actinophage derived from ⁇ C31 (att " ), hyg, tsr f pSM743B Recombinant vector, derived from pIJ922, It is containing the rimA gene under the control of the xylanase promoter invention Xy s A.
- pCNB5006 Vector derived from pIJ2925 containing the d ermEp.
- pSM721 promoter Internal 0.7-kb (Sacl ⁇ ) DNA fragment This is the rimG gene cloned into the Hincll site of invention pIJ2925 pSM768 0.7 kb fragment of AND Hindl ⁇ l-Xbal This of the vector pSM721 cloned into the Bam ⁇ l-invention site
- E. coli JMlOl strain was grown and transformed using previously described protocols (Maniatis et. Al., 1982, Molecular Cloning, CoId Spring Harbor, N. Y). Streptomyces strains were manipulated as previously described (Kieser T. et al., 2000, cited supra). Intraspecific conjugation was carried out as previously described in Example 1. DNA manipulations were carried out as previously described by Maniatis et al, 1982 (cited supra). Trials for the production of tetraenes
- Mass spectra were determined on an 1100MSD HPLC device connected to an Agilent Technology quadrupole detector, using electrospray as a source and a positive ionization mode.
- the chromatographic conditions were the same as those previously described (Pérez-Z ⁇ iga F.J., et al., 2004, cited supra). NMR analysis
- Streptomyces diastaticus var. 108 :: PMl-768 / 743B was cultured in solid SYM2 medium (Pérez-Z ⁇ iga FJ, et al, 2004, cited supra) supplemented with thiostreptone (50 ⁇ g / ml) and erythromycin (25 ⁇ g / ml) for the correct selection of the phage insertion PMl -768 on the chromosome and the presence of plasmid pSM743B, respectively. After 6 days, the complete solid medium where the microorganisms were grown, was fragmented and processed as previously described in Example 1.
- CE-108C (HIb) and rimocidine C (Illa) were purified by HPLC using a semi-preparative column (Supelcosil PLC-8, 250 x 21.2 mm); the gradient applied was similar to that described previously for analytical fractionation (cited above) and controlled by an automatic gradient controller (Waters Automated Gradient).
- the fractions carrying the pure polyenes were combined, subjected to a desalination stage using Sep-Pak (Waters) cartridges and, finally, they were lyophilized twice. This method can be used to purify any methylated polyene from the culture of the corresponding genetically modified microorganism.
- Hemolytic activity assays The assays were carried out on human blood enriched in erythrocytes as previously described in Example 1. Preparation of acellular extracts and "in yrtro" amidation assays
- the cells were collected by centrifugation as described above and resuspended in a 50 mM Tris-CIH buffer, pH 7.5, 0.5 mM EDTA, 5% glycerol, 50 mM ClNa, 0.5 mM PMSF and 1 mM beta-mercaptoethanol (PTSD buffer).
- Resuspended cells underwent ultrasound disruption; The homogenate was clarified by centrifugation twice at 8,000 g for 15 minutes and 4 0 C. Polyenes contaminating the acellular homogenate were partially removed by passing the supernatant through a Sep-Pak Cl 8 cartridge (Waters).
- amidotransferase assays were performed in 200 microliters containing 100 microliters of the solution described above, 4 x 10 6 Units of optical density measured at 340 nm of the solutions containing the different polyenes, 2.5 mM glutamine, 25 mM ClNa, 10 mM Cl 2 Mg, 4 mM ATP and 125 mM TES buffer at pH 7.2.
- rimG could be crucial: disruption of the rimG gene would give rise to a mutant capable of producing the corresponding amides by being a carrier of a plasmid involved in inducing the formation of tetraenes knotted if the mechanism were the (a) or incapable of it in the possibility (b).
- a mutant was generated by disruption in the rimG gene using actinophage PMl as a vector (Malpartida et. Al., 1986, cited supd).
- actinophage PMl actinophage PMl as a vector
- a 0.6 kbp Sac ⁇ l fragment internal to rimG (coordinates 8267-8849 of the sequence deposited in GeneBank AY442225) was cloned following the fragment containing the promoter of the ermE v gene and the set in phage PMl.
- the recombinant actinophagus PM1-768B was used to infect spores of S. diastaticus var. 108 giving rise to S. diastaticus var.
- plasmid pSM743B capable of complementing rimA disruption and inducing the formation of knotted polyenes (cited supra), was transferred by intraspecific conjugation from the wild strain S. diastaticus and ⁇ X. 108 / 743B to the lysogen S. diastaticus var. 108 :: PMl-768, where S. diastaticus var. 108 :: PMl-768 / 743B the resulting recombinant. Once the genotypes are confirmed corresponding, the fermentation broths were analyzed for the production of polyenes.
- the compound rimocidine C (Illa) was obtained as a yellow powder, which manifested the existence of ions / "ez / fo-molecular am / z 738 ([M + H]) and 760 [(MH-Na + ]) , which corresponds to the molecular formula C ⁇ H 63 NO 12 by high resolution (found 738.442217, calculated 738.442300 for [M + H]).
- this compound corresponds to the loss of two oxygen atoms and the addition of two protons in rimocidine C (Illa), which can formally be interpreted as a substitution of the group carboxyl in C-14 carbon by a methyl residue.
- the 1 H-NMR spectrum was very similar to that of rimocidine (lia) and showed three signals in the range of sp 2 , a doublet doublet (dd) at ⁇ 6.30, a multiplet at ⁇ 6.05- 6.18, and a second dd at ⁇ 5.90 (Table 2).
- the sugar protons appeared in the range of ⁇ 3.25-4.62.
- the aliphatic region of the 1 H-NMR spectrum also exhibited similarities with that of rimocidine (lia), especially with respect to five complex multiplet patterns in the range of ⁇ 1.30-2.50.
- rimocidine (lia) Four methyl groups instead of three as in rimocidine (lia) appeared as two triplets and two doublets at ⁇ 0.90, 0.95, and 1.26, 1.00, respectively.
- the 13 C-NMR magnetic resonance spectrum indicated 39 carbon signals as in rimocidine (lia), as required by the molecular formula. This and the similarities of the proton spectra allowed us to conclude that rimocidine (lia) and rimocidine C (Illa) have the same carbon skeleton including mycosamine sugar, the only difference being the presence of only two carbonyl groups instead of three as in rimocidine (lia). The signals at ⁇ 211.6 and 174.5 were attributed to a ketone group and a carbonyl lactone, respectively.
- the mass spectrum (+) - ESI NS determined the molecular weight of CE-108C (HIb) as miz 709, which corresponds to the molecular formula C 37 H 59 NO 12 by high resolution (found 710.410905, calculated 710.411000 for [ M + H] + ).
- the 13 C-NMR magnetic resonance spectrum confirmed the presence of 37 carbon signals as in CE-108 (Hb), as required by the molecular formula.
- Comparison with the 13 C-NMR magnetic resonance spectrum of CE-108B (I-lb) revealed the presence of only two carbonyl signals at ⁇ 211.3 and 174.3 again attributed to a ketone group and a carbonyl lactone.
- the antifungal activity of the new non-carboxylated tetraenes rimocidine C (Illa) and CE-108C (HIb) was measured against Penicillium chrysogenum, Candida albicans, Aspergillus niger, Candida h'usei and Criptococcus neoformans compared to that of native rimocidine tetraenes ( lia) and CE-108 (Hb).
- rimE gene is transcribed in a polyistron of approximately 9 Kb that also houses the rimF, rimG, HmH and rimA genes (Seco EM et al., 2004, Chem. Biol. 11: 357-366) ( Figure 4A) , it was necessary to prevent a polar effect on genes located downstream in the chromosome.
- the strong ermEp * promoter was cloned in front of the 0.8 kbp fragment I left internal to the rimE gene (coordinates 5629-6484 of the sequence deposited in GeneBank AY442225) in the correct orientation to allow transcription of the rest of the RNA delivery courier.
- the resulting construct was cloned into the PM1 phage in several steps described in Table 1.
- the resulting recombinant phage (PM1 -702B) was used to infect spores of Streptomyces diastaticus var. 108, allowing the isolation of S. diastaticus var. 108 :: PMl-702B.
- the correct integration into the chromosome was confirmed by the Southern blotting technique.
- the analysis of the HPLC fermentation broths and mass spectrometry analysis determined the presence of four major compounds (see Figure 5) that correspond to the CE-108 and rimocidine aglycones, as well as the rimocidine C aglycones ( Illa) and CE-108C (HIb).
- plasmid pSM743B was introduced by conjugation to this lysogen, capable of inducing S. diastaticus var. 108 the formation of the rimocidine B (I-la) and CE-108B (I-lb) amides, no formation of knotted aglycones was observed.
- the data is interpreted as that the substrate of the possible amidotransferase activity would actually be rimocidine (lia) and CE-108 (Hb) but not its aglycone.
- 108/784 cited in Example 1 was grown in SYM2 liquid medium for 3 days, as indicated in Experimental Procedures for obtaining acellular extracts. Initially, different parameters were tested: substrates, enzymatic co-factors, donors of the amide group, optimal reaction pH. The products of the reactions were analyzed by HPLC and the titration was optimized using for the enzymatic tests the sediment of several fractionations with ammonium sulfate, carried out according to the conditions of standardized use in the biochemical works of the field. Finally, the most optimal conditions for the assessment of amidotransferase activity are indicated in the Experimental Procedures section.
- acellular extracts of S. diastaticus var. 108/784 were also tested against heterologous substrates such as amphotericin B and pimaricin (IVa) although the results were only satisfactory using pimaricin (IVa) as a substrate.
- acellular extracts of S. diastaticus var.108 / 784 were able to convert pimaricin (IVa) to its corresponding amide AB-400 (IVb).
- the strain contains the complete route to produce rimocidine (lia) and CE-108 (Hb), being also able to produce the corresponding rhymoidin B (I-la) and CE-108B (I-lb) amidates.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Genetics & Genomics (AREA)
- Engineering & Computer Science (AREA)
- General Health & Medical Sciences (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Biotechnology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biochemistry (AREA)
- Molecular Biology (AREA)
- Medicinal Chemistry (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Biomedical Technology (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Mycology (AREA)
- Biophysics (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Plant Pathology (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Gastroenterology & Hepatology (AREA)
- Communicable Diseases (AREA)
- Oncology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Physics & Mathematics (AREA)
- Tropical Medicine & Parasitology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Preparation Of Compounds By Using Micro-Organisms (AREA)
- Saccharide Compounds (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Abstract
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP06743410A EP1862467A2 (en) | 2005-03-23 | 2006-03-23 | Polyene antibiotics, compositions containing said antibiotics, method and micro-organisms used to obtain same and applications thereof |
| US11/886,673 US20090221520A1 (en) | 2005-03-23 | 2006-03-23 | Polyene Antibiotics, Compositions Containing Said Antibiotics, Method and Micro-Organisms Used to Obtain Same and Applications Thereof |
| AU2006226257A AU2006226257A1 (en) | 2005-03-23 | 2006-03-23 | Polyene antibiotics, compositions containing said antibiotics, method and micro-organisms used to obtain same and applications thereof |
| JP2008502429A JP2008538895A (ja) | 2005-03-23 | 2006-03-23 | ポリエン抗生物質、該抗生物質を含有する組成物、それを取得するために用いられる方法および微生物ならびにその用途 |
| CA002602355A CA2602355A1 (en) | 2005-03-23 | 2006-03-23 | Polyene antibiotics, compositions containing said antibiotics, method and micro-organisms used to obtain same and applications thereof |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ESP200500701 | 2005-03-23 | ||
| ES200500701A ES2323253B1 (es) | 2005-03-23 | 2005-03-23 | Nuevos polienos amidados, procedimiento para su obtencion y aplicaciones. |
| ES200501952A ES2323397B1 (es) | 2005-08-03 | 2005-08-03 | Macrolidos polienos metilados, procedimiento para su obtencion y sus aplicaciones. |
| ESP200501952 | 2005-08-03 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| WO2006100330A2 true WO2006100330A2 (es) | 2006-09-28 |
| WO2006100330A3 WO2006100330A3 (es) | 2006-11-23 |
Family
ID=37024198
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/ES2006/000142 Ceased WO2006100330A2 (es) | 2005-03-23 | 2006-03-23 | Antibióticos polienos, composiciones que los contengan, procedimiento y microorganismos para su obtención y sus aplicaciones |
Country Status (8)
| Country | Link |
|---|---|
| US (1) | US20090221520A1 (es) |
| EP (1) | EP1862467A2 (es) |
| JP (1) | JP2008538895A (es) |
| KR (1) | KR20070116254A (es) |
| AU (1) | AU2006226257A1 (es) |
| CA (1) | CA2602355A1 (es) |
| RU (1) | RU2007138884A (es) |
| WO (1) | WO2006100330A2 (es) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009003595A3 (de) * | 2007-07-04 | 2009-04-09 | Sanofi Aventis | Makrolakton-derivate |
| WO2010069850A1 (en) * | 2008-12-17 | 2010-06-24 | Sanofi-Aventis | Macrolactone derivatives, method for the production thereof and use thereof for the treatment of cancer |
| ES2371615A1 (es) * | 2009-07-31 | 2012-01-05 | Consejo Superior De Investigaciones Científicas (Csic) | Macrólidos polienos con actividad antimicrobiana y su procedimiento biotecnológico de obtención. |
| WO2020103668A1 (zh) * | 2018-11-19 | 2020-05-28 | 常熟理工学院 | 一株产甲壳素酶菌株及应用 |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ITMI20120560A1 (it) * | 2012-04-05 | 2013-10-06 | Olon Spa | Procedimento per la purificazione della tiacumicina b |
| JP6600303B2 (ja) | 2013-10-07 | 2019-10-30 | ザ ボード オブ トラスティーズ オブ ザ ユニヴァーシティ オブ イリノイ | 治療指数が改善されたアンフォテリシンb誘導体 |
| WO2016014779A1 (en) * | 2014-07-23 | 2016-01-28 | The Board Of Trustees Of The University Of Illinois | Antifungal polyene macrolide derivatives with reduced mammalian toxicity |
| WO2016040779A1 (en) * | 2014-09-12 | 2016-03-17 | The Board Of Trustees Of The University Of Illinois | Urea derivatives of polyene macrolide antibiotics |
| US11230553B2 (en) | 2016-05-09 | 2022-01-25 | The Research Foundation For The State University Of New York | Nannocystin process and products |
| GB202406857D0 (en) * | 2024-05-15 | 2024-06-26 | Univ Manchester | Polyenes |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| PL122086B1 (en) * | 1979-04-09 | 1982-06-30 | Politechnika Gdanska | Process for preparing amides of antibiotics from the group of polyene macrolides and their derivativesvykh makrolidov i ikh proizvodnykh |
| PL124710B1 (en) * | 1979-07-18 | 1983-02-28 | Politechnika Gdanska | Process for preparing esters of antibiotics from polyene macrolids group and their n-substituted derivatives |
-
2006
- 2006-03-23 EP EP06743410A patent/EP1862467A2/en active Pending
- 2006-03-23 RU RU2007138884/04A patent/RU2007138884A/ru not_active Application Discontinuation
- 2006-03-23 WO PCT/ES2006/000142 patent/WO2006100330A2/es not_active Ceased
- 2006-03-23 AU AU2006226257A patent/AU2006226257A1/en not_active Abandoned
- 2006-03-23 CA CA002602355A patent/CA2602355A1/en not_active Abandoned
- 2006-03-23 JP JP2008502429A patent/JP2008538895A/ja not_active Withdrawn
- 2006-03-23 US US11/886,673 patent/US20090221520A1/en not_active Abandoned
- 2006-03-23 KR KR1020077023675A patent/KR20070116254A/ko not_active Withdrawn
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009003595A3 (de) * | 2007-07-04 | 2009-04-09 | Sanofi Aventis | Makrolakton-derivate |
| JP2010531823A (ja) * | 2007-07-04 | 2010-09-30 | サノフィ−アベンティス | マクロラクトン誘導体 |
| US8268775B2 (en) | 2007-07-04 | 2012-09-18 | Sanofi | Macrolactone derivatives |
| WO2010069850A1 (en) * | 2008-12-17 | 2010-06-24 | Sanofi-Aventis | Macrolactone derivatives, method for the production thereof and use thereof for the treatment of cancer |
| ES2371615A1 (es) * | 2009-07-31 | 2012-01-05 | Consejo Superior De Investigaciones Científicas (Csic) | Macrólidos polienos con actividad antimicrobiana y su procedimiento biotecnológico de obtención. |
| WO2020103668A1 (zh) * | 2018-11-19 | 2020-05-28 | 常熟理工学院 | 一株产甲壳素酶菌株及应用 |
Also Published As
| Publication number | Publication date |
|---|---|
| CA2602355A1 (en) | 2006-09-28 |
| AU2006226257A1 (en) | 2006-09-28 |
| US20090221520A1 (en) | 2009-09-03 |
| WO2006100330A3 (es) | 2006-11-23 |
| EP1862467A2 (en) | 2007-12-05 |
| JP2008538895A (ja) | 2008-11-13 |
| KR20070116254A (ko) | 2007-12-07 |
| RU2007138884A (ru) | 2009-04-27 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2006100330A2 (es) | Antibióticos polienos, composiciones que los contengan, procedimiento y microorganismos para su obtención y sus aplicaciones | |
| CN101333206B (zh) | 大环内酯类化合物及其制备和应用 | |
| JP5314680B2 (ja) | ナイスタチン誘導体およびその抗菌剤としての使用 | |
| US9605015B2 (en) | Polyene compound, method for preparing the same, and antifungal drug comprising novel polyene compound as active ingredient | |
| US10793590B2 (en) | Antifungal compounds | |
| KR100336964B1 (ko) | 오보바톨 또는 리도보바톨 함유 항진균제 | |
| KR102517926B1 (ko) | 나르제니신 a1 유도체를 포함하는 위암 예방 또는 치료용 조성물 | |
| ES2323253B1 (es) | Nuevos polienos amidados, procedimiento para su obtencion y aplicaciones. | |
| ES2323397B1 (es) | Macrolidos polienos metilados, procedimiento para su obtencion y sus aplicaciones. | |
| ES2255331B1 (es) | Procedimiento de obtencion de indolocarbazoles mediante la utilizacion de genes biosinteticos de rebecamicina. | |
| EP2327789B1 (en) | Signamycin, method for production thereof, and use thereof | |
| US20190127313A1 (en) | Antimicrobial agents | |
| AU729659B2 (en) | Sordarin and derivatives thereof for use as crop antifungal agents | |
| JP2004283174A (ja) | B2:b1アベルメクチンの比に関するストレプトミセス・アベルミティリス遺伝子 | |
| EP1137796A2 (en) | Micromonospora echinospora genes encoding for biosynthesis of calicheamicin and self-resistance thereto | |
| US11739122B2 (en) | Glycopeptide antibiotic compounds, methods for producing the same, and uses thereof | |
| WO2015145152A1 (en) | Antimicrobial agents | |
| CN102741243A (zh) | 新型化合物拟无枝酸菌糖衍生物、它们的生产方法和应用 | |
| WO2024082757A1 (zh) | 黄酮类化合物及其生物合成相关基因以及其应用 | |
| KR100316010B1 (ko) | 키틴 합성효소 2를 저해하는 신규 화합물 페린신 에이 및 이를함유하는 항진균제 조성물 | |
| HU203582B (en) | Process for producing amicin, amicin derivatives and pharmaceutical compositions containing them, and fungicide compositions containing them | |
| Park et al. | Y, Nah HJ, Choi SS and Kim ES (2020) Stimulated Biosynthesis of an C10-Deoxy Heptaene NPP B2 via Regulatory Genes Overexpression in Pseudonocardia autotrophica | |
| WO2025238361A1 (en) | Antifungal polyene macrolides | |
| CN105579064B (zh) | 并用抗抗酸菌药、抗抗酸菌药的筛选方法、和WecA及其直系同源的活性阻碍剂 | |
| JP2005506050A (ja) | カリケマイシンの生合成およびそれに対する自己耐性をコードするミクロモノスポラ・エチノスポラ(Micromonosporaechinospora)遺伝子 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 2006743410 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2602355 Country of ref document: CA |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 561817 Country of ref document: NZ |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2008502429 Country of ref document: JP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 3749/KOLNP/2007 Country of ref document: IN |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2006226257 Country of ref document: AU |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 1020077023675 Country of ref document: KR |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2007138884 Country of ref document: RU |
|
| ENP | Entry into the national phase |
Ref document number: 2006226257 Country of ref document: AU Date of ref document: 20060323 Kind code of ref document: A |
|
| WWP | Wipo information: published in national office |
Ref document number: 2006226257 Country of ref document: AU |
|
| WWP | Wipo information: published in national office |
Ref document number: 2006743410 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 11886673 Country of ref document: US |