WO2007105388A1 - イソプレン系化合物の重合用の重合触媒組成物 - Google Patents
イソプレン系化合物の重合用の重合触媒組成物 Download PDFInfo
- Publication number
- WO2007105388A1 WO2007105388A1 PCT/JP2007/051929 JP2007051929W WO2007105388A1 WO 2007105388 A1 WO2007105388 A1 WO 2007105388A1 JP 2007051929 W JP2007051929 W JP 2007051929W WO 2007105388 A1 WO2007105388 A1 WO 2007105388A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- group
- general formula
- isoprene
- polymerization
- catalyst composition
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F36/00—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds
- C08F36/02—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds
- C08F36/04—Homopolymers and copolymers of compounds having one or more unsaturated aliphatic radicals, at least one having two or more carbon-to-carbon double bonds the radical having only two carbon-to-carbon double bonds conjugated
- C08F36/08—Isoprene
Definitions
- the present invention relates to a method for producing an isoprene-based polymer, particularly a regioselective and high-tacticity isoprene-based polymer, preferably polyisoprene, and a polymerization catalyst composition used therefor.
- Polyisoprene may have the following four different structural units. That is, a 3,4-bonded structural unit represented by the general formula ( ⁇ ), a transformer 1,4-bonded structural unit represented by the general formula ( ⁇ ), a cis 1,4 represented by the general formula ( ⁇ ) Bonded structural units, and 1, 2 bonded structural units represented by general formula (IV).
- Non-Patent Document 1 It is reported that the above polymer is produced by polymerizing isoprene (see Non-Patent Document 1).
- the other is to use a complex in which sparteine is coordinated with FeCl as a polymerization catalyst.
- Non-patent Document 2 It is reported that the above polymer is produced by polymerizing isoprene (Non-patent Document 2).
- polyisoprene having selectively a structural unit represented by the general formula ( ⁇ ) is considered to have greatly different physical properties depending on the tacticity of the arrangement of the structural unit.
- Two types of stereoisomerism can occur in a polymer with two side chain substituents different from each other in the main chain atom, such as polyisoprene, which is a structural unit represented by the general formula ( ⁇ ).
- Tactic City is this solid It means the arrangement or order in the polymer main chain of the part showing isomerism.
- One of the two different side chain substituents is bonded to one side only with respect to the plane formed by the polymer main chain, and the resulting polymer is represented by a isotactic polymer (represented by the following general formula (V)).
- the polymer is a syndiotactic polymer (the following general formula (V)).
- Such a polymer having no regularity is referred to as atactic polymer.
- Non-Patent Document 1 it is described that the obtained polyisoprene is a atactic polymer, and in Non-Patent Document 2, there is no description regarding the tacticity of the obtained polyisoprene. Therefore, a polyisoprene having a general formula ( ⁇ ) selectively and having a high tacticity has been demanded.
- Patent Document 1 a method for producing polyisoprene having high tacticity has been reported.
- polyisoprene is polymerized using a meta-octacene catalyst.
- polyisoprene having high tacticity can be produced by polymerizing isoprene using such a catalyst, there is a problem that the cost of the catalyst is high at present.
- Non-patent Document 3 it has been reported that polyethylene is produced using a non-metacene catalyst containing amidine.
- the yield of polyethylene fluctuates by changing the central metal.
- isoprene-based polymers having high tacticity.
- Patent Document 1 International Publication No. 05Z085306 Pamphlet
- Non-patent literature l Makromolekulare Chem (1964), 77, pp.126-138.
- Non-Patent Document 2 Macromolecules (2003), 36, pp.7953-7958.
- Non-Patent Document 3 J. AM. CHEM. SOC. (2004), 126, pp. 9182-9183.
- the present invention has been made under such circumstances, and is an isoprene-based polymer selectively having a structural unit represented by the following general formula (Y), and the arrangement of the structural units.
- a polymerization catalyst composition for producing an isoprene-based polymer (particularly a isotactic-rich isoprene-based polymer) at a low cost with a high tacticity, and an isoprene having a high tacticity using the polymerization catalyst composition It is an object of the present invention to provide a method for producing a polymer.
- R 4 represents an alkyl group or a alkenyl group having 1 to 10 carbon atoms.
- the present invention is as follows.
- R 1 and R 2 each independently represents an alkyl group, a cyclohexyl group, an aryl group or an aralkyl group,
- R 3 represents an alkyl group, an alkyl group, an alkyl group, an alkyl group, an aryl group or an aralkyl group, an aliphatic, aromatic or cyclic amino group, or a phosphino group, a boryl group, an alkyl or arylthio group, an alkoxy group. Or an aryloxy group,
- M represents any of rare earth elements from lanthanum La to lutetium Lu excluding scandium Sc, yttrium Y or promethium Pm,
- Q 1 and Q 2 each independently represent a mono-on-type ligand
- L represents a neutral Lewis base
- w represents an integer of 0 to 3.
- R 4 represents an alkyl group or a alkenyl group having 1 to 10 carbon atoms.
- R 1 and R 2 in the general formula (A) are 2 , 6-Diisopropylphenol group, R 3 represents a phenyl group,
- M represents any of rare earth elements from lanthanum La to lutetium Lu, excluding scandium Sc, yttrium Y or promethium Pm.
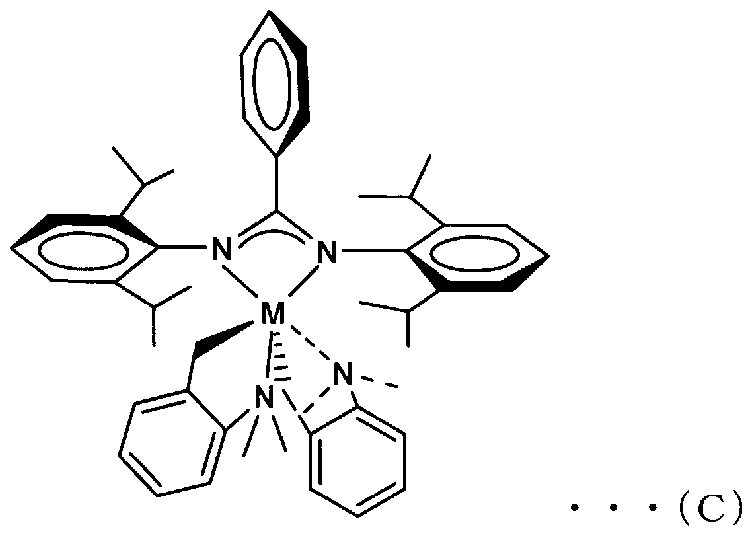
- the complex represented by the general formula (A) is a compound represented by the general formula (C).
- M represents any of rare earth elements from lanthanum La to lutetium Lu except scandium Sc, yttrium Y or promethium Pm.
- catalyst activator according to any one of (1) to (4), wherein the catalyst activator is an ionic compound comprising a non-coordinating cation and a cationic card. Polymerization catalyst composition.
- FIG. 1 is a 1 H-NMR spectrum chart of polyisoprene obtained in Example 1.
- FIG. 2 is a 13 C-NMR ⁇ vector chart of polyisoprene obtained in Example 1.
- FIG. 3 is a GPC chart of polyisoprene obtained in Example 1.
- FIG. 4 is a DSC chart of the polyisoprene obtained in Example 1.
- FIG. 5 is a 1 H-NMR spectrum chart of polyisoprene obtained in Example 4.
- FIG. 6 is a 13 C-NMR ⁇ vector chart of polyisoprene obtained in Example 4.
- FIG. 7 is a DSC chart of the polyisoprene obtained in Example 4.
- FIG. 8 is a 1 H-NMR spectrum chart of polyisoprene obtained in Reference Example 1.
- FIG. 9 is a 13 C-NMR ⁇ vector chart of polyisoprene obtained in Reference Example 1.
- the polymerization catalyst composition of the present invention comprises the complex represented by the general formula (A) and a catalyst activator.
- R 1 and R 2 are each independently an alkyl group, a substituted or unsubstituted cyclohexyl group, an aryl group, or an aralkyl group.
- alkyl group include a methyl group, an ethyl group, an isopropyl group, an n-butyl group, and a t-butyl group.
- substituted cyclohexyl group include a cyclohexyl group having an alkyl group as a substituent, for example, a methylcyclohexyl group.
- Examples of the unsubstituted aryl group include a phenyl group, and examples of the substituted aryl group include a phenyl group having an alkyl group as a substituent.
- Examples of the unsubstituted aralkyl group include a benzyl group, and examples of the substituted aralkyl group include a benzyl group having an alkyl group as a substituent.
- phenyl having an alkyl group as a substituent is preferred, and 2,6-diisopropylphenyl group is particularly preferred.
- R 1 and R 2 may be the same or different! However, both R 1 and R 2 are preferably a phenyl group having an alkyl group as a substituent, more preferably a 2,6-diisopropyl phenol group.
- R 3 represents an alkyl group, an alkyl group, an alkyl group, an alkyl group, an aryl group or an aralkyl group, an aliphatic, aromatic or cyclic amino group, or a phosphino group, a boryl group, an alkyl group or an arylthio group.
- the complex contained in the polymerization catalyst composition of the present invention is a 2, 6-diisopropyl phenol group for both R 1 and R 2 forces, and R 3 is a phenol group. It is preferable to have the structure of —'- bis (2,6-diisopropyl pyridine) benzamidinate (NCN)! /.
- the central metal ⁇ represents any of rare earth elements from lanthanum La to lutetium Lu excluding scandium Sc, yttrium Y or promethium Pm.
- the central metal M tries to polymerize. A force that can be appropriately selected according to the type of monomer, etc. Scandium Sc, yttrium Y or lutetium Lu is preferred, and scandium Sc is particularly preferred.
- Q 1 and Q 2 are mono-on-type ligands.
- Monoarion-type ligands include 1) hydride, 2) halide, 3) substituted or unsubstituted hydrocarbyl group having 1 to 20 carbon atoms, 4) substituted or unsubstituted, 1 to 20 carbon atoms Examples thereof include alkoxy groups or aryloxy groups, 5) substituted or unsubstituted amide groups having 1 to 20 carbon atoms (including silylamide groups), 6) phosphino groups, and the like, and hydrocarbyl groups are preferably exemplified. It is not limited to that.
- Q 1 and Q 2 may be combined with each other, or may be combined to form a di-on coordination.
- di-on ligands include alkylidene, gen, cyclometalated hydrocarbyl groups, or bidentate chelate ligands.
- the halide may be any of chloride, bromide, fluoride, and iodide! / ⁇ .
- the hydrocarbyl group having 1 to 20 carbon atoms is a methyl group, an ethyl group, a propyl group, an isopropyl group, a butyl group, an isobutyl group, a tbutyl group, a pentyl group, an amyl group, an isoamyl group, a hexyl group, or a cyclohexyl group.
- Alkyl groups such as xyl group, heptyl group, octyl group, nor group, decyl group, cetyl group, 2-ethylhexyl group, vinyl group, 1 probe group, isopropyl group, aryl group, Alkyl groups such as methallyl groups, crotyl groups, etc., ether groups, alkyl groups such as 3,3-dimethyl-1-buture groups, aryl groups such as phenol groups, tolyl groups, benzyl groups, diphenylmethyl groups, A aralkyl group such as a phenylalkyl group such as a phenylethyl group, a diphenylethyl group, a trialkylsilylmethyl group, a bis (trialkylsilyl) methyl group, a 2-phenyl-thuryl group, a 2- (trimethyl) Lil) Echuru group, main Chirufue - group, Jimechirufu
- Q 1 and Q 2 are preferably a trialkylsilylmethyl group or an aminobenzyl group.
- the three alkyl groups on the silyl element of the trialkylsilylmethyl group are linear or branched groups having about 1 to 6 carbon atoms, preferably about 1 to 4 carbon atoms. More preferably, a methyl group is mentioned.
- Examples of the trialkylsilyl include trimethylsilyl and t-butyldimethylsilyl.
- Preferred examples of the aminobenzyl group include 0-N, N dimethylaminobenzil group.
- the alkoxy group or aryloxy group is preferably a methoxy group, a substituted or unsubstituted phenoxy group, or the like.
- the amide group is preferably a dimethylamide group, a jetylamide group, a methylethylamide group, a dibutylamide group, a diisopropylamide group, an unsubstituted or substituted diphenylamide group, or a bis (trimethylsilyl) amide group.
- the phosphino group is preferably a diphenylphosphino group, a dicyclohexylphosphino group, a diisopropylphosphino group, a jetylphosphino group, a dimethylphosphino group, or the like.
- the alkylidene is preferably methylidene, ethylidene, propylidene, benzylidene, or the like.
- the cyclometallated hydrocarbyl group is preferably propylene, butylene, pentylene, hexylene, octylene or the like.
- the gen is preferably 1,3 butadiene, 1,3 pentagen, 1,4 pentagen, 1,3 hexagen, 1,4 monohexagen, 1,5 hexagen, 2,4 dimethyl 1,3 Pentagen, 2-methyl-1,3 hexagen, 2,4 monohexagen, etc.
- L in the general formula (I) is a neutral Lewis base.
- the neutral Lewis base include tetrahydrofuran (THF), jetyl ether, dimethylamine, trimethylphosphine, lithium chloride and the like. Among these, tetrahydrofuran is preferable.
- the neutral Lewis base L may be combined with Q 1 and Z or Q 2 to form a so-called multidentate ligand.
- the w of L in the general formula (I) represents the number of neutral Lewis bases.
- w is a force that varies depending on the type of the central metal M, and is usually an integer of 0 to 3, preferably 0 or 1.
- the complex represented by the general formula (A) contained in the polymerization catalyst composition of the present invention is preferably a compound represented by the general formula (B) or (C).
- the central metal M represents any of rare earth elements from lanthanum La to lutetium Lu excluding scandium Sc, yttrium Y or promethium Pm.
- the central metal M is a force that can be appropriately selected according to the type of monomer to be polymerized. Scandium Sc, yttrium Y or lutetium Lu is preferred, particularly scandium. Sc is preferred.
- the catalyst activator contained in the polymerization catalyst composition of the present invention is an ionic compound, an alkylaluminum compound, a Lewis acid, or the like, and preferably an ionicity composed of a non-coordinating cation and a cationic catalyst. Includes composites.
- the catalyst activator activates the complex of the present invention and exhibits activity as a polymerization catalyst. As its activation mechanism, the complex reacts with a catalyst activator, and a plurality of the rare earth metal atoms of the complex are coordinated! /, Q 1 or Q 2 is eliminated, and a cationic complex ( It can be considered that active species) are generated.
- non-coordinating key ion of the ionic compound for example, tetravalent boron key and tetrakis (monofluorophenyl) borate are preferable.
- Examples of the cation of the ionic compound include a carbo cation, an oxo cation, an ammonium cation, a phospho cation, a cycloheptatri cation, and a ph- ole cation cation having a transition metal.
- Specific examples of the carbo-cation include tri-substituted carbo-cations such as tri-phenyl cation and tri-substituted carboxylic cation.
- Specific examples of the tri-substituted phenolic cation include tris (methylphenol) carbocation and tris (dimethylphenol) carbocation.
- ammonium cation examples include trimethyl ammonium cation, triethyl ammonium cation, tripropyl ammonium cation, tri tert-butyl ammonium cation.
- Trialkyl ammonium cations such as tri-n-butyl ammonium cation, ,,-dialkyl aluminum cation such as N, N-jetylarium cation, ⁇ , ⁇ -2,4,6-pentamethylarium cation
- dialkylammonium cations such as di (isopropyl) ammonium cation and dicyclohexylammonium cation.
- phosphonium cation examples include triarylphosphonium cations such as triphenylphosphonium cation, tris (methylphenol) phosphonium cation, and tris (dimethylphenol) phosphonium cation.
- a combination of the above-mentioned non-coordinating cation and cation force can be used.
- a combination of the above-mentioned non-coordinating cation and cation force can be used.
- a combination of the above-mentioned non-coordinating cation and cation force can be used.
- triphenylcarbtetrakis (pentafluorophenol) borate triphenylcarbtetrakis (tetrafluorophenol) borate, ⁇ , ⁇ -dimethylarium tetrakis (pentafluorophenol) -L) borate, 1,1, and dimethyl ferroceum tetrax (pentafluorophenol) borate.
- triphenyl calve tetrakis (pentafluorophenol) borate and ⁇ , ⁇ -dimethyl arlium tetrakis (pentafluorophenol) borate it is preferable to use triphenyl calve tetrakis (pentafluorophenol) borate and ⁇ , ⁇ -dimethyl arlium tetrakis (pentafluorophenol) borate.
- One ionic compound may be used, or two or more ionic compounds may be used in combination.
- Lewis acids that can react with transition metal compounds to form cationic transition metal compounds include B (C F), A1 (C F)
- the polymerization catalyst composition of the present invention may contain at least one of the complexes represented by the general formula (A) and at least one of the catalyst activators, but preferably the general formulas (B) and ( At least one of the complexes represented by C) and triphenylcarbtetrakis (pentafluorophenol) borate ([Ph C] [B (CF)]) and ⁇ , ⁇ -dimethylayuyl-tetrakis ( Pentafluorofe
- the complex represented by the general formula (A) can be used in any amount, and the amount of the isoprene-based compound to be polymerized and the purpose of the production.
- Isoprene The molecular weight of the system polymer can be adjusted. Preferably, it can be an amount suitable for use in the production method of an isoprene-based polymer described later.
- the amount of the catalyst activator which can be adjusted similarly is usually 0.5 to 5 moles, preferably about 1 mole per mole of the complex.
- the polymerization catalyst used in the method for producing an isoprene-based polymer may contain a third component such as an organic aluminum compound or an aluminoxane. Addition of organoaluminum compound or aluminoxane is thought to promote removal of impurities in the reaction system and chain transfer, so it is expected that the catalytic activity and the molecular weight of the resulting polymer will change.
- the polymerization catalyst composition of the present invention is used for polymerization of the isoprene-based compound represented by the general formula (X).
- R 1 represents an alkyl group or an alkenyl group.
- the isoprene-based polymer having high isotacticity is obtained by polymerizing the isoprene-based compound represented by the general formula (X) using the complex represented by the general formula (A) and the catalyst activator. It can be manufactured from cocoon.
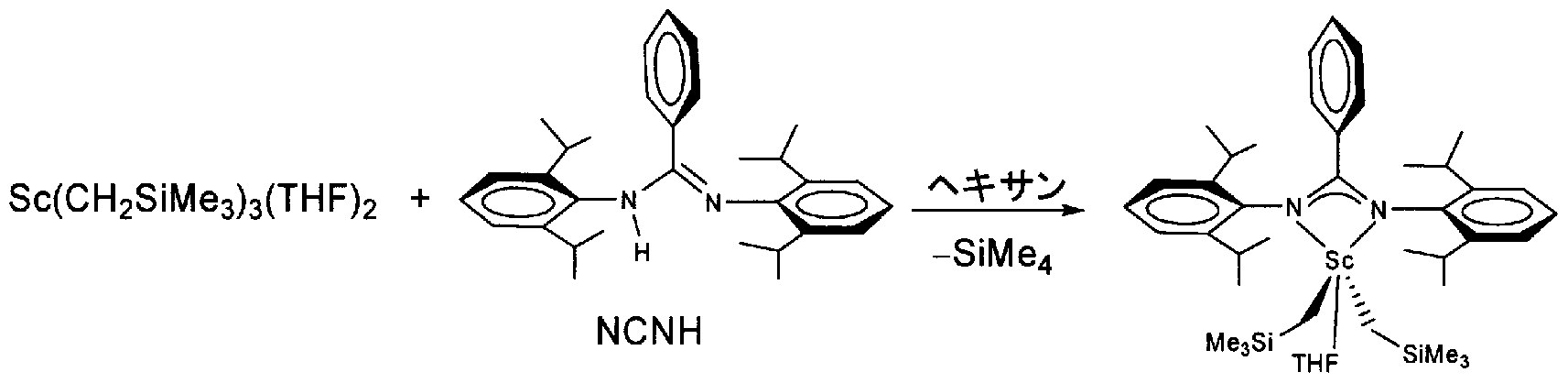
- the complex represented by the general formula (A) can be produced, for example, according to the following scheme.
- a person skilled in the art can appropriately select starting materials, reaction reagents, reaction conditions, etc., referring to the general synthesis scheme shown below, and appropriately modify or modify these methods as necessary.
- the complex represented by the formula (A) can be easily produced.
- the contents described in J. AM. CHEM. SOC. 2004, 126, 9182-9183 can also be referred to.
- the amount of the complex used is usually from 0.0001 force to 0.05 monolayer, preferably from 0.0001 force to 0.01 monolayer of an isoprene-based compound. It ’s mono. If the amount of the complex relative to isoprene is reduced, the molecular weight of the resulting isoprene-based polymer can be increased. Conversely, if the amount of the complex is increased, the molecular weight of the isoprene-based polymer can be decreased. .
- the amount of the catalyst activator is usually 0.5 to 5 mol, preferably 1 mol with respect to 1 mol of the complex represented by the general formula (A). About 1 mole.
- the method for producing the isoprene-based polymer of the present invention may be an addition polymerization method, a polycondensation method, a polyaddition method, or other methods, and is preferably an addition polymerization method.
- the production method of the isoprene-based polymer of the present invention may be any method such as a gas phase polymerization method, a solution polymerization method, and a slurry polymerization method.
- the solvent used is not particularly limited as long as it is inactive in the polymerization reaction and can dissolve the isoprene-based compound and the catalyst.
- saturated aliphatic hydrocarbons such as butane, pentane, hexane and heptane
- saturated alicyclic hydrocarbons such as cyclopentane and cyclohexane
- aromatic hydrocarbons such as benzene and toluene
- Halogenated hydrocarbons such as carbon tetrachloride, trichloroethylene, norchloroethylene, 1,2-dichloroethane, black benzene, bromobenzene, and black toluene
- ethers such as tetrahydrofuran and jetyl ether .
- solvents those having a melting point lower than 0 ° C are preferred-those having a melting point lower than 20 ° C are more preferred.
- aromatic hydrocarbons particularly black benzene is preferred.
- One solvent may be used alone, or a mixed solvent of two or more may be used.
- the amount of the solvent used can be usually adjusted so that the concentration of the complex contained in the polymerization catalyst is 0.000001 to 0.1M, preferably 0.0001-0.01M.
- the polymerization reaction temperature may be any temperature, for example, in the range of 100 to 100 ° C. Usually, it may be 25 ° C or lower, preferably 0 ° C or lower, more preferably ⁇ 10 ° C or lower, and further preferably ⁇ 20 ° C or lower.
- the tacticity (isotacticity) of the arrangement of the structural units (1 ′) contained in the obtained isoprene-based polymer can be increased. In other words, by adjusting the polymerization temperature The isotacticity can be adjusted.
- the reaction time is, for example, about 1 minute to 100 hours, usually 1 minute to 24 hours, preferably 5 to 60 minutes.
- these reaction conditions can be appropriately selected according to the polymerization reaction temperature, the type and amount of the monomer, the type and amount of the catalyst composition, etc., and should be limited to the ranges exemplified above. There is no.
- the method for producing an isoprene-based polymer of the present invention may be carried out by adding a complex, an isoprene-based compound, a catalyst activator, and other compounds in an arbitrary order to the reaction system.
- a catalyst activator is added to a mixture of a complex and an isoprene-based compound.
- the molecular weight distribution curve of the obtained isoprene-based polymer may have a plurality of peaks (that is, A mixture of isoprene-based polymers having different molecular weight distribution peaks may be obtained).
- a known polymerization terminator for example, BHT (methanol containing 2,6-bis (t-butyl) -4-methylphenol)
- BHT methanol containing 2,6-bis (t-butyl) -4-methylphenol
- the isoprene-based polymer obtained by polymerizing the isoprene-based compound represented by the general formula (X) using the production method of the present invention has the following general formulas (1), ( ⁇ ), (III),
- the structural unit represented by (IV) (hereinafter, also simply referred to as “structural units (1), ( ⁇ ), (III), (IV)”) may be included in any ratio.
- R 4 in the structural units (I) to (IV) is an alkyl group or an alkenyl group. More preferably, R 4 is a methyl group, that is, the most preferred isoprene-based polymer produced by the production method of the present invention is polyisoprene.
- R 4 is also preferably exemplified by a 4-methyl-3-pentenyl group, that is, a preferred polymer is a myrcene polymer.
- the proportion of the structural unit (I) contained in the isoprene-based polymer produced by the production method of the present invention in the microstructure of the polymer is usually 60% or more, preferably 90% or more. Preferably it is 95% or more, more preferably 99% or more.
- the isoprene-based polymer produced by the production method of the present invention can contain structural units (II) to (IV) in an arbitrary ratio in addition to the structural unit (I).
- the proportion of the structural unit (I) in the microstructure is calculated by measuring the NMR vector of the obtained isoprene-based polymer, obtaining the integral value of the peak attributed to each structural unit, and comparing it. be able to. This calculation will be described later in the specification of the present application.
- the structural unit (I) contained in the isoprene-based polymer is usually arranged in a head-to-tail manner, and the following two stereoisomerisms can occur in the arrangement.
- the structural units (I) contained in the isoprene-based polymer produced by the production method of the present invention are arranged with stereoregularity, preferably arranged in a highly isotactic manner.
- Highly isotactic arrangement means that the 1-alkylbule group or 1-alkenylvinyl group (or hydrogen atom) in general formula (I) is on one side of the plane formed by the polymer main chain. Is selectively arranged.
- the isotacticity of the arrangement of structural units (I) contained in the isoprene-based polymer produced by the production method of the present invention is at least 60% mm or more in triad display, usually It is 80% mm or more, preferably 90% mm or more, more preferably 95% mm or more, more preferably 99% mm or more, and most preferably 99% mm mm or more in the pentat display.
- I structural units in the isoprene-based polymer
- triazide Three types of structural units (I) in the isoprene-based polymer (referred to as “triazide”) can be considered as follows: three isotactic triads, heterotactic triads, and syndiotactic triads. It is done. Isotacticity in terms of triad means the ratio of “isotactic triad, heterotriad” in the polymer, and the percentage is expressed as '% mm'.
- isotacticity by pentad display refers to the proportion of isotactic pentads in the pentad, focusing on the five chains of structural units (I) (referred to as "pentads") in the same manner as triad display. The percentage of the percentage is displayed as '% mmmm'.
- the isotacticity of the sequence of the structural unit (I) contained in the isoprene-based polymer can be represented by triad display or pentad display as described above.
- the isotacticity of the isoprene-based polymer by triad display or pentad display can also calculate the NMR ⁇ vector data (preferably 13 C-NMR) force of the obtained isoprene-based polymer. This calculation is described later in this specification.
- the average molecular weight of the isoprene-based polymer produced by the production method of the present invention is an arbitrary power-average molecular weight of at least 5,000, usually 50,000 or more, preferably 100,000 or more.
- the upper limit of the number average molecular weight is not particularly limited, but can be 6 million or less as a guide.
- the number average molecular weight means a number average molecular weight measured by a GPC method, and can be measured using, for example, a GPC measuring apparatus (TOSOH HLC 8220 GPC).
- the molecular weight distribution of the isoprene-based polymer produced by the production method of the present invention is usually 6 or less, preferably 3 or less, more preferably 1.7 or less when expressed in M / M.
- the molecular weight distribution means a molecular weight distribution measured by a GPC method, and can be measured using, for example, a GPC measuring apparatus (TOS OH HLC 8220 GPC).
- the isoprene-based polymer produced by the production method of the present invention has a 1-alkylbutyl group or a 1-alkylcarbyl group containing a carbon double bond as a side chain.
- the carbon double bond of the bur group can be hydrosilylated or hydroborated or epoxyized.
- the isoprene-based polymer produced by the production method of the present invention may include not only a homopolymer but also a copolymer.
- a copolymer may be, for example, a copolymer of isoprene and an isoprene-based compound other than isoprene, or a copolymer of isoprene and a conjugate. Further, it may be a copolymer of an isoprene-based compound and a nonpolar monomer (including ethylene, styrene, etc.) or a polar monomer (including latathone, acrylate ester, etc.).
- the isoprene-based polymer can be identified by ⁇ H-NMR analysis, 13 C-NMR analysis, measurement of average molecular weight and molecular weight distribution by GPC method, IR measurement, mass spectrometry and the like.
- NMR analysis means analysis by nuclear magnetic resonance spectroscopy at a frequency of 400 MHz.
- the analysis can be performed by using JNM-AL-400RN manufactured by JEOL, which is an NMR analyzer.
- NMR ⁇ vector data means the analysis Means the spectrum data obtained by The measurement solvent is heavy black mouth form CDC1
- Measurement temperature is 25 ° C (room temperature).
- the proportion of the isoprene-based polymer in the microstructure of the structural unit (3,4-structure) represented by the general formula (I) is as follows (WM Dong, T. Masuda, J. Polym. Sci., Part A: Poly m. Chem., 40, 1838 (2002), AS Khatchaturov, ER Dolinskaya, LK Prozenko, EL Abramenko and VA Kormer, Polymer, 18, 871, (1976)). NMR spectrum data can be obtained.
- the isotacticity of the sequence of the structural unit (structural unit (I)) represented by the general formula (I) contained in the isoprene-based polymer can be determined from NMR vector data.
- FIGS. 8 and 9 show polyisoprene, the proportion of structural unit (I) in the microstructure is 92%, and the isotacticity of the structural unit (I) is 36% mm.
- 1 is a measurement chart of 1 H-NMR and 13 C-NMR of a polymer. In Figs.
- FIGS. 1 and 2 show polyisoprene, in which the proportion of structural units (I) in the microstructure is 99.8% and the isotacticity of the arrangement of structural units (I) is 99%. Measurement chart of 1 H-NMR and 13 C-NMR of a polymer of mmmm, FIGS.
- the compounds obtained in the following examples are 1 H-NMR, 13 C-NMR (JEOL JNM-AL 400RN), GPC (TOSOH HLC-8220), UV (SHIMAZDZU CORPRATION UV-PC SERIES U V-2400PC / UV -2500PC). Elemental analysis for RIKEN Chemical Analysis Laboratory More analyzed.
- the solution is dropped into a mixed solution containing isoprene and (NCN) Sc (CH 2 SiMe) (THF) in the flask,
- a polymer was obtained in the same manner as in Example 1 except that the reaction time in Example 1 was changed from 20 minutes to 10 minutes.
- Example 1 The reaction time in Example 1 was changed from 20 minutes to 5 minutes and (NCN) Sc (CH SiMe) (TH).
- Example 2 The same procedure as in Example 1 was conducted except that (NCN) Y (CH SiMe) (THF) was used instead of (F).
- Example 1 a polymer was obtained in the same manner as in Example 1 except that the reaction temperature was changed from ⁇ 10 ° C. to room temperature and the reaction time was changed from 20 minutes to 5 minutes.
- FIG. 5 shows a 1 H-NMR ⁇ vector chart of the obtained polymer
- FIG. 6 shows a 13 C-NMR ⁇ vector chart.
- NMR ⁇ vectors were measured at room temperature using heavy chloroform as a solvent.
- Figure 7 shows the DSC chart.
- Example 4 instead of [Ph C] [B (C F)], [PhMe NH] [B (C F)] was used.
- a polymer was obtained in the same manner as in Example 4 except for the above.
- Example 4 instead of (NCN) Sc (CH SiMe) (THF), (NCN) Y (CH SiMe) (THF)
- a polymer was obtained in the same manner as in Example 4 except that 2 3 2 2 3 2 was used.
- Example 6 instead of [Ph C] [B (C F)], [PhMe NH] [B (C F)] was used.
- FIG. 8 shows a 1 H-NMR ⁇ vector chart of the obtained polymer
- FIG. 9 shows a 13 C-NMR ⁇ vector chart.
- NMR ⁇ vector was measured at room temperature using deuterated form as solvent.
- a polymer was obtained in the same manner as in Example 4 except that.
- Example 7 instead of (NCN) Sc (CH SiMe) (THF), (NCN) Y (CH SiMe) (THF)
- a polymer was obtained in the same manner as in Example 7 except that 2 3 2 2 3 2 was used.
- Example 9 In Example 7, instead of (NCN) Sc (CH SiMe) (THF), (NCN) Lu (CH SiMe) (THF)
- a polymer was obtained in the same manner as in Example 7 except that 2 3 2 2 3 2 was used.
- Example 7 instead of (NCN) Sc (CH SiMe) (THF), (NCN) Sc (CH C H NMe -o)
- a polymer was obtained in the same manner as in Example 7 except that 2 3 2 2 6 4 2 was used.
- Example 7 instead of (NCN) Sc (CH SiMe) (THF), (NCN) Y (CH C H NMe -o)
- a polymer was obtained in the same manner as in Example 7 except that 2 3 2 2 6 4 2 2 was used.
- Example 7 a polymer was obtained in the same manner as in Example 7, except that the reaction temperature was changed from room temperature to -10 ° C and the reaction time was changed from 5 minutes to 20 minutes.
- Example 11 instead of (NCN) Sc (CH SiMe) (THF), (NCN) Y (CH SiMe) (THF)
- a polymer was obtained in the same manner as in Example 11 except that 2 3 2 2 3 2 was used.
- a polymer was obtained in the same manner as in Example 11 except that F) was used.
- Example 11 instead of (NCN) Sc (CH SiMe) (THF), (NCN) Sc (CH C H NMe-
- a polymer was obtained in the same manner as in Example 11 except that 2 3 2 2 6 4 2 o) was used.
- a polymer was obtained in the same manner as in Example 14, except that the reaction time was changed from 20 minutes to 30 minutes in Example 14.
- Example 14 (NCN) Sc (CH C H NMe -o) was previously added in [Ph C] [B (C F)] for 10 minutes.
- Example 17 In Example 14, instead of (NCN) Sc (CH CH NMe -o), (NCN) Y (CH CH NMe-
- a polymer was obtained in the same manner as in Example 14 except that 2 6 4 2 2 2 6 4 2 o) was used.
- Example 8 a polymer was obtained in the same manner as in Example 8 except that the reaction temperature was changed from room temperature to 20 ° C.
- Table 1 shows the yield (%) of polyisoprene obtained in Examples and Reference Examples, number average molecular weight M, molecular weight distribution M / M, ratio of 3,4-polyisoprene to total polyisoprene (%). , Isotacticity (%) in triad display and pentad display, glass transition temperature T (° C) g
- polyisoprene having a high isotacticity can be produced by appropriately selecting the reaction conditions using the polymerization catalyst composition of the present invention.
- (NCN) Sc (CH SiMe) (THF) or (NCN) Sc (CH C H NMe -o) is used as a complex and used as a catalyst activator.
- Len can be produced.
- NCN Sc (CH SiMe) (THF)
- NCN Y (CH SiMe) (THF)
- reaction temperature was set to room temperature, the reaction time was 30 minutes, and the reaction was carried out in the same manner as in the Examples.
- B and C represent complexes represented by the general formula (B) and the general formula (C), respectively, and the parenthesis represents the central metal M.
- a is [Ph 3 C] [B (C 6 F 5 ) 4]
- b is [PhMe 2 NH] [B (C 6 F 5 ) 4 ]
- c is B (C 6 F 5 ) 3 is shown.
- the isoprene-based polymer produced by the production method using the polymerization catalyst composition of the present invention is considered to exhibit excellent mechanical or thermal durability with high isotacticity. Therefore, it is expected to be used as a plastic material.
- the polymerization catalyst composition of the present invention is low in cost, the double bond of the 1-alkylvinyl group or 1-alkenylvinyl group in the side chain of the isoprene-based polymer is chemically modified. Therefore, it is considered useful for the development of new functional polymers.
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Transition And Organic Metals Composition Catalysts For Addition Polymerization (AREA)
- Addition Polymer Or Copolymer, Post-Treatments, Or Chemical Modifications (AREA)
- Polymerization Catalysts (AREA)
Description
イソプレン系化合物の重合用の重合触媒組成物
技術分野
[0001] 本発明はイソプレン系重合体、特に位置選択的であって、かつ高いタクチシティ一 を有するイソプレン系重合体、好ましくはポリイソプレンの製造方法及びこれに用いる 重合触媒組成物に関する。
背景技術
[0002] ポリイソプレンは、以下の 4つの異なる構造単位を有する可能性がある。すなわち、 一般式 (Γ)で表される 3, 4結合型構造単位、一般式 (ΙΓ)で表されるトランス 1, 4結合 型構造単位、一般式 (ΠΓ)で表されるシス 1, 4結合型構造単位、及び一般式 (IV)で 表される 1, 2結合型構造単位である。
[0003] [化 1]
[0004] 上記の構造単位のうち、一般式 (Γ)で表される構造単位を選択的に有するポリイソ プレンの製造について、以下の二つの報告がされている。一つは、アルミニウムアル キル—チタニウムアルコキシド (AlEt -Ti(OC H -n) )系の触媒を重合触媒として用
3 3 7 4
いてイソプレンを重合させて、上記重合体を製造するという報告である(非特許文献 1 参照)。もう一つは、 FeClにスパルティン (sparteine)が配位した錯体を重合触媒とし
2
て用いてイソプレンを重合させて、上記重合体を製造するという報告である(非特許 文献 2)。
[0005] 一方、一般式 (Γ)で表される構造単位を選択的に有するポリイソプレンは、該構造 単位の配列のタクチシティーによって物性が大きく異なると考えられる。一般式 (Γ)で 表される構造単位力 なるポリイソプレンのように、主鎖原子に相異なる二つの側鎖 置換基をもつ高分子には 2種類の立体異性が生じ得る。タクチシティーとはこの立体
異性を示す部分の高分子主鎖中での配列の仕方あるいは秩序を意味する。相違な る二つの側鎖置換基の一方が、高分子主鎖のつくる平面に対して片方にのみ結合 して 、る高分子をァイソタクチック重合体(下記一般式 (V)で表される)と称し、平面に 対して交互に両方向に結合して 、る高分子をシンジオタクチック重合体(下記一般式
(VI)で表される)と称する。また、このような規則性のない高分子をァタクチック重合 体と称する。
(V) (VI)
[0007] 上記した非特許文献 1では、得られたポリイソプレンについてァタクチック重合体で あると記載されており、また非特許文献 2では、得られたポリイソプレンのタクチシティ 一に関して記載がされていない。したがって、一般式 (Γ)を選択的に有するポリイソプ レンであって、かつ高いタクチシティ一を有するポリイソプレンが求められていた。
[0008] このような技術背景において、高いタクチシティ一を有するポリイソプレンを製造す る方法が報告されている(特許文献 1)。ここでは、メタ口セン系触媒を用いてポリイソ プレンの重合を行っている。このような触媒を用いてイソプレンの重合を行うことにより 、高いタクチシティ一を有するポリイソプレンを製造することができるものの、現時点で は触媒のコストが高くつくという問題がある。
従って、高 、タクチシティ一を有するポリイソプレンなどのイソプレン系重合体を低コ ストで製造するための他の触媒が求められている。
[0009] 一方、アミジンを含む非メタ口セン系触媒を用いたポリエチレンを製造することが報 告されている(非特許文献 3)。ここでは、中心金属を変えることにより、ポリエチレンの 収率が変動することが報告されている。しかしながら、高いタクチシティ一を有するィ ソプレン系重合体を製造することにつ 、ては報告されて 、な!/、。
特許文献 1:国際公開第 05Z085306号パンフレット
非特許文献 l : Makromolekulare Chem (1964), 77, pp.126- 138.
非特許文献 2 :Macromolecules (2003), 36, pp.7953- 7958.
非特許文献 3 : J. AM. CHEM. SOC. (2004), 126, pp.9182- 9183.
発明の開示
[0010] 本発明はこのような状況下でなされたものであり、下記一般式 (Y)で表される構造 単位を選択的に有するイソプレン系重合体であって、かつ該構造単位の配列のタク チシティ一が高 、イソプレン系重合体 (特にァイソタクチックリッチなイソプレン系重合 体)を低コストで製造するための重合触媒組成物及び該重合触媒組成物を用いて、 タクチシティーが高いイソプレン系重合体を製造する方法を提供することを課題とす る。
[0011] [化 3]
(一般式 (Y)中、 R4は炭素数 1〜10のアルキル基又はァルケ-ル基を示す。 )
[0012] すなわち本発明は以下の通りである。
(1)一般式 (A)で表される錯体及び触媒活性化剤を含むことを特徴とする、一般式 ( X)で表されるイソプレン系化合物の重合用の重合触媒組成物。
[0013] [化 4]
[0014] (一般式 (A)にお!/、て、
R1及び R2はそれぞれ独立して、アルキル基、シクロへキシル基、ァリール基又はァ ラルキル基を示し、
R3はアルキル基、ァルケ-ル基、アルキ-ル基、ァリール基又はァラルキル基、脂 肪族、芳香族又は環状のアミノ基、若しくはホスフイノ基、ボリル基、アルキル又はァリ 一ルチオ基、アルコキシ又はァリールォキシ基を示し、
Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除くランタン Laからルテ チウム Luまでの希土類元素の何れかを示し、
Q1および Q2はそれぞれ独立して、モノア-オン性配位子を示し、
Lは中性ルイス塩基を示し、 wは 0〜3の整数を示す。)
[0016] (一般式 (X)において R4は炭素数 1〜 10のアルキル基又はァルケ-ル基を示す。 ) [0017] (2)—般式 (A)における R1及び R2が 2, 6—ジイソプロピルフエ-ル基を示し、 R3がフ ェニル基を示すことを特徴とする、 (1)に記載の重合触媒組成物。
(3)一般式 (A)で表される錯体が、一般式 (B)で表される化合物であることを特徴と する、(1)又は(2)に記載の重合触媒組成物。
[0018]
[0019] (一般式(B)において、 Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除 くランタン Laからルテチウム Luまでの希土類元素の何れかを示す。)
(4)一般式 (A)で表される錯体が、一般式 (C)で表される化合物であることを特徴と
する、(1)又は(2)に記載の重合触媒組成物。
[化 7]
[0021] (一般式(C)にお!/、て、 Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除 くランタン Laからルテチウム Luまでの希土類元素の何れかを示す。)
(5)前記触媒活性化剤が、非配位性ァ-オンとカチオンカゝらなるイオン性ィ匕合物で あることを特徴とする、(1)〜 (4)の何れか一に記載の重合触媒組成物。
(6)前記非配位性ァ-オン力 価のホウ素ァ-オンであることを特徴とする、 (5)に記 載の重合触媒組成物。
[0022] (7)—般式 (X)で表されるイソプレン系化合物を、(1)〜(6)の何れか一に記載の重 合触媒組成物を用いて重合させることを特徴とする、イソプレン系重合体の製造方法
(8)—般式 (X)における R4力メチル基であることを特徴とする、 (7)に記載の製造方 法。
(9)前記重合が溶液重合であって、重合反応温度が 0°C以下であることを特徴とする 、(7)又は (8)に記載の製造方法。
図面の簡単な説明
[0023] [図 1]実施例 1で得られたポリイソプレンの1 H—NMRスペクトルチャートである。
[図 2]実施例 1で得られたポリイソプレンの13 C— NMR ^ベクトルチャートである。
[図 3]実施例 1で得られたポリイソプレンの GPCチャートである。
[図 4]実施例 1で得られたポリイソプレンの DSCチャートである。
[図 5]実施例 4で得られたポリイソプレンの1 H— NMRスペクトルチャートである。
[図 6]実施例 4で得られたポリイソプレンの13 C— NMR ^ベクトルチャートである。
[図 7]実施例 4で得られたポリイソプレンの DSCチャートである。
[図 8]参考例 1で得られたポリイソプレンの1 H— NMRスペクトルチャートである。
[図 9]参考例 1で得られたポリイソプレンの13 C— NMR ^ベクトルチャートである。 発明を実施するための最良の形態
[0024] 本発明の重合触媒組成物は、前記一般式 (A)で表される錯体及び触媒活性化剤 を含むことを特徴とする。
[0025] 一般式 (A)にお 、て、 R1及び R2はそれぞれ独立してアルキル基、置換若しくは無 置換のシクロへキシル基、ァリール基又はァラルキル基である。アルキル基としては、 メチル基、ェチル基、イソプロピル基、 n—ブチル基、 t—ブチル基等を例示できる。 置換のシクロへキシル基としては、アルキル基を置換基とするシクロへキシル基、例 えばメチルシクロへキシル基等を例示できる。無置換のァリール基としては、例えばフ ェニル基を例示でき、置換のァリール基としては、例えばアルキル基を置換基とする フエ二ル基等を例示できる。無置換のァラルキル基としては、例えばベンジル基を例 示でき、置換のァラルキル基としては、例えばアルキル基を置換基とするベンジル基 等を例示できる。この中でもアルキル基を置換基とするフエニルが好ましぐ特に 2, 6 ージイソプロピルフエ-ル基が好まし 、。 R1及び R2は同一でも異なって 、てもよ!/、が 、 R1及び R2は共にアルキル基を置換基とするフエ-ル基であることが好ましぐ共に 2 , 6—ジイソプロピルフエ-ル基であることがさらに好ましい。
[0026] R3はアルキル基、ァルケ-ル基、アルキ-ル基、ァリール基又はァラルキル基、脂 肪族、芳香族又は環状のアミノ基、若しくはホスフイノ基、ボリル基、アルキル又はァリ 一ルチオ基、アルコキシ又はァリールォキシ基を示す。この中でもァリール基が好ま しぐ特にフエニル基が好ましい。
[0027] さらに、本発明の重合触媒組成物に含まれる錯体は、 R1及び R2力 共に 2, 6—ジ イソプロピルフエ-ル基であり、かつ R3がフエ-ル基である Ν,Ν'-ビス(2, 6—ジイソプ 口ピルフエ-ル)ベンズアミジナート(NCN)の構造を有することが好まし!/、。
[0028] 一般式 (Α)において、中心金属 Μは、スカンジウム Sc、イットリウム Y又はプロメチウ ム Pmを除くランタン Laからルテチウム Luまでの希土類元素の何れかを示す。本発 明の重合触媒組成物に含まれる錯体においては、中心金属 Mは重合させようとする
モノマーの種類などに応じて適宜選択されうる力 スカンジウム Sc、イットリウム Y又は ルテチウム Luが好ましぐ特にスカンジウム Scが好ましい。
[0029] 一般式 (A)にお!/、て、 Q1および Q2はモノア-オン性配位子である。モノア-オン性 配位子としては、 1)ヒドリド、 2)ハライド、 3)置換もしくは無置換の、炭素数 1〜20のヒ ドロカルビル基、 4)置換もしくは無置換の、炭素数 1〜20のアルコキシ基もしくはァリ ールォキシ基、 5)置換もしくは無置換の、炭素数 1〜20のアミド基 (シリルアミド基を 含む)、 6)ホスフイノ基などが例示され、ヒドロカルビル基が好ましく例示される力 こ れらに限定されるわけではない。
また、 Q1および Q2は互いに結合する力、あるいは一緒になつてジァ-オン性配位 子となっていてもよい。ジァ-オン性配位子としては、アルキリデン、ジェン、シクロメ タルイ匕されたヒドロカルビル基、または二座のキレート配位子などが挙げられる。
[0030] 前記ハライドは、クロリド、ブロミド、フルオリド及びアイオダイドの 、ずれでもよ!/ヽ。
前記炭素数 1〜20のヒドロカルビル基は、メチル基、ェチル基、プロピル基、イソプ 口ピル基、ブチル基、イソブチル基、 t ブチル基、ペンチル基、アミル基、イソアミル 基、へキシル基、シクロへキシル基、ヘプチル基、ォクチル基、ノ-ル基、デシル基、 セチル基、 2—ェチルへキシル基などのアルキル基、ビニル基、 1 プロべ-ル基、 イソプロべ-ル基、ァリル基、メタリル基、クロチル基等のァルケ-ル基、ェチュル基、 3, 3 ジメチルー 1ーブチュル基等のアルキ-ル基、フエ-ル基、トリル基等のァリー ル基、ベンジル基、ジフエ-ルメチル基、フエ-ルェチル基、ジフエ-ルェチル基等 のフエ-ルアルキル基等のァラルキル基、トリアルキルシリルメチル基、ビス(トリアル キルシリル)メチル基、 2—フエ-ルェチュル基、 2—(トリメチルシリル)ェチュル基、メ チルフエ-ル基、ジメチルフエ-ル基、ァミノフエ-ル基、 o-N, N ジメチルァミノベン ジル基等のァミノべンジル基、 0- (メチルチオ)ベンジル基等のチォベンジル基、。-メト キシベンジル基等のアルコキシベンジル基、 0- (ジメチルホスフイノ)ベンジル基等のホ スフイノべンジル基などでもよ 、。
[0031] 本発明においては Q1及び Q2は、トリアルキルシリルメチル基又はアミノベンジル基 であることが好まし ヽ。トリアルキルシリルメチル基のシリル元素上の 3個のアルキル 基は、炭素原子数 1〜6程度、好ましくは炭素原子数 1〜4程度の直鎖又は分岐鎖基
が挙げられ、さらに好ましくはメチル基が挙げられる。該トリアルキルシリルとしては、 例えばトリメチルシリル、 t ブチルジメチルシリルなどが挙げられる。ァミノべンジル 基としては、 0-N, N ジメチルァミノべンジル基が好ましく挙げられる。
[0032] 前記アルコキシ基またはァリールォキシ基は、好ましくはメトキシ基、置換または無 置換のフエノキシ基などである。
前記アミド基は、好ましくはジメチルアミド基、ジェチルアミド基、メチルェチルアミド 基、ジー t ブチルアミド基、ジイソプロピルアミド基、無置換または置換ジフエ-ルァ ミド基、ビス(トリメチルシリル)アミド基などである。
前記ホスフイノ基は、好ましくはジフエ-ルホスフイノ基、ジシクロへキシルホスフイノ 基、ジイソプロピルホスフイノ基、ジェチルホスフイノ基、ジメチルホスフイノ基などであ る。
[0033] 前記アルキリデンは、好ましくはメチリデン、ェチリデン、プロピリデン、ベンジリデン などである。
前記シクロメタル化されたヒドロカルビル基は、好ましくはプロピレン、ブチレン、ペン チレン、へキシレン、オタチレンなどである。
前記ジェンは、好ましくは 1, 3 ブタジエン、 1, 3 ペンタジェン、 1, 4 ペンタジ ェン、 1, 3 へキサジェン、 1, 4一へキサジェン、 1, 5 へキサジェン、 2, 4ージメ チルー 1, 3 ペンタジェン、 2—メチルー 1, 3 へキサジェン、 2, 4一へキサジェン などである。
[0034] 前記一般式 (I)における Lは中性ルイス塩基である。中性ルイス塩基としてはテトラ ヒドロフラン (THF)、ジェチルエーテル、ジメチルァ-リン、トリメチルホスフィン、塩化 リチウムなどが例示される。この中でも、テトラヒドロフランが好ましい。
また中性ルイス塩基 Lは、 Q1および Zまたは Q2と結合して 、わゆる多座配位子とな つていてもよい。
一般式 (I)における Lの wは、中性ルイス塩基の個数を示す。 wは、中心金属 Mの 種類などに応じて異なる力 通常は 0〜3の整数であり、好ましくは 0または 1である。
[0035] また、本発明の重合用触媒組成物に含まれる一般式 (A)で表される錯体は、前記 一般式 (B)又は(C)で表される化合物であることが好ま 、。一般式 (B)又は(C)に
おいて中心金属 Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除くラン タン Laからルテチウム Luまでの希土類元素の何れかを示す。本発明の重合触媒組 成物に含まれる錯体においては、中心金属 Mは重合させようとするモノマーの種類 などに応じて適宜選択されうる力 スカンジウム Sc、イットリウム Y又はルテチウム Lu が好ましぐ特にスカンジウム Scが好ましい。
[0036] 本発明の重合触媒組成物に含まれる触媒活性化剤は、イオン性化合物、アルキル アルミニウム化合物又はルイス酸などであり、好ましくは非配位性ァ-オンとカチオン カゝらなるイオン性ィ匕合物を含む。前記触媒活性化剤は、本発明の錯体を活性化させ て重合触媒としての活性を発揮させる。その活性化メカニズムとして、前記錯体が触 媒活性化剤と反応して、前記錯体の希土類金属原子に複数個配位して!/、る Q1又は Q2が脱離し、カチオン性の錯体 (活性種)が生成すると考えることができる。
[0037] イオン性ィ匕合物の非配位性ァ-オンとしては、例えば、 4価のホウ素ァ-オンが好 ましぐテトラ(フエ-ル)ボレート、テトラキス(モノフルオロフェ -ル)ボレート、テトラキ ス(ジフルオロフェ -ル)ボレート、テトラキス(トリフルオロフェ -ル)ボレート、テトラキ ス(トリフルオロフェ -ル)ボレート、テトラキス(ペンタフルォロフエ-ル)ボレート、テト ラキス (テトラフルォロメチルフエニル)ボレート、テトラ(トリル)ボレート、テトラ(キシリ ル)ボレート、 (ペンタフルォロフエ-ル)トリフエ-ルポレート、 [トリス(ペンタフルォロ フエ-ル),フエ-ル]ボレート、トリデカハイドライド- 7,8-ジカルパウンデカボレートな どが挙げられる。
[0038] イオン性化合物のカチオンとしては、カルボ-ゥムカチオン、ォキソ-ゥムカチオン 、アンモ-ゥムカチオン、ホスホ-ゥムカチオン、シクロヘプタトリエ-ルカチオン、遷 移金属を有するフエ口セ-ゥムカチオンなどを挙げることができる。カルボ-ゥムカチ オンの具体例としては、トリフエ-ルカルポ-ゥムカチオン、トリ置換フエ-ルカルポ- ゥムカチオンなどの三置換カルボ-ゥムカチオンを挙げることができる。トリ置換フエ -ルカルボ-ゥムカチオンの具体例としては、トリス(メチルフエ-ル)カルボ-ゥムカ チオン、トリス(ジメチルフエ-ル)カルボ-ゥムカチオンを挙げることができる。アンモ ユウムカチオンの具体例としては、トリメチルアンモ-ゥムカチオン、トリェチルアンモ -ゥムカチオン、トリプロピルアンモ-ゥムカチオン、トリ tーブチルアンモ -ゥムカチォ
ン、トリ n—ブチルアンモ-ゥムカチオンなどのトリアルキルアンモ-ゥムカチオン、 N, N-ジェチルァ-リュウムカチオン、 Ν,Ν-2,4,6-ペンタメチルァ-リュウムカチオンなど の Ν,Ν-ジアルキルァ-リュウムカチオン、ジ (イソプロピル)アンモ-ゥムカチオン、ジ シクロへキシルアンモ-ゥムカチオンなどのジアルキルアンモ-ゥムカチオンを挙げ ることができる。ホスホ-ゥムカチオンの具体例としては、トリフエ-ルホスホ-ゥムカチ オン、トリス(メチルフエ-ル)ホスホ-ゥムカチオン、トリス(ジメチルフエ-ル)ホスホ- ゥムカチオンなどのトリアリールホスホ-ゥムカチオンを挙げることができる。
[0039] すなわち、前記イオン性ィ匕合物として、前記した非配位性ァ-オンおよびカチオン 力もそれぞれ選ばれるものを組み合わせたものを用いることができる。好ましくは例え ば、トリフエ-ルカルベ-ゥムテトラキス(ペンタフルォロフエ-ル)ボレート、トリフエ- ルカルべ-ゥムテトラキス(テトラフルオロフェ -ル)ボレート、 Ν,Ν-ジメチルァ-リュウ ムテトラキス(ペンタフルォロフエ-ル)ボレート、 1 , 1しジメチルフエロセ-ゥムテトラキ ス(ペンタフルォロフエ-ル)ボレートなどが例示される。この中でも、トリフエ-ルカル ベ-ゥムテトラキス(ペンタフルォロフエ-ル)ボレート、 Ν,Ν-ジメチルァ-リュウムテト ラキス(ペンタフルォロフエ-ル)ボレートを用いることが好まし 、。イオン性化合物は 1 種を用いてもよぐ 2種以上を組み合わせて用いてもよい。また、遷移金属化合物と 反応してカチオン性遷移金属化合物を生成できるルイス酸として、 B(C F ) 、 A1(C F )
6 5 3 6 5 などを用いることができ、これらを前記のイオン性ィ匕合物と組み合わせて用いてもよ
3
い。
[0040] 本発明の重合触媒組成物は、一般式 (A)で表される錯体の少なくとも 1つと触媒活 性化剤の少なくとも 1つを含みうるが、好ましくは、一般式 (B)及び (C)で表される錯 体の少なくとも 1つとトリフエ-ルカルベ-ゥムテトラキス(ペンタフルォロフエ-ル)ボレ ート([Ph C][B(C F ) ])及び Ν,Ν-ジメチルァユリ-ゥムテトラキス(ペンタフルオロフェ
3 6 5 4
-ル)ボレート([PhMe NH][B(C F ) ])の少なくとも 1つを含むことが好ましい。特に、(
2 6 5 4
NCN)Sc(CH SiMe ) (THF)、(NCN)Y(CH SiMe ) (THF)及び (NCN)Sc(CH C H NMe -
2 3 2 2 3 2 2 6 4 2 o)力 選ばれる錯体と、 [Ph C][B(C F ) ]を含むことが好ましい。
2 3 6 5 4
[0041] 本発明の重合触媒組成物にお!ヽて、一般式 (A)で表される錯体は任意の量を用 いることができ、重合させるイソプレン系化合物の量及び製造の目的とするイソプレン
系重合体の分子量に応じて調節することができる。好ましくは、後述するイソプレン系 重合体の製造方法に用いるのに適した量とすることができる。触媒活性化剤の量も 同様に調節することができる力 通常、前記錯体 1モルに対して 0. 5から 5モル、好ま しくは約 1倍モルである。
[0042] さらに、イソプレン系重合体の製造方法に用いられる重合触媒は、有機アルミ-ゥ ム系化合物やアルミノキサンなど第三成分を含んで 、てもよ 、。有機アルミ系化合物 やアルミノキサンを加えると、反応系内の不純物の除去や連鎖移動が促進されると考 えられるので、触媒活性や得られたポリマーの分子量などが変わることが予想される
[0043] 本発明の重合触媒組成物は、前記一般式 (X)で表されるイソプレン系化合物の重 合用として用いられる。一般式 (X)において R1はアルキル基又はアルケニル基を示 す。例えば、炭素数 1〜10 (好ましくは炭素数 1〜6)のアルキル基又はァルケ-ル基 であり、特に好ましくはメチル基又は 4—メチル— 3—ペンテニル基である。
[0044] <本発明のイソプレン系重合体の製造方法 >
高 、アイソタクチシティ一を有するイソプレン系重合体は、一般式 (A)で表される錯 体及び触媒活性化剤を用いて、前記一般式 (X)で表されるイソプレン系化合物を重 合させること〖こより製造することができる。
[0045] 一般式 (A)で表される錯体は、例えば下記のスキームに従って製造することが可能 である。当業者は下記に示す一般的合成スキームを参照しつつ、出発原料、反応試 薬、反応条件などを適宜選択し、必要に応じてこれらの方法に適宜の修飾ないし改 変を加えることにより、一般式 (A)で表される錯体を容易に製造することができる。な お、一般式 (A)で表される錯体の合成については、 J. AM. CHEM. SOC. 2004, 126, 9182-9183に記載の内容を参照することもできる。
[0046] [化 8]
[0047] イソプレン系重合体の製造において、該錯体の使用量は、イソプレン系化合物の 1 モノレに対して、通常は 0. 00001力ら 0. 05モノレ、好ましくは 0. 0001力ら 0. 01モノレ である。イソプレンに対して該錯体の量を減らせば、得られるイソプレン系重合体の 分子量を大きくすることができ、逆に該錯体の量を増やせばイソプレン系重合体の分 子量を小さくすることができる。
[0048] イソプレン系重合体の製造にぉ 、て、触媒活性化剤の量は、一般式 (A)で表され る錯体の 1モルに対して、通常は 0. 5から 5モル、好ましくは約 1倍モルである。
[0049] 本発明のイソプレン系重合体の製造方法は、付加重合法、重縮合法、重付加法、 又はその他の方法であり得るが、好ましくは付加重合法である。
[0050] また、本発明のイソプレン系重合体の製造方法は、気相重合法、溶液重合法、スラ リー重合法などの任意の方法であり得る。溶液重合法による場合、用いられる溶媒は 重合反応において不活性であり、イソプレン系化合物及び触媒を溶解させ得る溶媒 であれば特に限定されない。例えば、ブタン、ペンタン、へキサン、ヘプタン等の飽和 脂肪族炭化水素;シクロペンタン、シクロへキサン等の飽和脂環式炭化水素;ベンゼ ン、トルエン等の芳香族炭化水素;塩化メチレン、クロ口ホルム、四塩化炭素、トリクロ 口エチレン、ノ ークロノレエチレン、 1,2-ジクロロエタン、クロ口ベンゼン、ブロモベンゼ ン、クロ口トルエン等のハロゲン化炭化水素;テトラヒドロフランゃジェチルエーテルな どのエーテル類が挙げられる。これらの溶媒のうち、 0°Cより低い融点を有するものが 好ましぐ—20°Cより低い融点を有するものがより好ましい。具体的には、芳香族炭 化水素、特にクロ口ベンゼンが好ましい。溶媒は 1種を単独で用いてもよいが、 2種以 上組み合わせた混合溶媒を用いてもょ 、。
また、用いられる溶媒の量は、通常は重合触媒に含まれる錯体の濃度が 0. 00001 〜0. 1M、好ましくは 0. 0001-0. 01Mとなるように調節することができる。
[0051] 本発明の重合を溶液重合で行う場合の重合反応温度は、任意の温度、例えば 1 00〜100°Cの範囲で行いうる。通常は 25°C以下、好ましくは 0°C以下、より好ましく は— 10°C以下、さらに好ましくは— 20°C以下であり得る。重合温度を低下させること で、得られるイソプレン系重合体に含まれる構造単位 (1' )の配列のタクチシティー ( アイソタクチシティ一)を高めることができる。つまり、重合温度を調整することによって
該ァイソタクチシティ一を調整することができる。
[0052] 反応時間は、例えば 1分〜 100時間程度であり、通常は 1分〜 24時間、好ましくは 5〜60分である。もっとも、これらの反応条件は、重合反応温度、モノマーの種類や 量、触媒組成物の種類や量などに応じて、適宜選択することが可能であり、上記に例 示した範囲に限定されることはない。本発明は上記のようにより低温で重合させること が好ましいので、温度を下げることによって反応性が下がる場合には重合時間を長く することが好ましい。
[0053] 本発明のイソプレン系重合体の製造方法は、反応系中に錯体、イソプレン系化合 物および触媒活性化剤、ならびにその他の化合物を任意の順序で添加して実施す ればよいが、通常は錯体とイソプレン系化合物の混合物中に、触媒活性化剤を添加 して実施する。一方、錯体と触媒活性化剤の混合物中に、イソプレン系化合物を添 加して重合反応を行うと、得られるイソプレン系重合体の分子量分布曲線は、複数の ピークを有することがある(すなわち、分子量分布のピークが互いに異なるイソプレン 系重合体の混合物が得られることがある)。
[0054] 重合反応が所定の重合率に達した後、公知の重合停止剤(例えば BHT(2,6-ビス (t -ブチル) -4-メチルフエノールを含有するメタノール))を重合系に加えて停止させ、次 V、で通常の方法に従!、生成した重合体を反応系から分離することができる。
[0055] 本発明の製造方法を用いて一般式 (X)で表されるイソプレン系化合物を重合させ て得られるイソプレン系重合体は、下記一般式 (1)、 (Π)、 (III) , (IV)で表される構 造単位 (以下、それぞれについて、単に「構造単位 (1)、 (Π)、 (III) , (IV)」とも称する 。)を任意の比率で含みうる。構造単位 (I)〜(IV)における R4はアルキル基又はアル ケニル基である。さらに好ましくは、 R4はメチル基であり、すなわち本発明の製造方法 により製造される最も好ましいイソプレン系重合体はポリイソプレンである。また、 R4と して 4ーメチルー 3—ペンテ二ル基も好ましく例示され、すなわち、好ましい重合体と してミルセン重合体が挙げられる。
[0057] 本発明の製造方法により製造されるイソプレン系重合体に含まれる構造単位 (I)の 、該重合体のミクロ構造における割合は、通常は 60%以上、好ましくは 90%以上、よ り好ましくは 95%以上、さらに好ましくは 99%以上である。なお、本発明の製造方法 により製造されるイソプレン系重合体は、構造単位 (I)以外に、構造単位 (II)〜 (IV) を任意の比率で含みうる。構造単位 (I)のミクロ構造における割合は、得られるイソプ レン系重合体の NMR ^ベクトルを測定し、各構造単位に帰属されるピークの積分値 を求めて、それを比較することで算出することができる。該算出については、本願明 細書にぉ 、て後に説明されて 、る。
[0058] イソプレン系重合体に含まれる構造単位 (I)は通常、頭一尾 (head to tail)結合して 配列している力 その配列において下記するような 2つの立体異性が生じ得る。すな わち、高分子主鎖がつくる平面に対する 1-アルキルビニル基もしくは 1-ァルケ-ル ビュル基 (-C(R4)=CH )、又は水素原子の結合の方向により、 2つの立体異性が生じ
2
得る。本発明の製造方法により製造されるイソプレン系重合体に含まれる構造単位 (I )は、立体規則性をもって配列しており、好ましくは高ァイソタクチックに配列している 。高ァイソタクチックに配列しているとは、一般式 (I)における 1-アルキルビュル基も しくは 1-アルケニルビニル基 (又は水素原子)が、高分子主鎖がつくる平面に対して 一方の面側に選択的に配置されていることをいう。
[0059] [化 10]
[0060] 具体的には、本発明の製造方法により製造されるイソプレン系重合体に含まれる構 造単位 (I)の配列のアイソタクチシティ一は、トリアツド表示で少なくとも 60%mm以上 、通常は 80%mm以上、好ましくは 90%mm以上、より好ましくは 95%mm以上、さ らに好ましくは 99%mm以上、最も好ましくはペンタツト表示で 99%mmmm以上で ある。
[0061] ここで、トリアツド表示について簡単に説明する。イソプレン系重合体中の、構造単 位 (I)の三連鎖(「トリアツド」という)は、以下のように、ァイソタクチックトリアツド、ヘテロ タクチックトリアツド、シンジオタクチックトリアツドの 3種類が考えられる。トリアツド表示 によるアイソタクチシティ一とは、重合体中における「ァイソタクチックトリアツド、ヘテロ トリアツド」の割合を意味し、その割合の百分率が '%mm'で表示される。
[0062] [化 11]
ァイソタクチック トリアツド ヘテロタクチック トリアツド
[0063] また、ペンタッド表示によるアイソタクチシティ一とは、構造単位 (I)の五連鎖(「ペン タッド」という)に注目して、トリアツド表示と同様にして、ペンタッドのうちのアイソタクチ ックペンタッドの割合を示したものであり、その割合の百分率は '%mmmm'で表示さ れる。
[0064] イソプレン系重合体に含まれる構造単位 (I)の配列のアイソタクチシティ一は、上記 のとおりトリアツド表示又はペンタッド表示により表され得る。なお、イソプレン系重合 体のトリアツド表示又はペンタッド表示によるアイソタクチシティ一は、得られるイソプレ ン系重合体の NMR ^ベクトルデータ (好ましくは13 C— NMR)力も算出することができ る。この算出については、本願明細書において後に説明されている。
[0065] 本発明の製造方法により製造されるイソプレン系重合体の平均分子量は任意であ る力 数平均分子量で、少なくとも 5千以上、通常 5万以上、好ましくは 10万以上であ る。なお数平均分子量の上限は特に限定されないが、 目安として 600万以下であり 得る。該数平均分子量は、 GPC法により測定した数平均分子量を意味し、例えば G PC測定装置(TOSOH HLC 8220 GPC)を用いて測定することができる。
[0066] 本発明の製造方法により製造されるイソプレン系重合体の分子量分布は、 M /Mで 表した場合、通常は 6以下、好ましくは 3以下、より好ましくは 1. 7以下である。該分子 量分布は、 GPC法により測定した分子量分布を意味し、例えば GPC測定装置 (TOS OH HLC 8220 GPC)を用いて測定することができる。
[0067] 本発明の製造方法により製造されるイソプレン系重合体は、炭素二重結合を含む 1 -アルキルビュル基又は 1-ァルケ-ルビ-ル基を側鎖として有している。該ビュル 基の炭素二重結合はヒドロシリルイ匕ゃヒドロホウ素化、エポキシィ匕することができる。
[0068] 本発明の製造方法により製造されるイソプレン系重合体は、単独重合体は勿論の こと、共重合体も含みうる。この様な共重合体としては、例えばイソプレンとイソプレン 以外のイソプレン系化合物との共重合体や、イソプレンと共役ジェンとの共重合体で あり得る。また、イソプレン系化合物と非極性モノマー(エチレン、スチレンなどを含む )あるいは極性モノマー(ラタトン、アクリル酸エステルなどを含む)との共重合体でも あり得る。
[0069] イソプレン系重合体は、 ^H— NMR分析、 13C— NMR分析、 GPC法による平均分 子量および分子量分布の測定、 IR測定、質量分析などにより同定することができる。 なお、本願明細書において「NMR分析」とは、 400MHzの周波数における核磁気 共鳴分光法による分析を意味する。例えば NMR分析装置である JEOL製 JNM-AL- 400RNを用いて該分析を行うことができる。また「NMR ^ベクトルデータ」とは該分析
により得られたスペクトルデータを意味する。なお測定溶媒は重クロ口ホルム CDC1
3、 測定温度は 25°C (室温)である。
[0070] イソプレン系重合体の、一般式 (I)で表される構造単位 (3,4-構造)のミクロ構造にお ける割合は、以下の既知文献(W. M. Dong, T. Masuda, J. Polym. Sci., Part A: Poly m. Chem., 40, 1838(2002)、 A. S. Khatchaturov, E. R. Dolinskaya, L. K. Prozenko, E. L. Abramenko and V. A. Kormer, Polymer, 18, 871, (1976))の記載に基づき、 NM Rスペクトルデータから求めることができる。
[0071] また、イソプレン系重合体に含まれる一般式 (I)で表される構造単位 (構造単位 (I) ) の配列のアイソタクチシティ一は、 NMR ^ベクトルデータから求めることができる。例え ば、図 8及び図 9は、ポリイソプレンであって、ミクロ構造における構造単位 (I)の割合 力 92%であって、かつ構造単位(I)の配列のアイソタクチシティ一が 36%mmである 重合体の1 H- NMR及び13 C— NMRの測定チャートである。図 8及び図 9においては、 ァイソタクチックトリアツド (mm)に帰属されるピークの他、ヘテロタクチックトリアツド (m r)に帰属されるピークやシンジオタクチックトリアツド (rr)に帰属されるピークが認めら れる。一方、図 1及び図 2は、ポリイソプレンであって、ミクロ構造における構造単位 (I )の割合が 99. 8%であって、かつ構造単位 (I)の配列のアイソタクチシティ一が 99% mmmmである重合体の1 H- NMR及び13 C- NMRの測定チャート、図 5及び図 6はポリイ ソプレンであって、ミクロ構造における構造単位 (I)の割合が 99. 0%であって、かつ 構造単位 (I)の配列のアイソタクチシティ一が 80%mmmmである重合体の1 H- NMR及 び13 C- NMRの測定チャート、である。図 1、図 2、図 5、図 6においては、図 8及び 9に おいて観察された、ヘテロタクチックトリアツド (mr)に帰属されるピークやシンジオタク チックトリアツド (rr)に帰属されるピークがほぼ消失していることがわかる。さらに、アイ ソタクチックトリアツド (mm)に帰属されるピークも、選択的にアイソタクチックペンタッド (mmmm)〖こ帰属されることがわかる。したがって、これらのピークの積分値を比較す ることにより、イソプレン系重合体に含まれる構造単位 (I)の配列のアイソタクチシティ 一を求めることができる。
実施例
[0072] 以下、本発明を実施例によりさらに具体的に説明するが、本発明の範囲は下記の
実施例により限定されることはない。
<錯体の合成 >
Y(CH C H NMe - o) (0.384g, 0.781mmol)のトルエン (4ml)溶液の入った 100mlフラス
2 6 4 2 3
コに、(NCN)H (bis(2,6-diisopropylphenyl)benzamidine) (0.344 g, 0.781 mmol)の n—へ キサン (6ml)溶液を滴下し、一晩攪拌した。反応混合液は明るい淡黄色に変化した。 次いで反応混合液力 低沸点化合物を除去後、減圧乾燥し、定量的に淡黄色の粉 体を得た。これを冷却したへキサン 3mlで速やかに洗い、トルエン 3mlと少量の n-へキ サン中で再結晶させ、(NCN)Y(CH C H NMe - o)を結晶として単離した (0.529g,収率
2 6 4 2 2
85%)。また、 Y(CH C H NMe - o)の代わりに Scを用いることによって (NCN)Sc(CH C
2 6 4 2 3 2 6
H NMe - o)を得た。
4 2 2
[0073] [化 12]
[0074] J. AM. CHEM. SOC. 2004, 126, 9182-9183に記載の方法に従って、(NCN)Sc(CH SiMe ) (THF)、(NCN)Y(CH SiMe ) (THF)、 (NCN)Lu(CH SiMe ) (THF)を得た。
3 2 2 3 2 2 3 2
[0075] [化 13]
くポリイソプレンの製造 >
以下の実施例で得られた化合物は1 H— NMR, 13C— NMR(JEOL製 JNM-AL 400RN ) , GPC (TOSOH HLC-8220) , UV(SHIMAZDZU CORPRATION UV- PC SERIES U V-2400PC/UV-2500PC)により同定した。元素分析は、理化学研究所化学分析室に
より分析された。
[0077] [化 14]
[0078] <実施例 1 >
グローブボックス中で、滴下漏斗を取り付けたフラスコ(100 ml)に磁気攪拌子を入 れ、イソプレン (1.022 g, 15.0 mmol)、 (NCN)Sc(CH SiMe ) (THF) (0.015 g, 0.020mmo
2 3 2
1)、クロ口ベンゼン溶液 (4ml)をカ卩えた。次いで、 [Ph C][B(C F ) ] (0.018 g, 0.020mmol
3 6 5 4
)のクロ口ベンゼン溶液 (lml)を滴下漏斗へカ卩えた。この反応装置を、屋外に移動し、 クーリングバス(— 10°C)に設置した。 10分後、 [Ph C][B(C F ) ]のクロ口ベンゼン溶
3 6 5 4
液をフラスコ内のイソプレンと (NCN)Sc(CH SiMe ) (THF)を含む混合溶液に滴下し、
2 3 2
高速攪拌した。この混合溶液を一 10°Cで 20分攪拌した後、メタノールを加えることに より重合を終了させた。反応溶液を少量の塩酸および安定剤としてプチルヒドロキシ トルエン(BHT)を含むメタノール溶液 200 mlに注いだ。デカンテーシヨンにより沈殿し たポリマー生成物を単離し、小さく切断した後、メタノールで洗浄し、 60°Cにて減圧 乾燥し、 1.021 gのポリマーを得た(収率: 100%)。得られたポリマーの1 H—NMR^ ベクトルチャートを図 1に、 13C— NMR ^ベクトルチャートを図 2に示す。 NMR ^ベクトル は、室温で重クロ口ホルムを溶媒として測定した。また、 GPCチャートを図 3に、 DSCチ ヤートを図 4に示す。
[0079] <実施例 2>
実施例 1における反応時間を 20分間から 10分間に変更したこと以外は、実施例 1 と同様にしてポリマーを得た。
<実施例 3 >
実施例 1における反応時間を 20分間から 5分間に変更し、 (NCN)Sc(CH SiMe ) (TH
2 3 2
F)に代えて (NCN)Y(CH SiMe ) (THF)を用いたこと以外は、実施例 1と同様にしてポリ
2 3 2
マーを得た。
<実施例 4>
実施例 1において、反応温度を— 10°Cから室温に変更し、反応時間を 20分間から 5分間に変更したこと以外は、実施例 1と同様にしてポリマーを得た。
得られたポリマーの1 H— NMR ^ベクトルチャートを図 5に、 13C— NMR ^ベクトルチヤ 一トを図 6に示す。 NMR ^ベクトルは、室温で重クロ口ホルムを溶媒として測定した。ま た、 DSCチャートを図 7に示す。
[0080] <実施例 5 >
実施例 4において、 [Ph C][B(C F ) ]に代えて [PhMe NH][B(C F ) ]を用いたこと以
3 6 5 4 2 6 5 4
外は、実施例 4と同様にしてポリマーを得た。
<実施例 6 >
実施例 4において、 (NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Y(CH SiMe ) (THF)
2 3 2 2 3 2 を用いたこと以外は、実施例 4と同様にしてポリマーを得た。
[0081] <参考例 1 >
実施例 6において、 [Ph C][B(C F ) ]に代えて [PhMe NH][B(C F ) ]を用いたこと以
3 6 5 4 2 6 5 4
外は、実施例 6と同様にしてポリマーを得た。得られたポリマーの1 H— NMR ^ベクトル チャートを図 8に、 13C— NMR ^ベクトルチャートを図 9に示す。 NMR ^ベクトルは、室 温で重クロ口ホルムを溶媒として測定した。
<参考例 2>
実施例 6において、 [Ph C][B(C F ) ]に代えて B(C F )を用いたこと以外は、実施例
3 6 5 4 6 5 3
6と同様にしてポリマーを得た。
[0082] <実施例 7>
実施例 4において、 (NCN)Sc(CH SiMe ) (THF) (0.015 g, 0.020mmol)のクロ口べンゼ
2 3 2
ン溶液 (8ml)と [Ph C][B(C F ) ] (0.018 g, 0.020mmol)のクロ口ベンゼン溶液 (2ml)を用
3 6 5 4
いたこと以外は、実施例 4と同様にしてポリマーを得た。
<実施例 8 >
実施例 7において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Y(CH SiMe ) (THF)
2 3 2 2 3 2 を用いたこと以外は、実施例 7と同様にしてポリマーを得た。
<実施例 9 >
実施例 7において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Lu(CH SiMe ) (THF)
2 3 2 2 3 2 を用いたこと以外は、実施例 7と同様にしてポリマーを得た。
<実施例 10 >
実施例 7において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Sc(CH C H NMe - o)
2 3 2 2 6 4 2 を用いたこと以外は、実施例 7と同様にしてポリマーを得た。
2
[0083] <参考例 3〉
実施例 7において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Y(CH C H NMe - o)
2 3 2 2 6 4 2 2 を用いたこと以外は、実施例 7と同様にしてポリマーを得た。
<実施例 11 >
実施例 7において、反応温度を室温から— 10°Cに変更し、反応時間を 5分間から 2 0分間に変更したこと以外は、実施例 7と同様にしてポリマーを得た。
<実施例 12 >
実施例 11において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Y(CH SiMe ) (THF)
2 3 2 2 3 2 を用いたこと以外は、実施例 11と同様にしてポリマーを得た。
[0084] <実施例 13 >
実施例 11において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Lu(CH SiMe ) (TH
2 3 2 2 3 2
F)を用いたこと以外は、実施例 11と同様にしてポリマーを得た。
<実施例 14 >
実施例 11において、(NCN)Sc(CH SiMe ) (THF)に代えて (NCN)Sc(CH C H NMe -
2 3 2 2 6 4 2 o)を用いたこと以外は、実施例 11と同様にしてポリマーを得た。
2
<実施例 15 >
実施例 14において、反応時間を 20分間から 30分間に変更したこと以外は実施例 14と同様にしてポリマーを得た。
[0085] <実施例 16 >
実施例 14において、予め (NCN)Sc(CH C H NMe - o)を [Ph C][B(C F ) ]で 10分間
2 6 4 2 2 3 6 5 4
活性ィ匕した後、イソプレンを加えて 30分間攪拌したこと以外は実施例 14と同様にし てポリマーを得た。
<実施例 17 >
実施例 14において、(NCN)Sc(CH C H NMe - o)に代えて (NCN)Y(CH C H NMe -
2 6 4 2 2 2 6 4 2 o)を用いたこと以外は実施例 14と同様にしてポリマーを得た。
2
<実施例 18 >
実施例 8において、反応温度を室温から 20°Cに変更したこと以外は実施例 8と同 様にしてポリマーを得た。
[0086] 表 1に実施例及び参考例で得られたポリイソプレンの収率(%)、数平均分子量 M、 分子量分布 M /M、全ポリイソプレンに対する 3, 4—ポリイソプレンの割合(%)、トリ アツド表示及びペンタッド表示でのアイソタクチシティ一(%)、ガラス転移温度 T (°C) g
、融点 T (°C)を示す。なお、 3, 4 ポリイソプレン以外の生成物は、 1 , 4 ポリイソプ m
レンであった。
表 1から本発明の重合触媒組成物を用い、反応条件を適宜選択することにより、ァ イソタクチシティ一が高いポリイソプレンが製造できることが分かる。特に、錯体として( NCN)Sc(CH SiMe ) (THF)や (NCN)Sc(CH C H NMe - o)を用い、触媒活性化剤とし
2 3 2 2 6 4 2 2
て [Ph C][B(C F ) ]を用いた場合には、アイソタクチシティ一が高い 3, 4—ポリイソプ
3 6 5 4
レンが製造できることが分かる。
[0087] <比較例 >
(NCN)Sc(CH SiMe ) (THF), (NCN)Y(CH SiMe ) (THF)について、触媒活性化剤を
2 3 2 2 3 2
加えずに、反応温度を室温とし、反応時間を 30分間として実施例と同様にして反応 を行った力 ポリマーは得られな力つた。
[0088] [表 1]
反応 反応 ミクロ構造(%)
触媒活 収率 Mn
錯体 時間
性化剤 (%)
O (分) Cx104) 3, 4 mm mmmm
(。c) (。c) 実施例 1 B (Sc) a -10 20 100 19.9 1.6 99.8 100 99 25 156 実施例 2 B (Sc) a -10 10 23 7.0 1.7 99.8 100 99 26 15 実施例 3 B (Y) a -10 5 100 16.0 1.5 99.3 100 99 19 138 実施例 4 B (Sc) a r.t. 5 100 12.5 1.6 99 93 80 23 - 実施例 5 B (Sc) b r.t. 5 76 8.8 1.4 97 66 一 28 ― 実施例 6 B (Y) a r.t. 5 100 7.2 1.4 92 50 18 一 参考例 1 B (Y) b r.t 5 78 5.5 1.1 92 36 一 27 一 参考例 2 B (Y) c r.t 5 1 1 1.8 1.2 92 一 - 31 - 実施例 7 B (Sc) a r.t. 5 88 13.5 1.5 99 93 80 25 一 実施例 8 B (Y) a r.t. 5 100 8.2 1.4 92 50 ― 18 - 実施例 9 B (Lu) a r.t. 5 100 12.2 1.6 98 76 27 - 実施例 1 0 C (Sc) a r.t 5 100 16.7 2.1 97 93 30 23 一 参考例 3 C (Y) a r.t. 5 100 10.2 1.5 93 21 - 実施例 1 1 B (Sc) a -10 20 57 13.1 1.6 99.8 100 99 26 158 実施例 1 2 B (Y) a - 10 20 100 22.9 1.5 99.3 100 99 22 実施例 1 3 B (Lu) a -10 20 100 21.1 1.8 99 90 一 26 一 実施例 1 4 C (Sc) a -10 20 77 14.9 2.0 99.8 100 99 27 153 実施例 1 5 C (Sc) a -10 30 89 24.0 2.0 99.8 100 99 26 152 実施例 1 6 C (Sc) a - 10 10+30 77 26.4 2.1 〜100 100 99 26 150 実施例 1 7 C (Y) a -10 20 100 18.3 1.3 99 97 70 24 ― 実施例 1 8 B (Y) a -20 5 85 23.3 1.3 99.5 100 99 22 142
B (Sc)
比較例 - r.t 30 0 一 - - 一 ― 又は B (Y)
表 1の錯体の欄中、 B及び Cはそれぞれ一般式 (B)及び一般式 (C)で表される錯体を示し、括弧内は中心金属 Mを示す。 触媒活性化剤の欄中、 aは [Ph3C][B(C6F5)4]、 bは [PhMe2NH][B(C6F5)4]、 cは B(C6F5)3を示す。
反応温度の欄中、 r は室温を示す。 産業上の利用の可能性
本発明の重合触媒組成物を用いた製造方法により製造されるイソプレン系重合体 はアイソタクチシティ一が高ぐ力学的又は熱的な耐久力に優れた特徴を示すと考え られる。そのため、プラスチック材料として利用されることが期待される。特に、本発明 の重合触媒組成物は低コストであることから、イソプレン系重合体の側鎖の 1-アルキ ルビ-ル基又は 1-アルケニルビニル基の二重結合をィ匕学的に修飾することで、新規 な機能性ポリマーの開発に有用であると考えられる。
Claims
請求の範囲
一般式 (A)で表される錯体及び触媒活性化剤を含むことを特徴とする、一般式 (X )で表されるイソプレン系化合物の重合用の重合触媒組成物。
R1
(一般式 (A)において、
R1及び R2はそれぞれ独立して、アルキル基、シクロへキシル基、ァリール基又はァ ラルキル基を示し、
R3はアルキル基、ァルケ-ル基、アルキ-ル基、ァリール基又はァラルキル基、脂 肪族、芳香族又は環状のアミノ基、若しくはホスフイノ基、ボリル基、アルキル又はァリ 一ルチオ基、アルコキシ又はァリールォキシ基を示し、
Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除くランタン Laからルテ チウム Luまでの希土類元素の何れかを示し、
Q1および Q2はそれぞれ独立して、モノア-オン性配位子を示し、
Lは中性ルイス塩基を示し、 wは 0〜3の整数を示す。)
[化 2]
(一般式 (X)において Rは炭素数 1〜 10のアルキル基又はァルケ-ル基を示す。 ) 一般式 (A)における R1及び R2が 2, 6—ジイソプロピルフエ-ル基を示し、 R3がフエ
二ル基を示すことを特徴とする、請求項 1に記載の重合触媒組成物。
一般式 (A)で表される錯体が、一般式 (B)で表される化合物であることを特徴とす る、請求項 1又は 2に記載の重合触媒組成物。
[化 3]
(一般式(B)において、 Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除 くランタン Laからルテチウム Luまでの希土類元素の何れかを示す。)
一般式 (A)で表される錯体が、一般式 (C)で表される化合物であることを特徴とす る、請求項 1又は 2に記載の重合触媒組成物。
[化 4]
(一般式(C)において、 Mは、スカンジウム Sc、イットリウム Y又はプロメチウム Pmを除 くランタン Laからルテチウム Luまでの希土類元素のうち何れかを示す。 )
[5] 前記触媒活性化剤が、非配位性ァ-オンとカチオン力もなるイオン性ィ匕合物である ことを特徴とする、請求項 1〜4の何れか一項に記載の重合触媒組成物。
[6] 前記非配位性ァ-オン力 価のホウ素ァ-オンであることを特徴とする、請求項 5に 記載の重合触媒組成物。
[7] 一般式 (X)で表されるイソプレン系化合物を、請求項 1〜6の何れか一項に記載の
重合触媒組成物を用いて重合させることを特徴とする、イソプレン系重合体の製造方 法。
[8] 一般式 (X)における R4カ^チル基であることを特徴とする、請求項 7に記載の製造 方法。
[9] 前記重合が溶液重合であって、重合反応温度が 0°C以下であることを特徴とする、 請求項 7又は 8に記載の製造方法。
Priority Applications (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US12/282,148 US7829642B2 (en) | 2006-03-10 | 2007-02-05 | Polymerization catalyst composition for polymerization of isoprene compound |
| EP07708047.1A EP1995257A4 (en) | 2006-03-10 | 2007-02-05 | POLYMERIZATION CATALYST COMPOSITION FOR THE POLYMERIZATION OF AN ISOPRENE COMPOUND |
| CN2007800086250A CN101400707B (zh) | 2006-03-10 | 2007-02-05 | 用于异戊二烯系化合物聚合的聚合催化剂组合物 |
| US12/897,750 US8563457B2 (en) | 2006-03-10 | 2010-10-04 | Polymerization catalyst composition for polymerization of isoprene compound |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2006065855A JP2007238857A (ja) | 2006-03-10 | 2006-03-10 | イソプレン系化合物の重合用の重合触媒組成物 |
| JP2006-065855 | 2006-03-10 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2007105388A1 true WO2007105388A1 (ja) | 2007-09-20 |
Family
ID=38509226
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2007/051929 Ceased WO2007105388A1 (ja) | 2006-03-10 | 2007-02-05 | イソプレン系化合物の重合用の重合触媒組成物 |
Country Status (5)
| Country | Link |
|---|---|
| US (2) | US7829642B2 (ja) |
| EP (1) | EP1995257A4 (ja) |
| JP (1) | JP2007238857A (ja) |
| CN (1) | CN101400707B (ja) |
| WO (1) | WO2007105388A1 (ja) |
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008222791A (ja) * | 2007-03-09 | 2008-09-25 | Institute Of Physical & Chemical Research | イソプレン系化合物の重合用の重合触媒組成物 |
| JP2011012169A (ja) * | 2009-07-01 | 2011-01-20 | Idemitsu Kosan Co Ltd | 重合触媒および芳香族ビニル化合物重合体の製造方法 |
| US20130197174A1 (en) * | 2010-07-30 | 2013-08-01 | Bridgestone Corporation | Copolymer and method of manufacturing the same |
Families Citing this family (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US20110098434A1 (en) | 2008-04-18 | 2011-04-28 | Zeon Corporation | Isoprene-based polymer cyclized product, alicyclic polymer, and optical resin |
| CN102234342B (zh) * | 2010-04-30 | 2013-03-06 | 青岛伊科思新材料股份有限公司 | 应用于异戊橡胶生产的稀土催化剂的制备方法 |
| WO2012106695A2 (en) | 2011-02-05 | 2012-08-09 | Bridgestone Corporation | Metal complex catalysts and polymerization methods employing same |
| US20140088276A1 (en) | 2011-05-09 | 2014-03-27 | Riken | Manufacturing method for multidimensional polymer, and multidimensional polymer |
| CN106084108A (zh) * | 2016-06-14 | 2016-11-09 | 郭云琴 | 一种脒基稀土烷基化合物制备异戊橡胶的方法 |
| CN112592421B (zh) * | 2020-11-22 | 2021-09-17 | 复旦大学 | 通过链穿梭反应制备异戊二烯多嵌段区域共聚物的方法 |
Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004000894A1 (en) * | 2002-06-21 | 2003-12-31 | Exxonmobil Chemical Patents Inc. | Yttrium-based ethylene polymerization catalysts with bulky amidinate ancillary ligands |
| WO2005085306A1 (ja) * | 2004-03-04 | 2005-09-15 | Riken | アイソタクチック3,4−イソプレン系重合体 |
| WO2006078021A1 (ja) * | 2005-01-21 | 2006-07-27 | Riken | 三座配位子を含む金属錯体、およびそれを含む重合用触媒 |
Family Cites Families (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| IT1265048B1 (it) * | 1993-08-06 | 1996-10-28 | Eniricerche Spa | Complessi metallorganici dei lantanidi e loro uso nella polimerizzazione di monomeri insaturi |
| JP2007161919A (ja) * | 2005-12-15 | 2007-06-28 | Ube Ind Ltd | ポリイソプレンの製造方法 |
| JP5024755B2 (ja) * | 2007-03-09 | 2012-09-12 | 独立行政法人理化学研究所 | イソプレン系化合物の重合用の重合触媒組成物 |
-
2006
- 2006-03-10 JP JP2006065855A patent/JP2007238857A/ja active Pending
-
2007
- 2007-02-05 EP EP07708047.1A patent/EP1995257A4/en not_active Withdrawn
- 2007-02-05 WO PCT/JP2007/051929 patent/WO2007105388A1/ja not_active Ceased
- 2007-02-05 CN CN2007800086250A patent/CN101400707B/zh not_active Expired - Fee Related
- 2007-02-05 US US12/282,148 patent/US7829642B2/en not_active Expired - Fee Related
-
2010
- 2010-10-04 US US12/897,750 patent/US8563457B2/en not_active Expired - Fee Related
Patent Citations (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2004000894A1 (en) * | 2002-06-21 | 2003-12-31 | Exxonmobil Chemical Patents Inc. | Yttrium-based ethylene polymerization catalysts with bulky amidinate ancillary ligands |
| WO2005085306A1 (ja) * | 2004-03-04 | 2005-09-15 | Riken | アイソタクチック3,4−イソプレン系重合体 |
| WO2006078021A1 (ja) * | 2005-01-21 | 2006-07-27 | Riken | 三座配位子を含む金属錯体、およびそれを含む重合用触媒 |
Non-Patent Citations (8)
| Title |
|---|
| A. S. KHATCHATUROV ET AL., POLYMER, vol. 18, 1976, pages 871 |
| BAMBIRRA S. ET AL.: "One Ligand Fits All: Cationic Mono(amidinate) Alkyl Catalysts over the Full Size Range of the Group 3 and Lanthanide Metals", J. AM. CHEM. SOC., vol. 126, no. 30, August 2004 (2004-08-01), pages 9182 - 9183, XP003017763 * |
| BAMBIRRA S. ET AL.: "Yttrium alkyl complexes with a sterically demanding benzamidinate ligand: synthesis, structure and catalytic ethene polymerisation", CHEM. COMMUN., no. 4, February 2003 (2003-02-01), pages 522 - 523, XP003017764 * |
| J. AM. CHEM. SOC., vol. 126, 2004, pages 9182 - 9183 |
| MACROMOLECULES, vol. 36, 2003, pages 7953 - 7958 |
| MAKROMOLEKULARE CHEM, vol. 77, 1964, pages 126 - 138 |
| See also references of EP1995257A4 * |
| W. M. DONG; T. MASUDA, J. POLYM. SCI., PART A: POLYM. CHEM., vol. 40, 2002, pages 1838 |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2008222791A (ja) * | 2007-03-09 | 2008-09-25 | Institute Of Physical & Chemical Research | イソプレン系化合物の重合用の重合触媒組成物 |
| JP2011012169A (ja) * | 2009-07-01 | 2011-01-20 | Idemitsu Kosan Co Ltd | 重合触媒および芳香族ビニル化合物重合体の製造方法 |
| US20130197174A1 (en) * | 2010-07-30 | 2013-08-01 | Bridgestone Corporation | Copolymer and method of manufacturing the same |
| US9266978B2 (en) * | 2010-07-30 | 2016-02-23 | Bridgestone Corporation | Copolymer and method of manufacturing the same |
Also Published As
| Publication number | Publication date |
|---|---|
| US7829642B2 (en) | 2010-11-09 |
| US8563457B2 (en) | 2013-10-22 |
| JP2007238857A (ja) | 2007-09-20 |
| EP1995257A4 (en) | 2013-06-05 |
| CN101400707B (zh) | 2011-08-03 |
| US20110021346A1 (en) | 2011-01-27 |
| US20090030167A1 (en) | 2009-01-29 |
| CN101400707A (zh) | 2009-04-01 |
| EP1995257A1 (en) | 2008-11-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| WO2007105388A1 (ja) | イソプレン系化合物の重合用の重合触媒組成物 | |
| JP4925297B2 (ja) | 三座配位子を含む金属錯体、およびそれを含む重合用触媒 | |
| Li et al. | β-diketiminato rare-earth metal complexes. Structures, catalysis, and active species for highly cis-1, 4-selective polymerization of isoprene | |
| JP2020045500A (ja) | 多元共重合体、ゴム組成物及びタイヤ | |
| WO2006004068A1 (ja) | メタロセン錯体を含む重合触媒組成物、およびそれを用いて製造される重合体 | |
| JP5942172B2 (ja) | 共役ジエン系モノマーの重合触媒組成物 | |
| CN104428323B (zh) | 聚丁二烯的制造方法、聚丁二烯、橡胶组合物和轮胎 | |
| JPWO2016027402A1 (ja) | 共役ジエン重合体の製造方法、共役ジエン重合体、ゴム組成物、タイヤ | |
| JP2013216850A (ja) | 合成ポリイソプレンの製造方法、合成ポリイソプレン、ゴム組成物及びタイヤ | |
| JP5024755B2 (ja) | イソプレン系化合物の重合用の重合触媒組成物 | |
| Nuyken | Neodymium based ziegler catalysts-fundamental chemistry | |
| EP1721914B1 (en) | Isotactic 3,4-isoprene polymer | |
| Chen et al. | Synthetic rubbers prepared by lanthanide coordination catalysts | |
| JP7402820B2 (ja) | ポリブタジエン、ポリブタジエンの製造方法、ポリブタジエン組成物、タイヤ、及び樹脂部材 | |
| TR201906505T4 (tr) | Lantanitlerin bis-imin piridin bileşiği, bahsi geçen bis-imin piridin bileşği içeren katalitik sistem ve konjuge dienlerin (ko)polimerizasyonu için işlem. | |
| KR102682765B1 (ko) | 액상 고무 제조방법 및 이로부터 제조된 액상 고무 | |
| CN105073791B (zh) | 异戊二烯聚合催化剂组合物、合成聚异戊二烯的制造方法及合成聚异戊二烯 | |
| CN104470985B (zh) | 聚合物组合物的制造方法和聚合物组合物 | |
| Wang et al. | Polymerization of isoprene and butadiene with unparalleled stereoselectivity catalysed by rare-earth metal cationic species bearing a novel tridentate ligand | |
| JP2017039929A (ja) | ペンタジエン単独又は共重合体の製造方法及びペンタジエン単独又は共重合体 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 07708047 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 12282148 Country of ref document: US Ref document number: 2007708047 Country of ref document: EP |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 200780008625.0 Country of ref document: CN |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |