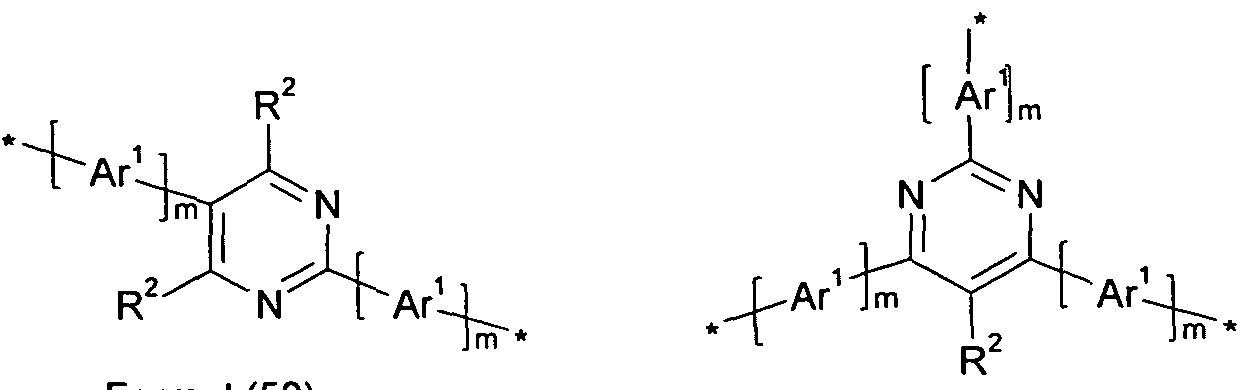WO2011060867A1 - Stickstoffhaltige kondensierte heterozyklen für oleds - Google Patents
Stickstoffhaltige kondensierte heterozyklen für oleds Download PDFInfo
- Publication number
- WO2011060867A1 WO2011060867A1 PCT/EP2010/006414 EP2010006414W WO2011060867A1 WO 2011060867 A1 WO2011060867 A1 WO 2011060867A1 EP 2010006414 W EP2010006414 W EP 2010006414W WO 2011060867 A1 WO2011060867 A1 WO 2011060867A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- formula
- group
- compounds
- atoms
- substituted
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
- 0 Cc1c(*)c(*)nc(-c2nc(*)c(*)c(*c3c(*)c(*)c4*)c22)c1*2c3c4NC1IC1 Chemical compound Cc1c(*)c(*)nc(-c2nc(*)c(*)c(*c3c(*)c(*)c4*)c22)c1*2c3c4NC1IC1 0.000 description 15
- LTOCSSDMGZBSIF-UHFFFAOYSA-N CC1(C)c(cncc2)c2-[n]2c3c1cccc3c1c2ccc(S(O)O)c1 Chemical compound CC1(C)c(cncc2)c2-[n]2c3c1cccc3c1c2ccc(S(O)O)c1 LTOCSSDMGZBSIF-UHFFFAOYSA-N 0.000 description 1
- SJPGXAKQUZZLMC-UHFFFAOYSA-N CC1(C)c(cncc2)c2-[n]2c3c1cccc3c1cc(-c(cc3)cc4c3[n]3-c5ccncc5C(C)(C)c5c3c4ccc5)ccc21 Chemical compound CC1(C)c(cncc2)c2-[n]2c3c1cccc3c1cc(-c(cc3)cc4c3[n]3-c5ccncc5C(C)(C)c5c3c4ccc5)ccc21 SJPGXAKQUZZLMC-UHFFFAOYSA-N 0.000 description 1
- LNJTUXVIEWWDRS-UHFFFAOYSA-N CC1(C)c(cncc2)c2-[n]2c3c1cccc3c1cc(B(O)O)ccc21 Chemical compound CC1(C)c(cncc2)c2-[n]2c3c1cccc3c1cc(B(O)O)ccc21 LNJTUXVIEWWDRS-UHFFFAOYSA-N 0.000 description 1
- FEAOFOVUMDNZKX-UHFFFAOYSA-N CC1(C)c2cnccc2-[n]2c3c1cccc3c1cc(-c(cc3)cc(c4c5cccc4)c3[n]5-c3ccccc3)ccc21 Chemical compound CC1(C)c2cnccc2-[n]2c3c1cccc3c1cc(-c(cc3)cc(c4c5cccc4)c3[n]5-c3ccccc3)ccc21 FEAOFOVUMDNZKX-UHFFFAOYSA-N 0.000 description 1
- ZNELINRXVBNSSV-UHFFFAOYSA-N N#Cc(cccc1C#N)c1-[n]1c(ccnc2)c2c2c1cccc2 Chemical compound N#Cc(cccc1C#N)c1-[n]1c(ccnc2)c2c2c1cccc2 ZNELINRXVBNSSV-UHFFFAOYSA-N 0.000 description 1
- LIXDLBIUJIOBOK-UHFFFAOYSA-N OC(c(cc1c2c3cccc2)nc2c1[n]3-c1ccccc1C2=O)=O Chemical compound OC(c(cc1c2c3cccc2)nc2c1[n]3-c1ccccc1C2=O)=O LIXDLBIUJIOBOK-UHFFFAOYSA-N 0.000 description 1
- ILJXDUUYRQURAT-UHFFFAOYSA-N c(cc1)cc(C23c4cccc(C5(c6ccccc6-c6ccccc56)c5cnc6)c4-[n]4c5c6c5cccc2c45)c1-c1c3cccc1 Chemical compound c(cc1)cc(C23c4cccc(C5(c6ccccc6-c6ccccc56)c5cnc6)c4-[n]4c5c6c5cccc2c45)c1-c1c3cccc1 ILJXDUUYRQURAT-UHFFFAOYSA-N 0.000 description 1
- YXDXONQABVWRTO-UHFFFAOYSA-N c(cc1)cc(c2cccc3c22)c1[n]2c1c3nccn1 Chemical compound c(cc1)cc(c2cccc3c22)c1[n]2c1c3nccn1 YXDXONQABVWRTO-UHFFFAOYSA-N 0.000 description 1
- RDMFHRSPDKWERA-UHFFFAOYSA-N c(cc1)cc2c1[nH]c1c2cncc1 Chemical compound c(cc1)cc2c1[nH]c1c2cncc1 RDMFHRSPDKWERA-UHFFFAOYSA-N 0.000 description 1
- UISREQMUWWRLIS-UHFFFAOYSA-N c(cc1)cc2c1[n]1c(nccc3)c3c3cccc2c13 Chemical compound c(cc1)cc2c1[n]1c(nccc3)c3c3cccc2c13 UISREQMUWWRLIS-UHFFFAOYSA-N 0.000 description 1
- LLOMWOCJQZBHCO-UHFFFAOYSA-N c(cc1)cc2c1[n]1c3c2cncc3c2c1cccc2 Chemical compound c(cc1)cc2c1[n]1c3c2cncc3c2c1cccc2 LLOMWOCJQZBHCO-UHFFFAOYSA-N 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D455/00—Heterocyclic compounds containing quinolizine ring systems, e.g. emetine alkaloids, protoberberine; Alkylenedioxy derivatives of dibenzo [a, g] quinolizines, e.g. berberine
- C07D455/03—Heterocyclic compounds containing quinolizine ring systems, e.g. emetine alkaloids, protoberberine; Alkylenedioxy derivatives of dibenzo [a, g] quinolizines, e.g. berberine containing quinolizine ring systems directly condensed with at least one six-membered carbocyclic ring, e.g. protoberberine; Alkylenedioxy derivatives of dibenzo [a, g] quinolizines, e.g. berberine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/12—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains three hetero rings
- C07D471/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/22—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed systems contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains three hetero rings
- C07D498/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D498/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms
- C07D498/22—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and oxygen atoms as the only ring hetero atoms in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/02—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains two hetero rings
- C07D513/04—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/12—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains three hetero rings
- C07D513/14—Ortho-condensed systems
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D513/00—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00
- C07D513/22—Heterocyclic compounds containing in the condensed system at least one hetero ring having nitrogen and sulfur atoms as the only ring hetero atoms, not provided for in groups C07D463/00, C07D477/00 or C07D499/00 - C07D507/00 in which the condensed system contains four or more hetero rings
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/002—Osmium compounds
- C07F15/0026—Osmium compounds without a metal-carbon linkage
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0033—Iridium compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F15/00—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table
- C07F15/0006—Compounds containing elements of Groups 8, 9, 10 or 18 of the Periodic Table compounds of the platinum group
- C07F15/0086—Platinum compounds
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F7/00—Compounds containing elements of Groups 4 or 14 of the Periodic Table
- C07F7/02—Silicon compounds
- C07F7/08—Compounds having one or more C—Si linkages
- C07F7/0803—Compounds with Si-C or Si-Si linkages
- C07F7/081—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te
- C07F7/0812—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring
- C07F7/0816—Compounds with Si-C or Si-Si linkages comprising at least one atom selected from the elements N, O, halogen, S, Se or Te comprising a heterocyclic ring said ring comprising Si as a ring atom
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6568—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms
- C07F9/65683—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms the ring phosphorus atom being part of a phosphine
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07F—ACYCLIC, CARBOCYCLIC OR HETEROCYCLIC COMPOUNDS CONTAINING ELEMENTS OTHER THAN CARBON, HYDROGEN, HALOGEN, OXYGEN, NITROGEN, SULFUR, SELENIUM OR TELLURIUM
- C07F9/00—Compounds containing elements of Groups 5 or 15 of the Periodic Table
- C07F9/02—Phosphorus compounds
- C07F9/547—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom
- C07F9/6564—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms
- C07F9/6568—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms
- C07F9/65685—Heterocyclic compounds, e.g. containing phosphorus as a ring hetero atom having phosphorus atoms, with or without nitrogen, oxygen, sulfur, selenium or tellurium atoms, as ring hetero atoms having phosphorus atoms as the only ring hetero atoms the ring phosphorus atom being part of a phosphine oxide or thioxide
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09B—ORGANIC DYES OR CLOSELY-RELATED COMPOUNDS FOR PRODUCING DYES, e.g. PIGMENTS; MORDANTS; LAKES
- C09B57/00—Other synthetic dyes of known constitution
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K11/00—Luminescent materials, e.g. electroluminescent or chemiluminescent
- C09K11/06—Luminescent materials, e.g. electroluminescent or chemiluminescent containing organic luminescent materials
-
- H—ELECTRICITY
- H05—ELECTRIC TECHNIQUES NOT OTHERWISE PROVIDED FOR
- H05B—ELECTRIC HEATING; ELECTRIC LIGHT SOURCES NOT OTHERWISE PROVIDED FOR; CIRCUIT ARRANGEMENTS FOR ELECTRIC LIGHT SOURCES, IN GENERAL
- H05B33/00—Electroluminescent light sources
- H05B33/12—Light sources with substantially two-dimensional [2D] radiating surfaces
- H05B33/14—Light sources with substantially two-dimensional [2D] radiating surfaces characterised by the chemical or physical composition or the arrangement of the electroluminescent material, or by the simultaneous addition of the electroluminescent material in or onto the light source
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1003—Carbocyclic compounds
- C09K2211/1011—Condensed systems
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1033—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/1037—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with sulfur
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1029—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom
- C09K2211/104—Heterocyclic compounds characterised by ligands containing one nitrogen atom as the heteroatom with other heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1044—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms
- C09K2211/1048—Heterocyclic compounds characterised by ligands containing two nitrogen atoms as heteroatoms with oxygen
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1059—Heterocyclic compounds characterised by ligands containing three nitrogen atoms as heteroatoms
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1088—Heterocyclic compounds characterised by ligands containing oxygen as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1092—Heterocyclic compounds characterised by ligands containing sulfur as the only heteroatom
-
- C—CHEMISTRY; METALLURGY
- C09—DYES; PAINTS; POLISHES; NATURAL RESINS; ADHESIVES; COMPOSITIONS NOT OTHERWISE PROVIDED FOR; APPLICATIONS OF MATERIALS NOT OTHERWISE PROVIDED FOR
- C09K—MATERIALS FOR MISCELLANEOUS APPLICATIONS, NOT PROVIDED FOR ELSEWHERE
- C09K2211/00—Chemical nature of organic luminescent or tenebrescent compounds
- C09K2211/10—Non-macromolecular compounds
- C09K2211/1018—Heterocyclic compounds
- C09K2211/1025—Heterocyclic compounds characterised by ligands
- C09K2211/1096—Heterocyclic compounds characterised by ligands containing other heteroatoms
Definitions
- alkyl, alkenyl, alkynyl, alkoxy or thioalkyl groups may be straight-chained, branched or cyclic, wherein one or more non-adjacent CH 2 groups may be replaced by the above-mentioned groups;
- one or more H atoms can also be replaced by D, F, Cl, Br, I, CN or NO 2 , preferably F, Cl or CN, more preferably F or CN, particularly preferably CN.
- aromatic or heteroaromatic ring system with 5-80 aromatic ring atoms which may be substituted in each case with the above-mentioned radicals R 2 or a hydrocarbon radical and which may be linked via any position on the aromatic or heteroaromatic, are understood in particular groups derived are benzene, naphthalene, anthracene, benzanthracene,
- At least one group Y in each unit is a single bond.
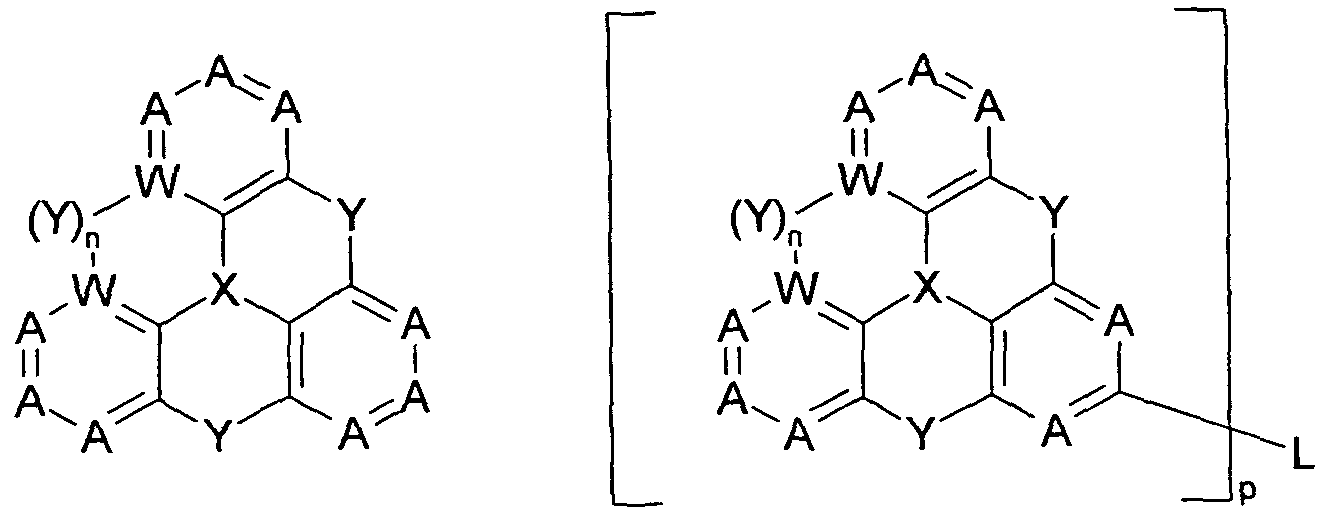
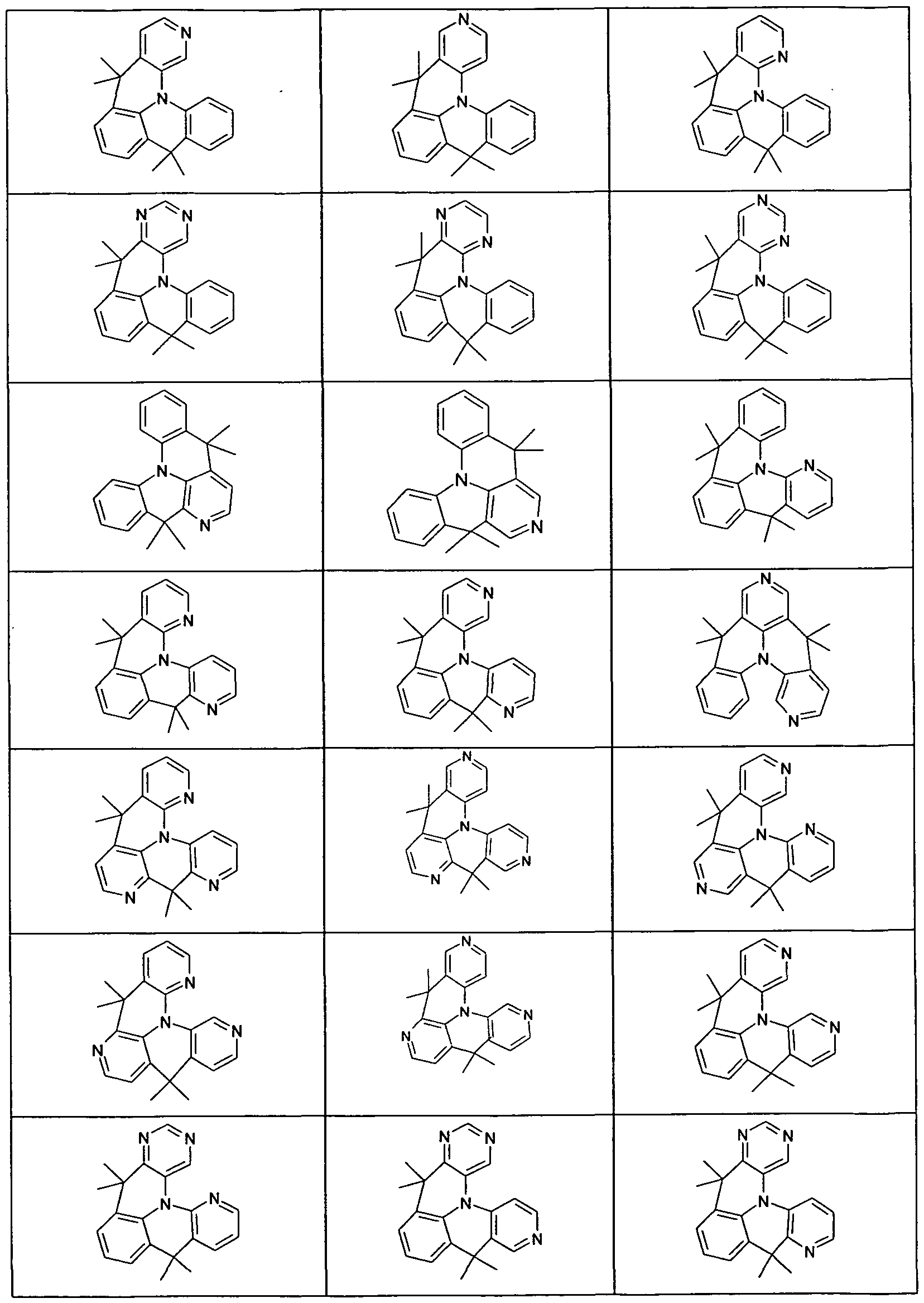
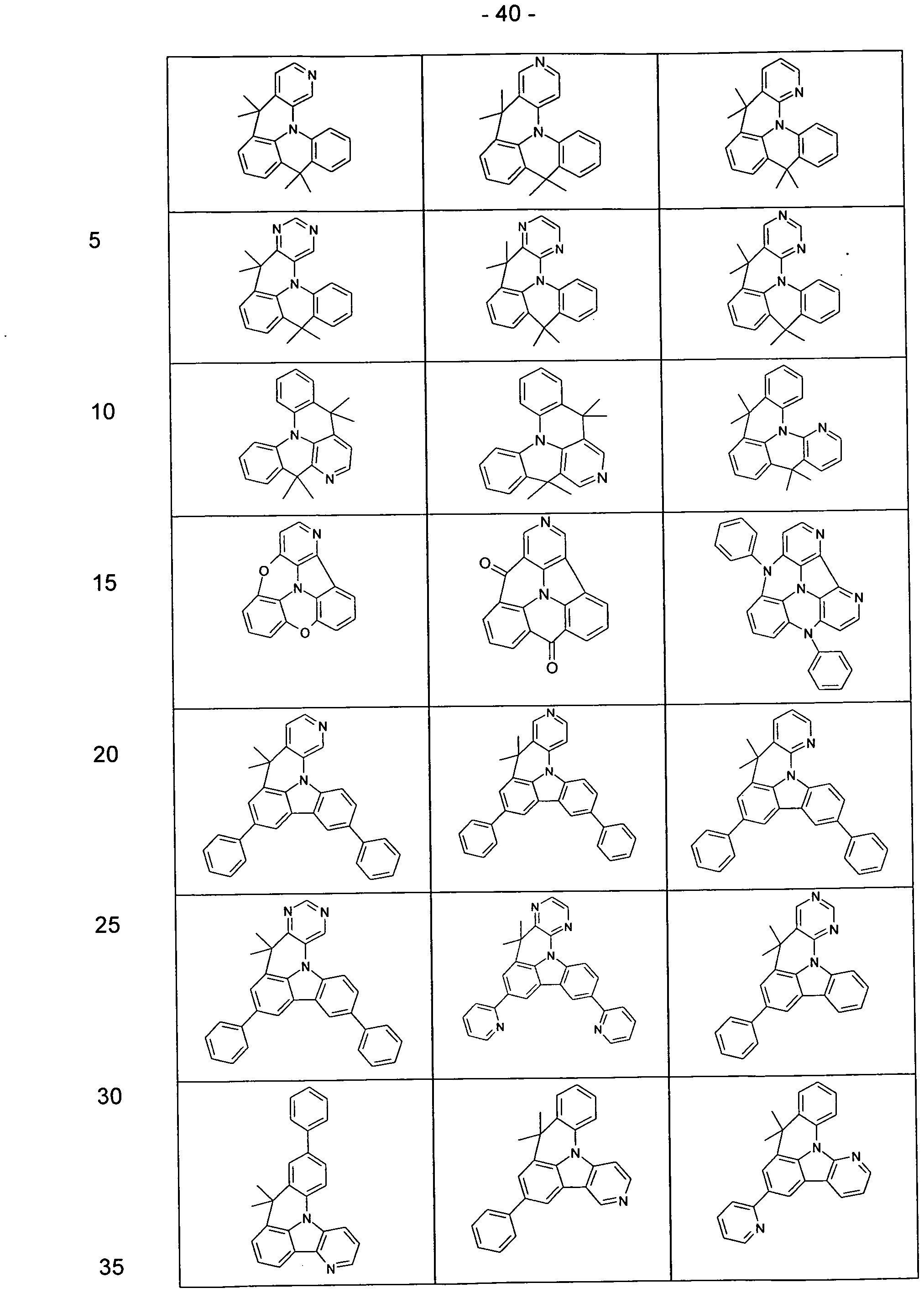
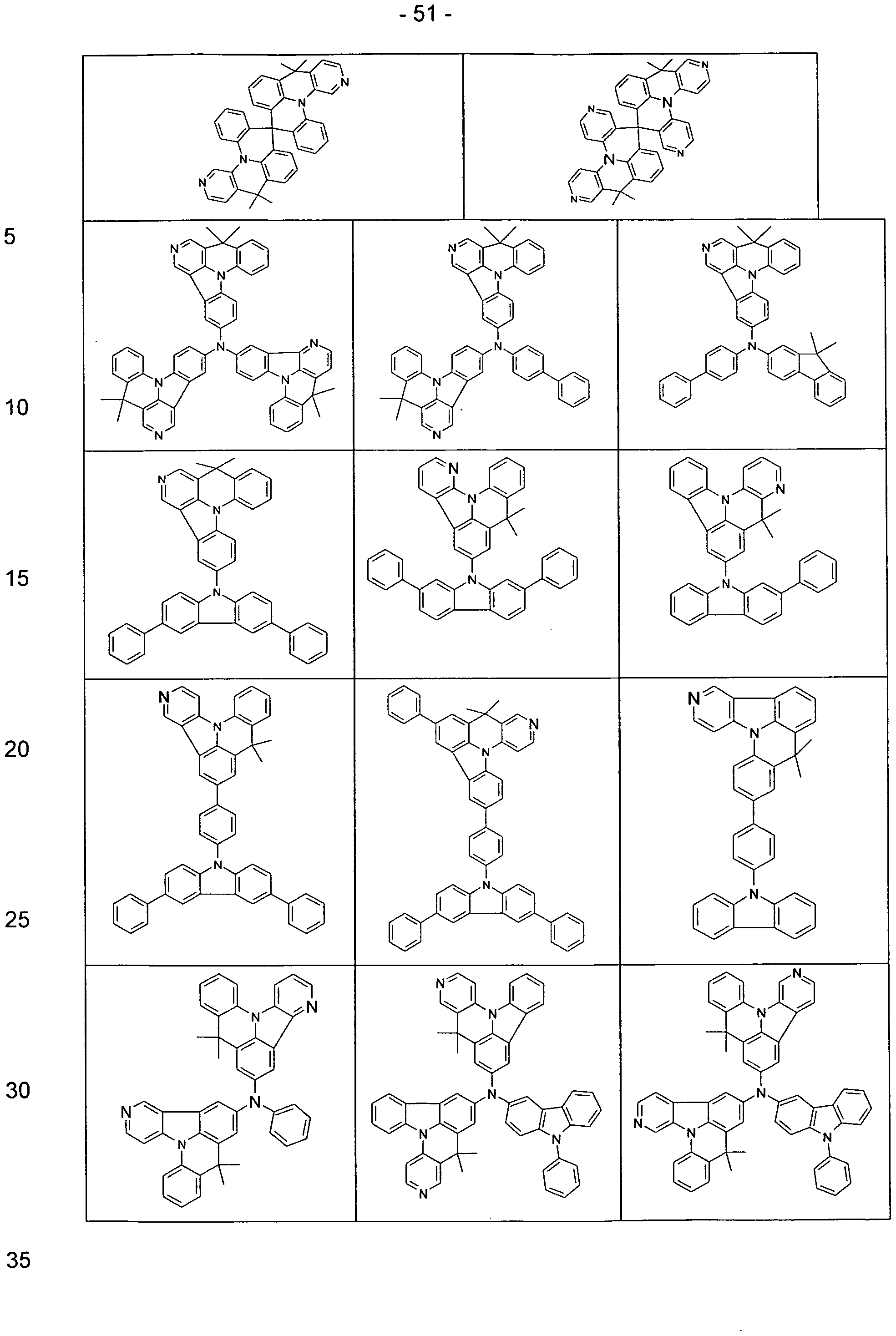
- Preferred compounds are therefore the compounds of the formula (5) to (0),
- one, two or three symbols A or W stand for N in total and the other symbols A and W stand for CR and C, respectively.
- the "unit” is understood to mean the structure according to formula (1) or in the formulas (2) and (3) each of the groups which binds to L or in the formula (4) in each case each of the groups which The same applies to the formulas (5) to (10).
- At least one group Y is a single bond. Particular preference is thus given to the compounds of the following formulas (11a) to (31b)
- X is, identically or differently on each occurrence, N or P. X is particularly preferably N.
- not all three groups Y in one unit are simultaneously one
- the groups Y which are different from a chemical bond, are identical or different at each occurrence for C (R 1 ) 2 , NR 1 , O or S, very particularly preferably for C (R 1 ) 2 or NR 1 , in particular for C (R 1 ) 2 .
- radicals R are substituted by radicals R other than hydrogen or deuterium, these radicals R are preferably bonded in each case in the para position to the group X. Therefore, preferred are the compounds according to the following formulas (11c) to (31c),
- radicals R other than hydrogen or deuterium, then these radicals R are preferably each bonded in the para position to the group X.
- R is the same or different selected from the group consisting of H, D, N (Ar) 2 , one for each occurrence straight-chain alkyl group having 1 to 4 carbon atoms or a branched alkyl group having 3 or 4 carbon atoms, each of which may be substituted by one or more radicals R 1 , wherein one or more HI atoms may be replaced by D, or an aromatic or heteroaromatic ring system having 6 to 18 aromatic ring atoms, each of which may be substituted by one or more R 2 radicals.
- Substituents R which are bonded in Y are preferably selected from the group consisting of alkyl groups having 1 to 10 C atoms or aromatic or heteroaromatic ring systems having 5 to 20 aromatic ring atoms, which may each be substituted by one or more radicals R 2 .
- Two radicals R 1 which are bonded in the same group Y, can also form a ring system with one another and thus form a spirosystem.
- R 2 in each occurrence is identically or differently selected from the group consisting of H, D, a straight-chain alkyl group having 1 to 4 C atoms or a branched alkyl group having 3 or 4 C atoms or an aromatic or heteroaromatic ring system having 6 to 18 aromatic ring atoms.
- L is a bivalent or higher valent straight-chain alkylene or alkylidene group having 1 to 10 C atoms or a branched or cyclic alkylene or alkylidene group having 3 to 10 C atoms, each having one or more radicals R 2 may be substituted, wherein one or more H atoms may be replaced by D or F, or an at least bivalent aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may be substituted by one or more radicals R 2 , or L is a chemical bond.
- At least one substituent R, R and / or R 2 , preferably R, is preferably an electron-deficient group, in particular selected from structures according to the following formulas (32) to (35),
- Formula (35) and / or at least one group L preferably represents a group of the following formulas (36) to (38),
- Formula (36) Formula (37) Formula (38) wherein R 2 has the abovementioned meaning, * indicates the position of the bond of the group according to formula (32) to (38) and furthermore:
- Z is the same or different CR 2 or N on each occurrence, with the proviso that one group Z, two groups Z or three groups Z are N;
- Ar 1 is the same or different each occurrence of a bivalent aryl or heteroaryl group having 5 to 16 carbon atoms, which may be substituted by one or more radicals R 2 ; m is identical or different 0, 1, 2 or 3 at each occurrence.
- at least one substituent R is a group of the abovementioned formula (32) and / or at least the group L is a group of the abovementioned formulas (36) to (38), where in each case two or three Symbols Z stand for N and the other symbols Z stand for CR 2 .
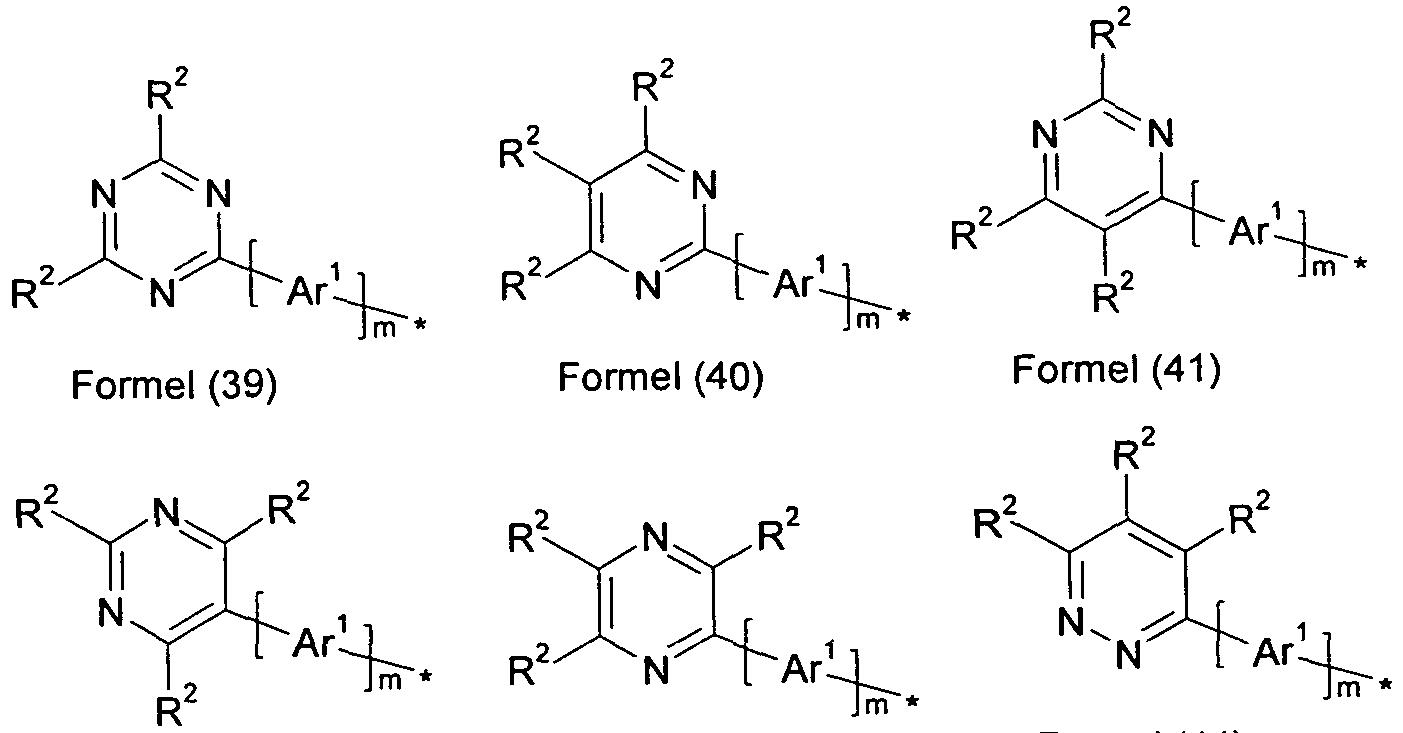
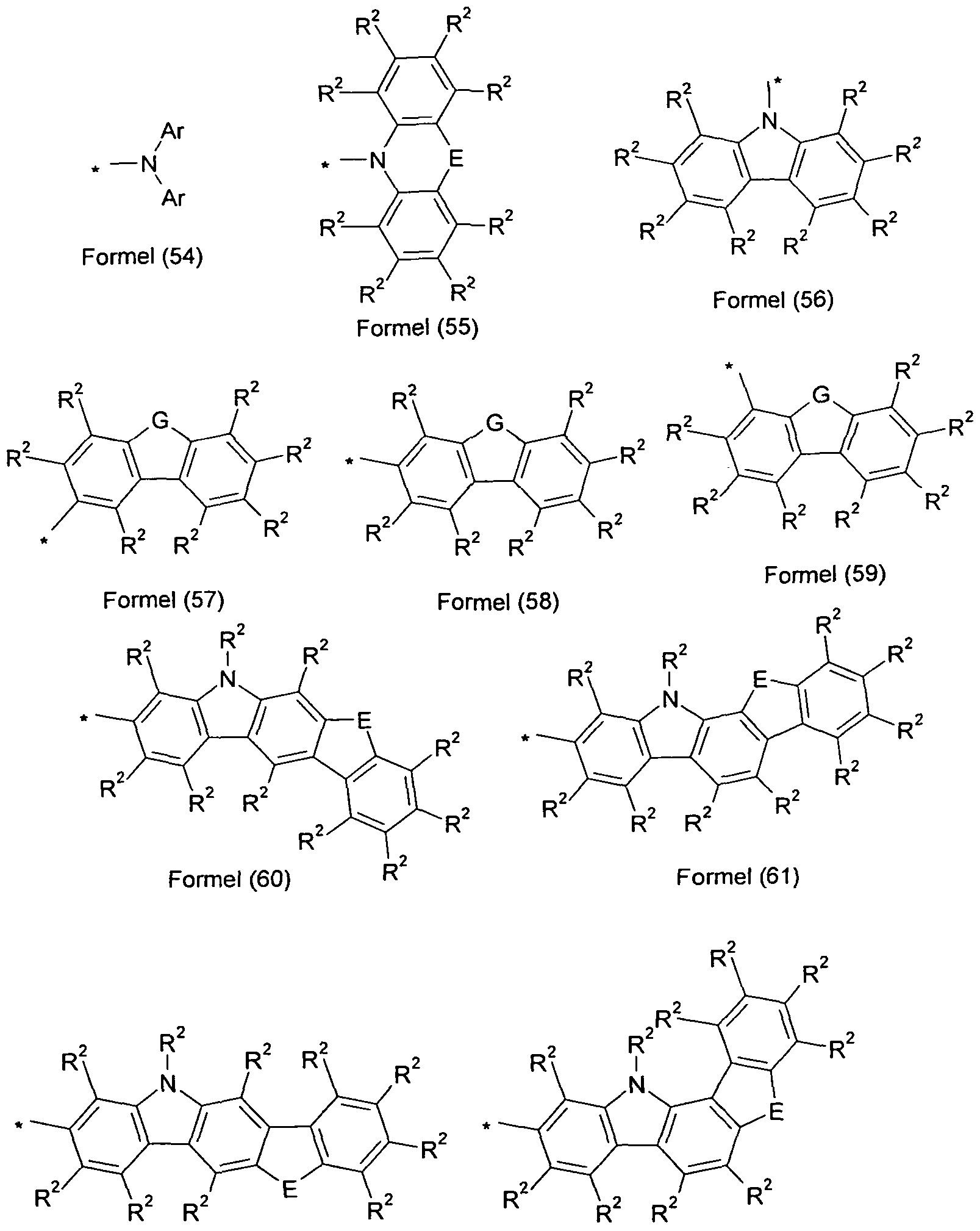
- Particularly preferred groups R are therefore the groups of the following formulas (39) to (45), and particularly preferred groups L are the groups of the following formulas (46) to (53)
- R 2 in this group is preferably an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms, which may be substituted by one or more radicals R 3 , in particular phenyl, ortho -, meta- or para-biphenyl, ortho, meta, para or branched terphenyl or ortho, meta, para or branched quarterphenyl.
- R 2 in these groups is preferably the same or different at each occurrence of H, D or an aromatic or heteroaromatic ring system having 5 to 24 aromatic ring atoms which is represented by a or more radicals R 3 may be substituted, in particular phenyl, ortho-, meta- or para-biphenyl, ortho, meta, para or branched terphenyl or ortho, meta, para or branched quarterphenyl.
- E is selected from the group consisting of C (R 2 ) 2 , NR 2 , O or S;
- one or two groups R or R 1 is a group of the abovementioned formulas (32) to (67), more preferably exactly one group R, and the other groups R stand for H or D. ,
- the abovementioned preferences occur simultaneously.
- Particularly preferred embodiments are therefore compounds according to the abovementioned formulas (1) to (31) and (11a) to (31 e), in which the preferences mentioned above apply simultaneously, in which
- R 1 is selected from the group consisting of alkyl groups having 1 to 5 carbon atoms or aromatic or heteroaromatic ring systems having 5 to 18 aromatic ring atoms, each of which may be substituted by one or more radicals R 2 , where also two radicals R, which in the same group Y are bound together, form a ring system with each other and so can span a spirosystem;
- L is a bivalent or higher valent straight-chain alkylene or alkylidene group having 1 to 4 C atoms or a branched or cyclic alkylene or alkylidene group having 3 or 4 C atoms, which may each be substituted by one or more R 2 radicals, where one or more H atoms can be replaced by D or F, or an at least bivalent aromatic or heteroaromatic ring system having 5 to 18 aromatic ring atoms, which may be substituted by one or more radicals R 2 ; or L is a chemical bond; or L is a group according to any one of the above
- Another object of the present invention is therefore a
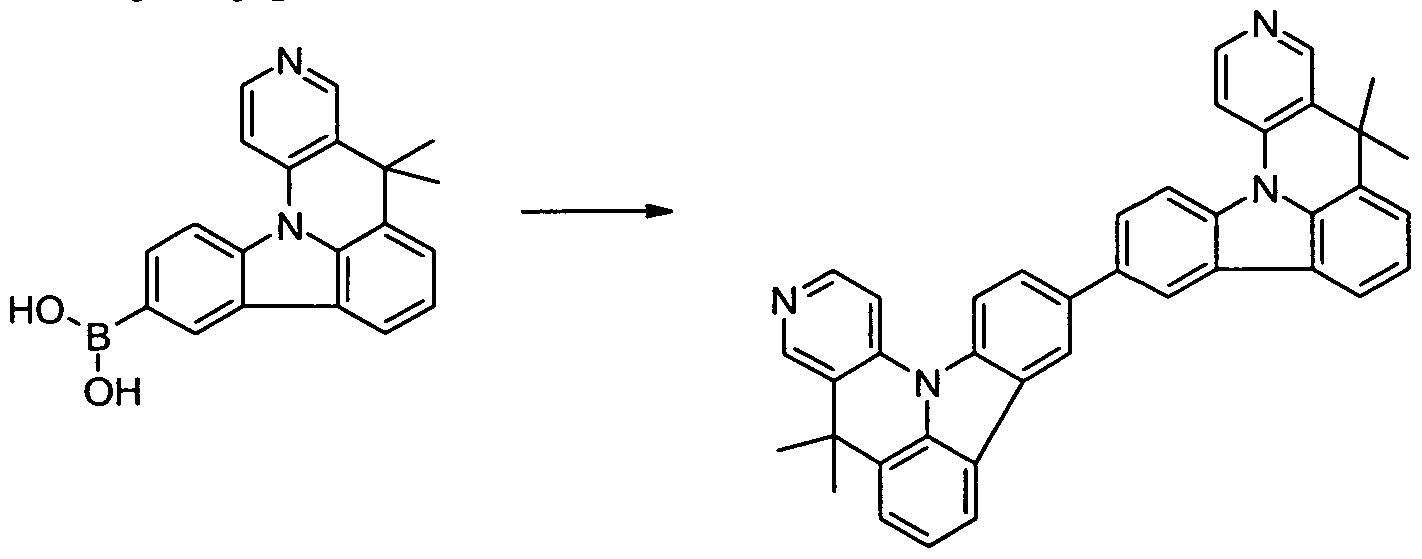
- the oligomerization or polymerization takes place preferably via the halogen functionality or the boronic acid functionality or via the polymerizable group. It is also possible to crosslink the polymers via such groups.
- Dendrimers can be used as a crosslinked or uncrosslinked layer.
- the monomers according to the invention are homopolymerized or copolymerized with further monomers.
- Suitable and preferred comonomers which form the polymer backbone are selected from fluorenes (for example according to EP 842208 or WO 00/22026), spirobifluorenes (for example according to EP 707020, EP 894107 or WO 06/061181), para- phenylenes (for example according to WO 92/18552), carbazoles (for example according to WO 04/070772 or US Pat
- solutions or from the liquid phase for processing from solution or from the liquid phase, for example by spin coating or by printing processes, solutions or
- Formulations of the compounds of the invention required. It may be preferred to use mixtures of two or more solvents. Suitable and preferred solvents are, for example, toluene, anisole, o-, m- or p-xylene, methyl benzoate, dimethylanisole,
- Formulation in particular a solution, a suspension or a miniemulsion containing at least one compound of the invention and one or more solvents, in particular organic solvents.
- solvents in particular organic solvents.
- an electronic device is understood to mean a device which contains at least one layer which contains at least one organic compound.
- the component may also contain inorganic materials or even layers which are completely composed of inorganic materials.
- the organic electroluminescent device includes cathode, anode and at least one emitting layer. In addition to these layers, they may also contain further layers, for example one or more hole injection layers, hole transport layers, hole blocking layers, electron transport layers, electron injection layers, exciton blocking layers, electron blocking layers and / or
- Embodiments can be used in different layers, depending on the exact structure. Preference is given to an organic electroluminescent device comprising a compound according to formula (1) to (31) or formula (11a) to (31e) as matrix material for fluorescent or phosphorescent emitters, in particular for phosphorescent emitters, and / or in a hole blocking layer and / or in one
- the compound of the formula (1) to (31) or formula (11a) to (31 e) is used as the matrix material for a fluorescent or phosphorescent compound, in particular for a phosphorescent compound, in an emitting layer.
- the organic electroluminescent device may comprise an emitting layer, or it may comprise a plurality of emitting layers, wherein at least one emitting layer contains at least one compound according to the invention as matrix material.
- a further preferred embodiment of the present invention is the use of the compound of the formula (1) to (31) or formula (11a) to (31e) as matrix material for a phosphorescent emitter in combination with another matrix material.
- Particularly suitable matrix materials which can be used in combination with the compounds of the formulas (1) to (31) or (11a) to (31e) are aromatic ketones, aromatic phosphine oxides or aromatic sulfoxides or sulfones, eg. Example, according to WO 04/013080, WO 04/093207, WO 06/005627 or WO 2010/006680, triarylamines, carbazole derivatives, for. B. CBP ( ⁇ , ⁇ -Biscarbazolylbiphenyl) or in WO 05/039246, US
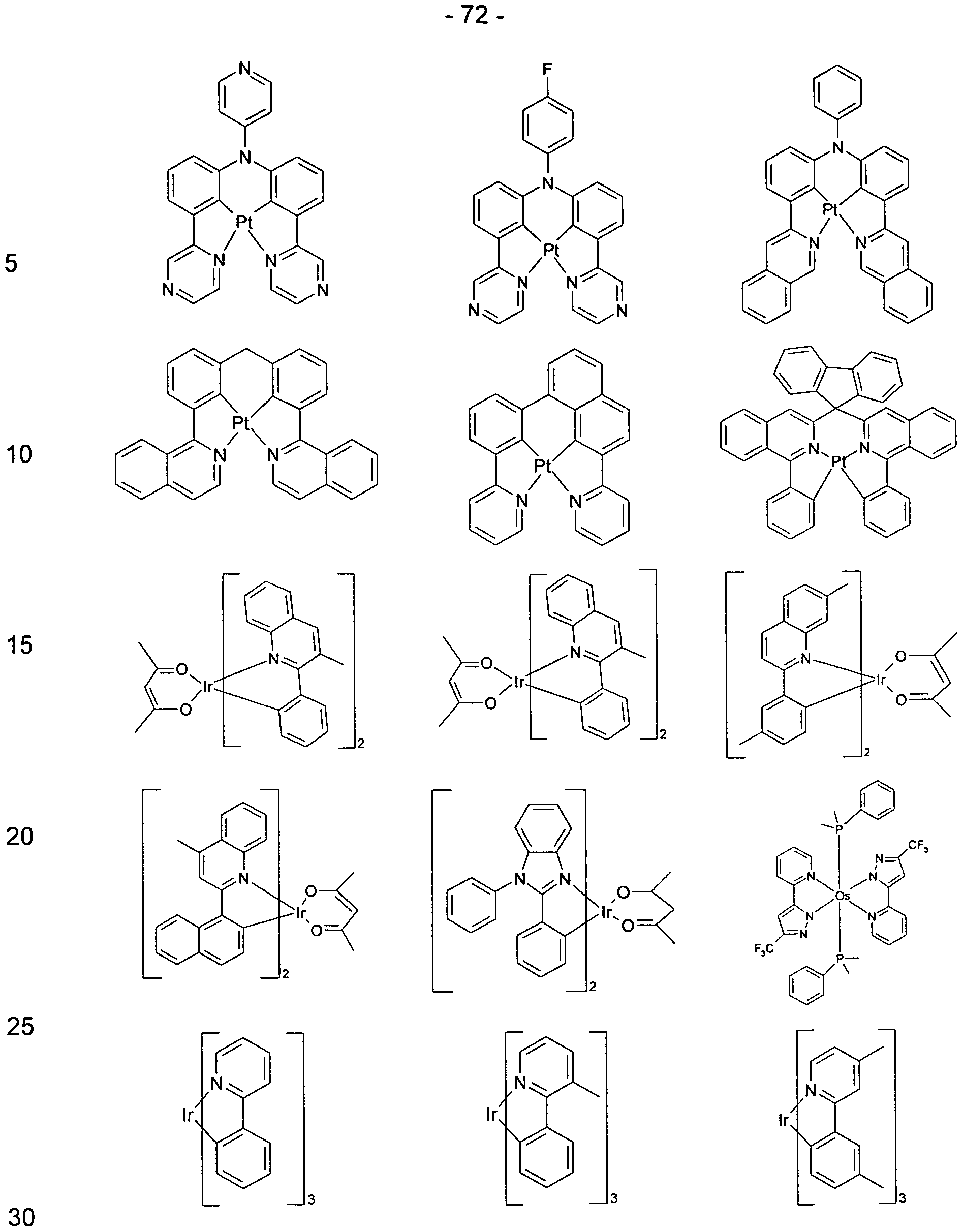
- Suitable phosphorescent compounds are, in particular, compounds which emit light, preferably in the visible range, with suitable excitation and also contain at least one atom of atomic number greater than 20, preferably greater than 38 and less than 84, particularly preferably greater than 56 and less than 80, in particular a metal with this atomic number.
- Preferred phosphorescence emitters are compounds comprising copper, molybdenum, tungsten, rhenium,
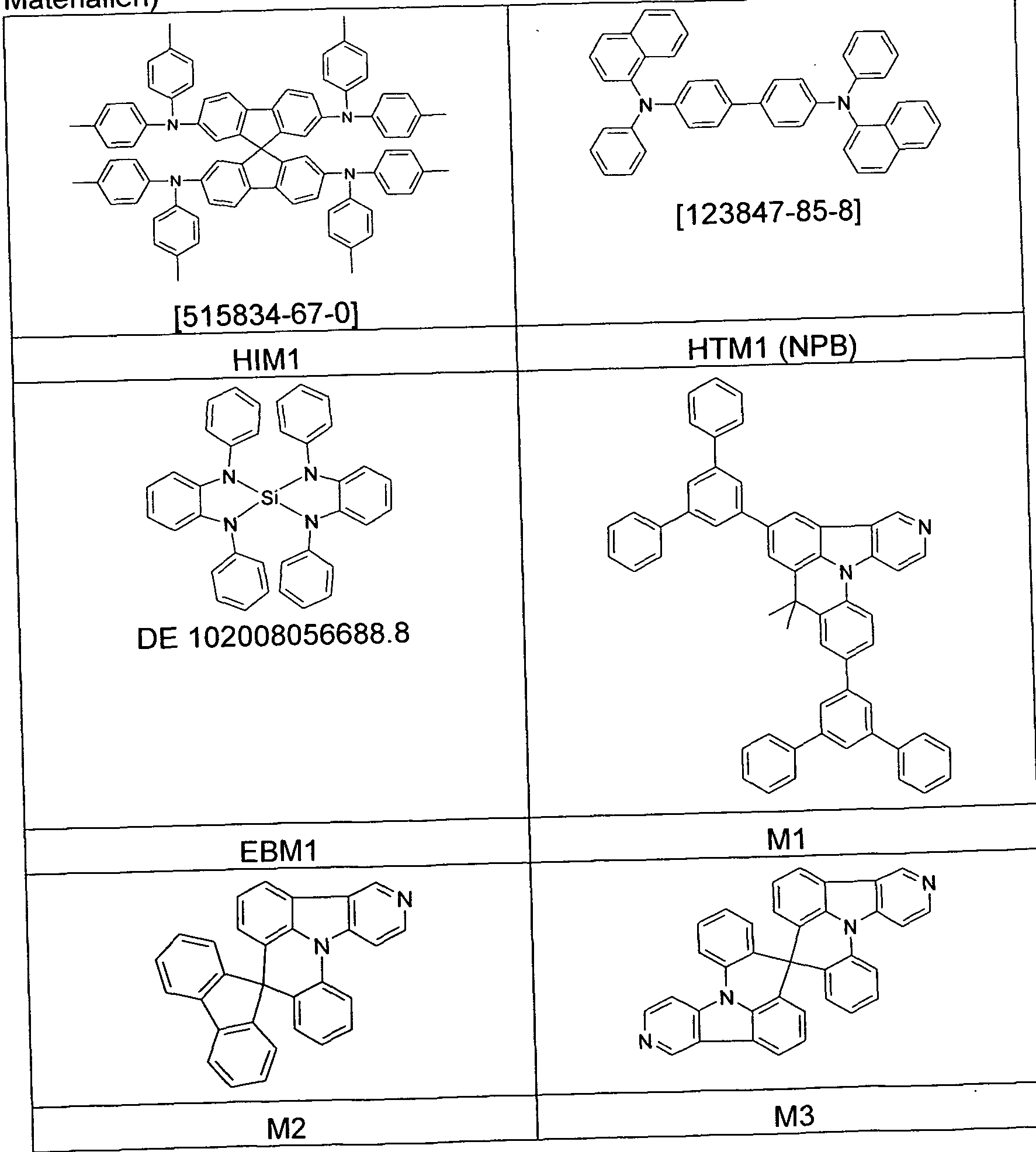
- the OLEDs have in principle the following layer structure: substrate / hole injection layer (HIL, with HIM1, 20 nm) / hole transport layer (HTL, with HTM1, 20 nm) / electron blocking layer (EBL, with EBM1, 20 nm) / emission layer (EML, 40 nm) / Electron transport layer (ETL, with ETM1, 20 nm) / electron injection layer (EIL, LiF, 1 nm) and
- E6 HIL1 HATCN BPA1 12c TEG2 - ST1: LiQ -
- E36 HIL1 HATCN 8e ST1 TEG2 - ST1: LiQ -
- HIL1 HATCN 8g ST1 TEG2 - ST1: LiQ -
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Biochemistry (AREA)
- General Health & Medical Sciences (AREA)
- Molecular Biology (AREA)
- Engineering & Computer Science (AREA)
- Materials Engineering (AREA)
- Electroluminescent Light Sources (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
Abstract
Description
Claims
Priority Applications (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2010800523644A CN102612518A (zh) | 2009-11-18 | 2010-10-20 | 用于oled的含氮稠合杂环化合物 |
| DE112010004482T DE112010004482A5 (de) | 2009-11-18 | 2010-10-20 | Stickstoffhaltige kondensierte Heterozyklen für Oleds |
| US13/510,425 US9012599B2 (en) | 2009-11-18 | 2010-10-20 | Nitrogen-containing condensed heterocyclic compounds for OLEDs |
| JP2012539209A JP6009356B2 (ja) | 2009-11-18 | 2010-10-20 | Oledのための窒素含有縮合ヘテロ環化合物 |
| KR1020127015799A KR101781235B1 (ko) | 2009-11-18 | 2010-10-20 | Oled 용 질소-함유 축합 헤테로시클릭 화합물 |
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE102009053836A DE102009053836A1 (de) | 2009-11-18 | 2009-11-18 | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009053836.4 | 2009-11-18 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2011060867A1 true WO2011060867A1 (de) | 2011-05-26 |
Family
ID=43560745
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/EP2010/006414 Ceased WO2011060867A1 (de) | 2009-11-18 | 2010-10-20 | Stickstoffhaltige kondensierte heterozyklen für oleds |
Country Status (7)
| Country | Link |
|---|---|
| US (1) | US9012599B2 (de) |
| JP (1) | JP6009356B2 (de) |
| KR (1) | KR101781235B1 (de) |
| CN (1) | CN102612518A (de) |
| DE (2) | DE102009053836A1 (de) |
| TW (1) | TW201134819A (de) |
| WO (1) | WO2011060867A1 (de) |
Cited By (133)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012050103A1 (ja) * | 2010-10-13 | 2012-04-19 | 住友化学株式会社 | 縮合芳香族化合物、有機半導体材料及び有機トランジスタ素子 |
| WO2012048781A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien auf basis von triphenylen für organische elektrolumineszenzvorrichtungen |
| WO2012069121A1 (de) | 2010-11-24 | 2012-05-31 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102012000064A1 (de) | 2011-01-21 | 2012-07-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP2012191031A (ja) * | 2011-03-11 | 2012-10-04 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2012136295A1 (de) | 2011-04-05 | 2012-10-11 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2013012296A1 (en) * | 2011-07-21 | 2013-01-24 | Rohm And Haas Electronic Materials Korea Ltd. | Novel organic electroluminescence compounds and organic electroluminescence device using the same |
| CN102945928A (zh) * | 2012-12-06 | 2013-02-27 | 吉林大学 | 一种光谱可调且色坐标稳定的白光有机电致发光器件 |
| WO2013026515A1 (de) | 2011-08-22 | 2013-02-28 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| WO2013077344A1 (ja) * | 2011-11-22 | 2013-05-30 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| WO2013083216A1 (de) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen |
| JP2013175698A (ja) * | 2012-01-23 | 2013-09-05 | Udc Ireland Ltd | 有機電界発光素子、有機電界発光素子用電荷輸送材料、並びに、該素子を用いた発光装置、表示装置及び照明装置 |
| WO2013139431A1 (de) | 2012-03-23 | 2013-09-26 | Merck Patent Gmbh | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| JP2013243300A (ja) * | 2012-05-22 | 2013-12-05 | Udc Ireland Ltd | 電荷輸送材料、有機電界発光素子、発光装置、表示装置および照明装置 |
| KR20130135187A (ko) * | 2012-05-31 | 2013-12-10 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| CN103619986A (zh) * | 2011-06-03 | 2014-03-05 | 默克专利有限公司 | 有机电致发光器件 |
| JP2014132002A (ja) * | 2012-09-03 | 2014-07-17 | Hodogaya Chem Co Ltd | インデノアクリダン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| JP2014517524A (ja) * | 2011-06-01 | 2014-07-17 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | ハイブリッド両極性tft |
| CN104039921A (zh) * | 2011-11-16 | 2014-09-10 | 罗门哈斯电子材料韩国有限公司 | 新有机电致发光化合物和使用该化合物的有机电致发光器件 |
| US9000421B2 (en) | 2012-03-01 | 2015-04-07 | Udc Ireland Limited | Organic electroluminescent element, materials for organic electroluminescent element, and light emitting device, display device, or illumination device, each using the element, and compounds used in the element |
| JP2015159305A (ja) * | 2015-04-01 | 2015-09-03 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置、並びに照明装置 |
| WO2015197156A1 (de) | 2014-06-25 | 2015-12-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| EP2837622A4 (de) * | 2012-04-10 | 2016-03-09 | Hodogaya Chemical Co Ltd | Verbindung mit einer acridanringstruktur und einem organischen elektrolumineszenzelement |
| CN105693749A (zh) * | 2016-03-09 | 2016-06-22 | 中节能万润股份有限公司 | 一种含有吩噻嗪结构的有机光电材料及其应用 |
| WO2016198144A1 (en) | 2015-06-10 | 2016-12-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017016630A1 (en) | 2015-07-30 | 2017-02-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017071791A1 (en) | 2015-10-27 | 2017-05-04 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP3137467A4 (de) * | 2014-05-02 | 2017-10-25 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszenzverbindung und organische elektrolumineszenzvorrichtung damit |
| WO2018104193A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018138306A1 (de) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018149769A1 (de) | 2017-02-14 | 2018-08-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10312455B2 (en) | 2017-03-26 | 2019-06-04 | Feng-wen Yen | Delayed fluorescence material for organic electroluminescence device |
| WO2019145316A1 (de) | 2018-01-25 | 2019-08-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019233904A1 (de) | 2018-06-07 | 2019-12-12 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020094542A1 (de) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | 5,6-diphenyl-5,6-dihydro-dibenz[c,e][1,2]azaphosphorin- und 6-phenyl-6h-dibenzo[c,e][1,2]thiazin-5,5-dioxid-derivate und ähnliche verbindungen als organische elektrolumineszenzmaterialien für oleds |
| US10658594B2 (en) | 2017-12-06 | 2020-05-19 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and novel compound |
| WO2020099307A1 (de) | 2018-11-15 | 2020-05-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020127165A1 (de) | 2018-12-19 | 2020-06-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020182779A1 (de) | 2019-03-12 | 2020-09-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020187865A1 (de) | 2019-03-20 | 2020-09-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021037401A1 (de) | 2019-08-26 | 2021-03-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043703A1 (de) | 2019-09-02 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043755A1 (de) | 2019-09-03 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021053046A1 (de) | 2019-09-20 | 2021-03-25 | Merck Patent Gmbh | Peri-kondensierte heterozyklische verbindungen als materialien für elektronische vorrichtungen |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2021122740A1 (de) | 2019-12-19 | 2021-06-24 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122538A1 (de) | 2019-12-18 | 2021-06-24 | Merck Patent Gmbh | Aromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122535A1 (de) | 2019-12-17 | 2021-06-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021151922A1 (de) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Benzimidazol-derivate |
| WO2021170522A1 (de) | 2020-02-25 | 2021-09-02 | Merck Patent Gmbh | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021185829A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191183A1 (de) | 2020-03-26 | 2021-09-30 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191117A1 (de) | 2020-03-24 | 2021-09-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021204646A1 (de) | 2020-04-06 | 2021-10-14 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002772A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002771A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022029096A1 (de) | 2020-08-06 | 2022-02-10 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038065A1 (de) | 2020-08-18 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038066A1 (de) | 2020-08-19 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022069422A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Verbindungen zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen |
| WO2022069421A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen einsetzbare verbindungen |
| WO2022079067A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022101171A1 (de) | 2020-11-10 | 2022-05-19 | Merck Patent Gmbh | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022117473A1 (de) | 2020-12-02 | 2022-06-09 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022148717A1 (de) | 2021-01-05 | 2022-07-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022184601A1 (de) | 2021-03-02 | 2022-09-09 | Merck Patent Gmbh | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022194799A1 (de) | 2021-03-18 | 2022-09-22 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022200638A1 (de) | 2021-07-06 | 2022-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229126A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229298A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023110742A1 (de) | 2021-12-13 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152063A1 (de) | 2022-02-09 | 2023-08-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023161168A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023247345A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Heterocyclen für photoelektrische vorrichtungen |
| WO2023247338A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Organische heterocyclen für photoelektrische vorrichtungen |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024094592A2 (de) | 2022-11-01 | 2024-05-10 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024133048A1 (en) | 2022-12-20 | 2024-06-27 | Merck Patent Gmbh | Method for preparing deuterated aromatic compounds |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024153568A1 (de) | 2023-01-17 | 2024-07-25 | Merck Patent Gmbh | Heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024194264A1 (de) | 2023-03-20 | 2024-09-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024240725A1 (de) | 2023-05-25 | 2024-11-28 | Merck Patent Gmbh | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| WO2024256357A1 (de) | 2023-06-12 | 2024-12-19 | Merck Patent Gmbh | Organische heterocyclen für photoelektrische vorrichtungen |
| EP4486099A1 (de) | 2023-06-30 | 2025-01-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025003084A1 (de) | 2023-06-28 | 2025-01-02 | Merck Patent Gmbh | Dicyanoarylverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045935A1 (de) | 2023-08-31 | 2025-03-06 | Merck Patent Gmbh | Cyanogruppen-enthaltende aromaten für organische elektrolumineszenzvorrichtungen |
| WO2025045842A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025132547A1 (en) | 2023-12-21 | 2025-06-26 | Merck Patent Gmbh | Mechanochemical method for deuterating organic compounds |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2025210013A1 (de) | 2024-04-04 | 2025-10-09 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen, insbesondere verbindungen für oleds |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2026041632A1 (de) | 2024-08-21 | 2026-02-26 | Merck Patent Gmbh | Heterocyclische materialien für organische lichtemittierende vorrichtungen |
Families Citing this family (37)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009041289A1 (de) * | 2009-09-16 | 2011-03-17 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102010010481A1 (de) | 2010-03-06 | 2011-09-08 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtung |
| DE102010012738A1 (de) | 2010-03-25 | 2011-09-29 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102010019306B4 (de) | 2010-05-04 | 2021-05-20 | Merck Patent Gmbh | Organische Elektrolumineszenzvorrichtungen |
| JP6215192B2 (ja) | 2011-04-18 | 2017-10-18 | メルク パテント ゲーエムベーハー | 有機エレクトロルミネッセンス素子用材料 |
| KR101390362B1 (ko) * | 2012-09-21 | 2014-04-30 | 주식회사 엘엠에스 | 신규한 화합물, 이를 포함하는 발광 소자 및 전자 장치 |
| WO2014046495A1 (ko) * | 2012-09-21 | 2014-03-27 | 주식회사 엘엠에스 | 신규 구조의 발광 소자 및 이를 포함하는 전자 장치 |
| CN103130812B (zh) * | 2013-03-05 | 2014-12-24 | 华东师范大学 | 一种吲哚并[3,2,1-jk]咔唑衍生物及其制备方法和应用 |
| JP6576929B2 (ja) * | 2013-09-11 | 2019-09-18 | メルク パテント ゲーエムベーハー | ヘテロ環化合物 |
| KR102420202B1 (ko) | 2014-06-27 | 2022-07-14 | 롬엔드하스전자재료코리아유한회사 | 신규한 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| KR102419711B1 (ko) | 2014-07-09 | 2022-07-13 | 롬엔드하스전자재료코리아유한회사 | 유기 전계 발광 화합물 및 이를 포함하는 유기 전계 발광 소자 |
| JP6651712B2 (ja) * | 2015-05-15 | 2020-02-19 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子、その製造方法、表示装置、照明装置、有機エレクトロルミネッセンス素子材料及び新規化合物 |
| US10211411B2 (en) | 2015-08-25 | 2019-02-19 | Arizona Board Of Regents On Behalf Of Arizona State University | Thermally activated delayed fluorescent material based on 9,10-dihydro-9,9-dimethylacridine analogues for prolonging device longevity |
| CN105348300B (zh) * | 2015-11-10 | 2018-04-10 | 中节能万润股份有限公司 | 一种有机光电材料及其制备方法和用途 |
| KR101834433B1 (ko) | 2016-06-08 | 2018-03-05 | 주식회사 엘지화학 | 신규한 화합물 및 이를 포함하는 유기발광 소자 |
| KR102477259B1 (ko) * | 2016-07-18 | 2022-12-14 | 삼성디스플레이 주식회사 | 유기 전계 발광 표시 장치 |
| TW201833118A (zh) * | 2016-11-22 | 2018-09-16 | 德商麥克專利有限公司 | 用於電子裝置之材料 |
| CN109792001B (zh) * | 2016-11-23 | 2021-04-20 | 广州华睿光电材料有限公司 | 有机化合物、有机混合物、有机电子器件 |
| US10615349B2 (en) | 2017-05-19 | 2020-04-07 | Arizona Board Of Regents On Behalf Of Arizona State University | Donor-acceptor type thermally activated delayed fluorescent materials based on imidazo[1,2-F]phenanthridine and analogues |
| US10392387B2 (en) | 2017-05-19 | 2019-08-27 | Arizona Board Of Regents On Behalf Of Arizona State University | Substituted benzo[4,5]imidazo[1,2-a]phenanthro[9,10-c][1,8]naphthyridines, benzo[4,5]imidazo[1,2-a]phenanthro[9,10-c][1,5]naphthyridines and dibenzo[f,h]benzo[4,5]imidazo[2,1-a]pyrazino[2,3-c]isoquinolines as thermally assisted delayed fluorescent materials |
| WO2019111971A1 (ja) | 2017-12-06 | 2019-06-13 | 出光興産株式会社 | 有機エレクトロルミネッセンス素子及び新規化合物 |
| CN108997345B (zh) * | 2018-08-20 | 2024-08-02 | 上海弗屈尔光电科技有限公司 | 一种氮杂螺环化合物及含有该化合物的有机光电器件 |
| US10593889B1 (en) | 2018-09-26 | 2020-03-17 | Idemitsu Kosan Co., Ltd. | Compound and organic electroluminescence device |
| CN110759910A (zh) * | 2018-12-06 | 2020-02-07 | 广州华睿光电材料有限公司 | 吡啶化合物及其用途 |
| KR20200075193A (ko) | 2018-12-17 | 2020-06-26 | 삼성디스플레이 주식회사 | 축합환 화합물, 이를 포함하는 유기 발광 소자 및 이를 포함하는 표시 장치 |
| CN111848620A (zh) * | 2019-04-30 | 2020-10-30 | 江西冠能光电材料有限公司 | 一种有机发光化合物及其有机发光器件应用 |
| KR102786420B1 (ko) | 2019-06-19 | 2025-03-27 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 아민 화합물 |
| KR102890850B1 (ko) | 2019-10-24 | 2025-11-27 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 다환 화합물 |
| CN110746426A (zh) * | 2019-10-25 | 2020-02-04 | 武汉华星光电半导体显示技术有限公司 | 一种双极主体材料及其应用 |
| KR102806909B1 (ko) | 2019-11-08 | 2025-05-15 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 다환 화합물 |
| US20220348822A1 (en) * | 2020-01-07 | 2022-11-03 | Arizona Board Of Regents On Behalf Of Arizona State University | Donor-acceptor type stable thermally activated delayed fluorescent materials based on rigid molecular structure design |
| US12168661B2 (en) | 2020-02-21 | 2024-12-17 | Arizona Board Of Regents On Behalf Of Arizona State University | Functional materials based on stable chemical structure |
| CN111675709B (zh) | 2020-03-31 | 2021-12-24 | 武汉华星光电半导体显示技术有限公司 | 一种荧光材料及其合成方法 |
| KR102900610B1 (ko) | 2020-07-31 | 2025-12-19 | 삼성디스플레이 주식회사 | 유기 전계 발광 소자 및 유기 전계 발광 소자용 다환 화합물 |
| US12545678B2 (en) | 2020-09-09 | 2026-02-10 | Arizona Board Of Regents On Behalf Of Arizon State University | Blue thermally activated delayed fluorescent emitters and hosts based on functionalized imidazolyl groups |
| KR102936425B1 (ko) | 2020-12-15 | 2026-03-10 | 삼성디스플레이 주식회사 | 발광 소자 및 발광 소자용 다환 화합물 |
| CN116333726A (zh) * | 2023-03-08 | 2023-06-27 | 季华实验室 | 一种有机晶体材料、有机晶体材料的制备方法及其应用 |
Citations (67)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| WO1992018552A1 (de) | 1991-04-11 | 1992-10-29 | Wacker-Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| EP1028136A2 (de) | 1999-02-10 | 2000-08-16 | Carnegie-Mellon University | Ein Verfahren zur Herstellung von Poly(3-substituierten)thiophenen |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| WO2002002714A2 (en) | 2000-06-30 | 2002-01-10 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191612A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191613A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191614A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung und dafür verwendete Metallkoordinationsverbindung |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2002072714A1 (de) | 2001-03-10 | 2002-09-19 | Covion Organic Semiconductors Gmbh | Lösung und dispersionen organischer halbleiter |
| WO2003019694A2 (de) | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors Gmbh | Lösungen polymerer halbleiter |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004041901A1 (en) | 2002-11-08 | 2004-05-21 | Covion Organic Semiconductors Gmbh | Aryl-substituted polyindenofluorenes for use in organic electroluminiscent devices |
| WO2004058911A2 (de) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2004070772A2 (de) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| WO2004113412A2 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Polymer |
| WO2004113468A1 (de) | 2003-06-26 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Neue materialien für die elektrolumineszenz |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005019373A2 (de) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005033244A1 (de) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
| WO2005053051A1 (de) | 2003-11-25 | 2005-06-09 | Merck Patent Gmbh | Organisches elektrolumineszenzelement |
| WO2005104264A1 (de) | 2004-04-26 | 2005-11-03 | Merck Patent Gmbh | Elektrolumineszierende polymere und deren verwendung |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| EP1617711A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organisches elektrolumineszenzbauelement und anzeige |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006061181A1 (de) | 2004-12-06 | 2006-06-15 | Merck Patent Gmbh | Teilkonjugierte polymere, deren darstellung und verwendung |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2007017066A1 (de) | 2005-08-10 | 2007-02-15 | Merck Patent Gmbh | Elektrolumineszierende polymere und ihre verwendung |
| WO2007031165A2 (de) | 2005-09-12 | 2007-03-22 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009030981A2 (en) | 2006-12-28 | 2009-03-12 | Universal Display Corporation | Long lifetime phosphorescent organic light emitting device (oled) structures |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| US20090136779A1 (en) | 2007-11-26 | 2009-05-28 | Chien-Hong Cheng | Conjugated compounds containing hydroindoloacridine structural elements, and their use |
| US20090230857A1 (en) * | 2008-03-14 | 2009-09-17 | Byoung-Ki Choi | Aromatic heterocyclic compound, organic light emitting diode comprising organic layer comprising the same and method of manufacturing the organic light emitting diode |
| WO2009146770A2 (de) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Elektronische vorrichtung enthaltend metallkomplexe |
| WO2010006680A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010015307A1 (de) | 2008-08-04 | 2010-02-11 | Merck Patent Gmbh | Elektronische vorrichtung enthaltend metallkomplexe mit isonitrilliganden |
| WO2010015306A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organische elektrolumineszenzvorrichtung |
| US20100051928A1 (en) * | 2008-09-04 | 2010-03-04 | Fujifilm Corporation | Organic electroluminescence device |
| WO2010031485A1 (de) | 2008-09-22 | 2010-03-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054731A1 (de) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054729A2 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054730A1 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2010054728A1 (de) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010086089A1 (de) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
Family Cites Families (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE102009011223A1 (de) | 2009-03-02 | 2010-09-23 | Merck Patent Gmbh | Metallkomplexe |
| DE102009013041A1 (de) | 2009-03-13 | 2010-09-16 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009023155A1 (de) | 2009-05-29 | 2010-12-02 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009031021A1 (de) | 2009-06-30 | 2011-01-05 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| DE102009048791A1 (de) | 2009-10-08 | 2011-04-14 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
-
2009
- 2009-11-18 DE DE102009053836A patent/DE102009053836A1/de not_active Withdrawn
-
2010
- 2010-10-20 CN CN2010800523644A patent/CN102612518A/zh active Pending
- 2010-10-20 WO PCT/EP2010/006414 patent/WO2011060867A1/de not_active Ceased
- 2010-10-20 JP JP2012539209A patent/JP6009356B2/ja not_active Expired - Fee Related
- 2010-10-20 KR KR1020127015799A patent/KR101781235B1/ko active Active
- 2010-10-20 US US13/510,425 patent/US9012599B2/en active Active
- 2010-10-20 DE DE112010004482T patent/DE112010004482A5/de not_active Withdrawn
- 2010-11-15 TW TW099139205A patent/TW201134819A/zh unknown
Patent Citations (69)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US4539507A (en) | 1983-03-25 | 1985-09-03 | Eastman Kodak Company | Organic electroluminescent devices having improved power conversion efficiencies |
| WO1992018552A1 (de) | 1991-04-11 | 1992-10-29 | Wacker-Chemie Gmbh | Leiterpolymere mit konjugierten doppelbindungen |
| US5151629A (en) | 1991-08-01 | 1992-09-29 | Eastman Kodak Company | Blue emitting internal junction organic electroluminescent device (I) |
| EP0652273A1 (de) | 1993-11-09 | 1995-05-10 | Shinko Electric Industries Co. Ltd. | Organisches Material für elektrolumineszente Vorrichtung und elektrolumineszente Vorrichtung |
| EP0676461A2 (de) | 1994-04-07 | 1995-10-11 | Hoechst Aktiengesellschaft | Spiroverbindungen und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0707020A2 (de) | 1994-10-14 | 1996-04-17 | Hoechst Aktiengesellschaft | Konjugierte Polymere mit Spirozentren und ihre Verwendung als Elektrolumineszenzmaterialien |
| EP0842208A1 (de) | 1995-07-28 | 1998-05-20 | The Dow Chemical Company | 2,7-aryl-9-substituierte fluorene und 9-substituierte fluorenoligomere und polymere |
| EP0894107A1 (de) | 1996-04-17 | 1999-02-03 | Hoechst Research & Technology Deutschland GmbH & Co. KG | Polymere mit spiroatomen und ihre verwendung als elektrolumineszenzmaterialien |
| WO1998027136A1 (de) | 1996-12-16 | 1998-06-25 | Aventis Research & Technologies Gmbh & Co Kg | ARYLSUBSTITUIERTE POLY(p-ARYLENVINYLENE), VERFAHREN ZUR HERSTELLUNG UND DEREN VERWENDUNG IN ELEKTROLUMINESZENZBAUELEMENTEN |
| WO2000022026A1 (de) | 1998-10-10 | 2000-04-20 | Celanese Ventures Gmbh | Konjugierte polymere, enthaltend spezielle fluoren-bausteine mit verbesserten eigenschaften |
| EP1028136A2 (de) | 1999-02-10 | 2000-08-16 | Carnegie-Mellon University | Ein Verfahren zur Herstellung von Poly(3-substituierten)thiophenen |
| WO2000070655A2 (en) | 1999-05-13 | 2000-11-23 | The Trustees Of Princeton University | Very high efficiency organic light emitting devices based on electrophosphorescence |
| WO2001041512A1 (en) | 1999-12-01 | 2001-06-07 | The Trustees Of Princeton University | Complexes of form l2mx as phosphorescent dopants for organic leds |
| EP1205527A1 (de) | 2000-03-27 | 2002-05-15 | Idemitsu Kosan Co., Ltd. | Organische elektrolumineszierende vorrichtung |
| WO2002002714A2 (en) | 2000-06-30 | 2002-01-10 | E.I. Du Pont De Nemours And Company | Electroluminescent iridium compounds with fluorinated phenylpyridines, phenylpyrimidines, and phenylquinolines and devices made with such compounds |
| WO2002015645A1 (en) | 2000-08-11 | 2002-02-21 | The Trustees Of Princeton University | Organometallic compounds and emission-shifting organic electrophosphorescence |
| EP1191612A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191613A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung, Bildanzeigevorrichtung und Metallkoordinationsverbindung |
| EP1191614A2 (de) | 2000-09-26 | 2002-03-27 | Canon Kabushiki Kaisha | Lumineszente Vorrichtung und dafür verwendete Metallkoordinationsverbindung |
| WO2002072714A1 (de) | 2001-03-10 | 2002-09-19 | Covion Organic Semiconductors Gmbh | Lösung und dispersionen organischer halbleiter |
| WO2003019694A2 (de) | 2001-08-24 | 2003-03-06 | Covion Organic Semiconductors Gmbh | Lösungen polymerer halbleiter |
| WO2004013080A1 (en) | 2002-08-01 | 2004-02-12 | Covion Organic Semiconductors Gmbh | Spirobifluorene derivatives, their preparation and uses thereof |
| WO2004041901A1 (en) | 2002-11-08 | 2004-05-21 | Covion Organic Semiconductors Gmbh | Aryl-substituted polyindenofluorenes for use in organic electroluminiscent devices |
| WO2004058911A2 (de) | 2002-12-23 | 2004-07-15 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2004070772A2 (de) | 2003-02-06 | 2004-08-19 | Covion Organic Semiconductors Gmbh | Carbazol-enthaltende konjugierte polymere und blends, deren darstellung und verwendung |
| JP2004288381A (ja) | 2003-03-19 | 2004-10-14 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子 |
| WO2004093207A2 (de) | 2003-04-15 | 2004-10-28 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialien, deren verwendung und elektronikbauteile enthaltend diese mischungen |
| EP1617711A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Organisches elektrolumineszenzbauelement und anzeige |
| EP1617710A1 (de) | 2003-04-23 | 2006-01-18 | Konica Minolta Holdings, Inc. | Material für ein organisches elektrolumineszenzgerät, organisches elektrolumineszenzgerät, beleuchtungsvorrichtung und anzeige |
| WO2004113412A2 (en) | 2003-06-23 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Polymer |
| WO2004113468A1 (de) | 2003-06-26 | 2004-12-29 | Covion Organic Semiconductors Gmbh | Neue materialien für die elektrolumineszenz |
| WO2005003253A2 (de) | 2003-07-07 | 2005-01-13 | Covion Organic Semiconductors Gmbh | Mischungen von organischen zur emission befähigten halbleitern und matrixmaterialen, deren verwendung und elektronikbauteile enthaltend diese |
| WO2005011013A1 (de) | 2003-07-21 | 2005-02-03 | Covion Organic Semiconductors Gmbh | Organisches elektrolumineszenzelement |
| WO2005014689A2 (de) | 2003-08-12 | 2005-02-17 | Covion Organic Semiconductors Gmbh | Konjugierte polymere enthaltend dihydrophenanthren-einheiten und deren verwendung |
| WO2005019373A2 (de) | 2003-08-19 | 2005-03-03 | Basf Aktiengesellschaft | Übergangsmetallkomplexe mit carbenliganden als emitter für organische licht-emittierende dioden (oleds) |
| WO2005033244A1 (de) | 2003-09-29 | 2005-04-14 | Covion Organic Semiconductors Gmbh | Metallkomplexe |
| US20050069729A1 (en) | 2003-09-30 | 2005-03-31 | Konica Minolta Holdings, Inc. | Organic electroluminescent element, illuminator, display and compound |
| WO2005039246A1 (ja) | 2003-09-30 | 2005-04-28 | Konica Minolta Holdings, Inc. | 有機エレクトロルミネッセンス素子、照明装置、表示装置 |
| WO2005040302A1 (de) | 2003-10-22 | 2005-05-06 | Merck Patent Gmbh | Neue materialien für die elektrolumineszenz und deren verwendung |
| WO2005053051A1 (de) | 2003-11-25 | 2005-06-09 | Merck Patent Gmbh | Organisches elektrolumineszenzelement |
| EP1731584A1 (de) | 2004-03-31 | 2006-12-13 | Konica Minolta Holdings, Inc. | Organischer elektrolumineszenzvorrichtungsstoff, organische elektrolumineszenzvorrichtung, display und beleuchtungsvorrichtung |
| WO2005104264A1 (de) | 2004-04-26 | 2005-11-03 | Merck Patent Gmbh | Elektrolumineszierende polymere und deren verwendung |
| WO2005111172A2 (de) | 2004-05-11 | 2005-11-24 | Merck Patent Gmbh | Neue materialmischungen für die elektrolumineszenz |
| US20050258742A1 (en) | 2004-05-18 | 2005-11-24 | Yui-Yi Tsai | Carbene containing metal complexes as OLEDs |
| JP2005347160A (ja) | 2004-06-04 | 2005-12-15 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、照明装置及び表示装置 |
| WO2006005627A1 (en) | 2004-07-15 | 2006-01-19 | Merck Patent Gmbh | Oligomeric derivatives of spirobifluorene, their preparation and use |
| WO2006061181A1 (de) | 2004-12-06 | 2006-06-15 | Merck Patent Gmbh | Teilkonjugierte polymere, deren darstellung und verwendung |
| WO2006117052A1 (de) | 2005-05-03 | 2006-11-09 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung und in deren herstellung verwendete boronsäure- und borinsäure-derivate |
| WO2007017066A1 (de) | 2005-08-10 | 2007-02-15 | Merck Patent Gmbh | Elektrolumineszierende polymere und ihre verwendung |
| WO2007031165A2 (de) | 2005-09-12 | 2007-03-22 | Merck Patent Gmbh | Verbindungen für organische elektronische vorrichtungen |
| WO2007063754A1 (ja) | 2005-12-01 | 2007-06-07 | Nippon Steel Chemical Co., Ltd. | 有機電界発光素子用化合物及び有機電界発光素子 |
| WO2007137725A1 (de) | 2006-05-31 | 2007-12-06 | Merck Patent Gmbh | Neue materialien für organische elektrolumineszenzvorrichtungen |
| WO2008056746A1 (en) | 2006-11-09 | 2008-05-15 | Nippon Steel Chemical Co., Ltd. | Compound for organic electroluminescent device and organic electroluminescent device |
| WO2009030981A2 (en) | 2006-12-28 | 2009-03-12 | Universal Display Corporation | Long lifetime phosphorescent organic light emitting device (oled) structures |
| WO2008086851A1 (de) | 2007-01-18 | 2008-07-24 | Merck Patent Gmbh | Carbazol-derivate für organische elektrolumineszenzvorrichtungen |
| WO2009062578A1 (de) | 2007-11-12 | 2009-05-22 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen enthaltend azomethin-metall-komplexe |
| US20090136779A1 (en) | 2007-11-26 | 2009-05-28 | Chien-Hong Cheng | Conjugated compounds containing hydroindoloacridine structural elements, and their use |
| US20090230857A1 (en) * | 2008-03-14 | 2009-09-17 | Byoung-Ki Choi | Aromatic heterocyclic compound, organic light emitting diode comprising organic layer comprising the same and method of manufacturing the organic light emitting diode |
| WO2009146770A2 (de) | 2008-06-05 | 2009-12-10 | Merck Patent Gmbh | Elektronische vorrichtung enthaltend metallkomplexe |
| WO2010006680A1 (de) | 2008-07-18 | 2010-01-21 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010015307A1 (de) | 2008-08-04 | 2010-02-11 | Merck Patent Gmbh | Elektronische vorrichtung enthaltend metallkomplexe mit isonitrilliganden |
| WO2010015306A1 (de) | 2008-08-08 | 2010-02-11 | Merck Patent Gmbh, | Organische elektrolumineszenzvorrichtung |
| US20100051928A1 (en) * | 2008-09-04 | 2010-03-04 | Fujifilm Corporation | Organic electroluminescence device |
| WO2010031485A1 (de) | 2008-09-22 | 2010-03-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054729A2 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054730A1 (de) | 2008-11-11 | 2010-05-20 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2010054731A1 (de) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010054728A1 (de) | 2008-11-13 | 2010-05-20 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2010086089A1 (de) | 2009-02-02 | 2010-08-05 | Merck Patent Gmbh | Metallkomplexe |
Non-Patent Citations (10)
| Title |
|---|
| B. M. S. ARNOLD ET AL., APPL. PHYS. LETT., vol. 92, 2008, pages 053301 |
| D. M. KOLLER ET AL., NATURE PHOTONICS, 2008, pages 1 - 4 |
| DATABASE CA [online] CHEMICAL ABSTRACTS SERVICE, COLUMBUS, OHIO, US; 1 January 2007 (2007-01-01), I.G.ABRAMOV ET AL: "Synthesis of six-membered O-, N- and S-containing heterocyclic compounds condensed with phthalonitrile fragment", XP002623205, Database accession no. 2005:1029337 * |
| ESHIMBETOV A G ET AL: "Theoretical and UV spectral study of isomeric 1-(quinolinyl)-beta-carbolines conformations", SPECTROCHIMICA ACTA. PART A: MOLECULAR AND BIOMOLECULAR SPECTROSCOPY, ELSEVIER, AMSTERDAM, NL, vol. 67, no. 3-4, 1 July 2007 (2007-07-01), pages 1139 - 1143, XP025319153, ISSN: 1386-1425, [retrieved on 20070525], DOI: DOI:10.1016/J.SAA.2006.07.054 * |
| I. HELD ET AL: "The stability of acylpyridinium cations and their relation to the catalytic activity of pyridine bases", SYNTHESIS, vol. 9, 13 April 2005 (2005-04-13) - 13 April 2005 (2005-04-13), pages 1425 - 1430, XP002623206 * |
| IZVESTIYA VYSSHIKH UCHEBNYKH ZAVEDENII, KHIMIYA I KHIMICHESKAYA TEKHNOLOGIYA, vol. 47, no. 6, 1 January 2007 (2007-01-01) - 1 January 2007 (2007-01-01), pages 18 - 23 * |
| J.B HENRY ET AL: "Calculation of the Redox Properties of Aromatics and Prediction of Their Coupling Mechanism and Oligomer Redox Properties", J. OF PHYSICAL CHEMISTRY A, vol. 113, no. 46, 10 February 2009 (2009-02-10) - 10 February 2009 (2009-02-10), pages 13023 - 13028, XP002623204 * |
| L. CRAWFORD ET AL: "Synthesis of azapyrrolo[3,2,1-jk]carbazoles, azaindolo[3,2,1-jk]carbazoles, and carbazole-1-carbonitriles by gas-phase cyclization of aryl radicals", SYNTHESIS, vol. 6, 8 January 2010 (2010-01-08) - 8 January 2010 (2010-01-08), pages 923 - 928, XP002623203 * |
| M. A. BALDO ET AL., APPL. PHYS. LETT., vol. 75, 1999, pages 4 - 6 |
| P. MOLINA ET AL: "Iminophosphorane-mediated syntheses of the fascaplysin alkaloid of marine origin and nitramarine", TETRAHEDRON LETTERS, vol. 35, no. 47, 1 January 1994 (1994-01-01) - 1 January 1994 (1994-01-01), pages 8851 - 8854, XP002623207 * |
Cited By (149)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2012050103A1 (ja) * | 2010-10-13 | 2012-04-19 | 住友化学株式会社 | 縮合芳香族化合物、有機半導体材料及び有機トランジスタ素子 |
| WO2012048781A1 (de) | 2010-10-15 | 2012-04-19 | Merck Patent Gmbh | Materialien auf basis von triphenylen für organische elektrolumineszenzvorrichtungen |
| WO2012069121A1 (de) | 2010-11-24 | 2012-05-31 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| DE102012000064A1 (de) | 2011-01-21 | 2012-07-26 | Merck Patent Gmbh | Materialien für organische Elektrolumineszenzvorrichtungen |
| JP2012191031A (ja) * | 2011-03-11 | 2012-10-04 | Konica Minolta Holdings Inc | 有機エレクトロルミネッセンス素子、表示装置及び照明装置 |
| WO2012136295A1 (de) | 2011-04-05 | 2012-10-11 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| JP2014517524A (ja) * | 2011-06-01 | 2014-07-17 | メルク パテント ゲゼルシャフト ミット ベシュレンクテル ハフツング | ハイブリッド両極性tft |
| US9118022B2 (en) * | 2011-06-03 | 2015-08-25 | Merck Patent Gmbh | Organic electroluminescent device |
| US20140088305A1 (en) * | 2011-06-03 | 2014-03-27 | Merck Patent Gmbh | Organic electroluminescent device |
| CN103619986A (zh) * | 2011-06-03 | 2014-03-05 | 默克专利有限公司 | 有机电致发光器件 |
| WO2013012296A1 (en) * | 2011-07-21 | 2013-01-24 | Rohm And Haas Electronic Materials Korea Ltd. | Novel organic electroluminescence compounds and organic electroluminescence device using the same |
| JP2014520882A (ja) * | 2011-07-21 | 2014-08-25 | ローム・アンド・ハース・エレクトロニック・マテリアルズ・コリア・リミテッド | 新規有機エレクトロルミネセンス化合物およびこれを使用した有機エレクトロルミネセンス素子 |
| CN103797014A (zh) * | 2011-07-21 | 2014-05-14 | 罗门哈斯电子材料韩国有限公司 | 新有机电致发光化合物和使用该化合物的有机电致发光器件 |
| WO2013026515A1 (de) | 2011-08-22 | 2013-02-28 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtung |
| CN104039921A (zh) * | 2011-11-16 | 2014-09-10 | 罗门哈斯电子材料韩国有限公司 | 新有机电致发光化合物和使用该化合物的有机电致发光器件 |
| WO2013083216A1 (de) | 2011-11-17 | 2013-06-13 | Merck Patent Gmbh | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen |
| US12552803B2 (en) | 2011-11-22 | 2026-02-17 | Udc Ireland Limited | Organic electroluminescent element, material for organic electroluminescent element, light emitting device, display device and lighting device each using said element, and compound used for said element |
| JP7379619B2 (ja) | 2011-11-22 | 2023-11-14 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| WO2013077344A1 (ja) * | 2011-11-22 | 2013-05-30 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| JP2022188018A (ja) * | 2011-11-22 | 2022-12-20 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| US11171293B2 (en) | 2011-11-22 | 2021-11-09 | Udc Ireland Limited | Organic electroluminescent element, material for organic electroluminescent element, light emitting device, display device and lighting device each using said element, and compound used for said element |
| JP2020004964A (ja) * | 2011-11-22 | 2020-01-09 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| JPWO2013077344A1 (ja) * | 2011-11-22 | 2015-04-27 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| JP2017199925A (ja) * | 2011-11-22 | 2017-11-02 | ユー・ディー・シー アイルランド リミテッド | 有機電界発光素子、有機電界発光素子用材料、並びに、該素子を用いた発光装置、表示装置、照明装置及び該素子に用いられる化合物 |
| JP2013175698A (ja) * | 2012-01-23 | 2013-09-05 | Udc Ireland Ltd | 有機電界発光素子、有機電界発光素子用電荷輸送材料、並びに、該素子を用いた発光装置、表示装置及び照明装置 |
| US9000421B2 (en) | 2012-03-01 | 2015-04-07 | Udc Ireland Limited | Organic electroluminescent element, materials for organic electroluminescent element, and light emitting device, display device, or illumination device, each using the element, and compounds used in the element |
| WO2013139431A1 (de) | 2012-03-23 | 2013-09-26 | Merck Patent Gmbh | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen |
| EP2837622A4 (de) * | 2012-04-10 | 2016-03-09 | Hodogaya Chemical Co Ltd | Verbindung mit einer acridanringstruktur und einem organischen elektrolumineszenzelement |
| JP2013243300A (ja) * | 2012-05-22 | 2013-12-05 | Udc Ireland Ltd | 電荷輸送材料、有機電界発光素子、発光装置、表示装置および照明装置 |
| KR20130135187A (ko) * | 2012-05-31 | 2013-12-10 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| KR101640285B1 (ko) | 2012-05-31 | 2016-07-15 | 주식회사 엘지화학 | 신규한 화합물 및 이를 이용한 유기 발광 소자 |
| JP2014132002A (ja) * | 2012-09-03 | 2014-07-17 | Hodogaya Chem Co Ltd | インデノアクリダン環構造を有する化合物および有機エレクトロルミネッセンス素子 |
| EP2894155A4 (de) * | 2012-09-03 | 2016-01-20 | Hodogaya Chemical Co Ltd | Verbindung mit einer indenoacridanringstruktur und einem organischen elektrolumineszenzelement |
| CN102945928A (zh) * | 2012-12-06 | 2013-02-27 | 吉林大学 | 一种光谱可调且色坐标稳定的白光有机电致发光器件 |
| EP3137467A4 (de) * | 2014-05-02 | 2017-10-25 | Rohm And Haas Electronic Materials Korea Ltd. | Organische elektrolumineszenzverbindung und organische elektrolumineszenzvorrichtung damit |
| WO2015197156A1 (de) | 2014-06-25 | 2015-12-30 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| JP2015159305A (ja) * | 2015-04-01 | 2015-09-03 | コニカミノルタ株式会社 | 有機エレクトロルミネッセンス素子材料、有機エレクトロルミネッセンス素子、表示装置、並びに照明装置 |
| WO2016198144A1 (en) | 2015-06-10 | 2016-12-15 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2017016630A1 (en) | 2015-07-30 | 2017-02-02 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| EP4301110A2 (de) | 2015-07-30 | 2024-01-03 | Merck Patent GmbH | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2017071791A1 (en) | 2015-10-27 | 2017-05-04 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| CN105693749A (zh) * | 2016-03-09 | 2016-06-22 | 中节能万润股份有限公司 | 一种含有吩噻嗪结构的有机光电材料及其应用 |
| WO2018104193A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018104194A1 (de) | 2016-12-05 | 2018-06-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018127465A1 (de) | 2017-01-04 | 2018-07-12 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018138306A1 (de) | 2017-01-30 | 2018-08-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2018149769A1 (de) | 2017-02-14 | 2018-08-23 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10312455B2 (en) | 2017-03-26 | 2019-06-04 | Feng-wen Yen | Delayed fluorescence material for organic electroluminescence device |
| WO2019081391A1 (de) | 2017-10-24 | 2019-05-02 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| US10658594B2 (en) | 2017-12-06 | 2020-05-19 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and novel compound |
| US10672989B2 (en) | 2017-12-06 | 2020-06-02 | Idemitsu Kosan Co., Ltd. | Organic electroluminescence device and novel compound |
| WO2019145316A1 (de) | 2018-01-25 | 2019-08-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2019233904A1 (de) | 2018-06-07 | 2019-12-12 | Merck Patent Gmbh | Organische elektrolumineszenzvorrichtungen |
| WO2020011686A1 (de) | 2018-07-09 | 2020-01-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020094542A1 (de) | 2018-11-06 | 2020-05-14 | Merck Patent Gmbh | 5,6-diphenyl-5,6-dihydro-dibenz[c,e][1,2]azaphosphorin- und 6-phenyl-6h-dibenzo[c,e][1,2]thiazin-5,5-dioxid-derivate und ähnliche verbindungen als organische elektrolumineszenzmaterialien für oleds |
| WO2020099307A1 (de) | 2018-11-15 | 2020-05-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020127165A1 (de) | 2018-12-19 | 2020-06-25 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020182779A1 (de) | 2019-03-12 | 2020-09-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020187865A1 (de) | 2019-03-20 | 2020-09-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2020193447A1 (de) | 2019-03-25 | 2020-10-01 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021037401A1 (de) | 2019-08-26 | 2021-03-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043703A1 (de) | 2019-09-02 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021043755A1 (de) | 2019-09-03 | 2021-03-11 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021053046A1 (de) | 2019-09-20 | 2021-03-25 | Merck Patent Gmbh | Peri-kondensierte heterozyklische verbindungen als materialien für elektronische vorrichtungen |
| WO2021078710A1 (en) | 2019-10-22 | 2021-04-29 | Merck Patent Gmbh | Materials for organic electroluminescent devices |
| WO2021078831A1 (de) | 2019-10-25 | 2021-04-29 | Merck Patent Gmbh | In einer organischen elektronischen vorrichtung einsetzbare verbindungen |
| WO2021122535A1 (de) | 2019-12-17 | 2021-06-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021122538A1 (de) | 2019-12-18 | 2021-06-24 | Merck Patent Gmbh | Aromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021122740A1 (de) | 2019-12-19 | 2021-06-24 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021151922A1 (de) | 2020-01-29 | 2021-08-05 | Merck Patent Gmbh | Benzimidazol-derivate |
| WO2021170522A1 (de) | 2020-02-25 | 2021-09-02 | Merck Patent Gmbh | Verwendung von heterocyclischen verbindungen in einer organischen elektronischen vorrichtung |
| WO2021175706A1 (de) | 2020-03-02 | 2021-09-10 | Merck Patent Gmbh | Verwendung von sulfonverbindungen in einer organischen elektronischen vorrichtung |
| WO2021185712A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021185829A1 (de) | 2020-03-17 | 2021-09-23 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021191117A1 (de) | 2020-03-24 | 2021-09-30 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2021191183A1 (de) | 2020-03-26 | 2021-09-30 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2021198213A1 (de) | 2020-04-02 | 2021-10-07 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2021204646A1 (de) | 2020-04-06 | 2021-10-14 | Merck Patent Gmbh | Polycyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002772A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022002771A1 (de) | 2020-06-29 | 2022-01-06 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022029096A1 (de) | 2020-08-06 | 2022-02-10 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038065A1 (de) | 2020-08-18 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022038066A1 (de) | 2020-08-19 | 2022-02-24 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022069421A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen einsetzbare verbindungen |
| WO2022069422A1 (de) | 2020-09-30 | 2022-04-07 | Merck Patent Gmbh | Verbindungen zur strukturierung von funktionalen schichten organischer elektrolumineszenzvorrichtungen |
| WO2022079067A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Verbindungen mit heteroatomen für organische elektrolumineszenzvorrichtungen |
| WO2022079068A1 (de) | 2020-10-16 | 2022-04-21 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022101171A1 (de) | 2020-11-10 | 2022-05-19 | Merck Patent Gmbh | Schwefelhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022117473A1 (de) | 2020-12-02 | 2022-06-09 | Merck Patent Gmbh | Heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022122682A2 (de) | 2020-12-10 | 2022-06-16 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022129116A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Indolo[3.2.1-jk]carbazole-6-carbonitril-derivate als blau fluoreszierende emitter zur verwendung in oleds |
| WO2022129113A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022129114A1 (de) | 2020-12-18 | 2022-06-23 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| EP4676208A2 (de) | 2020-12-18 | 2026-01-07 | Merck Patent GmbH | Stickstoffhaltige heteroaromaten für organische elektrolumineszenzvorrichtungen |
| WO2022148717A1 (de) | 2021-01-05 | 2022-07-14 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022157343A1 (de) | 2021-01-25 | 2022-07-28 | Merck Patent Gmbh | Stickstoffhaltige verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022184601A1 (de) | 2021-03-02 | 2022-09-09 | Merck Patent Gmbh | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022194799A1 (de) | 2021-03-18 | 2022-09-22 | Merck Patent Gmbh | Heteroaromatische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022229298A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229126A1 (de) | 2021-04-29 | 2022-11-03 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2022229234A1 (de) | 2021-04-30 | 2022-11-03 | Merck Patent Gmbh | Stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2022200638A1 (de) | 2021-07-06 | 2022-09-29 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023041454A1 (de) | 2021-09-14 | 2023-03-23 | Merck Patent Gmbh | Borhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023052314A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052313A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052272A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023052275A1 (de) | 2021-09-28 | 2023-04-06 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023072799A1 (de) | 2021-10-27 | 2023-05-04 | Merck Patent Gmbh | Bor- und stickstoffhaltige, heterocyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023094412A1 (de) | 2021-11-25 | 2023-06-01 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023110742A1 (de) | 2021-12-13 | 2023-06-22 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023117837A1 (de) | 2021-12-21 | 2023-06-29 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023152063A1 (de) | 2022-02-09 | 2023-08-17 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2023152346A1 (de) | 2022-02-14 | 2023-08-17 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2023161167A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023161168A1 (de) | 2022-02-23 | 2023-08-31 | Merck Patent Gmbh | Aromatische heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2023213837A1 (de) | 2022-05-06 | 2023-11-09 | Merck Patent Gmbh | Cyclische verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2023222559A1 (de) | 2022-05-18 | 2023-11-23 | Merck Patent Gmbh | Verfahren zur herstellung von deuterierten organischen verbindungen |
| WO2023247338A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Organische heterocyclen für photoelektrische vorrichtungen |
| WO2023247345A1 (de) | 2022-06-20 | 2023-12-28 | Merck Patent Gmbh | Heterocyclen für photoelektrische vorrichtungen |
| WO2024013004A1 (de) | 2022-07-11 | 2024-01-18 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024061942A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024061948A1 (de) | 2022-09-22 | 2024-03-28 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024094592A2 (de) | 2022-11-01 | 2024-05-10 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024132993A1 (de) | 2022-12-19 | 2024-06-27 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024133048A1 (en) | 2022-12-20 | 2024-06-27 | Merck Patent Gmbh | Method for preparing deuterated aromatic compounds |
| WO2024149694A1 (de) | 2023-01-10 | 2024-07-18 | Merck Patent Gmbh | Stickstoffhaltige heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024153568A1 (de) | 2023-01-17 | 2024-07-25 | Merck Patent Gmbh | Heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2024184050A1 (de) | 2023-03-07 | 2024-09-12 | Merck Patent Gmbh | Cyclische stickstoffverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2024194264A1 (de) | 2023-03-20 | 2024-09-26 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2024218109A1 (de) | 2023-04-20 | 2024-10-24 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2024240725A1 (de) | 2023-05-25 | 2024-11-28 | Merck Patent Gmbh | Tris[1,2,4]triazolo[1,5-a:1',5'-c:1'',5''-e][1,3,5]triazin-derivate zur verwendung in organischen elektrolumineszenzvorrichtungen |
| WO2024256357A1 (de) | 2023-06-12 | 2024-12-19 | Merck Patent Gmbh | Organische heterocyclen für photoelektrische vorrichtungen |
| WO2025003084A1 (de) | 2023-06-28 | 2025-01-02 | Merck Patent Gmbh | Dicyanoarylverbindungen für organische elektrolumineszenzvorrichtungen |
| EP4486099A1 (de) | 2023-06-30 | 2025-01-01 | Merck Patent GmbH | Verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025021855A1 (de) | 2023-07-27 | 2025-01-30 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen und organische sensoren |
| WO2025045843A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045842A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045851A1 (de) | 2023-08-30 | 2025-03-06 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2025045935A1 (de) | 2023-08-31 | 2025-03-06 | Merck Patent Gmbh | Cyanogruppen-enthaltende aromaten für organische elektrolumineszenzvorrichtungen |
| WO2025109056A1 (de) | 2023-11-24 | 2025-05-30 | Merck Patent Gmbh | Sauerstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025132547A1 (en) | 2023-12-21 | 2025-06-26 | Merck Patent Gmbh | Mechanochemical method for deuterating organic compounds |
| WO2025132551A1 (de) | 2023-12-22 | 2025-06-26 | Merck Patent Gmbh | Materialien für elektronische vorrichtungen |
| WO2025181097A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende heterocyclen für organische elektrolumineszenzvorrichtungen |
| WO2025181044A1 (de) | 2024-02-29 | 2025-09-04 | Merck Patent Gmbh | Stickstoffenthaltende verbindungen für organische elektrolumineszenzvorrichtungen |
| WO2025181124A1 (de) | 2024-03-01 | 2025-09-04 | Merck Patent Gmbh | Materialien für organische elektrolumineszenzvorrichtungen |
| WO2025210013A1 (de) | 2024-04-04 | 2025-10-09 | Merck Patent Gmbh | Verbindungen für elektronische vorrichtungen, insbesondere verbindungen für oleds |
| WO2026008710A1 (de) | 2024-07-05 | 2026-01-08 | Merck Patent Gmbh | Cyclische siliciumverbindungen für organische elektrolumineszenzvorrichtungen |
| WO2026022016A1 (de) | 2024-07-22 | 2026-01-29 | Merck Patent Gmbh | Materialien für organische lichtemittierende vorrichtungen |
| WO2026041632A1 (de) | 2024-08-21 | 2026-02-26 | Merck Patent Gmbh | Heterocyclische materialien für organische lichtemittierende vorrichtungen |
Also Published As
| Publication number | Publication date |
|---|---|
| TW201134819A (en) | 2011-10-16 |
| JP2013511476A (ja) | 2013-04-04 |
| DE112010004482A5 (de) | 2012-10-11 |
| KR101781235B1 (ko) | 2017-09-22 |
| CN102612518A (zh) | 2012-07-25 |
| US9012599B2 (en) | 2015-04-21 |
| JP6009356B2 (ja) | 2016-10-19 |
| US20120232241A1 (en) | 2012-09-13 |
| DE102009053836A1 (de) | 2011-05-26 |
| KR20120095997A (ko) | 2012-08-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP2935276B1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| EP3180411B1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| DE102010019306B4 (de) | Organische Elektrolumineszenzvorrichtungen | |
| WO2011060867A1 (de) | Stickstoffhaltige kondensierte heterozyklen für oleds | |
| EP3016952B1 (de) | Spirokondensierte lactamverbindungen für organische elektrolumineszenzvorrichtungen | |
| EP2699571A2 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| WO2011042107A2 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| EP2780325A1 (de) | Spiro -dihydroacridinderivate und ihre verwendung als materialien für organische elektrolumineszenzvorrichtungen | |
| WO2016015810A1 (de) | Materialien f?r organische elektrolumineszenzvorrichtungen | |
| DE102010005697A1 (de) | Verbindungen für elektronische Vorrichtungen | |
| WO2012048781A1 (de) | Materialien auf basis von triphenylen für organische elektrolumineszenzvorrichtungen | |
| WO2011116865A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| WO2011128017A1 (de) | Überbrückte triarylamine und -phosphine als materialien für elektronische vorrichtungen | |
| WO2013056776A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| WO2011107186A2 (de) | Verbindungen für elektronische vorrichtungen | |
| EP2828266A1 (de) | 9,9'-spirobixanthenderivate für elektrolumineszenzvorrichtungen | |
| WO2012048780A1 (de) | Verbindungen für elektronische vorrichtungen | |
| EP2737554A1 (de) | Verbindungen für elektronische vorrichtungen | |
| WO2013041176A1 (de) | Carbazolderivate für organische elektrolumineszenzvorrichtungen | |
| WO2012016630A1 (de) | Materialien für elektronische vorrichtungen | |
| WO2011057701A1 (de) | Organische verbindungen für elektroluminiszenz vorrichtungen | |
| EP3218368A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| WO2011157346A1 (de) | Verbindungen für elektronische vorrichtungen | |
| EP3110796A1 (de) | Materialien für organische elektrolumineszenzvorrichtungen | |
| EP2697225A1 (de) | Materialien für elektronische vorrichtungen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| WWE | Wipo information: entry into national phase |
Ref document number: 201080052364.4 Country of ref document: CN |
|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 10771021 Country of ref document: EP Kind code of ref document: A1 |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 13510425 Country of ref document: US |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2012539209 Country of ref document: JP Ref document number: 112010004482 Country of ref document: DE Ref document number: 1120100044821 Country of ref document: DE |
|
| ENP | Entry into the national phase |
Ref document number: 20127015799 Country of ref document: KR Kind code of ref document: A |
|
| REG | Reference to national code |
Ref country code: DE Ref legal event code: R225 Ref document number: 112010004482 Country of ref document: DE Effective date: 20121011 |
|
| 122 | Ep: pct application non-entry in european phase |
Ref document number: 10771021 Country of ref document: EP Kind code of ref document: A1 |