이하, 본 명세서에 대하여 더욱 상세하게 설명한다.
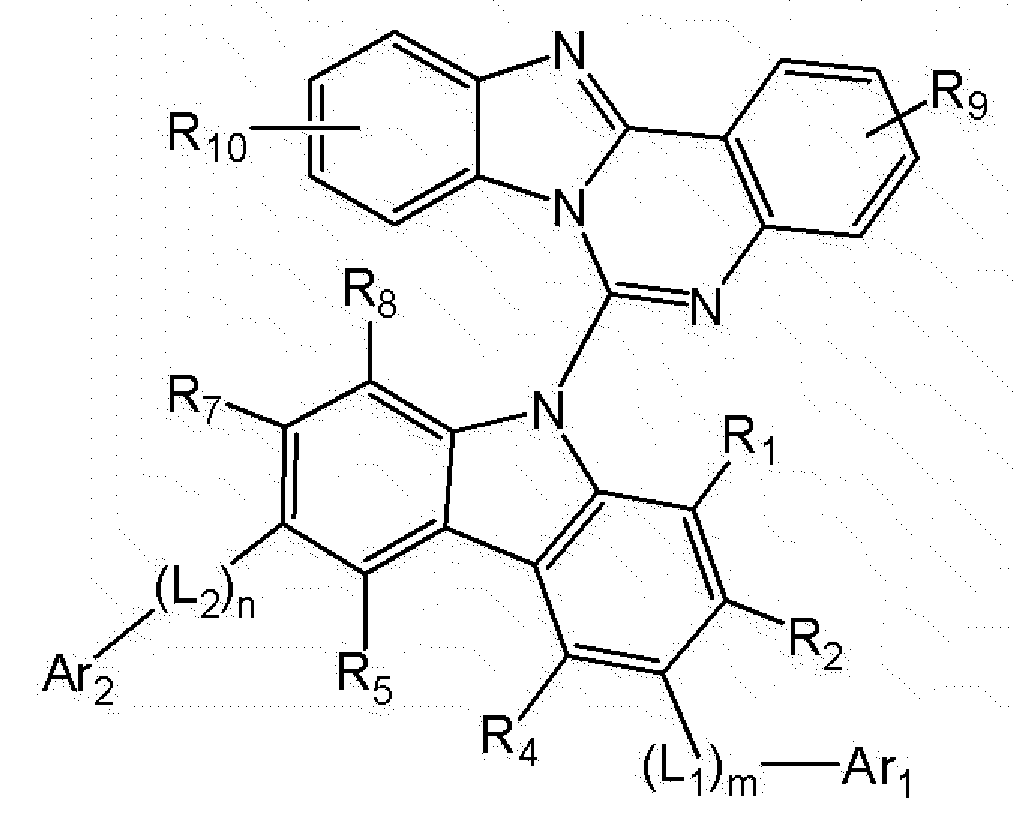
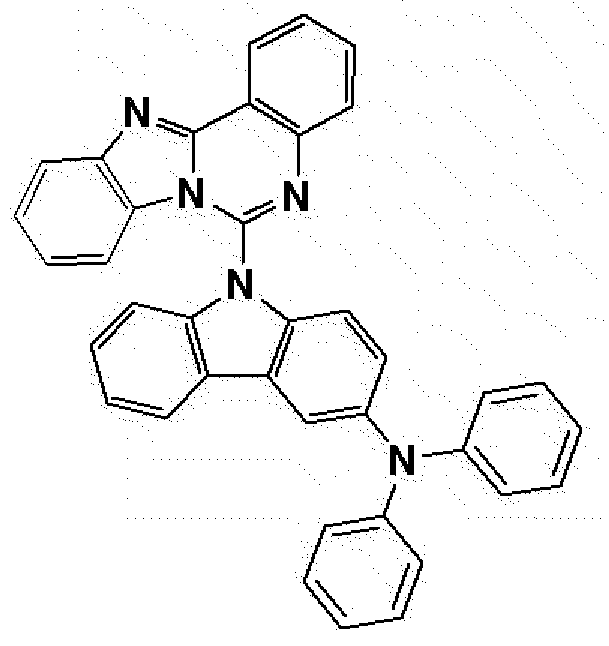
본 명세서는 상기 화학식 1로 표시되는 화합물를 제공한다.
본 출원의 일 실시상태에 따르면, 상기 화학식 1의 화합물은 이미다조퀴나졸린기와 카바졸기가 직접연결된 코어 구조를 가짐으로써 컨쥬게이션(conjugation)을 제한하는 역할을 한다. 화합물의 컨쥬게이션 길이와 에너지 밴드갭은 밀접한 관계가 있다. 구체적으로, 화합물의 컨쥬게이션 길이가 길수록 에너지 밴드갭이 작아진다. 전술한 바와 같이, 상기 화학식 1의 화합물의 코어는 제한된 컨쥬게이션을 포함하고 있으므로, 에너지 밴드 갭이 큰 성질을 갖는다. 통상 에너지 밴드 갭이 큰 코어 구조에 치환기를 도입하여 에너지 밴드 갭을 조절하는 것은 용이하나, 코어 구조가 에너지 밴드 갭이 작은 경우에는 치환기를 도입하여 에너지 밴드 갭을 크게 조절하기 어렵다. 이러한 관점에서, 상기 화학식 1의 화합물은 밴드 갭이 큰 구조를 가지므로, 밴드 갭의 조절이 용이하며, 예컨대 화학식 1의 R1 내지 R8 위치에 다양한 치환기를 도입함으로써 다양한 에너지 밴드 갭을 갖는 화합물을 합성할 수 있다. 따라서, 상기 화학식 1의 R1 내지 R8 및 다양한 치환기를 도입함으로써 화합물의 HOMO 및 LUMO 에너지 준위도 조절할 수 있다.
예컨대, 유기발광소자 제조시 사용되는 정공주입층 물질, 정공수송층 물질, 발광층 물질, 전자 수송층 물질에 주로 사용되는 치환기를 상기 코어구조에 도입함으로써 각 유기물층에서 요구하는 조건들을 충족시키는 물질을 합성할 수 있다. 예컨대, 상기 화학식 1이 코어 구조에 아릴 아민 구조를 포함하고 있으면, 유기 발광 소자에서 정공주입 및/또는 정공수송 물질로서의 적절한 에너지 준위를 가질 수 있다. 따라서, 본 출원에서는 상기 화학식 1의 화합물 중 치환기에 따라 적절한 에너지 준위를 갖는 화합물을 선택하여 유기 발광 소자에 사용함으로써 구동 전압이 낮고 광효율이 높은 소자를 구현할 수 있다.
또한, 상기 코어구조에 다양한 치환기를 대칭 또는 비대칭으로 도입함으로써 에너지 밴드 갭을 미세하게 조절이 가능하게 하며, 한편으로 유기물 사이에서의 계면에서의 특성을 향상되게 하며 물질의 용도를 다양하게 할 수 있다.
또한, 상기 화학식 1의 화합물은 안정한 산화 환원 특성을 나타낸다. 산화 환원에 대한 안정성은 CV(cyclovoltammetry) 방법을 이용하여 확인할 수 있다. 구체적인 예로서, 상기 화학식 1의 화합물은 여러 번의 반복 산화 전압을 가하였을 때 동일한 전압에서 산화가 일어나고 같은 전류 양을 보이는 것으로 나타났으며, 이것은 상기 화합물이 산화에 대한 안정성이 우수함을 나타낸다.
한편, 상기 화학식 1의 화합물은 유리 전이 온도(Tg)가 높아 열적 안정성이 우수하다. 예컨대, 화학식 1의 화합물은 유리 전이온도가 131℃로서, 기존에 일반적으로 사용되던 NPB(Tg: 96℃)에 비해 현저히 높음을 알 수 있다. 이러한 열적 안정성의 증가는 소자에 구동 안정성을 제공하는 중요한 요인이 된다.
또한, 상기 화학식 1의 화합물은 소자의 제조 공정 중 이용되는 용매, 예를 들어 자일렌, 디클로로 에탄, 혹은 NMP등과 같은 극성 용매등에 대한 용해도가 매우 우수하고, 용액을 이용한 방법을 통한 박막 형성에 용이한 특성을 가진다. 이에 따라, 제조 시 진공 증착법 뿐만 아니라 용액 도포법을 사용할 수 있다. 여기서, 용액 도포법이라 함은 스핀코팅, 딥코팅, 잉크젯프린팅, 스크린 프린팅, 스프레이법, 롤 코팅 등을 의미하지만, 이들만으로 한정되는 것은 아니다. 통상 용액 도포법에 의해 형성된 박막이나 고체 상태에서의 발광파장은 분자간 상호 작용에 의해 용액 상태의 발광 파장에 비해 장파장으로 이동하는 것을 흔히 볼 수 있는데, 상기 화학식 1의 화합물과 같은 구조를 갖는 화합물에서는 상기와 같은 파장의 이동이 거의 나타나지 않는 장점이 있다.
본 명세서에서 치환기의 예시들은 아래에서 설명하나, 이에 한정되는 것은 아니다.
상기 "치환"이라는 용어는 화합물의 탄소 원자에 결합된 수소 원자가 다른 치환기로 바뀌는 것을 의미하며, 치환되는 위치는 수소 원자가 치환되는 위치 즉, 치환기가 치환 가능한 위치라면 한정하지 않으며, 2 이상 치환되는 경우, 2 이상의 치환기는 서로 동일하거나 상이할 수 있다.
본 명세서에서 "치환 또는 비치환된" 이라는 용어는 중수소; 할로겐기; 시아노기; 니트로기; 히드록시기; 게르마늄기; 알킬기; 시클로알킬기; 알케닐기; 아민기; 실릴기; 포스포릴기; 아릴기; 및 헤테로고리기로 이루어진 군에서 선택된 1 또는 2 이상의 치환기로 치환되었거나 상기 예시된 치환기 중 2 이상의 치환기가 연결된 치환기로 치환되거나, 또는 어떠한 치환기도 갖지 않는 것을 의미한다. 예컨대, "2 이상의 치환기가 연결된 치환기"는 비페닐기일 수 있다. 즉, 비페닐기는 아릴기일 수도 있고, 2개의 페닐기가 연결된 치환기로 해석될 수 있다.
본 명세서에 있어서, 할로겐기의 예로는 불소, 염소, 브롬 또는 요오드가 있다.
본 명세서에 있어서, 에스테르기의 탄소수는 특별히 한정되지 않으나, 탄소수 1 내지 50인 것이 바람직하다. 구체적으로, 하기 구조식의 화합물이 될 수 있으나, 이에 한정되는 것은 아니다.
본 명세서에서 카보닐기의 탄소수는 특별히 한정되지 않으나, 탄소수 1 내지 50인 것이 바람직하다. 구체적으로 하기와 같은 구조의 화합물이 될 수 있으나, 이에 한정되는 것은 아니다.
본 명세서에 있어서, 상기 알킬기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나 1 내지 50인 것이 바람직하다. 구체적인 예로는 메틸기, 에틸기, 프로필기, n-프로필기, 이소프로필기, 부틸기, n-부틸기, 이소부틸기, tert-부틸기, sec-부틸기, 1-메틸-부틸기, 1-에틸-부틸기, 펜틸기, n-펜틸기, 이소펜틸기, 네오펜틸기, tert-펜틸기, 헥실기, n-헥실기, 1-메틸펜틸기, 2-메틸펜틸기, 4-메틸-2-펜틸기, 3,3-디메틸부틸기, 2-에틸부틸기, 헵틸기, n-헵틸기, 1-메틸헥실기, 시클로펜틸메틸기, 시클로헥실메틸기, 옥틸기, n-옥틸기, tert-옥틸기, 1-메틸헵틸기, 2-에틸헥실기, 2-프로필펜틸기, n-노닐기, 2,2-디메틸헵틸기, 1-에틸-프로필기, 1,1-디메틸-프로필기, 이소헥실기, 2-메틸펜틸기, 4-메틸헥실기, 5-메틸헥실기 등이 있으나, 이들에 한정되지 않는다.
본 명세서에 있어서, 시클로알킬기는 특별히 한정되지 않으나, 탄소수 3 내지 60인 것이 바람직하며, 구체적으로 시클로프로필기, 시클로부틸기, 시클로펜틸기, 3-메틸시클로펜틸기, 2,3-디메틸시클로펜틸기, 시클로헥실기, 3-메틸시클로헥실기, 4-메틸시클로헥실기, 2,3-디메틸시클로헥실기, 3,4,5-트리메틸시클로헥실기, 4-tert-부틸시클로헥실기, 시클로헵틸기, 시클로옥틸기 등이 있으나, 이에 한정되지 않는다.
본 명세서에 있어서, 상기 알콕시기는 직쇄, 분지쇄 또는 고리쇄일 수 있다. 알콕시기의 탄소수는 특별히 한정되지 않으나, 탄소수 1 내지 20인 것이 바람직하다. 구체적으로, 메톡시기, 에톡시기, n-프로폭시기, 이소프로폭시기, i-프로필옥시기, n-부톡시기, 이소부톡시기, tert-부톡시기, sec-부톡시기, n-펜틸옥시기, 네오펜틸옥시기, 이소펜틸옥시기, n-헥실옥시기, 3,3-디메틸부틸옥시기, 2-에틸부틸옥시기, n-옥틸옥시기, n-노닐옥시기, n-데실옥시기, 벤질옥시기, p-메틸벤질옥시기 등이 될 수 있으나, 이에 한정되는 것은 아니다.
본 명세서에 있어서, 상기 알케닐기는 직쇄 또는 분지쇄일 수 있고, 탄소수는 특별히 한정되지 않으나, 2 내지 40인 것이 바람직하다. 구체적인 예로는 비닐기, 1-프로페닐기, 이소프로페닐기, 1-부테닐기, 2-부테닐기, 3-부테닐기, 1-펜테닐기, 2-펜테닐기, 3-펜테닐기, 3-메틸-1-부테닐기, 1,3-부타디에닐기, 알릴기, 1-페닐비닐-1-일기, 2-페닐비닐-1-일기, 2,2-디페닐비닐-1-일기, 2-페닐-2-(나프틸-1-일)비닐-1-일기, 2,2-비스(디페닐-1-일)비닐-1-일기, 스틸베닐기, 스티레닐기 등이 있으나 이들에 한정되지 않는다.
본 명세서에서 상기 아릴기가 단환식 아릴기인 경우 탄소수는 특별히 한정되지 않으나, 탄소수 6 내지 25인 것이 바람직하다. 구체적으로 단환식 아릴기로는 페닐기, 비페닐기, 터페닐기 등이 될 수 있으나, 이에 한정되는 것은 아니다.
상기 아릴기가 다환식 아릴기인 경우 탄소수는 특별히 한정되지 않으나. 탄소수 10 내지 24인 것이 바람직하다. 구체적으로 다환식 아릴기로는 나프틸기, 안트라세닐기, 페난트릴기, 파이레닐기, 페릴레닐기, 크라이세닐기, 플루오레닐기 등이 될 수 있으나, 이에 한정되는 것은 아니다.
본 명세서에 있어서, 상기 플루오레닐기는 치환될 수 있으며, 인접한 치환기들이 서로 결합하여 고리를 형성할 수 있다.
상기 플루오레닐기가 치환되는 경우,
,
,
,
,
,
등이 될 수 있으나, 이에 한정되는 것은 아니다.
본 명세서에 있어서, 헤테로고리기는 탄소가 아닌 원자, 이종원자를 1 이상 포함하는 것으로서, 구체적으로 상기 이종 원자는 O, N, Se 및 S 등으로 이루어진 군에서 선택되는 원자를 1 이상 포함할 수 있다. 헤테로고리기의 탄소수는 특별히 한정되지 않으나, 탄소수 2 내지 60인 것이 바람직하다. 헤테로고리기의 예로는 티오페닐기, 퓨라닐기, 피롤기, 이미다졸릴기, 티아졸릴기, 옥사졸릴기, 옥사디아졸릴기, 트리아졸릴기, 피리딜기, 비피리딜기, 피리미딜기, 트리아지닐기, 아크리딜기, 피리다지닐기, 피라지닐기, 퀴놀리닐기, 퀴나졸리닐기, 퀴녹살리닐기, 프탈라지닐기, 피리도피리미디닐기, 피리도피라지닐기, 피라지노피라지닐기, 이소퀴놀리닐기, 인돌기, 카바졸릴기, 벤즈옥사졸릴기, 벤즈이미다졸릴기, 벤조티아졸릴기, 벤조카바졸릴기, 디벤조카바졸릴기, 벤조티오페닐기, 디벤조티오페닐기, 벤조퓨라닐기, 페난트롤리닐기(phenanthrolinyl group), 티아졸릴기, 이소옥사졸릴기, 옥사디아졸릴기, 티아디아졸릴기, 벤조티아졸릴기, 페노티아지닐기, 페노옥사지닐기, 디벤조퓨란기 및 이들의 축합구조 등이 있으나, 이들에만 한정되는 것은 아니다. 이외에도 헤테로고리기의 예로서, 술포닐기를 포함하는 헤테로고리 구조, 예컨대,
등이 있다.
본 명세서에 있어서, 상기 축합구조는 해당 치환기에 방향족 탄화수소 고리가 축합된 구조일 수 있다. 예컨대, 벤즈이미다졸의 축합고리로서
,
,
등이 될 수 있으나, 이에 한정되는 것은 아니다.
본 명세서에 있어서, "인접한" 기는 해당 치환기가 치환된 원자와 직접 연결된 원자에 치환된 치환기, 해당 치환기와 입체구조적으로 가장 가깝게 위치한 치환기, 또는 해당 치환기가 치환된 원자에 치환된 다른 치환기를 의미할 수 있다. 예컨대, 벤젠고리에서 오쏘(ortho)위치로 치환된 2개의 치환기 및 지방족 고리에서 동일 탄소에 치환된 2개의 치환기는 서로 "인접한" 기로 해석될 수 있다.
본 명세서에 있어서, 인접한 기가 서로 결합하여 고리를 형성하는 것의 의미는 전술한 바와 같이 인접한 기가 서로 결합하여, 5원 내지 8원의 탄화수소 고리 또는 5원 내지 8원의 헤테로고리를 형성하는 것을 의미하며, 단환 또는 다환일 수 있으며, 지방족, 방향족 또는 이들의 축합된 형태일 수 있으며 이를 한정하지 않는다.
본 명세서에서 탄화수소고리 또는 헤테로고리는 1 가기인 것을 제외하고, 전술한 시클로알킬기, 아릴기 또는 헤테로고리기의 예시 중에서 선택될 수 있으며, 단환 또는 다환, 지방족 또는 방향족 또는 이들의 축합된 형태일 수 있으나. 이들에만 한정되는 것은 아니다.
본 명세서에서 아민기는 아미노기(-NH2)의 적어도 하나의 수소 원자가 다른 치환체로 치환된 1가의 아민을 의미한다. 예컨대, 상기 아민기는 -NR100R101로 표시되고, R100 및 R101은 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 할로겐기; 알킬기; 알케닐기; 알콕시기; 시클로알킬기; 아릴기; 및 헤테로고리기 중 적어도 하나로 이루어진 치환기일 수 있다(단, R100 및 R101 중 적어도 하나는 수소가 아니다). 예컨대, 상기 아민기가 치환체로 알킬기 및 아릴기를 가지는 경우의 구체적인 예로는 디페닐아민기, 비페닐비페닐아민기, 페닐비페닐아민기, 페닐터페닐아민기, 페닐플루오레닐아민, 페닐(디메틸플루오레닐)아민기, 비페닐(디메틸플루오레닐)아민기 등이 있으나, 이에만 한정되는 것은 아니다.
본 명세서에서 포스포릴기는 P(=O)를 포함하고 상기 P 원자가 라디칼로서 직접 연결되는 치환기이며, -P(=O)R102R103로 표시되고, R102 및 R103은 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 할로겐기; 알킬기; 알케닐기; 알콕시기; 시클로알킬기; 아릴기; 및 헤테로고리기 중 적어도 하나로 이루어진 치환기일 수 있다. 예컨대, 상기 포스포릴기가 치환체로 아릴기를 가지는 경우의 구체적인 예로는 디페닐포스포릴기, 페닐비페닐포스포릴기, 비페닐비페닐포스포릴기, 페닐터페닐포스포릴기, 비페닐터페닐포스포릴기 등이 있으나, 이에만 한정되는 것은 아니다.
본 명세서에서 실릴기는 Si를 포함하고 상기 Si 원자가 라디칼로서 직접 연결되는 치환기이며, -SiR104R105R106로 표시되고, R104 내지 R106은 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 할로겐기; 알킬기; 알케닐기; 알콕시기; 시클로알킬기; 아릴기; 및 헤테로고리기 중 적어도 하나로 이루어진 치환기일 수 있다. 예컨대, 상기 실릴기가 치환체로 알킬기를 가지는 경우의 구체적인 예로는 트리메틸실릴기가 있으나, 이에만 한정되는 것은 아니다. 또한, 상기 실릴기가 치환체로 아릴기를 가지는 경우의 구체적인 예로는 트리페닐실릴기가 있으나, 이에만 한정되는 것은 아니다.
본 명세서에 있어서, 게르마늄기는 -GeRaRbRc의 화학식으로 표시될 수 있고, 상기 Ra, Rb 및 Rc는 각각 수소; 치환 또는 비치환된 알킬기; 또는 치환 또는 비치환된 아릴기일 수 있다. 상기 게르마늄기는 구체적으로 트리메틸게르마늄기, 트리에틸게르마늄기, t-부틸디메틸게르마늄기 등이 있으나, 이에 한정되지 않는다.
본 명세서에서 아릴옥시기, 아릴싸이오기 중의 아릴기는 전술한 아릴기에 관한 설명이 적용될 수 있다.
본 명세서에서 아르알킬기 중 알킬기는 전술한 알킬기에 관한 설명이 적용될 수 있다.
본 명세서에서 헤테로아릴기는 방향족인 것을 제외하고는 전술한 헤테로고리기에 관한 설명이 적용될 수 있다.
본 명세서에서 알콕시카보닐기 중 알콕시기는 전술한 알킬기에 관한 설명이 적용되고, 알콕시카보닐기 중 카보닐기는 전술한 카보닐기에 관한 설명이 적용될 수 있다.
본 출원의 일 실시상태에 따르면, R1 내지 R4 중 인접한 하나의 쌍은 서로 결합하여 고리를 형성한다.
본 출원의 일 실시상태에 따르면, R1 내지 R4 중 인접한 하나의 쌍은 서로 결합하여 방향족 탄화수소 고리를 형성한다.
본 출원의 일 실시상태에 따르면, R1 내지 R4 중 인접한 하나의 쌍은 서로 결합하여 방향족 6원고리를 형성한다.
본 출원의 일 실시상태에 따르면, R5 내지 R8 중 인접한 하나의 쌍은 서로 결합하여 고리를 형성한다.
본 출원의 일 실시상태에 따르면, R5 내지 R8 중 인접한 하나의 쌍은 서로 결합하여 방향족 탄화수소 고리를 형성한다.
본 출원의 일 실시상태에 따르면, R5 내지 R8 중 인접한 하나의 쌍은 서로 결합하여 방향족 6원고리를 형성한다.
본 출원의 일 실시상태에 따르면, 상기 화학식 1은 하기 화학식 2 또는 3으로 표시된다.
[화학식 2]
[화학식 3]
상기 화학식 2 및 3에 있어서,
R1 내지 R10은 화학식 1에서 정의한 바와 동일하고,
R11 및 R12는 서로 동일하거나 상이하며, 각각 독립적으로 수소; 중수소; 할로겐기; 니트로기; 시아노기; 에스테르기; 카보닐기; 치환 또는 비치환된 알킬기; 치환 또는 비치환된 시클로알킬기; 치환 또는 비치환된 알콕시기; 치환 또는 비치환된 알케닐기; 치환 또는 비치환된 아릴기; 또는 치환 또는 비치환된 헤테로고리기이고,
p 및 q는 각각 0 내지 4의 정수이다.
본 출원의 일 실시상태에 따르면, 상기 R3는 -(L)m-(Ar)n이다.
본 출원의 일 실시상태에 따르면, 상기 R2는 -(L)m-(Ar)n이다.
본 출원의 일 실시상태에 따르면, 상기 R3 및 R6는 -(L)m-(Ar)n이고, 상기 R3 및 R6는 서로 동일하거나 상이하다.
본 출원의 일 실시상태에 따르면, 상기 R2 및 R7은 -(L)m-(Ar)n이고, 상기 R2 및 R7은 서로 동일하거나 상이하다.
본 출원의 일 실시상태에 따르면, 상기 화학식 1은 하기 화학식 4 내지 7 중 어느 하나로 표시된다.
[화학식 4]
[화학식 5]
[화학식 6]
[화학식 7]
상기 화학식 4 내지 7에 있어서, L, L1 및 L2는 상기 화학식 1의 L의 정의와 동일하고, Ar, Ar1 및 Ar2는 상기 화학식 1의 Ar의 정의와 동일하며, m 및 n은 화학식 1의 m의 정의와 동일하며, R1 내지 R10은 화학식 1에서 정의한 바와 동일하다.
본 출원의 일 실시상태에 따르면, 상기 L은 직접결합 또는 치환 또는 비치환된 아릴렌기이다.
본 출원의 일 실시상태에 따르면, 상기 L은 직접결합; 치환 또는 비치환된 페닐렌기; 치환 또는 비치환된 비페닐렌기; 치환 또는 비치환된 나프틸렌기; 치환 또는 비치환된 안트라세닐렌기; 치환 또는 비치환된 플루오레닐렌기; 치환 또는 비치환된 페난트레닐렌기; 치환 또는 비치환된 파이레닐렌기; 및 치환 또는 비치환된 크라이세닐렌기로 이루어진 군에서 선택된다.
본 출원의 일 실시상태에 따르면, 상기 L은 직접결합; 페닐렌기; 비페닐렌기; 나프틸렌기; 안트라세닐렌기; 플루오레닐렌기; 페난트레닐렌기; 파이레닐렌기; 및 크라이세닐렌기로 이루어진 군에서 선택된다.
본 출원의 일 실시상태에 따르면, 상기 L은 직접결합; 또는 치환 또는 비치환된 페닐렌기이다.
본 출원의 일 실시상태에 따르면, 상기 L은 직접결합; 또는 페닐렌기이다.
본 출원의 일 실시상태에 따르면 m은 1이다.
본 출원의 일 실시상태에 따르면 m은 2이고, 2개의 L은 서로 동일하거나 상이하다.
본 출원의 일 실시상태에 따르면 m은 3이고, 3개의 L은 서로 동일하거나 상이하다.
본 출원의 일 실시상태에 따르면, 상기 L1 및 L2는 전술한 L의 정의와 동일하다.
본 출원의 일 실시상태에 따르면, 상기 Ar은 치환된 단환의 아릴기; 치환 또는 비치환된 다환의 아릴기; 치환 또는 비치환된 헤테로고리기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 실릴기; 또는 치환 또는 비치환된 포스포릴기이다.
본 출원의 일 실시상태에 따르면, 상기 Ar은 치환된 단환의 아릴기; 치환 또는 비치환된 다환의 아릴기; 치환 또는 비치환된 헤테로고리기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 실릴기; 또는 치환 또는 비치환된 포스포릴기이고, 상기 치환 또는 비치환된은 중수소; 할로겐기; 시아노기; C1 내지 C60의 알킬기; C6 내지 C60의 시클로알킬기; C6 내지 C60의 아릴기; 및 C2 내지 C60의 헤테로고리기로 이루어진 군으로부터 선택되는 적어도 하나로 치환 또는 비치환된 것을 의미한다.
본 출원의 일 실시상태에 따르면, 상기 Ar은 치환된 단환의 아릴기; 치환 또는 비치환된 다환의 아릴기; 치환 또는 비치환된 헤테로고리기; 치환 또는 비치환된 아민기; 치환 또는 비치환된 실릴기; 또는 치환 또는 비치환된 포스포릴기이고, 상기 치환 또는 비치환된은 중수소; 할로겐기; C1 내지 C20의 알킬기; 시아노기; C6 내지 C20의 아릴기; 및 C2 내지 C20의 헤테로고리기로 이루어진 군으로부터 선택되는 적어도 하나로 치환 또는 비치환된 것을 의미한다.
본 출원의 일 실시상태에 따르면, 상기 치환된 단환의 아릴기는 중수소; 할로겐기; C1 내지 C20의 알킬기; 시아노기; C6 내지 C20의 아릴기; 및 C2 내지 C20의 헤테로고리기로 이루어진 군으로부터 선택되는 적어도 하나로 치환된 페닐기이다.
본 출원의 일 실시상태에 따르면, 상기 치환된 단환의 아릴기는 중수소; 할로겐기; 메틸기; t-부틸기; 시아노기; 페닐기; 비페닐기; 나프틸기; 안트라세닐기; 페난트레닐기; 피리딜기; 피리미딜기; 및 트리아지닐기로 이루어진 군으로부터 선택되는 적어도 하나로 치환된 페닐기이다.
본 출원의 일 실시상태에 따르면, 상기 다환의 아릴기는 치환 또는 비치환된 나프틸기; 치환 또는 비치환된 안트라세닐기; 치환 또는 비치환된 페난트레닐기; 치환 또는 비치환된 크라이세닐기; 치환 또는 비치환된 파이레닐기; 치환 또는 비치환된 트리페닐레닐기; 또는 치환 또는 비치환된 플루오레닐기이다.
본 출원의 일 실시상태에 따르면, 상기 다환의 아릴기는 치환 또는 비치환된 나프틸기; 치환 또는 비치환된 안트라세닐기; 치환 또는 비치환된 페난트레닐기; 치환 또는 비치환된 크라이세닐기; 치환 또는 비치환된 파이레닐기; 치환 또는 비치환된 트리페닐레닐기; 또는 치환 또는 비치환된 플루오레닐기이고, 상기 치환 또는 비치환된은 중수소; 할로겐기; C1 내지 C20의 알킬기; 시아노기; C6 내지 C20의 아릴기; 및 C2 내지 C20의 헤테로고리기로 이루어진 군으로부터 선택되는 적어도 하나로 치환 또는 비치환된 것을 의미한다.
본 출원의 일 실시상태에 따르면, 상기 다환의 아릴기는 치환 또는 비치환된 나프틸기; 치환 또는 비치환된 안트라세닐기; 치환 또는 비치환된 페난트레닐기; 치환 또는 비치환된 크라이세닐기; 치환 또는 비치환된 파이레닐기; 치환 또는 비치환된 트리페닐레닐기; 또는 치환 또는 비치환된 플루오레닐기이고, 상기 치환 또는 비치환된은 중수소; 할로겐기; 메틸기; t-부틸기; 시아노기; 페닐기; 비페닐기; 나프틸기; 안트라세닐기; 페난트레닐기; 피리딜기; 피리미딜기; 및 트리아지닐기로 이루어진 군으로부터 선택되는 적어도 하나로 치환 또는 비치환된 것을 의미한다.
본 출원의 일 실시상태에 따르면, 상기 헤테로고리기는 치환 또는 비치환된 피리딜기; 치환 또는 비치환된 피리미딜기; 치환 또는 비치환된 트리아지닐기; 치환 또는 비치환된 티오페닐기; 치환 또는 비치환된 퓨라닐기; 치환 또는 비치환된 벤조퓨라닐기; 치환 또는 비치환된 벤조티오페닐기; 치환 또는 비치환된 디벤조퓨라닐기; 치환 또는 비치환된 디벤조티오페닐기; 치환 또는 비치환된 카바졸릴기; 치환 또는 비치환된 벤조카바졸릴기; 치환 또는 비치환된 디벤조카바졸릴기; 치환 또는 비치환된 이미다졸릴기; 치환 또는 비치환된 벤즈이미다졸릴기; 치환 또는 비치환된 디벤즈이미다졸릴기; 치환 또는 비치환된 티아졸릴기; 치환 또는 비치환된 벤조티아졸릴기; 치환 또는 비치환된 옥사졸릴기; 치환 또는 비치환된 벤즈옥사졸릴기; 치환 또는 비치환된 페난트롤리닐기; 치환 또는 비치환된 페노티아지닐기; 치환 또는 비치환된 페노옥사지닐기; 치환 또는 비치환된 퀴놀리닐기; 치환 또는 비치환된 1가의
기; 치환 또는 비치환된 1가의
기; 치환 또는 비치환된 1가의
기; 또는 치환 또는 비치환된 1가의
기 이고, 상기 치환 또는 비치환된은 중수소; 할로겐기; C
1 내지 C
20의 알킬기; 시아노기; C
6 내지 C
20의 아릴기; 및 C
2 내지 C
20의 헤테로고리기로 이루어진 군으로부터 선택되는 적어도 하나로 치환 또는 비치환된 것을 의미한다.
본 출원의 일 실시상태에 따르면, 상기 헤테로고리기는 치환 또는 비치환된 피리딜기; 치환 또는 비치환된 피리미딜기; 치환 또는 비치환된 트리아지닐기; 치환 또는 비치환된 티오페닐기; 치환 또는 비치환된 퓨라닐기; 치환 또는 비치환된 벤조퓨라닐기; 치환 또는 비치환된 벤조티오페닐기; 치환 또는 비치환된 디벤조퓨라닐기; 치환 또는 비치환된 디벤조티오페닐기; 치환 또는 비치환된 카바졸릴기; 치환 또는 비치환된 벤조카바졸릴기; 치환 또는 비치환된 디벤조카바졸릴기; 치환 또는 비치환된 이미다졸릴기; 치환 또는 비치환된 벤즈이미다졸릴기; 치환 또는 비치환된 디벤즈이미다졸릴기; 치환 또는 비치환된 티아졸릴기; 치환 또는 비치환된 벤조티아졸릴기; 치환 또는 비치환된 옥사졸릴기; 치환 또는 비치환된 벤즈옥사졸릴기; 치환 또는 비치환된 페난트롤리닐기; 치환 또는 비치환된 페노티아지닐기; 치환 또는 비치환된 페노옥사지닐기; 치환 또는 비치환된 퀴놀리닐기; 치환 또는 비치환된 1가의
기; 치환 또는 비치환된 1가의
기; 치환 또는 비치환된 1가의
기; 또는 치환 또는 비치환된 1가의
기 이고, 상기 치환 또는 비치환된은 중수소; 할로겐기; 메틸기; t-부틸기; 시아노기; 페닐기; 비페닐기; 나프틸기; 안트라세닐기; 페난트레닐기; 피리딜기; 피리미딜기; 및 트리아지닐기로 이루어진 군으로부터 선택되는 적어도 하나로 치환 또는 비치환된 것을 의미한다.
본 출원의 일 실시상태에 따르면, 상기 Ar1 및 Ar2는 전술한 Ar의 정의와 동일하다.
본 출원의 일 실시상태에 따르면, 상기 아민기는 -NR100R101로 표시되고, 상기 R100 및 R101은 서로 동일하거나 상이하며, 각각 독립적으로 치환 또는 비치환된 C1 내지 C60의 알킬기; 치환 또는 비치환된 C6 내지 C60의 시클로알킬기; 치환 또는 비치환된 C6 내지 C60의 아릴기; 또는 치환 또는 비치환된 C2 내지 C60의 헤테로고리기일 수 있다.
본 출원의 일 실시상태에 따르면, 상기 R100 및 R101은 치환 또는 비치환된 C6 내지 C60의 아릴기이고, R100 및 R101은 서로 동일하거나 상이할 수 있다.
본 출원의 일 실시상태에 따르면, 상기 상기 R100 및 R101은 C1 내지 C60의 알킬기로 치환 또는 비치환된 C6 내지 C60의 아릴기이고, 상기 R100 및 R101은 서로 동일하거나 상이할 수 있다.
본 출원의 일 실시상태에 따르면, 상기 상기 R100 및 R101은 서로 동일하거나 상이하고, 각각 독립적으로 페닐기, 비페닐기, 나프틸기, 터페닐기, 플루오렌기 또는 디메틸 플루오렌기일 수 있다.
본 출원의 일 실시상태에 따르면, 상기 포스포릴기는 -P(=O)R102R103로 표시되고, 상기 R102 및 R103은 서로 동일하거나 상이하며, 각각 독립적으로 치환 또는 비치환된 C1 내지 C60의 알킬기; 치환 또는 비치환된 C6 내지 C60의 시클로알킬기; 치환 또는 비치환된 C6 내지 C60의 아릴기; 또는 치환 또는 비치환된 C2 내지 C60의 헤테로고리기일 수 있다.
본 출원의 일 실시상태에 따르면, 상기 R102 및 R103은 치환 또는 비치환된 C6 내지 C60의 아릴기이고, R102 및 R103은 서로 동일하거나 상이할 수 있다.
본 출원의 일 실시상태에 따르면, 상기 상기 R102 및 R103은 서로 동일하거나 상이하고, 각각 독립적으로 페닐기, 비페닐기, 나프틸기, 터페닐기, 플루오렌기 또는 디메틸 플루오렌기일 수 있다.
본 출원의 일 실시상태에 따르면, 상기 실릴기는 -SiR104R105R106으로 표시되고, 상기 R104 내지 R106은 서로 동일하거나 상이하며, 각각 독립적으로 치환 또는 비치환된 C1 내지 C60의 알킬기; 치환 또는 비치환된 C6 내지 C60의 시클로알킬기; 치환 또는 비치환된 C6 내지 C60의 아릴기; 또는 치환 또는 비치환된 C2 내지 C60의 헤테로고리기일 수 있다.
본 출원의 일 실시상태에 따르면, 상기 R104 내지 R106은 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 C1 내지 C60의 알킬기; 또는 치환 또는 비치환된 C6 내지 C60의 아릴기이다.
본 출원의 일 실시상태에 따르면, 상기 상기 R104 내지 R106은 서로 동일하거나 상이하고, 각각 독립적으로 메틸기, 에틸기, 페닐기, 비페닐기, 나프틸기, 터페닐기, 플루오렌기 또는 디메틸 플루오렌기일 수 있다.
본 출원의 일 실시상태에 따르면, 상기 -(L)m-(Ar)n은 하기 그룹 1 내지 4의 구조식들 중에서 선택되는 어느 하나일 수 있다.
[그룹 1]
[그룹 2]
[그룹 3]
[그룹 4]
상기 그룹 1, 2 및 4에서 "
"는 결합하는 위치를 의미한다.
상기 그룹 2에서 플루오렌기에 치환된 메틸기를 제외한 "
"는 결합하는 위치를 의미한다.
상기 그룹 3에서 플루오렌기에 치환된 메틸기를 제외한 "
"는 결합하는 위치를 의미한다. 즉, N에 연결된 "
"는 결합하는 위치를 의미한다.
본 출원의 일 실시상태에 따르면 n은 1이다.
본 출원의 일 실시상태에 따르면 n은 2이고, 2개의 Ar은 서로 동일하거나 상이하다.
본 출원의 일 실시상태에 따르면, 상기 화학식 1로 표시되는 화합물은 하기 구조식들 중에서 선택되는 어느 하나일 수 있다.
본 출원의 일 실시상태에 따른 화합물은 후술하는 제조 방법으로 제조될 수 있다.
예컨대, 상기 화학식 1의 화합물은 하기 일반식 1 내지 6과 같이 코어 구조가 제조될 수 있다. 치환기는 당기술분야에 알려져 있는 방법에 의하여 결합될 수 있으며, 치환기의 종류, 위치 또는 개수는 당기술분야에 알려져 있는 기술에 따라 변경될 수 있다.
[일반식 1]
[일반식 2]
[일반식 3]
[일반식 4]
[일반식 5]
[일반식 6]
상기 일반식 1 내지 6에서 제조된 코어에서 Br의 위치가 상기 -(L)m-Ar로 치환되는 위치일 수 있다.
전술한 바와 같이, 치환기는 당기술분야에 알려져 있는 방법에 의하여 결합될 수 있으며, 치환기의 종류, 위치 또는 개수는 당기술분야에 알려져 있는 기술에 따라 변경될 수 있다. 예컨대, 하기 일반식 7 내지 9에 의하여 아민기, 아릴기, 헤테로고리기 등의 치환기를 연결할 수 있다.
[일반식 7]
[일반식 8]
[일반식 9]
상기 일반식 7은 부끄발드 아미네이션(Buchwald amination)을 이용하여 아민, 아릴아민 등의 치환체를 연결하는 반응식을 나타낸 것이다. 여기서, 상기 Ar은 수소 또는 추가의 치환기를 의미한다.
상기 일반식 8 및 9는 보릴레이션 방법 및 스즈키커플링(Suzuki coupling)을 이용하여 아릴기, 헤테로고리기 등의 치환체를 연결하는 반응식을 나타낸 것이다. 특히, 상기 일반식 9는 단환의 아릴기 또는 단환의 N함유 헤테로고리기의 치환체를 연결하는 반응식을 나타낸 것이다. 상기 X1 내지 X3는 탄소 또는 질소이며, 상기 Ar은 수소 또는 추가의 치환기를 의미한다.
상기 일반식 1 내지 9는 본 출원의 일 실시상태에 따른 화합물의 코어 구조를 제조하고, 치환체를 연결하는 방법의 예들일 뿐, 이에만 한정되는 것은 아니다.
또한, 본 명세서는 상기 전술한 화합물을 포함하는 유기 전자 소자를 제공한다.
본 출원의 일 실시상태에 있어서, 제1 전극; 상기 제1 전극과 대향하여 구비된 제2 전극; 및 상기 제1 전극과 상기 제2 전극 사이에 구비된 1층 이상의 유기물층을 포함하는 유기 전자 소자로서, 상기 유기물층 중 1 층 이상은 상기 화합물을 포함하는 것인 유기 전자 소자를 제공한다.
본 명세서의 일 실시상태는 상기 유기물층 중 1층 이상은 상기 화학식 1로 표시되는 화합물을 포함하고, 하기 화학식 4의 화합물을 포함하는 발광층을 포함하는 것인 유기 전자 소자이다,
[화학식 4]
상기 화학식 4에 있어서,
Ar3는 벤조플루오렌 골격, 플루오란텐 골격, 피렌 골격 또는 크리센 골격이고,
L3는 단일결합, C6 내지 C30의 아릴렌기 또는 C5 내지 C30의 2가의 헤테로고리기이며,
X1 및 X2는 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 C6 내지 C30의 아릴기, 치환 또는 비치환된 C5 내지 C30의 헤테로 고리기, 치환 또는 비치환된 C1 내지 C30의 알킬기 및 치환 또는 비치환된 C7 내지 C30의 아르알킬기로 이루어진 군에서 선택되고, X1 및 X2는 서로 결합하여 포화 또는 불포화 고리를 형성할 수 있고,
r은 1 이상의 정수이며,
상기 r이 2 이상인 경우, X1은 서로 동일하거나 상이하고, X2는 서로 동일하거나 상이하다.
본 명세서의 일 실시상태에 있어서, 상기 L3는 단일결합 또는 C6 내지 C30의 아릴렌기이다.
또 하나의 일 실시상태에 있어서, 상기 L3는 단일결합이다.
본 명세서의 일 실시상태에 있어서, 상기 Ar3는 벤조플루오렌 골격, 플루오란텐 골격 또는 피렌골격이다.
또 하나의 일 실시상태에 있어서, 상기 Ar3는 피렌골격이다.
본 명세서의 일 실시상태에 있어서, 상기 X1 및 X2는 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 C6 내지 C30의 아릴기, 치환 또는 비치환된 C5 및 C30의 헤테로 고리기 또는 치환 또는 비치환된 C1 내지 C30의 알킬기이다.
또 하나의 일 실시상태에 있어서, 상기 X1 및 X2는 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 C6 내지 C30의 아릴기이다.
또 하나의 일 실시상태에 있어서, 상기 X1 및 X2는 서로 동일하거나 상이하고, 각각 독립적으로 게르마늄기로 치환 또는 비치환된 페닐기이다.
또 하나의 일 실시상태에 있어서, 상기 X1 및 X2는 서로 동일하거나 상이하고, 각각 독립적으로 트리메틸게르마늄기로 치환 또는 비치환된 페닐기이다.
본 명세서의 일 실시상태에 있어서, 상기 Ar3는 피렌 골격이고, L3는 단일결합이며, X1 및 X2는 서로 동일하거나 상이하고, 각각 독립적으로 게르마늄기로 치환 또는 비치환된 아릴기이고, r이 2인 유기 전자 소자이다.
또 하나의 일 실시상태에 있어서, 상기 Ar3는 피렌 골격이고 L3는 단일결합이며, X1은 페닐기이고, X2는 트리메틸게르마늄기로 치환된 페닐기이고, r은 2인 유기 전자 소자이다.
본 명세서의 일 실시상태에 있어서, 상기 화학식 4의 화합물을 발광층의 도펀트로 포함될 수 있다.
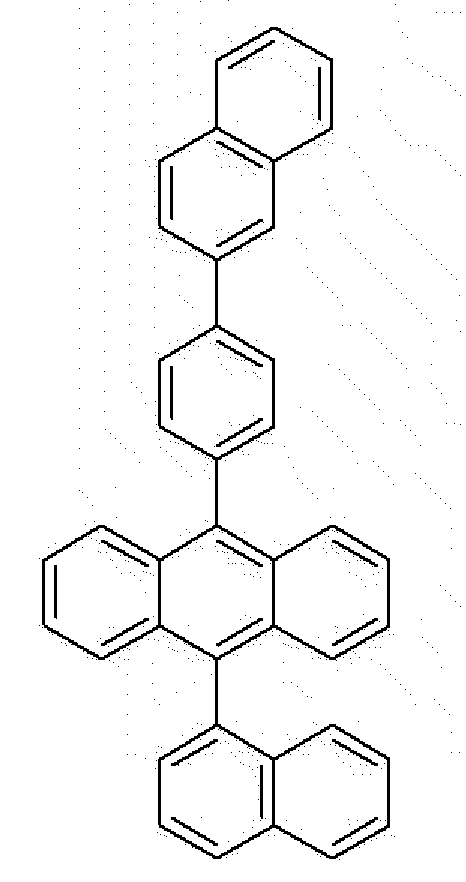
본 명세서의 일 실시상태는 상기 유기물층 중 1층 이상은 상기 화학식 1로 표시되는 화합물을 포함하고, 하기 화학식 5의 화합물을 상기 유기물층 중 발광층에 포함하는 것인 유기 전자 소자이다.
[화학식 5]
상기 화학식 5에 있어서,
X
5는 치환 또는 비치환된 1-나프틸기, 치환 또는 비치환된 2-나프틸기, 치환 또는 비치환된 1-안트릴기, 치환 또는 비치환된 2-안트릴기, 치환 또는 비치환된 1-페난트릴기, 치환 또는 비치환된 2-페난트릴기, 치환 또는 비치환된 3-페난트릴기, 치환 또는 비치환된 4-페난트릴기, 치환 또는 비치환된 9-페난트릴기, 치환 또는 비치환된 1-나프타센일기, 치환 또는 비치환된 2-나프타센일기, 치환 또는 비치환된 9-나프타센일기, 치환 또는 비치환된 1-피렌일기, 치환 또는 비치환된 2-피렌일기, 치환 또는 비치환된 4-피렌일기, 치환 또는 비치환된 3-메틸-2-나프틸기, 치환 또는 비치환된 4-메틸-1-나프틸기 또는 하기 구조식
이고,
X6는 페닐기, 1-나프틸기, 2-나프틸기, 1-안트릴기, 2-안트릴기, 9-안트릴기, 1-페난트릴기, 2-페난트릴기, 3-페난트릴기, 4-페난트릴기, 9-페난트릴기, 1-나프타센일기, 2-나프타센일기, 9-나프타센일기, 1-피렌일기, 2-피렌일기, 4-피렌일기, 2-바이페닐릴기, 3-바이페닐릴기, 4-바이페닐릴기, p-터페닐-4-일기, p-터페닐-3-일기, p-터페닐-2-일기, m-터페닐-4-일기, m-터페닐-3-일기, m-터페닐-2-일기, o-톨릴기, m-톨릴기, p-톨릴기, p-t-뷰틸페닐기, p-(2-페닐프로필)페닐기, 3-메틸-2-나프틸기, 4-메틸-1-나프틸기, 4-메틸-1-안트릴기, 4'-메틸바이페닐릴기, 4"-t-뷰틸-p-터페닐-4-일기, 및 3-플루오란텐일기로 이루어진 군으로부터 선택되는 기이며,
X3 및 X4는 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 탄소수 6 내지 50의 아릴기, 치환 또는 비치환된 핵원자수 5 내지 50의 헤테로 아릴기, 치환 또는 비치환된 탄소수 1 내지 50의 알킬기, 치환 또는 비치환된 탄소수 1 내지 50의 알콕시기, 치환 또는 비치환된 탄소수 6 내지 50의 아르알킬기, 치환 또는 비치환된 핵원자수 5 내지 50의 아릴옥시기, 치환 또는 비치환된 핵원자수 5 내지 50의 아릴싸이오기, 치환 또는 비치환된 탄소수 1 내지 50의 알콕시카보닐기, 카복실기, 할로젠 원자, 사이아노기, 니트로기 또는 하이드록실기이고,
s1 및 s2는 각각 0 내지 4의 정수이다.
본 명세서의 일 실시상태에 있어서, 상기 X5는 치환 또는 비치환된 1-나프틸기 또는 치환 또는 비치환된 2-나프틸기이다.
또 하나의 일 실시상태에 있어서, 상기 X5는 치환 또는 비치환된 1- 나프틸기이다.
또 하나의 일 실시상태에 있어서, 상기 X5는 1-나프틸기이다.
본 명세서의 일 실시상태에 있어서, 상기 X6는 페닐기, 1-나프틸기 또는 2-나프틸기이다.
또 하나의 일 실시상태에 있어서, 상기 X6는 2-나프틸기이다.
본 명세서의 일 실시상태에 있어서, 상기 X3 및 X4는 서로 동일하거나 상이하고, 각각 독립적으로 치환 또는 비치환된 C6 내지 C50의 아릴기 또는 치환 또는 비치환된 C5 내지 C50의 헤테로아릴기이다.
본 명세서의 일 실시상태에 있어서, 상기 s1 및 s2는 각각 0 내지 2의 정수이다.
또 하나의 일 실시상태에 있어서, 상기 s1 및 s2는 0이다.
본 명세서의 일 실시상태에 있어서, 상기 X5 및 X6는 서로 동일하거나 상이하고, 각각 독립적으로 1-나프틸기 또는 2-나프틸기이고, s1 및 s2는 0인 유기 전자 소자이다.
본 명세서의 일 실시상태에 있어서, 상기 화학식5의 화합물은 발광층의 호스트로 포함될 수 있다.
본 명세서의 일 실시상태에 있어서, 상기 유기물층 중 1층 이상은 상기 화학식 1로 표시되는 화합물을 포함하고, 상기 화학식 4의 화합물 및 상기 화학식 5의 화합물을 상기 유기물층 중 발광층에 포함하는 유기 전자 소자이다.
또 하나의 일 실시상태에 있어서, 상기 유기물층 중 1층 이상은 상기 화학식 1로 표시되는 화합물을 포함하고, 상기 화학식 4의 Ar3는 피렌골격이고, L3는 단일결합이며, X1 및 X2는 게르마늄기로 치환 또는 비치환된 아릴기이고, r은 2인 화합물 및 상기 화학식 5의 X5 및 X6는 서로 동일하거나 상이하고, 각각 독립적으로 1-나프틸기 또는 2-나프틸기이고, s1 및 s2는 0인 유기 전자 소자이다.
본 명세서에서 어떤 부재가 다른 부재 "상에" 위치하고 있다고 할 때, 이는 어떤 부재가 다른 부재에 접해 있는 경우뿐 아니라 두 부재 사이에 또 다른 부재가 존재하는 경우도 포함한다.
본 명세서에서 어떤 부분이 어떤 구성요소를 "포함" 한다고 할 때, 이는 특별히 반대되는 기재가 없는 한 다른 구성요소를 제외하는 것이 아니라 다른 구성 요소를 더 포함할 수 있는 것을 의미한다.
본 출원의 유기 전자 소자의 유기물층은 단층 구조로 이루어질 수도 있으나, 2층 이상의 유기물층이 적층된 다층 구조로 이루어질 수 있다. 예컨대, 본 출원의 유기 전자 소자의 대표 적인 예로서, 유기 발광 소자는 유기물층으로서 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층 등을 포함하는 구조를 가질 수 있다. 그러나 유기 전자 소자의 구조는 이에 한정되지 않고 더 적은 수의 유기층을 포함할 수 있다.
본 출원의 일 실시상태에 따르면, 상기 유기 전자 소자는 유기발광소자, 유기인광소자, 유기태양전지, 유기감광체(OPC) 및 유기트랜지스터로 이루어진 군으로부터 선택될 수 있다.
이하에서는 유기발광소자에 대하여 예시한다.
본 출원의 일 실시상태에 있어서, 상기 유기물층은 정공주입층 또는 정공수송층을 포함하고, 상기 정공주입층 또는 정공수송층은 상기 화합물을 포함한다.
본 출원의 일 실시상태에 있어서, 상기 유기물층은 발광층을 포함하고, 상기 발광층은 상기 화합물을 포함한다.
또 하나의 실시상태에 있어서, 상기 유기물층은 발광층을 포함하고, 상기 발광층은 상기 화합물을 포함한다.
본 출원의 일 실시상태에 있어서, 상기 유기물층은 전자수송층 또는 전자주입층을 포함하고, 상기 전자수송층 또는 전자주입층은 상기 화합물을 포함한다.
본 출원의 일 실시상태에 있어서, 상기 유기 발광 소자는 정공주입층, 정공수송층, 발광층, 전자수송층, 전자주입층, 전자저지층 및 정공저지층으로 이루어진 군에서 선택되는 2층 이상을 포함한다.
본 출원의 일 실시상태에 있어서, 상기 유기 발광 소자는 제1 전극; 상기 제1 전극과 대향하여 구비된 제2 전극; 및 상기 제1 전극과 상기 제2 전극 사이에 구비된 발광층; 상기 발광층과 상기 제1 전극 사이, 또는 상기 발광층과 상기 제2 전극 사이에 구비된 2층 이상의 유기물층을 포함하고, 상기 2층 이상의 유기물층 중 적어도 하나는 상기 화합물을 포함한다. 본 출원의 일 실시상태에 있어서, 상기 2층 이상의 유기물층은 전자수송층, 전자주입층, 전자 수송과 전자주입을 동시에 하는 층 및 정공저지층으로 이루어진 군에서 2 이상이 선택될 수 있다.
본 출원의 일 실시상태에 있어서, 상기 유기물층은 2층 이상의 전자수송층을 포함하고, 상기 2층 이상의 전자수송층 중 적어도 하나는 상기 화합물을 포함한다. 구체적으로 본 명세서의 일 실시상태에 있어서, 상기 화합물은 상기 2층 이상의 전자수송층 중 1층에 포함될 수도 있으며, 각각의 2층 이상의 전자수송층에 포함될 수 있다.
또한, 본 출원의 일 실시상태에 있어서, 상기 화합물이 상기 각각의 2층 이상의 전자수송층에 포함되는 경우, 상기 화합물을 제외한 다른 재료들은 서로 동일하거나 상이할 수 있다.
본 출원의 일 실시상태에 있어서, 상기 유기물층은 상기 화합물을 포함하는 유기물층 이외에 아릴아미노기, 카바졸기 또는 벤조카바졸기를 포함하는 화합물을 포함하는 정공주입층 또는 정공수송층을 더 포함한다.
또 하나의 실시상태에 있어서, 유기 발광 소자는 기판 상에 양극, 1층 이상의 유기물층 및 음극이 순차적으로 적층된 구조(normal type)의 유기 발광 소자일 수 있다.
또 하나의 실시상태에 있어서, 유기 발광 소자는 기판 상에 음극, 1층 이상의 유기물층 및 양극이 순차적으로 적층된 역방향 구조(inverted type)의 유기 발광 소자일 수 있다.
예컨대, 본 출원의 일 실시상태에 따른 유기 발광 소자의 구조는 도 1 및 2에 예시되어 있다.
도 1은 기판(1), 양극(2), 발광층(3), 음극(4)이 순차적으로 적층된 유기 전자 소자의 구조가 예시되어 있다. 이와 같은 구조에 있어서, 상기 화합물은 상기 발광층(3)에 포함될 수 있다.
도 2는 기판 (1), 양극(2), 정공주입층(5), 정공수송층(6), 발광층(3), 전자수송층(7) 및 음극(4)이 순차적으로 적층된 유기 전자 소자의 구조가 예시되어 있다. 이와 같은 구조에 있어서 상기 화합물은 상기 정공주입층(5), 정공 수송층(6), 발광층(3) 및 전자 수송층(7) 중 1층 이상에 포함될 수 있다.
이와 같은 구조에 있어서, 상기 화합물은 상기 정공주입층, 정공수송층, 발광층 및 전자수송층 중 1층 이상에 포함될 수 있다.
본 출원의 유기 발광 소자는 유기물층 중 1층 이상이 본 출원의 화합물, 즉 상기 화합물을 포함하는 것을 제외하고는 당 기술분야에 알려져 있는 재료와 방법으로 제조될 수 있다.
상기 유기 발광 소자가 복수개의 유기물층을 포함하는 경우, 상기 유기물층은 동일한 물질 또는 다른 물질로 형성될 수 있다.
본 출원의 유기 발광 소자는 유기물층 중 1층 이상이 상기 화합물, 즉 상기 화학식 1로 표시되는 화합물을 포함하는 것을 제외하고는 당 기술분야에 알려져 있는 재료와 방법으로 제조될 수 있다.
예컨대, 본 출원의 유기 발광 소자는 기판 상에 제1 전극, 유기물층 및 제2 전극을 순차적으로 적층시킴으로써 제조할 수 있다. 이 때 스퍼터링법(sputtering)이나 전자빔 증발법(e-beam evaporation)과 같은 PVD(physical Vapor Deposition)방법을 이용하여, 기판 상에 금속 또는 전도성을 가지는 금속 산화물 또는 이들의 합금을 증착시켜 양극을 형성하고, 그 위에 정공 주입층, 정공 수송층, 발광층 및 전자 수송층을 포함하는 유기물층을 형성한 후, 그 위에 음극으로 사용할 수 있는 물질을 증착시킴으로써 제조될 수 있다. 이와 같은 방법 외에도, 기판 상에 음극 물질부터 유기물층, 양극 물질을 차례로 증착시켜 유기 발광 소자를 만들 수 있다.
또한, 상기 화학식 1의 화합물은 유기 발광 소자의 제조시 진공 증착법 뿐만 아니라 용액 도포법에 의하여 유기물층으로 형성될 수 있다. 여기서, 용액 도포법이라 함은 스핀 코팅, 딥코팅, 닥터 블레이딩, 잉크젯프린팅, 스크린 프린팅, 스프레이법, 롤 코팅 등을 의미하지만, 이들만으로 한정되는 것은 아니다.
이와 같은 방법 외에도, 기판 상에 음극 물질로부터 유기물층, 양극 물질을 차례로 증착시켜 유기 발광 소자를 만들 수도 있다 (국제 특허 출원 공개 제 2003/012890호). 다만, 제조 방법이 이에 한정되는 것은 아니다.
본 출원의 일 실시상태에 있어서, 상기 제1 전극은 양극이고, 상기 제2 전극은 음극이다.
또 하나의 실시상태에 있어서, 상기 제1 전극은 음극이고, 상기 제2 전극은 양극이다.
상기 양극 물질로는 통상 유기물층으로 정공 주입이 원활할 수 있도록 일함수가 큰 물질이 바람직하다. 본 출원에서 사용될 수 있는 양극 물질의 구체적인 예로는 바나듐, 크롬, 구리, 아연, 금과 같은 금속 또는 이들의 합금; 아연 산화물, 인듐 산화물, 인듐주석 산화물(ITO), 인듐아연 산화물(IZO)과 같은 금속 산화물; ZnO:Al 또는 SnO2 : Sb와 같은 금속과 산화물의 조합; 폴리(3-메틸티오펜), 폴리[3,4-(에틸렌-1,2-디옥시)티오펜](PEDOT), 폴리피롤 및 폴리아닐린과 같은 전도성 고분자 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 음극 물질로는 통상 유기물층으로 전자 주입이 용이하도록 일함수가 작은 물질인 것이 바람직하다. 음극 물질의 구체적인 예로는 마그네슘, 칼슘, 나트륨, 칼륨, 티타늄, 인듐, 이트륨, 리튬, 가돌리늄, 알루미늄, 은, 주석 및 납과 같은 금속 또는 이들의 합금; LiF/Al 또는 LiO2/Al과 같은 다층 구조 물질 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 정공 주입 물질로는 정공을 수송하는 능력을 가져 양극에서의 정공 주입효과, 발광층 또는 발광재료에 대하여 우수한 정공 주입 효과를 갖고, 발광층에서 생성된 여기자의 전자주입층 또는 전자주입재료에의 이동을 방지하며, 또한, 박막 형성 능력이 우수한 화합물이 바람직하다. 정공 주입 물질의 HOMO(highest occupied molecular orbital)가 양극 물질의 일함수와 주변 유기물층의 HOMO 사이인 것이 바람직하다. 정공 주입 물질의 구체적인 예로는 금속 포피린(porphyrin), 올리고티오펜, 아릴아민 계열의 유기물, 헥사니트릴헥사아자트리페닐렌 계열의 유기물, 퀴나크리돈(quinacridone)계열의 유기물, 페릴렌(perylene) 계열의 유기물, 안트라퀴논 및 폴리아닐린과 폴리티오펜 계열의 전도성 고분자 등이 있으나, 이들에만 한정 되는 것은 아니다.
상기 정공수송층은 정공주입층으로부터 정공을 수취하여 발광층까지 정공을 수송하는 층으로, 정공 수송 물질로는 양극이나 정공 주입층으로부터 정공을 수송받아 발광층으로 옮겨줄 수 있는 물질로 정공에 대한 이동성이 큰 물질이 적합하다. 구체적인 예로는 아릴아민 계열의 유기물, 전도성 고분자, 및 공액 부분과 비공액 부분이 함께 있는 블록 공중합체 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 발광 물질로는 정공 수송층과 전자 수송층으로부터 정공과 전자를 각각 수송받아 결합시킴으로써 가시광선 영역의 빛을 낼 수 있는 물질로서, 형광이나 인광에 대한 양자 효율이 좋은 물질이 바람직하다. 구체적인 예로는 8-히드록시-퀴놀린 알루미늄 착물(Alq3); 카르바졸 계열 화합물; 이량체화 스티릴(dimerized styryl) 화합물; BAlq; 10-히드록시벤조 퀴놀린-금속 화합물; 벤족사졸, 벤즈티아졸 및 벤즈이미다졸 계열의 화합물; 폴리(p-페닐렌비닐렌)(PPV) 계열의 고분자; 스피로(spiro) 화합물; 폴리플루오렌, 루브렌 등이 있으나, 이들에만 한정되는 것은 아니다.
상기 발광층은 호스트 재료 및 도펀트 재료를 포함할 수 있다. 호스트 재료는 축합 방향족환 유도체 또는 헤테로환 함유 화합물 등이 있다. 구체적으로 축합 방향족환 유도체로는 안트라센 유도체, 피렌 유도체, 나프탈렌 유도체, 펜타센 유도체, 페난트렌 화합물, 플루오란텐 화합물 등이 있고, 헤테로환 함유 화합물로는 화합물, 디벤조퓨란 유도체, 래더형 퓨란 화합물, 피리미딘 유도체 등이 있으나, 이에 한정되지 않는다.
상기 전자 수송 물질로는 전자주입층으로부터 전자를 수취하여 발광층까지 전자를 수송하는 층으로 전자 수송 물질로는 음극으로부터 전자를 잘 주입 받아 발광층으로 옮겨줄 수 있는 물질로서, 전자에 대한 이동성이 큰 물질이 적합하다. 구체적인 예로는 8-히드록시퀴놀린의 Al착물; Alq3를 포함한 착물; 유기 라디칼 화합물; 히드록시플라본-금속 착물 등이 있으나, 이들에만 한정되는 것은 아니다. 전자 수송층은 종래기술에 따라 사용된 바와 같이 임의의 원하는 캐소드 물질과 함께 사용할 수 있다. 특히, 적절한 캐소드 물질의 예는 낮은 일함수를 가지고 알루미늄층 또는 실버층이 뒤따르는 통상적인 물질이다. 구체적으로 세슘, 바륨, 칼슘, 이테르븀 및 사마륨이고, 각 경우 알루미늄 층 또는 실버층이 뒤따른다.
상기 전자주입층은 전극으로부터 전자를 주입하는 층으로, 전자를 수송하는 능력을 갖고, 음극으로부터의 전자주입 효과, 발광층 또는 발광 재료에 대하여 우수한 전자주입 효과를 가지며, 발광층에서 생성된 여기자의 정공 주입층에의 이동을 방지하고, 또한, 박막형성능력이 우수한 화합물이 바람직하다. 구체적으로는 플루오레논, 안트라퀴노다이메탄, 다이페노퀴논, 티오피란 다이옥사이드, 옥사졸, 옥사다이아졸, 트리아졸, 이미다졸, 페릴렌테트라카복실산, 프레오레닐리덴 메탄, 안트론 등과 그들의 유도체, 금속 착체 화합물 및 함질소 5원환 유도체 등이 있으나, 이에 한정되지 않는다.
상기 금속 착체 화합물로서는 8-하이드록시퀴놀리나토 리튬, 비스(8-하이드록시퀴놀리나토)아연, 비스(8-하이드록시퀴놀리나토)구리, 비스(8-하이드록시퀴놀리나토)망간, 트리스(8-하이드록시퀴놀리나토)알루미늄, 트리스(2-메틸-8-하이드록시퀴놀리나토)알루미늄, 트리스(8-하이드록시퀴놀리나토)갈륨, 비스(10-하이드록시벤조[h]퀴놀리나토)베릴륨, 비스(10-하이드록시벤조[h]퀴놀리나토)아연, 비스(2-메틸-8-퀴놀리나토)클로로갈륨, 비스(2-메틸-8-퀴놀리나토)(o-크레졸라토)갈륨, 비스(2-메틸-8-퀴놀리나토)(1-나프톨라토)알루미늄, 비스(2-메틸-8-퀴놀리나토)(2-나프톨라토)갈륨 등이 있으나, 이에 한정되지 않는다.
상기 정공저지층은 정공의 음극 도달을 저지하는 층으로, 일반적으로 정공주입층과 동일한 조건으로 형성될 수 있다. 구체적으로 옥사디아졸 유도체나 트리아졸 유도체, 페난트롤린 유도체, BCP, 알루미늄 착물(aluminum complex) 등이 있으나, 이에 한정되지 않는다.
본 명세서에 따른 유기 발광 소자는 사용되는 재료에 따라 전면 발광형, 후면 발광형 또는 양면 발광형일 수 있다.
본 출원의 일 실시상태에 있어서, 상기 화합물은 유기 발광 소자 외에도 유기 태양 전지 또는 유기 트랜지스터에 포함될 수 있다.
본 출원에 따른 화합물은 유기인광소자, 유기태양전지, 유기감광체, 유기트랜지스터 등을 비롯한 유기 전자 소자에서도 유기 발광 소자에 적용되는 것과 유사한 원리로 작용할 수 있다.
이하, 본 명세서를 구체적으로 설명하기 위해 실시예를 들어 상세하게 설명하기로 한다. 그러나, 본 명세서에 따른 실시예들은 여러 가지 다른 형태로 변형될 수 있으며, 본 출원의 범위가 아래에서 상술하는 실시예들에 한정되는 것으로 해석되지 않는다. 본 출원의 실시예들은 당업계에서 평균적인 지식을 가진 자에게 본 명세서를 보다 완전하게 설명하기 위해 제공되는 것이다.
<제조예 1> 화합물 1의 합성
화합물 A(10g, 21.6mmol), 디페닐아민(4.03g, 23.81mmol) 그리고 NaOt-Bu (2.51g, 25.9mmol)을 톨루엔 200ml에 넣은 후 교반하면서 온도를 높였다. 승온한 후 환류되기 시작하면 비스(트리-tert-부틸포스핀)팔라듐(0.06g, 0.11mmol)을 천천히 떨어뜨리며 넣었다. 3시간 후 반응을 종료하여 온도를 상온으로 낮추고 감압 하에서 농축한 후 컬럼 정제하여 9.64g(81%)의 화합물 1을 제조하였다.
MS[M+H]+= 552
<제조예 2> 화합물 2의 합성
화합물 A(10g, 21.6mmol), 비스바이페닐아민(8.08g, 23.81mmol) 그리고 NaOt-Bu (2.51g, 25.9mmol)을 톨루엔 200ml에 넣은 후 교반하면서 온도를 높였다. 승온한 후 환류되기 시작하면 비스(트리-tert-부틸포스핀)팔라듐(0.06g, 0.11mmol)을 천천히 떨어뜨리며 넣었다. 3시간 후 반응을 종료하여 온도를 상온으로 낮추고 감압 하에서 농축한 후 컬럼 정제하여 13.85g(91%)의 화합물 2를 제조하였다.
MS[M+H]+= 704
<제조예 3> 화합물 3의 합성
화합물 A(10g, 21.6mmol), 9,9-디메틸플루오렌바이페닐아민(9.05g, 23.81mmol) 그리고 NaOt-Bu (2.51g, 25.9mmol)을 톨루엔 200ml에 넣은 후 교반하면서 온도를 높였다. 승온한 후 환류되기 시작하면 비스(트리-tert-부틸포스핀)팔라듐(0.06g, 0.11mmol)을 천천히 떨어뜨리며 넣었다. 3시간 후 반응을 종료하여 온도를 상온으로 낮추고 감압 하에서 농축한 후 컬럼 정제하여 14.77g(92%)의 화합물 3을 제조하였다.
MS[M+H]+= 744
<제조예 4> 화합물 4의 합성
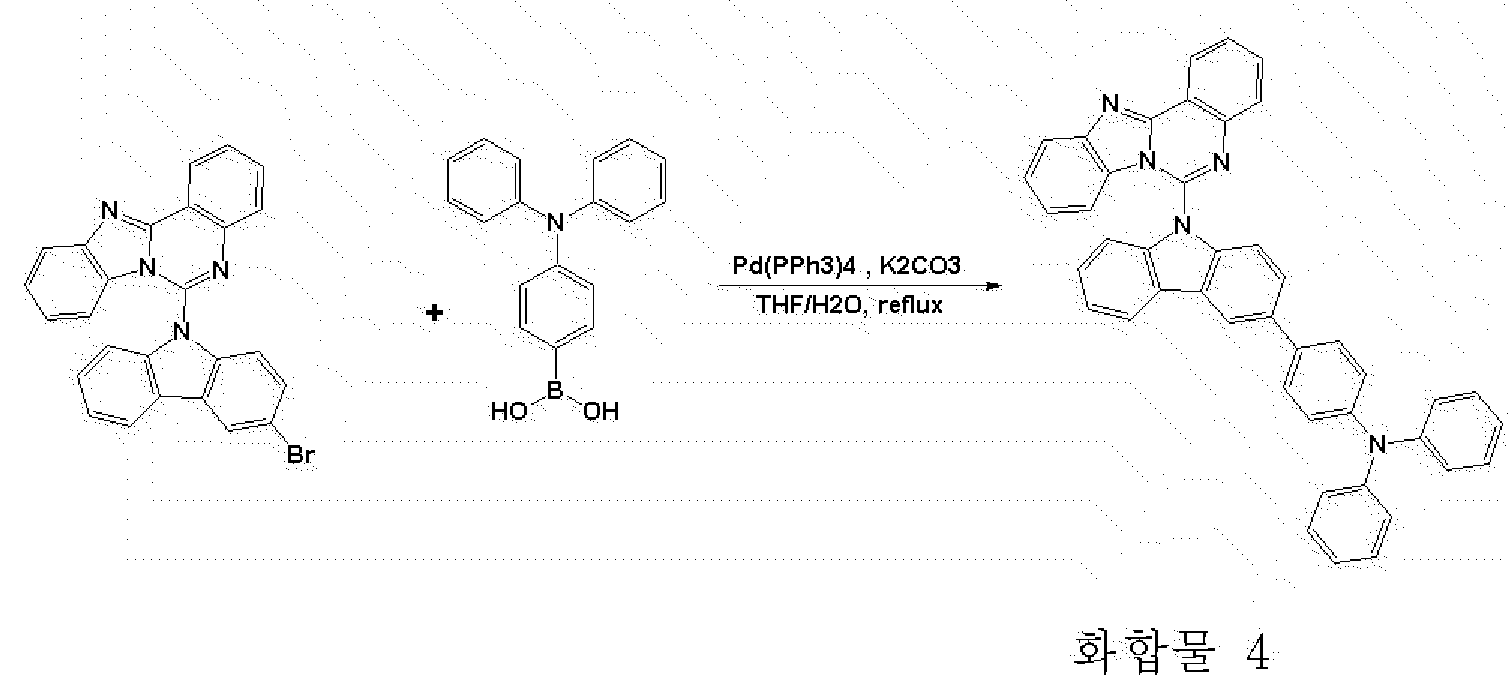
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(디페닐아미노)페닐)보론산 (6.88g, 23.81mmol)을 테트라하이드로퓨란 200ml에 완전히 녹인 후 2M 탄산칼륨수용액(100ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 3 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에탄올 300ml로 재결정하여 화합물 4 (11.31g, 83%)를 제조하였다.
MS[M+H]+= 628
<제조예 5> 화합물 5의 합성
화합물 A(10g, 21.6mmol), 카바졸(4.01g, 23.81mmol) 그리고 NaOt-Bu (2.51g, 25.9mmol)을 톨루엔 200ml에 넣은 후 교반하면서 온도를 높였다. 승온한 후 환류되기 시작하면 비스(트리-tert-부틸포스핀)팔라듐(0.06g, 0.11mmol)을 천천히 떨어뜨리며 넣었다. 5시간 후 반응을 종료하여 온도를 상온으로 낮추고 감압 하에서 농축한 후 컬럼 정제하여 10.72g(90%)의 화합물 5를 제조하였다.
MS[M+H]+= 550
<제조예 6> 화합물 6의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(9H-카바졸-9-yl)페닐)보론산 (6.88g, 23.81mmol)을 테트라하이드로퓨란 280ml에 완전히 녹인 후 2M 탄산칼륨수용액(140ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 6 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 6 (10.31g, 78%)을 제조하였다.
MS[M+H]+= 626
<제조예 7> 화합물 7의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (9-페닐-9H-카바졸-3-yl)보론산 (6.88g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 2 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 7 (12.09g, 91%)을 제조하였다.
MS[M+H]+= 626
<제조예 8> 화합물 8의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 G (10g, 19.61mmol), 2-클로로-4,6-디페닐-1,3,5-트리아진 (4.76g, 17.83mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.62g, 0.53mmol)을 넣은 후 8 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 8 (12.41g, 93%)을 제조하였다.
MS[M+H]+= 616
<제조예 9> 화합물 9의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 G (10g, 19.61mmol), 2-클로로-4,6-디페닐피리미딘 (4.74g, 17.83mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.62g, 0.53mmol)을 넣은 후 5 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 250ml로 재결정하여 화합물 9 (10.15g, 78%)를 제조하였다.
MS[M+H]+= 615
<제조예 10> 화합물 10의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 G (10g, 19.61mmol), 4-클로로-2,6-디페닐피리미딘 (4.74g, 17.83mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.62g, 0.53mmol)을 넣은 후 4 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 250ml로 재결정하여 화합물 10 (11.32g, 86%)을 제조하였다.
MS[M+H]+= 615
<제조예 11> 화합물 11의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 G (10g, 19.61mmol), 2-클로로-4,6-디페닐피리미딘 (4.71g, 17.83mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.62g, 0.53mmol)을 넣은 후 2 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 280ml로 재결정하여 화합물 11 (11.32g, 86%)을 제조하였다.
MS[M+H]+= 614
<제조예 12> 화합물 12의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 G (10g, 19.61mmol), 2-(4-브로모페닐)-4,6-디페닐-1,3,5-트리아진 (6.91g, 17.83mmol)을 테트라하이드로퓨란 400ml에 완전히 녹인 후 2M 탄산칼륨수용액(200ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(1.24g, 1.06mmol)을 넣은 후 12 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 500ml로 재결정하여 화합물 12 (12.41g, 93%)를 제조하였다.
MS[M+H]+= 692
<제조예 13> 화합물 13의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 G (10g, 19.61mmol), 2-(3-브로모페닐)-4,6-디페닐-1,3,5-트리아진 (6.91g, 17.83mmol)을 테트라하이드로퓨란 400ml에 완전히 녹인 후 2M 탄산칼륨수용액(200ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(1.24g, 1.06mmol)을 넣은 후 7 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 400ml로 재결정하여 화합물 13 (9.55g, 64%)을 제조하였다.
MS[M+H]+= 693
<제조예 14> 화합물 14의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), 디벤조bs,d]퓨란-2-일보론산 (5.26g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 6 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 14 (10.82g, 91%)를 제조하였다.
MS[M+H]+= 551
<제조예 15> 화합물 15의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), 디벤조[b,d]티오펜-2-일보론산 (5.32g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 5 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 15 (9.44g, 80%)를 제조하였다.
MS[M+H]+= 567
<제조예 16> 화합물 16의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), [1,1':3',1"-터페닐]-5'-일보론산 (6.52g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 6 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 16 (10.42g, 78%)을 제조하였다.
MS[M+H]+= 613
<제조예 17> 화합물 17의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (9,9-디메틸-9H-플루오렌-2-일)보론산 (5.66g, 23.81mmol)을 테트라하이드로퓨란 320ml에 완전히 녹인 후 2M 탄산칼륨수용액(160ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 3 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 17 (9.56g, 76%)을 제조하였다.
MS[M+H]+= 577
<제조예 18> 화합물 18의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(나프탈렌-2-일)페닐)보론산 (6.51g, 23.81mmol)을 테트라하이드로퓨란 320ml에 완전히 녹인 후 2M 탄산칼륨수용액(160ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 5 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 18 (10.22g, 84%)을 제조하였다.
MS[M+H]+= 587
<제조예 19> 화합물 19의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), 9,9'-스피로비[플루오렌]-2-일보론산 (8.57g, 23.81mmol)을 테트라하이드로퓨란 400ml에 완전히 녹인 후 2M 탄산칼륨수용액(200ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 5 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 19 (13.74g, 91%)를 제조하였다.
MS[M+H]+= 699
<제조예 20> 화합물 20의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(1-페닐-1H-benzo[d]이미다졸-2-일)페닐)보론산 (7.48g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(140ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 8 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 20 (12.42g, 87%)을 제조하였다.
MS[M+H]+= 653
<제조예 21> 화합물 21의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(벤조[d]옥사졸-2-일)페닐)보론산 (5.69g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(140ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 3 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 21 (10.11g, 81%)을 제조하였다.
MS[M+H]+= 578
<제조예 22> 화합물 22의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(벤조[d]티아졸-2-일)페닐)보론산 (5.69g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(140ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 3 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 22 (9.53g, 74%)를 제조하였다.
MS[M+H]+= 594
<제조예 23> 화합물 23의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 A (10g, 21.6mmol), (4-(벤조[d]티아졸-2-일)페닐)보론산 (6.84g, 23.81mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(140ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.75g, 0.65mmol)을 넣은 후 2 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 23 (9.53g, 74%)을 제조하였다.
MS[M+H]+= 662
<제조예 24> 화합물 24 내지 46의 합성
제조예 1 내지 23 에서 출발물질을 화합물 A 대신 화합물 B를 사용하고, 화합물 G 대신 화합물 H를 사용한 것을 제외하고, 상기 화합물 1 내지 23을 제조하는 방법과 동일하게 하기 화합물 24 내지 46을 제조하였다.
<제조예 25> 화합물 47 내지 69의 합성
제조예 1 내지 23 에서 출발물질을 화합물 A 대신 화합물 E 를 사용한 것을 제외하고, 상기 화합물 1 내지 23을 제조하는 방법과 동일하게 하기 화합물 47 내지 69를 제조하였다.
<제조예 26> 화합물 70 내지 92의 합성
제조예 1 내지 23 에서 출발물질을 화합물 A 대신 화합물 F 를 사용한 것을 제외하고, 상기 화합물 1 내지 23을 제조하는 방법과 동일하게 하기 화합물 70 내지 92를 제조하였다.
<제조예 27> 화합물 93의 합성
화합물 C(10g, 18.52mmol), 디페닐아민(6.88g, 40.74mmol) 그리고 NaOt-Bu (4.62g, 48.2mmol)을 톨루엔 200ml에 넣은 후 교반하면서 온도를 높였다. 승온한 후 환류되기 시작하면 비스(트리-tert-부틸포스핀)팔라듐(0.09g, 0.18mmol)을 천천히 떨어뜨리며 넣었다. 5시간 후 반응을 종료하여 온도를 상온으로 낮추고 감압 하에서 농축한 후 컬럼 정제하여 10.42g(80%)의 화합물 93을 제조하였다.
MS[M+H]+= 719
<제조예 28> 화합물 94의 합성
화합물 C(10g, 18.52mmol), 카바졸(6.85g, 40.74mmol) 그리고 NaOt-Bu (4.62g, 48.2mmol)을 톨루엔 200ml에 넣은 후 교반하면서 온도를 높였다. 승온한 후 환류되기 시작하면 비스(트리-tert-부틸포스핀)팔라듐(0.09g, 0.18mmol)을 천천히 떨어뜨리며 넣었다. 5시간 후 반응을 종료하여 온도를 상온으로 낮추고 감압 하에서 농축한 후 컬럼 정제하여 8.42g(71%)의 화합물 94를 제조하였다.
MS[M+H]+= 715
<제조예 29> 화합물 95의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 C(10g, 18.52mmol), (4-(디페닐아미노)페닐)보론산 (11.40g, 40.74mmol)을 테트라하이드로퓨란 320ml에 완전히 녹인 후 2M 탄산칼륨수용액(110ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.65g, 0.56mmol)을 넣은 후 3 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 200ml로 재결정하여 화합물 95 (13.54g, 84%)를 제조하였다.
MS[M+H]+= 871
<제조예 30> 화합물 96의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 C(10g, 18.52mmol), 나프탈렌-일보론산 (7.01g, 40.74mmol)을 테트라하이드로퓨란 280ml에 완전히 녹인 후 2M 탄산칼륨수용액(120ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.65g, 0.56mmol)을 넣은 후 1 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 96 (9.45g, 80%)을 제조하였다.
MS[M+H]+= 637
<제조예 31> 화합물 97의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 C(10g, 18.52mmol), 디벤조[b,d]퓨란-4-일보론산 (8.64g, 40.74mmol)을 테트라하이드로퓨란 300ml에 완전히 녹인 후 2M 탄산칼륨수용액(150ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.65g, 0.56mmol)을 넣은 후 3 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 97 (11.24g, 84%)을 제조하였다.
MS[M+H]+= 717
<제조예 32> 화합물 98의 합성
질소 분위기에서 500ml 둥근 바닥 플라스크에 화합물 C(10g, 18.52mmol), 디벤조[b,d]퓨란-4-일보론산 (13.12g, 40.74mmol)을 테트라하이드로퓨란 360ml에 완전히 녹인 후 2M 탄산칼륨수용액(180ml)을 첨가하고, 테트라키스-(트리페닐포스핀)팔라듐(0.65g, 0.56mmol)을 넣은 후 15 시간 동안 가열 교반하였다. 상온으로 온도를 낮추고 물 층을 제거하고 무수황산마그네슘으로 건조한 후 감압농축 시키고 에틸아세테이트 300ml로 재결정하여 화합물 98 (14.15g, 81%)을 제조하였다.
MS[M+H]+= 937
<제조예 33> 화합물 99 내지 104의 합성
제조예 27 내지 32 에서 출발물질을 화합물 C 대신 화합물 D 를 사용한 것을 제외하고, 상기 화합물 93 내지 98을 제조하는 방법과 동일하게 하기 화합물 99 내지 104를 제조하였다.
<실험예 1-1>
ITO(indium tin oxide)가 1,000Å의 두께로 박막 코팅된 유리 기판을 세제를 녹인 증류수에 넣고 초음파로 세척하였다. 이 때, 세제로는 피셔사(Fischer Co.) 제품을 사용하였으며, 증류수로는 밀러포어사(Millipore Co.) 제품의 필터(Filter)로 2차로 걸러진 증류수를 사용하였다. ITO를 30분간 세척한 후 증류수로 2회 반복하여 초음파 세척을 10분간 진행하였다. 증류수 세척이 끝난 후, 이소프로필알콜, 아세톤, 메탄올의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 수송시켰다. 또한, 산소 플라즈마를 이용하여 상기 기판을 5분간 세정한 후 진공 증착기로 기판을 수송시켰다.
이렇게 준비된 ITO 투명 전극 위에 하기 화학식의 헥사니트릴 헥사아자트리페닐렌 (hexaazatriphenylene; HAT)를 500Å의 두께로 열 진공 증착하여 정공 주입층을 형성하였다.
[HAT]
상기 정공 주입층 위에 정공을 수송하는 물질인 하기 화합물 4-4'-비스[N-(1-나프틸)-N-페닐아미노]비페닐(NPB)(300Å)를 진공 증착하여 정공 수송층을 형성하였다.
[NPB]
이어서, 상기 정공 수송층 위에 막 두께 100Å으로 하기 화합물 1을 진공 증착하여 전자 저지층을 형성하였다.
[화합물 1]
이어서, 상기 전자 저지층 위에 막 두께 300Å으로 아래와 같은 BH와 BD를 25:1의 중량비로 진공증착하여 발광층을 형성하였다.
[BH]
[BD]
[ET1]
[LiQ]
상기 발광층 위에 상기 화합물 ET1과 상기 화합물 LiQ(Lithium Quinolate)를 1:1의 중량비로 진공증착하여 300Å의 두께로 전자 주입 및 수송층을 형성하였다. 상기 전자 주입 및 수송층 위에 순차적으로 12Å두께로 리튬플로라이드(LiF)와 2,000Å 두께로 알루미늄을 증착하여 음극을 형성하였다.
상기의 과정에서 유기물의 증착속도는 0.4~ 0.7Å/sec를 유지하였고, 음극의 리튬플로라이드는 0.3Å/sec, 알루미늄은 2Å/sec의 증착 속도를 유지하였으며, 증착시 진공도는 2 × 10-7 ~5 × 10-6 torr를 유지하여, 유기 발광 소자를 제작하였다.
<실험예 1-2>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 2를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-3>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 3을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-4>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 4를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-5>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 5를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-6>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 6을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-7>
상기 실험예 1-1에서 화합물1 대신 상기 화합물 7을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-8>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 24를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-9>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 25를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-10>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 26을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-11>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 27를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-12>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 28를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-13>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 29를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-14>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 30를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-15>
상기 실험예1-1에서 화합물 1 대신 상기 화합물 47를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-16>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 48을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-17>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 49를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-18>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 50을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-19>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 51를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-20>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 52를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-21>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 53을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-22>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 70를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-23>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 71을 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-24>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 72를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-25>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 73를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-26>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 74를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-27>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 75를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-28>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 76를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-29>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 93를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-30>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 94를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-31>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 95를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-32>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 99를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-33>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 100를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 1-34>
상기 실험예 1-1에서 화합물 1 대신 상기 화합물 101를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<비교예 1-1>
상기 실험예 1-1에서 화합물 1 대신 하기 화합물 EB 1(TCTA)를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
[EB 1]
<비교예 1-2>
상기 실험예 1-1에서 화합물 1 대신 하기 화합물 EB 2를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
[EB 2]
<비교예 1-3>
상기 실험예 1-1에서 화합물 1 대신 하기 화합물 EB 3를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
[EB 3]
<비교예 1-4>
상기 실험예 1-1에서 화합물 1 대신 하기 화합물 EB 4를 사용한 것을 제외하고는 실험예 1-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
[EB 4]
실험예 1-1 내지 1-34 및 비교예 1-1 및 1-4에 의해 제작된 유기 발광 소자에 전류를 인가하였을 때, 성능평가를 하기 표 1에 나타내었다.
| |
화합물(전자억제층) |
전압(V@10mA/cm2) |
효율(cd/A@10mA/cm2) |
색좌표(x,y) |
| 실험예 1-1 |
화합물 1 |
3.75 |
5.85 |
(0.139, 0.122) |
| 실험예 1-2 |
화합물 2 |
3.72 |
5.88 |
(0.138, 0.126) |
| 실험예 1-3 |
화합물 3 |
3.77 |
5.81 |
(0.138, 0.127) |
| 실험예 1-4 |
화합물 4 |
3.78 |
5.82 |
(0.137, 0.125) |
| 실험예 1-5 |
화합물 5 |
3.79 |
5.83 |
(0.136, 0.125) |
| 실험예 1-6 |
화합물 6 |
3.74 |
5.87 |
(0.136, 0.127) |
| 실험예 1-7 |
화합물 7 |
3.73 |
5.88 |
(0.136, 0.125) |
| 실험예 1-8 |
화합물 24 |
3.74 |
5.71 |
(0.137, 0.125) |
| 실험예 1-9 |
화합물 25 |
3.73 |
5.78 |
(0.138, 0.125) |
| 실험예 1-10 |
화합물 26 |
3.74 |
5.62 |
(0.136, 0.125) |
| 실험예 1-11 |
화합물 27 |
3.73 |
5.77 |
(0.137, 0.125) |
| 실험예 1-12 |
화합물 28 |
3.85 |
5.75 |
(0.136, 0.125) |
| 실험예 1-13 |
화합물 29 |
3.82 |
5.68 |
(0.138, 0.126) |
| 실험예 1-14 |
화합물 30 |
3.87 |
5.71 |
(0.137, 0.125) |
| 실험예 1-15 |
화합물 47 |
3.88 |
5.72 |
(0.136, 0.127) |
| 실험예 1-16 |
화합물 48 |
3.89 |
5.73 |
(0.135, 0.127) |
| 실험예 1-17 |
화합물 49 |
3.84 |
5.77 |
(0.138, 0.127) |
| 실험예 1-18 |
화합물 50 |
3.83 |
5.78 |
(0.137, 0.125) |
| 실험예 1-19 |
화합물 51 |
3.84 |
5.71 |
(0.137, 0.125) |
| 실험예 1-20 |
화합물 52 |
3.83 |
5.78 |
(0.136, 0.127) |
| 실험예 1-21 |
화합물 53 |
3.84 |
5.72 |
(0.135, 0.127) |
| 실험예 1-22 |
화합물 70 |
3.83 |
5.77 |
(0.138, 0.127) |
| 실험예 1-23 |
화합물 71 |
3.89 |
5.75 |
(0.137, 0.125) |
| 실험예 1-24 |
화합물 72 |
3.88 |
5.78 |
(0.137, 0.125) |
| 실험예 1-25 |
화합물 73 |
3.87 |
5.71 |
(0.136, 0.125) |
| 실험예 1-26 |
화합물 74 |
3.61 |
5.65 |
(0.139, 0.122) |
| 실험예 1-27 |
화합물 75 |
3.63 |
5.68 |
(0.138, 0.126) |
| 실험예 1-28 |
화합물 76 |
3.62 |
5.61 |
(0.138, 0.127) |
| 실험예 1-29 |
화합물 93 |
3.74 |
5.62 |
(0.137, 0.125) |
| 실험예 1-30 |
화합물 94 |
3.70 |
5.63 |
(0.136, 0.125) |
| 실험예 1-31 |
화합물 95 |
3.75 |
5.67 |
(0.136, 0.127) |
| 실험예 1-32 |
화합물 99 |
3.80 |
5.58 |
(0.136, 0.125) |
| 실험예 1-33 |
화합물 100 |
3.84 |
5.51 |
(0.137, 0.125) |
| 실험예 1-34 |
화합물 101 |
3.82 |
5.54 |
(0.138, 0.125) |
| 비교예 1-1 |
EB1 |
4.37 |
4.68 |
(0.138, 0.125) |
| 비교예 1-2 |
EB2 |
4.15 |
4.85 |
(0.138, 0.125) |
| 비교예 1-3 |
EB3 |
4.63 |
4.32 |
(0.138, 0.126) |
| 비교예 1-4 |
EB4 |
4.52 |
4.41 |
(0.138, 0.125) |
상기 표 1에서 나타난 바와 같이, 실험예 1-1 내지 1-34의 화합물로 이루어진 유기발광소자는 전자억제층으로 자주 사용되는 TCTA(비교예 1-1), 비교예 1-2, -L-Ar이 페닐기인 비교예 1-3 및 이미다조 퀴나졸린과 카바졸 사이에 링커로 나프탈렌이 연결된 비교예 1-4 보다 저전압, 고효율의 특성을 나타내는 것을 알 수 있다. 특히 화합물 A로부터 제조된 화합물 1 내지 7을 사용한 유기 발광 소자에서 저전압 고효율 특성이 가장 뛰어난 것을 알 수 있다.
따라서, 본 출원에 따른 화학식의 화합물 유도체는 전자 억제 능력이 우수하여 저전압 및 고효율의 특성을 보이며 유기 발광 소자에 적용 가능함을 확인할 수 있었다.
<실험예 2>
<실험예 2-1 내지 실험예 2-34>
상기 실험예 1에서 전자 저지층으로 TCTA을 사용하고, 정공 수송층으로 NPB 대신 실험예 1-1 내지 1-34의 화합물들을 사용한 것을 제외하고는 동일하게 실험하였다.
<비교예 2-1>
상기 실험예 1에서 전자 저지층으로 TCTA을 사용하고, 정공 수송층으로 HT 1(NPB)을 사용한 것을 제외하고는 동일하게 실험하였다.
<비교예 2-2>
상기 실험예 1에서 전자 저지층으로 TCTA을 사용하고, 정공 수송층으로 HT 2를 사용한 것을 제외하고는 동일하게 실험하였다.
[HT 2]
<비교예 2-3>
상기 실험예 1에서 전자 저지층으로 TCTA을 사용하고, 정공 수송층으로 HT 3를 사용한 것을 제외하고는 동일하게 실험하였다.
[HT 3]
<비교예 2-4>
상기 실험예 1에서 전자 저지층으로 TCTA을 사용하고, 정공 수송층으로 HT 4를 사용한 것을 제외하고는 동일하게 실험하였다.
[HT 4]
실험예 2-1 내지 2-25 및 비교예 2-1 및 2-4에 의해 제작된 유기 발광 소자에 전류를 인가하였을 때, 성능평가를 하기 표 2에 나타내었다.
| |
화합물(정공수송층) |
전압(V@10mA/cm2) |
효율(cd/A@10mA/cm2) |
색좌표(x,y) |
| 실험예 2-1 |
화합물 1 |
4.35 |
5.95 |
(0.139, 0.122) |
| 실험예 2-2 |
화합물 2 |
4.32 |
5.98 |
(0.138, 0.126) |
| 실험예 2-3 |
화합물 3 |
4.37 |
5.91 |
(0.138, 0.127) |
| 실험예 2-4 |
화합물 4 |
4.38 |
5.92 |
(0.137, 0.125) |
| 실험예 2-5 |
화합물 5 |
4.39 |
5.93 |
(0.136, 0.125) |
| 실험예 2-6 |
화합물 6 |
4.34 |
5.97 |
(0.136, 0.127) |
| 실험예 2-7 |
화합물 7 |
4.33 |
5.98 |
(0.136, 0.125) |
| 실험예 2-8 |
화합물 24 |
4.34 |
5.91 |
(0.137, 0.125) |
| 실험예 2-9 |
화합물 25 |
4.33 |
5.98 |
(0.138, 0.125) |
| 실험예 2-10 |
화합물 26 |
4.34 |
5.92 |
(0.136, 0.125) |
| 실험예 2-11 |
화합물 27 |
4.33 |
5.97 |
(0.137, 0.125) |
| 실험예 2-12 |
화합물 28 |
4.45 |
5.85 |
(0.136, 0.125) |
| 실험예 2-13 |
화합물 29 |
4.42 |
5.88 |
(0.138, 0.126) |
| 실험예 2-14 |
화합물 30 |
4.47 |
5.81 |
(0.137, 0.125) |
| 실험예 2-15 |
화합물 47 |
4.48 |
5.82 |
(0.136, 0.127) |
| 실험예 2-16 |
화합물 48 |
4.49 |
5.83 |
(0.135, 0.127) |
| 실험예 2-17 |
화합물 49 |
4.44 |
5.87 |
(0.138, 0.127) |
| 실험예 2-18 |
화합물 50 |
4.43 |
5.88 |
(0.137, 0.125) |
| 실험예 2-19 |
화합물 51 |
4.44 |
5.81 |
(0.137, 0.125) |
| 실험예 2-20 |
화합물 52 |
4.43 |
5.88 |
(0.136, 0.127) |
| 실험예 2-21 |
화합물 53 |
4.44 |
5.82 |
(0.135, 0.127) |
| 실험예 2-22 |
화합물 70 |
4.43 |
5.87 |
(0.138, 0.127) |
| 실험예 2-23 |
화합물 71 |
4.59 |
5.75 |
(0.137, 0.125) |
| 실험예 2-24 |
화합물 72 |
4.48 |
5.88 |
(0.137, 0.125) |
| 실험예 2-25 |
화합물 73 |
4.37 |
5.94 |
(0.136, 0.125) |
| 실험예 2-26 |
화합물 74 |
4.35 |
5.95 |
(0.139, 0.122) |
| 실험예 2-27 |
화합물 75 |
4.32 |
5.98 |
(0.138, 0.126) |
| 실험예 2-28 |
화합물 76 |
4.37 |
5.91 |
(0.138, 0.127) |
| 실험예 2-29 |
화합물 93 |
4.58 |
5.82 |
(0.137, 0.125) |
| 실험예 2-30 |
화합물 94 |
4.59 |
5.83 |
(0.136, 0.125) |
| 실험예 2-31 |
화합물 95 |
4.54 |
5.87 |
(0.136, 0.127) |
| 실험예 2-32 |
화합물 99 |
4.53 |
5.88 |
(0.136, 0.125) |
| 실험예 2-33 |
화합물 100 |
4.54 |
5.81 |
(0.137, 0.125) |
| 실험예 2-34 |
화합물 101 |
4.53 |
5.88 |
(0.138, 0.125) |
| 비교예 2-1 |
HT1 |
5.85 |
4.12 |
(0.136, 0.125) |
| 비교예 2-2 |
HT2 |
5.63 |
4.37 |
(0.137, 0.125) |
| 비교예 2-3 |
HT3 |
5.72 |
4.25 |
(0.136, 0.126) |
| 비교예 2-4 |
HT4 |
5.56 |
4.43 |
(0.137, 0.126) |
상기 표 2에서 나타난 바와 같이, 실험예 2-1 내지 2-34의 화합물로 이루어진 유기발광소자는 정공수송층으로 자주 사용되는 NPB(비교예 2-1), 비교예 2-2, -L-Ar이 페닐기인 비교예 2-3 및 이미다조 퀴나졸린과 카바졸 사이에 링커로 나프탈렌이 연결된 비교예 2-4 보다 저전압, 고효율의 특성을 나타내는 것을 알 수 있다. 특히 화합물 A로부터 제조된 화합물 1 내지 7을 사용한 유기 발광 소자에서 저전압 고효율 특성이 가장 뛰어난 것을 알 수 있다.
따라서, 본 출원에 따른 화학식의 화합물 유도체는 전자 억제 능력뿐만 아니라 정공 수송 능력 또한 우수하여 저전압 및 고효율의 특성을 보이며 유기 발광 소자에 적용 가능함을 확인할 수 있었다.
<실험예 3-1>
합성예 에서 합성된 화합물들을 통상적으로 알려진 방법으로 고순도 승화정제를 한 후, 하기와 같은 방법으로 녹색 유기 발광 소자를 제조하였다.
ITO(ndium tin oxide)가 1,000Å의 두께로 박막 코팅된 유리 기판을 세제를 녹인 증류수에 넣고 초음파로 세척하였다. 이 때, 세제로는 피셔사(Fischer Co.) 제품을 사용하였으며, 증류수로는 밀러포어사(Millipore Co.) 제품의 필터(Filter)로 2차로 걸러진 증류수를 사용하였다. ITO를 30분간 세척한 후 증류수로 2회 반복하여 초음파 세척을 10분간 진행하였다. 증류수 세척이 끝난 후, 이소프로필알콜, 아세톤, 메탄올의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 수송시켰다. 또한, 산소 플라즈마를 이용하여 상기 기판을 5분간 세정한 후 진공 증착기로 기판을 수송시켰다.
이렇게 준비된 ITO 투명 전극 위에 화합물 5를 호스트로 이용하여, m-MTDATA(60nm) / TCTA(80 nm) / 화합물 5 + 10 % Ir(ppy)3(300nm)/ BCP(10 nm) / Alq3(30 nm) / LiF(1 nm) / Al (200nm) 순으로 발광 소자를 구성하여 유기 EL 소자를 제조하였다.
m-MTDATA, TCTA, Ir(ppy)3 및 BCP의 구조는 각각 하기와 같다.
[m-MTDATA] [TCTA]
[Ir(ppy)3] [BCP]
[화합물 5]
<실험예 3-2>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 6을 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-3>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 7을 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-4>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 8를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-5>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 9를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-6>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 10을 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다. .
<실험예 3-7>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 11를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-8>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 12를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-9>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 13를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-10>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 14를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-11>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 15를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-12>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 28를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-13>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 29를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-14>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 30을 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다. .
<실험예 3-15>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 31를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-16>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 32를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-17>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 33를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-18>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 34를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-19>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 35를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-20>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 36를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-21>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 37를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-22>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 38를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-23>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 51를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-24>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 52를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-25>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 53를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-26>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 54를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-27>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 55를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-28>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 56를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-29>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 57를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-30>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 58를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-31>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 59를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-32>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 60를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-33>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 61를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-34>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 74를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-35>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 75를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-36>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 76를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-37>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 77를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-38>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 78를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-39>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 79를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-40>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 80를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-41>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 81를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-42>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 82를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-43>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 83를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<실험예 3-44>
상기 실험예 3-1에서 화합물 5 대신 상기 화합물 84를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
<비교예 3-1>
상기 실험예 3-1에서 화합물 5 대신 GH 1(CBP)를 사용한 것을 제외하고는 실험예 3-1과 동일한 방법으로 유기 발광 소자를 제작하였다.
[GH 1]
실험예 3-1 내지 3-44, 비교예 3-1(CBP)에 의해 제작된 유기 발광 소자에 전류를 인가하였을 때, 성능평가를 하기 표 3에 나타내었다.
| |
화합물(호스트) |
전압(V@10mA/cm2) |
효율(cd/A@10mA/cm2) |
EL 피크(nm) |
| 실험예 3-1 |
화합물 5 |
6.88 |
41.93 |
517 |
| 실험예 3-2 |
화합물 6 |
6.96 |
42.24 |
516 |
| 실험예 3-3 |
화합물 7 |
6.85 |
41.79 |
518 |
| 실험예 3-4 |
화합물 8 |
6.19 |
46.15 |
517 |
| 실험예 3-5 |
화합물 9 |
6.28 |
44.31 |
515 |
| 실험예 3-6 |
화합물 10 |
6.23 |
45.63 |
516 |
| 실험예 3-7 |
화합물 11 |
6.29 |
45.62 |
516 |
| 실험예 3-8 |
화합물 12 |
6.17 |
46.64 |
517 |
| 실험예 3-9 |
화합물 13 |
6.14 |
46.68 |
518 |
| 실험예 3-10 |
화합물 14 |
6.48 |
44.83 |
517 |
| 실험예 3-11 |
화합물 15 |
6.46 |
45.24 |
516 |
| 실험예 3-12 |
화합물 28 |
6.84 |
41.94 |
518 |
| 실험예 3-13 |
화합물 29 |
6.95 |
42.22 |
517 |
| 실험예 3-14 |
화합물 30 |
6.83 |
41.75 |
515 |
| 실험예 3-15 |
화합물 31 |
6.15 |
46.16 |
516 |
| 실험예 3-16 |
화합물 32 |
6.24 |
44.34 |
516 |
| 실험예 3-17 |
화합물 33 |
6.25 |
45.62 |
517 |
| 실험예 3-18 |
화합물 34 |
6.27 |
45.64 |
518 |
| 실험예 3-19 |
화합물 35 |
6.15 |
46.66 |
517 |
| 실험예 3-20 |
화합물 36 |
6.13 |
46.67 |
516 |
| 실험예 3-21 |
화합물 37 |
6.42 |
44.41 |
518 |
| 실험예 3-22 |
화합물 38 |
6.47 |
45.55 |
517 |
| 실험예 3-23 |
화합물 51 |
6.82 |
41.74 |
515 |
| 실험예 3-24 |
화합물 52 |
6.94 |
42.62 |
516 |
| 실험예 3-25 |
화합물 53 |
6.81 |
41.55 |
516 |
| 실험예 3-26 |
화합물 54 |
6.18 |
46.16 |
517 |
| 실험예 3-27 |
화합물 55 |
6.27 |
44.94 |
518 |
| 실험예 3-28 |
화합물 56 |
6.23 |
45.32 |
517 |
| 실험예 3-29 |
화합물 57 |
6.24 |
45.14 |
516 |
| 실험예 3-30 |
화합물 58 |
6.11 |
46.46 |
518 |
| 실험예 3-31 |
화합물 59 |
6.16 |
46.37 |
517 |
| 실험예 3-32 |
화합물 60 |
6.45 |
44.71 |
515 |
| 실험예 3-33 |
화합물 61 |
6.44 |
45.65 |
516 |
| 실험예 3-34 |
화합물 74 |
6.85 |
41.44 |
516 |
| 실험예 3-35 |
화합물 75 |
6.9 |
42.82 |
517 |
| 실험예 3-36 |
화합물 76 |
6.81 |
41.65 |
518 |
| 실험예 3-37 |
화합물 77 |
6.16 |
46.46 |
518 |
| 실험예 3-38 |
화합물 78 |
6.24 |
44.54 |
517 |
| 실험예 3-39 |
화합물 79 |
6.28 |
45.32 |
515 |
| 실험예 3-40 |
화합물 80 |
6.24 |
45.44 |
516 |
| 실험예 3-41 |
화합물 81 |
6.16 |
46.16 |
516 |
| 실험예 3-42 |
화합물 82 |
6.15 |
46.67 |
517 |
| 실험예 3-43 |
화합물 83 |
6.41 |
44.71 |
518 |
| 실험예 3-44 |
화합물 84 |
6.43 |
45.55 |
518 |
| 비교예 3-1 |
GH 1(CBP) |
7.27 |
32.52 |
517 |
상기 표 3에 나타난 바와 같이, 본 출원의 일 실시상태에 따른 화합물을 발광층의 녹색 호스트 물질로 사용하는 실험예 3-1 내지 3-44의 유기 발광 소자는 종래 CBP를 사용하는 비교예 3-1의 유기 발광 소자보다 전류효율 및 구동전압 면에서 우수한 성능을 나타내는 것을 확인할 수 있었다.
<실험예 4-1>
ITO(indium tin oxide)가 1,000Å의 두께로 박막 코팅된 유리 기판을 세제를 녹인 증류수에 넣고 초음파로 세척하였다. 이 때, 세제로는 피셔사(Fischer Co.) 제품을 사용하였으며, 증류수로는 밀러포어사(Millipore Co.) 제품의 필터(Filter)로 2차로 걸러진 증류수를 사용하였다. ITO를 30분간 세척한 후 증류수로 2회 반복하여 초음파 세척을 10분간 진행하였다. 증류수 세척이 끝난 후, 이소프로필알콜, 아세톤, 메탄올의 용제로 초음파 세척을 하고 건조시킨 후 플라즈마 세정기로 수송시켰다. 또한, 산소 플라즈마를 이용하여 상기 기판을 5분간 세정한 후 진공 증착기로 기판을 수송시켰다.
이렇게 준비된 ITO 투명 전극 위에 하기 화학식의 헥사니트릴 헥사아자트리페닐렌 (hexaazatriphenylene; HAT)를 500Å의 두께로 열 진공 증착하여 정공 주입층을 형성하였다.
[HAT]
상기 정공 주입층 위에 정공을 수송하는 물질인 하기 화합물 4-4'-비스[N-(1-나프틸)-N-페닐아미노]비페닐(NPB)(400Å)를 진공 증착하여 정공 수송층을 형성하였다.
[NPB]
이어서, 상기 정공 수송층 위에 막 두께 300Å으로 아래와 같은 BH와 BD를 25:1의 중량비로 진공증착하여 발광층을 형성하였다.
[BH]
[BD]
[LiQ]
상기 발광층 위에 제조예 8에서 제조한 화합물 8과 상기 화합물 LiQ(Lithium Quinolate)를 1:1의 중량비로 진공증착하여 300Å의 두께로 전자 주입 및 수송층을 형성하였다. 상기 전자 주입 및 수송층 위에 순차적으로 12Å두께로 리튬플로라이드(LiF)와 2,000Å 두께로 알루미늄을 증착하여 음극을 형성하였다.
상기의 과정에서 유기물의 증착속도는 0.4~ 0.7Å/sec를 유지하였고, 음극의 리튬플로라이드는 0.3Å/sec, 알루미늄은 2Å/sec의 증착 속도를 유지하였으며, 증착시 진공도는 2 × 10-7 ~5 × 10-6 torr를 유지하여, 유기 발광 소자를 제작하였다.
<실험예 4-2>
상기 실험예 4-1 에서 전자 수송층으로 화합물 8 대신 화합물 9를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-3>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 10을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-4>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 11을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-5>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 12를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-6>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 13을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-7>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 14를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-8>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 15를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-9>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 16을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-10>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 17을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-11>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 19를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-12>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 20을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-13>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 21을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-14>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 22를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-15>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 23을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-16>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 31을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-17>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 35를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-18>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 40을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-19>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 42를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-20>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 43을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-21>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 44를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-22>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 45를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-23>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 46을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-24>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 54를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-25>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 58을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-26>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 63을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-27>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 65를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-28>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 66을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-29>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 67을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-30>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 68을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-31>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 69를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-32>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 77을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-33>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 81을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-34>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 84를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-35>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 85를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-36>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 86을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-37>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 88을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-38>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 89를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-39>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 90을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-40>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 91을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-41>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 92를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-42>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 94를 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-43>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 98을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-44>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 100을 사용한 것을 제외하고는 동일하게 실험하였다.
<실험예 4-45>
상기 실험예 4 에서 전자 수송층으로 화합물 8 대신 화합물 104를 사용한 것을 제외하고는 동일하게 실험하였다.
<비교예 4-1>
상기 실험예 1에서 전자 수송층으로 화합물 8 대신 하기 화합물 ET 1을 사용한 것을 제외하고는 동일하게 실험하였다.
[ET 1]
<비교예 4-2>
상기 실험예 1에서 전자 수송층으로 화합물 8 대신 하기 화합물 ET 2을 사용한 것을 제외하고는 동일하게 실험하였다.
[ET 2]
실험예 4-1 내지 4-44, 비교예 4-1 및 4-2 에 의해 제작된 유기 발광 소자에 전류를 인가하였을 때, 표 4의 결과를 얻었다.
| |
화합물(전자수송층) |
전압(V@10mA/cm2) |
효율(cd/A@10mA/cm2) |
EL 피크(nm) |
| 실험예 4-1 |
화합물 8 |
6.88 |
41.93 |
517 |
| 실험예 4-2 |
화합물 9 |
6.96 |
42.24 |
516 |
| 실험예 4-3 |
화합물 10 |
6.85 |
41.79 |
518 |
| 실험예 4-4 |
화합물 11 |
6.19 |
46.15 |
517 |
| 실험예 4-5 |
화합물 12 |
6.28 |
44.31 |
515 |
| 실험예 4-6 |
화합물 13 |
6.23 |
45.63 |
516 |
| 실험예 4-7 |
화합물 14 |
6.29 |
45.62 |
516 |
| 실험예 4-8 |
화합물 15 |
6.17 |
46.64 |
517 |
| 실험예 4-9 |
화합물 17 |
6.14 |
46.68 |
518 |
| 실험예 4-10 |
화합물 19 |
6.48 |
44.83 |
517 |
| 실험예 4-11 |
화합물 20 |
6.46 |
45.24 |
516 |
| 실험예 4-12 |
화합물 21 |
6.84 |
41.94 |
518 |
| 실험예 4-13 |
화합물 22 |
6.95 |
42.22 |
517 |
| 실험예 4-14 |
화합물 23 |
6.83 |
41.75 |
515 |
| 실험예 4-15 |
화합물 31 |
6.15 |
46.16 |
516 |
| 실험예 4-16 |
화합물 35 |
6.24 |
44.34 |
516 |
| 실험예 4-17 |
화합물 40 |
6.25 |
45.62 |
517 |
| 실험예 4-18 |
화합물 42 |
6.27 |
45.64 |
518 |
| 실험예 4-19 |
화합물 43 |
6.15 |
46.66 |
517 |
| 실험예 4-20 |
화합물 44 |
6.13 |
46.67 |
516 |
| 실험예 4-21 |
화합물 45 |
6.42 |
44.41 |
518 |
| 실험예 4-22 |
화합물 46 |
6.47 |
45.55 |
517 |
| 실험예 4-23 |
화합물 54 |
6.82 |
41.74 |
515 |
| 실험예 4-24 |
화합물 58 |
6.94 |
42.62 |
516 |
| 실험예 4-25 |
화합물 63 |
6.81 |
41.55 |
516 |
| 실험예 4-26 |
화합물 65 |
6.18 |
46.16 |
517 |
| 실험예 4-27 |
화합물 66 |
6.27 |
44.94 |
518 |
| 실험예 4-28 |
화합물 67 |
6.23 |
45.32 |
517 |
| 실험예 4-29 |
화합물 68 |
6.24 |
45.14 |
516 |
| 실험예 4-30 |
화합물 69 |
6.11 |
46.46 |
518 |
| 실험예 4-31 |
화합물 77 |
6.16 |
46.37 |
517 |
| 실험예 4-32 |
화합물 81 |
6.45 |
44.71 |
515 |
| 실험예 4-33 |
화합물 84 |
6.44 |
45.65 |
516 |
| 실험예 4-34 |
화합물 85 |
6.85 |
41.44 |
516 |
| 실험예 4-35 |
화합물 86 |
6.9 |
42.82 |
517 |
| 실험예 4-36 |
화합물 88 |
6.81 |
41.65 |
518 |
| 실험예 4-37 |
화합물 89 |
6.16 |
46.46 |
518 |
| 실험예 4-38 |
화합물 90 |
6.24 |
44.54 |
517 |
| 실험예 4-39 |
화합물 91 |
6.28 |
45.32 |
515 |
| 실험예 4-40 |
화합물 92 |
6.24 |
45.44 |
516 |
| 실험예 4-41 |
화합물 94 |
6.16 |
46.16 |
516 |
| 실험예 4-42 |
화합물 98 |
6.15 |
46.67 |
517 |
| 실험예 4-43 |
화합물 100 |
6.41 |
44.71 |
518 |
| 실험예 4-44 |
화합물 104 |
6.43 |
45.55 |
518 |
| 비교예 4-1 |
ET 1 |
7.27 |
32.52 |
517 |
| 비교예 4-2 |
ET 2 |
7.45 |
30.16 |
517 |
상기 표 4에서 나타난 바와 같이, 본 출원의 일 실시상태에 따른 화합물은 전자 수송 및 주입 능력이 우수하여 유기 발광 소자에 적용 가능함을 확인할 수 있었다.
이상을 통해 본 출원의 바람직한 실시예(전자억제층, 정공수송층, 녹색발광층, 적색발광층, 전자주입층)에 대하여 설명하였지만, 본 출원은 이에 한정되는 것이 아니고 특허청구범위와 발명의 상세한 설명의 범위 안에서 여러 가지로 변형하여 실시하는 것이 가능하고 이 또한 출원의 범주에 속한다.