WO2024253069A1 - 温度応答性マイクロキャリア - Google Patents
温度応答性マイクロキャリア Download PDFInfo
- Publication number
- WO2024253069A1 WO2024253069A1 PCT/JP2024/020256 JP2024020256W WO2024253069A1 WO 2024253069 A1 WO2024253069 A1 WO 2024253069A1 JP 2024020256 W JP2024020256 W JP 2024020256W WO 2024253069 A1 WO2024253069 A1 WO 2024253069A1
- Authority
- WO
- WIPO (PCT)
- Prior art keywords
- cells
- temperature
- cooling
- microcarrier
- polymer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Ceased
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08F—MACROMOLECULAR COMPOUNDS OBTAINED BY REACTIONS ONLY INVOLVING CARBON-TO-CARBON UNSATURATED BONDS
- C08F293/00—Macromolecular compounds obtained by polymerisation on to a macromolecule having groups capable of inducing the formation of new polymer chains bound exclusively at one or both ends of the starting macromolecule
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08J—WORKING-UP; GENERAL PROCESSES OF COMPOUNDING; AFTER-TREATMENT NOT COVERED BY SUBCLASSES C08B, C08C, C08F, C08G or C08H
- C08J3/00—Processes of treating or compounding macromolecular substances
- C08J3/12—Powdering or granulating
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12M—APPARATUS FOR ENZYMOLOGY OR MICROBIOLOGY; APPARATUS FOR CULTURING MICROORGANISMS FOR PRODUCING BIOMASS, FOR GROWING CELLS OR FOR OBTAINING FERMENTATION OR METABOLIC PRODUCTS, i.e. BIOREACTORS OR FERMENTERS
- C12M3/00—Tissue, human, animal or plant cell, or virus culture apparatus
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N11/00—Carrier-bound or immobilised enzymes; Carrier-bound or immobilised microbial cells; Preparation thereof
- C12N11/02—Enzymes or microbial cells immobilised on or in an organic carrier
- C12N11/08—Enzymes or microbial cells immobilised on or in an organic carrier the carrier being a synthetic polymer
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
Definitions
- the present invention relates to a temperature-responsive microcarrier consisting of beads coated with a polymer coating film that contains a temperature-responsive polymer and a negatively charged polymer.
- Patent Document 1 describes a microcarrier made of beads made from synthetic polymers and natural polymers such as polysaccharides. By placing the microcarrier in a container containing a cell suspension and culturing it, the cells grow on the surface of the microcarrier, and cell growth per unit volume of medium can be increased.
- the temperature-responsive microcarrier described in Patent Document 2 when using the temperature-responsive microcarrier described in Patent Document 2, cells can be detached from the microcarrier surface by cooling without the need for proteolytic enzymes, simplifying the process.
- the temperature-responsive microcarrier described in Patent Document 2 does not always detach cells sufficiently, and there is a demand for a temperature-responsive microcarrier that exhibits more suitable temperature responsiveness.
- the present inventors have conducted extensive research and found that a suitable temperature responsiveness can be achieved by using a microcarrier made of beads coated with a polymer coating film containing a temperature-responsive polymer having a lower critical solution temperature of 0° C. to 50° C. and a negatively charged polymer, and have thus completed the present invention. That is, the present invention includes the following aspects. ⁇ 1> A microcarrier comprising beads coated with a polymer coating film containing a temperature-responsive polymer having a lower critical solution temperature of 0°C to 50°C and a negatively charged polymer. ⁇ 2> The microcarrier according to ⁇ 1>, wherein the proportion of the negatively charged polymer is 0.1 to 20 wt %.
- ⁇ 3> The microcarrier according to ⁇ 1> or ⁇ 2>, wherein the negatively charged polymer contains a carboxy group.
- ⁇ 4> The microcarrier according to any one of ⁇ 1> to ⁇ 3>, wherein the ratio of carboxyl groups in the negatively charged polymer is 10 to 50 wt %.
- ⁇ 5> The microcarrier according to any one of ⁇ 1> to ⁇ 4>, wherein the bead surface is cationic.
- ⁇ 6> The microcarrier according to any one of ⁇ 1> to ⁇ 5>, wherein the beads are modified with a functional group having a positive charge.
- ⁇ 7> The microcarrier according to any one of ⁇ 1> to ⁇ 6>, wherein the beads are trimethylammonium chloride-modified polystyrene.
- ⁇ 8> The microcarrier according to any one of ⁇ 1> to ⁇ 7>, wherein the particle size of the beads is 20 ⁇ m to 1000 ⁇ m.
- ⁇ 9> The microcarrier according to any one of ⁇ 1> to ⁇ 8>, wherein the temperature-responsive polymer is a block copolymer containing the following blocks (A), (B), and (C): (A) A polymer block having an HLB value (Griffin method) in the range of 7 or more and 20 or less.
- HLB value Griffin method
- (B) A polymer block having an HLB value (Griffin method) in the range of 0 or more and less than 7.
- C A temperature-responsive polymer block having a lower critical solution temperature (LCST) in water in the range of 0°C to 50°C.
- LCST lower critical solution temperature
- ⁇ 10> A method for producing a microcarrier according to any one of ⁇ 1> to ⁇ 9>.
- ⁇ 11> A method for producing a microcarrier according to any one of ⁇ 1> to ⁇ 9>, comprising a step of coating the beads with a polymer coating film containing a temperature-responsive polymer having a lower critical solution temperature of 0°C to 50°C and a polymer having a negative charge.
- ⁇ 12> A cell culture method using the microcarrier according to any one of ⁇ 1> to ⁇ 9>.
- a cell culture method comprising the step of culturing cells in a medium containing the microcarrier according to any one of ⁇ 1> to ⁇ 9>.
- a microcarrier consisting of beads coated with a polymer coating film containing a temperature-responsive polymer with a lower critical dissolution temperature between 0°C and 50°C and a negatively charged polymer can exhibit suitable temperature responsiveness.
- the present invention is a microcarrier consisting of beads coated with a polymer coating film that contains a temperature-responsive polymer with a lower critical solution temperature between 0°C and 50°C and a negatively charged polymer.
- the temperature-responsive polymer in the present invention is not particularly limited as long as the compatibility changes when the lower critical solution temperature is from 0° C. to 50° C. However, in order to significantly exhibit the change in compatibility, it is preferable that the temperature-responsive polymer is a block copolymer.
- An example of the block copolymer is a block copolymer containing the following blocks (A), (B), and (C).
- B A polymer block having an HLB value (Griffin method) in the range of 0 or more and less than 7.
- C A temperature-responsive polymer block having a lower critical solution temperature (LCST) in water in the range of 0°C to 50°C.
- the HLB value (Hydrophile-Lipophile Balance: HLB) is a value expressing the degree of affinity for water and oil, as described in W. C. Griffin, Journal of the Society of Cosmetic Chemists, 1, 311 (1949). It takes a value from 0 to 20, and the closer to 0, the higher the hydrophobicity, and the closer to 20, the higher the hydrophilicity.
- Methods for calculating the HLB value by a formula include the Atlas method, the Griffin method, the Davis method, and the Kawakami method.
- the value calculated by the Griffin method is used, and the value is calculated by the following formula based on the formula weight of the hydrophilic portion in the repeating unit of each block constituting the block copolymer of the present invention and the total formula weight of the repeating units.
- HLB value 20 x (formula weight of hydrophilic portion in repeating unit) ⁇ (total formula weight of repeating units)
- hydrophilic moieties in the repeating units of each block include a sulfone moiety (-SO 3 -), a phosphono group (-PO 3 -), a carboxyl group (-COOH), an ester group (-COO-), an amide group (-CONH-), an imide group (-CON-), an aldehyde group (-CHO), a carbonyl group (-CO-), a hydroxyl group (-OH), an amino group (-NH 2 ), an acetyl group (-COCH 3 ), an ethyleneamine group (-CH 2 CH 2 N-), an ethyleneoxy group (-CH 2 CH 2 O-), an alkali metal ion, an alkaline earth metal ion, an ammonium ion, a halide ion, and an acetate ion.
- the atoms constituting the hydrophilic portion must not overlap with the atoms constituting other hydrophilic portions.
- An example of calculating the HLB value in a repeating unit is shown below.
- the hydrophilic portion is one part ester portion, one part phosphono group portion, and one part ethyleneamine portion, and the molecular weight of the hydrophilic portion is 181.04, so the HLB value is 12.3.
- the hydrophilic portion is one part ester portion and one part ethyleneamine portion, and the molecular weight of the hydrophilic portion is 86.07, so the HLB value is 11.0.
- the hydrophilic portion is one part ester portion, and the molecular weight of the hydrophilic portion is 44.01, so the HLB value is 8.8.
- the hydrophilic portion is one part ester, and the molecular weight of the hydrophilic portion is 44.01, so the HLB value is 6.2.
- the lower critical solution temperature is the temperature below which a polymer dissolves in water to form a transparent solution, but above which it becomes insoluble and either becomes cloudy or precipitates, resulting in phase separation.
- temperature-responsive polymers include homopolymers composed only of component (C), copolymers composed of components (A) and (C), and copolymers composed of components (B) and (C).
- the copolymers may be random or block copolymers.
- the number average molecular weight of the temperature-responsive polymer is not particularly limited, but an example is 1,000 to 1,000,000, preferably 5,000 to 500,000, and more preferably 10,000 to 200,000.
- a negatively charged polymer is a polymer having a functional group that ionizes in water and exhibits anionic properties.
- the functional group that exhibits anionic properties examples include hydroxyl groups, carboxy groups, and sulfo groups. Among these, carboxy groups are preferred because of the ease of controlling the acidity.
- the repeating units of the negatively charged polymer examples include vinylphenol, acrylic acid, methacrylic acid, and styrene sulfonic acid.
- the negatively charged polymer may also contain repeating units of a polymer that does not have a negative charge, and an example is a copolymer of styrene sulfonic acid and styrene.
- the copolymer may also be a random copolymer or a block copolymer.
- the functional group of the negatively charged polymer is a carboxy group
- the proportion of carboxy groups in the negatively charged polymer is 10 to 50 wt%, preferably 15 to 40 wt%, and more preferably 20 to 30 wt%.
- the number average molecular weight of the negatively charged polymer is not particularly limited, but an example is 1,000 to 1,000,000, preferably 5,000 to 500,000, and more preferably 10,000 to 200,000.
- beads are powder particles.
- the particle size of the beads there is no particular limitation on the particle size of the beads, and examples thereof are 1 ⁇ m to 10 mm, 5 ⁇ m to 5 mm, and 20 ⁇ m to 1000 ⁇ m.
- the shape of the beads there is no particular limitation on the shape of the beads, and examples thereof include a sphere, a rectangular parallelepiped, a cylindrical column, a cylindrical shape, and a star shape.
- the true density of the beads but the higher the density of the polymer solution used in producing the temperature-responsive microcarrier, the more preferable it is, and an example thereof is 0.9 to 20.0 g/cm 2.
- the beads may or may not have pores.
- the specific surface area per dry weight of the beads there is no particular limitation on the specific surface area per dry weight of the beads, and an example thereof is 10 to 100,000 cm 2 /g.
- the specific surface area per dry weight can be measured by the BET (Brunauer Emmett Teller) method, but in this application, it is calculated from the average particle size and particle specific gravity obtained from SEM images.
- the material of the beads there is no particular limit to the material of the beads, and various materials can be used, such as metals, metal oxides, inorganic salts, synthetic polymers, biopolymers, or composites of these.
- the surface of the beads it is preferable that the surface is cationic or modified with a positively charged functional group in order to enhance cell proliferation.
- positively charged functional groups include ammonium groups and ammonium group derivatives.
- Specific examples of beads include polystyrene, and trimethylammonium chloride-modified polystyrene is preferred.
- the method for producing the temperature-responsive microcarrier is not particularly limited, but examples include a general method of physically coating the beads by adsorbing a polymer, or a chemical coating method by fixing a polymer to the beads by covalent bonding.
- the coating method is not particularly limited, and examples include the impregnation method, immersion method, and Henschel mixer method. In the impregnation method and immersion method, the beads are immersed or sprayed with a polymer solution, and the solvent is removed by reducing the pressure to obtain a temperature-responsive microcarrier.
- the beads are stirred with an impeller in a reaction vessel equipped with an impeller, and a polymer coating solution is added while blowing a drying gas into the reaction vessel, thereby obtaining a temperature-responsive microcarrier in a short time.
- the Henschel mixer method and the impregnation method have the advantage that the entire amount of the polymer solution used can be adsorbed, making it easy to adjust the composition ratio and coating amount of the temperature-responsive polymer and the negatively charged polymer.
- the polymer is fixed to the beads by a chemical covalent bond, there is no particular limitation on the type of chemical covalent bond, examples of which include ester bonds, amide bonds, ether bonds, and thioether bonds.
- Temperature-responsive microcarriers can be obtained by removing unreacted compounds by washing after the reaction.
- the drying gas there is no particular limitation on the drying gas, and any gas that is not reactive with the beads and polymer coating solution, such as nitrogen, air, argon, and neon, can be used.
- the method for producing a temperature-responsive microcarrier may be, for example, a method characterized by comprising a step of coating beads with a polymer coating film containing a temperature-responsive polymer having a lower critical solution temperature of 0°C to 50°C and a polymer having a negative charge.
- the proportion of the negatively charged polymer in the temperature-responsive microcarrier is not particularly limited, but is, for example, 0.1 to 20 wt %, and in order to exhibit suitable temperature responsiveness, is preferably 0.3 to 10 wt %, more preferably 0.5 to 5 wt %, even more preferably 0.5 to 4 wt %, and particularly preferably 0.5 to 3 wt %.
- the temperature-responsive microcarriers can be used for cell culture, particularly for cell culture of adherent cells.
- Adherent cells are cells that grow while adhering to the surface of a cell culture substrate such as a microcarrier.
- a cell culture substrate such as a microcarrier.
- adherent cells There are no particular limitations on the origin of the adherent cells to be cultured, but examples include mammals such as humans, monkeys, dogs, cats, rabbits, rats, nude mice, mice, guinea pigs, pigs, sheep, Chinese hamsters, and cows, and birds such as chickens and ducks.
- the type of cells (adherent cells) to be cultured is not particularly limited, and examples thereof include human or animal-derived mesenchymal stem cells, CHO cells derived from Chinese hamster ovaries, VERO cells derived from African green monkey kidney epithelium, MDCK cells derived from dog kidneys, MRC-5 cells derived from normal human fetal lung tissue, CEF cells derived from chicken fetuses, BHK cells derived from hamster kidneys, L929 cells derived from mouse connective tissue, HEK293 cells derived from human fetal kidneys, MDBK cells derived from bovine kidneys, CRFK cells derived from cat kidneys, CPK cells derived from guinea pig kidneys, HeLa cells derived from human cervical cancer, and further, epithelial cells and endothelial cells constituting each tissue and organ in the body, skeletal muscle cells that exhibit contractility, smooth muscle cells, cardiac muscle cells, neuron cells that constitute the nervous system, glial cells, fibros,
- cell lines in which the above-mentioned cell types have been immortalized.
- Other examples include cells contained in blood, lymph, cerebrospinal fluid, sputum, urine, or feces, and microorganisms, viruses, protozoa, etc. present in the body or in the environment.
- the type of medium used it may be a serum medium or a serum-free medium, and can be selected appropriately depending on the type of cell.
- the type of basal medium used in the culture of the present invention is not particularly limited, and examples of the medium that can be used include MEM, ⁇ MEM, DMEM, EMEM, GMEM, DMEM/Ham's F-12, Ham's F-12, Ham's F-10, Medium 199, and RPMI 1640.
- the medium may be a serum medium or a serum-free medium, and the serum used is not particularly limited, and examples of the serum that can be used include fetal bovine serum (FBS), calf serum, adult bovine serum, horse serum, sheep serum, goat serum, pig serum, chicken serum, rabbit serum, and human serum.
- FBS fetal bovine serum
- the complete medium may or may not contain antibiotics, and can be selected appropriately depending on the type of cells.
- the cells may be cultured under stationary conditions or under agitated conditions.
- the agitation speed there is no particular limitation on the agitation speed, and one example is 1 to 1000 rpm.
- the culture temperature during culture but it is preferable to perform the culture at or above the LCST, which can provide an environment in which the surface of the temperature-responsive polymer-coated microcarrier becomes hydrophobic and cells can easily adhere. After culture, the cells on the microcarrier can be recovered by cooling to a temperature below the LCST.
- the cells may be directly cooled using a cooler, or the medium may be replaced with a cooling liquid.
- the cooling liquid may be a basal medium, a complete medium containing growth factors and serum, or a phosphate buffer, but by selecting a phosphate buffer, the cells are easily detached from the microcarrier. If a chelating agent such as EDTA or EGTA is introduced into the phosphate buffer for cooling, the cells are more easily detached from the microcarrier as single cells.
- single cells mean that the cells have left the state in which they were connected to each other and have been separated into individual cells.
- the concentration of the chelating agent in the phosphate buffer is not particularly limited and is between 1 ⁇ M and 1 mM.
- the cooling liquid it is preferable for the cooling liquid to have a flow, as this can promote cooling of the temperature-responsive microcarriers. For example, a flow can be obtained by stirring or pipetting.
- the cell culture method using the temperature-responsive microcarrier of the present invention may be, for example, a method characterized by including a step of culturing cells in a medium containing the microcarrier of the present invention.
- the cell culture method using the temperature-responsive microcarrier of the present invention may further include a cooling cell detachment step of detaching the cells from the microcarrier using a cooling liquid containing a chelating agent.
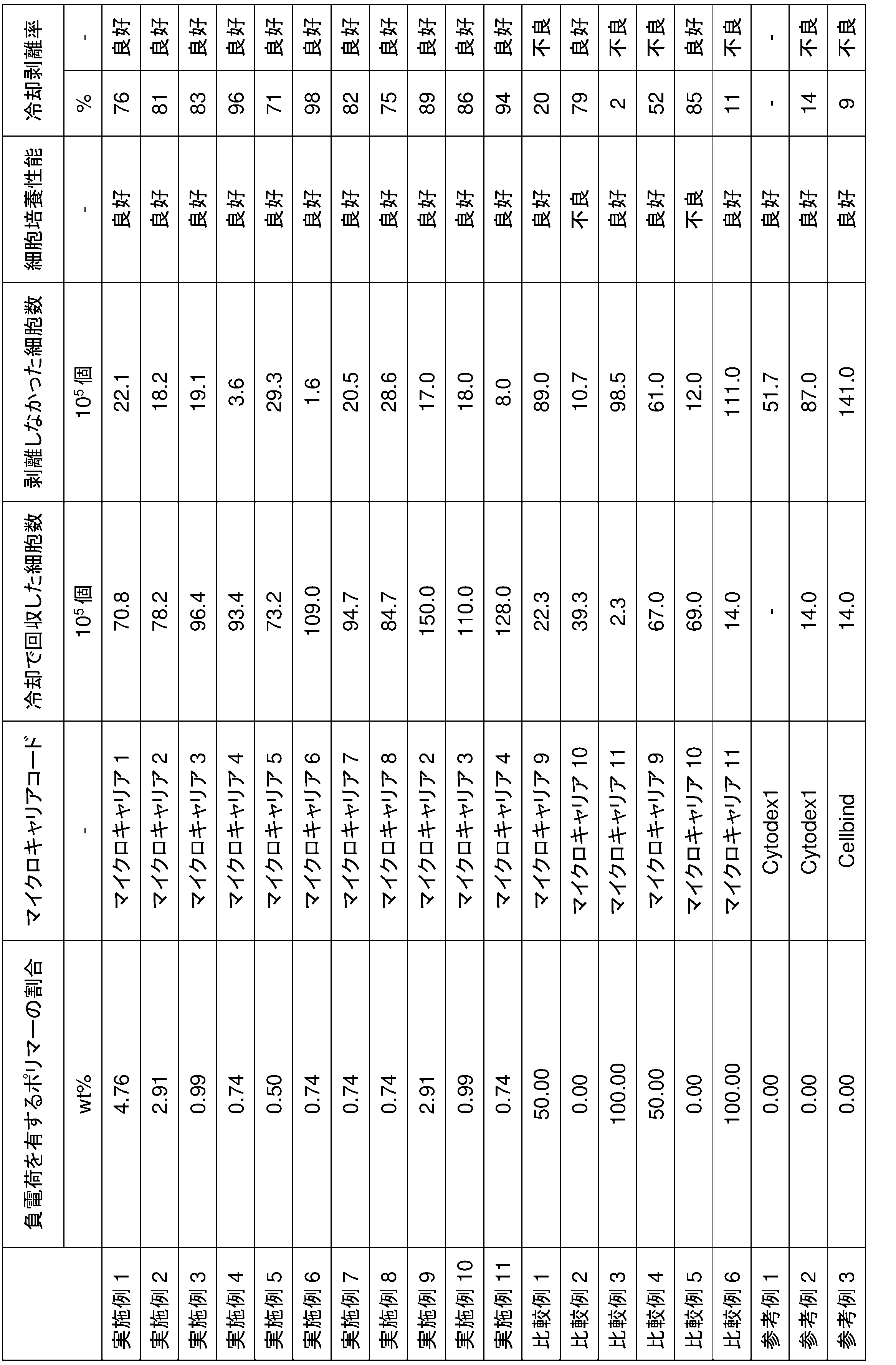
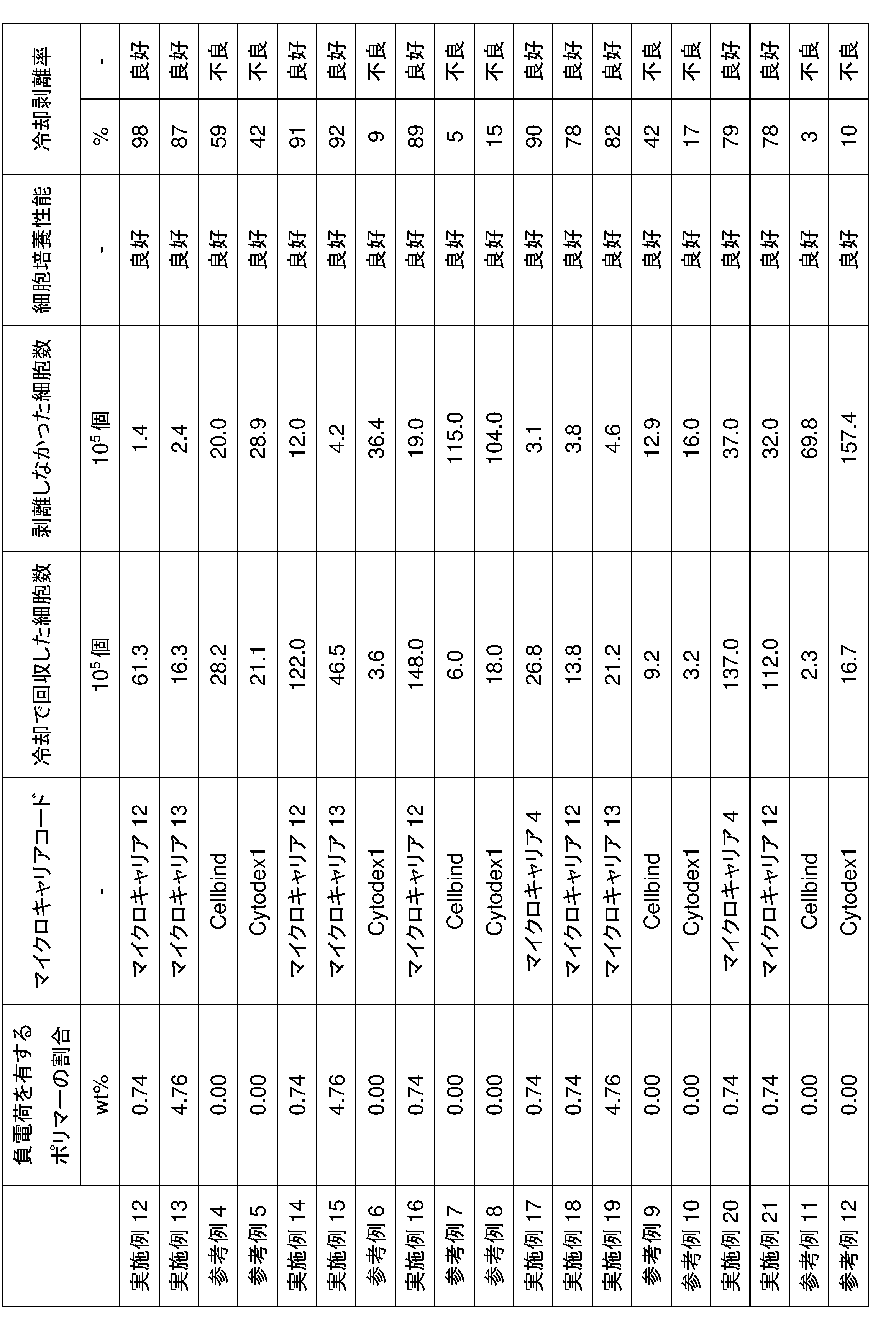
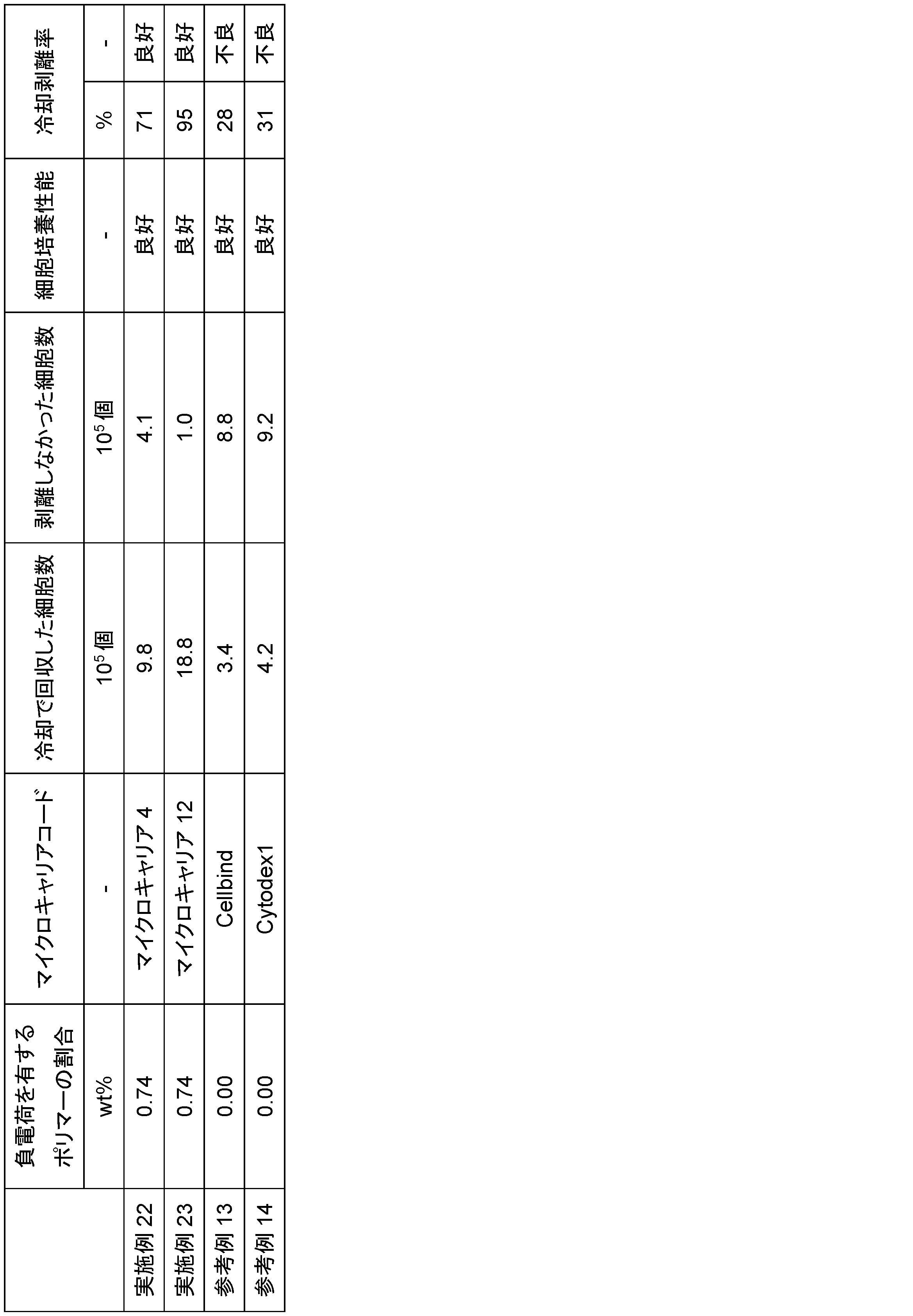
- the culture performance of the temperature-responsive microcarrier of the present invention is evaluated by the total cell number and the cooling detachment rate. If the total cell number is equal to or lower than the total cell number cultured in a current general-purpose microcarrier with the same culture area, it is judged to have poor culture performance.
- the current general-purpose microcarrier is Cytodex1 with a cationic surface from Cytiva and/or Cellbind with an anionic surface from Corning.
- the method for evaluating the temperature-responsive cooling detachment rate there is no particular limitation on the method for evaluating the temperature-responsive cooling detachment rate, but as an example, (1) the number of cells recovered by cooling is measured, and (2) the number of cells that were not detached by cooling is measured using a protease, and the number of cells in (1) is divided by the sum of the number of cells in (1) and (2), and the result is multiplied by 100 to evaluate the cooling detachment rate.
- the method for measuring the number of cells but it can be evaluated using a hemocytometer or the like.
- the GPC device used was a Tosoh Corporation HLC-8320GPC, and two Tosoh Corporation TSKgel SuperAWM-H columns were used. The column temperature was set to 40°C, and the eluent was 2,2,2-trifluoroethanol containing 10 mM sodium trifluoroacetate.
- the measurement sample was prepared at 1.0 mg/mL and measured.
- polymethylmethacrylate Sigma-Aldrich
- the reaction solution was purified by reprecipitation with water and dried under reduced pressure to obtain a yellow solid.
- the obtained yellow solid was dissolved in chloroform, and the chloroform phase was collected using a separatory funnel.
- the collected chloroform phase was concentrated in an evaporator and purified by reprecipitation with hexane.
- the precipitate was collected by filtration and dried under reduced pressure to obtain 5.805 g of polymer MBI.
- ⁇ Polymer CStS having negative charge> 1.156 g (8 mmol) of p-carboxystyrene (CSt) and 1.271 g (12 mmol) of styrene (St) were added to a 100 mL two-neck flask, and 3.3 mg (20 ⁇ mol) of azobisisobutyronitrile and 20 mL of tert-butyl alcohol were added. After argon gas replacement, the mixture was heated and stirred at 64° C. for 24 hours. The reaction solution was purified by reprecipitation with n-heptane and dried under reduced pressure to obtain 0.92 g of polymer CStS. The composition ratio of polymer CStS was CSt/St 33/67 (mol%), the number average molecular weight Mn was 106,000, and the molecular weight distribution Mw/Mn was 1.84.
- the rotary evaporator was a Tokyo Rika Kikai N-1300
- the small cooling water circulation device was a Tokyo Rika Kikai CCA-1112A
- the diaphragm type vacuum pump was a Tokyo Rika Kikai NVP-2100V
- the water bath was a Tokyo Rika Kikai OSB-2200.
- Water was used as the fluid for the small cooling water circulation device, and the temperature was set to 3°C. The temperature of the water bath was set to 50°C.
- Example 1 10 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 10 g of 1-methoxy-2-propanol solution of 0.0025 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were further added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute.
- the mixture was further subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the mixture was finally subjected to vacuum impregnation treatment by reducing the pressure to 1,500 Pa by treating for 30 minutes with the vacuum pump at its maximum output.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarrier 1, which contains 4.76 wt% of negatively charged polymer.
- ⁇ Human bone marrow-derived mesenchymal stem cell culture> To a 30 mL single-use bioreactor manufactured by Able, 204 mg (culture area 87 cm2 ) of temperature-responsive microcarrier 1 and 30 mL of mesenchymal stem cell proliferation medium 2 manufactured by PromoCell were added. Furthermore, 5 x 105 cells of human bone marrow-derived mesenchymal stem cells (passage number 2) manufactured by Lonza were added and cultured for 6 days under stirring conditions of 100 rpm in an incubator with a 5 vol% CO2 atmosphere at 37°C.
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, left to settle the microcarriers, 22.5 mL of the medium was removed, and 22.5 mL of phosphate buffered saline (PBS(-)) containing 1 mM EDTA at 4 ° C. without calcium and magnesium was added and left to stand for 10 minutes. After standing, the mixture was stirred at 300 rpm for 3 minutes at room temperature.
- the cell suspension was passed through a 50 mL tube with a cell strainer with a 70 ⁇ m opening, and 5 mL of PBS(-) was added twice on the cell strainer, the cells were collected in the tube, concentrated by centrifugation, and the cell number was counted.
- the number of cells collected by cooling was 70.8 ⁇ 10 5 cells.
- the microcarriers on the cell strainer were then transferred to a 15 mL tube, 5 mL of TrypLE Express Enzyme (manufactured by Thermo Fisher Scientific) was added, and the tube was left to stand for 5 minutes in a 5 vol% CO2 atmosphere at 37 °C.
- the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a 70 ⁇ m opening, and 5 mL of PBS (-) was added twice onto the cell strainer to collect the cells in the tube, which were then concentrated by centrifugation to count the number of cells.
- the number of cells that could not be collected by cooling was 22.1 ⁇ 105.
- the cooling detachment rate was 76%.
- Example 2 10 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 10 g of 1-methoxy-2-propanol solution of 0.0015 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were added and left to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was treated at a constant pressure of 12,000 Pa for 1 minute.
- the mixture was further treated at a constant pressure of 10,000 Pa for 1 minute, at 8,000 Pa for 1 minute, at 6,000 Pa for 2 minutes, and at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the mixture was finally treated for 30 minutes with the vacuum pump at its maximum output, reducing the pressure to 1,500 Pa and performing vacuum impregnation.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, and the flask was left to stand for 10 minutes while being exposed to ultrasonic waves.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarrier 2, which contains 2.91 wt% of negatively charged polymer.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that temperature-responsive microcarrier 2 was used.
- the number of cells recovered by cooling was 78.2 x 105
- the number of cells that could not be recovered by cooling was 18.2 x 105.
- the cooling detachment rate was 81%.
- Example 3 10 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 10 g of 1-methoxy-2-propanol solution of 0.0005 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were further added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12000 Pa for 1 minute.
- the mixture was further subjected to constant pressure treatment at 10000 Pa for 1 minute, constant pressure treatment at 8000 Pa for 1 minute, constant pressure treatment at 6000 Pa for 2 minutes, and constant pressure treatment at 4000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the vacuum pump was finally set to maximum output for 30 minutes to reduce the pressure to 1500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarrier 3, which contains 0.99 wt% of negatively charged polymer.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except for using temperature-responsive microcarrier 3.
- the number of cells recovered by cooling was 96.4 x 105
- the number of cells that could not be recovered by cooling was 19.1 x 105.
- the cooling detachment rate was 83%.
- Example 4 10 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 10 g of 1-methoxy-2-propanol solution of 0.00038 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were further added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12000 Pa for 1 minute. The mixture was further subjected to constant pressure treatment at 10000 Pa for 1 minute, constant pressure treatment at 8000 Pa for 1 minute, constant pressure treatment at 6000 Pa for 2 minutes, and constant pressure treatment at 4000 Pa for 3 minutes, for vacuum impregnation treatment.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarrier 4, which contains 0.74 wt% of negatively charged polymer.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that temperature-responsive microcarrier 4 was used.
- the number of cells recovered by cooling was 93.4 x 105
- the number of cells that could not be recovered by cooling was 3.6 x 105.
- the cooling detachment rate was 96%.
- Example 5 10 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 10 g of 1-methoxy-2-propanol solution of 0.00025 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were further added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute.
- the mixture was further subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the vacuum pump was finally set to maximum output for 30 minutes to reduce the pressure to 1,500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarrier 5, which contains 0.50 wt% of negatively charged polymer.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that temperature-responsive microcarrier 5 was used.
- the number of cells recovered by cooling was 73.2 x 105
- the number of cells that could not be recovered by cooling was 29.3 x 105.
- the cooling detachment rate was 71%.
- Example 6 12 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 12 g of 1-methoxy-2-propanol solution of 0.00038 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute.
- the mixture was further subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the vacuum pump was set to maximum output for 30 minutes to reduce the pressure to 1,500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, and the mixture was exposed to ultrasound and left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the mixture was treated for 30 minutes to obtain temperature-responsive microcarriers 6 with a negatively charged polymer ratio of 0.74 wt%.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that temperature-responsive microcarriers 6 were used.
- the number of cells recovered by cooling was 109.0 x 105
- the number of cells that could not be recovered by cooling was 1.6 x 105.
- the cooling detachment rate was 98%.
- the mixture was further subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the vacuum pump was set to maximum output for 30 minutes to reduce the pressure to 1,500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarrier 7, which contains 0.74 wt% of negatively charged polymer.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except for using temperature-responsive microcarriers 7.
- the number of cells recovered by cooling was 94.7 x 105 , and the number of cells that could not be recovered by cooling was 20.5 x 105.
- the cooling detachment rate was 82%.
- Example 8 In a 200 mL flask, 6 g of a 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 6 g of a 1-methoxy-2-propanol solution of 0.00038 wt% polymer CStS were added. Furthermore, 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) having a diameter of 130 ⁇ m were added and left to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12000 Pa for 1 minute.
- a 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 6 g of a 1-methoxy-2-propanol solution of 0.00038 wt% polymer CStS were added. Furthermore, 10 g of dried polystyrene
- constant pressure treatment was performed at 10000 Pa for 1 minute, constant pressure treatment at 8000 Pa for 1 minute, constant pressure treatment at 6000 Pa for 2 minutes, and constant pressure treatment at 4000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and finally, the vacuum pump was set to maximum output and treated for 30 minutes to reduce the pressure to 1500 Pa, and vacuum impregnation treatment was performed.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that temperature-responsive microcarriers 8 were used.
- the number of cells recovered by cooling was 84.7 x 105
- the number of cells that could not be recovered by cooling was 28.6 x 105.
- the cooling detachment rate was 75%.
- Example 9 ⁇ VERO cell culture> 356 mg (culture area 150 cm 2 ) of temperature-responsive microcarrier 2 and 30 mL of DMEM (Dulbecco's Modified Eagle Medium, Wako Pure Chemical Industries) containing 10% fetal bovine serum (Biowest Co., Ltd.) and 1% antibiotic-antimycotic solution (Wako Pure Chemical Industries, Ltd.) were added to a 30 mL single-use bioreactor manufactured by Able Co., Ltd. Furthermore, 1 x 10 6 cells of VERO cells (passage number 16) manufactured by JCRB Cell Bank were added and cultured for 8 days under stirring conditions of 120 rpm in an incubator with a 5 vol% CO 2 atmosphere at 37°C.
- DMEM Dynamic Eagle Medium
- fetal bovine serum Biowest Co., Ltd.
- antibiotic-antimycotic solution (Wako Pure Chemical Industries, Ltd.)
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, the cell suspension was passed through a 50 mL tube with a cell strainer with a mesh size of 70 ⁇ m, the floating cells were removed, and only the microcarriers to which the cells on the cell strainer were attached were collected, and phosphate buffered saline (PBS (-)) free of calcium and magnesium at 4 ° C was added and allowed to stand for 10 minutes. After standing, pipetting was performed 60 times, and the detached cells were collected by passing them through a 50 mL tube with a cell strainer with a mesh size of 70 ⁇ m, and the cells were concentrated by centrifugation and counted.
- PBS (-) phosphate buffered saline
- Example 10 ⁇ VERO cell culture> VERO cells were cultured and the number of cells was counted in the same manner as in ⁇ VERO cell culture> of Example 9, except that temperature-responsive microcarrier 3 was used.
- the number of cells recovered by cooling was 11.0 x 106
- the number of cells that could not be recovered by cooling was 1.8 x 106.
- the cooling detachment rate was 86%.
- Example 11 ⁇ VERO cell culture> VERO cells were cultured and the number of cells was counted in the same manner as in ⁇ VERO cell culture> of Example 9, except that temperature-responsive microcarrier 4 was used.
- the number of cells recovered by cooling was 12.8 x 106
- the number of cells that could not be recovered by cooling was 0.8 x 106.
- the cooling detachment rate was 94%.
- Comparative Example 1 10 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 10 g of 1-methoxy-2-propanol solution of 0.050 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m were further added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that temperature-responsive microcarrier 9 was used.
- the number of cells recovered by cooling was 22.3 x 105
- the number of cells that could not be recovered by cooling was 89.0 x 105.
- the cooling detachment rate was 20%.
- Comparative Example 2 10 g of a 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI was added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m was further added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute.
- the mixture was further subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the vacuum pump was set to maximum output for 30 minutes to reduce the pressure to 1,500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, and the flask was left to stand for 10 minutes while being exposed to ultrasonic waves.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarriers 10 with a negatively charged polymer ratio of 0.00 wt%.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that the temperature-responsive microcarrier 10 was used.
- the number of cells recovered by cooling was 39.3 x 105
- the number of cells that could not be recovered by cooling was 10.7 x 105.
- the cooling detachment rate was 79%, but the total number of cells was lower than the total number of cells cultured using the current general-purpose microcarrier described in Reference Example 1.
- Comparative Example 3 10 g of 1-methoxy-2-propanol solution of 0.050 wt% polymer CStS was added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m was added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute. The mixture was then subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes. The stirring speed was set to 120 rpm, and the vacuum pump was set to maximum output for 30 minutes to reduce the pressure to 1,500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain microcarriers 11 with a negatively charged polymer ratio of 100.00 wt%.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except for using the temperature-responsive microcarrier 11.
- the number of cells recovered by cooling was 2.3 x 105
- the number of cells that could not be recovered by cooling was 98.5 x 105.
- the cooling detachment rate was 2%.
- VERO cells were cultured and the number of cells was counted in the same manner as in ⁇ VERO cell culture> of Example 9, except that temperature-responsive microcarrier 11 was used.
- the number of cells recovered by cooling was 1.4 x 106
- the number of cells that could not be recovered by cooling was 11.1 x 106.
- the cooling detachment rate was 85%.
- Reference Example 1 Human bone marrow-derived mesenchymal stem cell culture> 20 mg (culture area 87 cm2 ) of autoclave-sterilized Cytodex1 (surface: cationic, average specific gravity: 1.03) was added to a 30 mL single-use bioreactor manufactured by Able Co., Ltd. Furthermore, 5 x 105 cells of human bone marrow-derived mesenchymal stem cells (passage number 2) manufactured by Lonza were added and cultured for 6 days under stirring conditions of 60 rpm in an incubator with a 5 vol% CO2 atmosphere at 37°C.
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, left to settle Cytodex1, 27 mL of medium was removed, and 27 mL of PBS(-) was added. Cytodex1 was left to settle, 27 mL of liquid was removed, 5 mL of TrypLE Express Enzyme (manufactured by Thermo Fisher Scientific) was added, and the mixture was left to stand for 5 minutes in a 5 vol% CO2 atmosphere at 37 ° C.
- the cell suspension was passed through a 50 mL tube with a cell strainer with a 70 ⁇ m opening, and 5 mL of PBS(-) was added twice on the cell strainer, the cells were collected in the tube, concentrated by centrifugation, and the cell number was measured. The cell number was 51.7 ⁇ 10 5 cells.
- Reference Example 2 ⁇ VERO cell culture> VERO cells were cultured and the number of cells was counted in the same manner as in ⁇ VERO cell culture> in Example 9, except that 34.1 mg (culture area 150 cm2 ) of the microcarrier of Reference Example 1 (Cytodex 1, surface: cationic, average specific gravity: 1.03) was used and the stirring speed was set to 60 rpm.
- the number of cells recovered by cooling was 1.4 x 106
- the number of cells that could not be recovered by cooling was 8.7 x 106.
- the cooling detachment rate was 14%.
- Reference Example 3 ⁇ VERO cell culture> 416 mg (culture area 150 cm 2 ) of autoclave-sterilized Cellbind (surface: anionic, average specific gravity: 1.026) was added to a 30 mL single-use bioreactor manufactured by Able. 30 mL of DMEM (Dulbecco's Modified Eagle Medium, Wako Pure Chemical Industries) containing 10% fetal bovine serum (Biowest) and 1% antibiotic-antimycotic solution (Wako Pure Chemical Industries) was then added. 1 ⁇ 10 6 cells of VERO cells (passage number 16) manufactured by JCRB Cell Bank were then added and cultured for 8 days at 37° C. in an incubator with a 5 vol% CO 2 atmosphere at 120 rpm.
- DMEM Disulbecco's Modified Eagle Medium, Wako Pure Chemical Industries
- VERO cells were cultured and the number of cells was counted in the same manner as in ⁇ VERO cell culture> in Example 9, except that Cellbind microcarriers were used.
- the number of cells recovered by cooling was 1.4 x 106
- the number of cells that could not be recovered by cooling was 14.1 x 106.
- the cooling detachment rate was 9%.
- Example 12 12 g of 1-methoxy-2-propanol solution of 0.050 wt% temperature-responsive block copolymer MBI and 12 g of 1-methoxy-2-propanol solution of 0.00038 wt% polymer CStS were added to a 200 mL flask. 10 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.03) with a diameter of 130 ⁇ m were added and allowed to stand for 1 minute. The flask was placed in an evaporator, the stirring speed was set to 60 rpm, and the mixture was subjected to constant pressure treatment at 12,000 Pa for 1 minute.
- the mixture was further subjected to constant pressure treatment at 10,000 Pa for 1 minute, constant pressure treatment at 8,000 Pa for 1 minute, constant pressure treatment at 6,000 Pa for 2 minutes, and constant pressure treatment at 4,000 Pa for 3 minutes.
- the stirring speed was set to 120 rpm, and the vacuum pump was set to maximum output for 30 minutes to reduce the pressure to 1,500 Pa, and vacuum impregnation treatment was performed.
- the flask was removed from the evaporator, 150 mL of ion-exchanged water was added, ultrasonic waves were applied, and the flask was left to stand for 10 minutes.
- the beads collected by filtration were transferred to a 200 mL flask, and the stirring speed in the evaporator was set to 120 rpm.
- the vacuum pump was set to maximum output and the flask was left to stand for 30 minutes to obtain temperature-responsive microcarriers 12 with a negatively charged polymer ratio of 0.74 wt%.
- Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that 195 mg (culture area 87 cm2 ) of temperature-responsive microcarriers 12 were used and the stirring speed was set to 60 rpm.
- the number of cells recovered by cooling was 61.3 x 105 , and the number of cells that could not be recovered by cooling was 1.4 x 105.
- the cooling detachment rate was 98%.
- Example 13 A 500 mL separable flask was set and equipped with a PTFE (poly(1,1,2,2-tetrafluoroethylene)) stirring blade. 40 g of dried polystyrene beads (surface: cationic, average specific gravity: 1.08) with a diameter of 130 ⁇ m was added and purged with nitrogen gas in the flask while stirring at 100 rpm.
- PTFE poly(1,1,2,2-tetrafluoroethylene)
- Example 4 Human bone marrow-derived mesenchymal stem cell culture> Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that 238 mg (culture area 87 cm2 ) of Cellbind (surface: anionic, average specific gravity: 1.026) microcarriers sterilized by autoclave were used and the stirring speed was set to 60 rpm. The number of cells recovered by cooling was 20.0 x 105 , and the number of cells that could not be recovered by cooling was 28.2 x 105. The cooling detachment rate was 59%.
- Example 5 Human bone marrow-derived mesenchymal stem cell culture> Human bone marrow-derived mesenchymal stem cells were cultured and the number of cells was counted in the same manner as in Example 1 ⁇ Human bone marrow-derived mesenchymal stem cell culture>, except that 20 mg (culture area 87 cm2 ) of autoclave-sterilized Cytodex1 microcarriers (surface: cationic, average specific gravity: 1.03) was used and the stirring speed was set to 60 rpm. The number of cells recovered by cooling was 21.1 x 105 , and the number of cells that could not be recovered by cooling was 28.9 x 105. The cooling detachment rate was 42%.
- Example 14 ⁇ VERO cell culture> VERO cells were cultured and the number of cells was counted in the same manner as in ⁇ VERO cell culture> of Example 9, except that 340 mg (culture area 150 cm2 ) of temperature-responsive microcarriers 13 were used and the stirring speed was set to 60 rpm. The number of cells recovered by cooling was 122.0 x 105 , and the number of cells that could not be recovered by cooling was 12.0 x 105. The cooling detachment rate was 91%.
- Example 15 Serum-free culture of VERO cells 356 mg (culture area 150 cm 2 ) of temperature-responsive microcarrier 13 and 1 L of VP-SFM (1X) (Thermo Fisher Scientific, product number: 11681020) were added to a 30 mL single-use bioreactor manufactured by Able, and 20 mL of 200 mM L-Glutamine Solution (1X) (ATCC, product number: 30-2214) were added to the VP-SFM (1X) and 30 mL of a final medium with a final concentration of 20 mM were added. Furthermore, 1 x 10 6 cells of Vero cells (American Type Culture Collection (ATCC), product number: CCL-81) were added and cultured for 8 days at 37 ° C. in an incubator with a 5 vol % CO 2 atmosphere at 100 rpm stirring condition.
- ATCC American Type Culture Collection
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, the cell suspension was passed through a 50 mL tube with a cell strainer with a mesh size of 70 ⁇ m, the floating cells were removed, and only the microcarriers to which the cells on the cell strainer were attached were collected, and phosphate buffered saline (PBS (-)) free of calcium and magnesium at 4 ° C was added and allowed to stand for 10 minutes. After standing, pipetting was performed 60 times, and the detached cells were collected by passing them through a 50 mL tube with a cell strainer with a mesh size of 70 ⁇ m, and the cells were concentrated by centrifugation and counted.
- PBS (-) phosphate buffered saline
- the number of cells collected by cooling was 46.5 ⁇ 10 5 cells. Furthermore, the microcarriers on the cell strainer were transferred to a 15 mL tube, 5 mL of CTS TrypLE Select Enzyme (manufactured by Thermo Fisher Scientific) was added, and the mixture was allowed to stand for 5 minutes in a 5 vol% CO 2 atmosphere at 37 ° C. The cell suspension was passed through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, the cells were collected, concentrated by centrifugation, and the cell number was counted. The number of cells that could not be collected by cooling was 4.2 ⁇ 10 5 cells. The cooling detachment rate was 92%.
- Example 16 ⁇ BHK-21 cell culture> 340 mg (culture area 150 cm 2 ) of temperature-responsive microcarrier 12 and 30 mL of complete medium of DMEM (Dulbecco's Modified Eagle Medium, Wako Pure Chemical Industries) containing 10% fetal bovine serum (FBS, Biowest Co., Ltd.) and 1% antibiotic-antimycotic solution (Wako Pure Chemical Industries, Ltd.) were added to a 30 mL single-use bioreactor manufactured by Able Co., Ltd. Furthermore, 1 x 10 6 cells of BHK-21 cells (ATCC, product number: CCL-10) were added and cultured for 7 days at 60 rpm stirring in an incubator with a 5 vol% CO 2 atmosphere at 37°C.
- DMEM Dynamic fetal bovine serum
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, the floating cells were removed, and only the microcarriers to which the cells on the cell strainer were attached were collected, and phosphate buffered saline (PBS (-)) containing no calcium or magnesium at 4 ° C was added and allowed to stand for 10 minutes. After standing, pipetting was performed 60 times, and the detached cells were collected by passing them through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, and the cells were concentrated by centrifugation and counted.
- PBS (-) phosphate buffered saline
- the number of cells collected by cooling was 148.0 ⁇ 10 5 cells.
- the microcarriers on the cell strainer were then transferred to a 15 mL tube, 5 mL of CTS TrypLE Select Enzyme (manufactured by Thermo Fisher Scientific) was added, and the mixture was allowed to stand for 5 minutes in a 5 vol% CO2 atmosphere at 37 °C.
- the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a 70 ⁇ m opening, the cells were collected, and the cells were concentrated by centrifugation to count the number of cells.
- the number of cells that could not be collected by cooling was 19.0 ⁇ 105.
- the cooling detachment rate was 89%.
- Example 17 ⁇ CRFK cell culture> 356 mg (culture area 150 cm 2 ) of temperature-responsive microcarrier 4 and 30 mL of complete medium of EMEM (ATCC-formulated Eagle's Minimum Essential Medium, ATCC, product number: 30-2003) containing 10% horse serum (HS, Sigma-Aldrich Japan, LLC) were added to a 30 mL single-use bioreactor manufactured by Able Co., Ltd. Furthermore, 0.8 x 10 6 cells of CRFK cells (ATCC, product number: CCL-94) were added and cultured for 7 days at 100 rpm stirring in an incubator with a 5 vol% CO 2 atmosphere at 37°C.
- EMEM ATCC-formulated Eagle's Minimum Essential Medium, ATCC, product number: 30-2003
- horse serum HS, Sigma-Aldrich Japan, LLC
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, the floating cells were removed, and only the microcarriers to which the cells on the cell strainer were attached were collected, and phosphate buffered saline (PBS (-)) containing no calcium or magnesium at 4 ° C was added and allowed to stand for 10 minutes. After standing, pipetting was performed 60 times, and the detached cells were collected by passing them through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, and the cells were concentrated by centrifugation and counted.
- PBS (-) phosphate buffered saline
- the number of cells collected by cooling was 26.8.0 ⁇ 10 5 cells.
- the microcarriers on the cell strainer were then transferred to a 15 mL tube, 5 mL of CTS TrypLE Select Enzyme (manufactured by Thermo Fisher Scientific) was added, and the mixture was allowed to stand for 5 minutes in a 5 vol% CO2 atmosphere at 37 °C.
- the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a 70 ⁇ m opening, the cells were collected, and the cells were concentrated by centrifugation to count the number of cells.
- the number of cells that could not be collected by cooling was 3.1 ⁇ 10 5 cells.
- the cooling detachment rate was 90%.
- Example 18 CRFK cell culture> CRFK cells were cultured and the number of cells was counted in the same manner as in ⁇ CRFK cell culture> in Example 17, except that 340 mg of microcarriers 12 (culture area 150 cm 2 ) was used and the stirring speed was set to 60 rpm. The number of cells recovered by cooling was 13.8 ⁇ 10 5 , and the number of cells that could not be recovered by cooling was 3.8 ⁇ 10 5 . The cooling detachment rate was 78%.
- Example 19 CRFK cell culture> CRFK cells were cultured and the number of cells was counted in the same manner as in ⁇ CRFK cell culture> in Example 17, except that 356 mg of microcarrier 13 (culture area 150 cm 2 ) was used. The number of cells recovered by cooling was 21.2 ⁇ 10 5 , and the number of cells that could not be recovered by cooling was 4.6 ⁇ 10 5 . The cooling detachment rate was 82%.
- Example 20 ⁇ MDCK cell culture> 356 mg (culture area 150 cm 2 ) of temperature-responsive microcarrier 4 and 30 mL of complete medium of DMEM (Dulbecco's Modified Eagle Medium, Wako Pure Chemical Industries) containing 10% fetal bovine serum (FBS, Biowest Co., Ltd.) and 1% antibiotic-antimycotic solution (Wako Pure Chemical Industries, Ltd.) were added to a 30 mL single-use bioreactor manufactured by Able Co., Ltd. Furthermore, 0.6 x 10 6 cells of MDCK cells (manufactured by Japanese Collection of Research Bioresources (JCRB), product number: JCRB9029) were added and cultured for 7 days at 37 ° C. in an incubator with 5 vol % CO 2 atmosphere at 100 rpm stirring conditions.
- DMEM Dynamic Eagle Medium
- FBS fetal bovine serum
- antibiotic-antimycotic solution Wako Pure Chemical Industries, Ltd.
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, the floating cells were removed, and only the microcarriers to which the cells on the cell strainer were attached were collected, and phosphate buffered saline (PBS (-)) containing no calcium or magnesium at 4 ° C was added and allowed to stand for 10 minutes. After standing, pipetting was performed 60 times, and the detached cells were collected by passing them through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, and the cells were concentrated by centrifugation and counted.
- PBS (-) phosphate buffered saline
- the number of cells collected by cooling was 137.0 ⁇ 10 5 cells.
- the microcarriers on the cell strainer were then transferred to a 15 mL tube, 5 mL of CTS TrypLE Select Enzyme (manufactured by Thermo Fisher Scientific) was added, and the mixture was allowed to stand for 5 minutes in a 5 vol% CO2 atmosphere at 37 °C.
- the cell suspension was passed through a 50 mL tube equipped with a cell strainer with a 70 ⁇ m opening, the cells were collected, and the cells were concentrated by centrifugation to count the number of cells.
- the number of cells that could not be collected by cooling was 37.0 ⁇ 10 5 cells.
- the cooling detachment rate was 79%.
- Example 21 ⁇ MDCK cell culture> MDCK cells were cultured and the number of cells was counted in the same manner as in ⁇ MDCK cell culture> of Example 19, except that 340 mg of microcarriers 12 (culture area 150 cm 2 ) was used and the stirring speed was set to 60 rpm. The number of cells recovered by cooling was 112.0 ⁇ 10 5 , and the number of cells that could not be recovered by cooling was 32.0 ⁇ 10 5 . The cooling detachment rate was 78%.
- Example 11 MDCK cells were cultured and the number of cells was counted in the same manner as in ⁇ MDCK cell culture> of Example 20, except that 416 mg (culture area 150 cm2 ) of Cellbind (surface: anionic, average specific gravity: 1.026) microcarriers sterilized by autoclave were used and the stirring speed was set to 60 rpm.
- the number of cells recovered by cooling was 2.3 x 105
- the number of cells that could not be recovered by cooling was 68.8 x 105.
- the cooling detachment rate was 3%.
- Example 12 MDCK cell culture> MDCK cells were cultured and the number of cells was counted in the same manner as in ⁇ MDCK cell culture> of Example 20, except that 34.1 mg (culture area 150 cm2 ) of autoclave-sterilized Cytodex1 (surface: cationic, average specific gravity: 1.03) microcarriers were used and the stirring speed was set to 60 rpm.
- the number of cells recovered by cooling was 16.7 x 105
- the number of cells that could not be recovered by cooling was 157.4 x 105.
- the cooling detachment rate was 10%.
- Example 22 ⁇ MRC-5 cell culture> 204 mg (culture area 87 cm 2 ) of temperature-responsive microcarrier 4 and 30 mL of complete medium of DMEM (Dulbecco's Modified Eagle Medium, Wako Pure Chemical Industries) containing 10% fetal bovine serum (FBS, Biowest Co., Ltd.) and 1% antibiotic-antimycotic solution (Wako Pure Chemical Industries, Ltd.) were added to a 30 mL single-use bioreactor manufactured by Able Co., Ltd. Furthermore, 0.5 x 10 6 cells of MRC-5 cells (manufactured by Japanese Collection of Research Bioresources (JCRB), product number: JCRB9008) were added and cultured for 6 days at 37 ° C. in an incubator with 5 vol % CO 2 atmosphere at 100 rpm stirring conditions.
- DMEM Dynamic Eagle Medium
- FBS fetal bovine serum
- antibiotic-antimycotic solution Wako Pure Chemical Industries, Ltd.
- the 30 mL single-use bioreactor was transferred to a safety cabinet at room temperature, the cell suspension was passed through a 50 mL tube with a cell strainer with a mesh size of 70 ⁇ m, the floating cells were removed, and only the microcarriers to which the cells on the cell strainer were attached were collected, and phosphate buffered saline (PBS (-)) free of calcium and magnesium at 4 ° C was added and allowed to stand for 10 minutes. After standing, pipetting was performed 60 times, and the detached cells were collected by passing them through a 50 mL tube with a cell strainer with a mesh size of 70 ⁇ m, and the cells were concentrated by centrifugation and counted.
- PBS (-) phosphate buffered saline
- the number of cells collected by cooling was 9.8 ⁇ 10 5 cells. Furthermore, the microcarriers on the cell strainer were transferred to a 15 mL tube, 5 mL of CTS TrypLE Select Enzyme (manufactured by Thermo Fisher Scientific) was added, and the mixture was allowed to stand for 5 minutes in a 5 vol% CO 2 atmosphere at 37 ° C. The cell suspension was passed through a 50 mL tube equipped with a cell strainer with a mesh size of 70 ⁇ m, the cells were collected, concentrated by centrifugation, and the number of cells was counted. The number of cells that could not be collected by cooling was 4.1 ⁇ 10 5 cells. The cooling detachment rate was 71%.
- Example 23 ⁇ MRC-5 cell culture> MRC-5 cells were cultured and the number of cells was counted in the same manner as in ⁇ MRC-5 cell culture> in Example 22, except that 195 mg of microcarriers 12 (culture area 87 cm 2 ) were used and the stirring speed was 60 rpm.
- the number of cells recovered by cooling was 18.8 ⁇ 10 5
- the number of cells that could not be recovered by cooling was 1.0 ⁇ 10 5 .
- the cooling detachment rate was 95%.
- MRC-5 cells were cultured and the number of cells was counted in the same manner as in ⁇ MRC-5 cell culture> in Example 22, except that 238 mg (culture area 87 cm 2 ) of Cellbind (surface: anionic, average specific gravity: 1.026) microcarriers sterilized by autoclave were used and the stirring speed was set to 60 rpm.
- the number of cells recovered by cooling was 3.4 ⁇ 10 5
- the number of cells that could not be recovered by cooling was 8.8 ⁇ 10 5 .
- the cooling detachment rate was 28%.
- MRC-5 cells were cultured and the number of cells was counted in the same manner as in ⁇ MRC-5 cell culture> in Example 22, except that 20 mg (culture area 87 cm 2 ) of autoclave-sterilized Cytodex 1 (surface: cationic, average specific gravity: 1.03) microcarriers were used and the stirring speed was set to 60 rpm.
- the number of cells recovered by cooling was 4.2 ⁇ 10 5
- the number of cells that could not be recovered by cooling was 9.2 ⁇ 10 5 .
- the cooling detachment rate was 31%.
Landscapes
- Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Zoology (AREA)
- Biomedical Technology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Biotechnology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- General Engineering & Computer Science (AREA)
- Microbiology (AREA)
- Cell Biology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Sustainable Development (AREA)
- Virology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
本発明は、下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリアに関する。
Description
本発明は、温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなる温度応答性マイクロキャリアに関する。
細胞を原料にして製造する細胞医薬品は難治疾患の治療薬として注目を集めている。また、抗体医薬品やワクチンなどの生産のため大量細胞培養法が注目を集めており、原料細胞を効率的に製造する技術が求められている。一般的にヒト細胞を含め多くの動物細胞は足場依存性があり、細胞を増殖する際は細胞が接着し安定的に増殖できる適切な足場が必要である。コスト低減に当たり、単位培地量当たりの細胞増殖が高くなる足場の設計を行う必要があった。これを解決するため、合成高分子や多糖などの天然高分子を原料としたビーズから構成されるマイクロキャリアが特許文献1に記載されている。マイクロキャリアを細胞懸濁液入りの容器に投入し培養することで、細胞はマイクロキャリア表面で増殖し、単位培地量当たりの細胞増殖を高めることができる。
細胞がマイクロキャリア表面を全て覆うまで培養した後は、細胞をマイクロキャリアから剥がして新しいマイクロキャリアに植え継ぐ拡大培養を行う。一般的なマイクロキャリアではトリプシンなどのタンパク質分解酵素を用いてマイクロキャリアから細胞を剥がすが、タンパク質分解酵素が残存すると培養に悪影響を与えるため、タンパク質分解酵素を除去ないし中和する工程が必要となる。
これに対し、特許文献2記載の温度応答性マイクロキャリアを用いる場合は、冷却することで細胞をタンパク質分解酵素不要でマイクロキャリア表面から剥離できるため工程の簡略化が可能になる。しかしながら特許文献2記載の温度応答性マイクロキャリアでは必ずしも十分に細胞を剥離できず、より好適な温度応答性を発現する温度応答性マイクロキャリアが求められた。
本特許の目的は、好適な温度応答性を発現する温度応答性マイクロキャリアを提供することにある。
本発明者らは、以上の点を鑑み、鋭意研究を重ねた結果、下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリアにより、好適な温度応答性を発現することを見出し、本発明を完成した。すなわち本発明は以下の態様を含包する。
<1>下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリア。
<2>負電荷を有するポリマーの割合が0.1~20wt%であることを特徴とする<1>記載のマイクロキャリア。
<3>負電荷を有するポリマー中にカルボキシ基が含まれることを特徴とする<1>又は<2>記載のマイクロキャリア。
<4>負電荷を有するポリマー中のカルボキシ基の割合が10~50wt%であることを特徴とする<1>~<3>記載のマイクロキャリア。
<5>ビーズ表面がカチオン性であることを特徴とする<1>~<4>記載のマイクロキャリア。
<6>ビーズに正電荷を有する官能基が修飾していることを特徴とする<1>~<5>記載のマイクロキャリア。
<7>ビーズがトリメチルアンモニウムクロライド修飾ポリスチレンであることを特徴とする<1>~<6>記載のマイクロキャリア。
<8>ビーズの粒径が20μm~1000μmであることを特徴とする<1>~<7>記載のマイクロキャリア。
<9>温度応答性ポリマーが下記(A)、(B)、(C)のブロックを含むブロック共重合体であることを特徴とする<1>~<8>記載のマイクロキャリア。
(A)HLB値(グリフィン法)が7以上20以下の範囲にある重合体ブロック。
(B)HLB値(グリフィン法)が0以上7未満の範囲にある重合体ブロック。
(C)水に対する下限臨界溶解温度(LCST)が0℃~50℃の範囲にある温度応答性重合体ブロック。
<10><1>~<9>記載のマイクロキャリアの製造方法。
<11>ビーズを、下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーとを含むポリマーコート膜で被覆する工程を備えることを特徴とする<1>~<9>記載のマイクロキャリアの製造方法。
<12><1>~<9>記載のマイクロキャリアを用いた細胞培養方法。
<13><1>~<9>記載のマイクロキャリアを含有する培地で、細胞を培養する工程を含むことを特徴とする細胞培養方法。
<14>キレート剤を導入した冷却液を用いて、細胞をマイクロキャリアから剥離する冷却細胞剥離工程を含むことを特徴とする<12>又は<13>記載の細胞培養方法。
<1>下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリア。
<2>負電荷を有するポリマーの割合が0.1~20wt%であることを特徴とする<1>記載のマイクロキャリア。
<3>負電荷を有するポリマー中にカルボキシ基が含まれることを特徴とする<1>又は<2>記載のマイクロキャリア。
<4>負電荷を有するポリマー中のカルボキシ基の割合が10~50wt%であることを特徴とする<1>~<3>記載のマイクロキャリア。
<5>ビーズ表面がカチオン性であることを特徴とする<1>~<4>記載のマイクロキャリア。
<6>ビーズに正電荷を有する官能基が修飾していることを特徴とする<1>~<5>記載のマイクロキャリア。
<7>ビーズがトリメチルアンモニウムクロライド修飾ポリスチレンであることを特徴とする<1>~<6>記載のマイクロキャリア。
<8>ビーズの粒径が20μm~1000μmであることを特徴とする<1>~<7>記載のマイクロキャリア。
<9>温度応答性ポリマーが下記(A)、(B)、(C)のブロックを含むブロック共重合体であることを特徴とする<1>~<8>記載のマイクロキャリア。
(A)HLB値(グリフィン法)が7以上20以下の範囲にある重合体ブロック。
(B)HLB値(グリフィン法)が0以上7未満の範囲にある重合体ブロック。
(C)水に対する下限臨界溶解温度(LCST)が0℃~50℃の範囲にある温度応答性重合体ブロック。
<10><1>~<9>記載のマイクロキャリアの製造方法。
<11>ビーズを、下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーとを含むポリマーコート膜で被覆する工程を備えることを特徴とする<1>~<9>記載のマイクロキャリアの製造方法。
<12><1>~<9>記載のマイクロキャリアを用いた細胞培養方法。
<13><1>~<9>記載のマイクロキャリアを含有する培地で、細胞を培養する工程を含むことを特徴とする細胞培養方法。
<14>キレート剤を導入した冷却液を用いて、細胞をマイクロキャリアから剥離する冷却細胞剥離工程を含むことを特徴とする<12>又は<13>記載の細胞培養方法。
下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリアにより、好適な温度応答性を発現することができる。
以下、本発明を実施するための形態について詳細に説明するが、本発明を以下の内容に限定する趣旨ではない。本発明は、その趣旨の範囲内で適宜変更して実施できる。
本発明は下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリアである。
本発明における温度応答性ポリマーは下限臨界溶解温度が0℃~50℃で相溶性が変化すれば特に限定はないが、相溶性の変化を顕著に表すためにブロック共重合体であることが好ましく、一例として下記(A)、(B)、(C)のブロックを含むブロック共重合体を例示できる。
(A)HLB値(グリフィン法)が7以上20以下の範囲にある重合体ブロック。
(B)HLB値(グリフィン法)が0以上7未満の範囲にある重合体ブロック。
(C)水に対する下限臨界溶解温度(LCST)が0℃~50℃の範囲にある温度応答性重合体ブロック。
(A)HLB値(グリフィン法)が7以上20以下の範囲にある重合体ブロック。
(B)HLB値(グリフィン法)が0以上7未満の範囲にある重合体ブロック。
(C)水に対する下限臨界溶解温度(LCST)が0℃~50℃の範囲にある温度応答性重合体ブロック。
HLB値(Hydrophile-Lipophile Balance:HLB)とは、W.C.Griffin, Journal of the Society of Cosmetic Chemists, 1, 311(1949).に記載の、水と油への親和性の程度を表す値であり、0から20までの値を取り、0に近いほど疎水性が高く、20に近いほど親水性が高くなる。計算式によりHLB値を算出方法として、アトラス法、グリフィン法、デイビス法、川上法があるが、本明細書においては、グリフィン法により算出した値を使用し、本発明のブロック共重合体を構成する各ブロックの繰り返し単位中の親水部の式量と繰り返し単位の総式量を元に、下記の計算式により算出した。
HLB値=20×(繰り返し単位中の親水部の式量)÷(繰り返し単位の総式量)
HLB値=20×(繰り返し単位中の親水部の式量)÷(繰り返し単位の総式量)
前述の、各ブロックの繰り返し単位中の親水部の定義として、スルホン部(-SO3-)、ホスホノ基部(-PO3-)、カルボキシル基部(-COOH)、エステル部(-COO-)、アミド部(-CONH-)、イミド部(-CON-)、アルデヒド基部(-CHO)、カルボニル基部(-CO-)、ヒドロキシル基部(-OH)、アミノ基部(-NH2)、アセチル基部(-COCH3)、エチレンアミン部(-CH2CH2N-)、エチレンオキシ部(-CH2CH2O-)、アルカリ金属イオン、アルカリ土類金属イオン、アンモニウムイオン、ハロゲン化物イオン、酢酸イオンを例示することができる。
繰り返し単位中の親水部の算出では、親水部を構成する原子が、他の親水部を構成する原子として重複してはならない。繰り返し単位中のHLB値の算出例を以下に記載した。例えば、2-メタクリロイルオキシエチルホスホリルコリン(分子量:295.27)の場合、親水部は、エステル部が1部、ホスホノ基部が1部およびエチレンアミン部が1部であり、親水部の分子量は181.04であるから、HLB値は12.3である。2-ジメチルアミノエチルメタクリレート(分子量:157.11)の場合、親水部は、エステル部が1部およびエチレンアミン部が1部であり、親水部の分子量は86.07であるから、HLB値は11.0である。メチルメタクリレート(分子量:100.12)の場合、親水部は、エステル部が1部であり、親水部の分子量は44.01であるから、HLB値は8.8である。n-ブチルメタクリレート(分子量:142.20)の場合、親水部は、エステル部が1部であり、親水部の分子量は44.01であるから、HLB値は6.2である。
下限臨界溶解温度(LCST;Lower Critical Solution Temperature)とは、この温度よりも低い温度では高分子が水に溶解して透明の溶液になるが、この温度よりも高い温度では不溶化して白濁するか沈殿が生じ、相分離する温度である。ブロック(C)に含まれる繰返し単位とその水に対するLCSTは、例えば、N-イソプロピルアクリルアミド(LCST=32℃)、N-n-プロピルメタクリルアミド(LCST=22℃)、N-テトラヒドロフルフリルアクリルアミド(LCST=28℃)、N-エトキシエチルアクリルアミド(LCST=35℃)、N,N-ジエチルアクリルアミド(LCST=32℃)、N-イソプロピルメタクリルアミド(LCST=44℃)、N-n-プロピルメタクリルアミド(LCST=28℃)、N-テトラヒドロフルフリルメタクリルアミド(LCST=35℃)、N-メチル-N-イソプロピルアクリルアミド(LCST=23℃)、またはN-メチル-N-n-プロピルアクリルアミド(LCST=20℃)などが例示できる。本発明におけるブロック(C)は、前記繰り返し単位を1種類のみ用いてもよく、2種類以上を組み合わせて用いてもよい。また温度応答性を有するのであれば、前記温度応答性繰返し単位の他に、異なる繰返し単位を含んでも良い。
(A)、(B)、(C)のブロックを含むブロック共重合体の一例として、(A)2-メトキシエチルアクリレート(HLB値=13.5)の繰り返し単位、(B)n-ブチルアクリレート(HLB値=6.9)の繰り返し単位、(C)N-イソプロピルアクリルアミド(LCST=32℃)の繰り返し単位からなるブロック共重合体が挙げられる。
温度応答性ポリマーのその他の例として、(C)成分のみから構成されるホモポリマーや、(A)成分と(C)成分から構成される共重合体、(B)成分と(C)成分から構成される共重合体が挙げられる。共重合体はランダム共重合体であっても、ブロック共重合体であっても良い。
温度応答性ポリマーの数平均分子量は特に限定はないが、一例として1000~1000000であり、好ましくは5000~500000、さらに好ましくは10000~200000である。
本発明において負電荷を有するポリマーとは、水中で電離してアニオン性を示す官能基を有するポリマーである。アニオン性を示す官能基は特に限定はないが、一例としてヒドロキシ基、カルボキシ基、スルホ基であり、これらの中でも酸性の制御が容易なことからカルボキシ基が好ましい。負電荷を有するポリマーの繰り返し単位は特に限定はないが、一例として、ビニルフェノール、アクリル酸、メタクリル酸、スチレンスルホン酸が挙げられる。負電荷を有するポリマーに、負電荷を有するポリマーの繰り返し単位の他に、負電荷を有さないポリマーの繰り返し単位を含んでも良く、一例としてスチレンスルホン酸とスチレンの共重合体が挙げられる。また共重合体はランダム共重合体やブロック共重合体であっても良い。
負電荷を有するポリマーの官能基がカルボキシ基である場合、負電荷を有するポリマー中のカルボキシ基の割合は特に限定はないが、温度応答性を良好に発現するために、一例として10~50wt%であり、好ましく15~40wt%、より好ましくは20~30wt%である。
負電荷を有するポリマーの数平均分子量は特に限定はないが、一例として1000~1000000であり、好ましくは5000~500000、さらに好ましくは10000~200000である。
本発明においてビーズとは粉粒体である。ビーズの粒径に特に限定はなく、一例として1μm~10mm、5μm~5mm、20μm~1000μmである。ビーズの形状は特に限定はなく、一例として球形、直方形、円柱形、円筒形、星形などが挙げられる。ビーズの真密度は特に限定はないが、温度応答性マイクロキャリアを製造する際に使用するポリマー溶液の密度より高いほど好ましく、一例として0.9~20.0g/cm2である。またビーズに細孔があってもなくても良い。ビーズの乾燥重量当たりの比表面積は特に限定はないが、一例として10~100000cm2/gである。乾燥重量当たりの比表面積はBET(Brunauer Emmett Teller)法で測定した値を用いることもできるが、本出願ではSEM画像から求めた平均粒子径と粒子比重から計算して求めた。
ビーズの素材に特に限定はなく、一例として金属、金属酸化物、無機塩、合成高分子、生体高分子、またはそれらの複合物など様々な素材に適用できる。ビーズの表面は特に限定はないが、細胞増殖を高めるためにカチオン性であること、又は正電荷を有する官能基が修飾していることが好ましい。正電荷を有する官能基の一例として、アンモニウム基やアンモニウム基誘導体が挙げられる。具体的なビーズとしては例えば、ポリスチレン等が挙げられ、トリメチルアンモニウムクロライド修飾ポリスチレンが好ましい。
本発明において温度応答性マイクロキャリアの製法は特に限定はないが、一般的な、ビーズにポリマーを吸着させるなどの物理的に被覆する方法又はビーズにポリマーを共有結合で固定するなどの化学的に被覆する方法が挙げられる。ビーズにポリマーを吸着させるなどビーズを物理的に被覆する場合は、被覆する方法に特に限定はなく、一例として含浸法や浸漬法、ヘンシェルミキサー法が挙げられる。含浸法及び浸漬法はビーズにポリマー溶液を浸漬ないし吹付を行い、減圧して溶媒を除去することで温度応答性マイクロキャリアが得られる。ヘンシェルミキサー法は、撹拌翼付きの反応槽でビーズを撹拌翼により撹拌させながら、乾燥用の気体を反応槽内に吹き込みつつ、ポリマーコート溶液を加えることで、短時間で温度応答性マイクロキャリアを得る方法である。ヘンシェルミキサー法及び含浸法は用いたポリマー溶液を全量吸着できるため温度応答性ポリマーと負電荷を有するポリマーの組成比調整や被覆量調整が容易な利点がある。また、後者のビーズにポリマーを化学共有結合で固定する場合は、化学共有結合の種類に特に限定はなく、一例としてエステル結合、アミド結合、エーテル結合、チオエーテル結合などが挙げられ、反応後に洗浄して未反応化合物を除去することで温度応答性マイクロキャリアが得られる。被覆後の乾燥工程において、乾燥用の気体に制限はなく、例えば窒素、空気、アルゴン、ネオン等、ビーズ及びポリマーコート溶液と反応性の無い気体であれば特に制限はない。
本発明において温度応答性マイクロキャリアの製造方法は、例えば、ビーズを、下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーとを含むポリマーコート膜で被覆する工程を備えることを特徴とする方法であってもよい。
本発明において温度応答性マイクロキャリアの負電荷を有するポリマーの割合は特に限定はないが、一例として0.1~20wt%であり、好適な温度応答性を発現するために、好ましくは0.3~10wt%、より好ましくは0.5~5wt%、更に好ましくは0.5~4wt%であり、特に好ましくは0.5~3wt%である。
本発明において温度応答性マイクロキャリアは細胞培養、特に接着性細胞の細胞培養に使用できる。接着性細胞とはマイクロキャリア等の細胞培養基材の表面に付着しながら増殖する細胞である。培養する接着細胞の由来は特に限定はないが、一例としてヒト、サル、イヌ、ネコ、ウサギ、ラット、ヌードマウス、マウス、モルモット、ブタ、ヒツジ、チャイニーズハムスター、ウシ等の哺乳類やニワトリ、アヒル等の鳥類等が挙げられる。また、培養する細胞(接着細胞)の種類に特に限定はなく、一例としてヒト又は動物由来間葉系幹細胞、チャイニーズハムスター卵巣由来のCHO細胞、アフリカミドリザルの腎臓上皮由来のVERO細胞、イヌ腎臓由来のMDCK細胞、ヒト胎児正常肺組織由来のMRC-5細胞、ニワトリ胎児由来のCEF細胞、ハムスター腎臓由来のBHK細胞、マウス結合組織由来のL929細胞、ヒト胎児腎臓由来細胞HEK293細胞、ウシ腎由来のMDBK細胞、ネコ腎臓由来のCRFK細胞、モルモット腎臓由来のCPK細胞、ヒト子宮頸癌由来のHeLa細胞、更に生体内の各組織、臓器を構成する上皮細胞や内皮細胞、収縮性を示す骨格筋細胞、平滑筋細胞、心筋細胞、神経系を構成するニューロン細胞、グリア細胞、繊維芽細胞、生体の代謝に関与する肝実質細胞、肝非実質細胞や脂肪細胞、分化能を有する細胞として、種々の組織に存在する幹細胞、さらにはそれらから分化誘導した細胞が挙げられる。また、上述の細胞種が不死化された細胞株などが挙げられる。これら以外でも、血液、リンパ液、髄液、喀痰、尿又は便に含まれる細胞や、体内あるいは環境中に存在する微生物、ウイルス、原虫等を例示できる。使用する培地の種類は特に限定はなく、血清培地であっても無血清培地であっても良く、細胞の種類に応じて適宜選択できる。
本発明の培養で使用される基礎培地の種類は特に限定はなく、例えば、MEM、αMEM、DMEM、EMEM、GMEM、DMEM/Ham’sF-12、Ham’sF-12、Ham’sF-10、Medium199、RPMI1640などを用いることができる。また、血清培地であっても無血清培地であっても良いが、使用血清は特に限定はなく、例えば、牛胎児血清(Fetal Bovine Serum:FBS)、児牛血清、成牛血清、ウマ血清、ヒツジ血清、ヤギ血清、ブタ血清、ニワトリ血清、ウサギ血清、ヒト血清が使用できる。また、完成培地は抗生物質を含有してもしなくても良く、細胞の種類に応じて適宜選択できる。
本発明の温度応答性マイクロキャリアを用いた細胞培養方法は特に限定はなく、静置条件で培養しても良いし、撹拌条件で培養しても良い。撹拌条件で培養する場合は撹拌速度に特に限定はなく、一例として1~1000rpmである。培養時の培養温度は特に限定はないが、温度応答性ポリマー被覆されたマイクロキャリアの表面が疎水化し細胞が接着しやすい環境の提供ができるLCST以上で行うことが好ましい。培養後はLCST未満の温度に冷却することでマイクロキャリア上の細胞を回収できる。冷却方法は特に限定はなく、冷却器を使用して直接冷却しても良いし、培地を冷却液で交換しても良い。冷却液は基礎培地であっても、成長因子や血清等を含む完成培地であっても、リン酸緩衝液であっても良いが、リン酸緩衝液を選択することで細胞がマイクロキャリアから剥離しやすくなる。冷却用のリン酸緩衝液にEDTA、EGTAなどのキレート剤を導入すると細胞がさらにシングルセルとしてマイクロキャリアから剥離しやすくなる。ここでシングルセルとは、細胞同士が繋がっている状態から脱し、1細胞ごとに分離していることを意味している。リン酸緩衝液中のキレート剤の濃度は特に限定はなく、1μM~1mMである。細胞を回収する際は、冷却液に流動があると温度応答性マイクロキャリアの冷却を促進できるため好ましく、一例として撹拌やピペッティングで流動を得ることができる。
本発明の温度応答性マイクロキャリアを用いた細胞培養方法は、例えば、本発明のマイクロキャリアを含有する培地で、細胞を培養する工程を含むことを特徴とする方法であってもよい。本発明の温度応答性マイクロキャリアを用いた細胞培養方法は、キレート剤を導入した冷却液を用いて、細胞をマイクロキャリアから剥離する冷却細胞剥離工程を更に含んでいてもよい。
本発明の温度応答性マイクロキャリアの培養性能は全細胞数と冷却剥離率で評価する。全細胞数が同じ培養面積の現行の汎用マイクロキャリアで培養した全細胞数と同等もしくは下回る場合は培養性能不良と判断する。現行の汎用マイクロキャリアは、Cytiva社の表面がカチオン性であるCytodex1又は/及びCorning社の表面がアニオン性であるCellbindとする。温度応答性冷却剥離率の評価方法は特に限定はないが、一例として(1)冷却で回収した細胞数を測定し、さらに(2)冷却で剥離しなかった細胞はタンパク質分解酵素を用いて回収した細胞数を測定し、(1)の細胞数を、(1)と(2)の細胞数の和で割り、100を掛けた値で冷却剥離率として評価することができる。細胞数の計測方法は特に限定はないが、血球計算板などを用いて評価できる。
以下に本発明の実施例を説明するが、本発明はこれら実施例により何ら制限されるものではない。なお、断りのない限り、試薬は市販品を用いた。
<ブロック共重合体の組成解析>
核磁気共鳴測定装置(日本電子製、商品名JNM-ECZ400S/L1)を用いたプロトン核磁気共鳴分光(1H-NMR)スペクトル分析より求めた。
核磁気共鳴測定装置(日本電子製、商品名JNM-ECZ400S/L1)を用いたプロトン核磁気共鳴分光(1H-NMR)スペクトル分析より求めた。
<ブロック共重合体の分子量、分子量分布の解析>
重量平均分子量(Mw)、数平均分子量(Mn)及び分子量分布(Mw/Mn)は、ゲル・パーミエーション・クロマトグラフィー(GPC)によって測定した。GPC装置は東ソー(株)製 HLC-8320GPCを用い、カラムは東ソー(株)製 TSKgel SuperAWM-Hを2本用い、カラム温度を40℃に設定し、溶離液は10mMトリフルオロ酢酸ナトリウムを含む2,2,2-トリフルオロエタノールを用いて測定した。測定試料は1.0mg/mLで調製して測定した。分子量の検量線は、分子量既知のポリメタクリル酸メチル(Sigma-Aldrich社製)を用いた。
重量平均分子量(Mw)、数平均分子量(Mn)及び分子量分布(Mw/Mn)は、ゲル・パーミエーション・クロマトグラフィー(GPC)によって測定した。GPC装置は東ソー(株)製 HLC-8320GPCを用い、カラムは東ソー(株)製 TSKgel SuperAWM-Hを2本用い、カラム温度を40℃に設定し、溶離液は10mMトリフルオロ酢酸ナトリウムを含む2,2,2-トリフルオロエタノールを用いて測定した。測定試料は1.0mg/mLで調製して測定した。分子量の検量線は、分子量既知のポリメタクリル酸メチル(Sigma-Aldrich社製)を用いた。
<温度応答性ポリマーMBIの合成>
100mL2口フラスコに2-メトキシエチルアクリレート(MEA)0.650g(5mmol)を加え、さらにシアノメチルドデシルカルボナトを31.8mg(100μmol)とアゾビスイソブチロニトリル1.6mg(10μmol)と1,4-ジオキサン10mLを加え、アルゴンガス置換後、62℃で24時間加熱撹拌した。
100mL2口フラスコに2-メトキシエチルアクリレート(MEA)0.650g(5mmol)を加え、さらにシアノメチルドデシルカルボナトを31.8mg(100μmol)とアゾビスイソブチロニトリル1.6mg(10μmol)と1,4-ジオキサン10mLを加え、アルゴンガス置換後、62℃で24時間加熱撹拌した。
1回目の加熱撹拌後、上記にn-ブチルアクリレート(BA)3.845g(30mmol)を加え、さらにアゾビスイソブチロニトリル1.6mg(10μmol)と1,4-ジオキサン5mLを加え、アルゴンガス置換後、62℃で48時間加熱撹拌した。
2回目の加熱撹拌後、上記にN-イソプロピルアクリルアミド(IPAAm,LCST=32℃)7.355g(65mmol)を加え、さらにアゾビスイソブチロニトリル1.6mg(10μmol)と1,4-ジオキサン35mLを加え、アルゴンガス置換後、62℃で48時間加熱撹拌した。
3回目の加熱撹拌後、反応液を水で再沈精製し、減圧乾燥することで黄色固体を得た。得られた黄色固体をクロロホルムに溶解し、分液ロートを用いクロロホルム相を回収した。回収したクロロホルム相をエバポレーターで濃縮し、ヘキサンで再沈精製した。沈殿物をろ過で回収し、減圧乾燥することで、ポリマーMBIを5.805g得た。得られたブロック共重合体MBIの組成比はMEA/BA/IPAAm=5/26/69(mol%)であり、数平均分子量Mnは8.5万、分子量分布Mw/Mnは1.78であった。
<負電荷を有するポリマーCStS>
100mL2口フラスコにp-カルボキシスチレン(CSt)1.156g(8mmol)とスチレン(St)1.271g(12mmol)を加え、さらにアゾビスイソブチロニトリル3.3mg(20μmol)とtert-ブチルアルコール20mLを加え、アルゴンガス置換後、64℃で24時間加熱撹拌した。反応液をn-ヘプタンで再沈精製し、減圧乾燥することで、ポリマーCStSを0.92g得た。ポリマーCStSの組成比はCSt/St=33/67(mol%)、数平均分子量Mnは10.6万、分子量分布Mw/Mnは1.84であった。
100mL2口フラスコにp-カルボキシスチレン(CSt)1.156g(8mmol)とスチレン(St)1.271g(12mmol)を加え、さらにアゾビスイソブチロニトリル3.3mg(20μmol)とtert-ブチルアルコール20mLを加え、アルゴンガス置換後、64℃で24時間加熱撹拌した。反応液をn-ヘプタンで再沈精製し、減圧乾燥することで、ポリマーCStSを0.92g得た。ポリマーCStSの組成比はCSt/St=33/67(mol%)、数平均分子量Mnは10.6万、分子量分布Mw/Mnは1.84であった。
<エバポレーターの設置>
ロータリーエバポレーターとして東京理化器械製のN-1300、小型冷却水循環装置として東京理化器械製のCCA-1112A、ダイヤフラム型真空ポンプとして東京理化器械製のNVP-2100V、ウォーターバスとして東京理化器械製のOSB-2200をそれぞれ設置した。小型冷却水循環装置の流体に水を使用し、温度は3℃にした。ウォーターバスの温度は50℃にした。
ロータリーエバポレーターとして東京理化器械製のN-1300、小型冷却水循環装置として東京理化器械製のCCA-1112A、ダイヤフラム型真空ポンプとして東京理化器械製のNVP-2100V、ウォーターバスとして東京理化器械製のOSB-2200をそれぞれ設置した。小型冷却水循環装置の流体に水を使用し、温度は3℃にした。ウォーターバスの温度は50℃にした。
<細胞数と細胞生存率の計測>
細胞懸濁液中から10μLを細胞数測定用スライド(Thermo Fisher Scientific製、商品名Countess Cell Counting Chamber Slid)に添加し自動セルカウンター(Thermo Fisher Scientific製、商品名CountessII)を用いて、細胞数を測定した。
細胞懸濁液中から10μLを細胞数測定用スライド(Thermo Fisher Scientific製、商品名Countess Cell Counting Chamber Slid)に添加し自動セルカウンター(Thermo Fisher Scientific製、商品名CountessII)を用いて、細胞数を測定した。
実施例1
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.0025wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.0025wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が4.76wt%である温度応答性マイクロキャリア1を得た。
<ヒト骨髄由来間葉系幹細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに204mg(培養面積87cm2)の温度応答性マイクロキャリア1と30mLのPromoCell社製間葉系幹細胞増殖培地2を加えた。さらにロンザ製のヒト骨髄由来間葉系幹細胞(継代数2)を5×105cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で6日間培養した。
エイブル社製の30mLシングルユースバイオリアクターに204mg(培養面積87cm2)の温度応答性マイクロキャリア1と30mLのPromoCell社製間葉系幹細胞増殖培地2を加えた。さらにロンザ製のヒト骨髄由来間葉系幹細胞(継代数2)を5×105cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で6日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、静置してマイクロキャリアを沈降させ、22.5mLの培地を抜取り、新たに22.5mLの1mMのEDTAを含む4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に室温で3分間、300rpmで撹拌した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、さらにセルストレーナー上に5mLのPBS(-)を2回加え、細胞をチューブ内に回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は70.8×105個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのTrypLE Express Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、さらにセルストレーナー上に5mLのPBS(-)を2回加え、細胞をチューブ内に回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は22.1×105個であった。冷却剥離率は76%だった。
実施例2
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.0015wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.0015wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が2.91wt%である温度応答性マイクロキャリア2を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア2を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は78.2×105個で、冷却で回収できなかった細胞数は18.2×105個であった。冷却剥離率は81%だった。
温度応答性マイクロキャリア2を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は78.2×105個で、冷却で回収できなかった細胞数は18.2×105個であった。冷却剥離率は81%だった。
実施例3
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.0005wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.0005wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.99wt%である温度応答性マイクロキャリア3を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア3を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は96.4×105個で、冷却で回収できなかった細胞数は19.1×105個であった。冷却剥離率は83%だった。
温度応答性マイクロキャリア3を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は96.4×105個で、冷却で回収できなかった細胞数は19.1×105個であった。冷却剥離率は83%だった。
実施例4
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.74wt%である温度応答性マイクロキャリア4を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア4を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は93.4×105個で、冷却で回収できなかった細胞数は3.6×105個であった。冷却剥離率は96%だった。
温度応答性マイクロキャリア4を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は93.4×105個で、冷却で回収できなかった細胞数は3.6×105個であった。冷却剥離率は96%だった。
実施例5
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.00025wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.00025wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.50wt%である温度応答性マイクロキャリア5を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア5を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は73.2×105個で、冷却で回収できなかった細胞数は29.3×105個であった。冷却剥離率は71%だった。
温度応答性マイクロキャリア5を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は73.2×105個で、冷却で回収できなかった細胞数は29.3×105個であった。冷却剥離率は71%だった。
実施例6
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を12gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を12g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を12gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を12g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.74wt%である温度応答性マイクロキャリア6を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア6を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は109.0×105個で、冷却で回収できなかった細胞数は1.6×105個であった。冷却剥離率は98%だった。
温度応答性マイクロキャリア6を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は109.0×105個で、冷却で回収できなかった細胞数は1.6×105個であった。冷却剥離率は98%だった。
実施例7
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を8gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を8g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を8gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を8g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.74wt%である温度応答性マイクロキャリア7を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア7を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は94.7×105個で、冷却で回収できなかった細胞数は20.5×105個であった。冷却剥離率は82%だった。
温度応答性マイクロキャリア7を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は94.7×105個で、冷却で回収できなかった細胞数は20.5×105個であった。冷却剥離率は82%だった。
実施例8
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を6gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を6g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を6gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を6g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.74wt%である温度応答性マイクロキャリア8を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア8を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は84.7×105個で、冷却で回収できなかった細胞数は28.6×105個であった。冷却剥離率は75%だった。
温度応答性マイクロキャリア8を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は84.7×105個で、冷却で回収できなかった細胞数は28.6×105個であった。冷却剥離率は75%だった。
実施例9
<VERO細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア2と30mLの10%のウシ胎児血清(Fetal bovine serum、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)を加えた。さらにJCRB細胞バンク製のVERO細胞(継代数16)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で120rpmの撹拌条件で8日間培養した。
<VERO細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア2と30mLの10%のウシ胎児血清(Fetal bovine serum、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)を加えた。さらにJCRB細胞バンク製のVERO細胞(継代数16)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で120rpmの撹拌条件で8日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、浮遊細胞を除去し、セルストレーナー上の細胞が接着されているマイクロキャリアのみ回収し、4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に60回ピペッティング操作を行い、剥離細胞を目開き70μmのセルストレーナーをセットした50mLのチューブに通すことで回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は15.0×106個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのCTS TrypLE Select Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、細胞を回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は1.7×106個であった。冷却剥離率は89%だった。
実施例10
<VERO細胞培養>
温度応答性マイクロキャリア3を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は11.0×106個で、冷却で回収できなかった細胞数は1.8×106個であった。冷却剥離率は86%だった。
<VERO細胞培養>
温度応答性マイクロキャリア3を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は11.0×106個で、冷却で回収できなかった細胞数は1.8×106個であった。冷却剥離率は86%だった。
実施例11
<VERO細胞培養>
温度応答性マイクロキャリア4を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は12.8×106個で、冷却で回収できなかった細胞数は0.8×106個であった。冷却剥離率は94%だった。
<VERO細胞培養>
温度応答性マイクロキャリア4を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は12.8×106個で、冷却で回収できなかった細胞数は0.8×106個であった。冷却剥離率は94%だった。
比較例1
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.050wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10gと0.050wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が50.00wt%である温度応答性マイクロキャリア9を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア9を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は22.3×105個で、冷却で回収できなかった細胞数は89.0×105個であった。冷却剥離率は20%だった。
温度応答性マイクロキャリア9を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は22.3×105個で、冷却で回収できなかった細胞数は89.0×105個であった。冷却剥離率は20%だった。
比較例2
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.00wt%である温度応答性マイクロキャリア10を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア10を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は39.3×105個で、冷却で回収できなかった細胞数は10.7×105個であった。冷却剥離率は79%だが、全細胞数が参考例1記載の現行の汎用マイクロキャリアで培養した全細胞数を下回った。
温度応答性マイクロキャリア10を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は39.3×105個で、冷却で回収できなかった細胞数は10.7×105個であった。冷却剥離率は79%だが、全細胞数が参考例1記載の現行の汎用マイクロキャリアで培養した全細胞数を下回った。
比較例3
200mLのフラスコに0.050wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を10g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が100.00wt%であるマイクロキャリア11を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア11を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は2.3×105個で、冷却で回収できなかった細胞数は98.5×105個であった。冷却剥離率は2%だった。
温度応答性マイクロキャリア11を用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は2.3×105個で、冷却で回収できなかった細胞数は98.5×105個であった。冷却剥離率は2%だった。
比較例4
<VERO細胞培養>
温度応答性マイクロキャリア9を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は6.7×106個で、冷却で回収できなかった細胞数は6.1×106個であった。冷却剥離率は52%だった。
<VERO細胞培養>
温度応答性マイクロキャリア9を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は6.7×106個で、冷却で回収できなかった細胞数は6.1×106個であった。冷却剥離率は52%だった。
比較例5
<VERO細胞培養>
温度応答性マイクロキャリア10を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は6.9×106個で、冷却で回収できなかった細胞数は1.2×106個であった。冷却剥離率は85%だった。
<VERO細胞培養>
温度応答性マイクロキャリア10を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は6.9×106個で、冷却で回収できなかった細胞数は1.2×106個であった。冷却剥離率は85%だった。
比較例6
<VERO細胞培養>
温度応答性マイクロキャリア11を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は1.4×106個で、冷却で回収できなかった細胞数は11.1×106個であった。冷却剥離率は85%だった。
<VERO細胞培養>
温度応答性マイクロキャリア11を用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は1.4×106個で、冷却で回収できなかった細胞数は11.1×106個であった。冷却剥離率は85%だった。
参考例1
<ヒト骨髄由来間葉系幹細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに20mg(培養面積87cm2)のオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を加えた。さらにロンザ製のヒト骨髄由来間葉系幹細胞(継代数2)を5×105cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で60rpmの撹拌条件で6日間培養した。
<ヒト骨髄由来間葉系幹細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに20mg(培養面積87cm2)のオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を加えた。さらにロンザ製のヒト骨髄由来間葉系幹細胞(継代数2)を5×105cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で60rpmの撹拌条件で6日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、静置してCytodex1を沈降させ、27mLの培地を抜取り、新たに27mLのPBS(-)を加えた。静置してCytodex1を沈降させ、27mLの液を抜取り、5mLのTrypLE Express Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、さらにセルストレーナー上に5mLのPBS(-)を2回加え、細胞をチューブ内に回収し、遠心分離で濃縮して細胞数を計測した。細胞数は51.7×105個であった。
参考例2
<VERO細胞培養>
参考例1のマイクロキャリア(Cytodex1、表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにしたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は1.4×106個で、冷却で回収できなかった細胞数は8.7×106個であった。冷却剥離率は14%だった。
<VERO細胞培養>
参考例1のマイクロキャリア(Cytodex1、表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにしたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は1.4×106個で、冷却で回収できなかった細胞数は8.7×106個であった。冷却剥離率は14%だった。
参考例3
<VERO細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに416mg(培養面積150cm2)のオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を加えた。さらに30mLの10%のウシ胎児血清(Fetal bovine serum、バイオウエスト社)と1%の抗生物質-抗真菌剤溶液(和光純薬社)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社)を加えた。さらにJCRB細胞バンク製のVERO細胞(継代数16)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で120rpmの撹拌条件で8日間培養した。Cellbindマイクロキャリアを用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は1.4×106個で、冷却で回収できなかった細胞数は14.1×106個であった。冷却剥離率は9%だった。
<VERO細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに416mg(培養面積150cm2)のオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を加えた。さらに30mLの10%のウシ胎児血清(Fetal bovine serum、バイオウエスト社)と1%の抗生物質-抗真菌剤溶液(和光純薬社)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社)を加えた。さらにJCRB細胞バンク製のVERO細胞(継代数16)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で120rpmの撹拌条件で8日間培養した。Cellbindマイクロキャリアを用いたこと以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は1.4×106個で、冷却で回収できなかった細胞数は14.1×106個であった。冷却剥離率は9%だった。
実施例12
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を12gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を12g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.03)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
200mLのフラスコに0.050wt%の温度応答性ブロック共重合体MBIの1-メトキシ-2-プロパノール溶液を12gと0.00038wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を12g加えた。さらに直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.03)を10g加え、1分間静置した。フラスコをエバポレーターに設置し、撹拌速度60rpmに設定の上、12000Paで1分間定圧処理した。さらに10000Paで1分間定圧処理、8000Paで1分間定圧処理、6000Paで2分間定圧処理、4000Paで3分間定圧処理した。撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで1500Paまで減圧し真空含浸処理を行った。
フラスコをエバポレーターから取り外し、イオン交換水を150mL加え、超音波を照射し10分間静置した。ろ過で回収したビーズを200mLのフラスコに移し、エバポレーターで撹拌速度120rpmに設定の上、最終的に真空ポンプの出力を最大にして30分間処理することで負電荷を有するポリマーの割合が0.74wt%である温度応答性マイクロキャリア12を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア12を195mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は61.3×105個で、冷却で回収できなかった細胞数は1.4×105個であった。冷却剥離率は98%だった。
温度応答性マイクロキャリア12を195mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は61.3×105個で、冷却で回収できなかった細胞数は1.4×105個であった。冷却剥離率は98%だった。
実施例13
500mLのセパラブルフラスコをセットしPTFE(poly(1,1,2,2-tetrafluoroethylene)製)撹拌翼を装着し、直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)40gを加え100rpmで攪拌しながらフラスコ内窒素ガスでパージした。ポリスチレンビーズを80℃まで予熱させた後、攪拌速度を300rpmまで上げ、0.014wt%の温度応答性ブロックコポリマーMBIの1-メトキシ-2-プロパノール溶液を7gと0.0001wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を1g加え4分間混合した。80℃の熱風乾燥機で20時間追加乾燥後、負電荷を有するポリマーの割合が4.76wt%である温度応答性マイクロキャリア13を得た。
500mLのセパラブルフラスコをセットしPTFE(poly(1,1,2,2-tetrafluoroethylene)製)撹拌翼を装着し、直径130μmの乾燥したポリスチレンビーズ(表面:カチオン性、平均比重:1.08)40gを加え100rpmで攪拌しながらフラスコ内窒素ガスでパージした。ポリスチレンビーズを80℃まで予熱させた後、攪拌速度を300rpmまで上げ、0.014wt%の温度応答性ブロックコポリマーMBIの1-メトキシ-2-プロパノール溶液を7gと0.0001wt%のポリマーCStSの1-メトキシ-2-プロパノール溶液を1g加え4分間混合した。80℃の熱風乾燥機で20時間追加乾燥後、負電荷を有するポリマーの割合が4.76wt%である温度応答性マイクロキャリア13を得た。
<ヒト骨髄由来間葉系幹細胞培養>
温度応答性マイクロキャリア13を204mg(培養面積87cm2)用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は16.3×105個で、冷却で回収できなかった細胞数は2.4×105個であった。冷却剥離率は87%だった。
温度応答性マイクロキャリア13を204mg(培養面積87cm2)用いたこと以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は16.3×105個で、冷却で回収できなかった細胞数は2.4×105個であった。冷却剥離率は87%だった。
参考例4
<ヒト骨髄由来間葉系幹細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を238mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は20.0×105個で、冷却で回収できなかった細胞数は28.2×105個であった。冷却剥離率は59%だった。
<ヒト骨髄由来間葉系幹細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を238mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は20.0×105個で、冷却で回収できなかった細胞数は28.2×105個であった。冷却剥離率は59%だった。
参考例5
<ヒト骨髄由来間葉系幹細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を20mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は21.1×105個で、冷却で回収できなかった細胞数は28.9×105個であった。冷却剥離率は42%だった。
<ヒト骨髄由来間葉系幹細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を20mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例1の<ヒト骨髄由来間葉系幹細胞培養>と同じ方法でヒト骨髄由来間葉系幹細胞を培養し、細胞数を計測した。冷却で回収した細胞数は21.1×105個で、冷却で回収できなかった細胞数は28.9×105個であった。冷却剥離率は42%だった。
実施例14
<VERO細胞培養>
温度応答性マイクロキャリア13を340mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は122.0×105個で、冷却で回収できなかった細胞数は12.0×105個であった。冷却剥離率は91%だった。
<VERO細胞培養>
温度応答性マイクロキャリア13を340mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例9の<VERO細胞培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は122.0×105個で、冷却で回収できなかった細胞数は12.0×105個であった。冷却剥離率は91%だった。
実施例15
<VERO細胞の無血清培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア13とVP-SFM(1X)(Thermo Fisher Scientific製、製品番号:11681020)1Lに200mMのL-Glutamine Solution(1X)(ATCC製、製品番号:30-2214)20mLを加え最終濃度が20mMの完成培地30mLを加えた。さらに、Vero細胞(American Type Culture Collection(ATCC)製、製品番号:CCL-81)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で8日間培養した。
<VERO細胞の無血清培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア13とVP-SFM(1X)(Thermo Fisher Scientific製、製品番号:11681020)1Lに200mMのL-Glutamine Solution(1X)(ATCC製、製品番号:30-2214)20mLを加え最終濃度が20mMの完成培地30mLを加えた。さらに、Vero細胞(American Type Culture Collection(ATCC)製、製品番号:CCL-81)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で8日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、浮遊細胞を除去し、セルストレーナー上の細胞が接着されているマイクロキャリアのみ回収し、4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に60回ピペッティング操作を行い、剥離細胞を目開き70μmのセルストレーナーをセットした50mLのチューブに通すことで回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は46.5×105個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのCTS TrypLE Select Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、細胞を回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は4.2×105個であった。冷却剥離率は92%だった。
参考例6
<VERO細胞の無血清培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例15の<VERO細胞の無血清培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は3.6×105個で、冷却で回収できなかった細胞数は36.4×105個であった。冷却剥離率は9%だった。
<VERO細胞の無血清培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例15の<VERO細胞の無血清培養>と同じ方法でVERO細胞を培養し、細胞数を計測した。冷却で回収した細胞数は3.6×105個で、冷却で回収できなかった細胞数は36.4×105個であった。冷却剥離率は9%だった。
実施例16
<BHK-21細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに340mg(培養面積150cm2)の温度応答性マイクロキャリア12と10%のウシ胎児血清(FBS、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)の完成培地30mLを加えた。さらに、BHK-21細胞(ATCC製、製品番号:CCL-10)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で60rpmの撹拌条件で7日間培養した。
<BHK-21細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに340mg(培養面積150cm2)の温度応答性マイクロキャリア12と10%のウシ胎児血清(FBS、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)の完成培地30mLを加えた。さらに、BHK-21細胞(ATCC製、製品番号:CCL-10)を1×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で60rpmの撹拌条件で7日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、浮遊細胞を除去し、セルストレーナー上の細胞が接着されているマイクロキャリアのみ回収し、4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に60回ピペッティング操作を行い、剥離細胞を目開き70μmのセルストレーナーをセットした50mLのチューブに通すことで回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は148.0×105個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのCTS TrypLE Select Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、細胞を回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は19.0×105個であった。冷却剥離率は89%だった。
参考例7
<BHK-21細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を416mg(培養面積150cm2)用いたこと以外は実施例16の<BHK-21細胞培養>と同じ方法でBHK-21細胞を培養し、細胞数を計測した。冷却で回収した細胞数は6.0×105個で、冷却で回収できなかった細胞数は115.0×105個であった。冷却剥離率は5%だった。
<BHK-21細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を416mg(培養面積150cm2)用いたこと以外は実施例16の<BHK-21細胞培養>と同じ方法でBHK-21細胞を培養し、細胞数を計測した。冷却で回収した細胞数は6.0×105個で、冷却で回収できなかった細胞数は115.0×105個であった。冷却剥離率は5%だった。
参考例8
<BHK-21細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと以外は実施例16の<BHK-21細胞培養>と同じ方法でBHK-21細胞を培養し、細胞数を計測した。冷却で回収した細胞数は18.0×105個で、冷却で回収できなかった細胞数は104.0×105個であった。冷却剥離率は15%だった。
<BHK-21細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと以外は実施例16の<BHK-21細胞培養>と同じ方法でBHK-21細胞を培養し、細胞数を計測した。冷却で回収した細胞数は18.0×105個で、冷却で回収できなかった細胞数は104.0×105個であった。冷却剥離率は15%だった。
実施例17
<CRFK細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア4と10%のウマ血清(HS、シグマアルドリッチジャパン合同会社製)を含有するEMEM(ATCC-formulated Eagle’s Minimum Essential Medium、ATCC製、製品番号:30-2003)の完成培地30mLを加えた。さらに、CRFK細胞(ATCC製、製品番号:CCL-94)を0.8×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で7日間培養した。
<CRFK細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア4と10%のウマ血清(HS、シグマアルドリッチジャパン合同会社製)を含有するEMEM(ATCC-formulated Eagle’s Minimum Essential Medium、ATCC製、製品番号:30-2003)の完成培地30mLを加えた。さらに、CRFK細胞(ATCC製、製品番号:CCL-94)を0.8×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で7日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、浮遊細胞を除去し、セルストレーナー上の細胞が接着されているマイクロキャリアのみ回収し、4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に60回ピペッティング操作を行い、剥離細胞を目開き70μmのセルストレーナーをセットした50mLのチューブに通すことで回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は26.8.0×105個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのCTS TrypLE Select Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、細胞を回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は3.1×105個であった。冷却剥離率は90%だった。
実施例18
<CRFK細胞培養>
マイクロキャリア12を340mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は13.8×105個で、冷却で回収できなかった細胞数は3.8×105個であった。冷却剥離率は78%だった。
<CRFK細胞培養>
マイクロキャリア12を340mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は13.8×105個で、冷却で回収できなかった細胞数は3.8×105個であった。冷却剥離率は78%だった。
実施例19
<CRFK細胞培養>
マイクロキャリア13を356mg(培養面積150cm2)用いたこと以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は21.2×105個で、冷却で回収できなかった細胞数は4.6×105個であった。冷却剥離率は82%だった。
<CRFK細胞培養>
マイクロキャリア13を356mg(培養面積150cm2)用いたこと以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は21.2×105個で、冷却で回収できなかった細胞数は4.6×105個であった。冷却剥離率は82%だった。
参考例9
<CRFK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を416mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は9.2×105個で、冷却で回収できなかった細胞数は12.9×105個であった。冷却剥離率は42%だった。
<CRFK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を416mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は9.2×105個で、冷却で回収できなかった細胞数は12.9×105個であった。冷却剥離率は42%だった。
参考例10
<CRFK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は3.2×105個で、冷却で回収できなかった細胞数は16.0×105個であった。冷却剥離率は17%だった。
<CRFK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例17の<CRFK細胞培養>と同じ方法でCRFK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は3.2×105個で、冷却で回収できなかった細胞数は16.0×105個であった。冷却剥離率は17%だった。
実施例20
<MDCK細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア4と10%のウシ胎児血清(FBS、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)の完成培地30mLを加えた。さらに、MDCK細胞(Japanese Collection of Research Bioresources(JCRB)製、製品番号:JCRB9029)を0.6×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で7日間培養した。
<MDCK細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに356mg(培養面積150cm2)の温度応答性マイクロキャリア4と10%のウシ胎児血清(FBS、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)の完成培地30mLを加えた。さらに、MDCK細胞(Japanese Collection of Research Bioresources(JCRB)製、製品番号:JCRB9029)を0.6×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で7日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、浮遊細胞を除去し、セルストレーナー上の細胞が接着されているマイクロキャリアのみ回収し、4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に60回ピペッティング操作を行い、剥離細胞を目開き70μmのセルストレーナーをセットした50mLのチューブに通すことで回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は137.0×105個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのCTS TrypLE Select Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、細胞を回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は37.0×105個であった。冷却剥離率は79%だった。
実施例21
<MDCK細胞培養>
マイクロキャリア12を340mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例19の<MDCK細胞培養>と同じ方法でMDCK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は112.0×105個で、冷却で回収できなかった細胞数は32.0×105個であった。冷却剥離率は78%だった。
<MDCK細胞培養>
マイクロキャリア12を340mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例19の<MDCK細胞培養>と同じ方法でMDCK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は112.0×105個で、冷却で回収できなかった細胞数は32.0×105個であった。冷却剥離率は78%だった。
参考例11
<MDCK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を416mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例20の<MDCK細胞培養>と同じ方法でMDCK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は2.3×105個で、冷却で回収できなかった細胞数は68.8×105個であった。冷却剥離率は3%だった。
<MDCK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を416mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例20の<MDCK細胞培養>と同じ方法でMDCK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は2.3×105個で、冷却で回収できなかった細胞数は68.8×105個であった。冷却剥離率は3%だった。
参考例12
<MDCK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例20の<MDCK細胞培養>と同じ方法でMDCK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は16.7×105個で、冷却で回収できなかった細胞数は157.4×105個であった。冷却剥離率は10%だった。
<MDCK細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を34.1mg(培養面積150cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例20の<MDCK細胞培養>と同じ方法でMDCK細胞を培養し、細胞数を計測した。冷却で回収した細胞数は16.7×105個で、冷却で回収できなかった細胞数は157.4×105個であった。冷却剥離率は10%だった。
実施例22
<MRC-5細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに204mg(培養面積87cm2)の温度応答性マイクロキャリア4と10%のウシ胎児血清(FBS、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)の完成培地30mLを加えた。さらに、MRC-5細胞(Japanese Collection of Research Bioresources(JCRB)製、製品番号:JCRB9008)を0.5×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で6日間培養した。
<MRC-5細胞培養>
エイブル社製の30mLシングルユースバイオリアクターに204mg(培養面積87cm2)の温度応答性マイクロキャリア4と10%のウシ胎児血清(FBS、バイオウエスト社製)と1%の抗生物質-抗真菌剤溶液(和光純薬社製)を含有するDMEM(Dulbecco’s Modified Eagle Medium、和光純薬社製)の完成培地30mLを加えた。さらに、MRC-5細胞(Japanese Collection of Research Bioresources(JCRB)製、製品番号:JCRB9008)を0.5×106cells加えて37℃の5vol%CO2雰囲気のインキュベーター内で100rpmの撹拌条件で6日間培養した。
培養後、30mLシングルユースバイオリアクターを室温の安全キャビネットに移し、細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、浮遊細胞を除去し、セルストレーナー上の細胞が接着されているマイクロキャリアのみ回収し、4℃のカルシウムとマグネシウムが不含のリン酸緩衝生理食塩水(PBS(-))を加え、10分間静置した。静置後に60回ピペッティング操作を行い、剥離細胞を目開き70μmのセルストレーナーをセットした50mLのチューブに通すことで回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収した細胞数は9.8×105個であった。さらにセルストレーナー上のマイクロキャリアを15mLのチューブに移し、5mLのCTS TrypLE Select Enzyme(Thermo Fisher Scientific製)を加え、37℃の5vol%CO2雰囲気で5分間静置した。細胞懸濁液を目開き70μmのセルストレーナーをセットした50mLのチューブに通し、細胞を回収し、遠心分離で濃縮して細胞数を計測した。冷却で回収できなかった細胞数は4.1×105個であった。冷却剥離率は71%だった。
実施例23
<MRC-5細胞培養>
マイクロキャリア12を195mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例22の<MRC-5細胞培養>と同じ方法でMRC-5細胞を培養し、細胞数を計測した。冷却で回収した細胞数は18.8×105個で、冷却で回収できなかった細胞数は1.0×105個であった。冷却剥離率は95%だった。
<MRC-5細胞培養>
マイクロキャリア12を195mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例22の<MRC-5細胞培養>と同じ方法でMRC-5細胞を培養し、細胞数を計測した。冷却で回収した細胞数は18.8×105個で、冷却で回収できなかった細胞数は1.0×105個であった。冷却剥離率は95%だった。
参考例13
<MRC-5細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を238mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例22の<MRC-5細胞培養>と同じ方法でMRC-5細胞を培養し、細胞数を計測した。冷却で回収した細胞数は3.4×105個で、冷却で回収できなかった細胞数は8.8×105個であった。冷却剥離率は28%だった。
<MRC-5細胞培養>
マイクロキャリアをオートクレーブ滅菌したCellbind(表面:アニオン性、平均比重:1.026)を238mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例22の<MRC-5細胞培養>と同じ方法でMRC-5細胞を培養し、細胞数を計測した。冷却で回収した細胞数は3.4×105個で、冷却で回収できなかった細胞数は8.8×105個であった。冷却剥離率は28%だった。
参考例14
<MRC-5細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を20mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例22の<MRC-5細胞培養>と同じ方法でMRC-5細胞を培養し、細胞数を計測した。冷却で回収した細胞数は4.2×105個で、冷却で回収できなかった細胞数は9.2×105個であった。冷却剥離率は31%だった。
<MRC-5細胞培養>
マイクロキャリアをオートクレーブ滅菌したCytodex1(表面:カチオン性、平均比重:1.03)を20mg(培養面積87cm2)用いたこと及び攪拌速度を60rpmにした以外は実施例22の<MRC-5細胞培養>と同じ方法でMRC-5細胞を培養し、細胞数を計測した。冷却で回収した細胞数は4.2×105個で、冷却で回収できなかった細胞数は9.2×105個であった。冷却剥離率は31%だった。
Claims (14)
- 下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーを含むポリマーコート膜を被覆したビーズからなるマイクロキャリア。
- 負電荷を有するポリマーの割合が0.1~20wt%であることを特徴とする請求項1記載のマイクロキャリア。
- 負電荷を有するポリマー中にカルボキシ基が含まれることを特徴とする請求項2記載のマイクロキャリア。
- 負電荷を有するポリマー中のカルボキシ基の割合が10~50wt%であることを特徴とする請求項3記載のマイクロキャリア。
- ビーズ表面がカチオン性であることを特徴とする請求項4記載のマイクロキャリア。
- ビーズに正電荷を有する官能基が修飾していることを特徴とする請求項4記載のマイクロキャリア。
- ビーズがトリメチルアンモニウムクロライド修飾ポリスチレンであることを特徴とする請求項6記載のマイクロキャリア。
- ビーズの粒径が20μm~1000μmであることを特徴とする請求項7記載のマイクロキャリア。
- 温度応答性ポリマーが下記(A)、(B)、(C)のブロックを含むブロック共重合体であることを特徴とする請求項8記載のマイクロキャリア。
(A)HLB値(グリフィン法)が7以上20以下の範囲にある重合体ブロック。
(B)HLB値(グリフィン法)が0以上7未満の範囲にある重合体ブロック。
(C)水に対する下限臨界溶解温度(LCST)が0℃~50℃の範囲にある温度応答性重合体ブロック。 - 請求項1~9記載のマイクロキャリアの製造方法。
- ビーズを、下限臨界溶解温度を0℃~50℃に有する温度応答性ポリマーと負電荷を有するポリマーとを含むポリマーコート膜で被覆する工程を備えることを特徴とする請求項1~9記載のマイクロキャリアの製造方法。
- 請求項1~9記載のマイクロキャリアを用いた細胞培養方法。
- 請求項1~9記載のマイクロキャリアを含有する培地で、細胞を培養する工程を含むことを特徴とする細胞培養方法。
- キレート剤を含む冷却液を用いて、細胞をマイクロキャリアから剥離する冷却細胞剥離工程を含むことを特徴とする請求項12記載の細胞培養方法。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2025526105A JPWO2024253069A1 (ja) | 2023-06-06 | 2024-06-03 |
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| JP2023-093312 | 2023-06-06 | ||
| JP2023093312 | 2023-06-06 | ||
| JP2023147342 | 2023-09-12 | ||
| JP2023-147342 | 2023-09-12 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| WO2024253069A1 true WO2024253069A1 (ja) | 2024-12-12 |
Family
ID=93796011
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| PCT/JP2024/020256 Ceased WO2024253069A1 (ja) | 2023-06-06 | 2024-06-03 | 温度応答性マイクロキャリア |
Country Status (2)
| Country | Link |
|---|---|
| JP (1) | JPWO2024253069A1 (ja) |
| WO (1) | WO2024253069A1 (ja) |
Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010508851A (ja) * | 2006-11-13 | 2010-03-25 | エシコン・インコーポレイテッド | マイクロキャリアを使用した、産褥由来の細胞の生体外での拡大 |
| JP2011514169A (ja) * | 2008-03-17 | 2011-05-06 | エージェンシー フォー サイエンス,テクノロジー アンド リサーチ | 幹細胞培養のためのマイクロキャリア |
| WO2015093393A1 (ja) * | 2013-12-20 | 2015-06-25 | Dic株式会社 | 温度応答性細胞培養基材及びその製造方法 |
| WO2015111686A1 (ja) * | 2014-01-23 | 2015-07-30 | 日産化学工業株式会社 | 培地組成物 |
| JP2016501026A (ja) * | 2012-12-14 | 2016-01-18 | デピュイ・シンセス・プロダクツ・インコーポレイテッド | hUTC増殖用栄養強化培地 |
| JP2016036274A (ja) * | 2014-08-06 | 2016-03-22 | 株式会社Ihi | 細胞剥離方法、細胞剥離装置、及び、細胞培養システム |
| JP2019094421A (ja) * | 2017-11-22 | 2019-06-20 | 東ソー株式会社 | ブロック共重合体コートビーズおよびその製造方法 |
| WO2020054755A1 (ja) * | 2018-09-11 | 2020-03-19 | 日産化学株式会社 | 分離デバイスおよびそれを用いて分離対象物を分離する方法 |
| WO2022202911A1 (ja) * | 2021-03-26 | 2022-09-29 | 東ソー株式会社 | 温度応答性高分子表面処理剤 |
-
2024
- 2024-06-03 WO PCT/JP2024/020256 patent/WO2024253069A1/ja not_active Ceased
- 2024-06-03 JP JP2025526105A patent/JPWO2024253069A1/ja active Pending
Patent Citations (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JP2010508851A (ja) * | 2006-11-13 | 2010-03-25 | エシコン・インコーポレイテッド | マイクロキャリアを使用した、産褥由来の細胞の生体外での拡大 |
| JP2011514169A (ja) * | 2008-03-17 | 2011-05-06 | エージェンシー フォー サイエンス,テクノロジー アンド リサーチ | 幹細胞培養のためのマイクロキャリア |
| JP2016501026A (ja) * | 2012-12-14 | 2016-01-18 | デピュイ・シンセス・プロダクツ・インコーポレイテッド | hUTC増殖用栄養強化培地 |
| WO2015093393A1 (ja) * | 2013-12-20 | 2015-06-25 | Dic株式会社 | 温度応答性細胞培養基材及びその製造方法 |
| WO2015111686A1 (ja) * | 2014-01-23 | 2015-07-30 | 日産化学工業株式会社 | 培地組成物 |
| JP2016036274A (ja) * | 2014-08-06 | 2016-03-22 | 株式会社Ihi | 細胞剥離方法、細胞剥離装置、及び、細胞培養システム |
| JP2019094421A (ja) * | 2017-11-22 | 2019-06-20 | 東ソー株式会社 | ブロック共重合体コートビーズおよびその製造方法 |
| WO2020054755A1 (ja) * | 2018-09-11 | 2020-03-19 | 日産化学株式会社 | 分離デバイスおよびそれを用いて分離対象物を分離する方法 |
| WO2022202911A1 (ja) * | 2021-03-26 | 2022-09-29 | 東ソー株式会社 | 温度応答性高分子表面処理剤 |
Also Published As
| Publication number | Publication date |
|---|---|
| JPWO2024253069A1 (ja) | 2024-12-12 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US11046803B2 (en) | Block copolymer and surface treatment agent using same | |
| EP0914835B1 (en) | Biocompatible polymeric coatings | |
| JP2018174919A (ja) | ブロック共重合体およびそれを用いた表面処理剤 | |
| US20120156781A1 (en) | Temperature-responsive cell culture substrate on which a straight-chain temperature-responsive polymer is immobilized, and manufacturing method therefor | |
| WO2016159153A1 (ja) | 細胞培養基材、その製造方法、およびそれを用いた細胞培養方法 | |
| JP6150071B2 (ja) | 有機ケイ素化合物及びそれを含むシランカップリング剤 | |
| JP2020110140A (ja) | 細胞培養方法 | |
| CN103224679A (zh) | 壳聚糖聚丙烯酰胺水凝胶基底材料及其制备方法 | |
| Xia et al. | Cell attachment/detachment behavior on poly (N-isopropylacrylamide)-based microgel films: the effect of microgel structure and swelling ratio | |
| Darge et al. | Preparation of thermosensitive PNIPAm‐based copolymer coated cytodex 3 microcarriers for efficient nonenzymatic cell harvesting during 3D culturing | |
| WO2019035436A1 (ja) | 多能性幹細胞の培養基材及び多能性幹細胞の製造方法 | |
| WO2024253069A1 (ja) | 温度応答性マイクロキャリア | |
| JP7700843B2 (ja) | 温度応答性高分子表面処理剤 | |
| JP7250248B2 (ja) | ブロック共重合体、それを含む表面処理剤及び膜、並びに、それを用いた細胞培養用器材及び細胞培養方法 | |
| JP7480485B2 (ja) | 細胞分離方法 | |
| WO2024253070A1 (ja) | 温度応答性不織布 | |
| JP6954047B2 (ja) | ブロック共重合体コートビーズおよびその製造方法 | |
| JP2018164412A (ja) | 細胞凝集塊形成用基材、細胞凝集塊の形成方法、物質のスクリーニング方法、細胞の機能探索方法、細胞培養基材用コーティング剤、及び細胞凝集塊形成促進剤 | |
| JP2025134229A (ja) | 温度応答性ビーズの製造方法 | |
| JPWO2024075722A5 (ja) | ||
| WO2024075722A1 (ja) | 温度応答性マイクロキャリアを用いた細胞培養方法及び温度応答性細胞培養用ビーズ | |
| JP2025127417A (ja) | 温度応答性マイクロキャリアを用いた拡大培養方法 | |
| JP2021159049A (ja) | 接着性細胞を増殖させる方法、及びその方法のために用いられるマイクロキャリア | |
| JP2021151210A (ja) | マイクロキャリアおよびそれを用いた細胞の培養方法 | |
| US20240158660A1 (en) | Surface treatment agent |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| 121 | Ep: the epo has been informed by wipo that ep was designated in this application |
Ref document number: 24819299 Country of ref document: EP Kind code of ref document: A1 |
|
| ENP | Entry into the national phase |
Ref document number: 2025526105 Country of ref document: JP Kind code of ref document: A |
|
| WWE | Wipo information: entry into national phase |
Ref document number: 2025526105 Country of ref document: JP |
|
| NENP | Non-entry into the national phase |
Ref country code: DE |