BRPI0407255B1 - Composições de resina, artigo conformado, processos para provimento de uma poliolefina e para o aumento de temperatura de cristalização desta, filme orientado monoaxial ou biaxialmente, sistemas multicamadas, compostos e seus usos, e mistura - Google Patents
Composições de resina, artigo conformado, processos para provimento de uma poliolefina e para o aumento de temperatura de cristalização desta, filme orientado monoaxial ou biaxialmente, sistemas multicamadas, compostos e seus usos, e mistura Download PDFInfo
- Publication number
- BRPI0407255B1 BRPI0407255B1 BRPI0407255-3A BRPI0407255A BRPI0407255B1 BR PI0407255 B1 BRPI0407255 B1 BR PI0407255B1 BR PI0407255 A BRPI0407255 A BR PI0407255A BR PI0407255 B1 BRPI0407255 B1 BR PI0407255B1
- Authority
- BR
- Brazil
- Prior art keywords
- bis
- butyl
- benzamide
- methyl
- fact
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 100
- 238000000034 method Methods 0.000 title claims description 65
- 230000008569 process Effects 0.000 title claims description 44
- 238000002425 crystallisation Methods 0.000 title claims description 13
- 230000008025 crystallization Effects 0.000 title claims description 13
- 239000011342 resin composition Substances 0.000 title abstract description 4
- 238000002156 mixing Methods 0.000 title description 3
- 239000000203 mixture Substances 0.000 claims abstract description 119
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 113
- 229920001059 synthetic polymer Polymers 0.000 claims abstract description 19
- -1 -tert-butyl diamide Chemical compound 0.000 claims description 321
- 229910052757 nitrogen Inorganic materials 0.000 claims description 79
- 229920001577 copolymer Polymers 0.000 claims description 70
- 239000000654 additive Substances 0.000 claims description 32
- 239000004743 Polypropylene Substances 0.000 claims description 25
- 150000001412 amines Chemical class 0.000 claims description 23
- 150000003254 radicals Chemical class 0.000 claims description 23
- 239000002253 acid Substances 0.000 claims description 20
- 229920001155 polypropylene Polymers 0.000 claims description 20
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 20
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 claims description 19
- 239000005977 Ethylene Substances 0.000 claims description 19
- 230000000996 additive effect Effects 0.000 claims description 18
- 238000002347 injection Methods 0.000 claims description 17
- 239000007924 injection Substances 0.000 claims description 17
- 239000002667 nucleating agent Substances 0.000 claims description 16
- 229920000098 polyolefin Polymers 0.000 claims description 15
- 229920002554 vinyl polymer Polymers 0.000 claims description 15
- 125000001973 tert-pentyl group Chemical group [H]C([H])([H])C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 14
- 239000004952 Polyamide Substances 0.000 claims description 12
- 150000002148 esters Chemical class 0.000 claims description 12
- 229920002647 polyamide Polymers 0.000 claims description 12
- 238000001125 extrusion Methods 0.000 claims description 11
- 125000001972 isopentyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])C([H])([H])* 0.000 claims description 10
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 10
- 239000000835 fiber Substances 0.000 claims description 9
- 238000000465 moulding Methods 0.000 claims description 9
- YARNUSSCRCMUME-UHFFFAOYSA-N 5-(2,2-dimethylpropanoylamino)benzene-1,3-dicarboxylic acid Chemical compound CC(C)(C)C(=O)NC1=CC(C(O)=O)=CC(C(O)=O)=C1 YARNUSSCRCMUME-UHFFFAOYSA-N 0.000 claims description 8
- 150000001252 acrylic acid derivatives Chemical class 0.000 claims description 8
- 125000002914 sec-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 8
- 229920001519 homopolymer Polymers 0.000 claims description 7
- 239000000314 lubricant Substances 0.000 claims description 7
- 239000004711 α-olefin Substances 0.000 claims description 7
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 claims description 6
- AVXURJPOCDRRFD-UHFFFAOYSA-N Hydroxylamine Chemical compound ON AVXURJPOCDRRFD-UHFFFAOYSA-N 0.000 claims description 6
- 239000003638 chemical reducing agent Substances 0.000 claims description 6
- XGPSTLRFHJVMTP-UHFFFAOYSA-N n'-(2,2-dimethylpropanoyl)benzohydrazide Chemical compound CC(C)(C)C(=O)NNC(=O)C1=CC=CC=C1 XGPSTLRFHJVMTP-UHFFFAOYSA-N 0.000 claims description 6
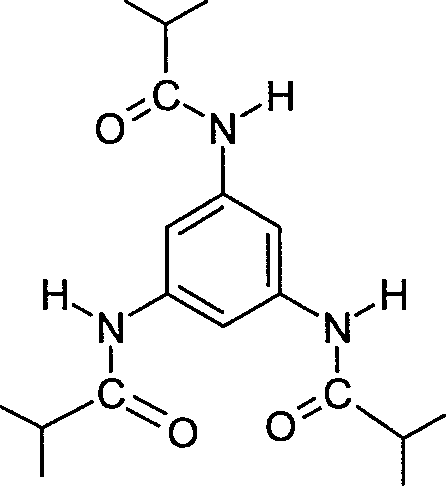
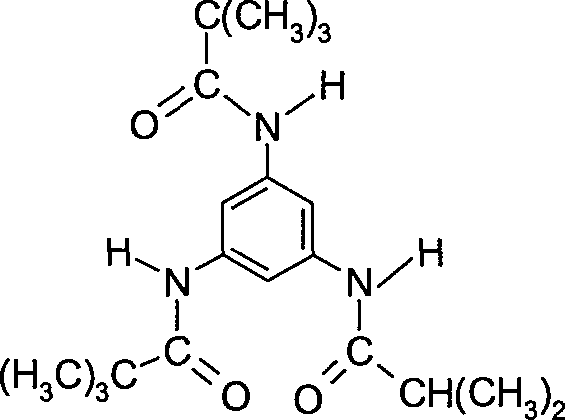
- CPEULHAPWXMDDV-UHFFFAOYSA-N n-[3,5-bis(2,2-dimethylpropanoylamino)phenyl]-2,2-dimethylpropanamide Chemical compound CC(C)(C)C(=O)NC1=CC(NC(=O)C(C)(C)C)=CC(NC(=O)C(C)(C)C)=C1 CPEULHAPWXMDDV-UHFFFAOYSA-N 0.000 claims description 6
- 229920005629 polypropylene homopolymer Polymers 0.000 claims description 6
- 239000003381 stabilizer Substances 0.000 claims description 6
- 125000003538 pentan-3-yl group Chemical group [H]C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 claims description 5
- 150000002978 peroxides Chemical class 0.000 claims description 5
- 125000003548 sec-pentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])[H] 0.000 claims description 5
- 150000005208 1,4-dihydroxybenzenes Chemical class 0.000 claims description 4
- XXNOZIMYHXRVAG-UHFFFAOYSA-N 3,5-bis(2,2-dimethylpropanoylamino)-n-propan-2-ylbenzamide Chemical compound CC(C)NC(=O)C1=CC(NC(=O)C(C)(C)C)=CC(NC(=O)C(C)(C)C)=C1 XXNOZIMYHXRVAG-UHFFFAOYSA-N 0.000 claims description 4
- CPYKOJLWWVNMQZ-UHFFFAOYSA-N 3,5-bis(2-methylpropanoylamino)-n-(2,4,4-trimethylpentan-2-yl)benzamide Chemical compound CC(C)C(=O)NC1=CC(NC(=O)C(C)C)=CC(C(=O)NC(C)(C)CC(C)(C)C)=C1 CPYKOJLWWVNMQZ-UHFFFAOYSA-N 0.000 claims description 4
- HXRKJMFSXYOVOW-UHFFFAOYSA-N 3,5-bis(2-methylpropanoylamino)-n-propan-2-ylbenzamide Chemical compound CC(C)NC(=O)C1=CC(NC(=O)C(C)C)=CC(NC(=O)C(C)C)=C1 HXRKJMFSXYOVOW-UHFFFAOYSA-N 0.000 claims description 4
- 239000003963 antioxidant agent Substances 0.000 claims description 4
- 235000006708 antioxidants Nutrition 0.000 claims description 4
- 229920001400 block copolymer Polymers 0.000 claims description 4
- 238000010348 incorporation Methods 0.000 claims description 4
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 4
- CMLHEHXOWQWJKX-UHFFFAOYSA-N n-(3-methylbutyl)-3,5-bis(4-methylpentanoylamino)benzamide Chemical compound CC(C)CCNC(=O)C1=CC(NC(=O)CCC(C)C)=CC(NC(=O)CCC(C)C)=C1 CMLHEHXOWQWJKX-UHFFFAOYSA-N 0.000 claims description 4
- SQDFHQJTAWCFIB-UHFFFAOYSA-N n-methylidenehydroxylamine Chemical compound ON=C SQDFHQJTAWCFIB-UHFFFAOYSA-N 0.000 claims description 4
- 125000001971 neopentyl group Chemical group [H]C([*])([H])C(C([H])([H])[H])(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 4
- 229920005604 random copolymer Polymers 0.000 claims description 4
- 125000004493 2-methylbut-1-yl group Chemical group CC(C*)CC 0.000 claims description 3
- YOUSVCIYWQHESX-UHFFFAOYSA-N 3,5-bis(3-methylbutanoylamino)-n-(3-methylbutyl)benzamide Chemical compound CC(C)CCNC(=O)C1=CC(NC(=O)CC(C)C)=CC(NC(=O)CC(C)C)=C1 YOUSVCIYWQHESX-UHFFFAOYSA-N 0.000 claims description 3
- ACZGCWSMSTYWDQ-UHFFFAOYSA-N 3h-1-benzofuran-2-one Chemical class C1=CC=C2OC(=O)CC2=C1 ACZGCWSMSTYWDQ-UHFFFAOYSA-N 0.000 claims description 3
- 235000010233 benzoic acid Nutrition 0.000 claims description 3
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 3
- 238000007664 blowing Methods 0.000 claims description 3
- RNMNIWCXWPCKEN-UHFFFAOYSA-N n-[3,5-bis(2,2-dimethylpropanoylamino)phenyl]-3,3-dimethylbutanamide Chemical compound CC(C)(C)CC(=O)NC1=CC(NC(=O)C(C)(C)C)=CC(NC(=O)C(C)(C)C)=C1 RNMNIWCXWPCKEN-UHFFFAOYSA-N 0.000 claims description 3
- GYXDNDSUBCPBNZ-UHFFFAOYSA-N n-[3-(2,2-dimethylpropanoylamino)-5-(2-methylpropanoylamino)phenyl]-2,2-dimethylpropanamide Chemical compound CC(C)C(=O)NC1=CC(NC(=O)C(C)(C)C)=CC(NC(=O)C(C)(C)C)=C1 GYXDNDSUBCPBNZ-UHFFFAOYSA-N 0.000 claims description 3
- 150000002989 phenols Chemical class 0.000 claims description 3
- AQSJGOWTSHOLKH-UHFFFAOYSA-N phosphite(3-) Chemical class [O-]P([O-])[O-] AQSJGOWTSHOLKH-UHFFFAOYSA-N 0.000 claims description 3
- 238000001175 rotational moulding Methods 0.000 claims description 3
- 238000009987 spinning Methods 0.000 claims description 3
- HJIAMFHSAAEUKR-UHFFFAOYSA-N (2-hydroxyphenyl)-phenylmethanone Chemical class OC1=CC=CC=C1C(=O)C1=CC=CC=C1 HJIAMFHSAAEUKR-UHFFFAOYSA-N 0.000 claims description 2
- 125000006219 1-ethylpentyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C([H])([H])[H] 0.000 claims description 2
- HWRLEEPNFJNTOP-UHFFFAOYSA-N 2-(1,3,5-triazin-2-yl)phenol Chemical class OC1=CC=CC=C1C1=NC=NC=N1 HWRLEEPNFJNTOP-UHFFFAOYSA-N 0.000 claims description 2
- QLMGIWHWWWXXME-UHFFFAOYSA-N 2-(3,5-ditert-butyl-4-hydroxyphenyl)acetic acid Chemical class CC(C)(C)C1=CC(CC(O)=O)=CC(C(C)(C)C)=C1O QLMGIWHWWWXXME-UHFFFAOYSA-N 0.000 claims description 2
- FJGQBLRYBUAASW-UHFFFAOYSA-N 2-(benzotriazol-2-yl)phenol Chemical class OC1=CC=CC=C1N1N=C2C=CC=CC2=N1 FJGQBLRYBUAASW-UHFFFAOYSA-N 0.000 claims description 2
- WPMYUUITDBHVQZ-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoic acid Chemical class CC(C)(C)C1=CC(CCC(O)=O)=CC(C(C)(C)C)=C1O WPMYUUITDBHVQZ-UHFFFAOYSA-N 0.000 claims description 2
- FLZYQMOKBVFXJS-UHFFFAOYSA-N 3-(3-tert-butyl-4-hydroxy-5-methylphenyl)propanoic acid Chemical class CC1=CC(CCC(O)=O)=CC(C(C)(C)C)=C1O FLZYQMOKBVFXJS-UHFFFAOYSA-N 0.000 claims description 2
- VPWLFOOAVIRLEF-UHFFFAOYSA-N 3-hydroperoxy-3-oxopropanoic acid Chemical class OOC(=O)CC(O)=O VPWLFOOAVIRLEF-UHFFFAOYSA-N 0.000 claims description 2
- 125000003542 3-methylbutan-2-yl group Chemical group [H]C([H])([H])C([H])(*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 claims description 2
- 229930185605 Bisphenol Natural products 0.000 claims description 2
- LTBRACVJRXLQHC-UHFFFAOYSA-N OP(=O)OCC1=CC=CC=C1 Chemical class OP(=O)OCC1=CC=CC=C1 LTBRACVJRXLQHC-UHFFFAOYSA-N 0.000 claims description 2
- YIKSCQDJHCMVMK-UHFFFAOYSA-N Oxamide Chemical class NC(=O)C(N)=O YIKSCQDJHCMVMK-UHFFFAOYSA-N 0.000 claims description 2
- 235000010323 ascorbic acid Nutrition 0.000 claims description 2
- 239000011668 ascorbic acid Substances 0.000 claims description 2
- 229960005070 ascorbic acid Drugs 0.000 claims description 2
- 150000001559 benzoic acids Chemical class 0.000 claims description 2
- HGCIXCUEYOPUTN-UHFFFAOYSA-N cis-cyclohexene Natural products C1CCC=CC1 HGCIXCUEYOPUTN-UHFFFAOYSA-N 0.000 claims description 2
- 238000007906 compression Methods 0.000 claims description 2
- 230000006835 compression Effects 0.000 claims description 2
- 150000002443 hydroxylamines Chemical class 0.000 claims description 2
- JYGFTBXVXVMTGB-UHFFFAOYSA-N indolin-2-one Chemical class C1=CC=C2NC(=O)CC2=C1 JYGFTBXVXVMTGB-UHFFFAOYSA-N 0.000 claims description 2
- 239000006078 metal deactivator Substances 0.000 claims description 2
- ZOPZLMGYAAOUQM-UHFFFAOYSA-N n-[3,5-bis(2-methylpropanoylamino)phenyl]-3,3-dimethylbutanamide Chemical compound CC(C)C(=O)NC1=CC(NC(=O)CC(C)(C)C)=CC(NC(=O)C(C)C)=C1 ZOPZLMGYAAOUQM-UHFFFAOYSA-N 0.000 claims description 2
- GNEBSLDFZWGFSB-UHFFFAOYSA-N n-[3-(3,3-dimethylbutanoylamino)-5-(2,2-dimethylpropanoylamino)phenyl]-3,3-dimethylbutanamide Chemical compound CC(C)(C)CC(=O)NC1=CC(NC(=O)CC(C)(C)C)=CC(NC(=O)C(C)(C)C)=C1 GNEBSLDFZWGFSB-UHFFFAOYSA-N 0.000 claims description 2
- 150000002816 nickel compounds Chemical class 0.000 claims description 2
- XRBCRPZXSCBRTK-UHFFFAOYSA-N phosphonous acid Chemical class OPO XRBCRPZXSCBRTK-UHFFFAOYSA-N 0.000 claims description 2
- 229930003799 tocopherol Natural products 0.000 claims description 2
- 239000011732 tocopherol Substances 0.000 claims description 2
- 235000019149 tocopherols Nutrition 0.000 claims description 2
- 150000003918 triazines Chemical class 0.000 claims description 2
- JSPLKZUTYZBBKA-UHFFFAOYSA-N trioxidane Chemical class OOO JSPLKZUTYZBBKA-UHFFFAOYSA-N 0.000 claims description 2
- QUEDXNHFTDJVIY-UHFFFAOYSA-N γ-tocopherol Chemical class OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1 QUEDXNHFTDJVIY-UHFFFAOYSA-N 0.000 claims description 2
- GZUZMDDAJCZRRI-UHFFFAOYSA-N 5-(2,2-dimethylbutanoylamino)benzene-1,3-dicarboxylic acid Chemical compound CCC(C)(C)C(=O)NC1=CC(C(O)=O)=CC(C(O)=O)=C1 GZUZMDDAJCZRRI-UHFFFAOYSA-N 0.000 claims 4
- 239000004744 fabric Substances 0.000 claims 4
- NEZORLJFVGEQNO-UHFFFAOYSA-N CC(CC(=O)NC1=C(C(=CC(=C1)NC(C(CC)(C)C)=O)NC(CC(C)(C)C)=O)N)(C)C Chemical compound CC(CC(=O)NC1=C(C(=CC(=C1)NC(C(CC)(C)C)=O)NC(CC(C)(C)C)=O)N)(C)C NEZORLJFVGEQNO-UHFFFAOYSA-N 0.000 claims 1
- 230000009977 dual effect Effects 0.000 claims 1
- 125000003518 norbornenyl group Chemical class C12(C=CC(CC1)C2)* 0.000 claims 1
- 229920005615 natural polymer Polymers 0.000 abstract description 3
- SECXISVLQFMRJM-UHFFFAOYSA-N N-Methylpyrrolidone Chemical compound CN1CCCC1=O SECXISVLQFMRJM-UHFFFAOYSA-N 0.000 description 201
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 120
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 105
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 104
- 238000002360 preparation method Methods 0.000 description 96
- 238000002844 melting Methods 0.000 description 83
- 230000008018 melting Effects 0.000 description 83
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 75
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 description 68
- KWGKDLIKAYFUFQ-UHFFFAOYSA-M lithium chloride Chemical compound [Li+].[Cl-] KWGKDLIKAYFUFQ-UHFFFAOYSA-M 0.000 description 54
- KDLHZDBZIXYQEI-UHFFFAOYSA-N palladium Substances [Pd] KDLHZDBZIXYQEI-UHFFFAOYSA-N 0.000 description 52
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 52
- PPBRXRYQALVLMV-UHFFFAOYSA-N Styrene Chemical group C=CC1=CC=CC=C1 PPBRXRYQALVLMV-UHFFFAOYSA-N 0.000 description 49
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 48
- 238000001953 recrystallisation Methods 0.000 description 45
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 42
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 42
- 238000000746 purification Methods 0.000 description 42
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 41
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 40
- 239000000047 product Substances 0.000 description 36
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 36
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 35
- QQVIHTHCMHWDBS-UHFFFAOYSA-N perisophthalic acid Natural products OC(=O)C1=CC=CC(C(O)=O)=C1 QQVIHTHCMHWDBS-UHFFFAOYSA-N 0.000 description 33
- OAKJQQAXSVQMHS-UHFFFAOYSA-N Hydrazine Chemical compound NN OAKJQQAXSVQMHS-UHFFFAOYSA-N 0.000 description 32
- 239000000843 powder Substances 0.000 description 32
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 31
- 239000003054 catalyst Substances 0.000 description 30
- 239000011541 reaction mixture Substances 0.000 description 29
- 239000000243 solution Substances 0.000 description 29
- 229920000642 polymer Polymers 0.000 description 28
- 239000007787 solid Substances 0.000 description 28
- 229940086542 triethylamine Drugs 0.000 description 25
- YXFVVABEGXRONW-UHFFFAOYSA-N Toluene Natural products CC1=CC=CC=C1 YXFVVABEGXRONW-UHFFFAOYSA-N 0.000 description 23
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 22
- 239000001993 wax Substances 0.000 description 22
- NLHHRLWOUZZQLW-UHFFFAOYSA-N Acrylonitrile Chemical compound C=CC#N NLHHRLWOUZZQLW-UHFFFAOYSA-N 0.000 description 20
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 20
- ZUOUZKKEUPVFJK-UHFFFAOYSA-N diphenyl Chemical compound C1=CC=CC=C1C1=CC=CC=C1 ZUOUZKKEUPVFJK-UHFFFAOYSA-N 0.000 description 19
- 125000004356 hydroxy functional group Chemical group O* 0.000 description 18
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 18
- 239000002904 solvent Substances 0.000 description 17
- 125000003837 (C1-C20) alkyl group Chemical group 0.000 description 16
- 238000006243 chemical reaction Methods 0.000 description 16
- 239000002244 precipitate Substances 0.000 description 16
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 description 15
- 239000004305 biphenyl Substances 0.000 description 15
- 229910052751 metal Inorganic materials 0.000 description 15
- 239000002184 metal Substances 0.000 description 15
- 229910052763 palladium Inorganic materials 0.000 description 15
- ISWSIDIOOBJBQZ-UHFFFAOYSA-N Phenol Chemical compound OC1=CC=CC=C1 ISWSIDIOOBJBQZ-UHFFFAOYSA-N 0.000 description 14
- 239000004698 Polyethylene Substances 0.000 description 14
- 239000007983 Tris buffer Substances 0.000 description 14
- 235000010290 biphenyl Nutrition 0.000 description 14
- 238000000354 decomposition reaction Methods 0.000 description 14
- 238000002330 electrospray ionisation mass spectrometry Methods 0.000 description 14
- 239000002585 base Substances 0.000 description 13
- 239000000543 intermediate Substances 0.000 description 13
- 239000000155 melt Substances 0.000 description 13
- 239000003960 organic solvent Substances 0.000 description 13
- KBZFDRWPMZESDI-UHFFFAOYSA-N 5-aminobenzene-1,3-dicarboxylic acid Chemical compound NC1=CC(C(O)=O)=CC(C(O)=O)=C1 KBZFDRWPMZESDI-UHFFFAOYSA-N 0.000 description 12
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 12
- 238000005917 acylation reaction Methods 0.000 description 12
- MTHSVFCYNBDYFN-UHFFFAOYSA-N diethylene glycol Chemical compound OCCOCCO MTHSVFCYNBDYFN-UHFFFAOYSA-N 0.000 description 12
- 238000005984 hydrogenation reaction Methods 0.000 description 12
- PGZVFRAEAAXREB-UHFFFAOYSA-N 2,2-dimethylpropanoyl 2,2-dimethylpropanoate Chemical compound CC(C)(C)C(=O)OC(=O)C(C)(C)C PGZVFRAEAAXREB-UHFFFAOYSA-N 0.000 description 11
- 230000010933 acylation Effects 0.000 description 11
- 125000000753 cycloalkyl group Chemical group 0.000 description 11
- 229920000573 polyethylene Polymers 0.000 description 11
- 238000000859 sublimation Methods 0.000 description 11
- 230000008022 sublimation Effects 0.000 description 11
- NBDAHKQJXVLAID-UHFFFAOYSA-N 5-nitroisophthalic acid Chemical compound OC(=O)C1=CC(C(O)=O)=CC([N+]([O-])=O)=C1 NBDAHKQJXVLAID-UHFFFAOYSA-N 0.000 description 10
- XBDQKXXYIPTUBI-UHFFFAOYSA-M Propionate Chemical compound CCC([O-])=O XBDQKXXYIPTUBI-UHFFFAOYSA-M 0.000 description 10
- 239000003795 chemical substances by application Substances 0.000 description 10
- 239000012141 concentrate Substances 0.000 description 10
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 10
- RFFLAFLAYFXFSW-UHFFFAOYSA-N 1,2-dichlorobenzene Chemical compound ClC1=CC=CC=C1Cl RFFLAFLAYFXFSW-UHFFFAOYSA-N 0.000 description 9
- VXNZUUAINFGPBY-UHFFFAOYSA-N 1-Butene Chemical compound CCC=C VXNZUUAINFGPBY-UHFFFAOYSA-N 0.000 description 9
- RGSFGYAAUTVSQA-UHFFFAOYSA-N Cyclopentane Chemical compound C1CCCC1 RGSFGYAAUTVSQA-UHFFFAOYSA-N 0.000 description 9
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 9
- JKIJEFPNVSHHEI-UHFFFAOYSA-N Phenol, 2,4-bis(1,1-dimethylethyl)-, phosphite (3:1) Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC=C1OP(OC=1C(=CC(=CC=1)C(C)(C)C)C(C)(C)C)OC1=CC=C(C(C)(C)C)C=C1C(C)(C)C JKIJEFPNVSHHEI-UHFFFAOYSA-N 0.000 description 9
- 230000015572 biosynthetic process Effects 0.000 description 9
- 239000007789 gas Substances 0.000 description 9
- 239000001257 hydrogen Substances 0.000 description 9
- 229910052739 hydrogen Inorganic materials 0.000 description 9
- 239000005457 ice water Substances 0.000 description 9
- 238000002955 isolation Methods 0.000 description 9
- 229920001684 low density polyethylene Polymers 0.000 description 9
- 239000004702 low-density polyethylene Substances 0.000 description 9
- 229920002857 polybutadiene Polymers 0.000 description 9
- 238000003786 synthesis reaction Methods 0.000 description 9
- 238000005406 washing Methods 0.000 description 9
- JVSFQJZRHXAUGT-UHFFFAOYSA-N 2,2-dimethylpropanoyl chloride Chemical compound CC(C)(C)C(Cl)=O JVSFQJZRHXAUGT-UHFFFAOYSA-N 0.000 description 8
- 239000004215 Carbon black (E152) Substances 0.000 description 8
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 8
- 239000005062 Polybutadiene Substances 0.000 description 8
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 8
- 125000003545 alkoxy group Chemical group 0.000 description 8
- 239000012298 atmosphere Substances 0.000 description 8
- ZPHQBFRCXUIIAZ-UHFFFAOYSA-N benzene;hydrochloride Chemical compound Cl.C1=CC=CC=C1 ZPHQBFRCXUIIAZ-UHFFFAOYSA-N 0.000 description 8
- 125000003236 benzoyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C(*)=O 0.000 description 8
- 150000001993 dienes Chemical class 0.000 description 8
- 229930195733 hydrocarbon Natural products 0.000 description 8
- 238000001746 injection moulding Methods 0.000 description 8
- 239000004417 polycarbonate Substances 0.000 description 8
- 239000000600 sorbitol Substances 0.000 description 8
- 230000006641 stabilisation Effects 0.000 description 8
- 238000011105 stabilization Methods 0.000 description 8
- MPBZUKLDHPOCLS-UHFFFAOYSA-N 3,5-dinitroaniline Chemical compound NC1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 MPBZUKLDHPOCLS-UHFFFAOYSA-N 0.000 description 7
- OHIVUAREQFICPK-UHFFFAOYSA-N 5-nitrobenzene-1,3-dicarbonyl chloride Chemical compound [O-][N+](=O)C1=CC(C(Cl)=O)=CC(C(Cl)=O)=C1 OHIVUAREQFICPK-UHFFFAOYSA-N 0.000 description 7
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 description 7
- PXHVJJICTQNCMI-UHFFFAOYSA-N Nickel Chemical compound [Ni] PXHVJJICTQNCMI-UHFFFAOYSA-N 0.000 description 7
- ABLZXFCXXLZCGV-UHFFFAOYSA-N Phosphorous acid Chemical compound OP(O)=O ABLZXFCXXLZCGV-UHFFFAOYSA-N 0.000 description 7
- 239000007868 Raney catalyst Substances 0.000 description 7
- 229910000564 Raney nickel Inorganic materials 0.000 description 7
- 229920000122 acrylonitrile butadiene styrene Polymers 0.000 description 7
- 125000003282 alkyl amino group Chemical group 0.000 description 7
- QRUDEWIWKLJBPS-UHFFFAOYSA-N benzotriazole Chemical compound C1=CC=C2N[N][N]C2=C1 QRUDEWIWKLJBPS-UHFFFAOYSA-N 0.000 description 7
- 239000012964 benzotriazole Substances 0.000 description 7
- 229910052799 carbon Inorganic materials 0.000 description 7
- 238000001816 cooling Methods 0.000 description 7
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 7
- 238000001914 filtration Methods 0.000 description 7
- 229920001903 high density polyethylene Polymers 0.000 description 7
- 239000004700 high-density polyethylene Substances 0.000 description 7
- 125000000449 nitro group Chemical group [O-][N+](*)=O 0.000 description 7
- 229910052760 oxygen Inorganic materials 0.000 description 7
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 7
- 238000010561 standard procedure Methods 0.000 description 7
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 6
- WQHXNDJZMBNEEH-UHFFFAOYSA-N 3,5-diamino-n-(3-methylbutyl)benzamide Chemical compound CC(C)CCNC(=O)C1=CC(N)=CC(N)=C1 WQHXNDJZMBNEEH-UHFFFAOYSA-N 0.000 description 6
- MZYKJELLDPAXNE-UHFFFAOYSA-N 3,5-diamino-n-cyclohexylbenzamide Chemical compound NC1=CC(N)=CC(C(=O)NC2CCCCC2)=C1 MZYKJELLDPAXNE-UHFFFAOYSA-N 0.000 description 6
- LOINHEQEMJNBMX-UHFFFAOYSA-N 3,5-diamino-n-cyclopentylbenzamide Chemical compound NC1=CC(N)=CC(C(=O)NC2CCCC2)=C1 LOINHEQEMJNBMX-UHFFFAOYSA-N 0.000 description 6
- WSSSPWUEQFSQQG-UHFFFAOYSA-N 4-methyl-1-pentene Chemical compound CC(C)CC=C WSSSPWUEQFSQQG-UHFFFAOYSA-N 0.000 description 6
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 6
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 6
- XDTMQSROBMDMFD-UHFFFAOYSA-N Cyclohexane Chemical compound C1CCCCC1 XDTMQSROBMDMFD-UHFFFAOYSA-N 0.000 description 6
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 6
- 150000001408 amides Chemical class 0.000 description 6
- 125000003118 aryl group Chemical group 0.000 description 6
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 6
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 6
- 235000013539 calcium stearate Nutrition 0.000 description 6
- 239000008116 calcium stearate Substances 0.000 description 6
- KBPLFHHGFOOTCA-UHFFFAOYSA-N caprylic alcohol Natural products CCCCCCCCO KBPLFHHGFOOTCA-UHFFFAOYSA-N 0.000 description 6
- 125000004432 carbon atom Chemical group C* 0.000 description 6
- 239000011248 coating agent Substances 0.000 description 6
- 238000000576 coating method Methods 0.000 description 6
- 238000004440 column chromatography Methods 0.000 description 6
- RVOJTCZRIKWHDX-UHFFFAOYSA-N cyclohexanecarbonyl chloride Chemical compound ClC(=O)C1CCCCC1 RVOJTCZRIKWHDX-UHFFFAOYSA-N 0.000 description 6
- WEPUZBYKXNKSDH-UHFFFAOYSA-N cyclopentanecarbonyl chloride Chemical compound ClC(=O)C1CCCC1 WEPUZBYKXNKSDH-UHFFFAOYSA-N 0.000 description 6
- 229920001971 elastomer Polymers 0.000 description 6
- 239000011521 glass Substances 0.000 description 6
- 239000000178 monomer Substances 0.000 description 6
- 239000001301 oxygen Substances 0.000 description 6
- 238000004806 packaging method and process Methods 0.000 description 6
- NFHFRUOZVGFOOS-UHFFFAOYSA-N palladium;triphenylphosphane Chemical compound [Pd].C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=CC=C1P(C=1C=CC=CC=1)C1=CC=CC=C1 NFHFRUOZVGFOOS-UHFFFAOYSA-N 0.000 description 6
- 238000006116 polymerization reaction Methods 0.000 description 6
- 229920006324 polyoxymethylene Polymers 0.000 description 6
- 239000004800 polyvinyl chloride Substances 0.000 description 6
- 229920000915 polyvinyl chloride Polymers 0.000 description 6
- 230000009467 reduction Effects 0.000 description 6
- 229910002027 silica gel Inorganic materials 0.000 description 6
- 239000000741 silica gel Substances 0.000 description 6
- 238000004809 thin layer chromatography Methods 0.000 description 6
- KAKZBPTYRLMSJV-UHFFFAOYSA-N vinyl-ethylene Natural products C=CC=C KAKZBPTYRLMSJV-UHFFFAOYSA-N 0.000 description 6
- HECLRDQVFMWTQS-RGOKHQFPSA-N 1755-01-7 Chemical compound C1[C@H]2[C@@H]3CC=C[C@@H]3[C@@H]1C=C2 HECLRDQVFMWTQS-RGOKHQFPSA-N 0.000 description 5
- LDJUYMIFFNTKOI-UHFFFAOYSA-N 2,2-dimethylbutanoyl chloride Chemical compound CCC(C)(C)C(Cl)=O LDJUYMIFFNTKOI-UHFFFAOYSA-N 0.000 description 5
- ISULZYQDGYXDFW-UHFFFAOYSA-N 3-methylbutanoyl chloride Chemical compound CC(C)CC(Cl)=O ISULZYQDGYXDFW-UHFFFAOYSA-N 0.000 description 5
- DFWXYHZQNLIBLY-UHFFFAOYSA-N 5-nitrobenzene-1,3-diamine Chemical compound NC1=CC(N)=CC([N+]([O-])=O)=C1 DFWXYHZQNLIBLY-UHFFFAOYSA-N 0.000 description 5
- 125000003860 C1-C20 alkoxy group Chemical group 0.000 description 5
- 239000004712 Metallocene polyethylene (PE-MC) Substances 0.000 description 5
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N N-phenyl amine Natural products NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 5
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 5
- 239000004721 Polyphenylene oxide Substances 0.000 description 5
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 5
- XITRBUPOXXBIJN-UHFFFAOYSA-N bis(2,2,6,6-tetramethylpiperidin-4-yl) decanedioate Chemical compound C1C(C)(C)NC(C)(C)CC1OC(=O)CCCCCCCCC(=O)OC1CC(C)(C)NC(C)(C)C1 XITRBUPOXXBIJN-UHFFFAOYSA-N 0.000 description 5
- 238000010790 dilution Methods 0.000 description 5
- 239000012895 dilution Substances 0.000 description 5
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 5
- 239000000499 gel Substances 0.000 description 5
- 229910052736 halogen Inorganic materials 0.000 description 5
- 150000002367 halogens Chemical class 0.000 description 5
- DMEGYFMYUHOHGS-UHFFFAOYSA-N heptamethylene Natural products C1CCCCCC1 DMEGYFMYUHOHGS-UHFFFAOYSA-N 0.000 description 5
- NAQMVNRVTILPCV-UHFFFAOYSA-N hexane-1,6-diamine Chemical compound NCCCCCCN NAQMVNRVTILPCV-UHFFFAOYSA-N 0.000 description 5
- LSACYLWPPQLVSM-UHFFFAOYSA-N isobutyric acid anhydride Chemical compound CC(C)C(=O)OC(=O)C(C)C LSACYLWPPQLVSM-UHFFFAOYSA-N 0.000 description 5
- ZFSLODLOARCGLH-UHFFFAOYSA-N isocyanuric acid Chemical compound OC1=NC(O)=NC(O)=N1 ZFSLODLOARCGLH-UHFFFAOYSA-N 0.000 description 5
- 239000000463 material Substances 0.000 description 5
- ZGEGCLOFRBLKSE-UHFFFAOYSA-N methylene hexane Natural products CCCCCC=C ZGEGCLOFRBLKSE-UHFFFAOYSA-N 0.000 description 5
- 125000001624 naphthyl group Chemical group 0.000 description 5
- WXZMFSXDPGVJKK-UHFFFAOYSA-N pentaerythritol Chemical compound OCC(CO)(CO)CO WXZMFSXDPGVJKK-UHFFFAOYSA-N 0.000 description 5
- 229920000728 polyester Polymers 0.000 description 5
- 229920006380 polyphenylene oxide Polymers 0.000 description 5
- KUKFKAPJCRZILJ-UHFFFAOYSA-N prop-2-enenitrile;prop-2-enoic acid Chemical class C=CC#N.OC(=O)C=C KUKFKAPJCRZILJ-UHFFFAOYSA-N 0.000 description 5
- 229920005989 resin Polymers 0.000 description 5
- 239000011347 resin Substances 0.000 description 5
- 239000000126 substance Substances 0.000 description 5
- 150000005846 sugar alcohols Polymers 0.000 description 5
- 229920001897 terpolymer Polymers 0.000 description 5
- 239000008096 xylene Substances 0.000 description 5
- OJOWICOBYCXEKR-APPZFPTMSA-N (1S,4R)-5-ethylidenebicyclo[2.2.1]hept-2-ene Chemical compound CC=C1C[C@@H]2C[C@@H]1C=C2 OJOWICOBYCXEKR-APPZFPTMSA-N 0.000 description 4
- 125000006652 (C3-C12) cycloalkyl group Chemical group 0.000 description 4
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 description 4
- DNIAPMSPPWPWGF-GSVOUGTGSA-N (R)-(-)-Propylene glycol Chemical compound C[C@@H](O)CO DNIAPMSPPWPWGF-GSVOUGTGSA-N 0.000 description 4
- ALVZNPYWJMLXKV-UHFFFAOYSA-N 1,9-Nonanediol Chemical compound OCCCCCCCCCO ALVZNPYWJMLXKV-UHFFFAOYSA-N 0.000 description 4
- AFFLGGQVNFXPEV-UHFFFAOYSA-N 1-decene Chemical compound CCCCCCCCC=C AFFLGGQVNFXPEV-UHFFFAOYSA-N 0.000 description 4
- CRSBERNSMYQZNG-UHFFFAOYSA-N 1-dodecene Chemical compound CCCCCCCCCCC=C CRSBERNSMYQZNG-UHFFFAOYSA-N 0.000 description 4
- GQEZCXVZFLOKMC-UHFFFAOYSA-N 1-hexadecene Chemical compound CCCCCCCCCCCCCCC=C GQEZCXVZFLOKMC-UHFFFAOYSA-N 0.000 description 4
- LIKMAJRDDDTEIG-UHFFFAOYSA-N 1-hexene Chemical compound CCCCC=C LIKMAJRDDDTEIG-UHFFFAOYSA-N 0.000 description 4
- JRZJOMJEPLMPRA-UHFFFAOYSA-N 1-nonene Chemical compound CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 4
- KWKAKUADMBZCLK-UHFFFAOYSA-N 1-octene Chemical compound CCCCCCC=C KWKAKUADMBZCLK-UHFFFAOYSA-N 0.000 description 4
- HFDVRLIODXPAHB-UHFFFAOYSA-N 1-tetradecene Chemical compound CCCCCCCCCCCCC=C HFDVRLIODXPAHB-UHFFFAOYSA-N 0.000 description 4
- DCTOHCCUXLBQMS-UHFFFAOYSA-N 1-undecene Chemical compound CCCCCCCCCC=C DCTOHCCUXLBQMS-UHFFFAOYSA-N 0.000 description 4
- 238000005160 1H NMR spectroscopy Methods 0.000 description 4
- KXPXKNBDCUOENF-UHFFFAOYSA-N 2-(Octylthio)ethanol Chemical compound CCCCCCCCSCCO KXPXKNBDCUOENF-UHFFFAOYSA-N 0.000 description 4
- NGNBDVOYPDDBFK-UHFFFAOYSA-N 2-[2,4-di(pentan-2-yl)phenoxy]acetyl chloride Chemical compound CCCC(C)C1=CC=C(OCC(Cl)=O)C(C(C)CCC)=C1 NGNBDVOYPDDBFK-UHFFFAOYSA-N 0.000 description 4
- ZPIRWAHWDCHWLM-UHFFFAOYSA-N 2-dodecylsulfanylethanol Chemical compound CCCCCCCCCCCCSCCO ZPIRWAHWDCHWLM-UHFFFAOYSA-N 0.000 description 4
- 229920000089 Cyclic olefin copolymer Polymers 0.000 description 4
- 229920000877 Melamine resin Polymers 0.000 description 4
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 4
- ZJCCRDAZUWHFQH-UHFFFAOYSA-N Trimethylolpropane Chemical compound CCC(CO)(CO)CO ZJCCRDAZUWHFQH-UHFFFAOYSA-N 0.000 description 4
- BZHJMEDXRYGGRV-UHFFFAOYSA-N Vinyl chloride Chemical compound ClC=C BZHJMEDXRYGGRV-UHFFFAOYSA-N 0.000 description 4
- 150000007513 acids Chemical class 0.000 description 4
- 239000012190 activator Substances 0.000 description 4
- WNLRTRBMVRJNCN-UHFFFAOYSA-N adipic acid Chemical compound OC(=O)CCCCC(O)=O WNLRTRBMVRJNCN-UHFFFAOYSA-N 0.000 description 4
- 150000001298 alcohols Chemical class 0.000 description 4
- 125000003342 alkenyl group Chemical group 0.000 description 4
- 150000008064 anhydrides Chemical class 0.000 description 4
- 125000005428 anthryl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C3C(*)=C([H])C([H])=C([H])C3=C([H])C2=C1[H] 0.000 description 4
- 239000011230 binding agent Substances 0.000 description 4
- 125000002529 biphenylenyl group Chemical group C1(=CC=CC=2C3=CC=CC=C3C12)* 0.000 description 4
- MTAZNLWOLGHBHU-UHFFFAOYSA-N butadiene-styrene rubber Chemical compound C=CC=C.C=CC1=CC=CC=C1 MTAZNLWOLGHBHU-UHFFFAOYSA-N 0.000 description 4
- PAFZNILMFXTMIY-UHFFFAOYSA-N cyclohexylamine Chemical compound NC1CCCCC1 PAFZNILMFXTMIY-UHFFFAOYSA-N 0.000 description 4
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 4
- 150000004985 diamines Chemical class 0.000 description 4
- DMBHHRLKUKUOEG-UHFFFAOYSA-N diphenylamine Chemical compound C=1C=CC=CC=1NC1=CC=CC=C1 DMBHHRLKUKUOEG-UHFFFAOYSA-N 0.000 description 4
- 239000003480 eluent Substances 0.000 description 4
- LDLDYFCCDKENPD-UHFFFAOYSA-N ethenylcyclohexane Chemical compound C=CC1CCCCC1 LDLDYFCCDKENPD-UHFFFAOYSA-N 0.000 description 4
- 235000013305 food Nutrition 0.000 description 4
- XXMIOPMDWAUFGU-UHFFFAOYSA-N hexane-1,6-diol Chemical compound OCCCCCCO XXMIOPMDWAUFGU-UHFFFAOYSA-N 0.000 description 4
- 238000009413 insulation Methods 0.000 description 4
- 150000002739 metals Chemical class 0.000 description 4
- DNIAPMSPPWPWGF-UHFFFAOYSA-N monopropylene glycol Natural products CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 4
- TVMXDCGIABBOFY-UHFFFAOYSA-N n-Octanol Natural products CCCCCCCC TVMXDCGIABBOFY-UHFFFAOYSA-N 0.000 description 4
- XBGNERSKEKDZDS-UHFFFAOYSA-N n-[2-(dimethylamino)ethyl]acridine-4-carboxamide Chemical compound C1=CC=C2N=C3C(C(=O)NCCN(C)C)=CC=CC3=CC2=C1 XBGNERSKEKDZDS-UHFFFAOYSA-N 0.000 description 4
- VAMFXQBUQXONLZ-UHFFFAOYSA-N n-alpha-eicosene Natural products CCCCCCCCCCCCCCCCCCC=C VAMFXQBUQXONLZ-UHFFFAOYSA-N 0.000 description 4
- CCCMONHAUSKTEQ-UHFFFAOYSA-N octadec-1-ene Chemical compound CCCCCCCCCCCCCCCCC=C CCCMONHAUSKTEQ-UHFFFAOYSA-N 0.000 description 4
- GLDOVTGHNKAZLK-UHFFFAOYSA-N octadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCCCO GLDOVTGHNKAZLK-UHFFFAOYSA-N 0.000 description 4
- 239000003921 oil Substances 0.000 description 4
- YWAKXRMUMFPDSH-UHFFFAOYSA-N pentene Chemical compound CCCC=C YWAKXRMUMFPDSH-UHFFFAOYSA-N 0.000 description 4
- 230000000737 periodic effect Effects 0.000 description 4
- 229920001281 polyalkylene Polymers 0.000 description 4
- 229920001707 polybutylene terephthalate Polymers 0.000 description 4
- 229960004063 propylene glycol Drugs 0.000 description 4
- 235000013772 propylene glycol Nutrition 0.000 description 4
- 150000003839 salts Chemical class 0.000 description 4
- 238000000926 separation method Methods 0.000 description 4
- 229910052717 sulfur Inorganic materials 0.000 description 4
- 239000011593 sulfur Substances 0.000 description 4
- YODZTKMDCQEPHD-UHFFFAOYSA-N thiodiglycol Chemical compound OCCSCCO YODZTKMDCQEPHD-UHFFFAOYSA-N 0.000 description 4
- ZIBGPFATKBEMQZ-UHFFFAOYSA-N triethylene glycol Chemical compound OCCOCCOCCO ZIBGPFATKBEMQZ-UHFFFAOYSA-N 0.000 description 4
- XOOUIPVCVHRTMJ-UHFFFAOYSA-L zinc stearate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O XOOUIPVCVHRTMJ-UHFFFAOYSA-L 0.000 description 4
- BPXVHIRIPLPOPT-UHFFFAOYSA-N 1,3,5-tris(2-hydroxyethyl)-1,3,5-triazinane-2,4,6-trione Chemical compound OCCN1C(=O)N(CCO)C(=O)N(CCO)C1=O BPXVHIRIPLPOPT-UHFFFAOYSA-N 0.000 description 3
- DWUJDNHHQKEOPR-UHFFFAOYSA-N 2-(2-piperidin-4-ylethyl)pyridine Chemical compound C1CNCCC1CCC1=CC=CC=N1 DWUJDNHHQKEOPR-UHFFFAOYSA-N 0.000 description 3
- RXFCIXRFAJRBSG-UHFFFAOYSA-N 3,2,3-tetramine Chemical compound NCCCNCCNCCCN RXFCIXRFAJRBSG-UHFFFAOYSA-N 0.000 description 3
- NNOHXABAQAGKRZ-UHFFFAOYSA-N 3,5-dinitrobenzoyl chloride Chemical compound [O-][N+](=O)C1=CC(C(Cl)=O)=CC([N+]([O-])=O)=C1 NNOHXABAQAGKRZ-UHFFFAOYSA-N 0.000 description 3
- CKPKHTKLLYPGFM-UHFFFAOYSA-N 6,6-dimethylheptane-1,1-diol Chemical compound CC(CCCCC(O)O)(C)C CKPKHTKLLYPGFM-UHFFFAOYSA-N 0.000 description 3
- NIXOWILDQLNWCW-UHFFFAOYSA-M Acrylate Chemical compound [O-]C(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-M 0.000 description 3
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 3
- 229920002943 EPDM rubber Polymers 0.000 description 3
- UAUDZVJPLUQNMU-UHFFFAOYSA-N Erucasaeureamid Natural products CCCCCCCCC=CCCCCCCCCCCCC(N)=O UAUDZVJPLUQNMU-UHFFFAOYSA-N 0.000 description 3
- 241001024304 Mino Species 0.000 description 3
- 229920002367 Polyisobutene Polymers 0.000 description 3
- 239000006096 absorbing agent Substances 0.000 description 3
- 230000006978 adaptation Effects 0.000 description 3
- 230000000386 athletic effect Effects 0.000 description 3
- MQTYQCAVOMQEFJ-UHFFFAOYSA-N benzene;trihydrochloride Chemical compound Cl.Cl.Cl.C1=CC=CC=C1 MQTYQCAVOMQEFJ-UHFFFAOYSA-N 0.000 description 3
- 125000000649 benzylidene group Chemical group [H]C(=[*])C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 3
- 125000002619 bicyclic group Chemical group 0.000 description 3
- 229910002091 carbon monoxide Inorganic materials 0.000 description 3
- 150000001244 carboxylic acid anhydrides Chemical class 0.000 description 3
- 150000001732 carboxylic acid derivatives Chemical class 0.000 description 3
- 150000001991 dicarboxylic acids Chemical class 0.000 description 3
- 235000014113 dietary fatty acids Nutrition 0.000 description 3
- 238000004455 differential thermal analysis Methods 0.000 description 3
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical group [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 3
- 239000000806 elastomer Substances 0.000 description 3
- 238000005516 engineering process Methods 0.000 description 3
- UAUDZVJPLUQNMU-KTKRTIGZSA-N erucamide Chemical compound CCCCCCCC\C=C/CCCCCCCCCCCC(N)=O UAUDZVJPLUQNMU-KTKRTIGZSA-N 0.000 description 3
- HQQADJVZYDDRJT-UHFFFAOYSA-N ethene;prop-1-ene Chemical group C=C.CC=C HQQADJVZYDDRJT-UHFFFAOYSA-N 0.000 description 3
- 229920001038 ethylene copolymer Polymers 0.000 description 3
- 239000005038 ethylene vinyl acetate Substances 0.000 description 3
- 229920006226 ethylene-acrylic acid Polymers 0.000 description 3
- 238000000605 extraction Methods 0.000 description 3
- 229930195729 fatty acid Natural products 0.000 description 3
- 239000000194 fatty acid Substances 0.000 description 3
- 150000004665 fatty acids Chemical class 0.000 description 3
- 239000012467 final product Substances 0.000 description 3
- AHAREKHAZNPPMI-UHFFFAOYSA-N hexa-1,3-diene Chemical compound CCC=CC=C AHAREKHAZNPPMI-UHFFFAOYSA-N 0.000 description 3
- 229920000554 ionomer Polymers 0.000 description 3
- FPYJFEHAWHCUMM-UHFFFAOYSA-N maleic anhydride Chemical class O=C1OC(=O)C=C1 FPYJFEHAWHCUMM-UHFFFAOYSA-N 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 150000005673 monoalkenes Chemical class 0.000 description 3
- UKJARPDLRWBRAX-UHFFFAOYSA-N n,n'-bis(2,2,6,6-tetramethylpiperidin-4-yl)hexane-1,6-diamine Chemical compound C1C(C)(C)NC(C)(C)CC1NCCCCCCNC1CC(C)(C)NC(C)(C)C1 UKJARPDLRWBRAX-UHFFFAOYSA-N 0.000 description 3
- FPQJEXTVQZHURJ-UHFFFAOYSA-N n,n'-bis(2-hydroxyethyl)oxamide Chemical compound OCCNC(=O)C(=O)NCCO FPQJEXTVQZHURJ-UHFFFAOYSA-N 0.000 description 3
- FTWUXYZHDFCGSV-UHFFFAOYSA-N n,n'-diphenyloxamide Chemical compound C=1C=CC=CC=1NC(=O)C(=O)NC1=CC=CC=C1 FTWUXYZHDFCGSV-UHFFFAOYSA-N 0.000 description 3
- PMBAZUADXYLDHV-UHFFFAOYSA-N n-(3-methylbutyl)benzamide Chemical group CC(C)CCNC(=O)C1=CC=CC=C1 PMBAZUADXYLDHV-UHFFFAOYSA-N 0.000 description 3
- SLCVBVWXLSEKPL-UHFFFAOYSA-N neopentyl glycol Chemical compound OCC(C)(C)CO SLCVBVWXLSEKPL-UHFFFAOYSA-N 0.000 description 3
- 150000002815 nickel Chemical class 0.000 description 3
- 150000002848 norbornenes Chemical class 0.000 description 3
- 230000003287 optical effect Effects 0.000 description 3
- 125000001181 organosilyl group Chemical group [SiH3]* 0.000 description 3
- 239000008188 pellet Substances 0.000 description 3
- 229920000570 polyether Polymers 0.000 description 3
- 239000004814 polyurethane Substances 0.000 description 3
- HNJBEVLQSNELDL-UHFFFAOYSA-N pyrrolidin-2-one Chemical compound O=C1CCCN1 HNJBEVLQSNELDL-UHFFFAOYSA-N 0.000 description 3
- 239000005060 rubber Substances 0.000 description 3
- ZQBAKBUEJOMQEX-UHFFFAOYSA-N salicylic acid phenyl ester Natural products OC1=CC=CC=C1C(=O)OC1=CC=CC=C1 ZQBAKBUEJOMQEX-UHFFFAOYSA-N 0.000 description 3
- 238000005185 salting out Methods 0.000 description 3
- 238000003756 stirring Methods 0.000 description 3
- 230000009182 swimming Effects 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- IMFACGCPASFAPR-UHFFFAOYSA-N tributylamine Chemical compound CCCCN(CCCC)CCCC IMFACGCPASFAPR-UHFFFAOYSA-N 0.000 description 3
- 125000000026 trimethylsilyl group Chemical group [H]C([H])([H])[Si]([*])(C([H])([H])[H])C([H])([H])[H] 0.000 description 3
- YWEWWNPYDDHZDI-JJKKTNRVSA-N (1r)-1-[(4r,4ar,8as)-2,6-bis(3,4-dimethylphenyl)-4,4a,8,8a-tetrahydro-[1,3]dioxino[5,4-d][1,3]dioxin-4-yl]ethane-1,2-diol Chemical compound C1=C(C)C(C)=CC=C1C1O[C@H]2[C@@H]([C@H](O)CO)OC(C=3C=C(C)C(C)=CC=3)O[C@H]2CO1 YWEWWNPYDDHZDI-JJKKTNRVSA-N 0.000 description 2
- OJOWICOBYCXEKR-KRXBUXKQSA-N (5e)-5-ethylidenebicyclo[2.2.1]hept-2-ene Chemical compound C1C2C(=C/C)/CC1C=C2 OJOWICOBYCXEKR-KRXBUXKQSA-N 0.000 description 2
- 125000000008 (C1-C10) alkyl group Chemical group 0.000 description 2
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 2
- ZQMPWXFHAUDENN-UHFFFAOYSA-N 1,2-bis[(2-methylphenyl)amino]ethane Natural products CC1=CC=CC=C1NCCNC1=CC=CC=C1C ZQMPWXFHAUDENN-UHFFFAOYSA-N 0.000 description 2
- YHMYGUUIMTVXNW-UHFFFAOYSA-N 1,3-dihydrobenzimidazole-2-thione Chemical compound C1=CC=C2NC(S)=NC2=C1 YHMYGUUIMTVXNW-UHFFFAOYSA-N 0.000 description 2
- BUGAMLAPDQMYNZ-UHFFFAOYSA-N 1-(2,4,4-trimethylpentan-2-yl)-10h-phenothiazine Chemical class S1C2=CC=CC=C2NC2=C1C=CC=C2C(C)(C)CC(C)(C)C BUGAMLAPDQMYNZ-UHFFFAOYSA-N 0.000 description 2
- 229940106006 1-eicosene Drugs 0.000 description 2
- FIKTURVKRGQNQD-UHFFFAOYSA-N 1-eicosene Natural products CCCCCCCCCCCCCCCCCC=CC(O)=O FIKTURVKRGQNQD-UHFFFAOYSA-N 0.000 description 2
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 2
- BWJKLDGAAPQXGO-UHFFFAOYSA-N 2,2,6,6-tetramethyl-4-octadecoxypiperidine Chemical compound CCCCCCCCCCCCCCCCCCOC1CC(C)(C)NC(C)(C)C1 BWJKLDGAAPQXGO-UHFFFAOYSA-N 0.000 description 2
- QIJIUJYANDSEKG-UHFFFAOYSA-N 2,4,4-trimethylpentan-2-amine Chemical compound CC(C)(C)CC(C)(C)N QIJIUJYANDSEKG-UHFFFAOYSA-N 0.000 description 2
- ONTODYXHFBKCDK-UHFFFAOYSA-N 2-(2,4-dimethylphenyl)-1,3,5-triazine Chemical compound CC1=CC(C)=CC=C1C1=NC=NC=N1 ONTODYXHFBKCDK-UHFFFAOYSA-N 0.000 description 2
- HIXDQWDOVZUNNA-UHFFFAOYSA-N 2-(3,4-dimethoxyphenyl)-5-hydroxy-7-methoxychromen-4-one Chemical group C=1C(OC)=CC(O)=C(C(C=2)=O)C=1OC=2C1=CC=C(OC)C(OC)=C1 HIXDQWDOVZUNNA-UHFFFAOYSA-N 0.000 description 2
- OXWDLAHVJDUQJM-UHFFFAOYSA-N 2-[[2-[2-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyloxy]ethylamino]-2-oxoacetyl]amino]ethyl 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoate Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)OCCNC(=O)C(=O)NCCOC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 OXWDLAHVJDUQJM-UHFFFAOYSA-N 0.000 description 2
- 125000004189 3,4-dichlorophenyl group Chemical group [H]C1=C([H])C(Cl)=C(Cl)C([H])=C1* 0.000 description 2
- 125000002774 3,4-dimethoxybenzyl group Chemical group [H]C1=C([H])C(=C([H])C(OC([H])([H])[H])=C1OC([H])([H])[H])C([H])([H])* 0.000 description 2
- UENRXLSRMCSUSN-UHFFFAOYSA-N 3,5-diaminobenzoic acid Chemical compound NC1=CC(N)=CC(C(O)=O)=C1 UENRXLSRMCSUSN-UHFFFAOYSA-N 0.000 description 2
- ZMCQQCBOZIGNRV-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-[2-(1,2,4-triazol-1-yl)ethyl]benzamide Chemical compound NCC1=CC(OC2=CC=CC(=C2)C(=O)NCCN2C=NC=N2)=NC(=C1)C(F)(F)F ZMCQQCBOZIGNRV-UHFFFAOYSA-N 0.000 description 2
- FBIXXCXCZOZFCO-UHFFFAOYSA-N 3-dodecyl-1-(2,2,6,6-tetramethylpiperidin-4-yl)pyrrolidine-2,5-dione Chemical compound O=C1C(CCCCCCCCCCCC)CC(=O)N1C1CC(C)(C)NC(C)(C)C1 FBIXXCXCZOZFCO-UHFFFAOYSA-N 0.000 description 2
- 125000006180 3-methyl benzyl group Chemical group [H]C1=C([H])C(=C([H])C(=C1[H])C([H])([H])[H])C([H])([H])* 0.000 description 2
- JLBJTVDPSNHSKJ-UHFFFAOYSA-N 4-Methylstyrene Chemical group CC1=CC=C(C=C)C=C1 JLBJTVDPSNHSKJ-UHFFFAOYSA-N 0.000 description 2
- 125000004860 4-ethylphenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])C([H])([H])[H] 0.000 description 2
- 125000004861 4-isopropyl phenyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])(C([H])([H])[H])C([H])([H])[H] 0.000 description 2
- SVWCVXFHTHCJJB-UHFFFAOYSA-N 4-methylpentanoyl chloride Chemical compound CC(C)CCC(Cl)=O SVWCVXFHTHCJJB-UHFFFAOYSA-N 0.000 description 2
- UXPIWHPHEGRYLB-UHFFFAOYSA-N 5-aminobenzene-1,3-dicarboxamide Chemical compound NC(=O)C1=CC(N)=CC(C(N)=O)=C1 UXPIWHPHEGRYLB-UHFFFAOYSA-N 0.000 description 2
- RSWGJHLUYNHPMX-UHFFFAOYSA-N Abietic-Saeure Natural products C12CCC(C(C)C)=CC2=CCC2C1(C)CCCC2(C)C(O)=O RSWGJHLUYNHPMX-UHFFFAOYSA-N 0.000 description 2
- ZOXJGFHDIHLPTG-UHFFFAOYSA-N Boron Chemical compound [B] ZOXJGFHDIHLPTG-UHFFFAOYSA-N 0.000 description 2
- JGBQNDUNNCZLQX-UHFFFAOYSA-N C(C(C)C)(=O)NC1=C(C(=CC(=C1)C(C(CC)(C)C)=O)NC(C(C)C)=O)N Chemical compound C(C(C)C)(=O)NC1=C(C(=CC(=C1)C(C(CC)(C)C)=O)NC(C(C)C)=O)N JGBQNDUNNCZLQX-UHFFFAOYSA-N 0.000 description 2
- 239000004709 Chlorinated polyethylene Substances 0.000 description 2
- BRLQWZUYTZBJKN-UHFFFAOYSA-N Epichlorohydrin Chemical compound ClCC1CO1 BRLQWZUYTZBJKN-UHFFFAOYSA-N 0.000 description 2
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 2
- 229920010126 Linear Low Density Polyethylene (LLDPE) Polymers 0.000 description 2
- TWRXJAOTZQYOKJ-UHFFFAOYSA-L Magnesium chloride Chemical class [Mg+2].[Cl-].[Cl-] TWRXJAOTZQYOKJ-UHFFFAOYSA-L 0.000 description 2
- PEEHTFAAVSWFBL-UHFFFAOYSA-N Maleimide Chemical compound O=C1NC(=O)C=C1 PEEHTFAAVSWFBL-UHFFFAOYSA-N 0.000 description 2
- OFOBLEOULBTSOW-UHFFFAOYSA-L Malonate Chemical compound [O-]C(=O)CC([O-])=O OFOBLEOULBTSOW-UHFFFAOYSA-L 0.000 description 2
- BAPJBEWLBFYGME-UHFFFAOYSA-N Methyl acrylate Chemical compound COC(=O)C=C BAPJBEWLBFYGME-UHFFFAOYSA-N 0.000 description 2
- XQVWYOYUZDUNRW-UHFFFAOYSA-N N-Phenyl-1-naphthylamine Chemical compound C=1C=CC2=CC=CC=C2C=1NC1=CC=CC=C1 XQVWYOYUZDUNRW-UHFFFAOYSA-N 0.000 description 2
- KEQFTVQCIQJIQW-UHFFFAOYSA-N N-Phenyl-2-naphthylamine Chemical compound C=1C=C2C=CC=CC2=CC=1NC1=CC=CC=C1 KEQFTVQCIQJIQW-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- 239000006057 Non-nutritive feed additive Substances 0.000 description 2
- 229920002292 Nylon 6 Polymers 0.000 description 2
- REYJJPSVUYRZGE-UHFFFAOYSA-N Octadecylamine Chemical compound CCCCCCCCCCCCCCCCCCN REYJJPSVUYRZGE-UHFFFAOYSA-N 0.000 description 2
- 239000004793 Polystyrene Substances 0.000 description 2
- 229920002396 Polyurea Polymers 0.000 description 2
- KDYFGRWQOYBRFD-UHFFFAOYSA-N Succinic acid Natural products OC(=O)CCC(O)=O KDYFGRWQOYBRFD-UHFFFAOYSA-N 0.000 description 2
- KKEYFWRCBNTPAC-UHFFFAOYSA-N Terephthalic acid Chemical compound OC(=O)C1=CC=C(C(O)=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-N 0.000 description 2
- GWEVSGVZZGPLCZ-UHFFFAOYSA-N Titan oxide Chemical compound O=[Ti]=O GWEVSGVZZGPLCZ-UHFFFAOYSA-N 0.000 description 2
- JWUXJYZVKZKLTJ-UHFFFAOYSA-N Triacetonamine Chemical compound CC1(C)CC(=O)CC(C)(C)N1 JWUXJYZVKZKLTJ-UHFFFAOYSA-N 0.000 description 2
- XSQUKJJJFZCRTK-UHFFFAOYSA-N Urea Chemical compound NC(N)=O XSQUKJJJFZCRTK-UHFFFAOYSA-N 0.000 description 2
- XTXRWKRVRITETP-UHFFFAOYSA-N Vinyl acetate Chemical compound CC(=O)OC=C XTXRWKRVRITETP-UHFFFAOYSA-N 0.000 description 2
- KPCZJLGGXRGYIE-UHFFFAOYSA-N [C]1=CC=CN=C1 Chemical group [C]1=CC=CN=C1 KPCZJLGGXRGYIE-UHFFFAOYSA-N 0.000 description 2
- SZPWXAOBLNYOHY-UHFFFAOYSA-N [C]1=CC=NC2=CC=CC=C12 Chemical group [C]1=CC=NC2=CC=CC=C12 SZPWXAOBLNYOHY-UHFFFAOYSA-N 0.000 description 2
- 150000001241 acetals Chemical class 0.000 description 2
- 229920000800 acrylic rubber Polymers 0.000 description 2
- 239000000853 adhesive Substances 0.000 description 2
- 230000001070 adhesive effect Effects 0.000 description 2
- 239000001361 adipic acid Substances 0.000 description 2
- 235000011037 adipic acid Nutrition 0.000 description 2
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 2
- 229920000180 alkyd Polymers 0.000 description 2
- 125000005250 alkyl acrylate group Chemical group 0.000 description 2
- 125000005037 alkyl phenyl group Chemical group 0.000 description 2
- XYLMUPLGERFSHI-UHFFFAOYSA-N alpha-Methylstyrene Chemical compound CC(=C)C1=CC=CC=C1 XYLMUPLGERFSHI-UHFFFAOYSA-N 0.000 description 2
- AFVLVVWMAFSXCK-VMPITWQZSA-N alpha-cyano-4-hydroxycinnamic acid Chemical group OC(=O)C(\C#N)=C\C1=CC=C(O)C=C1 AFVLVVWMAFSXCK-VMPITWQZSA-N 0.000 description 2
- 229910052782 aluminium Inorganic materials 0.000 description 2
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 2
- PNEYBMLMFCGWSK-UHFFFAOYSA-N aluminium oxide Inorganic materials [O-2].[O-2].[O-2].[Al+3].[Al+3] PNEYBMLMFCGWSK-UHFFFAOYSA-N 0.000 description 2
- 238000004458 analytical method Methods 0.000 description 2
- 239000002216 antistatic agent Substances 0.000 description 2
- 238000013459 approach Methods 0.000 description 2
- 229940054066 benzamide antipsychotics Drugs 0.000 description 2
- IISBACLAFKSPIT-UHFFFAOYSA-N bisphenol A Chemical compound C=1C=C(O)C=CC=1C(C)(C)C1=CC=C(O)C=C1 IISBACLAFKSPIT-UHFFFAOYSA-N 0.000 description 2
- PXKLMJQFEQBVLD-UHFFFAOYSA-N bisphenol F Chemical compound C1=CC(O)=CC=C1CC1=CC=C(O)C=C1 PXKLMJQFEQBVLD-UHFFFAOYSA-N 0.000 description 2
- 229910052796 boron Inorganic materials 0.000 description 2
- DQXBYHZEEUGOBF-UHFFFAOYSA-N but-3-enoic acid;ethene Chemical compound C=C.OC(=O)CC=C DQXBYHZEEUGOBF-UHFFFAOYSA-N 0.000 description 2
- KDYFGRWQOYBRFD-NUQCWPJISA-N butanedioic acid Chemical compound O[14C](=O)CC[14C](O)=O KDYFGRWQOYBRFD-NUQCWPJISA-N 0.000 description 2
- 235000013877 carbamide Nutrition 0.000 description 2
- 150000004649 carbonic acid derivatives Chemical class 0.000 description 2
- 230000003197 catalytic effect Effects 0.000 description 2
- 239000007795 chemical reaction product Substances 0.000 description 2
- 239000002131 composite material Substances 0.000 description 2
- 238000010276 construction Methods 0.000 description 2
- 238000005520 cutting process Methods 0.000 description 2
- 125000004122 cyclic group Chemical group 0.000 description 2
- MGNZXYYWBUKAII-UHFFFAOYSA-N cyclohexa-1,3-diene Chemical compound C1CC=CC=C1 MGNZXYYWBUKAII-UHFFFAOYSA-N 0.000 description 2
- 125000004210 cyclohexylmethyl group Chemical group [H]C([H])(*)C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C1([H])[H] 0.000 description 2
- ZSWFCLXCOIISFI-UHFFFAOYSA-N cyclopentadiene Chemical compound C1C=CC=C1 ZSWFCLXCOIISFI-UHFFFAOYSA-N 0.000 description 2
- LPIQUOYDBNQMRZ-UHFFFAOYSA-N cyclopentene Chemical compound C1CC=CC1 LPIQUOYDBNQMRZ-UHFFFAOYSA-N 0.000 description 2
- 125000004851 cyclopentylmethyl group Chemical group C1(CCCC1)C* 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- 238000005034 decoration Methods 0.000 description 2
- MHDVGSVTJDSBDK-UHFFFAOYSA-N dibenzyl ether Chemical compound C=1C=CC=CC=1COCC1=CC=CC=C1 MHDVGSVTJDSBDK-UHFFFAOYSA-N 0.000 description 2
- 238000000113 differential scanning calorimetry Methods 0.000 description 2
- GYZLOYUZLJXAJU-UHFFFAOYSA-N diglycidyl ether Chemical class C1OC1COCC1CO1 GYZLOYUZLJXAJU-UHFFFAOYSA-N 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 229940035422 diphenylamine Drugs 0.000 description 2
- 229940069096 dodecene Drugs 0.000 description 2
- 238000001035 drying Methods 0.000 description 2
- 239000000428 dust Substances 0.000 description 2
- 239000003822 epoxy resin Substances 0.000 description 2
- RTZKZFJDLAIYFH-UHFFFAOYSA-N ether Chemical group CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 2
- 150000002170 ethers Chemical class 0.000 description 2
- 238000007765 extrusion coating Methods 0.000 description 2
- 239000000706 filtrate Substances 0.000 description 2
- 239000003063 flame retardant Substances 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000000446 fuel Substances 0.000 description 2
- 230000004927 fusion Effects 0.000 description 2
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 2
- 239000008187 granular material Substances 0.000 description 2
- 150000004820 halides Chemical class 0.000 description 2
- LNEPOXFFQSENCJ-UHFFFAOYSA-N haloperidol Chemical compound C1CC(O)(C=2C=CC(Cl)=CC=2)CCN1CCCC(=O)C1=CC=C(F)C=C1 LNEPOXFFQSENCJ-UHFFFAOYSA-N 0.000 description 2
- 150000002483 hydrogen compounds Chemical class 0.000 description 2
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 description 2
- 238000011065 in-situ storage Methods 0.000 description 2
- 238000003475 lamination Methods 0.000 description 2
- 229920000092 linear low density polyethylene Polymers 0.000 description 2
- 239000004707 linear low-density polyethylene Substances 0.000 description 2
- 125000000040 m-tolyl group Chemical group [H]C1=C([H])C(*)=C([H])C(=C1[H])C([H])([H])[H] 0.000 description 2
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 2
- 229920001179 medium density polyethylene Polymers 0.000 description 2
- 239000004701 medium-density polyethylene Substances 0.000 description 2
- JDSHMPZPIAZGSV-UHFFFAOYSA-N melamine Chemical compound NC1=NC(N)=NC(N)=N1 JDSHMPZPIAZGSV-UHFFFAOYSA-N 0.000 description 2
- 150000002734 metacrylic acid derivatives Chemical class 0.000 description 2
- 229910052987 metal hydride Inorganic materials 0.000 description 2
- 150000004681 metal hydrides Chemical class 0.000 description 2
- 229910044991 metal oxide Inorganic materials 0.000 description 2
- 125000001570 methylene group Chemical group [H]C([H])([*:1])[*:2] 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- FTRYJEGLDVMWIK-UHFFFAOYSA-N n-(3,5-dinitrophenyl)-2,2-dimethylpropanamide Chemical compound CC(C)(C)C(=O)NC1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 FTRYJEGLDVMWIK-UHFFFAOYSA-N 0.000 description 2
- YASWBJXTHOXPGK-UHFFFAOYSA-N n-(4-hydroxyphenyl)octadecanamide Chemical compound CCCCCCCCCCCCCCCCCC(=O)NC1=CC=C(O)C=C1 YASWBJXTHOXPGK-UHFFFAOYSA-N 0.000 description 2
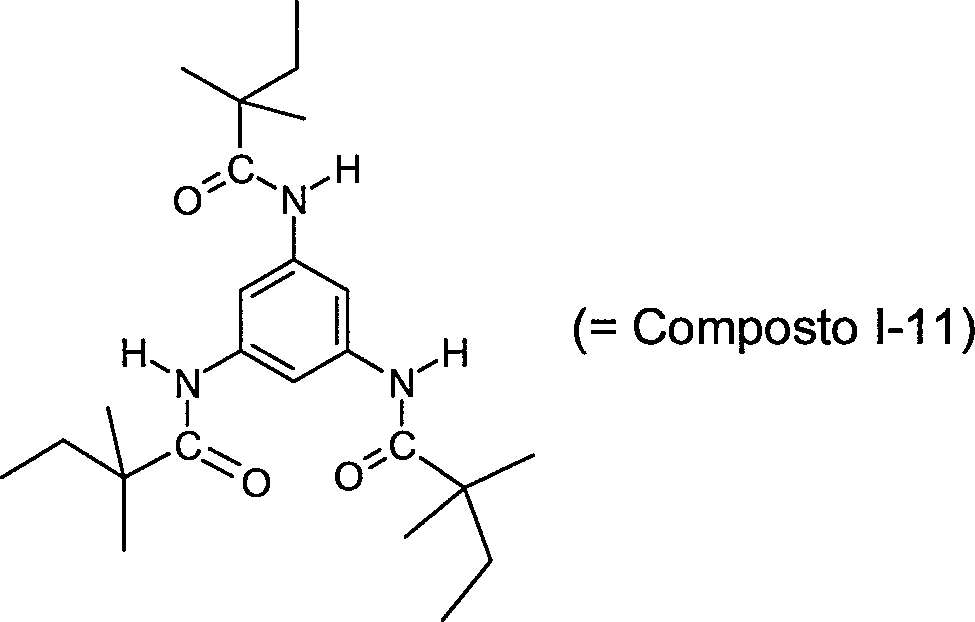
- UWJFKABGZXCEPV-UHFFFAOYSA-N n-[3,5-bis(2,2-dimethylpropanoylamino)phenyl]-2,2-dimethylbutanamide Chemical compound CCC(C)(C)C(=O)NC1=CC(NC(=O)C(C)(C)C)=CC(NC(=O)C(C)(C)C)=C1 UWJFKABGZXCEPV-UHFFFAOYSA-N 0.000 description 2
- IFSWAJUNOYSXGM-UHFFFAOYSA-N n-[3,5-bis(2-ethylbutanoylamino)phenyl]-2-ethylbutanamide Chemical compound CCC(CC)C(=O)NC1=CC(NC(=O)C(CC)CC)=CC(NC(=O)C(CC)CC)=C1 IFSWAJUNOYSXGM-UHFFFAOYSA-N 0.000 description 2
- PSBLVHHQEULUNH-UHFFFAOYSA-N n-[3,5-bis(2-methylpropanoylamino)phenyl]-2,2-dimethylpropanamide Chemical compound CC(C)C(=O)NC1=CC(NC(=O)C(C)C)=CC(NC(=O)C(C)(C)C)=C1 PSBLVHHQEULUNH-UHFFFAOYSA-N 0.000 description 2
- DUPGKFRRMSXUOP-UHFFFAOYSA-N n-[3-(2,2-dimethylbutanoylamino)-5-(2,2-dimethylpropanoylamino)phenyl]-2,2-dimethylbutanamide Chemical compound CCC(C)(C)C(=O)NC1=CC(NC(=O)C(C)(C)C)=CC(NC(=O)C(C)(C)CC)=C1 DUPGKFRRMSXUOP-UHFFFAOYSA-N 0.000 description 2
- LLANUGDMEAKGRA-UHFFFAOYSA-N n-[3-(2,2-dimethylbutanoylamino)-5-(2-methylpropanoylamino)phenyl]-2,2-dimethylbutanamide Chemical compound CCC(C)(C)C(=O)NC1=CC(NC(=O)C(C)C)=CC(NC(=O)C(C)(C)CC)=C1 LLANUGDMEAKGRA-UHFFFAOYSA-N 0.000 description 2
- FDAKZQLBIFPGSV-UHFFFAOYSA-N n-butyl-2,2,6,6-tetramethylpiperidin-4-amine Chemical compound CCCCNC1CC(C)(C)NC(C)(C)C1 FDAKZQLBIFPGSV-UHFFFAOYSA-N 0.000 description 2
- UVGSVVRGULNQAW-UHFFFAOYSA-N n-cyclopentyl-3,5-bis(4-methylpentanoylamino)benzamide Chemical compound CC(C)CCC(=O)NC1=CC(NC(=O)CCC(C)C)=CC(C(=O)NC2CCCC2)=C1 UVGSVVRGULNQAW-UHFFFAOYSA-N 0.000 description 2
- XLJIKAANBALQJD-UHFFFAOYSA-N n-tert-butyl-3,5-bis(3-methylbutanoylamino)benzamide Chemical compound CC(C)CC(=O)NC1=CC(NC(=O)CC(C)C)=CC(C(=O)NC(C)(C)C)=C1 XLJIKAANBALQJD-UHFFFAOYSA-N 0.000 description 2
- 239000012299 nitrogen atmosphere Substances 0.000 description 2
- LYRFLYHAGKPMFH-UHFFFAOYSA-N octadecanamide Chemical compound CCCCCCCCCCCCCCCCCC(N)=O LYRFLYHAGKPMFH-UHFFFAOYSA-N 0.000 description 2
- 125000003431 oxalo group Chemical group 0.000 description 2
- TWNQGVIAIRXVLR-UHFFFAOYSA-N oxo(oxoalumanyloxy)alumane Chemical compound O=[Al]O[Al]=O TWNQGVIAIRXVLR-UHFFFAOYSA-N 0.000 description 2
- 125000001037 p-tolyl group Chemical group [H]C1=C([H])C(=C([H])C([H])=C1*)C([H])([H])[H] 0.000 description 2
- 125000001147 pentyl group Chemical group C(CCCC)* 0.000 description 2
- 229960000969 phenyl salicylate Drugs 0.000 description 2
- 229920003023 plastic Polymers 0.000 description 2
- 239000004033 plastic Substances 0.000 description 2
- 229920001200 poly(ethylene-vinyl acetate) Polymers 0.000 description 2
- 229920000058 polyacrylate Polymers 0.000 description 2
- 229920002239 polyacrylonitrile Polymers 0.000 description 2
- 229920000515 polycarbonate Polymers 0.000 description 2
- 229920000647 polyepoxide Polymers 0.000 description 2
- 229920000139 polyethylene terephthalate Polymers 0.000 description 2
- 239000005020 polyethylene terephthalate Substances 0.000 description 2
- 239000005056 polyisocyanate Substances 0.000 description 2
- 229920001228 polyisocyanate Polymers 0.000 description 2
- 229920005606 polypropylene copolymer Polymers 0.000 description 2
- 229920001451 polypropylene glycol Polymers 0.000 description 2
- 229920002223 polystyrene Polymers 0.000 description 2
- 229920002635 polyurethane Polymers 0.000 description 2
- 238000012545 processing Methods 0.000 description 2
- 239000000523 sample Substances 0.000 description 2
- 229940116351 sebacate Drugs 0.000 description 2
- CXMXRPHRNRROMY-UHFFFAOYSA-L sebacate(2-) Chemical compound [O-]C(=O)CCCCCCCCC([O-])=O CXMXRPHRNRROMY-UHFFFAOYSA-L 0.000 description 2
- 239000004065 semiconductor Substances 0.000 description 2
- 230000035939 shock Effects 0.000 description 2
- 229910052814 silicon oxide Inorganic materials 0.000 description 2
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 2
- 235000010234 sodium benzoate Nutrition 0.000 description 2
- 239000004299 sodium benzoate Substances 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 125000004079 stearyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 239000000758 substrate Substances 0.000 description 2
- PXQLVRUNWNTZOS-UHFFFAOYSA-N sulfanyl Chemical class [SH] PXQLVRUNWNTZOS-UHFFFAOYSA-N 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 239000000454 talc Substances 0.000 description 2
- 235000012222 talc Nutrition 0.000 description 2
- 229910052623 talc Inorganic materials 0.000 description 2
- YBRBMKDOPFTVDT-UHFFFAOYSA-N tert-butylamine Chemical compound CC(C)(C)N YBRBMKDOPFTVDT-UHFFFAOYSA-N 0.000 description 2
- 239000004753 textile Substances 0.000 description 2
- 238000002411 thermogravimetry Methods 0.000 description 2
- YONPGGFAJWQGJC-UHFFFAOYSA-K titanium(iii) chloride Chemical compound Cl[Ti](Cl)Cl YONPGGFAJWQGJC-UHFFFAOYSA-K 0.000 description 2
- 125000002889 tridecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- HVLLSGMXQDNUAL-UHFFFAOYSA-N triphenyl phosphite Chemical compound C=1C=CC=CC=1OP(OC=1C=CC=CC=1)OC1=CC=CC=C1 HVLLSGMXQDNUAL-UHFFFAOYSA-N 0.000 description 2
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 2
- 229960000281 trometamol Drugs 0.000 description 2
- 150000003672 ureas Chemical class 0.000 description 2
- 125000000391 vinyl group Chemical group [H]C([*])=C([H])[H] 0.000 description 2
- 239000002023 wood Substances 0.000 description 2
- WGVKWNUPNGFDFJ-DQCZWYHMSA-N β-tocopherol Chemical compound OC1=CC(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C WGVKWNUPNGFDFJ-DQCZWYHMSA-N 0.000 description 2
- GZIFEOYASATJEH-VHFRWLAGSA-N δ-tocopherol Chemical compound OC1=CC(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1 GZIFEOYASATJEH-VHFRWLAGSA-N 0.000 description 2
- FMZUHGYZWYNSOA-VVBFYGJXSA-N (1r)-1-[(4r,4ar,8as)-2,6-diphenyl-4,4a,8,8a-tetrahydro-[1,3]dioxino[5,4-d][1,3]dioxin-4-yl]ethane-1,2-diol Chemical compound C([C@@H]1OC(O[C@@H]([C@@H]1O1)[C@H](O)CO)C=2C=CC=CC=2)OC1C1=CC=CC=C1 FMZUHGYZWYNSOA-VVBFYGJXSA-N 0.000 description 1
- RRKODOZNUZCUBN-CCAGOZQPSA-N (1z,3z)-cycloocta-1,3-diene Chemical compound C1CC\C=C/C=C\C1 RRKODOZNUZCUBN-CCAGOZQPSA-N 0.000 description 1
- HQEPZWYPQQKFLU-UHFFFAOYSA-N (2,6-dihydroxyphenyl)-phenylmethanone Chemical compound OC1=CC=CC(O)=C1C(=O)C1=CC=CC=C1 HQEPZWYPQQKFLU-UHFFFAOYSA-N 0.000 description 1
- ATLWFAZCZPSXII-UHFFFAOYSA-N (2-octylphenyl) 2-hydroxybenzoate Chemical compound CCCCCCCCC1=CC=CC=C1OC(=O)C1=CC=CC=C1O ATLWFAZCZPSXII-UHFFFAOYSA-N 0.000 description 1
- GOZHNJTXLALKRL-UHFFFAOYSA-N (5-benzoyl-2,4-dihydroxyphenyl)-phenylmethanone Chemical compound OC1=CC(O)=C(C(=O)C=2C=CC=CC=2)C=C1C(=O)C1=CC=CC=C1 GOZHNJTXLALKRL-UHFFFAOYSA-N 0.000 description 1
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 1
- DQXKOHDUMJLXKH-PHEQNACWSA-N (e)-n-[2-[2-[[(e)-oct-2-enoyl]amino]ethyldisulfanyl]ethyl]oct-2-enamide Chemical compound CCCCC\C=C\C(=O)NCCSSCCNC(=O)\C=C\CCCCC DQXKOHDUMJLXKH-PHEQNACWSA-N 0.000 description 1
- VCMZIKKVYXGKCI-UHFFFAOYSA-N 1,1-bis(2,4-ditert-butyl-6-methylphenyl)-2,2-bis(hydroxymethyl)propane-1,3-diol dihydroxyphosphanyl dihydrogen phosphite Chemical compound OP(O)OP(O)O.C(C)(C)(C)C1=C(C(=CC(=C1)C(C)(C)C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1C)C(C)(C)C)C(C)(C)C VCMZIKKVYXGKCI-UHFFFAOYSA-N 0.000 description 1
- RGASRBUYZODJTG-UHFFFAOYSA-N 1,1-bis(2,4-ditert-butylphenyl)-2,2-bis(hydroxymethyl)propane-1,3-diol dihydroxyphosphanyl dihydrogen phosphite Chemical compound OP(O)OP(O)O.C(C)(C)(C)C1=C(C=CC(=C1)C(C)(C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1)C(C)(C)C)C(C)(C)C RGASRBUYZODJTG-UHFFFAOYSA-N 0.000 description 1
- VKLDCBNUFZIAFK-UHFFFAOYSA-N 1,1-bis[2,4-bis(2-phenylpropan-2-yl)phenyl]-2,2-bis(hydroxymethyl)propane-1,3-diol dihydroxyphosphanyl dihydrogen phosphite Chemical compound OP(O)OP(O)O.C(C)(C)(C1=CC=CC=C1)C1=C(C=CC(=C1)C(C)(C)C1=CC=CC=C1)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1)C(C)(C)C1=CC=CC=C1)C(C)(C)C1=CC=CC=C1 VKLDCBNUFZIAFK-UHFFFAOYSA-N 0.000 description 1
- CGXOAAMIQPDTPE-UHFFFAOYSA-N 1,2,2,6,6-pentamethylpiperidin-4-amine Chemical compound CN1C(C)(C)CC(N)CC1(C)C CGXOAAMIQPDTPE-UHFFFAOYSA-N 0.000 description 1
- IKAACYWAXDLDPM-UHFFFAOYSA-N 1,2,3,4,4a,5-hexahydronaphthalene Chemical compound C1=CCC2CCCCC2=C1 IKAACYWAXDLDPM-UHFFFAOYSA-N 0.000 description 1
- JYEUMXHLPRZUAT-UHFFFAOYSA-N 1,2,3-triazine Chemical compound C1=CN=NN=C1 JYEUMXHLPRZUAT-UHFFFAOYSA-N 0.000 description 1
- GGQHNQQPLWRNHD-UHFFFAOYSA-N 1,3,7,9-tetratert-butyl-11-hydroxy-5h-benzo[d][1,3,2]benzodioxaphosphocine 11-oxide Chemical compound C1C2=CC(C(C)(C)C)=CC(C(C)(C)C)=C2OP(O)(=O)OC2=C1C=C(C(C)(C)C)C=C2C(C)(C)C GGQHNQQPLWRNHD-UHFFFAOYSA-N 0.000 description 1
- RIIVFNPHAKCXRK-UHFFFAOYSA-N 1,3,7,9-tetratert-butyl-4-(6-methylheptoxy)-5h-benzo[d][1,3,2]benzodioxaphosphocine Chemical compound O1POC2=C(C(C)(C)C)C=C(C(C)(C)C)C(OCCCCCC(C)C)=C2CC2=CC(C(C)(C)C)=CC(C(C)(C)C)=C21 RIIVFNPHAKCXRK-UHFFFAOYSA-N 0.000 description 1
- QTYUSOHYEPOHLV-FNORWQNLSA-N 1,3-Octadiene Chemical compound CCCC\C=C\C=C QTYUSOHYEPOHLV-FNORWQNLSA-N 0.000 description 1
- VMDYMJSKWCVEEB-UHFFFAOYSA-N 1-[3,5-bis[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyl]-1,3,5-triazinan-1-yl]-3-(3,5-ditert-butyl-4-hydroxyphenyl)propan-1-one Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)N2CN(CN(C2)C(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)C(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 VMDYMJSKWCVEEB-UHFFFAOYSA-N 0.000 description 1
- MNCMBBIFTVWHIP-UHFFFAOYSA-N 1-anthracen-9-yl-2,2,2-trifluoroethanone Chemical group C1=CC=C2C(C(=O)C(F)(F)F)=C(C=CC=C3)C3=CC2=C1 MNCMBBIFTVWHIP-UHFFFAOYSA-N 0.000 description 1
- YENQKAGAGMQTRZ-UHFFFAOYSA-N 1-cyanoethenyl prop-2-enoate Chemical compound C=CC(=O)OC(=C)C#N YENQKAGAGMQTRZ-UHFFFAOYSA-N 0.000 description 1
- XIRPMPKSZHNMST-UHFFFAOYSA-N 1-ethenyl-2-phenylbenzene Chemical group C=CC1=CC=CC=C1C1=CC=CC=C1 XIRPMPKSZHNMST-UHFFFAOYSA-N 0.000 description 1
- SDRZFSPCVYEJTP-UHFFFAOYSA-N 1-ethenylcyclohexene Chemical compound C=CC1=CCCCC1 SDRZFSPCVYEJTP-UHFFFAOYSA-N 0.000 description 1
- 125000004066 1-hydroxyethyl group Chemical group [H]OC([H])([*])C([H])([H])[H] 0.000 description 1
- 125000006028 1-methyl-2-butenyl group Chemical group 0.000 description 1
- 125000006021 1-methyl-2-propenyl group Chemical group 0.000 description 1
- BBRHQNMMUUMVDE-UHFFFAOYSA-N 1-n,2-n-diphenylpropane-1,2-diamine Chemical compound C=1C=CC=CC=1NC(C)CNC1=CC=CC=C1 BBRHQNMMUUMVDE-UHFFFAOYSA-N 0.000 description 1
- JUHXTONDLXIGGK-UHFFFAOYSA-N 1-n,4-n-bis(5-methylheptan-3-yl)benzene-1,4-diamine Chemical compound CCC(C)CC(CC)NC1=CC=C(NC(CC)CC(C)CC)C=C1 JUHXTONDLXIGGK-UHFFFAOYSA-N 0.000 description 1
- ZJNLYGOUHDJHMG-UHFFFAOYSA-N 1-n,4-n-bis(5-methylhexan-2-yl)benzene-1,4-diamine Chemical compound CC(C)CCC(C)NC1=CC=C(NC(C)CCC(C)C)C=C1 ZJNLYGOUHDJHMG-UHFFFAOYSA-N 0.000 description 1
- APTGHASZJUAUCP-UHFFFAOYSA-N 1-n,4-n-di(octan-2-yl)benzene-1,4-diamine Chemical compound CCCCCCC(C)NC1=CC=C(NC(C)CCCCCC)C=C1 APTGHASZJUAUCP-UHFFFAOYSA-N 0.000 description 1
- PWNBRRGFUVBTQG-UHFFFAOYSA-N 1-n,4-n-di(propan-2-yl)benzene-1,4-diamine Chemical compound CC(C)NC1=CC=C(NC(C)C)C=C1 PWNBRRGFUVBTQG-UHFFFAOYSA-N 0.000 description 1
- VETPHHXZEJAYOB-UHFFFAOYSA-N 1-n,4-n-dinaphthalen-2-ylbenzene-1,4-diamine Chemical compound C1=CC=CC2=CC(NC=3C=CC(NC=4C=C5C=CC=CC5=CC=4)=CC=3)=CC=C21 VETPHHXZEJAYOB-UHFFFAOYSA-N 0.000 description 1
- 125000001637 1-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C(*)=C([H])C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000004343 1-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])(*)C([H])([H])[H] 0.000 description 1
- IGGDKDTUCAWDAN-UHFFFAOYSA-N 1-vinylnaphthalene Chemical compound C1=CC=C2C(C=C)=CC=CC2=C1 IGGDKDTUCAWDAN-UHFFFAOYSA-N 0.000 description 1
- GFVSLJXVNAYUJE-UHFFFAOYSA-N 10-prop-2-enylphenothiazine Chemical compound C1=CC=C2N(CC=C)C3=CC=CC=C3SC2=C1 GFVSLJXVNAYUJE-UHFFFAOYSA-N 0.000 description 1
- WJFKNYWRSNBZNX-UHFFFAOYSA-N 10H-phenothiazine Chemical compound C1=CC=C2NC3=CC=CC=C3SC2=C1 WJFKNYWRSNBZNX-UHFFFAOYSA-N 0.000 description 1
- FTVFPPFZRRKJIH-UHFFFAOYSA-N 2,2,6,6-tetramethylpiperidin-4-amine Chemical compound CC1(C)CC(N)CC(C)(C)N1 FTVFPPFZRRKJIH-UHFFFAOYSA-N 0.000 description 1
- VDVUCLWJZJHFAV-UHFFFAOYSA-N 2,2,6,6-tetramethylpiperidin-4-ol Chemical compound CC1(C)CC(O)CC(C)(C)N1 VDVUCLWJZJHFAV-UHFFFAOYSA-N 0.000 description 1
- GXURZKWLMYOCDX-UHFFFAOYSA-N 2,2-bis(hydroxymethyl)propane-1,3-diol;dihydroxyphosphanyl dihydrogen phosphite Chemical compound OP(O)OP(O)O.OCC(CO)(CO)CO GXURZKWLMYOCDX-UHFFFAOYSA-N 0.000 description 1
- LKWOOKWVBNSLGN-UHFFFAOYSA-N 2,3-dimethylcyclohexan-1-amine Chemical compound CC1CCCC(N)C1C LKWOOKWVBNSLGN-UHFFFAOYSA-N 0.000 description 1
- UUAIOYWXCDLHKT-UHFFFAOYSA-N 2,4,6-tricyclohexylphenol Chemical compound OC1=C(C2CCCCC2)C=C(C2CCCCC2)C=C1C1CCCCC1 UUAIOYWXCDLHKT-UHFFFAOYSA-N 0.000 description 1
- OSPBEQGPLJSTKW-UHFFFAOYSA-N 2,4,6-tris[(3,5-ditert-butyl-4-hydroxyphenyl)methyl]phenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CC=2C=C(CC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)C(O)=C(CC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)C=2)=C1 OSPBEQGPLJSTKW-UHFFFAOYSA-N 0.000 description 1
- JUSNISPZXDHWQK-UHFFFAOYSA-N 2,4-dimethyl-6-octadecan-2-ylphenol Chemical compound CCCCCCCCCCCCCCCCC(C)C1=CC(C)=CC(C)=C1O JUSNISPZXDHWQK-UHFFFAOYSA-N 0.000 description 1
- OPLCSTZDXXUYDU-UHFFFAOYSA-N 2,4-dimethyl-6-tert-butylphenol Chemical compound CC1=CC(C)=C(O)C(C(C)(C)C)=C1 OPLCSTZDXXUYDU-UHFFFAOYSA-N 0.000 description 1
- LXWZXEJDKYWBOW-UHFFFAOYSA-N 2,4-ditert-butyl-6-[(3,5-ditert-butyl-2-hydroxyphenyl)methyl]phenol Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC(CC=2C(=C(C=C(C=2)C(C)(C)C)C(C)(C)C)O)=C1O LXWZXEJDKYWBOW-UHFFFAOYSA-N 0.000 description 1
- DXCHWXWXYPEZKM-UHFFFAOYSA-N 2,4-ditert-butyl-6-[1-(3,5-ditert-butyl-2-hydroxyphenyl)ethyl]phenol Chemical compound C=1C(C(C)(C)C)=CC(C(C)(C)C)=C(O)C=1C(C)C1=CC(C(C)(C)C)=CC(C(C)(C)C)=C1O DXCHWXWXYPEZKM-UHFFFAOYSA-N 0.000 description 1
- CZNRFEXEPBITDS-UHFFFAOYSA-N 2,5-bis(2-methylbutan-2-yl)benzene-1,4-diol Chemical compound CCC(C)(C)C1=CC(O)=C(C(C)(C)CC)C=C1O CZNRFEXEPBITDS-UHFFFAOYSA-N 0.000 description 1
- JZODKRWQWUWGCD-UHFFFAOYSA-N 2,5-di-tert-butylbenzene-1,4-diol Chemical compound CC(C)(C)C1=CC(O)=C(C(C)(C)C)C=C1O JZODKRWQWUWGCD-UHFFFAOYSA-N 0.000 description 1
- 150000003923 2,5-pyrrolediones Chemical class 0.000 description 1
- JFGVTUJBHHZRAB-UHFFFAOYSA-N 2,6-Di-tert-butyl-1,4-benzenediol Chemical compound CC(C)(C)C1=CC(O)=CC(C(C)(C)C)=C1O JFGVTUJBHHZRAB-UHFFFAOYSA-N 0.000 description 1
- LKALLEFLBKHPTQ-UHFFFAOYSA-N 2,6-bis[(3-tert-butyl-2-hydroxy-5-methylphenyl)methyl]-4-methylphenol Chemical compound OC=1C(CC=2C(=C(C=C(C)C=2)C(C)(C)C)O)=CC(C)=CC=1CC1=CC(C)=CC(C(C)(C)C)=C1O LKALLEFLBKHPTQ-UHFFFAOYSA-N 0.000 description 1
- BVUXDWXKPROUDO-UHFFFAOYSA-N 2,6-di-tert-butyl-4-ethylphenol Chemical compound CCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 BVUXDWXKPROUDO-UHFFFAOYSA-N 0.000 description 1
- SLUKQUGVTITNSY-UHFFFAOYSA-N 2,6-di-tert-butyl-4-methoxyphenol Chemical compound COC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 SLUKQUGVTITNSY-UHFFFAOYSA-N 0.000 description 1
- JBYWTKPHBLYYFJ-UHFFFAOYSA-N 2,6-ditert-butyl-4-(2-methylpropyl)phenol Chemical compound CC(C)CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 JBYWTKPHBLYYFJ-UHFFFAOYSA-N 0.000 description 1
- SCXYLTWTWUGEAA-UHFFFAOYSA-N 2,6-ditert-butyl-4-(methoxymethyl)phenol Chemical compound COCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 SCXYLTWTWUGEAA-UHFFFAOYSA-N 0.000 description 1
- UDFARPRXWMDFQU-UHFFFAOYSA-N 2,6-ditert-butyl-4-[(3,5-ditert-butyl-4-hydroxyphenyl)methylsulfanylmethyl]phenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CSCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 UDFARPRXWMDFQU-UHFFFAOYSA-N 0.000 description 1
- VMZVBRIIHDRYGK-UHFFFAOYSA-N 2,6-ditert-butyl-4-[(dimethylamino)methyl]phenol Chemical compound CN(C)CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 VMZVBRIIHDRYGK-UHFFFAOYSA-N 0.000 description 1
- QHPKIUDQDCWRKO-UHFFFAOYSA-N 2,6-ditert-butyl-4-[2-(3,5-ditert-butyl-4-hydroxyphenyl)propan-2-yl]phenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(C(C)(C)C=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 QHPKIUDQDCWRKO-UHFFFAOYSA-N 0.000 description 1
- KEZCYYOJCXNTLW-UHFFFAOYSA-N 2,6-ditert-butyl-4-[[6-(3,5-ditert-butyl-4-hydroxyanilino)-2-octyl-1-sulfanyl-2h-1,3,5-triazin-4-yl]amino]phenol Chemical compound N1=C(NC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)N(S)C(CCCCCCCC)N=C1NC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 KEZCYYOJCXNTLW-UHFFFAOYSA-N 0.000 description 1
- LBOGPIWNHXHYHN-UHFFFAOYSA-N 2-(2-hydroxy-5-octylphenyl)sulfanyl-4-octylphenol Chemical compound CCCCCCCCC1=CC=C(O)C(SC=2C(=CC=C(CCCCCCCC)C=2)O)=C1 LBOGPIWNHXHYHN-UHFFFAOYSA-N 0.000 description 1
- ZQQHQCZUIMXHDW-UHFFFAOYSA-N 2-(2H-benzotriazol-4-yl)-4-tert-butylphenol Chemical compound CC(C)(C)C1=CC=C(O)C(C=2C=3N=NNC=3C=CC=2)=C1 ZQQHQCZUIMXHDW-UHFFFAOYSA-N 0.000 description 1
- OEPOKWHJYJXUGD-UHFFFAOYSA-N 2-(3-phenylmethoxyphenyl)-1,3-thiazole-4-carbaldehyde Chemical compound O=CC1=CSC(C=2C=C(OCC=3C=CC=CC=3)C=CC=2)=N1 OEPOKWHJYJXUGD-UHFFFAOYSA-N 0.000 description 1
- UUINYPIVWRZHAG-UHFFFAOYSA-N 2-(4,6-diphenyl-1,3,5-triazin-2-yl)-5-methoxyphenol Chemical compound OC1=CC(OC)=CC=C1C1=NC(C=2C=CC=CC=2)=NC(C=2C=CC=CC=2)=N1 UUINYPIVWRZHAG-UHFFFAOYSA-N 0.000 description 1
- ZMWRRFHBXARRRT-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-4,6-bis(2-methylbutan-2-yl)phenol Chemical compound CCC(C)(C)C1=CC(C(C)(C)CC)=CC(N2N=C3C=CC=CC3=N2)=C1O ZMWRRFHBXARRRT-UHFFFAOYSA-N 0.000 description 1
- OLFNXLXEGXRUOI-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-4,6-bis(2-phenylpropan-2-yl)phenol Chemical compound C=1C(N2N=C3C=CC=CC3=N2)=C(O)C(C(C)(C)C=2C=CC=CC=2)=CC=1C(C)(C)C1=CC=CC=C1 OLFNXLXEGXRUOI-UHFFFAOYSA-N 0.000 description 1
- ITLDHFORLZTRJI-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-5-octoxyphenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1N1N=C2C=CC=CC2=N1 ITLDHFORLZTRJI-UHFFFAOYSA-N 0.000 description 1
- VQMHSKWEJGIXGA-UHFFFAOYSA-N 2-(benzotriazol-2-yl)-6-dodecyl-4-methylphenol Chemical compound CCCCCCCCCCCCC1=CC(C)=CC(N2N=C3C=CC=CC3=N2)=C1O VQMHSKWEJGIXGA-UHFFFAOYSA-N 0.000 description 1
- IUVCFHHAEHNCFT-INIZCTEOSA-N 2-[(1s)-1-[4-amino-3-(3-fluoro-4-propan-2-yloxyphenyl)pyrazolo[3,4-d]pyrimidin-1-yl]ethyl]-6-fluoro-3-(3-fluorophenyl)chromen-4-one Chemical compound C1=C(F)C(OC(C)C)=CC=C1C(C1=C(N)N=CN=C11)=NN1[C@@H](C)C1=C(C=2C=C(F)C=CC=2)C(=O)C2=CC(F)=CC=C2O1 IUVCFHHAEHNCFT-INIZCTEOSA-N 0.000 description 1
- XQESJWNDTICJHW-UHFFFAOYSA-N 2-[(2-hydroxy-5-methyl-3-nonylphenyl)methyl]-4-methyl-6-nonylphenol Chemical compound CCCCCCCCCC1=CC(C)=CC(CC=2C(=C(CCCCCCCCC)C=C(C)C=2)O)=C1O XQESJWNDTICJHW-UHFFFAOYSA-N 0.000 description 1
- UTNMPUFESIRPQP-UHFFFAOYSA-N 2-[(4-aminophenyl)methyl]aniline Chemical compound C1=CC(N)=CC=C1CC1=CC=CC=C1N UTNMPUFESIRPQP-UHFFFAOYSA-N 0.000 description 1
- YQQAAUCBTNZUQQ-UHFFFAOYSA-N 2-[1-(2-hydroxy-3,5-dimethylphenyl)butyl]-4,6-dimethylphenol Chemical compound C=1C(C)=CC(C)=C(O)C=1C(CCC)C1=CC(C)=CC(C)=C1O YQQAAUCBTNZUQQ-UHFFFAOYSA-N 0.000 description 1
- BVNPSIYFJSSEER-UHFFFAOYSA-H 2-[2-(1,3,2-benzodioxastibol-2-yloxy)phenoxy]-1,3,2-benzodioxastibole Chemical compound O([Sb]1Oc2ccccc2O1)c1ccccc1O[Sb]1Oc2ccccc2O1 BVNPSIYFJSSEER-UHFFFAOYSA-H 0.000 description 1
- TWISUSVXOIDKJG-UHFFFAOYSA-N 2-[2-hydroxy-5-(2,4,4-trimethylpentan-2-yl)phenyl]sulfanyl-4-(2,4,4-trimethylpentan-2-yl)phenol;nickel Chemical class [Ni].CC(C)(C)CC(C)(C)C1=CC=C(O)C(SC=2C(=CC=C(C=2)C(C)(C)CC(C)(C)C)O)=C1 TWISUSVXOIDKJG-UHFFFAOYSA-N 0.000 description 1
- SITYOOWCYAYOKL-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-(3-dodecoxy-2-hydroxypropoxy)phenol Chemical compound OC1=CC(OCC(O)COCCCCCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 SITYOOWCYAYOKL-UHFFFAOYSA-N 0.000 description 1
- ZSSVCEUEVMALRD-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-(octyloxy)phenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 ZSSVCEUEVMALRD-UHFFFAOYSA-N 0.000 description 1
- DBYBHKQEHCYBQV-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-dodecoxyphenol Chemical compound OC1=CC(OCCCCCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 DBYBHKQEHCYBQV-UHFFFAOYSA-N 0.000 description 1
- LSNNLZXIHSJCIE-UHFFFAOYSA-N 2-[4,6-bis(2,4-dimethylphenyl)-1,3,5-triazin-2-yl]-5-tridecoxyphenol Chemical compound OC1=CC(OCCCCCCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(C)=CC=2)C)=N1 LSNNLZXIHSJCIE-UHFFFAOYSA-N 0.000 description 1
- WPMUMRCRKFBYIH-UHFFFAOYSA-N 2-[4,6-bis(2-hydroxy-4-octoxyphenyl)-1,3,5-triazin-2-yl]-5-octoxyphenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1C1=NC(C=2C(=CC(OCCCCCCCC)=CC=2)O)=NC(C=2C(=CC(OCCCCCCCC)=CC=2)O)=N1 WPMUMRCRKFBYIH-UHFFFAOYSA-N 0.000 description 1
- NPUPWUDXQCOMBF-UHFFFAOYSA-N 2-[4,6-bis(4-methylphenyl)-1,3,5-triazin-2-yl]-5-octoxyphenol Chemical compound OC1=CC(OCCCCCCCC)=CC=C1C1=NC(C=2C=CC(C)=CC=2)=NC(C=2C=CC(C)=CC=2)=N1 NPUPWUDXQCOMBF-UHFFFAOYSA-N 0.000 description 1
- HHIVRACNDKRDTF-UHFFFAOYSA-N 2-[4-(2,4-dimethylphenyl)-6-(2-hydroxy-4-propoxyphenyl)-1,3,5-triazin-2-yl]-5-propoxyphenol Chemical compound OC1=CC(OCCC)=CC=C1C1=NC(C=2C(=CC(C)=CC=2)C)=NC(C=2C(=CC(OCCC)=CC=2)O)=N1 HHIVRACNDKRDTF-UHFFFAOYSA-N 0.000 description 1
- RDDIIAYGQFICIL-UHFFFAOYSA-N 2-[4-(5,7-ditert-butyl-2-oxo-3h-1-benzofuran-3-yl)phenoxy]ethyl acetate Chemical compound C1=CC(OCCOC(=O)C)=CC=C1C1C(C=C(C=C2C(C)(C)C)C(C)(C)C)=C2OC1=O RDDIIAYGQFICIL-UHFFFAOYSA-N 0.000 description 1
- YJWCUAHFSOAUKV-UHFFFAOYSA-N 2-[4-(5,7-ditert-butyl-2-oxo-3h-1-benzofuran-3-yl)phenoxy]ethyl octadecanoate Chemical compound C1=CC(OCCOC(=O)CCCCCCCCCCCCCCCCC)=CC=C1C1C(C=C(C=C2C(C)(C)C)C(C)(C)C)=C2OC1=O YJWCUAHFSOAUKV-UHFFFAOYSA-N 0.000 description 1
- FYELSNVLZVIGTI-UHFFFAOYSA-N 2-[4-[2-(2,3-dihydro-1H-inden-2-ylamino)pyrimidin-5-yl]-5-ethylpyrazol-1-yl]-1-(2,4,6,7-tetrahydrotriazolo[4,5-c]pyridin-5-yl)ethanone Chemical compound C1C(CC2=CC=CC=C12)NC1=NC=C(C=N1)C=1C=NN(C=1CC)CC(=O)N1CC2=C(CC1)NN=N2 FYELSNVLZVIGTI-UHFFFAOYSA-N 0.000 description 1
- VZBKFSFRDBYEDW-UHFFFAOYSA-N 2-[[2-hydroxy-5-nonyl-3-(2-phenylpropan-2-yl)phenyl]methyl]-4-nonyl-6-(2-phenylpropan-2-yl)phenol Chemical compound OC=1C(C(C)(C)C=2C=CC=CC=2)=CC(CCCCCCCCC)=CC=1CC(C=1O)=CC(CCCCCCCCC)=CC=1C(C)(C)C1=CC=CC=C1 VZBKFSFRDBYEDW-UHFFFAOYSA-N 0.000 description 1
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 1
- DGBKTJIQJQNAIN-UHFFFAOYSA-N 2-butyl-3-methylbutanedioic acid Chemical compound CCCCC(C(O)=O)C(C)C(O)=O DGBKTJIQJQNAIN-UHFFFAOYSA-N 0.000 description 1
- AKNMPWVTPUHKCG-UHFFFAOYSA-N 2-cyclohexyl-6-[(3-cyclohexyl-2-hydroxy-5-methylphenyl)methyl]-4-methylphenol Chemical compound OC=1C(C2CCCCC2)=CC(C)=CC=1CC(C=1O)=CC(C)=CC=1C1CCCCC1 AKNMPWVTPUHKCG-UHFFFAOYSA-N 0.000 description 1
- IXAKLSFFPBJWBS-UHFFFAOYSA-N 2-cycloundecyl-7,7,9,9-tetramethyl-1-oxa-3,8-diazaspiro[4.5]decan-4-one Chemical compound C1C(C)(C)NC(C)(C)CC21C(=O)NC(C1CCCCCCCCCC1)O2 IXAKLSFFPBJWBS-UHFFFAOYSA-N 0.000 description 1
- SMUKODJVMQOSAB-UHFFFAOYSA-N 2-ethylbutanoyl chloride Chemical compound CCC(CC)C(Cl)=O SMUKODJVMQOSAB-UHFFFAOYSA-N 0.000 description 1
- LHHLLQVLJAUUDT-UHFFFAOYSA-N 2-ethylhexyl 3-[3-(benzotriazol-2-yl)-5-tert-butyl-4-hydroxyphenyl]propanoate Chemical compound CC(C)(C)C1=CC(CCC(=O)OCC(CC)CCCC)=CC(N2N=C3C=CC=CC3=N2)=C1O LHHLLQVLJAUUDT-UHFFFAOYSA-N 0.000 description 1
- AWEVLIFGIMIQHY-UHFFFAOYSA-N 2-ethylhexyl 3-[3-tert-butyl-5-(5-chlorobenzotriazol-2-yl)-4-hydroxyphenyl]propanoate Chemical compound CC(C)(C)C1=CC(CCC(=O)OCC(CC)CCCC)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O AWEVLIFGIMIQHY-UHFFFAOYSA-N 0.000 description 1
- 125000002941 2-furyl group Chemical group O1C([*])=C([H])C([H])=C1[H] 0.000 description 1
- UORSDGBOJHYJLV-UHFFFAOYSA-N 2-hydroxy-n'-(2-hydroxybenzoyl)benzohydrazide Chemical compound OC1=CC=CC=C1C(=O)NNC(=O)C1=CC=CC=C1O UORSDGBOJHYJLV-UHFFFAOYSA-N 0.000 description 1
- MZZYGYNZAOVRTG-UHFFFAOYSA-N 2-hydroxy-n-(1h-1,2,4-triazol-5-yl)benzamide Chemical compound OC1=CC=CC=C1C(=O)NC1=NC=NN1 MZZYGYNZAOVRTG-UHFFFAOYSA-N 0.000 description 1
- WBJWXIQDBDZMAW-UHFFFAOYSA-N 2-hydroxynaphthalene-1-carbonyl chloride Chemical compound C1=CC=CC2=C(C(Cl)=O)C(O)=CC=C21 WBJWXIQDBDZMAW-UHFFFAOYSA-N 0.000 description 1
- VSKJLJHPAFKHBX-UHFFFAOYSA-N 2-methylbuta-1,3-diene;styrene Chemical compound CC(=C)C=C.C=CC1=CC=CC=C1.C=CC1=CC=CC=C1 VSKJLJHPAFKHBX-UHFFFAOYSA-N 0.000 description 1
- FEUISMYEFPANSS-UHFFFAOYSA-N 2-methylcyclohexan-1-amine Chemical compound CC1CCCCC1N FEUISMYEFPANSS-UHFFFAOYSA-N 0.000 description 1
- KGMWXVAUXAJKIV-UHFFFAOYSA-N 2-methylcyclohexane-1-carbonyl chloride Chemical compound CC1CCCCC1C(Cl)=O KGMWXVAUXAJKIV-UHFFFAOYSA-N 0.000 description 1
- DGMOBVGABMBZSB-UHFFFAOYSA-N 2-methylpropanoyl chloride Chemical compound CC(C)C(Cl)=O DGMOBVGABMBZSB-UHFFFAOYSA-N 0.000 description 1
- 125000001622 2-naphthyl group Chemical group [H]C1=C([H])C([H])=C2C([H])=C(*)C([H])=C([H])C2=C1[H] 0.000 description 1
- 125000000094 2-phenylethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])* 0.000 description 1
- YFHKLSPMRRWLKI-UHFFFAOYSA-N 2-tert-butyl-4-(3-tert-butyl-4-hydroxy-5-methylphenyl)sulfanyl-6-methylphenol Chemical compound CC(C)(C)C1=C(O)C(C)=CC(SC=2C=C(C(O)=C(C)C=2)C(C)(C)C)=C1 YFHKLSPMRRWLKI-UHFFFAOYSA-N 0.000 description 1
- HXIQYSLFEXIOAV-UHFFFAOYSA-N 2-tert-butyl-4-(5-tert-butyl-4-hydroxy-2-methylphenyl)sulfanyl-5-methylphenol Chemical compound CC1=CC(O)=C(C(C)(C)C)C=C1SC1=CC(C(C)(C)C)=C(O)C=C1C HXIQYSLFEXIOAV-UHFFFAOYSA-N 0.000 description 1
- RKLRVTKRKFEVQG-UHFFFAOYSA-N 2-tert-butyl-4-[(3-tert-butyl-4-hydroxy-5-methylphenyl)methyl]-6-methylphenol Chemical compound CC(C)(C)C1=C(O)C(C)=CC(CC=2C=C(C(O)=C(C)C=2)C(C)(C)C)=C1 RKLRVTKRKFEVQG-UHFFFAOYSA-N 0.000 description 1
- MOOLTXVOHPAOAP-UHFFFAOYSA-N 2-tert-butyl-4-[1-(5-tert-butyl-4-hydroxy-2-methylphenyl)-3-methyl-1-sulfanylpentadecyl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(S)(CC(C)CCCCCCCCCCCC)C1=CC(C(C)(C)C)=C(O)C=C1C MOOLTXVOHPAOAP-UHFFFAOYSA-N 0.000 description 1
- PFANXOISJYKQRP-UHFFFAOYSA-N 2-tert-butyl-4-[1-(5-tert-butyl-4-hydroxy-2-methylphenyl)butyl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(CCC)C1=CC(C(C)(C)C)=C(O)C=C1C PFANXOISJYKQRP-UHFFFAOYSA-N 0.000 description 1
- UGXGWRYMSRRFMQ-UHFFFAOYSA-N 2-tert-butyl-4-[2-(5-tert-butyl-4-hydroxy-2-methylphenyl)-1-sulfanylhexadecan-2-yl]-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(CS)(CCCCCCCCCCCCCC)C1=CC(C(C)(C)C)=C(O)C=C1C UGXGWRYMSRRFMQ-UHFFFAOYSA-N 0.000 description 1
- LZHCVNIARUXHAL-UHFFFAOYSA-N 2-tert-butyl-4-ethylphenol Chemical compound CCC1=CC=C(O)C(C(C)(C)C)=C1 LZHCVNIARUXHAL-UHFFFAOYSA-N 0.000 description 1
- XMUNJUUYEJAAHG-UHFFFAOYSA-N 2-tert-butyl-5-methyl-4-[1,5,5-tris(5-tert-butyl-4-hydroxy-2-methylphenyl)pentyl]phenol Chemical compound CC1=CC(O)=C(C(C)(C)C)C=C1C(C=1C(=CC(O)=C(C=1)C(C)(C)C)C)CCCC(C=1C(=CC(O)=C(C=1)C(C)(C)C)C)C1=CC(C(C)(C)C)=C(O)C=C1C XMUNJUUYEJAAHG-UHFFFAOYSA-N 0.000 description 1
- UHLYPUYAVHSKBN-UHFFFAOYSA-N 2-tert-butyl-6-[1-[3-tert-butyl-2-hydroxy-5-(2-methylpropyl)phenyl]ethyl]-4-(2-methylpropyl)phenol Chemical compound CC(C)(C)C1=CC(CC(C)C)=CC(C(C)C=2C(=C(C=C(CC(C)C)C=2)C(C)(C)C)O)=C1O UHLYPUYAVHSKBN-UHFFFAOYSA-N 0.000 description 1
- ODJQKYXPKWQWNK-UHFFFAOYSA-N 3,3'-Thiobispropanoic acid Chemical compound OC(=O)CCSCCC(O)=O ODJQKYXPKWQWNK-UHFFFAOYSA-N 0.000 description 1
- GUCMKIKYKIHUTM-UHFFFAOYSA-N 3,3,5,5-tetramethyl-1-[2-(3,3,5,5-tetramethyl-2-oxopiperazin-1-yl)ethyl]piperazin-2-one Chemical compound O=C1C(C)(C)NC(C)(C)CN1CCN1C(=O)C(C)(C)NC(C)(C)C1 GUCMKIKYKIHUTM-UHFFFAOYSA-N 0.000 description 1
- RWYIKYWUOWLWHZ-UHFFFAOYSA-N 3,3-dimethyl-2,4-dihydro-1,4-benzothiazine Chemical compound C1=CC=C2NC(C)(C)CSC2=C1 RWYIKYWUOWLWHZ-UHFFFAOYSA-N 0.000 description 1
- BUTKIHRNYUEGKB-UHFFFAOYSA-N 3,3-dimethylbutanoyl chloride Chemical compound CC(C)(C)CC(Cl)=O BUTKIHRNYUEGKB-UHFFFAOYSA-N 0.000 description 1
- RGAKSNQOIIYQRM-UHFFFAOYSA-N 3,4-dimethylbenzoyl chloride Chemical compound CC1=CC=C(C(Cl)=O)C=C1C RGAKSNQOIIYQRM-UHFFFAOYSA-N 0.000 description 1
- ZJIOBDJEKDUUCI-UHFFFAOYSA-N 3,5-dimethylbenzoyl chloride Chemical compound CC1=CC(C)=CC(C(Cl)=O)=C1 ZJIOBDJEKDUUCI-UHFFFAOYSA-N 0.000 description 1
- VZZQLSBTVGMMQK-UHFFFAOYSA-N 3,5-dinitro-n-(2,4,4-trimethylpentan-2-yl)benzamide Chemical compound CC(C)(C)CC(C)(C)NC(=O)C1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 VZZQLSBTVGMMQK-UHFFFAOYSA-N 0.000 description 1
- HDBVLHIQSYYAII-UHFFFAOYSA-N 3,5-dinitro-n-propan-2-ylbenzamide Chemical compound CC(C)NC(=O)C1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 HDBVLHIQSYYAII-UHFFFAOYSA-N 0.000 description 1
- VYWYYJYRVSBHJQ-UHFFFAOYSA-N 3,5-dinitrobenzoic acid Chemical compound OC(=O)C1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 VYWYYJYRVSBHJQ-UHFFFAOYSA-N 0.000 description 1
- YLUZWKKWWSCRSR-UHFFFAOYSA-N 3,9-bis(8-methylnonoxy)-2,4,8,10-tetraoxa-3,9-diphosphaspiro[5.5]undecane Chemical compound C1OP(OCCCCCCCC(C)C)OCC21COP(OCCCCCCCC(C)C)OC2 YLUZWKKWWSCRSR-UHFFFAOYSA-N 0.000 description 1
- HCILJBJJZALOAL-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)-n'-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoyl]propanehydrazide Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)NNC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 HCILJBJJZALOAL-UHFFFAOYSA-N 0.000 description 1
- KJEKRODBOPOEGG-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)-n-[3-[3-(3,5-ditert-butyl-4-hydroxyphenyl)propanoylamino]propyl]propanamide Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)NCCCNC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 KJEKRODBOPOEGG-UHFFFAOYSA-N 0.000 description 1
- FJDLQLIRZFKEKJ-UHFFFAOYSA-N 3-(3,5-ditert-butyl-4-hydroxyphenyl)propanamide Chemical class CC(C)(C)C1=CC(CCC(N)=O)=CC(C(C)(C)C)=C1O FJDLQLIRZFKEKJ-UHFFFAOYSA-N 0.000 description 1
- YCGKJPVUGMBDDS-UHFFFAOYSA-N 3-(6-azabicyclo[3.1.1]hepta-1(7),2,4-triene-6-carbonyl)benzamide Chemical compound NC(=O)C1=CC=CC(C(=O)N2C=3C=C2C=CC=3)=C1 YCGKJPVUGMBDDS-UHFFFAOYSA-N 0.000 description 1
- WSNKEJIFARPOSQ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-(1-benzothiophen-2-ylmethyl)benzamide Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C(=O)NCC2=CC3=C(S2)C=CC=C3)C=CC=1 WSNKEJIFARPOSQ-UHFFFAOYSA-N 0.000 description 1
- MROVZCRMXJZHCN-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-(2-hydroxyethyl)benzamide Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C(=O)NCCO)C=CC=1 MROVZCRMXJZHCN-UHFFFAOYSA-N 0.000 description 1
- VTNULXUEOJMRKZ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-(2H-tetrazol-5-ylmethyl)benzamide Chemical compound N=1NN=NC=1CNC(C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)=O VTNULXUEOJMRKZ-UHFFFAOYSA-N 0.000 description 1
- AJZDHLHTTJRNQJ-UHFFFAOYSA-N 3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxy-N-[2-(tetrazol-1-yl)ethyl]benzamide Chemical compound N1(N=NN=C1)CCNC(C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F)=O AJZDHLHTTJRNQJ-UHFFFAOYSA-N 0.000 description 1
- XHLMMVDCYIXUAX-UHFFFAOYSA-N 3-amino-5-carbamoylbenzoic acid Chemical compound NC(=O)C1=CC(N)=CC(C(O)=O)=C1 XHLMMVDCYIXUAX-UHFFFAOYSA-N 0.000 description 1
- 125000003682 3-furyl group Chemical group O1C([H])=C([*])C([H])=C1[H] 0.000 description 1
- 125000004207 3-methoxyphenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(OC([H])([H])[H])=C1[H] 0.000 description 1
- 125000006201 3-phenylpropyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- MDWVSAYEQPLWMX-UHFFFAOYSA-N 4,4'-Methylenebis(2,6-di-tert-butylphenol) Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 MDWVSAYEQPLWMX-UHFFFAOYSA-N 0.000 description 1
- BTXXTMOWISPQSJ-UHFFFAOYSA-N 4,4,4-trifluorobutan-2-one Chemical compound CC(=O)CC(F)(F)F BTXXTMOWISPQSJ-UHFFFAOYSA-N 0.000 description 1
- HPFWYRKGZUGGPB-UHFFFAOYSA-N 4,6-dichloro-n-(2,4,4-trimethylpentan-2-yl)-1,3,5-triazin-2-amine Chemical compound CC(C)(C)CC(C)(C)NC1=NC(Cl)=NC(Cl)=N1 HPFWYRKGZUGGPB-UHFFFAOYSA-N 0.000 description 1
- UQAMDAUJTXFNAD-UHFFFAOYSA-N 4-(4,6-dichloro-1,3,5-triazin-2-yl)morpholine Chemical compound ClC1=NC(Cl)=NC(N2CCOCC2)=N1 UQAMDAUJTXFNAD-UHFFFAOYSA-N 0.000 description 1
- PGGROMGHWHXWJL-UHFFFAOYSA-N 4-(azepane-1-carbonyl)benzamide Chemical compound C1=CC(C(=O)N)=CC=C1C(=O)N1CCCCCC1 PGGROMGHWHXWJL-UHFFFAOYSA-N 0.000 description 1
- VAMBUGIXOVLJEA-UHFFFAOYSA-N 4-(butylamino)phenol Chemical compound CCCCNC1=CC=C(O)C=C1 VAMBUGIXOVLJEA-UHFFFAOYSA-N 0.000 description 1
- STEYNUVPFMIUOY-UHFFFAOYSA-N 4-Hydroxy-1-(2-hydroxyethyl)-2,2,6,6-tetramethylpiperidine Chemical compound CC1(C)CC(O)CC(C)(C)N1CCO STEYNUVPFMIUOY-UHFFFAOYSA-N 0.000 description 1
- SWZOQAGVRGQLDV-UHFFFAOYSA-N 4-[2-(4-hydroxy-2,2,6,6-tetramethylpiperidin-1-yl)ethoxy]-4-oxobutanoic acid Chemical compound CC1(C)CC(O)CC(C)(C)N1CCOC(=O)CCC(O)=O SWZOQAGVRGQLDV-UHFFFAOYSA-N 0.000 description 1
- VGEJJASMUCILJT-UHFFFAOYSA-N 4-[2-[4,6-bis[2-(3,5-ditert-butyl-4-hydroxyphenyl)ethyl]-1,3,5-triazin-2-yl]ethyl]-2,6-ditert-butylphenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC=2N=C(CCC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)N=C(CCC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)N=2)=C1 VGEJJASMUCILJT-UHFFFAOYSA-N 0.000 description 1
- PRWJPWSKLXYEPD-UHFFFAOYSA-N 4-[4,4-bis(5-tert-butyl-4-hydroxy-2-methylphenyl)butan-2-yl]-2-tert-butyl-5-methylphenol Chemical compound C=1C(C(C)(C)C)=C(O)C=C(C)C=1C(C)CC(C=1C(=CC(O)=C(C=1)C(C)(C)C)C)C1=CC(C(C)(C)C)=C(O)C=C1C PRWJPWSKLXYEPD-UHFFFAOYSA-N 0.000 description 1
- IYUSCCOBICHICG-UHFFFAOYSA-N 4-[[2,4-bis(3,5-ditert-butyl-4-hydroxyphenoxy)-1h-triazin-6-yl]oxy]-2,6-ditert-butylphenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(ON2N=C(OC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)C=C(OC=3C=C(C(O)=C(C=3)C(C)(C)C)C(C)(C)C)N2)=C1 IYUSCCOBICHICG-UHFFFAOYSA-N 0.000 description 1
- VSAWBBYYMBQKIK-UHFFFAOYSA-N 4-[[3,5-bis[(3,5-ditert-butyl-4-hydroxyphenyl)methyl]-2,4,6-trimethylphenyl]methyl]-2,6-ditert-butylphenol Chemical compound CC1=C(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)C(C)=C(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)C(C)=C1CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 VSAWBBYYMBQKIK-UHFFFAOYSA-N 0.000 description 1
- BOQNWBDBDUWBMT-UHFFFAOYSA-N 4-[[bis[(3,5-ditert-butyl-4-hydroxyphenyl)methyl]amino]methyl]-2,6-ditert-butylphenol Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CN(CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)CC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 BOQNWBDBDUWBMT-UHFFFAOYSA-N 0.000 description 1
- WTWGHNZAQVTLSQ-UHFFFAOYSA-N 4-butyl-2,6-ditert-butylphenol Chemical compound CCCCC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 WTWGHNZAQVTLSQ-UHFFFAOYSA-N 0.000 description 1
- UVRJPVCMHKFQKP-UHFFFAOYSA-N 4-butyl-3-(4-ethoxyphenyl)-3h-1-benzofuran-2-one Chemical compound C1=2C(CCCC)=CC=CC=2OC(=O)C1C1=CC=C(OCC)C=C1 UVRJPVCMHKFQKP-UHFFFAOYSA-N 0.000 description 1
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 1
- UXMKUNDWNZNECH-UHFFFAOYSA-N 4-methyl-2,6-di(nonyl)phenol Chemical compound CCCCCCCCCC1=CC(C)=CC(CCCCCCCCC)=C1O UXMKUNDWNZNECH-UHFFFAOYSA-N 0.000 description 1
- LZAIWKMQABZIDI-UHFFFAOYSA-N 4-methyl-2,6-dioctadecylphenol Chemical compound CCCCCCCCCCCCCCCCCCC1=CC(C)=CC(CCCCCCCCCCCCCCCCCC)=C1O LZAIWKMQABZIDI-UHFFFAOYSA-N 0.000 description 1
- NQUVCRCCRXRJCK-UHFFFAOYSA-N 4-methylbenzoyl chloride Chemical compound CC1=CC=C(C(Cl)=O)C=C1 NQUVCRCCRXRJCK-UHFFFAOYSA-N 0.000 description 1
- ZZMVLMVFYMGSMY-UHFFFAOYSA-N 4-n-(4-methylpentan-2-yl)-1-n-phenylbenzene-1,4-diamine Chemical compound C1=CC(NC(C)CC(C)C)=CC=C1NC1=CC=CC=C1 ZZMVLMVFYMGSMY-UHFFFAOYSA-N 0.000 description 1
- JQTYAZKTBXWQOM-UHFFFAOYSA-N 4-n-octan-2-yl-1-n-phenylbenzene-1,4-diamine Chemical compound C1=CC(NC(C)CCCCCC)=CC=C1NC1=CC=CC=C1 JQTYAZKTBXWQOM-UHFFFAOYSA-N 0.000 description 1
- JJHKARPEMHIIQC-UHFFFAOYSA-N 4-octadecoxy-2,6-diphenylphenol Chemical compound C=1C(OCCCCCCCCCCCCCCCCCC)=CC(C=2C=CC=CC=2)=C(O)C=1C1=CC=CC=C1 JJHKARPEMHIIQC-UHFFFAOYSA-N 0.000 description 1
- GQMRGZGKJOOBFR-UHFFFAOYSA-N 4-octylperoxy-4-oxobutanoic acid Chemical compound CCCCCCCCOOC(=O)CCC(O)=O GQMRGZGKJOOBFR-UHFFFAOYSA-N 0.000 description 1
- KDVYCTOWXSLNNI-UHFFFAOYSA-N 4-t-Butylbenzoic acid Chemical compound CC(C)(C)C1=CC=C(C(O)=O)C=C1 KDVYCTOWXSLNNI-UHFFFAOYSA-N 0.000 description 1
- 125000002373 5 membered heterocyclic group Chemical group 0.000 description 1
- JFYKXFLSIZYLRY-UHFFFAOYSA-N 5,7-ditert-butyl-3-(2,3-dimethylphenyl)-3h-1-benzofuran-2-one Chemical compound CC1=CC=CC(C2C3=C(C(=CC(=C3)C(C)(C)C)C(C)(C)C)OC2=O)=C1C JFYKXFLSIZYLRY-UHFFFAOYSA-N 0.000 description 1
- CYHYIIFODCKQNP-UHFFFAOYSA-N 5,7-ditert-butyl-3-(3,4-dimethylphenyl)-3h-1-benzofuran-2-one Chemical compound C1=C(C)C(C)=CC=C1C1C(C=C(C=C2C(C)(C)C)C(C)(C)C)=C2OC1=O CYHYIIFODCKQNP-UHFFFAOYSA-N 0.000 description 1
- VQCLDAPPPUUUQC-UHFFFAOYSA-N 5-(3-methylbutanoylamino)benzene-1,3-dicarboxylic acid Chemical compound CC(C)CC(=O)NC1=CC(C(O)=O)=CC(C(O)=O)=C1 VQCLDAPPPUUUQC-UHFFFAOYSA-N 0.000 description 1
- ARUFLXLCEGMMDU-UHFFFAOYSA-N 5-(cyclopentanecarbonylamino)benzene-1,3-dicarboxylic acid Chemical compound OC(=O)C1=CC(C(=O)O)=CC(NC(=O)C2CCCC2)=C1 ARUFLXLCEGMMDU-UHFFFAOYSA-N 0.000 description 1
- UWSMKYBKUPAEJQ-UHFFFAOYSA-N 5-Chloro-2-(3,5-di-tert-butyl-2-hydroxyphenyl)-2H-benzotriazole Chemical compound CC(C)(C)C1=CC(C(C)(C)C)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O UWSMKYBKUPAEJQ-UHFFFAOYSA-N 0.000 description 1
- SROJCNHFTOAYCO-UHFFFAOYSA-N 5-[(2-methylcyclohexanecarbonyl)amino]benzene-1,3-dicarboxylic acid Chemical compound CC1CCCCC1C(=O)NC1=CC(C(O)=O)=CC(C(O)=O)=C1 SROJCNHFTOAYCO-UHFFFAOYSA-N 0.000 description 1
- SDQJTJLJXCWVQR-UHFFFAOYSA-N 5-nitrobenzene-1,3-dicarboxamide Chemical compound NC(=O)C1=CC(C(N)=O)=CC([N+]([O-])=O)=C1 SDQJTJLJXCWVQR-UHFFFAOYSA-N 0.000 description 1
- IPRLZACALWPEGS-UHFFFAOYSA-N 7,7,9,9-tetramethyl-2-undecyl-1-oxa-3,8-diazaspiro[4.5]decan-4-one Chemical compound O1C(CCCCCCCCCCC)NC(=O)C11CC(C)(C)NC(C)(C)C1 IPRLZACALWPEGS-UHFFFAOYSA-N 0.000 description 1
- NRLQBVLOUUPAMI-UHFFFAOYSA-N 8-[3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxybenzoyl]-1-oxa-3,8-diazaspiro[4.5]decan-2-one Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C(=O)N2CCC3(CNC(O3)=O)CC2)C=CC=1 NRLQBVLOUUPAMI-UHFFFAOYSA-N 0.000 description 1
- RAZWNFJQEZAVOT-UHFFFAOYSA-N 8-acetyl-3-dodecyl-7,7,9,9-tetramethyl-1,3,8-triazaspiro[4.5]decane-2,4-dione Chemical compound O=C1N(CCCCCCCCCCCC)C(=O)NC11CC(C)(C)N(C(C)=O)C(C)(C)C1 RAZWNFJQEZAVOT-UHFFFAOYSA-N 0.000 description 1
- BQACOLQNOUYJCE-FYZZASKESA-N Abietic acid Natural products CC(C)C1=CC2=CC[C@]3(C)[C@](C)(CCC[C@@]3(C)C(=O)O)[C@H]2CC1 BQACOLQNOUYJCE-FYZZASKESA-N 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 229920000178 Acrylic resin Polymers 0.000 description 1
- 239000004925 Acrylic resin Substances 0.000 description 1
- 241000251468 Actinopterygii Species 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 101001053401 Arabidopsis thaliana Acid beta-fructofuranosidase 3, vacuolar Proteins 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- XNCOSPRUTUOJCJ-UHFFFAOYSA-N Biguanide Chemical compound NC(N)=NC(N)=N XNCOSPRUTUOJCJ-UHFFFAOYSA-N 0.000 description 1
- 229940123208 Biguanide Drugs 0.000 description 1
- 239000004604 Blowing Agent Substances 0.000 description 1
- YCIIUHGCNOPWJL-UHFFFAOYSA-N C(CCC)(=O)O.C(C)(C)(C)C=1C=C(C=CC1O)C(CO)O Chemical compound C(CCC)(=O)O.C(C)(C)(C)C=1C=C(C=CC1O)C(CO)O YCIIUHGCNOPWJL-UHFFFAOYSA-N 0.000 description 1
- XIQYTULRWXHXOM-UHFFFAOYSA-N C(CCCCCCCCCCC)C1C(N(C(C1)=O)C=1CC(N(C(C1)(C)C)C)(C)C)=O Chemical compound C(CCCCCCCCCCC)C1C(N(C(C1)=O)C=1CC(N(C(C1)(C)C)C)(C)C)=O XIQYTULRWXHXOM-UHFFFAOYSA-N 0.000 description 1
- 125000003358 C2-C20 alkenyl group Chemical group 0.000 description 1
- ZRZFCHCIMYNMST-UHFFFAOYSA-L C=1([O-])C([O-])=CC=CC1.[Zn+2] Chemical compound C=1([O-])C([O-])=CC=CC1.[Zn+2] ZRZFCHCIMYNMST-UHFFFAOYSA-L 0.000 description 1
- OQBNLWNGPPUNSI-UHFFFAOYSA-N CC(C)(C)C(Nc1cc(C(NC(C)(C)C)=O)cc(C(NC(C)(C)C)=O)c1)=O Chemical compound CC(C)(C)C(Nc1cc(C(NC(C)(C)C)=O)cc(C(NC(C)(C)C)=O)c1)=O OQBNLWNGPPUNSI-UHFFFAOYSA-N 0.000 description 1
- HACCXQMVURYHJQ-UHFFFAOYSA-N CC(C)(C)CC(C)(C)NC(c1cc(NC(C(C)(C)C)=O)cc(NC(C(C)(C)C)=O)c1)=O Chemical compound CC(C)(C)CC(C)(C)NC(c1cc(NC(C(C)(C)C)=O)cc(NC(C(C)(C)C)=O)c1)=O HACCXQMVURYHJQ-UHFFFAOYSA-N 0.000 description 1
- DYIVQZACWIEVOU-UHFFFAOYSA-N CC(C)(C)NC(c1cc(NC(C2CCCC2)=O)cc(NC(C2CCCC2)=O)c1)=O Chemical compound CC(C)(C)NC(c1cc(NC(C2CCCC2)=O)cc(NC(C2CCCC2)=O)c1)=O DYIVQZACWIEVOU-UHFFFAOYSA-N 0.000 description 1
- SRTPJGXNDRVVHB-UHFFFAOYSA-N CC(C)CC(Nc1cc(NC(CC(C)C)=O)cc(C(N)=O)c1)=O Chemical compound CC(C)CC(Nc1cc(NC(CC(C)C)=O)cc(C(N)=O)c1)=O SRTPJGXNDRVVHB-UHFFFAOYSA-N 0.000 description 1
- WBBFAUMLECBIEL-UHFFFAOYSA-N CC(C)CCNC(c1cc(NC(C2CCCCC2)=O)cc(NC(C2CCCCC2)=O)c1)=O Chemical compound CC(C)CCNC(c1cc(NC(C2CCCCC2)=O)cc(NC(C2CCCCC2)=O)c1)=O WBBFAUMLECBIEL-UHFFFAOYSA-N 0.000 description 1
- 0 CCC(C)(C)C(Nc1cc(NC(*C)=O)cc(NC(C(C)(C)CC)=O)c1)=O Chemical compound CCC(C)(C)C(Nc1cc(NC(*C)=O)cc(NC(C(C)(C)CC)=O)c1)=O 0.000 description 1
- DJRCMVCFUPOPKC-UHFFFAOYSA-N CCCCCCCCCCCC(=NO)C1=CC=C(C)C=C1O Chemical compound CCCCCCCCCCCC(=NO)C1=CC=C(C)C=C1O DJRCMVCFUPOPKC-UHFFFAOYSA-N 0.000 description 1
- BDHFRTCKAVRGLD-UHFFFAOYSA-N CCCCCCCCCCON(CCCCCC)CCCCCC Chemical compound CCCCCCCCCCON(CCCCCC)CCCCCC BDHFRTCKAVRGLD-UHFFFAOYSA-N 0.000 description 1
- GAWIXWVDTYZWAW-UHFFFAOYSA-N C[CH]O Chemical group C[CH]O GAWIXWVDTYZWAW-UHFFFAOYSA-N 0.000 description 1
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 1
- 244000025254 Cannabis sativa Species 0.000 description 1
- KXDHJXZQYSOELW-UHFFFAOYSA-N Carbamic acid Chemical class NC(O)=O KXDHJXZQYSOELW-UHFFFAOYSA-N 0.000 description 1
- 229920001634 Copolyester Polymers 0.000 description 1
- LVZWSLJZHVFIQJ-UHFFFAOYSA-N Cyclopropane Chemical compound C1CC1 LVZWSLJZHVFIQJ-UHFFFAOYSA-N 0.000 description 1
- GZIFEOYASATJEH-UHFFFAOYSA-N D-delta tocopherol Natural products OC1=CC(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1 GZIFEOYASATJEH-UHFFFAOYSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- GHKOFFNLGXMVNJ-UHFFFAOYSA-N Didodecyl thiobispropanoate Chemical compound CCCCCCCCCCCCOC(=O)CCSCCC(=O)OCCCCCCCCCCCC GHKOFFNLGXMVNJ-UHFFFAOYSA-N 0.000 description 1
- 239000003508 Dilauryl thiodipropionate Substances 0.000 description 1
- QXNVGIXVLWOKEQ-UHFFFAOYSA-N Disodium Chemical class [Na][Na] QXNVGIXVLWOKEQ-UHFFFAOYSA-N 0.000 description 1
- 239000002656 Distearyl thiodipropionate Substances 0.000 description 1
- SNRUBQQJIBEYMU-UHFFFAOYSA-N Dodecane Natural products CCCCCCCCCCCC SNRUBQQJIBEYMU-UHFFFAOYSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 239000004593 Epoxy Substances 0.000 description 1
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 1
- XPDWGBQVDMORPB-UHFFFAOYSA-N Fluoroform Chemical compound FC(F)F XPDWGBQVDMORPB-UHFFFAOYSA-N 0.000 description 1
- 239000004705 High-molecular-weight polyethylene Substances 0.000 description 1
- 101000939500 Homo sapiens UBX domain-containing protein 11 Proteins 0.000 description 1
- 239000013032 Hydrocarbon resin Substances 0.000 description 1
- 206010021639 Incontinence Diseases 0.000 description 1
- OKOBUGCCXMIKDM-UHFFFAOYSA-N Irganox 1098 Chemical compound CC(C)(C)C1=C(O)C(C(C)(C)C)=CC(CCC(=O)NCCCCCCNC(=O)CCC=2C=C(C(O)=C(C=2)C(C)(C)C)C(C)(C)C)=C1 OKOBUGCCXMIKDM-UHFFFAOYSA-N 0.000 description 1
- VQTUBCCKSQIDNK-UHFFFAOYSA-N Isobutene Chemical group CC(C)=C VQTUBCCKSQIDNK-UHFFFAOYSA-N 0.000 description 1
- VHOQXEIFYTTXJU-UHFFFAOYSA-N Isobutylene-isoprene copolymer Chemical class CC(C)=C.CC(=C)C=C VHOQXEIFYTTXJU-UHFFFAOYSA-N 0.000 description 1
- RRHGJUQNOFWUDK-UHFFFAOYSA-N Isoprene Natural products CC(=C)C=C RRHGJUQNOFWUDK-UHFFFAOYSA-N 0.000 description 1
- VVQNEPGJFQJSBK-UHFFFAOYSA-N Methyl methacrylate Chemical compound COC(=O)C(C)=C VVQNEPGJFQJSBK-UHFFFAOYSA-N 0.000 description 1
- GYCMBHHDWRMZGG-UHFFFAOYSA-N Methylacrylonitrile Chemical compound CC(=C)C#N GYCMBHHDWRMZGG-UHFFFAOYSA-N 0.000 description 1
- 241001139947 Mida Species 0.000 description 1
- 101100113998 Mus musculus Cnbd2 gene Proteins 0.000 description 1
- XXNMZOHRQLOGQL-UHFFFAOYSA-N N,N'-diethoxyoxamide Chemical compound CCONC(=O)C(=O)NOCC XXNMZOHRQLOGQL-UHFFFAOYSA-N 0.000 description 1
- UTGQNNCQYDRXCH-UHFFFAOYSA-N N,N'-diphenyl-1,4-phenylenediamine Chemical compound C=1C=C(NC=2C=CC=CC=2)C=CC=1NC1=CC=CC=C1 UTGQNNCQYDRXCH-UHFFFAOYSA-N 0.000 description 1
- OUBMGJOQLXMSNT-UHFFFAOYSA-N N-isopropyl-N'-phenyl-p-phenylenediamine Chemical compound C1=CC(NC(C)C)=CC=C1NC1=CC=CC=C1 OUBMGJOQLXMSNT-UHFFFAOYSA-N 0.000 description 1
- 229920000571 Nylon 11 Polymers 0.000 description 1
- 229920000299 Nylon 12 Polymers 0.000 description 1
- 229920001007 Nylon 4 Polymers 0.000 description 1
- 229920002302 Nylon 6,6 Polymers 0.000 description 1
- IWGBGUINMSOOKP-UHFFFAOYSA-N OC1=C(C(=O)CCCCCCCCCCC)C=NN1C1=CC=CC=C1 Chemical compound OC1=C(C(=O)CCCCCCCCCCC)C=NN1C1=CC=CC=C1 IWGBGUINMSOOKP-UHFFFAOYSA-N 0.000 description 1
- FDBMBOYIVUGUSL-UHFFFAOYSA-N OP(O)OP(O)O.C(C)(C)(C)C1=C(C(=CC(=C1)C)C(C)(C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1C(C)(C)C)C)C(C)(C)C Chemical compound OP(O)OP(O)O.C(C)(C)(C)C1=C(C(=CC(=C1)C)C(C)(C)C)C(O)(C(CO)(CO)CO)C1=C(C=C(C=C1C(C)(C)C)C)C(C)(C)C FDBMBOYIVUGUSL-UHFFFAOYSA-N 0.000 description 1
- 229910019142 PO4 Inorganic materials 0.000 description 1
- 239000002033 PVDF binder Substances 0.000 description 1
- 229930040373 Paraformaldehyde Natural products 0.000 description 1
- 229920001944 Plastisol Polymers 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000004962 Polyamide-imide Substances 0.000 description 1
- 229920003006 Polybutadiene acrylonitrile Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004642 Polyimide Substances 0.000 description 1
- 239000004734 Polyphenylene sulfide Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 229920001328 Polyvinylidene chloride Polymers 0.000 description 1
- 229910019020 PtO2 Inorganic materials 0.000 description 1
- KHPCPRHQVVSZAH-HUOMCSJISA-N Rosin Natural products O(C/C=C/c1ccccc1)[C@H]1[C@H](O)[C@@H](O)[C@@H](O)[C@@H](CO)O1 KHPCPRHQVVSZAH-HUOMCSJISA-N 0.000 description 1
- BLRPTPMANUNPDV-UHFFFAOYSA-N Silane Chemical compound [SiH4] BLRPTPMANUNPDV-UHFFFAOYSA-N 0.000 description 1
- 229920002472 Starch Polymers 0.000 description 1
- 229910000831 Steel Inorganic materials 0.000 description 1
- 244000269722 Thea sinensis Species 0.000 description 1
- 239000004433 Thermoplastic polyurethane Substances 0.000 description 1
- 239000003490 Thiodipropionic acid Substances 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical compound OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- UATJOMSPNYCXIX-UHFFFAOYSA-N Trinitrobenzene Chemical compound [O-][N+](=O)C1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 UATJOMSPNYCXIX-UHFFFAOYSA-N 0.000 description 1
- 102100029645 UBX domain-containing protein 11 Human genes 0.000 description 1
- 229920001807 Urea-formaldehyde Polymers 0.000 description 1
- 239000004708 Very-low-density polyethylene Substances 0.000 description 1
- 241000750042 Vini Species 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 1
- FJDRHAOQERROCN-UHFFFAOYSA-N [1,3-bis(dodecan-2-ylsulfanyl)-2,2-bis[dodecan-2-ylsulfanyl(hydroxy)methyl]-3-hydroxypropyl] propanoate Chemical compound C(CC)(=O)OC(C(C(O)SC(C)CCCCCCCCCC)(C(O)SC(C)CCCCCCCCCC)C(O)SC(C)CCCCCCCCCC)SC(C)CCCCCCCCCC FJDRHAOQERROCN-UHFFFAOYSA-N 0.000 description 1
- SAHIZENKTPRYSN-UHFFFAOYSA-N [2-[3-(phenoxymethyl)phenoxy]-6-(trifluoromethyl)pyridin-4-yl]methanamine Chemical compound O(C1=CC=CC=C1)CC=1C=C(OC2=NC(=CC(=C2)CN)C(F)(F)F)C=CC=1 SAHIZENKTPRYSN-UHFFFAOYSA-N 0.000 description 1
- YQYBUJYBXOVWQW-UHFFFAOYSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-(3,4-dihydro-1H-isoquinolin-2-yl)methanone Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C=CC=1)C(=O)N1CC2=CC=CC=C2CC1 YQYBUJYBXOVWQW-UHFFFAOYSA-N 0.000 description 1
- YKKPYMXANSSQCA-UHFFFAOYSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-(3-pyrazol-1-ylazetidin-1-yl)methanone Chemical compound N1(N=CC=C1)C1CN(C1)C(=O)C1=CC(=CC=C1)OC1=NC(=CC(=C1)CN)C(F)(F)F YKKPYMXANSSQCA-UHFFFAOYSA-N 0.000 description 1
- LJHFUFVRZNYVMK-CYBMUJFWSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-[(3R)-3-hydroxypyrrolidin-1-yl]methanone Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C=CC=1)C(=O)N1C[C@@H](CC1)O LJHFUFVRZNYVMK-CYBMUJFWSA-N 0.000 description 1
- LJHFUFVRZNYVMK-ZDUSSCGKSA-N [3-[4-(aminomethyl)-6-(trifluoromethyl)pyridin-2-yl]oxyphenyl]-[(3S)-3-hydroxypyrrolidin-1-yl]methanone Chemical compound NCC1=CC(=NC(=C1)C(F)(F)F)OC=1C=C(C=CC=1)C(=O)N1C[C@H](CC1)O LJHFUFVRZNYVMK-ZDUSSCGKSA-N 0.000 description 1
- ZSFWKZUHCKWKGK-UHFFFAOYSA-N [4-(5,7-ditert-butyl-2-oxo-3h-1-benzofuran-3-yl)-2,6-dimethylphenyl] 2,2-dimethylpropanoate Chemical compound CC1=C(OC(=O)C(C)(C)C)C(C)=CC(C2C3=C(C(=CC(=C3)C(C)(C)C)C(C)(C)C)OC2=O)=C1 ZSFWKZUHCKWKGK-UHFFFAOYSA-N 0.000 description 1
- FXOMJIWKCOCWOU-UHFFFAOYSA-N [4-(5,7-ditert-butyl-2-oxo-3h-1-benzofuran-3-yl)-2,6-dimethylphenyl] acetate Chemical compound C1=C(C)C(OC(=O)C)=C(C)C=C1C1C(C=C(C=C2C(C)(C)C)C(C)(C)C)=C2OC1=O FXOMJIWKCOCWOU-UHFFFAOYSA-N 0.000 description 1
- YIMQCDZDWXUDCA-UHFFFAOYSA-N [4-(hydroxymethyl)cyclohexyl]methanol Chemical compound OCC1CCC(CO)CC1 YIMQCDZDWXUDCA-UHFFFAOYSA-N 0.000 description 1
- HHFMFWAFQGUGOB-UHFFFAOYSA-N [5-(4-tert-butylbenzoyl)-2,4-dihydroxyphenyl]-(4-tert-butylphenyl)methanone Chemical compound C1=CC(C(C)(C)C)=CC=C1C(=O)C1=CC(C(=O)C=2C=CC(=CC=2)C(C)(C)C)=C(O)C=C1O HHFMFWAFQGUGOB-UHFFFAOYSA-N 0.000 description 1
- BVPRUAZVDOHSHP-UHFFFAOYSA-N [S-][S-].[Zn+2] Chemical compound [S-][S-].[Zn+2] BVPRUAZVDOHSHP-UHFFFAOYSA-N 0.000 description 1
- DHKHKXVYLBGOIT-UHFFFAOYSA-N acetaldehyde Diethyl Acetal Natural products CCOC(C)OCC DHKHKXVYLBGOIT-UHFFFAOYSA-N 0.000 description 1
- 229940022663 acetate Drugs 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 125000002252 acyl group Chemical group 0.000 description 1
- MIBQYWIOHFTKHD-UHFFFAOYSA-N adamantane-1-carbonyl chloride Chemical compound C1C(C2)CC3CC2CC1(C(=O)Cl)C3 MIBQYWIOHFTKHD-UHFFFAOYSA-N 0.000 description 1
- YKIOKAURTKXMSB-UHFFFAOYSA-N adams's catalyst Chemical compound O=[Pt]=O YKIOKAURTKXMSB-UHFFFAOYSA-N 0.000 description 1
- 239000002390 adhesive tape Substances 0.000 description 1
- WNLRTRBMVRJNCN-UHFFFAOYSA-L adipate(2-) Chemical compound [O-]C(=O)CCCCC([O-])=O WNLRTRBMVRJNCN-UHFFFAOYSA-L 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 238000013019 agitation Methods 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- 150000001342 alkaline earth metals Chemical class 0.000 description 1
- 125000005735 alkanylene group Chemical group 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 125000005907 alkyl ester group Chemical group 0.000 description 1
- 150000001350 alkyl halides Chemical class 0.000 description 1
- PYHXGXCGESYPCW-UHFFFAOYSA-N alpha-phenylbenzeneacetic acid Natural products C=1C=CC=CC=1C(C(=O)O)C1=CC=CC=C1 PYHXGXCGESYPCW-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- OYFUVZBROQZLCL-UHFFFAOYSA-K aluminum;4-tert-butylbenzoate;hydroxide Chemical compound [OH-].[Al+3].CC(C)(C)C1=CC=C(C([O-])=O)C=C1.CC(C)(C)C1=CC=C(C([O-])=O)C=C1 OYFUVZBROQZLCL-UHFFFAOYSA-K 0.000 description 1
- 238000000137 annealing Methods 0.000 description 1
- MWPLVEDNUUSJAV-UHFFFAOYSA-N anthracene Natural products C1=CC=CC2=CC3=CC=CC=C3C=C21 MWPLVEDNUUSJAV-UHFFFAOYSA-N 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 239000004760 aramid Substances 0.000 description 1
- 229920003235 aromatic polyamide Polymers 0.000 description 1
- 239000010425 asbestos Substances 0.000 description 1
- 238000005452 bending Methods 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 150000003936 benzamides Chemical class 0.000 description 1
- 229940007550 benzyl acetate Drugs 0.000 description 1
- QUKGYYKBILRGFE-UHFFFAOYSA-N benzyloxyacetoaldehyde Natural products CC(=O)OCC1=CC=CC=C1 QUKGYYKBILRGFE-UHFFFAOYSA-N 0.000 description 1
- 229940066595 beta tocopherol Drugs 0.000 description 1
- 229920006378 biaxially oriented polypropylene Polymers 0.000 description 1
- 239000011127 biaxially oriented polypropylene Substances 0.000 description 1
- SFFFIHNOEGSAIH-UHFFFAOYSA-N bicyclo[2.2.1]hept-2-ene;ethene Chemical compound C=C.C1C2CCC1C=C2 SFFFIHNOEGSAIH-UHFFFAOYSA-N 0.000 description 1
- 125000006267 biphenyl group Chemical group 0.000 description 1
- NLMFVJSIGDIJBB-UHFFFAOYSA-N bis(2,2,6,6-tetramethyl-1-octoxypiperidin-3-yl) decanedioate Chemical compound CC1(C)N(OCCCCCCCC)C(C)(C)CCC1OC(=O)CCCCCCCCC(=O)OC1C(C)(C)N(OCCCCCCCC)C(C)(C)CC1 NLMFVJSIGDIJBB-UHFFFAOYSA-N 0.000 description 1
- OSIVCXJNIBEGCL-UHFFFAOYSA-N bis(2,2,6,6-tetramethyl-1-octoxypiperidin-4-yl) decanedioate Chemical compound C1C(C)(C)N(OCCCCCCCC)C(C)(C)CC1OC(=O)CCCCCCCCC(=O)OC1CC(C)(C)N(OCCCCCCCC)C(C)(C)C1 OSIVCXJNIBEGCL-UHFFFAOYSA-N 0.000 description 1
- GOJOVSYIGHASEI-UHFFFAOYSA-N bis(2,2,6,6-tetramethylpiperidin-4-yl) butanedioate Chemical compound C1C(C)(C)NC(C)(C)CC1OC(=O)CCC(=O)OC1CC(C)(C)NC(C)(C)C1 GOJOVSYIGHASEI-UHFFFAOYSA-N 0.000 description 1
- ZEFSGHVBJCEKAZ-UHFFFAOYSA-N bis(2,4-ditert-butyl-6-methylphenyl) ethyl phosphite Chemical compound CC=1C=C(C(C)(C)C)C=C(C(C)(C)C)C=1OP(OCC)OC1=C(C)C=C(C(C)(C)C)C=C1C(C)(C)C ZEFSGHVBJCEKAZ-UHFFFAOYSA-N 0.000 description 1
- FQUNFJULCYSSOP-UHFFFAOYSA-N bisoctrizole Chemical compound N1=C2C=CC=CC2=NN1C1=CC(C(C)(C)CC(C)(C)C)=CC(CC=2C(=C(C=C(C=2)C(C)(C)CC(C)(C)C)N2N=C3C=CC=CC3=N2)O)=C1O FQUNFJULCYSSOP-UHFFFAOYSA-N 0.000 description 1
- 239000002981 blocking agent Substances 0.000 description 1
- 238000000071 blow moulding Methods 0.000 description 1
- MPMBRWOOISTHJV-UHFFFAOYSA-N but-1-enylbenzene Chemical compound CCC=CC1=CC=CC=C1 MPMBRWOOISTHJV-UHFFFAOYSA-N 0.000 description 1
- HQABUPZFAYXKJW-UHFFFAOYSA-N butan-1-amine Chemical compound CCCCN HQABUPZFAYXKJW-UHFFFAOYSA-N 0.000 description 1
- GGAUUQHSCNMCAU-UHFFFAOYSA-N butane-1,2,3,4-tetracarboxylic acid Chemical compound OC(=O)CC(C(O)=O)C(C(O)=O)CC(O)=O GGAUUQHSCNMCAU-UHFFFAOYSA-N 0.000 description 1
- 239000001405 butyl (E)-3-phenylprop-2-enoate Substances 0.000 description 1
- CQEYYJKEWSMYFG-UHFFFAOYSA-N butyl acrylate Chemical compound CCCCOC(=O)C=C CQEYYJKEWSMYFG-UHFFFAOYSA-N 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 239000011575 calcium Substances 0.000 description 1
- 229910052791 calcium Inorganic materials 0.000 description 1
- 159000000007 calcium salts Chemical class 0.000 description 1
- 238000003490 calendering Methods 0.000 description 1
- 239000004202 carbamide Substances 0.000 description 1
- 239000006229 carbon black Substances 0.000 description 1
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical class OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 description 1
- 239000012876 carrier material Substances 0.000 description 1
- 238000009903 catalytic hydrogenation reaction Methods 0.000 description 1
- UOCJDOLVGGIYIQ-PBFPGSCMSA-N cefatrizine Chemical group S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)[C@H](N)C=2C=CC(O)=CC=2)CC=1CSC=1C=NNN=1 UOCJDOLVGGIYIQ-PBFPGSCMSA-N 0.000 description 1
- 229920002301 cellulose acetate Polymers 0.000 description 1
- 229920001727 cellulose butyrate Polymers 0.000 description 1
- 229920003086 cellulose ether Polymers 0.000 description 1
- 229920006218 cellulose propionate Polymers 0.000 description 1
- 239000004568 cement Substances 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- CCRCUPLGCSFEDV-UHFFFAOYSA-N cinnamic acid methyl ester Natural products COC(=O)C=CC1=CC=CC=C1 CCRCUPLGCSFEDV-UHFFFAOYSA-N 0.000 description 1
- 238000005253 cladding Methods 0.000 description 1
- 238000013037 co-molding Methods 0.000 description 1
- 238000000748 compression moulding Methods 0.000 description 1
- 239000004567 concrete Substances 0.000 description 1
- 239000013068 control sample Substances 0.000 description 1
- 238000010411 cooking Methods 0.000 description 1
- 150000001879 copper Chemical class 0.000 description 1
- 239000002537 cosmetic Substances 0.000 description 1
- 229920006037 cross link polymer Polymers 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 239000003431 cross linking reagent Substances 0.000 description 1
- 239000012045 crude solution Substances 0.000 description 1
- 239000013078 crystal Substances 0.000 description 1
- MGNCLNQXLYJVJD-UHFFFAOYSA-N cyanuric chloride Chemical compound ClC1=NC(Cl)=NC(Cl)=N1 MGNCLNQXLYJVJD-UHFFFAOYSA-N 0.000 description 1
- 150000004292 cyclic ethers Chemical class 0.000 description 1
- 150000001925 cycloalkenes Chemical class 0.000 description 1
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 1
- 125000000582 cycloheptyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 1
- NISGSNTVMOOSJQ-UHFFFAOYSA-N cyclopentanamine Chemical compound NC1CCCC1 NISGSNTVMOOSJQ-UHFFFAOYSA-N 0.000 description 1
- 125000002704 decyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 235000010389 delta-tocopherol Nutrition 0.000 description 1
- 238000010612 desalination reaction Methods 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 239000003599 detergent Substances 0.000 description 1
- GDVKFRBCXAPAQJ-UHFFFAOYSA-A dialuminum;hexamagnesium;carbonate;hexadecahydroxide Chemical compound [OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[OH-].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Mg+2].[Al+3].[Al+3].[O-]C([O-])=O GDVKFRBCXAPAQJ-UHFFFAOYSA-A 0.000 description 1
- 150000001470 diamides Chemical class 0.000 description 1
- SZRLKIKBPASKQH-UHFFFAOYSA-M dibutyldithiocarbamate Chemical compound CCCCN(C([S-])=S)CCCC SZRLKIKBPASKQH-UHFFFAOYSA-M 0.000 description 1
- 150000005690 diesters Chemical class 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 229940043237 diethanolamine Drugs 0.000 description 1
- 235000019304 dilauryl thiodipropionate Nutrition 0.000 description 1
- 229910001873 dinitrogen Inorganic materials 0.000 description 1
- 150000002009 diols Chemical class 0.000 description 1
- ZZTCPWRAHWXWCH-UHFFFAOYSA-N diphenylmethanediamine Chemical compound C=1C=CC=CC=1C(N)(N)C1=CC=CC=C1 ZZTCPWRAHWXWCH-UHFFFAOYSA-N 0.000 description 1
- 125000005982 diphenylmethyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])(*)C1=C([H])C([H])=C([H])C([H])=C1[H] 0.000 description 1
- FXDGCBFGSXNGQD-FAESFXMKSA-L disodium;(1s,2s,3r,4r)-bicyclo[2.2.1]heptane-2,3-dicarboxylate Chemical compound [Na+].[Na+].C1C[C@H]2[C@@H](C([O-])=O)[C@@H](C(=O)[O-])[C@@H]1C2 FXDGCBFGSXNGQD-FAESFXMKSA-L 0.000 description 1
- UZUODNWWWUQRIR-UHFFFAOYSA-L disodium;3-aminonaphthalene-1,5-disulfonate Chemical compound [Na+].[Na+].C1=CC=C(S([O-])(=O)=O)C2=CC(N)=CC(S([O-])(=O)=O)=C21 UZUODNWWWUQRIR-UHFFFAOYSA-L 0.000 description 1
- PWWSSIYVTQUJQQ-UHFFFAOYSA-N distearyl thiodipropionate Chemical compound CCCCCCCCCCCCCCCCCCOC(=O)CCSCCC(=O)OCCCCCCCCCCCCCCCCCC PWWSSIYVTQUJQQ-UHFFFAOYSA-N 0.000 description 1
- 235000019305 distearyl thiodipropionate Nutrition 0.000 description 1
- 238000004821 distillation Methods 0.000 description 1
- 125000003438 dodecyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 239000010459 dolomite Substances 0.000 description 1
- 229910000514 dolomite Inorganic materials 0.000 description 1
- MCPKSFINULVDNX-UHFFFAOYSA-N drometrizole Chemical compound CC1=CC=C(O)C(N2N=C3C=CC=CC3=N2)=C1 MCPKSFINULVDNX-UHFFFAOYSA-N 0.000 description 1
- 235000013399 edible fruits Nutrition 0.000 description 1
- 238000010894 electron beam technology Methods 0.000 description 1
- 238000005538 encapsulation Methods 0.000 description 1
- QGEOKXWFGANCJL-UHFFFAOYSA-N ethenyl acetate;hydrochloride Chemical compound Cl.CC(=O)OC=C QGEOKXWFGANCJL-UHFFFAOYSA-N 0.000 description 1
- UHESRSKEBRADOO-UHFFFAOYSA-N ethyl carbamate;prop-2-enoic acid Chemical class OC(=O)C=C.CCOC(N)=O UHESRSKEBRADOO-UHFFFAOYSA-N 0.000 description 1
- 125000004494 ethyl ester group Chemical group 0.000 description 1
- 229920006228 ethylene acrylate copolymer Polymers 0.000 description 1
- 125000000816 ethylene group Chemical group [H]C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 239000000284 extract Substances 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 235000019688 fish Nutrition 0.000 description 1
- 238000005188 flotation Methods 0.000 description 1
- 238000005187 foaming Methods 0.000 description 1
- 239000004088 foaming agent Substances 0.000 description 1
- 239000011888 foil Substances 0.000 description 1
- IVJISJACKSSFGE-UHFFFAOYSA-N formaldehyde;1,3,5-triazine-2,4,6-triamine Chemical compound O=C.NC1=NC(N)=NC(N)=N1 IVJISJACKSSFGE-UHFFFAOYSA-N 0.000 description 1
- 239000002828 fuel tank Substances 0.000 description 1
- WOLATMHLPFJRGC-UHFFFAOYSA-N furan-2,5-dione;styrene Chemical compound O=C1OC(=O)C=C1.C=CC1=CC=CC=C1 WOLATMHLPFJRGC-UHFFFAOYSA-N 0.000 description 1
- 235000010382 gamma-tocopherol Nutrition 0.000 description 1
- 239000003502 gasoline Substances 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 239000004746 geotextile Substances 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- 239000004519 grease Substances 0.000 description 1
- 229920005555 halobutyl Polymers 0.000 description 1
- 125000004968 halobutyl group Chemical group 0.000 description 1
- 238000010438 heat treatment Methods 0.000 description 1
- 229910001385 heavy metal Inorganic materials 0.000 description 1
- 125000000623 heterocyclic group Chemical group 0.000 description 1
- 125000004051 hexyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- 229920005669 high impact polystyrene Polymers 0.000 description 1
- 239000004797 high-impact polystyrene Substances 0.000 description 1
- 238000003898 horticulture Methods 0.000 description 1
- 150000001469 hydantoins Chemical class 0.000 description 1
- 230000036571 hydration Effects 0.000 description 1
- 238000006703 hydration reaction Methods 0.000 description 1
- 150000002429 hydrazines Chemical class 0.000 description 1
- 229920006270 hydrocarbon resin Polymers 0.000 description 1
- 229960001545 hydrotalcite Drugs 0.000 description 1
- 229910001701 hydrotalcite Inorganic materials 0.000 description 1
- 238000005286 illumination Methods 0.000 description 1
- 230000000415 inactivating effect Effects 0.000 description 1
- 239000011261 inert gas Substances 0.000 description 1
- 238000010102 injection blow moulding Methods 0.000 description 1
- 150000007529 inorganic bases Chemical class 0.000 description 1
- 150000004694 iodide salts Chemical class 0.000 description 1
- 235000000396 iron Nutrition 0.000 description 1
- QTBFPMKWQKYFLR-UHFFFAOYSA-N isobutyl chloride Chemical compound CC(C)CCl QTBFPMKWQKYFLR-UHFFFAOYSA-N 0.000 description 1
- 239000012948 isocyanate Substances 0.000 description 1
- 150000002513 isocyanates Chemical class 0.000 description 1
- BMFVGAAISNGQNM-UHFFFAOYSA-N isopentylamine Chemical compound CC(C)CCN BMFVGAAISNGQNM-UHFFFAOYSA-N 0.000 description 1
- QZUPTXGVPYNUIT-UHFFFAOYSA-N isophthalamide Chemical compound NC(=O)C1=CC=CC(C(N)=O)=C1 QZUPTXGVPYNUIT-UHFFFAOYSA-N 0.000 description 1
- JJWLVOIRVHMVIS-UHFFFAOYSA-O isopropylaminium Chemical compound CC(C)[NH3+] JJWLVOIRVHMVIS-UHFFFAOYSA-O 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 238000004898 kneading Methods 0.000 description 1
- 150000003951 lactams Chemical class 0.000 description 1
- 150000002596 lactones Chemical class 0.000 description 1
- 210000001699 lower leg Anatomy 0.000 description 1
- 239000001095 magnesium carbonate Substances 0.000 description 1
- 235000011160 magnesium carbonates Nutrition 0.000 description 1
- 239000000395 magnesium oxide Substances 0.000 description 1
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 description 1
- 235000012245 magnesium oxide Nutrition 0.000 description 1
- 239000004137 magnesium phosphate Substances 0.000 description 1
- 235000010994 magnesium phosphates Nutrition 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 235000019341 magnesium sulphate Nutrition 0.000 description 1
- OBQVOBQZMOXRAL-UHFFFAOYSA-L magnesium;docosanoate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCCCCCC([O-])=O OBQVOBQZMOXRAL-UHFFFAOYSA-L 0.000 description 1
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- 150000002696 manganese Chemical class 0.000 description 1
- 235000013372 meat Nutrition 0.000 description 1
- 150000007974 melamines Chemical class 0.000 description 1
- 229910001507 metal halide Inorganic materials 0.000 description 1
- 150000004706 metal oxides Chemical class 0.000 description 1
- 239000003863 metallic catalyst Substances 0.000 description 1
- 125000004184 methoxymethyl group Chemical group [H]C([H])([H])OC([H])([H])* 0.000 description 1
- UJRDRFZCRQNLJM-UHFFFAOYSA-N methyl 3-[3-(benzotriazol-2-yl)-5-tert-butyl-4-hydroxyphenyl]propanoate Chemical compound CC(C)(C)C1=CC(CCC(=O)OC)=CC(N2N=C3C=CC=CC3=N2)=C1O UJRDRFZCRQNLJM-UHFFFAOYSA-N 0.000 description 1
- 125000006178 methyl benzyl group Chemical group 0.000 description 1
- 229920000609 methyl cellulose Polymers 0.000 description 1
- 239000001923 methylcellulose Substances 0.000 description 1
- 235000010981 methylcellulose Nutrition 0.000 description 1
- 239000010445 mica Substances 0.000 description 1
- 229910052618 mica group Inorganic materials 0.000 description 1
- 239000003607 modifier Substances 0.000 description 1
- 239000012170 montan wax Substances 0.000 description 1
- 238000009740 moulding (composite fabrication) Methods 0.000 description 1
- 125000001421 myristyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- YIMHRDBSVCPJOV-UHFFFAOYSA-N n'-(2-ethoxyphenyl)-n-(2-ethylphenyl)oxamide Chemical compound CCOC1=CC=CC=C1NC(=O)C(=O)NC1=CC=CC=C1CC YIMHRDBSVCPJOV-UHFFFAOYSA-N 0.000 description 1
- ZJFPXDGPJMHQMW-UHFFFAOYSA-N n,n'-bis[3-(dimethylamino)propyl]oxamide Chemical compound CN(C)CCCNC(=O)C(=O)NCCCN(C)C ZJFPXDGPJMHQMW-UHFFFAOYSA-N 0.000 description 1
- KIMPOEOLEXUJEX-UHFFFAOYSA-N n-(3,5-diacetamidophenyl)acetamide Chemical compound CC(=O)NC1=CC(NC(C)=O)=CC(NC(C)=O)=C1 KIMPOEOLEXUJEX-UHFFFAOYSA-N 0.000 description 1
- OYYUNSUFKIUCOI-UHFFFAOYSA-N n-(3,5-dinitrophenyl)-2-methylpropanamide Chemical compound CC(C)C(=O)NC1=CC([N+]([O-])=O)=CC([N+]([O-])=O)=C1 OYYUNSUFKIUCOI-UHFFFAOYSA-N 0.000 description 1
- KESXDDATSRRGAH-UHFFFAOYSA-N n-(4-hydroxyphenyl)butanamide Chemical compound CCCC(=O)NC1=CC=C(O)C=C1 KESXDDATSRRGAH-UHFFFAOYSA-N 0.000 description 1
- JVKWTDRHWOSRFT-UHFFFAOYSA-N n-(4-hydroxyphenyl)dodecanamide Chemical compound CCCCCCCCCCCC(=O)NC1=CC=C(O)C=C1 JVKWTDRHWOSRFT-UHFFFAOYSA-N 0.000 description 1
- VQLURHRLTDWRLX-UHFFFAOYSA-N n-(4-hydroxyphenyl)nonanamide Chemical compound CCCCCCCCC(=O)NC1=CC=C(O)C=C1 VQLURHRLTDWRLX-UHFFFAOYSA-N 0.000 description 1
- XEEBADPDYKMRAS-UHFFFAOYSA-N n-[3,5-bis(2,2-dimethylbutanoylamino)phenyl]-2,2-dimethylbutanamide Chemical compound CCC(C)(C)C(=O)NC1=CC(NC(=O)C(C)(C)CC)=CC(NC(=O)C(C)(C)CC)=C1 XEEBADPDYKMRAS-UHFFFAOYSA-N 0.000 description 1
- LXXDLUDACKWILX-UHFFFAOYSA-N n-[3,5-bis(2-methylpropanoylamino)phenyl]-2-methylpropanamide Chemical compound CC(C)C(=O)NC1=CC(NC(=O)C(C)C)=CC(NC(=O)C(C)C)=C1 LXXDLUDACKWILX-UHFFFAOYSA-N 0.000 description 1
- PRWJYTOHVYEMMO-UHFFFAOYSA-N n-[3,5-bis(3,3-dimethylbutanoylamino)phenyl]-3,3-dimethylbutanamide Chemical compound CC(C)(C)CC(=O)NC1=CC(NC(=O)CC(C)(C)C)=CC(NC(=O)CC(C)(C)C)=C1 PRWJYTOHVYEMMO-UHFFFAOYSA-N 0.000 description 1
- SEFUPFRSFIYQRS-UHFFFAOYSA-N n-[3,5-bis(3-cyclohexylpropanoylamino)phenyl]-3-cyclohexylpropanamide Chemical compound C=1C(NC(=O)CCC2CCCCC2)=CC(NC(=O)CCC2CCCCC2)=CC=1NC(=O)CCC1CCCCC1 SEFUPFRSFIYQRS-UHFFFAOYSA-N 0.000 description 1
- YUIRELOVBCFFSG-UHFFFAOYSA-N n-[3,5-bis(4-cyclohexylbutanoylamino)phenyl]-4-cyclohexylbutanamide Chemical compound C=1C(NC(=O)CCCC2CCCCC2)=CC(NC(=O)CCCC2CCCCC2)=CC=1NC(=O)CCCC1CCCCC1 YUIRELOVBCFFSG-UHFFFAOYSA-N 0.000 description 1
- VTEKCCOVZIZGSM-UHFFFAOYSA-N n-[3,5-bis(cyclohexanecarbonylamino)phenyl]cyclohexanecarboxamide Chemical compound C1CCCCC1C(=O)NC(C=C(NC(=O)C1CCCCC1)C=1)=CC=1NC(=O)C1CCCCC1 VTEKCCOVZIZGSM-UHFFFAOYSA-N 0.000 description 1
- XVRLQZZWTLWXNH-UHFFFAOYSA-N n-[3,5-bis(propanoylamino)phenyl]propanamide Chemical class CCC(=O)NC1=CC(NC(=O)CC)=CC(NC(=O)CC)=C1 XVRLQZZWTLWXNH-UHFFFAOYSA-N 0.000 description 1
- WAMQOOPSJGJDMX-UHFFFAOYSA-N n-[3,5-bis[(2-cyclohexylacetyl)amino]phenyl]-2-cyclohexylacetamide Chemical compound C=1C(NC(=O)CC2CCCCC2)=CC(NC(=O)CC2CCCCC2)=CC=1NC(=O)CC1CCCCC1 WAMQOOPSJGJDMX-UHFFFAOYSA-N 0.000 description 1
- YBVFVIALKPNQBZ-UHFFFAOYSA-N n-[3-(3,3-dimethylbutanoylamino)-5-(2-methylpropanoylamino)phenyl]-3,3-dimethylbutanamide Chemical compound CC(C)C(=O)NC1=CC(NC(=O)CC(C)(C)C)=CC(NC(=O)CC(C)(C)C)=C1 YBVFVIALKPNQBZ-UHFFFAOYSA-N 0.000 description 1
- 125000004108 n-butyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- ABHDKVZBLKFKIJ-UHFFFAOYSA-N n-cyclohexyl-3,5-bis(4-methylpentanoylamino)benzamide Chemical compound CC(C)CCC(=O)NC1=CC(NC(=O)CCC(C)C)=CC(C(=O)NC2CCCCC2)=C1 ABHDKVZBLKFKIJ-UHFFFAOYSA-N 0.000 description 1
- FRWXQLZHBMHNTQ-UHFFFAOYSA-N n-cyclopentyl-3,5-bis(3-methylbutanoylamino)benzamide Chemical compound CC(C)CC(=O)NC1=CC(NC(=O)CC(C)C)=CC(C(=O)NC2CCCC2)=C1 FRWXQLZHBMHNTQ-UHFFFAOYSA-N 0.000 description 1
- QOSAXOJJXBSPPQ-UHFFFAOYSA-N n-decylhydroxylamine Chemical compound CCCCCCCCCCNO QOSAXOJJXBSPPQ-UHFFFAOYSA-N 0.000 description 1
- ZRPOKHXBOZQSOX-UHFFFAOYSA-N n-heptadecyl-n-octadecylhydroxylamine Chemical compound CCCCCCCCCCCCCCCCCCN(O)CCCCCCCCCCCCCCCCC ZRPOKHXBOZQSOX-UHFFFAOYSA-N 0.000 description 1
- WGCBLWIBXXQTAW-UHFFFAOYSA-N n-hexadecyl-n-octadecylhydroxylamine Chemical compound CCCCCCCCCCCCCCCCCCN(O)CCCCCCCCCCCCCCCC WGCBLWIBXXQTAW-UHFFFAOYSA-N 0.000 description 1
- FWBBTCULLJSJCS-UHFFFAOYSA-N n-octadecylidenehydroxylamine Chemical compound CCCCCCCCCCCCCCCCCC=NO FWBBTCULLJSJCS-UHFFFAOYSA-N 0.000 description 1
- CVVFFUKULYKOJR-UHFFFAOYSA-N n-phenyl-4-propan-2-yloxyaniline Chemical compound C1=CC(OC(C)C)=CC=C1NC1=CC=CC=C1 CVVFFUKULYKOJR-UHFFFAOYSA-N 0.000 description 1
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 1
- ZPONZGGBGJYFHY-UHFFFAOYSA-N n-tetradecylidenehydroxylamine Chemical compound CCCCCCCCCCCCCC=NO ZPONZGGBGJYFHY-UHFFFAOYSA-N 0.000 description 1
- 239000002114 nanocomposite Substances 0.000 description 1
- 125000005487 naphthalate group Chemical group 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 150000002828 nitro derivatives Chemical class 0.000 description 1
- HDKLIZDXVUCLHQ-UHFFFAOYSA-N non-3-en-2-one Chemical compound CCCCCC=CC(C)=O HDKLIZDXVUCLHQ-UHFFFAOYSA-N 0.000 description 1
- 125000001400 nonyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- SNQQPOLDUKLAAF-UHFFFAOYSA-N nonylphenol Chemical class CCCCCCCCCC1=CC=CC=C1O SNQQPOLDUKLAAF-UHFFFAOYSA-N 0.000 description 1
- JFNLZVQOOSMTJK-KNVOCYPGSA-N norbornene Chemical compound C1[C@@H]2CC[C@H]1C=C2 JFNLZVQOOSMTJK-KNVOCYPGSA-N 0.000 description 1
- 125000003261 o-tolyl group Chemical group [H]C1=C([H])C(*)=C(C([H])=C1[H])C([H])([H])[H] 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- DMFXLIFZVRXRRR-UHFFFAOYSA-N octyl 3-[3-tert-butyl-5-(5-chlorobenzotriazol-2-yl)-4-hydroxyphenyl]propanoate Chemical compound CC(C)(C)C1=CC(CCC(=O)OCCCCCCCC)=CC(N2N=C3C=C(Cl)C=CC3=N2)=C1O DMFXLIFZVRXRRR-UHFFFAOYSA-N 0.000 description 1
- 125000002347 octyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- FATBGEAMYMYZAF-KTKRTIGZSA-N oleamide Chemical compound CCCCCCCC\C=C/CCCCCCCC(N)=O FATBGEAMYMYZAF-KTKRTIGZSA-N 0.000 description 1
- FATBGEAMYMYZAF-UHFFFAOYSA-N oleicacidamide-heptaglycolether Natural products CCCCCCCCC=CCCCCCCCC(N)=O FATBGEAMYMYZAF-UHFFFAOYSA-N 0.000 description 1
- 150000007530 organic bases Chemical class 0.000 description 1
- 150000002894 organic compounds Chemical class 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 235000019809 paraffin wax Nutrition 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 238000005192 partition Methods 0.000 description 1
- KHMYONNPZWOTKW-UHFFFAOYSA-N pent-1-enylbenzene Chemical compound CCCC=CC1=CC=CC=C1 KHMYONNPZWOTKW-UHFFFAOYSA-N 0.000 description 1
- 125000002958 pentadecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- PNJWIWWMYCMZRO-UHFFFAOYSA-N pent‐4‐en‐2‐one Natural products CC(=O)CC=C PNJWIWWMYCMZRO-UHFFFAOYSA-N 0.000 description 1
- 239000002304 perfume Substances 0.000 description 1
- 235000019271 petrolatum Nutrition 0.000 description 1
- 229950000688 phenothiazine Drugs 0.000 description 1
- VCAFTIGPOYBOIC-UHFFFAOYSA-N phenyl dihydrogen phosphite Chemical class OP(O)OC1=CC=CC=C1 VCAFTIGPOYBOIC-UHFFFAOYSA-N 0.000 description 1
- ZPNJBTBYIHBSIG-UHFFFAOYSA-N phenyl-(2,2,6,6-tetramethylpiperidin-4-yl)methanone Chemical compound C1C(C)(C)NC(C)(C)CC1C(=O)C1=CC=CC=C1 ZPNJBTBYIHBSIG-UHFFFAOYSA-N 0.000 description 1
- 239000011990 phillips catalyst Substances 0.000 description 1
- UEZVMMHDMIWARA-UHFFFAOYSA-M phosphonate Chemical compound [O-]P(=O)=O UEZVMMHDMIWARA-UHFFFAOYSA-M 0.000 description 1
- 150000003013 phosphoric acid derivatives Chemical class 0.000 description 1
- 150000003016 phosphoric acids Chemical class 0.000 description 1
- 150000003018 phosphorus compounds Chemical class 0.000 description 1
- 239000012994 photoredox catalyst Substances 0.000 description 1
- XNGIFLGASWRNHJ-UHFFFAOYSA-L phthalate(2-) Chemical compound [O-]C(=O)C1=CC=CC=C1C([O-])=O XNGIFLGASWRNHJ-UHFFFAOYSA-L 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 125000005936 piperidyl group Chemical group 0.000 description 1
- 239000004014 plasticizer Substances 0.000 description 1
- 239000004999 plastisol Substances 0.000 description 1
- 229920001627 poly(4-methyl styrene) Polymers 0.000 description 1
- 229920001084 poly(chloroprene) Polymers 0.000 description 1
- 229920001643 poly(ether ketone) Polymers 0.000 description 1
- 229920003229 poly(methyl methacrylate) Polymers 0.000 description 1
- 229920002492 poly(sulfone) Polymers 0.000 description 1
- 229920002037 poly(vinyl butyral) polymer Polymers 0.000 description 1
- 229920003251 poly(α-methylstyrene) Polymers 0.000 description 1
- 229920002401 polyacrylamide Polymers 0.000 description 1
- 229920001515 polyalkylene glycol Polymers 0.000 description 1
- 229920002312 polyamide-imide Polymers 0.000 description 1
- 229920002480 polybenzimidazole Polymers 0.000 description 1
- 229920001083 polybutene Polymers 0.000 description 1
- 229920001225 polyester resin Polymers 0.000 description 1
- 239000004645 polyester resin Substances 0.000 description 1
- 229920006393 polyether sulfone Polymers 0.000 description 1
- 229920001601 polyetherimide Polymers 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229940068886 polyethylene glycol 300 Drugs 0.000 description 1
- 239000004848 polyfunctional curative Substances 0.000 description 1
- 229920001721 polyimide Polymers 0.000 description 1
- 229920001195 polyisoprene Polymers 0.000 description 1
- 229920001470 polyketone Polymers 0.000 description 1
- 229920000193 polymethacrylate Polymers 0.000 description 1
- 229920000069 polyphenylene sulfide Polymers 0.000 description 1
- 229920002689 polyvinyl acetate Polymers 0.000 description 1
- 239000011118 polyvinyl acetate Substances 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 229920002620 polyvinyl fluoride Polymers 0.000 description 1
- 239000005033 polyvinylidene chloride Substances 0.000 description 1
- 229920002981 polyvinylidene fluoride Polymers 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- MQOCIYICOGDBSG-UHFFFAOYSA-M potassium;hexadecanoate Chemical compound [K+].CCCCCCCCCCCCCCCC([O-])=O MQOCIYICOGDBSG-UHFFFAOYSA-M 0.000 description 1
- 239000002243 precursor Substances 0.000 description 1
- 238000003825 pressing Methods 0.000 description 1
- 238000007639 printing Methods 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- 125000001501 propionyl group Chemical group O=C([*])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000010526 radical polymerization reaction Methods 0.000 description 1
- 230000003134 recirculating effect Effects 0.000 description 1
- 238000004064 recycling Methods 0.000 description 1
- 230000002787 reinforcement Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 238000000518 rheometry Methods 0.000 description 1
- 229910052895 riebeckite Inorganic materials 0.000 description 1
- 238000005096 rolling process Methods 0.000 description 1
- 229920006395 saturated elastomer Polymers 0.000 description 1
- 238000007789 sealing Methods 0.000 description 1
- 239000004460 silage Substances 0.000 description 1
- 229910000077 silane Inorganic materials 0.000 description 1
- 150000004760 silicates Chemical class 0.000 description 1
- 238000005245 sintering Methods 0.000 description 1
- IJRHDFLHUATAOS-DPMBMXLASA-M sodium ricinoleate Chemical compound [Na+].CCCCCC[C@@H](O)C\C=C/CCCCCCCC([O-])=O IJRHDFLHUATAOS-DPMBMXLASA-M 0.000 description 1
- 229940074404 sodium succinate Drugs 0.000 description 1
- ZDQYSKICYIVCPN-UHFFFAOYSA-L sodium succinate (anhydrous) Chemical compound [Na+].[Na+].[O-]C(=O)CCC([O-])=O ZDQYSKICYIVCPN-UHFFFAOYSA-L 0.000 description 1
- ZHROMWXOTYBIMF-UHFFFAOYSA-M sodium;1,3,7,9-tetratert-butyl-11-oxido-5h-benzo[d][1,3,2]benzodioxaphosphocine 11-oxide Chemical compound [Na+].C1C2=CC(C(C)(C)C)=CC(C(C)(C)C)=C2OP([O-])(=O)OC2=C1C=C(C(C)(C)C)C=C2C(C)(C)C ZHROMWXOTYBIMF-UHFFFAOYSA-M 0.000 description 1
- 239000012265 solid product Substances 0.000 description 1
- 125000006850 spacer group Chemical group 0.000 description 1
- 238000004611 spectroscopical analysis Methods 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 235000019698 starch Nutrition 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 229940037312 stearamide Drugs 0.000 description 1
- 239000010959 steel Substances 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 229920006302 stretch film Polymers 0.000 description 1
- 229920000638 styrene acrylonitrile Polymers 0.000 description 1
- 229920006132 styrene block copolymer Polymers 0.000 description 1
- IAHFWCOBPZCAEA-UHFFFAOYSA-N succinonitrile Chemical compound N#CCCC#N IAHFWCOBPZCAEA-UHFFFAOYSA-N 0.000 description 1
- 150000003467 sulfuric acid derivatives Chemical class 0.000 description 1
- 230000037072 sun protection Effects 0.000 description 1
- 238000004381 surface treatment Methods 0.000 description 1
- 229920003002 synthetic resin Polymers 0.000 description 1
- 239000000057 synthetic resin Substances 0.000 description 1
- KKEYFWRCBNTPAC-UHFFFAOYSA-L terephthalate(2-) Chemical compound [O-]C(=O)C1=CC=C(C([O-])=O)C=C1 KKEYFWRCBNTPAC-UHFFFAOYSA-L 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 125000000383 tetramethylene group Chemical group [H]C([H])([*:1])C([H])([H])C([H])([H])C([H])([H])[*:2] 0.000 description 1
- 238000003856 thermoforming Methods 0.000 description 1
- 238000001757 thermogravimetry curve Methods 0.000 description 1
- 229920001169 thermoplastic Polymers 0.000 description 1
- 229920002803 thermoplastic polyurethane Polymers 0.000 description 1
- 239000004416 thermosoftening plastic Substances 0.000 description 1
- 235000019303 thiodipropionic acid Nutrition 0.000 description 1
- 150000003568 thioethers Chemical class 0.000 description 1
- 239000004408 titanium dioxide Substances 0.000 description 1
- 235000010215 titanium dioxide Nutrition 0.000 description 1
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 1
- KHPCPRHQVVSZAH-UHFFFAOYSA-N trans-cinnamyl beta-D-glucopyranoside Natural products OC1C(O)C(O)C(CO)OC1OCC=CC1=CC=CC=C1 KHPCPRHQVVSZAH-UHFFFAOYSA-N 0.000 description 1
- 238000005809 transesterification reaction Methods 0.000 description 1
- 230000009466 transformation Effects 0.000 description 1
- 230000007704 transition Effects 0.000 description 1
- 238000002834 transmittance Methods 0.000 description 1
- IVIIAEVMQHEPAY-UHFFFAOYSA-N tridodecyl phosphite Chemical compound CCCCCCCCCCCCOP(OCCCCCCCCCCCC)OCCCCCCCCCCCC IVIIAEVMQHEPAY-UHFFFAOYSA-N 0.000 description 1
- WGKLOLBTFWFKOD-UHFFFAOYSA-N tris(2-nonylphenyl) phosphite Chemical compound CCCCCCCCCC1=CC=CC=C1OP(OC=1C(=CC=CC=1)CCCCCCCCC)OC1=CC=CC=C1CCCCCCCCC WGKLOLBTFWFKOD-UHFFFAOYSA-N 0.000 description 1
- 229920001862 ultra low molecular weight polyethylene Polymers 0.000 description 1
- 125000002948 undecyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 229920006337 unsaturated polyester resin Polymers 0.000 description 1
- 238000007740 vapor deposition Methods 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 229920001866 very low density polyethylene Polymers 0.000 description 1
- 229920006163 vinyl copolymer Polymers 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 238000004073 vulcanization Methods 0.000 description 1
- 239000002699 waste material Substances 0.000 description 1
- 239000002351 wastewater Substances 0.000 description 1
- 238000003466 welding Methods 0.000 description 1
- 239000002983 wood substitute Substances 0.000 description 1
- 239000002759 woven fabric Substances 0.000 description 1
- 150000003751 zinc Chemical class 0.000 description 1
- BOXSVZNGTQTENJ-UHFFFAOYSA-L zinc dibutyldithiocarbamate Chemical compound [Zn+2].CCCCN(C([S-])=S)CCCC.CCCCN(C([S-])=S)CCCC BOXSVZNGTQTENJ-UHFFFAOYSA-L 0.000 description 1
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 1
- 235000007680 β-tocopherol Nutrition 0.000 description 1
- 239000011590 β-tocopherol Substances 0.000 description 1
- 239000002478 γ-tocopherol Substances 0.000 description 1
- QUEDXNHFTDJVIY-DQCZWYHMSA-N γ-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1 QUEDXNHFTDJVIY-DQCZWYHMSA-N 0.000 description 1
- 239000002446 δ-tocopherol Substances 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/0008—Organic ingredients according to more than one of the "one dot" groups of C08K5/01 - C08K5/59
- C08K5/0083—Nucleating agents promoting the crystallisation of the polymer matrix
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/02—Halogenated hydrocarbons
- C08K5/03—Halogenated hydrocarbons aromatic, e.g. C6H5-CH2-Cl
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/16—Nitrogen-containing compounds
-
- C—CHEMISTRY; METALLURGY
- C08—ORGANIC MACROMOLECULAR COMPOUNDS; THEIR PREPARATION OR CHEMICAL WORKING-UP; COMPOSITIONS BASED THEREON
- C08K—Use of inorganic or non-macromolecular organic substances as compounding ingredients
- C08K5/00—Use of organic ingredients
- C08K5/16—Nitrogen-containing compounds
- C08K5/20—Carboxylic acid amides
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Medicinal Chemistry (AREA)
- Polymers & Plastics (AREA)
- Organic Chemistry (AREA)
- Crystallography & Structural Chemistry (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Compositions Of Macromolecular Compounds (AREA)
Abstract
"composições de resina". uma composição contendo a) um polímero natural ou sintético e b) um ou mais compostos da fórmula (1), (11) ou (111) onde r~ 1~, r~ 2~ e r~ 3~, ou y~ 1~, y~ 2~ e y~ 3~, ou z~ 1~, z~ 2~ e z~ 3~ são, por exemplo, alquila c~ 3-20~ ramificado.
Description
(54) Título: COMPOSIÇÕES DE RESINA, ARTIGO CONFORMADO, PROCESSOS PARA PROVIMENTO DE UMA POLIOLEFINA E PARA O AUMENTO DE TEMPERATURA DE CRISTALIZAÇÃO DESTA, FILME ORIENTADO MONOAXIAL OU BIAXIALMENTE, SISTEMAS MULTICAMADAS, COMPOSTOS E SEUS USOS, E MISTURA (51) Int.CI.: C08K 5/20; C08K 5/00 (30) Prioridade Unionista: 14/02/2003 EP 03 405084.9, 16/10/2003 EP 03 103835.9 (73) Titular(es): CIBA SPECIALTY CHEMICALS HOLDING INC.
(72) Inventor(es): HANS-WERNER SCHMIDT; MARKUS BLOMENHOFER; KLAUS STOLL; HANSRUDOLF MEIER
Relatório Descritivo da Patente de Invenção para COMPOSIÇÕES DE RESINA, ARTIGO CONFORMADO, PROCESSOS PARA PROVIMENTO DE UMA POLIOLEFINA E PARA O AUMENTO DE TEMPERATURA DE CRISTALIZAÇÃO DESTA, FILME ORIENTADO MONOAXIAL OU BIAXIALMENTE, SISTEMAS MULTICAMADAS, COMPOSTOS E SEUS USOS, E MISTURA.
A presente invenção refere-se a uma composição contendo um polímero sintético ou natural e uma amida, a um artigo conformado obtenível a partir da dita composição, ao uso das amidas como agentes nucleantes, em particular como agentes de redução de turvação, e a novas amidas.
Composições de resina sintética cristalina são, por exemplo, descritas nas EP-A-776 933, JP-A-Hei 8-157-640, JP-A-Hei 6-271 762, e EP-A-940 431.
Os compostos 1,3,5-tris[acetilamino]benzeno e 1,3,5-tris[propionilamino]benzeno são por exemplo, descritos em Chem. Ber. 103, 200-204 (1970) por H. Stetter et al.
O composto 1,3,5-tris[2,3-diidróxi benzoilamino]benzeno é por exemplo, descrito em J. Am. Chem. Soc., 123, 8923-8938 (2001) por D.L. Caulder et al.
A presente invenção refere-se em particular a uma composição contendo
a) um polímero natural ou sintético, preferivelmente um polímero sinté-tico, e
b) um ou mais compostos da fórmula (I), (II) ou (III) (I)
R1
Y
I1
H (II)
Petição 870160037195, de 19/07/2016, pág. 4/18 il
onde
Ri, R2 e R3) ou Yi, Y2 θ Y3, ou Zi, Z2 e Z3 independentemente um do outro são alquila C^o não-substituído ou substituído com um ou mais hidróxi; alquenila C2.20 não-substituído ou substituído com um ou mais hidróxi; alquila C2.2o interrompido por oxigênio ou enxofre; cicloalquila C3.i2 nãosubstituído ou substituído com um ou mais alquila Ci-20; (cicloalquil C3.12) alquila Ci-10 não-substituído ou substituído com um ou mais alquila C-i2obis[cicloalquil C3_-j2] alquila C1-10 não-substituído ou substituído com um ou mais alquila Ci_2o; um radical hidrocarboneto bicíclico ou tricíclico com 5 a 20 átomos de carbono não-substituído ou substituído com um ou mais alquila C1-20;
fenila não-substituído ou substituído com um ou mais radicais selecionados de alquila Ci.20> alcóxi Ci_2o, alquilamino Ci.2O, di(alquil Ci_20) amino, hidróxi e nitro; fenil alquila C-|.2o não-substituído ou substituído com um ou mais radicais selecionados de alquila Ci.2O, cicloalquila C3_i2, fenila, alcóxi Ci-2o e hidróxi;
fenil etenila não-substituído ou substituído com um ou mais alquila C-t.2O; bifenil (alquila C-mo) não-substituído ou substituído com um ou mais alquila Ci-20; naftila não-substituído ou substituído com um ou mais alquila C-i_20; naftil alquila Ci.2O não-substituído ou substituído com um ou mais alquila C1 -2oi naftóxi metila não-substituído ou substituído com um ou mais alquila C-|.2O; bifenilenila, flourenila, antrila; um radical heterocíclico de 5 a 6 membros não-substituído ou substituído com um ou mais alquila Ci-20; um radical hidrocarboneto C-i-20 contendo um ou mais halogênio; ou tri(alquil Cmo) silil (alquila Cmo);
com a condição de que pelo menos um dos radicais R-ι, R2 e R3, ou Y-ι, Y2 e Y3, ou Ζι, Z2 e Z3 seja alquila C3.2o ramificado não-substituído ou substituído com um ou mais hidróxi; alquila C2-20 interrompido por oxigênio ou enxofre; cicloalquila C3.-i2 não-substituído ou substituído com um ou mais alquila C1-20; (cicloalquil C3_12) alquila Cmo não-substituído ou substituído com um ou mais alquila C-|. 20; um radical hidrocarboneto bicíclico ou tricíclico com 5 a 20 átomos de carbono não-substituído ou substituído com um ou mais alquila C1-20; fenila não-substituído ou substituído com um ou mais radicais selecionados de alquila C1-20, alcóxi C1-20, alquilamino C1-20, di(alquil C1-20) amino, hidróxi e nitro; fenil alquila Cmo não-substituído ou substituído com um ou mais radicais selecionados de alquila C-i-20, cicloalquila C3.12, fenila, alcóxi C1-20 θ hidróxi; bifenil alquila Cmo não-substituído ou substituído com um ou mais alquila C-i20; naftil alquila C1-20 não-substituído ou substituído com um ou mais alquila Ci-20; ou tri(alquil Cmo) silil (alquila Cmo)·
De acordo com uma realização preferida da presente invenção pelo menos um dos radicais R1s R2 e R3, ou Y-ι, Y2 e Y3, ou Ζι, Ζ2 e Z3 é alquila C3.-io ramificado, ou cicloalquila C3.12 não-substituído ou substituído com um ou mais alquila C1-20.
De acordo com uma particular realização preferida da presente invenção pelo menos um dos radicais R-ι, R2 e R3, ou Υ-ι, Y2 e Y3, ou Z-j, Ζ2 e Z3 é alquila C3.10 ramificado.
Exemplos de alquila C-i-20, por exemplo, alquila C3.2o ramificado, não-substituído ou substituído com um ou mais hidróxi, por exemplo, 1, 2 ou 3 hidróxi, são etila, n-propila, 1-metil etila, n-butila, 2-metil propila, 1-metil propila, t-butila, pentila, 1-metil butila, 2-metil butila, 3-metil butila, 1,1-dimetil propila, 1-etil propila, t-butil metila, hexila, 1-metil pentila, heptila, issoheptila, 1-etil hexila, 2-etil pentila, 1-propil butila, octila, nonila, isononila, neononila, 2,4,4-trimetil pentila, undecila, tridecila, pentadecila, hepta decila, hidróxi metila e 1-hidróxi etila. Alquila Cmo ramificado é particularmente preferido. Um dos significados preferidos dos radicais R-ι, R2 e R3, ou Y1, Y2 e Y3, ou Ζ1, Z2 e Z3 é alquila C3.-io ramificado com um átomo de C quaternário em posição 1, em particular -C(CH3)2-H ou -C(CH3)2-(alquila Ci-7).
Ο
Exemplos de alquenila C2-20 não-substituído ou substituído com um ou mais hidróxi, por exemplo, 1, 2 ou 3 hidróxi, são 9-decenila, 8-hepta decenila e 11-hidróxi-8-hepta decenila.
Exemplos de alquila C2-20 interrompido por oxigênio são t-butóxi metila, t-butóxi etila, t-butóxi propila e t-butóxi butila.
Exemplos de alquila C2-20 interrompido por enxofre são (H3C)3CS-CH2-, (H3C)3C-S-C2H4-, (H3C)3C-S-C3H6- e (H3C)3C-S-C4H8-.
Exemplos de cicloalquila C3.12 não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1, 2, 3 ou 4 alquila C-m, são ciclopropila, 3- metilciclopropila, 2,2,3,3-tetrametilciclopropila, ciclobutila, ciclopentila, ciclohexila, 1-metilciclohexila, 2-metilciclohexila, 3-metilciclohexila, 4metilciclohexila, 4-t-butil ciclohexila e cicloheptila.
Exemplos de (cicloalquil C3.i2) alquila C1.10 não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1, 2 ou 3 alquila C-m, são ciclopentil metila, 2-ciclopentil etila, ciclohexil metila, 2-ciclohexil etila, 3ciclohexil propila, 4-ciclohexil butila e (4-metilciclohexil) metila.
Um exemplo de bis[cicloalquil C3.i2] alquila Cmo não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1, 2 ou 3 alquila C1-4, é diciclohexil metila.
Exemplos de um radical hidrocarboneto bicíclico ou tricíclico com 5 a 20 átomos de carbono não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1, 2 ou 3 alquila C1-4, são
ϊΜ
Exemplos de fenila não-substituído ou substituído com um ou mais radicais, por exemplo, 1, 2 ou 3 radicais, selecionados de alquila C-1-20, alcóxi C-i-20, alquilamino C-i-20, di(alquil C-i-20) amino, hidróxi e nitro, preferivelmente alquila C1.4, alcóxi C1.4, alquilamino C1-4, di(alqui) C1-4) amino, hidróxi e nitro, são fenila, 3-metil fenila, 3-metóxi fenila, 4-metil fenila, 4- etil fenila, 4-propil fenila, 4-isopropil fenila, 4-t-butil fenila, 4-isopropóxi fenila,
2.3- dimetóxi fenila, 2-nitro fenila, 3-metil-6-nitro fenila, 4-dimetilamino fenila,
2.3- dimetil fenila, 2,6-dimetil fenila, 2,4-dimetil fenila, 3,4-dimetil fenila, 3,5dimetil fenila, 3,5-di-t-butil fenila, 2,4,6-trimetil fenila, e 3,5-di-t-butil-4-hidróxi fenila.
Exemplos de fenil alquila C1.20 não-substituído ou substituído com um ou mais radicais, por exemplo, 1, 2 ou 3 radicais, selecionados de alquila C-i-20, cicloalquila C3.12, fenila, alcóxi C1-20 e hidróxi, preferivelmente alquila Cm, cicloalquila C3-6, fenila, alcóxi C1.4 e hidróxi, são benzila, alfa ciclohexil benzila, difenil metila, 1-fenil etila, alfa hidróxi benzila, 2-fenil etila, 2fenil propila, 3-fenil propila, 3-metil benzila, 3,4-dimetóxi benzila, e 2-(3,4dimetóxi fenil) etila.
Um exemplo de fenil etenila não-substituído ou substituído com um ou mais alquila C1-20, por exemplo 1, 2 ou 3 alquila C1-4, θ 2-(4-metil fnil) etenila.
Um exemplo de bifenil (alquila Cuo) não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1, 2 ou 3 alquila Ci-4> θ 4bifenil metila.
Exemplos de naftila não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1,2 ou 3 alquila C1.4, são 1-naftila e 2-naftila.
Exemplos de naftil C1-20 alquila não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1, 2 0 u3 alquila C1.4, são 1-naftil metila e 2-naftil metila.
Um exemplo de naftóxi metila não-substituído ou substituído com um ou mais alquila C1-20, por exemplo, 1,2 ou 3 alquila C-μ, é naftóxi metila.
Exemplos de bifenilenila, flourenila ou antrila é 2-bifenilenila, 9flourenila, 1-flourenila ou 9-antrila, respectivamente.
Exemplos de um radical heterocíclico de 5- ou 6-membros nãosubstituído ou substituído com um ou mais alquila Ci-20, por exemplo, 1,2 ou 3 alquila Cm, são 3-piridinila, 4-piridinila, 2-hidróxi piridin-3-ila, 3-quinolinila, 4-quinolinila, 2-furifa, 3-furila, e 1 -metil-2-pirrila.
Exemplos de um radical hidrocarboneto C1-20 contendo um ou mais halogênios, por exemplo, 1,2, 3, 4, 5, ou 6 -F, -Cl ou -J, são 1-bromo2-metil propila, dicloro metila, pentaflúor etila, 3,5-bis[triflúor metil] fenila, 2,3,5,6-tetraflúor p-toiila, 2,3-dicloro fenila, 3,4-dicloro fenila e 2,4-bis[triflúor metil] fenila.
R1, R2 e R3, ou Y1, Y2 e Y3, ou Zy, Z2 e Z3 são preferivelmente independentemente um do outro alquila C-mo não-substituído ou substituído com 1, 2 ou 3 hidróxi; alquenila C2.2o não-substituído ou substituído com 1, 2 ou 3 hidróxi; alquila C2.10 interrompido com oxigênio; cicloalquila C3_6 nãosubstituído ou substituído com 1, 2, 3 ou 4 alquila Cy.4, (cicloalquil C3-6) alquila C-mo não-substituído ou substituído com 1, 2 ou 3 alquila Cm; bis[cicloalquil C3.6] alquila Cmo não-substituído ou substituído com 1, 2 ou 3 alquila Cm;
fenila não-substituído ou substituído com 1, 2 ou 3 radicais selecionados de alquila Cm, alcóxi Cm, alquilamino Cm, di(alquil Cm) amino, hidróxi e nitro;
fenil alquila Cmo não-substituído ou substituído com 1, 2 ou 3 radicais sele7 cionados de alquila Cm, cicloalquila C3.6, fenila, alcoxi C1-4 e hidróxi; fenil etenila não-substituído ou substituído com 1, 2 ou 3 alquila C1-4; bifenil (alquila C-mo) não-substituído ou substituído com 1, 2 ou 3 alquila C-1.4; naftila não-substituído ou substituído com 1, 2 ou 3 alquila Ci_4; naftil alquila C1-10 não-substituído ou substituído com 1, 2 ou 3 alquila C1.4; naftóxi metila nãosubstituído ou substituído com 1, 2 ou 3 alquila Ci-4; bifenilenila, flourenila, antrila; 3-piridinila, 4-piridinila, 2-hidróxi piridin-3-ila, 3-quinolinila, 4-quinolinila, 2-furila, 3-furila, 1-metil-2-pirrila; 1-bromo-2-metil propila; dicloro metila, pentaflúor etila, 3,5-bis[triflúor metil] fenila, 2,3,5,6-tetraflúor p-tolila, 2,3dicloro fenila, 3,4-dicloro fenila ou 2,4-bis[triflúor metil] fenila.
R-ι, R2 e R3, ou Y-i, Y2 e Y3, ou Z-ι, Z2 e Z3 independentemente uns dos outros são em particular alquila C3-i0 interrompido por oxigênio;
cicloalquila C3.6 não-substituído ou substituído com 1, 2, 3 ou 4 alquila mCi-4;
(cicloalquil Ο3.β) alquila C1.10 não-substituído ou substituído com 1,2 ou 3 alquila C-|.4;
fenila não-substituído ou substituído com 1,2 ou 3 alquila C-|.4; fenil alquila C1.10 não-substituído ou substituído com 1, 2 ou 3 radicais selecionados de alquila C1-4 e alcoxi C1.4; bifenil (alquila CMo); naftil alquila C1-10; ou
ΊΎ tri(alquil C-m) silil (alquila C1-5).
Exemplos de compostos da fórmula (I) são:
1.3.5- tris[ciclohexil carbonilaminojbenzeno,
1.3.5- tris[2,2-dimetilpropionilamino]benzeno,
1.3.5- tris[4-metil benzoilaminojbenzeno,
1.3.5- tris[3,4-dimetil benzoilamino]benzeno,
1.3.5- tris[3,5-dimetil benzoilaminojbenzeno,
1.3.5- tris[ciclopentano carbonilaminojbenzeno,
1.3.5- tris[1-adamantano carbonilaminojbenzeno,
1.3.5- tris[2-metilpropionilamino]benzeno,
1.3.5- tris[3,3-dimetilbutirilamino]benzeno,
1.3.5- tris[2-etilbutirilamino]benzeno,
1.3.5- tris[2,2-dimetilbutirilamino]benzeno,
1.3.5- tris[2-ciclohexilacetilamino]benzeno,
1.3.5- tris[3-ciclohexilpropionilamino]benzeno,
1.3.5- tris[4-ciclohexilbutirilamino]benzeno,
1.3.5- tris[5-ciclohexilvaleroilamino]benzeno, 1-isobutirilamino-3,5-bis[pivaloilamino]benzeno,
2.2- dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno,
3.3- dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno,
1.3- bis[isobutirilamino]-5-pivaloilamino benzeno,
1.3- bis[isobutirilamino]-5-(2,2-dimetilbutiril)aminobenzeno,
1.3- bis-[isobutirilamino]-5-(3,3-dimetilbutiril)aminobenzeno,
1.3- bis-[2,2-dimetilbutirilamino]-5-pivaloilaminobenzeno,
1.3- bis-[2,2-dimetilbutirilamino-5-isobutirilaminobenzeno,
1.3- bis[2,2-dimetilbutirilamino]-5-(3,3-dimetilbutiril)aminobenzeno,
1.3- bis[3,3-dimetilbutirilamino]-5-pivaloilaminobenzeno,
1.3- bis[3,3-dimetilbutirilamino]-5-isobutirilaminobenzeno,
1.3- bis-[3,3-dimetilbutirilamino)-5-(2,2-dimetilbutirilamino aminobenzeno,e
1.3.5- tris[3-(trimetil silil) propionilaminojbenzeno.
Ainda exemplos de compostos da fórmula (I) são:
1.3.5- tris-[2,2-dimetilvaleroilamino]benzeno,
1.3.5- tris-[3,3-climetilvaleroilamino]benzeno,
1.3.5- tris-[2,4-dimetilvaleroilamino]benzeno,
1.3.5- tris-[4,4-dimetilvaleroilamino]benzeno,
1.3.5- tris-[4-metilvaleroilamino]benzeno,
1.3.5- tris-[2-metilbutirilamino]benzeno,
1.3.5- tris-[2-metilvaleroilamino]benzeno,
1.3.5- tris-[3-metilvaleroilamino]benzeno,
1.3.5- tris-[2,2,3,3-tetrametil ciclopropano carbonilamino]benzeno,
1.3.5- tris-[ciclopentilacetilamino]benzeno,
1.3.5- tris-[3-ciclopentilpropionilamino]benzeno,
1.3.5- tris-[2-norbornilacetilamino]benzeno,
1.3.5- tris-[4-t-butil ciclohexano-1-carbonilamino]benzeno,
1.3.5- tris[2-(t-butóxi) acetilamino]benzeno,
1.3.5- tris[3-(t-butóxi) propionilamino]benzeno,
1.3.5- tris[4-(t-butóxi) butirilamino]benzeno,
1.3.5- tris-[5-t-butóxi valeroilamino]benzeno,
1.3.5- tris[ciclopropano carbonilaminojbenzeno,
1.3.5- tris[2-metil ciclopropano-1-carbonilaminojbenzeno,
1.3.5- tris[3-noradamantano-1 -carbonilamino]benzeno,
1.3.5- tris[bifenil-4-acetilamino]benzeno,
1.3.5- tris-[2-naftilacetilamino]benzeno,
1.3.5- tris-[3-metil fenilacetilaminojbenzeno,
1.3.5- tris[(3,4-dimetóxi fenil) acetilamino]benzeno,
1.3.5- tris-[(3-trimetil sililpropionilamino]benzeno, e
1.3.5- tris-[(4-trimetil sililbutirilamino]benzeno.
Exemplos de compostos da fórmula (II) são:
N-t-butil-3,5-bis-(3-metilbutirilamino)benzamida,
N-t-butil-3,5-bis-(pivaloilamino)benzamida,
N-t-octil-3,5-bis-(pivaloilamino)benzamida,
N-(1,1 -dimetil propil)-3,5-bis-(pivaloilamino)benzamida, le>
N-(t-octil)-3,5-bis(isobutirilamino)benzamida,
N-(t-butil)-3,5-bis(pivaloilamino)benzamida,
N-(2,3-dimetilciclohexil)-3,5-bis-(pivaloilamino)benzamida, N-t-butil-3,5-bis-(ciclopentanocarbonilamino)benzamida, N-(3-metil butil)-3,5-bis-(3-metilbutirilamino)benzamida, N-(3-metil butil)-3,5-bis-(pivaloilamino)benzamida,
N-(3-metil butil)-3,5-bis-(4-metilpentanoilamino)benzamida,
N-(3-metil butil)-3,5-bis-(ciclopentanocarbonilamino)benzamida,
N-(3-metil butil)-3,5-bis-(ciclohexanocarbonilamino)benzamida,
N-ciclopentil-3,5-bis-(3-metilbutirilamino)benzamida,
N-ciclopentil-3,5-bis-(pivaloilamino)benzamida,
N-ciclopentil-3,5-bis-(4-metilpentanoilamino)benzamida,
N-ciclopentil-3,5-bis-(ciclopentanocarbonilamino)benzamida,
N-ciclopentil-3,5-bis-(ciclohexanocarbonilamino)benzamida,
N-ciclohexil-3,5-bis-(3-metilbutirilamino)benzamida,
N-ciclohexil-3,5-bis-(pivaloilamino)benzamida,
N-ciclohexil-3,5-bis-(4-metilpentanoilamino)benzannida,
N-ciclohexil-3,5-bis-(ciclopentanocarbonilamino)benzamida,
N-ciclohexil-3,5-bis.(ciclohexanocarbonilamino)benzamida,
N-isopropil-3,5-bis-(pivaloilamino)benzamida,
N-isopropil-3,5-bis-(isobutirilamino)benzamida,
N-t-butil-3,5-bis-(2,2-dimetilbutirilamino)benzamida, e
N-t-octil-3,5-bis-(2,2-dimetilbutirilamino)benzamida.
Exemplos de compostos da fórmula (lll) são Ν,Ν’-di-t-butil diamida de ácido 5-pivaloilamino isoftálico, Ν,Ν'-di-t-octil diamida de ácido 5-pivaloilamino isofátlico, Ν,Ν'-di-t-butil diamida de ácido 5-(2,2-dimetilbutirilamino) isoftálico, Ν,Ν'-di-t-octil diamida de ácido 5-(2,2-dimetilbutirilamino) isoftálico, Ν,Ν'-di-ciclohexil diamida de ácido 5-(3-metil butirilamino) isoftáN,N'-di-ciclohexil diamida de ácido 5-(pivaloilamino) isoftálico, Ν,Ν'-di-ciclohexil diamida de ácido 5-(ciclopentano carbonilami11 no) isoftálico,
Ν,Ν'-di-ciclohexil diamida de ácido 5-(ciclohexil carbonilamino) isofálico,
N,N'-bis-(2-metilciclohexil)diamida de ácido 5-(ciclopentano carbonilamino) isoftálico,
N,N'-bis-(2-metilciclohexil) diamida,
N,N'-bis-(2-metilciclohexil)diamida de ácido 5-((1metilciclohexanocarbonil)amino)isoftálico, e
N,N'-bis-(2-metilciclohexil)diamida de ácido 5-((2-metil ciclohexnao carbonil) amino) isoftálico.
Ainda de acordo com uma realização preferida Ri,R2e R3 ou Y1, Y2 e Y3 ou Zu Z2 e Z3 são independentemente um do outro 1-metil etila, 2metil propila, 1-metil propila, t-butila, 1-metil butila, 2-metil butila, 3-metil butila, 1,1-dimetil propila, 1-etil propila, t-butil metila, ciclopropila, 3-metilciclopropila, 2,2,3,3-tetrametilciclopropila, ciclopentila, ciclopentil metila, 2-ciclopentil etila, ciclohexila, ciclohexil metila, 2-ciclohexil etila, 4-t-butil ciclohexila, (4metilciclohexila) metila,
alfa-ciclohexil benzila, 3-metil benzila, 3,4-dimetóxi benzila, 4-bifenil metila, 2-naftil metila, m-tolila, m-metóxi fenila, p-tolila, 4-etil fenila, 4-isopropil fenila, 4-t-butil fenila, 2,3-dimetil fenila, 2,6-dimetil fenila, 2,4-dimetil fenila, ou 3,5di-t-butil-4-hidróxi fenila.
Os radicais R-ι, R2 e R3 ou ΥΊ, Y2 e Y3 ou ΖΊ, Z2 e Z3 são preferivelmente idênticos.
Realizações particularmente preferidas da presente invenção são listadas abaixo.
• uma composição onde R-ι, R2 e R3 ou Y-ι, Y2 e Y3 ou Z-ι, Z2 e Z3 independentemente um do outro são alquila C-mo ramificado; ou cicioalquila C3-6 não-substituído ou substituído com 1, 2, 3 ou 4 alquila C1-4.
• uma composição onde R1t R2 e R3 ou Y-ι, Y2 e Y3 ou Z1t Z2 e Z3 independentemente um do outro são alquila C3-10 ramificado.
· uma composição onde R-ι, R2 e R3 ou Y1# e Y3 ou Z-ι, independentemente um do outro são isopropila, s-butila, t-butila, 1-metil butila, 1metil pentila, 1-etil pentila, 1,1-dimetil propila, 2,2-dimetil propila, 1,1-dimetil butila, 1,1-dimetil hexila, 1-etil propila, 1-propil butila, 1-metil etenila, 1-metil2-propenila, 1-metil-2-butenila, ciclopentila ou ciclohexila.
· uma composição onde Y2, ou Z2 e Z3 independentemente um do outro são isopropila, s-butila, t-butila, 1,1-dimetil propila, 1,2-dimetil propila, 2,2-dimetil propila, t-octila, ciclopentila, ciclohexila, 2-metilciclohexila, 2,3dimetilciclohexila, 1-ciclohexil etila ou 1-adamantila.
• uma composição onde os radicais R1, R2 e R3 ou Y1, Y2 e Y3 ou
Z1, Z2 e Z3 são t-butila.
Exemplos preferidos de compostos da fórmula (I) são:
CH, I 3
Um particular exemplo preferido de um composto da fórmula (I) é
as composições de acordo com a presente invenção têm, por exemplo, excelente capacidade de cristalização, alta transmitância, alta claridade, baixa turvação e/ou aperfeiçoada estabilidade térmica.
Uma composição preferida da presente invenção é caracterizada por um valor de turvação que é menor que 62%; o valor de turvação sendo medido em uma placa de 1,0-1,2 mm de espessura, em particular 1,1-1,2 mm de espessura.
A turvação é determinada de acordo com ASTM D 1003. Turva10 ção é definida como aquela porcentagem de luz transmitida que passando através de um espécime (placa) desvia do feixe incidente por mais que 2,5° em média. Claridade é avaliada na faixa de ângulo menor que 2,5°. O espécime deve ter superfícies paralelas - substancialmente planas livre de pó, graxa, arranhões, e manchas, e deve ser livre de vazios internos distintos e partículas.
Uma composição que é caracterizada por uma turvação de 2 a
62%, em particular 2 a 50%, é preferida.
Uma composição que é caracterizada por uma turvação de 2 a 40%, em particular 5 a 15%, é ainda de interesse.
Exemplos de turvação são 2 a 55%, 2 a 50%, 2 a 45%, 2 a 40%, 2 a 35%, 2 a 30%, 2 a 25%, 2 a 20%, 2 a 15%, 2 a 10%, 5 a 55%, 5 a 50%, a 45%, 5 a 40%, 5 a 35%, 5 a 30%, 5 a 25%, 5 a 20%, 5 a 15%, 5 a 10%, a 55%, 7 a 50%, 7 a 45%, 7 a 40%, 7 a 35%, 7 a 30%, 7 a 25%, 7 a 20%, a 15%, 7 a 10%, 10 a 55%, 10 a 50%, 10 a 45%, 10 a 40%, 10 a 35%, 10 a 30%, 10 a 25%, 10 a 20% e 10 a 15%, em particular 10 a 40% or 13 a 40%.
Exemplos do polímero sintético (componente a)) são:
1. Polímeros de mono olefinas e diolefinas, por exemplo, poli propileno, poli isobutileno, poli but-1-eno, poli-4-metilo pent-1-eno, poli vinil ciclohexano, poli isopreno, ou poli butadieno, assim como polímeros de cicloolefinas, por exemplo, de ciclopenteno ou norborneno, polietileno (que opcionalmente pode ser reticulado), por exmeplo, polietileno de alta densidade (HDPE), polietileno de alta densidade e alto peso molecular (HDPEHMW), polietileno de alta densidade e peso molecular ultra alto (HDPEUHMW), polietileno de densidade média (MDPE), polietileno de baixa densidade (LDPE), polietileno de baixa densidade linear (LLDPE), (VLDPE) e (ULDPE).
Poliolefinas, isto é, os polímeros de mono olefinas exemplificados no parágrafo anterior, preferivelmente polietileno e polipropileno, podem ser preparados por diferentes, e especialmente pelos seguintes, processos:
a) polimerização de radical (normalmente sob alta pressão e em temperatura elevada).
b) polimerização catalítica usando um catalisador que normalmente contem um ou mais de um metal de grupos IVb, Vb, Vlb, ou VIII da Tabela Periódica. Estes metais usualmente têm um ou mais que um ligante, tipicamente óxidos, haletos, alcoolatos, ésteres, éteres, aminas, alquilas, alquenilas, e/ou arilas que podem ser tanto π- como σ-coordenados. Estes complexos de metais podem estar na forma livre ou fixados sobre substratos, tipicamente sobre cloreto de magnésio ativado, cloreto de titânio (III), alumina ou óxido de silício. Estes catalisadores podem ser solúveis ou insolúveis no meio de polimerização. Os catalisadores podem ser usados por si mesmos na polimerização ou ainda ativadores podem ser usados, tipicamente alquil metais, hidretos de metais, alquil haletos de metais, alquil óxidos de metais, ou metal alquiloxanos, os ditos metais sendo elementos de grupos Ia, Ila e/ou 11Ia da Tabela Periódica. Os ativadores podem ser convenientemente modificados com ainda grupos éster, éter, amina ou silil éter. Estes sistemas catalisadores são usualmente chamados catalisadores Phillips, Standard Oil Indiana, Ziegler (-Natta), ΤΝΖ (DuPont), metaloceno ou de sítio simples (SSC).
2. Misturas dos polímeros mencionados sob 1), por exemplo, misturas de polipropileno com poli isobutileno, polipropileno com polietileno (por exemplo, PP/HDPE, PP/LDPE) e misturas de diferentes tipos de polietileno (por exemplo, LDPE/HDPE).
3. Copolímeros de mono olefinas e diolefinas uns com os outros ou com outros monômeros vinila, por exemplo, copolímeros de etileno/propileno, polietileno de baixa densidade linear (LLDPE) e suas misturas com polietileno de baixa densidade (LDPE), copolímeros de propileno/but-1eno, copolímeros de propileno/isobutileno, copolímeros de etileno/but-1-eno, copolímeros de etileno/hexeno, copolímeros de etileno/metil penteno, copolímeros de etileno/hepteno, copolímeros de etileno/octeno, copolímeros de etileno/vinil ciclohexano, copolímeros de etileno/cicloolefina (por exmeplo, etileno/norborneno como COC), copolímeros de etileno/1-olefinas, onde a 1olefina é gerada in-situ; copolímeros de propileno/butadieno, copolímeros de isobutileno/isopreno, copolímeros de etileno/vinil ciclohexano, copolímeros de etileno/acrilato de alquila, copolímeros de etileno/metacrilato de alquila, copolímeros de etileno/acetato de vinila ou copolímeros de etileno/ácido acrílico e seus sais (ionômeros) assim como terpolímeros de etileno com propileno e um dieno tal como hexadieno, diciclopentadieno ou etilideno - norborneno; e misturas de tais copolímeros uns com os outros e com polímeros mencionados em 1) acima, por exemplo, copolímeros de polipropileno/ etileno-propileno, copolímeros de LDPE/etileno-acetato de vinila (EVA), copolí16 ι6 meros de LDPE/etileno-ácido acrílico (EAA), LLDPE/EVA, LLDPE/EAA e copolímeros de polialquileno/monóxido de carbono alternantes ou randômicos e suas misturas com outros polímeros, por exemplo, poliamidas.
4. Resinas hidrocarbonetos (por exemplo, C5-9) incluindo suas modificações hidrogenadas (por exemplo, formadores de pegajosice) e misturas de polialquilenos e amido.
Homopolímeros e copolímeros de 1 .)-4.) podem ter qualquer estrutura estéreo incluindo sindiotática, isotática, hemi-isotática ou atática. Polímeros de bloco estéreo também são incluídos.
5. Poliestireno, poli(p-metil estireno), poli (alfa metil estireno).
6. Homopolímeros e copolímeros aromáticos derivados de monômeros aromáticos vinila incluindo estireno, alfa metil estireno, todos os isômeros de vinil tolueno, especialmente p-vinil tolueno, todos os isômeros de etil estireno, propil estireno, vinil bifenila, vinil naftaleno, e vinil antraceno, e suas misturas. Homopolímeros e copolímeros podem ter qualquer estéreoestrutura incluindo sindiotática, isotática, hemi-isotática ou atática. Polímeros de bloco estéreo também são incluídos.
6a. Copolímeros incluindo os monômeros e comonômeros aromáticos vinila mencionados anteriormente selecionados de etileno, propile20 no, dienos, nitrilas, ácidos, anidridos maléicos, maleimidas, acetato de vinila e cloreto de vinila ou derivados acrílicos e suas misturas, por exemplo, estireno/butadieno, estireno/acrilontrila, estireno/etileno (interpolímeros), estireno/metacrilato de alquila, estireno/butadieno/acrilato de alquila, estireno/ butadieno/metacrilato de alquila, estireno/anidrido maléico, estireno/ acrilonitri25 la/acrilato de metila; misturas de copolímeros de estireno de alta resistência a impacto e um outro polímero, por exemplo, um poliacrilato, um polímero dieno ou um terpolímero etileno/propileno/dieno; e copolímeros de bloco de estireno como estireno/butadieno/estireno, estireno/isopreno/estireno, estireno/etileno/butileno/estireno ou estireno/etileno/propileno/estireno.
6b. Polímeros aromáticos hidrogenados derivados de hidrogenação de polímeros mencionados sob 6.), especialmente incluindo poli ciclohexil etileno (PCHE) preparado por hidrogenação de poliestireno atático, fre17
qüentemente referido como poli vinil ciclohexano (PVCH).
6c. polímeros aromáticos hidrogenados derivados de hidrogenação de polímeros mencionados sob 6a.).
Homopolímeros e copolímeros podem ter qualquer estéreoestrutura incluindo sindiotática, isotática, hemi-isotática ou atática. Polímeros de bloco estéreo também são incluídos.
7. Copolímeros de enxerto de monômeros aromáticos vinila tais como estireno ou alfa-metil estireno, por exemplo, copolímeros de estireno sobre polibutadieno, estireno sobre polibutadieno-estireno ou polibutadienoacrilonitrila;estireno e acrilonitrila (ou metacrilonitrila) sobre polibutadieno; estireno, acrilonitrila e metacrilato de metila sobre polibutadieno; estireno e anidrido maléico sobre polibutadieno; estireno, acrilonitrila e anidrido maléico ou maleimida sobre polibutadieno; estireno e maleimida sobre polibutadieno; estireno e acrilatos ou metacrilatos de alquila sobre polibutadieno; estireno e acrilotrila sobre terpolímeros de etileno/propileno/dieno; estireno e acrilonitrila sobre acrilatos de polialquila ou metacrilatos de polialquila, estireno e acrilontrila sobre copolímeros de acrilato/butadieno, assim como suas misturas com os copolímeros listados sob 6), por exemplo, as misturas de copolímeros conhecidas como polímeros ABS, MBS, ASA ou AES.
8. Polímeros contendo halogênio tais como policloropreno, borrachas cloradas, copolímero clorado e bromado de isobutileno-isopreno (borracha halo butila), polietileno clorado ou sulfo-clorado, copolímeros de etileno e etileno clorado, homo- e copolímeros de epicloroidrina, especialmente polímeros de compostos vinila contendo hjalogênio, por exemplo, cloreto de polivinila, cloreto de polivinilideno, fluoreto de polivinila, fluoreto de polivinilideno, assim como seus copolímeros como copolímeros de cloreto de vinila/cloreto de vinilideno, cloreto de vinila/acetato de vinila ou cloreto de viniiideno/acetato de vinila.
9. Polímeros derivados de ácidos alfa,beta-insaturados e seus derivados como poliacrilatos e polimetacrilatos; metacrilatos de poli metila, poliacrilamidas e poliacrilonitrilas, modificadas - impacto com acrilato de butila.
αν
10. Copolímeros dos monômeros mencionados sob 9) uns com outros ou com outros monômeros insaturados, por exemplo, copolímeros de acrilonitrila/butadieno, copolímeros de acrilonitrila/acriiato de alquila, copolímeros de acrilonitrila/acriiato de alcoxi alquila ou acrilonitrila/haleto de vinila ou terpolímeros de acrilonitrila/metacrilato de alquila/butadieno.
11. Polímeros derivados de álcoois insaturados e aminas ou os derivados acila ou seus acetais, por exemplo, álcool polivinílico, acetato de polivinila, estearato de polivinila, benzoato de polivinila, maleato de polivinila, polivinil butiral, ftalato de polialila ou poli alil melamina; assim como seus co10 polímeros com olefinas mecionadas em 1) acima.
12. Homopolímeros e copolímeros de éter cíclicos tais como polialquileno glicóis, óxido de polietileno, óxido de poli propileno, ou seus copolímeros com bis-glicidil éteres.
13. Poliacetais tais como polioximetileno e aqueles polioximetile15 nos que contêm óxido de etileno como um comonômero, poliacetais modificados com poliuretanos termoplásticos, acrilatos ou MBS.
14. Óxidos de polifenileno e sulfetos, e misturas de óxidos de polifenileno com polímeros de estireno ou poliamidas.
15. Poliuretanos derivados de poliéteres terminados com hidroxi20 la, poliésteres ou polibutadienos por um lado e poliisocianatos alifáticos ou arompor outro, assim como seus precursores.
16. Poliamidas e copoliamidas derivadas de diaminas e ácidos dicarboxílicos e/ou de ácidos aminocarboxílicos ou os correspondentes lactams, por exemplo poliamida 4, poliamida 6, poliamida 6/6, 6/10, 6/9, 6/12,
4/6, 12/12, poliamida 11, poliamida 12, poliamidas aromáticas partindo de mxileno diamina e ácido adípico; poliamidas preparadas de hexa metileno diamina e ácido isoftálico e/ou tereftálico e com ou sem um elastômero como modificador, por exemplo, poIi-2,4,4-trimetil hexa metileno tereftalamida ou poli-m-fenileno isoftalamida; e também copolímeros de bloco das poliamidas mencionadas anteriormente com poliolefinas, copolímeros de olefinas, ionômeros ou elastômeros enxertados ou ligados quimicamente; ou com poliéteres, por exemplo, com polietileno glicol, polipropileno glicol, ou poli tetrameti19
Μ leno glicol; assim como poliamidas ou copoliamidas modificadas com EPDM ou ABS; e poliamidas condensadas durante processamento (sistemas de poliamida RIM).
17. Poliuréias, poliimidas, poliamida-imidas, poli éter imidas, poli 5 éster imidas, poli hidantoínas e poli benzimidazóis.
18. Poliésteres derivados de ácidos dicarboxílicos e diõis e/ou de ácidos hidróxi carboxílicos ou as correspondentes lactonas, por exemplo, tereftalato de polietileno, tereftalato de polibutileno, tereftalato de poli-1,4dimetilol ciclohexano, naftalato de polialquileno (PAN) e poliidróxi benzoatos, assim como copoliéter ésteres em bloco derivados de poliéteres terminados com hidroxila; e também poliésteres modificados com policarbonatos ou MBS.
19. Policarbonatos e poliéster carbonatos.
20. Poli cetonas.
21. Poli sulfonas, poliéter sulfonas e poliéter cetonas.
22. Polímeros reticulados derivados de aldeídos por um lado e fenóis, uréias e melaminas por outro lado, tais como resinas fenol/ formaldeído, resinas uréia/formaldeído e resinas melamina/formaldeído.
23. Resinas alquida de secagem e não-secagem.
24. Resinas poliéster insaturadas derivadas de copoliésteres de ácidos dicarboxílicos saturados e insaturados com álcoois poliídricos e compostos vinila como agentes de reticulação, e também suas modificações contendo halogênio de baixa inflamabilidade.
25. Resinas acrílicas reticuláveis derivadas de acrilatos substitu25 idos, por exemplo, epóxi acrilatos, uretano acrilatos, ou poliéster acrilatos.
26. Resinas alquida, resinas poliéster e resinas acrilato reticuladas com resinas melamina, resinas uréia, isocianatos, isocianurratos, poliisocianatos ou resinas epóxi.
27. Resinas epóxi reticuladas derivadas de compostos glicidiia a30 lifáticos, cicloalifáticos, hetero cíclicos ou aromáticos, por exemplo, produtos de diglicidil éteres de bisfenol A e bisfenol F, que são reticulados com endurecedores usuais tais como anidridos ou aminas, com ou sem aceleradores.
28. Acetatos de celulose, propionatos de celulose, e butiratos de celulose, ou os éteres celulose tais como metil celulose; assim como colofônias e seus derivados.
29. Combinações dos polímeros (policombinações) mencionados acima, por exemplo, PP/EPDM, poliamida/EPDM ou ABS, PVC/EVA, PVC/ABS, PVC/MBS, PC/ABS, PBTP/ABS, PC/ASA, PC/PBT, PVC/CPE, PVC/acrilatos, POM/PUR termoplástico, PC/PURtermoplástico, POM/ acrilato, POM/MBS, PPO/HIPS, PPO/PA 6.6 e copolímeros, PA/HDPE, PA/PP, PA/PPO, PBT/PC/ABS ou PBT/PET/PC.
Copolímero baseado em catalisador metaloceno-polipropileno, metaloceno-polietileno e qualquer metaloceno de propileno e etileno, respectivamente, com outras alfa olefinas também são apropriados para aplicação na presente invenção e para ilustração de benefícios técnicos.
Os compostos da fórmula (I), (II) ou (III) ainda são úteis como agentes gelificantes na preparação de bastões de gel e aperfeiçoam estabilidade de gel de sistemas baseados em solvente orgânico e água.
Polímeros sintéticos preferidos (componente (a)) são listados sob os itens 1 a 3 acima.
Exemplos preferidos particulares do polímero sintético são um homopolímero de polipropileno, copolímero randômico, copolímero alternante ou segmentado, copolímero de bloco ou uma combinação de polipropileno com um outro polímero sintético.
Um homopolímero de polipropileno como componente a) é ainda preferido.
Homopolímero de polipropileno também cobre polipropileno ramificado de cadeia longa.
Poliopropileno, pode ser preparado por diferentes, por exemplo, pelos seguintes, processos:
Polimerização catalítica usando um catalisador que normalmente contem um ou mais de um metal de grupos IVb, Vb, Vlb, ou VIII da Tabela
Periódica. Estes metais usualmente têm um ou mais de um ligante, tipicamente óxidos, haletos, alcoolatos, ésteres, éteres, aminas, alquilas, alqueni21
Ias, e/ou arilas que podem ser π- ou σ-coordenadas. Estes complexos de metais podem estar na forma livre ou fixados sobre substratos, tipicamente sobre cloreto de magnésio ativado, cloreto de titânio (III), alumina ou óxido de silício. Estes catalisadores podem ser solúveis ou insolúveis no meio de polimerização. Os catalisadores podem ser usados por si próprios na polimerização ou ainda ativadores podem ser usados, tipicamente metal alquilas, hidretos de metais, alquil haletos de metais, alquil óxidos de metais, ou metais alquiloxanos, os ditos metais sendo elementos dos grupos Ia, lia, e/ou 11la da Tabela Periódica. Os ativadores podem ser convenientemente modificados com ainda grupos éster, éter, amina, ou silil éter. Estes sistemas catalisadores são usualmente chamados catalisadores de Phillips, Standard Oil Indiana, Ziegler (-Natta), TNZ (DuPont), metaloceno ou de sítio simples (SSC).
Ainda de acordo com uma realização preferida da presente invenção, componente a) é um copolímero randômico de polipropileno, copolímero alternante ou segmentado ou copolímero de bloco contendo um ou mais comonômeros selecionados do grupo consistindo em etileno, alfa olefina C4-20, vinil ciclohexano, vinil ciclohexeno, alcanodieno C4-20, cicloalcano dieno C5-12 e derivados de norborneno; a quantidade total de propileno eo comonômero(s) sendo 100%.
Copolímero de polipropileno também cobre copolímero de polipropileno ramificado de cadeia longa.
Exemplos de apropriadas alfa olefinas C4.2o são 1-buteno, 1penteno, 1-hexeno, 1-hepteno, 1-octeno, 1-noneno, 1-deceno, 1-undeceno,
1- dodeceno, 1-tetradeceno, 1-hexadeceno, 1-octadeceno, 1-eicoseno e 4metil-1-penteno.
Exemplos de apropriados alcanodienos C4.20 são hexadieno e octadieno.
Exemplos de apropriados cicloalcano dienos C5.12 são ciclopentadieno, ciclohexadieno, e ciclooctadieno.
Exemplos de apropriados derivados norborneno são 5-etilideno2- norborneno (ENB), diciclopentadieno (DCP) e metileno domethylene he22 xaidro naftalina (ΜΕΝ).
Um copolímero de propileno/etileno contem por exemplo 50 a 99,9%, preferivelmente 809 a 99,9%, em particular 90 a 99,9% em peso de propileno.
Um copolímero de propileno onde o comonômero é uma alfa olefina C9.20 tal como, por exemplo, 1-noneno, 1-deceno, 1-undeceno, 1-dodeceno, 1-tetradeceno, 1-hexadeceno, 1-octadeceno ou 1-eicoseno; alcanodieno C9.20, cicloalcanodieno Cg.12 ou um derivado norborneno tal como, por exemplo, 5-etilideno-2-norborneno (ENB) ou metileno domethylene hexaidro naftalina (MEN) contem preferivelmente mais que 90 moles %, em particular 90 a 99,9 moles % ou 90 a 99 moles %, de propileno.
Um copolímero de propileno onde o comonômero é uma alfa olefina C4.8 tal como, por exemplo, 1-buteno, 1-penteno, 1-hexeno, 1-hepteno, 1-octeno, ou 4-metil-1-penteno; vini ciclohexano, vinil ciclohexeno, alcandieno C4-8 ou cicloalcanodieno C5.8 contem preferivelmente mais que 80 moles %, em particular 80 a 99,9 moles % ou 80 a 99 moles %, de propileno.
Ainda exemplos de componente a) são copolímero de propileno/isobutileno, copolímero de propileno/butadieno, copolímero de propileno/cicloolefina, terpolímeros de propileno com etileno e um dieno tal como hexadieno, diciclopentadieno ou etilideno-norborneno; copolímeros de propileno/1-olefina onde a 1-olefina é gerada in situ; e copolímeros de propileno/monóxido de carbono.
Outros exemplos de componente a) são combinações de polipropileno com copolímeros de propileno/etileno, copolímeros de propileno/butileno, polietileno, por exemplo, HDPE ou LDPE; polibuteno, poliisobutileno, poli-4-metil penteno ou copolímeros de polialquileno/monóxido de carbono alternantes ou randômicos. Estas combinações podem conter pelo menos 50% em peso, em relação ao peso da combinação total, de polipropileno.
Componente b) é preferivelmente 0,0001 a 5%, por exemplo,
0,001 a 5%, 0,001 a 2%, 0,005 a 1%, 0,01 a 1% ou 0,01 a 0,05%, em relação ao peso de componente a), de um ou mais compostos da fórmula (I), (II) ou (III).
Ainda uma realização preferida da presente invenção refere-se a uma composição contendo como componente adicional c-1) por exemplo, 0,001 a 5%, preferivelmente 0,001 a 5%, preferivelmente 0,01 a 5%, em relação ao peso de componente a), de um ou mais agentes nucleantes convencionais.
Exemplos de agentes nucleantes convencionais são
1) sorbitol acetais aromáticos, por exemplo • 1,3:2,4-bis(benzilideno) sorbitol, comercialmente disponível como Irgaclear D (RTM), Millad 3905 (RTM) e Gel AII D (RTM).
• 1,3:2,4-bis(4-metil benzilideno) sorbitol, comercialmente disponível como Irgaclear DM (RTM), Millad 3940 (RTM), NC-6 (Mitsui (RTM)) e Gel AII MD (RTM).
• 1,3:2,4-bis(3,4-dimetil benzilideno) sorbitol, comercialmente disponível como Millad 3988 (RTM).
• 1,3:2,4-bis(4-etil benzilideno) sorbitol, comercialmente disponível como NC-4 (Mitsui (RTM))
2) Agentes nucleantes baseados em sais de ácido fosfórico, por exemplo • fosfato de 2,2'-metilen-bis-(4,6-di-t-butil fenila), comercialmente disponível como Adeka Stab NA11 (RTM) e Adeka Stab NA21 (RTM).
3) Agentes nucleantes baseados em sais de ácido carboxílico, por exemplo, benzoato de sódio.
4) Agentes nucleantes baseados em carbóxi hidróxido de alumínio, por exemplo, hidróxi-bis[4-(t-butil) benzoato] de alumínio, comercialmente disponível como Sandostab 4030 (RTM).
5) Agentes nucleantes baseados em sais de colofônica, respectivamente ácido abiético, por exemplo, . Pinecrystal KM-1300 (RTM) . Pinecrystal KM-1600 (RTM). ·
6) Outros agentes nucleantes, por exemplo, monoglicerolato de zinco (II) comercialmente disponível como Priferr 3888 (RTM) e Prifer 3881 (RTM).
7) sal dissódio de ácido cis-endo-biciclo(2.2.21) heptano-2,3dicarboxílico (=Chemical Abstracts Registry No. 351870-33-2), comercialmente disponível como Hyperform HPN-68 (RTM).
Uma outra realização da presente invenção refere-se a uma composição contendo
a) um polímero sintético cristalizável e
b) um agente nucleante, em particular um agente de redução de turvação;
caracterizada em que componente b) é capaz de prover a composição com o valor de turvação mais baixo possível, que é pelo menos 80% do valor de turvação original, preferivelmente 10 a 80% ou 10 a 50% ou 10 a 40% ou 20 a 80% ou 20 a 50% ou 20 a 40%, na faixa de concentração de 0,001 a 0,3%, preferivelmente 0,0025 a 0,15% ou 0,005 a 0,10% ou 0,0075 a 0,05% ou 0,01 a 0,02%, em relação ao peso de componente a); o valor de turvação original da composição é o valor de turvação obtido sem uso de componente b) e medido sobre placas de 1,0-1,2 mm de espessura.
Ainda uma realização da presente invenção é um processo para provimento de um polímero sintético com um valor de turvação que é menor que 62%; o valor de turvação sendo medido em uma placa de 1,0-1,2 mm de espessura; que compreende incorporação no polímero sintético de um ou mais compostos da fórmula (I), (II) ou (III) como definida acima.
Uma outra realização da presente invenção é o uso de um composto da fórmula (I), (II), ou (III) como agente de redução de turvação para um polímero sintético.
Aqui, um valor de turvação normalizado (TurvaçãonOrm) θ definido como indicado abaixo.
Turvação de uma composição da presente invenção
TurvaçãOnorm =- x 100%
Turvação da correspondente composição sem componente b
Exemplos de TurvaçãonOrm são 1 a 80%, 2 a 80%, 4 a 80%, 10 a
80%, 1 a 70%, 2 a 70%, 4 a 70%, 10 a 70%, 1 a 60%, 2 a 60%, 4 a 60%, 10 a 60%, 1 a 50%, 2 a 50%, 4 a 50%, 10 a 50%, 1 a 40%, 2 a 40%, 4 a 40%, 10 a 40%, 1 a 30%, 2 a 30%, 4 a 30%, 10 a 30%,
TurvaçãOnorm θ preferivelmente 5 a 30%. De particular interesse é uma TurvaçãOnorm de 10 a 20%.
Ainda uma realização da presente invenção refere-se a um processo para aumento de temperatura de cristalização de um polímero sintético, que compreende incorporação no polímero sintético de um ou mais compostos da fórmula (I), (II) ou (III) como definidos acima. A temperatura de cristalização pode ser aumentada, por exemplo, por mais de 3°C, em particular mais que 5°C. Um aumento na temperatura de cristalização de 4 a 40°C, por exemplo, 4 a 25°C ou 4 a 20°C, em particular 10 a 25°C é especialmente preferido.
Uma outra realização da presente invenção é o uso de um composto da fórmula (I), (II) ou (III) como agente nucleante para polímeros sintéticos.
As composições da presente invenção podem ser preparadas através de procedimentos padrões, bem conhecidos por aqueles versados na técnica, de composição, tal como mistura de componentes prescritos em um misturador convencional e fundindo e amassando a mistura com um extrusor de parafuso simples ou duplo, ou semelhante.
Os compostos da fórmula (I), (II) ou (III) podem ser adicionados ao polímero sintético através do uso de qualquer tecnologia conhecida na técnica, por exemplo, na forma de um pulverizado, grânulos, concentrados, revestimentos de spray ou bateladas mestres, que contêm estes compostos em uma concentração de, por exemplo, 1 a 50%, em particular 1 a 10% em peso, tanto em forma pura como junto com outros co-aditivos e opcionalmente apropriados materiais carreadores de acordo com tecnologias estabelecidas e bem conhecidas.
Adicionais materiais opcionalmente podem ser adicionados às composições da presente invenção em uma faixa de concentração que não afeta adversamente os efeitos benéficos da invenção. Estes materiais podem incluir estabilizadores, antioxidantes, agentes antibacteriais, absorvedo26 res de ultravioleta, termoestabilizadores, foto-estabilizadores, neutralizadores, agentes antiestáticos, agentes anti-bloqueio, agentes de inativação de metal pesado, retardadores de chama, lubrificantes, peróxidos, hidrotalcita, agentes espumantes, elastômeros, auxiliares de processamento, agentes nucleantes adicionais, e semelhantes e suas misturas.
Exemplos mais detalhados destes aditivos convencionais são listados abaixo.
1. Antioxidantes
1.1. Mono fenóis alquilados, por exemplo, 2,6-di-t-butil-4-metil 10 fenol, 2-t-butil-4,6-dimetil fenol, 2,6-di-t-butil-4-etil fenol, 2,6-di-t-butil-4-n-butil fenol, 2,6-di-t-butil-4-isobutil fenol, 2.6-diciclopentil-4-metil fenol, 2-(alfa metilciclohexil)-4,6-dimetil fenol, 2,6-diocta decil-4-metil fenol, 2,4,6-triciclohexil fenol, 2,6-di-t-butil-4-metóxi metil fenol, nonil fenóis que são lineares ou ramificados nas cadeias laterais, por exemplo, 2,6-dinonil-4-metil fenol, 2,415 dimetil-6-(1'-metil undec-T-il) fenol, 2,4-dimetil-6-(1'-metil hepta dec-1-il) fenol, 2,4-dimetil-6-(T-metil tridec-Γ-ϋ) fenol e suas misturas.
1.2. Alquil tiometil fenóis. por exemplo, 2,4-dioctil tiometü-6-t-butil fenol, 2,4-dioctil tiometii-6-metil fenol, 2,4-dioctil tiometil-6-etil fenol, 2,6-didodecil tiometil-4-nonil fenol.
1,3. Hidroquinonas e hidroquinonas alquiladas, por exemplo, 2,6di-t-butil-4-metóxi fenol, 2,5-di-t-butil hidroquinona, 2,5-di-t-amil hidroquinona,
2,6-difenil-4-octa decilóxi fenol, 2,6-di-t-butil hidroquinona, 2,5-di-t-butil-4hidróxi anisol, 3,5-di-t-butil-4-hidróxi anisol, estearato de 3,5-di-t-butil-4hidróxi fenila, adipato de bis(3,5-di-t-butil-4-hidróxi fenila).
1,4. Tocoferóis, por exemplo, a-tocoferol, β-tocoferol, γ-tocoferol, δ-tocoferol e suas misturas (vitamina E).
1.5. Tiodifenil éteres hidroxilados. por exemplo, 2,2'-tiobis (6-tbutil-4-metil fenoi), 2,2'-tiobis(4-octil fenol), 4,4’-tiobis(6-t-butil-3-metil fenol), 4,4'-tiobis-(6-t-butil-2-metil fenol), 4,4'-tiobis-(3,6-dissec-amil fenol), dissulfeto de 4,4'-bis-(2,6-dimetil-4-hidróxi fenila).
1.6. Alquilideno bisfenóis, por exemplo, 2,2'-metileno bis-(6-tbutil-4-metil fenol), 2,2-metileno bis-(6-t-butil-4-etil fenol), 2,2-metileno bis[427 ?>£ metil-6-(alfa metilciclohexil) fenol], 2,2'-metileno bis(4-metil-6-ciclohexil fenol), 2,2'-metileno bis-(6-nonil-4-metil fenol), 2,2'-metileno bis-(4,6-di-t-butil fenol), 2,2'-etilideno bis-(4,6-di-t-butil fenol), 2,2'-etilideno bis-(6-t-butil-4-isobutil fenol), 2,2'-metileno bis[6-alfa metil benzil)-4-nonil fenol], 2,2'-metileno bis-[6-(alfa, alfa-dimetil benzil)-4-nonil fenol], 4,4'-metileno bis-(2,6-di-t-butil fenol), 4,4'-metileno bis-(6-t-butil-2-metil fenol), 1,1-bis-(5-t-butil-4-hidróxi-2metil fenil) butano, 2,6-bis-(3-t-butil-5-metil-2-hidróxi benzil)-4-metil fenol, 1,1,3-tris(5-t-butil-4-hidróxi-2-metil fenil)butano, 1,1 -bis-(5-t-butil-4-hidróxi-2metil fenil)-3-n-dodecil mercapto butano, bis-[3,3-bis(3'-t-butil-4'-hidróxi fenil) butirato de etileno glicol, bis-(3-t-butil-4-hidróxi-5-metil fenil) diciclopentadieno, tereftalato de bis[2-3'-t-butil-2'-hidróxi-5'-metil benzil)-6-t-butil-4-metil fenila], 1,1-bis-(3,5-dimetil-2-hidróxi fenil) butano, 2,2-bis-(3,5-di-t-butil-4-hidróxi fenil) propano, 2,2-bis-(5-t-butil-4-hidróxi-2-metil fenil)-4-n-dodecil mercapto butano, 1,1,5,5-tetra-(5-t-butil-4-hidróxi-2-metil fenil) pentano.
1.7. Compostos O-, N- e S-. por exemplo, 3,5,3',5'-tetra-t-butil4,4’-diidróxi dibenzil éter, mercapto acetato de octadecil-4-hidróxi-3,5-dimetil benzila, mercapto acetato de tridecil-4-hidróxi-3,5-di-t-butil benzila, tris-(3,5di-t-butil-4-hidróxi benzil) amina, ditio tereftalato de bis-(4-t-butil-3-hidróxi-2,6dimetil benzila), sulfeto de bis-(3,5-di-t-butil-4-hidróxi benzila), mercapto acetato de isooctil-3,5-di-t-butil-4-hidróxi benzila.
1.8. Malonatos hidróxi benzilados, por exemplo, malonato de dioctadecil-2,2-bis-(3,5-di-t-butil-2-hidróxi benzila), malonato de dioctadecil-2(3-t-butil-4-hidróxi-5-metil benzila), malonato de didodecil mercapto etil-2,2bis-(3,5-di-t-butil-4-hidróxi benzila), malonato de bis-[4-(1,1,3,3-tetrametil butil) fenil]-2,2-bis-(3,5-di-t-butil-4-hidróxi benzila).
1.9. Compostos hidróxi benzila aromáticos, por exemplo, 1,3,5tris-(3,5-di-t-butil-4-hidróxi benzil)-2,4,6-trimetil benzeno, 1,4-bis-(3,5-di-tbutil-4-hidróxi benzil)-2,3,5,6-tetrametil benzeno, 2,4,6-tris-(3,5-di-t-butil-4hidróxi benzil) fenol.
1.10. Compostos triazina, por exemplo, 2,4-bis-(octil mercapto)6-(3,5-di-t-butii-4-hidróxi anilino)-1,3,5-triazina, 2-octil mercapto-4,6-bis-(3,5di-t-butil-4-hidróxi anilino)-1,3,5-triazina, 2-octil mercapto-4,6-bis-(3,5-di-t28 butil-4-hidróxi fenóxi)-1,3,5-triazina, 2,4,6-tris-(3,5-di-t-butil-4-hidróxi fenóxi)1,2,3-triazina, isocianurato de 1,3,5-tris-(3,5-di-t-butil-4-hidróxi benzila), isocianurato de 1,3,5-tris-(4-t-butil-3-hidróxi-2,6-dimetil benzila), 2,4,6-tris-(3,5di-t-butil-4-hidroxifeniletil)-1,3,5-triazina, 1,3,5-tris-(3,5-di-t-butil-4-hidróxi fenil propionil) hexidro-1,3,5-triazina, isocianurato de 1,3,5-tris-(3,5-diciclohexil-4hidróxi benzila).
1.11. Benzil fosfonatos, por exemplo, 2,5-di-t-butil-4-hidróxi benzil fosfonato de dimetila, 3,5-di-t-butil-4-hidróxi benzil fosfonato de dietila,
3,5-di-t-butil-4-hidróxi benzil fosfonato de dioctadecila, 5-t-butil-4-hidróxi-3metil benzil fosfonato de dioctadecila, o sal de cálcio do mono etil éster de ácido 3,5-di-t-butil-4-hidróxi benzil fosfônico.
1.12. Acilamino fenóis, por exemplo, 4-hidróxi lauranilida, 4hidróxi estearanilida, N-(3,5-di-t-butil-4-hidróxi fenil) carbamato de octila.
1.13. Ésteres de ácido beta-(3,5-di-t-butil-4-hidróxi fenil) propiônico com álcoois mono- ou poliídricos, por exemplo, com metanol, etanol, noctanol, i-octanol, octadecanol, 1,6-hexanodiol, 1,9-nonanodiol, etileno glicol, 1,2-propanodiol, neopentil glicol, tiodietileno glicol, dietileno glicol, trietileno glicol, pentaeritritol, isocianurato de tris-(hidróxi etila), N,N'-bis-(hidróxi etil) oxamida, 3-tiaundecanol, 3-tiapentadecanol, trimetil hexanodiol, trimetilol propano, 4-hidróxi metil-1-fosfa-2,6,7-trioxa biciclo[2.2.2] octano.
1.14. Ésteres de ácido beta-(5-t-butil-4-hidróxi-3-metil fenil) propiônico com álcoois mono- ou poliídricos, por exemplo, com metanol, etanol, n-octanol, i-octanol, octadecanol, 1,6-hexanodiol, 1,9-nonanodiol, etileno glicol, 1,2-propanodiol, neopentil glicol, tiodietileno glicol, dietileno glicol, trietileno glicol, pentaeritritol, isocianurato de tris-(hidróxi etila), N,N'-bis-(hidróxi etil) oxamida, 3-tiaundecanol, 3-tiapentadecanol, trimetil hexanodiol, trimetilol propano, 4-hidróxi metil-1-fosfa-2,6,7-trioxa biciclo[2.2.] octano; 3,9-bis-[2-{3(3-t-butil-4-hidróxi-5-metil fenil) propionilóxi}-1,1-2,4,8,10-tetraoxa spiro[5.5] undecano.
1.15. Ésteres de ácido beta-(3.5-diciclohexil-4-hidróxi fenil) propiônico com álcoois mono- ou poliídricos, por exemplo, com metanol, etanol, octanol, 1,6-hexanodiol, 1,9-nonanodiol, etileno glicol, 1,2-propanodiol, neo29 pentil glicol, tiodietileno glicol, dietileno glicol, trietileno glicol, pentaeritritol, isocianurato de tris-(hidróxi etila), N,N'-bis-(hidróxi etil) oxamida, 3tiaundecanol, 3-tia pentadecanol, trimetil hexanodiol, trimetilol propano, 4hidróxi metil-1-fosfa-2,6,7-trioxa biciclo[2.2.2] octano.
1.16. Ésteres de ácido 3,5-di-t-butil-4-hidróxi fenil acético, com álcoois mono- ou poliídricos, por exemplo, com metanol, etanol, octanol, 1,6hexanodiol, 1,9-nonanodiol, etileno glicol, 1,2-propanodiol, neopentil glicol, tiodietileno glicol, dietileno glicol, trietileno glicol, pentaeritritol, isocianurato de tris-(hidróxi etila), N,N'-bis-(hidróxi etil) oxamida, 3-tiaundecanol, 3-tia pentadecanol, trimetil hexanodiol, trimetilol propano, 4-hidróxi metil-1-fosfa2,6,7-trioxa biciclo[2.2.2] octano.
1.17. Amidas de ácido beta-(3.5-di-t-butil-4-hidróxi fenil) propiôniço, por exemplo, N,N'-bis-(3,5-di-t-butil-4-hidróxi fenil propionil) hexa metileno diamida, N,N'-bis-(3,5-di-t-butil-4-hidróxi fenil propionil) trimetileno diamida, N,N'-bis-(3,5-di-t-butil-4-hidróxi fenil propionil) hidrazida, N,N'-bis-[2-(3[3,5-di-t-butil-4-hidróxi fenil] propionilóxi) etil] oxamida (Naugard XL-1, fornecido por Uniroyal).
1.18. Ácido ascórbico (vitamina C)
1.19. Antioxidantes amínicos, por exemplo, N,N'-diisopropil-pfenileno diamina, Ν,Ν'-dissec-butil-p-fenileno diamina, N,N'-bis-(1,4-dimetil pentil)-p-fenileno diamina, N,N'-bis-(1-etil-3-metil pentil)-p-fenileno diamina, N,N'-bis-(1-metil heptil)-p-fenileno diamina, Ν,Ν'-diciclohexil-p-fenileno diamina, N,N'-difenil-p-fenileno diamina, N,N'-bis-(2-naftil)-p-fenileno diamina, N-isopropil-N'-fenil-p-fenileno diamina, N-(1,3-dimetil butil)-N'-fenil-p-fenileno diamina, N-(1-metil heptil)-N'-fenil-p-fenileno diamina, N-ciclohexil-N'-fenil-pfenileno diamina, 4-(p-tolueno sulfamoil) difenil amina, N,N'-dimetil-N,N'-di-sbutil-p-fenileno diamina, difenil amina, N-alil difenil amina, 4-isopropóxi difenil amina, N-fenil-1-naftil amina, N-(4-t-octil fenii)-1 -naftil amina, N-fenil-2-naftil amina, difenil amina octilada, por exemplo, p,p'-di-t-octil difenil amina, 4-nbutilamino fenol, 4-butirilamino fenol, 4-nonanoilamino fenol, 4dodecanoilamino fenol, 4-octa decanoilamino fenol, bis-(4-metóxi fenil) amina, 2,6-di-t-butil-4-dimetilamino metil fenol, 2,4'-diamino difenil metano, 4,4'30 diamino difenil metano, N,N,N\N'-tetrametil-4,4'-diamino difenil metano, 1,2bis-[(2-metil fenil) amino] etano, 1,2-bis-(fenilamino) propano, (o-tolil) biguanida, bis-[4-(1',3'-dimetil butil) fenil] amina, N-fenil-1-naftil amina t-octilado, uma mistura de t-butil/t-octil difenil aminas mono- e dialquiladas, uma mistura de nonil difenil aminas mono- e dialquiladas, uma mistura de dodecil difenil aminas mono- e dialquiladas, uma mistura de isopropil/isoexil difenil aminas mono- e dialquiladas, uma mistura de t-butil difenil aminas mono- e dialquiladas, 2,3-diidro-3,3-dimetil-4H-1,4-benzotiazina, fenotiazina, uma mistura de t-butil/t-octil fenotiazinas mono- e dialquiladas, uma mistura de t-octil fenotiazinas mono- ou dialquiladas, N-alil fenotiazina, N,N,N',N'-tetrafenil-1,4diamino but-2-eno, N,N-bis-(2,2,6,6-tetrametil piperid-4-il hexa metileno diamina, sebacato de bis(2,2,6,6-tetrametil piperid-4-ila), 2,2,6,6-tetrametil piperidin-4-ona, 2,2,6,6-tetrametil piperidin-4-ol.
2. Absorvedores de UV e fotoestabilizadores
2.1. 2-(2'-hidróxi fenil) benzo triazóis, por exemplo, 2-(2'-hidróxi5'-metil fenil) benzo triazol, 2-(3',5'-di-t-butil-2,-hidróxi fenil) benzo triazol, 2(5'-t-butil-2'-hidróxi fenil) benzo triazol, 2-(2,-hidróxi-5,-(1,1,3,3-tetrametil butil) fenil) benzo triazol, 2-(3',5'-di-t-butil-2'-hidróxi fenil)-5-cloro benzo triazol, 2(Sq-butil^-hidróxi-õ-metil fenil)-5-cloro benzo triazol, 2-(3'-sec-butil-5'-tbutil-2'-hidróxi fenil) benzo triazol, 2-(2'-hidróxi-4'-octilóxi fenil) benzo triazol, 2-(3',5'-di-t-amil-2'-hidróxi fenil) benzo triazol, 2-(3',5'-bis-(alfa, alfa-dimetil benzil)-2'-hidróxi fenil) benzo triazol, 2-(3'-t-butil-2'-hidróxi-5'-(2-octilóxi carbonil etil) fenil)-5-cloro benzo triazol, 2-(3'-t-butil-5'-[2-(2-etil hexilóxi) carbonil etil]-2'-hidróxi fenil)-5-cloro benzo triazol, 2-(3'-t-butil-2'-hidróxi-5,-(2-metóxi carbonil etil) fenil)-5-cloro benzo triazol, 2-(3'-t-butil-2'-hidróxi-5'-(2-metóxi carbonil etil) fenil) benzo triazol, 2-(3'-t-butil-2'-hidróxi-5’-(2-octilóxi carbonil etil) fenil) benzotriazol, 2-(3'-t-butil-5'-[2-(2-etil hexilóxi) carbonil etil]-2’-hidróxi fenil) benzo triazol, 2-(3'-dodecil-2'-hidróxi-5'-metil fenil) benzo triazol, 2-(3'-tbutil-2'-hidróxi-5'-(2-isooctilóxi carbonil etil) fenil benzo triazol, 2,2-metileno bis [4-(1,1,3,3-tetrametil butil)-6-benzo triazol-2-il fenol]; o produto de transesterificação de 2-[3'-t-butil-5'-(2-metóxi carbonil etil)-2'-hidróxi fenil]-2H31 benzo triazol com polietileno glicol 300; [r-ch2ch2—C00-CH2CH2-9^ onde
R = 3'-t-butil-4,-hidróxi-5'-2H-benzotriazol-2-il fenila, 2-[2'-hidróxi-3'-(alfa, alfadimetil benzil)-5'-(1,1,3,3-tetrametil butil) fenil] benzo triazol; 2-[2'-hidróxi-3'(1,1,3,3-tetrametil butiI)-5'-(alfa, alfa-diemtil benzil) fenil] benzo triazol.
2.2. 2-hidróxi benzo fenonas. por exemplo, derivados 4-hidróxi, 4-metóxi, 4-octilóxi, 4-decilóxi, 4-dodecilóxi, 4-benzilóxi, 4,2’,4,-triidróxi e 2'hidróxi-4,4'-dimetóxi.
2.3. Ésteres de ácidos benzóicos substituídos e não-substituídos. por exemplo, salicilato de 4-t-butil fenila, salicilato de fenila, salicilato de octil fenila, dibenzoil resorcinol, bis-(4-t-butil benzoil) resorcinol, benzoil resorcinol, 3,5-di-t-butil-4-hidróxi benzoato de 2,4-di-t-butil fenila, 3,5-di-t-butil-4hidróxi benzoato de hexa decila, 3,5-di-t-butil-4-hidróxi benzoato de octa decila, 3,5-di-t-butil-4-hidróxi benzoato de 2-metil-4,6-di-t-butil fenila.
2.4. Acrilatos, por exemplo, alfa-ciano beta, beta-difenil acrilato de etila, alfa-ciano-beta, beta-difenil acrilato de isooctila, alfa-carbo metóxi cinamato de metila, alfa ciano beta-metil-p-metóxi cinamato de metila, alfa ciano beta metil-p-metóxi cinamato de butila, alfa carbo metóxi-p-metóxi cinamato de metila, e N-(beta-carbo metóxi-beta-ciano vinil)-2-metil indolina.
2.5. Compostos de níquel, por exemplo, complexos de níquel de 2,2'-tiobis[4-(1,1,3,3-tetrametil butil) fenol] tal como o complexo 1:1 ou 1:2, com ou sem adicionais ligantes como n-butil amina, trietanolamina ou Nciclohexil dietanol amina, dibutil ditio carbamato de níquel, sais de níquel dos mono alquil ésteres, por exemplo, o metil ou etil éster, de ácido 4-hidróxi-3,5di-t-butil benzil fosfônico, complexos de níquel de cetoximas, por exemplo, de 2-hidróxi-4-metil fenil undecil cetoxima, complexos de níquel de 1-fenil-4lauroil-5-hidróxi pirazol, com ou sem ligantes adicionais.
2.6. Aminas estereamente impedidas, por exemplo, sebacato de bis-(2,2,6,6-tetrametil-4-piperidila), succinato de bis-(2,2,6,6-tetrametil-4-piperidila), sebacato de bis-(1,2,2,6,6-pentametil-4-piperidila), sebacato de bis(1 -octilóxi-2,2,6,6-tetrametil-4-piperidila), n-butil-3,5-di-t-butil-4-hidróxi benzil malonato de bis-(1,2,2,6,6-pentametil-4-piperidila), o condensado de 1-(232 hidróxi etil)-2,2,6,6-tetrametil-4-hidróxi piperidina e ácido succínico, condensados lineares ou cíclicos de N,N'-bis-(2,2,6,6-tetrametil-4-piperidil) hexa metileno diamina e 4-t-octilamino-2,6-dicloro-1,3,5-triazina, nitrilo triacetato de de tris-(2,2,6,6-tetrametil-4-piperidila), 1,2,3,4-butano tetracarboxilato de tetrakis-(2,2,6,6-tetrametil-4-piperidila), 1,1'-(1,2-etanodiil)-bis-(3,3,5,5-tetrametil piperazinona), 4-benzoil-2,2,6,6-tetrametil piperidina, 4-estearilóxi-2,2,6,6tetrametil piperidina, malonato de bis-(1,2,2,6,6-pentametil piperidil)-2-n-butil2-(2-hidróxi-3,5-di-t-butil benzila), 3-n-octil-7,7,9,9-tetrametil-1,3,8-triaza spiro[4.5] decano-2,4-diona, sebacato de bis-(1-octilóxi-2,2,6,6-tetrametil piperidila), succinato de bis-(1-octilóxi-2,2,6,6-tetrametil piperidila), condensados lineares ou cíclicos de N,N'-bis-(2,2,6,6-tetrametil-4-piperidil) hexa metileno diamina e 4-morfolino-2,6-dicloro-1,3,5-triazina, o condensado de 2-cloro4.6- bis-(4-n-butilamino-2,2,6,6-tetrametil piperidil)-1,3,5-triazina e 1,2-bis-(3amino propilamino) etano, o condensado de 2-cloro-4,6-di-(4-n-butilamino1.2.2.6.6- pentametil piperidil)-1,3,5-triazina e 1,2-bis-(3-amino propilamino) etano, 8-acetil-3-dodecil-7,7,9,9-tetrametil-1,3,8-triaza spiro[4.5] decano-2,4diona, 3-dodecil-1-(2,2,6,6-tetrametil-4-piperidil) pirrolidino-2,5-diona, 3dodecil-1-(1,2,2,6,6-pentametil-4-piperidil) pirrolidino-2,5-diona, uma mistura de 4-hexa decilóxi- e 4-estearilóxi-2,2,6,6-tetrametil piperidina, um condensado de N,N'-bis-(2,2,6,6-tetrametil-4-piperidil) hexa metileno diamina e 4ciclohexilamino-2,6-dicloro-1,3,5-triazina, um condensado de 1,2-bis-(3amino propilamino) etano e 2,4,6-tricloro-1,35-triazina assim como 4butilamino-2,2,6,6-tetrametil piperidina (CAS Reg. No. {136504-96-6]); um condensado de 1,6-hexano diamina e 2,4,6-tricloro-1,3,5-triazina assim como Ν,Ν-dibutil amina e 4-butilamino-2,2,6,6-tetrametil piperidina (CAS Reg. No. [192268-64-7]); N-(2,2,6,6-tetrametil-4-piperidil)-n-dodecil succinimida, N-(1,2,2,6,6-pentametil-4-píperidil)-n-dodecil succinimida, 2-undecil-7,7,9,9tetrametil-1-oxa-3,8-diaza-4-oxo spiro[4,5] decano, um produto de reação de 7,7,9,9-tetrametil-2-cicloundecil-1-oxa-3,8-diaza-4-oxo spiro-[4,5] decano e epicloroidrina, 1,1 -bis-(1,2,2,6,6-pentametil-4-piperidilóxi carbonii)-2-(4metóxi fenil) eteno, N,N,-bis-formil-N,N,-bis-(2,2,6,6-tetrametil-4-piperidil) hexa metileno diamina, um diéster de ácido 4-metóxi metileno malônico com
Μ.Ρ
1.2.2.6.6- pentametil-4-hidróxi piperidina, poli[metil propil-3-óxi-4-(2,2,6,6tetrametil-4-piperidil)] siloxano, um produto de reação de copolímero de anidrido de ácido maléico-alfa olefina com 2,2,6,6-tetrametil-4-amino piperidina ou 1,2,2,6,6-pentametil-4-amino piperidina.
2.7. Oxamidas, por exemplo, 4,4'-dioctilóxi oxanilida, 2,2'-dietóxi oxanilida, 2,2'-dioctilóxi-5,5'-di-t-butoxanilida, 2,2'-didodecilóxi-5,5'-di-tbutoxanilida, 2-etóxi-2'-etiloxanilida, N,N'-bis-(3-dimetilamino propil) oxamida, 2-etóxi-5-t-butil-2'-etoxanilida e suas misturas com 2-etóxi-2'-etil-5,4’-di-tbutoxanilida, misturas de oxanilidas dissubstituídas com o- ou p-metóxi e misturas de oxanilidas dissubstituídas com o- e p-etóxi.
2.8. 2-(2-hidróxi fenil)-1.3.5-triazinas, por exemplo, 2,4,6-tris-(2hidróxi-4-octilóxi fenil)-1,3,5-triazina, 2-(2-hidróxi-4-octilóxi fenil)-4,6-bis-(2,4dimetil fenil)-1,3,5-triazina, 2-(2,4-diidróxi fenil)-4,6-bis-(2,4-dimetil fenil-1,3,5triazina, 2,4-bis-(2-hidróxi-4-propilóxi fenil)-6-(2,4-dimetil fenil)-1,3,5-triazina,
2-(2-hidróxi-4-octilóxi fenil)-4,6-bis-(4-metil fenil)-1,3,5-triazina, 2-(2-hidróxi-4dodecilóxi fenil)-4,6-bis-(2,4-dimetil fenil)-1,3,5-triazina, 2-(2-hidróxi-4tridecilóxi fenil)-4,6-bis-(2,.4-dimetilfenil)-1,3,5-triazina, 2-[2-hidróxi-4-(2hidróxi-3-butilóxi propóxi) fenil]-4,6-bis-(2,4-dimetil)-1,3,5-triazina, 2-[2hidróxi-4—(2-hidróxi-3-octilóxi propilóxi) fenil]-4,6-bis-(2,4-dimetil)-1,3,520 triazina, 2-[4-(dodecilóxi/tridecilóxi-2-hidróxi propóxi)-2-hidróxi fenil]-4,6-bis(2,4-dimetil fenil)-1,3,5-triazina, 2-[2-hidróxi -4-(2-hidróxi-3-dodecilóxi propóxi) fenil]-4,6-bis-(2,4-dimetil fenil)-1,3,5-triazina, 2-(2-hidróxi-4-hexilóxi) fenil4.6- difenil-1,3,5-triazina, 2-(2-hidróxi-4-metóxi fenil)-4,6-difenil-1,3,5-triazina,
2.4.6- tris-[2-hidróxi-4-(3-butóxi-2-hidróxi propóxi) fenil]-1,3,5-triazina, 2-(225 hidróxi fenil)-4-(4-metóxi fenii)-6-fenil-1,3,5-triazina, 2-{2-hidróxi-4-[3-(2-etil hexil-1-óxi)-2-hidróxi propilóxi] fenil}-4,6-bis-(2,4-dimetil fenil)-1,3,5-triazina.
3. Desativadores de metais, por exemplo, Ν,Ν'-difenil oxamida,
N-salicilal-N-saliciloil hidrazina, N,N'-bis-(saliciloil) hidrazina, N,N'-bis-(3,5-dit-butil-4-hidróxi fenil propionil) hidrazina, 3-saliciloilamino-1,2,4-triazol, bis30 (benzilideno) oxalil diidrazida, oxanilida, isoftaloil diidrazida, sebacoil bis-fenil hidrazida, Ν,Ν'-diacetil adipoil diidrazida, N,N'-bis-(saliciloil) oxalil diidrazida,
N,N-bis-(saliciloil) tiopropionil diidrazida.
4. Fosfitos e fosfonitos, por exemplo, fosfito de trifenila, fosfitos de difenil alquila, fosfitos de fenil dialquila, fosfito de tris(nonil fenila), fosfito de trilaurila, fosfito de triocta decila, difosfito de diestearil pentaeritritol, fosfito de tris-(2,4-di-t-butil fenila), difosfito de diisodecil pentaeritritol, difosfito de bis-(2,4-di-t-butil fenil) pentaeritritol, difosfito de bis-(2,4-di-cumil fenil) pentaeritritol, difosfito de bis-(2,6-di-t-butil-4-metil fenil) pentaeritritol, difosfito de diisodecilóxi pentaeritritol, difosfito de bis-(2,4-di-t-butil-6-metil fenil) pentaeritritol, difosfito de bis-(2,4,6-tris-(t-butil fenil) pentaeritritol, trifosfitos de trestearil sorbitol, difosfonito de tetrakis-(2,4-di-t-butil fenil)-4,4'-bifenileno, 610 isooctilóxi-2,4,8,10-tetra-t-butil-12H-dibenz[d,g]-1,3,2-dioxafosfocina, fosfito de bis-(2,4-di-t-butil-6-metil fenil) metila, fosfito de bis-(2,4-di-t-butiI-6-metil fenil) etila, 6-flúor-2,4,8,10-tetrat-butil-12-metil dibenz[d,g]-1,3,2-dioxafosfocina, fosfito de 2,2',2-ηΙΙπΙο-Ρ:ΓΐβίΙΙ tris-(3,3',5,5'-tetrat-butil-1,1 '-bifenil-2,2'diila), fosfito de 2-etil hexil-(3,3,5,5'-tetrat-butil-1,r-bifenil-2,2'-diila), 5-butil-515 eti 1-2-(2,4,6-tri-t-butil fenóxi)-1,3,2-dioxafosfirano.
Os seguintes fosfitos são especialmente preferidos:
Fosfito de tris-(2,4-di-t-butil fenila) (Irgafos 168, Ciba-Geigy), fosfito de tris(nonil fenila),
(CH3)3C
(C)
ΜΜ
C(CH3)3 (D) h3c
3'3 (CH3)3C chq (E)
C(CH3): p—\ /—É (F) H37C1-J O P y f θ θ18^37 0-^ V_o
(G)
5. Hidroxilaminas. por exemplo, Ν,Ν-dibenzil hidroxilamina, N,Ndietil hidroxilamina, Ν,Ν-dioctil hidroxilamina, Ν,Ν-dilauril hidroxilamina, N,Nditetradeci I hidroxilamina, N,N-di-hexa decil hidroxilamina, Ν,Ν-diocta decil hidroxilamina, N-hexa decil-N-octa decil hidroxilamina, N-hepta decil-N-octa decil hidroxilamina, Ν,Ν-dialquil hidroximamina derivada de amina de sebo hidrogenada.
6. Nitronas, por exemplo, N-benzil alfa fenil nitrona, N-etil alfa metil nitrona, N-octilalfa heptil nitrona, N-lauril alfa undecil nitrona, Ntetradecil alfa tridecil nitrona, N-hexa decil alfa pentadecil nitrona, N-octa de10 cil alfa hepta decil nitrona, N-hexa decil alfa hepta decil nitrona, N-octa decil alfa pentadecinl nitrona, N-hepta decil alfa hepta decil nitrona, N-octa decil alfa hexa decil nitrona, nitrona derivada de Ν,Ν-dialquil hidroxilamina derivada de amina de sebo hidrogenada.
7. Tiosinergísticos, por exemplo, tiodipropionato de dilaurila ou tiodipropionato de diestearila.
8. Limpadores de peróxido, por exemplo, ésteres de ácido beta tio dipropiônico, por exemplo, o lauril, estearil, miristil ou tridecil ésteres, mercapto benzimidazol ou o sal de zinco de 2-mercapto benzimidazol, dibutil ditio carbamato de zinco, dissulfeto de diocta decila, tetrakis-(beta dodecil mercapto) propionato de pentaeritritol.
9. Estabilizadores de poliamida. por exemplo, sais de cobre em combinação com iodetos e/ou compostos de fósforo e sais de manganês divalentes.
10. Co-estabilizadores básicos, por exemplo, melamina, poli vinil pirrolidona, dician diamida, cianurato de trialila, derivados de uréia, derivados de hidrazina, aminas, poliamidas, poliuretanos, sais de metais alcalinos, e sais de metais alcalinos terrosos de ácidos graxos superiores, por exemplo, estearato de cálcio, estearato de zinco, behenato de magnésio, estearato de magnésio, ricinoleato de sódio, e palmitato de potássio, pirocatecolato de antimônio ou pirocatecolato de zinco.
11. Agentes nucleantes convencionais, por exemplo, substâncias inorgânicas, tais como talcum, óxidos de metais, como dióxido de titânio ou óxido de magnésio, fosfatos, carbonatos ou sulfatos de, preferivelmente, metais alcalinos terrosos; compostos orgânicos, como ácidos mono- ou policarboxílicos e seus sais, por exemplo, ácido 4-t-butil benzóico, ácido adípico, ácido difenil acético, succinato de sódio ou benzoato de sódio; compostos poliméricos, tais como copolímeros iônicos (ionômeros). Especialmente preferidos são 1,3:2,4-bis-(3',4'-dimetil benzilideno) sorbitol, 1,3:2,4-di-(para metil dibenzilideno) sorbitol, e 1,3:2,4-di(benzilideno) sorbitol.
12. Outros aditivos, por exemplo, plastificantes, lubrificantes, aditivos de reologia, catalisadores, agentes de controle de fluxo, abrilhantadores óticos, agentes à provba de chamas, agentes antiestáticos e agentes de sopro.
13. Benzofuranonas e indolinonas, por exemplo, aquelas mostradas em US-A-4 325 863; US-A-4 338 244; US-A-5 175 312; US-A-5 216 052; US-A-5 252 643; DE-A-4316611; DE-A-4316622; DE-A-4316876; EP-A0589839 ou EP-A-0591102 ou 3-[4-(2-acetóxi etóxi) fenil]-5,7-di-t-butil benzo furan-2-ona, 5,7-di-t-butil-3-[4-(2-estearoilóxi etóxi) fenil] benzo furan-2-ona, 3,3'-bis-[5,7-di-t-butil-3-(4-[2-hidróxi etóxi] fenil) benzo furan-2-ona], 5,7-di-t37
butil-3-(4-etóxi fenil) benzo furan-2-ona, 3-(4-acetóxi-3,5-dimetil fenil)-5,7-dit-butil benzo furan-2-ona, 3-(3,5-dimetil-4-pivaloilóxi fenil)-5,7-di-t-butil benzo furan-2-ona, 3-(3,4-dimetil fenil)-5,7-di-t-butil benzo furan-2-ona, 3-(2,3dimetil fenil)-5,7-di-t-butil benzo furan-2-ona.
A razão em peso do componente b) descrito acima para o aditivo convencional é preferivelmente 1:100 a 100:1, por exemplo, 1:90 a 90:1, 1:80 a 80:1, 1:70 a 70:1, 1:60 a 60:1, 1:50 a 50:1, 1:40 a 40:1, 1:30 a 30:1, 1:20 a 20:1, 1:10 a 10:1, 1:5 a 5:1, 1:4 a 4:1, 1:3 a 3:1, 1:1 a 2:1 ou 1:1.
Uma realização preferida da invenção refere-se a uma composição contendo como componente adicional c-2) um ou mais compostos amina estereamente impedida.
Exemplos preferidos destes compostos amina estereamente impedida são aqueles listados acima sob o item 2.6. O uso combinado de componentes b) e c-2) pode mesmo conduzir a um efeito sinergístico em ainda redução de turvação de um polímero sintético cristalizável. Componente c-2) é preferivelmente usado em uma quantidade de 5-70%, mais preferivelmente 10-30% e mais preferivelmente 15-25%, em relação ao peso de componente b).
Uma outra realização preferida da presente invenção refere-se a uma composição contendo como componente adicional c-3) um ou mais lubrificantes.
Componente c-3) é preferivelmente pleo menos um lubrificante selecionado do grupo consistindo em ceras sintéticas ou naturais e amidas de ácidos graxos. Uma definição compreensiva e revisão sobre ceras é dada, por exemplo, em Ullmann's Encyclopedia Of Industrial Chemistry, Vol. A28, VCH Verlagsgesellschaft mbH, D-69451 Weinheim, 1996 (em particular, ver páginas 104 ff. Ali), que é aqui incorporada por referência.
Preferivelmente apropriadas são ceras sintéticas, mais preferivelmente ceras inteiramente sintéticas de baixa polaridade. São exemplos ceras Fischer-Tropssch, ceras de polietileno de alta pressão, ceras de polietileno Ziegler-Natta, ceras de polietileno metaloceno e ceras de polipropileno de Ziegler-Natta.
Μϊ
Uma cera Fischer-Tropsch comercialmente disponível mais apropriada é, por exmeplo, AdSperse 868 (RTM), disponível de SASOL (RTM), Republic of South África. Exemplos de ceras Ziegler-Natta mais apropriadas são Licowax PE 520 (RTM) e Licowax PP 230 (RTM) comercialmente disponíveis de Clariant GmbH, Germany.
Ceras de poliolefina mais apropriadas preferivelmente t~em um peso molecular Mw de mais que 800 g/mol e menos que 20 000 g/mol.
Exemplos de ceras naturais apropriadas são ésteres refinados de cera montan e ceras de parafina descoloridas.
Exemplos de amidas de ácido graxo são estearamida, erucamida e oleamida que são comercialmente disponíveis como Atmer SA 1750 (RTM), Atmer SA 1753 (RTM), respectivamente Atmer SA 1756 (RTM), Atmer SA 1758 (RTM) e Atmer SA 1759 (RTM).
Componente c-3) é em particular pelo menos um lubrificante selecionado do grupo consistindo em cera Fischer-Tropsch, cera de polietileno de alta pressão, cera de polietileno de Ziegler-Natta, cera de polietileno metaloceno, cera de polipropileno de Ziegler-Natta, ceras naturais e amidas de ácidos graxos.
A combinação de componente |b) e componente c-3) também pode mostrar um efeito sinergístico na redução de turvação de um polímero sintético cristalizável. O componente c-3) está preferivelmente presente em uma quantidade de 0,01-5%, mais preferivelmente 0,1-1%, mais preferível 0,2-0,7%, em relação ao peso de componente a).
Exemplos de processamento das composições de acordo com a presente invenção são: moldagem de sopro de injeção, extrusão, moldagem de sopro, roto-moldagem, em decoração de molde (contra-injeção), moldagem de lama, moldagem de injeção, moldagem de co-injeção, formação, moldagem de compressão, prensagem, extrusão de filme (filme de fusão; filme soprado), fiação de fibra (tecida, não-tecida), estiramento (uniaxial, biaxial), recozimento, estiramento profundo, calandragem, transformação mecânica, sinterização, co-extrusão, revestimento, laminação, reticulação (radiação, peróxido, silano), deposição de vapor, soldagem, cola, vulcanização, termoformação, extrusão de tubo, extrusão de perfil, extrusão de folha; moldagem de folha, revestimento de rotação, strapping, formação de espuma, reciclagem/re-trabalho, revestimentos de extrusão, visbreaking (peróxido, térmico), sopro de fusão de fibra, ligado por fiação, tratamento de superfície (descarga corona, chama, plasma), esterilização (por raios gama, feixes de elétrons), revestimento com gel, extrusão de fita, processo SMC ou plastisol.
As composições de acordo com a presente invenção podem ser vantajosamente usadas para a preparação de vários artigos conformados. Exemplos são:
1-1) Dispositivos de flutuação, aplicações marinhas, pontões, bóias, madeira de construção plástica para deques, píers, barcos, caiaques, remos, e reforços de prais.
I-2) Aplicações automotivas, em particular pára-choques, painéis de instrumentos, bateria, forros traseiros e frontais, partes de moldagem sob a capota, estante de chapéu, forros de caminhão, forros de interior, coberturas de bolsas de ar, moldagens eletrônicas para adaptações (luzes), vidraças para painéis, vidro de farol, painel de instrumentos, forros exteriores, estofamento, luzes automotivas, faróis, luzes de estacionamento, luzes traseiras; forro de assento, painéis exteriores, isolamento de fio, extrusão de perfil para selagem, revestimento, coberturas de pilar, partes de chassis, sistemas de exaustão, filtro/enchedor de combustível, bombas de combustível, tanque de combustível, moldagens de lado de corpo, capotas conversíveis, espelhos exteriores, antena exterior, fixadores/fixações, módulo de extremidade frontal, vidro, articulações, sistemas de fecho, estantes de lagagem/teto, partes prensadas/seladas, selos, proteção lateral de impacto, amortecedor/isolante de som, e teto solar.
I-3) Dispositivos de tráfego de estrada, em particular sinais de postes, postes para marcação de estrada, acessórios de carros, triângulos de aviso, estojos médicos, capacetes, pneus.
I-4) Dispositivos para avião, trem, carros a motor (carro, motocicleta) incluindo enfeites.
I-5) Dispositivos para aplicações espaciais, em particular fogue40 tes e satélites, por exemplo, escudos de reentrada.
I- 6) Dispositivos para arquitetura e desenho, aplicações em minas, sistemas de tratamento acústico, refúgios de rua, e abrigos.
II- 1) Aparelhos, estojos, e coberturas em geral e dispositivos elé5 tricos/eletrônicos (computador pessoal, telefone, fone portátil, impressora, aparelhos de televisão, dispositivos de áudio e vídeo), vasos de flores, antenas de TV a satélite, e dispositivos de painel.
II-2) Encamisamento para outros materiais como aço ou têxteis.
II-3) Dispositivos para a indústria eletrônica, em particular isola10 mento de plugs, especialmente plugs de computadores, estojos para partes elétricas e eletrônicas, painéis impressos, e materiais para estocagem de dados eletrônicos tais como chips, cartões de cheque ou cartões de crédito.
II-4) Aparelhos elétricos, em particular máquinas de lavar, amassadoras, fornos (forno de microondas), lavadoras de pratos, misturadores e ferros.
II-5) coberturas para luzes (por exemplo, luzes de rua, abajures). II-6) aplicações em fio e cabo (semi-condutor, isolamento e encamisamento de cabo).
II- 7) Folhas para condensadores, refrigeradores, dispositivos a20 quecedors, condicionadores de ar, encapsulaçãop de eletrônicos, semicondutores, máquinas de café e limpadores à vácuo.
III- 1) Artigos técnicos como roda dentada (engrenagem), adaptações de lâminas, espaçadores, parafusos, cavilhas, pegadores e maçanetas.
III-2) Lâminas de rotor, ventiladores e paletas de monho de ven25 to, dispositivos solares, piscinas de natação, coberturas de piscina de natação, forros de piscinas, forros de tanque, closets, armários, paredes divisórias, paredes de persianas, paredes dobráveis, tetos, persiana de enrolar, adaptações, conexões entre tubos, luvas, e correias transportadoras.
III-3) Artigos sanitários, em particular cubículos de chuveiro, as30 sentos lavatórios, tampas e pias.
III-4) Artigos sanitários, em particular fraldas (bebês, incontinência adulta), artigos de higiene feminina, curtinas de chuveiro, escovas, estei41 ras, banhieras, móveis de toilet, escovas de dentes, e bed pans.
III-5) Tubulações reticuladas ou não) para água, água de despejo, e compostos químicos, tubulações para proteção de fios e cabos, tubulações para gás, óleo e despejo, calhas, tubulações descendentes e sistemas de drenagem.
III-6) Perfis de qualquer geometria (vidraças de janela e parede lateral.
III-7) Substitutos de vidro, em particular placas extrudadas, acabamento brilhante para construções (monolítica, dupla ou multiparedes), avião, escolas, folhas extrudadas, filme de janela para acabamento brilhante de arquitetura, trem, transporte, artigos sanitários, e estufa.
III-8) Placas (paredes, painel de corte), revestimento - extrusão (papel fotográfico, tetrapack e revestimento de tubo), silos, substituto de madeira, tabuado plástico, compósitos de madeira, paredes, superfícies, mobília, folha decorativa, coberturas de piso (aplicações interiores e exteriores), pavimento, assoalhos engradados de trincheiras, e telhas.
III-9) Distribuidores de entrada e saída.
III- 10) Aplicações e coberturas, parede lateral e revestimento de cimento, concreto, compósito, corrimões, superfícies de trabalho de cozinha, folhas de telhado, telhas e encerados.
IV- 1) Placas (paredes e painel de corte), bandejas, grama artificial, astroturf, cobertura artificial para anéis de estádios (atléticos), piso artificial para anéis de estádios (atléticos), e fitas.
IV-2) tecidos tecidos contínuos e comprimento padrão, fibras (carpetes/artigos higiênicos/geotêxteis/monofilamentos; filtros; esfregões/ cortinas (persianas)/aplicações médicas), fibras volumosas (aplicações tais como vstido/roupas de proteção), malhas, cordas, cabos, cordas, filamentos, correais - assento de segurança, roupas, roupas de baixo, luvas; botas; botas de borracha; vestuário íntimo; vestidos, roupas de banho, roupas de esportes, guarda-chuvas (pára-sol e filtro de sol), páraquedas, paraglides, velas, seda de balãom artigos de camping, tendas, camas de ar, camas de sol, bolsas volumosas e sacos.
IV-3) Membranas, isolamento, coberturas e selos para tetos, túneis, depósitos de lixo, pequenos lagos, membranas de cobertura de parede, geo-membranas, piscinas de natação, cortinas (persianas)/proteção solar, toldos, dosséis, papel de parede, embalagem de alimento e envoltório (flexí5 vel e sólido), embalagem médica (flexível e sólida), bolsas de ar/cintos de segurança e descanso de cabeça, carpetes, console de centro, painel de instrumentos, cabinas, porta, modulo de console acima da cabeça, enfeite de porta, forros de teto, iluminação interior, espelhos interiores, prateleira de embrulho, cobertura de bagagem traseira, assentos, coluna de direção, roda de direção, têxteis, e forro de baú.
V) Filmes (embalagem, despejo, laminação, agricultura e horticultura, estufa, cobertura de raiz de planta, túnel, silagem), envoltório de bala, sacos de despejo, papel de parede, filme de estirar, ráfia, filme de dessalinização, baterias e conectores.
VI-1) Embalagem de alimento e envoltório (flexível e sólido),
BOPP, BOPET, garrafas.
VI- 2) Sistemas de estocagem tais como caixas (engradados), bagageiro, cofres, caixas domésticas, paletes, prateleiras, pistas, caixas de parafusos, embalagns e latas.
VI-3) Cartuchos, seringas, aplicações médicas, recipientes para qualquer transporte, latas de lixo, e compartimentos de despejo, sacos de lixo, compartimentos, compartimentos de pó, forros de compartimento, recipientes em geral, tanques para água/água usada/química/gás/óleo/ gasolina/diesel; forros de tanque, caixas, engradados, caixa de bateria, cochos, dispositivos médicos como pistão, aplicações oftálmicas, dispositivos diagnósticos, e embalagem para bolhas farmacêuticas.
VII- 1) Revestimento de extrusão papel de fotografia, tetrapack, revestimento de tubo), artigos domésticos de qualquer tipo (por exemplo, aparelhos, garrafa térmica/cabide de roupas), sistemas de fixação como plugs, grampos de fio e cabo, zíper, fechos, fechaduras e fechaduras de estalo.
VII-2) Dispositivos de suporte, artigos para momentos de lazer como dispositivos de esportes e boa forma, esteiras de ginástica, botas de esqui, skate em linha, esquis, superfícies atléticas (por exemplo, pisos de tênis), tampas de aparafusar, tampas e rolhas para garrafas e latas.
VII-3) Mobília em geral, artigos espumados (estofamentos, absorvedores de impacto), espumas, esponjas, panos de prato, esteiras, cadeiras de jardim, assentos de estádio, mesas, sofás, brinquedos, kits de construção (painéis/figuras/bolas), teatros, escorregadores, e veículos de brinquedo.
VII-4) Materiais para estocagem de dados magnéticos e óticos.
VII-5) Utensílios de cozinha (comida, bebida, cozinhar, estocar).
VII-6) Caixas para CDs, cassetes e vídeoteipe; artigos eletrônicos de DVD, suprimentos de escritório de qualquer tipo (canetas de ponta de bola, estampas e almofadas de tinta, mouse, prateleiras, pistas), garrafas de qualquer volume e conteúdo (drinques, detergentes, cosméticos incluindo perfumes), e fitas adesivas.
VII-7) Artigos de pés (sapatos/solas de sapatos), palmilhas, polainas, adesivos, adesivos estruturais, caixas de alimentos (frutas, vegetais, carne, peixe), papel sintético, rótulos para garrafas, sofás, juntas artificiais (humanas), placas de impressão (flexográficas), painéis de circuito impresso, e tecnologias de mostradores.
VII-8) Dispositivos de polímeros enchidos(talco, greda, argila da China (caolin), wolastonita, pigmentos, negro de fumo, T1O2, mica, nanocompósitos, dolomita, silicatos, vidro, asbestos).
Assim, ainda uma realização da presente invenção refere-se a um artigo conformado, em particular uma fibra de filme, perfil, tubo, garrafa, tanque ou recipiente, obtenível a partir de uma composição como descrita acima.
Um artigo moldado é preferido. A moldagem é em particular efetuada por injeção, sopro, compressão, roto-moldagem, ou moldagem de lama ou extrusão.
Ainda uma realização da presente invenção refere-se a um filme orientado mono-axialmente ou um filme orientado bi-axialmente obtenível a partir de uma composição como descrita acima.
A presente invenção ainda refere-se a um sistema multicamadas
ÓÒ onde uma ou mais camadas contêm uma composição como descrita acima.
Alguns compostos das fórmulas (I), (II) e (III) são novos. Assim, a presente invenção também refere-se a um composto da fórmula (IA), (IIA) ou (IIIA).
(HA) (IIIA) onde R-ι, R2 e R3, ou Y1f Y2 e Y3, ou Z-ι, Z2 e Z3 independentemente um do outro são alquila Ci-2o ou alquila C3.2o substituído com um ou mais hidróxi;
alquenila C2.2o não-substituído ou substituído com um ou mais hidróxi;
alquila C2.2o interrompido por oxigênio ou enxofre;
cicloalquila C3-i2 não-substituído ou substituído com um ou mais alquila C1-20;
(cicloalquil C3.i2) alquila C-mo não-substituído ou substituído com um ou mais alquila Ci.2o:
bis-[cicloalquil C3-12] alquila C1-10 não-substituído ou substituído com um ou mais alquila C1.20;
um radical hidrocarboneto bicíclico ou tricíclico com 5 a 20 átomos de carbono não-substituído ou substituído com um ou mais alquila Ci_20;
fenila substituído com um ou mais radicais selecionados de alquila C1-20, alquilamino Ci_20, di(alquil C-|.2O) amino e hidróxi; com a condição de que 2,3-diidróxi fenila é renunciado; m-metóxi fenila;
fenil alquila Ci_2o não-substituído ou substituído por um ou mais radicais selecionados de alquila Ci.2O, cicloalquila C3-i2, fenila, alcóxi Ci-2o e hidróxi;
fenil etenila não-substituído ou substituído com um ou mais alquila Ci-20;
bifenil alquila C1-10 não-substituído ou substituído com um ou mais alquila Ci_2o!
naftila não-substituído ou substituído com um ou mais alquila C-i2θΐ naftil alquila C-|.2o não-substituído ou substituído com um ou mais alquila C1-20;
naftóxi metila n~]ao-substituído ou substituído com um ou mais alquila Ci_20;
bifenilenila, flourenila, antrila;
um radical hetero cíclico de 5 a 6 membros não-substituído ou substituído com um ou mais alquila C-i-2o;
um radical hidrocargboneto Cp2o contendo um ou mais halogênios; ou tri-(alquii Cmo) silil alquila C1-10; com a condição de que (1) R2, R3, Y1( Y2, Y3, Z-i, Z2 e Z3 independentemente uns dos outros são adicionalmente metila, etila ou 2,3-diidro fenila;
(2) pelo menos um dos radicais R-ι, R2 e R3, ou Y1, Y2 e Y3, ou
Zi,Z2eZ3é alquila C3-20 ramificado, não-substituído ou substituído com um ou mais hidróxi;
alquila C2-20 interrompido por oxigênio ou enxofre; cicloalquila C3-12 não-substituído ou substituído por um ou mais alquila C-i_2o;
(cicloalquil C3-12) alquila C1-10 não-substituído ou substituído com um ou mais alquila Ci-20;
um radical hidrocarboneto bicíclico ou tricílico com 5 a 20 átomos de carbono não-substituído ou substituído com um ou mais alquila Ci.2o;
fenila não-substituído ou substituído com um ou mais radicais selecionados de alquila C-|.2o, alcóxi C-i-2o, alquilamino C-|.2o, di(alquil C-|.2o) amino, hidróxi e nitro;
fenil alquila C1-20 não-substituído ou substituído com um ou mais radicais selecionados de alquila Ci-20, cicloalquila C3.i2, fenila, alcóxi C1.20 e hidróxi;
bifenil alquila C-mo não-substituído ou substituído com um ou mais alquila Ci.2O;
naftil alquila C-i_20 não-substituído ou substituído com um ou mais alquila C-j_20; ou tri-(alquil Cmq) silil alquila C1-10; e (3) 0 composto N-t-butil-3,5-bis-(pivaloilamino)benzamida é renunciado.
Compostos preferidos da presente invenção são aqueles onde pelo menos um dos radicais R1f R2 e R3, ou Y-ι, Y2 e Y3, ou ZpZ2eZ3é alquila C3_20 ramificado, ou cicloalquila C3-12 não-substituído ou substituído co m um ou mais alquila C-|.2O.
Os compostos descritos nos exemplos de trabalho são de particular interesse.
Os particulares usos e preferências descritas acima para os compostos das fórmulas (I), (II) e (III) também são aplicáveis aos compostos das fórmulas (ΙΑ), (IIA) e (IIIA).
Os compostos das fórmulas (I), (II), ou (III) podem ser preparados em analogia a processos conhecidos como mostrado nos exemplos de trabalho que se seguem. Os compostos também podem ser preparados por exemplo, sem o uso de qualquer solvente. À menos que de outro modo indicado, anteriormente e a seguir, todas as partes e porcentagens são em peso e todas as temperaturas são dadas em gruas Celsius (°C). Trabalho usual significa: adição a água, filtração de precipitado, extração com solvente orgânico e/ou purificação de produto por cristalização e/ou cromatografia e/ou sublimação.
Um exemplo genérico da preparação dos compostos da fórmula (I)
Os coimpostos da fórmula (I) podem ser sintetizados, por exemplo, por hidrogenação de 1,3,5-trinitro benzeno, 3,5-dinitro anilina ou 1,3diamino-5-nitrobenzeno com hidrogênio e um apropriado catalisador metal em um apropriado solvente orgânico. O 1,3,5-triamino benzeno assim obtido pode ser isolado ou opcionalmente transferido no correspondente cloridrato e pode ser purificado em ambas as formas por recristalização a partir de um solvente apropriado. É também possível usar a solução da triamina bruta ou a triamina bruta isolada (com ou sem remoção da água formada na hidrogenação) para a subseqüente reação de acilação. Possíveis catalisadores são, por exemplo, Pd, PtO2, níquel Raney, etc., preferivelmente as versões comercialmente disponíveis sobre suporte de carbono. A hidrogenação pode ser realizada sob pressão normal ou sob pressão em temperaturas entre 20 e 120°C (Verificações de segurança são altamente recomendadas antes de aumentar a escala). Apropriados solventes para a hidrogenação são, por exmeplo, tetraidrofurano (THF), THF/metanol, dimetil formamida (DMF) ou N-metil pirrolidinona (NMP). Um procedimento alternativo é redução com níquel Raney e hidrazina como fonte de hidrogênio (ver, por exemplo, Organikum, chapter 8.1, Reduktion von Nitroverbindungen und Nitrosoverbindubg, Berlin, 1970) ou outras reduções padrões conhecidas. Recristalização pode ser realizada, por exemplo, com metanol, etanol, ou outros álcoois. A amina livre (ou a amina obtida do cloridrato e uma base apropriada) pode ser achada com uma quantidade estequiométrica ou um excesso do correspondente cloreto ácido, preferivelmente na presença de uma base orgânica ou inorgânica não-interagindo, por exemplo, trietilamina, tributil amina, piridina; um outro processo usa uma quantidade estequiométrica ou um excesso do anidrido do ácido carboxílico como agente aci lante; neste caso nenhuma base é requerida. A reação é realizada na ausência ou preferivelmente na presença de um solvente. A temperatura de reação ideal depende da natureza dos agentes acilantes (por exemplo, o-100°C). Isolamento/purificação do produto final é realizado por precipitação/recristalização/lavagem com uma apropriada mistura de água/solvente orgânico ou solvente orgânico/solvente orgânico ou com um solvente puro, por exemplo, DMF/água, NMP/água, etanol, metanol, etc.
Exemplo A: Preparação de 1,3,5-tris-[ciclohexil carbonilamino]benzeno
1) Preparação de tris-cloridrato de 1,3,5-triamino benzeno:
16,85 g (0,092 moles) de 3,5-dinitro anilina são dissolvidos em uma mistura de 60 mL de metanol e 300 mL de tetraidrofurano. A mistura é colocada em um reator de vidro Buechi e 1,2 g de paládio 10% em peso sobre carvão ativado são adicionados. O reator é fechadoi e sob agitação 3 vezes purgado com nitrogênio e 3 vezes com hidrogênio. A hidratação é realizada a 40°C e uma pressão de hidrogênio de 4 bar por 24 horas. A mistura de reação é transferida sob atmosfera de gás inerte em um frasco e filtrada sobre 40 g de óxido de alumínio (Alox N) para remoção de carvão ativo, o catalisador e água. A solução levemente colorida é imediatamente convertida no tris-cloridrato através de adição de uma mistura de ácido clorídrico concentrado (100 mL) e metanol (200 mL). O produto precipitado é filtrado e lavado com metanol e secado para render um sólido branco a cinza claro.
Rendimento: 13,61 g (0,059 moles) = 64% de teoria.
1H-NMR (D2O): um singleto (3H) em 6,86 ppm.
2) Preparação de 1,3,5-tris[ciclohexil carbonilaminojbenzeno.
1,00 g (4,3 mmoles) de tris-cloridrato de 1,3,5-triamino benzeno e 0,1 g de LiCI seco são adiei onados sob atmosfera inerte a 50 mL de Nmetil pirrolidinona (NMP) e 10 mL de piridina anidra e resfriado para 5°C.
2,10 g (14,3 mmoles) de cloreto de ciclohexano carbonila são adicionados. A mistura de reação é aquecida a 60°C e agitada. Após 24 horas a mistura de reação é adicionada a 1000 mL de água gelada. O precipitado é filtrado. Trabalho usual (recristalização a partir de tolueno/n-hexano (mistura 1:1)) rende o desejado produto.
Rendimento: 1,33 g (2,93 mmoles) = 68,2% de teoria.
Ponto de fusão: 286°C EM (El): 453 (M+).
Exemplo B: Preparação de 1,3,5-tris-[2,2-dimetilpropionilamino]benzeno.
(= Composto I-2)
I) 1,00 g (4,3 mmoles) de tris-cloridrato de 1,3,5-triamino benzeno (Ver Exemplo A) e 0,1 g de LiCI são adicionados sob atmosfera inerte a 50 mL de NMP anidra e 10 mL de piridina anidra e resfriados para 5°C. 1,73 g (14,3 mmoles) de cloreto de pivaloíla são adicionados. A mistura de reação é aquecida a 60°C e agitada. Após 24 horas a mistura de reação é adicionada a 1000 mL de água gelada. O precipitado é filtrado. Trabalhos usual (recristalização a partir de tetraidrofurano) rende o desejado produto.
Rendimento: 0,64 g (1,70 mmoles) = 39,6% de teoria.
Ponto de fusão: nenhum ponto de fusão detectado, sublimação.
EM(EI): 375 (M+).
II) Um processo de preparação de 1,3,5-triamino benzeno:
g (0,0983 moles) de 3,5-dinitro anilina em 180 mL de tetraidrofurano são hidrogenados na presença de 1,8 g de Pd/C (10%) por 6 horas a 20-40°C sob pressão normal. Após separação do catalisador por filtração, o filtrado é concentrado e uma parte do produto precipitou da solução. O produto restante é isolado por destilação de solvente.
Rendimento toai: 10,77 g (= 89% de teoria).
Ponto de fusão: 117° (decomposição)
EM(CI): 124 (MH+).
III) Síntese direta do composto I-2 a partir de 1,3-diamino-5nitrobenzeno sem isolamento do intermediário trisamina:
g (0,12 moles) de 1,3-diamino-5-nitro benzeno e 500 mL de N-metilk pirrolidona (NMP) são hidrogenados a 25°C na presença de 2 g Pd/C (10%) por 5 horas em 1-2 bar em uma autoclave. Após adição de 35 mL de anidrido piválico e agitação por 10 horas a 100°C, o resíduo é filtrado e extraído (Soxhlet) com 300 mL de metanol por 20 horas. O extrato é resfriado para 25°C e o precipitado é filtrado e secado. O desejado produto é obtido como um pó incolor.
Rendimento: 4,9 g (= 50% de teoria).
1H-NMR e EM são idênticos com o produto descrito em I).
IV) Síntese direta do composto I-2 a partir de 1,3-diamino-5nitrobenzeno sem isolamento do intermediário trisamina.
g (0,12 moles) de 1,3-diamino-5-nitrobenzeno e 500 mL de Nmetil pirrolidona (NMP) são hidrogenados a 25°C na presença de 2 g Pd/C (10%) por 5 horas/1-2 bar em uma autoclave. Agora, 120 g de anidrido piválico são adicionados e a solução é agitada por 10 horas a 90°C. O catalisador é filtrado a 90°C. Então, a solução é resfriada para 10°C e o precipitado é filtrado. O precipitado é então lavado com 200 mL de metanol e secado para render 35 g (71,7%) de cristais quase brancos. Após recristalização a partir de DMF e DMF/água um pó branco é obtido.
Rendimento: 31,5 g (= 66,4% de teoria).
1H-NMR e EM são idênticos com o produto descrito em I).
V) Em uma maneira similar, composto I-2 também pode ser obtido por acilação de 1,3,5-triamino benzeno obtido por hidrogenação catalítica de 100,1 g (0,546 moles) de 3,5-dinitro anilina em 1 L de NMP com 5 g de Pt/C (10%) por 6 horas a 50°C, separação do catalisador (filtração) e subseqüente acilação com 615 mL (3,03 moles) de anidrido piválico como descrito em IV).
Rendimento: 91,5% de teoria.
1H-NMR e EM são idênticos com o produto descrito em I). Exemplo C: Preparação de 1,3,5-tris-[4-metil benzoilaminojbenzeno.
Composto I-3 é obtido como um pó quase branco em analogia ao Exemplo A a partir de 3,48 g (15,0 mmoles) de cloridrato de 1,3,5triamino benzeno, 8,34 g (54,0 mmoles) de cloreto de 4-metil benzoíla, 200 mL de NMP, 40 mL de trietil amina e 0,4 g de LiCI.
Rendimento: 1,92 g (= 26,8% de teoria).
Ponto de fusão: 278°C.
EM(EI): 477 (M+).
Exemplo D: Preparação de 1,3,5-tris-[3,4-dimetil benzoilaminojbenzeno.
Composto 1-4 é obtido como um pó incolor em analogia ao Exemplo A a partir de 1,23 g (10,09 mmoles) de cloridrato de 1,3,5-triamino benzeno, 6,07 g (36,0 mmoles) de cloreto de 3,4-dimetil benzoíla, 100 mL de NMP, 20 mL de trietilamina e 0,3 g de LiCI.
Rendimento: 2,55 g (=49,1 % de teoria).
Ponto de fusão: 304°C.
EM(EI): 519 (M+).
Exemplo E: Preparação de 1,3,5-tris-[3,5-dimetil benzoilaminojbenzeno.
Composto I-5 é obtido como um pó incolor em analogia ao E10 xemplo A a partir de 1,23 g (10,0 mmoles) de cloridrato de 1,3,5-triamino benzeno, 6,00 g (35,6 mmoles) de cloreto de 3,5-dimetil benzoíla, 100 mL de NMP, 20 mL de trietil amina e 0,3 g de LiCI. Rendimento: 2,00 g (= 38,5% de teoria).
Ponto de fusão: 282°C (polimorof, pico de endoterma mais alto). EM(EI): 519 (M+).
Exemplo F: Preparação de 1,3,5-tris-[ciclopentano carbonilaminojbenzeno.
Composto I-6 é obtido como um pó incolor em analogia ao Exemplo A a partir de 2,50 g (10,75 mmoles) de cloridrato de 1,3,5-triamino benzeno, 4,75 g (35,83 mmoles) de cioreto de ciclopentano carbonila, 70 mL de NMP, 15 mL de piridina e 0,3 g de LiCI.
Rendimento: 1,00 g (= 22,6% de teoria).
Ponto de fusão: 285°C.
EM(EI): 411(M+).
Exemplo G: Preparação de 1,3,5-tris-[1-adamantano carbonilaminojbenzeno.
Composto I-7 é obtido como um pó incolor em analogia ao Exemplo A a partir de 1,68 g (13,6 mmoles) de cloridrato de 1,3,5-triamino benzeno, 9,03 g (45,0 mmoles) de cloreto de 1-adamantano carbonila, 150 mL de NMP, 30 mL de piridina e 0,3 g de LiCI.
Rendimento: 6,75 g (= 81,4% de teoria).
Ponto de fusão: sublimação (nenhum ponto de fusão observado).
EM(EI): 609 (M+).
Exemplo H: Preparação de 1,3,5-tris-[2-metilpropionilamino]benzeno.
fc>
(= Composto I-8)
Composto I-8 é obtido como um pó quase branco em analogia ao Exemplo A a partir de 1,67 g (13,6 mmoles) de cloridrato de 1,3,5-triamino benzeno, 5,22 g (49,0 mmoles) de cloreto de ácido isobutírico, 150 mL de NMP, 30 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 0,95 g (= 20,9% de teoria).
Ponto de fusão: 290°C.
EM(EI): 333 (M+).
Exemplo I: Preparação de 1,3,5-tris-[3,3-dimetilbutirilamino]benzeno.
Composto I-9 é obtido como um pó quase branco em analogia ao exemplo A a partir de 4,65 g (20,0 mmoles) de cloridrato de 1,3,5-triamino benzeo, 9,42 g (70,0 mmoles) de cloreto de ácido 3,3-dimetil butírico, 250 mL de NMP, 50 mL de trietil amina e 0,5 g de LiCI.
Rendimento: 3,82 g (=45,7% de teoria).
Ponto de fusão: 316°C.
EM(EI): 417(M+).
Exemplo J: Preparação de 1,3,5-tris-[2-etilbutirilamino]benzeno.
Composto 1-10 é obtido como um pó quase branco em analogia ao Exmeplo A a partir de 4,65 g (20,0 mmoles) de cloridrato de 1,3,5triamino benzeno, 9,42 g (70,0 mmoles) de cloreto de ácido 2-etil butírico,
250 mL de NMP, 50 mL de trietilamina e 0,5 g de LiCI.
Rendimento: 4,04 g (=48,4% de teoria).
Ponto de fusão: 363°C (sob sublimação).
EM(EI): 417(M+).
Exemplo K: Preparação de 1,3,5-tris-[2,2-dimetilbutirilamino]benzeno.
Composto 1-11 é obtido como um produto sólido felpudo, incolor em analogia ao Exemplo A a partir de 1,23 g (10,0 mmoles) de 1,3,5-triamino benzeno, 4,84g (36,0 mmoles) de cloreto de ácido 2,2-dimetil butírico, 150 mL de NMP, 20 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 2,93 g (= 70,3% de teoria).
Ponto de fusão: 368°C (sob sublimação).
EM(EI): 417(M+).
Exemplo L: Preparação de 1,3,5-tris-[2-ciclohexilacetilamino]benzeno.
Composto 1-12 é obtido como um pulverizado incolor em analogia ao Exemplo A a partir de 1,23 g (10,0 mmoles) de 1,3,5-triamino benzeno, 5,78 g (36,0 mmoles) de cloreto de 2-ciclohexila, 100 mL de NMP, 20 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 3,42 g (= 69,1% de teoria).
Ponto de fusão: 204°C.
EM(EI): 495(M+).
Exemplo M: Preparação de 1,3,5-tris-[3-ciclohexilpropionilamino]benzeno.
Composto 1-13 é obtido como um pó incolor em analogia ao Exemplo A a partir de 1,17 g (9,5 mmoles) de 1,3,5-triamino benzeno, 5,0 g (28,0 mmoles) de cloreto de 3-ciclohexil propionila, 100 mL de NMP, 20 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 1,87 g (= 69,1% de teoria).
Ponto de fusão: 215°C.
EM(EI): 537 (M+).
Exemplo N: Prpearação de 1,3,5-tris-[4-ciclohexilbutirilamino]benzeno.
Composto 1-14 é obtido como um pó incolor em analogia ao E5 xemplo A a partir de 1,23 g (10 mmoles) de 1,3,5-triamino benzeno, 6,79 g (28,0 mmoles) de cloreto de 4-ciclohexil butirila, 100 mL de NMP, 20 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 2,30 g (= 40% de teoria).
Ponto de fusão:191°C.
EM(EI): 579 (M+).
Exemplo O: Preparação de 1,3,5-tris-[5-ciclohexilvaIeroilamino]benzeno.
H·
H (= Composto 1-14)
Composto 1-15 é obtido como um pó incolor em analogia ao Exemplo A a partir de 1,23 g (10 mmoles) de 1,3,5-triamino benzeno, 7,3 g (36,0 mmoles) de cloreto de 5-ciclohexil valeroíla, 100 mL de NMP, 20 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 1,40 g (= 23% de teoria).
Ponto de fusão: 141°C.
EM(EI): 621 (M+).
Exemplo P: Preparação de 1-isobutirilamino-3-5,-bis-[pivaloilamino]benzeno.
(= Composto 1-16)
a) N-isobutiril-3,5-dinitro anilina é obtida de 45,8 g (0,25 moles) de 3,5-dinitro anilina, 29,3 g (0,275 moles) de cloreto de isobutila, 98,9 g (1,25 moles) de piridina, 250 mL de NMP e 0,2 g de LiCI. A acilação é realizada como descrito no Exemplo A.
Rendimento: 62,0 g (= 98% de teoria).
Ponto de fusão: 168-170°C.
EM(CI): 254 (MH+).
b) 24,2 g (0,096 moles) do produto obtido sob a) são hidrogenados em 100 mL de NMP com 1g de Pd/C (10%) a 50°C em analogia ao Exemplo B-V. A solução é usada após separação do catalisador por filtração para a etapa seguinte sem isolamento do intermediário N-isobutiril-1,3,5triamino benzeno (100% de conversão de acordo com TLC (cromatografia de camada fina) : RF (N-isobutiril-1,3,5-triamino benzeno) = 0,05; RF (Nisobutiril-3,5-dinitro anilina) = 0,65; sílica gel, eluente: hexano/acetato de etila 1:1).
A esta solução 68,6 g (0,368 moles) de anidrido piválico são adicionados a 60°C e a mistura de reação é agitada por 1 hora a 60°C. Diluição com água precipitou o produto que é separado por filtração e lavado com
tolueno e hexano. O produto obtido é um pó quase branco.
Rendimento: 30,9 g (= 86% de teoria). Ponto de fusão: 370°C sob sublimação. EM(CI): 362(MH+).
Exemplo Q: Preparação de 2,2-dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno.
C(CH3)3
H (= Composto 1-17)
H
a) N-2,2-dimetil butiril-3,5-dinitro anilina é obtida de 45,8 g (0,25 moles) de 3,5-dinitro anilina, 37,0 g (0,275 moles) de cloreto de 2,2-dimetil butirila, 98,9 g (1,25 moles) de piridina, 250 mL de NMP e 0,25 g de LiCI. A acilação é realizada como descrito no Exemplo A.
Rendimento: 67,0 g (= 95% de teoria).
Ponto de fusão: 171-173°C.
EM(CI): 282(MH+).
b) 16,7 g (0,06 moles) do produto obtido sob a) são hidrogenados em 75 mL de NMP com 1 g de Pd/C (10%) a 90°C em analogia ao Exemplo B-V. A solução é usada após separação do catalisador por filtração para a etapa seguinte sem isolamento do intermediário N-(2,2-dimetil butiril)1,3,5-triamino benzeno (100% de conversão de acordo com TLC: RF (N-2,2dimetil butiril-1,3,5-triamino benzeno) = 0,13; RF (N-2,2-dimetil butiril-3,5dinitro anilina) = 0,83; sílica gel, eluente: hexano/acetato de etila 1:1). A esta solução 40,65 g (0,218 moles) de anidrido piválico são adicionados e a mistura de reação é agitada por 1 hora em 60°C. Após trabalho em analogia ao Exemplo P e recristalização de DMF o desejado produto é obtido como um um produto penugento incolor.
Rendimento: 14,7 g (= 63,8% de teoria).
Q&
Ponto de fusão: nenhum ponto de fusão detectado (sublimado).
EM(CI): 390 (MH+).
Exemplo_R: Preparação de 3,3-dimetilbutirilamino-3,5bis[pivaloilamino]benzeno.
(= Composto 1-18)
a) N-3,3-dimetil butiril-3,5-dinitro anilina é obtida de 45,8 g (0,25 moles) de 3,5-dinitro anilina, 37,0 g (0,275 moles) de cloreto de 3,3-dimetil butirila, 98,9 g (1,25 moles) de piridina, 250 mL de NMP e 0,25 g de LiCI. A acilação é realizada como descrito no Exemplo A.
Rendimento: 70 g (= 100% de teoria).
Ponto de fusão: 145°C.
EM(CI): 282 (MH+).
b) 16,7 g (0,059 moles) do composto obtido sob a) são hidrogenados em 75 mL de NMP com 1 g de Pd/C (10%) a 85°C em analogia ao Exemplo B-V. A solução é usada após separação do catalisador por filtração para a etapa seguinte sem isolamento do intermediário N-3,3-dimetil butiril1,3,5-triamino benzeno (100% de conversão de acordo com TLC: RF (N-3,3dimetil butiril-1,3,5-triamino benzeno) = 0,07; RF (N-3,3-dimetil butiril-3,5dinitro anilina) = 0,73; sílica gel, eluente: hexano/acetato de etila 1:1). A esta solução 40,65 g de anidrido piválico (0,218 moles) são adicionados e a mistura de reação é agitada por 3 horas a 60°C. Após trablaho em analogia ao Exemplo P, o desejado produto é obtido como um pó branco.
jRendimento: 16,0 g (= 69,5% de teoria).
Ponto de fusão: 368°C sob sublimação.
EM(CI): 390 (MH+).
Exemplo S: Preparação de 1,3-bis-[isobutirilamino]-5-pivaloilaminobenzeno.
(= Composto 1-19)
a) N-pivaloil-3,5-dinitro anilina é obtida de 45,8 g (0,25 moles) de
3,5-dinitro anilina, 33,2 g (0,275 moles) de cloreto de pivaloíla, 98,9 g (1,25 moles) de piridina, 250 mL de NMP e 0,2 g de LiCI. A acilação é realizada como descrito no Exemplo A.
Rendimento: 67,0 g (= 100% de teoria).
Ponto de fusão: 206-208°C.
EM(CI): 268(MH+).
b) 26,2 g (0,1 mol) do produto obtido sob a) são hidrogenados em 100 mL de NMP com 1 g Pd/C a 90°C em analogia ao Exemplo B-V. A solução é usada após separação do catalisador por filtração para a etapa seguitne sem isolamento do intermediário N-pivaloil-1,3,5-triamino benzeno (100% de conversão de acordo com TLC: Rf (N-pivaloil-1,3,5-triamino benzeno) = 0,08; RF (N-pivaloil-3,5-dinitro anilina) = 0,65; sílica gel, eluente: hexano/acetato de etila 1:1). A esta solução 58,5 g (0,37 moles) de anidrido de isobutirila são adicionados a 60°C e a mistura de reação é agitada por 1 hora a 60°C. Diluição com água precipita o produto como um pó quase branco.
Rendimento: 20,4 g (= 59% de teoria).
Ponto de fusão: 288°C
EM(CI): 348(MH+).
Exemplo T: Preparação de 1,3-bis-[isobutirilamino]-5-(2,2dimetilbutiril)aminobenzeno.
(= Composto 1-20)
A uma solução de 13,1 g (0,059 moles) de N-(2,2-dimetil butiril)1,3,5-triamino benzeno obtida como descrito no Exemplo Q) em 75 mL de NMP, 34,5 g (0,22 moles) de anidrido isobutírico são adicionados a 60°C e a mistura de reação é agitada por 2 horas a 60°C. Diluição com água precipita o desejado produto como um pó quase branco.
Rendimento: 19,2 g (= 91% de teoria).
Ponto de fusão: 302-303°C.
EM(CI): 362(MH+).
Exemplo U: Preparação de 1,3-bis-[isobutirilamino]-5-(3,3dimetilbutiril)aminobenzeno.
(= Composto 1-21)
A uma solução de 13,1 g (0,059 moles) de N-(3,3-dimetil butiril)1,3,5-triamino benzeno (obtido como descrito no Exemplo R) em 75 mL de NMP, 34,5 g (0,22 moles) de anidrido isobutírico são adicionados a 60°C e a mistura de reação é agitada por 1 hora a 60°C. Diluição com água precipita o desejado produto como um pó incolor.
Rendimento: 15,2 g (= 71% de teoria)
Ponto de fusão: 227-228°C
EM(CI): 362 (MH+).
Exemplo V: Preparação de 1,3-bis-[2,2-dimetilbutirilamino]-5pivaloilaminobenzeno
(= Composto I-22)
A uma solução de 18,3 g (0,088 moles) de N-pivaloil-1,3,5triamino benzeno (obtida como descrito no Exemplo S) em 180 mL de NMP,
34,8 g (0,44 moles) de piridina e 35,5 g (0,264 moles) de cloreto de 2,2dimetil butirila são adicionados a 5°C e a mistura de reação é agitada por 5 horas a 100°C. Trabalho como descrito no Exemplo P e lavagem com hexano rendem um pó quase branco.
Rendimento: 28,0 g (=79% de teoria).
Ponto de fusão: nenhum ponto de fusão observado (sublimação).
EM(CI): 404(MH+).
Exemplo W: Preparação de 1,3-bis-[2,2-dimetilbutirilamino]-5isobutirilaminobenzeno.
(= Composto I-23)
A uma solução de 18,45 g (0,096 moles) de N-isobutiril-1,3,515 triamino benzeno (obtida como descrito no Exemplo P) em 100 mL de NMP,
37,8 g (0,478 moles) de piridina e 38,6 g (0,287 moles) de cloreto de 2,2dimetil butirila são adicionados a 5°C e a mistura de reação é agitada por 5 horas a 100°C. Trabalho como descrito no Exemplo P e lavagem com metanol e hexano rendem um pó incolor.
Ú3
Rendimento: 31,9 g (=83% de teoria).
Ponto de fusão: 363°C sob sublimação.
EM(CI): 390(MH+).
Exemplo X: Preparação de 1,3-bis[2,2-dimetilbutirilamino]-5-(3,35 dimetilbutiril)aminobenzeno
A uma solução de 13,1 g (0,059 moles) de N-(3,3-dimetil butiril)1,3,5-triamino benzeno (obtida como descrito no Exemplo R) em 75 mL de NMP, 23,3 g (0,295 moles) de piridina e 23,8 g (0,177 moles) de cloreto de 2,2-dimetil butirila são adicionados a 5°C e a mistura de reação é agitada por 5 horas a 100°C. Trabalho como descrito no Exemplo R e lavagem com metanol e hexano rendem o desejado produto como um pó quase branco.
Rendimento: 20,2 g (=82% de teoria).
Ponto de fusão: 364-367°C.
EM(CI): 418(MH+).
Exemplo Y: Preparação de 1,3-bis-[3,3-dimetilbutirilamino]-5pivaloilaminobenzeno.
H
H (= Composto I-25)
A uma solução de 18,3 g (0,088 moles) de N-pivaloil-1,3,5triamino benzeno (obtida como descrito no Exemplo S) em 100 mL de NMP, 34,8 g (0,44 moles) de piridina e 35,5 g (0,264 moles) de cloreto de 3,3dimetil butirila são adicionados a 5°C e a mistura de reação é agitada por 5 horas a 100°C. Trabalho como descrito no Exemplo P e lavagem com hexano rendem um pó quase branco.
Rendimento: 30,3 g (=85% de teoria).
Ponto de fusão: 315-318°C.
EM(CI): 404(MH+).
Exemplo Z: Preparação de 1,3-bis-[3,3-dimetilbutirilamino]-5isobutirilaminobenzeno.
(= Composto I-26)
A uma solução de 18,45 g (0,096 moles) de N-isobutiril-1,3,5triamino benzeno (obtida como descrito no Exemplo P) em 100 mL de NMP, 37,8 g (0,478 moles) de piridina e 38,6 g (0,287 moles) de cloreto de 3,3dimetil butirila são adicionados a 5°C e a mistura de reação é agitada por 5 horas a 100°C. Trabalho como descrito no Exemplo P e lavagem com metanol e hexano rendem um pó quase branco.
Rendimento: 33,9 g (= 88% de teoria).
Ponto de fusão: 266-268°C.
EM(CI): 390 (MH+).
Exemplo A1: Preparação de 1,3-bis[3,3-dimetilbutirilamino)-5-(2,2dimetilbutirilamino)aminobenzeno.
(= Composto 1-27)
A uma solução de 13,1 g (0,059 moles) de N-(2,2-dimetil butiril)1,3,5-triamino benzeno (obtida como descrito no Exemplo Q) em 75 mL de NMP, 23,3 g (0,295 moles) de piridina e 23,8 g (0,177 moles) de cloreto de 3,3-dimetil butirila são adicionados a 5°C e a mistura de reação é agitada por 5 horas a 100°C. Diluição com água precipita o produto. Recristalização a partir de DMF/água rende o desejado produto como um pó quase branco.
Rendimento: 20,9 g (=85%de teoria).
Ponto de fusão: 332-334°C.
EM(CI): 418(MH+).
Exemplo B1: Preparação de 1,3,5-tris-[3-(trimetil silil) propionilaminojbenzeno.
Si / \ (= Composto I-28)
Composto I-28 é obtido como um pó incolor em analogia ao Exemplo A a partir de 0,96 g (7,8 mmoles) de 1,3,5-triamino benzeno, 4,61 g (28,0 mmoles) de cloreto de 3-(trimetil silil) propionila, 80 mL de NMP, 17 mL de trietil amina e 0,3 g de LiCI.
Rendimento: 2,37 g (= 60% de teoria).
Ponto de fusão: 237°C.
EM(EI): 507(M+).
No que se segue, exemplos da preparação dos compostos da fórmula (II) são descritos em detalhes.
Os compostos da fórmula (II) pode ser sintetizados, por exemplo, por hidrogenação de 3,5-dinitro benzamidas (WWW)(preparadas através de procedimento padrão a partir de cloreto de 3,5-dinitro benzoíla (VW) e a correspondente amina) com hidrogênio e um apropriado catalisador metálico em um apropriado solvente orgânico e subseqüente acilação das assim obtidas 3,5-diamino benzamidas (YYY). Os compostos (YYY) podem ser isolados ou transferidos no correspondente dicloridrato; ambos podem ser purificados por recristalização a partir de um apropriado solvente. Também é possível usar uma solução do bruto (YYY) ou o bruto isolado (YYY) para a seguinte acilação com o cloreto ou anidrido de ácido carboxílico. Catalisadores possíveis são, por exemplo, Pd, PtO2, níquel Raney, etc, preferivelmente a versão comercialmente disponível sobre suporte de carbono. A hidrogenação pode ser realizada sob pressão normal ou sob pressão em temperaturas entre 20 e 120°C (verificaç ões de segurança são recomendadas antes de aumento de escala). Uma outra abordagem é redução com níquel Raney/hidrazina ou o uso de outros agentes redutores comuns, por exemplo, redução Béchamps ou uso de compostos de boro/hidrogênio. Apropriados solventes para a hidrogenação são, por exemplo, tetraidrofurano (THF), THF/metanol, dimetil formamida (DMF) ou N-metil pirrolidona (NMP). Recristalização pode ser realizada por exemplo, com metanol, etanol ou outros álcoois.
Α amina livre (ΥΥΥ) (ou a amina obtida a partir do cloridrato e uma base apropriada) pode ser acilada com uma quantidade estequiométrica ou um excesso do correspondente cloreto ácido, preferivelmente na presença de uma base não-interagindo orgânica ou inorgânica, por exemplo, trietil amina, tributil amina, piridina; um outro processo usa uma quantidade estequiométrica ou excesso do anidrido do ácido carboxílico como agente acilante; neste caso nenhuma base é requerida. A reação é realizada na ausência ou preferivelmente na presença de um solvente. A temperatura de reação ideal depende da natureza dos agentes acilantes (0°-100°C). Isolmento/purificação do produto final da fórmula (II) é realizado através de precipitação/recristalização/lavagem com uma apropriada mistura de água/solvente orgânico ou solvente orgânico/solvente orgânico ou com um solvente puro, por exemplo, DMF/água, NMP/água, etanol, metanol, etc. Síntese dos intermediários amida de ácido 3,5-dinitro benzóico da fórmula
Procedimento Genérico:
Em uma atmosfera inerte o cloreto de 3,5-dinitro benzoíla (VW) é adicionado a uma mistura de N-metil pirrolidona (NMP), piridina, LiCI e a requerida amina a 0°C. A mistura de reação é subseqüentemente aquecida a 75°C e mantida nesta temperatura por 2 horas. Após rsfriamento a mistura de reação é vertida em cinco vezes a quantiodade de água gelada. O produto precipitado é deixado em repouso por toda noite e subseqüentemente filtrado e secado em vácuo (0,1 mbar) em temperatura ambiente por 24 horas. Exemplo WWWa: Preparação de 3,5-dinitro-(N-t-butil) benzamida (WWWa) a partir de 8,00 g (34,7 mmoles) de cloreto de 3,5-dinitro benzoíola, 3,39 g (46,3 mmoles) de t-butil amina, 150 mL de NMP, 20 mL de piridina e 0,1 g de LiCI de acordo com o procedimento genérico descrito acima.
Purificação: recristalização a partir de xileno.
Ή
Rendimento: 5,70 g (61,5% de teoria; sólido branco).
EM(EI): 267(M+).
Exemplo WWWb: Preparação de 3,5-dinitro-(n-1,1-dimetil propil) benzamida (WWWb) a partir de 16,1 g (0,07 moles) de cloreto de 3,5-dinitro benzoíla,
7,3 g (0,084 moles) de t-amil amina, 50 mL de NMP e 12 mL de triatil amina de acordo com o procedimento genérico descrito acima.
Purificação: recristalização a partir de metanol.
Rendimento: 11 g (56% de teoria; sólido amarelo).
Ponto de fusão: 163-164°C.
Exemplo WWWc: Preparação de 3,5-dinitro-[N-(3-metil butil) benzamida (WWWc) a partir de 8,00 g (34,7 mmoles) de cloreto de 3,5-dinitro benzoíla,
4,04 g (46,3 mmoles) de 3-metil butil amina, 150 mL de NMP, 20 mL de piridina e 0,1 g de LiCI de acordo com o procedimento genérico descrito acima.
Purificação: recristalização a partir de tolueno Rendimento: 5,10 g (52,3% de teoria; sólido incolor).
13C-NMR (DMSO-d6): δ= 22,3; 25,2; 37,7; 37,9; 120,6; 127,4;
137,1; 148,1; 161,7.
Exemplo WWWd: Preparação de 3,5-dinitro-(N-t-octil) benzamida (WWWd) a partir de 106 g (0,45 moles) de cloreto de 3,5-dinitro benzoíla, 73,5 g (0,54 moles) de t-octil amina, 200 mL de NMP e 75 mL de trietil amina de acordo com o procedimento genérico descrito acima.
Purificação: recristalização a partir de metanol.
Rendimento: 92 g (63% de teoria; sólido amarelo).
Ponto de fusão: 129-130°C.
Exemplo WWWe: Preparação de 3,5-dinitro-(N-ciclopentil) benzamida (WWWe) a partir de 8,00 g (34,7 mmoles) de cloreto de 3,5-dinitro benzoíla,
3,94 g (46,3 mmoles) de ciclopentil amina, 150 mL de NMP, 20 mL de piridina e 0,1 g de LiCI de acordo com o procedimento genérico descrito acima.
Purificação: recristalização a partir de xileno.
Rendimento: 5,60 g (57,8% de teoria; sólido incolor).
EM(EI): 279(M+).
Exemplo WWWf: Preparação de 3,5-dinitro-(N-ciclohexil) benzamida
'............τϋ (WWWf) a partir de 8,00 g (34,7 mmoles) de cloreto de 3,5-dinitro benzoíla,
4,59 g (46,3 mmoles) de ciclohexil amina, 150 mL de NMP, 20 mL de piridina e 0,1 g de LiCI de acordo com o procedimento genérico descrito acima.
Purificação; recristalização a partir de xileno.
Rendimento: 5,34 g (52,5% de teoria; sólido incolor).
EM(EI): 293 (M+).
Exemplo WWWg: Preparação de 3,5-dinitro-(N-2,3-dimetilciclohexil) benzamida (WWWg) a partir de 11,5 g (0,05 moles) de cloreto de 3,5-dinitro benzoíla, 7,6 g (0,06 moles) de 2,3-dimetilciclohexil amina, 50 mL de NMP, e 10 mL de trietil amina de acordo com o procedimento genérico descrito acima.
Purificação: recristalização a partir de metanol.
Rendimento: 6,5 g (40% de teoria; sólido âmbar).
Ponto de fusão; 173-175°C.
Exemplo WWWh: Preparação de 3,5-dinitro-(N-isopropil) benzamida (WWWh) a partir de 46,11 g (0,2 moles) de cloreto de 3,5-dinitro benzoíla, 14,18 g (0,24 moles) de isopropil amina, 150 mL de NMP e 25 mL de trietil amina de acordo com o procedimento genérico descrito acima.
Purificação; recristalização a partir de isopropanol.
Rendimento: 37 g (73% de teoria; sólido âmbar).
Ponto de fusão: 179-181 °C.
Síntese dos intermediários amida de ácido 3,5-diamino benzóico da fórmula
Procedimento Genérico:
Uma mistura do correspondente derivado amida de ácido 3,5dinitro benzóico (WWW), tetraidrofurano (THF), metanol e paládio sobre carvão ativado (10% Pd) é tratada com gás H2 por 24 horas. O catalisador é subseqüentemente filtrado e o solvente é evaporado sob pressão reduzida. Exemplo YYYa: Preparação de 3,5-diamino-N-t-butil benzamida (YYYa) a partir de 1,75 g (6,55 mmoles) de 3,5-dinitro-N-t-butil benzamida, 0,2 g de paládio sobre carvão ativado (Pd 10%), 200 mL de THF e 50 mL de metanol em uma temperatura de reação de 35°C e uma pressão de hidrogênio de 3 bar de acordo com o procedimento genérico descrito acima.
Rendimento: 1,31 g (96,5% de teoria; sólido amarelo).
EM(EI): 207(M+).
Exemplo YYYb: Preparação de 3,5-diamino-N-t-octil benzamida (YYYb).
O produto que é preparado de acordo com o procedimento genérico descrito acima não é isolado. Uma solução de (YYYb) é diretamente acilada como descrito no Exemplo II-3.
Exemplo YYYc: Preparação de 3,5-diamino-N-(3-metil butil) benzamida (YYYc) a partir de 4,98 g (17,7 mmoles) de 3,5-dinitro-N-(3-metil butil) benzamida, 0,2 g de palsobre carvão ativado (Pd 10%), 200 mL de THF e 50 mL de metanol em uma temperatura de reação de 35°C e uma pressão de hidrogênio de 3 bar de acordo com o procedimento genérico descrito acima.
Rendimento: 3,16 g (80,7% de teoria; sólido amarelo). 13C-NMR(DMSO-d6): δ = 22,5; 25,3; 37,2; 38,2; 101,9; 102,1;
136,7; 148,9; 167,6.
Exemplo YYYd: Preparação de 3,5-diamino-N-ciclopentil benzamida (YYYd) a partir de 4,41 g (15,8 mmoles) de 3,5-dinitro-N-ciclopentil benzamida, 0,2 g de paládio sobre carvão ativado (Pd 10%), 200 mL de THF e 50 mL de metanol em uma temperatura de reação de 35°C e uma pressão de hidrogênio de 3 bar de acordo com o procedimento genérico descrito acima.
Rendimento: 3,10 g(89,5% de teoria; sólido amarronzado). EM(EI): 219(M+).
Exemplo YYYe: Preparação de 3,5-diamino-N-ciclohexil benzamida (YYYe) a partir de 4,78 g (16,3 mmoles) de 3,5-dinitro-N-ciclohexil benzamida, 0,2 g de paládio sobre carvão ativado (Pd 10%), 200 mL de THF e 50 mL de metanol em uma temperatura de reação de 35°C e uma pressão de hidrogênio de 3 bar de acordo com o procedimento genérico descrito acima.
Rendimento: 3,09 g (81,2% de teoria; sólido amarelo).
EM(EI): 233(M+).
Síntese dos compostos da fórmula II
Procedimento Genérico:
Processo A:
Em uma atmosfera inerte o derivado de ácido 3,5-diamino ben5 zóico é adicionado a uma mistura de N-metil pirrolidona (NMP), piridina, LiCI e o requerido cloreto ácido ou anidrido (neste caso nenhuma amina terciária é requerida) a 0°C. A mistura de reação é subseqüentemente aquecida a 75°C e mantida nesta temperatura por 2 horas. Após resfriamento a mistura de reação é vertida em cinco vezes a quantidade de água gelada. O produto precipitado é deixado em repouso por toda noite e subseqüentemente filtrado e secado em vácuo (0,1 mbar) em temperatura ambiente por 24 horas. Um pó incolor é obtido.
Processo B:
Uma outra síntese inicia-se a partir do derivado 1,3-dinitro ben15 zeno (WWW), que é hidrogenado em NMP à diamina (YYY). Este intermediário não é isolado e diretamente acilado. O isolamento do produto pode ser em analogia ao processo A
Exemplo 11-1: Preparação de N-t-butil-3,5-bis-(3-metilbutirilamino)benzamida
7>>
a partir de 0,50 g (2,41 mmoles) de 3,5-diamino-N-t-butil benzamida, 0,68 g (5,64 mmoles) de cloreto de ácido 3-metil butírico, 30 mL de NMP, 5 mL de piridina e 0,1 g de LiCI de acordo com o Processo A
Purificação: recristalização a partir de xileno.
Rendimento: 0,63 g (69,6% de teoria).
Ponto de fusão: 237°C.
EM(EI): 375 (M+).
Exemplo II-2: Preparação de N-t-butil-3,5-bis-(pivaloilamino)benzamida
(ZZZb) a partir de 1,24 g (6,0 mmoles) de 3,5-diamino-N-t-butil benzamida, 1,69 g (14,0 mmoles) de cloreto de pivaloíla, 50 mL de NMP, 10 mL de piridina e 0,1 g de LiCI de acordo com o Processo A
Purificação: recristalização a partir de etanol.
Rendimento: 1,54 g (68,4% de teoria).
EM(EI): 375(M+).
Ponto de fusão: sublimação inicia-se em 294°C.
Exemplo II-3: Preparação de N-t-octil-3,5-bis-(pivaloilamino)benzamida de acordo com o Processo B.
Uma mistura de 10 g (31 mmoles) de 3,5-dinitro-(N-t-octil) benzamida, 75 mL de NMP e 0,5 g de paládio sobre carvão ativado (Pd 10%) é
1)2>
tratada com gás H2 por 30 horas a 100°C. O catalisador é subseqüentemente filtrado e 17,3 g (93 mmoles) de anidrido de pivaloíla são adicionados ao filtrado. Esta mistura de reação é então aquecida por 12 horas a 100°C. Após resfriamento a mistura de reação é vertida em cinco vezes a quantidade de água gelada. O produto precipitado é filtrado e o resíduo é recristalizado de etanol.
Rendimento: 4,7 g (35% de teoria; pó levemente cinza).
Ponto de fusão: 327°C (decomposição).
Exemplo il-4: Preparação de N-(1,1 -dimetil propil)-3,5-bis10 (pivaloilamino)benzamida de acordo com Processo B.
Em analogia ao Exemplo il-3, 9,9 g (71%) de composto (ZZZd) são obtidos como um sólido branco a partir de 7,88 g (0,036 moles) de 3,5dinitro-(N-1,1-dimetil propil) benzamida, 75 mL de NMP, 0,5 g de Pd/C (Pd 10%) e 19,9 g (0,11 moles) de anidrido piválico.
Ponto de fusão: 378°C (decomposição).
Exemplo il-5: Preparação de N-(t-octil)-3,5-bis-(isobutirilamino)benzamida de acordo com o Processo B.
Em analogia ao Exemplo il-3, 6,7 g (51%) de composto (ZZZe) são obtidos como um sólido levemente cinza a partir de 8,2 g (0,031 moles) de 3,5-dinitro-(N-t-octil) benzamida (composto WWWb), 75 mL de NMP, 0,5 g de Pd/C (Pd 10%) e 14,7 g (0,093 moles) de anidrido isobutírico.
Ponto de fusão: 256°C (decomposição).
Exemplo II-6: Preparação de N-(t-butil)-3,5-bis-(pivaloilamino)benzamida de acordo com o Processo B.
(ZZZb) em analogia ao Exemplo II-3, 129 g (92%) de composto (ZZZb) são obtidos na forma de um sólido branco a partir de 77,5 g (0,37 moles) de 3,5-dinitro(N-t-butil) benzamida (composto WWWa), 1200 mL de NMP, 5 g de Pd/C (Pd 10%) e 209 g (1,12 moles) de anidrido de pivaloíla.
Ponto de fusão: O produto sublima a 294°C.
Exemplo II-7: Preparação de N-(2,3-dimetilciclohexil)-3,5-bis(pivaloilamino)benzamida de acordo com o Processo B.
Em analogia ao Exemplo II-3, 7,6 g (56%) de composto (ZZZf) 15 são obtidos como um sólido levemente cinza a partir de 8,2 g (0,031 moles) de 3,5-dinitro-(N-2,3-dimetilciclohexil) benzamida, 75 mL de NMP, 0,5 g de
Pd/C (Pd 10%) e 17,5 g (0,094 moles de anidrido piválico.
Ponto de fusão: 337°C (decomposição).
Exemplo II-8: Preparação de N-t-butil-3,5-bis76 (ciclopentanocarbonilamino)benzamida
a partir de 0,50 g (2,41 mmoles) de 3,5-diamino-N-t-butil benzamida, 0,75 g (5,66 mmoles) de cloreto de ciclopentano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o processo A.
Purificação: recristalização a partir de diclorometano.
Rendimento: 0,45 g (46,7% de teoria).
Ponto de fusão: 281 °C (decomposição).
EM(EI): 399(M+).
Exemplo II-9: Preparação de N-(3-metil butil)-3,5-bis-(310 metilbutirilamino)benzamida
a partir de 0,50 g (2,26 mmoles) de 3,5-diamino-N-(3-metil butil) benzamida, 0,64 g (5,31 mmoles) de cloreto de ácido 3-metil butírico, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: cromatografia de coluna (hexano/acetato de etila
2:1).
Rendimento: 0,58 g (65,9% de teoria).
EM(EI): 389(M+).
Ponto de fusão: decomposição inicia-se em 300°C.
%
Exemplo 11-10: Preparação de N-(3-metil butil)-3,5-bis(pivaloilamino)benzamida
(ZZZi) a partir de 0,50 g (2,26 mmoles) de 3,5-diamino-N-(3-metil butil) benzamida, 0,64 g (5,31 mmoles) de cloreto de pivaloíla, 30 mL de NMP, 5 mL de piridi5 na e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização a partir de clorofórmio.
Rendimento: 0,42 g (47,7% de teoria).
Ponto de fusão: 312°C (decomposição).
EM(EI): 389(M+).
Exemplo 11-11: Preparação de N-(3-metil butil )-3,5-bis-(4metilpentanoilamino)benzamida.
(ZZZj) a partir de 0,50 g (2,26 mmoles) de 3,5-diamino-N-(3-metil butil) benzamida, 0,71 g (5,27 mmoles) de cloreto de ácido 4-metil valérico, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A
Purificação: cromatografia de coluna (ciclohexano/acetato de etila 2:1).
Rendimento: 0,52 g (55,1 % de teoria).
EM(EI): 417(M+).
Ponto de fusão: decomposição começa em 290°C.
Exemplo 11-12: Preparação de N-(3-metil butil)-3,5-bis(ciclopentanocarbonilamino)benzamida.
a partir de 0,50 g (2,26 mmoles) de 3,5-diamino-N-(3-metil butil) benzamida, 0,70 g (5,28 mmoles) de cloreto de ciclopentano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: cromatografia de coluna (ciclohexano/acetato de etila 2:1).
Rendimento: 0,67 g (71,7% de teoria).
Ponto de fusão: 225°C.
EM(EI): 413 (M+).
Exemplo 11-13: Preparação de N-(3-metil butil)-3,5-bis(ciclohexanocarbonilamino)benzamida.
(ZZZI) a partir de 0,63 g (2,85 mmoles) de 3,5-diamino-N-(3-metil butil) benzamida, 0,97 g (6,62 mmoles) de cloreto de ciclohexano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: cromatografia de coluna (ciclohexano/acetato de etila 2:1). Rendimento: 0,75 g (59,6% de teoria).
Ponto de fusão: 234°C.
EM(EI): 441 (M+).
Exemplo 11-14: Preparação de N-ciclopentil-3,5-bis-(379 metilbutirilamino)benzamida
a partir de 0,50 g (2,28 mmoles) de 3,5-diamino-N-ciclopentil benzamida, 064 g (5,31 mmoles) de cloreto de ácido 3-metil butírico, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização de tolueno.
Rendimento: 0,55 g (62,2% de teoria).
Ponto de fusão: 241 °C.
EM(EI): 387(M+).
Exemplo 11-15: Prpearação de N-ciclopentil-3,5-bis10 (pivaloilamino)benzamida.
a partir de 0,50 g (2,28 mmoles) de 3,5-diamino-N-ciclopentil benzamida, 0,64 g (5,31 mmoles) de cloreto de pivaloíla, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização a partir de clorofórmio.
Rendimento: 0,35 g (39,6% de teoria).
Ponto de fusão: 361 °C.
EM(70 eV), m/z(%): 387(M+).
Exemplo 11-16: Prparação de N-ciclopentil-3,5-bis-(4metilpentanoilamino)benzamida.
a partir de 0,50 g (2,28 mmoles) de 3,5-diamino-N-ciclopentil benzamida, 0,72 g (5,35 mmoles) de cloreto de ácido 4-metil valérico, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização a partir de tolueno.
Rendimento: 0,82 g (86,5% de teoria).
Ponto de fusão: 207°C.
EM(EI): 415(M+).
Exemplo 11-17: Preparação de N-ciclopentil-3,5-bis(ciclopentanocarbonilamino)benzamida
(ZZZp) a partir de 0,50 g (2,28 mmoles) de 3,5-diamino-N-ciclopentil benzamida, 0,71 g (5,35 mmoles) de cloreto de ciclopentano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização a partir de 1,2-dicloro benzeno. Rendimento: 0,72 g (76,7% de teoria).
Ponto de fusão: 301 °C.
EM(EI): 411(M+).
Exemplo 11-18: Preparação de N-ciclopentil-3,5-bis(ciclohexanocarbonilamino)benzamida
(ZZZq) a partir de 0,62 g (2,83 mmoles) de 3,5-diamino-N-ciclopentil benzamida, 0,97 g (6,62 mmoles) de cloreto de ciclohexano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização a partir de 1,2-dicloro benzeno. Rendimento: 1,03 g (82,8% de teoria).
Ponto de fusão: 305°C.
EM(El): 439(M+).
Exemplo 11-19: Preparação de N-ciclohexil-3,5-bis-(3metilbutirilamino)benzamida
(ZZZr) a partir de 0,50 g (2,14 mmoles) de 3,5-diamino-N-ciclohexil benzamida, 0,60 g (4,98 mmoles) de cloreto de ácido 3-metil butírico, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: cromatografia de coluna (ciclohexano/acetato de etila 1:1). Rendimento: 0,60 g (69,8% de teoria)
Ponto de fusão: 212°C.
EM(EI): 401 (M+).
Exemplo H-20: Preparação de N-ciclohexil-3,5-bis-(pivaloilamino)benzamida
a partir de 0,50 g (2,14 mmoles) de 3,5-diamino-N-ciclohexil benzamida, 0,60 g (4,98 mmoles) de cloreto de pivaloíla, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o Processo A.
Purificação: recristalização a partir de clorofórmio.
Rendimento: 0,39 g (45,4% de teoria).
Ponto de fusão: 347°C.
EM(EI): (M+).
Exemplo 11-21: Preparação de N-ciclohexil-3,5-bis-(4metilpentanoilamino)benzamida
a partir de 0,50 g (2,14 mmoles) de 3,5-diamino-N-ciclohexil benzamida, 0,67 g (4,98 mmoles) de cloreto de ácido 4-metil valérico, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI de acordo com o processo A.
Purificação: recristalização a partir de tolueno.
Rendimento: 0,77 g (83,8% de teoria).
Ponto de fusão: 200°C.
EM(El): 429(M+).
Exemplo li-22: Preparação de N-ciclohexil-3,5-bis(ciclopentanocarbonilamino)benzamida
a partir de 0,50 g (2,14 mmoles) de 3,5-diamino-N-ciclohexil benzamida, 0,66 g (4,98 mmoles) de cloreto de ciclopentano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de LiCI seco de acordo com o Processo A.
Purificação: recristalização a partir de xileno.
Rendimento: 0,66 g (72,5% de teoria).
Ponto de fusão: 279°C.
EM(EI): 425(M+).
Exemplo II-23: Preparação de N-ciclohexil-3,5-bis(ciclohexanocarbonilamino)benzamida
a partir de 0,50 g (2,14 mmoles) de 3,5-diamino-N-ciclohexil benzamida, 0,73 g (4,98 mmoles) de cloreto de ciclohexano carbonila, 30 mL de NMP, 5 mL de piridina e 0,05 g de Li Cl de acordo com o Processo A.
Purificação: cromatografia de coluna (ciclohexano/acetato de etila 2:1). Rendimento: 0,83 g (85,5% de teoria).
Ponto de fusão: 290°C.
EM(EI):453(M+)
Exemplo II-24: Preparação de N-isopropil-3,5-bis-(pivaloilamino)benzamida de acordo com o Processo B.
V
(ZZZw)
Em analogia ao Exemplo 11-3, o composto (ZZZw) é obtido como um sólido levemente cinza a partir de 18,7 g (0,074 moles) de 3,5-dinitro-(Nisopropil) benzamida, 150 mL de NMP, 1,25 g de Pd/C (Pd 10%) e 41,2 g (0,22 moles) de anidrido piválico.
Rendimento: 17,35 g
Ponto de fusão: 360°C (decomposição).
Exemplo II-25: Preparação de N-isopropil-3,5-bis-(isobutirilamino)benzamida de acordo com o Processo B.
(ZZZx)
Em analogia ao Exemplo II-3, o composto (ZZZx) é obtido como um sólido levemente cinza a partir de 18,7 g (0,074 moles) de 3,5-dinitro-(Nisopropil) benzamida, 150 mL de NMP, 1,25 g de Pd/C (Pd 10%) e 35,0 g (0,22 moles) de anidrido isobutírico.
Rendimento: 6,3 g
Ponto de fusão: 239°C (decomposição).
Exemplo II-26: Preparação de N-t-butil-3,5-bis-(2,2-dimetilbutirilamino) benzamida de acordo com o Processo B.
(ZZZy)
Em analogia ao Exemplo II-3, o composto (ZZZy) é obtido como um sólido levemente cinza a partir de 20,0 g (0,075 moles) de 3,5-dinitro-(Nt-butil) benzamida, 100 mL de NMP, e 30,3 g (0,225 moles) de cloreto de 2,2-dimetil butirila.
Rendimento: 25,7 g.
Ponto de fusão: 390°C (decomposição).
No seguinte, exemplos da preparação dos compostos da fórmula (III) são descritos em detalhes.
Os compostos da fórmula (III) são sintetizados, por exemplo, através de redução de diamidas de ácido 5-nitro isoftálico (YYY) (preparado através de procedimento padrão a partir de dicloreto de ácido 5-nitro isoftálico (QQQ) e a correspondente amina) e subseqüente acilação. O intermediário diamida de ácido 5-amino isoftálico (TTT) pode ser isolado ou transferido para o correspondente cloridrato e pode ser purificado por recristalização a partir de um apropriado solvente. É também possível usar a solução do bruto (TTT) ou o bruto isolado (TTT)para a seguinte reação com o cloreto ou anidrido de ácido carboxílico.
Catalisadores possíveis para a reação são, por exemplo, Pd, PtO2, níquel Raney, etc., preferivelmente a versão comercialmente disponível sobre suporte de carbono. A hidrogenação pode ser realizada sob pressão normal ou sob pressão em temperaturas entre 20 e 120°C (verificações de segurança são recomendadas antes de aumentar a escala). Uma outra abordagem é redução com níquel Raney/hidrazina ou o uso de outros agentes redutores comuns, por exemplo, redução Béchamps ou o uso de compostos de boro/hidrogênio. Solventes apropriados para a hidrogenação são, por exemplo, tetraidrofurano (THF), THF/metanol, dimetil formamida (DMF) ou N-metil pirrolidona (NMP). Recristalização pode ser realizada, por exemplo, com metanol, etanol ou outros álcoois.
A amina livre (TTT) (ou a amina obtida a partir do cloridrato e uma apropriada base) pode ser acilada com uma quantidade estequiométrica ou um excesso do correspondente cloreto ácido, preferivelmente na presença de uma base não-interagindo orgânica ou inorgânica, por exemplo, trietilamina, tributil amina, piridina; um outro processo usa uma quantidade estequiométrica ou excesso o anidrido do ácido carboxílico como agente acilante; neste caso nenhuma base é requerida. A reação é realizada na ausência ou preferivelmente na presença de um solvente. A temperatura de reação ideal depende da natureza dos agentes acilantes (0°-100°C). Isolamento/purificação do produto final é realizado, por exemplo, através de precipitação/recristalização/lavagem com uma mistura apropriada de água/ solvente orgânico ou solvente orgânico/solvente orgânico ou com um solvente puro, por exemplo, DMF/água, NMP/água, etanol, metanol, etc.
Síntese dos intermediários diamida de ácido 5-nitro isoftálico da fórmula
Procedimento Geral
Em uma atmosfera inerte o dicloreto de ácido 5-nitro isoftálico (obtido através de procedimento padrão a partir de ácido isoftálico e SOCb) é adicionado a uma mistura de N-metil pirrolidona, piridina e trietil amina, LiCI e a requerida amina a 0°C. A mistura de reação é subseqüentemente aquecida a 75°C e mantida nesta temperatura por 2 horas. Após resfriamento a mistura de reação é vertida em cinco vezes a quantidade de água gelada. O produto precipitado é deixado em repouso por toda noite e subseqüentemente filtrado e secado em vácuo (0,1 mbar) em temperatura ambiente por 24 horas.
Exemplo RRRa-1: Preparação de Ν,Ν'-di-t-butil diamida de ácido 5-nitro isoftálico.
(RRRa)
500g de dicloreto de ácido 5-nitro isoftálico (2,0 moles; obtido através de procedimento padrão de ácido isoftálico e SOCI2), em 1 L de
NMP são adicionados a 0°C dentro de 2 horas a uma solução de 345 g (4,7 moles) de t-butil amina, 1,3 L de piridina e 25 g de LiCI em 1 L de NMP. Após 2 horas de agitação a 75°C, a solução é resfriada com gelo/água. O precipitado é filtrado, lavado com água e etanol e secado em vácuo.
Rendimento: 462,4 g (72% de teoria; pó incolor). Ponto de fusão: 307-308°C.
EM(EI): 321(M+).
Exemplo RRRa-2: Preparação de Ν,Ν'-di-t-butil diamida de ácido 5-nitro isoftálico (RRRa).
O mesmo composto como descrito no Exemplo RRRa-1 é obtido, 15 partindo de 1,98 g (8,0 mmoles) de dicloreto de ácido 5-nitro isoftálico, 1,38 g (18,8 mmoles) de t-butil aminas, 50 mL de NMP, 7 mL de piridina e 0,1 g de LiCI.
Purificação: recristalização a partir de acetato de etila. Rendimento: 1,30 g (50,6% de teoria; sólido branco). EM(EI): 321 (M+).
Exemplo RRRb: Preparação de Ν,Ν'-di-t-octil diamida de ácido 5-nitro isoftalico.
Hr c
g de dicloreto de ácido 5-nitro isoftálico (0,20 moles; obtido
3>Ύ através de procedimento padrão a partir de ácido isoftálico e SOCI2) em 100 mL de NMP são adicionados a 0°C dentro de 30 minutos a uma solução de 60,8 g (0,47 moles) de t-octil amina, 130 mL de piridina e 2,5 g de LiCI em 100 mL de NMP. Após 2 horas de agitação a 75°C, a solução é resfriada com gelo/água. O precipitado é filtrado, lavado com água e etanol e secado. Rendimento: 55 g (63% de teoria; pó quase branco).
Ponto de fusão após recristalização: 169-172°C.
EM(CI): 434(MH+).
Exemplo RRRc: Preparação de Ν,Ν'-diciclohexil diamida de ácido 5-nitro 10 isoftálico
(RRRc) a partir de 49,60 g (0,20 moles) de dicloreto de ácido 5-nitro isoftálico, 51,57 g (0,52 moles) de ciclohexil amina, 900 mL de NMP, 250 mL de trietil amina e 1,0 g de LiCI.
Purificação: recristalização a partir de DMF.
Rendimento: 48,50 g (64,9% de teoria; sólido branco).
EM(EI): 373 (M+).
Exemplo RRRd: Preparação de N,N'-bis-(2-metilciclohexil)diamida de ácido
5-nitro isoftálico
(RRRd) a partir de 24,80 g (0,10 moles) de dicloreto de ácido 5-nitro isoftálico, 28,30 20 g (0,25 moles) de 2-metilciclohexil amina (mistura isomérica), 778 mL de
NMP, 167 mL de piridina e 1,0 g de LiCI.
Purificação: recristalização a partir de 1,2-dicloro benzeno.
Rendimento: 30,06 g (74,9% de teoria; sólido branco).
EM(EI): 401 (M+).
Síntese dos intermediários diamida de ácido 5-amino isoftálico da fórmula
Exemplo TTTa-1: Preparação de Ν,Ν'-di-t-butil diamida de ácido 5-amino isoftálico.
Uma mistura de 1,22 g (3,80 mmoles) de N,Ν'-di-t-butil diamida de ácido 5-nitro isoftálico, 200 mL de THF, 50 mL de metanol e 0,2 g de paládio sobre carvão ativado (Pd 10%) é tratada com gás H2 (3 bar) a 35°C por 24 horas. O catalisador é subseqüentemente filtrado e o solvente é evapora10 do sob pressão reduzida.
Rendimento: 1,10 g (99,3% de teoria).
EM(EI): 291 (M+).
Exemplo TTTa-2: Preparação de Ν,Ν'-di-t-butil diamida de ácido 5-amino isoftálico (TTTa).
100,4 g (0,312 moles) de Ν,Ν'-di-t-butil diamida de ácido 5-nitro isoftálico, 5 g de paládio sobre carvão ativado (Pd 10%) e 1000 mL de nMP são tratados com gás H2 (5 bar) a 50°C por 6 horas. É verificado por TLC que nenhum composto nitro de partida (RRRa) permanece (sílica gel, hexano/acetato de etila 1:1, Rf (TTTa) = 0,32; RF (RRRa) = 0,76); rendimento
100%. O catalisador é subseqüentemente filtrado e a solução é usada diretamente para a acilação.
Exemplo TTTb: Preparação de Ν,Ν'-di-t-octil diamida de ácido 5-amino isoftálico.
30,0 g (0,069 moles) de Ν,Ν'-di-t-octil diamida de ácido 5-nitro isoftálico, 1 g de paládio sobre carvão (Pd 10%) e 125 mL de NMP são tra5 tados com gás H2 (5 bar) a 70-75°C por 8 horas. É verificado por TLC que nenhum composto nitro de partida (RRRb) permanece (sílica gel, hexano/acetato de etila 1:2, Rf (TTTb) = 0,43, Rf (RRRb) = 0,83); rendimento 100%. O catalisador é subseqüentemente filtrado e a solução é usada diretamente para a acilação.
Exemplo TTTc: Preparação de Ν,Ν'-diciclohexil diamida de ácido 5-amino isoftálico.
(TTTc)
Uma mistura 47,47 g (127,1 mmoles) de Ν,Ν'-diciclohexil diamida de ácido 5-nitro isoftálico, 800 mL de DMF, 20 mL de água e 1,0 g de paládio sobre carvão ativado (Pd 10%) é tratada com gás H2 (3 bar) a 60°C por 24 horas. O catalisador é subseqüentemente filtrado. A mistura de reação é vertida em 4 L de água gelada. O precipitado é filtrado, secado e recristalizado de DMF.
Rendimento: 31,0 g (71,0% de teoria; sólido amarelo claro).
EM(EI): 343(M+).
Exemplo TTTd: Preparação de N,N'-bis-(2-metiiciclohexil)diamida de ácido
5-amino isoftálico
(TTTd)
Uma mistura de 14,86 g (37,0 mmoles) de N,N'-bis-(2metilciclohexil)diamida de ácido 5-nitro isoftálico, 500 mL de THF, 10 mL de metanol e 5,0 g de níquel Raney é tratada com gás H2 (3 bar) a 40°C por 24 horas. O catalisador é subseqüentemente filtrado e o solvente é evaporado sob pressão reduzida.
Rendimento: 8,08 g (58,8% de teoria; sólido amarelo).
EM(EI): 371 (M+).
Síntese dos compostos da fórmula (III)
(III)
Procedimento Geral:
Em uma atmosfera inerte o intermediário diamida de ácido 5amino isoftálico é adicionado a uma mistura de N-metil pirrolidona, piridina ou trietil amina, LiCI e o requerido cloreto ácido a 0°C. A mistura de reação é subseqüentemente aquecida a 75°C e mantida nesta temperatura por 2 horas. Após resfriamento a temperatura ambiente é vertida em cinco vezes o volume de água gelada. O produto precipitado é deixado em repouso por toda noite e subseqüentemente filtrado e secado em vácuo (0,1 mbar) em temperatura ambiente por 24 horas. Um pó incolor é obtido.
Exemplo 111-1: Preparação de Ν,Ν'-di-t-butil diamida de ácido 5-pivaloilamino isoftálico.
íol
Em uma atmosfera inerte, 1,10 g (3,77 mmoles) de N,N'-di-t-butil diamida de ácido 5-amino isoftálico são adicionados a uma mistura de 50 mL de N-metil pirrolidona, 10 mL de piridina, 0,05 g de LiCI e 0,61 g (5 mmoles) de cloreto de pivaloíla a 0°C. A mistura de reação é subseqüentemente aquecida a 75°C e mantida nesta temperatura por 2 horas. Após resfriamento a mistura de reação é vertida em cinco vezes a quantidade de água gelada. O precipitado é filtrado e secado em vácuo.
Rendimento: 0,83 g (58,6% de teoria).
Ainda purificação por recristalização a partir de metanol.
Ponto de fusão: sublimação começa a 294°C; nenhum ponto de fusão.
EM(CI): 376 (MH+).
Exemplo III-2: Preparação de N,N'-di-t-butil diamida de ácido 5-pivaloilamino isoftálico.
90,6 g (0,311 moles) de N,N'-di-t-butil diamida de ácido 5-amino isoftálico (I l la), 126 mL (0,62 mmoles) de anidrido piválico e 1,2 L de NMP são agitados por 18 horas a 90°C. O precipitado é filtrado a 25°C, lavado com metanol e secado.
Rendimento: 81,7 g (70% de teoria; pó incolor).
De acordo com dados espectroscópicos, o produto é idêntico ao
1ΰ>
produto obtido no Exemplo 111-1.
Exemplo III-3: Preparação de N,N'-di-t-octil diamida de ácido 5-pivaloilamino isoftálico.
28,25 g (0,07 moles) de N,N'-di-t-octil diamida de ácido 5-amino isoftálico (TTTb), 28,4 ml (0,14 mmoles) de anidrido piválico e 150 mL de NMP são agitados por 20 horas a 90°C. O precipitado é filtrado a 25°C, lavado com metanol e secado.
Rendimento: 27,3 g (80,8% de teoria; pó incolor).
Ponto de fusão: 298-299°C.
EM(CI): 488(MH+).
Exemplo III-4: Preparação de Ν,Ν'-diciclohexil diamida de ácido 5-(3-metil butirilamino) isoftálico
a partir de 6,87 g (20,0 mmoles) de Ν,Ν'-di-ciclohexil diamida de ácido 5amino isoftálico, 3,14 g (26,0 mmoles) de cloreto de ácido 3-metil butírico,
100 mL de NMP, 15 mL de trietil amina e 0,1 g de LiCI.
Purificação: recristalização a partir de metanol.
lod
Rendimento: 7,23 g (84,5% de teoria).
Ponto de fusão: 260°C.
EM(EI): 427(M+).
Exemplo II1-5: Preparação de Ν,Ν'-di-ciclohexil diamida de ácido 55 (pivaloilamino) isoftálico
a partir de 6,87 g (20,0 mmoles) de Ν,Ν'-diciclohexil diamida de ácido 5amino isoftálico, 3,14 g (26,0 mmoles) de cloreto de pivaloíla, 100 mL de NMP, 15 mL de trietil amina e 0,1 g de LiCI.
Purificação: recristalização a partir de metanol.
Rendimento: 4,90 g (57,3% de teoria).
Ponto de fusão: 327°C (decomposição).
EM(EI): 427(M+).
lExemplo II1-6: Preparação de Ν,Ν'-diciclohexil diamida de ácido 5(ciclopentano carbonilamino) isoftálico
a partir de 6,87 g (20,0 mmoles) de Ν,Ν'-diciclohexil diamida de ácido 5amino isoftálico, 3,45 g (26,0 mmoles) de cloreto de ciclopentano carbonila, 100 mL de NMP, 15 mL de trietil amina e 0,1 g de LiCI.
ΙοΗ
Purificação: recristalização a partir de metanol.
Rendimento: 4,60 g (52,3% de teoria).
Ponto de fusão: 306°C.
EM(EI): 439(M+).
Exemplo 111-7: Preparação de Ν,Ν'-diciclohexil diamida de ácido 5-(ciclohexil carbonilamino) isoftálico.
(UUUf) a partir de 6,87 g (20,0 mmoles) de Ν,Ν'-diciclohexil diamida de ácido 5amino isoftálico, 3,81 g (26,0 mmoles) de cloreto de ciclohexano carbonila, 100 mL de NMP, 15 mL de trietil amina e 0,1 g de LiCI.
Purificação: recristalização a partir de metanol.
Rendimento: 5,11 g (56,3% de teoria).
Ponto de fusão: 291 °C.
EM(EI): 453(M+).
Exemplo III-8: Preparação de N,N'-bis-(2-metilciclohexil)diamida de ácido 515 (ciclopentano carbonilamino) isoftálico.
a partir de 2,02 g (5,44 mmoles) de N,N'-bis-(2-metilciclohexil)diamida de ácido 5-amnio isoftálico, 0,96 g (7,24 mmoies) de cloreto de ciclopentano iüó carbonila, 70 mL de NMP, 15 mL de piridina e 0,1 g de LiCI.
Purificação: extração com tolueno (72 horas).
Rendimento: 1,66 g (65,2% de teoria).
Ponto de fusão: 312°C.
EM(EI): 467(M+).
Exemplo HI-9: Preparação de N,N'-bis-(2-metilciclohexil)diamida de ácido 5(ciclohexano carbonilamino) isoftálico
a partir de 2,02 g (5,44 mmoles) de N,N'-bis-(2-metilciclohexil)diamida de ácido 5-amino isoftálico, 1,06 g (7,23 mmoles) de cloreto ciclohexano carbonila, 70 mL de NMP, 15 mL de piridina e 0,1 g de LiCI.
Purificação: extração com acetato de etila (12 h).
Rendimento: 1,64 g (62,6% de teoria).
Ponto de fusão: 327°C (decomposição).
EM(EI): 481 (M+).
Exemplo 111-10: Preparação de N,N'-bis-(2-metilciclohexiI)diamida de ácido 5((1-metilciclohexanocarbonil)amino)isoftálico
a partir de 2,02 g (5,44 mmoles) de N,N'-bis-92-metilciclohexil) amida de áci97 do 5-amino isoftálico, 1,16 g(7,22 mmoles) de cloreto 1-metil ciclohexano carbonila, 70 mL de NMP, 15 mL de piridina e 0,1 g de LiCI.
Purificação: recristaiização a partir de metanol.
Rendimento: 1,16 g (43,0% de teoria).
Ponto de fusão: 354°C.
EM(EI): 495 (M+).
Exemplo 111-11: Preparação de N,N'-bis-(2-metilciclohexil)diamida 5-((2metilciclohexanocarbonil)amino)isoftálico.
a partir 2,02 g (5,44 mmoles) de N,N'-bis-(2-metilciclohexil)diamida de ácido
5-amino isoftálico, 1,16 g (7,22 mmole) de cloreto de 2-metil ciclohexano carbonila, 70 mL de NMP, 15 mL de piridina e 0,1 g de LiCI.
Purificação: recristaiização a partir de metanol.
Rendimento: 1,57 g (58,2% de teoria).
Ponto de fusão: 334°C.
EM(EI): 495(M+).
Os seguintes procedimentos genéricos são usados nos exemplos de trabalho à menos que de outro modo indicado.
Procedimento de mistura:
A 59,91 g do polímero de aditivos pulverizados como indicado abaixo são adicionados, e misturados - amassados por 24 horas em um recipiente de vidro. Em geral, 4,5 g desta mistura são compostos a 230-240°C em um extrusor de pequena escala, parafuso duplo, de laboratório, recirculante e de co-rotação, por exemplo, o MicroCompounder de DACA Instruments (RTM), por um período de cerca de 4 minutos em uma velocidade de parafuso de 40 rpm, e subseqüentemente coletados em temperatura ambi98 ente. O polipropileno puro é similarmente tratado para produzir uma amostra controle branco.
Calorimetria de Exploração Diferencial (DSC):
Um instrumento Perkin-Elmer DSC (RTM) (Model DSC 7), operado em uma atmosfera de nitrogênio seco, é usado para as análises do comportamento de cristalização das várias misturas e amostras controles, de acordo com procedimentos padrões. Cerca de 5 a 10 mg de amostra são selados em um copo de alumínio, aquecidos de 130 a 230°C em uma taxa de 10°C/minuto, mantidos em 230°C por 5 minutos, e então subseqüentemente resfriados em uma taxa de 10°C/minuto para 50°C. Os dados representados como temperaturas de cristalização são as temperaturas de pico das exotermas nos termogramas que são anotados com resfriamento.
Análises termo-gravimétricas (TGA), Análises térmicas diferenciais (DTA):
Um instrumento automatizado Netzsch TGA/DTA (STA 409) (RTM) operado em nitrogênio é usado para as análises da estabilidade térmica e a temperatura de fusão. Como temperaturas de fusão o pico máximo da transição endotérmica é apresentado. Cerca de 10 mg de amostra são colocados em um cadinho de óxido de alumínio e aquecidos a partir de 50°C a 640°C em uma taxa de 10°C/minuto.
Moldagem de injeção:
A moldagem de injeção é realizada com um instrumento Microlnjector (DACA Instruments (RTM)). Cerca de 3,0 g do fio pelotizado são colocados sob uma camada de nitrogênio no barril a 260°C. Após o granulado ser completamente fundido, a fusão é injetada em um molde polido com uma pressão de cerca de 8 bar. A temperatura de molde é de 20°C. O espécime teste coletado tem um diâmetro de 2,5 cm e uma espessura de cerca de 1,11,2 mm.
Caracterização ótica (turvação):
A turvação é medida em um instrumento haze-gard plus (BYK,
Gardner (RTM), illumination CIE-C) em temperatura ambiente. O instrumento haze-gard plus conforma-se a ASTM D-1003. Os valores de turvação são
medidos entre 12-24 horas após obtenção de amostras por moldagem de injeção.
Módulos de flexão:
Os módulos de flexão de espécimes de polímeros são medidos de acordo com condições padrões como descrito em ISSO 178.
Exemplo 1:
Homopolímero propileno pulverizado (PP homo) de índice de escoamento de fusão de 3,8 dg/minuto (medido a 230°C e 2,16 kg) é intensamente misturado com adequadas quantidades do respectivo agente nucleante como indicado nas tabelas abaixo e, além disso em qualquer caso, com 0,05% de estearato de cálcio (limpador de ácido) e 0,10% de fosfito de tris-[2,4-di-t-butil fenila] e 0,05% de tetrakis-[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila como co-aditivos.
Composição das formulações é realizada a 240°C sobre um extrusor de parafuso duplo de laboratório de co-rotação, como o MicroCompounder de DACA Instruments (RTM), por um período de cerca de 4 minutos em uma velocidade de parafuso de 40 rpm, então resfriada para temperatura ambiente e pelotizada.
Moldagem de injeção é subseqüentemente realizada em um Microlnjector (DACA Instruments (RTM)). O composto pelotizado é completamente fundido sob atmosfera de nitrogênio em uma temperatura de barril de 260°C e então injetado fundido em um molde polido em uma pressão de cerca de 8 bar em 20°C de temperatura de molde. Os resultantes espécimes com um diâmetro de 2,5 cm e uma espessura de cerca de 1,1-1,2 mm são usados para ainda caracterização de propriedades do polímero nucleado.
A temperatura de cristalizçaão (TcrjSt.) θ turvação da composição de polipropileno assim como a espessura do espécime de teste (placa) e a concentração do aditivo de acordo com a presente invenção são listadas nas tabelas que se seguem.
100
Tabela 1a:
| Aditivo de acordo com a presente invenção | Composto | T cryst, [°C] | Turvação [%] | Concentração [% em peso] | Espessura [mm] |
| Nonhum | - | 110,3 | 67,2 | - | 1,0 |
| 1,3,5-tris-[2,2-di metil propionilamino]benzeno | I-2 (Exemplo B) | 124,8 | 17,0 | 0,15 | 1,1 |
| 1,3,5-tris-[2-etil butirilamino]benzeno | 1-10 (Exemplo J) | 119,3 | 24,2 | 0,15 | 1,1 |
| 1,3,5-tris-[2,2-d imetilbutirilamino]benzeno | 1-11 (Exemplo K) | 124,9 | 19,5 | 0,15 | 1,1 |
| 1 -isobutilamino-3,5-bis[pivaloilamino]benzeno | 1-16 (Exemplo P) | 122,3 | 27,6 | 0,15 | 1,1 |
| 2,2-dimetilbutirilamino- 3,5-bis-[pivaloilamino] benzeno | 1-17 (Exemplo Q) | 125,4 | 20,0 | 0,15 | 1,1 |
| 3,3-dimetilbutirilamino- 3,5-bis-[pivaloilamino] benzeno | 1-18 (Exemplo R) | 120,2 | 24,0 | 0,15 | 1,1 |
| 1,3-bis-[isobutirilamino]-5pivaloilaminobenzeno | 1-19 (Exemplo S) | 116,8 | 26,9 | 0,15 | 1,1 |
| 1,3-bis-[isobutirilamino]-5- (2,2-dimetilbutiril)amino- benzeno | I-20 (Exemplo T) | 120,3 | 24,8 | 0,15 | 1,1 |
| 1,3-bis-[2,2-dimetil butiril- amino]-5-pivaloilamino- benzeno | I-22 (Exemplo V) | 126,0 | 23,1 | 0,15 | 1,1 |
| 1,3-bis-[2,2-dimetil butirilamino]-5-isobutirilaminobenzeno | I-23 (Exemplo W) | 122,5 | 20,2 | 0,15 | 1,1 |
| 1,3-bis-[2,2-d imetil butiril- amino]-5-(3,3-dimetilbu- tiril)aminobenzeno | I-24 (Exemplo X) | 119,6 | 25,2 | 0,15 | 1,1 |
Tabela 1b:
| Aditivo de acordo com a presente invenção | Composto | Tcryst, [°C] | Turvação [%] | Concentração [% em peso] | Espessura [mm] |
| Nonhum | - | 110,3 | 67,2 | - | 1,0 |
| Ν,Ν'-di-t-butil diamida de ácido 5-pivaloilamino isoftálico | UUUa (Exemplo III-2) | 124,7 | 26,0 | 0,15 | 1,1 |
| Ν,Ν'-diciclohexil diamida de ácido 5-pivaloil- amino isoftálico | UUUd (Exemplo III-5) | 117,2 | 32,1 | 0,15 | 1,2 |
| N-t-butil-3,5-bis-[piva- loilamino]benzamida | ZZZb (Exemplo II-2) | 123,1 | 23,7 | 0,15 | 1,1 |
101
| Aditivo de acordo com a presente invenção | Composto | Tcryst, [°C] | Turvação [%] | Concentração [% em peso] | Espessura [mm] |
| N-ciclopentil-3,5-bis-[pi- valoilamino]benzamida | ZZZn (Exemplo 11-15) | 119,0 | 32,3 | 0,15 | 1,2 |
| N-ciclohexil-3,5-bis-[pi- valoilamino]benzamida | ZZZs (Exemplo il-20) | 116,4 | 33,2 | 0,15 | 1,1 |
| N-isopropil-3,5-bis-[pi- valoilamino]benzamida | ZZZw (Exemplo II-24) | 120,5 | 26,8 | 0,15 | 1,1 |
| N-t-butil-3,5-bis-[2,2-di- metilbutirilamino]ben- zamida | ZZZy (Exemplo II-26) | 124,1 | 20,5 | 0,15 | 1,1 |
Exemplo 2
O polímero pulverizado (copolímero randômico de propileno (PP raco); um tipo com um índice de escoamento de fusão de 7,5 dg/minuto; um outro tipo com um índice de fusão de 12 dg/minuto; medido a 230°C e 2,16 kg, respectivamente; ou polietileno metaloceno grau de densidade média com um índice de escoamento de fusão de 2,8 dg/minuto; medido a 190°C e 5,0 kg) é intensamente homogeneizado em um misturador Henschel com adequadas quantidades do respectivo agente nucleante e opcionalmente com ainda co-aditivos, tal como uma combinação de antioxidante de fosfito de tris-[2,4-di-t-butil fenila] e tetrakis-[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila em uma razão em peso de 2:1; limpadores de ácido, por exemplo, estearato de cálcio ou zinco; e/ou opcionalmente outros auxiliares de procesamento ou ainda aditivos, como aqueles indicados nas tabelas abaixo.
Então cada formulação é composta sobre um Berstorff ZE
25x46D (RTM) a 220-250°C. O fio obtido é resfriado em água e pelotizado. As pelotas obtidas são usadas para moldagem de injeção sobre um Arburg 320 S (RTM) a 200-240°C para preparar placas de cerca de 1 mm de tamanho de 85 mm x 90 mm. A turvação das placas é medida em um Haze-Gard plus (BYK Gardner (RTM)) de acordo com ASTM D-1003.
A temperatura de cristalizçaão (Tcrist.) e turvação da composição de polímero assim como a espessura do espécime de teste (placa) e a concentração do aditivo de acordo com a presente invenção são listadas nas
102
1U tabelas que se seguem.
Tabela 2a:
Copolímero randômico de propileno com um índice de escoamento de fusão de 7,5 dg/minuto (medido a 230°C e 2,16 kg); composto a
240°C e moldado por injeção em 235°C.
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil fenila]
0,033% de tetrakis-[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila
0,020% de estearato de cálcio
O aditivo de acordo com a presente invenção é primeiro combinado-seco com o copolímero randômico de propileno e composto em um concentrado 1%. Então, o concentrado é combinado - sacola com o copolímero randômico de propileno e novamente composto antes de subseqüente moldagem de injeção.
| Aditivo de acordo com a presente invenção | Composto | fcryst, [°C] | Turvação [%] | Concentração [% em peso] | Espessura [mm] |
| Nonhum | - | 97,2 | 35,1 | - | 1,0 |
| 1,3,5-tris-[2,2- dimetilpropionila- mino]benzeno | I-2 (Exemplo B) | 105,7 | 14,2 | 0,010 | 1,0 |
| 1,3,5-tris-[2,2- dimetilpropionila- mino]benzeno | I-2 (Exemplo B) | 108,2 | 13,4 | 0,015 | 1,0 |
| 1,3,5-tris-[2,2- dimetilpropionila- mino]benzeno | I-2 (Exemplo B) | 105,5 | 15,4 | 0,020 | 1,0 |
Tabela 2b:
Copolímero randômico de propileno com um índice de escoamento de fusão de 7,5 dg/minuto (medido em 230°C e 2,16 kg); composto a 250°C e moldado por injeção em 235°C.
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil feni20 la]
0,033% de tetrakis-[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de
103 pentaeritritila
0,020% de estearato de cálcio
1% do aditivo de acordo com a presente invenção e 0,2% dos co-aditivos individuais, respectivamente, como indicado na tabela abaixo são cada um combinados secos com copolímero randômico de propileno pulverizado e compostos em concentrados. Então, pelotas de copolímero randômico de propileno são combinadas - bolsa com estes concentrados em apropriadas razões de let-down de acordo com as concentrações finais dadas na tabela.
| Aditivo de acordo com a presente invenção (Concentração em % em peso) | Composto | Co-aditivo (Concentração em peso) | T cryst, [°Cj | Turvação [%] | Espessura [mm] |
| 1,3,5-tris-[2,2dimetilpropionilaminojbenzeno (0,02) | I-2 (Exemplo B) | Nonhum | 105,4 | 14,2 | 1,0 |
| 1,3,5-tris-[2,2dimetilpropionilaminojbenzeno (0,02) | I-2 (Exemplo B) | HALS-1 (50 ppm) | 103,6 | 12,7 | 1,0 |
| 1,3,5-tris-[2,2dimetilpropionilamino]benzeno (0,02) | i-2 (Exemplo B) | HALS-2 (20 ppm) | 105,3 | 12,3 | 1,0 |
| 1,3,5-tris-[2,2dimetilpropionilaminojbenzeno (0,02) | i-2 (Exemplo B) | Erucamide (50 ppm) | 104,0 | 12,5 | 1,0 |
HALS-1 é sebacato de bis-(2,2,6,6-tetrametil-4-piperidila), comercialmente disponível, por exemplo, como TINUVIN 770 (RTM).
HALS-2 é o condensado de 1 -(2-hidróxi etil)-2,2,6,6-tetrametil-4hidróxi piperidina e ácido succínico, comercialmente disponível, por exemplo como TINUVIN 622 (RTM).
Erucamida é, por exemplo, comercialmente disponível como
ATMER 1753 (RTM).
Tabela 2c:
Copolímero randômico de propileno com um índice de escoamento de fusão de 7,5 dg/minuto (medido em 230°C e 2,16 kg); composto e moldado por injeção em 240°C.
104
U3
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil fenila]
0,033% de tetrakis-[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila
0,075% de estearato de zinco
O aditivo de acordo com a presente invenção e o co-aditivo indicado na tabela abaixo são combinados secos com copolímero randômico de propileno pulverizado, subseqüentemente composto e moldado por injeção em placas.
| Aditivo de acordo com a presente invenção (Concentração em % em peso) | Composto | Co-aditivo (Concentração em peso) | Tcryst, [°C] | Turvação [%] | Espessura [mm] |
| Nonhum | - | Nonhum | 96,9 | 36,4 | 1,0 |
| Nonhum | - | AdSperse 868 (RTM) (0.50) | 95,3 | 36,3 | 1,0 |
| Nonhum | - | Licowax PE 520 (RTM) (0.50) | 97,3 | 35,2 | 1,0 |
| 1,3,5-tris-[2,2-dimetilpropionilaminojbenzeno (0,02) | I-2 (Exemplo B) | Nonhum | 104,3 | 14,2 | 1,0 |
| 1,3,5-tris-[2,2-dimetilpropionilaminojbenzeno (0,02) | I-2 (Exemplo B) | AdSperse 868 (RTM) (0.50) | 106,1 | 13,8 | 1,0 |
| 1,3,5-tris-[2,2-d imetilpropionilaminojbenzeno (0,02) | I-2 (Exemplo B) | Licowax PE 520 (RTM) (0.50) | 105,6 | 13,5 | 1,0 |
AsSperse 868 (RTM) é uma cera Fischer-Tropsch comercialmente disponível.
Licowax PE 520 (RTM) é uma cera de polietileno Ziegler-Natta comercialmente disponível.
Tabela 2d:
Copolímero randômico de propileno com um índice de escoamento de fusão de 12 dg/minuto (medido a 230°C e 2,16 kg); composto duas vezes a 250°C e moldado por injeção em 235°C.
105
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butii fenila]
0,033% de tetrakis[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila
0,075% de estearato de zinco
Todos os componentes são combinados pulverizados para composição, então, moldados por injeção em placas.
| Aditivo de acordo com a presente invenção | Composto | T crist. [°C] | Turva- ção [%] | Concen- tração [% em peso] | Espes- sura [mm] |
| Nenhum | - | 96,7 | 50,7 | - | 1,0 |
| Ν,Ν'-di-t-butil diamida de ácido 5-pivaloilamino isoftálico | UUUa (Exemplo III-2) | 106,8 | 30,2 | 0,05 | 1,0 |
| Ν,Ν’-di-t-octil diamida de ácido 5-pivaloilamino isoftálico | UUUb (Exemplo III-3) | 98,3 | 39,3 | 0,05 | 1,0 |
| N-t-butil-3,5-bis-(pivaloil- amino)benzamida | ZZZb Exemplo II-2) | 109,2 | 24,4 | 0,15 | 1,0 |
Tabela 2e:
Copolímero randômico de propileno com um índice de escoa10 mento de fusão de 7,5 dg/minuto (medido a 230°C e 2,16 kg); composto a
240°C e moldado por injeção a 235°C.
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil fenila]
0,033% de tetrakis[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila
Os aditivos de acordo com a presente invenção e todos os coaditivos indicados são primeiro combinados - secos, então compostos e subseqüentemente moldados por injeção em placas.
106
| Aditivo de acordo com a presente invenção | Composto | Tcrist. [°C] | Turvação [%] | Concen- tração [% em peso] | Espes- sura [mm] |
| Nenhun | - | 96,9 | 36,4 | - | 1,0 |
| N-(t-octil)-3,5-bis- (pivaloilamino)benzamida | ZZZc (Exemplo II-3) | 97,4 | 34,9 | 0,020 | 1,0 |
| N-(1,1 -dimetilpropil)-3,5- bis-(pivaloilamino)benza- mida | ZZZd (Exemplo II-4) | 107,6 | 22,7 | 0,015 | 1,0 |
| N-(t-octil)-3,5-bis-(isobu- tirilamino)benzamida | ZZZe (Exemplo II-5) | 98,5 | 32,0 | 0,020 | 1,0 |
Tabela 2f:
Copolímero randômico de propileno com um índice de escoamento de fusão de 7,5 dg/minuto (medido a 230°C e 2,16 kg); composto a 250°C e moldado por injeção a 235°C.
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil fenila]
0,033% de tetrakis[3-(3,5-di-t-butil-4-hidróxi fenil) propionato] de pentaeritritila
0,020% de estearato de cálcio
O aditivo de acordo com a presente invenção é primeiro combi10 nado seco com o copolímero randômico de propileno e composto em um concentrado 1%. Então, o concentrado é combinado - sacola com as pelotas de copolímero randômico de propileno e novamente composto antes de moldagem de injeção.
| Aditivo de acordo com a presente invenção | Composto | Tcrist. [°C] | Turvação [%] | Concen- tração [% em peso] | Espes- sura [mm] |
| Nenhun | - | 93,6 | 36,7 | - | 1,0 |
| N-t-Butil-3,5-bis- (pivaloilamino)benzamida | ZZZb (Exemplo II-2) | 105,4 | 16,2 | 0,010 | 1,0 |
| N-t-Butil-3,5-bis- (pivaloilamino)benzamida | ZZZb (Exemplo II-2) | 107,3 | 15,4 | 0,015 | 1,0 |
| N-t-Butil-3,5-bis- (pivaloilamino)benzamida | ZZZb (Exemplo II-2) | 107,2 | 17,3 | 0,020 | 1,0 |
107 /Llé
Tabela 2q:
Copolímero randômico de propileno com um índice de escoamento de fusão de 7,5 dg/minuto (medido a 230°C e 2,16 kg); composto duas vezes 240°C e moldado por injeção a 235°C.
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil fenila]
0,033% de tetrakis[3-(3,5-di-t-butil-4-hidróxi fenil) propionatoj de pentaeritritila
O aditivo de acordo com a presente invenção e todos os coaditivos indicados são combinados - secos, então compostos e moldados por injeção em placas.
| Aditivo de acordo com a presente invenção (concentração em % em peso) | Composto | Co-aditivo (concnetração em % em peso) | T crist [°C], | Turva- ção [%] | Espessura [mm] |
| Nenhum | - | Nenhum | 99,9 | 34,7 | 1,0 |
| N-t-butil-3,5-bis-(piva- loilamino)benzamida (0,015) | ZZZb (Exemplo II-2) | AdSperce 868 (RTM) (0,50) | 106,9 | 18,3 | 1,0 |
| N-(1,1 -dimetilpropil)3,5-bis-(pivaloilamino) benzamida (0,015) | ZZZd (Exemplo ll-4) | AdSperce 868 (RTM) (0,50) | 106,6 | 20,4 | 1,0 |
AdSperse 868 (RTM) é uma cera Fischer-Tropsch comercialmente disponível.
Tabela 2h:
Polietileno metaloceno grau de densidade média com um índice 15 de escoamento de fusão de 2,8 dg/minuto (medido a 190°C e 5,0 kg); composto em 220°C e moldado por injeção em 230°C.
Estabilização base: 0,067% de fosfito de tris-[2,4-di-t-butil fenila] 0,033% de tetrakis[3-(3,5-di-t-butil-4-hidróxi fenil) propionatoj de pentaeritritila
0,050% de estearato de cálcio
Todos os componentes são combinados pulverizados antes de composição, então, moldados por injeção em placas.
108
| Aditivo de acordo com a presente invenção | Composto | Módulo de flexão [MPa] | Turvação [%] | Concentração [% em peso] | Espessura [mm] |
| Nenhum | - | 409 | 71,4 | - | 1,0 |
| 1,3,5-tris-[2,2- dimetilpropionila- minojbenzeno | i-2 (Exemplo B) | 427 | 62,6 | 0,15 | 1,0 |
Claims (42)
- REIVINDICAÇÕES1. Composição, caracterizada pelo fato de que contém (a) poliolefina e (b) 0,0001 a 5%, em relação ao peso do componente (a), de um ou mais compostos da fórmula (I), (II) ou (III)I I zC .C.o r2 o r3 ondeRi, R2 e R3, ou Yi, Y2 e Y3, ou Zi, Z2 e Z3 independentemente um do outro são alquila C3-Cw ramificada.
- 2. Composição de acordo com a reivindicação 1, caracterizada 10 pelo fato de que o composto da fórmula (I) é1,3,5-tris[2,2-dimetilpropionilamino]benzeno,Petição 870160037195, de 19/07/2016, pág. 5/181.3.5- tris[2-metilpropionilamino]benzeno,1.3.5- tris[3,3-dimetilbutirilamino]benzeno,1.3.5- tris[2-etilbutirilamino]benzeno,1.3.5- tris[2,2-dimetilbutirilamino]benzeno,5 1 -isobutirilamino-3,5-bis[pivaloilamino]benzeno,2.2- dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno,
- 3.3- dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno,1.3- bis[isobutirilamino]-5-pivaloilamino benzeno,1.3- bis[isobutirilamino]-5-(2,2-dimetilbutiril)aminobenzeno,10 1,3-bis-[isobutirilamino]-5-(3,3-dimetilbutiril)aminobenzeno,1.3- bis-[2,2-dimetilbutirilamino]-5-pivaloilaminobenzeno,1.3- bis-[2,2-dimetilbutirilamino]-5-isobutirilaminobenzeno,1.3- bis[2,2-dimetilbutirilamino]-5-(3,3dimetilbutiril)aminobenzeno,15 1,3-bis[3,3-dimetilbutirilamino]-5-pivaloilaminobenzeno,1.3- bis[3,3-dimetilbutirilamino]-5-isobutirilaminobenzeno ou1.3- bis-[3,3-dimetilbutirilamino]-5-(2,2dimetilbutirilamino)aminobenzeno.3. Composição de acordo com a reivindicação 1, caracterizada20 pelo fato de que o composto da fórmula (II) éN-terc-butil-3,5-bis-(3-metilbutirilamino)benzamida,N-terc-butil-3,5-bis-(pivaloilamino)benzamida,N-t-octil-3,5-bis-(pivaloilamino)benzamida,N-(1,1 -dimetil propil)-3,5-bis-(pivaloilamino)benzamida,25 N-(t-octil)-3,5-bis-(isobutirilamino)benzamida,N-(terc-butil)-3,5-bis(pivaloilamino)benzamida,N-(3-metil butil)-3,5-bis-(3-metilbutirilamino)benzamida, N-(3-metil butil)-3,5-bis-(pivaloilamino)benzamida,N-(3-metil butil)-3,5-bis-(4-metilpentanoilamino)benzamida,30 N-isopropil-3,5-bis-(pivaloilamino)benzamida,N-isopropil-3,5-bis-(isobutirilamino)benzamida,N-terc-butil-3,5-bis-(2,2-dimetilbutirilamino)benzamida, ouPetição 870160037195, de 19/07/2016, pág. 6/18N-t-octil-3,5-bis-(2,2-dimetilbutirilamino)benzamida.
- 4. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que o composto da fórmula (III) éN,N'-di-terc-butil diamida de ácido 5-pivaloilamino isoftálico,
- 5 N,N'-di-t-octil diamida de ácido 5-pivaloilamino isofátlico,N,N'-di-terc-butil diamida de ácido 5-(2,2-dimetilbutirilamino) isoftálico ouN,N'-di-t-octil diamida de ácido 5-(2,2-dimetilbutirilamino) isoftálico.10 5. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que R1, R2 e R3 ou Y1, Y2 e Y3 ou Z1, Z2 e Z3 independentemente um do outro são 1-metil etila, 2-metil propila, 1-metil propila, terc-butila, 1metil butila, 2-metil butila, 3-metil butila, 1,1-dimetil propila, 1-etil propila, ou terc-butil metila.15
- 6. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que R1, R2 e R3 ou Y1, Y2 e Y3 ou Z1, Z2 e Z3 são idênticos.
- 7. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que R1, R2 e R3 ou Y1, Y2 e Y3 ou Z1, Z2 e Z3 são idênticos e são 1-metil etila, 1-metil propila, 2-metil propila, terc-butila, 1,1-dimetil propila, ou20 terc-butil metila.
- 8. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que o componente (b) é um composto da fórmula (I), onde R1, R2 e R3 são terc-butila.
- 9. Composição de acordo com a reivindicação 1, caracterizada 25 pelo fato de que R1, R2 e R3 ou Y1, e Y3 ou Z1, independentemente uns dos outros são isopropila, s-butila, terc-butila, 1-metil butila, 1-metil pentila, 1-etil pentila, 1,1-dimetil propila, 2,2-dimetil propila, 1,1-dimetil butila, 1,1-dimetil hexila, 1-etil propila ou 1-propil butila.
- 10. Composição de acordo com a reivindicação 1, caracteriza30 da pelo fato de que Y2, ou Z2 e Z3 independentemente uns dos outros são isopropila, s-butila, terc-butila, 1,1-dimetil propila, 1,2-dimetil propila, 2,2dimetil propila ou t-octila.Petição 870160037195, de 19/07/2016, pág. 7/18
- 11. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que os radicais R1, R2 e R3 ou Y1, Y2 e Y3 ou Z1, Z2 e Z3 são terc-butila.
- 12. Composição de acordo com a reivindicação 1, caracteriza5 da pelo fato de que contém como componente adicional (c-1) um ou mais agentes nucleantes convencionais.
- 13. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que contém como componente adicional (c-2) um ou mais compostos amina estereamente impedida.10
- 14. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que contém como componente adicional (c-3) um ou mais lubrificantes.
- 15. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que tem um valor de turvação que é menor que 62%; o valor15 de turvação sendo medido em uma placa de 1,0 - 1,2 mm de espessura.
- 16. Composição de acordo com a reivindicação 15, caracterizada pelo fato de que tem uma turvação de 2 a 62%.
- 17. Composição de acordo com a reivindicação 15, caracterizada pelo fato de que a composição tem uma turvação de 2 a 50%.20
- 18. Composição de acordo com a reivindicação 15, caracterizada pelo fato de que a composição tem uma turvação de 2 a 40%.
- 19. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que componente (a) é um homopolímero de polipropileno, copolímero randômico, copolímero alternante ou segmentado, copolímero de25 bloco ou uma combinação de polipropileno com um outro polímero sintético.
- 20. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que componente (a) é um homopolímero de polipropileno.
- 21. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que componente (a) é um copolímero randômico de polipro30 pileno, copolímero alternante ou segmentado ou copolímero de bloco contendo um ou mais comonômeros selecionados do grupo consistindo em etileno, alfa-olefina C4-C20, vinil ciclohexano, vinil ciclohexeno, alcanodieno C4Petição 870160037195, de 19/07/2016, pág. 8/18C20, cicloalcanodieno C5-Ci2 e derivados norborneno.
- 22. Processo para provimento de uma poliolefina com um valor de turvação que é menor que 62%; o valor de turvação sendo medido em uma placa de 1,0 - 1,2 mm de espessura, caracterizado pelo fato de que5 compreende incorporação na poliolefina de 0,0001 a 5%, em relação ao peso da poliolefina, de um ou mais compostos da fórmula (I), (II) ou (III), como definidos na reivindicação 1.
- 23. Uso de um composto da fórmula (I), (II), ou (III), como definido na reivindicação 1, caracterizado pelo fato de ser como agente de redu10 ção de turvação para poliolefinas.
- 24. Processo para aumento de temperatura de cristalização de uma poliolefina, caracterizado pelo fato de que compreende a incorporação na poliolefina de 0,0001 a 5%, em relação ao peso da poliolefina, de um ou mais compostos da fórmula (I), (II) ou (III), como definidos na reivindicação15 1.
- 25. Uso de um composto da fórmula (I), (II), ou (III), como definido na reivindicação 1, caracterizado pelo fato de ser como agente nucleante para poliolefinas.
- 26. Artigo conformado, caracterizado pelo fato de ser obtenível 20 a partir de uma composição como definida na reivindicação 1.
- 27. Artigo conformado de acordo com a reivindicação 26, caracterizado pelo fato de que é um artigo moldado.
- 28. Artigo conformado de acordo com a reivindicação 26, caracterizado pelo fato de que a moldagem é efetuada por injeção, sopro,25 compressão, roto-moldagem, ou moldagem de lama ou extrusão.
- 29. Artigo conformado de acordo com a reivindicação 26, caracterizado pelo fato de que é um filme, fibra, perfil, tubo, garrafa, tanque ou recipiente.
- 30. Filme orientado monoaxialmente ou um filme orientado bia30 xialmente, caracterizado pelo fato de ser obtenível a partir de uma composição como definida na reivindicação 1.
- 31. Sistema multicamadas, caracterizado pelo fato de que umaPetição 870160037195, de 19/07/2016, pág. 9/18 ou mais camadas contêm uma composição como definida na reivindicação 1.
- 32. Composto, caracterizado pelo fato de que apresenta fórmula (IA), (IIA), ou (IIIA) (IA) onde Ri, R2 e R3, ou Yi, Y2 e Y3, ou Zi, Z2 e Z3 independentemente um do outro são alquila C3-Cw ramificada e o composto N-terc-butil-3,5-bis-(pivaloilamino)benzamida é renunciado.
- 33. Composto da fórmula (IA) de acordo com a reivindicação 32, caracterizado pelo fato de que Ri, R2 e R3 são terc-butila.
- 34. Composto da fórmula (IA), (IIA) ou (IIIA) de acordo com a reivindicação 32, caracterizado pelo fato de que é1.3.5- tris[2,2-dimetilpropionilamino]benzeno,1.3.5- tris[2-metilpropionilamino]benzeno,1.3.5- tris[3,3-dimetilbutirilamino]benzeno,Petição 870160037195, de 19/07/2016, pág. 10/181.3.5- tris[2-etilbutirilamino]benzeno,1.3.5- tris[2,2-dimetilbutirilamino]benzeno, 1-isobutirilamino-3,5-bis[pivaloilamino]benzeno,2.2- dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno,5 3,3-dimetilbutirilamino-3,5-bis[pivaloilamino]benzeno,1.3- bis[isobutirilamino]-5-pivaloilamino benzeno,1.3- bis[isobutirilamino]-5-(2,2-dimetilbutiril)aminobenzeno,1.3- bis-[isobutirilamino]-5-(3,3-dimetilbutiril)aminobenzeno,1.3- bis-[2,2-dimetilbutirilamino]-5-pivaloilaminobenzeno,10 1,3-bis-[2,2-dimetilbutirilamino-5-isobutirilaminobenzeno,1.3- bis[2,2-dimetilbutirilamino]-5-(3,3dimetilbutiril)aminobenzeno,1.3- bis[3,3-dimetilbutirilamino]-5-pivaloilaminobenzeno,1.3- bis[3,3-dimetilbutirilamino]-5-isobutirilaminobenzeno,15 1,3-bis-[3,3-dimetilbutirilamino]-5-(2,2dimetilbutirilamino)aminobenzeno,N-terc-butil-3,5-bis-(3-metilbutirilamino)benzamida,N-t-octil-3,5-bis-(pivaloilamino)benzamida,N-(1,1 -dimetil propil)-3,5-bis-(pivaloilamino)benzamida,20 N-(t-octil)-3,5-bis(isobutirilamino)benzamida,N-(terc-butil)-3,5-bis-(pivaloilamino)benzamida,N-(3-metil butil)-3,5-bis-(3-metilbutirilamino)benzamida, N-(3-metil butil)-3,5-bis-(pivaloilamino)benzamida,N-(3-metil butil)-3,5-bis-(4-metilpentanoilamino)benzamida,25 N-isopropil-3,5-bis-(pivaloilamino)benzamida,N-isopropil-3,5-bis-(isobutirilamino)benzamida, N-terc-butil-3,5-bis-(2,2-dimetilbutirilamino)benzamida, N-t-octil-3,5-bis-(2,2-dimetilbutirilamino)benzamida N,N'-di-terc-butil diamida de ácido 5-pivaloilamino isoftálico,30 N,N'-di-t-octil diamida de ácido 5-pivaloilamino isofátlico,N,N'-di-terc-butil diamida de ácido 5-(2,2-dimetilbutirilamino) isoftálico ouPetição 870160037195, de 19/07/2016, pág. 11/18N,N'-di-t-octil diamida de ácido 5-(2,2-dimetilbutirilamino) isoftálico.
- 35. Mistura, caracterizada pelo fato de que contém um composto da fórmula (IA), (IIA), ou (IIIA), como definido na reivindicação 32, e um5 composto de amina estereamente impedida ou um lubrificante.
- 36. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que adicionalmente contém um aditivo convencional selecionado do grupo consistindo em mono fenóis alquilados,10 alquil tiometil fenóis, hidroquinonas e hidroquinonas alquiladas, tocoferóis, tiodifenil éteres hidroxilados, alquilideno bisfenóis,15 compostos O-, N- e S- de benzila, malonatos hidróxi benzilados, compostos hidróxi benzila aromáticos, compostos triazina, benzil fosfonatos,20 acilamino fenóis, ésteres de ácido beta-(3,5-di-t-butil-4-hidróxi fenil) propiônico, ésteres de ácido beta-(5-t-butil-4-hidróxi-3-metil fenil) propiônico, ésteres de ácido beta-(3,5-diciclohexil-4-hidróxi fenil) propiôni25 co, ésteres de ácido 3,5-di-t-butil-4-hidróxifenil acético, amidas de ácido beta-(3,5-di-t-butil-4-hidróxi fenil) propiônico, ácido ascórbico, antioxidantes amínicos,30 2-(2'-hidróxi fenil) benzo triazóis,2-hidróxi benzo fenonas, ésteres de ácidos benzoicos substituídos e não-substituídosPetição 870160037195, de 19/07/2016, pág. 12/18 acrilatos, compostos de níquel, aminas estereamente impedidas, oxamidas,2-(2-hidróxi fenil)-1,3,5-triazinas, desativadores de metais, fosfitos e fosfonitos, hidroxilaminas, nitronas, tiosinergísticos, limpadores de peróxido, estabilizadores de poliamida, co-estabilizadores básicos, agentes nucleantes convencionais, e benzofuranonas e indolinonas.
- 37. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que adicionalmente contém uma hidroxilamina ou uma nitrona.
- 38. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que superfície é tratada por descarga de corona.
- 39. Composição de acordo com a reivindicação 1, caracterizada pelo fato de que superfície é tratada por descarga de corona, onde o componente (a) é um homopolímero de polipropileno, e o componente (b) é1,3,5-tris[2,2-dimetilpropionilamino]benzeno.
- 40. Artigo conformado de acordo com a reivindicação 26, caracterizado pelo fato de que é um tecido ou não-tecido obtenível por fiação de fibra a partir de uma composição como definida na reivindicação 1.
- 41. Artigo conformado de acordo com a reivindicação 26, caracterizado pelo fato de que é um tecido ou não-tecido obtenível por fiação de fibra a partir de uma composição contendo, como componente (a), um homopolímero de polipropileno, e, como componente (b), 1,3,5-tris[2,2dimetilpropionilamino]benzeno.Petição 870160037195, de 19/07/2016, pág. 13/18
- 42. Artigo conformado de acordo com a reivindicação 26, caracterizado pelo fato de que é um filtro feito de fibras.Petição 870160037195, de 19/07/2016, pág. 14/18
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP03405084.9 | 2003-02-14 | ||
| EP03405084 | 2003-02-14 | ||
| EP03103835 | 2003-10-16 | ||
| EP03103835.9 | 2003-10-16 | ||
| PCT/EP2004/050095 WO2004072168A2 (en) | 2003-02-14 | 2004-02-09 | Resin compositions |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0407255A BRPI0407255A (pt) | 2006-01-31 |
| BRPI0407255B1 true BRPI0407255B1 (pt) | 2018-03-13 |
Family
ID=32870778
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0407255-3A BRPI0407255B1 (pt) | 2003-02-14 | 2004-02-09 | Composições de resina, artigo conformado, processos para provimento de uma poliolefina e para o aumento de temperatura de cristalização desta, filme orientado monoaxial ou biaxialmente, sistemas multicamadas, compostos e seus usos, e mistura |
Country Status (12)
| Country | Link |
|---|---|
| US (1) | US7790793B2 (pt) |
| EP (1) | EP1592738B1 (pt) |
| JP (1) | JP4654177B2 (pt) |
| KR (1) | KR101074723B1 (pt) |
| AU (1) | AU2004210907B2 (pt) |
| BR (1) | BRPI0407255B1 (pt) |
| CA (1) | CA2514034C (pt) |
| ES (1) | ES2825902T3 (pt) |
| MY (1) | MY140740A (pt) |
| RU (1) | RU2358990C2 (pt) |
| TW (1) | TWI348477B (pt) |
| WO (1) | WO2004072168A2 (pt) |
Families Citing this family (74)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| MY145424A (en) * | 2005-02-07 | 2012-02-15 | Ciba Holding Inc | Functionalized esters, amides or urethanes of perfluorinated alcohols or amines as surface modifiers |
| US7786203B2 (en) | 2005-09-16 | 2010-08-31 | Milliken & Company | Polymer compositions comprising nucleating or clarifying agents and articles made using such compositions |
| KR20080049067A (ko) * | 2005-09-28 | 2008-06-03 | 시바 홀딩 인코포레이티드 | 중합체 용융물의 유동성을 개선하는 방법 |
| WO2007039521A1 (en) * | 2005-09-30 | 2007-04-12 | Ciba Specialty Chemicals Holding Inc. | Microporous films |
| US7572849B2 (en) | 2005-11-18 | 2009-08-11 | Chemtura Corporation | Urea phenyl derivatives and their use as polypropylene nucleating agents |
| US7585909B2 (en) | 2005-11-22 | 2009-09-08 | Chemtura Corporation | β-crystalline polypropylenes |
| US7390351B2 (en) * | 2006-02-09 | 2008-06-24 | 3M Innovative Properties Company | Electrets and compounds useful in electrets |
| BRPI0711647B1 (pt) | 2006-05-16 | 2018-06-05 | Basf Schweiz Ag | Películas sopradas por mono e múltiplas camadas |
| US7569630B2 (en) | 2006-06-14 | 2009-08-04 | Chemtura Corporation | β-Crystalline polypropylenes |
| US7714035B1 (en) * | 2006-07-05 | 2010-05-11 | Nibco, Inc. | Plumbing manifolds |
| US20080249269A1 (en) * | 2007-04-05 | 2008-10-09 | Hui Chin | Electret materials |
| US7920780B2 (en) * | 2008-04-16 | 2011-04-05 | Canon Kabushiki Kaisha | Image stabilization apparatus, imaging apparatus, and optical apparatus |
| CN102137893B (zh) * | 2008-08-28 | 2013-03-27 | 株式会社Adeka | 聚烯烃系树脂组合物 |
| WO2010068971A1 (en) * | 2008-12-18 | 2010-06-24 | Dymon Pallets Pty Ltd | Biaxially oriented polyethylene terephthalate (pet) pallet |
| WO2010069854A2 (en) * | 2008-12-19 | 2010-06-24 | Basf Se | Modified polyolefin waxes |
| CA2745372C (en) | 2008-12-22 | 2015-05-05 | Basf Se | Method of improving scratch resistance and related products and uses |
| CN102498165B (zh) * | 2009-09-18 | 2015-02-11 | 巴斯夫欧洲公司 | 具有改善抗刮性、改善机械稳定性和改善雾度的聚合物组合物 |
| WO2011071718A2 (en) * | 2009-12-07 | 2011-06-16 | Basf Se | Clarified polypropylene articles with improved optical properties and/or increased temperature of crystallization |
| CZ306740B6 (cs) | 2010-10-05 | 2017-06-07 | Basf Se | Způsob přípravy nukleovaného semikrystalického polyolefinu |
| WO2012055797A1 (en) | 2010-10-28 | 2012-05-03 | Lummus Novolen Technology Gmbh | Nonwoven and yarn polypropylene with additivation |
| JP5722002B2 (ja) * | 2010-11-10 | 2015-05-20 | 株式会社Adeka | ポリプロピレン系樹脂組成物 |
| US9855682B2 (en) | 2011-06-10 | 2018-01-02 | Columbia Insurance Company | Methods of recycling synthetic turf, methods of using reclaimed synthetic turf, and products comprising same |
| EP2537868B1 (en) * | 2011-06-21 | 2016-08-10 | Borealis AG | Process for the manufacture of alpha-nucleated polypropylene |
| KR20140057360A (ko) | 2011-08-29 | 2014-05-12 | 티코나 엘엘씨 | 고유동성 액정 중합체 조성물 |
| TW201319223A (zh) | 2011-08-29 | 2013-05-16 | Ticona Llc | 高流量液晶聚合物組合物 |
| US8906258B2 (en) | 2011-08-29 | 2014-12-09 | Ticona Llc | Heat-resistant liquid crystalline polymer composition having a low melting temperature |
| TW201319022A (zh) | 2011-08-29 | 2013-05-16 | Ticona Llc | 芳族醯胺化合物 |
| WO2013032979A1 (en) | 2011-08-29 | 2013-03-07 | Ticona Llc | Melt polymerization of low melt viscosity liquid crystalline polymers |
| TW201313884A (zh) | 2011-08-29 | 2013-04-01 | Ticona Llc | 液晶聚合物之固態聚合 |
| US8852730B2 (en) | 2011-08-29 | 2014-10-07 | Ticona Llc | Melt-extruded substrate for use in thermoformed articles |
| WO2013032967A1 (en) | 2011-08-29 | 2013-03-07 | Ticona Llc | Cast molded parts formed form a liquid crystalline polymer |
| WO2013032975A1 (en) | 2011-08-29 | 2013-03-07 | Ticona Llc | Thermotropic liquid crystalline polymer with improved low shear viscosity |
| US10259984B2 (en) | 2011-09-23 | 2019-04-16 | Synoil Fluids Holdings Inc. | Pyromellitamide gelling agents |
| EP2758483A4 (en) | 2011-09-23 | 2015-04-22 | Synoil Fluids Holdings Inc | PYROMELLITAMIDGELIERMITTEL |
| DE102011083434B4 (de) | 2011-09-26 | 2016-11-17 | Neue Materialien Bayreuth Gmbh | Verfahren zur Herstellung eines offenzelligen Polymerschaums |
| JP2014533321A (ja) | 2011-11-10 | 2014-12-11 | エフアールエックス ポリマーズ、インク. | 難燃性ポリアミド組成物 |
| US9328219B2 (en) | 2012-03-20 | 2016-05-03 | Basf Se | Polyamide compositions with improved optical properties |
| ES2563855T3 (es) | 2012-03-20 | 2016-03-16 | Basf Se | Composiciones de poliamida con propiedades ópticas mejoradas |
| US9882136B2 (en) * | 2012-05-31 | 2018-01-30 | Hodogaya Chemical Co., Ltd. | Organic electroluminescent device |
| EA032320B1 (ru) | 2012-10-15 | 2019-05-31 | Сауди Бейсик Индастриз Корпорейшн | Полиэтиленовая композиция, содержащая полипропилен, способ ее получения, ее применение и содержащее ее изделие |
| EP2948464A4 (en) | 2013-01-22 | 2016-12-07 | Frx Polymers Inc | PHOSPHORUS-BASED EPOXY BINDINGS AND COMPOSITIONS THEREOF |
| WO2014130275A2 (en) * | 2013-02-22 | 2014-08-28 | Ticona Llc | High performance polymer composition with improved flow properties |
| CN105264041A (zh) * | 2013-03-22 | 2016-01-20 | SynOil流体控股有限公司 | 酰胺支链芳烃胶凝剂 |
| US9217102B2 (en) | 2013-03-22 | 2015-12-22 | Synoil Fluids Holdings Inc. | Amide branched aromatic gelling agents |
| CN105358657A (zh) | 2013-06-07 | 2016-02-24 | 提克纳有限责任公司 | 高强度热致液晶聚合物 |
| CZ305857B6 (cs) | 2013-08-12 | 2016-04-13 | Polymer Institute Brno, Spol. S R.O. | Použití činidla pro nukleaci polyolefinů pro eliminaci tvorby úsad polyolefinového prášku v plynofázních polymeračních reaktorech |
| WO2015044785A2 (en) | 2013-09-27 | 2015-04-02 | Basf Se | Polyolefin compositions for building materials |
| US20150166752A1 (en) * | 2013-12-16 | 2015-06-18 | Clariant International, Ltd. | Polymeric Foam |
| US9534086B2 (en) | 2014-05-07 | 2017-01-03 | International Business Machines Corporation | Methods of forming poly(aryl ether sulfone)s and articles therefrom |
| US10597522B2 (en) | 2014-11-20 | 2020-03-24 | Sabic Global Technologies B.V. | Polypropylene compositions |
| EP3037466A1 (en) | 2014-12-23 | 2016-06-29 | Dow Global Technologies LLC | Polyethylene compositions with improved optical properties |
| FR3037588B1 (fr) | 2015-06-19 | 2017-05-19 | Michelin & Cie | Copolymere elastomere thermoplastique a base d'elastomere dienique et de polypropylene, compositions le comprenant et procede de preparation |
| FR3037587A1 (fr) | 2015-06-19 | 2016-12-23 | Michelin & Cie | Copolymere elastomere thermoplastique a base de polyethylene et polypropylene, compositions le comprenant et procede de preparation |
| WO2017009193A1 (en) | 2015-07-13 | 2017-01-19 | Sabic Global Technologies B.V. | Composition comprising heterophasic propylene copolymer |
| WO2017009409A1 (en) | 2015-07-16 | 2017-01-19 | Total Research & Technology Feluy | Polypropylene composition and thermoformed sheet thereof |
| EP3347413B1 (en) | 2015-09-09 | 2019-08-07 | SABIC Global Technologies B.V. | Polyolefin compositions |
| EP3420027B1 (en) | 2016-02-22 | 2019-10-23 | SABIC Global Technologies B.V. | Composition comprising heterophasic propylene copolymer |
| KR102182908B1 (ko) * | 2016-03-09 | 2020-11-25 | 밀리켄 앤드 캄파니 | 트리스아미드 화합물 및 이를 포함하는 조성물 |
| EP3704191A1 (en) | 2017-10-31 | 2020-09-09 | Total Research & Technology Feluy | Polymer composition comprising recycled polypropylene |
| US12540122B2 (en) | 2018-09-26 | 2026-02-03 | Adeka Corporation | Nucleating agent, synthetic-resin composition containing same, and molded object thereof |
| JP6728506B1 (ja) | 2018-12-27 | 2020-07-22 | 株式会社Adeka | ポリオレフィン系樹脂用核剤、これを含有するポリオレフィン系樹脂用核剤組成物、ポリオレフィン系樹脂用マスターバッチ、ポリオレフィン系樹脂組成物、その成形品、そのフィルム、多孔質フィルムの製造方法および包装体 |
| US12202959B2 (en) | 2019-02-18 | 2025-01-21 | Sabic Global Technologies B.V. | Composition comprising heterophasic propylene copolymer |
| US11667603B2 (en) * | 2019-12-12 | 2023-06-06 | Milliken & Company | Trisamide compounds and compositions comprising the same |
| ES3038874T3 (en) * | 2019-12-12 | 2025-10-15 | Milliken & Co | Trisamide compounds and compositions comprising the same |
| EP3838985A1 (en) | 2019-12-20 | 2021-06-23 | Total Research & Technology Feluy | Conductive composite material and thermoformed sheet thereof |
| US20230227627A1 (en) | 2020-05-19 | 2023-07-20 | Ineos Styrolution Group Gmbh | Small-cell polystyrene foams, and process for producing same |
| RU2751889C1 (ru) * | 2020-07-03 | 2021-07-19 | Владимир Ильич Денисенко | Полимерная композиция и плавучий понтон, изготовленный на основе полимерной композиции |
| EP4185633A2 (en) * | 2020-07-23 | 2023-05-31 | Borealis AG | Polymer composition for moulded article |
| US20230363858A1 (en) * | 2020-10-13 | 2023-11-16 | 3M Innovative Properties Company | Methods of controlling haze in orthodontic appliances including semi-crystalline polymers |
| WO2022132455A1 (en) | 2020-12-14 | 2022-06-23 | Milliken & Company | Trisamide compounds and compositions comprising the same |
| WO2023036716A1 (en) | 2021-09-09 | 2023-03-16 | Totalenergies Onetech | Polypropylene-based compositions with transparency and elongational properties |
| EP4296307A1 (en) * | 2022-06-22 | 2023-12-27 | Basell Poliolefine Italia S.r.l. | Process for recycling propylene based polymers |
| EP4573154A1 (en) | 2022-08-19 | 2025-06-25 | Basf Se | Use of additives for improving the processing of polyethylenes |
| WO2026012954A1 (en) | 2024-07-09 | 2026-01-15 | Sabic Global Technologies B.V. | Polypropylene composition |
Family Cites Families (16)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3223764A (en) * | 1961-11-28 | 1965-12-14 | Nat Distillers Chem Corp | Process for production of biaxially oriented polypropylene film |
| ES2021944A6 (es) | 1990-02-14 | 1991-11-16 | Rhone Poulenc Farma Sa | Procedimiento para preparar nuevos derivados de 1,3,5,-triamino-2,4,6-triyodobenceno. |
| TW254955B (pt) | 1992-09-25 | 1995-08-21 | Ciba Geigy | |
| JP3430609B2 (ja) * | 1993-01-13 | 2003-07-28 | 新日本理化株式会社 | ポリエステル樹脂組成物 |
| JP3477787B2 (ja) | 1993-01-20 | 2003-12-10 | 新日本理化株式会社 | ポリアミド系樹脂組成物 |
| JP3401818B2 (ja) * | 1993-02-08 | 2003-04-28 | 新日本理化株式会社 | ポリエチレン系樹脂組成物 |
| US5491188A (en) * | 1993-05-20 | 1996-02-13 | New Japan Chemical Co., Ltd. | Porous stretched article of polypropylene-based resin and process for its preparation |
| US5973076A (en) | 1995-05-31 | 1999-10-26 | New Japan Chemical Co., Ltd. | Polybutene-1 resin composition and a method of accelerating the crystal transformation thereof |
| JP3991085B2 (ja) * | 1994-10-04 | 2007-10-17 | 新日本理化株式会社 | 結晶性合成樹脂組成物 |
| JP3671547B2 (ja) * | 1996-09-13 | 2005-07-13 | 新日本理化株式会社 | ポリ乳酸系樹脂組成物 |
| EP1277790A3 (en) | 1998-03-04 | 2004-07-28 | Ciba SC Holding AG | Nucleators for crystallizable thermoplastic polymers |
| US6639038B2 (en) * | 1998-05-22 | 2003-10-28 | Idemitsu Petrochemical Co., Ltd. | Crystalline polypropylene and its moldings and films |
| FR2796276B1 (fr) * | 1999-07-15 | 2003-05-16 | Oreal | Composition sous forme solide comprenant une huile et un compose gelifiant particulier, procede de traitement cosmetique et utilisation dudit compose |
| IL155902A0 (en) | 2000-12-06 | 2003-12-23 | Ciba Sc Holding Ag | Polypropylene resin compositions |
| CA2486415C (en) | 2002-05-30 | 2010-10-26 | Ciba Specialty Chemicals Holding Inc. | Amorphous solid modification of bis(2,4-dicumylphenyl) pentaerythritol diphosphite |
| MXPA04011840A (es) * | 2002-05-30 | 2005-03-31 | Ciba Sc Holding Ag | Polipropilenos b-cristalinos. |
-
2004
- 2004-02-09 AU AU2004210907A patent/AU2004210907B2/en not_active Expired
- 2004-02-09 US US10/544,508 patent/US7790793B2/en active Active
- 2004-02-09 JP JP2006502010A patent/JP4654177B2/ja not_active Expired - Lifetime
- 2004-02-09 BR BRPI0407255-3A patent/BRPI0407255B1/pt not_active IP Right Cessation
- 2004-02-09 CA CA2514034A patent/CA2514034C/en not_active Expired - Lifetime
- 2004-02-09 RU RU2005128347/04A patent/RU2358990C2/ru active
- 2004-02-09 KR KR1020057014991A patent/KR101074723B1/ko not_active Expired - Lifetime
- 2004-02-09 ES ES04709244T patent/ES2825902T3/es not_active Expired - Lifetime
- 2004-02-09 WO PCT/EP2004/050095 patent/WO2004072168A2/en not_active Ceased
- 2004-02-09 EP EP04709244.0A patent/EP1592738B1/en not_active Expired - Lifetime
- 2004-02-10 MY MYPI20040394A patent/MY140740A/en unknown
- 2004-02-12 TW TW093103289A patent/TWI348477B/zh not_active IP Right Cessation
Also Published As
| Publication number | Publication date |
|---|---|
| JP4654177B2 (ja) | 2011-03-16 |
| MY140740A (en) | 2010-01-15 |
| WO2004072168A3 (en) | 2004-10-28 |
| KR20050109491A (ko) | 2005-11-21 |
| RU2005128347A (ru) | 2006-05-10 |
| JP2006518402A (ja) | 2006-08-10 |
| KR101074723B1 (ko) | 2011-10-19 |
| AU2004210907A1 (en) | 2004-08-26 |
| AU2004210907B2 (en) | 2009-02-19 |
| CA2514034C (en) | 2013-04-16 |
| BRPI0407255A (pt) | 2006-01-31 |
| TW200420641A (en) | 2004-10-16 |
| US20070149663A1 (en) | 2007-06-28 |
| EP1592738B1 (en) | 2020-07-29 |
| ES2825902T3 (es) | 2021-05-17 |
| TWI348477B (en) | 2011-09-11 |
| EP1592738A2 (en) | 2005-11-09 |
| CA2514034A1 (en) | 2004-08-26 |
| US7790793B2 (en) | 2010-09-07 |
| RU2358990C2 (ru) | 2009-06-20 |
| WO2004072168A2 (en) | 2004-08-26 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0407255B1 (pt) | Composições de resina, artigo conformado, processos para provimento de uma poliolefina e para o aumento de temperatura de cristalização desta, filme orientado monoaxial ou biaxialmente, sistemas multicamadas, compostos e seus usos, e mistura | |
| TWI314568B (en) | B-crystalline polypropylenes | |
| TW200407377A (en) | Beta-nucleating, light stabilizing agents for polypropylene | |
| ES2499019T3 (es) | Forma cristalina de 2-(4,6-bis-bifenil-4-il-1,3,5-triazin-2-il)-5-(2-etil-(n)-hexiloxi)fenol | |
| ES2203344B1 (es) | "mezcla estabilizantes". | |
| CN105693698B (zh) | 多功能位阻胺光稳定剂 | |
| ES2715646T3 (es) | Estabilizantes contra la luz, de amina impedida a base de triazina, piperidina y pirrolidina | |
| KR20160121560A (ko) | 안정화제로서의 인을 함유하는 3-페닐-벤조푸란-2-온 유도체 | |
| TWI588137B (zh) | 作爲有機材料穩定劑之二-[3-(7-第三丁基-2-酮基-3-苯基-3h-苯并呋喃-5-基)丙醯基]聚二醇衍生物 | |
| KR20190053880A (ko) | 첨가제 혼합물 | |
| BR112020025321A2 (pt) | Composição, processo para proteção de um material orgânico suscetível a degradação oxidante, térmica ou induzida por luz, uso de um composto, composto, composição de aditivo, e, composto intermediário | |
| CN105358528A (zh) | 新型光稳定剂 | |
| TWI601770B (zh) | 用於使有機材料安定化之吲哚并[2,1-a]喹唑啉衍生物 | |
| CN103502342B (zh) | 用于稳定有机材料的5h-呋喃-2-酮衍生物 | |
| KR20090010066A (ko) | 표면 개질제로서 n-치환된 퍼플루오로알킬화된 피롤리딘 | |
| KR20190098265A (ko) | 혼합된 작용화를 지니는 입체 장애 아민 광 안정제 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] | ||
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 21A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2813 DE 03-12-2024 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |