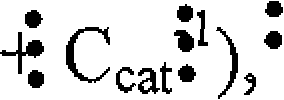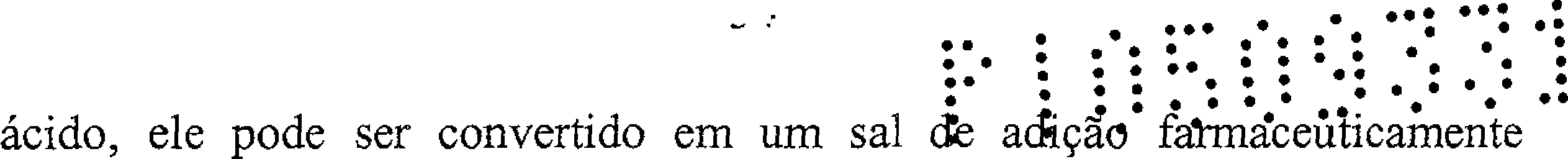(54) Título: USO DE UMA COMPOSIÇÃO DE LIGAÇÃO DE SÓDIO (73) Titular: RELYPSA, INC.. Endereço: 5301 Patrick Henry Drive, Santa Clara, Califórnia 95054, ESTADOS UNIDOS DA AMÉRICA(US) (72) Inventor: ROBERT ALPERN; JERRY M. BUYSSE; HAN TING CHANG; DOMINIQUE CHARMOT; MICHAEL JAMES COPE; JOHN FORDTRAN; GERRIT KLAERNER.
Prazo de Validade: 10 (dez) anos contados a partir de 27/11/2018, observadas as condições legais
Expedida em: 27/11/2018
Assinado digitalmente por:
Alexandre Gomes Ciancio
Diretor Substituto de Patentes, Programas de Computador e Topografias de Circuitos Integrados “USO DE UMA COMPOSIÇÃO DE LIGAÇÃO DE SÓDIO”
REFERÊNCIA RELACIONADA
Este pedido é uma continuação em parte do Pedido U.S. de N° Serial 10/ 965. 274, depositado em 13 de outubro de 2004, que é um pedido 5 de continuação em parte do Pedido U.S. de N° serial 10/ 814. 527, depositado em 30 de março de 2004; Pedido U. S. de N° Serial 10/ 814. 749, depositado em 30 de março de 2004; e Pedido U.S. de N° Serial 10/ 813.872, depositado em 30 de março de 2004, que são incorporados a este a título referencial, em sua totalidade.
FUNDAMENTOS DA INVENÇÃO:
Presentemente, aproximadamente 58 milhões de adultos americanos possuem hipertensão, e seus custos diretos e indiretos são estimados como sendo superiores a um quarto de trilhão de dólares por ano. A hipertensão é considerada como sendo o principal fator para o derrame e está 15 associada com uma alta taxa de morbidez e mortalidade quando diagnosticada em seus últimos estágios. A hipertensão é um distúrbio caracterizado por pressão sangüínea elevada, isto é, pressão sistólica consistentemente superior a cerca de 140 ou pressão sangüínea diastólica consistentemente superior a cerca de 90. Muitos fatores afetam a pressão sangüínea, incluindo o volume 20 de fluido no corpo, o conteúdo de sal no corpo, as condições dos rins, sistema nervoso, ou vasos sangüíneos, e níveis de vários hormônios no corpo. 35% de indivíduos de hipertensão caucasianos e 65% de africano- americanos são caracterizados por retenção de sal/ água. A hipertensão e a diabetes são as causas mais comuns da Doença Renal de Estágio Terminal (ESRD). A 25 abordagem não- farmacológica ao tratamento de hipertensão consiste na restrição de sal, controle de peso, e controle do estresse. O controle da ingestão de sódio evita um terço dos casos de hipertensão e é uma terapia auxiliar útil em outro terço dos casos.
Petição 870180127847, de 06/09/2018, pág. 9/12
O National Heart Lung and recomenda como parte de uma dieta saudável total, que os americanos não devem consumir mais do que 2,4 g (100 mmol) de sódio por dia. Isto equivale a cerca de 6 gramas de cloreto de sódio. No entanto, a dieta americana média 5 consiste de uma estimativa de 8 - 12 g de sal por dia. De fato, a ingestão de sal recomendada é ainda mais baixa para indivíduos com doença renal de estágio terminal e para aqueles com um risco de desenvolver hipertensão.
Tratamentos de hipertensão comuns incluem bloqueadores do
canal de cálcio, diuréticos, beta bloqueadores, alfa bloqueadores, medicação para ansiedade, inibidores de ACE e vasodilatadores. Estudos recentes recomendaram que diuréticos podem ser usados como o tratamento isolado inicial preferido, ou como parte de um tratamento combinado para indivíduos que sofrem de hipertensão.
Diuréticos são drogas que aumentam a taxa de fluxo de urina através de interferência com a reabsorção de água e sódio nos nefrônios. De modo geral, eles aumentam a taxa de excreção de sódio a partir do corpo. O sódio é o principal determinante do volume de água fora das células (referido como à água extracelular). Um diurético, que causa com que o sódio seja | excretado na urina diminui o volume da água extracelular. O aumento da excreção de sódio restaura a homeoestase do sal e a tonicidàde mais baixa, que é fmalmente traduzida em pressão sangüínea inferior. À medida em que o corpo regula a concentração de sódio intracelular e extracelular dentro de uma faixa muito estreita, a excreção de sal é usualmente acompanhada pela perda de uma quantidade proporcional de água. Os diuréticos recaem em quatro classes, dependendo de seu modo e local de ação:
a. inibidores de anidrase carbônica, tais que acetazolamida inibem a absorção de NaHCO3 e de NaCl no tubulo proximal;
b. diuréticos de circuito completo, tais que furosemida, que agem sobre o circuito de Henle pela absorção dos transportadores Na+/K7 2C1;
* · • ·· « • ·· · • ·,·· ·· · · ··♦ • · · · · · ·· * * * **·
c. diuréticos tipo tiazida, que inibem os cotrànsportâcfofaS mTGF no túbulo distai;
d. diuréticos poupadores de potássio, que agem sobre o duto coletor, eles diminuem a absorção de sódio ao mesmo tempo em que 5 poupam K+ (isto é, em oposição às outras três categorias, que promovem a perda de potássio).
Diuréticos nem sempre são terapias eficazes, pois eles possuem efeitos colaterais indesejáveis. O desequilíbrio nos ânions induzido

pela modificação de transporte de sódio tende a criar complicações, tais que acidose ou alcalose. Uma das limitações da terapia diurética é a “resistência diurética”. Uma definição de resistência diurética é a falha em excretar pelo menos 90 mmol de sódio dentro de 72 horas de uma dose de 160 mg de furosemida oral, dada duas vezes ao dia. Este efeito é causado por um ou uma combinação de mecanismos: (i) uma alteração do perfil farmacocinético de diuréticos de circuito completo, (ii) compensação da absorção de sódio no nefrônio distai, e (iii) resposta de nefrônio diminuída. Diuréticos de circuito completo, tais que furosemida, exibem uma concentração de teto no sangue, em que a excreção fracionária e sódio é máxima. Este efeito de teto apresenta sérias implicações para indivíduos, que dificilmente respondem a concentrações de subteto. Estes indivíduos requerem a infusão contínua da droga para que seja alcançado o nível de excreção de sódio desejado. Apesar de várias tentativas para aperfeiçoar o perfil da droga ou a sua biodisponibilidade, os resultados destas terapias permanecem inferiores aos que seriam desejados.
A resistência diurética é tida como ocorrendo em um de três indivíduos com falha cardíaca congestiva (CHF). Como os indivíduos, aos quais é prescrito um diurético precisam aderir a uma dieta de baixo teor de sódio, outra causa da falha da terapia diurética é a incapacidade dos indivíduos para observarem uma dieta um tal baixo teor de sal.
«*« ♦ ·· :% ; :·· .·. .*<. · .* · :* *·ί · β ·
Ο edema refere-se ao acúmulo jde yohtfhes· de* 41úi*dõ · · anormalmente grandes no espaço intracelular do corpo como um resultado da retenção de sódio excessiva. O edema pode estar associado com insuficiência renal, síndrome nefrítica, síndrome nefrótica, insuficiência cardíaca, ou falha hepática. Quando os mecanismos que regulam o equilíbrio de sódio no corpo são rompidos, o acúmulo de sódio conduz a um acúmulo compensador de fluido (para retificar o desequilíbrio osmótico) e edemas observáveis. Em indivíduos com rins que funcionam, o edema pode ser tratado pela limitação

da ingestão de sódio e pelo uso de diuréticos, que causam com que o corpo excrete mais água na urina (Brater, D.C (1992) “Clinicai pharmacology of loop diuretics in health and disease.” Eur. Heart. J. 13 Suppl. G : 10-4 e Brater, D.C. (1993) “Resistance to diuretics: mechanisms and clinicai implications”. Adv. Nephrol Necker Hosp. 22: 349-69). Os diuréticos são ineficazes em indivíduos, que possuem funções renais reduzidas e também em 15 certas populações de indivíduos que não respondem a diuréticos (Brater, D.C.
(1981) “Resistance to diuretics: emphasis on a pharmacological perspective “. Drugs 22 (6) : 477- 94 e Brater, D.C. (1985) “Resistance to loop diuretics.
Why it happens and what to do about it”. Drugs 30 (5): 427- 43).
Vários estudos demonstraram que a varredura do sódio intestinal é possível. No entanto, a quantidade de resina requerida para este propósito (em geral de 60- 100 g/ dia) é considerada inaceitavelmente alta para a terapia moderna. As grandes doses refletem a baixa capacidade de ligação in vitro e mais baixa in vivo destes resinas. Mesmo na presença de dietas de alto teor de sal, resinas sulfônicas não removem mais do que ImEq 25 Na+ /g e resinas fosfônicas não mais do que 0,8 mEq Na7 g (Fourman, P.
(1953) “ Capacity of a cationic exchange resin (zeo- karb 225) in vivo. “Br Med. J. 1 (4809) : 544-6; Heming, A. E. and T. L. Flanagan (1953). “Considerations in the selection of cation exchange resins for therapeutic use.” Ann. N.Y. Acad. Sei. 57 (3): 329- 51; e McChesney, E. W., F. C.
·· ;;»····· · ·
Nachod, et al. (1953) “ Some aspects of cation exchgnge fessps a^thetapéufkf *·* agents for sodium removal “ Ann. N. Y. Acad. Sei 57 (3): 252- 9). De modo típico, as resinas retiveram apenas cerca de 25%, ou menos, de sua capacidade de ligação de sódio in vitro quando usadas clinicamente em indivíduos. Estas resinas não foram bem toleradas pelos indivíduos devido a sua textura gredosa ou arenosa e devido a sua tendência a causar constipação (Heming A. E. and T. L. Flanagan (1953) “Considerations in the selection of cation exchange resins for therapeutic use’’. Ann. N. Y. Acad. Sei 57 (3): 239
-51).
Deste modo, seria benéfico desenvolver composições poliméricas que removessem sal e/ou água a partir do trato gastrintestinal de modo eficiente.
Em adição a indivíduos de hipertensão, indivíduos que sofrem de doença renal de estágio terminal, insuficiente renal, diarréia crônica, incontinência, falha cardíaca congestiva, cirrose hepática, edema idiopático, e outras condições, podem se beneficiar da ligação de Na+ intestinal e/ ou água.
Em geral, os tratamentos correntes para a redução dos níveis de sal e/ água no corpo são sub- ótimos. Portanto, existe uma necessidade para desenvolver terapias com alta capacidade de remoção de sal e/ ou água, seletivas, com menos efeitos colaterais para os indivíduos.
BREVE DESCRIÇÃO DAS FIGURAS
A Figura 1 é uma representação esquemática da formação de um complexo de polieletrólito.
A Figura 2 ilustra a permeabilidade de uma membrana sódio em diferentes pHs.
BREVE SUMÁRIO DA INVENÇÃO
A presente invenção provê métodos para a remoção de sódio a partir do trato gastrintestinal de um animal. Em algumas modalidades, os métodos envolvem geralmente a administração de uma quantidade eficaz de ··· :· ::: ···:: ’♦* J· um polímero de ligação de sódio. De modo preferido; os polftrtefoS de*ligáça€> de sódio possuem uma capacidade de ligação de sódio in vivo em um ser humano de 4 mmol ou mais por grama de polímero. Em outras modalidades, os métodos envolvem a administração de composições de núcleo- casca para a remoção de sódio a partir do trato gastrintestinal. Os métodos e as composições descritos nesta são úteis no tratamento de distúrbios, nos quais a remoção de sódio e/ ou água a partir do corpo de um ser humano é desejável.
Doenças que podem ser tratadas com os métodos e as composições aqui descritos incluem, mas não estão limitadas a, hipertensão, falha cardíaca crônica, e doença renal em estágio terminal, cirrose hepática, insuficiência renal crônica, sobrecarga de fluido, ou sobrecarga de sódio.
DESCRIÇÃO DETALHADA DA INVENÇÃO: Composições Poliméricas de Ligação de Sódio
A presente invenção provê métodos, composições farmacêuticas, e kits para o tratamento de indivíduos humanos. Os termos indivíduo humano e animal como aqui usados, incluem tanto seres humanos como outros mamíferos. Em particular, a presente invenção provê composições poliméricas para a remoção de íons de sódio. De modo preferido, estas composições são usadas para a remoção de íons de sódio a partir do trato gastrintestinal de indivíduos animais.
Um aspecto da invenção consiste em um método para a remoção de íons e sódio com uma composição polimérica de ligação de sódio. Em uma modalidade, a composição polimérica de ligação de sódio possui alta capacidade e/ ou seletividade para a ligação de sódio e não libera, de modo significativo, o sódio ligado no trato gastrintestinal. De modo preferido, a composição polimérica de ligação de sódio não libera o sódio ligado no cólon. De modo ainda mais preferido, a composição polimérica de ligação de sódio não introduz íons prejudiciais. É preferido que a composição polimérica exiba ligação seletiva para íons de sódio. Em uma modalidade, devido à ligação :·. : :- .·. .·. -: ’ ;· ·.: ·. e seletiva de sódio pela composição polimérica jle ljga^o*.de’*Sódi’o,**à · composição não exaure potássio a partir do corpo.
É preferido que as composições poliméricas da presente invenção exibam uma alta capacidade e/ ou seletividade para sódio. O termo “alta capacidade”, como aqui usado, abrange a ligação in vivo de 4 mmol ou mais de sódio por grama de polímero. De modo típico, esta capacidade de
ligação in vivo é determinada em um ser humano. Técnicas para a determinação da capacidade de ligação de sódio in vivo em um ser humano são bem conhecidas na técnica. Por exemplo, seguindo-se à administração de um polímero de ligação de sódio a um indivíduo, a quantidade de sódio nas fezes pode ser usada para calcular a capacidade de ligação de sódio in vivo. De modo típico, a capacidade de ligação de sódio in vivo é determinada em um ser humano sem deficiência de um hormônio que controla a excreção de sal, por exemplo, aldosteronas.
Em algumas modalidades, a capacidade de ligação de sódio in vivo pode ser igual a ou superior a 4 mmol por grama de polímero em um ser humano. De modo preferido, a capacidade de ligação de sódio in vivo em um ser humano é de cerca de 5 mmol ou mais por grama, de modo preferido é de cerca de 6 mmol ou mais por grama, de modo ainda mais preferido é de cerca de 7 mmol ou mais por grama, e de modo mais preferido é de cerca de 8 mmol ou mais por grama. Em uma modalidade preferida, a capacidade de ligação de sódio in vivo em um ser humano é de cerca de 8 mmol a cerca de 15 mmol por grama em um ser humano.
A capacidade dos polímeros de ligação de sódio pode ser também determinada in vitro. É preferido que a capacidade de ligação de sódio in vitro seja determinada em condições que simulem as condições físicas do trato gastrintestinal. Em algumas modalidades, a capacidade de ligação de sódio in vitro é determinada em soluções com um pH de cerca de
7,5 ou menos. Em várias modalidades, a capacidade de ligação de sódio in
• · · ·« · ......... · • * · ··· · · · · · ·· · ···· ****ζ * · vitro em um pH de cerca de 7,5 ou menos é igual ou-maiqr (ÍQ:qn^6’mmoí pol· * grama de polímero. Uma faixa preferida de capacidade de ligação de sódio in vitro em um pH de cerca de 7,5 ou menos, é de cerca de 6 mmol a cerca de 15 mmol por grama de polímero. De modo preferido, a capacidade de ligação de sódio in vitro em um pH de cerca de 7,5 é menor ou igual a cerca de 6 mmol ou mais por grama, de modo preferido é de cerca de 8 mmol ou mais por grama, de modo ainda mais preferido é de cerca de 10 mmol ou mais por grama, e de modo mais preferido é de cerca de 15 mmol ou mais por grama.
A capacidade mais alta da composição polimérica possibilita a administração de uma dose mais baixa da composição. De modo típico, a dose da composição polimérica usada para obter os benefícios terapêuticos e/ ou profiláticos é de cerca de 0,5 g/ dia a cerca de 25 g/ dia. De modo mais preferido, é de cerca de 15 g/ dia, ou menos. Uma faixa de dose preferida é de cerca de 5 g/ dia a cerca de 20 g/ dia, de modo mais preferido é de cerca de 5 g/ dia e cerca de 15 g/ dia, de modo ainda mais preferido é de cerca de 10 g/ dia a cerca de 20 g/ dia, e de modo mais preferido é de cerca de 10 g/ dia a cerca de 15 g/ dia.
O termo “íons prejudiciais” é aqui usado para fazer referência | a íons, que não se deseja que sejam liberados ao interior do corpo pelas composições descritas nesta durante o seu período de uso. De modo típico, os íons prejudiciais para uma composição dependem da condição sendo tratada, das propriedades químicas, e/ ou das propriedades de ligação da composição. Por exemplo, quando a hipertensão está sendo tratada e a composição é usada para remover íons de sódio, o íon prejudicial deveria ser cloreto ou OH', pois 25 estes indivíduos frequentemente possuem alcalose. Quando a falha renal está sendo tratada, exemplos de íons prejudiciais são K+ e Ca2+.
É também preferido que as composições nesta descrita retenham uma quantidade significativa de sódio ligado. De modo preferido, o sódio é ligado pelo polímero no trato gastrintestinal superior e não é liberado • · · • · · · · no trato gastrintestinal inferior. O termo
..;····· · · “ quantiqade ;sigutfk#tiv^’\Zofnb aqui usado, não tem a intenção de significar que a quantidade total de s ódio ligado é retida. É preferido que pelo menos algum do sódio ligado seja retido, de tal modo que um benefício terapêutico e/ ou profilático seja obtido.
Quantidades preferidas de sódio ligado estão na faixa de cerca de 25% do sódio ligado, de modo mais preferido de cerca de 50%, de modo ainda mais preferido de cerca de 75%, e de modo mais preferido a retenção é de 100% do sódio ligado. É preferido que o período de retenção seja durante o período de tempo em que a composição está sendo usada terapeuticamente e/ ou profílaticamente. Na modalidade, na qual a composição é usada para ligar e remover sódio a partir do trato gastrintestinal, o período de retenção é o período de tempo de residência da composição no trato gastrintestinal.
Em uma modalidade, a composição polimérica de ligação de sódio troca prótons por íons de sódio no trato gastrintestinal e mantém o sódio ligado no interior da composição polimérica no cólon, em que a concentração de sódio é, de modo típico, muito inferior em comparação com outros cátions. Os últimos são, de modo típico, K+, Mg++, Ca++, NH44, H+ e aminas protonadas derivadas a partir de desaminação de aminoácido enzimática e aqui referida como a “cátions competitivos”.
Em outra modalidade, a composição polimérica de ligação de sódio é caracterizada por uma alta taxa de ligação a íons de sódio (contra cátions competitivos), mesmo em um ambiente em que a razão de sódio: cátions competitivos é tão baixa quando de 1: 4, tal que no cólon.
Em ainda uma outra modalidade, a composição polimérica de ligação de sódio é caracterizada por uma alta ligação, mas não- específica de sódio no trato superior, acoplado a um decréscimo na permeabilidade iônica da resina disparada por uma alteração nas condições fisiológicas do trato gastrintestinal. Esta alteração na permeabilidade pode ser efetuada pela alteração de PH do estômago para o duodeno ou alteração de pH do íleo para · · *·« · · ......
........... · · •· · ίί** ·**·· *· · ο cólon. Em outra modalidade, a alteração de fermçaKiJtdaffe*pocfc ser ·.· efetuada na presença de secreção (tais que ácidos biliares) ou metabólitos (tais que ácidos graxos) ou atividade enzimática localizada.
Em uma modalidade, a composição polimérica de ligação de sódio compreende uma resina tipo ácido, de modo preferido carregada com
H+ ou NH4 +, e possivelmente K+. De modo típico, H+, NH/ são deslocadas no trato superior principalmente Na+ e a permeabilidade da resina a íons é reduzida à medida em que a resina se desloca a partir do trato gastrintestinal
superior para o trato gastrintestinal inferior. De modo típico, esta alteração na permeabilidade é modulada pelas alterações fisiológicas no ambiente de vários segmentos gastrintestinais.
Em outra modalidade, a composição polimérica de ligação de sódio compreende sulfonato ou polímeros fosfônicos.
Composições de Núcleo- Casca de Ligação de Sódio.
Em um aspecto da invenção, uma composição de núcleocasca é usada para a remoção de sódio. De modo típico, nas composições de núcleo- casca, o núcleo compreende um polímero com uma alta capacidade de ligação para sódio. As várias composições poliméricas de ligação de sódio nesta descritas podem ser usadas como o componente de núcleo das 20 composições núcleo- casca. Em algumas modalidades, a casca modula a entrada de solutos competitivos através da casca para o componente de núcleo. Em uma modalidade, a permeabilidade da membrana ao sódio ligado é diminuída à medida em que a composição núcleo- casca se move através do trato gastrintestinal. De modo típico, esta alteração de permeabilidade é 25 produzida pela hidrofobicidade aumentada e/ ou desentumescência da casca.
É preferido que a casca da composição núcleo- casca não seja essencialmente desintegrada durante o período de residência e passagem através do trato gastrintestinal.
O termo “soluto competitivo”, como aqui usado, compreende • · · ··· · · · solutos que competem com sódio para a ligação a um coijipóçfeiTtps Ué núcleo* V ·*· mas que não se deseja que sejam contatados e/ ou ligados ao componente do núcleo. De modo típico, o soluto competitivo para uma composição de núcleo- casca depende das características de ligação do núcleo e/ ou das características de permeabilidade do componente da casca. Pode ser evitado com que um soluto competitivo seja contatado e/ ou ligado a uma partícula de núcleo- casca, devido às características da ligação preferenciais do componente do núcleo e/ou à permeabilidade diminuída do componente de casca para o soluto competitivo a partir do ambiente externo. De modo típico, o soluto competitivo possui uma permeabilidade mais baixa a partir do ambiente externo através da casca, comparado àquele de íons de sódio. Exemplos de solutos competitivos incluem, mas não estão limitados a, K+, Mg~, Ca++, NH4+, H+ e aminas protonadas.
Em uma modalidade preferida, a composição núcleo- casca liga sódio em todo o trato gastrintestinal, mas evita a liberação de sódio no cólon. Estas propriedades do núcleo- casca são moduladas pela fato de que a casca é permeável a sódio nas partes superiores do trato gastrintestinal e pelo fato de que é menos permeável a sódio no trato gastrintestinal inferior, tal que o cólon proximal. Esta modulação da permeabilidade da casca através do trato gastrintestinal é aqui referida como “captura de permeabilidade”.
Em algumas modalidades, a casca é permeável tanto a cátions mono valentes, como a cátions di valentes. Em algumas das modalidades, nas quais a casca é permeável tanto a cátions monovalentes como a cátions divalentes, o núcleo liga apenas cátions monovalentes, de modo preferido sódio, devido às características de ligação do núcleo. Em outras modalidades, a casca exibe permeabilidade preferida a íons de sódio.
É particularmente preferido que as composições de núcleocasca e as composições poliméricas de ligação de sódio descritas nesta liguem sódio nas partes do trato gastrintestinal que possuem uma concentração
• · · ·· · · ··· · · ··? ··· *·*»·· · · · · · · relativamente alta de sódio, tal que de cerca de 70 mM ajceíçâ 1^0 mM*J? ·.· então preferido que o sódio ligado permaneça ligado às composições e não seja liberado nas porções do trato gastrintestinal com concentrações, tal que de cerca de 10 mM a cerca de 40 mM.
Em uma modalidade, o material de casca protege o componente do núcleo contra o ambiente GI externo. O material de casca, em algumas modalidades, protege os grupos ácidos do polímero do núcleo e evita a sua exposição ao ambiente GI. Em uma modalidade, o componente do núcleo é protegido com um componente de casca, que compreende um 10 revestimento entérico. Exemplos adequados de revestimentos entéricos são descritos na técnica. Por exemplo, vide Remington: The Science and Practice of Pharmacy por A. R. Gennaro, (Editor), 20a Edição, 2000.
Em outra modalidade, o material de casca é engenheirado para

responder a alterações fisiológicas no trato gastrintestinal, de tal modo que a permeabilidade da casca seja alterada. A permeabilidade da casca é diminuída, de tal modo que os íons hidrofílicos não mais sejam capazes de cruzar a membrana após estes íons serem ligados ao núcleo. De modo preferido, esta permeabilidade diminuída ocorre durante o período de uso da composição polimérica, isto é, durante o período em que a composição polimérica reside no trato gastrintestinal. A perda de permeabilidade para os íons hidrofílicos pode ser executada através do decréscimo ou mesmo da eliminação do volume livre de permeação da membrana. Como a última é principalmente controlada pela taxa de hidratação da casca, é possível quase paralisar a taxa de permeação através da indução de um colapso da casca. Muitas técnicas de indução de uma tal fase são conhecidas na técnica. A abordagem preferida consiste em tomar o material da membrana crescentemente hidrofóbico, de tal modo que a taxa de hidratação diminua a até quase zero. Esta pode ser alcançada através de vários modos, dependendo do tipo de mecanismo de disparo.
• · · · · ♦ · ♦ · ♦ · ·· · * · ι * *·· ·♦
Por exemplo, a alteração de fase |)ode· séç· alteração do pH. O perfil do pH do trato gastríntestinal pode ser alterado como uma função do tempo, mas apresentar algumas constantes, tal como indicado abaixo na TABELA I (Fallinborg et al. Aliment. Pharm. Therap. 5 (1989),3,605 - 613).
TABELA 1
|
Segmento do trato gastríntestinal |
Faixa de pH |
|
Estômago |
1-2 |
|
Duodeno- intestino delgado distai |
6-7 |
|
Ceco- cólon ascendente |
7- 5,5 |
|
Transverso - cólon descendente |
5,5-6 |
|
Fezes |
6,5 |
Os polímeros de casca, que exibem um colapso de cadeia em qualquer destas regiões de pH, podem ser usados para causar alterações de permeabilidade. Uma modalidade das partículas núcleo- casca liga íons de 10 sódio seletivamente no estômago e os mantém no núcleo da partícula

enquanto as partículas estão se deslocando no intestino grosso e intestino delgado, e exibem uma alta permeabilidade a íons de sódio em baixo pH e permeabilidade muito baixa em pH neutro. Isto pode ser alcançado por meio de um polímero de casca com grupos hidrofóbicos e grupos que ionizam quando submetidos a uma alteração de pH. Por exemplo, polímeros formados a partir de monômeros hidrofóbicos (por exemplo, (met)acrilatos de álcool de cadeia longa, N-alquil (met)acrilamida, monômeros aromáticos), e monômeros básicos que ionizam em pH baixo e permanecem neutros além de seu pKa (por exemplo, vinil piridina, dialquilaminoetil (met)acrilamida). A reação entre o pH e a razão de intumescência da casca, e portanto a permeabilidade, é controlada pelo equilíbrio de monômeros hidrofóbicos e monômeros não- ionizáveis. Exemplos de tais sistemas são relatados na literatura (Batich e al., Macromolecules, 26, 4675- 4680. Em uma modalidade, a composição da casca ou do núcleo casca é caracterizada por uma alta permeabilidade para sódio em baixos pHs, tal que um pH de cerca de a cerca de 5. Um núcleo- casca com estas propriedades pode ligar sódio no estômago e à medida em que a
.. · · ··· · ♦ *·· *·· ; . * · « · » ♦ * · · * ·· · ···· · · * · * * composição ipassa ãtravps ♦.do. 1 trato ·.· gastrintestinal inferior, e permeabilidade é paralisada, de modo típico em pH neutro.
Em uma modalidade, a casca de uma composição núcleo5 casca é caracterizada por uma alta permeabilidade a sódio em pHs cerca de neutros e acima. Um núcleo- casca com esta propriedade pode absorver e ligar sódio no trato gastrintestinal superior, a partir de secreções que são principalmente ricas em sódio (por exemplo, cerca de 140 mM de sódio e
cerca de 20 mM de potássio) e quando a composição penetra no ceco, em que a faixa de pH é de cerca de 5 a cerca de 6, a casca entra em colapso e reduz a sua permeabilidade a cátions competitivos. O material da casca passa a partir de um estado hidratado a um estado impermeável em colapso à medida em que o pH se toma ligeiramente ácido. Neste caso particular, os polímeros da casca contêm, de modo típico, uma quantidade balanceada de monômeros hidrofóbicos e ácidos. Sistemas que podem ser usados na casca desta modalidade são descritos na literatura. Por exemplo, vide Kraft et al.
Langmuir, 2003, 19, 910 - 915; Ito et al., Macromolecules, (1992), 25, 7313 7316.
Em outra modalidade, a casca de uma composição núcleocasca exibe uma alteração de permeabilidade por absorção passiva, ao mesmo tempo em que passa através do trato GI superior. Muitos componentes presentes no trato GI, que incluem os componentes da dieta, metabólitos, secreção, etc., são suscetíveis de serem adsorvidos sobre e no interior da casca em um modo quase irreversível e modificam fortemente o padrão de 25 permeabilidade da casca. A vasta maioria destes materiais solúveis são negativamente carregados e apresentam vários níveis de hidrofobicidade.
Algumas daquelas espécies possuem um caráter anfifílico típico, tais que os ácidos graxos, fosfolipídios, sais da bile e se comportam como tensoativos. Tensoativos podem ser adsorvidos, de modo não- específico, a superfícies ·♦ · * ·*♦ * **Ι **ί· ♦ · ♦ ··· **·· * ·· ♦♦ · * · ·· · · ·φ* ·#·, através de interações hidrofóbicas, interação iônjca | €pmbjnãç©eX*dQS ♦.·.
mesmos. Nesta modalidade, este fenômeno é usado para alterar a permeabilidade da composição polimérica quando do curso da ligação de íons de sódio. Em uma modalidade, os ácidos graxos podem ser usados para modificar a permeabilidade da casca e, em outra modalidade, ácidos biliares podem ser usados. Ácidos graxos e ácidos biliares formam ambos agregados (micelas ou vesículas) e podem também formar complexos insolúveis quando misturados com polímeros positivamente carregados (vide, por exemplo, kaneko et al, Macromolecular Rapid Communications (2003), 24 (13), 78910 792). Ambos os ácidos graxos e os ácidos biliares exibem similaridades com tensoativos aniônicos sintéticos e numerosos estudos relatam a formação de complexos insolúveis entre tensoativos aniônicos sintéticos e polímeros cationicamente carregados (por exemplo, Chen, L. et al., Macromolecules (1998), 31 (3), 787- 794). Nesta modalidade, o material da casca é selecionado a partir de copolímeros contendo tanto grupos hidrofóbicos e catiônicos, de tal modo que a casca forma um complexo íntimo com hidrófobos anionicamente carregados, tipicamente encontrados no trato GI, tais que ácidos biliares, ácidos graxos, bilirrubina e compostos relacionados.
| Composições adequadas também incluem materiais poliméricos descritos como agentes de sequestro de ácidos biliares, tais que aqueles relatados nas Patentes US 5. 607. 669; 6. 294. 163; e 5. 374. 422; Figuly et al., Macromolecules, 1997, 30, 6174- 6184. A formação do complexo induz um colapso da membrana da casca, que, por sua vez, pode reduzir ou até mesmo paralisar a taxa de permeação através da membrana. Um núcleo- casca com estas propriedades pode absorver e ligar sódio no trato gastrintestinal superior, tal que o estômago e o duodeno, e à medida em que as moléculas do ácido biliar e as moléculas do ácido graxo se ligam adicionalmente à casca no trato gastrintestinal, a permeabilidade da casca para os íons, incluindo sódio, é diminuída à medida em que a porosidade da casca é impedida pelas moléculas », < · »♦· · ♦ ·♦* ·♦· • « · ♦·· ···· · · ·· · · · **φ ζ t *»ζ ·♦ *· do ácido biliar e/ ou ácido graxo. Além disso, uma iiterajãó ártòp ájíil&e e^· \· ácidos graxos com a casca evita a sua interação com o núcleo e pode, deste modo, preservar a capacidade de ligação de sódio do componente do núcleo.
Em ainda outra modalidade, a permeabilidade da casca de uma
composição de núcleo- casca é modulada pela atividade enzimática no trato gastrintestinal. Existe um número de enzimas secretadas produzidas pela microflora colônica comum. Por exemplo, Bacteroides, Prevotella,
Porphyromonas, e Fusobacterium produzem uma variedade de enzimas
secretadas, incluindo colagenase, neuramidase, desoxirribonuclease [ Dnase], heparinase, e proteinases. Nesta modalidade, a casca compreende uma espinha dorsal hidrofóbica com entidades hidrofilicas pendentes, que são clivadas através de uma reação enzimática no intestino. À medida em que a reação enzimática prossegue, a membrana do polímero se toma mais e mais hidrofóbica, e passa de um estado altamente intumescido, de um material de 15 alta taxa de permeabilidade, a uma membrana de baixa hidratação inteiramente em colapso, com permeabilidade mínima. Entidades hidrofilicas podem ser selecionadas a partir de substratos naturais de enzimas comumente secretadas no trato GI. Tais entidades incluem aminoácidos, peptídeos,

carboidratos, ésteres, ésteres de fosfato, monoésteres de oxifosfato, O- e Sfosforotioatos, fosforamidas, tiofosfato, grupos azo, e os similares. Exemplos de enzimas entéricas, suscetíveis de alterar quimicamente o polímero da casca incluem, mas não estão limitadas a, lipases, fosfolipases, carboxilesterase, glicosidases, azorredutases, fosfatases, amidases e proteases. A casca pode ser permeável a íons de sódio até que ela entre no cólon proximal e então as 25 enzimas presentes no cólon proximal iriam reagir quimicamente com a casca de modo a reduzir a sua permeabilidade aos íons de sódio.
Em algumas modalidades, a espessura da casca pode estar entre cerca de 0,002 mícrons a cerca de 50 mícrons, de modo preferido de cerca de 0,005 mícrons a cerca de 20 mícrons. Preferivelmente, a espessura da
casca é de mais do que cerca de 1 mícrons, de modo jnaisipreicriCMu c ec ·· ·· do que cerca de 40 mícrons. Preferivelmente, a espessura da casca é inferior a cerca de 50 mícrons, de modo mais preferido é inferior a cerca de 40 mícrons, de modo ainda mais preferido é inferior a cerca de 20 mícrons, e de modo 5 mais preferido é inferior a menos do que cerca de 10 mícrons.
O tamanho das partículas de núcleo casca está, de modo típico,
na faixa de cerca de 200 nm a cerca de 2 mm, sendo preferivelmente de cerca de 500 pm. De modo preferido, o tamanho das partículas de núcleo casca é de mais do que 1 pm, de modo mais preferido é de mais do que cerca de 100 pm, 0 de modo ainda mais preferido é de mais do que cerca de 200 pm, e de modo mais preferido é de mais do que cerca de 400 pm. Preferivelmente, o tamanho das partículas de núcleo- casca é inferior a cerca de 500 pm, de modo mais preferido é inferior a cerca de 400 pm, e de modo ainda mais preferido é de cerca de 200 pm, e mais preferencialmente é de menos do que cerca de 100 pm.
Polímeros de Ligação de Sódio
Em uma modalidade, o polímero de ligação de sódio usado nas composições poliméricas e nas composições de núcleo- casca é um polímero ) funcional do tipo sulfônico (-SO3“), sulfurico (-OSO3), carboxílico (-CO2'), 20 fosfônico (-PO3‘), fosfórico (-OPO3‘), ou sulfamato (-NHSO3‘). Polímeros radicais livres, derivados de monômeros, tais que sulfonato de vinila, fosfonato de vinila, ou sulfamato de vinila podem ser usados. De modo preferido, os polímeros usados podem ligar sódio em uma ampla faixa de pHs.
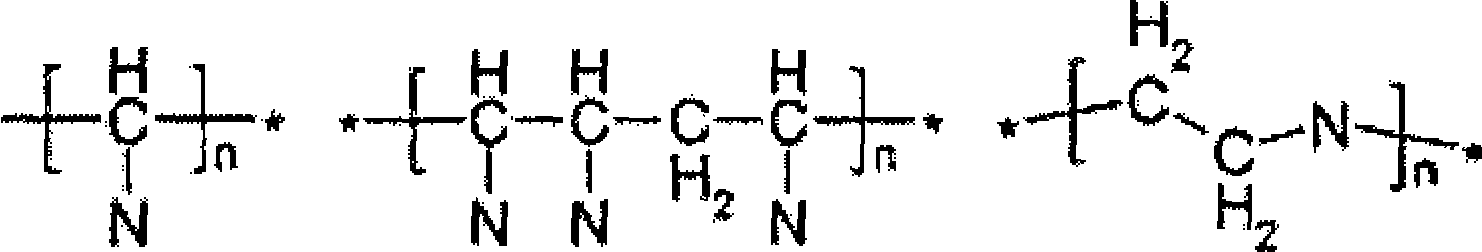
Exemplos de outros monômeros adequados para polímeros de ligação de sódio estão incluídos na Tabela 2.
Fração de H Fração de H Capacidade Capacidade ·· · . . ; · · · · · • · ;.íi* · · · ·,·
TABELA 2: Exemplos de porções de trocá dei câtion· - 'estfutufas e capacidades de ligação teóricas
Massa
Outras porções de troca de cátion adequadas incluem:
ζ
ζ
em que η é igual ou maior do que m e Z representa ou SO3H ou PO3H. De modo preferido, n é cerca de 50 ou mais, mais preferivelmente n é cerca de 100 ou mais, de modo ainda mais preferido n é cerca de 200 ou mais, e de modo mais preferido n é cerca de 500 ou mais.
Monômeros de fosfonato adequados incluem fosfonato de vinila, 1,1-bis fosfonato de vinila, e derivados etilênicos de ésteres de fosfonocarboxilato, oligo(metilenofosfonatos), e ácidos hidroxietano-1,1difosfônico. Métodos de síntese destes monômeros são bem conhecidos na técnica. Polímeros sulfâmicos (isto é, quando Z = SO3H) ou fosforamídicos • * ·· ··· ·>··· (isto é, quando Z = PO3H) podem ser obtidos a partis dê .polímeros* amina oti precursores de monômero tratados com um agente de sulfonação, tal que produtos de adição de trióxido de enxofre / amina ou um agente de fosfonação, tal que P2O5, respectivamente. De modo típico, os prótons ácidos 5 dos grupos fosfônicos podem ser trocados por cátions, tais que sódio, em um pH de cerca de 6 a cerca de 7.
Outro exemplo de um monômero adequado para o uso nesta é um ct-fluoroacrilato. Este monômero é preparado, de modo típico, a partir de
um éster de cloroacetato. Vide, KF Pittman, C. U. M., Ueda, et al. (1980). Macromolecules 13 (5): 1031- 1036. Outros métodos compreendem a polimerização de crescimento gradual a partir de compostos funcionais fosfonato, carboxílico, fosfato, sulfinato, sulfato e sulfonato. Polifosfonatos de alta densidade, tais que aqueles comercializados pela Rhodia sob a marca registrada Briquest são particularmente úteis.
Os polímeros da invenção também incluem resinas de troca iônica sintetizadas a partir de polímeros de ocorrência natural, tais que polímeros de sacarídeo e polímeros semi- sintéticos, opcionalmente funcionalizados para criar sítios de troca iônica na espinha dorsal ou nos resíduos pendentes. Exemplos de polissacarídeos de interesse incluem materiais de origens vegetais ou animais, tais que materiais celulósicos, hemicelulose, alquil celulose, hidroxialquil celulose, carboximetil celulose, sulfoetil celulose, amido, xilano, amilopectina, condroitina, hialuronato, heparina, guar, cantano, manano, glactomanano, quitina e quitosano. São mais preferidos polímeros que não se degradam sob as condições fisiológicas do 25 trato gastrintestinal e permanecem não- adsorvidos, tais que carboximetil celulose, quitosano e sulfoetil celulose.
Polímeros de Ligação de Cátion e Ânion
Uma modalidade da invenção utiliza tanto uma resina ácida (por exemplo, sulfonato na forma de próton) e uma resina de base forte (por • · * • * ·*♦··· ·····.*· exemplo, amônio quaternário sjna forma OH') Ou uína* resina de base frac*a (por exemplo, uma amina livre). Esta composição pode liberar água quando da troca de H+ para Na+ e OH' para Cf. Em ainda outra modalidade, o polímero contém um sal interno de um ácido e uma função de base, livre de 5 contraíons. Nesta modalidade, a combinação com uma resina de ligação aniônica possui a vantagem de aumentar a excreção de íons de cloreto a partir do corpo (o ânion mais dominante no ambiente GI superior) e portanto minimiza a acidose nos indivíduos com rins comprometidos.
Em uma modalidade, a composição polimérica que pode ligar 10 sódio possui a capacidade de intumescer de cerca de 2 a cerca de 100 vezes o seu peso em uma composição de fluido isotônico. O polímero em uma modalidade é um polímero de absorção de fluido estável a ácido, que pode absorver cerca de 10- a cerca de 50 vezes o seu peso em solução salina e ter a capacidade de reter este fluido absorvido sob pressão, por exemplo, sob 15 pressão que ocorre mediante a redução de volume no cólon humano. Com base na estrutura de polímero, a absorção de fluido pode ser dependente do pH e a absorção da solução salina pode ser evitada no estômago e ocorrer no trato gastrintestinal. O sítio de absorção de fluido pode ser modificado com base na estrutura do polímero, incluindo através de reticulação, contraíons, 20 peso molecular, densidade de carga, densidade de reticulação ou revestimentos.
Em uma modalidade, a invenção utiliza uma resina de troca catiônica em forma ácida e uma resina de troca aniônica em forma básica, isto é, o sítio de troca aniônica positivamente carregado no polímero é 25 compensado por OH'. Em alternativa, o polímero pode ser uma base livre, que é protonada quando do contato com o fluido gastrintestinal aquoso. As resinas podem ser independentemente materiais solúveis em água ou reticulado; de modo preferido ambas as resinas são reticuladas. A razão molar de troca do ânion (OH') para o cátion (H+) é preferivelmente de cerca de 0, 5 a cerca de • · ; . · · · ·· · · · • · · · 1,5, de modo mais preferido de cerca de 0,9 a certa dd 1,1·.* ··· • · · ·· • · · · ·♦ ·
• · · ··.· ♦ · ·· ·
As resinas de troca iônica podem ser obtidas através de polimerização de radical livre, através de copolimerização de monômeros funcionais, pós- funcionalização de polímero ou combinações dos mesmos.
Exemplos de grupos de troca de cátion são aqueles relacionados na Tabela 2.
Exemplos de grupos de troca de ânion são : amina (~NR3), amónio quaternário (-NR?), amidina (- C(=NH)-NH2), gunidina (-NH-C(+NH)-NH2), fosfônio (PR3 +).
Métodos de preparação dos polímeros com resinas de troca iônica são bem conhecidos de uma pessoa versada na técnica. Por exemplo, vide Ion Exchange, Charles Dickert, Kirk- Othmer Encyclopedia of Chemical
Technology,© 1995 por John Wiley & Sons, Inc. Resinas de troca iônica podem ser preparadas através de uma variedade de processos incluindo em massa, solução, emulsão, suspensão, dispersão, precipitação, ou com o uso de 15 água ou solventes orgânicos. Quando necessário, são usados auxiliares de processo, incluindo iniciadores de radical livre, sistemas de iniciação redox, agentes de reticulação, agentes de ramificação, agentes de transferência de cadeia, agentes de suspensão, agentes umectantes, estabilizadores, porogênio, diluentes, estabilizadores de luz e calor, e plastificantes. O polímero pode ser 20 moldado sob a forma de, por exemplo, um pó, conta, folha, fibra, cápsula ou membrana.
É preferido que as capacidades de troca iônica dos polímeros nesta descritos sejam máximas para reter a carga de sal mais alta (por exemplo, expressa como NaCl). Quando mais elevada a capacidade, mais 25 baixa a dose de polímero requerida para excretar uma determinada quantidade de sal. A capacidade pode ser expressa como mEq de íon que pode ser trocado por grama de polímero. O peso de cloreto de sódio absorvido por uma grama de polímero como uma função da capacidade do polímero pode ser computado como se segue:
• · ·
·«· ···
WNacl= 58, 44, 10'7 (Cna·* em que Cna é a capacidade da resina de troca aniônica, e Ccat é a capacidade da resina de troca catiônica. Em modalidades preferidas da presente invenção, WNaci está na faixa de cerca de 0,05 a cerca de 1, preferivelmente de cerca de 0,2 a cerca de 0,7, de modo mais preferido de 5 cerca de 0,3 a cerca de 0,5. Can e Ccat estão, de modo preferido, entre cerca de a cerca de 30mEq/ g, preferivelmente de cerca de 5 a cerca de 25 mEq/g, de modo mais preferido entre cerca de 10 e cerca de 20 mEq/ g.
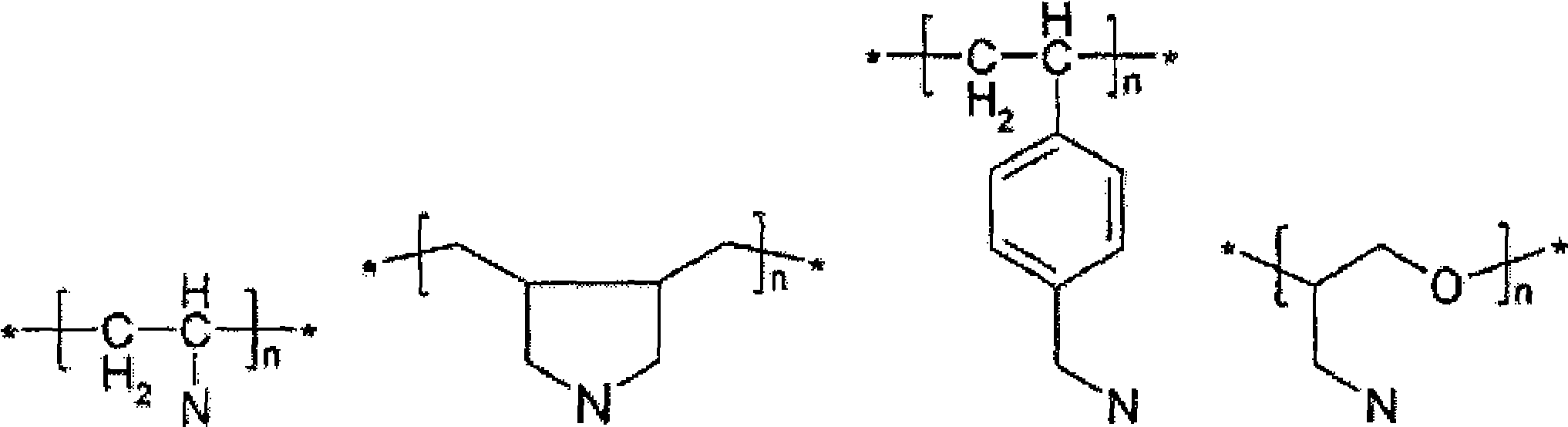
Exemplos de polímeros de troca aniônica adequados são:
*+Νγ'Νγ'ΝΊΤ· *+Νγ>Ν4τ*
N N N
Nestas estruturas, N representa um átomo de nitrogênio ligado a substituintes de modo a respeitar a valência de nitrogênio: exemplos de substituintes estão relacionados a seguir (mas não limitados a): - NR2, -NR-CH=NR, - NR-C(=NR) NR2, com R sendo H, alquila, arila, acila, opcionalmente substituídos.
As resinas de troca aniônica podem ser também sintetizadas a partir de polímeros de ocorrência natural, tais que polímeros de sacarídeo e polímeros semi- sintéticos, opcionalmente funcionalizados para introduzir funcionalidade amina na espinha dorsal ou nos resíduos pendentes. Eles podem ser preparados através de reações de substituição nucleofílica, sob condições alcalinas. Uma adição de Michael pode ser usada para preparar ·:· ί Γ;ΰ. < • * ··>··· · · · · · celulose cianoetilada ou carbamoil celulose pelct tratâmênto de eelaiosef cofti

acrilonitrila ou acrilamida, respectivamente. A preparação de aminoalquil celulósicos primários envolve, de modo geral, a reação de celulose ativada com halogenetos de aminoalquila, ácido amnoalquil sulfurico, ou etileno imina. Outro método para preparar aminoalquil celulósicos envolve a redução direta do grupo nitrila de celulose cianoetilada para fornecer aminopropil celulose. O rearranjo de Hofmann de carbamoil etil celulose com bromo / NaOH durante 30 - 120 minutos também fornecer aminopropil celulose. A reação de celulose ativada com epicloroidrina, seguida por reação subsequente com várias diaminas fornecer O-[ 2-Hidróxi-3 (ωaminoalquilamino) propil celulose. Uma 2-aminoetil-carbamoil celulose com um baixo grau de substituição (DS < 0,02) pode ser preparada pelo tratamento de carboximetil celulose de sódio com etileno diamina em excesso, na presença de carbodiimidas solúveis em água.
Em uma modalidade, as resinas básicas e ácidas estão encerradas em um compartimento isolado do fluido gastrintestinal por uma membrana permeável a íon. O uso de uma membrana para circundar as resinas que estão em proximidade adjacente reduz a variação de pH seguindo-
se à absorção de sal. Por exemplo, os dois tipos de resinas podem ser encerrados em um saco de diálise, saco de papel, matriz microporosa, gel de polímero, fibras ocas, vesículas, cápsulas, comprimido ou um filme.
Em uma modalidade, o polímero de remoção de sal compreende um sal interno de um complexo de polieletrólito, preparado a partir de polímeros de cargas opostas, o polímero sendo capaz de remover 25 íons a partir do trato gastrintestinal e não introduzir íons prejudiciais. Este material é aqui referido como a um complexo de eletrólito (PEC). A formação de um complexo é representada esquematicamente na Figura 1. Um policátion e um poliânion são misturados em uma razão estequiométrica, até que um complexo insolúvel seja precipitado.
··· ·*· . ··· · · ··· ··· ρ : : : ··. · : /. < Ο PEC forma como um resultado dl iHtbr’aç*ãô*eletrostâtiea
cooperativa entre os polímeros de cargas opostas e de um ganho de entropia produzido pela liberação de contraíons de molécula pequena. A lavagem adicional ou diálise conduz a um material isento de sal: quase todas as cargas nos polímeros são compensadas intemamente. Quando este material é colocado em contato com uma solução aquosa de uma concentração de sal finita, e se a concentração de sal for suficientemente alta, então a interação coulômbica entre o policátion e o poliânion é varrida pelo campo elétrico
produzido pelo eletrólito adicionado, e o complexo se toma solúvel. Nesta situação, cada carga em ambos os polímeros é compensada por um contraíon oriundo da solução circundante. O resultado líquido é uma absorção de sal pelo polímero a partir da solução aquosa, através de um processo de troca iônica. Quando o PEC é inteiramente solubilizado, a quantidade de sal retida pelo polímero é igual ao conteúdo molar de sal interno inicialmente presente no complexo de polímero.
Em uma modalidade, é primeiramente formado um complexo pela adição dos dois polímeros na razão molar requerida para formar um precipitado complexo, que é subsequentemente lavado do sal liberado. Quando o complexo de polímero isento de sal é ingerido oralmente, quando do contato com o conteúdo gastrintestinal, a resistência iônica fisiológica é suficiente para anular a interação coulômbica dentro do PEC, de tal modo que cada filamento de polímero carregado se toma solúvel, ao mesmo tempo em que varre um equivalente de sal (principalmente NaCl). Os polieletrólitos permanecem solúveis no trato gastrintestinal e evitam com que os seus contraíons associados sejam reabsorvidos, até a excreção nas fezes.
A preparação e a química física de PECs é bem conhecida na técnica. Por exemplo, vide A. S. Michael et al., J. Phys. Chem, 65, 1765 (1961); J. Phys. Chem. 69, 1447 (1965); J. Phys. Chem. 69, 1456 (1965); J.
Phy. Chem. 65, 1765 (1961); Bixler et al., Encycl. Polym. Sei. Pech. 10, 765 •·· ··· :·. : ·*· · : : : : / ·* ·· : :: ···: : ·* . : . :
(1969); Kabanov et al., Chem. Reviews, 4, 207-Í83 (i982); TFsuctiida et ãl., J. Polym. Sei. Polym. Chem. Ed. 10, 3397 (1972). PECs são amplamente usados na técnica na microencapsulação de drogas, enzimas, células, microorganismos, ilhotas de Langerhans, multicamadas de polieletrólitos 5 como sensores, imobilização de proteínas pela formação de complexo, e complexos de policátion com DNA como vetores em terapia genérica. Nestes pedidos da técnica anterior, os PECs retêm uma estrutura de gel sólido em concentrações de sal fisiológicas. No entanto, os PECs da presente invenção são submetidos à ressolubilização induzida por sal em concentrações de sal 10 fisiológicas, que então permitem que o polímero remova sais a partir do fluido fisiológico no trato gastrintestinal.
É preferido que os PECs e os polímeros que constituem os PECs preencham uma ou mais condições para prover propriedades de remoção de sal sob condições prevalecentes no trato gastrintestinal: os 15 polímeros e seus complexos são não- absorvíveis, não- irritáveis, não- tóxicos e não- inflamatórios. É também preferido que os polímeros, uma vez liberados do complexo, não produzam pressão osmótica elevada, de tal modo que não ocorram eventos intestinais significativamente indesejáveis, tais que o movimento intestinal e a diarréia osmótica. A solubilização do PEC pode 20 ser disparada em uma concentração de eletrólito típica do trato gastrintestinal.
A solubilização do PEC pode ocorrer a cerca de 50-200 mM expressos em NaCl, usualmente a cerca de 100 mM. É ainda preferido que o polímero, seja como um gel ou como uma solução aquosa, não altere adversamente a consistência das fezes, ou provoque constipação.
Os PECs da presente invenção com propriedades de remoção de sal recaem em 3 categorias em algumas modalidades: (i) ambos os polímeros são solúveis e distintos um do outro; (ii) um polímero é um gel reticulado, enquanto que o outro polímero é solúvel, o material reticulado sendo preferivelmente o componente catiônico; ou (iii) ambos os polímeros
: ··· ζ ζ Ζ ♦ · · · · são co-reticulados em um material de gel. Q PBC/rfo*«qu^ ambos oS polímeros são co-reticulados em uma material de gel, ocorre uma transição a partir de um estado em colapso a um estado intumescido na presença de um sal, em que o gel em colapso (sal interno) começa a absorver o sal 5 circundante, incluindo NaCl.
De modo típico, cada PEC possui uma concentração de sal, acima da qual o complexo é desintegrado, isto é, é solubilizado ou intumesce. Esta é uma das características do PEC, que controla a propriedade de remoção de sal requerida no ambiente gastrintestinal. A concentração de sal de 10 solubilização (ou a concentração de sal de intumescência de gel quando se trata de um gel reticulado) depende de um número de fatores, tais que a densidade de carga em ambos os polímeros, as restrições geométricas para formar um sal interno (equiparação da densidade de carga entre os componentes aniônicos e catiônicos), os pesos moleculares, a hidrofobicidade 15 total das espinhas dorsais do polímero, e a razão molar entre sítios catiônicos e aniônicos.
Os polímeros da presente invenção podem ser polímeros hidrofílicos com densidades de carga moderadas, uma desproporção nas densidades de carga entre cátions e ânions, e razões não- estequioméricas que 20 exibem propriedades de solubilização de sal em concentrações de sal nas faixas fisiológicas desejadas. As faixas preferidas de densidades de carga (expressas como capacidade de ânion ou cátion em mEq/g) são de cerca de 5 mEq / g a cerca de 25 mEq/ g, de modo mais preferido de 5 mEq/ g a 10 mEq/ g. Uma desproporção de densidade de carga preferida (medida como a razão 25 da capacidade de ânion para a capacidade de cátion; uma razão que se afasta de 1 é traduzida em uma desproporção de densidade) é de cerca de 0,2 a cerca de 0,8 e de cerca de 1, 2 a 1,8, de modo mais preferido sendo de cerca de 0, 5 a cerca de 0,8 e de cerca de 1,3 a cerca de 1,5. Uma razão estequiométrica preferida de cátion/ ânion é de cerca de 1, 00 +/ - 0,01 a cerca de 1,00 + / 28 ?·; η :··: η μ /. ?;
0,5, sendo de modo mais preferido de cerca de 1*00 +:/ -CrjOS^abêroa dê4,Ô0 + /-0,3.
Os polímeros da presente invenção podem ser homopolímeros ou copolímeros, em que a fração molar de monômero iônico pode estar na 5 faixa de cerca de 0,10 a cerca de 1. Outras arquiteturas de polímero, tais que em bloco, em estrela e de enxerto, e copolímeros em gradiente podem ser também vantajosas. Copolímeros em bloco são conhecidos como sendo reunidos em micelas, estas micelas podendo ser reticuladas no núcleo ou no
domínio da casca. Tais arquiteturas segmentadas podem ser produzidas através de métodos de polimerização de radical livre vivo, tais que RAFT ou
ATRP. Quando são usados polímeros solúveis, o peso molecular está, de modo preferido, entre cerca de 5000 g/ mol a cerca de 5.000.000 g/ mol, de modo preferido de cerca de 50.000 g/ mol a 1.000. 000 g/ mol. Quando são usados polímero do tipo estrela e micelar, os pesos moleculares estão 15 compreendidos, de modo típico, entre 50.000 a 100.000.000 g/ mol.
Finalmente, quando os polímeros são reticulados, o peso molecular é, por definição, infinito. Polímeros reticulados, usados de acordo com as várias modalidades da invenção, podem adotar vários formatos, incluindo contas
com diâmetros na faixa de a partir de cerca de 10 nanômetros a várias centenas de mícrons.
Síntese de Composições Núcleo- Casca
Exemplos de processos, que podem ser usados para a síntese de composições núcleo- casca adequadas, são o processo de suspensão inversa e o processo de suspensão direta.
No processo de suspensão inversa, o núcleo hidrofílico pode ser produzido através de polimerização de radical livre inversa usando um copolímero em bloco como o tensoativo. Monômeros adequados incluem sulfonato de vinila, ácido maleico, fosfonato de vinila, bis- fosfonato de vinila, ácido acrílico, ácido a- fluoro acrílico, sulfonato de estireno, e ácido
..... * ·♦? ··;
• · *· * : ·. *· * * *
• ♦ acrilamido- metil- propano sulfônico (AMPS), cçu ostseüs*sãis. Ά* casca *pocte ser produzida por um copolímero em bloco com um bloco compreendendo o
material de casca (por exemplo, catiônico e hidrofóbico) e o outro bloco sendo solúvel e co- reativo com o polímero do núcleo.
Outras técnicas para a síntese de composições núcleo- casca são descritas no pedido de patente co-pendente intitulado, “Ion Binding Compositions”, número do documento de procuração: 29329- 715. 201; depositado em 30 de março de 2004, Número do Pedido: 10/ 814. 749.
Um processo útil consiste na conversão de monômeros sulfônicos a suas formas de éster, que então se tomam muito menos solúveis em água e que podem portanto, ser conduzidas à polimerização em miniemulsão direta. A casca pode ser produzida pela adição de um monômero de segundo estágio para encapsular o núcleo. O material final é hidrolisado em condições ácidas.
Em uma modalidade, o material de casca é projetado para interagir com os ácidos biliares e/ ou ácidos graxos, de modo preferido em um modo irreversível. Aglutinantes do ácido biliar adequados, que podem ser usados na casca, incluem colestirilamina, Welchol, e as composições
adequadas expostas na Patente U.S. 5633344, Macromolecules, 1997, 30,
6174 - 84 e J. Pharma Sei. 86, 1, 1997. Um exemplo de um monômero adequado, que pode ser usado na casca, é 11- undecilmetacrilato de trimetilamônio.
Outro processo útil compreende primeiramente a formação de um polímero funcional amina, tal que polialil amina, polivinil amina ou 25 polietileno imina, e a seguir tratamento com um agente de sulfonação, tal que SO3/ trimetil amina, ou altemativamente um agente de fosfonação, tal que P2O5. Outros precursores de polímero podem ser também usados, por exemplo poliestireno, polibutadieno, poliisopreno, polipropileno, borracha de EPDM e os similares.
Em outro processo, os polímerçs a&artiÂife/s WTonãdcrs õu altamente fosfonados são obtidos a partir de polímeros funcionais amina, que são então pós - reagidos com ácido vinil sulfônico, vinil fosfônico ou vinil difosfônico, através de adições de Michael.
Tratamento de Desequilíbrios Iônicos e de Sobrecarga de Fluido
A presente invenção inclui métodos de tratamento usando os polímeros acima descritos. As composições poliméricas de ligação de sódio e composições de núcleo- casca de ligação de sódio nesta descritas podem ser usadas para tratar doenças, em que uma redução nos níveis fisiológicos de sal 10 e/ ou água seja desejada. As populações de indivíduos, nas quais as composições e métodos nesta descritos são particularmente úteis, incluem, mas não estão limitadas a falha cardíaca congestiva, hipertensão, diabetes, insuficiência renal crônica, doença renal de estágio terminal, e cirrose

hepática. Além disso, populações de indivíduos adequadas incluem indivíduos que sofrem de sobrecarga de fluido e/ou sobrecarga de sal. Outra população de indivíduos adequados incluem indivíduos que são resistentes à terapia de diurético e que estão sofrendo de hipertensão, falha cardíaca crônica e doença renal de estágio terminal, cirrose hepática, insuficiência renal crônica, sobrecarga de fluido, ou uma combinação dos mesmos. As composições descritas nesta são também úteis no tratamento de edema periférico, incluindo edema pré- menstruai e edema do tipo mistura, e edema de gravidez com ou sem hipertensão, incluindo pré-eclâmpsia.
Em uma modalidade, os indivíduos tratados com as composições descritas nesta se beneficiam da remoção de pequenas 25 quantidades de sal constantemente ao longo de um período de tempo estendido. Em outra modalidade, os indivíduos e beneficiam da remoção de água extra- celular e, deste modo, possuem um efeito benéfico sobre o controle de fluido, controle da pressão sangüínea, ganho de peso interdialítico e outros aspectos comumente relacionados à sobrecarga de fluido quando ·· · ♦ · ♦ · ·· ·. · sofrendo de hipertensão, falha cardíaca crônicía, djença TétiâTcte* estágio terminal, cirrose hepática, e/ou insuficiência renal crônica. A remoção tanto de sódio como de cloreto auxilia no tratamento de acidose. O uso das composições nesta descritas podem evitar a formação de edema após um evento cardíaco em um indivíduo. Além disso, as composições são adequadas para o tratamento de indivíduos, que sofrem de falha cardíaca diastólica sensível a volume/ sal.
Em indivíduos com doença renal de estágio terminal, as
composições da presente invenção causam a remoção de sódio e, deste modo, causam uma redução na sobrecarga de fluido. A remoção de sódio auxilia a manter o volume sanguíneo sob controle para tratar hipertensão. O tratamento com as composições da presente invenção pode permitir uma redução na dosagem e/ ou substituição de tratamentos de hipertensão corrente, tais que bloqueadores de canal de cálcio e minimizar ganhos de peso de água entre 15 sessões de diálise, que possuem um impacto significativo sobre o coração, duração da diálise e qualidade de vida geral.
Os polímeros da presente invenção são também úteis no tratamento de indivíduos com nefropatia diabética e hipertensiva. De modo típico, estes indivíduos desenvolvem resistência à terapia com diurético 20 devido à função renal reduzida. Nesta população de indivíduos, os polímeros da presente invenção causam a remoção de sódio, o que, por sua vez, permite reduzir a hipertensão e preservar a função renal. Os polímeros podem ser usados isoladamente ou em combinação com vasodilatadores.
As presentes composições podem ser também usadas para tratar indivíduos com hipertensão. Outros indivíduos que podem se beneficiar do tratamento com as composições da presente invenção incluem indivíduos que sofrem de falha cardíaca crônica, diarréia, incontinência, e indivíduos com cirrose hepática.
O termo “tratamento” e seus equivalentes gramaticais, como aqui usados, incluem que seja alcançado um benefício fçrapAAA)·®/ ôu*um benefício profilático. Por benefício terapêutico, é compreendida a erradicação ou a melhora do distúrbio subjacente sendo tratado. Por exemplo, em um indivíduo de hipertensão, o benefício terapêutico inclui a erradicação ou a 5 melhora da hipertensão subjacente. Além disso, é alcançado um benefício terapêutico com a erradicação ou melhora de um ou mais dos sintomas fisiológicos associados com o distúrbio subjacente, de tal modo que seja observada uma melhora no indivíduo, apesar do fato de que o indivíduo possa

estar ainda afligido com o distúrbio subjacente. Por exemplo, a administração de um polímero da presente invenção a um indivíduo que sofra de hipertensão, provê o benefício terapêutico não apenas quando a pressão sangüínea é diminuída, mas também quando é observado um aperfeiçoamento no indivíduo com relação a outros sintomas que acompanham a hipertensão, tais que dores de cabeça. Para o benefício profilático, pode ser administrado um polímero a um indivíduo, que esteja e risco de desenvolver hipertensão, ou a um indivíduo que relate um ou mais dos sintomas fisiológicos de hipertensão, mesmo que um diagnóstico de hipertensão não tenha sido feito.
A presente invenção também inclui kits, que compreendem as composições nesta descritas. Estes kits compreendem pelo menos uma das composições da presente invenção e instruções, que ensinam o uso do kit de acordo com os vários métodos nesta descritos.
Terapias Combinadas
Em todas as populações de indivíduo adequadas, as composições poliméricas presente invenção podem ser administradas em 25 conjunto com outros tratamentos. Por exemplo, as composições podem ser administradas com outros tratamentos de hipertensão e de falha cardíaca congestiva convencionais. Em indivíduos de hipertensão, os polímeros podem ser administrados de modo conjunto com terapia de hipertensão incluindo, mas não limitados a, bloqueadores de canal de cálcio, diuréticos, beta , * ··· ··· :: ’ ;· * · · iií····.· bloqueadores, alfa bloque adores, e medicação cõntra* ansiedade,'inibidores ae
ACE, vasodilatadores, e bloqueadores de receptor de angiotensina II. Por “ administração conjunta” é intencionado compreender aqui a administração simultânea dos agentes terapêuticos na mesma forma de dosagem, a administração simultânea em formas de dosagem separada, e a administração
separada dos agentes terapêuticos. Por exemplo, um polímero da presente invenção pode ser administrado simultaneamente com um diurético, em que ambos o polímero e o diurético são formulados, de modo conjunto, em um
mesmo comprimido. Em alternativa, o polímero podería ser administrado simultaneamente com o diurético, em cujo caso o polímero e o diurético estão presentes em dois comprimidos separados. Em outra alternativa, o polímero podería ser administrado primeiramente seguido pela administração do diurético ou vice-versa. Em uma modalidade, as composições nesta descritas podem ser administradas em conjunto com um laxante.
Formulações e Vias de Administração
As composições poliméricas e as composições de núcleocasca nesta descritas ou sais farmaceuticamente aceitáveis das mesmas,
podem ser fornecidos ao indivíduo usando uma ampla variedade de vias ou modos de administração. As vias mais preferidas para a administração são a oral ou a intestinal.
O termo “sal farmaceuticamente aceitável” compreende aqueles sais, que retêm a eficácia biológica e as propriedades dos polímeros usados na presente invenção e que não biologicamente ou de outro modo indesejáveis. Tais sais incluem sais com ácidos orgânicos ou inorgânicos, tais 25 que ácido clorídrico, ácido bromídrico, ácido fosfórico, ácido nítrico, ácido sulfurico, ácido metano sulfônico, ácido p-tolueno sulfônico, ácido acético, ácido fumárico, ácido succínico, ácido láctico, ácido mandélico, ácido málico, ácido cítrico, ácido tartárico ou ácido maleico. Em adição, se os polímeros usados na presente invenção contiverem um grupo carbóxi ou outro grupo
aceitável com bases orgânicas ou inorgânicas. Exemplos de bases adequadas incluem hidróxido de sódio, hidróxido de potássio, amônia, cicloexil amina, dicicloexil amina, etanol amina, dietanol amina, e trietanol amina.
Se necessário, os polímeros e as composições de núcleo- casca podem ser administrados em combinação com outros agentes terapêuticos. A escolha dos agentes terapêuticos, que podem ser administrados em conjunto com os compostos da invenção, irá depender, em parte, da condição que está sendo tratada.
Os polímeros (ou sais farmaceuticamente aceitáveis dos mesmos) podem ser administrados per se ou sob a forma de uma composição farmacêutica, em que o (s) composto (s) ativo(s) está (ão) em mistura com um ou mais veículos farmaceuticamente aceitáveis, excipientes ou diluentes. Composições farmacêuticas para o uso de acordo com a presente invenção 15 podem ser formuladas de modo convencional usando um ou mais veículos fisiologicamente aceitáveis compreendendo excipientes e auxiliares, que facilitam o processamento dos compostos ativos sob a forma de preparações que podem ser usadas farmaceuticamente. A formulação apropriada depende I da via de administração selecionada.
Para a administração oral, os compostos podem ser prontamente formulados pela combinação do(s) composto(s) ativo(s) com veículos farmaceuticamente aceitáveis, bem conhecidos na técnica. Tais veículos possibilitam com que os compostos da invenção sejam formulados como comprimidos, pílulas, drágeas, cápsulas, líquidos, géis xaropes, pastas, 25 suspensões, pastilhas e os similares, para a ingestão oral por um indivíduo a ser tratado. Em uma modalidade, a formulação oral não possui um revestimento entérico. Preparações farmacêuticas para o uso oral podem ser obtidas como um excipiente sólido, opcionalmente moagem de uma mistura resultante, e processamento da mistura de grânulos, após a adição de • · · :> : : : ··.: : /: /:
auxiliares adequados, se desejado, para a of)tençjão*-de* wrnprífnidòs ou núcleos de drágeas. Alguns excipientes são, em particular, cargas, tais que açúcares, incluindo lactose, sacarose, manitol, ou sorbitol; preparações de celulose, tais que, por exemplo, amido de milho, amido de trigo, amido de arroz, amido de batata, gelatina, goma tragacanto, metil celulose, hidroxipropilmetil celulose, carboximetil celulose sólida, e/ ou polivinil pirrolidona (PVP). Se desejado, podem ser adicionados agentes de desintegração, tais que polivinil pirrolidona reticulada, ágar, ou ácido algínico
ou um sal do mesmo, tal que alginato de sódio.
Núcleos de drágeas podem ser providos com revestimentos adequados. Para este propósito, soluções de açúcar concentradas podem ser usadas, que podem conter opcionalmente goma arábica, talco, polivinil pirrolidona, carbopol gel, polietileno glicol, e/ ou dióxido de titânio, soluções de verniz, e solventes orgânicos adequados ou misturas de solventes. Corantes 15 ou pigmentos podem ser adicionados aos revestimentos de drágeas ou comprimidos para a identificação ou para caracterizar diferentes combinações de doses de compostos ativos.
Apenas para a administração por via oral, os compostos podem
ser formulados como uma preparação para a liberação sustentada. Numerosas técnicas para a formulação de preparação para a liberação sustentada são conhecidas na técnica.
Preparações farmacêuticas, que podem ser usadas oralmente, incluem cápsulas de encaixe, produzidas de gelatina, tais que cápsulas seladas, moles, produzidas de gelatina e um plastificante, tal que glicerol ou 25 sorbitol. As cápsulas de encaixe, que contêm os ingredientes ativos em mistura com carga, tais que lactose, aglutinantes, tais que amidos, e/ou lubrificantes, tais que talco ou estearato de magnésio e, opcionalmente e estabilizadores. Em cápsulas moles, os compostos ativos podem ser dissolvidos ou suspensos em líquidos adequados, tais que óleos graxos, • · · parafina líquida, ou polietileno glicóis líquidoá Em atfição, eStabiliza’dores podem ser adicionados. Todas as formulações para a administração oral devem estar em dosagem adequadas para a administração.
Dosagens Eficazes
Composições farmacêuticas adequadas para o uso na presente invenção incluem composições, em que os polímeros de ligação de sódio estão presentes em uma quantidade eficaz, isto é, em uma quantidade eficaz para que seja alcançado o benefício terapêutico e/ ou profilático. A quantidade eficaz, eficaz para uma aplicação particular, irá depender da condição sendo 10 tratada e da via de administração. A determinação da quantidade eficaz está bem dentro das capacidades daqueles versados na técnica, em especial à luz
do aqui exposto.
A quantidade eficaz para o uso em seres humanos pode ser determinada a partir de modelos de animal. Por exemplo, uma dose para seres humanos pode ser formulada de modo a alcançar concentrações gastrintestinais, que foram verificadas como sendo eficazes em animais.
Uma pessoa versada na técnica, usando técnicas conhecidas na técnica, pode determinar a quantidade eficaz de polímero. Em uma modalidade, uma quantidade eficaz de polímero de ligação de sódio é a quantidade que irá diminuir a pressão diastólica e/ ou sistólica em um indivíduo com hipertensão; de modo preferido reduzindo a pressão sanguínea a uma faixa normal. Em algumas modalidades, o decréscimo é de cerca de
20% a cerca de 40%. A quantidade eficaz pode também ser uma quantidade que aumenta a excreção fecal de sódio. Um aumento na excreção de sódio de cerca de 10 a cerca de 150 mmol por dia é preferido, um aumento de cerca de mmol a cerca de 100 mmol por dia é ainda mais preferido; e é mais preferido um aumento de cerca de 40 mmol a cerca de 80 mmol por dia.
EXEMPLOS
EXEMPLO 1:
• · • · t :· ;
Medição da capacidade de ligação de sódio, bt vitr&
O material de resina é tratado com HC1 1 M e lavado repetidamente com água. Uma alíquota pesada é então titulada com NaOH 0,1 Mea capacidade registrada como a quantidade molar de base requerida para alcançar o pH desejado (usualmente 6). Em alternativa, a resina é embebida com uma solução e NaCl 1 M tamponada no pH desejado, lavada com água, e finalmente tratada com KC1 0,5 Μ. O sódio liberado é então titulado por cromatografia de troca iônica e a capacidade de ligação de sódio correspondentemente calculada. Contas de polímero descritas nos exemplos 10 que se seguem, fornecem, de modo típico, uma capacidade de ligação de Na na faixa de cerca de 6 a 10 mmol/g.
EXEMPLO 2
Síntese de composições poliméricas de ligação de sódio
A. Síntese de contas de polímero de sulfonato de polivinila
O monômero sulfonato de vinila é primeiramente polimerizado em água com persulfato de sódio como o iniciador de radical livre em um reator à prova de pressão a 110°C. Oligômeros de sulfonato de polivinila são isolados através de precipitação em acetona. Os oligômeros são então tratados
com cloreto de tionila para formar copolímeros de sulfonato de vinila-cocloreto de vinilsulfonila. As contas são obtidas pela dispersão de uma solução de oligômero de sulfonato de vinila-co-cloreto de vinilsulfonila em tolueno, e então adição de diamino- propano para formar as contas desejadas. As contas finais são lavadas extensivamente com água, HCL 1 M, e água, sucessivamente.
B. Síntese de contas de polímero de sulfamato de polivinila através de polimerização em suspensão inversa
100 partes de vinil formamida/ metileno-bis-acrilamida em uma razão de 90/10, em peso, são solubilizadas em 100 partes de água com 1 parte de persulfato de sódio como um iniciador; a mistura é então dispersada
em 200 partes de tolueno e uma parte de sesqúioleato de íorbitol como um
tensoativo, usando um homogeneizado de alto cisalhamento. A emulsão é mantida sob agitação mecânica a 80°C, durante 8 horas. As contas são então filtradas, lavadas com acetona, e hidrolisadas em HCL 1 M durante 6 horas, a 5 50°C, para contas reticuladas de poli vinil amina. As contas são então tratadas com trimetilamina/ SO3 para fornecer as partículas de sulfamato de polivinila desejadas.
C. Síntese de contas de copolímero de sulfamato de polivinila/ sulfato de vinila
O processo acima (Exemplo 2 B) é repetido, exceto que 30 mol % de vinil formamida são substituídos por acetato de vinila.
D. Síntese de contas de polímero de polivinilfosforamídico
O processo acima (Exemplo 2B) é repetido, exceto que os grupos poli vinil amina são tratados com P2O5.
E. Síntese de contas de N-fbis-fosfônico- etiDpolivinil amina
O processo acima (Exemplo 2B) é repetido, exceto que os grupos polivinilamina são adicionalmente tratados com vinil fosfonato de dietila, e o polímero resultante é hidrolisado à forma fosfônica.
F. Síntese de contas do ácido poli-cc-fluoroacrílico
Primeiramente o ácido cc- fluoroacrílico é preparado a partir de éster de cloroacetato de KF, seguindo o procedimento descrito em Pittman, C.
U. M., Ueda et al. (1980), Macromolecules 13 (5) : 1031-1036. As contas são preparadas através de um processo de suspensão direta, em que uma mistura de éster metílico a-fluoroacrílico/ divinil benzeno/ peróxido de benzoíla, em 25 uma razão, em peso, de 90/ 9/ 1, são dispersadas em água sob alto cisalhamento, com hidroetilcelulose como um agente de suspensão. A suspensão é agitada e aquecida a 80°C durante 10 horas. O monômero residual é eliminado por extração com vapor. As contas são então filtradas e tratadas com HC1 para hidrolisar o polímero à forma de partículas de ácido
poli oc-fluoroacrílico desejadas.
G. Partícula de núcleo de (ácido poli - a-fluoroacrílico)/ casca de (poli-11 undecilmetacrilato de trimetilamônio)
Partículas de polímero de éster metílico a- fluoroacrílico reticuladas são preparadas através de polimerização em miniemulsão. Uma mistura de éster metílico a-fluoroacrílico/ dimetacrilato de etileno glicol/ ΑΙΒΝ7 Hexadecanol em uma razão em peso de 88/ 9/1/2 é dispersada em uma solução aquosa de SDS a 0,5%, em peso, usando um homogeneizador de alto
cisalhamento Ultra Turrax. A temperatura é ajustada a 85°C durante 15 horas e então a 75°C durante mais 5 horas, após o que uma mistura de monômero de segundo estágio, composta de 25 partes de metacrilato de 11dimetilaminodecila e cinco partes de divinil benzeno é dosada junto com 5 partes de uma solução aquosa a 5%, em peso, de persulfato de sódio. A dispersão é então resfriada à temperatura ambiente e tratada com sulfato de 15 dimetila para converter os grupos diamino a grupos de sulfato de trimetil amónio. A suspensão é adicionalmente tratada com HCI para converter o éster metílico do núcleo às porções ácidas desejadas. O diâmetro de partícula médio é medido por um classificador de partículas por difração a laser
Malvem a 0,5 mícrons.
H. Síntese de contas de copolímero de fosfonato de vinila/ ácido acrílico
Fosfonato de vinila e ácido acrílico são primeiramente neutralizados com 50 mol % com NaOH para formar uma solução aquosa a %, em peso; a esta mistura, é adicionado metileno- bis- acrilamida em 10 %, em peso, para monômeros. 100 partes da mistura de monômeros são então emulsificadas em 200 partes de hexano e 1 parte de sesquioleato sorbitol como um tensoativo. 10 partes de uma solução aquosa a 5%, em peso, de persulfato de sódio são ainda adicionadas à suspensão, reação é mantida @ 80°C durante 10 horas, enquanto que 10 partes de solução de persulfato de sódio são adicionadas. A água é então extraída através de um aparelho Dean40 *·· ···
Stark, as contas são filtradas e repetidamente iavaàas* *por'metanol e água, nesta ordem.
I. Síntese de contas do copolímero de fosfonato de vinila/ ácido qfluoroacrílico
O processo acima descrito no Exemplo 2H é repetido, exceto que o ácido acrílico é substituído por ácido a-fluoroacrílico.
J. Síntese de contas de sulfato de polivinila
Contas de acetato de polivinila reticuladas são preparadas através de polimerização em suspensão direta, filtradas, e hidrolisadas para 10 contas de álcool polivinílico através de hidrólise básica em metanol / NaOH. Após lavagem extensiva, as contas são adicionalmente tratadas com trióxido de enxofre/ trimetil amina para fornecer as partículas de sulfato de polivinila desejadas.
K. Síntese de núcleo de (poli-fosfonato de vinila / ácido acrílico)/ casca de 15 (estireno- vinil piridina) usando uma abordagem de copolímero em bloco.
É preparado um copolímero dibloco, que compreende um bloco de poli- acrilato de etila e um segundo bloco de um copolímero de estireno/ 4-vinil piridina em uma razão de 50: 50, em peso; a razão do bloco é
selecionada a 1: 1, 5 e o peso molecular total é de 50.000 g/ mol. A seguir, é executado um processo em emulsão, em que 1 parte do copolímero em bloco é solubilizada em 100 partes de água deionizada, à qual são adicionadas 20 partes de uma mistura composta de acrilato de terc-butila, etil fosfonato de vinila, dimetacrilato de etileno glicol, peróxido de benzoíla em uma razão de
78: 18: 3:1, em peso. A temperatura é elevada para 70°C e a reação é deixada 25 prosseguir durante 10 horas. Os monômeros residuais são extraídos com um dispositivo Dean- Stark e as partículas são então fervidas em HC1 1 M durante a noite, neutralizadas com NaOH, lavadas com água e finalmente novamente acidificadas em HC1 diluído para fornecer as partículas de núcleo- casca.
L. Preparação de partículas núcleo- casca compreendendo um núcleo de • * · : ϊ · · < . ··. · · ·: .:.: *«.··· · * * sulfamato de polivinila reticulado e uma chsca* de* cobolímero de 11aminodecilmetacrilato de dimetila/ metacrilato de laurila
O polímero da casca é preparado separadamente através de polimerização por adição de radical livre de uma razão a 50: 50, em peso, de uma mistura de monômero de 11-aminodecilmetacrilato de dimetila/ metacrilato de laurila a 20%, em peso, em DMF, usando AIBN como um iniciador. As contas obtidas a partir do Exemplo 2B são revestidas por pulverização usando a solução de casca de polímero acima mencionada usando um aparelho de revestimento de leito fluido Wurster de unidade 10 portátil de 2”- 4”/ 6” (5,08 cm - 10, 16 cm/ 15, 24 cm). A unidade de leito fluidizado é operada de tal modo que um revestimento de espessura média de 5 mícrons seja depositado sobre as partículas do núcleo.
M. Partículas de núcleo- casca usando um processo de deposição de látex
O polímero da casca é preparado como uma emulsão usando 15 ou técnicas de emulsificação diretas ou polimerização em emulsão. As contas são então contatadas com o látex durante um determinado período de tempo, decantadas, e secadas por pulverização. As taxas de deposição de casca mais altas são alcançadas pela indução da coagulação incipiente do látex sobre as
contas do núcleo, ou pela alteração da temperatura, adição de eletrólito, variação de pH, ou uma combinação dos mesmos.
N. Partículas de núcleo- casca preparadas a partir de partículas de núcleo de ácido a~ acrílico e casca de multícamadas de polialil amina / sulfonato de poliestireno.
Contas de núcleo negativamente carregadas do Exemplo 21 25 são primeiramente suspensas em uma solução aquosa diluída de poli (hidrocloreto de alilamina) em temperatura ambiente durante 20 minutos e as contas são separadas da solução através de centrifugação e subseqüentemente lavadas com água. As contas são então suspensas em uma solução aquosa diluída de sulfonato de poliestireno sódico durante 20 minutos e separadas
....... ··: ··:
·*· ζ ζ··· *·*.ζ *· *· ·” : : : · · ·/· .,· ·.* *·β através de centrifugação e lavadas com água. Eáte processo é repetido até que seja obtida uma casca de 20 nm de espessura.
O. Contas de núcleo de ácido poliacrilico/ casca contendo lactose
Um derivado estireno de lactose (glicomonômero) é preparado de acordo com o procedimento descrito por Kobayashi, et al., Macromolecules, 1997, 30, 2016- 2020. Um glicopolímero é preparado pela polimerização do glicomonômero, metacrilato de glicidila e acrilato de butila em DMF, usando AIBN como o iniciador. O glicopolímero é ligado às contas
de poli (ácido acrílico) pela suspensão das contas em solução de 10 glicopolímero em DMF, a 60°C, durante 8 horas, e as contas de núcleo/ casca são isoladas através de centrifugação e lavadas com DMF e água.
EXEMPLO 3
Medição da capacidade de ligação de sódio em condições fisiológicas representativas do trato GI superior
Partículas dos Exemplos 2A - 20 são condicionadas sob a forma de próton e adicionadas a um fluido do GI reconstituído, representativo do segmento do jejuno, incluindo ácidos biliares, ácidos graxos e enzimas intestinais. Os cátions Na e K são ajustados a 80 mM e 15 mM,
respectivamente. Após a incubação a 37°C durante 30 minutos, as contas são isoladas a través de filtração e lavadas com água deionizada. Então, uma solução de LiCl a 0,5 M é adicionada para deslocar ambos os cátions Na e K. A capacidade de ligação de cátion é então calculada e encontrada na faixa de 3 mmol/ g a 10 mmol/ g para sódio e 0,2 mmol/ g a 2 mmol /g para potássio.
Medição da capacidade de ligação de sódio em condições fisiológicas, representativas do trato GI inferior
Partículas dos Exemplos 2 A - 2 O são incubadas no fluido do trato superior simulado e isoladas e lavadas, como acima indicado, e então adicionadas a um fluido simulado, representativo do ambiente do cólon, em que concentrações de íons de sódio e potássio são ajustadas a 70 nM e 0 mM.
• · ;····· · ·
Após uma incubação de 30 minutos, as partículas são Centrifugadas e o sobrenadante testado quanto ao Na liberado a partir da conta e a capacidade de ligação de Na resultante computada. Um exemplo comparativo é executado com uma resina de sulfonato de poliestireno comercial na forma 5 ácida com uma capacidade nominal de 5 mmol/ g. Todas as partículas da presente invenção demonstram ligação superior de Na em ambos os fluidos do trato superior e inferior.
EXEMPLO 4
Modelo Animal para Demonstrar a Natureza Não - absorvida da Resina 10 de Ligação de Na
Estes estudos são executados usando uma administração de bolo única de resina rotulada com 3E1 ou 14C dada a ratos alojados em câmaras

metabólicas. O projeto de estudo consiste de dois grupos de seis ratos Sprague-Dawley; os animais no grupo 1 recebem uma dose oral única de resina radiorrotulada (250 mg/ kg de peso corpóreo), enquanto que os animais no grupo 2 foram previamente tratados com resina não rotulada na dieta a ~6 g/ kg/ dia durante 28 dias, seguida por uma administração única de resina rotulada no dia 29 (250 mg/ kg de peso corpóreo). O grupo 1 é usado para medir a absorção e a eliminação em animais não habituados à resina, enquanto que o Grupo 2 é usado para monitorar a absorção e a eliminação em animais cronicamente tratados, como pode ser observado em indivíduos que recebem a resina em uma base diária. A urina e fezes totais são coletadas e analisadas quanto à radiorrotulação em 0, 6, 12, 18, 24, 18 e 72 horas após a administração de resina rotulada. No sacrifício, alíquotas de sangue são 25 removidas e o plasma coletado através de centrifugação; o conteúdo do trato
GI é coletado e as amostras de tecido do estômago, ceco, intestino delgado, intestino grosso, reto, fígado, baço, músculo esquelético e nodos linfáticos são coletadas. Os pesos da urina, tecido e do conteúdo do GI são determinados e o tecido é picado. A radioatividade na urina e no plasma é determinada através


de contagem por cintilação líquida. O tecSdo 'fecal ê as substâncias homogeneizadas sangüíneas totais são ffacionadas e queimadas com a radioatividade retida na fase aquosa determinada através de contagem por cintilação líquida. As propriedades de uma resina não- absorvida são (i) 5 nenhuma excreção urinária significativa de radioatividade (< 0,05% da dose para ambos os grupos); (ii) radioatividade total média excretada nas fezes entre 97% - 100% da dose total para ambos os grupos, recuperada dentro de 72 horas do período de coleta; (iii) sangue, plasma, fígado, rins, baço, músculo esquelético e nodo linfático (isto é, tecidos não- gastrintestinais) 10 possuem < 0,07 % da dose de resina rotulada total em um ponto de coleta em horas; e (iv) estômago, intestino delgado, intestino grosso, ceco, e reto possuem < 0,1% da dose total de resina rotulada em um ponto de coleta de 72 horas.
EXEMPLO 5
Estudos de voluntário humano para demonstrar a natureza nãoabsorvida da resina de ligação de Na
A resina rotulada 14C é preparada para fornecer, a grosso modo, 0,2 m Ci/g de resina. Em um projeto de estudo típico, vinte voluntários ! recebem cápsulas 3 x 600 mg de resina não- rotulada, três vezes ao dia, 20 durante 28 dias (dose diária total = 5400 mg). Dezesseis indivíduos são admitidos na unidade metabólica de pesquisa clínica em um centro designado, para continuar com a porção de radiorrotulação do estudo. Na manhã do primeiro dia de confinamento, os indivíduos recebem uma dose oral única de 2,4 g (cápsulas 4 x 600 mg) de resina rotulada 14C para um total de 480 uCI 25 de 14C por indivíduo. A resina não- rotulada é então administrada antes, durante os próximos três dias. Amostras de sangue são extraídas em 0, 4, 8, 12, 24, 48, 72 e 96 horas. Urina e fezes esvaziadas são coletadas na linha de referência durante os intervalos de 0- 24 horas, 24- 48 horas, 48- 72 horas, 7296 horas. Amostras de sangue totais e fecais homogeneizadas são secadas e • · ··· ·*! .
• « · *· :· : ··· *·
- ί < : ··♦·..· *·* · · oxidadas antes da contagem por cintilação. A râdioátividadé no* sangue, urina
e fezes é expressa como um percentual da dose administrada para cada intervalo de tempo e como um percentual total. As propriedades de uma resina não- absorvida são (i) quantidades não- detectáveis de resina 14C no sangue total de qualquer indivíduo em qualquer momento durante o estudo;
(ii) para cada indivíduo, < 0,009% da dose de resina rotulada nas amostras de mina coletadas, cobrindo um período de 96 horas seguindo-se à administração da resina rotulada; e (iii) para cada indivíduo, > 99% da dose são recuperados na fezes, durante um período de 10 dias seguindo-se à administração da resina 10 14C.
EXEMPLO 6
Modelos de Animal para Demonstrar a Capacidade de Ligação de Na de Resinas
Modelos de animal são usados para demonstrar a ligação de cátions de sódio pelas resinas, que são suplementadas em uma dieta controlada, administrada a ratos ou cachorros. Estes estudos são geralmente conduzidos em animais normais para demonstrar um efeito da resina, então em modelos de animal doentes, em que um desequilíbrio sustentado de
eletrólitos, que conduz a edema extravascular é criado comprometendo a função renal, do fígado ou cardíaca do animal de teste.
Um experimento típico com ratos normais para determinar a eficiência de ligação relativa dos polímeros de teste usa três grupos (n= 6/ grupo) de ratos fêmeas Sprague-Dawley colocados em gaiolas metabólicas individuais em uma dieta consistindo de biscoitos de baixo conteúdo de sódio e de água destilada. O sódio é administrado diariamente através de um tubo de alimentação oral, em três doses, como uma solução 200 mM (2, 4 mEq). Durante os primeiros três dias do teste, os dados da linha de referência são coletados sob a forma de mEq/ dia de sódio na urina e mEq/ dia de sódio nas fezes; o sódio usual mede 2, 25 - 2, 5 mEq/ dia na urina e 0,05- 0,3 mEq / dia
....... /. ··: ··:. :·♦ : : : :· · · ·.: ·· :· : : ; . :·.· ·.· .
nas fezes. Nos três dias subseqüentes, os três grupos* de *animais de teste recebem doses fixas da resina de teste (500, 1000, 2000 mg/ kg/ dia) em adição à solução salina administrada por tubo endogástrico durante três doses. No final de três dias de teste, a resina é removida a partir do tubo endogástrico e a solução salina é administrada como no primeiro período para prover um
segundo período de controle de monitoração. Resinas ativas são aquelas que diminuem o sódio na urina durante o segundo período de dosagem abaixo de 2,25 mEq/ dia (faixas típicas são de 0,25 - 1,5 mEq/ dia) e aumento do conteúdo de sódio nas fezes (valores típicos estão na faixa de 2 mEq/ g 10 5mEq/ g de resina). O conteúdo de sódio na urina e nas fezes é determinado através de extração e cromatografia de troca iônica ou através de fotometria de chama.
Um experimento típico com ratos que apresentam função renal comprometida, usado para simular a hipertensão e a retenção de fluido no indivíduo de ESRD, utiliza a indução química do dano renal (acetato de

uranila, gentamicina, cefaloradina, etc.) ou a resseção cirúrgica do rim (nefrectomia de 5/ 6 s) para induzir a falha renal crônica. Após a manipulação química ou cirúrgica dos animais e a estabilização da função renal em um estado reduzido, os animais são divididos em três grupos de teste (n = 10/ grupo). Como em testes de animal normal, os animais de teste são mantidos durante 3 dias em biscoitos com baixo conteúdo de sódio e recebem solução de NaCl 75 mM à vontade; os valores de sódio de linha de referência são determinados para urina e fezes. Aos animais em cada grupo são fornecidas quantidades fixas da resina através de tubo endogástrico oral (3 doses, doses 25 diárias de 500, 1000 e 2000 mg/ kg/ dia), durante três dias, com um período de “limpeza“ durante três dias, seguindo-se à dosagem de resina. O sódio na urina e nas fezes é determinado através da linha de referência, teste e períodos de limpeza; o conteúdo de sódio na urina é, em geral, elevado na linha de referência e nos períodos de limpeza (4-5 mEq/ dia), mas é reduzido na fase
...... · ··: ··:.
:*♦ : :: :· ; '< *· ·/ ..· ·.· *.* de tratamento (1-2 mEq/ dia). De modo similar, o sódio* fecal na linha e referência e grupos de limpeza é de 0,03 - 0,56 mEq/ dia e aumenta para 3,8 5 mEq/ g de resina nos animais tratados.
EXEMPLO 7
Estudos de voluntários humanos para demonstrar a capacidade de ligação de sódio de resinas
O término da análise farmacológica e toxicológica de segurança que permite IND das resinas irá possibilitar estudos de voluntários humanos em indivíduos normais, para avaliar a capacidade de ligação in vivo 10 das resinas de teste. O projeto de um estudo típico compreende 24 indivíduos normais alojados em uma unidade metabólica clínica; os indivíduos apresentam peso corpóreo, teste hematológicos e químicos normais e não apresentam história de doença gastrintestinal, renal ou hepática. Após a triagem, os voluntários são colocados aleatoriamente em 3 grupos de 8 15 indivíduos cada; seis dos indivíduos em cada grupo são selecionados aleatoriamente para receber uma dose específica de resina (25 mg/ kg; 70 mg/ kg; 140 mg/ kg) e dois recebem placebo. Os voluntários são alojados nas unidades metabólicas durante 18 dias e consomem uma dieta controlada de

sódio e 5 g de sódio elementar por dia (3 refeições, além de um lanche). O projeto de estudo é o que se segue; no dia 1, os indivíduos recebem uma dose oral única de resina ou placebo de acordo com o grupo de tratamento. Durante os próximos sete dias (d2- d8), os indivíduos não recebem droga; a partir da manha do dia 5 até a manhã do dia 9, urina e fezes de 24 horas são coletadas e o conteúdo de sódio e potássio das amostras determinado. Nos dias 9- 16, os 25 indivíduos recebem a mesma dosagem de acordo com o grupo, as doses sendo divididas ao longo de três doses diárias; urina e fezes totais são coletadas do dia 13 ao dia 17. Os indivíduos são descarregados no dia 18. O conteúdo de sódio fecal é levado nos grupos de tratamento, aproximando-se de 4- 5 mEq/ g de resina.
EXEMPLO 8 • · · « · :
• * ♦ > · ♦ · · ♦ · · • * • · .
Membrana disparadas por pH
Membranas com copolímeros de dibutil acrilamida e dimetil aminoetil metacrilato foram sintetizadas e seus perfis de permeabilidade 5 foram avaliados em diferentes pHs. A solução de doador usada para estudar a permeabilidade foi de tampão Na+ 50 mM em diferentes pHs. Os resultados são ilustrados na Figura 2. Com pH crescente (pH na faixa de 5 ~8), a permeabilidade da membrana diminuiu e se tomou até mesmo impermeável em alto pH. A composição da membrana também afetou a permeabilidade. 10 Para amostras com DBA < 50 % (D2, D3), a membrana era impermeável em alto pH (> 7,5).
Todas as publicações e pedidos de patentes mencionados neste relatório são incorporadas a este, a título referencial, e na mesma extensão em que cada publicação ou pedido de patente foi especificamente e 15 individualmente indicado para ser incorporado a título referencial.
Será evidente para aquele de habilidade na técnica que muitas alterações e modificações podem ser introduzidas no mesmo, sem que haja afastamento do espírito ou escopo das reivindicações apensas.