BRPI0606802B1 - uso de compostos de morfolino para a prevenção de contaminação bacteriana - Google Patents
uso de compostos de morfolino para a prevenção de contaminação bacteriana Download PDFInfo
- Publication number
- BRPI0606802B1 BRPI0606802B1 BRPI0606802-2A BRPI0606802A BRPI0606802B1 BR PI0606802 B1 BRPI0606802 B1 BR PI0606802B1 BR PI0606802 A BRPI0606802 A BR PI0606802A BR PI0606802 B1 BRPI0606802 B1 BR PI0606802B1
- Authority
- BR
- Brazil
- Prior art keywords
- compound
- biofilm
- carbon atoms
- compounds
- coated
- Prior art date
Links
- 125000004573 morpholin-4-yl group Chemical group N1(CCOCC1)* 0.000 title claims abstract description 5
- 230000001580 bacterial effect Effects 0.000 title abstract description 19
- 238000011109 contamination Methods 0.000 title abstract description 3
- 150000001875 compounds Chemical class 0.000 claims abstract description 63
- 230000032770 biofilm formation Effects 0.000 claims abstract description 12
- 125000004432 carbon atom Chemical group C* 0.000 claims abstract description 11
- 125000000217 alkyl group Chemical group 0.000 claims abstract description 7
- 230000002265 prevention Effects 0.000 claims abstract description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims abstract description 3
- 238000013270 controlled release Methods 0.000 claims description 6
- 239000000203 mixture Substances 0.000 claims description 6
- 229910052751 metal Inorganic materials 0.000 claims description 5
- 239000002184 metal Substances 0.000 claims description 5
- 238000009472 formulation Methods 0.000 claims description 4
- 230000009467 reduction Effects 0.000 claims description 4
- 230000000399 orthopedic effect Effects 0.000 claims description 3
- 150000003839 salts Chemical class 0.000 claims description 3
- 238000000576 coating method Methods 0.000 abstract description 8
- 239000011248 coating agent Substances 0.000 abstract description 4
- QSFOWAYMMZCQNF-UHFFFAOYSA-N delmopinol Chemical compound CCCC(CCC)CCCC1COCCN1CCO QSFOWAYMMZCQNF-UHFFFAOYSA-N 0.000 description 22
- 229960003854 delmopinol Drugs 0.000 description 21
- 210000004027 cell Anatomy 0.000 description 17
- 239000000463 material Substances 0.000 description 17
- 241000894006 Bacteria Species 0.000 description 15
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 15
- 239000007943 implant Substances 0.000 description 10
- 238000000034 method Methods 0.000 description 8
- 239000000243 solution Substances 0.000 description 8
- 238000012360 testing method Methods 0.000 description 8
- 239000012530 fluid Substances 0.000 description 7
- 239000011159 matrix material Substances 0.000 description 7
- 238000003860 storage Methods 0.000 description 7
- 229920002306 Glycocalyx Polymers 0.000 description 6
- 230000015572 biosynthetic process Effects 0.000 description 6
- 210000004517 glycocalyx Anatomy 0.000 description 6
- 230000035899 viability Effects 0.000 description 6
- 230000001464 adherent effect Effects 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- 230000000813 microbial effect Effects 0.000 description 5
- 235000015097 nutrients Nutrition 0.000 description 5
- -1 complement Proteins 0.000 description 4
- 230000007613 environmental effect Effects 0.000 description 4
- 244000005700 microbiome Species 0.000 description 4
- 241000894007 species Species 0.000 description 4
- 239000007864 aqueous solution Substances 0.000 description 3
- 238000009826 distribution Methods 0.000 description 3
- 230000000694 effects Effects 0.000 description 3
- 239000004744 fabric Substances 0.000 description 3
- 239000000017 hydrogel Substances 0.000 description 3
- 230000010412 perfusion Effects 0.000 description 3
- 239000004033 plastic Substances 0.000 description 3
- 229920003023 plastic Polymers 0.000 description 3
- 238000006748 scratching Methods 0.000 description 3
- 230000002393 scratching effect Effects 0.000 description 3
- 229920002444 Exopolysaccharide Polymers 0.000 description 2
- WOBHKFSMXKNTIM-UHFFFAOYSA-N Hydroxyethyl methacrylate Chemical compound CC(=C)C(=O)OCCO WOBHKFSMXKNTIM-UHFFFAOYSA-N 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 239000002202 Polyethylene glycol Substances 0.000 description 2
- 230000008901 benefit Effects 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 239000006161 blood agar Substances 0.000 description 2
- 230000001143 conditioned effect Effects 0.000 description 2
- 239000002537 cosmetic Substances 0.000 description 2
- 238000005516 engineering process Methods 0.000 description 2
- 238000000799 fluorescence microscopy Methods 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 210000003709 heart valve Anatomy 0.000 description 2
- 230000003993 interaction Effects 0.000 description 2
- 238000004519 manufacturing process Methods 0.000 description 2
- 230000035800 maturation Effects 0.000 description 2
- 229920000620 organic polymer Polymers 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000008057 potassium phosphate buffer Substances 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- XJMOSONTPMZWPB-UHFFFAOYSA-M propidium iodide Chemical compound [I-].[I-].C12=CC(N)=CC=C2C2=CC=C(N)C=C2[N+](CCC[N+](C)(CC)CC)=C1C1=CC=CC=C1 XJMOSONTPMZWPB-UHFFFAOYSA-M 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 238000001356 surgical procedure Methods 0.000 description 2
- 239000000725 suspension Substances 0.000 description 2
- 238000010998 test method Methods 0.000 description 2
- 208000034309 Bacterial disease carrier Diseases 0.000 description 1
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 1
- 102100026735 Coagulation factor VIII Human genes 0.000 description 1
- 229920000742 Cotton Polymers 0.000 description 1
- 241000195493 Cryptophyta Species 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 108700039887 Essential Genes Proteins 0.000 description 1
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 1
- 102000008946 Fibrinogen Human genes 0.000 description 1
- 108010049003 Fibrinogen Proteins 0.000 description 1
- 241000233866 Fungi Species 0.000 description 1
- 229920002683 Glycosaminoglycan Polymers 0.000 description 1
- 108060003393 Granulin Proteins 0.000 description 1
- 101000911390 Homo sapiens Coagulation factor VIII Proteins 0.000 description 1
- 108090001090 Lectins Proteins 0.000 description 1
- 102000004856 Lectins Human genes 0.000 description 1
- 239000004793 Polystyrene Substances 0.000 description 1
- 208000034809 Product contamination Diseases 0.000 description 1
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 1
- 241000191963 Staphylococcus epidermidis Species 0.000 description 1
- RTAQQCXQSZGOHL-UHFFFAOYSA-N Titanium Chemical compound [Ti] RTAQQCXQSZGOHL-UHFFFAOYSA-N 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000002411 adverse Effects 0.000 description 1
- 239000000443 aerosol Substances 0.000 description 1
- 238000005576 amination reaction Methods 0.000 description 1
- 238000004458 analytical method Methods 0.000 description 1
- 238000004873 anchoring Methods 0.000 description 1
- 125000000129 anionic group Chemical group 0.000 description 1
- 239000003242 anti bacterial agent Substances 0.000 description 1
- 229940088710 antibiotic agent Drugs 0.000 description 1
- 239000004599 antimicrobial Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 230000010065 bacterial adhesion Effects 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 229920000249 biocompatible polymer Polymers 0.000 description 1
- 239000012620 biological material Substances 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 239000007853 buffer solution Substances 0.000 description 1
- 239000006227 byproduct Substances 0.000 description 1
- 229940041514 candida albicans extract Drugs 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 239000000919 ceramic Substances 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 230000001332 colony forming effect Effects 0.000 description 1
- 230000000295 complement effect Effects 0.000 description 1
- 239000002361 compost Substances 0.000 description 1
- 238000007796 conventional method Methods 0.000 description 1
- 238000005260 corrosion Methods 0.000 description 1
- 230000007797 corrosion Effects 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 235000013365 dairy product Nutrition 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 239000004053 dental implant Substances 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 239000002552 dosage form Substances 0.000 description 1
- 239000003814 drug Substances 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000003628 erosive effect Effects 0.000 description 1
- 230000005284 excitation Effects 0.000 description 1
- 229920000912 exopolymer Polymers 0.000 description 1
- 229940012952 fibrinogen Drugs 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 239000003292 glue Substances 0.000 description 1
- 229910052736 halogen Inorganic materials 0.000 description 1
- 150000002367 halogens Chemical class 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 239000012535 impurity Substances 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- 208000015181 infectious disease Diseases 0.000 description 1
- 230000028709 inflammatory response Effects 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- 229910052500 inorganic mineral Inorganic materials 0.000 description 1
- 238000003780 insertion Methods 0.000 description 1
- 230000037431 insertion Effects 0.000 description 1
- 238000012977 invasive surgical procedure Methods 0.000 description 1
- 230000002427 irreversible effect Effects 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- 239000002523 lectin Substances 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000014759 maintenance of location Effects 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 239000002609 medium Substances 0.000 description 1
- 230000002503 metabolic effect Effects 0.000 description 1
- 239000011707 mineral Substances 0.000 description 1
- 239000003595 mist Substances 0.000 description 1
- 239000003068 molecular probe Substances 0.000 description 1
- 229920001778 nylon Polymers 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 125000000962 organic group Chemical group 0.000 description 1
- 229910052760 oxygen Inorganic materials 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- 244000052769 pathogen Species 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000008447 perception Effects 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000011505 plaster Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 229920002223 polystyrene Polymers 0.000 description 1
- 235000008476 powdered milk Nutrition 0.000 description 1
- 238000002360 preparation method Methods 0.000 description 1
- 230000008569 process Effects 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 108090000623 proteins and genes Proteins 0.000 description 1
- 102000004169 proteins and genes Human genes 0.000 description 1
- 238000000746 purification Methods 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 229910052710 silicon Inorganic materials 0.000 description 1
- 239000010703 silicon Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000002904 solvent Substances 0.000 description 1
- 238000005507 spraying Methods 0.000 description 1
- 229910001220 stainless steel Inorganic materials 0.000 description 1
- 239000010935 stainless steel Substances 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 229910000811 surgical stainless steel Inorganic materials 0.000 description 1
- 239000010966 surgical stainless steel Substances 0.000 description 1
- 239000010936 titanium Substances 0.000 description 1
- 229910052719 titanium Inorganic materials 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 239000011345 viscous material Substances 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- 239000012138 yeast extract Substances 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/72—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms
- A01N43/84—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with nitrogen atoms and oxygen or sulfur atoms as ring hetero atoms six-membered rings with one nitrogen atom and either one oxygen atom or one sulfur atom in positions 1,4
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
- A01N25/02—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests containing liquids as carriers, diluents or solvents
- A01N25/04—Dispersions, emulsions, suspoemulsions, suspension concentrates or gels
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N33/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic nitrogen compounds
- A01N33/02—Amines; Quaternary ammonium compounds
- A01N33/08—Amines; Quaternary ammonium compounds containing oxygen or sulfur
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61F—FILTERS IMPLANTABLE INTO BLOOD VESSELS; PROSTHESES; DEVICES PROVIDING PATENCY TO, OR PREVENTING COLLAPSING OF, TUBULAR STRUCTURES OF THE BODY, e.g. STENTS; ORTHOPAEDIC, NURSING OR CONTRACEPTIVE DEVICES; FOMENTATION; TREATMENT OR PROTECTION OF EYES OR EARS; BANDAGES, DRESSINGS OR ABSORBENT PADS; FIRST-AID KITS
- A61F13/00—Bandages or dressings; Absorbent pads
- A61F13/02—Adhesive bandages or dressings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/49—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing heterocyclic compounds
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L15/00—Chemical aspects of, or use of materials for, bandages, dressings or absorbent pads
- A61L15/16—Bandages, dressings or absorbent pads for physiological fluids such as urine or blood, e.g. sanitary towels, tampons
- A61L15/42—Use of materials characterised by their function or physical properties
- A61L15/44—Medicaments
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q11/00—Preparations for care of the teeth, of the oral cavity or of dentures; Dentifrices, e.g. toothpastes; Mouth rinses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q17/00—Barrier preparations; Preparations brought into direct contact with the skin for affording protection against external influences, e.g. sunlight, X-rays or other harmful rays, corrosive materials, bacteria or insect stings
- A61Q17/005—Antimicrobial preparations
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61L—METHODS OR APPARATUS FOR STERILISING MATERIALS OR OBJECTS IN GENERAL; DISINFECTION, STERILISATION OR DEODORISATION OF AIR; CHEMICAL ASPECTS OF BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES; MATERIALS FOR BANDAGES, DRESSINGS, ABSORBENT PADS OR SURGICAL ARTICLES
- A61L2300/00—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices
- A61L2300/40—Biologically active materials used in bandages, wound dressings, absorbent pads or medical devices characterised by a specific therapeutic activity or mode of action
- A61L2300/404—Biocides, antimicrobial agents, antiseptic agents
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y10—TECHNICAL SUBJECTS COVERED BY FORMER USPC
- Y10T—TECHNICAL SUBJECTS COVERED BY FORMER US CLASSIFICATION
- Y10T428/00—Stock material or miscellaneous articles
- Y10T428/13—Hollow or container type article [e.g., tube, vase, etc.]
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Engineering & Computer Science (AREA)
- Wood Science & Technology (AREA)
- Agronomy & Crop Science (AREA)
- Environmental Sciences (AREA)
- Zoology (AREA)
- Dentistry (AREA)
- Plant Pathology (AREA)
- Pest Control & Pesticides (AREA)
- Chemical & Material Sciences (AREA)
- Epidemiology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Dermatology (AREA)
- Birds (AREA)
- Oral & Maxillofacial Surgery (AREA)
- Communicable Diseases (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Oncology (AREA)
- Organic Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Biomedical Technology (AREA)
- Vascular Medicine (AREA)
- Heart & Thoracic Surgery (AREA)
- Materials Engineering (AREA)
- Toxicology (AREA)
- Hematology (AREA)
- Dispersion Chemistry (AREA)
- Materials For Medical Uses (AREA)
- Prostheses (AREA)
- Apparatus For Disinfection Or Sterilisation (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Eyeglasses (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Nitrogen And Oxygen As The Only Ring Hetero Atoms (AREA)
Abstract
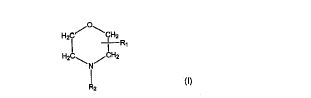
USO DE COMPOSTOS DE MORFOLINO PARA A PREVENÇÃO DE CONTAMINAÇÃO BACTERIANA. Um composto da fórmula 1: onde R~ 1~ é um grupo alguila linear ou ramificado contendo 8 a 16 átomos de carbono na posição 2 ou 3 do anel morfolino, e R~ 2~ é um grupo alquila linear ou ramificado contendo 2 a 10 átomos de carbono, substituído com um grupo hidróxi exceto na posição alfa, a soma dos átomos de carbono nos grupos R~ 1~ e R~ 2~ sendo pelo menos 10 e preferivelmente 10 a 20, é utilizado para evitar a formação de biofilme em uma superfície. Os compostos são particularmente úteis para revestimentos ou tratamentos de dispositivos médicos, incluindo stents, cateteres e fios-guia.
Description
A presente invenção refere-se à prevenção da formação de biofilme em disoositivos médicos e orodutos dearmazenagem contendo fluido.
Um biofilme pode ser descrito simplesmente como uma "comunidade de micróbios incorporados em uma matriz de 10 polímero orgânico, aderindo a uma superfície"(Carpentier, 1993, J. Appl. Bacteriol. 75:499-511). Todos os biofilmes compreendem três ingredientes básicos: micróbios, umglicocálix e uma superfície. Se um desses componentes for retirado, um biofilme não sedesenvolverá.
Um biofilme pode ser formado por uma únicaespécie bacteriana, porém frequentemente biofilmes consistem em muitas espécies de bactérias juntamente com fungos, algas, protozoários, resíduos e produtos de corrosão. Um biofilme pode se formar em quase qualquer superfície exposta a bactérias e alguma quantidade de água.
O processo de fixação bacteriana em uma superfície disponível (viva ou abiótica) e o desenvolvimento subsequente de um biofilme são examinados por W. Michael Dunne Jr., Clin. Microbiol. Rev. 2002 abril; 15(2): 155-66. A fixação bacteriana é determinada pordiversas variáveis, incluindo a espécie bacteriana, composição superficial, fatores ambientais e produtos essenciais de gene.
Em termos simples, um biofilme se forma quando as 30 bactérias aderem a uma superfície em um ambiente aquoso ecomeçam a excretar uma substância viscosa semelhante à cola, que pode fixar as mesmas em uma gama de materiais - implante médico, e tecido.
A adesão primária ocorre através do encontre casual de uma superfície condicionada e um microorganismo planctônico. Como uma simplificação em excesso, a adesão primária entre bactérias e superfícies abióticas é mediada por interações não especificas ip°r exempio, nidrotooicas), ao passo que a adesão a tecido vivo ou desvitaiizado é realizada através de mecanismos de acoplamento molecular específicos (lectina, por ligante ou adesão). Esse estágio é reversível e é determinado por variáveis f i sioquímicas definindo a interação entre a superfície de célula bacteriana e a superfície condicionada de interesse.
Após adesão primária, ocorre uma fase de ancoramento, onde organismos frouxamente ligados consolidam a adesão pela produção de exopolissacarídeos que complexam com a superfície, resultando em adesão irreversível à superfície.
Uma vez que as bactérias estão fixadas irreversivelmente, a maturação de biofilme tem início. A densidade total e complexidade do biofilme aumentam, à medida que os organismos ligados superficialmente replicam ativamente (e morrem) e componentes extracelulares (gerados por bactérias fixadas) interagem com moléculas orgânicas e inorgânicas no ambiente imediato para criar o glicocálix. Exopolissacarídeos formam o componente principal (excluindo água) do glicocálix que, na maioria das espécies, é predominantemente aniônico e retém nutrientes enquanto protege as bactérias contra insultos ambientais. No caso de implantes biomédicos infectados, o glicocálix pode incluir proteínas de resposta inflamatória derivada de hospedeiro ou proteínas de matriz como complemento, fibrinogênio, e glicosaminoglicanos fixados no implante. iimitado pela disponibilidade de nutri antes no ambiente imediato, a perfusão daqueles nutrientes para células dentro do biofilme e a remoção de resíduos. Um fluxo hidrodinâmico ótimo através do biofilme favorece o ores timent^ e perrusáu em vez de erosão oas camadas mais externas. Outros fatores que controlam a maturação de biofilme incluem pH interne, perfusão de oxigênio, fonte de carbono, e osmolaridade. Em uma massa crítica, um equilíbrio dinâmico é atingido no qual a camada mais externa de crescimento (mais distante da superfície) gera organismos planctônicos. Esses organismos são livres para escapar do biofilme e colonizar outras superfícies. As células mais próximas à superfície se tornam quiescentes ou morrem devido à falta de nutrientes ou perfusão, pH diminuído, pCp, ou um acúmulo de subprodutos metabólicos tóxicos.
Uma vez ancorados em uma superfície, microorganismos do biofilme realizam uma variedade de reações prejudiciais ou benéficas (por padrões humanos) dependendo das condições ambientais em volta. Biofilmes microbianos nas superfícies custam bilhões de dólares anualmente em dano a equipamentos, contaminação de produtos, perdas de energia e infecções médicas. Os métodos convencionais de exterminar bactérias (como antibióticos e desinfecção) são frequentemente ineficazes com bactérias de biofilme, em parte devido à natureza protetora do glicocálix. As imensas doses de antimicrobianos necessárias para livrar os sistemas de bactérias de biofilme são ambientalmente indesejáveis (e podem não ser permitidas por regulações ambientais) e medicamente impraticáveis (uma vez que a quantidade necessária para exterminar as bactérias de biofilme teria também um efeito adverso sobre o paciente) .
Embora as superfícies ou revestimentos de superfície que retardam a adesão bacteriana tenham sido descritos (por exemplo, Sheng e colaboradores, Diagn. Microbiol. Infec. Dis. 38:1-5), nada foi desenvolvido para evitar a mesma (pl-11, Lappin-Scott e Costerton, Microbial Biofilm 1995. Cambridge University Press). Por conseguinte, novas estratégias são necessárias para gerenciar a formação de biofilme.
A presente invenção se baseia na percepção de que delmopinol, e seus derivados, podem ser utilizados para evitar ou reduzir a formação de biofilme ou assegurar um estado de biofilme não patogênico (não viável). Isso pode ser utilizado em aplicações industriais, incluindo a prevenção de formação de biofilme em dispositivos cirúrgicos ou dispositivo de armazenagem de água ou dispositivos de distribuição.
De acordo com um primeiro aspecto da presente invenção, um composto tendo a fórmula (I), ou um sal do mesmo, é utilizado para a prevenção ou redução de formação de biofilme em uma superfície, ou para evitar ou reduzir crescimento microbiano viável em uma superfície, onde Ri é um grupo alquila linear ou ramificado contendo 8 a 16 átomos de carbono na posição 2 ou 3 do anel morfolino, e R2 é um grupo alquila linear ou ramificado C ,..X"x t <_i i 2 lA 1 u ciLi.7in.uo uciLijiJhu, OUJJ^! 1. L. U I K.,' 1...'.<..> J L L ...1(11 pUpOhidróxi exceto na posição a"! fa, a soma dos átomos de carbono nos grupos R; e R.. sendo pelo menos 10 epreferivelmente 10 a 20.
De acordo com um segundo aspecto da presenteinvenção, há o uso cie um composto como definido acima para tratai um implemento cirúrgico antes da cirurgia.
De acordo com um terceiro aspecto da presente invenção, há uma zaragatoa impregnada com um composto como definido acima.
De acordo com um quarto aspecto da presente invenção, há um dispositivo médico revestido com um composto como definido acima.
De acordo com um quinto aspecto da presente invenção, um filtro, tubo de distribuição de água ou tanque de armazenagem de fluido é revestido com um composto como definido acima.
De acordo com sexto aspecto da invenção, um recipiente compreendendo um composto como definido acima, é utilizado para o tratamento de uma superfície a fim de evitar ou reduzir formação de biofilme na superfície ou evitar ou reduzir crescimento microbiano viável na superfície.
De acordo com um sétimo aspecto da invenção, um recipiente compreende uma pluralidade de pacotes vedados individuais, cada pacote compreendendo uma forma de dosagem unitária de um composto como definido acima, em forma líquida.
A invenção se baseia na surpreendente revelação de que o delmopinol e seus derivados, podem evitar ou reduzir a formação de biofilme e/ou podem assegurar que qualquer biofilme bacteriano seja inativo, isto é, que ‘'VP ’V: esr. w r■ -■ \/ _dve i . i " U .i ■..<■ ). Lutilizado aqui, se refere ac significado reconhecido do termo na técnica, isto é, uma comunidade de micróbios e um glicocálix associado, fixado em uma superfície. Uma variedade de definições existe na técnica, cada uma das quais está compreendida no escopo oa presente invenção. Por exemp1 o, Caroent i.er ' supra ) descreve um oiotiime como "uma comunidade de micróbios incorporados em uma matriz de polímero orgânico, aderindo a uma superfície"; Costerton (1999 Science 284: 1318-1322) define um biofilme como "uma comunidade estruturada de células bacterianas anexadas em uma matriz polimérica de auto-produção e aderente a uma superfície inerte ou viva"; Elder (1995 Eye 9:102-109) descreve um biofilme em termos mais cooperativos como "um consórcio de funções de microorganismos organizados em uma matriz de exopolímero extensa".
Os compostos para uso na presente invenção têm a fórmula geral (1) como mostrado acima, onde Ri é um grupo alquila linear ou ramificado contendo 8 a 16 átomos de carbono na posição 2 ou 3 do anel morfolino, e R2 é um grupo de alquila reto ou ramificado contendo 2 a 10 átomos de carbono, substituído com um grupo hidróxi exceto na posição alfa, a soma dos átomos de carbono nos grupos Ri e R;_ sendo pelo menos 10 e preferivelmente 10 a 20. Em uma modalidade preferida, o composto é delmopinol, isto é, 3- (4-propil-heptil)-4-(2-hidróxietil) morfolina, um composto conhecido.
A preparação dos compostos utilizados na invenção é descrita em US 4894221, cujo conteúdo é aqui incorporado a título de referência.
Na descrição a seguir faz-se referência à "prevenção ou redução de formação de biofilme." Entretanto, a presente invenção também abrange o tratamento S 'V y : j ■ ' i es Ud l -.-i v i α 1 ..< I CU'J z_ _1_ _i_ biofilmes "ativos". Biofilmes ativos são aqueles caracterizados por microorganismos viáveis. Por conseguinte, a referência à prevenção de formação de biofilme inclui a prevenção ou redução da formação de complexos microbianos viáveis ou coiônias ou a reouçao na formação de tais comoiexos ou colônias. "Reoucao" e meoiua pela comparação com uma superfície não tratada.
Os compostos podem ser utilizados para tratar qualquer superficie. Virtualmente qualquer superfície - animal, mineral ou vegetal (isto é, biótica ou abiótica j - pode ser adequada para colonização bacteriana e formação de biofilme, incluindo lentes de contato, cascos de navio, tubulações de petróleo e laticínios e todas as variedades de implantes biomédicos e dispositivos transcutâneos; os compostos podem ser utilizados, portanto, para evitar a formação de biofilme em qualquer uma dessas superficies.
Os compostos são de beneficio especifico na prevenção de biofilmes em dispositivos médicos, por exemplo, implantes cirúrgicos incluindo juntas artificiais como quadris, ferragens ortopédicas como pinos, placas e fios, membros artificiais/protético, válvulas cardiacas, stents, lentes de contato e dispositivos para distribuir fluidos, nutrientes e remédios, ou para a remoção de fluidos e refugo, por exemplo, catereres. Para evitar dúvida, o termo "dispositivo médico", como utilizado aqui, inclui dispositivos e implantes utilizados em procedimentos cosméticos. Os compostos também podem ser utilizados para evitar formação de biofilme em etiquetas de informação e identificação ou chips eletrônicos que são implantados em um sujeito.
O composto da invenção também pode ser utilizadopara tratar implementos cirúrgicos, por exemplo, lâminas outro instrumento utilizado em um procedimento cirúrgico invasive.
O dispositivo médico pode ser um implanto, isto é, um dispositivo que é inserido no corpo de um sujeito. Em uma modalidade preferida, o dispositivo e um implante cirurcuco que requer que uma incisão seja ieita im corpo para permitir implantação. Em uma modalidade particularmente preferida, o dispositivo a ser tratado é um implante dental, por exemplo um parafuso ou pino dental para retenção de dente. Alternativamente, o dispositivo médico contata o corpo porém não penetra no mesmo, por exemplo, um membro profético, atadura gessada, lente de contato ou meio auxiliar de audição, externo.
No contexto de uma lente de contato, o composto da invenção pode ser impregnado sobre a superfície da lente de contato. Alternativamente, no contexto de lentes de contato de hidrogel, o composto pode ser impregnado na matriz de hidrogel. Alternativamente, o composto pode estar presente na solução utilizada para armazenar ou limpar lentes de contato.
O sujeito em (ou sobre) o qual o dispositivo é implantado (ou contatado) pode ser humano ou animal, isto é, aplicações veterinárias estão compreendidas no escopo da invenção.
O composto será normalmente revestido na superfície ou dispositivo a ser tratado. Há muitos modos nos quais os compostos podem ser revestidos sobre substâncias adequadas, incluindo revestimentos de pulverização, irradiação e cura por ultravioleta. As tecnologias para revestir dispositivos médicos com biomateriais são agora avançadas, e essas tecnologias podem ser aplicadas na presente invenção. Por conseguinte, a part) cu] ar dispositivos médicos revestidos com o composto da fórmula I. Filtro ou tubos de distribuição de água revestidos com o composto da fórmula I também estão 5 compreendidos no escopo da presente invenção, bem como osdisposit 1 vos cie d.i s L r .i. bu ição de t luido ou armazenagem de fj.uido, revestidos. o πiacemcu α ser revest^Oo pocm sei metal, plástico, cerâmica, poliestireno ou vidro. Preferivelmente, o material a ser revestido é metal, por 10 exemplo, aço inoxidável.
O composto da invenção pode ser ligado á superfície tratada em uma ligação covalente ou não covalente. Se ligado de forma covalente, uma molécula de ligação pode ser utilizada para ligar o composto àsuperfície. Por exemplo, polietilenoglicol (PEG) é um substrato ligante útil que pode ser utilizado na presente invenção. A aminação também pode ser utilizada para distribuir uma molécula ligante eficaz.
Alternativamente, o composto pode ser impregnadoem uma matriz, por exemplo, uma matriz de polímero.Matrizes de polímeros biocompativeis convencionais podem ser utilizadas para reter o composto na superficie. Por exemplo, poli(organo)fofazeno, hidrogéis hidrofilicos (por exemplo, metacrilato 2-hidróxietil; HEMA) ou revestimentosa base de em silicio (por exemplo, fluorosilicone) são todos utilizados como revestimentos convencionais em dispositivos médicos e podem ser utilizados para reter um composto da invenção. Um método de revestimento adequado é revelado em US2005/0187611, cujo conteúdo é pela presente incorporado a titulo de referência.
Em uma modalidade preferida, um dispositivo médico é contatado com um composto da fórmula I antes ou durante a inserção em (ou contato com) o sujeito em (ou SOI '■ r f-* O q 1.1 d I. <J l lllp lαhi.t: ue vc r; i o J L.:. u . . Mu 1 _■ preferivelmente, o dispositivo é rinçadc- no composto antes ■de ou durante contato com o sujeito. Mais preferivelmente, a rinçagem ocorre imediatamente antes do contato com o sujeito, com secagem subsequente para revestir o composto sobre o dispositivo.
Uma modalidade preterida da invenção compreende uma quantidade do composto da fórmula I adequada para uma aplicação única no dispositivo médico, ou outra superfície, dentro de um recipiente. Preferivelmente, as superficies internas do recipiente, seu ambiente interno e conteúdo (por exemplo, delmopinol) são assépticos, isto é, estéreis e substancialmente livres de patógenos e, portanto, adequados para uso em uma operação médica (ou cosmética) como cirurgia. Mais preferivelmente, as superfícies externas são também estéreis. Qualquer recipiente adequado para reter um líquido pode ser utilizado, prefere-se que o recipiente possa ser vedado. Um recipiente preferido é um sachê, ou bolsa, que pode ser vedado de forma asséptica na produção e cortado ou rasgado para ser aberto quando necessário. Preferivelmente, o sachê é feito de um material de metal ou plástico flexível; sachês adequados são conhecidos na técnica. Outros recipientes adequados incluem garrafas, jarros e tubos de qualquer material, preferivelmente vidro ou plástico. Em uma modalidade preferida, o recipiente é um vasilhame para a armazenagem ou 1 impeza de uma lente de contato. O tamanho do recipiente (e portanto a dosagem predeterminada de composto armazenado dentro do mesmo) adequado para diferentes aplicações será evidente para uma pessoa versada na técnica, por exemplo, um implante de quadril exigirá uma quantidade maior de delmopinol do que um cateter (padrão) . Prefere-se que cada recipiente seja "de uso único", isto é, eliminado, independente se todo o conteúdo foi ut i 1izado. Isso tem a vantagem de minimizar qualquer contaminação em potencial.
O composto da invenção pode estar presente no recipient em qualquer concent ração aoequaoa . 1'ipicament e , o composto esta presente em uma concentração de f ui-c. kp/ v; a 10% (p/v), preferivelmente de 0,1% (p/v) a 5% (p/v) e mais preferivelmente de 1% (p/v) a 3% (p/v), por exemplo 2% (p/v). 0 composto estará tipicamente presente em uma solução de água, embora qualquer outro solvente adequado possa ser utilizado, inclusive álcool.
Os compostos da fórmula I podem ser impregnados sobre um material que é utilizado para contatar a superfície sobre a qual a formação de biofilme deve ser evitada. O material pode ser de tecido ou não tecido. Um material de tecido será tipicamente utilizado para limpar a superfície; exemplos não limitados de materiais de tecidos adequados incluem uma zaragatoa, pano, lenço ou esfregão. O material de tecido pode compreender fibras naturais (por exemplo, algodão) ou sintéticas (por exemplo, náilon) ou uma combinação das duas. Em uma modalidade preferida, o material impregnado é um material de "uso único" asséptico/estéril, adequado para uso em um ambiente médico, por exemplo, uma bandagem. Mais preferivelmente, o material é fornecido em um recipiente como descrito acima; o recipiente pode compreender somente o material impregnado, ou o material impregnado e um excesso do composto adequado para rinçar a superfície (além de, ou em vez de, contatar o mesmo com o material impregnado) .
Os compostos da fórmula I são também úteis em outras aplicações industriais onde um fluido, por exemplo, água, é colocado em contato com uma superfície. Em uma evitar a formação de biofilme em sistemas de armazenagem ou distribuição de fluido ou água, incluindo sistemas de purificação ou transporte de água, incluindo tubos de água 5 e tanques de armazenagem de água.
Em outra modaliαade preferiαa, a própria superfície é revestida ou impregnada com um composto oe acordo com a invenção. Essa modalidade é particularmente adequada para superfícies que permanecerão no local por um 10 período prolongado de tempo, por exemplo, dispositivosmédicos e os sistemas de distribuição de fluido ou água descritos acima.
Os compostos podem ser colocados em contato com a superfície a ser tratada em um modo convencional. Por 15 exemplo, os compostos podem ser preparados em solução e asolução colocada em contato com a superfície.
Os compostos podem ser utilizados para rinçar ou limpar a superfície, como descrito acima. Em uma outra modalidade preferida, o composto é pulverizado sobre a 20 superfície. Nessa modalidade, o composto pode serpreparado em um canister de aerossol, frasco de pulverização de atomizador ou outro dispositivo similar, adequado para produzir uma névoa à basede gotícula contendo o composto. Esse é um método eficaz de contatar 25 superfícies grandes com o composto. Isso também éparticularmente eficaz para contatar superfícies de formato incômodo, ou superfícies delicadas como lentes de contato.
Os compostos podem ser fornecidos em qualquer forma adequada que obtenha o efeito desejado. Os compostos 30 podem ser incluídos em uma formulação de liberação controlada ou armazenados em um dispositivo que permita a liberação controlada do composto. Uma formulação de liberação controlada pode ser utilizada em combinação com 1’11 .qjer CUI M iπoα n l nidUt 1 uα .. ..10.0formulação de liberação control ada pode ser impregnada em uma superfície, ou fornecida utilizando uma pulverização.
O composto da invenção pode ser utilizado em qualquer de suas formas de sal. Em particular, o composto pode estar em sua forma o.e sai acido i por exemplo, delmopinol HC1) ou em sua baixa solubilidade em soluções de água. 0 composto será, portanto, retido na superfície do dispositivo tratado, mesmo após rinçagem.
A quantidade eficaz para evitar formação de biofilme será facilmente evidente para a pessoa versada e pode ser determinada com base na superfície a ser tratada.
A invenção é adicionalmente descrita no seguinte exemplo não limitador.
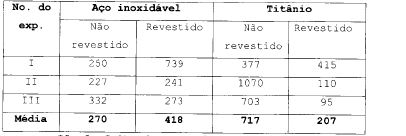
Os seguintes materiais de teste foram incluídos no estudo: . aço inoxidável cirúrgico 316 (por exemplo, para válvula do coração) titânio (por exemplo, para implantes nos quadris)
Os materiais diferentes foram obtidos como discos com um diâmetro aproximado de 30 mm e uma espessura de 1 mm. Esses discos foram então montados no fundo de pratos de Petri.
Cloridrato de delmopinol foi dissolvido em água do tipo UHQ a uma concentração de 20 mg/mL (2% p/v) . A solução foi armazenada no escuro em temperatura ambiente até uso.
Tratamento de superfícies de teste com delmopinol tratadas com 2 mL da solução aquosa de delmopinol HCI a 22 e deixadas nào agitadas por 15 minutos em temperatura ambiente. Toda solução de delmopinol foi retirada com uma pipeta. As cavidades foram então vigorosamente rinçadas três vetes com 4 ml., αe um tampão de f os fato cie potássio f .10 mH, pH "i,2. Uma vez que o pKa de aentiopinol e 7,1, uma parte substancial do composto será convertida em sua base, que tem uma solubilidade muito baixa em soluções aquosas e desse modo permanecerá na superfície e não será retirada totalmente por lavagem durante o procedimento de rinçagem.
Procedimento B: As superficies de teste foram tratadas com 2 mL da solução aquosa de delmopinol HCI a 2% e deixadas de pernoite para secar.
Uma cepa bacteriana fresca de Staphylococcus epidermidis foi isolada da pele e armazenada em leite em pó a ~80°C. No dia anterior ao uso experimental, bactérias foram transferidas para agar de sangue e incubadas em uma atmosfera de 95% H2 e 5% de CO2 a 37°C de pernoite. Unidades de formação de colônia foram coletadas do agar de sangue e suspensas em 10 mM de tampão de fosfato de potássio, pH 7,2, a uma densidade óptica a 600 nm de 0,4, correspondendo a aproximadamente 10scélulas/mL.
A viabilidade bacteriana da suspensão bacteriana, indicada pelas percentagens de vitalidade, foi avaliada por microscopia de fluorescência utilizando o método de Viabilidade Bacteriana Viva/Morta com Sondas Moleculares (Inc. Eugene, OR, EUA), de acordo com as instruções do fabricante. Desse modo, SYTO 9 (1,5 μL) e iodeto de propidio (1,5 μL) foram misturados com 1 mL de tampão de fosfato 10 mM, pH 7,2. Alíquotas de 10 μL foram adicionadas rt I1'jLl I (JH StlSpeilSdl; ue tje 1 !.l d_ d S id dlldllòdUdd d lUidlA elll relação a células verdes/VIVAS e vermelhas/MORTAS no microscópio de fluorescência (microscópio Le i t z Aristoplan equipado com uma lâmpada de halogênio e um filtro de excitação de 470-490 nm).
Em todos os casos a viabilidade de cultures de células foi maior do que 95r.
Quatro mL da suspensão bacteriana foram adicionados no topo de superficies de teste revestidas e não revestidas montadas em pratos de Petri. As células foram deixadas aderir por 60 min a 37°C. Células não aderentes foram removidas por rinçagem das superficies três vezes com 4 mL da solução de tampão. Todo liquido na superficie foi retirado e bactérias aderentes foram visualizadas utilizando as manchas de SYTO 9 e iodeto de propidio como descrito acima. Uma aliquota de 10 μL da mistura foi adicionada à superficie e analisada após 10 min de incubação no escuro. Imagens microscópicas de células aderentes foram analisadas a partir de 10 campos de cada disco. As imagens foram capturadas com uma câmera digital conectada ao microscópio e utilizadas para tirar a média do número de células fixadas em campos separados. O número de células fixadas, bem como a percentagem de células vitais, foi estimado utilizando o programa matemático MATLAB.
Populações de células aderentes foram preparadas em superficies revestidas com delmopinol como descrito acima. Para testar se as células foram retiradas da superficie com delmopinol, as superficies foram rinçadas três vezes com 2 % de delmopinol em água seguido por análise com microscopia de fluorescência. adesão
Galraras triplicadas das cepas bacterianas foram utilizadas e os valores médios das diferentes operações são apresentados. Os números totais (viáveis e não viáveis) de (’eiuias fixaoas sao apresentamos na Taioeia i .
Comparaçao de adesão cm superi_cies revestidas uu não revestidas com delmopinol. Os algarismos representam o número de células por mm2 em superficies dadas pré-tratadas ou não pré-tratadas com uma solução a 25 de delmopinol HCI. Tabela 1 II. 0 efeito de revestimento de delmopinol sobre a viabilidade bacteriana
Culturas triplicadas das cepas bacterianas foramtratadas como descrito acima e os valores médios das diferentes operações são apresentados na Tabela 2.
Comparação de viabilidade bacteriana em superficies revestidas ou não revestidas com delmopinol. Os algarismos representam percentagem de células viáveis em superficies de teste dadas. Tabela 2
III. Crescimento de bactérias aderentes em superfícies tratadas e não tratadas
A capacidade das bactérias crescerem em superfícies revestidas e não revestidas foi determinadapela adição de 4 mL de meio de Extrato de Levedura trípticoa cada cavidade e incubação a 37°C. Os resultados indicam que o crescimento em superfícies sólidas é inibido por revestimento de delmopinol (Tabela 3). Tabela 3
Em conclusão, as superfícies revestidas comdelmopinol mostraram uma redução significativa na viabilidade de células aderentes e o delmopinol inibiu significativamente o crescimento de bactérias associadas à superfície.
Claims (4)
1. Uso de um composto tendo a fórmula (I), ou um sal do mesmo, para a prevenção ou redução de formação de biofilme em uma superfície, sendo o composto de fórmula (I) caracterizadopelo fato de que R1 é um grupo alquila linear ou ramificado contendo 8 a 16 átomos de carbono na posição 2 ou 3 do anel morfolino, e R2 é um grupo alquila linear ou ramificado contendo 2 a 10 átomos de carbono, substituído com um grupo hidróxi exceto na posição alfa, a soma dos átomos de carbono nos grupos R1 e R2 sendo pelo menos 10 e preferivelmente 10 a 20; em que a superfície é, ou faz parte de, um dispositivo médico selecionado a partir de um dispositivotranscutâneo, cateter, stent, fio-guia ou prótese ortopédica; e em que a superfície compreende metal.
2. Uso, de acordo com a reivindicação 1, caracterizadopelo fato de que a superfície é impregnada ou revestida com o composto.
3. Uso, de acordo com a reivindicação 1 ou 2, caracterizadopelo fato de que o composto está em uma formulação de liberação controlada, ou está contido em um dispositivo que permite liberação controlada do composto.
4. Dispositivo médico caracterizadopelo fato de que o dispositivo é revestido com um composto conforme a reivindicação 1, em que o dispositivo médico é um dispositivo transcutâneo, cateter, stent, fio-guia ou prótese ortopédica; e em que a superfície do dispositivo médico compreende metal.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GB0502046.6 | 2005-02-01 | ||
| GBGB0502046.6A GB0502046D0 (en) | 2005-02-01 | 2005-02-01 | Method |
| PCT/GB2006/000335 WO2006082393A1 (en) | 2005-02-01 | 2006-02-01 | Use of morpholino compounds for the prevention of bacterial contamination |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0606802A2 BRPI0606802A2 (pt) | 2009-07-14 |
| BRPI0606802B1 true BRPI0606802B1 (pt) | 2021-02-02 |
Family
ID=34307787
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0606802-2A BRPI0606802B1 (pt) | 2005-02-01 | 2006-02-01 | uso de compostos de morfolino para a prevenção de contaminação bacteriana |
Country Status (20)
| Country | Link |
|---|---|
| US (2) | US8999365B2 (pt) |
| EP (1) | EP1850837B1 (pt) |
| JP (1) | JP5209322B2 (pt) |
| KR (3) | KR20070107078A (pt) |
| CN (1) | CN101111221B (pt) |
| AR (1) | AR056267A1 (pt) |
| AT (1) | ATE435011T1 (pt) |
| AU (1) | AU2006210711B2 (pt) |
| BR (1) | BRPI0606802B1 (pt) |
| CA (1) | CA2594836C (pt) |
| DE (1) | DE602006007549D1 (pt) |
| GB (1) | GB0502046D0 (pt) |
| IL (1) | IL184412A0 (pt) |
| MX (1) | MX2007009146A (pt) |
| NO (1) | NO338610B1 (pt) |
| NZ (1) | NZ556323A (pt) |
| RU (1) | RU2375043C2 (pt) |
| TW (1) | TWI365875B (pt) |
| WO (1) | WO2006082393A1 (pt) |
| ZA (1) | ZA200705983B (pt) |
Families Citing this family (8)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0502046D0 (en) | 2005-02-01 | 2005-03-09 | Sinclair Pharmaceuticals Ltd | Method |
| GB0615814D0 (en) | 2006-08-09 | 2006-09-20 | Sinclair Pharmaceuticals Ltd | Medicament |
| GB0714338D0 (en) * | 2007-07-23 | 2007-09-05 | Sinclair Pharmaceuticals Ltd | method |
| KR101594202B1 (ko) | 2008-09-24 | 2016-02-15 | 텔 하쇼머 메디컬 리서치 인프라스트럭쳐 앤드 서비시스 리미티드. | 세포 유착 방지를 위한 펩티드와 조성물 및 그것의 사용 방법 |
| US20150010479A1 (en) | 2012-03-20 | 2015-01-08 | Sinclair Pharmaceuticals Limited | Treatment of microbial infections |
| USD908214S1 (en) | 2018-07-10 | 2021-01-19 | United States Endoscopy Group, Inc. | Tip protector |
| US11780818B2 (en) | 2020-01-31 | 2023-10-10 | You First Services, Inc. | Methods of making delmopinol and salts thereof |
| US20250221412A1 (en) * | 2022-03-23 | 2025-07-10 | You First Services, Inc. | Methods for irrigation using delmopinol and delmopinol salts |
Family Cites Families (28)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| AT320163B (de) * | 1973-01-24 | 1975-01-27 | Hurka Wilhelm | Desinfektionstüchlein |
| SU536220A1 (ru) | 1974-06-14 | 1976-11-25 | Экспериментально-Конструкторский И Технологический Институт Автомобильной Промышленности | Моющее средство дл очстки металлической поверхности |
| SE439011B (sv) * | 1980-03-21 | 1985-05-28 | Ferrosan Ab | Morfolinoforeningar, kompositioner innehallande dessa och anvendning derav |
| DE3017767C2 (de) * | 1980-05-09 | 1984-11-15 | Deutsche Gesellschaft für Wiederaufarbeitung von Kernbrennstoffen mbH, 3000 Hannover | Schutzbehälter zum Transport, zur Lagerung und zur Strahlungsabschirmung von mit abgebrannten Reaktor-Brennelementen beladenen Brennelementbehältern |
| ATE11869T1 (de) * | 1980-12-18 | 1985-03-15 | Smith & Nephew Ass | Sterilisationszubereitungen fuer linsen und ihre anwendung. |
| US4894221A (en) * | 1981-03-19 | 1990-01-16 | Ab Ferrosan | Method of treating plaque using morpholine compounds |
| WO1987005779A1 (en) * | 1986-03-28 | 1987-10-08 | Jonah Shacknai | Prophylaxis method and composition therefor |
| NZ233503A (en) * | 1989-05-15 | 1991-06-25 | Janssen Pharmaceutica Nv | Substituted (thio)morpholinyl and piperazinyl alkylphenol ethers |
| AU1325792A (en) | 1992-02-03 | 1993-09-01 | Samuel Solomon | Granulins from leukocytes |
| US5500206A (en) * | 1994-04-29 | 1996-03-19 | The Procter & Gamble Company | Oral compositions comprising actinomyces viscosus fimbriae |
| US6096328A (en) * | 1997-06-06 | 2000-08-01 | The Procter & Gamble Company | Delivery system for an oral care substance using a strip of material having low flexural stiffness |
| US6132702A (en) * | 1998-02-27 | 2000-10-17 | The Procter & Gamble Company | Oral care compositions comprising chlorite and methods |
| US6350438B1 (en) | 1998-02-27 | 2002-02-26 | The Procter & Gamble Company | Oral care compositions comprising chlorite and methods |
| US7087661B1 (en) * | 1998-09-23 | 2006-08-08 | Cernofina, Llc | Safe and effective biofilm inhibitory compounds and health-related uses thereof |
| CZ20014709A3 (cs) * | 1999-07-02 | 2002-09-11 | The Procter & Gamble Company | Dávkovací systém pro dodávání látky ústní hygieny do dutiny ústní a způsob dávkování |
| CN1189012C (zh) * | 2000-07-18 | 2005-02-09 | 松下电器产业株式会社 | 图象读取装置及图象处理装置 |
| US6509007B2 (en) * | 2001-03-19 | 2003-01-21 | The Procter & Gamble Company | Oral care kits and compositions |
| FI20021126A0 (fi) | 2002-06-12 | 2002-06-12 | Pekka Vallittu | Antimikrobinen prepreg, komposiitti ja niiden käyttö |
| US20060105000A1 (en) * | 2002-11-21 | 2006-05-18 | J.P.M.E.D. Ltd | Compositions for treating infected skin and mucous membrane comprising an anti-microbial agent and an essential oil |
| ATE483724T1 (de) | 2003-02-26 | 2010-10-15 | A & G Pharmaceuticals Inc | Verfahren zur erhöhung der ausbreitung von b- zellen |
| BRPI0410505A (pt) * | 2003-05-07 | 2006-06-20 | Dmi Biosciences Inc | métodos e produtos para cuidados orais |
| GB0502046D0 (en) | 2005-02-01 | 2005-03-09 | Sinclair Pharmaceuticals Ltd | Method |
| WO2007000924A1 (ja) | 2005-06-28 | 2007-01-04 | Osaka University | プログラニュリン活性を抑制または促進する物質を含む医薬組成物、およびプログラニュリン活性を抑制または促進する物質のスクリーニング方法 |
| GB0515138D0 (en) | 2005-07-22 | 2005-08-31 | Sinclair Pharmaceuticals | Acne treatment |
| JP4994387B2 (ja) | 2005-11-22 | 2012-08-08 | シンクレア ファーマシューティカルズ リミテッド | 歯肉縁下ポケット感染症の治療 |
| EP2037948B1 (en) | 2006-05-30 | 2016-04-13 | Mayo Foundation For Medical Education And Research | Detecting and treating dementia |
| GB0708960D0 (en) | 2007-05-09 | 2007-06-20 | Sinclair Pharmaceuticals Ltd | Method |
| GB0714338D0 (en) * | 2007-07-23 | 2007-09-05 | Sinclair Pharmaceuticals Ltd | method |
-
2005
- 2005-02-01 GB GBGB0502046.6A patent/GB0502046D0/en not_active Ceased
-
2006
- 2006-02-01 AR ARP060100367A patent/AR056267A1/es unknown
- 2006-02-01 AU AU2006210711A patent/AU2006210711B2/en not_active Expired
- 2006-02-01 JP JP2007552729A patent/JP5209322B2/ja not_active Expired - Fee Related
- 2006-02-01 US US11/814,925 patent/US8999365B2/en active Active
- 2006-02-01 CN CN2006800037141A patent/CN101111221B/zh not_active Expired - Lifetime
- 2006-02-01 KR KR1020077019679A patent/KR20070107078A/ko not_active Ceased
- 2006-02-01 ZA ZA200705983A patent/ZA200705983B/xx unknown
- 2006-02-01 NZ NZ556323A patent/NZ556323A/en unknown
- 2006-02-01 KR KR1020147003744A patent/KR20140032498A/ko not_active Ceased
- 2006-02-01 AT AT06704067T patent/ATE435011T1/de not_active IP Right Cessation
- 2006-02-01 KR KR20157008034A patent/KR20150041177A/ko not_active Ceased
- 2006-02-01 RU RU2007127905/15A patent/RU2375043C2/ru active
- 2006-02-01 BR BRPI0606802-2A patent/BRPI0606802B1/pt active IP Right Grant
- 2006-02-01 CA CA2594836A patent/CA2594836C/en not_active Expired - Lifetime
- 2006-02-01 DE DE602006007549T patent/DE602006007549D1/de not_active Expired - Lifetime
- 2006-02-01 EP EP06704067A patent/EP1850837B1/en not_active Expired - Lifetime
- 2006-02-01 MX MX2007009146A patent/MX2007009146A/es active IP Right Grant
- 2006-02-01 WO PCT/GB2006/000335 patent/WO2006082393A1/en not_active Ceased
- 2006-02-03 TW TW095103747A patent/TWI365875B/zh not_active IP Right Cessation
-
2007
- 2007-07-04 IL IL184412A patent/IL184412A0/en active IP Right Grant
- 2007-08-22 NO NO20074291A patent/NO338610B1/no not_active IP Right Cessation
-
2015
- 2015-02-27 US US14/633,730 patent/US20150164080A1/en not_active Abandoned
Also Published As
| Publication number | Publication date |
|---|---|
| NZ556323A (en) | 2010-06-25 |
| JP2008528160A (ja) | 2008-07-31 |
| DE602006007549D1 (de) | 2009-08-13 |
| US20080152688A1 (en) | 2008-06-26 |
| EP1850837A1 (en) | 2007-11-07 |
| US8999365B2 (en) | 2015-04-07 |
| KR20150041177A (ko) | 2015-04-15 |
| CN101111221B (zh) | 2011-07-20 |
| NO20074291L (no) | 2007-10-19 |
| IL184412A0 (en) | 2007-10-31 |
| BRPI0606802A2 (pt) | 2009-07-14 |
| RU2375043C2 (ru) | 2009-12-10 |
| JP5209322B2 (ja) | 2013-06-12 |
| KR20140032498A (ko) | 2014-03-14 |
| AR056267A1 (es) | 2007-10-03 |
| TWI365875B (en) | 2012-06-11 |
| EP1850837B1 (en) | 2009-07-01 |
| KR20070107078A (ko) | 2007-11-06 |
| TW200639153A (en) | 2006-11-16 |
| CA2594836C (en) | 2014-03-11 |
| MX2007009146A (es) | 2007-09-06 |
| AU2006210711B2 (en) | 2010-05-13 |
| RU2007127905A (ru) | 2009-03-10 |
| GB0502046D0 (en) | 2005-03-09 |
| ZA200705983B (en) | 2009-01-28 |
| CA2594836A1 (en) | 2006-08-10 |
| HK1110527A1 (en) | 2008-07-18 |
| AU2006210711A1 (en) | 2006-08-10 |
| NO338610B1 (no) | 2016-09-12 |
| US20150164080A1 (en) | 2015-06-18 |
| WO2006082393A1 (en) | 2006-08-10 |
| ATE435011T1 (de) | 2009-07-15 |
| CN101111221A (zh) | 2008-01-23 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| DK1628655T3 (en) | Antiseptic compositions, methods and systems | |
| US20150164080A1 (en) | Prevention of bacterial contamination | |
| JP2008273984A (ja) | 抗菌性システムおよび方法 | |
| Fernández et al. | In vitro and in vivo comparisons of staphylococcal biofilm formation on a cross-linked poly (ethylene glycol)-based polymer coating | |
| ES2292566T3 (es) | Metodo de esterilizacion de articulos. | |
| EP2037969A1 (en) | Disinfectant having ozone | |
| HK1110527B (en) | Use of morpholino compounds for the prevention of bacterial contamination | |
| WO2008017814A1 (en) | Prevention and treatment of microbial infection | |
| CIOCHINDA et al. | Preliminary study on antimicrobial efficiency of some common chemical substances with a disinfecting character on impression materials used in implant-prosthetic rehabilitation. | |
| MXPA05013038A (en) | Antiseptic compositions, methods and systems |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B09B | Patent application refused [chapter 9.2 patent gazette] |
Free format text: INDEFIRO O PEDIDO DE ACORDO COM O(S) ARTIGO(S) 8 E 13 DA LPI |
|
| B12B | Appeal against refusal [chapter 12.2 patent gazette] | ||
| B25G | Requested change of headquarter approved |
Owner name: SINCLAIR PHARMACEUTICALS LIMITED (GB) |
|
| B25A | Requested transfer of rights approved |
Owner name: MAELOR LABORATOIES LIMITED (GB) |
|
| B25G | Requested change of headquarter approved |
Owner name: MAELOR LABORATOIES LIMITED (GB) |
|
| B25A | Requested transfer of rights approved |
Owner name: MERIAL LIMITED (US) ; MERIAL, INC. (US) |
|
| B25A | Requested transfer of rights approved |
Owner name: MERIAL, INC. (US) |
|
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 02/02/2021, OBSERVADAS AS CONDICOES LEGAIS. |