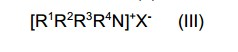[001] A presente invenção se refere ao uso de compostos de amônio quaternários para impedir precipitações de fluorquinolonas de suas soluções, bem como medicamentos toleráveis, estáveis, especialmente adequados para a aplicação parenteral, que em forma dissolvidacontêm uma fluorquinolona e um composto de amônio quaternário.
[002] Há uma extensa pesquisa científica no campo da solubili- zação de fluorquinolonas de ação antibiótica. Dessa maneira, na DE- OS-3 831 514 são descritas soluções com quinolonas através da aplicação de íons de metais, especialmente através de íons de cálcio. Uma melhor solubilidade de quinolonas é descrita também na JP 02264724, bem como por M. Nakano, M. Yamamoto, T. Arita em Chem. Pharm. Bull, Interactions of Aluminium, Magnesium and Calcium ions with Nalidixic acid, 26 (5) 1505-1510 (1978) através do uso de íons de metais, especialmente de íons de magnésio. Na EP-A 507 851 são descritos complexos de quinolonas com íons de metais bem como ácido; nesses complexos a solubilidade das quinolonas deve ser melhor. A melhor solubilidade de uma fluorquinolona através da adição de íons de metais, bem como co-solventes está fundamentada na US 5,811,130. A tolerância desses complexos é apresentada em vitelas. Complexos de quinolonas com íons de metais e especialmente com íons de magnésio também são descritos no WO 99/29322, pelo que deve ser obtida uma melhor solubilidade das quinolonas. Os complexos aqui descritos são descritos como sendo bem-toleráveis e estáveis ao armazenamento, sendo que a tolerância foi pesquisada em vitelas e ratos.
[003] Soluções para fins farmacêuticos devem ser livres de preci- pitações. Nas soluções, que são determinadas para a aplicação parenteral, isso é particularmente importante e também precipitações em pequena escala, designadas como formação de partículas, não são aceitáveis. Isso vale para toda a durabilidade de um produto farmaceu- ticamente utilizado. Por isso, há muitas publicações em relação ao tema do impedimento de formação de partículas, respectivamente, pre-cipitação de medicamentos das soluções. Por exemplo, o WO 98/18492 descreve o impedimento de formações de partículas em soluções com cefalosporinas através do uso de fosfolipídios.
[004] A EP-A 287 026 descreve um processo de purificação deta lhado especialmente para a síntese de fluorquinolonas, para que não ocorra formação de partículas na produção de soluções (injetáveis).
[005] Do mesmo modo, o WO 01/10408 descreve que para a produção de soluções injetáveis de uma fluorquinolona, devem ser usadas substâncias de aplicação com uma fração particularmente pequena de impurezas devido aos íons de metais, para assegurar que as soluções continuem livres de partículas.
[006] A liofilização de soluções representa, por exemplo, uma al ternativatambém freqüentemente selecionada para o problema da formação de partículas.
[007] De modo geral, sabe-se que substâncias tensoativas não são bem-toleráveis na administração parenteral. Isso é atribuído, entre outros, à afinidade das substâncias tensoativas em relação aos componentes das paredes celulares. Por isso, as substâncias tensoativas com uma afinidade particularmente pronunciada em relação às paredes celulares são usadas, entre outras, também como desinfetantes ou como conservantes. Isso vale também para conservantes do grupo dos compostos de amônio quaternário, tal como, por exemplo, cloreto de benzalcônio.
[008] Do mesmo modo, sabe-se de modo geral que o grupo dos compostos de amônio quaternário são irritantes da pele e da mucosa. Dessa maneira, K.H. Wallhauser (em Praxis der Sterilisation, Desin- fektion-Konservierung, Thieme Verlag, 1995, 5a edição, página 586598) descreve o efeito rubefaciente do cloreto de benzalcônio na pele de coelho sadio; também é descrita a formação de dermatites em camundongos (J. Amer. Ver. Med. Ass., 1972, 161 (6), 652-655. Dermatitis and death in mice accidentially exposed to quaternary ammonium disinfectants). Em J. Gen. Microbiol., 1967, 48 (3), 391-400 ("Effects of organic cations on the gram-negative cell wall and their bactericidal activity with EDTA and surface active agents") é apresentado o mecanismo do efeito de compostos de amônio quaternário, sendo explicitamente descrita a interação com as membranas celulares e o aumento daí resultante da permeabilidade para outras substâncias.
[009] Na verdade, a melhora da solubilidade de fluorquinolonas através da adição de íons de metais, tais como, por exemplo, de íons de magnésio ou íons de cálcio, em princípio, é descrita na literatura. Contudo, em alguns casos, as soluções de fluorquinolona, ao serem armazenadas, apresentam as precipitações conhecidas na forma de formações de partículas. Isso ocorre também com o uso de substâncias geralmente comuns para impedir precipitações ou cristalizações. Dessa maneira, por exemplo, a formação de partículas em soluções de pradofloxacina não é impedida através da aplicação de co- solventes descritos na US 5,811,130 ou também através de formulações contendo ácido, tais como descritas na EP-A 507 851.
[0010] Além disso, formulações de fluorquinolonas não são bem- toleráveis do mesmo modo nas diversas espécies animais, de maneira que não se pode partir de uma tolerância, que foi determinada em vitelas, para uma tolerância, por exemplo, em porcos ou cães ou mesmo gatos. Isso vale também para o caso inverso; soluções injetáveis, que são toleráveis por cães, não são obrigatoriamente toleráveis por gatos ou vitelas.
[0011] Diferentemente do campo dos animais domésticos (por exemplo, bovinos), além dos resultados locais objetivos, a avaliação da tolerância local de soluções injetáveis em animais de recreação (por exemplo, cães ou gatos) é mais crítica. Dessa maneira, a aceitação dos proprietários de animais em relação às leves intolerâncias locais (por exemplo, intumescimentos, algesia) no campo dos animais de recreação, é nitidamente inferior ao campo dos animais domésticos.Além disso, particularmente as variantes de criação a serem atingidas no campo dos animais de recreação, reagem muitas vezes de maneira mais sensível às injeções subcutâneas comparadas com os animais domésticos. Aqui mencionam-se particularmente os gatos como espécie animal muito sensível. Por conseguinte, também não é supreendente que a maioria das soluções injetáveis com fluorquinolo- nas, entre outras, com base nas tolerâncias deficientes, não estão à disposição de cães ou gatos.
[0012] Para formular a tolerância da melhor maneira possível, re comenda-se manter o pH das soluções o mais neutro possível (cerca de 7,4), mas o que contraria a solubilidade das fluorquinolonas, visto que geralmente essas têm uma solubilidade particularmente baixa na escala de pH neutro. Isso vale especialmente para sistemas aquosos preferivelmente empregados nas quinolonas, sendo que, devido à má solubilidade das quinolonas com pH em torno do ponto neutro, recorre- se a aditivos, tais como co-solventes. Na escala de pH neutro observa- se com freqüência uma formação de partículas da forma betaína das fluorquinolonas, razão pela qual soluções, quando já deveriam ser toleráveis, freqüentemente não são armazenáveis por muito tempo e ocorre a formação de partículas. Na prática, por exemplo, isso é con-tornado pelo fato de se desviar de produtos liofilizados. Mas o manuseio desses produtos liofilizados é complicado e a solução reconsti- tuinte apresenta, via de regra, uma curta durabilidade (por exemplo, de 4 semanas) após a reconstituição ou deve ser diretamente rejeitada devido a possível formação de partículas. Portanto, tais produtos têm claras desvantagens em relação a uma solução injetável pronta, dire-tamenteaplicável.
[0013] Por conseguinte, uma solução pronta para o uso é vantajo sa como solução injetável, também designada como "formulação ready to use". Além disso, é necessário que após a aplicação, tal como também descrito no WO 99/29322, a fluorquinolona converta-se no soro na quantidade correspondente. Isso também não é evidente com formulações injetáveis de fluorquinolonas e do mesmo modo pode depender das respectivas espécies animais.
[0014] Foi encontrada uma possibilidade de manter fluorquinolo- nas com substâncias aditivas farmaceuticamente aceitáveis em solução. Dessa maneira, é possível preparar formulações com fluorquino- lonas diretamente aplicáveis (ready to use), que após aplicação parenteral em diversas espécies animais, são localmente bem-toleráveis, que são estáveis em condições de armazenamento farmacêuticas, bem como são livres de formação de partículas e que apresentam um perfil cinético de soro vantajoso.
[0015] A invenção se refere:
[0016] ao uso de compostos de amônio quaternário para impedir precipitações de fluorquinolonas de suas soluções.
[0017] Além disso, a invenção se refere:
[0018] a um medicamento contendo em forma dissolvida: (a) uma fluorquinolona eventualmente na forma de um sal farmaceuticamente utilizável e (b) um composto de amônio quaternário.
[0019] Fluorquinolonas são compostos, tais como são publicadas, entre outras, nos seguintes documentos: US 4,670,444 (Bayer AG), US 4,472,405 (Riker Labs), US 4,730,000 (Abbott), US 4,861,779 (Pfizer), US 4,382,892 (Daiichi), US 4,704,459 (Toyama), como exemplos concretos sejam mencionados: benofloxacina, binfloxacina, cinoxaci- na, ciprofloxacina, danofloxacina, difloxacina, enoxacina, enrofloxaci- na, fleroxacina, ibafloxacina, levofloxacina, lomefloxacina, marbofloxa- cina, moxifloxacina, norfloxacina, ofloxacina, orbifloxacina, pefloxacina, temafloxacina, tosufloxacina, sarafloxacina, sparfloxacina.
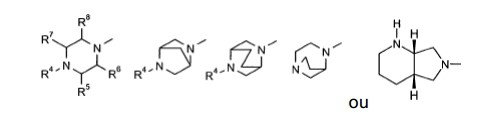
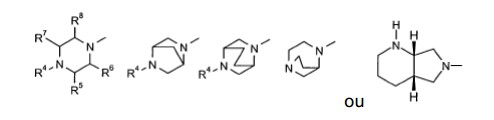
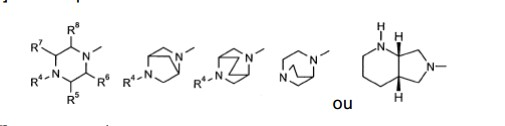
[0020] Um grupo preferido de fluorquinolonas são aquelas da Fórmula (I) ou (II):
[0021] na qual
[0022] X representa hidrogênio, halogênio, C1-4-alquila, C1-4- alcóxi, NH2,
[0023] Y representa radicais das estruturas
[0024] sendo que
[0025] R4 representa C1-4-alquila em cadeia linear ou ramificada eventualmente substituída por hidróxi ou metóxi, ciclopropila, acila com 1 a 3 átomos de carbono,
[0026] R5 representa hidrogênio, metila, fenila, tienila ou piridila,
[0027] R6 representa hidrogênio ou C1-4-alquila,
[0028] R7 representa hidrogênio ou C1-4-alquila,
[0029] R8 representa hidrogênio ou C1-4-alquila,
[0030] bem como
[0031] R1 representa um radical alquila com 1 a 3 átomos de car bono, ciclopropila, 2-fluoroetila, metóxi, 4-fluorofenila, 2,4-difluorofenila ou metilamino,
[0032] R2 representa hidrogênio ou alquila com 1 a 6 átomos de carbono eventualmente substituída por metóxi ou 2-metoxietóxi, bem como ciclohexila, benzila, 2-oxopropila, fenacila, etoxicarbonilmetila, pivaloiloximetila,
[0033] R3 representa hidrogênio, metila ou etila e
[0034] A representa nitrogênio, =CH-, =C(halogênio)-, =C(OCH3)-, =C (CH3)- ou =C(CN),
[0035] B representa oxigênio, =NH ou =CH2 eventualmente substi tuída por metila ou fenila,
[0036] Z representa =CH- ou =N-
[0037] e seus sais e hidratos farmaceuticamente utilizáveis.
[0038] São preferidos compostos da Fórmula (I),
[0039] na qual
[0040] A representa =CH- ou =C-CN,
[0041] R1 representa C1-C3-alquila eventualmente substituída por halogênio ou ciclopropila,
[0042] R2 representa hidrogênio ou C1-4-alquila,
[0043] Y representa radicais das estruturas
[0044] sendo que
[0045] R4 representa C1-C3-alquila em cadeia linear ou ramificada eventualmente substituída por hidróxi, oxalila com 1 a 4 átomos de carbono,
[0046] R5 representa hidrogênio, metila ou fenila,
[0047] R6 representa hidrogênio ou metila,
[0048] R7 representa hidrogênio ou metila,
[0049] R8 representa hidrogênio ou metila,
[0050] e seus hidratos e sais farmaceuticamente utilizáveis.
[0051] Particularmente, são preferidos compostos da Fórmula (I),
[0052] em que
[0053] A representa =CH- ou =C-CN,
[0054] R1 representa ciclopropila,
[0055] R2 representa hidrogênio, metila ou etila,
[0056] Y representa radicais das estruturas
[0057] nas quais
[0058] R4 representa metila, etila eventualmente substituída por hidróxi,
[0059] R5 representa hidrogênio ou metila,
[0060] R6 representa hidrogênio,
[0061] R7 representa hidrogênio ou metila,
[0062] R8 representa hidrogênio,
[0063] e seus sais e hidratos farmaceuticamente utilizáveis.
[0064] Como exemplo preferido de uma fluorquinolona da Fórmula (II) seja mencionada a marbofloxacina:
[0065] Como fluorquinolonas particularmente preferidas sejam mencionados os compostos descritos no WO 97/31001, especialmente ácido 8-ciano-1-ciclopropil-7-((1S,6S)-2,8-diazabiciclo[4.3.0]nonan-8- il)-6-flúor-1,4-dihidro-4-oxo-3-quinolinocarboxílico (pradofloxacina) com a Fórmula
[0066] Além disso, a enrofloxacina é usada de modo particular mente preferido:
[0067] ácido 1-ciclopropil-7-(4-etil-1-piperazinil)-6-flúor-1,4-dihidro- 4-oxo -3-quinolinocarboxílico
[0068] Do mesmo modo, é concebível o uso da substância ativa ciprofloxacina usada, ademais, na medicina humana.
[0069] As fluorquinolonas podem estar presentes na forma de seus racematos ou em formas enantioméricas. Tanto os enantiômeros puros, como também suas misturas podem ser usados de acordo com a invenção.
[0070] Como sais tomam-se em consideração os sais de adição de ácidos farmaceuticamente utilizáveis e sais básicos.
[0071] Como sais farmaceuticamente utilizáveis entendem-se, por exemplo, os sais do ácido clorídrico, ácido sulfúrico, ácido acético, áci-doglicólico, ácido lático, ácido succínico, ácido cítrico, ácido tartárico, ácido metanossulfônico, ácido 4-toluenossulfônico, ácido galacturôni- co, ácido glucônico, ácido embônico, ácido glutamínico ou ácido aspa- ragínico. Além disso, os compostos de acordo com a invenção podem ser ligados aos trocadores de íons ácidos ou básicos. Como sais básicos farmaceuticamente utilizáveis sejam mencionados, por exemplo, os sais de metais alcalinos, por exemplo, os sais de sódio ou potássio, os sais de metais alcalino-terrosos, por exemplo, os sais de magnésio ou cálcio; os sais de zinco, os sais de prata e os sais de guanidínio.
[0072] Por hidratos entendem-se tanto os hidratos das próprias fluorquinolonas, como também os hidratos de seus sais. Como exemplo seja mencionada a pradofloxacina, que forma um trihidrato estável (vide o WO 2005/097789).
[0073] Sob determinadas circunstâncias, as fluorquinolonas po dem formar, como sólido, diversas modificações cristalinas. Modificações vantajosas para os medicamentos da presente invenção são aquelas que têm propriedades de solubilidade correspondentes.
[0074] Nos medicamentos de acordo com a invenção, a fluorquino- lona para animais com um peso corporal de até aproximadamente 80 kg é tipicamente usada em uma proporção de 0,1 até 15 %, preferivelmente 0,5 até 15 % e de modo particularmente preferido, com 1 até 15 %. No caso de animais com um peso corporal a partir de aproximadamente 80 kg, a fluorquinolona é tipicamente usada em uma proporção de 1 até 30 %, preferivelmente 3 até 25 % e de modo particularmente preferido, com 4 até 20 %. Aqui e a seguir - desde que não indicado de outro modo - entende-se por dados de porcentagem, porcento (M/V). Isso significa: massa da respectiva substância em grama para 100 mL de solução pronta.
[0075] Os medicamentos de acordo com a invenção podem conter outras substâncias ativas adequadas, tais como, por exemplo, analgésicos, especialmente NSAID’s (substâncias não esteroidais, antiinfla- matórias). Tais NSAID’s podem ser, por exemplo: meloxicam, flunixina, cetoprofeno, carprofeno, metamizol ou ácido (acetil)-salicílico.
[0076] Compostos de amônio quaternário no sentido desta inven ção são compostos de amônio usualmente orgânicos, que apresentam substituintes apolares e que podem ter diversos contraíons, tais como, por exemplo, cloreto, brometo, iodeto ou fluoreto. Preferivelmente, esses são compostos da Fórmula Geral (II):
[0077] na qual
[0078] R1 a R4 são iguais ou diferentes e representam C1-18- alquila, que pode ser eventualmente interrompida uma ou mais vezes por oxigênio e pode ser eventualmente substituída com hidroxila ou com um radical arila eventualmente substituído com um ou mais átomos de halogênio ou radicais C1-8-alquila ou
[0079] R1 a R4 através de ciclização de três radicais formam radi cais heterocíclicos com 5 ou 6 membros, tais como, por exemplo, piri- dina ou tiazolina, que por seu lado são eventualmente substituídos uma ou mais vezes com C1-4-alquila ou C1-4-alquenila, que portam eventualmente um radical arila, que por seu lado, pode ser substituído com halogênio, especialmente cloro, amino ou dimetilamino e
[0080] X representa sulfato, halogeneto, especialmente cloreto, brometo ou iodeto ou um contra-íon semelhante.
[0081] Pelo menos um dos radicais R1 a R4 apresenta preferivel mente um comprimento de cadeia de 8 a 18, de modo particularmente preferido, 12 a 16 átomos de carbono.
[0082] Arila representa preferivelmente um radical fenila, que é eventualmente substituído com 1 ou 2 radicais selecionados de halo- gênio, especialmente cloro e C1-8-alquila.
[0083] São exemplos os cloretos de alquil-dimetil-benzilamônio, especialmente cloreto de benzalcônio [cloreto de (C8-18)-alquil-dimetil- benzil-amônio] ou cloreto de n-(C12-C18)-alquil-benzildimetilamônio com pesos moleculares médios de cerca de 380, cloreto de benzetônio (cloreto de diisobutil-fenoxietoxietil-dimetilbenzil-amônio), cloreto de diclorobenzil-dimetil-alquil-amônio, cloreto de benzoxônio (cloreto de benzil-dodecil-bis-(2-hidroxietil)-amônio, brometo de cetrimônio, brometo de (N-hexadecil-N,N-trimetil-amônio, cloreto de di-(C8-C18)- alquil-dimetil-amônio, tal como, por exemplo, cloreto de dioctil-dimetil- amônio ou cloreto de di-n-decil-dimetil-amônio, cloreto de cetilpiridínio (cloreto de 1-hexadecil-piridínio) bem como iodeto de tiazolínio (iodeto de 3-heptil-2-(3-heptil-4-metil-4-tiazolin-2-iliden-metil)-4-metil- tiazolínio). Desses, preferem-se particularmente o cloreto de benzetô- nio e cloreto de benzalcônio.
[0084] Os compostos de amônio quaternário são usualmente apli cados em concentrações de 0,001 até 10 %, preferivelmente de 0,005 até 6 % e de modo particularmente preferido, de 0,005 até 3 %. Os dados de porcentagem significam % (M/V).
[0085] Os medicamentos de acordo com a invenção podem conter outras substâncias adicionalmente aos compostos de amônio quaternário, que podem impedir a formação de partículas; por exemplo, po- loxâmeros, lecitinas, polivinilpirrolidonas, co-solventes, antioxidantes ou formadores de complexos. Também esses são usualmente aplicados em concentrações de 0,001 até 20 %, preferivelmente de 0,01 até 10 % e de modo particularmente preferido, de 0,05 até 3 %. Os dados de porcentagem significam % (M/V).
[0086] As formulações líquidas podem conter substâncias, que melhoram a tolerância local da aplicação. Como exemplos sejam men-cionados: captadores de radicais ou antioxidantes, tais como, por exemplo, vitamina E, ésteres de vitamina E hidrossolúveis ou vitamina C, butilhidroxianisol, butilhidroxitolueno, cisteamina, cisteína, glutation, tioglicol, ácido tiolático, dissulfeto de sódio ou também acetilcisteína. Formadores de complexos, tais como, por exemplo, ciclodextrinas (por exemplo, hidroxipropil-ciclodextrina), sódio-EDTA (ácido etilenodiami- notetraacético), polivinilpirrolidona, dexpantenol, sais de ácidos graxos, tais como, por exemplo, caprilato de sódio, sais de cátions de metais polivalentes (por exemplo, Me2+ ou Me3+), especialmente os metais alcalino-terrosos e aqui especialmente o magnésio e sua forma de sal, aminoácidos e entre estes, particularmente, arginina ou lisina, poloxâ- meros, poloxaminas, co-solventes, tais como, por exemplo, n-butanol, glicerina, polietilenoglicol, propilenoglicol ou dimetilacetamida, dextra- nos, creatina, creatinina, ácidos, tais como, por exemplo, o ácido glu- conolactônico, ácido lático, ácido embônico, ácido cítrico, ácido tartári- co, ácido múcico ou ácido hialurônico, lecitinas com um teor de fosfati- dilcolina de 70-100 % de soja ou albumina de galinha. Das substâncias mencionadas acima, aplicam-se preferivelmente os sais de cátions de metais polivalentes e, na verdade, preferivelmente os sais de metais alcalino-terrosos, especialmente sais de magnésio.
[0087] Substâncias, que melhoram a tolerância, são usualmente aplicadas em concentrações de 0,05 até 10 %, preferivelmente com 0,1 até 8 % e de modo particularmente preferido, com 0,5 até 5 %. Os dados de porcentagem significam % (M/V).
[0088] Como solventes, a formulação líquida pode conter água ou substâncias hidromiscíveis. Como exemplos são mencionados: glicerina, propilenoglicol, polietilenoglicol, álcoois toleráveis bem como eta- nol, álcool benzílico ou n-butanol, lactato de etila, acetato de etila, triacetina, N-metil-pirrolidona, propileno carbonato, glicofurol, dimetilace- tamida, 2-pirrolidona, isopropilideno glicerol, glicerinformal. Combinações dos solventes são também imagináveis. formulações preferidas à base de água, são contidas nesses outros solventes ou co-solventes naturais.
[0089] Como solventes, a formulação líquida, além de água ou substâncias hidromiscíveis, também pode conter óleos em forma de uma emulsão. Entre esses, sejam mencionados óleos vegetais, animais e sintéticos, tais como óleo de semente de algodão, óleo de sésamo,óleo de soja, triglicerídeos de cadeia média com um comprimento de cadeia de C12-C18, decanoato de propilenoglicoloctanoato ou também parafina.
[0090] O solvente está usualmente contido em concentrações de até 98,5 %, preferivelmente de até 97 %, de modo particularmente preferido, de até 96,5 %. Via de regra, as concentrações do solvente encontram-se acima de 50 %, preferivelmente acima de 60 %, de modo particularmente preferido, acima de 70 %. Os dados de porcentagem significam % (M/V).
[0091] As formulações de acordo com a invenção também podem conter co-solventes e, na verdade, preferivelmente, quando as formulações contêm água; os co-solventes podem melhorar a solubilidade de certos componentes da formulação. Os co-solventes são usualmente aplicados em proporções de 1 a 10 %, preferivelmente de 3 a 8 % (em cada caso os dados de porcentagem são M/V). Como co- solventes sejam mencionados, por exemplo: álcoois farmaceuticamen- te toleráveis, dimetilsulfóxido, etillactato, acetato de etila, triacetina, N- metilpirrolidona, propilenocarbonato, propilenoglicol, glicofurol, dimeti- lacetamida, 2-pirrolidona, isopropilidenoglicerol, glicerinformal, glicerina e polietilenoglicóis. Como co-solventes prestam-se especialmente álcoois farmaceuticamente toleráveis, tais como, por exemplo, etanol, álcool benzílico ou n-butanol. Misturas dos solventes mencionados acima também podem ser aplicados como co-solventes.
[0092] Conservantes podem estar contidos nas formulações líqui das. Os compostos de amônio quaternário mencionados acima têm, via de regra, efeito conservante, por exemplo, cloreto de benzalcônio, cloreto de benzetônio ou cloreto de cetilpiridínio. Como exemplos de outros conservantes utilizáveis sejam mencionados: álcoois alifático, tais como álcool benzílico, etanol, n-butanol, fenol, cresóis, clorobuta- nol, éster de ácido para-hidroxibenzóico (especialmente os ésteres metílico e propílico), sais ou os ácidos livres dos ácidos carboxílicos, tais como ácido sórbico, ácido benzóico, ácido lático ou ácido propiô- nico.
[0093] Dependendo do tipo de formulação e forma de aplicação, os medicamentos de acordo com a invenção, podem conter outros aditivos e coadjuvantes farmaceuticamente toleráveis. Como exemplos mencionam-se: • antioxidantes, tais como, por exemplo, sulfitos (sulfito de Na, metabissulfito de Na), sulfetos orgânicos (cistina, cisteína, cistea- mina, metionina, tioglicerol, ácido tioglicólico, ácido tiolático), fenóis (tocoferóis, tais como também vitamina E e vitamina E-TPGS (d-alfa- tocoferilpolietilenoglicol-1000-succinato)), butilhidroxianisol, butilhidro- xitolueno, octil- e dodecilgalato), ácidos orgânicos (ácido ascórbico, ácido cítrico, ácido tartárico, ácido lático) e seus sais e ésteres. • Umectantes, tais como, por exemplo, sais de ácido gra- xo, alquilsulfatos graxos, alquilsulfonatos graxos, alquilbenzenossulfo- natos lineares, sulfatos de éter alquilpolietilenoglicólico graxo, éter al- quilpolietilenoglicólico graxo, éter alquilfenolpolietilenoglicólico, alquil- poliglicosídeos, N-metilglucamidas de ácido graxo, polissorbatos, éster de ácido sorbitanograxo e poloxâmeros. • Substâncias para a isotonização, tais como, por exemplo, cloreto de sódio, glicose ou glicerina. • Corantes farmaceuticamente aceitáveis, tais como, por exemplo, óxidos de ferro, carotenóides e outros.
[0094] O pH das formulações líquidas importa em 2-11, preferi velmente 3-8 e de modo particularmente preferido, 4-7,6.
[0095] Os medicamentos de acordo com a invenção podem ser fabricados, em que a fluorquinolona é dispersa no solvente, as substâncias para melhorar a tolerância e eventualmente para impedir a formação de partículas são igualmente complementadas. Co- solventes, tais como outras substâncias constitutivas, tais como, por exemplo, conservantes, já podem ser acrescentados ao solvente ou misturados mais tarde.
[0096] Alternativamente, os co-solventes, conservantes, substân cias que influenciam na tolerância ou formação de partículas também podem ser inicialmente dissolvidos no solvente e em seguida, complementados primeiro à fluorquinolona.
[0097] As preparações farmacêuticas de acordo com a invenção, prestam-se geralmente para a aplicação no ser humano e animal. Pre-ferivelmente, elas são aplicadas na zootecnia e pecuária em animais domésticos, animais de criação, de zoológico, de laboratório, cobaias e de recreação.
[0098] Nos animais domésticos e pecuária incluem-se mamíferos, tais como, por exemplo, bovinos, eqüinos, ovinos, porcinos, caprinos, camelos, búfalos de água, muares, coelhos, caça, renas, animais que fornecem pele, tais como, por exemplo, martas, chinchilas, urso lavadeiro, bem como pássaros, tais como, por exemplo, codorniz, galinhas, gansos, perus, patos, pombos e espécies de pássaros para a criação doméstica ou zoológica.
[0099] Nos animais de laboratório e cobaias incluem-se camun dongos, ratos, porquinhos-da-Índia, hamster dourado, coelhos, macacos, cães e gatos.
[00100] Nos animais de recreação incluem-se coelhos, hamster, ratos, porquinhos-da-Índia, camundongos, cavalos, répteis, espécies de pássaros correspondentes, cães e gatos.
[00101] Além disso, sejam mencionados peixes e, na verdade, pei-xesdomésticos, de criação, de aquário e ornamentais de todos os es- tágios de idade, que vivem em água doce ou salgada.
[00102] Preferivelmente, as preparações de acordo com a invenção são usadas em animais de recreação, tais como cavalos, coelhos, gatos e cães. Elas são especialmente adequadas para a aplicação em gatos e cães.
[00103] Exemplos de animais domésticos preferidos são bovinos, ovinos, porcinos, caprinos, peru e galinha. Animais domésticos particularmente preferidos são bovinos e porco.
[00104] A aplicação pode ser efetuada tanto profilaticamente, meta- filaticamente, como também terapeuticamente.
[00105] Preferivelmente, as formulações líquidas de acordo com a invenção são administradas como soluções ou emulsão, as soluções homogêneas são particularmente preferidas.
[00106] As formulações aqui descritas podem ser administradas ao organismo-alvo (ser humano ou animal) de diferentes maneiras. Elas podem ser aplicadas, por exemplo, via parenteral, especialmente através de injeção (por exemplo, subcutânea, intramuscular, intravenosa, intramamária, intraperitonial), dérmica, oral, retal, vaginal ou nasal, sendo preferida a aplicação parenteral - especialmente através de injeção.
[00107] O uso com as substâncias mencionadas leva a medicamentos com boa solubilidade da substância ativa e boa estabilidade da formulação, especialmente em relação às precipitações. Além disso, o medicamento de acordo com a invenção destaca-se por boa tolerância e cinética de soro adequada nas diversas espécies animais mencionadas, especialmente após administração parenteral.
EXEMPLOS
[00108] As formulações dos seguintes exemplos são preparadas, em que as substâncias de aplicação são misturadas ou dissolvidas em água por injeção. O valor de pH das soluções pode ser ajustado atra- vés da adição de ácidos ou bases. As soluções para a injeção são fil-tradasestéreis e transferidas para recipientes adequados. Pradofloxa- cina pode ser usado como anidrato ou como trihidrato; os valores numéricos são calculados em cada caso para o anidrato.
[00109] (Dados de porcentagem em % em peso, em relação ao volume total do preparado pronto [M/V]). EXEMPLO 1 1 % de enrofloxacina 3,0 % de hexahidrato de cloreto de magnésio 0,02 % de cloreto de benzalcônio quantum satis hidróxido de potássio ad 100 % de água por injeção.
[00110] 0,5 g de enrofloxacina, 1,5 g de hexahidrato de cloreto de magnésio e 0,01 g de cloreto de benzalcônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de potássio. EXEMPLO 2 3,0 % de pradofloxacina (trihidrato) 3,0 % de hexahidrato de cloreto de magnésio 0,02 % de cloreto de benzalcônio quantum satis hidróxido de sódio ad 100 % de água por injeção
[00111] 1,5 g de pradofloxacina (calculado como pradofloxacina pu ra, usada como trihidrato), 1,5 g de hexahidrato de cloreto de magnésio e 0,01 g de cloreto de benzalcônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de sódio. EXEMPLO 3 1,5 % de pradofloxacina 3 % de hexahidrato de cloreto de magnésio 0,01 % de cloreto de benzetônio ad 100 % de água por injeção.
[00112] 0,75 g de pradofloxacina, 1,5 g de hexahidrato de cloreto de magnésio e 0,005 g de cloreto de benzetônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de sódio. EXEMPLO 4 1,5 % de pradofloxacina (trihidrato) 3 % de hexahidrato de cloreto de magnésio 0,02 % de cloreto de benzalcônio ad 100 % de água por injeção
[00113] 0,75 g de pradofloxacina (calculado como pradofloxacina pura, usada como trihidrato), 1,5 g de hexahidrato de cloreto de magnésio e 0,01 g de cloreto de benzalcônio são dissolvidos em água por injeção para 50 mL e eventualmente o valor de pH é ajustado para 6,0 com hidróxido de sódio. EXEMPLO 5 5 % de pradofloxacina (trihidrato) 0,02 % de cloreto de benzalcônio 3 % de hexahidrato de cloreto de magnésio ad 100 % de água por injeção
[00114] 80 g de água por injeção são misturados com 0,02 g de clo reto de benzalcônio e 3 g de hexahidrato de cloreto de magnésio. Nesses, são dissolvidos 5 g de pradofloxacina (calculado como prado- floxacina pura; usado como trihidrato). Com a água por injeção restante ajusta-se para o peso final para 100 mL e antes ajusta-se eventualmente o valor de pH para 6,0 com hidróxido de sódio. EXEMPLO 6 1,5 % de pradofloxacina (trihidrato) 0,015 % de cloreto de benzalcônio 3 % de hexahidrato de cloreto de magnésio ad 100 % de água por injeção
[00115] 80 g de água por injeção são misturados com 0,015 g de cloreto de benzalcônio e 3 g de hexahidrato de cloreto de magnésio. Nesses, são dissolvidos 1,5 g de pradofloxacina (calculado como pra- dofloxacina pura; usado como trihidrato). Com a água por injeção restante completa-se para o peso final de 100 mL e antes ajusta-se eventualmente o valor de pH para 6,0 com hidróxido de sódio. EXEMPLO 7 1,5 % de pradofloxacina (trihidrato) 0,01 % de cloreto de benzalcônio 3 % de hexahidrato de cloreto de magnésio ad 100 % de Aqua pro injection
[00116] 80 g de Aqua pro injection são misturados com 0,01 g de cloreto de benzalcônio e 3 g de hexahidrato de cloreto de magnésio. Nesses, são dissolvidos 1,5 g de pradofloxacina (calculado como pra- dofloxacina pura; usado como trihidrato). Com a Aqua pro injection restante completa-se para o peso final de 100 mL e antes ajusta-se eventualmente o valor de pH para 6,0 com hidróxido de sódio.
TOLERÂNCIA IN VIVO
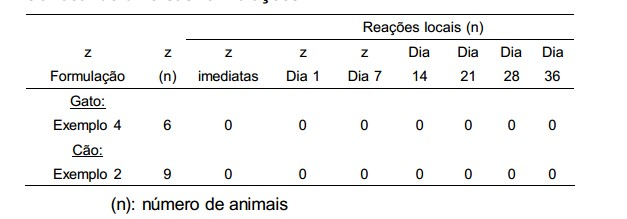
[00117] No ensaio clínico, as formulações aqui descritas demonstraram um melhor tolerância local em relação a outras formulações. Irritações de tecidos e intumescimentos causados pela substância ativa no local da injeção manifestam-se de acordo com as formulações usadas. Exemplos para esse fim são relacionados na seguinte tabela.
[00118] O sistema de teste aplicado consiste em uma prova combinada de tolerância local inicial e durante 36 dias e farmacocinética do soro de 0 - 72 horas. Cada formulação é testada em 6 animais cada das duas espécies cão e gato após injeção subcutânea única. As amostras de soro (n = 11/animal) são testadas para sua concentração de substância por meio de HPLC e dessas são calculados os parâme-trosfarmacocinéticos. A tolerância local é avaliada com base nos parâmetros intumescimento, algesia, rubefação e irritação/modificação da pele e avaliada por apalpação. TABELA 1. Resultados selecionados do teste clínico para tolerância local de diversas formulações
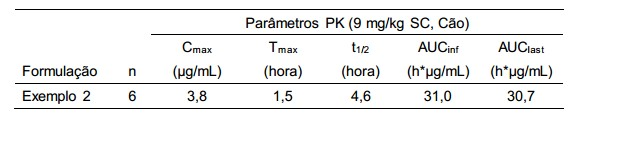
[00119] Além das diversas tolerâncias, a formulação tem também uma influência sobre o perfil farmacocinético do soro (PK). Diversas formulações apresentam nítidas diferenças na curva do tempo da concentração de soro. Para as quinolonas, preferem-se curvas com rápida absorção, altas concentrações de pico e fases de eliminação lentas. A tabela abaixo mostra o perfil PK de uma formulação de acordo com a invenção. O sistema de teste usado foi descrito no parágrafo "tolerância local". TABELA 2. Resultados da farmacocinética do soro