BRPI0902242B1 - Uso do agonista do receptor mas da angiotensina (1-7) ave 0991 para tratamento ou prevenção da artrite reumatóide - Google Patents
Uso do agonista do receptor mas da angiotensina (1-7) ave 0991 para tratamento ou prevenção da artrite reumatóide Download PDFInfo
- Publication number
- BRPI0902242B1 BRPI0902242B1 BRPI0902242-2A BRPI0902242A BRPI0902242B1 BR PI0902242 B1 BRPI0902242 B1 BR PI0902242B1 BR PI0902242 A BRPI0902242 A BR PI0902242A BR PI0902242 B1 BRPI0902242 B1 BR PI0902242B1
- Authority
- BR
- Brazil
- Prior art keywords
- ave
- inflammatory
- angiotensin
- ang
- mbsa
- Prior art date
Links
- 229940044601 receptor agonist Drugs 0.000 title claims abstract description 28
- 239000000018 receptor agonist Substances 0.000 title claims abstract description 28
- 206010039073 rheumatoid arthritis Diseases 0.000 title claims abstract description 20
- PVHLMTREZMEJCG-GDTLVBQBSA-N Ile(5)-angiotensin II (1-7) Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N1[C@@H](CCC1)C([O-])=O)NC(=O)[C@@H](NC(=O)[C@H](CCCNC(N)=[NH2+])NC(=O)[C@@H]([NH3+])CC([O-])=O)C(C)C)C1=CC=C(O)C=C1 PVHLMTREZMEJCG-GDTLVBQBSA-N 0.000 title abstract description 42
- 108010021281 angiotensin I (1-7) Proteins 0.000 title abstract description 19
- 238000011282 treatment Methods 0.000 title description 29
- 230000002265 prevention Effects 0.000 title description 3
- QTOZBSNPDCWHPV-UHFFFAOYSA-N 1-ethyl-3-[3-[4-[(5-formyl-4-methoxy-2-phenylimidazol-1-yl)methyl]phenyl]-5-(2-methylpropyl)thiophen-2-yl]sulfonylurea Chemical compound S1C(CC(C)C)=CC(C=2C=CC(CN3C(=NC(OC)=C3C=O)C=3C=CC=CC=3)=CC=2)=C1S(=O)(=O)NC(=O)NCC QTOZBSNPDCWHPV-UHFFFAOYSA-N 0.000 claims abstract description 53
- 108010064733 Angiotensins Proteins 0.000 claims abstract description 9
- 102000015427 Angiotensins Human genes 0.000 claims abstract description 9
- 239000003814 drug Substances 0.000 claims abstract description 6
- 206010003246 arthritis Diseases 0.000 abstract description 27
- 102000015925 Proto-oncogene Mas Human genes 0.000 abstract description 23
- 108050004181 Proto-oncogene Mas Proteins 0.000 abstract description 23
- 239000000203 mixture Substances 0.000 abstract description 16
- 108090000765 processed proteins & peptides Proteins 0.000 abstract description 14
- 230000002757 inflammatory effect Effects 0.000 abstract description 12
- 230000004044 response Effects 0.000 abstract description 11
- 208000027866 inflammatory disease Diseases 0.000 abstract description 8
- 230000028709 inflammatory response Effects 0.000 abstract description 8
- 230000000202 analgesic effect Effects 0.000 abstract description 7
- 230000000144 pharmacologic effect Effects 0.000 abstract description 7
- 230000001225 therapeutic effect Effects 0.000 abstract description 7
- 230000003110 anti-inflammatory effect Effects 0.000 abstract description 5
- 238000002360 preparation method Methods 0.000 abstract description 5
- 150000003839 salts Chemical class 0.000 abstract description 5
- 239000012453 solvate Substances 0.000 abstract description 5
- 239000000470 constituent Substances 0.000 abstract description 4
- 238000013459 approach Methods 0.000 abstract description 3
- 102000053723 Angiotensin-converting enzyme 2 Human genes 0.000 abstract 1
- 108090000975 Angiotensin-converting enzyme 2 Proteins 0.000 abstract 1
- 241001465754 Metazoa Species 0.000 description 46
- 230000000694 effects Effects 0.000 description 29
- 210000001519 tissue Anatomy 0.000 description 28
- 210000000265 leukocyte Anatomy 0.000 description 22
- 210000000440 neutrophil Anatomy 0.000 description 22
- 102000004127 Cytokines Human genes 0.000 description 20
- 108090000695 Cytokines Proteins 0.000 description 20
- 238000000034 method Methods 0.000 description 20
- 239000003981 vehicle Substances 0.000 description 18
- 230000035488 systolic blood pressure Effects 0.000 description 17
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 16
- 102000000852 Tumor Necrosis Factor-alpha Human genes 0.000 description 16
- MZOFCQQQCNRIBI-VMXHOPILSA-N (3s)-4-[[(2s)-1-[[(2s)-1-[[(1s)-1-carboxy-2-hydroxyethyl]amino]-4-methyl-1-oxopentan-2-yl]amino]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-3-[[2-[[(2s)-2,6-diaminohexanoyl]amino]acetyl]amino]-4-oxobutanoic acid Chemical compound OC[C@@H](C(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN MZOFCQQQCNRIBI-VMXHOPILSA-N 0.000 description 15
- 230000036454 renin-angiotensin system Effects 0.000 description 14
- 210000004027 cell Anatomy 0.000 description 13
- 238000012360 testing method Methods 0.000 description 13
- 230000005012 migration Effects 0.000 description 11
- 238000013508 migration Methods 0.000 description 11
- 230000004054 inflammatory process Effects 0.000 description 10
- 238000005096 rolling process Methods 0.000 description 10
- 239000000243 solution Substances 0.000 description 10
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 9
- 238000002474 experimental method Methods 0.000 description 9
- 206010061218 Inflammation Diseases 0.000 description 8
- 102000003896 Myeloperoxidases Human genes 0.000 description 8
- 108090000235 Myeloperoxidases Proteins 0.000 description 8
- 230000004913 activation Effects 0.000 description 8
- 238000000540 analysis of variance Methods 0.000 description 8
- 210000003038 endothelium Anatomy 0.000 description 8
- 210000003127 knee Anatomy 0.000 description 8
- 230000008569 process Effects 0.000 description 8
- 108010002352 Interleukin-1 Proteins 0.000 description 7
- 241000699670 Mus sp. Species 0.000 description 7
- 239000000556 agonist Substances 0.000 description 7
- 230000003993 interaction Effects 0.000 description 7
- 102000004190 Enzymes Human genes 0.000 description 6
- 108090000790 Enzymes Proteins 0.000 description 6
- 230000009471 action Effects 0.000 description 6
- 238000004519 manufacturing process Methods 0.000 description 6
- 230000007115 recruitment Effects 0.000 description 6
- 239000006228 supernatant Substances 0.000 description 6
- 108010012236 Chemokines Proteins 0.000 description 5
- 102000019034 Chemokines Human genes 0.000 description 5
- 238000002965 ELISA Methods 0.000 description 5
- 238000003639 Student–Newman–Keuls (SNK) method Methods 0.000 description 5
- 238000004458 analytical method Methods 0.000 description 5
- 239000003937 drug carrier Substances 0.000 description 5
- 238000001727 in vivo Methods 0.000 description 5
- 210000004969 inflammatory cell Anatomy 0.000 description 5
- -1 polypropylene Polymers 0.000 description 5
- 230000009467 reduction Effects 0.000 description 5
- UUUHXMGGBIUAPW-UHFFFAOYSA-N 1-[1-[2-[[5-amino-2-[[1-[5-(diaminomethylideneamino)-2-[[1-[3-(1h-indol-3-yl)-2-[(5-oxopyrrolidine-2-carbonyl)amino]propanoyl]pyrrolidine-2-carbonyl]amino]pentanoyl]pyrrolidine-2-carbonyl]amino]-5-oxopentanoyl]amino]-3-methylpentanoyl]pyrrolidine-2-carbon Chemical compound C1CCC(C(=O)N2C(CCC2)C(O)=O)N1C(=O)C(C(C)CC)NC(=O)C(CCC(N)=O)NC(=O)C1CCCN1C(=O)C(CCCN=C(N)N)NC(=O)C1CCCN1C(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C1CCC(=O)N1 UUUHXMGGBIUAPW-UHFFFAOYSA-N 0.000 description 4
- 101150059573 AGTR1 gene Proteins 0.000 description 4
- WZUVPPKBWHMQCE-UHFFFAOYSA-N Haematoxylin Chemical compound C12=CC(O)=C(O)C=C2CC2(O)C1C1=CC=C(O)C(O)=C1OC2 WZUVPPKBWHMQCE-UHFFFAOYSA-N 0.000 description 4
- 241000282412 Homo Species 0.000 description 4
- 241000699666 Mus <mouse, genus> Species 0.000 description 4
- 102000004270 Peptidyl-Dipeptidase A Human genes 0.000 description 4
- 108090000882 Peptidyl-Dipeptidase A Proteins 0.000 description 4
- QAOWNCQODCNURD-UHFFFAOYSA-N Sulfuric acid Chemical compound OS(O)(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-N 0.000 description 4
- 230000015572 biosynthetic process Effects 0.000 description 4
- 230000001413 cellular effect Effects 0.000 description 4
- 239000003795 chemical substances by application Substances 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 4
- 239000000839 emulsion Substances 0.000 description 4
- 238000012771 intravital microscopy Methods 0.000 description 4
- 210000001503 joint Anatomy 0.000 description 4
- 238000005259 measurement Methods 0.000 description 4
- QYSGYZVSCZSLHT-UHFFFAOYSA-N octafluoropropane Chemical class FC(F)(F)C(F)(F)C(F)(F)F QYSGYZVSCZSLHT-UHFFFAOYSA-N 0.000 description 4
- UOHMMEJUHBCKEE-UHFFFAOYSA-N prehnitene Chemical compound CC1=CC=C(C)C(C)=C1C UOHMMEJUHBCKEE-UHFFFAOYSA-N 0.000 description 4
- 102000005962 receptors Human genes 0.000 description 4
- 108020003175 receptors Proteins 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- 102000008873 Angiotensin II receptor Human genes 0.000 description 3
- 108050000824 Angiotensin II receptor Proteins 0.000 description 3
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 229930006000 Sucrose Natural products 0.000 description 3
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 3
- 239000004480 active ingredient Substances 0.000 description 3
- 239000002671 adjuvant Substances 0.000 description 3
- 238000010171 animal model Methods 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 230000000903 blocking effect Effects 0.000 description 3
- 230000036772 blood pressure Effects 0.000 description 3
- 239000000872 buffer Substances 0.000 description 3
- 230000021164 cell adhesion Effects 0.000 description 3
- 238000005119 centrifugation Methods 0.000 description 3
- VYXSBFYARXAAKO-WTKGSRSZSA-N chembl402140 Chemical compound Cl.C1=2C=C(C)C(NCC)=CC=2OC2=C\C(=N/CC)C(C)=CC2=C1C1=CC=CC=C1C(=O)OCC VYXSBFYARXAAKO-WTKGSRSZSA-N 0.000 description 3
- 150000001875 compounds Chemical class 0.000 description 3
- 230000001419 dependent effect Effects 0.000 description 3
- 210000002889 endothelial cell Anatomy 0.000 description 3
- 210000003989 endothelium vascular Anatomy 0.000 description 3
- 206010020718 hyperplasia Diseases 0.000 description 3
- 230000003053 immunization Effects 0.000 description 3
- 238000002649 immunization Methods 0.000 description 3
- 239000008188 pellet Substances 0.000 description 3
- 102000004196 processed proteins & peptides Human genes 0.000 description 3
- 230000000770 proinflammatory effect Effects 0.000 description 3
- 238000012552 review Methods 0.000 description 3
- 239000005720 sucrose Substances 0.000 description 3
- 239000000725 suspension Substances 0.000 description 3
- 210000001258 synovial membrane Anatomy 0.000 description 3
- 239000006188 syrup Substances 0.000 description 3
- 235000020357 syrup Nutrition 0.000 description 3
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 3
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- 238000011740 C57BL/6 mouse Methods 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 2
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 2
- 238000012286 ELISA Assay Methods 0.000 description 2
- 208000009386 Experimental Arthritis Diseases 0.000 description 2
- 206010016654 Fibrosis Diseases 0.000 description 2
- WSFSSNUMVMOOMR-UHFFFAOYSA-N Formaldehyde Chemical compound O=C WSFSSNUMVMOOMR-UHFFFAOYSA-N 0.000 description 2
- 108091006027 G proteins Proteins 0.000 description 2
- 102000030782 GTP binding Human genes 0.000 description 2
- 108091000058 GTP-Binding Proteins 0.000 description 2
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 2
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 2
- 206010020880 Hypertrophy Diseases 0.000 description 2
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 2
- 229930195725 Mannitol Natural products 0.000 description 2
- 241001529936 Murinae Species 0.000 description 2
- MWUXSHHQAYIFBG-UHFFFAOYSA-N Nitric oxide Chemical compound O=[N] MWUXSHHQAYIFBG-UHFFFAOYSA-N 0.000 description 2
- 102000035195 Peptidases Human genes 0.000 description 2
- 108091005804 Peptidases Proteins 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 2
- 229920002472 Starch Polymers 0.000 description 2
- 238000000692 Student's t-test Methods 0.000 description 2
- 210000001744 T-lymphocyte Anatomy 0.000 description 2
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 2
- 238000009825 accumulation Methods 0.000 description 2
- NIXOWILDQLNWCW-UHFFFAOYSA-N acrylic acid group Chemical group C(C=C)(=O)O NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 2
- 235000010443 alginic acid Nutrition 0.000 description 2
- 229920000615 alginic acid Polymers 0.000 description 2
- 239000002333 angiotensin II receptor antagonist Substances 0.000 description 2
- 239000002416 angiotensin derivative Substances 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 102000036639 antigens Human genes 0.000 description 2
- 108091007433 antigens Proteins 0.000 description 2
- 239000011230 binding agent Substances 0.000 description 2
- 230000004071 biological effect Effects 0.000 description 2
- 230000017531 blood circulation Effects 0.000 description 2
- 210000004204 blood vessel Anatomy 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 239000001768 carboxy methyl cellulose Substances 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 230000012292 cell migration Effects 0.000 description 2
- 230000008859 change Effects 0.000 description 2
- 238000006243 chemical reaction Methods 0.000 description 2
- 208000037976 chronic inflammation Diseases 0.000 description 2
- 208000037893 chronic inflammatory disorder Diseases 0.000 description 2
- 230000004087 circulation Effects 0.000 description 2
- 238000004737 colorimetric analysis Methods 0.000 description 2
- 230000001276 controlling effect Effects 0.000 description 2
- 230000001517 counterregulatory effect Effects 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- YQGOJNYOYNNSMM-UHFFFAOYSA-N eosin Chemical compound [Na+].OC(=O)C1=CC=CC=C1C1=C2C=C(Br)C(=O)C(Br)=C2OC2=C(Br)C(O)=C(Br)C=C21 YQGOJNYOYNNSMM-UHFFFAOYSA-N 0.000 description 2
- 238000011156 evaluation Methods 0.000 description 2
- 210000000416 exudates and transudate Anatomy 0.000 description 2
- 210000002950 fibroblast Anatomy 0.000 description 2
- 230000004761 fibrosis Effects 0.000 description 2
- 238000009472 formulation Methods 0.000 description 2
- 239000012634 fragment Substances 0.000 description 2
- 238000007489 histopathology method Methods 0.000 description 2
- 238000000265 homogenisation Methods 0.000 description 2
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Substances C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 description 2
- 230000002519 immonomodulatory effect Effects 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000008595 infiltration Effects 0.000 description 2
- 238000001764 infiltration Methods 0.000 description 2
- 230000004941 influx Effects 0.000 description 2
- 208000018937 joint inflammation Diseases 0.000 description 2
- 229960003299 ketamine Drugs 0.000 description 2
- 230000023404 leukocyte cell-cell adhesion Effects 0.000 description 2
- 239000007788 liquid Substances 0.000 description 2
- 210000002540 macrophage Anatomy 0.000 description 2
- 239000000594 mannitol Substances 0.000 description 2
- 235000010355 mannitol Nutrition 0.000 description 2
- 229920000609 methyl cellulose Polymers 0.000 description 2
- 239000001923 methylcellulose Substances 0.000 description 2
- 235000010981 methylcellulose Nutrition 0.000 description 2
- 230000003278 mimic effect Effects 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 230000004963 pathophysiological condition Effects 0.000 description 2
- 230000008447 perception Effects 0.000 description 2
- 239000008194 pharmaceutical composition Substances 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 238000002203 pretreatment Methods 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 235000019833 protease Nutrition 0.000 description 2
- 230000001105 regulatory effect Effects 0.000 description 2
- 235000019698 starch Nutrition 0.000 description 2
- 208000024891 symptom Diseases 0.000 description 2
- 230000001960 triggered effect Effects 0.000 description 2
- 230000024883 vasodilation Effects 0.000 description 2
- 238000012800 visualization Methods 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- BPICBUSOMSTKRF-UHFFFAOYSA-N xylazine Chemical compound CC1=CC=CC(C)=C1NC1=NCCCS1 BPICBUSOMSTKRF-UHFFFAOYSA-N 0.000 description 2
- 229960001600 xylazine Drugs 0.000 description 2
- GEYOCULIXLDCMW-UHFFFAOYSA-N 1,2-phenylenediamine Chemical compound NC1=CC=CC=C1N GEYOCULIXLDCMW-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 1
- 239000005541 ACE inhibitor Substances 0.000 description 1
- 101150116411 AGTR2 gene Proteins 0.000 description 1
- 208000030090 Acute Disease Diseases 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- PQSUYGKTWSAVDQ-ZVIOFETBSA-N Aldosterone Chemical compound C([C@@]1([C@@H](C(=O)CO)CC[C@H]1[C@@H]1CC2)C=O)[C@H](O)[C@@H]1[C@]1(C)C2=CC(=O)CC1 PQSUYGKTWSAVDQ-ZVIOFETBSA-N 0.000 description 1
- PQSUYGKTWSAVDQ-UHFFFAOYSA-N Aldosterone Natural products C1CC2C3CCC(C(=O)CO)C3(C=O)CC(O)C2C2(C)C1=CC(=O)CC2 PQSUYGKTWSAVDQ-UHFFFAOYSA-N 0.000 description 1
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 1
- 101800000734 Angiotensin-1 Proteins 0.000 description 1
- 102400000344 Angiotensin-1 Human genes 0.000 description 1
- 102400000345 Angiotensin-2 Human genes 0.000 description 1
- 101800000733 Angiotensin-2 Proteins 0.000 description 1
- 101100332655 Arabidopsis thaliana ECA2 gene Proteins 0.000 description 1
- 239000002083 C09CA01 - Losartan Substances 0.000 description 1
- 101100289995 Caenorhabditis elegans mac-1 gene Proteins 0.000 description 1
- 208000024172 Cardiovascular disease Diseases 0.000 description 1
- 102000000503 Collagen Type II Human genes 0.000 description 1
- 108010041390 Collagen Type II Proteins 0.000 description 1
- 229920002261 Corn starch Polymers 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- 241000196324 Embryophyta Species 0.000 description 1
- 108050009340 Endothelin Proteins 0.000 description 1
- 102000002045 Endothelin Human genes 0.000 description 1
- 208000010228 Erectile Dysfunction Diseases 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 102000017703 GABRG2 Human genes 0.000 description 1
- 108010010803 Gelatin Proteins 0.000 description 1
- 238000002738 Giemsa staining Methods 0.000 description 1
- 206010019280 Heart failures Diseases 0.000 description 1
- 101001055222 Homo sapiens Interleukin-8 Proteins 0.000 description 1
- 208000004454 Hyperalgesia Diseases 0.000 description 1
- 208000035154 Hyperesthesia Diseases 0.000 description 1
- 206010020772 Hypertension Diseases 0.000 description 1
- CZGUSIXMZVURDU-JZXHSEFVSA-N Ile(5)-angiotensin II Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC=1C=CC=CC=1)C([O-])=O)NC(=O)[C@@H](NC(=O)[C@H](CCCNC(N)=[NH2+])NC(=O)[C@@H]([NH3+])CC([O-])=O)C(C)C)C1=CC=C(O)C=C1 CZGUSIXMZVURDU-JZXHSEFVSA-N 0.000 description 1
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 1
- 108090001007 Interleukin-8 Proteins 0.000 description 1
- 108010063738 Interleukins Proteins 0.000 description 1
- 102000015696 Interleukins Human genes 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 101710151803 Mitochondrial intermediate peptidase 2 Proteins 0.000 description 1
- CTQNGGLPUBDAKN-UHFFFAOYSA-N O-Xylene Chemical compound CC1=CC=CC=C1C CTQNGGLPUBDAKN-UHFFFAOYSA-N 0.000 description 1
- 206010030113 Oedema Diseases 0.000 description 1
- 241001536563 Panus Species 0.000 description 1
- 102000003992 Peroxidases Human genes 0.000 description 1
- 239000004743 Polypropylene Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 206010037660 Pyrexia Diseases 0.000 description 1
- 206010041277 Sodium retention Diseases 0.000 description 1
- 235000021355 Stearic acid Nutrition 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 238000010161 Student-Newman-Keuls test Methods 0.000 description 1
- OUUQCZGPVNCOIJ-UHFFFAOYSA-M Superoxide Chemical compound [O-][O] OUUQCZGPVNCOIJ-UHFFFAOYSA-M 0.000 description 1
- 230000006044 T cell activation Effects 0.000 description 1
- 206010047139 Vasoconstriction Diseases 0.000 description 1
- GXBMIBRIOWHPDT-UHFFFAOYSA-N Vasopressin Natural products N1C(=O)C(CC=2C=C(O)C=CC=2)NC(=O)C(N)CSSCC(C(=O)N2C(CCC2)C(=O)NC(CCCN=C(N)N)C(=O)NCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(CCC(N)=O)NC(=O)C1CC1=CC=CC=C1 GXBMIBRIOWHPDT-UHFFFAOYSA-N 0.000 description 1
- 108010004977 Vasopressins Proteins 0.000 description 1
- 102000002852 Vasopressins Human genes 0.000 description 1
- 235000010724 Wisteria floribunda Nutrition 0.000 description 1
- 229920000392 Zymosan Polymers 0.000 description 1
- 230000003213 activating effect Effects 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 230000010398 acute inflammatory response Effects 0.000 description 1
- 230000006978 adaptation Effects 0.000 description 1
- 230000001464 adherent effect Effects 0.000 description 1
- 230000001919 adrenal effect Effects 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 229960002478 aldosterone Drugs 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 150000004781 alginic acids Chemical class 0.000 description 1
- 230000003444 anaesthetic effect Effects 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- ORWYRWWVDCYOMK-HBZPZAIKSA-N angiotensin I Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC(C)C)C(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CCCN=C(N)N)NC(=O)[C@@H](N)CC(O)=O)C(C)C)C1=CC=C(O)C=C1 ORWYRWWVDCYOMK-HBZPZAIKSA-N 0.000 description 1
- 239000000400 angiotensin II type 1 receptor blocker Substances 0.000 description 1
- 229950006323 angiotensin ii Drugs 0.000 description 1
- 229940044094 angiotensin-converting-enzyme inhibitor Drugs 0.000 description 1
- 230000003042 antagnostic effect Effects 0.000 description 1
- 230000002663 anti-arrhythmogenic effect Effects 0.000 description 1
- 230000001028 anti-proliverative effect Effects 0.000 description 1
- 239000000427 antigen Substances 0.000 description 1
- 210000000709 aorta Anatomy 0.000 description 1
- 230000001640 apoptogenic effect Effects 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- KBZOIRJILGZLEJ-LGYYRGKSSA-N argipressin Chemical compound C([C@H]1C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CSSC[C@@H](C(N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N1)=O)N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCN=C(N)N)C(=O)NCC(N)=O)C1=CC=CC=C1 KBZOIRJILGZLEJ-LGYYRGKSSA-N 0.000 description 1
- 230000006793 arrhythmia Effects 0.000 description 1
- 206010003119 arrhythmia Diseases 0.000 description 1
- 208000037849 arterial hypertension Diseases 0.000 description 1
- 210000001188 articular cartilage Anatomy 0.000 description 1
- 230000002238 attenuated effect Effects 0.000 description 1
- 230000001363 autoimmune Effects 0.000 description 1
- 210000003719 b-lymphocyte Anatomy 0.000 description 1
- 210000003651 basophil Anatomy 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 229940098773 bovine serum albumin Drugs 0.000 description 1
- CJZGTCYPCWQAJB-UHFFFAOYSA-L calcium stearate Chemical compound [Ca+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O CJZGTCYPCWQAJB-UHFFFAOYSA-L 0.000 description 1
- 239000008116 calcium stearate Substances 0.000 description 1
- 235000013539 calcium stearate Nutrition 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 230000000747 cardiac effect Effects 0.000 description 1
- 239000002327 cardiovascular agent Substances 0.000 description 1
- 229940125692 cardiovascular agent Drugs 0.000 description 1
- 235000010418 carrageenan Nutrition 0.000 description 1
- 239000000679 carrageenan Substances 0.000 description 1
- 229920001525 carrageenan Polymers 0.000 description 1
- 229940113118 carrageenan Drugs 0.000 description 1
- 210000000845 cartilage Anatomy 0.000 description 1
- 238000004113 cell culture Methods 0.000 description 1
- 230000024245 cell differentiation Effects 0.000 description 1
- 230000004663 cell proliferation Effects 0.000 description 1
- 239000001913 cellulose Substances 0.000 description 1
- 229920002678 cellulose Polymers 0.000 description 1
- 239000003153 chemical reaction reagent Substances 0.000 description 1
- 239000005482 chemotactic factor Substances 0.000 description 1
- 210000001612 chondrocyte Anatomy 0.000 description 1
- 230000001684 chronic effect Effects 0.000 description 1
- 230000012085 chronic inflammatory response Effects 0.000 description 1
- 230000036474 chronotropism Effects 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 239000008120 corn starch Substances 0.000 description 1
- 238000009109 curative therapy Methods 0.000 description 1
- 229940097362 cyclodextrins Drugs 0.000 description 1
- 230000003013 cytotoxicity Effects 0.000 description 1
- 231100000135 cytotoxicity Toxicity 0.000 description 1
- 230000003247 decreasing effect Effects 0.000 description 1
- 230000006735 deficit Effects 0.000 description 1
- 238000001514 detection method Methods 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- 238000003745 diagnosis Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- MOTZDAYCYVMXPC-UHFFFAOYSA-N dodecyl hydrogen sulfate Chemical class CCCCCCCCCCCCOS(O)(=O)=O MOTZDAYCYVMXPC-UHFFFAOYSA-N 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 229940079593 drug Drugs 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000002526 effect on cardiovascular system Effects 0.000 description 1
- 239000003792 electrolyte Substances 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- ZUBDGKVDJUIMQQ-UBFCDGJISA-N endothelin-1 Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(O)=O)NC(=O)[C@H]1NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](C(C)C)NC(=O)[C@H]2CSSC[C@@H](C(N[C@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)NC(=O)[C@@H](CO)NC(=O)[C@H](N)CSSC1)C1=CNC=N1 ZUBDGKVDJUIMQQ-UBFCDGJISA-N 0.000 description 1
- 230000003628 erosive effect Effects 0.000 description 1
- 210000003743 erythrocyte Anatomy 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 239000007888 film coating Substances 0.000 description 1
- 238000009501 film coating Methods 0.000 description 1
- 239000012530 fluid Substances 0.000 description 1
- 230000006870 function Effects 0.000 description 1
- 239000008273 gelatin Substances 0.000 description 1
- 229920000159 gelatin Polymers 0.000 description 1
- 235000019322 gelatine Nutrition 0.000 description 1
- 235000011852 gelatine desserts Nutrition 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 235000011187 glycerol Nutrition 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 230000036433 growing body Effects 0.000 description 1
- 230000012010 growth Effects 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000000004 hemodynamic effect Effects 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 150000002460 imidazoles Chemical group 0.000 description 1
- 238000007654 immersion Methods 0.000 description 1
- 201000001881 impotence Diseases 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 230000004968 inflammatory condition Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000036450 inotropism Effects 0.000 description 1
- 229940047122 interleukins Drugs 0.000 description 1
- 230000031146 intracellular signal transduction Effects 0.000 description 1
- 238000007918 intramuscular administration Methods 0.000 description 1
- 239000007927 intramuscular injection Substances 0.000 description 1
- 238000010255 intramuscular injection Methods 0.000 description 1
- 238000010253 intravenous injection Methods 0.000 description 1
- 210000002510 keratinocyte Anatomy 0.000 description 1
- 230000003907 kidney function Effects 0.000 description 1
- 238000011813 knockout mouse model Methods 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- 235000010445 lecithin Nutrition 0.000 description 1
- 239000000787 lecithin Substances 0.000 description 1
- 229940067606 lecithin Drugs 0.000 description 1
- 229960004393 lidocaine hydrochloride Drugs 0.000 description 1
- YECIFGHRMFEPJK-UHFFFAOYSA-N lidocaine hydrochloride monohydrate Chemical compound O.[Cl-].CC[NH+](CC)CC(=O)NC1=C(C)C=CC=C1C YECIFGHRMFEPJK-UHFFFAOYSA-N 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 230000003908 liver function Effects 0.000 description 1
- 230000008752 local inflammatory process Effects 0.000 description 1
- KJJZZJSZUJXYEA-UHFFFAOYSA-N losartan Chemical compound CCCCC1=NC(Cl)=C(CO)N1CC1=CC=C(C=2C(=CC=CC=2)C=2[N]N=NN=2)C=C1 KJJZZJSZUJXYEA-UHFFFAOYSA-N 0.000 description 1
- 229960004773 losartan Drugs 0.000 description 1
- 239000000314 lubricant Substances 0.000 description 1
- 210000004072 lung Anatomy 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Substances [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 1
- 235000019359 magnesium stearate Nutrition 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 239000000463 material Substances 0.000 description 1
- 210000003622 mature neutrocyte Anatomy 0.000 description 1
- 102000006240 membrane receptors Human genes 0.000 description 1
- 108020004084 membrane receptors Proteins 0.000 description 1
- QSHDDOUJBYECFT-UHFFFAOYSA-N mercury Chemical compound [Hg] QSHDDOUJBYECFT-UHFFFAOYSA-N 0.000 description 1
- 229910052753 mercury Inorganic materials 0.000 description 1
- 238000007431 microscopic evaluation Methods 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 210000001616 monocyte Anatomy 0.000 description 1
- 210000005087 mononuclear cell Anatomy 0.000 description 1
- 230000000877 morphologic effect Effects 0.000 description 1
- 230000003387 muscular Effects 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 229920001206 natural gum Polymers 0.000 description 1
- 230000017095 negative regulation of cell growth Effects 0.000 description 1
- 238000006386 neutralization reaction Methods 0.000 description 1
- 230000011242 neutrophil chemotaxis Effects 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 230000003040 nociceptive effect Effects 0.000 description 1
- 229940127264 non-peptide agonist Drugs 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 1
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 1
- 239000003921 oil Substances 0.000 description 1
- 235000019198 oils Nutrition 0.000 description 1
- 239000004006 olive oil Substances 0.000 description 1
- 235000008390 olive oil Nutrition 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 210000000056 organ Anatomy 0.000 description 1
- 210000002997 osteoclast Anatomy 0.000 description 1
- 230000003647 oxidation Effects 0.000 description 1
- 238000007254 oxidation reaction Methods 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 210000000426 patellar ligament Anatomy 0.000 description 1
- 230000007310 pathophysiology Effects 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 108040007629 peroxidase activity proteins Proteins 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 229940127557 pharmaceutical product Drugs 0.000 description 1
- 230000003285 pharmacodynamic effect Effects 0.000 description 1
- 239000008363 phosphate buffer Substances 0.000 description 1
- 239000006187 pill Substances 0.000 description 1
- 229920001223 polyethylene glycol Polymers 0.000 description 1
- 229920001155 polypropylene Polymers 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 1
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 1
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 238000004321 preservation Methods 0.000 description 1
- 230000002062 proliferating effect Effects 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000000069 prophylactic effect Effects 0.000 description 1
- 238000011321 prophylaxis Methods 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 230000001681 protective effect Effects 0.000 description 1
- 230000002685 pulmonary effect Effects 0.000 description 1
- 238000011002 quantification Methods 0.000 description 1
- 230000002829 reductive effect Effects 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- 238000002271 resection Methods 0.000 description 1
- 229940069575 rompun Drugs 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- 229940080313 sodium starch Drugs 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 241000894007 species Species 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 229940032147 starch Drugs 0.000 description 1
- 238000007619 statistical method Methods 0.000 description 1
- 239000008117 stearic acid Substances 0.000 description 1
- 239000008223 sterile water Substances 0.000 description 1
- 230000000638 stimulation Effects 0.000 description 1
- 238000007920 subcutaneous administration Methods 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 239000000758 substrate Substances 0.000 description 1
- 238000009495 sugar coating Methods 0.000 description 1
- 238000013268 sustained release Methods 0.000 description 1
- 239000012730 sustained-release form Substances 0.000 description 1
- 230000008700 sympathetic activation Effects 0.000 description 1
- 210000001179 synovial fluid Anatomy 0.000 description 1
- 210000005222 synovial tissue Anatomy 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 238000009475 tablet pressing Methods 0.000 description 1
- 239000000454 talc Substances 0.000 description 1
- 229910052623 talc Inorganic materials 0.000 description 1
- 235000012222 talc Nutrition 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 239000003440 toxic substance Substances 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 230000025033 vasoconstriction Effects 0.000 description 1
- 229940124549 vasodilator Drugs 0.000 description 1
- 239000003071 vasodilator agent Substances 0.000 description 1
- 229960003726 vasopressin Drugs 0.000 description 1
- 210000003462 vein Anatomy 0.000 description 1
- 210000000264 venule Anatomy 0.000 description 1
- 239000011534 wash buffer Substances 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- QYEFBJRXKKSABU-UHFFFAOYSA-N xylazine hydrochloride Chemical compound Cl.CC1=CC=CC(C)=C1NC1=NCCCS1 QYEFBJRXKKSABU-UHFFFAOYSA-N 0.000 description 1
- 239000008096 xylene Substances 0.000 description 1
- UHVMMEOXYDMDKI-JKYCWFKZSA-L zinc;1-(5-cyanopyridin-2-yl)-3-[(1s,2s)-2-(6-fluoro-2-hydroxy-3-propanoylphenyl)cyclopropyl]urea;diacetate Chemical compound [Zn+2].CC([O-])=O.CC([O-])=O.CCC(=O)C1=CC=C(F)C([C@H]2[C@H](C2)NC(=O)NC=2N=CC(=CC=2)C#N)=C1O UHVMMEOXYDMDKI-JKYCWFKZSA-L 0.000 description 1
Images
Landscapes
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
COMPOSIÇÃO COMPREENDENDO AGONISTA DO RECEPTOR MAS DA ANGIOTENSINA (1-7) E SEU USO PARA A MODULAÇÃO DA RESPOSTA INFLAMATÓRIA E/OU ANALGÉSICA. A presente invenção proporciona o uso de agonistas do receptor Mas da Angiotensina (1-7), como alternativa farmacológica e terapêutica no contexto das doenças inflamatórias, como a artrite reumatóide. A invenção proporciona composições compreendendo angiotensina(1-7), seus análogos peptídicos ou não peptídicos, ou um sal, solvato e/ou hidrato farmaceuticamente aceitável e seu uso na preparação de medicamentos, para a modulação da resposta inflamatória e/ou analgésica. Entre outros, os efeitos antiinflamatórios dos agonistas do receptor Mas de angiotensina (1-7), em especial do AVE 0991, inibem importantes parâmetros da resposta inflamatória no modelo de artrite induzida por mBSA. A presente invenção proporciona ainda uma nova abordagem de constituintes do SRA, como o eixo ECA2/Ang(1-7)/Mas, associados a eventos específicos da cascata da resposta inflamatória.
Description
[01] A presente invenção está no campo dos produtos e processos farmacêuticos. Em seu aspecto mais geral, se refere ao uso de agonista do receptor, Mas da Angiotensina (1-7), como angiotensina(1-7), seus análogos peptídicos ou não peptídicos, ou um sal, solvato e/ou hidrato farmaceuticamente aceitável como alternativa farmacológica e terapêutica no contexto das doenças inflamatórias, como a artrite reumatóide. A invenção proporciona composições compreendendo agonistas do receptor, Mas da Angiotensina (1-7), seu uso na preparação de medicamentos para modulação e diagnóstico da resposta inflamatória e/ou analgésica. Entre outros, os efeitos anti-inflamatórios dos agonistas do receptor, Mas de angiotensina (1-7), em especial o AVE 0991, inibem importantes parâmetros da resposta inflamatória no modelo de artrite induzida por mBSA (albumina bovina metilada). A presente invenção proporciona ainda uma nova abordagem de constituintes do SRA, como o eixo ECA2/Ang(1-7)/Mas, associados a eventos específicos da cascata da resposta inflamatória.
[02] A artrite reumatóide (AR) é uma doença inflamatória crônica sistêmica de base autoimune que afeta aproximadamente 1% da população mundial e acomete com maior frequência as mulheres adultas. A AR se inicia com o processo proliferativo da membrana sinovial, causando erosão da cartilagem articular e destruição do osso subjacente, sendo caracterizada pelo infiltrado celular de neutrófilos, células T, células B e macrófagos na membrana sinovial e nos espaços periarticulares. O acúmulo de neutrófilos na cavidade articular é uma característica marcante inflamação articular, pois estas células regulam e compõem tanto a resposta inflamatória aguda como a crônica [ver Wipke, BT e Allen, PM. J Immunology, 167 (3): 1601-1608 (2001)].
[03] As citocinas participam do recrutamento de neutrófilos em várias condições inflamatórias, incluindo a AR. A importância das citocinas e quimiocinas na fisiopatologia da AR foi demonstrada tanto em humanos como em modelos experimentais [ver Feldmann et al., Annual review of immunology,14, 397 (1996)].
[04] As interleucinas 1 e 8 (IL-1, IL-8) e o Fator de Necrose Tumoral -α (TNF-α), têm sido encontradas no líquido sinovial de pacientes com artrite. Embora os modelos experimentais não mimetizem a complexidade da AR humana, no modelo de artrite induzida por antígeno (AIA), que utiliza albumina bovina metilada (mBSA) como antígeno protéico e adjuvante completo de Freund (CFA), muitas das características histopatológicas, como o intenso influxo de neutrófilos, exsudato inflamatório articular e formação de panus, são semelhantes à doença humana.
[05] A IL-1 e o TNF-α são citocinas produzidas por uma variedade de células como os monócitos e os macrófagos e tem sido atribuído a estas citocinas importantes papéis na imunomodulação e em condições fisiopatológicas como a inflamação. Uma das principais atividades biológicas da IL-1 inclui a ativação de células T, estimulação da produção de prostaglandinas, indução de febre e quimiotaxia de neutrófilos. A inapropriada produção de IL-1 pode implicar no surgimento ou na manutenção do quadro agudo ou crônico de doenças inflamatórias como a artrite reumatóide.
[06] O TNF-α é uma citocina pró-inflamatória que possui papel chave em diversos processos, como inflamação, imunomodulação, crescimento, angiogênese e citotoxidade [ver Taylor et al., Current Opinion in biotechnology, 15(6): 557-563, (2004)]. Ela induz o aumento da expressão das moléculas de adesão tanto em PMN circulantes, quanto em células endoteliais. Estimula a síntese de outras citocinas, ativando células endoteliais, fibroblastos, eosteoclastos e condrócitos. O TNF-α também participa na migração de neutrófilos em modelos de reação inflamatória, tais como artrite induzida por colágeno, e em doenças inflamatórias humanas como a doença inflamatória intestinal e a AR.
[07] A quimiocina KC (homóloga murina da IL-8 humana) tem sido demonstrada como um fator quimiotático para linfócitos T, basófilos e principalmente para neutrófilos. Ela pode ser produzida por células mononucleares, fibroblastos, queratinócitos e células endoteliais. A sua produção por estas últimas células é induzida por IL-1 e TNF-α. Doenças caracterizadas por uma significativa infiltração de neutrófilos, como a AR, têm sido associadas ao aumento da produção de KC. Visto que a capacidade de KC em aumentar a expressão de moléculas como Mac-1 sobre a superfície de neutrófilos promove o aumento da adesão desse leucócito ao endotélio vascular.
[08] A neutralização de citocinas pró-inflamatórias como IL-1, TNF-α e KC por receptores solúveis ou anticorpos monoclonais é uma estratégia clínica comumente empregada no tratamento de pacientes com AR. Entretanto, o envolvimento de quimiocinas no modelo de AIA ainda não está bem elucidado. Apesar da relevância clínica, o tratamento da hiperalgesia articular ainda é limitado. Mesmo com diferentes formas para induzir artrite em ratos e camundongos, como carragenina, zymosan, colágeno tipo II e mBSA, os modelos que permitem o estudo da hipernocicepção articular são limitados.
[09] O sistema renina-angiotensina (SRA) é classicamente conceituado como uma cascata hormonal com ações voltadas para o controle das funções cardiovasculares, renais e adrenais, controlando o balanço de fluidos e eletrólitos, e também os níveis da pressão arterial. Esse controle era atribuído, exclusivamente às ações da Angiotensina II (Ang II).
[010] A Ang II exerce muitos dos efeitos biológicas do SRA, através a ativação do receptor AT1, um receptor de sete domínios transmembrânicos acoplado à proteína G. Dentre os efeitos decorrentes dessa ativação, destacam-se: vasoconstrição, retenção de sódio (relacionada à produção de aldosterona), retenção de água (relacionada à liberação de vasopressina), hipertrofia celular, fibrose, inotropismo/contratilidade, cronotropismo/arritmia, formação de superóxido, ativação do sistema nervoso simpático, secreção de endotelinas, etc. A Ang II também pode se ligar ao receptor AT2, que também é um receptor de membrana, os efeitos da sua ativação podem ser opostos aos da ativação de AT1: promove diferenciação celular, reparo tecidual, apoptose, vasodilatação, inibição do crescimento celular e efeitos anti-proliferativos. Contudo, há um corpo crescente de evidências documentando o envolvimento da Ang II em doenças inflamatórias. Levando-se em conta o perfil dos principais parâmetros desencadeados nessas patologias (recrutamento de células inflamatórias associadas com a liberação de citocinas para o local da inflamação) somado aos efeitos observados até então a partir da utilização de agentes do SRA. Estudos demonstram, inclusive, a presença de constituintes do sistema renina-angiotensina em células inflamatórias [ver Owen,CA e Campbel EJ, J Immunol, 160, 1436 (1998)].
[011] Outras enzimas também têm a habilidade de formar a Ang II a partir de Ang I. Ambas, Ang I e Ang II são susceptíveis à ação de peptidases. A ação dessas peptidases produz fragmentos menores de angiotensinas como a Ang III, 2-8 peptídeos; Ang IV, 3-8 peptídeos; Ang 1-7, etc., encontrados na circulação ou no tecido.
[012] A angiotensina-(1-7) é um desses “fragmentos” de angiotensina, que por muito tempo foi descrito como um produto inativo do sistema renina-angiotensina. O significado biológico desses novos peptídeos tem sido investigado há pouco tempo por vários grupos de pesquisa. Isso porque os recentes avanços na biologia celular e molecular, bem como as novas estratégias farmacologias e fisiológicas têm produzido novos conceitos sobre as ações do SRA.
[013] Dentre as recentes descobertas que produziram alterações conceituais de fundamental importância para relacionadas à Ang-(1-7), destaca-se a identificação da ECA2 (enzima conversora da angiotensina I 2) como uma importante enzima formadora de Ang-(1-7) [ver Donoghue et al., Circ Res, 87, E1-E9 (2000)] e a identificação do receptor acoplado a proteína G, Mas, como um receptor de Ang-(1-7) (ver Santos et al., Proc Natl Acad Sci USA,100, 8258 (2003)].
[014] A ativação do receptor, Mas pela Ang-(1-7) têm efeitos antagônicos àqueles promovidos pela Ang II via ativação de receptor AT1, dentre estes efeitos pode-se destacar: vasodilatação, anti-arritmogênico, redução de fibrose, redução da proliferação celular, redução da hipertrofia entre outros. Levando-se em conta tais efeitos da Ang-(1-7), pode-se afirmar que ela também é um importante mediador do sistema renina-angiotensina. De maneira geral esta invenção é dirigida justamente para esta nova abordagem do SRA e de seus constituintes, mediando outras condições fisiopatológicas do organismo, como a inflamação e às doenças associados a processos inflamatórios. Deixando para o passado a visão clássica de um sistema unidirecional e promovendo uma visão, ainda panorâmica, de um sistema mais complexo que funciona embasado em dois eixos opostos: o principal, responsável pela maioria das ações deste sistema - o eixo ECA - Ang II - ATI, e o segundo, um eixo contra-regulatório - ECA2 - Ang - (1-7) - Mas.
[015] AVE 0991, 5-formyl-4-methoxy-2-phenyl-1[[4-[2- ethylaminocarbonylsulfonamido)-5-isobutyl-3-thienyl]-phenyl]-methyl]- imidazole, é um derivado imidazol substituído e análogo da Ang (1-7). AVE 0991 mimetiza os efeitos da Ang - (1-7) em vários órgãos, e a sua identificação como um agonista do receptor Mas viabilizou estudos e possibilidades terapêuticas no tratamento de doenças cardiovasculares (Wiemer, G. et al “AVE 0991, a Nonpeptide Mimic of the Effects of Angiotensin-(1-7) on the endothelium” Hypertension, Dec. 2002; Santos RAS & Ferreira, AJ. “Pharmacological Effects of AVE 0991, a Nonpeptide Angiotensin-(1-7) Receptor Agonist” Cardiovascular Drug Reviews, Vol. 24, No. 3-4, pp. 239-246, 2006; Lemos, V. et al “The EndotheliumDependent Vasodilator Effect of the Nonpeptide Ang(1-7) Mimic AVE 0991 Is Abolished in the Aorta of Mas-Knockout Mice” J Cardiovasc Pharmacol. Volume 46, Number 3, September 2005; Ferreira, AJ et al “The nonpeptide angiotensin-(1-7) receptor Mas agonist AVE-0991 attenuates heart failure induced by myocardial infarction”, Am J Physiol Heart Circ Physiol 292: H1113-H1119, 2007; Toda, N. et al “Interaction of Endothelial Nitric Oxide and Angiotensin in the Circulation” Pharmacological Reviews, Vol. 59, No. 1, 2007). Entretanto, ao conhecimento dos presentes inventores, era até então inédita sua aplicabilidade no contexto das doenças inflamatórias, e especificamente nesta invenção na AIA.
[016] A literatura patentária contempla alguns documentos relacionados ao uso de AVE0991, porém sem antecipar ou sequer sugerir os objetos da presente invenção.
[017] O pedido internacional de patente WO 2008/089532, depositado pela Universidade Federal de Minas Gerais, Biolab Sanus, União Química e Farmacêutica Nacional e Biosintética Farmacêutica, revela o uso de Ang (1-7), um agonista de receptor Ang (1-7) e/ou um análogo de Ang (1-7) no tratamento da disfunção erétil. Apesar de citar o uso de AVE 0991, a invenção do referido documento é destinada a resolver outro problema técnico.
[018] O pedido internacional de patente WO 2007/000036, depositado pela Universidade Federal de Minas Gerais, revela o uso de agonistas e antagonistas de receptor Mas acoplado à proteína G como moduladores da atividade apoptótica, sendo, portanto, útil no estudo prevenção e tratamento de doenças. Um dos exemplos citados é uso de Ang (1-7) ou análogos, agonistas ou antagonistas. Além de ser destinada a resolver outro problema técnico, a invenção do referido documento não cita o uso de AVE 0991.
[019] O pedido internacional de patente WO 2002/080910, depositado pela Universidade Federal de Minas Gerais, revela formulações compreendendo antagonistas de receptor Angiotensina II AT1 em combinação com ciclodextrinas e derivados, visando o tratamento de hipertensão arterial. Além de ser destinada a resolver outro problema técnico, a invenção do referido documento não cita o uso de AVE 0991.
[020] A presente invenção tem como conceito inventivo o uso de agonista do receptor Mas da Angiotensina (1-7), como angiotensina(1-7), seus análogos peptídicos ou não peptídicos, ou um sal, solvato e/ou hidrato farmaceuticamente aceitável como modulador da resposta inflamatória e/ou analgésica em vertebrados.
[021] Em um aspecto, sendo, portanto, um dos objetos da invenção, são reveladas composições compreendendo agonistas do receptor Mas da Angiotensina (1-7), como alternativa farmacológica e terapêutica no contexto das doenças inflamatórias. Em um aspecto preferencial, as composições da presente invenção são potencialmente úteis no tratamento prevenção ou diagnóstico da artrite reumatóide.
[022] Em outro aspecto, sendo, portanto, outro dos objetos da invenção, é revelado o uso de agonista do receptor Mas da Angiotensina (1-7), como angiotensina(1-7), seus análogos peptídicos ou não peptídicos, ou um sal, solvato e/ou hidrato farmaceuticamente aceitável na preparação de medicamentos úteis para a modulação da resposta inflamatória e/ou analgésica. Em um aspecto preferencial, os efeitos anti-inflamatórios dos agonistas do receptor Mas de angiotensina (1-7), em especial o AVE 0991 inibem importantes parâmetros da resposta inflamatória no modelo de artrite induzida por mBSA. Em um aspecto preferencial, o uso do AVE 0991 proporciona influência sobre a interação in vivo de leucócitos circulantes ao endotélio sinovial da microvasculatura do joelho durante os processos de rolamento e adesão celular no modelo de artrite induzida por mBSA. Em um outro aspecto preferencial, o uso de AVE 0991 proporciona influência sobre a percepção do estímulo de hipernocicepção e sobre a pressão arterial sistólica no modelo de artrite induzida por mBSA.
[023] Estes e outros objetos da presente invenção serão valorizados a partir da descrição detalhada a seguir.
[024] A figura 1 representa a fórmula estrutural do AVE 0991 (podendo também ser referida simplesmente como AVE): 5-formil-4-metoxi-2-fenil- 1[[4-[2-etilaminocarbonilsulfonamido)-5-isobutil-3-tienil]-fenil]-metil]- imidazol.
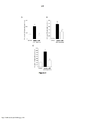
[025] A figura 2 representa o efeito do tratamento com o agonista do receptor de angiotensina (1-7), AVE 0991, na migração de células totais (A), e de neutrófilos para o espaço articular (B) e na migração de neutrófilos para os tecidos periarticulares (C). Os animais foram imunizados com mBSA+adjuvante de Freund e 14 dias depois, desafiados e tratados. O grupo controle não foi desafiado nem recebeu qualquer tratamento, o grupo veículo foi desafiado e recebeu NaCl 0,9% e os grupos AVE 0991 receberam diferentes concentrações do composto: 0,6mg/kg, 3,0 mg/kg e 15mg/kg (i.p.), duas vezes: 30 minutos antes e 6 horas após o desafio (10μL de mBSA). As análises foram realizadas 24 horas após o desafio. Os resultados foram expressos como média ± EPM. (*): médias diferem do grupo veículo e (#): médias diferem do grupo controle. Para ambas as comparações, foi considerado o critério estatístico p<0,05. A análise utilizada foi ANOVA, seguida pelo pós-teste Student-Newman-Keuls.
[026] A figura 3 representa o efeito do tratamento com o agonista do receptor de Angiotensina (1-7), AVE 0991, sobre os níveis de TNF-α, IL- 1β e KC nos tecidos periarticulares de animais submetidos a um modelo de artrite induzida por mBSA. As concentrações das citocinas TNF-α (A), IL-1β (B) e KC (C) foram avaliadas por ELISA (Enzyme Linked Immuno Sorbent Assay). Os animais do grupo controle foram imunizados com mBSA e desafiados com PBS e os animais do grupo tratado foram desafiados e imunizados com mBSA seguido por tratamento com AVE 0991 3mg/kg. Uma dose de 3mg/kg de AVE 0991 foi administrada (i.p.) 30 minutos antes do desfio e outra dose 6 horas após. Os resultados foram expressos como média ± EPM. (*): médias diferem do grupo veículo e (#): médias diferem do grupo controle. Para ambas as comparações, foi considerado o critério estatístico p<0,05. A análise utilizada foi ANOVA, seguida pelo pós-teste Student-Newman-Keuls.
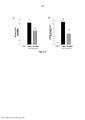
[027] A figura 4 representa o efeito do tratamento com o agonista do receptor de Angiotensina (1-7), AVE 0991, sobre a interação dos leucócitos com o endotélio sinovial de animais submetidos a um modelo de artrite induzida por m BSA. AVE 0991 (3mg/kg, i.p.) ou NaCl (0,9% i.p.) foram administrados 30 minutos antes da avaliação do fluxo sangüíneo sinovial pela técnica de microscopia intravital. O rolamento (A) e a adesão (B) dos leucócitos ao longo do endotélio sinovial foram avaliados 24 horas após o desafio dos animais previamente imunizados com mBSA. Os resultados foram expressos como média ± EPM. (*): médias diferem do grupo veículo (#): médias diferem do grupo controle. Para ambas as comparações, foi considerado o critério estatístico p<0,05. A análise utilizada foi ANOVA, seguida pelo pós-teste Student- Newman-Keuls.
[028] A figura 5 representa o efeito do tratamento com o agonista do receptor de Angiotensina (1-7), AVE 0991, sobre Δ do limiar do estímulo de hipernocicepção, sobre o Δ da pressão arterial sistólica e o índice de acometimento histológico em um modelo de artrite induzida por mBSA. A intensidade de hipernocicepção foi quantificada a partir da utilização do teste de pressão, utilizando-se um anestesiômetro, onde concentrações crescentes de AVE 0991 foram avaliadas: 0,6mg/kg, 3,0mg/kg e 15mg/kg (A). O gráfico B representa a diferença de pressão arterial sistólica resultante da subtração da pressão pré-tratamento (avaliada anteriormente ao desafio) da pressão pós-tratamento (24 horas após o desafio). O método utilizado foi de pletismografia de cauda. O grau de lesão articular foi quantificado a partir da utilização de um índice (C). As articulações foram obtidas 24 horas após o desafio, processadas e coradas com Hematoxilina & Eosina para avaliação microscopica. Uma dose de 3mg/kg de AVE 0991 foi administrada (i.p.) 30 minutos antes do desfio e outra dose 6 horas após. Os animais do grupo controle forma imunizados com mBSA e desafiados com PBS e, os animais do grupo veículo e do grupo tratado com AVE 3mg/kg foram imunizados e desafiados com mBSA. As análises foram realizadas 24 horas após o desafio. Os resultados foram expressos como média ± EPM. (*): médias diferem do grupo veículo (#): médias diferem do grupo controle. Para ambas as comparações, foi considerado o critério estatístico p<0,05. A análise utilizada foi o teste t de Student ou ANOVA, seguida pelo pós- teste Student-Newman-Keuls.
[029] A presente invenção tem como conceito inventivo o uso do AVE 0991 como modulador da resposta inflamatória e/ou analgésica em vertebrados.
[030] São reveladas composições compreendendo AVE 0991, um agonista do receptor Mas da Angiotensina (1-7), como alternativa farmacológica e terapêutica no contexto das doenças inflamatórias. Em um aspecto preferencial, as composições da presente invenção são potencialmente úteis no tratamento curativo ou profilático da artrite reumatóide.
[031] É também revelado o uso de pelo menos um agonista do receptor Mas da Angiotensina (1-7) compreendendo angiotensina(1-7), seus análogos peptídicos ou não peptídicos, ou um sal, solvato e/ou hidrato farmaceuticamente aceitável do mesmo na preparação de medicamentos úteis para a modulação da resposta inflamatória e/ou analgésica. Em um aspecto preferencial, os efeitos anti-inflamatórios do análogo não peptídico, AVE 0991 inibem importantes parâmetros da resposta inflamatória no modelo de artrite induzida por mBSA. Em um aspecto preferencial, o uso do AVE 0991 proporciona influência sobre a interação in vivo de leucócitos circulantes ao endotélio sinovial da microvasculatura do joelho durante os processos de rolamento e adesão celular no modelo de artrite induzida por mBSA. Em um outro aspecto preferencial, o uso de AVE 0991 proporciona influência sobre a percepção do estímulo de hipernocicepção e sobre a pressão arterial sistólica no modelo de artrite induzida por mBSA.
[032] Os exemplos a seguir ilustram, mas não limitam, as formas preferenciais de concretizar a invenção.
[033] Revendo os trabalhos que estudam a implicação do sistema renina-angiotensina com o processo inflamatório local, pôde-se verificar uma expressiva participação desse sistema na regulação da migração de células inflamatórias, na produção e liberação de citocinas e na modulação direta de importantes vias de sinalização intracelular que culminam nas respostas inflamatórias. Estas respostas foram observadas in vivo, nos tecidos renal, cardíaco, pulmonar e vascular, e in vitro, em algumas culturas de células; outros poucos estudos em humanos. São raros os trabalhos avaliando a participação da Ang-(1-7), menos ainda do agonista do seu receptor, o AVE 0991, nos processos inflamatórios. Indiscutivelmente, o papel da Ang II tem sido mais bem explorado e mais bem compreendido. Pode-se dizer, resumidamente, que Ang II tem um efeito pró-inflamatório quando ligada ao seu receptor AT1. Por outro lado, alguns estudos têm avaliado o papel de uma importante enzima envolvida na formação das angiotensinas: ECA 2. Estes estudos demonstram um papel protetor dessa enzima na inflamação. ECA 2 é a principal enzima formadora de Ang-(1-7), logo a melhora dos parâmetros inflamatórios pode ser um efeito indireto da ECA2, possivelmente diretamente relacionado ao aumento da concentração local da Ang-(1-7).
[034] Considerando-se que ECA2-Ang-(1-7)-Mas é o eixo contra- regulatório do SRA, podemos concluir que existem evidências suficientes que sustentem a hipótese de que a ativação do receptor Mas, quer pela Ang-(1-7) quer pelo AVE 0991, seja capaz de exercer efeitos anti- inflamatórios potentes.
[035] O alvo de interesse desta invenção é a artrite reumatóide, doença inflamatória crônica, que acomete uma grande parcela da população, na qual os sintomas evoluem muitas vezes para incapacitação funcional do paciente gerando gastos financeiros altíssimos aos governos. Além disto, os tratamentos disponíveis até a atualidade são bastante limitados e pouco eficientes.
[036] Levando-se em conta o perfil das principais respostas inflamatórias desencadeadas nessa patologia (recrutamento de células inflamatórias associada com a liberação de citocinas para o local da inflamação) somado aos efeitos observados até então a partir da utilização de agentes do SRA, verificamos que há uma coincidência de alvos: migração celular e liberação de citocinas. Há um potencial terapêutico à vista para artrite reumatóide envolvendo o SRA, como verificado recentemente por alguns poucos pesquisadores avaliando modelos animais e também dados em humanos.
[037] O primeiro passo neste sentido foi demonstrar a existência de componentes do SRA no tecido sinovial humano. [ver Walsh et al., J Pharmacol, 112, 435 (1994)] demonstraram aumentos dos níveis de enzima conversora da angiotensina (ECA) e do receptor AT1 em amostras de sinóvia de pacientes com artrite reumatóide. Posteriormente, em um modelo murino de artrite induzido por colágeno, a utilização de inibidores da ECA promoveu benefícios terapêuticos para os animais, diminuindo a inflamação articular [ver Dalbeth et al., Rheumatology, 44(1), 24 (2005)]. Em um estudo mais recente, Price et al., Arthritis & Rheumatism, 56(2),441 (2007), demonstraram que o bloqueio do receptor de Ang II com o antagonista seletivo do receptor AT1, Losartan, atenuou a inflamação de forma dose-dependente em humanos e em modelo animal, ocorrendo diminuição de edema articular e da quantidade de TNF-α local. Não foram encontrados relatos de estudos, em modelos animais ou em humanos, avaliando a participação do eixo ECA2-Ang-(1-7)-Mas na artrite reumatóide. Desta forma, será abordado abaixo o efeito da ativação do receptor Mas através da utilização do agonista não-peptídico, AVE 0991, em um modelo de artrite induzido por mBSA em camundongos, mas sem limitação do escopo de proteção.
[038] Exemplos de testes biológicos. Para avaliação dos efeitos do tratamento in vivo com o AVE 0991 foram utilizados camundongos da linhagem C57BL/6 com idade entre 8-10 semanas. Os procedimentos experimentais foram aprovados pelo respectivo Comitê de Ética.
[039] Camundongos C57BL/6 foram imunizados, através de injeção por via subcutânea (s.c.), com uma emulsão contendo 200μL de volumes iguais de PBS e adjuvante completo de Freund (CFA), na qual foi dissolvida 500 μg de mBSA. No 14° dia após a imunização com mBSA/CFA, os animais foram desafiados com mBSA (10 μg/cavidade) através de injeção intra-articular (articulação fêmur-tibial).
[040] Avaliação da migração de neutrófilos para a cavidade articular. Após 24h do desafio, os camundongos foram anestesiados com uma mistura de cetamina, 150 mg/Kg e xilazina, 10 mg/ Kg e sacrificados. Para avaliar a migração de neutrófilos para a cavidade articular, foi realizado um lavado intra-articular. Este procedimento consistiu em injetar 20μL de uma solução de albumina bovina 3% na cavidade articular, lavando-a três vezes para que uma amostra das células presentes no interior da cavidade fosse coletada juntamente com a solução de albumina recapturada com uma pipeta. Este lavado de células da articular foi diluído em 180 μL de albumina bovina 3% para a posterior contagem total e diferencial dos leucócitos.
[041] Contagem total dos leucócitos. Alíquotas de 30μL do lavado articular foram diluídas em 60μL de solução Turk, sendo a contagem total dos leucócitos realizada em câmara de Neubauer, com o auxílio de microscópio óptico (aumento de 100x) e contador manual. O número total de leucócitos foi utilizado para cálculo da percentagem dos diferentes leucócitos após a contagem em lâminas preparadas por citocentrifugação.
[042] Contagem diferencial dos leucócitos. As lâminas para contagem diferencial foram preparadas por citocentrifugação de uma alíquota de 70μL do lavado articular (citospin; Shandon Lipshaw Inc., Pittsburgh, Pennsylvania, USA). As lâminas foram coradas segundo a técnica de coloração de May-Grumwald e giemsa. As células foram examinadas em microscópio óptico através da objetiva de imersão em óleo (aumento de 1.000x) usando os critérios morfológicos padrões para diferenciar os tipos celulares. Os resultados foram expressos como número de neutrófilos x 104/ cavidade articular.
[043] Atividade da mieloperoxidase (MPO). Para avaliar o acúmulo de neutrófilos no tecido periarticular do joelho, foi utilizado o método de quantificação da atividade de MPO como descrito previamente (DE MATOS e col., 2001). Em suma, o componente residual (pellet) foi ressuspendido em 5% salina EDTA (Buffer 1) submetido à homogeneização e centrifugação (10.000g, 10 minutos). O sobrenadante foi desprezado e o pellet foi ressuspendido em 1,5 mL de NaCl 0.2% gelado e 1,5 mL de NaCl 1.6% com glicose 5% gelada para cada 100 mg de tecido. Realizou-se nova centrifugação 10.000g por 10 minutos. Novamente, o sobrenadante foi descartado e o pellet ressuspendido em tampão fosfato com HETAB (Buffer 2) e re-homogeneizado por 30 segundos. As amostras foram congeladas e descongeladas seguidamente (3 vezes) em nitrogênio líquido, submetidas novamente a centrifugação (10.000g, 15 minutos) e o sobrenadante coletado para ensaio de MPO. As amostras do tecido periarticular foram diluídas três vezes antes do ensaio. Em seguida foram adicionadas as amostras (25μl/poço). Foi adicionado 25μl/poço de tetrametilbenzeno (TMB) a 1,6 mM e incubado a 37°C por 5 minutos, em seguida foi adicionado 100μl/poço de H202 (0,002%) e a reação foi parada com ácido sulfúrico 1M. A atividade da MPO das amostras foi detectada por colorimetria em um leitor de ELISA (450 nm). Os resultados foram expressos como número total de neutrófilos (Unidades Relativas) por comparação da O.D. do sobrenadante do tecido com neutrófilos do pulmão de camundongos processados da mesma maneira.
[044] A Tabela 1 representa os resultados do exemplo 1 que se refere ao efeito do tratamento com o agonista do receptor de Ang-(1-7), AVE 0991 na migração de células para a cavidade e para o tecido periarticular no modelo de artrite induzida por mBSA. Tabela 1 - Efeito do AVE 0991 na migração de células totais para a cavidade articular e, neutrófilos para a cavidade e tecido periarticular no modelo de artrite induzida por mBSA.
[045] Os resultados foram expressos como média ± EPM. (*): médias diferem do grupo veículo e (#): médias diferem do grupo controle. Para ambas as comparações, foi considerado estatístico p<0,05. A análise utilizada foi ANOVA seguida pelo pós-teste Student-Newman-Keuls).
[046] Nos experimentos em questão, os animais imunizados e desafiados com mBSA (10μg/cavidade) apresentaram um expressivo aumento no número total de células inflamatórias para a cavidade articular afetada. Tal aumento não foi alterado pelo tratamento com o agonista do receptor da Ang (1-7), AVE 0991, conforme observado na figura 2A. Entretanto, quando se avaliou especificamente a migração de neutrófilos para a cavidade, verificou-se que o AVE 0991 reduziu, significativamente, o influxo de neutrófilos para o sítio inflamatório nas três concentrações avaliadas, 0,6 mg/kg, 3,0mg/Kg e 15mg/kg (fig. 2B). O mesmo efeito de redução da migração de neutrófilos foi verificado nos tecidos adjacentes à articulação, ocorrendo, no entanto, um efeito dose- dependente em resposta ao uso do AVE 0991 (fig.2C). Os valores foram expressos como média ± erro padrão da média e estão reunidos na tabela 1.
[047] A região da articulação fêmur-tibial foi removida cirurgicamente e dissecada mantendo-se o invólucro muscular. Os espécimes obtidos foram fixados em formol 10% tamponado durante 24 horas. Inicialmente, as amostras foram lavadas em água corrente e desmineralizadas em solução de EDTA 10%, ph 7.2, em temperatura ambiente, por um período de três semanas. Em seguida, as peças foram novamente lavadas em água corrente, desidratadas em banhos de álcool 70%, 80%, 90% e álcool absoluto; diafanizadas em xilol e incluídas em parafina. O material foi seccionado em micrótomo RM2125RT (Leica, Heerbrugg, St. Gallen, Switzerland) obtendo-se cortes consecutivos de 5 Dm, que foram corados pela técnica da Hematoxilina & Eosina (HE).
[048] A avaliação histopatológica da articulação dos animais permitiu quantificar o grau de acometimento da articulação a partir da utilização de score que levava em consideração a ocorrência de hiperplasia sinovial, presença de exudado celular, comprometimento da cartilagem ou de estruturas ósseas e da intensidade do infiltrado sinovial. Através de um índice, pôde-se determinar claramente que as estruturas articulares dos animais tratados com o AVE 0991 na dose de 3 mg/kg apresentaram melhora em relação ao grupo não tratado (Fig. 5A). Intenso infiltrado periarticular e desorganização e hiperplasia sinovial foram observados nas articulações dos animais do grupo veículo quando comparado com os controles. Por outro lado, os animais tratados com 3mg/kg de AVE 0991, apresentaram uma significativa redução do infiltrado inflamatório, bem como uma preservação da sinóvia, apresentando apenas pequenas áreas de hiperplasia focal.
[049] A figura 5 representa os resultados obtidos do exemplo 2 que se refere a análise histopatológica da articulação fêmur-tibial de animais submetidos ao modelo de artrite induzida por mBSA.
[050] Determinação de citocinas por ELISA. O tecido periarticular do joelho foi retirado para realização do ensaio de ELISA e da atividade da mieloperoxidase (MPO). O tecido foi pesado, e em seguida foi colocada a solução de extração de citocinas (1mL da para cada 100mg de tecido). Após homogeneização e centrifugação (10.000g, 10 minutos, 40C). Foi retirado o sobrenadante para o ensaio de ELISA e usado a fração residual decantada para o ensaio de MPO. Os kits para ELISA de camundongo para TNF-α, KC e IL1-β foram obtidos da R&D Systems (DuoSet) e utilizados de acordo com os procedimentos previamente descritos pelo fabricante. Brevemente, as concentrações das citocina e quimiocinas (TNF-α, KC e MIP-2) foram avaliadas no sobrenadante de tecido periarticular diluídas 1:3 em PBS:BSA1%. Em uma placa de 96 poços foram adicionados 100 μl/poço de uma solução contendo concentração adequada do anticorpo captura específico. Essa solução permaneceu em contato com a placa durante 18 h a 4°C. Posteriormente, as placas foram lavadas (4 vezes) com tampão de lavagem (PBS/Tween 0,1%) em um lavador de placas automático. Logo após, foram adicionados 200 μl/poço da solução de bloqueio contendo 1% de albumina de soro bovino em PBS. O tempo de bloqueio foi de no mínimo 1 hora. Em seguida, foram adicionados aos padrões de citocinas em concentração conhecida e as amostras (50μl/ poço). Dezoito horas após a incubação a 4°C, as placas foram lavadas, sendo adicionados 100 μl de uma solução de anticorpo de detecção, seguida de incubação de 1 h. Transcorrido esse período e após lavagem, foi adicionado à placa uma solução contendo estreptavidina ligada à peroxidase R&D Systems (DuoSet). Após 30 min, a placa foi novamente lavada, sendo adicionado o tampão substrato contendo o-fenilenodiamina (OPD, Sigma) e H2O2 (Merck). A reação foi parada com ácido sulfúrico 1M. O produto de oxidação do OPD foi detectado por colorimetria em um leitor de placas de ELISA no comprimento de onda de 492 nm.
[051] Às 24 horas subsequentes ao desafio, os tecidos periarticulares continham elevados níveis de citocinas inflamatórias quando comparados aos animais controle. TNF-α aumentou de 75,50±30,2 pg/100mg de tecido, nos animais controle, para 206,25±25,7 pg/100mg de tecido, no grupo veículo (fig.3A). A quimiocina KC aumentou de 547,70±62,9 pg/100mg de tecido, no grupo controle, para 1836,24±204,6 pg/100mg de tecido, no grupo veículo (fig.3C). Além destas, o nível de IL-1 também foi regulado, aumentou de n.i pg/100mg de tecido, no grupo controle, para 1204±97,7 pg/100mg de tecido, no grupo veículo (fig 3B).
[052] O tratamento com o agonista da Ang-(1-7) foi eficaz em reduziu os níveis das três citocinas avaliadas nos tecidos periarticulares. Os animais tratados com AVE 3mg/kg apresentaram níveis de TNF-α, KC e IL-1β iguais a 49,15±28,5pg/100mg de tecido, 770,08±134,7 pg/100mg de tecido e 591,5±132,2 pg/100mg de tecido, respectivamente.
[053] Um aumento do recrutamento de neutrófilos para a cavidade articular e para os tecidos adjacentes foi verificado, associados a um aumento nos níveis de TNF-α, KC e IL-1β em decorrência da artrite. Além disso, ocorreu uma significativa redução da migração celular e dos níveis destas citocinas após o tratamento com o agonista do receptor de Ang-(1-7), AVE 0991. Estes dados sugerem que as interações dos leucócitos com endotélio vascular sinovial podem estar sendo reguladas.
[054] A figura 3 representa os resultados do exemplo 2 e se refere ao efeito do tratamento com o agonista do receptor de Ang (1-7), AVE 0991, sobre os níveis de TNF-α, IL1-β e KC nos tecidos periarticulares de animas submetidos ao modelo de artrite induzida por mBSA.
[055] A técnica de microscopia intravital foi utilizada com o intuito de visualizar o recrutamento de leucócitos através do endotélio da microvasculatura do joelho de camundongos. Os animais foram anestesiados com uma mistura de xilazina (10mg/kg, Rompun®, Bayer) e Ketamina S+ (200mg/kg, Cristália, SP) e PBS injetada via intraperitoneal (i.p.). A veia da cauda foi canulada para administração de substância fluorescente, Rodamina 6G, reagentes experimentais e volume adicional de anestésico. Para a visualização dos vasos sanguíneos na região do joelho, foi realizada uma ressecção do tendão patelar. Para a avaliação do processo de recrutamento de leucócitos nos vasos do joelho, os animais receberam, inicialmente, uma injeção por via intravenosa de Rodamina 6G (0,3 mg/kg) para marcação dos leucócitos. A Rodamina 6G foi utilizada por sua capacidade de marcar leucócitos, permitindo a visualização destes numa elevada velocidade de fluxo sanguíneo. Um microscópio (Olympus BX40) com objetiva de 20X, foi utilizado para observar os eventos de rolamento e adesão celular na parede dos vasos. Uma câmera de vídeo (Optronics) instalada ao microscópio projetava a imagem em um monitor e as imagens eram, então, gravadas em vídeo-cassete (VHS, Semp Toshiba, modelo x685) para posterior contagem do número de leucócitos em rolamento e aderidos ao longo da parede dos vasos. Foram considerados aderidos os leucócitos que permaneceram estacionados no endotélio vascular por um período mínimo de 30 segundos, e esta adesão foi quantificada pelo número total de células aderentes em 100 m de comprimento da vênula. O rolamento foi considerado para os leucócitos que migravam da região central para a margem do vaso e se moviam a uma velocidade menor que a velocidade dos eritrócitos. Foram avaliados três a quatro vasos sanguíneos por animal e os resultados de rolamento e adesão foram expressos como número de células/min e número de c6lulas/100μm, respectivamente.
[056] Experimentos de microscopia intravital permitiram avaliar in vivo o processo de rolamento e de adesão leucocitária, demonstrando que os camundongos imunizados e desafiados com mBSA (veículos) apresentaram aumentos tanto no número de leucócitos em rolamento quanto no número de leucócitos aderidos ao longo das paredes dos vasos, quando comparado com os camundongos imunizados com mBSA e desafiados com PBS (controles). A utilização do agonista do receptor de Ang-(1-7), AVE 0991, provocou uma expressiva alteração no perfil de interação leucócito-endotélio: ocorreu uma queda de 38% na taxa de rolamento (Fig. 4A) e uma queda de 53% na adesão (Fig. 4B) leucocitária ao longo dos vasos sinoviais, 24 horas após o desafio dos animais previamente imunizados com mBSA
[057] A figura 4 representa os resultados do exemplo 3, relacionando o feito do tratamento com o agonista do receptor de Ang-(1-7), AVE 0991, sobre interação dos leucócitos com o endotélio sinovial de animais submetidos a um modelo de artrite induzida por mBSA.
[058] Os experimentos foram realizados utilizando o teste de pressão com um anestesiômetro eletrônico, que consiste em um transdutor de pressão conectado a um contador digital de força expressa em gramas (g). A precisão do aparelho é de 0,1 g. O aparelho é calibrado para registrar uma força máxima de 150 g, mantendo a precisão de 0,1 g até a força de 80 g. O contato do transdutor de pressão à pata é realizado através de uma ponteira descartável de polipropileno com 0.5 ou 4,15 mm2 de diâmetro adaptada a esse. Os animais são colocados em caixas de acrílico, medindo 12 x 10 x 17 cm cujo assoalho é uma rede de malha igual a 5 mm2 constituída de arame não maleável de 1 mm de espessura, durante 15 minutos antes do experimento para adaptação ao ambiente. Espelhos são posicionados 25 cm abaixo das caixas de experimentação para facilitar a visualização das plantas das patas dos animais. O experimentador deve aplicar, por entre as malhas da rede, uma pressão linearmente crescente no centro da planta da pata do camundongo até que o animal produza uma resposta caracterizada como sacudida (“flinch”) da pata estimulada. Os estímulos são repetidos por até seis vezes, em geral até o animal apresentar 3 medidas similares com uma clara resposta de “flinch” após a retirada da pata. A intensidade de hipernocicepção foi quantificada como a variação na pressão (em gramas) obtida subtraindo-se a média de três valores expressos em gramas (força) observados antes do procedimento experimental (0 hora) da média de três valores em gramas (força) após a administração dos estímulos que variaram conforme o protocolo experimental. Os testes nociceptivos foram realizados entre 08:00 e 16:00 h. Todos os experimentos seguiram as normas e éticas estabelecidas para experimentação com animais conscientes, recomendadas pelo IASP (ZIMMERMANN, 1983).
[059] Para este ensaio em questão os animais foram imunizados e, 14 dias depois, foram desafiados. Antes da imunização, a intensidade da hipernocicepção avaliada. Os animais foram tratados com veículo (NaCl 0,9%) ou com AVE 0991(i.p.), na dose de 3,0mg/kg. Após 30 minutos, foram desafiados com mBSA. Receberam uma nova dose de AVE 0991 3,0 mg/kg 6 horas após o desafio. A intensidade de hipernocicepção dos animais foi novamente avaliada 24 horas do desafio.
[060] A intensidade de hipernocicepção foi quantificada como a variação da pressão (em gramas) obtida a partir da subtração da média de três valores expressos em gramas (força) observados antes do procedimento experimental (0 hora) da média de três valores em gramas (força) 24 horas após o desafio com mBSA.
[061] Avaliação da pressão arterial sistólica por pletismografia de cauda. A avaliação da pressão arterial sistólica (PAS) foi realizada a partir da adaptação de um método não-invasivo muito utilizado (Fuji e cols, 2006; Whitesall e cols, 2004; Krege e cols, 1995). Os camundongos, acordados, foram condicionados a ocuparem um contensor acrílico com temperatura interna constante (37°C) por um período máximo de 5 minutos para cada medida de PAS. Sobre a cauda dos animais, foi acoplado um manguito e um sensor de frequência cardíaca, interligados a um programa de aquisição de dados (XBP1000 Series Rat Blood Pressure Systm - Kent Scientifc, Torrington, CT - USA) onde era possível visualizar a PAS a cada tomada em um monitor. Foram realizadas 3 a 5 tomadas, da PAS, no mínimo, respeitando um intervalo mínimo de 60 segundos entre as tomadas. Para minimizar o estresse causado pela contenção e manipulação do animal durante o procedimento, cada animal era submetido ao procedimento acima pelo menos 5 vezes nos 2 dias que antecederam o início do experimento em questão. Esse período era chamado período de adaptação ao pletismógrafo. Para este ensaio em questão os animais foram imunizados com mBSA, 12 dias após iniciou-se a adaptação dos animais ao plestismógrafo. No 140 dia, realizou-se a medida da PAS dos animais momentos antes do tratamento e desafio. Uma nova medida de PAS foi realizada no dia seguinte, 24h após o desafio. Os dados apresentados foram as variações da pressão arterial sistólica (ΔPAS= PAS final - PAS inicial) e a unidade utilizada foi milímetros de mercúrio (mmHg).
[062] A figura 5 representa os resultados do exemplo 4 que se refere ao efeito do agonista de Ang-(1-7), AVE 0991, sobre a hipernocicepção, sobre a pressão arterial sistólica e índice de acometimento articular no modelo de artrite induzida por mBSA.
[063] Neste ensaio em questão foram associados os elevados níveis de citocinas à consequente migração de neutrófilos para a articulação, e verificou-se a ocorrência de um aumento da variação do limiar do estímulo hipernociceptivo nos animais imunizados e desfiados com mBSA (veículo) quando comparados aos animais imunizados com mBSA e desafiados com PBS (controle): 1,99±0,5 g vs 7,23±0,7 g. Após o tratamento com o agonista do receptor de Ang-(1-7), AVE 0991, houve uma diminuição da hipernocicepção nas três concentrações avaliadas: AVE 0,6 mg/kg, AVE 3 mg/kg e AVE15 mg/kg (4,91±0,6 g, 2,89±0,6g e 2,30±0,5 g, respectivamente) (Fig. 5A).
[064] A pressão arterial sistólica dos animais foi verificada para excluir possíveis ocorrências de uma queda da pressão arterial pós-tratamento que pudesse comprometer a avaliação do limiar de hipernocicepção articular dos animais tratados. Conforme observado na figura 5B, a pressão arterial sistólica dos animais tratados com AVE 3mg/kg no apresentou variação significativa, ou seja, os valores pré-tratamento foram muito semelhantes ao pós-tratamento, gerando uma ΔPAS de - 1,75±7,18 mmHg. Nenhuma diferença foi observada em relação ao grupo controle (ΔPAS=6,71±7,9 mmHg). Este dado foi importante para demonstrar que os efeitos apresentados pelo agonista do receptor de Ang-(1-7), AVE 0991, na concentração de 3mg/kg não alterou a hemodinâmica dos animais no modelo de artrite induzida por BSA.
[065] Análises estatísticas. Os dados foram expressos como a média, erro padrão da média (EPM) de pelo menos 6 animais por grupo. O teste t de Student ou a análise de variância (ANOVA) foram realizados para comparar, respectivamente, dois ou mais grupos experimentais. No caso de observação de significância estatística na ANOVA, foi realizado pós- teste Student-Newman-Keuls. A significância estatística foi ajustada em p<0,05.
[066] Composições contendo AVE 0991 e uso na preparação de medicamento. Para efeitos desta invenção, por "composições farmacêuticas" entende-se toda e qualquer composição que contenha um princípio ativo, com fins profiláticos, paliativos e/ou curativos, e um veículo farmaceuticamente aceitável, dita composição atuando de forma a manter e/ou restaurar a homeostase, podendo ser administrada de forma oral, tópica, parenteral, enteral e/ou intratecal. Os compostos da presente invenção podem ser administrados em forma de dosagem oral, como comprimidos, cápsulas (cada qual inclui a liberação sustentada ou formulações com tempo de liberação), pílulas, pós, granulados, elixires, tinturas, suspensões, xaropes, e emulsões. Eles podem também ser opcionalmente administrados em infusão, intraperitoneal, subcutânea, ou em formas intramusculares, todas utilizando dosagens conhecidas para aqueles com habilidade ordinária que praticam a arte farmacêutica. Eles podem ser administrados sozinhos, mas geralmente serão administrados com um veículo farmaceuticamente aceitável selecionado na base de rota de administração escolhida e da prática farmacêutica padrão. O regime de dosagens para os compostos da presente invenção, naturalmente, variará dependendo de fatores já conhecidos, como as características farmacodinâmicas de um agente particular e modalidade e rota de administração, as espécies, idade, sexo, saúde, condição medica, e peso do receptor, a natureza e extensão dos sintomas; o tipo de tratamento simultâneo; a frequência do tratamento; a rota de administração, a função hepática e renal do paciente/usuário, e o efeito desejado. Por exemplo, as formas orais sólidas preferencialmente contêm, adicionalmente ao princípio ativo, um veículo farmaceuticamente aceitável compreendendo um ou mais diluentes, como por exemplo, lactose, dextrose, sacarose, celulose, amido de milho ou amido de batata; um ou mais lubrificantes, como por exemplo, sílica, talco, ácido esteárico, estearato de magnésio ou de cálcio, ou glicóis de polietileno; um ou mais agentes de ligação (aglutinantes), como, por exemplo, amidos, goma arábica, gelatina, metilcelulose, carboximetilcelulose ou polivinil pirrolidona; um ou mais agentes desagregantes, como, por exemplo, amido, ácido algínico, alginatos ou glicolato de amido de sódio; misturas efervescentes; corantes; açucarados; um ou mais agentes umectantes, como por exemplo, lecitina, polisorbatos, laurilsulfatos; e substâncias inativas farmacologicamente e não-tóxicas usadas comumente em formulações farmacêuticas e amplamente conhecidas dos técnicos em farmacotecnia. As composições da invenção podem ser manufaturadas de forma conhecida, como, por exemplo, por meios de mistura, granulação, prensagem em pastilha, cobertura de açúcar, ou processos de revestimento de filme. As formas líquidas para administração oral podem ser, por exemplo, xaropes, emulsões ou suspensões. Os xaropes podem conter um carreador ou veículo farmaceuticamente aceitável, como por exemplo, sacarose ou sacarose com glicerina e/ou manita (manitol) e/ou sorbitol. As suspensões e as emulsões podem conter um carreador ou veículo farmaceuticamente aceitável, como, por exemplo, uma goma natural, ágar, alginato de sódio, pectina, metilcelulose, carboximetilcelulose ou álcool polivinílico. As formas destinadas a injeções intramusculares podem conter, adicionalmente ao princípio ativo AVE 0991, um carreador ou veículo farmaceuticamente aceitável, como por exemplo, água estéril, óleo de oliva, oleato de etila, glicol de propileno e, uma quantidade apropriada de hidrocloreto de lidocaína. Na presente invenção, as formas orais são preferidas.
[067] Os versados na arte valorizarão os ensinamentos da presente invenção e entenderão que podem ser feitas diferentes formas de concretizar o conceito inventivo, se comparadas com as aqui reveladas exemplificativamente, devendo ser consideradas como dentro do escopo das reivindicações anexas.
Claims (1)
1. USO do agonista do receptor Mas da angiotensina (1-7) AVE 0991, caracterizado por ser para preparar um medicamento para tratamento ou prevenção da artrite reumato ide.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BRPI0902242-2A BRPI0902242B1 (pt) | 2009-06-30 | 2009-06-30 | Uso do agonista do receptor mas da angiotensina (1-7) ave 0991 para tratamento ou prevenção da artrite reumatóide |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BRPI0902242-2A BRPI0902242B1 (pt) | 2009-06-30 | 2009-06-30 | Uso do agonista do receptor mas da angiotensina (1-7) ave 0991 para tratamento ou prevenção da artrite reumatóide |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0902242A2 BRPI0902242A2 (pt) | 2011-03-09 |
| BRPI0902242B1 true BRPI0902242B1 (pt) | 2022-05-10 |
Family
ID=43661629
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0902242-2A BRPI0902242B1 (pt) | 2009-06-30 | 2009-06-30 | Uso do agonista do receptor mas da angiotensina (1-7) ave 0991 para tratamento ou prevenção da artrite reumatóide |
Country Status (1)
| Country | Link |
|---|---|
| BR (1) | BRPI0902242B1 (pt) |
-
2009
- 2009-06-30 BR BRPI0902242-2A patent/BRPI0902242B1/pt active IP Right Grant
Also Published As
| Publication number | Publication date |
|---|---|
| BRPI0902242A2 (pt) | 2011-03-09 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Dalghi et al. | The urothelium: life in a liquid environment | |
| Chen et al. | Angiotensin-(1–7) ameliorates sepsis-induced cardiomyopathy by alleviating inflammatory response and mitochondrial damage through the NF-κB and MAPK pathways | |
| Cunha et al. | Treatment with DF 2162, a non‐competitive allosteric inhibitor of CXCR1/2, diminishes neutrophil influx and inflammatory hypernociception in mice | |
| Shen et al. | Losartan prevents sepsis-induced acute lung injury and decreases activation of nuclear factorκB and mitogen-activated protein kinases | |
| Luo et al. | MCC950 attenuated early brain injury by suppressing NLRP3 inflammasome after experimental SAH in rats | |
| US9808501B2 (en) | Compositions and methods for treating and preventing hyperlipidemia, fatty liver, atherosclerosis and other disorders associated with metabolic syndrome | |
| Napimoga et al. | Lonchocarpus sericeus lectin decreases leukocyte migration and mechanical hypernociception by inhibiting cytokine and chemokines production | |
| Eid et al. | Subacute ghrelin administration inhibits apoptosis and improves ultrastructural abnormalities in remote myocardium post-myocardial infarction | |
| CN110338139B (zh) | 一种痛风动物模型的构建方法及应用 | |
| Grimsholm et al. | Unexpected finding of a marked non-neuronal cholinergic system in human knee joint synovial tissue | |
| Tang et al. | Formononetin attenuates myocardial ischemia/reperfusion injury by regulating neutrophil extracellular traps formation and platelet activation via platelet CD36 | |
| BRPI0716833A2 (pt) | Uso de agonistas de lxr para o tratamento de osteoartrite | |
| Chen et al. | Caspase-12 exhibits non-redundant functions in response to endoplasmic reticulum stress to promote GSDMD-mediated NETosis, leading to thoracic aortic dissection | |
| Lv et al. | Role of G protein coupled receptors in acute kidney injury | |
| CN109152767A (zh) | 用血栓烷-a2受体拮抗剂治疗肌营养不良的组合物和方法 | |
| Tenti et al. | The emerging role of bradykinin in the pathogenesis of osteoarthritis and its possible clinical implications | |
| US6972175B2 (en) | Inhibition of Egr-1 expression by ppar-gamma agonists and related compositions and methods | |
| US10105411B2 (en) | Compositions and methods for modulating AT2R activity | |
| BRPI0902242B1 (pt) | Uso do agonista do receptor mas da angiotensina (1-7) ave 0991 para tratamento ou prevenção da artrite reumatóide | |
| CN101095668B (zh) | 迷迭香酸在制备治疗或预防肝纤维化和肾纤维化的药物中的应用 | |
| Wu et al. | Spatiotemporally targeted nanocapsules combined with mild photothermal therapy regulate the synovial microenvironment in rheumatoid arthritis | |
| US10272133B2 (en) | Compositions and methods for treating and preventing hyperlipidemia, fatty liver, atherosclerosis and other disorders associated with metabolic syndrome | |
| Okechukwu et al. | Evidence that angiotensin II does not directly stimulate the MD2-TLR4 innate inflammatory pathway | |
| Paffoni et al. | Follicular fluid levels of the long pentraxin PTX3 | |
| Choudhary et al. | An indole derivative of Ursolic acid, inhibits RANKL-induced osteoclast differentiation via modulating the Nrf2 and NFATc1/c-Fos axis: Targeting oxidative stress and osteoclastogenesis in managing rheumatoid arthritis |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B03A | Publication of a patent application or of a certificate of addition of invention [chapter 3.1 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B08F | Application dismissed because of non-payment of annual fees [chapter 8.6 patent gazette] | ||
| B08H | Application fees: decision cancelled [chapter 8.8 patent gazette] |
Free format text: ANULADA A PUBLICACAO CODIGO 8.6 NA RPI NO 2469 DE 02/05/2018 POR TER SIDO INDEVIDA. |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] |
Free format text: NOTIFICACAO DE ANUENCIA RELACIONADA COM O ART 229 DA LPI |
|
| B06V | Preliminary requirement: patent application procedure suspended [chapter 6.22 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B08F | Application dismissed because of non-payment of annual fees [chapter 8.6 patent gazette] |
Free format text: REFERENTE A 9A ANUIDADE. |
|
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 30/06/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |
|
| B08H | Application fees: decision cancelled [chapter 8.8 patent gazette] |
Free format text: ANULADA A PUBLICACAO CODIGO 8.6 NA RPI NO 2677 DE 26/04/2022 POR TER SIDO INDEVIDA. |