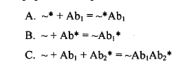CAMPO DA INVENÇÃO
[001] A presente invenção refere-se ao transportador de membrana NaPi2b (SLC34A2) como um alvo em terapia de câncer, incluindo imunoterapia. A invenção adicionalmente se refere à região extracelular de SLC34A2 como um alvo e epítopo específicos em terapia e imunoterapia. A invenção refere-se aos anticorpos e seus fragmentos que se ligam nos mesmos, e particularmente que são direcionados contra o peptídeo de epítopo de aminoácidos de domínio extracelular, particularmente aminoácidos 312 a 340. Composições imunogênicas e anticorpos SLC34A2 da presente invenção também podem ser usados em terapia em combinação com agentes quimioterapêuticos ou de anti-câncer.
FUNDAMENTOS DA INVENÇÃO
[002] Câncer ovariano epitelial é uma das malignidades ginecológicas mais comuns e a quinta causa mais freqüente de morte por câncer em mulheres com uma incidência estimada em cerca de 15.000 em 2006 apenas nos E.U.A. As pacientes apresentam em sua maioria doença avançada e taxa de mortalidade é de aproximadamente 65% da taxa de incidência. Cirurgia citorredutora e quimioterapia de combinação baseada em platina (incluindo taxanos) são as modalidades de tratamento correntes; contudo a maioria dos pacientes com câncer ovariano epitelial recidivo sucumbem à doença. Assim, há uma necessidade de novas modalidades de tratamento em câncer ovariano, terapias selecionadas tal como imunoterapia com anticorpos monoclonais ou abordagens baseadas em vacina contra câncer.
[003] Anticorpo monoclonal MX35 foi gerado de camundongos imunizados com um coquetel de células de carcinoma ovariano de humano preparadas de quatro espécimes cirúrgicos diferentes. Reatividade por imuno- histoquímica com seções de criostato de um painel de tecidos de humano congelados foi usada como os maiores critérios de seleção de hibridoma (1). Mab MX35 mostra reatividade homogênea com aproximadamente 90% dos cânceres ovarianos epiteliais de humano e um número limitado de tecidos normais. Subseqüentemente, a localização e a biodistribuição de anticorpo murino radiomarcado foram estudadas em pacientes com carcinoma ovariano em testes clínicos de fase I. Anticorpo MX35 intacto selecionou bem tumores em pacientes com câncer ovariano (2) e foi mostrado que F(ab)2 de MX35 está localizado em depósitos de carcinoma ovariano micrometastático dentro da cavidade peritoneal (3). Em preparação para o uso do anticorpo para radioimunoterapia, e.g. como um carreador selecionado de radionuclídeos em pacientes com carcinoma ovariano, o anticorpo murino e seus fragmentos estão sendo correntemente investigados em modelos pré-clínicos (4, 5) e em um teste clínico de fase I em pacientes com câncer ovariano como carreador do nuclídeo emissor de partícula alfa astato-211 (6).
[004] Apesar do uso de mAb MX35 em testes clínicos a natureza molecular detalhada do antígeno reconhecido por mAb MX35 ainda não tem sido identificada. Caracterização imunoquímica inicial tem descrito o antígeno de MX35 como uma glicoproteína de superfície celular de 95 kDa com o epítopo antigênico estabilizado por ligações de dissulfeto (7).
[005] A identificação e a caracterização do epítopo e do antígeno de mAb MX35 proporcionariam um alvo para imunoterapia de câncer com anticorpos monoclonais e para outras modalidades de tratamento de câncer, incluindo compostos terapêuticos de câncer controlados e aperfeiçoados, e um marcador reconhecido para propósitos de diagnose e monitoração.
[006] As referências aqui citadas não devem ser entendidas como uma admissão de que elas são a técnica anterior à presente invenção.
SUMÁRIO DA INVENÇÃO
[007] Em um aspecto amplo, a presente invenção fornece um alvo antígeno ou epítopo para terapia de câncer, incluindo imunoterapia. E particular um epítopo de câncer ovariano chave, que também é um alvo terapêutico ou marcador diagnóstico, tem sido identificado. O transportador de membrana, particularmente um transportador de fosfato dependente de sódio (NaPi2b) correspondendo a SLC34A2 tem sido agora identificado como o antígeno reconhecido pelo anticorpo mAb MX35. Em particular, o anticorpo MX35 reconhece e é específico para o epítopo incluído pelos aminoácidos 312-340 de SLC34A2. Anticorpos ou seus fragmentos isolados que reconhecem aminoácidos 312-340 de SLC34A2 são aqui fornecidos. Os anticorpos da invenção reconhecem o epítopo 312-340, que é evidente ou reativo em células tumorigênicas, particularmente células de câncer ovariano, tumores e linhagens de célula. SLC34A2 fornece um alvo terapêutico novo e moderno para câncer, particularmente câncer ovariano.
[008] A identificação do antígeno MX35 como a proteína transportadora de fosfato dependente de sódio 2b (NaPi2b) SLC34A2, agora fornece uma família nova de alvos de superfície celular potenciais para imunoterapia de câncer com anticorpos monoclonais. Mais geralmente, SLC34A2 fornece um alvo para desenvolvimento e seleção de agentes terapêuticos, incluindo compostos de anti-câncer. Ensaios e métodos utilizando e baseados no domínio extracelular de SLC34A2, particularmente aminoácidos 312-340 de região de domínio extracelular ou seus fragmentos, são aqui fornecidos.
[009] Os presentes inventores têm identificado anticorpos monoclonais novos e adicionais, que especificamente reconhecem SLC34A2, e particularmente são reativos com e se ligam no epítopo de aminoácidos 312- 340 de SLC34A2. Em particular, os anticorpos da presente invenção reconhecem um epítopo de SLC34A2 que é encontrado particularmente em células tumorigênicas, incluindo células de câncer ovariano. Os anticorpos da presente invenção são adicionalmente exemplificados pelos anticorpos mAb aqui descritos. Os anticorpos da presente invenção especificamente reconhecem o domínio extracelular de SLC34A2, que inclui os aminoácidos 188-361, e mais particularmente o epítopo incluído em aminoácidos 312-340 de SLC34A2.
[0010] Os anticorpos da presente invenção podem especificamente categorizar a natureza de células, por coloração ou diferentemente reconhecer aquelas células nas quais câncer, incluindo câncer de tiróide, câncer ovariano, câncer de pulmão, câncer de rim, e câncer de mama, particularmente câncer ovariano, está presente. Ademais, os anticorpos da presente invenção, podem ser usados em imunoterapia, imunodiagnóstico, imunosseleção,e vacinas contra câncer para mediação terapêutica e/ou profilática de câncer.
[0011] Em um aspecto preferido, o anticorpo é um que tem as características do anticorpo que os inventores têm identificado e caracterizado, em particular reconhecendo SLC34A2, particularmente direcionado contra ou reativo com os aminoácidos 312-340 de SLC34A2. Em um aspecto particularmente preferido o anticorpo é selecionado de anticorpos MX35, L2(20/3), L3(28/1) ou seus fragmentos ativos, ou anticorpos quiméricos, superficialmente modificados ou humanizados e anticorpos de cadeia única baseados nos mesmos. Em um aspecto particular o anticorpo da presente invenção compreende as seqüências de aminoácidos de região variável de cadeia pesada e de região variável de cadeia leve do anticorpo MX35 mostradas em Figura 5 e Figura 6 respectivamente. Em um outro aspecto um anticorpo derivado de MX35 compreende os domínios CDR de região variável das cadeia pesada e/ou leve como mostrado em Figuras 5 e 6. Em um tal aspecto, um anticorpo da presente invenção compreende uma cadeia pesada e leve, sendo que a região variável de cadeia pesada compreende as seqüências de região CDR SEQ ID NO: 26, 27 e 28, e a região variável de cadeia leve compreende as seqüências de região CDR SEQ ID NO: 31, 32 e 33.
[0012] A invenção fornece vários anticorpos direcionados contra SLC34A2 e capazes de se ligarem em ou de reconhecerem SLC34A2, particularmente aminoácidos 312-340, particularmente o peptídeo SLC34A2 e SEQ ID NO: 8. A seqüência de região variável de MX35 compreendo as regiões CDR SEQ ID NO: 26-28, para a cadeia pesada, e SEQ ID NO: 31-32, serviram como a base para gerar anticorpos adicionais. MX35 superficialmente modificado é aqui fornecido, um tal anticorpo superficialmente modificado exemplar compreendendo a seqüência de região variável de cadeia pesada SEQ ID NO:38 e a seqüência de região variável de cadeia leve SEQ ID NO: 39. MX 35 quimérico é aqui fornecido, um tal anticorpo quimérico exemplar compreendendo a seqüência de região variável de cadeia pesada SEQ ID NO:40 e a seqüência de região variável de cadeia leve SEQ ID NO: 41. Anticorpos de cadeia única têm sido gerados baseado nos anticorpos MX35 quiméricos e superficialmente modificados e são aqui fornecidos. Anticorpo ScFv baseado em MX35 superficialmente modificado é mostrado em FIGURA 16 e tem a seqüência de aminoácidos de SEQ ID NO: 42 e a seqüência de ácido nucleico de SEQ ID NO:43. Anticorpo ScFv baseado em MX35 quimérico é mostrado em FIGURA 17 e tem a seqüência de aminoácidos de SEQ ID NO: 44 e a seqüência de ácido nucleico de SEQ ID NO:45. Anticorpo MX35 humanizado é outro aspecto da invenção e é aqui fornecido. O anticorpo MX35 humanizado exemplar compreende uma seqüência de região variável de cadeia leve SEQ ID NO: 35 e uma seqüência de região variável de cadeia pesada de SEQ ID NO: 37 e é mostrada em FIGURAS 11A e 11B. A região variável de cadeia pesada de MX35 humanizado compreende as regiões CDR mostradas em SEQ ID NO: 26, 27 e 28. A região variável de cadeia leve de MX35 humanizado compreende as regiões CDR como mostrado em SEQ ID NO: 31, 32 e 33.
[0013] Assim, a invenção fornece epítopos de transportador de membrana, particularmente o epítopo incluído em aminoácidos 312-340 de SLC34A2, que pode ser utilizado em geração de anticorpos que têm atividade ou capacidade de anti-tumor ou uso em estimulação uma resposta imunológica que é uma resposta de anti-tumor. A invenção fornece epítopos de transportador de membrana, particularmente epítopos de SLC34A2, principalmente o epítopo incluído em aminoácidos 312-340 de SLC34A2, que pode ser utilizado em geração de aminoácidos que têm atividade ou capacidade de anti-tumor ou uso em estimulação de uma resposta imunológica que é um resposta de anti-tumor. Em um aspecto geral a invenção fornece um epítopo de SLC34A2, particularmente os aminoácidos 312-340 de epítopo de SLC34A2, que é encontrado em células tumorigênicas, particularmente células de câncer ovariano.
[0014] De acordo com a presente invenção, são fornecidos peptídeos SLC34A2, particularmente peptídeos compreendendo aminoácidos 312-340 de SLC34A2, que são capazes de gerar anticorpos, particularmente anticorpos monoclonais, que reconhecem células de câncer ou tumor e têm atividade de anti-tumor e anti-câncer.
[0015] Os peptídeos SLC34A2, particularmente peptídeos compreendendo aminoácidos 312-340 de SLC34A2, da presente invenção fornecem usos diagnósticos e terapêuticos para identificar, caracterizar e selecionar numerosos tipos de tumor, por exemplo, câncer ovariano, de tiróide, de mama, de pulmão, e de rim, particularmente câncer ovariano.
[0016] Em seu aspecto mais amplo, a presente invenção inclui polipeptídeos isolados compreendendo uma seqüência de aminoácidos de um peptídeo SLC34A2, particularmente aminoácidos 312-340 de SLC34A2. Os peptídeos isolados, incluindo combinações de um ou mais dos mesmos, são adequados para uso em geração de anticorpos que reconhecem SLC34A2 e têm atividade de anti-tumor em imunização de animais, particularmente mamíferos, mais particularmente humanos, que têm doença de câncer ou tumor.
[0017] A presente invenção é direcionada a um polipeptídeo receptor isolado que compreende a seqüência de aminoácidos mostrada em qualquer uma de SEQ ID NOS: 1-8 e seus fragmentos imunogênicos.
[0018] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos INVTVPSTANCTSPSLCWTDGIQNWTMKN (SEQ ID NO: 1).
[0019] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos INVTVPSTANATSPSLCWTDGIQNWTMKN (SEQ ID NO: 2).
[0020] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos INVTVPSTANCTSPSLAWTDGIQNWTMKN (SEQ ID NO: 3).
[0021] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos INVTVPSTANATSPSLAWTDGIQNWTMKN (SEQ ID NO: 4).
[0022] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos PSTANCTSPSLCWTDGIQNWTMKN (SEQ ID NO: 5).
[0023] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos ANCTSPSLCWTDGIQNWTMKN (SEQ ID NO: 6).
[0024] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos TSPSLCWTDGIQNWTMKN (SEQ ID NO: 7).
[0025] A invenção fornece um peptídeo isolado tendo a seqüência de aminoácidos SPSLCWTDGIQNWTM (SEQ ID NO: 8).
[0026] A presente invenção se estende a um peptídeo receptor imunogênico, particularmente selecionado de qualquer uma de SEQ ID NOS: 1-8, ou um seu fragmento imunogênico. A presente invenção também se estende aos peptídeos receptores imunogênicos sendo que tais polipeptídeos compreendem uma combinação de pelo menos um peptídeo receptor imunogênico, selecionado de qualquer uma de SEQ ID NOS: 1-8, ou seu fragmento de peptídeo imunogênico.
[0027] A invenção fornece um método para imunizar um mamífero compreendendo administrar um peptídeo de epítopo de SLC34A2 ou um seu fragmento imunogênico, por meio do qual são produzidos anticorpos que são imunorreativos com o peptídeo de epítopo exposto sobre as células expressando receptor de fator de crescimento anormal ou sobre-expressado, mas não exposto sobre células de tipo selvagem. A invenção adicionalmente fornece um método para imunizar um mamífero compreendendo administrar um peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8 ou um seu fragmento imunogênico, por meio do qual são produzidos anticorpos que são imunorreativos com células de câncer, particularmente células de câncer ovariano. A invenção fornece um método para imunizar um mamífero compreendendo administrar um peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8 ou um seu fragmento imunogênico, por meio do qual são produzidos anticorpos que são imunorreativos com domínio extracelular de SLC34A2 e SLC34A2 sobre células.
[0028] Em um outro aspecto, a presente invenção se estende às vacinas e composições imunogênicas baseadas nos peptídeos receptores aqui descritos. A presente invenção fornece uma vacina compreendendo um ou mais peptídeos SLC34A2, particularmente aminoácidos 312-340 de SLC34A2, incluindo selecionados de qualquer uma das EQ ID NOS: 1-8, e um adjuvante farmaceuticamente aceitável. A presente invenção fornece uma vacina compreendendo um ou mais peptídeos selecionados de qualquer uma de SEQ ID NOS: 1-8, e um adjuvante farmaceuticamente aceitável. A presente invenção fornece uma composição imunogênica compreendendo um ou mais peptídeos de LC34A2 selecionados de qualquer uma de SEQ ID NOS: 1-8, e um adjuvante farmaceuticamente aceitável. A presente invenção fornece uma composição imunogênica compreendendo um ou mais peptídeos selecionados de qualquer uma de SEQ ID NOS: 1-8, e um adjuvante farmaceuticamente aceitável.
[0029] A presente invenção adicionalmente fornece uma vacina de anti-câncer ou anti-tumor compreendendo um ou mais peptídeos SLC34A2 selecionados do grupo de SEQ ID NOS: 1-8, adicionalmente compreendendo um ou mais antígenos de tumor adicionais. A presente invenção adicionalmente fornece uma vacina de anti-câncer ou tumor compreendendo um ou mais peptídeos SLC34A2, particularmente um peptídeo correspondendo aos aminoácidos 312-340 de SLC34A2 ou seus fragmentos, particularmente selecionados do grupo de qualquer uma de SEQ ID NOS: 1-8. A composição pode adicionalmente compreender um ou mais antígenos adicionais de SLC34A2 ou outros antígenos de tumor.
[0030] Em outro aspecto, a invenção é direcionada a uma vacina para tratamento de um mamífero, particularmente um sujeito humano sofrendo de câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano, incluindo compreendendo uma quantidade imunogênica de um ou mais peptídeos SLC34A2, particularmente compreendendo aminoácidos 312-340 de SLC34A2 selecionados do grupo de qualquer uma de SEQ ID NOS: 1-8 ou seu fragmento imunogênico. Uma tal vacina pode conter o peptídeo e um adjuvante farmaceuticamente aceitável. Uma tal vacina adicionalmente contém o peptídeo conjugado em um carreador.
[0031] Em outro aspecto, a invenção é direcionada a uma vacina para tratamento de um mamífero, particularmente um sujeito humano sofrendo de câncer ovariano, particularmente câncer ovariano epitelial, particularmente carcinomas serosos papilares e tumores endometriais de grau baixo, incluindo compreendendo uma quantidade imunogênica de um ou mais peptídeos SLC34A2, particularmente compreendendo aminoácidos 312-340 de SLC34A2 selecionados do grupo de qualquer uma de SEQ ID NOS: 1-8 ou seu fragmento imunogênico. Uma tal vacina pode conter o peptídeo e um adjuvante farmaceuticamente aceitável. Uma tal vacina adicionalmente contém o peptídeo conjugado em um carreador.
[0032] A invenção fornece composições farmacêuticas compreendendo um peptídeo SLC34A2, particularmente peptídeos de aminoácidos 312-340, um carreador farmaceuticamente aceitável. A invenção fornece composições farmacêuticas compreendendo um peptídeo SLC34A2 selecionado de um ou mais peptídeos selecionados de qualquer uma de SEQ ID NOS: 1-8, um carreador farmaceuticamente aceitável. A invenção fornece composições farmacêuticas compreendendo um anticorpo para peptídeo SLC34A2 e um carreador farmaceuticamente aceitável. A invenção fornece composições farmacêuticas compreendendo um anticorpo para peptídeo SLC34A2 imunorreativo com um ou mais peptídeos selecionados de qualquer uma de SEQ ID NOS: 1-8, um carreador farmaceuticamente aceitável. A invenção adicionalmente fornece uma composição farmacêutica compreendendo uma combinação de pelo menos dois anticorpos para peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8 e um carreador farmaceuticamente aceitável.
[0033] Em ainda um outro aspecto, a presente invenção fornece um anticorpo purificado para um peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8.
[0034] Anticorpos contra os polipeptídeos isolados da presente invenção incluem os anticorpos naturalmente produzidos e recombinantemente preparados ou seus fragmentos, incluindo variantes de cadeia única e Fv. Estes podem incluir ambos anticorpos monoclonais e policlonais preparados por técnicas genéticas conhecidas, bem como anticorpos bi-específicos, e anticorpos incluindo outras funcionalidades adequando-os para uso diagnóstico e terapêutico. Os anticorpos incluem anticorpos quiméricos, anticorpos superficialmente modificados, anticorpos humanizados, anticorpos de domínio, anticorpos calemizados e anticorpos de cadeia única. Tais anticorpos podem ser usados em imunoensaios para caracterizar tumores ou diagnosticar câncer incluindo, mas não limitado a câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano. Os anticorpos também podem ser usados para imunização passiva para reduzir tumores ou tratar câncer incluindo, mas não limitado a, câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano.
[0035] Um anticorpo para um peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8 marcado com um marcador detectável é adicionalmente fornecido. Em modalidades particulares, o marcador pode ser selecionado do grupo consistindo de uma enzima, um agente químico que manifesta fluorescência, e um elemento radioativo. Na situação aqui um mαTY'αrlAT1 AZA lol AC ICÀÍAAAC3^J 14^^ 32^) 35 O 36^^1 51 57 58Co, 59Fe, 86Y, 90Y, 124I, 125I, 131I, 111I , 99Tc e 186Re são usados, procedimentos de contagem conhecidos correntemente disponíveis podem ser utilizados. No caso onde o marcador é uma enzima, detecção pode ser realizada por qualquer uma das técnicas colorimétrica, espectrofotométrica, fluoroespectrométrica, amperométrica ou gasométrica conhecidas na técnica.
[0036] Em uma outra modalidade, a presente invenção refere-se a certos métodos terapêuticos que seriam baseados na atividade de um anticorpo, ou seus fragmentos ativos, para um peptídeo SLC34A2 selecionadode qualquer uma de SEQ ID NOS: 1-8, ou em agentes ou outras drogas determinados para modular SLC34A2 por ligação em ou interação com o peptídeo SLC34A2. Um primeiro método terapêutico está associado com a prevenção ou o tratamento de câncer, incluindo mas não limitado a câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano.
[0037] Em particular, os anticorpos da presente invenção, ou seus fragmentos ativos, e anticorpos quiméricos ou sintéticos derivados dos mesmos podem ser preparados em composições farmacêuticas, incluindo um veículo, portador ou diluente adequado, para administração em casos nos quais terapia é apropriada, tal como para tratar câncer. Tais composições farmacêuticas também podem incluir métodos de modular a meia-vida dos membros de ligação, anticorpos ou fragmentos por métodos conhecidos na técnica tal como peguilação. Tais composições farmacêuticas podem adicionalmente compreender anticorpos ou agentes terapêuticos adicionais.
[0038] A presente invenção também inclui anticorpos para um peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8, e quaisquer de seus fragmentos, que são covalentemente ligados em ou diferentemente associados com outras moléculas ou agentes a serem usados para propósitos terapêuticos ou diagnósticos. Estas outras moléculas ou agentes incluem, mas não são limitados a, moléculas (incluindo outros anticorpos ou fragmentos de anticorpo) com distintas características, toxinas, ligantes, isótopos radioativos e agentes quimioterapêuticos. Dentro da técnica há muitas moléculas ou agentes bem conhecidos que têm sido covalentemente ligados ou diferentemente associados para serem usados paras propósitos terapêuticos. Exemplos de tais moléculas ou agentes incluem, mas não são limitados a: toxinas tais como caliqueamicina, maitansinoide, duocarmicina, ricina, toxina de difteria e exotoxina de Pseudomonas; ligantes tal como fator de necrose de tumor (TNF); isótopos radioativos tais como 90Y, 125I, 131I, 211At, 225Ac, 213Bi e outro isótopo emissor de partículas α, β ou y; e drogas quimioterapêuticas tais como paclitaxel (Taxol®) e doxorubicina (Adriamycin®).
[0039] A presente invenção contempla o uso de peptídeos receptores e anticorpos para os mesmos da presente invenção em testes e métodos diagnósticos para determinar e/ou monitorar tumores e câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano.
[0040] A presente invenção refere-se às vacinas de ácido nucleico ou vacinas de DNA compreendendo ácidos nucleicos codificadores de peptídeos SLC34A2, particularmente selecionados de qualquer uma de SEQ ID NOS: 18. A presente invenção refere-se às vacinas de ácido nucleico ou vacinas de DNA compreendendo ácidos nucleicos codificadores de um ou mais peptídeos imunogênicos de SLC34A2 selecionados de qualquer uma de SEQ ID NOS: 1-8 com pelo menos um outro polipeptídeo, particularmente um antígeno de tumor ou peptídeo de molécula imunomodulatória.
[0041] A presente invenção inclui métodos para determinar e monitorar tumores e câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano por detecção da presença ou exposição de um peptídeo SLC34A2 selecionado do grupo de qualquer uma de SEQ ID NOS: 1-8. Em um tal método particular, o peptídeo SLC34A2 é medido por: a.contato de uma amostra na qual a presença ou exposição de um peptídeo SLC34A2 selecionado do grupo de qualquer uma de SEQ ID NOS: 1-8 é suspeito com um anticorpo para o dito peptídeo SLC34A2 sob condições que permitem a ocorrência da ligação do peptídeo no anticorpo; e b.detecção de se a ligação tem ocorrido entre o peptídeo SLC34A2 da amostra e o anticorpo; sendo que a detecção de ligação indica a presença ou exposição do peptídeo SLC34A2 na amostra.
[0042] Este método pode incluir o contato da amostra com um anticorpo selecionado de anticorpo MX35, um anticorpo tendo uma cadeia pesada e uma cadeia leve sendo que a região variável de cadeia pesada compreende CDRs de SEQ ID NO: 26, 27 e 28 e a região variável de cadeia leve compreende CDRs de SEQ ID NO: 31, 32 e 33, anticorpo MX35 humanizado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 37 e uma região variável de cadeia leve de SEQ ID NO: 35, anticorpo MX35 superficialmente modificado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 38 e uma região variável de cadeia leve de SEQ ID NO: 39, anticorpo MX35 quimérico compreendendo uma região variável de cadeia pesada de SEQ ID NO: 40 e uma região variável de cadeia leve de SEQ ID NO: 41, anticorpo Fv de cadeia única tendo a seqüência de SEQ ID NO: 42 ou SEQ ID NO: 44.
[0043] A invenção inclui um sistema de ensaio para triagem de compostos potenciais eficazes para modular o SLC34A2 por ligação, interação com ou diferentemente modular o peptídeo SLC34A2 da presente invenção. Em um caso, o composto de teste, ou um extrato contendo o composto, poderia ser administrado a uma amostra celular expressando o peptídeo particular de SLC34A2 para determinar o efeito do composto sobre SLC34A2 ou, o peptídeo SLC34A2 da presente invenção ou a atividade de SLC34A2 por comparação com um controle.
[0044] Ainda um outro objetivo da presente invenção é fornecer um método para o tratamento de mamíferos sofrendo de tumores ou câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano. A invenção fornece um método para o tratamento de mamíferos sofrendo de tumores ou câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano compreendendo administrar uma dose imunogenicamente eficaz de uma vacina compreendendo um peptídeo SLC34A2 selecionado do grupo de qualquer uma de SEQ ID NOS: 1 -8 a um sujeito.
[0045] Em um outro aspecto a invenção fornece um método de tratamento ou diagnose de câncer ovariano, particularmente de tumores ovarianos endometrióides e serosos papilares. A invenção fornece um método para o tratamento de mamíferos sofrendo de tumores ovarianos endometrióides e serosos papilares compreendendo administrar uma dose imunogenicamente eficaz de uma vacina compreendendo um peptídeo SLC34A2 selecionado do grupo de qualquer uma de SEQ ID NOS: 1-8 a um sujeito. A invenção fornece um método para o tratamento de mamíferos sofrendo de tumores ovarianos endometrióides e serosos papilares compreendendo administrar um anticorpo para SLC34A2 selecionado de anticorpo MX35, um anticorpo tendo uma cadeia leve e uma cadeia pesada sendo que a região variável de cadeia pesada compreende CDRs de SEQ ID NO: 26, 27 e 28 e a região variável de cadeia leve compreende CDRs de SEQ ID NO: 31,32 e 33, anticorpo MX35 humanizado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 37 e uma região variável de cadeia leve de SEQ ID NO: 35, anticorpo MX35 superficialmente modificado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 38 e uma região variável de cadeia leve de SEQ ID NO: 39, anticorpo MX35 quimérico compreendendo uma região variável de cadeia pesada de SEQ ID NO: 40 e uma região variável de cadeia leve de SEQ ID NO: 41, anticorpo Fv de cadeia única tendo a seqüência de SEQ ID NO: 42 ou SEQ ID NO: 44.
[0046] Em um outro aspecto, a invenção fornece um método de induzir uma resposta imune em um sujeito que tem tumores ou câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano compreendendo administrar ao sujeito uma quantidade da composição farmacêutica compreendendo um peptídeo SLC34A2 selecionado do grupo de qualquer uma de SEQ ID NOS: 1-8, um carreador farmaceuticamente aceitável, induzindo deste modo uma resposta imune.
[0047] Um objetivo adicional da presente invenção é fornecer um método para o tratamento de mamíferos sofrendo de tumores ou câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano. A invenção fornece um método para o tratamento de mamíferos sofrendo de tumores ou câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano, particularmente câncer ovariano epitelial, compreendendo administrar ao dito mamífero uma quantidade terapeuticamente eficaz de um anticorpo para SLC34A2 selecionado de anticorpo MX35, um anticorpo tendo uma cadeia pesada e uma cadeia leve sendo que a região variável de cadeia pesada compreende CDRs de SEQ ID NO: 26, 27 e 28 e a região variável de cadeia leve compreende CDRs de SEQ ID NO: 31, 32 e 33, anticorpo MX35 humanizado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 37 e uma região variável de cadeia leve de SEQ ID NO: 35, anticorpo MX35 superficialmente modificado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 38 e uma região variável de cadeia leve de SEQ ID NO: 39, anticorpo MX35 quimérico compreendendo uma região variável de cadeia pesada de SEQ ID NO: 40 e uma região variável de cadeia leve de SEQ ID NO: 41, e anticorpo Fv de cadeia única tendo a seqüência de SEQ ID NO: 42 ou SEQ ID NO: 44.
[0048] A invenção fornece um método para o tratamento de mamíferos sofrendo de tumores ou câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano, particularmente câncer ovariano epitelial, compreendendo administrar ao dito mamífero uma quantidade terapeuticamente eficaz de um anticorpo para SLC34A2 selecionado de um anticorpo tendo uma cadeia pesada e uma cadeia leve sendo que a região variável de cadeia pesada compreende CDRs de SEQ ID NO: 26, 27 e 28 e a região variável de cadeia leve compreende CDRs de SEQ ID NO: 31, 32 e 33, anticorpo MX35 humanizado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 37 e uma região variável de cadeia leve de SEQ ID NO: 35, anticorpo MX35 superficialmente modificado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 38 e uma região variável de cadeia leve de SEQ ID NO: 39, anticorpo MX35 quimérico compreendendo uma região variável de cadeia pesada de SEQ ID NO: 40 e uma região variável de cadeia leve de SEQ ID NO: 41, e anticorpo Fv de cadeia única tendo a seqüência de SEQ ID NO: 42 ou SEQ ID NO: 44.
[0049] A invenção fornece um método para inibir transporte de fosfato em células de um mamífero compreendendo administrar ao dito paciente uma quantidade eficaz de um anticorpo para SLC34A2. Em um aspecto particular o anticorpo é selecionado de um anticorpo tendo uma cadeia pesada e uma cadeia leve sendo que a região variável de cadeia pesada compreende CDRs de SEQ ID NO: 26, 27 e 28 e a região variável de cadeia leve compreende CDRs de SEQ ID NO: 31, 32 e 33, anticorpo MX35 humanizado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 37 e uma região variável de cadeia leve de SEQ ID NO: 35, anticorpo MX35 superficialmente modificado compreendendo uma região variável de cadeia pesada de SEQ ID NO: 38 e uma região variável de cadeia leve de SEQ ID NO: 39, anticorpo MX35 quimérico compreendendo uma região variável de cadeia pesada de SEQ ID NO: 40 e uma região variável de cadeia leve de SEQ ID NO: 41, e anticorpo Fv de cadeia única tendo a seqüência de SEQ ID NO: 42 ou SEQ ID NO: 44. Em um aspecto do método transporte de fosfato é inibido em células incluindo células ovarianas, células de rim, células de pulmão, células de tiróide, células de mama, particularmente células ovarianas, particularmente células epiteliais ovarianas.
[0050] A ligação de um anticorpo em seu antígeno alvo é mediada através da região variável, particularmente as regiões determinantes de complementaridade (CDRs) de suas cadeias pesada e leve. Conformemente, os membros de ligação específica baseados na região variável, particularmente as regiões CDR da cadeia pesada ou leve, e preferivelmente de ambas, de mAb MX35 serão membros de anticorpo úteis para terapia in vivo. As região variável e CDRs do anticorpo mAb MX35 são mostradas em Figuras 5 e 6. As CDRs de cadeia pesada correspondem às SEQ ID NOS: 2628 e as CDRs de cadeia leve correspondem às SEQIDNOS: 31-33.
[0051] Em outros aspectos, a invenção fornece um ácido nucleico isolado que compreende uma seqüência codificadora de um anticorpo ou seu fragmento como definido acima, e métodos de preparar anticorpos da invenção que compreendem expressar ditos ácidos nucleicos sob condições para causar a expressão de dito anticorpo, e recuperar o anticorpo.
[0052] Outros objetivos e vantagens se tornarão evidentes para aquelas pessoas experientes na técnica a partir de uma revisão da seguinte descrição detalhada, que procede com referência aos seguintes desenhos ilustrativos, e as reivindicações anexadas.
DESCRIÇÃO BREVE DOS DESENHOS
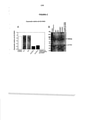
[0053] FIGURA 1: Antígeno MX35 expressado em superfície de célula foi isolado de duas linhagens de células diferentes positivas para antígeno MX35, OVCAR-3 e SK-RC-18 por imunoprecipitação após marcação metabólica de proteínas com 35S metionina e 35S cisteína. (A) SDS- PAGE de complexos imunes de MX35 marcados com 35S e visualizados por autorradiografia ou por coloração de prata. MAb MX35 precipitou o antígeno em duas formas, bandas #1 e #2, diferindo em tamanho; (B) impressão digital de massa de peptídeo de proteína sulfonada e marcada com lisina digerida com tripsina; (C) Seqüência da proteína transportadora de fosfato dependente de sódio 2b. Peptídeos detectados por espectrometria de massa são mostrados em negrito. A alça ligada por dissulfeto putativa (aa 303-350) também é mostrada. A região contendo o epítopo reconhecido por mAb MX35 é mostrada em itálico. Resíduos de asparagina(N) que são prováveis sítios de glicosilação N-ligada são mostrados em letras maiúsculas.
[0054] FIGURA 2: Efeitos de interferência de siRNA sobre o nível de expressão de SLC34A2 mRNA e de proteína MX35 em células SK-RC-18. Células são transfectadas com SLC34A2 siRNA ou siRNA de controle na presença de Lipofectamine 2000. Células são ensaiadas 72 horas após a transfecção. (A) RNA total foi extraído e níveis de SLC34A2 mRNA foram determinados por RT-PCR de tempo real. (B) Células são lisadas e o nível de expressão de proteína foi analisado por SDS-PAGE e Western blotting usando mAb MX35 e um anticorpo anti-actina.
[0055] FIGURA 3: (A) Diagrama esquemático da topologia de membrana predita da proteína transportadora de fosfato dependente de sódio 2b; (B) Apresentação esquemática da proteína NaPi2b e das proteínas de fusão derivadas da região extracelular potencialmente maior aa188-361 e a localização do epítopo de MX35; (C) Proteínas de fusão de NaPi2b expressadas em bactérias e borradas por imuno-mancha ("immunoblotted") com MAb MX35 após separação por SDS-PAGE.
[0056] FIGURA 4: Caracterização bioquímica de antígeno de NaPi2b/MX35. Precipitações imunes de MAb MX35 dos lisados de célula SK-RC-18 metabolicamente marcados separados por SDS-PAGE sob condições redutoras e visualizados por autorradiografia. (A) Análise por desglicosilação enzimática de complexos imunes marcados com 35S analisados; (B) Análise por desglicosilação enzimática de complexos imunes derivados de células marcadas com 3H-glicosamina; (C) Análise por acilação de complexos imunes de células marcadas com 3H -palmitato.
[0057] FIGURA 5 mostra as seqüências de nucleotídeos e de aminoácidos da região variável de cadeia pesada de anticorpo MX35, incluindo os domínios de CDR: CDR1, CDR2, e CDR3.
[0058] FIGURA 6 mostra as seqüências de nucleotídeos e de aminoácidos da região variável de cadeia leve de anticorpo MX35, incluindo os domínios de CDR: CDR1, CDR2, e CDR3.
[0059] FIGURA 7 mostra análise por SDS-PAGE de proteínas de fusão GST/NaPi2b bacterialmente expressadas e purificadas por afinidade. (A)Análise de expressão e purificação de GST/NaPi2b-L de fração insolúvel de lisado de célula bacteriana. Expressão de GST/NaPi2b-L em células BL21(DE3) foi induzida por IPTG por 3 horas a 27°C. A pelota de células bacterianas foi lisada e centrifugada para remover a fração insolúvel. Purificação de GST/NaPi2b-L da fração insolúvel foi realizada por eletroeluição do gel de SDS-PAGE. (B), (C). Perfis de expressão e qualidade de GST/NaPi2b-1L purificada por afinidade (188-300aa) (B) e GST/NaPi2b- 2L (291-361aa) (C) analisadas por eletroforese SDS-PAGE. A expressão de GST/NaPi2b-1L e GST/NaPi2b-2L foi induzida por IPTG por 1, 2 e 3 horas. Células colhidas foram lisadas e centrifugadas a 13.000 rpm para remover a fração insolúvel. O extrato de proteínas solúveis foi usado para purificação por cromatografia de afinidade em Glutathione Sepharose.
[0060] FIGURA 8 mostra análise por Western blot (A) e imunoprecipitação (B) de NaPi2b transientemente expressada e endógena. (A) Reconhecimento específico de NaPi2b endógena pelos anticorpos gerados em análise por Western blot. Lisados de célula totais (10 μg) de linhagens de célula OVCAR3, SKRC18 e SKRC01 foram separados por SDS-PAGE sob condições não-redutoras (sem DTT) e sondadas com anticorpos monoclonais gerados. (B). Imunoprecipitação de myc-NaPi2b transientemente sobre- expressada. Células Hek293 foram transientemente transfectadas com pcDNA3.1/myc-NaPi2b. Os sobrenadantes de células transfectadas foram incubados com Protein A Sepharose contendo IgGs de clones de hibridoma L2(2/1), L2(20/3), L3(28/1). Os complexos imunes foram resolvidos por SDS-PAGE e borrados por imuno-mancha com L2(20/3) MAb.
[0061] FIGURA 9 fornece análise por imuno-histoquímica de tecidos ovarianos com NaPi2b/(20/3) e NaPi2b/(28/1) MAb. Coloração imuno- histoquímica de seções embebidas em parafina de ovário normal e carcinoma ovariano com anticorpos L2(20/3) (A) e L3(28/1) (B).
[0062] FIGURA 10 mostra o mapeamento de epítopo para anticorpos monoclonais anti-NaPi2b. (A) Representação esquemática de proteínas de fusão GST/NaPi2b usadas neste estudo. A região de NaPi2b que possui os epítopos para anticorpos gerados está marcada e mostrada por seqüência de aminoácidos. (B) Análise por Western-blot de GST apenas e de proteínas de fusão GST/NaPi2b com L2(20/3) e anticorpos monoclonais anti-GST. Quantidades iguais de GST apenas ou várias proteínas de fusão GST/NaPi2b (2 μg cada) foram resolvidas por SDS-PAGE, eletro-borradas sobre membrana de PVDF e sondadas com L2(20/3) e anticorpos monoclonais antiGST.
[0063] FIGURA 11 mostra um alinhamento de seqüências de aminoácidos de regiões variáveis de cadeia pesada (A) e cadeia leve (B) das versões murina e humanizada de anticorpo MX35. Regiões CDR estão dentro de retângulos.
[0064] FIGURA 12 fornece análise por citometria de fluxo avaliando a ligação do anticorpo MX35 humanizado em células OVCAR-3 de carcinoma ovariano. Resultados são comparados com aqueles obtidos com "células sozinhas", "controle murino FITC-conjugado", controles "MX35 murino" e "Zenapax®".
[0065] FIGURA 13 fornece análise por citometria de fluxo avaliando a ligação do anticorpo MX35 humanizado em células SK-RC-18 de carcinoma renal. Resultados são comparados com aqueles obtidos com "células sozinhas", "controle murino FITC-conjugado", controles "MX35 murino" e "Zenapax®".
[0066] FIGURA 14 fornece análise por citometria de fluxo avaliando a ligação do anticorpo MX35 humanizado em células SW626, derivadas de uma metástase ovariana (tumor primário está em cólon). Resultados são comparados com aqueles obtidos com "células sozinhas", "controle murino FITC-conjugado", controles "huH3S193", "MX35 murino" e "Zenapax®".
[0067] FIGURA 15 fornece análise por citometria de fluxo avaliando a ligação do anticorpo MX35 humanizado em células LoVo de carcinoma colorretal. Resultados são comparados com aqueles obtidos com "células sozinhas", "controle murino FITC-conjugado", controles "huH3S193", "MX35 murino" e "Zenapax®".
[0068] FIGURA 16 mostra a seqüência de ácido nucleico (SEQ ID NO: 43) e seqüência de aminoácidos (SEQ ID NO: 42) de anticorpo Fv de cadeia única baseada no MX35 superficialmente modificado (VMX35 ScFv #6). A seqüência de sinal é mostrada primeiro em preto; a cadeia pesada variável está a seguir em verde; segue a região de ligador em vermelho; a cadeia leve variável é mostrada a seguir em azul; e as últimas seqüências são a etiqueta-E, mostrada em vermelho.
[0069] FIGURA 17 mostra a seqüência de ácido nucleico (SEQ ID NO: 45) e seqüência de aminoácidos (SEQ ID NO: 44) de anticorpo Fv de cadeia única baseado em MX35 quimérico MX35 (chMX35 ScFv #8). A primeira seção de seqüência mostrada em preto é a seqüência de sinal; seguida pela seqüência de cadeia pesada variável em verde; a região de ligador em vermelho é mostrada a seguir; a cadeia leve variável segue em azul; e a última seqüência me vermelho é a etiqueta-E.
[0070] FIGURA 18 mostra os resultados de ELISA de anticorpo de cadeia única recombinante MX35 mostrando diluições de MX35, MX35 ScFv superficialmente modificado e MX35 ScFv quimérico versus peptídeo MX35, ou com peptídeo de controle negativo ou uma placa bloqueada.
[0071] FIGURE 19 mostra absorbância a 450 nm de ELISA de MX35 de controle, MX35 ScFv superficialmente modificado ou MX35 ScFv quimérico versus peptídeo MX35, peptídeo irrelevante, e sem peptídeo.
[0072] FIGURA 20 mostra um borrão de manchas de anticorpos MX35, L2, L3 e controle G250 versus peptídeo S2L34AZ, incluindo 312-340 de tipo selvagem e 312-340 T330M.
[0073] FIGURA 21 fornece uma representação esquemática de organização de domínio de Napi2b e a localização de substituição T330V, deleção de aa 6 e 59.
[0074] FIGURA 22 mostra a expressão de formas de tipo selvagem e mutante de NaPi2b em células HEK293 estavelmente transfectadas. A. Análise WB de lisados de células HEK293 com: anticorpo anti-etiqueta-EE (A): anticorpo anti-Napi2b (L2(20/3) (B) e anticorpo anti-GAPDH (C). Células HEK293 transfectadas com pcDNA3.1/Napi2b-WT (1), pcDNA3.1/Napi2b-δ6aa, pcDNA3.1/Napi2b-T330V (3) e pcDNA3.1 (4).
[0075] FIGURA 23 mostra a ligação de anticorpo por Western em forma de tipo selvagem e mutante (T330V) de NaPi2b em células HEK293 estavelmente transfectadas. Células HEK 293 transfectadas com pcDNA3.1/NaPi2b-_WT, pcDNA3.1/NaPi2b_T330V, e pcDNA3.1 estão em pistas como anotado. Análise por Western blot de lisados de células HEK293 é mostrada com (A) MAb MX35, (B) anticorpo policlonal para NaPi2b e (C) controle positivo MAb anti-beta actina.
[0076] FIGURA 24 mostra análise por Western-blot de proteína NaPi2b com um MAb anti-NaPi2b gerado contra alça extracelular (ECL) de NaPi2b. (A) Expressão de GST/NaPi2b-ECL em bactérias foi induzida por IPTG 1 mM. Lisados totais foram resolvidos por SDS-PAGE e sondados com MAb anti-NaPi2b; B) Expressão endógena de proteína NaPi2b em linhagens de células OVCAR-3, SKRC-18 e células HEK293 estavelmente expressando NaPi2b; C) Expressão de NaPi2b em tipos diferentes de câncer ovariano e ovário normal (figura superior), pistas 1-8 - carcinoma seroso papilar, pista 9 - cistadenoma seroso papilar, pista 10 - cistadenoma seroso, pista 11 - cistadenoma endometrióide, pista 12 - carcinoma endometrióide fracamente diferenciado, pista 13-16 - carcinoma endometrióide bem diferenciado, pista 17- cistadenoma mucinoso, 18 - carcinoma mucinoso, pistas 19-21 - ovário normal. GAPDH foi usado como um controle de carga (figura inferior).
[0077] FIGURA 25 fornece imuno-histoquímica de amostras de tumores ovarianos e de ovários normais com MAb anti-NaPi2b. A - ovário normal, B - carcinoma seroso papilar, C - cistadenoma seroso papilar, D - cistadenoma seroso, E - carcinoma endometrióide bem diferenciado, F - cistadenoma mucinoso.
[0078] FIGURA 26 fornece imuno-histoquímica de tubas de Falópio normais (A), endométrio (B), epitélio endocervical (C) com MAb anti-NaPi2b
[0079] FIGURA 27 mostra análise por RT-PCR de amostras de tumor ovariano com iniciadores SLC34A2 (A) e iniciadores para b-actina (B). Pista 1 - carcinoma seroso papilar, pista 2 - cistadenoma seroso papilar, pista 3 - cistadenoma seroso, pista 4 - cistadenoma endometrióide, pista 5 - carcinoma endometrióide bem diferenciado, pista 6 - cistadenoma mucinoso, pista 7 - carcinoma mucinoso, pista 8 - ovário normal.
[0080] FIGURA 28 mostra os resultados de pré-incubação de células HEK293 expressando NaPi2b de tipo selvagem com MAb MX35. Células HEK293 expressando tipo selvagem de NaPi2b foram pré-incubadas com anticorpos monoclonais MX35 (50mkg/mL) por um período de 1h, 24h ou 48h. Análise WB de lisados de células HEK293 com MAb MX35 (A), conjugado anti-camundongo (B), e MAb anti-beta actina (C).
[0081] FIGURA 29 mostra regulação positiva de MAb MX35 do nível de NaPi2b de tipo selvagem mas não sua forma mutante T330V em células HEK293 estáveis. HEK293 expressando forma de tipo selvagem e mutante T330V de transportador NaPi2b foram pré-incubadas com MAb MX35 (50mkg/mL) durante 24 h. Análise WB de lisados de células HEK.293 é mostrada com MAb MX35 (A), soro policlonal anti-NaPi2b (B) e MAb anti-beta actina (C).
[0082] FIGURA 30 mostra inibição de transporte de fosfato por pré- incubação de células HEK293 expressando NaPi2b de tipo selvagem com MAb MX35. Células HEK293 (expressando forma WT, forma mutante T330V de vetor vazio NaPi2band) foram pré-incubadas com MAb MX35 (50mkg/mL) durante 24h. Ensaio de captação de fosfato foi realizado na presença de P33 durante 15 min. Os resultados foram reproduzidos em 5 experimentos independentes.
DESCRIÇÃO DETALHADA
[0083] De acordo com a presente invenção podem ser utilizadas técnicas de biologia molecular, microbiologia, e DNA recombinante convencionais dentro da habilidade da técnica. Tais técnicas são explicadas completamente na literatura. Veja, e.g., Sambrook et al., "Molecular Cloning: A Laboratory Manual" (1989); "Current Protocols in Molecular Biology"Volumes I-III [Ausubel, R. M., ed. (1994)]; "Cell Biology: A Laboratory Handbook" Volumes I-III [J. E. Celis, ed. (1994))]; "Current Protocols in Immunology" Volumes I-III [Coligan, J. E., ed. (1994)]; "Oligonucleotide Synthesis" (M.J. Gait ed. 1984); "Nucleic Acid Hybridization" [B.D. Hames & S.J. Higgins eds. (1985)]; "Transcription And Translation" [B.D. Hames & S.J. Higgins, eds. (1984)]; "Animal Cell Culture" [R.I. Freshney, ed. (1986)]; "Immobilized Cells And Enzymes" [IRL Press, (1986)]; B. Perbal, "A Practical Guide To Molecular Cloning" (1984).
[0084] Portanto, se aqui aparecendo, os seguintes termos devem ter as definições mostradas abaixo.
[0085] Os termos "peptídeo de transportador de membrana", "peptídeos NaPi2B ", "peptídeos SLC34A2", "peptídeos de epítopo de SLC34A" e quaisquer variantes não especificamente listadas, podem ser usados aqui intercambiavelmente, e como usados em todo o presente pedido e nas reivindicações referem-se ao material de peptídeo incluindo peptídeos únicos ou múltiplos, e se estende àqueles peptídeos compreendendo região extracelular de SLC34A2, incluindo aminoácidos 312-340, e tendo o perfil de atividades e características aqui descritos e nas reivindicações. Particularmente estão incluídos os peptídeos tendo os dados de seqüência de aminoácidos aqui descritos e apresentados em qualquer uma de SEQ ID NOS: 1-8, e suas variantes. Conformemente, proteínas exibindo atividade substancialmente equivalente ou alterada são igualmente contempladas. Estas modificações podem ser deliberadas, por exemplo, tais como modificações obtidas através de mutagênese sítio-direcionada, ou podem ser acidentais, tais como aquelas obtidas através de mutações em hospedeiros que são produtores do complexo ou suas subunidades nomeadas. Métodos para gerar e testar modificações dos peptídeos de epítopo receptor, incluindo suas variantes, incluindo mas não limitados a, mutagênese sítio-direcionada ou mutagênese aleatória são bem conhecidos por aquelas pessoas experientes na técnica, e incluem aqueles aqui descritos e exemplificados. Também, os termos "peptídeos de transportador de membrana", "peptídeos NaPi2B ", "peptídeos SLC34A2", peptídeos de epítopo de SLC34A2" são intencionados para incluírem dentro de seu escopo proteínas especificamente aqui citadas bem como análogos homólogos e variantes alélicas.
[0086] É preferido que os resíduos de aminoácido aqui descritos estejam na forma isomérica "L". Contudo, resíduos na forma isomérica "D" podem ser substituídos por qualquer resíduo de L-aminoácido, desde que a propriedade funcional desejada da ligação de imunoglobulina seja mantida pelo polipeptídeo. NH2 refere-se ao grupo amino livre presente na terminação amino de um polipeptídeo. COOH refere-se ao grupo carboxila livre de um polipeptídeo. Estando de acordo com a nomenclatura de polipeptídeo padrão, J. Biol. Chem., 243:3552-59 (1969), abreviações para resíduos de aminoácido são mostradas na seguinte Tabela de Correspondência:
[0087] Deve ser notado que todas as seqüências de resíduos de aminoácido são aqui apresentadas por fórmulas cuja orientação esquerda e direita está na direção convencional de terminação amino para terminação carboxila. Ademais, deve ser notado que um travessão no início ou no final de uma seqüência de resíduos de aminoácido indica uma ligação peptídica em uma outra seqüência de um ou mais resíduos de aminoácido. A Tabela acima é apresentada para correlacionar as anotações de uma letra e de três letras que podem aparecer aqui alternativamente.
[0088] Um "replicon" é qualquer elemento genético (e.g., plasmídeo, cromossomo, vírus) que funciona como uma unidade autônoma de replicação de DNA in vivo; i.e., capaz de replicação sob seu próprio controle.
[0089] Um "vetor" é um replicon, tal como um plasmídeo, fago ou cosmídeo, no qual outro segmento de DNA pode ser ligado de modo a causar a replicação do segmento ligado.
[0090] Uma "molécula de DNA" refere-se à forma polimérica de desoxirribonucleotídeos (adenina, guanina, timina, ou citosina) em quer sua forma de fita única, quer uma hélice de fita dupla. Este termo refere-se às estruturas primária e secundária da molécula, e não a limita a qualquer uma de suas formas terciárias particulares. Assim, este termo inclui DNA de fita dupla encontrado, inter alia, em moléculas de DNA linear (e.g., fragmentos de restrição), vírus, plasmídeos, e cromossomos. Na discussão da estrutura de moléculas de DNA de fita dupla particulares, seqüências podem ser aqui descritas de acordo com a convenção normal de dar apenas a seqüência na direção de 5' para 3' ao longo da fita não-traduzida de DNA (i.e., a fita tendo um homólogo de seqüência ao mRNA).
[0091] Uma "origem de replicação" refere-se àquelas seqüências de DNA que participam na síntese de DNA.
[0092] Uma "seqüência codificadora"de DNA é uma seqüência de DNA de fita dupla que é transcrita e traduzida em um polipeptídeo in vivo quando posta sob o controle das seqüências regulatórias apropriadas. Os limites da seqüência codificadora são determinados por um códon de iniciação na terminação 5'(amino) e um códon de tradução na terminação 3' (carboxila). Uma seqüência codificadora pode incluir, mas não é limitada a, seqüências procarióticas, cDNA de mRNA eucariótico, seqüência de DNA genômico de DNA eucariótico (e.g., de mamífero), e até mesmo seqüências de DNA sintéticas. Uma seqüência de sinal de poliadenilação e seqüência de terminação de transcrição estarão costumeiramente localizadas 3' em relação à seqüência codificadora.
[0093] Seqüências de controle de transcrição e de tradução são seqüências regulatórias de DNA, tais como promotores, intensificadores, sinais de poliadenilação, terminadores, e semelhantes, que fornecem a expressão de uma seqüência codificadora em uma célula hospedeira.
[0094] Uma "seqüência de promotor" é uma região regulatória de DNA capaz de ligar RNA polimerase em uma célula e iniciar a transcrição de uma seqüência codificadora a jusante (direção 3'). Para os propósitos de definição da presente invenção, a seqüência de promotor é ligada em sua terminação 3' pelo sítio de iniciação de transcrição e se estende a montante (direção 5') para incluir o número mínimo de bases ou elementos necessários para iniciar a transcrição em níveis detectáveis acima do background. Dentro da seqüência de promotor serão encontrados um sítio de iniciação de transcrição (convenientemente definido por mapeamento com nuclease S1), bem como domínios de ligação de proteína (seqüências de consenso) responsáveis pela ligação de RNA polimerase. Promotores eucarióticos freqüentemente, mas nem sempre, conterão os boxes "TATA"e boxes "CAT". Promotores procarióticos contêm as seqüências de Shine-Dalgarno em adição às seqüências de consenso -10 e -35.
[0095] Uma "seqüência de controle de expressão" é uma seqüência de DNA que controla e regula a transcrição e a tradução de outra seqüência de DNA. Uma seqüência codificadora está "sob o controle" de seqüências de controle de transcrição e de tradução em uma célula quando RNA polimerase transcreve a seqüência codificadora em mRNA, que é então traduzida na proteína codificada pela seqüência codificadora.
[0096] Uma "seqüência de sinal" pode ser incluída antes da seqüência codificadora. A seqüência codifica um peptídeo de sinal, N-terminal ao polipeptídeo, que se comunica com a célula hospedeira para direcionar o polipeptídeo para a superfície da célula ou secretar o polipeptídeo para dentro do meio, e este peptídeo de sinal é cortado pela célula hospedeira antes de a proteína deixar a célula. Seqüências de sinal podem ser encontradas associadas com uma variedade de proteínas nativas de procariotos e eucariotos.
[0097] O termo "oligonucleotídeo", como aqui usado em referência à sonda da presente invenção, é definido como uma molécula compreendida de dois ou mais ribonucleotídeos, preferivelmente mais do que três. seu tamanho exato dependerá de muitos fatores que, por sua vez, dependem da função e do uso finais do oligonucleotídeo.
[0098] O termo "iniciador" como aqui usado refere-se a um oligonucleotídeo, seja ocorrendo naturalmente como em um digesto de restrição purificado seja produzido sinteticamente, o qual é capaz de atuar como um ponto de iniciação de síntese quando posto sob condições nas quais a síntese de um produto de extensão de iniciador, que é complementar a uma fita de ácido nucleico, é induzida, i.e., na presença de nucleotídeos e um agente indutor tal como uma DNA polimerase e em uma temperatura e um pH adequados. O iniciador pode ser de fita quer única quer dupla e precisa ser suficientemente longo para iniciar a síntese do produto de extensão desejado na presença do agente indutor. O comprimento exato do iniciador dependerá da muitos fatores, incluindo temperatura, fonte de iniciador e uso do método. Por exemplo, para aplicações diagnósticas, dependendo da complexidade da seqüência alvo, o iniciador oligonucleotídeo tipicamente contém 15-25 ou mais nucleotídeos, embora possa conter menos nucleotídeos.
[0099] Os iniciadores aqui são selecionados para serem "substancialmente" complementares às fitas diferentes de uma seqüência de DNA alvo particular. Isto significa que os iniciadores precisam ser suficientemente complementares para hibridizarem com suas fitas respectivas. Portanto, a seqüência de iniciador não necessita refletir a seqüência exata do modelo. For exemplo, um fragmento de nucleotídeos não-complementar pode ser ligado na extremidade 5' do iniciador, com o restante da seqüência de iniciador sendo complementar à fita. Alternativamente, seqüências mais longas ou bases não-complementares podem ser entremeadas no iniciador, desde que a seqüência de iniciador tenha complementaridade suficiente com a seqüência da fita para hibridizar com a mesma e deste modo formar o modelo para a síntese do produto de extensão.
[00100] Como aqui usados, os termos "endonucleases de restrição" e "enzimas de restrição"referem-se às enzimas bacterianas, cada uma das quais cortam DNA de fita dupla em uma ou próximo de uma seqüência de nucleotídeos específica.
[00101] Uma célula tem sido "transformada" por DNA exógeno ou endógeno quando tal DNA tem sido introduzido dentro da célula. O DNA transformante pode ou não estar integrado (covalentemente ligado) em DNA cromossômico compondo o genoma da célula. Em procariotos, levedura, e células de mamífero por exemplo, o DNA transformante pode ser mantido em um elemento epissomal tal como um plasmídeo. Com respeito às células eucarióticas, uma célula estavelmente transformada é uma na qual o DNA transformante tem se tornado integrado dentro de um cromossomo de modo que ele é herdado pelas células filhas através de replicação de cromossomo. Esta estabilidade é demonstrada pela capacidade da célula eucariótica de estabelecer clones ou linhagens de célula compreendidos de uma população de células filhas contendo o DNA transformante. Um "clone" é uma população de células derivadas de uma única célula ou ancestre comum por mitose. Uma "linhagem de célula" é um clone de uma célula primária que é capaz de crescimento estável in vitro por muitas gerações.
[00102] Duas seqüências de DNA são "substancialmente homólogas" quando pelo menos cerca de 75% (preferivelmente pelo menos cerca de 80%, e mais preferivelmente pelo menos cerca de 90 ou 95%) dos nucleotídeos combinam sobre o comprimento definido das seqüências de DNA. Seqüências que são substancialmente homólogas podem ser identificadas por comparação das seqüências usando programa de computador padrão disponível em bancos de dados de seqüências, ou em um experimento de hibridização de Southern sob, por exemplo, condições estringentes como definidas para aquele sistema particular. Definição de condições de hibridização apropriadas está dentro da habilidade da técnica. Veja, e.g., Maniatis et al., supra; DNA Cloning, Vols. I & II, supra; Nucleic Acid Hybridization, supra.
[00103] Deve ser reconhecido que também estão dentro do escopo da presente invenção as seqüências de DNA codificadoras de peptídeos SLC34A2 e/ou da anticorpos específicos para peptídeo SLC34A2 da presente invenção. Ácidos nucleicos codificadores do peptídeo SLC34A2 codificam um polipeptídeo compreendendo a seqüência de aminoácidos ou qualquer uma das SEQ ID NOS: 1-8, e podem ser degenerados em um outro.
[00104] Ácidos nucleicos codificadores dos anticorpos específicos direcionados contra SLC34A2 também estão incluídos na invenção. Tais ácidos nucleicos incluem aqueles codificadores de anticorpos selecionados de MX35, L2(20/3) e L3(28/1) ou seus fragmentos ativos. Ácidos nucleicos, incluindo seqüências de DNA, codificadores de polipeptídeos de cadeia pesada e leve de anticorpo MX35 como mostrados em Figura 5 (SEQ ID NO: 24) e Figura 6 (SEQ ID NO: 29) são fornecidos por esta invenção. Tais ácidos nucleicos incluem aqueles codificadores das regiões CDR (SEQ ID NOS: 2628 e 31-33) de anticorpo MX35. Ácidos nucleicos codificadores de um anticorpo MX35 humanizado são adicionalmente aqui fornecidos incluindo os mostrados em FIGURA 11, a região variável de cadeia leve de anticorpo humanizado é mostrada em SEQ ID NO: 34 e a região variável de cadeia pesada de anticorpo humanizado é mostrada em SEQ ID NO: 36. "Degenerado em" significa que um códon de três letras diferente é usado para especificar um aminoácido particular. É bem sabido na técnica que os seguintes códons podem ser usados intercambiavelmente para codificar cada aminoácido específico:
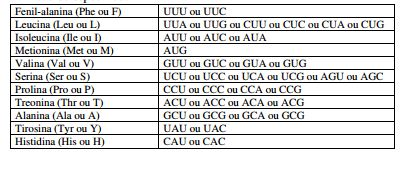

[00105] Deve ser entendido que os códons especificados acima são para seqüências de RNA. Os codons correspondentes para DNA têm U substituída por T.
[00106] Mutações podem ser feitas em seqüências de DNA codificadoras de anticorpos ou peptídeos aqui fornecidos, tais como mostrados em Figuras 5 e 6, as suas CDRs SEQ ID NOS 26-28 e 31-33, ou em peptídeos tais como SEQ ID NOS: 1-8, de tal modo que um códon particular é trocado por um códon que codifica um aminoácido diferente. Uma tal mutação é geralmente feita fazendo-se o mínimo possível de trocas. Uma mutação de substituição deste tipo pode ser feita para trocar um aminoácido na proteína resultante em uma maneira não-conservativa (i.e., por troca do códon de um aminoácido pertencendo a um agrupamento de aminoácidos tendo um tamanho ou uma característica particular por um aminoácido pertencendo a outro agrupamento) ou em uma maneira conservativa (i.e, por troca do códon de um aminoácido pertencendo a um agrupamento de aminoácidos tendo um tamanho ou uma característica particular por um aminoácido pertencendo ao mesmo agrupamento). Uma tal troca conservativa geralmente causa uma mudança menor na estrutura e na função da proteína resultante. Uma troca não-conservativa provavelmente altera mais a estrutura, atividade ou função da proteína resultante. Deve ser considerado que a presente invenção inclui seqüências contendo trocas conservativas que não alteram significativamente a atividade ou características de ligação da proteína resultante.
[00107] O seguinte é um exemplo de vários agrupamentos de aminoácidos: Aminoácidos com grupos R não-polares
[00108] Alanina, Valina, Leucina, Isoleucina, Prolina, Fenil-alanina, Triptofano, Metionina Aminoácidos com grupos R não-carregados
[00109] Glicina, Serina, Treonina, Cisteína, Tirosina, Asparagina, Glutamina Aminoácidos com grupos R polares carregados (negativamente carregados em pH 6,0)
[00110] Ácido Aspártico, Ácido Glutâmico Aminoácidos básicos (positivamente carregados em pH 6,0)
[00111] Lisina, Arginina, Histidina (em pH 6,0)
[00112] Outro agrupamento pode ser aqueles aminoácidos com grupos fenila:
[00113] Fenil-alanina, Triptofano, Tirosina
[00114] Outro agrupamento pode ser de acordo com o peso molecular (i.e., tamanho de grupos R):
[00115] Substituições particularmente preferidas são: - Lys no lugar de Arg e vice versa de tal modo que uma carga positiva possa ser mantida; - Glu no lugar de Asp e vice versa de tal modo que uma carga negativa possa ser mantida; - Ser no lugar de Thr de tal modo que uma -OH livre possa ser mantida; e - Gln no lugar de Asn de tal modo que um NH2 livre possa ser mantido.
[00116] Substituições de aminoácido também podem ser introduzidas para substituir um aminoácido com uma propriedade particularmente preferível. Por exemplo, uma Cys pode ser introduzida em um sítio potencial para pontes de dissulfeto com outra Cys. Uma His pode ser introduzida como um sítio particularmente "catalítico" (i.e., His pode atuar como um ácido ou uma base e é o aminoácido mais comum em catálise bioquímica). Pro pode ser introduzida por causa de sua estrutura particularmente plana, que induz torções na estrutura da proteína.
[00117] Duas seqüências de aminoácidos são "substancialmente homólogas" quando pelo menos cerca de 70% dos resíduos de aminoácido (preferivelmente pelo menos cerca de 80%, e mais preferivelmente pelo menos cerca de 90 ou 95%) são idênticos, ou representam substituições conservativas.
[00118] Uma região "heteróloga" do construto de DNA é um segmento identificável de DNA dentro de uma molécula de DNA maior que não é encontrado em associação com a molécula maior na natureza. Assim, quando a região heteróloga codifica um gene de mamífero, o gene costumeiramente estará flanqueado por DNA que não flanqueia o DNA genômico de mamífero no genoma do organismo fonte. Outro exemplo de uma seqüência codificadora heteróloga é um construto onde a própria seqüência codificadora não é encontrada na natureza (e.g., um cDNA onde a seqüência codificadora genômica contém íntrons, ou seqüências sintéticas tendo códons diferentes do gene nativo). Variações alélicas ou eventos mutacionais naturalmente ocorrentes não ocasionam uma região heteróloga de DNA como aqui definida.
[00119] Uma seqüência de DNA está "operacionalmente ligada" em uma seqüência de controle de expressão quando a seqüência de controle de expressão controla e regula a transcrição e a tradução daquela seqüência de DNA. O termo "operacionalmente ligada" inclui ter um sinal de iniciação apropriado (e.g., ATG) na frente da seqüência de DNA a ser expressada e manutenção da matriz de leitura correta para permitir expressão da seqüência de DNA sob o controle da seqüência de controle de expressão e produção do produto desejado codificado pela seqüência de DNA. Se um gene que se deseja inserir em uma molécula de DNA recombinante não contém um sinal de iniciação apropriado, um tal sinal de iniciação pode ser inserido em frente do gene.
[00120] O termo "condições de hibridização padrão"refere-se às condições de sal e de temperatura substancialmente equivalentes a 5 x SSC e 65°C para ambas hibridização e lavagem. Contudo, uma pessoa experiente na técnica reconhecerá que tais "condições de hibridização padrão" são dependentes das condições particulares incluindo a concentração de sódio e de magnésio no tampão, a concentração e o comprimento de seqüência de nucleotídeos, má combinação percentual, formamida percentual, e semelhantes. Também importante na determinação das "condições de hibridização padrão" é se as duas seqüências hibridizando são RNA-RNA, DNA-DNA ou RNA-DNA. Tais condições de hibridização padrão são facilmente determinadas por uma pessoa experiente na técnica de acordo com fórmulas bem conhecidas, nas quais hibridização é tipicamente 10-20°C abaixo da Tm predita ou determinada com lavagens de estringência maior, se desejadas.
[00121] Um "anticorpo" é qualquer imunoglobulina, incluindo anticorpos e seus fragmentos, que se liga em um epítopo específico. O termo inclui anticorpos policlonais, monoclonais, e quiméricos, os últimos mencionados descritos com mais detalhe em Patentes U.S. de Nos. 4.816.397 e 4.816.567. O termo "anticorpo(s)" inclui uma molécula de imunoglobulina (Ig) de tipo selvagem, geralmente compreendendo quatro cadeias de polipeptídeo de comprimento total, duas cadeias pesadas (H) e duas cadeias leves (L), ou um seu homólogo de Ig equivalente (e.g., um nanocorpo de camelídeo, que compreende apenas uma cadeia pesada); incluindo seus mutantes, variantes ou derivados funcionais de comprimento total, que mantêm as características de ligação em epítopo essenciais de uma molécula de Ig, e incluindo anticorpos de domínio dual específico, biespecífico, multiespecífico, e variável dual; moléculas de Imunoglobulina podem ser de qualquer classe (e.g., IgG, IgE, IgM, IgD, IgA, e IgY), ou subclasse (e.g., IgG1, IgG2, IgG3, IgG4, IgA1, e IgA2). Também está incluído dentro do significado do termo "anticorpo" qualquer "fragmento de anticorpo".
[00122] Visto que anticorpos podem ser modificados em numerosas maneiras, o termo "anticorpo" deve ser entendido como cobrindo qualquer molécula ou substância tendo um domínio de ligação com a especificidade exigida. Assim, este termo cobre fragmentos de anticorpo, derivados, equivalentes funcionais e homólogos de anticorpos, incluindo qualquer polipeptídeo compreendendo um domínio de ligação de imunoglobulina, seja natural seja total ou parcialmente sintético. Moléculas quiméricas compreendendo um domínio de ligação de imunoglobulina, ou equivalente, fusionado em outro polipeptídeo são conseqüentemente incluídas. Clonagem e expressão de anticorpos quiméricos são descritas em EP-A-0120694 e EP- A-0125023 e em Patentes U.S. de Nos. 4.816.397 e 4.816.567.
[00123] Tem sido mostrado que fragmentos de um anticorpo inteiro podem desempenhar a função de ligação de antígenos. Exemplos de fragmentos de ligação são (i) o fragmento Fab consistindo de domínios VL, VH, CL e CHI; (ii) o fragmento Fd consistindo dos domínios VH e CHI; (iii) o fragmento Fv consistindo dos domínios VL e VH de um anticorpo único; (iv) o fragmento dAb (Ward, E.S. et al., Nature 341, 544-546 (1989)) que consiste de um domínio VH; (v) regiões CDR isoladas; (vi) fragmentos F(ab')2, um fragmento bivalente compreendendo dois fragmentos Fab ligados (vii) moléculas Fv de cadeia única (scFv), nas quais um domínio VH e um domínio VL estão ligados por um linker peptídico que permite que os dois domínios se associem para formarem um sítio de ligação de antígeno (Bird et al., Science, 242, 423-426, 1988; Huston et al., PNAS USA, 85, 5879-5883, 1988); (viii) fragmentos de anticorpo multivalentes (dímeros, trímeros e/ou tetrâmeros de scFv (Power e Hudson, J Immunol. Methods 242: 193-204 9 (2000)) (ix) dímeros de Fv de cadeia única biespecíficos (PCT/US92/09965) e (x) "diacorpos", fragmentos multivalentes ou multiespecíficos construídos por fusão de gene (WO94/13804; P. Holliger et al. Proc. Natl. Acad. Sci. USA 90 6444-6448, (1993)).
[00124] Um "sítio de combinação de anticorpo" é aquela porção estrutural de uma molécula de anticorpo compreendida de regiões variáveis e hipervariáveis de cadeias pesada e leve que especificamente se liga em antígeno.
[00125] A frase "molécula de anticorpo" em suas várias formas gramaticais como aqui usada contempla ambas uma molécula de imunoglobulina intacta e uma porção imunologicamente ativa de uma molécula de imunoglobulina.
[00126] Moléculas de anticorpo exemplares são moléculas de imunoglobulina intactas, moléculas de imunoglobulina substancialmente intactas e aquelas porções de uma molécula de imunoglobulina que contém paratopo, incluindo aquelas porções conhecidas na técnica como Fab, Fab', F(ab')2 e F(v), cujas porções são preferidas para uso nos métodos terapêuticos aqui descritos.
[00127] Porções Fab e F(ab')2 de moléculas de anticorpo são preparadas por reação proteolítica de papaína e pepsina, respectivamente, em moléculas de anticorpo substancialmente intactas por métodos que são bem conhecidos. Veja por exemplo, Patente U.S. de No. 4.342.566 de Theofilopolous et al. Porções de molécula de anticorpo Fab' também são bem conhecidas e são produzidas a partir de porções F(ab')2 seguido por redução das ligações de dissulfeto ligando as duas porções de cadeia pesada como com mercapto-etanol, e seguido por alquilação do ao proteína-mercaptano resultante com um reagente tal como iodo-acetamida. Um anticorpo contendo moléculas de anticorpo intactas é aqui preferido.
[00128] A frase "anticorpo monoclonal"em suas várias formas gramaticais refere-se a um anticorpo tendo apenas uma espécie de sítio de combinação de anticorpo capaz de imunorreagir com um antígeno particular. Um anticorpo monoclonal assim tipicamente exibe uma única afinidade de ligação por qualquer antígeno com o qual ele imunorreage. Um anticorpo monoclonal pode portanto conter uma molécula de anticorpo tendo uma pluralidade de sítios de combinação de anticorpo, cada um imunoespecífico para um antígeno diferente; e.g., um anticorpo monoclonal biespecífico (quimérico).
[00129] A frase "farmaceuticamente aceitável"refere-se à entidades moleculares e composições que são fisiologicamente toleráveis e tipicamente não produzem reação alérgica ou adversa similar, tal como distúrbio gástrico, vertigem e semelhantes, quando administradas a um humano.
[00130] A frase "quantidade terapeuticamente eficaz" é aqui usada para significar uma quantidade suficiente para prevenir, e preferivelmente reduzir em pelo menos cerca de 30 por cento, mais preferivelmente em pelo menos cerca de 50 por cento, muito mais preferivelmente em pelo menos cerca de 90 por cento, um tamanho de mudança clinicamente significativa ou na atividade de fase S de uma massa celular alvo, ou outra característica de patologia tal como por exemplo resposta de anticorpo, resposta de célula T ou célula B, redução em expressão de EGFR.
[00131] O termo "adjuvante"refere-se a um composto ou mistura que intensifica a resposta imune, particularmente a um antígeno. Um adjuvante pode servir como um depósito de tecido que lentamente libera o antígeno e também como um ativador de sistema linfóide que não-especificamente intensifica a resposta imune (Hood et al., Immunology, Second Ed., 1984, Benjamin/Cummings: Menlo Park, Califórnia, p. 384). Freqüentemente, um desafio primário com um antígeno sozinho, na ausência de um adjuvante, falhará em induzir uma resposta imune celular ou humoral. Adjuvantes previamente conhecidos e utilizados incluem, mas não são limitados a, adjuvante completo de Freund, adjuvante incompleto de Freund, saponina, geles minerais tal como hidróxido de alumínio, substâncias tensoativas tais como lisolecitina, polióis plurônicos, poliânions, peptídeos, emulsões de hidrogênio ou óleo, hemocianinas de lapa, dinitro-fenol, e adjuvantes de humano potencialmente úteis tais como BCG (bacille Calmette-Gueriri) e Corynebacterium parvum. Adjuvantes de sal mineral incluem mas não são limitados a: hidróxido de alumínio, fosfato de alumínio, fosfato de cálcio, hidróxido de zinco e hidróxido de cálcio. Preferivelmente, a composição de adjuvante adicionalmente compreende um lipídeo de emulsão gordurosa compreendendo cerca de 10% (em peso) de óleo vegetal e cerca de 1-2% (em peso) de fosfolipídeos. Preferivelmente, a composição de adjuvante adicionalmente opcionalmente compreende uma forma de emulsão tendo partículas oleosas dispersadas em uma fase aquosa contínua, tendo um poliol formador de emulsão em uma quantidade de cerca de 0,2% (em peso) a cerca de 49% (em peso), opcionalmente um óleo metabolizável em uma quantidade de formação de emulsão de até 15% (em peso), e opcionalmente um tensoativo baseado em glicol-éter em uma quantidade estabilizadora de emulsão de até cerca de 5% (em peso). Outros exemplos de adjuvantes incluem monofosforil-lipídeo A (MPL, SmithKline Beecham), um congênere obtido após purificação e hidrólise ácida de lipopolissacarídeo de Salmonella Minnesota Re 595; saponinas incluindo QS21 (SmithKline Beecham), uma saponina QA-21 pura purificada de extrato de Quillja saponaria; DQS21, descrita em Pedido PCT de número W096/33739 (SmithKline Beecham); ISCOM (CSL Ltd., Parkville, Victoria, Austrália) derivada da casca da árvore Quillaia saponaria molina; QS-7, QS-17, QS-18, e QS-L1 (So et al., Mol. Cells 7:178-186, 1997); montanida; alume; oligonucleotídeos CpG (veja e.g. Kreig et al., Nature 374:546-9, 1995); várias emulsões de água-em-óleo preparadas de óleos biodegradáveis tais como esqualeno e/ou tocoferol; e fatores que são capturados pelo denominado 'receptor 7 tipo ferramenta’ sobre certas células imunes que são encontradas na parte externa da pele, tal como imiquimod (3M, St. Paul, Minnesota). Particularmente, os antígenos podem ser administrados misturados com uma combinação de DQS21/MPL. A razão de DQS21 para MPL tipicamente será cerca de 1:10 a 10:1, preferivelmente cerca de 1:5 a 5:1 e mais preferivelmente cerca de 1:1. Tipicamente para administração humana, DQS21 e MPL estarão presentes em uma formulação de vacina dentro da faixa de cerca de 1 μg a cerca de 100 μg. Outros adjuvantes são conhecidos na técnica e podem ser usados na invenção (veja, e.g. Goding, Monoclonal Antibodies: Principles and Practice, 2ndEd., 1986). Métodos para a preparação de misturas ou emulsões de polipeptídeo e adjuvante são bem conhecidos por aquelas pessoas experientes na técnica de indução e/ou intensificação de uma resposta imune e na técnica de vacinação.
[00132] Como aqui usado, o termo "imunomodulador" refere-se a um agente que é capaz de modular uma resposta imune ou resposta imunológica. Tal modulação inclui a intensificação de produção de anticorpo, de resposta humoral, de resposta imune celular. Exemplos de imunomoduladores incluem, mas não são limitados a, adjuvantes, citoquinas, interleucinas, quimiocinas e fatores de crescimento.
[00133] O termo "quantidade eficaz" de um imunomodulador refere-se a uma quantidade de um imunomodulador suficiente para intensificar uma resposta imune induzida por vacina, seja ela mediada por célula, humoral ou mediada por anticorpo. Uma quantidade eficaz de um imunomodulador, se injetada, pode estar dentro da faixa de cerca de 0,1-1.000 μg, preferivelmente 1-900 μg, mais preferivelmente 5-500 μg, para um sujeito humano ou dentro da faixa de cerca de 0,01-10,0 μg/kg de peso corporal do animal sujeito. Esta quantidade pode variar em algum grau dependendo do modo de administração, mas estará dentro da mesma faixa geral. Se mais do que um imunomodulador é usado, cada um pode estar presente nestas quantidades ou a quantidade total pode cair dentro desta faixa. Uma quantidade eficaz de um antígeno pode ser uma quantidade capaz de induzir uma resposta imune demonstrável na ausência de um imunomodulador. A quantidade apropriada de antígeno a ser usada é dependente do antígeno específico e é bem conhecida na técnica.
[00134] A quantidade eficaz exata necessária variará de sujeito para sujeito, dependendo da espécie, da idade e da condição geral do sujeito, da severidade da condição sendo tratada, do modo de administração, etc. Assim, não é possível especificar uma quantidade eficaz exata. Contudo, a quantidade eficaz apropriada pode ser determinada por uma pessoa ordinariamente experiente na técnica usando apenas experimentação rotineira ou conhecimento anterior na técnica de vacina.
[00135] Uma "resposta imunológica" a uma composição ou vacina compreendida de um antígeno é o desenvolvimento no hospedeiro de uma resposta imune mediada por anticorpo e/ou célula à composição ou vacina de interesse. Costumeiramente, uma tal resposta consiste de o sujeito produzir anticorpos, células B, células T auxiliadoras, células T supressoras, e/ou células T citotóxicas direcionadas especificamente para um antígeno ou antígenos incluído(s) na composição ou vacina de interesse.
[00136] Como aqui usado, "pg" significa picograma, "ng" significa nanograma, "ug" ou "μg"significa micrograma, "mg" significa miligrama, "ul" ou "μL"significa microlitro, "mL" significa mililitro, "L" significa litro.
[00137] A presente invenção refere-se aos epítopos e peptídeos SLC34A2, particularmente peptídeos incluindo aminoácidos 312-340 de SLC34A2, que podem ser utilizados em geração de anticorpos que têm atividade e capacidade de anti-tumor ou estimulação de uma resposta imunológica que é uma resposta de anti-tumor. A invenção fornece epítopos e peptídeos SLC34A2, particularmente peptídeos de aminoácidos 312-340 de SLC34A2, que podem ser utilizados em seleção de agentes compostos que têm atividade ou capacidade de anti-tumor e uso em estimulação de uma resposta de anti-tumor.
[00138] SLC34A2 é um membro da família de gene de carreador de soluto e tem sido relatado que medeia o transporte de fosfato inorgânico para dentro de células epiteliais via co-transporte de sódio, tendo assim um papel potencial em homeostasia de fosfato. SLC34A2 também tem sido chamado de proteína de transporte de fosfato dependente de sódio 2b (NaPi2b) e foi isolado e clonado de uma biblioteca de cDNA de pulmão e de intestino delgado de humano (Field, J.A. et al. (1999) Biocehm Biophys Res Commun 258:578-582; Xu, H. et al. (1999) Genomics 62:281-284). O gene SLC34A2 codifica uma proteína de 690 aminoácidos, como mostrada emk Figura 1C, que é uma proteína de membrana predita em passar através da membrana múltiplas vezes, com 8 domínios de transmembrana. SLC34A2 também corresponde ao e é chamado de transportador de fosfato dependente de sódio IPT-1, cujas seqüências de polipeptídeo e de ácido nucleico de humano são fornecidas em Fields et al. Patentes U.S. de Nos. 6.319.688 e 6.350.858, cada uma das quais é aqui incorporada como referência.
[00139] Os peptídeos SLC34A2, particularmente de aminoácidos 312340 de peptídeos SLC34A2, da presente invenção fornecem usos diagnósticos e terapêuticos para identificar, caracterizar e selecionar numerosos tipos de tumor, por exemplo, câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano.
[00140] A presente invenção inclui polipeptídeos isolados compreendendo uma seqüência de aminoácidos de um peptídeo SLC34A2 tendo uma seqüência de aminoácidos selecionada de qualquer uma de SEQ ID NOS: 1-8. A presente invenção adicionalmente inclui variantes ou mutantes de qualquer uma das SEQ ID NOS: 1-8, nas quais um ou mais aminoácidos são substituídos, incluindo por um aminoácido conservativo ou não- conservativo. Qualquer tal peptídeo variante ou mutante que é capaz de ser reconhecido ou ligado pelo anticorpo mAb MX35, ou um anticorpo recombinante ou sintético derivado do mesmo, ou que é capaz de gerar anticorpo(s) tendo uma característica de mAb MX35 é incluído pela presente invenção. Em particular, qualquer um de tal(ais) peptídeo(s) pode(m) ser capaz(es) de gerar anticorpos que reconhecem receptor de fator de crescimento e têm atividade de anti-tumor. Os peptídeos isolados, incluindo combinações de um ou mais dos mesmos, são adequados para uso em geração de anticorpos que reconhecem SLC34A2 e têm atividade de anti-tumor e em imunização de animais, particularmente mamíferos, mais particularmente humanos, que têm doença de tumor ou câncer.
[00141] Como indicado acima, a presente invenção também se refere a uma molécula de DNA recombinante ou gene clonado, ou uma sua variante degenerada, que codifica epítopo SLC34A2, ou um seu fragmento imunogênico, que tem uma seqüência de aminoácidos mostrada em qualquer uma das SEQ ID NOS: 1-8; preferivelmente uma molécula de ácido nucleico, em particular uma molécula de DNA recombinante ou gene clonado, codificador(a) de peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8.
[00142] Anticorpos
[00143] Em ainda um outro aspecto, a presente invenção fornece um anticorpo purificado para um peptídeo SLC34A2 selecionado de qualquer uma de SEQ ID NOS: 1-8. A invenção adicionalmente fornece um anticorpo MX35 tendo as seqüências de cadeias pesada e leve de região variável de ácido nucleico e de aminoácidos como mostradas em Figuras 5 e 6. São fornecidos fragmentos, derivados, de anticorpo, ou anticorpos recombinantes compreendendo a seqüência de região variável de Figuras 5 e 6. São fornecidos anticorpos compreendendo as seqüências de domínio CDR como mostradas em Figuras 5 e 6. Em um tal aspecto, um anticorpo da presente invenção compreende uma cadeia pesada e uma cadeia leve, sendo que a região variável de cadeia pesada compreende as seqüências de região CDR SEQ ID NO: 26, 27 e 28, e a região variável de cadeia leve compreende as seqüências de região CDR SEQ ID NO: 31, 32 e 33.
[00144] A invenção fornece vários anticorpos direcionados contra SLC34A2 e capazes de se ligarem em ou reconhecerem SLC34A2, particularmente aminoácidos 312-340, particularmente o peptídeo SLC34A2 e SEQ ID NO: 8. A seqüência de região variável de MX35 compreendendo as SEQ ID NO: 26-28 de regiões CDR, para a cadeia pesada, e SEQ ID NO: 3132, serviu como a base para gerar anticorpos adicionais. MX35 superficialmente modificado é aqui fornecido, um tal anticorpo superficialmente modificado exemplar compreendendo a seqüência de região variável de cadeia pesada SEQ ID NO:38 e a seqüência de região variável de cadeia leve SEQ ID NO: 39. MX 35 quimérico é aqui fornecido, um tal anticorpo quimérico exemplar compreendendo a seqüência de região variável de cadeia pesada SEQ ID NO:40 e a seqüência de região variável de cadeia leve SEQ ID NO: 41. Anticorpos de cadeia única têm sido gerados baseado nos anticorpos superficialmente modificado e quimérico MX35 e são aqui fornecidos. Anticorpo ScFv baseado em MX35 superficialmente modificado é mostrado em FIGURA 16 e tem a seqüência de aminoácidos de SEQ ID NO: 42 e a seqüência de ácido nucleico de SEQ ID NO:43. Anticorpo ScFv baseado em MX35 quimérico é mostrado em FIGURA 17 e tem a seqüência de aminoácidos de SEQ ID NO: 44 e a seqüência de ácido nucleico de SEQ ID NO:45. Anticorpo MX35 humanizado é outro aspecto da invenção e é aqui fornecido. O anticorpo MX35 humanizado exemplar compreende uma seqüência de região variável de cadeia leve SEQ ID NO: 35 e uma seqüência de região variável de cadeia pesada de SEQ ID NO: 37 e é mostrado em FIGURA 11A e 11B. A região variável de cadeia pesada de MX35 humanizado compreende as regiões CDR como mostrado em SEQ ID NO: 26, 27 e 28. A região variável de cadeia leve de MX35 humanizado compreende as regiões CDR como mostrado em SEQ ID NO: 31, 32 e 33.
[00145] Anticorpos contra os polipeptídeos isolados da presente invenção incluem anticorpos naturalmente produzidos e recombinantemente preparados. Estes podem incluir anticorpos tanto monoclonais quanto policlonais preparados por técnicas genéticas conhecidas, bem como anticorpos bi-específicos, e anticorpos incluindo outras funcionalidades adequando-os para uso diagnóstico.
[00146] Tais anticorpos podem ser usados terapeuticamente para tratar pacientes com tumores expressando SLC34A2, incluindo mas não limitados a câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano. Tais anticorpos também podem ser usados em imunoensaios para caracterizar tumores ou diagnosticar câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano. Os anticorpos também podem ser usados para imunização passiva para reduzir tumores ou tratar câncer incluindo câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovarianos.
[00147] Também, anticorpos incluindo anticorpos tanto monoclonais quanto policlonais, e drogas que modulam a exposição ou atividade dos peptídeos SLC34A2 e/ou suas subunidades podem possuir certas aplicações diagnósticas e podem por exemplo, ser utilizados para o propósito de detectar e/ou medir condições tais como infecção viral ou semelhantes. Por exemplo, os peptídeos receptores ou seus fragmentos imunogênicos podem ser usados para produzir anticorpos tanto monoclonais quanto policlonais em uma variedade de meios celulares, por técnicas conhecidas tal como técnica de hibridoma utilizando, por exemplo, células de mieloma e linfócitos de baço de camundongo fusionados. Igualmente, moléculas pequenas que imitam ou antagonizam a(s) atividade(s) dos peptídeos receptores ou das seqüências de epítopo da invenção podem ser descobertas ou sintetizadas, e podem ser usadas em protocolos diagnósticos e/ou terapêuticos.
[00148] Painéis de anticorpos monoclonais produzidos contra os peptídeos receptores podem ser selecionados para várias propriedades; i.e., isótipo, epítopo, afinidade, etc. De interesse particular são os anticorpos monoclonais que neutralizam ou modulam a atividade do receptor. Tais monoclonais podem ser prontamente identificados em ensaios de sinalização ou de atividade de receptor ou em ensaios de tumorigenicidade. Anticorpos de afinidade alta também são úteis quando é desejada purificação por imunoafinidade de SLC34A2 mutante.
[00149] Particularmente, o anticorpo anti-peptídeo SLC34A2 usado nos métodos diagnósticos desta invenção pode ser um anticorpo policlonal purificado por afinidade. Mais particularmente, o anticorpo é um anticorpo monoclonal (mAb). Em adição, as moléculas de anticorpo anti-peptídeo receptor aqui usadas podem estar na forma de porções Fab, Fab', F(ab')2 ou F(v) de moléculas de anticorpo inteiras. Anticorpos humanizados, recombinantes ou totalmente de humano são particularmente preferidos e fornecidos.
[00150] Usos terapêuticos de anticorpos são bem conhecidos dentro da técnica. Há várias maneiras de usar anticorpos para propósitos terapêuticos, por exemplo, como anticorpo nu em combinação com drogas quimioterapêuticas conhecidas, como anticorpos radiomarcados para radioimunoterapia, ou como anticorpos conjugados / copulados com drogas citotóxicas, toxinas, ou outros agentes tóxicos.
[00151] Anticorpos radiomarcados e seus fragmentos, particularmente radioimunoconjugados, são úteis em radioimunoterapia, particularmente como anticorpos radiomarcados para terapia de câncer. Em ainda um outro aspecto, os anticorpos radiomarcados e seus fragmentos, são úteis em técnicas de cirurgia radioimuno-conduzidas, nas quais podem identificar e indicar a presença e/ou localização de células de câncer, células pré-cancerosas, células de tumor, e células hiperproliferativas, antes da, durante a ou após a cirurgia para remover tais células.
[00152] Imunoconjugados ou proteínas de fusão de anticorpo da presente invenção, nos(as) quais os anticorpos e seus fragmentos, da presente invenção estão conjugados ou ligados em outras moléculas ou outros agentes adicionalmente incluem, mas não são limitados aos membros de ligação conjugados em um agente de ablação química, toxina, imunomodulador, citoquina, agente citotóxico, droga ou agente quimioterapêutico.
[00153] Os anticorpos, ou fragmentos de anticorpo, da presente invenção podem ser administrados sozinhos ou em combinação com outros tratamentos, agentes terapêuticos ou agentes, quer simultânea quer seqüencialmente dependentes da condição a ser tratada. Em adição, a presente invenção contempla e inclui composições compreendendo o anticorpo ou seu fragmento, aqui descrito e outros agentes ou agentes terapêuticos tais como agentes terapêuticos ou agentes de anti-câncer, hormônios, anticorpos ou agentes anti-SLC34A2, ou moduladores imunes. Mais geralmente estes agentes de anti-câncer podem ser inibidores de tirosina quinase ou inibidores da cascata de fosforilação, moduladores de pós-tradução, inibidores de crescimento ou divisão celular (e.g., anti-mitóticos), ou inibidores de transdução de sinal. Outros tratamentos ou agentes terapêuticos podem incluir a administração de doses adequadas de drogas de alívio de dor tais como drogas antiinflamatórias não-estereoidais (e.g., aspirina, paracetamol, ibuprofeno ou cetoprofeno) ou opiatos tais como morfina, ou anti-eméticos. A composição pode ser administrada em combinação (quer seqüencialmente (i.e. antes ou após) quer simultaneamente) com inibidores de tirosina quinase, inibidores de transporte de fosfato, doxorubicina, temozolomida, cisplatina, carboplatina, nitroso-uréias, procarbazina, vincristina, hidróxi-uréia, 5-fluoro- uracil, citosina arabinosídeo, ciclofosfamida, epipodofilotoxina, carmustina, lomustina, e/ou outros agentes quimioterapêuticos. Em adição, a composição pode ser administrada com hormônios tais como dexametasona, moduladores imunes, tais como interleucinas, fator de necrose de tumor (TNF), fator estimulante de colônia de granulócito-macrófago (GM-CSF) ou outros fatores de crescimento ou citoquinas que estimulam a resposta imune e redução ou eliminação de tumores ou células de câncer.
[00154] Métodos para produzir anticorpos policlonais anti-peptídeo receptor são bem conhecidos na técnica. Veja Patente U.S. de No. 4.493.795 de Nestor et al. Um anticorpo monoclonal, tipicamente contendo porções Fab e/ou F(ab')2 de moléculas de anticorpo úteis, pode ser preparado usando a tecnologia de hibridoma descrita em Antibodies - A Laboratory Manual, Harlow e Lane, eds., Cold Spring Harbor Laboratory, New York (1988), que é aqui incorporado como referência. Resumidamente, para formar o hibridoma do qual a composição de anticorpo monoclonal é produzida, um mieloma ou outra linhagem de célula auto-perpétua é fusionado com linfócitos obtidos do baço de um mamífero hiper-imunizado com um peptídeo receptor ou um seu fragmento imunogênico. Esplenócitos são tipicamente fusionados com células de mieloma usando poli(etileno-glicol) (PEG) 6000. Híbridos fusionados são selecionados por sua sensibilidade a HAT. Hibridomas produzindo um anticorpo monoclonal útil na prática desta invenção são identificados por sua capacidade para imunorreagirem com os peptídeos receptores presentes e sua capacidade para inibir peptídeo receptor específico ou atividade de receptor em células alvo.
[00155] Um anticorpo monoclonal útil na prática da presente invenção pode ser produzido por iniciação de uma cultura de hibridoma monoclonal compreendendo um meio nutriente contendo um hibridoma que secreta moléculas de anticorpo da especificidade de antígeno apropriado. A cultura é mantida sob condições e por um período de tempo suficientes para o hibridoma secretar as moléculas de anticorpo para dentro do meio. O meio contendo anticorpo é então coletado. As moléculas de anticorpo podem ser então mais adiante isoladas por técnicas bem conhecidas. Meios úteis para a preparação destas composições tanto são conhecidas na técnica quanto estão comercialmente disponíveis e incluem meios de cultura sintéticos, camundongos congênitos e semelhantes. Um meio sintético exemplar é meio essencial mínimo de Dulbecco (DMEM; Dulbecco et al., Virol. 8:396 (1959)) suplementado com 4,5 g/1 de glicose, 20 mm de glutamina, e 20% de soro fetal bovino. Uma cepa de camundongo congênito exemplar é o Balb/c.
[00156] A metodologia geral para preparar anticorpos monoclonais por hibridomas é bem conhecida. Linhagens de célula produtoras de anticorpo, imortais também podem ser criadas por técnicas diferentes de fusão, tal como transformação direta de linfócitos B com DNA oncogênico, ou transfecção com vírus Epstein-Barr. Veja, e.g., M. Schreier et al., "Hybridoma Techniques"(1980); Hammerling et al., "Monoclonal Antibodies And T-cell Hybridomas" (1981); Kennett et al., "Monoclonal Antibodies" (1980); veja também Patentes U.S. de Nos. 4.341.761; 4.399.121; 4.427.783; 4.444.887; 4.451.570; 4.466.917; 4.472.500; 4.491.632; 4.493.890.
[00157] À parte da técnica de hibridoma tradicional há numerosas outras técnicas bem conhecidas para preparar anticorpos monoclonais. Particularmente úteis são os métodos de preparar anticorpos totalmente de humano. Um método é tecnologia de exibição de fago que pode ser usada para selecionar uma variedade de anticorpos de humano ligando especificamente no antígeno usando métodos de enriquecimento por afinidade. Exibição de fago tem sido completamente descrita na literatura e a construção e a triagem de bibliotecas de exibição de fago são bem conhecidas na técnica, veja, e.g., Hoogenboom et al. Trends Biotechnol, 15:62-70 (1997); Hoogenboom, et al. Immunotechnology 4:1-20 (1998); McGregor et al. Mol. Biotechnol, 6:155-62 (1996); e Bird et al., Science, 242:423-426 (1988). Anticorpos totalmente de humano também podem ser preparados por imunização de camundongos transgênicos trazendo porções grandes das cadeias pesada e leve de imunoglobulina de humano, com um imunógeno. Exemplos de tais camundongos são bem conhecidos na técnica, e. g., o Xenomouse® (Abgenix, Inc.) e o HuMAb-Mouse (Medarex, Inc.,), veja também Patentes U. S. de No. 6.207.418, No. 6.150.584, No. 6.111.166, No. 6.075.181, No. 5.922.545, No. 5.545.806 e No. 5.569.825. Anticorpos podem ser preparados por técnicas padrão, e.g. técnicas de hibridoma padrão ou por exibição de fago.
[00158] Anticorpos monoclonais derivados por técnica de hibridoma a partir de espécie diferente de espécie humana, tal como camundongo, podem ser humanizados, o que significa que um anticorpo de não-humano geneticamente engenhado para ser mais humano com o propósito de se evitar HAMA quando infundido em humanos. Os métodos de humanização de anticorpos são bem conhecidos na técnica, dentre os métodos mais comuns estão enxerto de região determinante de complementaridade (CDR) e modificação superficial (também conhecida como fornecimento de superfície nova). Estes métodos tem sido extensivamente descritos na literatura e em patentes, veja e.g.; King "Applications and Engineering of Monoclonal Antibodies" Taylor & Francis, 1998; Patentes U.S. 5.225.539; 5.530.101; 5.585.089. 5.859.205 e 6.797.492, cada uma aqui incorporada como referência.
[00159] Outra possibilidade em desenvolvimento de moléculas que se ligam em / bloqueiam / selecionam ou interagem de alguma outra maneira com os epítopos aqui descritos, são pela preparação de peptídeos. Estes peptídeos poderiam ser qualquer peptídeo aleatório que tem uma afinidade pelos epítopos e necessariamente não têm que ser da família de imunoglobulinas. Estes peptídeos são freqüentemente isolados por técnicas similares àquelas para anticorpos de exibição de fago (Szardenings, J Recept Signal Transduct Res. 2003;23(4):307-49). O uso de peptídeos de tais bibliotecas de peptídeos aleatórios é similar ao dos anticorpos e fragmentos de anticorpo.
[00160] Como descrito em detalhe acima, anticorpo(s) para o peptídeo pode(m) ser produzido(s) e isolado(s) por métodos padrão incluindo técnicas de hibridoma. Para conveniência, o(s) anticorpo(s) para o peptídeo receptor serão aqui chamados de Ab1 e anticorpo(s) produzido(s) em outras espécies será(ão) chamado(s) de Ab2. Será visto a partir do discutido abaixo, que uma propriedade característica de Ab2 é que ele reagirá com o Ab1. Para propósitos desta descrição e das reivindicações, Ab1 será chamado de um anticorpo primário ou anti-peptídeo receptor, e Ab2 será chamada de um anticorpo secundário ou anti-Ab1.
[00161] A presença de peptídeo de epítopo exposto em células pode ser avaliada por procedimentos imunológicos costumeiros aplicáveis a tais determinações. Numerosos procedimentos úteis são conhecidos. Três tais procedimentos que são especialmente úteis utilizam quer o peptídeo receptor marcado com um marcador detectável, anticorpo Abi marcado com um marcador detectável, quer anticorpos Ab2 marcado com um marcador detectável. Os procedimentos podem ser resumidos pelas seguintes equações nas quais o asterisco indica que a partícula está marcada, e "~" representa o peptídeo receptor:
[00162] Os procedimentos e sua aplicação são familiares para aquelas pessoas experientes na técnica e conformemente podem ser utilizados dentro do escopo da presente invenção. O procedimento "competitivo", Procedimento A, é descrito em Patentes U.S. de Nos. 3.654.090 e 3.850.752. Procedimento C, o procedimento de "sanduíche", é descrito em Patentes U.S. de Nos. RE 31.006 e 4.016.043. Ainda outros procedimentos são conhecidos tal como o procedimento de "anticorpo duplo" ou "DASP".
[00163] Em cada caso, o peptídeo forma complexos com um ou mais anticorpos ou parceiros de ligação e um membro do complexo é marcado com um marcador detectável. O fato de que um complexo tem formado e, se desejado, a sua quantidade, pode ser determinado por métodos conhecidos aplicáveis para a detecção de marcadores. Os marcadores, mais comumente utilizados para estes estudos são elementos radioativos, enzimas, agentes químicos que fluorescem quando expostos à luz ultravioleta, e outros. Numerosos materiais fluorescentes são conhecidos e podem ser utilizados como marcadores. Estes incluem, por exemplo, fluoresceína, rodamina, auramina, Vermelho Texas, azul AMCA e Amarelo Lúcifer. Um material de detecção particular é anticorpo anti-coelho preparado em cabras e conjugado com fluoresceína através de isotiocianato. O peptídeo SLC34A2 ou seu(s) parceiro(s) de ligação também pode(m) ser marcado(s) com um elemento radioativo ou com uma enzima. O marcador radioativo pode ser detectado por qualquer um dos procedimentos de contagem correntemente disponíveis. O içnfnnn TM’A'FAT’Irlcpr rlí3 isótopo preferido pode ser selecionado de 3H, 14C, 32P, 35S, 36C1, 51Cr, 57Co, 58Co,59Fe,90Y,125I,131I, e 186Re.
[00164] Marcadores de enzima são igualmente úteis, e podem ser detectados por qualquer uma das técnicas colorimétrica, espectrofotométrica, fluoroespectrofotométrica, amperométrica ou gasométrica presentemente utilizadas. A enzima é conjugada na partícula selecionada pela reação com moléculas de ponte tais como carbodiimidas, diisocianatos, glutaraldeído e semelhante. Muitas enzimas que podem ser usadas nestes procedimentos são conhecidas e podem ser utilizadas. As preferidas são peroxidase, β- glicuronidase, β-D-glicosidase, β-D-galactosidase, urease, glicose oxidase mais peroxidase e fosfatase alcalina. Patentes U.S. de Nos. 3.654.090; 3.850.752; e 4.016.043 são referidas por meio de exemplo para sua revelação de métodos e material de marcação alternativos.
[00165] Em uma outra modalidade desta invenção, kits ou ensaios podem ser preparados para determinar a presença ou ausência de ou a modulação de peptídeo SLC34A2 em células alvo. De acordo com as técnicas de teste discutidas acima. Uma classe de tais kits ou ensaios conterá pelo menos o peptídeo SLC34A2 marcado ou seu parceiro de ligação, por exemplo um anticorpo específico para o mesmo, e orientações, naturalmente, dependendo do método selecionado, e.g., "competitivo", "sanduíche", "DASP"e semelhante. Os kits ou ensaios também podem conter reagentes periféricos tais como tampões, estabilizadores, etc.
[00166] Conformemente, um kit pode ser preparado para a demonstração da presença ou atividade de SLC34A2, compreendendo: (a) uma quantidade predeterminada de pelo menos um componente marcado imunoquimicamente reativo obtido por ligação direta ou indireta do peptídeo SLC34A2 ou um parceiro de ligação específica para o mesmo, em um marcador detectável; (b) outros reagentes; e (c) orientações para uso de dito kit.
[00167] Mais especificamente, o kit pode compreender: (a) uma quantidade conhecida do peptídeo SLC34A2 como descrito acima (ou um parceiro de ligação) geralmente ligado em uma fase sólida para formar um imunossorbente, ou alternativamente, ligado em uma etiqueta adequada, ou pluralidade de tais produtos finais, etc. (ou seus parceiros de ligação) um de cada; (b) se necessários, outros reagentes; e (c) orientações para uso de dito kit.
[00168] Um sistema de ensaio para seleção de drogas potenciais eficazes para modular a atividade do peptídeo SLC34A2, ou um anticorpo para o mesmo pode ser preparado. O peptídeo SLC34A2 ou anticorpo pode ser introduzido em um sistema de teste, e a droga esperada também pode ser introduzida na cultura de célula resultante, e a cultura depois é examinada para observar quaisquer mudanças na atividade de SLC34A2 das células, quer devido à adição da droga prospectiva sozinha, quer devido ao efeito das quantidades adicionadas do peptídeo SLC34A2 conhecido, ou de um anticorpo para o mesmo. Composições
[00169] A presente invenção adicionalmente contempla composições terapêuticas úteis na prática dos métodos terapêuticos desta invenção. Uma presente composição terapêutica inclui, em mistura, um excipiente (veículo) farmaceuticamente aceitável e um ou mais de um peptídeo SLC34A2, particularmente selecionado de um peptídeo tendo qualquer uma seqüência de qualquer uma das SEQ ID NOS: 1-8, ou seu fragmento imunogênico, como aqui descrito como um ingrediente ativo. A invenção adicionalmente contempla composições terapêuticas do anticorpo para SLC34A2, incluindo anticorpos recombinantes ou fragmento de anticorpo, anticorpos variantes, anticorpos quiméricos compreendendo seqüências de região variável de anticorpo MX35, como mostradas em Figuras 5 e 6, ou as suas CDRS.
[00170] A preparação de composições terapêuticas que contêm polipeptídeos, anticorpos, análogos ou fragmentos como ingredientes ativos será entendida na técnica. Tipicamente, tais composições são preparadas como injetáveis, quer como suspensões quer como soluções líquidas, contudo, formas sólidas adequadas para solução em, ou suspensão em, líquido antes da injeção também podem ser preparadas. A preparação também pode ser emulsificada. O ingrediente ativo terapêutico é freqüentemente misturado com excipientes que são farmaceuticamente aceitáveis e compatíveis com o ingrediente ativo. Excipientes adequados são, por exemplo, água, solução salina, dextrose, glicerol, etanol, ou semelhante e suas combinações. Em adição, se desejado, a composição pode conter quantidades menores de substâncias auxiliares tais como agentes umectantes ou emulsificadores, agentes tamponantes de pH que intensificam a efetividade do ingrediente ativo.
[00171] Um polipeptídeo, anticorpo, análogo ou fragmento ativo pode ser formulado na composição terapêutica como formas de sal farmaceuticamente aceitáveis neutralizadas. Sais farmaceuticamente aceitáveis incluem os sais de adição de ácido (formados com os grupos amino livres do polipeptídeo ou da molécula de anticorpo) e que são formados com ácidos inorgânicos tais como, por exemplo, ácidos clorídrico ou fosfórico, ou tais ácidos orgânicos como ácidos acético, oxálico, tartárico, mandélico, e semelhantes. Sais formados dos grupos carboxila livres também podem ser derivados de bases inorgânicas tais como, por exemplo, hidróxidos de sódio, de potássio, de amônio, de cálcio, ou férrico, e de tais bases orgânicas como isopropil-amina, trimetil-amina, 2-etil-amino-etanol, histidina, procaína, e semelhantes.
[00172] As composições terapêuticas contendo peptídeo, anticorpo ou fragmento imunogênico podem ser administradas oral, intramuscular, intraperitoneal ou intravenosamente, ou por injeção ou administração em uma dose unitária, por exemplo. O termo "dose unitária" quando usado com referência a uma composição terapêutica da presente invenção refere-se às unidades fisicamente discretas adequadas como dosagem unitária para humanos, cada unidade contendo uma quantidade predeterminada de material ativo calculada para produzir o efeito terapêutico desejado em associação com o diluente exigido; i.e., portador, ou veículo. As composições terapêuticas contendo o peptídeo receptor ou fragmento imunogênico podem ser administradas múltiplas vezes em série, como em um planejamento de imunização.
[00173] As composições são administradas em uma maneira compatível com a formulação de dosagem, e em uma quantidade terapeuticamente eficaz. A quantidade a ser administrada depende do sujeito a ser tratado, da capacidade do sistema imune do sujeito para utilizar o ingrediente ativo, e do grau de inibição ou neutralização de capacidade de sinalização e ligação de receptor de fator de crescimento desejado. Quantidades precisas de ingrediente ativo exigidas para serem administradas dependem do julgamento do médico e são peculiares a cada indivíduo. Contudo, dosagens adequadas podem variar de cerca de 0,1 a 20, preferivelmente cerca de 0,5 a cerca de 10, e mais preferivelmente um a vários, miligramas de ingrediente ativo por quilograma de peso corporal de indivíduo por dia e depende da rota de administração. Regimes adequados para administração inicial e administrações de reforço também são variáveis, mas são tipicamente por meio de uma administração inicial seguida por doses repetidas em um ou mais intervalos de hora por uma injeção subseqüente ou outra administração. Alternativamente, infusão intravenosa contínua suficiente para manter concentrações freqüentemente nanomolar a dez micromolar no sangue são contempladas.
[00174] As composições terapêuticas podem adicionalmente incluir uma quantidade eficaz do peptídeo SLC34A2, ou anticorpo para o mesmo, e um ou mais dos seguintes ingredientes ativos: um agente anti-mitótico, um agente quimioterapêutico, um imunomodulador.
Ácidos nucleicos
[00175] Outra característica desta invenção é a expressão de seqüências de DNA codificadoras dos peptídeos ou anticorpos aqui revelados. Como é bem conhecido na técnica, seqüências de DNA podem ser expressadas por ligação operacional delas em uma seqüência de controle de expressão em um vetor de expressão apropriado e empregando aquele vetor de expressão para transformar um hospedeiro unicelular apropriado. Tal ligação operativa de uma seqüência de DNA desta invenção em uma seqüência de controle de expressão, naturalmente, inclui, se não já parte da seqüência de DNA, o fornecimento de um códon de iniciação, ATG, na matriz de leitura correta a montante da seqüência de DNA.
[00176] Uma ampla variedade de combinações de hospedeiro / vetor de expressão pode ser utilizada na expressão de seqüências de DNA desta invenção. Vetores de expressão úteis, por exemplo, podem consistir de segmentos de seqüências de DNA cromossômico, não-cromossômico e sintético. Vetores adequados incluem derivados de SV40 e plasmídeos bacterianos conhecidos, e.g., plasmídeos de E. coli col E1, pCR1, pBR322, pMB9 e seus derivados, plasmídeos tal como RP4; DNAS de fago, e.g., os numerosos derivados de fago X, e.g., NM989, e outro DNA de fago, e.g., M13 e DNA de fago de fita única filamentoso; plasmídeos de levedura tal como o plasmídeo 2μ ou seus derivados; vetores úteis em células eucarióticas, tais como vetores úteis em células de mamífero ou de inseto; vetores derivados de combinações de plasmídeos e DNAs de fago, tais como plasmídeos que têm sido modificados para utilizar DNA de fago ou outras seqüências de controle de expressão; e semelhantes.
[00177] Qualquer uma de uma ampla variedade de seqüências de controle de expressão - seqüências que controlam a expressão de uma seqüência de DNA operacionalmente ligada na mesma - pode ser usada nestes vetores para expressar as seqüências de DNA desta invenção. Tais seqüências de controle de expressão úteis incluem, por exemplo, os promotores precoce e tardio de SV40, CMV, vacínia, polioma ou adenovírus, o sistema lac, o sistema trp, o sistema TAC, o sistema TRC, o sistema LTR, o operador maior e regiões de promotor de fago X, as regiões de controle de proteína de capa fd, o promotor para 3-fosfo-glicerato quinase ou outras enzimas glicolíticas, os promotores de dita fosfatase (e.g., Pho5), os promotores dos fatores de acasalamento-α de levedura, e outras seqüências conhecidas para controlar a expressão de genes de células procarióticas ou eucarióticas ou seus vírus, e suas várias combinações.
[00178] Uma ampla variedade de células hospedeiras unicelulares também é útil na expressão de seqüências de DNA desta invenção. Estes hospedeiros podem incluir hospedeiros eucarióticos e procarióticos bem conhecidos, tais como cepas de E. coli, Pseudomonas, Bacillus, Streptomyces, fungos tais como leveduras, e células de animal, tais como células CHO, R1.1, B-W e L-M, células de rim de Macaco Verde Africano (e.g., COS 1, COS 7, BSC1, BSC40, e BMT10), células de inseto (e.g., Sf9), e células de humano e células de planta em cultura de tecido.
[00179] Será entendido que nem todos os vetores, seqüências de controle de expressão e hospedeiros funcionarão igualmente bem para expressarem as seqüências de DNA desta invenção. Nem todos os hospedeiros funcionarão igualmente bem com o mesmo sistema de expressão. Contudo, uma pessoa experiente na técnica será capaz de selecionar os vetores, seqüências de controle de expressão, e hospedeiros apropriados sem experimentação indevida para realizar a expressão desejada sem se desviar do escopo desta invenção. Por exemplo, na seleção de um vetor, o hospedeiro precisa ser considerado porque o vetor precisa funcionar nele. O número de cópias de vetor, a capacidade para controlar aquele número de cópias, e a expressão de qualquer outras proteínas codificadas pelo vetor, tais como marcadores antibióticos, também serão considerados.
[00180] Na seleção de uma seqüência de controle de expressão, uma variedade de fatores normalmente será considerada. Estas incluem, por exemplo, a força relativa do sistema, sua compatibilidade com a seqüência de DNA ou gene particular a ser expressada(o), particularmente com relação às estruturas secundárias potenciais. Hospedeiros unicelulares adequados serão selecionados pela consideração de, e.g., sua compatibilidade com o vetor escolhido, suas características de secreção, sua capacidade para dobrar proteínas corretamente, e suas exigências de fermentação, bem como a toxicidade para o hospedeiro do produto codificado pelas seqüências de DNA a serem expressadas, e a facilidade de purificação dos produtos de expressão.
[00181] Considerando estes e outros fatores uma pessoa experiente na técnica será capaz de construir uma variedade de combinações de vetor / seqüência de controle de expressão / hospedeiro que expressará as seqüências de DNA desta invenção sob fermentação ou em cultura animal de grande escala.
[00182] É adicionalmente intencionado que análogos de peptídeo, análogos, variantes ou derivados de anticorpo, incluindo fragmentos ction, podem ser preparados a partir de seqüências de nucleotídeos da subunidade / complexo de proteína dentro do escopo da presente invenção. Análogos, tais como fragmentos, podem ser produzidos, por exemplo, por digestão proteolítica, incluindo digestão com pepsina, dos peptídeos ou anticorpos. Outros análogos, tais como muteínas, podem ser produzidos por mutagênese sítio-direcionada padrão das seqüências codificadoras de anticorpo ou peptídeo. Análogos exibindo "atividade de peptídeo SLC34A2" ou "atividade de anticorpo SLC34A2"tais como moléculas pequenas, funcionando quer como promotores quer como inibidores, podem ser identificados por ensaios in vivo e/ou in vitro conhecidos.
[00183] Como mencionado acima, uma seqüência de DNA codificadora do(s) peptídeo(s) ou anticorpo(s) pode ser preparada sinteticamente em vez de ser clonada. A seqüência de DNA pode ser planejada com os códons apropriados para a seqüência de aminoácidos de peptídeo receptor. Em geral, serão selecionados os códons preferidos para o hospedeiro intencionado se a seqüência for usada para expressão. A seqüência completa é montada a partir de oligonucleotídeos sobrepostos preparados por métodos padrão e montada em uma seqüência codificadora completa. Veja, e.g., Edge, Nature, 292:756 (1981); Nambair et al., Science, 223:1299 (1984); Jay et al., J. Biol. Chem., 259:6311 (1984).
[00184] Seqüências de DNA sintéticas permitem construção conveniente de genes que expressarão análogos de peptídeo receptor ou "muteínas". Alternativamente, DNA codificador de muteínas pode ser preparado por mutagênese sítio-direcionada dos genes de receptor de fator de crescimento nativo ou cDNAs, e muteínas podem ser preparadas diretamente usando síntese de polipeptídeo convencional.
[00185] Um método geral para incorporação sítio-específica de aminoácidos não-naturais em proteínas é descrito em Christopher J. Noren, Spencer J. Anthony-Cahill, Michael C. Griffith, Peter G. Schultz, Science, 244:182-188 (April 1989). Este método pode ser usado para criar análogos com aminoácidos não-naturais.
Antígenos e Vacinas
[00186] A caracterização de antígenos de tumor reconhecidos por células T tem revolucionado a abordagem de vacina contra câncer, fornecendo pela primeira vez a oportunidade de imunizar pacientes pelo uso de antígenos bem definidos.
[00187] Antígenos sintéticos, incluindo vacinas, podem ser preparados por síntese química de peptídeos SLC34A2 da presente invenção, opcionalmente incluindo outros antígenos de tumor. Estes peptídeos, combinações de carreador de peptídeo, derivados de lipídeo de tais peptídeos bem como antígenos de tumor, podem ser usados quer individualmente quer combinados como um coquetel, e formulados com um adjuvante para fornecer uma composição imunogênica. Como aqui contemplado, um antígeno pode ser covalentemente ligado em um análogo de glicolipídeo para fornecer uma molécula discreta que exibe um efeito adjuvante intensificado sobre o antígeno que é maior do que o efeito adjuvante alcançável na ausência de tal ligação covalente. Estas composições podem ser usadas para imunizar mamíferos, por exemplo, por rotas intramuscular ou parenteral, ou por liberação em superfícies mucosais usando micropartículas, cápsulas, lipossomos e moléculas alvo, tais como toxinas e anticorpos.
[00188] Vacinas contendo peptídeos são geralmente bem conhecidas na técnica, como exemplificadas por Patentes U.S. de Nos. 4.601.903; 4.599.231; 4.599.230; e 4.596.792; todas as quais são aqui incorporadas como referências. O uso de peptídeos in vivo pode primeiro exigir sua modificação química porque os próprios peptídeos podem não ter uma meia-vida longa em tecido e/ou em soro e/ou imunogenicidade suficiente. Em adição, pode ser vantajoso modificar os peptídeos com o propósito de impor neles uma restrição conformacional. Isto pode ser útil, por exemplo, para imitar uma conformação naturalmente ocorrente do peptídeo no contexto da proteína nativa com o propósito de otimizar as respostas imunes efetoras que são induzidas.
[00189] Esta invenção fornece uma composição imunogênica compreendendo uma quantidade do peptídeo SLC34A2, ou seus fragmentos imunogênicos e suas combinações. Em uma modalidade o peptídeo SLC34A2 é selecionado de SEQ ID NOS: 1-8.
[00190] Esta invenção fornece um método de estimular ou intensificar uma resposta imune mediada por célula específica para antígeno que compreende administrar a um sujeito uma quantidade de um peptídeo receptor, ou seu fragmento imunogênico, e um adjuvante adequado.
[00191] Esta invenção fornece um método de tratar um sujeito com um tumor ou câncer compreendendo administrar a um sujeito uma quantidade de composição de peptídeo SLC34A2 e adjuvante da presente invenção como um imunomodulador, e um diluente ou veículo adequado. Em particular, um sujeito tendo câncer pode ser tratado com a composição de peptídeo receptor - adjuvante. Tais cânceres incluem mas não são limitados a câncer ovariano, câncer de tiróide, câncer de pulmão, câncer de mama, câncer de rim, particularmente câncer ovariano.
[00192] Ademais o sujeito pode ser tratado com o peptídeo SLC34A2 ou sua composição imunogênica em combinação com terapia quimioterapêutica, quimiopreventiva, ou de radiação. É contemplado por esta invenção que a composição de peptídeo receptor poderia ser usada conjuntamente com intervenção quimio- ou radioterapêutica. Em outra modalidade, tratamento com a composição de peptídeo receptor pode preceder ou seguir o tratamento de agente danificador de DNA por intervalos variando de minutos a semanas. Protocolos e métodos são conhecidos por aquelas pessoas experientes na técnica. Fatores ou agentes danificadores de DNA são conhecidos por aquelas pessoas experientes na técnica e significam qualquer composto químico ou método de tratamento que induz dano em DNA tais como irradiação gama, raios-X, irradiação UV, microondas, emissões eletrônicas, e semelhantes. Uma variedade de compostos químicos, também descritos como "agentes quimioterapêuticos", funcionam para induzir dano em DNA, todos os quais são intencionados para serem usados nos métodos de tratamento combinado aqui revelados. Agentes quimioterapêuticos contemplados para serem usados, incluem, e.g., adriamicina, 5-fluoro-uracil (5FU), etoposida (VP-16), camptotecina, actinomicina-D, mitomicina C, cisplatina (CDDP) e até mesmo peróxido de hidrogênio.
[00193] Combinações de um ou mais agentes danificadores de DNA podem ser usadas com EHA, quer baseado em radiação quer compostos reais, tal como o uso de raios-X com cisplatina ou o uso de cisplatina com etoposida. Outros agentes tóxicos ou neoplásicos incluem mas não são limitados a: 5-fluoro-uracil, metotrexato e adriamicina que podem estar ligados em cada caso, por exemplo, em uma cefalosporina (veja WO- A94.01.137 e EP-A-0.382.411) ou mostardas de cefalosporina (veja EP-A- 0.484.870).
[00194] O peptídeo SLC34A2 ou as composições imunogênicas pode(m) ser preparo(as) como injetáveis, como emulsões ou soluções líquidas. Os antígenos e as composições imunogênicas podem ser misturados com veículos fisiologicamente aceitáveis que são compatíveis com os(as) mesmos(as). Estes podem incluir água, solução salina, dextrose, glicerol, etanol e suas combinações. A vacina pode adicionalmente conter substâncias auxiliares, tais como agentes umectantes ou emulsificadores e agentes tamponantes de pH, para adicionalmente intensificar sua efetividade. Vacinas podem ser administradas por injeção subcutânea ou intramuscular.
[00195] Alternativamente, as composições imunogênicas formadas de acordo com a presente invenção, podem ser formuladas e liberadas em uma maneira para evocar uma resposta imune em superfícies mucosais. Assim, a composição imunogênica pode ser administrada às superfícies mucosais por, por exemplo, rotas nasal ou oral (intragástrica). Alternativamente, outros modos de administração incluindo supositórios podem ser desejáveis. Para supositórios, aglutinantes e veículos podem incluir, por exemplo, poli(alquileno-glicóis) e triglicerídeos. Formulações orais podem incluir excipientes normalmente utilizados, tais como graus farmacêuticos de sacarina, celulose e carbonato de magnésio.
[00196] Os modos de administração podem compreender o uso de quaisquer meios e/ou métodos adequados para liberar o adjuvante ou a vacina contendo adjuvante em um local corporal do animal hospedeiro onde o adjuvante e os antígenos associados são imunoestimulantemente eficazes. Modos de liberação podem incluir, sem limitação, métodos de administração parenteral, tais como paracanceral, transmucosal, transdermal, intramuscular, intravenosa, intradermal, subcutânea, intraperitoneal, intraventricular, intracranial e intratumoralmente.
Anticorpos recombinantes, quiméricos, biespecíficos e fragmentos
[00197] Anticorpos recombinantes, quiméricos, biespecíficos, fragmentos, etc. dos anticorpos direcionados contra SLC34A2, particularmente contra aminoácidos 312-340 de SLC34A2 são fornecidos e incluídos nesta invenção. Anticorpos compreendendo as seqüências de região variável mostradas em Figuras 5 e 6, particularmente incluindo as regiões CDR são contemplados. Em geral, as regiões CDR, compreendendo seqüências de aminoácidos substancialmente como mostradas como regiões CDR de Figuras 5 e 6 serão transportadas em uma estrutura que permite a ligação das regiões CDR em um antígeno de tumor, incluindo SLC34A2.
[00198] "Substancialmente como mostradas" significa que as regiões CDR da invenção serão quer idênticas quer elevadamente homólogas às regiões especificadas de Figuras 5 e 6. Por "elevadamente homólogas" é contemplado que apenas umas poucas substituições, preferivelmente de 1 a 8, preferivelmente de 1 a 5, preferivelmente de 1 a 4, ou de 1 a 3 ou 1 ou 2 substituições podem ser feitas nas CDRs. É contemplado que anticorpos tendo poucas ou várias, tais como 1 a 3 ou 1 ou 2 substituições nas CDRs como aqui mostradas, neste caso em SEQ ID NOS: 26-28 e/ou 31-33, são incluídas pela invenção e o termo como substancialmente mostradas.
[00199] A estrutura para transportar a(s) região(ões) CDR da invenção geralmente será de uma seqüência de cadeia pesada ou leve de anticorpo ou sua porção substancial na qual as regiões CDR estão localizadas em localizações correspondendo à região CDR dos domínios variáveis de anticorpo VH e VL naturalmente ocorrentes codificados por genes de imunoglobulina rearranjados. As estruturas e as localizações de domínios variáveis de imunoglobulina podem ser determinadas referindo-se a Kabat, E.A. et al., Sequences of Proteins of Immunological Interest. 4thEdition. US Department of Health and Human Services. 1987, e suas atualizações, agira disponível na Internet (http://imnuno.bme.nwu.edu)).
[00200] Preferivelmente, a(s) seqüência(s) de aminoácidos substancialmente como mostrada(s) nas CDRs de Figura 5 (incluindo como mostradas em SEQ ID NOS: 26-28) são transportadas como as CDRs em um domínio variável de cadeia pesada de humano ou como uma sua porção substancial, e a(s) seqüência(s) de aminoácidos substancialmente como mostrada(s) como as CDRs de Figura 6 (incluindo como mostrada(s) em SEQ ID NOS: 31-33) são transportadas como as CDRs respectivamente em um domínio variável de cadeia leve de humano ou uma sua porção substancial. Os domínios variáveis podem ser derivados de linhagem germinativa ou de domínio variável de humano rearranjado, ou podem ser um domínio variável sintético baseado em seqüências de consenso de domínios variáveis de humano conhecidos.
[00201] Vários anticorpos SLC34A2 exemplares são aqui fornecidos. Assim, um anticorpo da presente invenção compreende uma cadeia pesada e uma cadeia leve, sendo que a região variável de cadeia pesada compreende as seqüências de região CDR SEQ ID NO: 26, 27 e 28, e a região variável de cadeia leve compreende as seqüências de região CDR SEQ ID NO: 31, 32 e 33. A invenção fornece vários anticorpos direcionados contra SLC34A2 e capazes de ligação em ou reconhecimento de SLC34A2, particularmente aminoácidos 312-340, particularmente o peptídeo SLC34A2 e SEQ ID NO: 8. A seqüência de região variável de MX35 compreendendo regiões CDR SEQ ID NO: 26-28, para a cadeia pesada, e SEQ ID NO: 31-32, serviu como a base para gerar anticorpos adicionais. MX 35 superficialmente modificado é aqui fornecido, um tal exemplar de anticorpo superficialmente modificado compreendendo a seqüência de região variável de cadeia pesada SEQ ID NO:38 e a seqüência de região variável de cadeia leve SEQ ID NO: 39. MX 35 quimérico é aqui fornecido, um tal anticorpo quimérico exemplar compreendendo a seqüência de região variável de cadeia pesada SEQ ID NO:40 e a seqüência de região variável de cadeia leve SEQ ID NO: 41. Anticorpos de cadeia única têm sido gerados baseado nos anticorpos MX35 quiméricos e superficialmente modificados e são aqui fornecidos. Anticorpo ScFv baseado em MX35 superficialmente modificado é mostrado em FIGURA 16 e tem a seqüência de aminoácidos de SEQ ID NO: 42 e a seqüência de ácido nucleico de SEQ ID NO:43. Anticorpo ScFv baseado em MX35 quimérico é mostrado em FIGURA 17 e tem a seqüência de aminoácidos de SEQ ID NO: 44 e a seqüência de ácido nucleico de SEQ ID NO:45. Anticorpo MX35 humanizado é outro aspecto da invenção e é aqui fornecido. O anticorpo MX35 humanizado exemplar compreende uma seqüência de região variável de cadeia leve SEQ ID NO: 35 e uma seqüência de região variável de cadeia pesada de SEQ ID NO: 37 e é mostrado em FIGURA 11A e 11B. A região variável de cadeia pesada de MX35 humanizado compreende as regiões CDR como mostradas em SEQ ID NO: 26, 27 e 28. A região variável de cadeia leve de MX35 humanizado compreende as regiões CDR como mostradas em SEQ ID NO: 31, 32 e 33.
[00202] Por exemplo, Marks et al. (Bio/Technology, 1992, 10:779783) descrevem métodos de produzir repertórios de domínios variáveis de anticorpo nos quais iniciadores de consenso direcionados na ou adjacentes à extremidade 5' da área de domínio variável são usados conjuntamente com iniciadores de consenso para a terceira região de molde de genes VH de humano para fornecer um repertório de domínios variáveis VH faltantes de uma CDR.
[00203] Técnicas combinatórias ou de rearranjo também são reveladas por Stemmer (Nature, 1994, 370:389-391), que descreve a técnica em relação a um gene de β-lactamase mas observa que a abordagem pode ser usada para a geração de anticorpos. Uma outra alternativa é gerar novas regiões VH ou VL transportando seqüências derivadas de CDR3 da invenção usando mutagênese aleatória de, por exemplo, os genes VH ou VL de mAb para gerar mutações dentro do domínio variável inteiro. Uma tal técnica é descrita por Gram et al. (1992, Proc. Natl. Acad. Sci., USA, 89:3576-3580), que usam error-prone PCR. Outro método que pode ser utilizado é conduzir mutagênese nas regiões CDR de genes VH ou VL. Tais técnicas são reveladas por Barbas et al., (1994, Proc. Natl. Acad. Sci., USA, 91:3809-3813) e Schier et al. (1996, J. Mol. Biol. 263:551-567).
[00204] Todas as técnicas descritas acima são conhecidas como tais na técnica e em si mesmas não formam parte da presente invenção. A pessoa experiente será capaz de usar tais técnicas para fornecer membros de ligação específica da invenção usando metodologia de rotina na técnica.
[00205] Domínios de ligação única quer baseados em seqüências de região variável como mostradas em Figuras 5 e 6, quer baseados em anticorpos SLC34A2 mais geralmente aqui revelados e fornecidos, formam outros aspectos da invenção. No caso de qualquer um destes domínios de ligação específica de cadeia única, estes domínios podem ser usados para selecionar domínios complementares capazes de formarem um membro de ligação específica de dois domínios que tem propriedades in vivo tão boas quanto ou iguais às do(s) anticorpo(s) mAb aqui revelado(s). Isto pode ser realizado por métodos de seleção por exibição de fago usando a denominada abordagem combinatória dual hierárquica como revelada em Patente U.S. 5.969.108 na qual uma colônia individual contendo um clone de cadeia quer H quer L é usada para infectar uma biblioteca completa de clones codificadores da outra cadeia (L ou H) e o membro de ligação específica de duas cadeias é selecionado de acordo com as técnicas de exibição de fago tais como aquelas descritas naquela referência. Esta técnica também é mostrada em et al., ibid.
[00206] Anticorpos da presente invenção podem adicionalmente compreender regiões constantes de anticorpo ou suas partes. Por exemplo, membros de ligação específica baseados nas seqüências de MX35 ou outros anticorpos aqui, podem ser ligados em sua extremidade C-terminal nos domínios constantes de cadeia leve de anticorpo incluindo cadeias CK ou CX, preferivelmente cadeias CX. Similarmente, membros de ligação específica baseados em SEQ ID NO: [sic] podem ser ligados em sua extremidade de ligação C-terminal em toda ou em parte de uma cadeia pesada de imunoglobulina derivada de qualquer isótipo de anticorpo e.g. IgG, IgA, IgE, IgD e IgM e qualquer uma das subclasses de isótipo, particularmente IgG1, IgG2b, e IgG4. IgG1 é preferida.
[00207] A invenção pode ser melhor entendida por referência aos seguintes Exemplos não limitantes, que são fornecidos como modalidades exemplares da invenção. Os seguintes exemplos são apresentados com o propósito de mais completamente ilustrar as modalidades preferidas da invenção e contudo não devem ser em nenhuma maneira entendidos como limitando o escopo amplo da invenção.
EXEMPLO 1
Anticorpo monoclonal MX35 detecta o transportador de membrana NaPi2b (SLC34A2) em carcinomas de humano: um alvo novo para imunoterapia de câncer
[00208] Anticorpo monoclonal de camundongo MX35 foi desenvolvido contra câncer ovariano e o anticorpo mostrou reatividade homogênea com aproximadamente 90% dos cânceres epiteliais ovarianos de humano mas com apenas um número limitado de tecidos normais por imuno- histoquímica. Embora mAb MX35 tenha sido usado em numerosos testes clínicos em câncer ovariano, foi difícil definir a identidade molecular de MX35. Relatamos aqui que mAb MX35 reconhece a proteína de transporte de fosfato dependente de sódio 2b (NaPi2b) em células de câncer de humano. Esta conclusão é baseada em várias linhas de evidência experimental, incluindo 1) identificação de SLC34A2, o gene codificador de NaPi2b, por imunosseleção de uma linhagem de célula de câncer ovariano derivada de biblioteca de expressão de cDNA com mAb MX35; 2) seqüenciamento por espectrometria de massa de peptídeos obtidos por fermentação de antígeno purificado por afinidade de mAb MX35, que mostrou homologia de seqüência completa com seqüências de aminoácidos em NaPi2b; 3) regulação positiva seletiva de expressão de gene SLC34A2 por interferência de RNA e a perda resultante de mAb MX35 ligando em células de câncer de humano expressando MX35; e 4) demonstração de reatividade específica mAb MX35 com proteínas de fusão recombinantes e com peptídeos sintéticos da alça extracelular maior putativa de NaPi2b. Adicionalmente mostramos que NaPi2b em células de câncer é expressada sobre a superfície celular como uma proteína elevadamente N-glicosilada, com evidência de modificação de pós-tradução adicionais, tais como palmitoilação e formação de pontes de dissulfeto na alça extracelular maior. Moléculas transportadoras de membrana, tal como NaPi2b, representam uma família nova de alvos de superfície celular potenciais para imunoterapia de câncer com anticorpos monoclonais.
MATERIAIS E MÉTODOS
[00209] Linhagens de células e anticorpos: Todas as linhagens de células foram obtidas do banco de células do Ludwig Institute for Cancer Research, New York Branch em Memorial Sloan-Kettering Cancer Center. mAb MX35 Murino (IgG1) foi purificado do sobrenadante de hibridoma por cromatografia em proteína G.
[00210] Imunosseleção de biblioteca de OVCAR-3 cDNA: A biblioteca de expressão de cDNA de linhagem de célula OVCAR-3 tem sido descrita (19). Um total de 1x106 fagos recombinantes foi selecionado com o anticorpo monoclonal MX35 (5 μg/mL TBS com 0,2% de leite desnatado em pó) por 15 h na temperatura ambiente. Clones positivos para MX35 foram mais adiante confirmados por seleção secundária e terciária. Fagos positivos isolados foram convertidos em fagomídeo pBK-CMV usando o protocolo de excisão in vivo de Stratagene (La Jolla, CA). DNAs plasmídeo resgatados foram purificados usando um miniprep kit (Qiagen, Valencia, CA) e submetidos à análise de restrição e seqüenciamento de DNA.
[00211] Radiomarcação metabólica de células cultivadas: Células cultivadas foram metabolicamente marcadas com mistura de Tran 35S-label (MP Biomedicals, Inc. Irvine, CA) e 3H-Glicosamina (Amersham Biosciences UK, Buckinghamshire, UK) como previamente descrito (20). Palmoilação metabólica usando ácido 3H-palmítico foi realizada como descrito (21).
[00212] Radioimunoprecipitação, SDS-PAGE, Autorradiografia e Immunoblotting:Radioimunoprecipitação, SDS-PAGE, autorradiografia e immunoblotting foram realizadas como descrito (21).
[00213] Espectrometria de massa MALDI-TOF/TOF: Marcação metabólica, imunoprecipitação, SDS-PAGE e detecção de proteínas marcadas com 35S foram realizadas como descrito no início. Digestão tríptica em gel e impressão digital de massa de peptídeo foram realizadas como descrito (22) com tratamento adicional de bandas de proteína excisadas com DTT antes de descoloração e digestão. Experimentos em paralelo, peptídeos extraídos foram submetidos à marcação de resíduos de aminoácido lisina usando 2-metóxi-4,5 di-hidro-1H-imidazol (23) e à sulfonação da terminação-N de peptídeos para melhorar a fragmentação (Ettan CAF MALDI sequencing kit, GE healthcare Amersham Biosciences AB, Uppsala, Suécia). Peptídeos foram submetidos ao seqüenciamento "de-novo" por fragmentação usando decaimento pós-fonte em um instrumento Bruker Ultraflex MALDI TOF/TOF (Bruker Daltonics, Bremen, Alemanha). Os espectros de PSD foram interpretados manualmente. Experimentos foram realizados com duas linhagens celulares diferentes, OVCAR-3 e SK-RC-18, e três repetições para cada linhagem de célula.
[00214] Ensaio de interferência de RNA: Dois conjuntos diferentes de SMARTpool siRNA específico para SLC34A2 (ON-Targetplus™ e siGENOME) e controles SMARTpool siRNA não-selecionadores (ON- Targetplus™ siCONTROL e standard siCONTROL) foram adquiridos de Dharmacon, Inc. (Lafayette, CO). A transfecção de siRNA foi realizada na presença de meios Lipofectamine 2000 e Opti-MEM (Invitrogen, Carlsbad, CA) de acordo com as instruções do fabricante em uma concentração final de 40nM. Células foram tratadas com Lipofectamine 2000 sozinho e siRNA pools não-selecionadores foram usados como controles. Setenta e duas horas após a transfecção, as células foram processadas para análise MHA, PCR em tempo real e Western blot.
[00215] Isolamento de RNA, análise por PCR com Transcrição Reversa [(RT)-PCR] e PCR em Tempo Real: Isolamento de RNA, análise por PCR com transcrição reversa (24) e por PCR em tempo real foram realizados usando técnicas de biologia molecular padrão. Iniciadores específicos de gene utilizados para amplificar SLC34A2 por RT-PCR foram 5'-TCA GCC AAA TTG CAA TGA AC-3' e 3'-ATC ATG ATC AGG CAA CCA CA-5'.
[00216] Clonagem, expressão e purificação de proteínas de fusão GST/NaPi2b: Várias regiões da alça extracelular grande de NaPi2b de humano foram amplificadas por PCR e clonadas em vetor pGEX4T1 em matriz com GST. Expressão de fusões GST/NaPi2b em células BL21 DE3 foi induzida por IPTG 1mM por 3 horas a 37°C. Pelotas celulares foram rompidas por sonificação em tampão de lise (Tris-HCl 25 mM, pH 7,5, NaCl 150 mM, EDTA 1 mM, Triton 0,5% e coquetel de inibidor de protease (Boehringer Mannheim, Alemanha) e proteínas de fusão GST foram purificadas dos sobrenadantes clarificados por cromatografia de afinidade usando GST-Sepharose como recomendado pelo fabricante. Detalhes de expressão de His-NaPi2b-ECD em células de inseto Sf9 são dados em SI- texto.
[00217] Ensaios de hemadsorção mista: O ensaio de hemadsorção mista (MHA), que detecta IgG ligada em superfície por aderência de células vermelhas de sangue de humano (grupo sanguíneo O) revestidas com IgG de coelho anti-camundongo para selecionar células, foi realizado como descrito (25).
[00218] Microarranjo de peptídeo sintético: Arranjos de membrana de peptídeos sintéticos abarcando os aminoácidos 312-340 da seqüência de proteína NaPi2b foram preparados sob encomenda (JPT Peptide Technologies, Inc., Springfield, VA). Para mapeamento de epítopo, membranas foram incubadas por 3 horas com 1 μg/mL de anticorpo primário, seguido por incubação com anticorpos policlonais de cabra anti-camundongo marcados com HRP (Jackson ImmunoResearch Laboratories, West Grove, PA) por 2 horas. Anticorpo ligado foi visualizado por quimioluminescência (Western Lightning Plus). Para mapeamento de epítopo sob condições redutoras, as membranas foram incubadas em DTT 1 mM na temperatura ambiente, e então lavadas extensivamente antes da incubação de anticorpo.
[00219] Bloqueio de peptídeo e ELISA de peptídeo: Um peptídeo correspondendo aos aminoácidos 312-340 de NaPi2b foi quimicamente sintetizado (Bio-Synthesis, Inc. Lewisville, TX) e co-incubado em concentrações variadas com mAb MX35 antes do ensaio de ligação de mAb MX35 em células MX35-positivas e MX35-negativas por MHA. Ligação de mAb MX35 no peptídeo sintético 312-340 também foi ensaiada por ELISA usando placas NUNC Maxisorp, nas quais o peptídeo (10 ug/mL em água) fora absorvido por 2 goras na RT.
[00220] Extração em Triton X-114 e tratamentos com glicosidase e análise por acilação: Extração em Triton X-114 das proteínas de membrana é descrita em detalhe em SI-texto. Alíquotas de complexos imunes marcados com 35S ou com 3H-glicosamina foram submetidas ao tratamento com várias glicosidases: N-Glicanase; PNGaseF (5mU), Sialidase A (5mU), O-Glicanase (1,25 mU), β(1-4)Galactosidase (3mU), e β-N-Acetil-glicosaminidase (40mU) usando o Prozyme Enzymatic Deglycosylation Kit (Glyko, San Leandro, CA) de acordo com a instrução do fabricante. Desglicosilação foi monitorada por SDS-PAGE, autorradiografia e análise por Western blot como descrito acima. NaPi2b marcada com 3H-palmitoíla foi obtida por imunoprecipitação das células SK-RC-18 cultivadas na presença de ácido 3H-palmítico, separada por gel Bis-Tris SDS-PAGE 4-12 %, e visualizada por autorradiografia. Para testar ácido palmítico ligado por tioéster-geles SDS-PAGE foram pré- incubados com hidróxido de potássio 0,2 M em metanol, ou hidroxil-amina - ácido clorídrico 1M, pH 7,5 ou Tris 1 M, pH 7,5, seguido por autorradiografia (21).
RESULTADOS
Clonagem molecular do antígeno MX35 por imunotriagem de uma biblioteca de expressão de OVCAR-3 cDNA
[00221] Triagem de uma biblioteca de cDNA gerada de linhagem de célula de câncer ovariano OVCAR-3, que expressa antígeno MX35 sobre sua superfície celular, identificou três clones distintos reativos a mAb MX35 (N1, N4 e N6). Reatividade dos três clones foi confirmada em uma triagem secundária. Subseqüentes seqüenciamento e análise de restrição de cDNA identificaram o clone N1 reativo mais forte a mAb MX35 como codificador de uma forma N-terminalmente truncada da proteína de transporte de fosfato dependente de sódio 2b (gene SLC34A2, tamanho 3394pb; fragmento 742pb - 4135pb), clone N4 uma forma N-terminalmente truncada da proteína dedo de Zinco 638 (ZN638; tamanho 4637pb; fragmento 1798pb - 6434pb), e clone N6 uma forma N-terminalmente truncada da mesma proteína dedo de Zinco 638 (tamanho 3585pb; fragmento 2850pb - 6434pb). Confirmação da identidade de antígeno MX35 como a proteína de transporte de fosfato dependente de sódio 2b (gene SLC34A2) (i) Co-tipificação de expressão de mRNA e expressão em superfície celular de antígeno MX35
[00222] Um painel de linhagens de célula de câncer foi co-tipificado para expressão de SLC34A2 mRNA por RT-PCR e para expressão em superfície celular de antígeno de proteína MX35 em um ensaio de hemadsorção misto (MHA) usando mAb MX35 como sonda. Em adição, lisados de célula foram sondados por análise por Western blot para expressão de MX35. Um painel de linhagens de célula de câncer com expressão conhecida de antígeno MX35 foi incluído. A expressão forte de SLC34A2 mRNA correlacionou com a expressão em superfície celular de antígeno MX35 em todas as células analisadas (Tabela 1). Nenhuma tal correlação foi encontrada para a proteína dedo de Zinco 638 (dados não mostrados). TABELA 1 Expressão de proteína MX35 e SLC34A2 mRNA em um painel de linhagens de célula de câncer diferentes
(ii) Seqüenciamento de peptídeos por fragmentação usando espectrometria de massa
[00223] Imunoprecipitação de antígeno MX35 de duas linhagens diferentes de células OVCAR-3 e SK-RC-18 positivas para antígeno MX35, após marcação metabólica de proteínas com [35S] metionina e [35S] cisteína mostrou uma banda maior (~90kDa) e uma banda menor (~180kDa) sobre SDS-PAGE (Figura 1 A). Subseqüentemente, quantidades preparativas dos complexos imunes de MX35 foram separadas por SDS-PAGE e bandas de proteína marcada com 35S foram excisadas e submetidas à digestão tríptica seguida por seqüenciamento por fragmentação de peptídeos usando espectrometria de massa. Fragmentação de quatro peptídeos selecionados forneceu seqüências de aminoácidos VITKPFTK, LIVQLDKK, IWCK e SLKPWDAVVSK (Fig. 1B) , que mostrou alinhamento completo com aminoácidos 266-273, 274-281, 301-304 e 599-609 na seqüência de proteína NaPi2b (Fig. 1C). Os peptídeos NaPi2b foram identificados em ambas as bandas de proteína. Isto identifica proteína de transporte de fosfato dependente de sódio 2b como o antígeno MX35, em vez de a proteína dedo de Zn também selecionada na triagem molecular inicial. (iii) Interferência de RNA
[00224] Dois conjuntos de siRNAs "on-target" específicos para SLC34A2 foram preparados para analisar se regulação positiva seletiva de expressão de gene SLC34A2 por interferência de RNA resultaria em uma perda ou ligação reduzida de anticorpo MX35 em células de câncer expressando MX35. Ambos os conjuntos de siRNA específico para SLC34A2 seletivamente regularam positivamente SLC34A2 mRNA em células SK-RC- 18 e OVCAR-3 conforme determinado por PCR em tempo real (RT-PCR) (Fig. 2A). Ligação de anticorpo MX35 antígeno MX35 expressado em superfície celular foi significativamente reduzida em MHA (dados não mostrados). Regulação positiva específica de níveis de antígeno de proteína MX35 foi confirmada por análise Western blot (Fig. 2B). siRNA "não- selecionador" não teve efeito sobre níveis de expressão de SLC34A2 mRNA e antígeno de proteína MX35 em ambas as linhagens celulares. Estes resultados adicionalmente validam NaPi2b como o antígeno MX35.
Mapeamento do sítio de ligação de anticorpo em NaPi2b
[00225] Análise bioinformática sugeriu que a proteína codificada por SLC34A2 tem pelo menos 8 domínios de transmembrana potenciais, 5 sítios de domínio intracelular putativos e 4 alças de domínio extracelular putativo com ambas as regiões N- e C-terminais faceando o citoplasma (Fig. 3A). Levando-se em consideração que mAb MX35 reconhece um epítopo expressado sobre a superfície celular, a alça ECD potencial potencialmente maior foi expressada como uma proteína de fusão de GST (cobrindo aa 188361 de NaPi2b) (Fig. 3B) em E. coli e como uma proteína etiquetada com His em células de inseto Sf9 usando um sistema de expressão de baculovírus, e foram sondadas para reatividade com Mab MX35 em Western blots. Ambas as proteínas de fusão foram reconhecidas por mAb MX35. Pré-incubação de mAb MX35 com a proteína de fusão bacteriana pôde seletivamente bloquear a ligação de mAb MX35 em antígeno MX35 naturalmente expressado em tecido de câncer ovariano por imunocitoquímica (dados não mostrados). Subseqüentemente, proteínas de fusão mais curtas, truncadas da terminação-N e da terminação-C (Fig. 3B) foram estudadas e o epítopo de ligação de mAb MX35 foi diminuído para uma proteína de fusão contendo aminoácidos 311340 da seqüência de proteína NaPi2b (Fig. 3C). Ligação de mAb MX35 nesta seqüência de peptídeo foi mais adiante confirmada por ELISA e imuno- mancha dot blot usando como o antígeno um peptídeo 29mer sintético representando aminoácidos 312-340 da proteína NaPi2b. Este peptídeo foi depois truncado da terminação-N e da terminação-C e o epítopo reativo a MX35 foi diminuído para aminoácidos 324-338 como determinado em uma análise de mancha de peptídeo (Tabela 2). Dentro desta região a seqüência WTM (aa 336-338) parece ser elevadamente crítica para reconhecimento de antígeno. Embora a região de aminoácidos 324-338 (SPSLCWTDGIQNWTM) da proteína de humano seja elevadamente homóloga à contra-parte murina (SPSYCWTDGIQNWTI) na proteína NaPi2b, a proteína murina não foi reconhecida pelo mAb MX35 em uma análise Western blot de vários tecidos de camundongo, adicionalmente confirmando WTM como crítico para reconhecimento de anticorpo MX35 (dados não mostrados). De maneira interessante, os resíduos Cys em posições 322 e 328 não são exigidos, porque poderiam ser substituídos por resíduos Ala, embora a reatividade de anticorpo com a NaPi2b de tipo selvagem de comprimento total seja reduzida em sensibilidade. Estes aminoácidos provavelmente não estão envolvidos na alça de cisteína postulada em estabilizar o epítopo; esta alça provavelmente abarca aa 303 até aa 350 (Fig. 1C; UniProtKB/Swiss-Prot entry 005436). TABELA 2 Mapeamento de epítopo de MAb MX35 usando uma série de peptídeos sintéticos localizados em um domínio extracelular putativo (aa 312340) da proteína NaPi2b


[00226] Análise Western blot e experimentos de radioimunoprecipitação com mAb MX35 mostraram que a proteína é expressada em células OVCAR-3 e SK-RC-18 em pelo menos duas formas maiores, uma migrando em um SDS-PAGE a ~90 kDa e uma segunda migrando a cerca de 180 k (Fig. 1A); estas poderiam ser formas monoméricas e diméricas da proteína. Embora reconhecimento de mAb MX35 de seu antígeno seja sensível à redução, imunoprecipitação de antígeno MX35 metabolicamente marcado não mostrou diferença óbvia no padrão de migração em SDS-PAGE entre condições redutoras e não-redutoras. Extração da proteína de células OVCAR-3 com o detergente Triton-X114 mostrou que quase toda a proteína reativa a mAb MX35 dividiu para dentro da fração enriquecida em detergente, inferior, confirmando que NaPi2b é uma proteína de membrana integral (dados não mostrados).
(ii) Características de glicosilação
[00227] Análise de seqüência de produto de gene SLC34A2 prediz 5 sítios de N-glicosilação potenciais em N295, N308, N313, N321 e N340 (Fig. 1C). De modo interessante, todos os 5 sítios de glicosilação putativos parecem agrupados dentro de uma região de peptídeo bastante curto (aa 295-340) localizada na alça de domínio extracelular maior na qual o epítopo de mAb MX35 também foi mapeado (Fig. 1C). Marcação metabólica de células SK- RC-18 com 3H-glicosamina seguida por imunoprecipitação com mAb MX35 mostrou que NaPi2b está de fato elevadamente glicosilada (Fig. 4B) e tratamento com N-glicanase mas não com O-glicanase removeu a maioria deste marcador. Tratamento de imunoprecipitados marcados com [35S] Met e Cys com várias glicosidases mostrou que as cadeia de glicano foram sensíveis à N-glicosidase confirmando que quase todos os açúcares no antígeno MX35 estavam N-ligados como predito. Apenas uma proporção menor do carboidrato foi sensível à O-glicosidase e sialidase ou a uma mistura de O- glicosidase, sialidase, β-galactosidase e N-acetil-glicosaminidase. Tratamento com uma combinação de N- e O-glicosidases resultou em um deslocamento de migração das bandas reativas MX35em SDS-PAGE de ~90 kDa para 5560 kDa e de ~180 kDa para 130-140 kDa. A primeiro número é muito menor do que o tamanho de peptídeo predito para a proteína não processada desta seqüência de cDNA (75,7 kDa) mas a proteína pode migrar anomalamente sobre SDS-PAGE por causa de muitas de suas regiões hidrofóbicas.
(iii) Características de acilação
[00228] Estudos de bioinformática revelaram uma região rica em cisteína na extremidade C-terminal, que poderia ser sítios potenciais para palmitoilação. De fato, marcação metabólica de células SK-RC-18 com ácido 3H-palmítico seguida por imunoprecipitação com mAb MX35 e análise por SDS-PAGE sugere que proteína MX35 está acilada (Fig. 4C). Tratamento com base mostrou que acilação é parcialmente reversível.
DISCUSSÃO:
[00229] MAb MX35 foi desenvolvido como um reagente terapêutico para o tratamento de câncer ovariano. Em testes clínicos de fase I anticorpo MX35 murino radiomarcado selecionou bem tumores em pacientes com câncer ovariano (2, 3) e o anticorpo está correntemente sendo estudado em um teste clínico de fase I como carreador de radionuclídeo emissor de partícula alfa astato-211 para radioimunoterapia de câncer ovariano (6). Embora, tenha havido esta exploração clínica de mAb MX35 tem sido difícil definir a identidade molecular do antígeno MX35. Agora temos identificado de modo claro a proteína de transporte de fosfato dependente de sódio 2b (NaPi2b) como o alvo molecular reconhecido por mAb MX35. Esta conclusão é baseada na seguinte evidência experimental:
[00230] 1) Um clone codificador de uma forma N-terminalmente truncada de NaPi2b (gene SLC34A2, tamanho 3394pb; fragmento 742pb - 4135pb) foi isolado de uma biblioteca de cDNA gerada da linhagem de célula de câncer ovariano OVCAR-3, que expressa MX35 sobre sua superfície celular; 2) Co-tipificação de um painel de linhagens de células de câncer mostrou uma correlação boa de expressão de SLC34A2 RNA por RT-PCR e expressão sobre superfície celular de MX35 conforme determinado por ensaios de hemadsorção mista; 3) Isolamento de MX35 de linhagens de células de câncer OVCAR-3 e SK-RC-18 expressando MX35 e subseqüente seqüenciamento de proteína por fragmentação de peptídeos usando espectrometria de massa forneceu seqüências de aminoácidos que mostraram alinhamento completo com as seqüências de aminoácidos em NaPi2b; 4) Regulação positiva seletiva de expressão de gene SLC34A2 em células de câncer expressando MX35 por interferência de RNA resultou na perda ou ligação reduzida de mAb MX35; 5) A alça extracelular putativa maior da proteína de multi-transmembrana NaPi2b foi expressada em células de inseto e de E. coli e ambos os produtos de expressão foram reconhecidos por mAb MX35 em ensaios Western blot e bloquearam a ligação de mAb MX35 em tecidos de câncer ovariano em imuno-histoquímica; 6) Um peptídeo sintético pequeno com 100% de homologia de seqüência com aminoácidos 312-340 da alça extracelular maior de NaPi2b foi reativo com mAb MX35 em ensaios dot blot e por ELISA.
[00231] SLC34A2 é um membro da família de gene de carreador de soluto (8, 9) e dos mapas de gene para cromossomo 4p15.2. O gene SLC34A2 codifica uma proteína de membrana de multi-passagem de 690 aminoácidos (Fig 3A). Tem sido relatado que esta proteína medeia o transporte de fosfato inorgânico para dentro de células epiteliais via co-transporte de íon sódio e pode ter um papel em homeostasia de fosfato (para revisão veja (10, 11)) e na síntese de tensoativos em alvéolos pulmonares (12). A proteína de humano, proteína de transporte de fosfato dependente de sódio 2b (NaPi2b) ou membro 2 da família 34 de carreador de soluto, também tem vários outros sinônimos. SLC34A2 cDNA foi primeiro isolado e clonado de uma biblioteca de cDNA de pulmão e intestino delgado de humano (8, 9) e subseqüente análise de expressão de gene por Northern Blot mostrou que SLC34A2 era elevadamente expressado no pulmão e em níveis baixo a moderado em vários outros tecidos normais de humano incluindo traquéia, rim, intestino delgado, ovário, placenta, útero, testículo, próstata, pâncreas, glândula mamária, glândula tiróide, glândula salivar. Uma pesquisa em banco de dados de EST confirmou expressão do gene SLC34A2 em tiróide, ovário, traquéia e glândula mamária mas mostrou aquelas pessoas experientes na apenas umas poucas contagens de EST em rim, intestino delgado, placenta, útero, testículo e próstata. Expressão no pulmão adicionalmente confirmada por varreduras de genoma (13, 14) e visualização de mRNA por hibridização "in-situ" mostrou a expressão mais alta em células alveolares de tipo II (13). Expressão aumentada de gene SLC34A2 tem sido relatada em câncer ovariano (15) e câncer papilar de tiróide (16).
[00232] Até agora, o SLC34A2 de humano tem sido caracterizado largamente em nível de gene e atividades de transportador NaPi2b foram geralmente estudadas com proteína recombinante expressada em oócitos de xenopus (8, 9, 13, 17, 18). Pouco tem sido relatado sobre a bioquímica do produto de proteína naturalmente expressado de SLC34A2. Neste relato, fornecemos evidência experimental de que NaPi2b é naturalmente expressada como uma proteína de membrana plasmática elevadamente glicosilada em células de câncer. Poderíamos mostrar que o ECD potencialmente maior predito (aa 188-361) de NaPi2b é de fato expressado sobre a superfície da célula, ou pelo menos a sua parte maior, como o epítopo antigênico reconhecido por mAb MX35 (aa 324-338) está localizada dentro do ECD predito e mAb MX35 ligado em células de câncer expressando NaPi2b em um ensaio de ligação de superfície de célula MHA. Também fornecemos evidência experimental de que a ponte de dissulfeto predita no ECD de NaPi2b está formada entre C303 e C350 e não envolve C322 e C328. Isto é baseado na observação de que mAb MX35 apenas pode reagir com NaPi2b não-reduzida, naturalmente expressada, mas reconheceu o peptídeo sintético 311-340 (contendo C322 e C328) em ambas as formas reduzida e não- reduzida. NaPi2b está elevadamente glicosilada e temos mostrado por clivagem por exoglicosidase que as carboidrases, em sua vasta maioria, estão N-ligadas. Sítios de N-glicosilação preditos estão localizados no ECD em aminoácidos N295, N308, N313, N321 e N340. É de interesse que todos os sítios de glicosilação preditos estejam dentro ou intimamente próximos do epítopo de aminoácidos reconhecido por mAb MX35 (aa 324-338) mas não interfiram com ligação do anticorpo porque NaPi2v glicosilada e não- glicosilada liga-se igualmente bem em mAb MX35 em ensaios Western blot e ensaios de imunoprecipitação. Também fornecemos evidência experimental para outras modificações de pós-tradução de NaPi2b, mostrando por marcação metabólica que palmitato foi incorporado na proteína indicando que NaPi2b está provavelmente naturalmente palmitoilada. Sítios de palmitoilação potenciais podem estar localizados dentro do domínio citoplásmico C- terminal, que contém um segmento rico em cisteína de 17 cisteínas dentro de aminoácidos 613-645. Acilação de NaPi2b foi parcialmente reversível por tratamento com hidroxil-amina sugerindo que NaPi2b pode ser palmitoilada tanto transientemente quanto permanentemente. Parece que a proteína é expressada na membrana plasmática em pelo menos duas formas maiores distinguíveis por seu peso molecular aparente (90 kDa e 180 kDa) por SDS- PAGE, e que provavelmente representa formas monoméricas e diméricas da proteína conforme determinadas por espectrometria de massa. Presença de formas homodiméricas de NaPi2b têm sido propostas baseado em análise de microfotografia de fratura congelada de oócitos expressando NaPi2b recombinante de linguado (11).
[00233] Com a identificação de mAb MX35 reconhecendo um produto de proteína de SLC34A2 agora tem se tornado possível ligar os perfis de expressão de mRNA do gene SLC34A2 aos seus produtos de gene em nível de proteína e estudar a expressão de NaPi2b em tecidos normais e em câncer. Se os produtos de gene SLC34A2 em câncer e em tecidos normais são iguais ou diferentes necessitará ser determinado porque expressão de gene SLC34A2 anômala tem sido recentemente relatada. Tem sido recentemente descrito que mutações de exon em SLC34A2 (o gene contém 13 exons dos quais 12 são exons codificadores) ocorrem em pacientes com microlitíase alveolar pulmonar (13, 14). Foi predito que estas mutações afetam tradução, potencialmente resultando em vários produtos de gene alterados incluindo, expressão de proteínas truncadas ou proteínas com substituições de aminoácido, e editoração aberrante ou incapacidade para expressar a proteína. Várias daquelas traduções aberrantes resultaram em uma perda funcional da proteína NaPi2b, quando expressada como proteína recombinante in-vitro. Visto que SLC34A2 é aparentemente o único transportador de fosfato conhecido elevadamente expressado no pulmão, mutações inativadoras do gene SLC34A2 foram associadas com acúmulos de micrólitos de fosfato de cálcio no espaço alveolar e tem sido relatado que SLC34A2 é o gene causador de microlitíase alveolar pulmonar em dois estudos independentes (13, 14). Agora temos iniciado uma análise mutacional do gene SLC34A2 em vários tipos de câncer expressando antígeno MX35, incluindo câncer ovariano, de pulmão e câncer de rim, para investigar se formas mutadas do gene também podem estar presentes em câncer em certos tipos de tumor.
[00234] O anticorpo MX35, que agora temos mostrado que reconhece NaPi2b, havia sido inicialmente desenvolvido contra câncer ovariano e o anticorpo mostrou reatividade homogênea com aproximadamente 90% dos cânceres epiteliais ovarianos de humano mas com apenas um número limitado de tecidos normais por imuno-histoquímica. Em seções de tecido congelado, a reatividade de mAb MX35 foi detectada com células epiteliais normais de pulmão, brônquio, tiróide, útero, cérvix, tuba de falópio, glândulas sudoríparas e dos dutos coletoras no rim (1). Embora este perfil de expressão em tecido de MX35 em nível de proteína pareça estar bem correlacionado com o perfil de expressão de gene relatado para SLC34A2, a análise de expressão de proteína NaPi2b em tecido de humano necessitará ser revisada com metodologias imuno-histoquímicas mais avançadas. Temos agora iniciado um estudo abrangente investigando expressão de NaPi2b em tecido humano normal e em uma ampla variedade de tipos diferentes de câncer de humano utilizando novas técnicas de recuperação de antígeno, que facilitam a reatividade de MX35 em material de arquivo.
[00235] Quais são as perspectivas para NaPi2b como um alvo para terapias de câncer baseadas em anticorpo em humanos? O interesse principal seria a expressão em tecido normal, particularmente no pulmão. Contudo, em análise de biodistribuição / farmacocinética inicial de mAb MX35 em humanos, houve boa localização de tumor sem evidência de acúmulo no pulmão ou em outros tecidos normais. De outros estudos com seleção de anticorpo monoclonal em testes clínicos expressão "in-vitro" de antígeno por imuno-histoquímica não necessariamente prediz localização de anticorpo "in- vivo", e isto é melhor explicado pela inacessibilidade de células expressando antígeno ao anticorpo proveniente do sangue. A outra questão que necessita ser solucionada é o impacto relativo desta bomba de fosfato e outros membros SLC relacionados em células de câncer comparadas com células normais com relação à viabilidade e à proliferação. Solução destas questões de acessibilidade in-vivo e o papel destes genes em células de câncer serão críticos na determinação das estratégias terapêuticas ótimas para mAb MX35. Com a identificação de NaPi2b como o alvo molecular de mAb MX35 se tornou evidente que o antígeno MX35 é não apenas expressado em cânceres ovarianos mas também em uma série de outros cânceres epiteliais, incluindo câncer de pulmão, câncer de tiróide e câncer renal potencialmente utilizando a aplicação terapêutica do anticorpo MX35 naqueles e outros tipos de câncer. NaPi2b é o primeiro exemplo de um transportador de fosfato que pode ser selecionado como antígeno de câncer com um anticorpo monoclonal. É concebível que também outros membros da família de transportadores de soluto, a maioria deles como SLC34A2/NaPi2b sob controle regulatório rigoroso se tornam anormalmente expressados em câncer, e conseqüentemente vêm a ser alvos potenciais para imunoterapia de câncer com anticorpos e vacinas.
REFERÊNCIAS
[00236] 1. Mattes, M. J., Look, K., Furukawa, K., Pierce, V. K., Old, L. J., Lewis, J. L., Jr., e Lloyd, K. O. (1987) Mouse monoclonal antibodies to human epithelial differentiation antigens expressed on the surface of ovarian carcinoma ascites cells. Cancer Res 47, 6741-50. (PMID: 3677104).
[00237] 2. Rubin, S. C, Kostakoglu, L., Divgi, C, Federici, M. G., Finstad, C. L., Lloyd, K. O., Larson, S. M., e Hoskins, W. J. (1993) Biodistribution and intraoperative evaluation of radiolabeled monoclonal antibody MX35 in patients with epithelial ovarian cancer. Gynecol Oncol 51, 61-6. (PMID: 8244176).
[00238] 3. Finstad, C. L., Lloyd, K. O., Federici, M. G., Divgi, C, Venkatraman, E., Barakat, R. R., Finn, R. D., Larson, S. M., Hoskins, W. J., e Humm, J. L. (1997) Distribution of radiolabeled monoclonal antibody MX35 F(ab')2 in tissue samples by storage phosphor screen imageanalysis: evaluation of antibody localization to micrometastatic disease in epithelial ovarian cancer. Clin Cancer Res 3, 1433-42. (PMID: 9815829).
[00239] 4. Back, T., Andersson, H., Divgi, C. R., Hultborn, R., Jensen, H., Lindegren, S., Palm, S., e Jacobsson, L. (2005) 211At radioimmunotherapy of subcutaneous human ovarian cancer xenografts: evaluation of relative biologic effectiveness of an alpha-emitter in vivo. J Nucl Med 46, 2061-7. (PMID: 16330571).
[00240] 5. Elgqvist, J., Andersson, H., Back, T., Claesson, I., Hultborn, R., Jensen, H., Lindegren, S., Olsson, M., Palm, S., Warnhammar, E., e Jacobsson, L. (2006) Fractionated radioimmunotherapy of intraperitoneally growing ovarian cancer in nude mice with 211At-MX35 F(ab')2: therapeutic efficacy and myelotoxicity. Nuclear Med Biol 33, 1065-72. (PMID: 17127181).
[00241] 6. Hultborn R, A. H., Back T, Divgi C, Elgqvist J, Himmelman J, Horvath G, Jensen H, Lindegren S, Palm S, Jacobsson L (2006) Pharmacokinetics and dosimetry of 211At-MX35 F(ab')2 in therapy of ovarian cancer—preliminary results from an ongoing phase I study [abstract]. Cancer Biother Radiopharm 21, 373 -81.
[00242] 7. Welshinger, M., Yin, B. W., and Lloyd, K. O. (1997) Initial immunochemical characterization of MX35 ovarian cancer antigen. Gynecol Oncol 67, 188-192.
[00243] 8. Feild, J. A., Zhang, L., Brun, K. A., Brooks, D. P., e Edwards, R. M. (1999) Cloning and functional characterization of a sodiumdependent phosphate transporter expressed in human lung and small intestine. Biochem Biophys Res Commun 258, 578-82. (PMID: 10329428).
[00244] 9. Xu, H., Bai, L., Collins, J. F., e Ghishan, F. K. (1999) Molecular cloning, functional characterization, tissue distribution, and chromosomal localization of a human, small intestinal sodium-phosphate (Na+-Pi) transporter (SLC34A2). Genomics 62, 281-4. (PMID: 10610722)
[00245] 10. Murer, H., Forster, I., e Biber, J. (2004) The sodium phosphate cotransporter family SLC34. Pflugers Arch 447, 763-7. (PMID: 12750889).
[00246] 11. Forster, I. C, Hernando, N., Biber, J., e Murer, H. (2006) Proximal tubular handling of phosphate: A molecular perspective. Kidney Ml 70, 1548-59. (PMID: 16955105).
[00247] 12. Traebert, M., Hattenhauer, O., Murer, H., Kaissling, B., e Biber, J. (1999) Expression of type II Na-P(i) cotransporter in alveolar type II cells. Am J Physiol 277, L868-73. (PMID: 10564169).
[00248] 13. Huqun, Izumi, S., Miyazawa, H., Ishii, K., Uchiyama, B., Ishida, T., Tanaka, S., Tazawa, R., Fukuyama, S., Tanaka, T., Nagai, Y., Yokote, A., Takahashi, H., Fukushima, T., Kobayashi, K., Chiba, H., Nagata, M., Sakamoto, S., Nakata, K., Takebayashi, Y., Shimizu, Y., Kaneko, K., Shimizu, M., Kanazawa, M., Abe, S., Inoue, Y., Takenoshita, S., Yoshimura, K., Kudo,K., Tachibana, T., Nukiwa, T., e Hagiwara, K. (2007) Mutations in the SLC34A2 gene are associated with microlitíase alveolar pulmonar. Am JRespi Crit Care Med 175, 263-8. (PMID: 17095743).
[00249] 14. Corut, A., Senyigit, A., Ugur, S. A., Altin, S., Ozcelik, U., Calisir, H., Yildirim, Z., Gocmen, A., e Tolun, A. (2006) Mutations in SLC34A2 cause microlitíase alveolar pulmonar and are possibly associated with testicular microlithiasis. Am J Hum Genet 79, 650-6. (PMID: 16960801).
[00250] 15. Rangel, L. B., Sherman-Baust, C. A., Wernyj, R. P., Schwartz, D. R., Cho, K. R., e Morin, P. J. (2003) Characterization of novel human ovarian cancer-specific transcripts (HOSTs) identified by serial analysis of gene expression. Oncogene 22, 7225-32. (PMID: 14562052).
[00251] 16. Jarzab, B., Wiench, M., Fujarewicz, K., Simek, K., Jarzab, M., Oczko-Wojciechowska, M., Wloch, J., Czarniecka, A., Chmielik, E., Lange, D., Pawlaczek, A., Szpak, S., Gubala, E., e Swierniak, A. (2005) Gene expression profile of papillary thyroid cancer: sources of variability and diagnostic implications. Cancer Res 65, 1587-97. (PMID: 15735049).
[00252] 17. Xu, H., Uno, J. K., Inouye, M., Xu, L., Drees, J. B., Collins, J. F., e Ghishan, F. K. (2003) Regulation of intestinal NaPi-IIb cotransporter gene expression by estrogen. Am J Physiol 285, Gl 317-24. (PMID: 12893629).
[00253] 18. Matsuo, A., Negoro, T., Seo, T., Kitao, Y., Shindo, M., Segawa, H., e Miyamoto, K. (2005) Inhibitory effect of JTP-59557, a new triazole derivative, on intestinal phosphate transport in vitro and in vivo. Eur J Pharmacol 517, 111-9. (PMID: 15961073).
[00254] 19. Yin, B. W., e Lloyd, K. O. (2001) Molecular cloning of the CA125 ovarian cancer antigen: identification as a new mucin, MUC16. J Biol Chem 276, 27371-5. (PMID: 11369781).
[00255] 20. Yin, B. W., Finstad, C. L., Kitamura, K., Federici, M. G., Welshinger, M., Kudryashov, V., Hoskins, W. J., Welt, S., e Lloyd, K. O. (1996) Serological and immunochemical analysis of Lewis y (Ley) blood group antigen expression in epithelial ovarian cancer. Int J Cancer 65, 406-12. (PMID: 8621218).
[00256] 21. Ritter, G., Cohen, L. S., Nice, E. C, Catimel, B., Burgess, A. W., Moritz, R. L., Ji, H., Heath, J. K., White, S. J., Welt, S., Old, L. J., e Simpson, R. J. (1997) Characterization of posttranslational modifications of human A3 3 antigen, a novel palmitoylated surface glycoprotein of human gastrointestinal epithelium. Biochem Biophys Res Commun 236, 682-6. (PMID: 9245713).
[00257] 22. Iwahana, H., Yakymovych, I., Dubrovska, A., Hellman, U., e Souchelnytskyi, S. (2006) Glycoproteome profiling of transforming growth factor-beta (TGFbeta) signaling:nonglycosylated cell death-inducing DFF-like effector A inhibits TGFbetal-dependent apoptosis. Proteomics 6, 6168-80. (PMID: 17080483).
[00258] 23. Peters, E. C, Horn, D. M., Tully, D. C, e Brock, A. (2001) A novel multifunctional labeling reagent for enhanced protein characterization with mass spectrometry. Rapid Commun Mass Spectrom 15, 2387-92. (PMID: 11746907).
[00259] 24. Gure, A. O., Chua, R., Williamson, B., Gonen, M., Ferrera, C. A., Gnjatic, S., Ritter, G., Simpson, A. J., Chen, Y. T., Old, L. J., e Altorki, N. K. (2005) Cancer-testis genes are coordinately expressed and are markers of poor outcome in non-small cell lung cancer. Clin Cancer Res 11, 8055-62. (PMID: 16299236)
[00260] 25. Pfreundschuh, M., Shiku, H., Takahashi, T., Ueda, R., Ransohoff, J., Oettgen, H. F., e Old, L. J. (1978) Serological analysis of cell surface antigens of malignant human brain tumors. Proc Natl Acad Sci USA 75, 5122-6. (PMID: 283420).
[00261] EXEMPLO 2
[00262] As seqüências de nucleotídeos e de polipeptídeo do anticorpo MX35 de camundongo agora têm sido determinadas. As seqüência de região variável de cadeia pesada é fornecida em FIGURA 5. A seqüência de região variável de cadeia pesada inclui as seqüências dos três domínios CDR, CDR1 (GYTFTGYNIH), CDR2 (AIYPGNGDTSYKQKFRG) e CDR3 (GETARATFAY). A seqüência de região variável de cadeia leve é fornecida em FIGURA 6. A seqüência de região variável de cadeia leve inclui as seqüências dos três domínios CDR, CDR1 (SASQDIGNFLN), CDR2 (YTSSLYS) e CDR3 (QQYSKLPLT).
EXEMPLO 3
Desenvolvimento de anticorpos monoclonais específicos para co- transportador de fosfato dependente de sódio NaPi2b
[00263] A homeostasia de fosfato inorgânico em corpo humano é mantida por absorção, metabolismo e excreção regulados. Transportadores de fosfato dependentes de sódio (NaPi) medeiam o transporte de fosfato inorgânico (Pi) dentro de células em resposta ao consumo de fosfato dietético, hormônios, e fatores de crescimento. NaPi2b é um membro da família de transportadores de fosfato dependentes de sódio com um padrão distinto de expressão e regulação. Rotas de sinalização ativadas por mitógenos, glicocorticóides e fatores metabólicos têm estado implicadas em regulação de transporte de Pi via NaP2b. Inativação da função de NaPi2b por mutações tem estado ligada às patologias de humano, tal como microlitíase alveolar pulmonar. Neste estudo, descrevemos a produção e a caracterização de anticorpos monoclonais direcionados contra NaPi2b. Foi mostrado que anticorpos gerados reconhecem NaPi2b endógeno e transientemente expressado em imunoensaios comumente usados, tais como Western blotting, imunoprecipitação e imuno-histoquímica. Estas propriedades os tornam particularmente valiosos para elucidar a função de NaPi2b em saúde e doença.
INTRODUÇÃO
[00264] Concentração celular de fosfato inorgânico (Pi) deve ser mantida constante para regulação apropriada de crescimento, metabolismo e rotas de sinalização, bem como para formação de osso. Homeostasia de fosfato inorgânico é mantida por vários mecanismos, principalmente através da regulação de sua absorção e de seu metabolismo. Captação celular de Pi é mediada pelos transportadores de fosfato dependentes de sódio (pertencendo à série de carreadores de soluto, SLC) que poderiam ser agrupados em três subtipos baseados em identidade de seqüência: NaPi-I (SLC 17), NaPi-II (SLC34) e NaPi-III (SLC20). NaPi2b (NaPi-IIb, SLC34A2, NaPi3b, NPT-2) pertence à família de tipo II de transportadores de fosfato dependentes de sódio que também inclui NaPi2a (NaPi-IIa) e NaPi2b (NaPi-IIc). Co-transportadores Na/Pi de tipo II são expressados em vários tecidos e desempenham um papel maior na homeostasia de fosfato inorgânico. NaPi2b foi identificado por dois laboratórios independentes pela utilização de triagens de homologia bioinformática (1,2). NaPi2b é uma proteína de transmembrana que está ancorada nas membranas celulares através de pelo menos 8 regiões α-helicoidais elevadamente hidrofóbicas. Na topologia predita de NaPi2b, ambas as caudas N- e C-terminais faceiam o citoplasma, expondo alças de vários comprimentos aos compartimentos extracelulares e intracelulares. A alça extracelular maior contém vários sítios potenciais de glicosilação e uma região rica em resíduos de cisteína que poderiam estar envolvidos em formação de ligação de dissulfeto. Sobre o gel SDS-PAGE, NaPi2b corre como uma banda difusa de aproximadamente 95-108 kDa (3). Ademais, NaPi2b também pode existir como um dímero (4). Estudos de expressão indicaram que NaPi2b é expressada em intestino delgado, pulmão, testículo, fígado, ovário, glândulas mamárias secretórias, glândulas salivares e osteoblastos (1, 5-9). Foi verificado que o nível de NaPi2b é controlado por muitos hormônios e fatores metabólicos de acordo com as necessidades de Pi do corpo. Tem sido relatado que o nível aumentado de NaPi2b é induzido por dieta baixa em fosfato, por vitamina D, por estrogênios (10, 11). Regulação positiva de nível de NaPi2b em resposta a FGF 23, EGF e glicocorticóides foi demonstrada em modelos celulares (12, 13, e 14). Em adição, é sabido que Pi e carbonato tamponam prótons em sangue durante acidose metabólica. Para servir em tamponamento de prótons, Pi é liberado de osso junto com carbonato ou reposto por absorção intestinal de NaPi2b (15). Estudos imuno- histoquímicos mostraram que NaPi2b está localizada principalmente em bordas em escova de enterócitos ou em membranas apicais de células epiteliais de mamífero (2,16). NaPi2b transporta Pi divalente junto com três íons Na+ por mecanismo eletrogênico. Rotas de sinalização que regulam a função de NaPi2b não estão bem entendidas. Recentemente, a capacidade de quinase induzível por soro e glicocorticóide (SGK1) em estimular o transporte de fosfato via NaPi2b foi demonstrada (17). Ademais, foi mostrado que a atividade de NaPi2b é inibida por rapamicina, indicando o envolvimento de rota de sinalização mTor na regulação de homeostasia de fosfato (18).
[00265] Desregulação de função de NaPi2b tem estado ligada às patologias humanas. Tem sido recentemente demonstrado que mutações em NaPi2b causam microlitíase alveolar pulmonar (19). Ademais, a sobre- expressão de NaPi2b foi observada em tumores ovariano, de mama e papilar de tiróide (20, 21, 22). Ademais ligação de NaPi2b ao câncer tem sido recentemente estabelecida. O consórcio comandado pelo Ludwig Institute for Cancer Research identificou NaPi2b como antígeno de câncer MX35, que tem estado associado com câncer ovariano há muitos anos (23).
[00266] Neste estudo, descrevemos a produção e a caracterização de anticorpos monoclonais específicos para NaPi2b. Um fragmento de NaPi2b foi expressado em bactérias como proteína de fusão GST e usado para procedimentos de imunização e triagem. Várias rodadas de triagem permitiram que selecionássemos dois anticorpos monoclonais, chamados L2(20/3) e L3(28/1), que reconhecem NaPi2b especificamente endógena em vários ensaios imunológicos, incluindo Western blotting, imunoprecipitação e imuno-histoquímica. Anticorpos gerados e caracterizados seriam úteis e estariam disponíveis para comunidade acadêmica estudar a função de NaPi2b.
MATERIAIS E MÉTODOS
[00267] Linhagens de célula. Todas as linhagens de célula foram obtidas do banco de células do Ludwig Institute for Cancer Research, New Y ork Branch em Memorial Sloan-Kettering Cancer Center.
[00268] Produção e purificação de proteínas de fusão GST-NaPi2b. O domínio (alça) extracelular de NaPi2b de humano (L, alça, 188-361aa) e vários fragmentos deste domínio (1L, 188-300aa; 2L 291-361aa; 3L, 291- 340aa; 4L, 311-340aa; 5L, 311-361aa) foram amplificados por PCR usando iniciadores oligonucleotídeo específicos com sítios de restrição BamHl e EcoRl e clonados em vetor pGEX4Tl (Novagen) em matriz com a seqüência de etiqueta-GST C-terminal. Os construtos resultantes, chamados de pGEX- 4T1-NaPi2b-L, pGEX-4T1-NaPi2b-1L, pGEX-4T1-NaPi2b-2L, pGEX-4T1- NaPi2b-3L, pGEX-4T1-NaPi2b-4L, pGEX-4T1-NaPi2b-5L foram transformados em células de cepa de E. coli BL21(DE3). A expressão de proteínas recombinantes foi induzida com iso-propil-b-D(2)-tio-galacto- piranosídeo (IPTG) 1 mM por 1-3 ha 30°C. Purificação de proteínas recombinantes GST-NaPi2b da fração solúvel de lisado bacteriano foi realizada usando GST Agarose (Qiagen, UK) de acordo com as recomendações do fabricante. Purificação de GST-NaPi2b-L da fração insolúvel foi realizada usando eletro-eluição do gel.
[00269] Produção de células de hibridoma. Camundongos fêmeas BALB/c de 6-8 semanas de idade foram imunizados por injeção intraperitoneal (i.p.) com 15 μg de proteína de fusão recombinante GST- NaPi2b-L(188-361aa) em adjuvante completo de Freund 4 vezes em intervalo de duas semanas. Então, os camundongos imunizados (com título em soro menor do que 10-5-10-6) foram reforçados com 20 μg de antígeno em PBS por injeção i.p. Três dias mais tarde esplenócitos de camundongos imunizados foram fusionados na presença de PEG (MW2000, Merck, Alemanha) com células de mieloma SP2/0 cultivadas em meio RPMI 1640 contendo 20% de soro fetal bovino (FCS). Triagem primária de sobrenadantes de hibridoma foi realizada usando técnica de ELISA e clones positivos isolados foram subclonados pelo método de diluição limitada usando GST-NaPi2b-L como antígeno (24).
[00270] Análise Western blot de proteínas recombinantes. Para triagem de hibridoma proteínas recombinantes GST-NaPi2b bacterialmente expressadas: GST-NaPi2b-L 188-361aa, ou GST-NaPi2b-1L 188-300 aa, ou GST-NaPi2b-2L 291-361aa foram separadas por um 10% SDS/PAGE e eletrotransferidas para membrana Immobilon-P (Millipore, USA). A membrana foi bloqueada por leite desnatado 5% em PBS, contendo 0,1% de Tween 20 (PBST) por 1 h na temperatura ambiente e dividida em tiras seguido por uma lavagem única com PBST. Tiras foram incubadas com PBS, soro pós-imune (1:1000), meio de hibridoma de clones positivos, ou meio de cultura celular sozinho por 2 h na temperatura ambiente. Anticorpo secundário conjugado com peroxidase (Promega, USA) foi adicionado nas tiras após três lavagens e incubado por 1 h na temperatura ambiente. Tiras foram lavadas três vezes, e a imunorreatividade foi detectada pelo sistema ECL (Amersham, Suécia).
[00271] Para mapeamento de epítopo de mAbs peptídeos recombinantes (GST-NaPi2b-L, GST-NaPi2b-1L, GST-NaPi2b-2L, GST- NaPi2b-3L, GST-NaPi2b-4L, GST-NaPi2b-5L) têm sido analisados em WB como descrito acima e incubados com mAbs L2(2/1), L2(20/3) e L3(28/1). mAbs Anti-GST foram usados como um controle para expressão de proteínas recombinantes.
[00272] Purificação de mAbs. Camundongos BALB/c foram injetados com 0,5 mL de pristane e 7-10 dias mais tarde inoculados com 5-106 de células de hibridoma (18). O fluido ascítico foi coletado após 7-10 dias, e após centrifugação por 20 min a 14000 rpm, e filtração por filtro de 0,4μm (Millipore, USA) foi usado para purificação por afinidade por cromatografia em Protein A-Sepharose CL-4B (Amersham, Suécia). As frações de IgG foram reunidas e dialisadas em uma solução salina tamponada com fosfato (PBS), pH 7,4. As alíquotas de anticorpos purificados foram armazenadas a - 20°C.
[00273] Preparação e immunoblotting de lisado celular. Células OVCAR3, SK-RC-18, SK-RC-01 foram lisadas em tampão contendo Tris- HCl 10 mM, pH 7,5, NaCl 150 mM, MgCh 10mM, NP-40 0,5% e uma mistura de Coquetel de Inibidor de Protease Halt (Pierce). Concentração de proteína foi estimada pelo ensaio BSA (Pierce), e quantidades iguais de proteínas (10 μg) foram resolvidas em 8% SDS-PAGE. Geles foram transferidos para membrana de poli(difluoreto de vinilideno) (PVDF) (Millipore, USA). A membrana foi bloqueada com BSA 5% em 1x PBST por 1 h na RT. mAbs anti-NaPi2b foram incubados com membranas a 4°C durante a noite. Após lavagem com PBST, IgG de cabra anti-camundongo conjugada com HRP 1:5000 (Promega, USA) foi adicionada na membrana por 1 h na RT. Western blots foram desenvolvidos usando o sistema ECL (Amersham, Suécia) e então expostos ao filme Agfa de raios-X.
[00274] Análise imuno-histoquímica. mAbs anti-NaPi2b foram usados para análise imuno-histoquímica de amostras de câncer ovariano de acordo com um protocolo padrão. Resumidamente, seções representativas de tumores ovarianos foram preparadas de blocos de parafina. Peroxidase endógena foi extinta com H2O2 (3%) em PBS 0,01%. Após bloqueio de coloração não- específica com solução de bloqueio de avidina-biotina (Vector Laboratories, Burlinghame, CA, USA), seções de tecido foram incubadas durante a noite a 4°C com mAb anti-NaPi2b (10 mkg/mL). Então seções foram incubadas com anticorpos secundários biotinilados por 2 horas na temperatura ambiente (1:400, IgG de cabra anti-camundongo biotinilada, Sigma), seguido por incubação com complexo de avidina-biotina-peroxidase (Vector Laboratories, Burlinghame, CA, USA; 30 min, temperatura ambiente) e revelado com solução de diamino-benzidina. Hematoxilina foi usada para contra-coloração. Microscopia padrão foi realizada usando um microscópio Zeiss Universal (Zeiss, Alemanha), e imagens foram capturadas usando programa de computador Axiocam digital.
[00275] Transfecção transiente de células Hek293. Transfecção de células Hek293 foi realizada com reagente de transfecção FuGene (Roshe, Suíça) de acordo com as instruções do fabricante. Resumidamente, para cada transfecção 5 mkg de DNA plasmídeo (pcDNA3.1/Glu-Napi2b ou vetor vazio) e 10 mkl de FuGene foram usados. Após incubação de 48 h células foram lisadas e analisadas.
[00276] Imunoprecipitação. 25 μl de suspensão 50% de Protein A- Sepharose CL-4B (Amersham, Suécia) foram incubados com meio de hibridoma de clones positivos selecionados por 1 h a 4°C em rotação e então analisados por tampão de lise. Sobrenadantes (500 μg de proteína total) de células Hek 293 transfectadas com pcDNA3.1/NaPi2b ou pcDNA3.1 sozinho foram adicionados em glóbulos. Após incubação em roda a 4°C por 3h, glóbulos foram lavados quatro vezes com 1 mL de tampão de lise como descrito acima. Glóbulos foram fervidos em tampão de amostra Laemmli e complexos imunes foram separados por 8% SDS-PAGE para posteriores immunoblotting ou coloração Coomassie.
[00277] Ensaios de hemadsorção mista. O ensaio de hemadsorção mista (MHA), que detecta IgG ligada em superfície por aderência de células vermelhas de sangue de humano (grupo sanguíneo O) revestidas com IgG de coelho anti-camundongo em células alvo, foi realizado como descrito (25).
[00278] Detecção de isótipo de anticorpo. Isótipos de anticorpos foram definidos com kit de teste de isotipificação monoclonal de camundongo (AbD Serotec, UK) usando sobrenadantes de cultura de clones KL2(2/1), KL2(20/3), KL3 (28/1).
RESULTADOS E DISCUSSÃO
[00279] Transporte de Pi através de membrana por cotransportadores de NaPi é reconhecido como um evento regulatório chave em manutenção de homeostasia de fosfato em organismos tão diversos quanto bactérias e humano. Transportador de fosfato NaPi2b é responsável por medição de transporte de Pi epitelial em vários tecidos de humano. Desregulação de função de NaPi2b tem estado ligada à microlitíase alveolar pulmonar. Recentemente sobre-expressão de NaPi2b em câncer de mama, de tiróide e ovariano tem sido estabelecida. O mecanismo e a importância da sobre- expressão de NaPi2b em tumores de humano, especialmente câncer ovariano, são conhecidos. Estas descobertas identificam NaPi2b com o um candidato adequado para o desenvolvimento de novas intervenções terapêuticas e diagnósticas em patologias humanas.
[00280] O foco principal deste estudo foi gerar anticorpos monoclonais que podem especificamente reconhecer NaPi2b em vários ensaios imunológicos, incluindo Western blotting, imunoprecipitação e imuno- histoquímica. Com o propósito de obter o anticorpo que pode ter o epítopo na região extracelular de NaPi2b, selecionamos a alça extracelular maior (188- 361aa) para estudos de expressão e imunização. O fragmento de NaPi2b, correspondendo aos resíduos de aminoácido 188-361 foi amplificado por PCR e clonado em vetor pGEX4Tl em matriz com a seqüência GST N- terminalmente localizada. A expressão da proteína de fusão do plasmídeo resultante pGEX4Tl/NaPi2b-L foi realizada em células BL21 (DE3). Análise de expressão indicou que GST/NaPi2b-L foi expressado em um nível muito alto após indução com IPTG. Contudo, a proteína de fusão foi insolúvel e instável (Fig.1A). Nossas tentativas para aumentar a solubilidade da proteína GST/NaPi2b-L por mudança das condições de expressão não foram bem sucedidas. Portanto, a purificação de GST/NaPi2b-L foi realizada sob condições desnaturadas da fração insolúvel como descrito em Materiais e Métodos. Esta abordagem permitiu-nos purificar a proteína de fusão GST/NaPi2b -L com pelo menos 80% de pureza em quantidades suficientes para imunização e triagem por ELISA (Fig. 1A). Em adição, as regiões N- e C-terminais da alça extracelular maior foram expressados em bactérias como fusão GST e chamadas de GST/NaPi2b-1L (188-300aa) e GST/NaPi2b-2L (291-361aa). Como mostrado em Figuras 1B e C, ambas as proteínas de fusão expressaram bem, mas foram apenas parcialmente solúveis. Purificação por afinidade em Glutathione Sepharose permitiu-nos obter quantidades significativas de GST/NaPi2b-1L e GST/NaPi2b-2L recombinantes de aproximadamente 95% de pureza (Figuras 1B, C).
[00281] Geração de hibridomas foi realizada por um procedimento padrão como descrito em Materiais e Métodos. Triagem por ELISA primária de meio de hibridoma dos híbridos gerados com proteína de fusão GST/NaPi2b-L acarretou a detecção de 110 clones positivos. Uma triagem de segunda rodada, a especificidade para GST/NaPi2b-L foi adicionalmente confirmada para 83 clones selecionados. Triagem subseqüente por ELISA contra GST sozinha indicou que 27 clones possuíam epítopos localizados em seqüências GST e GST/NaPi2b-L.
[00282] A especificidade de 56 clones híbridos positivos restantes foi examinada por Western blotting para GST/NaPi2b-L. Esta análise identificou 24 clones que reconheceram especificamente, mas com eficiência diferente, uma banda de 45 kDa correspondendo a GST/NaPi2b-L (dados não mostrados). Clones positivos que mostraram a atividade mais forte para GST/NaPi2b-L foram adicionalmente testados por immunoblotting contra GST/NaPi2b-1L e GST/NaPi2b-2L. De modo interessante, nenhum dos clones selecionados reconheceu a proteína de fusão GST/NaPi2b-1L (dados não mostrados). Estes dados indicam claramente que a região C-terminal da alça extracelular de NaPi2b é muito mais imunogênica do que sua região N- terminal. Esta descoberta correlaciona-se com análise bioinformática de imunogenicidade de NaPi2b (www.imtech.res.in/raghava/bcepred). Os melhores respondedores (7 clones de hibridoma) foram subclonados em monoclonalidade e de novo confirmados por ELISA e Western blotting.
[00283] Para determinar se mAbs selecionados podem reconhecer NaPi2b endógena, testamos sua especificidade em Western blotting, imunoprecipitação, ensaio de hemadsorção mista e imuno-histoquímica usando tecidos e linhagens de célula de mamífero. Inicialmente, os lisados de linhagens de células negativas para NaPi2b (SK-RC-01) e positivas para NaPi2b (OVCAR3 e SK-RC-18) foram sondadas em Western blotting com meio de hibridoma de clones selecionados. Todas as linhagens de célula têm sido previamente tipificadas por RT-PCR para a expressão de SLC34A2 mRNA (23). Esta análise permitiu-nos identificar três clones que reconheceram especificamente NaPi2b endógena em immunoblotting. Como mostrado em Figura 2A, anticorpos monoclonais chamados de L2(20/3), L3(28/1) e em menor extensão L2(2/1) detectam uma banda difusa de aproximadamente 95 kDa em células OVCAR3 e SK-RC-18, mas não em células SK-RC-01 sob condições não-redutoras (Fig. 2, A). Quando extratos celulares totais foram resolvidos sob condições redutoras e sondados com NaPi2b mAbs, a banda de 95 kDa de reconhecimento de NaPi2b endogenamente expressada em lisados de células OVCAR3 e SK-RC-18 foi menos difusa e observada apenas com mAbs L2(20/3), L3(28/1) mas não com mAb L2(2/1) (dados não mostrados). Estes resultados indicam que todos os três anticorpos monoclonais reconhecem epítopo(s) conformacional(ais) na região C-terminal da alça extracelular maior.
[00284] Então, testamos a capacidade de clones híbridos selecionados para imunoprecipitar NaPi2b transientemente sobre-expressada. Neste experimento, células Hek293 foram transientemente transfectadas com pcDNA3.1/Glu-NaPi2b ou pcDNA3.1 sozinho. Verificamos que anticorpos monoclonais f L2(20/3) e L3(28/1) foram particularmente bons em imunoprecipitação de NaPi2b transientemente sobre-expressada (Fig 2B). Ademais, verificamos que ambos anticorpos monoclonais L2(20/3) e L3(28/1 podem especificamente imunoprecipitar NaPi2b endógena de células SK-RC-18 (dados não mostrados). Temos testado anticorpos monoclonais L2(20/3) e L3(28/1) em ensaio de hemadsorção mista onde mostraram reatividade forte com as linhagens de células OVCAR-3 e SK-RC-18, que expressaram NaPi2b sobre sua superfície celular mas não reagiram com SK-RC-1, que não expressa NaPi2b (Tabela 3). TABELA 3. Ensaio de hemadsorção mista de anticorpos monoclonais novos contra NaPi2b
[00285] A eficiência de anticorpos gerados também foi examinada por imuno-histoquímica. Levando-se em consideração que sobre-expressão de NaPi2b foi observada em câncer ovariano de humano, temos sondado as amostras de carcinoma ovariano e de ovário normal com anticorpos monoclonais gerais. Os resultados em Figuras 3A e B indicam que clones L2(20/3) e L3(28/1) reconhecem antígeno correspondente em seções embebidas em parafina de carcinoma ovariano com coloração positiva localizada em sua maior parte sobre a borda luminal da amostra de tumor. Nenhum ou muito pouco sinal imunorreativo é detectado em ovário normal sob as mesmas condições experimentais. Estes resultados confirmam os dados previamente publicados indicando que NaPi2b é sobre-expressada em câncer ovariano (20).
[00286] Para restringir os epítopos de anticorpos monoclonais gerados usamos um painel de construtos de fusão GST/NaPi2b, expressando várias regiões da alça extracelular maior. A apresentação esquemática das proteínas de fusão geradas usadas neste estudo é mostrada em Figura 4A. Proteínas de fusão GST/NaPi2b e GST sozinho foram resolvidas por SDS-PAGE sob condições não-redutoras, transfectadas para a membrana de PVDF e sondadas com mAbs L2(2/1), L2(20/3) e L3(28/1). Este estudo claramente indicou que os sítios de ligação para todos os três anticorpos gerados estão localizados na região entre os resíduos de aminoácido 311 e 340. Figura 4B mostra o mapeamento de epítopo para anticorpo monoclonal L2(20/3). Análise bioinformática confirmou esta região como antigênica em seqüência de NaPi2b. Além disso, também contém dois resíduos de cisteína (C322 e C328) que poderiam estar envolvidos em formação de ligação de dissulfeto. A presença de três sítios potenciais de glicosilação (N313, N321 e N340) dentro da região de 311-340aa também tem sido predita pela análise bioinformática. Portanto, o padrão de glicosilação, bem como a formação de pontes de dissulfeto, poderiam determinar a eficiência e a especificidade de reconhecimento de epítopo nesta região elevadamente antigênica sob condições fisiológicas e patológicas.
[00287] Finalmente, determinamos os isótopos de anticorpos gerados. Pelo uso de kit de isotipificação de anticorpo monoclonal de Serotec, verificamos que os clones L2(2/1) e L3(28/1) produzem IgG1, enquanto que o clone L2(20/3) é específico para IgG2b.
[00288] Em resumo, temos gerado um painel de anticorpos monoclonais contra domínio extracelular bacterialmente expressado de transportador de fosfato dependente de sódio NaPi2b. Dois clones híbridos, chamados L2(20/3) e L3(28/1), reconhecem especificamente e com eficiência alta NaPi2b endógena em vários imunoensaios, incluindo Western blotting, imunoprecipitação e imuno-histoquímica. As propriedades de ambos anticorpos torna-os particularmente úteis para estudo da função de NaPi2b sob condições fisiológicas e patológicas.
REFERÊNCIAS
[00289] 1. Feild JA, Zhang L, Brun KA, Brooks DP, Edwards RM. Cloning and functional characterization of a sodium-dependent phosphate transporter expressed in human lung and small intestine. Biochem Biophys Res Commun. 1999; 258(3):578-82.
[00290] 2. Xu H, Bai L, Collins JF, Ghishan FK. Molecular cloning, functional characterization, tissue distribution, and chromosomal localization of a human, small intestinal sodium-phosphate (Na+-Pi) transporter (SLC34A2). Genomics 1999; 62(2):281-4.
[00291] 3. Hilfiker H, Hattenhauer O, Traebert M, Forster I., Murer H, Biber J. Characterization of a new murine type II sodium-phosphate cotransporter expressed in mammalian small intestine. Proc Natl Acad Sci USA 1998; 95:14564-14569.
[00292] 4. Forster 1C, Hernando N, Biber J, Murer H, Proximal tubular handling of phosphate: A molecular perspective. Kidney International 2006; 70:1548-1559.
[00293] 5. Traebert M, Hattenhauer O, Murer H, Kaissling B, Biber J. Expression of type II Na-P(i) cotransporter in alveolar type II cells. Am J Physiol 1999; 277:868-73.
[00294] 6. Homann V, Rosin-Steiner S, Stratmann T, Arnold WH, Gaengler P, Kinne RK. Sodium-phosphate cotransporter in human salivary glands: molecular evidence for the involvement of NPT2b in acinar phosphate secretion and ductal phosphate reabsorption. Arch Oral Biol. 2005; 50(9):759- 68.
[00295] 7. Xu Y, Yeung C-H, Setiawan I, Avram C, Biber J, Wagenfeld A, Lang F, e Cooper TG. Sodium-Inorganic Phosphate Cotransporter NaPi2b in the Epididymis and Its Potential Role in Male Fertility Studied in a Transgenic Mouse Model. Biology of reproduction. 2003;69:1135-1141.
[00296] 8. Frei P, Gao B, Hagenbuch B, Mate A, Biber J, Murer H, Meier PJ, Stieger B. Identification and localization of sodium-phosphate cotransporters in hepatocytes and cholangiocytes of rat liver. Am J Physiol Gastrointest Liver Physiol. 2005; 288:G771-G778.
[00297] 9. Lundquist P, Murer H, Biber J. Type II Na+-P cotransporters in osteoblast mineral formation; regulation by inorganic phosphate. Cell Physiol Biochem 2007; 19:43-56.
[00298] 10. Katai K, Miyamoto K, Kishida S, Segawa H, Nii T, Tanaka H, Tani Y, Arai H, Tatsumi S, Morita K, Taketani Y, e Takeda E. Regulation of intestinal Na+-dependent phosphate co-transporters by a low- phosphate diet and 1,25-dihydroxyvitamin D3. Biochem J 1999; 343:705-712.
[00299] 11. Xu H, Uno JK, Inouye M, Xu L, Drees JB, Collins JF, and Ghishan FK. Regulation of intestinal NaPi2b cotransporter gene expression by estrogen. Am J Physiol Gastrointest Liver Physiol 2003; 285:G1317- G1324.
[00300] 12. Miyamoto K-I, Ito M, Kuwahata M, Kato S e Segawa H. Inhibition of intestinal sodium-dependent inorganic phosphate transport by fibroblast growth factor 23. Ther Apher Dial. 2005; 9 (4):331-5.
[00301] 13. Xu H, Collins JF, Bai L, Kiela PR, Ghishan FK. Regulation of the human sodium-phosphate cotransporter NaPi2b gene promoter by epidermal growth factor. Am J Physiol 2001; 280:C628-C636.
[00302] 14. Arima K, Hines ER, Kiela PR, Drees JB, Collins JF, Ghishan FK. Glucocorticoid regulation and glycosylation of mouse intestinal type lib Na-Pi cotransporter during ontogeny. Am J Physiol 2002; 283:G426- G434.
[00303] 15. Stauber A, Radanovic T, Stange G, Murer H, Wagner CA, Biber J. Regulation of intestinal phosphate transport. II. Metabolic acidosis stimulates Na(+)-dependent phosphate absorption and expression of the Na(+)-P(i) cotransporter NaPi2b in small intestine. Am J Physiol Gastrointest Liver Physiol. 2005; 288(3):G501-6.
[00304] 16. Miyoshi K, Shillingford JM, Smith GH, Grimm SL, Wagner, KU, Oka T, Rosen JM, Robinson GW, Hennighausen L. Signal transducer and activator of transcription (Stat) 5 controls the proliferation and differentiation of mammary alveolar epithelium. J Cell Biol 2001; 155:531542.
[00305] 17. Palmada M, Dieter M, Speil A, Bohmer C, Mack AF, Wagner HJ, Klingel K, Kandolf R, Murer H, Biber J, Closs EI and Lang F. Regulation of intestinal phosphate cotransporter NaPi lib by ubiquitin ligase Nedd4-2 and by serum- and glucocorticoid-dependent kinase 1, Am. J. Physiol. Gastrointest. Liver Physiol. 2004; 287:G143-G150.
[00306] 18. Shojaiefard M, Lang F. Stimulation of the intestinal phosphate transporter SLC34A2 by the protein kinase mTOR. Biochem Biophys Res Commun. 2006; 345(4):1611-4.
[00307] 19. Corut A, Senyigit A, Ugur SA, Altin S, Ozcelik U, Calisir H, Yildirim Z, Gocmen A, Tolun A. Mutations in SLC34A2 cause microlitíase alveolar pulmonar and are possibly associated with testicular microlithiasis. Am J Hum Genet. 2006; 79 (4):650-6.
[00308] 20. Rangel LB, Sherman-Baust CA, Wernyj RP, Schwartz DR, Cho KR, Morin PJ Characterization of novel human ovarian cancer-specific transcripts (HOSTs) identified by serial analysis of gene expression. Oncogene. 2003; 22(46):7225-32.
[00309] 21. Blanchard A, Shiu R, Booth S, Sorensen G, DeCorby N, Nistor A, Wong P, Leygue E, Myal Y. Gene expression profiling of early involuting mammary glands reveals novel gene potentially relevant to human breast cancer. Frontiers in Bioscience 2007; 12:2221-32.
[00310] 22. Jarzab B, Wiench M, Fujarewicz K, Simek K, Jarzab M, Oczko-Wojciechowska M, Wloch J, Czarniecka A, Chmielik E, Lange D, Pawlaczek A, Szpak S, Gubala E, Swierniak A. Gene expression profile of papillary thyroid cancer: sources of variability and diagnostic implications. Cancer Res. 2005; 65(4): 1587-97.
[00311] 23. Beatrice W.T. Yin, Ramziya Kiyamova, Ramon Chua, Otavia L. Caballero, Ivan Gout, Vitalina Gryshkova, Nimesh Bhaskaran, Serhiy Souchelnytskyi, Ulf Hellman, Valeriy Filonenko, Achim A. Jungbluth, Kunle Odunsi, Kenneth O. Lloyd, Lloyd J. Old, G. Ritter. Monoclonal antibody MX35 detects the membrane transporter NaPi2b (SLC34A2) in human carcinomas; a new target for cancer immunotherapy. Accepted for publication in cancer Immunity, MS No. 080103
[00312] 24. Harlow, E. & Lane, D. Antibodies: A Laboratory Manual 1998; Cold Spring Harbor Lab. Press, Plainview, NY.
[00313] 25. Pfreundschuh M, Shiku H, Takahashi T, Ueda R, Ransohoff J, Oettgen HF, Old LJ. Serological analysis of cell surface antigens of malignant human brain tumors. Proceedings of the National Academy of Sciences of the United States of America. 1978; 75:5122-6.
EXEMPLO 4
ANTICORPO MONOCLONAL HUMANIZADO MX35 (huMX35)
Planejamento e síntese de anticorpo monoclonal humanizado MX35 (huMX25):
[00314] As regiões variáveis de cadeia leve e pesada de MAb MX35 murino foram humanizadas in silico seguindo procedimentos de modificação superficial como esboçados por Dauherty et al. (Patente U.S. de No. 6.797.492 B2) e Gonzalez et al. (Tumour Biol., v. 26, n. 1, pp. 31-43, 2005), resultando nas seqüências de ácido nucleico como mostradas em SEQ ID NO: XX (região variável de cadeia leve humanizada) e SEQ ID NO: YY (região variável de cadeia pesada humanizada). Destas seqüências de nucleotídeos, as regiões variáveis de cadeia leve e pesada codificadas tendo respectivamente, as seqüências de aminoácidos de SEQ ID NO: ZZ e PP podem ser expressadas. FIGURA 11 mostra análise de alinhamento de seqüências (programa Clustal 2.0.1) entre as regiões variáveis de cadeias leve e pesada murinas e humanizadas. As regiões CDR de ambas as cadeias leve e pesada estão dentro de retângulo. As CDRs de cadeia leve do MX35 humanizado correspondem às CDRs do anticorpo MX35 de camundongo e são mostradas em SEQ ID NOs: 31-33. As CDRs de cadeia pesada de MX35 humanizado correspondem às CDRs do anticorpo MX35 de camundongo e são mostradas em SEQ ID NOs: 26-28.
[00315] Após o procedimento de modificação superficial in silico, o alinhamento Clustal mostrou a falta de seqüências de sinal líder para ambas as cadeias pesada e leve. O planejamento das seqüências inteiras, sinais de peptídeo conservados foram pesquisados e chegados por teste de processamento virtual. O processamento correto da seqüência líder foi checado pelo algoritmo SignalP 3.0 Server (Center for Biological Sequence Analysis) disponível no website SignalP.
[00316] O anticorpo MX35 humanizado foi construído de modo a se terem as regiões variáveis pesada e leve murinas conectadas nas regiões constantes de humano IgGl e kappa (Crucell, Países-baixos), respectivamente. Várias seqüências de regiões constantes de IgG1 de humano foram analisadas, todas exibindo um índice de homologia alto e também puderam ser usadas para a construção de cadeia pesada completa. Sítios de restrição, HpaI para extremidade 3' e AscI para extremidade 5' da cadeia leve, NheI para extremidade 3' e BamHI para extremidade 5' da cadeia pesada foram adicionados no planejamento de gene com o propósito de permitir sua clonagem eficiente no vetor pcDNA3002Neo (Jones et al., Biotechnol. Prog. V. 19, pp. 163-168, 2003) para expressão em células de mamífero. A escolha das enzimas de restrição também foi feita para permitir a clonagem dos genes no vetor pcDNA3002Neo. Seqüências de consenso de Kozak também foram adicionadas para permitir tradução adequada.
[00317] As seqüências de éxon foram otimizadas para células hospedeiras de humano levando-se em consideração os códons mais usados pelas células de humano para sintetizar proteínas e assim evitar a expressão baixa de proteína para a falta ou deficiência de códons específicos disponíveis na espécie humana quando se usam células de humano como o sistema de expressão.
[00318] A seqüência de DNA final foi analisada pelo programa de computador Genscan (MIT, USA), que prediz sítios de editoração nos limites de éxon-íntron. As seqüências de nucleotídeos completas de ambas as cadeias pesada e leve foram sinteticamente sintetizadas (GeneArt, Suíça).
Clonagem de anticorpo monoclonal MX35 humanizado:
[00319] Os dois vetores, cada um contendo o gene quer para cadeia leve quer para cadeia pesada do huMX35 foram digeridos com as enzimas de restrição (New England Biolabs) descritas acima. O vetor pcDNA3002Neo vazio (Crucell, Paízes-Baixos) foi digerido com as mesmas enzimas de modo a receber os genes de cadeia leve e pesada de MX35, em uma ordem de seqüência detalhada abaixo.
[00320] Para checar a correção, seqüenciamento de DNA de cadeias leve e pesada de anticorpo foi realizado por reações cíclicas de seqüenciamento por PCR com terminadores de cadeias didesóxi fluorescentes (Big Dye® Terminator V3.1 Cycle Sequencing Kit, Applied Biosystems) de acordo com as instruções do fabricante. As reações de seqüenciamento foram analisadas em um ABI 3130 XL DNA Sequencer (Applied Biosystems).
[00321] Para a clonagem da cadeia leve da versão humanizada de anticorpo monoclonal MX35, o vetor vazio pcDNA3002Neo e o vetor transportador contendo a seqüência de gene leve MX35 humanizada foram tanto clivados com enzimas de restrição HpaI e AscI (New England Biolabs) quanto analisados por eletroforese em gel de agarose 1%. O vetor vazio e o fragmento de cadeia leve foram ambos purificados por Wizard SV Gel e PCR Clean-Up System (Promega) das bandas de gel de agarose e usados para reação de ligação com T4 DNA Ligase (Invitrogen) entre o vetor e o gene de cadeia leve. O produto foi usado para transformação de bactérias ("Heat Shock Transformation"descrita por Sambrook e Russell. (Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, 3rdedition, 2001)). Clones foram amplificados e analisados por digestão com enzimas de restrição apropriadas confirmando a inserção esperada. O clone resultante contendo a cadeia leve de anticorpo MX35 foi identificado como pcDNA3002Neo-MX35-LC e usado para a clonagem da cadeia pesada de MX35 humanizado. O vetor transportador contendo o gene de cadeia pesada de MX35 humanizado e o pcDNA3002Neo-MX35-LC foram ambos clivados com as enzimas de restrição NheI e BamRI (New England Biolabs) em extremidades 3' e 5' respectivamente e o protocolo acima foi usado para clonagem do gene de cadeia pesada de MX35 humanizado no pcDNA3002Neo-MX35-LC. Após análise final confirmando a inserção correta, o vetor final foi identificado por pcDNA3002Neo-MX35-LC-HC.
[00322] Um endo-free maxi-prep kit (Endo-Free Plasmid Purification, Qyagen) foi usado para a extração e a purificação do vetor pcDNA3002Neo- MX35-LC-HC contendo as seqüências de gene MX35 humanizado completo. Um procedimento similar foi usado para purificar o vetor vazio pcDNA3002Neo destinado para controle de transfecção de células Per.C6®. Um seqüenciamento de DNA completo foi realizado para ambas as cadeias leve e pesada do MX35 humanizado, como descrito acima, confirmando a precisão da clonagem. As seqüências de nucleotídeos para as cadeias variáveis leve e pesada do XM35 humanizado são mostradas em SEQ ID NOS: 34 e 36 e as seqüências de aminoácidos para as cadeias variáveis leve e pesada do MX35 humanizado são mostradas em SEQ ID NOS: 35 e 37. Transfecção de célula de humano:
[00323] Para a transfecção, um frasco de células congeladas aderentes Per.C6®, passagem 41 (Crucell, Países-Baixos), foi descongelado e mantido em meio de cultura DME-F12 (Invitrogen) suplementado com 10% de soro fetal bovino e cloreto de magnésio 10 mM, e permitido expandir. Para a transfecção, as células foram plaqueadas um dia depois em placas de Petri P60 com 2x10E6 células por placa. No dia de transfecção as células foram 50% confluentes. Uma mistura de DNA (2,5 μg), cultura de meio livre de soro com MgCl210 mM, e 10 μL de solução Lipofectamine™ LTX (Invitrogen) foi distribuída em tubos Eppendorf®. Os tubos foram mantidos na temperatura ambiente por 30 min para permitir a formação de complexos de lipossomo-DNA.
[00324] As células aderentes foram lavadas três vezes com meio livre de soro, com 2 mL de volume de meio no final das lavagens. A mistura de DNA-lipossomo foi cuidadosamente adicionada sobre o meio com células Per.C6® (Crucell, Países-Baixos). As placas foram incubadas e após 48 h o meio de seleção contendo geneticina (G418) (Invitrogen) (500μg/mL) foi adicionado com o objetivo de gerar um pool estável. Cada 3-4 dias o meio foi removido, centrifugado e mantido congelado para uso posterior. Meio novo foi adicionado nas células. Este regime demorou mais de 30 dias, quando as células foram congeladas com o marcador "Per.C6 huMX35 Pool 1". Após 48 h uma amostra foi tirada para análise. Teste de ELISA usando detecção de cadeias pesada e leve separadas (IgG de cabra anti-humano (específica para cadeia-Y) e kappa de cabra anti-humano (específica para cadeia-K (Southern Biotech) confirmou a síntese do anticorpo monoclonal MX35 humanizado. Análise por citometria de fluxo confirmou que o anticorpo produzido podia se ligar na linhagem de célula OVCAR-3, conhecida pelos resultados prévios (veja exemplos anteriores) como uma célula positiva para a versão murina de anticorpo monoclonal MX35.
[00325] Com estes resultados positivos, este pool estável de células aderentes foi então adaptado para crescimento em suspensão em meio livre de soro (meio CDM4PerMab®, Hyclone, Thermo Scientific).
Produção de anticorpo monoclonal MX35 humanizado:
[00326] Um frasco de "Per.C6 huMX35 Pool 1" com células produzindo MX35 humanizado foi descongelado e as células foram expandidas para adaptação de crescimento em suspensão. Usando um frasco de cultura T-75 com 80% de confluência, as células foram tripsinizadas, centrifugadas, ressuspensas em meio CDM4PerMab® (Hyclone, Thermo Scientific) sem soro e mantidas em um frasco T-75 em condições de cultura estática por 4 dias. As células em suspensão foram transferidas para frascos agitadores sob condições de agitador orbital, com concentrações de célula de pelo menos 0,6 x 106/mL. O meio condicionado colhido entre as mudanças de meio foi mantido em temperatura de 4°C-8°C.
[00327] Purificação do meio condicionado foi realizada em uma sala fria usando uma Hytrap® Protein A (GE Healthcare). O meio condicionado foi filtrado e diluído 1:1 com um tampão de glicina 1,5 M, NaCl 3 M, pH 9,0. Dez volumes de coluna do sobrenadante diluído foram aplicados na coluna. Quando a aplicação de amostra acabou, a coluna foi lavada com dez volumes do tampão acima. Um tampão de citrato 50 mM, NaCl 150mM, pH 6,0 foi usado como primeira eluição para a remoção de contaminantes de proteína. O anticorpo foi eluído com o tampão de citrato 50 mM, NaCl 150mM, pH 3,0.
[00328] Materiais eluídos de pH 6,0 e 3,0 foram dialisados contra solução salina tamponada com fosfato. Amostras de cada etapa da cromatografia em proteína A foram aplicadas sobre geles SDS-PAGE, 7% para eletroforese não-reduzida e 12% para eletroforese reduzida. O anticorpo foi eluído em pH 3,0 sem contaminantes e a concentração foi determinada pelo método de Bradford.
Propriedades de ligação do anticorpo monoclonal MX35 humanizado:
[00329] A eficácia de ligação de anticorpo MX35 humanizado, sintetizado e purificado como descrito acima, foi comparada com a versão murina do anticorpo MX35, usando marcador fluoresceína isotiocianato - FITC - para avaliar a ligação específica em linhagens celulares diferentes em citometria de fluxo. As linhagens celulares listadas em TABELA 4 foram tripsinizadas, ajustadas para uma concentração de 2,5 x 105células e distribuídas em tubos de ensaio de 1,5 mL. Após centrifugação a pelota foi ressuspensa em 100 μL de anticorpo primário (quer MX35 murino, MX35 humanizado, hu3S193 quer Zenapax®) diluído no mesmo meio de cultura usado para cultivar as células na concentração de 20 μg/mL. No caso de controles de "células sozinhas" e FITC-conjugados, as células foram ressuspensas em 100 μL de meio de cultura. As misturas foram incubadas por 1 ha 4°C e então lavadas duas vezes com 200 μL de solução salina tamponada com fosfato. As células foram ressuspensas em 100 μL de conjugado de FITC - anticorpo secundário, quer murino quer humano dependendo da versão de anticorpo MX35 usada. O tubo de controle "células apenas" recebeu apenas meio de cultura. Os conjugados de FITC - anticorpo secundário foram "fragmento F(ab')2 de IgG (molécula inteira) anti- camundongo produzido em ovelha" e "fragmento F(ab')2 de IgG (específico para cadeia-y) anti-humano produzido em cabra", ambos de Sigma Aldrich. As misturas dos conjugados de células - FITC foram incubadas por 30 min a 4°C e então lavadas duas vezes com solução salina tamponada com fosfato. As células pelotizadas foram ressuspensas em 300 μL de solução de fixação (glicose 3,2%, formaldeído 1% em solução salina tamponada com fosfato). Coloração das células com as sondas fluorescentes foi medida em uma corrente de fluido na citometria de fluxo Guava® ExpressPro (Guava EasyCyte Mini System). Para cada experimento individual 10.000 eventos foram adquiridos e contados. Programa de computador incluído no equipamento foi usado para analisar os resultados, com certos resultados exemplares apresentados em FIGURAS 12 a 15.
[00330] TABELAS 4 e 5 resumem os resultados de análise de citometria de linhagens celulares diferentes com anticorpo MX35 quer humanizado quer murino. Os resultados de células de origem de tumor de estão tabulados em TABELA 4. Os resultados de células normais, de humano e de macaco rhesus estão tabulados em TABELA 5.
[00331] Além dos anticorpos murino e humanizado, as análises de citometria de fluxo utilizaram e mostraram dois outros anticorpos humanizados. Um (hu3S193) seleciona o antígeno LewisY, presente em um número grande de carcinomas epiteliais de humano, e aqui utilizado como um controle positivo. Um anticorpo IgG1 humanizado comercial (Zenapax®, Roche) que seleciona a forma de afinidade alta de IL-2Rα presente apenas sobre a membrana de linfócitos ativados foi escolhido como um controle negativo pareado.
[00332] Os resultados totais obtidos pelas análises de citometria de fluxo confirmaram a especificidade de ligação de anticorpo MX35em células de tumores ovariano e renal de humano. Os anticorpos MX35, cada um e ambos de camundongo e de humano, não mostraram ligação detectável por citometria de fluxo com várias outras linhagens de células de câncer, células DLD-1 de carcinoma colorretal, células H358 de carcinoma de pulmão, células LNCaP de carcinoma de próstata, células MCF-7 de carcinoma e mama, células SK-MEL-28 de melanoma, células de MK.N45 de carcinoma gástrico, células HeLa de carcinoma cervical. Estas células foram linhagens celulares e não células de tumor ou câncer primário. A versão humanizada de anticorpo MX35 seguiu o mesmo perfil mostrado pela versão murina original de anticorpo MX35. Como a versão murina já tem estado em testes clínicos de Fase I (referências citadas), a versão humanizada de MX35, tendo as mesmas propriedades de ligação que as do antígeno de superfície de célula, pode ser útil em intervenção clínica contra câncer ovariano. TABELA 4 Resultados de ligação de anticorpo huMX35 em células de tumor de humano de origens diferentes

TABELA 5 Resultados de ligação de MX35 em células normais de origens diferentes (3 humanas e 1 primata)
[00333] Daugherty et al. Method for reducing the immunogenicity of antibody variable domains. Patent USP 6.797.492 B2; Sept 28, 2004.
[00334] Gonzalez, N.R. et al. "Minimizing the immunogenicity of antibodies for clinical application". Tumour Biol., 26(1): 31-43, 2005.
[00335] Rubin SC, KJA Kairemo, AL Brownell, F Daghighian, MG Federici, KS Pentlow, RD Finn, RM Lambrecht, WJ Hoskins, JL Lewis & SM Larson. High-resolution positron emission tomography of human ovarian cancer in nude rats using 124I-labeled monoclonal antibodies. Gynecol. Oncol. 1993; 48: 61-67.
[00336] Rubin SC, L Kostakoglu, C Divgi, MG Federici, CL Finstad, KO Lloyd, SM Larson & WJ Hoskins. Biodistribution and intraoperative evaluation of radiolabeled monoclonal antibody MX35 in patients with epithelial ovarian cancer. Gynecol. Oncol. 1993; 51: 61-66.
[00337] Finstad CL, KO Lloyd, MG Federici, C Divgi, E Venkatraman, RR Barakat, RD Finn, SM Larson, WJ Hoskins & JL Humm. Distribution of radiolabeled monoclonal antibody MX35 F(ab')2 in tissue samples by storage phosphor screen image analysis: Evaluation of antibody localization to micrometastatic disease in epithelial ovarian cancer. Clin. Cancer Res.1997; 3: 1433-1442.
[00338] Elgqvist J, Andersson H, Back T, Hultborn R, Jensen H, Karlsson B, Lindegren S, Palm S, Warnhammar E & Jacobsson L. Therapeutic efficacy and tumor dose estimations in radioimmunotherapy of intraperitoneally growing OVCAR-3 cells in nude mice with 211At-labeled monoclonal antibody MX35. J Nucl Med 2005; 46:1907-1915.
[00339] Back T, Andersson H, Divgi CR, Hultborn R, Jensen H, Lindegren S, Palm S & Jacobsson L. 211At radioimmunotherapy of subcutaneous human ovarian cancer xenografts: Evaluation of relative biological effectiveness of an α-emitter in vivo. J Nucl Med 2005; 46:20612067.
[00340] Elqqvist J, Andersson H, Back T, Claesson I, Hultborn R, Jensen J, Lindegren S, Olsson M, Palm S, Warnhammar E & Jacobsson L. Fractioned radioimmunotherapy of intraperitoneally growing ovarian cancer in nude mice with 211At-MX35 F(ab')2: therapeutic efficacy and mielotoxicity. Nuclear Med Biol 2006; 33:1065-1072.
[00341] Elqgvist J, Andersson H, Back T, Claesson I, Hultborn R, Jensen J, Johansson B, Lindegren S, Olsson M, Palm S, Warnhammar E & Jacobsson L. α-radioimmunotherapy of intraperitoneally growing OVCAR-3 tumors of variable dimensions: outcome related to measured tumor size and mean absorbed dose. J Nucl Med 2006; 47:1342-1350.
[00342] Elgqvist J, Andersson H, Bernhardt P, Back T, Claesson I, Hultborn R, Jensen H, Johansson B, Lindegren S, Olsson M, Palm S, Warnhammar E & Jacobsson L. Administered activity and metastatic cure probability during radioimmunotherapy of ovarian cancer in nude mice with 211At-MX35 F(ab')2- Int. J. Radiation Oncology Biol. Phys. 2006; 66(4):1228- 1237.
[00343] Howard M. Shapiro. Practical Flow Cytometry. 4thEdition, 2003.
[00344] Jones et al. High-level expression of recombinant IgG in the human cell line per.c6. Biotechnol. Prog. V. 19, pp. 163-169,2003.
[00345] Sambrook, J. e Russell, D.W. Molecular Cloning: A Laboratory Manual, Cold Spring Harbor Laboratory Press, 3rdedition, 2001. EXEMPLO 5
CONSTRUÇÃO DE ANTICORPOS MX35 DE CADEIA ÚNICA
[00346] Procuramos criar versões de cadeia única (ScFv) do anticorpo MX35 superficialmente modificado (vMX35) e de um anticorpo MX35 quimérico códon-otimizado (chMX35), e usar estes anticorpos para confirmar que vMX35 e chMX35 podem ser ligar em peptídeo MX35 em ELISA. Anticorpos de cadeia única foram produzidos, e anticorpos de cadeia única baseados em ambos um anticorpo MX35 superficialmente modificado e quimérico reconhecem o peptídeo MX35 (correspondendo aos aminoácidos 324-338 de NaPi2b (SLC34A2) (SEQ ID NO:8)).
[00347] Seqüências de aminoácidos de região variável do anticorpos MX35 superficialmente modificado são fornecidas em SEQ ID NO: 38 (cadeia pesada) e SEQ ID NO: 39 (região variável de cadeia leve). Seqüências de aminoácidos de regiões variáveis de anticorpos MX35 quimérico de códon-otimizado são fornecidas em SEQ ID NO: 40 (cadeia pesada) e SEQ ID NO: 41 (região variável de cadeia leve).
Planejamento de iniciador ScFv
[00348] Iniciadores foram planejados para criar as versões de cadeia única dos anticorpos superficialmente modificado e quimérico. Anticorpos de fragmento variável de cadeia única (ScFv) são compostos da seqüência codificadora de cadeia pesada variável ligada em uma região de linker flexível (Gly4Ser)3, seguida pela seqüência codificadora de cadeia leve variável, e fechando com uma etiqueta-E. A seqüência de etiqueta-E foi codificada no plasmídeo pCANTAB 5E. Este plasmídeo, juntamente com as células TG1 usadas para produzir ScFv solúvel, foi parte do Sistema de Anticorpo de Fago Recombinante (GE Biosciences).
[00349] Iniciadores MX35 ScFv foram os seguintes:
[00350] Iniciadores de seqüência codificadora vH, início da seqüência vH está em NEGRITO HCupstreamPD: CACGGCCCAGCCGGCCCAGGTGCAGCTCCAAGAGAG (SEQ ID NO: 46) vMX35vHup-PD: CACGGCCCAGCCGGCCCAGGTGCAGCTGGTGCAGAGC (SEQ ID NO: 47) chMX35vHup-PD: CACGGCCCAGCCGGCCCAGGTGCAATTGAAGCAGTCT (SEQ ID NO: 48)
[00351] Iniciadores para seqüência codificadora vH para linker; final de seqüência vH está em NEGRITO, sobreposição de iniciador linker está sublinhada HCdownstreamPD: CCACCTCCGCCTGAACCGCCTCCACCGCTGCTCACTGTCACTAGGG (SEQ ID NO: 49) RC: CCCTAGTGACAGTGAGCAGCGGTGGAGGCGGTTCAGGCGGAGGTGG (SEQ ID I NO: 50) vMX35vHdown-PD: CCACCTCCGCCTGAACCGCCTCCACCGGATGATACAGTCACCAGGG (SEQ ID NO: 51) RC: CCCTGGTGACTGTATCATCCGGTGGAGGCGGTTCAGGCGGAGGTGG (SEQ ID NO: 52) chMX35vHdown-PD: CCACCTCCGCCTGAACCGCCTCCACCGGATGACACGGTCACCAGGG (SEQ ID NO: 53) RC: CCCTGGTGACCGTGTCATCCGGTGGAGGCGGTTCAGGCGGAGGTGG (SEQ ID NO: 54)
[00352] Iniciadores para linker em seqüência codificadora vL; iniciador linker está sublinhado, início de seqüência vL está em NEGRITO LCupstreamPD: CAGGCGGAGGTGGCTCTGGCGGTGGCGGATCGGATATTCAGATGACTCAGAGTC (SEQ ID NO: 55) vMX35vLup-PD: CAGGCGGAGGTGGCTCTGGCGGTGGCGG ATCGG AC ATCC AG ATG ACCCAGAGCC (SEQ ID NO: 56) chMX35vLup-PD: CAGGCGGAGGTGGCTCTGGCGGTGGCGGATCGGATATCCAGATGACCCAGACCA (SEQ ID NO: 57)
[00353] Iniciadores para extremidade de vL; final de seqüência codificadora vL está em NEGRITO. LCdownstreamPD: CCTGCGGCCGCTTTGATTTCCAGTπTGTGCCGCC (SEQ ID NO: 58) RC: GGCGGCACAAAACTGGAAATCAAAGCGGCCGCAGG (SEQ ID NO: 59) vMX35vLdown-PD: CCTGCGGCCGCTTTGAGTTCCAGTTTGGTGCCCTG (SEQ ID NO: 60) RC: CAGGGCACCAAACTGGAACTCAAAGCGGCCGCAGG (SEQ ID NO: 61) chMX35vLdown-PD: CCTGCGGCCGCTTTCAGCTCCAGCTTGGTGCCGGC (SEQ ID NO: 62) RC: GCCGGCACCAAGCTGGAGCTGAAAGCGGCCGCAGG (SEQ ID NO: 63) Produção de genes vMX35 e chMX35 ScFv
[00354] Criação de seqüência ScFv completa exigiu duas rodadas de PCR. O produto final foi então digerido com SfiI e NotI, e ligado no plasmídeo pCANTAB 5E.
[00355] Protocolo de PCR2 é idêntico àquele de PCR1. Correr produtos através de coluna de limpeza de reação (coluna Qiagen Qiaspin), eluir em 50ul H2O e proceder com Digestão por Restrição. Digerir produtos
de PCR2 usando SfiI e NotI, ligar em plasmídeo pCANTAB 5E.
[00356] Incubar os digestos duplos por uma hora a 37°C. Isolar as bandas digeridas para inserto e plasmídeo por eletroforese em gel de agarose 1%. Purificar DNA em minicoluna (coluna Qiagen MinElute) e eluir em 10 μl de H2O. Ligação de MX35ScFv + pCANTAB 5E 1μl T4 DNA Ligase 2μl Tampão de T4 DNA Ligase 2μl Inserto digerido (vMX35 ou chMX35 PCR2) 6μl Vetor digerido (pCANTAB 5E) 9μl H2O
[00357] Incubar Reação de Ligação por 15min a 22°C. Limpar DNA por preparação em minicoluna e eluir em 10μl de H2O.
[00358] Transformar células Top 10 quimicamente competentes com plasmídeos ScFv de acordo com o protocolo publicado (Invitrogen Top 10 Chemically Competent E.coli).
[00359] Checar as colônias isoladas para a presença de plasmídeo por PCR de colônia. Coletar colônias isoladas, e usando um palito de dente estéril, transferir bactérias de cada colônia para tubos separados contendo 100 μl de água estéril. Lisar as células por incubação a 95°C por 5 minutos. Usar 5μl de cada tubo na seguinte reação PCR: PCR de colônia 0,5μl vMX35vLup-PD ou chMX35vLup-PD 0,5μl R2 5,0μl DNA Modelo de células lisadas 7,0μl Mistura Padrão RedTaq 1,0μl H2O
[00360] Protocolo de PCR é idêntico àquele de PCR1. Após PCR, correr a reação de PCR inteira (4μl) em uma cavidade de um gel de agarose 1,5%. Colônias que têm sido transformadas com plasmídeo contendo inserto ScFv terão uma banda de ~450pb. Crescer 10ml de culturas líquidas derivadas de colônias verificadas por PCR sobre LB + Amp durante a noite. Preparar estoques em glicerol: em 1 ml de cultura noturna, adicionar 75 μl de glicerol, agitar para misturar, e armazenar a -80°C. Purificar plasmídeo dos 9 ml restantes de cada cultura usando uma coluna-spin para purificação de DNA plasmídeo (Promega Wizard Plus Miniprep).
[00361] Seqüenciar plasmídeos usando iniciadores R1 & R2, que agrupam a seqüência ScFv, anelar ~80bases a montante ou a jusante, respectivamente. Iniciadores de seqüenciamento: R1: 5' - CCATGATTACGCCAAGCTTTGGAGCC - 3' (SEQ ID NO: 64) R2: 5' - CGATCTAAAGTTTTGTCGTCTTTCC - 3' (SEQ ID NO: 65)
[00362] Nota: A região dentro e ao redor do sítio sfiI é rica em GC. Esta foi provavelmente a causa dos erros durante a PCR e as reações de ligação. Como um resultado, a eficiência de transformação foi baixa para estes construtos, e houve uma freqüência de inserção relativamente alta ou erros de deleção relativamente elevados dentro desta parte da seqüência. Apenas um clone perfeito foi encontrado para vMX35 ScFv; clone #6. Como para chMX35, todos os clones tiveram erros na rodada inicial de seqüenciamento. ChMX35 ScFv clone #5 foi subseqüentemente modificado para corrigir uma mutação de deslocamento de matriz nesta região. Iniciadores foram planejados para se beneficiarem do único sítio MunI/MfiI dentro da seqüência de chMX35 ScFv precoce. Uma seqüência correta foi obtida por PCR de chMX35 ScFv clone #5 usando os seguintes iniciadores: Iniciadores de modificação de cMX35scfv: PD HindiII up: 5’- GATTACGCCAAGCTTTGGAG-3’ (SEQ ID NO: 66) Ch5 sfil muni: 5’- CTTCAATTGCACCTGGGCCGGCTGGGCCGCATAGAAAGGAAC -3’ (SEQ ID NO: 67)
[00363] Após digestão em HindlII e MfiI, esta seqüência foi ligada em HindIII-MfiI digerido e CIP'd chMX35 ScFv clone #5. Foi provado que dois clones derivados das subseqüentes ligação e transformação, chMX35 ScFv clone #6 e chMX35 ScFv clone #8 têm seqüências perfeitas, idênticas. Clone #8 foi usado em aplicações a jusante. Clones contendo seqüências corretas, usados para ELISA:
[00364] vMX35 ScFv clone #6
[00365] chMX35 ScFv clone #8
[00366] A seqüência de aminoácidos para o vMX35 ScFv clone #6 é mostrada em FIGURA 16 (SEQ ID NO: 42). A seqüência de ácido nucleico para vMX35 ScFv clone #6 é mostrada em FIGURA 16 (SEQ ID NO: 43). A seqüência de aminoácidos para ScFv clone #8 quimérico é mostrada em FIGURA 17 (SEQ ID NO: 44). A seqüência de ácido nucleico para ScFv clone #8 quimérico é mostrada em FIGURA 17 (SEQ ID NO: 45).
Eletroporação de células TG1
[00367] Plasmídeos purificados de seqüência verificada de vMX35 ScFv clone #6 e de chMX35 ScFv clone #8 foram então usados para transformar E.coli TG1 eletrocompetente. Estas células foram parte do RPAS kit, e poderiam ser utilizadas para produzir tanto anticorpos exibidos em fago quanto anticorpos de cadeia única solúveis que poderiam ser então usados em ELISA.
[00368] Protocolo: Descongelar frasco de TG1 eletrocompetente sobre gelo. Transferir 50 μl de células para uma cubeta de 0,2 cm pré-esfriada. Adicionar 50 μl de água d.i. e 2 μl de plasmídeo pCANTAB 5E purificado livre de sal com seqüência ScFv. Agitar no fundo da cubeta. Deixar sobre gelo por 1 minuto. Programar o eletroporator para dar 25 μF, 2,5 kV a 200 ohms. Secar a cubeta com um tecido e deixá-la dentro da câmara de eletroporação. Pulsar uma vez. Imediatamente adicionar 1 mL de meio LB-G ou 2x YT-G novo na cubeta e cobrir e inverter para ressuspender as células. Incubar as células eletroporadas restantes por 1 hora a 37°C com agitação a 250 rpm. Plaquear 100 μl de células transformadas não diluídas bem como diluições 1:100 e 1:10.000 sobre placas SOB AG separadas usando um espalhador estéril. Quando secas, inverter as placas e incubar durante a noite a 37°C. Preparar estoques congelados de uma cultura noturna de uma colônia única em 10ml de 2x-YT-AG, cultivada a 37°C. Em 1ml desta cultura, adicionar 75μl de glicerol e armazenar a - 80°C.
Extrato periplásmico
[00369] Anticorpos ScFv marcados com etiqueta-E podem ser extraídos do espaço periplásmico de E. coli TG1 ou HB2151 transfectada com uma seqüência de anticorpo de cadeia única inserida em um plasmídeo pCANTAB 5E e cultivada em meio contendo IPTG. Embora a literatura sugira que anticorpos ScFv também podem ser colhidos do sobrenadante ou das frações intracelulares de tais culturas, havia sido determinado em experimentos prévios que extratos periplásmicos deram o rendimento mais alto. Assim, ScFv's solúveis marcados com etiqueta-E foram extraídos para uso em ELISA.
[00370] Protocolo: Crescer clone TG1 contendo gene ScFv codificador de plasmídeo (vMX35 #6, e chMX35 #8) por três horas em 10ml de meio 2x- YT-AG. Incubar a 37°C, agitar a 250rpm. Pelotizar as células por centrifugação por 20 minutos a 1000 x g. Jogar fora o sobrenadante e ressuspender as células em 10ml de meio 2x-YT-AI. Incubar durante a noite a 30°C ou 37°C, agitando a 250rpm. Pelotizar as células por centrifugação por 20 minutos a 1000 x g. Jogar fora o sobrenadante. Ressuspender a pelota celular em 0,5 ml de tampão 1x TES gelado e transferir o conteúdo para um tubo de microcentrífuga de 1,5ml. Imediatamente adicionar 0,75ml de tampão 1/5x TES gelado (uma parte de 1xTES, quatro partes de água d.i.), e agitar para induzir choque osmótico suave. Incubar sobre gelo por 30 minutos. Centrifugar a 14000rpm por 10 minutos. Reter o sobrenadante, que contém ScFvs e será usado para dot-blots e ELISAs. Neste ponto, DNA pode ser extraído da pelota celular por ebulição, e a presença da seqüência de interesse pode ser detectada por PCR de colônia. Dot-Blot
[00371] Dot-Blots foram realizados como um meio simples de determinar a presença de ScFvs dos extratos periplásmicos. Embora este ensaio, como esboçado, de modo algum pudesse mostrar a capacidade dos anticorpos ScFv de se ligarem em peptídeo, ele deu uma indicação de se o anticorpo ScFv havia sido extraído, bem como uma idéia aproximada da concentração.
[00372] Protocolo: Aplicar mancha (blot) de 2μl de cada amostra de extrato periplásmico sobre nitro-celulose e deixar secar.
[00373] Amostras: (C) - Controle Positivo; 806 ScFv superficialmente modificado colhido de células HB2151
[00374] (V) - vMX35 ScFv (de clone #6)
[00375] (CH) - chMX35 (de clone #8)
[00376] Bloquear mancha (blot) por uma hora em PBS + BSA 3% (10ml). Incubar por uma hora sobre anticorpo anti-etiqueta-E conjugado com HRP diluído 1:1000 em PBS + BSA 3%. Lavar 5x com PBS + Tween20 0,05% em um minuto por lavagem. Seguir com uma lavagem com água deionizada. Revelar em tampão de revelação 4Cn por <20 minutos. Interromper a reação de cor com lavagem aquosa. (Tampão 4Cn: Dissolver um tablete 4Cn triturado em 500μl de Etanol 100%; Adicionar 75ml de PBS; Esterilizar por filtração; Adicionar 100μl de H2O2 imediatamente antes do uso). Resultados indicam a presença de anticorpos ScFv marcados com etiqueta-E solúveis em extratos periplásmicos. ELISA
[00377] Os resultados deste ELISA de peptídeo estabeleceram que anticorpos ScFV solúveis, vMX35 ScFv #6, e chMX35 ScFv #8, de fato reconhecem o peptídeo MX35 (SEQ ID NO:8).
[00378] Protocolo: placa de ELISA (NUNC) é revestida com 100μl por cavidade de 4μg/mL de peptídeo MX35 (ou peptídeo EMEE (806) para controle negativo) dissolvido em tampão Carbonato-Bicarbonato em pH 9,6 e incubado durante a noite a 4°C. Peptídeo é removido e a placa é bloqueada usando 250μl/cavidade de PBS + BSA 3% por uma hora na temperatura ambiente. Uma placa de diluição é bloqueada na mesma maneira. Tampão de bloqueio é removido da placa de diluição e as diluições de anticorpo são preparadas. 100μl de tampão de diluição (PBS + BSA 3%+ Tween20 0,05%) são adicionados em cada cavidade da placa de diluição (exceto nas cavidades mais concentradas do controle positivo, A1 e B1). 100μl de extrato periplásmico são adicionados na cavidade inicial para cada série de diluição (rotulada "2"). A amostra é misturada por pipetação para ascendente e descendente, e 100μl da amostra misturada são transferidos para a cavidade seguinte, onde o processo é repetido. A série continua por 11 diluições. Nenhum anticorpo é adicionado na 12a cavidade, está é uma cavidade de controle negativo. O controle positivo também é diluído como descrito, mas uma concentração inicial de 2μg/mL é preparada e adicionada nas primeiras cavidades. Controles negativos são apenas diluídos para 1:32.
[00379] A placa de ELISA bloqueada e revestida com peptídeo é esvaziada, e 100μl de cada cavidade da placa de diluição são adicionados na cavidade correspondente na placa de ELISA. A placa é incubada por 1,5 horas na temperatura ambiente. A placa é lavada 4x usando PBS + Tween20 0,05%. 100μl de anticorpos secundário conjugado com HRP são adicionados em cada cavidade da placa de ELISA. No caso do controle positivo, este é gama Fc de cabra anti-camundongo conjugado com HRP diluído 1:20.000 em PBS + BSA 3%+ Tween20 0,05%. Para os anticorpos ScFV marcados com etiqueta-E, o anticorpo secundário é um anticorpo anti-etiqueta-E conjugado com HRP (GE Biosciences) diluído para 1:8.000 no PBS + BSA 3%+ Tween20 0,05%. A placa é incubada por 1 hora na temperatura ambiente. A placa é lavada 4x usando PBS + Tween20 0,05%.
[00380] Sinal é detectado usando 100μl/cavidade de Dako© TMB+ substrato. Cor desenvolvida dentro de 10 minutos, e a reação foi interrompida com 100μl/cavidade de Ácido Sulfúrico 1M. A Absorbância em 450nm é lida e registrada.
[00381] Uma comparação das primeiro oito diluições é mostrada em FIGURA 18. Resultados de ELISA de anticorpo MX35 de controle, e de anticorpos scFV superficialmente modificado e quimérico versus peptídeo MX35, peptídeo irrelevante e sem peptídeo, em uma única concentração de anticorpo são fornecidos em FIGURA 19. Os anticorpos superficialmente modificado e quimérico Fv de cadeia única reagiram com células SK-RC-18 (linhagem de célula renal) pelo ensaio de hemaglutinação mista (dados não mostrados).
EXEMPLO 6
SLC34A2 VARIANTE T330 M NÃO É RECONHECIDA PELO ANTICORPO MX35
[00382] SLC34A2, envolvido em homeostasia de fosfato em vários órgãos, tem sido verificado em ser o gene responsável por microlitíase alveolar pulmonar (PAM), uma doença rara caracterizada pela deposição de micrólitos de fosfato de cálcio em toda parte dos pulmões. Corut et al. têm estudado e identificado mutações em SLC34A2 que são preditas em causarem microlitíase alveolar pulmonar e possivelmente também estão associadas com microlitíase testicular (Corut, A. et al. (2006) AM J. Hum Genet 79:650-656). Enquanto analisava controles normais, Corut identificou uma variante nova c.989C-T (p. T330M) em uma fêmea não afetada, por meio da qual treonina é substituída por metionina, substituindo um resíduo polar por um resíduo não- polar. É presumido que isto inativa a proteína SLC34A2. Esta mutação T330M está localizada dentro da região de peptídeo de epítopo MX35 de SLC34A2. Para testar se o anticorpo MX35 é capaz de se ligar em ou de reconhecer a variante T330M SLC34A2 mutante e presumida inativa, ligação de anticorpo MX35 em peptídeo 312-340 variante T330M (SLC34A p312340 T330M) (SEQ ID NO: 68) versus peptídeo 312-340 de tipo selvagem (SEQ ID NO: 8) foi avaliada por dot blot. Os resultados são mostrados em FIGURA 20. Embora anticorpos MX35, L2 e L3 se ligam em peptídeo p312340 SEQ ID NO: 8, nenhum destes anticorpos se liga em peptídeo T330M P312-340 por análise dot blot.
EXEMPLO 7
ESTABELECIMENTO DE MODELOS CELULARES PARA A ANÁLISE DE TRANSPORTADOR DE FOSFATO DEPENDNETE DE SÓDIO NaPi2b. UM MARCADOR POTENCIAL PARA CÂNCER OVARIANO
[00383] O objetivo do presente estudo foi estabelecer um modelo para análise funcional de um marcador recentemente identificado de câncer ovariano - transportador de fosfato dependente de sódio NaPi2b. Para este propósito, temos criado linhagens de células estáveis HEK293 expressando as formas de tipo selvagem e mutante de NaPi2b (substituição T330V em uma alça extracelular grande e uma deleção de 6 resíduos de aminoácido na cauda citoplásmica C-terminal) que foram revelados em linhagens de célula de câncer ovariano. A expressão de formas de tipo selvagem e mutante de NaPi2b em linhagens de células estáveis criadas foi confirmada por análise Western-blot com anticorpo monoclonal contra NaPi2b. Os modelos celulares estabelecidos aqui descritos serão úteis para estudar a função de transportador de fosfato dependente de sódio NaPi2b em saúde e doença.
[00384] Câncer ovariano epitelial (EOC) é uma das causas líderes de morte relacionada com câncer em mulheres e a causa líder de morte por câncer ginecológico. A falta de marcadores específicos para EOC torna difícil alcançar o objetivo clínico para detecção precoce e terapia. Assim, a identificação e a caracterização de novos marcadores de câncer ovariano são cruciais para o desenvolvimento de novas abordagens diagnósticas e imunoterapêuticas em oncologia ginecológica e para entendimento dos mecanismos moleculares de crescimento maligno.
[00385] Descobertas recentes sugerem que o transportador de fosfato dependente de sódio NaPi2b poderia ser considerado como um marcador esperado potencial de câncer ovariano. Em primeiro lugar, NaPi2b é sobre- expressado em câncer ovariano em comparação com tecidos normais e outros tipos de câncer [1]. Em segundo lugar, NaPi2b foi recentemente identificado como antígeno de câncer MX35 por duas abordagens independentes: a) triagem de biblioteca de cDNA de linhagem de célula de câncer ovariano OVCAR3 com anticorpo monoclonal MX35; e b) purificação por afinidade de antígeno MX35 seguida por análise por espectrometria de massa [2]. MAb MX35 foi gerado mais do que 20 anos atrás em Memorial Sloan-Kettering Cancer Center por imunização de camundongos com células de carcinoma ovariano novas e triagem de hibridomas gerados com um painel de linhagens de célula de câncer ovariano [3]. Outros estudos mostraram que o antígeno MX35 é expressado em nível alto em aproximadamente 90% dos cânceres epiteliais ovarianos de humano, o que criou a base para usar MAb MX35 humanizado em testes clínicos de fase inicial [3, 4]. Em tecidos normais, a expressão de transportador de fosfato dependente de sódio 2b em nível de proteína é restrita ao intestino delgado [5], pulmão [6], fígado [7], glândulas mamárias e salivar [8,9].
[00386] O transportador de fosfato dependente de sódio de humano NaPi2b é codificado pelo gene SLC34A2 que pertence à família de tipo II de transportadores de fosfato dependentes de sódio (família SLC34). Ele está envolvido em regulação de hemostasia de fosfato inorgânico em corpo humano por absorção de Pi inorgânico, enquanto que cotransportador de fosfato dependente de sódio homólogo NaPi2a é crítico para reabsorção de Pi renal [10].
[00387] NaPi2b é uma proteína de transmembrana com peso molecular dentro da faixa de 76-110 kDa dependendo do estado de glicosilação [6-9, 11, 12]. É predito que ela é ancorada na membrana plasmática através de pelo menos 8 regiões α-helicoidais elevadamente hidrofóbicas [13]. Tem sido previamente proposto que NaPi2b possui uma alça extracelular grande (188- 360aa), 8 domínios de transmembrana e as caudas citoplásmicas N- e C- terminais. A alça extracelular maior contém vários sítios potenciais de glicosilação e uma região rica em resíduos de cisteína, que poderia estar envolvida em formação de ligação de dissulfeto [2]. Temos recentemente descrito a produção de vários anticorpos monoclonais direcionados contra alça extracelular de NaPi2b (188-360aa) e estreitado seus epítopos entre resíduos de aminoácido 311 e 340 [14]. Estes anticorpos poderiam ter um valor terapêutico, porque NaPi2b é uma proteína de membrana e é sobre- expressada em câncer ovariano.
[00388] Estudos recentes forneceram a evidência de que mutações em gene SLC34A2 estão associadas com microlitíase alveolar pulmonar (PAM) que é caracterizada pela deposição de micrólitos de fosfato de cálcio nos pulmões [15]. Até o presente, não há dados que poderiam ligar mutações em gene SLC34A2 com transformação maligna.
[00389] Neste estudo descrevemos duas mutações em gene NaPi2b que poderiam potencialmente estar associadas com câncer ovariano: T330V em uma alça extracelular grande e uma deleção de 6 aa na extremidade C- terminal de transportador. Estas mutações, bem como outras foram identificadas por análise bioinformática de seqüências de NaPi2b em vários bancos de dados de DNA. Ademais, temos criado construtos de expressão de formas de tipo selvagem e mutante de NaPi2b adequados para tornar estáveis as linhagens celulares. Nível alto de expressão de formas de tipo selvagem e mutante de NaPi2b em linhagens de células HEK293 estáveis foi confirmado por análise Western-blot. Linhagens celulares gerais serão usadas para estudar a regulação de NaPi2b sob várias condições experimentais, tais como estimulação mitogênica, tratamento de células com inibidores de transdução de sinal, exposição a estresses celulares etc.
Material e métodos
Abordagens bioinformáticas
[00390] Bancos de dados GeneBank foram pesquisados para mutações potenciais em cotransportador dependente de sódio Napi2b. Programa CLUSTALW (1.82) (www.ebi.ac.uk/clustalw/)foi usado para alinhamento de múltiplas seqüências de clones EST diferentes correspondendo a Napi2b.
Clonagem de Napi2b de tipo selvagem em pcDNA3.1
[00391] O clone de cDNA de comprimento total de NaPi2b de humano (Napi2b_WT) foi amplificado do clone original DKFZp6860655Q2 (recebido do banco de genes RZPD) com iniciadores contendo sítios de clonagem e seqüências para a etiqueta-EE (Tabela 6). O fragmento de cDNA amplificado foi então ligado em vetor de expressão em mamífero pcDNA3.1+ (Invitrogen, USA) quer permite a expressão de cDNA clonado em células de mamífero sob o controle do promotor CMV. Plasmídeos de cDNA gerados foram confirmados por análise de restrição e seqüenciamento de DNA. DNA plasmídeo usado nos estudos subseqüentes foi purificado pelo kit de purificação de DNA (Promega, USA). TABELA 6
[00392] Iniciadores oligonucleotídeo usados para clonagem e mutagênese sítio-direcionada
Mutagênese sítio-direcionada
[00393] 20 ng do plasmídeo pcDNA3.1/NaPi2b foram amplificados com 2,5U de Pfu DNA polimerase na presença de iniciadores sobrepostos para mutagênese (9 pmol de cada). Os iniciadores continham uma mutação (ac 988 gt para T330V e dell768-1785nt para del6aa, veja tabela 1) no meio da seqüência. Amplificação por PCR foi realizada em 50μl com 18-22 ciclos térmicos (95°C por 30s, 55°C por 1 min e 68°C por 16 min). DNA amplificado foi precipitado, redissolvido em 15μl de água e então DNA dam- metilado parental foi digerido com 10U de DpnI por 1 h a 37°C. 100 μl de células ultracompetentes XL1-Blue foram transformadas com 4μl da mistura reacional, crescidas por 45 min em meio SOC e plaqueadas sobre placa de ampicilina-LB. DNA plasmídeo foi purificado pelo kit de purificação de DNA (Promega, USA). Mutações geradas foram verificadas por análise de seqüenciamento.
Produção de células HEK293 estáveis
[00394] Inicialmente, construtos de DNA produzidos foram linearizados com enzima de restrição Sca1 (Fermentas, Lituânia) de acordo com as recomendações do fabricante. Transfecção de células HEK293 com FuGene (Roche, Suíça) foi realizada em placas de 6 cm quando densidade de células alcançou 60-70%. 5 μg de cada DNA plasmídeo (pcDNA3.1/NaPi2b- WT, pcDNA3.1/NaPi2b-T330V, pcDNA3.1/NaPi2b-A6aa ou vetor vazio) foram misturados com 500 μl de meio DMEM padrão. Reagente FuGene (10 μl) foi adicionado em cada amostra e incubados na temperatura ambiente por 10 min antes da adição nas células. Após incubação de 24h, o meio foi substituído por meio DMEM completo (FBS 10%, Glutamina 1 mM, antibióticos penicilina (50 U/mL)/estreptomicina (0,25mkg/mL)). Após 48 h, o meio foi substituído por meio DMEM completo contendo 1 mg/mL de antibiótico G418 (Gibco, USA). Células transfectadas foram cultivadas na presença de G418 por 7-10 dias com o propósito de eliminar células não- transfectadas. Linhagens de células estáveis geradas foram cultivadas na presença de G418.
Lise celular e análise Western-blot
[00395] Células HEK293 estavelmente transfectadas foram lisadas em tampão contendo Tris-HCl 10 mM, pH 7,5, NaCl 150 mM, MgCl210 mM, NP-40 0,5%, e uma mistura de Coquetel de Inibidor de Protease Halt (Pierce, USA). Concentração de proteína foi medida pelo ensaio Bradford (Pierce, USA), e quantidades iguais de proteínas (10 μg) foram separadas em 8% SDS-PAGE e aplicadas como manchas (blotted) em membrana de poli(difluoreto de vinilideno) (PVDF) (Millipore, USA). A membrana foi bloqueada com BSA 3% em PBS (tampão de solução salina tamponada com fosfato) contendo 0,1% d Tween-20 (PBST) por 1 h. Anticorpos anti-NaPi2b e anti-etiqueta-EE foram incubados com membranas a 4°C durante a noite. Geração de anticorpos monoclonais contra a alça extracelular do transportados foi previamente descrita [5]. Após lavagem com PBST, IgG1 de cabra anti-camundongo conjugada com HRP 1:5000 (Promega, USA) foi adicionada na membrana por 1 h na RT. Western blots foram desenvolvidos com o sistema ECL (Amersham, Suécia) e então expostos ao filme Agfa de raios-X.
Resultados e discussão
[00396] Temos recentemente identificado cotransportador de fosfato dependente de sódio NaPi2b como antígeno MX35 que é sobre-expressado em 90% dos casos de câncer ovariano epitelial de humano [2, 3]. Em células normais, NaPi2b medeia efluxo trans-epitelial de fosfato inorgânico e de íons sódio através de membrana apical de enterócitos em intestino delgado e desempenha um papel importante na manutenção de homeostasia de fosfato em corpo humano [16]. NaPi2b também é expressado na superfície apical de células epiteliais em outros órgãos para proporcionar nível de fosfato inorgânico apropriado em tensoativo alveolar [6], bile [7], saliva [9], e fluido epididimal [11]. Notavelmente, NaPi2b é expressado em um nível muito baixo em ovário normal, ao contrário da expressão alta em câncer ovariano epitelial [1,5]. Até agora, não está clara a base lógica para expressão em nível alto de transportador NaPi2b em câncer ovariano. Isto poderia refletir a demanda aumentada em células de câncer por fosfato inorgânico que é exigido para processos de biossíntese e transdução de sinal. É sabido que a função de transportador de fosfato é regulada por diversos estímulos extracelulares, incluindo, incluindo FGF 23, EGF, glicocorticóides, vitamina D e estrógenos [17-21]. Por essa razão, desregulação de rotas de sinalização induzidas por transformação oncogênica pode causar o aumento da captação de nutrientes através da expressão aumentada de transportadores no nível de transcrição e tradução.
[00397] Temos realizado análise bioinformática detalhada das mutações potenciais em gene SLC34A2 em banco de dados disponíveis e composto o mapa de variações de seqüência em seqüência de NaPi2b de humano (dados não mostrados). Este estudo permitiu-nos identificar 15 diferenças na seqüência codificadora de NaPi2b de humano: sete delas foram encontradas em DNA genômico de pacientes sofrendo de microlitíase alveolar pulmonar; uma em DNA genômico de paciente com microlitíase testicular; três em clones de cDNA de linhagens de célula de câncer ovariano quatro de tecidos aparentemente normais.
[00398] Análise bioinformática de seqüências de NaPi2b de linhagens de células de câncer ovariano revelou três mutações potencialmente associadas ao câncer ovariano: a) uma substituição de único aminoácido T330V em uma alça extracelular grande; b) deleção de 6 aa (591-596aa); e c) uma deleção de 56 aa (461-519aa) em terminação-C do transportador (FIGURA 21).
[00399] Mutação pontual T330V está localizada em uma alça extracelular grande de proteína Napi2b e por essa razão poderia influenciar propriedades antigênicas de transportador. Corut et al. têm descrito substituição T330M em NaPi2b e têm indicado que esta mutação poderia inativar transportador NaPi2b devido à substituição de resíduo polar por um não-polar [15]. Assim, esta posição pode representar um ponto quente de mutação em NaPi2b, especialmente em câncer ovariano.
[00400] As deleções identificadas em NaPi2b estão localizadas na cauda C-terminal - esta região do transportador de fosfato é possivelmente responsável pela interação com parceiros de ligação implicados na regulação de localização celular e similaridade de função com NaPi2a [22]. Uma deleção de 6aa é flanqueada por repetições diretas curtas, que poderiam estar envolvidas no mecanismo de mutagênese por deslizamento na replicação [23], mutagênese sítio-direcionada e outros. Propomos que estas mutações podem existir em câncer ovariano e podem influenciar a função e a localização celular de NaPi2b.
[00401] Temos criado construtos de cDNA mutantes de NaPi2b com uma mutação pontual T330V e uma deleção de 6aa de 591...596 aa por mutagênese sítio-direcionada. Infelizmente, não fomos bem sucedidos na preparação de um mutante de deleção de 59 aa em plasmídeo de expressão de mamífero. Clonagem de NaPi2b de tipo selvagem em matriz com o epítopo de etiqueta-EE N-terminalmente localizada em vetor pcDNA3.1 foi realizada como descrita em Materiais e Métodos. Todos os construtos gerados foram linearizados e usados para transfecção estável de células HEK293. Após seleção de 7-10 dias de células transfectadas sobre meio contendo geneticina temos selecionado colônias parta testar expressão de NaPi2b.
[00402] A expressão de NaPi2b (formas de tipo selvagem e mutante) em HEK293 foi confirmada por análise Western blot de lisados celulares totais com anticorpo monoclonal anti-EE (FIGURA 22A) ou anticorpos monoclonais anti-NaPi2b (FIGURA 22B). Ademais, temos verificado que MAb anti-NaPi2b gerado contra a alça extracelular de transportador (L2(20/3)) especificamente reconhece tipo selvagem e um mutante de deleção de 6 aa, mas não detecta mutante NaPi2b trazendo substituição T330V na alça extracelular de NaPi2b localizada dentro de uma região de epítopo para L2(20/3) MAb (311-340aa). Estes dados indicam claramente que a substituição T330V de aminoácido hidrofílico por não-polar poderia ser crucial para reconhecimento de epítopo por L2(20/3) MAb. O epítopo de anticorpo MX35 também está localizado na mesma região da alça extracelular grande [2] e o MAb MX35 não detecta o mutante NaPi2b trazendo substituição T330V em células HEK293 estavelmente transfectadas como avaliado por Western blot (FIGURA 23).
Conclusões
[00403] Temos criado linhagens de célula estáveis expressando formas de tipo selvagem e mutante de transportador de fosfato NaPi2b e temos mostrado que mutação T330V na alça extracelular não é reconhecida pelo anticorpo MX35L2 ou L2(20/3) mAb anti-Napi2b por análise Western-blot. Este resultado poderia ser explicado pela destruição ou alteração do epítopo para estes anticorpos sob substituição da treonina por valina na região de epítopo de proteína NaPi2b (SLC34A2) e está consistente com os resultados de T330M em Exemplo 6 acima.
[00404] Linhagens de célula estáveis serão usadas para análise adicional de transportador de fosfato NaPi2b em células normais e transformadas. Investigaremos o impacto de mutações geradas sobre a função de transporte de fosfato e processos celulares, tais como biossíntese de DNA, crescimento e proliferação.
Referências
[00405] 1. Rangel L.B., Sherman-Baust C.A., Wernyj RP., Schwartz D.R, Cho K.R, Morin P.J. Characterization of novel human ovarian cancerspecific transcripts (HOSTs) identified by serial analysis of gene expression // Oncogene. - 2003. -22, N 46.-P. 7225-7232.
[00406] 2. Yin B.W.T., Kiyamova R, Chua R, Caballero O. L, Gout I., Gryshkova V., Bhaskaran N., Souchelnytskyi S., Hellman U., Filonenko V., Jungbluth A.A., Odunsi K., Lloyd K.O., Old L.J., Ritter G. Monoclonal antibody MX35 detects the membrane transporter NaPi2b (SLC34A2) in humancarcinomas; a new target for cancer immunotherapy // Cancer Immun. [serial online]. - 2008. -8, N 3. -URL: http://www.cancerimmunity.org/v8p3/080103.htm.
[00407] 3. Mattes M.J., Look K., Furukawa K., Pierce V.K., Old L.J., Lewis J. L, Lloyd K.O. Mouse monoclonal antibodies to human epithelial differentiation antigens expressed on the surface of ovarian carcinoma ascites cells // Cancer Res.- 1987.- 47.-P. 6741-6750.
[00408] 4. Rubin S.C., Kostakoglu L., Divgi C, Federici M.G., Finstad C.L., Lloyd K.O, Larson, S.M., Hoskins, W.J. Biodistribution and intraoperative evaluation of radiolabeled monoclonal antibody MX35 in patients with epithelial ovarian cancer//Gynecol. Oncol.- 1993 .-51.-P. 61-66.
[00409] 5. Feild J.A., Zhang L., Brun K.A., Brooks D.P., Edwards ./iMCloning and functional characterization of a sodium-dependent phosphate transporter expressed in human lung and small intestine // Biochem. Biophys. Res. Commun. - 1999. - 258, N 3.-578-582.
[00410] 6. Traebert M., Hattenhauer O., Murer K, Kaissling B., Biber J. Expression of a type II sodium-phosphate cotransporter in murine type II alveolar epithelial cells // Am. J. Physiol.- 1999.- 277.-P.L868-L873.
[00411] 7. Frei P., Gao B., Hagenbuch B., Mate A., Biber J., Murer K, Meier P.J., Stieger B. Identification and localization of sodium-phosphate cotransporters in hepatocytes and cholangiocytes of rat liver // Am. J. Physiol. Gastrointest. Liver Physiol.-2005.-288.-P. G771-G778.
[00412] 8. Huber K., Muscher A., Breves G. Sodium-dependent phosphate transport across the apical membrane of alveolar epithelium in caprine mammary gland // Comparative Biochemistry and Physiology.- 2007.-146.-P. 215-222.
[00413] 9. Homann V., Rosin-Steiner S., Stratmann T., Arnold W.H., Gaengler P., Kinne R.K. Sodium-phosphate cotransporter in human salivary glands: molecular evidence for the involvement of NPT2b in acinar phosphate secretion and ductal phosphate reabsorption // Arch. Oral Biol.- 2005.-50, N 9.-P. 759-768.
[00414] 10. Murer K, Forster I., Biber J. The sodium phosphate cotransporter family SLC34 // Pflugers Arch. -Eur. J. Physiol.-2004.-447.-P. 763-767.
[00415] 11. Xu Y., Yeung C.-H., Setiawan I., Avram C., Biber J., Wagenfeld A., Lang F., and Cooper T.G. Sodium-Inorganic Phosphate Cotransporter NaPi2b in the Epididymis and Its Potential Role in Male Fertility Studied in a Transgenic Mouse Model // Biology of reproduction.- 2003.- 69.-P. 1135-1141.
[00416] 12. Lundquist P., Murer H., Biber J. Type II Na+-P cotransporters in osteoblast mineral formation; regulation by inorganic phosphate // Cell. Physiol. Biochem.- 2007.-19.-P. 43-56.
[00417] 13. Hilfiker K, Hattenhauer O., Traebert M., Forster I., Murer H., Biber J. Characterization of a new murine type II sodium-phosphate cotransporter expressed in mammalian small intestine // PNAS USA.-1998.-P. 14564-14569.
[00418] 14. Kiyamova R, Gryshkova V., Ovcharenko G, Lituyev D., Malyuchik S., Usenko V., Khozhayenko Yu., Gurtovyy V., Yin B., Ritter G., Old L., Filonenko V., Gout I. Development of monoclonal antibodies specific for the human sodium-dependent phosphate cotransporter NaPi2b // Hybridoma.-2008.- 27, N 4.- P.277-284.
[00419] 15. Corut A., Senyigit A., Ugur S.A., Altin S., Ozcelik U., Calisir K, Yildirim Z, Gocmen A., Tolun A. Mutations in SLC34A2 cause pulmonary alveolar microlithiasis and are possibly associated with testicular microlithiasis // Am. J. Hum. Genet.-2006.-79, N 4.-P. 650-656.
[00420] 16. Murer H., Hernando N., Forster I., Biber J. Molecular mechanisms in proximal tubular and small intestinal phosphate // Molecular Membrane Biology.- 2001.- 18.-P. 3-11.
[00421] 17. Miyamoto K, Ito M., Kuwahata M., Kato S., e Segawa H. Inhibition of intestinal sodium-dependent inorganic phosphate transport by fibroblast growth factor 23 // Ther. Apher. Dial.- 2005.-9, N4.-P. 331-335.
[00422] 18. Xu H., Collins J., Bai L., Kiela P., Ghishan F. Regulation of the human sodium-phosphate cotransporter NaPi2b gene promoter by epidermal growth factor // Am. J. Physiol.- 2001.-280.-P.C628-C636.
[00423] 19. Arima K, Hines E.R., Kiela P.R., Drees J.B., Collins J.F., Ghishan F.K. Glucocorticoid regulation and glycosylation of mouse intestinal type lib Na-Pi cotransporter during ontogeny // Am. J. Physiol.-2002.- 283.-P. G426-G434.
[00424] 20. Katai K., Miyamoto K., Kishida S., Segawa H., Nii T., Tanaka H., Tani Y., Arai H., Tatsumi S., Morita K., Taketani Y., and Takeda E. Regulation of intestinal Na+-dependent phosphate co-transporters by a low-phosphate diet and 1,25-dihydroxyvitamin D3 // Biochem. J.- 1999.343.- P. 705-712.
[00425] 21. Xu H., Uno J.K., Inouye M., Xu L., Drees J.B., Collins J.F., e Ghishan F.K. Regulation of intestinal NaPi2b cotransporter gene expression by estrogen // Am. J. Physiol. Gastrointest. Liver Physiol.- 2003.- 285.-P. G1317-G1324.
[00426] 22. Lanaspa M.A., Giral K, Breusegem S.Y, Halaihel N., Baile G, Catalan J., Carrodeguas J.A., Barry N.P., Levi M., Sorribas V. Interaction of MAPI 7 with NHERF3/4 induces translocation of the renal Na/Pi Ha transporter to the trans-Golgi II Am. J. Physiol. Renal Physiol.-2007.-292.-P. 230-242.
[00427] 23. Ball E.V., Stenson P.D., Abeysinghe S.S. Microdeletions and microinsertions causing human genetic disease common mechanisms of mutagenesis and the role of local DNA sequence complexity // Human mutation.-2005.-26, N 3.-P. 205-213.
EXEMPLO 8
INVESTIGAÇÃO DE EXPRESSÃO DE TRANSPORTADOR DE FOSFATO NaPi2b EM DIFERENTES HISTOTIPOS DE CÂNCER OVARIANO EPITELIAL
[00428] A identificação de marcadores específicos que são expressados por tipos histológicos diferentes de câncer ovariano epitelial (EOC) pode levar ao desenvolvimento de novas estratégias terapêuticas e diagnósticas mais específicas. Transportador de fosfato dependente de sódio NaPi2b (ou antígeno MX35 de câncer ovariano) é um novo marcador esperado de EOC. Até o presente momento, os estudos sobre expressão de NaPi2b/MX35 em histotipos diferentes de EOC são limitados. O objetivo do presente estudo foi a investigação de expressão de NaPi2b/MX35 em histotipos diferentes de câncer ovariano epitelial.
[00429] Métodos: Aqui, descrevemos a análise de expressão de NaPi2b em tumores ovarianos mucinosos, endometrióides, serosos pela utilização de Western blotting, imuno-histoquímica e RT-PCR.
[00430] Resultados: Os resultados de análise imuno-histoquímica e immunoblot mostraram que tumores serosos papilares benignos e malignos bem diferenciados bem como tumores endometrióides malignos bem diferenciados sobre-expressam proteína NaPi2b. Contudo, nenhuma sobre- expressão de NaPi2b foi detectada em tumores mucinosos benignos e malignos bem como em tumores endometrióides insatisfatoriamente diferenciados. Notavelmente, a expressão de NaPi2b mRNA foi detectada em todos os tipos histológicos investigados de EOC, indicando a regulação de expressão de NaPi2b em nível de tradução de estabilidade de proteína.
[00431] Conclusão: Visto que pacientes com tumores ovarianos endometrióides e serosos papilares bem diferenciados têm bom prognóstico, a expressão de NaPi2b poderia ser considerada como um marcador de boa prognose destes tipos de malignidades ovarianas.
[00432] Câncer ovariano é a causa mais comum de morte de cânceres do trato genital feminino [1-4]. A taxa de fatalidade alta resulta em parte da diagnose freqüente de câncer ovariano em estágios avançados. Tumores epiteliais de ovário compreendem 58% de todas as neoplasias ovarianas e mais do que 90% de tumores malignos de ovário [5]. EOC resulta de epitélio de superfície ovariana (OSE) que tem fenótipo "não-comprometido" e mantêm a capacidade para diferenciar em tipos diferentes de células em resposta aos sinais ambientais [6]. Durante cancerogênese ovariana, o epitélio de ovário poderia se diferenciar em epitélio de tuba de Falópio (tumores serosos papilares), epitélio endometrial (tumores endometrióides), epitélio colônico ou endocervical (tumores mucinosos) e componente de endometriose (tumores de célula clara). A análise histológica de EOC indica que tumores serosos papilares representam 50-60% de todos os cânceres ovarianos e os tumores restantes exibem histologia endometrióide (25%), mucinoso (4%) e de célula clara (4%) [7]. É óbvio que a heterogeneidade de tumor observada tem uma base molecular e a identificação marcadores moleculares específicos para tipos histológicos diferentes de câncer ovariano epitelial pode levar ao desenvolvimento de abordagens de tratamento mais eficazes.
[00433] Recentemente, estudos de um consórcio colaborador tem levado à identificação de transportador de fosfato dependente de sódio NaPi2b como antígeno de câncer ovariano, chamado MX35 [8]. A identidade de antígeno MX35 foi confirmada por triagem de biblioteca de expressão de OVCAR3 cDNA de linhagem de célula de câncer ovariano com anticorpo monoclonal MX35 e por purificação por afinidade de antígeno MX35 seguida por espectrometria de massa. Antígeno MX35 foi originalmente identificado com o uso de anticorpo monoclonal MX35, obtido de camundongos imunizados com células de carcinoma ovariano novas e selecionado por análise extensiva de linhagens de célula e tecidos malignos e normais. Estudos bioquímicos e imuno-histoquímicos revelaram que MAb MX35 reconhece uma glicoproteína de superfície celular de cerca de 95 kDa que é sobre-expressada em 90% dos espécimes de câncer ovariano mas mostra expressão restrita em tecidos normais. Estudos clínicos com fragmentos Fab de anticorpo MX35 radiomarcado sugerem um potencial terapêutico em pacientes com câncer ovariano [9, 10].
[00434] O transportador de fosfato dependente de sódio NaPi2b de humano é codificado pelo gene SLC34A2 que pertence à família de tipo II de transportadores de fosfato dependentes de sódio (família SLC34). Está envolvido em manutenção da homeostasia de fosfato inorgânico em corpo humano por regulação de absorção de Pi intestinal [11]. Em tecidos normais, a expressão de NaPi2b em nível de proteína é restrita ao intestino delgado [12], pulmão [13], fígado [14], glândulas mamária e salivar [15, 16]. A sobre- expressão de transportador NaPi2b em câncer foi relatada em carcinomas ovarianos epiteliais por análise SAGE e RT-PCR em tempo real [17]. Contudo, quase não há dados em relação à expressão de proteína NaPi2b/MX35 por tipos histológicos diferentes de EOC. A investigação de expressão de NaPi2b por histotipos diferentes de EOC poderia proporcionar o entendimento de seu valor prognóstico e o potencial para desenvolver abordagens imunoterapêuticas em câncer ovariano.
[00435] Neste estudo, comparamos a expressão de proteína NaPi2b entre tecidos ovarianos normais e tipos histológicos diferentes de EOC, tais como tumores ovarianos serosos, endometrióides e mucinosos.
Materiais e Métodos
Amostras de tecido
[00436] Amostras de tumor foram obtidas de pacientes com câncer ovariano (28 no total) admitidos para resseção de tumor no Oncology Institute (NAMS of Ukraine, Kyiv, Ucrânia). Os tipos de EOC foram confirmados por exame histopatológico no Department of Pathology, Oncology Institute (NAMS of Ukraine, Kyiv, Ucrânia). Tecidos ovarianos normais foram usados como amostras de controle. A idade média de pacientes com câncer ovariano e controles foi 47 (faixa de 22-69) e 46 (faixa de 19-69), respectivamente. O estudo foi aprovado pelo Ethics Committee of the Institute of Molecular Biology and Genetics, e formulários de consentimento foram obtidos de todos os pacientes.
Análise Western-blot
[00437] Temos analisado a expressão de NaPi2b em 28 amostras de câncer ovariano e 10 ovários normais. Amostras de tecido foram homogeneizadas em tampão RIPA (TrisHCl 20mM, pH 7,5, 0, NaCl 150mM, EDTA 1mM, NP-40 1%, SDS 0,1%) suplementado com PMSF (Sigma, Steinheim, IL), e Coquetel de Inibidor de Protease (Sigma, Steinheim, IL) e então foram centrifugadas a 4°C por 30 min. Frações solúveis de lisados (50 μg por amostra) foram separadas por 8% SDS-PAGE em condições não- redutoras. Proteínas separadas foram transferidas para uma membrana de PVDF por 2 horas a 80V (Perkin Elmer, Boston, MA) usando uma célula de transferência úmida (Pharmacia Biotech). Após a transferência, a membrana foi bloqueada em tampão PBST (1x PBS com 0,05 % de Tween), contendo 3% de BSA e então incubada em mAb anti-NaPi2b (0,5 mg/mL) [18] a 4°C durante a noite. Após lavagem extensiva em tampão PBST, a membrana foi incubada com anticorpo secundário IgG anti-camundongo (1:5000) por 1 h (Promega, Madison, WI). Os complexos imunes foram detectados pelo sistema ECL (Amersham, Uppsala, Suécia). GAPDH foi usado como um controle de carregamento.
Imuno-histoquímica
[00438] Análise imuno-histoquímica de amostras de câncer com MAbs anti-NaPi2b foi realizada de acordo com um protocolo padrão. Resumidamente, seções representativas de tumores ovarianos foram preparadas de blocos de parafina. Peroxidase endógena foi extinta com H2O2 (3%) em PBS 0,01%. Após bloqueio de ligação não-específica com solução de bloqueio de avidina-biotina (Vector Laboratories, Burlingame, CA, USA), seções de tecido foram incubadas durante a noite a 4°C com mAb anti- NaPi2b (10 mkg/mL). Então, seções foram incubadas com anticorpos secundários biotinilados por 2 horas na temperatura ambiente em diluição 1:400, (IgG de cabra anti-camundongo biotinilada, Sigma, Steinheim, Alemanha), seguido por incubação com complexo de avidina-biotina- peroxidase (Vector Laboratories, Burlingame, CA, USA) por 30 min na RT e revelado com solução de diamino-benzidina. Hematoxilina foi usada para contra-coloração. Microscopia padrão foi realizada usando um microscópio Zeiss Universal (Zeiss, Jena, Alemanha), e imagens foram capturadas usando programa de computador Axiocam digital.
Purificação de RNA total e análise por RT-PCR
[00439] RNA total foi isolado pelo procedimento de extração ácida em tiocianato-de-guanidínio-fenol-clorofórmio [19]. Resumidamente, 1 ml de solução de desnaturação (tiocianato de guanidínio 4 M, citrato de sódio 25 mM, pH 7,0, sarcosil 5%, 2-mercapto-etanol 0,1M) foi adicionado em 100 mg de tecidos homogeneizados. Seqüencialmente, 0,1 mL de acetato de sódio 2M, pH 4, 1 mL de fenol (aquoso saturado), e 0,2ml de mistura de clorofórmio-isoamil-álcool (49:1) foram adicionados no homogeneizado. Após centrifugação a 10.000g por 20 min a 4°C, RNA total foi precipitado da fase aquosa com o mesmo volume de isopropanol a -20°C por 1 h. A pelota foi ressuspensa em etanol 75%, seco com ar e dissolvido em 50 μl de água livre de nuclease.
[00440] RNA total purificado (5 μg) foi convertido em cDNA com Transcriptase Reversa M-MuLV (Fermentas) a 37°C por 60 min usando iniciadores oligo dT. cDNA produzido (100 ng) foram amplificados usando os seguintes iniciadores - direto GTCATCACTAAGCCCTTCACA (SEQ ID NO: 75) e inverso CAGGCAACCACAGAGGAC (SEQ ID NO: 76) - por 30 ciclos em 50 μl de volume total de tampão de PCR 5x PCR (Fermentas) contendo dNTP 10 mM, uma unidade de Taq polimerase, 20 pmoles de cada iniciador. A amplificação foi realizada em Ciclador Térmico de DNA (Perkin Elmer) sob as seguintes condições: 94°C por 60 s, 60°C por 30 s e 72°C por 60 s. Produtos amplificados foram separados sobre um gel de agarose 1% e visualizados.
Resultados
[00441] Neste estudo, examinamos expressão de NaPi2b em tumores ovarianos de histologia serosa, endometrióide e mucinoso. Em um painel de 28 tumores ovarianos, houve 17 tumores serosos (3-cistadenomas, 1 cistadenoma papilar e 13 carcinomas papilares); 8 tumores endometrióides (1 cistadenoma, 4 carcinomas de grau baixo e 3 carcinomas de grau alto); e 3 tumores mucinosos (1 cistadenoma, e 2 carcinomas). As técnicas de Western blot, imuno-histoquímica e RT-PCR foram utilizadas para examinar o perfil de expressão de NaPi2b nestes tumores e para compará-los com tecidos ovarianos normais.
Análise Western-blot de expressão de NaPi2b
[00442] Análise immunoblot de expressão de NaPi2b em amostras ovarianas foi realizada sob condições não-redutoras usando anticorpo monoclonal produzido contra a alça extracelular de NaPi2b de humano (188- 360aa). A especificidade de MAb anti-NaPi2b foi testada com o uso de NaPi2b recombinante expressada em bactérias como proteína de fusão GST (FIGURA 24A). Ademais, confirmamos a expressão de proteína endógena NaPi2b em linhagem de célula de câncer (OVCAR3), linhagem de célula de carcinoma de rim (SKRC18) que são linhagens celulases positivas para MX35 e em HEK293 estavelmente expressando proteína NaPi2b (FIGURA 24B) em Western-blotting.
[00443] Tem sido previamente demonstrado que proteína NaPi2b é reconhecida em WB como painel de bandas imunorreativas com peso molecular diferente, refletindo o estado de glicosilação [12-16, 20-22]. Os resultados apresentados em FIGURA 24C mostram que NaPi2b é reconhecida em lisados de tumor ovariano como banda de 100 kDa. Notavelmente, apenas alguns tumores ovarianos sobre-expressam NaPi2b.
[00444] Análise adicional indicou que a expressão de NaPi2b é detectada em todos (13/13) os cânceres serosos papilares. No caso de tumores serosos benignos expressão de NaPi2b foi detectada apenas em cistadenoma papilar (1/1), enquanto que cistadenomas serosos com estrutura não-papilar não expressaram NaPi2b (3/3) (FIGURA 24C).
[00445] Em tumores endometrióides expressão de NaPi2b foi encontrada em alguns dos tumores testados. De modo interessante, carcinomas endometrióides de grau baixo (4/4) mostraram sobre-expressão de NaPi2b, enquanto que carcinomas endometrióides de grau alto (3/3) e cistadenoma endometrióide (1/1) não expressaram nível detectável de Napi2b (FIGURA 24C).
[00446] A expressão de proteína NaPi2b em WB não foi detectada em cistadenoma mucinoso (1/1) e em carcinomas mucinosos bem como em lisados ovarianos de controle (10/10) (FIGURA 24C).
Análise imuno-histoquímica de tumores ovarianos e tecidos normais do trato ginecológico com MAb anti-NaPi2b
[00447] Realizamos detecção imuno-histoquímica de NaPi2b em todas as amostras de tumor de câncer ovariano mencionadas acima e em tecidos normais de ovário. A presença deNaPi2b por coloração imuno-histológica foi observada apenas na superfície apical de células epiteliais que é uma feição característica de expressão de NaPi2b.
[00448] Verificamos que o epitélio superficial de ovário normal bem como o estroma de ovário foram negativos para coloração de NaPi2b (FIGURA 25A). Análise IH de tumores serosos mostrou coloração forte com MAb anti-NaPi2b em carcinomas serosos papilares (FIGURA 25B) e cistadenomas serosos papilares (FIGURA 25C) mas nenhuma coloração foi detectada em cistadenomas serosos com estruturas não-papilares (FIGURA 25D). Além, disso, tumores endometriais de grau baixo exibiram coloração forte com NaPi2b MAb (FIGURA 25E) que estava ausente em tumores endometrióides benignos e de grau alto. Em todos os casos examinados, tumores ovarianos mucinosos benignos e malignos foram negativos para NaPi2b (FIGURA 25F). Os resultados apresentados acima indicam uma correlação boa entre a expressão de proteína NaPi2b e o tipo de tumor. Padrão diferencial de expressão de proteína NaPi2b em vários tipos de tumores ovarianos sugeriu-nos para examinarmos a expressão de proteína NaPi2b em tecidos normais do trato ginecológico tais como tubas de Falópio, endométrio e endocérvix. Observamos que a coloração positiva com NaPi2b MAb em epitélio de tuba de Falópio normal (FIGURA 26A) e endométrio de tuba de Falópio normal (FIGURA 26B) mas não em epitélio endocervical (FIGURA 26C).
Análise por RT-PCR de SLC34A2
[00449] RNA total derivado de 28 tecidos de câncer ovariano e 10 ovários normais foram investigados em análise por RT-PCR com iniciadores específicos para SLC34A2 (veja materiais e métodos) que foram planejados para seqüências únicas de gene SLC34A2. O produto de amplificação (350 pb) foi analisado sobre um gel de agarose. Os resultados apresentados em FIGURA 27A mostram expressão de gene SLC34A2 no nível de mRNA em todos os tecidos analisados.
[00450] Discussão
[00451] Temos recentemente identificado cotransportador de fosfato dependente de sódio NaPi2b como antígeno MX35 que é conhecidamente sobre-expressado em 90% de cânceres ovarianos de humano [8, 9]. O padrão de expressão de NaPi2b em tecidos normais e em câncer ovariano torna o antígeno NaPi2b/MX35 um alvo potencial para o desenvolvimento de abordagens imunoterapêuticas e diagnósticas de EOC.
[00452] NaPi2b é uma glicoproteína de transmembrana que possui 8 domínios de transmembrana, uma alça extracelular grande (188-360aa) com vários sítios potenciais de glicosilação, e as caudas citoplásmicas N- e C- terminais faceando o citosol [8]. Em adição ao anticorpo MX35, temos recentemente desenvolvido vários anticorpos monoclonais reconhecedores da alça extracelular de NaPi2b de humano [18]. Para nosso conhecimento, a expressão de proteína NaPi2b/MX35 em histotipos diferentes de EOC não tem sido analisada até agora. A elucidação de perfil de expressão de NaPi2b em vários tipos de câncer ovariano poderia ser útil não apenas para o entendimento dos mecanismos celulares de cancerogênese, mas também para a verificação de estratégias de diagnose, prognose e tratamento.
[00453] Neste estudo, temos analisado a expressão de NaPi2b em níveis de proteína e de mRNA em tipos diferentes de câncer ovariano epitelial e tecidos normais de trato ginecológico. Temos observado uma correlação boa de expressão de proteína NaPi2b detectada por WB e IH em amostras de câncer ovariano com tipos histológicos diferentes de tumor. Nossos resultados mostraram que proteína NaPi2b é sobre-expressada em tumores serosos papilares e tumores endometrióides de grau baixo quando comparados com câncer ovariano mucinoso. O tipo histológico mais comum de EOC é o de carcinomas serosos papilares que estão freqüentemente associados com anéis concêntricos de calcificação conhecidos como corpos de psammoma [23]. Notavelmente, cânceres de mama e de tiróide papilar, que são caracterizados por expressão aberrante de NaPi2b, também são afetados por calcificações [24, 25]. Tem sido demonstrado que a regulação positiva da função de transporte de NaPi2b resulta na deposição de micrólitos de fosfato de cálcio em pulmões de paciente. Este fenômeno é causado por mutações em gene SLC34A2 de transportador de fosfato que culmina no desenvolvimento de microlitíase alveolar pulmonar (PAM) [26]. Baseado nestes dados propomos que a calcificação em câncer ovariano seroso papilar poderia estar associada com falha de homeostasia de fosfato de cálcio devido à expressão aberrante em gene de transportador de fosfato NaPi2b.
[00454] Visto que grau de tumor baixo tem estado associado com bons resultado e sobrevivência [27,28], a sobre-expressão de NaPi2b em carcinomas endometrióide e seroso papilar bem diferenciados poderia ser um marcador de uma prognose boa. Nossos dados correlacionam-se bem como aqueles publicados por Rangel et al., mostrando que tumores ovarianos epiteliais bem diferenciados tendem a expressar nível alto de NaPi2b [17].
[00455] Análise por imuno-histoquímica (IH) de tecidos de trato ginecológico normal com NaPi2b MAb revelou sua expressão em endométrio e epitélio de tuba de Falópio, mas não em epitélio endocervical. Visto que epitélio de superfície ovariana de tumores serosos papilares parece-se com epitélio de tuba de Falópio, e tumores endometrióides - epitélio do endométrio e tumores mucinosos - epitélio colônico ou endocervical [29], não é surpreendente que apenas tumores endometrióides e serosos papilares de grau baixo sobre-expressassem a proteína NaPi2b. Assim, a sobre-expressão de proteína NaPi2b em tumores endometrióides e serosos papilares bem diferenciados está ligada à diferenciação de epitélio de superfície ovariana em epitélio e endométrio de tubas de Falópio, respectivamente.
[00456] A expressão de NaPi2b mRNA em tipos diferentes de EOC não mostrou correlação com aquela de proteína NaPi2b detectada por IH e WB. Observamos expressão de mRNA NaPi2b em todos os tipos histológicos investigados de EOC e não houve revelação de diferença significativa entre amostras com níveis alto e baixo de expressão de proteína NaPi2b. A ausência de correlação entre expressão de proteína e NaPi2b mRNA poderia indicar a regulação de expressão de NaPi2b no nível de tradução ou estabilidade de proteína. Estes resultados correlacionam-se com os dados de Rangel et al. mostrando supra-regulação de expressão de SLC34A2 em tumores de célula clara, mucinosos, endometrióides, e serosos de EOC por análise de RT-PCR em tempo real [17].
[00457] Em resumo, nossos dados demonstram que o transportador de fosfato NaPi2b é sobre-expressado em tumores ovarianos endometrióides e serosos papilares bem diferenciados associados como prognose boa. Além disso, verificamos que expressão diferencial de NaPi2b em EOC pode ser a conseqüência de mudanças em diferenciação de epitélio ovariano durante processo maligno. As descobertas deste estudo poderiam facilitar o desenvolvimento racional de novas modalidades diagnósticas e terapias adaptadas para malignidades ovarianas.
Referências
[00458] 1. Jemal A, Siegel R, Ward E, et al. Cancer statistics. CA Cancer J Clin 2008; 58:71-96.
[00459] 2. Cannistra SA. Cancer of the ovary. N Engl J Med 2004; 351:2519-2529.
[00460] 3. Bhoola S, Hoskins WJ. Diagnosis and management of epithelial ovarian cancer. Obstet Gynecol 2006; 107:1399-1410.
[00461] 4. Ozols RF, Rubin SC, Thomas GM, Robboy SJ. Epithelial ovarian cancer. Em: Hoskins WJ, Young RC, Markman M, Perez CA, Barakat R, Randall M, eds. Principles and Practice of Gynecologic Oncology. Philadelphia, PA: Lippincott Williams & Wilkins 2005; 895-988.
[00462] 5. Zoloudek CF. Tumors of the ovary. Em: Fletcher C. Diagnostic Histopathology of Tumors. New-York, NY: Churchill Livingstone, third edition; 2007: 501-555.
[00463] 6. Auersperg N, Wong AS, Choi KC, Rang SK, Leung PC. Ovarian surface epithelium: biology, endocrinology, and pathology. Endocr Rev. 2001; 22(2):255-88.
[00464] 7. Farley J, Ozbun LL, Birrer MJ. Genomic analysis of epithelial ovarian cancer. Cell Res. 2008;18(5):538-48.
[00465] 8. Yin B. W.T., Kiyamova R., Chua R., Caballero O. L, Gout I., Gryshkova V., Bhaskaran N., Souchelnytskyi S., Hellman U., Filonenko V., Jungbluth A. A., Odunsi K., Lloyd K. O., Old LJ., Ritter G. Monoclonal antibody MX35 detects the membrane transporter NaPi2b (SLC34A2) in human carcinomas; a new target for cancer immunotherapy. Cancer Immun [serial online] 2008; 8:3. URL:cancerimmunity.org/v8p3/080103.htm.
[00466] 9. Mattes M. J, Look K, Furukawa K, Pierce V. K, Old L. J, Lewis J. L, Lloyd K. O. Mouse monoclonal antibodies to human epithelial differentiation antigens expressed on the surface of ovarian carcinoma ascites cells. Cancer Res 1987; 47, 6741-6750.
[00467] 10. Rubin S. C, Kostakoglu L, Divgi C, Federici M. G, Finstad C. L, Lloyd K. O, Larson, S. M, Hoskins, W. J. Biodistribution and intraoperative evaluation of radiolabeled monoclonal antibody MX35 in patients with epithelial ovarian cancer. Gynecol Oncol 1993; 51, 61-66.
[00468] 11. Murer H, Forster I, Biber J. The sodium phosphate cotransporter family SLC34. Pflugers Arch -Eur J Physiol 2004; 447: 763767.
[00469] 12. Feild JA, Zhang L, Brun KA, Brooks DP, Edwards RM. Cloning and functional characterization of a sodium-dependent phosphate transporter expressed in human lung and small intestine. Biochem Biophys Res Commun 1999; 258(3):578-82.
[00470] 13. Traebert M, Hattenhauer O, Murer H, Kaissling B, Biber J. Expression of a type II sodium-phosphate cotransporter in murine type II alveolar epithelial cells. Am J Physiol 1999; 277:L868-L873.
[00471] 14. Frei P, Gao B, Hagenbuch B, Mate A, Biber J, Murer H, Meier PJ, Stieger B. Identification and localization of sodium-phosphate cotransporters in hepatocytes and cholangiocytes of rat liver. Am J Physiol Gastrointest Liver Physiol 2005; 288:G771-G778.
[00472] 15. Huber K, Muscher A, Breves G. Sodium-dependent phosphate transport across the apical membrane of alveolar epithelium in caprine mammary gland. Comparative Biochemistry and Physiology 2007; 146: 215-222.
[00473] 16. Homann V, Rosin-Steiner S, Stratmann T, Arnold WH, Gaengler P, Kinne RK. Sodium-phosphate cotransporter in human salivary glands: molecular evidence for the involvement of NPT2b in acinar phosphate secretion and ductal phosphate reabsorption. Arch Oral Biol. 2005; 50(9):759- 68
[00474] 17. Rangel LB, Sherman-Baust CA, Wernyj RP, Schwartz DR, Cho KR, Morin PJ. Characterization of novel human ovarian cancer-specific transcripts (HOSTs) identified by serial analysis of gene expression. Oncogene 2003; 22(46):7225-32.
[00475] 18. Kiyamova R, Gryshkova V, Ovcharenko G, Lituyev D, Malyuchik S, Usenko V, Khozhayenko Yu, Gurtovyy V, Yin B, Ritter G, Old L, Filonenko V, Gout I. Development of monoclonal antibodies specific for the human sodium-dependent phosphate cotransporter NaPi2b. Hybridoma 2008; 27(4):277-284.
[00476] 19. Siebert PD, Chenchik A. Modified acid guanidinium thiocyanate-phenol-chloroform RNA extraction method which greatly reduces DNA contamination. Nucleic Acids Res. 1993; 21(8):2019-20.
[00477] 20. Xu Y, Yeung C-H, Setiawan I, Avram C, Biber J, Wagenfeld A, Lang F, and Cooper TG: Sodium-Inorganic Phosphate Cotransporter NaPi2b in the Epididymis and Its Potential Role in Male Fertility Studied in a Transgenic Mouse Model. Biology of reproduction 2003; 69:1135-1141.
[00478] 21. Lundquist P, Murer H, Biber J. Type II Na+-P cotransporters in osteoblast mineral formation; regulation by inorganic phosphate. Cell Physiol Biochem 2007; 19:43-56.
[00479] 22. Hilfiker H, Hattenhauer O, Traebert M, Forster I., Murer H, Biber J Characterization of a new murine type II sodium-phosphate cotransporter expressed in mammalian small intestine. Proc Natl Acad Sci USA 1998; 14564-14569.
[00480] 23. Maki, M.; Hirota, S.; Kaneko, Y.; Morohoshi, T. Expression of osteopontin messenger RNA by macrophages in ovarian serous papillary cystadenocarcinoma: a possible association with calcification of psammoma bodies. Pathol Int. 2000; 50(7):531-5.
[00481] 24. Blanchard, A.; Shiu,R.; Booth, S. et al. Gene expression profiling of early involuting mammary gland reveals novel genes potentially relevant to human breast cancer. Frontiers in Bioscience 2007;12: 2221-2232.
[00482] 25. Galeza -Kulik M, Zebracka J, Szpak-Ulczok S, et al., Expression of selected genes involved in transport of ions in papillary thyroid carcinoma.[Article in Polish] Endokrynol Pol. 2006;57:26-31.
[00483] 26. Corut A, Senyigit A, Ugur SA, Altin S, Ozcelik U, Calisir H, Yildirim Z, Gocmen A, Tolun A: Mutations in SLC34A2 cause pulmonary alveolar microlithiasis and are possibly associated with testicular microlithiasis. Am J Hum Genet 2006; 79 (4):650-656.
[00484] 27. Makar AP, Beakeland M, Trope CG, et al. The prognostic significance of residual disease, FIGO substage, tumor histology, and grade in patients with FIGO stage 111 ovarian cancer. Gynecol Oncol 1995; 56(2): 175-180.
[00485] 28. Shimuzu Y, Kamoi S, Amada S, et al. Toward the development of a universal grading system of ovarian epithelial carcinoma. 1. Prognostic significance of hystopathologic features - problems involved in the architectural grading system. Gynecol Oncol 1998; 70 (1): 2-12.
[00486] 29. Seidman JD, Kurman RJ. Pathology of ovarian carcinoma. Hematol Oncol Clin North Am 2003; 17:909-925.
EXEMPLO 9
ANTICORPO MX35 INTRA-REGULA NaPi2b E INIBE O TRANSPORTE DE FOSFATO
[00487] Pré-incubação de anticorpos MX35 com células HEK293 estavelmente transfectadas com NaPi2b de tipo selvagem (SLC34A2) resultou em inibição do transporte de fosfato dependente de sódio. Células HEK 293 expressando NaPi2b de tipo selvagem (SLC34A2) foram pré-incubadas com anticorpo MX35 (50 μg/mL) por um período de 1 hora, 24 h ou 48 h. Análise Western blot de lisados de células HEK293 com anticorpo MX35, MAb anti- camundongo conjugado e MAb anti-beta-actina de controle é mostrada em FIGURA 28. Níveis de NaPi2b foram reduzidos em pré-incubação com anticorpo MX35.
[00488] Embora anticorpo MX35 regulasse positivamente o nível de NaPi2b de tipo selvagem em células HEK293 estáveis, o nível de forma mutante T330V de NaPi2b não foi alterado ou reduzido sob pré-incubação com MX35. Estes resultados são mostrados em FIGURA 29.
[00489] Pré-incubação de células HEK293 expressando NaPi2b de tipo selvagem (SLC34A2) com MX35 MAb inibiu o transporte de fosfato. Isto é mostrado em FIGURA 30. O ensaio de fosfato foi realizado na presença de P33 por 15 min. nMol de Pi por mg de proteína é tabulado.
[00490] Esta invenção pode ser representada como modalidade em outras formas ou realizada em outras maneiras sem se desviar do espírito ou das características essenciais da mesma. Portanto a presente revelação é para ser considerada como em todos os aspectos ilustrativa e não restritiva, o escopo da invenção sendo indicado pelas reivindicações anexadas, e todas as mudanças que caem dentro do significado e da extensão de equivalência são intencionadas para serem incluídas nela.
[00491] Várias referências são citadas em todo este relatório descritivo, cada uma das quais é aqui incorporada como referência em sua totalidade.