BRPI0909317B1 - Imidazoquinolinas substituídas - Google Patents
Imidazoquinolinas substituídas Download PDFInfo
- Publication number
- BRPI0909317B1 BRPI0909317B1 BRPI0909317-6A BRPI0909317A BRPI0909317B1 BR PI0909317 B1 BRPI0909317 B1 BR PI0909317B1 BR PI0909317 A BRPI0909317 A BR PI0909317A BR PI0909317 B1 BRPI0909317 B1 BR PI0909317B1
- Authority
- BR
- Brazil
- Prior art keywords
- alkyl
- aryl
- butyl
- heterocyclyl
- group
- Prior art date
Links
Images
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D471/00—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00
- C07D471/02—Heterocyclic compounds containing nitrogen atoms as the only ring hetero atoms in the condensed system, at least one ring being a six-membered ring with one nitrogen atom, not provided for by groups C07D451/00 - C07D463/00 in which the condensed system contains two hetero rings
- C07D471/04—Ortho-condensed systems
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/02—Stomatological preparations, e.g. drugs for caries, aphtae, periodontitis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/02—Nasal agents, e.g. decongestants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P11/00—Drugs for disorders of the respiratory system
- A61P11/06—Antiasthmatics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
- A61P31/06—Antibacterial agents for tuberculosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
- A61P31/22—Antivirals for DNA viruses for herpes viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P33/00—Antiparasitic agents
- A61P33/02—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis
- A61P33/08—Antiprotozoals, e.g. for leishmaniasis, trichomoniasis, toxoplasmosis for Pneumocystis carinii
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/08—Antiallergic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D453/00—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids
- C07D453/02—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids containing not further condensed quinuclidine ring systems
- C07D453/04—Heterocyclic compounds containing quinuclidine or iso-quinuclidine ring systems, e.g. quinine alkaloids containing not further condensed quinuclidine ring systems having a quinolyl-4, a substituted quinolyl-4 or a alkylenedioxy-quinolyl-4 radical linked through only one carbon atom, attached in position 2, e.g. quinine
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Engineering & Computer Science (AREA)
- Oncology (AREA)
- Virology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Communicable Diseases (AREA)
- Pulmonology (AREA)
- Molecular Biology (AREA)
- Tropical Medicine & Parasitology (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Biotechnology (AREA)
- AIDS & HIV (AREA)
- Neurology (AREA)
- Neurosurgery (AREA)
- Biomedical Technology (AREA)
- Otolaryngology (AREA)
- Diabetes (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
Abstract
IMIDAZOQUINOLINAS SUBSTITUÍDAS. A presente invenção refere-se a imidazoquinolinas de fórmula l que contêm funcionalidade de amina substituída ou funcionalidade de amida na posição 1 e que são eficazes como ativadores de Receptor 7 do tipo dobre de sino. Estes compostos são úteis como agentes anticâncer.
Description
A presente invenção refere-se a derivados de imidazoquinolina e a composições farmacêuticas contendo os derivados de imidazoquinolina. Os derivados de imidazoquinolina são úteis como ativadores de agonis- ta/TRL7 receptor do tipo dobre de sino.
Os receptores do tipo dobre de sino (TLR) atualmente compreendendo um gene familiar de 10 receptores com especificidades diferentes são parte do sistema de reconhecimento padrão patógeno celular, que evoluiu para defesa contra uma variedade de infecções (bactérias, vírus, fungos). A ativação de TLRs leva às respostas de citocinas, por exemplo, com liberação de interferons e ativação de células imunes especificadas. A ex-pressão funcional de TLRs selecionados em tecidos é altamente diferente. Parte dos receptores é localizada na superfície da célula tal como TLR4 (estimulado por lipopolissacarídeo LPS de E.coli), por exemplo, sobre células epiteliais, ou TLR3, 7, 8 e 9 localizados em membranas endossômicas em células imunes especificadas. Os últimos são todos ativados pelos ácidos nucleicos, porém identificam-se vários tipos deles. Por exemplo, o TLR9 é ativado por DNA de fita única contendo subsequências CpG, TLR7 e 8 são ativados por RNA de fita única, e TLR3 é ativado por RNA de fita dupla.
Alguns agonistas de TRL7 ou TRL8 (SMOL) de molécula pequena foram identificados. Aqueles agonistas podem ser agrupados em moléculas do tipo purina, tal como 7-tia-8-oxoguanosina (TOG, isatoribina) ou o imi- quimod de imidazoquinolina. Imiquimod é, até aqui, o único agonista de TLR definitivo aprovado, comercializado como 5 % de creme (por Aldara). Ele gera aproximadamente 80 % de purificação em 5 anos de carcinomas de célula basal superficiais, que é o câncer mais frequente por todo o mundo. O imiquimod ativa o TLR7. A expressão funcional de TLR7 parece ser restrita às células imunes especificadas, isto é, em seres humanos, até aqui, somente células dendríticas plasmacitoides, células B e provavelmente eosinó- filos são conhecidos serem ativados por agonistas de TLR7.
Durante vários anos fortes esforços estão em andamento por todo o mundo na tentativa de explorar a forte ativação imune induzida por a- gonistas de TLR7, 8 ou 9 para o tratamento de câncer. A imunoterapia de câncer, entretanto, experimentou uma longa história de falhas. Em anos recentes, contudo, o conhecimento sobre vigilância imune de câncer e a função de subgrupos de terapia de células imunes foi melhorado drasticamente. Os agonistas de TLR7 ou TLR9 estão em desenvolvimento clínico para mo- noterapías ou terapias de combinação de câncer, ou como adjuvantes de vacina.
O método agonista de TLR para imunoterapias de câncer é diferente de esforços anteriores usando, por exemplo, citocinas, interferons ou vacinações monovalentes, a ativação imune mediada por agonista de TLR é pleiotrópica por meio de células imunes especificadas (células dendríticas primárias e células B, subsequentemente outras células), que geram uma resposta imune inata e adaptável. Entretanto, não apenas um interferon é induzido, porém de preferência as muito diferentes isoformas conjuntamente, e não apenas o tipo I (alfa, beta), mas também (indiretamente) o tipo II (gama, células NK). Pelo menos para a aplicação local, a Aldara deu uma prova de conceito notável. Isto demonstra que os antígenos são liberados por tumores, e que terapia imune pode ajudar nas indicações de câncer em princípio, e ainda em monoterapia. Para uma via de administração sistêmica, con-tudo, o POC clínico é dependente dos agonistas de TLR7 ou TLR9, que estão em testes clínicos. Para cânceres avançados e aplicações sistêmicas (preferivelmente via de administração s.c. ou i.v.) parece estar claro que tais agonistas de TLR devem ser combinados com outras terapias.
No caso de estágios precoces de câncer a situação pode ser diferente. A metástase é um aspecto mais grave de desenvolvimento de tumor em pacientes, em grande parte porque os tumores são detectados muito tarde, quando a metástase já ocorreu. As terapias de tumor estabelecidas na maioria das vezes incluem fármacos citotóxicos com janelas terapêuticas de preferência reduzidas. Consequentemente, para o tratamento em estágios de tumor precoces, quando a supressão de disseminação de metástase pode também ser possível, a necessidade é alta de novas terapias com boa tolerabilidade e segurança.
A ativação do sistema imune, e em particular, a ativação de sinalização de receptor do tipo dobre de sino (TLR) fornece novos métodos promissores. Os oligos CpG agonísticos de TLR9 tipo H2006 ou H 1826, e os agonistas de TLR7 tipo isatoribina derivada de guanosina ou um derivado de imiquimod foram testados no modelo de metástase de pulmão de Renca de murina. Todas as moléculas testadas virtualmente completamente suprimiram a emergência de metástase de pulmão com boa tolerabilidade.
Isto fornece uma razão convincente para o desenvolvimento clínico de tais moléculas para supressão de metástase de câncer e pontos para a estabilidade de aplicação sistêmica de tais fármacos. Entretanto, os a- gonistas de TLR7 do tipo SMOL têm a vantagem de síntese eficaz e custo estabelecido se comparados aos agonistas de TRL9 do tipo ácido nucleico, e são bem adaptados para aplicação tópica. US-B-6,573,273 descreve compostos de imidazoquinolina e te- tra-hidroimidazoquinolina que contêm funcionalidade de ureia, tioureia, acilu- reia, sulfonilureia ou carbamato. Os compostos são ditos serem úteis como imunomoduladores. US-B-6,677,349 descreve compostos de imidazoquinolina e te- tra-hidroimidazoquinolina que contêm funcionalidade de sulfonamida na posição 1. Os compostos são ditos serem úteis como imunomoduladores. US-A-2003/0144283 e WO-A-00/76505 descrevem compostos de imidazoquinolina e tetra-hidroimidazoquinolina que contêm funcionalidade de amida na posição 1. Os compostos são ditos serem úteis como imunomoduladores. WO-A-2005/051324 descreve sistemas de anel imidazoquinolina, piridina e naftiridina substituído na posição 1 com oxima ou uma funcionalidade de N-óxido especial. Os compostos são ditos serem úteis como imunomoduladores.
Descobriu-se que moléculas pequenas, em particular, derivados de imidazoquinolinas-4-amina são ativadores de TLR7 com alta potência. Estes derivados de imidazoquinolina têm propriedades físicoquímicas e far- macocinéticas favoráveis. Consequentemente, esta invenção fornece compostos, que constataram ser ativadores de TLR7 e que são definidos pela fórmula estrutural geral I: em que: R1, A e B são como definidos abaixo. Os compostos de fórmula I são úteis como ativadores de TLR7.
A invenção também fornece composições farmacêuticas conten do uma quantidade eficaz de composto de fórmula I. Além disso, métodos de sinterização de compostos de fórmula I são descritos.
Descrição das Figuras A figura 1 mostra o efeito de cloroquina sobre indução de citoci- na de agonistas de TRL em células PCIR-I. A expressão de mRNA IL8 foi medida com PCR de TaqMan após 16 horas de incubação de células com H2006, LPS ou Resiquimod apenas e em incubação com cloroquina. A figura 2 mostra a cascata de análise de agonista de TLR. A figura 3 mostra a indução de mRNA de citocina em hPBMC tratado com 3-{acetil[4-(4-amino-2-etil-1H-imidazo[4, 5-c]quinolin-1- il)butil]amino}-2,5- anidro-1,3,4-trideoxipentitol (TLR ago 1, exemplo III). A figura 4 mostra estudos com compostos de referência no modelo de metástase de pulmão de Renca (Leia A, Hofmann HP, Maier T, Dra- che D, Grebe C, Fischer S, Gimmnich P, Sanders K, Gekeler V. Metastasis of murine Renca kidney cancer cells to the lungs of Balb/c mice is strongly suppressed by TLR9 or TLR7 agonists. Abstract 3552, Proc Am Cancer Res 48, 2007), TOG = 7-tia-8-oxoguanosina; IMDZQ = derivado de imidazoquinolina). Em particular, os camundongos Balb/c fêmeas (n=10) foram tratados durante 4 dias consecutivos iniciando 1 dia ou 8 dias após a injeção de célula tumoral LacZ Renca. Os compostos (moléculas pequenas (SMOLs)) foram aplicados em 20 % de PEG, ODNs em 0,9 % de NaCI como indicado. Os pulmões foram excisados 25 dias após a injeção de célula tumoral (veja figura 4A). Além disso, camundongos Balb/c fêmeas (n=5) foram tratados durante 4 dias consecutivos como indicado. Os compostos (SMOLs) foram aplicados em 20 % de PEG, ODNs em 0,9 % de NaCI. Em 4 dias de tratamento, o sangue foi coletado por meio do plexo orbital e os baços foram excisados. Subsequentemente, o mRNA foi isolado para análise de expressão por meio de qPCR. Os dados foram normalizados para controle de veículo (a média fixada em 1). A avaliação estatística foi realizada por meio de teste de Mann-Whitney (veja Figura 4B). A figura 5 mostra estudos similares à figura 4, entretanto, realizados com 3-{acetil[4-(4-amino-2-etil-1 H-imidazo[4,5-c]quinolin-1- il)butil]amino)-2,5-anidro-1,3,4-trideoxipentitol (TLR ago 1, exemplo III) e N- [4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N-(1,1-dioxidotetra- hidro-3-tienil)acetamida (TLR ago 2, exemplo I) no modelo de metástase de pulmão de Renca.
Descobriu-se que os derivados de imidazoquinolinas, que são descritos com maiores detalhes abaixo, são ativadores eficazes de TLR7 e têm propriedades surpreendentes e particularmente vantajosas. Além disso, e com base nos antecedentes, descobriu-se também, que certos solvatos, sais, N-óxidos ou estereoisômeros farmaceutica- mente aceitáveis, destes derivados de imidazoquinolinas, ou combinações dos mesmos, têm propriedades surpreendentes e particularmente vantajo- sas. A presente invenção fornece compostos de fórmula I: em que Ri é selecionado do grupo consistindo em: - H, alquila, alquinila, arila, alcóxi, heterociclila e heteroarila, em que alquila, alquinila, arila, alcóxi, heterociclila ou heteroarila pode ser opcionalmente substituída por um ou mais grupos, que são, por exemplo, selecionados do grupo consistindo em: -H, -OH, halogênio, -CO-N(R4)2, -N(R4)2, - CO-CMO alquila, -CO-O-C1.10 alquila, -N3, arila opcionalmente substituída, heterociclila, ou -CO-arila; cada R4 é independentemente selecionado do grupo consistindo em: - H, -Ci-io alquila, -CMO alquil-arila, arila; A é Ci-C3 alquila; B é - N(R2)(R3); R2 θ hidrogênio ou -(CO)-R5; Rs é selecionado do grupo consistindo em: alquila, alquinila, arila, heterociclila e heteroarila, cada da qual pode ser opcionalmente substituída por um ou mais grupos, que são, por exemplo, selecionados do grupo consistindo em: - H, -OH, halogênio, -CN, -NO2, -COOH, -SH, -CO-C^e alquila, - CO-O-C1-6 alquila, -N3, arila opcionalmente substituída, heterociclila, -CO- arila ou -CO-heterociclila; R3 é selecionado do grupo consistindo em: - H, alquila, alquenila, arila, heteroarila, cicloalquila e heterociclila, em que alquila, alquenila, arila, heteroarila, cicloalquila, ou heterociclila pode ser não substituída ou substituída por um ou mais substituintes, que são, por exemplo, selecionados do grupo consistindo em: -H, alquila, alquenila, alcóxi, halogênio, -OH, -N3, trifluorometila, -alquil-arila, -O-alquil-arila, -CO-arila, arila, heterociclila, heteroarila, -CO-heteroarila, -CO-arila substituída, -CO- heteroarila substituída, -CO-O-alquila, -CO-N-alquila, -CO-N-arila; ou solva- tos, sais, N-óxidos farmaceuticamente aceitáveis ou estereoisômeros dos mesmos, ou combinações dos mesmos.
Como usados aqui, os termos "alquila", "alquenila", "alquinila" e o prefixo "alqu" são inclusive tanto de grupos de cadeia linear e cadeia ramificada quanto de grupos cíclicos, isto é, cicloalquila e cicloalquenila. A menos que de outro modo especificado, esses grupos contêm de 1 a 20 átomos de carbono, com grupos alquenila e alquinila contendo de 2 a 20 átomos de carbono. Os grupos preferidos têm um total de até 10 átomos de carbono. Os grupos cíclicos podem ser monocíclicos ou policíclicos e preferivelmente têm de 3 a 10 átomos de carbono no anel. Os grupos cíclicos exemplares incluem ciclopropila, ciclopentila, ciclo-hexila e adamantila.
Em particular, o termo "alquila" refere-se a um radical de alquila de cadeia linear ou ramificada tendo 1 a 4 átomos de carbono. Os exemplos incluem metila, etila, propila, isopropila, butila, isobutila, sec-butila, terc- butila. A alquila substituída é como acima definido.
Além disso, o termo "alquinila" refere-se a um grupo alquila tendo pelo menos dois átomos de carbono e incluindo uma ligação tripla de carbono-carbono. Alquinila substituída é como acima definido.
Igualmente, "alquenila" refere-se a um grupo alquila tendo pelo menos dois átomos de carbono e incluindo uma ligação dupla de carbono- carbono.
Além disso, o termo "alcóxi" refere-se a um grupo alquila sendo ligado por meio de um átomo de oxigênio.
O termo "arila" como usado aqui inclui anéis aromáticos carbocí- clicos ou sistemas de anel. Os exemplos de grupos de arila incluem fenila, naftila, bifenila, fluorenila e indenila. Em particular, o termo "arila" refere-se a fenila ou naftaleno. Em uma modalidade preferida, arila é fenila. A arila substituída é como acima definido.
O termo "heteroarila" inclui anéis aromáticos ou sistemas de anel que contêm pelo menos um heteroátomo de anel (por exemplo, O, S, N). Em particular, os grupos de heteroarila exemplares incluem furila, tienila, pirroli- la, pirazolila, imidazolila, triazolila, tetrazolila, isoxazolila, oxazolila, tiazolila, isotiazolila, oxadiazolila, oxatriazolila, tiadiazolila, piridila, piridazinila, pirimi- dinila, benzofuranila, isobenzofuranila, tionaftenila, isotionaftenila, indolila, isoindolila, indazolila, benzisoxazolila, benzoxazolila, benztiazolila, benzisoti- azolila, purinila, benzopiranila, quinolinila, isoquinolinila, cinolinila, quinazoli- nila, naftiridinila, e benzoxazinila, que em cada caso é não substituída ou pode opcionalmente ser substituída em um ou mais lugares.
Heteroarila substituída é substituída, por exemplo, por um ou mais de halogênio, hidroxila, arila, alquila, aralquila, alcóxi, carbóxi, ciano, trifluorometila, nitro, amino, alquilamino, dialquilamino, ou combinações dos mesmos.
Como usado aqui, o termo "heterociclila" refere-se a anéis não aromáticos ou sistemas de anéis mono- ou bicíclicos que contêm pelo menos um heteroátomo de anel (por exemplo, preferivelmente selecionado de O, SOX ou N, em que x = 0, 1 ou 2). Os grupos heterocíclicos exemplares incluem pirrolidinila, tetra-hidrofuranila, morfolinila, tiomorfolinila, piperidinila, piperazinila, tiazolidinila, imidazolidinila, tetra-hidropiranila, azabiciclooctani- la, tal como 1-azabiciclo[2,2,2]-octanila, 1-oxo e dioxo-tetra-hidrotiofenila ou ciclopentilsulfonila, bem como formas benzocondensadas e/ou n-óxidos dos mesmos, que em cada caso são não substituídos ou podem opcionalmente ser substituídos em um ou mais lugares. A heterociclila substituída é, por exemplo, substituída por um ou mais de halogênio, hidroxila, arila, alquila, aralquila, alcóxi, carbóxi, ciano, trifluorometila, nitro, amino, alquilamino, dialquilamino, ou combinações dos mesmos.
Deve ser entendido que a invenção cobre todas as combinações de grupos substituintes referidos aqui anteriormente. Em particular, a invenção cobre todas as combinações de grupos preferidos descritos aqui anteriormente.
Os sais farmaceuticamente aceitáveis dos compostos de acordo com a invenção incluem todos os sais de adição de ácido inorgânicos e orgânicos e sais com bases, especialmente todos os sais de adição de ácido inorgânicos e orgânicos farmaceuticamente aceitáveis e sais com bases, particularmente todos os sais de adição de ácido inorgânicos e orgânicos farmaceuticamente aceitáveis e sais com bases costumeiramente usadas na farmácia.
Os exemplos de sais de adição de ácido incluem, porém não são limitados a, cloridratos, bromidratos, fosfatos, nitratos, sulfates, acetatos, citratos, D-gliconatos, benzoatos, 2-(4-hidroxibenzoil)benzoatos, butiratos, sulfossalicilatos, maleatos, lauratos, malatos, fumaratos, sucinatos, oxalatos, tartaratos, estearatos, toluenossulfonatos, metanossulfonatos, 3-hidróxi-2- naftoatos e trifluoroacetatos.
Os exemplos de sais com bases incluem, porém não são limitados a, sais de lítio, sódio, potássio, cálcio, alumínio, magnésio, titânio, amónio, meglumina e guanidínio. Destes, sais de sódio e amónio são preferidos.
Os sais incluem sais insolúveis em água e, particularmente, solúveis em água.
Os compostos da invenção e os sais dos mesmos podem conter, por exemplo, quando isolados na forma cristalina, variando as quantidades de solventes. São incluídos no escopo da invenção, portanto, todos os solva- tos dos compostos de fórmula (I) e os sais dos mesmos. Os hidratos são um exemplo preferido de referidos solvatos.
Os N-óxidos dos compostos de acordo com a invenção e os sais dos mesmos incluem compostos, em que um átomo de nitrogênio de uma porção de substituinte é oxidado.
Em certas modalidades, os compostos de acordo com a invenção e os sais dos mesmos podem incluir estereoisômeros. Cada dos centros estereogênicos presentes em referidos estereoisômeros podem ter a configuração absoluta R ou a configuração absoluta S (de acordo com as normas de Cahn, Ingold e Prelog). Todos os tais estereoisômeros e os sais dos mesmos são parte da invenção. A invenção também inclui todas as misturas dos estereoisômeros acima mencionados independente da relação, incluindo os racematos.
Compostos da invenção e sais dos mesmos contendo uma liga- ção dupla podem existir como isômeros E e isômeros Z. Ambos os referidos isômeros são incluídos na invenção. O isômero Z é o isômero geométrico em que os átomos de carbono conectados pela ligação dupla, cada qual tem dois grupos de classificação mais elevadas no mesmo lado da ligação dupla. O isômero E é o isômero geométrico em que os átomos de carbono conectados pela ligação dupla, cada qual tem dois grupos de classificação mais elevada nos lados opostos da ligação dupla.
Alguns dos compostos e sais de acordo com a invenção podem existir em diferentes formas cristalinas (polimorfos) que estão incluídos no escopo da invenção.
Além disso, os derivados dos compostos de fórmula (I) e os sais dos mesmos que são convertidos em composto (I) ou um sal dos mesmos em um sistema biológico (bioprecursores ou profármacos) são cobertos pela invenção. O referido sistema biológico é, por exemplo, um organismo de mamífero, particularmente um paciente humano. O bioprecursor é, por e- xemplo, convertido no composto de fórmula (I) ou em um sal dos mesmos por um processo metabólico.
De acordo com uma modalidade preferida da presente invenção, os compostos de fórmula I em que Ri é -H, alquila, arila opcionalmente substituída, heterociclila, ou heteroarila opcionalmente substituída; R2 é - (CO)-R5, em que R5 é alquila, arila, ou heteroarila, e R3é -H, ou alquila, são excluídos da presente invenção.
Em outra modalidade preferida, a presente invenção refere-se a um composto de fórmula la, que é um composto de fórmula I como definido acima, em que R2 é hidrogênio.
Em outra modalidade preferida, a presente invenção refere-se a um composto de fórmula lb, que é um composto de fórmula I como definido acima, em que R2 é -(CO)-Rs; e R3 é selecionado de grupos consistindo em: alquenila, arila, heteroarila, cicloalquila e heterociclila, cada da qual pode ser não substituída ou substituída por um ou mais substituintes.
Em outra modalidade preferida, a presente invenção refere-se a
um composto de fórmula lc, que é um composto de fórmula I como definido acima, em que Ri é alquinila ou alcóxi; e R2 é -(CO)-Rs.
Em uma modalidade preferida do composto de fórmula I, incluindo os compostos de fórmulas la, lb e lc, de acordo com a presente invenção, R3 é heterociclila, que pode ser não substituída ou substituída por um ou mais substituintes, como definido acima.
Em outra modalidade preferida do composto de fórmula I, incluindo os compostos de fórmulas la, lb e lc, Ri é alquila, mais preferivelmente etila.
Em outra modalidade preferida do composto de fórmula I, incluindo os compostos de fórmulas la, lb e lc, R5 é alquila, mais preferivelmente metila.
Em outra modalidade preferida do composto de fórmula I, incluindo os compostos de fórmulas la, lb e lc, R3 é heterociclila, que pode ser não substituída ou substituída por um ou mais substituintes selecionados do grupo consistindo em: hidrogênio, alquila, alquenila, halogênio, ou -OH.
Em outra modalidade preferida do composto de fórmula I, incluindo os compostos de fórmulas la, lb e lc, A is C2-4 alquila, mais preferivelmente C4 alquila.
Outra modalidade preferida dos compostos de acordo com a presente invenção refere-se a compostos de fórmula I selecionados de: N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N-(1,1- dioxidotetra-hidro-3-tienil)acetamida, N-[4-(4-amino-2-etil-1 H-imidazo[4,5-c]quinolin-1 -i l)b util]-N-( 1 - metil-1 - oxidopiperidin-4-il)acetamida, 3-{acetil[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil]amino}-2,5-anidro-1,3,4-trideoxipentitol, N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N-(1- benzil-2-metil-1-oxidopirrolidin-3-il)acetamida, 2-etil-1-[4-(tetra-hidro-2H-piran-4-ilamino)butil]-1H-imidazo[4,5- c]quinolin-4-amina, 1-[4-(1-azabiciclo[2,2,2]oct-3 -ilamino)butil]-2-etil-1H-imidazo[4,5- c]quinolin-4-amina ou 1-{4-[(1,1-dióxido-3,4-di-hidro-2H-tiocromen-4-il)amino]butil}-2- etil-1 H-imidazo[4, 5-c]quinolin-4-amina ou solvatos, sais, N-óxidos farmaceuticamente aceitáveis ou es- tereoisômeros dos mesmos, ou combinações dos mesmos.
As composições farmacêuticas da invenção contêm uma quantidade terapeuticamente eficaz de um composto de fórmula I (incluindo fórmulas la, lb e lc) de acordo com a presente invenção em combinação com um veículo farmaceuticamente aceitável.
O termo "quantidade terapeuticamente eficaz" significa uma quantidade do composto suficiente para induzir um efeito terapêutico, tal como ativação de TLR7. Isto pode causar indução de citocina, atividade anti- tumor e/ou atividade antiviral. Mesmo que a quantidade exata de composto ativo usada em uma composição farmacêutica da invenção variar de acordo com fatores conhecidos por aqueles versados na técnica, tal como a natureza física e química do composto bem como a natureza do veículo e o regime de dosagem pretendido, antecipa-se que as composições da invenção conterão ingrediente ativo suficiente para fornecer uma dose de cerca de 100 ng/kg a cerca de 50 mg/kg, preferivelmente de cerca de 10 μg/kg a cerca de 5 mg/kg, do composto ao paciente.
Quaisquer das formas de dosagem convencionais podem ser usadas, tal como comprimidos, losangos, formulações parenterais, xaropes, cremes, unguentos, formulações de aerossol, emplastros transdérmicos, emplastros transmucosos e similares.
Os compostos da invenção podem ser administrados como o agente terapêutico único em um regime de tratamento, ou podem ser administrados em combinação com um outro ou com outros agentes ativos, incluindo agentes anticâncer adicionais, modificadores de resposta imune, antivirals, antibióticos, e similares.
A invenção, além disso, refere-se a composições farmacêuticas que compreendem pelo menos um dos compostos e sais farmaceuticamente aceitáveis de acordo com a invenção junto com pelo menos um auxiliar far- maceiiticamente aceitável.
Preferivelmente, as composições farmacêuticas compreendem um ou dois dos compostos e sais famnaceuticamente aceitáveis de acordo com invenção. Mais preferivelmente, as composições farmacêuticas compreendem um dos compostos e sais farmaceuticamente aceitáveis de acordo com invenção.
Em uma modalidade particularmente preferida da invenção, as composições farmacêuticas compreendem um composto dos exemplos de acordo com a invenção junto com pelo menos um auxiliar farmaceuticamente aceitável.
As composições farmacêuticas podem conter pelo menos um dos compostos e sais farmaceuticamente aceitáveis de acordo com a invenção (referido aqui a seguir como "o composto ativo") em uma quantidade total de 0,1 a 99,9 % em peso, preferivelmente 5 a 95 % em peso, mais preferivelmente 20 a 80 % em peso.
Como auxiliares farmaceuticamente aceitáveis, qualquer auxiliar conhecido como sendo adequado para preparar composições farmacêuticas pode ser usado. Os exemplos destes incluem, porém não são limitados a, solventes, excipientes, dispersantes, emulsificantes, solubilizantes, formadores de gel, bases de unguento, antioxidantes, conservantes, estabilizadores, veículoss, enchimentos, aglutinantes, espessantes, agentes de complexa- ção, agentes de desintegração, tampões, promotores de permeação, polímeros, lubrificantes, agentes de revestimento, propelentes, agentes de ajuste de tonicidade, tensoativos, corantes, flavorizantes, adoçantes e tinturas. Em particular, auxiliaries de um tipo apropriado à formulação desejada e o modo desejado de administração são usados.
As composições farmacêuticas podem ser formuladas, por e- xemplo, em comprimidos, comprimidos revestidos (drágeas), pílulas, selos, cápsulas (capselas), grânulos, pós, supositórios, soluções (por exemplo, soluções estéreis), emulsões, suspensões, unguentos, cremes, loções, pastas, óleos, géis, sprays e emplastros (por exemplo, sistemas transdérmicos terapêuticos). Adicionalmente, as composições farmacêuticas podem ser prepa radas como, por exemplo, sistemas de liberação de lipossomas, sistemas em que o composto ativo é acoplado aos anticorpos monoclonais e sistemas em que o composto ativo é acoplado a polímeros (por exemplo, polímeros solúveis ou biodegradáveis).
As composições farmacêuticas compreendem o composto ativo e pelo menos um auxiliar pode ser fabricado de maneira conhecida por uma pessoa versada na técnica, por exemplo, dissolvendo, misturando, granulando, misturando para drágea, preparar em pó, emulsificando, encapsulando, pinçando ou liofilizando processos.
A formulação selecionada depende entre outros da via de administração da composição farmacêutica. As composições farmacêuticas da invenção podem ser administradas por qualquer via adequada, por exemplo, pela via oral, sublingual, bucal, intravenosa, intra-arterial, intramuscular, subcutânea, intracutânea, tópica, transdérmica, intranasal, intraocular, intraperitoneal, intraesternal, intracoronária, transuretral, via retal ou vaginal, por inalação ou por insuflação. A administração oral é preferida.
Comprimidos, comprimidos revestidos (drágeas), pílulas, selos, cápsulas (capselas), grânulos, soluções, emulsões e suspensões são, por exemplo, adequados para administração oral. Em particular, referidas formulações podem ser adaptadas para representar, por exemplo, uma forma entérica, uma forma de liberação imediata, uma forma de liberação retardada, uma forma de liberação de dose repetida, uma forma de liberação prolongada ou uma forma de liberação sustentada. Referidas formas podem ser obtidas, por exemplo, revestindo-se comprimidos, dissolvendo-se comprimidos em vários compartimentos separados por camadas desintegrantes sob condições diferentes (por exemplo, condições de pH) ou acoplando-se o composto ativo a um polímero biodegradável.
A administração por inalação é preferivelmente feita usando um aerossol. O aerossol é uma dispersão líquido-gasosa, uma dispersão sólido- gasosa ou uma dispersão líquido/sólido-gasosa misturada.
O aerossol pode ser gerado por meio de dispositivos de produção de aerossol tais como inaladores de pó seco (DPIs), inaladores com do- símetro pressurizado (PMDIs) e nebulizadores. Dependendo da espécie do composto ativo a ser administrado, o dispositivo de produção de aerossol pode conter o composto ativo na forma de um pó, uma solução ou uma dispersão. O pó pode conter, por exemplo, um ou mais dos seguintes auxiliaries: veículos, estabilizadores e enchimentos. A solução pode conter além do solvente, por exemplo, um ou mais dos seguintes auxiliares: propelentes, solubilizantes (cossolventes), tensoativos, estabilizadores, tampões, agentes de ajuste de tonicidade, conservantes e flavorizantes. A dispersão pode conter além do dispersante, por exemplo, um ou mais dos seguintes auxiliares: propelentes, tensoativos, estabilizadores, tampões, conservantes e flavorizantes. Exemplos de veículos incluem, porém não são limitados a, sacarí- deos, por exemplo, lactose e glicose. Exemplos de propelentes incluem, porém não são limitados a, fluoro-hidrocarbonetos, por exemplo, 1,1,1,2- tetrafluoroetano e 1,1,1,2,3,3,3-heptafluoropropano.
O tamanho de partícula das partículas de aerossol (partículas sólidas, líquidas ou sólidas/líquidas) é preferivelmente menor do que 100 μm, mais preferivelmente ela é na faixa de 0,5 a 10 μm, em particular, na faixa de 2 a 6 μm (valor de ID50, medido por difração de laser).
Os dispositivos de produção de aerossol específicos que podem ser usados para administração inalada incluem, porém não são limitados a, inaladores Ciclohaler®, Diskhaler®, Rotadisk®, Turbohaler®, Autohaler®, Turbohaler®, Novolizer®, Easyhaler®, Aerolizer®, Jethaler®, Diskus®, Ul- trahalei® e Mystic®. Os dispositivos de produção de aerossol podem ser combinados com espaçadores ou dilatadores, por exemplo, Aerochamber®, Nebulator®, Volumatic® e Rondo®, para melhorar a eficiência de inalação.
Em caso de administração tópica, as formulações farmacêuticas adequadas são, por exemplo, unguentos, cremes, loções, pastas, géis, pós, soluções, emulsões, suspensões, óleos, sprays e emplastros (por exemplo, sistemas transdérmicos terapêuticos).
Para modos parenterais de administração tais como, por exemplo, administração intravenosa, intra-arterial, intramuscular, subcutânea, in- tracutânea, intraperitoneal e intraesternal, preferivelmente soluções (por e- xemplo, soluções estéreis, soluções isotônicas) são usadas. Elas são preferivelmente administradas por técnicas de injeção ou infusão.
Em caso de administração intranasal, por exemplo, sprays e soluções a serem aplicadas em forma de gota são formulações preferidas.
Para administração intraocular, as soluções a serem aplicadas em forma de gota, géis e unguentos são formulações exemplificadas.
Geralmente, as composições farmacêuticas de acordo com a invenção podem ser administradas tal que a dose do composto ativo seja na faixa habitual para ativadores de TLR7. Em particular, a dose na faixa de 0,01 a 4000 mg, preferivelmente 0,1 mg a 2000 mg, mais preferivelmente 0,5 mg a 1000 mg e mais preferivelmente 1 mg a 500 mg, do composto ativo por dia é preferida para um paciente adulto mediano tendo um peso corporal de 70 kg. Neste aspecto, deve ser observado que a dose é dependente, por exemplo, do composto específico usado, das espécies tratadas, idade, peso corporal, saúde geral, sexo e dieta do paciente tratado, modo e tempo de administração, taxa de excreção, gravidade da doença a ser tratada e combinação de fármaco.
A composição farmacêutica pode ser administrada em uma dose única por dia ou em múltiplas subdoses, por exemplo, 2 a 4 doses por dia. Uma unidade de dose única da composição farmacêutica pode conter, por exemplo, de 0,01 mg a 4000 mg, preferivelmente 0,1 mg a 2000 mg, mais preferivelmente 0,5 a 1000 mg, mais preferivelmente 1 a 500 mg, do composto ativo. Além disso, uma composição farmacêutica pode ser adaptada à administração semanal, mensal, ou ainda mais raro, por exemplo usando-se um implante, por exemplo, um implante subcutâneo ou intramuscular, usando-se o composto ativo em forma de um sal ligeiramente solúvel ou usando- se o composto ativo acoplado a um polímero.
Mostrou-se que compostos da invenção ativam TLR7 em experimentos realizados de acordo com testes apresentados abaixo. Os compostos da presente invenção são úteis como agentes anticâncer para cânceres que são responsivos à ativação de TLR7.
Os cânceres ilustrativos incluem, porém não são limitados a, câncer de mama, vesícula biliar, ósseo, cérebro, sistema nervoso central e periférico, cólon, glândulas endócrinas, esôfago, endométrico, células germi- nativas, cabeça e pescoço, rim, fígado, pulmão, laringe e hipofaringe, meso- telioma, sarcoma, ovário, pâncreas, próstata, reto, renal, intestino pequeno, tecido mole, testículos, estômago, pele, uretra, vagina e vulva; cânceres herdados, retinoblastoma e tumor de Wilms; leucemia, linfoma, doença de não-Hodgkin, leucemia mileoide aguda e crônica, leucemia linfoblástica aguda, doença de Hodgkin, mieloma múltiplo e linfoma de célula T; síndrome mielodisplástica, neoplasia de célula de plasma, síndromes paraneoplásti- cas, cânceres de sítios primários não conhecidos e malignidades relacionadas à AIDS.
Preferivelmente, os agonistas de TRL7 podem ser usados para tratar os cânceres da pele ou rim. A sensibilidade de um determinado câncer à ativação de TLR7 pode ser avaliada por, porém não limitada à medição de um decréscimo em carga primária ou metastática (regressão menor, parcial ou completa), alterações no hemograma, hormônio alterado ou concentrações de citocina no sangue, inibição de outro aumento de carga de tumor, estabilização da doença no paciente, avaliação de biomarcadores ou marcadores substitutos relevantes para a doença, sobrevivência global prolongada de um paciente, tempo prolongado para progressão da doença de um paciente, sobrevivência livre de progressão prolongada de um paciente, sobrevivência livre de doença prolongada de um paciente, qualidade melhorada de vida de um paciente, ou modulação da comorbidez da doença (por exemplo, porém não limitada a dor, caquexia, mobilização, hospitalização, hemograma alterado, perda de peso, cicatrização de ferida, febre).
Os compostos de acordo com a presente invenção podem também ser úteis como modificadores de resposta imune que podem modular a resposta imune em diversos modos diferentes, tornando eles úteis no tratamento de uma variedade de distúrbios.
As citocinas que podem ser induzidas pela administração de compostos de acordo com a invenção geralmente incluem interferon (IFN) e/ou fator-a de necrose de tumoral (TNF-α) bem como certas interleucinas (IL). As citocinas das quais a biossíntese pode ser induzida por compostos da invenção incluem IFN- α, TNF- α, IL-I, 6, 10 e 12, e uma variedade de outras citocinas. Entre os efeitos, as citocinas inibem a produção de vírus e crescimento de célula tumoral, tornando os compostos úteis no tratamento de tumores e doenças virais.
Além disso, para a capacidade induzir à produção de citocinas, os compostos da invenção afetam outros aspectos da resposta imune inata. Por exemplo, a atividade de célula exterminadora natural pode ser estimulada, um efeito que pode ser devido à indução de citocina. Os compostos podem também ativar os macrófagos, que sucessivamente estimulam a secreção de óxido nítrico e a produção de citocinas adicionais. Além disso, os compostos podem causar proliferação e diferenciação de linfócitos B.
Os compostos da invenção podem também ter um efeito sobre a resposta imune adquirida. Por exemplo, ao mesmo tempo que não se destinam a ser ligados por qualquer teoria particular, não se acredita que tenham qualquer efeito direto sobre as células T ou indução direta de citocinas de célula T, porém a produção da citocina IFN-y de tipo 1 auxiliar T (Th 1) é induzida indiretamente e a produção das citocinas IL-4, IL-5 and IL- 13 de tipo 2 auxiliar (Th2) é inibida sob administração dos compostos. Esta atividade significa que os compostos são úteis no tratamento de doenças onde a su- per-regulação da resposta a Th1 e/ou sub-regulação da resposta a Th2 é desejada. Em vista da capacidade de certos compostos de fórmula I de inibir a resposta imune a Th2, espera-se que os compostos sejam úteis no tratamento de condições que são associadas com superestimulação de uma resposta a Th2 tal como doenças atópicas, por exemplo, dermatite atópica; asma; alergia; rinite alérgica; lúpus eritematoso sistêmico; como um adjuvante de vacina para imunidade mediada por célula; e possivelmente como um tratamento para doenças fúngicas recorrentes, periodontite e clamídia.
Os efeitos de modificação de resposta imune dos compostos os tornam úteis no tratamento de uma ampla variedade de condições. Por causa de sua capacidade de induzir à produção de citocinas tais como IFN-a e/ou TNF-a, e IL-12, os compostos são particularmente úteis no tratamento de doenças virais e tumores. Esta atividade de imunomodulação sugere que os compostos da invenção são úteis no tratamento de doenças tais como, porém não limitadas às doenças virais incluindo verrugas genitais; verrugas comuns; verrugas plantares; Hepatite B; Hepatite C; Herpes Simples do Tipo I e Tipo II; molusco contagioso; HIV; CMV; VZV; neoplasias intraepiteliais tal como neoplasia intraepitelial cervical; papilomavírus humano (HPV) e neo-plasias associadas; doenças fúngicas, por exemplo, Cândida, aspergillus, e meningite criptocócica; doenças neoplásicas, por exemplo, carcinoma de célula basal, leucemia de célula capilar, sarcoma de Kaposi, carcinoma de célula renal, carcinoma de célula escamosa, leucemia mielogenosa, mieloma múltiplo, melanoma, linfoma de não-Hodgkin, linfoma de célula T cutânea, e outros cânceres; doenças parasíticas, por exemplo, Pneumocystis camii, criptosporidiose, histoplasmose, toxoplasmose, infecção por tripanossoma, e leislimaniase; e infecções bacterianas, por exemplo, tuberculose, e mycobacterium avium. Doenças ou condições adicionais que podem ser tratadas usando os compostos da invenção incluem eczema; eosinofilia; trombocte- mia essencial; lepra; esclerose múltipla; síndrome de Ommen; lúpus discoi- de; doença de Bowen; papulose Bowenoide; e para realçar ou estimular a cicatrização de feridas, incluindo feridas crônicas.
Consequentemente, a invenção fornece um método de ativação de TLR7 em um animal, especialmente um mamífero, preferivelmente um ser humano que compreende administrar uma quantidade eficaz de um composto de fórmula I ao animal. Uma quantidade eficaz de um composto variará de acordo com os fatores conhecidos na técnica, porém é esperada ser uma dose de cerca de 100 ng/kg a cerca de 60 mg/kg, preferivelmente cerca de 10 μg/kg a cerca de 30 mg/kg, mais preferivelmente cerca de 10 μg/kg a cerca de 5 mg/kg.
A invenção também fornece um método de tratamento de infecção viral em um animal que compreende administrar uma quantidade eficaz de um composto de fórmula I ao animal. Uma quantidade eficaz para tratar ou inibir uma infecção viral que causará uma redução em uma ou mais das manifestações de infecção viral, tais como lesões virais, cargas virais, taxa de produção de vírus, e mortalidade em relação aos animais de controle não tratados. A quantidade precisa variará de acordo com fatores conhecidos na técnica, porém é esperada ser uma dose como acima indicado com respeito à ativação de TLR7, ou uma dose de cerca de 100 ng/kg a cerca de 50 mg/kg, preferivelmente cerca de 10 μg/kg a cerca de 5 mg/kg.
Uma quantidade eficaz para tratar uma condição neoplásica é uma quantidade que causará uma redução no tamanho de tumor ou no número de focos de tumor. Novamente, a quantidade precisa variará de acordo com os fatores conhecidos na técnica, porém é esperada ser uma dose como acima indicado com respeito à ativação de TLR7, ou uma dose de cerca de 100 mg/kg a cerca de 50 mg/kg, preferivelmente cerca de 10 mg/kg a cerca de 5 mg/kg.
Os compostos de acordo com a invenção podem ser preparados, por exemplo, como descrito como segue e de acordo com as seguintes etapas de reação especificadas, ou, particularmente, de uma maneira como descrito por meio de exemplo nos seguintes exemplos.
Como mostrado no esquema de reação A, um composto de fórmula 7 em que R3 tendo o significado como definido acima pode ser obtido pelo tratamento quinolin-4-ol como ácido nítrico para fornecer seu derivado de nitro de fórmula 1 que é também reagido com oxicloreto fosforoso na presença de N,N-dimetil formaldeído para produzir 4-cloro-3-nitroquinolina de fórmula 2. O composto de fórmula 2 na reação com terc-butil éster de ácido (4-amino-butil)-carbâmico resultou no composto de fórmula 4 que é em seguida reagido com trietilortopropionato na presença de tolueno para fornecer composto de fórmula 5. Terc-butil éster de ácido [4-(2-etil-imidazo[4,5- c]quinolin-1-il)-butil]-carbâmico de fórmula 5 é em seguida desprotegido para fornecer 4-(2-etil-imidazo[4,5-c]quinolin-1-il)-butilamina de fórmula 6. Um composto de fórmula 6 é em seguida tratado com cetonas heterocíclicas a- dequadas para obter um composto desejado de fórmula 7. Esquema A
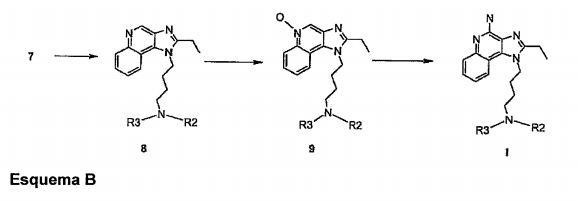
Como mostrado no esquema de reação B, o composto de fórmula I, em que R2 é -CO-R5 e todos os outros símbolos têm os significados como definido acima, pode ser obtido reagindo o composto de fórmula 7 com o 5 anidrido ácido adequado de fórmula R5 -CO-O-CO-Rs para obter um composto de fórmula 8 que é em seguida tratado com ácido m-cloroperbenzoico para produzir seu derivado de N-óxido de fórmula 9. Um composto de fórmula 9 é também submetido à aminação usando solução de amónia aquosa (aq.) para obter o composto desejado de fórmula I. Esquema B
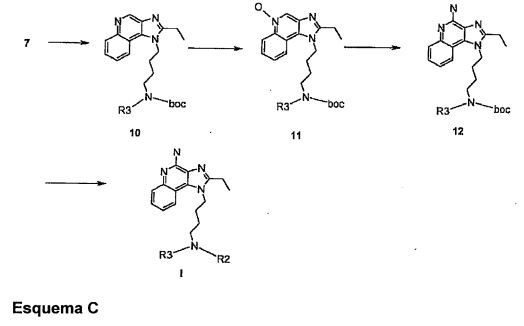
Como mostrado no esquema de reação C um composto de fórmula I, em que R2 é hidrogênio e todos os símbolos têm os significados como definido acima, pode ser obtido reagindo o composto de fórmula 7 com di-terc-butil-dicarbonato para obter um composto de fórmula 10, que é em seguida tratado com ácido m-cloroperbenzoico para produzir seu derivado de N-óxido de fórmula 11.0 composto de fórmula 11 é em seguida também submetido à aminação usando amónia aquosa para obter um composto de fórmula 12 que é desprotegido usando condições acídicas para obter o com posto desejado de fórmula I. Esquema C
É conhecido pela pessoa versada na técnica que, existem diversos centros reativos em um composto de partida ou intermediário, pode ser necessário bloquear um ou mais centros reativos temporariamente por grupos protetores a fim de permitir a reação prosseguir especificamente no centro de reação desejado.
Os compostos de acordo com a invenção são isolados e purificados de maneira conhecida de per si, por exemplo, destilando o solvente em vácuo e recristalizando o resíduo obtido de um solvente adequado ou submetendo-o a um dos métodos de purificação habituais, tal como croma- tografia de coluna em um material de suporte adequado.
Os sais dos compostos de fórmula (I) de acordo com a invenção podem ser obtidos dissolvendo o composto livre em um solvente adequado (por exemplo, uma cetona tal como acetona, metiletilcetona ou metilisobutil- cetona, um éter tal como dietil éter, tetra-hidrofurano ou dioxano, um hidro- carboneto clorado tal como cloreto de metileno ou clorofórmio, ou um álcool alifático de baixo peso molecular tal como metanol, etanol ou isopropanol) que contém o ácido ou base desejada, ou ao qual o ácido ou base desejada é em seguida adicionado. O ácido ou base pode ser empregado em uma preparação de sal, dependendo se um sal mono- ou polibásico ou base está envolvido e dependendo de que sal é desejado, em uma relação quantitativa equimolar ou uma diferença a partir desta. Os sais são obtidos por filtragem, reprecipitação, precipitação com um não-solvente para o sal ou por evaporação do solvente. Os sais obtidos podem ser convertidos nos compostos livres que, por sua vez, podem ser convertidos em sais. Desta maneira, os sais farmaceuticamente inaceitáveis, que podem ser obtidos, por exemplo, como produto de processamento na fabricação em uma escala industrial, podem ser convertidos em sais farmaceuticamente aceitáveis por processos conhecidos pela pessoa versada na técnica.
Os compostos de fórmula (I) de acordo com a invenção podem ser convertidos em seus N-óxidos, por exemplo, com o auxílio de peróxido de hidrogênio em metanol ou com o auxílio de ácido m-cloroperoxibenzoico em diclorometano. A pessoa versada na técnica está familiar com as condições de reação para realização da N-oxidação.
Os diastereômeros puros e enantiômeros puros dos compostos e sais de acordo com a invenção que estão presentes na forma de tais este- reoisômeros podem ser obtidos, por exemplo, por síntese assimétrica, usando-se compostos de partida quirais na síntese e dividindo-se as misturas enantioméricas e diastereoméricas obtidas na síntese.
As misturas enantioméricas e diastereoméricas podem ser divididas nos enantiômeros puros e diastereômeros puros por métodos conhecidos por uma pessoa versada na técnica. Preferivelmente, as misturas diastereoméricas são separadas por cristalização, em particular, cristalização fracionai, ou cromatografia. As misturas enantioméricas podem ser separadas, por exemplo, formando diastereômeros com um agente auxiliar quiral, resolvendo os diastereômeros obtidos e removendo o agente auxiliar quiral. Como agentes auxiliares quirais, por exemplo, ácidos quirais podem ser u- sados para separar bases enantioméricas e bases quirais podem ser usadas para separar ácidos enantioméricos por meio de formação de sais diastere- oméricos. Além disso, derivados diastereoméricos tais como ésteres diaste- reoméricos podem ser formados de misturas enantioméricas de alcoóis ou misturas enantioméricas de ácidos, respectivamente, usando ácidos quirais ou alcoóis quirais, respectivamente, como agentes auxiliares quirais. Adicionalmente, complexos diastereoméricos ou clatratos diastereoméricos podem ser usados para separação de misturas enantioméricas. Alternativamente, as misturas enantioméricas podem ser divididas usando colunas de separa-ção quirais em cromatografia. Outro método adequado para isolamento de enantiômeros é a separação enzimática.
Como será apreciado pelas pessoas versadas na técnica, a invenção não é limitada às modalidades particulares descritas aqui, porém cobre todas as modificações de referidas modalidades que estão incluídas no espírito e escopo da invenção como definido pelas reivindicações anexadas.
Os exemplos seguintes ilustram a invenção com maior detalhe, sem restringi-la. Outros compostos de acordo com invenção, dos quais a preparação não é explicitamente descrita, podem ser preparados de um modo análogo.
Os compostos que são mencionados nos exemplos e os sais dos mesmos representam modalidades preferidas da invenção.
Exemplos: Preparação de 4-(2-etil-imidazo[4,5-c]quinolin-1-il)-butilamina de fórmula 6 Etapa-1: 3-nitro-quinolina-4-ol
Uma mistura de quinolin-4-ol (1 equivalente) em ácido propiônico foi aquecida para 125°C com agitação. Ácido nítrico (2,2 equivalentes) foi adicionado gota a gota à solução agitada ao mesmo tempo em que mantendo a temperatura de mistura reacional a 125°C. A reação foi agitada a 125°C durante 15 minutos e resfriada para temperatura ambiente. A reação foi diluída com etanol e o sólido foi coletado por filtragem a vácuo. O sólido foi lavado sucessivamente com etanol, água e etanol. O sólido amarelo resultante foi aquecido em etanol refluxante e filtrado por mistura quente para fornecer 3-nitro-quinolina-4-ol puro. Etapa-ll: 4-cloro-3-nitro-quinolina
Oxicloreto fosforoso (1,2 equivalente) foi adicionado lentamente à suspensão bem agitada de composto de fórmula 1 obtido na etapa I em N,N-dimetilformamida. A mistura reacional foi também aquecida para 50°C com agitação durante 30 minutos. A solução resultante foi resfriada em temperatura ambiente e despejada em uma mistura de gelo/água. Um sólido foi coletado por filtragem e secado para fornecer 4-cloro-3-nitro-quinolina. Etapa-111: {4-[(3-nitroquinolin-4-il) amino]butil}carbamato de terc-butila
Um composto de fórmula 2 (1 equivalente) foi adicionado a uma solução de terc-butiléster de ácido (4-amino-butil)-carbâmico (1,2 equivalente) e trietilamina (1,5 equivalente) em etanol. A mistura reacional foi em seguida refluxada durante 15 minutos e em seguida diluída com água ao produto impuro precipitado, que foi separado por filtragem. Solução de hidróxido de amónio saturada foi adicionada ao filtrado e o sólido precipitado foi coletado por filtragem a vácuo e secado para fornecer {4-[(3-nitroquinolin-4- il)amino] butiljcarbamato de terc-butila de fórmula 3.
Etapa-IV: {4-[(3-aminoquinolin-4-il)amino]butil}carbamato de terc-butila
Uma suspensão de composto de fórmula 3 (1 equivalente), 5 % de paládio em carbono (2 % em peso) e sulfato de magnésio em acetato de etila foi hidrogenada em um aparelho de parr em 3,51 kg/cm2 (50 psi) de gás de hidrogênio durante 4 horas. A mistura reacional resultante foi em seguida filtrada e o filtrado foi concentrado em pressão reduzida para produzir sólido bruto, que em seguida purificou por cromatografia de coluna em sílica-gel para fornecer {4-[(3-aminoquinolin-4-il) amino] butil} carbamato de terc-butila de fórmula 4. Etapa-V: [4-(2-etiI-1H-imidazo[4,5-c]quinolin-1-il)butil]carbamato de terc- butila
A uma solução de composto de fórmula 4(1 equivalente) em to- lueno foi adicionado trietilortopropionato (2 equivalentes) e a mistura reacional resultante foi aquecida a 80-90 °C durante 5 horas. A mistura reacional foi em seguida resfriada e o solvente foi evaporado para remover 50 % de tolueno. A uma mistura reacional restante foi adicionada água gelada e o produto foi precipitado como sólido branco que foi em seguida separado por filtragem a vácuo e secado para fornecer [4-(2-etil-1H-imidazo[4,5-c]quinolin- 1-il)butil]carbamato de terc-butila de fórmula 5. Etapa- VI: 4-(2-etil-1H-imidazo[4,5-c]quinolin-1-il)butan-1-amina
Uma solução de terc-butil éster de ácido [4-(2-etil-imidazo[4,5- c]quinolin-1-il)-butil]-carbâmico de fórmula 5 obtido na etapa V em ácido tri- fluoroacético foi agitada a 40°C durante 4 horas.
A mistura reacional foi em seguida despejada em mistura de á- gua gelada e extraída com clorofórmio.
A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para fornecer 4-(2-etil-1H-imidazo[4,5-c]quinolin- 1-il) butan-1-amina de fórmula 6.
Exemplo I: N-[4-(4-amino-2-etil-1 H-imidazo[4,5-c]quinolin-1 -il)butil]-N- (1,1 -dioxidotetra-hidro-3-tienil)acetamida Etapa-I: N-[4-(2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]tetra-hidrotiofen- 3-amina.
A uma suspensão de 4-(2-etil-imidazo[4,5-c]quinolin-1-il)- butilamina obtida na etapa VI em tetra-hidrofurano foram adicionados ácido acético (1 equivalente) e di-hidrotiofen-3-ona (1,1 equivalente). A mistura reacional resultante foi agitada durante 10 minutos. Triacetoxiboroidreto de sódio (2,2 equivalentes) foi adicionado à mistura reacional durante um período de 1 hora e a suspensão resultante foi em seguida agitada durante 4-5 horas. Reação foi em seguida extinta com metanol e concentrada até secura. A mistura reacional foi basificada usando solução de hidróxido de sódio aquosa e extraída com clorofórmio. A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para produzir sólido pegajoso. O produto foi em seguida purificado por cromatografia de coluna em sílica-gel para fornecer [4-(2-etil-imidazo[4,5-c]quinolin-1-il)-butil]-(tetraidro- tiofen-3-il)-amina. Etapa-ll: N-[4-(2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N-(tetra-hidro-3- tienil)acetamida
A uma solução de [4-(2-etil-imidazo[4,5-c]quinolin-1-il)-butil]- (tetra-hidro-tiofen-3-il)-amina em diclorometano foram adicionados trietilami- na (1,5 equivalente) e anidrido acético (1,5 equivalente) e agitada em temperatura ambiente durante 4 horas. A mistura reacional foi em seguida diluída com diclorometano e lavada com solução de bicarbonato de sódio saturada. A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para fornecer N-[4-(2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil]-N-(tetra-hidro-3-tienil)acetamida. Etapa-III: N-(1,1-dioxidotetra-hidro-3-tienil)-N-[4-(2-etil-5-óxido-1H- imidazo[4,5- c]quinolin-1 -il)butil]acetamida
A uma solução de N-[4-(2-etil-imidazo[4,5-c]quinolin-1 -il)-butil]-N- (tetra-hidrotiofen-3-il)-acetamida em clorofórmio foi adicionado ácido m- clroperbenzoico (4 equivalentes) e agitada em temperatura ambiente durante 2 horas. A mistura reacional foi em seguida diluída com clorofórmio e lavada com solução de bicarbonato de sódio saturada. A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para produzir massa pegajosa. O produto foi em seguida purificado usando cromatografia de coluna em sílica-gel para fornecer N-(1,1-dioxidotetra-hidro-3-tienil)-N-[4- (2-etil-5-óxido-1H-imidazo[4,5-c]quinolin-1-il)butil]acetamida. Etapa-IV: N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N-(1,1- dioxidotetra-hidro-3-tienil)acetamida
A uma solução de (1,1-dioxo-tetra-hidro1 lambda* 6 *-tiofen-3-il)- N-[4-(2-etil-5-óxi-imidazo[4,5-c]quinolin-1-il)-butil]-acetamida em clorofórmio foi adicionado cloreto de p-tolueno sulfonila (1,2 equivalente) seguido por solução de hidróxido de amónio aquosa. A mistura reacional resultante foi agitada em temperatura ambiente durante a noite. A mistura reacional foi em seguida diluída com clorofórmio e lavada com solução de bicarbonato de sódio saturada. A camada orgânica foi secada sobre sulfato de sódio e con-centrada sob pressão reduzida para produzir sólido pegajoso, que foi em seguida purificado usando cromatografia de coluna em sílica-gel para forne- cer o composto do título. 1H RMN (300 MHZ1CDCI3) δ (ppm): 8,29(dd, 1H, J=S ,4&J=3,0Hz), 8,21 (dd, 1H, J=8,4Hz, J=3,0Hz), 7,65(m, 2H), 5,49(s, 2H)3 4,58(t, 2H), 3,78(t, 2H),3,3(t, 2H)-| 3,02(q, 2H),2,34(d, 2H), 2,2(t, 1H), 2,1(s, 3H), 2,09(m, 2H), 1,9(m, 2H),1,79(m, 2H), 1,55(t, 3H)
Os exemplos de 2 a 4 foram também preparados seguindo o procedimento de exemplo I. Exemplo II: N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N- (1-metil-1-oxidopiperidin-4-il)acetamida 1H RMN (300 MHZ3CDCI3) δ (ppm): 8,24(dd, 1H, J=8,4&J=3,0Hz), 8,19(dd, 1H, J=S,4&J=3,0Hz), 7,60(m, 2H), 5,60(s, 2H), 4,52(t, 2H), 3,75(t, 2H), 3,4(m, 1H), 3,2(m, 4H), 3,12(q, 2H), 2,16(s, 3H), 2,01 (m, 2H), 1,99(m, 4H), 1,70(m, 2H), 1,51 (t, 3H) Exemplo III: 3-{acetil[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil] amino}-2,5-anidro-l,3,4-trideoxipentitol 1H RMN (300 MHZ3CDCI3) δ (ppm):8,35(dd, 1H, J=8,4&J=3,0Hz), 8,29(dd, 1H, J=8,4&J-3,0Hz), 7,63(m5 2H), 5,56(s, 2H), 4,50(t, 2H), 4,42(m, 1H), 3,70(t, 2H),3,62(m, 1H)5 3,35(t, 2H), 3,12(q, 2H),2,15(s, 3H), 2,05(m, 2H),1,92(d, 3H),1,8(t, 2H) 1,70(m, 2H), 1,51(t, 3H) Exemplo IV: N-[4-(4-amino-2-etil-1 H-imidazo[4,5-c]quinolin-1 -i I) b u ti I]-N - (I- benzil-2-metil-1 -oxidopirrolidin-3-il)acetamida 1H RMN (300 MHz.CDCI,) δ (ppm): 8,31 (dd, 1H, J-8,4&J=3,0Hz), 8,15(dd, 1H, J=8,4Hz, J=3,0Hz), 7,62(111, 2H), 7,55(m, 5H), 5,59(s, 2H), 4,50(t, 2H), 3,71(t, 2H),3,35(t, 2H), 3,23(s, 2H), 3,21(q, 2H),2,19(d, 2H), 2,15(t, 1H), 2,10(s, 3H), 2,09(m, 2H), 1,9(m, 2H),1,79(m, 2H), 1,55(t, 3H). Exemplo V: 2-eti I-1 -[4-(tetra-hidro-2H-piran-4-ilamino)butil]-1 H- imidazo[4,5- c]quinolin-4-amina Etapa-I: N-[4-(2-etil-1 H-imidazo[4,5-c]quinolin-1 -il)butiltetra-hidro-2H- piran-4-amina
A uma suspensão de 4-(2-etil-1H-imidazo[4,5-c]quinolin-1- il)butan-1-amina obtida na etapa VI de exemplo I em tetra-hidrofurano foram adicionados ácido acético (1 equivalente) e tetra-hidro-piran-4-ona (1,1 equi- valente). A mistura reacional resultante foi agitada durante 10 minutos. Tria- cetoxiboroidreto de sódio (2,2 equivalentes) foi adicionado à mistura reacional durante um período de 1 hora e a suspensão resultante foi em seguida agitada durante 4-5 horas. A reação foi em seguida extinta com metanol e concentrada até secura. A mistura reacional foi basificada usando solução de hidróxido de sódio aquosa e extraída com clorofórmio. A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para produzir sólido pegajoso. O produto foi em seguida purificado por cro- matografia de coluna em sílica-gel para fornecer N-[4-(2-etil-1H-imidazo[4,5- c]quinolin-1 -il)butil]tetra-hidro-2H-piran-4- amina. Etapa-ll: [4-(2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]tetra-hidro-2H-piran-4- ilcarbamato de terc-butila
A uma solução de N-[4-(2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil]tetra-hidro-2H-piran-4-amina em diclorometano foi adicionada trietila- mina (1,5 equivalente) seguido por di-terc-butil-dicarbonato (1,5 equivalente) e a mistura reacional resultante foi agitada durante 4 horas em temperatura ambiente. A mistura reacional foi em seguida evaporada completamente e dissolvida em diclorometano, lavada com água e a camada orgânica foi se-cada sobre sulfato de sódio e concentrada sob pressão reduzida para fornecer [4-(2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]tetra-hidro-2H-piran-4- ilcarbamato de terc-butila. Etapa-lll: [4-(2-etil-5-óxido-1H-imidazo[4,5-c]quinolin-1-il)butil]tetra-hidro-2H- piran-4-ilcarbamato de terc-butila
A uma solução de [4-(2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil]tetra-hidro-2H-piran-4-ilcarbamato de terc-butila em clorofórmio foi adicionado ácido m-clroperbenzoico (4 equivalente) e agitada em temperatura ambiente durante 2 horas. A mistura reacional foi em seguida diluída com clorofórmio e lavada com solução de bicarbonato de sódio saturada. A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para produzir massa pegajosa. O produto foi em seguida purificado usando cromatografia de coluna em sílica-gel para fornecer [4-(2-etil-5- óxido-1H-imidazo[4,5-c]quinolin-1-il)butil]tetra-hidro-2H-piran-4-ilcarbamato de terc-butila. Etapa-IV: [4-(4-amino-2-etil-1 H-imidazo[4,5-c]quinolin-1 -i I) b uti l]tetra-h id ro- 2H-piran-4-ilcarbamato de terc-butila
A uma solução de [4-(2-etil-5-óxido-1H-imidazo[4,5-c]quinolin-1- il)butil]tetra-hidro-2H-piran-4-ilcarbamato de terc-butila em clorofórmio foi adicionado cloreto de p-tolueno sulfonila (1,2 equivalente) seguido por solução de hidróxido de amónio aquosa. A mistura reacional resultante foi agitada em temperatura ambiente durante a noite. A mistura reacional foi lavada com solução de bicarbonato de sódio saturada. A camada orgânica separada, secada sobre sulfato de sódio anidro e concentrada sob pressão reduzida para produzir sólido pegajoso, que foi em seguida purificado usando cromatografia de coluna em sílica-gel para fornecer [4-(4-amino-2-etil-1 H- imidazo[4,5-c]quinolin-1 -il)butil]tetra-hidro-2H-piran-4-ilcarbamato de terc- butila. Etapa-V: 2-etil-1-[4-(tetra-hidro-2H-piran-4-ilamino)butil]-1H-imidazo[4,5-c] quinolin-4-amina
Uma solução de [4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil]tetra-hidro-2H-piran-4-ilcarbamato de terc-butila em ácido trifluoroacé- tico foi agitada a 40°C durante 4 horas. A mistura reacional foi em seguida despejada em mistura de água gelada e extraída com clorofórmio.
A camada orgânica foi secada sobre sulfato de sódio e concentrada sob pressão reduzida para fornecer o composto do título. 1H RMN (300 MHz5MeOD) δ (ppm):8,2(d, 1H, J=8JHz), 7,75(m, 2H), 7,6(dt, 1H, J=1,5 & 7,2Hz),4,69(t, 2H), 4,0 l(d, 1H), 3,98(d, 1H), 3,4(m, 3H), 3,2(m, 2H), 3,1(m, 2H), 2,0(m, 4H), 1,9(m, 4H), 1,5(t, 3H) Exemplos 6-7 foram também preparados seguindo o procedimento de e- xemplo 5. Exemplo VI: 1-[4-(l-azabiciclo[2,2,2]oct-3-ilamino)butil]-2-etil-1 H-imidazo[4,5- c]quinolin-4-amina 1H RMN (300 MHz, MeOD) δ (ppm): 8,01 (d, 1H, J=8,4Hz), 7,67(dd, 1H, J=1,2 & 8,4 Hz), 7,4(dt, 1H, J=1,5 & 7,8Hz), 7,33(dt, 1H, J=l ,2 & 7,5Hz), 4,5 (m, 2H), 4,2(m, 2H), 3,6(m, 1H), 3,4(m, 1H), 3,1(m, 2H), 3,0(q, 2H), 2,7(m, 2H), 1,9(m, 3H), 1,7(m, 2H), 1,5(t, 3H), 1,4(m, 2H), 1,3(m, 3H). Exemplo VII: l-{4-[(1,1-dióxido-3,4-di-hidro-2H-tiocromen-4-il)amino]butil}-2- etil-1H-Tmidazo[4,5-c]quinolin-4-amina 1H RMN (300 MHz, MeOD) δ (ppm);8,2(d, 1H, J=8,1Hz), 7,80(dt, 1H, J=l ,5 & 6,3Hz),7,73(d, 1H, J=7,5Hz), 7,64(dt, 1H, J=l ,5 & 7,5Hz), 7,5(m, 4H), 4,59(t, 2H), 3,97(t, 1H), 3,70(m, 1H), 3,02(q, 2H), 2,71 (m, 3H), 2,50(m, 2H), 1,99(m, 2H), 1,69(m, 2H), 1,48(t, 3H). Exemplo A - Representação in vitro:
Ensaios celulares usando uma linhagem de células de câncer humana (PCIR-I) ou frações de PBMC humana para testar compostos para ativar TLR7 são estabelecidos.
A especificidade de TLR7 e 9 foi checada adicionando-se cloroquina, que ab-roga a sinalização por meio dos TLRs endossômicos. O sistema PCIR-I é adequado para medir a citocina IPIO ligada por interferon por um ensaio com base em conta no formato de 384 cavidades.
Expressão de mRNA de TLR em PCIR-I (análise de TaqMan PCR) TLRI ++, TLR2 (+). TLR3 +, TLR4 ++, TLR5 (+), TLR6 ++, TLR7 ++, TLR8 - TLR9 +++, TLRIO -.
O tratamento desta linhagem de células com LPS de compostos de referência de agonista de TLR (TLR4 ago), resiquimod (imidazoquinolina) e H2006 (oligonucleotídeo CpG) resulta em indução de mRNA de citocina forte. Além disso, a resposta a RNA de filamento duplo de poli l-C (agonista de TLR 3; 40 vezes indução de IP-IO após 15 horas) e MALP-2 (agonista de TLR 2/6 heterodímero, 100 vezes indução de IP-IO após 15 horas) é detectada.
Os dados de indução de RNA foram confirmados por análise de Luminex paralela mostrando forte liberação de citocinas IP-10 e IL8, em particular, e também níveis de proteína significantes de IL6, IL12p40/p70 e ILI0.
A sinalização por meio de TLR7 e TLR9 (ambos expressados em endossomas) pode ser completamente bloqueada pela adição de cloro- quina, que é conhecida por perturbar o gradiente do pH endossômico. Em contraste, a sinalização de TLR4 por LPS não é afetada (figura 1).
O conceito atual para uma cascata de análise de agonista de TLR em um formato de alta ou média produtividade é sumariado na figura 2.
Os compostos da presente invenção são testados para indução de citocina especificada no mRNA ou níveis proteínas. Os compostos mostram eficácia nos ensaios celulares (figura 3). Exemplo B - Representação de PD in vivo\
Nos seguintes, os estudos com os compostos de referência e compostos de acordo com a invenção são mostrados no modelo de metástase pulmonar de Renca como descrito em Leja A, Hofmann HP, Maier T, Drache D, Grebe C, Fischer S, Gimmnich P, Sanders K, Gekeler V. A metástase de células de câncer de rim Renca de murino para os pulmões de camundongos Balb/c é fortemente suprimida por agonistas de TLR9 ou TLR7. Abstract 3552, Proc Am câncer Res 48, 2007.
As figuras 4A e 4B mostram os resultados de compostos de referência (agonistas de TLR9 bem como de TLR7, que são SMOLs ou oligonu- cleotídeos; TOG = 7-tia-8-oxoguanosina; IMDZQ - derivado de imidazoquinolina).
Em particular, camundongos Balb/c fêmeas (n-10) foram tratados durante 4 dias consecutivos iniciando 1 dia ou 8 dias após a injeção de células de tumor LacZ Renca, respectivamente. Os SMOLs foram aplicados em 20 % de PEG, os oligonucleotídeos em 0,9 % de NaCI como indicado. Os pulmões foram excisados 25 dias após a injeção de células de tumor (veja figura 4A). Além disso, camundongos Balb/c fêmeas (n=5) foram tratados durante 4 dias consecutivos como indicado. Os SMOLs foram aplicados em 20 % de PEG, oligonucleotídeos em 0,9 % de NaCI. Em 4 dias de tratamento, o sangue foi coletado por meio do plexo orbital e os baços foram excisados. Subsequentemente, o mRNA foi isolado para análise de expressão por meio do qPCR. Os dados foram normalizados para controle de veículo (a média fixada em 1). A avaliação estatística foi realizada por meio de teste de Mann- Whitney (veja a figura 4B).
Sob as mesmas condições descritas acima para os SMOLs como compostos de referência, 3-{acetil[4-(4-amino-2-etil-1H-imidazo[4,5- c]quinolin-1-il)butil]amino}-2,5-anidro-1,3,4-trideoxipentitol (agonista de TLR 1, exemplo III) e N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N- 5 (1,1-dioxidotetra-hidro-3-tienil)acetamida (agonista de TLR 2, exemplo I) a- gonista de TLR 1, ambos compostos de acordo com a invenção, são examinados no modelo de metástase de pulmão de Renca. 3-{acetil[4-(4-amino-2-etil-1 H-imidazo[4,5-c]quinolin-1 - il)butil]amino}-2,5-anidro-1,3,4-trideoxipentitol(agonista de TLR 1, exemplo 10 III) demonstra um forte efeito antimetastático com purificação virtualmente completa dos pulmões após um breve tratamento (dl - 4) (figura 5).
Claims (12)
1. Composto, caracterizado pelo fato de que apresenta a fórmula I: em que R1 é selecionado do grupo consistindo em: -H, alquila, al- quinila, arila, alcóxi, heterociclila e heteroarila, em que alquila, alquini- la, arila, alcóxi, heterociclila ou heteroarila pode ser não substituída ou substituída por um ou mais substituintes que são selecionados do grupo consistindo em: -H, -OH, halogênio, -CO-N(R4)2, -N(R4)2, -CO-C1-10 alquila, -CO-O-C1-10 alquila, -N3, arila e heterociclila, em que cada R4 é independentemente selecionado do grupo consistindo em: -H, -C1-10 alquila, -C1-10 alquil-arila, ou arila; A é C1-C6 alquila; B é-N(R2)(R3); R2 é -(CO)-R5; R5 é selecionado do grupo consistindo em: alquila incluindo grupos de cadeia linear e cadeia ramificada e de grupos cíclicos, al- quinila, arila, heterociclila e heteroarila, cada da qual pode ser não substituída ou substituída por um ou mais substituintes que são seleci-onados do grupo consistindo em: -H, - OH, halogênio, -CN, -NO2, - COOH, -SH, -CO-C1-6 alquila, -CO-O-C1-6 alquila, -N3, arila, heterocicli- la, -CO-arila e -CO-heterociclila; R3 é selecionado do grupo consistindo em: alquenila, hete- roarila, cicloalquila, e heterociclila, em que alquenila, heteroarila, ci- cloalquila ou heterociclila pode ser não substituída ou substituída por um ou mais substituintes H, alquila, alquenila, alcóxi, halogênio, -OH, - N3, trifluorometila, -alquil-arila, -O-alquil-arila, -CO-arila, arila, heteroci- clila, heteroarila, - CO-heteroarila, -CO-O-alquila, - CO-N-alquila, -CO- N-arila; ou sais, N-óxidos farmaceuticamente aceitáveis dos mesmos, ou combinações dos mesmos; em que alquila se refere a um radical de alquila de cadeia linear ou ramificada tendo 1 a 4 átomos de carbono; em que alquinila se refere a um grupo alquila tendo pelo menos dois átomos de carbono e incluindo uma ligação tripla de carbono-carbono; em que alquenila se refere a um grupo alquila tendo pelo menos dois átomos de carbono e incluindo uma ligação dupla de car-bono-carbono; em que alcóxi se refere a um grupo alquila sendo ligado por meio de um átomo de oxigênio; em que arila se refere a fenila, naftila, bifenila, fluorenila e indenila; em que heteroarila se refere a furila, tienila, pirrolila, pira- zolila, imidazolila, triazolila, tetrazolila, isoxazolila, oxazolila, tiazolila, isotiazolila, oxadiazolila, oxatriazolila, tiadiazolila, piridila, piridazinila, pirimidinila, benzofuranila, isobenzofuranila, tionaftenila, isotionaf- tenila, indolila, isoindolila, indazolila, benzisoxazolila, benzoxazolila, ben-ztiazolila, benzisotiazolila, purinila, benzopiranila, quinolinila, iso- quinolinila, cinolinila, quinazolinila, naftiridinila, e benzoxazinila, que em cada caso é não substituída ou pode ser substituída em um ou mais lugares, e inclui anéis aromáticos ou sistemas de anel que contêm pelo menos um heteroátomo de anel entre O, S ou N; em que heterociclila se refere a pirrolidinila, tetra-hidrofuranila, morfolinila, tiomorfolinila, piperidinila, piperazinila, tiazolidinila, imidazoli- dinila, tetra-hidropiranila, azabiciclooctanila, tal como 1-azabiciclo[2,2,2]- octanila, 1-oxo e dioxo-tetra-hidrotiofenila ou ciclopentilsulfonila, bem como formas benzocondensadas e/ou n-óxidos dos mesmos, que em cada caso são não substituídos ou podem ser substituídos em um ou mais lugares, e inclui anéis não aromáticos ou sistemas de anéis mono- ou bicí- clicos que contêm pelo menos um heteroátomo de anel entre O, SOx ou N, em que x = 0, 1 ou 2; e em que cicloalquila se refere a ciclopropila, ciclopentila, ci- clo-hexila e adamantila.
2. Composto de acordo com a reivindicação 1, caracterizado pelo fato de que R1 é alquinila ou alcóxi.
3. Composto de acordo com a reivindicação 1 ou 2, carac-terizado pelo fato de que: R3 é heterociclila, que pode ser não substituída ou substituída por um ou mais substituintes selecionados do grupo consistindo em: -H, alquila, alquenila, halogênio e -OH.
4. Composto de acordo com qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que R3 é selecionado do grupo consis-tindo em: dioxo-tetra-hidrotiofenila, piperidinila, tetra-hidrofuranila, pirididi- na, tetra-hidropiranila e azabiciclo-octanila, cada da qual pode ser opcio-nalmente substituída por um ou mais grupos selecionados do grupo que compreende halogênio, hidroxila, arila, alquila, alcoxi, trifluorometila ou combinações dos mesmos.
5. Composto de acordo com qualquer uma das reivindicações 1 a 4, caracterizado pelo fato de que R1 é alquila, preferivelmente etila.
6. Composto de acordo com qualquer uma das reivindicações 1 a 5, caracterizado pelo fato de que R5 é alquila, preferivelmente metila.
7. Composto de acordo com a reivindicação 1, caracte- rizado pelo fato de ser: N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N- (1,1-dioxidotetra-hidro-3 -tienil)acetamida, N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N- (1-metil-1- oxidopiperidin-4-il)acetamida, 3-{acetil[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1- il)butil]amino}-2,5-anidro-1,3,4-trideoxipentitol, N-[4-(4-amino-2-etil-1H-imidazo[4,5-c]quinolin-1-il)butil]-N-(l- benzil-2-metil-1-oxidopirrolidin-3-il)acetamida, ou sais, N-óxidos farmaceuticamente aceitáveis dos mesmos, ou combinações dos mesmos.
8. Composto de acordo com qualquer uma das reivindicações 1 a 7, caracterizado pelo fato de ser para uso como um medicamento.
9. Composição farmacêutica, caracterizada pelo fato de que compreende uma quantidade terapeuticamente eficaz de um composto de fórmula I como definido em qualquer uma das reivindicações 1 a 7, em combinação com um veículo farmaceuticamente aceitável.
10. Uso de um composto como definido em qualquer uma das reivindicações 1 a 7, caracterizado pelo fato de ser para a fabricação de um medicamento e/ou uma composição farmacêutica para o tratamento de uma doença viral ou neoplástica.
11. Composto de acordo com qualquer uma das reivindi-cações 1 a 7 ou composição farmacêutica de acordo com a reivindicação 9, caracterizado(a) pelo fato de ser para uso no tratamento de um câncer selecionado do grupo que compreende câncer de mama, bexiga, osso, cérebro, sistema nervoso central e periférico. sistema, cólon, glândulas endócrinas, esôfago, endométrio, células germinativas, cabeça e pesco-ço, rim, fígado, pulmão, laringe e hipofaringe, mesotelioma, sarcoma, ovário, pâncreas, próstata, reto, renal, intestino delgado, tecidos moles, testículos, estômago, pele, ureter, vagina e vulva; cancros herdados, reti- nomblastoma e tumor de Wilms; leucemia, linfoma, doença não- Hodgkins, leucemia mielóide crônica e aguda, leucemia linfoblástica agu-da, doença de Hodgkins, mieloma múltiplo e linfoma de células T; sín- drome mielodisplásica, neoplasia das células plasmáticas, síndromes paraneoplásicas, câncer de sítio primário desconhecido e neoplasias re-lacionadas à AIDS.
12. Composto de acordo com qualquer uma das reivindi-cações 1 a 7 ou composição farmacêutica de acordo com a reivindicação 9, caracterizado(a) pelo fato de ser para uso no tratamento de uma con-dição médica selecionada do grupo que compreende verrugas genitais; verrugas comuns; verrugas plantares; Hepatite B; Hepatite C; Herpes Simplex Tipo I e Tipo II; molusco contagioso; HIV; CMV; VZV; neoplasias intra-epiteliais incluindo neoplasia intra-epitelial cervical, papilomavírus humano (HPV) e neoplasias associadas; doenças fúngicas incluindo candida, aspergillus e meningite criptocócica; doenças neoplásicas inclu-indo carcinoma basocelular, leucemia de células cabeludas, sarcoma de Kaposi, carcinoma de células renais, carcinoma de células escamosas, leucemia mielóide, mieloma múltiplo, melanoma, linfoma não-Hodgkin, linfoma cutâneo de células T e outros cânceres; doenças parasitárias, incluindo pneumocystis carinii, criptosporidiose, histoplasmose, toxo- plasmose, infecção por tripanossoma e leishmaniose; infecções bacteria- nas incluindo tuberculose e mycobacterium avium; eczema; eosinofilia; trombocitemia essencial; lepra; esclerose múltipla; Sindrome de Ommen; lúpus discóide; Doença de Bowen; Papulose bowenóide; doenças atópi- cas incluindo dermatite atópica; asma; alergia; rinite alérgica; lúpus erite- matoso sistêmico; doenças fúngicas recorrentes, periodontite e clamídia; ou para o uso como adjuvante de vacina para imunidade mediada por células; ou pelo uso para melhorar ou estimular a cicatrização de feridas, incluindo feridas crônicas.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| IN614/MUM/2008 | 2008-03-24 | ||
| IN614MU2008 | 2008-03-24 | ||
| PCT/EP2009/053399 WO2009118296A2 (en) | 2008-03-24 | 2009-03-23 | Novel substituted imidazoquinolines |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0909317A2 BRPI0909317A2 (pt) | 2017-04-11 |
| BRPI0909317B1 true BRPI0909317B1 (pt) | 2021-05-25 |
Family
ID=40718842
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0909317-6A BRPI0909317B1 (pt) | 2008-03-24 | 2009-03-23 | Imidazoquinolinas substituídas |
Country Status (24)
| Country | Link |
|---|---|
| US (3) | US9073913B2 (pt) |
| EP (2) | EP2386557B1 (pt) |
| JP (3) | JP5670876B2 (pt) |
| KR (1) | KR101606219B1 (pt) |
| CN (2) | CN101980707B (pt) |
| AU (2) | AU2009228769C1 (pt) |
| BR (1) | BRPI0909317B1 (pt) |
| CA (1) | CA2719544C (pt) |
| CY (1) | CY1114648T1 (pt) |
| DK (2) | DK2276486T3 (pt) |
| EA (2) | EA029926B1 (pt) |
| ES (2) | ES2436540T3 (pt) |
| HR (1) | HRP20131139T1 (pt) |
| IL (1) | IL208220A (pt) |
| ME (1) | ME02124B (pt) |
| MX (2) | MX344330B (pt) |
| NZ (2) | NZ588183A (pt) |
| PL (1) | PL2276486T3 (pt) |
| PT (1) | PT2276486E (pt) |
| RS (1) | RS53059B (pt) |
| SG (1) | SG189692A1 (pt) |
| SI (1) | SI2276486T1 (pt) |
| UA (1) | UA105764C2 (pt) |
| WO (1) | WO2009118296A2 (pt) |
Families Citing this family (45)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE10347710B4 (de) | 2003-10-14 | 2006-03-30 | Johannes-Gutenberg-Universität Mainz | Rekombinante Impfstoffe und deren Verwendung |
| DE102005046490A1 (de) | 2005-09-28 | 2007-03-29 | Johannes-Gutenberg-Universität Mainz | Modifikationen von RNA, die zu einer erhöhten Transkriptstabilität und Translationseffizienz führen |
| SI2276486T1 (sl) * | 2008-03-24 | 2014-01-31 | 4Sc Discovery Gmbh | Novi substituirani imidazokinolini |
| JP5988492B2 (ja) | 2009-09-02 | 2016-09-07 | ノバルティス アーゲー | Tlr活性モジュレーターを含む免疫原性組成物 |
| ES2644286T3 (es) | 2009-10-22 | 2017-11-28 | Gilead Sciences, Inc. | Derivados de purina o deazapurina útiles para el tratamiento de (entre otros) infecciones víricas |
| EP2480253B1 (en) | 2010-09-01 | 2014-01-22 | Novartis AG | Adsorption of immunopotentiators to insoluble metal salts |
| AU2012222883A1 (en) | 2011-03-02 | 2013-10-17 | Novartis Ag | Combination vaccines with lower doses of antigen and/or adjuvant |
| HUE046152T2 (hu) | 2011-05-24 | 2020-02-28 | Biontech Rna Pharmaceuticals Gmbh | Rák elleni egyedi vakcinák |
| BR112014004782A2 (pt) | 2011-09-01 | 2017-03-21 | Novartis Ag | formulações adjuvantes de antígenos de staphylococcus aureus |
| JP2015509520A (ja) | 2012-03-07 | 2015-03-30 | ノバルティス アーゲー | 狂犬病ウイルス免疫原のアジュバント化製剤 |
| JP2015510872A (ja) | 2012-03-07 | 2015-04-13 | ノバルティス アーゲー | Streptococcuspneumoniae抗原の増強された製剤 |
| CN104159602B (zh) | 2012-03-08 | 2017-10-24 | 葛兰素史密丝克莱恩生物有限公司 | 加强疫苗的含佐剂制剂 |
| WO2013143555A1 (en) | 2012-03-26 | 2013-10-03 | Biontech Ag | Rna formulation for immunotherapy |
| EP2659908A1 (en) | 2012-05-01 | 2013-11-06 | Affiris AG | Compositions |
| EP2659907A1 (en) | 2012-05-01 | 2013-11-06 | Affiris AG | Compositions |
| EP2659906A1 (en) | 2012-05-01 | 2013-11-06 | Affiris AG | Compositions |
| RU2015106930A (ru) | 2012-09-06 | 2016-10-20 | Новартис Аг | Комбинированные вакцины с менингококком серогруппы в и к/д/с |
| CN104918634A (zh) | 2012-10-12 | 2015-09-16 | 葛兰素史密丝克莱恩生物有限公司 | 用于组合疫苗的非交联无细胞百日咳抗原 |
| CA2892391C (en) | 2012-11-28 | 2023-10-17 | Biontech Rna Pharmaceuticals Gmbh | Individualized vaccines for cancer |
| US9827190B2 (en) | 2013-02-01 | 2017-11-28 | Glaxosmithkline Biologicals Sa | Intradermal delivery of immunological compositions comprising toll-like receptor 7 agonists |
| WO2014180490A1 (en) | 2013-05-10 | 2014-11-13 | Biontech Ag | Predicting immunogenicity of t cell epitopes |
| CN105828835A (zh) | 2013-05-10 | 2016-08-03 | 诺华股份有限公司 | 避免流感疫苗中的发作性嗜睡病风险 |
| ES2959398T3 (es) | 2013-08-28 | 2024-02-26 | Pci Biotech As | Compuesto y método para vacunación e inmunización |
| BE1022744B1 (fr) | 2014-03-26 | 2016-08-29 | Glaxosmithkline Biologicals Sa | Antigenes staphylococciques mutants |
| WO2016045732A1 (en) | 2014-09-25 | 2016-03-31 | Biontech Rna Pharmaceuticals Gmbh | Stable formulations of lipids and liposomes |
| WO2016128060A1 (en) | 2015-02-12 | 2016-08-18 | Biontech Ag | Predicting t cell epitopes useful for vaccination |
| CN104800843B (zh) * | 2015-04-02 | 2017-07-04 | 中国农业科学院兰州兽医研究所 | 一种用于弓形虫感染预防的药剂及应用 |
| EP3302536A1 (en) | 2015-06-03 | 2018-04-11 | Affiris AG | Il-23-p19 vaccines |
| AU2016289497A1 (en) | 2015-07-07 | 2017-12-07 | Affiris Ag | Vaccines for the treatment and prevention of IgE mediated diseases |
| WO2017059902A1 (en) | 2015-10-07 | 2017-04-13 | Biontech Rna Pharmaceuticals Gmbh | 3' utr sequences for stabilization of rna |
| EP3380126A4 (en) | 2015-11-25 | 2019-07-24 | LegoChem Biosciences, Inc. | ANTIBODY-ACTIVE CONJUGATES WITH BRANCHED LINKERS AND ASSOCIATED METHODS |
| BE1024097B1 (fr) * | 2015-12-14 | 2017-11-16 | Glaxosmithkline Biologicals Sa | Imidazoquinoleines pegylees |
| CN109790171B (zh) | 2017-03-29 | 2022-07-26 | 乐高化学生物科学股份有限公司 | 吡咯并苯并二氮杂二聚物前体及其配体-连接体缀合化合物 |
| WO2018224166A1 (en) | 2017-06-09 | 2018-12-13 | Biontech Rna Pharmaceuticals Gmbh | Methods for predicting the usefulness of disease specific amino acid modifications for immunotherapy |
| BR112020004505A2 (pt) | 2017-09-06 | 2020-09-15 | BioNTech SE | imidazoquinolinas substituídas como agonistas de tlr7 |
| WO2019048036A1 (en) * | 2017-09-06 | 2019-03-14 | Biontech Ag | SUBSTITUTED IMIDAZOQUINOLINES |
| WO2019123178A1 (en) * | 2017-12-20 | 2019-06-27 | 3M Innovative Properties Company | Amide substitued imidazo[4,5-c]quinoline compounds with a branched chain linking group for use as an immune response modifier |
| TW202012395A (zh) | 2018-04-14 | 2020-04-01 | 德商4Sc製藥公司 | 用於治療癌症的包含組蛋白去乙醯酶(hdac)抑制劑和tlr7 激動劑和/或tlr8 激動劑的藥物組合產品 |
| CN114616234B (zh) * | 2019-02-07 | 2024-04-12 | 康威(广州)生物科技有限公司 | 磷咪唑并喹啉胺衍生物、及其药物组合物和应用 |
| CU24679B1 (es) * | 2019-03-07 | 2023-09-07 | BioNTech SE | Proceso para la preparación de una imidazoquinolina sustituida |
| CN114599360A (zh) * | 2019-10-29 | 2022-06-07 | 骏达贸易有限公司 | 4-氨基-咪唑并喹啉化合物及其用途 |
| CN117736210A (zh) * | 2021-01-28 | 2024-03-22 | 上海翊石医药科技有限公司 | 一类芳杂环类化合物及其制备方法和用途 |
| US20250313557A1 (en) * | 2022-04-29 | 2025-10-09 | Ligachem Biosciences Inc. | Imidazo[4,5-c]pyridine derivative compounds as tlr7/8 modulators |
| CN115181117B (zh) * | 2022-08-08 | 2024-05-17 | 中国医学科学院医学生物学研究所 | 一种s构型手性分子化合物及其制备方法和作为疫苗佐剂的应用 |
| CN116731015B (zh) * | 2023-05-18 | 2024-09-27 | 深圳威科森生物医药科技有限公司 | 咪唑并喹啉化合物及其制备方法、应用和组合物 |
Family Cites Families (31)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| UA32546C2 (uk) * | 1991-03-01 | 2001-02-15 | Міннесота Майнінг Енд Мен'Юфекчурінг Компані | 1,2-заміщені 1н-імідазо[4,5-с]хінолін-4-аміни, проміжні сполуки для їх синтезу, антивірусна фармацевтична композиція, спосіб лікування інфікованих ссавців, спосіб індукування біосинтезу інтерферону у ссавців, спосіб уповільнення росту бластом |
| WO1998030562A1 (en) * | 1997-01-09 | 1998-07-16 | Terumo Kabushiki Kaisha | Novel amide derivatives and intermediates for the synthesis thereof |
| JPH11222432A (ja) * | 1998-02-03 | 1999-08-17 | Terumo Corp | インターフェロンを誘起するアミド誘導体を含有する外用剤 |
| US6451810B1 (en) | 1999-06-10 | 2002-09-17 | 3M Innovative Properties Company | Amide substituted imidazoquinolines |
| US6756382B2 (en) | 1999-06-10 | 2004-06-29 | 3M Innovative Properties Company | Amide substituted imidazoquinolines |
| US6573273B1 (en) * | 1999-06-10 | 2003-06-03 | 3M Innovative Properties Company | Urea substituted imidazoquinolines |
| US6376669B1 (en) * | 1999-11-05 | 2002-04-23 | 3M Innovative Properties Company | Dye labeled imidazoquinoline compounds |
| DE60230340D1 (de) * | 2001-11-16 | 2009-01-22 | 3M Innovative Properties Co | N-Ä4-(4-Amino-2-ethyl-1H-imidazoÄ4,5-cÜchinolin-1-yl)butylÜmethanesulfonamide, diese enthaltende pharmazeutische Zusammensetzung und deren Verwendung |
| CN100473384C (zh) * | 2001-11-29 | 2009-04-01 | 3M创新有限公司 | 包括免疫反应改性剂的药物制剂 |
| US6677349B1 (en) | 2001-12-21 | 2004-01-13 | 3M Innovative Properties Company | Sulfonamide and sulfamide substituted imidazoquinolines |
| JP2006517974A (ja) * | 2003-02-13 | 2006-08-03 | スリーエム イノベイティブ プロパティズ カンパニー | Irm化合物およびトル様受容体8に関する方法および組成物 |
| EP1599726A4 (en) * | 2003-02-27 | 2009-07-22 | 3M Innovative Properties Co | SELECTIVE MODULATION OF TLR-MEDIATED BIOLOGICAL ACTIVITY |
| US20040176367A1 (en) | 2003-03-07 | 2004-09-09 | 3M Innovative Properties Company | 1-Amino 1H-imidazoquinolines |
| EP1613956A2 (en) * | 2003-03-25 | 2006-01-11 | 3M Innovative Properties Company | Selective activation of cellular activities mediated through a common toll-like receptor |
| MY157827A (en) * | 2003-06-27 | 2016-07-29 | 3M Innovative Properties Co | Sulfonamide substituted imidazoquinolines |
| ES2545826T3 (es) * | 2003-08-14 | 2015-09-16 | 3M Innovative Properties Company | Modificadores de la respuesta inmune modificados con lípidos |
| JP2007511535A (ja) * | 2003-11-14 | 2007-05-10 | スリーエム イノベイティブ プロパティズ カンパニー | ヒドロキシルアミン置換イミダゾ環化合物 |
| CA2545774A1 (en) | 2003-11-14 | 2005-06-02 | 3M Innovative Properties Company | Oxime substituted imidazo ring compounds |
| US8778963B2 (en) | 2003-11-25 | 2014-07-15 | 3M Innovative Properties Company | Hydroxylamine and oxime substituted imidazoquinolines, imidazopyridines, and imidazonaphthyridines |
| WO2005110013A2 (en) * | 2004-04-09 | 2005-11-24 | 3M Innovative Properties Company | Methods, compositions, and preparations for delivery of immune response modifiers |
| EP1755665A4 (en) * | 2004-04-28 | 2010-03-03 | 3M Innovative Properties Co | COMPOSITIONS AND METHODS FOR MUCOSAL VACCINATION |
| US20080015184A1 (en) | 2004-06-14 | 2008-01-17 | 3M Innovative Properties Company | Urea Substituted Imidazopyridines, Imidazoquinolines, and Imidazonaphthyridines |
| US20070259881A1 (en) | 2004-06-18 | 2007-11-08 | Dellaria Joseph F Jr | Substituted Imidazo Ring Systems and Methods |
| WO2006028451A1 (en) * | 2004-09-03 | 2006-03-16 | 3M Innovative Properties Company | 1-amino 1-h-imidazoquinolines |
| CA2598695A1 (en) * | 2005-02-23 | 2006-09-21 | Coley Pharmaceutical Group, Inc. | Hydroxyalkyl substituted imidazoquinolines |
| WO2006091647A2 (en) * | 2005-02-23 | 2006-08-31 | Coley Pharmaceutical Group, Inc. | Method of preferentially inducing the biosynthesis of interferon |
| WO2006116475A2 (en) * | 2005-04-25 | 2006-11-02 | 3M Innovative Properties Company | Immunostimulatory compositions |
| US8088790B2 (en) * | 2005-11-04 | 2012-01-03 | 3M Innovative Properties Company | Hydroxy and alkoxy substituted 1H-imidazoquinolines and methods |
| EP1988896A4 (en) * | 2006-02-22 | 2011-07-27 | 3M Innovative Properties Co | CONJUGATES TO MODIFY IMMUNE REACTIONS |
| DK2155743T3 (da) * | 2007-05-08 | 2012-11-05 | Astrazeneca Ab | Imidazoquinoliner med immunmodulerende egenskaber |
| SI2276486T1 (sl) * | 2008-03-24 | 2014-01-31 | 4Sc Discovery Gmbh | Novi substituirani imidazokinolini |
-
2009
- 2009-03-23 SI SI200930788T patent/SI2276486T1/sl unknown
- 2009-03-23 PT PT97247845T patent/PT2276486E/pt unknown
- 2009-03-23 EP EP11175040.2A patent/EP2386557B1/en active Active
- 2009-03-23 ES ES09724784.5T patent/ES2436540T3/es active Active
- 2009-03-23 NZ NZ588183A patent/NZ588183A/en not_active IP Right Cessation
- 2009-03-23 EA EA201590628A patent/EA029926B1/ru unknown
- 2009-03-23 CA CA2719544A patent/CA2719544C/en active Active
- 2009-03-23 MX MX2012005484A patent/MX344330B/es unknown
- 2009-03-23 BR BRPI0909317-6A patent/BRPI0909317B1/pt not_active IP Right Cessation
- 2009-03-23 UA UAA201012523A patent/UA105764C2/uk unknown
- 2009-03-23 MX MX2010010511A patent/MX2010010511A/es active IP Right Grant
- 2009-03-23 ES ES11175040.2T patent/ES2667054T3/es active Active
- 2009-03-23 KR KR1020107023633A patent/KR101606219B1/ko not_active Expired - Fee Related
- 2009-03-23 CN CN200980111136.7A patent/CN101980707B/zh not_active Expired - Fee Related
- 2009-03-23 RS RS20130525A patent/RS53059B/sr unknown
- 2009-03-23 WO PCT/EP2009/053399 patent/WO2009118296A2/en not_active Ceased
- 2009-03-23 DK DK09724784.5T patent/DK2276486T3/da active
- 2009-03-23 US US12/934,228 patent/US9073913B2/en active Active
- 2009-03-23 EA EA201001356A patent/EA023556B1/ru not_active IP Right Cessation
- 2009-03-23 DK DK11175040.2T patent/DK2386557T3/en active
- 2009-03-23 PL PL09724784T patent/PL2276486T3/pl unknown
- 2009-03-23 JP JP2011501192A patent/JP5670876B2/ja active Active
- 2009-03-23 AU AU2009228769A patent/AU2009228769C1/en not_active Ceased
- 2009-03-23 CN CN201310241620.XA patent/CN103396415B/zh not_active Expired - Fee Related
- 2009-03-23 NZ NZ599446A patent/NZ599446A/xx not_active IP Right Cessation
- 2009-03-23 SG SG2013020649A patent/SG189692A1/en unknown
- 2009-03-23 EP EP09724784.5A patent/EP2276486B1/en active Active
- 2009-03-23 HR HRP20131139AT patent/HRP20131139T1/hr unknown
-
2010
- 2010-09-19 IL IL208220A patent/IL208220A/en active IP Right Grant
-
2013
- 2013-11-21 JP JP2013240978A patent/JP5837549B2/ja active Active
- 2013-11-26 CY CY20131101056T patent/CY1114648T1/el unknown
-
2014
- 2014-08-01 JP JP2014157662A patent/JP2014208704A/ja active Pending
- 2014-08-06 AU AU2014210573A patent/AU2014210573B2/en not_active Ceased
-
2015
- 2015-06-03 US US14/729,698 patent/US9446040B2/en active Active
-
2016
- 2016-09-19 US US15/269,363 patent/US9908880B2/en active Active
- 2016-10-27 ME MEP-2013-525A patent/ME02124B/me unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0909317B1 (pt) | Imidazoquinolinas substituídas | |
| UA77710C2 (en) | Amide-substituted imidazopyridine compounds | |
| PT1198233E (pt) | Imidazoquinilinas substituídas com sulfonamida e sulfamida | |
| CN108026092A (zh) | 胍取代的咪唑并[4,5-c]环化合物 | |
| BR112020004505A2 (pt) | imidazoquinolinas substituídas como agonistas de tlr7 | |
| HK1152238B (en) | Novel substituted imidazoquinolines | |
| HK1086762B (en) | Sulfonamide substituted imidazoquinolines |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B25G | Requested change of headquarter approved |
Owner name: 4SC AG (DE) |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B25A | Requested transfer of rights approved |
Owner name: BIONTECH SE (DE) |
|
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 23/03/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |
|
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 17A ANUIDADE. |