BRPI0909866B1 - Método de produção de um meio condicionado de células progenitoras de fígado, meio condicionado e composição farmacêutica - Google Patents
Método de produção de um meio condicionado de células progenitoras de fígado, meio condicionado e composição farmacêutica Download PDFInfo
- Publication number
- BRPI0909866B1 BRPI0909866B1 BRPI0909866-6A BRPI0909866A BRPI0909866B1 BR PI0909866 B1 BRPI0909866 B1 BR PI0909866B1 BR PI0909866 A BRPI0909866 A BR PI0909866A BR PI0909866 B1 BRPI0909866 B1 BR PI0909866B1
- Authority
- BR
- Brazil
- Prior art keywords
- pharmaceutical composition
- conditioned medium
- cells
- cell
- human
- Prior art date
Links
- 239000003636 conditioned culture medium Substances 0.000 title claims abstract description 85
- 210000004185 liver Anatomy 0.000 title claims abstract description 50
- 210000000130 stem cell Anatomy 0.000 title claims abstract description 43
- 239000008194 pharmaceutical composition Substances 0.000 title claims description 26
- 238000000034 method Methods 0.000 title claims description 19
- 238000004519 manufacturing process Methods 0.000 title description 4
- 210000004027 cell Anatomy 0.000 claims description 58
- 239000000203 mixture Substances 0.000 claims description 35
- 210000003494 hepatocyte Anatomy 0.000 claims description 25
- 102000004889 Interleukin-6 Human genes 0.000 claims description 22
- 108090001005 Interleukin-6 Proteins 0.000 claims description 22
- 102000004890 Interleukin-8 Human genes 0.000 claims description 22
- 108090001007 Interleukin-8 Proteins 0.000 claims description 22
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 claims description 21
- 102000003745 Hepatocyte Growth Factor Human genes 0.000 claims description 21
- 229940100601 interleukin-6 Drugs 0.000 claims description 19
- 229940096397 interleukin-8 Drugs 0.000 claims description 19
- 108010073929 Vascular Endothelial Growth Factor A Proteins 0.000 claims description 18
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 claims description 18
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 claims description 18
- XKTZWUACRZHVAN-VADRZIEHSA-N interleukin-8 Chemical compound C([C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@@H](NC(C)=O)CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N[C@@H](CCSC)C(=O)N1[C@H](CCC1)C(=O)N1[C@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC=1C=CC(O)=CC=1)C(=O)N[C@H](CO)C(=O)N1[C@H](CCC1)C(N)=O)C1=CC=CC=C1 XKTZWUACRZHVAN-VADRZIEHSA-N 0.000 claims description 17
- 238000012258 culturing Methods 0.000 claims description 16
- 210000002966 serum Anatomy 0.000 claims description 14
- 239000007758 minimum essential medium Substances 0.000 claims description 13
- 239000001963 growth medium Substances 0.000 claims description 10
- 102000003974 Fibroblast growth factor 2 Human genes 0.000 claims description 8
- 108090000379 Fibroblast growth factor 2 Proteins 0.000 claims description 8
- 239000003102 growth factor Substances 0.000 claims description 8
- 238000004113 cell culture Methods 0.000 claims description 6
- 230000034994 death Effects 0.000 claims description 6
- 231100000517 death Toxicity 0.000 claims description 6
- 239000006143 cell culture medium Substances 0.000 claims description 5
- 230000008472 epithelial growth Effects 0.000 claims description 3
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 2
- 150000001413 amino acids Chemical class 0.000 claims description 2
- 239000002577 cryoprotective agent Substances 0.000 claims description 2
- 239000008103 glucose Substances 0.000 claims description 2
- 210000005228 liver tissue Anatomy 0.000 claims description 2
- 210000004962 mammalian cell Anatomy 0.000 claims description 2
- 150000003839 salts Chemical class 0.000 claims description 2
- 235000013343 vitamin Nutrition 0.000 claims description 2
- 239000011782 vitamin Substances 0.000 claims description 2
- 229940088594 vitamin Drugs 0.000 claims description 2
- 229930003231 vitamin Natural products 0.000 claims description 2
- 102000049853 macrophage stimulating protein Human genes 0.000 claims 2
- 108010053292 macrophage stimulating protein Proteins 0.000 claims 2
- 230000010261 cell growth Effects 0.000 claims 1
- 230000001172 regenerating effect Effects 0.000 abstract description 10
- 238000011282 treatment Methods 0.000 abstract description 10
- 239000003814 drug Substances 0.000 abstract description 8
- 230000006378 damage Effects 0.000 abstract description 7
- 208000027418 Wounds and injury Diseases 0.000 abstract description 6
- 208000014674 injury Diseases 0.000 abstract description 6
- 210000000056 organ Anatomy 0.000 abstract description 2
- 238000011177 media preparation Methods 0.000 abstract 1
- MSWZFWKMSRAUBD-GASJEMHNSA-N 2-amino-2-deoxy-D-galactopyranose Chemical compound N[C@H]1C(O)O[C@H](CO)[C@H](O)[C@@H]1O MSWZFWKMSRAUBD-GASJEMHNSA-N 0.000 description 51
- MSWZFWKMSRAUBD-UHFFFAOYSA-N beta-D-galactosamine Natural products NC1C(O)OC(CO)C(O)C1O MSWZFWKMSRAUBD-UHFFFAOYSA-N 0.000 description 49
- 102000004127 Cytokines Human genes 0.000 description 42
- 108090000695 Cytokines Proteins 0.000 description 42
- 210000002901 mesenchymal stem cell Anatomy 0.000 description 39
- 239000002158 endotoxin Substances 0.000 description 38
- 229920006008 lipopolysaccharide Polymers 0.000 description 35
- 102000004169 proteins and genes Human genes 0.000 description 27
- 108090000623 proteins and genes Proteins 0.000 description 27
- 235000018102 proteins Nutrition 0.000 description 25
- 238000002474 experimental method Methods 0.000 description 23
- 239000007924 injection Substances 0.000 description 20
- 238000002347 injection Methods 0.000 description 20
- 239000002609 medium Substances 0.000 description 20
- 238000011579 SCID mouse model Methods 0.000 description 19
- 238000002360 preparation method Methods 0.000 description 18
- 241001465754 Metazoa Species 0.000 description 16
- 108091006905 Human Serum Albumin Proteins 0.000 description 15
- 102000008100 Human Serum Albumin Human genes 0.000 description 15
- 241000699670 Mus sp. Species 0.000 description 15
- YBJHBAHKTGYVGT-ZKWXMUAHSA-N (+)-Biotin Chemical compound N1C(=O)N[C@@H]2[C@H](CCCCC(=O)O)SC[C@@H]21 YBJHBAHKTGYVGT-ZKWXMUAHSA-N 0.000 description 14
- 238000011194 good manufacturing practice Methods 0.000 description 14
- 101000958041 Homo sapiens Musculin Proteins 0.000 description 13
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 13
- 239000006228 supernatant Substances 0.000 description 13
- 230000004083 survival effect Effects 0.000 description 12
- 238000000108 ultra-filtration Methods 0.000 description 11
- 235000002639 sodium chloride Nutrition 0.000 description 10
- 239000006146 Roswell Park Memorial Institute medium Substances 0.000 description 9
- 238000004458 analytical method Methods 0.000 description 9
- 238000003556 assay Methods 0.000 description 9
- 238000000338 in vitro Methods 0.000 description 9
- 238000001727 in vivo Methods 0.000 description 9
- 230000006698 induction Effects 0.000 description 9
- 239000011780 sodium chloride Substances 0.000 description 9
- 108010057081 Merozoite Surface Protein 1 Proteins 0.000 description 8
- 231100000518 lethal Toxicity 0.000 description 8
- 230000001665 lethal effect Effects 0.000 description 8
- 239000012528 membrane Substances 0.000 description 8
- 210000001519 tissue Anatomy 0.000 description 8
- 238000001262 western blot Methods 0.000 description 8
- 102100036475 Alanine aminotransferase 1 Human genes 0.000 description 7
- 108010082126 Alanine transaminase Proteins 0.000 description 7
- 229960002685 biotin Drugs 0.000 description 7
- 235000020958 biotin Nutrition 0.000 description 7
- 239000011616 biotin Substances 0.000 description 7
- 230000014509 gene expression Effects 0.000 description 7
- 230000012010 growth Effects 0.000 description 7
- 239000011159 matrix material Substances 0.000 description 7
- QAPSNMNOIOSXSQ-YNEHKIRRSA-N 1-[(2r,4s,5r)-4-[tert-butyl(dimethyl)silyl]oxy-5-(hydroxymethyl)oxolan-2-yl]-5-methylpyrimidine-2,4-dione Chemical compound O=C1NC(=O)C(C)=CN1[C@@H]1O[C@H](CO)[C@@H](O[Si](C)(C)C(C)(C)C)C1 QAPSNMNOIOSXSQ-YNEHKIRRSA-N 0.000 description 6
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 6
- 108050006400 Cyclin Proteins 0.000 description 6
- 238000002965 ELISA Methods 0.000 description 6
- 102100036691 Proliferating cell nuclear antigen Human genes 0.000 description 6
- 230000006907 apoptotic process Effects 0.000 description 6
- 210000001185 bone marrow Anatomy 0.000 description 6
- 230000003247 decreasing effect Effects 0.000 description 6
- 230000000694 effects Effects 0.000 description 6
- 208000007788 Acute Liver Failure Diseases 0.000 description 5
- 102000019034 Chemokines Human genes 0.000 description 5
- 108010012236 Chemokines Proteins 0.000 description 5
- CKLJMWTZIZZHCS-REOHCLBHSA-N L-aspartic acid Chemical compound OC(=O)[C@@H](N)CC(O)=O CKLJMWTZIZZHCS-REOHCLBHSA-N 0.000 description 5
- 102000014962 Monocyte Chemoattractant Proteins Human genes 0.000 description 5
- 108010064136 Monocyte Chemoattractant Proteins Proteins 0.000 description 5
- 102100040247 Tumor necrosis factor Human genes 0.000 description 5
- 229940009098 aspartate Drugs 0.000 description 5
- 230000030833 cell death Effects 0.000 description 5
- 238000005119 centrifugation Methods 0.000 description 5
- 238000001514 detection method Methods 0.000 description 5
- 230000028974 hepatocyte apoptotic process Effects 0.000 description 5
- 239000007928 intraperitoneal injection Substances 0.000 description 5
- 238000010186 staining Methods 0.000 description 5
- QKNYBSVHEMOAJP-UHFFFAOYSA-N 2-amino-2-(hydroxymethyl)propane-1,3-diol;hydron;chloride Chemical compound Cl.OCC(N)(CO)CO QKNYBSVHEMOAJP-UHFFFAOYSA-N 0.000 description 4
- 108010063104 Apoptosis Regulatory Proteins Proteins 0.000 description 4
- 102000010565 Apoptosis Regulatory Proteins Human genes 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- 206010019663 Hepatic failure Diseases 0.000 description 4
- 108060008682 Tumor Necrosis Factor Proteins 0.000 description 4
- 239000000872 buffer Substances 0.000 description 4
- 230000004069 differentiation Effects 0.000 description 4
- 238000001114 immunoprecipitation Methods 0.000 description 4
- 208000007903 liver failure Diseases 0.000 description 4
- 239000003550 marker Substances 0.000 description 4
- 239000000463 material Substances 0.000 description 4
- YBYRMVIVWMBXKQ-UHFFFAOYSA-N phenylmethanesulfonyl fluoride Chemical compound FS(=O)(=O)CC1=CC=CC=C1 YBYRMVIVWMBXKQ-UHFFFAOYSA-N 0.000 description 4
- 230000002829 reductive effect Effects 0.000 description 4
- 238000012360 testing method Methods 0.000 description 4
- 231100000419 toxicity Toxicity 0.000 description 4
- 230000001988 toxicity Effects 0.000 description 4
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 3
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 3
- 238000009010 Bradford assay Methods 0.000 description 3
- 102100021943 C-C motif chemokine 2 Human genes 0.000 description 3
- 102100037362 Fibronectin Human genes 0.000 description 3
- 108010067306 Fibronectins Proteins 0.000 description 3
- 102100039620 Granulocyte-macrophage colony-stimulating factor Human genes 0.000 description 3
- 206010021143 Hypoxia Diseases 0.000 description 3
- 108091058560 IL8 Proteins 0.000 description 3
- 101710091439 Major capsid protein 1 Proteins 0.000 description 3
- 239000000020 Nitrocellulose Substances 0.000 description 3
- 206010053159 Organ failure Diseases 0.000 description 3
- 241000700159 Rattus Species 0.000 description 3
- 208000001647 Renal Insufficiency Diseases 0.000 description 3
- 230000001640 apoptogenic effect Effects 0.000 description 3
- 230000008901 benefit Effects 0.000 description 3
- 229940098773 bovine serum albumin Drugs 0.000 description 3
- 239000003153 chemical reaction reagent Substances 0.000 description 3
- 238000011496 digital image analysis Methods 0.000 description 3
- 239000012091 fetal bovine serum Substances 0.000 description 3
- 238000007490 hematoxylin and eosin (H&E) staining Methods 0.000 description 3
- 230000001146 hypoxic effect Effects 0.000 description 3
- 230000005764 inhibitory process Effects 0.000 description 3
- 201000006370 kidney failure Diseases 0.000 description 3
- 231100000225 lethality Toxicity 0.000 description 3
- 238000005259 measurement Methods 0.000 description 3
- 229920001220 nitrocellulos Polymers 0.000 description 3
- 238000010899 nucleation Methods 0.000 description 3
- 230000033667 organ regeneration Effects 0.000 description 3
- 230000035755 proliferation Effects 0.000 description 3
- 235000020183 skimmed milk Nutrition 0.000 description 3
- 239000000243 solution Substances 0.000 description 3
- IMGXDCAOBSTOQJ-CFTXMQDWSA-N (3R,4R,5R,6R)-3-amino-6-(hydroxymethyl)oxane-2,4,5-triol (2R,3R,4R,5R)-2-amino-3,4,5,6-tetrahydroxyhexanal Chemical compound O=C[C@H](N)[C@@H](O)[C@@H](O)[C@H](O)CO.N[C@H]1C(O)O[C@H](CO)[C@H](O)[C@@H]1O IMGXDCAOBSTOQJ-CFTXMQDWSA-N 0.000 description 2
- 108010039627 Aprotinin Proteins 0.000 description 2
- 101150008012 Bcl2l1 gene Proteins 0.000 description 2
- 108010071942 Colony-Stimulating Factors Proteins 0.000 description 2
- 102000005754 Cytokine Receptor gp130 Human genes 0.000 description 2
- 108010006197 Cytokine Receptor gp130 Proteins 0.000 description 2
- 102000006975 Ectodysplasins Human genes 0.000 description 2
- 108010072589 Ectodysplasins Proteins 0.000 description 2
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 2
- 102000003886 Glycoproteins Human genes 0.000 description 2
- 108090000288 Glycoproteins Proteins 0.000 description 2
- 238000012404 In vitro experiment Methods 0.000 description 2
- 102000004883 Insulin-like growth factor-binding protein 6 Human genes 0.000 description 2
- 108090001014 Insulin-like growth factor-binding protein 6 Proteins 0.000 description 2
- GDBQQVLCIARPGH-UHFFFAOYSA-N Leupeptin Natural products CC(C)CC(NC(C)=O)C(=O)NC(CC(C)C)C(=O)NC(C=O)CCCN=C(N)N GDBQQVLCIARPGH-UHFFFAOYSA-N 0.000 description 2
- 206010067125 Liver injury Diseases 0.000 description 2
- 206010028851 Necrosis Diseases 0.000 description 2
- 102100039867 Outer mitochondrial transmembrane helix translocase Human genes 0.000 description 2
- -1 PDGF Proteins 0.000 description 2
- BELBBZDIHDAJOR-UHFFFAOYSA-N Phenolsulfonephthalein Chemical compound C1=CC(O)=CC=C1C1(C=2C=CC(O)=CC=2)C2=CC=CC=C2S(=O)(=O)O1 BELBBZDIHDAJOR-UHFFFAOYSA-N 0.000 description 2
- 238000012288 TUNEL assay Methods 0.000 description 2
- 239000013504 Triton X-100 Substances 0.000 description 2
- 229920004890 Triton X-100 Polymers 0.000 description 2
- 230000009815 adipogenic differentiation Effects 0.000 description 2
- 238000003782 apoptosis assay Methods 0.000 description 2
- 229960004405 aprotinin Drugs 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 239000012228 culture supernatant Substances 0.000 description 2
- 235000018417 cysteine Nutrition 0.000 description 2
- XUJNEKJLAYXESH-UHFFFAOYSA-N cysteine Natural products SCC(N)C(O)=O XUJNEKJLAYXESH-UHFFFAOYSA-N 0.000 description 2
- 230000001419 dependent effect Effects 0.000 description 2
- 238000000502 dialysis Methods 0.000 description 2
- 230000003828 downregulation Effects 0.000 description 2
- 231100000234 hepatic damage Toxicity 0.000 description 2
- 206010019692 hepatic necrosis Diseases 0.000 description 2
- 102000046949 human MSC Human genes 0.000 description 2
- 239000003547 immunosorbent Substances 0.000 description 2
- 238000011534 incubation Methods 0.000 description 2
- 230000002401 inhibitory effect Effects 0.000 description 2
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 2
- GDBQQVLCIARPGH-ULQDDVLXSA-N leupeptin Chemical compound CC(C)C[C@H](NC(C)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](C=O)CCCN=C(N)N GDBQQVLCIARPGH-ULQDDVLXSA-N 0.000 description 2
- 108010052968 leupeptin Proteins 0.000 description 2
- 230000008818 liver damage Effects 0.000 description 2
- 231100000149 liver necrosis Toxicity 0.000 description 2
- 239000006166 lysate Substances 0.000 description 2
- 239000012139 lysis buffer Substances 0.000 description 2
- 230000007246 mechanism Effects 0.000 description 2
- 238000007837 multiplex assay Methods 0.000 description 2
- 230000017074 necrotic cell death Effects 0.000 description 2
- 230000009818 osteogenic differentiation Effects 0.000 description 2
- 102000013415 peroxidase activity proteins Human genes 0.000 description 2
- 108040007629 peroxidase activity proteins Proteins 0.000 description 2
- 229960003531 phenolsulfonphthalein Drugs 0.000 description 2
- 238000002264 polyacrylamide gel electrophoresis Methods 0.000 description 2
- 229920000136 polysorbate Polymers 0.000 description 2
- 239000011148 porous material Substances 0.000 description 2
- 230000008569 process Effects 0.000 description 2
- 235000019624 protein content Nutrition 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 238000002415 sodium dodecyl sulfate polyacrylamide gel electrophoresis Methods 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 230000003827 upregulation Effects 0.000 description 2
- 238000005406 washing Methods 0.000 description 2
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 2
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 1
- UAIUNKRWKOVEES-UHFFFAOYSA-N 3,3',5,5'-tetramethylbenzidine Chemical compound CC1=C(N)C(C)=CC(C=2C=C(C)C(N)=C(C)C=2)=C1 UAIUNKRWKOVEES-UHFFFAOYSA-N 0.000 description 1
- WOVKYSAHUYNSMH-RRKCRQDMSA-N 5-bromodeoxyuridine Chemical compound C1[C@H](O)[C@@H](CO)O[C@H]1N1C(=O)NC(=O)C(Br)=C1 WOVKYSAHUYNSMH-RRKCRQDMSA-N 0.000 description 1
- HRPVXLWXLXDGHG-UHFFFAOYSA-N Acrylamide Chemical compound NC(=O)C=C HRPVXLWXLXDGHG-UHFFFAOYSA-N 0.000 description 1
- 108010075348 Activated-Leukocyte Cell Adhesion Molecule Proteins 0.000 description 1
- 108010059616 Activins Proteins 0.000 description 1
- 206010000804 Acute hepatic failure Diseases 0.000 description 1
- 108010078606 Adipokines Proteins 0.000 description 1
- 102000014777 Adipokines Human genes 0.000 description 1
- 102000009027 Albumins Human genes 0.000 description 1
- 108010088751 Albumins Proteins 0.000 description 1
- 102100025248 C-X-C motif chemokine 10 Human genes 0.000 description 1
- 101710098275 C-X-C motif chemokine 10 Proteins 0.000 description 1
- 108700012434 CCL3 Proteins 0.000 description 1
- 102100024210 CD166 antigen Human genes 0.000 description 1
- 241000283707 Capra Species 0.000 description 1
- 102000000013 Chemokine CCL3 Human genes 0.000 description 1
- 102000001326 Chemokine CCL4 Human genes 0.000 description 1
- 108010055165 Chemokine CCL4 Proteins 0.000 description 1
- 102000001327 Chemokine CCL5 Human genes 0.000 description 1
- 108010055166 Chemokine CCL5 Proteins 0.000 description 1
- 108090000738 Decorin Proteins 0.000 description 1
- 102000004237 Decorin Human genes 0.000 description 1
- 238000012286 ELISA Assay Methods 0.000 description 1
- 238000008157 ELISA kit Methods 0.000 description 1
- 108050009340 Endothelin Proteins 0.000 description 1
- 102000002045 Endothelin Human genes 0.000 description 1
- 102100023688 Eotaxin Human genes 0.000 description 1
- 101710139422 Eotaxin Proteins 0.000 description 1
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 1
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 1
- 229920002527 Glycogen Polymers 0.000 description 1
- 102000010956 Glypican Human genes 0.000 description 1
- 108050001154 Glypican Proteins 0.000 description 1
- 108050007237 Glypican-3 Proteins 0.000 description 1
- 102000004269 Granulocyte Colony-Stimulating Factor Human genes 0.000 description 1
- 108010017080 Granulocyte Colony-Stimulating Factor Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000599951 Homo sapiens Insulin-like growth factor I Proteins 0.000 description 1
- 101001044893 Homo sapiens Interleukin-20 receptor subunit alpha Proteins 0.000 description 1
- 101001055222 Homo sapiens Interleukin-8 Proteins 0.000 description 1
- 101000798130 Homo sapiens Tumor necrosis factor receptor superfamily member 11B Proteins 0.000 description 1
- 108010001336 Horseradish Peroxidase Proteins 0.000 description 1
- 101150088952 IGF1 gene Proteins 0.000 description 1
- 102100026818 Inhibin beta E chain Human genes 0.000 description 1
- 102100037852 Insulin-like growth factor I Human genes 0.000 description 1
- 102000003814 Interleukin-10 Human genes 0.000 description 1
- 108090000174 Interleukin-10 Proteins 0.000 description 1
- 102000003816 Interleukin-13 Human genes 0.000 description 1
- 108090000176 Interleukin-13 Proteins 0.000 description 1
- 102000003812 Interleukin-15 Human genes 0.000 description 1
- 108090000172 Interleukin-15 Proteins 0.000 description 1
- 102000013691 Interleukin-17 Human genes 0.000 description 1
- 108050003558 Interleukin-17 Proteins 0.000 description 1
- 108010002350 Interleukin-2 Proteins 0.000 description 1
- 102000000588 Interleukin-2 Human genes 0.000 description 1
- 102100022706 Interleukin-20 receptor subunit alpha Human genes 0.000 description 1
- 102000004388 Interleukin-4 Human genes 0.000 description 1
- 108090000978 Interleukin-4 Proteins 0.000 description 1
- 108010002616 Interleukin-5 Proteins 0.000 description 1
- 102100039897 Interleukin-5 Human genes 0.000 description 1
- 108010002586 Interleukin-7 Proteins 0.000 description 1
- 102100021592 Interleukin-7 Human genes 0.000 description 1
- 102100026236 Interleukin-8 Human genes 0.000 description 1
- 108010002335 Interleukin-9 Proteins 0.000 description 1
- 102000000585 Interleukin-9 Human genes 0.000 description 1
- 102100020880 Kit ligand Human genes 0.000 description 1
- 101710177504 Kit ligand Proteins 0.000 description 1
- 102100027000 Latent-transforming growth factor beta-binding protein 1 Human genes 0.000 description 1
- 101710178954 Latent-transforming growth factor beta-binding protein 1 Proteins 0.000 description 1
- 108060004872 MIF Proteins 0.000 description 1
- 108010046938 Macrophage Colony-Stimulating Factor Proteins 0.000 description 1
- 102000007651 Macrophage Colony-Stimulating Factor Human genes 0.000 description 1
- 102000009571 Macrophage Inflammatory Proteins Human genes 0.000 description 1
- 108010009474 Macrophage Inflammatory Proteins Proteins 0.000 description 1
- 101710151803 Mitochondrial intermediate peptidase 2 Proteins 0.000 description 1
- 102100030173 Muellerian-inhibiting factor Human genes 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 102000009890 Osteonectin Human genes 0.000 description 1
- 108010077077 Osteonectin Proteins 0.000 description 1
- 108010035042 Osteoprotegerin Proteins 0.000 description 1
- 102000008108 Osteoprotegerin Human genes 0.000 description 1
- 102000035195 Peptidases Human genes 0.000 description 1
- 108091005804 Peptidases Proteins 0.000 description 1
- 229920001213 Polysorbate 20 Polymers 0.000 description 1
- 239000004365 Protease Substances 0.000 description 1
- 239000012083 RIPA buffer Substances 0.000 description 1
- 229920002684 Sepharose Polymers 0.000 description 1
- 108010090804 Streptavidin Proteins 0.000 description 1
- 108090000340 Transaminases Proteins 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 108060008683 Tumor Necrosis Factor Receptor Proteins 0.000 description 1
- 102100032236 Tumor necrosis factor receptor superfamily member 11B Human genes 0.000 description 1
- CYKLRRKFBPBYEI-KBQKSTHMSA-N UDP-alpha-D-galactosamine Chemical class O1[C@H](CO)[C@H](O)[C@H](O)[C@@H](N)[C@H]1OP(O)(=O)OP(O)(=O)OC[C@@H]1[C@@H](O)[C@@H](O)[C@H](N2C(NC(=O)C=C2)=O)O1 CYKLRRKFBPBYEI-KBQKSTHMSA-N 0.000 description 1
- 238000002835 absorbance Methods 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 230000002378 acidificating effect Effects 0.000 description 1
- 230000009471 action Effects 0.000 description 1
- 239000000488 activin Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 239000000478 adipokine Substances 0.000 description 1
- 229940024606 amino acid Drugs 0.000 description 1
- 235000001014 amino acid Nutrition 0.000 description 1
- 238000010171 animal model Methods 0.000 description 1
- 239000011324 bead Substances 0.000 description 1
- 238000012742 biochemical analysis Methods 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 230000000903 blocking effect Effects 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 230000021164 cell adhesion Effects 0.000 description 1
- 230000005779 cell damage Effects 0.000 description 1
- 208000037887 cell injury Diseases 0.000 description 1
- 230000003833 cell viability Effects 0.000 description 1
- 210000003169 central nervous system Anatomy 0.000 description 1
- 238000006243 chemical reaction Methods 0.000 description 1
- 239000007376 cm-medium Substances 0.000 description 1
- 230000001143 conditioned effect Effects 0.000 description 1
- 230000016396 cytokine production Effects 0.000 description 1
- 239000012153 distilled water Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 230000000816 effect on animals Effects 0.000 description 1
- 230000003511 endothelial effect Effects 0.000 description 1
- ZUBDGKVDJUIMQQ-UBFCDGJISA-N endothelin-1 Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(O)=O)NC(=O)[C@H]1NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](C(C)C)NC(=O)[C@H]2CSSC[C@@H](C(N[C@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)NC(=O)[C@@H](CO)NC(=O)[C@H](N)CSSC1)C1=CNC=N1 ZUBDGKVDJUIMQQ-UBFCDGJISA-N 0.000 description 1
- 210000002744 extracellular matrix Anatomy 0.000 description 1
- 239000000835 fiber Substances 0.000 description 1
- 210000002950 fibroblast Anatomy 0.000 description 1
- 238000001914 filtration Methods 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 229940096919 glycogen Drugs 0.000 description 1
- 210000003714 granulocyte Anatomy 0.000 description 1
- 230000035876 healing Effects 0.000 description 1
- 230000011132 hemopoiesis Effects 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 208000006454 hepatitis Diseases 0.000 description 1
- 231100000283 hepatitis Toxicity 0.000 description 1
- 230000002443 hepatoprotective effect Effects 0.000 description 1
- 230000003082 hepatotoxic effect Effects 0.000 description 1
- 238000007489 histopathology method Methods 0.000 description 1
- 230000008105 immune reaction Effects 0.000 description 1
- 238000003018 immunoassay Methods 0.000 description 1
- 230000004968 inflammatory condition Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 102000004114 interleukin 20 Human genes 0.000 description 1
- 108090000681 interleukin 20 Proteins 0.000 description 1
- 102000009634 interleukin-1 receptor antagonist activity proteins Human genes 0.000 description 1
- 108040001669 interleukin-1 receptor antagonist activity proteins Proteins 0.000 description 1
- 238000002372 labelling Methods 0.000 description 1
- 210000000265 leukocyte Anatomy 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 210000005229 liver cell Anatomy 0.000 description 1
- 231100000835 liver failure Toxicity 0.000 description 1
- 229920002521 macromolecule Polymers 0.000 description 1
- 210000002540 macrophage Anatomy 0.000 description 1
- 238000001000 micrograph Methods 0.000 description 1
- 239000004005 microsphere Substances 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 230000006654 negative regulation of apoptotic process Effects 0.000 description 1
- XXUPLYBCNPLTIW-UHFFFAOYSA-N octadec-7-ynoic acid Chemical compound CCCCCCCCCCC#CCCCCCC(O)=O XXUPLYBCNPLTIW-UHFFFAOYSA-N 0.000 description 1
- 102000027450 oncoproteins Human genes 0.000 description 1
- 108091008819 oncoproteins Proteins 0.000 description 1
- 230000003287 optical effect Effects 0.000 description 1
- 239000008188 pellet Substances 0.000 description 1
- 239000000825 pharmaceutical preparation Substances 0.000 description 1
- 210000001778 pluripotent stem cell Anatomy 0.000 description 1
- 239000000256 polyoxyethylene sorbitan monolaurate Substances 0.000 description 1
- 235000010486 polyoxyethylene sorbitan monolaurate Nutrition 0.000 description 1
- 230000002265 prevention Effects 0.000 description 1
- 150000003141 primary amines Chemical class 0.000 description 1
- 230000006920 protein precipitation Effects 0.000 description 1
- 238000013139 quantization Methods 0.000 description 1
- 238000011552 rat model Methods 0.000 description 1
- 238000011084 recovery Methods 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000008439 repair process Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000002441 reversible effect Effects 0.000 description 1
- 230000003248 secreting effect Effects 0.000 description 1
- 230000035945 sensitivity Effects 0.000 description 1
- 238000002660 stem cell treatment Methods 0.000 description 1
- 230000004936 stimulating effect Effects 0.000 description 1
- 239000012089 stop solution Substances 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 230000001225 therapeutic effect Effects 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 231100000331 toxic Toxicity 0.000 description 1
- 230000002588 toxic effect Effects 0.000 description 1
- 102000014898 transaminase activity proteins Human genes 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 230000001228 trophic effect Effects 0.000 description 1
- 238000003211 trypan blue cell staining Methods 0.000 description 1
- 102000003298 tumor necrosis factor receptor Human genes 0.000 description 1
- 230000002792 vascular Effects 0.000 description 1
- 230000035899 viability Effects 0.000 description 1
Images
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K35/00—Medicinal preparations containing materials or reaction products thereof with undetermined constitution
- A61K35/12—Materials from mammals; Compositions comprising non-specified tissues or cells; Compositions comprising non-embryonic stem cells; Genetically modified cells
- A61K35/37—Digestive system
- A61K35/407—Liver; Hepatocytes
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/1703—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans from vertebrates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/177—Receptors; Cell surface antigens; Cell surface determinants
- A61K38/1793—Receptors; Cell surface antigens; Cell surface determinants for cytokines; for lymphokines; for interferons
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1833—Hepatocyte growth factor; Scatter factor; Tumor cytotoxic factor II
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1858—Platelet-derived growth factor [PDGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/18—Growth factors; Growth regulators
- A61K38/1858—Platelet-derived growth factor [PDGF]
- A61K38/1866—Vascular endothelial growth factor [VEGF]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/204—IL-6
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/19—Cytokines; Lymphokines; Interferons
- A61K38/20—Interleukins [IL]
- A61K38/2053—IL-8
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/16—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- A61K38/17—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- A61K38/22—Hormones
- A61K38/30—Insulin-like growth factors, i.e. somatomedins, e.g. IGF-1, IGF-2
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P39/00—General protective or antinoxious agents
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/0018—Culture media for cell or tissue culture
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/067—Hepatocytes
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/067—Hepatocytes
- C12N5/0672—Stem cells; Progenitor cells; Precursor cells; Oval cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/05—Inorganic components
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/32—Amino acids
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/30—Organic components
- C12N2500/38—Vitamins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/70—Undefined extracts
- C12N2500/80—Undefined extracts from animals
- C12N2500/84—Undefined extracts from animals from mammals
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/11—Epidermal growth factor [EGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/115—Basic fibroblast growth factor (bFGF, FGF-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/998—Proteins not provided for elsewhere
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Chemical & Material Sciences (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- General Health & Medical Sciences (AREA)
- Gastroenterology & Hepatology (AREA)
- Medicinal Chemistry (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Immunology (AREA)
- Epidemiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Biomedical Technology (AREA)
- Biotechnology (AREA)
- Organic Chemistry (AREA)
- Wood Science & Technology (AREA)
- Genetics & Genomics (AREA)
- Cell Biology (AREA)
- Biochemistry (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Developmental Biology & Embryology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Virology (AREA)
- Physiology (AREA)
- Nutrition Science (AREA)
- Marine Sciences & Fisheries (AREA)
- Vascular Medicine (AREA)
- Diabetes (AREA)
- Molecular Biology (AREA)
- Endocrinology (AREA)
- Toxicology (AREA)
- Urology & Nephrology (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
Abstract
meio condicionado de células progenitoras de fígado. o presente invento está no campo da medicina regenerativa. foi descoberto que o meio condicionado de células progenitoras pluripotentes do fígado não ovais exerce um efeito regenerador de tecido. uma preparação do meio condicionado livre de células é portanto útil no tratamento de ferimentos e falha do órgão, preferencialmente do fígado, e/ou ferimento ou falha.
Description
O presente invento pertence ao campo das preparações farmacêuticas biológicas e medicina regenerativa.
Os preparados de células tronco mostraram exercer um efeito regenerativo em tecidos humanos ou animais. Testes clínicos testando a eficácia de suporte de fígado bio-artificial no tratamento de falha hepática fulminante (FHF) produziram alguns resultados promissores, ainda que a geração atual de dispositivos não tenha demonstrado confiabilidade e eficácia suficientes para uso rotineiro, primeiramente devido à falta de uma fonte de hepatócitos humanos funcionalmente estável (Kobayashi N, Okitsu T, Tanaka N. Cell choice for bioartificial livers. Keio J Med. 2003;52(3):151-7). As células tronco do fígado, ou mesmo células tronco derivadas de outros tecidos, poderiam potencialmente prover uma fonte alternativa de hepatócitos humanos. Em adição à medula óssea, as células tronco residem em tecidos adultos tais como fígado e sistema nervoso central, e tem uma plasticidade muito maior que aquela conhecida anteriormente.
As células tronco/progenitoras pluripotentes do fígado humano descritas no pedido de patente internacional WO2006/126236 mostraram sofrer diferenciação numa variedade de tipos de células de tecidos e exercer efeitos de regeneração de órgãos. Estas células são derivadas de uma linhagem celular progenitora pluripotente de fígado humano não oval que expressa marcadores de células hepáticas.
O pedido de patente internacional WO2006/126236 também descreve um método para isolar as células tronco/progenitoras pluripotentes de fígado humano mencionadas acima, capazes de sofrer diferenciação numa variedade de tipos de células, o método compreendendo as etapas de: (i) cultivar hepatócitos humanos maduros derivados de fígado adulto num meio de cultura celular até a morte dos hepatócitos maduros e seleção de uma população de células sobreviventes tendo morfologia epitelioide; (ii) expandir a população de células sobreviventes tendo morfologia epitelióide por cultura num meio de cultura contendo soro e glicose suplementado com hEGF (fator de crescimento epitelial humano) e bFGF (fator de crescimento de fibroblasto básico) e compreendendo os usuais sais inorgânicos, aminoácidos e vitaminas necessários para o crescimento de células de mamíferos e em particular em que os hepatócitos maduros são congelados em um meio de cultura contendo soro na presença de um agente crio-protetor e então descongelados antes da cultura de acordo com a etapa (i).
As células progenitoras pluripotentes humanas do pedido de patente internacional WO2006/126236 (designadas como HLSCs na descrição da patente) e o método de sua preparação são completamente incorporados aqui por referência.
Preparações de células tronco mesenquimais (MSCs) mostraram exercer um efeito regenerativo em tecidos. Por exemplo, sabe-se que as células tronco mesenquimais naturalmente suportam a hematopoiese secretando várias moléculas tróficas, incluindo glicoproteínas de matriz extracelular solúveis, citocinas e fatores de crescimento.
Entretanto, as preparações de células troncas têm a desvantagem principal de causar reações imunes quando administradas. Algumas preparações de células troncas têm até o potencial de causar câncer.
Parekkadan et al. (Parekkadan B, van Poll D, Suganuma K, Carter EA, Berthiaume F, Tilles AW, Yarmush ML. Mesenchymal stem cell-derived molecules reverse fulminant hepatic failure. PLoS ONE. 2007 Sep 26;2(9):e941) avaliaram primeiro vários tratamentos com MSC, tais como a entrega de um meio condicionado (CM), para testar a eficácia em um modelo de ratos de dano grave induzido no fígado. Nesta publicação, foram administradas intraperitonealmente aos ratos um total de duas injeções de D-galactosamina (GalN). Num segundo estudo (Van Poll D, Parekkadan B, Cho CH, Berthiaume F, Nahmias Y, Tilles AW, Yarmush ML. Mesenchymal stem cell-derived molecules directly modulate hepatocellular death and regeneration in vitro and in vivo. Hepatology. 2008 Jan 24;47(5):1634-1643) o grupo de Parekkadan investigou se a infusão sistêmica de MSC-CM poderia levar a uma resposta hepatoprotetora no fígado agudamente ferido, especificamente inibindo a morte celular e estimulando programas reparativos. Este grupo usou um regime sub-letal de indução D- galactosamina, demonstrando um beneficio de sobrevivência significativo e prevenção de liberação de enzima no fígado após o tratamento MSC-CM.
Em vista das desvantagens mencionadas acima dos tratamentos com células tronco, o fato de os preparados altamente eficientes no campo da medicina regenerativa usualmente conterem células é um problema técnico que deve ser superado.
Assim, o objetivo do presente invento é o de prover uma preparação que seja efetiva como uma composição farmacêutica no campo da medicina regenerativa mas que não contenha células, evitando com isso as desvantagens causadas pelas preparações do estado da técnica que contêm células, particularmente células tronco.
Um outro objetivo do presente invento é prover um método para preparar uma composição farmacêutica que seja efetiva no campo da medicina regenerativa mas que não contenha células, evitando com isso as desvantagens causadas pelas preparações do estado da técnica que contêm células, particularmente células tronco.
Estes e outros objetivos são alcançados pelas preparações e pelo método como definido nas reivindicações independentes. As reivindicações dependentes se referem a formas de realização preferidas do presente invento. A matéria objeto de ambas reivindicações dependentes e independentes forma uma parte integral da descrição.
Usando um modelo de camundongo de falha hepática fulminante (FHF), o meio condicionado livre de células (CM livre de células) produzido pela cultura de uma linhagem de células progenitoras do fígado, tais como p.ex. a linhagem de células progenitoras pluripotentes de fígado humano não ovais descrita no pedido de patente internacional WO2006/126236, foi mostrado pelos inventores exercer um efeito regenerativo sobre o fígado. O meio condicionado livre de células (CM livre de células) produzido pela cultura da linhagem de células progenitoras do fígado mostrou ser efetivo na terapia de falha do órgão, em particular na terapia de falha do fígado e rins. Surpreendentemente, também foi verificado que um CM de linhagem de células progenitoras do fígado é significativamente mais efetivo que um CM de células tronco mesenquimais preparado sob as mesmas condições.
Em particular, nos estudos descritos no exemplo 1 da presente descrição, camundongos SCID machos de 6 a 7 semanas de idade receberam uma injeção intraperitoneal de 500 μL de tampão salino contendo 0,125 μg de LPS e 18 mg de D-galactosamina (GalN) para induzir FHF. 30 minutos, 1 hora e 3 horas após a administração de LPS e GalN, os camundongos foram injetados intraperitonealmente com 3 mL de meio condicionado derivado de HLSCs cultivadas em um bio-reator rotatório. A análise preliminar do meio condicionado revelou uma grande fração de citocinas, quimiocinas e fatores de crescimento. Os níveis de soro de transaminase alanina e transaminase aspartato aumentaram notavelmente após a indução do dano e diminuíram significativamente após 6 dias da injeção com o tratamento de meio condicionado. Por um lado, a análise histopatológica do tecido do fígado avaliada por ensaios BrdU, PCNA e Túnel revelou um índice diminuído de apoptose e necrose e uma recuperação da morfologia do tecido.
Estes estudos proveram a primeira evidência experimental de uso terapêutico potencial de meio condicionado derivado de HLSCs no tratamento de condições inflamatórias e regeneração de órgãos.
Assim, um primeiro aspecto do presente invento é um preparado consistindo de um meio condicionado livre de células obtido pela cultura de uma linhagem de células progenitoras do fígado, preferencialmente uma linhagem de células progenitoras pluripotentes de fígado humano não ovais, mais preferencialmente a linhagem de células progenitoras pluripotentes de fígado humano não ovais descrita no pedido de patente internacional WO2006/126236, que é aqui incorporada por referência.
Uma composição farmacêutica compreendendo uma quantidade efetiva da preparação definida acima também cai dentro do escopo do presente invento.
A seguir, o meio condicionado livre de células derivado de uma linhagem de células progenitoras do fígado que forma o objetivo do presente invento deve ser chamado de "CM-HLSC livre de células"
O termo "HLSC" se refere a uma linhagem de células progenitoras/tronco pluripotentes de fígado. Preferencialmente, o termo "HLSC" se refere a uma linhagem de células pluripotentes de fígado não ovais, mais preferencialmente à linhagem de células progenitoras pluripotentes de fígado humano não ovais descrita no pedido de patente internacional WO2006/126236. Mais preferencialmente, a linhagem de células HLSC tem as características definidas em qualquer uma das reivindicações de 1 a 10 de WO2006/126236 e/ou as características resumidas na Tabela I, página 7, do pedido de patente internacional WO2006/126236. Tais características são aqui incorporadas por referência.
O CM-HLSC livre de células que forma a matéria-objeto do presente invento é adequado para uso como uma composição farmacêutica como tal ou numa forma concentrada. Uma forma concentrada é concentrada por exemplo pelo menos 5 vezes, preferencialmente pelo menos aproximadamente 10 vezes, mais preferencialmente pelo menos aproximadamente 20 vezes, ainda mais preferencialmente aproximadamente 25 vezes.
Preferencialmente o CM-HLSC livre de células do presente invento é obtido a partir de células progenitoras/tronco pluripotentes de fígado, preferencialmente a linhagem de células HLSC descrita no pedido de patente internacional WO2006/126236, cultivadas sob condições GMP (boas práticas de fabricação), que são conhecidas dos técnicos da área. Alternativamente, ele pode ser obtido a partir de células progenitoras/tronco pluripotentes de fígado, preferencialmente a linhagem de células HLSC descrita no pedido de patente internacional WO2006/126236, cultivadas num sistema BAL (fígado bio-artificial), que também é conhecido dos técnicos da área.
Um exemplo de condições GMP para crescimento de células progenitoras/tronco pluripotentes de fígado e coletar o seu meio condicionado livre de células (CM) é como segue.
As células progenitoras/tronco pluripotentes do fígado são isoladas por um método descrito no pedido de patente internacional WO2006/126236, em que a etapa de expansão é executada cultivando-se as células tronco progenitoras na presença de soro fetal bovino (FCS) preferencialmente numa concentração de cerca de 10%, hEGF (fator de crescimento epitelial humano) e bFGF (fator de crescimento de fibroblasto básico). O FCS, bFGF e hEGF têm preferencialmente o grau GMP, p.ex. aquele produzido por Invitrogen.
Para coletar o meio condicionado nas condições GMP, o FCS é removido da cultura uma vez que esta é uma proteína heteróloga que não é adequada para injeção em humanos. Para isto, as células são lavadas e cultivadas por 24 horas num meio de coleta compreendendo por exemplo a-MEM suplementado com albumina humana grau GMP. A albumina está preferencialmente numa concentração de 0,05%. O meio condicionado livre de células é então coletado por centrifugação ou filtração.
No experimento in vivo mencionado acima, a administração do CM-HLSC livre de células do presente invento a um modelo animal (camundongo SCID) de falha hepática fulminante (FHF) mostrou prover um benefício de sobrevida significativo sobre camundongos SCID tratados com CM-MSC.
Assim, um outro aspecto do presente invento é um meio de cultura celular condicionado livre de células obtido ao cultivar uma linhagem de células progenitoras de fígado, preferencialmente uma linhagem de células progenitoras pluripotentes de fígado humano não ovais, ainda mais preferencialmente a linhagem de células progenitoras pluripotentes de fígado humano não ovais descrita no pedido de patente internacional WO2006/126236, para uso como um medicamento.
De acordo com uma forma preferida de realização, o medicamento é para o tratamento de uma falha de órgão e/ou ferimento, preferencialmente falha de fígado e/ou rins e/ou ferimento.
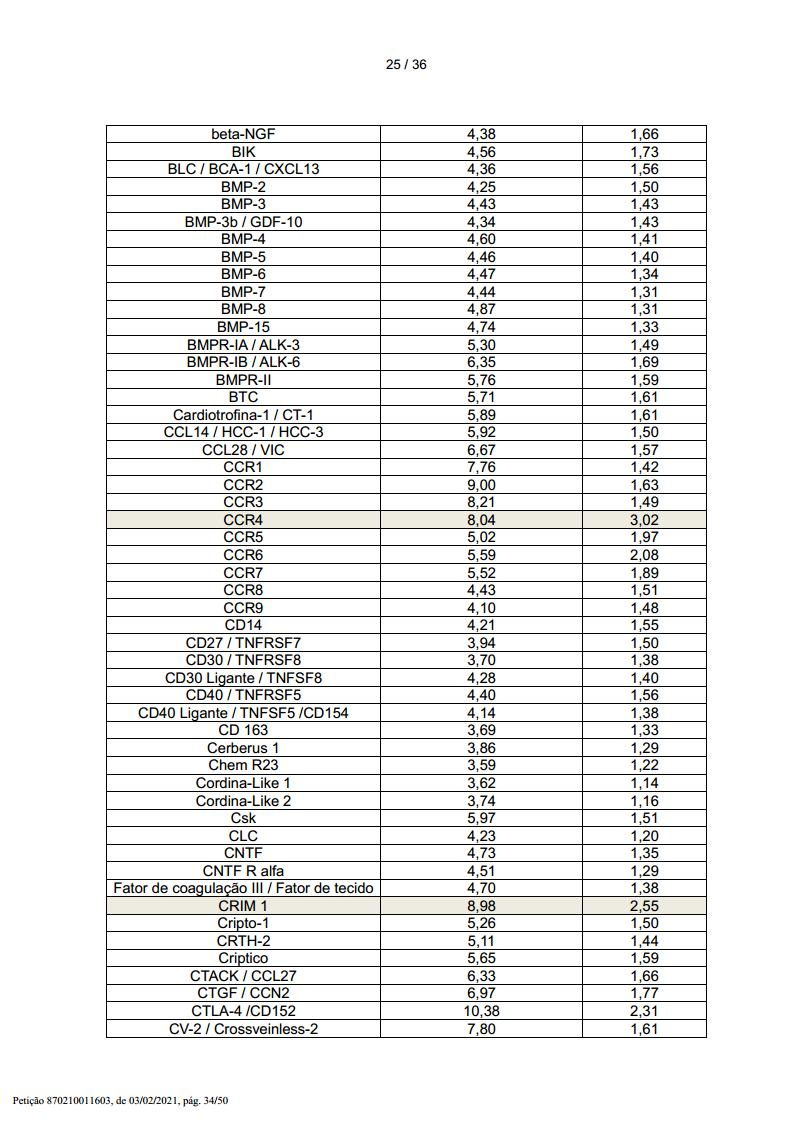
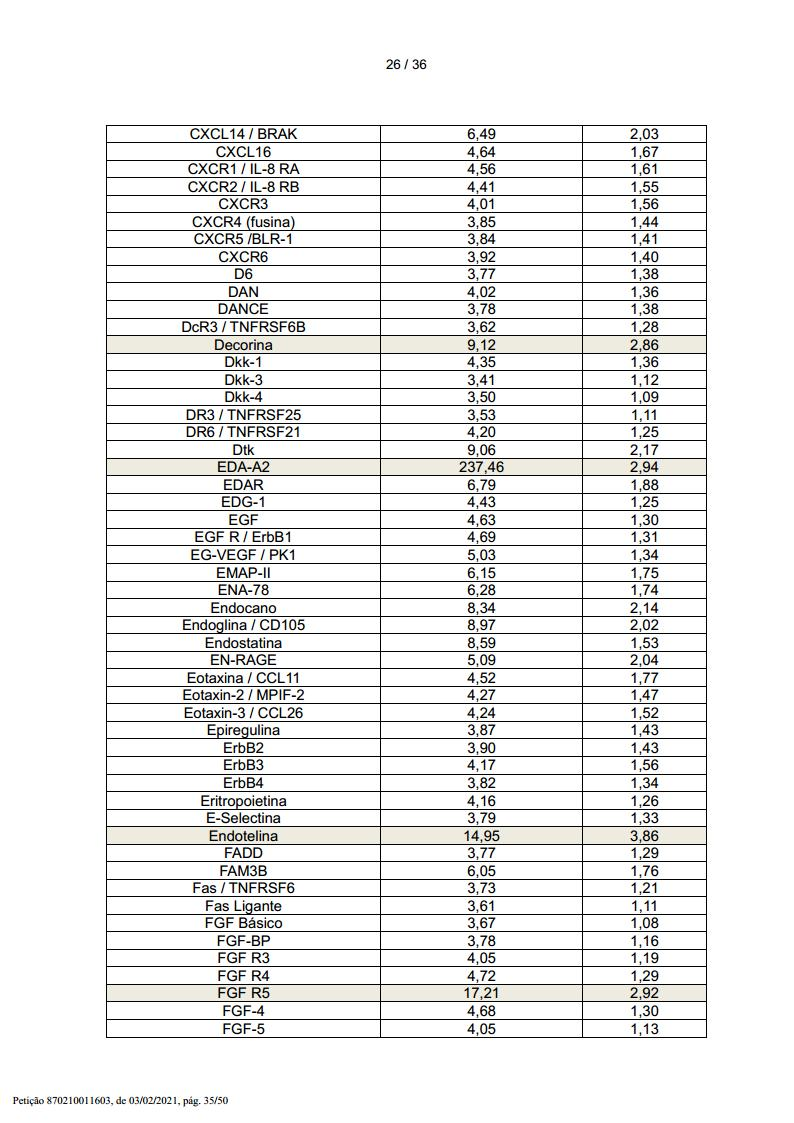
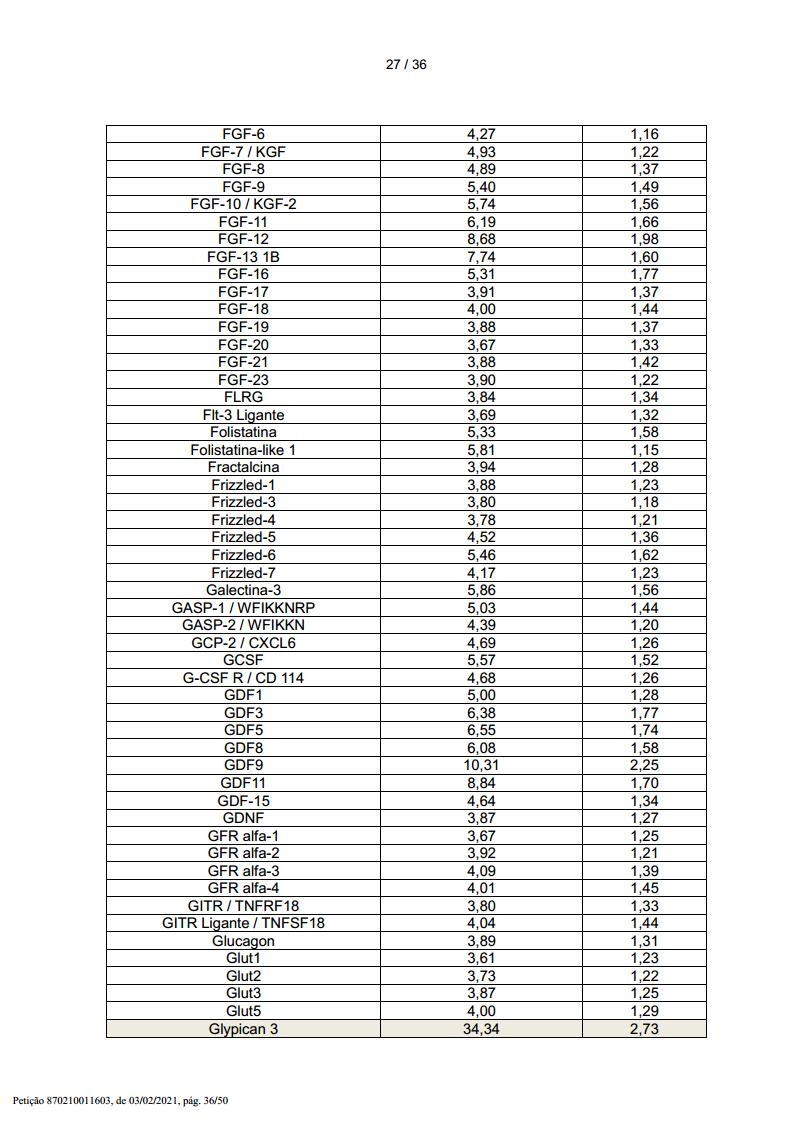
Em adição, os inventores analisaram a composição do CM- HLSC livre de células do presente invento, a fim de identificar aquelas proteínas (p.ex. citocinas, quimiocinas, fatores de crescimento e/ou outras proteínas), que são mais prováveis de prover uma contribuição significativa aos efeitos benéficos do CM mencionado acima, para prover composições farmacêuticas simplificadas compreendendo uma mistura de proteínas capaz de mimetizar, ao menos em parte, as capacidades regeneradoras de órgão do CM produzido pela cultura das HLSCs descrita acima.
Assim, um outro aspecto do presente invento é uma composição farmacêutica simplificada compreendendo uma quantidade farmaceuticamente efetiva de uma mistura de pelo menos um fator de crescimento de hepatócito (HGF), interleucina 6 (IL-6) e interleucina 8 (IL-8).
Numa forma preferida de realização, a composição farmacêutica simplificada compreende uma quantidade farmaceuticamente efetiva de uma mistura de pelo menos um fator de crescimento de hepatócito (HGF), interleucina 6 (IL-6), interleucina 8 (IL-8) e fator de crescimento endotelial vascular (VEGF).
Numa outra forma preferida de realização, a composição farmacêutica simplificada compreende uma quantidade farmaceuticamente efetiva de uma mistura de pelo menos fator de crescimento de hepatócito (HGF), interleucina 6 (IL- 6), interleucina 8 (IL-8) e proteína estimulante de macrófago (MSP) e opcionalmente fator de crescimento endotelial vascular (VEGF).
Numa outra forma de realização preferida, a composição farmacêutica simplificada compreende uma quantidade farmaceuticamente efetiva de uma mistura de proteínas de acordo com qualquer uma das formas de realização definidas acima e pelo menos uma proteína adicional escolhida dentre o grupo que consiste de Activina C, molécula de adesão celular ativada por leucócito (ALCAM), quimiocina (motivo C-C) receptor 4 (CCR4), regulador 1 (similar a cordina) BMP transmembrana rico em cisteína (CRIM), decorina, ectodisplasina A2 (EDA-A2), endotelina, fator de crescimento de fibroblasto 1 similar a receptor (FGF R5), glipicano 3, oncoproteína relacionada ao crescimento (GRO), proteína de ligação 6 de fator de crescimento similar a insulina (IGFBP-6), fator de crescimento similar a insulina 1 (IGF-1), receptor interleucina 20, alfa (IL-20 R alfa), Kremen-2, proteína de ligação 1 do fator de crescimento de transformação beta latente, proteína principal intrínseca de fibra de lentes (MIP-2), cadeia beta MSP, oesteoprotegerina / TNFRSF11B (membro 11b da superfamília de receptores do fator de necrose de tumor), gp130 solúvel (sgp130), proteína secretada, acídica, rica em cisteína (osteonectina) (SPARC).
A concentração preferida de citocina varia na composição farmacêutica simplificada como segue: - HGF: de 1 a 100 ng/mL, preferencialmente de 5 a 80 ng/mL, mais preferencialmente de 10 a 65 ng/mL; - IL-6: de 10 a 200 ng/mL, preferencialmente de 20 a 100 ng/mL, mais preferencialmente de 30 a 50 ng/mL; - IL-8: > 35 ng/mL, preferencialmente de 50 a 600 ng/mL, mais preferencialmente de 100 a 300 ng/mL; - VEGF (se presente): de 10 a 400 ng/mL, preferencialmente de 20 a 250 ng/mL, mais preferencialmente de 35 a 175 ng/mL; e - MSP (se presente): de 1 a 100 pg/mL, preferencialmente de 5 a 80 pg/mL, mais preferencialmente de 5 a 65 pg/mL.
Entretanto, o escopo do presente invento também inclui qualquer forma diluída ou concentrada da composição farmacêutica simplificada. Uma forma concentrada é concentrada, por exemplo, em aproximadamente 5 vezes, preferencialmente pelo menos aproximadamente 10 vezes, mais preferencialmente pelo menos aproximadamente 20 vezes, ainda mais preferencialmente aproximadamente 25 vezes. Uma forma diluída é diluída, por exemplo, pelo menos aproximadamente 5 vezes, preferencialmente pelo menos aproximadamente 10 vezes, mais preferencialmente pelo menos aproximadamente 20 vezes, ainda mais preferencialmente aproximadamente 25.
A composição farmacêutica simplificada do presente invento é adequada para uso como um medicamento, particularmente para o tratamento de falha e/ou ferimento em órgão, preferencialmente falha e/ou ferimento no fígado e/ou rins. De acordo com uma forma preferida de realização, a composição farmacêutica é formulada para administrar as seguintes doses de citocina: - HGF: de 0,01 a 1 mg/kg, preferencialmente de 0,03 a 0,8 mg/kg, mais preferencialmente de 0,05 a 0,5 mg/kg; - interleucina 6 (IL-6): de 0,01 a 1 mg/kg, preferencialmente de 0,03 a 0,8 mg/kg, mais preferencialmente de 0,05 a 0,5 mg/kg; - interleucina 8 (IL-8): de 0,01 a 1 mg/kg, preferencialmente de 0,02 a 0,8 mg/kg, mais preferencialmente de 0,03 a 0,5 mg/kg; - VEGF (se presente): de 0,01 a 1 mg/kg, preferencialmente de 0,02 a 0,8 mg/kg, mais preferencialmente de 0,04 a 0,5 mg/kg; - MSP (se presente): de 0,01 a 1 mg/kg, preferencialmente de 0,02 a 0,8 mg/kg, mais preferencialmente de 0,08 a 0,5 mg/kg. Numa forma de realização particularmente preferida, estas doses de citocina são administradas uma vez ao dia.
Deve ser entendido que as composições farmacêuticas simplificadas definidas acima são providas puramente como exemplos não limitativos de composições farmacêuticas simplificadas capazes de mimetizar, pelo menos em parte, as capacidades de regeneração de órgãos de um CM obtenível pela cultura de HLSCs como descrito acima.
Objetivos adicionais e vantagens do presente invento aparecerão mais claramente a partir dos exemplos a seguir, que são providos puramente a título de ilustração.
Também deve ser entendido que formas de realização adicionais das composições farmacêuticas reivindicadas e métodos podem ser previstas com base nos exemplos providos aqui a seguir, sem com isso fugir ao escopo do presente invento.
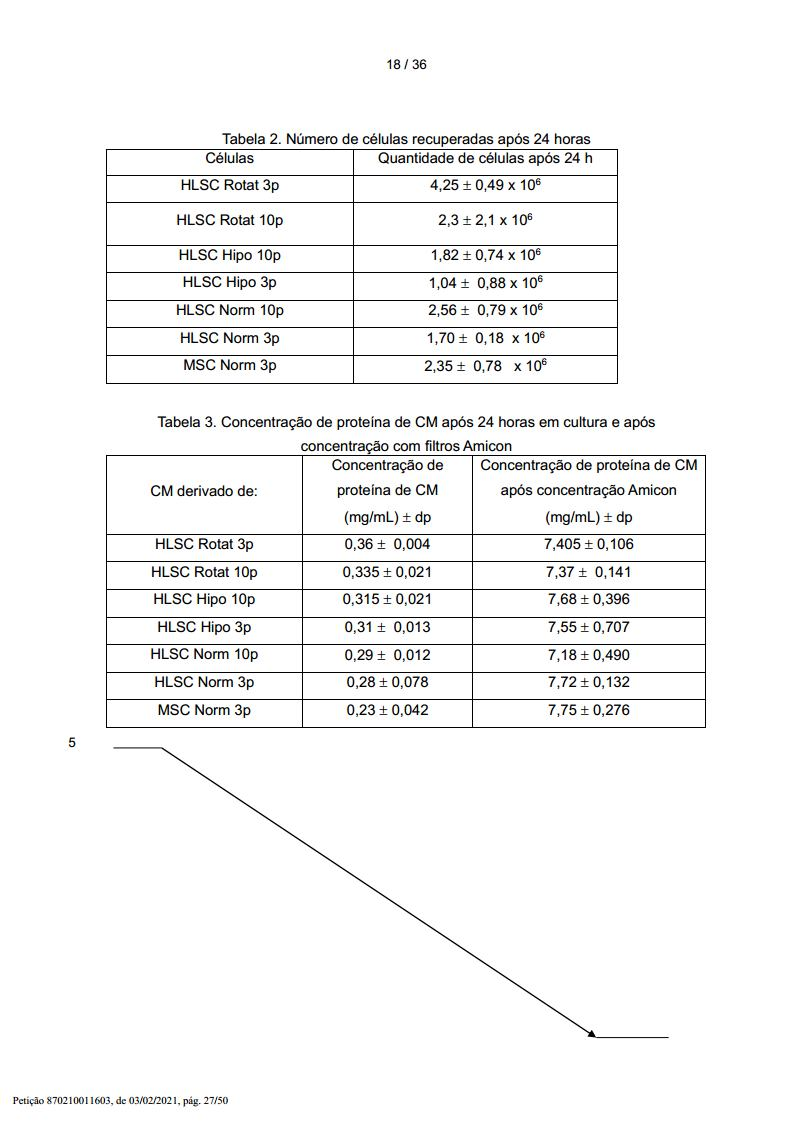
Preparação das culturas de células HLSC e MSC Células progenitoras de fígado humano (HLSCs) foram isoladas como descrito no pedido de patente internacional WO2006/126236. As células foram deixadas a crescer a de 60 a 70% de confluência (aproximadamente 2 x 106
HLSCs por frasco de 75 cm2), lavadas cuidadosamente, e cultivadas em 10 mL de meio alfa-MEM (meio mínimo essencial alfa) livre de soro suplementado com 0,05% de albumina de soro humano (produzida em grau GMP). As células tronco mesenquimais humanas (MSCs) fora isoladas a partir de aspirados de medula óssea e cresceram e foram caracterizadas como previamente relatado. As MSCs foram cultivadas em meio MesenPRO RSTM que é um meio de soro reduzido (2% FCS) especificamente formulado para suportar o crescimento de MSCs. Preparação do meio condicionado
O meio condicionado livre de células foi preparado coletando-se o meio após 24 horas de cultura de MSCs e HLSCs por centrifugação. Os experimentos foram realizados com uma massa celular de 2 x 106 células. O meio foi então concentrado, aproximadamente 25 vezes, usando unidades de ultrafiltração (Amicon Ultra-PL 3, Millipore) com um corte de peso molecular de 3 kDa. Foi obtido um total de 250 μL de meio condicionado. O meio concentrado foi diluído em 3 mL de a-MEM (sem FCS) até um volume final de 3 mL. 1 mL de meio condicionado foi administrado intraperitonealmente 30 minutos, 1 hora e 3 horas após a indução de dano ao fígado.
Para indução de falha hepática fulminante (FHF), a toxicidade letal de lipopolisacarídeo (LPS) em animais em tratamento com D- galactosamina (2-amino-2-desoxi-D-galactose) foi desenvolvida como descrito previamente (Lehmann V, Freudenberg MA, Galanos C. Lethal toxicity of lipopolysaccharide and tumor necrosis factor in normal and D-galactosamine-treated mice. J Exp Med. 1987;165(3):657-63). Brevemente, um grupo de 10 camundongos SCID recebeu uma injeção intraperitoneal de D-galactosamina (GalN) (600 mg/kg) e 0,125 μg de LPS por animal. Os inventores determinaram previamente que 100% de letalidade foram induzidos em camundongos tratados com GalN (600 mg/kg) e LPS (0,125 μg por animal) dentro de 8 horas. GalN e LPS foram administrados como uma mistura em 500 μL de solução NaCl livre de pirogênio. As mortes foram registradas até 24 horas após a injeção. A 30 minutos, 1 hora e 3 horas após a injeção de LPS e GalN, os camundongos foram injetados intraperitonealmente três vezes com 1 mL de meio condicionado concentrado de HLSC e MSC. Como mostrado na figura 1, quatro dentre 5 ratos injetados com o CM derivado de HLSC sobreviveram, enquanto nenhum dos ratos tratados com o CM derivado de MSC sobreviveu.
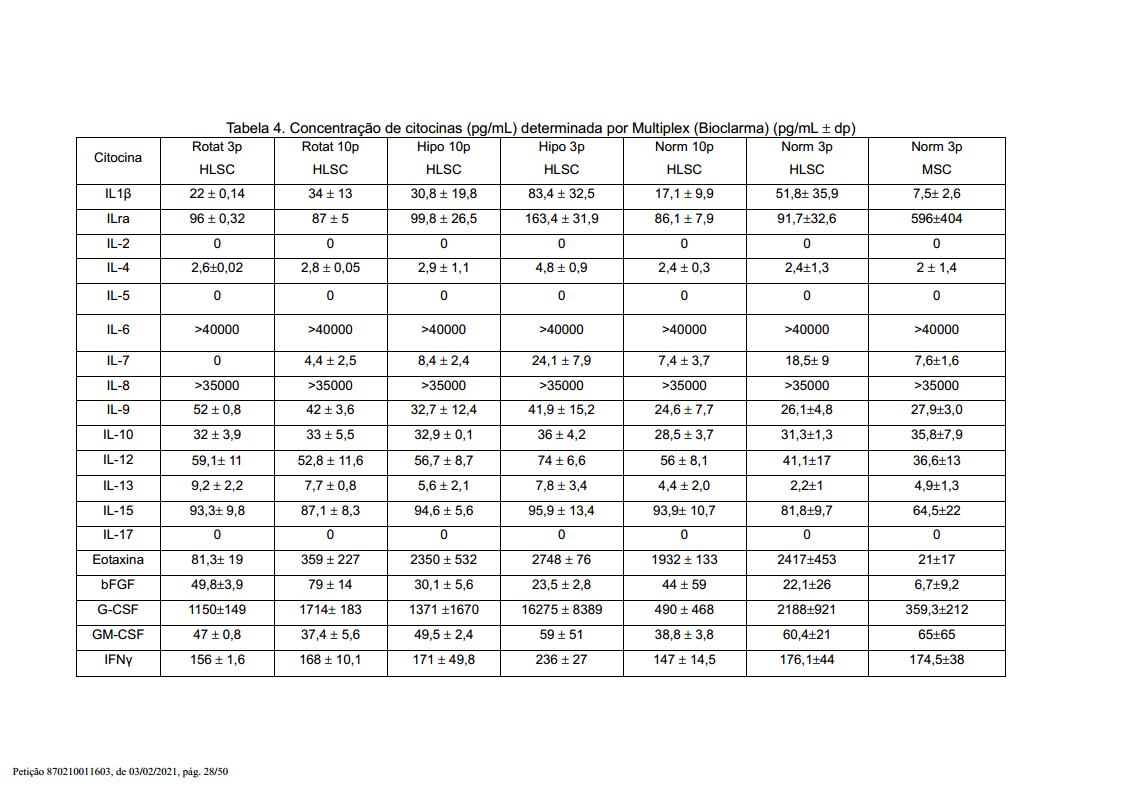
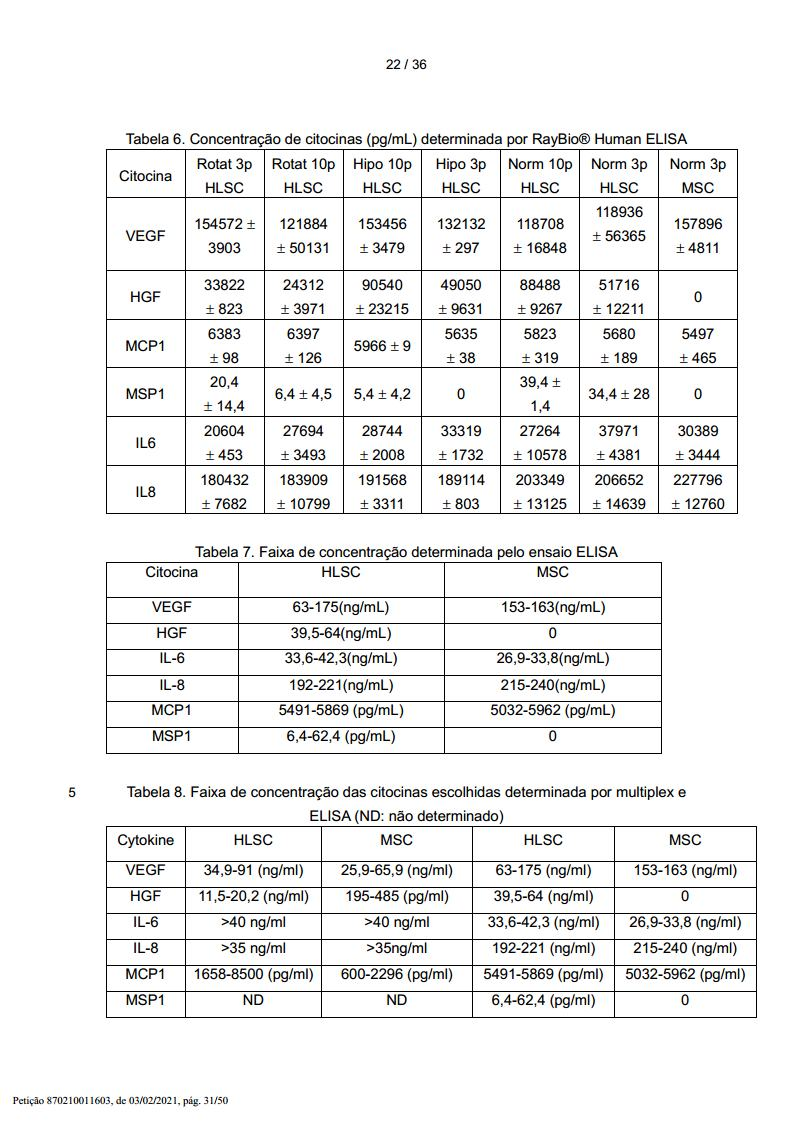
Composição de citocinas de meio condicionado HLSC e MSC
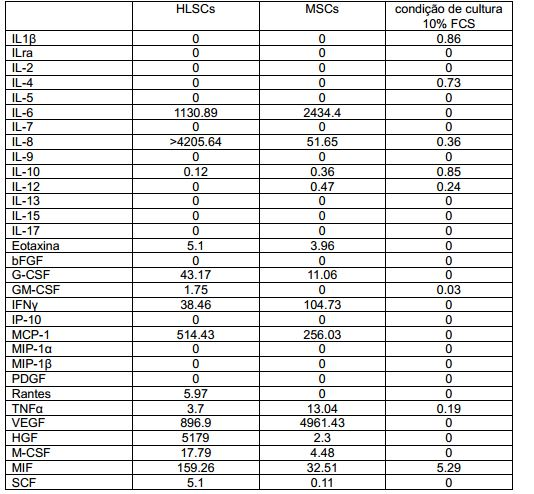
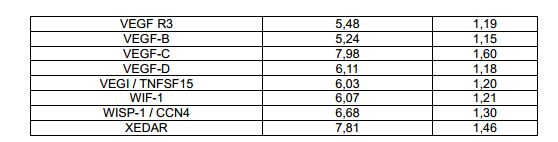
Para estudar a composição do meio condicionado obtido pela cultura de HLSCs e MSCs como descrito acima, um painel de 31 citocinas diferentes foi medido por múltiplos testes ELISA (Bioclarma). Ambos tipos de células foram cultivados em um meio com 10% de FCS. Os meios condicionados foram coletados após 24 horas de cultura. A composição de citocinas do meio sozinho também foi medida. Os resultados são providos abaixo na Tabela 1.
Tabela 1. HLSCs vs. MSCs: Produção de citocinas* HLSCs MSCs condição de cultura 10% FCS administrada em 30 minutos, 1 hora e 3 horas após a indução de FHF por injeção de D-GalN/LPS. Doze camundongos SCID foram tratados no total. 2) O segundo protocolo experimental consistiu na injeção de uma mistura de citocinas. Um total de 10 camundongos SCID foram injetados com a seguinte mistura de citocina recombinante. HGF: 870,75 ng/mL x 30 mL de alfa-MEM (injeções i.v.) = 26 μg. IL-6: 340,5 ng/mL x 30 (injeções i.v.) = 10,4 μg. IL-8: 261 ng/mL x 30 (injeções i.v.) = 8 μg. VEGF: 202 ng/mL x 30 (injeções i.v.) = 6 μg. 30 mL desta mistura foram preparados a fim de ter 3 mL de mistura para um total de 10 camundongos SCID. Cada camundongo SCID foi injetado com 1 mL desta mistura de citocinas em 30 minutos, 1 hora e 3 horas após a injeção intraperitoneal de GALN/LPS. Cada camundongo SCID recebeu: [HGF]: 2,59 μg, [IL-6]: 1,02 μg, [IL-8]: 0,79 μg, [VEGF]: 0,6 μg. Esta mistura foi designada como MIX 4. 3) O terceiro protocolo experimental consistiu na injeção do MIX 4 mais MSP-1. Um total de 5 camundongos SCID foram injetados. Cada camundongo SCID recebeu: [HGF]: 2,59 μg, [IL-6]: 1,02 μg, [IL-8]: 0,79 μg, [VEGF]: 0,6 μg (que são as concentrações de citocinas obtidas dos experimentos BAL) mais [MSP-1]: 2 μg. 4) O quarto protocolo experimental consistiu na injeção de CM-MSC ou CM-HLSC. A fim de obter CM-MSCs, as MSCs foram deixadas a crescer até 90% de confluência (aproximadamente 2 x 106 MSCs por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de MesenPRO RSTM, um meio de cultura com 2% de FCS. O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA), com um corte de 3 kDa. Para produzir CM-HLSCs, as HLSCs foram deixadas a crescer até de 60 a 70% de confluência (aproximadamente 2 x 106 HLSC por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de meio alfa-MEM livre de soro suplementado com 0,05% de albumina de soro humano (produzida em grau GMP). O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA) com um corte de 3 kDa.
O peso médio dos camundongos SCID usados nestes experimentos foi de cerca de 25 g.
Modelo FHF in vivo. Para indução de FHF, a toxicidade letal de lipopolisacarídeo (LPS) nos animais em tratamento com D-galactosamina (2-amino-2-desoxi-D-galactose) foi desenvolvida como previamente descrito (Lehmann V, Freudenberg MA, Galanos C. Lethal toxicity of lipopolysaccharide and tumor necrosis factor in normal and D- galactosamine-treated mice. J Exp Med. 1987;165(3):657-63). Brevemente, os camundongos SCID receberam uma injeção intraperitoneal de D-galactosamina (GalN) (600 mg/kg, 18 mg por animal) e 0,125 μg de LPS por animal. Os inventores determinaram previamente que 100% de letalidade foram induzidos em camundongos tratados com GalN (600 mg/kg) e LPS (0,125 μg por animal) dentro de 8 horas. GalN e LPS foram administrados como uma mistura de 500 μL de solução NaCl livre de pirogênio. As mortes foram registradas até 24 horas após a injeção. A 30 minutos, 1 hora e 3 horas após a injeção de LPS e GalN, os camundongos foram injetados intraperitonealmente com 1 mL de meio condicionado HLSC, meio condicionado MSC ou mistura de citocinas.
Cultura de células. As células tronco mesenquimais humanas (MSCs) foram isoladas de aspirados de medula óssea e cresceram e foram caracterizadas como relatado anteriormente. As MSCs foram cultivadas em meio MesenPRO RSTM que é um meio de soro reduzido (2% de FCS) especificamente formulado para suportar o crescimento de MSC. As células foram usadas para experimentos durante as passagens de 3 a 5.
Preparação do meio condicionado (CM) de MSCs. As MSCs humanas foram cultivadas e caracterizadas para expressão de marcador de superfície e capacidade de diferenciação adipogênica e osteogênica como previamente descrito. Para obter o CM- MSCs, as células foram deixadas a crescer até 90% de confluência (aproximadamente 2 x 106 MSCs por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de MesenPRO RSTM, um meio de cultura com 2% de FCS. O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA) com um corte de 3 kDa.
Preparação de CM-HLSCs. As HLSCs foram obtidas a partir de hepatócitos humanos congelados. As HLSCs humanas foram cultivadas e caracterizadas para expressão de marcador de superfície e capacidade de diferenciação como previamente descrito. Para obter o CM-HLSCs, as células foram deixadas a crescer até de 60 a 70% de confluência (aproximadamente 2 x 106 MSCs por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de meio alfa-MEM livre de soro suplementado com 0,05% de albumina de soro humano (produzida em grau GMP). O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA) com um corte de 3 kDa.
Concentração do meio condicionado. Os sobrenadantes foram coletados a partir do frasco T após 24 horas de cultura. O sobrenadante foi então concentrado, aproximadamente 25 vezes, usando unidades de ultrafiltração com um corte de peso molecular de 3 kDa de Millipore.
Análise histológica. A necrose do fígado foi analisada através de manchamento H&E (manchamento com hematoxilina e eosina), proliferação (manchamento PCNA) e TUNEL (células apoptóticas).
Análise bioquímica. Os níveis de transaminase alanina (ALT) e transaminase aspartato (AST) no soro foram medidos usando um analisador automático clínico padrão.
Western Blot. O ensaio Western Blot foi realizado para a detecção de BAX e BclXS/L. Os fígados foram homogeneizados e lisados a 4oC por 1 hora em tampão de lise (50 mmol/L Tris-HCl, pH 8,3, 1% de Triton X-100, 10 μmol/L de fluoreto de fenilmetil sulfonila, 10 μmol/L de leupeptina e 100 U/mL de aprotinina) e centrifugado a 15000 g. Os teores de proteínas dos sobrenadantes foram medidos pelo método Bradford. Alíquotas contendo 200 μg de proteínas de lisados de fígados foram submetidas à eletroforese em gel de dodecilsulfato-poliacrilamida sob condições redutoras e eletro-manchados em filtros de membrana de nitrocelulose. As manchas foram bloqueadas com 5% de leite desnatado em 20 mmol/L de Tris-HCL, pH 7,5, 500 mmol/L de NaCl mais 0,1% de Tween (TBS-T). A membranas foram subseqüentemente imunomanchadas de um dia para o outro a 4oC com os relevantes anticorpos primários na concentração apropriada. Após lavagens extensivas com TBS-T, as manchas foram incubadas por 1 hora à temperatura ambiente com anticorpos secundários específicos a isotipo conjugado com peroxidase, lavados com TBS-T, desenvolvidos com reagentes de detecção ECL por 1 minutos e expostos a filme X-Omat. Os seguintes anticorpos foram usados: anticorpo monoclonal anti-BAX e anticorpo policlonal BclXS/L de Santa Cruz Biotechnology.
Os resultados obtidos são ilustrados nas figuras de 2 a 4.
A figura 2 mostra a taxa de sobrevivência (%) de camundongos SCID feridos com GalN/LPS tratados com CM-HLSC (n = 22; 73% de sobrevivência), CM-MSC (n = 5; 0% de sobrevivência) ou com uma mistura de citocinas (citocinas: VEGF, IL6, IL8, HGF; n = 10; 40% de sobrevivência), e a mistura de citocinas mais MSP-1 (citocinas: VEGF, IL6, IL8, HGF + MSP-1; n = 5, 100% de sobrevivência).
A figura 3 mostra os níveis de aminotransferase aspartato (AST) e aminotransferase alanina (ALT) no soro de controle, camundongos tratados com GalN/LPS e camundongos tratados com GalN/LPS injetados com CM-HLSC após 6 dias de indução de FHF.
A figura 4 é uma imagem mostrando o manchamento H&E e PCNA de camundongos SCID tratados com GalN/LPS injetados com CM-HLSC após 3 e 6 dias de indução FHF.
Neste protocolo experimental, foi investigada a capacidade do CM-HLSCs de inibir diretamente a apoptose em hepatócitos primários humanos cultivados. Usando ensaios de apoptose in vitro, o meio condicionado derivado de HLSCs demonstrou exercer um efeito inibitório direto sobre a morte de hepatócitos. Esta atividade in vitro também foi comparada com a atividade in vitro de CM-MSCs. O efeito de 6 citocinas recombinantes humanas presentes no meio condicionado produzido pelas células também foi estudado no ensaio de apoptose de hepatócitos humanos.
Materiais e métodos Cultura de células. As células tronco mesenquimais humanas (MSCs) foram isoladas de aspirados de medula óssea, cresceram e foram caracterizadas como relatado anteriormente. As MSCs foram cultivadas em meio MesenPRO RSTM que é um meio de soro reduzido (2% de FCS) especificamente formulado para suportar o crescimento de MSC. As células foram usadas para experimentos durante as passagens de 3 a 5. As células progenitoras de fígado humano (HLSCs) foram isoladas como previamente descrito e cultivadas em alfa-MEM/EBM (3:1) contendo 10% de FCS (soro fetal bovino, GMP) suplementado com 4 ng/mL de ambos hEGF e hFGF.
Meio condicionado (CM) de MSCs. As MSCs humanas foram cultivadas e caracterizadas para expressão de marcador de superfície e capacidade de diferenciação adipogênica e osteogênica como previamente descrito. Para obter o CM-MSCs, as células foram deixadas a crescer até 90% de confluência (aproximadamente 2 x 106 MSCs por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de MesenPRO RSTM, um meio de cultura com 2% de FCS. O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA) com um corte de 3 kDa.
CM-HLSCs. As HLSCs foram obtidas a partir de hepatócitos humanos congelados. As HLSCs humanas foram cultivadas e caracterizadas para expressão de marcador de superfície e capacidade de diferenciação como previamente descrito. Para obter o CM- HLSCs, as células foram deixadas a crescer até de 60 a 70% de confluência (aproximadamente 2 x 106 MSCs por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de meio alfa-MEM livre de soro suplementado com 0,05% de albumina de soro humano (produzida em grau GMP). O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA) com um corte de 3 kDa.
Apoptose de hepatócitos in vitro (TUNEL). Os hepatócitos foram cultivados por 1 dia em placas de 96 cavidades a 30000 células/cavidade em placas revestidas com fibronectina. A galactosamina-D foi adicionada a uma concentração de 5 mM por 24 horas, seguida de diferentes doses de meio condicionado derivados de HLSC e MSC obtidos como previamente descrito (de 0,5% a 16%), mistura de quatro citocinas (MIX 4 significa IL-8, IL-6, HGF, VEGF). Os resultados são expressos como média ± dp de 8 experimentos diferentes.
Concentração de citocinas. A concentração das citocinas recombinantes humanas usadas no experimentos in vitro foi escolhida a partir das concentrações produzidas por HLSCs após 24 horas em condições de cultura em frasco, concentradas 25 vezes. No caso de MSP, foi usada a concentração obtida em condições de cultura BAL. A primeira concentração é considerada a mesma do estoque de meio condicionado, as células foram então estimuladas com os 16% de cada concentração estoque que representa a mais alta concentração do meio condicionado usado in vitro.
IL-6=56,5 ng/mL, concentração final usada = 9 ng/mL IL-8=210 ng/mL, concentração final usada= 33,6 ng/mL HGF=259 ng/mL, concentração final usada = 41,4 ng/mL VEGF= 44,8 ng/mL, concentração final usada= 7,2 ng/mL MCP-1= 25,7 ng/mL, concentração final usada = 4,1 ng/mL MSP= 60 ng/mL, concentração final usada= 9,6 ng/mL Os resultados são ilustrados nas figuras de 5 a 10.
A figura 5 mostra a inibição in vitro de apoptose de hepatócito por CM-HLSCs em baixas concentrações. Os hepatócitos humanos primários foram cultivados em placas revestidas com fibronectina. A apoptose foi induzida com D- galactosamina (GalN). Durante a exposição à GalN, os hepatócitos foram cultivados em um meio de cultura celular suplementado com 0,5; 2; 8 ou 16% de CM-HLSCs concentrado 25 vezes (produzido em grau GMP). A morte das células foi quantificada usando análise de imagem digital de quatro imagens por cavidade. Os dados mostrados são média ± dp de 8 experimentos. P < 0,05.
A figura 6 mostra micrografias representativas do ensaio TUNEL de hepatócitos humanos tratados com GalN. (A) hepatócitos tratados com 5 mM GalN após 24 horas e (B) hepatócitos tratados com 5 mM GalN estimulados com 2% CM- HLSCs após 24 horas.
A figura 7 mostra a inibição in vitro de apoptose de hepatócitos por CM-MSCs em baixas concentrações. Os hepatócitos humanos primários foram cultivados em placas revestidas com fibronectina. A apoptose foi induzida com D- galactosamina (GalN). Durante a exposição à GalN, os hepatócitos foram cultivados em um meio de cultura celular suplementado com 0,5; 2; 8 ou 16% de CM-MSCs concentrado 25 vezes (produzido em grau GMP). A morte das células foi quantificada usando análise de imagem digital de quatro imagens por cavidade. Os dados mostrados são média ± dp de 8 experimentos. P < 0,05.
A figura 8 mostra a inibição in vitro de apoptose de hepatócitos por várias misturas de citocinas. Os hepatócitos humanos primários foram cultivados na presença de D-galactosamina (GalN; 5 mM) por 24 horas. O uso de MIX 4 + MSP em hepatócitos tratados com GalN resultou na inibição da apoptose após 24 horas. Os hepatócitos tratados com GalN também foram cultivados com MIX 4 + MCP-1 ou com a combinação de MIX 4 + MSP + MCP-1. A morte das células foi quantificada usando análise de imagem digital de quatro imagens por cavidade. Os dados mostrados são média ± dp de 8 experimentos. *P < 0,05.
As citocinas solúveis produzidas no meio de cultura pelas células tronco do fígado humano (HLSCs) mostraram intensificar a cura do fígado. A fim de elucidar ainda mais os mecanismos envolvidos, foram determinadas as citocinas liberadas pelas HLSCs e comparadas com as citocinas produzidas pelas células tronco mesenquimais (MSCs) da medula óssea humana. A análise do perfil das citocinas secretadas foi estendida pela produção de meio condicionado sob diferentes condições de cultura de células, tais como garrafa rolante, frasco T em condições normóxicas e frasco T sob condições hipóxicas. No caso de MSCs, as células foram cultivadas somente em frasco T em condições de cultura normóxicas. Foi obtido um total de 16 meios condicionados diferentes. Todas as análises feitas com o sistema Multiplex (de BioRad) do meio condicionado produzidas em 24 horas de cultura por HLSCs e MSCs, indicaram a presença de citocinas e quimiocinas, tais como quantidades principais de, inter alia, HGF, IL6, IL8, VEGF, MCP1, com um total de 31 proteínas diferentes. Vários anticorpos usados para o ensaio multiplex humano Bio-Rad foram também avaliados pelo ensaio ELISA (IL-6, IL-8, HGF, VEGF, MCP1 e MSP1). O teste ELISA foi executado com kits RayBio® Human ELISA de acordo com as instruções do fabricante. Os inventores também avaliaram comparativamente os ensaios multiplex e imunosorvente ligado a enzima (ELISA). A comparação foi baseada na medida de seis citocinas presentes nos 16 meios condicionados diferentes produzidos. As concentrações de citocinas, medidas pelos diferentes kits, mostraram tendências similares, embora as concentrações absolutas medidas fossem diferentes. Materiais e métodos Cultura de células HLSCs. Células progenitoras de fígado humano (HLSC) foram isoladas como previamente descrito e cultivadas em alfa-MEM/EBM (3:1) contendo 10% de FCS (soro fetal bovino, GMP) suplementado com 4 ng/mL de ambos rhEGF e rhFGF.
A semeadura celular inicial e composições dos meios, para a coleção de meio condicionado (CM), em todos os experimentos executados com HLSCs cultivadas por 24 horas, foram como descrito abaixo: - 2 experimentos com células na passagem 3 cultivadas numa garrafa rotatória: cultura de 20 x 106 HLSC em 100 mL de RPMI + 0,05% de albumina humana - 2 experimentos com células na passagem 10 cultivadas numa garrafa rotatória: cultura de 20 x 106 HLSC em 100 mL de RPMI + 0,05% de albumina humana - 3 experimentos com células na passagem 3 cultivadas em frasco T em condições normóxicas: cultura de 2 x 106 HLSC em 10 mL de RPMI + 0,05% de albumina humana - 3 experimentos com células na passagem 10 cultivadas em frasco T em condições normóxicas: cultura de 2 x 106 HLSC em 10 mL de RPMI + 0,05% de albumina humana - 2 experimentos com células na passagem 3 cultivadas em frasco T em condições hipóxicas: cultura de 2 x 106 HLSC em 10 mL de RPMI + 0,05% de albumina humana - 2 experimentos com células na passagem 10 cultivadas em frasco T em condições hipóxicas: cultura de 2 x 106 HLSC em 10 mL de RPMI + 0,05% de albumina humana hMSCs. As células tronco mesenquimais humanas (hMSCs) foram isoladas de aspirados de medula óssea humana e cresceram e foram caracterizadas como previamente relatado. As MSCs foram cultivadas em meio MesenPRO RSTM que é um meio de soro reduzido (2% FCS) especificamente formulado para suportar o crescimento de MSCs. As células foram usadas nos experimentos durante a passagem 3.
A semeadura celular inicial e composições dos meios, para a coleção de meio condicionado (CM), dos experimentos executados com hMSCs cultivadas por 24 horas, foram como descrito abaixo: - 2 experimentos com células na passagem 3 cultivadas em frasco T em condições normóxicas: cultura de 2 x 106 HLSC em 10 mL de RPMI + 0,05% de albumina humana
Preparação do CM. Os CMs derivados de HLSCs foram obtidos pela semeadura das células numa concentração de 2 x 106 em frascos T e incubando-as de um dia para o outro na incubadora. No dia seguinte, as células foram cuidadosamente lavadas, e cultivadas em 10 mL de RPMI (sem o vermelho fenol) na presença de 0,05% de albumina humana. O meio CM foi coletado 24 horas mais tarde e todas as alíquotas de cada experimento foram congeladas a -20oC. O CM foi concentrado por centrifugação por 1, 30 horas a 4oC, a 2700 g usando as unidades de ultrafiltração de Millipore com um corte de 3 kDa de tamanhos de poros.
Os CMs derivados de hMSCs foram obtidos deixando crescer até 90% de confluência (aproximadamente 2 x 106 MSCs por frasco de 75 cm2), lavando cuidadosamente, e cultivando em 10 mL de RPMI (sem o vermelho fenol) na presença de 0,05% de albumina humana. O meio condicionado foi coletado 24 horas mais tarde e todas as alíquotas de cada experimento foram congeladas a -20oC. O CM foi concentrado por centrifugação por 1, 30 horas a 4oC, a 2700 g usando as unidades de ultrafiltração de Millipore com um corte de 3 kDa de tamanhos de poros.
Após a coleta do CM, as células foram recuperadas, a viabilidade celular foi avaliada por exclusão pelo corante azul de tripano obtendo mais de 95% de viabilidade em todos os experimentos.
Quantização total de proteína. A concentração total de proteína no CM foi determinada de acordo com o método Bradford (Bio-Rad Laboratories) seguindo-se o protocolo do fabricante. A albumina de soro bovino (BSA) foi usada para criar uma referência padrão. 5 μL de cada amostra foram adicionados a 1 mL do corante do regente de Bradford diluído 1 para 5 com água destilada e misturado. Após incubação por 5 min. à temperatura ambiente, a absorbância óptica a luz de 595 nm foi determinada com um fluorofotômetro. 5 A concentração de proteína para cada amostra foi calculada de acordo com a curva BSA linearizada.
ELISA. Foi usado o ensaio RayBio® Human ELISA (ensaio imunosorvente ligado à enzima) para a medição quantitativa de IL-8, IL-6, VEGF, HGF, MCP1 e MSP1. Este ensaio emprega anticorpos específicos para as citocinas humanas mencionadas, 10 revestido numa placa de 96 cavidades. Os padrões e amostras foram pipetados nas cavidades e as citocinas presentes na amostra são ligadas às cavidades pelos anticorpos imobilizados. As cavidades foram lavadas e anticorpos biotinilados anti- citocinas humanas foram adicionados. Após lavar os anticorpos biotililados não ligados, estreptavidina conjugada com HRP foi pipetada nas cavidades. As cavidades foram 15 novamente lavadas, uma solução substrato de TMB foi adicionada às cavidades e desenvolveu cor em proporção à quantidade de citocinas ligadas. A solução de parada muda a cor de azul para amarelo, e a intensidade da cor é medida em 450 nm.
Ensaio Bioclarma. Um imuno ensaio biométrico multiplex de Bio-Rad, contendo microesferas coradas fluorescentes conjugadas com um anticorpo monoclonal específico 20 para as proteínas alvo, foi usado para medição de citocinas de acordo com as instruções do fabricante (Bio-Plex Human Cytokine Assay; Bio-Rad). As seguintes citocinas foram ensaiadas: IL-1β, IL-1ra, IL-2, IL-4, IL-5, IL-6, IL-7, CXCL8 (IL-8), IL-9, IL-10, HGF, M- CSF, MIF, SCF, PDGF, Rantes, VEGF, Eotaxina, bFGF, IP-10, IFNy, IL-12 (p70), IL-13, IL- 15, IL-17, fator de estimulação de colônia de granulocito (G-CSF), fator de estimulação de 25 colônia de granulocito-monocito (GM-CSF), proteína quimioatrativa de monócito (MCP-1), proteína inflamatória de macrófago (MIP-1β/CCL4), MIP-1α e TNF-a.
Brevemente, 250 μL de CM não diluídos foram incubados com contas acopladas a anticorpos. Os complexos foram lavados, então incubados com anticorpos biotinilados de detecção e, finalmente, com estreptavidina-ficoeritrina antes de avaliar a concentração de 30 citocinas. Uma faixa de 1,95 a 40000 pg/mL de citocinas recombinantes foi usada para estabelecer curvas padrão e maximizar a sensibilidade e faixa dinâmica do ensaio. Os níveis de citocina foram determinados usando um leitor de matriz multiplex de LuminexTM Instrumentation System. A concentração foi calculada usando o software provido pelo fabricante. Os resultados obtidos são ilustrados abaixo nas Tabelas de 2 a 8. 35
Imunoprecipitação de MSP-1 a partir de meio condicionado HLSC e Western Blot
Os sobrenadantes MSP-1 em cultura de HLSC foram determinados por imunoprecipitação e Western Blot. 15 mL de sobrenadante de cultura após 24 horas de cultura foram centrifugados por 70 minutos a 4000 g a 4oC, concentrados em um Amicon 3KD ultrafiltro em 250 μL. Para precipitação de proteína, 1 mL de etanol puro frio (-20o) foi adicionado aos 250 μL de sobrenadante concentrado e incubado a -80oC de um dia para o outro. As proteínas precipitadas foram coletadas após centrifugação a 1200 g e lisada com 500 μL de tampão RIPA. A imunoprecipitação foi executada por 18 horas usando um anticorpo anti-MSP (R&D System) reticulado à proteína a-sefarose. Para SDS-PAGE, péletes foram suspensos em 40 μL de 2-beta- mercaptoetanol e aquecidos a 100oC. As proteínas foram separadas por SDS-PAGE em gel acrilamida 8%, transferidas para uma membrana de nitrocelulose. Após 1 horas de bloqueio com 5% leite desnatado seco em tampão salino Tris contendo 0,05% de Tween 20, a membrana foi incubada de um dia para o outro com 2 μg/mL de anticorpo anti-MSP humano a 4oC e, após lavada três vezes, incubada 1 hora à temperatura ambiente com goat anti-mouse IgG conjugada com peroxidase de raiz-forte (Bio-Rad). A membrana foi revelada com reagente quimioluminescente e analisada com quimiodoc.
Os resultados são ilustrados na figura 9, mostrando a imunoprecipitação de MSP a partir do meio condicionado de HLSCs em três passagens diferentes (1, 2 , 5). As bandas de 85 kDa representam MSP monomérico (pro-MSP) e as bandas de 55 kDA a cadeia alfa de MSP dimérico (ativo).
Os níveis de expressão de 507 proteínas humanas alvo derivadas de CM HLSC e MSC foram simultaneamente detectados. Os CMs foram coletados após 48 horas de cultura de 1 x 106 células na presença de aMEM suplementado com 0,2% de FCS como descrito no protocolo de matriz de proteína. O painel de moléculas incluía citocinas, quimiocinas, adipocina, fatores de crescimento, proteases, receptores solúveis, moléculas de adesão solúveis e outras proteínas no sobrenadante de cultura de células.
Materiais e métodos Preparação do CM. Para preparar CM HLSCs e MSC, as células foram depositadas em pratos de cultura de tecido de 100 mm a uma densidade de 1 x 106 células por prato. As células foram então cultivadas com meio de cultura completo por de 24 a 48 horas. Após o que, o meio foi substituído por baixo teor de soro (0,2% FCS) e então as células foram cultivadas por 48 horas mais uma vez. Os CMs foram coletados e centrifugados a 1000 g. Os CMs de ambos tipos de células sofreram diálise antes da etapa de marcação com biotina. Através de um processo simples, a amina primária das proteínas nas amostras foi biotinilada, seguido por diálise para remover a biotina livre. A partir daqui, as amostras recém biotiniladas foram adicionadas sobre a membrana da matriz e incubadas à temperatura ambiente. Após a incubação com HRP-estreptavidina, os sinais foram visualizados por quimioluminescência. Nesta 5 matriz, foi usado um controle interno para monitorar todo o processo incluindo o rótulo- biotina e a matriz de anticorpos. Os resultados foram analisados com RayBio Analysis Tool, que é um programa especificamente projetado para análise de matriz de anticorpos RayBio baseada em rótulo biotina. Detalhes adicionais deste ensaio podem ser encontrados em RayBio® Biotin Label-based Human Antibody Array I User Manual.
A figura 10 mostra o mapa da matriz humana do RayBio Biotin Label-based a partir dos sobrenadantes derivados de HLSCs (A) e MSC (B).
O resultado completo do ensaio de matriz de anticorpos RayBio® Biotin Label-based é resumido abaixo na Tabela 9. Tabela 9
Com base numa razão HLSC/MSC igual ou maior que 2,5, foi identificado um total de 25 proteínas como aquelas mais prováveis de dar uma contribuição para a atividade do CM. Tais proteínas são destacadas na Tabela 9.
FHF in vivo Modelo in vivo D-galactosamina/endotoxina de hepatite letal tóxica aguda
Os mecanismos subjacentes à ação hepatotóxica de galactosamina ocorrem devido a uma elevada acumulação de derivados UDP- galactosamina no fígado, levando a uma exaustão de UTP hepático. Como resultado, pára a biossíntese de macromoléculas (RNA, proteínas, glicoproteínas, glicogênio, etc.). Estas alterações levam a um eventual dano celular e morte celular, que em estágios avançados da reação podem ser identificados pelo aumento das enzimas do fígado no sangue e por histologia. Ao mesmo tempo, a endotoxina induziu a produção de fator de necrose tumoral a (TNF-a) que desenvolveu uma apoptose massiva de hepatócitos. Este modelo in vivo foi desenvolvido em camundongos SCID para estudar a ação de HLSC neste sistema letal in vivo.
Animais e protocolos experimentais. Camundongos SCID de seis a sete semanas de idade foram alojados em instalações animais com acesso livre a comida e água. Estes animais receberam uma injeção intraperitoneal de 500 μL de tampão salino contendo 0,125 μg de LPS e 18 mg de GalN. Os camundongos foram injetados intraperitonealmente com 30 x 106 de HLSC após 2 horas da injeção D-GalN/LPS. Um segundo grupo de camundongos SCID foi inoculado intraperitonealmente com 1 mL de sobrenadante de HLSC em tampão salino ao mesmo tempo, 30 minutos e 2 horas após a injeção de LPS e GalN. Os camundongos de controle receberam uma injeção de uma mistura de LPS e GalN.
Produção de sobrenadante a partir de HLSC no frasco T. Para a geração de CM a partir de HLSC (CM-HLSC), as células foram deixadas a crescer até de 60 a 70% de confluência (aproximadamente 2 x 106 HLSC por frasco de 75 cm2), lavadas cuidadosamente e cultivadas em 10 mL de meio alfa-MEM livre de soro suplementado com 0,05% de albumina de soro humano (produzida em grau GMP). O meio condicionado foi coletado 24 horas mais tarde e concentrado 25 vezes usando unidades de ultrafiltração (Millipore, Bedford, MA) com um corte de 3 kDa.
Análise histológica. A necrose do fígado foi analisada através de manchamento H&E, proliferação (manchamento PCNA) e TUNEL (células apoptóticas).
Western Blot. O ensaio Western Blot foi realizado para a detecção de BAX e BclXS/L. Os fígados foram homogeneizados e lisados a 4oC por 1 hora em tampão de lise (50 mmol/L Tris-HCl, pH 8,3, 1% de Triton X-100, 10 μmol/L de fluoreto de fenilmetil sulfonila, 10 μmol/L de leupeptina e 100 U/mL de aprotinina) e centrifugado a 15000 g. Os teores de proteínas dos sobrenadantes foram medidos pelo método Bradford. Alíquotas contendo 200 μg de proteínas de lisados de fígados foram submetidas à eletroforese em gel de dodecilsulfato-poliacrilamida sob condições redutoras e eletro-manchados em filtros de membrana de nitrocelulose. As manchas foram bloqueadas com 5% de leite desnatado em 20 mmol/L de Tris-HCL, pH 7,5, 500 mmol/L de NaCl mais 0,1% de Tween (TBS-T). A membranas foram subseqüentemente imunomanchadas de um dia para o outro a 4oC com os relevantes anticorpos primários na concentração apropriada. Após lavagens extensivas com TBS-T, as manchas foram incubadas por 1 hora à temperatura ambiente com anticorpos secundários específicos a isotipo conjugado com peroxidase, lavados com TBS-T, desenvolvidos com reagentes de detecção ECL por 1 minutos e expostos a filme X-Omat. Os seguintes anticorpos foram usados: anticorpo monoclonal anti-BAX e anticorpo policlonal BclXS/L de Santa Cruz Biotechnology.
Para avaliar efeitos benéficos possíveis de HLSC sobre a letalidade de camundongos que receberam endotoxina (LPS) e GalN, foram realizados estudos de sobrevivência usando 6 camundongos. A % de sobrevivência animal injetada com 0,125 μg de LPS e 18 mg de GalN e 30 x 106 HLSC foi de 75%. A % de sobrevivência animal injetada com 1 mL de sobrenadante concentrado em tampão salino ao mesmo tempo, 30 minutos e 2 horas após a injeção de LPS e 18 mg de GalN foi de 70% (n = 17). Os níveis de transaminase alanina (ALT) no soro diminuíram de 273 U/L para 57 U/L e de transaminase aspartato (AST) no soro diminuíram de 1693 U/L para 291 U/L, ambos após 7 dias da injeção de HLSC. Os níveis de AST diminuíram de 1693 U/L para 1000 U/L ambos após 6 dias de injeção de CM-HLSC.
A análise histológica de seções de fígado após 3 e 6 dias do tratamento com sobrenadante mostraram um índice diminuído de apoptose (TUNEL) e necrose. Uma regeneração massiva de tecido foi observada. Esta descoberta se correlaciona com um aumento do índice de proliferação de tecido (manchamento PCNA). Pelo Western Blot, foi mostrado que houve uma regulação para cima da proteína pró- apoptótica BAX nos animais tratados com GalN/LPS e uma regulação para baixo no ponto diferente no tempo em ambos sobrenadantes concentrados. No caso da expressão da proteína pró-apoptótica BcLX/L, foi observada uma regulação para cima desta proteína nos animais tratados com o sobrenadante concentrado e uma regulação para baixo da expressão nos animais tratados somente com GalN/LPS.
Os resultados mencionados acima são ilustrados nas figuras de 11 a 13. A figura 11a mostra a sobrevivência de camundongos no modelo letal LPS/GalN injetados com HLSC (n = 6).
A figura 11b mostra a sobrevivência de camundongos no modelo letal LPS/GalN injetados com HLSC concentrado (n = 17).
A figura 12 mostra o manchamento H&E e PCNA de camundongos SCID tratados com GalN/LPS injetados com CM concentrado a partir de
HLSC purificado a partir do frasco T após 3 e 6 dias de indução de falha hepática (GalN/LPS).
A figura 13 mostra os resultados do ensaio TUNEL para avaliar os hepatócitos apoptóticos. A presença da proteína pró-apoptótica BAX e da proteína anti-apoptótica BclX foi avaliada por análise Western Blot.
Claims (13)
1. Meio condicionado, caracterizado pelo fato de ser obtido pela cultura de uma linhagem de células progenitoras pluripotentes de fígado humano, em que compreende uma mistura de fator de crescimento de hepatócito (HGF) em uma concentração variando de 1 a 100 ng/mL, interleucina 6 (IL-6) em uma concentração variando de 10 a 200ng/mL, interleucina 8 (IL-8) em uma concentração maior do que ou igual a 35ng/mL, um fator de crescimento endotelial vascular (VEGF) em uma concentração variando de 10 a 400ng/mL, e proteína estimulante de macrófagos (MSP) em uma concentração variando de 1 a 100 pg/mL, e em que é livre de células.
2. Método de produção de um meio condicionado livre de células como definido na reivindicação 1, caracterizado pelo fato de que o referido método compreende as etapas de: (i) cultivar hepatócitos humanos maduros derivados de uma amostra de tecido do fígado adulto num meio de cultura celular até a morte dos hepatócitos maduros e seleção de uma população de células sobreviventes tendo morfologia epitelioide, as referidas células tendo morfologia epitelioide sendo células progenitoras pluripotentes de fígado humano; (ii) expandir a população de células sobreviventes tendo morfologia epitelióide por cultura num meio de cultura contendo soro e glicose suplementado com hEGF (fator de crescimento epitelial humano) e bFGF (fator de crescimento de fibroblasto básico) e compreendendo os usuais sais inorgânicos, aminoácidos e vitaminas necessários para o crescimento de células de mamíferos; e (iii) separar as células do meio de cultura das células.
3. Método, de acordo com a reivindicação 2, caracterizado pelo fato que os hepatócitos maduros são congelados em um meio de cultura contendo soro na presença de um agente crio-protetor e então descongelados antes da cultura de acordo com a etapa (i).
4. Método, de acordo com a reivindicação 2 ou 3, caracterizado pelo fato que o meio de cultura compreende alfa-MEM (meio mínimo essencial alfa) suplementado com pelo fato de ser concentrada 20 vezes.
5. Composição farmacêutica, caracterizada pelo fato de compreender o meio condicionado como definido na reivindicação 1.
6. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser concentrada 5 vezes.
7. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser concentrada 10 vezes.
8. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser concentrada 20 vezes.
9. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser concentrada 25 vezes.
10. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser diluída 5 vezes.
11. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser diluída 10 vezes.
12. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser diluída 20 vezes.
13. Composição farmacêutica, de acordo com a reivindicação 5, caracterizada pelo fato de ser diluída 25 vezes.
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08010651.1 | 2008-06-11 | ||
| EP08010651 | 2008-06-11 | ||
| PCT/EP2009/057232 WO2009150199A1 (en) | 2008-06-11 | 2009-06-11 | Conditioned medium of liver progenitor cells |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0909866A2 BRPI0909866A2 (pt) | 2015-08-11 |
| BRPI0909866B1 true BRPI0909866B1 (pt) | 2021-08-24 |
Family
ID=40905279
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0909866-6A BRPI0909866B1 (pt) | 2008-06-11 | 2009-06-11 | Método de produção de um meio condicionado de células progenitoras de fígado, meio condicionado e composição farmacêutica |
Country Status (12)
| Country | Link |
|---|---|
| US (2) | US10456425B2 (pt) |
| EP (1) | EP2296672B1 (pt) |
| JP (1) | JP5632833B2 (pt) |
| CN (2) | CN103800895B (pt) |
| BR (1) | BRPI0909866B1 (pt) |
| CA (1) | CA2727392C (pt) |
| DK (1) | DK2296672T3 (pt) |
| ES (1) | ES2556630T3 (pt) |
| HU (1) | HUE028676T2 (pt) |
| PL (1) | PL2296672T3 (pt) |
| PT (1) | PT2296672E (pt) |
| WO (1) | WO2009150199A1 (pt) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2333047A1 (en) * | 2009-12-09 | 2011-06-15 | Fresenius Medical Care Deutschland GmbH | Adult stem cell derived conditioned medium and/or adult stem cells for use in the therapeutic treatment of a tumor disease |
| US8603470B1 (en) | 2012-08-07 | 2013-12-10 | National Cheng Kung University | Use of IL-20 antagonists for treating liver diseases |
| WO2015001124A1 (en) | 2013-07-05 | 2015-01-08 | Université Catholique de Louvain | Conditioned medium from human adult liver stem cells and its use in the treatment of liver disorders |
| BR112016004911A2 (pt) | 2013-09-05 | 2017-09-05 | Inis Biotech Llc | Proteína secretada, acídica e rica em cisteína, um novo alvo para o tratamento e prevenção de insuficiência aguda do fígado |
| RU2644650C2 (ru) * | 2014-12-01 | 2018-02-13 | Общество с ограниченной ответственностью "Т-Хелпер Клеточные Технологии" | Материал стволовых клеток и способ его получения |
| CN104818245B (zh) * | 2015-05-29 | 2020-02-04 | 广州赛莱拉干细胞科技股份有限公司 | 一种肝脏干细胞的培养基及培养方法 |
| WO2017139455A1 (en) | 2016-02-10 | 2017-08-17 | Wake Forest University Health Sciences | Model system of liver fibrosis and method of making and using the same |
| RU2708329C2 (ru) | 2016-05-31 | 2019-12-05 | Общество с ограниченной ответственностью "Т-Хелпер Клеточные Технологии" | Материал стволовых клеток, композиции и способы применения |
| EP4467565A3 (en) | 2016-12-21 | 2025-03-12 | Amgen Inc. | Anti-tnf alpha antibody formulations |
| US12453743B2 (en) | 2018-05-30 | 2025-10-28 | Direct Biologics, Llc | Mesenchymal stem cell (MSC) growth factor and extracellular vesicle preparation in frozen or powdered form and methods of use |
| CN109628377A (zh) * | 2019-01-02 | 2019-04-16 | 贵州省人民医院 | 一种小鼠原代肝细胞灌注式分离及离体培养方法 |
| CN111607556B (zh) * | 2019-01-25 | 2022-06-07 | 中国科学院广州生物医药与健康研究院 | 一种培养扩增人肝祖细胞的培养基及其应用 |
| EP3920946A4 (en) | 2019-02-07 | 2022-11-09 | Direct Biologics LLC | METHOD FOR TREATING OSTEOARTHRITIS USING A COMBINATION OF EXOSOMES OF MESENCHYMATE STEM CELLS, SYNOVIAL MESENCHYMATE STEM CELLS AND SCAFFOLDS |
| LT3963050T (lt) * | 2019-04-30 | 2023-12-27 | Cellaïon SA | Žmogaus alogeninių kepenų progenitorinių ląstelių paruošimas |
| CN111394391B (zh) * | 2019-07-11 | 2022-12-06 | 上海赛立维生物科技有限公司 | 肝祖细胞样细胞库的构建方法及其制备的细胞株与应用 |
| EP3999083A4 (en) | 2019-07-18 | 2023-07-26 | Direct Biologics LLC | Preparations comprising mesenchymal stem cells and cannabinoids and methods of their use |
| MX2022013301A (es) | 2020-04-22 | 2023-02-14 | Direct Biologics Llc | Métodos y composiciones para tratar las afecciones inflamatorias asociadas con una enfermedad infecciosa. |
| US12502407B2 (en) | 2024-04-25 | 2025-12-23 | Direct Biologics, Llc | Treatment of fistula with bone marrow mesenchymal stem cell derived extracellular vesicles |
Family Cites Families (13)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| JPH093099A (ja) * | 1995-06-20 | 1997-01-07 | Toyobo Co Ltd | マクロファージ刺激蛋白質改変体およびその製造法 |
| US6475490B1 (en) * | 1998-10-19 | 2002-11-05 | Fordham University | Compositions and methods for promoting tissue repair using heat shock proteins |
| US6372494B1 (en) * | 1999-05-14 | 2002-04-16 | Advanced Tissue Sciences, Inc. | Methods of making conditioned cell culture medium compositions |
| US6719969B1 (en) * | 1999-08-09 | 2004-04-13 | The Regents Of The University Of Michigan | Treatment of liver disease and injury with CXC chemokines |
| CA2290240C (en) * | 1999-11-24 | 2008-03-11 | Stergios Stergiopoulos | High resolution 3d ultrasound imaging system deploying a multi-dimensional array of sensors and method for multi-dimensional beamforming sensor signals |
| US7547674B2 (en) * | 2001-06-06 | 2009-06-16 | New York Medical College | Methods and compositions for the repair and/or regeneration of damaged myocardium |
| US6916770B2 (en) | 2001-04-27 | 2005-07-12 | Polyone Corporation | Multi-functional color concentrate compositions |
| AU2002345603B2 (en) * | 2001-06-07 | 2006-10-12 | Skinmedica, Inc. | Conditioned cell culture media and uses thereof |
| EP1444345A4 (en) * | 2001-10-18 | 2004-12-08 | Ixion Biotechnology Inc | TRANSFORMATION OF STEM CELLS AND LIVER PROGENITORS INTO FUNCTIONAL CELLS OF PANCREAS |
| WO2006126219A1 (en) * | 2005-05-26 | 2006-11-30 | Fresenius Medical Care Deutschland G.M.B.H. | Liver progenitor cells |
| US20070292400A1 (en) * | 2006-02-16 | 2007-12-20 | Lipton Stuart A | Media conditioned by human embryonic stem cells or other progenitor cells and uses therefor |
| EP2422794A3 (en) * | 2006-03-07 | 2013-03-13 | Geeta Shroff | Compositions comprising human embryonic stem cells and their derivatives, methods of use, and methods of preparation |
| FR2912916B1 (fr) * | 2007-02-26 | 2009-05-22 | Oreal | Composition cosmetique ou dermatologique comprenant un milieu de culture cellulaire |
-
2009
- 2009-06-11 BR BRPI0909866-6A patent/BRPI0909866B1/pt active IP Right Grant
- 2009-06-11 PT PT97617617T patent/PT2296672E/pt unknown
- 2009-06-11 PL PL09761761T patent/PL2296672T3/pl unknown
- 2009-06-11 HU HUE09761761A patent/HUE028676T2/en unknown
- 2009-06-11 EP EP09761761.7A patent/EP2296672B1/en active Active
- 2009-06-11 ES ES09761761.7T patent/ES2556630T3/es active Active
- 2009-06-11 CN CN201310348088.1A patent/CN103800895B/zh active Active
- 2009-06-11 CN CN200980131229.6A patent/CN102119031B/zh active Active
- 2009-06-11 CA CA2727392A patent/CA2727392C/en active Active
- 2009-06-11 JP JP2011512983A patent/JP5632833B2/ja active Active
- 2009-06-11 DK DK09761761.7T patent/DK2296672T3/en active
- 2009-06-11 WO PCT/EP2009/057232 patent/WO2009150199A1/en not_active Ceased
- 2009-06-11 US US12/737,143 patent/US10456425B2/en active Active
-
2017
- 2017-01-23 US US15/412,142 patent/US10357519B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| PL2296672T3 (pl) | 2016-03-31 |
| PT2296672E (pt) | 2016-01-22 |
| EP2296672B1 (en) | 2015-09-16 |
| US10456425B2 (en) | 2019-10-29 |
| CN103800895B (zh) | 2016-12-28 |
| HUE028676T2 (en) | 2016-12-28 |
| BRPI0909866A2 (pt) | 2015-08-11 |
| EP2296672A1 (en) | 2011-03-23 |
| CA2727392C (en) | 2017-08-22 |
| US20170182100A1 (en) | 2017-06-29 |
| ES2556630T3 (es) | 2016-01-19 |
| JP2011522553A (ja) | 2011-08-04 |
| US10357519B2 (en) | 2019-07-23 |
| US20110129439A1 (en) | 2011-06-02 |
| CA2727392A1 (en) | 2009-12-17 |
| JP5632833B2 (ja) | 2014-11-26 |
| WO2009150199A1 (en) | 2009-12-17 |
| CN103800895A (zh) | 2014-05-21 |
| DK2296672T3 (en) | 2016-01-04 |
| CN102119031A (zh) | 2011-07-06 |
| CN102119031B (zh) | 2014-09-10 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0909866B1 (pt) | Método de produção de um meio condicionado de células progenitoras de fígado, meio condicionado e composição farmacêutica | |
| Jiang et al. | Potentiation of hepatic stellate cell activation by extracellular ATP is dependent on P2X7R-mediated NLRP3 inflammasome activation | |
| Yang et al. | Mitochondrial Ca2+ and membrane potential, an alternative pathway for Interleukin 6 to regulate CD4 cell effector function | |
| Mao et al. | Exosomes derived from human umbilical cord mesenchymal stem cells relieve inflammatory bowel disease in mice | |
| Kopp et al. | Innate immunity and adipocyte function: ligand‐specific activation of multiple Toll‐like receptors modulates cytokine, adipokine, and chemokine secretion in adipocytes | |
| ES2589311T3 (es) | Poblaciones de células que tienen actividad inmunorreguladora, método de aislamiento y usos | |
| Chang et al. | Activated hepatic stellate cells mediate the differentiation of macrophages | |
| JP2022095884A (ja) | 単離ミトコンドリアを含む関節リウマチの予防または治療のための医薬組成物 | |
| US20190048314A1 (en) | Modulation of Angiogenesis | |
| CN105748514A (zh) | 用于治疗肝脏疾病的间叶干细胞 | |
| KR20140042824A (ko) | 인공 근위세뇨관 시스템 및 사용 방법 | |
| Bigildeev et al. | Interleukin-1 beta is an irradiation-induced stromal growth factor | |
| JP2021058218A (ja) | 血管形成の調節 | |
| Shi et al. | Effect evaluation of interleukin-1 receptor antagonist nanoparticles for mesenchymal stem cell transplantation | |
| CN114517177A (zh) | 用于增强间充质干细胞效能的组合物及其应用 | |
| Puolakkainen et al. | Novel delivery system for inducing quiescence in intestinal stem cells in rats by transforming growth factor β1 | |
| Milara et al. | Targeting IL‐11 to reduce fibrocyte circulation and lung accumulation in animal models of pulmonary hypertension‐associated lung fibrosis | |
| CN115518077A (zh) | 一种治疗炎症性肠病的细胞药物 | |
| White et al. | Myofibroblast differentiation is governed by adhesion mechanics, and inhibition of the stress sensor Talin2 reverses lung fibrosis | |
| White et al. | Inhibition of Talin2 dedifferentiates myofibroblasts and reverses lung and kidney fibrosis | |
| Boby et al. | Identification, Characterization, and Transcriptional Reprogramming of Epithelial Stem Cells and Intestinal Enteroids in Simian Immunodeficiency Virus Infected Rhesus Macaques | |
| CN120305413B (zh) | Caspase8在制备非酒精性脂肪肝的药物中的应用 | |
| KR20200140294A (ko) | 환자를 위한 세포 요법 | |
| TWI720031B (zh) | 具免疫調節功能之多胜肽組成物的製備方法 | |
| CN121370715A (zh) | 一种用于延缓细胞衰老、维持组织稳态的组合物及其制备方法和应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B07G | Grant request does not fulfill article 229-c lpi (prior consent of anvisa) [chapter 7.7 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 11/06/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |