BRPI0910345B1 - Compostos análogos de oxitocina, composição farmacêutica compreendendo os mesmos e uso dos ditos análogos - Google Patents
Compostos análogos de oxitocina, composição farmacêutica compreendendo os mesmos e uso dos ditos análogos Download PDFInfo
- Publication number
- BRPI0910345B1 BRPI0910345B1 BRPI0910345-7A BRPI0910345A BRPI0910345B1 BR PI0910345 B1 BRPI0910345 B1 BR PI0910345B1 BR PI0910345 A BRPI0910345 A BR PI0910345A BR PI0910345 B1 BRPI0910345 B1 BR PI0910345B1
- Authority
- BR
- Brazil
- Prior art keywords
- fmoc
- compound
- conditions
- compounds
- compound according
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K7/00—Peptides having 5 to 20 amino acids in a fully defined sequence; Derivatives thereof
- C07K7/04—Linear peptides containing only normal peptide links
- C07K7/16—Oxytocins; Vasopressins; Related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/10—Laxatives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/10—Drugs for genital or sexual disorders; Contraceptives for impotence
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/14—Drugs for genital or sexual disorders; Contraceptives for lactation disorders, e.g. galactorrhoea
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/08—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease
- A61P19/10—Drugs for skeletal disorders for bone diseases, e.g. rachitism, Paget's disease for osteoporosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/04—Centrally acting analgesics, e.g. opioids
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/22—Anxiolytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
- A61P25/26—Psychostimulants, e.g. nicotine, cocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/10—Drugs for disorders of the endocrine system of the posterior pituitary hormones, e.g. oxytocin, ADH
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P7/00—Drugs for disorders of the blood or the extracellular fluid
- A61P7/04—Antihaemorrhagics; Procoagulants; Haemostatic agents; Antifibrinolytic agents
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/53—Immunoassay; Biospecific binding assay; Materials therefor
- G01N33/575—Immunoassay; Biospecific binding assay; Materials therefor for cancer
-
- G—PHYSICS
- G01—MEASURING; TESTING
- G01N—INVESTIGATING OR ANALYSING MATERIALS BY DETERMINING THEIR CHEMICAL OR PHYSICAL PROPERTIES
- G01N33/00—Investigating or analysing materials by specific methods not covered by groups G01N1/00 - G01N31/00
- G01N33/48—Biological material, e.g. blood, urine; Haemocytometers
- G01N33/50—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing
- G01N33/68—Chemical analysis of biological material, e.g. blood, urine; Testing involving biospecific ligand binding methods; Immunological testing involving proteins, peptides or amino acids
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Engineering & Computer Science (AREA)
- Veterinary Medicine (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- Public Health (AREA)
- General Chemical & Material Sciences (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Biomedical Technology (AREA)
- Molecular Biology (AREA)
- Hematology (AREA)
- Immunology (AREA)
- Biochemistry (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Endocrinology (AREA)
- Neurosurgery (AREA)
- Urology & Nephrology (AREA)
- Rheumatology (AREA)
- Neurology (AREA)
- Physical Education & Sports Medicine (AREA)
- Genetics & Genomics (AREA)
- Biophysics (AREA)
- Reproductive Health (AREA)
- Diabetes (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physics & Mathematics (AREA)
- General Physics & Mathematics (AREA)
- Gynecology & Obstetrics (AREA)
- Pathology (AREA)
- Analytical Chemistry (AREA)
- Dermatology (AREA)
- Biotechnology (AREA)
- Cell Biology (AREA)
Abstract
análogos de oxitocina, composição farmacêutica compreendendo os mesmo e uso dos ditos análogos. a presente invenção refere-se a novos composto, composições farmacêuticas que compreendem os mesmos, uso dos ditos compostos para a fabricação de um medicamento para tratamento inter alia de condições comprometidas de lactação, bem como um método para tratamento das ditas condições, em que os ditos compostos são administrados. os compostos são representados pela fórmula genérica (i), como definida ainda no relatório descritivo.
Description
A presente invenção refere-se a novos compostos, composições farmacêuticas que compreendem os mesmos, uso dos ditos compostos para a fabricação de um medicamento para tratamento inter alia de condições comprometidas de lactação, bem como um método para tratamento das ditas condições, em que os ditos compostos são administrados.
Os agonistas de receptores peptídicos de oxitocina incluem o hormônio natural oxitocina, e carbetocina.
A oxitocina é um agente uterotônico potente, usado clinicamente para induzir o parto, e demonstrou intensificar o início e manutenção da lactação (Gimpl, G. et al., Physiol Rev. 81:629-683 (2001); Ruis, H. et al., British Medical Jornal 283:340-342 (1981)). A carbetocina (1-desamino-1-carba-2- tirosina-(O-metil)-oxitocina) também é um agente uterotônico potente usado clinicamente para o controle de atonia uterina e sangramento excessivo. Outra pesquisa indica que os agonistas de oxitocina são úteis para o tratamento de inflamação e dor, incluindo dor abdominal e dorsal; disfunção sexual, ma- culina e feminina; síndrome do intestino irritável (IBS), constipação e obstrução gastrointestinal; autismo, tensão, ansiedade (incluindo distúrbio de ansiedade) e depressão (Pitman, R. et al., Psychiatry Research, 48:107-117; Kirsch, P. et al., The Journal of Neuroscience 25(49):11489-11493); perda cirúrgica de sangue, controle de hemorragia pós-parto, cicatrização de feridas e infecção; mastite e expulsão placentária; e osteoporose. Adicionalmente, os agonistas de oxitocina podem ser úteis para o diagnóstico de câncer e insuficiência placentária.
Uma desvantagem de oxitocina e também carbetocina é sua falta de seletividade sobre receptores de vasopressinas, especialmente o receptor V2. Durante a administração de oxitocina, esta desvantagem é observada por efeitos colaterais tais como antidiurese e hiponatremia.
Para melhorar as propriedades farmacológicas de oxitocina, análogos de oxitocina foram sintetizados. Tais análogos são descritos por Grozonka, Z. et al., em J. Med. Chem. 26:555-559 (1983) e J. Med. Chem. 26:1786-1787 (1983), e por Engstrom, T. et al. em E. J. Pharmacol.355:203- 210 (1998). Adicionalmente, os análogos de oxitocina com atividade antagonista no receptor de oxitocina foram descritos por Fragiadaki, M. et al., em E. J. Med. Chem. 799-806 (2007).
A presente invenção pode prover compostos eficazes e seletivos, fornecendo alternativas e/ou melhoras possíveis, por exemplo, no tratamento de condições de lactação comprometidas.
A presente invenção refere-se a compostos representados pela formula generica (I): em que: n é selecionado entre 0, 1 e 2; p é selecionado entre 0, 1, 2, 3, 4, 5 e 6; Ri é selecionado entre arila opcionalmente substituída com pelo menos um substituinte OH, F, Cl, Br, alquila ou O-alquila; R2 é selecionado entre R4, H, alquila, cicloalquila, arila e sistemas anelares heteroaromáticos com 5 e 6 membros; R3 é selecionado entre H e uma ligação covalente a R2, quando R2 é R4, para formar uma estrutura anelar; R4 é um grupamento alquileno de Ci_6 com pelo menos um substituinte O-alquila, S-alquila ou OH; W e X são selecionados, um independentemente do outro, entre CH2 e S, mas não podem ser ambos CH2; - a alquila é selecionada entre alquila com cadeia linear de Ci-6 e ramificada de C4-8 e tem opcionalmente pelo menos um substituinte hidroxila; - a arila é selecionada entre fenila e fenila monossubstituída ou polissubstituída; desde que, quando R2 é H, p é 1, R3 é H, n é 1 e We X são ambos S, Ri não seja 4-hidróxi-fenila; - a cicloalquila é selecionada entre cicloalquila de C3.6 e tem op-cionalmente pelo menos um substituinte hidroxila; e seus solvatos e sais farmaceuticamente aceitáveis.
A presente invenção pode se referir ainda a compostos representados pela fórmula (I) acima com outra ressalva que, quando R2 é H, p é 0, R3 é H, n é 1, e W e X são ambos S, Ri não seja 4-hidróxi-fenila. Assim sendo, a presente invenção pode se referir a compostos da fórmula (I) acima com a ressalva que o composto não seja [1-β-Mpa,7-Sar]OT e/ou não {dea- m i no-[7-g liei na]-oxitocina}.
Para os propósitos da presente invenção, a terminologia que se segue é utilizada.
Alquila com cadeia linear de denota que tem entre um e seis átomos de carbono, incluindo qualquer número entre eles.
Alquila com cadeia ramificada de C4.8 denota todos grupos alquila ramificados contendo quatro a oito átomos de carbono, incluindo as configurações iso-, see- e terc-, pois a dita expressão não está relacionada ao local de ligação da cadeia alquila em questão.
Cicloalquila de C3-6 denota um sistema anelar carbocíclico que contém entre três e seis átomos de carbono, incluindo qualquer número entre eles. O sistema anelar pode conter ligações insaturadas entre átomos de carbono.
Um sistema anelar heteroaromático com cinco membros é um sistema anelar aromático monocíclico que tem cinco átomos no anel, em que 1, 2, 3 ou 4 átomos do anel são selecionados independentemente entre N, O e S. Os sistemas anelares preferidos são selecionados no grupo que consis- te em tienila, furila, imidazolila, tiazolila, tiadiazolila e tetrazolila.
Um sistema anelar heteroaromático com seis membros é um sistema anelar aromático monocíclico que tem seis átomos no anel, em que 1, 2, 3 ou 4 átomos do anel são selecionados independentemente entre N, O e S. Os sistemas anelares preferidos são selecionados no grupo que consiste em piridila.
Arila denota um grupo aromático selecionado entre fenila e fenila monossubstituída ou polissubstituída.
As porções substituintes podem ser selecionadas entre átomos de flúor (F), cloro (F) e bromo (BR), e alquila, hidróxi (-OH), alcóxi (-O-alquila) e alquil-tio (-S-alquila).
Os exemplos de sais farmaceuticamente aceitáveis compreendem sais de adição de ácidos, por exemplo, um sal formado pela reação com ácidos halogenídricos tais como ácido clorídrico e ácidos minerais, tais como ácido sulfúrico, ácido fosfórico e ácido nítrico, bem como ácidos car- boxílicos alifáticos, aromáticos ou heterocíclicos, sulfônicos, tais como ácido fórmico, ácido acético, ácido propiônico, ácido succínico, ácido glicólico, ácido lático, ácido málico, ácido tartárico, ácido cítrico, ácido benzoico, ácido ascórbico, ácido maleico, ácido hidróxi-maleico, ácido pirúvico, ácido p-hi- dróxi-benzoico, ácido embônico, ácido metanossulfônico, ácido halo-benze- nossulfônico, ácido triflúor-acético, ácido triflúor-metanossulfônico, ácido to- luenossulfônico, e ácido naftalenossulfônico.
Em uma modalidade preferida, n é 1.
Em modalidades preferidas, p é selecionado entre 1, 2, 3, 4 e 5.
Em modalidades preferidas, R1 é selecionado entre fenila, 4-hi- dróxi-fenila, 4-metóxi-fenila e 4 etil-fenila.
Em modalidades preferidas, R2 é selecionado entre etila, n-propila, n-butila, ciclopropila, 2-hidróxi-etila, 2-metóxi-etila, 2-fenil-etila, fenila, benzila, 2-metil-fenila, 3-metil-fenila, 4-metil-fenila, 4-metóxi-fenila, 4-flúor-fenila, 3,4-di- flúor-fenila, 2-tienila, 2-tetra-hidrofurila, 2-furila, 2-piridila e 4-piridila.
Em modalidades preferidas, R3 é H.
Em modalidades preferidas, a dita estrutura anelar é selecionadaentre (R)-4-met6xi-pirrolidinila, (R)-4-metil-tiopirrolidinila, e (S)-4-hidroxi-pirrolidinila.
Em modalidades preferidas, W e CH2, eXeS.
Em modalidades preferidas, WeSeXe CH2.
Em modalidades preferidas, W e X sao ambos S.
Além disso, a presente invenção refere-se a um composto como enunciado acima para uso como um produto farmacêutico.
Consequentemente, a presente invenção refere-se também a 5 uma composição farmacêutica que compreende um composto como enunciado acima como ingrediente ativo em associação com um adjuvante, diluen- te ou veículo farmaceuticamente aceitável.
A composição farmacêutica pode ser adaptada para administração oral, intravenosa, tópica, intraperitoneal, nasal, bucal, intraocular, intra- aural, sublingual ou subcutânea ou para administração por intermédio do trato respiratório, por exemplo, na forma de um aerossol ou pó fino em suspensão no ar. A composição pode assim, por exemplo, estar na forma de comprimidos, cápsulas, pós, micropartículas, grânulos, xaropes, suspensões, soluções emplastros transdérmicos ou supositórios.
Deve-se assinalar que a composição de acordo com a presente invenção pode incluir opcionalmente dois ou mais dos compostos delineados acima.
A presente composição farmacêutica pode compreender opcionalmente, por exemplo, pelo menos um outro aditivo selecionado entre um agente desintegrador, ligante, lubrificante, agente saporífero, conservante, colorante e qualquer mistura deles. Os exemplos desses outros aditivos são encontrados em "Handbook of Pharmaceutical Excipients", editor A. H. Kib- be, 3- edição, American Pharmaceutical Association, USA and Pharmaceutical Press UK, 2000.
A presente composição farmacêutica pode ser adaptada para administração nasal. Ela pode compreender uma preparação aquosa estéril, de preferência, isotônica com o sangue do recebedor. Esta preparação a- quosa pode ser formulada de acordo com métodos conhecidos, usando a- gentes dispersantes ou umectantes e agentes de suspensão apropriados. A formulação de spray nasal SYNTOCINON® (oxitocina) é exemplificativa de uma formulação farmacêutica apropriada aplicável também para os compostos da invenção aqui descritos. Água, solução de Ringer, e solução isotônica de cloreto de sódio são diluentes exemplificativos aceitáveis. A preparação pode incluir também excipientes tais como fosfato de sódio, ácido cítrico, cloreto de sódio, glicerina, solução de sorbitol, para-hidróxi-benzoato de me- tila (metilparaben), para-hidróxi-benzoato de propila (propilparaben) e cloro- butanol.
Além disso, a presente invenção refere-se ao uso de um composto como delineado acima para tratamento, ou para a fabricação de um medicamento para o tratamento de uma ou mais condições médicas, tais como condições comprometidas de lactação; enfraquecimento de indução do parto; condições de atonia uterina; sangramento excessivo; inflamação e dor, incluindo dor abdominal e dorsal; disfunção sexual, masculina e também feminina; síndrome do intestino irritável (IBS), constipação e obstrução gastrointestinal; autismo, tensão, ansiedade (incluindo distúrbio de ansiedade) e depressão; perda cirúrgica de sangue, hemorragia pós-parto, cicatrização e infecção de feridas; mastite e enfraquecimento de expulsão placentária; e osteoporose; e para o diagnóstico de câncer e insuficiência placentária. Neste relatório descritivo, o termo "ansiedade" inclui distúrbio de ansiedade. O distúrbio de ansiedade inclui as indicações dependentes distúrbio de ansiedade generalizada, distúrbio do pânico, agorafobia, fobias, distúrbio de ansiedade social, distúrbio obsessivo-compulsivo, distúrbio de tensão pós- traumática, e ansiedade da separação.
Em outra modalidade a invenção refere-se a um método para o tratamento de condições comprometidas de lactação; enfraquecimento de indução do parto; condições de atonia uterina; sangramento excessivo; inflamação e dor, incluindo dor abdominal e dorsal; disfunção sexual, masculina e também feminina; síndrome do intestino irritável (IBS), constipação e obstrução gastrointestinal; autismo, tensão, ansiedade (incluindo distúrbio de ansiedade) e depressão; perda cirúrgica de sangue, hemorragia pós-parto, cicatrização e infecção de feridas; mastite e enfraquecimento de expulsão placentária; e osteoporose; e para o diagnóstico de câncer e insuficiência placentária.
A dosagem típica dos compostos de acordo com a presente invenção varia dentro de uma ampla faixa e dependerá de vários fatores, tais como as necessidades individuais de cada paciente, e da via de administração. Um médico versado na técnica será capaz de otimizar a dosagem para a situação em questão.
Por exemplo, caso a composição da invenção seja para intensificar o início e manutenção de lactação (por exemplo, para administração nasal), uma dose típica pode ficar na faixa de 0,05 a 1,0 μg/kg de peso corporal para cada sessão de bombeamento das mamas. Uma dose intranasal pode ser dividida, por exemplo, em 1, 2 ou 3 doses menores (por exemplo, fungadas), por exemplo, distribuídas para uma ou ambas narinas, conforme necessário. Os versados nessas técnicas ou um médico podem considerar relevantes variantes desta faixa de dosagem e implementações práticas para adaptar à situação em questão.
Em outro exemplo, a composição da invenção pode ser adminis- trada como uma infusão intravenosa, por exemplo, para o tratamento de hemorragia pós-parto ou perda cirúrgica de sangue. Neste exemplo, ela pode ser administrada durante um período mais longo. Uma dosagem exempli- ficativa para administração por infusão intravenosa é 0,5-200 pg/kg em peso corporal por hora.
Em outro exemplo, a composição da invenção pode ser para administração subcutânea, intranasal ou bucal, por exemplo, para tratar distúrbio de ansiedade ou depressão. Uma dosagem exemplificativa para administração subcutânea , intranasal ou bucal é 0,5-1.000 pg/kg em peso corporal. A dosagem pode ser, por exemplo, para administração tantas vezes ao dia quanto necessário, por exemplo, uma ou duas vezes ao dia.
As abreviaturas usadas são: AcOH ácido acético Boc t-butóxi-carbonila BOP benzotriazol-1-iloxi hexaflúrofosfato de trisdimetilaminofosfônio Bua ácido butírico Bu resíduos de butil-alquila podem ser denotados ainda um resíduo n (normal, isto é, não ramificado), i (isso), s (see) e terc (terciário) CH3CN acetonitrila DCC N,N'-diciclo-hexil-carbodi-imida DCM dicloro-metano DIC N,N'-di-isopropil-carbodi-imida DIPEA N,N-di-isopropil-etil-amina DMF N,N-dimetil-formamida 4-FBzlGly N-(4-flúor-benzil)-glicina Fmoc 9-fluorenil-metóxi-carbonila Fmoc-CI cloreto de 9-fluorenil-metóxi-carbonila Fmoc-OSu N-(9-fluorenil-metóxi-carbonil)-succinimida h hora(s) HBTU O-(benzotriazol-1-il)-N,N,N',N'-hexaflúor-fosfato de terametil -urônio Hcy homocisteína HF ácido fluorídrico HObt 1-hidróxi-benzotriazol HPLC cromatografia líquida de alto desempenho I PA álcool isopropilico MeOH metanol MBHA 4-metil-benzidril-amina NMM 4-metil-morfolina 4-Pic 4-picolil-(4-piridil-metila) PyBOP benzotriazol-1 -iloxi-hexafluorofosfato trispirrolidinofosfônico tBu terc-butila tBuOH álcool t-butilico TEA trietilamina TFA ácido trifluoroacético TIS tri-isopropil-silano Trt tritil-[trifenil-metil, (C6H5)3C-] A menos que diferentemente especificado, foram usados L-ami- noácidos, e a terminologia convencional de aminoácidos é seguida. Seção Experimental (síntese)
Os derivados de aminoácidos e as resinas foram adquiridas em fornecedores comerciais (Bachem, Novabiochem e Peptides International). N-Fmoc-N-(R2(CH2)p)-glicina, Fmoc-Hcy(t-butóxi-carbonil-etil)-OH foram sintetizados de acordo com a literatura [Weber e tal., J. Med.Chem. 46:1918 (2003); Prochaska et al., Collect. Crech. Chem. Commun. 57:1335 (1992); e Wisnieski et al. no documento ns WO 03/072597]. Outros produtos químicos e solventes foram fornecidos pela Sigma-Aldrich, fluka e Across Organics.
Os compostos desta invenção foram sintetizados por métodos usuais com química de peptídeos em fase sólida, utilizando metodologia Fmoc e Boc. Todo acoplamento de aminoácidos protegidos com Fmoc foi mediado com DIC/HOBt/DMF e todo acoplamento de aminoácidos protegidos com Boc foi mediado com DIC ou DCC em DCM. A remoção do grupo Fmoc foi realizada com piperidina a 20% em DMF e a remoção do grupo Boc foi realizada em uma mistura de 50% de TFA/DCM com 1% de m-cresol por 5 e 25 minutos. As lavagens requeridas da resina foram realizadas com DCM, IPA e MeOH. A neutralização, conforme necessária, foi realizada com 2 lavagens da resina de 10% de TEA/DCM por 5 minutos.
A menos que diferentemente mencionado, todas reações foram realizadas à temperatura ambiente. Além das referências citadas acima, a seguinte literatura referencial padrão fornece orientação adicional sobre a organização experimental geral, bem como sobre a disponibilidade das matérias-primas e reagentes necessários: Kates, S.A., Albericio, F., Editores, "Solid Phase Synthesis: A Practical Guide", Marcel Dekker, Nova Iorque, Basel, 2000; Stewart, J.M., Young, J.D., "Solid Phase Synthesis", Pierce Chemical Company, 1984; Bisello etal., J. Biol. Chem. 273:22498-22505 (1998); e Merrifield, J. Am. Chem. Soc. 85:2149-2154 (1963).
A pureza do peptídeo sintetizado pode ser determinada por H- PLC em fase reversa. A integridade estrutural dos peptídeos pode ser conformada usando análise de aminoácidos e espectrometria de massas por eletrospray. Metodologias de Fmoc e Boc foram usadas para sintetizar o di- peptídeo (Leu) na posição 8 e (Gly) na posição 9 ligado à resina.
O derivado de aminoácido na posição 7 do resíduo de aminoácidos foi introduzido por intermédio de uma das seguinte rotas: ácido bromoa- cético foi acoplado ao dipeptídeo ligado à resina sob condições de DIC/ HOBt/DMF e o átomode bromo foi deslocado com (R2(CH2)P)NH2, produzindo uma N-(R2(CH2)p)-glicina ou um derivado de Fmoc-pro-OH foi acoplado ao dipeptídeo ligado à resina, de acordo com a metodologia de Fmoc. Todos os acoplamentos de aminoácidos subsequentes seguiram a metodologia de Fmoc, a menos que diferentemente especificado.
O derivado de aminoácido introduzido na posição 6 foi um dos seguintes: Fmoc-Cys(Trt)-OH; FmocHcy(t-butóxi-acarbonil-etil)-OH ou Fmoc- Cys(t-butóxi-carbonil-propil)-OH. Os análogos de peptídeos nos quais a posição 6 era Fmoc-Cys(Trt)-OH requereu acoplamento de Mpa(Trt)-OH ao terminal N do resíduo de nonapeptídeo ligado à resina.
Os peptídeos sintetizados usando um suporte de resina amida Rink foram clivados da resina, junto com quaisquer grupos protetores lábeis a ácidos tais como Boc, tritila e terc-butila, com solução de TFA/TIS/H2O 95/2,5/2,5 (v/v/v). Os ditos peptídeos foram ciclizados depois da clivagem do peptídeo da resina. Os peptídeos sintetizados usando um suporte de resina de MBHA foram clivados da resina com solução de HF/anisol 14/1 (v/v). Os ditos peptídeos foram ciclizados antes da clivagem do peptídeo da resina.
A ciclização do nonapeptídeo linear através da formação de dis- sulfeto (anel) foi realizada por oxidação de peptídeos lineares dissolvidos em solução aquosa de TFA a 10% com iodo. A ciclização do nonapeptídeo através da formação de ligação amida foi realizada por mediação com HB- TU/DIPEA/DMF ou PyBOP/DIPEA/DMF em uma alta diluição.
Os peptídeos foram purificados por HPLC preparatória em tampões de fosfato de trietilamônio (aquosos) e dessalinizados com um sistema de tampão de ácido acético (aquoso)/acetonitrila. As frações com uma pureza maior do que 97% foram selecionadas e liofilizadas.
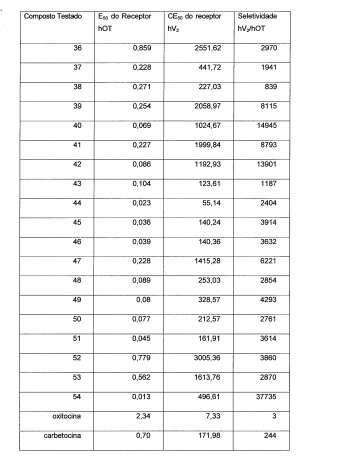
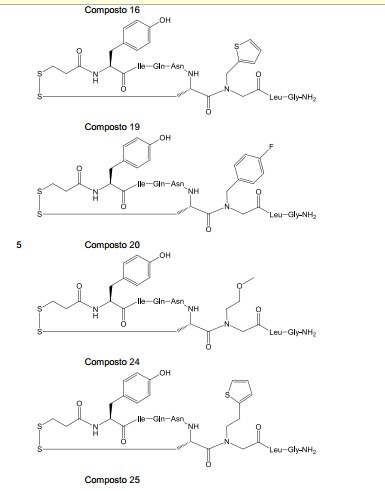
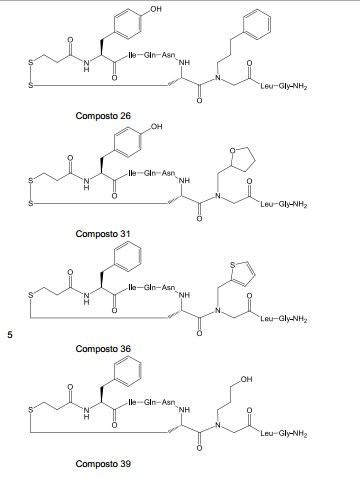
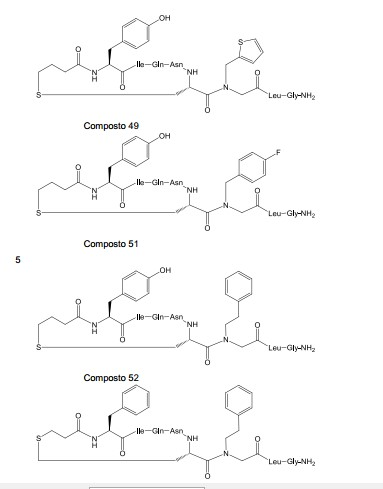
A tabela 1 lista os compostos preparados pelo procedimento a- cima. Um asterisco "*" marca as modalidades mais preferidas. Tabela 1
Os exemplos detalhados que se seguem são foram fornecidos para ilustrar ainda mais a síntese.
Em todas as sínteses, foi realizada HPLC analítica em um cro- matógrafo de Líquido Waters 600, usando uma coluna Vydac C18, 5 μm, 4,6 x 250 mm, em uma vazão de 2 mL/min. A HPLC preparatória foi realizada em um cromatógrafo de líquido Waters 2000, usando um cartucho PrePak de 47 x 300 mm em uma vazão de 100 mL/min. A análise do composto final foi realizada em um cromatógrafo de líquido Agilent 1100, usando uma coluna Vydac C18, 5 μm, 2,1 x 250 mm, em uma vazão de 0,3 ml_/min. Os espectros de massas foram registrados em um espectrômetro Finnigan MAT.
Composto 49: carba-1-[4-FBzlGly7]dOT
Os derivados de aminoácidos usados foram Fmoc-Gly-OH, Fmoc -Leu-OH, Fmoc-Cys(t-butóxi-carbonil-propil)-OH, Fmoc-Asn(Trt)-OH, Fmoc-GIn (Trt)-OH, Fmoc-lle-OH, e Boc-Tyr(tBtu)-OH (Peptides International). Fmoc-Cys (t-butóxi-carbonil-propil)-OH foi sintetizado como descrito acima.
A resina com peptídeo completamente protegida foi sintetizada manualmente, partindo de 1,45 g (0,87 mol) de resina Amida AM Rink de 0,074-0,037 mm (200-400 mesh, Novabiochem). Foram realizados acopla-mentos individuais mediados com DIC/HOBt/DMF com um excesso de 3 vezes de derivados dos aminoácidos Gly e Leu. O resíduo N-(4-flúorbenzil)- glicina foi introduzido com um excesso de 4 vezes de BrC^CC^H/DIC/HOBt em DMF e subsequente substituição de bromo por um excesso de 10 vezes de 4-flúorbenzil-amina em DMF. O acoplamento mediado por DIC/DCM com um excesso de 4 vezes de Fmoc-Cys(t-butóxi-carbonil-propil)-OH foi realizado. Foram realizados subsequentes acoplamentos individuais mediados por DIC/HOBt/DMF com um excesso de 3 vezes de derivados de aminoácidos Asn, Gin, He e Tyr. Os grupos Fmoc foram removidos com solução de piperi- dina a 20% em DMF. Depois de completada a síntese em fase sólida, a resina foi tratada com uma solução de TFA/TIS/H2O 96/2,5/1,5 (y/vlv) (50 mL) por 1,5 h, e removida por filtração. O filtrado foi concentrado sob vácuo e o peptídeo linear bruto foi precipitado com etóxi-etano. O precipitado em DMF (300 mL) foi adicionado em 3 parcelas (3 x 100 mL) a uma solução sob agi- tação intensa de DIPEA (1 mL) em DMF (100 mL). HBTU (150 mg) em DMF (5 mL) foi adicionado à mistura reativa depois da adição de cada parcela de 100 mL da solução de peptídeo; o pH da solução reativa foi mantido em pH 9 pela adição de DIPEA pura, conforme necessário. A reação foi monitorada por HPLC analítica. A solução reativa foi concentrada sob vácuo e o resíduo foi dissolvido em ACOH/CH3CN/H2O. A mistura foi carregada em uma coluna de HPLC e purificada usando um tampão de fosfato de trietil-amônio com pH 5,2. O composto foi eluído com um gradiente de acetonitrila. As frações com uma pureza maior do que 97% foram selecionadas, diluídas com água (2 volumes), e carregadas em uma coluna pré-equilibrada com solução aquosa de AcOH a 2%. O composto desejado foi eluído com um gradiente rápido (3%/min) de CH3CN. As frações que continham o produto desejado foram selecionadas e liofilizadas. 434 mg (rendimento de ~40%, baseado no carregamento da resina inicial e presumindo 85% de teor do peptídeo) do composto amorfo em pó foram obtidos. HPLC: Rt = 19,4 min; gradiente: 5% de B por 5 min, t = 40 °C; solvente A: solução de TFA a 0,01%, solvente B: CH3CN a 70%, 0,01% de TFA (aquoso); pureza: 99,3%; MS (M+H+): esperado 1.042,4, observado 1.042,5.
O texto que se segue é uma síntese em larga escala (isto é, au-mento de escala) do Composto 49: carba-1-[4-FBzlGly7]dOT
Os derivados de aminoácidos usados foram Fmoc-Gly-OH, Fmoc - Leu-OH, Fmoc-4-FBzlGly-OH, Fmoc-Cys(t-butóxi-carbonil-propil)-OH, Fmoc- Asn(Trt)-OH, Fmoc-Gln(Trt)-OH, Fmoc-lle-OH, e Boc-Tyr(tBtu)-OH (Peptides International). Fmoc-4-FBzlGly-OH e Fmoc-Cys(t-butóxi-carbonil-propil)-OH foram sintetizados como descrito acima. O peptídeo foi sintetizado por acoplamentos individuais mediados por DIC/HOBt/DMF com um excesso de 3 vezes de derivado de aminoácido. A síntese remanescente e a caracterização do composto 49 foram seguidas como fornecido acima. 434 mg (rendimento de ~40%, baseado no carregamento da resina inicial e presumindo 85% de teor do peptídeo) de um pó amorfo branco foram obtidos.
Composto 10: [4-PicGly7]dOT
Os derivados de aminoácidos usados foram Fmoc-Gly-OH, Fmoc- Leu-OH, Fmoc-Cys(Trt)-OH, Fmoc-Asn(Trt)-OH, Fmoc-Gln(Trt)-OH, Fmoc-lle- OH, Fmoc-Tyr(tBu)-OH, e Mpa(Trt)-OH (Peptides International). A resina com peptídeo completamente protegida foi sintetizada manualmente, partindo de 1,33 g (0,65 mol) de resina Rink AM de 0,074-0,037 mm (200-400 mesh, Novabiochem). Foram realizados acoplamentos individuais mediados por DIC/HOBt/DMF com um excesso de 3 vezes dos derivados de aminoácidos Gly e Leu. O resíduo N-(4-picolil)-glicina foi introduzido com um excesso de 4 vezes de BrCH2CO2H/DIC/HOBt em DMF e a subsequente substituição de bromo por um excesso de 10 vezes de 4-picolil-amina em DMF. O acoplamento mediado por DIC/DCM com um excesso de 4 vezes de Fmoc-Cys (Trt)-OHe os acoplamentos individuais mediados por DIC/HOBt/DMF com um excessso de 3 vezes dos derivados de aminoácidos Asn, He, tyr e Mpa foram realizados. Os grupos Fmoc foram removidos com piperidina a 20% em DMF. Depois de completada a síntese em fase sólida, a resina foi tratada com uma solução de TFA/TIS/H2O 96/2/2 (vMv) (50 mL) por 1,5 h, e removida por filtração. O filtrado foi concentrado sob vácuo e o peptídeo linear bruto foi precipitado com etóxi-etano. O precipitado foi dissolvido em TFA ouro (50 mL), vertido sobre uma solução aquosa de acetonitrila a 5% (600 mL) sob agitação com um agitador magnético, e o peptídeo foi oxidado adicionando l2 a 0,1 M em metanol até que persistisse uma cor amarela. O excesso de iodo foi reduzido com ácido ascórbico sólido (Sigma-Aldrich) e o pH da solução foi ajustado até cerca de 4 adicionando amônea concentrada (aquosa). A mistura foi carregada em uma coluna de HPLC e purificada u- sando um tampão de fosfato de trietil-amônio com pH 5,2. O composto foi eluído com um gradiente de acetonitrila. As frações com uma pureza maior do que 97% foram selecionadas, diluídas com água (2 volumes), e carregadas em uma coluna pré-equilibrada com solução aquosa de AcOH a 2%. O composto desejado foi eluído com um gradiente rápido (3%/min) de acetonitrila. As frações que continham o produto desejado foram selecionadas e liofilizadas. 348,7 mg (rendimento de ~44%, baseado no carregamento da resina inicial e presumindo 85% de teor do peptídeo) de um pó amorfo branco foram obtidos. HPLC: Rt = 21,7 min; gradiente: 5% de B por 0,5 min, >10% de B em 0,5 min, 10—>30% de B durante 20 min e 100% de B por 5 min, t = 40 °C; solvente A: solução aquosa de TFA a 0,01%, solvente B: CH3CN a 70%, 0,01% de TFA (aquoso); pureza: 99,9%; MS (M+H+): esperado 1.043,4, observado 1.043,4. Composto 29: carba-6-[Phe2,MeOEtGly7]doT
Os derivados de aminoácidos usados foram Boc-Gly-OH e Boc- Leu-OH (Bachem), Fmoc-Hcy(t-butóxi-carbonil-etil)-OH, Fmoc-Asn(Trt)-OH, Fmoc-Gln(Trt)-OH, Fmoc-lle-OH, e Boc-Phe-OH (Peptides International). Fmoc-Hcy(t-butóxi-carbonil-etil)-OH foi sintetizado como descrito acima.
A resina com peptídeo completamente protegido foi sintetizada manualmente, partindo de 1,33 g (0,94 mol) de resina MBHA (Novabio- chem). A resina foi neutralizada com TEA a 10% em DCM. Foram realizados acoplamentos individuais mediados por DIC/DCM com um excesso de 1,7 vez dos aminoácidos Boc-Gly-OH e Boc-Leu-OH. O resíduo N-(2-metóxi-etil) -glicina foi introduzido com um excesso de 3,6 vezes de BrCH2CO2H/ DIC/HOBt em DMF e subsequente substituição do bromo por um excesso de 7 vezes de 2-metóxi-etila e um excesso de 4 vezes de DIPEA em DMF (10 ml_); a reação foi agitada por 5 h. Foram realizados o acoplamento mediado por DIC/DCM com um excesso de 4 vezes dos derivados de Fmoc-Hcy(t- butóxi-carbonil-etil)-OH e os acoplamentos individuais mediados por DIC/HOBt/DMF com um excesso de 3 vezes dos derivados de aminoácidos Asn e Gin. Os dois acoplamentos individuais finais com Fmoc-lle-OH e Boc- Phe-OH foram realizados com DIC/DCM para produzir o peptídeo linear ligado à resina protegida. Os grupos Fmoc foram removidos com piperidina a 20% em DMF. A resina foi tratada com TFA/H2O/TIS 95/3/2 (v/v/v) por 2 h, para remover os grupos tritila, Boc e t-butila. BOP (4 eq) e DIPEA (10 eq) foram adicionados a uma suspensão da resina em DMF (10 ml_) sob agitação; deoiis de 2 h, PyBOP (2 eq) e DIPEA (5 eq) foram adicionados. O peptídeo foi clivado da resina usando 70 mL de HF anidro contendo 5 ml_ de anisol a 0 °C por 90 min. O HF foi removido sob vácuo e o peptídeo linear bruto foi lavado com etóxi-etila (300 mL). O peptídeo foi dissolvido em A- cOH/CH3CN/H2O 1/2/7 (v/v/v) (400 mL). A mistura resultante foi carregada diretamente em uma coluna de HPLC e purificada usando tampão de fosfato de trietil-amônio em pH 2,3. O composto foi eluído com um gradiente de ace- tonitrila. As frações com uma pureza maior do que 97% foram selecionadas, diluídas com água (2 volumes), e carregadas em uma coluna pré-equilibrada com solução aquosa de AcOH a 2%. O composto desejado foi eluído com um gradiente de 1% de AcOH/CH3CN. As frações que continham o produto desejado foram selecionadas e liofilizadas. 292,7 mg (rendimento de ~27%, baseado no carregamento da resina inicial e presumindo 85% de teor do peptídeo) de um pó amorfo branco foram obtidos. HPLC: Rt = 16,7 min; gradiente: 5% de B por 0,5 min, 5^-30% de B em 0,5 min, 30->50% de B durante 20 min e 100% de B por 5 min, t = 40 °C; solvente A: solução aquosa de TFA a 0,01%, solvente B: CH3CN a 70%, 0,01% de TFA (aquoso); pureza: 100,0%; MS (M+H+): esperado 976,5, observado 976,3.
Os outros compostos foram preparados por variação análoga destes procedimentos sintéticos.
A atividade agonista de compostos sobre o receptor hOT foi determinada em um ensaio de gene repórter de transcrição transfectando de forma transiente um DNA com expressão do receptor hOT dentro da linhagem de células do ovário do hamster chinês (CHO) conjuntamente com um DNA repórter que contém elementos promotores responsivos a cálcio intracelular que regulam a expressão de luciferase de pirilampo. Vide Boss, V., Talpade, D.J., Murphy, T.J., J. Biol. Chem. 271 (18):10429-10432 (3 de maio de 1996) para obter informações adicionais sobre este ensaio. As células foram expostas a diluições seriais de compostos diluídos 10 vezes por dose durante 5 h, e em seguida, lise das células, determinação de eficácias dos compostos e valor de CE50 através de regressão não-linear. Oxitocina (OT) foi usada como controle interno em cada experimento, e os compostos foram testados em pelo menos três experimentos independentes. Para determinar a seletividade, os compostos foram testados ainda em ensaios de gene re pórter de transcrição baseados em luciferase, expressando o receptor de vasopressina (hV2) humano.
Com propósitos comparativos adicionais, carbetocina foi usada como composto referencial.
Os resultados nos ensaios in vivo estão representados na tabe la 2 abaixo. O valor de CE50 fornecido é a média geométrica expressa em nanomol/L (nM). Os valores de seletividade são fornecidos em relações de CEÕO- Tabela 2
Os resultados precedentes indicam que os compostos exemplifi- cativos estão dentro do âmbito de invenção e podem ser úteis, por exemplo, no tratamento seguro e eficaz de seres humanos, para induzir parto, controlar atonia uterina, promover e manter lactação, etc.
O âmbito de presente invenção está definido ainda nas reivindi cações que se seguem.
Claims (9)
4. Composto de acordo com qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de ser para uso como produto farmacêutico.
5. Composição farmacêutica, caracterizada pelo fato de que compreende um composto como definido em qualquer uma das reivindica- 10 ções 1 a 3, como ingrediente ativo, em associação com um adjuvante, dilu- ente ou veículo farmaceuticamente aceitável.
6. Composto de acordo com qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de ser para uso no tratamento de uma ou mais dentre condições comprometidas de lactação, enfraquecimento de indução do parto, condições de atonia uterina, sangramento excessivo, inflamação, dor, dor abdominal, dor dorsal, disfunção sexual masculina e feminina, sín- drome do intestino irritável (IBS), constipação, obstrução gastrointestinal, autismo, tensão, ansiedade, depressão, distúrbio de ansiedade, perda cirúr-gica de sangue, hemorragia pós-parto, cicatrização de feridas, infecção, mastite, enfraquecimento de expulsão placentária e osteoporose.
7. Composto de acordo com qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de ser para uso no diagnóstico de câncer ou in-suficiência placentária.
8. Uso de um composto como definido em qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de ser para a fabricação de um medicamento para tratamento de condições comprometidas de lactação, enfraquecimento de indução do parto, condições de atonia uterina, sangra- mento excessivo, inflamação, dor, dor abdominal, dor dorsal, disfunção se-xual masculina e feminina, síndrome do intestino irritável (IBS), constipação, obstrução gastrointestinal, autismo, tensão, ansiedade, depressão, distúrbio de ansiedade, perda cirúrgica de sangue, hemorragia pós-parto, cicatrização de feridas, infecção, mastite, enfraquecimento de expulsão placentária ou osteoporose.
9. Uso de um composto como definido em qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de ser na fabricação de um medicamento para o diagnóstico de câncer ou insuficiência placentária.
Applications Claiming Priority (5)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US4097308P | 2008-03-31 | 2008-03-31 | |
| US61/040,973 | 2008-03-31 | ||
| EP08251739 | 2008-05-19 | ||
| EP08251739.2 | 2008-05-19 | ||
| PCT/IB2009/005351 WO2009122285A1 (en) | 2008-03-31 | 2009-03-30 | Oxitocin analogues |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0910345A2 BRPI0910345A2 (pt) | 2015-10-06 |
| BRPI0910345B1 true BRPI0910345B1 (pt) | 2021-08-17 |
Family
ID=39722695
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0910345-7A BRPI0910345B1 (pt) | 2008-03-31 | 2009-03-30 | Compostos análogos de oxitocina, composição farmacêutica compreendendo os mesmos e uso dos ditos análogos |
Country Status (20)
| Country | Link |
|---|---|
| US (1) | US8673841B2 (pt) |
| EP (2) | EP2260053B1 (pt) |
| JP (1) | JP5539310B2 (pt) |
| KR (1) | KR101558404B1 (pt) |
| CN (1) | CN101983205B (pt) |
| AU (1) | AU2009233429B2 (pt) |
| BR (1) | BRPI0910345B1 (pt) |
| CA (1) | CA2718148C (pt) |
| DK (1) | DK2260053T3 (pt) |
| ES (1) | ES2488992T3 (pt) |
| HR (1) | HRP20140716T1 (pt) |
| IL (1) | IL208039A (pt) |
| MX (1) | MX2010010743A (pt) |
| NZ (1) | NZ587817A (pt) |
| PL (1) | PL2260053T3 (pt) |
| PT (1) | PT2260053E (pt) |
| RU (1) | RU2496788C2 (pt) |
| SI (1) | SI2260053T1 (pt) |
| WO (1) | WO2009122285A1 (pt) |
| ZA (1) | ZA201006733B (pt) |
Families Citing this family (18)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2575853B1 (en) | 2010-05-25 | 2016-08-24 | INSERM - Institut National de la Santé et de la Recherche Médicale | Methods and pharmaceutical composition for the treatment of a feeding disorder with early-onset in a patient |
| JO3400B1 (ar) * | 2010-09-30 | 2019-10-20 | Ferring Bv | مركب صيدلاني من كاربيتوسين |
| EP2935312B1 (en) | 2012-12-21 | 2018-08-08 | F.Hoffmann-La Roche Ag | Peptides as oxytocin agonists |
| AU2015270723A1 (en) * | 2014-06-03 | 2016-11-17 | F. Hoffmann-La Roche Ag | Peptides as oxytocin agonists |
| CR20160562A (es) * | 2014-06-06 | 2017-01-06 | Hoffmann La Roche | Péptidos como agonistas de la oxitocina |
| US10588980B2 (en) | 2014-06-23 | 2020-03-17 | Novartis Ag | Fatty acids and their use in conjugation to biomolecules |
| ES2970059T3 (es) | 2014-09-19 | 2024-05-24 | Ferring Bv | Método de tratamiento del síndrome de Prader-Willi |
| CN106084015B (zh) * | 2016-08-25 | 2020-01-31 | 成都圣诺生物制药有限公司 | 一种合成卡贝缩宫素的方法 |
| US20190135859A1 (en) | 2017-08-11 | 2019-05-09 | Ferring B.V. | Method of manufacturing a pharmaceutical composition |
| BR112020001832A2 (pt) * | 2017-08-11 | 2020-07-28 | Ferring B.V. | método de produção de uma composição farmacêuti-ca |
| CN107628975B (zh) * | 2017-09-17 | 2019-10-29 | 贵州医科大学 | 赖氨酸衍生物类组蛋白去乙酰化酶抑制剂及其合成和应用 |
| EP3852724A4 (en) | 2018-09-20 | 2022-07-06 | Levo Therapeutics, Inc. | CARBETOCIN DRUG PRODUCT AND PROCESS FOR ITS MANUFACTURE |
| TW202031283A (zh) | 2018-09-20 | 2020-09-01 | 馬克 C 曼寧 | 穩定卡貝縮宮素鼻內製劑 |
| JP7390031B2 (ja) * | 2018-12-27 | 2023-12-01 | 国立大学法人金沢大学 | オキシトシン誘導体及びその使用 |
| JP2023500763A (ja) * | 2019-11-04 | 2023-01-11 | フェリング ベスローテン フェンノートシャップ | 泌乳の改善のためのメロトシンの鼻腔内投与 |
| WO2022026463A1 (en) * | 2020-07-27 | 2022-02-03 | Arizona Board Of Regents On Behalf Of The University Of Arizona | Oxytocin analogues and methods for using the same |
| ES3010259T3 (en) | 2021-03-26 | 2025-04-01 | Ot4B | Treatment of dysphagia |
| WO2024044633A2 (en) * | 2022-08-23 | 2024-02-29 | Seattle Children's Hospital (D/B/A Seattle Children's Research Institute) | Oxytocin derivatives and methods of use |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| SE9604341D0 (sv) * | 1996-11-26 | 1996-11-26 | Ferring Bv | Hepta-peptide oxytocin analogue |
| EP1480998B1 (en) * | 2002-02-27 | 2006-11-22 | Ferring BV | Intermediates and methods for making heptapeptide oxytocin analogues |
-
2009
- 2009-03-30 EP EP09727031.8A patent/EP2260053B1/en active Active
- 2009-03-30 AU AU2009233429A patent/AU2009233429B2/en active Active
- 2009-03-30 PT PT97270318T patent/PT2260053E/pt unknown
- 2009-03-30 JP JP2011502454A patent/JP5539310B2/ja active Active
- 2009-03-30 SI SI200930966T patent/SI2260053T1/sl unknown
- 2009-03-30 DK DK09727031.8T patent/DK2260053T3/da active
- 2009-03-30 KR KR1020107024207A patent/KR101558404B1/ko active Active
- 2009-03-30 CN CN200980111919.5A patent/CN101983205B/zh active Active
- 2009-03-30 HR HRP20140716AT patent/HRP20140716T1/hr unknown
- 2009-03-30 ES ES09727031.8T patent/ES2488992T3/es active Active
- 2009-03-30 NZ NZ587817A patent/NZ587817A/en unknown
- 2009-03-30 US US12/933,858 patent/US8673841B2/en active Active
- 2009-03-30 MX MX2010010743A patent/MX2010010743A/es active IP Right Grant
- 2009-03-30 PL PL09727031T patent/PL2260053T3/pl unknown
- 2009-03-30 EP EP13156710.9A patent/EP2626364A1/en not_active Withdrawn
- 2009-03-30 WO PCT/IB2009/005351 patent/WO2009122285A1/en not_active Ceased
- 2009-03-30 RU RU2010139634/04A patent/RU2496788C2/ru active
- 2009-03-30 CA CA2718148A patent/CA2718148C/en active Active
- 2009-03-30 BR BRPI0910345-7A patent/BRPI0910345B1/pt active IP Right Grant
-
2010
- 2010-09-07 IL IL208039A patent/IL208039A/en active IP Right Grant
- 2010-09-20 ZA ZA2010/06733A patent/ZA201006733B/en unknown
Also Published As
| Publication number | Publication date |
|---|---|
| CA2718148C (en) | 2017-11-07 |
| NZ587817A (en) | 2012-05-25 |
| ES2488992T3 (es) | 2014-09-01 |
| IL208039A0 (en) | 2010-12-30 |
| HK1146064A1 (en) | 2011-05-13 |
| MX2010010743A (es) | 2010-11-04 |
| US8673841B2 (en) | 2014-03-18 |
| US20110044905A1 (en) | 2011-02-24 |
| EP2260053A1 (en) | 2010-12-15 |
| CN101983205B (zh) | 2015-08-19 |
| SI2260053T1 (sl) | 2014-08-29 |
| KR101558404B1 (ko) | 2015-10-08 |
| BRPI0910345A2 (pt) | 2015-10-06 |
| CN101983205A (zh) | 2011-03-02 |
| DK2260053T3 (da) | 2014-06-23 |
| RU2010139634A (ru) | 2012-05-10 |
| AU2009233429B2 (en) | 2014-02-13 |
| WO2009122285A8 (en) | 2009-12-10 |
| HRP20140716T1 (hr) | 2014-08-29 |
| JP2011516460A (ja) | 2011-05-26 |
| EP2260053B1 (en) | 2014-05-14 |
| AU2009233429A1 (en) | 2009-10-08 |
| RU2496788C2 (ru) | 2013-10-27 |
| JP5539310B2 (ja) | 2014-07-02 |
| ZA201006733B (en) | 2011-06-29 |
| EP2626364A1 (en) | 2013-08-14 |
| IL208039A (en) | 2016-03-31 |
| PL2260053T3 (pl) | 2014-11-28 |
| KR20110005705A (ko) | 2011-01-18 |
| PT2260053E (pt) | 2014-08-29 |
| CA2718148A1 (en) | 2009-10-08 |
| WO2009122285A1 (en) | 2009-10-08 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0910345B1 (pt) | Compostos análogos de oxitocina, composição farmacêutica compreendendo os mesmos e uso dos ditos análogos | |
| RU2539692C2 (ru) | Агонисты окситоциновых рецепторов | |
| ES2366702T3 (es) | Agonistas peptídicos de receptores de vasopresina. | |
| CN101379076B (zh) | 新化合物 | |
| HK1146064B (en) | Oxytocin analogues | |
| WO2002000688A1 (en) | Peptide compound and pharmaceutical compositions and medicines containing the same as the active ingredient |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001, QUE MODIFICOU A LEI NO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUENCIA PREVIA DA ANVISA. CONSIDERANDO A APROVACAO DOS TERMOS DO PARECER NO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDENCIAS CABIVEIS. |
|
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 30/03/2009, OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF, QUE DETERMINA A ALTERACAO DO PRAZO DE CONCESSAO. |