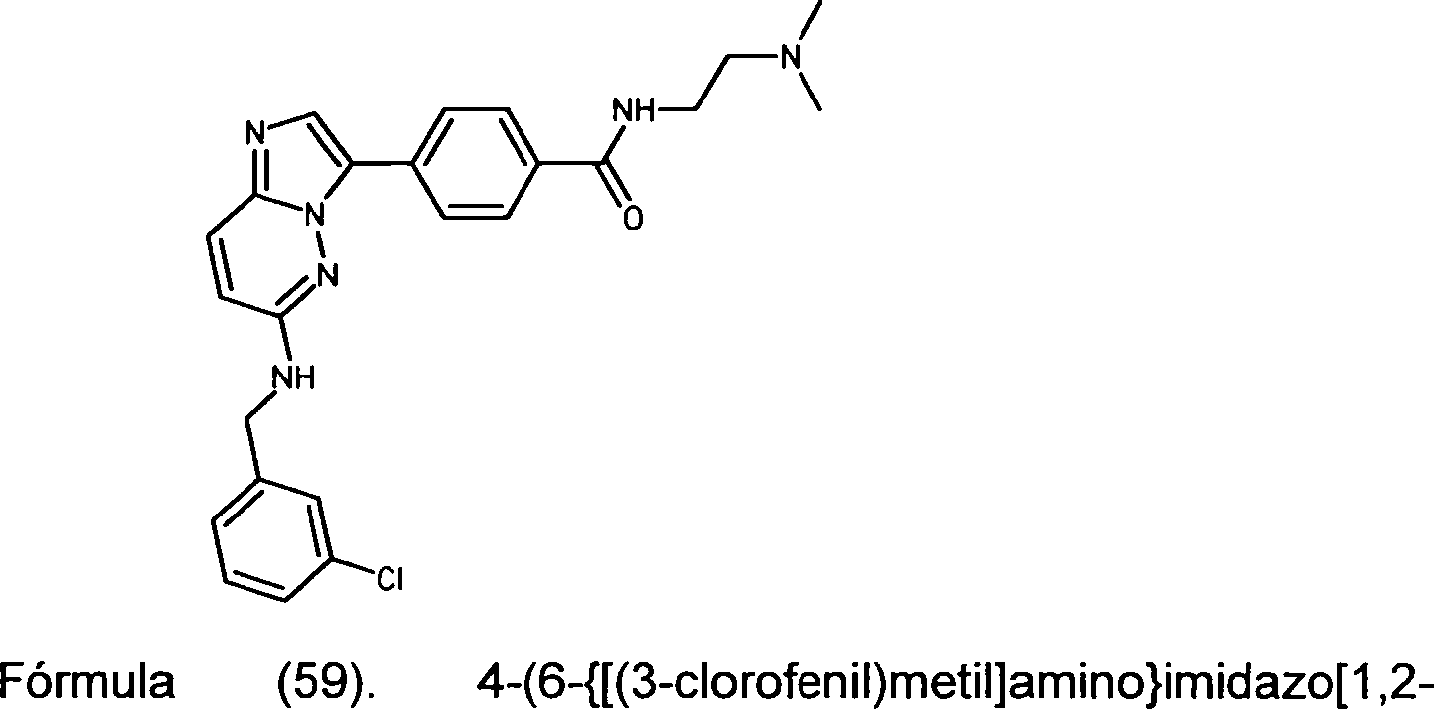
BRPI0914116A2 - diferenciação de células-tronco pluripotentes - Google Patents
diferenciação de células-tronco pluripotentes Download PDFInfo
- Publication number
- BRPI0914116A2 BRPI0914116A2 BRPI0914116A BRPI0914116A BRPI0914116A2 BR PI0914116 A2 BRPI0914116 A2 BR PI0914116A2 BR PI0914116 A BRPI0914116 A BR PI0914116A BR PI0914116 A BRPI0914116 A BR PI0914116A BR PI0914116 A2 BRPI0914116 A2 BR PI0914116A2
- Authority
- BR
- Brazil
- Prior art keywords
- cells
- cat
- compound
- cell
- test
- Prior art date
Links
- 210000001778 pluripotent stem cell Anatomy 0.000 title claims abstract description 70
- 230000024245 cell differentiation Effects 0.000 title abstract description 9
- 210000004027 cell Anatomy 0.000 claims abstract description 821
- 210000001900 endoderm Anatomy 0.000 claims abstract description 174
- 238000000034 method Methods 0.000 claims abstract description 126
- 150000001875 compounds Chemical class 0.000 claims description 330
- 108010023082 activin A Proteins 0.000 claims description 198
- 102100039939 Growth/differentiation factor 8 Human genes 0.000 claims description 194
- 108010056852 Myostatin Proteins 0.000 claims description 187
- -1 PDGF-B Proteins 0.000 claims description 71
- SCVDQROBPYCNAO-UHFFFAOYSA-N aniline;pyrido[3,2-d]triazine Chemical compound NC1=CC=CC=C1.C1=NN=NC2=CC=CN=C21 SCVDQROBPYCNAO-UHFFFAOYSA-N 0.000 claims description 58
- ZJQHPWUVQPJPQT-UHFFFAOYSA-N muscimol Chemical compound NCC1=CC(=O)NO1 ZJQHPWUVQPJPQT-UHFFFAOYSA-N 0.000 claims description 50
- 125000004122 cyclic group Chemical group 0.000 claims description 41
- 102100028072 Fibroblast growth factor 4 Human genes 0.000 claims description 35
- 101001060274 Homo sapiens Fibroblast growth factor 4 Proteins 0.000 claims description 35
- 102100037596 Platelet-derived growth factor subunit A Human genes 0.000 claims description 32
- 108010017843 platelet-derived growth factor A Proteins 0.000 claims description 32
- 102000005789 Vascular Endothelial Growth Factors Human genes 0.000 claims description 26
- 108010019530 Vascular Endothelial Growth Factors Proteins 0.000 claims description 26
- 101710170209 Platelet-derived growth factor D Proteins 0.000 claims description 17
- 102100040682 Platelet-derived growth factor D Human genes 0.000 claims description 16
- MFBOGIVSZKQAPD-UHFFFAOYSA-M sodium butyrate Chemical compound [Na+].CCCC([O-])=O MFBOGIVSZKQAPD-UHFFFAOYSA-M 0.000 claims description 10
- 108010017992 platelet-derived growth factor C Proteins 0.000 claims description 9
- 102100040681 Platelet-derived growth factor C Human genes 0.000 claims description 8
- 102000009024 Epidermal Growth Factor Human genes 0.000 claims 1
- 101710098940 Pro-epidermal growth factor Proteins 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 9
- 238000012258 culturing Methods 0.000 abstract description 5
- 101150004578 gdf-8 gene Proteins 0.000 abstract description 4
- 238000012360 testing method Methods 0.000 description 331
- 230000004069 differentiation Effects 0.000 description 274
- 238000011282 treatment Methods 0.000 description 172
- 230000014509 gene expression Effects 0.000 description 165
- 239000003102 growth factor Substances 0.000 description 158
- 239000002609 medium Substances 0.000 description 153
- 210000001671 embryonic stem cell Anatomy 0.000 description 124
- 102100030243 Transcription factor SOX-17 Human genes 0.000 description 122
- 101000652324 Homo sapiens Transcription factor SOX-17 Proteins 0.000 description 120
- 238000004458 analytical method Methods 0.000 description 85
- NOESYZHRGYRDHS-UHFFFAOYSA-N insulin Chemical compound N1C(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(NC(=O)CN)C(C)CC)CSSCC(C(NC(CO)C(=O)NC(CC(C)C)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CCC(N)=O)C(=O)NC(CC(C)C)C(=O)NC(CCC(O)=O)C(=O)NC(CC(N)=O)C(=O)NC(CC=2C=CC(O)=CC=2)C(=O)NC(CSSCC(NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2C=CC(O)=CC=2)NC(=O)C(CC(C)C)NC(=O)C(C)NC(=O)C(CCC(O)=O)NC(=O)C(C(C)C)NC(=O)C(CC(C)C)NC(=O)C(CC=2NC=NC=2)NC(=O)C(CO)NC(=O)CNC2=O)C(=O)NCC(=O)NC(CCC(O)=O)C(=O)NC(CCCNC(N)=N)C(=O)NCC(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC=CC=3)C(=O)NC(CC=3C=CC(O)=CC=3)C(=O)NC(C(C)O)C(=O)N3C(CCC3)C(=O)NC(CCCCN)C(=O)NC(C)C(O)=O)C(=O)NC(CC(N)=O)C(O)=O)=O)NC(=O)C(C(C)CC)NC(=O)C(CO)NC(=O)C(C(C)O)NC(=O)C1CSSCC2NC(=O)C(CC(C)C)NC(=O)C(NC(=O)C(CCC(N)=O)NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(N)CC=1C=CC=CC=1)C(C)C)CC1=CN=CN1 NOESYZHRGYRDHS-UHFFFAOYSA-N 0.000 description 82
- SMNRFWMNPDABKZ-WVALLCKVSA-N [[(2R,3S,4R,5S)-5-(2,6-dioxo-3H-pyridin-3-yl)-3,4-dihydroxyoxolan-2-yl]methoxy-hydroxyphosphoryl] [[[(2R,3S,4S,5R,6R)-4-fluoro-3,5-dihydroxy-6-(hydroxymethyl)oxan-2-yl]oxy-hydroxyphosphoryl]oxy-hydroxyphosphoryl] hydrogen phosphate Chemical compound OC[C@H]1O[C@H](OP(O)(=O)OP(O)(=O)OP(O)(=O)OP(O)(=O)OC[C@H]2O[C@H]([C@H](O)[C@@H]2O)C2C=CC(=O)NC2=O)[C@H](O)[C@@H](F)[C@@H]1O SMNRFWMNPDABKZ-WVALLCKVSA-N 0.000 description 75
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 69
- 239000013641 positive control Substances 0.000 description 65
- 108090000623 proteins and genes Proteins 0.000 description 60
- 239000006144 Dulbecco’s modified Eagle's medium Substances 0.000 description 59
- 108010082117 matrigel Proteins 0.000 description 57
- 241000287828 Gallus gallus Species 0.000 description 56
- 125000000217 alkyl group Chemical group 0.000 description 53
- 239000000523 sample Substances 0.000 description 51
- 210000002966 serum Anatomy 0.000 description 50
- 230000002829 reductive effect Effects 0.000 description 49
- 102000004169 proteins and genes Human genes 0.000 description 47
- 102000004877 Insulin Human genes 0.000 description 42
- 108090001061 Insulin Proteins 0.000 description 42
- 239000012103 Alexa Fluor 488 Substances 0.000 description 41
- 239000001963 growth medium Substances 0.000 description 41
- 229940125396 insulin Drugs 0.000 description 41
- 230000002354 daily effect Effects 0.000 description 40
- 239000003112 inhibitor Substances 0.000 description 39
- 150000003384 small molecules Chemical class 0.000 description 38
- 210000001519 tissue Anatomy 0.000 description 38
- 238000012216 screening Methods 0.000 description 37
- PRDFBSVERLRRMY-UHFFFAOYSA-N 2'-(4-ethoxyphenyl)-5-(4-methylpiperazin-1-yl)-2,5'-bibenzimidazole Chemical compound C1=CC(OCC)=CC=C1C1=NC2=CC=C(C=3NC4=CC(=CC=C4N=3)N3CCN(C)CC3)C=C2N1 PRDFBSVERLRRMY-UHFFFAOYSA-N 0.000 description 36
- 101710183548 Pyridoxal 5'-phosphate synthase subunit PdxS Proteins 0.000 description 36
- VBEQCZHXXJYVRD-GACYYNSASA-N uroanthelone Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CS)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CS)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)NCC(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CS)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C(C)C)[C@@H](C)O)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H](CCSC)NC(=O)[C@H](CS)NC(=O)[C@@H](NC(=O)CNC(=O)CNC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CS)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CS)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC(N)=O)C(C)C)[C@@H](C)CC)C1=CC=C(O)C=C1 VBEQCZHXXJYVRD-GACYYNSASA-N 0.000 description 36
- 239000003636 conditioned culture medium Substances 0.000 description 35
- 230000000694 effects Effects 0.000 description 35
- 210000004940 nucleus Anatomy 0.000 description 35
- 102400001368 Epidermal growth factor Human genes 0.000 description 34
- 101800003838 Epidermal growth factor Proteins 0.000 description 34
- 229940116977 epidermal growth factor Drugs 0.000 description 34
- 238000010790 dilution Methods 0.000 description 33
- 239000012895 dilution Substances 0.000 description 33
- 230000009996 pancreatic endocrine effect Effects 0.000 description 33
- 102100031650 C-X-C chemokine receptor type 4 Human genes 0.000 description 32
- 101000922348 Homo sapiens C-X-C chemokine receptor type 4 Proteins 0.000 description 32
- 239000013642 negative control Substances 0.000 description 32
- 238000002360 preparation method Methods 0.000 description 29
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 27
- 241000699670 Mus sp. Species 0.000 description 27
- HUWSZNZAROKDRZ-RRLWZMAJSA-N (3r,4r)-3-azaniumyl-5-[[(2s,3r)-1-[(2s)-2,3-dicarboxypyrrolidin-1-yl]-3-methyl-1-oxopentan-2-yl]amino]-5-oxo-4-sulfanylpentane-1-sulfonate Chemical compound OS(=O)(=O)CC[C@@H](N)[C@@H](S)C(=O)N[C@@H]([C@H](C)CC)C(=O)N1CCC(C(O)=O)[C@H]1C(O)=O HUWSZNZAROKDRZ-RRLWZMAJSA-N 0.000 description 26
- 230000015572 biosynthetic process Effects 0.000 description 26
- 239000008103 glucose Substances 0.000 description 25
- 108090000765 processed proteins & peptides Proteins 0.000 description 25
- 239000012980 RPMI-1640 medium Substances 0.000 description 23
- 238000005406 washing Methods 0.000 description 22
- 108020004414 DNA Proteins 0.000 description 21
- 210000000227 basophil cell of anterior lobe of hypophysis Anatomy 0.000 description 21
- 238000013100 final test Methods 0.000 description 21
- 241000283707 Capra Species 0.000 description 20
- 239000003550 marker Substances 0.000 description 20
- 239000008188 pellet Substances 0.000 description 20
- 238000007790 scraping Methods 0.000 description 20
- 102000051325 Glucagon Human genes 0.000 description 19
- 108060003199 Glucagon Proteins 0.000 description 19
- 241000699666 Mus <mouse, genus> Species 0.000 description 19
- 125000003545 alkoxy group Chemical group 0.000 description 19
- 108010007093 dispase Proteins 0.000 description 19
- 238000002054 transplantation Methods 0.000 description 19
- 102000001267 GSK3 Human genes 0.000 description 18
- 108060006662 GSK3 Proteins 0.000 description 18
- 102100041030 Pancreas/duodenum homeobox protein 1 Human genes 0.000 description 18
- 229930040373 Paraformaldehyde Natural products 0.000 description 18
- 238000010240 RT-PCR analysis Methods 0.000 description 18
- 229920004890 Triton X-100 Polymers 0.000 description 18
- 239000013504 Triton X-100 Substances 0.000 description 18
- 229960004666 glucagon Drugs 0.000 description 18
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 18
- 125000000623 heterocyclic group Chemical group 0.000 description 18
- 238000005259 measurement Methods 0.000 description 18
- NFVJNJQRWPQVOA-UHFFFAOYSA-N n-[2-chloro-5-(trifluoromethyl)phenyl]-2-[3-(4-ethyl-5-ethylsulfanyl-1,2,4-triazol-3-yl)piperidin-1-yl]acetamide Chemical compound CCN1C(SCC)=NN=C1C1CN(CC(=O)NC=2C(=CC=C(C=2)C(F)(F)F)Cl)CCC1 NFVJNJQRWPQVOA-UHFFFAOYSA-N 0.000 description 18
- 229920002866 paraformaldehyde Polymers 0.000 description 18
- 125000003386 piperidinyl group Chemical group 0.000 description 18
- 230000035755 proliferation Effects 0.000 description 18
- 125000000719 pyrrolidinyl group Chemical group 0.000 description 18
- 230000011218 segmentation Effects 0.000 description 18
- IWZSHWBGHQBIML-ZGGLMWTQSA-N (3S,8S,10R,13S,14S,17S)-17-isoquinolin-7-yl-N,N,10,13-tetramethyl-2,3,4,7,8,9,11,12,14,15,16,17-dodecahydro-1H-cyclopenta[a]phenanthren-3-amine Chemical compound CN(C)[C@H]1CC[C@]2(C)C3CC[C@@]4(C)[C@@H](CC[C@@H]4c4ccc5ccncc5c4)[C@@H]3CC=C2C1 IWZSHWBGHQBIML-ZGGLMWTQSA-N 0.000 description 17
- 108010059616 Activins Proteins 0.000 description 17
- 239000000488 activin Substances 0.000 description 17
- 125000001424 substituent group Chemical group 0.000 description 17
- 239000000758 substrate Substances 0.000 description 17
- SHGAZHPCJJPHSC-YCNIQYBTSA-N all-trans-retinoic acid Chemical compound OC(=O)\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C SHGAZHPCJJPHSC-YCNIQYBTSA-N 0.000 description 16
- 238000004166 bioassay Methods 0.000 description 16
- 230000002124 endocrine Effects 0.000 description 16
- 238000003384 imaging method Methods 0.000 description 16
- 210000004039 endoderm cell Anatomy 0.000 description 15
- 125000004193 piperazinyl group Chemical group 0.000 description 15
- 239000000243 solution Substances 0.000 description 15
- 238000009331 sowing Methods 0.000 description 15
- 102100026818 Inhibin beta E chain Human genes 0.000 description 14
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 14
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 description 13
- 102100024506 Bone morphogenetic protein 2 Human genes 0.000 description 13
- 108060005980 Collagenase Proteins 0.000 description 13
- 102000029816 Collagenase Human genes 0.000 description 13
- 238000012413 Fluorescence activated cell sorting analysis Methods 0.000 description 13
- 238000004113 cell culture Methods 0.000 description 13
- 229960002424 collagenase Drugs 0.000 description 13
- 238000000684 flow cytometry Methods 0.000 description 13
- 230000012010 growth Effects 0.000 description 13
- 229920003023 plastic Polymers 0.000 description 13
- 239000004033 plastic Substances 0.000 description 13
- 229930002330 retinoic acid Natural products 0.000 description 13
- 108091032973 (ribonucleotides)n+m Proteins 0.000 description 12
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 12
- 230000006727 cell loss Effects 0.000 description 12
- 229910052739 hydrogen Inorganic materials 0.000 description 12
- 239000001257 hydrogen Substances 0.000 description 12
- 238000000338 in vitro Methods 0.000 description 12
- 238000010186 staining Methods 0.000 description 12
- VOUAQYXWVJDEQY-QENPJCQMSA-N 33017-11-7 Chemical compound OC(=O)CC[C@H](N)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)NCC(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)NCC(=O)NCC(=O)N1CCC[C@H]1C(=O)NCC(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N1[C@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(O)=O)CCC1 VOUAQYXWVJDEQY-QENPJCQMSA-N 0.000 description 11
- 102000004190 Enzymes Human genes 0.000 description 11
- 108090000790 Enzymes Proteins 0.000 description 11
- 102100028071 Fibroblast growth factor 7 Human genes 0.000 description 11
- 101001060261 Homo sapiens Fibroblast growth factor 7 Proteins 0.000 description 11
- 239000003795 chemical substances by application Substances 0.000 description 11
- 230000001143 conditioned effect Effects 0.000 description 11
- 229940088598 enzyme Drugs 0.000 description 11
- 238000001943 fluorescence-activated cell sorting Methods 0.000 description 11
- 229940088597 hormone Drugs 0.000 description 11
- 239000005556 hormone Substances 0.000 description 11
- 239000003068 molecular probe Substances 0.000 description 11
- 229960001727 tretinoin Drugs 0.000 description 11
- 108010011459 Exenatide Proteins 0.000 description 10
- 108090000723 Insulin-Like Growth Factor I Proteins 0.000 description 10
- 241000204031 Mycoplasma Species 0.000 description 10
- JUFFVKRROAPVBI-PVOYSMBESA-N chembl1210015 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(=O)N[C@H]1[C@@H]([C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O)[C@@H](O)[C@@H](CO[C@]3(O[C@@H](C[C@H](O)[C@H](O)CO)[C@H](NC(C)=O)[C@@H](O)C3)C(O)=O)O2)O)[C@@H](CO)O1)NC(C)=O)C(=O)NCC(=O)NCC(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)NCC(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)CNC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 JUFFVKRROAPVBI-PVOYSMBESA-N 0.000 description 10
- 229960001519 exenatide Drugs 0.000 description 10
- 150000002431 hydrogen Chemical class 0.000 description 10
- 125000002757 morpholinyl group Chemical group 0.000 description 10
- 238000003757 reverse transcription PCR Methods 0.000 description 10
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 9
- 108010049931 Bone Morphogenetic Protein 2 Proteins 0.000 description 9
- 108010075254 C-Peptide Proteins 0.000 description 9
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 9
- 108010037362 Extracellular Matrix Proteins Proteins 0.000 description 9
- 102000010834 Extracellular Matrix Proteins Human genes 0.000 description 9
- 102000018233 Fibroblast Growth Factor Human genes 0.000 description 9
- 108050007372 Fibroblast Growth Factor Proteins 0.000 description 9
- 108010090254 Growth Differentiation Factor 5 Proteins 0.000 description 9
- 102100035379 Growth/differentiation factor 5 Human genes 0.000 description 9
- 239000007995 HEPES buffer Substances 0.000 description 9
- 102000040945 Transcription factor Human genes 0.000 description 9
- 108091023040 Transcription factor Proteins 0.000 description 9
- 210000004369 blood Anatomy 0.000 description 9
- 239000008280 blood Substances 0.000 description 9
- 239000000872 buffer Substances 0.000 description 9
- 239000002775 capsule Substances 0.000 description 9
- 239000002299 complementary DNA Substances 0.000 description 9
- 238000001514 detection method Methods 0.000 description 9
- 239000006185 dispersion Substances 0.000 description 9
- 210000003890 endocrine cell Anatomy 0.000 description 9
- 210000002744 extracellular matrix Anatomy 0.000 description 9
- WDHRPWOAMDJICD-FOAQWNCLSA-N n-[2-[(3'r,3'as,6's,6as,6bs,7'ar,9r,11as,11br)-3',6',10,11b-tetramethyl-3-oxospiro[1,2,4,6,6a,6b,7,8,11,11a-decahydrobenzo[a]fluorene-9,2'-3,3a,5,6,7,7a-hexahydrofuro[3,2-b]pyridine]-4'-yl]ethyl]-6-(3-phenylpropanoylamino)hexanamide Chemical compound C([C@@H](C)C[C@@H]1[C@@H]2[C@H]([C@]3(C(=C4C[C@@H]5[C@@]6(C)CCC(=O)CC6=CC[C@H]5[C@@H]4CC3)C)O1)C)N2CCNC(=O)CCCCCNC(=O)CCC1=CC=CC=C1 WDHRPWOAMDJICD-FOAQWNCLSA-N 0.000 description 9
- 230000004044 response Effects 0.000 description 9
- 239000002356 single layer Substances 0.000 description 9
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 description 8
- 102100024505 Bone morphogenetic protein 4 Human genes 0.000 description 8
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 8
- 102100038553 Neurogenin-3 Human genes 0.000 description 8
- 238000001727 in vivo Methods 0.000 description 8
- 210000003734 kidney Anatomy 0.000 description 8
- 238000012423 maintenance Methods 0.000 description 8
- 239000004005 microsphere Substances 0.000 description 8
- 239000002243 precursor Substances 0.000 description 8
- 230000003248 secreting effect Effects 0.000 description 8
- 102000024905 CD99 Human genes 0.000 description 7
- 108060001253 CD99 Proteins 0.000 description 7
- 108010083123 CDX2 Transcription Factor Proteins 0.000 description 7
- 102000006277 CDX2 Transcription Factor Human genes 0.000 description 7
- 102100040896 Growth/differentiation factor 15 Human genes 0.000 description 7
- 102100035364 Growth/differentiation factor 3 Human genes 0.000 description 7
- 102100028096 Homeobox protein Nkx-6.2 Human genes 0.000 description 7
- 101000886562 Homo sapiens Growth/differentiation factor 8 Proteins 0.000 description 7
- 101000578254 Homo sapiens Homeobox protein Nkx-6.1 Proteins 0.000 description 7
- 101000578258 Homo sapiens Homeobox protein Nkx-6.2 Proteins 0.000 description 7
- 101001053263 Homo sapiens Insulin gene enhancer protein ISL-1 Proteins 0.000 description 7
- 101000603702 Homo sapiens Neurogenin-3 Proteins 0.000 description 7
- 102100024392 Insulin gene enhancer protein ISL-1 Human genes 0.000 description 7
- 102000052651 Pancreatic hormone Human genes 0.000 description 7
- 239000004743 Polypropylene Substances 0.000 description 7
- 235000014113 dietary fatty acids Nutrition 0.000 description 7
- 229930195729 fatty acid Natural products 0.000 description 7
- 239000000194 fatty acid Substances 0.000 description 7
- 150000004665 fatty acids Chemical class 0.000 description 7
- 125000001475 halogen functional group Chemical group 0.000 description 7
- QYSGYZVSCZSLHT-UHFFFAOYSA-N octafluoropropane Chemical compound FC(F)(F)C(F)(F)C(F)(F)F QYSGYZVSCZSLHT-UHFFFAOYSA-N 0.000 description 7
- 239000004025 pancreas hormone Substances 0.000 description 7
- 229940032957 pancreatic hormone Drugs 0.000 description 7
- 229920001155 polypropylene Polymers 0.000 description 7
- 125000002924 primary amino group Chemical group [H]N([H])* 0.000 description 7
- 101710201246 Eomesodermin Proteins 0.000 description 6
- 102100030751 Eomesodermin homolog Human genes 0.000 description 6
- 102100040895 Growth/differentiation factor 10 Human genes 0.000 description 6
- 102000003693 Hedgehog Proteins Human genes 0.000 description 6
- 108090000031 Hedgehog Proteins Proteins 0.000 description 6
- 102100029087 Hepatocyte nuclear factor 6 Human genes 0.000 description 6
- 101000613495 Homo sapiens Paired box protein Pax-4 Proteins 0.000 description 6
- 102000004218 Insulin-Like Growth Factor I Human genes 0.000 description 6
- 101150079937 NEUROD1 gene Proteins 0.000 description 6
- 102100032063 Neurogenic differentiation factor 1 Human genes 0.000 description 6
- 102100040909 Paired box protein Pax-4 Human genes 0.000 description 6
- 101800001268 Pancreatic hormone Proteins 0.000 description 6
- 108010056088 Somatostatin Proteins 0.000 description 6
- 102000005157 Somatostatin Human genes 0.000 description 6
- 102000043168 TGF-beta family Human genes 0.000 description 6
- 108091085018 TGF-beta family Proteins 0.000 description 6
- 230000003321 amplification Effects 0.000 description 6
- 230000000875 corresponding effect Effects 0.000 description 6
- 210000001654 germ layer Anatomy 0.000 description 6
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 6
- 125000002632 imidazolidinyl group Chemical group 0.000 description 6
- 230000000968 intestinal effect Effects 0.000 description 6
- 239000000463 material Substances 0.000 description 6
- 238000003199 nucleic acid amplification method Methods 0.000 description 6
- 239000008177 pharmaceutical agent Substances 0.000 description 6
- 125000003373 pyrazinyl group Chemical group 0.000 description 6
- 125000003072 pyrazolidinyl group Chemical group 0.000 description 6
- 125000004076 pyridyl group Chemical group 0.000 description 6
- 125000000714 pyrimidinyl group Chemical group 0.000 description 6
- 229910052711 selenium Inorganic materials 0.000 description 6
- 239000011669 selenium Substances 0.000 description 6
- 229960000553 somatostatin Drugs 0.000 description 6
- NHXLMOGPVYXJNR-ATOGVRKGSA-N somatostatin Chemical compound C([C@H]1C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CSSC[C@@H](C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2C3=CC=CC=C3NC=2)C(=O)N[C@@H](CCCCN)C(=O)N[C@H](C(=O)N1)[C@@H](C)O)NC(=O)CNC(=O)[C@H](C)N)C(O)=O)=O)[C@H](O)C)C1=CC=CC=C1 NHXLMOGPVYXJNR-ATOGVRKGSA-N 0.000 description 6
- WWTBZEKOSBFBEM-SPWPXUSOSA-N (2s)-2-[[2-benzyl-3-[hydroxy-[(1r)-2-phenyl-1-(phenylmethoxycarbonylamino)ethyl]phosphoryl]propanoyl]amino]-3-(1h-indol-3-yl)propanoic acid Chemical compound N([C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)O)C(=O)C(CP(O)(=O)[C@H](CC=1C=CC=CC=1)NC(=O)OCC=1C=CC=CC=1)CC1=CC=CC=C1 WWTBZEKOSBFBEM-SPWPXUSOSA-N 0.000 description 5
- 125000005913 (C3-C6) cycloalkyl group Chemical group 0.000 description 5
- HFDKKNHCYWNNNQ-YOGANYHLSA-N 75976-10-2 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]1N(CCC1)C(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@H]1N(CCC1)C(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@@H](NC(=O)[C@H]1N(CCC1)C(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]1N(CCC1)C(=O)[C@H](C)N)C(C)C)[C@@H](C)O)C1=CC=C(O)C=C1 HFDKKNHCYWNNNQ-YOGANYHLSA-N 0.000 description 5
- 239000012114 Alexa Fluor 647 Substances 0.000 description 5
- 108010041834 Growth Differentiation Factor 15 Proteins 0.000 description 5
- 108010090293 Growth Differentiation Factor 3 Proteins 0.000 description 5
- 102100040898 Growth/differentiation factor 11 Human genes 0.000 description 5
- 108090000100 Hepatocyte Growth Factor Proteins 0.000 description 5
- 102100021866 Hepatocyte growth factor Human genes 0.000 description 5
- 101000988619 Homo sapiens Hepatocyte nuclear factor 6 Proteins 0.000 description 5
- 102000018886 Pancreatic Polypeptide Human genes 0.000 description 5
- 101000983124 Sus scrofa Pancreatic prohormone precursor Proteins 0.000 description 5
- 125000003342 alkenyl group Chemical group 0.000 description 5
- 238000013459 approach Methods 0.000 description 5
- 238000003556 assay Methods 0.000 description 5
- 239000007640 basal medium Substances 0.000 description 5
- 230000000052 comparative effect Effects 0.000 description 5
- 229940126208 compound 22 Drugs 0.000 description 5
- 125000000753 cycloalkyl group Chemical group 0.000 description 5
- 206010012601 diabetes mellitus Diseases 0.000 description 5
- 239000000975 dye Substances 0.000 description 5
- 229940126864 fibroblast growth factor Drugs 0.000 description 5
- 230000005484 gravity Effects 0.000 description 5
- 239000003966 growth inhibitor Substances 0.000 description 5
- 230000001965 increasing effect Effects 0.000 description 5
- 230000006698 induction Effects 0.000 description 5
- 230000001939 inductive effect Effects 0.000 description 5
- 239000010410 layer Substances 0.000 description 5
- 238000010899 nucleation Methods 0.000 description 5
- 102000039446 nucleic acids Human genes 0.000 description 5
- 108020004707 nucleic acids Proteins 0.000 description 5
- 150000007523 nucleic acids Chemical class 0.000 description 5
- 210000000496 pancreas Anatomy 0.000 description 5
- 230000008569 process Effects 0.000 description 5
- 239000012474 protein marker Substances 0.000 description 5
- 230000011664 signaling Effects 0.000 description 5
- 210000000130 stem cell Anatomy 0.000 description 5
- 239000011550 stock solution Substances 0.000 description 5
- 238000007920 subcutaneous administration Methods 0.000 description 5
- 239000013589 supplement Substances 0.000 description 5
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 5
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 4
- 108010049955 Bone Morphogenetic Protein 4 Proteins 0.000 description 4
- 108010049870 Bone Morphogenetic Protein 7 Proteins 0.000 description 4
- 102100024504 Bone morphogenetic protein 3 Human genes 0.000 description 4
- 102100022544 Bone morphogenetic protein 7 Human genes 0.000 description 4
- 241000283690 Bos taurus Species 0.000 description 4
- DWJXYEABWRJFSP-XOBRGWDASA-N DAPT Chemical compound N([C@@H](C)C(=O)N[C@H](C(=O)OC(C)(C)C)C=1C=CC=CC=1)C(=O)CC1=CC(F)=CC(F)=C1 DWJXYEABWRJFSP-XOBRGWDASA-N 0.000 description 4
- 101100518002 Danio rerio nkx2.2a gene Proteins 0.000 description 4
- 238000002965 ELISA Methods 0.000 description 4
- OHCQJHSOBUTRHG-KGGHGJDLSA-N FORSKOLIN Chemical compound O=C([C@@]12O)C[C@](C)(C=C)O[C@]1(C)[C@@H](OC(=O)C)[C@@H](O)[C@@H]1[C@]2(C)[C@@H](O)CCC1(C)C OHCQJHSOBUTRHG-KGGHGJDLSA-N 0.000 description 4
- 102000003972 Fibroblast growth factor 7 Human genes 0.000 description 4
- 108090000385 Fibroblast growth factor 7 Proteins 0.000 description 4
- 108010041881 Growth Differentiation Factor 10 Proteins 0.000 description 4
- 108700014808 Homeobox Protein Nkx-2.2 Proteins 0.000 description 4
- 102100027886 Homeobox protein Nkx-2.2 Human genes 0.000 description 4
- 101000762366 Homo sapiens Bone morphogenetic protein 2 Proteins 0.000 description 4
- 101000762379 Homo sapiens Bone morphogenetic protein 4 Proteins 0.000 description 4
- 101000971533 Homo sapiens Killer cell lectin-like receptor subfamily G member 1 Proteins 0.000 description 4
- 101100460496 Homo sapiens NKX2-2 gene Proteins 0.000 description 4
- 101000819074 Homo sapiens Transcription factor GATA-4 Proteins 0.000 description 4
- 101000979205 Homo sapiens Transcription factor MafA Proteins 0.000 description 4
- 102000003982 Parathyroid hormone Human genes 0.000 description 4
- 108090000445 Parathyroid hormone Proteins 0.000 description 4
- RJKFOVLPORLFTN-LEKSSAKUSA-N Progesterone Chemical compound C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 RJKFOVLPORLFTN-LEKSSAKUSA-N 0.000 description 4
- 238000011579 SCID mouse model Methods 0.000 description 4
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 4
- 102000013275 Somatomedins Human genes 0.000 description 4
- 102100021380 Transcription factor GATA-4 Human genes 0.000 description 4
- 102100023237 Transcription factor MafA Human genes 0.000 description 4
- 102000004887 Transforming Growth Factor beta Human genes 0.000 description 4
- 108090001012 Transforming Growth Factor beta Proteins 0.000 description 4
- DFPAKSUCGFBDDF-ZQBYOMGUSA-N [14c]-nicotinamide Chemical compound N[14C](=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-ZQBYOMGUSA-N 0.000 description 4
- 239000003153 chemical reaction reagent Substances 0.000 description 4
- 239000000306 component Substances 0.000 description 4
- 238000011109 contamination Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 238000011977 dual antiplatelet therapy Methods 0.000 description 4
- 210000002308 embryonic cell Anatomy 0.000 description 4
- 238000011156 evaluation Methods 0.000 description 4
- JYGXADMDTFJGBT-VWUMJDOOSA-N hydrocortisone Chemical compound O=C1CC[C@]2(C)[C@H]3[C@@H](O)C[C@](C)([C@@](CC4)(O)C(=O)CO)[C@@H]4[C@@H]3CCC2=C1 JYGXADMDTFJGBT-VWUMJDOOSA-N 0.000 description 4
- ZPNFWUPYTFPOJU-LPYSRVMUSA-N iniprol Chemical compound C([C@H]1C(=O)NCC(=O)NCC(=O)N[C@H]2CSSC[C@H]3C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@H](C(N[C@H](C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC=4C=CC=CC=4)C(=O)N[C@@H](CC=4C=CC(O)=CC=4)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](C)C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CC=4C=CC=CC=4)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC2=O)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H]2N(CCC2)C(=O)[C@@H](N)CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2[C@@H](CCC2)C(=O)N2[C@@H](CCC2)C(=O)N[C@@H](CC=2C=CC(O)=CC=2)C(=O)N[C@@H]([C@@H](C)O)C(=O)NCC(=O)N2[C@@H](CCC2)C(=O)N3)C(=O)NCC(=O)NCC(=O)N[C@@H](C)C(O)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@H](C(=O)N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@H](C(=O)N1)C(C)C)[C@@H](C)O)[C@@H](C)CC)=O)[C@@H](C)CC)C1=CC=C(O)C=C1 ZPNFWUPYTFPOJU-LPYSRVMUSA-N 0.000 description 4
- OGQSCIYDJSNCMY-UHFFFAOYSA-H iron(3+);methyl-dioxido-oxo-$l^{5}-arsane Chemical compound [Fe+3].[Fe+3].C[As]([O-])([O-])=O.C[As]([O-])([O-])=O.C[As]([O-])([O-])=O OGQSCIYDJSNCMY-UHFFFAOYSA-H 0.000 description 4
- 210000003205 muscle Anatomy 0.000 description 4
- 239000000199 parathyroid hormone Substances 0.000 description 4
- 229960001319 parathyroid hormone Drugs 0.000 description 4
- 210000004623 platelet-rich plasma Anatomy 0.000 description 4
- 102000004196 processed proteins & peptides Human genes 0.000 description 4
- 125000000168 pyrrolyl group Chemical group 0.000 description 4
- 210000003491 skin Anatomy 0.000 description 4
- 239000006228 supernatant Substances 0.000 description 4
- 238000001356 surgical procedure Methods 0.000 description 4
- 230000004083 survival effect Effects 0.000 description 4
- ZRKFYGHZFMAOKI-QMGMOQQFSA-N tgfbeta Chemical compound C([C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CC(C)C)NC(=O)CNC(=O)[C@H](C)NC(=O)[C@H](CO)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](N)CCSC)C(C)C)[C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C)C(=O)N[C@@H](CC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(O)=O)C1=CC=C(O)C=C1 ZRKFYGHZFMAOKI-QMGMOQQFSA-N 0.000 description 4
- 238000004448 titration Methods 0.000 description 4
- UBWXUGDQUBIEIZ-UHFFFAOYSA-N (13-methyl-3-oxo-2,6,7,8,9,10,11,12,14,15,16,17-dodecahydro-1h-cyclopenta[a]phenanthren-17-yl) 3-phenylpropanoate Chemical compound CC12CCC(C3CCC(=O)C=C3CC3)C3C1CCC2OC(=O)CCC1=CC=CC=C1 UBWXUGDQUBIEIZ-UHFFFAOYSA-N 0.000 description 3
- ABJSOROVZZKJGI-OCYUSGCXSA-N (1r,2r,4r)-2-(4-bromophenyl)-n-[(4-chlorophenyl)-(2-fluoropyridin-4-yl)methyl]-4-morpholin-4-ylcyclohexane-1-carboxamide Chemical compound C1=NC(F)=CC(C(NC(=O)[C@H]2[C@@H](C[C@@H](CC2)N2CCOCC2)C=2C=CC(Br)=CC=2)C=2C=CC(Cl)=CC=2)=C1 ABJSOROVZZKJGI-OCYUSGCXSA-N 0.000 description 3
- 125000004180 3-fluorophenyl group Chemical group [H]C1=C([H])C(*)=C([H])C(F)=C1[H] 0.000 description 3
- 102000005606 Activins Human genes 0.000 description 3
- WPYMKLBDIGXBTP-UHFFFAOYSA-N Benzoic acid Natural products OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 3
- 101800001382 Betacellulin Proteins 0.000 description 3
- 102400001242 Betacellulin Human genes 0.000 description 3
- 108010049974 Bone Morphogenetic Protein 6 Proteins 0.000 description 3
- 102100022525 Bone morphogenetic protein 6 Human genes 0.000 description 3
- 102100036008 CD48 antigen Human genes 0.000 description 3
- CURLTUGMZLYLDI-UHFFFAOYSA-N Carbon dioxide Chemical compound O=C=O CURLTUGMZLYLDI-UHFFFAOYSA-N 0.000 description 3
- 102100025745 Cerberus Human genes 0.000 description 3
- QASFUMOKHFSJGL-LAFRSMQTSA-N Cyclopamine Chemical compound C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H](CC2=C3C)[C@@H]1[C@@H]2CC[C@@]13O[C@@H]2C[C@H](C)CN[C@H]2[C@H]1C QASFUMOKHFSJGL-LAFRSMQTSA-N 0.000 description 3
- 102100037986 Dickkopf-related protein 4 Human genes 0.000 description 3
- 102100035308 Fibroblast growth factor 17 Human genes 0.000 description 3
- 102100037680 Fibroblast growth factor 8 Human genes 0.000 description 3
- 102100037362 Fibronectin Human genes 0.000 description 3
- 108010067306 Fibronectins Proteins 0.000 description 3
- 102100023374 Forkhead box protein M1 Human genes 0.000 description 3
- 101800000221 Glucagon-like peptide 2 Proteins 0.000 description 3
- 102400000326 Glucagon-like peptide 2 Human genes 0.000 description 3
- 101710194452 Growth/differentiation factor 11 Proteins 0.000 description 3
- HTTJABKRGRZYRN-UHFFFAOYSA-N Heparin Chemical compound OC1C(NC(=O)C)C(O)OC(COS(O)(=O)=O)C1OC1C(OS(O)(=O)=O)C(O)C(OC2C(C(OS(O)(=O)=O)C(OC3C(C(O)C(O)C(O3)C(O)=O)OS(O)(=O)=O)C(CO)O2)NS(O)(=O)=O)C(C(O)=O)O1 HTTJABKRGRZYRN-UHFFFAOYSA-N 0.000 description 3
- 102100022057 Hepatocyte nuclear factor 1-alpha Human genes 0.000 description 3
- 102100030634 Homeobox protein OTX2 Human genes 0.000 description 3
- 102000009331 Homeodomain Proteins Human genes 0.000 description 3
- 108010048671 Homeodomain Proteins Proteins 0.000 description 3
- 101000762375 Homo sapiens Bone morphogenetic protein 3 Proteins 0.000 description 3
- 101000716130 Homo sapiens CD48 antigen Proteins 0.000 description 3
- 101000951340 Homo sapiens Dickkopf-related protein 4 Proteins 0.000 description 3
- 101000878124 Homo sapiens Fibroblast growth factor 17 Proteins 0.000 description 3
- 101001027382 Homo sapiens Fibroblast growth factor 8 Proteins 0.000 description 3
- 101000907578 Homo sapiens Forkhead box protein M1 Proteins 0.000 description 3
- 101001066129 Homo sapiens Glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 3
- 101001045751 Homo sapiens Hepatocyte nuclear factor 1-alpha Proteins 0.000 description 3
- 101000584400 Homo sapiens Homeobox protein OTX2 Proteins 0.000 description 3
- 102100034343 Integrase Human genes 0.000 description 3
- 102100027754 Mast/stem cell growth factor receptor Kit Human genes 0.000 description 3
- 101500028740 Mus musculus Glucagon Proteins 0.000 description 3
- 238000000636 Northern blotting Methods 0.000 description 3
- 230000005913 Notch signaling pathway Effects 0.000 description 3
- 239000013614 RNA sample Substances 0.000 description 3
- 108010092799 RNA-directed DNA polymerase Proteins 0.000 description 3
- 238000011530 RNeasy Mini Kit Methods 0.000 description 3
- 241000283984 Rodentia Species 0.000 description 3
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 3
- 102000009618 Transforming Growth Factors Human genes 0.000 description 3
- 108010009583 Transforming Growth Factors Proteins 0.000 description 3
- 238000000137 annealing Methods 0.000 description 3
- 210000002469 basement membrane Anatomy 0.000 description 3
- 239000000090 biomarker Substances 0.000 description 3
- 210000002459 blastocyst Anatomy 0.000 description 3
- 235000011089 carbon dioxide Nutrition 0.000 description 3
- 230000005754 cellular signaling Effects 0.000 description 3
- 238000006243 chemical reaction Methods 0.000 description 3
- 239000011248 coating agent Substances 0.000 description 3
- 238000000576 coating method Methods 0.000 description 3
- 229940125898 compound 5 Drugs 0.000 description 3
- 230000001010 compromised effect Effects 0.000 description 3
- 239000000356 contaminant Substances 0.000 description 3
- QASFUMOKHFSJGL-UHFFFAOYSA-N cyclopamine Natural products C1C=C2CC(O)CCC2(C)C(CC2=C3C)C1C2CCC13OC2CC(C)CNC2C1C QASFUMOKHFSJGL-UHFFFAOYSA-N 0.000 description 3
- 238000007405 data analysis Methods 0.000 description 3
- 238000004925 denaturation Methods 0.000 description 3
- 230000036425 denaturation Effects 0.000 description 3
- 238000011161 development Methods 0.000 description 3
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 3
- 230000003203 everyday effect Effects 0.000 description 3
- 108010074605 gamma-Globulins Proteins 0.000 description 3
- 230000007045 gastrulation Effects 0.000 description 3
- TWSALRJGPBVBQU-PKQQPRCHSA-N glucagon-like peptide 2 Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CC(O)=O)C(O)=O)[C@@H](C)CC)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@@H](NC(=O)[C@H](CC(N)=O)NC(=O)[C@H](CCSC)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@H](CO)NC(=O)CNC(=O)[C@H](CC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)CC)C1=CC=CC=C1 TWSALRJGPBVBQU-PKQQPRCHSA-N 0.000 description 3
- 102000006602 glyceraldehyde-3-phosphate dehydrogenase Human genes 0.000 description 3
- 108020004445 glyceraldehyde-3-phosphate dehydrogenase Proteins 0.000 description 3
- 210000003958 hematopoietic stem cell Anatomy 0.000 description 3
- 229920000669 heparin Polymers 0.000 description 3
- 229960002897 heparin Drugs 0.000 description 3
- 102000047486 human GAPDH Human genes 0.000 description 3
- 238000003018 immunoassay Methods 0.000 description 3
- 238000002991 immunohistochemical analysis Methods 0.000 description 3
- 238000002513 implantation Methods 0.000 description 3
- 238000007901 in situ hybridization Methods 0.000 description 3
- 238000011534 incubation Methods 0.000 description 3
- 210000004153 islets of langerhan Anatomy 0.000 description 3
- 238000002955 isolation Methods 0.000 description 3
- 230000014759 maintenance of location Effects 0.000 description 3
- 238000004519 manufacturing process Methods 0.000 description 3
- 210000004379 membrane Anatomy 0.000 description 3
- 239000012528 membrane Substances 0.000 description 3
- 108010000685 platelet-derived growth factor AB Proteins 0.000 description 3
- 238000003752 polymerase chain reaction Methods 0.000 description 3
- 230000003389 potentiating effect Effects 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- 125000004307 pyrazin-2-yl group Chemical group [H]C1=C([H])N=C(*)C([H])=N1 0.000 description 3
- 238000003753 real-time PCR Methods 0.000 description 3
- 230000001105 regulatory effect Effects 0.000 description 3
- 230000002441 reversible effect Effects 0.000 description 3
- 239000000741 silica gel Substances 0.000 description 3
- 229910002027 silica gel Inorganic materials 0.000 description 3
- 239000000126 substance Substances 0.000 description 3
- 230000002195 synergetic effect Effects 0.000 description 3
- 230000035899 viability Effects 0.000 description 3
- 238000001262 western blot Methods 0.000 description 3
- DGVVWUTYPXICAM-UHFFFAOYSA-N β‐Mercaptoethanol Chemical compound OCCS DGVVWUTYPXICAM-UHFFFAOYSA-N 0.000 description 3
- ASGMFNBUXDJWJJ-JLCFBVMHSA-N (1R,3R)-3-[[3-bromo-1-[4-(5-methyl-1,3,4-thiadiazol-2-yl)phenyl]pyrazolo[3,4-d]pyrimidin-6-yl]amino]-N,1-dimethylcyclopentane-1-carboxamide Chemical compound BrC1=NN(C2=NC(=NC=C21)N[C@H]1C[C@@](CC1)(C(=O)NC)C)C1=CC=C(C=C1)C=1SC(=NN=1)C ASGMFNBUXDJWJJ-JLCFBVMHSA-N 0.000 description 2
- UAOUIVVJBYDFKD-XKCDOFEDSA-N (1R,9R,10S,11R,12R,15S,18S,21R)-10,11,21-trihydroxy-8,8-dimethyl-14-methylidene-4-(prop-2-enylamino)-20-oxa-5-thia-3-azahexacyclo[9.7.2.112,15.01,9.02,6.012,18]henicosa-2(6),3-dien-13-one Chemical compound C([C@@H]1[C@@H](O)[C@@]23C(C1=C)=O)C[C@H]2[C@]12C(N=C(NCC=C)S4)=C4CC(C)(C)[C@H]1[C@H](O)[C@]3(O)OC2 UAOUIVVJBYDFKD-XKCDOFEDSA-N 0.000 description 2
- NAWXUBYGYWOOIX-SFHVURJKSA-N (2s)-2-[[4-[2-(2,4-diaminoquinazolin-6-yl)ethyl]benzoyl]amino]-4-methylidenepentanedioic acid Chemical compound C1=CC2=NC(N)=NC(N)=C2C=C1CCC1=CC=C(C(=O)N[C@@H](CC(=C)C(O)=O)C(O)=O)C=C1 NAWXUBYGYWOOIX-SFHVURJKSA-N 0.000 description 2
- MPDDTAJMJCESGV-CTUHWIOQSA-M (3r,5r)-7-[2-(4-fluorophenyl)-5-[methyl-[(1r)-1-phenylethyl]carbamoyl]-4-propan-2-ylpyrazol-3-yl]-3,5-dihydroxyheptanoate Chemical compound C1([C@@H](C)N(C)C(=O)C2=NN(C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C2C(C)C)C=2C=CC(F)=CC=2)=CC=CC=C1 MPDDTAJMJCESGV-CTUHWIOQSA-M 0.000 description 2
- 125000000229 (C1-C4)alkoxy group Chemical group 0.000 description 2
- 125000001399 1,2,3-triazolyl group Chemical group N1N=NC(=C1)* 0.000 description 2
- TVTJUIAKQFIXCE-HUKYDQBMSA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynyl-1H-purine-6,8-dione Chemical compound NC=1NC(C=2N(C(N(C=2N=1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C)=O TVTJUIAKQFIXCE-HUKYDQBMSA-N 0.000 description 2
- 125000000175 2-thienyl group Chemical group S1C([*])=C([H])C([H])=C1[H] 0.000 description 2
- LCSKNASZPVZHEG-UHFFFAOYSA-N 3,6-dimethyl-1,4-dioxane-2,5-dione;1,4-dioxane-2,5-dione Chemical compound O=C1COC(=O)CO1.CC1OC(=O)C(C)OC1=O LCSKNASZPVZHEG-UHFFFAOYSA-N 0.000 description 2
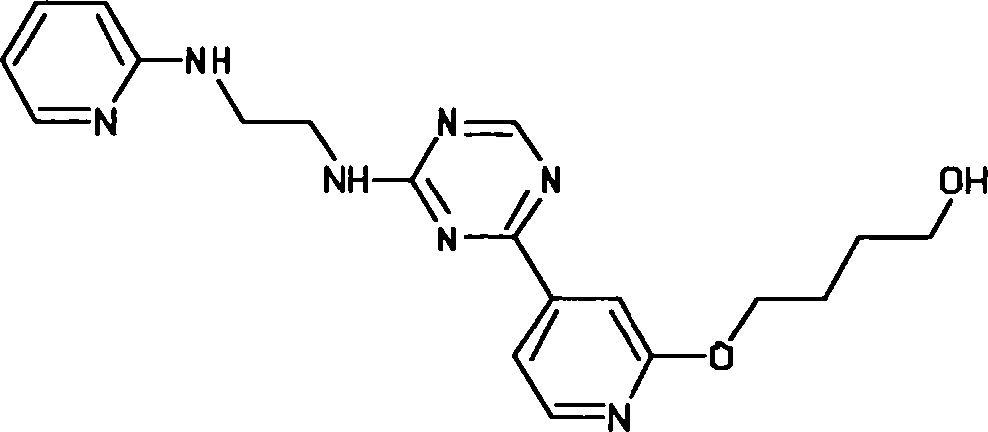
- PHFWAZUKMCGITC-UHFFFAOYSA-N 3-[[3-[4-[2-[methyl(pyridin-2-yl)amino]ethylamino]-1,3,5-triazin-2-yl]pyridin-2-yl]amino]propan-1-ol Chemical compound C=1C=CC=NC=1N(C)CCNC(N=1)=NC=NC=1C1=CC=CN=C1NCCCO PHFWAZUKMCGITC-UHFFFAOYSA-N 0.000 description 2
- DPBWFNDFMCCGGJ-UHFFFAOYSA-N 4-Piperidine carboxamide Chemical compound NC(=O)C1CCNCC1 DPBWFNDFMCCGGJ-UHFFFAOYSA-N 0.000 description 2
- OVHALSXVZABRDM-UHFFFAOYSA-N 4-[4-[4-[2-(pyridin-2-ylamino)ethylamino]-1,3,5-triazin-2-yl]pyridin-2-yl]oxybutan-1-ol Chemical compound C1=NC(OCCCCO)=CC(C=2N=C(NCCNC=3N=CC=CC=3)N=CN=2)=C1 OVHALSXVZABRDM-UHFFFAOYSA-N 0.000 description 2
- 125000004195 4-methylpiperazin-1-yl group Chemical group [H]C([H])([H])N1C([H])([H])C([H])([H])N(*)C([H])([H])C1([H])[H] 0.000 description 2
- 102100027211 Albumin Human genes 0.000 description 2
- 108010088751 Albumins Proteins 0.000 description 2
- 206010002091 Anaesthesia Diseases 0.000 description 2
- 108010039627 Aprotinin Proteins 0.000 description 2
- KXDAEFPNCMNJSK-UHFFFAOYSA-N Benzamide Chemical compound NC(=O)C1=CC=CC=C1 KXDAEFPNCMNJSK-UHFFFAOYSA-N 0.000 description 2
- 239000005711 Benzoic acid Substances 0.000 description 2
- IYGYMKDQCDOMRE-QRWMCTBCSA-N Bicculine Chemical compound O([C@H]1C2C3=CC=4OCOC=4C=C3CCN2C)C(=O)C2=C1C=CC1=C2OCO1 IYGYMKDQCDOMRE-QRWMCTBCSA-N 0.000 description 2
- 102100028728 Bone morphogenetic protein 1 Human genes 0.000 description 2
- 108090000654 Bone morphogenetic protein 1 Proteins 0.000 description 2
- 229940127007 Compound 39 Drugs 0.000 description 2
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 2
- SUZLHDUTVMZSEV-UHFFFAOYSA-N Deoxycoleonol Natural products C12C(=O)CC(C)(C=C)OC2(C)C(OC(=O)C)C(O)C2C1(C)C(O)CCC2(C)C SUZLHDUTVMZSEV-UHFFFAOYSA-N 0.000 description 2
- 238000009007 Diagnostic Kit Methods 0.000 description 2
- 102000002045 Endothelin Human genes 0.000 description 2
- 108050009340 Endothelin Proteins 0.000 description 2
- 241000283074 Equus asinus Species 0.000 description 2
- 101150021185 FGF gene Proteins 0.000 description 2
- 108090000368 Fibroblast growth factor 8 Proteins 0.000 description 2
- 102100037060 Forkhead box protein D3 Human genes 0.000 description 2
- 102000027484 GABAA receptors Human genes 0.000 description 2
- 108091008681 GABAA receptors Proteins 0.000 description 2
- 108010086512 Hepatocyte Nuclear Factor 1 Proteins 0.000 description 2
- 102000006754 Hepatocyte Nuclear Factor 1 Human genes 0.000 description 2
- 102000009094 Hepatocyte Nuclear Factor 3-beta Human genes 0.000 description 2
- 108010087745 Hepatocyte Nuclear Factor 3-beta Proteins 0.000 description 2
- 102100035108 High affinity nerve growth factor receptor Human genes 0.000 description 2
- 102100024208 Homeobox protein MIXL1 Human genes 0.000 description 2
- 101000914195 Homo sapiens Cerberus Proteins 0.000 description 2
- 101001029308 Homo sapiens Forkhead box protein D3 Proteins 0.000 description 2
- 101000893563 Homo sapiens Growth/differentiation factor 10 Proteins 0.000 description 2
- 101000893545 Homo sapiens Growth/differentiation factor 11 Proteins 0.000 description 2
- 101000893549 Homo sapiens Growth/differentiation factor 15 Proteins 0.000 description 2
- 101001023986 Homo sapiens Growth/differentiation factor 3 Proteins 0.000 description 2
- 101001052462 Homo sapiens Homeobox protein MIXL1 Proteins 0.000 description 2
- 101000576323 Homo sapiens Motor neuron and pancreas homeobox protein 1 Proteins 0.000 description 2
- 101000819088 Homo sapiens Transcription factor GATA-6 Proteins 0.000 description 2
- 101000687905 Homo sapiens Transcription factor SOX-2 Proteins 0.000 description 2
- 101000976622 Homo sapiens Zinc finger protein 42 homolog Proteins 0.000 description 2
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 description 2
- PIWKPBJCKXDKJR-UHFFFAOYSA-N Isoflurane Chemical compound FC(F)OC(Cl)C(F)(F)F PIWKPBJCKXDKJR-UHFFFAOYSA-N 0.000 description 2
- 108090000581 Leukemia inhibitory factor Proteins 0.000 description 2
- 102000043136 MAP kinase family Human genes 0.000 description 2
- 108091054455 MAP kinase family Proteins 0.000 description 2
- ZRVUJXDFFKFLMG-UHFFFAOYSA-N Meloxicam Chemical compound OC=1C2=CC=CC=C2S(=O)(=O)N(C)C=1C(=O)NC1=NC=C(C)S1 ZRVUJXDFFKFLMG-UHFFFAOYSA-N 0.000 description 2
- 102000013013 Member 2 Subfamily G ATP Binding Cassette Transporter Human genes 0.000 description 2
- 108010090306 Member 2 Subfamily G ATP Binding Cassette Transporter Proteins 0.000 description 2
- 101100189458 Mesocricetus auratus INGAP gene Proteins 0.000 description 2
- 241001465754 Metazoa Species 0.000 description 2
- 102100025170 Motor neuron and pancreas homeobox protein 1 Human genes 0.000 description 2
- 101100220212 Mus musculus Cdx2 gene Proteins 0.000 description 2
- 101100310648 Mus musculus Sox17 gene Proteins 0.000 description 2
- 125000000815 N-oxide group Chemical group 0.000 description 2
- DFPAKSUCGFBDDF-UHFFFAOYSA-N Nicotinamide Chemical compound NC(=O)C1=CC=CN=C1 DFPAKSUCGFBDDF-UHFFFAOYSA-N 0.000 description 2
- 102000014736 Notch Human genes 0.000 description 2
- 108010070047 Notch Receptors Proteins 0.000 description 2
- 108010032788 PAX6 Transcription Factor Proteins 0.000 description 2
- 102000007354 PAX6 Transcription Factor Human genes 0.000 description 2
- 101150081664 PAX6 gene Proteins 0.000 description 2
- 102100035423 POU domain, class 5, transcription factor 1 Human genes 0.000 description 2
- 101710126211 POU domain, class 5, transcription factor 1 Proteins 0.000 description 2
- 102100037506 Paired box protein Pax-6 Human genes 0.000 description 2
- 101710144033 Pancreas/duodenum homeobox protein 1 Proteins 0.000 description 2
- 102100039277 Pleiotrophin Human genes 0.000 description 2
- 102100033880 Prospero homeobox protein 1 Human genes 0.000 description 2
- 229940079156 Proteasome inhibitor Drugs 0.000 description 2
- 101001032756 Rattus norvegicus Granzyme-like protein 1 Proteins 0.000 description 2
- 108010071390 Serum Albumin Proteins 0.000 description 2
- 102000007562 Serum Albumin Human genes 0.000 description 2
- 102100021382 Transcription factor GATA-6 Human genes 0.000 description 2
- 101710176387 Transcription factor SOX-17 Proteins 0.000 description 2
- 102100024270 Transcription factor SOX-2 Human genes 0.000 description 2
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 2
- 102000013814 Wnt Human genes 0.000 description 2
- 108050003627 Wnt Proteins 0.000 description 2
- 102100023550 Zinc finger protein 42 homolog Human genes 0.000 description 2
- 108010076089 accutase Proteins 0.000 description 2
- 239000000654 additive Substances 0.000 description 2
- 239000000556 agonist Substances 0.000 description 2
- 229930013930 alkaloid Natural products 0.000 description 2
- 150000003797 alkaloid derivatives Chemical class 0.000 description 2
- 125000005137 alkenylsulfonyl group Chemical group 0.000 description 2
- 125000004457 alkyl amino carbonyl group Chemical group 0.000 description 2
- 125000004448 alkyl carbonyl group Chemical group 0.000 description 2
- 125000004397 aminosulfonyl group Chemical group NS(=O)(=O)* 0.000 description 2
- 230000037005 anaesthesia Effects 0.000 description 2
- 229960004405 aprotinin Drugs 0.000 description 2
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 2
- 229910000063 azene Inorganic materials 0.000 description 2
- 230000009286 beneficial effect Effects 0.000 description 2
- 235000010233 benzoic acid Nutrition 0.000 description 2
- AACMFFIUYXGCOC-UHFFFAOYSA-N bicuculline Natural products CN1CCc2cc3OCOc3cc2C1C4OCc5c6OCOc6ccc45 AACMFFIUYXGCOC-UHFFFAOYSA-N 0.000 description 2
- 229960000074 biopharmaceutical Drugs 0.000 description 2
- 230000037396 body weight Effects 0.000 description 2
- 210000000988 bone and bone Anatomy 0.000 description 2
- 229940087828 buprenex Drugs 0.000 description 2
- UAIXRPCCYXNJMQ-RZIPZOSSSA-N buprenorphine hydrochlorie Chemical compound [Cl-].C([C@]12[C@H]3OC=4C(O)=CC=C(C2=4)C[C@@H]2[C@]11CC[C@]3([C@H](C1)[C@](C)(O)C(C)(C)C)OC)C[NH+]2CC1CC1 UAIXRPCCYXNJMQ-RZIPZOSSSA-N 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 238000007444 cell Immobilization Methods 0.000 description 2
- 230000011712 cell development Effects 0.000 description 2
- 238000005119 centrifugation Methods 0.000 description 2
- 239000002738 chelating agent Substances 0.000 description 2
- OHCQJHSOBUTRHG-UHFFFAOYSA-N colforsin Natural products OC12C(=O)CC(C)(C=C)OC1(C)C(OC(=O)C)C(O)C1C2(C)C(O)CCC1(C)C OHCQJHSOBUTRHG-UHFFFAOYSA-N 0.000 description 2
- 229940125851 compound 27 Drugs 0.000 description 2
- 239000013068 control sample Substances 0.000 description 2
- 229910052802 copper Inorganic materials 0.000 description 2
- 239000010949 copper Substances 0.000 description 2
- 125000004093 cyano group Chemical group *C#N 0.000 description 2
- IYGYMKDQCDOMRE-UHFFFAOYSA-N d-Bicucullin Natural products CN1CCC2=CC=3OCOC=3C=C2C1C1OC(=O)C2=C1C=CC1=C2OCO1 IYGYMKDQCDOMRE-UHFFFAOYSA-N 0.000 description 2
- 230000007423 decrease Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- NIJJYAXOARWZEE-UHFFFAOYSA-N di-n-propyl-acetic acid Natural products CCCC(C(O)=O)CCC NIJJYAXOARWZEE-UHFFFAOYSA-N 0.000 description 2
- 238000006073 displacement reaction Methods 0.000 description 2
- 238000009826 distribution Methods 0.000 description 2
- 210000003981 ectoderm Anatomy 0.000 description 2
- ZUBDGKVDJUIMQQ-UBFCDGJISA-N endothelin-1 Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(O)=O)NC(=O)[C@H]1NC(=O)[C@H](CC=2C=CC=CC=2)NC(=O)[C@@H](CC=2C=CC(O)=CC=2)NC(=O)[C@H](C(C)C)NC(=O)[C@H]2CSSC[C@@H](C(N[C@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)NC(=O)[C@@H](CO)NC(=O)[C@H](N)CSSC1)C1=CNC=N1 ZUBDGKVDJUIMQQ-UBFCDGJISA-N 0.000 description 2
- 230000002255 enzymatic effect Effects 0.000 description 2
- 229940031098 ethanolamine Drugs 0.000 description 2
- UPCIBFUJJLCOQG-UHFFFAOYSA-L ethyl-[2-[2-[ethyl(dimethyl)azaniumyl]ethyl-methylamino]ethyl]-dimethylazanium;dibromide Chemical compound [Br-].[Br-].CC[N+](C)(C)CCN(C)CC[N+](C)(C)CC UPCIBFUJJLCOQG-UHFFFAOYSA-L 0.000 description 2
- 238000002474 experimental method Methods 0.000 description 2
- 239000012091 fetal bovine serum Substances 0.000 description 2
- 210000002950 fibroblast Anatomy 0.000 description 2
- 235000013305 food Nutrition 0.000 description 2
- 108010043649 gastrin I Proteins 0.000 description 2
- 210000001035 gastrointestinal tract Anatomy 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 230000002068 genetic effect Effects 0.000 description 2
- 210000004602 germ cell Anatomy 0.000 description 2
- 229940093181 glucose injection Drugs 0.000 description 2
- 108010069764 helospectin I Proteins 0.000 description 2
- HTMVMVKJOPFRMK-OYZAELBCSA-N helospectin i Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC(C)C)C(=O)NCC(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CO)C(=O)N[C@@H](CO)C(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)[C@H](C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=C(O)C=C1 HTMVMVKJOPFRMK-OYZAELBCSA-N 0.000 description 2
- 229960000890 hydrocortisone Drugs 0.000 description 2
- 125000002883 imidazolyl group Chemical group 0.000 description 2
- 239000007943 implant Substances 0.000 description 2
- 230000001976 improved effect Effects 0.000 description 2
- 239000000893 inhibin Substances 0.000 description 2
- HHMSPIAOYISBOU-IYQBICMXSA-N insulin rabbit Chemical compound C([C@@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@H]1CSSC[C@H]2C(=O)N[C@H](C(=O)N[C@@H](CO)C(=O)N[C@H](C(=O)N[C@H](C(N[C@@H](CO)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@@H](CSSC[C@H](NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3C=CC(O)=CC=3)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=3NC=NC=3)NC(=O)[C@H](CO)NC(=O)CNC1=O)C(=O)NCC(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](CC=1C=CC(O)=CC=1)C(=O)N[C@@H]([C@@H](C)O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CO)C(O)=O)C(=O)N[C@@H](CC(N)=O)C(O)=O)=O)CSSC[C@@H](C(N2)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C(C)C)NC(=O)[C@@H](NC(=O)CN)[C@@H](C)CC)[C@@H](C)CC)[C@@H](C)O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CC(N)=O)NC(=O)[C@@H](NC(=O)[C@@H](N)CC=1C=CC=CC=1)C(C)C)C1=CN=CN1 HHMSPIAOYISBOU-IYQBICMXSA-N 0.000 description 2
- 210000002660 insulin-secreting cell Anatomy 0.000 description 2
- 210000000936 intestine Anatomy 0.000 description 2
- 229960002725 isoflurane Drugs 0.000 description 2
- 239000003446 ligand Substances 0.000 description 2
- 230000000670 limiting effect Effects 0.000 description 2
- 210000004185 liver Anatomy 0.000 description 2
- 210000005229 liver cell Anatomy 0.000 description 2
- 230000010534 mechanism of action Effects 0.000 description 2
- 230000001404 mediated effect Effects 0.000 description 2
- 210000003716 mesoderm Anatomy 0.000 description 2
- 108020004999 messenger RNA Proteins 0.000 description 2
- 229940001676 metacam Drugs 0.000 description 2
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 2
- 238000002156 mixing Methods 0.000 description 2
- 230000000921 morphogenic effect Effects 0.000 description 2
- WYVMHMJLOOLNFJ-UHFFFAOYSA-N n-[(1-benzylazepan-4-yl)methyl]-2-pyridin-3-ylacetamide Chemical compound C1CCN(CC=2C=CC=CC=2)CCC1CNC(=O)CC1=CC=CN=C1 WYVMHMJLOOLNFJ-UHFFFAOYSA-N 0.000 description 2
- 230000009707 neogenesis Effects 0.000 description 2
- 230000014511 neuron projection development Effects 0.000 description 2
- 229910052757 nitrogen Inorganic materials 0.000 description 2
- 238000005457 optimization Methods 0.000 description 2
- 210000000056 organ Anatomy 0.000 description 2
- 230000005305 organ development Effects 0.000 description 2
- 229910052760 oxygen Inorganic materials 0.000 description 2
- 239000001301 oxygen Substances 0.000 description 2
- 230000037361 pathway Effects 0.000 description 2
- 230000026731 phosphorylation Effects 0.000 description 2
- 238000006366 phosphorylation reaction Methods 0.000 description 2
- 230000001817 pituitary effect Effects 0.000 description 2
- 210000002381 plasma Anatomy 0.000 description 2
- 229920001184 polypeptide Polymers 0.000 description 2
- 230000035935 pregnancy Effects 0.000 description 2
- 239000000186 progesterone Substances 0.000 description 2
- 229960003387 progesterone Drugs 0.000 description 2
- 239000003207 proteasome inhibitor Substances 0.000 description 2
- 125000003226 pyrazolyl group Chemical group 0.000 description 2
- 125000004528 pyrimidin-5-yl group Chemical group N1=CN=CC(=C1)* 0.000 description 2
- 229940044601 receptor agonist Drugs 0.000 description 2
- 239000000018 receptor agonist Substances 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 238000011084 recovery Methods 0.000 description 2
- 150000003839 salts Chemical class 0.000 description 2
- 239000013049 sediment Substances 0.000 description 2
- 239000011780 sodium chloride Substances 0.000 description 2
- 230000003637 steroidlike Effects 0.000 description 2
- 238000003860 storage Methods 0.000 description 2
- 238000004114 suspension culture Methods 0.000 description 2
- 230000005737 synergistic response Effects 0.000 description 2
- 238000002560 therapeutic procedure Methods 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 230000032258 transport Effects 0.000 description 2
- RTKIYFITIVXBLE-QEQCGCAPSA-N trichostatin A Chemical compound ONC(=O)/C=C/C(/C)=C/[C@@H](C)C(=O)C1=CC=C(N(C)C)C=C1 RTKIYFITIVXBLE-QEQCGCAPSA-N 0.000 description 2
- 238000010200 validation analysis Methods 0.000 description 2
- MSRILKIQRXUYCT-UHFFFAOYSA-M valproate semisodium Chemical compound [Na+].CCCC(C(O)=O)CCC.CCCC(C([O-])=O)CCC MSRILKIQRXUYCT-UHFFFAOYSA-M 0.000 description 2
- 229960000604 valproic acid Drugs 0.000 description 2
- 210000003556 vascular endothelial cell Anatomy 0.000 description 2
- AOSZTAHDEDLTLQ-AZKQZHLXSA-N (1S,2S,4R,8S,9S,11S,12R,13S,19S)-6-[(3-chlorophenyl)methyl]-12,19-difluoro-11-hydroxy-8-(2-hydroxyacetyl)-9,13-dimethyl-6-azapentacyclo[10.8.0.02,9.04,8.013,18]icosa-14,17-dien-16-one Chemical compound C([C@@H]1C[C@H]2[C@H]3[C@]([C@]4(C=CC(=O)C=C4[C@@H](F)C3)C)(F)[C@@H](O)C[C@@]2([C@@]1(C1)C(=O)CO)C)N1CC1=CC=CC(Cl)=C1 AOSZTAHDEDLTLQ-AZKQZHLXSA-N 0.000 description 1
- GLGNXYJARSMNGJ-VKTIVEEGSA-N (1s,2s,3r,4r)-3-[[5-chloro-2-[(1-ethyl-6-methoxy-2-oxo-4,5-dihydro-3h-1-benzazepin-7-yl)amino]pyrimidin-4-yl]amino]bicyclo[2.2.1]hept-5-ene-2-carboxamide Chemical compound CCN1C(=O)CCCC2=C(OC)C(NC=3N=C(C(=CN=3)Cl)N[C@H]3[C@H]([C@@]4([H])C[C@@]3(C=C4)[H])C(N)=O)=CC=C21 GLGNXYJARSMNGJ-VKTIVEEGSA-N 0.000 description 1
- SZUVGFMDDVSKSI-WIFOCOSTSA-N (1s,2s,3s,5r)-1-(carboxymethyl)-3,5-bis[(4-phenoxyphenyl)methyl-propylcarbamoyl]cyclopentane-1,2-dicarboxylic acid Chemical compound O=C([C@@H]1[C@@H]([C@](CC(O)=O)([C@H](C(=O)N(CCC)CC=2C=CC(OC=3C=CC=CC=3)=CC=2)C1)C(O)=O)C(O)=O)N(CCC)CC(C=C1)=CC=C1OC1=CC=CC=C1 SZUVGFMDDVSKSI-WIFOCOSTSA-N 0.000 description 1
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 1
- IUSARDYWEPUTPN-OZBXUNDUSA-N (2r)-n-[(2s,3r)-4-[[(4s)-6-(2,2-dimethylpropyl)spiro[3,4-dihydropyrano[2,3-b]pyridine-2,1'-cyclobutane]-4-yl]amino]-3-hydroxy-1-[3-(1,3-thiazol-2-yl)phenyl]butan-2-yl]-2-methoxypropanamide Chemical compound C([C@H](NC(=O)[C@@H](C)OC)[C@H](O)CN[C@@H]1C2=CC(CC(C)(C)C)=CN=C2OC2(CCC2)C1)C(C=1)=CC=CC=1C1=NC=CS1 IUSARDYWEPUTPN-OZBXUNDUSA-N 0.000 description 1
- YJLIKUSWRSEPSM-WGQQHEPDSA-N (2r,3r,4s,5r)-2-[6-amino-8-[(4-phenylphenyl)methylamino]purin-9-yl]-5-(hydroxymethyl)oxolane-3,4-diol Chemical compound C=1C=C(C=2C=CC=CC=2)C=CC=1CNC1=NC=2C(N)=NC=NC=2N1[C@@H]1O[C@H](CO)[C@@H](O)[C@H]1O YJLIKUSWRSEPSM-WGQQHEPDSA-N 0.000 description 1
- VIJSPAIQWVPKQZ-BLECARSGSA-N (2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-[[(2s)-2-acetamido-5-(diaminomethylideneamino)pentanoyl]amino]-4-methylpentanoyl]amino]-4,4-dimethylpentanoyl]amino]-4-methylpentanoyl]amino]propanoyl]amino]-5-(diaminomethylideneamino)pentanoic acid Chemical compound NC(=N)NCCC[C@@H](C(O)=O)NC(=O)[C@H](C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC(C)(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CCCNC(N)=N)NC(C)=O VIJSPAIQWVPKQZ-BLECARSGSA-N 0.000 description 1
- STBLNCCBQMHSRC-BATDWUPUSA-N (2s)-n-[(3s,4s)-5-acetyl-7-cyano-4-methyl-1-[(2-methylnaphthalen-1-yl)methyl]-2-oxo-3,4-dihydro-1,5-benzodiazepin-3-yl]-2-(methylamino)propanamide Chemical compound O=C1[C@@H](NC(=O)[C@H](C)NC)[C@H](C)N(C(C)=O)C2=CC(C#N)=CC=C2N1CC1=C(C)C=CC2=CC=CC=C12 STBLNCCBQMHSRC-BATDWUPUSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- UDQTXCHQKHIQMH-KYGLGHNPSA-N (3ar,5s,6s,7r,7ar)-5-(difluoromethyl)-2-(ethylamino)-5,6,7,7a-tetrahydro-3ah-pyrano[3,2-d][1,3]thiazole-6,7-diol Chemical compound S1C(NCC)=N[C@H]2[C@@H]1O[C@H](C(F)F)[C@@H](O)[C@@H]2O UDQTXCHQKHIQMH-KYGLGHNPSA-N 0.000 description 1
- OMBVEVHRIQULKW-DNQXCXABSA-M (3r,5r)-7-[3-(4-fluorophenyl)-8-oxo-7-phenyl-1-propan-2-yl-5,6-dihydro-4h-pyrrolo[2,3-c]azepin-2-yl]-3,5-dihydroxyheptanoate Chemical compound O=C1C=2N(C(C)C)C(CC[C@@H](O)C[C@@H](O)CC([O-])=O)=C(C=3C=CC(F)=CC=3)C=2CCCN1C1=CC=CC=C1 OMBVEVHRIQULKW-DNQXCXABSA-M 0.000 description 1
- YQOLEILXOBUDMU-KRWDZBQOSA-N (4R)-5-[(6-bromo-3-methyl-2-pyrrolidin-1-ylquinoline-4-carbonyl)amino]-4-(2-chlorophenyl)pentanoic acid Chemical compound CC1=C(C2=C(C=CC(=C2)Br)N=C1N3CCCC3)C(=O)NC[C@H](CCC(=O)O)C4=CC=CC=C4Cl YQOLEILXOBUDMU-KRWDZBQOSA-N 0.000 description 1
- KPYXMALABCDPGN-HYOZMBHHSA-N (4s)-5-[[(2s)-6-amino-1-[[(2s,3s)-1-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2r)-1-[[2-[[2-[[(1s)-3-amino-1-carboxy-3-oxopropyl]amino]-2-oxoethyl]amino]-2-oxoethyl]amino]-1-oxo-3-sulfanylpropan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-1-oxopropan-2-yl]a Chemical compound NC(=O)C[C@@H](C(O)=O)NC(=O)CNC(=O)CNC(=O)[C@H](CS)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](C)NC(=O)[C@H](C(C)C)NC(=O)[C@H](CC(C)C)NC(=O)[C@H]([C@@H](C)CC)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)CNC(=O)[C@@H](N)CCCCN)CC1=CC=C(O)C=C1 KPYXMALABCDPGN-HYOZMBHHSA-N 0.000 description 1
- KQZLRWGGWXJPOS-NLFPWZOASA-N 1-[(1R)-1-(2,4-dichlorophenyl)ethyl]-6-[(4S,5R)-4-[(2S)-2-(hydroxymethyl)pyrrolidin-1-yl]-5-methylcyclohexen-1-yl]pyrazolo[3,4-b]pyrazine-3-carbonitrile Chemical compound ClC1=C(C=CC(=C1)Cl)[C@@H](C)N1N=C(C=2C1=NC(=CN=2)C1=CC[C@@H]([C@@H](C1)C)N1[C@@H](CCC1)CO)C#N KQZLRWGGWXJPOS-NLFPWZOASA-N 0.000 description 1
- WZZBNLYBHUDSHF-DHLKQENFSA-N 1-[(3s,4s)-4-[8-(2-chloro-4-pyrimidin-2-yloxyphenyl)-7-fluoro-2-methylimidazo[4,5-c]quinolin-1-yl]-3-fluoropiperidin-1-yl]-2-hydroxyethanone Chemical compound CC1=NC2=CN=C3C=C(F)C(C=4C(=CC(OC=5N=CC=CN=5)=CC=4)Cl)=CC3=C2N1[C@H]1CCN(C(=O)CO)C[C@@H]1F WZZBNLYBHUDSHF-DHLKQENFSA-N 0.000 description 1
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 1
- BFLCELFLUWTJSN-UHFFFAOYSA-N 2-(4-propan-2-ylanilino)-n-(2-thiophen-2-ylethyl)-7,8-dihydro-5h-pyrido[4,3-d]pyrimidine-6-carboxamide Chemical compound C1=CC(C(C)C)=CC=C1NC1=NC=C(CN(CC2)C(=O)NCCC=3SC=CC=3)C2=N1 BFLCELFLUWTJSN-UHFFFAOYSA-N 0.000 description 1
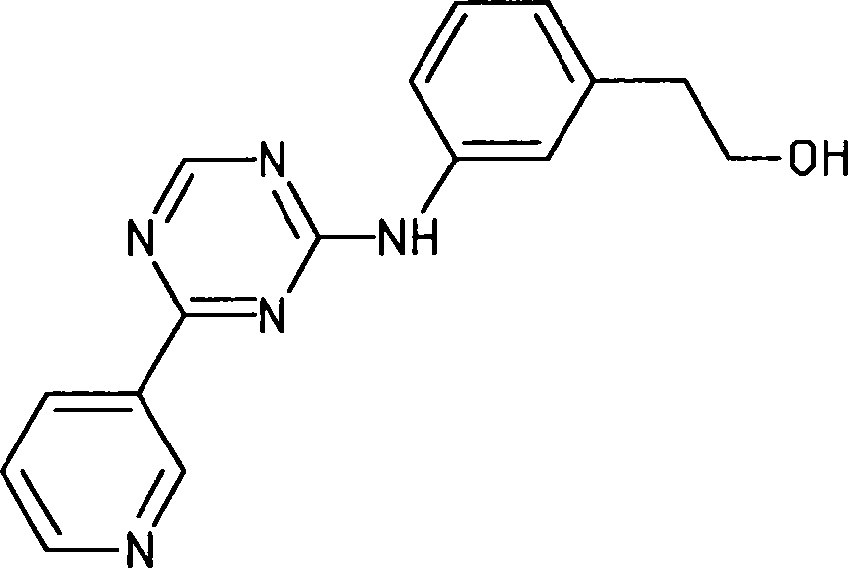
- LWHMNNIAPAZAOT-UHFFFAOYSA-N 2-[3-[(4-pyridin-3-yl-1,3,5-triazin-2-yl)amino]phenyl]ethanol Chemical compound OCCC1=CC=CC(NC=2N=C(N=CN=2)C=2C=NC=CC=2)=C1 LWHMNNIAPAZAOT-UHFFFAOYSA-N 0.000 description 1
- PYRKKGOKRMZEIT-UHFFFAOYSA-N 2-[6-(2-cyclopropylethoxy)-9-(2-hydroxy-2-methylpropyl)-1h-phenanthro[9,10-d]imidazol-2-yl]-5-fluorobenzene-1,3-dicarbonitrile Chemical compound C1=C2C3=CC(CC(C)(O)C)=CC=C3C=3NC(C=4C(=CC(F)=CC=4C#N)C#N)=NC=3C2=CC=C1OCCC1CC1 PYRKKGOKRMZEIT-UHFFFAOYSA-N 0.000 description 1
- FMKGJQHNYMWDFJ-CVEARBPZSA-N 2-[[4-(2,2-difluoropropoxy)pyrimidin-5-yl]methylamino]-4-[[(1R,4S)-4-hydroxy-3,3-dimethylcyclohexyl]amino]pyrimidine-5-carbonitrile Chemical compound FC(COC1=NC=NC=C1CNC1=NC=C(C(=N1)N[C@H]1CC([C@H](CC1)O)(C)C)C#N)(C)F FMKGJQHNYMWDFJ-CVEARBPZSA-N 0.000 description 1
- NPRYCHLHHVWLQZ-TURQNECASA-N 2-amino-9-[(2R,3S,4S,5R)-4-fluoro-3-hydroxy-5-(hydroxymethyl)oxolan-2-yl]-7-prop-2-ynylpurin-8-one Chemical compound NC1=NC=C2N(C(N(C2=N1)[C@@H]1O[C@@H]([C@H]([C@H]1O)F)CO)=O)CC#C NPRYCHLHHVWLQZ-TURQNECASA-N 0.000 description 1
- LFOIDLOIBZFWDO-UHFFFAOYSA-N 2-methoxy-6-[6-methoxy-4-[(3-phenylmethoxyphenyl)methoxy]-1-benzofuran-2-yl]imidazo[2,1-b][1,3,4]thiadiazole Chemical compound N1=C2SC(OC)=NN2C=C1C(OC1=CC(OC)=C2)=CC1=C2OCC(C=1)=CC=CC=1OCC1=CC=CC=C1 LFOIDLOIBZFWDO-UHFFFAOYSA-N 0.000 description 1
- QBWKPGNFQQJGFY-QLFBSQMISA-N 3-[(1r)-1-[(2r,6s)-2,6-dimethylmorpholin-4-yl]ethyl]-n-[6-methyl-3-(1h-pyrazol-4-yl)imidazo[1,2-a]pyrazin-8-yl]-1,2-thiazol-5-amine Chemical compound N1([C@H](C)C2=NSC(NC=3C4=NC=C(N4C=C(C)N=3)C3=CNN=C3)=C2)C[C@H](C)O[C@H](C)C1 QBWKPGNFQQJGFY-QLFBSQMISA-N 0.000 description 1
- BGAJNPLDJJBRHK-UHFFFAOYSA-N 3-[2-[5-(3-chloro-4-propan-2-yloxyphenyl)-1,3,4-thiadiazol-2-yl]-3-methyl-6,7-dihydro-4h-pyrazolo[4,3-c]pyridin-5-yl]propanoic acid Chemical compound C1=C(Cl)C(OC(C)C)=CC=C1C1=NN=C(N2C(=C3CN(CCC(O)=O)CCC3=N2)C)S1 BGAJNPLDJJBRHK-UHFFFAOYSA-N 0.000 description 1
- HQHSJJZIICGOIX-UHFFFAOYSA-N 4-(1h-pyrrolo[2,3-b]pyridin-3-yl)pyrimidin-2-amine Chemical compound NC1=NC=CC(C=2C3=CC=CN=C3NC=2)=N1 HQHSJJZIICGOIX-UHFFFAOYSA-N 0.000 description 1
- WYFCZWSWFGJODV-MIANJLSGSA-N 4-[[(1s)-2-[(e)-3-[3-chloro-2-fluoro-6-(tetrazol-1-yl)phenyl]prop-2-enoyl]-5-(4-methyl-2-oxopiperazin-1-yl)-3,4-dihydro-1h-isoquinoline-1-carbonyl]amino]benzoic acid Chemical compound O=C1CN(C)CCN1C1=CC=CC2=C1CCN(C(=O)\C=C\C=1C(=CC=C(Cl)C=1F)N1N=NN=C1)[C@@H]2C(=O)NC1=CC=C(C(O)=O)C=C1 WYFCZWSWFGJODV-MIANJLSGSA-N 0.000 description 1
- HCKIZAIKIHWWFE-UHFFFAOYSA-N 4-chloro-2-[[6-[3-(chloromethyl)-4-methoxyanilino]pyrimidin-4-yl]amino]phenol Chemical compound C1=C(CCl)C(OC)=CC=C1NC1=CC(NC=2C(=CC=C(Cl)C=2)O)=NC=N1 HCKIZAIKIHWWFE-UHFFFAOYSA-N 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- YXHLJMWYDTXDHS-IRFLANFNSA-N 7-aminoactinomycin D Chemical compound C[C@H]1OC(=O)[C@H](C(C)C)N(C)C(=O)CN(C)C(=O)[C@@H]2CCCN2C(=O)[C@@H](C(C)C)NC(=O)[C@H]1NC(=O)C1=C(N)C(=O)C(C)=C2OC(C(C)=C(N)C=C3C(=O)N[C@@H]4C(=O)N[C@@H](C(N5CCC[C@H]5C(=O)N(C)CC(=O)N(C)[C@@H](C(C)C)C(=O)O[C@@H]4C)=O)C(C)C)=C3N=C21 YXHLJMWYDTXDHS-IRFLANFNSA-N 0.000 description 1
- 108700012813 7-aminoactinomycin D Proteins 0.000 description 1
- 102100034134 Activin receptor type-1B Human genes 0.000 description 1
- 239000004382 Amylase Substances 0.000 description 1
- 102000013142 Amylases Human genes 0.000 description 1
- 108010065511 Amylases Proteins 0.000 description 1
- 101000810330 Arabidopsis thaliana Eukaryotic translation initiation factor 3 subunit E Proteins 0.000 description 1
- 108010049951 Bone Morphogenetic Protein 3 Proteins 0.000 description 1
- OBMZMSLWNNWEJA-XNCRXQDQSA-N C1=CC=2C(C[C@@H]3NC(=O)[C@@H](NC(=O)[C@H](NC(=O)N(CC#CCN(CCCC[C@H](NC(=O)[C@@H](CC4=CC=CC=C4)NC3=O)C(=O)N)CC=C)NC(=O)[C@@H](N)C)CC3=CNC4=C3C=CC=C4)C)=CNC=2C=C1 Chemical compound C1=CC=2C(C[C@@H]3NC(=O)[C@@H](NC(=O)[C@H](NC(=O)N(CC#CCN(CCCC[C@H](NC(=O)[C@@H](CC4=CC=CC=C4)NC3=O)C(=O)N)CC=C)NC(=O)[C@@H](N)C)CC3=CNC4=C3C=CC=C4)C)=CNC=2C=C1 OBMZMSLWNNWEJA-XNCRXQDQSA-N 0.000 description 1
- 102100037904 CD9 antigen Human genes 0.000 description 1
- AQGNHMOJWBZFQQ-UHFFFAOYSA-N CT 99021 Chemical compound CC1=CNC(C=2C(=NC(NCCNC=3N=CC(=CC=3)C#N)=NC=2)C=2C(=CC(Cl)=CC=2)Cl)=N1 AQGNHMOJWBZFQQ-UHFFFAOYSA-N 0.000 description 1
- 101100468275 Caenorhabditis elegans rep-1 gene Proteins 0.000 description 1
- 101710010675 Cerberus Proteins 0.000 description 1
- 241000202252 Cerberus Species 0.000 description 1
- 206010010099 Combined immunodeficiency Diseases 0.000 description 1
- 229940126657 Compound 17 Drugs 0.000 description 1
- 229940126639 Compound 33 Drugs 0.000 description 1
- 102000000541 Defensins Human genes 0.000 description 1
- 108010002069 Defensins Proteins 0.000 description 1
- QMMFVYPAHWMCMS-UHFFFAOYSA-N Dimethyl sulfide Chemical compound CSC QMMFVYPAHWMCMS-UHFFFAOYSA-N 0.000 description 1
- 102100033167 Elastin Human genes 0.000 description 1
- 108010014258 Elastin Proteins 0.000 description 1
- 101000704130 Escherichia coli (strain K12) Signal recognition particle protein Proteins 0.000 description 1
- 102100028412 Fibroblast growth factor 10 Human genes 0.000 description 1
- 206010016654 Fibrosis Diseases 0.000 description 1
- 101800001586 Ghrelin Proteins 0.000 description 1
- 102400000442 Ghrelin-28 Human genes 0.000 description 1
- 108700031316 Goosecoid Proteins 0.000 description 1
- 102000050057 Goosecoid Human genes 0.000 description 1
- 229920002971 Heparan sulfate Polymers 0.000 description 1
- 102000012046 Hepatocyte Nuclear Factor 1-beta Human genes 0.000 description 1
- 108010061414 Hepatocyte Nuclear Factor 1-beta Proteins 0.000 description 1
- 108010086527 Hepatocyte Nuclear Factor 6 Proteins 0.000 description 1
- 101150068639 Hnf4a gene Proteins 0.000 description 1
- 108700005087 Homeobox Genes Proteins 0.000 description 1
- 241000282412 Homo Species 0.000 description 1
- 101000799189 Homo sapiens Activin receptor type-1B Proteins 0.000 description 1
- 101000738354 Homo sapiens CD9 antigen Proteins 0.000 description 1
- 101000917237 Homo sapiens Fibroblast growth factor 10 Proteins 0.000 description 1
- 101000911772 Homo sapiens Hsc70-interacting protein Proteins 0.000 description 1
- 101000738523 Homo sapiens Pancreas transcription factor 1 subunit alpha Proteins 0.000 description 1
- 101001069749 Homo sapiens Prospero homeobox protein 1 Proteins 0.000 description 1
- 101000642523 Homo sapiens Transcription factor SOX-7 Proteins 0.000 description 1
- 102100027037 Hsc70-interacting protein Human genes 0.000 description 1
- 206010062767 Hypophysitis Diseases 0.000 description 1
- 102100022875 Hypoxia-inducible factor 1-alpha Human genes 0.000 description 1
- 108050009527 Hypoxia-inducible factor-1 alpha Proteins 0.000 description 1
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 1
- 229930182816 L-glutamine Natural products 0.000 description 1
- 108010085895 Laminin Proteins 0.000 description 1
- 102000007547 Laminin Human genes 0.000 description 1
- 102000004058 Leukemia inhibitory factor Human genes 0.000 description 1
- 102100032352 Leukemia inhibitory factor Human genes 0.000 description 1
- 108010052014 Liberase Proteins 0.000 description 1
- 101500016415 Lophius americanus Glucagon-like peptide 1 Proteins 0.000 description 1
- 101500016432 Lophius americanus Glucagon-like peptide 2 Proteins 0.000 description 1
- 241000124008 Mammalia Species 0.000 description 1
- 102100025751 Mothers against decapentaplegic homolog 2 Human genes 0.000 description 1
- 101710143123 Mothers against decapentaplegic homolog 2 Proteins 0.000 description 1
- 102100025748 Mothers against decapentaplegic homolog 3 Human genes 0.000 description 1
- 101710143111 Mothers against decapentaplegic homolog 3 Proteins 0.000 description 1
- 101000720386 Mus musculus Acyl-coenzyme A thioesterase 9, mitochondrial Proteins 0.000 description 1
- 101100446513 Mus musculus Fgf4 gene Proteins 0.000 description 1
- 101000607573 Mus musculus Unknown protein from 2D-PAGE of fibroblasts Proteins 0.000 description 1
- OPFJDXRVMFKJJO-ZHHKINOHSA-N N-{[3-(2-benzamido-4-methyl-1,3-thiazol-5-yl)-pyrazol-5-yl]carbonyl}-G-dR-G-dD-dD-dD-NH2 Chemical compound S1C(C=2NN=C(C=2)C(=O)NCC(=O)N[C@H](CCCN=C(N)N)C(=O)NCC(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(=O)N[C@H](CC(O)=O)C(N)=O)=C(C)N=C1NC(=O)C1=CC=CC=C1 OPFJDXRVMFKJJO-ZHHKINOHSA-N 0.000 description 1
- NDKUBLKSJQPEBQ-UHFFFAOYSA-N N=1C=NCCC1C(=O)N Chemical compound N=1C=NCCC1C(=O)N NDKUBLKSJQPEBQ-UHFFFAOYSA-N 0.000 description 1
- 102100034388 Netrin-4 Human genes 0.000 description 1
- 101710121532 Netrin-4 Proteins 0.000 description 1
- 101710096141 Neurogenin-3 Proteins 0.000 description 1
- 101100519293 Neurospora crassa (strain ATCC 24698 / 74-OR23-1A / CBS 708.71 / DSM 1257 / FGSC 987) pdx-1 gene Proteins 0.000 description 1
- 102100037369 Nidogen-1 Human genes 0.000 description 1
- 101000741177 Oat chlorotic stunt virus (isolate United Kingdom) Capsid protein Proteins 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 102100037878 Pancreas transcription factor 1 subunit alpha Human genes 0.000 description 1
- 108700020479 Pancreatic hormone Proteins 0.000 description 1
- 101150075928 Pax4 gene Proteins 0.000 description 1
- 101710176384 Peptide 1 Proteins 0.000 description 1
- 108091000080 Phosphotransferase Proteins 0.000 description 1
- 102100040990 Platelet-derived growth factor subunit B Human genes 0.000 description 1
- 229920000954 Polyglycolide Polymers 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- 108050000980 Prospero homeobox protein 1 Proteins 0.000 description 1
- 108010067787 Proteoglycans Proteins 0.000 description 1
- 102000016611 Proteoglycans Human genes 0.000 description 1
- 108010019674 Proto-Oncogene Proteins c-sis Proteins 0.000 description 1
- 108091005682 Receptor kinases Proteins 0.000 description 1
- 102000007056 Recombinant Fusion Proteins Human genes 0.000 description 1
- 108010008281 Recombinant Fusion Proteins Proteins 0.000 description 1
- 206010039491 Sarcoma Diseases 0.000 description 1
- PNUZDKCDAWUEGK-CYZMBNFOSA-N Sitafloxacin Chemical compound C([C@H]1N)N(C=2C(=C3C(C(C(C(O)=O)=CN3[C@H]3[C@H](C3)F)=O)=CC=2F)Cl)CC11CC1 PNUZDKCDAWUEGK-CYZMBNFOSA-N 0.000 description 1
- ZSJLQEPLLKMAKR-UHFFFAOYSA-N Streptozotocin Natural products O=NN(C)C(=O)NC1C(O)OC(CO)C(O)C1O ZSJLQEPLLKMAKR-UHFFFAOYSA-N 0.000 description 1
- 108010008125 Tenascin Proteins 0.000 description 1
- 102000007000 Tenascin Human genes 0.000 description 1
- 206010043276 Teratoma Diseases 0.000 description 1
- 108090000190 Thrombin Proteins 0.000 description 1
- 102100036730 Transcription factor SOX-7 Human genes 0.000 description 1
- RTKIYFITIVXBLE-UHFFFAOYSA-N Trichostatin A Natural products ONC(=O)C=CC(C)=CC(C)C(=O)C1=CC=C(N(C)C)C=C1 RTKIYFITIVXBLE-UHFFFAOYSA-N 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- 108010031318 Vitronectin Proteins 0.000 description 1
- 102100035140 Vitronectin Human genes 0.000 description 1
- LJOOWESTVASNOG-UFJKPHDISA-N [(1s,3r,4ar,7s,8s,8as)-3-hydroxy-8-[2-[(4r)-4-hydroxy-6-oxooxan-2-yl]ethyl]-7-methyl-1,2,3,4,4a,7,8,8a-octahydronaphthalen-1-yl] (2s)-2-methylbutanoate Chemical compound C([C@H]1[C@@H](C)C=C[C@H]2C[C@@H](O)C[C@@H]([C@H]12)OC(=O)[C@@H](C)CC)CC1C[C@@H](O)CC(=O)O1 LJOOWESTVASNOG-UFJKPHDISA-N 0.000 description 1
- SPXSEZMVRJLHQG-XMMPIXPASA-N [(2R)-1-[[4-[(3-phenylmethoxyphenoxy)methyl]phenyl]methyl]pyrrolidin-2-yl]methanol Chemical compound C(C1=CC=CC=C1)OC=1C=C(OCC2=CC=C(CN3[C@H](CCC3)CO)C=C2)C=CC=1 SPXSEZMVRJLHQG-XMMPIXPASA-N 0.000 description 1
- LNUFLCYMSVYYNW-ZPJMAFJPSA-N [(2r,3r,4s,5r,6r)-2-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[(2r,3r,4s,5r,6r)-6-[[(3s,5s,8r,9s,10s,13r,14s,17r)-10,13-dimethyl-17-[(2r)-6-methylheptan-2-yl]-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-3-yl]oxy]-4,5-disulfo Chemical compound O([C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1[C@@H](COS(O)(=O)=O)O[C@H]([C@@H]([C@H]1OS(O)(=O)=O)OS(O)(=O)=O)O[C@@H]1C[C@@H]2CC[C@H]3[C@@H]4CC[C@@H]([C@]4(CC[C@@H]3[C@@]2(C)CC1)C)[C@H](C)CCCC(C)C)[C@H]1O[C@H](COS(O)(=O)=O)[C@@H](OS(O)(=O)=O)[C@H](OS(O)(=O)=O)[C@H]1OS(O)(=O)=O LNUFLCYMSVYYNW-ZPJMAFJPSA-N 0.000 description 1
- PSLUFJFHTBIXMW-WYEYVKMPSA-N [(3r,4ar,5s,6s,6as,10s,10ar,10bs)-3-ethenyl-10,10b-dihydroxy-3,4a,7,7,10a-pentamethyl-1-oxo-6-(2-pyridin-2-ylethylcarbamoyloxy)-5,6,6a,8,9,10-hexahydro-2h-benzo[f]chromen-5-yl] acetate Chemical compound O([C@@H]1[C@@H]([C@]2(O[C@](C)(CC(=O)[C@]2(O)[C@@]2(C)[C@@H](O)CCC(C)(C)[C@@H]21)C=C)C)OC(=O)C)C(=O)NCCC1=CC=CC=N1 PSLUFJFHTBIXMW-WYEYVKMPSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 230000004913 activation Effects 0.000 description 1
- 239000000853 adhesive Substances 0.000 description 1
- 230000001070 adhesive effect Effects 0.000 description 1
- 125000000304 alkynyl group Chemical group 0.000 description 1
- 235000019418 amylase Nutrition 0.000 description 1
- 230000033115 angiogenesis Effects 0.000 description 1
- 230000002424 anti-apoptotic effect Effects 0.000 description 1
- 229940121363 anti-inflammatory agent Drugs 0.000 description 1
- 239000002260 anti-inflammatory agent Substances 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 239000003963 antioxidant agent Substances 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 230000006907 apoptotic process Effects 0.000 description 1
- XRWSZZJLZRKHHD-WVWIJVSJSA-N asunaprevir Chemical compound O=C([C@@H]1C[C@H](CN1C(=O)[C@@H](NC(=O)OC(C)(C)C)C(C)(C)C)OC1=NC=C(C2=CC=C(Cl)C=C21)OC)N[C@]1(C(=O)NS(=O)(=O)C2CC2)C[C@H]1C=C XRWSZZJLZRKHHD-WVWIJVSJSA-N 0.000 description 1
- 230000004888 barrier function Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- KGNDCEVUMONOKF-UGPLYTSKSA-N benzyl n-[(2r)-1-[(2s,4r)-2-[[(2s)-6-amino-1-(1,3-benzoxazol-2-yl)-1,1-dihydroxyhexan-2-yl]carbamoyl]-4-[(4-methylphenyl)methoxy]pyrrolidin-1-yl]-1-oxo-4-phenylbutan-2-yl]carbamate Chemical compound C1=CC(C)=CC=C1CO[C@H]1CN(C(=O)[C@@H](CCC=2C=CC=CC=2)NC(=O)OCC=2C=CC=CC=2)[C@H](C(=O)N[C@@H](CCCCN)C(O)(O)C=2OC3=CC=CC=C3N=2)C1 KGNDCEVUMONOKF-UGPLYTSKSA-N 0.000 description 1
- 239000002876 beta blocker Substances 0.000 description 1
- 239000012867 bioactive agent Substances 0.000 description 1
- 230000000975 bioactive effect Effects 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 210000000601 blood cell Anatomy 0.000 description 1
- 239000012503 blood component Substances 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 230000022131 cell cycle Effects 0.000 description 1
- 230000036755 cellular response Effects 0.000 description 1
- 230000008859 change Effects 0.000 description 1
- 238000012512 characterization method Methods 0.000 description 1
- 230000003399 chemotactic effect Effects 0.000 description 1
- 210000001612 chondrocyte Anatomy 0.000 description 1
- 238000005352 clarification Methods 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940125797 compound 12 Drugs 0.000 description 1
- 229940126543 compound 14 Drugs 0.000 description 1
- 229940125758 compound 15 Drugs 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940125810 compound 20 Drugs 0.000 description 1
- 229940126086 compound 21 Drugs 0.000 description 1
- 229940125833 compound 23 Drugs 0.000 description 1
- 229940125961 compound 24 Drugs 0.000 description 1
- 229940125846 compound 25 Drugs 0.000 description 1
- 229940127204 compound 29 Drugs 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 229940125877 compound 31 Drugs 0.000 description 1
- 229940125878 compound 36 Drugs 0.000 description 1
- 229940125807 compound 37 Drugs 0.000 description 1
- 229940127573 compound 38 Drugs 0.000 description 1
- 229940126540 compound 41 Drugs 0.000 description 1
- 229940125936 compound 42 Drugs 0.000 description 1
- 229940125844 compound 46 Drugs 0.000 description 1
- 229940127271 compound 49 Drugs 0.000 description 1
- 229940126545 compound 53 Drugs 0.000 description 1
- 229940127113 compound 57 Drugs 0.000 description 1
- 230000008878 coupling Effects 0.000 description 1
- 238000010168 coupling process Methods 0.000 description 1
- 238000005859 coupling reaction Methods 0.000 description 1
- 210000004748 cultured cell Anatomy 0.000 description 1
- 125000004802 cyanophenyl group Chemical group 0.000 description 1
- 230000032459 dedifferentiation Effects 0.000 description 1
- 238000000151 deposition Methods 0.000 description 1
- 230000001627 detrimental effect Effects 0.000 description 1
- 238000009792 diffusion process Methods 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000000539 dimer Substances 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 239000003937 drug carrier Substances 0.000 description 1
- 230000002900 effect on cell Effects 0.000 description 1
- 230000013020 embryo development Effects 0.000 description 1
- 238000005516 engineering process Methods 0.000 description 1
- 239000002532 enzyme inhibitor Substances 0.000 description 1
- 239000003797 essential amino acid Substances 0.000 description 1
- 235000020776 essential amino acid Nutrition 0.000 description 1
- 210000000646 extraembryonic cell Anatomy 0.000 description 1
- 230000001605 fetal effect Effects 0.000 description 1
- 210000003754 fetus Anatomy 0.000 description 1
- 230000004761 fibrosis Effects 0.000 description 1
- 239000006260 foam Substances 0.000 description 1
- 230000002496 gastric effect Effects 0.000 description 1
- GNKDKYIHGQKHHM-RJKLHVOGSA-N ghrelin Chemical compound C([C@H](NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)CN)COC(=O)CCCCCCC)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CO)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CC=1N=CNC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](CO)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N1[C@@H](CCC1)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCC(N)=O)C(=O)N1[C@@H](CCC1)C(=O)N[C@@H](CCCNC(N)=N)C(O)=O)C1=CC=CC=C1 GNKDKYIHGQKHHM-RJKLHVOGSA-N 0.000 description 1
- 230000002710 gonadal effect Effects 0.000 description 1
- JAXFJECJQZDFJS-XHEPKHHKSA-N gtpl8555 Chemical compound OC(=O)C[C@H](N)C(=O)N[C@@H](CCC(O)=O)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@@H]1C(=O)N[C@H](B1O[C@@]2(C)[C@H]3C[C@H](C3(C)C)C[C@H]2O1)CCC1=CC=C(F)C=C1 JAXFJECJQZDFJS-XHEPKHHKSA-N 0.000 description 1
- 230000036541 health Effects 0.000 description 1
- 230000002440 hepatic effect Effects 0.000 description 1
- 210000003494 hepatocyte Anatomy 0.000 description 1
- 210000003917 human chromosome Anatomy 0.000 description 1
- 239000000017 hydrogel Substances 0.000 description 1
- ORTFAQDWJHRMNX-UHFFFAOYSA-N hydroxidooxidocarbon(.) Chemical group O[C]=O ORTFAQDWJHRMNX-UHFFFAOYSA-N 0.000 description 1
- 125000004029 hydroxymethyl group Chemical group [H]OC([H])([H])* 0.000 description 1
- 125000004464 hydroxyphenyl group Chemical group 0.000 description 1
- 230000028993 immune response Effects 0.000 description 1
- 230000001506 immunosuppresive effect Effects 0.000 description 1
- 230000006872 improvement Effects 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- 238000010348 incorporation Methods 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 230000005764 inhibitory process Effects 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 230000000977 initiatory effect Effects 0.000 description 1
- 229940090044 injection Drugs 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 230000003914 insulin secretion Effects 0.000 description 1
- 230000003993 interaction Effects 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 229940043355 kinase inhibitor Drugs 0.000 description 1
- 239000007788 liquid Substances 0.000 description 1
- 210000001161 mammalian embryo Anatomy 0.000 description 1
- 230000003278 mimic effect Effects 0.000 description 1
- 238000010172 mouse model Methods 0.000 description 1
- 210000002894 multi-fate stem cell Anatomy 0.000 description 1
- 210000000663 muscle cell Anatomy 0.000 description 1
- QTICHSHQWLMGCX-UHFFFAOYSA-N n-[[3-[5-[3-(2-aminopyrimidin-4-yl)anilino]triazolo[4,5-d]pyrimidin-3-yl]phenyl]methyl]cyclopropanecarboxamide Chemical compound NC1=NC=CC(C=2C=C(NC=3N=C4N(C=5C=C(CNC(=O)C6CC6)C=CC=5)N=NC4=CN=3)C=CC=2)=N1 QTICHSHQWLMGCX-UHFFFAOYSA-N 0.000 description 1
- IOMMMLWIABWRKL-WUTDNEBXSA-N nazartinib Chemical compound C1N(C(=O)/C=C/CN(C)C)CCCC[C@H]1N1C2=C(Cl)C=CC=C2N=C1NC(=O)C1=CC=NC(C)=C1 IOMMMLWIABWRKL-WUTDNEBXSA-N 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- 230000006576 neuronal survival Effects 0.000 description 1
- 229960003966 nicotinamide Drugs 0.000 description 1
- 235000005152 nicotinamide Nutrition 0.000 description 1
- 239000011570 nicotinamide Substances 0.000 description 1
- 108010008217 nidogen Proteins 0.000 description 1
- 230000005937 nuclear translocation Effects 0.000 description 1
- 230000000474 nursing effect Effects 0.000 description 1
- PIDFDZJZLOTZTM-KHVQSSSXSA-N ombitasvir Chemical compound COC(=O)N[C@@H](C(C)C)C(=O)N1CCC[C@H]1C(=O)NC1=CC=C([C@H]2N([C@@H](CC2)C=2C=CC(NC(=O)[C@H]3N(CCC3)C(=O)[C@@H](NC(=O)OC)C(C)C)=CC=2)C=2C=CC(=CC=2)C(C)(C)C)C=C1 PIDFDZJZLOTZTM-KHVQSSSXSA-N 0.000 description 1
- 210000002747 omentum Anatomy 0.000 description 1
- 230000000399 orthopedic effect Effects 0.000 description 1
- 230000002018 overexpression Effects 0.000 description 1
- AICOOMRHRUFYCM-ZRRPKQBOSA-N oxazine, 1 Chemical compound C([C@@H]1[C@H](C(C[C@]2(C)[C@@H]([C@H](C)N(C)C)[C@H](O)C[C@]21C)=O)CC1=CC2)C[C@H]1[C@@]1(C)[C@H]2N=C(C(C)C)OC1 AICOOMRHRUFYCM-ZRRPKQBOSA-N 0.000 description 1
- 210000004303 peritoneum Anatomy 0.000 description 1
- 239000000546 pharmaceutical excipient Substances 0.000 description 1
- 239000002935 phosphatidylinositol 3 kinase inhibitor Substances 0.000 description 1
- 229940043441 phosphoinositide 3-kinase inhibitor Drugs 0.000 description 1
- 102000020233 phosphotransferase Human genes 0.000 description 1
- 239000003757 phosphotransferase inhibitor Substances 0.000 description 1
- HDOWRFHMPULYOA-UHFFFAOYSA-N piperidin-4-ol Chemical compound OC1CCNCC1 HDOWRFHMPULYOA-UHFFFAOYSA-N 0.000 description 1
- 210000003635 pituitary gland Anatomy 0.000 description 1
- 238000007747 plating Methods 0.000 description 1
- 239000004633 polyglycolic acid Substances 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 210000003240 portal vein Anatomy 0.000 description 1
- 230000036515 potency Effects 0.000 description 1
- GCYXWQUSHADNBF-AAEALURTSA-N preproglucagon 78-108 Chemical compound C([C@@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCNC(N)=N)C(=O)NCC(O)=O)NC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CCCCN)NC(=O)[C@H](C)NC(=O)[C@H](C)NC(=O)[C@H](CCC(N)=O)NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1N=CNC=1)[C@@H](C)O)[C@@H](C)O)C(C)C)C1=CC=CC=C1 GCYXWQUSHADNBF-AAEALURTSA-N 0.000 description 1
- 238000012545 processing Methods 0.000 description 1
- 230000001737 promoting effect Effects 0.000 description 1
- 230000000644 propagated effect Effects 0.000 description 1
- 125000002206 pyridazin-3-yl group Chemical group [H]C1=C([H])C([H])=C(*)N=N1 0.000 description 1
- 125000000246 pyrimidin-2-yl group Chemical group [H]C1=NC(*)=NC([H])=C1[H] 0.000 description 1
- 230000009703 regulation of cell differentiation Effects 0.000 description 1
- 230000025053 regulation of cell proliferation Effects 0.000 description 1
- 230000022917 regulation of follicle-stimulating hormone secretion Effects 0.000 description 1
- 238000009256 replacement therapy Methods 0.000 description 1
- 238000011160 research Methods 0.000 description 1
- FDBYIYFVSAHJLY-UHFFFAOYSA-N resmetirom Chemical compound N1C(=O)C(C(C)C)=CC(OC=2C(=CC(=CC=2Cl)N2C(NC(=O)C(C#N)=N2)=O)Cl)=N1 FDBYIYFVSAHJLY-UHFFFAOYSA-N 0.000 description 1
- 230000000717 retained effect Effects 0.000 description 1
- 238000012552 review Methods 0.000 description 1
- 208000002491 severe combined immunodeficiency Diseases 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 230000008410 smoothened signaling pathway Effects 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 230000000920 spermatogeneic effect Effects 0.000 description 1
- 230000006641 stabilisation Effects 0.000 description 1
- 238000011105 stabilization Methods 0.000 description 1
- 239000007858 starting material Substances 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- ZSJLQEPLLKMAKR-GKHCUFPYSA-N streptozocin Chemical compound O=NN(C)C(=O)N[C@H]1[C@@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O ZSJLQEPLLKMAKR-GKHCUFPYSA-N 0.000 description 1
- 229960001052 streptozocin Drugs 0.000 description 1
- 125000000472 sulfonyl group Chemical group *S(*)(=O)=O 0.000 description 1
- 238000003786 synthesis reaction Methods 0.000 description 1
- 230000002194 synthesizing effect Effects 0.000 description 1
- 239000004753 textile Substances 0.000 description 1
- 150000003573 thiols Chemical class 0.000 description 1
- 229960004072 thrombin Drugs 0.000 description 1
- 210000001541 thymus gland Anatomy 0.000 description 1
- 210000001685 thyroid gland Anatomy 0.000 description 1
- 238000013334 tissue model Methods 0.000 description 1
- 230000017423 tissue regeneration Effects 0.000 description 1
- 238000000954 titration curve Methods 0.000 description 1
- 230000001988 toxicity Effects 0.000 description 1
- 231100000419 toxicity Toxicity 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 238000012546 transfer Methods 0.000 description 1
- 210000004881 tumor cell Anatomy 0.000 description 1
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 1
- 230000036266 weeks of gestation Effects 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0603—Embryonic cells ; Embryoid bodies
- C12N5/0606—Pluripotent embryonic cells, e.g. embryonic stem cells [ES]
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07K—PEPTIDES
- C07K14/00—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof
- C07K14/435—Peptides having more than 20 amino acids; Gastrins; Somatostatins; Melanotropins; Derivatives thereof from animals; from humans
- C07K14/475—Growth factors; Growth regulators
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/0018—Culture media for cell or tissue culture
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0676—Pancreatic cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0676—Pancreatic cells
- C12N5/0678—Stem cells; Progenitor cells; Precursor cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N5/00—Undifferentiated human, animal or plant cells, e.g. cell lines; Tissues; Cultivation or maintenance thereof; Culture media therefor
- C12N5/06—Animal cells or tissues; Human cells or tissues
- C12N5/0602—Vertebrate cells
- C12N5/0696—Artificially induced pluripotent stem cells, e.g. iPS
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2500/00—Specific components of cell culture medium
- C12N2500/05—Inorganic components
- C12N2500/10—Metals; Metal chelators
- C12N2500/20—Transition metals
- C12N2500/24—Iron; Fe chelators; Transferrin
- C12N2500/25—Insulin-transferrin; Insulin-transferrin-selenium
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/11—Epidermal growth factor [EGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/115—Basic fibroblast growth factor (bFGF, FGF-2)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/119—Other fibroblast growth factors, e.g. FGF-4, FGF-8, FGF-10
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/135—Platelet-derived growth factor [PDGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/15—Transforming growth factor beta (TGF-β)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/155—Bone morphogenic proteins [BMP]; Osteogenins; Osteogenic factor; Bone inducing factor
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/16—Activin; Inhibin; Mullerian inhibiting substance
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/165—Vascular endothelial growth factor [VEGF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/10—Growth factors
- C12N2501/19—Growth and differentiation factors [GDF]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/30—Hormones
- C12N2501/38—Hormones with nuclear receptors
- C12N2501/385—Hormones with nuclear receptors of the family of the retinoic acid recptor, e.g. RAR, RXR; Peroxisome proliferator-activated receptor [PPAR]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/41—Hedgehog proteins; Cyclopamine (inhibitor)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/415—Wnt; Frizzeled
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/40—Regulators of development
- C12N2501/42—Notch; Delta; Jagged; Serrate
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/70—Enzymes
- C12N2501/72—Transferases [EC 2.]
- C12N2501/727—Kinases (EC 2.7.)
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/80—Neurotransmitters; Neurohormones
- C12N2501/845—Gamma amino butyric acid [GABA]
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2501/00—Active agents used in cell culture processes, e.g. differentation
- C12N2501/999—Small molecules not provided for elsewhere
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2506/00—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells
- C12N2506/02—Differentiation of animal cells from one lineage to another; Differentiation of pluripotent cells from embryonic cells
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2531/00—Microcarriers
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/50—Proteins
-
- C—CHEMISTRY; METALLURGY
- C12—BIOCHEMISTRY; BEER; SPIRITS; WINE; VINEGAR; MICROBIOLOGY; ENZYMOLOGY; MUTATION OR GENETIC ENGINEERING
- C12N—MICROORGANISMS OR ENZYMES; COMPOSITIONS THEREOF; PROPAGATING, PRESERVING, OR MAINTAINING MICROORGANISMS; MUTATION OR GENETIC ENGINEERING; CULTURE MEDIA
- C12N2533/00—Supports or coatings for cell culture, characterised by material
- C12N2533/90—Substrates of biological origin, e.g. extracellular matrix, decellularised tissue
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Engineering & Computer Science (AREA)
- Biomedical Technology (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Biotechnology (AREA)
- Genetics & Genomics (AREA)
- Zoology (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Wood Science & Technology (AREA)
- General Health & Medical Sciences (AREA)
- Biochemistry (AREA)
- Cell Biology (AREA)
- Microbiology (AREA)
- General Engineering & Computer Science (AREA)
- Developmental Biology & Embryology (AREA)
- Reproductive Health (AREA)
- Gynecology & Obstetrics (AREA)
- Biophysics (AREA)
- Gastroenterology & Hepatology (AREA)
- Medicinal Chemistry (AREA)
- Molecular Biology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Toxicology (AREA)
- Transplantation (AREA)
- Micro-Organisms Or Cultivation Processes Thereof (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
diferenciação de células-tronco pluripotentes a presente invenção refere-se a métodos para diferenciar células-tronco pluripotentes. em particular, a presente invenção refere-se a métodos e composições para diferenciar células-tronco pluripotentes em células que expressam marcadores característicos da linhagem do endoderma definitivo que compreendem o cultivo das células-tronco pluripotentes em meio que compreende uma quantidade suficiente de gdf-8 para ocasionar a diferenciação das células-tronco pluripotentes em células que expressam marcadores característicos da linhagem do endoderma definitivo .
Description
Relatório Descritivo da Patente de Invenção para DIFERENCIAÇÃO DE CÉLULAS-TRONCO PLURIPOTENTES.
A presente invenção reivindica a prioridade ao pedido de número de série 61/076.900, depositado em 30 de junho de 2008, pedido de número de série 61/076.908, depositado em 30 de junho de 2008, e pedido de número de série 61/076.915, depositado em 30 de junho de 2008.
CAMPO DA INVENÇÃO
A presente invenção refere-se a métodos para diferentciar células-tronco pluripotentes. Em particular, a presente invenção refere-se a métodos e composições para diferenciar células-tronco pluripotentes em células que expressam marcadores característicos da linhagem do endoderma definitivo que compreendem o cultivo das células-tronco pluripotentes em meio que compreende uma quantidade suficiente de GDF-8 para ocasionar a diferenciação das células-tronco pluripotentes em células que expressam marcadores característicos da linhagem do endoderma definitivo.
ANTECEDENTES
Os avanços na terapia de reposição celular para a diabetes melito tipo I e a escassez de ilhotas de Langerhans transplantáveis concentraram interesses no desenvolvimento de fontes de células produtoras de insulina, ou células β, adequadas para enxerto. Uma abordagem trata da geração de células β funcionais a partir de células-tronco pluripotentes, como, por exemplo, células-tronco embrionárias.
No desenvolvimento embrionário de vertebrados, uma célula pluripotente dá origem a um grupo de células compreendendo três camadas germinativas (ectoderme, mesoderme e endoderme), em um processo conhecido como gastrulação. Tecidos como tireoide, timo, pâncreas, intestinos e fígado se desenvolvem a partir da endoderme, por meio de um estágio intermediário. O estágio intermediário nesse processo consiste na formação da endoderme definitivo. As células de endoderme definitiva expressam inúmeros marcadores, como HNF-3beta, GATA4, MIXL1, CXCR4 e SOX17.
A formação do pâncreas tem origem na diferenciação da endoderme definitiva em endoderme pancreática. As células da endoderme
2/247 pancreática expressam o gene homeobox pancreático-duodenal, Pdx1. Na ausência de Pdx1, o pâncreas não desenvolve além da formação dos ramos ventral e dorsal. Portanto, a expressão do Pdx1 marca uma etapa de importância crítica na organogênese pancreática. O pâncreas maduro contém, entre outros tipos de célula, tecido exócrino e tecido endócrino. Os tecidos exócrino e endócrino têm origem na diferenciação da endoderme pancreática.
Há relatos de que células dotadas de características das célulasilhota tenham sido obtidas a partir de células embrionárias de camundongo. Por exemplo, Lumelsky et al. (Science 292:1389, 2001) relataram a diferenciação de células-tronco embrionárias de camundongo em estruturas secretoras de insulina similares a ilhotas pancreáticas. Soria et al. (Diabetes 49:157, 2000) relatam que células secretoras de insulina derivadas de células-tronco embrionárias de camundongo normalizam a glicemia em camundongos com diabetes induzida por estreptozotocina.
Em um exemplo, Hori et al. (PNAS 99: 16105, 2002) descreve que o tratamento de células-tronco embrionárias de camundongo com inibidores de fosfoinositídieo 3-quinase (LY294002) produziu células que se assemelhavam às células β.
Em outro exemplo, Blyszczuk et al. (PNAS 100:998, 2003) relatam a geração de células produtoras de insulina a partir de células-tronco embrionárias de camundongo expressando constitutivamente Pax4.
Micallef et al., dizem que o ácido retinoico pode regular as células-tronco embrionárias comprometidas com a formação do endoderma pancreático positivo Pdx1. O ácido retinoico é mais eficaz para induzir a expressão de Pdx1 quando adicionado a culturas no dia 4 da diferenciação da célula-tronco embrionária durante um período correspondente ao final da gastrulação no embrião (Diabetes 54:301, 2005).
Miyazaki et al. relatam uma linhagem de célula-tronco embrionária de camundongo que superexpressa Pdx1. Seus resultados mostram que a expressão exógena do Pdx1 intensificou claramente a expressão dos genes de insulina, somatostatina, glicoquinase, neurogenina3, P48, Pax6 e
3/247
HNF6 nas células diferenciadas resultantes (Diabetes 53: 1030, 2004).
Skoudy et al. relatam que a ativina A (um membro da superfamília TGF-β) regula para cima a expressão de genes pancreáticos exócrinos (p48 e amilase) e endócrinos (Pdx1, insulina e glucagon) em células-tronco embrionárias de camundongo.
O efeito máximo foi observado com o uso de 1 nM de ativina A. Observou-se também que o nível de expressão de mRNA de insulina e Pdx1 não foi afetado pelo ácido retinoico; entretanto, o tratamento com 3 nM de FGF7 resultou em um nível aumentado da transcrição para Pdx1 (Biochem. J. 379: 749, 2004).
Shiraki et al. estudaram os efeitos de fatores de crescimento que acentuam especificamente a diferenciação das células-tronco embrionárias nas células positivas para Pdx1. Observou-se que o TGFp2 rendeu, reprodutivelmente, uma maior proporção de células positivas para Pdx1 (Genes Cells., junho de 2005, 10(6): 503 a 16).
Gordon et al. demonstraram a indução de células de endoderma braquiúria [positivo]/ HNF-3beta [positivo] a partir de células-tronco embrionárias de camundongo, na ausência de soro e na presença de ativina juntamente com um inibidor de sinalização Wnt (US 2006/0003446A 1).
Gordon et al. (PNAS, Volume 103, página 16806, 2006) declaram que foi necessária a sinalização simultânea de Wnt e TGF-beta/nodal/ativina para a geração da linha primitiva anterior.
Entretanto, o modelo de camundongo para desenvolvimento de célula-tronco embrionária pode não imitar exatamente o programa de desenvolvimento em mamíferos superiores, como seres humanos.
Thomson et al. isolou células-tronco embrionárias de blastocistos humanos (Science 282:114, 1998). Ao mesmo tempo, Gearhart e seus colaboradores derivaram linhagens de células germinativas embrionárias humanas (hEG) a partir do tecido gonadal de feto (Shamblott et al., Proc. Natl. Acad. Sei. USA 95:13726, 1998). Ao contrário das células-tronco embrionárias de camundongo, cuja diferenciação pode ser impedida simplesmente por realizar-se cultura com o Fator Inibitório de Leucemia
4/247 (LIF), as células-tronco embrionárias de seres humanos têm que ser mantidas sob condições muito especiais (patente U.S. n° 6.200.806; WO
99/20741; WO 01/51616).
D'Amour et al. descreve a produção de culturas enriquecidas de endoderma definitivo derivado de células-tronco embrionárias humanas na presença de uma alta concentração de ativina e baixo teor de soro (D'Amour K A et al. 2005). O transplante dessas células sob a cápsula renal de camundongos resultou na diferenciação em células mais maduras com características de alguns órgãos endodémnicos. As células de endoderma definitivo derivadas de células-tronco embrionárias humanas podem ser ainda diferenciadas em células positivas para Pdx1, após a adição de FGF10 (US 2005/0266554A1).
D'Amour et al., (Nature Biotechnology - 24, 1392 a 1401 (2006)) declaram: desenvolvemos um processo de diferenciação que converte células-tronco embrionárias de ser humano (hES) em células endócrinas capazes de sintetizarem a insulina dos hormônios pancreáticos, glucagon, somatostatina, polipeptídeo pancreático e grelina. Este processo imita a organogenese pancreática in vivo, mediante o direcionamento das células através de estágios que se assemelham ao endoderma definitivo, ao endoderma do tubo gastrointestinal, ao endoderma pancreático e ao precursor endócrino, em rota para células que expressam hormônios endócrinos.
Em outro exemplo, Fisk et al. relata um sistema para a produção de células de ilhota pancreática a partir de células-tronco embrionárias humanas (US2006/0040387A1). Nesse caso, a via de diferenciação foi dividida em três estágios. As células-tronco embrionárias humanas foram primeiro diferenciadas em endoderme com o uso de uma combinação de nbutirato e ativina A. As células foram então cultivadas com antagonistas de TGF-β como noguina em combinação com EGF ou betacelulina para gerar células positivas para Pdx1. A diferenciação terminal foi induzida por nicotinamida.
Em um exemplo, Benvenistry et al. declaram: concluímos que a
5/247 superexpressão de PDX1 acentuou a expressão de genes pancreáticos enriquecidos, a indução da expressão de insulina pode requerer sinais adicionais que só estão presentes in vivo (Benvenistry et ai., Stem Cells
2006; 24:1923-1930).
A ativina A é um membro da família TGF-beta que exibe uma ampla gama de atividades biológicas, inclusive regulação de proliferação e diferenciação celular, bem como promoção da sobrevivência neuronal. O isolamento e a purificação da ativina A são frequentemente complexos e podem, frequentemente, resultar em um rendimento insatisfatório. Por exemplo, Pangas, S.A. e Woodruff, T.K. declaram: a inibina e a ativina são hormônios proteicos com papéis fisiológicos diversos, inclusive a regulação da secreção de FSH pela hipófise. Como outros membros da família do gene para fator de transformação do crescimento β, sofrem processamento a partir de moléculas precursoras maiores, bem como montagem em dímeros funcionais. O isolamento de inibina e ativina a partir de fontes naturais só pode produzir quantidades limitadas de proteína bioativa. (J. Endocrinol. 172 (2002) 199-210).
Em outro exemplo, Arai, K. Y. et al. declaram: as ativinas são fatores de crescimento multifuncionais que pertencem à superfamília do fator de transformação do crescimento β. O isolamento de ativinas a partir de fontes naturais requer muitas etapas e só produz quantidades limitadas. Embora preparações recombinantes venham sendo usadas em estudos recentes, a purificação de ativinas ainda exige múltiplas etapas. (Protein Expression and Purification 49 (2006) 78-82).
Portanto, ainda permanece uma necessidade significativa por alternativas à ativina A para facilitar a diferenciação de células-tronco pluripotentes.
SUMÁRIO
Em uma modalidade, a presente invenção apresenta um método para diferenciar células-tronco pluripotentes em células que expressam marcadores característicos da linhagem de endoderma definitivo, compreendendo o cultivo das células-tronco pluripotentes em um meio que
6/247 compreende uma quantidade suficiente de GDF-8 para ocasionar a diferenciação das células-tronco pluripotentes em células que expressam marcadores característicos da linhagem de endoderma definitivo.
Em uma modalidade, o meio que compreende uma quantidade suficiente de GDF-8 também contém pelo menos um outro composto. Em uma modalidade, esse pelo menos um outro composto é uma anilinapiridinotriazina. Em uma modalidade alternativa, esse pelo menos um outro composto é uma anilina-piridinotriazina cíclica.
BREVE DESCRIÇÃO DAS FIGURAS
A figura 1 mostra a diferenciação de células-tronco embrionárias humanas H1 em células expressoras de marcadores característicos da linhagem de endoderma definitivo. A diferenciação foi determinada mediante a medição do número de células (Painel A) e da intensidade de SOX17 (Painel B) com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare). As células-tronco embrionárias humanas foram tratadas durante um total de quatro dias com um meio contendo 20 ng/mL de Wnt3a, mais ativina A, nas concentrações indicadas (barras pretas), ou com um meio desprovido de Wnt3a mas com ativina A nas concentrações indicadas (barras brancas).
A figura 2 mostra a relação entre dose e resposta de ativina A e GDF8 usados para diferenciar células da linhagem H1 de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo. As células foram tratadas por um total de três dias com ativina A ou GDF8 nas concentrações mostradas, em combinação com 20 ng/mL de Wnt3a no primeiro dia de teste. A diferenciação foi determinada mediante a medição da intensidade de SOX17, com o uso de uma sonda de anticorpo fluorescente e análise de alto conteúdo em um equipamento de análise celular GE Healthcare IN Cell Analyzer.
A figura 3 mostra a expressão de CXCR4 nas células, em seguida à primeira etapa de diferenciação, de acordo com os métodos descritos no Exemplo 12. As células H1 foram tratadas com 100 ng/mL de
7/247 ativina A ou 200 ng/mL de GDF-8 durante um total de três dias, em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 34, ou 2,5 μΜ do Composto 56, durante todos os três dias. A expressão de CXCR4 foi medida com o uso de uma sonda de anticorpo fluorescente e citometria de fluxo, produzindo as porcentagens mostradas de células positivas.
A figura 4 mostra a expressão de SOX17 em células após três dias de diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 12. As células H1 foram tratadas durante um total de três dias com 100 ng/mL de ativina A ou 200 ng/mL de GDF-8 em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 34, ou 2,5 μΜ do Composto 56, durante todos os três dias. A diferenciação foi determinada mediante a medição da intensidade de SOX17 (barras pretas) e o número de células resultante (barras brancas) com sondas de anticorpo fluorescentes e análise de alto conteúdo em um equipamento de análise celular GE Healthcare IN Cell Analyzer.
A figura 5 mostra a expressão de proteína PDX1 e CDX2 nas células, em seguida à terceira etapa de diferenciação, de acordo com os métodos descritos no Exemplo 12. As células H1 foram tratadas durante um total de três dias com 100 ng/mL de ativina A ou 200 ng/mL de GDF-8 em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 34, ou 2,5 μΜ do Composto 56, durante todos os três dias, seguido de subsequente diferenciação por meio das segunda e terceira etapas de diferenciação. A expressão de proteína e os números de células, conforme determinado com sondas de anticorpo fluorescentes e análise de alto conteúdo, são representados para cada grupo de tratamento. Para propósitos de comparação, os valores são normalizados em relação ao tratamento com ativina A/Wnt3a.
A figura 6 mostra a expressão de proteína PDX1 (barras brancas) e o número de células (barras pretas) para células em seguida à quarta etapa de diferenciação, de acordo com os métodos descritos no Exemplo 12. As células H1 foram tratadas durante um total de três dias com
8/247
100 ng/mL de ativina A ou 200 ng/mL de GDF-8 em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 34, ou 2,5 μΜ de Composto 56, durante todos os três dias, seguido de subsequente diferenciação por meio das segunda, terceira e quarta etapas de diferenciação. A expressão de proteína e os números de células, conforme determinado com sondas de anticorpo fluorescentes e análise de alto conteúdo, são representados para cada grupo de tratamento. Para propósitos de comparação, os valores são normalizados em relação ao tratamento com ativina A/Wnt3a.
A figura 7 mostra a expressão de proteína para insulina e glucagon, bem como o número de células, para células diferenciadas de acordo com os métodos descritos no Exemplo 12. As células H1 foram tratadas durante um total de três dias com 100 ng/mL de ativina A ou 200 ng/mL de GDF-8 em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 34, ou 2,5 μΜ de Composto 56, durante todos os três dias, seguido de subsequente diferenciação por meio das segunda, terceira, quarta e quinta etapas de diferenciação. A expressão de proteína e os números de células, conforme determinado com sondas de anticorpo fluorescentes e análise de alto conteúdo, são representados para cada grupo de tratamento. Para propósitos de comparação, os valores são normalizados em relação ao tratamento com ativina A/Wnt3a.
A figura 8 mostra a expressão de proteína SOX17 e o número de células para células-tronco embrionárias humanas, após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo
13. As células H1 foram tratadas durante um total de quatro dias com 100 ng/mL de ativina A ou 100 ng/mL de um fator de crescimento GDF em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 34, ou 2,5 μΜ de Composto 56 durante os primeiros dois dias de teste. A expressão de proteína SOX17 (barras pretas) e os números de células (barras brancas), conforme determinado com sondas de anticorpo fluorescentes e análise de alto conteúdo, são representados para cada grupo de tratamento. Para propósitos de comparação, os valores são
9/247 normalizados em relação ao tratamento com ativina A/Wnt3a. O painel 8A mostra uma série de condições de controle para diferenciação na ausência de quaisquer fatores de crescimento (NENHUM), ou com tratamento de ativina A/Wnt3a (AA/Wnt3a), ou com reagentes individuais por si sós. O painel 8B mostra a diferenciação com GDF-3, por si só ou em múltiplas combinações com Wnt3a, Composto 34 ou Composto 56. O painel 8C mostra a diferenciação com GDF-5, por si só ou em múltiplas combinações com Wnt3a, Composto 34 ou Composto 56. O painel 8D mostra a diferenciação com GDF-8, por si só ou em múltiplas combinações com Wnt3a, Composto 34 ou Composto 56. O painel 8E mostra a diferenciação com GDF-10, por si só ou em múltiplas combinações com Wnt3a, Composto 34 ou Composto 56. O painel 8F mostra a diferenciação com GDF-11, por si só ou em múltiplas combinações com Wnt3a, Composto 34 ou Composto 56. O painel 8G mostra a diferenciação com GDF-15, por si só ou em múltiplas combinações com Wnt3a, Composto 34 ou Composto 56.
A figura 9 mostra a expressão de proteína SOX17 em célulastronco embrionárias humanas após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 14. As células H1 foram tratadas durante um total de três dias com 100 ng/mL de ativina A, ou vários fatores de crescimento nas concentrações mostradas, em combinação com 20 ng/mL de Wnt3a, ou 2,5 μΜ de Composto 34 durante o primeiro dia do teste. A expressão de proteína SOX17 (barras pretas) e os números de células (barras brancas), conforme determinado com sondas de anticorpo fluorescentes e análise de alto conteúdo, são representados para cada grupo de tratamento. Para propósitos de comparação, os valores são normalizados em relação ao tratamento com ativina A/Wnt3a. O painel 9A mostra uma série de condições de controle para diferenciação com Wnt3a por si só, ou na ausência de quaisquer fatores de crescimento (Nenhum), ou com tratamento de ativina A/Wnt3a (AA/Wnt3a). O painel 9B mostra a diferenciação com GDF-8 (fornecedor: PeproTech), nas concentrações mostradas, em combinação com 20 ng/mL de Wnt3a. O painel 9C mostra a diferenciação com GDF-8 (fornecedor: Shenendoah), nas concentrações
10/247 mostradas, em combinação com 20 ng/mL de Wnt3a. O painel 9D mostra a diferenciação com ΤΘΕβ1, nas concentrações mostradas, em múltiplas combinações com Wnt3a ou Composto 34. O painel 9E mostra a diferenciação com BMP2, nas concentrações mostradas, em múltiplas combinações com Wnt3a ou Composto 34. O painel 9F mostra a diferenciação com BMP3, nas concentrações mostradas, em múltiplas combinações com Wnt3a ou Composto 34. O painel 9G mostra a diferenciação com BMP4, nas concentrações mostradas, em múltiplas combinações com Wnt3a ou Composto 34.
A figura 10 mostra a expressão de proteína SOX17 em célulastronco embrionárias humanas após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias em várias exposições temporizadas com 100 ng/mL de ativina A ou 100 ng/mL de GDF-8, em combinação com 20 ng/mL de Wnt3a. A expressão de proteína SOX17, conforme determinada por sondas de anticorpo fluorescentes e análise de alto conteúdo, é mostrada sob a forma de valores de intensidade total para cada grupo de tratamento, sendo as condições de controle testadas quanto à diferenciação sem a adição de quaisquer fatores de crescimento (nenhum tratamento), com Wnt3a por si só, com ativina A ou GDF-8 por si só, ou com tratamento por ativina A/Wnt3a ou GDF-8/Wnt3a, sendo que o Wnt3a foi adicionado somente durante o primeiro dia do teste, ou durante os três dias de teste, conforme mostrado.
A figura 11 mostra a expressão de proteína SOX17 em célulastronco embrionárias humanas após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de ativina A em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado somente no
11/247 primeiro dia do teste. A expressão de proteína para SOX17, conforme determinado por sondas de anticorpo fluorescentes e análise de alto conteúdo, é representada por valores de intensidade total.
A figura 12 mostra a expressão de proteína SOX17 em célulastronco embrionárias humanas após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de ativina A em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado durante todos os três dias do teste. A expressão de proteína para SOX17, conforme determinado por sondas de anticorpo fluorescentes e análise de alto conteúdo, é representada por valores de intensidade total.
A figura 13 mostra a expressão de proteína SOX17 em célulastronco embrionárias humanas após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de GDF-8 em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado somente no primeiro dia do teste. A expressão de proteína para SOX17, conforme determinado por sondas de anticorpo fluorescentes e análise de alto conteúdo, é representada por valores de intensidade total.
A figura 14 mostra a expressão de proteína SOX17 em célulastronco embrionárias humanas após a diferenciação para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de GDF-8 em combinação com o composto
12/247 de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado durante todos os três dias do teste. A expressão de proteína para SOX17, conforme determinado por sondas de anticorpo fluorescentes e análise de alto conteúdo, é representada por valores de intensidade total.
A figura 15 mostra os rendimentos do número de células após a diferenciação de células-tronco embrionárias humanas para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias em várias exposições temporizadas com 100 ng/mL de ativina A ou 100 ng/mL de GDF-8, em combinação com 20 ng/mL de Wnt3a. Os números de células, conforme determinado por uma sonda nuclear fluorescente e por análise de alto conteúdo, são mostrados para cada grupo de tratamento, testando-se as condições de controle para diferenciação sem a adição de nenhum fator de crescimento (nenhum tratamento), com Wnt3a por si só, com ativina A ou GDF-8 por si só, ou com tratamento por ativina A/Wnt3a ou por GDF8/Wnt3a, sendo que o Wnt3a foi adicionado somente para o primeiro dia do teste, ou para todos os três dias do teste, conforme mostrado.
A figura 16 mostra os rendimentos do número de células após a diferenciação de células-tronco embrionárias humanas para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de ativina A em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado somente no primeiro dia do teste. São mostrados os rendimentos do número de células, conforme determinado por uma sonda nuclear fluorescente e por análise de alto conteúdo.
13/247
A figura 17 mostra os rendimentos do número de células após a diferenciação de células-tronco embrionárias humanas para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de ativina A em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado durante todos os três dias do teste. São mostrados os rendimentos do número de células, conforme determinado por uma sonda nuclear fluorescente e por análise de alto conteúdo.
A figura 18 mostra os rendimentos do número de células após a diferenciação de células-tronco embrionárias humanas para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de GDF-8 em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações mostradas, sendo que o composto de teste foi adicionado somente no primeiro dia do teste. São mostrados os rendimentos do número de células, conforme determinado por uma sonda nuclear fluorescente e por análise de alto conteúdo.
A figura 19 mostra os rendimentos do número de células após a diferenciação de células-tronco embrionárias humanas para endoderma definitivo, de acordo com os métodos descritos no Exemplo 15. As células H1 foram tratadas durante um total de três dias, em várias exposições temporizadas, com 100 ng/mL de GDF-8 em combinação com o composto de teste (Composto 181 (Painel A), Composto 180 (Painel B), Composto 19 (Painel C), Composto 202 (Painel D), Composto 40 (Painel E), Composto 34 (Painel F) ou inibidor de GSK3 BIO (Painel G)) nas concentrações
14/247 mostradas, sendo que o composto de teste foi adicionado durante todos os três dias do teste. São mostrados os rendimentos do número de células, conforme determinado por uma sonda nuclear fluorescente e por análise de alto conteúdo.
A figura 20 mostra a expressão de vários marcadores de proteína em células através das múltiplas etapas de diferenciação, de acordo com os métodos descritos no Exemplo 16. As células H1 foram tratadas com 100 ng/mL de ativina A ou 100 ng/mL de GDF-8 durante um total de três dias, em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de vários compostos (Composto 19, Composto 202, Composto 40 ou inibidor GSK3 BIO) adicionados somente no primeiro dia. A figura 20, painel A mostra a análise de FACS para o marcador de endoderma definitivo, CXCR4, em células após a primeira etapa de diferenciação. A expressão de CXCR4 foi medida com o uso de uma sonda de anticorpo fluorescente e citometria de fluxo, produzindo as porcentagens de células positivas conforme mostrado. A figura 20, painel B mostra a análise de imagens de alto conteúdo para expressão de proteína SOX17 normalizada (barras pretas) e números de células recuperadas (barras brancas) resultantes da primeira etapa de diferenciação, testando os tratamentos correspondentes mostrados. A figura 20, painel C, mostra a análise de imagens de alto conteúdo para números relativos de células recuperadas de culturas tratadas por meio da etapa de diferenciação 5. A figura 20, painel D, mostra a análise de imagens de alto conteúdo para expressão de proteína glucagon a partir de culturas tratadas por meio da etapa de diferenciação 5. A figura 20, painel E, mostra a análise de imagens de alto conteúdo para expressão de proteína insulina a partir de culturas tratadas por meio da etapa de diferenciação 5. A figura 20, painel F mostra a razão entre as expressões de glucagon e de insulina em células de culturas tratadas por meio da etapa de diferenciação 5. Para propósitos de comparação, os valores de expressão nos painéis B, C, D, E e F são normalizados em relação ao tratamento de controle com ativina A e Wnt3a durante a etapa 1.
15/247
A figura 21 mostra a expressão de vários marcadores de proteína e de RT-PCR em células através das múltiplas etapas de diferenciação, de acordo com os métodos descritos no Exemplo 17. As células H1 foram tratadas com 100 ng/mL de ativina A ou 100 ng/mL de GDF-8 durante um total de três dias, em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou vários compostos nas concentrações apresentadas a seguir (Composto 181, Composto 180, Composto 19, Composto 202, Composto 40, Composto 56 ou inibidor GSK3 BIO) adicionados somente no primeiro dia. A análise FACS quanto ao marcador de endoderma definitivo CXCR4 é mostrada em células após a primeira etapa de diferenciação, em que o tratamento combinou ativina A (Painel A) ou GDF-8 (Painel B) com Wnt3a ou vários compostos. A expressão de CXCR4 foi medida com o uso de uma sonda de anticorpo fluorescente e citometria de fluxo, produzindo as porcentagens de células positivas conforme mostrado. Nos painéis subsequentes da figura 21, valores normalizados de RT-PCR para vários marcadores de diferenciação são mostrados com os respectivos tratamentos usando ativina A ou GDF-8 durante a primeira etapa de diferenciação, conforme exposto a seguir: marcadores ao final da primeira etapa de diferenciação para tratamentos combinando ativina A (Painel C) ou GDF-8 (Painel D); marcadores ao final da terceira etapa de diferenciação para tratamentos combinando ativina A (Painel E) ou GDF-8 (Painel F); marcadores ao final da quarta etapa de diferenciação para tratamentos combinando ativina A (Painel G) ou GDF-8 (Painel H); marcadores ao final da quinta etapa de diferenciação para tratamentos combinando ativina A (Painel I) ou GDF-8 (Painel J). Na conclusão da quinta etapa de diferenciação, realizou-se uma análise de alto conteúdo para medir os números de células recuperadas para os tratamentos correspondentes durante a primeira etapa de diferenciação usando ativina A (Painel K) ou GDF-8 (Painel Μ). A análise de alto conteúdo foi, também, usada para medir a intensidade de glucagon e insulina nas populações de células recuperadas ao final da quinta etapa de diferenciação, correspondente ao tratamento com ativina A (Painel L) ou
16/247
GDF-8 (Painel N) durante a primeira etapa de diferenciação.
A figura 22 mostra a expressão de vários marcadores de proteína e RT-PCR em células tratadas de acordo com os métodos descritos no Exemplo 18. As células H1 foram tratadas com 100 ng/mL de ativina A ou 100 ng/mL de GDF-8 durante um total de três dias, em combinação com 20 ng/mL de Wnt3a durante o primeiro dia, ou 2,5 μΜ de Composto 40, ou
2,5 μΜ de Composto 202, somente no primeiro dia. A figura 22, painel A mostra a análise de FACS quanto ao marcador de endoderma definitivo, CXCR4, em células após a primeira etapa de diferenciação. A expressão de CXCR4 foi medida com o uso de uma sonda de anticorpo fluorescente e citometria de fluxo, produzindo as porcentagens de células positivas conforme mostrado. Na figura 22, painel B, valores normalizados de RTPCR para vários marcadores de diferenciação em células recuperadas após a quarta etapa de diferenciação são mostrados correspondendo aos respectivos tratamentos usando ativina A/Wnt3a, ou GDF-8/Composto 40, ou GDF-8/Composto 202, durante a primeira etapa de diferenciação.
A figura 23 mostra o teor de peptídeo C detectado em camundongos SCID beges que receberam células ao final da quarta etapa do protocolo de diferenciação, conforme descrito no Exemplo 18.
A figura 24, painel A, mostra a expressão de CXCR4, conforme determinado por FACS, em células ao final da primeira etapa do protocolo de diferenciação descrito no Exemplo 19. O painel B mostra a expressão de vários genes, conforme determinado por RT-PCR em células ao final da quarta etapa do protocolo de diferenciação descrito no Exemplo 19. São mostradas duas réplicas experimentais diferentes (Rep-1 e Rep-2), cada qual submetida a protocolos de tratamento idênticos. O painel C mostra o teor de peptídeo C detectado em camundongos SCID beges que receberam células ao final da etapa quatro do protocolo de diferenciação, conforme tratado com GDF-8 e Wnt3a durante a primeira etapa da diferenciação in vitro. O painel D mostra o teor de peptídeo C detectado em camundongos SCID beges que receberam células ao final da etapa quatro do protocolo de diferenciação, conforme tratado com GDF-8 e Composto 28 durante a
17/247 primeira etapa da diferenciação in vitro.
A figura 25 mostra o número de células (painel A) e a expressão de CXCR4 (painel B) oriundos de células cultivadas em microesferas portadoras, tratadas de acordo com os métodos da presente invenção, conforme descrito no Exemplo 22. As células foram cultivadas sobre microesferas de Cytodex3 sem tratamento (não diferenciadas), ou com tratamento combinando 100 ng/mL de ativina A com 20 ng/mL de Wnt3a (AA/Wnt3a), ou com vários tratamentos combinando GDF-8, conforme mostrado: 50 ng/mL de GDF-8 com 2,5 μΜ de Composto 34 (Cmp 34+8); ou 50 ng/mL de GDF-8 com 2,5 μΜ de Composto 34 e 50 ng/mL de PDGF (Cmp 34+8+D); ou 50 ng/mL de GDF-8 com 2,5 μΜ de Composto 34, 50 ng/mL de PDGF e 50 ng/mL de VEGF (Cmp 34+8+D+V); ou 50 ng/mL de GDF-8 com 2,5 μΜ de Composto 34, 50 ng/mL de PDGF, 50 ng/mL de VEGF e 20 ng/mL de muscimol (Cmp 34+8+D+V+M).
A figura 26 mostra a proliferação de células em seguida ao tratamento dos compostos da presente invenção, conforme descrito no Exemplo 23. Os painéis B a I mostram resultados de teste para tratamento com o uso de um composto em combinação com GDF-8 e medindo-se as leituras de MTS OD a 1 dia, 2 dias e 3 dias após o início do teste de diferenciação.
A figura 27 mostra a expressão de várias proteínas e genes oriundos de células cultivadas em microesferas portadoras, tratadas de acordo com os métodos da presente invenção. O painel A mostra a porcentagem de expressão positiva de CXCR4, CD99 e CD9, conforme determinado por FACS em células ao final da primeira etapa do protocolo de diferenciação descrito no Exemplo 24. O painel B mostra células recuperadas de tratamentos conforme mostrado, diferenciadas através da etapa três do protocolo de diferenciação. O painel C mostra os valores de ddCT para vários marcadores genéticos expressos nas células tratadas conforme mostrado na etapa, e diferenciado através da etapa três do protocolo.
DESCRIÇÃO DETALHADA
Com propósitos de esclarecimento da descrição, e sem propó18/247 sitos de limitação, a descrição detalhada da invenção é dividida nas subseções a seguir que descrevem ou ilustram determinadas características, modalidades ou aplicações da presente invenção.
Definições
Células-tronco são células não diferenciadas definidas por sua capacidade, em nível unicelular, tanto para autorrrenovação como para diferenciação a fim de produzir células-progênie, inclusive progenitoras autorrenováveis, progenitoras não renováveis e células terminalmente diferenciadas. As células-tronco são também caracterizadas por sua capacidade de se diferenciar, in vitro, em células funcionais de várias linhagens celulares de múltiplas camadas germinativas (endoderma, mesoderma e ectoderma), bem como por sua capacidade de originar, após transplante, tecidos de múltiplas camadas germinativas e de contribuir substancialmente para a maioria, senão todos, dos tecidos após a injeção em blastocistos.
As células-tronco são classificadas de acordo com seu potencial de desenvolvimento como: (1) totipotentes, o que significa que são capazes de dar origem a todos os tipos de células embrionárias e extraembrionárias; (2) pluripotentes, o que significa que são capazes de dar origem a todos os tipos de célula embrionária; (3) multipotentes, o que significa que são capazes de dar origem a um subconjunto de linhagens celulares, porém todos dentro de um tecido, órgão ou sistema fisiológico específico (por exemplo, células-tronco hematopoiéticas (HSC) podem produzir progênie que inclui HSC (autorrenovação), progenitoras oligopotentes restritas a células sanguíneas e todos os tipos de células e elementos (por exemplo, plaquetas) que são componentes normais do sangue); (4) oligopotentes, o que significa que são capazes de dar origem a subconjuntos de linhagens celulares mais restritos que aqueles das células-tronco multipotentes; e (5) unipotentes, o que significa que são capazes de dar origem a uma única linhagem celular (por exemplo, células-tronco espermatogênicas).
A diferenciação é o processo pelo qual uma célula não especializada (não comprometida) ou menos especializada adquire as características de uma célula especializada, como uma célula nervosa ou muscular.
19/247
Uma célula diferenciada ou induzida por diferenciação é aquela que assumiu uma posição mais especializada (comprometida) dentro da linhagem de uma célula. O termo comprometida, quando aplicado ao processo de diferenciação, refere-se a uma célula que avançou na rota de diferenciação até um ponto em que, sob circunstâncias normais, continuará a se diferenciar em um tipo específico de célula, ou em um subconjunto de tipos de célula, e não poderá, sob circunstâncias normais, diferenciar-se em um tipo de célula diferente, ou reverter para um tipo de célula menos diferenciado. A desdiferenciação refere-se ao processo pelo qual uma célula reverte a uma posição menos especializada (ou menos comprometida) dentro da linhagem celular. Para uso na presente invenção, a linhagem de uma célula define a hereditariedade da mesma, isto é, de quais células se originou e a quais células pode dar origem. A linhagem de uma célula a coloca dentro de um esquema hereditário de desenvolvimento e diferenciação. Um marcador específico de linhagem refere-se a uma característica especificamente associada ao fenótipo das células de uma linhagem em questão, e pode ser usado para avaliar a diferenciação de uma célula não comprometida em relação à linhagem em questão.
A expressão linhagem de células β refere-se a células com expressão gênica positiva para o fator de transcrição PDX-1 e pelo menos um dentre os seguintes fatores de transcrição: NGN3, NKX2.2, NKX6.1, NEUROD, ISL1, HNF-3 beta, MAFA, PAX4 ou PAX6. Células que expressam marcadores característicos da linhagem de célula β incluem células β.
A expressão células expressoras de marcadores característicos da linhagem de endoderma definitivo, ou células em Estágio 1, ou Estágio 1, para uso na presente invenção, refere-se a células que expressam pelo menos um dentre os seguintes marcadores: SOX17, GATA4, HNF-3 beta, GSC, CER1, Nodal, FGF8, braquiúria, proteína homeobox similar a Mix, FGF4 CD48, eomesodermina (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99 ou OTX2. Células que expressam marcadores característicos da linhagem de endoderma definitivo incluem
20/247 células precursoras da linha primitiva, células da linha primitiva, células de mesendoderma e células do endoderma definitivo.
A expressão células expressoras de marcadores característicos da linhagem de endoderma pancreático, para uso na presente invenção, refere-se a células que expressam pelo menos um dentre os seguintes marcadores: PDX1, HNF-1 beta, PTF1 alfa, HNF6 ou HB9. Células que expressam marcadores característicos da linhagem endodérmica pancreática incluem células endodérmicas pancreáticas, células do tubo intestinal primitivo, e células do trato digestivo superior posterior.
A expressão células expressoras de marcadores característicos da linhagem endócrina pancreática, ou células em Estágio 5, ou Estágio 5, para uso na presente invenção, refere-se a células que expressam pelo menos um dentre os seguintes marcadores: NGN3, NEUROD, ISL1, PDX1, NKX6.1, PAX4 ou PTF-1 alfa. As células expressoras de marcadores característicos da linhagem endócrina pancreática incluem células pancreáticas endócrinas, células pancreáticas expressoras de hormônio e células pancreáticas secretoras de hormônio, bem como células da linhagem de células β.
A expressão endoderma definitivo, para uso na presente invenção, refere-se a células que apresentam as características de células oriundas do epiblasto durante a gastrulação, e que formam o trato gastrointestinal e seus derivados. As células de endoderma definitivo expressam os seguintes marcadores: HNF-3 beta, GATA4, SOX-17, Cerberus, OTX2, goosecoide, C-Kit, CD99 ou MIXL1.
A expressão endoderma extraembrionário, para uso na presente invenção, refere-se a uma população de células que expressam pelo menos um dentre os seguintes marcadores: SOX7, AFP ou SPARC.
Marcadores, para uso na presente invenção, são moléculas de ácido nucléico ou polipeptídeo que são expressas diferencialmente em uma célula de interesse. Nesse contexto, expressão diferencial significa um nível aumentado para um marcador positivo e um nível diminuído para um marcador negativo. O nível detectável do ácido nucléico ou polipeptídeo do
21/247 marcador é suficientemente maior ou menor nas células em questão, em comparação com outras células, de modo que a célula em questão pode ser identificada e distinguida de outras células com o uso de qualquer um de uma variedade de métodos conhecidos na técnica.
A expressão célula de mesendoderma, para uso na presente invenção, refere-se a uma célula que expressa pelo menos um dentre os seguintes marcadores: CD48, eomesodermina (EOMES), SOX17, DKK4, HNF-3 beta, GSC, FGF17 ou GATA-6.
Os termos célula pancreática endócrina, ou célula que expressa hormônio pancreático, para uso na presente invenção, referem-se a uma célula capaz de expressar pelo menos um dentre os seguintes hormônios: insulina, glucagon, somatostatina e polipeptídeo pancreático.
A expressão célula de endoderma pancreático, ou células em Estágio 4, ou Estágio 4, para uso na presente invenção, refere-se a uma célula capaz de expressar pelo menos um dentre os seguintes marcadores: NGN3, NEUROD, ISL1, PDX1, PAX4 ou NKX2.2.
Célula produtora de hormônio pancreático, para uso na presente invenção, refere-se a uma célula capaz de produzir pelo menos um dos seguintes hormônios: insulina, glucagon, somatostatina, e polipeptídeo pancreático.
A expressão célula pancreática secretora de hormônio, para uso na presente invenção, refere-se a uma célula capaz de secretar pelo menos um dentre os seguintes hormônios: insulina, glucagon, somatostatina e polipeptídeo pancreático.
A expressão célula posterior do intestino anterior, ou células em Estágio 3, ou Estágio 3, para uso na presente invenção, refere-se a uma célula capaz de secretar pelo menos um dentre os seguintes marcadores: PDX1, HNF1, PTF-1 alfa, HNF6, HB-9 ou PROX-1.
Célula pré-linha primitiva, para uso na presente invenção, refere-se a uma célula que expressa pelo menos um dos seguintes marcadores: Nodal, ou FGF8.
A expressão célula do tubo intestinal primitivo, ou células em
22/247
Estágio 2, ou Estágio 2, para uso na presente invenção, refere-se a uma célula capaz de secretar pelo menos um dentre os seguintes marcadores:
HNF1, HNF-4 alfa.
Célula da linha primitiva, para uso na presente invenção, refere-se a uma célula que expressa pelo menos um dos seguintes marcadores: Brachyury, proteína Mix-like homeobox, ou FGF4.
Isolamento, expansão e cultura de células-tronco pluripotentes
Caracterização de células-tronco pluripotentes
A pluripotência das células-tronco pluripotentes pode ser confirmada, por exemplo, injetando-se as células em camundongos com imunodeficiência combinada grave (SCID), fixando-se os teratomas que se formam com o uso de 4% de paraformaldeído e, então, examinando-os histologicamente quanto a evidências dos tipos de célula oriundos das três camadas germinativas. Alternativamente, a pluripotência pode ser determinada criando-se corpos embroides e avaliando-os quanto à presença de marcadores associados às três camadas germinais.
As linhagens de células-tronco pluripotentes propagadas podem ser submetidas a cariotipagem com o uso de uma técnica-padrão de bandamento G, sendo então comparadas aos cariótipos publicados das espécies de primata correspondentes. É desejável a obtenção de células que tenham um cariótipo normal, o que significa que as células são euploides, em que todos os cromossomos humanos estão presentes e sem alterações perceptíveis.
Fontes de células-tronco pluripotentes
Os tipos de células-tronco pluripotentes que podem ser usados incluem linhagens estabelecidas de células pluripotentes derivadas de tecido formado após a gestação, inclusive tecido pré-embrionário (como um blastocisto), tecido embrionário ou tecido fetal coletado a qualquer tempo durante a gestação, tipicamente porém não necessariamente antes de aproximadamente 10 a 12 semanas de gestação. Alguns exemplos não limitadores consistem em linhagens estabelecidas de células-tronco embrionárias humanas ou células germinativas embrionárias humanas, como as
23/247 linhagens de célula-tronco embrionária humana H1, H7 e H9 (WiCell). É também contemplado o uso das composições desta descrição durante o estabelecimento inicial ou a estabilização dessas células, caso no qual as células-fonte seriam células pluripotentes primárias coletadas diretamente dos tecidos-fonte. São adequadas, também, as células coletadas de uma população de células-tronco pluripotentes já cultivadas na ausência de células mantenedoras. São adequadas, também, as linhagens de célulatronco embrionária humana mutantes, como BG01v (BresaGen, Athens, GA, EUA).
Em uma modalidade, as células-tronco embrionárias humanas são preparadas conforme descrito por Thomson et al. (patente US n° 5.843.780; Science 282:1145, 1998; Curr. Top. Dev. Biol. 38:133 ff., 1998; Proc. Natl. Acad. Sei. EUA 92:7844, 1995).
Em uma modalidade, as células-tronco pluripotentes são preparadas conforme descrito por Takahashi et al. (Cell 131: 1-12, 2007).
Cultura de células-tronco pluripotentes
Em uma modalidade, as células-tronco pluripotentes são tipicamente cultivadas sobre uma camada de células alimentadoras que de várias maneiras oferecem suporte às células-tronco pluripotentes. Alternativamente, as células-tronco pluripotentes são cultivadas em um sistema de cultura que é essencialmente isento de células nutrizes mas que, mesmo assim, suporte a proliferação de células-tronco pluripotentes sem que ocorra uma diferenciação substancial. A proliferação de células-tronco pluripotentes em um meio de cultura isento de células nutrizes sem diferenciação é suportado com o uso de um meio condicionado pelo cultivo prévio com outro tipo de célula. Alternativamente, o crescimento de células-tronco pluripotentes em meio de cultura isento de células nutrizes sem diferenciação é suportado com o uso de um meio quimicamente definido.
As células-tronco pluripotentes podem ser aplicadas sobre um substrato de cultura adequado. Em uma modalidade, o substrato de cultura adequado é um componente de matriz extracelular, como aqueles derivados de membrana basal, que possa fazer parte dos acoplamentos receptor
24/247 ligante das moléculas de adesão. Em uma modalidade, o substrato de cultura adequado consiste em MATRIGEL® (Becton Dickenson). MATRIGEL® é uma preparação solúvel feita a partir de células tumorais Engelbreth-Holm-Swarm, que se gelifica à temperatura ambiente para formar uma membrana basal reconstituída.
Outros componentes e misturas de componentes de arranjo extracelular são adequados como alternativa. Dependendo do tipo de célula sendo submetido à proliferação, isto pode incluir laminina, fibronectina, proteoglicano, entactina, sulfato de heparano, e similares, sozinhos ou em várias combinações.
As células-tronco pluripotentes podem ser aplicadas sobre o substrato em uma distribuição adequada e na presença de um meio que promova a sobrevivência, a propagação e a retenção das características desejáveis. Todas essas características se beneficiam da cuidadosa atenção à distribuição da semeadura, e podem ser prontamente determinadas pelo versado na técnica.
O meio de cultura adequado pode ser produzido a partir dos seguintes componentes, como o meio Eagle modificado da Dulbecco (DMEM), Gibco n° 11965-092; meio Eagle modificado Knockout da Dulbecco (KO DMEM), Gibco n° 10829-018; meio basal DMEM F12/50% da Ham; 200 mM de L-glutamina, Gibco n° 15039-027; solução de aminoâcidos não essenciais, Gibco 11140-050; β-mercapto etanol, Sigma n° M7522; fator de crescimento de fibroblastos básico recombinante humano (bFGF), Gibco n° 13256-029.
Formação de células produtoras de hormônio pancreático a partir de células-tronco pluripotentes
Em uma modalidade, a presente invenção apresenta um método para produção de células produtoras de hormônio pancreático a partir de células-tronco pluripotentes, compreendendo as etapas de:
a. cultivar células-tronco pluripotentes,
b. diferenciar as células-tronco pluripotentes nas células que expressam características de marcadores da linhagem endodérmica
25/247 definitiva,
c. diferenciar as células que expressam características de marcadores da linhagem endodérmica definitiva em células que expressam características de marcadores da linhagem endodérmica pancreática, e
d. diferenciar as células que expressam características de marcadores da linhagem endodérmica pancreática em células que expressam características de marcadores da linhagem endodérmica pancreática.
Em um aspecto da presente invenção, a célula pancreática endócrina é uma célula produtora de hormônio pancreático. Em um aspecto alternativo, a célula pancreática endócrina é uma célula que expressa marcadores característicos da linhagem de células β. Uma célula que expressa marcadores característicos da linhagem de células β expressa PDX1 e pelo menos um dentre os seguintes fatores de transcrição: NGN3, NKX2.2, NKX6.1, NEUROD, ISL1, HNF-3 beta, MAFA, PAX4 ou Pax6. Em um aspecto da presente invenção, uma célula que expressa marcadores característicos da linhagem de células β é uma célula β.
As células-tronco pluripotentes adequadas ao uso na presente invenção incluem, por exemplo, a linhagem H9 de células-tronco embrionárias humanas (código NIH: WA09), a linhagem H1 de células-tronco embrionárias humanas (código NIH: WA01), a linhagem H7 de células-tronco embrionárias humanas (código NIH: WA07) e a linhagem SA002 de célulastronco embrionárias humanas (Cellartis, Suécia). São adequadas ao uso na presente invenção, também, as células que expressam pelo menos um dentre os seguintes marcadores característicos de células pluripotentes: ABCG2, cripto, CD9, FOXD3, Conexina43, Conexina45, OCT4, SOX2, Nanog, hTERT, UTF-1, ZFP42, SSEA-3, SSEA-4, Tra1-60, ou Tra1-81.
As células-tronco pluripotentes podem ser cultivadas sobre uma camada de células nutrizes. Alternativamente, as células-tronco pluripotentes podem ser cultivadas sobre uma matriz extracelular. A matriz extracelular pode consistir em uma preparação de membrana basal solubilizada, extraída de células de sarcoma de camundongo (conforme vendida pela BD Biosciences sob o nome comercial de MATRIGEL®). Alternativamente, a
26/247 matriz extracelular pode consistir em MATRIGEL® com teor reduzido de fator de crescimento. Alternativamente, a matriz extracelular pode consistir em fibronectina. Em uma modalidade alternativa, as células-tronco pluripotentes são cultivadas e diferenciadas sobre substrato para cultura de tecidos revestido com soro humano.
O arranjo extracelular pode ser diluída antes do revestimento do substrato para cultura de tecidos. Exemplos de métodos adequados para diluição da matriz extracelular e para revestimento do substrato para cultura de tecidos podem ser encontrados em Kleinman, H.K., et al., Biochemistry 25:312 (1986), e em Hadley, M.A., et al., J.Cell.Biol. 101:1511 (1985).
Em uma modalidade, a matriz extracelular consiste em MATRIGEL®. Em uma modalidade, o substrato para cultura de tecidos é revestido com MATRIGEL® a uma diluição de 1:10. Em uma modalidade alternativa, o substrato para cultura de tecidos é revestido com MATRIGEL® a uma diluição de 1:15. Em uma modalidade alternativa, o substrato para cultura de tecidos é revestido com MATRIGEL® a uma diluição de 1:30. Em uma modalidade alternativa, o substrato para cultura de tecidos é revestido com MATRIGEL® a uma diluição de 1:60.
Em uma modalidade, a matriz extracelular consiste em MATRIGEL® com teor reduzido de fator de crescimento. Em uma modalidade, o substrato para cultura de tecidos é revestido com MATRIGEL® com teor reduzido de fator de crescimento a uma diluição de 1:10. Em uma modalidade alternativa, o substrato para cultura de tecidos é revestido com MATRIGEL® com teor reduzido de fator de crescimento a uma diluição de 1:15. Em uma modalidade alternativa, o substrato para cultura de tecidos é revestido com MATRIGEL® com teor reduzido de fator de crescimento a uma diluição de 1:30. Em uma modalidade alternativa, o substrato para cultura de tecidos é revestido com MATRIGEL® com teor reduzido de fator de crescimento a uma diluição de 1:60.
Marcadores característicos da linhagem de endoderma definitivo são selecionados a partir do grupo consistindo em SOX17, GATA4, 3HNF-, GSC, CER1, Nodal, FGF8, Brachyury, proteína Mix-like homeobox, FGF4
27/247
CD48, eomesodermina (EOMES), DKK4, FGF17, GATA6, CXCR4, C-Kit, CD99, e OTX2. Uma célula que expressa pelo menos um dos marcadores característicos da linhagem de endoderma definitivo é adequada para uso na presente invenção. Em um aspecto da presente invenção, uma célula que expressa marcadores característicos da linhagem do endoderma definitivo é uma célula precursora da linha primitiva. Em um aspecto alternativo, uma célula que expressa marcadores característicos da linhagem do endoderma definitivo é uma célula do mesendoderma. Em um aspecto alternativo, uma célula que expressa marcadores característicos da linhagem do endoderma definitivo é uma célula do endoderma definitivo.
Os marcadores característicos da linhagem de endoderma pancreático são selecionados a partir do grupo consistindo em PDX1, HNF-1 beta, PTF1 alfa, HNF6, HB9 e PROX1. Uma célula que expressa pelo menos um dos marcadores característicos da linhagem endodérmica pancreática é adequada para uso na presente invenção. Em um aspecto da presente invenção, uma célula que expressa marcadores característicos da linhagem do endoderma pancreático é uma célula do endoderma pancreático.
Os marcadores característicos da linhagem endócrina pancreática são selecionados a partir do grupo consistindo em NGN3, NEUROD, ISL1, PDX1, NKX6.1, PAX4 e PTF-1 alfa. Em uma modalidade, uma célula pancreática endócrina é capaz de expressar pelo menos um dentre os seguintes hormônios: insulina, glucagon, somatostatina e polipeptídeo pancreático. É adequada ao uso na presente invenção uma célula que expressa pelo menos um dos marcadores característicos da linhagem endócrina pancreática. Em um aspecto da presente invenção, uma célula que expressa marcadores característicos da linhagem endócrina pancreática é uma célula pancreática endócrina. A célula pancreática endócrina pode ser uma célula pancreática que expressa de hormônio. Alternativamente, a célula pancreática endócrina pode ser uma célula pancreática secretora de hormônio.
Formação de células que expressam marcadores característicos
28/247 da linhagem de endoderma definitivo
Em um aspecto da presente invenção, as células-tronco pluripotentes podem ser diferenciadas em células expressoras de marcadores característicos da linhagem de endoderma definitivo mediante cultivo das células-tronco pluripotentes em um meio compreendendo uma quantidade suficiente de GDF-8 para causar a diferenciação das células-tronco pluripotentes em células expressoras de marcadores característicos da linhagem de endoderma definitivo.
As células-tronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF-8 durante cerca de um dia a cerca de sete dias. Alternativamente, as células-tronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF-8 durante cerca de um dia a cerca de seis dias. Alternativamente, as célulastronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF-8 durante cerca de um dia a cerca de cinco dias. Alternativamente, as células-tronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF-8 durante cerca de um dia a cerca de quatro dias. Alternativamente, as células-tronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF8 durante cerca de um dia a cerca de três dias. Alternativamente, as célulastronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF-8 durante cerca de um dia a cerca de dois dias. Alternativamente, as células-tronco pluripotentes podem ser cultivadas no meio contendo uma quantidade suficiente de GDF-8 durante cerca de um dia.
Em uma modalidade, o GDF-8 é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o GDF-8 é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o GDF-8 é usado a uma concentração de cerca de 5 ng/mL a cerca de 25 ng/mL. Em uma modalidade alternativa, o GDF-8 é usado a uma concentração de cerca de 25 ng/mL.
Em uma modalidade, o meio compreendendo uma quantidade suficiente de GDF-8 também contém pelo menos um outro fator. Em uma
29/247 modalidade, o pelo menos um outro fator é selecionado do grupo consistindo em: EGF, FGF4, PDGF-A, PDGF-B, PDGF-C, PDGF-D, VEGF, muscimol,
PD98059, LY294002, U0124, U0126 e butirato de sódio.
Em uma modalidade, o EGF é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o EGF é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o EGF é usado a uma concentração de cerca de 50 ng/mL.
Em uma modalidade, o FGF4 é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o FGF4 é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o FGF4 é usado a uma concentração de cerca de 50 ng/mL.
Em uma modalidade, o PDGF-A é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o PDGF-A é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o PDGF-A é usado a uma concentração de cerca de 50 ng/mL.
Em uma modalidade, o PDGF-B é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o PDGF-B é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o PDGF-B é usado a uma concentração de cerca de 50 ng/mL.
Em uma modalidade, o PDGF-C é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o PDGF-C é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o PDGF-C é usado a uma concentração de cerca de 50 ng/mL.
Em uma modalidade, o PDGF-D é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o PDGF-D é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o PDGF-D é usado a uma
30/247 concentração de cerca de 50 ng/mL.
Em uma modalidade, o VEGF é usado a uma concentração de cerca de 5 ng/mL a cerca de 500 ng/mL. Em uma modalidade alternativa, o VEGF é usado a uma concentração de cerca de 5 ng/mL a cerca de 50 ng/mL. Em uma modalidade alternativa, o VEGF é usado a uma concentração de cerca de 50 ng/mL.
Em uma modalidade, o muscimol é usado a uma concentração de cerca de 1 pM a cerca de 200 pM. Em uma modalidade alternativa, o muscimol é usado a uma concentração de cerca de 1 pM a cerca de 20 pM. Em uma modalidade alternativa, o muscimol é usado a uma concentração de cerca de 20 pM.
Em uma modalidade, o PD98059 é usado a uma concentração de cerca de 0,1 pM a cerca de 10 pM. Em uma modalidade alternativa, o PD98059 é usado a uma concentração de cerca de 0,1 pMa cerca de 1 pM. Em uma modalidade alternativa, o PD98059 é usado a uma concentração de cerca de 1 pM.
Em uma modalidade, o LY294002 é usado a uma concentração de cerca de 0,25 pM a cerca de 25 pM. Em uma modalidade alternativa, o LY294002 é usado a uma concentração de cerca de 0,25 pM a cerca de 2,5 pM. Em uma modalidade alternativa, o LY294002 é usado a uma concentração de cerca de 2,5 pM.
Em uma modalidade, o U0124 é usado a uma concentração de cerca de 0,1 pM a cerca de 10 pM. Em uma modalidade alternativa, o U0124 é usado a uma concentração de cerca de 0,1 pMa cerca de 1 pM. Em uma modalidade alternativa, o U0124 é usado a uma concentração de cerca de 1 pM.
Em uma modalidade, o U0126 é usado a uma concentração de cerca de 0,1 pM a cerca de 10 pM. Em uma modalidade alternativa, o U0126 é usado a uma concentração de cerca de 0,1 pM a cerca de 1 pM. Em uma modalidade alternativa, o U0126 é usado a uma concentração de cerca de 1 pM.
Em uma modalidade, o butirato de sódio é usado a uma
31/247 concentração de cerca de 0,05 μΜ a cerca de 5 μΜ. Em uma modalidade alternativa, o butirato de sódio é usado a uma concentração de cerca de 0,05 μΜ a cerca de 0,5 μΜ. Em uma modalidade alternativa, o butirato de sódio é usado a uma concentração de cerca de 0,5 μΜ.
Em uma modalidade alternativa, esse pelo menos um outro fator é selecionado do grupo consistindo em: uma anilina-piridinotriazina, uma anilina-piridinotriazina cíclica, N-{[1-(fenil metil)azepan-4-il]metil}-2-piridin-3ilacetamida, 4-{[4-(4-{[2-(piridin-2-ilamino)etil]amino}-1,3,5-triazin-2-il)piridin2-il]óxi}butan-1 -ol, 3-({3-[4-({2-[metil(piridin-2-il)amino]etil}amino)-1,3,5triazin-2-il]piridin-2-il}amino)propan-1-ol, N~4~-[2-(3-fluorofenil)etil]-N~2~-[3(4-metil piperazin-1-il)propil]pirido[2,3-d]pirimidina-2,4-diamina, 1-metil-N-[(4piridin-3-il-2-{[3-(trifluorometil)fenil]amino}-1,3-tiazol-5-il)metil]piperidina-4carboxamida, {2-[4-({5-[3-(3-hid róxi propil)fenil]-4H-1,2,4-triazol-3-il}amino)fenil]etil}carbamato de 1,1-dimetiletila, {[3-({5-[5-(3-hidróxi propil)-2(metilóxi)fenil]-1,3-oxazol-2-il}amino)fenil]metil}carbamato de 1,1-dimetiletila, 1-({5-[6-({4-[(4-metil piperazin-1-il)sulfonil]fenil}amino)pirazin-2-il]tiofen-2i IJmeti l)p i perid i n-4-ol, 1 -({4-[6-({4-[(4-metil piperazin-1 -il)sulfonil]fenil}amino)pirazin-2-il]tiofen-2-il}metil)piperidina-4-carboxamida, e 2-{[4-( 1 metiletil)fenil]amino}-N-(2-tiofen-2-iletil)-7,8-diidropirido[4,3-d]pirimidina6(5H)-carboxamida.
Os compostos da presente invenção
A presente invenção apresenta compostos que são capazes de diferenciar células-tronco pluripotentes em células expressoras de marcadores característicos da linhagem de endoderma definitivo.
Em uma modalidade, o composto que é capaz de diferenciar células-tronco pluripotentes em células expressoras de marcadores característicos da linhagem de endoderma definitivo é uma anilina-piridinotriazina com a Fórmula (1):
32/247
As formas de N-óxido, os sais de adição farmaceuticamente aceitáveis e as formas estereoquimicamente isoméricas da mesma, em que:
m representa um número inteiro de 1 a 4; n representa um número inteiro de 1 a 4; Z representa N ou C;
cada um dentre R1 e R8 representa, independentemente, hidrogênio, Het14, ciano, halo, hidróxi, Ci^alcóxi-, Ci^alquil-, mono ou di(C-|. 4alquil)amino-carbonil-, mono ou di(Ci^alquil)amino-sulfonila, Ci^alcóxisubstituído com halo ou R1 representa C^alquila substituída com um ou, quando possível, dois ou mais substituintes selecionados a partir de hidróxi ou halo;
cada um dentre R2 e R9 representa, independentemente, hidrogênio, Ci^alquila, C2^alquenila, Het3, Het4-Ci^alquil-, Het5-Ci_ 4alquilcarbonil-, mono ou d^C^alquiOamino-Ci^alquil-carbonil- ou fenila opcionalmente substituída com um ou, quando possível, dois ou mais substituintes selecionados a partir de hidrogênio, hidróxi, amino ou Ci_ 4alquilóxi-;
cada um dentre R3 e R7 representa, independentemente, hidrogênio, Ci^alquila, Het6, Hef-C^alquil-, C2^alquenilcarbonil-opcionalmente substituído com Het8-C1^alquilaminocarbonil-, C2^alquenilsulfonil-, 4alquilóxi, Ci^alquil- ou fenila opcionalmente substituído com um ou, quando possível, dois ou mais substituintes selecionados a partir de hidrogênio, hidróxi, amino ou Ci^alquilóxi-;
cada um dentre R4, R5, R6 e R10 representa, independentemente, hidrogênio ou C^alquila opcionalmente substituído com hidróxi, Het9 ou Ci^alquilóxi;
cada um dentre Het1 e Het2 representa, independentemente, um
33/247 heterociclo selecionado a partir de pirrolidinila, piperidinila, piperazinila, piridinila, pirimidinila, pirazinila, imidazolidinila ou pirazolidinila, sendo que os ditos Het1 e Het2 são, opcionalmente, substituídos com amino, hidróxi, Cv 4alquila, hidróxi-CMalquil-, fenila, fenil-C^alquil-, Ci^alquil-óxi-Ci^alquilmono ou di(Ci^alquil) amino- ou amino-carbonil-;
cada um dentre Het3 e Het6 representa, independentemente, um heterociclo selecionado a partir de pirrolidinila ou piperidinila, sendo que os ditos Het3 e Het6 são, opcionalmente, substituídos com um ou, quando possível, dois ou mais substítuintes selecionados de Ci^alquila, C3_ 6cicloalquila, hidróxi-C^alquil-, Ci^alquilóxi C^alquila ou poliidróxi-Cv 4alquil-;
cada um dentre Het4, Het7 e Het9 representa, independentemente, um heterociclo selecionado a partir de morfolinila, pirrolidinila, piperazinila ou piperidinila, sendo que os ditos Het4, Het7 e Het9 são, opcionalmente, substituídos com um ou, quando possível, dois ou mais substítuintes selecionados de Ci^alquila, C3^cicloalquila, hidróxi-Ci^alquil-, Ci^alquilóxi Ci^alquila ou poli-hidróxi-Ci^alquil-;
Het5 representa um heterociclo selecionado a partir de morfolinila, pirrolidinila, piperazinila ou piperidinila, sendo que o dito Het5 é, opcionalmente, substituído com um ou, quando possível, dois ou mais substítuintes selecionados a partir de C^alquila, C3.6cicloalquila, hidróxi-Ci_ 4alquil-, Ci^alquilóxi Ci^alquila ou poli-hidróxi-Ci^alquil-;
cada um dentre Het10, Het11 e Het13 representa, independentemente, um heterociclo selecionado a partir de pirrolidinila, piperidinila, piperazinila, piridinila, pirimidinila, pirazinila, imidazolidinila ou pirazolidinila, sendo que os ditos Het10, Het11 e Het13 são, opcionalmente, substituídos com amino, hidróxi, CMalquila, hidróxi-C^alquil-, fenila, fenil-C^alquil-, Ci. 4alquil-óxi-Ci^alquil-, amino-carbonil- ou mono ou di(C-i^alquil)amino-;
Het12 representa um heterociclo selecionado a partir de pirrolidinila, piperidinila, piperazinila, piridinila, pirimidinila, pirazinila, imidazolidinila ou pirazolidinila, sendo que o dito Het12 é, opcionalmente, substituído com amino, hidróxi, CMalquila, hidróxi-C^alquil-, fenila, fenil-C^alquil-, ϋμ
34/247 4alquil-0xi-Ci^alquil-; mono ou di(Ci^alquil)amino- ou amino-carbonil-;
Het14 representa um heterociclo selecionado a partir de morfolinila, pirrolidinila, piperazinila, imidazolila, pirrolila, 2,3,4-triazapirrolila,
1,2,3-triazolila, pirazolila ou piperidinila, sendo que o dito Het14 é, opcionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de C^alquila, C^cicloalquila, hidróxi-C^alquil-, Ci^alquilóxi C^alquila ou poli-hidróxi-Ci^alquil-; particularmente, Het14 representa urn heterociclo selecionado a partir de morfolinila, pirrolidinila, pirrolila, 2,3,4-triazapirrolila, piperazinila ou piperidinila, sendo que o dito Het14 é, opcionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de Ci^alquila, C3^cicloalquila, hidróxi-Ci_ 4alquil-, Ci^alquilóxi Ci^alquila ou poli-hidróxi-Ci^alquil-; mais particularmente, Het14 representa um heterociclo selecionado a partir de morfolinila, pirrolidinila, piperazinila ou piperidinila, sendo que o dito Het14 é, opcionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de C^alquila, C^cicloalquila, hidróxi-C^alquil-, Ci 4alquilóxi Ci^alquila ou poli-hidróxi-Ci_4alquil-.
Em uma modalidade, a anilina-piridinotriazina é um composto da Fórmula (1).
Em uma modalidade, a anilina-piridinotriazina é um composto da Fórmula (2).
Fórmula (2): ácido 3-{3-[(4-piridin-3-il-1,3,5-triazin-2-il)amino]feniljpropanoico. Chamado, na presente invenção, de Composto 1.
Em uma modalidade, a anilina-piridinotriazina é um composto da
35/247
Fórmula (3).
Fórmula (3): 2-{3-[(4-piridin-3-il-1,3,5-triazin-2-il)amino]fenil}etanol. chamado, na presente invenção, de Composto 2.
Em uma modalidade, a anilina-piridinotriazina é um composto da
Fórmula (4).
Fórmula (4): {2-[3-({4-[2-(3-hidroxiprop-1 -in-1 -il)piridin-4-il]-1,3,5triazin-2-il}amino)fenil]etil}carbamato de 1,1-dimetiletila. Chamado, na 10 presente invenção, de Composto 3.
Em uma modalidade, a anilina-piridinotriazina é um composto da Fórmula (5).
Fórmula (5): {4-[4-(4-{[3-(hidroximetil)fenil]amino}-1,3,5-triazin-2
36/247 il)piridin-2-il]butil}carbamato de 1,1 -dimetiletila. Chamado, na presente invenção, de Composto 4.
Em uma modalidade, a anilina-piridinotriazina é um composto da Fórmula (6).
Fórmula (6): {3-[{[5-(2-{[3-bromo-5-(hidroximetil)fenil]amino}pirimidin-4-il)-2-(metilóxi)fenil]metil}(metil)amino]propil}carbamato de 1,1-dimetiletila. Chamado, na presente invenção, de Composto 5.
Em uma modalidade, a anilina-piridinotriazina é um composto da
Fórmula (7): ácido 4-{[3-(3-fluorofenil)-3H-[1,2,3]triazolo[4,5d]pirimidin-5-il]amino}benzoico. Chamado, na presente invenção, de 15 Composto 6.
Em uma modalidade, a anilina-piridinotriazina é um composto da
Fórmula (8).
37/247
Fórmula (8): ácido 2-fluoro-5-[(3-fenil-3H-[1,2,3]triazolo[4,5d]pirimidin-5-il)amino]benzoico. Chamado, na presente invenção, de Composto 7.
Em uma modalidade, a anilina-piridinotriazina é um composto da
Fórmula (9).
Fórmula (9): N-{[3-(5-{[3-(2-aminopirimidin-4-il)fenil]amino}-3H[1,2,3]triazolo[4,5-d]pirimidin-3-il)fenil]metil}ciclopropanocarboxamida.
Chamado, na presente invenção, de Composto 8.
Em uma modalidade, a anilina-piridinotriazina é um composto da
Fórmula (10).
Fórmula (10): 4-[(1-ciclo-hexil-1H-pirazolo[3,4-d]pirimidin-615 il)amino]-N-[3-(metilóxi)propil]benzenossulfonamida. Chamado, na presente invenção, de Composto 9.
Em uma modalidade, a anilina-piridinotriazina é um composto da Fórmula (11).
38/247
OH
Cl
Fórmula (11): 4-cloro-2-[(6-{[3-(clorometil)-4-metoxifenil]amino}pirimidin-4-il)amino]fenol. Chamado, na presente invenção, de Composto 10.
Em uma modalidade, a anilina-piridinotriazina é um composto da
Fórmula (12).
Fórmula (12): 4-{[4-(4-metil-3,4-di-hidroquinoxalin-1 (2 H)-il)pirimidin-2-il]amino}-N-(1-metilpiperidin-4-il)benzamida. Chamado, na presente 10 invenção, de Composto 11
Em uma modalidade, a anilina-piridinotriazina é um composto da Fórmula (13).
Fórmula (13): N-(2-metóxi-4-{[(3-metóxi propil)amino]metil}fenil)15 4-(1H-pirrolo[2,3-b]piridin-3-il)pirimidin-2-amina. Chamado, na presente invenção, de Composto 12.
Em uma modalidade, o composto que é capaz de diferenciar células-tronco pluripotentes em células expressoras de marcadores caracte
39/247 rísticos da linhagem de endoderma definitivo é uma anilina-piridinotriazina cíclica com a Fórmula (14):
1 Fórmula (14).
As formas de N-óxido, os sais de adição farmaceuticamente aceitáveis e as formas estereoquimicamente isoméricas da mesma, em que:
m representa um número inteiro de 1 a 4; n representa um número inteiro de 1 a 4; Z representa N ou C;
Y representa -NR2-Ci_6alquil-CO-NR4-, -Ci^alkyl-NR9-Ci^alquil-, Ci_6alquil-CO-Het10-, -Het11-CO-Ci^alquil-, -Het12-C^alquil-, -CO-Het13-Ci_ 6alquil-, -CO-NR10-CV6alquil-, -Het1-Ci^alquil-CO-NR5-, or-Het^CO-NR6-, sendo que o ligante -Ci^alquil- em -NR2-C1 6alquil-CO-NR4- ou -Het1-Ci_ ealquil-CO-NR5- é, opcionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de hidróxi, metóxi, amino carbonila, halo, fenila, indolila, sulfeto de metila, tiol, hidróxi fenila, cianofenila, amino e hidroxicarbonila;
X1 representa uma ligação direta, Ci^alquila, Ci^alquilóxi-, Ci4alquil-CO-, C^alquenila, C2-4alquinila, ou Ci^alquil-NR3-, sendo que a dita Ci^alquila ou C^alquenila é, opcionalmente, substituída com um ou, quando possível, dois ou mais substituintes halo;
X2 representa uma ligação direta, Ci^alquila, C^alquilóxi-, Ci. 4alquil-CO-, C^alquenila, C2^alquinila, ou C^alquil-NR7-, sendo que a dita Cí^alquila ou C^alquenila é, opcionalmente, substituída com um ou, quando possível, dois ou mais substituintes halo;
cada um dentre R1 e R8 representa, independentemente,
40/247 hidrogênio, Het14, ciano, halo, hidróxi, Ci^alcóxi-, Ci^alquil-, mono ou di(Ci. 4alquil)amino-carbonil-, mono ou di(Ci^alquil)amino-sulfonila, C^alcóxisubstituído com halo ou R1 representa Ci^alquila substituída com um ou, quando possível, dois ou mais substituintes selecionados a partir de hidróxi ou halo;
cada um dentre R2 e R9 representa, independentemente, hidrogênio, Ci^alquila, C2^alquenila, Het3, Het4-Ci^alquil-, Het5-Ci^alquil carbonil-, mono ou di(C1^alquil)amino-Ci^alquil-carbonil- ou fenila opcionalmente substituída com um ou, quando possível, dois ou mais substituintes selecionados a partir de hidrogênio, hidróxi, amino ou Ci^alquilóxi-;
cada um dentre R3 e R7 representa, independentemente, hidrogênio, C^alquila, Het6, Hef-C^alquil-, C2^alquenilcarbonil-opcionalmente substituído com He^-C^alquilaminocarbonil-, C24alquenilsulfonil-, Ci_ 4alquilóxi, Ci^alquil- ou fenil opcionalmente substituído com um ou, quando possível, dois ou mais substituintes selecionados a partir de hidrogênio, hidróxi, amino ou C^alquilóxi-;
cada um dentre R4, R5, R6 e R10 representa, independentemente, hidrogênio ou C^alquila opcionalmente substituído com hidróxi, Het9 ou Ci_4alquilóxi;
cada um dentre Het1 e Het2 representa, independentemente, um heterociclo selecionado a partir de pirrolidinila, piperidinila, piperazinila, piridinila, pirimidinila, pirazinila, imidazolidinila ou pirazolidinila, sendo que os ditos Het1 e Het2 são, opcionalmente, substituídos com amino, hidróxi, 4alquila, hidróxi-Ci^alquil-, fenila, fenil-Ci^alquil-, Ci^alquil-óxi-Ci^alquilmono ou di(Ci^alquil) amino- ou amino-carbonil-;
cada um dentre Het3 e Het6 representa, independentemente, um heterociclo selecionado a partir de pirrolidinila ou piperidinila, sendo que os ditos Het3 e Het6 são, opcionalmente, substituídos com um ou, quando possível, dois ou mais substituintes selecionados de C^alquila, C3_6cicloalquila, hidróxi-Ci^alquil-, C^alquilóxi C^alquila ou poli-hidróxi-Ci^alquil-;
cada um dentre Het4, Het7 e Het9 representa, independentemente, um heterociclo selecionado a partir de morfolinila, pirrolidinila, pipera41/247 zinila ou piperidinila, sendo que os ditos Het4, Het7 e Het9 são, opcionalmente, substituídos com um ou, quando possível, dois ou mais substituintes selecionados de Ci^alquila, C3^cicloalquila, hidróxi-Ci^alquil-, C^alquilóxi
Ci^alquila ou poli-hidróxi-Ci^alquil-;
Het5 representa um heterociclo selecionado a partir de morfolinila, pirrolidinila, piperazinila ou piperidinila, sendo que o dito Het5 é, opeionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados a partir de C^alquila, C3_6cicloalquila, hidróxi-Ci_ 4alquil-, C^alquilóxi Ci^alquila ou poli-hidróxi-C^alquil-;
cada um dentre Het10, Het11 e Het13 representa, independentemente, um heterociclo selecionado a partir de pirrolidinila, piperidinila, piperazinila, piridinila, pirimidinila, pirazinila, imidazolidinila ou pirazolidinila, sendo que os ditos Het10, Het11 e Het13 são, opeionalmente, substituídos com amino, hidróxi, Ci^alquila, hidróxi-Ci^alquil-, fenila, fenil-Ci^alquil-, Cv 4alquil-0xi-Ci^alquil-, amino-carbonil- ou mono ou d^C^alquiQamino-;
Het12 representa um heterociclo selecionado a partir de pirrolidinila, piperidinila, piperazinila, piridinila, pirimidinila, pirazinila, imidazolidinila ou pirazolidinila, sendo que o dito Het12 é, opeionalmente, substituído com amino, hidróxi, C-i^alquila, hidróxi-C-i^alquil-, fenila, fenil-Ci^alquil-, C-j. 4alquil-óxi-Ci^alquil-; mono ou di(Ci-4alquil)amino- ou amino-carbonil-;
Het14 representa um heterociclo selecionado a partir de morfolinila, pirrolidinila, piperazinila, imidazolila, pirrolila, 2,3,4-triazapirrolila, 1,2,3triazolila, pirazolila ou piperidinila, sendo que o dito Het14 é, opeionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de Ci^alquila, C3^cicloalquila, hidróxi-Ci^alquil-, C14alquilóxi Ci^alquila ou poli-hidróxi-Ci-^alquil-; particularmente, Het14 representa um heterociclo selecionado a partir de morfolinila, pirrolidinila, pirrolila, 2,3,4triazapirrolila, piperazinila ou piperidinila, sendo que o dito Het14 é, opcionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de Ci^alquila, C3_6cicloalquila, hidróxi-Ci^alquil-, C^alquilóxi Ci^alquila ou poli-hidróxi-Ci_4alquil-; mais particularmente, Het14 representa um heterociclo selecionado a partir de morfolinila', pirrolidinila, piperazinila
42/247 ou piperidinila, sendo que o dito Het14 é, opcionalmente, substituído com um ou, quando possível, dois ou mais substituintes selecionados de Ci^alquila,
C3-6cicloalquila, hidróxi-Ci^alquil-, C^alquilóxi Ci^alquila ou poli-hidróxi-C-i4alquil-.
Os compostos de Fórmula (7) são descritos em W02007/003525, atribuída à Janssen Pharmaceutica N.V.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (14).
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (15).
Fórmula (15): 1,8,10,12,17,19,23,27,33-nona-azapentaciclo[25.2.2.1 -3,7-.1 -9,13-.1-14,18~]tetratriaconta-3(34),4,6,9(33), 10,12, 14(32),15,17-nonaen-24-ona. Chamado, na presente invenção, de Composto 13.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (16).
Fórmula (16): 10-cloro-14-etil-3,5,7,14,17,22,27-hepta-azatetraci
43/247 clo[19.3.1.1-2,6-.1-8,12~]heptacosa-1 (25),2(27),3,5,8(26),9,11,21,23nonaen-16-ona. Chamado, na presente invenção, de Composto 14.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (17).
Fórmula (17): 14-etil-3,5,7,14,17,27-hexa-azatetraciclo[19.3.1.1 -2,6-.1 -8,12~]heptacosa-1 (25),2(27),3,5,8(26),9,11,21,23nonaen-16-ona. Chamado, na presente invenção, de Composto 15.
Em uma modalidade, a anilina-piridinotriazina cíclica é um 10 composto da Fórmula (18).
Fórmula (18): 10-cloro-14-etil-3,5,7,14,17,27-hexa-azatetraciclo[19.3.1.1-2,6-.1-8,12~]heptacosa-1(25),2(27),3,5,8(26),9,11,21,23nonaen-16-ona. Chamado, na presente invenção, de Composto 16.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (19).
44/247
Fórmula (19): 3,5,7,14,20,26,31-hepta-azapentaciclo[22.3.1.1 ~2,6~. 1 ~8,12~. 1 ~14,18~]hentriaconta-1 (28),2(31 ),3,5,8(30),9,
11,24,26-nonaen-19-ona. Chamado, na presente invenção, de Composto 5 17.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (20).
Fórmula (20): (18S)-3,5,7,14,20,26,30-hepta-azapentaci10 clo[22.3.1.1~2,6~.1~8,12-0-14,18~]triaconta-1(28),2(30),3,5,8(29),9,11,
24,26-nonaen-19-ona. Chamado, na presente invenção, de Composto 18.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (21).
45/247
Fórmula (21): 14-metil-3,5,7,14,18,24,28-hepta-azatetraciclo[20.3.1.1~2,6~.1~8,12~]octacosa-1(26),2(28),3,5,8(27),9,11,22,24nonaen-17-ona. Chamado, na presente invenção, de Composto 19.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (22).
Fórmula (22): 14-metil-3,5,7,14,19,25,29-hepta-azatetraciclo[21.3.1.1 ~2,6~. 1-8,12~]nonacosa-1 (27),2(29),3,5,8(28),9,11,23,2510 nonaen-18-ona. Chamado, na presente invenção, de Composto 20.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (23).
Fórmula (23):
14-metil-3,5,7,14,18,22,29-hepta-azatetraci46/247 clo[21.3.1.1-2,6-.1-8,12~]nonacosa-1(27),2(29),3,5,8(28),9,11,23,25nonaen-17-ona. Chamado, na presente invenção, de Composto 21.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (24).
Fórmula (24): 1,8,10,12,16,22,30-hepta-azapentaciclo[22.2.2.1 -3,7-. 1-9,13-.1-14,18~]hentriaconta-3(31 ),4,6,9(30), 10,12, 14(29),15,17-nonaen-23-ona. Chamado, na presente invenção, de Composto 22.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (25).
Fórmula (25): 1,8,10,12,16,22,26,32-octa-azapentaciclo[24.2.2.1 -3,7-. 1-9,13-.1-14,18~]tritriaconta-3(33),4,6,9(32), 10,12,
14(31),15,17-nonaen-23-ona. Chamado, na presente invenção, de
Composto 23.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (26).
47/247
Fórmula (26): 5-cloro-17-fluoro-1,8,10,12,22,26,32-heptaazapentaciclo[24.2.2.1 -3,7-. 1-9,13-1-14,18~]tritriaconta-3(33),4,6,9(32), 10,12,14(31),15,17-nonaen-23-ona. Chamado, na presente invenção, de 5 Composto 24.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (27).
Fórmula (27): 10-cloro-14-etil-22-fIuoro-3,5,7,14,17,27-hexa10 azatetraciclo[19.3.1.1~2,6~.1~8,12~]heptacosa-1(25),2(27),3,5,8(26),9, 11,21,23-nonaen-16-ona. Chamado, na presente invenção, de Composto 25.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (28).
48/247
Fórmula (28): 10-cloro-25-fluoro-3,5,7,14,20,31-hexa-azapentaciclo[22.3.1.1~2,6~.1~8,12~.1~14,18~]hentriaconta-1(28),2(31),3,5,8(30),9,
11,24,26-nonaen-19-ona. Chamado, na presente invenção, de Composto 5 26.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (29).
Fórmula (29): 4-cloro-1,8,10,12,17,22,26,32-octa-azapentaciclo[24.2.2.1 -3,7-.1 ~9,13~. 1-14,18~]tritriaconta-3(33),4,6,9(32), 10,12, 14(31), 15,17-nonaen-23-ona. Chamado, na presente invenção, de Composto 27.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (30).
49/247
Fórmula (30): 18-metil-3,5,7,15,18,28-hexa-azatetraciclo[20.3.1.1-2,6-.1-8,12~]octacosa-1 (26),2(28),3,5,8(27),9,11,22,24nonaen-16-ona. Chamado, na presente invenção, de Composto 28.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (31).
Fórmula (31): 18-etil-3,5,7,15,18,28-hexa-azatetraciclo[20.3.1.1~2,6~.1~8,12~]octacosa-1(26),2(28),3,5,8(27),9,1 í,22,2410 nonaen-16-ona. Chamado, na presente invenção, de Composto 29.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (32).
Fórmula (32): 1,8,10,12,17,19,23,27,33-nona-azapentaci50/247 clo[25.2.2.1-3,7-.1-9,13-.1-14,18~]tetratriaconta-3(34),4,6,9(33), 10,12,
14(32),15,17-nonaen-24-ona. Chamado, na presente invenção, de Composto 30.
Em uma modalidade, a anilina-piridinotriazina cíclica é um 5 composto da Fórmula (33).
Fórmula (33): 1,11,13,15,23,31-hexa-azapentaciclo[23.2.2.1-5,9-1-10,14~. 1 -16,20~]dotriaconta-5(32),6,8,10(31), 11, 13,16(30),17,19-nonaen-24-ona. Chamado, na presente invenção, de 10 Composto 31.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (34).
Fórmula (34): 15-etil-13,14,15,16,18,19-hexa-hidro-1H-6,215 (azeno)-7,11 -(meteno)-1,3,5,15,18-benzopenta-azaciclo-henicosin-17(12H)ona. Chamado, na presente invenção, de Composto 32.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (35).
51/247
Fórmula (35): 20-metil-3,5,7,15,20,30-hexa-azatetraciclo[22.3.1.1-2,6-.1 ~8,12~]triaconta-1 (28),2(30),3,5,8(29),9,11,24,26nonaen-16-ona. Chamado, na presente invenção, de Composto 33.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (36).
Fórmula (36): 5-cloro-1,8,10,12,16,22,26,32-octa-azapentaciclo[24.2.2.1 ~3,7~. 1 ~9,13~. 1 ~14,18~]tritriaconta-3(33),4,6,9(32), 10,12,
14(31),15,17-nonaen-23-ona. Chamado, na presente invenção, de Composto 34.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (37).
52/247
Fórmula (37): 10-cloro-14-etil-3,5,7,14,17,23,27-hepta-azatetraciclo[ 19.3.1.1-2,6-.1-8,12~]heptacosa-1 (25),2(27),3,5,8(26),9,11,21,23nonaen-16-ona. Chamado, na presente invenção, de Composto 35.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (38).
Fórmula (38): (18S)-10-cloro-3,5,7,14,20,26,30-hepta-azapentaciclo[22.3.1.1 -2,6-. 1-8,12-.0-14,18~]triaconta10 1(28),2(30),3,5,8(29),9,11,24,26-nonaen-19-ona. Chamado, na presente invenção, de Composto 36.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (39).
53/247
Cl
Fórmula (39): 10-cloro-3,5,7,14,20,26,31-hepta-azapentaciclo[22.3.1.1-2,6-.1-8,12-.1-14,18~]hentriaconta-1(28),2(31),3,5,8(30),9,
11,24,26-nonaen-19-ona. Chamado, na presente invenção, de Composto 37.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (40).
α
Fórmula (40): 5-cloro-1,8,10,12,16,22,30-hepta-azapentaciclo[22.2.2.1 -3,7-.1-9,13-.1-14,18~]hentriaconta-3(31 ),4,6,9(30), 10,12, 14(29),15,17-nonaen-23-ona. Chamado, na presente invenção, de Composto 38.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (41).
54/247
Fórmula (41): 9-metil-2,3,4,5,7,8,9,10-octa-hidro-16H-17,21(azeno)-11,15-(meteno)pirido[3,2-g][1,3,5,9,13,17]hexa-azaciclotricosin6(1H)-ona. Chamado, na presente invenção, de Composto 39.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (42).
Fórmula (42): 14-prop-2-en-1-il-3,5,7,14,17,23,27-hepta-azatetraciclo[19.3.1.1 ~2,6~. 1 -8,12~]heptacosa-1 (25),2(27),3,5,8(26),9,11,21,2310 nonaen-16-ona. Chamado, na presente invenção, de Composto 40.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (43).
55/247
Fórmula (43): 18-oxo-14-oxa-2,4,8,17,25-penta-azatetraciclo[17.3.1.1-3,7-.1-9,13~]pentacosa-1 (23),3(25),4,6,9(24), 10,12,19,21nonaeno-6-carbonitrila. Chamado, na presente invenção, de Composto 41.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (44).
Fórmula (44): 14,21-dioxa-2,4,8,18,28-penta-azatetraciclo[20.3.1.1-3,7-.1-9,13~]octacosa-1 (26),3(28),4,6,9(27), 10,12,22,24nonaen-19-ona. Chamado, na presente invenção, de Composto 42.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (45).
Fórmula (45): 21-metil-1,8,10,11,21,24,30-hepta-azapentaciclo[22.2.2.1 -3,7-.1-9,12-.1-13,17~]hentriaconta-3(31 ),4,6,9,11,13(29), 14,
16-octaen-23-ona. Chamado, na presente invenção, de Composto 43.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (46).
56/247
ο
Fórmula (46): (18S)-11-(morfolin-4-ilcarbonil)-5,7,14,20,28penta-azapentaciclo[20.3.1.1 ~2,6~. 1 ~8,12~.0~14,18~]octacosa1(26),2(28),3,5,8(27),9,11,22,24-nonaen-19-ona. Chamado, na presente 5 invenção, de Composto 44.
Em uma modalidade, a anilina-piridinotriazina cíclica é um composto da Fórmula (47).
Fórmula (47): 10-metóxi-17-metil-2,14,15,17,18,19,20,22-octa10 hidro-6H-19,21 -metano-7,11 -(meteno)-12-oxa-2,3,5,6,17,21 -hexa-azacicloicosa[1,2,3-cd]inden-16(13H)-ona. Chamado, na presente invenção, de Composto 45.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (48):
57/247
Fórmula (48). N-{[1 -(fenilmetil)azepan-4-il]metil}-2-piridin-3-ilacetamida. Chamado, na presente invenção, de Composto 46.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (49):
Fórmula (49). 4-{[4-(4-{[2-(piridin-2-ilamino)etil]amino}-1,3,5-triazin-2-il)piridin-2-il]óxi}butan-1-ol. Chamado, na presente invenção, de Composto 47.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (50):
Fórmula (50). 3-({3-[4-({2-[metil(piridin-2-il)amino]etil}amino)1,3,5-triazin-2-il]piridin-2-il}amino)propan-1-ol. Chamado, na presente inven58/247 ção, de Composto 48.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (51):
Fórmula (51). N~4~-[2-(3-fluorofenil)etil]-N~2~-[3-(4-metil piperazin-1-il)propil]pirido[2,3-d]pirimidina-2,4-diamina. Chamado, na presente invenção, de Composto 49.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (52):
Fórmula (52).
1-metil-N-[(4-piridin-3-il-2-{[3-(trifluorometil)fenil]amino}-1,3-tiazol-5-il)metil]piperidina-4-carboxamida. Chamado, na presente invenção, de Composto 50.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (53):
59/247
Fórmula (53). {2-[4-({5-[3-(3-hidróxi propil)fenil]-4H-1,2,4-triazol3-il}amino)fenil]etil}carbamato de 1,1-dimetiletila. Chamado, na presente invenção, de Composto 51.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (54):
Fórmula (54). {[3-({5-[5-(3-hidróxi propil)-2-(metilóxi)fenil]-1,3oxazol-2-il}amino)fenil]metil}carbamato de 1,1-dimetiletila. Chamado, na 10 presente invenção, de Composto 52.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (55):
Fórmula (55). 1-({5-[6-({4-[(4-metil piperazin-1-il)sulfonil]fe
60/247 nil}amino)pirazin-2-il]tiofen-2-il}metil)piperidin-4-ol. Chamado, na presente invenção, de Composto 53.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (56):
NH»
Fórmula (56). 1 -({4-[6-({4-[(4-metilpiperazin-1 -il)suIfoniljfenil}amino)pirazin-2-il]tiofen-2-il}metil)piperidina-4-carboxamida. Chamado, na presente invenção, de Composto 54.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (57):
Fórmula (57). 2-{[4-(1 -metiletil)fenil]amino}-N-(2-tiofen-2-iletil)7,8-di-hidropirido[4,3-d]pirimidina-6(5H)-carboxamida. Chamado, na presente 15 invenção, de Composto 55.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (58):
61/247
Fórmula (58). 6-[(2-{[4-(2,4-diclorofenil)-5-(4-metil-1 H-imidazol-2il)pirimidin-2-il]amino}etil)amino]piridina-3-carbonitrila. Chamado, na presente invenção, de Composto 56.
Em uma modalidade, esse pelo menos um outro fator é um composto da Fórmula (59):
b]piridazin-3-il)-N-[2-(dimetilamino)etil]benzamida. Chamado, na presente 10 invenção, de Composto 57.
Detecção de células que expressam marcadores característicos da linhagem de endoderma definitivo
A formação de células expressoras de marcadores característicos da linhagem de endoderma definitiva pode ser determinada 15 testando-se quanto à presença dos marcadores antes e depois de seguir um determinado protocolo. As células-tronco pluripotentes tipicamente não expressam esses marcadores. Portanto, a diferenciação das células pluripotentes é detectada quando as células começam a expressá-los.
A eficiência da diferenciação pode ser determinada expondo-se
62/247 uma população de células tratadas a um agente (como um anticorpo) que especificamente reconhece um marcador de proteína expresso por células que expressam marcadores característicos da linhagem de endoderma definitivo.
Os métodos para avaliar a expressão de marcadores de proteína e de ácido nucléico em células cultivadas ou isoladas são padrão na técnica. Estes incluem reação em cadeia de polimerase via transcriptase reversa quantitativa (RT-PCR), Northern blots, in situ hibridização (vide, por exemplo, Current Protocols in Molecular Biology (Ausubel et al., Editores, suplemento de 2001)), e imunoensaios como análise imuno-histoquimica de material seccionado, Western blotting e, para marcadores que são acessíveis em células intactas, análise de citometria de fluxo (FACS) (vide, por exemplo, Harlow e Lane, Using Antibodies: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press (1998)).
Por exemplo, as características de células-tronco pluripotentes são bem-conhecidas dos versados na técnica, e características adicionais de células-tronco pluripotentes continuam a ser identificadas. Os marcadores de células-tronco pluripotentes incluem, por exemplo, a expressão de um ou mais dentre os seguintes: ABCG2, cripto, FOXD3, Conexina43, Conexina45, OCT4, SOX2, Nanog, hTERT, UTF-1, ZFP42, SSEA-3, SSEA-4, Tra1-60, ou Tra1-81.
Após o tratamento das células-tronco pluripotentes com os métodos da presente invenção, as células diferenciadas podem ser purificadas mediante exposição de uma população de células tratadas a um agente (como um anticorpo) que especificamente reconhece um marcador de proteína, como CXCR4, expresso por células que expressam marcadores característicos da linhagem de endoderma definitivo.
Formação de células que expressam marcadores característicos da linhagem endodérmica pancreática
As células que expressam marcadores característicos da linhagem de endoderma definitivo podem ser diferenciadas em células que expressam marcadores característicos da linhagem endodérmica pan
63/247 creática por meio de qualquer método na técnica, ou por meio de qualquer método proposto na presente invenção.
Por exemplo, as células que expressam marcadores característicos da linhagem de endoderma definitivo podem ser diferenciados em células que expressam marcadores característicos da linhagem endodérmica pancreática, de acordo com os métodos apresentados em D’Amour et al, Nature Biotechnology 24, 1392 a 1401 (2006).
Por exemplo, as células que expressam marcadores característicos da linhagem de endoderma definitivo são adicionalmente diferenciadas em células que expressam marcadores característicos da linhagem endodérmica pancreática, tratando-se as células que expressam marcadores característicos da linhagem de endoderma definitivo com um fator de crescimento de fibroblastos e o inibidor da rota de sinalização hedgehog KAAD-ciclopamina, então removendo-se o meio contendo o fator de crescimento de fibroblastos e o KAAD-ciclopamina e, subsequentemente, cultivando-se as células em um meio contendo ácido retinoico, um fator de crescimento de fibroblastos e KAAD-ciclopamina. Um exemplo desse método é descrito em Nature Biotechnology 24, 1392 - 1401 (2006).
Em um aspecto da presente invenção, células que expressam marcadores característicos da linhagem de endoderma definitivo são diferenciadas, adicionalmente, em células que expressam marcadores característicos da linhagem endodérmica pancreática, mediante tratamento das células que expressam marcadores característicos da linhagem de endoderma definitivo com ácido retinoico e pelo menos um fator de crescimento de fibroblasto durante um período de tempo, de acordo com os métodos descritos no pedido de patente US No. de série 11/736,908, atribuído a LifeScan, Inc.
Em um aspecto da presente invenção, células que expressam marcadores característicos da linhagem de endoderma definitivo são diferenciadas, adicionalmente, em células que expressam marcadores característicos da linhagem endodérmica pancreática, por tratar as células que expressam marcadores característicos da linhagem de endoderma definitivo
64/247 com ácido retinoico e pelo menos um fator de crescimento de fibroblasto durante um período de tempo, de acordo com os métodos descritos no pedido de patente US No. de série 11/779.311, atribuído a LifeScan, Inc.
Em um aspecto da presente invenção, as células que expressam marcadores característicos da linhagem de endoderma definitivo são diferenciadas, adicionalmente, em células que expressam marcadores característicos da linhagem endodérmica pancreática, mediante tratamento das células que expressam marcadores característicos da linhagem de endoderma definitivo de acordo com os métodos descritos no pedido de patente com n° de série US 60/990.529.
As células que expressam marcadores característicos da linhagem de endoderma definitivo podem ser tratadas com pelo menos um outro fator adicional que pode aumentar a formação de células que expressam marcadores característicos da linhagem endodérmica pancreática. Alternativamente, o pelo menos um outro fator adicional pode otimizar a proliferação das células que expressam marcadores característicos da linhagem endodérmica pancreática formada pelos métodos da presente invenção. Adicionalmente, esse pelo menos um outro fator adicional pode otimizar a capacidade das células que expressam marcadores característicos da linhagem endodérmica pancreática formada pelos métodos da presente invenção para formar outros tipos de célula, ou otimizar a eficiência de quaisquer outras etapas adicionais de diferenciação.
Esse pelo menos um fator adicional pode ser, por exemplo, nicotinamida, membros de TGF-β família, inclusive TGF-βΙ, 2 e 3, albumina sérica, membros da família do fator de crescimento de fibroblastos, fatores AA e BB de crescimento derivados de plaqueta, plasma rico em plaquetas, fator de crescimento similar a insulina (IGF-I, II), fator de diferenciação de crescimento (como GDF-5, 6, 8, 10, 11), peptídeo I e II similar a glucagon (GLP-I e II), mimetocorpo GLP-1 e GLP-2, exendina-4, ácido retinoico, hormônio da paratiroide, insulina, progesterona, aprotinina, hidrocortisona, etanolamina, beta mercaptoetanol, fator de crescimento epidérmico (EGF), gastrina I e II, queladores de cobre, como trietileno pentamina, forscolina,
65/247
Na-butirato, ativina, betacelulina, ITS, noguina, fator de crescimento de neuritos, nodal, ácido valproico, tricostatina A, butirato de sódio, fator de crescimento de hepatócitos (HGF), esfingosina-1, VEGF, MG132 (EMD, CA), suplementos N2 e B27 (Gibco, CA), alcalóide esteroidal, como ciclopamina (EMD, CA), fator de crescimento de queratinócitos (KGF), família de proteínas Dickkopf, extrato de hipófise bovina, proteína associada à neogênese de ilhotas (INGAP), Indian hedgehog, Sonic hedgehog, inibidores de proteassoma, inibidores da via notch, inibidores de sonic hedgehog ou combinações dos mesmos.
Esse pelo menos um outro fator adicional pode ser fornecido pelo meio condicionado obtido a partir de linhagens de células pancreáticas, como PANC-1 (ATCC n°: CRL-1469), CAPAN-1 (ATCC n°: HTB-79), BxPC-3 (ATCC n°: CRL-1687), HPAF-II (ATCC n°: CRL-1997), linhagens de células hepáticas, como HepG2 (ATCC n°: HTB-8065), e linhagens de células intestinais, como FHs 74 (ATCC n°: CCL-241).
Detecção de células expressoras de marcadores característicos da linhagem de endoderme pancreática
Os marcadores característicos da linhagem endodérmica pancreática são bem-conhecidos dos versados na técnica, e marcadores adicionais característicos da linhagem endodérmica pancreática continuam a ser identificados. Esses marcadores podem ser usados para confirmar que as células tratadas de acordo com a presente invenção se diferenciaram para adquirir as propriedades características da linhagem endodérmica pancreática. Os marcadores específicos para linhagem endodérmica pancreática incluem a expressão de um ou mais fatores de transcrição, como Hlxb9, PTF-1a, PDX-1, HNF-6 e HNF-1beta.
A eficiência da diferenciação pode ser determinada expondo-se uma população de células tratadas a um agente (como um anticorpo) que especificamente reconhece um marcador de proteína expresso por células que expressam marcadores característicos da linhagem endodérmica pancreática.
Os métodos para avaliar a expressão de marcadores de proteína
66/247 e de ácido nucleico em células cultivadas ou isoladas são padrão na técnica. Estes incluem reação em cadeia de polimerase via transcriptase reversa quantitativa (RT-PCR), Northern blots, in situ hibridização (vide, por exemplo, Current Protocols in Molecular Biology (Ausubel et al., Editores, suplemento de 2001)), e imunoensaios como análise imuno-histoquimica de material seccionado, Western blotting e, para marcadores que são acessíveis em células intactas, análise de citometria de fluxo (FACS) (vide, por exemplo, Harlow e Lane, Using Antibodies: A Laboratory Manual, New York: Cold Spring Harbor Laboratory Press (1998)).
Formação de células expressoras de marcadores da linhagem endócrina pancreática
As células que expressam marcadores característicos da linhagem endodérmica pancreática podem ser diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática por meio de qualquer método na técnica, ou por meio de qualquer método descrito nesta invenção.
Por exemplo, as células que expressam marcadores característicos da linhagem endodérmica pancreática podem ser diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, de acordo com os métodos descritos em D’Amour et al, Nature Biotechnology 24, 1392a1401 (2006).
Por exemplo, as células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, cultivando-se as células que expressam marcadores característicos da linhagem endodérmica pancreática em meio contendo DAPT e exendina 4, então removendo-se o meio contendo DAPT e exendina 4 e, subsequentemente, cultivando-se as células em um meio contendo exendina 1, IGF-1 e HGF. Um exemplo desse método é descrito em Nature Biotechnology 24, 1392 -1401 (2006).
Por exemplo, as células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferen
67/247 ciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, cultivando-se as células que expressam marcadores característicos da linhagem endodérmica pancreática em meio contendo exendina 4, então removendo-se o meio contendo exendina 4 e, subsequentemente, cultivando-se as células em um meio contendo exendina 1, IGF-1 e HGF. Um Exemplo desse método é descrito em D’ Amour et al., Nature Biotechnology, 2006.
Por exemplo, as células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, cultivando-se as células que expressam marcadores característicos da linhagem endodérmica pancreática em um meio contendo DAPT e exendina 4. Um Exemplo desse método é descrito em D’ Amour et al., Nature Biotechnology, 2006.
Por exemplo, células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, através do cultivo das células que expressam marcadores característicos da linhagem endodérmica pancreática em meio contendo exendina 4. Um Exemplo desse método é descrito em D’ Amour et al., Nature Biotechnology, 2006.
Em um aspecto da presente invenção, as células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, através do tratamento das células que expressam marcadores característicos da linhagem endodérmica pancreática com um fator que inibe a via de sinalização de Notch, de acordo com os métodos descritos no pedido de patente US No. de série 11/736.908, atribuído a LifeScan, Inc.
Em um aspecto da presente invenção, as células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferenciadas em células que expressam marcadores carac
68/247 terísticos da linhagem endócrina pancreática, através do tratamento das células que expressam marcadores característicos da linhagem endodérmica pancreática com um fator que inibe a via de sinalização de Notch, de acordo com os métodos descritos no pedido de patente US No. de série 11/779.311, atribuído a LifeScan, Inc.
Em um aspecto da presente invenção, as células que expressam marcadores característicos da linhagem endodérmica pancreática são adicionalmente diferenciadas em células que expressam marcadores característicos da linhagem endócrina pancreática, através do tratamento das células que expressam marcadores característicos da linhagem endodérmica pancreática com um fator que inibe a via de sinalização de Notch, de acordo com os métodos descritos no pedido de patente US No. de série 60/953.178, atribuído a LifeScan, Inc.
Em um aspecto da presente invenção, as células expressoras de marcadores característicos da linhagem de endoderma pancreático são adicionalmente diferenciadas em células expressoras de marcadores característicos da linhagem endócrina pancreática, mediante tratamento das células expressoras de marcadores característicos da linhagem de endoderma pancreático de acordo com os métodos descritos no pedido de patente com n° serial 60/990.529.
As células que expressam marcadores característicos da linhagem endodérmica pancreática podem ser tratadas com pelo menos um outro fator adicional que pode amplificar a formação de células que expressam marcadores característicos da linhagem endócrina pancreática. Alternativamente, esse pelo menos um outro fator adicional pode otimizar a proliferação das células que expressam marcadores característicos da linhagem endócrina pancreática formada pelos métodos da presente invenção. Além disso, o pelo menos um outro fator adicional pode melhorar a capacidade das células que expressam marcadores característicos da linhagem endócrina pancreática formadas pelos métodos da presente invenção em formar outros tipos de células, ou aperfeiçoar a eficiência de quaisquer outras etapas de diferenciação adicional.
69/247
O pelo menos um fator adicional pode ser, por exemplo, nicotinamida, membros de TGF-β família, inclusive TGF-βΙ, 2 e 3, albumina sérica, membros da família do fator de crescimento de fibroblastos, fatores AA e BB de crescimento derivados de plaqueta, plasma rico em plaquetas, fator de crescimento similar a insulina (IGF-I, II), fator de diferenciação de crescimento (como GDF-5, -6, -8, -10, -11), peptídeo I e II similar a glucagon (GLP-I e II), mimetocorpo GLP-1 e GLP-2, exendina-4, ácido retinoico, hormônio da paratiroide, insulina, progesterona, aprotinina, hidrocortisona, etanolamina, beta mercaptoetanol, fator de crescimento epidérmico (EGF), gastrina I e II, queladores de cobre, como trietileno pentamina, forscolina, Na-butirato, ativina, betacelulina, ITS, noguina, fator de crescimento de neuritos, nodal, ácido valproico, tricostatina A, butirato de sódio, fator de crescimento de hepatócitos (HGF), esfingosina-1, VEGF, MG132 (EMD, CA), suplementos N2 e B27 (Gibco, CA), alcalóide esteroidal, como ciclopamina (EMD, CA), fator de crescimento de queratinócitos (KGF), família de proteínas Dickkopf, extrato de hipófise bovina, proteína associada à neogênese de ilhotas (INGAP), Indian hedgehog, Sonic hedgehog, inibidores de proteassoma, inibidores da via notch, inibidores de sonic hedgehog ou combinações dos mesmos.
O pelo menos um outro fator adicional pode ser fornecido pelo meio condicionado obtido a partir de linhagens de células pancreáticas, como PANC-1 (ATCC n°: CRL-1469), CAPAN-1 (ATCC n°: HTB-79), BxPC-3 (ATCC n°: CRL-1687), HPAF-II (ATCC n°: CRL-1997), linhagens de células hepáticas, como HepG2 (ATCC n°: HTB-8065), e linhagens de células intestinais, como FHs 74 (ATCC n°: CCL-241).
Detecção de células expressoras de marcadores característicos da linhagem endócrina pancreática
Os marcadores característicos das células da linhagem endócrina pancreática são bem-conhecidos dos versados na técnica, e marcadores adicionais característicos da linhagem endócrina pancreática continuam a ser identificados. Esses marcadores podem ser usados para confirmar que as células tratadas de acordo com a presente invenção se diferenciaram
70/247 para adquirir as propriedades características da linhagem endócrina pancreática. Os marcadores específicos para linhagem endócrina pancreática incluem a expressão de um ou mais fatores de transcrição, como NGN3,
NEURO ou ISL1
Os marcadores característicos das células da linhagem celular β são bem-conhecidos dos versados na técnica, e marcadores adicionais característicos da linhagem celular β continuam a ser identificados. Esses marcadores podem ser usados para confirmar que as células tratadas de acordo com a presente invenção foram diferenciadas para adquirir as propriedades características da linhagem de célula β. As características específicas da linhagem de células β incluem a expressão de um ou mais fatores de transcrição como PDX1, NKX2.2, NKX6.1, ISL1, PAX6, PAX4, NEUROD, HNF1 beta, HNF6, HNF3 beta ou MAFA, entre outros. Esses fatores de transcrição são bem-estabelecidos na técnica para identificação de células endócrinas. Vide, por exemplo, Edlund (Nature Reviews Genetics 3: 524-632 (2002)).
A eficiência da diferenciação pode ser determinada expondo-se uma população de células tratadas a um agente (como um anticorpo) que especificamente reconhece um marcador de proteína expresso por células que expressam marcadores característicos da linhagem endócrina pancreática. Alternativamente, a eficiência de diferenciação pode ser determinada expondo-se uma população de células tratadas a um agente (como um anticorpo) que especificamente reconhece um marcador de proteína expresso pelas células expressoras de marcadores característicos da linhagem celular β.
Os métodos para avaliar a expressão de marcadores de proteína e de ácido nucléico em células cultivadas ou isoladas são padrão na técnica. Estes incluem reação em cadeia de polimerase via transcriptase reversa quantitativa (RT-PCR), Northern blots, in situ hibridização (vide, por exemplo, Current Protocols in Molecular Biology (Ausubel et al., Editores, suplemento de 2001)), e imunoensaios como análise imuno-histoquimica de material seccionado, Western blotting e, para marcadores que são acessíveis em
71/247 células intactas, análise de citometria de fluxo (FACS) (vide, por exemplo,
Harlow e Lane, Using Antibodies: A Laboratory Manual, New York: Cold
Spring Harbor Laboratory Press (1998)).
Em um aspecto da presente invenção, a eficiência da diferenciação é determinada mediante a medição da porcentagem de células positivas para insulina em uma determinada cultura celular após tratamento. Em uma modalidade, os métodos da presente invenção produzem cerca de 100% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 90% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 80% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 70% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 60% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 50% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 40% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 30% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 20% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 10% de células positivas para insulina em uma determinada cultura. Em uma modalidade alternativa, os métodos da presente invenção produzem cerca de 5% de células positivas para insulina em uma determinada cultura.
Em um aspecto da presente invenção, a eficiência da diferenciação é determinada mediante a medição da secreção de insulina estimulada por glicose, conforme detectado mediante a medição da quantidade de
72/247 peptídeo C liberado pelas células. Em uma modalidade, as células produzidas pelos métodos da presente invenção produzem cerca de 1000 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 900 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 800 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 700 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 600 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 500 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 400 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 500 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 400 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 300 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 200 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 100 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 90 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 80 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 70 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 60 ng
73/247 de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 50 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 40 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 30 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 20 ng de peptídeo C/pg DNA. Em uma modalidade alternativa, as células produzidas pelos métodos da presente invenção produzem cerca de 10 ng de peptídeo C/pg DNA.
Terapias
Em um aspecto, a presente invenção apresenta um método para tratar um paciente que sofre de, ou que está em risco de desenvolver, diabetes tipo 1. Esse método envolve cultivar células-tronco pluripotentes, diferenciar as células-tronco pluripotentes in vitro em uma linhagem celular β, e implantar em um paciente as células de uma linhagem celular β.
Em ainda um outro aspecto, esta invenção apresenta um método para tratamento de um paciente que sofra de, ou esteja em risco de desenvolver, diabetes tipo 2. Esse método envolve cultivar células-tronco pluripotentes, diferenciar as células cultivadas in vitro em uma linhagem celular β, e implantar no paciente as células da linhagem celular β.
Se for adequado, o paciente pode ser adicionalmente tratado com agentes farmacêuticos ou bioativos que facilitem a sobrevivência e a função das células transplantadas. Esses agentes podem incluir, por exemplo, insulina, membros da família TGF-β, inclusive TGF-βΙ, 2 e 3, proteínas morfogênicas ósseas (BMP-2, 3, 4, 5, 6, 7, 11, 12 e 13), fatores 1 e 2 de crescimento de fibroblastos, fatores AA e BB de crescimento derivado de plaqueta, plasma rico em plaquetas, fator de crescimento similar a insulina (IGF-I, II), fator de diferenciação de crescimento (como GDF-5, 6, 7, 8, 10, 15), fator de crescimento derivado de célula endotelial vascular (VEGF), pleiotrofina e endotelina, entre outros. Outros compostos farmacêuticos podem incluir, por exemplo, nicotinamida, peptídeo-l tipo glucacon (GLP-1) e
74/247
II, mimeticorpo GLP-1 e 2, Exendina-4, ácido retinoico, hormônio da paratiroide, inibidores MAPK, por exemplo os compostos descritos no pedido publicado US 2004/0209901 e no pedido publicado US 2004/0132729.
As células-tronco pluripotentes podem ser diferenciadas em uma célula produtora de insulina, antes do transplante para um recipiente. Em uma modalidade específica, as células-tronco pluripotentes são totalmente diferenciadas em células β, antes de serem transplantadas para um recipiente. Alternativamente, as células-tronco pluripotentes podem ser transplantadas para um recipiente em um estado não diferenciado ou parcialmente 10 diferenciado. Uma diferenciação adicional pode ocorrer no recipiente.
As células de endoderme definitiva ou, alternativamente, as células de endoderme pancreática ou, alternativamente, as células β, podem ser implantadas sob a forma de células dispersas ou formadas em agrupamentos que podem ser aplicados ao paciente por infusão pela veia porta 15 hepática. Alternativamente, as células podem ser fornecidas em suportes poliméricos biocompatíveis e degradáveis, dispositivos porosos não degradáveis, ou encapsulados para proteção contra a resposta imunológica do hospedeiro. As células podem ser implantadas em um sítio adequado do recipiente. Os sítios de implantação incluem, por exemplo, o fígado, o pân20 creas natural, o espaço subcapsular renal, o omento, o peritônio, o espaço subseroso, o intestino, o estômago ou um bolso subcutâneo.
Para otimizar a diferenciação adicional, a sobrevivência ou a atividade das células implantadas, fatores adicionais como fatores de crescimento e agentes antioxidantes ou anti-inflamatórios podem ser admi25 nistrados antes, simultaneamente, ou após a administração das células. Em certas modalidades, os fatores de crescimento são usados para diferenciar in vivo as células administradas. Esses fatores podem ser secretados por células endógenas e expostos in situ às células administradas. As células implantadas podem ser induzidas a se diferenciar por qualquer combinação 30 de fatores de crescimento conhecidos na técnica, tanto endógenos como administrados exogenamente.
A quantidade de células usadas na implantação depende de
75/247 inúmeros fatores diferentes, inclusive a condição de saúde do paciente e sua resposta à terapia, e pode ser determinada pelo versado na técnica.
Em um aspecto, a presente invenção apresenta um método para tratar um paciente que sofra de, ou que esteja em risco de desenvolver, diabetes. Esse método envolve cultivar células-tronco pluripotentes, diferenciar as células cultivadas in vitro em uma linhagem celular β, e incorporar as células a um suporte tridimensional. As células podem ser mantidas in vitro nesse suporte, antes da implantação no paciente. Alternativamente, o suporte contendo as células pode ser diretamente implantado no paciente sem cultura in vitro adicional. O suporte pode, opcionalmente, ser incorporado com pelo menos um agente farmacêutico que facilite a sobrevivência e o funcionamento das células transplantadas.
Os materiais de suporte adequados ao uso para os propósitos da presente invenção incluem modelos de tecidos, conduítes, barreiras e reservatórios úteis para reparo de tecidos. Em particular, materiais sintéticos e naturais sob a forma de espumas, esponjas, géis, hidrogéis, produtos têxteis e estruturas não tecidas, que têm sido usadas in vitro e in vivo para reconstruir ou regenerar tecido biológico, bem como para liberar agentes quimiotácticos a fim de induzir a proliferação de tecidos, são adequadas ao uso na prática dos métodos da presente invenção. Vide, por exemplo, os materiais descritos nas patentes US n° 5.770.417, 6.022.743, 5.567.612, 5.759.830, 6.626.950, 6.534.084, 6.306.424, 6.365.149, 6.599.323, 6.656.488, no pedido de patente publicado US 2004/0062753 A1, e nas patentes US n° 4.557.264 e 6.333.029.
Para formar um suporte incorporado com um agente farmacêutico, este pode ser misturado à solução de polímero antes da formação do suporte. Altemativamente, um agente farmacêutico podería ser aplicado como revestimento sobre um suporte fabricado, de preferência na presença de um portador farmacêutico. O agente farmacêutico pode estar presente sob a forma de um líquido, um sólido finamente dividido, ou qualquer outro formato físico adequado. Alternativamente, os excipientes podem ser adicionados ao suporte para alterar a taxa de liberação do agente farmacêutico.
76/247
Em uma modalidade alternativa, o suporte é incorporado a pelo menos um composto farmacêutico que é um composto anti-inflamatório, como os compostos apresentados na patente US n° 6.509.369.
O suporte pode ser incorporado a pelo menos um composto farmacêutico que é um composto antiapoptótico, como os compostos descritos na patente US n° 6.793.945.
O suporte pode, também, ser incorporado a pelo menos um composto farmacêutico que é um inibidor de fibrose, como os compostos descritos na patente US n° 6.331.298.
O suporte pode, também, ser incorporado a pelo menos um composto farmacêutico que é capaz de acentuar a angiogênese, como os compostos descritos nos pedidos de patente publicados US 2004/0220393 e US 2004/0209901.
O suporte pode, também, ser incorporado a pelo menos um composto farmacêutico que é um composto imunossuppressivo, como os compostos descritos no pedido publicado US 2004/0171623.
O suporte pode, também, ser incorporado com pelo menos um composto farmacêutico que é um fator de crescimento, como os membros da família TGF-β, inclusive TGF-βΙ, 2 e 3, proteínas morfogênicas ósseas (BMP-2, 3, 4, 5, 6, 7, 11, 12 e 13), fatores 1 e 2 de crescimento de fibroblastos, fatores AA e BB de crescimento derivado de plaqueta, plasma rico em plaquetas, fator de crescimento similar a insulina (IGF-I, II), fator de diferenciação de crescimento (como GDF-5, 6, 8, 10, 15), fator de crescimento derivado de célula endotelial vascular (VEGF), pleiotrofina e endotelina, entre outros. Outros compostos farmacêuticos podem incluir, por exemplo, nicotinamida, fator 1-alfa induzível por hipóxia, peptídeo-l (GLP-1) similar a glucagon, mimeticorpo GLP-1, GLP-2 e II, exendina-4, nodal, noguina, NGF, ácido retinoico, hormônio da paratiroide, tenascina-C, tropoelastina, peptídeos derivados de trombina, catelicidinas, defensinas, laminina, peptídeos biológicos contendo domínios de ligação a célula e a heparina das proteínas adesivas da matriz extracelular, como fibronectina e vitronectina, inibidores MAPK, como os compostos descritos nos pedidos
77/247 publicados US 2004/0209901 e US 2004/0132729.
A incorporação das células da presente invenção em um arcabouço pode ser obtida mediante a simples deposição das células sobre o mesmo. As células podem entrar no arcabouço por difusão simples (J. Pediatr. Surg. 23 (1 Pt 2): 3 a 9 (1988)). Várias outras abordagens foram desenvolvidas para acentuar a eficiência da semeadura de células. Por exemplo, frascos de agitação foram usados na semeadura de condrócitos sobre arcabouços de ácido poliglicólico (Biotechnol. Prog. 14(2): 193 a 202 (1998)). Uma outra abordagem para a semeadura de células é o uso de centrifugação, que resulta em estresse mínimo para as células semeadas, otimizando a eficiência da semeadura. Por exemplo, Yang et al. desenvolveu um método para semeadura de células (J. Biomed. Mater. Res. 55(3): 37986 (2001)), chamado de imobilização centrifugacional da célula (CCI, ou Centrifugational Cell Immobilization).
A presente invenção é ilustrada com mais detalhes pelos exemplos a seguir, porém não é limitada pelos mesmos.
Exemplos
Para esclarecimento da descrição, e sem propósitos de limitação, a descrição detalhada da invenção é dividida nas subseções a seguir que descrevem ou ilustram determinadas características, modalidades ou aplicações da presente invenção.
Exemplo 1
Cultura de célula-tronco embrionária humana
As linhagens H1, H7 e H9 de células-tronco embrionárias humanas foram obtidas junto ao WiCell Research Institute, Inc., (Madison, Wl, EUA) e cultivadas de acordo com as instruções fornecidas pelo instituto de origem. As células-tronco embrionárias humanas foram, também, semeadas sobre placas revestidas com uma diluição a 1:30 de MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), e cultivadas em meio condicionado com MEF e suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As células cultivadas sobre MATRIGEL® foram rotineiramente passadas como aglomerados com o uso
78/247 de colagenase IV (Invitrogen/GIBCO, Cat. n° 17104-019), Dispase (Invitrogen, Cat. n° 17105-041) ou enzima Liberase Cl (Roche, Cat. n°
11814435001). Em alguns casos, as células foram passadas como células individuais com o uso de ACCUTASE (Sigma, Cat. n° A6964).
As células-tronco embrionárias humanas usadas nesses exemplos foram mantidas em um estado não diferenciado, pluripotente, com passagem em média a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de colagenase (1 ou 10 mg/mL, Sigma-Aldrich) durante 10 a 30 minutos a 37°C, seguida de raspagem suave com a ponta de uma pipeta para recuperar aglomerados celulares. Os aglomerados foram deixados sedimentar por gravidade, sendo em seguida lavados para remover a colagenase residual. Os aglomerados celulares foram divididos a uma razão de 1:3 para cultura de manutenção de rotina ou a uma razão de 1:1 para teste posterior. Todas as linhagens de células ES humanas foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao fenótipo cariotípico normal e à ausência de contaminação por micoplasma.
Exemplo 2
Bioensaio para formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo
A ativina A é um importante mediador da diferenciação em uma ampla gama de tipos de célula, inclusive na diferenciação de células-tronco embrionárias para endoderma definitivo. Quando as células-tronco embrionárias humanas são tratadas com uma combinação de ativina A e Wnt3a, vários genes representativos do endoderma definitivo são regulados para cima. Um bioensaio que mede essa diferenciação em células-tronco embrionárias humanas foi adaptado em um formato miniaturizado para placas com 96 poços para propósitos de triagem. A validação foi concluída usando-se o tratamento com fontes comerciais de ativina A e Wnt3a proteínas recombinantes e medindo-se a expressão de proteína do fator de transcrição SOX17, considerado como sendo um marcador representativo do endoderma definitivo.
79/247
Live Cell Assay, em resumo, aglomerados de células-tronco embrionárias humanas H1 foram cultivados em plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzimas, e folheadas a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, Perkin Elmer, Cat. n° 6005182). As células foram deixadas unir-se sob a forma de aglomerados e, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de 100 μΙ, por poço, de meio condicionado com fibroblasto embriônico de camundongo (MEF) suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB).
O teste foi iniciado com a lavagem dos poços de cada placa duas vezes em PBS (Invitrogen, Cat. n° 14190), seguida pela adição, a cada poço, de uma alíquota (100 μΙ) da amostra de teste em meio basal DMEM:F12 (Invitrogen, Cat. n° 11330-032). As condições de teste foram realizadas em triplicata, com alimentação em dias alternados mediante aspiração e substituição do meio de cada poço com amostras para teste, ao longo de um período de teste total de quatro dias. No primeiro e no segundo dias de teste, as amostras para teste adicionadas aos poços de teste foram diluídas em DMEM:F12 com 0,5% de FCS (HyClone, Cat. n° SH30070.03) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN). No terceiro e no quarto dias de teste, as amostras para teste adicionadas aos poços de teste foram diluídas em DMEM:F12 com 2% de FCS, sem qualquer Wnt3a. As amostras de controle positivo consistiam em ativina A humana recombinante (PeproTech, Cat. n° 120-14) adicionada a uma concentração de 100 ng/mL por todo o teste, mais Wnt3a (20 ng/mL) nos dias 1 e 2. Nas amostras de controle negativo foi omitido o tratamento tanto com ativina A como com Wnt3a.
Análise de alto conteúdo: na conclusão de quatro dias de
80/247 cultura, as placas de teste foram lavadas duas vezes com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anticabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para captura de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, coradas somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida
81/247 como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
A figura 1 mostra a validação do teste de triagem, testando uma curva de diluição dupla de uma fonte comercial de ativina A (PeproTech) e medindo tanto o número de células (figura 1A) como a intensidade de SOX17 (figura 1B). Os efeitos ideais da ativina A para indução da expressão de SOX17 foram geralmente observados na faixa de 100 a 200 ng/mL, com um EC50 de 30 a 50 ng/mL. Omitindo-se o Wnt3a do tratamento nos dias 1 e 2 do teste, deixou de produzir uma expressão mensurável de SOX17 (figura 1B, barras brancas). A ausência de ativina A também deixou de resultar na expressão de SOX17 (figura 1B).
Exemplo 3
Triagem primária: efeitos dos compostos da presente invenção sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo na ausência de ativina A
A diferenciação de células-tronco pluripotentes em células expressoras de marcadores característicos da linhagem de endoderma definitivo é mediado através de uma série de interações receptor-ligante que, por sua vez, ativam as quinases receptoras levando à fosforilação e à translocação nuclear de substratos a jusante, eventualmente regulando a expressão de genes-alvo específicos. A ativação ótima dessas cascatas de sinalização em alguns tipos de célula pode requerer a inibição de rotaspadrão opostas. Em outros casos, as rotas redundantes envolvendo membros alternativos de uma família quinase maior podem substituir, em parte, uma ou mais moléculas sinalizadoras. Em outros casos, as rotas canônicas e não canônicas podem divergir com diferentes estímulos iniciadores, mas podem levar a um resultado funcional similar.
82/247
As triagens funcionais baseadas em células são uma abordagem para identificação de alvos e métodos inovadores que podem ter um impacto sobre respostas celulares específicas. Uma abordagem muito poderosa envolve uma série de triagens iterativas por meio das quais as pistas ou os acertos de uma triagem são integrados a outra triagem subsequente. Alternativamente, uma série de variáveis diferentes é integrada de maneira combinatória (por exemplo, fatores de crescimento com inibidores da quinase) para identificar efeitos inovadores sobre a diferenciação celular. Nesse caso, uma biblioteca de moléculas pequenas, compreendendo anilina-piridinotriazinas, anilina-piridinotriazinas cíclicas e estruturas intermediárias em sua síntese, foi testada quanto a propriedades importantes durante a diferenciação do endoderma definitivo de células-tronco embrionárias humanas, especificamente quanto a efeitos para reter ou otimizar o número de células na conclusão de uma ‘primeira’ etapa de diferenciação em meio com baixo teor de soro e na ausência do fator de crescimento ativina A.
Teste de triagem
Semeadura para teste das células: em resumo, aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, PerkinElmer, Cat. n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do
83/247 ensaio.
Preparação de compostos e teste: os compostos testados foram disponibilizados como estoques de 5 mM no formato de placas com 96 poços, solubilizados em 100% de DMSO (Sigma, Cat. n° D2650) e armazenados a -80°C. Os compostos da biblioteca foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. As condições de teste foram realizadas em triplicata, com alimentação em dias alternados ao longo de um período de teste de quatro dias. Ensaios de triagem primários foram iniciados por se aspirar o meio de cultura de cada um dos poços seguido de três lavagens em PBS (Invitrogen, Cat. n° 14190) para remover quantidades residuais de fatores de crescimento e soro. No primeiro dia do teste, os volumes de teste de 200 pl por poço foram adicionados de volta contendo o meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032), suplementado com 0,5% FCS (HyClone, Cat. n° SH30070.03) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN), mais 2,5 mM do composto de teste. No terceiro dia do teste, os volumes de teste de 200 μΙ por poço foram adicionados de volta contendo o meio base DMEM:F12 suplementado com 2% de FCS mais 2,5 mM de composto de teste, sem Wnt3a. As amostras de controle positivo continham o mesmo meio base suplementado com FCS, substituindo-se 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14) pelo composto de teste por todo o período de testes de quatro dias, juntamente com Wnt3a (20 ng/mL) adicionadas somente nos dias 1 e 2. As amostras de controle negativo continham meio base DMEM:F12 suplementado com FCS, adicionando-se Wnt3a nos dias 1 e 2, mas omitindo-se a ativina A.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As
84/247 células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anticabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram
85/247 calculados para médias e desvios-padrão de cada conjunto de réplicas.
A tabela 1 mostra os resultados da triagem primária para os compostos testados, mostrando seus efeitos sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo, na ausência de ativina A. Os resultados incluem medidas quantitativas tanto do número de células como da intensidade de SOX17, tendo sido calculada a média dos respectivos pontos de dados a partir de poços em triplicata, e analisada quanto a cada parâmetro com o uso de campos idênticos em cada poço. A expressão do fator de transcrição SOX17 é considerada indicativa de diferenciação do endoderma definitivo. Os resultados da triagem primária foram capturados a partir de oito placas de triagem com 96 poços. A variabilidade de uma placa para outra foi reduzida com a inclusão de controles positivo e negativo individuais em cada placa. Os resultados são normalizados e expressos como uma porcentagem do controle positivo. Deu-se ênfase à retenção ou amplificação do número de células na conclusão do teste.
A tabela 2 lista um subconjunto de 27 compostos e seus resultados analisados a partir da triagem primária, onde esses acertos pareceram reter um número de células em teor equivalente a, ou melhor que, o do controle positivo, apesar da ausência de ativina A no teste de triagem.
Em alguns casos, a expressão de SOX17 foi induzida na ausência de ativina A (por exemplo, os Compostos 35 e 22, à base de anilinapiridinotriazinas cíclicas).
Os compostos mostrados na tabela 2 foram selecionados para avaliação adicional quanto aos efeitos sobre a diferenciação de célulastronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo, na ausência de ativina A.
Exemplo 4
Triagem secundária: efeitos dos compostos da presente invenção sobre a diferenciação de células-tronco embrionárias humanas em
86/247 células expressoras de marcadores característicos da linhagem de endoderma definitivo com EGF/FGF4 na ausência de ativina A
Uma curva de titulação para ativina A com uma quantidade constante de Wnt3a mostrou pelo menos dois efeitos durante a diferenciação de endoderma definitivo: 1) manutenção dos números de células ou prevenção de perda celular, e 2) indução de um marcador de endoderma definitivo, por exemplo expressão de SOX17 (exemplo 2). A triagem primária do exemplo 3 identificou compostos que poderíam manter, em um teste, números de células similares ou otimizados em relação à adição de ativina A/Wnt3a por si sós. Conduziu-se um teste de triagem secundária para avaliar o efeito das combinações dos compostos identificados com outros fatores de crescimento, especificamente EGF e FGF4, sobre a geração de endoderma definitivo.
Semeadura para teste das células: aglomerados de célulastronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, PerkinElmer, Cat. n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e fatores de crescimento: as concentrações de estoque para EGF (R&D Systems Cat. n° 236-EG) e FGF4 (R&D Systems, Cat. n° 235-F4) eram de 250 ng/mL, cada qual solubilizado em
87/247
PBS com 0,1% de BSA (Sigma, Cat. n° A7888). Os compostos foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO (Sigma, Cat. n° D2650) e armazenados a -80°C. Os compostos foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. Todos os fatores de crescimento e inibidores foram preparados em uma placa de polipropileno com 96 poços profundas, diluídos até 5x com soluções de estoque intermediárias em meio base DMEM:F12 no início do teste, e armazenados a 4°C.
Foi conduzido um teste de triagem secundária, com teste em triplicata e alimentação em dias alternados ao longo do período de teste de quatro dias. Os testes foram iniciados mediante aspiração do meio de cultura de cada um dos poços, seguida de três lavagens em PBS para remover quantidades residuais de fatores de crescimento e soro. Os volumes de teste de 80 pl por poço foram adicionados de volta, contendo meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,625% de FCS (HyClone, Cat. n° SH30070.03), 25 ng/mL de Wnt3a (R&D Systems) e
3,125 μΜ de composto mais 20 μΙ de estoque a 5x de fatores de crescimento, para produzir uma concentração final de 0,5% de FCS, 20 ng/mL de Wnt3a e 2,5 μΜ de composto mais 50 ng/mL de EGF e 50 ng/mL de FGF4 no teste. Os poços com controle positivo (100 μΙ/poço) continham o mesmo meio base suplementado com 0,5% de FCS, 20 ng/mL de Wnt3a e 100 ng/mL de ativina A. Os poços com controle negativo (100 μΙ/poço) continham o mesmo meio base suplementado com 0,5% de FCS e 20 ng/mL de Wnt3a, omitindo-se a ativina A.
No dia 3, os poços foram aspirados e alimentados com 80 μΙ de meio base DMEM:F12 suplementado com 2,5% de FCS (HyClone) e 3,125 μΜ de composto mais 20 μΙ de estoque a 5x de fatores de crescimento por poço, para produzir uma concentração final de 2% de FCS e 2,5 μΜ de composto (omitindo-se o Wnt3a), mais 50 ng/mL de EGF e FGF4 no teste. Os poços com controle positivo (100 μΙ/poço) continham o mesmo meio base
88/247 suplementado com 2% de FCS e 100 ng/mL de ativina A, omitindo-se
Wnt3a. Os poços com controle negativo (100 μΙ/poço) continham o mesmo meio base com 2% de FCS, omitindo-se tanto a ativina A como o Wnt3a.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS, fixadas com 4% de paraformaldeido (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, coradas somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determi
89/247 nada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
A tabela 3A mostra os resultados para dois fatores de crescimento, EGF e FGF 4 (50 ng/mL cada), testados em combinação com os compostos de anilina-piridinotriazina mostrados na tabela 2, por seus efeitos sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo, na ausência de ativina A. Os resultados são classificados em ordem descendente quanto aos melhores efeitos sobre a expressão de SOX17. Embora os efeitos desses compostos sobre a expressão de SOX17 tenham sido considerados fracos em relação ao controle positivo com ativina A/Wnt3a, as respostas para alguns desses compostos foram consideradas significativas. Por exemplo, uma seleção dos compostos parece ter propriedades exclusivas no que diz respeito à retenção de altos números de células por poço durante o teste, presumivelmente mediante a prevenção da apoptose ou mediante a modulação do ciclo celular. Além disso, esses compostos parecem criar uma sinergia com EGF e FGF4 para promover uma modesta diferenciação do endoderma definitivo, conforme medido pela expressão de SOX17. Os compostos mais potentes são mencionados na tabela 3B. Outros compostos testados em combinação com EGF e FGF4 neste teste foram ineficazes para induzir a expressão de SOX17, mas poderíam reter os números de células em teste (por exemplo o Composto 90, com 85% do número de células e 2% de expressão de SOX17).
90/247
Exemplo 5
Efeitos dos compostos da presente invenção, em combinação com outros fatores, sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo na ausência de ativina A
Um teste secundário foi conduzido para avaliar o efeito dos compostos da presente invenção com combinações de outros fatores de crescimento individuais, ou compostos conhecidos na literatura por regular a diferenciação do endoderma definitivo.
Semeadura para teste das células: aglomerados de célulastronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, PerkinElmer, Cat. n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e fatores de crescimento: os estoques de fatores de crescimento adquiridos junto à R&D Systems foram: EGF (Cat. n° 236-EG), FGF4 (Cat. n° 235-F4), PDGF-A (Cat. n° 221-A-A), PDGF-B (Cat. n° 220-BB), PDGF-C (Cat. n° 1687-CC), PDGF-D (Cat. n° 1159-SB), PDGF-A/B (Cat. n° 222-AB), VEGF (Cat. n° 293-VE), BMP-1 (Cat. n° 1927ZN)BMP-2 (Cat. n° 355-BM), BMP-4 (Cat. n° 314-BP), BMP-6 (Cat. n° 507BP), BMP-7 (Cat. n° 222-AB), BMP-2/7 (Cat. n° 3229-BM). Outros agentes
91/247 testados foram adquiridos conforme exposto a seguir: BMP-7 (Sigma, Cat. n° B1434), LY294002 (Cayman, Cat. n° 70920), PD98059, U0126, U0124 (EMD Biosciences, Cat. n° 453710), muscimol (Tocris, Cat. n° 0289), bicuculina (Tocris, Cat. n° 0130), butirato de sódio (Sigma, Cat. n° B5887). Todos os 5 fatores de crescimento foram solubilizados em PBS com 0,1% de BSA (Sigma, Cat. n° A7888) e armazenados congelados a -80°C. As moléculas pequenas foram solubilizadas em 100% de DMSO (Sigma, Cat. n° D2650) e armazenadas congeladas a — 80°C. Os compostos foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, 10 solubilizados em 100% de DMSO e armazenados a —80°C. Os compostos da presente invenção foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630080) e 20% de DMSO, e armazenados a 4°C. Todos os fatores de crescimento e inibidores foram preparados em uma placa de polipropileno com 15 96 poços profundas, diluídos até 5x com soluções de estoque intermediárias em meio base DMEM:F12 no início do teste, e armazenados a 4°C.
Foi conduzido um teste de triagem secundária, com teste em triplicata e alimentação em dias alternados ao longo do período de teste de quatro dias. Os testes foram iniciados mediante aspiração do meio de cultura 20 de cada um dos poços, seguida de três lavagens em PBS para remover quantidades residuais de fatores de crescimento e soro. Os volumes de teste de 80 pl por poço foram adicionados de volta, contendo meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,625% de FCS (HyClone, Cat. n° SH30070.03), 25 ng/mL de Wnt3a (R&D Systems) e 25 3,125 μΜ de composto mais 20 μΙ de estoque a 5x de fatores de crescimento ou moléculas pequenas, para produzir uma concentração final de 0,5% de FCS, 20 ng/mL de Wnt3a e 2,5 μΜ de composto. Todos os fatores de crescimento restantes foram testados a uma concentração final de teste de 50 ng/mL (EGF, FGF4, PDGF-A, PDGF-B, PDGF-C, PDGF-D, PDGF-A/B, 30 VEGF, BMP-1, BMP-2, BMP-4, BMP-6, BMP-7 e BMP-2/7). As concentrações finais de teste das moléculas pequenas testadas eram conforme exposto a seguir: muscimol (20 μΜ), PD98059 (1 μΜ), LY294002 (2,5 μΜ),
92/247
U0124 (1 μΜ), U0126 (1 μΜ), butirato de sódio (0,5 mM). Os poços com controle positivo (100 μΙ/poço) continham o mesmo meio base suplementado com 0,5% de FCS, 20 ng/mL de Wnt3a e 100 ng/mL de ativina A. Os poços com controle negativo (100 μΙ/poço) continham o mesmo meio base suplementado com 0,5% de FCS e 20 ng/mL de Wnt3a, omitindo-se a ativina A.
No dia 3, os poços foram aspirados e alimentados com 80 μΙ de meio base DMEM:F12 suplementado com 2,5% de FCS (HyClone) e
3,125 μΜ de composto de anilina-piridinotriazina cíclica mais 20 μΙ de estoque a 5x de fatores de crescimento ou moléculas pequenas por poço, para produzir uma concentração final de 2% de FCS e 2,5 mM de composto (omitindo-se o Wnt3a) e, conforme denotado no primeiro dia para todos os fatores de crescimento ou moléculas pequenas restantes. Os poços com controle positivo (100 μΙ/poço) continham o mesmo meio base suplementado com 2% de FCS e 100 ng/mL de ativina A, omitindo-se Wnt3a. Os poços com controle negativo (100 μΙ/poço) continham o mesmo meio base com 2% de FCS, omitindo-se tanto a ativina A como o Wnt3a.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS, fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570)
93/247 durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100pl/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
A tabela 4 mostra os resultados para a diferenciação de célulastronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo, em seguida a tratamento com os compostos da presente invenção, em combinação com fatores de crescimento individuais ou outras moléculas pequenas. Em geral, os membros da família BMP (BMP-1, BMP-2, BMP-4, BMP-6, BMP-7 e BMP-2/7) inibiram ou tiveram efeitos desprezíveis sobre a expressão de
94/247
SOX17. O mesmo era verdadeiro para a maioria dos inibidores de enzimas de molécula pequena testadas nesse ensaio (LY294002, PD98059, U0126, U0124 e butirato de sódio). Entretanto, alguns membros da família PDGF (PDGF-A, AB, C e D) forneceram um aumento na expressão de SOX17 (de 10 a 25% do controle com ativina A/Wnt3a). Outros fatores de crescimento mostrando aumentos similares na expressão de SOX17 incluíam EGF (34%), VEGF (18%) e FGF4 (17%), embora o FGF4 não tenha sido capaz de suportar a retenção dos números de células. O muscimol (agonista do receptor GABAa) de molécula pequena, testado em combinação com o Composto 35, também ofereceu um modesto aumento na expressão de SOX17, enquanto o agonista do receptor GABAa, bicuculina, não teve qualquer efeito sobre a expressão de SOX17. EGF, FGF4, PDGF-A, PDGFB, PDGF-AB, PDGF-C, PDGF-D e muscimol foram selecionados para avaliação adicional durante a diferenciação do endoderma definitivo.
Exemplo 6
Efeitos dos compostos da presente invenção, em combinação com outros fatores, sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo na ausência de ativina A
Um teste secundário foi conduzido para avaliar o efeito das combinações de diferentes compostos com outros agentes individuais sobre a diferenciação do endoderma definitivo. Os outros agentes selecionados para esta triagem tinham previamente mostrado um modesto aumento na formação de endoderma definitivo, conforme testado com o Composto 17 e conforme denotado na tabela 5. Nesta triagem, um painel mais amplo de compostos foi avaliado com esses agentes, seja em comparações individuais em pares, seja em combinações agrupadas.
Semeadura para teste das células: aglomerados de célulastronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e
95/247 raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, PerkinElmer, Cat. n° 6005182), usando-se volumes de 100 μ/poço. As células foram deixadas unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% CO2, em uma caixa umidificada por toda a duração do teste.
Preparação de compostos e fatores de crescimento: os estoques de fatores de crescimento adquiridos junto à R&D Systems foram EGF (Cat. n° 236-EG), FGF4 (Cat. n° 235-F4), PDGF-A (Cat. n° 221-AA), PDGF-D (Cat. n° 1159-SB), PDGF-A/B (Cat. n° 222-AB) e VEGF (Cat. n° 293-VE). O muscimol foi adquirido junto à Tocris (Cat. n° 0289). Todos os fatores de crescimento foram solubilizados em PBS com 0,1% de BSA (Sigma, Cat. n° A7888) e armazenados congelados a -80°C. O muscimol foi solubilizado em 100% de DMSO (Sigma, Cat. n° D2650) e armazenado congelado a -80°C. Os compostos foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO e armazenados a -80°C. Os compostos foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. Todos os fatores de crescimento e inibidores foram preparados em uma placa de polipropileno com 96 poços profundos, diluídos até 5x com soluções de estoque intermediárias em meio base DMEM:F12 no início do teste, e armazenados a 4°C.
Foi conduzido um teste de triagem secundária, com teste em triplicate e alimentação em dias alternados ao longo do período de teste de quatro dias. Os testes foram iniciados mediante aspiração do meio de cultura de cada um dos poços, seguido de três lavagens em PBS para remover quantidades residuais de fatores de crescimento e soro. Os volumes de teste
96/247 de 80 μΙ por poço foram adicionados de volta, contendo meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,625% de FCS (HyClone, Cat. n° SH30070.03), 25 ng/mL de Wnt3a (R&D Systems) e
3,125 μΜ de composto mais 20 μΙ de estoque a 5x de fator de crescimento ou moléculas pequenas, para produzir uma concentração final de 0,5% de FCS, 20 ng/mL de Wnt3a e 2,5 μΜ. Todos os fatores de crescimento restantes foram testados a uma concentração final de teste de 50 ng/mL (EGF, FGF4, PDGF-A, PDGF-A/B e VEGF). A concentração final de teste do muscimol era de 20 μΜ. Os poços com controle positivo (100 μ/poço) continham o mesmo meio base suplementado com 0,5% de FCS, 20 ng/mL de Wnt3a e 100 ng/mL de ativina A. Os poços com controle negativo (100 μ/poço) continham o mesmo meio base suplementado com 0,5% de FCS e 20 ng/mL de Wnt3a, omitindo-se a ativina A.
No dia 3, os poços foram aspirados e alimentados com 80 μΙ de meio base DMEM:F12 suplementado com 2,5% de FCS (HyClone) e 3,125 μΜ de composto mais 20 μΙ de estoque a 5x de fatores de crescimento ou moléculas pequenas por poço, para produzir uma concentração final de 2% de FCS e 2,5 μΜ de composto (omitindo-se o Wnt3a) e, conforme denotado no primeiro dia para todos os fatores de crescimento ou moléculas pequenas restantes. Os poços com controle positivo (100 μ/poço) continham o mesmo meio base suplementado com 2% de FCS e 100 ng/mL de ativina A, omitindo-se Wnt3a. Os poços com controle negativo (100 μ/poço) continham o mesmo meio base com 2% de FCS, omitindo-se tanto a ativina A como o Wnt3a.
Análise de alto conteúdo', na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS, fixadas com 4% de parafomnaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura
97/247 ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para captura de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
98/247
A tabela 5 mostra compostos previamente identificados como acertos (tabela 2), testados em um bioensaio de endoderma definitivo em várias combinações com fatores de crescimento e muscimol, sem ativina A. Alguns compostos tiveram efeitos mínimos ou fracos sobre a expressão de SOX17 com todas as combinações de fator de crescimento testadas. Entretanto, alguns compostos foram capazes de induzir expressão de SOX17 significativa com algumas, mas não com todas, as combinações de fator de crescimento. Um composto em particular, o Composto 34, teve respostas sinérgicas significativas com todos os fatores de crescimento testados, e mediou aumentos tanto nos números de células como na expressão de SOX17 neste teste: Composto 39 com 1) EGF+FGF4 = 77% da resposta do controle positivo; ou 2) EGF+FGF4+PDGF-AB = 68% da resposta do controle positivo; ou 3) EGF+FGF4+PDGF-A+VEGF = 31% da resposta do controle positivo.
Exemplo 7
Efeitos do Composto 34, em combinação com outros fatores, sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo na ausência de ativina A
Neste exemplo, fez-se um esforço para analisar o número mínimo de fatores de crescimento requeridos, em combinação com o composto de anilina-piridinotriazina cíclica, Composto 34, para produzir uma robusta resposta de SOX17, na ausência de ativina A. Também neste exemplo um novo fator de crescimento, GDF-8, foi adicionado para avaliação. O GDF-8, também conhecido como miostatina, é um membro da família TGF-β e foi demonstrado seu uso nos receptores de ativina tipo II e TGF-β tipo I (ALK4/5) para induzir a fosforilação de SMAD 2/3.
Semeadura para teste das células: aglomerados de célulastronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e
99/247 raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, PerkinElmer, Cat. n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e fatores de crescimento: estoques de fatores de crescimento adquiridos junto à R&D Systems foram: EGF (Cat. n° 236-EG), FGF4 (Cat. n°235-F4), PDGF-A (Cat. n°221-A-A), PDGF-D (Cat. n°1159-SB), PDGF-A/B (Cat. n°222-AB), VEGF (Cat. n°293-VE) e GDF-8 (Cat. n° 788-G8). O muscimol foi adquirido junto à Tocris (Cat. n° 0289). Todos os fatores de crescimento foram solubilizados em PBS com 0,1% de BSA (Sigma, Cat. n° A7888) e armazenados congelados a -80°C. O muscimol foi solubilizado em 100% de DMSO (Sigma, Cat. n° D2650) e armazenado congelado a -80°C. Os compostos de anilina-piridinotriazina cíclica foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO e armazenados a 80°C. O composto 34 foi adicionalmente diluído até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630080) e 20% de DMSO, e armazenado a 4°C. Todos os fatores de crescimento e inibidores foram preparados em uma placa de polipropileno com 96 poços profundos, diluídos até 5x com soluções de estoque intermediárias em meio base DMEM:F12 no início do teste, e armazenados a 4°C.
Foi conduzido um teste de triagem secundária, com teste em triplicata e alimentação em dias alternados ao longo do período de teste de quatro dias. Os testes foram iniciados mediante aspiração do meio de cultura de cada uma das poços, seguida de três lavagens em PBS para remover
100/247 quantidades residuais de fatores de crescimento e soro. Os volumes de teste de 80 pl por poço foram adicionados de volta, contendo meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,625% de FCS (HyClone, Cat. n° SH30070.03), 25 ng/mL de Wnt3a (R&D Systems) e
3,125 μΜ de Composto 27 mais 20 μΙ de estoque a 5x de fatores de crescimento ou moléculas pequenas, para produzir uma concentração final de 0,5% de FCS, 20 ng/mL de Wnt3a e 2,5 μΜ de Composto 34. Todos os fatores de crescimento restantes foram testados a uma concentração final de teste de 50 ng/mL (EGF, FGF4, PDGF-A, PDGF-A/B e VEGF), com a exceção de GDF-8, que foi testado a 25 ng/mL. A concentração final de teste do muscimol era de 20 μΜ. Os poços com controle positivo (100 μΙ/poço) continham o mesmo meio base suplementado com 0,5% de FCS, 20 ng/mL de Wnt3a e 100 ng/mL de ativina A. Os poços com controle negativo (100 μΙ/poço) continham o mesmo meio base suplementado com 0,5% de FCS e 20 ng/mL de Wnt3a, omitindo-se a ativina A.
No dia 3, os poços foram aspirados e alimentados com 80 μΙ de meio base DMEM:F12 suplementado com 2,5% de FCS (HyClone) e 3,125 μΜ do Composto 34 mais 20 μΙ de estoque a 5x de fatores de crescimento ou moléculas pequenas por poço, para produzir uma concentração final de 2% de FCS e 2,5 μΜ de Composto 34 (omitindo-se o Wnt3a) e, conforme denotado no primeiro dia para todos os fatores de crescimento ou moléculas pequenas restantes. Os poços com controle positivo (100 μΙ/poço) continham o mesmo meio base suplementado com 2% de FCS e 100 ng/mL de ativina A, omitindo-se Wnt3a. Os poços com controle negativo (100 μΙ/poço) continham o mesmo meio base com 2% de FCS, omitindo-se tanto a ativina A como o Wnt3a.
Análise de alto conteúdo', na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS, fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas
101/247 novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. η·° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, coradas somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados
102/247 foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
A tabela 6 mostra os resultados desse teste. Quando o GDF-8 estava presente em qualquer combinação com o Composto 34, observou-se um aumento substancial na expressão de SOX17. Além disso, o GDF-8 e o Wnt3a com o Composto 34 foram suficientes para produzir uma expressão de SOX17 (88% do controle) em uma faixa similar àquela observada em um tratamento com 100 ng/mL de ativina A/Wnt3a. Parece que o fator de crescimento GDF-8 pode servir como uma substituição à ativina A durante a diferenciação do endoderma definitivo de células-tronco embrionárias humanas.
Exemplo 8
Triagem adicional para compostos capazes de diferenciar células-tronco pluripotentes em células expressoras de marcadores característicos da linhagem de endoderma definitivo
Com base nas estruturas de composto para os acertos identificados até então, conduziu-se uma busca por análogos, a fim de encontrar compostos relacionados adicionais para testar no bioensaio de endoderma definitivo. A busca por subestruturas resultou em compostos para triagem. Os parâmetros de triagem para este teste foram designados com a combinação de fatores que rendeu ótimos resultados em testes anteriores, especificamente combinando EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol e GDF-8 com o composto de moléculas pequenas.
Semeadura para teste das células: em resumo, aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates,
103/247
PerkinElmer, Cat n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e teste: os fatores de crescimento adquiridos junto à R&D Systems foram: EGF (Cat. n° 236-EG), FGF4 (Cat. n°235-F4), PDGF-A (Cat. n°221-AA), PDGF-D (Cat. n°1159-SB), PDGF-A/B (Cat. n°222-AB), VEGF (Cat. n°293-VE) e GDF-8 (Cat. n° 788-G8). O muscimol foi adquirido junto à Tocris (Cat. n° 0289). A triagem foi conduzida com o uso de uma biblioteca de compostos que foram disponibilizados como estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO (Sigma, Cat. n° D2650) e armazenados a -80°C. Os compostos foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. As condições de teste foram realizadas em poços individuais, com alimentação em dias alternados ao longo de um período de teste de quatro dias. Ensaios de triagem primários foram iniciados por se aspirar o meio de cultura de cada um dos poços seguido de três lavagens em PBS (Invitrogen, Cat. n° 14190) para remover quantidades residuais de fatores de crescimento e soro. No primeiro dia do teste, os volumes de teste de 200 μΙ por poço foram adicionados de volta contendo o meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032), suplementado com 0,5% FCS (HyClone, Cat. n° SH30070.03) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN), mais 2,5 μΜ do composto. Todos os fatores de crescimento restantes foram testados a uma concentração final de teste de 50 ng/mL (EGF, FGF4, PDGF-A, PDGF-A/B e VEGF), com a exceção de GDF-8, que foi testado a 25 ng/mL. A concentração final de teste do muscimol era de 20 μΜ. As amostras de controle positivo continham o mesmo meio base suplementado com 0,5% de FCS mais 20 ng/mL de
104/247
Wnt3a e 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14). As amostras de controle negativo continham o meio base DMEM:F12 suplementado com 0,5% de FCS e 20 ng/mL Wnt3a. No terceiro dia do teste, os volumes de teste de 200 pl por poço foram adicionados de volta contendo o meio base DMEM:F12 suplementado com 2% de FCS mais
2,5 μΜ de composto, sem Wnt3a. Todos os fatores de crescimento restantes foram testados a uma concentração final de teste de 50 ng/mL (EGF, FGF4, PDGF-A, PDGF-A/B e VEGF), com a exceção de GDF-8, que foi testado a 25 ng/mL. A concentração final de teste do muscimol era de 20 μΜ. As amostras de controle positivo continham o mesmo meio base suplementado com 2% de FCS mais 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14). As amostras de controle negativo continham o meio base DMEM:F12 suplementado com 2% de FCS. As amostras de controle positivo continham o mesmo meio base suplementado com FCS, substituindo-se 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14) pelo composto de anilina-piridinotriazina por todo o período de testes de quatro dias, juntamente com Wnt3a (20 ng/mL) nos dias 1 e 2. As amostras de controle negativo continham meio base DMEM:F12 suplementado com FCS, adicionando-se Wnt3a nos dias 1 e 2, mas omitindo-se o tratamento com ativina A.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG,
105/247 sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total da proteína SOX17 foi relatada como a intensidade total ou intensidade integrada, definida como a fluorescência total da célula vezes a área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
Na tabela 7, o GDF-8 e uma combinação de fatores de crescimento/agonistas (EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol) foram testados com um novo conjunto de compostos à base de anilinapiridinotriazina. Os resultados de duas placas de teste neste experimento individual são classificadas em relação às respostas de SOX17 (como uma
106/247 porcentagem do tratamento do controle positivo com ativina A e Wnt3a). Foram identificados compostos adicionais que mostram atividade sinérgica significativa com o grupo de fator de crescimento/agonista. Esses compostos foram eficazes tanto para reter o número de células de teste, como para produzir expressão de SOX17 durante a diferenciação de células-tronco embrionárias humanas na ausência de ativina A. Uma lista desses acertos com atividade maior que 25% do controle positivo é mostrada na tabela 8.
Deve-se observar que quatro acertos oriundos da triagem primária inicial (tabela 2) foram duplicados na biblioteca de análogos. Dois desses compostos repetiram-se como acertos na triagem de análogos (Composto 34 e Composto 35, mostrados em uma caixa na tabela 8), um foi um acerto fraco na triagem de análogos, e um composto não repetiu o resultado.
Exemplo 9
Efeitos dos compostos da presente invenção sobre a diferenciação de células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo na presença de baixas concentrações de ativina A
É importante determinar se os compostos que foram identificados como acertos nos bioensaios de endoderma definitivo, acima, também poderíam exibir uma atividade sinérgica com doses muito baixas de ativina A. Realizou-se uma avaliação inicial com o uso da lista curta de acertos dos compostos à base de anilina-piridinotriazina cíclica apontados na tabela 3B.
Semeadura para teste das células: aglomerados de célulastronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Packard ViewPlates, PerkinElmer, Cat. n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas
107/247 unir-se sob a forma de aglomerados para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e fatores de crescimento: estoques de fatores de crescimento adquiridos junto à R&D Systems foram: EGF (Cat. n° 236-EG), FGF4 (Cat. n°235-F4), PDGF-A (Cat. n°221-AA), PDGF-D (Cat. n°1159-SB), PDGF-A/B (Cat. n°222-AB), VEGF (Cat. n°293-VE) e GDF-8 (Cat. n° 788-G8). A ativina A foi adquirida junto à PeproTech (Cat. n°). O muscimol foi adquirido junto à Tocris (Cat. n° 0289). Todos os fatores de crescimento foram solubilizados em PBS com 0,1% de BSA (Sigma, Cat. n° A7888) e armazenados congelados a -80°C. O muscimol foi solubilizado em 100% de DMSO (Sigma, Cat. n° D2650) e armazenado congelado a -80°C. Os compostos foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO e armazenados a -80°C. Os compostos foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. Todos os fatores de crescimento e inibidores foram preparados em uma placa de polipropileno com 96 poços profundas, diluídos até 5x com soluções de estoque intermediárias em meio base DMEM:F12 no início do teste, e armazenados a 4°C.
Foi conduzido um teste de triagem secundária, com teste em triplicata e alimentação em dias alternados ao longo do período de teste de quatro dias. Os testes foram iniciados mediante aspiração do meio de cultura de cada um dos poços, seguido de três lavagens em PBS para remover quantidades residuais de fatores de crescimento e soro. Os volumes de teste de 80 pl por poço foram adicionados de volta, contendo meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,625% de FCS (HyClone, Cat. n° SH30070.03), 25 ng/mL de Wnt3a (R&D Systems),
12,5 ng/mL de ativina A e 3,125 μΜ de composto mais 20 μΙ de estoque a 5x
108/247 de fator de crescimento ou moléculas pequenas para produzir uma concentração final de 0,5% de FCS, 20 ng/mL de Wnt3a, 10 ng/mL de ativina A e
2,5 μΜ de composto. Todos os fatores de crescimento restantes foram testados a uma concentração final de teste de 50 ng/mL (EGF, FGF4, PDGF-A, PDGF-A/B e VEGF), com a exceção de GDF-8, que foi usado a 25 ng/mL. A concentração final de teste do muscimol era de 20 μΜ. Os poços com controle positivo (100 pl/poço) continham o mesmo meio base suplementado com 0,5% de FCS, 20 ng/mL de Wnt3a e 10 ng/mL (dose baixa) ou 100 ng/mL (dose alta) de ativina A. Os poços com controle negativo (100 pl/poço) continham o mesmo meio base suplementado com 0,5% de FCS e 20 ng/mL de Wnt3a, omitindo-se a ativina A.
No dia 3, os poços foram aspirados e alimentados com 80 pl de meio base DMEM:F12 suplementado com 2,5% de FCS (HyClone), 12,5 ng/mL de ativina A e 3,125 pM de composto mais 20 pl de estoque a 5x de fatores de crescimento ou moléculas pequenas por poço, para produzir uma concentração final de 2% de FCS, 10 ng/mL de ativina A e 2,5 pM de composto (omitindo-se o Wnt3a) e, conforme denotado no primeiro dia para todos os fatores de crescimento ou moléculas pequenas restantes. Os poços com controle positivo (100 pl/poço) continham o mesmo meio base suplementado com 2% de FCS e 10 ng/mL ou 100 ng/mL de ativina A, omitindose Wnt3a. Os poços com controle negativo (100 pl/poço) continham o mesmo meio base com 2% de FCS, omitindo-se tanto a ativina A como o Wnt3a.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS, fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems,
109/247
Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
A tabela 9 mostra os resultados do teste de vários compostos e
110/247 diferentes combinações de fatores de crescimento com baixas doses de ativina A. Alguns compostos exibiram respostas sinérgicas robustas com vários fatores de crescimento. Em outros casos, os efeitos sinérgicos foram mais modestos, porém significativos em relação a um controle com baixa dose de ativina A. Outros compostos não apresentaram qualquer atividade em relação ao controle com baixa dose de ativina A.
Exemplo 10
Efeitos dos compostos da presente invenção sobre a diferenciação de células-tronco embrionárias humanas individuais em células expressoras de marcadores da linhagem de endoderma definitivo, na ausência de ativina A
Os compostos à base de anilina-piridinotriazina cíclica foram, também, testados em um formato de triagem usando células dispersas, por meio de tratamento enzimático, em células individuais e folheadas em uma camada única para teste. O teste também fez alterações para eliminar o soro que poderia fornecer fatores de crescimento, ainda que em baixas doses. Para isso, o meio basal foi alterado, e o soro foi substituído por BSA isento de ácido graxo. O teste foi encurtado de quatro dias para três dias, de modo a oferecer um período mais estreito para a medição de resultados. Finalmente, o teste incluiu dois fatores de crescimento, EGF e FGF4, que haviam previamente mostrado efeitos significativos porém abaixo do ótimo sobre a diferenciação do endoderma definitivo na ausência de ativina A.
Teste de triagem
Semeadura para teste das células: em resumo, aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As culturas foram tratadas com Accutase (Sigma, Cat. n° A6964), usando-se volumes equivalentes a 10 pL por 10 cm2 de área superficial durante 5 minutos a 37°C e, então, foram delicadamente ressuspensas, peletizadas por centrífugação, e ressuspensas em meio condicionado com MEF para contagem. Para semeadura para o teste, as células foram folheadas a 50.000 células/cm2 sobre placas pretas
111/247 com 96 poços revestidas por MATRIGEL® com fator de crescimento reduzido (Packard ViewPlates, Cat. n° 6005182), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se e recuperar a proliferação na fase log ao longo de um período de 3 a 5 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e teste: estoques de EGF e FGF4 foram preparados em uma placa de polipropileno com 96 poços (Corning, Inc., Cat. n° 3960). O Composto 22 estava disponível como um estoque de 5 mM solubilizado em 100% de DMSO (Sigma, Cat. n° D2650) e armazenado a -80°C. Os testes foram iniciados mediante aspiração do meio de cultura de cada um dos poços, seguido de três lavagens em PBS para remover quantidades residuais de fatores de crescimento e soro. Os volumes de teste de 80 pl por poço foram adicionados de volta, contendo meio base RPMI 1640 (Invitrogen, Cat. n° 22400-089) suplementado com 2,5% de BSA isento de ácido graxo (MP Biomedicals LLC, Cat. n° 152401), 10 ng/mL de bFGF (PeproTech Inc, Cat. n° 100-18B), 25 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN) e 3,125 μΜ de Composto 22 mais 20 μΙ de estoque a 5x de fatores de crescimento, para produzir uma concentração final de 2% de BSA isento de ácido graxo, 8 ng/mL de bFGF (PeproTech Inc; Cat. n° 100-18B), 20 ng/mL de Wnt3a, e 2,5 μΜ de Composto 22 no teste. Os poços de controle positivo continham o mesmo meio base suplementado com 2% de BSA isento de ácido graxo, 8 ng/mL de bFGF, 20 ng/mL de Wnt3a e 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14). Os poços de controle negativo continham o mesmo meio base suplementado com 2% de BSA isento de ácido graxo, 8 ng/mL de bFGF e 20 ng/mL de Wnt3a, mas omitiu-se o tratamento com ativina A.
No segundo dia de teste, os poços foram novamente aspiradas e alimentadas com 80 μΙ por poço que foram adicionados de volta, contendo meio base RPMI 1640 suplementado com 2,5% de BSA isento de ácido graxo, 10 ng/mL de bFGF e 3,125 μΜ de Composto 22 mais 20 μΙ de
112/247 estoque a 5x de fatores de crescimento, para produzir uma concentração final de 2% de BSA isento de ácido graxo, 8 ng/mL de bFGF e 2,5 pM de Composto 22 no teste. Os poços de controle positivo continham o mesmo meio base suplementado com 2% de BSA isento de ácido graxo, 8 ng/mL de bFGF e 100 ng/mL de ativina A humana recombinante. As amostras de controle negativo continham o mesmo meio base suplementado com 2% de BSA isento de ácido graxo e 8 ng/mL de bFGF, mas omitiu-se o tratamento com ativina A.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS, fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 pl/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15
113/247 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
A tabela 10 mostra os resultados desse teste com o Composto 34. As amostras de controle com EGF e/ou FGF4 sozinho, sem o Composto 34, apresentaram baixa expressão de SOX17. A adição do Composto 34 adicionou um otimização significativa da expressão de SOX17.
Exemplo 11
Comparação entre a capacidade da ativina A e do GDF-8 para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo
Um exemplo anterior mostrou que o GDF-8 é capaz de substituir a ativina A para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo. Foi importante conhecer as potências relativas de GDF-8GDF-8 e ativina A, no que se refere a sua capacidade para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo. Um teste de resposta à dosagem foi conduzido com o uso de concentrações equivalentes de cada fator de
114/247 crescimento, para comparar os resultados durante a diferenciação das células-tronco embrionárias.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL com teor reduzido de fator de crescimento, em meio condicionado com MEF e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de células tronco embrionárias de ser humano foram mantidas com números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao fenótipo cariotípico normal e quanto à ausência de contaminação por micoplasma.
Os aglomerados celulares usados no teste foram uniformemente ressuspensos em meio condicionado com MEF e suplementado com 8 ng/mL de bFGF, e foram semeados sobre placas com 96 poços Packard VIEWPLATES (PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento, em volumes de 100 μΙ/poço. Usou-se um meio condicionado MEF suplementado com 8 ng/ml de bFGF para o plaqueamento inicial e expansão. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2, em uma caixa umidificada por toda a duração do teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta uma alíquota de 100 μΙ do
115/247 meio para teste. As condições de teste foram realizadas em quadruplicate ao longo de um período de teste total de três dias, com alimentação nos dias 1 e 2, mediante aspiração e substituição do meio em cada poço com meio de teste sem uso. Duas cubas de polipropileno com 12 canaletas (Argos 5 Technologies, Inc, Cat. n° B3135) foram usadas para produzir o meio de teste contendo diferentes concentrações de ativina A (PeproTech, Cat. n°120-14) ou GDF-8 (R&D Systems, Cat. n° 788-G8). As canaletas numeradas de 2 a 12 de cada cuba continham 1 ml_ de meio para teste composto de meio RPMI-1640 (Invitrogen, Cat. n°: 22400) suplementado 10 com 2% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (MP Biomedicals, Inc, Cat. n° 152401) e 8 ng/mL de bFGF (PeproTech Inc., Cat. n°: 100-18B), e com 20 ng/mL de Wnt3a (R&D Systems Cat. n° 1324WN/CF) adicionados no dia 1, e omitidos nos dias 2 e 3. A canaleta número 1 de cada cuba continha 1.600 ng/mL de ativina A ou 1.600 ng/mL de GDF15 8, diluídos no mesmo meio para teste. Transferiu-se 1 mL de meio da canaleta número 1 para a canaleta número 2, misturando-se bem. Uma ponta de pipeta sem uso foi usada para transferir um mL do meio da canaleta número 2 ao canal número 3, seguido de misturação cuidadosa. Ο mesmo procedimento foi repetido em sequência até a canaleta número 11, para cada respectiva cuba. A canaleta número 12 de cada cuba continha meio sem ativina A ou GDF-8. Desse modo, criou-se uma série de diluições para teste a duas vezes, contendo ativina A ou GDF-8 a concentrações na faixa de 1,6 ng/mL a 1.600 ng/mL, para adição aos respectivos poços de teste.
Análise de alto conteúdo: na conclusão de três dias de cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma,
Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à
116/247 temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467) diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total de SOX17 em cada poço foram obtidas com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada conjunto de dados quadruplicado. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 4.500. Os dados da intensidade total de SOX17 foram calculados usando-se GraphPad Prism 4.02 (GraphPad Software, Inc., La Jolla, CA, EUA). Os dados foram normalizados para definir os menores e maiores valores em cada conjunto de dados como 0% e 100%, respectivamente. A tabela 11 mostra os valores normalizados para cada um dentre os conjuntos de dados de ativina A e GDF-8. Duas curvas sigmoidais dose-resposta são mostradas na figura 2 conforme geradas com o uso dos valores normalizados mostrados na tabela 11. Os valores de R2, indicando o ajuste de curva, foram calculados com o uso de GraphPad Prism e determinados como sendo 0,9944 para ativina A e 0,9964 para GDF-8. Usando o GraphPad
117/247
Prism, os valores EC50 para cada fator de crescimento foram calculados e determinados como sendo 13,9 ng/mL para a ativina A e 184,8 ng/mL para o GDF-8. Esses dados indicam que o GDF-8 é menos potente que a ativina A, no que se refere a induzir células-tronco embrionárias humanas à diferenciação para células expressoras de marcadores característicos da linhagem de endoderma definitivo. Ainda assim, o GDF-8 pode substituir a ativina A e, a concentrações específicas, pode induzir uma população equivalente de células de endoderma definitivo, conforme denotado pela expressão de SOX17.
Exemplo 12
Células expressoras de marcadores característicos da linhagem de endoderma definitivo, que são formadas de acordo com os métodos da presente invenção, são capazes de diferenciar-se adicionalmente em células expressoras de marcadores característicos da linhagem endócrina pancreática
Populações paralelas de células-tronco embrionárias humanas foram diferenciadas em células expressoras de marcadores característicos da linhagem de endoderma definitivo com o uso de GDF-8 em combinação com o Composto 34 ou o Composto 56. Em seguida, um protocolo de diferenciação gradual foi aplicado às células tratadas para promover a diferenciação para endoderma pancreático e linhagens endócrinas. Um controle paralelo, consistindo em células tratadas com ativina A e Wnt3a, foi mantido para propósitos de comparação durante todo o processo de diferenciação gradual. As amostras foram tomadas a cada estágio da diferenciação, para determinar o aparecimento de biomarcadores para proteínas e mRNA, representativos dos vários estágios de diferenciação.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL® com teor reduzido de fator de crescimento, em meio condicionado com MEF e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição
118/247 das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de células ES humanas foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de micoplasma.
Os aglomerados celulares foram uniformemente ressuspensos em meio condicionado com MEF suplementado com 8 ng/mL de bFGF e semeado sobre as placas de cultura de paredes pretas com 24 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Arctic White, Cat. n° AWLS-303012) em volumes de 0,5 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por toda a duração do teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta uma alíquota (0,5 mL) de meio para teste. As condições de teste para a primeira etapa de diferenciação foram conduzidos ao longo de um período de três dias, com alimentação diária mediante aspiração e substituição do meio de cada poço com meio de teste sem uso. No primeiro dia do teste, 100 ng/mL de ativina A (PeproTech, Cat. n°120-14) ou 200 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) foram adicionados aos respectivos poços de teste nas quais cada fator de crescimento foi diluído em meio RPMI-1640 (Invitrogen, Cat. n° 22400) com 1% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (MP Biomedicals, Inc, Cat. n° 152401), 1% de Probumin (Millipore, Cat. n° 81-068-3) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF). No segundo dia de teste, diluiu-se 100 ng/mL de ativina A ou 200 ng/mL de
119/247
GDF-8 em meio RPMI-1640 suplementado com 2% de FAF BSA sem Wnt3a. Em algumas amostras para teste usando GDF-8, o Wnt3a foi substituído por um Composto 34 ou um Composto 56, a uma concentração de 2,5 μΜ, e um Composto 34 ou um Composto 56 foi adicionado diariamente durante todos os três dias de diferenciação do endoderma definitivo. Na conclusão da primeira etapa de diferenciação, as células de alguns poços foram coletadas para análise de citometria de fluxo, de modo a avaliar os níveis de CXCR4, um marcador de formação de endoderma definitivo. Os poços adicionais foram coletadas para análise RT-PCR, de modo a medir outros marcadores de diferenciação.
Na conclusão da primeira etapa de diferenciação, os conjuntos replicados de poços paralelos de cada grupo de tratamento foram submetidos a uma diferenciação gradual adicional. É importante notar que, após a primeira etapa de diferenciação, todos os poços passando por cultura e diferenciação contínuas receberam o mesmo tratamento. O protocolo para essa diferenciação contínua é descrito abaixo.
A etapa 2 do protocolo de diferenciação foi realizada ao longo de dois dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de meio DMEM:F12 (Invitrogen, Cat. n° 11330-032) contendo 2% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (MP Biomedicals, Inc, Cat. n° 152401), 50 ng/mL de FGF7 (PeproTech, Cat. n° 100-19) e 250 nM de ciclopamina (Calbiochem, Cat. n° 239804).
A etapa 3 do protocolo de diferenciação foi realizada ao longo de quatro dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de glicose com alto teor de DMEM (Invitrogen, Cat. n° 10569) suplementado com 1% de B27 (Invitrogen, Cat. n° 17504-044), 50 ng/mL de FGF7, 100 ng/mL de noguina (R&D Systems, Cat. n° 3344-NG), 250 nM de KAAD-ciclopamina (Calbiochem, Cat. n° 239804) e 2 mM de ácido todotransretinoico (RA) (Sigma-Aldrich, Cat. n° R2625). Na conclusão da terceira etapa de diferenciação, as células de alguns poços foram coletadas para
120/247 análise de RT-PCR, de modo a medir os marcadores de diferenciação. Outros poços de cultura foram submetidos a análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para Pdx1, um fator de transcrição associado ao endoderma pancreático, e Cdx2, um fator de transcrição associado ao endoderma intestinal.
A etapa 4 do protocolo de diferenciação foi realizada ao longo de três dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de glicose com alto teor de DMEM suplementado com 1% de B27, 100 ng/mL de noguina, 100 ng/mL de netrina-4, 1 μΜ de DAPT (EMD Biosciences, Cat. n°565770) e 1 pM de inibidor Alk 5 (Axxora, Cat. n° ALX270-445). Na conclusão da quarta etapa de diferenciação, as células de alguns poços foram coletadas para análise de RT-PCR, de modo a medir os marcadores de diferenciação. Outros poços de cultura foram submetidos a análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para PDX1.
A etapa 5 do protocolo de diferenciação foi realizada ao longo de sete dias em glicose com alto teor de DMEM com 1% de B27 e 1 pM de inibidor Alk 5. O meio em cada poço foi aspirado e substituído por uma alíquota sem uso (0,5 mL) em todos os dias. Na conclusão da quinta etapa de diferenciação, as células de alguns poços foram coletadas para análise de RT-PCR, de modo a medir os marcadores de diferenciação. Outros poços de cultura foram submetidos a análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para insulina e glucagon.
A etapa 6 do protocolo de diferenciação foi realizada ao longo de sete dias em glicose com alto teor de DMEM com 1% de B27. O meio em cada poço foi aspirado e substituído por uma alíquota sem uso (0,5 mL) em dias alternados. Na conclusão da sexta etapa de diferenciação, as células de alguns poços foram coletadas para análise de RT-PCR, de modo a medir os marcadores de diferenciação.
Análise FACS: as células para análise FACS foram bloqueadas em uma solução a 1:5 de 0,5% de gama-globulina humana (Sigma, Cat. n°
121/247
G-4386) em PBS (Invitrogen, Cat. n° 14040-133): tampão corante BD FACS - BSA (BD, Cat. n° 554657) durante 15 minutos a 4°C. As células foram, então, coradas com anticorpos para CD9 PE (BD, Cat. n° 555372), CD99 PE (Caltag, Cat. n° MHCD9904) e CXCR4 APC (R&D Systems, Cat. n° FAB173A) durante 30 minutos a 4°C. Após uma série de lavagens em tampão corante BD FACS, as células foram coradas para viabilidade com 7-AAD (BD, Cat. n° 559925) e analisadas em um BD FACSArray. Um anticorpo de controle de isotipo IgGIK de camundongo, tanto para PE como para APC, foi usado para delimitar a porcentagem de células positivas.
Análise RT-PCR: amostras de RNA foram purificadas mediante ligação a uma membrana de sílica-gel (Rneasy Mini Kit, Qiagen, CA) na presença de um tampão de alta salinidade contendo etanol, seguido de lavagem para remover os contaminantes. O RNA foi adicionalmente purificado com o uso de um kit TURBO isento de DNA (Ambion, INC), e o RNA de alta qualidade foi então eluído em água. O rendimento e a pureza foram avaliados por leituras A260 e A280 em um espectrofotômetro. As cópias de CDNA foram produzidas a partir de RNA purificado com o uso de um kit de arquivo de cDNA de alta capacidade ABI (ABI, CA, EUA).
Exceto onde especificado em contrário, todos os reagentes foram obtidos junto à Applied Biosystems. As reações de PCR em tempo real foram executadas com o uso do sistema de detecção de sequência ABI PRISM® 7900. TAQMAN® UNIVERSAL PCR MASTER MIX® (ABI, CA, EUA) foi usado com 20 ng de RNA transcrito reverso em um volume de reação total de 20 pL. Cada amostra de cDNA foi analisada em duplicata para correção quanto a erros de pipetagem. Os iniciadores e sondas TAQMAN® identificadas com FAM foram usados em concentrações de 200 nM. O nível de expressão para cada gene-alvo foi normalizado com o uso um controle endógeno de gliceraldeído-3-fosfato desidrogenase humana (GAPDH) anteriormente desenvolvido por Applied Biosistemas. Os conjuntos de iniciador e sonda são mencionados na tabela 12. Após uma incubação inicial a 50°C durante 2 min, seguida de 95°C durante 10 min, as amostras foram submetidas 40 vezes a ciclos em dois estágios, sendo uma etapa de
122/247 desnaturação a 95°C durante 15 s seguida de uma etapa de recozimento/extensão a 60°C durante 1 minuto. A análise de dados foi realizada com o uso do software de detecção de sequências GENEAMP®7000 Sequence Detection System. Para cada conjunto de iniciador/ponta de prova, um valor Ct foi determinado como o número de ciclo no qual a intensidade de fluorescência alcançou um valor específico no meio da região exponencial de amplificação. Os níveis de expressão genética relativos foram calculados com o uso do método Ct comparativo. Brevemente, para cada amostra de cDNA, o valor Ct de controle endógeno Ct foi subtraído do gene de interesse Ct para proporcionar o valor de delta Ct (ACt). A quantidade normalizada de alvo foi calculada como 2-ACt, assumindo a amplificação em 100% de eficiência. Os dados finais foram expressos em relação a uma amostra de calibração.
Análise de alto conteúdo: na conclusão da cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467) diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens. Outros anticorpos primários usados para análise incluíram diluição a 1:100 de CDX2 de camundongo anti-humano (Invitrogen, Cat. n° 397800), diluição a 1:100
123/247 de Pdx1 de cabra anti-humano (Santa Cruz Biotechnology, Cat. n° SC14664), diluição a 1:200 de insulina de coelho anti-humano (Cell Signaling, Cat. n° C27C9), e diluição a 1:1500 de glucagon de camundongo antihumano (Sigma-Aldrich, Cat. n° G2654). Os anticorpos secundários usados para análise incluíram diluição a 1:400 de Alexa Fluor 647 IgG de galinha anti-camundongo (Invitrogen, Cat. n° A-21463), diluição a 1:200 de Alexa Fluor 488 IgG de jumento anti-cabra (Invitrogen, Cat. n° A11055), diluição a 1:1000 de Alexa Fluor 647 IgG de galinha anti-coelho (Invitrogen, Cat. n° A21443), e diluição a 1:1000 de Alexa Fluor 488 IgG de galinha anticamundongo (Invitrogen, Cat. n° A21200).
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 4.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo.
Os resultados de PCR para marcadores de diferenciação representativos são mostrados na tabela 13 para células coletadas a partir de cada etapa de diferenciação. As amostras tratadas com GDF-8 e Wnt3a, ou com GDF-8 e Composto 34 ou Composto 56, mostraram níveis de expressão similares ou, em alguns casos, otimizados para marcadores de expressão associados a diferenciação endodérmica e endócrina.
A figura 3 mostra os resultados da análise de FACS, mostrando
124/247 a expressão do marcador de endoderma definitivo, CXCR4, após a primeira etapa de diferenciação. O tratamento de células-tronco embrionárias humanas com GDF-8 e Wnt3a rendeu uma porcentagem equivalente de células positivas para CXCR4, em comparação ao tratamento com ativina A e Wnt3a. De modo similar, o tratamento de células-tronco embrionárias humanas com GDF-8 e uma molécula pequena (Composto 34 ou Composto 56) também rendeu uma porcentagem equivalente ou ligeiramente mais alta de células positivas para CXC4. A figura 4 mostra a análise de imagens de alto conteúdo para expressão de proteína SOX17 normalizada em células-tronco embrionárias humanas, após três dias de diferenciação para endoderma definitivo. Os níveis de expressão para os grupos de tratamento usando GDF-8 com Wnt3a, ou GDF-8 com uma molécula pequena, são similares ao tratamento com ativina A e Wnt3a.
A figura 5 mostra a análise de imagens de alto conteúdo para expressão de proteínas Pdx1 e Cdx2 normalizada em células-tronco embrionárias humanas, após a terceira etapa de diferenciação para endoderma pancreático. Os níveis de expressão para grupos de tratamento usando GDF-8 com Wnt3a, ou GDF-8 com Wnt3a, ou GDF-8 com um composto da presente invenção, mostra níveis equivalentes de PDX1 e CDX2. Em alguns grupos de tratamento, diminuiu o número de células retidas após diferenciação, aumentando assim a razão entre as células que expressam PDX1. Foram obtidos resultados similares mostrando expressão de PDX1 normalizada equivalente em todos os grupos de tratamento após a quarta etapa de diferenciação, conforme mostrado na figura 6. Na figura 7, são mostrados níveis normalizados de proteína para insulina e glucagon, demonstrando expressão equivalente entre os grupos de tratamento com ativina A e com GDF-8.
Esses resultados coletivos demonstram que o GDF-8, em combinação com Wnt3a ou Composto 34 ou Composto 56, pode substituir a ativina A durante a diferenciação do endoderma definitivo e a subsequente diferenciação de endoderma pancreático e endócrino.
125/247
Exemplo 13
Formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo com outros membros da família de proteínas GDF
É importante determinar se o tratamento de células-tronco embrionárias humanas com outros membros da família GDF podería resultar na formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo. Testou-se o Wnt3a, em combinação com o Composto 34 ou o Composto 56, em células-tronco embrionárias humanas em combinação com seis diferentes fatores de crescimento GDF [GDF-3, GDF-5, GDF-8, GDF-10, GDF-11 e GDF-15], para determinara capacidade dos membros da família de proteínas GDF para diferenciar as células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo. Um controle paralelo de células tratadas com ativina A e Wnt3a foi mantido para propósitos de comparação.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), em meio condicionado com MEF e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de células ES humanas foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de micoplasma.
126/247
Os aglomerados celulares foram uniformemente ressuspensos em meio condicionado com MEF e suplementado com 8 ng/mL de bFGF, e foram semeados sobre placas com 96 poços Packard VIEWPLATES (PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento, em volumes de 0,1 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por toda a duração do teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta alíquotas de 100 do meio para teste. As condições de teste foram realizadas em triplicata ao longo de um período de teste total de quatro dias, com alimentação nos dias 1 e 3, mediante aspiração e substituição do meio em cada poço com meio de teste sem uso. Vários membros da família de proteínas GDF foram obtidos para teste conforme exposto a seguir: GDF-3 (PeproTech, Cat. n° 120-22), GDF-5 (DePuy Orthopaedics, Inc., uma empresa Johnson & Johnson), GDF-8 (R&D Systems, Cat. n° 788-G8), GDF-10 (R&D Systems, Cat. n° 1543-BP), GDF11 (PeproTech, Cat. n° 120-11), GDF-15 (R&D Systems, Cat. n° 957GD). No primeiro dia do teste, todas os poços receberam uma alíquota (80 μΙ) de meio basal DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,5% de soro fetal bovino (Hyclone, Cat. n° SH30070.03). Foi criada uma série de cinco amostras diferentes, de controle ou experimentais para teste, a fim de avaliar a ativina A ou vários GDFs em combinação com Wnt3a ou com o Composto 34 ou o Composto 56. Essas amostras para teste foram adicionadas em alíquotas de 20 μΙ (concentradas a 5x) a poços de teste adequadamente combinadas, para produzir um volume de teste final de 100 μΙ em cada poço, nas condições de teste finais indicadas. No primeiro conjunto de amostras de controle, foram testadas as seguintes condições: 1) nenhum aditivo (isto é, nenhum fator de crescimento ou molécula pequena suplementar); 2) 100 ng/mL de ativina A (PeproTech, Cat. n° 120-14) em combinação com 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF); 3) 20 ng/mL de Wnt3a por si só; 4) Composto 34 por si só
127/247 (2,5 μΜ) sem qualquer fator de crescimento ou molécula pequena; 5) Composto 56 por si só (2,5 μΜ) sem qualquer fator de crescimento ou molécula pequena. No segundo conjunto de amostras para teste, as seguintes condições foram testadas em combinação com 100ng/mL de GDF3: 1) nenhum aditivo (isto é, GDF-3 por si só); 2) 20 ng/mL de Wnt3a; 3) 20 ng/mL de Wnt3a com o Composto 34 (2,5 μΜ); 4) Composto 34 (2,5 μΜ); 5) Composto 56 (2,5 μΜ); e 6) 20 ng/mL de Wnt3a com o Composto 56 (2,5 μΜ). No terceiro conjunto de amostras para teste, cada uma das seis condições foi combinada com 100 ng/mL de GDF-5. No quarto conjunto de amostras para teste, cada uma das seis condições foi combinada com 100 ng/mL de GDF-8. No quinto conjunto de amostras para teste, cada uma das seis condições foi combinada com 100 ng/mL de GDF-10. No sexto conjunto de amostras para teste, cada uma das seis condições foi combinada com 100 ng/mL de GDF-11. No sétimo conjunto de amostras para teste, cada uma das seis condições foi combinada com 100 ng/mL de GDF-15. No terceiro dia de teste, todos os poços para todas as amostras para teste, receberam 100 ng/mL de ativina A ou 100 ng/mL do respectivo fator de crescimento GDF, sem Wnt3a ou Composto 34 ou Composto 56, diluído em meio DMEM:F12 suplementado com 2% de FBS.
Análise de alto conteúdo: na conclusão da cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467)
128/247 diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 4.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo.
A figura 8 mostra a análise de imagens de alto conteúdo para expressão de proteína SOX17 em células-tronco embrionárias humanas, após quatro dias de diferenciação para endoderma definitivo. Em cada caso, os resultados são normalizados em relação ao tratamento do controle positivo com ativina A e Wnt3a. Na figura 8A, somente o tratamento do controle positivo rendeu uma expressão significativa de SOX17, sendo que o tratamento com Wnt3a por si só, ou qualquer dos Compostos 34 ou 56 por si sós deixou de induzir a expressão de SOX17. Na figura 8, painéis B a G, são mostrados os níveis de expressão de SOX17 normalizada para cada fator de crescimento GDF substituindo a ativina A nos respectivos tratamentos. GDF-3 (figura 8B) e GDF-5 (figura 8C) induziram uma expressão fraca de SOX17, e somente em amostras para teste nas quais estava presente um dos compostos da presente invenção. GDF10 (figura
129/247
8D), GDF11 (figura 8E) e GDF15 (figura 8G) induziram níveis significativos de expressão de SOX17, mais do que foi observado em tratamentos com GDF3 ou 5, porém menos do que foi observado em tratamentos com ativina A e Wnt3a. Em geral, a expressão de SOX17 foi desprezível quando GDF10, GDF-11 ou GDF-15 foi combinado com Wnt3a, mas melhorou em combinação com um dos compostos da presente invenção, em particular quando combinado ao Composto 34. A figura 8D mostra os resultados para os grupos de tratamento usando GDF-8, nos quais o GDF-8 em combinação com o Composto 34 ou o Composto 56 causou uma indução robusta de SOX17, excedendo os resultados observados no controle positivo de ativina A/Wnt3a. Em alguns desse exemplos, a presença do Composto 34 ou do Composto 56, em combinação com um fator de crescimento GDF, também causou um aumento no número de células durante a diferenciação.
Esses resultados coletivos demonstram que o GDF-8 foi superior a todos os demais membros da família GDF testados, quando usado em combinação com o Composto 34 ou o Composto 56, e poderia substituir a ativina A durante a diferenciação do endoderma definitivo.
Exemplo 14
Formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo com outros membros da superfamília de proteínas TGF
É importante determinar se o tratamento de células-tronco embrionárias humanas com outros membros da superfamília TGF poderia facilitar a formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo. O Composto 34 e Wnt3a foram testados em células-tronco embrionárias humanas em combinação com TGFp-1, BMP2, BMP3 ou BMP4, para determinar a capacidade dos membros da superfamília TGF para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo. Em paralelo, duas fontes comerciais diferentes de GDF-8 foram testadas com Wnt3a quanto à sua capacidade para diferenciar células-tronco embrionárias humanas em células expressoras de marca130/247 dores característicos da linhagem de endoderma definitivo. Um controle positivo usando-se ativina A com Wnt3a foi mantido para propósitos de comparação.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), em meio condicionado com MEF e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de célula-tronco embrionária humana foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de micoplasma.
Os aglomerados celulares foram uniformemente ressuspensos em meio condicionado com MEF e suplementado com 8 ng/mL de bFGF, e foram semeados sobre placas com 96 poços Packard VIEWPLATES (PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento, em volumes de 0,1 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por todo o teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta alíquotas de 100 do meio para teste. As condições de teste foram realizadas em triplicata ao longo de um período de teste total de três dias, com alimentação nos dias 1 e 2, mediante
131/247 aspiração e substituição do meio em cada poço com meio de teste sem uso. Vários proteínas de fator de crescimento foram obtidas para teste, conforme exposto a seguir: BMP-2 (R&D Systems, Cat. n° 355-BM); BMP-3 (R&D Systems, Cat. n° 113-BP); BMP-4 (R&D Systems, Cat. n° 314-BP); ΤΟΡβ-1 (R&D Systems, Cat. n° 240-B); GDF-8 (PeproTech, Cat. n° 120-00); GDF-8 (Shenandoah, Cat. n° 100-22); e ativina A (PeproTech, Cat. n° 120-14). No primeiro dia do teste, cada poço foi tratado com 80 pl de meio de crescimento [RPMI-1640 (Invitrogen, Cat. n° 22400) contendo 2,5% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (MP Biomedicals, Inc, Cat. n° 152401) e 10 ng/mL de bFGF], Em alguns poços, adicionou-se 25 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF) ao meio de crescimento, para produzir uma concentração final de teste de 20 ng/mL. Em alguns poços, adicionou-se ativina A ao meio de crescimento, para produzir uma concentração final de teste de 100 ng/mL. Em alguns poços, adicionou-se 3,125 μΜ de Composto 34 ao meio de crescimento, para produzir uma concentração final de teste de 2,5 μΜ. Uma titulação de dose de fatores de crescimento adicionais (concentrada 5x, diluída em RPMI-1640) também foi adicionada aos respectivos poços de teste, para produzir um volume de teste final de 100 μΙ em cada poço, para todas as condições de tratamento. No segundo dia de teste, o Wnt3a e o Composto 34 foram omitidos do teste. Todos os poços receberam 80 μΙ de meio de crescimento [RPMI-1640 contendo 2,5% de FAF BSA e 10 ng/mL de bFGF] e 20 μΙ da respectiva diluição de fator de crescimento (concentrada 5x, diluída em RPMI-1640). Os controles comparativos para esse teste incluíam: 1) nenhum fator de crescimento adicionado; 2) Wnt3a por si só; e 3) ativina A com Wnt3a. Cada fonte comercial de GDF-8 foi testada em combinação com Wnt3a. Cada um dos fatores de crescimento BMP, bem como ΤΟΡβ-1, foi testado em combinação com Wnt3a, com o Composto 34, e com Wnt3a em combinação com o Composto 34.
Análise de alto conteúdo: na conclusão da cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à
132/247 temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467) diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 4.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo.
A figura 9 mostra a análise de imagens de alto conteúdo para expressão de proteína SOX17 em células-tronco embrionárias humanas, após três dias de diferenciação para endoderma definitivo. Em cada caso, os
133/247 resultados são normalizados em relação ao tratamento do controle positivo com ativina A e Wnt3a. Os resultados na figura 9A mostram que o tratamento com o meio de crescimento por si só, ou com Wnt3a por si só, deixou de induzir a expressão de SOX17, sendo que somente a adição de ativina A causou uma expressão robusta de SOX17. Na figura 9, painéis B e C, são representados os resultados para cada uma das fontes comerciais de GDF-8, mostrando diferenças de potência entre os dois fornecedores. Embora menos potente que a ativina A, houve indução significativa da expressão de SOX17 nas células tratadas com GDF-8 em combinação com Wnt3a. Na figura 9, painéis D, E, F e G, são mostrados resultados para a diferenciação do endoderma definitivo com o uso de BMP2, BMP3, BMP4 e TGFP-1, incorporando-se uma titulação de dose para cada fator de crescimento em combinação com Wnt3a, ou o Composto 34, ou Wnt3a juntamente com o Composto 34. Embora alguns tratamentos tenham apresentado um efeito significativo sobre os números de células na conclusão do teste (por exemplo BMP2 e BMP4), a indução da expressão de SOX17 resultante de qualquer dessas combinações de fatores de crescimento e tratamentos foi fraca ou desprezível em comparação ao tratamento com Wnt3a por si só.
Exemplo 15
Estudo de faixas de dose para a formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo com uma seleção dos compostos da presente invenção
É importante conhecer as concentrações ótimas de trabalho para o Composto 181, o Composto 180, o Composto 19, o Composto 202, o Composto 40 e o Composto 34, que poderíam mediar a formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo. Em conjunto, foram realizadas comparações lado a lado para titulações de cada composto em combinação com ativina A ou GDF-8 no teste de endoderma definitivo. Finalmente, a duração da exposição para cada composto foi testada nos ensaios, também em combinação com ativina A ou GDF-8, adicionando o composto somente no primeiro dia do teste ou
134/247 ao longo de todos os três dias de formação de endoderma definitivo.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), em meio condicionado com MEF suplementado com 8 ng/mL de bFGF (PeproTech Inc., Cat. n° 10018B) e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletarse um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de célula-tronco embrionária humana foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de micoplasma.
Os aglomerados celulares foram uniformemente ressuspensos em meio condicionado com MEF e suplementado com 8 ng/mL de bFGF, e foram semeados sobre placas com 96 poços Packard VIEWPLATES (PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento, em volumes de 0,1 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por toda a duração do teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta alíquotas de 100 do meio para teste. As condições de teste foram realizadas em quadruplicata ao longo de um período de teste total de quatro dias, com alimentação diária mediante aspiração e substituição do meio em cada poço com meio de teste sem uso.
135/247
Cada poço foi tratado com 80 μΙ de meio de crescimento [RPMI-1640 (Invitrogen, Cat. n° 22400) contendo 2,5% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (MP Biomedicals, Inc, Cat. n° 152401), 10 ng/mL de bFGF e fatores de crescimento adicionais (concentrados a 1,25x)J e 20 μΙ do composto de teste (concentrado a 5x e diluído em RPMI1640) para produzir um volume de teste final de 100 ul em cada poço. Os compostos para teste neste ensaio incluíam seis dos compostos da presente invenção: Composto 181, Composto 180, Composto 19, Composto 202, Composto 40 e Composto 34, bem como um inibidor GSK3i BIO comercialmente disponível (EMD Chemicals, Inc., Cat. n° 361550). No primeiro dia do teste, os poços foram tratados com vários controles ou condições experimentais. As condições de controle, com concentrações finais de teste conforme indicadas, eram conforme exposto a seguir: 1) meio de crescimento por si só; 2) somente 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF); 3) 100 ng/mL de ativina A (PeproTech, Cat. n° 120-14); 4) 100 ng/mL de ativina A e 20 ng/mL de Wnt3a; 5) 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8); 6) 100 ng/mL GDF-8 e 20 ng/mL de Wnt3a. Os compostos para teste foram diluídos duas vezes em série, para produzir uma faixa de concentração de 78 nM a 10 μΜ no teste final. As amostras para teste experimentais combinavam cada série de diluição do composto individual com 100 ng/mL de ativina A ou 100 ng/mL de GDF-8, sendo ambos os conjuntos de tratamento na ausência de Wnt3a. No segundo e no terceiro dias do teste, alguns poços continuaram a ser tratados com 20 ng/mL de Wnt3a ou com o composto de teste diluído em combinação com ativina A ou GDF-8. Em outros poços, o tratamento com ativina A ou GDF-8 continuou no segundo e no terceiro dias de teste, mas removeu-se o Wnt3a ou o composto de teste diluído.
Análise de alto conteúdo: na conclusão da cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2)
136/247 durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467) diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos for determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 4.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo.
Resultados: os resultados da análise de alto conteúdo são mostrados para a expressão de SOX17 nas figuras 10 a 14, e o número de células resultante na conclusão do teste é mostrado nas figuras 15 a 19. Na figura 10, os resultados são mostrados para a expressão de SOX 17 resultante dos tratamentos de controle usando ativina A ou GDF-8, por si sós
137/247 ou em combinação com Wnt3a. Os tratamentos com ativina A resultaram em uma expressão de SOX17 significativamente mais alta do que a observada no tratamento com GDF-8. De modo similar, conforme visto na figura 15, o tratamento com ativina A resultou em um número mais alto de células na conclusão do teste do que o observado no tratamento com GDF-8, independentemente da presença do Wnt3a por um ou três dias durante o teste. A adição de qualquer um dentre os Compostos 181, 180, 19, 202, 40 ou 34 ao tratamento com ativina A não otimizou a expressão de SOX17 (figuras 11 a 12), nem aumentou o número de células (figuras 17 a 18), independentemente de o composto ter estado presente durante um dia no início do teste, ou durante três dias por toda a duração do teste. Entretanto, o tratamento com um dentre os Compostos 181, 180, 19, 202, 40 ou 34 em combinação com GDF-8 aprimorou significativamente a expressão de SOX17 (figuras 13 a 14), além de aumentar também o número de células no final do teste (figuras 18 a 19). Quando um dos Compostos 181, 180, 19, 202, 40 ou 34 foi usado em combinação com o GDF-8, a otimização da expressão de SOX17 e do número de células foi, em muitos casos, equivalente aos resultados observados no tratamento com ativina A. A melhor diferenciação na combinação com GDF-8 ficou evidente em um efeito de titulação de dose para muitos dos compostos, embora por vezes fosse observada toxicidade nas concentrações mais altas. Na maioria dos casos, os melhores efeitos benéficos do tratamento com o composto e o GDF-8 ficaram evidentes com somente um dia de exposição ao composto, no início do teste. Em alguns casos, a presença do composto ao longo da duração do teste não teve qualquer efeito prejudicial, ou teve um efeito ligeiramente benéfico. A partir desses resultados coletivos, foi determinada uma faixa de concentrações funcionais ótimas para cada composto em combinação com o tratamento por GDF8. Os resultados foram específicos para cada composto, geralmente na faixa de 1 a 10 μΜ, conforme testado neste ensaio.
Exemplo 16
Células expressoras de marcadores característicos da linhagem
138/247 de endoderma definitivo, que são formadas sem estar de acordo com os métodos da presente invenção, são capazes de diferenciar-se adicionalmente em células expressoras de marcadores característicos da linhagem endócrina pancreática
Moléculas pequenas adicionais foram testadas em combinação com GDF-8 para diferenciação do endoderma definitivo. Estas incluíram um inibidor de GSK3 comercialmente disponível, bem como compostos da presente invenção. Um protocolo de diferenciação gradual foi aplicado a células tratadas com GDF-8 em combinação com várias moléculas pequenas. A eficácia da diferenciação foi determinada por expressão gênica para biomarcadores representativos do endoderma pancreático, ou de linhagens endócrinas pancreáticas. Uma amostra de controle paralela de células tratadas com ativina A e Wnt3a foi mantida para propósitos de comparação durante todo o processo de diferenciação gradual.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL™ com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), em meio condicionado com MEF e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de célula-tronco embrionária humana foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de micoplasma.
Os aglomerados celulares foram uniformemente ressuspensos
139/247 em meio condicionado com MEF suplementado com 8 ng/mL de bFGF e folheado sobre as placas de cultura de paredes pretas com 24 poços revestidas por MATRIGEL com teor reduzido de fator de crescimento (Arctic White, Cat n° AWLS-303012) em volumes de 0,5 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por toda a duração do teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta uma alíquota (0,5 mL) de meio para teste. As condições de teste para a primeira etapa de diferenciação foram conduzidos ao longo de um período de três dias, com alimentação diária mediante aspiração e substituição do meio de cada poço com meio de teste sem uso. No primeiro dia do teste, 100 ng/mL de ativina A (PeproTech, Cat. n°120-14) ou 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) foram adicionados aos respectivos poços de teste nas quais cada fator de crescimento foi diluído em meio RPMI-1640 (Invitrogen, Cat. n° 22400) com 2% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (Proliant Inc., Cat n° SKU 68700) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF). No segundo dia de teste, diluiu-se 100 ng/mL de ativina A ou 100 ng/mL de GDF-8 em meio RPMI-1640 suplementado com 2% de FAF BSA sem Wnt3a. Em algumas amostras para teste usando GDF-8, o Wnt3a foi substituído por um composto de moléculas pequenas, adicionado somente no primeiro dia da diferenciação do endoderma definitivo. Essas moléculas pequenas incluíam o Composto 19 (2,5 μΜ no teste), o Composto 202 (2,5 pM no teste), o Composto 40 (2,5 pM no teste), ou um inibidor de GSK3 BIO disponível comercialmente (0,5 pM no teste) (EMD Chemicals, Inc., Cat. n° 361550). Na conclusão da primeira etapa de diferenciação, as células de alguns poços foram coletados para análise de citometria de fluxo, de modo a avaliar os níveis de CXCR4, um marcador de formação de endoderma definitivo. Os poços adicionais foram coletados para análise RT-PCR, de modo a medir outros marcadores de diferenciação.
140/247
Na conclusão da primeira etapa de diferenciação para endoderma definitivo, os conjuntos replicados de poços paralelos de cada grupo de tratamento foram submetidos a uma diferenciação gradual adicional. É importante notar que, após a primeira etapa de diferenciação, todas os poços passando por cultura e diferenciação subsequente receberam o mesmo tratamento. O protocolo para essa diferenciação contínua é descrito abaixo.
A etapa 2 do protocolo de diferenciação foi realizada ao longo de dois dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de meio DMEM:F12 (Invitrogen, Cat n° 11330-032) contendo 2% de FAF BSA, 50 ng/mL de FGF7 (PeproTech, Cat. n° 100-19) e 250 nM de ciclopamina-KAAD (Calbiochem, Cat. n° 239804).
A etapa 3 do protocolo de diferenciação foi realizada ao longo de sete dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de glicose com alto teor de DMEM (Invitrogen, Cat. n° 10569) suplementada com 0,1% de Albumax (Invitrogen, Cat. n° 11020-021), 0,5x de insulina-transferrina-selênio (ITS-X, Invitrogen, Cat. n° 51500056), 50 ng/mL de FGF7, 100 ng/mL de noguina (R&D Systems, Cat. n° 3344NG), 250 nM KAAD-ciclopamina, e 2 pM ácido todo-transretinoico (RA) (Sigma-Aldrich, Cat. n° R2625). Na conclusão da terceira etapa de diferenciação, as células de alguns poços foram coletadas para análise de RT-PCR, de modo a medir os marcadores de diferenciação. Outros poços de cultura foram submetidos a análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para Pdx1 e Cdx2.
A etapa 4 do protocolo de diferenciação foi realizada ao longo de três dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de glicose com alto teor de DMEM suplementada com 0,1% de Albumax, 0,5x de insulina-transferrina-selênio, 100 ng/mL de noguina e 1 pM de inibidor Alk 5 (Axxora, Cat. n° ALX-270-445). Na conclusão da quarta
141/247 etapa de diferenciação, as células de alguns poços foram coletadas para análise de RT-PCR, de modo a medir os marcadores de diferenciação.
Outros poços de cultura foram submetidos a análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para Pdx1.
A etapa 5 do protocolo de diferenciação foi realizada ao longo de sete dias em glicose com alto teor de DMEM com 0,1% de Albumax, 0,5x de insulina-transferrina-selênio e 1 μΜ de inibidor Alk 5. O meio em cada poço foi aspirado e substituído por uma alíquota sem uso (0,5 mL) em todos os dias. Na conclusão da quinta etapa de diferenciação, as células de alguns poços foram coletados para análise de RT-PCR, de modo a medir os marcadores de diferenciação. Outros poços de cultura foram submetidos à análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para insulina e glucagon.
Análise FACS: as células para análise FACS foram bloqueadas em uma solução a 1:5 de 0,5% de gama-globulina humana (Sigma, Cat. n° G-4386) em PBS (Invitrogen, Cat. n° 14040-133): tampão corante BD FACS - BSA (BD, Cat. n° 554657) durante 15 minutos a 4°C. As células foram, então, coradas com anticorpos para CD9 PE (BD, Cat. n° 555372), CD99 PE (Caltag, Cat. n° MHCD9904) e CXCR4 APC (R&D Systems, Cat. n° FAB173A) durante 30 minutos a 4°C. Após uma série de lavagens em tampão corante BD FACS, as células foram coradas para viabilidade com 7AAD (BD, Cat. n° 559925) e analisadas em um BD FACSArray. Um anticorpo de controle de isotipo IgGIK de camundongo, tanto para PE como para APC, foi usado para delimitar a porcentagem de células positivas.
Análise RT-PCR: amostras de RNA foram purificadas mediante ligação a uma membrana de sílica-gel (Rneasy Mini Kit, Qiagen, CA) na presença de um tampão de alta salinidade contendo etanol, seguido de lavagem para remover os contaminantes. O RNA foi adicionalmente purificado com o uso de um kit TURBO isento de DNA (Ambion, INC), e o RNA de alta qualidade foi então eluído em água. O rendimento e a pureza foram avaliados por leituras A260 e A280 em um espectrofotômetro. As cópias de CDNA foram produzidas a partir de RNA purificado com o uso de um kit de
142/247 arquivo de cDNA de alta capacidade ABI (ABI, CA, EUA).
Exceto onde especificado em contrário, todos os reagentes foram obtidos junto à Applied Biosystems. As reações de PCR em tempo real foram executadas com o uso do sistema de detecção de sequência ABI PRISM® 7900. TAQMAN® UNIVERSAL PCR MASTER MIX® (ABI, CA, EUA) foi usado com 20 ng de RNA transcrito reverso em um volume de reação total de 20 pL. Cada amostra de cDNA foi analisada em duplicata para correção quanto a erros de pipetagem. Os iniciadores e sondas TAQMAN® identificadas com FAM foram usados em concentrações de 200 nM. O nível de expressão para cada gene-alvo foi normalizado com o uso um controle endógeno de gliceraldeído-3-fosfato desidrogenase humana (GAPDH) anteriormente desenvolvido por Applied Biosistemas. Os conjuntos de iniciador e sonda são mencionados na tabela 12. Após uma incubação inicial a 50°C durante 2 min, seguida de 95°C durante 10 min, as amostras foram submetidas 40 vezes a ciclos em dois estágios, sendo uma etapa de desnaturação a 95°C durante 15 s seguida de uma etapa de recozimento/extensão a 60°C durante 1 minuto. A análise de dados foi realizada com o uso do software de detecção de sequências GENEAMP®7000 Sequence Detection System. Para cada conjunto de iniciador/ponta de prova, um valor Ct foi determinado como o número de ciclo no qual a intensidade de fluorescência alcançou um valor específico no meio da região exponencial de amplificação. Os níveis de expressão genética relativos foram calculados com o uso do método Ct comparativo. Brevemente, para cada amostra de cDNA, o valor Ct de controle endógeno Ct foi subtraído do gene de interesse Ct para proporcionar o valor de delta Ct (ACt). A quantidade normalizada de alvo foi calculada como 2-ACt, assumindo a amplificação em 100% de eficiência. Os dados finais foram expressos em relação a uma amostra de calibração.
Análise de alto conteúdo: na conclusão da cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com
143/247
PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467) diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 pl/poço de PBS para formação de imagens. Outros anticorpos primários usados para análise incluíram diluição a 1:200 de insulina de coelho anti-humano (Cell Signaling, Cat. n° C27C9) e diluição a 1:1.500 de glucagon de camundongo anti-humano (Sigma-Aldrich, Cat. n° G2654). Os anticorpos secundários usados para análise incluíram diluição a 1:1.000 de Alexa Fluor 647 IgG de galinha anti-coelho (Invitrogen, Cat. n° A21443) e diluição a 1:1000 de Alexa Fluor 488 IgG de galinha anti-camundongo (Invitrogen, Cat. n° A21200).
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação
144/247 das faixas de escala de tons cinza entre 200 e 4.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo.
Os resultados de PCR para marcadores de diferenciação representativos são mostrados na tabela 14 para células coletadas a partir de cada etapa de diferenciação. As amostras tratadas com GDF-8 e Wnt3a, ou com GDF-8 e uma molécula pequena, mostraram níveis de expressão similares para marcadores associados à diferenciação endodérmica e endócrina.
A figura 20, painel A mostra a análise de FACS para o marcador de endoderma definitivo, CXCR4, após a primeira etapa de diferenciação. O tratamento de células-tronco embrionárias humanas com GDF-8 e Wnt3a rendeu uma porcentagem similar de células positivas para CXCR4, em comparação ao tratamento com ativina A e Wnt3a. O tratamento de células-tronco embrionárias humanas com GDF-8 e um composto da presente invenção (Composto 19, Composto 202, Composto 40 ou inibidor GSK3 IX BIO) também rendeu uma porcentagem equivalente ou ligeiramente mais alta de células positivas para CXC4. A figura 20, painel B mostra a análise de imagens de alto conteúdo para expressão de proteína SOX17 normalizada em células-tronco embrionárias humanas, após três dias de diferenciação para endoderma definitivo. Em alguns casos, o tratamento com GDF-8 resultou em um número de células mais baixo na conclusão da primeira etapa de diferenciação. Entretanto, o tratamento com GDF-8 em combinação com Wnt3a ou com os inibidores de molécula pequena claramente induziu a expressão de SOX17, um marcador de endoderma definitivo. Em um exemplo, o tratamento com GDF-8 e o Composto 40 rendeu um número de células em cultura e uma expressão de SOX17 equivalentes ao tratamento com ativina A e Wnt3a.
A figura 20, painel C, mostra a análise de imagens de alto conteúdo para números relativos de células recuperadas de culturas tratadas por meio da etapa de diferenciação 5. Conforme observado anteriormente, ao final da etapa 1, alguns tratamentos causaram uma queda na recupe
145/247 ração celular em relação ao tratamento com ativina A e Wnt3a. Essa diminuição no número de células foi observada, especificamente, em grupos de tratamento usando GDF-8 com inibidor GSK3 BIO, e também usando GDF-8 com o Composto 19. Os grupos de tratamento com GDF-8 adicionais apresentaram recuperação celular similar à do tratamento com activin A e Wnt3a. Na figura 20, painéis D a F, são mostrados os níveis normalizados de proteína para insulina e glucagon, juntamente com sua respectiva razão em cada grupo de tratamento. Níveis similares de insulina e glucagon poderíam ser obtidos em cada um dos tratamentos com GDF-8, em relação ao tratamento com ativina A e Wnt3a, demonstrando que o GDF-8, em combinação com Wnt3a ou uma molécula pequena, pode substituir a ativina A durante a diferenciação do endoderma definitivo e a subsequente diferenciação de endoderma pancreático e endócrino.
Exemplo 17
Células expressoras de marcadores característicos da linhagem de endoderma definitivo, gue são formadas com o uso de GDF-8 e um composto da presente invenção, são capazes de diferenciar-se adicionalmente em células expressoras de marcadores característicos da linhagem endócrina pancreática
Moléculas pequenas adicionais foram testadas em combinação com GDF-8 e ativina A para diferenciação do endoderma definitivo. Estas incluíram um inibidor de GSK3 comercialmente disponível, bem como os compostos da presente invenção. Um protocolo de diferenciação gradual foi aplicado a células tratadas com GDF-8 em combinação com várias moléculas pequenas. A eficácia da diferenciação foi determinada por expressão gênica para biomarcadores representativos do endoderma pancreático e de linhagens endócrinas pancreáticas. Uma amostra de controle paralela de células tratadas com ativina A e Wnt3a foi mantida para propósitos de comparação durante todo o processo de diferenciação gradual.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferen
146/247 ciado sobre placas revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), em meio condicionado com MEF suplementado com 8 ng/mL de bFGF (PeproTech Inc., Cat. n° 10018B) e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de células ES humanas foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de micoplasma.
Os aglomerados celulares foram uniformemente ressuspensos em meio condicionado com MEF suplementado com 8 ng/mL de bFGF e folheado sobre as placas de cultura de paredes pretas com 24 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento (Arctic White, Cat n° AWLS-303012) em volumes de 0,5 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por todo o teste.
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta uma alíquota (0,5 mL) de meio para teste. As condições de teste para a primeira etapa de diferenciação foram conduzidos ao longo de um período de três dias, com alimentação diária mediante aspiração e substituição do meio de cada poço com meio de teste sem uso. No primeiro dia do teste, 100 ng/mL de ativina A (PeproTech, Cat. n° 120-14) ou 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) foram adicionados aos respectivos poços de teste nas quais cada fator de crescimento foi diluído em meio RPMI-1640 (Invitrogen, Cat. n° 22400) com
147/247
2% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (MP Biomedicals, Inc; Cat # 152401). Em algumas amostras, incluiu-se também 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF). No segundo dia de teste, diluiu-se 100 ng/mL de ativina A ou 100 ng/mL de GDF-8 em meio RPMI-1640 suplementado com 2% de FAF BSA, omitindo-se o Wnt3a de todas as amostras. Em algumas amostras para teste usando GDF-8, o Wnt3a foi substituído por uma determinada concentração de composto de moléculas pequenas, adicionado somente no primeiro dia da diferenciação do endoderma definitivo. Essas moléculas pequenas incluíam: Composto 181 (1,25 μΜ no teste), Composto 180 (2,5 μΜ no teste), Composto 19 (10 μΜ no teste), Composto 202 (2,5 μΜ no teste), Composto 40 (5 μΜ no teste), Composto 34 (2,5 μΜ no teste), Composto 206 (2,5 μΜ no teste), e um inibidor GSK3 IX BIO disponível comercialmente (10 μΜ no teste) (EMD Chemicals, Inc., Cat. n° 361550). Na conclusão da primeira etapa de diferenciação, as células de alguns poços foram coletadas para análise de citometria de fluxo, de modo a avaliar os níveis de CXCR4, um marcador de formação de endoderma definitivo. Os poços adicionais foram coletadas para análise RT-PCR, de modo a medir outros marcadores de diferenciação.
Na conclusão da primeira etapa de diferenciação para endoderma definitivo, os conjuntos replicados de poços paralelos de cada grupo de tratamento foram submetidos a uma diferenciação gradual adicional. É importante notar que, após a primeira etapa de diferenciação, todos os poços passando por cultura e diferenciação subsequente receberam o mesmo tratamento. O protocolo para essa diferenciação contínua é descrito abaixo.
A etapa 2 do protocolo de diferenciação foi realizada ao longo de dois dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de meio DMEM:F12 (Invitrogen, Cat. n° 11330-032) contendo 2% de FAF BSA, 50 ng/mL de FGF7 (PeproTech, Cat. n° 100-19) e 250 nM de ciclopamina-KAAD (Calbiochem, Cat. n° 239804).
A etapa 3 do protocolo de diferenciação foi realizada ao longo de
148/247 quatro dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de glicose com alto teor de DMEM (Invitrogen, Cat. n° 10569) suplementada com 0,1% de Albumax (Invitrogen, Cat. n° 11020-021), 0,5x de insulina-transferrina-selênio (ITS-X, Invitrogen, Cat. n° 51500056), 50 ng/mL de FGF7, 100 ng/mL de noguina (R&D Systems, Cat. n° 3344-NG), 250 nM KAAD-ciclopamina, e 2 mM ácido todo-transretinoico (RA) (SigmaAldrich, Cat. n° R2625). Na conclusão da terceira etapa de diferenciação, as células de alguns poços foram coletados para análise de RT-PCR, de modo a medir os marcadores de diferenciação.
A etapa 4 do protocolo de diferenciação foi realizada ao longo de três dias. As células foram alimentadas diariamente mediante aspiração do meio de cada poço, substituindo-se o mesmo por uma alíquota sem uso (0,5 mL) de glicose com alto teor de DMEM suplementada com 0,1% de Albumax, 0,5x de insulina-transferrina-selênio, 100 ng/mL de noguina e 1 μΜ de inibidor Alk 5 (Axxora, Cat. n° ALX-270-445). Na conclusão da quarta etapa de diferenciação, as células de alguns poços foram coletados para análise de RT-PCR, de modo a medir os marcadores de diferenciação.
A etapa 5 do protocolo de diferenciação foi realizada ao longo de sete dias em glicose com alto teor de DMEM com 0,1% de Albumax, 0,5x de insulina-transferrina-selênio e 1 μΜ de inibidor Alk 5. O meio em cada poço foi aspirado e substituído por uma alíquota sem uso (0,5 mL) em todos os dias. Na conclusão da quinta etapa de diferenciação, as células de alguns poços foram coletados para análise de RT-PCR, de modo a medir os marcadores de diferenciação. Outros poços de cultura foram submetidos a análise de imagens de alto conteúdo quanto a níveis de expressão de proteína para insulina e glucagon.
Análise FACS: as células para análise FACS foram bloqueadas em uma solução a 1:5 de 0,5% de gama-globulina humana (Sigma, Cat. n° G-4386) em PBS (Invitrogen, Cat. n° 14040-133): tampão corante BD FACS - BSA (BD, Cat. n° 554657) durante 15 minutos a 4°C. As células foram, então, coradas com anticorpos para CD9 PE (BD, Cat. n° 555372), CD99 PE
149/247 (Caltag, Cat. n° MHCD9904) e CXCR4 APC (R&D Systems, Cat. n° FAB173A) durante 30 minutos a 4°C. Após uma série de lavagens em tampão corante BD FACS, as células foram coradas para viabilidade com 7AAD (BD, Cat. n° 559925) e analisadas em um BD FACSArray. Um anticorpo de controle de isotipo IgGIK de camundongo, tanto para PE como para APC, foi usado para delimitar a porcentagem de células positivas.
Análise RT-PCR: amostras de RNA foram purificadas mediante ligação a uma membrana de sílica-gel (Rneasy Mini Kit, Qiagen, CA) na presença de um tampão de alta salinidade contendo etanol, seguido de lavagem para remover os contaminantes. O RNA foi adicionalmente purificado com o uso de um kit TURBO livre de DNA (Ambion, INC), e o RNA de alta qualidade foi então eluído em água. O rendimento e a pureza foram avaliados por leituras A260 e A280 em um espectrofotômetro. As cópias de CDNA foram produzidas a partir de RNA purificado com o uso de um kit de arquivo de cDNA de alta capacidade ABI (ABI, CA, EUA).
Exceto onde especificado em contrário, todos os reagentes foram obtidos junto à Applied Biosystems. As reações de PCR em tempo real foram executadas com o uso do sistema de detecção de sequência ABI PRISM® 7900. TAQMAN® UNIVERSAL PCR MASTER MIX® (ABI, CA, EUA) foi usado com 20 ng de RNA transcrito reverso em um volume de reação total de 20 pL. Cada amostra de cDNA foi analisada em duplicata para correção quanto a erros de pipetagem. Os iniciadores e sondas TAQMAN® identificadas com FAM foram usados em concentrações de 200 nM. O nível de expressão para cada gene alvo foi normalizado com o uso um controle endógeno de gliceraldeído-3-fosfato desidrogenase humana (GAPDH) anteriormente desenvolvido por Applied Biosistemas. Os conjuntos de iníciador e sonda são mencionados na tabela 12. Após uma incubação inicial a 50°C durante 2 min, seguida de 95°C durante 10 min, as amostras foram submetidas 40 vezes a ciclos em dois estágios, sendo uma etapa de desnaturação a 95°C durante 15 s seguida de uma etapa de recozimento/extensão a 60°C durante 1 minuto. A análise de dados foi realizada com o uso do software de detecção de sequências GENEAMP®7000 Sequence
150/247
Detection System. Para cada conjunto de iniciador/ponta de prova, urn valor Ct foi determinado como o número de ciclo no qual a intensidade de fluorescência alcançou um valor específico no meio da região exponencial de amplificação. Os níveis de expressão genética relativos foram calculados com o uso do método Ct comparativo. Brevemente, para cada amostra de cDNA, o valor Ct de controle endógeno Ct foi subtraído do gene de interesse Ct para proporcionar o valor de delta Ct (ACt). A quantidade normalizada de alvo foi calculada como 2-ACt, assumindo a amplificação em 100% de eficiência. Os dados finais foram expressos em relação a uma amostra de calibração.
Análise de alto conteúdo: na conclusão da cultura, as placas de teste foram lavadas uma vez com PBS (Invitrogen, Cat. n° 14190), fixas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha, e adicionado a cada poço durante duas horas, à temperatura ambiente. Após lavar três vezes com PBS, adicionou-se a cada poço o anticorpo secundário conjugado Alexa Fluor 488 (galinha anti-cabra IgG, Invitrogen, Cat. n° A21467) diluído a 1:200 em PBS. Para contracorar os núcleos, adicionou-se 5 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante quinze minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens. Outros anticorpos primários usados para análise incluíram diluição a 1:100 de CDX2 de camundongo anti-humano (Invitrogen, Cat. n° 397800), diluição a 1:100 de Pdx1 de cabra anti-humano (Santa Cruz Biotechnology, Cat. n° SC-14664), diluição a 1:200 de insulina de coelho anti-humano (Cell Signaling, Cat. n° C27C9), e diluição a 1:1500 de glucagon de camundongo anti-humano
151/247 (Sigma-Aldrich, Cat. n° G2654). Os anticorpos secundários usados para análise incluíram diluição a 1:400 de Alexa Fluor 647 IgG de galinha anticamundongo (Invitrogen, Cat. n° A-21463), diluição a 1:200 de Alexa Fluor 488 IgG de jumento anti-cabra (Invitrogen, Cat. n° A11055), diluição a 1:1000 de Alexa Fluor 647 IgG de galinha anti-coelho (Invitrogen, Cat. n° A21443), e diluição a 1:1000 de Alexa Fluor 488 IgG de galinha anticamundongo (Invitrogen, Cat. n° A21200).
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Foram capturadas imagens de 25 campos por poço. As medições quanto à intensidade total foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total de proteína foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de tons cinza entre 200 e 4.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo.
Resultados: os resultados para os marcadores de diferenciação representativos são mostrados na figura 21 e na tabela 15, para células coletadas a partir de cada etapa de diferenciação. Nas figuras 21A e B, os resultados da citometria de fluxo para CXCR4 são mostrados para vários tratamentos durante a primeira etapa da diferenciação do endoderma definitivo. A figura 21A mostra os efeitos sobre a expressão de CXCR4 do tratamento com vários compostos em combinação com ativina A. A figura 21B mostra os efeitos sobre o CXCR4 do tratamento com vários compostos em combinação com GDF-8. Os compostos da presente invenção em combinação com ativina A não acentuaram a expressão de CXCR4. Entre
152/247 tanto, todos os compostos da presente invenção testados neste exemplo acentuaram a expressão de CXCR4 em combinação com GDF-8.
Nas figuras 21C e 21 D, os valores de RT-PCR normalizados para vários marcadores de diferenciação, ao final da primeira etapa de diferenciação, são mostrados para tratamentos aplicados durante a primeira etapa do protocolo, usando-se os compostos selecionados da presente invenção, em combinação com ativina A (figura 21C) ou em combinação com GDF-8 (figura 21 D). Valores similares de RT-PCR normalizados foram avaliados na conclusão da etapa três do protocolo de diferenciação (figuras 21E e 21F), ao final da etapa quatro do protocolo de diferenciação (figuras 21G e 21H) e ao final da etapa 5 do protocolo de diferenciação (figuras 211 e 21J). Os tratamentos durante a etapa de diferenciação 1, que combinavam um composto da presente invenção com GDF-8, apresentaram expressão acentuada de vários marcadores endodérmicos e pancreáticos em relação ao tratamento com GDF-8 por si só (figuras 21 F, 21H e 21J). Os tratamentos combinando compostos da presente invenção com ativina A tiveram pouca ou nenhuma melhoria nos marcadores de expressão, em relação ao tratamento com ativina A por si só ou com ativina A e Wnt3a (figuras 21E, 21G e 211). A tabela 15 resume os valores de CT comparativos para marcadores genéticos adicionais ao final de cada etapa de diferenciação, comparando tratamentos durante a primeira etapa que combinavam ativina A ou GDF-8, com ou sem um composto da presente invenção. Na conclusão da quinta etapa de diferenciação, realizou-se uma análise de alto conteúdo para medir os números de células (figuras 21K e 21M) e a expressão de proteína para insulina e glucagon (figuras 21L e 21N). O tratamento com GDF-8 durante a primeira etapa de diferenciação, sozinho ou em combinação com um composto da presente invenção, resultou na expressão de insulina e glucagon na conclusão da quinta etapa de diferenciação, demonstrando que o GDF-8 foi capaz de substituir a ativina A durante a iniciação da formação de endoderma definitivo, levando subsequentemente a células hormonais pancreáticas. Coletivamente, esses dados mostram que a adição de qualquer das respectivas moléculas pequenas
153/247 teve efeitos mínimos sobre os marcadores de diferenciação para tratamentos em combinação com ativina A. Entretanto, a adição de uma molécula pequena em combinação com tratamento por GDF8 teve efeitos aprimorados significativos sobre a imediata diferenciação do endoderma definitivo, na conclusão da primeira etapa de diferenciação e também em marcadores de diferenciação a jusante, na conclusão das etapas 3, 4 e 5. Foi observada uma variabilidade dentro do painel de moléculas pequenas, talvez atribuível à concentração do composto usado no teste, e/ou de seu mecanismo de ação.
Exemplo 18
Células expressoras de marcadores característicos da linhagem de endoderma definitivo gue foram formadas com o uso de GDF-8 e um composto da presente invenção são capazes de liberar peptídeo C em seguida ao transplante para um roedor
É importante determinar se as células expressoras de marcadores característicos da linhagem de endoderma pancreático geradas in vitro por tratamento com GDF-8 e uma molécula peguena poderíam produzir células endócrinas funcionais in vivo. Foi feito um estudo de transplante in vivo, para comparar as células diferenciadas por tratamento com ativina A e Wnt3a versus tratamento com GDF-8 e compostos de molécula pequena.
Preparação de células: aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231), com passagem em média a cada quatro dias. Um meio condicionado com MEF e suplementado com 8 ng/ml de bFGF foi usado para semeadura inicial e expansão. Todas as linhagens de células ES humanas foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de contaminação por micoplasma.
A passagem das células foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada
154/247 única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados celulares foram centrifugados a baixa velocidade em meio condicionado com MEF, para remover quantidades residuais de dispase e, então, uniformemente ressuspensos em meio condicionado com MEF suplementado com 8 ng/mL de bFGF (PeproTech Inc., Cat. n° 100-18B) para semeadura sobre placas com 6 poços (Nunc, Cat. n° 140685) revestidas por MATRIGEL com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231) a uma razão de 1:3, usando volumes de 2,5 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 por toda o tempo em cultura.
Diferenciação celular, o processo de diferenciação foi iniciado três dias depois de as células serem semeadas sobre placas com 6 poços revestidas por MATRIGEL® com teor reduzido de fator de crescimento. Um protocolo em quatro etapas foi usado para diferenciação in vitro de célulastronco embrionárias humanas H1 em células expressoras de marcadores característicos da linhagem de endoderma pancreático. A etapa 1 foi conduzida ao longo de três dias para gerar células de endoderma definitivo. No primeiro dia da etapa 1, a diferenciação foi iniciada mediante a aspiração do meio de cultura gasto, seguida da adição de um volume igual de meio basal RPMI-1640 (Invitrogen, Cat. n° 22400) com 2% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (Proliant Biologicals, Cat. n° SKU 68700) e 8 ng/mL de bFGF. Em um grupo de tratamento, as células foram expostas a 100 ng/mL de ativina A (PeproTech, Cat. n° 120-14) com 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF). Em um segundo grupo de tratamento, as células foram expostas a 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) com 2,5 μΜ de Composto 40. Em um terceiro grupo de tratamento, as células foram expostas a 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) com 2,5 μΜ de Composto 202. No segundo e no terceiro dias da etapa 1 de diferenciação, as células em todos os grupos de tratamento foram alimentadas com RPMI-1640 contendo 2%
155/247 de FAF BSA, 8 ng/mL de bFGF e ou 100 ng/mL de ativina A (grupo de tratamento 1), ou 100 ng/mL de GDF-8 (grupos de tratamento 2 e 3), sem a adição de Wnt3a ou um composto da presente invenção. Ao final do terceiro dia de cultura, um poço de cada grupo de tratamento foi coletado para análise de FACS.
A etapa 2 do protocolo de diferenciação foi conduzida ao longo de três dias. As células de todos os grupos de tratamento foram alimentadas diariamente com DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 2% de FAF BSA e 50 ng/mL de FGF7 (PeproTech, Cat. n° 100-19).
A etapa 3 do protocolo de diferenciação foi conduzida ao longo de quatro dias. As células de todos os grupos de tratamento foram alimentadas diariamente com glicose com alto teor de DMEM (Invitrogen, Cat. n°10569) suplementado com 1% de B27 (Invitrogen, Cat. n° 17504044), 50 ng/mL de FGF7, 100 ng/mL de noguina (R&D Systems, Cat. n° 3344-NG), 250 nM de KAAD-ciclopamina (Calbiochem, Cat. n° 239804) e 2 μΜ de ácido todo-transretinoico (RA) (Sigma-Aldrich, Cat. n° R2625).
A etapa 4 do protocolo de diferenciação foi conduzida ao longo de três dias. As células de todos os grupos de tratamento foram alimentadas diariamente, durante os primeiros dois dias, com glicose com alto teor de DMEM suplementado com 1% de B27, 100 ng/mL de noguina e 1 μΜ de inibidor ALK5 (Axxora, Cat. n° ALX-270-445). No terceiro dia, as células foram coletadas do substrato mediante o uso de uma ponta de 20 μΙ (Rainin, Cat. n° RT-L10F) e um raspador de células (Corning, Cat. n° 3008) e, então, transferidas para um tubo de 50 mL. As células foram deixadas sedimentar por gravidade, e o sobrenadante foi aspirado sem perturbar o pélete de células. As células foram ressuspensas em glicose com alto teor de DMEM suplementado com 1% de B27, 100 ng/mL de noguina e 1 mM de inibidor ALK5 e, então, cultivadas de um dia para o outro em microplacas de seis poços com fixação ultrabaixa Costar (Corning Inc., Cat. n° 3471). No dia seguinte, as células na cultura em suspensão foram coletadas e contadas. Alíquotas de 10x106 células/camundongo foram usadas para transplante. Alíquotas de 0,5 x 106 células foram coletadas para análise por RT-PCR.
156/247
A figura 22 mostra os resultados da citometria de fluxo para células de endoderma definitivo geradas ao final da etapa 1 para cada um dos respectivos grupos de tratamento. O tratamento com ativina A e Wnt3a, ou o tratamento com GDF-8 e um composto da presente invenção, resultou em células que expressam níveis similares de CXCR4 (mais que 85%) ao final da etapa 1, sugerindo que uma população equivalente de células de endoderma definitivo foi derivada de cada grupo de tratamento.
Os resultados da análise de RT-PCR para células de cada grupo de tratamento na conclusão da etapa 4 do protocolo de diferenciação são mostrados na figura 22, painel B. As células diferenciadas em endoderma pancreático (PE) com o uso de ativina A e Wnt3a, ou com o uso de GDF-8 e o Composto 40, ou com o uso de GDF-8 e o Composto 202, expressaram níveis equivalentes de marcadores para PE: CDX2, MAFA, NGN3, NKX6.1, PDX1 e Ptf1 alfa. Esses resultados sugerem que o protocolo de diferenciação usando GDF-8 e uma molécula pequena foi igualmente eficaz na criação de uma população de células precursoras de endoderma pancreático.
Transplante, para camundongos, de células-tronco embrionárias humanas tratadas de acordo com os métodos da presente invenção: camundongos SCID beges machos (C.B-lgh-Vo/GbmsTac-Prkdc^-Lyst139 N7) com cinco a seis semanas de idade foram adquiridos junto à Taconic Farms. Os camundongos foram acomodados em gaiolas microisoladoras com livre acesso a alimento e água esterilizados. Em preparação para a cirurgia, os camundongos foram identificados por etiquetas na orelha, seu peso corporal foi medido, e sua glicose sanguínea foi determinada com o uso de um glicosímetro manual (LifeScan, One Touch). No dia da cirurgia, os camundongos foram anestesiados com uma mistura de isoflurano e oxigênio, e o sítio cirúrgico foi raspado com aparadores próprios para pequenos animais. No pré-operatório, os camundongos receberam uma dose subcutânea de 0,1 mg.kg de Buprenex. O sítio cirúrgico foi preparado com sucessivas lavagens de 70% de álcool isopropílico, 10% de povidonaiodeto e 70% de álcool isopropílico, e uma incisão lateral esquerda foi feita através das camadas de pele e músculo. O rim esquerdo foi externalizado e
157/247 mantido úmido com cloreto de sódio a 0,9%. Um cateter I.V. de 24G x %” foi usado para penetrar a cápsula renal, e a agulha foi removida. O cateter foi, então, avançado sob a cápsula renal até o pólo distal do rim. Durante a preparação pré-operatória dos camundongos, as células para transplante foram centrifugadas em um tubo de 1,5 mL para microfuga, e a maior parte do sobrenadante foi removida, deixando uma quantidade suficiente de meio para coletar o pélete de células. As células foram coletadas em uma ponta de pipeta Rainin Pos-D para deslocamento positivo, e a pipeta foi invertida para deixar as células decantarem por gravidade. O excesso de meio foi dispensado, deixando uma preparação de células pronta para transplante. Para o transplante, a ponta de pipeta Pos-D foi colocada firmemente na parte central do cateter, e as células foram dispensadas da pipeta através do cateter sob a cápsula renal, para aplicação ao pólo distal do rim. O lúmen do cateter foi purgado com um pequeno volume de meio de cultura, para transportar quaisquer células restantes, e o cateter foi removido. A cápsula renal foi selada com um cautério de baixa temperatura, e o rim foi retornado a sua posição anatômica original. O músculo foi fechado por suturas contínuas com o uso de suturas 5-0 VICRYL, e a pele foi fechada com grampos cirúrgicos. O camundongo foi removido da anestesia e deixado recuperar-se totalmente. No pós-operatório, os camundongos receberam uma dose subcutânea de 1,0 mg.kg de Metacam.
Em seguida ao transplante, os camundongos foram pesados uma vez por semana, e a glicose sanguínea foi medida duas vezes por semana. Em vários intervalos em seguida ao transplante, os camundongos receberam doses de 3 g/kg de glicose IP e, 60 minutos após a injeção de glicose, foi coletado sangue via sinus retro-orbital e colocado em tubos para microfuga contendo uma pequena quantidade de heparina. O sangue foi centrifugado, e o plasma foi colocado em um segundo tubo de microfuga, e congelado em gelo seco para armazenamento a -80°C, até que fosse realizado o teste de peptideo C humano. Os níveis de peptideo C humano foram determinados com o uso do kit para diagnóstico Mercodia/ALPCO Diagnotics Ultrasensitive C-peptide ELISA, de acordo com as instruções do
158/247 fabricante.
Os resultados do teste ELISA para peptídeo C humano são mostrados na figura 23 para camundongos transplantados com células obtidas de cada um dos respectivos grupos de tratamento. Nenhum peptídeo C humano circulante foi detectado quatro semanas após o transplante, para qualquer dos camundongos que receberam células de qualquer dos grupos de tratamento. Oito semanas após o transplante, peptídeo C detectável foi encontrado em um dentre dois camundongos que receberam células tratadas com ativina A e Wnt3a, um dentre três camundongos que receberam células tratadas com GDF-8 e Composto 40, e duas dentre três camundongos que receberam células tratadas com GDF-8 e Composto 202. Esses resultados sugerem que uma população equivalente de células precursoras endócrinas poderia ser derivada do protocolo de diferenciação com GDF-8 e uma molécula pequena, e que as células adicionalmente maturaram in vivo para uma célula secretora de insulina e responsiva a glicose.
Exemplo 19
Células expressoras de marcadores característicos da linhagem de endoderma definitivo que foram formadas com o uso de GDF-8 são capazes de liberar peptídeo C em seguida ao transplante para um roedor
É importante demonstrar que as células diferenciadas com GDF8 na ausência de ativina A poderíam, também, ser adicionalmente diferenciadas para uma população de células endócrinas capaz de secretar peptídeo C humano em um modelo de transplante de roedor in vivo.
Preparação de células: aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por MATRIGEL® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231), com passagem em média a cada quatro dias. Um meio condicionado com MEF e suplementado com 8 ng/ml de bFGF foi usado para semeadura inicial e expansão. Todas as linhagens de células ES humanas foram mantidas em números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao cariótipo normal e à ausência de contaminação por micoplasma.
159/247
A passagem das células foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados celulares foram centrifugados a baixa velocidade em meio condicionado com MEF, para remover quantidades residuais de dispase e, então, uniformemente ressuspensos em meio condicionado com MEF suplementado com 8 ng/mL de bFGF (PeproTech Inc., Cat. n° 100-18B) para semeadura sobre placas com 6 poços (Nunc, Cat. n° 140685) revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231) a uma razão de 1:3, usando volumes de 2,5 mL/poço. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. As placas foram mantidas a 37°C, com 5% de CO2 durante toda a cultura.
Diferenciação celular, o processo de diferenciação foi iniciado três dias depois de as células serem semeadas em placas com 6 poços. Um protocolo em quatro etapas foi usado para diferenciação in vitro de célulastronco embrionárias humanas H1 em células expressoras de marcadores característicos da linhagem de endoderma pancreático. A etapa 1 foi conduzida ao longo de três dias, para gerar células expressoras de marcadores característicos da linhagem de endoderma definitivo. No primeiro dia da etapa 1, a diferenciação foi iniciada mediante a aspiração do meio de cultura gasto, seguida da adição de um volume igual de meio basal RPMI-1640 (Invitrogen, Cat. n° 22400) com 2% de fração V de albumina bovina isenta de ácido graxo (FAF BSA) (Proliant Biologicals, Cat. n° SKU 68700) e 8 ng/mL de bFGF. Em um grupo de tratamento, conjuntos de células em duplicata foram tratados com 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF). Em um segundo grupo de tratamento, conjuntos de células em duplicata foram tratados com 100 ng/mL de GDF-8 e 2,5 mM do Composto 40. No segundo e no terceiro dias da primeira etapa de diferenciação, as células em todos os
160/247 grupos de tratamento foram alimentadas com RPMI-1640 contendo 2% de
FAF BSA, 8 ng/mL de bFGF e 100 ng/mL de GDF-8, porém sem a adição de
Wnt3a ou do Composto 40. Ao final do terceiro dia de cultura, um poço de cada grupo de tratamento foi coletado para análise de FACS.
A etapa 2 do protocolo de diferenciação foi realizada ao longo de três dias. As células de todos os grupos de tratamento foram alimentadas diariamente com DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 2% de FAF BSA e 50 ng/mL de FGF7 (PeproTech, Cat. n° 100-19).
A etapa 3 do protocolo de diferenciação foi realizada ao longo de quatro dias. As células de todos os grupos de tratamento foram alimentadas diariamente com glicose com alto teor de DMEM (Invitrogen, Cat. n° 10569) suplementado com 1% de B27 (Invitrogen, Cat. n° 17504-044), 50 ng/mL de FGF7, 100 ng/mL de noguina (R&D Systems, Cat. n° 3344-NG), 250 nM de KA-AD-ciclopamina (Calbiochem, Cat. n° 239804) e 2 μΜ de ácido todotrans-retinoico (RA) (Sigma-Aldrich, Cat. n° R2625).
A etapa 4 do protocolo de diferenciação foi realizada ao longo de três dias. As células de todos os grupos de tratamento foram alimentadas diariamente com glicose com alto teor de DMEM suplementada com 1% de B27, 100 ng/mL de noguina e 1 μΜ de inibidor ALK5 (Axxora, Cat. n° ALX270-445), e 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) durante os primeiros dois dias. No terceiro dia da etapa 4, as células foram coletadas das placas com 6 poços usando-se uma ponta de 20 μΙ (Rainin, Cat. n° RTL10F) e um raspador de células (Corning, Cat. n° 3008), sendo então transferidas para um tubo de 50 mL. As células foram deixadas sedimentar por gravidade, e o sobrenadante foi aspirado sem perturbar o pélete de células. As células foram ressuspensas em glicose com alto teor de DMEM suplementado com 1% de B27, 100 ng/mL de noguina e 1 mM de inibidor ALK5 e, então, cultivadas de um dia para o outro em microplacas de seis poços com fixação ultrabaixa Costar (Corning Inc., Cat. n° 3471). No dia seguinte, as células na cultura em suspensão foram coletadas e contadas. Alíquotas de 10 x 106 células/camundongo foram usadas para transplante. Alíquotas de 0,5 x 106 células foram coletadas para análise por RT-RCR.
161/247
A figura 24A mostra os resultados da citometria de fluxo para células de endoderma definitivo geradas ao final da etapa 1 para cada um dos respectivos grupos de tratamento. Os resultados para tratamento com GDF-8 e Wnt3a, ou tratamento com GDF-8 e Composto 40, expressaram níveis similares de CXCR4 ao final da etapa 1, sugerindo que uma população celular de endoderma definitivo equivalente e robusta resultou de cada grupo de tratamento. Conjuntos de tratamento em duplicata apresentaram forte concordância. Os resultados antes do transplante para análise de RTPCR na conclusão da etapa 4 do protocolo de diferenciação são mostrados na figura 24B. As células diferenciadas para endoderma pancreático (PE) com o uso de GDF-8 e Wnt3a, ou GDF-8 e Composto 40, expressaram níveis equivalentes de marcadores característicos da linhagem de endoderma pancreático, como: CDX2, MafA, Ngn3, NKX6.1, Pdx-1 e Ptf1A. Esses resultados demonstram que o protocolo de diferenciação usando GDF-8 e Wnt3a, ou GDF-8 e um composto da presente invenção, foi igualmente eficaz na criação de uma população de células precursoras de endoderma pancreático. O protocolo de diferenciação foi conduzido em dois conjuntos de tratamento independentes porém idênticos. Os resultados dos conjuntos de tratamento em duplicata apresentaram forte concordância, conforme mostrado por análise de RT-PCR.
Transplante, para camundongos, de células-tronco embrionárias humanas: camundongos SCID beges machos (C.B-/gri-1b/GbmsTacPrkdc^-Lys?9 N7) com cinco a seis semanas de idade foram adquiridos junto à Taconic Farms. Os camundongos foram acomodados em gaiolas microisoladoras com livre acesso a alimento e água esterilizados. Em preparação para a cirurgia, os camundongos foram identificados por etiquetas na orelha, seu peso corporal foi medido, e sua glicose sanguínea foi determinada com o uso de um glicosímetro manual (LifeScan, One Touch). No dia da cirurgia, os camundongos foram anestesiados com uma mistura de isoflurano e oxigênio, e o sítio cirúrgico foi raspado com aparadores próprios para pequenos animais. No pré -operatório, os camundongos receberam uma dose subcutânea de 0,1 mg.kg de Buprenex. O sítio cirúrgico foi
162/247 preparado com sucessivas lavagens de 70% de álcool isopropílico, 10% de povidona-iodeto e 70% de álcool isopropílico, e uma incisão lateral esquerda foi feita através das camadas de pele e músculo. O rim esquerdo foi externalizado e mantido úmido com cloreto de sódio a 0,9%. Um cateter I.V. de 24G x %” foi usado para penetrar a cápsula renal, e a agulha foi removida. O cateter foi, então, avançado sob a cápsula renal até o pólo distal do rim. Durante a preparação pré-operatória dos camundongos, as células para transplante foram centrifugadas em um tubo de 1,5 mL para microfuga, e a maior parte do sobrenadante foi removida, deixando uma quantidade suficiente de meio para coletar o pélete de células. As células foram coletadas em uma ponta de pipeta Rainin Pos-D para deslocamento positivo, e a pipeta foi invertida para deixar as células decantarem por gravidade. O excesso de meio foi dispensado, deixando uma preparação de células pronta para o transplante. Para o transplante, a ponta de pipeta PosD foi colocada firmemente na parte central do cateter, e as células foram dispensadas da pipeta através do cateter sob a cápsula renal, para aplicação ao pólo distai do rim. O lúmen do cateter foi purgado com um pequeno volume de meio de cultura, para transportar quaisquer células restantes, e o cateter foi removido. A cápsula renal foi selada com um cautério de baixa temperatura, e o rim foi retornado a sua posição anatômica original. O músculo foi fechado por suturas contínuas com o uso de 5-0 VICRYL, e a pele foi fechada com grampos cirúrgicos. O camundongo foi removido da anestesia e deixado recuperar-se totalmente. No pósoperatório, os camundongos receberam uma dose subcutânea de 1,0 mg.kg de Metacam.
Em seguida ao transplante, os camundongos foram pesados uma vez por semana, e a glicose sanguínea foi medida duas vezes por semana. Em vários intervalos em seguida ao transplante, os camundongos receberam doses de 3 g/kg de glicose IP e, 60 minutos após a injeção de glicose, foi coletado sangue via sinus retro-orbital e colocado em tubos para microfuga contendo uma pequena quantidade de heparina. O sangue foi centrifugado, e o plasma foi colocado em um segundo tubo de microfuga, e
163/247 congelado em gelo seco para armazenamento a -80°C, até que fosse realizado o teste de peptídeo C humano. Os níveis de peptídeo C humano foram determinados com o uso do kit para diagnóstico Mercodia/ALPCO Diagnotics Ultrasensitive C-peptide ELISA, de acordo com as instruções do fabricante. Os resultados do teste ELISA para peptídeo C humano são mostrados nas figuras 29C e D para camundongos transplantados com células obtidas de cada um dos respectivos grupos de tratamento. Níveis similares de peptídeo C humano eram detectáveis 8 semanas após o transplante, para cada categoria de tratamento, indicando que uma população equivalente de células endócrinas precursoras podería ser derivada do protocolo de diferenciação com o uso de GDF-8 e Wnt3a, ou de GDF-8 e um composto da presente invenção.
Exemplo 20
Avaliação do potencial dos inibidores de CDK, GSK3 e TRK para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo
Um subconjunto de 14 moléculas pequenas proprietárias, conhecidas por terem especificidade para rotas de sinalização de CDK, GSK3 e/ou TRK, foram avaliadas quanto a seu potencial para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo.
Semeadura para teste das células: em resumo, aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico para cultura de tecidos revestido por Matrigel® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços (Packard ViewPlates, PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), usandose volumes de 100 μΙ/poço. As células foram deixadas unir-se para, então,
164/247 recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e teste: a triagem foi realizada usando-se os compostos descritos na tabela 16. Além disso, o Composto 34 foi incluído como um controle positivo, conforme demonstrado nos exemplos anteriores. Os compostos foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO (Sigma, Cat. n° D2650) e armazenados a -80°C. Os compostos da biblioteca foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. As condições de teste foram realizadas em triplicata, com alimentação em dias alternados ao longo de um período de teste de quatro dias. O teste foi iniciado mediante aspiração do meio de cultura de cada poço, seguido de três lavagens em PBS (Invitrogen, Cat. n° 14190) para remover quantidades residuais de fatores de crescimento. No primeiro dia do teste, os volumes de teste de 200 μΙ por poço foram adicionados a cada poço usando-se meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,5% de FCS (HyClone, Cat. n° SH30070.03) e 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) mais 2,5 mM de composto. Um conjunto paralelo de amostras para teste foi tratado de maneira idêntica, porém omitindo-se o GDF-8 do meio. No terceiro dia do teste, os volumes de teste de 100 μΙ por poço foram adicionados a cada poço usando-se meio base DMEM:F12 suplementado com 2% de FCS mais 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8). O GDF-8 foi omitido das amostras para teste que não foram tratadas com GDF-8 no primeiro dia do teste. As amostras de controle positivo continham o mesmo meio base suplementado com FCS e 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14) durante todo o teste de quatro dias, juntamente com adição de Wnt3a (20 ng/mL) nos dias 1 e 2. As amostras de controle negativo conti165/247 nham meio base DMEM:F12 suplementado com FCS.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anticabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, corados somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calcula
166/247 dos para cada réplica de conjunto de dados. A expressão total de proteína SOX17 foi relatada como intensidade total ou intensidade integrada, definida como a fluorescência total da célula multiplicada pela área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de cinza entre 200 e 3.500. Coletou-se a média de dados das poços em triplicata. A porcentagem de poços tratados em relação ao controle positivo foi calculada.
Os resultados para essa triagem são mostrados na tabela 17. Nenhuma das moléculas pequenas induziu uma expressão de SOX17 significativa na ausência de GDF-8 durante o processo de diferenciação em quatro dias. O Composto 34 serviu como um controle experimental, e induziu uma expressão de SOX17 significativa na presença de GDF-8, equivalente aos níveis observados com o controle positivo usando ativina A e Wnt3a. Os demais compostos da presente invenção testados neste exemplo apresentaram uma faixa de atividades com indução entre fraca e moderada para expressão de SOX17. Deve-se observar que a atividade de diferenciação nesse subconjunto de compostos foi observada em associação com a seletividade para todas as três rotas sinalizadoras enzimáticas, tornando difícil determinar conclusivamente um mecanismo de ação claro.
Exemplo 21
Triagem quanto a análogos dos compostos da presente invenção que são capazes de mediar a formação de células expressoras de marcadores característicos da linhagem de endoderma definitivo
Com base nas estruturas dos compostos da presente invenção, conduziu-se uma busca por análogos e 118 análogos foram encontrados. A triagem inicial determinou que alguns análogos eram capazes de induzir diferenciação do endoderma definitivo na ausência de ativina A, em combinação com outros fatores de crescimento. É importante determinar se esses análogos também poderíam induzir a diferenciação do endoderma definitivo em combinação apenas com GDF-8.
Semeadura para teste das células: em resumo, aglomerados de células-tronco embrionárias humanas H1 foram cultivados sobre plástico
167/247 para cultura de tecidos revestido por Matrigel® com teor reduzido de fator de crescimento (Invitrogen, Cat. n° 356231). As células foram passadas usando-se tratamento com colagenase (Invitrogen, Cat. n° 17104-019) e raspagem delicada, foram lavadas para remover quantidades residuais de enzima, e folheadas com dispersão uniforme a uma razão de 1:1 (área superficial) sobre placas pretas com 96 poços (Packard ViewPlates, PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), usando-se volumes de 100 μΙ/poço. As células foram deixadas unir-se para, então, recuperar a proliferação na fase log ao longo de um período de 1 a 3 dias, com alimentação diária de meio condicionado com MEF suplementado com 8 ng/mL de bFGF (R&D Systems, Cat. n° 233-FB). As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
Preparação de compostos e teste: a triagem foi realizada usando-se uma biblioteca de compostos análogos. Os compostos dessa biblioteca foram disponibilizados sob a forma de estoques de 5 mM no formato de placa com 96 poços, solubilizados em 100% de DMSO (Sigma, Cat. n° D2650) e armazenados a -80°C. Os compostos da biblioteca foram adicionalmente diluídos até uma concentração intermediária de 0,2 mM em 50 mM de HEPES (Invitrogen, Cat. n° 15630-080) e 20% de DMSO, e armazenados a 4°C. As condições de teste foram realizadas em triplicata, com alimentação em dias alternados ao longo de um período de teste de quatro dias. Os testes foram iniciados mediante aspiração do meio de cultura de cada poço, seguido de três lavagens em PBS (Invitrogen, Cat. n° 14190) para remover quantidades residuais de fatores de crescimento. No primeiro dia do teste, os volumes de teste de 200 μΙ por poço foram adicionados a cada poço usando-se meio base DMEM:F12 (Invitrogen, Cat. n° 11330-032) suplementado com 0,5% de FCS (HyClone, Cat. n° SH30070.03) e 200 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) mais 2,5 μΜ de composto. No terceiro dia do teste, os volumes de teste de 100 μΙ por poço foram adicionados a cada poço usando-se meio base DMEM:F12 suplementado com 2% de FCS mais 200 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8).
168/247
As amostras de controle positivo continham o mesmo meio base suplementado com FCS e 100 ng/mL de ativina A humana recombinante (PeproTech, Cat. n° 120-14) durante todo o teste de quatro dias, juntamente com Wnt3a (20 ng/mL) nos dias 1 e 2. As amostras de controle negativo continham meio base DMEM:F12 suplementado com FCS, adicionando-se Wnt3a nos dias 1 e 2, mas omitindo-se o tratamento com ativina A.
Análise de alto conteúdo: na conclusão de quatro dias de cultura, as placas de teste foram lavadas duas vezes com PBS (Invitrogen, Cat. n° 14190), fixadas com 4% de paraformaldeído (Alexis Biochemical, Cat. n° ALX-350-011) à temperatura ambiente durante 20 minutos e, então, lavadas três vezes com PBS e permeabilizadas com 0,5% de Triton X-100 (Sigma, Cat. n° T8760-2) durante 20 minutos à temperatura ambiente. As células foram lavadas novamente três vezes com PBS e bloqueadas com 4% de soro de galinha (Invitrogen, Cat. n° 16110082) em PBS durante 30 minutos à temperatura ambiente. O anticorpo primário (cabra anti-humano SOX17, R&D Systems, Cat. n° AF1924) foi diluído a 1:100 e 4% de soro de galinha e adicionado a cada poço durante uma hora, à temperatura ambiente. O anticorpo secundário conjugado Alexa Fluor 488 (galinha anticabra IgG, sondas moleculares, Cat. n° AZ1467) foi diluído a 1:200 em PBS e adicionado a cada poço de amostra, após lavagem por três vezes com PBS. Para contracorar os núcleos, adicionou-se 4 pg/mL de Hoechst 33342 (Invitrogen, Cat. n° H3570) durante dez minutos à temperatura ambiente. As placas foram lavadas uma vez com PBS e deixadas em 100 μΙ/poço de PBS para formação de imagens.
A captura de imagens foi realizada com o uso de um equipamento de análise celular IN Cell Analyzer 1000 (GE Healthcare), usando o filtro dicroico 51008bs para células coradas com Hoechst 33342 e Alexa Fluor 488. Os tempos de exposição foram otimizados a partir de poços com controle positivo e de poços com controle negativo não tratado, coradas somente com anticorpo secundário. Foram capturadas imagens de 15 campos por poço, para compensar por qualquer perda celular ocorrida durante o bioensaio e os procedimentos de coloração subsequentes. As medições
169/247 quanto ao número total de células e à intensidade total de SOX17 foram obtidas a partir de cada poço com o uso do software IN Cell Developer
Toolbox 1.7 (GE Healthcare). A segmentação para os núcleos foi determinada com base em níveis de escala de tons de cinza (linha de base na faixa de 100 a 300) e tamanho nuclear. Médias e desvios-padrão foram calculados para cada réplica de conjunto de dados. A expressão total da proteína SOX17 foi relatada como a intensidade total ou intensidade integrada, definida como a fluorescência total da célula vezes a área da célula. O fundo foi eliminado com base no critério de aceitação das faixas de escala de cinza 10 entre 200 e 3.500. Os dados de intensidade total foram normalizados mediante a divisão das intensidades totais para cada poço pela intensidade total média para o controle positivo. Dados normalizados foram calculados para médias e desvios-padrão de cada conjunto de réplicas.
Os resultados da triagem são mostrados na tabela 18, a partir 15 de quatro placas de teste neste único experimento. Os compostos são classificados em relação à expressão de SOX17 como uma porcentagem do tratamento do controle positivo com ativina A e Wnt3a. Esse teste identificou uma lista de 12 novos acertos de análogo, conforme mostrado na tabela 19.
Exemplo 22
Células-tronco embrionárias humanas cultivadas em microportadores podem ser diferenciadas em células expressoras de marcadores característicos da linhagem de endoderma definitivo de acordo com os métodos da presente invenção
Para os propósitos de diferenciação e produção de grandes números de células endócrinas sob condições escalonáveis, foi importante mostrar gue as células-tronco embrionárias humanas podiam ser cultivadas e diferenciadas para endoderme definitiva sobre microesferas portadoras com o uso dos métodos da presente invenção.
Preparação de células para teste e diferenciação: células H1 p49C3 foram rotineiramente cultivadas sobre microesferas Cytodex3 (GE
Healthcare Life Sciences, NJ, EUA) em um 125 mL frasco de agitação, de acordo com os métodos descritos no pedido de patente US n° 61/116.447.
170/247
Após sete dias, as células e as microesferas foram transferidas para uma placa com 6 poços (Vendor; Cat # XXX) a uma razão de 30 cm2 de área superficial da microesfera por poço, e a placa foi colocada em uma plataforma de agitação. As células sobre as microesferas no poço para tratamento do controle positivo (designada AA/Wnt3a) foram diferenciadas com adição de 100 ng/mL de ativina A (PeproTech, Cat. n° 120-14) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF) durante dois dias, seguido de 100 ng/mL de ativina A e 8 ng/mL de bFGF (PeproTech Inc., Cat. n° 100-18B) durante um dia em RPMI-1640 (Invitrogen, Cat. n° 22400) com 2% de BSA isento de ácido graxo (MP Biomedicals, Inc, Cat. n° 152401), usando volumes de 2 mL/poço. O Composto 34, a uma concentração final de 2,5 μΜ, foi adicionado a uma poço de tratamento para controle negativo (designada CMP por si só) em RPMI-1640 com 2% de BSA isento de ácido graxo (2 mL/poço) durante três dias, na ausência de qualquer outro tratamento por fator de crescimento. Um terceiro poço de tratamento (designada CMP+8) recebeu o Composto 34 a 2,5 μΜ mais 50 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) em RPMI-1640 com 2% de BSA isento de ácido graxo (2 mL/poço) durante três dias. Um quarto poço de tratamento (designada CMP+8+D) recebeu o Composto 34 a 2,5 μΜ com 50 ng/mL de GDF-8 e 50 ng/mL de PDGF-D me RPMI-1640 com 2% de BSA isento de ácido graxo (2 mL/poço) durante três dias. Um quinto poço de tratamento (designada CMP+8+D+V) recebeu o Composto 34 a 2,5 μΜ com 50 ng/mL de GDF-8, 50 ng/mL de PDGF-D e 50 ng/mL de VEGF em RPMI1640 com 2% de BSA isento de ácido graxo (2 mL/poço) durante três dias. Um sexto poço de tratamento (designada CMP+8+D+V+M) recebeu o Composto 34 a 2,5 μΜ com 50 ng/mL de GDF-8, 50 ng/mL de PDGF-D, 50 ng/mL de VEGF e 20 ng/mL de Muscimol em RPMI-1640 com 2% de BSA isento de ácido graxo (2 mL/poço) durante três dias. Todos os meios e tratamentos foram trocados diariamente.
Na conclusão do tratamento e do cultivo, as células foram coletadas das microesferas, de acordo com os métodos descritos no pedido de patente US n° 61/116.447. As células coletadas foram contadas e analisa171/247 das por citometria de fluxo, de acordo com os métodos acima descritos.
Os resultados são mostrados na figura 25. Conforme mostrado no painel A, números similares de células foram recuperados para todos os grupos de tratamento passando por diferenciação. Conforme mostrado no painel B, as células tratadas somente com o Composto 34 não se diferenciaram em células positivas para CXCR4. O tratamento do controle positivo, adicionando ativina A e Wnt3a durante a diferenciação, induziu a expressão de CXCR4 em 68% da população celular resultante. O Composto 34, adicionado com as várias combinações de fator de crescimento, induziu a expressão de CXCR4 em 50% da células, em média. Deve-se notar que níveis equivalentes de expressão de CXCR4 foram observados durante o tratamento com o Composto 34 em combinação com um único fator de crescimento, GDF-8, ou em combinação com múltiplos fatores de crescimento que incluíam GDF-8. Isso prova que o Composto 34, em combinação com pelo menos GDF-8, pode substituir a ativina A e o Wnt3a para promover a diferenciação do endoderma definitivo. Esse exemplo mostra, também, que o procedimento para tratamento é eficaz para células cultivadas e diferenciadas sobre microesferas portadoras.
Exemplo 23
Os compostos da presente invenção, juntamente com GDF-8, acentuam a proliferação celular
Um exemplo anterior mostrou que o GDF-8 é capaz de substituir a ativina A para diferenciar células-tronco embrionárias humanas em células expressoras de marcadores característicos da linhagem de endoderma definitivo. Foi importante conhecer as potências relativas do GDF-8 e da ativina A em relação à formação de endoderma definitivo. Um teste de resposta à dosagem foi conduzido com o uso de concentrações equivalentes de cada fator de crescimento, para comparar os resultados durante a diferenciação das células-tronco embrionárias humanas.
Os compostos da presente invenção usados em combinação com GDF-8 durante a diferenciação do endoderma definitivo foram avaliados quanto a sua capacidade para induzir a proliferação celular. Os resultados
172/247 foram comparados ao tratamento com ativina A ou GDF-8 por si sós.
Preparação de células para teste: culturas de estoque de células-tronco embrionárias humanas (linhagem de células-tronco embrionárias humanas H1) foram mantidas em um estado pluripotente não diferenciado sobre placas revestidas por MATRIGEL® com teor reduzido de fator de crescimento (BD Biosciences, Cat. n° 356231), em meio condicionado com MEF e com passagem, em média, a cada quatro dias. A passagem foi realizada mediante a exposição das culturas celulares a uma solução de 1 mg/mL de dispase (Invitrogen, Cat. n° 17105-041) durante 5 a 7 minutos a 37°C, seguida de enxágue da camada única com meio de cultura condicionado com MEF e raspagem delicada para recuperar os aglomerados celulares. Os aglomerados foram centrifugados a baixa velocidade para coletar-se um pélete de células e para remover quantidades residuais de dispase. Os aglomerados celulares foram divididos a uma razão de 1:3 ou 1:4 para cultura de manutenção de rotina, ou a uma razão de 1:1 para teste imediato. Todas as linhagens de células-tronco embrionárias de ser humano foram mantidas com números de passagem menores que 50, e foram rotineiramente avaliadas quanto ao fenótipo cariotípico normal e quanto à ausência de contaminação por micoplasma.
Os aglomerados celulares usados no teste foram uniformemente ressuspensos em meio condicionado com MEF e suplementado com 8 ng/mL de bFGF, e foram semeados sobre placas com 96 poços Packard VIEWPLATES (PerkinElmer, Cat. n° 6005182) revestidas por MATRIGEL® com teor reduzido de fator de crescimento, em volumes de 100 μΙ/poço. Um meio condicionado com MEF e suplementado com 8 ng/ml de bFGF foi usado para semeadura inicial e expansão. A alimentação diária foi conduzida aspirando-se o meio de cultura gasto de cada poço, e substituindo o mesmo por um volume igual de meio sem uso. Um conjunto de poços de fundo em cada placa de teste não foi semeado com células, mas foi tratado durante todo o teste com condições de meio basal. As placas foram mantidas a 37°C, 5% de CO2, em uma caixa umidificada por toda a duração do ensaio.
173/247
Teste: o teste foi iniciado mediante a aspiração do meio de cultura de cada poço, adicionando-se de volta uma alíquota final de 100 pl do meio para teste. As condições de teste foram realizadas em triplicata ao longo de um período de teste total de três dias, com alimentação diária 5 mediante aspiração e substituição do meio em cada poço com meio de teste sem uso. Testes idênticos foram preparados simultaneamente em paralelo, para avaliação ao final de 24, 48 e 72 horas.
No primeiro dia do teste, todos os poços contendo células receberam uma alíquota (80 μΙ) de meio RPMI-1640 (Invitrogen, Cat. n° 10 22400) suplementado com 2,5% de fração V de albumina bovina isenta de ácido graxo (FAF BSA, 2% no teste final) (Proliant Inc., Cat. n° SKU 68700). Várias amostras para controle e para teste foram criadas a uma concentração de 5x para serem adicionadas a poços adequados (20 μΙ por poço). As condições de controle incluíam o seguinte, com concentrações 15 finais de fator de crescimento conforme indicado: 1) meio basal com 2% de FAF BSA; 2) 100 ng/mL de ativina A (PeproTech, Cat. n°120-14) com 8 ng/mL de bFGF (PeproTech, Cat. n° 100-18B); 3) 100 ng/mL de ativina A com 8 ng/mL de bFGF e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324WN/CF); 4) 100 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) com 8 20 ng/mL de bFGF; 5) GDF-8 com 8 ng/mL de bFGF e 20 ng/mL de Wnt3a. As células em um conjunto adicional de poços de controle foram tratadas com meio condicionado com MEF durante todo o teste. Em algumas amostras de controle usando GDF-8, o Wnt3a foi substituído por um composto da presente invenção. Para as amostras para teste experimentais, os oito 25 diferentes compostos foram diluídos duas vezes em série, para criar três diferentes concentrações de dose, então combinadas com 100 ng/mL de GDF-8 e 8 ng/mL de bFGF. Essas moléculas pequenas incluíam os compostos proprietários Composto 181, Composto 180, Composto 19, Composto 202, Composto 40, Composto 34 e Composto 56, e um inibidor 30 GSK3 BIO disponível comercialmente (EMD Chemicals, Inc., Cat. n° 361550). No segundo e no terceiro dias de teste, todos os poços para amostras de controle e experimentais foram aspirados e alimentados novamente
174/247 usando-se condições de tratamento idênticas, exceto pelo fato de que o Wnt3a foi removido de alguns poços de controle.
Teste de MTS: na conclusão de 24, 48 ou 72 horas de cultura, um conjunto de placas de teste foi submetido a um teste de MTS (Promega, Cat. n° G3581), seguindo-se as instruções do fabricante. Em resumo, adicionou-se 20 pl de MTS a cada poço, e as placas de teste foram incubadas a 37°C e 5% de CO2 durante quatro horas, antes de serem tomadas as leituras de OD490. As medidas estatísticas foram calculadas menos o plano de fundo (isto é, poços de tratamento sem células), para determinar os valores médios para cada conjunto em triplicata, em adição a um erropadrão da média.
O teste de MTS é uma medida de atividade metabólica celular na redução enzimática de um composto de tetrazólio para um produto de formazano. Em um único ponto no tempo, o teste de MTS pode ser usado como um indicador comparativo da viabilidade celular. Os testes de MTS avaliados em paralelo e a pontos sequenciais no tempo, podem agregar informações adicionais referentes a aumentos na atividade metabólica celular que, por sua vez, podem ser correlacionados com a proliferação celular para cada condição de tratamento. A figura 26, painel A mostra as leituras de OD490 para todos os tratamentos de controle ao longo do período de teste de três dias. As células tratadas com meio condicionado mostraram pouca alteração em OD490 ao longo de três dias, indicando que os números de células nesse grupo de tratamento permaneceram estáticos. Em contraste, as células cultivadas em meio basal sem fatores de crescimento (nenhum tratamento), mostraram um declínio constante em OD490, correlacionado com uma perda no número de células ao longo do tempo. Os tratamentos com ativina A durante o processo de diferenciação, com e sem Wnt3a, mostraram aumentos incrementais em OD490, indicando expansão significativa da população celular ao longo do tempo. O tratamento com GDF-8 na ausência de Wnt3a resultou em uma diminuição de OD490, em relação ao tratamento com ativina A, sendo isso perceptível no primeiro dia e mantido ao longo dos três dias de cultivo. A adição de Wnt3a ao grupo de
175/247 tratamento com GDF-8 resultou em recuperação e aumento de OD490 pelo terceiro dia de cultivo.
Da figura 26, painel B, até a figura 26, painel I, são mostrados os resultados do teste MTS para tratamento com um inibidor de molécula pequena em combinação com GDF-8. As leituras de OD490 referentes aos tratamentos com um composto da presente invenção e GDF-8 apresentaram resultados equivalentes a, ou melhores que, aqueles do tratamento com ativina A. Em todos os casos, uma concentração ótima de cada molécula pequena combinada com GDF-8 resultou em leituras de OD490 otimizadas ao longo dos três dias de teste em relação ao tratamento com GDF-8 por si só. Isso sugere que os compostos da presente invenção são importantes para induzir a proliferação e a expansão de uma população celular durante a diferenciação do endoderma definitivo.
Exemplo 24
Células-tronco embrionárias humanas cultivadas em microportadores podem ser diferenciadas em células proqenitoras endócrinas de acordo com os métodos da presente invenção
Para os propósitos de diferenciação e produção de grandes números de células endócrinas sob condições industriais, foi importante mostrar que as células-tronco embrionárias humanas podiam ser cultivadas e diferenciadas para células progenitoras endócrinas sobre microesferas portadoras, com o uso de um protocolo sem ativina A.
Preparação de células para teste e diferenciação: células H1 p45 foram cultivadas sobre microesferas Cytodex3 (GE Healthcare, Cat. n° 170485-01) em uma placa de fixação ultrabaixa com 6 poços (Costar, Cat. n° 3471) colocada sobre uma plataforma de agitação com cerca de 1 rotação a cada 10 segundos (Vari Mix, Thermo Scientific, Cat. n° M79735). Um meio condicionado em MEF foi trocado diariamente durante seis dias. Então, o meio foi alterado para os tratamentos apresentados a seguir, para iniciar a diferenciação de endoderma. As células sobre as microesferas no poço para tratamento do controle positivo (designada AA+Wnt) foram diferenciadas com adição de 100 ng/mL de ativina A (PeproTech, Cat. n° 120-14), 8 ng/mL
176/247 de bFGF (PeproTech Inc., Cat. n° 100-18B) e 20 ng/mL de Wnt3a (R&D Systems, Cat. n° 1324-WN/CF) durante um dia, seguido de 100 ng/mL de ativina A e 8 ng/mL de bFGF (PeproTech Inc., Cat. n° 100-18B) durante dois dias em RPMI-1640 (Invitrogen, Cat n° 22400) com 2% de BSA isento de ácido graxo (Proliant Biomedicals, Inc, SKU n° 68700), usando volumes de 2 mL/poço. Um segundo poço de tratamento (designada GDF-8+MCX) recebeu o Composto 202 a 2,5 μΜ mais 200 ng/mL de GDF-8 (R&D Systems, Cat. n° 788-G8) e 8 ng/mL de bFGF durante um dia, seguido de dois dias com 200 ng/mL de GDF-8 e 8 ng/mL de bFGF em meio RPMI-1640 com 2% de BSA isento de ácido graxo (2 mL/poço). Um terceiro poço de tratamento (designada GDF-8+Wnt) recebeu 200 ng/mL de GDF-8 com 20 ng/mL de Wnt3a e 8 ng/mL de bFGF durante um dia, seguido de dois dias com 200 ng/mL de GDF-8 e 8 ng/mL de bFGF em meio RPMI-1640 com 2% de BSA isento de ácido graxo (2 mL/poço). Todos os meios e tratamentos foram trocados diariamente.
Na conclusão do tratamento e do cultivo, as células foram coletadas e contadas para se determinar a recuperação celular e para submetêlas a citometria de fluxo. Observou-se altos teores de CXCR4 e CD99 em seguida a todos os três regimes de tratamento (figura 27A). O número de células variou entre amostras (figura 27B). Um menor número de células foi observado em amostras tratadas com GDF-8 e nos grupos de endoderma definitivo e quarto estágio, em comparação a outros grupos de tratamento. Isso sugere que os compostos da presente invenção podem aumentar a proliferação das células durante a diferenciação.
Ao final do estágio 3, os genes para endoderma PDX1, HNF4 alfa e CDX2 são expressos nas células (figuras 27C e 27D). O tratamento das células com GDF-8 e um composto na presente invenção durante o primeiro estágio de diferenciação resultou em uma melhor expressão de Pdx1, em comparação ao tratamento de diferenciação para controle. Ao final do estágio 4, os genes para endoderma estavam adicionalmente regulados para cima (figuras 27E e 27F). Esses resultados concluem que o GDF-8 mais o Composto 202 podem substituir a ativina A e o Wnt3a para diferen
177/247 ciação do endoderma definitivo, resultando na formação de endoderma pancreático.
As publicações citadas ao longo deste documento estão aqui incorporadas a título de referência, em sua totalidade. Embora os vários 5 aspectos da invenção tenham sido ilustrados acima, por meio de referência a exemplos e modalidades preferenciais, deve-se compreender que o escopo da invenção é definido não pela supracitada descrição, mas pelas reivindicações apresentadas a seguir, adequadamente interpretadas sob os princípios da legislação de patentes.
| Tabela 1 | |||||
| Placa n° | Composto n° | Número de célula | Expressão de Sox17 | ||
| Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos | ||
| placa 5 | nenhuma ativina A (com Wnt3a) | 7159 | 67,42 | 8.12E+06 | 2,51 |
| placa 5 | Ativina A / Wnt3a | 10619 | 100,00 | 3.23E+08 | 100,00 |
| placa 5 | Composto 58 | 4848 | 45,66 | -1.60E+06 | -0,49 |
| placa 5 | Composto 59 | 20 | 0,19 | -4.62E+06 | -1,43 |
| placa 5 | Composto 60 | 3348 | 31,52 | -2.33E+05 | -0,07 |
| placa 5 | Composto 61 | 2931 | 27,60 | -3.05E+06 | -0,94 |
| placa 5 | Composto 62 | 7171 | 67,53 | -2.04E+06 | -0,63 |
| placa 5 | Composto 3 | 14211 | 133,82 | -2.34E+06 | -0,73 |
| placa 6 | nenhuma ativina A (com Wnt3a) | 3264 | 32,97 | 2.52E+06 | 0,80 |
| placa 6 | Ativina A / Wnt3a | 9902 | 100,00 | 3.14E+08 | 100,00 |
| placa 6 | Composto 63 | 1917 | 19,36 | 4.75E+05 | 0,15 |
| placa 6 | Composto 26 | 5434 | 54,88 | -6.33E+05 | -0,20 |
| placa 6 | Composto 27 | 6288 | 63,50 | -1.13E+06 | -0,36 |
| placa 6 | Composto 28 | 4121 | 41,62 | -1.89E+06 | -0,60 |
178/247
| placa 6 | Composto 39 | 5164 | 52,15 | -1.66E+06 | -0,53 |
| placa 6 | Composto 30 | 4726 | 47,73 | -1.23E+06 | -0,39 |
| placa 7 | nenhuma ativina A (com Wnt3a) | 9545 | 47,57 | -4.87E+06 | -0,99 |
| placa 7 | Ativina A / Wnt3a | 20064 | 100,00 | 4.92E+08 | 100,00 |
| placa 7 | Composto 31 | 7230 | 36,03 | -3.45E+06 | -0,70 |
| placa 7 | Composto 32 | 14655 | 73,04 | -3.03E+06 | -0,62 |
| placa 7 | Composto 33 | 13891 | 69,23 | -8,11 E+06 | -1,65 |
| placa 7 | Composto 34 | 11674 | 58,18 | -2.24E+06 | -0,46 |
| placa 7 | Composto 35 | 15379 | 76,65 | -7.30E+06 | -1,48 |
| placa 7 | Composto 36 | 8356 | 41,65 | -4.57E+06 | -0,93 |
| placa 8 | nenhuma ativina A (com Wnt3a) | 6868 | 36,97 | -2,31 E+06 | -0,52 |
| placa 8 | Ativina A / Wnt3a | 18575 | 100,00 | 4.47E+08 | 100,00 |
| placa 8 | Composto 37 | 9048 | 48,71 | -3,51 E+06 | -0,79 |
| placa 8 | Composto 38 | 11361 | 61,16 | -4,31 E+06 | -0,96 |
| placa 8 | Composto 39 | 7054 | 37,98 | -3.83E+06 | -0,86 |
| placa 8 | Composto 40 | 8104 | 43,63 | -4.59E+06 | -1,03 |
| placa 1 | nenhuma ativina A (com Wnt3a) | 2972 | 27,98 | 1.64E+07 | 19,74 |
| placa 1 | Ativina A / Wnt3a | 3126 | 29,44 | 8.33E+07 | 100,00 |
| placa 1 | Composto 64 | 2201 | 20,72 | 1,71 E+07 | 20,52 |
| placa 1 | Composto 65 | 3030 | 28,53 | 2.83E+07 | 33,95 |
| placa 1 | Composto 66 | 1990 | 18,74 | 2.36E+07 | 28,30 |
| placa 1 | Composto 67 | 2074 | 19,53 | 2.63E+07 | 31,55 |
| placa 1 | Composto 68 | 1432 | 13,48 | 1.03E+07 | 12,39 |
| placa 1 | Composto 69 | 2593 | 24,42 | 2.62E+07 | 31,43 |
| placa 1 | Composto 70 | 2236 | 21,05 | 2.59E+07 | 31,11 |
| placa 1 | Composto 71 | 2996 | 28,22 | 3.07E+07 | 36,92 |
| placa 1 | Composto 72 | 2179 | 20,52 | 1,21E+07 | 14,50 |
| placa 1 | Composto 73 | 2817 | 26,53 | 2.93E+07 | 35,25 |
179/247
| placa 1 | Composto 74 | 2853 | 26,86 | 2.25E+07 | 27,01 |
| placa 1 | Composto 75 | 1689 | 15,91 | 1,42E+07 | 17,05 |
| placa 1 | Composto 76 | 2324 | 21,89 | 1.48E+07 | 17,81 |
| placa 1 | Composto 77 | 2306 | 21,71 | 2.04E+07 | 24,55 |
| placa 1 | Composto 78 | 3298 | 31,06 | 2.58E+07 | 31,00 |
| placa 1 | Composto 79 | 2855 | 26,88 | 2.79E+07 | 33,47 |
| placa 1 | Composto 80 | 3603 | 33,93 | 3.22E+07 | 38,62 |
| placa 1 | Composto 81 | 2263 | 21,31 | 1.07E+07 | 12,91 |
| placa 1 | Composto 82 | 1210 | 11,39 | 1.36E+07 | 16,33 |
| placa 1 | Composto 83 | 1805 | 17,00 | 1.82E+07 | 21,87 |
| placa 1 | Composto 84 | 2024 | 19,06 | 2.48E+07 | 29,80 |
| placa 1 | Composto 85 | 2840 | 26,74 | 3.45E+07 | 41,44 |
| placa 1 | Composto 86 | 1447 | 13,63 | 8,43E+06 | 10,13 |
| placa 1 | Composto 87 | 5336 | 50,25 | 4.20E+07 | 50,38 |
| placa 2 | nenhuma ativina A (com Wnt3a) | 4033 | 35,50 | 2.14E+07 | 21,70 |
| placa 2 | Ativina A / Wnt3a | 4292 | 37,78 | 9.86E+07 | 100,00 |
| placa 2 | Composto 88 | 3416 | 30,06 | 4.17E+07 | 42,28 |
| placa 2 | Composto 89 | 4751 | 41,82 | 2.11E+07 | 21,40 |
| placa 2 | Composto 90 | 4542 | 39,98 | 3.03E+07 | 30,70 |
| placa 2 | Composto 91 | 1401 | 12,33 | 1.29E+06 | 1,31 |
| placa 2 | Composto 92 | 4210 | 37,06 | 2.95E+07 | 29,90 |
| placa 2 | Composto 93 | 4157 | 36,59 | 2.29E+07 | 23,26 |
| placa 2 | Composto 94 | 4046 | 35,61 | 2.85E+07 | 28,91 |
| placa 2 | Composto 95 | 8368 | 73,66 | 4.02E+07 | 40,72 |
| placa 2 | Composto 96 | 3695 | 32,53 | 2.92E+07 | 29,57 |
| placa 2 | Composto 97 | 3437 | 30,26 | 2,41 E+07 | 24,44 |
| placa 2 | Composto 98 | 4178 | 36,77 | 3.75E+07 | 38,07 |
| placa 2 | Composto 99 | 3739 | 32,91 | 2.10E+07 | 21,29 |
| placa 2 | Composto 100 | 2275 | 20,02 | 1.27E+07 | 12,86 |
| placa 2 | Composto 101 | 3496 | 30,77 | 2.98E+07 | 30,17 |
180/247
| placa 2 | Composto 102 | 4874 | 42,90 | 2.10E+07 | 21,32 |
| placa 2 | Composto 103 | 4228 | 37,22 | 2.69E+07 | 27,32 |
| placa 2 | Composto 104 | 6115 | 53,82 | 4.93E+07 | 49,99 |
| placa 2 | Composto 105 | 6484 | 57,07 | 5.03E+07 | 50,95 |
| placa 2 | Composto 106 | 4211 | 37,06 | 3.94E+07 | 40,00 |
| placa 2 | Composto 107 | 2853 | 25,11 | 1.78E+07 | 18,04 |
| placa 2 | Composto 108 | 3779 | 33,27 | 2.39E+07 | 24,26 |
| placa 2 | Composto 108 | 2869 | 25,26 | 2.04E+07 | 20,71 |
| placa 2 | Composto 110 | 4398 | 38,71 | 2.53E+07 | 25,65 |
| placa 3 | nenhuma ativina A (com Wnt3a) | 2589 | 91,17 | 1.17E+07 | 5,89 |
| placa 3 | Ativina A / Wnt3a | 6933 | 244,13 | 1.98E+08 | 100,00 |
| placa 3 | Composto 111 | 6816 | 240,04 | 5.33E+07 | 26,90 |
| placa 3 | Composto 112 | 5357 | 188,66 | 3.52E+07 | 17,74 |
| placa 3 | Composto 113 | 6002 | 211,37 | 8.55E+07 | 43,11 |
| placa 3 | Composto 114 | 3308 | 116,49 | 3.85E+07 | 19,44 |
| placa 3 | Composto 115 | 5007 | 176,31 | 3.96E+07 | 19,95 |
| placa 3 | Composto 116 | 3802 | 133,89 | 3J2E+07 | 15,75 |
| placa 3 | Composto 117 | 6521 | 229,64 | 4.16E+07 | 20,97 |
| placa 3 | Composto 118 | 6128 | 215,81 | 5.53E+07 | 27,91 |
| placa 3 | Composto 119 | 4184 | 147,35 | 3,41 E+07 | 17,21 |
| placa 3 | Composto 120 | 2489 | 87,66 | 2.87E+07 | 14,49 |
| placa 3 | Composto 121 | 4985 | 175,54 | 3.94E+07 | 19,87 |
| placa 3 | Composto 25 | 4151 | 146,17 | 4.03E+07 | 20,32 |
| placa 3 | Composto 122 | 6407 | 225,61 | 4.15E+07 | 20,95 |
| placa 3 | Composto 123 | 4465 | 157,24 | 5.35E+07 | 26,99 |
| placa 3 | Composto 124 | 4417 | 155,53 | 4.67E+07 | 23,55 |
| placa 3 | Composto 125 | 6367 | 224,23 | 5.73E+07 | 28,93 |
| placa 3 | Composto 126 | 6157 | 216,82 | 7.47E+07 | 37,70 |
| placa 3 | Composto 127 | 5593 | 196,97 | 5,61 E+07 | 28,28 |
| placa 3 | Composto 128 | 4160 | 146,50 | 4,91 E+07 | 24,77 |
181/247
| placa 3 | Composto 129 | 3778 | 133,03 | 3.54E+07 | 17,88 |
| placa 3 | Composto 130 | 4357 | 153,43 | 4.15E+07 | 20,92 |
| placa 3 | Composto 131 | 6135 | 216,05 | 4.28E+07 | 21,61 |
| placa 3 | Composto 132 | 4421 | 155,69 | 4.58E+07 | 23,12 |
| placa 3 | Composto 133 | 7069 | 248,94 | 6.52E+07 | 32,88 |
| placa 4 | nenhuma ativina A (com Wnt3a) | 3274 | 86,62 | 1.25E+07 | 12,79 |
| placa 4 | Ativina A / Wnt3a | 4158 | 110,03 | 9.79E+07 | 100,00 |
| placa 4 | Composto 134 | 5277 | 139,62 | 3.43E+07 | 35,04 |
| placa 4 | Composto 64 | 5657 | 149,67 | 3.38E+07 | 34,48 |
| placa 4 | Composto 135 | 2790 | 73,83 | 1.63E+07 | 16,63 |
| placa 4 | Composto 34 | 4774 | 126,33 | 4.35E+07 | 44,47 |
| placa 4 | Composto 136 | 4881 | 129,16 | 3.20E+07 | 32,73 |
| placa 4 | Composto 137 | 1740 | 46,05 | 9.16E+06 | 9,35 |
| placa 4 | Composto 30 | 6367 | 168,46 | 4.22E+07 | 43,13 |
| placa 4 | Composto 37 | 5377 | 142,27 | 2.85E+07 | 29,14 |
| placa 4 | Composto 138 | 7722 | 204,32 | 3.07E+07 | 31,37 |
| placa 4 | Composto 139 | 3574 | 94,56 | 1.30E+07 | 13,32 |
| placa 4 | Composto 140 | 3893 | 103,00 | 1.12E+07 | 11,46 |
| placa 4 | Composto 39 | 6114 | 161,77 | 3.45E+07 | 35,22 |
| placa 4 | Composto 141 | 4310 | 114,04 | 1.61E+07 | 16,48 |
| placa 4 | Composto 142 | 5091 | 134,71 | 3.74E+07 | 38,22 |
| placa 4 | Composto 35 | 6601 | 174,65 | 8.50E+07 | 86,77 |
| placa 4 | Composto 143 | 3582 | 94,79 | 2.17E+07 | 22,14 |
| placa 4 | Composto 144 | 6787 | 179,57 | 5.45E+07 | 55,69 |
| placa 4 | Composto 145 | 3752 | 99,29 | 2.23E+07 | 22,81 |
| placa 4 | Composto 146 | 2554 | 67,59 | 1.83E+07 | 18,71 |
| placa 4 | Composto 112 | 3289 | 87,03 | 1.48E+07 | 15,11 |
| placa 4 | Composto 113 | 3819 | 101,06 | 2.34E+07 | 23,93 |
| placa 4 | Composto 114 | 1259 | 33,32 | 1.34E+07 | 13,67 |
| placa 4 | Composto 22 | 5517 | 145,98 | 7.09E+07 | 72,39 |
182/247
| placa 4 | Composto 150 | 5104 | 135,04 | 3.34E+07 | 34,11 |
| placa 5 | nenhuma ativina A (com Wnt3a) | 7159 | 116,70 | 8.12E+06 | 2,51 |
| placa 5 | Ativina A / Wnt3a | 10619 | 173,09 | 3.23E+08 | 100,00 |
| placa 5 | Composto 151 | 2785 | 45,39 | -1.03E+06 | -0,32 |
| placa 5 | Composto 152 | 4693 | 76,50 | -3.08E+06 | -0,95 |
| placa 5 | Composto 153 | 9718 | 158,40 | -1.20E+06 | -0,37 |
| placa 5 | Composto 154 | 3479 | 56,70 | -1.97E+06 | -0,61 |
| placa 5 | Composto 155 | 9343 | 152,28 | -3,45E+06 | -1,07 |
| placa 5 | Composto 156 | 3813 | 62,16 | -2.58E+05 | -0,08 |
| placa 6 | nenhuma ativina A (com Wnt3a) | 3264 | 68,37 | 2.52E+06 | 0,80 |
| placa 6 | Ativina A / Wnt3a | 9902 | 207,40 | 3.14E+08 | 100,00 |
| placa 6 | Composto 157 | 2480 | 51,94 | -1.22E+06 | -0,39 |
| placa 6 | Composto 158 | 5271 | 110,41 | -1.30E+06 | -0,41 |
| placa 6 | Composto 159 | 6478 | 135,68 | -1.84E+06 | -0,59 |
| placa 6 | Composto 160 | 4212 | 88,21 | 1.30E+05 | 0,04 |
| placa 6 | Composto 161 | 2439 | 51,09 | -9.20E+05 | -0,29 |
| placa 6 | Composto 162 | 1260 | 26,39 | -1.35E+06 | -0,43 |
| placa 7 | nenhuma ativina A (com Wnt3a) | 9545 | 156,12 | -4.87E+06 | -0,99 |
| placa 7 | Ativina A / Wnt3a | 20064 | 328,17 | 4.92E+08 | 100,00 |
| placa 7 | Composto 163 | 16557 | 270,81 | -7,31 E+06 | -1,49 |
| placa 7 | Composto 164 | 16472 | 269,42 | -7.37E+06 | -1,50 |
| placa 7 | Composto 165 | 3015 | 49,32 | -7.34E+06 | -1,49 |
| placa 7 | Composto 166 | 13845 | 226,45 | -7.98E+06 | -1,62 |
| placa 7 | Composto 167 | 10325 | 168,87 | -7.35E+06 | -1,49 |
| placa 7 | Composto 168 | 14139 | 231,26 | -6.49E+06 | -1,32 |
| placa 7 | Composto 169 | 4468 | 73,08 | -6.38E+06 | -1,30 |
| placa 8 | nenhuma ativina A (com Wnt3a) | 6868 | 179,83 | -2,31 E+06 | -0,52 |
183/247
| placa 8 | Ativina A / Wnt3a | 18575 | 486,35 | 4.47E+08 | 100,00 |
| placa 8 | Composto 170 | 13140 | 344,04 | -4.13E+06 | -0,93 |
| placa 8 | Composto 171 | 10894 | 285,22 | -2,61 E+06 | -0,58 |
| placa 8 | Composto 172 | 3416 | 89,44 | -4.72E+06 | -1,06 |
| placa 8 | Composto 173 | 8815 | 230,81 | -4.25E+06 | -0,95 |
| placa 8 | Composto 174 | 11760 | 307,91 | -3.33E+06 | -0,75 |
| placa 8 | Composto 175 | 5 | 0,13 | -4,91 E+06 | -1,10 |
| placa 8 | Composto 176 | 10139 | 265,47 | -4.73E+06 | -1,06 |
| placa 8 | Composto 177 | 9994 | 261,68 | -2.95E+06 | -0,66 |
| placa 8 | Composto 178 | 8998 | 235,58 | -3.74E+06 | -0,84 |
| placa 5 | nenhuma ativina A (com Wnt3a) | 7159 | 67,42 | 8,12E+06 | 2,51 |
| placa 5 | Ativina A / Wnt3a | 10619 | 100,00 | 3.23E+08 | 100,00 |
| placa 5 | Composto 21 | 4719 | 44,44 | -1.96E+06 | -0,61 |
| placa 5 | Composto 22 | 2036 | 19,18 | -1.79E+06 | -0,55 |
| placa 5 | Composto 23 | 2563 | 24,13 | -1.56E+06 | -0,48 |
| placa 5 | Composto 24 | 4470 | 42,09 | -7.05E+05 | -0,22 |
| placa 5 | Composto 24 | 6085 | 57,30 | -3.08E+06 | -0,95 |
| placa 5 | Composto 26 | 7276 | 68,52 | -2.38E+06 | -0,74 |
| placa 5 | Composto 27 | 4588 | 43,20 | -5.63E+05 | -0,17 |
| placa 5 | Composto 28 | 2682 | 25,26 | -1.37E+06 | -0,43 |
| placa 5 | Composto 29 | 5778 | 54,41 | -1.94E+06 | -0,60 |
| placa 5 | Composto 30 | 620 | 5,84 | -5.05E+06 | -1,56 |
| placa 5 | Composto 31 | 3419 | 32,19 | -1.42E+06 | -0,44 |
| placa 6 | nenhuma ativina A (com Wnt3a) | 3264 | 69,07 | 2.52E+06 | 0,80 |
| placa 6 | Ativina A / Wnt3a | 9902 | 209,51 | 3.14E+08 | 100,00 |
| placa 6 | Composto 32 | 2142 | 45,32 | -1.33E+06 | -0,42 |
| placa 6 | Composto 33 | 5564 | 117,73 | -8.63E+05 | -0,27 |
| placa 6 | Composto 34 | 5927 | 125,41 | -2,01 E+06 | -0,64 |
| placa 6 | Composto 35 | 10068 | 213,01 | -2.15E+06 | -0,68 |
184/247
| placa 6 | Composto 36 | 5170 | 109,39 | -1.22E+06 | -0,39 |
| placa 6 | Composto 37 | 3098 | 65,55 | 1,91 E+06 | 0,61 |
| placa 6 | Composto 38 | 1537 | 32,52 | 4.48E+04 | 0,01 |
| placa 6 | Composto 39 | 3650 | 77,23 | -2,01 E+06 | -0,64 |
| placa 6 | Composto 40 | 5817 | 123,07 | 4,91 E+05 | 0,16 |
| placa 6 | Composto 64 | 4359 | 92,23 | -1.07E+05 | -0,03 |
| placa 6 | Composto 30 | 4035 | 85,38 | 2.09E+06 | 0,66 |
| placa 6 | Composto 65 | 3279 | 69,37 | -5.63E+05 | -0,18 |
| placa 6 | Composto 67 | 2698 | 57,08 | -1.95E+06 | -0,62 |
| placa 7 | nenhuma ativina A (com Wnt3a) | 9545 | 321,22 | -4.87E+06 | -0,99 |
| placa 7 | Ativina A / Wnt3a | 20064 | 675,20 | 4.92E+08 | 100,00 |
| placa 7 | Composto 68 | 10894 | 366,62 | -5.15E+06 | -1,05 |
| placa 7 | Composto 69 | 9734 | 327,58 | -3.97E+06 | -0,81 |
| placa 7 | Composto 70 | 16736 | 563,21 | -6,51 E+06 | -1,32 |
| placa 7 | Composto 71 | 17999 | 605,71 | -7.38E+06 | -1,50 |
| placa 7 | Composto 72 | 7309 | 245,96 | -6,47E+06 | -1,32 |
| placa 7 | Composto 73 | 8888 | 299,10 | -3.03E+06 | -0,62 |
| placa 7 | Composto 74 | 11496 | 386,85 | -2.67E+06 | -0,54 |
| placa 7 | COMPOSTO 75 | 9739 | 327,74 | -7.75E+06 | -1,57 |
| placa 7 | Composto 76 | 14439 | 485,89 | -4.19E+06 | -0,85 |
| placa 7 | Composto 77 | 12331 | 414,95 | -6.03E+06 | -1,22 |
| placa 7 | Composto 78 | 9702 | 326,49 | -6.57E+06 | -1,33 |
| placa 7 | Composto 79 | 8535 | 287,22 | -6.92E+06 | -1,41 |
| placa 8 | nenhuma ativina A (com Wnt3a) | 6868 | 295,49 | -2,31 E+06 | -0,52 |
| placa 8 | Ativina A / Wnt3a | 18575 | 799,17 | 4.47E+08 | 100,00 |
| placa 8 | Composto 80 | 13939 | 599,68 | -4.23E+06 | -0,95 |
| placa 8 | Composto 81 | 10466 | 450,29 | -4,91 E+06 | -1,10 |
| placa 8 | Composto 82 | 10323 | 444,14 | -4.90E+06 | -1,10 |
| placa 8 | Composto 83 | 14619 | 628,95 | 1.48E+06 | 0,33 |
185/247
| placa 8 | Composto 84 | 14105 | 606,84 | -4.44E+06 | -0,99 |
| placa 8 | Composto 85 | 12172 | 523,66 | -3.48E+06 | -0,78 |
| placa 8 | Composto 86 | 7218 | 310,54 | -4.22E+06 | -0,94 |
| placa 8 | Composto 87 | 5383 | 231,58 | -4.07E+06 | -0,91 |
| placa 8 | Composto 88 | 10419 | 448,27 | -4.27E+06 | -0,96 |
| placa 8 | Composto 89 | 11780 | 506,83 | -3.94E+06 | -0,88 |
| placa 8 | Composto 90 | 7002 | 301,25 | -1.54E+06 | -0,35 |
| placa 8 | Composto 91 | 6224 | 267,78 | -4.53E+06 | -1,01 |
| Tabela 2 | ||
| Composto n° | Número de célula | Intensidade de Sox17 |
| % de controles positivos | % de controles positivos | |
| Composto 17 | 133,8 | -0,7 |
| Composto 95 | 195,0 | 40,7 |
| Composto 138 | 185,7 | 31,4 |
| Composto 87 | 170,7 | 50,4 |
| Composto 144 | 163,2 | 55,7 |
| Composto 35 | 158,7 | 86,8 |
| Composto 30 | 153,1 | 43,1 |
| Composto 105 | 151,0 | 51,0 |
| Composto 39 | 147,0 | 35,2 |
| Composto 104 | 142,5 | 50,0 |
| Composto 29 | 136,0 | 34,5 |
| Composto 22 | 132,7 | 72,4 |
| Composto 37 | 129,3 | 29,1 |
| Composto 134 | 126,9 | 35,0 |
| Composto 150 | 122,7 | 34,1 |
| Composto 142 | 122,4 | 38,2 |
| Composto 136 | 117,4 | 32,7 |
| Composto 80 | 115,2 | 38,6 |
| Composto 34 | 114,8 | 44,5 |
| Composto 102 | 113,5 | 21,3 |
ΛΒΒΓΪΑΤ
| Composto 89 | 110,7 | 21,4 |
| Composto 105 | 105,8 | 30,7 |
| Composto 78 | 105,5 | 31,0 |
| Composto 141 | 103,6 | 16,5 |
| Composto 110 | 102,5 | 25,7 |
| Composto 133 | 102,0 | 32,9 |
| Tabela 3 | ||||||
| Composto n° | tratamentos | Número de célula | Expressão de Sox17 | |||
| Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos | |||
| Nenhum | nenhuma ativina A, com Wnt3a | 23253 | 124,16 | 1.97E+07 | 10,59 | |
| Nenhum | Ativina A / Wnt3a | 18728 | 100,00 | 1.86E+08 | 100,00 | |
| Composto 17 | nenhuma AA (com Wnt3a) | 21445 | 114,51 | 3.43E+07 | 18,48 | |
| Nenhum | nenhuma ativina A, com Wnt3a | 23253 | 124,16 | 1.97E+07 | 10,59 | |
| Nenhum | Ativina A / Wnt3a | 18728 | 100,00 | 1.86E+08 | 100,00 | |
| Composto 22 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 18336 | 97,91 | 3.72E+07 | 20,05 |
| Composto 34 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 18891 | 100,87 | 3.26E+07 | 17,55 |
| Composto 29 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 20221 | 107,97 | 2.83E+07 | 15,27 |
| Composto 39 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 17095 | 91,28 | 2.82E+07 | 15,19 |
| Composto 37 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 15605 | 83,32 | 2.67E+07 | 14,37 |
| Composto 35 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 23823 | 127,20 | 2.54E+07 | 13,69 |
187/247
| Composto 80 | nenhuma AA (com Wnt3a) | EGF+FGF4 | 19864 | 106,07 | 2.33E+07 | 12,54 |
| Composto 141 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 17719 | 94,61 | 2.24E+07 | 12,04 |
| Composto 30 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 18063 | 96,45 | 2.18E+07 | 11,73 |
| Composto 150 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 16833 | 89,88 | 2.16E+07 | 11,63 |
| Composto 144 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 17100 | 91,31 | 2.04E+07 | 11,01 |
| Composto 104 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 17863 | 95,38 | 1.89E+07 | 10,19 |
| Composto 142 | nenhuma AAfcom Wnt3a) | EGF+FGF4 | 18955 | 101,21 | 1.84E+07 | 9,90 |
| Composto 110 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 17534 | 93,62 | 1.76E+07 | 9,45 |
| Composto 78 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 17703 | 94,52 | 1.71E+07 | 9,23 |
| Composto 133 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 16521 | 88,22 | 1.67E+07 | 8,97 |
| Composto 87 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 16495 | 88,07 | 1,55E+07 | 8,33 |
188/247
| Composto 95 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 16900 | 90,24 | 1.43E+07 | 7,72 |
| Composto 136 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 19167 | 102,34 | 7,91 E+06 | 4,26 |
| Composto 105 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 15217 | 81,25 | 7.45E+06 | 4,01 |
| Composto 134 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 17208 | 91,88 | 7.40E+06 | 3,99 |
| Composto 138 | nenhuma AAfcom Wnt3a) | EGF+FGF4 | 16695 | 89,14 | 6.65E+06 | 3,58 |
| Composto 89 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 14652 | 78,24 | 3.89E+06 | 2,10 |
| Composto 90 | nenhuma AAfcom Wnt3a) | EGF+FGF4 | 15903 | 84,92 | 3.53E+06 | 1,90 |
| Composto 102 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 12943 | 69,11 | 2.85E+05 | 0,15 |
| Nenhum | nenhuma ativina A, com Wnt3a | 23253 | 124,16 | 1.97E+07 | 10,59 | |
| Nenhum | Ativina A / Wnt3a | 18728 | 100,00 | 1.86E+08 | 100,00 | |
| Composto 35 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 18294 | 97,68 | 1,99E+07 | 10,70 |
189/247
| Tabela 3B | ||
| Composto n° | Número de célula | Intensidade de Sox17 |
| % de controles positivos | % de controles positivos | |
| Composto 22 | 97,91 | 20,05 |
| Composto 34 | 100,87 | 17,55 |
| Composto 29 | 107,97 | 15,27 |
| Composto 39 | 91,28 | 15,19 |
| Composto 37 | 83,32 | 14,37 |
| Composto 35 | 127,20 | 13,69 |
| Tabela 4 | ||||||
| Composto n° | tratamentos | Número de célula | Expressão de Sox17 | |||
| Número total médio de células | % de controles positivos | Intensidad e total média | % de controles positivos | |||
| Nenhum | nenhuma ativina A (com Wnt3a) | 7107 | 67,96 | -1.27E+07 | -7,94 | |
| Nenhum | Ativina A / Wnt3a | 10459 | 100,00 | 1.60E+08 | 100,00 | |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF | 6942 | 73,43 | 1.27E+06 | 0,74 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 5738 | 60,69 | 3.14E+06 | 1,83 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PD GF-AB | 4453 | 47,10 | 9.30E+05 | 0,54 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PD GF- AB+Muscimol | 10391 | 109,91 | 8.92E+06 | 5,20 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+PDGF- A+VEGF | 5728 | 60,59 | 2.14E+06 | 1,24 |
| Composto 17 | nenhuma AA(com Wnt3a) | FGF4+PDGF- A+VEGF | 13198 | 139,59 | 1.29E+07 | 7,54 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PD GF-A+VEGF | 10480 | 110,85 | 8.97E+06 | 5,23 |
190/247
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PD GF- A+Muscimol | 13649 | 144,37 | 1.45E+07 | 8,43 |
| Nenhum | nenhuma ativina A (com Wnt3a) | 3117 | 34,86 | -1,41 E+06 | -0,72 | |
| Nenhum | Ativina A / Wnt3a | 8942 | 100,00 | 1.95E+08 | 100,00 | |
| Composto 35 | nenhuma AA(com Wnt3a) | EGF | 19334 | 216,23 | 6.62E+07 | 33,86 |
| Composto 35 | nenhuma AA(com Wnt3a) | PDGF-AB | 16662 | 186,34 | 4.95E+07 | 25,33 |
| Composto 35 | nenhuma AA(com Wnt3a) | PDGF-A | 16885 | 188,84 | 4.48E+07 | 22,94 |
| Composto 35 | nenhuma AA(com Wnt3a) | VEGF | 18263 | 204,25 | 3,51 E+07 | 17,98 |
| Composto 35 | nenhuma AAfcom Wnt3a) | FGF4 | 4410 | 49,32 | 3.33E+07 | 17,04 |
| Composto 35 | nenhuma AA(com Wnt3a) | Muscimol | 18867 | 211,00 | 2,61 E+07 | 13,35 |
| Composto 35 | nenhuma AA(com Wnt3a) | PDGF-C | 16642 | 186,12 | 1,85E+07 | 9,46 |
| Composto 35 | nenhuma AA(com Wnt3a) | PDGF-D | 17618 | 197,03 | 1.84E+07 | 9,41 |
| Composto 35 | nenhuma AA(com Wnt3a) | PDGF-B | 14168 | 158,46 | 1.52E+07 | 7,76 |
| Composto 35 | nenhuma AA(com Wnt3a) | PD98059 | 18877 | 211,11 | 1.30E+07 | 6,64 |
| Composto 35 | nenhuma AA(com Wnt3a) | BMP1 | 18849 | 210,81 | 1.29E+07 | 6,59 |
| Composto 35 | nenhuma AA(com Wnt3a) | LY294002 | 18374 | 205,49 | 1.03E+07 | 5,28 |
| Composto 35 | nenhuma AA(com Wnt3a) | BMP4 | 16748 | 187,31 | 8.97E+06 | 4,59 |
191/247
| Composto 35 | nenhuma AA(com Wnt3a) | BMP2 | 16218 | 181,38 | 8.89E+06 | 4,55 |
| Composto 35 | nenhuma AA(com Wnt3a) | BMP7 | 20111 | 224,91 | 8.05E+06 | 4,12 |
| Composto 35 | nenhuma AA(com Wnt3a) | U0124 | 16539 | 184,97 | 7.54E+06 | 3,86 |
| Composto 35 | nenhuma AA(com Wnt3a) | BMP6 | 17838 | 199,50 | 7.32E+06 | 3,75 |
| Composto 35 | nenhuma AA(com Wnt3a) | BMP2/7 | 12042 | 134,67 | 7.08E+06 | 3,62 |
| Composto 35 | nenhuma AA(com Wnt3a) | bicuculina | 19312 | 215,98 | 1.95E+06 | 1,00 |
| Composto 35 | nenhuma AA(com Wnt3a) | U0126 | 19961 | 223,24 | -5.75E+05 | -0,29 |
| Composto 35 | nenhuma AA(com Wnt3a) | bu ti rato | 14238 | 159,24 | -1.85E+06 | -0,94 |
| Nenhum | nenhuma ativina A (com Wnt3a) | 6049 | 45,2 | -1.31E+07 | -5,2 | |
| Nenhum | Ativina A/Wnt3a | 13392 | 100,0 | 2.50E+08 | 100,0 | |
| Composto 20 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 9434 | 70,4 | 1,48E+08 | 59,1 | |
| Composto 17 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 7988 | 59,6 | 1.13E+08 | 45,0 |
192/247
| Composto 16 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 8303 | 62,0 | 9.20E+07 | 36,7 | |
| Composto 13 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 7045 | 52,6 | 7.22E+07 | 28,8 | |
| Composto 19 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 7799 | 58,2 | 6.82E+07 | 27,2 | |
| Composto 92 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 5886 | 44,0 | 5.63E+07 | 22,5 | |
| Composto 93 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 5463 | 40,8 | 4.38E+07 | 17,5 | |
| Composto 94 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 5100 | 38,1 | 4.18E+07 | 16,7 |
193/247
| Composto 95 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 4510 | 33,7 | 3.32E+07 | 13,3 | |
| Composto 96 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 4570 | 34,1 | 3.09E+07 | 12,3 | |
| Composto 97 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 4561 | 34,1 | 2.15E+07 | 8,6 | |
| Composto 98 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3176 | 23,7 | 9.86E+06 | 3,9 | |
| Composto 99 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 1209 | 9,0 | -1.56E+07 | -6,2 | |
| Nenhum | nenhuma ativina A (com Wnt3a) | 15494 | 98,0 | -1,25E+07 | -4,4 | |
| Nenhum | Ativina A/Wnt3a | 15807 | 100,0 | 2.86E+08 | 100,0 |
194/247
| Composto 18 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 8742 | 55,3 | 1.01E+08 | 35,4 | |
| Composto 14 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 8464 | 53,5 | 8.33E+07 | 29,1 | |
| Composto 15 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 7234 | 45,8 | 7.95E+07 | 27,8 | |
| Composto 100 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 6805 | 43,0 | 5.88E+07 | 20,6 | |
| Composto 101 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 5668 | 35,9 | 5.34E+07 | 18,7 | |
| Composto 102 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 6195 | 39,2 | 5.29E+07 | 18,5 |
195/247
| Composto 103 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 7545 | 47,7 | 5.13E+07 | 18,0 | |
| Composto 104 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 4757 | 30,1 | 4.58E+07 | 16,0 | |
| Composto 105 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 6285 | 39,8 | 4.29E+07 | 15,0 | |
| Composto 106 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 5622 | 35,6 | 2.86E+07 | 10,0 | |
| Composto 107 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3951 | 25,0 | 1.72E+07 | 6,0 | |
| Composto 108 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3226 | 20,4 | 1.58E+07 | 5,5 |
196/247
| Composto 109 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3473 | 22,0 | 1.46E+07 | 5,1 | |
| Composto 110 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3703 | 23,4 | 1.32E+07 | 4,6 | |
| Composto 111 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2918 | 18,5 | 1.22E+07 | 4,3 | |
| Composto 112 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2975 | 18,8 | 1.04E+07 | 3,6 | |
| Composto 113 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2910 | 18,4 | 9.18E+06 | 3,2 | |
| Composto 114 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2734 | 17,3 | 6.13E+06 | 2,1 |
197/247
| Composto 115 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2169 | 13,7 | 3.77E+06 | 1,3 | |
| Composto 116 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3107 | 19,7 | 3.52E+06 | 1,2 | |
| Composto 117 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3343 | 21,1 | 5.35E+05 | 0,2 | |
| Composto 118 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 3034 | 19,2 | 2.37E+05 | 0,1 | |
| Composto 119 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2263 | 14,3 | -1.66E+06 | -0,6 | |
| Composto 120 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 1771 | 11,2 | -5.57E+06 | -2,0 |
198/247
| Composto 121 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 1136 | 7,2 | -1.79E+07 | -6,3 | |
| Composto 122 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | 2021 | 12,8 | -2.09E+07 | -7,3 |
| Tabela 5 | ||||||
| Composto n° | tratamentos | Número de célula | Expressão de Sox17 | |||
| Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos | |||
| Nenhum | nenhuma ativina A (com Wnt3a) | 7107 | 67,96 | -1.27E+07 | -7,94 | |
| Nenhum | Ativina A / Wnt3a | 10459 | 100,00 | 1.60E+08 | 100,00 | |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF | 6942 | 73,43 | 1.27E+06 | 0,74 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4 | 5738 | 60,69 | 3.14E+06 | 1,83 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PDG F-AB | 4453 | 47,10 | 9.30E+05 | 0,54 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PDG F-AB+Muscimol | 10391 | 109,91 | 8.92E+06 | 5,20 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+PDGFA+VEGF | 5728 | 60,59 | 2.14E+06 | 1,24 |
| Composto 17 | nenhuma AA(com Wnt3a) | FGF4+PDGF- A+VEGF | 13198 | 139,59 | 1.29E+07 | 7,54 |
| Composto 17 | nenhuma AA(com Wnt3a) | EGF+FGF4+PDG F-A+VEGF | 10480 | 110,85 | 8.97E+06 | 5,23 |
199/247
| Composto 17 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+Muscimol | 13649 | 144,37 | 1.45E+07 | 8,43 |
| Nenhum | nenhuma ativina A (com Wnt3a) | 7107 | 67,96 | -1.27E+07 | -7,94 | ||
| Nenhum | Ativina AZ Wnt3a | 10459 | 100,00 | 1.60Ε+Ό8 | 100,00 | ||
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF | 23887 | 228,40 | -1.01E+07 | -6,32 |
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF+FGF4 | 21268 | 203,36 | 1.36E+06 | 0,85 |
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB | 17611 | 168,39 | 1.28E+07 | 8,03 |
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB+Muscimol | 17949 | 171,62 | 1.54E+06 | 0,96 |
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF+PDGF- A+VEGF | 23242 | 222,23 | 1.23E+07 | 7,72 |
| Composto 35 | nenhuma Wnt3a) | AA(com | FGF4+PDGF- A+VEGF | 16068 | 153,63 | 3.92E+07 | 24,57 |
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+VEGF | 16132 | 154,25 | 9.11E+07 | 57,04 |
| Composto 35 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+Muscimol | 15457 | 147,80 | 6.89E+07 | 43,15 |
| Composto 29 | nenhuma Wnt3a) | AA(com | EGF | 1971 | 18,84 | -1.44E+07 | -9,00 |
| Composto 29 | nenhuma Wnt3a) | AA(com | EGF+FGF4 | 7436 | 71,10 | -4.35E+06 | -2,72 |
| Composto 29 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB | 6535 | 62,48 | -7.52E+06 | -4,71 |
| Composto 29 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB+Muscimol | 1376 | 13,15 | -1.42E+07 | -8,91 |
| Composto 29 | nenhuma Wnt3a) | AA(com | EGF+PDGF- A+VEGF | 8880 | 84,91 | -8.53E+06 | -5,34 |
| Composto 29 | nenhuma Wnt3a) | AA(com | FGF4+PDGF- A+VEGF | 8146 | 77,89 | -4.82E+06 | -3,02 |
200/247
| Composto 29 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-A+VEGF | 8858 | 84,70 | -7.15E+06 | -4,48 |
| Composto 29 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-A+Muscimol | 10071 | 96,30 | 2.95E+06 | 1,85 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF | 7966 | 76,17 | -1.19E+07 | -7,42 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF+FGF4 | 6932 | 66,28 | -4.62E+06 | -2,89 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-AB | 7473 | 71,46 | -2,61 E+06 | -1,63 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-AB+Muscimol | 7914 | 75,67 | -1.91E+06 | -1,20 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF+PDGF- A+VEGF | 12956 | 123,88 | -1.25E+07 | -7,82 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | FGF4+PDGF- A+VEGF | 6731 | 64,36 | -1.10E+07 | -6,89 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-A+VEGF | 8778 | 83,93 | 1.39E+05 | 0,09 |
| Composto 37 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-A+Muscimol | 5821 | 55,66 | -1,22E+07 | -7,64 |
| Composto 34 | nenhuma Wnt3a) | AAfcom | EGF | 13062 | 124,89 | 2.78E+07 | 17,39 |
| Composto 34 | nenhuma Wnt3a) | AAfcom | EGF+FGF4 | 13133 | 125,58 | 1.23E+08 | 76,85 |
| Composto 34 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-AB | 12532 | 119,83 | 1.09E+08 | 68,41 |
| Composto 34 | nenhuma Wnt3a) | AAfcom | EGF+FGF4+PDG F-AB+Muscimol | 15811 | 151,18 | 6.90Ε+Ό6 | 4,32 |
| Composto 34 | nenhuma Wnt3a) | AAfcom | EGF+PDGF- A+VEGF | 11801 | 112,84 | 4.04E+06 | 2,53 |
| Composto 34 | nenhuma Wnt3a) | AAfcom | FGF4+PDGF- A+VEGF | 15262 | 145,93 | 1.15E+07 | 7,18 |
201/247
| Composto 34 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+VEGF | 12901 | 123,36 | 5,01 E+07 | 31,35 |
| Composto 34 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+Muscimol | 12208 | 116,72 | 5.56E+07 | 34,83 |
| Nenhum | nenhuma ativina A (com Wnt3a) | 10224 | 108,14 | 7.36E+05 | 0,43 | ||
| Nenhum | Ativina A / Wnt3a | 9455 | 100,00 | 1.72E+08 | 100,00 | ||
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF | 11615 | 122,85 | 1.49E+05 | 0,09 |
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF+FGF4 | 10456 | 110,59 | 5.11E+06 | 2,98 |
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB | 9972 | 105,47 | 1.62E+06 | 0,94 |
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB+Muscimol | 10540 | 111,48 | 2.22E+06 | 1,29 |
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF+PDGF- A+VEGF | 17050 | 180,34 | 4.84E+06 | 2,82 |
| Composto 39 | nenhuma Wnt3a) | AA(com | FGF4+PDGF- A+VEGF | 8856 | 93,67 | 7,01 E+05 | 0,41 |
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+VEGF | 7973 | 84,33 | 5.30E+06 | 3,09 |
| Composto 39 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+Muscimol | 9103 | 96,28 | 7.32E+05 | 0,43 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF | 14105 | 149,19 | 1.75E+06 | 1,02 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF+FGF4 | 12971 | 137,19 | 1.04E+07 | 6,05 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB | 16580 | 175,36 | 8.60E+06 | 5,01 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-AB+Muscimol | 14676 | 155,23 | 5,61 E+06 | 3,27 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF+PDGF- A+VEGF | 20372 | 215,48 | 4.99E+06 | 2,91 |
202/247
| Composto 22 | nenhuma Wnt3a) | AA(com | FGF4+PDGF- A+VEGF | 12277 | 129,85 | 4.90E+06 | 2,86 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+VEGF | 12522 | 132,44 | 7.88E+06 | 4,59 |
| Composto 22 | nenhuma Wnt3a) | AA(com | EGF+FGF4+PDG F-A+Muscimol | 11610 | 122,80 | 1.33E+07 | 7,77 |
| Tabela 6 | ||||||
| Composto n° | tratamentos | Número de célula | Expressão de Sox17 | |||
| Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos | |||
| Nenhum | nenhuma ativina A (com Wnt3a) | 477 | 6,64 | 7.4E+04 | 0,09 | |
| Nenhum | Ativina A1 Wnt3a | 7185 | 100,00 | 8.0E+07 | 100,00 | |
| Composto 34 | nenhuma AA(com Wnt3a) | Nenhum | 4611 | 64,18 | 1.4E+07 | 17,21 |
| Composto 34 | nenhuma AA(com Wnt3a) | EGF | 6145 | 85,53 | 1,5E+07 | 19,18 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF4 | 5323 | 74,09 | 2.7E+07 | 33,75 |
| Composto 34 | nenhuma AA(com Wnt3a) | PDGF-D | 5017 | 69,84 | 1.5E+07 | 18,76 |
| Composto 34 | nenhuma AA(com Wnt3a) | PDGF-A | 4175 | 58,11 | 1.1E+07 | 13,43 |
| Composto 34 | nenhuma AA(com Wnt3a) | VEGF | 4713 | 65,60 | 1,0E+07 | 12,49 |
| Composto 34 | nenhuma AA(com Wnt3a) | GDF8 | 6354 | 88,44 | 7.1E+07 | 88,59 |
| Composto 34 | nenhuma AA(com Wnt3a) | Muscimol | 7286 | 101,41 | 3.1E+07 | 38,38 |
203/247
| Composto 34 | nenhuma AA(com Wnt3a) | PDGF-D+VEGF | 5030 | 70,01 | 1.2E+07 | 14,58 |
| Composto 34 | nenhuma AA(com Wnt3a) | VEGF+Muscimol | 776 | 10,81 | 1,3E+06 | 1,56 |
| Composto 34 | nenhuma AA(com Wnt3a) | PDGF-D+Muscimol | 3490 | 48,57 | 6.5E+06 | 8,02 |
| Composto 34 | nenhuma AA(com Wnt3a) | GDF8+PDGF-D | 6889 | 95,88 | 5.8E+07 | 72,59 |
| Composto 34 | nenhuma AA(com Wnt3a) | PDGF- D+Muscimol+VEGF | 2133 | 29,68 | 2.7E+06 | 3,32 |
| Composto 34 | nenhuma AA(com Wnt3a) | GDF8+PDGF- D+VEGF | 5585 | 77,74 | 6.6E+07 | 81,75 |
| Composto 34 | nenhuma AA(com Wnt3a) | GDF8+VEGF+Musci mol | 6083 | 84,67 | 5.6E+07 | 69,62 |
| Composto 34 | nenhuma AA(com Wnt3a) | GDF8+PDGF- D+VEGF+Muscimol | 9455 | 131,60 | 9.6E+07 | 119,24 |
| Composto 34 | nenhuma A-A, nenhum Wnt3a | EGF+FGF4+PDGF- A+VEGF+PDGF- D+Muscimol+GDF8 | 4757 | 66,21 | 3.9E+07 | 48,77 |
| Composto 34 | nenhuma AA(com Wnt3a) | EGF+FGF4+PDGF- A+VEGF+PDGF- D+Muscimol+GDF8 | 6028 | 83,90 | 7.0E+07 | 87,44 |
204/247
| Tabela 7 | ||||||
| Número de célula | Expressão de Sox17 | |||||
| Piaca | Tratamento | Composto n° | Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos |
| 1 | nenhuma ativina A (com Wnt3a) | Nenhum | 6049 | 45,2 | -1.31E+07 | -5,2 |
| 1 | Ativina A/Wnt3a | Nenhum | 13392 | 100,0 | 2.50E+08 | 100,0 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 18 | 13037 | 97,3 | 1.63E+O8 | 65,2 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 14 | 9344 | 69,8 | 1.23E+08 | 49,0 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 15 | 8448 | 63,1 | 8.64E+07 | 34,5 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 16 | 5498 | 41,1 | 6.56E+O7 | 26,2 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 64 | 5063 | 37,8 | 5.88E+07 | 23,5 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 65 | 4788 | 35,8 | 4.57E+07 | 18,2 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 66 | 8129 | 60,7 | 3.53E+07 | 14,1 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 67 | 6791 | 50,7 | 3.18E+07 | 12,7 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 68 | 3456 | 25,8 | 2.30E+07 | 9,2 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 69 | 3995 | 29,8 | 1.69E+07 | 6,8 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 70 | 474 | 3,5 | -1.80E+07 | -7,2 |
| 2 | nenhuma ativina A (com Wnt3a) | Nenhum | 15494 | 98,0 | -1.25E+07 | -4,4 |
205/247
| 2 | Ativina A/Wnt3a | Nenhum | 15807 | 100,0 | 2.86E+08 | 100,0 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 19 | 8425 | 53,3 | 1.19E+08 | 41,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 13 | 9123 | 57,7 | 1.13E+08 | 39,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 71 | 6048 | 38,3 | 5,51 E+07 | 19,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 72 | 6060 | 38,3 | 5.46E+07 | 19,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 73 | 5545 | 35,1 | 3.99E+07 | 14,0 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 74 | 10898 | 68,9 | 3,91 E+07 | 13,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 75 | 4117 | 26,0 | 3,01 E+07 | 10,5 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 76 | 3825 | 24,2 | 2.74E+O7 | 9,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 77 | 5928 | 37,5 | 2.44E+07 | 8,5 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 78 | 3303 | 20,9 | 2.03E+07 | 7,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 79 | 4767 | 30,2 | 1.85E+07 | 6,5 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 80 | 2194 | 13,9 | 1.22E+07 | 4,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 81 | 2920 | 18,5 | 9.16E+05 | 0,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 82 | 1819 | 11,5 | -1.05E+07 | -3,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 83 | 2153 | 13,6 | -1.19E+07 | -4,2 |
206/247
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 84 | 58 | 0,4 | -2.94E+07 | -10,3 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 85 | 57 | 0,4 | -3.03E+07 | -10,6 |
| 1 | nenhuma ativina A (com Wnt3a) | Nenhum | 6049 | 45,2 | -1.31E+07 | -5,2 |
| 1 | Ativina A/Wnt3a | Nenhum | 13392 | 100,0 | 2.50E+08 | 100,0 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 20 | 9434 | 70,4 | 1.48E+08 | 59,1 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 17 | 7988 | 59,6 | 1.13E+O8 | 45,0 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 16 | 8303 | 62,0 | 9.20E+07 | 36,7 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 13 | 7045 | 52,6 | 7.22E+07 | 28,8 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 19 | 7799 | 58,2 | 6.82E+07 | 27,2 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 92 | 5886 | 44,0 | 5.63E+07 | 22,5 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 93 | 5463 | 40,8 | 4.38Ε+Ό7 | 17,5 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 94 | 5100 | 38,1 | 4.18E+07 | 16,7 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 95 | 4510 | 33,7 | 3.32E+07 | 13,3 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 96 | 4570 | 34,1 | 3.Ο9Ε+Ό7 | 12,3 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 97 | 4561 | 34,1 | 2.15E+07 | 8,6 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 98 | 3176 | 23,7 | 9.86E+O6 | 3,9 |
207/247
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 99 | 1209 | 9,0 | -1.56E+07 | -6,2 |
| 2 | nenhuma ativina A (com Wnt3a) | Nenhum | 15494 | 98,0 | -1.25E+07 | -4,4 |
| 2 | Ativina A/Wnt3a | Nenhum | 15807 | 100,0 | 2.86E+08 | 100,0 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 18 | 8742 | 55,3 | 1.01E+08 | 35,4 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 14 | 8464 | 53,5 | 8.33E+O7 | 29,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 15 | 7234 | 45,8 | 7.95E+07 | 27,8 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 100 | 6805 | 43,0 | 5.88E+07 | 20,6 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 101 | 5668 | 35,9 | 5.34E+07 | 18,7 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 102 | 6195 | 39,2 | 5.29E+07 | 18,5 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 103 | 7545 | 47,7 | 5.13E+07 | 18,0 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 104 | 4757 | 30,1 | 4.58E+07 | 16,0 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 105 | 6285 | 39,8 | 4.29E+07 | 15,0 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 106 | 5622 | 35,6 | 2.86E+O7 | 10,0 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 107 | 3951 | 25,0 | 1.72E+07 | 6,0 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 108 | 3226 | 20,4 | 1.58E+07 | 5,5 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 109 | 3473 | 22,0 | 1.46E+07 | 5,1 |
208/247
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 110 | 3703 | 23,4 | 1.32E+07 | 4,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 111 | 2918 | 18,5 | 1.22E+07 | 4,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 112 | 2975 | 18,8 | 1.04E+07 | 3,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 113 | 2910 | 18,4 | 9.18E+06 | 3,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 114 | 2734 | 17,3 | 6.13E+O6 | 2,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 115 | 2169 | 13,7 | 3.77E+06 | 1,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 116 | 3107 | 19,7 | 3.52E+06 | 1,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 117 | 3343 | 21,1 | 5.35E+05 | 0,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 118 | 3034 | 19,2 | 2.37E+05 | 0,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 119 | 2263 | 14,3 | -1.66E+06 | -0,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 120 | 1771 | 11,2 | -5.57E+06 | -2,0 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 121 | 1136 | 7,2 | -1.79E+07 | -6,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 122 | 2021 | 12,8 | -2.09E+07 | -7,3 |
| 1 | nenhuma ativina A (com Wnt3a) | Nenhum | 6049 | 45,2 | -1.31E+07 | -5,2 |
| 1 | Ativina A/Wnt3a | Nenhum | 13392 | 100,0 | 2.50E+08 | 100,0 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 19 | 15878 | 118,6 | 2.67E+08 | 106,5 |
209/247
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 24 | 12714 | 94,9 | 2.46E+08 | 98,2 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 23 | 12165 | 90,8 | 2.15E+08 | 86,0 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 21 | 12640 | 94,4 | 1.65E+08 | 65,9 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 13 | 11491 | 85,8 | 1.61E+08 | 64,3 |
| 1 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 30 | 11396 | 85,1 | 1.34E+08 | 53,4 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 36 | 7964 | 59,5 | 9.47E+07 | 37,8 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 32 | 8066 | 60,2 | 9.29E+07 | 37,1 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 26 | 7415 | 55,4 | 8.30E+07 | 33,1 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 17 | 6994 | 52,2 | 7.76E+07 | 31,0 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 31 | 6957 | 51,9 | 6.59E+07 | 26,3 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 179 | 3573 | 26,7 | 2.43E+07 | 9,7 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 180 | 922 | 6,9 | -2.20E+07 | -8,8 |
| 1 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 181 | 8 | 0,1 | -2.68E+07 | -10,7 |
| 2 | nenhuma ativina A (com Wnt3a) | Nenhum | 15494 | 98,0 | -1.25E+07 | -4,4 |
| 2 | Ativina A/Wnt3a | Nenhum | 15807 | 100,0 | 2.86E+08 | 100,0 |
| 2 | EGF, FGF, PDGF-A VEGF, PDGF-D, muscimol, GDF8 | Composto 18 | 21102 | 133,5 | 4.18E+08 | 146,3 |
210/247
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 15 | 15373 | 97,3 | 3.74E+08 | 130,8 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 14 | 9008 | 57,0 | 2.62E+08 | 91,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 38 | 9650 | 61,0 | 2.46E+08 | 86,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 35 | 10461 | 66,2 | 1.59E+08 | 55,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 16 | 9064 | 57,3 | 1.48E+08 | 51,8 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 34 | 8907 | 56,3 | 9.99E+07 | 35,0 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 20 | 7346 | 46,5 | 8.90E+07 | 31,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 27 | 8044 | 50,9 | 8,81 E+07 | 30,8 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 28 | 7591 | 48,0 | 8.77E+07 | 30,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 40 | 4049 | 25,6 | 8.23E+07 | 28,8 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 33 | 7485 | 47,4 | 8.10E+07 | 28,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 25 | 6571 | 41,6 | 7.60E+07 | 26,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 182 | 7631 | 48,3 | 6.74E+07 | 23,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 183 | 6777 | 42,9 | 5.93E+07 | 20,8 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 184 | 5475 | 34,6 | 5.44E+07 | 19,0 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 185 | 4093 | 25,9 | 4.92E+07 | 17,2 |
211/247
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 186 | 5274 | 33,4 | 4.63E+O7 | 16,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 187 | 5342 | 33,8 | 4.02E+07 | 14,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 188 | 5533 | 35,0 | 3.98E+07 | 13,9 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 189 | 5928 | 37,5 | 3.96E+07 | 13,9 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 190 | 4822 | 30,5 | 3.90E+07 | 13,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 191 | 4249 | 26,9 | 3,81 E+07 | 13,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 192 | 5616 | 35,5 | 3.54E+07 | 12,4 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 193 | 4158 | 26,3 | 3.23E+07 | 11,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 194 | 3470 | 22,0 | 2.96E+07 | 10,4 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 195 | 3800 | 24,0 | 2.95E+07 | 10,3 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 196 | 4619 | 29,2 | 2.78E+07 | 9,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 197 | 4011 | 25,4 | 2.45E+07 | 8,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 198 | 4367 | 27,6 | 1.92E+07 | 6,7 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 199 | 3162 | 20,0 | 1.20E+07 | 4,2 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 200 | 2087 | 13,2 | 4.43E+06 | 1,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 201 | 1568 | 9,9 | -6.17E+06 | -2,2 |
212/247
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 202 | 5213 | 33,0 | -1,41 E+07 | -4,9 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 203 | 7 | 0,0 | -3.04E+07 | -10,6 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 204 | 11 | 0,1 | -3.18E+07 | -11,1 |
| 2 | EGF, FGF, PDGF-A, VEGF, PDGF-D, muscimol, GDF8 | Composto 205 | 10 | 0,1 | -3.20E+07 | -11,2 |
| Tabela 8 | ||||
| Número de célula | Expressão de Sox17 | |||
| Número total médio | % de controles | Intensidade | % de controles | |
| Composto n° | de células | positivos | TOTAL MÉDIA | positivos |
| Composto 18 | 21102 | 133,5 | 4.18E+08 | 146,3 |
| Composto 15 | 15373 | 97,3 | 3.74E+08 | 130,8 |
| Composto 19 | 15878 | 118,6 | 2.67E+08 | 106,5 |
| Composto 24 | 12714 | 94,9 | 2.46E+08 | 98,2 |
| Composto 14 | 9008 | 57,0 | 2.62E+08 | 91,6 |
| Composto 38 | 9650 | 61,0 | 2.46E+O8 | 86,2 |
| Composto 23 | 12165 | 90,8 | 2.15E+08 | 86,0 |
| Composto 21 | 12640 | 94,4 | 1.65E+08 | 65,9 |
| Composto 13 | 11491 | 85,8 | 1.61E+08 | 64,3 |
| Composto 35 | 10461 | 66,2 | 1.59E+08 | 55,7 |
| Composto 30 | 11396 | 85,1 | 1.34E+08 | 53,4 |
| Composto 16 | 9064 | 57,3 | 1.48E+08 | 51,8 |
| Composto 36 | 7964 | 59,5 | 9.47E+07 | 37,8 |
| Composto 32 | 8066 | 60,2 | 9.29E+07 | 37,1 |
| Composto 34 | 8907 | 56,3 | 9.99E+07 | 35,0 |
| Composto 26 | 7415 | 55,4 | 8.30E+07 | 33,1 |
| Composto 20 | 7346 | 46,5 | 8.90E+07 | 31,2 |
| Composto 17 | 6994 | 52,2 | 7.76E+07 | 31,0 |
| Composto 27 | 8044 | 50,9 | 8,81 E+07 | 30,8 |
213/247
| Composto 28 | 7591 | 48,0 | 8.77E+07 | 30,7 |
| Composto 40 | 4049 | 25,6 | 8.23E+07 | 28,8 |
| Composto 33 | 7485 | 47,4 | 8.10E+07 | 28,3 |
| Composto 25 | 6571 | 41,6 | 7.60E+07 | 26,6 |
| Composto 31 | 6957 | 51,9 | 6.59E+07 | 26,3 |
| Composto 20 | 9434 | 70,4 | 1.48E+08 | 59,1 |
| Composto 17 | 7988 | 59,6 | 1.13E+08 | 45,0 |
| Composto 16 | 8303 | 62,0 | 9.20E+07 | 36,7 |
| Composto 18 | 8742 | 55,3 | 1.01E+08 | 35,4 |
| Composto 14 | 8464 | 53,5 | 8.33E+07 | 29,1 |
| Composto 13 | 7045 | 52,6 | 7.22E+07 | 28,8 |
| Composto 15 | 7234 | 45,8 | 7.95E+07 | 27,8 |
| Composto 19 | 7799 | 58,2 | 6.82E+07 | 27,2 |
| Tabela 9 | |||||||
| tratamentos | Número de célula | Expressão de Sox17 | |||||
| Placa n° | Ativina A | Composto n° | Fatores de crescimento | Número total médio de células | % de controles positivos | Intensidade TOTAL MÉDIA | % de controles positivos |
| 1 | Nenhum | Nenhum | Nenhum | 9164 | 149,46 | -5,91 E+06 | -5,17 |
| 1 | 10 ng/mL de A-A | Nenhum | Nenhum | 6132 | 100,00 | 1.52E+06 | 1,33 |
| 1 | 100 ng/mL de A-A | Nenhum | Nenhum | 9658 | 157,51 | 1.14E+08 | 100,00 |
| 1 | 10 ng/mL de A-A | Composto 22 | EGF+FGF4+PDGF -A+VEGF+PDGFD+Muscimol+GDF 8+Wnt3a | 8556 | 139,53 | 8.78E+07 | 76,82 |
| 1 | 10 ng/mL de A-A | Composto 22 | EGF+FGF4+PDGF -AB+VEGF+Wnt3a | 7657 | 124,87 | 4.70E+07 | 41,09 |
| 1 | 10 ng/mL de A-A | Composto 22 | EGF+FGF4+PDGF | 8100 | 132,10 | 4.42E+07 | 38,65 |
214/247
| A+Muscimol+Wnt 3a | |||||||
| 1 | 10 ng/mL de A-A | Composto 22 | EGF+FGF4+PDGF -AB+Wrrt3a | 7975 | 130,06 | 3.43E+07 | 30,03 |
| 1 | 10 ng/mL de A-A | Composto 22 | EGF+FGF4+Wnt3a | 9800 | 159,83 | 4.59E+O7 | 40,13 |
| 1 | 10 ng/mL de A-A | Composto 22 | FGF4+Wnt3a | 6490 | 105,84 | 4.28E+07 | 37,43 |
| 1 | 10 ng/mL de A-A | Composto 22 | EGF+Wnt3a | 5001 | 81,55 | 2.80E+07 | 24,45 |
| 1 | 10 ng/mL de A-A | Composto 22 | wnt3a | 4543 | 74,09 | 3.05E+07 | 26,65 |
| 1 | 10 ng/mL de A-A | Composto 35 | EGF+FGF4+PDGF -A+VEGF+PDGFD+Muscimol+GDF 8+Wnt3a | 2522 | 41,14 | -4.86E+06 | -4,25 |
| 1 | 10 ng/mL de A-A | Composto 35 | EGF+FGF4+PDGF -AB+VEGF+Wnt3a | 3479 | 56,74 | -3.96E+06 | -3,46 |
| 1 | 10 ng/mL de A-A | Composto 35 | EGF+FGF4+PDGF A+Muscimol+Wnt 3a | 3820 | 62,29 | -1.67E+06 | -1,46 |
| 1 | 10 ng/mL de A-A | Composto 35 | EGF+FGF4+PDGF -AB+Wnt3a | 3263 | 53,21 | -4.56E+06 | -3,99 |
| 1 | 10 ng/mL de A-A | Composto 35 | EGF+FGF4+Wnt3a | 2704 | 44,10 | -4.17E+06 | -3,65 |
| 1 | 10 ng/mL de A-A | Composto 35 | FGF4+Wnt3a | 284 | 4,64 | -7.54E+06 | -6,59 |
| 1 | 10 ng/mL de A-A | Composto 35 | EGF+Wnt3a | 155 | 2,53 | -7.82E+06 | -6,84 |
| 1 | 10 ng/mL de A-A | Composto 35 | wnt3a | 173 | 2,83 | -7,61 E+06 | -6,66 |
215/247
| 1 | 10 ng/mL de A-A | Composto 29 | EGF+FGF4+PDGF -A+VEGF+PDGFD+Muscimol+GDF 8+Wnt3a | 2737 | 44,63 | 2,41 E+07 | 21,10 |
| 1 | 10 ng/mL de A-A | Composto 29 | EGF+FGF4+PDGF -AB+VEGF+Wnt3a | 2283 | 37,23 | 5.59E+06 | 4,88 |
| 1 | 10 ng/mL de A-A | Composto 29 | EGF+FGF4+PDGF A+Muscim ol+Wnt 3a | 4676 | 76,26 | 2,41 E+07 | 21,11 |
| 1 | 10 ng/mL de A-A | Composto 29 | EGF+FGF4+PDGF -AB+Wnt3a | 3964 | 64,65 | 2.27E+07 | 19,89 |
| 1 | 10 ng/mL de A-A | Composto 29 | EGF+FGF4+Wnt3a | 1736 | 28,31 | 1.98E+06 | 1,73 |
| 1 | 10 ng/mL de A-A | Composto 29 | FGF4+Wnt3a | 2139 | 34,89 | 6.98E+06 | 6,10 |
| 1 | 10 ng/mL de A-A | Composto 29 | EGF+Wnt3a | 365 | 5,96 | -4.86E+06 | -4,25 |
| 1 | 10 ng/mL de A-A | Composto 29 | wnt3a | 2090 | 34,09 | 4.89E+06 | 4,28 |
| 2 | Nenhum | Nenhum | Nenhum | 9325 | 121,89 | -3.35E+06 | -3,01 |
| 2 | 10 ng/mL de A-A | Nenhum | Nenhum | 5177 | 67,67 | 3.89E+06 | 3,49 |
| 2 | 100 ng/mL de A-A | Nenhum | Nenhum | 7650 | 100,00 | 1.11E+08 | 100,00 |
| 2 | 10 ng/mL de A-A | Composto 34 | EGF+FGF4+PDGF -A+VEGF+PDGFD+Muscimol+GDF 8+Wnt3a | 18362 | 240,02 | 3.45E+08 | 309,74 |
| 2 | 10 ng/mL de AA | Composto 34 | EGF+FGF4+PDGF -AB+VEGF+Wnt3a | 15574 | 203,58 | 2.59E+O8 | 232,70 |
216/247
| 2 | 10 ng/mL de A-A | Composto 34 | EGF+FGF4+PDGF A+Muscimol+Wnt 3a | 17890 | 233,85 | 2.88E+O8 | 258,30 |
| 2 | 10 ng/mL de A-A | Composto 34 | EGF+FGF4+PDGF -AB+Wnt3a | 17875 | 233,65 | 2.68E+08 | 241,07 |
| 2 | 10 ng/mL de A-A | Composto 34 | EGF+FGF4+Wnt3a | 14158 | 185,07 | 2.40E+08 | 215,35 |
| 2 | 10 ng/mL de A-A | Composto 34 | FGF4+Wnt3a | 13323 | 174,15 | 2.19E+O8 | 196,86 |
| 2 | 10 ng/mL de A-A | Composto 34 | EGF+Wnt3a | 14527 | 189,89 | 2.28E+08 | 204,84 |
| 2 | 10 ng/mL de A-A | Composto 34 | wnt3a | 3589 | 46,91 | 7.02E+07 | 63,08 |
| 2 | 10 ng/mL de A-A | Composto 39 | EGF+FGF4+PDGF -A+VEGF+PDGFD+Muscimol+GDF 8+Wnt3a | 5738 | 75,00 | 2.14E+O7 | 19,24 |
| 2 | 10 ng/mL de A-A | Composto 39 | EGF+FGF4+PDGF -AB+VEGF+Wnt3a | 2531 | 33,08 | 2.82E+06 | 2,53 |
| 2 | 10 ng/mL de A-A | Composto 39 | EGF+FGF4+PDGF A+Muscimol+Wnt 3a | 2879 | 37,64 | 3,61 E+06 | 3,24 |
| 2 | 10 ng/mL de A-A | Composto 39 | EGF+FGF4+PDGF -AB+Wnt3a | 2989 | 39,07 | -1.78E+04 | -0,02 |
| 2 | 10 ng/mL de A-A | Composto 39 | EGF+FGF4+Wnt3a | 734 | 9,59 | -3.93E+06 | -3,53 |
| 2 | 10 ng/mL de A-A | Composto 39 | FGF4+Wnt3a | 521 | 6,81 | -4.46E+06 | -4,01 |
| 2 | 10 ng/mL de A-A | Composto 39 | EGF+Wnt3a | 211 | 2,75 | -4.54E+06 | -4,08 |
217/247
| 2 | 10 ng/mL de A-A | Composto 39 | wnt3a | 518 | 6,78 | -2.37E+06 | -2,13 |
| 2 | 10 ng/mL de A-A | Composto 37 | EGF+FGF4+PDGF -A+VEGF+PDGFD+Muscimol+GDF 8+Wnt3a | 5711 | 74,65 | 1.21E+07 | 10,82 |
| 2 | 10 ng/mL de A-A | Composto 37 | EGF+FGF4+PDGF -AB+VEGF+Wnt3a | 4767 | 62,31 | -5.16E+05 | -0,46 |
| 2 | 10 ng/mL de A-A | Composto 37 | EGF+FGF4+PDGF A+Muscimol+Wnt 3a | 4540 | 59,34 | 9.23E+05 | 0,83 |
| 2 | 10 ng/mL de A-A | Composto 37 | EGF+FGF4+PDGF -AB+Wnt3a | 4223 | 55,20 | -6.15E+05 | -0,55 |
| 2 | 10 ng/mL de A-A | Composto 37 | EGF+FGF4+Wnt3a | 3501 | 45,77 | 5.60E+05 | 0,50 |
| 2 | 10 ng/mL de A-A | Composto 37 | FGF4+Wnt3a | 3930 | 51,37 | -1.88E+06 | -1,69 |
| 2 | 10 ng/mL de A-A | Composto 37 | EGF+Wnt3a | 1431 | 18,70 | -2.75E+06 | -2,47 |
| 2 | 10 ng/mL de A-A | Composto 37 | wnt3a | 791 | 10,34 | -2.99E+06 | -2,68 |
| Tabela 10 | |||||
| Composto n° | tratamentos | Número de célula | Expressão de Sox17 | ||
| Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos | ||
| Nenhum | Nenhuma ativina A (com Wnt3a) | 4273 | 33,70 | 4.75E+07 | 17,49 |
| Nenhum | Ativina A (com Wnt3a) | 12676 | 100,00 | 2.72E+08 | 100,00 |
218/247
| Composto 34 | Nenhuma AA(sem Wnt3a) | FGF (50 ng/mL) | EGF (50 ng/mL) | 13317 | 105,06 | 2,01 E+08 | 74,08 |
| Composto 34 | Nenhuma AAfsem Wnt3a) | FGF (50 ng/mL) | EGF (100 ng/mL) | 14189 | 111,93 | 2,01 E+08 | 73,90 |
| Composto 34 | Nenhuma AA(sem Wnt3a) | FGF (100 ng/mL) | EGF (50 ng/mL) | 12616 | 99,52 | 1.80E+08 | 66,21 |
| Composto 34 | Nenhuma AA(sem Wnt3a) | FGF (100 ng/mL) | EGF (100 ng/mL) | 8269 | 65,23 | 1.13E+08 | 41,73 |
| Composto 34 | nenhuma AA(com Wnt3a) | Nenhum | Nenhum | 11711 | 92,38 | 1.65E+08 | 60,68 |
| Composto 34 | nenhuma AA(com Wnt3a) | Nenhum | EGF (25 ng/mL) | 16052 | 126,63 | 2.14E+08 | 78,82 |
| Composto 34 | nenhuma AA(com Wnt3a) | Nenhum | EGF (50 ng/mL) | 13593 | 107,23 | 1.94E+08 | 71,52 |
| Composto 34 | nenhuma AA(com Wnt3a) | Nenhum | EGF (100 ng/mL) | 13170 | 103,90 | 1.93E+08 | 71,04 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (25 ng/mL) | Nenhum | 18433 | 145,41 | 2.49E+08 | 91,72 |
| Composto 34 | nenhuma AAfcom Wnt3a) | FGF (25 ng/mL) | EGF (25 ng/mL) | 18841 | 148,63 | 2.60E+08 | 95,72 |
219/247
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (25 ng/mL) | EGF (50 ng/mL) | 16232 | 128,05 | 2.30E+08 | 84,79 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (25 ng/mL) | EGF (100 ng/mL) | 9309 | 73,44 | 1.39E+08 | 51,00 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (50 ng/mL) | Nenhum | 12757 | 100,64 | 1.66E+08 | 61,10 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (50 ng/mL) | EGF (25 ng/mL) | 17720 | 139,79 | 2,31 E+08 | 85,01 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (50 ng/mL) | EGF (50 ng/mL) | 16331 | 128,83 | 2.26E+08 | 83,11 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (50 ng/mL) | EGF (100 ng/mL) | 16336 | 128,87 | 2.32E+08 | 85,24 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (100 ng/mL) | Nenhum | 19853 | 156,61 | 2.59E+08 | 95,45 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (100 ng/mL) | EGF (25 ng/mL) | 19880 | 156,83 | 2.59E+08 | 95,47 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (100 ng/mL) | EGF (50 ng/mL) | 18166 | 143,30 | 2.35E+08 | 86,30 |
| Composto 34 | nenhuma AA(com Wnt3a) | FGF (100 ng/mL) | EGF (100 ng/mL) | 11241 | 88,68 | 1,55E+08 | 57,10 |
220/247
| Nenhum | nenhuma AAfcom Wnt3a) | Nenhum | EGF (50 ng/mL) | 5558 | 43,85 | 5,01 E+07 | 18,44 |
| Nenhum | nenhuma AA(com Wnt3a) | Nenhum | EGF (100 ng/mL) | 6818 | 53,79 | 6.42E+07 | 23,62 |
| Nenhum | nenhuma AAfcom Wnt3a) | FGF (50 ng/mL) | Nenhum | 8494 | 67,01 | 6.62E+07 | 24,35 |
| Nenhum | nenhuma AAfcom Wnt3a) | FGF (50 ng/mL) | EGF (50 ng/mL) | 10138 | 79,98 | 7.30E+07 | 26,87 |
| Nenhum | nenhuma AAfcom Wnt3a) | FGF (50 ng/mL) | EGF (100 ng/mL) | 10219 | 80,62 | 7.75E+07 | 28,51 |
| Nenhum | nenhuma AAfcom Wnt3a) | FGF (100 ng/mL) | Nenhum | 9944 | 78,45 | 6.68E+07 | 24,59 |
| Nenhum | nenhuma AAfcom Wnt3a) | FGF (100 ng/mL) | EGF (50 ng/mL) | 11046 | 87,14 | 8.17E+07 | 30,07 |
| Nenhum | nenhuma AAfcom Wnt3a) | FGF (100 ng/mL) | EGF (100 ng/mL) | 7695 | 60,71 | 6.87E+07 | 25,28 |
| Tabela 11 | ||||
| Intensidade de SOX17 normalizada | ||||
| Ativina A | GDF8 | |||
| ng/mL | Média | SD | Média | SD |
| 1600 | 100,00 | 9,20 | 100,00 | 9,00 |
| 800 | 100,00 | 6,60 | 84,90 | 6,30 |
221/247
| 400 | 100,00 | 3,30 | 72,20 | 7,50 |
| 200 | 100,00 | 1,90 | 51,30 | 5,30 |
| 100 | 90,70 | 8,70 | 32,70 | 5,10 |
| 50 | 85,20 | 4,70 | 17,60 | 4,80 |
| 25 | 73,10 | 2,80 | 5,10 | 3,60 |
| 12,50 | 50,90 | 6,20 | 0,90 | 0,80 |
| 6,25 | 18,40 | 4,80 | 0,70 | 1,40 |
| 3,13 | 3,00 | 1,90 | 0,10 | 0,20 |
| 1,56 | 0,10 | 0,00 | 0,00 | 0,20 |
| 0,00 | 0,00 | 0,20 | 0,30 | 0,30 |
| Tabela 12 | |
| nome do marcador | n° de catálogo * |
| AFP | Hs00173490 m1 |
| CD99 | Hs00365982 m1 |
| CD9 | Hs00233521 m1 |
| CDH1 | Hs00170423 m1 |
| CDH2 | Hs00169953 m1 |
| CDX2 | Hs00230919 m1 |
| CER1 | Hs00193796 m1 |
| CXCR4 | Hs00237052 m1 |
| FGF17 | Hs00182599 m1 |
| FGF4 | Hs00173564 m1 |
| FOXA2 | Hs00232764 m1 |
| GAPDH | Hs99999905 m1 |
| GATA4 | HS00171403 m1 |
| GATA6 | Hs00232018 m1 |
| GSC | Hs00418279 m1 |
| HLXB9 | Hs00232128 m1 |
| KIT | Hs00174029 m1 |
| MIXL1 | HS00430824 g1 |
222/247
| NANOG | HS02387400 g1 |
| OTX2 | Hs00222238 ml |
| POU5F1 | HS00742896 s1 |
| SOX17 | Hs00751752 s1 |
| SOX7 | HS00846731 s1 |
| T | Hs00610080 ml |
| ALB | Hs00609411 ml |
| AMY2A | HS00420710 q1 |
| ARX | Hs00292465 ml |
| CDX2 | Hs00230919 ml |
| GAPDH | Hs99999905 ml |
| GCG | Hs00174967 ml |
| HNF4A | Hs00230853 ml |
| INS | Hs00355773 ml |
| ISL1 | Hs00158126 ml |
| MAFA | Hs01651425 s1 |
| MAFB | Hs00534343 s1 |
| NEUROD1 | Hs00159598 ml |
| NEUROG3 | Hs00360700 g1 |
| NKX2-2 | Hs00159616 ml |
| NKX2-5 | Hs00231763 ml |
| NKX6-1 | HS00232355 ml |
| PAX4 | Hs00173014 ml |
| PAX6 | Hs00240871 ml |
| PDX1 | Hs00236830 ml |
| PECAM1 | Hs00169777 ml |
| POU3F4 | HS00264887 s1 |
| PTF1A | Hs00603586 g1 |
| SST | HS00356144 ml |
| ZIC1 | Hs00602749 ml |
223I2A7
| CO 04 m | 04 04 m | CM m | 30.3 | 32.7 | ’’t ci m | 04 co’ m | 04' m | |||||||
| δ ω | 04 oi m | O> rõ | S | s | SST | CO o' m | σ> ΓΜ | CD_ CM | Λ ni | |||||
| δ ω b- | LO CO CM | CO TM | 23,2 | 21,8 | < | 1--------------------------------------------------------------------------------------------- 1 38.4 | ID co m | cd m | CO 3 | |||||
| ll jn Õ D- | rn | CD CD* fM | 30,1 | 27,9 | CO Z> O Q | I---------------------------------------------------------------------------------------------------------------------- 29,5 | o' m | m | £ | |||||
| £ _Q___ | CD —Si | σ>_ ΓΜ | u> CM | 19,3 | 5 δ LU CL | 28,3 | cn | co CM | CD co' CM | |||||
| MANOG | 23,8 | CO CM | 04 CO* CM | CM | δ a | (0 id' | io | CO <d“ ΓΜ | ID CM | |||||
| 5 | CO esL | CD CO* CM. | io | JO | ID CO | ID cd | cm | |||||||
| VIIXL1 | 23,4 | 23,1 | co ΓΜ | 21,5 | 1 | CD o CO. | cn | CM co' CO | 00 o' eft | |||||
| t | id ^»| | 23,9 | s | 21,5 | z | 38,5 | CD m | rn | 04 CO’ m | |||||
| O CO « | co 04' cm | 0Í CM | O)_ CM | o CM | Z ID | CO m | cd m | CO co' m | CO co m | |||||
| oi CM | CD_ fM | CM | 19,6 | É Z CM | CO CD* ΓΜ | Ο cn | 32,2 | O m | ||||||
| JL· | c6 CM | co 04 | OJ CO CM | 20,8 | o o a. Q LU z n | co CM | co | m | O)_ | |||||
| -0XA2 | CO CO* CM | S | s. | s o a: Q LU z | co o' m | IO o’ m | co co' m | CD o’ m | ||||||
| O LL | m co' m | corn | CO 04* co | 29,7 | £ . | 26,8 | σ> cd' | co CD ΓΜ | nJ | |||||
| O U- b* | o | CD σ>* | o' | 04 | £ | ID | CD s | 34,2 | 34,4 | |||||
| a. o X o | oi CM | σ> CM | co CM | CD* 3“ | Lj ω | O_ | ID_ | C0- | ||||||
| SE LU ω | CO* | CO | O>_ | 15,5 | ω z | CD 3 | S' | co | id | |||||
| § o | 00 corn | 04 co m | CO ID m | 35,3 | z T | T— | 21,2 | |||||||
| 04 T Q | tf) fM | CM | CD o' 04. | co' 1=. | o o CD | S' | ID s | CD cd | CO s~ | |||||
| T Q ü | iD_ S | co CO* 04 | 23,6 | 21,2 | a Q O | 04 | ID ci CM | ID 04' | ID 04 CM | |||||
| 8 Q O | (M | ID co' | CO CM | 20,9 | g | 00 o’ | O) o' | S' | (D_ m | |||||
| s o | CO CO CM | co CM | CO CM | 20,8 | 04 o' | cd’ | CD | O) CM | ||||||
| Q S | 0. u_ <r | S' | s | CO m | CM cn | Q o> | 3 .<r | co' | co | CO co' | ID co ΓΜ | |||
| £ o CG > | r Q à | io CD* | co* | ID co' 3=. | c/> £ P co ·> | GAPDH | CO* | S' | S' | 04 CO~ | ||||
| Tabela 13 | Etapa de diferenciação 1 | Tratamento | CG 1 | co S2 c Q Q | 3DF8/ Composto 34 | s £ s § o g Q Q | Etapa de diferenciação 3 | Tratamento Us | c 1 | co 1 Q fO | s f Q. E o O g Q a | 3DF8/ Composto 56 |
224/247
| b φ Τ5 eft & ο co > | S | ro | co | <n o> CM | CN m | Ι- Ο φ Ό CO £ ο co > | □ | 03 σ> CM | 32,1 | 40 CO | COcn | ||
| te cd | CN in cm | 03- | (M | co CN CM | te CD | ID CN CM | CN CM | CD- CM | CN CM | ||||
| < | O | CN CO m | OS O | < É CL | iO_ <O | to ro | ID 3 | 3’ | |||||
| co ZD O | CD cm | CO o> cm | co CM | 40- CM | CO O O o | 03 CM | 03 03 CM | o m | 4O_ ro | ||||
| 1 LU n T- | 03 cd' cm | 40 o> CM | LO rM | CO- CM | ! LU n -τ- | 03 CO CM | 03 03' ΓΜ | 03' CM | O> CM | ||||
| X Q | cm | in | 03 co CM | CN co' CM | § | CN ΛΙ | CD_ | CD_ X | 03 40 CM | ||||
| CD CM | co co’ CM | co CM | CO co CM | 40' CM | •Ν’ 4D‘ CM | CD lD* CM | CO- CM | ||||||
| 1 | 40 | nj | o>_ CM | in in* CM | CO CM | ®' CM | CD* CM | 03* CM | |||||
| 4O_ | 4O_ co | CD os’ CM | os CM | t z | CN CO | 4D O co | CN ro | CN £ | |||||
| Z ID | 40 | ’’T in co | CD_ | CN m | É Z IO | 03' CM | 03 03' CM | CO_ ro | 3 | ||||
| É Z CN | CD s | m CM | co to CM | CN co' CM | g Z CN | 40* CM | (D ID' CN | co 4D* CM | CO cd' CM | ||||
| o 2 a Z_ CO | o>_ ΓΜ | co CM | O> CM | ID ID CM | O O a: Q LU Z CO | 4D CN co | CO CN ro | CN CO | CD CO CO | ||||
| NEDR0D1 | CO cm | 40 co’ CM | CD S | CN CM | s 2 a z | CD- | CO- (M | ||||||
| MAF B | CD co’ cm | CN cm | CD CM | OS CN CM | co' CM | CO* CM | CM | 03 (M | |||||
| £ | m | CN co | CO_ | 03 OS CM | VIAFA | CO CO | V- CO | CO- | CN co | ||||
| Zj co | CO co' ΓΜ | co CM | CN CM | s CD | cb CM | co' CM | co CM | CD- | |||||
| co z | in o’ CM | o' CM | CN CN CM | CD co' | CD Z | 4D co | CD | co CD~ | r— | ||||
| z I | CD o’ cm | CN CM | CM | CO- CM | z X | CM | CN CM | CN CM | CN co' CM | ||||
| CD o co | m σ> | 03 σ> | CO- CM | <D_ | o o o | CN co' | CN co' | CO- | CO co | ||||
| g o | S | CN CN CM | co CN CM | CD CN CM | § Cl | CO CN CM | co' CM | co' CM | co_ s | ||||
| g | co co' CM | IO CM | CO CN CM | g | CN | CN (M | S | to CM | |||||
| CN 1 < | CM | CM | CM | CM | £! | C0_ CM | 4D co' CM | 03 CM | 03 CM | ||||
| 3 <r | CO co | CO σ> | OS CD | CO co' | CQ —1 <r | m co | 03 | CD o CM | <M | ||||
| X Q ã | co co | os co' | 03 co | CO CO* | X Q Q_ ã | (O co' | CO 03 _ | 03 03* n | O .CM | ||||
| Etapa de diferenciação 4 | rratamento\CTs | c I | co $2 c | Q Q | 3 o ω a E o O S3 Q Q | 3DF8/ Composto 56 | Etapa de diferenciação 5 | Tratamento Us | rc co I | 3DF8/Wnt3a | 3DF8/ Composto 34 | 3DF8/ Composto 56 |
225/247
| 7alores de CT | g | co 3' | CM | 34,5 | CD 3 | (0 a> JO co |
| fc co | CM cm cm | cm CM | cm' CM | CM | ||
| É n | co | 33,9 | CM ID* m | |||
| o n | CO cm’ m | ID m | cn co | CM co | ||
| ! LU n | CO. | co cm | 32,9 | CO co | ||
| § n_ | CM σ> CM | ID oo CM | CD CM | cn. CM | ||
| 1 | CD co CM | oo. CM | co CM | CM. | ||
| CD o' m | o' m | o' | CO CD CM | |||
| i z -- | co co | 30,5 | 33,1 | o' CO | ||
| É Z <n | o' co | 32,3 | CO. | CO co m | ||
| â Z CN | 29,6 | CD CM | CM σ> CM | 28,1 | ||
| 0 § Q LU Z co | o | m m | ID 3 | co 3‘ | ||
| Q O CC Q LU Z | CM | in CD CM | co CM | |||
| LL m | cm | co co rxi | co | σ> id ΓΜ | ||
| Í $ | <0 | 35,2 | 34,8 | 34,7 | ||
| Zj co | cd CM | CM co CM. | CO co CM | 25,7 | ||
| co z | 20,5 | 19,3 | o’ CM | CD a> | ||
| z X | ΓΜ | CO s | Si | Si | ||
| 0 o 0 | cn | co | co | |||
| § O | id | CM id CM | CO CM | σ> id CM | ||
| & <r | CD. CM | co co CM | CM | co CM | ||
| CM 1 < | o' | o' | CO. | CD o’ m | ||
| co -J <r | CO. S | m co CM | CO. S | ID CM | ||
| 3APDH | o' CM | o' CM | 21,3 | CM. CM | ||
| Etapa de diferenciação 6 | ξ c Φ E 3 E l- | s c | co co tz | Q 0 | 3 £ g § o & Q 0 | s o to g E o O g5 Q Q |
| Etapa de diferenciação 1 Valor de Ct | t | CO $ | CN 3 | co' co | CD CN CO | CM CO | |
| SOX7 | co CO | 33,3 | 33,7 | CO co | 32,6 | ||
| X o W r- | CM co CM | co CN | CO CN | CO CN CM | CN CN | ||
| POU5F 1 | CO cm CO | CO | 30,8 | 31,3 | 33,3 | ||
| CM g | CO CN | 00. CN | 21,8 | 21,9 | |||
| NANOG | ID. S| | OS Si | co CN | CO. Si | CO CM | co CM | |
| MIXL1 | CD CM | co OO CN | OO CN | oo CM | CO_ _ | ||
| X. | CM co CM | ID id CN | 24,2 | 24,3 | 24,8 | ||
| HLXB9 | 23,4 | CO. | CO CN | 23,1 | Si | CM | |
| O co 0 | CD. CM | CO co CN | CO- CM | 21,9 | 22,3 | CO CM | |
| GATA6 | cm CM | CO CO* CN | CN CM | ID CN CM | co cm CM | CO CM | |
| GATA4 | 23,8 | ID Si | 24,2 | 23,6 | 23,4 | ||
| FOXA2 | s | id CN | 24,2 | 24,2 | 3 | ||
| 0 | 00 | CO 3 | ID —s | 34,4 | 36,5 | ||
| FGF1 7 | 19,8 | CN | 20,1 | o CM | 20,3 | ||
| CXCR4 | cm CM | CO co CN. | CO CM | 22,3 | 22,2 | ||
| CER 1 | ID | 19,5 | co | 18,8 | 18,8 | ||
| CDX2 | O | o | s | CO | o | ||
| CDH | cn o’ CN | co. CM | co CM | o' CM | 00 o’ CM | ||
| CDH1 | co CN | CO. Si | CO. Si | CO. Si | 25,9 | ||
| 8 o Q | CN. Si | ID. Si | Si | Si | ID co’ CM | ||
| CD9 | x— Si | 23,8 | 23,7 | COCO CM | 24,5 | ||
| Q. £ | co id co | 3 | 3 | 34,8 | o | ||
| Q | o CN | o CN | CD | 19,8 | 19,8 | ||
| Tratamento | CU co | CU £2 c i ll Q Ω | GDF8/GSK3 inh BIO | CD O to g E o O Sj LL. O 0 | s CM O to O Q. E o Q co Q 0 | GDF8/ Composto 40 |
226/247
Valor de Ct
| o NJ | CO | o' co | T“ CO | co co | 34,6 | 35,5 | Etapa de diferenciação 4____________________Valor de Ct_____________________________________________________________________________________________________________________________ | o N | CD CXÍ CO | CD S | ID S | |
| ω ω | (N CN co | 31,3 | 32,4 | 32,4 | 32,4 | SST | CO id' CN | CN | 25,6 | |||
| .ο | 30,8 | 30,7 | 30,6 | o CO | 32,4 | 31,5 | Ê< | co CN | co CN | tD co CN | ||
| P0U3F 4 | CD co CXI | g | to σ>~ CN | σ>' CN | 30,2 | 30,2 | POU3F 4 | CN | CN | _ | ||
| PECAM | CO co CXI | 32,2 | 32,2 | co | 30,9 | 31,5 | PECAM | CN σί CN | 31,2 | 30,7 | ||
| PDX1 | CN CN | CO co' CN | 23,2 | σ> CN CN | 23,7 | 23,2 | PDX1 | CO CN | CN co CN | 23,2 | ||
| PAX6 | 35,2 | co | 32,9 | CO co CO | 36,2 | CO | PAX6 | CN | CO_ CN | CN | ||
| PAX Í4 | CD cxi | CN σ> CN | 28,7 | 28,3 | σ> CN | CD CN | PAX 4 | CD ID CXI | 26,2 | CD CN | ||
| NKX6-1 | 28,3 | cd CN | 28,8 | 27,8 | 3 | 29,5 | ΝΚΧ6-1 | CD ID' CN | CO in CN | 26,1 | ||
| NKX2-5 | 34,1 | 37,8 | LD co | 37,6 | o | 37,2 | ΝΚΧ2-5 | CT> co co | 35,4 | 35,4 | ||
| NKX2-2 | 27,3 | 27,9 | CD CN | 27,5 | CO CN | 27,8 | CN 8 z | 24,2 | CÍ | s | ||
| NEUR 0G3 | CXI IO CXI | 26,4 | 26,2 | 25,9 | cxi | 26,2 | NEUR OG3 | co co CN | 24,2 | cxi | ||
| NEURO b, | co ID CXI | CN CN | CO CD CN | CD cd' CN | 27,2 | 27,2 | NEURO D1 | 23,7 | COs | §L | ||
| MAFB | cxi | cxi | CD_ & | CO CN | 27,8 | 27,9 | m i | 24,9 | 24,9 | 25,4 | ||
| MAFA | 3 | s | 34,7 | 3' | 34,2 | 34,5 | Í | 32,4 | 33,1 | ID CN CO | ||
| Σ3 ω | 29,4 | cd CN | 29,3 | 8 | 31,6 | CO | Zj ω | 25,2 | 25,7 | 25,7 | ||
| INS | CXI σ> cxi | σ> CN | 28,8 | 28,5 | 30,3 | o co | INS | CD_ CN | o> CN | CN CN | ||
| z X < | 21,8 | co CN CN | 22,6 | 22,5 | CN CN | 22,5 | z X < | CD_ CN | σ> .s | O>_ 5. | ||
| 0 o 0 | 34,1 | 34,2 | 32,8 | 33,1 | cd 3 | 37,6 | 0 0 0 | CN | 22,6 | 22,3 | ||
| § o | 23,3 | σ> co CN | 23,6 | 3 | CN | 23,8 | § 0 | co CN | co CN | 23,3 | ||
| I | co CXI | σϊ CN | σ>' CN | σ> CN | CD σ> CN | 29,6 | i | CD_ s | 25,3 | CO id ÇN | ||
| CN 1 < | ID cd CN | 30,4 | 30,3 | 30,2 | T“ CO | 30,5 | CN 1 < | co co CN | ID co CN | 28,7 | ||
| 3 | id CN | 26,5 | 25,2 | 26,1 | 26,7 | 25,8 | ? | CO- CN | CO. CN | CN | ||
| GAPD H | σ>. | 18,5 | 18,5 | co' | co | 18,6 | Q L | 18,9 | 18,3 | σ> | ||
| Tratamento | <§ | CO $2 c | s | GDF8/GSK3 inh BIO | GDF8/Composto 19 | CN CN I ε o o «5 Q Q | GDF8/ Composto 40 | Tratamento | CD 1 | GDF8/Wnt3a | GDF8/GSK3 inh BIO |
227/247
| cõ | tf> co | t}4,4 | Etapa de diferenciação 5 Valor de Ct | ZIC1 | 34,1 | 25,6 | 26,3 | 28,8 | 33,8 | 34,8 | |
| tf) to' CM | 26,1 | CO co CM | SST | Rl | 22,7 | CO CM | 22,9 | 22,6 | 22,3 | ||
| CO aõ CM | CO co CM | 28,4 | E <r | to_ CM | 29,1 | 28,7 | 28,2 | 26,4 | |||
| CM | tO_ CM | 27,6 | POU3F 4 | co CM | 28,9 | 28,1 | 28,2 | 29,1 | 29,2 | ||
| eo | 30,2 | 1 | PECAM | _ | 29,2 | 29,2 | 29,8 | 29,9 | 29,9 | ||
| 23,1 | 23,4 | (23,1 | PDX1 | 22,6 | 23,6 | 23,6 | 23,4 | 23,4 | 23,4 | ||
| CO CM | co_ CM | co CM | PAX6 | 5. | 25,6 | 25,6 | 25,6 | 25,8 | 26,4 | ||
| to' CM | 25,8 | σ> tO~ CM | PAX 4 | 26,4 | 27,2 | 27,3 | 26,8 | 27,2 | 27,3 | ||
| tf)' CM | CO CM | CD tf) CM | ΝΚΧ6-1 | tf> CM | CO to CM | tf) CM | tf) CM | CO Cl | ID CM | ||
| σ> tf)' CO | 35,7 | 37,3 | NKX2-5 | CO CO | co co | O | 34,6 | o | CO 3 | ||
| 24,6 | 24,5 | 24,6 | ΝΚΧ2-2 | (N | 24,2 | s | CM | 23,2 | 23,5 | ||
| σ> co CM | CM | 24,2 | NEUR OG3 | CM | CO co' CM | 28,4 | 28,6 | 28,2 | co CM | ||
| CD co' CM | 24,2 | NEURO D1 | CM | 22,6 | 22,9 | CO cm CM | CO Rí | tf) cm' Cl | |||
| id CM | IO tf) CM | co to CM | m 1 | CO_ 8 | σ> CO Cl | 23,8 | 23,8 | CO CO CM | 23,9 | ||
| s | 33,3 | 33,5 | MAFA | 33,7 | 32,6 | 33,5 | 33,2 | cm Q. | CM J | ||
| 25,6 | 25,5 | CO CM | Zj ω | 23,4 | s | 23,8 | 23,2 | 23,9 | |||
| CM CM | CO cm CM | INS | 16,9 | CD | l< | 16,8 | 17,1 | ||||
| 22,2 | 22.1 | CO R| | HNF4 | o>_ 5. | 22,3 | 22,4 | 22,6 | 22,2 | 22,2 | ||
| 5 | cm CM | co Rl | GCG | 16,2 | CM_ | CM_ | r- | co | 16,9 | ||
| to co’ CM | 23,6 | h,7 | CDX2 | CD co CM | CO co' Cl | CM S | 24,2 | σ> co CM | CM_ §L | ||
| CM tf) CM | tf) CM | 25,5 | 1 | co’ CM | 23,8 | S | 23,4 | co CM | 23,7 | ||
| O) co' CM | 29,2 | 29,4 | CM 1 < | CO co Cl | co Cl | o> Cl | CO co CM | σ> CM | CD CM | ||
| CM | CD o CM | ▼— CM | CD _ | 19,5 | 19,9 | 19,2 | O CM | o Cl | 19,5 | ||
| 18,9 | σ> | 19,2 | GAPD H | σ> | co | σ> | σ> | 19,2 | 19,6 | ||
| σ> o Io a E o O 5δ u_ Q Ω. | GDF8/ Composto 202 | o o I <3 & Q Ç2. | Tratamento | δ | GDF8A/Vnt3a_______ | GDF8/GSK3 inh BIO | σ> ο ü) a E Ο Ο cõ LL Q £ | CM O CM O 1» a 1 Si Q 2 | GDF8/ Composto 40 |
228/247
| Η U a. ο £ •8 g O | H | tf | á | 33,8 | 32,7 | 29,6 | m to co | 32,8 | tf) co co | 34,6 | CD CM CO | |
| δ w | CO CM CO | 31,2 | 33,0 | 32,0 | 33,0 | 32,1 | m cm co | cm co | 32,4 | 29,8 | ||
| δ ω r- | CD CN | CM_ CM | CM cm CM | CM | 22,3 | 22,6 | co cm CM | co CM | 23,3 | 25,2 | ||
| POU5F 1 | CM CM CO | CD cõ | 32,8 | 32,1 | 32,1 | 32,7 | 33,6 | co s | 33,2 | 29,5 | ||
| 0TX2 | tf) tf | 19,9 | CO cm ÇM | 20,3 | 22,9 | 22,5 | 22,0 | co CM ÇM | O tf | 24,3 | ||
| 8 z 2 | s | 22,7 | 24,8 | co CM | 3 | 24,5 | 23,8 | 24,9 | 23,9 | 25,0 | ||
| Sd s | O) CO CM | CM | CO CM | 27,9 | m σ> CM | & | 28,0 | tf) co CM | CD CM | CD O CO | ||
| ΚΓΤ | tf | σ> cm CM | OÍ | CD tf | CD tf | 23,9 I | 22,9 | co CM | co CM | tf) CM | ||
| HLXB9 | CO 3 | (O co CM | m tf) CM | 24,8 | o co CM | CM tf) CM | tf) tf) CM | CM tf) CM | 3 | CO tf) CM | ||
| O w O | cm CM | CO cm CM | 00 o CM | 22,5 | CO S | co S | O) o CM | CM cm CM | CD cm CM | CM 3 | ||
| <: δ <o | 22,9 | 21,8 | 22,9 | 22,6 | 22,7 | 23,0 | 22,5 | CM CO CM | tf | 24,8 | ||
| GATA4 I___________________________________________________________________________ | 25,0 | 23,1 | s | 23,1 | 25,1 | 24,5 | 24,6 | O tf) CM | cq 3 | 27,5 | ||
| F0XA2 | tf) CM | 22,9 | 25,6 | 24,0 | 25,6 | 25,7 | 25,5 | 25,8 | 3 | 25,9 | ||
| FGF4 | 34,0 | 33,4 | 35,1 | 34,0 | 32,8 | 36,0 | 35,1 | 36,0 | 36,2 | 34,9 | ||
| fe | 20,7 | co | 20,1 | 18,9 | 20,5 | 20,4 | 20,2 | σ> o ÇM | o CM | 22,1 | ||
| 2 O X o | o CM | o cm ÇM | O —tf | 22,0 | 17,7 | 22,0 | cm CM | 22,2 | 19,6 | CD 3 | ||
| te LU O T- | 18,3 | 17,1 | 18,2 | CM | CD | 18,3 | r-_ | 18,5 | 18,3 | o CM | ||
| o | 36,0 | O o | σ> m' co | 35,2 | O o | O o | o o | tf) tf) Q | O o | O o ’í | ||
| r Q O | 21,8 | 20,9 | 20,7 | CM | 20,8 | CM | 20,4 | 21,9 | CM | 22,3 | ||
| CDH 1 | 26,1 | s | O CD Ç1 | 25,9 | 26,3 | 25,9 | 25,8 | cm CM | 25,5 | 25,2 | ||
| 6 600 | 24,0 | 22,0 | 23,3 | 21,6 | 24,9 | I 23,7 _________________________________________________________________________! | 23,6 | 23,7 | 23,7 | 25,9 | ||
| CD9 | CM m CM | tf) co CM | tf) 3 | 23,6 | s | tf) CM | CD 3 | tf) CM | CD 3 | tf) tf) Cl | ||
| CL £ | CO cm <o | O o | o o | 34,2 | 35,4 | O tf | O tf | O tf) CO | o o ’’T | 40,0 | ||
| Q È^ | 194 | 18,2 | 20,1 | co | 20,1 | co o CM | 19,9 | 20,2 | 19,8 | 21,6 | ||
| Tabela 15 | Etapa 1 | Tratamento | CO ! | cõ I 8 E O O 1 | AA+Composto 180 | O) i 8 E O O í | AA+Composto 202 | O 8 § o â | AA+GSK3 inhib BIO | AA+Composto 206 | GDF8 |
229/247
| 32,6 | 31,9 | 32,3 | CO o' CN | 32,5 | CN co | CD X | CO co’ co |
| m χ· | 32,8 | CO CN CO | CN <O | 32,0 | CN CO | 33,7 | co CN CO |
| ο in CN | 23,7 | CN S | CD CN CN | CO X | CO CN | CO CO' CN | S |
| x— cõ | CO s | CN co' g> . | CO_ CO | 30,0 | CD S | CO | X |
| 24,4 | 23,3 | 23,0 | & | 21,5 | 22,2 | 21,8 | 22,2 |
| CO s | in CN | CO cd' CN | co CN | 25,1 | s | CO ni | X |
| 30,5 | 28,1 | 28,3 | 28,5 | CN | 28,5 | 29,3 | 29,7 |
| m CN | CO co £N | 25,8 | CD CN CN | 25,9 | in CN | o in CN | in CN |
| 25,0 | 24,3 | 24,2 | 24,0 | 23,1 | 23,4 | a | 23,8 |
| 23,8 | 23,6 | 23,6 | 22,1 | 23,5 | 23,4 | 22,7 | 23,6 |
| a | 23,9 | 23,9 | CO CN CN | 22,5 | 22,6 | —S | o —X |
| 27,3 | 25,4 | 25,2 | O in CN | —S | CN s | 24,5 | 24,9 |
| 25,7 | 25,2 | 25,0 | 24,2 | 23,6 | 24,9 | a | 25,3 |
| 34,8 | 36,3 | 36,6 | 33,2 | 34,3 | 35,4 | 34,8 | 34,5 |
| 22,0 | tn S | CN | 20,4 | 19,9 | 20,5 | 20,1 | 20,3 |
| CD CO CN | 23,0 | X | co CN | S | 22,4 | 23,3 | o CO CN |
| cn | o o' CN | 19,9 | 18,0 | 18,5 | 18,2 | 17,7 | CO |
| o o’ Ν’ | o o' | X | 40,0 | 35,8 | 33,8 | 33,4 | 29,9 |
| CD CN CN | 22,4 | 22,1 | 20,7 | o' | 20,5 | 20,0 | o CM |
| in CN | m in CN | 26,9 | 24,6 | co —Si | 24,7 | 24,3 | 23,2 |
| 25,8 | 23,6 | 24,0 | 23,7 | 20,2 | 22,6 | 21,8 | 22,5 |
| o in CN | in CN | CD m CN | 23,9 | 22,1 | o co CN | CO CN | X |
| 40,0 | 40,0 | 40,0 | o o' | 30,6 | 40,0 | 30,1 | o o' Ν' |
| 21,2 | 20,7 | 20,9 | 19,6 | 18,5 | o' | 19,6 | σ> |
| CO $2 E co Q <2 | GDF8+Compostol 81 | GDF8+Composto 180 | GDF8+Compostol 9 | GDF8+Composto 202 | GDF8+Composto 40 | GDF8+GSK3 inhib BIO | GDF8+Composto 206 |
230/247
| Valores de RT-PCR CT | δ Ν | 34,8 | o o’ | 34,8 | 34,4 | o o’ | 40,0 | in” Q | O) X | o o’ s | cd' £1 | CM co £1 |
| SST L | CM CO’ co | 32,8 | 34,6 | 34,7 | o o’ | 34,2 | 35,3 | 35,2 | 31,9 | 29,5 | CM | |
| iPTF1 | 34,6 | o o’ | 36,0 | 40,0 | o | o o' | 35,6 | 40,0 | 35,0 | 34,2 | 34,0 | |
| POU3F | 30,5 | 30,7 | 30,8 | 31,3 | 40,0 | 31,9 | 31,3 | 32,4 | 31,2 | 30,8 | 29,8 | |
| PECA Μ | 31,0 | 30,9 | 30,0 | 28,9 | o o’ | 29,7 | 30,3 | 31,0 | 29,7 | 30,0 | 32,2 | |
| PDX1 L. | 23,3 | 23,8 | 25,0 | 26,3 | 40,0 | CM | 24,8 | 26,1 | 23,9 | 25,5 | 23,1 | |
| ΡΑΧ6 | o o’ | 38,1 | 40,0 | 36,2 | o | CD s | o o’ | o o’ | g | co_ S | co in CM | |
| ΡΑΧ4 | co | 31,9 | 33,3 | 35,3 | 40,0 | 32,0 | 32,9 | 34,9 | 31,5 | 32,4 | 31,5 | |
| ΝΚΧ6-1 | 32,2 | σ> s | 35,8 | 35,3 | 40,0 | 33,9 | 34,4 | 40,0 | 35,0 | o in' co | 32,9 | |
| ΝΚΧ2- 5 | CD 3 | o o’ | 33,9 | 32,5 | o o’ | CD 8 | 33,6 | 32,6 | CO cm CO | 34,4 | o o | |
| ΝΚΧ2- 2 | 29,3 | 29,0 | 30,3 I | CO | o o' | m CT> CM | 30,3 | 31,8 | CO σ> CM | 30,3 | 29,1 | |
| NEUROG 3_______ | o co CM | co CM | 29,0 | 30,3 | o o’ | 28,5 | 29,1 | o_ δ | CD co* CM | CD CM | IO CM | |
| NEMOD1 | o’ CO | 30,4 | CO | 32,6 | 40,0 | 30,0 | 30,8 | o 3 | £ | CO o' £9. | 30,1 | |
| MAFB i____________________________________________________________________________________________ | CM | CM | 28,5 | 28,6 | 34,9 | 28,2 | co' CM | co δ | CO δ | 27,2 | 26,1 | |
| MAFA | 36,4 | 33,9 | 34,6 | 34,3 | 40,0 | 35,1 | 34,1 | 34,9 | 34,4 | 33,6 | I 30,5 | |
| L ω | 29,3 | 28,8 | 30,4 | 29,4 | o o | 29,8 | 29,7 | 30,2 | co CM | 28,5 | 26,3 | |
| INS | 34,8 | ko | 40,0 | o o | o o' | 35,1 | o o’ _ | o o’ | o o’ | o o’ | 40,0 | |
| z I < | 22,4 | 22,4 | 22,3 | 1O _ | co | CD cm' CM | 22,3 | in CM | in _ | CD co £1 | 22,4 | |
| O 0 0 | 34,7 | 40,0 | 35,1 | o ? | CO 3 | o | o o’ | 35,7 | 40,0 | 35,1 | ||
| g o | σ> | o co' CM | 22,3 | 22,5 | o —s | m Rí | CM CM' n | 22,0 | 23,8 | 23,1 | ||
| 32,0 | 33,0 | 34,2 | 33,3 | 40,0 | 33,0 | 34,9 | 34,6 | co' co | 35,3 | 33,8 | ||
| 1 <r | 30,6 | 30,2 | 30,1 | 30,0 | o | 30,7 | o’ co | o’ co | co o’ co | 30,4 | 29,5 | |
| m | 26,9 | CO CM | o co CM | 25,5 | o o’ | 26,2 | 25,8 | 24,9 | o CM | 28,7 | 27,0 | |
| GAPD H | 18,5 | co | 18,6 | 18,8 | 34,1 | 18,5 | 18,5 | 18,5 | 18,3 | 18,0 | 17,4 | |
| CO CO Q 43 UI | Tratamento | AA | CO CO Έ 1 | AA+Composto 181 | AA+Composto 180 | σ> g g 1 | AA+Composto 202 | o 1 g E o Q + $ | AA+GSK3 inhib BIO | AA+Composto 206 | GDF8 | (0 £2 co O _____<2. |
231/247
| 34,5 | o 3 | 10 CO CO | o 3 | o o | 40,0 | 30,3 |
| CN <o | 34,4 | 3' | 30,9 | 33,7 | 33,6 | 29,2 |
| 33,9 | CD 3 | 40,0 | 31,6 | 36,3 | 34,8 ! | 33,0 |
| 10 ο CO | CO 8 | 31,6 _ | 30,2 | 30,5 | 30,0 | 30,8 |
| 29,4 | 31,6 | 29,4 | 30,1 | 29,2 | 30,4 | 32,7 |
| 23,5 | 23,7 | 25,0 | 23,0 | 23,2 | 24,0 | 23,3 |
| 10 co | 40,0 | 35,0 | 31,8 | o o | 35,1 | CN |
| 30,5 | 31,2 | 34,4 | 30,4 | 31,5 | 30,6 | 31,3 |
| 32,5 | 32,6 | 35,2 | 30,5 | 32,9 | 33,9 | 32,3 |
| 10' co | 35,4 | 134,4 | 35,7 | 35,3 | 34,6 | 40,0 |
| o co' CN | 29,0 | 32,2 | 28,4 | 28,8 | 27,9 | 29,3 |
| O CN | 10- CN | io_ cõ | CN | CO δ | 26,8 | £5 |
| CD 00 CN | 30,0 i______________________________________________________________________________________________________________________________________________ | CO co co | CD cd CN | o'oe | 29,2 | 29,9 |
| CO CN | CN | CO* CN | CD CN | 27,5 | 27,6 | T~ CN |
| 35,5 | 35,9 | 10 3 | CN 3 | 34,3 | 35,3 | 35,1 |
| co co CN | 29,5 | CD CN | 10 co CN | I I 29,1 | 29,9 | 27,9 |
| 34,5 | 40,0 | O o | CD 3 | o o | 34,5 | 40,0 |
| CN CN | & | CN 8 | CD RÍ | 22,4 | 5 | 22,9 |
| O O | CD 3 | o o | o | 35,1 | 34,7 | 40,0 |
| co CN | 22,8 1 | o CN CN | co co CN | o co ÇN | CN CN _ | 23,8 |
| cOcõ | 32,4 | co CO | CO CN CO | 32,5 | 31,5 | 33,5 |
| 30,2 | CD 8 | σ> CN | 8 | 8 | 30,3 | 30,2 |
| CO- CN | CO CN | σ> CN | CO CN | CN | 24,9 | 27,6 |
| CO co | CO co | co co | CO | co | co | 18,2 |
| GDF8+Compostol 81 | GDF8+Composto 180 | Õ (0 o CL E o o + co Q 0 CD | GDF8+Composto 202 | GDF8+Composto 40 __________ | GDF8+GSK3 inhib BIO ________ | GDF8+Composto 206 |
232/247
| b a. o Q. έ 0) D ω £ o £ | 5 | 32,5 | 32,4 | 31,2 | 31,2 | 35,1 | 32,7 | CN CO | 32,9 | |
| SST | CO. s | O) ID CN | ID in CN | 27,1 | 24,0 | 25,6 | CN CN | CD co CN | ||
| <0 O) CN | CO | o co | 32,6 | 29,5 | 31,2 | 33,7 | CO σ> CN | |||
| POU3F 4 | m <0 CN | CN CN | in CN | 28,5 | CN | ID co CN | ID o CO | <0 (D CN | ||
| PECA M | 29,8 | 30,4 | 27,9 | 26,7 | 29,6 | 30,3 | 29,6 | 29,7 | ||
| PDX1 | 23,7 | Si | 24,0 | 24,0 | 24,3 | ID CN | 26,5 | 23,6 | ||
| ΡΑΧ6 | t— CN | CD_ CN | o to CN | 28,9 | CT> co CN | CN CD CN | 30,0 | 26,3 | ||
| PAX4 | in CN | co' CN | CO to CN | CN | CO to CN | CN | O) CM | ID in CN | ||
| NKX6- 1 | CN | tf) CM | CO CN | 28,9 | CN | CO CN | 32,9 | CN & | ||
| NKX2- 5 | 31,9 | 31,8 | 30,9 | 29,4 | 32,1 | CN CM co | 31,5 | 31,9 | ||
| NKX2- I? | 24,0 | S | CD S | 25,0 | 25,0 | 26,2 | 23,8 | |||
| NEUROG 3 | co co' CN | s | tD S | 25,8 | s | CO 10 CN | S | co co CM | ||
| NEUROD 1 | co CN | s | CN S | 25,5 | 24,0 | S | 26,3 | 23,3 | ||
| MAFB | U> co CN | s | s | 24,6 | 23,9 | S | in CM | m co CN | ||
| MAFA I______________________________________________________________________________________________ | 30,6 | 5“ CO | 31,6 | S' | CO | 31,5 | 33,0 | 30,4 | ||
| ω | 25,1 | 24,5 | 26,1 | 24,4 | 25,3 | 26,5 | 24,0 | |||
| INS | <0 co’ CN | CN 10 CN | 24,6 | 26,7 | CN CN | 23,5 | 26,3 | 22,8 | ||
| z T < | CN CN | o CN | 20,6 | O CN | CO CN | CN | CN | |||
| o 0 o | 22,8 | 25,1 | ID S | 25,4 | CO_ CN | CN CN CN | CN in CM | CM CN | ||
| CDX2 | 23,7 | 22,1 | 21,6 | CO co CN | CD R| | CN CN | CD CN CN | |||
| < | 23,9 | 24,6 | o s | 26,3 | 24,0 | s | 26,7 | 23,3 | ||
| 1 < | CD co’ CN | 29,3 | CN | 27,3 | (Mostra de ARN insuficiente) | cd CN | σΓ CN | 29,2 | co CN | |
| co < | 22,4 | in co ÇN | O s | 21,0 | 20,7 | CD o’ CN | CD | 20,9 | ||
| 0 0. <5 X | 19,0 | 19,5 | 18,0 | 19,4 | 19,2 | 19,2 | 19,0 | 18,8 | ||
| to Q 5 Lil | Tratamento | <0 CO •c J | o to a E o Q £ g | 5 a E o O t o $ 5 | AA+Composto 19 | AA+Composto 202 | AA+Composto 40 | AA+GSK3 inhib BIO | AA+Composto 206 |
233I2A7
| CO CN CM | 29,0 | cd cõ | 33,4 | CO | 34,1 | 32,6 | 32,7 | 28,9 |
| O CD CM | Si | CN Si | CO co CM | 27,9 | 8 | CN CM | 23,4 | 24,0 |
| O O | m s | co co’ CM | 30,7 | 32,6 | cd CM | 28,4 | 29,5 | |
| CD CM | CN | ID CN | σ> co . CM | 29,2 | cd' CN | 26,4 | 27,8 | 26,9 |
| CD CM | co CO | CD CN | !30,6 I I_____________________________________________________________________________________________________ | 30,2 | ID σ> CM | 29,3 | 30,0 | 31,4 |
| ID cd CM | CO co’ CN | CO a | 23,8 | 25,1 | O co CM | 23,4 | 24,2 | 23,5 |
| cd_ CM | CO CO’ CM | o_ CN | 28,3 | 30,0 | 26,5 | 26,1 | 27,0 | 27,2 |
| CO | co’ CM | 24,2 | 26,0 | 28,2 | 24,8 | 24,8 | 26,1 | 25,5 |
| 31,2 | O co CN | 25,7 | CN | 30,2 | 25,9 | 26,6 | 27,9 | 26,3 |
| CO cn co | 33,3 | 32,1 | ID co CO | 34,0 | 33,4 | 33,2 | 33,3 | 35,3 |
| o cd CM | o ID CN | CM co CM | Si | 25,6 | 23,4 | 23,7 | 24,2 | 24,0 |
| 28,7 | 24,0 | co CN | co CN | 26,4 | 22,2 | £ | 23,8 | 23,0 |
| 29,2 | ID CM | 22,9 i______________________________________________________________________________________________________________________________________________ | 24,3 | 26,2 | 22,9 | 23,2 | 23,8 | 23,7 |
| s* | 25,1 | 23,0 | S’ | 25,5 | ID co’ _ | 23,3 | 24,0 | 24,2 |
| co cm co | 32,7 | 30,6 | CO | 32,6 | 30,3 | 30,2 | 31,0 | 30,9 |
| co CN | ID CM | CO co’ CM | Si | co io CM | 24,3 | 23,8 | 24,6 | 24,9 |
| 30,9 | ID m' CN | cm’ CM | 24,5 | CN 5 | c\i | 21,5 | 21,8 | CN CM |
| CO co CN | 23,0 | 21,4 | ID a | 22,1 | co CN CN | 22,0 | CN | 22,3 |
| CO | CN | 24,6 | id' CM | 26,7 | CO | 21,0 | 21,5 | 22,6 |
| CO s | Si | co CN | 23,9 | 22,9 | 24,5 | CD CO* CN | 23,0 | 24,0 |
| 29.8 | id' CM | tD co CM | Si | ID ID~ CM | CO CN | co CN | 24,3 | Si |
| σ> CN | O σ> CN | co CN | 29,3 | co CM | o co CN | O CD CM | 29,1 | 28,9 |
| m IO CM | co s | CO a | 24,0 | 22,6 | o CN CN | CN | σ> | 21,6 |
| O co | 19,0 | o co | 19,5 | σ> | O σΓ | O cd | cd' ▼*- | 18,9 |
| GDF8 | CO CO c ? co u. D Q | GDF8+Compostol 81 | GDF8+Compostol 80 | GDF8+Composto 19 | GDF8+Composto 202 | GDF8+Composto 40 | GDF8+GSK3 inhib BIO | GDF8+Composto 206 |
234/247
| _________________________________________Valores de RT-PCR CT_______________________________________________________ | 6 N | 34,4 | 32,5 | 31,2 | CO 8 | O s | 32,8 | σ>_ cõ | o cm co | cm ¢0 | 22,5 |
| SST | 19,6 | σ> | 18,8 | co | co' CM | aí | σ>~ | 19,5 | cd | CM | |
| PTF1 A | CO CM | 27,5 | 28,0 | co Cl | CÍ CO | o ci | 28,1 | 29,7 | 27,5 | 29,5 | |
| POU3F 4 | CO oo CM | 28,8 | 28,8 | o σ> Cl | CM CO CM | CM σ> CM | 29,2 | 29,9 | 28,7 | 27,8 | |
| PECA M | 30,1 | 29,6 | 27,5 | co Cl | in cõ | ÇM | 28,1 | CO co CM | 29,0 | cn cm | |
| PDX1 | CM co Cl | 23,3 | co Cl | Cl co Cl | o CM | 23,6 | 23,2 | CO co CM | 23,3 | 25,6 | |
| PAX6 | q ci | (θ' Cl | cq ci | <O cm | CD CO CM | ci | cm | CD s | CM | CD co CM | |
| PAX4 | <o_ CM | co CM | co CD Cl | CM_ CM | IO co | σ> co CM | cm | CM | CM | σί CM | |
| NKX6- 1 | 25,5 | CD Cl | co Cl | m cd CM | 00 to CM | 25,8 | co Cl | LO CM | cd to CM | CD cd CM | |
| NKX2- 5 | 34,1 | CO —s | 32,2 | CM 8 | 8’ | σ> σ> CM | σ> cm co | CO co CO. | 35,8 | CO | |
| NKX2- 2 | 23,7 | 23,4 | 23,3 | OO co Cl | O co CM | 23,7 | 23,5 | 24,2 | CD co .CM | 25,9 | |
| NEUROG 3 | oo’ Cl | O co CM | a> co d | m σΓ Cl | CM_ cõ | CD CO CM | o σ> CM | *o σ> CM | 28,0 | 30,1 | |
| NEUROD 1 | 00 R| | 21,6 | 21,5 | cm | CM CM | 21,9 | 21,6 | 22,1 | CM | 24,2 | |
| m í | CM CÍ CM | O cT CM | CM cT <M- | CD CM CM | ci | CD RÍ | ^· cm CM | 22,8 | RÍ | co' CM | |
| MAFA | 31,8 | 31,6 | 31,4 | σ> co | O cm CO | CO co | 31,5 | 31,8 | CO | 31,8 | |
| Zj ω | 22,4 | 22,3 | 22,1 | 26,2 | & | 22,5 | 22,8 | 22,5 | co_ s | ||
| INS | σ> | CD | tO | 26,9 | 15,0 | 14,7 | to | cq | 17,7 | ||
| HNF4A | 21,3 | 20,9 | 20,9 | o CM | 24,2 | 21,3 | CM | 20,5 | 21,3 | 22,9 | |
| Ο 0 0 | 14,1 | o_ | CO | σ> | 27,0 | CT> | CD | to | 14,4 | co | |
| i Q | 23,4 | 23,1 | 22,9 | σ> Rí | 25,4 | 23,4 | O co CM | CD RÍ | co' CM | s | |
| 22,0 | 21,9 | 22,0 | 5 | 28,2 | 22,6 | 22,3 | 23,0 | CM RÍ | 25,2 | ||
| 27,6 | Cl | 27,6 | CD CM | 28,6 | o co - CM | σ>_ cn | o CO CM | cn CM | CM co CM | ||
| 03 | Cl o cm | o o’ CL | CO co | OO 00 | 23,6 | 19,2 | 18,9 | r— | 19,5 | 20,5 | |
| o JL x | 18,3 | 18,0 | 18,0 | O oo | σ>_ | 18,6 | 18,3 | 18,3 | 18,2 | 17,4 | |
| to co Q s LU | Tratamento | s c ! | AA+Com posto 181 | AA+Composto 180 | AA+Composto 19 | AA+Composto 202 | § a E o J | AA+GSK3 inhib BIO | AA+Composto 206 | GDF8 |
235/247
| 22,8 | 31,9 | 31,5 | 31,9 | 30,9 | 32,0 | 32,4 | σ> co CN |
| ID 5. | 19,5 | 18,8 | 20,5 | 20,8 | 20,4 | 19,3 | co o CN |
| 30,7 | 27,3 | 27,3 | 31,0 | CN | CN | ID CO* CN | o co CN |
| 28,1 | CO co CN | 28,7 | o Q | ID O) CN | 28,9 | o' CO | CO co* CN |
| 29,8 | 27,5 | 29,6 | 29,0 | O CD CN | 27,3 | co CN | 03 CN |
| 25,6 | 23,0 | 22,9 | 24,2 | 23,2 | σ> 8 | o Si | O_ <N |
| 26,5 | CN | 23,8 | 25,2 | 25,2 | ▼— | CO s | ID CN |
| CO σ> _ | CO CD Π | co Cl | 27,3 | CN | 26,6 | 27,3 | lD_ CN |
| 27,0 | 25,0 | 25,1 | 28,6 | 24,8 | 25,0 | 26,7 | 25,9 |
| 31,9 | 33,8 | o o | 33,9 | co ÍÕ | 33,2 | o •D co | ID 3 |
| CD iD~ Cl | co Cl | 23,2 | COs | co co Cl | 23,2 | CN s | s |
| 30,2 i | CN | 27,9 | 31,2 | 27,8 | 27,3 | 28,2 | 28,5 |
| 24,0 | CN | 21,2 | 22,6 ______________________________________________________________________________________________________________________________________________i | 22,3 | 21,5 | 22,1 | 22,8 |
| ID CO Cl | CO CN Cl | 22,1 | 23,2 | 23,3 | 22,5 | 22,6 I______________________________________________________________________________________________ | σ> cn CN |
| 31,9 | 31,5 | CO | 32,2 | 32,8 | 31,5 | 32,6 | !32,1 |
| CN CN | m a | CN tf | 23,2 | ID co Cl | CO Rl | 23,1 | CO co CN |
| id_ x— | 00 | 14,4 | 15,6 | 15,8 | CO | 15,5 | 16,0 |
| 22,9 | 21,2 | 20,9 | 21,2 | 21,9 | x— CN | CO o' CN | S' |
| IO_ | CN | 16,2 | id | CO | 15,2 | 16,0 | |
| 24,3 | 23,4 | 22,9 | 23,0 | 24,0 | 23,0 | 22,8 | o Si |
| -----------------------------------------------------------------------1 24,8 | 22,4 | 22,2 | 23,4 | 23,1 | 22,3 | 23,2 | co’ CN |
| CM co' CN | CO_ CN | co_ CN | CO CN | CO co CN | 27,9 | 27,6 | 27,9 |
| 20,6 | σΓ | 18,0 | 18,5 | 19,6 | co | o o CN | |
| co | 18,0 | 18,0 | 18,3 | co | co | CO' y— | 18,0 |
| co co Έ § co Q 0 | GDF8+Compostol 81 | GDF8+Compostol 80 | GDF8+Composto 19 | GDF8+Composto 202 | GDF8+Composto 40 | GDF8+GSK3 inhib BIO | GDF8+Composto 206 |
236/247
| Tabela 16 | |
| Composto n° | Seletividade primária |
| Composto 6 | Seletivo para GSK |
| Composto 7 | Seletivo para GSK |
| Composto 8 | Seletivo para GSK |
| Composto 9 | Seletivo para CDK |
| Composto 57 | Seletivo para Trk |
| Composto 41 | Seletivo para GSK |
| Composto 42 | Seletivo para CDK |
| Composto 10 | Seletivo para CDK |
| Composto 34 | controle positivo |
| Composto 11 | Seletivo para CDK |
| Composto 43 | Seletivo para Trk |
| Composto 44 | Seletivo para GSK |
| Composto 12 | Seletivo para CDK |
| Composto 45 | Seletivo para Trk |
| Tabela 17 | |||||||
| Número de célula | Expressão de Sox17 | ||||||
| Placa | Tratame nto | Composto n° | Seletividade do composto | Número total médio de células | % de controles positivos | Intensidade total média | % de controles positivos |
| 1 | nenhum a Ativina A | Nenhum | N/D | 9809 | 67,8 | -4.0E+05 | -0,2 |
| 1 | Ativina A/Wnt3a | Nenhum | N/D | 14476 | 100,0 | 2.3E+08 | 100,0 |
| 1 | Nenhum GDF8 | Composto 11 | Seletivo para CDK | 565 | 3,9 | -1.1E+06 | -0,5 |
| 1 | Nenhum GDF8 | Composto 44 | Seletivo para GSK | 14 | 0,1 | -1.1E+06 | -0,5 |
| 1 | Nenhum | Composto 43 | Seletivo para Trk | 8610 | 59,5 | -2.1E+05 | -0,1 |
237/247
| GDF8 | |||||||
| 1 | Nenhum GDF8 | Composto 42 | Seletivo para CDK | 8700 | 60,1 | -2.4E+05 | -0,1 |
| 1 | Nenhum GDF8 | Composto 57 | Seletivo para Trk | 1222 | 8,4 | -7.1E+05 | -0,3 |
| 1 | Nenhum GDF8 | Composto 10 | Seletivo para CDK | 7011 | 48,4 | -6.6E+05 | -0,3 |
| 1 | Nenhum GDF8 | Composto 41 | Seletivo para GSK | 9995 | 69,0 | 5.9E+04 | 0,0 |
| 1 | Nenhum GDF8 | Composto 7 | Seletivo para CDK | 3 | 0,0 | -1.4E+06 | -0,6 |
| 1 | Nenhum GDF8 | Composto 45 | Seletivo para Trk | 8857 | 61,2 | -4.5E+05 | -0,2 |
| 1 | Nenhum GDF8 | Composto 6 | Seletivo para GSK | 14827 | 102,4 | -1,8E+05 | -0,1 |
| 1 | Nenhum GDF8 | Composto 9 | Seletivo para CDK | 7156 | 49,4 | -4.2E+04 | 0,0 |
| 1 | Nenhum GDF8 | Composto 12 | Seletivo para GSK | 13124 | 90,7 | -2.3E+05 | -0,1 |
| 1 | Nenhum GDF8 | Composto 8 | Seletivo para GSK | 13235 | 91,4 | 3,8E+05 | 0,2 |
| 1 | GDF8 | Composto 34 | controle positivo | 13926 | 96,2 | 2.6E+08 | 111,8 |
| 1 | GDF8 | Composto 45 | Seletivo para Trk | 9540 | 65,9 | 1.1E+08 | 47,9 |
| 1 | GDF8 | Composto 7 | Seletivo para GSK | 5296 | 36,6 | 7.0E+07 | 30,4 |
| 1 | GDF8 | Composto 10 | Seletivo para CDK | 4627 | 32,0 | 6.6E+07 | 28,6 |
| 1 | GDF8 | Composto 6 | Seletivo para GSK | 5118 | 35,4 | 5.8E+07 | 25,2 |
| 1 | GDF8 | Composto 43 | Seletivo para Trk | 6682 | 46,2 | 5.4E+07 | 23,4 |
| 1 | GDF8 | Composto 42 | Seletivo para CDK | 5686 | 39,3 | 4.9E+07 | 21,2 |
| 1 | GDF8 | Composto 8 | Seletivo para GSK | 5018 | 34,7 | 4.7E+07 | 20,4 |
| 1 | GDF8 | Composto 9 | Seletivo para CDK | 4816 | 33,3 | 4.5E+07 | 19,4 |
| 1 | GDF8 | Composto 41 | Seletivo para GSK | 4455 | 30,8 | 3.4E+07 | 14,8 |
| 1 | GDF8 | N/D | N/D | 2856 | 19,7 | 2.2E+07 | 9,4 |
238/247
| 1 | GDF8 | Composto 57 | Seletivo para Trk | 2110 | 14,6 | 1,1 E+07 | 4,8 |
| 1 | GDF8 | Composto 11 | Seletivo para CDK | 210 | 1,4 | -4.9E+05 | -0,2 |
| 1 | GDF8 | Composto 44 | Seletivo para GSK | 226 | 1,6 | -9.5E+05 | -0,4 |
| 1 | GDF8 | Composto 12 | Seletivo para CDK | 31 | 0,2 | -1.3E+06 | -0,6 |
| Tabela 18 | ||||||||||
| Número de célula | Expressão de Sox17 | |||||||||
| Placa | Tratame nto | Composto N° | Número total médio de células | SD | % de CV | % de controles positivos | Intensida de total média | SD | % de CV | % de controles positivos |
| 1 | nenhum a ativina A (com Wnt3a) | Nenhum | 15489 | 0 | 0,00 | 103,2 | 3.75E+07 | O.00E+ 00 | 0,00 | 10,9 |
| 1 | Ativina A/Wnt3a | Nenhum | 15007 | 1991 | 13,27 | 100,0 | 3.45E+08 | 7.16E+ 07 | 20,75 | 100,0 |
| 1 | GDF8 | Composto 206 | 20568 | 1683 | 8,18 | 137,1 | 5.19E+08 | 4,41 E+ 07 | 8,51 | 150,3 |
| 1 | GDF8 | Composto 207 | 19224 | 1091 | 5,68 | 128,1 | 2.54E+08 | 5.69E+ 07 | 22,41 | 73,6 |
| 1 | GDF8 | Composto 19 | 12569 | 1524 | 12,13 | 83,8 | 2.40E+08 | 6.34E+ 07 | 26,44 | 69,5 |
| 1 | GDF8 | Composto 23 | 8758 | 474 | 5,41 | 58,4 | 1.16E+08 | 9.07E+ 06 | 7,80 | 33,7 |
| 1 | GDF8 | Composto 170 | 6460 | 2305 | 35,68 | 43,0 | 9.44E+07 | 6.98E+ 07 | 73,93 | 27,4 |
| 1 | GDF8 | Composto 208 | 4848 | 1225 | 25,27 | 32,3 | 2.26E+07 | 2.15E+ 07 | 94,96 | 23,6 |
| 1 | GDF8 | Composto 209 | 4831 | 1243 | 25,74 | 32,2 | 3.97Ê+07 | 1.61E+ 07 | 40,56 | 11,5 |
| 1 | GDF8 | Composto | 4338 | 1520 | 35,04 | 28,9 | 3.63E+07 | 3.27E+ | 90,14 | 10,5 |
239/247
| 32 | 07 | |||||||||
| 1 | GDF8 | Composto 30 | 4679 | 435 | 9,29 | 31,2 | 3.47E+07 | 1.04E+ 07 | 30,03 | 10,1 |
| 1 | GDF8 | Composto 223 | 3704 | 1077 | 29,08 | 24,7 | 3.45E+07 | 2.74E+ 07 | 79,43 | 10,0 |
| 1 | GDF8 | Composto 2 | 4538 | 632 | 13,93 | 30,2 | 2.95E+07 | 2,81 E+ 06 | 9,50 | 8,6 |
| 1 | GDF8 | Composto 210 | 2645 | 817 | 30,88 | 17,6 | 2.90E+07 | 2.45E+ 07 | 84,73 | 8,4 |
| 1 | GDF8 | Composto 24 | 5012 | 1263 | 25,21 | 33,4 | 2.64E+07 | 1.66E+ 07 | 62,95 | 7,7 |
| 1 | GDF8 | Composto 211 | 5165 | 796 | 15,41 | 34,4 | 2,61 E+07 | 5.02E+ 06 | 19,23 | 7,6 |
| 1 | GDF8 | Composto 212 | 5476 | 1445 | 26,39 | 36,5 | 2.54E+07 | 1,18E+ 07 | 46,53 | 7,4 |
| 1 | GDF8 | Composto 224 | 5188 | 761 | 14,67 | 34,6 | 2.46E+07 | 8.26E+ 06 | 33,56 | 7,1 |
| 1 | GDF8 | Composto 225 | 4431 | 1149 | 25,92 | 29,5 | 2.45E+07 | 2.65E+ 07 | 108,19 | 7,1 |
| 1 | GDF8 | Composto 13 | 3123 | 1508 | 48,27 | 20,8 | 2.44E+07 | 2.30E+ 07 | 94,13 | 7,1 |
| 1 | GDF8 | Composto 213 | 1261 | 1028 | 81,49 | 8,4 | 2.07E+07 | 1,97E+ 07 | 95,03 | 6,0 |
| 1 | GDF8 | Composto 52 | 4932 | 386 | 7,82 | 32,9 | 1.99E+07 | 6.90E+ 06 | 34,67 | 5,8 |
| 1 | GDF8 | Composto 214 | 3345 | 335 | 10,01 | 22,3 | 1.93E+07 | 1.39E+ 07 | 72,18 | 5,6 |
| 1 | GDF8 | Composto 51 | 4289 | 940 | 21,91 | 28,6 | 1,70E+07 | 1.10E+ 07 | 64,86 | 4,9 |
| 1 | GDF8 | Composto 26 | 4896 | 545 | 11,14 | 32,6 | 1.65E+07 | 5.93E+ 06 | 36,02 | 4,8 |
| 1 | GDF8 | Composto | 3617 | 577 | 15,94 | 24,1 | 1.59E+07 | 4.96E+ | 31,21 | 4,6 |
240/247
| 226 | 06 | |||||||||
| 1 | GDF8 | Composto 215 | 4326 | 165 | 3,81 | 28,8 | 1.45E+07 | 2.69E+ 06 | 18,53 | 4,2 |
| 1 | GDF8 | Composto 31 | 3619 | 1011 | 27,92 | 24,1 | 1.36E+07 | 4.63E+ 06 | 34,15 | 3,9 |
| 1 | GDF8 | Composto 216 | 3364 | 629 | 18,70 | 22,4 | 8.75E+06 | 2.30E+ 06 | 26,32 | 2,5 |
| 1 | GDF8 | Composto 217 | 2859 | 544 | 19,03 | 19,1 | 8.75E+06 | 1.94E+ 06 | 22,16 | 2,5 |
| 1 | GDF8 | Composto 218 | 1327 | 118 | 8,92 | 8,8 | 6.44E+06 | 9.70E+ 05 | 15,05 | 1,9 |
| 1 | GDF8 | Composto 219 | 368 | 168 | 45,67 | 2,5 | 1.79E+06 | 1,29E+ 06 | 72,17 | 0,5 |
| 2 | nenhum a ativina A (com Wnt3a) | Nenhum | 15778 | 0 | 0,00 | 103,2 | 2.24E+07 | O.OOE+ 00 | 0,00 | 6,7 |
| 2 | Ativina A/Wnt3a | Nenhum | 15290 | 1119 | 7,32 | 100,0 | 3.37E+08 | 2.84E+ 07 | 8,44 | 100,0 |
| 2 | GDF8 | Composto 202 | 20177 | 987 | 4,89 | 132,0 | 4.85E+08 | 1.94E+ 07 | 4,00 | 144,0 |
| 2 | GDF8 | Composto 227 | 2911 | 4619 | 158,6 9 | 19,0 | 3.89E+07 | 6.69E+ 07 | 172,00 | 11,5 |
| 2 | GDF8 | Composto 15 | 4383 | 1775 | 40,49 | 28,7 | 3.57E+07 | 3.57E+ 07 | 100,03 | 10,6 |
| 2 | GDF8 | Composto 228 | 4043 | 1253 | 30,98 | 26,4 | 3.10E+07 | 2.53E+ 07 | 81,62 | 9,2 |
| 2 | GDF8 | Composto 229 | 3451 | 892 | 25,85 | 22,6 | 1.80E+07 | 1,46E+ 07 | 81,07 | 5,4 |
| 2 | GDF8 | Composto 4 | 3163 | 805 | 25,44 | 20,7 | 1.58E+07 | 3.54E+ 06 | 22,32 | 4,7 |
| 2 | GDF8 | Composto | 2791 | 1453 | 52,05 | 18,3 | 1.40E+07 | 9.00E+ | 64,28 | 4,2 |
241/247
| 220 | 06 | |||||||||
| 2 | GDF8 | Composto 5 | 3137 | 1172 | 37,34 | 20,5 | 1.30E+07 | 7.52E+ 06 | 57,85 | 3,9 |
| 2 | GDF8 | Composto 230 | 2624 | 248 | 9,46 | 17,2 | 1.24E+07 | 1,55E+ 07 | 124,73 | 3,7 |
| 2 | GDF8 | Composto 231 | 4773 | 2651 | 55,55 | 31,2 | 1.22E+07 | 6,51 E+ 06 | 53,37 | 3,6 |
| 2 | GDF8 | Composto 232 | 3273 | 1290 | 39,41 | 21,4 | 1.18E+07 | 1.51E+ 07 | 127,98 | 3,5 |
| 2 | GDF8 | Composto 221 | 1950 | 361 | 18,52 | 12,8 | 1.18E+07 | 1.54E+ 07 | 131,11 | 3,5 |
| 2 | GDF8 | Composto 233 | 3041 | 180 | 5,93 | 19,9 | 1.12E+07 | 1.09E+ 07 | 97,44 | 3,3 |
| 2 | GDF8 | Composto 147 | 3434 | 1199 | 34,91 | 22,5 | 1.12E+07 | 9.80E+ 06 | 87,75 | 3,3 |
| 2 | GDF8 | Composto 234 | 2835 | 623 | 21,98 | 18,5 | 9.47E+06 | 5.67E+ 06 | 59,84 | 2,8 |
| 2 | GDF8 | Composto 235 | 3391 | 2269 | 66,91 | 22,2 | 9.10E+06 | 6,51 E+ 06 | 71,52 | 2,7 |
| 2 | GDF8 | Composto 236 | 2868 | 561 | 19,57 | 18,8 | 6.73E+06 | 6.32E+ 06 | 93,82 | 2,0 |
| 2 | GDF8 | Composto 33 | 2362 | 511 | 21,66 | 15,4 | 6.60E+06 | 2.45E+ 06 | 37,20 | 2,0 |
| 2 | GDF8 | Composto 1 | 3213 | 166 | 5,16 | 21,0 | 6.48E+06 | 3.09E+ 06 | 47,67 | 1,9 |
| 2 | GDF8 | Composto 53 | 2783 | 441 | 15,86 | 18,2 | 6.36E+06 | 2.89E+ 06 | 45,36 | 1,9 |
| 2 | GDF8 | Composto 237 | 2973 | 292 | 9,83 | 19,4 | 6.02E+06 | 3.00E+ 06 | 49,79 | 1,8 |
| 2 | GDF8 | Composto 238 | 2739 | 485 | 17,70 | 17,9 | 5.97E+06 | 6,10E+ 06 | 102,07 | 1,8 |
| 2 | GDF8 | Composto | 3156 | 667 | 21,15 | 20,6 | 5.60E+06 | 2.42E+ | 43,24 | 1,7 |
242/247
| 239 | 06 | |||||||||
| 2 | GDF8 | Composto 240 | 3002 | 287 | 9,55 | 19,6 | 4.68E+06 | 3.13E+ 06 | 66,80 | 1,4 |
| 2 | GDF8 | Composto 200 | 2308 | 209 | 9,04 | 15,1 | 4.39E+06 | 1.88E+ 06 | 42,83 | 1,3 |
| 2 | GDF8 | Composto 222 | 1776 | 719 | 40,47 | 11,6 | 3.33E+06 | 2.52E+ 06 | 75,78 | 1,0 |
| 2 | GDF8 | Composto 241 | 2949 | 446 | 15,14 | 19,3 | 3.29E+06 | 1.55E+ 06 | 47,03 | 1,0 |
| 2 | GDF8 | Composto 242 | 385 | 184 | 47,83 | 2,5 | 1.08E+06 | 8.85E+ 05 | 81,61 | 0,3 |
| 2 | GDF8 | Composto 243 | 249 | 55 | 22,21 | 1,6 | 2.53E+05 | 3.07E+ 05 | 121,25 | 0,1 |
| 2 | GDF8 | Composto 204 | 250 | 21 | 8,38 | 1,6 | 1.36E+05 | 2.27E+ 04 | 16,66 | 0,0 |
| 3 | nenhum a ativina A (com Wnt3a) | Nenhum | 15796 | 0 | 0,00 | 99,6 | 2.82E+07 | O.OOE+ 00 | 0,00 | 8,0 |
| 3 | Ativina A/Wnt3a | Nenhum | 15867 | 785 | 4,95 | 100,0 | 3.54E+08 | 2.40E+ 07 | 6,77 | 100,0 |
| 3 | GDF8 | Composto 34 | 6974 | 3723 | 53,38 | 44,0 | 2.07E+08 | 9,51 E+ 07 | 45,85 | 58,6 |
| 3 | GDF8 | Composto 185 | 10892 | 1552 | 14,24 | 68,6 | 1.53E+08 | 4.08E+ 07 | 26,72 | 43,1 |
| 3 | GDF8 | Composto 35 | 7746 | 1873 | 24,17 | 48,8 | 1.35E+08 | 4.86E+ 07 | 36,08 | 38,0 |
| 3 | GDF8 | Composto 22 | 6727 | 1927 | 28,64 | 42,4 | 1.06E+08 | 5.04E+ 07 | 47,73 | 29,8 |
| 3 | GDF8 | Composto 34 | 4889 | 1152 | 23,57 | 30,8 | 4,31 E+07 | 2,11E+ 07 | 48,95 | 12,2 |
| 3 | GDF8 | Composto | 4173 | 1758 | 42,14 | 26,3 | 3.94E+07 | 2.24E+ | 56,78 | 11,1 |
243/247
| 184 | 07 | |||||||||
| 3 | GDF8 | Composto 223 | 4234 | 1604 | 37,88 | 26,7 | 3.55E+07 | 2.51E+ 07 | 70,56 | 10,0 |
| 3 | GDF8 | Composto 37 | 4187 | 338 | 8,06 | 26,4 | 3.11E+07 | 1,56E+ 07 | 50,18 | 8,8 |
| 3 | GDF8 | Composto 244 | 4479 | 1229 | 27,43 | 28,2 | 2.73E+07 | 1.52E+ 07 | 55,71 | 7,7 |
| 3 | GDF8 | Composto 245 | 4725 | 99 | 2,09 | 29,8 | 2.59E+07 | 1.03E+ 07 | 39,90 | 7,3 |
| 3 | GDF8 | Composto 246 | 3820 | 1091 | 28,57 | 24,1 | 2.30E+07 | 2.69E+ 07 | 117,08 | 6,5 |
| 3 | GDF8 | Composto 247 | 3730 | 966 | 25,90 | 23,5 | 2.14E+07 | 1.04E+ 07 | 48,63 | 6,1 |
| 3 | GDF8 | Composto 248 | 3875 | 445 | 11,48 | 24,4 | 2.13E+07 | 9.45E+ 06 | 44,45 | 6,0 |
| 3 | GDF8 | Composto 25 | 3879 | 658 | 16,95 | 24,4 | 1.76E+07 | 1.21E+ 07 | 69,04 | 5,0 |
| 3 | GDF8 | Composto 195 | 3703 | 405 | 10,94 | 23,3 | 1.61E+07 | 3.27E+ 06 | 20,34 | 4,5 |
| 3 | GDF8 | Composto 227 | 2904 | 397 | 13,68 | 18,3 | 1.43E+07 | 1,35E+ 07 | 94,25 | 4,0 |
| 3 | GDF8 | Composto 183 | 3306 | 969 | 29,32 | 20,8 | 1.35E+07 | 1.14E+ 07 | 84,25 | 3,8 |
| 3 | GDF8 | Composto 187 | 2768 | 1426 | 51,51 | 17,4 | 1.35E+07 | 9.02E+ 06 | 66,67 | 3,8 |
| 3 | GDF8 | Composto 201 | 3213 | 1114 | 34,66 | 20,3 | 1.35E+07 | 1.69E+ 07 | 125,02 | 3,8 |
| 3 | GDF8 | Composto 197 | 3268 | 211 | 6,46 | 20,6 | 1.30E+07 | 5.25E+ 06 | 40,51 | 3,7 |
| 3 | GDF8 | Composto 249 | 3840 | 348 | 9,06 | 24,2 | 1.29E+07 | 6,79E+ 06 | 52,72 | 3,6 |
| 3 | GDF8 | Composto | 2404 | 213 | 8,86 | 15,1 | 1.12E+07 | 4.95E+ | 44,30 | 3,2 |
244/247
| 141 | 06 | |||||||||
| 3 | GDF8 | Composto 194 | 3177 | 354 | 11,14 | 20,0 | 9.75E+06 | 2,11E+ 06 | 21,63 | 2,8 |
| 3 | GDF8 | Composto 250 | 3683 | 420 | 11,40 | 23,2 | 9.14E+06 | 4.78E+ 06 | 52,32 | 2,6 |
| 3 | GDF8 | Composto 251 | 3021 | 668 | 22,10 | 19,0 | 8,41 E+06 | 4.59E+ 06 | 54,60 | 2,4 |
| 3 | GDF8 | Composto 20 | 2793 | 205 | 7,35 | 17,6 | 6.77E+06 | 1.86E+ 06 | 27,45 | 1.9 |
| 3 | GDF8 | Composto 252 | 2580 | 135 | 5,24 | 16,3 | 6.20E+06 | 2,31 E+ 05 | 3,72 | 1.8 |
| 3 | GDF8 | Composto 253 | 2485 | 820 | 32,98 | 15,7 | 5.83E+06 | 1.47E+ 06 | 25,20 | 1.6 |
| 3 | GDF8 | Composto 202 | 2095 | 518 | 24,71 | 13,2 | 5.75E+06 | 2.62E+ 06 | 45,66 | 1.6 |
| 3 | GDF8 | Composto 21 | 371 | 294 | 79,19 | 2,3 | 2.36E+06 | 3.07E+ 06 | 129,78 | 0,7 |
| 4 | nenhum a ativina A (com Wnt3a) | Nenhum | 16629 | 0 | 0,00 | 119,3 | 2.42E+07 | O.OOE+ 00 | 0,00 | 7,8 |
| 4 | Ativina A/Wnt3a | Nenhum | 13945 | 1535 | 11,01 | 100,0 | 3.09E+08 | 4.77E+ 07 | 15,46 | 100,0 |
| 4 | GDF8 | Composto 34 | 7416 | 6482 | 87,41 | 53,2 | 2.10E+08 | 1.82E+ 08 | 86,70 | 68,0 |
| 4 | GDF8 | Composto 240 | 11283 | 2023 | 17,93 | 80,9 | 1.61E+08 | 4,41 E+ 07 | 27,34 | 52,2 |
| 4 | GDF8 | Composto 28 | 5236 | 1787 | 34,12 | 37,5 | 4.03E+07 | 3.08E+ 07 | 76,36 | 13,1 |
| 4 | GDF8 | Composto 198 | 3985 | 2674 | 67,10 | 28,6 | 3.89E+07 | 5.55E+ 07 | 142,91 | 12,6 |
| 4 | GDF8 | Composto | 4861 | 1501 | 30,87 | 34,9 | 3.03E+07 | 1,98E+ | 65,37 | 9,8 |
245/247
| 196 | 07 | |||||||||
| 4 | GDF8 | Composto 18 | 1921 | 1759 | 91,56 | 13,8 | 2.94E+07 | 3.65E+ 07 | 123,90 | 9,5 |
| 4 | GDF8 | Composto 186 | 3486 | 425 | 12,19 | 25,0 | 2.34E+07 | 1.42E+ 07 | 60,78 | 7,6 |
| 4 | GDF8 | Composto 254 | 3960 | 1521 | 38,42 | 28,4 | 2,31 E+07 | 2.27E+ 07 | 98,10 | 7,5 |
| 4 | GDF8 | Composto 168 | 3460 | 324 | 9,36 | 24,8 | 2.28E+07 | 7.13E+ 06 | 31,23 | 7,4 |
| 4 | GDF8 | Composto 190 | 3402 | 1318 | 38,74 | 24,4 | 1.87E+07 | 1.58E+ 07 | 84,61 | 6,1 |
| 4 | GDF8 | Composto 255 | 4006 | 1625 | 40,57 | 28,7 | 1.52E+07 | 1.05E+ 07 | 68,91 | 4,9 |
| 4 | GDF8 | Composto 50 | 2666 | 743 | 27,86 | 19,1 | 1.48E+07 | 8.30E+ 06 | 56,15 | 4,8 |
| 4 | GDF8 | Composto 27 | 3721 | 721 | 19,37 | 26,7 | 1.19E+07 | 9.69E+ 06 | 81,29 | 3,9 |
| 4 | GDF8 | Composto 256 | 2922 | 1275 | 43,64 | 21,0 | 9,41 E+06 | 8.65E+ 06 | 92,01 | 3,0 |
| 4 | GDF8 | Composto 257 | 3182 | 705 | 22,14 | 22,8 | 8.06E+06 | 4.49E+ 06 | 55,75 | 2,6 |
| 4 | GDF8 | Composto 258 | 2731 | 472 | 17,29 | 19,6 | 7.89E+06 | 7.24E+ 06 | 91,70 | 2,6 |
| 4 | GDF8 | Composto 189 | 2350 | 1625 | 69,16 | 16,9 | 7.72E+06 | 5.36E+ 06 | 69,41 | 2,5 |
| 4 | GDF8 | Composto 259 | 2195 | 955 | 43,49 | 15,7 | 6.92E+06 | 2.58E+ 06 | 37,29 | 2,2 |
| 4 | GDF8 | Composto 260 | 2468 | 741 | 30,04 | 17,7 | 6.64E+06 | 3.33E+ 06 | 50,18 | 2,2 |
| 4 | GDF8 | Composto 261 | 2965 | 456 | 15,38 | 21,3 | 6.23E+06 | 2.10E+ 06 | 33,61 | 2,0 |
| 4 | GDF8 | Composto | 2377 | 572 | 24,08 | 17,0 | 6.17E+06 | 2.76E+ | 44,65 | 2,0 |
246/247
| 192 | 06 | |||||||||
| 4 | GDF8 | Composto 262 | 2894 | 399 | 13,78 | 20,8 | 5.75E+06 | 3.00E+ 06 | 52,20 | 1,9 |
| 4 | GDF8 | Composto 188 | 3005 | 759 | 25,26 | 21,6 | 5.02E+06 | 3.97E+ 06 | 79,06 | 1,6 |
| 4 | GDF8 | Composto 263 | 2129 | 230 | 10,79 | 15,3 | 4.77E+06 | 1.14E+ 06 | 23,93 | 1,5 |
| 4 | GDF8 | Composto 264 | 2630 | 342 | 13,00 | 18,9 | 4.28E+06 | 2.17E+ 06 | 50,73 | 1,4 |
| 4 | GDF8 | Composto 265 | 2636 | 1372 | 52,04 | 18,9 | 4.27E+06 | 1.15E+ 06 | 26,86 | 1,4 |
| 4 | GDF8 | Composto 14 | 274 | 14 | 5,02 | 2,0 | 1.56E+05 | 9,51 E+ 04 | 60,91 | 0,1 |
| 4 | GDF8 | Composto 205 | 241 | 3 | 1,20 | 1,7 | 1.36E+05 | 6.83E+ 04 | 50,42 | 0,0 |
| 4 | GDF8 | Composto 266 | 271 | 7 | 2,67 | 1,9 | 1.18E+05 | 3.34E+ 04 | 28,43 | 0,0 |
| 4 | GDF8 | Composto 203 | 253 | 4 | 1,49 | 1,8 | 1.09E+05 | 3.49E+ 04 | 32,09 | 0,0 |
| Tabela 19 | |
| Expressão de Sox17 | |
| Composto n° | % de controles positivos |
| Composto 181 | 150,3 |
| Composto 202 | 144,0 |
| Composto 180 | 73,6 |
| Composto 19 | 69,5 |
| Composto 34 | 68,0 |
| Composto 40 | 52,2 |
| Composto 185 | 43,1 |
| Composto 185 | 38,0 |
247/247
| Composto 35 | 33,7 |
| Composto 23 | 29,8 |
| Composto 22 | 27,4 |
| Composto 17 | 23,6 |
1/1
Claims (2)
- REIVINDICAÇÕES1. Método para diferenciar células-tronco pluripotentes em células que expressam marcadores característicos da linhagem do endoderma definitivo que compreende tratar as células-tronco pluripotentes com um5 meio desprovido de activina A, e contendo um composto selecionado do grupo consistindo em: EGF, FGF4, PDGF-A, PDGF-B, PDGF-C, PDGF-D, VEGF, GDF-8, muscimol, PD98059, LY294002, U0124, U0126, e butirato de sódio, durante um período de tempo suficiente para a diferenciação das células-tronco pluripotentes em células que expressam marcadores caracte10 rísticos da linhagem do endoderma definitivo.
- 2. Método, de acordo com a reivindicação 1, em que a activina A ausente também contém pelo menos um outro composto selecionado do grupo consistindo em: uma anilina-piridinotriazina e uma anilina-piridinotriazina cíclica.
Applications Claiming Priority (4)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US7691508P | 2008-06-30 | 2008-06-30 | |
| US7690008P | 2008-06-30 | 2008-06-30 | |
| US7690808P | 2008-06-30 | 2008-06-30 | |
| PCT/US2009/049183 WO2010002846A1 (en) | 2008-06-30 | 2009-06-30 | Differentiation of pluripotent stem cells |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| BRPI0914116A2 true BRPI0914116A2 (pt) | 2019-09-17 |
Family
ID=41100882
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0914116A BRPI0914116A2 (pt) | 2008-06-30 | 2009-06-30 | diferenciação de células-tronco pluripotentes |
Country Status (15)
| Country | Link |
|---|---|
| US (6) | US20100015711A1 (pt) |
| EP (2) | EP2310492B1 (pt) |
| JP (1) | JP5734183B2 (pt) |
| KR (4) | KR101651661B1 (pt) |
| CN (1) | CN102159703B (pt) |
| AU (1) | AU2009267137A1 (pt) |
| BR (1) | BRPI0914116A2 (pt) |
| CA (1) | CA2729121C (pt) |
| ES (2) | ES2552240T3 (pt) |
| HK (1) | HK1216905A1 (pt) |
| MX (1) | MX2011000125A (pt) |
| PL (2) | PL2942392T3 (pt) |
| RU (2) | RU2533805C2 (pt) |
| WO (1) | WO2010002846A1 (pt) |
| ZA (1) | ZA201100758B (pt) |
Families Citing this family (73)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US8017395B2 (en) | 2004-12-17 | 2011-09-13 | Lifescan, Inc. | Seeding cells on porous supports |
| CA2613889A1 (en) | 2005-06-08 | 2006-12-14 | Centocor, Inc. | A cellular therapy for ocular degeneration |
| US8741643B2 (en) * | 2006-04-28 | 2014-06-03 | Lifescan, Inc. | Differentiation of pluripotent stem cells to definitive endoderm lineage |
| US9080145B2 (en) | 2007-07-01 | 2015-07-14 | Lifescan Corporation | Single pluripotent stem cell culture |
| MX2010001335A (es) | 2007-07-31 | 2010-06-02 | Lifescan Inc | Diferenciacion de celulas madre embrionarias humanas. |
| CN107574142B (zh) | 2007-11-27 | 2021-07-06 | 生命扫描有限公司 | 人胚胎干细胞的分化 |
| CN102046779A (zh) | 2008-02-21 | 2011-05-04 | 森托科尔奥索生物科技公司 | 用于细胞粘附、培养和分离的方法、表面改性培养板和组合物 |
| US8623648B2 (en) * | 2008-04-24 | 2014-01-07 | Janssen Biotech, Inc. | Treatment of pluripotent cells |
| JP2011526784A (ja) * | 2008-06-30 | 2011-10-20 | セントコア・オーソ・バイオテツク・インコーポレーテツド | 多能性幹細胞の分化 |
| RU2533805C2 (ru) | 2008-06-30 | 2014-11-20 | Сентокор Орто Байотек Инк. | Дифференцирование плюрипотентных стволовых клеток, представляющих собой линию клеток человека |
| EP2350265B1 (en) | 2008-10-31 | 2019-04-17 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells to the pancreatic endocrine lineage |
| WO2010051223A1 (en) | 2008-10-31 | 2010-05-06 | Centocor Ortho Biotech Inc. | Differentiation of human embryonic stem cells to the pancreatic endocrine lineage |
| CA2744234C (en) | 2008-11-20 | 2018-11-06 | Centocor Ortho Biotech Inc. | Pluripotent stem cell culture on micro-carriers |
| AU2009316583B2 (en) | 2008-11-20 | 2016-04-21 | Janssen Biotech, Inc. | Methods and compositions for cell attachment and cultivation on planar substrates |
| EP2412800A1 (en) * | 2010-07-29 | 2012-02-01 | Koninklijke Nederlandse Akademie van Wetenschappen | Liver organoid, uses thereof and culture method for obtaining them |
| SG174471A1 (en) | 2009-03-20 | 2011-10-28 | Agency Science Tech & Res | Culture of pluripotent and multipotent cells on microcarriers |
| EP2456862A4 (en) | 2009-07-20 | 2013-02-27 | Janssen Biotech Inc | DIFFERENTIATION OF HUMAN EMBRYONIC STEM CELLS |
| US8785184B2 (en) | 2009-07-20 | 2014-07-22 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells |
| GB2485113B (en) | 2009-07-20 | 2016-12-28 | Janssen Biotech Inc | Differentiation of human embryonic stem cells into cells of the pancreatic endoderm lineage |
| MX339669B (es) * | 2009-12-23 | 2016-06-02 | Janssen Biotech Inc | Diferenciacion de celulas madres embrionarias humanas. |
| RU2701335C2 (ru) | 2009-12-23 | 2019-09-25 | Янссен Байотек, Инк. | Способ получения популяции панкреатических эндокринных клеток, соэкспрессирующих nkx6.1 и инсулин, и способ лечения диабета |
| CN102791851B (zh) | 2010-03-01 | 2017-07-14 | 詹森生物科技公司 | 纯化衍生自多能干细胞的细胞的方法 |
| WO2011139628A1 (en) * | 2010-04-25 | 2011-11-10 | Mount Sinai School Of Medicine | Generation of anterior foregut endoderm from pluripotent cells |
| SG185511A1 (en) * | 2010-05-12 | 2012-12-28 | Centocor Ortho Biotech Inc | Differentiation of human embryonic stem cells |
| CA2809305C (en) | 2010-08-31 | 2019-06-11 | Janssen Biotech, Inc. | Differentiation of pluripotent stem cells |
| PH12013500367A1 (en) | 2010-08-31 | 2013-04-01 | Janssen Biotech Inc | Differentiation of human embryonic stem cells |
| EP2853589B1 (en) * | 2010-08-31 | 2017-12-27 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells |
| US9046992B2 (en) | 2010-10-01 | 2015-06-02 | Z124 | Gesture controls for multi-screen user interface |
| JP2013541951A (ja) | 2010-10-01 | 2013-11-21 | アメリカ合衆国 | p53アイソフォームによる幹細胞機能の操作 |
| EP2723852B1 (en) | 2011-06-21 | 2021-11-17 | Novo Nordisk A/S | Efficient induction of definitive endoderm from pluripotent stem cells |
| US20140242038A1 (en) * | 2011-10-11 | 2014-08-28 | The Trustees Of Columbia University In The City Of New York | Method for generating beta cells |
| EP2794857B1 (en) | 2011-12-22 | 2026-02-11 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells into single hormonal insulin positive cells |
| RU2664467C2 (ru) | 2012-03-07 | 2018-08-17 | Янссен Байотек, Инк. | Среда определенного состава для размножения и обновления плюрипотентных стволовых клеток |
| WO2013141133A1 (ja) * | 2012-03-22 | 2013-09-26 | タカラバイオ株式会社 | ウイルスベクターの製造方法 |
| WO2013146480A1 (ja) * | 2012-03-29 | 2013-10-03 | タカラバイオ株式会社 | 遺伝子導入方法 |
| CA2872770A1 (en) * | 2012-05-07 | 2013-11-14 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells into pancreatic endoderm |
| KR102468315B1 (ko) | 2012-06-08 | 2022-11-16 | 얀센 바이오테크 인코포레이티드 | 인간 배아 줄기 세포의 췌장 내분비 세포로의 분화 |
| EP2893000B1 (en) | 2012-09-03 | 2019-04-10 | Novo Nordisk A/S | Generation of pancreatic endoderm from pluripotent stem cells using small molecules |
| WO2014078802A1 (en) | 2012-11-19 | 2014-05-22 | Irm Llc | Compounds and compositions for the treatment of parasitic diseases |
| BR112015015701A2 (pt) | 2012-12-31 | 2017-07-11 | Janssen Biotech Inc | diferenciação de células-tronco embrionárias humanas em células pancreáticas endócrinas com o uso de reguladores hb9 |
| AU2013370228B2 (en) * | 2012-12-31 | 2018-10-18 | Janssen Biotech, Inc. | Suspension and clustering of human pluripotent cells for differentiation into pancreatic endocrine cells |
| DK2938724T3 (da) | 2012-12-31 | 2020-12-14 | Janssen Biotech Inc | Dyrkning af humane embryonale stamceller ved luft-væskegrænsefladen til differentiering til endokrine pankreasceller |
| US10370644B2 (en) | 2012-12-31 | 2019-08-06 | Janssen Biotech, Inc. | Method for making human pluripotent suspension cultures and cells derived therefrom |
| WO2014134213A1 (en) | 2013-02-27 | 2014-09-04 | The Regents Of The University Of California | Generation of thymic epithelial progenitor cells in vitro |
| JP2016510764A (ja) | 2013-03-07 | 2016-04-11 | カリフィア バイオ, インク.Califia Bio, Inc. | 混合系キナーゼ阻害剤および治療法 |
| EP3008168B1 (en) | 2013-06-11 | 2020-02-19 | President and Fellows of Harvard College | Sc- cells and compositions and methods for generating the same |
| GB201317869D0 (en) * | 2013-10-09 | 2013-11-20 | Cambridge Entpr Ltd | In vitro production of foregut stem cells |
| KR20160079072A (ko) * | 2013-11-01 | 2016-07-05 | 얀센 바이오테크 인코포레이티드 | 췌장 내분비 세포로의 분화를 위한 인간 만능 줄기세포의 현탁 및 클러스터링 |
| JP6261430B2 (ja) * | 2014-04-01 | 2018-01-17 | キヤノン株式会社 | 撮像装置及び画像処理システム |
| SG11201609473XA (en) | 2014-05-16 | 2016-12-29 | Janssen Biotech Inc | Use of small molecules to enhance mafa expression in pancreatic endocrine cells |
| US10443042B2 (en) | 2014-12-18 | 2019-10-15 | President And Fellows Of Harvard College | Serum-free in vitro directed differentiation protocol for generating stem cell-derived beta cells and uses thereof |
| US10253298B2 (en) | 2014-12-18 | 2019-04-09 | President And Fellows Of Harvard College | Methods for generating stem cell-derived beta cells and methods of use thereof |
| EP3234110B1 (en) | 2014-12-18 | 2024-02-28 | President and Fellows of Harvard College | METHODS FOR GENERATING STEM CELL-DERIVED ß CELLS AND USES THEREOF |
| WO2016100035A1 (en) * | 2014-12-19 | 2016-06-23 | Janssen Biotech, Inc. | Suspension culturing of pluripotent stem cells |
| KR101686229B1 (ko) * | 2015-04-03 | 2016-12-13 | 연세대학교 산학협력단 | D형 혈소판유래성장인자로 처리된 지방줄기세포를 유효성분으로 함유하는 발모 촉진용 조성물 |
| EP4450076A2 (en) | 2016-04-14 | 2024-10-23 | Janssen Biotech, Inc. | Differentiation of pluripotent stem cells to intestinal midgut endoderm cells |
| KR102785694B1 (ko) | 2016-06-21 | 2025-03-21 | 얀센 바이오테크 인코포레이티드 | 글루코스-의존성 미토콘드리아 호흡 및 2-상 인슐린 분비 반응을 나타내는 인간 만능 줄기 세포 유래 기능성 베타 세포의 생성 |
| US10767164B2 (en) | 2017-03-30 | 2020-09-08 | The Research Foundation For The State University Of New York | Microenvironments for self-assembly of islet organoids from stem cells differentiation |
| MX2020004830A (es) | 2017-11-08 | 2020-11-11 | Avexis Inc | Medios y metodo para preparar vectores virales y usos de los mismos. |
| JP7428653B2 (ja) | 2017-11-15 | 2024-02-06 | バーテックス ファーマシューティカルズ インコーポレイテッド | 島細胞製造組成物および使用方法 |
| WO2019236949A1 (en) | 2018-06-08 | 2019-12-12 | Avexis Inc. | Cell-based assay for measuring drug product potency |
| EP3833365A4 (en) | 2018-08-10 | 2022-05-11 | Vertex Pharmaceuticals Incorporated | Stem cell derived islet differentiation |
| AU2020283150B2 (en) | 2019-05-31 | 2023-08-17 | Viacyte, Inc. | Cell encapsulation devices with controlled oxygen diffusion distances |
| EP3976236A1 (en) | 2019-05-31 | 2022-04-06 | W.L. Gore & Associates Inc. | A biocompatible membrane composite |
| WO2020243665A1 (en) | 2019-05-31 | 2020-12-03 | W. L. Gore & Associates, Inc. | A biocompatible membrane composite |
| JP2022535239A (ja) | 2019-05-31 | 2022-08-05 | ダブリュ.エル.ゴア アンド アソシエイツ,インコーポレイティド | 生体適合性メンブレン複合体 |
| US11344859B2 (en) | 2019-11-27 | 2022-05-31 | Smartdyelivery Gmbh | Reactor for the preparation of a formulation |
| EP4103183A4 (en) * | 2020-02-14 | 2024-02-28 | Salk Institute for Biological Studies | MACROCYCLIC INHIBITORS OF ULK1/2 |
| AU2021319209A1 (en) | 2020-07-31 | 2023-03-02 | Vertex Pharmaceuticals Incorporated | Differentiation of pancreatic endocrine cells |
| CN115612661B (zh) * | 2021-07-14 | 2026-02-13 | 中山大学中山眼科中心 | Pdgf-d在调控干细胞增殖和/或分化中的应用 |
| JP2024542041A (ja) | 2021-11-01 | 2024-11-13 | バーテックス ファーマシューティカルズ インコーポレイテッド | 幹細胞由来の膵臓島分化 |
| CN115851581B (zh) * | 2022-10-24 | 2026-01-02 | 贵州医科大学 | 一种诱导性多功能干细胞分化为窦房结起搏细胞的方法 |
| WO2025012643A1 (en) * | 2023-07-11 | 2025-01-16 | Tay Therapeutics Limited | Compounds comprising a naphthyridine or pyridopyrimidine core as ptc read-through agents |
Family Cites Families (267)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3209652A (en) | 1961-03-30 | 1965-10-05 | Burgsmueller Karl | Thread whirling method |
| AT326803B (de) | 1968-08-26 | 1975-12-29 | Binder Fa G | Maschenware sowie verfahren zur herstellung derselben |
| US3935067A (en) | 1974-11-22 | 1976-01-27 | Wyo-Ben Products, Inc. | Inorganic support for culture media |
| CA1201400A (en) | 1982-04-16 | 1986-03-04 | Joel L. Williams | Chemically specific surfaces for influencing cell activity during culture |
| US4499802A (en) | 1982-09-29 | 1985-02-19 | Container Graphics Corporation | Rotary cutting die with scrap ejection |
| US4537773A (en) | 1983-12-05 | 1985-08-27 | E. I. Du Pont De Nemours And Company | α-Aminoboronic acid derivatives |
| US4557264A (en) | 1984-04-09 | 1985-12-10 | Ethicon Inc. | Surgical filament from polypropylene blended with polyethylene |
| US5215893A (en) | 1985-10-03 | 1993-06-01 | Genentech, Inc. | Nucleic acid encoding the ba chain prodomains of inhibin and method for synthesizing polypeptides using such nucleic acid |
| US5089396A (en) | 1985-10-03 | 1992-02-18 | Genentech, Inc. | Nucleic acid encoding β chain prodomains of inhibin and method for synthesizing polypeptides using such nucleic acid |
| US4737578A (en) | 1986-02-10 | 1988-04-12 | The Salk Institute For Biological Studies | Human inhibin |
| US5863531A (en) * | 1986-04-18 | 1999-01-26 | Advanced Tissue Sciences, Inc. | In vitro preparation of tubular tissue structures by stromal cell culture on a three-dimensional framework |
| US5759830A (en) | 1986-11-20 | 1998-06-02 | Massachusetts Institute Of Technology | Three-dimensional fibrous scaffold containing attached cells for producing vascularized tissue in vivo |
| US5567612A (en) | 1986-11-20 | 1996-10-22 | Massachusetts Institute Of Technology | Genitourinary cell-matrix structure for implantation into a human and a method of making |
| CA1340581C (en) | 1986-11-20 | 1999-06-08 | Joseph P. Vacanti | Chimeric neomorphogenesis of organs by controlled cellular implantation using artificial matrices |
| NZ229354A (en) | 1988-07-01 | 1990-09-26 | Becton Dickinson Co | Treating polymer surfaces with a gas plasma and then applying a layer of endothelial cells to the surface |
| EP0363125A3 (en) | 1988-10-03 | 1990-08-16 | Hana Biologics Inc. | Proliferated pancreatic endocrine cell product and process |
| SU1767433A1 (ru) | 1989-11-27 | 1992-10-07 | Пермский государственный медицинский институт | Способ определени инсулинорезистентности имунного генеза у больных сахарным диабетом I типа |
| US5837539A (en) | 1990-11-16 | 1998-11-17 | Osiris Therapeutics, Inc. | Monoclonal antibodies for human mesenchymal stem cells |
| KR100249937B1 (ko) | 1991-04-25 | 2000-04-01 | 나가야마 오사무 | 인간 인터루킨-6 수용체에 대한 재구성 인간 항체 |
| US5449383A (en) | 1992-03-18 | 1995-09-12 | Chatelier; Ronald C. | Cell growth substrates |
| GB9206861D0 (en) * | 1992-03-28 | 1992-05-13 | Univ Manchester | Wound healing and treatment of fibrotic disorders |
| CA2114282A1 (en) | 1993-01-28 | 1994-07-29 | Lothar Schilder | Multi-layered implant |
| JP3525221B2 (ja) | 1993-02-17 | 2004-05-10 | 味の素株式会社 | 免疫抑制剤 |
| WO1994022915A1 (en) * | 1993-03-31 | 1994-10-13 | Pro-Neuron, Inc. | Inhibitor of stem cell proliferation and uses thereof |
| WO1994023572A1 (en) | 1993-04-08 | 1994-10-27 | Human Cell Cultures, Inc. | Cell culturing method and medium |
| US5523226A (en) | 1993-05-14 | 1996-06-04 | Biotechnology Research And Development Corp. | Transgenic swine compositions and methods |
| GB9310557D0 (en) | 1993-05-21 | 1993-07-07 | Smithkline Beecham Plc | Novel process and apparatus |
| TW257671B (pt) | 1993-11-19 | 1995-09-21 | Ciba Geigy | |
| US6703017B1 (en) | 1994-04-28 | 2004-03-09 | Ixion Biotechnology, Inc. | Reversal of insulin-dependent diabetes by islet-producing stem cells, islet progenitor cells and islet-like structures |
| US6001647A (en) | 1994-04-28 | 1999-12-14 | Ixion Biotechnology, Inc. | In vitro growth of functional islets of Langerhans and in vivo uses thereof |
| US5834308A (en) * | 1994-04-28 | 1998-11-10 | University Of Florida Research Foundation, Inc. | In vitro growth of functional islets of Langerhans |
| US6083903A (en) | 1994-10-28 | 2000-07-04 | Leukosite, Inc. | Boronic ester and acid compounds, synthesis and uses |
| CN1075387C (zh) | 1994-12-29 | 2001-11-28 | 中外制药株式会社 | 含有il-6拮抗剂的抗肿瘤剂的作用增强剂 |
| US5843780A (en) * | 1995-01-20 | 1998-12-01 | Wisconsin Alumni Research Foundation | Primate embryonic stem cells |
| US5718922A (en) | 1995-05-31 | 1998-02-17 | Schepens Eye Research Institute, Inc. | Intravitreal microsphere drug delivery and method of preparation |
| US5908782A (en) | 1995-06-05 | 1999-06-01 | Osiris Therapeutics, Inc. | Chemically defined medium for human mesenchymal stem cells |
| US5681561A (en) | 1995-06-07 | 1997-10-28 | Life Medical Sciences, Inc. | Compositions and methods for improving autologous fat grafting |
| AU5734998A (en) | 1997-01-10 | 1998-08-03 | Life Technologies, Inc. | Embryonic stem cell serum replacement |
| HUP0002842A3 (en) | 1997-04-24 | 2002-01-28 | Ortho Mcneil Pharm Inc | Substituted imidazoles, process for producing them, pharmaceutical compositions containing them, their use and their intermediates |
| ES2285779T3 (es) | 1997-07-03 | 2007-11-16 | Osiris Therapeutics, Inc. | Celulas madre mesenquimatosas humanas de sangre periferica. |
| DK1015576T3 (da) | 1997-09-16 | 2005-08-29 | Egea Biosciences Llc | Fremgangsmåde til fuldstændig kemisk syntese og aggregering af gener og genomer |
| US6670127B2 (en) | 1997-09-16 | 2003-12-30 | Egea Biosciences, Inc. | Method for assembly of a polynucleotide encoding a target polypeptide |
| EP1025204A4 (en) | 1997-10-23 | 2001-02-28 | Geron Corp | Methods and materials for the growth of primate-derived primordial stem cells |
| CO4980885A1 (es) | 1997-12-29 | 2000-11-27 | Ortho Mcneil Pharm Inc | Compuestos de trifenilpropanamida utiles en el tratamiento de inflamaciones y metodos para preparar dicho compuesto |
| EP1066052B1 (en) | 1998-03-18 | 2006-02-01 | Osiris Therapeutics, Inc. | Mesenchymal stem cells for prevention and treatment of immune responses in transplantation |
| MY132496A (en) * | 1998-05-11 | 2007-10-31 | Vertex Pharma | Inhibitors of p38 |
| US6413773B1 (en) | 1998-06-01 | 2002-07-02 | The Regents Of The University Of California | Phosphatidylinositol 3-kinase inhibitors as stimulators of endocrine differentiation |
| US6667176B1 (en) | 2000-01-11 | 2003-12-23 | Geron Corporation | cDNA libraries reflecting gene expression during growth and differentiation of human pluripotent stem cells |
| US7410798B2 (en) | 2001-01-10 | 2008-08-12 | Geron Corporation | Culture system for rapid expansion of human embryonic stem cells |
| EP1131407B1 (en) * | 1998-11-09 | 2006-10-11 | Consorzio per la Gestione del Centro di Biotecnologie Avanzate | Serum free medium for chondrocyte-like cells |
| US6610540B1 (en) | 1998-11-18 | 2003-08-26 | California Institute Of Technology | Low oxygen culturing of central nervous system progenitor cells |
| US6413556B1 (en) | 1999-01-08 | 2002-07-02 | Sky High, Llc | Aqueous anti-apoptotic compositions |
| US6458593B1 (en) * | 1999-01-21 | 2002-10-01 | Vitro Diagnostics, Inc. | Immortalized cell lines and methods of making the same |
| US6815203B1 (en) | 1999-06-23 | 2004-11-09 | Joslin Diabetes Center, Inc. | Methods of making pancreatic islet cells |
| US6333029B1 (en) | 1999-06-30 | 2001-12-25 | Ethicon, Inc. | Porous tissue scaffoldings for the repair of regeneration of tissue |
| US6306424B1 (en) * | 1999-06-30 | 2001-10-23 | Ethicon, Inc. | Foam composite for the repair or regeneration of tissue |
| EP1224259A4 (en) | 1999-09-27 | 2005-04-27 | Univ Florida | INVERSION OF INSULIN DEPENDENT DIABETES BY ISOLATED STEM CELLS, PROGENITOR ISLANDIC CELLS, AND INSULAR TYPE STRUCTURES |
| US6685936B2 (en) | 1999-10-12 | 2004-02-03 | Osiris Therapeutics, Inc. | Suppressor cells induced by culture with mesenchymal stem cells for treatment of immune responses in transplantation |
| US20030082155A1 (en) * | 1999-12-06 | 2003-05-01 | Habener Joel F. | Stem cells of the islets of langerhans and their use in treating diabetes mellitus |
| EP1240518A4 (en) * | 1999-12-13 | 2006-05-17 | Scripps Research Inst | MARKERS TO IDENTIFY AND ISOLATE PROGENITORS OF PANCREATIC ISLAND ALPHA AND BETA CELLS |
| US7005252B1 (en) | 2000-03-09 | 2006-02-28 | Wisconsin Alumni Research Foundation | Serum free cultivation of primate embryonic stem cells |
| US7439064B2 (en) * | 2000-03-09 | 2008-10-21 | Wicell Research Institute, Inc. | Cultivation of human embryonic stem cells in the absence of feeder cells or without conditioned medium |
| US6436704B1 (en) | 2000-04-10 | 2002-08-20 | Raven Biotechnologies, Inc. | Human pancreatic epithelial progenitor cells and methods of isolation and use thereof |
| US6458589B1 (en) * | 2000-04-27 | 2002-10-01 | Geron Corporation | Hepatocyte lineage cells derived from pluripotent stem cells |
| CN1449439A (zh) | 2000-06-26 | 2003-10-15 | 株式会社雷诺再生医学研究所 | 细胞级分包括能分化为神经细胞的细胞 |
| CN100525768C (zh) | 2000-10-23 | 2009-08-12 | 史密丝克莱恩比彻姆公司 | 新化合物 |
| MXPA03005139A (es) | 2000-12-08 | 2004-01-29 | Ortho Mcneil Pharm Inc | Compuestos macroheterociclicos utiles como inhibidores de cinasa. |
| DE60119790T2 (de) | 2000-12-08 | 2007-01-25 | Ortho-Mcneil Pharmaceutical, Inc. | Indazolyl-substituierte pyrrolidin-verbindungen als kinase inhibitoren |
| US6599323B2 (en) * | 2000-12-21 | 2003-07-29 | Ethicon, Inc. | Reinforced tissue implants and methods of manufacture and use |
| CA2435826A1 (en) | 2001-01-24 | 2002-08-01 | The Government Of The United States Of America | Differentiation of stem cells to pancreatic endocrine cells |
| ES2571219T3 (es) | 2001-01-25 | 2024-09-23 | The United States Of America Represented By The Sec Dep Of Health And Human Services | Formulación de compuestos de ácido borónico |
| DE10117563B4 (de) | 2001-04-07 | 2006-04-13 | Interessengemeinschaft für Rundfunkschutzrechte GmbH Schutzrechtsverwertung & Co. KG. | Verfahren zur Verstärkung eines amplituden- und/oder phasenmodulierten Hochfrequenzsignals nach dem Prinzip des Envelope Elimination und Restoration und Schaltungsanordnung |
| US6656488B2 (en) | 2001-04-11 | 2003-12-02 | Ethicon Endo-Surgery, Inc. | Bioabsorbable bag containing bioabsorbable materials of different bioabsorption rates for tissue engineering |
| WO2002086107A2 (en) | 2001-04-19 | 2002-10-31 | DeveloGen Aktiengesellschaft für entwicklungsbiologische Forschung | A method for differentiating stem cells into insulin-producing cells |
| CN100516204C (zh) | 2001-04-24 | 2009-07-22 | 味之素株式会社 | 干细胞及其分离方法 |
| EP1393066A4 (en) | 2001-05-15 | 2006-01-25 | Rappaport Family Inst For Res | INSULIN-PRODUCING CELLS DERIVED FROM HUMAN EMBRYONIC STEM CELLS |
| US6626950B2 (en) | 2001-06-28 | 2003-09-30 | Ethicon, Inc. | Composite scaffold with post anchor for the repair and regeneration of tissue |
| KR100418195B1 (ko) | 2001-07-05 | 2004-02-11 | 주식회사 우리기술 | 전력케이블의 다중절연진단장치 및 그 방법 |
| GB0117583D0 (en) * | 2001-07-19 | 2001-09-12 | Astrazeneca Ab | Novel compounds |
| CA2456981C (en) * | 2001-08-06 | 2012-02-28 | Bresagen, Inc. | Alternative compositions and methods for the culture of stem cells |
| US6617152B2 (en) | 2001-09-04 | 2003-09-09 | Corning Inc | Method for creating a cell growth surface on a polymeric substrate |
| EP1298201A1 (en) | 2001-09-27 | 2003-04-02 | Cardion AG | Process for the production of cells exhibiting an islet-beta-cell-like state |
| EP1444345A4 (en) | 2001-10-18 | 2004-12-08 | Ixion Biotechnology Inc | TRANSFORMATION OF STEM CELLS AND LIVER PROGENITORS INTO FUNCTIONAL CELLS OF PANCREAS |
| CA2468171C (en) | 2001-11-15 | 2015-10-06 | Children's Medical Center Corporation | Methods of isolation, expansion and differentiation of fetal stem cells from chorionic villus, amniotic fluid, and placenta and therapeutic uses thereof |
| KR101150666B1 (ko) | 2001-12-07 | 2012-07-05 | 사이토리 테라퓨틱스, 인크. | 처리된 리포애스퍼레이트 세포로 환자를 치료하기 위한 시스템 및 방법 |
| CA2470539C (en) * | 2001-12-07 | 2011-10-04 | Geron Corporation | Islet cells from human embryonic stem cells |
| AU2002218893A1 (en) | 2001-12-21 | 2003-07-09 | Thromb-X Nv | Compositions for the in vitro derivation and culture of embryonic stem (es) cell lines with germline transmission capability |
| CA2471540A1 (en) | 2001-12-28 | 2003-07-10 | Cellartis Ab | A method for the establishment of a pluripotent human blastocyst-derived stem cell line |
| US20030162290A1 (en) | 2002-01-25 | 2003-08-28 | Kazutomo Inoue | Method for inducing differentiation of embryonic stem cells into functioning cells |
| US20030180268A1 (en) | 2002-02-05 | 2003-09-25 | Anthony Atala | Tissue engineered construct for supplementing or replacing a damaged organ |
| EP1498478A1 (en) | 2002-04-17 | 2005-01-19 | Otsuka Pharmaceutical Co., Ltd. | Method of forming pancreatic beta cells from mesenchymal cells |
| US20040161419A1 (en) | 2002-04-19 | 2004-08-19 | Strom Stephen C. | Placental stem cells and uses thereof |
| ATE387444T1 (de) | 2002-05-08 | 2008-03-15 | Janssen Pharmaceutica Nv | Substituierte pyrroline als kinase inhibitoren |
| GB0210539D0 (en) | 2002-05-08 | 2002-06-19 | Univ Edinburgh | Control of es cell self renewal and lineage specification, and medium therefor |
| US20060003446A1 (en) * | 2002-05-17 | 2006-01-05 | Gordon Keller | Mesoderm and definitive endoderm cell populations |
| BR0311413A (pt) | 2002-05-28 | 2005-03-22 | Becton Dickinson Co | Desenvolvimento e transdiferenciação de células acinares humanas |
| US6987110B2 (en) | 2002-06-05 | 2006-01-17 | Janssen Pharmaceutica N.V. | Substituted pyrrolines as kinase inhibitors |
| GB0212976D0 (en) | 2002-06-06 | 2002-07-17 | Tonejet Corp Pty Ltd | Ejection method and apparatus |
| CN1171991C (zh) | 2002-07-08 | 2004-10-20 | 徐如祥 | 人神经干细胞的培养方法 |
| US6877147B2 (en) * | 2002-07-22 | 2005-04-05 | Broadcom Corporation | Technique to assess timing delay by use of layout quality analyzer comparison |
| US7838290B2 (en) | 2002-07-25 | 2010-11-23 | The Scripps Research Institute | Hematopoietic stem cells and methods of treatment of neovascular eye diseases therewith |
| JP2005534345A (ja) | 2002-07-29 | 2005-11-17 | エス セル インターナショナル ピーティーイー リミテッド | インスリン陽性、グルコース応答性細胞の分化のための多段階方法 |
| US20040063204A1 (en) | 2002-08-14 | 2004-04-01 | Lijun Yang | Bone marrow cell differentiation |
| EP1539928A4 (en) | 2002-09-06 | 2006-09-06 | Amcyte Inc | CD56-POSITIVE HUMAN ADULTS PANCREATIC ENDOCRINE PRECURSOR CELLS |
| US9969977B2 (en) | 2002-09-20 | 2018-05-15 | Garnet Biotherapeutics | Cell populations which co-express CD49c and CD90 |
| US20040062753A1 (en) * | 2002-09-27 | 2004-04-01 | Alireza Rezania | Composite scaffolds seeded with mammalian cells |
| AU2003285172A1 (en) | 2002-11-08 | 2004-06-03 | The Johns Hopkins University | Human embryonic stem cell cultures, and compositions and methods for growing same |
| US7144999B2 (en) * | 2002-11-23 | 2006-12-05 | Isis Pharmaceuticals, Inc. | Modulation of hypoxia-inducible factor 1 alpha expression |
| EP1567639A4 (en) | 2002-12-05 | 2005-12-21 | Technion Res & Dev Foundation | CULTURE OF HUMAN PANCREATIC ISLANDS AND USES THEREOF |
| US7592175B2 (en) | 2002-12-16 | 2009-09-22 | Technion Research & Development Foundation Ltd. | Methods of preparing feeder cells-free, xeno-free human embryonic stem cells and cell cultures prepared using same |
| US20050118148A1 (en) | 2002-12-20 | 2005-06-02 | Roland Stein | Compositions and methods related to mammalian Maf-A |
| KR101114808B1 (ko) | 2003-01-29 | 2012-02-15 | 다케다 야쿠힌 고교 가부시키가이샤 | 피복 제제의 제조법 |
| RU2359671C2 (ru) | 2003-01-29 | 2009-06-27 | Такеда Фармасьютикал Компани Лимитед | Способ получения препарата с покрытием |
| WO2004073633A2 (en) * | 2003-02-14 | 2004-09-02 | The Board Of Trustees Of The Leland Stanford Junior University | Methods and compositions for modulating the development of stem cells |
| US20070154981A1 (en) | 2003-02-14 | 2007-07-05 | The Board Of Trustees Of The Leland Stanford Junior University | Insulin-producing cells derived from stem cells |
| KR100763477B1 (ko) * | 2003-03-12 | 2007-10-04 | 리라이언스 라이프 사이언시스 프라이빗. 리미티드 | 사람 배아 줄기세포로부터 최종적으로 분화된 도파민작용성 뉴런의 유도 |
| US20070020242A1 (en) | 2003-03-27 | 2007-01-25 | Ixion Biotechnology, Inc. | Method for transdifferentiation of non-pancreatic stem cells to the pancreatic pathway |
| US20060194315A1 (en) | 2003-03-31 | 2006-08-31 | Condie Brian G | Compositions and methods for the control, differentiaton and/or manipulation of pluripotent cells through a gamma-secretase signaling pathway |
| US20090203141A1 (en) | 2003-05-15 | 2009-08-13 | Shi-Lung Lin | Generation of tumor-free embryonic stem-like pluripotent cells using inducible recombinant RNA agents |
| CA2530732C (en) | 2003-06-27 | 2015-03-31 | DePuy Synthes Products, Inc. | Regeneration and repair of neural tissue using postpartum-derived cells |
| IL161903A0 (en) | 2003-07-17 | 2005-11-20 | Gamida Cell Ltd | Ex vivo progenitor and stem cell expansion for usein the treatment of disease of endodermally- deri ved organs |
| ITRM20030395A1 (it) | 2003-08-12 | 2005-02-13 | Istituto Naz Per Le Malattie Infettive Lazz | Terreno di coltura per il mantenimento, la proliferazione e il differenziamento di cellule di mammifero. |
| WO2005017117A2 (en) | 2003-08-14 | 2005-02-24 | Martin Haas | Multipotent amniotic fetal stem cells (mafsc) and banking of same |
| US7157275B2 (en) | 2003-08-15 | 2007-01-02 | Becton, Dickinson And Company | Peptides for enhanced cell attachment and growth |
| CA2536067A1 (en) | 2003-08-27 | 2005-03-10 | Stemcells California, Inc. | Enriched pancreatic stem cell and progenitor cell populations, and methods for identifying, isolating and enriching for these populations |
| EP1696899A1 (en) | 2003-12-17 | 2006-09-06 | Allergan, Inc. | Methods for treating retinoid responsive disorders using selective inhibitors of cyp26a and cyp26b |
| US20060030042A1 (en) | 2003-12-19 | 2006-02-09 | Ali Brivanlou | Maintenance of embryonic stem cells by the GSK-3 inhibitor 6-bromoindirubin-3'-oxime |
| US7541185B2 (en) | 2003-12-23 | 2009-06-02 | Cythera, Inc. | Methods for identifying factors for differentiating definitive endoderm |
| US7625753B2 (en) * | 2003-12-23 | 2009-12-01 | Cythera, Inc. | Expansion of definitive endoderm cells |
| US20050266554A1 (en) * | 2004-04-27 | 2005-12-01 | D Amour Kevin A | PDX1 expressing endoderm |
| SG149061A1 (en) | 2003-12-23 | 2009-01-29 | Cythera Inc | Definitive endoderm |
| CN112813019A (zh) | 2003-12-23 | 2021-05-18 | 维亚希特公司 | 定形内胚层 |
| US20050233446A1 (en) * | 2003-12-31 | 2005-10-20 | Parsons Xuejun H | Defined media for stem cell culture |
| TWI334443B (en) | 2003-12-31 | 2010-12-11 | Ind Tech Res Inst | Method of single cell culture of undifferentiated human embryonic stem cells |
| US7794704B2 (en) | 2004-01-23 | 2010-09-14 | Advanced Cell Technology, Inc. | Methods for producing enriched populations of human retinal pigment epithelium cells for treatment of retinal degeneration |
| WO2005071066A1 (en) | 2004-01-23 | 2005-08-04 | Board Of Regents, The University Of Texas System | Methods and compositions for preparing pancreatic insulin secreting cells |
| GB2441530B (en) | 2004-02-12 | 2009-09-23 | Univ Newcastle | Stem Cells |
| JP4901471B2 (ja) | 2004-02-19 | 2012-03-21 | 国立大学法人京都大学 | 体細胞核初期化物質のスクリーニング方法 |
| EP1737944A4 (en) | 2004-03-09 | 2010-03-24 | Lifescan Inc | METHOD FOR GENERATING INSULIN-PRODUCING CELLS |
| WO2005086845A2 (en) | 2004-03-10 | 2005-09-22 | Regents Of The University Of California | Compositions and methods for growth of embryonic stem cells |
| WO2005090557A1 (ja) | 2004-03-23 | 2005-09-29 | Daiichi Asubio Pharma Co., Ltd. | 多能性幹細胞の増殖方法 |
| WO2005097980A2 (en) * | 2004-03-26 | 2005-10-20 | Geron Corporation | New protocols for making hepatocytes from embryonic stem cells |
| WO2005097977A2 (en) | 2004-04-01 | 2005-10-20 | Wisconsin Alumni Research Foundation | Differentiation of stem cells to endoderm and pancreatic lineage |
| EA011953B1 (ru) | 2004-04-27 | 2009-06-30 | Китера, Инк. | Pdx1-экспрессирующая энтодерма |
| CA2573283C (en) | 2004-07-09 | 2023-03-14 | Cythera, Inc. | Methods for identifying factors for differentiating definitive endoderm |
| EP1791952A4 (en) | 2004-08-13 | 2008-06-11 | Univ Georgia Res Found | COMPOSITIONS AND METHODS OF SELF-RENEWAL AND DIFFERENTIATION IN HUMAN EMBRYONAL STEM CELLS |
| US20080268533A1 (en) | 2004-08-25 | 2008-10-30 | University Of Georgia Research Foundation, Inc. | Methods and Compositions Utilizing Myc and Gsk3Beta to Manipulate the Pluripotency of Embryonic Stem Cells |
| DE102004043256B4 (de) | 2004-09-07 | 2013-09-19 | Rheinische Friedrich-Wilhelms-Universität Bonn | Skalierbarer Prozess zur Kultivierung undifferenzierter Stammzellen in Suspension |
| JP5420837B2 (ja) | 2004-09-08 | 2014-02-19 | ウィスコンシン アラムニ リサーチ ファンデーション | 胚幹細胞の培地及び培養 |
| KR20070058584A (ko) | 2004-09-08 | 2007-06-08 | 위스콘신 얼럼나이 리서어치 화운데이션 | 인간 배아 줄기 세포의 배양 |
| WO2006073911A1 (en) | 2004-12-30 | 2006-07-13 | Stemlifeline, Inc. | Methods and compositions relating to embryonic stem cell lines |
| AU2006208944A1 (en) | 2005-01-28 | 2006-08-03 | Imperial College Innovations Limited | Methods for embryonic stem cell culture |
| US20060194321A1 (en) | 2005-01-31 | 2006-08-31 | Alan Colman | Directed differentiation of embryonic stem cells and uses thereof |
| US20060182724A1 (en) | 2005-02-15 | 2006-08-17 | Riordan Neil H | Method for expansion of stem cells |
| EP1860950B1 (en) | 2005-03-04 | 2017-04-19 | Lifescan, Inc. | Adult pancreatic derived stromal cells |
| GB0505970D0 (en) | 2005-03-23 | 2005-04-27 | Univ Edinburgh | Culture medium containing kinase inhibitor, and uses thereof |
| US7998938B2 (en) | 2005-04-15 | 2011-08-16 | Geron Corporation | Cancer treatment by combined inhibition of proteasome and telomerase activities |
| CN100425694C (zh) | 2005-04-15 | 2008-10-15 | 北京大学 | 诱导胚胎干细胞向胰腺细胞分化的方法 |
| US20080208351A1 (en) | 2005-04-26 | 2008-08-28 | Aarhus Universitet | Biocompatible Material for Surgical Implants and Cell Guiding Tissue Culture Surfaces |
| WO2006126574A1 (ja) | 2005-05-24 | 2006-11-30 | Kumamoto University | Es細胞の分化誘導方法 |
| AU2006202209B2 (en) | 2005-05-27 | 2011-04-14 | Lifescan, Inc. | Amniotic fluid derived cells |
| KR20080024194A (ko) | 2005-06-10 | 2008-03-17 | 아이알엠 엘엘씨 | 배아 줄기 세포의 다능성을 유지하는 화합물 |
| WO2006138433A2 (en) | 2005-06-14 | 2006-12-28 | The Regents Of The University Of California | Induction of cell differentiation by class i bhlh polypeptides |
| WO2006137787A1 (en) | 2005-06-21 | 2006-12-28 | Ge Healthcare Bio-Sciences Ab | Method for cell culture |
| US9074181B2 (en) | 2005-06-22 | 2015-07-07 | Asterias Biotherapeutics, Inc. | Suspension culture of human embryonic stem cells |
| BRPI0612888B8 (pt) | 2005-06-30 | 2022-12-27 | Janssen Pharmaceutica Nv | anilino-piridinotriazinas cíclicas como inibidoras de gsk-3, seus usos e composição farmacêutica, intermediário, seu uso e composição farmacêutica |
| WO2007117262A2 (en) * | 2005-07-29 | 2007-10-18 | Athersys, Inc. | Culture of non-embryonic cells at high cell density |
| US20090087907A1 (en) | 2005-07-29 | 2009-04-02 | Alice Pebay | Compositions and Methods for Growth of Pluripotent Cells |
| WO2007016485A2 (en) | 2005-07-29 | 2007-02-08 | Athersys, Inc. | Use of a gsk-3 inhibitor to maintain potency of cultured cells |
| WO2007025234A2 (en) | 2005-08-26 | 2007-03-01 | The Trustees Of Columbia University In The City Of New York | Generation of pancreatic endocrine cells from primary duct cell cultures and methods of use for treatment of diabetes |
| EP3354723B1 (en) | 2005-08-29 | 2023-12-13 | Technion Research & Development Foundation Ltd. | Media for culturing stem cells |
| EP1943334A1 (en) | 2005-09-02 | 2008-07-16 | Agency for Science, Technology and Research | Method of deriving progenitor cell line |
| US9422521B2 (en) | 2005-09-12 | 2016-08-23 | Es Cell International Pte Ltd. | Differentiation of pluripotent stem cells with a kinase inhibitor or PGI2 |
| WO2008048671A1 (en) | 2006-10-18 | 2008-04-24 | University Of Illinois | Embryonic-like stem cells derived from adult human peripheral blood and methods of use |
| US8409859B2 (en) | 2005-10-14 | 2013-04-02 | Regents Of The University Of Minnesota | Differentiation of non-embryonic stem cells to cells having a pancreatic phenotype |
| US7732202B2 (en) | 2005-10-21 | 2010-06-08 | International Stem Cell Corporation | Oxygen tension for the parthenogenic activation of human oocytes for the production of human embryonic stem cells |
| CA2627645C (en) | 2005-10-27 | 2015-07-07 | Cythera, Inc. | Pdx1-expressing dorsal and ventral foregut endoderm |
| CN103773804A (zh) | 2005-12-13 | 2014-05-07 | 国立大学法人京都大学 | 核重新编程因子 |
| WO2007082963A1 (es) | 2006-01-18 | 2007-07-26 | Fundación Instituto Valenciano De Infertilidad | Líneas de células madre embrionarias humanas y métodos para usar las mismas |
| JP5830217B2 (ja) | 2006-02-23 | 2015-12-09 | ヴィアサイト インコーポレイテッド | 分化可能細胞の培養に有用な組成物及び方法 |
| US7695965B2 (en) | 2006-03-02 | 2010-04-13 | Cythera, Inc. | Methods of producing pancreatic hormones |
| DK2650360T3 (da) | 2006-03-02 | 2019-10-07 | Viacyte Inc | Endokrine prekursorceller, pancreatiske hormon udtrykkende celler og fremgangsmåder til fremstilling |
| GB0615327D0 (en) | 2006-03-30 | 2006-09-13 | Univ Edinburgh | Culture medium containing kinase inhibitors and uses thereof |
| EP4438720A3 (en) | 2006-04-28 | 2025-02-26 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells |
| US8741643B2 (en) * | 2006-04-28 | 2014-06-03 | Lifescan, Inc. | Differentiation of pluripotent stem cells to definitive endoderm lineage |
| WO2007130474A2 (en) * | 2006-05-02 | 2007-11-15 | Wisconsin Alumni Research Foundation | Method of differentiating stem cells into cells of the endoderm and pancreatic lineage |
| US8685730B2 (en) | 2006-05-02 | 2014-04-01 | Wisconsin Alumni Research Foundation | Methods and devices for differentiating pluripotent stem cells into cells of the pancreatic lineage |
| US9598673B2 (en) | 2006-05-19 | 2017-03-21 | Creative Medical Health | Treatment of disc degenerative disease |
| US7964402B2 (en) | 2006-05-25 | 2011-06-21 | Sanford-Burnham Medical Research Institute | Methods for culture and production of single cell populations of human embryonic stem cells |
| WO2007143193A1 (en) | 2006-06-02 | 2007-12-13 | University Of Georgia Research Foundation, Inc. | Pancreatic and liver endoderm cells and tissue by differentiation of definitive endoderm cells obtained from human embryonic stems |
| CN101541953A (zh) | 2006-06-02 | 2009-09-23 | 佐治亚大学研究基金会 | 通过从人胚胎干细胞获得的定形内胚层细胞的分化得到胰和肝内胚层细胞及组织 |
| WO2007149182A2 (en) | 2006-06-19 | 2007-12-27 | Geron Corporation | Differentiation and enrichment of islet-like cells from human pluripotent stem cells |
| CN100494359C (zh) | 2006-06-23 | 2009-06-03 | 中日友好医院 | 神经干细胞三维立体培养体外扩增的方法 |
| CA2893679C (en) | 2006-06-26 | 2018-10-30 | Lifescan, Inc. | Conditioned medium for pluripotent stem cell culture |
| US20080003676A1 (en) | 2006-06-26 | 2008-01-03 | Millipore Corporation | Growth of embryonic stem cells |
| GB2454386B (en) | 2006-07-06 | 2011-07-06 | Es Cell Int Pte Ltd | Method for embryonic stem cell culture on a positively charged support surface |
| WO2008013664A2 (en) | 2006-07-26 | 2008-01-31 | Cythera, Inc. | Methods of producing pancreatic hormones |
| EP3441459B1 (en) | 2006-08-02 | 2021-03-17 | Technion Research & Development Foundation Limited | Methods of expanding embryonic stem cells in a suspension culture |
| KR101331510B1 (ko) | 2006-08-30 | 2013-11-20 | 재단법인서울대학교산학협력재단 | 저농도의 포도당을 함유하는 인간 배아줄기세포용 배지조성물 및 이를 이용한 인간 배아 줄기세포로부터 인슐린생산 세포 또는 세포괴로 분화시키는 방법, 그리고그로부터 유도된 인슐린 생산 세포 또는 세포괴 |
| JP2008099662A (ja) | 2006-09-22 | 2008-05-01 | Institute Of Physical & Chemical Research | 幹細胞の培養方法 |
| WO2008039521A2 (en) | 2006-09-26 | 2008-04-03 | Nmt Medical, Inc. | Method for modifying a medical implant surface for promoting tissue growth |
| WO2008048647A1 (en) * | 2006-10-17 | 2008-04-24 | Cythera, Inc. | Modulation of the phosphatidylinositol-3-kinase pathway in the differentiation of human embryonic stem cells |
| EP2114895A4 (en) | 2006-10-17 | 2011-06-22 | Stiefel Laboratories | TALARAZOLMETABOLITEN |
| US20110151554A1 (en) | 2006-11-09 | 2011-06-23 | Akira Yuo | Method for culturing and subculturing primate embryonic stem cell, as well as method for inducing differentiation thereof |
| WO2008086005A1 (en) | 2007-01-09 | 2008-07-17 | University Of South Florida | Compositions including triciribine and bortezomib and derivatives thereof and methods of use thereof |
| CN101641436A (zh) | 2007-01-30 | 2010-02-03 | 佐治亚大学研究基金会 | 用于产生内胚层和中胚层细胞系及多能游走细胞(mmc)的早期中胚层细胞即稳定的中内胚层细胞群 |
| GB0703188D0 (en) | 2007-02-19 | 2007-03-28 | Roger Land Building | Large scale production of stem cells |
| WO2008148105A1 (en) | 2007-05-25 | 2008-12-04 | Medistem Laboratories, Inc. | Endometrial stem cells and methods of making and using same |
| US7354310B1 (en) * | 2007-06-07 | 2008-04-08 | Fci Americas Technology, Inc. | Electrical connector housing cover |
| US8815585B2 (en) | 2007-06-29 | 2014-08-26 | Cellular Dynamics International, Inc. | Automated method and apparatus for embryonic stem cell culture |
| CN101861386A (zh) | 2007-07-18 | 2010-10-13 | 生命扫描有限公司 | 人胚胎干细胞的分化 |
| PL2185691T3 (pl) | 2007-07-31 | 2018-08-31 | Lifescan, Inc. | Różnicowanie pluripotencjalnych komórek macierzystych poprzez zastosowanie ludzkich komórek odżywczych |
| MX2010001335A (es) | 2007-07-31 | 2010-06-02 | Lifescan Inc | Diferenciacion de celulas madre embrionarias humanas. |
| CA2696622C (en) | 2007-08-24 | 2016-07-19 | Stichting Het Nederlands Kanker Instituut | Compositions for the treatment of neoplastic diseases |
| US20110151447A1 (en) | 2007-11-06 | 2011-06-23 | Children's Medical Center Corporation | Method to produce induced pluripotent stem (ips) cells from non-embryonic human cells |
| CN107574142B (zh) | 2007-11-27 | 2021-07-06 | 生命扫描有限公司 | 人胚胎干细胞的分化 |
| SG154367A1 (en) | 2008-01-31 | 2009-08-28 | Es Cell Int Pte Ltd | Method of differentiating stem cells |
| WO2009096049A1 (ja) | 2008-02-01 | 2009-08-06 | Kyoto University | 人工多能性幹細胞由来分化細胞 |
| US20100330677A1 (en) | 2008-02-11 | 2010-12-30 | Cambridge Enterprise Limited | Improved Reprogramming of Mammalian Cells, and Cells Obtained |
| CN102046779A (zh) | 2008-02-21 | 2011-05-04 | 森托科尔奥索生物科技公司 | 用于细胞粘附、培养和分离的方法、表面改性培养板和组合物 |
| WO2009110215A1 (ja) | 2008-03-03 | 2009-09-11 | 独立行政法人 科学技術振興機構 | 繊毛細胞の分化誘導方法 |
| US8716018B2 (en) | 2008-03-17 | 2014-05-06 | Agency For Science, Technology And Research | Microcarriers for stem cell culture |
| RU2359030C1 (ru) | 2008-03-19 | 2009-06-20 | Общество С Ограниченной Ответственностью "Лаборатория Клеточных Технологий" | Способ получения эндотелиальных клеток из эмбриональных стволовых клеток человека (варианты) |
| DK2727998T3 (da) | 2008-04-21 | 2019-08-26 | Viacyte Inc | Fremgangsmåder til oprensning af pancreatiske endodermceller afledt fra humane embryoniske stamceller |
| US8338170B2 (en) | 2008-04-21 | 2012-12-25 | Viacyte, Inc. | Methods for purifying endoderm and pancreatic endoderm cells derived from human embryonic stem cells |
| WO2009132083A2 (en) | 2008-04-22 | 2009-10-29 | President And Fellows Of Harvard College | Compositions and methods for promoting the generation of pdx1+ pancreatic cells |
| US8623648B2 (en) | 2008-04-24 | 2014-01-07 | Janssen Biotech, Inc. | Treatment of pluripotent cells |
| US7939322B2 (en) | 2008-04-24 | 2011-05-10 | Centocor Ortho Biotech Inc. | Cells expressing pluripotency markers and expressing markers characteristic of the definitive endoderm |
| US20090298178A1 (en) * | 2008-06-03 | 2009-12-03 | D Amour Kevin Allen | Growth factors for production of definitive endoderm |
| WO2009154606A1 (en) | 2008-06-03 | 2009-12-23 | Cythera, Inc. | Growth factors for production of definitive endoderm |
| RU2533805C2 (ru) | 2008-06-30 | 2014-11-20 | Сентокор Орто Байотек Инк. | Дифференцирование плюрипотентных стволовых клеток, представляющих собой линию клеток человека |
| DE102008032236A1 (de) | 2008-06-30 | 2010-04-01 | Eberhard-Karls-Universität Tübingen | Isolierung und/oder Identifizierung von Stammzellen mit adipozytärem, chondrozytärem und pankreatischem Differenzierungspotential |
| US20100028307A1 (en) | 2008-07-31 | 2010-02-04 | O'neil John J | Pluripotent stem cell differentiation |
| WO2010022395A2 (en) | 2008-08-22 | 2010-02-25 | President And Fellows Of Harvard College | Methods of reprogramming cells |
| WO2010051223A1 (en) | 2008-10-31 | 2010-05-06 | Centocor Ortho Biotech Inc. | Differentiation of human embryonic stem cells to the pancreatic endocrine lineage |
| EP2350265B1 (en) | 2008-10-31 | 2019-04-17 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells to the pancreatic endocrine lineage |
| ES2743204T3 (es) | 2008-11-04 | 2020-02-18 | Viacyte Inc | Composiciones de suspensión de agregados de células madre y métodos para su diferenciación |
| US8008075B2 (en) | 2008-11-04 | 2011-08-30 | Viacyte, Inc. | Stem cell aggregate suspension compositions and methods of differentiation thereof |
| PL2356227T3 (pl) | 2008-11-14 | 2018-07-31 | Viacyte, Inc. | Kapsułkowanie komórek trzustki pochodzących z ludzkich pluripotencjalnych komórek macierzystych |
| CA2744234C (en) | 2008-11-20 | 2018-11-06 | Centocor Ortho Biotech Inc. | Pluripotent stem cell culture on micro-carriers |
| JP5604766B2 (ja) | 2008-12-05 | 2014-10-15 | アンスティチュ ナショナル ドゥ ラ サンテ エ ドゥ ラ ルシェルシュ メディカル | 多能性細胞の神経分化のための方法および培地 |
| EP2456862A4 (en) | 2009-07-20 | 2013-02-27 | Janssen Biotech Inc | DIFFERENTIATION OF HUMAN EMBRYONIC STEM CELLS |
| GB2485113B (en) | 2009-07-20 | 2016-12-28 | Janssen Biotech Inc | Differentiation of human embryonic stem cells into cells of the pancreatic endoderm lineage |
| CN107058389A (zh) | 2009-10-29 | 2017-08-18 | 詹森生物科技公司 | 多能干细胞 |
| FI20096288A0 (fi) | 2009-12-04 | 2009-12-04 | Kristiina Rajala | Formulations and methods for culturing stem cells |
| RU2701335C2 (ru) | 2009-12-23 | 2019-09-25 | Янссен Байотек, Инк. | Способ получения популяции панкреатических эндокринных клеток, соэкспрессирующих nkx6.1 и инсулин, и способ лечения диабета |
| MX339669B (es) | 2009-12-23 | 2016-06-02 | Janssen Biotech Inc | Diferenciacion de celulas madres embrionarias humanas. |
| JP5812492B2 (ja) | 2010-02-03 | 2015-11-11 | 国立研究開発法人国立がん研究センター | 誘導肝幹細胞及びその製造方法、並びに、該細胞の応用 |
| WO2011108993A1 (en) | 2010-03-02 | 2011-09-09 | National University Of Singapore | Culture additives to boost stem cell proliferation and differentiation response |
| CN102959076B (zh) | 2010-03-31 | 2015-09-16 | 斯克里普斯研究所 | 重编程细胞 |
| WO2011139628A1 (en) | 2010-04-25 | 2011-11-10 | Mount Sinai School Of Medicine | Generation of anterior foregut endoderm from pluripotent cells |
| SG185511A1 (en) | 2010-05-12 | 2012-12-28 | Centocor Ortho Biotech Inc | Differentiation of human embryonic stem cells |
| EP2601288B1 (en) | 2010-08-05 | 2016-04-06 | Wisconsin Alumni Research Foundation | Simplified basic media for human pluripotent cell culture |
| CA2809305C (en) | 2010-08-31 | 2019-06-11 | Janssen Biotech, Inc. | Differentiation of pluripotent stem cells |
| EP2853589B1 (en) | 2010-08-31 | 2017-12-27 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells |
| WO2012117333A1 (en) | 2011-02-28 | 2012-09-07 | Stempeutics Research Malaysia Sdn Bhd | Isolation and expansion of adult stem cells, their therapeutic composition and uses thereof |
| WO2013055834A2 (en) | 2011-10-11 | 2013-04-18 | The New York Stem Cell Foundation | Er stress relievers in beta cell protection |
| WO2013055397A1 (en) | 2011-10-14 | 2013-04-18 | Children's Medical Center Corporation | Inhibition and enhancement of reprogramming by chromatin modifying enzymes |
| EP2794857B1 (en) | 2011-12-22 | 2026-02-11 | Janssen Biotech, Inc. | Differentiation of human embryonic stem cells into single hormonal insulin positive cells |
| US10519422B2 (en) | 2012-02-29 | 2019-12-31 | Riken | Method of producing human retinal pigment epithelial cells |
| KR102468315B1 (ko) | 2012-06-08 | 2022-11-16 | 얀센 바이오테크 인코포레이티드 | 인간 배아 줄기 세포의 췌장 내분비 세포로의 분화 |
| EP2893000B1 (en) | 2012-09-03 | 2019-04-10 | Novo Nordisk A/S | Generation of pancreatic endoderm from pluripotent stem cells using small molecules |
| BR112015015701A2 (pt) | 2012-12-31 | 2017-07-11 | Janssen Biotech Inc | diferenciação de células-tronco embrionárias humanas em células pancreáticas endócrinas com o uso de reguladores hb9 |
| US8859286B2 (en) | 2013-03-14 | 2014-10-14 | Viacyte, Inc. | In vitro differentiation of pluripotent stem cells to pancreatic endoderm cells (PEC) and endocrine cells |
| SG11201507510PA (en) | 2013-03-15 | 2015-10-29 | Jackson Lab | Isolation of non-embryonic stem cells and uses thereof |
| EP2981605B1 (en) | 2013-04-03 | 2019-06-19 | FUJIFILM Cellular Dynamics, Inc. | Methods and compositions for culturing endoderm progenitor cells in suspension |
| TWI768808B (zh) | 2021-04-01 | 2022-06-21 | 友達光電股份有限公司 | 遮光元件基板以及顯示裝置 |
-
2009
- 2009-06-30 RU RU2011103197/10A patent/RU2533805C2/ru active
- 2009-06-30 AU AU2009267137A patent/AU2009267137A1/en not_active Abandoned
- 2009-06-30 ES ES09774297.7T patent/ES2552240T3/es active Active
- 2009-06-30 PL PL15171064T patent/PL2942392T3/pl unknown
- 2009-06-30 WO PCT/US2009/049183 patent/WO2010002846A1/en not_active Ceased
- 2009-06-30 KR KR1020117001981A patent/KR101651661B1/ko active Active
- 2009-06-30 BR BRPI0914116A patent/BRPI0914116A2/pt not_active Application Discontinuation
- 2009-06-30 PL PL09774297T patent/PL2310492T3/pl unknown
- 2009-06-30 EP EP09774297.7A patent/EP2310492B1/en active Active
- 2009-06-30 EP EP15171064.7A patent/EP2942392B1/en active Active
- 2009-06-30 KR KR1020187003886A patent/KR20180018839A/ko not_active Abandoned
- 2009-06-30 MX MX2011000125A patent/MX2011000125A/es active IP Right Grant
- 2009-06-30 CA CA2729121A patent/CA2729121C/en active Active
- 2009-06-30 CN CN200980134123.1A patent/CN102159703B/zh active Active
- 2009-06-30 US US12/494,789 patent/US20100015711A1/en not_active Abandoned
- 2009-06-30 KR KR1020177012167A patent/KR101829310B1/ko not_active Expired - Fee Related
- 2009-06-30 JP JP2011516798A patent/JP5734183B2/ja not_active Expired - Fee Related
- 2009-06-30 KR KR1020167022553A patent/KR101734501B1/ko not_active Expired - Fee Related
- 2009-06-30 ES ES15171064T patent/ES2697798T3/es active Active
-
2011
- 2011-01-28 ZA ZA2011/00758A patent/ZA201100758B/en unknown
-
2012
- 2012-03-29 US US13/434,392 patent/US20120190112A1/en not_active Abandoned
- 2012-03-29 US US13/434,409 patent/US9593306B2/en active Active
- 2012-03-29 US US13/434,370 patent/US9593305B2/en active Active
-
2014
- 2014-06-10 RU RU2014123686A patent/RU2673750C2/ru active
-
2016
- 2016-04-28 HK HK16104895.0A patent/HK1216905A1/en unknown
-
2017
- 2017-03-13 US US15/457,893 patent/US10233421B2/en active Active
- 2017-03-13 US US15/457,864 patent/US10351820B2/en active Active
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US10233421B2 (en) | Differentiation of pluripotent stem cells | |
| KR102058901B1 (ko) | 인간 배아 줄기 세포의 분화 | |
| KR101893021B1 (ko) | 인간 배아 줄기 세포의 분화 | |
| KR20110077017A (ko) | 인간 배아 줄기 세포의 췌장 내분비 계통으로의 분화 | |
| AU2018201993B2 (en) | Differentiation of pluripotent stem cells | |
| HK1156665B (en) | Differentiation of pluripotent stem cells |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] |
Free format text: DE ACORDO COM O ARTIGO 229-C DA LEI NO 10196/2001, QUE MODIFICOU A LEI NO 9279/96, A CONCESSAO DA PATENTE ESTA CONDICIONADA A ANUENCIA PREVIA DA ANVISA. CONSIDERANDO A APROVACAO DOS TERMOS DO PARECER NO 337/PGF/EA/2010, BEM COMO A PORTARIA INTERMINISTERIAL NO 1065 DE 24/05/2012, ENCAMINHA-SE O PRESENTE PEDIDO PARA AS PROVIDENCIAS CABIVEIS. |
|
| B07G | Grant request does not fulfill article 229-c lpi (prior consent of anvisa) [chapter 7.7 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B08F | Application dismissed because of non-payment of annual fees [chapter 8.6 patent gazette] |
Free format text: REFERENTE A 11A ANUIDADE. |
|
| B11B | Dismissal acc. art. 36, par 1 of ipl - no reply within 90 days to fullfil the necessary requirements | ||
| B350 | Update of information on the portal [chapter 15.35 patent gazette] |