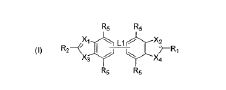
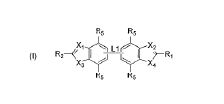
BRPI0922220B1 - uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos - Google Patents
uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos Download PDFInfo
- Publication number
- BRPI0922220B1 BRPI0922220B1 BRPI0922220-0A BRPI0922220A BRPI0922220B1 BR PI0922220 B1 BRPI0922220 B1 BR PI0922220B1 BR PI0922220 A BRPI0922220 A BR PI0922220A BR PI0922220 B1 BRPI0922220 B1 BR PI0922220B1
- Authority
- BR
- Brazil
- Prior art keywords
- compounds
- agents
- fact
- spp
- use according
- Prior art date
Links
- 150000001875 compounds Chemical class 0.000 title claims abstract description 247
- 230000000844 anti-bacterial effect Effects 0.000 title claims abstract description 34
- 239000008194 pharmaceutical composition Substances 0.000 title claims abstract description 27
- 241000193163 Clostridioides difficile Species 0.000 claims abstract description 78
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 claims abstract description 77
- 201000010099 disease Diseases 0.000 claims abstract description 73
- 238000011282 treatment Methods 0.000 claims abstract description 63
- 229910052739 hydrogen Inorganic materials 0.000 claims description 72
- -1 pyridine-4-yl Chemical group 0.000 claims description 59
- 230000000694 effects Effects 0.000 claims description 34
- 125000003118 aryl group Chemical group 0.000 claims description 21
- 230000003385 bacteriostatic effect Effects 0.000 claims description 21
- 230000000968 intestinal effect Effects 0.000 claims description 21
- 125000005843 halogen group Chemical group 0.000 claims description 19
- 238000002360 preparation method Methods 0.000 claims description 16
- RAXXELZNTBOGNW-UHFFFAOYSA-N imidazole Natural products C1=CNC=N1 RAXXELZNTBOGNW-UHFFFAOYSA-N 0.000 claims description 14
- 125000004169 (C1-C6) alkyl group Chemical group 0.000 claims description 13
- 125000004452 carbocyclyl group Chemical group 0.000 claims description 10
- 125000001072 heteroaryl group Chemical group 0.000 claims description 10
- 125000001424 substituent group Chemical group 0.000 claims description 10
- 125000000623 heterocyclic group Chemical group 0.000 claims description 9
- 125000004122 cyclic group Chemical group 0.000 claims description 7
- 241000606124 Bacteroides fragilis Species 0.000 claims description 6
- 241000186660 Lactobacillus Species 0.000 claims description 6
- 229940039696 lactobacillus Drugs 0.000 claims description 6
- 229910052760 oxygen Inorganic materials 0.000 claims description 6
- 238000006467 substitution reaction Methods 0.000 claims description 6
- 229910052717 sulfur Inorganic materials 0.000 claims description 6
- 101100134925 Gallus gallus COR6 gene Proteins 0.000 claims description 5
- 125000004178 (C1-C4) alkyl group Chemical group 0.000 claims description 4
- 241000423333 Bacteroides fragilis NCTC 9343 Species 0.000 claims description 4
- 241001148536 Bacteroides sp. Species 0.000 claims description 4
- 241000186000 Bifidobacterium Species 0.000 claims description 4
- 125000000882 C2-C6 alkenyl group Chemical group 0.000 claims description 4
- 241000588724 Escherichia coli Species 0.000 claims description 4
- 125000004435 hydrogen atom Chemical group [H]* 0.000 claims description 4
- 125000003601 C2-C6 alkynyl group Chemical group 0.000 claims description 3
- 241000186394 Eubacterium Species 0.000 claims description 3
- 241000206591 Peptococcus Species 0.000 claims description 3
- 241000191992 Peptostreptococcus Species 0.000 claims description 3
- 241000192031 Ruminococcus Species 0.000 claims description 3
- 239000001257 hydrogen Substances 0.000 claims description 3
- 125000005647 linker group Chemical group 0.000 claims description 3
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 3
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 3
- 241000588722 Escherichia Species 0.000 claims description 2
- 241000605909 Fusobacterium Species 0.000 claims description 2
- 125000004076 pyridyl group Chemical group 0.000 claims 2
- UHQFBTAJFNVZIV-UHFFFAOYSA-N 2-pyridin-4-yl-6-(2-pyridin-4-yl-3h-benzimidazol-5-yl)-1h-benzimidazole Chemical compound C1=NC=CC(C=2NC3=CC=C(C=C3N=2)C=2C=C3N=C(NC3=CC=2)C=2C=CN=CC=2)=C1 UHQFBTAJFNVZIV-UHFFFAOYSA-N 0.000 claims 1
- 241001360526 Escherichia coli ATCC 25922 Species 0.000 claims 1
- 239000000203 mixture Substances 0.000 abstract description 81
- 238000000034 method Methods 0.000 abstract description 47
- 208000035143 Bacterial infection Diseases 0.000 abstract description 20
- 208000015181 infectious disease Diseases 0.000 abstract description 20
- 208000022362 bacterial infectious disease Diseases 0.000 abstract description 15
- 239000003795 chemical substances by application Substances 0.000 description 90
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N Dimethylsulphoxide Chemical compound CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 66
- 241000894006 Bacteria Species 0.000 description 41
- 239000003242 anti bacterial agent Substances 0.000 description 41
- KYQCOXFCLRTKLS-UHFFFAOYSA-N Pyrazine Chemical compound C1=CN=CC=N1 KYQCOXFCLRTKLS-UHFFFAOYSA-N 0.000 description 38
- 229940088710 antibiotic agent Drugs 0.000 description 35
- 239000003814 drug Substances 0.000 description 25
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 24
- 238000009472 formulation Methods 0.000 description 24
- 239000002671 adjuvant Substances 0.000 description 23
- 238000002560 therapeutic procedure Methods 0.000 description 23
- 150000003839 salts Chemical class 0.000 description 22
- 238000005160 1H NMR spectroscopy Methods 0.000 description 21
- 206010009657 Clostridium difficile colitis Diseases 0.000 description 20
- 208000003100 Pseudomembranous Enterocolitis Diseases 0.000 description 20
- 239000007787 solid Substances 0.000 description 20
- 206010012735 Diarrhoea Diseases 0.000 description 19
- PCNDJXKNXGMECE-UHFFFAOYSA-N Phenazine Natural products C1=CC=CC2=NC3=CC=CC=C3N=C21 PCNDJXKNXGMECE-UHFFFAOYSA-N 0.000 description 19
- 229940079593 drug Drugs 0.000 description 19
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 19
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 18
- 241000193403 Clostridium Species 0.000 description 17
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 17
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 description 17
- 239000000243 solution Substances 0.000 description 17
- 206010037128 Pseudomembranous colitis Diseases 0.000 description 16
- 239000000463 material Substances 0.000 description 16
- 239000003826 tablet Substances 0.000 description 16
- 125000004432 carbon atom Chemical group C* 0.000 description 15
- 230000003115 biocidal effect Effects 0.000 description 14
- 210000004215 spore Anatomy 0.000 description 14
- 150000002430 hydrocarbons Chemical group 0.000 description 13
- 239000000546 pharmaceutical excipient Substances 0.000 description 13
- 239000000047 product Substances 0.000 description 13
- CSCPPACGZOOCGX-UHFFFAOYSA-N Acetone Chemical compound CC(C)=O CSCPPACGZOOCGX-UHFFFAOYSA-N 0.000 description 12
- BWHMMNNQKKPAPP-UHFFFAOYSA-L potassium carbonate Chemical compound [K+].[K+].[O-]C([O-])=O BWHMMNNQKKPAPP-UHFFFAOYSA-L 0.000 description 12
- 239000003755 preservative agent Substances 0.000 description 12
- 241000193738 Bacillus anthracis Species 0.000 description 11
- 235000019439 ethyl acetate Nutrition 0.000 description 11
- 238000011321 prophylaxis Methods 0.000 description 11
- 239000003053 toxin Substances 0.000 description 11
- 231100000765 toxin Toxicity 0.000 description 11
- 108700012359 toxins Proteins 0.000 description 11
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 10
- 108010059993 Vancomycin Proteins 0.000 description 10
- 206010009887 colitis Diseases 0.000 description 10
- 238000004440 column chromatography Methods 0.000 description 10
- 235000014113 dietary fatty acids Nutrition 0.000 description 10
- 239000000194 fatty acid Substances 0.000 description 10
- 229930195729 fatty acid Natural products 0.000 description 10
- 230000012010 growth Effects 0.000 description 10
- 230000002401 inhibitory effect Effects 0.000 description 10
- 229960000282 metronidazole Drugs 0.000 description 10
- VAOCPAMSLUNLGC-UHFFFAOYSA-N metronidazole Chemical compound CC1=NC=C([N+]([O-])=O)N1CCO VAOCPAMSLUNLGC-UHFFFAOYSA-N 0.000 description 10
- 229940002612 prodrug Drugs 0.000 description 10
- 239000000651 prodrug Substances 0.000 description 10
- 239000012453 solvate Substances 0.000 description 10
- 229960003165 vancomycin Drugs 0.000 description 10
- MYPYJXKWCTUITO-LYRMYLQWSA-N vancomycin Chemical compound O([C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC1=C2C=C3C=C1OC1=CC=C(C=C1Cl)[C@@H](O)[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@H]3C(=O)N[C@H]1C(=O)N[C@H](C(N[C@@H](C3=CC(O)=CC(O)=C3C=3C(O)=CC=C1C=3)C(O)=O)=O)[C@H](O)C1=CC=C(C(=C1)Cl)O2)=O)NC(=O)[C@@H](CC(C)C)NC)[C@H]1C[C@](C)(N)[C@H](O)[C@H](C)O1 MYPYJXKWCTUITO-LYRMYLQWSA-N 0.000 description 10
- MYPYJXKWCTUITO-UHFFFAOYSA-N vancomycin Natural products O1C(C(=C2)Cl)=CC=C2C(O)C(C(NC(C2=CC(O)=CC(O)=C2C=2C(O)=CC=C3C=2)C(O)=O)=O)NC(=O)C3NC(=O)C2NC(=O)C(CC(N)=O)NC(=O)C(NC(=O)C(CC(C)C)NC)C(O)C(C=C3Cl)=CC=C3OC3=CC2=CC1=C3OC1OC(CO)C(O)C(O)C1OC1CC(C)(N)C(O)C(C)O1 MYPYJXKWCTUITO-UHFFFAOYSA-N 0.000 description 10
- 239000004480 active ingredient Substances 0.000 description 9
- 244000005700 microbiome Species 0.000 description 9
- 239000002244 precipitate Substances 0.000 description 9
- 239000000725 suspension Substances 0.000 description 9
- 230000001225 therapeutic effect Effects 0.000 description 9
- SUBDBMMJDZJVOS-UHFFFAOYSA-N 5-methoxy-2-{[(4-methoxy-3,5-dimethylpyridin-2-yl)methyl]sulfinyl}-1H-benzimidazole Chemical compound N=1C2=CC(OC)=CC=C2NC=1S(=O)CC1=NC=C(C)C(OC)=C1C SUBDBMMJDZJVOS-UHFFFAOYSA-N 0.000 description 8
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 8
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 8
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 8
- DTQVDTLACAAQTR-UHFFFAOYSA-N Trifluoroacetic acid Chemical compound OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 8
- 239000007900 aqueous suspension Substances 0.000 description 8
- 230000001580 bacterial effect Effects 0.000 description 8
- 239000002585 base Substances 0.000 description 8
- FPPNZSSZRUTDAP-UWFZAAFLSA-N carbenicillin Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)C(C(O)=O)C1=CC=CC=C1 FPPNZSSZRUTDAP-UWFZAAFLSA-N 0.000 description 8
- 229960003669 carbenicillin Drugs 0.000 description 8
- 239000003086 colorant Substances 0.000 description 8
- 229940077716 histamine h2 receptor antagonists for peptic ulcer and gord Drugs 0.000 description 8
- 230000001965 increasing effect Effects 0.000 description 8
- 238000004519 manufacturing process Methods 0.000 description 8
- 239000003921 oil Substances 0.000 description 8
- 235000019198 oils Nutrition 0.000 description 8
- YNWDKZIIWCEDEE-UHFFFAOYSA-N pantoprazole sodium Chemical compound [Na+].COC1=CC=NC(CS(=O)C=2[N-]C3=CC=C(OC(F)F)C=C3N=2)=C1OC YNWDKZIIWCEDEE-UHFFFAOYSA-N 0.000 description 8
- 229920002261 Corn starch Polymers 0.000 description 7
- 241001465754 Metazoa Species 0.000 description 7
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 7
- 241000191967 Staphylococcus aureus Species 0.000 description 7
- 125000000217 alkyl group Chemical group 0.000 description 7
- 230000008901 benefit Effects 0.000 description 7
- 239000002775 capsule Substances 0.000 description 7
- 239000003085 diluting agent Substances 0.000 description 7
- 150000004665 fatty acids Chemical class 0.000 description 7
- 230000002550 fecal effect Effects 0.000 description 7
- 239000000796 flavoring agent Substances 0.000 description 7
- 150000004820 halides Chemical group 0.000 description 7
- 239000000314 lubricant Substances 0.000 description 7
- 239000002207 metabolite Substances 0.000 description 7
- 239000004094 surface-active agent Substances 0.000 description 7
- 239000000375 suspending agent Substances 0.000 description 7
- 239000003765 sweetening agent Substances 0.000 description 7
- 239000003981 vehicle Substances 0.000 description 7
- PAYRUJLWNCNPSJ-UHFFFAOYSA-N Aniline Chemical compound NC1=CC=CC=C1 PAYRUJLWNCNPSJ-UHFFFAOYSA-N 0.000 description 6
- 241000194033 Enterococcus Species 0.000 description 6
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 6
- GLUUGHFHXGJENI-UHFFFAOYSA-N Piperazine Chemical compound C1CNCCN1 GLUUGHFHXGJENI-UHFFFAOYSA-N 0.000 description 6
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 6
- 230000000845 anti-microbial effect Effects 0.000 description 6
- 125000004429 atom Chemical group 0.000 description 6
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid group Chemical group C(C1=CC=CC=C1)(=O)O WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 6
- 239000011230 binding agent Substances 0.000 description 6
- 239000008120 corn starch Substances 0.000 description 6
- 239000003599 detergent Substances 0.000 description 6
- XUFQPHANEAPEMJ-UHFFFAOYSA-N famotidine Chemical compound NC(N)=NC1=NC(CSCCC(N)=NS(N)(=O)=O)=CS1 XUFQPHANEAPEMJ-UHFFFAOYSA-N 0.000 description 6
- 235000003599 food sweetener Nutrition 0.000 description 6
- 238000000338 in vitro Methods 0.000 description 6
- MJIHNNLFOKEZEW-UHFFFAOYSA-N lansoprazole Chemical compound CC1=C(OCC(F)(F)F)C=CN=C1CS(=O)C1=NC2=CC=CC=C2N1 MJIHNNLFOKEZEW-UHFFFAOYSA-N 0.000 description 6
- HQKMJHAJHXVSDF-UHFFFAOYSA-L magnesium stearate Chemical compound [Mg+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O HQKMJHAJHXVSDF-UHFFFAOYSA-L 0.000 description 6
- 229910052757 nitrogen Inorganic materials 0.000 description 6
- 238000004806 packaging method and process Methods 0.000 description 6
- 235000015320 potassium carbonate Nutrition 0.000 description 6
- 229910000027 potassium carbonate Inorganic materials 0.000 description 6
- 239000000843 powder Substances 0.000 description 6
- 239000006041 probiotic Substances 0.000 description 6
- 235000018291 probiotics Nutrition 0.000 description 6
- YREYEVIYCVEVJK-UHFFFAOYSA-N rabeprazole Chemical compound COCCCOC1=CC=NC(CS(=O)C=2NC3=CC=CC=C3N=2)=C1C YREYEVIYCVEVJK-UHFFFAOYSA-N 0.000 description 6
- 239000002904 solvent Substances 0.000 description 6
- 238000001356 surgical procedure Methods 0.000 description 6
- 208000024891 symptom Diseases 0.000 description 6
- 238000012360 testing method Methods 0.000 description 6
- 229930195735 unsaturated hydrocarbon Natural products 0.000 description 6
- DGMYEDVRVIEGBG-UHFFFAOYSA-N 4-[6-[2-(4-aminophenyl)-3-methylbenzimidazol-5-yl]-1h-benzimidazol-2-yl]aniline Chemical compound C1=C2N(C)C(C=3C=CC(N)=CC=3)=NC2=CC=C1C(C=C1N=2)=CC=C1NC=2C1=CC=C(N)C=C1 DGMYEDVRVIEGBG-UHFFFAOYSA-N 0.000 description 5
- WZRJTRPJURQBRM-UHFFFAOYSA-N 4-amino-n-(5-methyl-1,2-oxazol-3-yl)benzenesulfonamide;5-[(3,4,5-trimethoxyphenyl)methyl]pyrimidine-2,4-diamine Chemical compound O1C(C)=CC(NS(=O)(=O)C=2C=CC(N)=CC=2)=N1.COC1=C(OC)C(OC)=CC(CC=2C(=NC(N)=NC=2)N)=C1 WZRJTRPJURQBRM-UHFFFAOYSA-N 0.000 description 5
- GUBGYTABKSRVRQ-XLOQQCSPSA-N Alpha-Lactose Chemical compound O[C@@H]1[C@@H](O)[C@@H](O)[C@@H](CO)O[C@H]1O[C@@H]1[C@@H](CO)O[C@H](O)[C@H](O)[C@H]1O GUBGYTABKSRVRQ-XLOQQCSPSA-N 0.000 description 5
- 229930186147 Cephalosporin Natural products 0.000 description 5
- 108010010803 Gelatin Proteins 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 5
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 5
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 5
- 241000191940 Staphylococcus Species 0.000 description 5
- 235000021355 Stearic acid Nutrition 0.000 description 5
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 5
- 229930006000 Sucrose Natural products 0.000 description 5
- 125000000304 alkynyl group Chemical group 0.000 description 5
- 230000027455 binding Effects 0.000 description 5
- 239000001506 calcium phosphate Substances 0.000 description 5
- 229910000389 calcium phosphate Inorganic materials 0.000 description 5
- 235000011010 calcium phosphates Nutrition 0.000 description 5
- 229940124587 cephalosporin Drugs 0.000 description 5
- 150000001780 cephalosporins Chemical class 0.000 description 5
- 229960002227 clindamycin Drugs 0.000 description 5
- KDLRVYVGXIQJDK-AWPVFWJPSA-N clindamycin Chemical compound CN1C[C@H](CCC)C[C@H]1C(=O)N[C@H]([C@H](C)Cl)[C@@H]1[C@H](O)[C@H](O)[C@@H](O)[C@@H](SC)O1 KDLRVYVGXIQJDK-AWPVFWJPSA-N 0.000 description 5
- 239000012043 crude product Substances 0.000 description 5
- 239000002552 dosage form Substances 0.000 description 5
- 235000013355 food flavoring agent Nutrition 0.000 description 5
- 229920000159 gelatin Polymers 0.000 description 5
- 239000008273 gelatin Substances 0.000 description 5
- 235000019322 gelatine Nutrition 0.000 description 5
- 235000011852 gelatine desserts Nutrition 0.000 description 5
- 239000003701 inert diluent Substances 0.000 description 5
- 239000003112 inhibitor Substances 0.000 description 5
- 230000035987 intoxication Effects 0.000 description 5
- 231100000566 intoxication Toxicity 0.000 description 5
- 239000008101 lactose Substances 0.000 description 5
- 239000007788 liquid Substances 0.000 description 5
- QIQXTHQIDYTFRH-UHFFFAOYSA-N octadecanoic acid Chemical compound CCCCCCCCCCCCCCCCCC(O)=O QIQXTHQIDYTFRH-UHFFFAOYSA-N 0.000 description 5
- OQCDKBAXFALNLD-UHFFFAOYSA-N octadecanoic acid Natural products CCCCCCCC(C)CCCCCCCCC(O)=O OQCDKBAXFALNLD-UHFFFAOYSA-N 0.000 description 5
- 229920006395 saturated elastomer Polymers 0.000 description 5
- 239000008117 stearic acid Substances 0.000 description 5
- 239000005720 sucrose Substances 0.000 description 5
- 231100000331 toxic Toxicity 0.000 description 5
- 230000002588 toxic effect Effects 0.000 description 5
- 231100000419 toxicity Toxicity 0.000 description 5
- 230000001988 toxicity Effects 0.000 description 5
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 5
- 239000000080 wetting agent Substances 0.000 description 5
- SGKRLCUYIXIAHR-AKNGSSGZSA-N (4s,4ar,5s,5ar,6r,12ar)-4-(dimethylamino)-1,5,10,11,12a-pentahydroxy-6-methyl-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1=CC=C2[C@H](C)[C@@H]([C@H](O)[C@@H]3[C@](C(O)=C(C(N)=O)C(=O)[C@H]3N(C)C)(O)C3=O)C3=C(O)C2=C1O SGKRLCUYIXIAHR-AKNGSSGZSA-N 0.000 description 4
- VBICKXHEKHSIBG-UHFFFAOYSA-N 1-monostearoylglycerol Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)CO VBICKXHEKHSIBG-UHFFFAOYSA-N 0.000 description 4
- IZHVBANLECCAGF-UHFFFAOYSA-N 2-hydroxy-3-(octadecanoyloxy)propyl octadecanoate Chemical compound CCCCCCCCCCCCCCCCCC(=O)OCC(O)COC(=O)CCCCCCCCCCCCCCCCC IZHVBANLECCAGF-UHFFFAOYSA-N 0.000 description 4
- BCCREUFCSIMJFS-UHFFFAOYSA-N 2-hydroxy-n-[3-[3-(piperidin-1-ylmethyl)phenoxy]propyl]acetamide Chemical compound OCC(=O)NCCCOC1=CC=CC(CN2CCCCC2)=C1 BCCREUFCSIMJFS-UHFFFAOYSA-N 0.000 description 4
- ALYNCZNDIQEVRV-UHFFFAOYSA-N 4-aminobenzoic acid Chemical compound NC1=CC=C(C(O)=O)C=C1 ALYNCZNDIQEVRV-UHFFFAOYSA-N 0.000 description 4
- 208000004998 Abdominal Pain Diseases 0.000 description 4
- 241000193830 Bacillus <bacterium> Species 0.000 description 4
- 241000193468 Clostridium perfringens Species 0.000 description 4
- 208000005156 Dehydration Diseases 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- IAZDPXIOMUYVGZ-WFGJKAKNSA-N Dimethyl sulfoxide Chemical compound [2H]C([2H])([2H])S(=O)C([2H])([2H])[2H] IAZDPXIOMUYVGZ-WFGJKAKNSA-N 0.000 description 4
- 241000194031 Enterococcus faecium Species 0.000 description 4
- 102000004190 Enzymes Human genes 0.000 description 4
- 108090000790 Enzymes Proteins 0.000 description 4
- ULGZDMOVFRHVEP-RWJQBGPGSA-N Erythromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 ULGZDMOVFRHVEP-RWJQBGPGSA-N 0.000 description 4
- IAYPIBMASNFSPL-UHFFFAOYSA-N Ethylene oxide Chemical compound C1CO1 IAYPIBMASNFSPL-UHFFFAOYSA-N 0.000 description 4
- KFZMGEQAYNKOFK-UHFFFAOYSA-N Isopropanol Chemical compound CC(C)O KFZMGEQAYNKOFK-UHFFFAOYSA-N 0.000 description 4
- GSDSWSVVBLHKDQ-JTQLQIEISA-N Levofloxacin Chemical compound C([C@@H](N1C2=C(C(C(C(O)=O)=C1)=O)C=C1F)C)OC2=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-JTQLQIEISA-N 0.000 description 4
- BAVYZALUXZFZLV-UHFFFAOYSA-N Methylamine Chemical compound NC BAVYZALUXZFZLV-UHFFFAOYSA-N 0.000 description 4
- YNAVUWVOSKDBBP-UHFFFAOYSA-N Morpholine Chemical compound C1COCCN1 YNAVUWVOSKDBBP-UHFFFAOYSA-N 0.000 description 4
- 150000001204 N-oxides Chemical class 0.000 description 4
- 206010028813 Nausea Diseases 0.000 description 4
- IQPSEEYGBUAQFF-UHFFFAOYSA-N Pantoprazole Chemical compound COC1=CC=NC(CS(=O)C=2NC3=CC=C(OC(F)F)C=C3N=2)=C1OC IQPSEEYGBUAQFF-UHFFFAOYSA-N 0.000 description 4
- 229930182555 Penicillin Natural products 0.000 description 4
- 206010037660 Pyrexia Diseases 0.000 description 4
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 4
- CDBYLPFSWZWCQE-UHFFFAOYSA-L Sodium Carbonate Chemical compound [Na+].[Na+].[O-]C([O-])=O CDBYLPFSWZWCQE-UHFFFAOYSA-L 0.000 description 4
- 235000010443 alginic acid Nutrition 0.000 description 4
- 229920000615 alginic acid Polymers 0.000 description 4
- 239000000783 alginic acid Substances 0.000 description 4
- 229960001126 alginic acid Drugs 0.000 description 4
- 150000004781 alginic acids Chemical class 0.000 description 4
- 125000003342 alkenyl group Chemical group 0.000 description 4
- 229960003022 amoxicillin Drugs 0.000 description 4
- LSQZJLSUYDQPKJ-NJBDSQKTSA-N amoxicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=C(O)C=C1 LSQZJLSUYDQPKJ-NJBDSQKTSA-N 0.000 description 4
- 229940121363 anti-inflammatory agent Drugs 0.000 description 4
- 239000002260 anti-inflammatory agent Substances 0.000 description 4
- 239000004599 antimicrobial Substances 0.000 description 4
- 125000002619 bicyclic group Chemical group 0.000 description 4
- 239000012267 brine Substances 0.000 description 4
- 229910000019 calcium carbonate Inorganic materials 0.000 description 4
- 235000010216 calcium carbonate Nutrition 0.000 description 4
- 210000004027 cell Anatomy 0.000 description 4
- 238000006243 chemical reaction Methods 0.000 description 4
- 229960002626 clarithromycin Drugs 0.000 description 4
- AGOYDEPGAOXOCK-KCBOHYOISA-N clarithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=O)[C@H](C)C[C@](C)([C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)OC)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 AGOYDEPGAOXOCK-KCBOHYOISA-N 0.000 description 4
- 229940047766 co-trimoxazole Drugs 0.000 description 4
- 238000002648 combination therapy Methods 0.000 description 4
- 239000007859 condensation product Substances 0.000 description 4
- 125000000753 cycloalkyl group Chemical group 0.000 description 4
- 230000034994 death Effects 0.000 description 4
- 231100000517 death Toxicity 0.000 description 4
- 230000018044 dehydration Effects 0.000 description 4
- 238000006297 dehydration reaction Methods 0.000 description 4
- 238000011161 development Methods 0.000 description 4
- 230000018109 developmental process Effects 0.000 description 4
- 231100000676 disease causative agent Toxicity 0.000 description 4
- 208000035475 disorder Diseases 0.000 description 4
- 239000002270 dispersing agent Substances 0.000 description 4
- 229960003722 doxycycline Drugs 0.000 description 4
- 239000000839 emulsion Substances 0.000 description 4
- AEUTYOVWOVBAKS-UWVGGRQHSA-N ethambutol Chemical compound CC[C@@H](CO)NCCN[C@@H](CC)CO AEUTYOVWOVBAKS-UWVGGRQHSA-N 0.000 description 4
- 239000002095 exotoxin Substances 0.000 description 4
- 231100000776 exotoxin Toxicity 0.000 description 4
- 239000000706 filtrate Substances 0.000 description 4
- 210000001035 gastrointestinal tract Anatomy 0.000 description 4
- 239000007903 gelatin capsule Substances 0.000 description 4
- 239000008187 granular material Substances 0.000 description 4
- 230000036541 health Effects 0.000 description 4
- BXWNKGSJHAJOGX-UHFFFAOYSA-N hexadecan-1-ol Chemical compound CCCCCCCCCCCCCCCCO BXWNKGSJHAJOGX-UHFFFAOYSA-N 0.000 description 4
- 238000004128 high performance liquid chromatography Methods 0.000 description 4
- 238000001990 intravenous administration Methods 0.000 description 4
- 230000007794 irritation Effects 0.000 description 4
- 229960003376 levofloxacin Drugs 0.000 description 4
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 4
- 235000019341 magnesium sulphate Nutrition 0.000 description 4
- 239000001788 mono and diglycerides of fatty acids Substances 0.000 description 4
- 230000008693 nausea Effects 0.000 description 4
- SGXXNSQHWDMGGP-IZZDOVSWSA-N nizatidine Chemical compound [O-][N+](=O)\C=C(/NC)NCCSCC1=CSC(CN(C)C)=N1 SGXXNSQHWDMGGP-IZZDOVSWSA-N 0.000 description 4
- 239000004006 olive oil Substances 0.000 description 4
- 235000008390 olive oil Nutrition 0.000 description 4
- LSQZJLSUYDQPKJ-UHFFFAOYSA-N p-Hydroxyampicillin Natural products O=C1N2C(C(O)=O)C(C)(C)SC2C1NC(=O)C(N)C1=CC=C(O)C=C1 LSQZJLSUYDQPKJ-UHFFFAOYSA-N 0.000 description 4
- 229960005019 pantoprazole Drugs 0.000 description 4
- 229920001223 polyethylene glycol Polymers 0.000 description 4
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 description 4
- 229940126409 proton pump inhibitor Drugs 0.000 description 4
- 239000000612 proton pump inhibitor Substances 0.000 description 4
- 229930195734 saturated hydrocarbon Natural products 0.000 description 4
- 239000011780 sodium chloride Substances 0.000 description 4
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- 239000000454 talc Substances 0.000 description 4
- 235000012222 talc Nutrition 0.000 description 4
- 229910052623 talc Inorganic materials 0.000 description 4
- NXKKZCYRNPHNSC-UHFFFAOYSA-N (4-carbamoyloxyphenyl) carbamate Chemical compound NC(=O)OC1=CC=C(OC(N)=O)C=C1 NXKKZCYRNPHNSC-UHFFFAOYSA-N 0.000 description 3
- QSHOHAZUJFNTGA-UHFFFAOYSA-N 2-(4-methoxyphenyl)-6-[2-(4-methoxyphenyl)-3h-benzimidazol-5-yl]-1h-benzimidazole Chemical compound C1=CC(OC)=CC=C1C1=NC2=CC(C=3C=C4N=C(NC4=CC=3)C=3C=CC(OC)=CC=3)=CC=C2N1 QSHOHAZUJFNTGA-UHFFFAOYSA-N 0.000 description 3
- HSTOKWSFWGCZMH-UHFFFAOYSA-N 3,3'-diaminobenzidine Chemical compound C1=C(N)C(N)=CC=C1C1=CC=C(N)C(N)=C1 HSTOKWSFWGCZMH-UHFFFAOYSA-N 0.000 description 3
- GGSCBDDPUMSULA-UHFFFAOYSA-N 4-[6-(3h-benzimidazol-5-yl)-1h-benzimidazol-2-yl]aniline Chemical compound C1=CC(N)=CC=C1C1=NC2=CC(C=3C=C4N=CNC4=CC=3)=CC=C2N1 GGSCBDDPUMSULA-UHFFFAOYSA-N 0.000 description 3
- HBAQYPYDRFILMT-UHFFFAOYSA-N 8-[3-(1-cyclopropylpyrazol-4-yl)-1H-pyrazolo[4,3-d]pyrimidin-5-yl]-3-methyl-3,8-diazabicyclo[3.2.1]octan-2-one Chemical class C1(CC1)N1N=CC(=C1)C1=NNC2=C1N=C(N=C2)N1C2C(N(CC1CC2)C)=O HBAQYPYDRFILMT-UHFFFAOYSA-N 0.000 description 3
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 description 3
- WEVYAHXRMPXWCK-UHFFFAOYSA-N Acetonitrile Chemical group CC#N WEVYAHXRMPXWCK-UHFFFAOYSA-N 0.000 description 3
- 108010001478 Bacitracin Proteins 0.000 description 3
- 108010062877 Bacteriocins Proteins 0.000 description 3
- UHOVQNZJYSORNB-UHFFFAOYSA-N Benzene Chemical compound C1=CC=CC=C1 UHOVQNZJYSORNB-UHFFFAOYSA-N 0.000 description 3
- 241000283690 Bos taurus Species 0.000 description 3
- 241001112696 Clostridia Species 0.000 description 3
- 241001112695 Clostridiales Species 0.000 description 3
- 102000004127 Cytokines Human genes 0.000 description 3
- 108090000695 Cytokines Proteins 0.000 description 3
- XTHFKEDIFFGKHM-UHFFFAOYSA-N Dimethoxyethane Chemical compound COCCOC XTHFKEDIFFGKHM-UHFFFAOYSA-N 0.000 description 3
- 241000194032 Enterococcus faecalis Species 0.000 description 3
- 241000283086 Equidae Species 0.000 description 3
- 241000192125 Firmicutes Species 0.000 description 3
- IECPWNUMDGFDKC-UHFFFAOYSA-N Fusicsaeure Natural products C12C(O)CC3C(=C(CCC=C(C)C)C(O)=O)C(OC(C)=O)CC3(C)C1(C)CCC1C2(C)CCC(O)C1C IECPWNUMDGFDKC-UHFFFAOYSA-N 0.000 description 3
- 241000282412 Homo Species 0.000 description 3
- 206010020751 Hypersensitivity Diseases 0.000 description 3
- SIKJAQJRHWYJAI-UHFFFAOYSA-N Indole Chemical compound C1=CC=C2NC=CC2=C1 SIKJAQJRHWYJAI-UHFFFAOYSA-N 0.000 description 3
- 206010061218 Inflammation Diseases 0.000 description 3
- 108090001007 Interleukin-8 Proteins 0.000 description 3
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 3
- 240000007472 Leucaena leucocephala Species 0.000 description 3
- RJQXTJLFIWVMTO-TYNCELHUSA-N Methicillin Chemical compound COC1=CC=CC(OC)=C1C(=O)N[C@@H]1C(=O)N2[C@@H](C(O)=O)C(C)(C)S[C@@H]21 RJQXTJLFIWVMTO-TYNCELHUSA-N 0.000 description 3
- 102100022389 Nucleosome assembly protein 1-like 1 Human genes 0.000 description 3
- 208000012868 Overgrowth Diseases 0.000 description 3
- 235000019483 Peanut oil Nutrition 0.000 description 3
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 3
- 208000005374 Poisoning Diseases 0.000 description 3
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 3
- RWRDLPDLKQPQOW-UHFFFAOYSA-N Pyrrolidine Chemical compound C1CCNC1 RWRDLPDLKQPQOW-UHFFFAOYSA-N 0.000 description 3
- XUIMIQQOPSSXEZ-UHFFFAOYSA-N Silicon Chemical compound [Si] XUIMIQQOPSSXEZ-UHFFFAOYSA-N 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- 239000004098 Tetracycline Substances 0.000 description 3
- 229920001615 Tragacanth Polymers 0.000 description 3
- 230000009471 action Effects 0.000 description 3
- 239000000443 aerosol Substances 0.000 description 3
- 150000001298 alcohols Chemical class 0.000 description 3
- 208000030961 allergic reaction Diseases 0.000 description 3
- QGZKDVFQNNGYKY-UHFFFAOYSA-O ammonium group Chemical group [NH4+] QGZKDVFQNNGYKY-UHFFFAOYSA-O 0.000 description 3
- 230000002924 anti-infective effect Effects 0.000 description 3
- 230000001857 anti-mycotic effect Effects 0.000 description 3
- 230000000840 anti-viral effect Effects 0.000 description 3
- 239000002543 antimycotic Substances 0.000 description 3
- 230000004596 appetite loss Effects 0.000 description 3
- 238000013459 approach Methods 0.000 description 3
- 239000012298 atmosphere Substances 0.000 description 3
- 229960004099 azithromycin Drugs 0.000 description 3
- MQTOSJVFKKJCRP-BICOPXKESA-N azithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)N(C)C[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 MQTOSJVFKKJCRP-BICOPXKESA-N 0.000 description 3
- 229940065181 bacillus anthracis Drugs 0.000 description 3
- 229960003071 bacitracin Drugs 0.000 description 3
- 229930184125 bacitracin Natural products 0.000 description 3
- CLKOFPXJLQSYAH-ABRJDSQDSA-N bacitracin A Chemical compound C1SC([C@@H](N)[C@@H](C)CC)=N[C@@H]1C(=O)N[C@@H](CC(C)C)C(=O)N[C@H](CCC(O)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]1C(=O)N[C@H](CCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC=2N=CNC=2)C(=O)N[C@H](CC(O)=O)C(=O)N[C@@H](CC(N)=O)C(=O)NCCCC1 CLKOFPXJLQSYAH-ABRJDSQDSA-N 0.000 description 3
- 244000052616 bacterial pathogen Species 0.000 description 3
- 210000004666 bacterial spore Anatomy 0.000 description 3
- 230000037396 body weight Effects 0.000 description 3
- 239000011203 carbon fibre reinforced carbon Substances 0.000 description 3
- 239000001768 carboxy methyl cellulose Substances 0.000 description 3
- JQXXHWHPUNPDRT-BQVAUQFYSA-N chembl1523493 Chemical compound O([C@](C1=O)(C)O\C=C/[C@@H]([C@H]([C@@H](OC(C)=O)[C@H](C)[C@H](O)[C@H](C)[C@@H](O)[C@@H](C)/C=C\C=C(C)/C(=O)NC=2C(O)=C3C(O)=C4C)C)OC)C4=C1C3=C(O)C=2C=NN1CCN(C)CC1 JQXXHWHPUNPDRT-BQVAUQFYSA-N 0.000 description 3
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 description 3
- 239000006184 cosolvent Substances 0.000 description 3
- 230000006378 damage Effects 0.000 description 3
- 238000009795 derivation Methods 0.000 description 3
- 238000001514 detection method Methods 0.000 description 3
- 239000003995 emulsifying agent Substances 0.000 description 3
- 239000002158 endotoxin Substances 0.000 description 3
- 150000002148 esters Chemical class 0.000 description 3
- UREBWPXBXRYXRJ-UHFFFAOYSA-N ethyl acetate;methanol Chemical compound OC.CCOC(C)=O UREBWPXBXRYXRJ-UHFFFAOYSA-N 0.000 description 3
- 235000013305 food Nutrition 0.000 description 3
- 239000012458 free base Substances 0.000 description 3
- 229960004675 fusidic acid Drugs 0.000 description 3
- IECPWNUMDGFDKC-MZJAQBGESA-N fusidic acid Chemical compound O[C@@H]([C@@H]12)C[C@H]3\C(=C(/CCC=C(C)C)C(O)=O)[C@@H](OC(C)=O)C[C@]3(C)[C@@]2(C)CC[C@@H]2[C@]1(C)CC[C@@H](O)[C@H]2C IECPWNUMDGFDKC-MZJAQBGESA-N 0.000 description 3
- 125000002887 hydroxy group Chemical group [H]O* 0.000 description 3
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 3
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 3
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 3
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 3
- 210000000987 immune system Anatomy 0.000 description 3
- 238000001727 in vivo Methods 0.000 description 3
- 238000007918 intramuscular administration Methods 0.000 description 3
- 239000010410 layer Substances 0.000 description 3
- 229940057995 liquid paraffin Drugs 0.000 description 3
- RDOIQAHITMMDAJ-UHFFFAOYSA-N loperamide Chemical compound C=1C=CC=CC=1C(C=1C=CC=CC=1)(C(=O)N(C)C)CCN(CC1)CCC1(O)C1=CC=C(Cl)C=C1 RDOIQAHITMMDAJ-UHFFFAOYSA-N 0.000 description 3
- 208000019017 loss of appetite Diseases 0.000 description 3
- 235000021266 loss of appetite Nutrition 0.000 description 3
- 239000007937 lozenge Substances 0.000 description 3
- 239000003120 macrolide antibiotic agent Substances 0.000 description 3
- 235000019359 magnesium stearate Nutrition 0.000 description 3
- 229910021645 metal ion Inorganic materials 0.000 description 3
- 229920000609 methyl cellulose Polymers 0.000 description 3
- 239000001923 methylcellulose Substances 0.000 description 3
- 235000010981 methylcellulose Nutrition 0.000 description 3
- 229960003085 meticillin Drugs 0.000 description 3
- 239000002480 mineral oil Substances 0.000 description 3
- 235000010446 mineral oil Nutrition 0.000 description 3
- 231100000252 nontoxic Toxicity 0.000 description 3
- 230000003000 nontoxic effect Effects 0.000 description 3
- 230000036961 partial effect Effects 0.000 description 3
- 244000052769 pathogen Species 0.000 description 3
- 239000000312 peanut oil Substances 0.000 description 3
- 229940049954 penicillin Drugs 0.000 description 3
- 238000009512 pharmaceutical packaging Methods 0.000 description 3
- 229960005141 piperazine Drugs 0.000 description 3
- 231100000572 poisoning Toxicity 0.000 description 3
- 230000000607 poisoning effect Effects 0.000 description 3
- 239000001267 polyvinylpyrrolidone Substances 0.000 description 3
- 229920000036 polyvinylpyrrolidone Polymers 0.000 description 3
- 235000013855 polyvinylpyrrolidone Nutrition 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 238000000746 purification Methods 0.000 description 3
- LISFMEBWQUVKPJ-UHFFFAOYSA-N quinolin-2-ol Chemical compound C1=CC=C2NC(=O)C=CC2=C1 LISFMEBWQUVKPJ-UHFFFAOYSA-N 0.000 description 3
- 230000009467 reduction Effects 0.000 description 3
- 238000012552 review Methods 0.000 description 3
- 229960001225 rifampicin Drugs 0.000 description 3
- 229960002181 saccharomyces boulardii Drugs 0.000 description 3
- 229910052710 silicon Inorganic materials 0.000 description 3
- 239000010703 silicon Substances 0.000 description 3
- 229910000029 sodium carbonate Inorganic materials 0.000 description 3
- FVAUCKIRQBBSSJ-UHFFFAOYSA-M sodium iodide Chemical compound [Na+].[I-] FVAUCKIRQBBSSJ-UHFFFAOYSA-M 0.000 description 3
- 239000001488 sodium phosphate Substances 0.000 description 3
- 230000004763 spore germination Effects 0.000 description 3
- 239000008107 starch Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- 150000003431 steroids Chemical class 0.000 description 3
- 238000007920 subcutaneous administration Methods 0.000 description 3
- 239000006188 syrup Substances 0.000 description 3
- 235000020357 syrup Nutrition 0.000 description 3
- 235000019364 tetracycline Nutrition 0.000 description 3
- 150000003522 tetracyclines Chemical class 0.000 description 3
- YLQBMQCUIZJEEH-UHFFFAOYSA-N tetrahydrofuran Natural products C=1C=COC=1 YLQBMQCUIZJEEH-UHFFFAOYSA-N 0.000 description 3
- 230000000699 topical effect Effects 0.000 description 3
- 238000002054 transplantation Methods 0.000 description 3
- PUPZLCDOIYMWBV-UHFFFAOYSA-N (+/-)-1,3-Butanediol Chemical compound CC(O)CCO PUPZLCDOIYMWBV-UHFFFAOYSA-N 0.000 description 2
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 2
- FFTVPQUHLQBXQZ-KVUCHLLUSA-N (4s,4as,5ar,12ar)-4,7-bis(dimethylamino)-1,10,11,12a-tetrahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1C2=C(N(C)C)C=CC(O)=C2C(O)=C2[C@@H]1C[C@H]1[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]1(O)C2=O FFTVPQUHLQBXQZ-KVUCHLLUSA-N 0.000 description 2
- GUXHBMASAHGULD-SEYHBJAFSA-N (4s,4as,5as,6s,12ar)-7-chloro-4-(dimethylamino)-1,6,10,11,12a-pentahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1([C@H]2O)=C(Cl)C=CC(O)=C1C(O)=C1[C@@H]2C[C@H]2[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]2(O)C1=O GUXHBMASAHGULD-SEYHBJAFSA-N 0.000 description 2
- 125000006727 (C1-C6) alkenyl group Chemical group 0.000 description 2
- 125000006570 (C5-C6) heteroaryl group Chemical group 0.000 description 2
- MINDHVHHQZYEEK-UHFFFAOYSA-N (E)-(2S,3R,4R,5S)-5-[(2S,3S,4S,5S)-2,3-epoxy-5-hydroxy-4-methylhexyl]tetrahydro-3,4-dihydroxy-(beta)-methyl-2H-pyran-2-crotonic acid ester with 9-hydroxynonanoic acid Natural products CC(O)C(C)C1OC1CC1C(O)C(O)C(CC(C)=CC(=O)OCCCCCCCCC(O)=O)OC1 MINDHVHHQZYEEK-UHFFFAOYSA-N 0.000 description 2
- UWYZHKAOTLEWKK-UHFFFAOYSA-N 1,2,3,4-tetrahydroisoquinoline Chemical compound C1=CC=C2CNCCC2=C1 UWYZHKAOTLEWKK-UHFFFAOYSA-N 0.000 description 2
- ZWNCJCPLPUBNCZ-UHFFFAOYSA-N 1,2-dimethoxyethane;hydrate Chemical compound O.COCCOC ZWNCJCPLPUBNCZ-UHFFFAOYSA-N 0.000 description 2
- HNSDLXPSAYFUHK-UHFFFAOYSA-N 1,4-bis(2-ethylhexyl) sulfosuccinate Chemical compound CCCCC(CC)COC(=O)CC(S(O)(=O)=O)C(=O)OCC(CC)CCCC HNSDLXPSAYFUHK-UHFFFAOYSA-N 0.000 description 2
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 2
- IIZPXYDJLKNOIY-JXPKJXOSSA-N 1-palmitoyl-2-arachidonoyl-sn-glycero-3-phosphocholine Chemical compound CCCCCCCCCCCCCCCC(=O)OC[C@H](COP([O-])(=O)OCC[N+](C)(C)C)OC(=O)CCC\C=C/C\C=C/C\C=C/C\C=C/CCCCC IIZPXYDJLKNOIY-JXPKJXOSSA-N 0.000 description 2
- XDOFQFKRPWOURC-UHFFFAOYSA-N 16-methylheptadecanoic acid Chemical compound CC(C)CCCCCCCCCCCCCCC(O)=O XDOFQFKRPWOURC-UHFFFAOYSA-N 0.000 description 2
- HZAXFHJVJLSVMW-UHFFFAOYSA-N 2-Aminoethan-1-ol Chemical compound NCCO HZAXFHJVJLSVMW-UHFFFAOYSA-N 0.000 description 2
- WRMNZCZEMHIOCP-UHFFFAOYSA-N 2-phenylethanol Chemical compound OCCC1=CC=CC=C1 WRMNZCZEMHIOCP-UHFFFAOYSA-N 0.000 description 2
- 125000003903 2-propenyl group Chemical group [H]C([*])([H])C([H])=C([H])[H] 0.000 description 2
- 125000006041 3-hexenyl group Chemical group 0.000 description 2
- NONOPSVXABRTPA-UHFFFAOYSA-N 4-(3-fluoro-4-nitrophenyl)-2-nitroaniline Chemical compound C1=C([N+]([O-])=O)C(N)=CC=C1C1=CC=C([N+]([O-])=O)C(F)=C1 NONOPSVXABRTPA-UHFFFAOYSA-N 0.000 description 2
- XHQRYVOPGLEZGC-UHFFFAOYSA-N 4-[2-(4-aminophenyl)-3h-benzimidazol-5-yl]benzene-1,2-diamine Chemical compound C1=CC(N)=CC=C1C1=NC2=CC=C(C=3C=C(N)C(N)=CC=3)C=C2N1 XHQRYVOPGLEZGC-UHFFFAOYSA-N 0.000 description 2
- DZRKIGIJCHMQML-UHFFFAOYSA-N 4-[3-amino-4-(methylamino)phenyl]benzene-1,2-diamine Chemical compound C1=C(N)C(NC)=CC=C1C1=CC=C(N)C(N)=C1 DZRKIGIJCHMQML-UHFFFAOYSA-N 0.000 description 2
- SYZQEVQDZRHNHU-UHFFFAOYSA-N 4-[6-(2-phenyl-3h-benzimidazol-5-yl)-1h-benzimidazol-2-yl]aniline Chemical compound C1=CC(N)=CC=C1C1=NC2=CC(C=3C=C4N=C(NC4=CC=3)C=3C=CC=CC=3)=CC=C2N1 SYZQEVQDZRHNHU-UHFFFAOYSA-N 0.000 description 2
- QGMGHALXLXKCBD-UHFFFAOYSA-N 4-amino-n-(2-aminophenyl)benzamide Chemical compound C1=CC(N)=CC=C1C(=O)NC1=CC=CC=C1N QGMGHALXLXKCBD-UHFFFAOYSA-N 0.000 description 2
- RGHHSNMVTDWUBI-UHFFFAOYSA-N 4-hydroxybenzaldehyde Chemical compound OC1=CC=C(C=O)C=C1 RGHHSNMVTDWUBI-UHFFFAOYSA-N 0.000 description 2
- GSDSWSVVBLHKDQ-UHFFFAOYSA-N 9-fluoro-3-methyl-10-(4-methylpiperazin-1-yl)-7-oxo-2,3-dihydro-7H-[1,4]oxazino[2,3,4-ij]quinoline-6-carboxylic acid Chemical compound FC1=CC(C(C(C(O)=O)=C2)=O)=C3N2C(C)COC3=C1N1CCN(C)CC1 GSDSWSVVBLHKDQ-UHFFFAOYSA-N 0.000 description 2
- 231100000699 Bacterial toxin Toxicity 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- 241000282472 Canis lupus familiaris Species 0.000 description 2
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 2
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 2
- 241000700198 Cavia Species 0.000 description 2
- HEDRZPFGACZZDS-UHFFFAOYSA-N Chloroform Chemical compound ClC(Cl)Cl HEDRZPFGACZZDS-UHFFFAOYSA-N 0.000 description 2
- 108010078777 Colistin Proteins 0.000 description 2
- 208000035473 Communicable disease Diseases 0.000 description 2
- 206010011409 Cross infection Diseases 0.000 description 2
- FMTDIUIBLCQGJB-UHFFFAOYSA-N Demethylchlortetracyclin Natural products C1C2C(O)C3=C(Cl)C=CC(O)=C3C(=O)C2=C(O)C2(O)C1C(N(C)C)C(O)=C(C(N)=O)C2=O FMTDIUIBLCQGJB-UHFFFAOYSA-N 0.000 description 2
- 241000792859 Enema Species 0.000 description 2
- VGGSQFUCUMXWEO-UHFFFAOYSA-N Ethene Chemical compound C=C VGGSQFUCUMXWEO-UHFFFAOYSA-N 0.000 description 2
- 239000005977 Ethylene Substances 0.000 description 2
- 241000282326 Felis catus Species 0.000 description 2
- 206010016952 Food poisoning Diseases 0.000 description 2
- 208000019331 Foodborne disease Diseases 0.000 description 2
- 206010019375 Helicobacter infections Diseases 0.000 description 2
- 108060003951 Immunoglobulin Proteins 0.000 description 2
- 206010022004 Influenza like illness Diseases 0.000 description 2
- 206010022678 Intestinal infections Diseases 0.000 description 2
- 240000001046 Lactobacillus acidophilus Species 0.000 description 2
- 235000013956 Lactobacillus acidophilus Nutrition 0.000 description 2
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 2
- 241000124008 Mammalia Species 0.000 description 2
- AFVFQIVMOAPDHO-UHFFFAOYSA-N Methanesulfonic acid Chemical compound CS(O)(=O)=O AFVFQIVMOAPDHO-UHFFFAOYSA-N 0.000 description 2
- 241000699670 Mus sp. Species 0.000 description 2
- MBBZMMPHUWSWHV-BDVNFPICSA-N N-methylglucamine Chemical compound CNC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO MBBZMMPHUWSWHV-BDVNFPICSA-N 0.000 description 2
- VMXUWOKSQNHOCA-UHFFFAOYSA-N N1'-[2-[[5-[(dimethylamino)methyl]-2-furanyl]methylthio]ethyl]-N1-methyl-2-nitroethene-1,1-diamine Chemical compound [O-][N+](=O)C=C(NC)NCCSCC1=CC=C(CN(C)C)O1 VMXUWOKSQNHOCA-UHFFFAOYSA-N 0.000 description 2
- UFWIBTONFRDIAS-UHFFFAOYSA-N Naphthalene Chemical compound C1=CC=CC2=CC=CC=C21 UFWIBTONFRDIAS-UHFFFAOYSA-N 0.000 description 2
- YJQPYGGHQPGBLI-UHFFFAOYSA-N Novobiocin Natural products O1C(C)(C)C(OC)C(OC(N)=O)C(O)C1OC1=CC=C(C(O)=C(NC(=O)C=2C=C(CC=C(C)C)C(O)=CC=2)C(=O)O2)C2=C1C YJQPYGGHQPGBLI-UHFFFAOYSA-N 0.000 description 2
- 239000004100 Oxytetracycline Substances 0.000 description 2
- 239000004264 Petrolatum Substances 0.000 description 2
- NQRYJNQNLNOLGT-UHFFFAOYSA-N Piperidine Chemical compound C1CCNCC1 NQRYJNQNLNOLGT-UHFFFAOYSA-N 0.000 description 2
- 206010035667 Pneumonia anthrax Diseases 0.000 description 2
- 239000004698 Polyethylene Substances 0.000 description 2
- 108010093965 Polymyxin B Proteins 0.000 description 2
- LOUPRKONTZGTKE-WZBLMQSHSA-N Quinine Chemical compound C([C@H]([C@H](C1)C=C)C2)C[N@@]1[C@@H]2[C@H](O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-WZBLMQSHSA-N 0.000 description 2
- 241000700159 Rattus Species 0.000 description 2
- 229930189077 Rifamycin Natural products 0.000 description 2
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical compound [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 2
- 241000193998 Streptococcus pneumoniae Species 0.000 description 2
- 108010053950 Teicoplanin Proteins 0.000 description 2
- WYURNTSHIVDZCO-UHFFFAOYSA-N Tetrahydrofuran Chemical compound C1CCOC1 WYURNTSHIVDZCO-UHFFFAOYSA-N 0.000 description 2
- YTPLMLYBLZKORZ-UHFFFAOYSA-N Thiophene Chemical compound C=1C=CSC=1 YTPLMLYBLZKORZ-UHFFFAOYSA-N 0.000 description 2
- HEDRZPFGACZZDS-MICDWDOJSA-N Trichloro(2H)methane Chemical compound [2H]C(Cl)(Cl)Cl HEDRZPFGACZZDS-MICDWDOJSA-N 0.000 description 2
- 206010057362 Underdose Diseases 0.000 description 2
- 206010047700 Vomiting Diseases 0.000 description 2
- 238000002679 ablation Methods 0.000 description 2
- 239000002250 absorbent Substances 0.000 description 2
- 230000002745 absorbent Effects 0.000 description 2
- 238000010521 absorption reaction Methods 0.000 description 2
- 229940062327 aciphex Drugs 0.000 description 2
- 125000005073 adamantyl group Chemical group C12(CC3CC(CC(C1)C3)C2)* 0.000 description 2
- 230000000996 additive effect Effects 0.000 description 2
- 238000009098 adjuvant therapy Methods 0.000 description 2
- 229910052783 alkali metal Inorganic materials 0.000 description 2
- 229960004821 amikacin Drugs 0.000 description 2
- LKCWBDHBTVXHDL-RMDFUYIESA-N amikacin Chemical compound O([C@@H]1[C@@H](N)C[C@H]([C@@H]([C@H]1O)O[C@@H]1[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O1)O)NC(=O)[C@@H](O)CCN)[C@H]1O[C@H](CN)[C@@H](O)[C@H](O)[C@H]1O LKCWBDHBTVXHDL-RMDFUYIESA-N 0.000 description 2
- 229960004050 aminobenzoic acid Drugs 0.000 description 2
- 229960000723 ampicillin Drugs 0.000 description 2
- AVKUERGKIZMTKX-NJBDSQKTSA-N ampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=CC=C1 AVKUERGKIZMTKX-NJBDSQKTSA-N 0.000 description 2
- 230000000202 analgesic effect Effects 0.000 description 2
- 230000001139 anti-pruritic effect Effects 0.000 description 2
- 229940124350 antibacterial drug Drugs 0.000 description 2
- 238000009635 antibiotic susceptibility testing Methods 0.000 description 2
- 239000003793 antidiarrheal agent Substances 0.000 description 2
- 239000003429 antifungal agent Substances 0.000 description 2
- 229940121375 antifungal agent Drugs 0.000 description 2
- 239000003963 antioxidant agent Substances 0.000 description 2
- 235000006708 antioxidants Nutrition 0.000 description 2
- 239000003904 antiprotozoal agent Substances 0.000 description 2
- 239000003908 antipruritic agent Substances 0.000 description 2
- 239000003443 antiviral agent Substances 0.000 description 2
- 239000000305 astragalus gummifer gum Substances 0.000 description 2
- 229940072293 axid Drugs 0.000 description 2
- JTWOMNBEOCYFNV-NFFDBFGFSA-N azlocillin Chemical compound N([C@@H](C(=O)N[C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C=1C=CC=CC=1)C(=O)N1CCNC1=O JTWOMNBEOCYFNV-NFFDBFGFSA-N 0.000 description 2
- 229960003623 azlocillin Drugs 0.000 description 2
- 239000000688 bacterial toxin Substances 0.000 description 2
- 239000003899 bactericide agent Substances 0.000 description 2
- 235000013871 bee wax Nutrition 0.000 description 2
- 239000012166 beeswax Substances 0.000 description 2
- 229940092738 beeswax Drugs 0.000 description 2
- HUMNYLRZRPPJDN-UHFFFAOYSA-N benzaldehyde Chemical compound O=CC1=CC=CC=C1 HUMNYLRZRPPJDN-UHFFFAOYSA-N 0.000 description 2
- 150000001556 benzimidazoles Chemical class 0.000 description 2
- IOJUPLGTWVMSFF-UHFFFAOYSA-N benzothiazole Chemical compound C1=CC=C2SC=NC2=C1 IOJUPLGTWVMSFF-UHFFFAOYSA-N 0.000 description 2
- 230000036760 body temperature Effects 0.000 description 2
- PPKJUHVNTMYXOD-PZGPJMECSA-N c49ws9n75l Chemical compound O=C([C@@H]1N(C2=O)CC[C@H]1S(=O)(=O)CCN(CC)CC)O[C@H](C(C)C)[C@H](C)\C=C\C(=O)NC\C=C\C(\C)=C\[C@@H](O)CC(=O)CC1=NC2=CO1.N([C@@H]1C(=O)N[C@@H](C(N2CCC[C@H]2C(=O)N(C)[C@@H](CC=2C=CC(=CC=2)N(C)C)C(=O)N2C[C@@H](CS[C@H]3C4CCN(CC4)C3)C(=O)C[C@H]2C(=O)N[C@H](C(=O)O[C@@H]1C)C=1C=CC=CC=1)=O)CC)C(=O)C1=NC=CC=C1O PPKJUHVNTMYXOD-PZGPJMECSA-N 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 235000001465 calcium Nutrition 0.000 description 2
- 229910052799 carbon Inorganic materials 0.000 description 2
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 2
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 2
- 239000012876 carrier material Substances 0.000 description 2
- 229960003719 cefdinir Drugs 0.000 description 2
- RTXOFQZKPXMALH-GHXIOONMSA-N cefdinir Chemical compound S1C(N)=NC(C(=N\O)\C(=O)N[C@@H]2C(N3C(=C(C=C)CS[C@@H]32)C(O)=O)=O)=C1 RTXOFQZKPXMALH-GHXIOONMSA-N 0.000 description 2
- 230000001413 cellular effect Effects 0.000 description 2
- 229940106164 cephalexin Drugs 0.000 description 2
- ZAIPMKNFIOOWCQ-UEKVPHQBSA-N cephalexin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=CC=C1 ZAIPMKNFIOOWCQ-UEKVPHQBSA-N 0.000 description 2
- DDTDNCYHLGRFBM-YZEKDTGTSA-N chembl2367892 Chemical compound CC(=O)N[C@H]1[C@@H](O)[C@H](O)[C@H](CO)O[C@H]1O[C@@H]([C@H]1C(N[C@@H](C2=CC(O)=CC(O[C@@H]3[C@H]([C@H](O)[C@H](O)[C@@H](CO)O3)O)=C2C=2C(O)=CC=C(C=2)[C@@H](NC(=O)[C@@H]2NC(=O)[C@@H]3C=4C=C(O)C=C(C=4)OC=4C(O)=CC=C(C=4)[C@@H](N)C(=O)N[C@H](CC=4C=C(Cl)C(O5)=CC=4)C(=O)N3)C(=O)N1)C(O)=O)=O)C(C=C1Cl)=CC=C1OC1=C(O[C@H]3[C@H]([C@@H](O)[C@H](O)[C@H](CO)O3)NC(C)=O)C5=CC2=C1 DDTDNCYHLGRFBM-YZEKDTGTSA-N 0.000 description 2
- 239000013043 chemical agent Substances 0.000 description 2
- 229960005091 chloramphenicol Drugs 0.000 description 2
- WIIZWVCIJKGZOK-RKDXNWHRSA-N chloramphenicol Chemical compound ClC(Cl)C(=O)N[C@H](CO)[C@H](O)C1=CC=C([N+]([O-])=O)C=C1 WIIZWVCIJKGZOK-RKDXNWHRSA-N 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- AQIXAKUUQRKLND-UHFFFAOYSA-N cimetidine Chemical compound N#C/N=C(/NC)NCCSCC=1N=CNC=1C AQIXAKUUQRKLND-UHFFFAOYSA-N 0.000 description 2
- MYSWGUAQZAJSOK-UHFFFAOYSA-N ciprofloxacin Chemical compound C12=CC(N3CCNCC3)=C(F)C=C2C(=O)C(C(=O)O)=CN1C1CC1 MYSWGUAQZAJSOK-UHFFFAOYSA-N 0.000 description 2
- 239000012459 cleaning agent Substances 0.000 description 2
- 229960003326 cloxacillin Drugs 0.000 description 2
- LQOLIRLGBULYKD-JKIFEVAISA-N cloxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=CC=CC=C1Cl LQOLIRLGBULYKD-JKIFEVAISA-N 0.000 description 2
- 229940110456 cocoa butter Drugs 0.000 description 2
- 235000019868 cocoa butter Nutrition 0.000 description 2
- 229960003346 colistin Drugs 0.000 description 2
- 210000001072 colon Anatomy 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 239000013058 crude material Substances 0.000 description 2
- 238000002425 crystallisation Methods 0.000 description 2
- 230000008025 crystallization Effects 0.000 description 2
- WZHCOOQXZCIUNC-UHFFFAOYSA-N cyclandelate Chemical compound C1C(C)(C)CC(C)CC1OC(=O)C(O)C1=CC=CC=C1 WZHCOOQXZCIUNC-UHFFFAOYSA-N 0.000 description 2
- 125000001995 cyclobutyl group Chemical group [H]C1([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000000113 cyclohexyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C([H])([H])C1([H])[H] 0.000 description 2
- 125000001511 cyclopentyl group Chemical group [H]C1([H])C([H])([H])C([H])([H])C([H])(*)C1([H])[H] 0.000 description 2
- 125000001559 cyclopropyl group Chemical group [H]C1([H])C([H])([H])C1([H])* 0.000 description 2
- 238000001804 debridement Methods 0.000 description 2
- 229960002398 demeclocycline Drugs 0.000 description 2
- 239000007933 dermal patch Substances 0.000 description 2
- YFAGHNZHGGCZAX-JKIFEVAISA-N dicloxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=C(Cl)C=CC=C1Cl YFAGHNZHGGCZAX-JKIFEVAISA-N 0.000 description 2
- 229960001585 dicloxacillin Drugs 0.000 description 2
- UFIVBRCCIRTJTN-UHFFFAOYSA-N difenoxin Chemical compound C1CC(C(=O)O)(C=2C=CC=CC=2)CCN1CCC(C#N)(C=1C=CC=CC=1)C1=CC=CC=C1 UFIVBRCCIRTJTN-UHFFFAOYSA-N 0.000 description 2
- 239000006185 dispersion Substances 0.000 description 2
- 239000003937 drug carrier Substances 0.000 description 2
- 239000007920 enema Substances 0.000 description 2
- 239000003623 enhancer Substances 0.000 description 2
- 229940032049 enterococcus faecalis Drugs 0.000 description 2
- 230000007613 environmental effect Effects 0.000 description 2
- 230000008029 eradication Effects 0.000 description 2
- 229960003276 erythromycin Drugs 0.000 description 2
- SUBDBMMJDZJVOS-DEOSSOPVSA-N esomeprazole Chemical compound C([S@](=O)C1=NC2=CC=C(C=C2N1)OC)C1=NC=C(C)C(OC)=C1C SUBDBMMJDZJVOS-DEOSSOPVSA-N 0.000 description 2
- 229960004770 esomeprazole Drugs 0.000 description 2
- KWORUUGOSLYAGD-YPPDDXJESA-N esomeprazole magnesium Chemical compound [Mg+2].C([S@](=O)C=1[N-]C2=CC=C(C=C2N=1)OC)C1=NC=C(C)C(OC)=C1C.C([S@](=O)C=1[N-]C2=CC=C(C=C2N=1)OC)C1=NC=C(C)C(OC)=C1C KWORUUGOSLYAGD-YPPDDXJESA-N 0.000 description 2
- 229960000285 ethambutol Drugs 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 239000000284 extract Substances 0.000 description 2
- 229960001596 famotidine Drugs 0.000 description 2
- 125000001153 fluoro group Chemical group F* 0.000 description 2
- 239000006260 foam Substances 0.000 description 2
- 229960001625 furazolidone Drugs 0.000 description 2
- PLHJDBGFXBMTGZ-WEVVVXLNSA-N furazolidone Chemical compound O1C([N+](=O)[O-])=CC=C1\C=N\N1C(=O)OCC1 PLHJDBGFXBMTGZ-WEVVVXLNSA-N 0.000 description 2
- 210000004211 gastric acid Anatomy 0.000 description 2
- 230000002496 gastric effect Effects 0.000 description 2
- 239000000499 gel Substances 0.000 description 2
- 229940074045 glyceryl distearate Drugs 0.000 description 2
- 229940075507 glyceryl monostearate Drugs 0.000 description 2
- 238000010438 heat treatment Methods 0.000 description 2
- 125000005842 heteroatom Chemical group 0.000 description 2
- 150000004677 hydrates Chemical class 0.000 description 2
- 102000018358 immunoglobulin Human genes 0.000 description 2
- 230000001506 immunosuppresive effect Effects 0.000 description 2
- 230000006872 improvement Effects 0.000 description 2
- 208000009449 inhalation anthrax Diseases 0.000 description 2
- 208000023372 inhalational anthrax Diseases 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 238000007912 intraperitoneal administration Methods 0.000 description 2
- 239000003456 ion exchange resin Substances 0.000 description 2
- 229920003303 ion-exchange polymer Polymers 0.000 description 2
- 229960003350 isoniazid Drugs 0.000 description 2
- QRXWMOHMRWLFEY-UHFFFAOYSA-N isoniazide Chemical compound NNC(=O)C1=CC=NC=C1 QRXWMOHMRWLFEY-UHFFFAOYSA-N 0.000 description 2
- AWJUIBRHMBBTKR-UHFFFAOYSA-N isoquinoline Chemical compound C1=NC=CC2=CC=CC=C21 AWJUIBRHMBBTKR-UHFFFAOYSA-N 0.000 description 2
- 229960000318 kanamycin Drugs 0.000 description 2
- 229930027917 kanamycin Natural products 0.000 description 2
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 2
- 229930182823 kanamycin A Natural products 0.000 description 2
- 229940039695 lactobacillus acidophilus Drugs 0.000 description 2
- 229960003174 lansoprazole Drugs 0.000 description 2
- 235000010445 lecithin Nutrition 0.000 description 2
- 239000000787 lecithin Substances 0.000 description 2
- 229940067606 lecithin Drugs 0.000 description 2
- 229960003907 linezolid Drugs 0.000 description 2
- TYZROVQLWOKYKF-ZDUSSCGKSA-N linezolid Chemical compound O=C1O[C@@H](CNC(=O)C)CN1C(C=C1F)=CC=C1N1CCOCC1 TYZROVQLWOKYKF-ZDUSSCGKSA-N 0.000 description 2
- 239000008297 liquid dosage form Substances 0.000 description 2
- HSZCZNFXUDYRKD-UHFFFAOYSA-M lithium iodide Chemical compound [Li+].[I-] HSZCZNFXUDYRKD-UHFFFAOYSA-M 0.000 description 2
- ZEKZLJVOYLTDKK-UHFFFAOYSA-N lomefloxacin Chemical compound FC1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNC(C)C1 ZEKZLJVOYLTDKK-UHFFFAOYSA-N 0.000 description 2
- 229960002422 lomefloxacin Drugs 0.000 description 2
- 229960001571 loperamide Drugs 0.000 description 2
- 229940041033 macrolides Drugs 0.000 description 2
- 239000011777 magnesium Substances 0.000 description 2
- 229910052749 magnesium Inorganic materials 0.000 description 2
- 235000001055 magnesium Nutrition 0.000 description 2
- 230000014759 maintenance of location Effects 0.000 description 2
- BDAGIHXWWSANSR-UHFFFAOYSA-N methanoic acid Natural products OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 2
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 description 2
- 230000000813 microbial effect Effects 0.000 description 2
- 150000007522 mineralic acids Chemical class 0.000 description 2
- 229960004023 minocycline Drugs 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 229960003128 mupirocin Drugs 0.000 description 2
- 229930187697 mupirocin Natural products 0.000 description 2
- DDHVILIIHBIMQU-YJGQQKNPSA-L mupirocin calcium hydrate Chemical compound O.O.[Ca+2].C[C@H](O)[C@H](C)[C@@H]1O[C@H]1C[C@@H]1[C@@H](O)[C@@H](O)[C@H](C\C(C)=C\C(=O)OCCCCCCCCC([O-])=O)OC1.C[C@H](O)[C@H](C)[C@@H]1O[C@H]1C[C@@H]1[C@@H](O)[C@@H](O)[C@H](C\C(C)=C\C(=O)OCCCCCCCCC([O-])=O)OC1 DDHVILIIHBIMQU-YJGQQKNPSA-L 0.000 description 2
- JORAUNFTUVJTNG-BSTBCYLQSA-N n-[(2s)-4-amino-1-[[(2s,3r)-1-[[(2s)-4-amino-1-oxo-1-[[(3s,6s,9s,12s,15r,18s,21s)-6,9,18-tris(2-aminoethyl)-3-[(1r)-1-hydroxyethyl]-12,15-bis(2-methylpropyl)-2,5,8,11,14,17,20-heptaoxo-1,4,7,10,13,16,19-heptazacyclotricos-21-yl]amino]butan-2-yl]amino]-3-h Chemical compound CC(C)CCCCC(=O)N[C@@H](CCN)C(=O)N[C@H]([C@@H](C)O)CN[C@@H](CCN)C(=O)N[C@H]1CCNC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCN)NC(=O)[C@H](CCN)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CCN)NC1=O.CCC(C)CCCCC(=O)N[C@@H](CCN)C(=O)N[C@H]([C@@H](C)O)CN[C@@H](CCN)C(=O)N[C@H]1CCNC(=O)[C@H]([C@@H](C)O)NC(=O)[C@H](CCN)NC(=O)[C@H](CCN)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@H](CCN)NC1=O JORAUNFTUVJTNG-BSTBCYLQSA-N 0.000 description 2
- 125000004123 n-propyl group Chemical group [H]C([H])([H])C([H])([H])C([H])([H])* 0.000 description 2
- GPXLMGHLHQJAGZ-JTDSTZFVSA-N nafcillin Chemical compound C1=CC=CC2=C(C(=O)N[C@@H]3C(N4[C@H](C(C)(C)S[C@@H]43)C(O)=O)=O)C(OCC)=CC=C21 GPXLMGHLHQJAGZ-JTDSTZFVSA-N 0.000 description 2
- 229960000515 nafcillin Drugs 0.000 description 2
- 229940112641 nexium Drugs 0.000 description 2
- 229960004872 nizatidine Drugs 0.000 description 2
- 239000000346 nonvolatile oil Substances 0.000 description 2
- 125000002868 norbornyl group Chemical group C12(CCC(CC1)C2)* 0.000 description 2
- OGJPXUAPXNRGGI-UHFFFAOYSA-N norfloxacin Chemical compound C1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 OGJPXUAPXNRGGI-UHFFFAOYSA-N 0.000 description 2
- 229960001180 norfloxacin Drugs 0.000 description 2
- 229960002950 novobiocin Drugs 0.000 description 2
- 229960001699 ofloxacin Drugs 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- JRZJOMJEPLMPRA-UHFFFAOYSA-N olefin Natural products CCCCCCCC=C JRZJOMJEPLMPRA-UHFFFAOYSA-N 0.000 description 2
- 235000020660 omega-3 fatty acid Nutrition 0.000 description 2
- 229960000381 omeprazole Drugs 0.000 description 2
- 238000011275 oncology therapy Methods 0.000 description 2
- 230000003287 optical effect Effects 0.000 description 2
- 229960000625 oxytetracycline Drugs 0.000 description 2
- IWVCMVBTMGNXQD-PXOLEDIWSA-N oxytetracycline Chemical compound C1=CC=C2[C@](O)(C)[C@H]3[C@H](O)[C@H]4[C@H](N(C)C)C(O)=C(C(N)=O)C(=O)[C@@]4(O)C(O)=C3C(=O)C2=C1O IWVCMVBTMGNXQD-PXOLEDIWSA-N 0.000 description 2
- 235000019366 oxytetracycline Nutrition 0.000 description 2
- ZRSNZINYAWTAHE-UHFFFAOYSA-N p-methoxybenzaldehyde Chemical compound COC1=CC=C(C=O)C=C1 ZRSNZINYAWTAHE-UHFFFAOYSA-N 0.000 description 2
- 230000007170 pathology Effects 0.000 description 2
- 229940072273 pepcid Drugs 0.000 description 2
- 235000019271 petrolatum Nutrition 0.000 description 2
- 229940066842 petrolatum Drugs 0.000 description 2
- 239000008180 pharmaceutical surfactant Substances 0.000 description 2
- 230000000144 pharmacologic effect Effects 0.000 description 2
- WLJVXDMOQOGPHL-UHFFFAOYSA-N phenylacetic acid Chemical compound OC(=O)CC1=CC=CC=C1 WLJVXDMOQOGPHL-UHFFFAOYSA-N 0.000 description 2
- 230000035790 physiological processes and functions Effects 0.000 description 2
- 239000006187 pill Substances 0.000 description 2
- IVBHGBMCVLDMKU-GXNBUGAJSA-N piperacillin Chemical compound O=C1C(=O)N(CC)CCN1C(=O)N[C@H](C=1C=CC=CC=1)C(=O)N[C@@H]1C(=O)N2[C@@H](C(O)=O)C(C)(C)S[C@@H]21 IVBHGBMCVLDMKU-GXNBUGAJSA-N 0.000 description 2
- 229960002292 piperacillin Drugs 0.000 description 2
- 229920000573 polyethylene Polymers 0.000 description 2
- 229940068917 polyethylene glycols Drugs 0.000 description 2
- 229920000024 polymyxin B Polymers 0.000 description 2
- XDJYMJULXQKGMM-UHFFFAOYSA-N polymyxin E1 Natural products CCC(C)CCCCC(=O)NC(CCN)C(=O)NC(C(C)O)C(=O)NC(CCN)C(=O)NC1CCNC(=O)C(C(C)O)NC(=O)C(CCN)NC(=O)C(CCN)NC(=O)C(CC(C)C)NC(=O)C(CC(C)C)NC(=O)C(CCN)NC1=O XDJYMJULXQKGMM-UHFFFAOYSA-N 0.000 description 2
- KNIWPHSUTGNZST-UHFFFAOYSA-N polymyxin E2 Natural products CC(C)CCCCC(=O)NC(CCN)C(=O)NC(C(C)O)C(=O)NC(CCN)C(=O)NC1CCNC(=O)C(C(C)O)NC(=O)C(CCN)NC(=O)C(CCN)NC(=O)C(CC(C)C)NC(=O)C(CC(C)C)NC(=O)C(CCN)NC1=O KNIWPHSUTGNZST-UHFFFAOYSA-N 0.000 description 2
- 229960005266 polymyxin b Drugs 0.000 description 2
- 229940032668 prevacid Drugs 0.000 description 2
- 229940089505 prilosec Drugs 0.000 description 2
- 230000000069 prophylactic effect Effects 0.000 description 2
- 229940061276 protonix Drugs 0.000 description 2
- 229960005206 pyrazinamide Drugs 0.000 description 2
- IPEHBUMCGVEMRF-UHFFFAOYSA-N pyrazinecarboxamide Chemical compound NC(=O)C1=CN=CC=N1 IPEHBUMCGVEMRF-UHFFFAOYSA-N 0.000 description 2
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 2
- 229940052337 quinupristin/dalfopristin Drugs 0.000 description 2
- 229960004157 rabeprazole Drugs 0.000 description 2
- KRCQSTCYZUOBHN-UHFFFAOYSA-N rabeprazole sodium Chemical compound [Na+].COCCCOC1=CC=NC(CS(=O)C=2[N-]C3=CC=CC=C3N=2)=C1C KRCQSTCYZUOBHN-UHFFFAOYSA-N 0.000 description 2
- VMXUWOKSQNHOCA-LCYFTJDESA-N ranitidine Chemical compound [O-][N+](=O)/C=C(/NC)NCCSCC1=CC=C(CN(C)C)O1 VMXUWOKSQNHOCA-LCYFTJDESA-N 0.000 description 2
- 229960000620 ranitidine Drugs 0.000 description 2
- 230000035484 reaction time Effects 0.000 description 2
- 230000000306 recurrent effect Effects 0.000 description 2
- 230000002829 reductive effect Effects 0.000 description 2
- 230000003362 replicative effect Effects 0.000 description 2
- 229960003292 rifamycin Drugs 0.000 description 2
- HJYYPODYNSCCOU-ODRIEIDWSA-N rifamycin SV Chemical compound OC1=C(C(O)=C2C)C3=C(O)C=C1NC(=O)\C(C)=C/C=C/[C@H](C)[C@H](O)[C@@H](C)[C@@H](O)[C@@H](C)[C@H](OC(C)=O)[C@H](C)[C@@H](OC)\C=C\O[C@@]1(C)OC2=C3C1=O HJYYPODYNSCCOU-ODRIEIDWSA-N 0.000 description 2
- 229960003320 roxatidine Drugs 0.000 description 2
- 239000008159 sesame oil Substances 0.000 description 2
- 235000011803 sesame oil Nutrition 0.000 description 2
- 208000026775 severe diarrhea Diseases 0.000 description 2
- 239000000344 soap Substances 0.000 description 2
- 229910052708 sodium Inorganic materials 0.000 description 2
- 239000011734 sodium Substances 0.000 description 2
- 235000010413 sodium alginate Nutrition 0.000 description 2
- 239000000661 sodium alginate Substances 0.000 description 2
- 229940005550 sodium alginate Drugs 0.000 description 2
- 229910000162 sodium phosphate Inorganic materials 0.000 description 2
- 238000000527 sonication Methods 0.000 description 2
- 239000007921 spray Substances 0.000 description 2
- 239000003381 stabilizer Substances 0.000 description 2
- 238000010186 staining Methods 0.000 description 2
- 230000004936 stimulating effect Effects 0.000 description 2
- 229940031000 streptococcus pneumoniae Drugs 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- 229940124530 sulfonamide Drugs 0.000 description 2
- 150000003456 sulfonamides Chemical class 0.000 description 2
- 239000000829 suppository Substances 0.000 description 2
- 208000011580 syndromic disease Diseases 0.000 description 2
- 230000002195 synergetic effect Effects 0.000 description 2
- 229960001608 teicoplanin Drugs 0.000 description 2
- IWVCMVBTMGNXQD-UHFFFAOYSA-N terramycin dehydrate Natural products C1=CC=C2C(O)(C)C3C(O)C4C(N(C)C)C(O)=C(C(N)=O)C(=O)C4(O)C(O)=C3C(=O)C2=C1O IWVCMVBTMGNXQD-UHFFFAOYSA-N 0.000 description 2
- 229960002180 tetracycline Drugs 0.000 description 2
- 229930101283 tetracycline Natural products 0.000 description 2
- 229940124597 therapeutic agent Drugs 0.000 description 2
- 238000004809 thin layer chromatography Methods 0.000 description 2
- FPZLLRFZJZRHSY-HJYUBDRYSA-N tigecycline Chemical class C([C@H]1C2)C3=C(N(C)C)C=C(NC(=O)CNC(C)(C)C)C(O)=C3C(=O)C1=C(O)[C@@]1(O)[C@@H]2[C@H](N(C)C)C(O)=C(C(N)=O)C1=O FPZLLRFZJZRHSY-HJYUBDRYSA-N 0.000 description 2
- 229960004089 tigecycline Drugs 0.000 description 2
- 238000011269 treatment regimen Methods 0.000 description 2
- GETQZCLCWQTVFV-UHFFFAOYSA-N trimethylamine Chemical compound CN(C)C GETQZCLCWQTVFV-UHFFFAOYSA-N 0.000 description 2
- 229960000497 trovafloxacin Drugs 0.000 description 2
- WVPSKSLAZQPAKQ-CDMJZVDBSA-N trovafloxacin Chemical compound C([C@H]1[C@@H]([C@H]1C1)N)N1C(C(=CC=1C(=O)C(C(O)=O)=C2)F)=NC=1N2C1=CC=C(F)C=C1F WVPSKSLAZQPAKQ-CDMJZVDBSA-N 0.000 description 2
- 230000008673 vomiting Effects 0.000 description 2
- 229940108322 zantac Drugs 0.000 description 2
- MQHLMHIZUIDKOO-OKZBNKHCSA-N (2R,6S)-2,6-dimethyl-4-[(2S)-2-methyl-3-[4-(2-methylbutan-2-yl)phenyl]propyl]morpholine Chemical compound C1=CC(C(C)(C)CC)=CC=C1C[C@H](C)CN1C[C@@H](C)O[C@@H](C)C1 MQHLMHIZUIDKOO-OKZBNKHCSA-N 0.000 description 1
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 1
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 1
- OQANPHBRHBJGNZ-FYJGNVAPSA-N (3e)-6-oxo-3-[[4-(pyridin-2-ylsulfamoyl)phenyl]hydrazinylidene]cyclohexa-1,4-diene-1-carboxylic acid Chemical compound C1=CC(=O)C(C(=O)O)=C\C1=N\NC1=CC=C(S(=O)(=O)NC=2N=CC=CC=2)C=C1 OQANPHBRHBJGNZ-FYJGNVAPSA-N 0.000 description 1
- VCOPTHOUUNAYKQ-WBTCAYNUSA-N (3s)-3,6-diamino-n-[[(2s,5s,8e,11s,15s)-15-amino-11-[(6r)-2-amino-1,4,5,6-tetrahydropyrimidin-6-yl]-8-[(carbamoylamino)methylidene]-2-(hydroxymethyl)-3,6,9,12,16-pentaoxo-1,4,7,10,13-pentazacyclohexadec-5-yl]methyl]hexanamide;(3s)-3,6-diamino-n-[[(2s,5s,8 Chemical compound N1C(=O)\C(=C/NC(N)=O)NC(=O)[C@H](CNC(=O)C[C@@H](N)CCCN)NC(=O)[C@H](C)NC(=O)[C@@H](N)CNC(=O)[C@@H]1[C@@H]1NC(N)=NCC1.N1C(=O)\C(=C/NC(N)=O)NC(=O)[C@H](CNC(=O)C[C@@H](N)CCCN)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CNC(=O)[C@@H]1[C@@H]1NC(N)=NCC1 VCOPTHOUUNAYKQ-WBTCAYNUSA-N 0.000 description 1
- HBUJYEUPIIJJOS-PBHICJAKSA-N (5r)-3-[4-[1-[(2s)-2,3-dihydroxypropanoyl]-3,6-dihydro-2h-pyridin-4-yl]-3,5-difluorophenyl]-5-(1,2-oxazol-3-yloxymethyl)-1,3-oxazolidin-2-one Chemical compound C1N(C(=O)[C@@H](O)CO)CCC(C=2C(=CC(=CC=2F)N2C(O[C@@H](COC3=NOC=C3)C2)=O)F)=C1 HBUJYEUPIIJJOS-PBHICJAKSA-N 0.000 description 1
- GPYKKBAAPVOCIW-HSASPSRMSA-N (6r,7s)-7-[[(2r)-2-amino-2-phenylacetyl]amino]-3-chloro-8-oxo-1-azabicyclo[4.2.0]oct-2-ene-2-carboxylic acid;hydrate Chemical compound O.C1([C@H](C(=O)N[C@@H]2C(N3C(=C(Cl)CC[C@@H]32)C(O)=O)=O)N)=CC=CC=C1 GPYKKBAAPVOCIW-HSASPSRMSA-N 0.000 description 1
- 125000006728 (C1-C6) alkynyl group Chemical group 0.000 description 1
- 125000000171 (C1-C6) haloalkyl group Chemical group 0.000 description 1
- WRIDQFICGBMAFQ-UHFFFAOYSA-N (E)-8-Octadecenoic acid Natural products CCCCCCCCCC=CCCCCCCC(O)=O WRIDQFICGBMAFQ-UHFFFAOYSA-N 0.000 description 1
- RXZBMPWDPOLZGW-XMRMVWPWSA-N (E)-roxithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H](O)[C@@H](C)C(=N/OCOCCOC)/[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 RXZBMPWDPOLZGW-XMRMVWPWSA-N 0.000 description 1
- XUBOMFCQGDBHNK-JTQLQIEISA-N (S)-gatifloxacin Chemical compound FC1=CC(C(C(C(O)=O)=CN2C3CC3)=O)=C2C(OC)=C1N1CCN[C@@H](C)C1 XUBOMFCQGDBHNK-JTQLQIEISA-N 0.000 description 1
- NNKXWRRDHYTHFP-HZQSTTLBSA-N (r)-[(2s,4s,5r)-5-ethenyl-1-azabicyclo[2.2.2]octan-2-yl]-(6-methoxyquinolin-4-yl)methanol;hydron;dichloride Chemical compound Cl.Cl.C([C@H]([C@H](C1)C=C)C2)CN1[C@@H]2[C@H](O)C1=CC=NC2=CC=C(OC)C=C21 NNKXWRRDHYTHFP-HZQSTTLBSA-N 0.000 description 1
- NCCJWSXETVVUHK-ZYSAIPPVSA-N (z)-7-[(2r)-2-amino-2-carboxyethyl]sulfanyl-2-[[(1s)-2,2-dimethylcyclopropanecarbonyl]amino]hept-2-enoic acid;(5r,6s)-3-[2-(aminomethylideneamino)ethylsulfanyl]-6-[(1r)-1-hydroxyethyl]-7-oxo-1-azabicyclo[3.2.0]hept-2-ene-2-carboxylic acid Chemical compound C1C(SCC\N=C/N)=C(C(O)=O)N2C(=O)[C@H]([C@H](O)C)[C@H]21.CC1(C)C[C@@H]1C(=O)N\C(=C/CCCCSC[C@H](N)C(O)=O)C(O)=O NCCJWSXETVVUHK-ZYSAIPPVSA-N 0.000 description 1
- KZPYGQFFRCFCPP-UHFFFAOYSA-N 1,1'-bis(diphenylphosphino)ferrocene Chemical compound [Fe+2].C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1.C1=CC=C[C-]1P(C=1C=CC=CC=1)C1=CC=CC=C1 KZPYGQFFRCFCPP-UHFFFAOYSA-N 0.000 description 1
- ZORQXIQZAOLNGE-UHFFFAOYSA-N 1,1-difluorocyclohexane Chemical compound FC1(F)CCCCC1 ZORQXIQZAOLNGE-UHFFFAOYSA-N 0.000 description 1
- BCMCBBGGLRIHSE-UHFFFAOYSA-N 1,3-benzoxazole Chemical compound C1=CC=C2OC=NC2=C1 BCMCBBGGLRIHSE-UHFFFAOYSA-N 0.000 description 1
- HYZJCKYKOHLVJF-UHFFFAOYSA-N 1H-benzimidazole Chemical compound C1=CC=C2NC=NC2=C1 HYZJCKYKOHLVJF-UHFFFAOYSA-N 0.000 description 1
- BAXOFTOLAUCFNW-UHFFFAOYSA-N 1H-indazole Chemical compound C1=CC=C2C=NNC2=C1 BAXOFTOLAUCFNW-UHFFFAOYSA-N 0.000 description 1
- GEJVGFCMKRDIAC-UHFFFAOYSA-N 1h-benzimidazole;quinoline Chemical compound C1=CC=C2NC=NC2=C1.N1=CC=CC2=CC=CC=C21 GEJVGFCMKRDIAC-UHFFFAOYSA-N 0.000 description 1
- ZAVJTSLIGAGALR-UHFFFAOYSA-N 2-(2,2,2-trifluoroacetyl)cyclooctan-1-one Chemical compound FC(F)(F)C(=O)C1CCCCCCC1=O ZAVJTSLIGAGALR-UHFFFAOYSA-N 0.000 description 1
- XKZQKPRCPNGNFR-UHFFFAOYSA-N 2-(3-hydroxyphenyl)phenol Chemical compound OC1=CC=CC(C=2C(=CC=CC=2)O)=C1 XKZQKPRCPNGNFR-UHFFFAOYSA-N 0.000 description 1
- IQEWIIWKWPCQIU-UHFFFAOYSA-N 2-(4-methoxyphenyl)-6-(2-phenyl-3h-benzimidazol-5-yl)-1h-benzimidazole Chemical compound C1=CC(OC)=CC=C1C1=NC2=CC=C(C=3C=C4N=C(NC4=CC=3)C=3C=CC=CC=3)C=C2N1 IQEWIIWKWPCQIU-UHFFFAOYSA-N 0.000 description 1
- IZXIZTKNFFYFOF-UHFFFAOYSA-N 2-Oxazolidone Chemical class O=C1NCCO1 IZXIZTKNFFYFOF-UHFFFAOYSA-N 0.000 description 1
- ODUOJXZPIYUATO-UHFFFAOYSA-N 2-[[2-[(acetylthio)methyl]-1-oxo-3-phenylpropyl]amino]acetic acid (phenylmethyl) ester Chemical compound C=1C=CC=CC=1COC(=O)CNC(=O)C(CSC(=O)C)CC1=CC=CC=C1 ODUOJXZPIYUATO-UHFFFAOYSA-N 0.000 description 1
- 125000005273 2-acetoxybenzoic acid group Chemical group 0.000 description 1
- JWYUFVNJZUSCSM-UHFFFAOYSA-N 2-aminobenzimidazole Chemical class C1=CC=C2NC(N)=NC2=C1 JWYUFVNJZUSCSM-UHFFFAOYSA-N 0.000 description 1
- UHGULLIUJBCTEF-UHFFFAOYSA-N 2-aminobenzothiazole Chemical class C1=CC=C2SC(N)=NC2=C1 UHGULLIUJBCTEF-UHFFFAOYSA-N 0.000 description 1
- NLEPLDKPYLYCSY-UHFFFAOYSA-N 2-fluoroquinoline Chemical compound C1=CC=CC2=NC(F)=CC=C21 NLEPLDKPYLYCSY-UHFFFAOYSA-N 0.000 description 1
- DPJCXCZTLWNFOH-UHFFFAOYSA-N 2-nitroaniline Chemical compound NC1=CC=CC=C1[N+]([O-])=O DPJCXCZTLWNFOH-UHFFFAOYSA-N 0.000 description 1
- 125000001494 2-propynyl group Chemical group [H]C#CC([H])([H])* 0.000 description 1
- LQJBNNIYVWPHFW-UHFFFAOYSA-N 20:1omega9c fatty acid Natural products CCCCCCCCCCC=CCCCCCCCC(O)=O LQJBNNIYVWPHFW-UHFFFAOYSA-N 0.000 description 1
- VHMICKWLTGFITH-UHFFFAOYSA-N 2H-isoindole Chemical compound C1=CC=CC2=CNC=C21 VHMICKWLTGFITH-UHFFFAOYSA-N 0.000 description 1
- QROWVLFOWUYBIG-UHFFFAOYSA-N 3-[6-[2-(3-aminophenyl)-3h-benzimidazol-5-yl]-1h-benzimidazol-2-yl]aniline Chemical compound NC1=CC=CC(C=2NC3=CC(=CC=C3N=2)C=2C=C3NC(=NC3=CC=2)C=2C=C(N)C=CC=2)=C1 QROWVLFOWUYBIG-UHFFFAOYSA-N 0.000 description 1
- QWZHDKGQKYEBKK-UHFFFAOYSA-N 3-aminochromen-2-one Chemical class C1=CC=C2OC(=O)C(N)=CC2=C1 QWZHDKGQKYEBKK-UHFFFAOYSA-N 0.000 description 1
- OSWFIVFLDKOXQC-UHFFFAOYSA-N 4-(3-methoxyphenyl)aniline Chemical compound COC1=CC=CC(C=2C=CC(N)=CC=2)=C1 OSWFIVFLDKOXQC-UHFFFAOYSA-N 0.000 description 1
- LXZLVPRVOHOQOS-UHFFFAOYSA-N 4-[2-(4-methoxyphenyl)-3h-benzimidazol-5-yl]benzene-1,2-diamine Chemical compound C1=CC(OC)=CC=C1C1=NC2=CC=C(C=3C=C(N)C(N)=CC=3)C=C2N1 LXZLVPRVOHOQOS-UHFFFAOYSA-N 0.000 description 1
- WUBBRNOQWQTFEX-UHFFFAOYSA-N 4-aminosalicylic acid Chemical compound NC1=CC=C(C(O)=O)C(O)=C1 WUBBRNOQWQTFEX-UHFFFAOYSA-N 0.000 description 1
- UQEANKGXXSENNF-UHFFFAOYSA-N 4-bromo-1-fluoro-2-nitrobenzene Chemical compound [O-][N+](=O)C1=CC(Br)=CC=C1F UQEANKGXXSENNF-UHFFFAOYSA-N 0.000 description 1
- VQCWSOYHHXXWSP-UHFFFAOYSA-N 4-bromo-2-fluoro-1-nitrobenzene Chemical compound [O-][N+](=O)C1=CC=C(Br)C=C1F VQCWSOYHHXXWSP-UHFFFAOYSA-N 0.000 description 1
- IFTUKVAJYOQKRS-UHFFFAOYSA-N 4-bromo-n-methyl-2-nitroaniline Chemical compound CNC1=CC=C(Br)C=C1[N+]([O-])=O IFTUKVAJYOQKRS-UHFFFAOYSA-N 0.000 description 1
- KCNVREFIOJIJGN-UHFFFAOYSA-N 4-chloro-n,n'-diphenylbenzenecarboximidamide Chemical class C1=CC(Cl)=CC=C1C(NC=1C=CC=CC=1)=NC1=CC=CC=C1 KCNVREFIOJIJGN-UHFFFAOYSA-N 0.000 description 1
- MAGFQRLKWCCTQJ-UHFFFAOYSA-N 4-ethenylbenzenesulfonic acid Chemical compound OS(=O)(=O)C1=CC=C(C=C)C=C1 MAGFQRLKWCCTQJ-UHFFFAOYSA-N 0.000 description 1
- HIQIXEFWDLTDED-UHFFFAOYSA-N 4-hydroxy-1-piperidin-4-ylpyrrolidin-2-one Chemical compound O=C1CC(O)CN1C1CCNCC1 HIQIXEFWDLTDED-UHFFFAOYSA-N 0.000 description 1
- SYQNUQSGEWNWKV-XUIVZRPNSA-N 4-hydroxy-3,5-dimethyl-5-(2-methyl-buta-1,3-dienyl)-5h-thiophen-2-one Chemical compound C=CC(/C)=C/[C@@]1(C)SC(=O)C(C)=C1O SYQNUQSGEWNWKV-XUIVZRPNSA-N 0.000 description 1
- 125000005274 4-hydroxybenzoic acid group Chemical group 0.000 description 1
- 125000004172 4-methoxyphenyl group Chemical group [H]C1=C([H])C(OC([H])([H])[H])=C([H])C([H])=C1* 0.000 description 1
- 125000000339 4-pyridyl group Chemical group N1=C([H])C([H])=C([*])C([H])=C1[H] 0.000 description 1
- SYQNUQSGEWNWKV-UHFFFAOYSA-N 5R-Thiolactomycin Natural products C=CC(C)=CC1(C)SC(=O)C(C)=C1O SYQNUQSGEWNWKV-UHFFFAOYSA-N 0.000 description 1
- QSBYPNXLFMSGKH-UHFFFAOYSA-N 9-Heptadecensaeure Natural products CCCCCCCC=CCCCCCCCC(O)=O QSBYPNXLFMSGKH-UHFFFAOYSA-N 0.000 description 1
- 208000030507 AIDS Diseases 0.000 description 1
- 206010000060 Abdominal distension Diseases 0.000 description 1
- 239000005995 Aluminium silicate Substances 0.000 description 1
- 229930183010 Amphotericin Natural products 0.000 description 1
- QGGFZZLFKABGNL-UHFFFAOYSA-N Amphotericin A Natural products OC1C(N)C(O)C(C)OC1OC1C=CC=CC=CC=CCCC=CC=CC(C)C(O)C(C)C(C)OC(=O)CC(O)CC(O)CCC(O)C(O)CC(O)CC(O)(CC(O)C2C(O)=O)OC2C1 QGGFZZLFKABGNL-UHFFFAOYSA-N 0.000 description 1
- WZPBZJONDBGPKJ-UHFFFAOYSA-N Antibiotic SQ 26917 Natural products O=C1N(S(O)(=O)=O)C(C)C1NC(=O)C(=NOC(C)(C)C(O)=O)C1=CSC(N)=N1 WZPBZJONDBGPKJ-UHFFFAOYSA-N 0.000 description 1
- 235000003911 Arachis Nutrition 0.000 description 1
- 244000105624 Arachis hypogaea Species 0.000 description 1
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Natural products OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- 244000063299 Bacillus subtilis Species 0.000 description 1
- 235000014469 Bacillus subtilis Nutrition 0.000 description 1
- 239000005711 Benzoic acid Substances 0.000 description 1
- 208000003508 Botulism Diseases 0.000 description 1
- COVZYZSDYWQREU-UHFFFAOYSA-N Busulfan Chemical compound CS(=O)(=O)OCCCCOS(C)(=O)=O COVZYZSDYWQREU-UHFFFAOYSA-N 0.000 description 1
- 240000001546 Byrsonima crassifolia Species 0.000 description 1
- 241000282421 Canidae Species 0.000 description 1
- 108010065839 Capreomycin Proteins 0.000 description 1
- 241000282693 Cercopithecidae Species 0.000 description 1
- 240000001817 Cereus hexagonus Species 0.000 description 1
- 241000282994 Cervidae Species 0.000 description 1
- 206010008631 Cholera Diseases 0.000 description 1
- 229920001268 Cholestyramine Polymers 0.000 description 1
- 235000001258 Cinchona calisaya Nutrition 0.000 description 1
- 241001470651 Clostridium perfringens ATCC 13124 Species 0.000 description 1
- 241000193449 Clostridium tetani Species 0.000 description 1
- 229920002911 Colestipol Polymers 0.000 description 1
- 208000002881 Colic Diseases 0.000 description 1
- 241000699800 Cricetinae Species 0.000 description 1
- 229920000858 Cyclodextrin Polymers 0.000 description 1
- DYDCUQKUCUHJBH-UWTATZPHSA-N D-Cycloserine Chemical compound N[C@@H]1CONC1=O DYDCUQKUCUHJBH-UWTATZPHSA-N 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- 230000004568 DNA-binding Effects 0.000 description 1
- 108010013198 Daptomycin Proteins 0.000 description 1
- 206010061818 Disease progression Diseases 0.000 description 1
- ZGTMUACCHSMWAC-UHFFFAOYSA-L EDTA disodium salt (anhydrous) Chemical compound [Na+].[Na+].OC(=O)CN(CC([O-])=O)CCN(CC(O)=O)CC([O-])=O ZGTMUACCHSMWAC-UHFFFAOYSA-L 0.000 description 1
- LVGKNOAMLMIIKO-UHFFFAOYSA-N Elaidinsaeure-aethylester Natural products CCCCCCCCC=CCCCCCCCC(=O)OCC LVGKNOAMLMIIKO-UHFFFAOYSA-N 0.000 description 1
- GDSYPXWUHMRTHT-UHFFFAOYSA-N Epidermin Natural products N#CCC(C)(C)OC1OC(CO)C(O)C(O)C1O GDSYPXWUHMRTHT-UHFFFAOYSA-N 0.000 description 1
- 241000283074 Equus asinus Species 0.000 description 1
- 241000283073 Equus caballus Species 0.000 description 1
- PIICEJLVQHRZGT-UHFFFAOYSA-N Ethylenediamine Chemical compound NCCN PIICEJLVQHRZGT-UHFFFAOYSA-N 0.000 description 1
- UIOFUWFRIANQPC-JKIFEVAISA-N Floxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=C(F)C=CC=C1Cl UIOFUWFRIANQPC-JKIFEVAISA-N 0.000 description 1
- 201000000628 Gas Gangrene Diseases 0.000 description 1
- JRZJKWGQFNTSRN-UHFFFAOYSA-N Geldanamycin Natural products C1C(C)CC(OC)C(O)C(C)C=C(C)C(OC(N)=O)C(OC)CCC=C(C)C(=O)NC2=CC(=O)C(OC)=C1C2=O JRZJKWGQFNTSRN-UHFFFAOYSA-N 0.000 description 1
- CEAZRRDELHUEMR-URQXQFDESA-N Gentamicin Chemical compound O1[C@H](C(C)NC)CC[C@@H](N)[C@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](NC)[C@@](C)(O)CO2)O)[C@H](N)C[C@@H]1N CEAZRRDELHUEMR-URQXQFDESA-N 0.000 description 1
- 229930182566 Gentamicin Natural products 0.000 description 1
- 241000282818 Giraffidae Species 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 108010015899 Glycopeptides Proteins 0.000 description 1
- 102000002068 Glycopeptides Human genes 0.000 description 1
- AIJTTZAVMXIJGM-UHFFFAOYSA-N Grepafloxacin Chemical compound C1CNC(C)CN1C(C(=C1C)F)=CC2=C1C(=O)C(C(O)=O)=CN2C1CC1 AIJTTZAVMXIJGM-UHFFFAOYSA-N 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- 229920000084 Gum arabic Polymers 0.000 description 1
- 241000589989 Helicobacter Species 0.000 description 1
- 206010019851 Hepatotoxicity Diseases 0.000 description 1
- 229940122957 Histamine H2 receptor antagonist Drugs 0.000 description 1
- 241001272567 Hominoidea Species 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 1
- 208000031226 Hyperlipidaemia Diseases 0.000 description 1
- JUZNIMUFDBIJCM-ANEDZVCMSA-N Invanz Chemical compound O=C([C@H]1NC[C@H](C1)SC=1[C@H](C)[C@@H]2[C@H](C(N2C=1C(O)=O)=O)[C@H](O)C)NC1=CC=CC(C(O)=O)=C1 JUZNIMUFDBIJCM-ANEDZVCMSA-N 0.000 description 1
- UETNIIAIRMUTSM-UHFFFAOYSA-N Jacareubin Natural products CC1(C)OC2=CC3Oc4c(O)c(O)ccc4C(=O)C3C(=C2C=C1)O UETNIIAIRMUTSM-UHFFFAOYSA-N 0.000 description 1
- YQEZLKZALYSWHR-UHFFFAOYSA-N Ketamine Chemical compound C=1C=CC=C(Cl)C=1C1(NC)CCCCC1=O YQEZLKZALYSWHR-UHFFFAOYSA-N 0.000 description 1
- 244000199866 Lactobacillus casei Species 0.000 description 1
- 235000013958 Lactobacillus casei Nutrition 0.000 description 1
- 240000006024 Lactobacillus plantarum Species 0.000 description 1
- 235000013965 Lactobacillus plantarum Nutrition 0.000 description 1
- 241000218588 Lactobacillus rhamnosus Species 0.000 description 1
- 239000004166 Lanolin Substances 0.000 description 1
- OJMMVQQUTAEWLP-UHFFFAOYSA-N Lincomycin Natural products CN1CC(CCC)CC1C(=O)NC(C(C)O)C1C(O)C(O)C(O)C(SC)O1 OJMMVQQUTAEWLP-UHFFFAOYSA-N 0.000 description 1
- 206010024604 Lipoatrophy Diseases 0.000 description 1
- 206010049287 Lipodystrophy acquired Diseases 0.000 description 1
- 108010028921 Lipopeptides Proteins 0.000 description 1
- 241000186781 Listeria Species 0.000 description 1
- WHXSMMKQMYFTQS-UHFFFAOYSA-N Lithium Chemical compound [Li] WHXSMMKQMYFTQS-UHFFFAOYSA-N 0.000 description 1
- TYMRLRRVMHJFTF-UHFFFAOYSA-N Mafenide Chemical compound NCC1=CC=C(S(N)(=O)=O)C=C1 TYMRLRRVMHJFTF-UHFFFAOYSA-N 0.000 description 1
- 235000019759 Maize starch Nutrition 0.000 description 1
- 208000002720 Malnutrition Diseases 0.000 description 1
- JCYZMTMYPZHVBF-UHFFFAOYSA-N Melarsoprol Chemical compound NC1=NC(N)=NC(NC=2C=CC(=CC=2)[As]2SC(CO)CS2)=N1 JCYZMTMYPZHVBF-UHFFFAOYSA-N 0.000 description 1
- 208000029725 Metabolic bone disease Diseases 0.000 description 1
- 108060004795 Methyltransferase Proteins 0.000 description 1
- MQGFYNRGFWXAKA-GXSYYHJRSA-N Micrococcin Chemical compound C[C@H](O)CNC(=O)C(=C/C)/NC(=O)C1=CSC(C=2N=C(SC=2)C=2N=C3C=4N=C(SC=4)[C@H]([C@@H](C)O)NC(=O)C=4N=C(SC=4)[C@@H](C(C)C)NC(=O)C=4N=C(SC=4)C(=C/C)/NC(=O)[C@H]([C@@H](C)O)NC(=O)C=4N=C(SC=4)C3=CC=2)=N1 MQGFYNRGFWXAKA-GXSYYHJRSA-N 0.000 description 1
- 241000238367 Mya arenaria Species 0.000 description 1
- 238000005481 NMR spectroscopy Methods 0.000 description 1
- 229910004879 Na2S2O5 Inorganic materials 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- 206010028980 Neoplasm Diseases 0.000 description 1
- 108010053775 Nisin Proteins 0.000 description 1
- NVNLLIYOARQCIX-MSHCCFNRSA-N Nisin Chemical compound N1C(=O)[C@@H](CC(C)C)NC(=O)C(=C)NC(=O)[C@@H]([C@H](C)CC)NC(=O)[C@@H](NC(=O)C(=C/C)/NC(=O)[C@H](N)[C@H](C)CC)CSC[C@@H]1C(=O)N[C@@H]1C(=O)N2CCC[C@@H]2C(=O)NCC(=O)N[C@@H](C(=O)N[C@H](CCCCN)C(=O)N[C@@H]2C(NCC(=O)N[C@H](C)C(=O)N[C@H](CC(C)C)C(=O)N[C@H](CCSC)C(=O)NCC(=O)N[C@H](CS[C@@H]2C)C(=O)N[C@H](CC(N)=O)C(=O)N[C@H](CCSC)C(=O)N[C@H](CCCCN)C(=O)N[C@@H]2C(N[C@H](C)C(=O)N[C@@H]3C(=O)N[C@@H](C(N[C@H](CC=4NC=NC=4)C(=O)N[C@H](CS[C@@H]3C)C(=O)N[C@H](CO)C(=O)N[C@H]([C@H](C)CC)C(=O)N[C@H](CC=3NC=NC=3)C(=O)N[C@H](C(C)C)C(=O)NC(=C)C(=O)N[C@H](CCCCN)C(O)=O)=O)CS[C@@H]2C)=O)=O)CS[C@@H]1C NVNLLIYOARQCIX-MSHCCFNRSA-N 0.000 description 1
- 240000007817 Olea europaea Species 0.000 description 1
- 239000005642 Oleic acid Substances 0.000 description 1
- ZQPPMHVWECSIRJ-UHFFFAOYSA-N Oleic acid Natural products CCCCCCCCC=CCCCCCCCC(O)=O ZQPPMHVWECSIRJ-UHFFFAOYSA-N 0.000 description 1
- 208000010195 Onychomycosis Diseases 0.000 description 1
- 241000283973 Oryctolagus cuniculus Species 0.000 description 1
- 206010049088 Osteopenia Diseases 0.000 description 1
- 208000001132 Osteoporosis Diseases 0.000 description 1
- 241000193465 Paeniclostridium sordellii Species 0.000 description 1
- 208000002193 Pain Diseases 0.000 description 1
- 241000282579 Pan Species 0.000 description 1
- 241000282320 Panthera leo Species 0.000 description 1
- 241000282376 Panthera tigris Species 0.000 description 1
- UOZODPSAJZTQNH-UHFFFAOYSA-N Paromomycin II Natural products NC1C(O)C(O)C(CN)OC1OC1C(O)C(OC2C(C(N)CC(N)C2O)OC2C(C(O)C(O)C(CO)O2)N)OC1CO UOZODPSAJZTQNH-UHFFFAOYSA-N 0.000 description 1
- 241001494479 Pecora Species 0.000 description 1
- RVGRUAULSDPKGF-UHFFFAOYSA-N Poloxamer Chemical compound C1CO1.CC1CO1 RVGRUAULSDPKGF-UHFFFAOYSA-N 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 241000282405 Pongo abelii Species 0.000 description 1
- ZLMJMSJWJFRBEC-UHFFFAOYSA-N Potassium Chemical compound [K] ZLMJMSJWJFRBEC-UHFFFAOYSA-N 0.000 description 1
- 241000288906 Primates Species 0.000 description 1
- CZPWVGJYEJSRLH-UHFFFAOYSA-N Pyrimidine Chemical compound C1=CN=CN=C1 CZPWVGJYEJSRLH-UHFFFAOYSA-N 0.000 description 1
- 206010057071 Rectal tenesmus Diseases 0.000 description 1
- 241000283984 Rodentia Species 0.000 description 1
- 241000235070 Saccharomyces Species 0.000 description 1
- 240000004808 Saccharomyces cerevisiae Species 0.000 description 1
- 235000014680 Saccharomyces cerevisiae Nutrition 0.000 description 1
- 206010039438 Salmonella Infections Diseases 0.000 description 1
- 101710084578 Short neurotoxin 1 Proteins 0.000 description 1
- 229920002125 Sokalan® Polymers 0.000 description 1
- 241000194017 Streptococcus Species 0.000 description 1
- 101001138042 Streptococcus mutans Lantibiotic mutacin-1140 Proteins 0.000 description 1
- 108010034396 Streptogramins Proteins 0.000 description 1
- 241000282887 Suidae Species 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- NHUHCSRWZMLRLA-UHFFFAOYSA-N Sulfisoxazole Chemical compound CC1=NOC(NS(=O)(=O)C=2C=CC(N)=CC=2)=C1C NHUHCSRWZMLRLA-UHFFFAOYSA-N 0.000 description 1
- NINIDFKCEFEMDL-UHFFFAOYSA-N Sulfur Chemical compound [S] NINIDFKCEFEMDL-UHFFFAOYSA-N 0.000 description 1
- PJSFRIWCGOHTNF-UHFFFAOYSA-N Sulphormetoxin Chemical compound COC1=NC=NC(NS(=O)(=O)C=2C=CC(N)=CC=2)=C1OC PJSFRIWCGOHTNF-UHFFFAOYSA-N 0.000 description 1
- 206010043376 Tetanus Diseases 0.000 description 1
- FZWLAAWBMGSTSO-UHFFFAOYSA-N Thiazole Chemical compound C1=CSC=N1 FZWLAAWBMGSTSO-UHFFFAOYSA-N 0.000 description 1
- NSFFHOGKXHRQEW-UHFFFAOYSA-N Thiostrepton B Natural products N1C(=O)C(C)NC(=O)C(=C)NC(=O)C(C)NC(=O)C(C(C)CC)NC(C(C2=N3)O)C=CC2=C(C(C)O)C=C3C(=O)OC(C)C(C=2SC=C(N=2)C2N=3)NC(=O)C(N=4)=CSC=4C(C(C)(O)C(C)O)NC(=O)C(N=4)CSC=4C(=CC)NC(=O)C(C(C)O)NC(=O)C(N=4)=CSC=4C21CCC=3C1=NC(C(=O)NC(=C)C(=O)NC(=C)C(N)=O)=CS1 NSFFHOGKXHRQEW-UHFFFAOYSA-N 0.000 description 1
- HJLSLZFTEKNLFI-UHFFFAOYSA-N Tinidazole Chemical compound CCS(=O)(=O)CCN1C(C)=NC=C1[N+]([O-])=O HJLSLZFTEKNLFI-UHFFFAOYSA-N 0.000 description 1
- 101710182223 Toxin B Proteins 0.000 description 1
- 101710182532 Toxin a Proteins 0.000 description 1
- GSEJCLTVZPLZKY-UHFFFAOYSA-N Triethanolamine Chemical class OCCN(CCO)CCO GSEJCLTVZPLZKY-UHFFFAOYSA-N 0.000 description 1
- 229940118555 Viral entry inhibitor Drugs 0.000 description 1
- 208000027418 Wounds and injury Diseases 0.000 description 1
- PTFCDOFLOPIGGS-UHFFFAOYSA-N Zinc dication Chemical compound [Zn+2] PTFCDOFLOPIGGS-UHFFFAOYSA-N 0.000 description 1
- WERKSKAQRVDLDW-ANOHMWSOSA-N [(2s,3r,4r,5r)-2,3,4,5,6-pentahydroxyhexyl] (z)-octadec-9-enoate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO WERKSKAQRVDLDW-ANOHMWSOSA-N 0.000 description 1
- ZWBTYMGEBZUQTK-PVLSIAFMSA-N [(7S,9E,11S,12R,13S,14R,15R,16R,17S,18S,19E,21Z)-2,15,17,32-tetrahydroxy-11-methoxy-3,7,12,14,16,18,22-heptamethyl-1'-(2-methylpropyl)-6,23-dioxospiro[8,33-dioxa-24,27,29-triazapentacyclo[23.6.1.14,7.05,31.026,30]tritriaconta-1(32),2,4,9,19,21,24,26,30-nonaene-28,4'-piperidine]-13-yl] acetate Chemical compound CO[C@H]1\C=C\O[C@@]2(C)Oc3c(C2=O)c2c4NC5(CCN(CC(C)C)CC5)N=c4c(=NC(=O)\C(C)=C/C=C/[C@H](C)[C@H](O)[C@@H](C)[C@@H](O)[C@@H](C)[C@H](OC(C)=O)[C@@H]1C)c(O)c2c(O)c3C ZWBTYMGEBZUQTK-PVLSIAFMSA-N 0.000 description 1
- 230000002159 abnormal effect Effects 0.000 description 1
- 230000005856 abnormality Effects 0.000 description 1
- 235000010489 acacia gum Nutrition 0.000 description 1
- 239000000205 acacia gum Substances 0.000 description 1
- DPXJVFZANSGRMM-UHFFFAOYSA-N acetic acid;2,3,4,5,6-pentahydroxyhexanal;sodium Chemical compound [Na].CC(O)=O.OCC(O)C(O)C(O)C(O)C=O DPXJVFZANSGRMM-UHFFFAOYSA-N 0.000 description 1
- 239000002253 acid Substances 0.000 description 1
- 239000011149 active material Substances 0.000 description 1
- 239000013543 active substance Substances 0.000 description 1
- 230000001154 acute effect Effects 0.000 description 1
- 208000038016 acute inflammation Diseases 0.000 description 1
- 230000006022 acute inflammation Effects 0.000 description 1
- 230000010933 acylation Effects 0.000 description 1
- 238000005917 acylation reaction Methods 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 238000005054 agglomeration Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 125000001931 aliphatic group Chemical group 0.000 description 1
- 229910001508 alkali metal halide Inorganic materials 0.000 description 1
- 150000008045 alkali metal halides Chemical class 0.000 description 1
- 150000001340 alkali metals Chemical class 0.000 description 1
- 229910052784 alkaline earth metal Inorganic materials 0.000 description 1
- 150000001336 alkenes Chemical class 0.000 description 1
- 230000029936 alkylation Effects 0.000 description 1
- 238000005804 alkylation reaction Methods 0.000 description 1
- 125000002947 alkylene group Chemical group 0.000 description 1
- 229910052782 aluminium Inorganic materials 0.000 description 1
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 1
- 235000012211 aluminium silicate Nutrition 0.000 description 1
- 150000001412 amines Chemical class 0.000 description 1
- 229940126575 aminoglycoside Drugs 0.000 description 1
- 229960004909 aminosalicylic acid Drugs 0.000 description 1
- 150000003863 ammonium salts Chemical class 0.000 description 1
- 229960003204 amorolfine Drugs 0.000 description 1
- 229940009444 amphotericin Drugs 0.000 description 1
- APKFDSVGJQXUKY-INPOYWNPSA-N amphotericin B Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/C=C/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 APKFDSVGJQXUKY-INPOYWNPSA-N 0.000 description 1
- 229940035676 analgesics Drugs 0.000 description 1
- 208000007502 anemia Diseases 0.000 description 1
- 239000000730 antalgic agent Substances 0.000 description 1
- 208000022338 anthrax infection Diseases 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 229940125714 antidiarrheal agent Drugs 0.000 description 1
- 229960005475 antiinfective agent Drugs 0.000 description 1
- 230000003078 antioxidant effect Effects 0.000 description 1
- 229940124575 antispasmodic agent Drugs 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 239000008135 aqueous vehicle Substances 0.000 description 1
- 229940003446 arsphenamine Drugs 0.000 description 1
- VLAXZGHHBIJLAD-UHFFFAOYSA-N arsphenamine Chemical compound [Cl-].[Cl-].C1=C(O)C([NH3+])=CC([As]=[As]C=2C=C([NH3+])C(O)=CC=2)=C1 VLAXZGHHBIJLAD-UHFFFAOYSA-N 0.000 description 1
- 235000010323 ascorbic acid Nutrition 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000011668 ascorbic acid Substances 0.000 description 1
- QVGXLLKOCUKJST-UHFFFAOYSA-N atomic oxygen Chemical compound [O] QVGXLLKOCUKJST-UHFFFAOYSA-N 0.000 description 1
- 229960003159 atovaquone Drugs 0.000 description 1
- KUCQYCKVKVOKAY-CTYIDZIISA-N atovaquone Chemical compound C1([C@H]2CC[C@@H](CC2)C2=C(C(C3=CC=CC=C3C2=O)=O)O)=CC=C(Cl)C=C1 KUCQYCKVKVOKAY-CTYIDZIISA-N 0.000 description 1
- 239000012752 auxiliary agent Substances 0.000 description 1
- 150000003851 azoles Chemical class 0.000 description 1
- WZPBZJONDBGPKJ-VEHQQRBSSA-N aztreonam Chemical compound O=C1N(S([O-])(=O)=O)[C@@H](C)[C@@H]1NC(=O)C(=N/OC(C)(C)C(O)=O)\C1=CSC([NH3+])=N1 WZPBZJONDBGPKJ-VEHQQRBSSA-N 0.000 description 1
- 229960003644 aztreonam Drugs 0.000 description 1
- PFOLLRNADZZWEX-FFGRCDKISA-N bacampicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)[C@H](C(S3)(C)C)C(=O)OC(C)OC(=O)OCC)=CC=CC=C1 PFOLLRNADZZWEX-FFGRCDKISA-N 0.000 description 1
- 229960002699 bacampicillin Drugs 0.000 description 1
- 229960000686 benzalkonium chloride Drugs 0.000 description 1
- RFRXIWQYSOIBDI-UHFFFAOYSA-N benzarone Chemical compound CCC=1OC2=CC=CC=C2C=1C(=O)C1=CC=C(O)C=C1 RFRXIWQYSOIBDI-UHFFFAOYSA-N 0.000 description 1
- JUHORIMYRDESRB-UHFFFAOYSA-N benzathine Chemical compound C=1C=CC=CC=1CNCCNCC1=CC=CC=C1 JUHORIMYRDESRB-UHFFFAOYSA-N 0.000 description 1
- 235000010233 benzoic acid Nutrition 0.000 description 1
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 1
- 239000003613 bile acid Substances 0.000 description 1
- 238000010876 biochemical test Methods 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 230000015572 biosynthetic process Effects 0.000 description 1
- 238000001815 biotherapy Methods 0.000 description 1
- 208000024330 bloating Diseases 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 125000001246 bromo group Chemical group Br* 0.000 description 1
- 238000002815 broth microdilution Methods 0.000 description 1
- 239000000872 buffer Substances 0.000 description 1
- HEJBMFPJLCJWER-CWPVBXIBSA-L calcium;7-[(2r,3r,4s,5r)-4-carbamoyloxy-3-hydroxy-5-methoxy-6,6-dimethyloxan-2-yl]oxy-3-[[4-hydroxy-3-(3-methylbut-2-enyl)benzoyl]amino]-8-methyl-2-oxochromen-4-olate Chemical compound [Ca+2].O1C(C)(C)[C@H](OC)[C@@H](OC(N)=O)[C@@H](O)[C@@H]1OC1=CC=C(C([O-])=C(NC(=O)C=2C=C(CC=C(C)C)C(O)=CC=2)C(=O)O2)C2=C1C.O1C(C)(C)[C@H](OC)[C@@H](OC(N)=O)[C@@H](O)[C@@H]1OC1=CC=C(C([O-])=C(NC(=O)C=2C=C(CC=C(C)C)C(O)=CC=2)C(=O)O2)C2=C1C HEJBMFPJLCJWER-CWPVBXIBSA-L 0.000 description 1
- 201000011510 cancer Diseases 0.000 description 1
- 229960004602 capreomycin Drugs 0.000 description 1
- 125000002837 carbocyclic group Chemical group 0.000 description 1
- 150000001735 carboxylic acids Chemical class 0.000 description 1
- 125000002091 cationic group Chemical group 0.000 description 1
- QYIYFLOTGYLRGG-GPCCPHFNSA-N cefaclor Chemical compound C1([C@H](C(=O)N[C@@H]2C(N3C(=C(Cl)CS[C@@H]32)C(O)=O)=O)N)=CC=CC=C1 QYIYFLOTGYLRGG-GPCCPHFNSA-N 0.000 description 1
- 229960005361 cefaclor Drugs 0.000 description 1
- 229960004841 cefadroxil Drugs 0.000 description 1
- NBFNMSULHIODTC-CYJZLJNKSA-N cefadroxil monohydrate Chemical compound O.C1([C@@H](N)C(=O)N[C@H]2[C@@H]3N(C2=O)C(=C(CS3)C)C(O)=O)=CC=C(O)C=C1 NBFNMSULHIODTC-CYJZLJNKSA-N 0.000 description 1
- XIURVHNZVLADCM-IUODEOHRSA-N cefalotin Chemical compound N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC(=O)C)C(O)=O)C(=O)CC1=CC=CS1 XIURVHNZVLADCM-IUODEOHRSA-N 0.000 description 1
- 229960000603 cefalotin Drugs 0.000 description 1
- OLVCFLKTBJRLHI-AXAPSJFSSA-N cefamandole Chemical compound CN1N=NN=C1SCC1=C(C(O)=O)N2C(=O)[C@@H](NC(=O)[C@H](O)C=3C=CC=CC=3)[C@H]2SC1 OLVCFLKTBJRLHI-AXAPSJFSSA-N 0.000 description 1
- 229960003012 cefamandole Drugs 0.000 description 1
- 229960001139 cefazolin Drugs 0.000 description 1
- MLYYVTUWGNIJIB-BXKDBHETSA-N cefazolin Chemical compound S1C(C)=NN=C1SCC1=C(C(O)=O)N2C(=O)[C@@H](NC(=O)CN3N=NN=C3)[C@H]2SC1 MLYYVTUWGNIJIB-BXKDBHETSA-N 0.000 description 1
- 229960004069 cefditoren Drugs 0.000 description 1
- KMIPKYQIOVAHOP-YLGJWRNMSA-N cefditoren Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1\C=C/C=1SC=NC=1C KMIPKYQIOVAHOP-YLGJWRNMSA-N 0.000 description 1
- HVFLCNVBZFFHBT-ZKDACBOMSA-N cefepime Chemical compound S([C@@H]1[C@@H](C(N1C=1C([O-])=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1C[N+]1(C)CCCC1 HVFLCNVBZFFHBT-ZKDACBOMSA-N 0.000 description 1
- 229960002100 cefepime Drugs 0.000 description 1
- 229960002129 cefixime Drugs 0.000 description 1
- OKBVVJOGVLARMR-QSWIMTSFSA-N cefixime Chemical compound S1C(N)=NC(C(=N\OCC(O)=O)\C(=O)N[C@@H]2C(N3C(=C(C=C)CS[C@@H]32)C(O)=O)=O)=C1 OKBVVJOGVLARMR-QSWIMTSFSA-N 0.000 description 1
- 229960004682 cefoperazone Drugs 0.000 description 1
- GCFBRXLSHGKWDP-XCGNWRKASA-N cefoperazone Chemical compound O=C1C(=O)N(CC)CCN1C(=O)N[C@H](C=1C=CC(O)=CC=1)C(=O)N[C@@H]1C(=O)N2C(C(O)=O)=C(CSC=3N(N=NN=3)C)CS[C@@H]21 GCFBRXLSHGKWDP-XCGNWRKASA-N 0.000 description 1
- 229960004261 cefotaxime Drugs 0.000 description 1
- GPRBEKHLDVQUJE-VINNURBNSA-N cefotaxime Chemical compound N([C@@H]1C(N2C(=C(COC(C)=O)CS[C@@H]21)C(O)=O)=O)C(=O)/C(=N/OC)C1=CSC(N)=N1 GPRBEKHLDVQUJE-VINNURBNSA-N 0.000 description 1
- WZOZEZRFJCJXNZ-ZBFHGGJFSA-N cefoxitin Chemical compound N([C@]1(OC)C(N2C(=C(COC(N)=O)CS[C@@H]21)C(O)=O)=O)C(=O)CC1=CC=CS1 WZOZEZRFJCJXNZ-ZBFHGGJFSA-N 0.000 description 1
- 229960002682 cefoxitin Drugs 0.000 description 1
- 229960005090 cefpodoxime Drugs 0.000 description 1
- WYUSVOMTXWRGEK-HBWVYFAYSA-N cefpodoxime Chemical compound N([C@H]1[C@@H]2N(C1=O)C(=C(CS2)COC)C(O)=O)C(=O)C(=N/OC)\C1=CSC(N)=N1 WYUSVOMTXWRGEK-HBWVYFAYSA-N 0.000 description 1
- 229960000484 ceftazidime Drugs 0.000 description 1
- NMVPEQXCMGEDNH-TZVUEUGBSA-N ceftazidime pentahydrate Chemical compound O.O.O.O.O.S([C@@H]1[C@@H](C(N1C=1C([O-])=O)=O)NC(=O)\C(=N/OC(C)(C)C(O)=O)C=2N=C(N)SC=2)CC=1C[N+]1=CC=CC=C1 NMVPEQXCMGEDNH-TZVUEUGBSA-N 0.000 description 1
- 229960004086 ceftibuten Drugs 0.000 description 1
- UNJFKXSSGBWRBZ-BJCIPQKHSA-N ceftibuten Chemical compound S1C(N)=NC(C(=C\CC(O)=O)\C(=O)N[C@@H]2C(N3C(=CCS[C@@H]32)C(O)=O)=O)=C1 UNJFKXSSGBWRBZ-BJCIPQKHSA-N 0.000 description 1
- 229960001991 ceftizoxime Drugs 0.000 description 1
- NNULBSISHYWZJU-LLKWHZGFSA-N ceftizoxime Chemical compound N([C@@H]1C(N2C(=CCS[C@@H]21)C(O)=O)=O)C(=O)\C(=N/OC)C1=CSC(N)=N1 NNULBSISHYWZJU-LLKWHZGFSA-N 0.000 description 1
- 229960004755 ceftriaxone Drugs 0.000 description 1
- VAAUVRVFOQPIGI-SPQHTLEESA-N ceftriaxone Chemical compound S([C@@H]1[C@@H](C(N1C=1C(O)=O)=O)NC(=O)\C(=N/OC)C=2N=C(N)SC=2)CC=1CSC1=NC(=O)C(=O)NN1C VAAUVRVFOQPIGI-SPQHTLEESA-N 0.000 description 1
- 229960001668 cefuroxime Drugs 0.000 description 1
- JFPVXVDWJQMJEE-IZRZKJBUSA-N cefuroxime Chemical compound N([C@@H]1C(N2C(=C(COC(N)=O)CS[C@@H]21)C(O)=O)=O)C(=O)\C(=N/OC)C1=CC=CO1 JFPVXVDWJQMJEE-IZRZKJBUSA-N 0.000 description 1
- 210000002421 cell wall Anatomy 0.000 description 1
- 229960000541 cetyl alcohol Drugs 0.000 description 1
- MYPYJXKWCTUITO-KIIOPKALSA-N chembl3301825 Chemical compound O([C@@H]1[C@@H](O)[C@H](O)[C@@H](CO)O[C@H]1OC1=C2C=C3C=C1OC1=CC=C(C=C1Cl)[C@@H](O)[C@H](C(N[C@@H](CC(N)=O)C(=O)N[C@H]3C(=O)N[C@H]1C(=O)N[C@H](C(N[C@H](C3=CC(O)=CC(O)=C3C=3C(O)=CC=C1C=3)C(O)=O)=O)[C@H](O)C1=CC=C(C(=C1)Cl)O2)=O)NC(=O)[C@@H](CC(C)C)NC)[C@H]1C[C@](C)(N)C(O)[C@H](C)O1 MYPYJXKWCTUITO-KIIOPKALSA-N 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- 125000001309 chloro group Chemical group Cl* 0.000 description 1
- HTMINPLANVJXLT-LOHKCFAQSA-N chlorobiocin Chemical compound O([C@H]1[C@@H](C(O[C@@H](OC=2C(=C3OC(=O)C(NC(=O)C=4C=C(CC=C(C)C)C(O)=CC=4)=C(O)C3=CC=2)Cl)[C@@H]1O)(C)C)OC)C(=O)C1=CC=C(C)[N]1 HTMINPLANVJXLT-LOHKCFAQSA-N 0.000 description 1
- FJAQNRBDVKIIKK-UHFFFAOYSA-N chlorobiocin Natural products OC1C(OC=2C(=C3OC(=O)C(NC(=O)C=4C=C(CC=C(C)C)C(O)=CC=4)=C(O)C3=CC=2)Cl)OC(C)(C)C(OC)C1OC(=O)C1=CC=C(C)N1 FJAQNRBDVKIIKK-UHFFFAOYSA-N 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- VDANGULDQQJODZ-UHFFFAOYSA-N chloroprocaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1Cl VDANGULDQQJODZ-UHFFFAOYSA-N 0.000 description 1
- 229960002023 chloroprocaine Drugs 0.000 description 1
- OEYIOHPDSNJKLS-UHFFFAOYSA-N choline Chemical compound C[N+](C)(C)CCO OEYIOHPDSNJKLS-UHFFFAOYSA-N 0.000 description 1
- 229960001231 choline Drugs 0.000 description 1
- 239000000812 cholinergic antagonist Substances 0.000 description 1
- 238000004587 chromatography analysis Methods 0.000 description 1
- LOUPRKONTZGTKE-UHFFFAOYSA-N cinchonine Natural products C1C(C(C2)C=C)CCN2C1C(O)C1=CC=NC2=CC=C(OC)C=C21 LOUPRKONTZGTKE-UHFFFAOYSA-N 0.000 description 1
- VDUWPHTZYNWKRN-UHFFFAOYSA-N cinoxacin Chemical compound C1=C2N(CC)N=C(C(O)=O)C(=O)C2=CC2=C1OCO2 VDUWPHTZYNWKRN-UHFFFAOYSA-N 0.000 description 1
- 229960004621 cinoxacin Drugs 0.000 description 1
- 229960003405 ciprofloxacin Drugs 0.000 description 1
- 238000004140 cleaning Methods 0.000 description 1
- 238000011260 co-administration Methods 0.000 description 1
- 238000000576 coating method Methods 0.000 description 1
- 239000003240 coconut oil Substances 0.000 description 1
- 235000019864 coconut oil Nutrition 0.000 description 1
- 238000012321 colectomy Methods 0.000 description 1
- GMRWGQCZJGVHKL-UHFFFAOYSA-N colestipol Chemical compound ClCC1CO1.NCCNCCNCCNCCN GMRWGQCZJGVHKL-UHFFFAOYSA-N 0.000 description 1
- 229960002604 colestipol Drugs 0.000 description 1
- 230000000112 colonic effect Effects 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940125782 compound 2 Drugs 0.000 description 1
- 229940126214 compound 3 Drugs 0.000 description 1
- 229940125898 compound 5 Drugs 0.000 description 1
- 230000001010 compromised effect Effects 0.000 description 1
- 238000009833 condensation Methods 0.000 description 1
- 230000005494 condensation Effects 0.000 description 1
- 238000011109 contamination Methods 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 235000005687 corn oil Nutrition 0.000 description 1
- 239000002285 corn oil Substances 0.000 description 1
- 229940099112 cornstarch Drugs 0.000 description 1
- 235000012343 cottonseed oil Nutrition 0.000 description 1
- 239000002385 cottonseed oil Substances 0.000 description 1
- 238000004132 cross linking Methods 0.000 description 1
- 238000000315 cryotherapy Methods 0.000 description 1
- 239000002178 crystalline material Substances 0.000 description 1
- 238000011461 current therapy Methods 0.000 description 1
- 125000000596 cyclohexenyl group Chemical group C1(=CCCCC1)* 0.000 description 1
- 231100000599 cytotoxic agent Toxicity 0.000 description 1
- 239000002619 cytotoxin Substances 0.000 description 1
- DOAKLVKFURWEDJ-QCMAZARJSA-N daptomycin Chemical compound C([C@H]1C(=O)O[C@H](C)[C@@H](C(NCC(=O)N[C@@H](CCCN)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@H](C)C(=O)N[C@@H](CC(O)=O)C(=O)NCC(=O)N[C@H](CO)C(=O)N[C@H](C(=O)N1)[C@H](C)CC(O)=O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@@H](CC(N)=O)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)CCCCCCCCC)C(=O)C1=CC=CC=C1N DOAKLVKFURWEDJ-QCMAZARJSA-N 0.000 description 1
- 229960005484 daptomycin Drugs 0.000 description 1
- 238000000354 decomposition reaction Methods 0.000 description 1
- 238000005202 decontamination Methods 0.000 description 1
- 230000003588 decontaminative effect Effects 0.000 description 1
- 230000001934 delay Effects 0.000 description 1
- CYQFCXCEBYINGO-IAGOWNOFSA-N delta1-THC Chemical compound C1=C(C)CC[C@H]2C(C)(C)OC3=CC(CCCCC)=CC(O)=C3[C@@H]21 CYQFCXCEBYINGO-IAGOWNOFSA-N 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- ZBCBWPMODOFKDW-UHFFFAOYSA-N diethanolamine Chemical compound OCCNCCO ZBCBWPMODOFKDW-UHFFFAOYSA-N 0.000 description 1
- 229940043237 diethanolamine Drugs 0.000 description 1
- HPNMFZURTQLUMO-UHFFFAOYSA-N diethylamine Chemical compound CCNCC HPNMFZURTQLUMO-UHFFFAOYSA-N 0.000 description 1
- 230000010339 dilation Effects 0.000 description 1
- 238000010790 dilution Methods 0.000 description 1
- 239000012895 dilution Substances 0.000 description 1
- HYPPXZBJBPSRLK-UHFFFAOYSA-N diphenoxylate Chemical compound C1CC(C(=O)OCC)(C=2C=CC=CC=2)CCN1CCC(C#N)(C=1C=CC=CC=1)C1=CC=CC=C1 HYPPXZBJBPSRLK-UHFFFAOYSA-N 0.000 description 1
- 229960004192 diphenoxylate Drugs 0.000 description 1
- 229940042399 direct acting antivirals protease inhibitors Drugs 0.000 description 1
- 229960004100 dirithromycin Drugs 0.000 description 1
- WLOHNSSYAXHWNR-NXPDYKKBSA-N dirithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)O[C@@H]([C@@]([C@H]2O[C@H](COCCOC)N[C@H]([C@@H]2C)[C@H](C)C[C@@](C)(O)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)O)[C@H]1C)(C)O)CC)[C@H]1C[C@@](C)(OC)[C@@H](O)[C@H](C)O1 WLOHNSSYAXHWNR-NXPDYKKBSA-N 0.000 description 1
- 230000006806 disease prevention Effects 0.000 description 1
- 230000005750 disease progression Effects 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 239000002934 diuretic Substances 0.000 description 1
- 229940030606 diuretics Drugs 0.000 description 1
- 229960000895 doripenem Drugs 0.000 description 1
- AVAACINZEOAHHE-VFZPANTDSA-N doripenem Chemical compound C=1([C@H](C)[C@@H]2[C@H](C(N2C=1C(O)=O)=O)[C@H](O)C)S[C@@H]1CN[C@H](CNS(N)(=O)=O)C1 AVAACINZEOAHHE-VFZPANTDSA-N 0.000 description 1
- 239000003107 drug analog Substances 0.000 description 1
- 239000000975 dye Substances 0.000 description 1
- 238000000132 electrospray ionisation Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 239000003974 emollient agent Substances 0.000 description 1
- 229940095399 enema Drugs 0.000 description 1
- 229940079360 enema for constipation Drugs 0.000 description 1
- 230000002708 enhancing effect Effects 0.000 description 1
- IDYZIJYBMGIQMJ-UHFFFAOYSA-N enoxacin Chemical compound N1=C2N(CC)C=C(C(O)=O)C(=O)C2=CC(F)=C1N1CCNCC1 IDYZIJYBMGIQMJ-UHFFFAOYSA-N 0.000 description 1
- 229960002549 enoxacin Drugs 0.000 description 1
- 239000002702 enteric coating Substances 0.000 description 1
- 238000009505 enteric coating Methods 0.000 description 1
- 244000000021 enteric pathogen Species 0.000 description 1
- 230000006353 environmental stress Effects 0.000 description 1
- 239000002532 enzyme inhibitor Substances 0.000 description 1
- 108010064962 epidermin Proteins 0.000 description 1
- CXTXHTVXPMOOSW-JUEJINBGSA-N epidermin Chemical compound C([C@H]1C(=O)N[C@H](C(=O)N[C@@H](CSC[C@H](C(N[C@@H](CCCCN)C(=O)N1)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)[C@@H](C)CC)C(=O)N[C@H]1C(N2CCC[C@H]2C(=O)NCC(=O)N[C@@H](CS[C@H]1C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCCCN)C(=O)N\C(=C/C)C(=O)NCC(=O)N[C@H]1C(N[C@@H](CC=2C=CC=CC=2)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@H]2C(=O)N[C@@H](CC=3C=CC(O)=CC=3)C(=O)N[C@H](C(N\C=C/SC2)=O)CSC1)=O)=O)[C@@H](C)CC)C1=CC=CC=C1 CXTXHTVXPMOOSW-JUEJINBGSA-N 0.000 description 1
- 229960002770 ertapenem Drugs 0.000 description 1
- 230000032050 esterification Effects 0.000 description 1
- 238000005886 esterification reaction Methods 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- 150000002170 ethers Chemical class 0.000 description 1
- AEOCXXJPGCBFJA-UHFFFAOYSA-N ethionamide Chemical compound CCC1=CC(C(N)=S)=CC=N1 AEOCXXJPGCBFJA-UHFFFAOYSA-N 0.000 description 1
- 229960002001 ethionamide Drugs 0.000 description 1
- LVGKNOAMLMIIKO-QXMHVHEDSA-N ethyl oleate Chemical compound CCCCCCCC\C=C/CCCCCCCC(=O)OCC LVGKNOAMLMIIKO-QXMHVHEDSA-N 0.000 description 1
- 229940093471 ethyl oleate Drugs 0.000 description 1
- 235000010228 ethyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004403 ethyl p-hydroxybenzoate Substances 0.000 description 1
- 229940043351 ethyl-p-hydroxybenzoate Drugs 0.000 description 1
- 229940012017 ethylenediamine Drugs 0.000 description 1
- NUVBSKCKDOMJSU-UHFFFAOYSA-N ethylparaben Chemical compound CCOC(=O)C1=CC=C(O)C=C1 NUVBSKCKDOMJSU-UHFFFAOYSA-N 0.000 description 1
- 125000002534 ethynyl group Chemical group [H]C#C* 0.000 description 1
- 230000007717 exclusion Effects 0.000 description 1
- 238000002474 experimental method Methods 0.000 description 1
- 239000003889 eye drop Substances 0.000 description 1
- 229940012356 eye drops Drugs 0.000 description 1
- 230000001815 facial effect Effects 0.000 description 1
- 230000002349 favourable effect Effects 0.000 description 1
- 210000003608 fece Anatomy 0.000 description 1
- 239000000945 filler Substances 0.000 description 1
- 238000009093 first-line therapy Methods 0.000 description 1
- 229960004273 floxacillin Drugs 0.000 description 1
- 229910052731 fluorine Inorganic materials 0.000 description 1
- 229940124307 fluoroquinolone Drugs 0.000 description 1
- 230000037406 food intake Effects 0.000 description 1
- 239000010794 food waste Substances 0.000 description 1
- 244000078673 foodborn pathogen Species 0.000 description 1
- 235000019253 formic acid Nutrition 0.000 description 1
- YMDXZJFXQJVXBF-STHAYSLISA-N fosfomycin Chemical compound C[C@@H]1O[C@@H]1P(O)(O)=O YMDXZJFXQJVXBF-STHAYSLISA-N 0.000 description 1
- GJXWDTUCERCKIX-UHFFFAOYSA-N fosmidomycin Chemical compound O=CN(O)CCCP(O)(O)=O GJXWDTUCERCKIX-UHFFFAOYSA-N 0.000 description 1
- 229950006501 fosmidomycin Drugs 0.000 description 1
- 230000004927 fusion Effects 0.000 description 1
- 229940125777 fusion inhibitor Drugs 0.000 description 1
- 108010070411 gardimycin Proteins 0.000 description 1
- LAWKVNVCUPIOMG-HWWYPGLISA-N gardimycin Chemical compound C1=CC=C2C(C[C@H](C(=O)NCC(=O)N[C@H](CO)C(=O)N[C@H](C)C(=O)NCC(=O)N[C@H](CC)C(=O)N[C@H](C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@H](C)C(=O)N[C@@H](C)C(=O)N[C@H](C)C(O)=O)C(C)C)NC(=O)[C@@H](NC(=O)[C@@H](C)NC(=O)[C@@H](CC)NC(=O)[C@@H](CCC(O)=O)NC(=O)[C@@H](NC(=O)[C@@H](CC)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](C)N)[C@@H](C)CC)C(C)C)=CNC2=C1 LAWKVNVCUPIOMG-HWWYPGLISA-N 0.000 description 1
- 229960003923 gatifloxacin Drugs 0.000 description 1
- QTQAWLPCGQOSGP-GBTDJJJQSA-N geldanamycin Chemical compound N1C(=O)\C(C)=C/C=C\[C@@H](OC)[C@H](OC(N)=O)\C(C)=C/[C@@H](C)[C@@H](O)[C@H](OC)C[C@@H](C)CC2=C(OC)C(=O)C=C1C2=O QTQAWLPCGQOSGP-GBTDJJJQSA-N 0.000 description 1
- 229960002518 gentamicin Drugs 0.000 description 1
- 230000002070 germicidal effect Effects 0.000 description 1
- 230000035784 germination Effects 0.000 description 1
- 230000005182 global health Effects 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 238000005469 granulation Methods 0.000 description 1
- 230000003179 granulation Effects 0.000 description 1
- 229960000642 grepafloxacin Drugs 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- 235000010417 guar gum Nutrition 0.000 description 1
- 229960002154 guar gum Drugs 0.000 description 1
- 244000005709 gut microbiome Species 0.000 description 1
- 230000007686 hepatotoxicity Effects 0.000 description 1
- 231100000304 hepatotoxicity Toxicity 0.000 description 1
- MCAHMSDENAOJFZ-BVXDHVRPSA-N herbimycin Chemical compound N1C(=O)\C(C)=C\C=C/[C@H](OC)[C@@H](OC(N)=O)\C(C)=C\[C@H](C)[C@@H](OC)[C@@H](OC)C[C@H](C)[C@@H](OC)C2=CC(=O)C=C1C2=O MCAHMSDENAOJFZ-BVXDHVRPSA-N 0.000 description 1
- 229930193320 herbimycin Natural products 0.000 description 1
- FBPFZTCFMRRESA-UHFFFAOYSA-N hexane-1,2,3,4,5,6-hexol Chemical compound OCC(O)C(O)C(O)C(O)CO FBPFZTCFMRRESA-UHFFFAOYSA-N 0.000 description 1
- 239000003485 histamine H2 receptor antagonist Substances 0.000 description 1
- 239000008240 homogeneous mixture Substances 0.000 description 1
- 235000003642 hunger Nutrition 0.000 description 1
- 230000007062 hydrolysis Effects 0.000 description 1
- 238000006460 hydrolysis reaction Methods 0.000 description 1
- 230000002209 hydrophobic effect Effects 0.000 description 1
- 229960002927 hydroxychloroquine sulfate Drugs 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 1
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 1
- 210000003405 ileum Anatomy 0.000 description 1
- 125000003037 imidazol-2-yl group Chemical group [H]N1C([*])=NC([H])=C1[H] 0.000 description 1
- 150000002460 imidazoles Chemical class 0.000 description 1
- 230000002519 immonomodulatory effect Effects 0.000 description 1
- 229940072221 immunoglobulins Drugs 0.000 description 1
- 230000003308 immunostimulating effect Effects 0.000 description 1
- 229960003444 immunosuppressant agent Drugs 0.000 description 1
- 239000003018 immunosuppressive agent Substances 0.000 description 1
- 229940095970 imodium Drugs 0.000 description 1
- 230000001771 impaired effect Effects 0.000 description 1
- 239000007943 implant Substances 0.000 description 1
- 238000002513 implantation Methods 0.000 description 1
- 238000011534 incubation Methods 0.000 description 1
- PZOUSPYUWWUPPK-UHFFFAOYSA-N indole Natural products CC1=CC=CC2=C1C=CN2 PZOUSPYUWWUPPK-UHFFFAOYSA-N 0.000 description 1
- RKJUIXBNRJVNHR-UHFFFAOYSA-N indolenine Natural products C1=CC=C2CC=NC2=C1 RKJUIXBNRJVNHR-UHFFFAOYSA-N 0.000 description 1
- 230000004054 inflammatory process Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000003999 initiator Substances 0.000 description 1
- 229940102223 injectable solution Drugs 0.000 description 1
- 229940102213 injectable suspension Drugs 0.000 description 1
- 238000002347 injection Methods 0.000 description 1
- 239000007924 injection Substances 0.000 description 1
- 229940124524 integrase inhibitor Drugs 0.000 description 1
- 239000002850 integrase inhibitor Substances 0.000 description 1
- 210000000936 intestine Anatomy 0.000 description 1
- 125000002346 iodo group Chemical group I* 0.000 description 1
- QXJSBBXBKPUZAA-UHFFFAOYSA-N isooleic acid Natural products CCCCCCCC=CCCCCCCCCC(O)=O QXJSBBXBKPUZAA-UHFFFAOYSA-N 0.000 description 1
- 125000001449 isopropyl group Chemical group [H]C([H])([H])C([H])(*)C([H])([H])[H] 0.000 description 1
- YWXYYJSYQOXTPL-SLPGGIOYSA-N isosorbide mononitrate Chemical compound [O-][N+](=O)O[C@@H]1CO[C@@H]2[C@@H](O)CO[C@@H]21 YWXYYJSYQOXTPL-SLPGGIOYSA-N 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- 235000015110 jellies Nutrition 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 229960003299 ketamine Drugs 0.000 description 1
- 230000002147 killing effect Effects 0.000 description 1
- TYQCGQRIZGCHNB-JLAZNSOCSA-N l-ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(O)=C(O)C1=O TYQCGQRIZGCHNB-JLAZNSOCSA-N 0.000 description 1
- 229940017800 lactobacillus casei Drugs 0.000 description 1
- 229940072205 lactobacillus plantarum Drugs 0.000 description 1
- 229940039717 lanolin Drugs 0.000 description 1
- 235000019388 lanolin Nutrition 0.000 description 1
- 230000000670 limiting effect Effects 0.000 description 1
- 229960005287 lincomycin Drugs 0.000 description 1
- OJMMVQQUTAEWLP-KIDUDLJLSA-N lincomycin Chemical compound CN1C[C@H](CCC)C[C@H]1C(=O)N[C@H]([C@@H](C)O)[C@@H]1[C@H](O)[C@H](O)[C@@H](O)[C@@H](SC)O1 OJMMVQQUTAEWLP-KIDUDLJLSA-N 0.000 description 1
- 150000002632 lipids Chemical class 0.000 description 1
- 208000006132 lipodystrophy Diseases 0.000 description 1
- 239000002502 liposome Substances 0.000 description 1
- 238000004811 liquid chromatography Methods 0.000 description 1
- 229910052744 lithium Inorganic materials 0.000 description 1
- 229960001977 loracarbef Drugs 0.000 description 1
- 229960003640 mafenide Drugs 0.000 description 1
- 238000004949 mass spectrometry Methods 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- OPXLLQIJSORQAM-UHFFFAOYSA-N mebendazole Chemical compound C=1C=C2NC(NC(=O)OC)=NC2=CC=1C(=O)C1=CC=CC=C1 OPXLLQIJSORQAM-UHFFFAOYSA-N 0.000 description 1
- 229960003439 mebendazole Drugs 0.000 description 1
- 238000005399 mechanical ventilation Methods 0.000 description 1
- 230000007246 mechanism Effects 0.000 description 1
- 230000001404 mediated effect Effects 0.000 description 1
- 238000002483 medication Methods 0.000 description 1
- 229960003194 meglumine Drugs 0.000 description 1
- 229960001728 melarsoprol Drugs 0.000 description 1
- 238000002844 melting Methods 0.000 description 1
- 230000008018 melting Effects 0.000 description 1
- 230000034217 membrane fusion Effects 0.000 description 1
- 229960002260 meropenem Drugs 0.000 description 1
- DMJNNHOOLUXYBV-PQTSNVLCSA-N meropenem Chemical compound C=1([C@H](C)[C@@H]2[C@H](C(N2C=1C(O)=O)=O)[C@H](O)C)S[C@@H]1CN[C@H](C(=O)N(C)C)C1 DMJNNHOOLUXYBV-PQTSNVLCSA-N 0.000 description 1
- 108010067215 mersacidin Proteins 0.000 description 1
- JSWKNDSDVHJUKY-CYGWNLPQSA-N mersacidin Chemical compound C([C@@H](C(=O)N[C@@H]1[C@H](C)SC[C@H](NC(=O)[C@H](C(C)C)NC(=O)CNC(=O)CNC(=O)CNC(=O)CNC(=O)[C@@H]2CCCN2C(=O)[C@H](CC(C)C)NC1=O)C(=O)N[C@@H]1[C@H](C)SC[C@H]2C(=O)N[C@H](C(N/C=C/S[C@@H](C)C(NC(=O)[C@H](CC(C)C)NC1=O)C(=O)NC(=C)C(=O)N[C@@H](CCC(O)=O)C(=O)N2)=O)[C@H](C)CC)NC(=O)[C@H]1[C@@H](SC[C@H](N)C(=O)N1)C)C1=CC=CC=C1 JSWKNDSDVHJUKY-CYGWNLPQSA-N 0.000 description 1
- 230000004060 metabolic process Effects 0.000 description 1
- 229940098779 methanesulfonic acid Drugs 0.000 description 1
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 description 1
- 229960002216 methylparaben Drugs 0.000 description 1
- 125000004170 methylsulfonyl group Chemical group [H]C([H])([H])S(*)(=O)=O 0.000 description 1
- YPBATNHYBCGSSN-VWPFQQQWSA-N mezlocillin Chemical compound N([C@@H](C(=O)N[C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C=1C=CC=CC=1)C(=O)N1CCN(S(C)(=O)=O)C1=O YPBATNHYBCGSSN-VWPFQQQWSA-N 0.000 description 1
- 229960000198 mezlocillin Drugs 0.000 description 1
- 238000009629 microbiological culture Methods 0.000 description 1
- 108010009882 micrococcin Proteins 0.000 description 1
- MQGFYNRGFWXAKA-TWSKATCCSA-N micrococcin P1 Natural products CC=C(NC(=O)c1csc(n1)c2csc(n2)c3ccc4c5nc(cs5)C(=O)N[C@@H]([C@@H](C)O)C(=O)NC(=CC)c6nc(cs6)C(=O)N[C@@H](C(C)C)c7nc(cs7)C(=O)N[C@@H]([C@@H](C)O)c8nc(cs8)c4n3)C(=O)NC[C@@H](C)O MQGFYNRGFWXAKA-TWSKATCCSA-N 0.000 description 1
- 244000005706 microflora Species 0.000 description 1
- 239000011859 microparticle Substances 0.000 description 1
- 238000000386 microscopy Methods 0.000 description 1
- 229940042472 mineral oil Drugs 0.000 description 1
- 238000002156 mixing Methods 0.000 description 1
- 238000012544 monitoring process Methods 0.000 description 1
- 229940041009 monobactams Drugs 0.000 description 1
- 238000009343 monoculture Methods 0.000 description 1
- 125000002950 monocyclic group Chemical group 0.000 description 1
- 229940102020 motofen Drugs 0.000 description 1
- 229960003702 moxifloxacin Drugs 0.000 description 1
- FABPRXSRWADJSP-MEDUHNTESA-N moxifloxacin Chemical compound COC1=C(N2C[C@H]3NCCC[C@H]3C2)C(F)=CC(C(C(C(O)=O)=C2)=O)=C1N2C1CC1 FABPRXSRWADJSP-MEDUHNTESA-N 0.000 description 1
- 108010093400 mutacin I Proteins 0.000 description 1
- 108010004592 mutacin II Proteins 0.000 description 1
- CSYNQJPENMOLHR-UHFFFAOYSA-N n,n-diethylethanamine;ethyl acetate Chemical compound CCOC(C)=O.CCN(CC)CC CSYNQJPENMOLHR-UHFFFAOYSA-N 0.000 description 1
- 125000001280 n-hexyl group Chemical group C(CCCCC)* 0.000 description 1
- MHWLWQUZZRMNGJ-UHFFFAOYSA-N nalidixic acid Chemical compound C1=C(C)N=C2N(CC)C=C(C(O)=O)C(=O)C2=C1 MHWLWQUZZRMNGJ-UHFFFAOYSA-N 0.000 description 1
- 229960000210 nalidixic acid Drugs 0.000 description 1
- 239000002105 nanoparticle Substances 0.000 description 1
- 230000037125 natural defense Effects 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 239000004309 nisin Substances 0.000 description 1
- 235000010297 nisin Nutrition 0.000 description 1
- 229960000564 nitrofurantoin Drugs 0.000 description 1
- NXFQHRVNIOXGAQ-YCRREMRBSA-N nitrofurantoin Chemical compound O1C([N+](=O)[O-])=CC=C1\C=N\N1C(=O)NC(=O)C1 NXFQHRVNIOXGAQ-YCRREMRBSA-N 0.000 description 1
- 231100000344 non-irritating Toxicity 0.000 description 1
- 229940042402 non-nucleoside reverse transcriptase inhibitor Drugs 0.000 description 1
- 239000002736 nonionic surfactant Substances 0.000 description 1
- 239000002726 nonnucleoside reverse transcriptase inhibitor Substances 0.000 description 1
- YJQPYGGHQPGBLI-KGSXXDOSSA-N novobiocin Chemical compound O1C(C)(C)[C@H](OC)[C@@H](OC(N)=O)[C@@H](O)[C@@H]1OC1=CC=C(C(O)=C(NC(=O)C=2C=C(CC=C(C)C)C(O)=CC=2)C(=O)O2)C2=C1C YJQPYGGHQPGBLI-KGSXXDOSSA-N 0.000 description 1
- 238000000655 nuclear magnetic resonance spectrum Methods 0.000 description 1
- 229940042404 nucleoside and nucleotide reverse transcriptase inhibitor Drugs 0.000 description 1
- 235000018343 nutrient deficiency Nutrition 0.000 description 1
- GYCKQBWUSACYIF-UHFFFAOYSA-N o-hydroxybenzoic acid ethyl ester Natural products CCOC(=O)C1=CC=CC=C1O GYCKQBWUSACYIF-UHFFFAOYSA-N 0.000 description 1
- 239000012053 oil suspension Substances 0.000 description 1
- ZQPPMHVWECSIRJ-KTKRTIGZSA-N oleic acid Chemical compound CCCCCCCC\C=C/CCCCCCCC(O)=O ZQPPMHVWECSIRJ-KTKRTIGZSA-N 0.000 description 1
- 229940012843 omega-3 fatty acid Drugs 0.000 description 1
- 229940127240 opiate Drugs 0.000 description 1
- 150000007524 organic acids Chemical class 0.000 description 1
- 239000012044 organic layer Substances 0.000 description 1
- 239000003960 organic solvent Substances 0.000 description 1
- UWYHMGVUTGAWSP-JKIFEVAISA-N oxacillin Chemical compound N([C@@H]1C(N2[C@H](C(C)(C)S[C@@H]21)C(O)=O)=O)C(=O)C1=C(C)ON=C1C1=CC=CC=C1 UWYHMGVUTGAWSP-JKIFEVAISA-N 0.000 description 1
- 229960001019 oxacillin Drugs 0.000 description 1
- 239000001301 oxygen Substances 0.000 description 1
- QNGNSVIICDLXHT-UHFFFAOYSA-N para-ethylbenzaldehyde Natural products CCC1=CC=C(C=O)C=C1 QNGNSVIICDLXHT-UHFFFAOYSA-N 0.000 description 1
- 239000012188 paraffin wax Substances 0.000 description 1
- 238000007911 parenteral administration Methods 0.000 description 1
- 229960001914 paromomycin Drugs 0.000 description 1
- UOZODPSAJZTQNH-LSWIJEOBSA-N paromomycin Chemical compound N[C@@H]1[C@@H](O)[C@H](O)[C@H](CN)O[C@@H]1O[C@H]1[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](N)C[C@@H](N)[C@@H]2O)O[C@@H]2[C@@H]([C@@H](O)[C@H](O)[C@@H](CO)O2)N)O[C@@H]1CO UOZODPSAJZTQNH-LSWIJEOBSA-N 0.000 description 1
- 239000002245 particle Substances 0.000 description 1
- 239000006072 paste Substances 0.000 description 1
- 230000001717 pathogenic effect Effects 0.000 description 1
- 230000001575 pathological effect Effects 0.000 description 1
- 235000010987 pectin Nutrition 0.000 description 1
- 239000001814 pectin Substances 0.000 description 1
- 229920001277 pectin Polymers 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 150000002960 penicillins Chemical class 0.000 description 1
- XDRYMKDFEDOLFX-UHFFFAOYSA-N pentamidine Chemical compound C1=CC(C(=N)N)=CC=C1OCCCCCOC1=CC=C(C(N)=N)C=C1 XDRYMKDFEDOLFX-UHFFFAOYSA-N 0.000 description 1
- 229960004448 pentamidine Drugs 0.000 description 1
- 239000000137 peptide hydrolase inhibitor Substances 0.000 description 1
- 208000033808 peripheral neuropathy Diseases 0.000 description 1
- 239000003208 petroleum Substances 0.000 description 1
- 229940124531 pharmaceutical excipient Drugs 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 229940067107 phenylethyl alcohol Drugs 0.000 description 1
- 235000011007 phosphoric acid Nutrition 0.000 description 1
- 150000003016 phosphoric acids Chemical class 0.000 description 1
- 230000004962 physiological condition Effects 0.000 description 1
- 239000000049 pigment Substances 0.000 description 1
- 229920001993 poloxamer 188 Polymers 0.000 description 1
- 229920000642 polymer Polymers 0.000 description 1
- 235000010482 polyoxyethylene sorbitan monooleate Nutrition 0.000 description 1
- 239000000244 polyoxyethylene sorbitan monooleate Substances 0.000 description 1
- 229920001184 polypeptide Polymers 0.000 description 1
- 229920005606 polypropylene copolymer Polymers 0.000 description 1
- 229920001451 polypropylene glycol Polymers 0.000 description 1
- 229920000136 polysorbate Polymers 0.000 description 1
- 229920000053 polysorbate 80 Polymers 0.000 description 1
- 229940068965 polysorbates Drugs 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 235000019422 polyvinyl alcohol Nutrition 0.000 description 1
- 229910052700 potassium Inorganic materials 0.000 description 1
- 239000011591 potassium Substances 0.000 description 1
- 229920001592 potato starch Polymers 0.000 description 1
- 229940116317 potato starch Drugs 0.000 description 1
- 235000013406 prebiotics Nutrition 0.000 description 1
- 230000002335 preservative effect Effects 0.000 description 1
- 230000000529 probiotic effect Effects 0.000 description 1
- MFDFERRIHVXMIY-UHFFFAOYSA-N procaine Chemical compound CCN(CC)CCOC(=O)C1=CC=C(N)C=C1 MFDFERRIHVXMIY-UHFFFAOYSA-N 0.000 description 1
- 229960004919 procaine Drugs 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 102000004196 processed proteins & peptides Human genes 0.000 description 1
- 229960005385 proguanil Drugs 0.000 description 1
- SSOLNOMRVKKSON-UHFFFAOYSA-N proguanil Chemical compound CC(C)\N=C(/N)N=C(N)NC1=CC=C(Cl)C=C1 SSOLNOMRVKKSON-UHFFFAOYSA-N 0.000 description 1
- 230000002035 prolonged effect Effects 0.000 description 1
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 description 1
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 description 1
- QQONPFPTGQHPMA-UHFFFAOYSA-N propylene Natural products CC=C QQONPFPTGQHPMA-UHFFFAOYSA-N 0.000 description 1
- 125000004805 propylene group Chemical group [H]C([H])([H])C([H])([*:1])C([H])([H])[*:2] 0.000 description 1
- 229960003415 propylparaben Drugs 0.000 description 1
- 238000000425 proton nuclear magnetic resonance spectrum Methods 0.000 description 1
- WKSAUQYGYAYLPV-UHFFFAOYSA-N pyrimethamine Chemical compound CCC1=NC(N)=NC(N)=C1C1=CC=C(Cl)C=C1 WKSAUQYGYAYLPV-UHFFFAOYSA-N 0.000 description 1
- 229960000611 pyrimethamine Drugs 0.000 description 1
- 150000003242 quaternary ammonium salts Chemical class 0.000 description 1
- JWVCLYRUEFBMGU-UHFFFAOYSA-N quinazoline Chemical compound N1=CN=CC2=CC=CC=C21 JWVCLYRUEFBMGU-UHFFFAOYSA-N 0.000 description 1
- XHKUDCCTVQUHJQ-LCYSNFERSA-N quinidine D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C(O)=O.C([C@H]([C@H](C1)C=C)C2)C[N@@]1[C@H]2[C@@H](O)C1=CC=NC2=CC=C(OC)C=C21 XHKUDCCTVQUHJQ-LCYSNFERSA-N 0.000 description 1
- 229960002454 quinidine gluconate Drugs 0.000 description 1
- 229960000948 quinine Drugs 0.000 description 1
- 229960002522 quinine dihydrochloride Drugs 0.000 description 1
- 150000007660 quinolones Chemical class 0.000 description 1
- 229960002281 racecadotril Drugs 0.000 description 1
- 108700040249 racecadotril Proteins 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 238000001959 radiotherapy Methods 0.000 description 1
- 239000002994 raw material Substances 0.000 description 1
- 238000001953 recrystallisation Methods 0.000 description 1
- 210000000664 rectum Anatomy 0.000 description 1
- 230000001850 reproductive effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 230000004043 responsiveness Effects 0.000 description 1
- 229960000885 rifabutin Drugs 0.000 description 1
- WDZCUPBHRAEYDL-GZAUEHORSA-N rifapentine Chemical compound O([C@](C1=O)(C)O/C=C/[C@@H]([C@H]([C@@H](OC(C)=O)[C@H](C)[C@H](O)[C@H](C)[C@@H](O)[C@@H](C)\C=C\C=C(C)/C(=O)NC=2C(O)=C3C(O)=C4C)C)OC)C4=C1C3=C(O)C=2\C=N\N(CC1)CCN1C1CCCC1 WDZCUPBHRAEYDL-GZAUEHORSA-N 0.000 description 1
- 229960002599 rifapentine Drugs 0.000 description 1
- 125000006413 ring segment Chemical group 0.000 description 1
- 229960005224 roxithromycin Drugs 0.000 description 1
- CVHZOJJKTDOEJC-UHFFFAOYSA-N saccharin Chemical compound C1=CC=C2C(=O)NS(=O)(=O)C2=C1 CVHZOJJKTDOEJC-UHFFFAOYSA-N 0.000 description 1
- 229940081974 saccharin Drugs 0.000 description 1
- 235000019204 saccharin Nutrition 0.000 description 1
- 239000000901 saccharin and its Na,K and Ca salt Substances 0.000 description 1
- YGSDEFSMJLZEOE-UHFFFAOYSA-M salicylate Chemical compound OC1=CC=CC=C1C([O-])=O YGSDEFSMJLZEOE-UHFFFAOYSA-M 0.000 description 1
- 229960001860 salicylate Drugs 0.000 description 1
- 206010039447 salmonellosis Diseases 0.000 description 1
- HFHDHCJBZVLPGP-UHFFFAOYSA-N schardinger α-dextrin Chemical compound O1C(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC(C(O)C2O)C(CO)OC2OC(C(C2O)O)C(CO)OC2OC2C(O)C(O)C1OC2CO HFHDHCJBZVLPGP-UHFFFAOYSA-N 0.000 description 1
- 238000013207 serial dilution Methods 0.000 description 1
- 238000009589 serological test Methods 0.000 description 1
- 208000026773 severe abdominal cramp Diseases 0.000 description 1
- 239000000741 silica gel Substances 0.000 description 1
- 229910002027 silica gel Inorganic materials 0.000 description 1
- 239000000377 silicon dioxide Substances 0.000 description 1
- 206010040872 skin infection Diseases 0.000 description 1
- 235000017557 sodium bicarbonate Nutrition 0.000 description 1
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 1
- 229910001467 sodium calcium phosphate Inorganic materials 0.000 description 1
- 235000019812 sodium carboxymethyl cellulose Nutrition 0.000 description 1
- 229920001027 sodium carboxymethylcellulose Polymers 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 235000009518 sodium iodide Nutrition 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 239000007909 solid dosage form Substances 0.000 description 1
- 238000003797 solvolysis reaction Methods 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 235000011069 sorbitan monooleate Nutrition 0.000 description 1
- 239000001593 sorbitan monooleate Substances 0.000 description 1
- 229940035049 sorbitan monooleate Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 239000003549 soybean oil Substances 0.000 description 1
- 235000012424 soybean oil Nutrition 0.000 description 1
- 241000894007 species Species 0.000 description 1
- UNFWWIHTNXNPBV-WXKVUWSESA-N spectinomycin Chemical compound O([C@@H]1[C@@H](NC)[C@@H](O)[C@H]([C@@H]([C@H]1O1)O)NC)[C@]2(O)[C@H]1O[C@H](C)CC2=O UNFWWIHTNXNPBV-WXKVUWSESA-N 0.000 description 1
- 229960000268 spectinomycin Drugs 0.000 description 1
- 238000001228 spectrum Methods 0.000 description 1
- 235000015096 spirit Nutrition 0.000 description 1
- 230000037351 starvation Effects 0.000 description 1
- 230000001954 sterilising effect Effects 0.000 description 1
- 238000004659 sterilization and disinfection Methods 0.000 description 1
- 210000002784 stomach Anatomy 0.000 description 1
- 229940041030 streptogramins Drugs 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 229960002673 sulfacetamide Drugs 0.000 description 1
- SKIVFJLNDNKQPD-UHFFFAOYSA-N sulfacetamide Chemical compound CC(=O)NS(=O)(=O)C1=CC=C(N)C=C1 SKIVFJLNDNKQPD-UHFFFAOYSA-N 0.000 description 1
- SEEPANYCNGTZFQ-UHFFFAOYSA-N sulfadiazine Chemical compound C1=CC(N)=CC=C1S(=O)(=O)NC1=NC=CC=N1 SEEPANYCNGTZFQ-UHFFFAOYSA-N 0.000 description 1
- 229960004306 sulfadiazine Drugs 0.000 description 1
- 229960004673 sulfadoxine Drugs 0.000 description 1
- 229960000654 sulfafurazole Drugs 0.000 description 1
- 229960005158 sulfamethizole Drugs 0.000 description 1
- VACCAVUAMIDAGB-UHFFFAOYSA-N sulfamethizole Chemical compound S1C(C)=NN=C1NS(=O)(=O)C1=CC=C(N)C=C1 VACCAVUAMIDAGB-UHFFFAOYSA-N 0.000 description 1
- 229960001940 sulfasalazine Drugs 0.000 description 1
- NCEXYHBECQHGNR-UHFFFAOYSA-N sulfasalazine Natural products C1=C(O)C(C(=O)O)=CC(N=NC=2C=CC(=CC=2)S(=O)(=O)NC=2N=CC=CC=2)=C1 NCEXYHBECQHGNR-UHFFFAOYSA-N 0.000 description 1
- 150000003460 sulfonic acids Chemical class 0.000 description 1
- 239000011593 sulfur Substances 0.000 description 1
- RAHZWNYVWXNFOC-UHFFFAOYSA-N sulfur dioxide Inorganic materials O=S=O RAHZWNYVWXNFOC-UHFFFAOYSA-N 0.000 description 1
- 229960005314 suramin Drugs 0.000 description 1
- FIAFUQMPZJWCLV-UHFFFAOYSA-N suramin Chemical compound OS(=O)(=O)C1=CC(S(O)(=O)=O)=C2C(NC(=O)C3=CC=C(C(=C3)NC(=O)C=3C=C(NC(=O)NC=4C=C(C=CC=4)C(=O)NC=4C(=CC=C(C=4)C(=O)NC=4C5=C(C=C(C=C5C(=CC=4)S(O)(=O)=O)S(O)(=O)=O)S(O)(=O)=O)C)C=CC=3)C)=CC=C(S(O)(=O)=O)C2=C1 FIAFUQMPZJWCLV-UHFFFAOYSA-N 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 230000009897 systematic effect Effects 0.000 description 1
- 230000009885 systemic effect Effects 0.000 description 1
- 231100000057 systemic toxicity Toxicity 0.000 description 1
- 230000008685 targeting Effects 0.000 description 1
- LJVAJPDWBABPEJ-PNUFFHFMSA-N telithromycin Chemical compound O([C@@H]1[C@@H](C)C(=O)[C@@H](C)C(=O)O[C@@H]([C@]2(OC(=O)N(CCCCN3C=C(N=C3)C=3C=NC=CC=3)[C@@H]2[C@@H](C)C(=O)[C@H](C)C[C@@]1(C)OC)C)CC)[C@@H]1O[C@H](C)C[C@H](N(C)C)[C@H]1O LJVAJPDWBABPEJ-PNUFFHFMSA-N 0.000 description 1
- 229960003250 telithromycin Drugs 0.000 description 1
- 208000012271 tenesmus Diseases 0.000 description 1
- DOMXUEMWDBAQBQ-WEVVVXLNSA-N terbinafine Chemical compound C1=CC=C2C(CN(C\C=C\C#CC(C)(C)C)C)=CC=CC2=C1 DOMXUEMWDBAQBQ-WEVVVXLNSA-N 0.000 description 1
- 229960002722 terbinafine Drugs 0.000 description 1
- 125000000999 tert-butyl group Chemical group [H]C([H])([H])C(*)(C([H])([H])[H])C([H])([H])[H] 0.000 description 1
- 150000003512 tertiary amines Chemical class 0.000 description 1
- 229940040944 tetracyclines Drugs 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- RTKIYNMVFMVABJ-UHFFFAOYSA-L thimerosal Chemical compound [Na+].CC[Hg]SC1=CC=CC=C1C([O-])=O RTKIYNMVFMVABJ-UHFFFAOYSA-L 0.000 description 1
- 229940033663 thimerosal Drugs 0.000 description 1
- 229930192474 thiophene Natural products 0.000 description 1
- 229940063214 thiostrepton Drugs 0.000 description 1
- NSFFHOGKXHRQEW-AIHSUZKVSA-N thiostrepton Chemical compound C([C@]12C=3SC=C(N=3)C(=O)N[C@H](C(=O)NC(/C=3SC[C@@H](N=3)C(=O)N[C@H](C=3SC=C(N=3)C(=O)N[C@H](C=3SC=C(N=3)[C@H]1N=1)[C@@H](C)OC(=O)C3=CC(=C4C=C[C@H]([C@@H](C4=N3)O)N[C@H](C(N[C@@H](C)C(=O)NC(=C)C(=O)N[C@@H](C)C(=O)N2)=O)[C@@H](C)CC)[C@H](C)O)[C@](C)(O)[C@@H](C)O)=C\C)[C@@H](C)O)CC=1C1=NC(C(=O)NC(=C)C(=O)NC(=C)C(N)=O)=CS1 NSFFHOGKXHRQEW-AIHSUZKVSA-N 0.000 description 1
- 229930188070 thiostrepton Natural products 0.000 description 1
- NSFFHOGKXHRQEW-OFMUQYBVSA-N thiostrepton A Natural products CC[C@H](C)[C@@H]1N[C@@H]2C=Cc3c(cc(nc3[C@H]2O)C(=O)O[C@H](C)[C@@H]4NC(=O)c5csc(n5)[C@@H](NC(=O)[C@H]6CSC(=N6)C(=CC)NC(=O)[C@@H](NC(=O)c7csc(n7)[C@]8(CCC(=N[C@@H]8c9csc4n9)c%10nc(cs%10)C(=O)NC(=C)C(=O)NC(=C)C(=O)N)NC(=O)[C@H](C)NC(=O)C(=C)NC(=O)[C@H](C)NC1=O)[C@@H](C)O)[C@](C)(O)[C@@H](C)O)[C@H](C)O NSFFHOGKXHRQEW-OFMUQYBVSA-N 0.000 description 1
- OHKOGUYZJXTSFX-KZFFXBSXSA-N ticarcillin Chemical compound C=1([C@@H](C(O)=O)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)C=CSC=1 OHKOGUYZJXTSFX-KZFFXBSXSA-N 0.000 description 1
- 229960004659 ticarcillin Drugs 0.000 description 1
- 201000005882 tinea unguium Diseases 0.000 description 1
- 229960005053 tinidazole Drugs 0.000 description 1
- 229960000707 tobramycin Drugs 0.000 description 1
- NLVFBUXFDBBNBW-PBSUHMDJSA-N tobramycin Chemical compound N[C@@H]1C[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N NLVFBUXFDBBNBW-PBSUHMDJSA-N 0.000 description 1
- 229950003754 tolevamer Drugs 0.000 description 1
- 239000012049 topical pharmaceutical composition Substances 0.000 description 1
- 201000002516 toxic megacolon Diseases 0.000 description 1
- 235000010487 tragacanth Nutrition 0.000 description 1
- 239000000196 tragacanth Substances 0.000 description 1
- 229940116362 tragacanth Drugs 0.000 description 1
- 230000008733 trauma Effects 0.000 description 1
- 125000006168 tricyclic group Chemical group 0.000 description 1
- IEDVJHCEMCRBQM-UHFFFAOYSA-N trimethoprim Chemical compound COC1=C(OC)C(OC)=CC(CC=2C(=NC(N)=NC=2)N)=C1 IEDVJHCEMCRBQM-UHFFFAOYSA-N 0.000 description 1
- 229960001082 trimethoprim Drugs 0.000 description 1
- LWIHDJKSTIGBAC-UHFFFAOYSA-K tripotassium phosphate Chemical compound [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 description 1
- 229910000404 tripotassium phosphate Inorganic materials 0.000 description 1
- 235000019798 tripotassium phosphate Nutrition 0.000 description 1
- RYFMWSXOAZQYPI-UHFFFAOYSA-K trisodium phosphate Chemical compound [Na+].[Na+].[Na+].[O-]P([O-])([O-])=O RYFMWSXOAZQYPI-UHFFFAOYSA-K 0.000 description 1
- 229960005041 troleandomycin Drugs 0.000 description 1
- LQCLVBQBTUVCEQ-QTFUVMRISA-N troleandomycin Chemical compound O1[C@@H](C)[C@H](OC(C)=O)[C@@H](OC)C[C@@H]1O[C@@H]1[C@@H](C)C(=O)O[C@H](C)[C@H](C)[C@H](OC(C)=O)[C@@H](C)C(=O)[C@@]2(OC2)C[C@H](C)[C@H](O[C@H]2[C@@H]([C@H](C[C@@H](C)O2)N(C)C)OC(C)=O)[C@H]1C LQCLVBQBTUVCEQ-QTFUVMRISA-N 0.000 description 1
- 241001148471 unidentified anaerobic bacterium Species 0.000 description 1
- 210000002438 upper gastrointestinal tract Anatomy 0.000 description 1
- 239000002966 varnish Substances 0.000 description 1
- 235000015112 vegetable and seed oil Nutrition 0.000 description 1
- 239000008158 vegetable oil Substances 0.000 description 1
- 235000013311 vegetables Nutrition 0.000 description 1
- 230000003612 virological effect Effects 0.000 description 1
- 230000001018 virulence Effects 0.000 description 1
- 238000005406 washing Methods 0.000 description 1
- XOOUIPVCVHRTMJ-UHFFFAOYSA-L zinc stearate Chemical compound [Zn+2].CCCCCCCCCCCCCCCCCC([O-])=O.CCCCCCCCCCCCCCCCCC([O-])=O XOOUIPVCVHRTMJ-UHFFFAOYSA-L 0.000 description 1
- 150000003952 β-lactams Chemical class 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/444—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a six-membered ring with nitrogen as a ring heteroatom, e.g. amrinone
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/20—Two benzimidazolyl-2 radicals linked together directly or via a hydrocarbon or substituted hydrocarbon radical
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/4427—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems
- A61K31/4439—Non condensed pyridines; Hydrogenated derivatives thereof containing further heterocyclic ring systems containing a five-membered ring with nitrogen as a ring hetero atom, e.g. omeprazole
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/12—Antidiarrhoeals
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/04—Antibacterial agents
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D235/00—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings
- C07D235/02—Heterocyclic compounds containing 1,3-diazole or hydrogenated 1,3-diazole rings, condensed with other rings condensed with carbocyclic rings or ring systems
- C07D235/04—Benzimidazoles; Hydrogenated benzimidazoles
- C07D235/18—Benzimidazoles; Hydrogenated benzimidazoles with aryl radicals directly attached in position 2
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D401/00—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom
- C07D401/14—Heterocyclic compounds containing two or more hetero rings, having nitrogen atoms as the only ring hetero atoms, at least one ring being a six-membered ring with only one nitrogen atom containing three or more hetero rings
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02A—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE
- Y02A50/00—TECHNOLOGIES FOR ADAPTATION TO CLIMATE CHANGE in human health protection, e.g. against extreme weather
- Y02A50/30—Against vector-borne diseases, e.g. mosquito-borne, fly-borne, tick-borne or waterborne diseases whose impact is exacerbated by climate change
Landscapes
- Chemical & Material Sciences (AREA)
- Health & Medical Sciences (AREA)
- Organic Chemistry (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Medicinal Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Life Sciences & Earth Sciences (AREA)
- Epidemiology (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Oncology (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Communicable Diseases (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Plural Heterocyclic Compounds (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicinal Preparation (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
Abstract
USO DE COMPOSTOS ANTIBACTERIANOS, COMPOSIÇÃO FARMACÊUTICA E COMBINAÇÃO COMPREENDENDO OS MESMOS. Apresente invenção refere-se aos compostos de fómula (I): os quais são de uso no tratamento de doenças e infecções bacterianas, a composições contendo estes compostos e a métodos de tratar doenças e infecções bacterianas usando os compostos. Em particular, os compostos são úteis para o tratamento de infecção com, e doenças causadas por, clostridium difficile.
Description
[001] A presente invenção refere-se a compostos os quais são de uso no tratamento de doenças e infecções bacterianas, a composições contendo estes compostos e a métodos de tratar doenças e infecções bacterianas usando os compostos. Em particular, os compostos da presente invenção são úteis para o tratamento de infecção com, e doenças causadas por, Clostridium difficile.
[002] O desenvolvimento de fármacos antibacterianos representa um dos avanços médicos mais importantes do século XX. Doenças previamente intratáveis podem agora ser prontamente controladas e se imaginou que muitas doenças seriam erradicadas com estes novos fármacos milagrosos. Apesar destes significativos avanços no tratamento, doenças infecciosas são a terceira causa principal de mortalidade nos Estados Unidos (Clin. Infect. Dis., 2004, 38, 12791286) e permanecem um dos problemas de saúde global mais importantes. As taxas de resistência em todas as principais bactérias patogênicas estão aumentando dramaticamente e é de particular interesse o número crescente e a gravidade das infecções nosocomiais (Infectious Disease Society of America, 2004, Bad Bugs, No Drugs). O surgimento de patógenos resistentes a multifármacos tem tornado muitos dos fármacos de linha de frente correntes completamente ineficazes no controle de muitas doenças.
[003] Um subgrupo particular de patógenos bacterianos de interesse é o daqueles classificados como bactérias formadoras de esporos. Esporos bacterianos (endosporos) são estruturas inativas, não-reprodutivas formadas por bactérias em resposta a stress ambiental. Um a vez que condições ambientais se tornam favoráveis, os esporos germinam e as bactérias proliferam. No caso de bactérias patogênicas, germinação em um hospedeiro humano pode resultar em doença.
[004] Esporos bacterianos são extremamente tolerantes a muitos agentes e condições ambientais incluindo radiação, dessecação, temperatura, inanição e agentes químicos. Esta tolerância natural a agentes químicos possibilita esporos persistentes por muitos meses em ambientes-chave tais como hospitais, outros centros de tratamento de saúde e instalações de produção de alimentos, onde agentes de limpeza de rotina, germicidas e processos de esterilização não erradicam as bactérias. No caso da produção de alimentos, a presença de esporos pode ter importantes consequências variando desde simples resíduo de alimento até a disseminação de patógenos transportados por alimentos e envenenamento alimentar. Mais recentemente, foi atraída atenção para os riscos associados com os esporos de Bacillus anthracis, o agente causador do anthrax. Os esporos podem ser prontamente preparados como um pó seco que pode ser disseminado por numerosos métodos e usado como um agente bioterrorista. Anthrax é considerado o agente bioterrorista único mais preocupante (CDC Emerg. Infect. Dis., 2004, 5 (4), 552-555). Isto pode ser salientado pelos ataques postais do anthrax nos Estados Unidos em 2001. Houve 22 infecções confirmadas resultando em 5 mortes com o custo de limpeza e descontaminação depois dos ataques estimados em 1 bilhão de dólares.
[005] Importantes bactérias formadoras de esporos são as bactérias formadoras de endosporos Gram-positivasdos gêneros Bacillus e Clostridium. Exemplos do gênero Bacillus de interesse de saúde para humanos incluem, mas não estão limitadas a, 6. anthracis e B. cereus. Bacillus anthracis é de particular interesse como o agente causador do anthrax. A infecção por anthrax pode ocorrer através de ingestão, inalação ou contato cutâneo com esporos de Bacillus anthracis resultando em três formas clínicas distintas. Infecção cutânea é responsável por cerca de 95% de todas as infecções e geralmente é bem controlada com o uso de antibióticos adequados. Cerca de 20% dos casos não tratados de anthrax cutâneo resultarão em morte. Infecção intestinal é caracterizada por uma inflamação aguda do trato intestinal resultando em náusea, perda de apetite, vômito, febre, dor abdominal, vômito de sangue e diarréia severa. Anthrax intestinal resulta em morte em 25% a 60% dos casos. A forma mais grave da doença é anthrax pulmonar o qual frequentemente é fatal, mesmo com administração de antibióticos agressiva e a tempo. A capacidade para dispersar prontamente esporos de anthrax através do ar e sobre uma ampla área para induzir anthrax pulmonar torna o anthrax o agente de bioterrorismo primário.
[006] Membros do gênero Clostridium são anaeróbios obrigatórios Gram-positivos, formadores de esporos. Espécies exemplares causadoras de doença humana incluem, mas não estão limitadas a, C. perfríngens, C. tetani, C. botulinium, C. sordellii e C. difficile. Clostrídios estão associados com diversas doenças humanas incluindo tétano, gangrena gasosa, botulismo e colite pseudomembranosa e pode ser um agente causador em envenenamento alimentar.
[007] De particular interesse é doença causada por Clostridium difficile. Clostridium difficile causa doenças associadas com Clostridium difficile (CDAD) e tem havido um aumento de dez vezes no número de casos dentro dos últimos 10 anos, com cepas hipervirulentas e resistentes a fármacos agora se tornando endêmicas. Recentes números do HPA mostram que houve 55.681 casos de infecção por C. difficile em pacientes com idades de 65 anos e acima na Inglaterra em 2006 (até 8% no ano anterior). Talvez mais preocupantes sejam os casos de doenças associadas com Clostridium difficile sem aplicação de antibiótico subjacente agora sendo reportados.
[008] Clostridium difficile é uma bactéria entérica comensal, cujos níveis são mantidos sob controle pela flora intestinal normal. No entanto, a bactéria é o agente causador de doença associada com C. difficile (CDAD) e tem sido identificada como a causa primária da manifestação mais grave de doença associada com Clostridium difficile, colite pseudomembranosa. A CDAD está associada com uma ampla gama de sintomas variando desde diarréia branda até colite pseudomembranosa, megacólon tóxico e morte. O fator de risco primário para o desenvolvimento de doença associada com Clostridium difficile é o uso de antibióticos perturbando a flora bacteriana entérica normal causando um crescimento excessivo de Clostridium difficile. Embora clindamicina seja o principal antibiótico associado com CDAD, a doença é agora associada com quase todos os antibióticos incluindo membros das classes das fluoroquinolonas, das cefalosporinas, dos macrolídeos, das P-lactamas e muitas outras classes.
[009] A doença associada com Clostridium difficile é essencialmente 5 de interesse no cenário hospitalar e é de particular interesse entre pacientes idosos onde as taxas de mortalidade são particularmente elevadas. As taxas reportadas de doença associada com Clostridium difficile aumentaram dramaticamente nos últimos anos com mais de 55.000 casos reportados no Reino Unido em 2006 (Health Protection Agency Surveillance of Healthcare Associated Infections Report2007).
[0010] As taxas de mortalidade nos Estados Unidos subiram de 5,7 por milhão da população em 1999 para 23,7 por milhão em 2004. As taxas de colonização de C. difficile na população geral são de até 3% embora hospitalisação aumente dramaticamente as taxas de colonização até 25%. De particular interesse é o surgimento de novas cepas endêmicas. Um exemplo particularmente pertinente é a cepa hipervirulenta BI/NAP1 (também conhecida como ribotipo 027) a qual apresenta aumentada produção de toxina A e B bem como a produção de novas toxinas binárias adicionais.
[0011] Um fator crucial associado com clostrídios são as altas taxas de esporos bacterianos presentes em ambientes hospitalares. Foi demonstrado recentemente que muitos dos agentes de limpeza hospitalar de rotina em aplicação são ineficazes para erradicar esporos de clostrídios do ambiente resultando em controle de doença ineficaz (Infect Cont. Hosp. Epidemiol., 2007, 28, 920-5). As características de hiperesporulação de cepas tais como BI/NAP1 contribuem significativamente para a questão.
[0012] Embora os fatores de risco primário associados com CDAD sejam uso de antibiótico subjacente e idade (CMAJ, 2008, 179 (8), 767-772; J. Antimicrob. Chem., 2003, 51, 1339-1350) existem numerosos outros fatores associados incluindo, por exemplo, o uso de inibidores da bomba de prótons, uso de antagonistas de receptores de H2, uso de diuréticos, duração da permanência hospitalar, uso de tubos de alimentação, ventilação mecânica e comorbidade subjacente.
[0013] A acidez gástrica é parte do mecanismo de defesa natural contra patógenos ingeridos e qualquer redução na acidez do estômago pode resultar em colonização do trato gastrointestinal superior normalmente estéril a qual pode resultar em um distúrbio da microflora entérica normal. Deste modo, o uso de agentes supressores do ácido gástrico, tais como inibidores da bomba de prótons (PPIs) e antagonistas de receptores de H2 de histamina (H2RAs) está associado com um risco aumentado de colonização por C. difficile e subsequente desenvolvimento de CDAD. O uso de PPIs e H2RAs foi associado previamente com outras infecções entéricas tais como diarréia do viajante, salmonelose e cólera. Dial et al. reportaram que o risco de doença associada com Clostridium difficile aumenta com o uso de agentes supressores do ácido gástrico tanto em cenários de comunidade (JAMA, 2005, 294(23), 2989-2995) quanto hospitalar (CMAJ, 2004, 171(1), 33-38).
[0014] Os inibidores da bomba de prótons incluem, mas não estão limitados a, omeprazol (Losec, Prilosec, Zegerid), lansoprazol (Prevacid, Zoton, Inhibitol), esomeprazol (Nexium), pantoprazol (Protonix, Somac, Pantoloc, Pantozol, Zurcal, Pan) e rabeprazol (Rabecid, Aciphex, Pariet, Rabeloc).
[0015] H2RAs incluem, mas não estão limitados a, cimetidina (Tagamet), ranitidina (Zinetac, Zantac), famotidina, (Pepcidine, Pepcid), roxatidina (Roxit) e nizatidina (Tazac, Axid).
[0016] Tripla terapia com PPIs ou H2RAs junto com uma combinação de dois antibióticos é um tratamento reconhecido para a erradicação de infecções por Helicobacter pylori (Aliment. Pharmacol. Ther., 2001, 15(5), 613-624; Helicobacter., 2005, 10 (3), 157-171). No entanto, existem uns poucos relatórios de que este regime de tripla terapia pode levar a efeitos colaterais de doença associada com Clostridium difficile (Am. J. Gastroenterol., 1998, 93(7), 1175-1176; J. Int. Med., 1998, 243(3), 251-253; Aliment. Pharm. Ther., 2001, 15(9), 1445-1452; Med. Sei. Monit., 2001, 7(4), 751-754). Antibacterianos típicos usados para tratar infecções por Helicobacter pylori são uma combinação de agentes selecionados entre, mas não limitados a metronidazol, amoxicilina, levofloxacina e claritromicina - muitos dos quais são fortemente associados com o desenvolvimento de CDAD.
[0017] As terapias correntes são extremamente limitadas; particularmente em vista do fato de que quase todas as classes de antibióticos são associadas com causar a doença. O único fármaco aprovado pela agência americana FDA para tratamento de doença associada com Clostridium difficile é vancomicina embora metronidazol também seja usado extensivamente. O uso disseminado de vancomicina para o tratamento de doença associada com Clostridium difficile é de interesse devido a sua ação bacteriostática contra clostrídios, seu custo relativamente elevado e a possível seleção de cepas de C. difficile resistentes bem como outras bactérias (particularmente Enterococcus spp.). Uma questão-chave tanto com metronidazol quanto com vancomicina é a alta taxa de recidiva com no mínimo 20% dos pacientes experimentando no mínimo um episódio recorrente. Propõe-se que ocorra recidiva devido à incapacidade de erradicar os esporos de clostrídio durante terapia resultando em crescimento excessivo subsequente para um estado patogênico. Esta incapacidade para controlar a formação de esporos possibilita contaminação contínua do ambiente hospitalar. Deste modo, agentes com capacidade para erradicar células vegetativas e controlar endosporos seriam de significativa vantagem.
[0018] A opção de terapia primária para o tratamento de doença associada com Clostridium difficile é descontinuação de qualquer tratamento antimicrobiano corrente seguida por aplicação apropriada de quer vancomicina ou metronidazol. Ambos os agentes são geralmente administrados por via oral embora metronidazol também possa ser administrado por via intravenosa e em caso graves, vancomicina também pode ser administrada através de numerosas outras vias incluindo intracolônica, através de tubo gástrico nasal ou como um enema de retenção de vancomicina. Agentes antibióticos adicionais que foram reportados para serem usados no tratamento de doença associada com Clostridium difficile incluem ácido fusídico, rifamicina e seus análogos, teicoplanina e bacitracina embora nenhum apresente eficácia em particular em relação à vancomicina ou ao metronidazol. Além de parar qualquer tratamento antibacteriano agressor, o uso de agentes antiperistálticos, opiáceos, ou loperamida deve ser evitado uma vez que eles podem reduzir a desobstrução das toxinas de C. difficile e exacerbar lesão colônica mediada por toxina. Os agentes referidos também podem precipitar íleo e causar dilatação tóxica do cólon (J. Med. Microbiol., 2005, 54, 101-111; JA-MA, 1993, 269, 71-5; Postgrad. Med. J.,1990, 66(777), 582).
[0019] Terapias alternativas, usadas como agentes isolados de rotina ou em combinação com antibacterianos, têm por alvo ou tentar restabelecer a população de micro-organismos intestinais nativos, reduzindo os níveis de toxinas de C. difficile ou estimular o sistema imune (para revisões vide Antibiotic Treatment for Clostridium - Associated Diarrhea in Adults (N.T.: Tratamento Antibiótico para Diarréia Associada com Clostridium difficile em Adultos), Cochrane Database of Systematic Reviews 2007, Issue 3. Art. N°: CD004610.; Clin. Inf. Dis., 2008, 46(S1), S32-S42; Clin. Inf. Dis., 2007, 45(S2), S122-S128; J. Med. Microbiol., 2005, 54, 101-111 e referências nos mesmos). Deste modo, terapias alternativas contra doença associada com Clostridium difficile incluem provisão de Saccharomyces boulardii ou Lactobacillus acidophilus em combinação com antibióticos, transplantação fecal e em casos graves onde todas as outras opções de terapias falharam, cirurgia. Embora as taxas de colectomia sejam baixas (até 3% dos casos) está associada com altas taxas de mortalidade (até 60%).
[0020] Deste modo, existe uma necessidade premente de agentes novos e eficazes para tratar doenças associadas com bactérias formadoras de esporos, particularmente aquelas causadas por membros dos gêneros Clostridium e Bacillus e em particular doença associada com infecção por Clostridium difficile. Esta necessidade é particularmente aguda à luz da natureza refratária do Clostridium difficile para muitos antibióticos de amplo espectro (incluindo antibióticos de p-lactama e de quinolona) e a frequência com a qual surge resistência (Antimicrob. Agents Chemother., 1985, 28(6): 842-844).
[0021] As publicações de patente internacional N°s WO 2007/056330, WO 2003/105846 e WO 2002/060879 revelam vários 2-amino benzimidazóis como agentes antibacterianos.
[0022] A publicação de patente internacional N° WO 2007/148093 revela vários 2-amino benzotiazóis como agentes antibacterianos.
[0023] As publicações de patente internacional N°s WO 2006/076009, WO 2004/041209 e Bowser et al. (Bioorg. Med. Chem. Lett., 2007, 17, 5652-5655) revelam vários compostos de benzimidazóis substituídos úteis como anti-infectivos que reduzem a resistência, virulência, ou crescimento de micróbios. Diz-se que os compostos não apresentam atividade antimicrobiana intrínseca in vitro.
[0024] A patente dos Estados Unidos N° US 5.824.698 revela vários di-benzimidazóis como antibióticos de amplo espectro, revelando atividade tanto contra bactérias Gram- negativas quanto contra Gram-positivas, incluindo Staphylococcus spp. e Enterococcus spp. No entanto, este documento não revela atividade contra bactérias anaeróbicas formadoras de esporos e em particular não revela atividade contra qualquer Clostridium spp. (incluindo C. difficile).
[0025] O requerimento de patente dos Estados Unidos N° US 2007/0112048 A1 revela várias bi- e triarilimidazolidinas e bi- e triarilamidinas como antibióticos de amplo espectro, revelando atividade contra tanto contra bactérias Gram-negativas quanto contra Gram- positivas, incluindo Staphylococcus spp., Enterococcus spp. e Clostridium spp. No entanto, este documento não revela compostos de fórmula geral (I) conforme descrito aqui, neste requerimento de patente.
[0026] Chaudhuri et al. (J.Org. Chem., 2007, 72, 1912-1923) descrevem vários bis-2-(piridil)-1H-benzimidazóis (incluindo compostos de fórmula I conforme descrito aqui, neste requerimento de patente) como agentes de ligação de DNA. Este documento não fala quanto a potencial atividade antibacteriana.
[0027] Portanto, em um primeiro aspecto da presente invenção, é proporcionado um composto de fórmula geral (I): em que: L1 é uma ligação direta ou um grupo ligante; R1 e R2 são cada um de modo independente selecionados entre H e C1-6 alquila, arila, heteroarila, carbociclila e heterociclila opcionalmente substituídos, a substituição opcional sendo com um ou mais substituintes selecionados entre halo, CN, NO2, R6, OR6, N(R6)2, COR6, CO2R6, SO2R6, NR7COR6, NR7CO2R6, NR7SO2R6, NR7CONR6R7, CONR6R7 e SO2NR6R7, contanto que no mínimo um de R1 e R2 seja cíclico; CadaR5é selecionadodemodoindependente entre H, halo, C1-6 alquila, OR7, N(R7)2, CN e NO2; X1 eX2 são cada umdemodoindependente selecionados entre N e CR3; X3 é selecionado entre NR4, O e S; X4 é NH; e R3 é selecionado entre H, halo e C1-6 alquila; R4 é selecionado entre H e C1-6 alquila; R6 é selecionado entre H, C1-6 alquila, C2-C6 alquenila, C2-C6 alquinila, C4-C7 carbociclila, C4-C7 heterociclila e arila ou heteroarila de 5 ou de 6 membros, qualquer um dos quais pode ser opcionalmente substituído com um ou mais átomos de halo; e R7 é selecionado entre hidrogênio e C1-C4 alquila, qualquer um dos quais é opcionalmente substituído com um ou mais átomos de halo; ou um N-óxido farmaceuticamente aceitável, sal, hidrato, solvato, complexo, bioisóstere, metabólito ou profármaco do mesmo, opcionalmente para o tratamento de uma infecção com, ou doença causada por, uma bactéria.
[0028] Alguns dos compostos de fórmula geral (I) são novos. Portanto, de acordo com a invenção, também foram proporcionados os compostos de fórmula geral (I) os quais são novos, junto com processos para sua preparação, composições contendo os mesmos, bem como seu uso como farmacêuticos.
[0029] Portanto, em outro aspecto, é proporcionado um composto de fórmula geral (I) em que: L1 é uma ligação direta ou um átomo ou grupo ligante; R1 e R2 são cada um de modo independente selecionados entre H e C1-6 alquila, arila, heteroarila, carbociclila e heterociclila opcionalmente substituídos, a substituição opcional sendo com um ou mais substituintes selecionados entre halo, CN, NO2, R6, OR6, N(R6)2, COR6, CO2R6, SO2R6, NR7COR6, NR7CO2R6, NR7SO2R6, NR7CONR6R7, CONR6R7 e SO2NR6R7, contanto que no mínimo um de R1 e R2 seja cíclico; CadaR5é selecionadodemodoindependente entre H, halo, C1-6 e alquila, OR7, N(R7)2, CN e NO2; X1 eX2são cada umdemodoindependente selecionados entre N e CR3; X3 é selecionado entre NR4, O e S; X4 é NH; e R3 é selecionado entre H, halo e C1-6 alquila; R4 é selecionado entre H e C1-6 alquila; R6 é selecionado entre H, C1-6 alquila, C2-C6 alquenila, C2-C6 alquinila, C4-C7 carbociclila, C4-C7 heterociclila e arila ou heteroarila de 5 ou de 6 membros, qualquer um dos quais pode ser opcionalmente substituído com um ou mais átomos de halo; e R7 é selecionado entre hidrogênio e C1-C4 alquila, qualquer um dos quais é opcionalmente substituído com um ou mais átomos de halo; ou um N-óxido farmaceuticamente aceitável, sal, hidrato, solvato, complexo, bioisóstere, metabólito ou profármaco do mesmo. L1 pode ser opcionalmente selecionado entre O, S, SO2, NR7, C(R7)2 e C=O.
[0030] O composto conforme definido acima pode ser para uso em terapia ou profilaxia, por exemplo, no tratamento de uma infecção ou doença bacteriana.
[0031] Em outro aspecto, é proporcionado um método de tratar uma infecção bacteriana ou doença bacteriana em um indivíduo compreendendo administrar uma quantidade eficaz de um composto conforme definido acima ao indivíduo referido.
[0032] Em outro aspecto, é proporcionado um método de matar uma bactéria ou inibir, reduzir ou prevenir o crescimento da mesma, compreendendo contactar a referida bactéria com um composto conforme definido acima.
[0033] Também são contempladas combinações compreendendo o composto da invenção conforme definido acima com vários agentes adjuvantes conforme definido abaixo.
[0034] Ainda outros aspectos da invenção são definidos nas reivindicações determinadas abaixo.
[0035] Todas as publicações, patentes, requerimentos de patente e outras referências mencionadas aqui, neste requerimento de patente, são por este incorporados por meio de referência em suas totalidades para todos os fins como se cada publicação, patente ou requerimento de patente individual fossem especificamente e individualmente indicados para serem incorporados por meio de referência e o conteúdo do mesmo citado na totalidade.
[0036] Onde usado aqui, neste requerimento de patente, e a menos que especificamente indicado de modo diverso, pretende-se que os seguintes termos tenham os seguintes significados além de quaisquer significados mais amplos (ou menos amplos) que os termos possam ter na técnica:
[0037] A menos que requerido de modo diverso pelo contexto, o uso do singular aqui, neste requerimento de patente, deve ser lido como incluindo o plural e vice versa. O termo “um” ou “uma” usados em relação a uma entidade deve ser lido como se referindo a uma ou mais daquela entidade. Deste modo, os termos “um” (ou “uma”), “um ou mais,” e “no mínimo um” são usados de modo intercambiável aqui, neste requerimento de patente.
[0038] Conforme usado aqui, neste requerimento de patente, o termo “compreendem,” ou variações do mesmo tais como “compreende” ou “compreendendo,” devem ser lidos como indicando a inclusão de qualquer inteiro mencionado (por exemplo, um aspecto, elemento, característica, propriedade, etapa do método / processo ou limitação) ou grupo de inteiros (por exemplo, aspectos, elemento, características, propriedades, etapas do método / processo ou limitações) mas não a exclusão de qualquer outro inteiro ou grupo de inteiros. Deste modo, conforme usado aqui, neste requerimento de patente, o termo “compreendendo” é inclusivo ou em aberto e não exclui inteiros ou etapas do método / processo adicionais, não mencionados.
[0039] A expressão “consistindo essencialmente de” é usada aqui, neste requerimento de patente, para requerer o um ou mais inteiros especificados ou etapas bem como aqueles os quais não afetam materialmente o caráter ou função da invenção reivindicada.
[0040] Conforme usado aqui, neste requerimento de patente, o termo “consistindo” é usado para indicar a presença do inteiro mencionado (por exemplo, um aspecto, elemento, característica, propriedade, etapa do método / processo ou limitação) ou grupo de inteiros (por exemplo, aspectos, elemento, características, propriedades, etapas do método / processo ou limitações) exclusivamente.
[0041] Conforme usado aqui, neste requerimento de patente, o termo “doença” é usado para definir qualquer condição anormal que prejudica a função fisiológica e está associada com sintomas específicos. O termo é usado amplamente para englobar qualquer distúrbio, doença, anormalidade, patologia, enfermidade, condição ou síndrome na qual a função fisiológica é prejudicada independente da natureza da etiologia (ou na verdade se a base etiológica para a doença é estabelecida). Portanto engloba condições originárias de trauma, lesão, cirurgia, ablação radiológica, envenenamento ou deficiências nutricionais.
[0042] Conforme usado aqui, neste requerimento de patente, o termo “doença bacteriana” se refere a qualquer doença que envolve (por exemplo, é causada, exacerbada, associada com ou caracterizada pela presença de) uma bactéria residente e/ou replicando no corpo e/ou células de um indivíduo. O termo, portanto, inclui doenças causadas ou exacerbadas por toxinas bacterianas (as quais também podem ser referidas aqui, neste requerimento de patente, como “intoxicação bacteriana”).
[0043] Conforme usado aqui, neste requerimento de patente, o termo doença associada com Clostridium difficile (CDAD) é usado para definir qualquer doença que envolve (por exemplo, é causada, exacerbada, associada com ou caracterizada pela presença de) Clostridium difficile residente e/ou replicando no corpo de um indivíduo. Deste modo, o termo cobre qualquer doença, distúrbio, patologia, sintoma, condição clínica ou síndrome na qual bactérias da espécie Clostridium difficile agem como agentes etiológicos ou na qual infecção com uma ou mais cepas de Clostridium difficile estão implicadas, são detectadas ou envolvidas. O termo, portanto, inclui as várias formas de colite, colite pseudomembranosa, diarréia e doença associada com antibiótico.
[0044] Conforme usado aqui, neste requerimento de patente, o termo “infecção bacteriana” é usado para definir uma condição na qual um indivíduo é infectado com uma bactéria. A infecção pode ser sintomática ou assintomática. No último caso, o indivíduo pode ser identificado como infectado com base em vários testes, incluindo, por exemplo, testes bioquímicos, testes sorológicos, cultura microbiológica e/ou microscopia.
[0045] Os termos bacteriostático e bactericida são termos da técnica usados para definir a capacidade para prevenir (ou reduzir a taxa de) crescimento bacteriano e para mediar (diretamente ou indiretamente) a destruição celular de células bacterianas, respectivamente. Os termos não são mutuamente exclusivos, e muitos agentes exercem tanto efeitos bacteriostáticos quanto bactericidas (em alguns casos em uma maneira dose-específica ou alvo- específica). Em geral, agentes bactericidas produzem melhores resultados terapêuticos e são preferenciais.
[0046] Conforme usado aqui, neste requerimento de patente, o termo “antibiótico de amplo espectro” define um agente o qual é bactericida e/oubacteriostático para uma gama de bactérias incluindo tanto bactérias Gram-positivas quanto Gram-negativas.
[0047] O termo “multifármaco resistente” (MDR) conforme aplicado a uma bactéria aqui, neste requerimento de patente, define uma bactéria a qual é resistente a duas ou mais classes de antibióticos incluindo, mas não limitados a, antibióticos selecionados entre penicilina, meticilina, quinolona, macrolídeo e/ou vancomicina.
[0048] Conforme usado aqui, neste requerimento de patente, o termo “tratamento” ou “tratar” se refere a uma intervenção (por exemplo, a administração de um agente a um indivíduo) a qual cura, melhora ou reduz os sintomas de uma doença ou remove (ou reduz o impacto de) sua ou suas causas (por exemplo, a bactéria causadora). Neste caso, o termo é usado de modo sinônimo com o termo “terapia”. Deste modo, o tratamento de infecção de acordo com a invenção pode ser caracterizado pela ação (direta ou indireta) bacteriostática e/ou bactericida dos compostos da invenção.
[0049] Adicionalmente, os termos “tratamento” ou “tratar” se refere a uma intervenção (por exemplo, a administração de um agente a um indivíduo) a qual previne ou retarda o início ou a progressão de uma doença ou reduz (ou erradica) sua incidência dentro de uma população tratada. Neste caso, o termo tratamento é usado de modo sinônimo com o termo “profilaxia”.
[0050] O termo “indivíduo” (o qual deve ser lido como incluindo “indivíduo”, “animal”, “paciente” ou “mamífero” onde o contexto permite) define qualquer indivíduo, particularmente um indivíduo mamífero, para o qual tratamento está indicado. Indivíduos mamíferos incluem, mas não estão limitados a, seres humanos, animais domésticos, animais de criação, animais de zoológico, animais de competição, animais de estimação tais como cães, gatos, porquinhos da índia, coelhos, ratos, camundongos, cavalos, gado, vacas; primatas tais como símios, macacos, orangotangos, e chimpanzés; canídeos tais como cães e lobos; felídeos tais como gatos, leões, e tigres; equídeos tais como cavalos, jumentos, e zebras; animais para alimento tais como vacas, porcos, e carneiro; ungulados tais como veados e girafas; roedores tais como camundongos, ratos, hamsters e porquinhos da índia; e assim por diante. Em preferenciais modalidades, o indivíduo é um ser humano, por exemplo, uma criança humana.
[0051] O termo bactéria Gram-positiva é um termo da técnica definindo uma classe particular de bactérias que são agrupadas juntas com base em algumas características de coloração da parede celular.
[0052] O termo bactéria Gram-positiva de baixo G+C Gram-positive bactéria (low G+C Gram-positive bacterium) é um termo da técnica definindo uma classe de subclasse particular de bactérias evolucionariamente relacionadas dentro das Gram-positivas com base na composição das bases no DNA. A subclasse inclui Streptococcus spp., Staphylococcus spp., Listeria spp., Bacillus spp., Clostridium spp., Enterococcus spp. e Lactobacillus spp.
[0053] O termo “concentração inibitória mínima” ou “MIC” define a menor concentração de um composto de teste que é necessário para inibir o crescimento de um isolado bacteriano in vitro. Um método comum para determinar a concentração inibitória mínima de um antibiótico é preparar vários tubos contendo diluições seriais do composto de teste que são então inoculados com o isolado bacteriano de interesse. Depois de incubação em atmosfera e temperatura apropriadas, a concentração inibitória mínima de um antibiótico pode ser determinada a partir do tubo com a menor concentração que não apresenta turvação.
[0054] Conforme usado aqui, neste requerimento de patente, o termo “combinação”, conforme aplicado a dois ou mais compostos e/ou agentes (também referidos aqui, neste requerimento de patente, como os componentes), pretende definir material no qual os dois ou mais compostos / agentes são associados. Os termos “combinados” e “combinar” neste contexto devem ser interpretados de acordo.
[0055] A associação dos dois ou mais compostos / agentes em uma combinação pode ser física ou não física. Exemplos de compostos / agentes combinados fisicamente associados incluem: •composições (por exemplo, formulações unitárias) compreendendo os dois ou mais compostos / agentes em mistura (por exemplo, dentro da mesma unidade de dose); •composições compreendendo material no qual os dois ou mais compostos / agentes são quimicamente / fisicoquimicamente encadeados (por exemplo, por reticulação, aglomeração molecular ou ligação a uma porção de veículo comum); •composições compreendendo material no qual os dois ou mais compostos / agentes são quimicamente / físico- quimicamente coembalados (por exemplo, dispostos sobre ou dentro de vesículas de lipídeos, partículas (por exemplo, micro- ou nanopartículas) ou gotículas de emulsão); •kits farmacêuticos, embalagens farmacêuticas ou embalagens para pacientes nas quais os dois ou mais compostos / agentes são coembalados ou coapresentados (por exemplo, como parte de uma série de unidades de doses);
[0056] Exemplos de compostos / agentes combinados não fisicamente associados incluem: •material (por exemplo, uma formulação não unitária) compreendendo no mínimo um dos dois ou mais compostos / agentes junto com instruções para a associação extemporânea do no mínimo um composto / agente para formar uma associação física dos dois ou mais compostos / agentes; •material (por exemplo, uma formulação não unitária) compreendendo no mínimo um dos dois ou mais compostos / agentes junto com instruções para terapia de combinação com os dois ou mais compostos / agentes; •material compreendendo no mínimo um dos dois ou mais compostos / agentes junto com instruções para administração a uma população de pacientes na qual o(s) outro(s) dos dois ou mais compostos / agentes foram (ou estão sendo) administrados; •material compreendendo no mínimo um dos dois ou mais compostos / agentes em uma quantidade ou em uma forma a qual é especificamente adaptada para uso em combinação com o(s) outro(s) dos dois ou mais compostos / agentes.
[0057] Conforme usado aqui, neste requerimento de patente, o termo “terapia de combinação” pretende definir terapias as quais compreendem o uso de uma combinação de dois ou mais compostos / agentes (conforme definido acima). Deste modo, referências à “terapia de combinação”, “combinações” e o uso de compostos / agentes “em combinação” neste requerimento pode se referir a compostos / agentes que são administrados como parte do mesmo regime de tratamento global. Deste modo, a posologia de cada um dos dois ou mais compostos / agentes pode diferir: cada um pode ser administrado ao mesmo tempo ou em momentos diferentes. Portanto será reconhecido que os compostos / agentes da combinação podem ser administrados sequencialmente (por exemplo, antes ou depois) ou simultaneamente, quer na mesma formulação farmacêutica (isto é, juntos), ou em diferentes formulações farmacêuticas (isto é, separadamente). Simultaneamente na mesma formulação é como uma formulação unitária ao passo que simultaneamente em diferentes formulações farmacêuticas é não unitária. As posologias de cada um dos dois ou mais compostos / agentes em uma terapia de combinação também podem diferir com respeito à via de administração.
[0058] Conforme usado aqui, neste requerimento de patente, o termo “kit farmacêutico” define uma série de uma ou mais unidades de doses de uma composição farmacêutica junto com meios de dosagem (por exemplo, dispositivo de medição) e/ou meios de liberação (por exemplo, inalador ou seringa), opcionalmente todos contidos dentro de embalagem externa comum. Em kits farmacêuticos compreendendo uma combinação de dois ou mais compostos / agentes, os compostos / agentes individuais podem ser formulações unitárias ou não unitárias. A dose unitária ou doses unitárias podem ser contidas dentro de um blister. O kit farmacêutico adicionalmente pode compreender opcionalmente instruções para aplicação.
[0059] Conforme usado aqui, neste requerimento de patente, o termo “embalagem farmacêutica” define uma série de uma ou mais unidades de doses de uma composição farmacêutica, opcionalmente contidas dentro de embalagem externa comum. Em embalagens farmacêuticas compreendendo uma combinação de dois ou mais compostos / agentes, os compostos / agentes individuais podem ser formulações unitárias ou não unitárias. A dose unitária ou doses unitárias podem ser contidas dentro de um blister. A embalagem farmacêutica adicionalmente pode compreender opcionalmente instruções para aplicação.
[0060] Conforme usado aqui, neste requerimento de patente, o termo “embalagem para paciente” define uma embalagem, prescrita a um paciente, a qual contém composições farmacêuticas para todo o curso do tratamento. Embalagens para pacientes geralmente contêm um ou mais blisters. Embalagens para pacientes têm uma vantagem em relação às prescrições tradicionais, onde um farmacêutico divide o suprimento de um paciente de um fármaco de um suprimento em volume, em que o paciente sempre tem acesso à bula contida na embalagem do paciente, normalmente ausente nas prescrições para o paciente. Foi demonstrado que a inclusão de uma bula melhora a observância do paciente às instruções do médico.
[0061] As combinações da invenção podem produzir um efeito terapeuticamente eficaz em relação ao efeito terapêutico dos compostos / agentes individuais quando administrados separadamente.
[0062] Conforme usado aqui, neste requerimento de patente, uma quantidade eficaz ou uma quantidade terapeuticamente eficaz de um composto define uma quantidade que pode ser administrada a um indivíduo sem excessiva toxicidade, irritação, reação alérgica, ou outro problema ou complicação, comensurado com uma razoável proporção de risco/ benefício, mas uma proporção que é suficiente para proporcionar o efeito desejado, por exemplo, o tratamento ou profilaxia manifestados por uma melhora permanente ou temporária na condição do indivíduo. A quantidade variará de indivíduo para indivíduo, dependendo da idade e da condição geral do indivíduo, modo de administração e outros fatores. Deste modo, apesar de não ser possível especificar uma quantidade eficaz exata, os versados na técnica serão capazes de determinar uma quantidade “eficaz” apropriada em qualquer caso individual usando experimentação de rotina e conhecimento geral de antecedentes. Um resultado terapêutico neste contexto inclui erradicação ou redução de sintomas, redução de dor ou desconforto, prolongada sobrevida, aprimorada mobilidade e outros marcadores de melhora clínica. Um resultado terapêutico não precisa ser uma cura completa.
[0063] Conforme usado aqui, neste requerimento de patente, uma “quantidade profilaticamente eficaz” se refere a uma quantidade eficaz, em dosagens e por períodos de tempo necessários, para obter o resultado profilático desejado. Tipicamente, desde que uma dose profilática seja usada em indivíduos antes de ou em um estágio de doença inicial, a quantidade profilaticamente eficaz será menor do que a quantidade terapeuticamente eficaz.
[0064] O termo “eficaz” inclui efeitos vantajosos tais como aditividade, sinergismo, efeitos colaterais reduzidos, reduzida toxicidade ou aprimorada performance ou atividade. Vantajosamente, um efeito eficaz pode possibilitar que doses menores de cada ou um ou outro componente sejam administradas a um paciente, deste modo reduzindo a toxicidade, enquanto produzindo e/ou mantendo o mesmo efeito terapêutico. Um efeito sinérgico no presente contexto se refere a um efeito terapêutico produzido pela combinação que é maior do que a soma dos efeitos terapêuticos dos componentes da combinação quando apresentados individualmente. Um efeito aditivo no presente contexto se refere a um efeito terapêutico produzido pela combinação o qual é maior do que o efeito terapêutico de quaisquer dos componentes da combinação quando apresentados individualmente.
[0065] O termo “composto auxiliar” (ou “agente auxiliar”) conforme usado aqui, neste requerimento de patente, pretende definir qualquer composto o qual produz uma combinação eficaz (conforme definido aqui, neste requerimento de patente) quando combinado com um composto da invenção. O composto auxiliar pode, portanto, agir como um acessório para o composto da invenção, ou pode contribuir de modo diverso para a eficácia da combinação (por exemplo, produzindo um efeito sinérgico ou aditivo ou potencializando a atividade do composto da invenção).
[0066] O termo “adjuvante” conforme aplicado à aplicação dos compostos e combinações da invenção em terapia ou profilaxia define aplicações nas quais os materiais são administrados junto com um ou mais outros fármacos, intervenções, regimes ou tratamentos (tais como cirurgia e/ou irradiação). As terapias adjuvantes referidas podem compreender a administração / aplicação concomitante, separada ou sequencial dos materiais da invenção e o outro ou outros tratamentos. Portanto, em algumas modalidades, aplicação adjuvante dos materiais da invenção é refletida na formulação das composições farmacêuticas da invenção. Por exemplo, aplicação adjuvante pode ser refletida em uma dosagem unitária específica, ou em formulações nas quais o composto da invenção está presente em mistura com o outro ou os outros fármacos com os quais deve ser usado acessoriamente (ou ainda fisicamente associado com o outro ou os outros fármacos dentro de uma única unidade de dose). Em outras modalidades, aplicação adjuvante dos compostos ou composições da invenção pode ser refletida na composição dos kits farmacêuticos da invenção, em que o composto da invenção é coembalado (por exemplo, como parte de uma série de doses unitárias) com o outro ou os outros fármacos com os quais deve ser usado acessoriamente. Em ainda outras modalidades, aplicação adjuvante dos compostos da invenção pode ser refletida no contento da informação e/ou instruções coembaladas com o composto relativas a formulação e/ou posologia.
[0067] O termo derivado farmaceuticamente aceitável conforme aplicado aos compostos da invenção define compostos os quais são obtidos (ou obteníveis) por derivação química dos compostos de origem da invenção. Os derivados farmaceuticamente aceitáveis são, portanto, adequados para administração a ou aplicação em contato com tecidos de mamífero sem indevida toxicidade, irritação ou reação alérgica (isto é, comensurado com uma razoável proporção risco / benefício). Derivados preferenciais são os obtidos (ou obteníveis) por alquilação, esterificação ou acilação dos compostos de origem da invenção. Os derivados podem ser ativos per se, ou podem ser inativos até serem processados in vivo. No último caso, os derivados da invenção agem como profármacos. Profármacos particularmente preferenciais são derivados de ésteres os quais são esterificados em uma ou mais das hidroxilas livres e os quais são ativados por hidrólise in vivo. Outros profármacos preferenciais são compostos ligados de modo covalente os quais liberam o fármaco de origem ativo de acordo com a fórmula geral (I) depois de divagem da ligação ou ligações covalentes in vivo.
[0068] Os derivados farmaceuticamente aceitáveis da invenção conservam parte ou toda a atividade do composto de origem. Em alguns casos, a atividade é aumentada por derivação. Derivação também pode aumentar outras atividades biológicas do composto, por exemplo, biodisponibilidade.
[0069] O termo sal farmaceuticamente aceitável conforme aplicado aos compostos da invenção define qualquer sal de adição de ácido orgânico ou inorgânico não-tóxico do composto de base livre o qual é adequado para uso em contato com tecidos de mamífero sem indevida toxicidade, irritação, reação alérgica e os quais são comensurados com uma razoável proporção risco / benefício. Sais farmaceuticamente aceitáveis adequados são de conhecimento geral na técnica. Exemplos são os sais com ácidos inorgânico (por exemplo, ácidos clorídricos, bromídricos, sulfúricos e fosfóricos), ácidos carboxílicos orgânicos (por exemplo, ácido acético, propiônico, glicólico, láctico, pirúvico, malônico, succínico, fumárico, málico, tartárico, cítrico, ascórbico, maleico, hidroximaleico, diidroximaleico, benzoico, fenilacético, 4-aminobenzoico, 4-hidroxibenzoico, antranílico, cinâmico, salicílico, 2- fenoxibenzoico, 2-acetoxibenzoico e mandélico) e ácidos sulfônicos orgânicos (por exemplo, ácido metanossulfônico e ácido p-toluenossulfônico). Os compostos da invenção também podem ser convertidos em sais por reação com um haleto de metal de álcali, por exemplo, cloreto de sódio, iodeto de sódio ou iodeto de lítio. Preferencialmente, os compostos da invenção são convertidos em seus sais por reação com uma quantidade estequiométrica de cloreto de sódio na presença de um solvente tal como acetona.
[0070] Estes sais e os compostos de base livre podem existir quer em uma forma hidratada ou em uma forma substancialmente anídrica. Formas cristalinas dos compostos da invenção também são contempladas e em geral os sais de adição ácidos dos compostos da invenção são materiais cristalinos os quais são solúveis em água e vários solventes orgânicos hidrofílicos e os quais em comparação com suas formas de base livre, demonstram pontos de fusão superiores e uma solubilidade crescente.
[0071] O termo solvato farmaceuticamente aceitável conforme aplicado aos compostos da invenção define qualquer forma de solvato farmaceuticamente aceitável de um composto especificado que conserva a eficácia biológica de semelhante composto. Exemplos de solvatos incluem compostos da invenção em combinação com água (hidratos), isopropanol, etanol, metanol, sulfóxido dimetila, acetato de etila, ácido acético, etanolamina, ou acetona. Além disso, são incluídas formulações miscíveis de misturas de solvatos tais como um composto da invenção em combinação com uma mistura de acetona e etanol. Em uma modalidade preferencial, o solvato inclui um composto da invenção em combinação com cerca de 20% de etanol e cerca de 80% de acetona. Deste modo, as fórmulas estruturais incluem compostos tendo a estrutura indicada, incluindo as formas hidratadas bem como as formas não hidratadas.
[0072] O termo profármaco farmaceuticamente aceitável conforme aplicado aos compostos da invenção define qualquer composto farmaceuticamente aceitável que pode ser convertidos sob condições fisiológicas ou por solvólise para o composto especificado, para um sal farmaceuticamente aceitável de semelhante composto ou para um composto que compartilha no mínimo um pouco da atividade antibacteriana do composto especificado (por exemplo, apresentando atividade contra Clostridium difficile).
[0073] O termo metabólito farmaceuticamente aceitável conforme aplicado aos compostos da invenção define um produto farmacologicamente ativo produzido através do metabolismo no corpo do composto especificado ou sal do mesmo.
[0074] Profármacos e metabólitos ativos dos compostos da invenção podem ser identificados usando técnicas de rotina conhecidas na arte (vide, por exemplo, Bertolini et al., J. Med. Chem., 1997, 40, 2011-2016).
[0075] O termo complexo farmaceuticamente aceitável conforme aplicado aos compostos da invenção define compostos ou composições nos quais o composto da invenção forma uma parte do componente. Deste modo, os complexos da invenção incluem derivados nos quais o composto da invenção é fisicamente associado (por exemplo, por ligação covalente ou não covalente) a outra porção ou porções. O termo, portanto, inclui formas multiméricas dos compostos da invenção. Os multímeros referidos podem ser gerados por encadeação ou colocando múltiplas cópias de um composto da invenção em íntima proximidade um com o outro (por exemplo, através de uma porção de arcabouço ou de veículo).
[0076] O termo bioisóstere (ou simplesmente isóstere) é um termo da técnica usado para definir análogos de fármacos nos quais um ou mais átomos (ou grupos de átomos) foram substituídos com átomos de reposição (ou grupos de átomos) tendo características estéricas e/ou eletrônicas similares aos átomos os quais substituem. A substituição de um átomo de hidrogênio ou um grupo hidroxila com um átomo de flúor é uma substituição bioisostérica comumente empregada. Substituição-Sila (troca C/Si) é uma técnica relativamente recente para produzir isósteres. Esta abordagem envolve a substituição de um ou mais átomos de carbono específicos em um composto com silício (para uma revisão, vide o artigo de Tacke e Zilch em Endeavour, New Series, 1986, 10. 191-197). Os isósteres sila-substituídos (isósteres de silício) podem apresentar propriedades farmacológicas aprimoradas, e pode ser, por exemplo, melhor tolerada, ter uma meia-vida mais longa ou apresentar potência aumentada (vide, por exemplo, o artigo de Englebienne em Med. Chem., 2005, 1(3), 215-226). Neste aspecto mais amplo, a presente invenção contempla todos os bioisósteres (e especificamente, todos os bioisósteres de silício) dos compostos da invenção.
[0077] Em seu aspecto mais amplo, a presente invenção contempla todos osisômerosóticos, formasracêmicas e diastereômeros doscompostos descritosaqui,neste requerimentodepatente.Osversadosnatécnica reconhecerãoque,devidoaosátomosdecarbono assimetricamente substituídospresentes noscompostos da invenção, os compostos podem ser produzidos em formas oticamente ativas e racêmicas. Se um centro quiral ou outra forma de centro isomérico estiver presente em um composto da presente invenção, pretende-se que sejam cobertas todas as formas de semelhante isômero ou isômeros, incluindo enantiômeros e diastereômeros, aqui, neste requerimento de patente. Compostos da invenção contendo um centro quiral (ou múltiplos centros quirais) podem ser usados como uma mistura racêmica, uma mistura enantiomericamente enriquecida, ou a mistura racêmica pode ser separada usando técnicas de conhecimento geral e um enantiômero individual pode ser usado exclusivamente. Deste modo, referências aos compostos da presente invenção englobam os produtos como uma mistura de diastereômeros, como diastereômeros individuais, como uma mistura de enantiômeros bem como sob a forma de enantiômeros individuais.
[0078] Portanto, a presente invenção contempla todos os isômeros óticos e formas racêmicas do mesmo dos compostos da invenção, e a menos que indicado de modo diverso (por exemplo, por uso de fórmulas estruturais de dash wedge) pretende-se que os compostos apresentados aqui, neste requerimento de patente, englobem todos os isômeros óticos possíveis dos compostos representados desta forma. Em casos onde a forma estereoquímica do composto é importante para utilidade farmacêutica, a invenção contempla o uso de um eutômero isolado.
[0079] Na presente especificação o termo “alquila” define uma cadeia de hidrocarboneto saturada reta ou ramificada. O termo “CrCe alquila” se refere a uma cadeia de hidrocarboneto saturada reta ou ramificada tendo um a seis átomos de carbono. Exemplos incluem metila, etila, n- propila, isopropila, t-butila, n-hexila. O termo “C1-C9 alquila” se refere a uma cadeia de hidrocarboneto saturada reta ou ramificada tendo um a nove átomos de carbono. O termo “CrCis alquila” se refere a uma cadeia de hidrocarboneto saturada reta ou ramificada tendo um a quinze átomos de carbono. Os grupos alquila da invenção podem ser opcionalmente substituídos por um ou mais átomos de halogeneto.
[0080] “C1-C4 alquila” tem um significado similar exceto que contém de um a quatro átomos de carbono.
[0081] “C2-C6 alquenila” se refere a uma cadeia de hidrocarboneto reta ou ramificada tendo de dois a seis átomos de carbono e contendo no mínimo uma ligação dupla carbono-carbono. Exemplos incluem etenila, 2-propenila, e 3-hexenila.
[0082] O termo “C1-C6 haloalquila” se refere a um grupo C1-6 alquila conforme definido acima substituído por um ou mais átomos de halogeneto.
[0083] Na presente especificação o termo “alquenila” define uma cadeia de hidrocarboneto reta ou ramificada tendo contendo no mínimo uma ligação dupla carbono-carbono. O termo “C1-C6 alquenila” se refere a uma cadeia de hidrocarboneto insaturada reta ou ramificada tendo um a seis átomos de carbono. O termo “C1-C9 alquenila” se refere a uma cadeia de hidrocarboneto insaturada reta ou ramificada tendo um a nove átomos de carbono. O termo “C1C15 alquenila” se refere a uma cadeia de hidrocarboneto insaturada reta ou ramificada tendo um a quinze átomos de carbono. É preferencial C1-C6 alquenila. Exemplos incluem etenila, 2-propenila, e 3-hexenila. Os grupos alquenila da invenção podem ser opcionalmente substituídos por um ou mais átomos de halogeneto.
[0084] Na presente especificação o termo “alquinila” define uma cadeia de hidrocarboneto reta ou ramificada tendo contendo no mínimo uma ligação tripla carbono- carbono. O termo “Ci-C6 alquinila” se refere a uma cadeia de hidrocarboneto insaturada reta ou ramificada tendo um a seis átomos de carbono. O termo “C1-C9 alquinila” se refere a uma cadeia de hidrocarboneto insaturada reta ou ramificada tendo um a nove átomos de carbono. O termo “C1C15 alquinila” se refere a uma cadeia de hidrocarboneto insaturada reta ou ramificada tendo um a quinze átomos de carbono. É preferencial Ci-C6 alquinila. Exemplos incluem etinila, 2-propinila, e 3-hexinila. Os grupos alquinila da invenção podem ser opcionalmente substituídos por um ou mais átomos de halogeneto.
[0085] O termo “heterociclila” define um sistema de anéis de 3 a 14 membros saturado ou parcialmente saturado (exceto quando números alternativos de átomos do anel são especificados) similar a cicloalquila, mas no qual no mínimo um dos átomos de carbono foi substituído por N, O, S, SO ou SO2. Exemplos incluem piperidina, piperazina, morfolina, tetra-hidrofurano e pirrolidina.
[0086] Conforme usado aqui, neste requerimento de patente, o termo “carbociclila” significa um resíduo monoou policíclico contendo 3 ou mais (por exemplo, 3a14, 3a10ou3a8) átomos de carbono. Os resíduos carbociclil da invenção podem ser opcionalmente substituídos por um ou mais átomos de halogeneto. Resíduos carbociclila mono- e bicíclico são preferenciais. Os resíduos carbociclila podem ser saturados ou parcialmente insaturados e incluem sistemas bicíclicos ou tricíclicos fundidos. Exemplos de semelhantes grupos incluem ciclopropila, ciclobutila, ciclopentila, ciclo-hexila, ciclo-hexenila e também sistemas ligados por ponte tais como norbornila e adamantila.
[0087] Resíduos carbociclila saturados são preferenciais e são referidos aqui, neste requerimento de patente, como “cicloalquilas” e o termo “cicloalquila” é usado aqui, neste requerimento de patente, para definir um anel carbocíclico de 3 a 14 membros saturado incluindo sistemas bicíclicos ou tricíclicos fundidos. Exemplos de semelhantes grupos incluem ciclopropila, ciclobutila, ciclopentila, ciclo-hexila e também sistemas ligados por ponte tais como norbornila e adamantila. Os resíduos cicloalquila da invenção podem ser opcionalmente substituídos por um ou mais átomos de halogeneto.
[0088] No presente relatório o termo “arila” define um grupo mono-, bi- ou tricíclico aromático de 5 a 14 (por exemplo, de 5 a 10) membros do qual no mínimo um anel é aromático. Deste modo, grupos aril bicíclico podem conter somente um anel aromático. Exemplos de porções aromáticas são benzeno, naftaleno, imidazol e piridina. O termo também inclui sistemas bicíclicos ou tricíclicos nos quais um ou mais dos anéis tem caráter aromático. Indano é um exemplo deste tipo de sistema.
[0089] Conforme usado aqui, neste requerimento de patente, o termo “heteroarila” são porções de arila conforme definido acima as quais contêm heteroátomos (por exemplo, nitrogênio, enxofre e/ou oxigênio). O termo também inclui sistemas nos quais um anel tendo caráter aromático é fundido a um anel saturado ou parcialmente saturado. Exemplos incluem sistemas de anéis piridina, pirimidina, furano, tiofeno, indol, isoindol, indolina, benzofu- rano, benzimidazol, benzimidazolina quinolina, isoquinolina, tetra- hidroisoquinolina, quinazolina, tiazol, benztiazol, benzoxazol, indazol e imidazol. A menos que indicado de modo diverso, o termo “arila” deve ser interpretado incluindo grupos heteroarila conforme definido acima.
[0090] Os grupos arila e heteroarila da invenção podem ser opcionalmente substituídos por um ou mais átomos de halogeneto.
[0091] No presente relatório, “halo” se refere a fluoro, cloro, bromo ou iodo.
[0092] Nas fórmulas gerais da presente invenção (e em particular na fórmula geral (I) conforme descrito abaixo), as ordens de ligação dos anéis especificados podem variar quando os vários heteroátomo(s) possíveis implicam específicos requisitos de modo a satisfazer aromaticidade, prevenir antiaromaticidade e estabilizar formas tautoméricas devido à localização. Em semelhantes casos, as ordens de ligação apropriadas das estruturas dos anéis nas fórmulas estruturais da presente invenção são contempladas aqui, neste requerimento de patente.
[0093] O termo “simétrico” conforme aplicado aos compostos de fórmula (I) pode definir compostos nos quais os substituintes R1 e R2 são os mesmos.
[0094] O termo “assimétrico” conforme aplicado aos compostos de fórmula (I) pode definir compostos nos quais os substituintes R1 e R2 são diferentes.
[0095] Os compostos da invenção têm a fórmula geral (I): em que os substituintes são conforme definido acima, ou podem ser um N-óxido farmaceuticamente aceitável, sal, hidrato, solvato, complexo, bioisóstere, metabólito ou profármaco do mesmo.
[0096] Compostos particularmente preferenciais de fórmula geral (I) são listados na Tabela 1 (abaixo): Tabela 1
[0097] Em cada caso, a invenção contempla saisfarmaceuticamente aceitáveis, hidratos, solvatos, complexos, bioisósteres, metabólitos ou pro- fármacos de cada um dos compostos listados.
[0098] Referências a números de compostos particulares aqui, neste 5 requerimento de patente, se referem aos números na Tabela 1.
[0099] Alguns dos compostos de fórmula geral (I) são novos. Deste modo, de acordo com a invenção, a invenção contempla os compostos de fórmula geral (I) os quais são novos como compostos per se, junto com processos para sua preparação, composições contendo os mesmos, bem como seu uso como farmacêuticos.
[00100] Deste modo, a invenção contempla um composto selecionado entre: 4,4'-(3'-metil-1H,3'H-5,5'-bibenzo[d]imidazol-2,2'- diil)dianilina 4,4'-(1-metil-1H,rH-5,5'-bibenzo[d]imidazol-2,2'- diil)dianilina 4,4'-(1H,1'H-5,5'-bibenzo[d]imidazol-2,2'-diil)bis(N- metilanilina) 4-(1H,1'H-5,5'-bibenzo[d]imidazol-2-il)anilina 4-(2'-fenil-1H,TH-5,5'-bibenzo[d]imidazol-2-il)anilina 2'-(4-metoxifenil)-2-fenil-1H,3'H-5,5'- bibenzo[d]imidazol 5,5'-(1H,TH-5,5'-bibenzo[d]imidazol-2,2'- diil)dipiridin-2-amina ou um N-óxido farmaceuticamente aceitável, sal, hidrato, solvato, complexo, bioisóstere, metabólito ou profármaco do mesmo, bem como composições (por exemplo, composições farmacêuticas) compreendendo os compostos referidos.
[00101] Compostos de fórmula geral (I) podem ser preparados por modificação de rotina dos métodos descritos na patente dos Estados Unidos N° US 5.824.698 (dujo conteúdo é por este incorporada aqui, a este requerimento de patente, por meio de referência) e conforme descrito no Exemplo 1 (abaixo).
[00102] Compostos preferenciais da invenção são agentes seletivos contra Clostridium difficile.
[00103] O termo “agente seletivo contra Clostridium difficile” é usado aqui, neste requerimento de patente, para definir compostos os quais apresentam atividade bacteriostática e/ou bactericida contra uma ou mais cepas de C. difficile, mas os quais não apresentam atividade bacteriostática e/ou bactericida contra um ou mais representantes da flora intestinal normal selecionados entre: (a) Escheríchia spp. (por exemplo, Escheríchia coli); (b) Bacteroides spp. (por exemplo, B. fragilis); (c) Fusobacteríum spp.; (d) Eubacterium spp. (e) Ruminococcus spp. (f) Peptococcus spp.; (g) Peptostreptococcus spp.; (h) Bifidobacterium spp; e (i) Lactobacillus spp.
[00104] Agentes seletivos contra Clostridium difficile particularmente preferenciais apresentam atividade bacteriostática e/ou bactericida contra uma ou mais cepas de C. difficile mas não apresentam atividade bacteriostática e/ou bactericida (MIC >64 pg/mL) contra B. fragilis ATCC25285.
[00105] Agentes seletivos contra Clostridium difficile ainda mais particularmente preferenciais apresentam atividade bacteriostática e/ou bactericida contra uma ou mais cepas de C. difficile, mas não apresentam atividade bacteriostática e/ou bactericida (MIC >64 pg/mL) contra tanto Bacteroides fragilis ATCC25285 quanto Escheríchia co//ATCC25922.
[00106] Os compostos preferenciais da invenção os quais são agentes seletivos contra Clostridium difficile podem, portanto, ser usados para tratar doença associada com Clostridium difficile sem perturbar a flora intestinal existente em uma extensão clinicamente significativa. Deste modo, os compostos referidos podem ser usados como agentes antimicrobianos sem causar doença associada com antibiótico (conforme definido aqui, neste requerimento de patente).
[00107] Compostos da invenção os quais agem como agentes seletivos contra Clostridium difficile podem ser identificados determinando as atividadeds antibacterianas relativas do composto para Clostridium difficile e um ou mais organismos indicadores representativos da flora intestinal normal. Organismos indicadores adequados para este fim incluem Escheríchia coli e/ou várias Bacteroides spp. (por exemplo, Bacteroides fragilis)
[00108] Alternativamente, ou além disso, compostos da invenção os quais agem como agentes seletivos contra Clostridium difficile podem ser identificados realizando culturas de fezes quantitativas sobre amostras de fezes seriais obtidas de indivíduos dosados com o um composto de teste. Uma variante in vitro desta abordagem se baseia na determinação de se o composto de teste produz importantes alterações da flora quando incubadas com amostras fecais diluídas e filtradas in vitro. Neste caso, alterações da flora podem ser detectadas determinando o efeito do composto de teste sobre os números relativos de bactérias representativas de dois ou mais dos gêneros seguintes: Bacteroides spp.; (c) Fusobacterium spp.; (d) Eubacterium spp. (e) Ruminococcus spp. (f) Peptococcus spp.; (g) Peptostreptococcus spp.; (h) Bifidobacterium spp; e (i) Lactobacillus spp.
[00109]Os compostos da invenção podem inibir ou prevenir a germinação de esporos.
[00110] Compostos os quais inibem a germinação de esporos podem ser identificados por detecção in vitro de alterações na refratividade de endosporos, resistência ao calor e coloração: endosporos germinando se tornam de fase escura, suscetíveis ao calor e tingíveis com alguns pigmentos.
[00111] Os compostos da invenção podem inibir ou prevenir o crescimento excessivo de esporos.
[00112] Compostos os quais inibem o crescimento excessivo de esporos podem ser identificados por examinação microscópica de esporos expostos a germinantes in vitro.
[00113] Os compostos da invenção podem ser bactericidas e/ou bacteriostáticos.
[00114] São preferenciais compostos bactericidas conforme definido acima. Os compostos bactericidas referidos também podem ser bacteriostáticos (por exemplo, dependendo da bactéria alvo e da concentração).
[00115] Os compostos da invenção encontram aplicação no tratamento de uma ampla gama de doenças. Deste modo, a invenção contempla os compostos de fórmula (I) conforme descrito aqui, neste requerimento de patente, para uso em medicina (por exemplo, para uso no tratamento ou profilaxia), métodos de tratamento medicinal ou profilaxia envolvendo a administração dos compostos de fórmula (I) conforme descrito aqui, neste requerimento de patente, bem como composições farmacêuticas compreendendo os compostos de fórmula (I) conforme descrito aqui, neste requerimento de patente.
[00116] Os compostos da invenção encontram aplicação em particular nas aplicações medicinais são descritos em mais detalhes abaixo:
[00117] A invenção encontra ampla aplicação no tratamento de qualquer infecção ou doença bacteriana Gram- positiva.
[00118] Particularmente preferencial é o tratamento de doença ou infecção causada por ou associada com uma bactéria anaeróbica Gram-positiva. Em semelhantes modalidades, a bactéria anaeróbica pode ser um anaeróbio facultativo ou um anaeróbio obrigatório.
[00119] Particularmente preferencial é o tratamento de doença ou infecção causada por ou associada com uma bactéria Gram-positiva formadora de endosporos. Em semelhantes modalidades, a bactéria Gram-positiva formadora de endosporos pode ser um anaeróbio (por exemplo, um anaeróbio facultativo ou um anaeróbio obrigatório).
[00120] Particularmente preferencial é o tratamento de doença ou infecção causada por ou associada com uma bactéria selecionada entre: (a) Clostridium spp.; (b) Staphylococcus spp.; (c) Enterococcus spp.; e (d) combinações de (a) a (c). Em semelhantes modalidades, é particularmente preferencial o tratamento de doença ou infecção causada por ou associada com uma bactéria selecionada entre: (a) Clostridium difficile (por exemplo, cepa BI/NAP1); (b) Clostridium perfringens', (c) Staphylococcus aureus; e (d) combinações das mesmas.
[00121] A doença bacteriana pode ser doença associada com Clostridium difficile, colite, colite pseudomembranosa, diarréia ou doença associada com antibiótico (incluindo diarréia associada com antibiótico e colite associada com antibiótico).
[00122] A doença ou infecção bacteriana pode envolver intoxicação com uma ou mais toxinas bacterianas, incluindo, por exemplo, endotoxinas, exotoxinas e/ou enzimas tóxicas.
[00123] Deste modo, os compostos da invenção encontram aplicação no tratamento de intoxicação bacteriana. Em semelhantes modalidades, é preferencial o tratamento de intoxicação com endotoxinas bacteriana, exotoxinas e/ou enzimas tóxicas, por exemplo, com endotoxinas, exotoxinas e/ou enzimas tóxicas produzidas pelas bactérias descritas nos parágrafos precedentes, incluindo em particular uma bactéria selecionada entre: (a) Clostridium spp.; (b) Staphylococcus spp.; (c) Enterococcus spp.; e (d) combinações de (a) a (c).
[00124] Particularmente preferencial é o tratamento de intoxicação com exotoxinas de clostrídios, incluindo toxina A (TcdA), toxina B (TcdB) e/ou toxina binária CDT de Clostridium difficile. Deste modo, os compostos da invenção encontram aplicação no tratamento de uma doença causada (ou exacerbada) pela presença de toxinas A (TcdA), B (TcdB) e/ou toxina binária CDT de Clostridium difficile.
[00125] Doença associada com Clostridium difficile (CDAD) define uma série de sintomas e doenças associadas com infecção e/ou intoxicação por C. difficile. Doença associada com Clostridium difficile inclui diarréiea, distensão, sintomas semelhantes a gripe, febre, perda de apetite, dor abdominal, náusea, desidratação e inflamação intestinal (colite). A manifestação mais grave de doença associada com Clostridium difficile é colite pseudomembranosa (PMC), a qual é manifestada histologicamente por colite com placas mucosas, e clinicamente por diarréia grave, cãibras abdominais e toxicidade sistêmica.
[00126] Os compostos da invenção encontram aplicação no tratamento de todas as formas de doença associada com Clostridium difficile, incluindo diarréia, distensão, sintomas semelhantes a gripe, febre, perda de apetite, dor abdominal, náusea, desidratação, colite e colite pseudomembranosa.
[00127] Doença associada com antibiótico define condições originárias de alterações nas quantidades relativas dos micro-organismos constituindo a flora intestinal normal causada por eliminação (parcial) da flora por administração de antibiótico. As doenças referidas surgem quando a administração de antibióticos (particularmente antibióticos de amplo espectro) permite o crescimento de organismos patogênicos (quer por crescimento excessivo de populações endógenas geralmente mantidas sob controle pela flora intestinal normal ou por colonização oportunista de sítios clareados da flora intestinal normal pelo antibiótico).
[00128] Doenças associadas com antibiótico tipicamente são manifestadas por diarréia (e desidratação associada), cãibras abdominais, tenesmo e febre. Também pode levar a várias formas de colite, incluindo colite pseudomembranosa (PMC). Deste modo, doença associada com antibiótico inclui diarréia associada com antibiótico (AAD) e colite associada com antibiótico (AAC).
[00129] Doença associada com antibiótico frequentemente é causada por cepas produtoras de toxina de Clostridium difficile, Staphylococcus aureus (incluindo meticilina resistente S. aureus) e Clostridium períringens. Clostridium diffícile é a causa mais comum de diarréia associada com antibiótico nosocomial e causa a maioria dos casos de colite associada com antibiótico. A bactéria prolifera no cólon de pacientes aos quais foram administrados antibióticos de amplo espectro ou quimioterapia contra câncer.
[00130] Portanto os compostos da invenção encontram aplicação no tratamento de doença associada com antibiótico, incluindo diarréia associada com antibiótico e colite associada com antibiótico. Particularmente preferencial é o tratamento de diarréia associada com antibiótico ou colite associada com antibiótico causadas por uma bactéria selecionada entre Clostridium diffícile, Staphylococcus aureus e Clostridium períringens, o mais preferencialmente AAD ou AAC causadas por Clostridium diffícile.
[00131] Particularmente preferencial para uso em semelhantes aplicações são compostos da invenção os quais são seletivos (conforme definido acima), uma vez que semelhantes compostos substancialmente poupam a flora intestinal normal.
[00132] Os compostos da invenção encontram aplicação em particular na profilaxia de doença associada com antibiótico, incluindo AAD e AAC. Em semelhantes aplicações, os compostos da invenção podem ser coadministrados com outros antibióticos ou tratamentos os quais podem induzir alterações nas quantidades relativas dos micro-organismos que constituem a flora intestinal normal.
[00133] Deste modo, os compostos da invenção podem ser usados para tratar indivíduos tratados (ou sendo submetidos a tratamento) com antibióticos de amplo espectro.
[00134] Conforme explicado acima, bactérias selecionadas entre Clostridium diffícile, Staphylococcus aureus e Clostridium períringens estão implicadas em colite, colite pseudomembranosa (PMC) e diarréia.
[00135] Por conseguinte, os compostos da invenção encontram aplicação no tratamento de colite, colite pseudomembranosa (PMC) ou diarréia.
[00136] Particularmente preferencial é o tratamento de colite pseudomembranosa.
[00137] Além do composto da invenção, a invenção também contempla o uso de um ou mais dos seguintes agentes adjuvantes como componentes adicionais da invenção.
[00138] Portanto, a invenção proporciona composições compreendendo o composto da invenção em combinação com um ou mais agentes adjuvantes selecionados entre os descritos abaixo.
[00139] As combinações preferencialmente compreendem adicionalmente um ou mais agentes antivirais auxiliares. Os agentes antivirais auxiliares referidos podem ser selecionados entre um ou mais de: (a) inibidores de enzimas virais (por exemplo, selecionados entre (i) inibidores de protease, (ii) inibidores de helicase e (iii) inibidores de polimerase); (b) inibidores da transcriptase reversa nucleosídeo/nucleotídeo; (c) inibidores da transcriptase reversa não nucleosídeo; (d) inibidores de integrase; (e) inibidores de maturação; (f) citocinas ou fatores estimuladores de citocina; (g) inibidores de entrada viral, por exemplo, selecionados entre: (i) um inibidor de ligação; (ii) um inibidor de ligação de correceptor; e (iii) um inibidor de fusão de membrana.
[00140] Os compostos da invenção podem ser usados em combinação com vários agentes antibacterianos incluindo, mas não limitados a um ou mais antibióticos selecionados entre os seguintes: •Aminoglicosídeos (por exemplo, amicacina, gentamicina, canamicina, neomicina, netilmicina, estreptomicina, tobramicina e paromomicina). •Ansamicinas (por exemplo, geldanamicina e herbimicina). •Carbacefenos (por exemplo, loracarbef). •Carbapenenos (por exemplo, ertapenem, doripenem, imipenem/cilastatin e meropenem) •Cefalosporinas (primeira geração), incluindo, por exemplo, cefadroxila, cefazolina, cefalotina / cefalotina e cefalexina). •Cefalosporinas (segunda geração), incluindo, por exemplo, cefaclor, cefamandol, cefoxitina, cefprozila e cefuroxima. •Cefalosporinas (terceira geração), incluindo, por exemplo, cefixima, cefdinir, cefditoren, cefoperazona, cefotaxima, cefpodoxima, ceftazidima, ceftibuten, ceftizoxima, ceftriaxona e cefdinir. •Cefalosporinas (quarta geração), incluindo, por exemplo, cefepima. •Glicopeptídeos (por exemplo, vancomicina e teicoplanina). •Macrolídeos (por exemplo, azitromicina, claritromicina, diritromicina, eritromicina, roxitromicina, troleandomicina, telitromicina e espectinomicina). •Monobactamas (por exemplo, aztreonam). •Penicilinas (por exemplo, amoxicilina, ampicilina, azlocilina, carbenicilina, cloxacilina, dicloxacilina, flucloxacilina, mezlocilina, nafcilina, penicilina, piperacilina e ticarcilina). •Polipeptídeos (por exemplo, bacitracina, polimixina B e colistina). •Quinolonas (por exemplo, ciprofloxacina, enoxacina, gatifloxacina, levofloxacina, lomefloxacina, moxifloxacina, norfloxacina, ofloxacina e trovafloxacina). •Sulfonamidas (por exemplo, mafenida, prontosila, sulfacetamida, sulfametizol, sulfanilimida, sulfasalazina, sulfisoxazol, trimetoprim, trimetoprim- sulfametoxazol (co-trimoxazol, TMP-SMX)). •Tetraciclinas (por exemplo, demeclociclina, doxiciclina, minociclina, oxitetraciclina e tetraciclina). •Aminocumarinas (por exemplo, novobiocina, albamicina, cumermicina e clorobiocina). •Oxazolidinonas (por exemplo, linezolid e AZD2563). •Lipopeptídeos (por exemplo, daptomicina). •Estreptograminas (por exemplo, quinupristina / dalfopristina). •Glicilciclinas (por exemplo, tigeciclina). •Lantibióticos (por exemplo, Lantibióticos Tipo A (tais como nisina, subtilina, epidermina, mutacina II, mutacina I e III) e Lantibióticos Tipo B (tais como mersacidina, actagardina e cinnamicina).
[00141] Outros antibióticos adequados úteis como agentes adjuvantes incluem um ou mais antibiótico(s) selecionados entre os seguintes:arsfenamina, cloranfenicol, clindamicina, lincoamicina, etambutol, fosfomicina, ácido fusídico, furazolidona, isoniazid, linezolid, metronidazol, mupirocina, nitrofurantoína, platensimicina, pirazinamida, quinupristina / dalfopristina, rifampina / rifampicina e tinidazol.
[00142] Deste modo, os compostos da invenção podem ser usados em combinação com um ou mais antibióticos selecionados entre: penicilina, cloxacilina, dicloxacilina, methicilina, nafcilina, oxacilina, ampicilina, amoxicilina, bacampicilina, capreomicina, cicloserina, azlocilina, carbenicilina, mezlocilina, piperacilina, ticarcilina, azitromicina, claritromicina, clindamicina, eritromicina, lincomicina, demeclociclina, doxiciclina, etambutol, etionamida, minociclina, oxitetraciclina, tetraciclina, quinolona, cinoxacina, ácido nalidíxico, fluoroquinolonas (por exemplo, levofloxacina, moxafloxacina e gatifloxacin, ciprofloxacina, enoxacina, grepafloxacina), canamicina, levofloxacina, lomefloxacina, norfloxacina, ofloxacina, ácido p-aminossalicílico, esparfloxacina, trovafloxacina, bacitracina, colistina, polimixina B, sulfonamida, trimetoprim- sulfametoxazol, co-amoxiclav, cefalotina, cefuroxima, ceftriaxone, vancomicina, gentamicina, amicacina, metronidazol, cloranfenicol, estreptomicina, nitrofurantoína, cotrimoxazol, rifamicina e derivados da mesma (por exemplo, rifampicina, rifabutina e rifapentina), isoniazid, pirazinamida, kirromicina, tiostrepton, micrococcina, ácido fusídico, tiolactomicina e fosmidomicina.
[00143] Outros agentes adjuvantes antibacterianos adequados podem ser selecionados entre os listados na tabela abaixo:
[00144] Os compostos da invenção podem ser usados em combinação com vários agentes antifúngicos (antimicóticos).
[00145] Os compostos da invenção podem ser usados em combinação com vários agentes antiprotozoários, incluindo mas não limitados a, cloroguina, doxiciclina, mefloguina, metronidazol, eplornitina, furazolidona, hidroxicloroguina, iodoguinol,pentamidina, mebendazol, piperazina, halofantrina, primaguina, pirimetamina sulfadoxina, doxiciclina, clindamicina, sulfato de guinina, gluconato de quinidina, diidrocloreto de quinina, sulfato de hidroxicloroquina, proguanila, quinina, clindamicina, atovaquone, azitromicina, suramin, melarsoprol, eflornitina, nifurtimox, anfotericina B, estibogluconato de sódio, isetionato de pentamidina, trimetoprim- sulfametoxazol, pirimetamina e sulfadiazina.
[00146] Os compostos da invenção podem ser coadministrados com uma variedade de outros agentes coterapêuticos os quais tratam ou previnem efeitos colaterais originários do tratamento anti-infeccioso e/ou se apresentando como sequelas da infecção. Agentes adjuvantes deste tipo podem ter ou não atividade anti- infecciosa e incluem, por exemplo, PPIs e H2RAs (conforme descrito acima).
[00147] Deste modo, os compostos da invenção podem ser usados acessoriamente com inibidores da bomba de prótons incluindo, mas não estão limitados a, omeprazol (Losec, Prilosec, Zegerid), lansoprazol (Prevacid, Zoton, Inhibitol), esomeprazol (Nexium), pantoprazol (Protonix, Somac, Pantoloc, Pantozol, Zurcal, Pan) e rabeprazol (Rabecid, Aciphex, Pariet, Rabeloc).
[00148] Os compostos da invenção também podem ser usados acessoriamente com H2RAs incluindo, mas não estão limitados a, cimetidina (Tagamet), ranitidina (Zinetac, Zantac), famotidina, (Pepcidine, Pepcid), roxatidina (Roxit) e nizatidina (Tazac, Axid).
[00149] Os compostos da invenção podem ser usados acessoriamente com tripla terapia com PPIs ou H2RAs junto com uma combinação de dois antibióticos (incluindo, mas não limitados a, antibióticos selecionados entre metronidazol, amoxicilina, levofloxacina e claritromicina).
[00150] Vários probióticos podem ser usados como agentes adjuvantes, incluindo por exemplo, células de Saccharomyces boulardii ou Lactobacillus acidophilus. Probióticos são monoculturas ou culturas mistas de microorganismos vivos os quais são propostos para ajudar a restabelecer a microflora intestinal natural do paciente que foi perturbada pelo antimicrobiano o-fensivo que induziu doença associada com Clostridium difficile ou mesmo o agente usado para tratar CDAD. Além disso, os microorganismos podem agir para estimular o sistema imune do paciente e provocar produção de enzimas que degradam as toxinas associadas com C. difficile. Microorganismos particulares de interesse são, mas não limitados a, Saccha- romyces spp. (por exemplo, Saccharomyces boulardii e Saccharomyces cerevisiae) e Lactobacillus spp. (por exemplo, Lactobacillus rhamnosus, Lactobacillus casei, Lactobaccillus acidophilus, Lactobacillus bulgarís e Lactobacillus plantarum). Qualquer outra composição de probióticos comuns ou microorganismo que seja um membro normal do trato intestinal humano também pode ser considerado.
[00151] Pré-bióticos, agentes tendo por objetivo estimular o crescimento da flora intestinal, também podem ser usados como agentes adjuvantes. Por exemplo, foi demonstrado que o uso de oligofrutose aumenta os níveis de Bifidobactéria spp. e reduz as taxas de recidiva subsequente nos pacientes. Deste modo, qualquer agente antibacteriano com um espectro limitado de atividade tendo por alvo a espécie Clostridium teria benefício significativco quando dosado em combinação com terapias tendo por objetivo restabelecer a população de microorganismos entéricos normais.
[00152] Outras abordagens tendo por objetivo restabelecer a flora entérica normal incluem bioterapia fecal e enemas fecais preparados a partir das fezes de indivíduos saudáveis as quais contêm os micro-organismos normais do intestino. Bacterioterapia fecal, portanto, também pode ser usada acessoriamente com os compostos da invenção.
[00153] De modo a sequestrar as toxinas produzidas por C. difficile, absorventes os quais ligam e sequestram bacteriotoxinas de vários tipos diferentes podem ser usados como agentes adjuvantes. Resinas de troca iônica, tais como os sequestrantes de ácido biliar colestiramina ou colestipol, ligam às citotoxinas de C. difficile e, portanto, têm por objetivo reduzir o grau de estímulo tóxico para o intestino. No entanto, resinas de troca iônica são conhecidas para ligar a agentes tais como vancomicina e, portanto, podem levar a níveis subótimos de agente antibacteriano no sítio de infecção. Outros absorventes que podem ser usados acessoriamente com os compostos da invenção incluem polímeros tais como Synsorb 90 e Tolevamer.
[00154] Embora terapia com probióticos seja sugerida para melhorar a reação do sistema imune em pacientes com doença associada com Clostridium difficile, imunoglobulina intravenosa (J. Antimicrob. Chem., 2004, 53, 882-884), por exemplo, também pode ser usada para tratar pacientes com doença associada com Clostridium difficile, particularmente casos recorrentes onde qualquer tratamento antimicrobiano adicional exacerbaria adicionalmente distúrbio da flora intestinal. Portanto, os compostos da invenção podem ser usados acessoriamente com várias imunoglobulinas.
[00155] Embora o uso de agentes com o fim de reduzir diarréia seja geralmente evitado em pacientes com doença associada com Clostridium difficile, em alguns casos pode ser previsto que o uso de semelhantes agentes em combinação com um antibacteriano possa ser de benefício ao tentar aumentar os níveis de um agente antimicrobiano no sítio de infecção e/ou ao tentar aumentar a extensão de tempo que um agente antibacteriano está em contato com o patógeno entérico. Os agentes referidos podem incluir, mas não estão limitados a, loperamida (Lopex, Imodium, Dimor, Pepto) difenoxilato (Lomotila, Cophenotrope) difenoxina (Motofen), e racecadotrila. Deste modo, os compostos da invenção podem ser usados acessoriamente com vários agentes antidiarreicos, incluindo quaisquer dos listados acima.
[00156] Agentes coterapêuticos os quais tratam ou previnem quaisquer dos seguintes efeitos colaterais podem ser usados como parte do mesmo regime de tratamento como os compostos da invenção: (a) lipodistrofia e debilitação; (b) lipoatrofia facial; (c) hiperlipidemia; (d) fadiga; (e) anemia; (f) neuropatia periférica; (g) náusea; (h) diarréia; (i) hepatotoxicidade; (j) osteopenia; (k) desidratação e (I) osteoporose.
[00157] O tratamento ou profilaxia pode compreender a administração de um composto conforme definido aqui, neste requerimento de patente, como um adjuvante a um ou mais dos seguintes tratamentos ou intervenções: (a)Terapia decâncer; (b)Terapia deAIDS; (c)Intervenções imunossupressoras; (d)Tratamentodeenxertopós-transplante / implante; (e)Cirurgia de unha onicomicótica ou debridamento; (f)Terapia antimicótica tópica (por exemplo, com um agente antimicótico selecionado entre azóis, alilaminas (por exemplo, terbinafina) ou uma morfolina (por exemplo, amorolfina); (g)Terapiaantimicótica sistêmica; (h)Terapiaantibacteriana; (i)Terapiaantiviral; (j)Terapia anti-inflamação(por exemplo, com esteroides); (k)Administração analgésica; (l)Administração antiprurítica; (m)Administração de probióticos; (n)Bacterioterapia fecal; ou (o)Enxerto de pele.
[00158] Portanto, a invenção pode compreender o tratamento ou profilaxia de uma população de pacientes na qual um ou mais dos tratamentos ou intervenções (a) a (o) estão sendo (ou foram) realizados.
[00159] O tratamento ou profilaxia pode compreender a administração de um composto conforme definido aqui, neste requerimento de patente, como um adjuvante a um ou mais dos seguintes tratamentos ou intervenções: 1.Terapia de câncer; 2.Intervençõesimunossupressoras; 3.Intervençõesimunoestimulatórias; 4.Tratamentode enxerto pós-transplante / implante; 5.Cirurgia de unha onicomicótica ou debridamento; 6.Terapia anti-inflamação (porexemplo, com steroids); 7.Administração analgésica; 8.Administração antiprurítica; 9.Cirurgia; 10.Ablação celular ou tecidual; 11.Radioterapia; 12.Crioterapia; 13.Terapia de transplantefecal (bacterioterapia fecal); 14.Terapia de probióticos;ou 15.Enxerto de pele.
[00160] Portanto, a invenção pode compreender o tratamento ou profilaxia de uma população de pacientes na qual um ou mais dos tratamentos ou intervenções (1) a (15) estão sendo (ou foram) realizados.
[00161] Os compostos da presente invenção podem ser administrados por vias orais ou parenterais, incluindo administração intravenosa, intramuscular, intraperitoneal, subcutânea, transdérmica, pelas vias aéreas (aerossol), retal, vaginal e tópica (incluindo bucal e sublingual).
[00162] A quantidade do composto administrado pode variar amplamente de acordo com a unidade de dosagem em particular empregada, o período de tratamento, a idade e o sexo do paciente tratado, a natureza e a extensão do distúrbio tratado, e o composto em particular selecionado.
[00163] Em geral, a quantidade eficaz do composto administrado geralmente variará a partir de cerca de 0,01 mg/kg a 10000 mg/kg diariamente. Uma dosagem unitária pode conter de 0,05 a 500 mg do composto, e pode ser tomada uma ou mais vezes por dia. O composto pode ser administrado com um veículo farmacêutico usando formas de unidades de dosagens convencionais quer por via oral, por via parenteral ou topicamente, conforme descrito abaixo.
[00164] A via de administração preferencial é administração oral. Em geral uma dose adequada será na faixa de 0,01 a 500 mg por quilograma de peso corporal do receptor por dia, preferencialmente na faixa de 0,1 a 1000 mg por quilograma de peso corporal por dia e o mais preferencialmente na faixa de 1 a 5 mg por quilograma de peso corporal por dia.
[00165] A dose desejada preferencialmente é apresentada como uma única dose para administração diária. No entanto, podem ser empregadas duas, três, quatro, cinco ou seis ou mais subdoses administradas em intervalos apropriados do início ao fim do dia. Estas subdoses podem ser administradas em formas de dosagens unitárias, por exemplo, contendo 0,001 a 100 mg, preferencialmente 0,01 a 10 mg, e o mais preferencialmente 0,5 a 1,0 mg de ingrediente ativo por forma de dosagem unitária.
[00166] Ao determinar uma quantidade ou dose eficaz, uma série de fatores são considerados pelo médico assistente, incluindo, mas não limitados a, a potência e duração de ação dos compostos usados, a natureza e gravidade da doença a ser tratada, bem como o sexo, a idade, o peso, saúde geral e responsividade individual do paciente a ser tratado, e outras circunstâncias relevantes. Os versados na técnica reconhecerão que as dosagens também podem ser determinadas com orientação do The Pharmacological Basis of Therapeutics de Goodman & Goldman, Ninth Edition (1996), Appendixll, pp. 1707-1711.
[00167] A quantidade do composto que pode ser combinada com materiais de veículo para produzir uma única forma de dosagem varia dependendo do indivíduo a ser tratado e do modo de administração em particular. Por exemplo, uma formulação pretendida para administração oral a humanos pode conter cerca de 0,5 mg a cerca de 7 g de agente ativo combinado opcionalmente com uma quantidade apropriada e conveniente de material de veículo o qual pode variar a partir de cerca de 5 a cerca de 95 por cento da composição total. Formas de unidade de dosagem para os compostos da invenção geralmente contêm cerca de 1 mg a cerca de 500 mg do ingrediente ativo, por exemplo, 5 mg, 10 mg, 20 mg, 25 mg, 50 mg, 100 mg, 200 mg, 300 mg, 400 mg, 500 mg, 600 mg, 800 mg ou 1000 mg.
[00168] A eficácia de uma dosagem particular do composto da invenção pode ser determinada monitorando o efeito de uma dada dosagem sobre a progressão da doença ou sua prevenção.
[00169] O composto da invenção pode tomar qualquer forma. Pode ser sintético, purificado ou isolado a partir de fontes naturais usando técnicas descritas na arte.
[00170] Sais farmaceuticamente aceitáveis ilustrativos são preparados a partir de ácidos fórmico, acético, propiônico, succínico, glicólico, glucônico, láctico, málico, tartárico, cítrico, ascórbico, glicurônico, maleico, fumárico, pirúvico, aspártico, glutâmico, benzoico, antranílico, mesílico, esteárico, salicílico, p-hidroxibenzoico, fenilacético, mandélico, embônico (pamoico), metanossulfônico, etanossulfônico, benzenosulfônico, pantotênico, toluenossulfônico, 2- hidroxietanossulfônico, sulfanílico, ciclo- hexilaminossulfônico, algênico, b-hidroxibutírico, galactárico e galacturônico.
[00171] Sais de adição de base farmaceuticamente aceitáveis incluem sais de íons metálicos e sais de íons orgânicos. Sais de íons metálicos incluem, mas não estão limitados a, sais de metais de álcali (grupo Ia) apropriados, sais de metais alcalinoterrosos (grupo lia) e outros íons de metais fisiologicamente aceitáveis. Os sais referidos podem ser preparados a partir dos íons de alumínio, cálcio, lítio, magnésio, potássio, sódio e zinco. Sais orgânicos podem ser preparados a partir aminas terciárias e sais de amônio quaternário, incluindo em parte, trimetilamina, dietilamina, N, N'- dibenziletilenodiamina, cloroprocaína, colina, dietanolamina, etileno diamina, meglumina (N- metilglucamina) e procaína. Todos os sais acima podem ser preparados por aqueles versados na técnica por meios convencionais a partir do composto correspondente.
[00172] Composições farmacêuticas podem incluir estabilizantes, antioxidantes, colorantes e diluentes. Veículos e aditivos farmaceuticamente aceitáveis são escolhidos de tal modo que os efeitos colaterais do composto farmacêutico são minimizados e a performance do composto não é comprometida em uma extensão tal que o tratamento é ineficaz.
[00173] As composições farmacêuticas podem ser administradas por via enteral e/ou por via parenteral. Oral (intragástrica) é uma via de administração típica. Veículos farmaceuticamente aceitáveis podem estar em formas de dosagens sólidas, incluindo comprimidos, cápsulas, pílulas e grânulos, os quais podem ser preparados com revestimentos e conchas, tais como revestimentos entéricos e outros de conhecimento geral na técnica. Formas de dosagens líquidas para administração oral incluem emulsões, soluções, suspensões, xaropes e elixires farmaceuticamente aceitáveis.
[00174] Administração parenteral inclui subcutânea, intramuscular, intradérmica, intravenosa, e outras vias conhecidas na técnica. Administração enteral inclui solução, comprimidos, cápsulas de liberação gradual, cápsulas com revestimento entérico, e xaropes.
[00175] Quando administrada, a composição farmacêutica pode estar na temperatura corporal ou próxima à temperatura corporal.
[00176] Composições pretendidas para aplicação oral podem ser preparadas de acordo com qualquer método conhecido na técnica para a fabricação de composições farmacêuticas e as composições referidas podem conter um ou mais agentes selecionados entre o grupo consistindo em agentes adoçantes, agentes aromatizantes, agentes colorantes e agentes conservantes de modo a proporcionar preparações farmaceuticamente elegantes e palatáveis. Comprimidos contêm o ingrediente ativo em mistura com excipientes farmaceuticamente aceitáveis não-tóxicos, os quais são adequados para a fabricação de comprimidos. Estes excipientes podem ser, por exemplo, diluentes inertes, tais como carbonato de cálcio, carbonato de sódio, lactose, fosfato de cálcio ou fosfato de sódio, agentes de granulação e desintegrantes, por exemplo, amido de milho, ou ácido algínico, agentes de ligação, por exemplo, amido, gelatina ou acácia, e agentes lubrificantes, por exemplo, estearato de magnésio, ácido esteárico, ou talco. Comprimidos podem ser não revestidos ou podem ser revestidos por técnicas conhecidas, por exemplo, para retardar desintegração e absorção no trato gastrointestinal e deste modo proporcionar ação gradual durante um período mais longo. Por exemplo, pode ser empregado um material de retardo de tempo tal como monoestearato de glicerila ou diestearato de glicerila.
[00177] Formulações para aplicação oral também podem ser apresentadas como cápsulas de gelatina dura em que os ingredientes ativos são misturados com um diluente sólido inerte, por exemplo, carbonato de cálcio, fosfato de cálcio ou caulim, ou como cápsulas de gelatina moles em que os ingredientes ativos estão presentes como se encontram, ou misturados com água ou um meio de óleo, por exemplo, óleo de amendoim, parafina líquida ou azeite de oliva.
[00178] Podem ser produzidas suspensões aquosas que contêm os materiais ativos em uma mistura com excipientes adequados para a fabricação de suspensões aquosas. Os excipientes referidos incluem agentes de suspensão, por exemplo, carboximetilcelulose de sódio, metilcelulose, hidroxipropilmetilcelulose, alginato de sódio, polivinilpirrolidona, goma tragacanto e goma acácia; agentes dispersantes ou umectantes podem ser fosfatídeos que ocorrem naturalmente, por exemplo, lecitina, ou produtos da condensação de um óxido de alquileno com ácidos graxos, por exemplo, estearato de polioxietileno, ou produtos da condensação de um óxido de etileno com alcoóis alifáticos de cadeia longa, por exemplo, heptadecaetilenooxicetanol, ou produtos da condensação de um óxido de etileno com ésteres parciais derivados de ácidos graxos e um hexitol tal como monooleato de sorbitol de polioxietileno, ou produtos da condensação de óxido de etileno com ésteres parciais derivados de ácidos graxos e anidridos de hexitol, por exemplo, monooleato de sorbitano de polioxietileno.
[00179] Suspensões aquosas também podem conter um ou mais conservantes, por exemplo, p-hidroxibenzoato de etila ou n-propila, um ou mais agentes colorantes, um ou mais agentes aromatizantes, ou um ou mais agentes adoçantes, tais como sacarose ou sacarina.
[00180] Suspensões oleosas podem ser formuladas suspendendo os ingredientes ativos em um ácido graxo ômega- 3, um óleo vegetal, por exemplo, óleo de araquis, azeite de oliva, óleo de gergelim ou óleo de coco, ou em um óleo mineral tal como parafina líquida. As suspensões oleosas podem conter um agente espessante, por exemplo, cera de abelhas, parafina dura ou álcool cetílico.
[00181] Agentes adoçantes, tais como os determinados acima, e agentes aromatizantes podem ser adicionados para proporcionar uma preparação oral palatável. Estas composições podem ser conservada por adição de um antioxidante tal como ácido ascórbico.
[00182] Pós e grânulos dispersíveis adequados para preparação de uma suspensão aquosa por adição de água proporcionam o ingrediente ativo em mistura com um agente dispersante ou umectante, um agente de suspensão e um ou mais conservantes. Agentes dispersantes ou umectantes adequados e agentes de suspensão são exemplificados por aqueles já mencionados acima. Excipientes adicionais, por exemplo, agentes adoçantes, aromatizantes e colorantes, também podem estar presentes.
[00183] Xaropes e elixires contendo o composto da invenção podem ser formulados com agentes adoçantes, por exemplo, glicerol, sorbitol, ou sacarose. As formulações referidas também podem conter um demulcente, umconservante e agentes aromatizantes e colorantes.
[00184] O composto da invenção pode ser administrado por via parenteral, por exemplo, por via subcutânea, por via intravenosa, ou por via intramuscular, ou por técnicas de infusão, sob a forma de suspensões aquosas ou oleaginosas injetáveis estéreis. As suspensões referidas podem ser formuladas de acordo com técnica conhecida usando agentes dispersantes ou umectantes adequados e agentes de suspensão tais como os mencionados acima ou outros agentes aceitáveis. Uma preparação injetável estéril pode ser uma solução ou suspensão injetável estérila em um diluente ou solvente não-tóxico aceitável por via parenteral, por exemplo, uma solução em 1,3-butanodiol. Entre veículos e solventes aceitáveis que podem ser empregados estão água, solução de Ringer e solução isotônica de cloreto de sódio. Além disso, óleos fixos estéreis são empregados convencionalmente como um solvente ou meio de suspensão. Para este fim, pode ser empregado qualquer óleo fixo suave, incluindo mono- ou diglicerídeos sintéticos. Além disso, ácidos graxos poli-insaturados ômega-3 encontram aplicação na preparação de injetáveis.
[00185] A administração também pode ser por inalação, sob a forma de aerossóis ou soluções para nebulizantes, ou por via retal, sob a forma de supositórios preparados misturando o fármaco com um excipiente não irritante adequado o qual é sólido em temperatura normal, mas líquido em temperatura retal e, portanto, derreterá no reto liberando o fármaco. Os materiais referidos são manteiga de cacau e polietileno glicóis.
[00186] Também é englobada pela presente invenção administração bu- cal e sublingual, incluindo administração sob a forma de losangos, pastilhas ou uma goma mastigável compreendendo os compostos determinados aqui, neste requerimento de patente. Os compostos podem ser depositados em uma base aromatizada, geralmente sacarose, e acácia ou tragacanto.
[00187] Outros métodos para administração dos compostos da invenção incluem emplastros dérmicos que liberam os medicamentos diretamente em e/ou através da pele de um indivíduo.
[00188] Sistemas de liberação tópica também são englobados pela presente invenção e incluem pomadas, pós, sprays, cremes, geleias, colírios, soluções ou suspensões.
[00189] As composições da presente invenção podem ser opcionalmente suplementadas com agentes adicional tais como, por exemplo, reforçadores da viscosidade, conservantes, tensoativos e reforçadores de penetração. Agentes de formação de viscosidade incluem, por exemplo, álcool polivinílico, polivinil pirrolidona, metilcelulose, hidroxipropilmetilcelulose, hidroxietilcelulose, carboximetilcelulose, hidroxipropilcelulose ou outros agentes conhecidos por aqueles versados na técnica. Os agentes referidos são tipicamente empregados em um nível de cerca de 0,01% a cerca de 2% em peso de uma composição farmacêutica.
[00190] Conservantes são opcionalmente empregados para prevenir crescimento microbiano antes ou durante o uso. Conservantes adequados incluem poliquatérnio-1, cloreto de benzalcônio, timerosal, clorobutanol, metilparabeno, propilparabeno, álcool feniletílico, edetato dissódio, ácido sórbico, ou outros agentes conhecidos por aqueles versados na técnica. Tipicamente, os conservantes referidos são empregados em um nível de cerca de 0,001% a cerca de 1,0% em peso de uma composição farmacêutica.
[00191] A solubilidade dos componentes das presentes composições pode ser reforçada por um tensoativo ou outro cossolvente apropriado na composição. Os cossolventes referidos incluem polissorbatos 20, 60 e 80, tensoativos de polioxietileno / polioxipropileno (por exemplo, Pluronic F- 68, F-84 e P-103), ciclodextrina, ou outros agentes de conhecimento daqueles versados na técnica. Tipicamente, os cossolventes referidos são empregados em um nível de cerca de 0,01% a cerca de 2% em peso de uma composição farmacêutica.
[00192] Excipientes e veículos farmaceuticamente aceitáveis englobam todos os precedentes e semelhantes. As considerações acima referentes a formulações e procedimentos de administração eficazes são de conhecimento geral na técnica e são descritas em compêndios de rotina. Vide, por exemplo, Remington: The Science and Practice of Pharmacy, 20th Edition (Lippincott, Williams e Wilkins), 2000; Lieberman et al., ed. , Pharmaceutical Dosage Forms, Marcei Decker, New York, N. Y. (1980) e Kibbe et aí, ed. , Handbook of Pharmaceutical Excipients (3rd Edition), American Pharmaceutical Association, Washington (1999).
[00193] Portanto, em modalidades onde o composto da invenção é formulado junto com um excipiente farmaceuticamente aceitável, pode ser usado qualquer excipiente adequado, incluindo, por exemplo, diluentes inertes, agentes desintegrantes, agentes de ligação, agentes lubrificantes, agentes adoçantes, agentes aromatizantes, agentes colorantes e preservantes. Diluentes inertes adequados incluem carbonato de sódio e de cálcio, fosfato de sódio e de cálcio, e lactose, ao passo que amido de milho e ácido algínico são agentes desintegrantes adequados. Agentes de ligação podem incluir amido e gelatina, ao passo que o agente lubrificante, caso presente, geralmente será estearato de magnésio, ácido esteárico ou talco. As composições farmacêuticas podem tomar qualquer forma adequada, e incluem, por exemplo, comprimidos, elixires, cápsulas, soluções, suspensões, pós, grânulos, esmaltes para as unhas, vernizes e folheados, emplastros para a pele e aerossóis.
[00194] A composição farmacêutica pode tomar a forma de um kit de partes, cujo kit pode compreender a composição da invenção junto com instruções para uso e/ou uma pluralidade de diferentes componentes em forma de unidade de dosagem.
[00195] Para administração oral o composto da invenção pode ser formulado em preparações sólidas ou líquidas tais como cápsulas, pílulas, comprimidos, trociscos, pastilhas, fusões, pós, grânulos, soluções, suspensões, dispersões ou emulsões (cujas soluções, suspensões dispersões ou emulsões podem ser aquosas ou não- aquosas). As formas de unidade de dosagem sólida podem ser uma cápsula a qual pode ser do tipo de gelatina de concha dura ou de concha mole ordinária contendo, por exemplo, tensoativos, lubrificantes, e enchimentos inertes tais como lactose, sacarose, fosfato de cálcio, e amido de milho. Comprimidos para aplicação oral podem incluir o composto da invenção, quer isolado ou junto com excipientes farma- ceuticamente aceitáveis, tais como diluentes inertes, agentes desintegrantes, agentes de ligação, agentes lubrificantes, agentes de adoçantes, agentes de aromatizantes, agentes de colorantes e conservantes. Diluentes inertes adequados incluem carbonato de sódio e de cálcio, fosfato de sódio e de cálcio, e lactose, ao passo que amido de milho e ácido algínico são agentes desintegrantes adequados. Agentes de ligação podem incluir amido e gelatina, ao passo que o agente lubrificante, caso presente, geralmente será estearato de magnésio, ácido esteárico ou talco. Caso desejado, os comprimidos podem ser revestidos com um material tal como monoestearato de glicerila ou diestearato de glicerila, para retardar a absorção no trato gastrointestinal. Cápsulas para aplicação oral incluem cápsulas de gelatina dura nas quais o composto da invenção é misturado com um diluente sólido, e cápsulas de gelatina mole em que o ingrediente ativo é misturado com água ou um óleo tal como óleo de amendoim, parafina líquida ou azeite de oliva.
[00196] Formulações para administração retal podem ser apresentadas como um supositório com uma base adequada compreendendo, por exemplo, manteiga de cacau ou um salicilato. Formulações adequadas para administração vaginal podem ser apresentadas como pessários, tampões, cremes, géis, pastas, espumas ou formulações de spray contendo além do ingrediente ativo veículo tais como são conhecidos na técnica como sendo apropriados.
[00197] Para aplicação intramuscular, intraperitoneal, subcutânea e intravenosa, os compostos da invenção geralmente serão proporiconados em soluções ou suspensões aquosas estéreis, tamponadas até um pH apropriado e isotonicidade.
[00198] Veículos aquosos adequados incluem solução de Ringer e cloreto de sódio isotônico. Suspensões aquosas de acordo com a invenção podem incluir agentes de suspensão tais como derivados celulósicos, alginato de sódio, polivinilpirrolidona e goma tragacanto, e um agente umectante tal como lecitina. Conservantes adequados para suspensões aquosas incluem p-hidroxibenzoato de etila e n- propila.
[00199] Os compostos da invenção também podem ser apresentados como formulações de lipossoma.
[00200] Em outra modalidade, os compostos da invenção são modelados em comprimidos com bases de comprimidos convencionais tais como lactose, sacarose, e amido de milho em combinação com aglutinantes tais como acácia, amido de milho, ou gelatina, agentes desintegrantes pretendidos para auxiliar a decomposição e dissolução do comprimido depois de administração tais como amido de batata, ácido algínico, amido de milho, e goma guar, lubrificantes pretendidos para aumentar o fluxo de granulações de comprimidos e para prevenir a adesão do material do comprimido às superfícies dos moldes de comprimidos e perfuradores, por exemplo, talco, ácido esteárico, ou estearato de magnésio, cálcio, ou zinco, corantes, agentes colorantes, e agentes aromatizantes pretendidos para reforçar as qualidades estéticas dos comprimidos e os tornar mais aceitáveis para o paciente.
[00201] Excipientes adequados para uso em formas de dosagem líquida oral incluem diluentes tais como água e alcoóis, por exemplo, etanol, álcool benzílico, e os alcoóis de polietileno, quer com ou sem a adição de um tensoativo farmaceuticamente aceitável, agente de suspensão ou agente emulsificante.
[00202] Os compostos da invenção também podem ser administrados por via parenteral, isto é, por via subcutânea, por via intravenosa, por via intramuscular, ou por via interperitoneal. Em semelhantes modalidades, o composto é proporcionado como doses injetáveis em um diluente fisiologicamente aceitável junto com um veículo farmacêutico (o qual pode ser um líquido estéril ou mistura de líquidos). Líquidos adequados incluem água, salina, dextrose aquosa e soluções de compostos relacionados, um álcool (tal como etanol, isopropanol, ou álcool hexadecílico), glicóis (tais como propileno glicol ou polietileno glicol), glicerol cetais (tais como 2,2- dimetil-1,3-dioxolana-4-metanol), éteres (tais como poli(etileno-glicol) 400), um óleo, um ácido graxo, um éster de ácido graxo ou glicerídeo, ou um glicerídeo de ácido graxo acetilado com ou sem a adição de um tensoativo farmaceuticamente aceitável (tal como um sabão ou um detergente), agente de suspensão (tal como pectina, carbômeros, metilcelulose, hidroxipropilmetilcelulose, ou carboximetilcelulose), ou agente emulsificante e outros adjuvantes farmacêuticos. Óleos adequados os quais podem ser usados nas formulações parenterais desta invenção são óleos de origem de petróleo, animal, vegetal, ou sintética, por exemplo, óleo de amendoim, óleo de soja, óleo de gergelim, óleo de semente de algodão, óleo de milho, azeite de oliva, petrolato, e óleo mineral.
[00203] Ácidos graxos adequados incluem ácido oleico, ácido esteárico, e ácido isoesteárico. Ésteres de ácidos graxos adequados são, por exemplo, oleato de etila e miristato de isopropila. Sabões adequados incluem sais de trietanolamina, amônio e metais de álcali graxos, e detergentes adequados incluem detergentes catiônicos, por exemplo, haletos dimetil dialquil de amônio, haletos de alquil piridínio, e acetatos de alquilaminas; detergentes aniônicos, por exemplo, sulfonatos de alquila, arila, e olefina, sulfatos e sulfossuccinatos de alquila, olefina, éter, e monoglicerídeo; detergentes não iônicos, por exemplo, óxidos de amina graxos, alcanolamidas de ácidos graxos, e copolímeros de polioxietilenopolipropileno; e detergentes anfotéricos, por exemplo, alquil-beta- aminopropionatos, e sais de amônio quarternário de 2- alquilimidazolina, bem como misturas.
[00204] As composições parenterais desta invenção tipicamente conterão a partir de cerca de 0,5 a cerca de 25% em peso do composto da invenção em solução. Conservantes e tampões também podem ser usados. De modo a minimizar ou eliminar irritação no sítio de injeção, as composições referidas podem conter um tensoativo não iônico tendo um balanço hidrófilolipófilo (HLB) de a partir de cerca de 12 a cerca de 17. A quantidade de tensoativo em semelhantes formulações varia a partir de cerca de 5 a cerca de 15% em peso. O tensoativo pode ser um único componente tendo o HLB acima ou pode ser uma mistura de dois ou mais componentes tendo o HLB desejado. Ilustrativa dos tensoativos usados em formulações parenterais são a classe de ésteres de ácidos graxos de sorbitano de polietileno, por exemplo, mono-oleato de sorbitano e os aductos de óxido de etileno de alto peso molecular com uma base hidrofóbica, formados pela condensação de óxido de propileno com propileno glicol.
[00205] Os compostos da invenção também podem ser administrados topicamente, e quando isso acontece o veículo pode compreender convenientemente uma solução, pomada ou base de gel. A base, por exemplo, pode compreender um ou mais dos seguintes: petrolato, lanolina, polietileno glicóis, cera de abelhas, óleo mineral, diluentes tais como água e álcool, e emulsificantes e estabilizantes. Formulações tópicas podem conter uma concentração do composto a partir de cerca de 0,1 a cerca de 10% em peso/ vol (peso por unidade de volume).
[00206] Quando usados acessoriamente, os compostos da invenção podem ser formulados para uso com um ou mais fármacos diversos. Em particular, os compostos da invenção podem ser usados em combinação com analgésicos, anti- inflamatórios (por exemplo, esteroides), agentes imunomodulatórios e antiespasmódicos.
[00207] Portanto, aplicação adjuvante pode ser refletida em uma unidade de dosagem específica designada para ser compatível (ou para sinergizar) com o outro ou outros fármacos, ou em formulações nas quais o composto é misturado com um ou mais agentes anti-inflamatórios, citocinas ou imunossupressivos (ou ainda fisicamente associados com o outro ou outros fármacos) dentro de uma única unidade de dose). Aplicações adjuvantes também podem ser refletidas na composição dos kits farmacêuticos da invenção, nas quais o composto da invenção é coembalado (por exemplo, como parte de uma série de unidades de doses) com os agentes antimicrobianos e/ou anti-inflamatórios. Aplicação adjuvante também pode ser refletida em informação e/ou instruções relativas à coadministração do composto com agentes antimicrobianos e/ou anti-inflamatórios.
[00208] A invenção será agora descrita com referência a Exemplos específicos. Estes são meramente exemplares e para fins ilustrativos somente: não se pretende que sejam limitantes de qualquer modo ao âmbito do monopólio reivindicado ou à invenção descrita. Estes exemplos constituem o melhor modo correntemente contemplado para praticar a invenção.
[00209] HPLC-UV-MS foi realizada em uma Gilson 321 HPLC com detecção realizada por um Gilson 170 DAD e um espectrômetro de massa Finnigan AQA operando em modo de ionização de eletrospray. A coluna de HPLC usada é uma Phenomenex Gemini C18 de 150x4,6 mm ou uma Phenomenex Gemini C18 de 50x4,6 mm de 3 p. Foi realizada HPLC do preparativo em um Gilson 321 com detecção realizada por um Gilson 170 DAD. As frações foram coletadas usando um coletor de fração Gilson 215. A coluna de HPLC do preparativo usada é uma Phenomenex Gemini C18 de 150x10 mm e a fase móvel é acetonitrila / água.
[00210] Os espectros de 1H RMN foram registrados em um instrumento Bruker operando a 300 MHz. Os espectros de RMN foram obtidos como soluções de CDCI3 ou de DMSO-d6 (reportadas em ppm), usando clorofórmio como o padrão de referência (7,26 ppm) ou DMSO-d6 (2,50 ppm). Quando são reportadas multiplicidades de picos, são usadas as seguintes abreviações: s (singleto), d (dubleto), t (tripleto), m (multipleto), br (ampliado), dd (dubleto de dubletos), dt (dubleto de tripletos), td (tripleto de dubletos), obsc. (obscurecido), app. (aparente). Constantes de ligação, quando dadas, são reportadas em Hertz (Hz).
[00211] Cromatografia de coluna foi realizada quer por cromatografia por cintilação (40 a 65 pm de sílica gel) ou usando um sistema de purificação automatizado (SP1® Purification System da Biotage® ou CombiFlash Companion da ISCO). Reações no micro-ondas foram realizadas em um Initiator 8® (Biotage) ou em um Explorer48 (CEM).
[00212] As abreviações usadas são DMSO (sulfóxido dimetila), DMF (dimetilformamida), IMS (aguardentes metilados industriais), TLC (cromatografia de camada fina), Boc (ferc-butiloxicarbonila), RT (tempo de retenção), DCM (diclorometano), TFA (ácido trifluoroacético), LCMS (cromatografia a líquido-espectrometria de massa), RMN (ressonância magnética nuclear), DME (1,2-dimetoxietano).
[00213] Dados de MIC foram determinados por microdiluição de caldo de acordo com protocolos de CLSI descritos em Methods for Antimicrobial Susceptibility Testing of Anaerobic Bactéria; Approved Standard-Seventh Edition [M11-A7, Vol. 27, No 2, Jan 2007] e Methods for Dilution Antimicrobial Susceptibility Tests for Bactéria That Grow Aerobically; Approved Standard- Seventh Edition[M7-A7, Vol. 26, No 2, Jan 2006],
[00214] Todos os compostos abaixo foram adquiridos da ChemDiv: 3,3'-(1H,1’H-5,5'-Bibenzo[d]imidazol-2,2'- diil)dianilina (Composto 2).
[00215] Uma mistura homogênea de bifenil-3,3',4,4'- tetra-amina (500 mg, 2,34 mmols) e ácido 4-aminobenzoico (640 mg, 4,67 mmols) foi adicionada em porções a PPA agitado (20 mL) a 200°C. A mistura foi agitada a 200°C por 2,5 horas. A mistura foi resfriada (até <100°C) e vertida em água. A mistura resultante foi agitada até ser formado um precipitado verde uniforme. O sólido foi filtrado e lavado com K2CO3 aquoso e água, e em seguida secado sob sucção. O produto bruto foi purificado por cromatografia de coluna (99:1 de EtOAc-NEt3 a 89:10:1 de EtOAc-MeOH-NEt3) para proporcionar um sólido amarelo. Este foi dissolvido em MeOH e HCI a 1 M, e em seguida concentrado a vácuo. O material foi em seguida triturado até um pó fino e agitado em NaHCO3 aquoso. O sólido foi filtrado, lavado com água e secado (forno a vácuo) para dar o produto como um sólido amarelo (475 mg, 49%).
[00216] LCMS TR=3,28 min, MH+ 417,3; 1H RMN (DMSO+D2O): 7,90- 7,84 (6 H, m), 7,74-7,65 (4 H, m) e 6,796,73 (4 H, m).
[00217] Os compostos que se seguem foram preparados em uma maneira similar, purificando por cristalização ou cromatografia de coluna onde necessário:
[00218] LCMS TR=1,46 min, MH+ 445,2; 1H RMN (DMSO): 12,52 (2 H, br s), 7,98-7,90 (4 H, m), 7,72 (2 H, br s), 7,60-7,52 (2 H, m), 7,48-7,43 (2 H, m), 6,66 (4 H, d, J 8,8), 6,24-6,17 (2 H, m) e 2,76 (6 H, d, J 4,8). 5,5'-(1H,1'H-5,5,-Bibenzo[d]imidazol-2,2,- diil)dipiridin-2-amina (Composto 11)
[00219] LCMS TR=1,36 min, MH+ 419,2; 1H RMN (DMSO): 12,82 (2 H, br s), 8,75 (2 H, d, J 2,4), 8,13 (2 H, dd, J 8,9 e 2,4), 7,76 (2 H, br s), 7,64- 7,57 (2 H, m), 7,537,47 (2 H, m) e 6,61-6,52 (6 H, m).
[00220] Uma mistura de bifenil-3,3',4,4'-tetra-amina (214 mg, 2,00 mmols), 4-hidroxibenzaldeído (489 mg, 4,00 mmols) e Na2S2O5 (380 mg, 2,00 mmols) em IMS-H2O (3:1, 20 mL) foi aquecida sob irradiação de microondas por 160°C por 10 min, em seguida 180°C por 10 min. A mistura foi filtrada e lavada com IMS. H2O foi adicionado ao filtrado, e o precipitado branco resultante foi filtrado, e lavado com água e Et2O. Cromatografia de coluna do sólido bruto (EtOAc a 95:5 a EtOAc-MeOH) proporcionou o produto como um sólido amarelo (50 mg, 6%).
[00221] LCMS TR=10,36 min [Dionex], MH+ 419,1; 1H RMN (DMSO): 12,75-12,66 (2 H, m), 10,00-9,96 (2 H, m), 8,06-7,99 (4 H, m), 7,86 (1 H, br s), 7,72-7,63 (2 H, m), 7,58-7,45 (3 H, m) e 6,96-6,89 (4 H, m).
[00222] N4-Metilbifenil-3,3',4,4'-tetra-amina (150 mg, 0,66 mmol) foi dissolvida em DMF (10 mL). Oxone® (810 mg, 1,32 mmol) foi adicionado, seguido por uma solução de /\/-Boc-4-aminobenzaldeído (preparado de acordo com J. Med. Chem., 1992, 35, 4150 e J. Med. Chem., 2004, 47, 2411) 320 mg, 1,45 mmol) em DMF (5 mL). A mistura foi agitada em temperatura ambiente por 5 horas. K2CÜ3 aquoso foi adicionado, e o precipitado resultante foi filtrado e lavado com água (3x100 mL). Este material bruto foi secado sob sucção, e purificado por cromatografia de coluna (75:25 de EtOAc-gasolina a 100% de EtOAc). O material foi adicionalmente purificado por recristalização de MeOH para dar o produto como um sólido branco (83 mg, 20%).
[00223] 1H RMN (DMSO): 12,81 (1 H, br s), 9,67 (2 H, d, J 6,1), 8,15- 8,05 (2 H, m), 7,96-7,89 (1,5 H, m), 7,867,77 (2,5 H, m), 7,73-7,49 (8 H, m), 3,91 (3 H, s) e 1,51 (18 H, s).
[00224] Os compostos que se seguem foram preparados em uma maneira similar, purificando por cristalização ou cromatografia de coluna onde necessário:
[00225] LCMS TR=1,52 min, MH+ 447,5; 1H RMN (DMSO):12,84-12,77 (2 H, m), 8,19-8,10 (4 H, m), 7,90 (1 H, br s), 7,75-7,66 (2 H, m), 7,61-7,48 (3 H, m), 7,17-7,09 (4 H, m) e 3,85 (6 H, s).
[00226] LCMS TR=1,46 min, MH+ 389,1; 1H RMN (DMSO+D2O): 8,79- 8,74 (4 H, m), 8,12-8,08 (4 H, m), 8,007,89 (2 H, br m), 7,81-7,73 (2 H, m) e 7,70-7,63 (2 H, br m).
[00227] 4-Bromo-2-fluoro-1-nitrobenzeno (500 mg, 2,27 mmols), 2-nitro- 4-(4,4,5,5-tetrametil-1,3,2- dioxaborolan-2-il)anilina (660 mg, 2,50 mmols) e K2CO2 (940 mg, 6,81 mmols) foram suspensos em DME-H2O (4:1, 15 mL) e purgados com nitrogênio. A solução foi desgaseificada por sonicação antes de Pd(dppf)CI2 (185 mg, 10% em mol) ser adicionado. A mistura foi aquecida até 130°C por 10 min sob irradiação de micro-ondas. A mistura resfriada foi particionada entre EtOAc e H2O. A camada aquosa foi extraída com EtOAc (2x50 mL). Os extratos orgânicos combinados foram lavados com salmoura, secados (MgSO4), filtrados e concentrados. O sólido preto resultante foi ab-sorvido sobre sílica e purificado por cromatografia de coluna (4:1 a 1:1 de gasolina-EtOAc) para dar o produto como um sólido laranja (285 mg, 45%).
[00228] 1H RMN (DMSO): 8,43 (1 H, d, J2,3), 8,19 (1 H, t, J 8,5), 7,96 (1 H, dd, J 4,8 e 2,1), 7,92 (1 H, d, J 2,0), 7,79-7,73 (3 H, m) e 7,15 (1 H, d, J 8,8).
[00229] 3'-Fluoro-3,4'-dinitrobifenil-4-amina (285 mg, 1,03 mmol) foi suspendido em DCM (10 mL). K2CO3 (284 mg, 2,06 mmols) foi adicionado, seguido por MeNH2 (40% em H2O, 10 mL). A mistura foi agitada em temperatura ambiente por 72 horas. A solução foi em seguida lavada com H2O e salmoura. A camada orgânica foi secada (MgSO4), filtrada e concentrada a vácuo para proporcionar o produto como um sólido vermelho (296 mg, 100%).
[00230]1H RMN (DMSO): 8,34 (1 H, d, J2,2), 8,33 8,26 (1 H, m), 8,11 (1 H, d, J 9,0), 7,91 (1 H, dd, J 8,8 e 2,1), 7,71 (2 H, br s), 7,15 (1 H, d, J 9,0), 7,11-7,08 (1 H, m), 6,97 (1 H, dd, J 9,0 e 1,8) e 3,05 (3 H, d, J 5,0). N3-Metilbifenil-3,3',4,4,-tetra-amina (Intermediário 3)
[00231]/V3-Metil-3',4-dinitrobifenil-3,4'-diamina (290 mg, 1,01 mmol) foi suspensa em IMS (25 ml_) e purgada com nitrogênio. Pd (10% sobre carbono, 30 mg, 10 % em mol) foi adicionado e a mistura foi colocada sob uma atmosfera de H2 (5 x ciclos de vácuo / balão). A mistura foi agitada em temperatura ambiente por 18 horas, ocasião na qual nenhuma matéria-prima permanecia por TLC (EtOAc). A mistura foi filtrada através de celite, lavando através com MeOH. O filtrado foi concentrado a vácuo para dar um óleo marrom. O produto bruto foi purificado por cromatografia de coluna (EtOAc a 97:3 de EtOAc-MeOH) para proporcionar o produto como uma espuma rosa (158 mg, 69%).
[00232] 1H RMN (DMSO): 6,74 (1 H, d, J 2,0), 6,616,47 (5 H, m), 4,62- 4,53 (1 H, m), 4,46-4,31 (6 H, m) e 2,75(3 H, d, J 2,8).
[00233] Preparado pelo Método 3 conforme descrito acima.
[00234] 1H RMN (DMSO): 12,81 (1 H, d, J 8,3), 9,699,75 (2 H, m), 8,12- 8,06 (2 H, m), 8,01-7,99 (0,5 H, m), 7,93-7,89 (1 H, m), 7,83-7,76 (2,5 H, m), 7,74-7,55 (8 H, m), 3,95 (3 H, s) e 1,51 (18 H, s).
[00235]4,4'-(3'-Metil-1H,3‘H-5,5'-bibenzo[d]imidazol-2,2'-diil)dianilina (Composto 4)
[00236]ferc-Butil-4,4'-(3'-metil-1H,3'H-5,5'- bibenzo[d]imidazol-2,2'- diil)bis(4,1-fenileno)dicarbamato (63 mg, 0,10 mmol) foi agitado em TFA (3 ml_) por 30 min. O solvente foi removido a vácuo e K2CO3 aquoso foi adicionado ao resíduo. O precipitado resultante foi filtrado e lavado com água e em seguida secado sob sucção para proporcionar o produto como um sólido amarelo-claro (36 mg, 86%).
[00237] LCMS TR=10,28 min [Dionex], MH+ 431,2; 1HRMN (DMSO): 12,48 (1 H, br s), 7,91-7,79 (4 H, m), 7,677,49 (6 H, m), 6,75-6,63 (4 H, m), 5,64-5,59 (4 H, br m) e 3,92 (3 H, s).
[00238] 4-Bromo-N-metil~2-nitroanilina (Intermediário 5)
[00239] 4-Bromo-1-fluoro-2-nitrobenzeno (1,50 g, 6,82 mmols) e K2CO3 (1,88 g, 13,6 mmols) foram suspensos em DCM (7 ml_). MeNH2(40% em H2O, 7 ml_) foi adicionado lentamente e a mistura foi agitada em temperatura ambiente por 4 horas. A mistura foi diluída com H2O e extraída com DCM (3x40 mL). As camadas de DCM combinadas foram lavadas com salmoura, secadas (MgSO4), filtradas e concentradas para proporcionar o produto como um sólido laranja brilhante (1,47 g, 93%).
[00240] 1H RMN (CDCI3): 8,32 (1 H, d, J2,4), 8,03 (1 H, br s), 7,52 (1 H, dd, J 9,2 e 2,5), 6,76 (1 H, d, J 9,2) e 3,02 (3 H, d, J 4,2). AA-Metil-SA-dinitrobifeniM/T- diamina (Intermediário 6)
[00241] 4-Bromo-N-metil-2-nitroanilina (100 mg, 0,43 mmol), 2-nitro-4-(4,4,5,5-tetrametil-1,3,2-dioxaborolan-2- il)anilina (115 mg, 0,43 mmol), bifenil-2-ildiciclo- hexilfosfina (30 mg, 20% em mol) e K3PO4 (275 mg, 1,3 mmol) foram suspensos em DME-H2O (4:1, 5 mL). A mistura foi purgada com nitrogênio e em seguida desgaseificada por sonicação. Pd(OAc)2 (5 mg, 5% em mol) foi adicionado, e a mistura foi aquecida até 130°C por 10 min sob irradiação de micro-ondas. A mistura resfriada foi diluída com EtOAc e H2O. Os orgânicos foram separados e a camada aquosa foi extraída com EtOAc (3x50 mL). Os extratos orgânicos combinados foram lavados com salmoura, secados (MgSO4), filtrados e concentrados a vácuo para dar o produto bruto como um sólido marrom escuro (210 mg). O material bruto foi aceito sem purificação adicional.
[00242] 1H RMN (DMSO): 8,29-8,14 (3 H, m), 7,90 (1 H, dd, J 9,1 e 2,3), 7,77 (1 H, td, J 8,5 e 2,3), 7,54 (2 H, br s), 7,15-7,05 (2 H, m) e 3,00 (3 H, d, J5,0).
[00243]N4-Metilbifenil-3,3',4,4'-tetra-amina(Intermediário 7)
[00244] AA-Metil-S.S-dinitrobifeniMA-diamina (bruta, 150 mg) foi suspensa em IMS (10 mL). O sistema foi purgado com nitrogênio antes de ser adicionado Pd (10% sobre carbono, 15 mg, 10% em mol). A mistura foi colocada sob uma atmosfera de H2 (3 x ciclos de vácuo / balão) e agitada em temperatura ambiente por 2,5 horas. A mistura foi filtrada através de celite e lavada através de MeOH. O filtrado foi concentrado a vácuo. O produto bruto foi purificado por cromatografia de coluna (EtOAc a 95:5 de EtOAc-MeOH) para proporcionar o produto como um óleo marrom claro (65 mg, 66% durante 2 etapas).
[00245]1H RMN (DMSO): 6,73-6,63 (3 H, m), 6,56-6,45(2 H, m), 6,37 (1 H, d, J 8,1), 4,42 (7 H, br s) e 2,71 (3 H, s).terc-Butil-4,4'-(1-metil-1H,1'H-5,5'-bibenzo[d]imidazol-2,2,-diil)bis(4,1-fenileno)dicarbamato (Intermediário 8)
[00246]Preparado pelo Método 3 conforme acima.
[00247]1H RMN (DMSO): 12,81 (1 H, br s), 9,67 (2 H, d, J 6,1), 8,15- 8,05 (2 H, m), 7,96-7,89 (1,5 H, m), 7,86- 7,77(2,5 H, m), 7,73-7,49 (8 H, m), 3,91 (3 H, s)e 1,51 (18 H, s). 4,4'-(1-Metil-1H,rH-5,5'-bibenzo[d]imidazol-2,2'- diil)dianilina (Composto 5)
[00248] terc-Butil-4,4'-(1 -metil-1 H, 1'H-5,5'- bibenzo[d]imidazol-2,2'-diil)bis(4,1-fenileno)dicarbamato (83 mg, 0,13 mmol) foi agitado em TFA (4 ml_) por 30 min. O solvente foi removido a vácuo e K2CO3 aquoso foi adicionado ao resíduo. O precipitado resultante foi filtrado e lavado com água e em seguida secado (forno a vácuo) para proporcionar o produto como um sólido branco (46 mg, 81%).
[00249] LCMS TR=1,44 min, MH+ 431,2; 1H RMN (DMSO): 12,49 (1 H, br s), 7,89-7,83 (3 H, m), 7,72 (1 H, br s), 7,63-7,42(6 H, m),6,74-6,64(6 H, m), 5,62(4 H, m) e3,88 (3 H, s).
[00250] Preparado pelo Método 1, usando uma proporção a 1:1 de bifenil-3,3',4,4,-tetra-amina para ácido 4-aminobenzoico e um tempo de reação de 2 horas.
[00251]1H RMN (DMSO): 12,33 (1 H, br s), 7,86-7,80 (2 H, m), 7,45 (2 H, brm), 7,25(1 H, dd, J 8,4 e 1,7), 6,86 (1 H, d, J2,1), 6,72 (1 H, dd, J7,9e 2,1), 6,69-6,63 (2 H, m), 6,57 (1 H, d, J7,9) e 5,80-4,40 (6 H, brs).
[00252] 4-(2-(4-Aminofenil)-1 H-benzo[d]imidazol-6- il)benzeno-1,2-diamina (200 mg, 0,64 mmol) e ácido fórmico (0,24 ml_, 6,35 mmols) foram dissolvidos em H2O (2 ml_) e a mistura foi aquecida até 160°C por 20 min sob irradiação de micro-ondas. No resfriamento, formou-se um precipitado, o qual foi filtrado e lavado com água. O filtrado foi basificado com K2CO3 e agitado por 30 min ocasião na qual um precipitado se tinha formado. A mistura foi filtrada e o precipitado foi lavado com água e secado sob sucção. O produto bruto foi purificado por cromatografia de coluna (EtOAc a 85:15 de E-tOAc-MeOH) para proporcionar o produto como um sólido branco (12 mg, 6%).
[00253] LCMS TR=1,35 min, MH+ 326,3; 1H RMN (DMSO): 12,48 (2 H, br s), 8,23 (1 H, br s), 7,91-7,68 (4 H, m), 7,65-7,41 (4 H, m), 6,70-6,64 (2 H, m) e 5,62 (2 H, br s).
[00254] Preparado pelo Método 1, usando somente 1 equivalente de ácido benzoico e um tempo de reação de 2 horas.
[00255] LCMS TR=1,48 min, MH+ 402,0; 1H RMN (DMSO): 12,97 (1 H, br s), 12,50 (1 H, br s), 8,24-8,18 (2 H, m), 7,96-7,80 (3,5 H, m), 7,76-7,70 (1,5 H, m), 7,68-7,43 (8 H, m), 6,67 (2 H, d, J 8,7) e 5,63 (2 H, br s).
[00256] Preparado pelo Método 2, usando uma proporção a 1:1 de bifenil-3,3',4,4'-tetra-amina para 4- metoxibenzaldeído, e aquecendo até 180°C por 10 min.
[00257]1H RMN (DMSO): 12,68-12,62(1 H, br m),8,14-8,07 (2 H, m), 7,66-7,54 (1 H, m), 7,51-7,43 (1 H, m), 7,35-7,27(1 H, m), 7,16-7,08(2 H, m),6,88(1 H, d, J2.1), 6,76-6,71 (1 H, m), 6,61-6,56 (1 H, m), 4,55 (4 H, br s) e 3,84 (3 H, s).
[00258] Preparado pelo Método 2, usando somente 1 equivalente de benzaldeído, e aquecendo até 180°C por 10 min.
[00259] LCMS TR=1,52 min, MH+ 417,0; 1H RMN (DMSO): 12,99 (1 H, br s), 12,82 (1 H, br s), 8,24-8,19 (2 H, m), 8,18-8,12 (2 H, m), 7,97-7,96 (1 H, br m), 7,80-7,66 (2 H, br m), 7,63-7,47 (4 H, m), 7,17-7,10 (2 H, m) e 3,85 (3 H, s).
[00260] Uma lista de compostos preferenciais de fórmula geral (I) junto com sua concentração inibitória mínima (MIC) contra Clostridium difficile ATCC700057 e um isolado clínico de Clostridium difficile (Cl) é resumida na Tabela 2 (abaixo):Tabela 2
[00261] Na tabela acima, os símbolos usados paraindicar os valores de MIC são: +++ = <1 gg/mL ++= 1-16pg/mL += 17-64 pg/mL -=>64 pg/mL
[00262] Uma lista de compostos junto com sua concentração inibitória mínima (MIC) contra Clostridium perfringens ATCC13124 e um isolado clínico de Clostridium perfringens (Cl) é resumida na Tabela 3 (abaixo). Os símbolos usados para indicar os valores da MIC são conforme para a Tabela 2 (acima).Tabela 3
[00263] Uma lista de compostos junto com sua concentração inibitória
[00264] mínima (MIC) contra Streptococcus pneumoniae ATCC49619 e uma cepa de Streptococcus pneumoniae resistente a múltiplos fármacos (MDR) é resumida na Tabela 4 (abaixo). Os símbolos usados para indicar os valores da MIC
[00266]
[00267] Uma lista de compostos junto com sua concentração inibitória mínima (MIC) contra Staphylococcus aureus ATCC29213 e uma cepa de Staphylococcus aureus resistente a múltiplos fármacos (MDR) é resumida na
[00268]5 Tabela 5 (abaixo). Os símbolos usados paraindicar os valores da MIC são conforme para a Tabela 2 (acima).Tabela 5
[00269] Uma lista de compostos junto com sua concentração inibitória 10 mínima (MIC) contra Enterococcus faecium e uma cepa de Enterococcus faecium resistente a múltiplos fármacos (MDR) é resumida na Tabela 6 (abaixo). Os símbolos usados para indicar os valores da MIC são conforme para a Tabela 2 (acima).Tabela 6
[00270] Uma lista de compostos junto com sua concentração inibitória mínima (MIC) contra uma cepa de Enterococcus faecalis resistente a vancomicina ATCC51299 (VR) é resumida na Tabela 7 (abaixo). Os símbolos usados para indicar os valores da MIC são conforme para a Tabela 2 (acima).Tabela 7
[00271] Nenhum dos compostos listados acima apresentou atividade significativa (MIC >64 pg/mL) contra a bactéria de Escherichia coli Gram-negativa facultativamente anaeróbica (ATCC25922). Somente os compostos 7 e 10 apresentaram qualquer atividade contra o anaeróbio Gram- negativo obrigatório Bacteroides fragilis (foram testados tanto ATCC25285 quanto um isolado clínico).
[00272] E. coli e Bacteroides fragilis são típicos da flora intestinal normal e portanto agem como substitutos para a flora intestinal microbiana.
[00273] Os dados determinados nos Exemplos 2 a 7 mostram que o composto 12 é altamente seletivo para Clostridium difficile em relação a C.perfringens, Staphylococcus aureus, Enterococcus faecium e Enterococcus faecalis. Este composto também não apresentou significativa atividade anti-bacteriana contra Bacillus subtilis ou Bacteroides fragilis.
[00274] Portanto, os dados mostram que os compostos da invenção podem encontrar utilidade no tratamento de doença associada com Clostridium difficile sem causar distúrbio patológico da flora intestinal normal.
[00275] A descrição precedente detalha modalidades presentemente preferenciais da presente invenção. Espera-se que numerosas modificações e variações na prática da mesma ocorram aos versados na técnica ao analisarem estas descrições. Pretende-se que estas modificações e variações sejam englobadas dentro das reivindicações anexadas a o presente requerimento.
Claims (17)
1. Uso de um composto de fórmula (l): em que: L1 é uma ligação direta ou um grupo ligante; R1 e R2 são cada um de modo independente selecionados entre H e C1-6 alquila, arila, heteroarila, carbociclila e heterociclil opcionalmente substituídos, a substituição opcional sendo com um ou mais substituintes selecionados entre halo, CN, NO2, R6, OR6, N(R6)2,COR6, CO2R6, SO2R6, NR7COR6, NR7CO2R6, NR7SO2R6, NR7CONR6R7, CONR6R7 e SO2NR6R7, contanto que no mínimo um de R1 e R2 seja cíclico; cada R5 é selecionado de modo independente entre H, halo, C1-6 alquila, OR7, N(R7)2, CN e NO2; X1 e X2 são cada um de modo independente selecionados entre N e CR3; X3 é selecionado entre NR4, O e S; X4 é NH; e R3 é selecionado entre H, halo e C1-6 alquila; R4 é selecionado entre H e C1-6 alquila; R6 é selecionado entre H, C1-C6 alquila, C2-C6 alqueniIa, C2-C6 alquinila, C4-C7 carbociclila, C4-C7 heterociclila e arila ou heteroarila de 5 ou de 6 membros, qualquer um dos quais pode ser opcionalmente substituído com um ou mais átomos de halo; e R7 é selecionado entre hidrogênio e C1-C4 alquila, qualquer um dos quais é opcionalmente substituído com um ou mais átomos de halo; caracterizado pelo fato de que é para preparação de uma composição farmacêutica para o tratamento de doença associada com Clostridium difficile (CDAD).
2.Uso, de acordo com a reivindicação 1, caracterizado pelo fato de que é para a preparação de uma composição farmacêutica direcionada seletivamente a Clostridium difficile.
3.Uso, de acordo com a reivindicação 2, caracterizado pelo fato de que é para a preparação de uma composição farmacêutica que tem efeito bacteriostático e/ou bactericida contra uma ou mais cepas de C. difficile, mas nenhum efeito bacteriostático e/ou . bactericida (MIC > 64 μg/mL) contra B. fragilis ATCC25285.
4.Uso, de acordo com a reivindicação 3, caracterizado pelo fato de que é para a preparação de uma composição farmacêutica que tem efeito bacteriostático e/ou bactericida contra uma ou mais cepas de C. difficile, mas nenhum efeito bacteriostático e/ou bactericida (MIC > 64 μg /mL) contra ambos Bacteroides fragilis ATCC25285 e Escherichia coli ATCC25922.
5.Uso, de acordo com a reivindicação 2, caracterizado pelo fato de que é para a preparação de uma composição farmacêutica que tem: (i)efeito bacteriostático e/ou bactericida contra uma ou mais cepas de C. difficile, mas nenhum efeito bacteriostático e/ou bactericida contra um ou mais representante(s) da flora intestinal normal selecionado(s) de: (a) Escherichia spp. (por exemplo, Escherichia coli); (b) Bacteroides spp. (por exemplo, B. fragilis); (c) Fusobacterium spp.; (d) Eubacterium spp. (e) Ruminococcus spp. (f) Peptococcus spp.; (g) Peptostreptococcus spp.; (h) Bifidobacterium spp; e (i) Lactobacillus spp.; ou (ii)nenhum efeito bacteriostático e/ou bactericida contra flora intestinal normal de uma forma clinicamente significativa.
6.Uso, de acordo com qualquer uma das reivindicações 1 a 5, caracterizado pelo fato de que é para a preparação de uma composição farmacêutica para o tratamento de CDAD enquanto poupa a flora intestinal normal.
7.Uso, de acordo com qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que X1 e/ou X2 é N.
8.Uso, de acordo com qualquer uma das reivindicações 1 a 7, caracterizado pelo fato de que X3 é: (a) NR4 ou (b) NR4 em que R4 é H ou metila.
9.Uso, de acordo com qualquer uma das reivindicações 1 a 8, caracterizado pelo fato de que R1 e R2 são: (a) cada um de modo independente selecionados entre H e arila; (b) cada um de modo independente selecionados entre H e arila opcionalmente substituída com OR6 e N(R6)2; (c) cada um cíclico; (d) os mesmos; (e) diferentes; ou (f) heterociclil ou heteroaril.
10.Uso, de acordo com qualquer uma das reivindicações 1 a 8, caracterizado pelo fato de que R1 e/ou R2 é (são): (a) heterociclil substituído com um ou mais substituintes selecionados entre halo, CN, NO2, R6, OR6, N(R6)2, COR6, CO2R6, SO2R6, NR7COR6, NR7CO2R6, NR7SO2R6, NR7CONR6R7, CONR6R7 e SO2NR6R7; ou (b) heteroaril substituído com um ou mais substituintes selecionados entre halo, CN, NO2, R6, OR6, N(R6)2, CO2R6, SO2R6, NR7COR6, NR7CO2R6, NR7SO2R6, NR7CONR6R7, CONR6R7 e SO2NR6R7.
11.Uso,deacordocomareivindicação10, caracterizado pelo fato de que R1 e/ou R2 é (são) piridila.
12.Uso,deacordocomareivindicação11, caracterizado pelo fato de que a piridila é substituída com um ou mais substituintes selecionados entre halo, CN, NO2, R6, OR6, N(R6)2, COR6, CO2R6, SO2R6, NR7COR6, NR7CO2R6, NR7SO2R6, NR7CONR6R7, CONR6R7 e SO2NR6R7.
13.Uso, de acordo com qualquer uma das reivindicações 1 a 12, caracterizado pelo fato de que R6 é selecionado de H e C1-C6 alquila e/ou cada R5 é H.
14.Uso, de acordo com qualquer uma das reivindicações 1 a 13, caracterizado pelo fato de que L1 é uma ligação direta, por exemplo, uma ligação direta entre as posições 5 e/ou 6 de cada ciclo.
15.Uso, de acordo com qualquer uma das reivindicações 1 a 14, caracterizado pelo fato de que: L1 é uma ligação direta R1 e R2 são cada um de modo independente selecionados entre H e arila, heteroarila opcionalmente substituídas, a substituição opcional 30 sendo com um ou mais substituintes selecionados dentre OR6, N(R6)2 contanto que pelo menos um de R1 e R2 é cíclico; R5 é H; X1 e X2 são N; X3 é NR4, em que R4 é H ou metila; e X4 é NH.
16.Uso, de acordo com qualquer uma das reivindicações 1 a 6, caracterizado pelo fato de que o composto é 2,2’- Di(piridina-4-il)-1H,1’H-5,5’-bibenzo[d]imidazol.
17.Composição farmacêutica caracterizada pelo fato de que compreende o composto 2,2’-Di(piridina-4-il)-1H,1’H- 5,5’-bibenzo[d]imidazol.
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| BR122020013025-3A BR122020013025B1 (pt) | 2008-12-02 | 2009-12-01 | uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos |
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| GBGB0821913.1A GB0821913D0 (en) | 2008-12-02 | 2008-12-02 | Antibacterial compounds |
| GB0821913.1 | 2008-12-02 | ||
| PCT/GB2009/002792 WO2010063996A2 (en) | 2008-12-02 | 2009-12-01 | Antibacterial compounds |
Publications (4)
| Publication Number | Publication Date |
|---|---|
| BRPI0922220A2 BRPI0922220A2 (pt) | 2015-12-29 |
| BRPI0922220A8 BRPI0922220A8 (pt) | 2018-04-03 |
| BRPI0922220B1 true BRPI0922220B1 (pt) | 2021-03-09 |
| BRPI0922220B8 BRPI0922220B8 (pt) | 2021-05-25 |
Family
ID=40262471
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0922220A BRPI0922220B8 (pt) | 2008-12-02 | 2009-12-01 | uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos |
| BR122020013025-3A BR122020013025B1 (pt) | 2008-12-02 | 2009-12-01 | uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos |
Family Applications After (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BR122020013025-3A BR122020013025B1 (pt) | 2008-12-02 | 2009-12-01 | uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos |
Country Status (27)
| Country | Link |
|---|---|
| US (3) | US8975416B2 (pt) |
| EP (3) | EP2373631B1 (pt) |
| JP (3) | JP5665756B2 (pt) |
| KR (1) | KR101643435B1 (pt) |
| CN (1) | CN102227411B (pt) |
| AU (1) | AU2009323854B2 (pt) |
| BR (2) | BRPI0922220B8 (pt) |
| CA (1) | CA2744962C (pt) |
| CY (2) | CY1116383T1 (pt) |
| DK (2) | DK2373631T3 (pt) |
| ES (2) | ES2575908T3 (pt) |
| GB (1) | GB0821913D0 (pt) |
| HR (2) | HRP20150518T1 (pt) |
| HU (1) | HUE029151T2 (pt) |
| IL (1) | IL213325A (pt) |
| LT (1) | LT2907813T (pt) |
| MX (1) | MX2011005837A (pt) |
| NZ (1) | NZ593111A (pt) |
| PL (2) | PL2907813T3 (pt) |
| PT (2) | PT2373631E (pt) |
| RS (1) | RS54904B1 (pt) |
| RU (1) | RU2525915C2 (pt) |
| SG (1) | SG171939A1 (pt) |
| SI (2) | SI2373631T1 (pt) |
| SM (2) | SMT201500117B (pt) |
| WO (1) | WO2010063996A2 (pt) |
| ZA (1) | ZA201103751B (pt) |
Families Citing this family (32)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB0821913D0 (en) | 2008-12-02 | 2009-01-07 | Price & Co | Antibacterial compounds |
| GB2480816A (en) * | 2010-06-01 | 2011-12-07 | Summit Corp Plc | Compounds for the treatment of Clostridium difficile associated diseases |
| WO2011151620A1 (en) * | 2010-06-01 | 2011-12-08 | Summit Corporation Plc | Compounds for the treatment of clostridium difficile associated disease |
| GB2480813A (en) * | 2010-06-01 | 2011-12-07 | Summit Corp Plc | Compounds for the treatment of clostridium difficile-associated disease |
| WO2011151619A1 (en) * | 2010-06-01 | 2011-12-08 | Summit Corporation Plc | Compounds for the treatment of clostridium difficile associated disease |
| GB2480814A (en) * | 2010-06-01 | 2011-12-07 | Summit Corp Plc | Compounds for the treatment of clostridium difficile-associated disease |
| ES2568455T3 (es) * | 2010-06-01 | 2016-04-29 | Summit Therapeutics Plc | Compuestos para el tratamiento de enfermedad asociada a Clostridium difficile |
| US9079935B2 (en) | 2012-08-13 | 2015-07-14 | The Board Of Regents Of The Nevada System Of Higher Education On Behalf Of The University Of Nevada, Las Vegas | Reducing risk of contracting Clostridium-difficile associated disease |
| CA3212215A1 (en) | 2012-11-23 | 2014-05-30 | Seres Therapeutics, Inc. | Synergistic bacterial compositions and methods of production and use thereof |
| US8906668B2 (en) | 2012-11-23 | 2014-12-09 | Seres Health, Inc. | Synergistic bacterial compositions and methods of production and use thereof |
| CA2899925A1 (en) * | 2013-02-04 | 2014-08-07 | Seres Therapeutics, Inc. | Compositions and methods for inhibition of pathogenic bacterial growth |
| HK1218560A1 (zh) | 2013-02-04 | 2017-02-24 | Seres Therapeutics, Inc. | 组成与方法 |
| EP2967077A4 (en) | 2013-03-15 | 2016-09-14 | Seres Therapeutics Inc | NETWORK-BASED MICROBIAL COMPOSITIONS AND METHOD |
| EP3074027B1 (en) | 2013-11-25 | 2024-12-18 | Seres Therapeutics, Inc. | Synergistic bacterial compositions and methods of production and use thereof |
| US9956282B2 (en) | 2013-12-16 | 2018-05-01 | Seres Therapeutics, Inc. | Bacterial compositions and methods of use thereof for treatment of immune system disorders |
| JP6526956B2 (ja) * | 2013-12-19 | 2019-06-05 | 花王株式会社 | 固形状組成物 |
| US9717711B2 (en) | 2014-06-16 | 2017-08-01 | The Lauridsen Group | Methods and compositions for treating Clostridium difficile associated disease |
| WO2016127102A2 (en) | 2015-02-06 | 2016-08-11 | Ernesto Abel-Santos | Inhibiting germination of clostridium perfringens spores to reduce necrotic enteritis |
| EP3668527A1 (en) | 2017-08-14 | 2020-06-24 | Seres Therapeutics, Inc. | Compositions and methods for treating cholestatic disease |
| US11512068B2 (en) | 2017-10-05 | 2022-11-29 | Sandoz Ag | Process for the preparation of crystalline ridinilazole using acid addition salts |
| JP2021501185A (ja) | 2017-10-30 | 2021-01-14 | セレス セラピューティクス インコーポレイテッド | 抗生物質耐性を処置するための組成物及び方法 |
| KR102737283B1 (ko) | 2019-07-17 | 2024-12-03 | 서밋 (옥스포드) 리미티드 | 리디닐라졸 및 이의 결정 형태의 제조방법 |
| CA3164134A1 (en) | 2019-12-06 | 2021-06-10 | Vertex Pharmaceuticals Incorporated | Substituted tetrahydrofurans as modulators of sodium channels |
| US20210324009A1 (en) * | 2020-04-17 | 2021-10-21 | The University Of Hong Kong | Anti-bacterial calcium-dependent antibiotic (cda) analogs and methods of treating bacterial infections |
| GB202100471D0 (en) | 2021-01-14 | 2021-03-03 | Summit Oxford Ltd | Preparation of antibacterial compounds |
| GB202100470D0 (en) * | 2021-01-14 | 2021-03-03 | Summit Oxford Ltd | Solid tablet dosage for of ridinilazole |
| WO2022251118A1 (en) * | 2021-05-24 | 2022-12-01 | Aimmax Therapeutics Inc. | Pristinamycin ia and flopristin combinations in treating or preventing bacterial infections |
| SI4347031T1 (sl) | 2021-06-04 | 2026-01-30 | Vertex Pharmaceuticals Incorporated | N-(hidroksialkil (hetero)aril) tetrahidrofuran karboksamidi kot modulatorji natrijevih kanalčkov |
| WO2022265993A1 (en) | 2021-06-14 | 2022-12-22 | Scorpion Therapeutics, Inc. | Urea derivatives which can be used to treat cancer |
| EP4398890A4 (en) | 2021-09-09 | 2025-07-30 | The Board Of Regents Of The Nevada System Of Higher Education On Behalf Of The Univ Of Nevada Las Ve | C. Difficile Spore Germination Inhibitors |
| WO2024112631A1 (en) * | 2022-11-22 | 2024-05-30 | Aimmax Therapeutics, Inc. | Streptogramin a monotherapy for treating or preventing bacterial infections |
| EP4418810A1 (de) | 2023-02-15 | 2024-08-21 | Siemens Aktiengesellschaft | Verfahren zur rechnergestützten überwachung einer industriellen anlage mittels eines funknetzes |
Family Cites Families (52)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3661849A (en) * | 1965-10-06 | 1972-05-09 | Ashland Oil Inc | Heterocyclic polyimides prepared from heterocyclic diamines |
| US3503929A (en) * | 1965-10-21 | 1970-03-31 | Minnesota Mining & Mfg | Polyimidazoquinazolines and polyamidobenzimidazoles |
| DE1670684A1 (de) | 1966-04-01 | 1970-12-03 | Hoechst Ag | Verfahren zur Herstellung von basisch substituierten Bis-benzimidazol-derivaten |
| US4087409A (en) * | 1966-11-07 | 1978-05-02 | Monsanto Company | Ordered heterocyclic copolymers |
| JPS50140445A (pt) * | 1974-04-30 | 1975-11-11 | ||
| JPS50154250A (pt) * | 1974-05-31 | 1975-12-12 | ||
| JPH03500661A (ja) * | 1988-06-09 | 1991-02-14 | ザ・ダウ・ケミカル・カンパニー | ベンゾキサゾール,ベンゾチアゾールまたはベンズイミダゾールの少なくとも1つの結合によって架橋したビスシクロブタレンのモノマー,オリゴマー及びポリマー |
| US5089592A (en) | 1988-06-09 | 1992-02-18 | The Dow Chemical Company | Biscyclobutarene monomer comprising two cyclobutarene moieties bridged by a divalent radical comprising at least one benzothiazole or benzimidazole linkage |
| GB9108279D0 (en) * | 1991-04-18 | 1991-06-05 | Ucb Sa | A method of preparing 1h-benzimidazoles |
| US5317078A (en) * | 1991-10-30 | 1994-05-31 | The United States Of America As Represented By The Administrator Of The National Aeronautics And Space Administration | Polybenzimidazole via aromatic nucleophilic displacement |
| WO1996016042A1 (de) * | 1994-11-17 | 1996-05-30 | F. Hoffmann-La Roche Ag | Antibakterielle dibenzimidazol-derivate |
| CN1164227A (zh) * | 1994-11-17 | 1997-11-05 | 弗·哈夫曼-拉罗切有限公司 | 联苯并咪唑衍生物 |
| US5770617A (en) | 1996-03-20 | 1998-06-23 | Rutgers, The State University Of New Jersey | Terbenzimidazoles useful as antifungal agents |
| JPH11158158A (ja) * | 1997-12-03 | 1999-06-15 | Snow Brand Milk Prod Co Ltd | 新規ベンゾイミダゾール誘導体 |
| JPH11158156A (ja) | 1997-12-03 | 1999-06-15 | Earth Chem Corp Ltd | 新規な1−(4−アルキルオキシフェニル)イミダゾール化合物 |
| US6358930B1 (en) | 1998-05-28 | 2002-03-19 | Synsorb Biotech Inc. | Treatment of C. difficile toxin B associated conditions |
| JP2000095767A (ja) * | 1998-09-28 | 2000-04-04 | Takeda Chem Ind Ltd | 性腺刺激ホルモン放出ホルモン拮抗剤 |
| GB9908828D0 (en) | 1999-04-16 | 1999-06-16 | Univ Reading The | Compounds |
| ES2232683T3 (es) | 2000-11-27 | 2005-06-01 | Ciba Specialty Chemicals Holding Inc. | Derivados de 2-(2-hiddroxifenil)-2h-benzotriazoles, sustituidos en posicion 5 por arilo y en posicion 5 por heteroarilo, como absorbentes uv. |
| HUP0303494A3 (en) | 2000-12-15 | 2009-08-28 | Vertex Pharma | Parmaceutical compositions containing bacterial gyrase inhibitors and uses thereof |
| FR2819180B1 (fr) | 2001-01-11 | 2003-02-21 | Oreal | Composition photoprotectrices a base de polymeres amphiphiles d'au moins un monomere a insaturation ethylique a groupement sulfonique et comportant une partie hydrophobe |
| AU2002228317A1 (en) * | 2001-01-29 | 2002-08-12 | Insight Strategy And Marketing Ltd | Benz-1,3-azole derivatives and their uses as heparanase inhibitors |
| WO2004001058A2 (en) | 2001-05-04 | 2003-12-31 | Paratek Pharmaceuticals, Inc. | Transcription factor modulating compounds and methods of use thereof |
| WO2003007955A2 (en) * | 2001-07-20 | 2003-01-30 | Cancer Research Technology Limited | Biphenyl apurinic/apyrimidinic site endonuclease inhibitors to treat cancer |
| JP5039268B2 (ja) | 2001-10-26 | 2012-10-03 | アベンティス・ファーマスーティカルズ・インコーポレイテツド | ベンゾイミダゾールおよび類縁体および蛋白キナーゼ阻害剤としてのその使用 |
| DE60309701T2 (de) | 2002-06-13 | 2007-09-06 | Vertex Pharmaceuticals Inc., Cambridge | 2-ureido-6-heteroaryl-3h-benzoimidazol-4-carbonsäurederivate und verwandte verbindungen als gyrase und/oder topoisomerase iv inhibitoren zur behandlung von bakteriellen infektionen |
| EP1547996A4 (en) * | 2002-08-30 | 2006-08-02 | Bf Res Inst Inc | DIAGNOSTIC PROBES AND REMEDIES FOR DISEASES IN WHICH PRION PROTEIN IS ACCUMULATED, AND ANIMAL FEVERING FOR PRION PROTEIN |
| WO2004041209A2 (en) | 2002-11-01 | 2004-05-21 | Paratek Pharmaceuticals, Inc. | Transcription factor modulating compounds and methods of use thereof |
| EP1742637A4 (en) | 2004-04-23 | 2011-06-08 | Paratek Pharm Innc | TRANSCRIPTION FACTOR MODULATION COMPOUNDS AND METHODS OF USE |
| KR100629060B1 (ko) | 2004-08-11 | 2006-09-26 | 주식회사 엘지화학 | 새로운 벤즈이미다졸계 화합물 |
| ATE482213T1 (de) | 2004-11-04 | 2010-10-15 | Vertex Pharma | Als inhibitoren von proteinkinasen geeignete pyrazoloä1,5-aüpyrimidine |
| US20090069384A1 (en) | 2005-01-19 | 2009-03-12 | Biolipox Ab | Thienopyrroles useful in the treatment of inflammation |
| US7825154B2 (en) | 2005-08-12 | 2010-11-02 | The United States Of America As Represented By The Secretary Of The Army | Small molecule inhibitors of botulinum neurotoxins |
| AU2006311729A1 (en) | 2005-11-07 | 2007-05-18 | Vertex Pharmaceuticals Incorporated | Benzimidazole derivatives as gyrase inhibitors |
| KR100744827B1 (ko) * | 2006-04-05 | 2007-08-01 | 한국화학연구원 | 트리플루오로비닐옥시기를 포함하는 불소계 벤즈이미다졸 단량체 및 이의 제조방법 |
| GB0612428D0 (en) | 2006-06-22 | 2006-08-02 | Prolysis Ltd | Antibacterial agents |
| JP5336375B2 (ja) | 2006-08-30 | 2013-11-06 | セルゾーム リミテッド | キナーゼ阻害剤としてのトリアゾール誘導体 |
| AR063311A1 (es) | 2006-10-18 | 2009-01-21 | Novartis Ag | Compuestos organicos |
| WO2008073451A2 (en) | 2006-12-11 | 2008-06-19 | Sirtris Pharmaceuticals, Inc. | Benzoimidazole derivatives as sirtuin (sir) modulating compounds |
| EP2121626A1 (en) | 2006-12-15 | 2009-11-25 | Pfizer Products Inc. | Benzimidazole derivatives |
| JP5502076B2 (ja) | 2008-06-05 | 2014-05-28 | グラクソ グループ リミテッド | 新規化合物 |
| KR101022649B1 (ko) | 2008-08-07 | 2011-03-22 | 삼성모바일디스플레이주식회사 | 헤테로고리 화합물 및 이를 이용한 유기 전계 발광 장치 |
| US7906655B2 (en) | 2008-08-07 | 2011-03-15 | Bristol-Myers Squibb Company | Hepatitis C virus inhibitors |
| GB0821913D0 (en) | 2008-12-02 | 2009-01-07 | Price & Co | Antibacterial compounds |
| KR101411889B1 (ko) | 2009-02-27 | 2014-06-27 | 이난타 파마슈티칼스, 인코포레이티드 | C형 간염 바이러스 억제제 |
| KR101219487B1 (ko) | 2009-03-03 | 2013-01-15 | 덕산하이메탈(주) | 비스벤조이미다졸 화합물 및 이를 이용한 유기전기소자, 그단말 |
| US8815918B2 (en) | 2009-04-02 | 2014-08-26 | Centro Nacional De Investigaciones Oncologicas (Cnio) | Imidazo [2, 1-B] [1, 3, 4] thiadiazole derivatives |
| US8536180B2 (en) | 2009-05-27 | 2013-09-17 | Abbvie Inc. | Pyrimidine inhibitors of kinase activity |
| CA2763140A1 (en) | 2009-05-29 | 2010-12-02 | Schering Corporation | Antiviral compounds composed of three linked aryl moieties to treat diseases such as hepatitis c |
| WO2010147898A2 (en) | 2009-06-15 | 2010-12-23 | Rigel Pharmaceuticals, Inc. | Small molecule inhibitors of spleen tyrosine kinase (syk) |
| JP5819305B2 (ja) | 2009-10-13 | 2015-11-24 | リガンド・ファーマシューティカルズ・インコーポレイテッド | 造血成長因子模倣小分子化合物およびそれらの使用 |
| ES2568455T3 (es) | 2010-06-01 | 2016-04-29 | Summit Therapeutics Plc | Compuestos para el tratamiento de enfermedad asociada a Clostridium difficile |
-
2008
- 2008-12-02 GB GBGB0821913.1A patent/GB0821913D0/en not_active Ceased
-
2009
- 2009-12-01 US US13/131,469 patent/US8975416B2/en active Active
- 2009-12-01 EP EP09795514.0A patent/EP2373631B1/en active Active
- 2009-12-01 PT PT97955140T patent/PT2373631E/pt unknown
- 2009-12-01 CN CN200980148065.8A patent/CN102227411B/zh active Active
- 2009-12-01 NZ NZ593111A patent/NZ593111A/xx unknown
- 2009-12-01 HR HRP20150518TT patent/HRP20150518T1/hr unknown
- 2009-12-01 SI SI200931191T patent/SI2373631T1/sl unknown
- 2009-12-01 AU AU2009323854A patent/AU2009323854B2/en active Active
- 2009-12-01 BR BRPI0922220A patent/BRPI0922220B8/pt active IP Right Grant
- 2009-12-01 PL PL14197877.5T patent/PL2907813T3/pl unknown
- 2009-12-01 WO PCT/GB2009/002792 patent/WO2010063996A2/en not_active Ceased
- 2009-12-01 DK DK09795514.0T patent/DK2373631T3/en active
- 2009-12-01 LT LTEP14197877.5T patent/LT2907813T/lt unknown
- 2009-12-01 HU HUE14197877A patent/HUE029151T2/hu unknown
- 2009-12-01 MX MX2011005837A patent/MX2011005837A/es active IP Right Grant
- 2009-12-01 RU RU2011127165/04A patent/RU2525915C2/ru active
- 2009-12-01 SG SG2011040458A patent/SG171939A1/en unknown
- 2009-12-01 PT PT141978775T patent/PT2907813T/pt unknown
- 2009-12-01 JP JP2011538052A patent/JP5665756B2/ja active Active
- 2009-12-01 EP EP16155561.0A patent/EP3095783A1/en not_active Withdrawn
- 2009-12-01 RS RS20160458A patent/RS54904B1/sr unknown
- 2009-12-01 BR BR122020013025-3A patent/BR122020013025B1/pt active IP Right Grant
- 2009-12-01 DK DK14197877.5T patent/DK2907813T3/en active
- 2009-12-01 PL PL09795514T patent/PL2373631T3/pl unknown
- 2009-12-01 CA CA2744962A patent/CA2744962C/en active Active
- 2009-12-01 EP EP14197877.5A patent/EP2907813B1/en active Active
- 2009-12-01 ES ES14197877.5T patent/ES2575908T3/es active Active
- 2009-12-01 KR KR1020117015273A patent/KR101643435B1/ko active Active
- 2009-12-01 SI SI200931456A patent/SI2907813T1/sl unknown
- 2009-12-01 ES ES09795514.0T patent/ES2537059T3/es active Active
-
2011
- 2011-05-23 ZA ZA2011/03751A patent/ZA201103751B/en unknown
- 2011-06-02 IL IL213325A patent/IL213325A/en active IP Right Grant
-
2014
- 2014-12-09 JP JP2014249071A patent/JP2015078220A/ja active Pending
-
2015
- 2015-02-06 US US14/616,006 patent/US9314456B2/en active Active
- 2015-05-15 CY CY20151100440T patent/CY1116383T1/el unknown
- 2015-05-18 SM SM201500117T patent/SMT201500117B/xx unknown
-
2016
- 2016-03-08 US US15/064,137 patent/US9763925B2/en active Active
- 2016-06-03 HR HRP20160597TT patent/HRP20160597T1/hr unknown
- 2016-06-24 CY CY20161100572T patent/CY1117934T1/el unknown
- 2016-08-03 SM SM201600259T patent/SMT201600259B/it unknown
- 2016-10-28 JP JP2016212160A patent/JP2017048217A/ja active Pending
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0922220B1 (pt) | uso de compostos antibacterianos, composição farmacêutica e combinação compreendendo os mesmos | |
| JP6150841B2 (ja) | クロストリジウム・ディフィシル関連疾患を治療するための化合物 | |
| WO2011151619A1 (en) | Compounds for the treatment of clostridium difficile associated disease | |
| HK1227868A1 (en) | Antibacterial compositions | |
| HK1227868A (en) | Antibacterial compositions | |
| HK1177706B (en) | Compounds for the treatment of clostridium difficile associated disease |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B25D | Requested change of name of applicant approved |
Owner name: SUMMIT THERAPEUTICS PLC (GB) |
|
| B25A | Requested transfer of rights approved |
Owner name: SUMMIT (OXFORD) LIMITED (GB) |
|
| B07D | Technical examination (opinion) related to article 229 of industrial property law [chapter 7.4 patent gazette] | ||
| B06F | Objections, documents and/or translations needed after an examination request according [chapter 6.6 patent gazette] | ||
| B07E | Notification of approval relating to section 229 industrial property law [chapter 7.5 patent gazette] | ||
| B06U | Preliminary requirement: requests with searches performed by other patent offices: procedure suspended [chapter 6.21 patent gazette] | ||
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] |
Free format text: PRAZO DE VALIDADE: 10 (DEZ) ANOS CONTADOS A PARTIR DE 09/03/2021, OBSERVADAS AS CONDICOES LEGAIS. |
|
| B16C | Correction of notification of the grant [chapter 16.3 patent gazette] |
Free format text: PRAZO DE VALIDADE: 20 (VINTE) ANOS CONTADOS A PARTIR DE 01/12/2009 OBSERVADAS AS CONDICOES LEGAIS. PATENTE CONCEDIDA CONFORME ADI 5.529/DF |