BRPI0922428B1 - 4-fenilpiridazinona e seu uso, composição herbicida, e método para combate de plantas indesejadas - Google Patents
4-fenilpiridazinona e seu uso, composição herbicida, e método para combate de plantas indesejadas Download PDFInfo
- Publication number
- BRPI0922428B1 BRPI0922428B1 BRPI0922428-9A BRPI0922428A BRPI0922428B1 BR PI0922428 B1 BRPI0922428 B1 BR PI0922428B1 BR PI0922428 A BRPI0922428 A BR PI0922428A BR PI0922428 B1 BRPI0922428 B1 BR PI0922428B1
- Authority
- BR
- Brazil
- Prior art keywords
- alkyl
- alkoxy
- phenyl
- halo
- cycloalkyl
- Prior art date
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D237/00—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings
- C07D237/02—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings
- C07D237/06—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members
- C07D237/10—Heterocyclic compounds containing 1,2-diazine or hydrogenated 1,2-diazine rings not condensed with other rings having three double bonds between ring members or between ring members and non-ring members with hetero atoms or with carbon atoms having three bonds to hetero atoms with at the most one bond to halogen, e.g. ester or nitrile radicals, directly attached to ring carbon atoms
- C07D237/14—Oxygen atoms
- C07D237/16—Two oxygen atoms
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N25/00—Biocides, pest repellants or attractants, or plant growth regulators, characterised by their forms, or by their non-active ingredients or by their methods of application, e.g. seed treatment or sequential application; Substances for reducing the noxious effect of the active ingredients to organisms other than pests
- A01N25/32—Ingredients for reducing the noxious effect of the active substances to organisms other than pests, e.g. toxicity reducing compositions, self-destructing compositions
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N43/00—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds
- A01N43/48—Biocides, pest repellants or attractants, or plant growth regulators containing heterocyclic compounds having rings with two nitrogen atoms as the only ring hetero atoms
- A01N43/58—1,2-Diazines; Hydrogenated 1,2-diazines
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01N—PRESERVATION OF BODIES OF HUMANS OR ANIMALS OR PLANTS OR PARTS THEREOF; BIOCIDES, e.g. AS DISINFECTANTS, AS PESTICIDES OR AS HERBICIDES; PEST REPELLANTS OR ATTRACTANTS; PLANT GROWTH REGULATORS
- A01N47/00—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid
- A01N47/02—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having no bond to a nitrogen atom
- A01N47/06—Biocides, pest repellants or attractants, or plant growth regulators containing organic compounds containing a carbon atom not being member of a ring and having no bond to a carbon or hydrogen atom, e.g. derivatives of carbonic acid the carbon atom having no bond to a nitrogen atom containing —O—CO—O— groups; Thio analogues thereof
Landscapes
- Chemical & Material Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Health & Medical Sciences (AREA)
- Pest Control & Pesticides (AREA)
- Engineering & Computer Science (AREA)
- Dentistry (AREA)
- Wood Science & Technology (AREA)
- Zoology (AREA)
- Environmental Sciences (AREA)
- Plant Pathology (AREA)
- Agronomy & Crop Science (AREA)
- Toxicology (AREA)
- Agricultural Chemicals And Associated Chemicals (AREA)
- Plural Heterocyclic Compounds (AREA)
Description
(54) Título: 4-FENILPIRIDAZINONA E SEU USO, COMPOSIÇÃO HERBICIDA, E MÉTODO PARA COMBATE DE PLANTAS INDESEJADAS (51) Int.CI.: C07D 237/16; A01N 43/58 (30) Prioridade Unionista: 19/12/2008 EP 08022104.7 (73) Titular(es): BAYER INTELLECTUAL PROPERTY GMBH (72) Inventor(es): ISOLDE HÀUSER-HAHN; STEFAN LEHR; THOMAS SCHENKE; CHRISTOPHER HUGH ROSINGER; REINER FISCHER; DIETER FEUCHT; JAN DITTGEN; PIERRE CRISTAU; OLIVER GAERTZEN; STEFAN HERRMANN; OLGA MALSAM; EVA MARIA FRANKEN
1/62
Relatório Descritivo da Patente de Invenção para 4FENILPIRIDAZINONA E SEU USO, COMPOSIÇÃO HERBICIDA, E MÉTODO PARA COMBATE DE PLANTAS INDESEJADAS.
A presente invenção refere-se ao campo técnico dos agentes fitoprotetores, particularmente dos herbicidas para o combate seletivo de ervas daninhas de folha larga e gramíneas daninhas em culturas de plantas úteis.
Ela refere-se especificamente a derivados de piridazinonas arilasubstituídas, a processos para sua preparação e ao seu uso como herbicidas e inseticidas.
Várias publicações descrevem 4-fenilpiridazinonas que apresentam propriedades herbicidas. 2-metil-4-fenilpiridazinonas são conhecidas a partir de Stevenson et. al, J. Het. Chem., (2005), 427 ff. O documento W02007/119434 A1 descreve 4-fenilpiridazinonas, que portam um radical alquila na 2a-posição do anel fenila. O documento W02009/035150 A2 descreve 4-fenilpiridazinonas, que podem portar um radical alquila ou alcóxi na 2a-posição do anel fenila e são opcionalmente substituídos nas outras posições por átomos de halogênio ou outros radicais.
Porém, os compostos conhecidos a partir dessas publicações muitas vezes apresentam atividade herbicida insuficiente. Correspondentemente, é objetivo da presente invenção prover compostos de ação herbicida.
Verificou-se que 4-fenilpiridazinonas cujo anel fenila porta determinados substituintes, são particularmente adequadas como herbicidas.
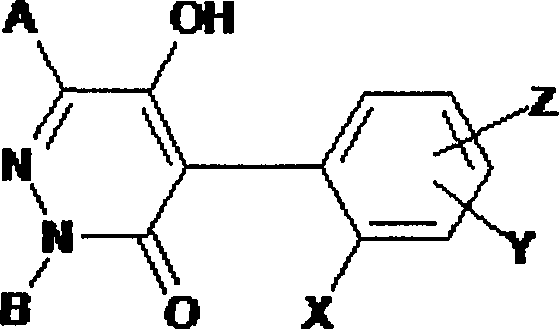
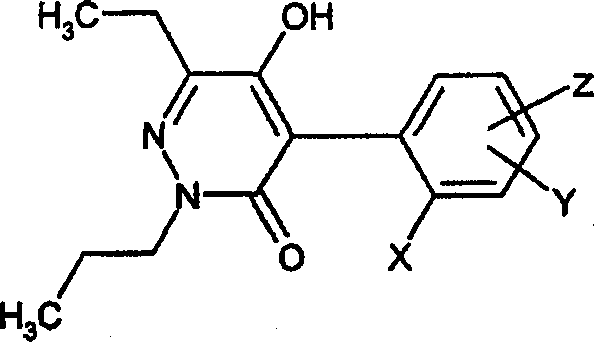
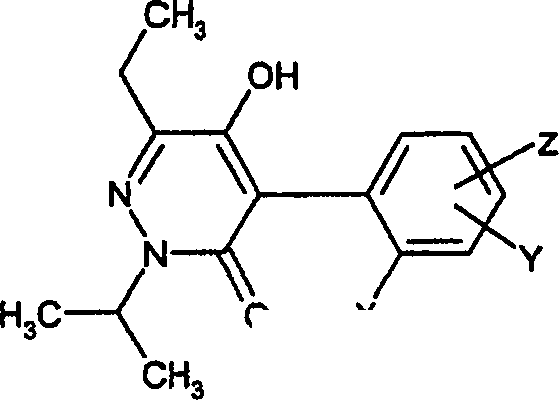
A presente invenção provê 4-fenilpiridazinonas da fórmula (I) ou sais destes
em que
A e B são respectivamente, independentemente entre si hidrogênio ou (Ci-C6)-alquila;
2/62
G é hidrogênio, C(=O)R1, C(=L)MR2, SO2R3, P(=L)R4R5
C(=L)NR6R7 ou E;
E é um equivalente de íon metálico ou um íon de amônio;
L é oxigênio ou enxofre;
M é oxigênio ou enxofre;
R1 é (Ci-C6)-alquila, (C2-C6)-alquenila, (Ci-C4)-alcóxi-(C1Cej-alquila, di-íCrC^-alcôxi-ÍCrCej-alquila ou (C-|-C4)-alquiltio-(C-|-C6)alquila, sendo cada um deles substituído por n átomos de halogênio, um anel de 3 a 6 membros totalmente saturado consistindo em 3 a 5 átomos de carbono e 1 a 3 heteroátomos do grupo consistindo em oxigênio, enxofre e nitrogênio, que é substituído por n radicais do grupo consistindo em halogênio, (CrC4)-alquila e (Ci-C4)-alcóxi, (C3-C6)-cicloalquila, fenila, fenil-(Ci-C4)-alquila, heteroarila, fenóxi-(Ci-C4)-alquila ou heteroarilóxi-(Ci-C4)-alquila substituído por n radicais do grupo consistindo em halogênio, (Ci-C4)-alquila e (Ci-C4)-alcóxi;
R2 é (Ci-C6)-alquila, (C2-C6)-aiquenila, (Ci-C4)-alcóxi-(Ci-C6)alquila ou di-(Ci-C4)-alcóxi-(C1-C6)-alquila, cada um deles sendo substituído por n átomos de halogênio, ou é (C3-C6)-cicloalquila, fenila ou benzila, cada um deles sendo substituído por n radicais do grupo consistindo em halogênio, (Ci-C4)-alquila e (Ci-C4)-alcóxi;
R3, R4 e R5 são respectivamente independentemente entre si (Ci-Ce)-alquila, que é substituída por n átomos de halogênio, (Ci-C4)-alcóxi, N-(Ci-C6)-alquilamino, N,N-di-(Ci-C6)-alquilamino, (Ci-C4)-alquiltio, (C2-C4)alquenila ou (C3-C6)-cicloalquiltio, ou fenila, benzila, fenóxi ou feniltio, que é substituído por n radicais do grupo consistindo em halogênio, (Ci-C4)-alquila e (CrC4)-alcóxi;
R6 e R7 são respectivamente independentemente entre si hidrogênio, (Ci-C6)-alquila que é substituída por n átomos de halogênio, (C3-C6)cicloalquila, (C2-C6)-alquenila, (Ci-C6)-alcóxi ou (Ci^j-alcóxi-ÍCi-Ce)alquiia, fenila ou benzila, sendo cada um deles substituído por n radicais do grupo consistindo em halogênio, (Ci-C4)-alquila e (CrC4)-alcóxi;
3/62 ou R6e R7 juntos com o átomo de nitrogênio ao qual eles estão ligados, formam um anel de 3 a 6 membros que contém 2 a 5 átomos de carbono e 0 ou 1 átomo de oxigênio ou de enxofre;
m é 1,2 ou 3; n é 0, 1,2 ou 3;
X é halogênio, ciano, (C3-C6)-cicloalquila, nitro ou é (CrCe)alquila ou (Ci-CeFalcóxi, sendo cada um deles substituído por m átomos de halogênio ou fenila substituída por n átomos de halogênio;
Y e Z são respectivamente independentemente entre si hidrogênio, halogênio, ciano, nitro, (C3-C6)-cicloalquila ou são (Ci-C6)-alquila, (CiC6)-alcóxi ou fenila, cada um sendo substituído por n átomos de halogênio, com a condição de que nem Y nem Z é um radical (Ci-C6)-alquila ou (Ci-Cej-alcóxi situado na posição 6, se n for 0.
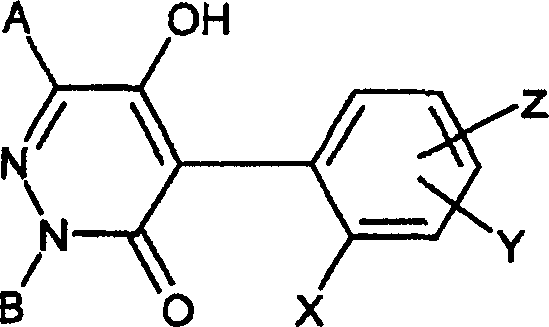
Se G e/ou B forem hidrogênio, os compostos da fórmula (I), de acordo com a invenção, dependendo de condições externas tais como pH, solvente e temperatura, podem estar presentes em várias estruturas tautoméricas que são todas abrangidas pela fórmula geral (I):
Em todas as estruturas abaixo, os substituintes, desde que nada diferente esteja definido, apresentam o mesmo significado conforme indica20 do acima para os compostos da fórmula (I).
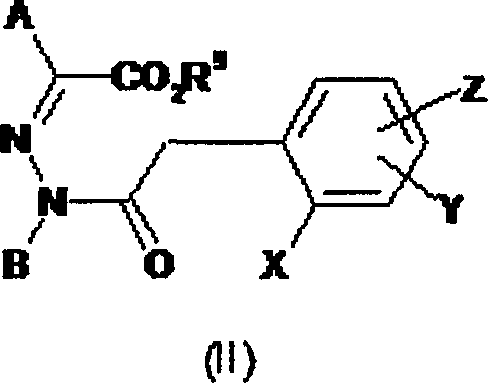
Compostos da fórmula (I), de acordo com a invenção, na qual G é hidrogênio, podem ser preparados, por exemplo, de acordo com o método indicado no esquema 1 pela reação de condensação base-induzida de com4/62 postos da fórmula (II). Neste caso, R9 é (Ci-C6)-alquila, particularmente metila ou etila.
Esquema 1
Os compostos da fórmula (II) podem ser preparados, por exemplo, de acordo com o método indicado no esquema 1a mediante reação de derivados de ácido hidrazonocarboxílico com derivados de ácido fenilacético. Neste caso, U é um grupo de saída introduzido por reagentes para ativação de ácidos carboxílicos, tais como carbonildiimidazóis, carbonildiimidas (tais como, por exemplo, diciclo-hexilcarbodiimida), agentes de fosforilação (tais como, por exemplo, POCI3, BOP-CI), agentes de halogenação tais como, por exemplo, cloreto de tionila, cloreto de oxalila, fosgênio ou ésteres clorofórmicos. Tais métodos também são conhecidos pelo versado na técnica, a partir do document W02007/119434, BCS07-3099 e dos documentos citados aqui.
Esquema 1a
Compostos da fórmula (II) também podem ser preparados, por exemplo, de acordo com o método apresentado no esquema 1b, mediante a reação, conhecido pelo versado na técnica na forma de Zh. Obs. Khim. 1992, 62, 2262, de hidrazidas (lia) com ácidos cetocarboxílicos da fórmula
A-CO-CO2R9·
5/62
Esquema 1b
As hidrazidas da fórmula (lia) mostradas no esquema 1b, podem ser preparadas, por exemplo, pela reação das hidrazinas da fórmula B-NHNH2 com os derivados de ácido fenilacético mostrados no esquema 1a, de acordo com o método descrito em J. Org. Chem. 1980, 45, 3673. As hidrazidas mostradas no esquema 1a podem ser preparadas a partir dos ácidos cetocarboxílicos A-CO-CO2R9 mostrados no esquema 1b, que são conhecidos per se, por exemplo de acordo com os métodos descritos em J. Med. Chem. 1985 (28), 1436.
Os ácidos livres fenilacéticos necessários para os derivados de ácido fenilacético mostrados no esquema 1a, isto é, aqueles nos quais U é hidroxila, são conhecidos ou podem ser preparados por processos conhecidos per se, por exemplo a partir dos documentos WO 2005/075401, WO 2001/96277, WO 1996/35664 e WO 1996/25395.
Porém, determinados derivados de ácido fenilacéticos também podem ser preparados utilizando-se enolatos de éster acético na presença de catalisadores de paládio, por exemplo, formados a partir da fonte de paládio (por exemplo Pd2(dba)3 ou Pd(Oac)2) e um ligante (por exemplo (t-Bu)3P, iMes*HCI ou 2'-(N,N-dimetilamino)-2-(diciclo-hexiÍfosfanil)bifenil) (WO 2005/048710, J. Am. Chem. Soc 2002. 124,. 12557, J. Am. Chem. Soc 2003. 125, 11176 or J. Am. Chem. Soc. 2001, 123, 799). Adicionalmente, determinados haletos de arila substituídos podem ser convertidos sob catálise de cobre nos ésteres malônicos substituídos correspondentes (por exemplo, descritos em Org. Lett. 2002, 2, 269, WO 2004/108727), que podem ser convertidos por métodos conhecidos em ácidos fenilacéticos.
Compostos da fórmula (I), de acordo com a invenção, na qual G é hidrogênio, podem ser preparados também, por exemplo, de acordo com o
6/62 método indicado no esquema 2, mediante reação dos compostos da fórmula (I), na qual G é alquila, preferivelmente metila, com bases minerais fortes tais como hidróxido de sódio ou hidróxido de potássio, ou em ácidos minerais concentrados tais como ácido bromídrico.
Compostos da fórmula (I) de acordo com a invenção, na qual G é C(=O)R1, também podem ser preparados, por exemplo, mediante reações conhecidas pelo versado na técnica no tipo de compostos da fórmula (I), na qual G é hidrogênio com haletos de carbonila da fórmula Hal-CO-R1 ou com anidridos carboxílicos da fórmula R1-CO-O-CO-R1
Compostos da fórmula (I), de acordo com a invenção, na qual G é C(=L)MR2 podem também ser preparados, por exemplo, mediante reações conhecidas pela versado na técnica no tipo de compostos da fórmula (I), na qual G é hidrogênio, com a) ésteres clorofórmicos ou tioésteres clorofórmicos da fórmula R2-M-COOR1 ou b) com haletos de cloroformila ou tiohaletos de cloroformila.
Compostos da fórmula (I), de acordo com a invenção, na qual G é SO2R3 também podem ser preparados, por exemplo, mediante reações conhecidas pelo versado na técnica no tipo de compostos da fórmula (I), na qual G é hidrogênio com cloretos de sulfonila da fórmula R3-SC>2-CI.
Compostos da fórmula (I), de acordo com a invenção, na qual G é P(=L)R4R5 podem também ser preparados, por exemplo, mediante reações conhecidas pelo versado na técnica o tipo de compostos da fórmula (I) na qual G é hidrogênio com cloretos de fosforila da fórmula Hal-P(=L)R4R5.
Compostos da fórmula (I) de acordo com a invenção, na qual G é E, também podem ser preparados, por exemplo, mediante reações conhecidas pelo versado na técnica no tipo de compostos da fórmula (I), na qual G
7/62 é hidrogênio com compostos metálicos da fórmula Me(OR10)t ou com aminas.Neste caso, um íon metálico mono- ou divalente, preferivelmente um metal alcalino ou alcalinoterroso tais como lítio, sódio, potássio, magnésio ou cálcio. O índice é 1 ou 2. Um íon de amônio é o grupo NH4+ ou r13r14r15r16N+ no qual R13, R14, R15e R16 independentemente entre si são preferivelmente (Ci-C6)-alquila ou benzila.
Compostos da fórmula (I) de acordo com a invenção na qual G é C(=L)NR®R7, também podem ser preparados, por exemplo, mediante reações conhecidas pelo versado na técnica de compostos da fórmula (I) na qual G é hidrogênio com isocianatos ou isotiocianatos da fórmula R6-N=C=L ou com cloretos de carbonila ou cloretos de tiocarbamoila da fórmula R6R7NC(=L)CI.
Compostos da fórmula (I), de acordo com a invenção, na qual G é alquila, preferivelmente metila, também podem ser preparados, por exemplo, de acordo com o esquema 3 mediante reações conhecidas pelo versado na técnica no tipo de compostos da fórmula (III) com compostos da fórmula (IV). Neste caso, Z’ é brometo ou iodeto e Q é um grupo trialquiltina, um grupo haleto de magnésio ou, preferivelmente, um ácido borônico ou um éster deste. Essas reações são usualmente feitas na presença de um catalisador (por exemplo um sal Pd ou um complexo Pd) e na presença de uma base (por exemplo carbonato de sódio, fosfato de potássio).
Dependendo da natureza dos substituintes acima definidos, os compostos da fórmula (I) apresentam propriedades acídicas ou básicas e também podem formar sais, se necessário sais internos ou adutos, com ácidos ou bases inorgânicos ou orgânicos ou com íons metálicos. Se os com8/62 postos da fórmula (I) portarem grupos amino, grupos alquilamino ou outros grupos que induzam propriedades básicas, estes compostos poderão ser reagidos com ácidos ou sais, ou eles serão diretamente obtidos como sais na síntese.
Exemplos de ácidos inorgânicos são ácidos hidroálicos tais como ácido fluorídrico, ácido clorídrico, ácido bromídrico e ácido iodídrico, ácido sulfúrico, ácido fosfórico e ácido nítrico, e sais acídicos tais como NaHSO4 e KHSO4.
Ácidos orgânicos adequados são, por exemplo, ácido fórmico, ácido carbônico e ácidos alcanoicos tais como ácido acético, ácido trifluoroacético, ácido tricloroacético e ácido propiônico e também ácido glicólico, ácido tiociânico, ácido lático, ácido succínico, ácido cítrico, ácido benzoico, ácido cinâmico, ácido oxálico, ácidos alquilsulfônicos (ácidos sulfônicos que apresentam cadeia linear ou radicais alquila ramificados de 1 a 20 átomos de carbono), ácidos arilsulfônicos ou ácidos dissulfônicos (radicais aromáticos tais como fenila e naftila que portam um ou dois grupos ácido sulfônico), ácidos alquilfosfônicos (ácidos fosfônicos que apresentam radicais alquila de cadeia linear ou ramificados contendo de 1 a 20 átomos de carbono), ácidos arilfosfônicos ou - ácidos difosfônicos (radicais aromáticos tais como fenila e naftila que portam um ou dois radicais ácido fosfônico), em que os radicais alquila ou arila podem portar outros substituintes, por exemplo ácido p-toluenossulfônico, ácido salicílico, ácido p-aminossalicílico, ácido 2-fenoxibenzoico, ácido 2-acetoxibenzoico, etc.
íons metálicos adequados são particularmente os íons dos elementos do Segundo grupo principal, particularmente cálcio e magnésio, o terceiro e quarto grupo principal, particularmente alumínio, estanho e chumbo, e também do primeiro ao oitavo grupo de transição, particularmente cromo, manganês, ferro, cobalto, níquel, cobre, zinco e outros. São particularmente preferidos íons metálicos dos elementos do quarto período. Neste caso, os metais podem estar presentes nas diferentes valências que eles podem assumir.
9/62
Se os compostos da fórmula (I) portarem grupos hidroxila, grupos carboxila ou outros grupos que induzam propriedades acídicas, esses compostos poderão ser reagidos com bases formando sais.
Base adequadas são, por exemplo, hidróxidos, carbonatos, bicarbonatos dos metais alcalinos ou alcalinoterrosos, particularmente aqueles de sódio, potássio, magnésio e cálcio, além disso amônio, aminas primárias, secundárias e terciárias contendo grupos (Ci-C4)-alquila, mono-, di- e trialcanolaminas de (Ci-C4)-alcanóis, colinas e também clorocolinas.
Halogênio é flúor, cloro, bromo e iodo.
Um equivalente de íon metálico é um íon metálico que apresenta uma carga positiva tais como Na+, K+, (Mg2+)i/2, (Ca2+)v2, MgH+, CaH+, (AI3+)i,3 (Fe2+)1/2 ou (Fe3+)1/3.
Alquila é um radical de cadeia linear ou ramificada saturado contendo de 1 a 8 átomos de carbono, por exemplo Ci-C6-alquila, tais como metila, etila, propila, 1-metiletila, butila, 1-metilpropila, 2-metilpropila, 1,1dimetiletila, pentila, 1-metilbutila, 2-metilbutila, 3-metilbutila, 2,2-dimetilpropila, 1-etilpropila, hexila, 1,1-dimetilpropila, 1,2-dimetilpropila,1-metilpentila,
2-metilpentila, 3-metilpentila, 4-metilpentila, 1,1-dimetilbutila, 1,2-dimetilbutila, 1,3-dimetilbutila, 2,2-dimetilbutila, 2,3-dimetilbutila, 3,3-dimetilbutila, 1-etilbutila, 2-etilbutila, 1,1,2-trimetilpropila, 1,2,2-trimetiipropila, 1-etil-1metilapropila e 1-etil-2-metilpropila.
Haloalquila é um grupo alquila de cadeia linear ou ramificado contendo de 1 a 8 átomos de carbono (conforme acima mencionado), em que alguns ou todos os átomos de hidrogênio neste grupo podem ser substituídos por átomos de halogênio, por exemplo Ci-C2-haloalquila tais como clorometila, bromometila, diclorometila, triclorometila, fluorometila, difluorometila, trifluorometila, clorofluorometila, diclorofluorometila, clorodifluorometila, 1-cloroetila, 1-bromoetila, 1-fluoroetila, 2-fluoroetila, 2,2difluoroetila, 2,2,2-trifluoroetila, 2-cloro-2-fluoroetila, 2-cloro-2,2-difluoroetila,
2,2-dicloro-2-fluoroetila, 2,2,2-tricloroetila, pentafluoroetila e 1,1,1trifluoroprop-2-ila.
Alquenila é um radical hidrocarboneto de cadeia linear ou ramifi10/62 cado insaturado contendo de 2 a 8 átomos de carbono e uma ligação dupla em qualquer posição, por exemplo C2-C6-alquenila tais como etenila, 1-propenila, 2-propenila, 1-metiletenila, 1-butenila, 2-butenila, 3-butenila, 1-metil1-propenila, 2-metil-1-propenila, 1-metil-2-propenila, 2-metil-2-propenila, 1-pentenila, 2-pentenila, 3-pentenila, 4-pentenila, 1-metil-1-butenila, 2-metíl1- butenila, 3-metil-1-buteníla, 1-metil-2-butenila, 2-metil-2-butenila, 3-metil-2butenila, 1-metil-3-butenila, 2-metil-3-butenila, 3-metil-3-butenila, 1,1-dimetil2- propenila, 1,2-dimetil-1-propenila, 1,2-dimetil-2-propenila, 1-etil-1-propenila, 1-etil-2-propenila, 1-hexenila, 2-hexenila, 3-hexenila, 4-hexenila, 5-hexenila, 1-metil-1-pentenila, 2-metil-1-pentenila, 3-metil-1-pentenila, 4-metil-1pentenila, 1-metil-2-pentenila, 2-metil-2-pentenila, 3-metil-2-pentenila, 4-metil-2-pentenila, 1-metil-3-pentenila, 2-metil-3-pentenila, 3-metil-3-pentenila, 4-metil-3-pentenila, 1-metil-4-pentenila, 2-metil-4-pentenila, 3-metil-4pentenila, 4-metil-4-pentenila, 1,1-dimetil-2-butenila, 1,1-dimetil-3-butenila,
1.2- dimetil-1-butenila, 1,2-dimetil-2-butenila, 1,2-dimetil-3-butenila, 1,3dimetil-1-butenila, 1,3-dimetil-2-butenila, 1,3-dimetil-3-butenila, 2,2-dimetil-3butenila, 2,3-dimetil-1-butenila, 2,3-dimetil-2-butenila, 2,3-dimetil-3-butenila,
3.3- dimetil-1-butenila, 3,3-dimetil-2-butenila, 1-etil-1-butenila, 1-etil-2-butenila, 1-etil-3-butenila, 2-etil-1-butenila, 2-etil-2-butenila, 2-etil-3-butenila,
1.1.2- trimetil-2-propenila, 1-etil-1-metil-2-propenila, 1-etil-2-metil-1-propenila e 1-etil-2-metil-2-propenila.
Alcóxi é um radical alcóxi de cadeia linear ou ramificado contendo de 1 a 8 átomos de carbono, por exemplo, Ci-C6-alcóxi tais como metóxi, etóxi, propóxi, 1-metiletóxi, butóxi, 1-metilpropóxi, 2-metilpropóxi, 1,1dimetiletóxi, pentóxi, 1-metilbutóxi, 2-metilbutóxi, 3-metilbutóxi, 2,2dimetilpropóxi, 1-etilpropóxi, hexóxi, 1,1-dimetilpropóxi, 1,2-dimetilpropóxi,1metilpentóxi, 2-metilpentóxi, 3-metilpentóxi, 4-metilpentóxi, 1,1-dimetilbutóxi,
1.2- dimetilbutóxi, 1,3-dimetilbutóxi, 2,2-dimetilbutóxi, 2,3-dimetilbutóxi, 3,3dimetilbutóxi, 1-etilbutóxi, 2-etilbutóxi, 1,1,2-trimetilpropóxi, 1,2,2-trimetilpropóxi, 1-etil-1-metilpropóxi e 1-etil-2-metilpropóxi;
Haloalcóxi é um grupo alcóxi de cadeia linear ou ramificado contend de 1a 8 átomos de carbono (conforme acima mencionado), sendo que
11/62 alguns ou todos os átomos de hidrogênio neste grupo podem ser substituídos por átomos de halogênio conforme acima mencionado, por exemplo CiC2-haloalcóxi, tais como clorometóxi, bromometóxi, diclorometóxi, triclorometóxi, fluorometóxi, difluorometóxi, trifluorometóxi, clorofluorometóxi, diclorofluorometóxi, clorodifluorometóxi, 1-cloroetóxi, 1-bromoetóxi, 1-fluoroetóxi, 2fluoroetóxi, 2,2-difluoroetóxi, 2,2,2-trifluoroetóxi, 2-cloro-2-fluoroetóxi, 2-clor2.2- difluoroetóxi, 2,2-dicloro-2-fluoroetóxi, 2,2,2-tricloroetóxi, pentafluoroetóxi e 1,1,1 -trifluoroprop-2-óxi.
Alquiltio é um radical alquiltio de cadeia linear ou ramificado saturado contendo de 1 a 8 átomos de carbono, por exemplo, Ci-C6-alquiltio tais como metiltio, etiltio, propiltio, 1-metiletiltio, butiltio, 1-metil-propiltio, 2metilpropiltio, 1,1-dimetiletiltio, pentiltio, 1-metilbutiltio, 2-metilbutiltio, 3-metilbutiltio, 2,2-di-metilpropiltio, 1-etilpropiltio, hexiltio, 1,1-dimetilpropiltio, 1,2-dimetilpropiltio,1-metilpentiltio, 2-metilpentiltio, 3-metilpentiltio, 4-metilpentiltio, 1,1-dimetilbutiltio, 1,2-dimetilbutiltio, 1,3-dimetil-butiltio, 2,2-dimetilbutiltio,
2.3- dimetilbutiltio, 3,3-dimetilbutiltio, 1-etilbutiltio, 2-etilbutiltio, 1,1,2-trimetilpropiltio, 1,2,2-trimetilpropiltio, 1-etil-1-metilpropiltio e 1-etil-2-metilpropiltio;
Haloalquiltio é um grupo alquiltio de cadeia linear ou ramificado contendo de 1 a 8 átomos de carbono (conforme acima mencionado), em que alguns ou todos os átomos de hidrogênio neste grupo podem ser substituídos por átomos de halogênio conforme acima mencionado, por exemplo Ci-C2-haloalquiltio tais cmo clorometiltio, bromometiltio, diclorometiltio, triclorometiltio, fluorometiltio, difluorometiltio, trifluorometiltio, clorofluorometiltio, diclorofluorometiltio, clorodifluorometiltio, 1-cloroetiltio, 1-bromoetiltio, 1fluoroetiltio, 2-fluoroetiltio, 2,2-difluoroetiltio, 2,2,2-trifluoroetiltio, 2-cloro-2fluoroetiltio, 2-cloro-2,2-difluoroetiltio, 2,2-dicloro-2-fluoroetiltio, 2,2,2tricloroetiltio, pentafluoroetiltio e 1,1,1-trifluoroprop-2-iltio.
Heteroarila é 2-furila, 3-furila, 2-tienila, 3-tienila, 1-pirrolila, 2pirrolila, 3-pirrolila, 3-isoxazolila, 4-isoxazolila, 5-isoxazolila, 3-isotiazolila, 4isotiazoiila, 5-isotiazolila, 1-pirazolila, 3-pirazolila, 4-pirazolila, 5-pirazolila, 2oxazolila, 4-oxazolila, 5-oxazolila, 2-tiazolila, 4-tiazolila, 5-tiazolila, 1-imidazolila, 2-imidazolila, 4-imidazolila, 5-imidazolila, 1,2,4-oxadiazol-3-ila, 1,2,4-oxadiazol12/62
5-ila, 1,2,4-tiadiazol-3-ila, 1,2,4-tiadiazol-5-ila, 1,3,4-oxadiazol-2-ila, 1,3,4tiadiazol-2-ila, 1,2,4-triazol-1-ila, 1,2,4-triazol-3-ila, 1,2,4-triazol-4-ila, 1,2,4triazol-5-ila, 1,2,3-triazol-1-ila, 1,2,3-triazol-2-ila, 1,2,3-triazol-4-ila, tetrazol-1-ila, tetrazol-2-ila, tetrazol-5-ila, indol-1-ila, indol-2-ila, indol-3-ila, isoindol-1-ila, isoindol-2-ila, benzofur-2-ila, benzotiofen-2-ila, benzofur-3-ila, benzotiofen-3-ila, benzoxazol-2-ila, benzotiazol-2-ila, benzimidazol-2-ila, indazol-1-ila, indazol-2-ila, indazol-3-ila, 2-piridinila, 3-piridinila, 4-piridinila, 3-piridazinila, 4-piridazinila, 2pirimidinila, 4-pirimidinila, 5-pirimidinila, 2-pirazinila, 1,3,5-triazin-2-ila, 1,2,4triazin-3-ila, 1,2,4-triazin-5-ila ou 1,2,4-triazin-6-ila. Este heteroarila é respectivamente não substituído ou mono- ou polissubstituído por radicais idênticos ou diferentes selecionados do grupo consistindo em flúor, cloro, bromo, iodo, ciano, hidroxila, mercapto, amino, metila, etila, n-propila, isopropila, n-butila, isobutila, sec-butila, tert-butila, ciciopropila, 1-clorociclopropila, vinila, etinila, metóxi, etóxi, isopropóxi, metiltio, etiltio, trifluorometiltio, clorodifluorometila, diclorofluorometila, clorofluorometila, clorometila, diclorometila, triclorometila, fluorometila, difluorometila, trifluorometila, 2,2,2-trifluoretila, trifluorometóxi, trifluorometiltio,
2,2,2-trifluoroetóxi, 2,2-dicloro-2-fluoroetila, 2,2-difluoro-2-cloroetila, 2-cloro-2fluoroetila, 2,2,2-tricloroetila, 2,2,2-trifluoroetila, 2-fluoroetila, 2,2-difluoroetila, 2metoxietóxi, acetila, propionila, metoxicarbonila, etoxicarbonila, N-metiiamino, Ν,Ν-dimetilamino, N-etilamino, Ν,Ν-dietilamino, aminocarbonila, metilaminocarbonila, dimetilaminocarbonila, dimetilacarbamoilamino, metoxicarbonilamino, metoxicarbonilóxi, etoxicarbonilamino, etoxicarbonilóxi, metilsulfamoila, dimetilsulfamoila, fenila ou fenóxi.
Dependendo da natureza dos substituintes, os compostos da fórmula (I) podem estar presentes como isômeros geométricos e/ou ópticos ou misturas isoméricas de composição variável que, se necessário, podem ser separados da forma convencional. A presente invenção provê tanto isômeros puros e as misturas isoméricas, à sua preparação e ao uso e composições que os compreendem. Porém, nas partes que se seguem, para fins de maior simplicidade, referem-se sempre a compostos da fórmula (I), embora isto implique tanto os compostos puros como, se necessário, misturas que apresentam proporções variáeis de compostos isoméricos.
13/62
Se um grupo for várias vezes substituído por radicais, isso implica que este grupo é substituído por um ou mais radicais idênticos ou diferentes a partir dos radicais mencionados.
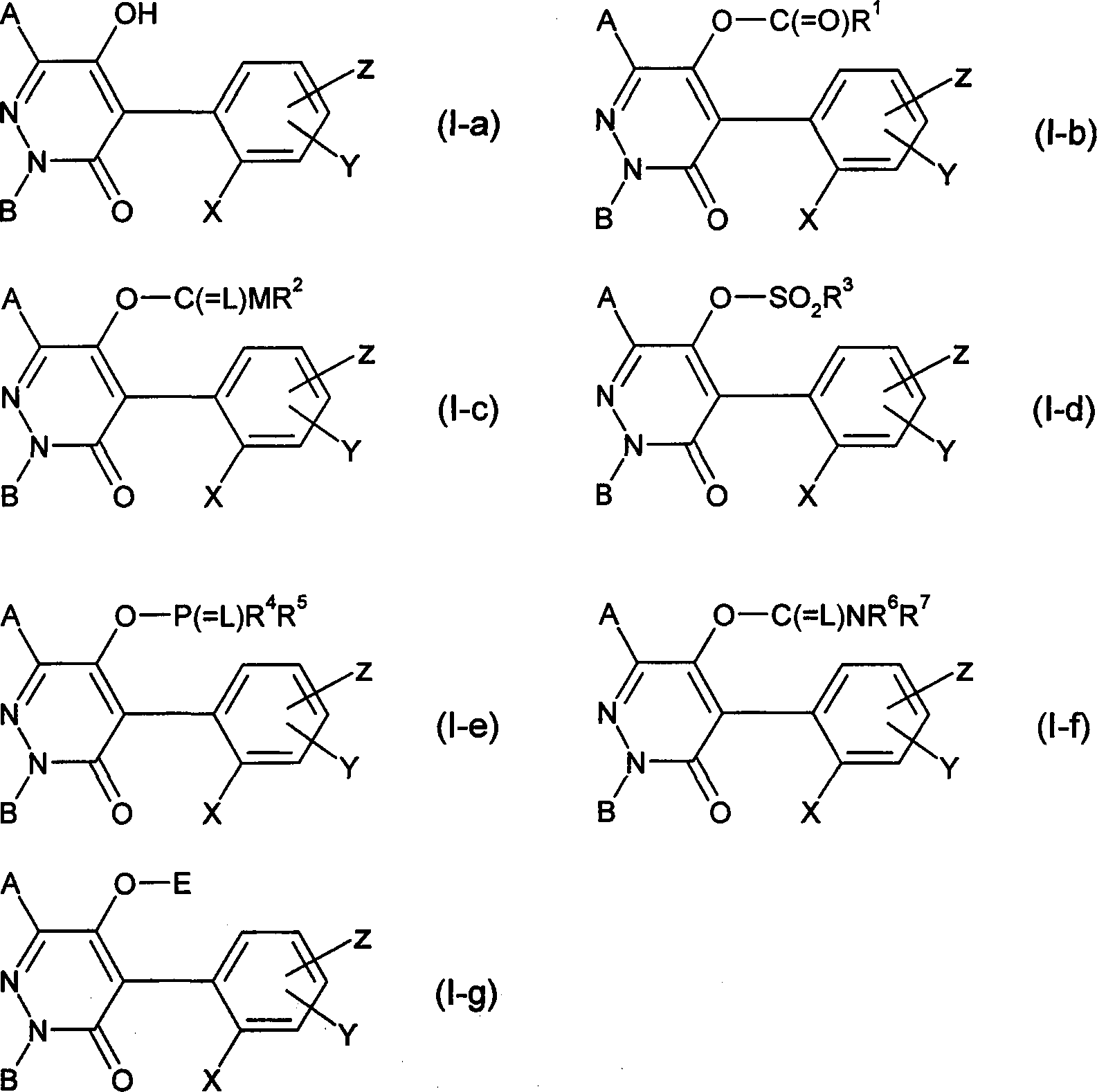
São preferidos compostos das fórmulas gerais (l-a), (l-b), (l-c), 5 (l-d), (l-e), (l-f) e (l-g)
São preferidos compostos da fórmula geral (I) na qual A é hidrogênio ou (Ci-C6)-alquila;
B é hidrogênio ou (Ci-Cej-alquila;
G é hidrogênio, C(=O)R1, C(=L)MR2, SO2R3, P(=L)R4R5,
C(=L)NR6R7, ou E;
E é Na+, K+, (Mg2+)i/2, (Ca2+)1/2, R13R14R15R16N+ ou NH4+;
R , R , R e R sao independentemente entre si (Ci-C6)alquila ou benzila;
14/62
L é oxigênio;
M é oxigênio;
R1 é (Ci-C6)-alquila, que é substituída por n átomos de halogênio ou é (C3-C6)-cicloalquila, fenila ou fenil-(Ci-C4)-alquila, é respectivamente substituída por n radicais do grupo consistindo em halogênio, (CiC4)-alquila e (Ci-C4)-alcóxi;
R2 é (Ci-Cej-alquila, que é substituída por n átomos de halogênio ou é (C3-C6)-cicloalquila, fenila ou benzila, respectivamente é substituída por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (Ci-C4)-alcóxi;
R3, R4e R5 respectivamente independentemente entre si (CiC6)-alquila, que é substituída por n átomos de halogênio ou são fenila ou benzila que são substituídas por n radicais do grupo consistindo em halogênio, (Ci-C4)-alquila e (Ci-C4)-alcóxi;
R6 e R7 são respectivamente independentemente entre si hidrogênio, (Ci-C6)-alquila, que é substituída por n átomos de halogênio ou fenila ou benzila que são substituídas por n radicais do grupo consistindo em halogênio, (Ci-C4)-alquila e (Ci-C4)-alcóxi;
m é 0, 1, 2 ou 3;
n é 0,1, 2, 3, com a condição de que m e n não são 0;
X é halogênio, ciano, (C3-C6)-cicloalquila, nitro ou é (Ci-C6)alquila ou (Ci-C6)-alcóxi, cada um sendo substituído por m átomos de halogênio;
Y e Z são respectivamente independentemente entre si hidrogênio, halogênio, ciano, nitro, (C3-C6)-cicloalquila ou são (Ci-C6)-alquila, (CiC6)-alcóxi ou fenila, sendo cada um substituído por n átomos de halogênio.
São preferidos compostos da fórmula geral (I), na qual
A é hidrogênio, metila, etila, isobutila;
B é hidrogênio, metila, etila, isobutila, ter-butila;
G é hidrogênio, C(=O)R1, C(=L)MR2, SO2R3, P(=L)R4R5, C(=L)NR6R7 ou E;
E é Na+, K+, (Mg2+)i/2, (Ca2+)i/2, (CH3)4N+ ou NH4 +;
15/62
L é oxigênio;
M é oxigênio;
R1 é (Ci-C6)-alquila ou (C3-C6)-cicloalquila;
R2 é (Ci-C6)-alquila, (C3-C6)-cicloalquila ou benzila;
R3, R4 e R5 são respectivamente independentemente entre si (Ci-C6)-aiquila, fenila ou benzila;
R6 e R7 são respectivamente independentemente entre si hidrogênio, (Ci-Cej-alquila, fenila ou benzila;
m é 1, 2 ou 3; n é 0, 1, 2 ou 3; e
X é flúor, bromo, cloro, iodo, ciano, nitro, trifluorometila, trifluorometóxi ou ciclopropila;
Y é hidrogênio, flúor, bromo, cloro, iodo, metila, etila, metóxi, etóxi, trifluorometila, trifluorometóxi ou ciclopropila;
Z é hidrogênio, flúor, bromo, cloro, iodo, metila, etila, metóxi, etóxi, trifluorometila, trifluorometóxi, ciclopropila, clorofenila ou fluorofenila.
São muito particularmente preferidos compostos da fórmula geral (I) relacionados nas tabelas 1 a 25, que podem ser obtidos de forma análoga aos métodos aqui mencionados.
As abreviações usadas são definidas abaixo:
| Bz = Benzila | c-Pr = Ciclopropila | Et | Etila |
| i-Bu = Isobutila | t-Bu = Butila terciária | i-Pr = | Isopropila |
| Me = metila | Ph = fenila |
16/62
Tabela 1: Compostos da fórmula geral (I), de acordo com a invenção na qual G é hidrogênio e A e B são respectivamente metila.
| N°. | X | Y | Z |
| 1 | F | H | H |
| 2 | Cl | H | H |
| 3 | Br | H | H |
| 4 | I | H | H |
| 5 | cf3 | H | H |
| 6 | CN | H | H |
| 7 | no2 | H | H |
| 8 | ocf3 | H | H |
| 9 | H | 3-CF3 | H |
| 10 | H | 3-Me | H |
| 11 | H | 3-F | H |
| 12 | H | 3-CI | H |
| 13 | H | 3-CN | H |
| 14 | H | 3-Brl | H |
| 15 | H | 3-I | H |
| 16 | H | 3-NO2 | H |
| 17 | H | 3-OCF3 | H |
| 18 | H | 3-OMe | H |
| 19 | H | 3-OEt | H |
| 20 | H | 4-CF3 | H |
| 21 | H | 4-Me | H |
| 22 | H | 4-F | H |
| 23 | H | 4-CI | H |
| 24 | H | 4-CN | H |
17/62
| Ν°. | X | Y | Z |
| 25 | Η | 4-Br | H |
| 26 | Η | 4-I | H |
| 27 | Η | 4-NO2 | H |
| 28 | Η | 4-OCF3 | H |
| 29 | Η | 4-OMe | H |
| 30 | Η | 4-OEt | H |
| 31 | CI | 4-CI | H |
| 32 | Η | 3-CI | 4-CI |
| 33 | Br | 4-CI | H |
| 34 | Cl | H | 6-CI |
| 35 | Cl | H | 6-F |
| 36 | F | H | 6-F |
| 37 | Cl | 4-CI | 6-CI |
| 38 | Br | 4-Me | 6-Br |
| 39 | Cl | 4-Me | 6-CI |
| 40 | I | H | 4-Me |
| 41 | I | 6-CI | 4-Me |
| 42 | c-Pr | 4H | H |
| 43 | c-Pr | 4-Me | H |
| 44 | c-Pr | 4-Me | 6-CI |
| 45 | Cl | 6-F | 3-Me |
| 46 | F | 6-F | 3-F |
| 47 | F | 6-F | 3-OEt |
| 48 | F | H | 5-CI |
| 49 | H | 3-CF3 | 5-CF3 |
| 50 | ocf3 | 4-Me | H |
| 51 | ocf3 | 5-Me | H |
| 52 | Br | 4-OCF3 | 6-CI |
| 53 | Br | 4-OCF3 | 6-Br |
| 54 | Cl | 4-OCF3 | 6-CI |
18/62
| N°. | X | Y | Z |
| 55 | ocf3 | 6-CI | 4-Br |
| 56 | ocf3 | 6-CI | 4-Me |
| 57 | Cl | 5-OCF3 | H |
| 58 | Br | 5-OCF3 | H |
| 59 | Cl | 6-CF3 | H |
| 60 | Cl | 3-CI | 6-CF3 |
| 61 | Cl | 3-F | 6-F |
| 62 | Cl | 4-CI | 6-c-Pr |
| 63 | Cl | 3-CI | H |
| 64 | Br | 4-Br | 6-OCF3 |
| 65 | Br | 4-CI | 6-OCF3 |
| 68 | Cl | 4-Br | 6-CF3 |
| 69 | Br | 4-CI | 6-CF3 |
| 70 | cf3 | 5-CF3 | H |
| 71 | F | 3-F | H |
| 72 | Cl | 4-CI | 6-c-Pr |
| 73 | F | 3-Me | 6-F |
| 74 |
Tabela 2: Compostos da fórmula geral (I), de acordo com a invenção na qual G é hidrogênio, A é hidrogênio e B é etila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
19/62
Tabela 3: Compostos da fórmula geral (I), de acordo com a invenção na qual G é hidrogênio, A é hidrogênio e B é n-propila e X, Y e Z respectivamente apresentam os significados indicados na tabela 1.
Tabela 4: Compostos da fórmula geral (I), de acordo com a in5 venção na qual G é hidrogênio, A é hidrogênio e B é isopropila e X, Y e Z respectivamente apresentam os significados indicados na tabela 1.
Tabela 5: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, e A é metila e B é metila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
20/62
Tabela 6: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, A é metila e B é etila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
Tabela 7: Compostos da fórmula geral (I) de acordo com a in5 venção, na qual G é hidrogênio, A é metila e B é n-propila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
Tabela 8: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, A é metila e B é isopropila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
21/62
Tabela 9: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, A é etila e B é metila e X, Ye Z, apresentam respectivamente os significados indicados na tabela 1.
Tabela 10: Compostos da fórmula geral (I) de acordo com a in5 venção, na qual G é hidrogênio, A é etila e B é etila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
Tabela 11: Compostos da fórmula geral (I), de acordo com a invenção, na qual G é hidrogênio, A é etila e B é n-propila e X, Y e apresentam respectivamente os significados indicados na tabela 1.
Tabela 12: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, A é etila e B é isopropila e X, Y e Z apresentam respectivamente os significados na tabela 1.
o x
22/62
Tabela 13: Compostos da fórmula geral (i) de acordo com a invenção na qual G é hidrogênio, e A é propila e B é metila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
Tabela 14: Compostos da fórmula geral (I), de acordo com a in5 venção na qual G é hidrogênio, A é propila e B é etila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
Tabela 15: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, A é propila e B é n-propila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
Tabela 16: Compostos da fórmula gerai (I), de acordo com a invenção na qual G é hidrogênio, A é propila e B é isopropila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
o x
23/62
Tabela 17: Compostos da fórmula geral (I), de acordo com a in venção na qual G é hidrogênio e A é isopropila e B é metila e X, Y e apre sentam respectivamente os significados indicados na tabela 1.
Tabela 18: Compostos da fórmula geral (I), de acordo com a in 5 venção na qual G é hidrogênio, A é isopropila e B é etila e X, Y e Z apresen tam respectivamente os significados indicados na tabela 1.
Tabela 19: Compostos da fórmula geral (I) de acordo com a in venção, na qual G é hidrogênio, A é isopropila e B é n-propila e X, Y e Z a presentam respectivamente os significados indicados na tabela 1.
24/62
Tabela 20: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio, A é isopropila e B é isopropila e X, Y e Z apresentam respectivamente os significados indicados na tabela 1.
São muito particularmente preferidos compostos nas tabelas 1 a 20 abaixo relacionados nas quais G é respectivamente C(=O)R1, C(=L)LR2, SO2R3, P(=L)R4R5, C(=L)NR6R7 ou E.
Coleções de compostos da fórmula (I) e/ou seis sais que podem ser sintetizados de acordo com as reações acima referidas também podem preparadas de forma paralelizada, que podem ser feitas manualmente ou de forma parcial ou totalmente automática. Neste caso, é possível, por exemplo, automatizar o procedimento da reação, a preparação ou a purificação dos produtos ou intermediários. Em suma, entende-se por um procedimento conforme descrito por exemplo por D. Tiebes em Combinatorial Chemistry Synthesis, Analysis, Screening (Editor Günther Jung), Wiley 1999, páginas 1 a 34.
Um número de aparelhagens comercialmente disponíveis pode ser usado para o procedimento de reação paralelizada e prepração, por exemplo blocos de reação Calpyso do Barnstead International, Dubuque, lowa 52004-0797, USA, ou estações de reação de Radleys, Shirehill, Saffron Walden, Essex, CB 11 3AZ, Inglaterra ou MultiPROBE Automated Workstations de Perkin Elmar, Waltham, Massachusetts 02451, EUA. Aparelhagens cromatográficas, por exemplo, de ISCO, Inc., 4700 Superior Street, Lincoln, NE 68504, EUA, estão disponíveis para a purificação paralelizada de compostos da fórmula (I) e seus sais ou de intermediários gerados no curso da preparação.
25/62
As aparelhagens relacionadas induzem a um procedimento modular no qual as etapas individuais são automatizadas, porém operações manuais podem ser realizadas entre as etapas. Isso pode ser evitado pelo uso de sistemas de automação parcial ou totalmente integrados, sendo que os módulos de automação relevantes são operados por exemplo por robôs. Tais sistemas de automação podem ser obtidos por exemplo do Caliper, Hopkinton, MA 01748, USA.
A execução de etapas de síntese individuais ou várias delas pode ser assistida pelo uso de reagentes polímero-suportados/resinas scavenger. A literatura especializada descreve uma séria de protocolos de teste por exemplo em ChemFiles, Vol. 4, N°. 1, Polymer-Supported Scavengers and Reagents for Solution-Phase Synthesis (Sigma-Aldrich).
Além dos métodos descritos aqui, a preparação de compostos da fórmula (I) e seus sais pode ser feita totalmente ou parcialmente através de métodos suportados por fase sólida. Para tanto, intermediários individuais, ou todos os intermediários da síntese ou de uma síntese adaptada ao procedimento relevante são ligados a uma resina intermediária. Métodos de síntese suportador por fase sólida são descritos suficientemente na literatura especializada por exemplo por Barry A. Bunin em The Combinatorial Index, Academic Press, 1998 and Combinatorial Chemistry - Synthesis, Analysis, Screening (Editor Günther Jung), Wiley, 1999. O uso de métodos de síntese suportados por fase sólida permite uma série de protocolos conhecidos da literatura especializada, que, novamente, podem ser feitos manualmente ou de forma automatizada. Por exemplo, as reações podem ser realizadas por meio da tecnologia IRORI em microrreatores da Nexus Biosystems, 12140 Community Road, Poway, CA92064, EUA.
A execução de etapas de síntese individuais ou uma pluralidade delas, tanto na fase sólida como na fase líquida, pode ser assistida peio uso da tecnologia de micro-ondas. Uma série de protocolos de teste é descrita na literatura especializada, por exemplo em Microwaves in Organic and Medicinal Chemistry (Editors C. O. Kappe and A. Stadler), Wiley, 2005.
26/62
A preparação de acordo com os processos descritos aqui gera compostos da fórmula (I) e seus sais na forma de coleções de substâncias, chamadas de bibliotecas. A presente invenção refere-se também a bibliotecas que compreendem pelo menos dois compostos da fórmula (I) e seus sais.
Os compostos da fórmula (I) de acordo com a invenção (e/ou seus sais), a seguir designados juntamente como compostos de acordo com a invenção, apresentam uma atividade de ação herbicida extraordinária contra um amplo espectro de plantas nocivas monodicotiledôneas e dicotiledôneas anuais economicamente importantes. As substâncias ativas também agem eficientemente em plantas nocivas pereniais que produzem brotos de rizomas, rizomas ou outros órgãos pereniais e que são difíceis de combater.
A presente invenção portanto refere-se a um método de combate de plantas indesejadas ou de regulação do crescimento de plantas, preferivelmente em culturas de plantas, onde um ou mais compostos de acordo com a invenção é/são aplicados às plantas (por exemplo plantas nocivas tais como ervas daninhas monodicotiledôneas e dicotiledôneas ou plantas de cultura indesejadas), às sementes (por exemplo grãos, sementes ou propágulos vegetativos tais como tubérculos ou partes de broto com botões) u a áreas nas quais as plantas crescem(por exemplo a área sob cultivo). Neste contexto, os compostos de acordo com a invenção podem ser aplicados por exemplo no método de pré-plantação (se necessário também mediante incorporação ao solo), de pré-emergência ou pós-emergência. Exemplos de representantes individuais da flora erva daninha monocotiledônea e dicotiledônea, que podem ser combatidos pelos compostos de acordo com a invenção, são mencionados, sem que seja feita limitação a determinadas espécies com referida menção.
Plantas nocivas monocotiledôneas dos gêneros: Aegilops, Agropyron, Agrostis, Alopecurus, Apera, Avena, Brachiaria, Bromus, Cenchrus, Commelina, Cynodon, Cyperus, Dactyloctenium, Digitaria, Echinochloa, Eleocharis, Eleusine, Eragrostis, Eriochloa, Festuca, Fimbristylis, Heteran27/62 thera, Imperata, Ischaemum, Leptochloa, Lolium, Monochoria, Panicum, Paspalum, Phalaris, Phleum, Poa, Rottboellia, Sagittaria, Scirpus, Setaria, Sorghum.
Ervas daninhas dicotiledôneas dos gêneros: Abutilon, Amaranthus, Ambrosia, Anoda, Anthemis, Aphanes, Artemisia, Atriplex, Bellis, Bidens, Capsella, Carduus, Cassia, Centaurea, Chenopodium, Cirsium, Convolvulus, Datura, Desmodium, Emex, Erysimum, Euphorbia, Galeopsis, Galinsoga, Gafium, Hibiscus, Ipomoea, Kochia, Lamium, Lepidium, Lindernia, Matricaria, Mentha, Mercurialis, Mullugo, Myosotis, Papaver, Pharbitis, Plantago, Polygonum, Portulaca, Ranunculus, Raphanus, Rorippa, Rotala, Rumex, Salsola, Senecio, Sesbania, Sida, Sinapis, Solanum, Sonchus, Sphenoclea, Stellaria, Taraxacum, Thlaspi, Trifolium, Urtica, Verônica, Viola, Xanthium.
Se os compostos de acordo com a invenção forem aplicados à superfície do solo antes da germinação, a emergência das sementeiras daninhas é evitada completamente ou o crescimento de ervas daninhas até eles terem atingido o estágio de cotiledônea, mas aí então estancam seu crescimento e finalmente as matam completamente após três até quatro semanas.
Se as substâncias ativas forem aplicadas no método de pósemergência às partes de planta verdes, o crescimento para após o tratamento, e as plantas nocivas permanecem no estágio de crescimento ocorrido no período de aplicação ou morrem totalmente após um determinado período de tempo de forma que a concorrência por ervas daninhas nocivas a plantas de cultura, seja assim eliminada bem antecipadamente e de forma duradoura.
Embora os compostos de acordo com a invenção apresentem uma ação herbicida extraordinária contra ervas daninhas monocotiledôneas e dicotiledôneas, plantas de cultura economicamente importantes, por exemplo, culturas dicotiledôneas dos gêneros Arachis, Beta, Brassica, Cucumis, Cucurbita, Helianthus, Daucus, Glycine, Gossypium, Ipomoea, Lactuca, Linum, Lycopersicon, Nicotiana, Phaseolus, Pisum, Solanum, Vicia, ou cultu28/62 ras monocotiledôneas dos gêneros Allium, Ananas, Asparagus, Avena, Hordeum, Oryza, Panicum, Saccharum, Secale, Sorghum, Triticale, Triticum, Zea, particularmente Zea e Triticum, são danificadas em uma extensão insignificante, ou nem são danificadas, dependendo da estrutura do respectivo composto de acordo com a invenção e sua taxa de aplicação. Esta é a razão de os presentes compostos serem perfeitamente adequados para o combate seletivo do crescimento de plantas indesejadas em culturas de planta como plantas úteis de agricultura ou ornamentais.
Além disso, os compostos de acordo com a invenção (dependendo de sua respectiva estrutura e da taxa de aplicação aplicada) apresentam extraordinárias propriedades reguladoras do crescimento em plantas de cultura. Eles intervém no metabolismo da planta de forma reguladora e podem portanto ser empregados para influenciar, seletivamente, constituintes de planta e para facilitar a colheita tais como por exemplo ao acionar a desicação e interromper o crescimento. Além disso, eles também são adequados para combater em geral e inibir o crescimento vegetativo sem destruir as plantas no processo. A inibição do crescimento vegetativo desempenha um importante papel em muitas culturas monocotiledôneas e dicotiledôneas já que por exemplo a deposição pode ser reduzida, ou evitada completamente neste caso.
Devido às suas propriedades herbicidas e reguladoras do crescimento de planta, as substâncias ativas também podem ser empregadas para combater plantas nocivas em culturas de plantas geneticamente modificadas ou plantas que foram modificadas por mutagênese convencional. Em geral, as plantas transgênicas são distinguidas por propriedades especialmente vantajosas, por exemplo por resistências a determinados pesticidas, principalmente a determinados herbicidas, resistências a doenças de plantas ou organismos causadores de doenças de plantas, tais como determinados insetos ou micro-organismos tais como fungos, bactérias ou vírus. Outras propriedades especiais referem-se por exemplo ao material colhido com relação à quantidade, qualidade, capacidade ao armazenamento, composição e constituintes específicos. Portanto, são conhecidas plantas transgênicas
29/62 com um teor de amido aumentado ou uma qualidade de amido modificada ou aquelas com uma composição de ácido graxo diferente do material colhido.
É preferido usar os compostos de acordo com a invenção ou seus sais em culturas transgênicas economicamente importantes de plantas úteis e ornamentais, por exemplo de cereais tais como trigo, cevada, arroz, aveias.sorgo e painço, arroz, mandioca e milho ou ainda culturas de beterraba sacarina, algodão, soja, semente de colza, batata, tomate, ervilhas e outros vegetais. É preferido empregar os compostos de acordo com a invenção como herbicidas em culturas de plantas úteis que são resistentes, ou se tornaram resistentes por meio recombinante, em relação aos efeitos fitotóxicos dos herbicidas.
Meios convencionais para gerar plantas novas que em comparação com plantas existentes apresentam propriedades modificadas são, por exemplo, métodos de reprodução tradicionais e a geração de mutantes. Alternativamente, plantas novas com propriedades modificadas podem ser geradas com o auxilio de métodos recombinantes (vide, por exemplo EP-A0221044, EP-A-0131624). Por exemplo, foi descrito o seguinte em diversos casos;
modificações recombinants de plantas de cultura para fins de modificação do amido sintetizado nas plantas (por exemplo WO 92/11376, WO 92/14827, WO 91/19806), plantas de cultura transgênicas são resistentes a determinados herbicidas do tipo glufosinato (cf., por exemplo, EP-A-0242236, EP-A242246) ou do tipo glifosato (WO 92/00377) ou do tipo sulfonilureia (EP-A0257993, US-A-5013659), plantas de cultura transgênicas, por exemplo, algodão, que é capaz de produzir toxinas Bacillus thuringiensis (toxinas Bt), que tornam as plantas resistentes a determinadas pestes (EP-A-0142924, EP-A-0193259),
Plantas de cultura transgênicas com uma composição de ácido graxo modificado (WO 91/13972),
Plantas de cultura geneticamente modificadas com constitu30/62 intes novos ou metabólitos secundários, por exemplo, fitoalexinas novas, que provocam uma melhor resistência à doença (EPA 309862, EPA0464461),
Plantas geneticamente modificadas com fotorrespiração reduzida que apresentam rendimentos maiores e melhor tolerância ao estresse (EPA 0305398),
Plantas de cultura transgênicas que produzem proteínas farmaceuticamente ou do ponto de vista de diagnóstico importantes (molecular pharming),
Plantas de cultura transgênicas que são distinguidas por rendimentos maiores ou melhor qualidade,
Plantas de cultura transgênicas que são distinguidas por uma combinação, por exemplo as novas propriedades acima referidas (gene stacking).
Um grande número de técnicas de biologia molecular por meio das quais podem ser produzidas novas plantas transgênicas com propriedades modificadas, são conhecidas a princípio; vide, por exemplo, I. Potrykus and G. Spangenberg (eds.) Gene Transfer to Plants, Springer Lab Manual (1995), Springer Verlag Berlin, Heidelberg. or Christou, Trends in Plant Science 1 (1996) 423-431).
Para realizar tais manipulações recombinantes, é possível introduzir moléculas de ácido nucieico em plasmídeos, que permitem uma mutagênese ou modificação de sequência mediante recombinação de sequências de DNA. Por exemplo, substituições de base podem ser feitas, sequências parciais podem ser removidas, ou sequências naturais ou sintéticas podem ser adicionadas com o auxílio de métodos convencionais. Para ligar os fragmentos de DNA entre si, é possível adicionar adaptadores ou ligantes aos fragmentos; vide, por exemplo, Sambrook et al., 1989, Molecular Cloning, A Laboratory Manual, 2nd ed., Cold Spring Harbor Laboratory Press, Cold Spring Harbor, NY; or Winnacker Gene and Klone, VCH Weinheim 2nd ed., 1996
A geração de células de planta com uma atividade reduzida para
31/62 o produto gênico pode ser obtida por exemplo mediante a expressão de pelo menos um RNA correspondente, um RNA senso para obtenção de um efeito de co-supressão ou pela expressão de pelo menos uma ribozima correspondentemente construída, que cliva especificamente transcritos do produto gênico acima referido.
Para tanto, é possível primeiramente usar moléculas de DNA que compreendem todas as sequências de codificação de um produto gênico, incluindo qualquer sequência flanqueadora que podem estar presentes ou ainda moléculas de DNA que compreendem apenas partes da sequência de codificação, sendo necessário para essas partes serem suficientemente longas para produzirem um efeito antissenso nas células. Também é possível, usar sequências de DNA que apresentam um elevado grau de homologia com as sequências de codificação de um produto gênico, mas que não são totalmente idênticas.
Ao expressar moléculas de ácido nucleico em plantas, a proteína sintetizada pode ser localizada em qualquer compartimento da célula de planta. Para obter localização em um compartimento particular, porém, é possível por exemplo ligar a região de codificação a sequências de DNA que asseguram a localização em um compartimento específico. Tais sequências são conhecidas pelo versado na técnica (vide, por exemplo, Braun et al., EMBO J. 11 (1992), 3219-3227; Wolter et al., Proc. Natl. Acad. Sci. USA 85 (1988), 846-850; Sonnewald et al., Plant J. 1 (1991), 95-106). As moléculas de ácido nucleico também são expressadas nas organelas das células de planta.
As células de planta transgênica podem ser regeneradas por técnicas conhecidas para formar plantas intactas. A princípio, as plantas transgênicas podem ser plantas de qualquer espécie de planta, isto é tanto plantas monocotiledôneas e dicotiledôneas.
Assim, podem ser obtidas plantas transgênicas que apresentam propriedades modificadas como resultado de superexpressão, supressão ou inibição de genes homólogos (= naturais) ou sequências gênicas ou expressão de genes heterólogos (= estranhos) ou sequências gênicas.
32/62
É preferido empregar os compostos de acordo com a invenção em culturas transgênicas que são resistentes a reguladores do crescimento tais como, por exemplo, dicamba, ou contra herbicidas que inibem enzimas de planta essenciais, por exemplo, sintase de acetolactato (ALS), sintase EPSP, sintase de glutamina (GS) ou dioxigenase de hidroxifenilpiruvato (HPPD), ou contra herbicidas do grupo consistindo das sulfoniluréias, glifosato, giufosinato ou benzoilisoxazóis e substâncias ativas análogas.
Quando as substâncias ativas de acordo com a invenção são usadas em culturas transgênicas, muitas vezes são observados efeitos - adicionalmente aos efeitos em plantas nocivas, que podem ser observados em outras culturas - que são específicos para a aplicação na cultura transgênica em questão, por exemplo, um espectro de ervas daninhas modificado ou especialmente amplo que pode ser combatido, taxas de aplicação modificadas que podem ser empregadas para aplicação, combinabilidade preferivelmente boa com os herbicidas em relação aos quais a cultura transgênica é resistente, e um efeito sobre crescimento e rendimento das plantas de cultura transgênica.
Portanto, a invenção refere-se também ao uso dos compostos de acordo com a invenção como herbicidas para o combate de plantas nocivas em plantas de cultura transgênica.
ι Os compostos de acordo com a invenção podem ser usados na forma de pós umedecíveis, concentrados emulsificáveis, soluções atomizáveis, produtos de pulverização ou grânulos nas formulações convencionais. Portanto, a invenção também provê composições herbicidas e reguladores dó crescimento de planta que compreendem os compostos de acordo com a iqvenção.
Os compostos de acordo com a invenção podem ser formulados de várias formas de acordo com as quais são necessários parâmetros biológicos e/ou fisicoquímicos. Possíveis formulações incluem, por exemplo: pós umedecíveis (WP), pós hidrossolúveis (SP), concentrados hidrossolúveis, concentrados emulfisicáveis (EC), emulsões (EW) tais como dispersões óleo-em-água e emulsões água-em-óleo, soluções atomizáveis,
I
33/62 concentrados em suspensão (SC), dispersões a base de óleo ou água, soluções miscíveis em óleo, suspensões em cápsulas (CS), produtos de pulverização (DP), produtos de revestimento de semente, grânulos para dispersão e aplicação em solo, grânulos (GR) na forma de microgrânulos, grânulos de atomização, grânulos revestidos e grânulos de adsorção, grânulos hidrodispersáveis (WG), grânulos hidrossolúveis (SG), formulações ULV, microcápsulas e ceras.
Esses tipos individuais de formulação são conhecidos a princípio e são descritos, por exemplo, em: Winnacker-Küchler, Chemische
Technologie [Chemical technology], Volume 7, C. Hanser Verlag Munich, 4th Ed. 1986, Wade van Valkenburg, Pesticide Formulations, Marcei Dekker, N.Y., 1973; K. Martens, Spray Drying Handbook, 3rd Ed. 1979, G. Goodwin Ltd. London.
Esses assistentes de formulação necessários tais como mate15 riais inertes, tensoativos, solventes e outros aditivos, são igualmente conhecidos e são descritos, por exemplo, em: Watkins, Handbook of Insecticide Dust Diluents and Carriers, 2nd Ed., Darland Books, Caldwell N.J., H.v. Olphen, Introduction to Clay Colloid Chemistry; 2nd Ed., J. Wiley & Sons, N.Y.; C. Marsden, Solvents Guide; 2nd Ed., Interscience, N.Y. 1963;
McCutcheon's Detergents and Emulsifiers Annual, MC Publ. Corp., Ridgewood N.J.; Sisley and Wood, Encyclopedia of Surface Active Agents”, Chem. Publ. Co. Inc., N.Y. 1964; Schõnfeldt, Grenzflãchenaktive Âthylenoxidaddukte [adutos de óxido de etileno Interface-ativos], Wiss. Verlagsgesell., Stuttgart 1976; Winnacker-Küchler, Chemische
Technologie, Volume 7, C. Hanser Verlag Munich, 4th Ed. 1986.
Pós umedecíveis são preparações que podem ser dispersadas uniformemente em água assim como o composto ativo, a não ser um diluente ou uma substância inerte, também compreendem tensoativos do tipo iônico e/ou não iônico (agentes umectantes, dispersantes), por exemplo alquilfenóis polioxietilados, alcoóis graxos polioxietilados, aminas graxas polioxietilados, sulfatos de poliglicol éter de álcool graxo, alcanossulfonatos, alquilbenzenossulfonatos, lignossulfonato de sódio, 2,2'-dinaftilmetano-6,6'34/62 dissuifonato de sódio, dibutilnaftalenossulfonato de sódio ou ainda oleilmetiltaurato de sódio. Para preparar os pós umedecíveis, as substâncias de ação herbicida são finamente moídas, por exemplo, em equipamentos convencionais tais como moinhos de martelo, moinhos de soprador e moinho a jato de ar simultaneamente ou em seguida misturadas com os assistentes de formulação.
Concentrados emulsificáveis são preparados mediante dissolvição do composto ativo em um solvente orgânico, por exemplo butanol, ciclohexanona, dimetilformamida, xileno ou ainda aromáticos com elevado ponto de ebulição ou hidrocarbonetos ou misturas dos solventes orgânicos com adição de um ou mais tensoativos do tipo iônico e/ou não iônico (emulsificantes). Os emulsificantes usados podem, por exemplo ser: alquilarilsulfonatos de cálcio, tais como dodecilbenzenosulfonato de cálcio, ou emulsificantes não iônicos tais como poliglicol ésteres de ácido graxo, alquilaril poliglicol éteres, poliglicol éteres de álcool graxo, produtos de condensação de óxido de propileno-óxido de etileno, alquil poliéteres, ésteres de sorbitano, por exemplo, ésteres de ácido graxo de sorbitano, ou ésteres de sorbitano de polioxietileno, por exemplo, éteres de ácido graxo de sorbitano de polioxietileno.
Produtos de pulverização são obtidos mediante moagem do composto ativo com substâncias sólidas finamente divididas, por exemplo talco, argilas naturais, tais como caulina, bentonita e pirofillita, ou terra diatomácea.
Concentrados em suspensão podem ser a base de água ou óleo. Eles podem ser preparados, por exemplo, por moagem úmida por meio de moinhos de esferas comerciais e adição opcional de tensoativos conforme já relacionado acima para os outros tipos de formulação.
Emulsões, por exemplo emulsões óleo-em-água (EW), podem ser preparadas, por exemplo, por meio de agitadores, moinhos coloidais e/ou misturadores estáticos utilizando-se solventes orgânicos aquosos e opcionalmente tensoativos, conforme por exemplo já relacionado acima para os outros tipos de formulação.
35/62
Grânulos podem ser produzidos ou por atomização do composto ativo sobre material inerte granulado adsortivo ou por aplicação dos concentrados de composto ativo por meio de adesivos, por exemplo, álcool polivinílico, poliacrilato de sódio ou óleos minerais, sobre a superfície de portadores tais como areia, caolinitas ou de material inerte granulado. Também é possível granular compostos ativos adequados de foma convencional para a produção de grânulos fertilizantes - se desejado em uma mistura com fertilizantes.
Grânulos dispersíveis em água são preparados geralmente pelos processos usuais tais como secagem por pulverização,granulação por leito fluídizado,granulação em disco,mistura com misturadores de alta velocidade e extrusão sem material inerte sólido. Para a preparação de grânulos de disco, de leito fluidifícado, de extrusora e de atomização vide, por exemplo, processos em Spray-Drying Handbook 3rd ed. 1979, G. Goodwin Ltd., London; J.E. Browning, Agglomeration, Chemical and Engineering 1967, pages 147 ff; Perry's Chemical Engineer's Handbook, 5th Ed., McGraw-HilI, New York 1973, p. 8-57.
Para maiores detalhes com relação à formulação de composições de fitoproteção, vide, por exemplo, G.C. Klingman, Weed Control as a Science, John Wiley and Sons, Inc., New York, 1961, pages 81-96 and J.D. Freyer, S.A. Evans, Weed Control Handbook, 5th Ed., Blackwell Scientific Publications, Oxford, 1968, páginas 101-103.
As formulações agroquímicas em geral contém de 0,1 a 99% em peso, particularmente de 0,1 a 95% em peso de composto ativo da fórmula (DEm pós umedecíveis, a concentração de composto ativo é, por exemplo, a partir de aproximadamente 10 a 90% em peso; o remanescente para 100% em peso consiste em constituintes de formulação convencionais. No caso de concentrados emulsificáveis, a concentração de composto ativo pode ser de aproximadamente. 1 a 90% em peso, preferivelmente de 5 a 80% em peso. Formulações tipo pó contém de 1 a 30% em peso de composto ativo, preferivelmente em geral de 5 a 20% em peso de composto
36/62 ativo; soluções atomizáveis contém de aproximadamente 0,05 a 80% em peso, preferivelmente de 2 a 50% em peso de composto ativo. Em grânulos dispersáveis em água, o teor de composto ativo depende em parte do composto ativo estar presente na forma sólida ou na forma líquida, e que são usados assistentes de granulação, cargas, etc. Nos grânulos dispersáveis em água, o teor de composto ativo, por exemplo, situa-se entre 1 e 95% em peso, preferivelmente entre 10 e 80% em peso.
Adicionalmente, as formulações de composto ativo mencionadas, compreendem opcionalmente os respectivos adesivos convencionais, agentes umectantes, dispersantes, emulsificantes, agentes promotores de penetração, conservantes, antes anticongelantes e solventes, cargas, portadores e corantes, antiespumantes, inibidores de evaporação e agentes que influenciam o pH e a viscosidade.
Baseado nessas formulações, também é possível preparar combinações com outros compostos de ação pesticida, tais como, por exemplo, inseticidas, acaricidas, herbicidas, fungicidas, e também com outros agentes protetores, fertilizantes e/ou reguladores do crescimento, por exemplo, na forma de uma formulação acabada ou como mistura de tanque. Agentes protetores adequados são, por exemplo, mefenpir-dietila, ciprossulfamida, isoxadifeno-etila, cloquintocet-mexila e dicloromida.
Compostos ativos que podem ser empregados em combinação com os compostos de acordo com a invenção em formulações mistas ou na mistura de tanque são, por exemplo, compostos ativos conhecidos que são baseados na inibição de, por exemplo, sintase de acetolactato, carboxilase de acetil-CoA, sintase de celulose, sintase de enolpiruviishikimate-3-fosfato, sintetase de glutamina, dioxigenase de p-hidroxifenilpiruvato, desaturase de fitoeno, fotossistema I, fotossistema II, oxidase de protoporfirinogênio, conforme descritos em, por exemplo, por exemplo, Weed Research 26 (1986) 441-445 or The Pesticide Manual, 14th edition, The British Crop Protection Council and the Royal Soc. of Chemistry, 2003 e a literatura citada aqui. Herbicidas conhecidos ou reguladores de crescimento de planta que podem ser combinados com os compostos de acordo com a invenção, são, por e37/62 xemplo,as seguintes substâncias ativas (os compostos são designados pelo nome comum de acordo com a Organização Internacional de Padronização (ISO) ou por um nome químico, se necessário junto com o número de código) e sempre compreendem todas as formas de uso tais como ácidos, sais, ésteres e isômeros tais como estereoisômeros e isômeros ópticos. Neste contexto, uma e, em alguns casos, diversas formas de uso são mencionadas a título de exemplo:
acetoclor, acibenzolar, acibenzolar-S-metila, acifluorfeno, acifluorfeno-sódio, aclonaifeno, alacloro, allidocloro, aloxidim, aloxidim-sódio, ametrina, amicarbazona, amidocloro, amidossulfurona, aminociclopiracloro, aminopiralida, amitrol, sulfamato de amônio a, ancimidol, anilofos, asulam, atrazina, azafenidina, azimsulfurona, aziprotrina, BAH-043, BAS-140H, BAS693H, BAS-714H, BAS-762H, BAS-776H, BAS-800H, beflubutamida, benazoiina, benazolina-etila, bencarbazona, benfluralina, benfuresato, bensulida, bensulfurona-metila, bentazona, benzfendizona, benzobiciclona, benzofenap, benzofluor, benzoilprop, bifenox, bilanafos, bilanafos-sódio, bispiribac, bispiribac-sódio, bromacila, bromobutida, bromofenoxim, bromoxinila, bromurona, buminafos, busoxinona, butacloro, butafenaciia, butamifos, butenacloro, butralina, butroxidim, butilato, cafenstrol, carbetamida, carfentrazona, carfentrazona-etila, clometoxifeno, cloroamben, cloroazifop, cloroazifop-butila, clorobromurona, clorobufam, clorofenac, clorofenac-sódio, clorofenprop, cloroflurenol, cloroflurenol-metila, cloroidazona, cloroimurona, cloroimuronaetila, cloromequat-cloroida, cloronitrofen, cloroftalim, clorotal-dimetila, clorotolurona, clorossulfurona, cinidona, cinidona-etila, cinmetilina, cinossulfurona, cletodim, clodinafop, clodinafop-propargila, clofencet, clomazona, clomeprop, cloprop, clopiralida, cloroansulam, cloroansulam-metila, cumilurona, cianamida, cianazina, ciclanilida, cicloato, ciclossulfamurona, cicloxidim, ciclurona, cihalofop, cihalofop-butila, ciperquat, ciprazina, ciprazol, 2,4-D, 2,4-DB, daimurona/dimrona, dalapona, daminozida, dazomet, n-decanol, desmedifam, desmetrín, detosil-pirazolato (DTP), dialato, dicamba, diclobenila, dicloroprop, dicloroprop-P, diclofop, diclofop-metila, diclofop-P-metila, diclosulam, dietatila, dietatil-etila, difenoxurona, difenzoquat, diflufenican, diflufenzopir,
38/62 diflufenzopir-sódio, dimefurona, diquegulac-sódio, dimefurona, dimepiperato, dimetacloro, dimetametrina, dimetenamida, dimetenamid-P, dimetipina, dimetrassulfurona, dinitramina, dinoseb, dinoterb, difenamida, dipropetrina, diquat, diquat-dibrometo, ditiopir, diurona, DNOC, eglinazina-etila, endotal, EPTC, esprocarb, etalfluralina, etametsulfurona-metila, etefona, etidimurona, etiozina, etofumesato, etoxifen, etoxifen-etila, etoxissulfurona, etobenzanida, F-5331, isto é N-[2-cloro-4-flúor-5-[4-(3-fluoropropil)-4,5-dihidro-5-oxo-1Htetrazol-1-ii]fenil]etanossulfonamida, fenoprop, fenoxaprop, fenoxaprop-P, fenoxaprop-etila, fenoxaprop-P-etila, fentrazamida, fenurona, flamprop, flamprop-M-isopropila, flamprop-M-metila, flazasulfurona, florasulam, fluazifop, fluazifop-P, fluazifop-butila, fluazifop-P-butila, fluazolato, flucarbazona, flucarbazona-sódio, flucetossulfurona, flucloroalina, flufenacet (tiafluamida), flufenpir, flufenpir-etila, flumetralina, flumetsulam, flumicloroac, flumicloroacpentila, flumioxazin, flumipropina, fluometurona, fluorodifen, fluoroglicofen, fluoroglicofen-etila, flupoxam, flupropacila, flupropanato, flupirsulfurona, flupirsulfurona-metil-sódio, flurenol, flurenol-butila, fluridona, flurocloroidona, fluroxipir, fluroxipir-meptila, flurprimidol, flurtamona, flutiaceto, flutiacetometila, flutiamida, fomesafen, foramsulfurona, forclorofenurona, fosamina, furiloxifen, ácido giberélico, glufosinato, L-glufosinato, L-glufosinato-amônio, glufosinato-amônio, glifosato, glifosato-isopropilamônio, H-9201, halosafen, halossulfurona, halossulfurona-metila, haloxifop, haloxifop-P, haloxifopetoxietila, haloxifop-P-etoxietila, haloxifop-metila, haloxifop-P-metila, hexazinona, HNPC-9908, HOC-201, HW-02, imazametabenz, imazametabenzmetila, imazamox, imazapic, imazapir, imazaquin, imazetapir, imazossulfurona, inabenfida, indanofan, ácido indoleacético (IAA), ácido 4-indol-3-iibutírico (IBA), iodossulfurona, iodossulfurona-metil-sódio, ioxinil, isocarbamid, isopropalin, isoproturona, isourona, isoxaben, isoxaclorotol, isoxafiutol, isoxapirifop, CUH-043, CUH-071, carbutilato, quetospiradox, lactofen, lenacil, linurona, hidrazida maléica, MCPA, MCPB, MCPB-metila, -etila e -sódio, mecoprop, mecoprop-sódio, mecoprop-butotila, mecoprop-P-butotila, mecoprop-Pdimetilamônio, mecoprop-P-2-etilhexil, mecoprop-P-potássio, mefenacet, mefluidida, mepiquat-cloroida, mesossulfurona, mesossulfurona-metila, me39/62 sotriona, metabenztiazurona, metam, metamifop, metamitrona, metazacloro, metazol, metoxifenona, metildimrona, 1-metilciclopropeno, isotiocianato de metila, metobenzurona, metobenzurona, metobromurona, metolacloro, Smetolacloro, metosulam, metoxurona, metribuzin, metsulfurona, metsulfurona-metila, molinato, monalida, monaocarbamida, di-hidrogênio sulfato de monocarbamida, monaolinurona, monaossulfurona, monaurona, MT 128, MT-5950, isto é N-[3-cloro-4-(1-metiletil)fenil]-2-metilpentanamida, NGGC011, naproanilida, napropamida, naptalam, NC-310, ou seja, 4-(2,4diclorobenzoil)-1-metil-5-benziloxipirazol, NC-620, neburona, nicossulfurona, nipiraclofen, nitralin, nitrofen, nitrofenolat-sodido (mistura isomérica), nitrofluorfen, ácido nonanoico, norflurazona, orbencarb, ortossulfamurona, orizalin, oxadiargil, oxadiazona, oxassulfurona, oxaziclomefona, oxifluorfen, paclobutrazol, paraquat, paraquat dicloreto, ácido pelargonáico (ácido nonanoico), pendimetalin, pendralin, penoxsulam, pentanocloro, pentoxazona, perfluidona, petoxamid, fenisofam, fenmedifam, fenmedifam-etila, picloroam, picolinafen, pinoxaden, piperofos, pirifenop, pirifenop-butila, pretilacloro, primissulfurona, primissulfurona-metila, probenazol, profluazol, prociazina, prodiamina, prifluralina, profoxidim, prohexadiona, prohexadiona-cálcio, prohidrojasmona, prometona, prometrin, propacloro, propanil, propaquizafop, propazina, profam, propisocloro, propoxicarbazona, propoxicarbazona-sódio, propizamida, prossulfalin, prosulfocarb, prosulfurona, prinacloro, piraclonail, piraflufen, piraflufen-etila, pirassulfotol, pirazolinato (pirazolato), pirazossulfurona-etila, pirazoxifen, piribambenz, piribambenz-isopropila, piribenzoxim, piributicarb, piridafol, piridato, piriftalid, piriminobac, piriminobac-metila, pirimissulfan, piritiobac, piritiobac-sódio, piroxassulfona, piroxsulam, quincloroac, quinmerac, quinoclamina, quizalofop, quizalofop-etila, quizalofop-P, quizalofop-P-etila, quizalofop-P-tefurila, rimsulfurona, saflufenacil, secbumetona, setoxidim, sidurona, simazina, simetrin, SN-106279, sulcotriona, sulfalato (CDEC), sulfentrazona, sulfometurona, sulfometurona-metila, sulfosato (glifosatotrimésio), sulfossulfurona, SIN-523, SIP-249, SIP-298, SIP-300, tebutam, tebutiurona, tecnazeno, tefuriltriona, tembotriona, tepraloxidim, terbacila, terbucarb, terbucloro, terbumetona, terbutilazina, terbutrina, T-547, ou seja pro40/62 pirissulfurona, tenilcloro, tiafluamida, tiazaflurona, tiazopir, tidiazimina, tidiazurona, tiencarbazona, tiencarbazona-metila, tifensulfurona, tifensulfuronametila, tiobencarb, tiocarbazil, topramezona, tralcoxidim, trialato, triassulfurona, triaziflam, triazofenamida, tribenurona, tribenurona-metila, ácido tricloro5 acético (TCA), triclopir, tridifano, trietazina, trifloxissulfurona, trifloxissulfurona-sódio, trifluralin, triflussulfurona, triflussulfurona-metila, trimeturona, trinexapac, trinexapac-etila, tritossulfurona, tsitodef, uniconazol, uniconazol-P, vernolato, ZJ-0166, ZJ-0270, ZJ-0543, ZJ-0862 e também os seguintes compostos:
Para uso, as formulações na forma comercial são, se apropriado, diluídas com água de forma convencional, por exemplo no caso de pós umedecíveis, dispersões e grânulos dispersáveis em água. Preparações na forma de pós, grânulos para aplicação no solo ou grânulos para difusão e
41/62 soluções atomizáveis não são usualmente diluídas com outras substâncias inertes antes da aplicação.
A taxa de aplicação dos compostos da fórmula (I) varia de acordo com as condições externas tais como, temperatura, umidade e o tipo de herbicida usado. Ela pode variar dentro de amplos limites, por exemplo entre 0,001 e 1,0 kg/ha ou mais de substância ativa; porém, preferivelmente entre 0,005 e 750 g/ha.
Adicíonalmente à ação herbicida, os compostos de acordo com a invenção também apresentam boa ação inseticida. Correspondentemente, a invenção também se refere ao seu uso como inseticida.
Os exemplos abaixo servem para ilustrar a invenção.
Exemplos químicos
1. Preparação_de_4-(2-cloro-6-fluorofenil)-5-hidróxi-2,6-dimetil3(2H)piridazinona (N°. 1 da tabela 21)
Uma solução de 2,1 g (2 eq) de t-butóxido de potássio em 10 ml de DMF foi inicialmente colocada, e 2,8 g (9,4 mmols) de 2-{[2-(2-cloro-6fluorofenil)acetil]metilhidrazono}propionato de etila foram lentamente adicionados em gotas em 10 ml de DMF sob < 0°C. A mistura foi deixada aquecer sob temperatura ambiente e em seguida agitada por mais 0,5 h. A solução de reação foi então derramada em 100 ml de ácido clorídrico a 1N resfriado e extraída duas vezes com respectivamente 250 ml de acetato de etila. As fases orgânicas combinadas foram lavadas com 50 ml de solução de cloreto de sódio saturada e depois secadas com sulfato de sódio, concentradas sob pressão reduzida e purificadas por cromatografia de coluna (sílica-gel, gradiente acetato de etila /n-heptano). Obteve-se 1,2 g de produto puro.
2. Preparação de 4-(3,4-diclorofenil)-5-hidr6xi-2-metil-3(2H)-piridazinona (No. 4 da tabela 21) ml de água/etanodiol (1:1) foram adicionados a 1,0 g (7,4 mmols) de 4-(3, 4-diclorofenil)-5-metóxi-2-metil-2H-piridazin-3-ona e 0,4 g de hidróxido de potássio (2 eq), e a mistura foi reagida sob 150°C durante a noite. A mistura de reação foi adicionada a 50 ml de água e ajustada ao pH 1 utilizando-se ácido clorídrico concentrado, e o precipitado resultante foi re42/62 movido por filtração. Recristalização de isopropanol resultou em 0,2 g de produto puro.
Os compostos a seguir foram preparados analogamente aos exemplos 1 e 2 acima referidos:
Tabela 21: Compostos da fórmula geral (I) de acordo com a invenção na qual G é hidrogênio.
| Ne. | X | Y | Z | A | B | Dados analíticos |
| 1-1-a-1 | Cl | 6-F | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,88 (bs, 1H), 7,48 (m, 1H), 7,40 (dd, 1H), 7,27 (t, 1H) 3,58 (s, 3H), 2,23 (s, 3H) |
| 1-1-a-2 | no2 | H | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,7 (bs, 1H), 8,10 (d, 1H), 7,78 (t, 1H), 7,62 (t, 1H), 7,45 (d, 1H) 3,53 (s, 3H), 2,28 (s, 3H) |
| 1-1 -a-3 | Cl | 3-CI | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,58 (bs, 1H), 7,58 (d, 1H), 7,42 (t, 1H), 7,25 (d, 1H) 3,58 (s, 3H), 2,21 (s, 3H) |
| 1-1-a-4 | H | 4-CI | 3-CI | H | Me | p.f.,: 315 °C |
| 1-1-a-5 | Cl | H | 4-CI | H | t-Bu | p.f.,: 250 °C |
| 1-1-a-6 | Cl | 6-CI | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,8 (bs, 1H), 7,52 (pseudo d, 2H), 7,43 (t, 1H), 3,58 (s, 3H), 2,23 (s, 3H) |
| 1-1-a-7 | H | 3-Ph | H | H | t-Bu | p.f.,: 244 °C |
| 1-1-a-8 | H | 5-CF3 | 3-CF3 | H | t-Bu | p.f.,: 239 °C |
| 1-1-a-9 | Cl | 4-Me | 6-Br | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,65 (bs, 1H), 7,52 (s, 1H), 7,38 (s, 1H), 3,57 (s, 3H), 2,33 (s, 3H), 2,23 (s, 3H) |
| 1-1-a-10 | Cl | 5-(4-CI-Ph) | H | H | t-Bu | p.f.,: 250 °C |
43/62
| Ν’. | X | Y | Z | A | B | Dados analíticos |
| l-1-a-11 | Br | 4-Me | Br | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,56 (s, 2H), 3,58 (s, 3H), 2,32 (s, 3H), 2,23 (s, 3H) |
| l-1-a-12 | Cl | H | 3-CI | H | t-Bu | pó amorfo |
| l-1-a-13 | Cl | 6-CI | H | i-Bu | Me | 1H-RMN, 400MHz, d6-DMSO, 10,8 (bs, 1H), 7,52 (d, 2H), 7,43 (t, 1H), 3,56 (s, 3H), 2,51 (m, 2H, obscurecido por solvente), 2,03 (m, 1H), 0,90 (d, 6H) |
| l-1-a-14 | Cl | 4-OCF3 | 6-CI | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 11,0 (bs, 1H), 7,72 (s, 2H), 3,58 (s, 3H), 2,23 (s, 3H) |
| l-1-a-15 | Cl | 4-Me | 6-c-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,07 (s, 1H), 6,82(s, 1H), 3,53 (s, 3H), 2,40 (s, 3H), 2,28 (s, 3H), 1,81 (m, 1H), 0,89 (m, 2H), 0,63 (m, 2H) |
| l-1-a-16 | Cl | 4-Me | 6- OCF3 | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,42 (s, 1H), 7,23 (s, 1H), 3,56 (s, 3H), 2,41 (s, 3H), 2,22 (s, 3H) |
| l-1-a-17 | F | 3-Me | 6-F | Me | Me | 1H-RMN, 400MHz, d6-DMS0, 7,37 (q, 1H), 7,03 (t, 1H), 3,56 (s, 3H), 2,23 (pseudo d, 6H) |
| l-1-a-18 | Cl | 3-Me | 6-F | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,37 (t, 1H), 7,12 (t, 1H), 3,52 (s, 3H), 2,32 (s, 3H), 2,23 (s, 3H) |
| l-1-a-19 | F | 3-OMe | 6-F | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,17 (m, 1H), 7,02 (t, 1H), 3,82 (s, 3H), 3,54 (s, 3H), 2,18 (s, 3H) |
| l-1-a-20 | Cl | 4-Br | 6-CI | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,82 (s, 2H), 3,54 (s, 3H), 2,21 (s, 3H) |
| l-1-a-21 | F | 6-F | H | Me | H | 1H-RMN, 400MHz, d6-DMSO, 7,50 (m, 1H), 7,12 (m, 1H), 2,23 (pseudo d, 6H) |
| l-1-a-22 | Cl | 6-CF3 | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,75 (bs, 1H), 7,88 (d, 1H), 7,81 (d, 1H), 7,67 (t, 1H), 3,56 (s, 3H), 2,23 (s, 3H) |
44/62
| Ν’. | X | Y | Z | A | B | Dados analíticos |
| l-1-a-23 | Cl | 4-CI | 6-Br | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,75 (bs, 1H), 7,88 (s, 1H), 7,68 (t, 1H), 3,58 (s, 3H), 2,23 (s, 3H) |
| l-1-a-24 | F | 3-F | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,8 (bs, 1H), 7,43 (m, 1H), 7,23 (m, 1H), 7,11 (m, 1H), 3,58 (s, 3H), 2,22 (s, 3H) |
| l-1-a-25 | OCF3 | 4-Br | 6-Br | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,92 (s, 1H), 7,59 (s, 1H), 3,48 (s, 3H), 2,11 (s, 3H) |
| l-1-a-26 | I | H | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,92 (d, 1H), 7,42 (t, 1H), 7,15 (m, 2H), 3,56 (s, 3H), 2,24 (s, 3H) |
| l-1-a-27 | Cl | 4-CI | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,54 (bs, 1H), 7,72 (d, 1H), 7,48 (dd, 1H), 7,16 (d, 1H) 3,58 (s, 3H), 2,23 (s, 3H) |
| l-1-a-28 | H | 4-CI | H | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 10,4 (bs, 1H), 7,50 (pseudo s, 4 H), 3,59 (s, 3H), 2,24 (s, 3H) |
| l-1-a-29 | H | 3-CI | H | Me | Me | 1H-RMN, 600MHz, d6-DMSO, 10,4 (bs, 1H), 7,47 (m, 3H) 7,39 (d, 2 H), 3,61 (s, 3H), 2,27 (s,3H) |
| l-1-a-30 | H | 3-CFa | H | Me | Me | 1H-RMN, 400MHz, CDCI3, 10,54 (bs, 1H), 7,72 (d, 1H), 7,75-7,55 (m, 4H), 3,71 (s, 3H), 2,31 (s, 3H) |
| l-1-a-31 | Cl | H | H | Me | Me | 1H-RMN, 600MHz, d6-DMSO, 10,4 (bs, 1H), 7,49 (m, 2H) 7,44 (d, 2 H), 7,41 (d, 2 H), 3,59 (s, 3H), 2,24 (s, 3H) |
45/62
| Ne. | X | Y | Z | A | B | Dados analíticos |
| l-1-a-32 | Cl | 6-F | H | Me | H | 1H-RMN 400 MHz, d6-DMSO : 12,27 ppm (amplo s, 1H), 7,41-7,47 (m, 1H); 7,36 (d, 1H); 7,19-7,23 (m, 1H); 2,22 (s, 3H) |
| l-1-a-33 | Cl | 6-F | 4-F | Me | H | Óleo |
| l-1-a-34 | Cl | 6-CI | 4-CI | Me | H | 1H-RMN 400 MHz, d6-DMSO : 12,27 ppm ((amplo s, 1H), 7,66 (s, 2H); 2,20 (s, 3H) |
| l-1-a-35 | Cl | 6-F | 3-Me | Me | H | 1H-RMN 400 MHz, d6-DMSO : 12,27 ppm (amplo s, 1H), 7,23-7,33 (m, 2H); 2,49 (s, 3H); 2,48 (s, 3H) |
| l-1-a-36 | F | 6-F | 3-F | Me | H | 1H-RMN 400 MHz, d6-DMSO : 12,38 ppm (amplo s, 1H), 7,50 (ddd, 1H); 7,10-7,16 (m, 1H); 2,22(8, 3H), |
3. Preparação de 5-isopropóxi-4-(2-cloro-6-fluorofenil)-2,6dimetil-3(2H)-piridazinona (N°. 1 de tabela 22)
0,15 g (0,55 mmol) do composto 1-1 -a-1 de acordo com a invenção da tabela 21 e 0,07 g de trietilamina (1,3 eq) foram inicialmente coloca5 dos em 10 ml de diclorometano. 0,06 g (1.0 eq) de cloreto de isobutirila foi em seguida adicionado em gotas durante um período de 10 minutos. A mistura foi agitada por uma hora, e 10 ml de 5 porcento de solução de bicarbonato de sódio adicionados. A fase orgânica foi separada e depois secada resultando, após a purificação cromatográfica (sílica-gel, gradiente acetato de etila /n-heptano), 0,18 g.
Os compostos da tabela 22 podem ser obtidos analogamente ao método acima.
46/62
Tabela 22: Compostos da fórmula geral (I) de acordo com a invenção na qual G é C(=O)R1.
| N°. | X | Y | Z | R1 | A | B | Dados analíticos |
| 1-1 -b-1 | Cl | 6-F | H | i-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,53 (m, 1H), 7,47 (d, 1H), 7,35 (t, 1H) 3,71 (s, 3H), 2,65 (m, 1H), 2,20 (s, 3H), 0,88 (m, 6H) |
| 1-1 -b-2 | H | 3-CI | 4-CI | i-Pr | Me | H | 89 °C |
| 1-1-b-3 | Cl | 6-CI | H | i-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,60 (pseudo d, 2H), 7,50 (t, 1H), 3,72 (s, 3H), 2,62 (m, 1H), 2,20 (s, 3H), 0,86 (d, 6H) |
| l-1-b-4 | NO2 | H | H | i-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 8,20 (d, 1H), 7,88 (t, 1H), 7,72 (t, 1H), 7,38 (d, 1H) 3,67 (s, 3H), 2,65 (m, 1H), 2,19 (s, 3H), 0,92 (m, 6H) |
| 1-1-b-5 | F | 3-F | H | i-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,55 (m, 1H), 7,30 (m, 1H), 7,07 (m, 1H), 3,70 (s, 3H), 2,68 (m, 1H), 2,19 (s, 3H), 0,93 (m, 6H) |
| 1-1-b-6 | Cl | 4-Me | 6-Br | i-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,58 (s, 1H), 7,44 (s, 1H), 3,71 (s, 3H), 2,31 (s, 3H), 2,19 (s, 3H) |
| 1-1-b-7 | Cl | 4-OCF3 | 6-CI | i-Pr | Me | Me | 1H-RMN, 400MHz, CDCI3, 7,32 (s, 2H), 3,85 (s, 3H), 2,62 (m, 1H), 2,28 (s, 3H), 1,01 (d, 6H) |
| 1-1-b-8 | Br | 4-Me | 6-Br | i-Pr | Me | Me | 1H-RMN, 400MHz, CDCI3, 7,41 (s, |
47/62
| Ν°. | X | Y | Z | R1 | A | B | Dados analíticos |
| 2H), 3,82 (s, 3H), 2,58 (m, 1H), 2,32 (s, 3H), 2,25 (s, 3H), 0,99 (d, 6H) | |||||||
| 1-1 -b-9 | Cl | 3-CI | H | i-Pr | Me | Me | 1H-RMN, 400MHz, CDCI3, 7,50 (d, 1H), 7,25 (t, 1H), 7,09 (d, 1H) 3,82 (s, 3H), 2,57 (m, 1H), 2,25 (s, 3H), 1,00 (dd, 6H) |
| 1-1-b-10 | Cl | 4-Me | 6-OCF3 | i-Pr | Me | Me | 1H-RMN, 400MHz, CDCI3, 7,21 (s, 1H), 7,02 (s, 1H), 3,75 (s, 3H), 2,57 (m, 1H), 2,38 (s, 6H), 0,99 (m, 6H) |
| 1-1-b-11 | F | 3-Me | 6-F | Et | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,43 (m, 1H), 7,12 (t, 1H), 3,68 (s, 3H), 2,40 (t, 1H), 2,21 (s, 6H), 0,89 (m, 6H) |
| l-1-b-12 | Cl | 3-Me | 6-F | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,52 (m, 1H), 7,22 (t, 1H), 3,70 (s, 3H), 2,32 (s, 3H), 2,22 (s, 3H), 2,09 (s, 3H) |
| l-1-b-13 | Cl | 4-Br | 6-CI | i-Pr | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,96 (s, 2H), 3,72 (s, 3H), 2,70 (m, 1H), 2,23 (s, 3H), 0,92 (m, 6H) |
| 1-1-b-14 | Cl | 4-CI | 6-Br | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,96 (d, 1H), 7,88 (d, 1H), 3,71 (s, 3H), 2,23 (s, 3H), 2,12 (s, 3H) |
| 1-1-b-15 | Cl | 4-Me | 6-c-Pr | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,58 (d, 1H), 7,22 (d, 1H), 3,68 (s, 3H), 2,29 8s, 3H), 2,21 (s, 3H), 2,05 (s, 3H) |
| 1-1-b-16 | Cl | 6-CI | H | i-Pr | i-Bu | Me | 1H-RMN, 400MHz, CDCI3, 7,39 (d, 2H), 7,28 (t, 1H), 3,87 (s, 3H), 2,53 (m, 1H), 2,42 (d, 2H), 2,06 (m, 1H), 0,96 (m, 12H) |
48/62
4. Preparação de 4-(2,6-diclorofenil)-5-etoxicarbonilóxi-2-metil6-isobutil-3(2H)-piridazinona (No. 1 da tabela 23)
0,5 g (1,52 mmol) do composto l-1-a-13 de acordo com a invenção da tabela 21 foi inicialmente colocado em 25 ml de diclorometano, e 0,2 g de trietilamina e 0,18 g de cloroformiato de etila adicionados. A mistura foi agitada sob temperatura ambiente por 15 minutos e depois adicionada a 30 ml de cinco porcento de solução de bicarbonato de sódio a 5%. A fase orgânica foi separada e depois secada, concentrada e purificada por cromatografia de coluna (sílica-gel, gradiente acetato de etila /n-heptano). Obtevese 0,47 g.
Os compostos da tabela 23 podem ser obtidos analogamente aos métodos acima referidos.
Tabela 23: Compostos da fórmula geral (I) de acordo com a invenção na qual G é C(=L)MR2.
A O—C(=L)MR2
| N°. | X | Y | z | A | B | L | M | R2 | Dados analíticos |
| H-o-1 | Cl | 6CI | H | i-Bu | Me | O | 0 | Et | 1H-RMN, 400MHz, CDCI3, 7,40 (d, 2H), 7,29 (t, 1H), 4,13 (q, 2H), 3,84 (s, 3H), 2,51 (d, 2H), 2,10 (m, 1H), 1,15 (t, 3H), 0,96 (d, 6H) |
| I-1-C-2 | F | 3-Me | 6-F | Me | Me | 0 | 0 | 5 | 1H-RMN, 400MHz, CDCfe, 7,46 (q 1H), 7,13 (t, 1H), 4,32 (q, 2H), 3,82 (s, 3H), 2,22 (s,3H), 1,32 (t,3H) |
| 1-1-03 | F | 3-OMe | 6-F | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, Õ6-DMSO, 7,32 (m, 1H), 7,17 (t, 1H), 4,13 (q, 2H), 3,85 (s, 3H), 3,71 (s, 3H), 2,25 (s, 3H), 1,09 (t, 3H) |
| I-1-&4 | Cl | 6-Br | 4-Me | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, Ó6-DMSO, 7,59 (s, 1H), 7,47 (s, 1H), 4,16 (q, 2H), 3,71 (s, 3H), 2,35 (s, 3H), 2,25 (s, 3H), 1,12 (t, 3H) |
49/62
| Ν°. | X | Y | Z | A | B | L | M | R2 | Dados analíticos |
| 1-1-05 | NO;. | H | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMS0, 8,23 (d, 1H), 7,88 (t, 1H), 7,75 (t, 1H), 7,43 (d, 1H), 4,15 (m, 2H), 3,68 (s, 3H), 2,28 (s, 3H), 0,92 (m, 6H) |
| 1-1-06 | Cl | 3-CI | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, DMSO, 7,72 (d, 1H), 7,47 (t, 1H), 7,22 (d, 1H), 4,13,(q, 2H), 3,72 (s, 3H), 2,25 (s, 3H), 1,07 (t, 3H) |
| 1-1-07 | Cl | 6-F | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMS0, 7,58 (m, 1H), 7,49 (d, 1H), 7,38 (t, 1H) 3,71 (s, 3H), 2,28 (s,3H), 1,08 (t,3H) |
| 1-1-οΒ | Cl | 6-CI | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, CDCIj, 7,60 (d, 2H), 7,52 (t, 1H), 4,13 (q, 2H), 3,72 (s, 3H), 2,28 (s,3H), 1,15 (t,3H) |
| l-1-οθ | Cl | 4-CI | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMS0, 7,79 (d, 1H), 7,53 (dd, 1H), 7,28 (d, 1H), 4,16 (q, 2H), 3,70 (S, 3H), 2,23 (s, 3H), 1,12 (t, 3H) |
| 1-1-010 | F | 3-F | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, dS-DMSO, 7,57 (m, 1H), 7,32 (m, 1H), 7,13 (m, 1H), 4,13 (q, 2H), 3,71 (s, 3H), 2,25 (s, 3H), 1,08 (t, 3H) |
| 1-1-011 | Br | 6-Br | 4-Me | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMSO, 7,61 (s, 2H), 4,18 (q, 2H), 3,72 (s, 3H), 2,33 (s, 3H), 2,26 (s,3H), 1,11 (t, 3H) |
| 1-1-012 | Cl | 6-CI | 4-OCF3 | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, CDCI3, 7,82 (s, 2H), 4,17 (q, 2H.) 3,72 (s, 3H) 2,28 (s, 3H), 1,07 (t,3H) |
| 1-1-0-13 | Cl | 6-OCF3 | 4-Me | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMSO, 7,48 (s, 1H), 7,32 (s, 1H), 4,18 (q, 2H), 3,71 (s, 3H), 2,42 (s, 3H), 2,21 (s, 3H), 1,12 (t, 3H) |
| 1-1-0-14 | OCF 3 | 4-Br | 6-Br | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6OMS0, 8,18 (s, 1H), 7,82 (s, 1H), 4,18 (q, 2H), 3,72 (s, 3H), 2,26 (s,3H), 1,13 (t, 3H) |
| 1-1-0-15 | H | 3-CFs | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, CDCU, 7,72 (d, 1H), 7,70-7,55 (m, 4H), 4,13 (q, 2H), 3,81 (s, 3H), 2,31 (s,3H), 1,17 (t, 3H) |
| H-o-16 | Cl | 3-Me | 6-F | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMSO, 7,52 (t, 1H), 7,28 (t, 1H), 4,12 (q, 2H), 3,72 (s, 3H), 2,35 (s, 3H), 2,28 (s, 3H), 1,08 (t, 3H) |
50/62
| N°. | X | Y | Z | A | B | L | M | R2 | Dados analíticos |
| I-1-O-17 | Cl | 4-Br | &CI | Me | Me | O | O | a | 1H-RMN, 400MHz, d6-DMSO, 7,95 (s, 2H), 4,18 (q, 2H), 3,71 (s, 3H), 2,27 (s, 3H), 1,13 (t, 3H) |
| I-1-C-18 | CF3 | 6-CI | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMSO, 7,97 (d, 1H), 7,89 (d, 1H), 7,73 (t, 1H), 4,16 (q, 2H), 3,73 (s, 3H), 2,28 (s, 3H), 1,12 (t, 3H) |
| H-o-19 | I | H | H | Me | Me | 0 | 0 | Et | 1H-RMN, 400MHz, d6-DMSO, 7,95 (d, 1H), 7,48 (t, 1H), 7,20 (t, 1H), 7,12 (d, 1H), 4,13 (q, 2H), 3,71 (s, 3H), 2,24 (s, 3H), 1,10 (t, 3H) |
| 1-1-0-20 | Cl | 4-Me | 6-Br | Me | Me | 0 | 0 | Me | 1H-RMN, 400MHz, d6-DMSO, 7,60 (d, 1H), 7,46 (d, 1H), 3,75 (s, 3H), 3,72 (s, 3H), 2,37 (s,3H), 2,26 (s,3H) |
| 1-1-0-21 | Cl | 3-Me | 6-F | Me | Me | 0 | 0 | Me | 1H-RMN, 400MHz, d6-DMSO, 7,52 (t, 1H), 7,28 (t, 1H), 3,72 (s, 6H), 2,35 (s, 3H), 2,28 (s, 3H) |
| 1-1-0-22 | F | 3-F | H | Me | Me | 0 | 0 | Bzl | 1H-RMN, 400MHz, d6-DMSO, 7,53 (m, 1H), 7,38 (m, 3H), 7,25 (m, 1H), 7,19 (m, 2H), 7,13 (m, 1H), 5,18 (s, 2H), 3,71 (s, 3H), 2,23 (s, 3H) |
| 1-1-0-23 | Cl | 3-CI | H | Me | Me | 0 | 0 | iBu | 1H-RMN, 400MHz, DMSO, 7,72 (d, 1H), 7,46 (t, 1H), 7,22 (d, 1H), 3,93,(m, 2H), 3,71 (s, 3H), 2,25 (s, 3H), 1,72 (m, 1H), 0,72 (d, 6H) |
| H-o-24 | Cl | 4-Me | 6-OCF3 | Me | Me | 0 | 0 | All | 1H-RMN, 400MHz, dfrOMSO, 7,49 (s, 1H), 7,32 (s, 1H), 5,78 (m, 1H), 5,18 (m, 2H), 4,62 (d, 2H), 3,71 (s, 3H), 2,40 (s, 3H), 2,26 (s, 3H) |
| 1-1-0-25 | Cl | 6-CI | H | i-Bu | Me | 0 | 0 | AO | 1H-RMN, 400MHz, CDCfe, 7,39 (d, 2H), 7,32 (t, 1H), 5,72 (m, 1H), 5,20 (m, 2H), 4,53 (d, 2H), 3,84 (s, 3H), 2,50 (d, 2H), 2,09 (m, 1H), 0,97 (d, 6H) |
5._Preparação de 4-(2-clorofenil)-5-metilsulfonilóxi-2, 6dimetil-3(2H)-piridazinona (N°. 1 da tabela 24)
0,03 g (0,12 mmol) do composto l-1-a-31 de acordo com a invenção da tabela 21 foi inicialmente colocado em 10 ml de acetato de etila,
51/62
0,02 g de trietilamina e a ponta de espátula de DMAP foram adicionados e a mistura aquecida sob 60°C. 0,015 g de cloreto de metanossulfonila foi adicionado em 2 ml de acetato de etila, e a mistura agitada por uma uma hora. Após adição de 6 ml de solução de cloreto de sódio saturada, a fase orgâni5 ca foi secada, concentrada e purificada por cromatografia de coluna (sílicagel, gradiente acetato de etila /n-heptano). Obteve-se 0,02 g de produto puro.
Os compostos da tabela 24 podem ser obtidos analogamente aos métodos acima mencionados.
Tabela 24: Compostos da fórmula geral (I) de acordo com a invenção na qual G é SO2R3.
| N°. | X | Y | Z | R3 | A | B | Dados analíticos |
| 1-1-d-1 | Cl | H | H | Me | Me | Me | 1H-RMN, 400MHz, CDCb, 7,55 (s, 1H), 7,42 (pseudo t, 3H), 3,81 (s, 3H), 2,51 (s, 3H), 2,48 (s, 3H) |
| 1-1-d-2 | Cl | 6-F | H | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,58 (m, 1H), 7,49 (d, 1H), 7,37 (t, 1H) 3,73 (s, 3H), 3,15 (s, 3H), 2,39 (t, 3H) |
| l-1-d-3 | Cl | 4-Me | 6-Br | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,61 (s, 1H), 7,48 (s, 1H), 3,71 (s, 3H), 3,11 (s, 3H), 2,38 (s, 3H), 2,33 (s, 3H) |
| l-1-d-4 | NO2 | H | H | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 8,23 (d, 1H), 7,88 (t, 1H), 7,77 (t, 1H), 7,60 (d, 1H) 3,67 (s, 3H), 3,05 (s, 3H), 2,39 (s, 3H) |
| 1-1-d-5 | Cl | 4-Br | 6-CI | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,96 (s, 2H), 3,71 (s, 3H), 3,35 (s, 3H), 2,40 (s, 3H) |
52/62
| N°. | X | Y | Z | R3 | A | B | Dados analíticos |
| 1-1 -d-6 | F | 3-F | H | Tolila | Me | Me | 1H-RMN, 400MHz, d6-DMSO: 7,43 (d, 2H); 7,33 (m, 1H), 7,25 (d, 2H), 7,09 (m, 1H), 7,02 (m, 1H), 3,68 (s, 3H), 2,38 (s, 3H), 2,35 (s, 3H) |
| 1-1 -d-7 | Cl | 4-OCF3 | 6-CI | Et | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,82 (s, 2H), 3,72 (s, 3H), 3,33 (q, 2H), 2,40 (s, 3H), 1,08 (t, 3H) |
| 1-1 -d-8 | F | 3-OCH3 | 6-F | Me | Me | Me | 1H-RMN, 400MHz, d6-DMSO: 7,33 (m, 1H); 7,18 (m, 1H), 3,86 (s, 3H), 3,72 (s, 3H), 3,21 (s, 3H), 2,41 (s, 3H) |
| 1-1-d-9 | Cl | 6-CI | H | Me | i-Bu | Me | 1H-RMN, 400MHz, CDCI3, 7,45 (d, 2H), 7,32 (t. 3H), 3,85 (s, 3H), 2,71 (d, 2H), 2,61 (s, 3H), 0,99 (d, 6H) |
6._Preparação de sal sódico de 4-(2-bromo-6-cloro-4metilfenil)-5-hidróxi-2,6-dimetil-3(2H)-piridazinona (N°. 1 da tabela 25)
0,1 g (0,12 mmol) do composto 1-1-a-9 de acordo com a invenção da tabela 21 e 0,011 g de hidróxido de sódio foram dissolvidos em 10 ml de metanol anidro e agitados por uma hora. A mistura foi concentrada sob pressão reduzida e recolhida em tolueno. O solvente foi removido mais uma vez, resultando em pó amorfo.
Os compostos da tabela 25 podem ser obtidos analogamente aos métodos acima referidos.
53/62
Tabela 25: Compostos da fórmula geral (I) de acordo com a invenção na qual G é E.
| N°. | X | Y | Z | E | A | B | Dados analíticos |
| l-1-g-1 | Br | 4-Me | 6-CI | Na+ | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,32 (s, 1H), 7,18 (s, 1H), 3,38 (s, 3H), 2,28 (s, 3H), 1,92 (s, 3H) |
| 1-1-g-2 | no2 | H | H | Na+ | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,78 (d, 1H), 7,65 (t, 1H), 7,43 (t, 1H), 7,20 (d, 1H)3,18(s, 3H), 1,93 (s, 3H) |
| 1-1-g-3 | NO2 | H | H | (Me)4N+ | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,78 (d, 1H), 7,65 (t, 1H), 7,43 (t, 1H), 7,22 (d, 1H) 3,38 (s, 3H), 3,12 (s, 12H), 1,95 (s, 3H) |
| 1-1 -g-4 | F | 3-F | H | (Me)4N+ | Me | Me | 1H-RMN, 400MHz, d6-DMSO, 7,08 (m, 1H), 6,98 (m, 1H), 7,13 (m, 1H), 3,38 (s, 3H), 3,13 (s, 12H), 1,96 (s, 3H) |
7. Descrição a título de exemplo da preparação da fórmula (H)
Exemplo 1:
0,45 g (9,7 mmols) de metil-hidrazina, junto com 0,99 g de trietilamina e 0,06 g de DMAP (0,05 eq), foram inicialmente colocados em 50 ml de diclorometano. 2,2 g de cloreto de 2,6-diclorofenilacetila,recém-preparado a partir de ácido 2,6-diclorofenilacético e cloreto de oxalila, em 50 ml de di10 clorometano foram lentamente adicionados em gotas sob 0°C. A mistura foi então agitada sob temperatura ambiente durante a noite, e adicionado clore54/62 to de amônio. A fase orgânica foi separada, secada e concentrada. A purificação por cromatografia de coluna resultou em 1,5 g de 1-(ácido 2, 6diclorofenilacético)-1 metil-hidrazida.
1,43 g de piruvato de metila foram adicionados, e a mistura dissolvida em 20 ml de etanol. A mistura de reação foi aquecida no ponto de ebulição sob refluxo durante duas horas e em seguida concentrada sob pressão reduzida e purificada por cromatografia de coluna (sílica-gel, fase móvel gradiente n-heptano/acetato de etila). Obteve-se 1,3 g de 2-{[2-(2,6diclorofenil)acetil]metil-hidrazono}propionato de metila.
Exemplo 2: 2 g (10,1 mmols) de ácido 2, 4-diclorofenilacético foram inicialmente colocados em 50 ml de diclorometano, 1,1 ml (1,67 eq) de cloreto de oxaiila e uma gota de DMF foram adicionados e a mistura aquecida no ponto de ebulição sob refluxo até a evolução de gás ter cessado. A mistura foi concentrada sob pressão reduzida, e duas vezes mais, adicionado diclorometano e a mistura novamente concentrada, e o resíduo então absorvido em 5 ml de diclorometano. A solução obtida assim foi adicionada em gotas a 0°C durante um período de 20 minutos a uma solução de 1,4 g (1,1 eq) de 2-(metil-hidrazono)propionato de metila e 2,9 ml de trietilamina (2,1 eq) em 20 ml de diclorometano. A mistura foi em seguida agitada sob temperatura ambiente durante a noite, e 30 ml de água adicionados. A fase aquosa foi removida e a fase orgânica concentrada. O resíduo obtido foi purificado por cromatografia de coluna (sílica-gel, gradiente n-heptano/acetato de etila). Obteve-se um total de 0,7 g de 2-{[2-(2,4-diclorofenil)acetil]metilhidrazonojpropionato de metila.
55/62
Tabela 26: Compostos da fórmula geral (II)
| N°. | X | Y | Z | A | B | R9 | Dados analíticos |
| ll-a-1 | Cl | 3-CI | H | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,54 (d, 1H), 7,34 (m, 2H), 4,10 (s, 2H), 3,78 (s, 3H), 3,36 (s, 3H), 2,27 (s, 3H) |
| ll-a-2 | Cl | 6-F | H | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,37 (m, 2H), 7,21 (t, 1H), 4,06 (s, 2H), 3,78 (s, 3H), 3,38 (s, 3H), 2,28 (s, 3H) |
| ll-a-3 | Cl | 6-CI | H | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,77 (d, 2H), 7,32 (t, 1H), 4,20 (s, 2H), 3,80 (s, 3H), 3,37 (s, 3H), 2,29 (s, 3H) |
| ll-a-4 | Cl | 4-CI | H | Me | Me | Me | 1H-RMN (400MHz, CDCI3, deslocamento em ppm): 7,45 - 7,04 (m, 3H), 4,10 (s, 2H), 3,89 (s, 3H), 3,42 (s, 3H), 2,29 (s, 3H) |
| ll-a-5 | H | 4-CI | H | Me | Me | Me | 1H-RMN (400MHz, CDCI3, deslocamento em ppm): 7,45 - 7,15 (m, 4H), 3,97 (s, 2H), 3,90 (s, 3H), 3,37 (s, 3H), 2,23 (s, 3H) |
| ll-a-6 | Cl | H | H | Me | Me | Me | 1H-RMN (400MHz, CDCI3, deslocamento em ppm): 7,45 - 7,05 (m, 4H), 4,14 (s, 2H), 3,88 (s, 3H), 3,41 (s, 3H), 2,27 (s, 3H) |
| ll-a-7 | H | 3-CI | H | Me | Me | Me | 1H-RMN (400MHz, CDCI3, deslocamento em ppm): 7,40 - 7,05 (m, 4H), 3,98 |
56/62
| Ν°. | X | Y | Z | A | B | R9 | Dados analíticos |
| (s, 2H), 3,93 (s, 3H), 3,38 (s, 3H), 2,21 (s, 3H) | |||||||
| ll-a-8 | H | 3-CF3 | H | Me | Me | Me | 1H-RMN (400MHz, CDCb, deslocamento em ppm): 7,70 - 7,35 (m, 4H), 4,06 (s, 2H), 3,90 (s, 3H), 3,38 (s, 3H), 2,23 (s, 3H) |
| ll-a-9 | Br | 4-Me | 6-Br | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,52 (s, 2H), 4,22 (s, 2H), 3,78 (s, 3H), 3,43 (s, 3H), 2,28 (s, 6H) |
| ll-a-10 | Cl | 4- OCF3 | Cl | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,64 (s, 2H), 4,22 (s, 2H), 3,78 (s, 3H), 3,38 (s, 3H), 2,28 (s, 3H) |
| ll-a-11 | Cl | 4-Me | 6-c-Pr | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,11 (s, 1H), 6,82 (s, 1H), 4,22 (s, 2H), 3,78 (s, 3H), 3,36 (s, 3H), 2,28 (s, 3H), 2,25 (s, 3H), 1,78 8m, 1H), 0,82 (m, 2H), 0,57 (m, 2H) |
| ll-a-12 | Cl | 4-Me | 6-OCF3 | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,38 (s, 1H), 7,22 (s, 1H), 4,05 (s, 2H), 3,77 (s, 3H), 3,36 (s, 3H), 2,35 (s, 3H), 2,28 (s, 3H) |
| ll-a-13 | F | 3-Me | 6-F | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,22 (m, 1H), 6,98 (t, 1H), 3,92 (s, 2H), 3,78 (s, 3H), 3,35 (s, 3H), 2,28 (s, 3H), 2,20 (s, 3H) |
| ll-a-14 | Br | 4-Br | 6-OCF3 | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,99 (s, 1H), 7,68 (s, 1H), 4,09 (s, 2H), 3,77 (s, 3H), 3,35 (s, 3H), 2,28 (s, 3H) |
57/62
| Ν°. | X | Y | Z | A | B | R9 | Dados analíticos |
| ll-a-15 | Cl | 3-Me | 6-F | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,32 (m, 1H), 7,13 (t, 1H), 4,05 (s, 2H), 3,78 (s, 3H), 3,35 (s, 3H), 2,53 (s, 3H), 2,28 (s, 3H) |
| ll-a-16 | F | 3- OMe | 6-F | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,12 (m, 1H), 7,02 (t, 1H), 3,92 (s, 2H), 3,82 (s, 3H), 3,78 (s, 3H), 3,35 (s, 3H), 2,25 (s. 3H), |
| ll-a-17 | Cl | 4-Br | 6-CI | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,79 (s, 2H), 4,15 (s, 2H), 3,79 (s, 3H), 3,35 (s, 3H), 2,28 (s, 3H) |
| ll-a-18 | Cl | 6-CI | H | Me | i-Bu | Et | 1H-RMN (400MHz, CDCI3, deslocamento em ppm): 7,32 (d, 2H), 7,15 (m, 1H), 4,32 (m, 4H), 3,40 e 3,22 (em cada caso s, juntamente 3H), 2,70 e 2,42 (em cada caso m, juntamente 2H) 2,00 (m, 1H), 1,42 (m, 3H), 0,95 (m, 6H) |
| ll-a-19 | I | H | H | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,82 (d, 2H), 7,32 (m, 2H), 7,02 (t, 1H), 4,03 (s, 2H), 3,80 (s, 3H), 3,36 (s, 3H), 2,26 (s, 3H) |
| ll-a-20 | Cl | 4-CI | 6-Br | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,82 (s, 1H), 7,72 (s, 1H), 4,21 (s, 2H), 3,79 (s, 3H), 3,38 (s, 3H), 2,28 (s, 3H) |
| ll-a-21 | Cl | 6-CF3 | H | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,82 (d, 1H), 7,75 (d, 1H), 7,54 (t, 1H), 4,21 (s, 2H), 3,79 (s, 3H), 3,30 (s, 3H), 2,28 (s, 3H) |
| ll-a-22 | 2-CF3 | 5-CF3 | H | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslo- |
58/62
| N°. | X | Y | Z | A | B | R9 | Dados analíticos |
| camento em ppm): 7,92 (t, 1H), 7,90 (s, 1H), 7,85 (d, 1H), 4,26 (s, 2H), 3,79 (s, 3H), 3,35 (s, 3H), 2,27 (s, 3H) | |||||||
| ll-a-23 | Cl | 4-CI | 6-c-Pr | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,42 (s, 1H), 7,05 (s, 1H), 4,23 (s, 2H), 3,79 (s, 3H), 3,38 (s, 3H), 2,28 (s, 3H), 1,82 (m, 1H), 0,88 (m, 2H), 0,68 (m, 2H) |
| ll-a-24 | Cl | 4-CI | 6-Br | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,81 (s, 1H), 7,71 (s, 1H), 4,22 (s, 2H), 3,78 (s, 3H), 3,38 (s, 3H), 2,28 (s, 3H) |
| ll-a-25 | Cl | 4-Br | 6-OCF3 | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,88 (s, 1H), 7,68 (s, 1H), 4,08 (s, 2H), 3,78 (s, 3H), 3,33 (s, 3H), 2,28 (s, 3H) |
| ll-a-26 | Br | 4-CI | 6-OCF3 | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 7,92 (s, 1H), 7,61 (s, 1H), 4,11 (s, 2H), 3,78 (s, 3H), 3,35 (s, 3H), 2,28 (s, 3H) |
| ll-a-27 | Cl | 4-Br | 6-OCF3 | Me | Me | Me | 1H-RMN (400MHz, d6-DMSO, deslocamento em ppm): 8,18 (s, 1H), 7,93 (s, 1H), 4,18 (s, 2H), 3,78 (s, 3H), 3,32 (s, 3H), 2,28 (s, 3H) |
B. Exemplos de formulação
a) Um pó é obtido misturando-se 10 partes em peso de um composto da fórmula (I) e/ou sal deste em 90 partes em peso de talco como substância inerte e triturado em um moinho de martelo.
b) Um pó umedecível que já é dispersável em água foi obtido mediante mistura de 25 partes em peso de um composto da fórmula (I) e/ou um sal deste, 64 partes em peso de um quartzo contendo caulina como
59/62 substância inerte, 10 partes em peso de lignossulfonato de potássio e uma parte em peso de oleoilmetiltaurato de sódio como agente umectante e dispersante, e moagem da mistura em um moinho de disco com pinos.
c) Um concentrado de dispersão hidrodispersável foi obtido mediante mistura de 20 partes em peso de um composto da fórmula (I) e/ou sal deste com 6 partes em peso de alquilfenol poliglicol éter(®Triton X 207), 3 partes em peso de isotridecanol poliglicol éter (õ EO) e 71 partes em peso de óleo mineral parafínico (faixa de ponto de ebulição por exemplo de aproximadamente 255 a acima de 277°C) e moagem da mistura em um moinho de esferas resultando em uma finura inferior a 5 mícrons.
d) Um concentrado emulsificante é obtido a partir de 15 partes em peso de um composto da fórmula (l)e/ou um sal deste, 75 partes em peso de ciclo-hexanona como solvente e 10 partes em peso de nonilfenol oxetilado como emulsificante.
e) Grânulos hidrodispersáveis foram obtidos mediante mistura de 75 partes em peso de um composto da fórmula (I) e/ou um sal deste, partes em peso de lignossulfonato de cálcio, partes em peso de laurilsulfato de sódio, partes em peso de álcool polivinílico e partes em peso de caulina,
Moagem da mistura em um moinho de disco com pinos e granulação do pó em um leito fluidificado mediante atomização em água como líquido de granulação.
f) grânulos hidrodispersáveis também são obtidos mediante homogeneização e pré-trituração de 25 partes em peso de um composto da fórmula (I), partes em peso de 2,2'-dinaftiimetano-6,6'-dissulfonato de sódio, partes em peso de oleoilmetiltaurato de sódio, parte em peso de álcool polivinílico, partes em peso de carbonato de cálcio e partes em peso de água
60/62
Em um moinho coloidal, em seguida moagem da mistura em um moinho de microesferas de vidro, e atomização e secagem da suspensão resultante em uma torre de pulverização, com o uso de um atomizador monofluido.
C. Exemplos biológicos
1. Efeito pré-emergência herbicida contra plantas nocivas
Sementes de ervas daninhas monocotiledôneas ou dicotiledôneas ou plantas de cultura são colocadas em um solo arenoso-limoso em potes de fibra de madeira e cobertos com terra. Os compostos de acordo com a invenção, formulados na forma de pós umedecíveis (WP) ou concentrados de emulsão (EC), são então aplicados à superfície da cobertura de terra na forma de uma suspensão aquosa ou emulsão a uma taxa de aplicação de água de 600 a 800 l/ha (convertida), com adição de 0,2% de agente umectante. Após o tratamento, os potes são colocados na estufa e mantidos sob boas condições de crescimento para as plantas de teste. O dano às plantas de teste foi verificado visualmente em comparação com controles não submetidos a tratamento após um período experimental de 3 semanas (ação herbicida em porcento (%): 100% de atividade = plantas morreram, 0% de atividade = como plantas de controle).Neste caso, por exemplo, os compostos Nos. 1-1-c-8, 1-1-a-16 e l-l-c-13 apresentam, a uma taxa de aplicação de 320 g/ha, respectivamente pelo menos 90% de atividade contra Matricaria inodora, Stellaria media e Verônica pérsica.
2. Atividade de pós-emergência herbicida contra plantas nocivas
Sementes de ervas daninhas monocotiledôneas e dicotiledôneas ou plantas de cultura foram colocadas em um solo arenoso-limoso em potes de fibra de madeira, cobertor com terra e desenvolvidos na estuda sob boas condições de crescimento. Duas a 3 semanas após a semeadura, as plantas de teste foram tratadas no estágio e 1-folha. Os compostos de acordo com a invenção, formulados na forma de pós umedecíveis (WP) ou concentrados de emulsão (EC), foram em seguida atomizados sobre as partes de planta verdes na forma de suspensão aquosa ou emulsão a uma taxa de aplicação de água de 600 a 800 l/ha (convertida), com adição de 0,2% de agente
61/62 umectante. Após as plantas de teste terem sido deixadas sob condições ideais de crescimento na estufa por aproximadamente 3 semanas, a atividade das preparações foi observada visualmente em comparação com controles não submetidos a tratamento (ação herbicida em porcento (%): 100% de atividade = plantas morreram, 0% de atividade = como plantas de controle). Neste caso, por exemplo, os compostos l-1-a-27, I-1-C-7, l-l-c-8, l-1-b-3, 1-1b-1, I-1-C-9, l-1-a-9, I-1-C-14, l-1-g-1 e l-1-a-25 apresentam, sob uma taxa de aplicação de 320 g/ha, pelo menos 80% de atividade contra Amaranthus retroflexus, Verônica pérsica e Viola tricolor.
3, Ação Inseticida
Exemplo A
Teste Myzus (tratamento por atomização MYZUPE)
Solventes: 78 partes em peso de acetona
1,5 parte em peso de dimetilformamida
Emulsificante: 0,5 parte em peso de alquilaril poliglicol éter
Para produzir uma preparação adequada de substância ativa, 1 parte em peso de substância ativa foi misturada às quantidades indicadas de solventes e emulsificantes, e o concentrado diluído com água contendo emulsificante formando a concentração desejada. Folhas de couve-chinesa (Brassica pekinensis) que foram infectadas em todos os estágios do pulgão verde (Myzus persicae) receberam aplicação de uma preparação de substância ativa na concentração desejada. Após o período desejado, o efeito foi determinado em %. 100% significam que todos os pulgões foram mortos;0% significa que nenhum dos pulgões foi morto. Neste teste, por exemplo, os compostos Nos. l-1-a-4 e l-1-a-8 apresentam, sob uma taxa de aplicação de 500 g/ha, pelo menos 80% de atividade.
Exemplo B
Teste de Heliothis virescens (tratamento por spray)
Solventes: 78,0 partes em peso de acetona
1,5 parte em peso de dimetilformamida
Emulsificante: 0,5 parte em peso de alquilaril poliglicol éter
Para produzir uma preparação adequada de substância ativa, 1
62/62 parte em peso de substância ativa foi misturada às quantidades indicadas de solventes e emulsificantes, e o concentrado diluído com água contendo emulsificante formando a concentração desejada. Folhas de soja (Glycine max.) receberam a aplicação de de uma preparação de substância ativa da concentração desejada e, após a secagem, populadas com ovos de lagarta de tabaco(Heliothis virescens). Após 7 dias, o efeito foi determinado em %. 100% significam que todos os ovos foram mortos; 0% significa que nenhum dos ovos foi morto. Neste teste, por exemplo, o composto N°. 1-1-a-5 apresenta sob uma taxa de aplicação de 500 g/ha, pelo menos 80% de atividade. Exemplo C
Teste de Meloidogyne incógnita (MELGIN)
Solventes: 78,0 partes em peso de acetona
1,5 parte em peso de dimetilformamida Emulsificante: 0,5 parte em peso de aiquilaril poliglicol éter Para produzir uma preparação adequada de substância ativa, 1 parte em peso de substância ativa foi misturada às quantidades indicadas de solventes e emulsificantes, e o concentrado diluído com água contendo emulsificante formando a concentração desejada. Recipientes foram preenchidos com areia, solução de substância ativa, suspensão de ovo/larva Meloidogyne e sementes de alface. As sementes de alface germinaram e as plantas cresceram. Nas raízes, foram formadas galhas. Após o período de tempo desejado, a atividade nematicidal foi determinada em % pela formação de galhas. 100% significam que nenhuma galha foi formada; 0% significa que o número de galhas nas plantas tratadas corresponde àquele do controle não submetido ao tratamento. Neste teste, por exemplo, o composto N°. 1-1-a-10 apresenta, a uma taxa de aplicação de 20 ppm, uma eficácia de pelo menos 80%.
1/5
1. 4-Fenilpiridazinona, caracterizada pelo fato de que apresenta
Claims (13)
- REIVINDICAÇÕES a fórmula (I) na qualA e B são cada, independentemente entre si, hidrogênio ou (C1C6)-alquila,G é hidrogênio, C(=O)R1, C(=L)MR2, SO2R3, P(=L)R4R5, C(=L)NR6R7 ou E;E é um equivalente de íon metálico ou um íon de amônio;L é oxigênio ou enxofre;M é oxigênio ou enxofre;R1 é (C1-C6)-alquila, (C2-C6)-alquenila, (C1-C4)-alcóxi-(C1-C6)alquila, di-(C1-C4)-alcóxi-(C1-C6)-alquila ou (C1-C4)-alquiltio-(C1-C6)-alquila, sendo cada uma substituída por n átomos de halogênio, um anel de 3 a 6 membros totalmente saturado consistindo em 3 a 5 átomos de carbono e 1 a 3 heteroátomos do grupo consistindo em oxigênio, enxofre e nitrogênio, o qual é substituído por n radicais do grupo consistindo em halogênio, (C1-C4)alquila e (C1-C4)-alcóxi,(C3-C6)-cicloalquila, fenila, fenil-(C1-C4)-alquila, heteroarila, fenóxi-(C1-C4)-alquila ou heteroarilóxi-(C1-C4)-alquila substituída por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (C1-C4)alcóxi;R2 é (C1-C6)-alquila, (C2-C6)-alquenila, (C1-C4)-alcóxi-(C1C6)-alquila ou di-(C1-C4)-alcóxi-(C1-C6)-alquila, sendo cada uma substituída por n átomos de halogênio, ou é (C3-C6)-cicloalquila, fenila ou benzila, sendo cada uma substituída por n radicais do grupo consistindo em halogênio, (C1C4)-alquila e (C1-C4)-alcóxi;R3, R4 e R5 são cada, independentemente entre si, (C1-C6)alquila, a qual é substituída por n átomos de halogênio, (C1-C4)-alcóxi, N-(C1Petição 870170089570, de 21/11/2017, pág. 4/11
- 2/5C6)-alquilamino, N,N-di-(C1-C6)-alquilamino, (C1-C4)-alquiltio, (C2-C4)alquenila ou (C3-C6)-cicloalquiltio, ou fenila, benzila, fenóxi ou feniltio, o qual é substituído por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (C1-C4)-alcóxi;R6 e R7 são cada, independentemente entre si, hidrogênio, (C1C6)-alquila, a qual é substituída por n átomos de halogênio, (C3-C6)cicloalquila, (C2-C6)-alquenila, (C1-C6)-alcóxi ou (C1-C4)-alcóxi-(C1-C6)alquila, fenila ou benzila, sendo cada uma substituída por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (C1-C4)-alcóxi;ou R6 e R7 ,juntamente com o átomo de nitrogênio ao qual estão ligados, formam um anel de 3 a 6 membros, que contém 2 a 5 átomos de carbono e 0 ou 1 átomo de oxigênio ou de enxofre;n é 0, 1, 2 ou 3;X é halogênio;Y e Z são cada, independentemente entre si, hidrogênio, halogênio, ciano, nitro, (C3-C6)-cicloalquila ou são (C1-C6)-alquila, (C1-C6)-alcóxi ou fenila, sendo cada um substituído por n átomos de halogênio, ou seus sais, com a condição de que nem Y nem Z seja um radical (C1-C6)-alquila ou (C1-C6)-alcóxi localizado na posição 6 se n for 0, e de que o composto 4-(2,4-diclorofenil)-5-hidróxi-2-metilpiridazin-3(2H)-ona esteja excluído.2. 4-Fenilpiridazinona, de acordo com a reivindicação 1, caracterizada pelo fato de que:A é hidrogênio ou (C1-C6)-alquila;B é hidrogênio ou (C1-C6)-alquila;G é hidrogênio, C(=O)R1, C(=L)MR2, SO2R3, P(=L)R4R5, C(=L)NR6R7, ou E;2+13d14d15d16m + é Na+, K+, (Mg2+)1/2, (Ca2+)1/2, R13R14R15R16N+ ou NH4+;E13 14 15 16R , R , R e R são, independentemente entre si, (C1-C6)alquila ou benzila;Petição 870170089570, de 21/11/2017, pág. 5/11
- 3/5L é oxigênio;M é oxigênio;R1 é (C1-C6)-alquila, a qual é substituída por n átomos de halogênio ou é (C3-C6)-cicloalquila, fenila ou fenil-(C1-C4)-alquila, sendo cada uma substituída por n radicais do grupo consistindo em halogênio, (C1-C4)alquila e (C1-C4)-alcóxi;R2 é (C1-C6)-alquila, a qual é substituída por n átomos de halogênio ou é (C3-C6)-cicloalquila, fenila ou benzila, sendo cada uma substituída por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (C1-C4)-alcóxi;R3, R4 e R5 são cada, independentemente entre si, (C1-C6)alquila, a qual é substituida por n átomos de halogênio ou são fenila ou benzila, as quais são substituídas por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (C1-C4)-alcóxi;R6 e R7 são cada, independentemente entre si, hidrogênio, (C1C6)-alquila, a qual é substituída por n átomos de halogênio ou fenila ou benzila, as quais são substituídas por n radicais do grupo consistindo em halogênio, (C1-C4)-alquila e (C1-C4)-alcóxi;n é 0, 1,2, ou 3;X é halogênio;Y e Z são cada, independentemente entre si, hidrogênio, halogênio, ciano, nitro, (C3-C6)-cicloalquila ou são (C1-C6)-alquila ou (C1-C6)alcóxi, sendo cada um substituído por n átomos de halogênio, com a condição de que nem Y nem Z seja um radical (C1-C6)-alquila ou (C1-C6)-alcóxi localizado na posição 6, se n for 0, e de que o composto 4-(2,4-diclorofenil)-5-hidróxi-2-metilpiridazin-3(2H)-ona esteja excluído.3. 4-Fenilpiridazinona, de acordo com a reivindicação 1 ou 2, caracterizada pelo fato de que:A é hidrogênio, metila, etila ou isobutila;B é hidrogênio, metila, etila, isobutila ou terc-butila;G é hidrogênio, C(=O)R1, C(=L)MR2, SO2R3, P(=L)R4R5,Petição 870170089570, de 21/11/2017, pág. 6/11
- 4/5C(=L)NR6R7 ou E;E é Na+, K+, (Mg2+)i/2, (Ca2+)i/2, (CH^N* ou NH4+;L é oxigênio;M é oxigênio;R1 é (C1-C6)-alquila ou (C3-C6)-cicloalquila;R2 é (C1-C6)-alquila, (C3-C6)-cicloalquila ou benzila;R3, R4 e R5 são cada, independentemente entre si, (C1-C6)alquila, fenila ou benzila;R6 e R7 são cada, independentemente entre si, hidrogênio, (C1C6)-alquila, fenila ou benzila;n é 0, 1, 2 ou 3; eX é flúor, bromo, cloro ou iodo;Y é hidrogênio, flúor, bromo, cloro, iodo, metila, etila, metóxi, etóxi, tri-flúor-metila, tri-flúor-metóxi ou ciclopropila;Z é hidrogênio, flúor, bromo, cloro, iodo, metila, etila, metóxi, etóxi, tri-flúor-metila, tri-flúor-metóxi ou ciclopropila, com a condição de que nem Y nem Z seja um radical (C1-C6)alquila ou (C1-C6)-alcóxi localizado na posição 6 se n for 0, e de que o composto 4-(2,4-diclorofenil)-5-hidróxi-2-metilpiridazin-3(2H)-ona esteja excluído.4. Composição herbicida, caracterizada pelo fato de que compreende uma quantidade eficaz de pelo menos uma 4-fenilpiridazinona, de acordo com a fórmula (I), como definida em qualquer uma das reivindicações 1 a 3.
- 5. Composição herbicida, de acordo com a reivindicação 4, caracterizada pelo fato de que é uma mistura com auxiliares de formulação.
- 6. Composição herbicida, de acordo com a reivindicação 4 ou 5, caracterizada pelo fato de que compreende pelo menos uma outra substância ativa de ação pesticida do grupo consistindo em inseticidas, acaricidas, herbicidas, fungicidas, agentes protetores e reguladores do crescimento.
- 7. Composição herbicida, de acordo com a reivindicação 6,Petição 870170089570, de 21/11/2017, pág. 7/115/5 caracterizada pelo fato de que compreende um agente protetor.
- 8. Composição herbicida, de acordo com a reivindicação 6 ou 7, caracterizada pelo fato de que compreende um outro herbicida.
- 9. Método para combate de plantas indesejadas, caracterizado pelo fato de que uma quantidade eficaz de pelo menos uma 4fenilpiridazinona, de acordo com a fórmula (I), como definida em qualquer uma das reivindicações 1 a 3, ou de uma composição herbicida, como definida em qualquer uma das reivindicações 4 a 8, é aplicada às plantas ou ao local onde as plantas indesejadas crescem.
- 10. Uso de uma 4-fenilpiridazinona, de acordo com a fórmula (I), como definida em qualquer uma das reivindicações 1 a 3, ou de uma composição herbicida, como definida em qualquer uma das reivindicações 4 a 8, caracterizado pelo fato de que é no combate de plantas indesejadas.
- 11. Uso, de acordo com a reivindicação 10, caracterizado pelo fato de que a 4-fenilpiridazinona, de acordo com a fórmula (I), é usada para o combate de plantas indesejadas em culturas de plantas úteis.
- 12. Uso, de acordo com a reivindicação 11, caracterizado pelo fato de que as plantas úteis são plantas úteis transgênicas.
- 13. Uso de uma 4-fenilpiridazinona, de acordo com a fórmula (I), como definida em qualquer uma das reivindicações 1 a 3, caracterizado pelo fato de que é como inseticida.Petição 870170089570, de 21/11/2017, pág. 8/11
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| EP08022104A EP2204366A1 (de) | 2008-12-19 | 2008-12-19 | Herbizid und insektizid wirksame phenylsubstituierte Pyridazinone |
| EP08022104.7 | 2008-12-19 | ||
| PCT/EP2009/008906 WO2010078912A1 (de) | 2008-12-19 | 2009-12-12 | Herbizid und insektizid wirksame phenyl-substituierte pyridazinone |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| BRPI0922428A2 BRPI0922428A2 (pt) | 2015-08-11 |
| BRPI0922428B1 true BRPI0922428B1 (pt) | 2018-07-10 |
Family
ID=40473702
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0923035A BRPI0923035A2 (pt) | 2008-12-19 | 2009-12-12 | piridazinonas 4-fenil-substituídas de ação herbicida e inseticida |
| BRPI0922428-9A BRPI0922428B1 (pt) | 2008-12-19 | 2009-12-12 | 4-fenilpiridazinona e seu uso, composição herbicida, e método para combate de plantas indesejadas |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| BRPI0923035A BRPI0923035A2 (pt) | 2008-12-19 | 2009-12-12 | piridazinonas 4-fenil-substituídas de ação herbicida e inseticida |
Country Status (9)
| Country | Link |
|---|---|
| US (3) | US20110003692A1 (pt) |
| EP (3) | EP2204366A1 (pt) |
| JP (2) | JP5651602B2 (pt) |
| CN (4) | CN102325757A (pt) |
| AR (3) | AR074773A1 (pt) |
| AU (2) | AU2009336854A1 (pt) |
| BR (2) | BRPI0923035A2 (pt) |
| CA (2) | CA2747639A1 (pt) |
| WO (3) | WO2010078912A1 (pt) |
Families Citing this family (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2006060122A2 (en) * | 2004-11-30 | 2006-06-08 | Artesian Therapeutics, Inc. | Cardiotonic compounds with inhibitory activity against beta-adrenergic receptors and phosphodiesterase |
| TWI375669B (en) * | 2006-03-17 | 2012-11-01 | Sumitomo Chemical Co | Pyridazinone compound and use thereof |
| US8097712B2 (en) | 2007-11-07 | 2012-01-17 | Beelogics Inc. | Compositions for conferring tolerance to viral disease in social insects, and the use thereof |
| GB201117019D0 (en) * | 2011-10-04 | 2011-11-16 | Syngenta Ltd | Herbicidal compounds |
| US8962584B2 (en) | 2009-10-14 | 2015-02-24 | Yissum Research Development Company Of The Hebrew University Of Jerusalem, Ltd. | Compositions for controlling Varroa mites in bees |
| WO2011045271A1 (de) | 2009-10-15 | 2011-04-21 | Bayer Cropscience Ag | Herbizid wirksame heterocyclylsubstituierte pyridazinone |
| MY163887A (en) | 2010-03-08 | 2017-11-15 | Monsanto Technology Llc | Polynucleotide molecules for gene regulations in plants |
| JP5842594B2 (ja) * | 2010-12-27 | 2016-01-13 | 住友化学株式会社 | ピリダジノン化合物、それを含有する除草剤及び有害節足動物防除剤 |
| CN107739737A (zh) | 2011-09-13 | 2018-02-27 | 孟山都技术公司 | 用于杂草控制的方法和组合物 |
| US10806146B2 (en) | 2011-09-13 | 2020-10-20 | Monsanto Technology Llc | Methods and compositions for weed control |
| UA115534C2 (uk) | 2011-09-13 | 2017-11-27 | Монсанто Текнолоджи Ллс | Спосіб та композиція для боротьби з бур'янами (варіанти) |
| EP3382027A3 (en) | 2011-09-13 | 2018-10-31 | Monsanto Technology LLC | Methods and compositions for weed control |
| US10829828B2 (en) | 2011-09-13 | 2020-11-10 | Monsanto Technology Llc | Methods and compositions for weed control |
| US10760086B2 (en) | 2011-09-13 | 2020-09-01 | Monsanto Technology Llc | Methods and compositions for weed control |
| CN110066794A (zh) | 2011-09-13 | 2019-07-30 | 孟山都技术公司 | 用于杂草控制的方法和组合物 |
| AR087862A1 (es) | 2011-09-13 | 2014-04-23 | Monsanto Technology Llc | Metodos y composiciones para el control de malezas |
| US9840715B1 (en) | 2011-09-13 | 2017-12-12 | Monsanto Technology Llc | Methods and compositions for delaying senescence and improving disease tolerance and yield in plants |
| EP2756084B1 (en) | 2011-09-13 | 2020-06-03 | Monsanto Technology LLC | Methods and compositions for weed control |
| WO2013040116A1 (en) | 2011-09-13 | 2013-03-21 | Monsanto Technology Llc | Methods and compositions for weed control |
| CN103930549B (zh) | 2011-09-13 | 2020-09-18 | 孟山都技术公司 | 用于杂草控制的方法和组合物 |
| US9920326B1 (en) | 2011-09-14 | 2018-03-20 | Monsanto Technology Llc | Methods and compositions for increasing invertase activity in plants |
| EP2855680B8 (en) | 2012-05-24 | 2020-04-15 | Monsanto Technology LLC | Compositions and methods for silencing gene expression |
| MX364070B (es) | 2012-10-18 | 2019-04-10 | Monsanto Technology Llc | Métodos y composiciones para el control de plagas vegetales. |
| UY35251A (es) | 2013-01-01 | 2014-07-31 | Seeds Ltd Ab | MOLÉCULAS DE dsRNA AISLADAS Y MÉTODOS PARA USARLAS PARA SILENCIAR MOLÉCULAS DIANA DE INTERÉS |
| US10683505B2 (en) | 2013-01-01 | 2020-06-16 | Monsanto Technology Llc | Methods of introducing dsRNA to plant seeds for modulating gene expression |
| US10000767B2 (en) | 2013-01-28 | 2018-06-19 | Monsanto Technology Llc | Methods and compositions for plant pest control |
| WO2014119770A1 (ja) * | 2013-01-30 | 2014-08-07 | 住友化学株式会社 | ピリダジノン化合物及びそれを含有する除草剤 |
| CN105074008A (zh) | 2013-03-13 | 2015-11-18 | 孟山都技术有限公司 | 用于杂草控制的方法和组合物 |
| UA121846C2 (uk) | 2013-03-13 | 2020-08-10 | Монсанто Текнолоджи Ллс | Спосіб та гербіцидна композиція для контролю видів рослини роду lolium |
| US20140283211A1 (en) | 2013-03-14 | 2014-09-18 | Monsanto Technology Llc | Methods and Compositions for Plant Pest Control |
| US10568328B2 (en) | 2013-03-15 | 2020-02-25 | Monsanto Technology Llc | Methods and compositions for weed control |
| US9850496B2 (en) | 2013-07-19 | 2017-12-26 | Monsanto Technology Llc | Compositions and methods for controlling Leptinotarsa |
| EP3608412A3 (en) | 2013-07-19 | 2020-04-08 | Monsanto Technology LLC | Compositions and methods for controlling leptinotarsa |
| US9540642B2 (en) | 2013-11-04 | 2017-01-10 | The United States Of America, As Represented By The Secretary Of Agriculture | Compositions and methods for controlling arthropod parasite and pest infestations |
| UA119253C2 (uk) | 2013-12-10 | 2019-05-27 | Біолоджикс, Інк. | Спосіб боротьби із вірусом у кліща varroa та у бджіл |
| MX368629B (es) | 2014-01-15 | 2019-10-08 | Monsanto Technology Llc | Metodos y composiciones para el control de malezas utilizando polinucleotidos de 5-enolpiruvilshikimato-3-fosfato sintasa (epsps). |
| WO2015153339A2 (en) | 2014-04-01 | 2015-10-08 | Monsanto Technology Llc | Compositions and methods for controlling insect pests |
| EP3137456B1 (en) * | 2014-04-29 | 2021-06-02 | FMC Corporation | Pyridazinone herbicides |
| AU2015280252A1 (en) | 2014-06-23 | 2017-01-12 | Monsanto Technology Llc | Compositions and methods for regulating gene expression via RNA interference |
| EP3161138A4 (en) | 2014-06-25 | 2017-12-06 | Monsanto Technology LLC | Methods and compositions for delivering nucleic acids to plant cells and regulating gene expression |
| GB201412735D0 (en) * | 2014-07-17 | 2014-09-03 | Syngenta Participations Ag | Herbicidal compounds |
| AR101348A1 (es) | 2014-07-29 | 2016-12-14 | Monsanto Technology Llc | Composiciones y métodos para el control de pestes por insectos |
| JP6942632B2 (ja) | 2015-01-22 | 2021-09-29 | モンサント テクノロジー エルエルシー | Leptinotarsa防除用組成物及びその方法 |
| GB201507464D0 (en) * | 2015-04-30 | 2015-06-17 | Syngenta Participations Ag | Herbicidal compounds |
| EP3302053B1 (en) | 2015-06-02 | 2021-03-17 | Monsanto Technology LLC | Compositions and methods for delivery of a polynucleotide into a plant |
| WO2016196782A1 (en) | 2015-06-03 | 2016-12-08 | Monsanto Technology Llc | Methods and compositions for introducing nucleic acids into plants |
| GB2546336A (en) * | 2016-01-18 | 2017-07-19 | Syngenta Participations Ag | Intermediate compounds |
| TWI780112B (zh) * | 2017-03-31 | 2022-10-11 | 美商科迪華農業科技有限責任公司 | 具有殺蟲效用之分子,及其相關之中間物、組成物暨方法 |
| JP2021008405A (ja) * | 2017-09-27 | 2021-01-28 | 石原産業株式会社 | ピリダジノン系化合物又はその塩、及びそれらを含有する除草剤 |
| GB201800305D0 (en) * | 2018-01-09 | 2018-02-21 | Syngenta Participations Ag | Herbicidal compounds |
| EP4330234A1 (en) | 2021-04-27 | 2024-03-06 | Bayer Aktiengesellschaft | Substituted pyridazinones, salts or n-oxides thereof and their use as herbicidally active substances |
| IL315190A (en) * | 2022-03-30 | 2024-10-01 | Ishihara Sangyo Kaisha | A pyridazinone compound or a salt thereof and a pesticide containing them |
| WO2025069918A1 (ja) * | 2023-09-27 | 2025-04-03 | 石原産業株式会社 | ピリダジノン系化合物又はその塩及びそれらを含有する有害生物防除剤 |
Family Cites Families (29)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA92064A (en) | 1905-02-23 | 1905-03-14 | James E. Toscan | Detachable ice creeper |
| EP0131624B1 (en) | 1983-01-17 | 1992-09-16 | Monsanto Company | Plasmids for transforming plant cells |
| BR8404834A (pt) | 1983-09-26 | 1985-08-13 | Agrigenetics Res Ass | Metodo para modificar geneticamente uma celula vegetal |
| BR8600161A (pt) | 1985-01-18 | 1986-09-23 | Plant Genetic Systems Nv | Gene quimerico,vetores de plasmidio hibrido,intermediario,processo para controlar insetos em agricultura ou horticultura,composicao inseticida,processo para transformar celulas de plantas para expressar uma toxina de polipeptideo produzida por bacillus thuringiensis,planta,semente de planta,cultura de celulas e plasmidio |
| EP0221044B1 (en) | 1985-10-25 | 1992-09-02 | Monsanto Company | Novel plant vectors |
| ES2018274T5 (es) | 1986-03-11 | 1996-12-16 | Plant Genetic Systems Nv | Celulas vegetales resistentes a los inhibidores de glutamina sintetasa, preparadas por ingenieria genetica. |
| IL83348A (en) | 1986-08-26 | 1995-12-08 | Du Pont | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| US5013659A (en) | 1987-07-27 | 1991-05-07 | E. I. Du Pont De Nemours And Company | Nucleic acid fragment encoding herbicide resistant plant acetolactate synthase |
| CA2077896C (en) | 1990-03-16 | 2008-02-19 | Gregory A. Thompson | Plant desaturases - compositions and uses |
| DE69132916T2 (de) | 1990-06-18 | 2002-10-31 | Monsanto Technology Llc, St. Louis | Erhöhter stärkegehalt in pflanzen |
| ATE213774T1 (de) | 1990-06-25 | 2002-03-15 | Monsanto Technology Llc | Glyphosattolerante pflanzen |
| SE467358B (sv) | 1990-12-21 | 1992-07-06 | Amylogene Hb | Genteknisk foeraendring av potatis foer bildning av staerkelse av amylopektintyp |
| DE4104782B4 (de) | 1991-02-13 | 2006-05-11 | Bayer Cropscience Gmbh | Neue Plasmide, enthaltend DNA-Sequenzen, die Veränderungen der Karbohydratkonzentration und Karbohydratzusammensetzung in Pflanzen hervorrufen, sowie Pflanzen und Pflanzenzellen enthaltend dieses Plasmide |
| GB9418545D0 (en) * | 1994-09-15 | 1994-11-02 | Merck Sharp & Dohme | Therapeutic agents |
| US6358887B1 (en) | 1995-02-13 | 2002-03-19 | Bayer Aktiengesellschaft | 2-Phenyl-substituted heterocyclic 1,3-ketonols as herbicides and pesticides |
| BR9608229A (pt) | 1995-05-09 | 1998-12-29 | Bayer Ag | Cetoenóis alquil-dihalogenofenil-substituídos |
| JPH11140055A (ja) * | 1997-09-01 | 1999-05-25 | Nissan Chem Ind Ltd | 6−ハロアルキル−3−置換フェニル−2(1h)−ピリジノン誘導体及び除草剤 |
| JPH11152273A (ja) * | 1997-11-19 | 1999-06-08 | Otsuka Chem Co Ltd | 窒素含有6員環ジオン誘導体 |
| DE10029413A1 (de) | 2000-06-15 | 2001-12-20 | Bayer Ag | Verfahren zur Herstellung von 2,3,4,6-Tetramethylmandelsäure und 2,3,4,6-Tetramethylmandelsäureacetat |
| DE10325133A1 (de) | 2003-06-04 | 2004-12-23 | Bayer Cropscience Ag | Triazolopyrimidine |
| DE10354628A1 (de) | 2003-11-22 | 2005-06-16 | Bayer Cropscience Ag | 2-Ethyl-4,6-dimethyl-phenyl-substituierte Tetramsäure-Derivate |
| DE102004005318A1 (de) | 2004-02-04 | 2005-08-25 | Bayer Cropscience Ag | Verfahren zur Herstellung von 2,5-Dimethylphenylessigsäure |
| WO2007014054A2 (en) * | 2005-07-22 | 2007-02-01 | Glaxo Group Limted | Benzenesulfonamide inhibitor of ccr2 chemokine receptor |
| JP5040383B2 (ja) * | 2006-03-17 | 2012-10-03 | 住友化学株式会社 | ピリダジノン化合物及びそれを含有する除草剤 |
| TWI375669B (en) | 2006-03-17 | 2012-11-01 | Sumitomo Chemical Co | Pyridazinone compound and use thereof |
| FR2903325B1 (fr) | 2006-07-06 | 2009-02-06 | Air Liquide | Procede et appareil d'injection d'un jet de fluide de direction et/ou d'ouverture variable |
| CL2008002703A1 (es) * | 2007-09-14 | 2009-11-20 | Sumitomo Chemical Co | Compuestos derivados de 1,4-dihidro-2h-piridazin-3-ona; composicion herbicida que comprende a dichos compuestos; metodo de control de malezas; uso de dichos compuestos para el control de malezas; y compuestos intermediarios. |
| JP2009067740A (ja) * | 2007-09-14 | 2009-04-02 | Sumitomo Chemical Co Ltd | 除草用組成物 |
| CL2008003785A1 (es) * | 2007-12-21 | 2009-10-09 | Du Pont | Compuestos derivados de piridazina; composiciones herbicidas que comprenden a dichos compuestos; y método para controlar el crecimiento de la vegetación indeseada. |
-
2008
- 2008-12-19 EP EP08022104A patent/EP2204366A1/de not_active Withdrawn
-
2009
- 2009-12-12 CN CN2009801572630A patent/CN102325757A/zh active Pending
- 2009-12-12 JP JP2011541180A patent/JP5651602B2/ja not_active Expired - Fee Related
- 2009-12-12 AU AU2009336854A patent/AU2009336854A1/en not_active Abandoned
- 2009-12-12 BR BRPI0923035A patent/BRPI0923035A2/pt not_active IP Right Cessation
- 2009-12-12 JP JP2011541178A patent/JP5651601B2/ja not_active Expired - Fee Related
- 2009-12-12 CA CA2747639A patent/CA2747639A1/en not_active Abandoned
- 2009-12-12 WO PCT/EP2009/008906 patent/WO2010078912A1/de not_active Ceased
- 2009-12-12 EP EP09768345.2A patent/EP2379508B1/de not_active Not-in-force
- 2009-12-12 BR BRPI0922428-9A patent/BRPI0922428B1/pt not_active IP Right Cessation
- 2009-12-12 CN CN201610945167.4A patent/CN106928148A/zh active Pending
- 2009-12-12 AU AU2009328607A patent/AU2009328607A1/en not_active Abandoned
- 2009-12-12 WO PCT/EP2009/008908 patent/WO2010069525A1/de not_active Ceased
- 2009-12-12 CN CN201610076960.5A patent/CN105732513A/zh active Pending
- 2009-12-12 EP EP09807666.4A patent/EP2379509B1/de not_active Not-in-force
- 2009-12-12 CN CN2009801572503A patent/CN102325756A/zh active Pending
- 2009-12-12 WO PCT/EP2009/008909 patent/WO2010069526A1/de not_active Ceased
- 2009-12-12 CA CA2747638A patent/CA2747638A1/en not_active Abandoned
- 2009-12-14 US US12/637,025 patent/US20110003692A1/en not_active Abandoned
- 2009-12-15 US US12/638,105 patent/US8188008B2/en active Active
- 2009-12-15 US US12/638,180 patent/US8242055B2/en not_active Expired - Fee Related
- 2009-12-17 AR ARP090104942A patent/AR074773A1/es not_active Application Discontinuation
- 2009-12-17 AR ARP090104941A patent/AR075673A1/es not_active Application Discontinuation
- 2009-12-17 AR ARP090104943A patent/AR074774A1/es unknown
Also Published As
| Publication number | Publication date |
|---|---|
| US8242055B2 (en) | 2012-08-14 |
| US20110003692A1 (en) | 2011-01-06 |
| WO2010069526A1 (de) | 2010-06-24 |
| CN102325756A (zh) | 2012-01-18 |
| AR074773A1 (es) | 2011-02-09 |
| EP2379508A1 (de) | 2011-10-26 |
| JP2012512209A (ja) | 2012-05-31 |
| CN106928148A (zh) | 2017-07-07 |
| EP2379508B1 (de) | 2014-06-04 |
| WO2010078912A1 (de) | 2010-07-15 |
| CA2747638A1 (en) | 2010-07-15 |
| JP5651601B2 (ja) | 2015-01-14 |
| AR074774A1 (es) | 2011-02-09 |
| BRPI0923035A2 (pt) | 2018-10-16 |
| AU2009336854A8 (en) | 2011-12-01 |
| AU2009328607A1 (en) | 2011-07-07 |
| EP2204366A1 (de) | 2010-07-07 |
| AU2009336854A1 (en) | 2011-07-21 |
| EP2379509A1 (de) | 2011-10-26 |
| AR075673A1 (es) | 2011-04-20 |
| US8188008B2 (en) | 2012-05-29 |
| JP5651602B2 (ja) | 2015-01-14 |
| CN102325757A (zh) | 2012-01-18 |
| BRPI0922428A2 (pt) | 2015-08-11 |
| EP2379509B1 (de) | 2016-02-17 |
| JP2012512211A (ja) | 2012-05-31 |
| CN105732513A (zh) | 2016-07-06 |
| US20100173775A1 (en) | 2010-07-08 |
| US20100184602A1 (en) | 2010-07-22 |
| CA2747639A1 (en) | 2010-06-24 |
| WO2010069525A1 (de) | 2010-06-24 |
| WO2010078912A8 (de) | 2011-07-14 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| BRPI0922428B1 (pt) | 4-fenilpiridazinona e seu uso, composição herbicida, e método para combate de plantas indesejadas | |
| AU2017204231C9 (en) | Substituted picolinic acids and pyrimidine-4-carboxylic acids, method for the production thereof, and use thereof as herbicides and plant growth regulators | |
| EP2691379B1 (de) | Herbizid und fungizid wirksame 3-phenylisoxazolin-5-carboxamide und 3- phenylisoxazolin-5-thioamide | |
| WO2011045271A1 (de) | Herbizid wirksame heterocyclylsubstituierte pyridazinone | |
| BR112014023995B1 (pt) | Tiazolopiridinonas herbicidamente ativas, composições herbicidas e inseticidas, métodos para o controle de plantas e insetos indesejados e utilização de compostos e composição herbicida | |
| US20110118118A1 (en) | Herbicidally active phenyl-substituted pyridazinones | |
| CN103189376B (zh) | 具有除草活性的酮基磺内酰胺和二酮基吡啶 | |
| US20120065065A1 (en) | Herbicidally active pyridylketosultams |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| B07A | Application suspended after technical examination (opinion) [chapter 7.1 patent gazette] | ||
| B25A | Requested transfer of rights approved |
Owner name: BAYER INTELLECTUAL PROPERTY GMBH (DE) |
|
| B06A | Patent application procedure suspended [chapter 6.1 patent gazette] | ||
| B09A | Decision: intention to grant [chapter 9.1 patent gazette] | ||
| B16A | Patent or certificate of addition of invention granted [chapter 16.1 patent gazette] | ||
| B25G | Requested change of headquarter approved | ||
| B25A | Requested transfer of rights approved | ||
| B21F | Lapse acc. art. 78, item iv - on non-payment of the annual fees in time |
Free format text: REFERENTE A 16A ANUIDADE. |
|
| B24J | Lapse because of non-payment of annual fees (definitively: art 78 iv lpi, resolution 113/2013 art. 12) |
Free format text: EM VIRTUDE DA EXTINCAO PUBLICADA NA RPI 2858 DE 14-10-2025 E CONSIDERANDO AUSENCIA DE MANIFESTACAO DENTRO DOS PRAZOS LEGAIS, INFORMO QUE CABE SER MANTIDA A EXTINCAO DA PATENTE E SEUS CERTIFICADOS, CONFORME O DISPOSTO NO ARTIGO 12, DA RESOLUCAO 113/2013. |