CN101007795B - 紫杉醇及多烯紫杉醇的合成方法 - Google Patents
紫杉醇及多烯紫杉醇的合成方法 Download PDFInfo
- Publication number
- CN101007795B CN101007795B CN2007100669400A CN200710066940A CN101007795B CN 101007795 B CN101007795 B CN 101007795B CN 2007100669400 A CN2007100669400 A CN 2007100669400A CN 200710066940 A CN200710066940 A CN 200710066940A CN 101007795 B CN101007795 B CN 101007795B
- Authority
- CN
- China
- Prior art keywords
- compound
- solvent
- docetaxel
- reaction
- acid
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Expired - Fee Related
Links
Classifications
-
- Y—GENERAL TAGGING OF NEW TECHNOLOGICAL DEVELOPMENTS; GENERAL TAGGING OF CROSS-SECTIONAL TECHNOLOGIES SPANNING OVER SEVERAL SECTIONS OF THE IPC; TECHNICAL SUBJECTS COVERED BY FORMER USPC CROSS-REFERENCE ART COLLECTIONS [XRACs] AND DIGESTS
- Y02—TECHNOLOGIES OR APPLICATIONS FOR MITIGATION OR ADAPTATION AGAINST CLIMATE CHANGE
- Y02P—CLIMATE CHANGE MITIGATION TECHNOLOGIES IN THE PRODUCTION OR PROCESSING OF GOODS
- Y02P20/00—Technologies relating to chemical industry
- Y02P20/50—Improvements relating to the production of bulk chemicals
- Y02P20/55—Design of synthesis routes, e.g. reducing the use of auxiliary or protecting groups
Landscapes
- Epoxy Compounds (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
本发明提供紫杉醇及多烯紫杉醇的合成方法,是以10-DAB III为中间体,先选择性地保护C-7羟基,然后对C-10羟基进行酰化或保护,接着用保护的侧链酸与C-13羟基进行偶联,最后水解脱除保护基即得目标化合物紫杉醇或多烯紫杉醇。本发明方法克服目前几种保护基存在的缺点,开发出一种新的保护基——咪唑基硫羰基;为了避免C-2’差向异构化的形成及剧烈的反应条件,合成了2-单取代-1,3-噁唑烷型侧链酸;设计合理,所用试剂价格低廉、反应步骤少以及反应条件温和。本发明方法为紫杉醇的工业化生产提供了有利条件。同时为多烯紫杉醇的合成提供了一种新途径。
Description
技术领域
本发明属化合物合成,主要涉及抗癌药物紫杉醇及多烯紫杉醇的合成方法。
背景技术
紫杉醇(Paclitaxel,商品名Taxol,Formula Ia)是从红豆杉属(Taxus)植物中分离出的一种紫杉烷二萜类化合物。其结构新颖、抗癌机理独特、抗癌效果显著、抗癌谱广,被认为是迄今所发现最好的抗癌药物之一。继美国之后,目前紫杉醇作为一线抗癌药物已在40多个国家被批准上市。然而,紫杉醇供应匮乏大大限制了它在临床上的应用。目前,药用紫杉醇的主要来源是从天然红豆杉属植物的树皮中提取分离。但由于该种属植物数量少,生长慢,含量低,且提取难度颇大,从长远考虑根本无法满足日益增长的临床需求。
多烯紫杉醇(Docetaxel,商品名Taxotere,Formula Ib)是抗癌新药紫杉醇经化学修饰的衍生物,其抗肿瘤效果和毒副作用明显优于紫杉醇。临床上多烯紫杉醇作为化疗药物已开始用于乳腺癌、肺癌、胃癌和食管癌等的治疗,具有较好效果,且副作用较少。然而,多烯紫杉醇的供应远远不能满足市场的需求。
近年来,紫杉醇化学全合成获得成功,但合成路线复杂,成本过高,故而仅具有研究意义,尚无商业价值。相比较而言,紫杉醇类化学半合成是具有实用价值的一种制备方法,因而显得尤为重要。
半合成研究一般都是以与紫杉醇大环结构类似的10—去乙酰基巴卡亭(10-deacetylbaccatin III,10-DAB III)为中间体,通过与紫杉醇或多烯紫杉醇的侧链对接而制得紫杉醇或多烯紫杉醇。10-DAB III可从来源丰富的红豆杉属植物的针叶中提取而得,且得率高,从而为紫杉醇和多烯紫杉醇的半合成提供了充足的保障。
一般来讲,以10-DAB III为前体物来半合成紫杉醇及多烯紫杉醇的路线包括以下几步:
(一)在C-7和C-10位羟基选择性地保护
在10-DAB III(Formula II)分子结构中存在四个羟基,分别位于C-1、7、10和13位。这些羟基的反应活性不同,反应活性顺序由快到慢是C-7>C-10>C-13>C-1。此外,C-7羟基在碱性条件下极易差向异构化。所以,C-7羟基的保护基必须要求在温和的反应条件下可选择性地上保护,又可选择性地脱保护。在紫杉醇的半合成研究中,已报道用作C-7羟基保护基的基团有四种:三乙基硅基(TES)、三氯乙氧羰酰基(Troc)、三氯乙酰基和氯乙酰基。其中,三乙基硅基是最常用的保护基,然而在C-7羟基保护的反应中,其最佳反应条件是需要大大过量(20倍等摩尔量)昂贵的三乙基硅基;采用三氯乙氧羰酰基作为C-7羟基保护基,由于该基团对C-7和C-10两羟基的反应几乎没有选择性,故而在合成得到紫杉醇的过程中需要多几步反应,另外在对C-7羟基进行保护与脱保护时均需要剧烈的反应条件(TetrahedronLetters,1992,pp5185-5188);专利US6130336采用间歇加入三氯乙酰基保护基的方法对C-7羟基进行选择性保护;至于氯乙酰基,由于其较低的反应活性选择性,所以在反应中需要其严格的量化条件。
在C-7羟基保护之后,对C-10羟基进行酰化作用得到7-位羟基保护的巴卡亭III;或在C-7羟基保护之后,采用氯乙酰氯等试剂对C-10羟基进行保护,可得到7,10-位羟基保护的10-去乙酰巴卡亭III。
(二)保护的苯基异丝氨酸侧链(C13侧链)与C-13羟基选择性地进行酯化对接
由于巴卡亭分子中的C-13羟基是位于半球形紫杉烷骨架的凹面区域,因而被遮挡的C-13羟基很难与侧链酸进行酯化作用,所以此步反应是合成过程中的关键。为了提高酯化产率及降低副产物的形成,苯基异丝氨酸侧链部分通常要进行适当的保护,常用保护的C-13侧链有三大类:直线型、四元环β—内酰胺型和五元环噁唑烷型。
(三)侧链及巴卡亭两部分的脱保护
在脱保护过程中,常常需要将侧链及巴卡亭两部分分步进行,同时也会脱掉侧链N-保护基。很明显,如果能在一步反应中同时在侧链及巴卡亭两部分脱保护,且能保留N-保护基,这样对合成紫杉醇及多烯紫杉醇将会大大简化合成工艺。
发明内容
本发明目的是为半合成紫杉醇及多烯紫杉醇提供一种新的合成方法,是以10-DABIII为中间体,先选择性地保护C-7羟基,然后对C-10羟基进行酰化或保护,接着用保护的侧链酸与C-13羟基进行偶联,最后水解脱除保护基即得目标化合物紫杉醇或多烯紫杉醇。
本发明所提供的半合成紫杉醇及多烯紫杉醇的合成方法具体通过以下步骤实现:
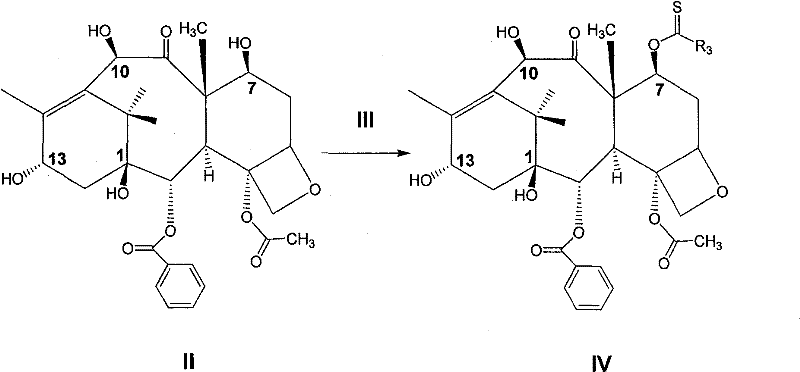
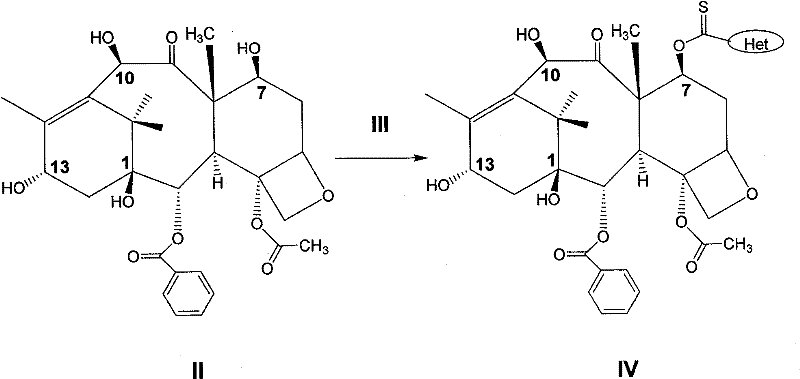
(1)10—去乙酰基巴卡亭(10-DAB III,化合物II)与化合物(III)在溶剂中进行反应,得到化合物(IV)。
或
上述为制备化合物(IV)的反应式,在该步反应中所用到的化合物(III)可以是酰卤化合物,也可以是杂环化合物,通常采用芳香酰卤或芳香杂环化合物,如硫代羰基二咪唑。反应的温度可以在-78~100℃之间,通常是在室温条件下进行,产率65~85%。所用到的溶剂可以是醚类溶剂,如1,4-二氧六环、二甲氧基乙烷、四氢呋喃等;也可以是芳香溶剂,如苯、甲苯、二甲苯等;还可以是氯代溶剂,如二氯甲烷、二氯乙烷、氯仿等,通常采用氯仿。所得产物(IV)的纯化可以通过重结晶的方法,如乙酸乙酯一正己烷;也可以进行快速硅胶柱层析。
(2)化合物(IV)与乙酰化试剂在溶剂中进行反应,得到化合物(Va);化合物(IV)与氯乙酰氯等试剂在溶剂中进行反应,对C-10羟基进行保护得到化合物(Vb)。
上述为制备化合物(V)的反应式,在该步反应中所用到的乙酰化试剂可以是乙酰氯、乙酸酐、冰乙酸等,通常采用乙酰氯或乙酸酐;对C-10羟基保护所用到的试剂可以是氯乙酰氯、三氯乙氧羰酰氯、苄氧羰酰氯、三氯乙酰氯。使用的捕酸剂是一些弱碱,如吡啶、三乙胺、哌啶等。反应的温度可以在-78~100℃之间,通常在0~30℃之间。使用的溶剂可以是醚类溶剂,如四氢呋喃等;也可以是氯代溶剂,如二氯甲烷、氯仿等,还可以是吡啶,通常采用的是吡啶。重结晶和快速柱层析均是可采用的纯化方法。
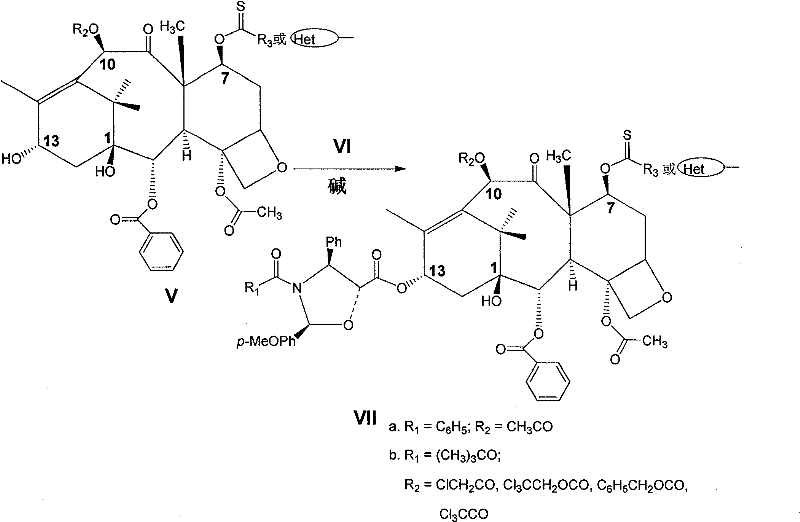
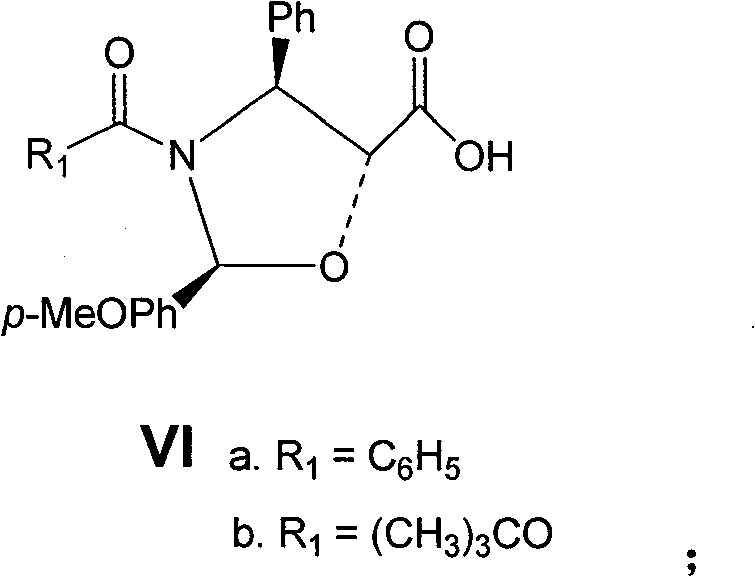
(3)化合物(Va)中的C-13羟基与保护的侧链酸(VIa)在碱存在下在溶剂中进行酯化偶联,得到化合物(VIIa);化合物(Vb)中的C-13羟基与保护的侧链酸(VIb)在碱存在下在溶剂中进行酯化偶联,得到化合物(VIIb)。
上述为制备化合物(VII)的反应式,在该步反应中所用到的碱包括两部分:一部分是缩合剂羰二酰亚胺类,如二环己基羰二酰亚胺(DCC)、二异丙基羰二酰亚胺(DIC)等;另一部分是激活剂,如4-二甲氨基吡啶等。可选用的溶剂可以是醚性溶剂,如1,4-二氧六环、二甲氧基乙烷、四氢呋喃等;可以是芳香溶剂,如苯、甲苯、二甲苯等;可以是氯代溶剂,如二氯甲烷、二氯乙烷、氯仿等;也可以是酰胺溶剂,如二甲基甲酰胺、二甲基乙酰胺等;还可以是它们的组合,如苯—四氢呋喃、甲苯—二氯甲烷等。该步反应可以温控在-78~100℃之间,通常在0~30℃之间。所得产物(VII)的粗品可采用快速柱层析进行纯化,也可不经纯化直接进入下一步反应。
(4)化合物(VIIa)在酸性条件下进行一步反应脱除C-7保护基及噁唑环保护基,得到目标产物紫杉醇(Ia);化合物(VIIb)在酸性条件下进行一步反应脱除C-7保护基、C-10保护基及噁唑环保护基,得到目标产物多烯紫杉醇(Ib)。
上述为制备目标化合物紫杉醇及多烯紫杉醇的反应式,在该步反应中所用到的弱酸可以是有机酸,如甲酸、乙酸、三氟乙酸、对甲苯磺酸等;也可以是无机酸的水溶液,如稀盐酸、稀硫酸、磷酸等;还可以是它们的组合,如对甲苯磺酸-稀盐酸、三氟乙酸-乙酸等。反应的温度可以在-78~100℃之间,通常是室温条件。可选用的溶剂可以是水、四氢呋喃、二氧六环、乙腈、甲醇、乙醇等。所得粗品经过柱层析可得纯产物。
本发明提供的紫杉醇合成新方法具有以下特点,(1)克服目前几种保护基存在的缺点,开发出一种新的保护基——咪唑基硫羰基。(2)为了避免C-2’差向异构化的形成及剧烈的反应条件,合成了2-单取代-1,3-噁唑烷型侧链酸。(3)设计合理,所用试剂价格低廉、反应步骤少以及反应条件温和等。本发明方法为紫杉醇的工业化生产提供了有利条件。同时,本发明为多烯紫杉醇的合成提供了一种新途径。
具体实施方式
下面将通过实施例对本发明作进一步的说明。
实施例1:7-(咪唑基)硫代羰氧基-10-去乙酰巴卡亭-III(IV)的制备
将1.25g(2.3mmol)10-去乙酰巴卡亭-III溶入110mL无水氯仿中,室温搅拌下加入0.82g(4.6mmol)1,1’-硫代羰基二咪唑,继续搅拌,体系呈亮黄透明,TLC监测反应进程。反应结束后,氯仿稀释,依次采用水和饱和的氯化钠溶液进行洗涤。无水硫酸钠干燥,过虑,减压除去溶剂。浓缩物经乙酸乙酯一正己烷重结晶纯化,得白色固体化合物IV1.24g(72.6%)。m.p.145-148℃;IR(KBr)v:3445,1717,1245cm-1;1HNMR(400MHz,DMSO-d6)δ:8.31(s,1H),8.05(d,J=7.2Hz,2H),7.69(m,1H),7.67(s,1H),7.58(t,J1=8.0Hz,J2=7.2Hz,2H),7.09(s,1H),6.11(t,J1=9.2Hz,J2=8.4Hz,1H),5.51(d,J=6.8Hz,1H),5.29(d,J=4.4Hz,1H),5.24(s,1H),5.18(s,1H),5.02(d,J=9.2Hz,1H),4.63(s,1H),4.46(s,1H),4.14(s,2H),4.04(d,J=6.8Hz,1H),2.73(m,1H),2.25(s,3H),2.21(m,2H),1.94(s,3H),1.90(m,1H),1.85(s,3H),0.96(s,3H),0.94(s,3H);13CNMR(100MHz,DMSO-d6)δ:209.23,182.74,169.99,165.29,141.88,136.91,134.40,133.28,130.76,130.11,129.53(2C),128.69(2C),118.56,82.70,81.86,79.45,76.93,75.39,74.69,74.39,69.95,55.38,46.16,42.27,39.09,31.21,26.57,22.14,20.07,14.79,11.22;LRMS calcd for C33H38N2O10S[M]+654.2,found654.4.
实施例2:7-(咪唑基)硫代羰氧基-巴卡亭-III(V)的制备
将1.11g(1.7mmol)化合物IV溶入15mL无水吡啶中,通氮气,搅拌,滴加3.3ml(34mmol)乙酸酐,室温下继续搅拌24h。加入等体积的乙酸乙酯和水,搅拌,静置分层,水相用乙酸乙酯提取两次,合并有机相,用饱和的硫酸铜溶液洗涤至完全除去吡啶,再依次用水和饱和的氯化钠溶液进行洗涤。无水硫酸钠干燥,过虑,减压除去溶剂。浓缩物经快速柱色谱纯化(洗脱剂为乙酸乙酯—环己烷,体积比为3∶4),得白色固体化合物V0.97g(71.7%)。m.p.241-244℃;IR(KBr)v:3466,1722,1236cm-1;1HNMR(400MHz,DMSO-d6)δ:8.15(s,1H),8.04(d,J=7.2Hz,2H),7.69(t,J1=7.2Hz,,J2=8.0Hz,1H),7.59(t,J=7.6Hz,2H),7.54(s,1H),7.03(s,1H),6.16(s,1H),6.12(m,1H),5.49(d,J=7.2Hz,1H),5.44(d,J=4.4Hz,1H),5.05(d,J=5.2Hz,1H),4.65(s,2H),4.13(s,2H),3.95(d,J=7.2Hz,1H),2.86(m,1H),2.25(s,3H),2.19(m,2H),1.95(s,6H),1.86(m,1H),1.84(s,3H),0.98(s,6H);13CNMR(100MHz,DMSO-d6):202.69,183.07,170.12,168.47,165.25,146.25,136.85,133.39,130.36,130.06,129.99,129.59(2C),128.76(2C),118.47,82.69,81.35,79.46,76.76,75.51,75.25,74.01,66.00,55.51,46.66,42.44,39.10,31.09,26.54,22.18,20.56,20.33,15.27,11.22;LRMS calcdfor C35H40N2O11S[M]+696.2,found 696.5.
实施例3:13-(2’-苯基-4’-对甲氧基苯基N-苯甲酰基-噁唑烷-1-羰氧基)-7-(咪唑基)硫代羰氧基-巴卡亭-III(VIIa)的制备
将0.77g(1.1mmol)化合物V溶入120mL无水甲苯和二氯甲烷(体积比为2∶1)中,搅拌下加入1.33g(3.3mmol)化合物VIa,40.3mg(0.33mmol)N,N’-二甲氨基吡啶(DMAP),搅拌10min后,加入340mg(1.65mmol)二环己基羰二酰亚胺(DCC),稍后体系变浑浊。室温条件下继续搅拌,TLC检测反应进程。反应完毕后,将浑浊物虑除,乙酸乙酯稀释,依次用饱和的氯化铵溶液、碳酸氢钠溶液和氯化钠溶液洗涤。无水硫酸钠干燥,过虑,减压除去溶剂。浓缩物经快速柱色谱纯化(洗脱剂为乙酸乙酯—环己烷,体积比为1∶2),得白色固体化合物VIIa 1.02g(75%)。m.p.157-161℃;IR(KBr)v:3428,1726,1653,1245 cm-1;1HNMR(400MHz,DMSO-d6)δ:8.18(s,1H),8.02(d,J=7.2Hz,2H),7.69(t,J1=7.6Hz,J2=7.2Hz,1H),7.59(t,J=7.6Hz,2H),7.56(s,1H),7.44-7.26(m,12H),7.04(s,1H),6.96(d,J=8.0Hz,2H),6.63(s,1H),6.20(s,1H),6.17-6.11(m,2H),5.58(d,J=6.8Hz,1H),5.51(s,1H),5.16(s,1H),5.09(s,1H),5.03(d,J=9.2Hz,1H),4.12(s,2H),3.95(d,J=7.2Hz,1H),3.78(s,3H),2.84(m,1H),2.38(m,1H),2.25(m,1H),2.14(s,3H),1.99(s,3H),1.96(s,3H),1.87(s,3H),1.86(m,1H),1.16(s,3H),1.03(s,3H);13CNMR(100MHz,DMSO-d6)δ:202.03,183.02,170.39,169.35,169.32,168.39,165.13,159.59(2C),156.58,140.14,139.08,136.86,135.79,133.53,132.62,130.39,129.68,129.58(2C),129.41,128.74,128.52(2C),128.39(2C),128.22(2C),127.91,126.84(2C),126.49(2C),118.46,113.63(2C),90.14,82.60,82.11,80.99,79.65,76.66,75.23,74.65,73.84,70.93,66.09,55.54,55.16,47.48,43.01,35.15,31.02,25.30,21.60,21.10,20.23,14.18,11.21;LRMS calcd for C59H59N3O15S[M]+1081.3,found1081.0.
实施例4:紫杉醇(Ia)的制备
将0.82g(0.76mmol)化合物VIIa溶入30mL甲醇中,室温搅拌下加入145mg(0.84mmol)对甲苯磺酸,反应3h后,再加入10mL 0.1N的盐酸水溶液,TLC检测反应进程。反应结束后,乙酸乙酯稀释,再依次用饱和的碳酸氢钠溶液、水和饱和的氯化钠溶液进行洗涤。无水硫酸钠干燥,过虑,减压浓缩,粗品经快速柱色谱纯化(洗脱剂为乙酸乙酯—环己烷,体积比为1∶1),得白色固体化合物Ia 0.56g(67%)。m.p.206-209℃;1HNMR(400MHz,DMSO-d6)δ:8.89(d,J=8.8Hz,1H),7.99(d,J=9.2Hz,1H),7.97(d,J=8.0Hz,2H),7.88(d,J=8.4Hz,2H),7.73-7.36(m,9H),7.22(d,J=8.4Hz,1H),6.29(s,1H),6.17(d,J=7.6Hz,1H),5.89(t,J1=8.8Hz,J2=9.2Hz,1H),5.42-5.40(m,2H),4.92-4.90(m,2H),4.70(s,1H),4.58(t,J1=7.6Hz,J2=8.4Hz,1H),4.41(d,J=4.0Hz,2H),4.11-4.09(m,1H),3.61(d,J=7.6Hz,1H),2.32(m,1H),2.22(s,3H),2.12(m,1H),2.11(s,3H),1.88(m,2H),1.79(s,3H),1.50(s,3H),1.07(s,3H),1.05(s,3H);LRMS calcd for C47H51NO14[M]+853.3,found 853.0.
实施例5:7-(苯基)硫代羰氧基-10-去乙酰巴卡亭-III(IV)的制备
将1.25g(2.3mmol)10-去乙酰巴卡亭-III溶入110mL无水氯仿中,室温搅拌下加入0.64g(4.6mmol)硫代苯甲酸,继续搅拌,TLC监测反应进程。反应结束后,氯仿稀释,依次采用水和饱和的氯化钠溶液进行洗涤。无水硫酸钠干燥,过虑,减压除去溶剂。浓缩物经乙酸乙酯—正己烷重结晶纯化,得化合物IV。
实施例6:7-(苯基)硫代羰氧基-10-三氯乙酰基-10-去乙酰巴卡亭-III(V)的制备
将1.13g(1.7mmol)化合物IV溶入15mL无水吡啶中,通氮气,搅拌,滴加6.18g(34mmol)三氯乙酰氯,室温下继续搅拌24h。加入等体积的乙酸乙酯和水,搅拌,静置分层,水相用乙酸乙酯提取两次,合并有机相,用饱和的硫酸铜溶液洗涤至完全除去吡啶,再依次用水和饱和的氯化钠溶液进行洗涤。无水硫酸钠干燥,过虑,减压除去溶剂。浓缩物经快速柱色谱纯化(洗脱剂为乙酸乙酯—环己烷,体积比为3∶4),得化合物V。
实施例7:13-(2’-苯基-4’-对甲氧基苯基-N-叔丁氧羰基-噁唑烷-1-羰氧基)-7-(苯基)硫代羰氧基-10-三氯乙酰基-10-去乙酰巴卡亭-III(VIIb)的制备
将0.89g(1.1mmol)化合物V溶入120mL无水甲苯和二氯甲烷(体积比为2∶1)中,搅拌下加入1.32g(3.3mmol)化合物VIb,40.3mg(0.33mmol)N’N’-二甲氨基吡啶(DMAP),搅拌10min后,加入340mg(1.65mmol)二环己基羰二酰亚胺(DCC),稍后体系变浑浊。室温条件下继续搅拌,TLC检测反应进程。反应完毕后,将浑浊物虑除,乙酸乙酯稀释,依次用饱和的氯化铵溶液、碳酸氢钠溶液和氯化钠溶液洗涤。无水硫酸钠干燥,过虑,减压除去溶剂。浓缩物经快速柱色谱纯化(洗脱剂为乙酸乙酯—环己烷,体积比为1∶2),得化合物VIIb。
实施例8:多烯紫杉醇(Ib)的制备
将0.91g(0.76mmol)化合物VIIb溶入30mL甲醇中,室温搅拌下加入145mg(0.84mmol)对甲苯磺酸,反应3h后,再加入10mL 0.1N的盐酸水溶液,TLC检测反应进程。反应结束后,乙酸乙酯稀释,再依次用饱和的碳酸氢钠溶液、水和饱和的氯化钠溶液进行洗涤。无水硫酸钠干燥,过虑,减压浓缩,粗品经快速柱色谱纯化(洗脱剂为乙酸乙酯—环己烷,体积比为1∶1),得化合物Ib。
Claims (6)
1.一种紫杉醇或多烯紫杉醇的合成方法,结构通式为:
其特征是通过以下步骤实现:
(1)10-去乙酰基巴卡亭II与化合物III在溶剂中进行反应,得到化合物IV,其中化合物III为酰卤化合物或杂环化合物,反应温度在-78~100℃,所用溶剂选用醚类溶剂、芳香溶剂或氯代溶剂,所得产物IV通过重结晶的方法纯化,或进行快速硅胶柱层析纯化,反应式为:
或
(2)化合物IV与乙酰化试剂在溶剂中进行反应,得到化合物Va,或化合物IV与氯乙酰氯试剂在溶剂中进行反应,对C-10羟基进行保护得到化合物Vb,所用乙酰化试剂选用乙酰氯、乙酸酐或冰乙酸,对C-10羟基保护所用的试剂选用氯乙酰氯、三氯乙氧羰酰氯、苄氧羰酰氯或三氯乙酰氯,反应温度为-78~100℃,产物的纯化方法同步骤(1),反应式为:
其中R3-为脂肪基或芳香基,为杂环基;
(3)化合物Va中的C-13羟基与保护的侧链酸VIa在碱存在下在溶剂中进行酯化偶联,得到化合物VIIa,化合物Vb中的C-13羟基与保护的侧链酸VIb在碱存在下在溶剂中进行酯化偶联,得到化合物VIIb,其中所用的碱包括缩合剂羰二酰亚胺类和激活剂,溶剂选用醚性溶剂、芳香溶剂、氯代溶剂、酰胺溶剂或它们的组合,反应的温度为-78~100℃,产物VII的纯化采用快速柱层析,或直接进入下一步,反应式为:
(4)化合物VIIa在酸性条件下进行一步反应脱除C-7保护基及噁唑环保护基,得到目标产物紫杉醇Ia,化合物VIIb在酸性条件下进行一步反应脱除C-7保护基、C-10保护基及噁唑环保护基,得到目标产物多烯紫杉醇Ib,所用的酸选用有机酸、无机酸的水溶液或它们的组合,反应温度在-78~100℃,选用的溶剂为水、四氢呋喃、二氧六环、乙腈、甲醇或乙醇,所得产物经过柱层析纯化,反应式为:
2.根据权利要求1所述的紫杉醇或多烯紫杉醇的合成方法,其特征是:步骤(1)中所用的化合物III中的R3-为芳香基,X-为卤素基。
3.根据权利要求1所述的紫杉醇或多烯紫杉醇的合成方法,其特征是:步骤(2)中所用的乙酰化试剂选用乙酰氯或乙酸酐,反应温度选用0~30℃。
4.根据权利要求1所述的紫杉醇或多烯紫杉醇的合成方法,其特征是:步骤(3)中缩合剂羰二酰亚胺类选用二环己基羰二酰亚胺或二异丙基羰二酰亚胺,激活剂选用4-二甲氨基吡啶,反应温度选用0~30℃。
5.根据权利要求1所述的紫杉醇或多烯紫杉醇的合成方法,其特征是:步骤(3)中选用的组合溶剂为苯-四氢呋喃或甲苯-二氯甲烷。
6.根据权利要求1所述的紫杉醇或多烯紫杉醇的合成方法,其特征是:步骤(4)中所用的组合酸选用甲苯磺酸-稀盐酸或三氟乙酸-乙酸。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2007100669400A CN101007795B (zh) | 2007-01-26 | 2007-01-26 | 紫杉醇及多烯紫杉醇的合成方法 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN2007100669400A CN101007795B (zh) | 2007-01-26 | 2007-01-26 | 紫杉醇及多烯紫杉醇的合成方法 |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN101007795A CN101007795A (zh) | 2007-08-01 |
| CN101007795B true CN101007795B (zh) | 2010-08-18 |
Family
ID=38696492
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN2007100669400A Expired - Fee Related CN101007795B (zh) | 2007-01-26 | 2007-01-26 | 紫杉醇及多烯紫杉醇的合成方法 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN101007795B (zh) |
Families Citing this family (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2011134067A1 (en) * | 2010-04-29 | 2011-11-03 | 6570763 Canada Inc. | Novel amino acid molecule and uses thereof |
| CN107056767B (zh) * | 2015-12-04 | 2022-07-15 | 江苏恩华络康药物研发有限公司 | 用于制备水溶性紫杉烷类衍生物的方法及中间体 |
Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1158126A (zh) * | 1995-06-20 | 1997-08-27 | 法玛西雅厄普约翰公司 | 制备紫杉醇及其衍生物的方法 |
| CN1670018A (zh) * | 2004-03-18 | 2005-09-21 | 中国科学院大连化学物理研究所 | 一种紫杉醇的制备方法 |
-
2007
- 2007-01-26 CN CN2007100669400A patent/CN101007795B/zh not_active Expired - Fee Related
Patent Citations (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN1158126A (zh) * | 1995-06-20 | 1997-08-27 | 法玛西雅厄普约翰公司 | 制备紫杉醇及其衍生物的方法 |
| CN1670018A (zh) * | 2004-03-18 | 2005-09-21 | 中国科学院大连化学物理研究所 | 一种紫杉醇的制备方法 |
Also Published As
| Publication number | Publication date |
|---|---|
| CN101007795A (zh) | 2007-08-01 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| AU678423B2 (en) | 2-debenzoyl-2-acyl taxol derivatives and methods for making same | |
| US20190142784A1 (en) | 9,10-Alpha,Alpha-OH-Taxane Analogs and Methods for Production Thereof | |
| US5821363A (en) | Antineoplastic use and pharmaceutical compositions containing them | |
| US6500966B1 (en) | Process for the preparation of taxanes from 10-deacetylbaccatin III | |
| JP2002505326A (ja) | 強塩基と求電子を用いる、7−ヒドロキシルの保護によるバッカチンiiiからのパクリタキセルの合成 | |
| CN101007795B (zh) | 紫杉醇及多烯紫杉醇的合成方法 | |
| CN103012328B (zh) | 一种制备第二代紫杉醇类抗癌药Cabazitaxel的方法 | |
| US6891050B2 (en) | Process for the preparation of taxanes such as paclitaxel, docetaxel and structurally similar analogs | |
| RS52438B (sr) | Priprema taksana od 9-dihidro-13-acetilbakcatina iii | |
| HU229373B1 (hu) | Eljárás paclitaxel elõállítására | |
| AU2002234535A1 (en) | A process for the preparation of paclitaxel | |
| CN103012330A (zh) | 一种紫杉醇类抗癌药xrp6258的制备方法 | |
| CN106632297A (zh) | 多烯紫杉醇侧链2′‑衍生的新型紫杉烷类抗肿瘤化合物及其合成方法与应用 | |
| CN101448839B (zh) | 制备紫杉烷衍生物的方法 | |
| CN101128448A (zh) | 制备紫杉醇的方法 | |
| CN102757410A (zh) | 一种简便高效地制备紫杉醇类似物Larotaxel的工艺 | |
| CN104610247A (zh) | 一种半合成紫杉烷衍生物及其制备方法和应用 | |
| JP5870197B2 (ja) | タキサン誘導体の製造方法 | |
| EP0747372A1 (en) | Taxane derivatives from 14-beta-hydroxy-10 deacetybaccatin III | |
| IL165436A (en) | 7, 10-bis-trichloroacetyl-10 deactylbaccatin iii |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| C17 | Cessation of patent right | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20100818 Termination date: 20110126 |