CN101977901A - 线性和环状胍衍生物及其制备和使用方法 - Google Patents
线性和环状胍衍生物及其制备和使用方法 Download PDFInfo
- Publication number
- CN101977901A CN101977901A CN2009801088746A CN200980108874A CN101977901A CN 101977901 A CN101977901 A CN 101977901A CN 2009801088746 A CN2009801088746 A CN 2009801088746A CN 200980108874 A CN200980108874 A CN 200980108874A CN 101977901 A CN101977901 A CN 101977901A
- Authority
- CN
- China
- Prior art keywords
- methyl
- ethyl
- allyl
- propargyl
- methacrylic
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Granted
Links
- 0 C*C(*C(C)C(C(*(C)C)N(C(*)C(*)C(C)C(*)C(*)C(*)C(*)N(*C)C(N[Re])=N*)C(*1)=O)*(C)=C)C(**)N(*2CC2)C1=C(*)*C Chemical compound C*C(*C(C)C(C(*(C)C)N(C(*)C(*)C(C)C(*)C(*)C(*)C(*)N(*C)C(N[Re])=N*)C(*1)=O)*(C)=C)C(**)N(*2CC2)C1=C(*)*C 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D255/00—Heterocyclic compounds containing rings having three nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D249/00 - C07D253/00
- C07D255/02—Heterocyclic compounds containing rings having three nitrogen atoms as the only ring hetero atoms, not provided for by groups C07D249/00 - C07D253/00 not condensed with other rings
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/10—Antimycotics
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C279/00—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups
- C07C279/04—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to acyclic carbon atoms of a carbon skeleton
- C07C279/12—Derivatives of guanidine, i.e. compounds containing the group, the singly-bound nitrogen atoms not being part of nitro or nitroso groups having nitrogen atoms of guanidine groups bound to acyclic carbon atoms of a carbon skeleton being further substituted by nitrogen atoms not being part of nitro or nitroso groups
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D259/00—Heterocyclic compounds containing rings having more than four nitrogen atoms as the only ring hetero atoms
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07C—ACYCLIC OR CARBOCYCLIC COMPOUNDS
- C07C2601/00—Systems containing only non-condensed rings
- C07C2601/02—Systems containing only non-condensed rings with a three-membered ring
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Health & Medical Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Life Sciences & Earth Sciences (AREA)
- General Chemical & Material Sciences (AREA)
- Medicinal Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Communicable Diseases (AREA)
- Pharmacology & Pharmacy (AREA)
- Oncology (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
- Acyclic And Carbocyclic Compounds In Medicinal Compositions (AREA)
- Hydrogenated Pyridines (AREA)
Abstract
本发明涉及线性和环状胍衍生物,其制备和使用方法,以及可以用作杀真菌剂的药学组合物,特别是用来抵抗假丝酵母类的药学组合物。
Description
技术领域
本发明涉及线性和环状胍衍生物,其制备和使用方法,以及可以用作杀真菌剂的药学组合物,特别是用来抵抗假丝酵母类的药学组合物。
背景技术
条件性病原微生物人类病原体白色假丝酵母和其它非白色类在临床中获得了广泛的关注,它们被看作免疫力降低的病人的传染物,是发病和死亡的重要成因。人们推荐的疗法依赖于氟康唑、伏立康唑和卡泊芬净。实际上,文献中出现的许多新的可能的抗真菌剂也都包括吡咯芯。
假丝酵母的致病物质不仅仅具有严重的传染性,而且能够产生对很多种抗真菌剂的耐药性。实际上,普遍地长期使用吡咯导致快速形成对多种药物的耐药性,这是抗真菌治疗的一个主要障碍。由于耐药性会快速出现,许多现有的药物对新的或重新出现的真菌变得无效。由于这些问题,使得人们需要开发新的有效的抗真菌药。因此,近年来,人们报道了具有新的结构类型的抗真菌药,其中证明胍衍生物具有非常有趣的抑制活性。例如,双胍盐(在农业中用作杀真菌剂的胍和聚胺的混合物)被归为中等毒性的抗真菌药,而通过体内动物研究获得的结果证明双胍盐和相关的化合物很有可能能够作为抗真菌药。作者最近报道了双胍盐的组分能够对白色假丝酵母和非白色假丝酵母类发挥作用。
发明内容
本发明涉及不同聚胺的新颖的环状胍化(guanilated)衍生物。基于用双胍盐的组分获得的结果,我们已经合成了不同聚胺的新的环状胍衍生物,使用这些衍生物对假丝酵母的8种临床分离物和3种参比种(白色假丝酵母(C.albicans)ATCC 60193,克鲁氏假丝酵母(C.krusei)ATCC 14243,近平滑假丝酵母(C.parapsilosis)ATCC 34136)进行了生物学评价。本发明的新的化合物对象具有极佳的抗真菌活性,而且具有以下性质:
1.对不同的假丝酵母种具有极高的活性;
2.具有低毒性;
3.对假丝酵母的耐药性菌株也具有活性。
在权利要求1-18中揭示了本发明的化合物。这些揭示的内容构成说明书的一部分。
本发明的另一个目的是权利要求1-18所述的任意化合物作为药物的应用。
本发明的另一个目的涉及权利要求1-18中任一项所述的化合物作为抗感染药的应用,优选作为抗真菌药,更优选作为抗假丝酵母种的抗真菌药,更优选作为下组的假丝酵母种的抗真菌药:白色假丝酵母,克鲁氏假丝酵母,近平滑假丝酵母。
本发明的另一个目的涉及一种药学组合物,该药学组合物包含权利要求1-18中任一项所述的任意化合物,或其任意混合物,以及合适的赋形剂和稀释剂。本领域的普通技术人员应当能够根据给药方式(局部给药,口服给药,肠胃外给药等)选择合适的赋形剂和稀释剂。在一个优选的实施方式中,所述组合物还包含至少一种其它的具有抗真菌活性的化合物。
本发明的另一个目的涉及一种用来制备如权利要求1-18中任一项所述的化合物的方法,所述方法包括以下步骤:
a)在合适的溶剂中,使得合适的胺R1-NH2与合适的S-甲基异硫脲反应,制得化合物2
式中:
n1和n2是4或6,n2可以是n1,或者n2可以与n1不同;
R1=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
R2=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
b)对步骤a)制得的化合物2进行萃取和/或纯化;
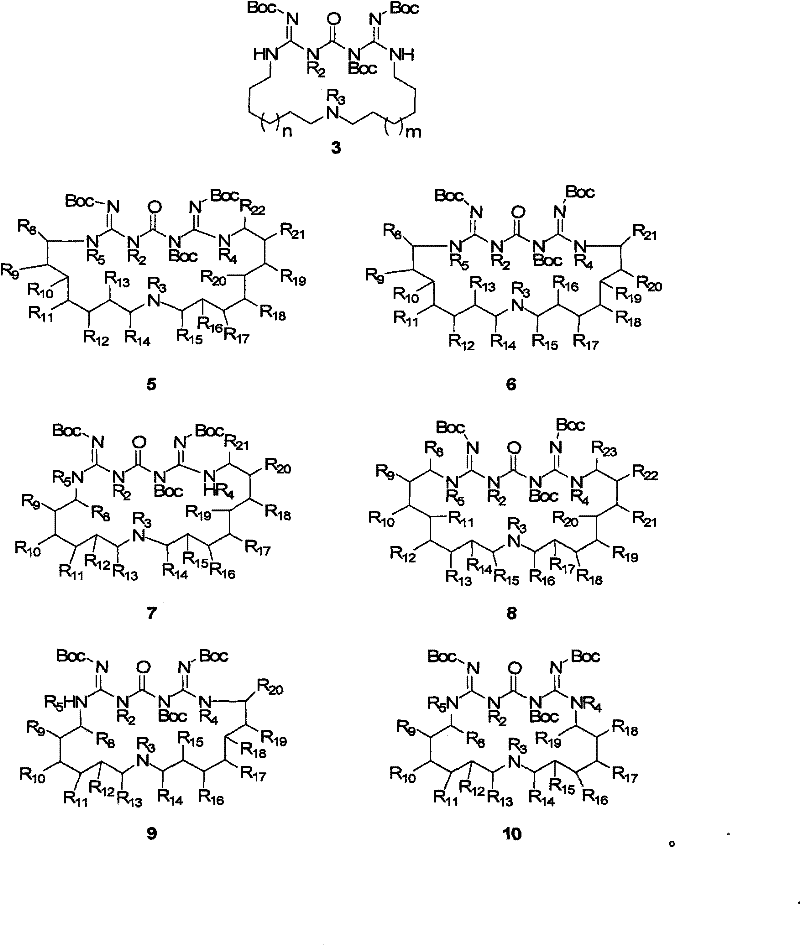
c)在适于制得化合物3或者以下结构式5-10所示的化合物的条件下,使得化合物2与合适的N,N’-二(叔丁氧基羰基)-N-(烷基)-S-甲基异硫脲反应:
式中:
R2=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
R3=H,甲基,乙基或苄基;
R4-R23=H,甲基或乙基;R4-R23可以是相同的或者不同的;
d)对步骤c)的化合物3,5-10进行纯化;
e)在适于制得权利要求1-18所述的化合物的条件下使得化合物3,5-10反应;
f)对步骤e)制得的化合物进行萃取和/或纯化。
本发明的另一个目的涉及任意结构式3,5-10所示的中间体:
具体实施方式
化学过程
本发明所述的化合物可以通过如下所述的方式合成:
a)THF:MeOH(5∶3),50℃;b)THF 60℃;c)10%TFA,无水CH2Cl2,24小时,室温。R1=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基或γ,γ-二甲基烯丙基,R2=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基或γ,γ-二甲基烯丙基,
n1=6-8,n2=6-8。
合成过程的实施例:
实施例1:1-氨基-17-[N2,N3-二(叔丁氧基羰基)胍基]-9-氮杂十七烷(12)的制备
在50℃的温度下,在1小时的时间内,向1,17-二氨基-9-氮杂十七烷3(4.9克,15.06毫摩)的THF/CH3OH 5/3(80毫升)搅拌溶液中滴加N,N’-二(叔丁氧基羰基)-S-甲基异硫脲(1.456克,5.02毫摩)的THF(25毫升)溶液。16小时之后,反应混合物在减压条件下浓缩,残余物用闪式色谱纯化(6%的甲醇,4%的三乙基胺,90%的乙酸乙酯),制得3.51克浅黄色油状物12(70%)。
实施例2:制备14的一般步骤。
在60℃下,向12(1.5毫摩)的THF(15毫升)搅拌溶液中滴加合适的N,N’-二(叔丁氧基羰基)-N-(烷基)-S-甲基异硫脲(1毫摩)的THF(5毫升)溶液。该反应混合物在60℃搅拌16小时,在室温下冷却,在减压条件下浓缩。该粗混合物通过闪式色谱纯化,制得黄色油状物14a-b。
化合物14a-b的NMR数据
2,6[(二叔丁氧基羰基)二亚氨基]-3-苄基-5-叔丁氧基羰基-1,3,5,7,16-五氮杂环二十四烷-4-酮(14a)。
1H NMR(CDCl3)δ12.06(NH,br s),8.73(NH,br s),8.06(NH,br s),7.26-7.24(5H,m),4.82(2H,s),3.47-3.32(2H,m),3.25-3.18(2H,m),3.00-2.93(4H,m),2.01-1.82(4H,m),1.48(9H,s),1.43(9H,s),1.41(9H,s),1.29-1.11(20H,m).MS(ESI):m/z=772.1[M+H]+。
2,6[(二叔丁氧基羰基)二亚氨基]-3-炔丙基-5-叔丁氧基羰基-1,3,5,7,16-五氮杂环二十四烷-4-酮(14b)。
1H NMR(CDCl3)δ8.09(NH,br s),4.45(2H,s),3.50(1H,s),3.45-3.20(4H,m),3.25-3.15(4H,m),2.01-1.82(4H,m),1.48(9H,s),1.43(9H,s),1.41(9H,s),1.32-1.11(20H,m)。MS(ESI):m/z=720.2[M+H]+。
实施例3:合成化合物4a-4e的一般过程。
用新鲜蒸馏的TFA的10%的无水DCM溶液(1毫摩用量30毫升)处理化合物3a-3e,该反应混合物在室温、氩气气氛下搅拌。24小时之后,反应混合物在减压条件下浓缩,以定量产率制得所需化合物,该化合物为三(三氟乙酸盐)(棕色油状物)的形式。所述混合物用半制备性HPLC纯化,制得最终化合物,该化合物为三(三甲酸盐)的形式。
化合物15a-15e的NMR数据
三(三氟乙酸)2,6-二亚氨基-3-苄基-1,3,5,7,16-五氮杂环二十四烷-4-酮(15a)。
1H NMR(CD3)2CO δ8.25(NH,br s),7.75(NH,br s),7.44(NH,br s),7.35-7.32(5H,m),4.55-4.52(2H,d,J=5Hz),3.75-3.44(4H,m),3.32-3.29(4H,m),1.64-1.57(8H,m),1.30(16H,br s)。MS(ESI):m/z=472.1[M+H]+。
三(三氟乙酸)2,6-二亚氨基-3-炔丙基-1,3,5,7,16-五氮杂环二十四烷-4-酮(15b)。
1H NMR(CD3)2CO δ8.26(NH,br s),7.60(NH,br s),7.44(NH,br s),4.16-4.14(2H,m),3.48-3.45(4H,m),3.33-3.27(4H,m),2.89(1H,s),1.68-1.59(8H,m),1.35-1.29(16H,m)。MS(ESI):m/z=420.1[M+H]+。
三(三甲酸)2,6-二亚氨基-3-(γ-甲基烯丙基)-1,3,5,7,16-五氮杂环二十四烷-4-酮(15c)。
1H NMR(CD3)2CO δ8.24(NH,br s),7.77(NH,br s),7.20(NH,br s),5.77-5.45(2H,m),3.74-3.71(2H,m),3.30-3.25(4H,m),3.19-3.12(4H,m),1.70-1.46(12H,m),1.34-1.26(16H,m)。MS(ESI):m/z=436.2[M+H]+。
三(三甲酸)2,6-二亚氨基-3-(β-甲基烯丙基)-1,3,5,7,16-五氮杂环二十四烷-4-酮(15d)。
1H NMR(CD3)2CO δ8.30(NH,br s),7.58(NH,br s),4.93-4.88(2H,d,J=10Hz),3.84-3.82(2H,m),3.46-3.40(4H,m),3.37-3.20(4H,m),1.72(3H,s),1.62(8H,br s),1.32-1.27(16H,m)。MS(ESI):m/z=436.3[M+H]+。
三(三甲酸)2,6-二亚氨基-3-(γ,γ-二甲基烯丙基)-1,3,5,7,16-五氮杂环二十四烷-4-酮(15e)。
1H NMR(CD3)2CO δ8.22(NH,br s),7.90(NH,br s),5.28-5.25(1H,m),3.74-3.71(2H,m),3.40-3.30(4H,m),3.20-3.10(4H,m),1.65-1.44(14H,m),1.30-1.28(16H,m)。MS(ESI):m/z=450.3[M+H]+。
生物学测试
通过AFST-EUCAST标准方法测定MIC。
实验培养基。实验培养基是RPMI 1604,其不含NaHCO3,包含L-谷氨酰胺(意大利,希格玛艾尔德里奇公司(Sigma Aldrich,Italy)),用0.165M的吗啉丙磺酸(意大利,希格玛艾尔德里奇公司)使得pH值缓冲至7.0,补充2%(w/v)的葡萄糖。所述培养基以双倍浓度溶液的形式制得,通过过滤灭菌,用在无菌蒸馏水中制备的真菌接种物以1∶2(v/v)的比例进行稀释。
接种准备
在测试之前,酵母分离物在37℃的温度下,在Sabouraud右旋糖琼胶(西班牙,马德里市的奥克斯尼德公司(Oxoid,Madrid,Spain))中培育48小时。通过将每种培养物的直径大于1毫米的五个独立的菌落合并起来,制备悬浮液。采用用于接种准备的分光光度法。在无菌蒸馏水中制备的最终接种物悬浮液包含0.5·105至2.5·105cfu/mL。
抗真菌药
在100%的二甲亚砜中制备测试化合物的储备用液。制备的储备用液的浓度是抗真菌活性测试中最高浓度的100倍,在-70℃冷冻,直至使用。
易感性测试
使用包括平底凹孔的无菌塑料微量滴定板。所述板包含抗真菌药的系列稀释样,实验培养基体积为100微升/凹孔。使用两个无药物的培养基孔作为无菌和生长参比。浅盘中以100微升最终接种物/凹孔的量进行培养,但是无菌参比凹孔例外。每种药物的被测浓度为1.25-80μM。微量滴定板在37℃下培养24小时。在24小时通过目视观察和分光光度法确定最小抑制浓度(MIC)。
目视观察终点测定
对于目视观察终点测定,MIC是根据S-I-R标度测定的,其中S(易受感)表示光学清晰的培养物,I(中等易受感)表示略微混浊的培养物,R(耐受性)表示混浊度无降低。MIC50定义为对应于S级培养物的药物最低浓度。
分光光度法终点测定
在读取结果之前,用微量滴定板振荡器搅拌微量滴定板,以确保浊度均匀。MIC是通过用微量滴定板读数器在450纳米处测定的吸光度。从其余的凹孔的读数减去空白值。每种被测的抗真菌药确定两个终点,其中MIC80表示相对于参比样的生长,生长减少80%或更多(通过分光光度法测定)时的最低药物浓度,MIC50表示相对于参比样的生长,生长减少50%(通过分光光度法测定)时的最低药物浓度。MIC50也定义为分光光度终点。
结果
生物学测试的结果列于表1和表2。具有体积最大的侧链(异戊二烯基)的化合物15e对白色假丝酵母(20-40μM),克鲁氏假丝酵母和热带假丝酵母(C.tropicalis)表现出令人感兴趣的活性,而近平滑假丝酵母和光滑假丝酵母(C.glabrata)对该化合物的易感性较低(40-80μM)。随着将不饱和链的尺寸减小到丁烯基(15c),活性发生显著提高,对白色假丝酵母(对所有的菌株均为2.5μM)和热带假丝酵母(1.25μM)均获得了极佳的结果。克鲁氏假丝酵母菌株也是易感的,但是在较低的浓度下(10μM)是易感的。将丁烯基链改为甲基丙烯基部分(15d),使得对所有真菌菌株的活性显著降低。发现该化合物对白色假丝酵母具有最佳的活性(对标样和15T菌株,MIC=20μM)。通过如15b所示,将侧链尺寸进一步减小到炔丙基部分,重新获得了对白色假丝酵母(白色假丝酵母4T除外,其对该化合物具有抗性)和热带假丝酵母(5μM)的良好活性。最后,对侧链进行芳化,改为苄基(15a),获得的活性数据与丁烯基衍生物15c获得的活性数据类似。总之,丁烯基衍生物和苄基衍生物都表现出最佳的抗真菌活性,其次是炔丙基化合物,其对很多种真菌菌株都保持了令人感兴趣的活性。
表1.双胍盐组分与线性和环状胍基衍生物的抗真菌活性。
在24小时通过目视观察和分光光度法测定aMIC的值。F是氟康唑。
表2.双胍盐组分与线性和环状胍基衍生物的抗真菌活性。
在24小时通过目视观察和分光光度法测定aMIC的值。
书目
Chamilos,G.;Kontoyiannis,D.P.Curr.Opin.Infect.Dis.2006,19,380。
Aperis,G.等,Expert Opin.Investig.Drugs 2006,15,1319。
Klepser,M.E.Pharmacotherapy 2006,26,68S。
Pauli,A.Med.Res.Rev.2006,26,223。
Buxbaum,A.等,Antimicrob.Chemother.2006,58,193。
Jana,G.H.;Jain,S.;Arora,S.K.;Sinha,N.Bioorg.Med.Chem.Lett.2005,15,3592。
Martin,D.W.等,Proc.Natl.Acad.Sci.USA 1993,90,8377。
Dreassi,E.等,.J.Pharm.Biomed.Anal.,出版中。
Sheehan,D.J.;Hitchcock,C.A.;Sibley,C.M.Clin.Microbiol.Rev.1999,12,40。
Pfaller,M.A.等,J.Clinical Microb.1999,37,870。
Herreros,E.等,Antimicrob.Agents Chemother.2001,45,3132。
Deschenes,R.J.等,Antimicrob.Agents Chemother.1999,43,1700。
Claims (27)
16.通式(31)所示的化合物,及其任意的盐,
R1=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
R2=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
R3=H,甲基,乙基或苄基;
R4-R22是相同的,或者各自独立地是H,甲基或乙基。
19.如以上权利要求中任一项所述的化合物作为药物的应用。
20.如权利要求1-18中任一项所述的化合物作为抗感染药的应用。
21.如权利要求20所述的化合物作为抗真菌药的应用。
22.如权利要求21所述的化合物作为抗假丝酵母种的抗真菌药的应用。
23.如权利要求22所述的化合物,其特征在于,所述假丝酵母种属于下组:白色假丝酵母,克鲁氏假丝酵母,近平滑假丝酵母。
24.一种药学组合物,其包含如权利要求1-18中任一项所述的化合物或其任意混合物,以及合适的赋形剂和稀释剂。
25.如权利要求24所述的药学组合物,其特征在于,所述组合物还包含至少一种其它的具有抗真菌活性的化合物。
26.一种用来制备如权利要求1-18中任一项所述的化合物的方法,该方法包括以下步骤:
a)在合适的溶剂中,使得合适的胺R1-NH2与合适的S-甲基异硫脲反应,制得化合物2
式中:
n1和n2是4或6,n2可以是n1,或者n2可以与n1不同;
R1=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
R2=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
b)对步骤a)制得的化合物2进行萃取和/或纯化;
c)在适于制得化合物3或者以下结构式5-10所示的化合物的条件下,使得化合物2与合适的N,N’-二(叔丁氧基羰基)-N-(烷基)-S-甲基异硫脲反应:
式中:
R2=H,炔丙基,环丙基甲基,γ-甲基烯丙基,β-甲基烯丙基,γ,γ-二甲基烯丙基,甲基或乙基;
R3=H,甲基,乙基或苄基;
R4-R23=H,甲基或乙基;R4-R23可以是相同的或者不同的;
d)对步骤c)的化合物3,5-10进行纯化;
e)在适于制得如权利要求1-17所述的化合物的条件下使得化合物3,5-10反应;
f)对步骤e)制得的化合物进行萃取和/或纯化。
Applications Claiming Priority (3)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US3616508P | 2008-03-13 | 2008-03-13 | |
| US61/036,165 | 2008-03-13 | ||
| PCT/IB2009/051032 WO2009113033A2 (en) | 2008-03-13 | 2009-03-12 | Linear and cyclic guanidine derivatives, method of preparation and uses thereof |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| CN101977901A true CN101977901A (zh) | 2011-02-16 |
| CN101977901B CN101977901B (zh) | 2015-04-01 |
Family
ID=40622063
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN200980108874.6A Expired - Fee Related CN101977901B (zh) | 2008-03-13 | 2009-03-12 | 线性和环状胍衍生物及其制备和使用方法 |
Country Status (13)
| Country | Link |
|---|---|
| US (1) | US8685953B2 (zh) |
| EP (1) | EP2274290B1 (zh) |
| JP (1) | JP5733988B2 (zh) |
| CN (1) | CN101977901B (zh) |
| AU (1) | AU2009223204B2 (zh) |
| BR (1) | BRPI0908953A2 (zh) |
| DK (1) | DK2274290T3 (zh) |
| EA (1) | EA018926B1 (zh) |
| ES (1) | ES2396288T3 (zh) |
| MX (1) | MX2010010017A (zh) |
| PL (1) | PL2274290T3 (zh) |
| PT (1) | PT2274290E (zh) |
| WO (1) | WO2009113033A2 (zh) |
Families Citing this family (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA2915767A1 (en) * | 2013-06-18 | 2014-12-24 | Cygnet Biosciences B.V. | New macrocyclic amidinourea derivatives, methods of preparation and uses thereof as chitinase inhibitors |
| JP6378179B2 (ja) | 2013-07-03 | 2018-08-22 | 株式会社新日本科学 | 新規化合物,有機カチオントランスポーター3の検出剤及び活性阻害剤 |
| WO2016055644A1 (en) | 2014-10-10 | 2016-04-14 | Lead Discovery Siena S.R.L. | Linear guanidine derivatives, methods of preparation and uses thereof |
| EP3854789A1 (en) * | 2020-01-22 | 2021-07-28 | Cygnet Biosciences B.V. | Macrocyclic compounds useful as chitinase inhibitors |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| GB1114155A (en) * | 1964-08-24 | 1968-05-15 | Evans Medical Ltd | Guanidino derivatives |
| US3988370A (en) * | 1970-10-08 | 1976-10-26 | Sterling Drug Inc. | Amidinoureas |
-
2009
- 2009-03-12 MX MX2010010017A patent/MX2010010017A/es active IP Right Grant
- 2009-03-12 AU AU2009223204A patent/AU2009223204B2/en not_active Ceased
- 2009-03-12 DK DK09719584.6T patent/DK2274290T3/da active
- 2009-03-12 EA EA201071072A patent/EA018926B1/ru not_active IP Right Cessation
- 2009-03-12 BR BRPI0908953A patent/BRPI0908953A2/pt not_active IP Right Cessation
- 2009-03-12 US US12/922,232 patent/US8685953B2/en not_active Expired - Fee Related
- 2009-03-12 ES ES09719584T patent/ES2396288T3/es active Active
- 2009-03-12 PL PL09719584T patent/PL2274290T3/pl unknown
- 2009-03-12 JP JP2010550321A patent/JP5733988B2/ja not_active Expired - Fee Related
- 2009-03-12 EP EP09719584A patent/EP2274290B1/en not_active Not-in-force
- 2009-03-12 CN CN200980108874.6A patent/CN101977901B/zh not_active Expired - Fee Related
- 2009-03-12 WO PCT/IB2009/051032 patent/WO2009113033A2/en not_active Ceased
- 2009-03-12 PT PT97195846T patent/PT2274290E/pt unknown
Also Published As
| Publication number | Publication date |
|---|---|
| JP5733988B2 (ja) | 2015-06-10 |
| EP2274290B1 (en) | 2012-09-26 |
| AU2009223204A1 (en) | 2009-09-17 |
| WO2009113033A3 (en) | 2009-12-30 |
| EP2274290A2 (en) | 2011-01-19 |
| JP2011513477A (ja) | 2011-04-28 |
| CN101977901B (zh) | 2015-04-01 |
| AU2009223204B2 (en) | 2014-07-24 |
| PL2274290T3 (pl) | 2013-03-29 |
| EA018926B1 (ru) | 2013-11-29 |
| US8685953B2 (en) | 2014-04-01 |
| US20110039854A1 (en) | 2011-02-17 |
| DK2274290T3 (da) | 2013-01-14 |
| WO2009113033A2 (en) | 2009-09-17 |
| MX2010010017A (es) | 2010-10-07 |
| BRPI0908953A2 (pt) | 2016-06-07 |
| PT2274290E (pt) | 2013-01-14 |
| ES2396288T3 (es) | 2013-02-20 |
| EA201071072A1 (ru) | 2011-04-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| US12552753B2 (en) | Methods and compositions for targeting Tregs using CCR8 inhibitors | |
| US8895561B2 (en) | Compounds and methods for treating candidiasis and aspergillus infections | |
| US8440720B2 (en) | Methods of use of antiviral compounds | |
| CN101977901B (zh) | 线性和环状胍衍生物及其制备和使用方法 | |
| AU2009276744A1 (en) | Anti-malarial compounds | |
| WO2001014331A2 (en) | Non-quinoline inhibitors of malaria parasites | |
| Singh et al. | Antiplasmodial activity of hydroxyethylamine analogs: synthesis, biological activity and structure activity relationship of plasmepsin inhibitors | |
| US20110065762A1 (en) | Methods of use of antiviral compounds | |
| US6872852B2 (en) | Polyamine analogues as cytotoxic agents | |
| CN1512982A (zh) | 可作为治疗剂和诊断剂的新多胺类似物 | |
| Prakasha et al. | Design, synthesis and antimicrobial screening of amino acids conjugated 2-amino-4-arylthiazole derivatives | |
| CN110325509B (zh) | 丙氨酸及脯氨酸氨基酸的功能性衍生物化合物及包含其的药学组合物 | |
| CN105131082A (zh) | 环肽类化合物及其应用 | |
| US9801861B2 (en) | Antimicrobial substituted thiazoles and methods of use | |
| CN109485607B (zh) | β-唑类-苯基酮衍生物及其用途 | |
| US20120165369A1 (en) | 3-SUBSTITUTED QUINOLINIUM AND 7H-INDOLO[2,3-c]QUINOLINIUM SALTS AS NEW ANTIINFECTIVES | |
| Osmaniye et al. | Synthesis and characterization of new series benzothiazole-dithiocarbamate derivatives as potential antifungal agents | |
| CN118598760B (zh) | 四苯乙烯衍生物及其应用 | |
| US20080312287A1 (en) | Compound and Methods For the Treatment of Cancer and Malaria | |
| Munnik | Development of new antimalarial ferrocenyl-artesunate complexes | |
| CN114426535A (zh) | N-取代含氟吡咯烷衍生物及其制备方法和用途 | |
| CN114181225A (zh) | 一种含笑内酯衍生物及其药物组合物、制备方法和用途 | |
| Onajole | Design, Synthesis and Pharmaceutical Application of Novel Polycyclic'cage'Diamines | |
| JPH06504796A (ja) | 抗真菌活性を有する3置換ピロール誘導体、該誘導体の製造方法および関連した薬理学的組成物 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C14 | Grant of patent or utility model | ||
| GR01 | Patent grant | ||
| CF01 | Termination of patent right due to non-payment of annual fee | ||
| CF01 | Termination of patent right due to non-payment of annual fee |
Granted publication date: 20150401 Termination date: 20200312 |