CN102755638A - Aggf1在制备促进血管形成的药物中的用途 - Google Patents
Aggf1在制备促进血管形成的药物中的用途 Download PDFInfo
- Publication number
- CN102755638A CN102755638A CN201210240339XA CN201210240339A CN102755638A CN 102755638 A CN102755638 A CN 102755638A CN 201210240339X A CN201210240339X A CN 201210240339XA CN 201210240339 A CN201210240339 A CN 201210240339A CN 102755638 A CN102755638 A CN 102755638A
- Authority
- CN
- China
- Prior art keywords
- aggf1
- albumen
- purposes
- active fragment
- coding
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Pending
Links
Images
Landscapes
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Medicines Containing Material From Animals Or Micro-Organisms (AREA)
Abstract
本发明涉及生长因子AGGF1在制备促进血管形成的药物中的用途,其中所述AGGF1可以是AGGF1蛋白、编码AGGF1的核苷酸序列或其活性片段。本发明涉及一种非治疗目的的促进血管新生的方法,包括给予血管刺激有效量的AGGF1蛋白或其活性片段、和/或编码AGGF1蛋白或其活性片段的核苷酸片段。
Description
发明领域
本发明涉及一种通过作用于骨骼肌和心肌的治疗心血管系统及其疾病的方法,更具体地说涉及一种利用生长因子刺激内皮细胞的增殖和生长,进而刺激血管新生来治疗心血管疾病的方法。本发明还涉及生长因子AGGF1在制备促进血管形成的药物中的用途,其中所述AGGF1可以是AGGF1蛋白、编码AGGF1的核苷酸序列或其活性片段。
背景技术
外周血管疾病,尤其是下肢血管疾病通常是由动脉粥样硬化导致血管的狭窄或者闭塞,从而阻止血流流向下肢(J Am Coll Cardiol47:1239-1312(2006);循环(Circulation)94:3026-3049(1994))。当今社会,尤其是老年化程度越来越高的时代,下肢血管疾病的发病率也越来越高,成年人的发病率达到了12%(J Am Coll Cardiol58:2020-2045(2011);新英格兰医学杂志(N Engl J Med)344:1608-1621(2001))。在美国大约有8百万到1千2百万的下肢血管疾病患者(循环(Circulation)110:738-743(2004))。而在德国,65岁以上的女性患病率甚至达到了17%,男性更高,其患病率达到20%(糖尿病治疗(Diabetes Care)26:3357-3358(2003))。
下肢缺血性疾病的临床症状也很多,有的呈现出典型的症状,例如间接性跛行,但很多情况下,下肢缺血疾病患者却表现出别的症状(J AmColl Cardiol 47:1239-1312(2006);国际流行病学杂志(IntJ Epidemiol)25: 1172-1181 (1996))。在一些严重的患者中,下肢缺血严重影响生活质量,并且导致了较高的发病率和死亡率(新英格兰医学杂志(N Engl J Med)326: 381-386 (1992))。严重的下肢缺血病人的一年生存率接近25%。更为重要的是,下肢缺血患者中46%同时患有冠状动脉疾病,10%以上的病人还有脑血管疾病(J ClinEpidemiol 45: 529-542(1992);循环(Circulation)122:1862-1875(2010))。
当前下肢血管疾病的治疗主要集中在降低心脑血管的发病率和死亡率上,同时缓解下肢血管疾病的症状等方面糖尿病治疗(梅奥临床进展(Mayo Clin Proc)85(7): 678-692(2010))。降脂类药物。降血压药物和抗血栓药物等药物用于预防心梗和脑梗等疾病(梅奥临床进展(Mayo Clin Proc)85(7): 678-692(2010))。但是一些下肢血管疾病患者可能遭受着巨大的疼痛,而不得不选择截肢。为了避免截肢等其他严重的病症,血管形成术,支架和外周血管搭桥等外科手术常常用于腿部的血流再灌(血栓研究(Thromb Res) 106(6): V285-294(2002))。但是,一些接受过血管外科手术的下肢血管患者比接受外科手术的冠心病患者的长期生存率明显低(J Am Coll Cardiol 51: 1588-1596(2008)。最为重要的是很多下肢缺血患者因为种种原因,不适合做血管外科或者介入手术(循环研究(Circ Res)105: 724-736(2009))。所以采用血管生成因子等促血管新生和改善微循环的治疗性血管新生的方法,越来越被人们认可,尤其是在下肢血管疾病的治疗中。一些血管生成因子,例如血管内皮生长因子(VEGF),成纤维生长因子(FGF),肝细胞生长因子(HGF)和胎盘来源的生长因子(PDGF)等,都已经在下肢缺血动物和严重的下肢缺血病人中进行了实验。
Tsurumi第一次将VEGF用于缺血性治疗,利用兔的下肢缺血模型,将VEGF质粒注射入缺血部位,从而促进血管新生,改善微循环(循环(Circulation)94: 3281-3290(1996))。
利用由水凝胶包裹的气囊导管将质粒DNA导入动脉血管内来进行基因治疗。随后,临床研究证实肌肉内注射也能够成功表达转入基因(循环(Circulation)94: 3281-3290(1996))。Baumgartner进行了前期临床试验,通过将VEGF165质粒注射到病人具有静息痛或者是难以治愈的溃疡的四肢肌肉进行治疗(循环(Circulation)97: 1114-1123(1998))。而Folkman认为这一结果需要通过解剖学和生理结构的证实,其中包括血液动力学、血管造影、疼痛的减轻效果、缺血性溃疡的恢复状况、肢端恢复、内皮增殖细胞的免疫组化来验证(循环(Circulation)97: 1108-1110(1998))。
Makinen等人比较了将VEGF165的质粒与其编码腺病毒对表现出跛行以及严重的肢端缺血(critical limb ischemia, CLI)的PAD的治疗效果。参与该经皮腔内血管成形术的45位PAD患者随机的接受了VEGF165的质粒、VEGF165编码腺病毒和乳酸林格氏安慰剂(分子治疗(Mol Ther)6: 127–133(2002))。而VEGF165的治疗均表现出一定的安全性以及显著的血管形成的疗效,但是VEGF165临床实验中,治疗组与对照组却没有显著区别。
在VEGF的异构体中,缺乏发卡结合域的VEGF121也被认为可以与蛋白复合体结合。这是由于区域性表达的VEGF121在组织中的半衰期比较短。因此,它只能诱导血管形成的早期阶段,也就是说它与内皮细胞松散的结合可能导致了组织水肿。而具有较长的组织半衰期的VEGF165可以有效的介导血管形成的整个时期。
RAVE (Regional Angiogenesis with Vascular EndothelialGrowth Factor)的临床实验是第一次随机双盲且设有安慰剂对照组的肌内注射腺病毒载体的PAD治疗(循环(Circulation)108: 1933-1938(2003))。其中,105名患有单侧运动受限的跛行被随机的分别进行肌内注射低浓度AdVEGF121、高浓度AdVEGF121以及安慰剂进行治疗。经过一个季度以及半年的治疗,研究人员在这三组患者中并没有发现主要疗效终点以及辅助疗效终点之间的区别,而AdVEGF121组的治疗表现出了与给药计量相关的外周水肿。这一结果非常引人注目,由于VEGF能够提高血管的渗透性,因此显示出AdVEGF121在该实验中是具有生物活性的。
Comerota等人发表了第一篇有关FGF1基因对CLI的临床治疗研究(血管外科杂志(J Vasc Surg)35:930-936(2002))。结果表明在外周动脉疾病患者肌肉注射FGF1(NV1FGF)的裸质粒的治疗过程中,对伤口愈合、疼痛减轻乃至经皮氧压力的改善方面都颇有成效。然而,Nikol等人在TALISMAN201 (Therapeutic Angiogenesiswith Intramuscular NV1FGF Improves Amputation-Free Survivalin Patients with Critical Limb Ischemia)的临床试验中对CLI的病人进行了临床II期的实验(分子治疗(Mol Ther)16: 972–978(2008))。这些病人随机的接受NV1FGF(n=59)或者是安慰剂(n=66)的肌肉内注射。在接受治疗的25周后,分别有19.6%来自于治疗组以及14.3%来自于对照组的病人到达了主要疗效终点。这一结果并不十分理想,但在实验组汇总截止率接近37.3%,相比较于对照组的55.4%有一个明显的减少(风险比率=0.498;P=0.015)。另外,接受NV1FGF治疗的患者的死亡率呈现出下降的趋势。而截肢与死亡均是作为CLI病人的NV1FGF的临床III期试验的主要疗效终点。
Taniyama等将外源性HGF作为治疗缺血性疾病的基因药物进行研究,在大鼠和兔子的下肢缺血模型中,都取得了很好的效果,可以促进血管新生,减轻溃烂程度,缓解坏死程度(基因治疗(Gene Ther)8:181-189(2001))。Morishita及同事们进行了一项有关HGF的基因治疗的预实验以及其安全性的评估,该项研究将会为临床II期的HGFSTAT研究提供依据(高血压(hypertension)44:203-209(2004);高血压(hypertension)33:1379-1384(1999))。参与这项实验的104名患者将随机的接受安慰剂以及三种不同剂量的HGF质粒的注射治疗(循环(Circulation)118: 58-65(2008))。在试验过程中出现了大约60%的严重的不良事件,但这一结果并不是出现在所有的分组中。而其也证明了我们无需对HGF质粒治疗安全性担忧。但是,当那些在治疗前就表现出15 mm汞柱高的TcPO2提高的病人被排除在外后,接受最大剂量的HGF质粒的病人该指标的提高最为明显。这一结论强调了当使用代理终结点来衡量严重的PAD患者时,传统的结果往往会遭到严峻的挑战。
另外一种HGF的载体在最近的早期临床研究中得到了应用。VM202包括了人类HGF基因和HGF-X7的基因组cDNA杂交,它可以通过不同的剪接方式来表达多种HGF的异构体。2009年3月,一项涵盖了12位CLI患者的治疗安全性以及计量梯度研究(ClinicalTrials. govIdentifier :NCT00696124)结果为该治疗方法的安全性以及生物活性提供了初步的证据。
HIF-1的转录作为一个典型的基因总开关可以在血管形成的生理学以及病理学过程中调控多个下游靶点。例如,学者已经对以HIF-1或者是其他氧气敏感型细胞中的调控因子为靶点的治疗缺血性疾病的方案进行了研究(自然医学(Nat Med)9:677-684(2003))。并且在年轻和老年小鼠的下肢缺血模型中开展了实验,发现HIF-1可以促进血管新生,提高血流再灌的情况,尤其是对于老年小鼠而言,这种情况更加明显(循环研究(Circ Res)101: 1310-1318(2007))。 Rajagopalan等人开展了针对利用修饰以及激活HIF-1来治疗38位PAD以及CLI患者的计量检定临床试验的安全性评估。他们并没有发现任何该方法的负面效应(循环(Circulation)115: 1234-1243(2007))。与此同时,尽管他们所选取的样本量比较小,但是在这些病人中,学者们观察到疼痛症状的减轻以及溃烂的恢复。在WALK这项临床研究中(ClinicalTrials.gov Identifier: NCT00117650),研究者们拥有了包括了289位病人,更为随机,病情也更为严重的病人样本。
AGGF1,又名VG5Q,是于2004年发现的一个先天性静脉畸形骨肥大综合征(Klippel-Trenaunay Syndrome,KTS)。KTS是一种罕见的先天性血管疾病,主要症状为毛细血管、静脉管、淋巴管畸形和过度增生,该病于1900年首次由法国医生Klippel和Tranaunay归类、描述并定义。承受疾病带来的疼痛等生理上的痛苦,还得承受由于残疾和畸形而引起的巨大的精神压力。
KTS临床最主要的特征有3个:皮肤毛细血管、淋巴管畸形和增生,常常伴有红色血管斑(port-wine stains);早发性静脉曲张或者静脉畸形(Venous malformations orvaricose veins);骨骼或者软组织生长过度,通常表现为单侧肢体肥大。一般而言,大多数病人具有上述2个特征,但KTS的临床诊断标准仍然为这三个基本特征。
由于KTS是一种综合征,所以常常伴有很多其他的临床症状:
毛细血管畸形(capillary malformations,CMs)是最常见的皮肤血管畸形,95-100%的KTS病人都有明显的毛细血管畸形,并且形成血管斑,由于症状不同其颜色也不同,从浅色到紫红色不等。KTS患者的毛细血管相对较薄,其内层的内皮细胞一般呈扁平状。
静脉畸形(Venous malformations)在70-80%的KTS病人中都会出现的,但其病症的表现差别较大,有的较轻,只有小的浅静脉异常,有的则比较也暗中,往往出现大面积的病变,并伴有溃烂。这种表征在婴儿时期不太明显,但伴随着年龄的增长,其症状逐渐严重。大多数静脉曲张不出现在皮肤表面,但是还是有很多KTS患者在病腿的内部的静脉出现畸形,例如内部静脉管腔曲张,静脉瓣缺失,静脉发育不全,以及某些深度静脉缺失,更有甚者,在有些病人中发现其腹腔或者盆腔的静脉出现畸形。
淋巴管异常(Lymphatic abnormalities,LMs)多指皮肤或皮下的淋巴管缺陷,这种情况多发于KTS患者的面颈部。而且大约20%KTS患者的淋巴管中的淋巴液渗漏出来。
Tian在KTS患者家系中,通过定位克隆的方法,发现一位KTS患者的淋巴细胞中出现了t(5;11)(q3.3;p15.1)平衡易位,采用PCR的方法,找到了这2条染色体的精确的易位断裂点,从而克隆出在易位断裂点附件的KTS候选基因,AGGF1(VG5Q)就是在5号染色体的断裂点附近克隆到的,也正是这个原因,这个基因一开始就被命名为VG5Q。
随后的研究发现VG5Q的全长蛋白有718个氨基酸,通过蛋白质结构分析发现VG5Q含有多个结构域,在N端有一个环状结构,还有个OCTamer重复结构域(OCRE),Forkhead相关结构域(FHA),C端有G-patch结构域。根据CG5Q的蛋白质结构域,所以,人们就把VG5Q重新命名为AGGF1(Angiogenic Factor with G-patch and FHA domains 1, AGGF1)
1995年Hofmann和Bucher发现FHA结构域(Forkhead-associated domain)是一个可以特异性识别苏氨酸的磷酸激酶的蛋白结构域。到目前为止,有200多种蛋白质含有这个结构域。这个结构域涉及到一系列的反应,例如信号传导通路,转录,蛋白翻译,DNA修复和蛋白质降解等,这个结构域常常在激酶,磷酸酶,驱动蛋白,转录因子,RNA结合蛋白,和一些代谢酶中。
AGGF1蛋白序列在各物种之间的保守性较高,尤其是Forkhead相关结构域(FHA)和C端的G-patch结构域,但是AGGF1的这些结构域的功能研究得却不深入。
目前在现有技术中,没有发现有关AGGF1的促血管生成能力的报道。
发明内容
本发明的目的是提供一种新的刺激和促进缺血组织的血管新生的方法,
依照本发明的第一方面,通过提供了一种促进生物体组织的血管重建的方法而实验这些和其他目的,包括给予上述需要这些治疗的生物体有效量的AGGF1蛋白,或它的有着AGGF1生物活性的片段或类似物。
所述的AGGF1可以是人类AGGF1,也可以是小鼠、大鼠等其他哺乳动物的AGGF1。人的AGGF1的氨基酸序列如序列表中SEQ ID NO:1所示;其编码核苷酸序列如序列表中SEQ ID NO:2所示;小鼠的AGGF1的氨基酸序列如序列表中SEQ ID NO:3所示;其编码核苷酸序列如序列表中SEQ ID NO:4所示。如序列表所示,人类AGGF1的氨基酸序列与小鼠的AGGF1的氨基酸序列具有很高的同源性。各物种中的AGGF1基因具有高度同源性,其氨基酸序列的具有高度的同一性,因此在本发明中可以相互替换使用。此外,还可使用各种AGGF1基因的变体、活性片段、缀合物和其他衍生物。
依照本发明的另外一方面,通过提供一种通过血管发生刺激缺血组织血管新生的方法而实现本发明的目的,包括给予有效的血管刺激量的AGGF1蛋白,或它的有着AGGF1生物学活性的片段或类似物的步骤。
梗死后的缺血性疾病状态时血流减少后引起的灌注减少所造成的。通过血液对梗死区域的再灌注可以减缓这个问题。因为梗死区域的绝大多数血管和肌肉细胞将坏死,只有通过增加血流才能达到再灌注,血流的增加依赖于梗死区域的新血管。
因此,利用AGGF1进行血管新生进行治疗的候选疾病包括,其中,(1)肢体缺血性或慢性静脉腿部溃疡患者;(2)脑梗患者;(3)血管造影证实的冠状动脉疾病引起的慢性稳定型心绞痛患者(CarmelietP和Collen D,血管发生和心血管疾病的转基因小鼠模型(综述),病理学杂志,2000;190(3)387-405);(4)出生后动脉不良患者;(5)球囊成形术后再狭窄患者(Carmeliet P,Moons L,及Collen D,血管发生、动脉狭窄、粥样硬化和止血的小鼠模型(综述),心血管研究,1998;39(1)8-33);(6)缺血性心血管疾病患者;以及(7)终末期冠状动脉疾病患者。
依照本发明,有很多种可以用于给予患者没能有效促进血管新生的AGGF1的技术,这些患有缺血性或者其他一些可以通过血管新生而缓解的病变的患者。给予的AGGF1,可以以裸DNA或其以载体基因给予,也可以是重组蛋白,也可以是病毒。当然了,如果需要,可以使用可调控的载体。这些给予方式,同样可以和一些辅料,例如一些高分子材料(树脂等),一起进行给予,从而提高转染效率,延长表达时间。可以采取肌肉直接注射或采取静脉注射,还可以采用电穿孔方法,同样也可以将其附着在支架上,缓慢释放,也可以采取超声微泡技术,或者纳米泡等手段进行给药治疗。
例如,在手术期间或者通过微开胸术,可以通过心肌直接注射编码AGGF1的裸质粒DNA,或者包裹AGGF1的病毒,或者AGGF1蛋白给予心肌缺血患者AGGF1。
同样在超声引导下,可以让超声微泡在心梗部位或者肢体缺血部位裂开,从而将AGGF1释放出来作用在目的部位。Mukherjee等 通过超声介导包裹有人重组VEGF蛋白的造影剂,从而明显促进血管新生(J AmColl Cardiol 2000;35:1678–86)。Enomoto等采用超声微泡的技术,将BMC细胞特异性释放到了大鼠心梗部位(Heart 2006;92:515–520)。
另一种AGGF1给药的可能性是在缺血肢体的肌肉内注射AGGF1质粒或者包裹AGGF1的病毒,以腺相关病毒或逆转录病毒等为主。Korpisalo等将腺病毒直接注射在下肢缺血兔稍微肌肉上(Circ. Res. 2008;103;1092-1099)。Shimpo等将包裹有VEGF的腺相关病毒直接打入到下肢缺血的大鼠的腿部肌肉中(Cardiovasc Res (2002) 53 (4):993-1001 )。Hiraoka等则是直接将裸质粒注射到下肢缺血大鼠的肌肉内(Circulation 2003;108;2689-2696)。有的人为了提高表达量,甚至采用电穿孔的技术。在下肢缺血的兔子的后肢肌肉上注射FGF质粒后,采用电穿孔的技术提高了FGF的表达量(Journal of SurgicalResearch 120, 37–46 (2004))。
重组AGGF1蛋白可以通过静脉注射,从而改善缺血部位的坏死程度,促进血管新生。Sumi等通过尾静脉注射重组高密度脂蛋白给下肢缺血小鼠,从而促进血管新生,改善缺血导致的不良反应(ArteriosclerThromb Vasc Biol 2007;27;813-818)。
此外,本发明还提供了AGGF1蛋白或其活性片段在制备促进血管形成药物中的用途;其中所述AGGF1蛋白可以是天然AGGF1蛋白蛋白或重组AGGF1蛋白;所述药物可以是注射剂。
本发明还提供了编码AGGF1蛋白或其活性片段的核苷酸片段在制备促进血管形成药物中的用途;其中所述核苷酸片段可以与质粒连接,也可以与腺病毒载体、腺相关病毒载体或者其他复制缺陷的逆转录病毒载体连接;所述含有AGGF1的质粒或者病毒包裹在微泡中。
上述药物用于可治疗选自冠状动脉疾病导致的慢性稳定型心绞痛、严重肢体缺血、慢性静脉性腿部溃疡、糖尿病神经病变、出生后动脉功能不全、再狭窄、缺血性心血管病和终末期冠状动脉病变的病症。
在另一实施方案中,所述AGGF1蛋白或其活性片段、或编码AGGF1蛋白或其活性片段的核苷酸片段与至少一种选自VEGF-A、VEGF-B、VEGF-C、PIGF、PDGF-A、PDGF-B、PDGF-C、HGF和FGF的生长因子一起用于促进血管形成。
在另一个实施方案中,所述AGGF1蛋白或其活性片段、或编码AGGF1蛋白或其活性片段的核苷酸片段与内皮祖细胞、骨髓干细胞和/或心肌干细胞等细胞一起用于促进血管的形成。
本发明的有益效果:针对缺血组织或者部位导入外源性的治疗性的AGGF1,发现能够明显提高缺血部位的血液流速,促进血管新生,提高缺氧部位的氧气供应,缓解缺血症状,提高运动能力,坏死程度明显降低。
附图说明
通过参照下面的实验可以进一步详细的描述本发明,这些实验说明了AGGF1在促进缺血组织的血管形成中的活性,附图显示了这些实验的结果,其中:
图1是手术前小鼠的股动脉的血流情况图。通过小动物高频超声多普勒,在彩色脉冲多普勒的模式下,检测正常小鼠的股动脉的血流情况。
图2是手术后小鼠的股动脉的血流情况图。通过小动物高频超声多普勒,在彩色脉冲多普勒的模式下,检测下肢缺血小鼠的股动脉的血流情况。通过频谱发现,股动脉近心端被结扎或者出现较大程度的狭窄,下肢供血明显不足,收缩期最大血流速度发生了明显的下降。若频谱,没有发生改变,且收缩期最大血流速度没有较大程度的降低,则认为手术不成功,应剔除造模失败小鼠。
图3是不同时间点超声检测的左右腿的血流速度的比率情况图。由于血流与温度的有一定相关性,所以为了排除这些因素的影响,所以采用血流比率的统计方法。
图4是不同时间点小鼠组织坏死情况图。0,没有坏死;1,一个脚趾坏死;2,2个或多个脚趾坏死;3,脚坏死;4,整条腿的坏死;5,自行截肢。所有组均为n=9。
图5是不同时间点小鼠后肢行为能力的评分图。1,对于尾部的牵拉,后肢能伸缩,但脚趾没有反应;2,后肢和脚趾皆没有反应;3,后肢拖行。所有组均为n=9。
图6是给药7天,14天和28天的小鼠腓肠肌的免疫组化结果图。血管特异性标记物CD31标记的新生血管的情况。
图7是给药28天的小鼠腓肠肌的新生血管的统计结果图。针对血管特异性标记物CD31标记的新生血管的进行统计,图7A是单位面积新生血管数量的情况图。图7B是相对于肌束而言新生血管的数量图。
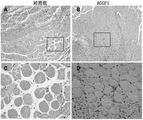
图8是小鼠腓肠肌肌肉组织切片的HE染色示意图。图8C是图8A图片中方框的放大图;图8D是图8C图片中方框的放大图。
具体实施方式
材料和实验方法
1)单侧下肢动脉结扎
10-12周雄性C57BL/6小鼠用戊巴比妥钠(50mg/kg)腹腔麻醉,并使其在手术中能自发呼吸。在小鼠左侧和右侧的腹股沟部到大腿部位用脱毛膏脱毛,使其表面干净。横向剪开皮肤,钝性分离出血管和神经。再小心将静脉和动脉分离开。右侧用6-0丝线将髂动脉结扎。顺着髂动脉往下分离血管,随后将股动脉进行结扎。在结扎过程中,不要伤及静脉和伴行的神经。左侧用6-0丝线将动脉绕一圈,在实验中作为对照,即假手术腿。
2)AGGF1和bFGF的质粒制备
使用已将目的基因整合进常用基因表达载体的重组表达载体,用于制备AGGF1和bFGF质粒的方法先前已有描述,根据Circulation 108:2689-2696(2003)中的方法制得AGGF1和bFGF质粒的。通过酚氯仿萃取和乙酸钾沉淀,纯化AGGF1和bFGF质粒,不含有内毒素。
3)小动物超声检测股动脉血流
采用Vevo 2100 高分辨率小动物超声系统(Visualsonics Inc,Toronto,Canada)检测小鼠血流。采用1%异戊烷麻醉小鼠,将其仰放在37℃的鼠板上,用脱毛膏将小鼠的两支腿的大腿部位到小腿部位的毛脱掉,减除毛发对超声检测的影响。采用MS550型探头进行检测。在彩色脉冲多普勒的模式下检测股动脉的血流速度。在手术前先检测小鼠股动脉的血流情况如图1所示,手术后第1天,再次通过超声检测如图2所示,判断下肢缺血模型是否成功。手术成功的标准为,脉冲多普勒的频谱出现了异常,基本上没有出现收缩期的最大血流,而且血流速度,明显降低,基本上小于手术前的10%。
4)组织坏死和行为能力的检测
未参加本实验的人,对小鼠的组织坏死和行为能力的情况进行评分。组织坏死的评分标准(Eur J Pharmacol 634(1-3): 121-131(2010))为:0,没有坏死;1,一个脚趾坏死;2,2个或多个脚趾坏死;3,脚坏死;4,整条腿的坏死;5,自行截肢,如图4所示。通过评分,我们发现相对于空质粒而言,AGGF1可以改善缺血组织坏死的情况,减轻小鼠的缺血症状,从而减轻因缺血而带来的病痛。
行为能力的评分标准(循环研究(Circ Res)101: 1310-1318(2007))为:0,对于尾部的牵拉,后肢有正常反应;1,对于尾部的牵拉,后肢能伸缩,但脚趾没有反应;2,后肢和脚趾皆没有反应;3,后肢拖行,如图5所示。下肢缺血小鼠的后肢的活动能力,在AGGF1的作用下,明显得到了增强,有利于缓解小鼠的缺血症状。运动能力的增强,也有利于缺血下肢的血管新生,从而改善由于缺血导致的各种不良的后果(循环(Circulation)122: 707-716(2010))。
5)免疫组化检测
手术后29天,将小鼠处死,分离出腓肠肌,4%的多聚甲醛固定过夜,石蜡包埋后,切片。采用新生血管的特异标记物CD31进行免疫组化检测,如图6所示。
实施例1
针对缺血组织,采用AGGF1基因进行血管新生的治疗
按照上述方法,建立小鼠下肢缺血模型。
采用肌肉注射DNA质粒的给药方式,对小鼠下肢缺血模型的缺血性部位进行血管新生治疗。手术1天后,在结扎部位下方,即腓肠肌部位,进行单点注射0.15ml的质粒。
在手术后8天,15天,29天进行血流检测,如图3所示。手术后8天,AGGF1治疗小鼠的左右腿血流流速比是0.22 ± 0.10,而对照组的小鼠的左右腿血流流速比为0.10± 0.04, (P < 0.05, n=9)。手术后29天的时候,AGGF1治疗小鼠的左右腿血流流速比是0.31±0.06,而对照组的小鼠的左右腿血流流速比为0.14±0.03, (P < 0.01, n=9)。发现通过AGGF1治疗确实可以明显提高血流速度,血流再灌能力增强。
根据免疫组化检测结果,发现外源性AGGF1能明显的刺激微血管的生成。AGGF1刺激28天后新生血管数量达到了0.934±0.413/mm2,而对照组仅仅0.538±0.388/mm2 (P < 0.01), 如图7A所示,同时相对于肌束而言新生血管的数量是439.2±250.1,对照组为172.5±109.4(P< 0.05),如图7B所示。
通过对切片进行HE染色,发现接受AGGF1注射的小鼠,细胞核的集中化并不显著。并且,坏死的肌肉纤维数量也明显下降,如图8所示。由此可见,AGGF1可以明显促进血管生成。
实施例2:
针对缺血组织,采用重组AGGF1蛋白进行血管新生的治疗
按照上述方法,建立小鼠下肢缺血模型。
建立小鼠下肢缺血模型后,在手术的第二天将纯化的AGGF1蛋白,通过尾静脉进行注射,诱导缺血组织中血管发生,缓解缺血导致的不良反应。按照上述方法进行组织坏死和行为能力的检测,发现给予AGGF1蛋白的小鼠的后肢运动能力明显增强,坏死程度也得到了改善。
实施例3:
针对缺血组织,采用AGGF1腺相关病毒进行血管新生的治疗
将编码AGGF1的cDNA克隆到腺相关病毒载体,转染,纯化,鉴定,测定其滴度,得到AGGF1腺相关病毒。
按照上述方法,建立小鼠下肢缺血模型。在手术的第二天,将纯化后得到AGGF1腺相关病毒,通过尾静脉进行注射。并在注射后的不同时间点检测股动脉血流、以及进行组织坏死和行为能力的检测。检测结果表明,与对照(缺乏编码AGGF1的cDNA的空腺相关病毒载体)相比,注射了AGGF1腺相关病毒的小鼠股动脉血流明显增加,小鼠的后肢运动能力明显增强,坏死程度也得到了改善。这些实验结果证实了AGGF1腺相关病毒能有效诱导缺血组织中血管发生,缓解缺血导致的不良反应。
上述三个实施例分别通过注射编码AGGF1的质粒、注射AGGF1蛋白、以及注射AGGF1腺相关病毒至小鼠下肢缺血模型中,结果均表明AGGF1能有效诱导缺血组织中血管发生,缓解缺血导致的不良反应。从而证实了AGGF1能够诱导血管发生,并治疗由局部缺血所导致的疾病和其他不良反应。
本发明虽然通过以上实施例进行了详细说明,但应当理解的是,这些实施例仅用于描述的目的,不应理解为对本发明的限制。
Claims (12)
1.AGGF1蛋白或其活性片段在制备促进血管形成的药物中的用途。
2.根据权利要求1的用途,其中所述AGGF1蛋白是重组AGGF1蛋白。
3.根据权利要求1或2的用途,其中所述药物是注射剂。
4.编码AGGF1蛋白或其活性片段的核苷酸片段在制备促进血管形成药物中的用途。
5.根据权利要求4的用途,其中所述编码AGGF1蛋白或其活性片段的核苷酸片段与质粒有效连接。
6.根据权利要求4的用途,其中所述编码AGGF1蛋白或其活性片段的核苷酸片段与腺病毒载体、腺相关病毒载体或者其他复制缺陷的逆转录病毒载体有效连接。
7.根据权利要求5或6的用途,其中所述含有AGGF1的质粒或者病毒包裹在微泡中。
8.根据权利要求1或4的用途,其中所述药物用于治疗局部缺血性疾病。
9.权利要求8的方法,其中所述疾病选自冠状动脉疾病导致的慢性稳定型心绞痛、严重肢体缺血、慢性静脉性腿部溃疡、糖尿病神经病变、出生后动脉功能不全、再狭窄、缺血性心血管病和终末期冠状动脉病变的病症。
10.根据权利要求1或4的用途,其中所述AGGF1蛋白或其活性片段、或编码AGGF1蛋白或其活性片段的核苷酸片段与至少一种选自VEGF-A、VEGF-B、VEGF-C、PIGF、PDGF-A、PDGF-B、PDGF-C、HGF和FGF的生长因子一起用于促进血管形成。
11.根据权利要求1或4的用途,其中所述AGGF1蛋白或其活性片段、或编码AGGF1蛋白或其活性片段的核苷酸片段与内皮祖细胞、骨髓干细胞和/或心肌干细胞等细胞一起用于促进血管的形成。
12.一种非治疗目的的促进血管形成的方法,包括给予血管刺激有效量的AGGF1蛋白或其活性片段、和/或编码AGGF1蛋白或其活性片段的核苷酸片段。
Priority Applications (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201210240339XA CN102755638A (zh) | 2012-07-12 | 2012-07-12 | Aggf1在制备促进血管形成的药物中的用途 |
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| CN201210240339XA CN102755638A (zh) | 2012-07-12 | 2012-07-12 | Aggf1在制备促进血管形成的药物中的用途 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| CN102755638A true CN102755638A (zh) | 2012-10-31 |
Family
ID=47050443
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| CN201210240339XA Pending CN102755638A (zh) | 2012-07-12 | 2012-07-12 | Aggf1在制备促进血管形成的药物中的用途 |
Country Status (1)
| Country | Link |
|---|---|
| CN (1) | CN102755638A (zh) |
Cited By (5)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103254296A (zh) * | 2013-04-28 | 2013-08-21 | 田小利 | 蛋白质aggf1及其fha多肽在制备抗炎药物中的应用 |
| CN106243212A (zh) * | 2016-07-29 | 2016-12-21 | 华中科技大学 | 一种重组蛋白及其应用 |
| CN115957300A (zh) * | 2022-12-22 | 2023-04-14 | 华中科技大学 | 一种重组蛋白用于制备抑制动脉瘤药物的应用 |
| CN116059319A (zh) * | 2022-07-13 | 2023-05-05 | 华中科技大学 | 一种重组蛋白用于制备抑制肌肉萎缩药物的应用 |
| WO2025208818A1 (zh) * | 2024-04-02 | 2025-10-09 | 深圳近邻生物科技有限公司 | 治疗下肢外周动脉疾病的核酸分子、药物组合物及其应用 |
Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005019432A2 (en) * | 2003-08-20 | 2005-03-03 | Cleveland Clinic Foundation Innovations | A novel gene and protein associated with angiogenesis and endothelial apoptosis |
-
2012
- 2012-07-12 CN CN201210240339XA patent/CN102755638A/zh active Pending
Patent Citations (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2005019432A2 (en) * | 2003-08-20 | 2005-03-03 | Cleveland Clinic Foundation Innovations | A novel gene and protein associated with angiogenesis and endothelial apoptosis |
Non-Patent Citations (1)
| Title |
|---|
| 刘木根: "先天性静脉畸形骨肥大综合征和长QT综合征的分子遗传学研究", 《万方学位论文》 * |
Cited By (7)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN103254296A (zh) * | 2013-04-28 | 2013-08-21 | 田小利 | 蛋白质aggf1及其fha多肽在制备抗炎药物中的应用 |
| CN106243212A (zh) * | 2016-07-29 | 2016-12-21 | 华中科技大学 | 一种重组蛋白及其应用 |
| CN116059319A (zh) * | 2022-07-13 | 2023-05-05 | 华中科技大学 | 一种重组蛋白用于制备抑制肌肉萎缩药物的应用 |
| CN115957300A (zh) * | 2022-12-22 | 2023-04-14 | 华中科技大学 | 一种重组蛋白用于制备抑制动脉瘤药物的应用 |
| CN115957300B (zh) * | 2022-12-22 | 2024-04-05 | 华中科技大学 | 一种重组蛋白用于制备抑制动脉瘤药物的应用 |
| WO2024130872A1 (zh) * | 2022-12-22 | 2024-06-27 | 华中科技大学 | 一种重组蛋白用于制备抑制动脉瘤药物的应用 |
| WO2025208818A1 (zh) * | 2024-04-02 | 2025-10-09 | 深圳近邻生物科技有限公司 | 治疗下肢外周动脉疾病的核酸分子、药物组合物及其应用 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| Collinson et al. | Therapeutic angiogenesis in peripheral arterial disease: can biotechnology produce an effective collateral circulation? | |
| JP5231587B2 (ja) | Vegf−cまたはvegf−d遺伝子またはタンパク質を用いた再狭窄の予防 | |
| Molin et al. | Therapeutic angiogenesis in the heart: protect and serve | |
| CN102755638A (zh) | Aggf1在制备促进血管形成的药物中的用途 | |
| Boodhwani et al. | The future of therapeutic myocardial angiogenesis | |
| AU772857B2 (en) | Method of inducing angiogenesis | |
| US7709450B2 (en) | Stimulation of vascularization with VEGF-B-186 | |
| Mikroulis et al. | Angiogenic growth factors in the treatment of peripheral arterial disease | |
| JP2006526592A (ja) | 血管由来の欠損に関連する高コレステロール血症または糖尿病の治療のための、線維芽細胞成長因子をコードするプラスミド | |
| Sedighiani et al. | Gene therapy in vascular disease | |
| Su et al. | APJ/apelin: A promising target for the treatment of retinopathy of prematurity | |
| US20200062820A1 (en) | Method for Treating Ischemic Tissue | |
| Shim et al. | Angiopoietin-1 promotes functional neovascularization that relieves ischemia by improving regional reperfusion in a swine chronic myocardial ischemia model | |
| Webster | Therapeutic angiogenesis: a case for targeted, regulated gene delivery | |
| Baklanov et al. | Arteriogenesis: lessons learned from clinical trials | |
| Khan et al. | Therapeutic angiogenesis for coronary artery disease | |
| Kaplan et al. | Cardiovascular gene therapy: angiogenesis and beyond | |
| Melillo et al. | Gene therapy in peripheral artery disease | |
| EP2007404A2 (en) | Methods and systems for treating injured cardiac tissue | |
| EP1402902A1 (en) | Method for treatment of vascular regeneration | |
| WO2025208818A1 (zh) | 治疗下肢外周动脉疾病的核酸分子、药物组合物及其应用 | |
| Rusiecka et al. | The cardiologists\'dream may come true–vascular therapy | |
| Charleston | 593. Delivery of Pleiotrophin Plasmid Induces Neovasculature Formation in Ischemic Myocardium | |
| Makeev et al. | THE NEW WAY TO THE GENE THERAPEUTIC CORRECTION OF THE PATHOGENETIC MECHANISMS OF CORONARY INSUFFICIENCY | |
| CN116251115A (zh) | 一种miR-342-5p在制备防治下肢缺血性疾病的药物中的应用 |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| C06 | Publication | ||
| PB01 | Publication | ||
| C10 | Entry into substantive examination | ||
| SE01 | Entry into force of request for substantive examination | ||
| C12 | Rejection of a patent application after its publication | ||
| RJ01 | Rejection of invention patent application after publication |
Application publication date: 20121031 |