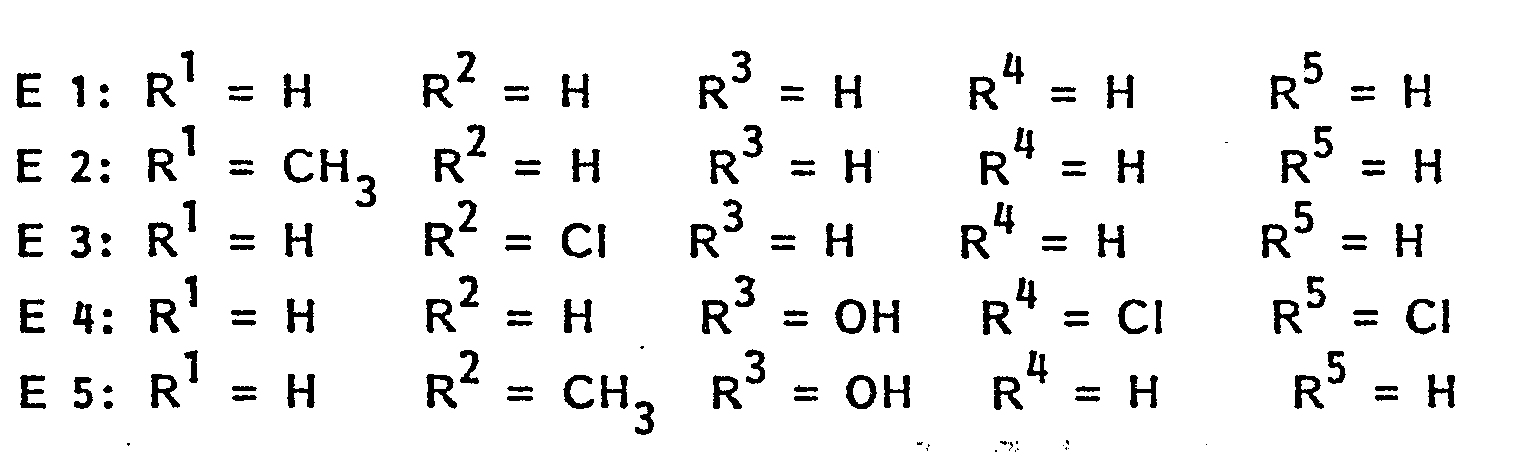EP0173932A2 - Haarfärbemittel - Google Patents
Haarfärbemittel Download PDFInfo
- Publication number
- EP0173932A2 EP0173932A2 EP85110640A EP85110640A EP0173932A2 EP 0173932 A2 EP0173932 A2 EP 0173932A2 EP 85110640 A EP85110640 A EP 85110640A EP 85110640 A EP85110640 A EP 85110640A EP 0173932 A2 EP0173932 A2 EP 0173932A2
- Authority
- EP
- European Patent Office
- Prior art keywords
- hair
- hydrogen
- benzyl
- amino
- oxidation
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K8/00—Cosmetics or similar toiletry preparations
- A61K8/18—Cosmetics or similar toiletry preparations characterised by the composition
- A61K8/30—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds
- A61K8/40—Cosmetics or similar toiletry preparations characterised by the composition containing organic compounds containing nitrogen
- A61K8/41—Amines
- A61K8/411—Aromatic amines, i.e. where the amino group is directly linked to the aromatic nucleus
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61Q—SPECIFIC USE OF COSMETICS OR SIMILAR TOILETRY PREPARATIONS
- A61Q5/00—Preparations for care of the hair
- A61Q5/10—Preparations for permanently dyeing the hair
Definitions
- the invention relates to hair colorants based on oxidation dyes.
- hair dyes contain oxidation dye precursors in a cosmetic carrier.
- Developer and coupler substances which form dyes under the influence of oxidizing agents or atmospheric oxygen are used as oxidation dye precursors.
- Creams, emulsions, gels, shampoos, foam aerosols or other preparations which are suitable for use on the hair serve as cosmetic carriers for the oxidation dye precursors.
- oxidation colors which result from the oxidative coupling of one or more developer components with one another or with one or more coupler components, play a preferred role because of their intense colors and good fastness properties.
- Primary aromatic amines with a further free or substituted hydroxy or amino group in the para or ortho position, furthermore diaminopyridine derivatives, heterocyclic hydrazone derivatives, 4-aminopyrazolone derivatives and tetraaminopyrimidines are usually used as developer substances.
- M-Phenylenediamine derivatives, naphthols, resorcinol derivatives and pyrazolones are used as so-called coupler substances.
- Good oxidation hair dye precursors must first of all meet the following requirements: They must develop the desired color shades with sufficient intensity and authenticity in the oxidative coupling. They must also have a good ability to draw on human hair without staining the scalp too much and they should above all be harmless from a toxicological and dermatological point of view.
- oxidation dye precursors P-phenylenediamine and many derivatives of this compound have long been known as oxidation dye precursors.
- many of these compounds are toxicologically and dermatologically questionable because they have mutagenic and / or allergic properties.
- oxidation dye precursors which, on the one hand, form intense colors with high fastness properties, but on the other hand are toxic in terms of toxicology and dermatology.
- hair colorants containing oxidation dye precursors in a cosmetic carrier the oxidation dye precursors N-benzyl-p-phenylenediamine or its derivatives of the general formula in which R is hydrogen or an alkyl group with 1 - 4 C atoms, R 2 is hydrogen, chlorine or an alkyl group with 1 - 4 C atoms, R 3 is hydrogen or a hydroxyl group and R 4 and R independently of one another are hydrogen or chlorine or whose salts and the coupler and / or developer substances common in oxidation colorants contain the requirements set out in to a high degree and, above all, are harmless and safe with regard to the toxicological and dermatological properties.
- the hair colorants according to the invention provide particularly intensive and brilliant hair colorations of high light and heat fastness, primarily in the area of the blue, red and brown shades.
- N-benzyl-p-phenylenediamines of the formula to be used according to the invention contain the substituents in the combinations E1, E2, E3, E4 or E5.
- N-benzyl-p-phenylenediamine (E1) to be used according to the invention as an oxidation hair dye precursor is a compound known from the literature (cf. Annalen der Chemie, 263, 302).
- the remaining compounds corresponding to general formula I can be obtained by synthesis processes known from the literature.
- an appropriately substituted p-nitroaniline can be substituted with an appropriately substituted benzyl alcohol according to the general reaction scheme or, if R 3 , R 4 and R are hydrogen or alkyl groups, a correspondingly substituted p-chloro-nitrobenzene with one correspondingly substituted benzylamine according to the general reaction scheme convert to N-benzyl-p-nitroaniline and catalytically hydrogenate it to N-benzyl-p-phenylenediamine.
- the preparation of the derivatives E 2 - E 5 which are not known in the literature, is described in more detail in the examples.
- the N-benzyl-p-phenylenediamines of the general formula 1 to be used according to the invention are developer substances, ie they are able to form dyes under the action of an oxidizing agent. However, particularly brilliant and intense colors are formed in the presence of coupler substances.
- Particularly suitable coupler substances are the m-phenylenediamines, m-aminophenols, resorcinols, naphthol-1, 1,5- and 2,7-dihydroxynaphthalene, hydroxy- and aminopyridines and aminopyrazolones.
- the developer compounds and the coupler compounds are generally used in approximately equimolar amounts in the hair colorants according to the invention. If the equimolar use also proves to be expedient, it is however not disadvantageous if individual oxidation dye precursors are used in excess. It is also not necessary that the N-benzyl-p-phenylenediamines or the oxidation dye precursors which are otherwise present are uniform compounds. Rather, mixtures of these compounds can also be used.
- the oxidative development of the coloring can in principle take place with atmospheric oxygen.
- a chemical oxidizing agent is preferably used, especially if, in addition to the coloring, a lightening effect on the hair is desired.
- Particularly suitable oxidizing agents are hydrogen peroxide or its adducts with urea, melamine or sodium borate and mixtures of such hydrogen peroxide adducts with potassium peroxide disulfate.
- the oxidation dye precursors are incorporated into a suitable cosmetic carrier.
- suitable cosmetic carrier are, for example, creams, emulsions, gels or also surfactant-containing, foaming solutions, for example shampoos or other preparations which are suitable for use on the hair.
- Typical components of such cosmetic preparations are, for example, wetting and emulsifying agents such as anionic, nonionic or ampholytic surfactants, for example fatty alcohol sulfates, alkane sulfonates, ⁇ -olefin sulfonates, fatty alcohol polyglycol ether sulfates, ethylene oxide addition products with fatty alcohols, fatty acids and alkylphenols, Sorbitan fatty acid esters and partial fatty acid glycerides, fatty acid alkanolamides and thickeners such as.
- wetting and emulsifying agents such as anionic, nonionic or ampholytic surfactants, for example fatty alcohol sulfates, alkane sulfonates, ⁇ -olefin sulfonates, fatty alcohol polyglycol ether sulfates, ethylene oxide addition products with fatty alcohols, fatty acids and alkylphenols, Sorbitan fatty acid esters and partial
- methyl or hydroxyethyl cellulose starch, fatty alcohols, paraffin oils, fatty acids, also perfume oils and hair care additives, such as water-soluble cationic polymers, protein derivatives, pantothenic acid and cholesterol.
- the constituents of the cosmetic carriers are used to produce the hair colorants according to the invention in amounts customary for these purposes; For example, emulsifiers are used in concentrations of 0.5 to 30% by weight and thickeners in concentrations of 0.1 to 25% by weight of the total colorant.
- the oxidation dye precursors are mixed into the carrier in amounts of 0.2% by weight, preferably 1% to 3% by weight, of the total colorant.
- the N-benzyl-p-phenylenediamines to be used according to the invention can be used in an amount of 0.05 to 10 millimoles per 100 g.
- the hair colorants according to the invention regardless of the type of cosmetic preparation, e.g. as a cream, gel or shampoo, in a slightly acidic, neutral or alkaline environment.
- the hair colorants are preferably used in a pH range of 8-10.
- the application temperatures can be in a range between 15 ° C. and 40 ° C.
- the hair dye is rinsed away from the hair to be colored.
- the hair is then washed with a mild shampoo and dried. Washing with a shampoo is not necessary if a carrier with a high tenside content, e.g. a coloring shampoo was used.
- the dyeings which can be achieved with the hair dye compositions according to the invention have a high brilliance and superior heat, light, wash and rub fastness properties.
- the following examples are intended to explain the subject of the invention in more detail, but without restricting it thereto.
- Hair colorants according to the invention were produced in the form of a hair color cream emulsion of the following composition:
- the ingredients were mixed together in order. After the oxidation dye precursors and the inhibitor had been added, the pH of the emulsion was first adjusted to 9.5 with concentrated ammonia solution, and the mixture was then made up to 100 g with water.
- the oxidative development of the color was carried out with 3% hydrogen peroxide solution as the oxidizing agent.
- 100 g of the emulsion were mixed with 50 g of hydrogen peroxide solution (3%) and mixed.
- the coloring cream was applied to approx. 5 cm long strands of standardized, 90% gray, but not specially pretreated human hair and left there for 30 minutes at 27 ° C. After the dyeing process was completed, the hair was rinsed, washed out with a customary shampoo and then dried.
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Birds (AREA)
- Epidemiology (AREA)
- Cosmetics (AREA)
Abstract
in der R1 Wasserstoff oder eine alkylgruppe mit 1 bis 4 C-Atomen, R2 Wasserstoff, Chlor oder eine Alkylgruppe mit 1 bis 4 C-Atomen, R3 Wasserstoff oder eine Hydroxylgruppe und R4 und R5 unabhängig voneinander Wasserstoff oder Chlor bedeuten, oder deren Salze eignen sich als Oxidationshaarfarbstoffvorprodukte für Haarfärbemittel. Die Verbindungen ergeben allein oder zusammen mit bekannten Kupplern und/oder Entwicklerverbindungen brillante Haarfärbungen von hoher Echtheit - vornehmlich im Bereich blauer, roter und brauner Nuancen.
Description
- Gegenstand der Erfindung sind Haarfärbemittel auf der Basis von Oxidationsfarbstoffen. Solche Haarfärbemittel enthalten Oxidationsfarbstoffvorprodukte in einem kosmetischen Träger. Als Oxidationsfarbstoffvorprodukte werden Entwicklersubstanzen und Kupplersubstanzen eingesetzt, die unter dem Einfiuß von Oxidationsmitteln oder von Luftsauerstoff Farbstoffe ausbilden. Als kosmetische Träger für die Oxidationsfarbstoffvorprodukte dienen Cremes, Emulsionen, Gele, Shampoos, Schaumaerosole oder andere Zubereitungen, die für die Anwendung auf dem Haar geeignet sind.
- Für das Färben von Haaren spielen die sogenannten Oxidationsfarben, die durch oxidative Kupplung einer oder mehrerer Entwicklerkomponenten untereinander oder mit einer oder mehreren Kupplerkomponenten entstehen, wegen ihrer intensiven Farben und guten Echtheitseigenschaften eine bevorzugte Rolle. Als Entwicklersubstanzen werden üblicherweise primäre aromatische Amine mit einer weiteren in Para- oder Orthoposition befindlichen freien oder substituierten Hydroxy- oder Aminogruppe, ferner Diaminopyridinderivate, hetero-cyclische Hydrazonderivate, 4-Aminopyrazolonderivate und Tetraaminopyrimidine eingesetzt. Als sogenannte Kupplersubstanzen werden m-Phenylendiaminderivate, Naphthole, Resorcinderivate und Pyrazolone verwendet.
- Gute Oxidationshaarfarbstoffvorprodukte müssen in erster Linie folgende Voraussetzungen erfüllen: Sie müssen bei der oxidativen Kupplung die gewünschten Farbnuancen in ausreichender Intensität und Echtheit ausbilden. Sie müssen ferner ein gutes Aufziehvermögen auf menschlichem Haar besitzen ohne die Kopfhaut zu stark anzufärben und sie sollen vor allem in toxikologischer und dermatologischer Hinsicht unbedenklich sein.
- P-Phenylendiamin und viele Derivate dieser Verbindung sind zwar als Oxidationsfarbstoffvorprodukte seit langem bekannt. Es ist aber auch bekannt, daß viele dieser Verbindungen toxikologisch und dermatologisch bedenklich sind, da sie mutagene undloder allergisierende Eigenschaften aufweisen. Es besteht daher ein hohes technisches Interesse an Oxidationsfarbstoffvorprodukten, die einerseits intensive Farben mit hohen Echtheitseigenschaften ausbilden, andererseits aber in toxikologischer und dermatologischer Hinsicht sjcher sind.
- Es wurde nun gefunden, daß Haarfärbemittel, enthaltend Oxidationsfarbstoffvorprodukte in einem kosmetischen Träger, die als Oxidationsfarbstoffvorprodukte N-Benzyl-p-phenylendiamin oder dessen Derivate der allgemeinen Formel
in der R Wasserstoff oder eine Alkylgruppe mit 1 - 4 C-Atomen, R2 Wasserstoff, Chlor- oder eine Alkylgruppe mit 1 - 4 C-Atomen, R3 Wasserstoff oder eine Hydroxylgruppe und R4 und R unabhängig voneinander Wasserstoff oder Chlor bedeuten oder deren Salze und die in Oxidationsfärbemitteln üblichen Kuppler- undloder Entwicklersubstanzen enthalten, die gestellten Anforderungen in hohem Maße erfüllen und vor allem in bezug auf die toxikologischen und dermatologischen Eigenschaften unbedenklich und sicher sind. Die erfindungsgemäßen Haarfärbemittel liefern besonders intensive und brillante Haarfärbungen von hoher Licht- und Wärmeechtheit, vornehmlich im Bereich der blauen, roten und braunen Nuancen. -
- Das erfindungsgemäß als Oxidationshaarfarbstoffvorprodukt zu verwendende N-Benzyl-p-phenylendiamin (E1) ist eine literaturbekannte Verbindung (vgl. Annalen der Chemie, 263, 302). Die übrigen der allgemeinen Formel I entsprechenden Verbindungen sind nach literaturbekannten Syntheseverfahren zugänglich. Allgemein kann man, wenn R3, R und R Halogen oder eine Hydroxylgruppe bedeuten, ein entsprechend substituiertes p-Nitroanilin mit einem entsprechend substituiertem Benzylalkohol nach dem allgemeinen Reaktionsschema
oder, wenn R3, R4 und R Wasserstoff oder Alkylgruppen sind, ein entsprechend substituiertes p-Chlor-nitrobenzol mit einem entsprechend substituierten Benzylamin nach dem allgemeinen Reaktionsschema
zum N-Benzyl-p-Nitroanilin umsetzen und dieses katalytisch zum N-Benzyl-p-phenylendiamin hydrieren. Die Herstellung der in der Literatur nicht bekannten Derivate E 2 - E 5 wird in den Beispielen näher beschrieben. - Die erfindungsgemäß zu verwendenden N-Benzyl-p-phenylendiamine der allgemeinen Formel 1 sind Entwicklersubstanzen, d.h. sie vermögen unter Einwirkung von Oxidationsmittein Farbstoffe auszubilden. In Gegenwart von Kupplersubstanzen werden jedoch besonders brillante und intensive Farben gebildet. Als Kupplersubstanzen eignen sich vor allem die m-Phenylendiamine, m-Aminophenole, Resorcine, Naphthol-1, 1,5- und 2,7-Dihydroxynaphthalin, Hydroxy- und Aminopyridine und Aminopyrazolone. Zur Modifikation der Farbnuance sind jedoch nicht nur die typischen, literaturbekannten Kupplerverbindungen geeignet, die selbst (ohne Entwickler) keine brauchbaren Färbungen anzubilden vermögen, sondern auch typische Entwicklersubstanzen, die mit den erfindungsgemäß zu verwendenden N-Benzyl-p-phenylendiaminen zu neuen Nuancen kuppeln. Solche zur Modifikation der Haaranfärbung geeignete Verbindungen sind vor allem aromatische Amine, die in Ortho- oder Paraposition eine zweite, substituierte oder freie Aminogruppe, eine Hydroxylgruppe, eine Phenolethergruppe oder eine Thiophenolethergruppe tragen, Diaminopyridine, 4-Aminopyrazolone sowie 2.4.5.6.-Tetraaminopyrimidin und deren Derivate. Auch direktziehende Farbstoffe, z. B. Nitrophenylendiaminderivate, Anthrachinonfarbstoffe oder Indophenole können zur Herstellung natürlicher Haarfarbnuancen mit den Oxidationsfarbstoffvorprodukten kombiniert und in die erfindungsgemäßen Haarfärbemittel eingesetzt werden.
- In den erfindungsgemäßen Haarfärbemitteln werden die Entwicklerverbindungen und die Kupplerverbindungen im allgemeinen in etwa äquimolaren Mengen eingesetzt. Wenn sich auch der äquimolare Einsatz als zweckmäßig erweist, so ist es jedoch nicht nachteilig, wenn einzelne Oxidationsfarbstoffvorprodukte im Überschuß zum Einsatz gelangen. Es ist auch nicht erforderlich, daß die N-Benzyl-p-Phenylendiamine oder die sonst vorhandenen Oxidationsfarbstoffvorprodukte einheitliche Verbindungen sind. Vielmehr können auch Gemische dieser Verbindungen zum Einsatz gelangen.
- Die oxidative Entwicklung der Färbung kann grundsätzlich mit Luftsauerstoff erfolgen. Bevorzugt wird jedoch ein chemisches Oxidationsmittel eingesetzt, besonders dann, wenn neben der Färbung ein Aufhelleffekt am Haar gewünscht wird. Als Oxidationsmittel kommen insbesondere Wasserstoffperoxid oder dessen Anlagerungsprodukte an Harnstoff, Melamin oder Natriumborat sowie Gemische aus derartigen Wasserstoffperoxidanlagerungsprodukten mit Kaliumperoxiddisulfat in Betracht.
- Zur Herstellung der erfindungsgemäßen Haarfärbemittel werden die Oxidationsfarbstoffvorprodukte in einen geeigneten kosmetischen Träger eingearbeitet. Solche Träger sind zum Beispiel Cremes, Emulsionen, Gele oder auch tensidhaltige, schäumende Lösungen, zum Beispiel Shampoos oder andere Zubereitungen, die für die Anwendung auf dem Haar geeignet sind. Übliche Bestandteile solcher kosmetischer Zubereitungen sind zum Beispiel Netz- und Emulgiermittel wie anionische, nichtionische oder ampholytische Tenside, zum Beispiel Fettalkoholsulfate, Alkansulfonate, α-Olefinsulfonate, Fettalkoholpolyglykolethersulfate, Ethylenoxidanlagerungsprodukte an Fettalkohole, Fettsäuren und Alkylphenole, Sorbitanfettsäureester und Fettsäurepartialglyceride, Fettsäurealkanolamide sowie Verdickungsmittel wie z. B. Methyl- oder Hydroxyethylcellulose, Stärke, Fettalkohole, Paraffinöle, Fettsäuren, ferner Parfümöle und haarpflegeride Zusätze, wie z.B. wasserlösliche kationische Polymere, Proteinderivate, Pantothensäure und Cholesterin. Die Bestandteile der kosmetischen Träger werden zur Herstellung der erfindungsgemäßen Haarfärbemittel in für diese Zwecke üblichen Mengen eingesetzt; z.B. werden Emulgiermittel in Konzentrationen von 0,5 bis 30 Gew.-% und Verdickungsmittel in Konzentrationen von 0,1 bis 25 Gew.-% des gesamten Färbemittels eingesetzt. Die Oxidationsfarbstoffvorprodukte werden in Mengen von 0,2 bis Gew.-%, vorzugsweise 1 bis 3 Gew.-% des gesamten Färbemittels in den Träger eingemischt. Die erfindungsgemäß zu verwendenden N-Benzyl-p-phenylendiamine können in einer Menge von 0,05 bis 10 Millimol pro 100 g eingesetzt werden.
- Die Anwendung der erfindungsgemäßen Haarfärbemittel kann, unabhängig von der Art der kosmetischen Zubereitung, z.B. als Creme, Gel oder Shampoo, im schwach sauren, neutralen oder alkalischen Milieu erfolgen. Bevorzugt ist die Anwendung der Haarfärbemittel in einem pH-Bereich von 8 - 10. Die Anwendungstemperaturen können in einem Bereich zwischen 15°C und 40°C liegen. Nach einer Einwirkungszeit von ca. 30 Minuten wird das Haarfärbemittel durch Ausspülen von dem zu färbenden Haar entfernt. Danach wird das Haar mit einem milden Shampoo nachgewaschen und getrocknet. Das Nachwaschen mit einem Shampoo entfällt, wenn ein stark tensidhaltiger Träger, z.B. ein Färbeshampoo, verwendet wurde.
- Die mit den erfindungsgemäßen Haarfärbemitteln erzielbaren Färbungen haben eine hohe Brillanz sowie überlegene Wärme-, Licht-, Wasch- und Reibechtheitseigenschaften. Die nachfolgenden Beispiele sollen den Erfindungsgegenstand näher erläutern, ohne ihn jedoch hierauf zu beschränken.
- Eine Mischung aus 7,9 g 1-Chlor-4-nitrobenzol (0,05 Mol) und 12,1 g Benzylmethylamin (0,1 Mol) wurde 6 Stunden unter Rühren auf 180°C erhitzt. Nach dem Abkühlen auf 20°C wurde das Reaktionsgemisch in verdünnter Salzsäure aufgenommen und der Niederschlag abfiltriert, mit Wasser gewaschen, getrocknet und aus Ethanol umkristaliisiert. Es wurden 8,2 g eines gelben Pulvers mit einem Schmelzpunkt von 66°C erhalten.
- Das Produkt der 1. Stufe wurde in ca. 200 ml Ethanol in Gegenwart von 0,5 g Palladium auf Aktivkohle (10 %ig) katalytisch hydriert. Nach beendeter Wasserstoffaufnahme wurde der Katalysator durch Filtration abgetrennt und das Filtrat zur Trockene eingeengt. Es wurde ein hellbraunes öl erhalten und durch infrarotspektrum identifiziert:
- IR-Spektrum (Film): 1615, 1520, 1470, 1450, 1430, 1415, 1335, 1310, 1260, 1180, 1150, 1125, 1050, 820.
- Eine Mischung aus 9,6 g 3.4-Dichlor-nitrobenzol (0,05 Mol) und 16g Benzylamin (0,15 Mol) wurde 30 Minuten auf 110°C und anschließend 2 Stunden auf 150° C erhitzt. Nach dem Abkühlen wurde das Reaktionsgemisch auf Eiswasser gegossen, der Niederschlag abfiltriert, mit Wasser gewaschen und aus Ethanol umkristallisiert. Es wurden 10,8 g eines gelben Pulvers mit einem Schmelzpunkt von 95° C erhalten.
- 2,6 g des Produktes der 1. Stufe wurden mit 11,3 g Sn Cl2 2H20 in 20 ml Ethanol 40 Minuten zum Sieden unter Rückflußkühlung erhitzt. Nach dem Abkühlen wurden 100 ml Eiswasser zugesetzt und unter Rühren ein pH-Wert von ca. 8 eingestellt. Das Reaktionsgemisch wurde dann 2 x mit je 50 ml Ethylacetat extrahiert. Nach Einengen des Estraktes zur Trockene wurde der Rückstand mit ca. 5 ml konzentrierter Salzsäure versetzt und erneut zur Trockene eingeengt. Es wurden 1,6 g des Produktes mit einem Schmelzpunkt von 1840 C (unter Zersetzung) erhäiten.
- Eine Mischung aus 9,65 g 2-Hydroxy-3.5-dichlorbenzylalkohol (0,05 Mol) und 6,9 g p-Nitroanilin (0,05 Mol) wurde 1 Stunde unter Rühren auf 160°C erhitzt. Nach dem Erkalten wurde das Reaktionsgemisch in verdünnter Natronlauge ( 45 ml 10 %ige Natronlauge in300 ml Wasser) aufgenommen. Durch Einleiten von CO2-Gas wurde das Produkt ausgefällt, dann abfiltriert, getrocknet und aus Ethanol umkristallisiert. Es wurden 8 g eines gelben Pulvers mit einem Schmelzpunkt von 129 - 132°C erhalten.
- 10 g des Produktes der 1. Stufe wurden in 400 ml Ethanol gelöst und nach Zugabe von O,5 g Raney-Nickel katalytisch hydriert. Nach beendeter Wasserstoff-Aufnahme wurde der Katalysator durch Filtration abgetrennt und das Filtrat mit konzentrierter Salzsäure angesäuert. Nach dem Einengen wurden 5 g des 1-(2-Hydroxy-3.5-dichlor)-benzylamino-4-aminobenzol-dihydrochlorid mit einem Schmelzpunkt ab 190°C (unter Zersetzung) erhalten.
- Eine Mischung aus 12,4 g 2-Hydroxybenzylalkohol (0,1 Mol) und 15,2 g 2-Methyl-4-nitroanilin (0,1 Mol) wurde 2 Stunden unter Rühren auf 160 C erhitzt. Nach dem Erkalten wurde das Reaktionsgemisch in verdünnter Natronlauge (45 ml 10%ige Natronlauge in 300 ml Wasser) aufgenommen. Durch Einleiten von CO-Gas wurde das Produkt ausgefällt, dann abfiltriert, getrocknet und aus Ethanol umkristallisiert. Es wurden 6 g eines olivgelben Pulvers mit einem Schmelzpunkt von 125 °C (unter Zersetzung) erhalten.
- 5 g des Produktes der 1. Stufe wurden in 400 ml Ethanol gelöst und nach Zugabe von 0,5 g Raney-Nickel katalytisch hydriert. Nach beendeter Wasserstoff-Aufnahme wurde der Katalysator durch Filtration abgetrennt und das Filtrat mit konzentrierter Salzsäure angesäuert. Nach dem Einengen wurden 4,2 g des 1-(2-Hydroxybenzyl)-amino-2-methyl-4-aminobenzol-dihydrochlorid mit einem Schmelzpunkt von 210 °C (unter Zersetzung) erhalten.
-
- Die Bestandteile wurden der Reihe nach miteinander vermischt. Nach Zugabe der Oxidationsfärbemittelvorprodukte und des Inhibitors wurde zunächst mit konzentrierter Ammoniak-Lösung der pH-Wert der Emulsion auf 9,5 eingestellt, dann wurde mit Wasser auf 100 g aufgefüllt.
- Die oxidative Entwicklung der Färbung wurde mit 3%iger Wasserstoffperoxidlösung als Oxidationsmittel durchgeführt. Hierzu wurden 100 g der Emulsion mit 50 g Wasserstoffperoxidiösung (3%ig) versetzt und vermischt.
- Die Färbecreme wurde auf ca. 5 cm lange Strähnen standardisierten, zu 90 % ergrauten, aber nicht besonders vorbehandelten Menschenhaars aufgetragen und dort 30 Minuten bei 27 ° C belassen. Nach Beendigung des Färbeprozesses wurde das Haar gespült, mit einem üblichen Haarwaschmittel ausgewaschen und anschließend getrocknet.
- Es wurden folgende N-Benzyl-p-phenylendiamine eingesetzt (Komponente E)
- E 1 : 1-Benzylamino-4-aminobenzol
- E 2 : 1-Benzyl-methyl-amino-4-aminobenzol
- E 3 : 1-Benzylamino-2-chlor-4-aminobenzol-dihydrochlorid
- E 4 : 1-(2-Hydroxy-3.5-dichlorbenzyl)-amino-4-aminobenzol- dihydrochlorid
- E 5 : 1-(2-Hydroxybenzyl)-amino-2-methyl-4-aminobenzol- dihydrochlorid
- Als zweites Oxidationsfarbstoffvorprodukt (Komponente M) zur Modifikation der Haaranfärbung wurden folgende Verbindungen eingesetzt:
- M 1 : Naphthol-1
- M 2 : 1.5-Dihydroxynaphthalin
- M 3 : 2.7-Dihydroxynaphthalin
- M 4 : Resorcin
- M 5 : 2-Methylresorcin
- M 6 : 4-Chlorresorcin
- M 7 : Diresorcylsulfoxid
- M 8 : m-Aminophenol
- M 9 : 5-Amino-2-methylphenol
- M 10: 2.4-Dichlor-3-aminophenol
- M 11: 2.4-Diaminophenol
- M 12: 3.4-Methylendioxyphenol
- M 13: 3.4-Methylendioxyanilin
- M 14: 2.4-Diaminophenoxyethanol
- M 15: 1.3-Bis-(2.4-diaminophenoxy)-propan
- M 16: 5-Chlor-2.3-pyridindiol
- M 17: 2-Amino-3-hydroxypyridin
- M 18: 3-Amino-2-methylamino-6-methoxypyridin
- M 19: 1-Phenyl-3-methyl-pyrazolon-5
- M 20: 1-Phenyl-4-amino-pyrazolon-5
- M 21: p-Phenylendiamin
- M 22: 2.5-Diaminotoluol
- M 23: N-Methyl-p-phenylendiamin
- M 24: 1-(2-Hydroxypropyl)-amino-4-aminobenzol
- M 25: 1-Ethyl-1-(2-hydroxyethyl)-amino-4-aminobenzol
- M 26: 1.1-Bis-(2-hydroxyethyl)-amino-4-aminobenzol
- M 27: 2.5-Diaminoanisol
- M 28: p-Aminophenol
- M 29: 2.4.5.6-Tetraaminopyrimidin
-
Claims (4)
in der R1 Wasserstoff oder eine Alkylgruppe mit 1 - 4 C-Atomen, R2 Wasserstoff, Chlor oder eine Alkylgruppe mit 1 - 4 C-Atomen, R3 Wasserstoff oder eine Hydroxylgruppe und R4 und R5 unabhängig voneinander Wasserstoff oder Chlor bedeuten, oder deren Salz und die in Oxidationsfärbemitteln üblichen Kuppler- und/oder Entwicklersubstanzen enthalten sind.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE3432214 | 1984-09-01 | ||
| DE19843432214 DE3432214A1 (de) | 1984-09-01 | 1984-09-01 | Haarfaerbemittel |
Publications (2)
| Publication Number | Publication Date |
|---|---|
| EP0173932A2 true EP0173932A2 (de) | 1986-03-12 |
| EP0173932A3 EP0173932A3 (de) | 1986-12-30 |
Family
ID=6244448
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP85110640A Withdrawn EP0173932A3 (de) | 1984-09-01 | 1985-08-23 | Haarfärbemittel |
Country Status (6)
| Country | Link |
|---|---|
| EP (1) | EP0173932A3 (de) |
| JP (1) | JPS6183112A (de) |
| DE (1) | DE3432214A1 (de) |
| DK (1) | DK398485A (de) |
| FI (1) | FI853314A7 (de) |
| NO (1) | NO853431L (de) |
Cited By (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0538195A3 (en) * | 1991-10-18 | 1993-06-23 | Ciba-Geigy Ag | N-allyl/benzyl substituted phenylenediamine stabilizers |
| EP1108708A1 (de) * | 1999-12-18 | 2001-06-20 | Wella Aktiengesellschaft | Neue 1,4-Diaminobenzol-Derivate und diese Verbindungen enthaltende Färbemittel |
Families Citing this family (1)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| USRE41549E1 (en) | 2000-08-31 | 2010-08-24 | Wella Ag | Dyes for keratin fibers, the dyes containing n-benzyl-p-phenylenediamine derivatives and novel n-benzyl-p-phenylenediamine derivatives |
Family Cites Families (2)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CA1025881A (en) * | 1973-10-15 | 1978-02-07 | Alexander Halasz | Dyeing keratin fibers with 2-substituted m-toluenediamines |
| DE2934330A1 (de) * | 1979-08-24 | 1981-03-12 | Henkel KGaA, 4000 Düsseldorf | Haarfaerbemittel. |
-
1984
- 1984-09-01 DE DE19843432214 patent/DE3432214A1/de not_active Withdrawn
-
1985
- 1985-08-23 EP EP85110640A patent/EP0173932A3/de not_active Withdrawn
- 1985-08-26 JP JP60185946A patent/JPS6183112A/ja active Pending
- 1985-08-29 FI FI853314A patent/FI853314A7/fi not_active Application Discontinuation
- 1985-08-30 NO NO853431A patent/NO853431L/no unknown
- 1985-08-30 DK DK398485A patent/DK398485A/da not_active Application Discontinuation
Cited By (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP0538195A3 (en) * | 1991-10-18 | 1993-06-23 | Ciba-Geigy Ag | N-allyl/benzyl substituted phenylenediamine stabilizers |
| EP1108708A1 (de) * | 1999-12-18 | 2001-06-20 | Wella Aktiengesellschaft | Neue 1,4-Diaminobenzol-Derivate und diese Verbindungen enthaltende Färbemittel |
| US6602302B1 (en) | 1999-12-18 | 2003-08-05 | Wella Ag | Substituted 1,4 diaminobenzene compounds and oxidation dye precursor compositions containing same |
Also Published As
| Publication number | Publication date |
|---|---|
| NO853431L (no) | 1986-03-03 |
| FI853314A0 (fi) | 1985-08-29 |
| FI853314L (fi) | 1986-03-02 |
| FI853314A7 (fi) | 1986-03-02 |
| DK398485A (da) | 1986-03-02 |
| DE3432214A1 (de) | 1986-03-13 |
| EP0173932A3 (de) | 1986-12-30 |
| JPS6183112A (ja) | 1986-04-26 |
| DK398485D0 (da) | 1985-08-30 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0211238B1 (de) | Neue Aminophenole und deren Verwendung in Oxidationshaarfärbemitteln | |
| EP0055386A2 (de) | Haarfärbemittel | |
| DE3627922A1 (de) | Neue tetraaminopyrimidin-derivate und deren verwendung in haarfaerbemitteln | |
| EP0319817A2 (de) | Phenylamino- und Phenylaminomethyl-pyridine und diese Enthaltende Haarfärbemittel | |
| EP0011844A1 (de) | Neue Kupplerkomponenten für Oxidationshaarfarben, deren Herstellung sowie diese enthaltende Haarfärbemittel | |
| EP0036591B1 (de) | Neue Kupplerkomponenten für Oxidationshaarfarben, deren Herstellung und Verwendung sowie diese enthaltende Haarfärbemittel | |
| EP0195361A2 (de) | Haarfärbemittel | |
| EP0569368A1 (de) | 2,5-diaminophenoxy-oxaalkane und deren verwendung als oxidationsfarbstoffvorprodukte | |
| EP0107027B1 (de) | Haarfärbemittel | |
| EP0470099B1 (de) | Haarfärbemittel | |
| DE2852156C2 (de) | Haarfärbemittel auf der Basis von Oxidationsfarbstoffen und Bis-(2,4-diaminophenoxy)-alkane | |
| EP0039806B1 (de) | Haarfärbemittel | |
| EP0270972A2 (de) | Oxidationshaarfärbemittel | |
| WO1993016679A1 (de) | p-PHENYLENDIAMINDERIVATE ALS OXIDATIONSFARBSTOFFVORPRODUKTE | |
| EP0195363B1 (de) | Haarfärbemittel | |
| EP0106089A1 (de) | Haarfärbemittel | |
| EP0173932A2 (de) | Haarfärbemittel | |
| EP0176798B1 (de) | Aminodiphenylamine und diese enthaltende Haarfärbemittel | |
| DE2934331A1 (de) | Neue entwicklerkomponenten fuer oxidationshaarfarben, deren herstellung und verwendung, sowie diese enthaltende haarfaerbemittel. | |
| DE2719424A1 (de) | Haarfaerbemittel | |
| EP0697854B1 (de) | Verwendung von hydroxynaphthalinen in färbemitteln | |
| EP0348849B1 (de) | Haarfärbemittel | |
| DE3045959C2 (de) | ||
| DE3537763A1 (de) | Haarfaerbemittel mit direktziehenden nitrodiphenylamin-derivaten | |
| DE3313905A1 (de) | Neue 2.4-diaminophenolether als kuppler fuer oxidationshaarfaerbemittel |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A2 Designated state(s): AT BE CH DE FR GB IT LI LU NL SE |
|
| PUAL | Search report despatched |
Free format text: ORIGINAL CODE: 0009013 |
|
| AK | Designated contracting states |
Kind code of ref document: A3 Designated state(s): AT BE CH DE FR GB IT LI LU NL SE |
|
| 17P | Request for examination filed |
Effective date: 19870522 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION HAS BEEN WITHDRAWN |
|
| 18W | Application withdrawn |
Withdrawal date: 19870730 |
|
| RIN1 | Information on inventor provided before grant (corrected) |
Inventor name: MAAK, NORBERT, DR. Inventor name: LIESKE, EDGAR Inventor name: ROSE, DAVID, DR. |