EP0554564A1 - Verfahren zur Herstellung von Benzaldehydacetalen - Google Patents
Verfahren zur Herstellung von Benzaldehydacetalen Download PDFInfo
- Publication number
- EP0554564A1 EP0554564A1 EP92121990A EP92121990A EP0554564A1 EP 0554564 A1 EP0554564 A1 EP 0554564A1 EP 92121990 A EP92121990 A EP 92121990A EP 92121990 A EP92121990 A EP 92121990A EP 0554564 A1 EP0554564 A1 EP 0554564A1
- Authority
- EP
- European Patent Office
- Prior art keywords
- alkyl
- general formula
- electrolysis
- substituents
- carried out
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Withdrawn
Links
Classifications
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25B—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES FOR THE PRODUCTION OF COMPOUNDS OR NON-METALS; APPARATUS THEREFOR
- C25B3/00—Electrolytic production of organic compounds
- C25B3/20—Processes
- C25B3/23—Oxidation
-
- C—CHEMISTRY; METALLURGY
- C25—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES; APPARATUS THEREFOR
- C25B—ELECTROLYTIC OR ELECTROPHORETIC PROCESSES FOR THE PRODUCTION OF COMPOUNDS OR NON-METALS; APPARATUS THEREFOR
- C25B3/00—Electrolytic production of organic compounds
- C25B3/01—Products
- C25B3/07—Oxygen containing compounds
Definitions
- the acetals I serve - especially in the form of the corresponding benzaldehydes - as fragrances or as intermediates for medicines or fragrances. Some of them are known or can be produced by known processes.
- Compounds I can also be prepared from dialkyl-substituted benzenes by electrooxidation.
- DE-A 3 322 399 the oxidation of p-xylene to p-methylbenzaldehyde dimethyl acetal proceeds with a selectivity of 79%.
- an alkyl substituent is branched, such as in p-cymene (p-isopropyltoluene)
- the selectivity of the reaction to compounds I drops drastically due to oxidation of the isopropyl group (ES 2 009 174).
- ES 2 009 174 According to J. Chem. Res. (S), 228-9 (1986), the electrooxidation of o-xylene also leads to a number of by-products.
- the object of the invention was to make acetals I from benzyl ethers II more selective and thus more economically accessible.
- the method according to the invention can be illustrated as follows:
- the starting compounds II are known and can be obtained by known methods, for example from the appropriately substituted benzyl chlorides.
- alkyl, cycloalkyl and aryl groups can carry substituents, C1-C2-alkyl radicals or halogen being preferred.
- the electrochemical oxidations can be carried out in divided, preferably undivided, flow cells.
- the electrolyte is composed of the starting compound II, an alcohol R1-OH and an auxiliary electrolyte.
- the electrolyte may contain a solvent which is inert under the electrolysis conditions, such as acetonitrile; however, the electrolysis is preferably carried out without such a solvent.
- the electrolyte preferably contains 1-49%, preferably 5-30% by weight of the benzyl ether II, 50-98.9%, preferably 70-95% by weight of the alkanol R1-OH and 0.1-5%, preferably 0.2-3% by weight of the auxiliary electrolyte
- Weakly basic or neutral or acidic salts are particularly suitable as auxiliary electrolytes. Examples are fluorides, tetrafluoroborates, sulfonates, sulfates, phosphates and phosphonates of alkali metals such as potassium fluoride and sodium phenyl sulfonate.
- Ammonium salts such as tetramethylammonium methyl sulfate and acidic compounds such as sulfuric acid, alkyl and aryl sulfonic acids such as methyl or benzenesulfonic acid are also suitable.
- the electrolysis is carried out in the acidic, neutral or weakly basic range. This range is indicated by the pH of the electrolyte.
- the pH of the electrolyte is determined in such a way that equal volumes of electrolyte and water are mixed and the pH of the resulting solution is measured using known methods. The measured pH should be less than 10, but a neutral or acidic solution is preferred.
- Precious metals such as platinum or oxides such as chromium and ruthenium oxide and mixed oxides such as Ti / RuO x are suitable as anode materials.
- the preferred material is graphite.
- the electrolysis can be carried out batchwise or continuously, it being possible, if desired, for unreacted starting material to be returned to the reaction.
- the current density for the process according to the invention can be chosen within wide limits from 0.1 to 25 A / dm2, preferably 1-10 A / dm2.
- the oxidations are carried out at temperatures from 0 to 120 ° C., preferably 20-80 ° C. There may be reduced pressure or normal pressure. In the presence of low-boiling components, it is also possible to work under increased pressure up to 10 bar, preferably up to 3 bar.
- the amounts of charge are generally 1.5 to 6 F / mol II, preferably 2 to 4 F / mol II.
- the reaction solution is worked up in a known manner, preferably by distillation.
- the process according to the invention allows the benzaldehyde acetals I to be prepared selectively, the product generally only having to be separated off from incompletely reacted starting material.
- the oxidation of the side group R3R4CH- is not observed or only to a minimal extent in the process according to the invention.
- the acetals I can be hydrolyzed to the corresponding benzaldehydes in a manner known per se. Some of these themselves serve as fragrances, for example o-tolylaldehyde and p-tolylaldehyde, or they are valuable intermediates. Cuminaldehyde, for example, is a precursor for the production of (4-isopropylcyclohexyl) methanol (mayol).
Landscapes
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Engineering & Computer Science (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Electrochemistry (AREA)
- Materials Engineering (AREA)
- Metallurgy (AREA)
- Electrolytic Production Of Non-Metals, Compounds, Apparatuses Therefor (AREA)
- Organic Low-Molecular-Weight Compounds And Preparation Thereof (AREA)
Abstract
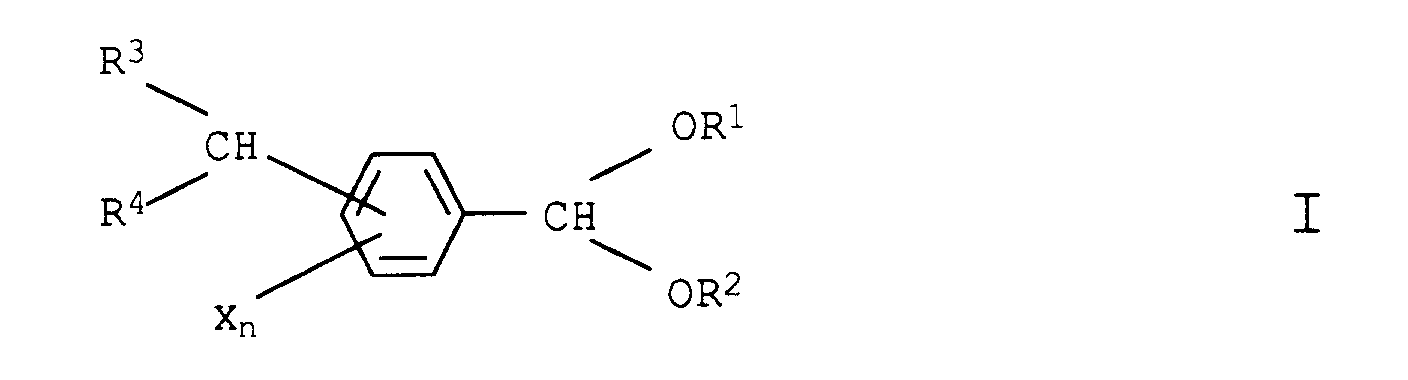
Verfahren zur Herstellung von Benzaldehydacetalen der allgemeinen Formel I
in der die Variablen folgende Bedeutung haben:
in der die Variablen folgende Bedeutung haben:
- R¹
- n-Alkyl
- R²
- ein Kohlenwasserstoffrest
- R³,R⁴
- Wasserstoff, Kohlenwasserstoffreste, Cyangruppen oder Alkoxycarbonylgruppen
- X
- inerte Substituenten
- n
- 0 bis 3, wobei die Substituenten X im Falle n > 1 gleich oder verschieden sein können
in Gegenwart eines Alkanols R¹-OH sowie in Gegenwart eines Hilfselektrolyten, indem man im sauren, neutralen oder schwach basischen Bereich elektrolysiert.
Description
-
- R¹
- n-Alkyl
- R²
- ein Kohlenwasserstoffrest
- R³,R⁴
- Wasserstoff, Kohlenwasserstoffreste, Cyangruppen oder Alkoxycarbonylgruppen
- X
- inerte Substituenten
- n
- 0 bis 3, wobei die Substituenten X im Falle n > 1 gleich oder verschieden sein können
- Die Acetale I dienen - vor allem in Form der entsprechenden Benzaldehyde - als Riechstoffe oder als Zwischenprodukte für Arzneimittel oder Riechstoffe. Sie sind zum Teil bekannt oder können durch bekannte Verfahren hergestellt werden.
- Die elektrochemische Oxidation von p-Methoxymethyltoluol in stark basischer Methanollösung führt nach Electrochim. Acta 29, 1639 - 41 (1984) zu einem Gemisch aus p-Methylbenzaldehyddimethylacetal und p-Xylylendimethylether im Verhältnis 10:1. Es findet hierbei teilweise eine Oxidation des Methylsubstituenten des Benzylethers statt.
- Aus dialkylsubstituierten Benzolen lassen sich die Verbindungen I ebenfalls durch Elektrooxidation herstellen. Nach DE-A 3 322 399 verläuft die Oxidation von p-Xylol zu p-Methylbenzaldehyddimethylacetal mit einer Selektivität von 79 %. Bei Verzweigung eines Alkylsubstituenten wie in p-Cymol (p-Isopropyltoluol) sinkt die Selektivität der Reaktion zu Verbindungen I durch Oxidation der Isopropylgruppe aber drastisch (ES 2 009 174). Auch die Elektrooxidation von o-Xylol führt nach J. Chem. Res. (S), 228-9 (1986) zu einer Reihe von Nebenprodukten.
- Der Erfindung lag die Aufgabe zugrunde, die Acetale I aus Benzylethern II selektiver und damit wirtschaftlicher zugänglich zu machen.
- Demgemäß wurde eine Verbesserung des eingangs definierten Verfahrens gefunden, welches dadurch gekennzeichnet ist, daß die Elektrolyse im sauren, neutralen oder schwach basischen Bereich durchgeführt wird.
-
- Unter den Verbindungen I werden solche bevorzugt, in denen die Substituenten folgende Bedeutung haben:
- R¹
- - C₁-C₆-n- Alkyl, vorzugsweise C₁-C₄-n-Alkyl, vor allem Methyl und Ethyl;
- R²
- - C₁-C₁₂-Alkyl, vorzugsweise C₁-C₆-Alkyl, darunter besonders Methyl, Ethyl, n-Propyl, iso-Propyl, n-Butyl, sek.-Butyl, iso-Butyl, tert.-Butyl, n-Pentyl, tert.-Amyl, n-Hexyl, 1,1-Dimethylbutyl;
- C₃-C₈-Cycloalkyl, vorzugsweise C₅-C₇-Cycloalkyl wie Cyclopentyl, Cyclohexyl, Cycloheptyl;
- C₇-C₁₄-Aralkyl, vorzugsweise C₇-C₁₀-Aralkyl wie 1-Phenylethyl, 2-Phenylethyl, 1-Phenylpropyl, 2-Phenylpropyl, 3-Phenylpropyl, 1-Methyl-1-phenylethyl und vor allem Benzyl;
- Aryl wie Phenyl; - R³,R⁴
- - wie R²; weiterhin:
- Wasserstoff;
- Alkoxycarbonyl wie Methoxycarbonyl, Ethoxycarbonyl, tert.-Butoxycarbonyl;
- Cyan; - X
- - wie R³; weiterhin:
- C₁-C₁₂-Alkoxy, vorzugsweise C₁-C₆-Alkoxy wie Methoxy, Ethoxy,n-Propoxy, iso-Propoxy, n-Butoxy, iso-Butoxy, sek-Butoxy, tert.-Butoxy, n-Pentoxy, tert.-Amyloxy, n-Hexyloxy;
- C₁-C₆-Dialkoxyalkyl, bevorzugt C₁-C₅-Dialkoxyalkyl wie 2,2-Dimethoxyethyl, Dimethoxymethyl, Diethoxymethyl;
- Halogen wie vorzugsweise Fluor, Chlor oder Brom. - Weiterhin können die Alkyl-, Cycloalkyl- und Arylgruppen Substituenten tragen, wobei C₁-C₂-Alkylreste oder Halogen bevorzugt sind.
- Die elektrochemischen Oxidationen können in geteilten, vorzugsweise in ungeteilten Durchflußzellen ausgeführt werden.
- Der Elektrolyt setzt sich aus der Ausgangsverbindung II, einem Alkohol R¹-OH und einem Hilfselektrolyten zusammen. Der Elektrolyt kann ein unter den Elektrolysebedingungen inertes Lösungsmittel wie Acetonitril enthalten; vorzugsweise führt man die Elektrolyse aber ohne ein solches Lösungsmittel aus.
- Bevorzugt enthält der Elektrolyt
1-49 %, vorzugsweise 5-30 Gew.% des Benzylethers II,
50-98,9 %, vorzugsweise 70-95 Gew.% des Alkanols R¹-OH und
0,1-5 %, vorzugsweise 0,2-3 Gew.% des Hilfselektrolyten
Als Hilfselektrolyte eignen sich besonders schwach basische oder neutrale oder saure Salze. Beispiele sind Fluoride, Tetrafluoroborate, Sulfonate, Sulfate, Phosphate und Phosphonate von Alkalimetallen wie Kaliumfluorid und Natriumphenylsulfonat. - Weiterhin kommen Ammoniumsalze wie Tetramethylammoniummethylsulfat in Betracht sowie saure Verbindungen wie Schwefelsäure, Alkyl- und Arylsulfonsäuren wie Methyl- oder Benzolsulfonsäure.
- Die Elektrolyse wird im sauren, neutralen oder schwach basischen Bereich ausgeführt. Dieser Bereich wird durch den pH-Wert des Elektrolyten angegeben. Definitionsgemäß wird der pH-Wert des Elektrolyten so ermittelt, daß gleiche Volumina Elektrolyt und Wasser gemischt werden und der pH-Wert der entstehenden Lösung nach bekannten Methoden gemessen wird. Der gemessene pH-Wert soll kleiner als 10 sein, bevorzugt wird aber eine neutrale oder saure Lösung.
- Als Anodenmaterialien kommen Edelmetalle wie Platin oder Oxide wie Chrom- und Rutheniumoxid sowie Mischoxide wie Ti/RuOx in Betracht. Bevorzugtes Material ist aber Graphit.
- Als Kathodenmaterial eignen sich im allgemeinen Stahl, Eisen, Kupfer, Nickel, Zink und Kohle sowie Edelmetalle wie Platin; bevorzugt wird jedoch Graphit.
- Die Elektrolyse kann diskontinuierlich oder kontinuierlich ausgeführt werden, wobei nicht umgesetztes Ausgangsmaterial gewünschtenfalls wieder in die Reaktion zurückgeführt werden kann.
- Die Stromdichte kann für das erfindungsgemäße Verfahren in weiten Grenzen von 0,1 bis 25 A/dm², vorzugsweise 1-10 A/dm² gewählt werden. Die Oxidationen werden bei Temperaturen von 0 bis 120°C, vorzugsweise 20-80°C durchgeführt. Dabei kann verminderter Druck oder Normaldruck herrschen. Bei Anwesenheit leichtsiedender Komponenten kann auch unter erhöhtem Druck bis 10 bar, vorzugsweise bis 3 bar gearbeitet werden. Die Ladungsmengen betragen in der Regel 1,5 bis 6 F/mol II, bevorzugt 2 bis 4 F/mol II.
- Die Aufarbeitung der Reaktionslösung wird in bekannter Weise, vorzugsweise destillativ, vorgenommen.
- Das erfindungsgemäße Verfahren erlaubt eine selektive Herstellung der Benzaldehydacetale I, wobei in der Regel das Produkt lediglich von nicht vollständig abreagiertem Ausgangsstoff abgetrennt zu werden braucht. Die Oxidation der Seitengruppe R³R⁴CH- ist im erfindungsgemäßen Verfahren nicht oder nur in minimalen Umfang zu beobachten.
- Die Acetale I können in an sich bekannter Weise zu den entsprechenden Benzaldehyden hydrolysiert werden. Diese dienen zum Teil selbst als Riechstoffe, z.B. o-Tolylaldehyd und p-Tolylaldehyd, oder sie sind wertvolle Zwischenprodukte. Cuminaldehyd beispielsweise ist ein Vorprodukt zur Herstellung von (4-Isopropyl-cyclohexyl)-methanol (Mayol).
-
- Apparatur:
- ungeteilte Zelle mit 11 bipolaren Elektroden
- Anode:
- Graphit
- Elektrolyt:
- 174 g (1,06 mol) p-Isopropylbenzylmethylether
30 g Natriumbenzolsulfonat
2,80 kg Methanol - Kathode:
- Graphit
- Elektrolysetemperatur:
- 60°C
- Nach Beendigung der Elektrolyse wurde das Methanol bei Normaldruck abdestilliert, und das ausgefallene Leitsalz wurde abfiltriert. Nach der Vakuumdestillation erhielt man bei 90 %igem Umsatz 70 % p-Isopropylbenzaldehyddimethylacetal, was einer Ausbeute bezogen auf umgesetzte Ausgangsverbindung (Selektivität) von 78 % entsprach. Daneben wurden nur höhersiedende Produkte gefunden.
-
- Apparatur:
- ungeteilte Zelle mit 8 bipolaren Elektroden
- Anode:
- Graphit
- Elektrolyt:
- 450 g (3,31 mol) 2-Methylbenzylmethylether
18 g Natriumbenzolsulfonat
2,53 kg Methanol - Kathode:
- Graphit
- Elektrolysetemperatur:
- 40°C
- Nach Durchführung und Aufarbeitung wie in Beispiel 1 wurden 73 % 2-Methylbenzaldehyddimethylacetal erhalten (Selektivität 76 %). Daneben wurden nur höhersiedende Produkte gefunden.
-
- Apparatur:
- ungeteilte Zelle mit 11 bipolaren Elektroden
- Anode:
- Graphit
- Elektrolyt:
- 67 g (345 mmol) 4-(Methoxymethyl)phenylessigsäuremethylester
8 g Natriumbenzolsulfonat
700 g Methanol - Kathode:
- Graphit
- Elektrolysetemperatur:
- 25°C
-
- Apparatur:
- ungeteilte Zelle mit 11 bipolaren Elektroden
- Anode:
- Graphit
- Elektrolyt:
- 300 g (2,21 mol) 4-Methylbenzylmethylether
30 g Natriumbenzolsulfonat
2,67 kg Methanol - Kathode:
- Graphit
- Elektrolysetemperatur:
- 52°C
- Nach Durchführung und Aufarbeitung wie in Beispiel 1 wurden 80 % 4-Methylbenzaldehyddimethylacetal isoliert (Selektivität 88 %). Daneben wurden nur höhersiedende Produkte gefunden.
in Gegenwart eines Alkanols R¹-OH sowie in Gegenwart eines Hilfselektrolyten.
Die Elektrolyse wurde mit 2 F/mol 4-Isopropylbenzylmethylether durchgeführt. Der Elektrolyt wurde während der Elektrolyse mit 200 l/h durch die Zelle geleitet.
Die Elektrolyse wurde mit 3,8 F/mol 2-Methylbenzylmethylether durchgeführt.
Die Elektrolyse wurde mit 3,25 F/mol 4-(Methoxymethyl)phenylessigsäuremethylester durchgeführt. Der Elektrolyt wurde mit 20 l/h durch die Zelle geleitet. Nach Aufarbeitung wie in Beispiel 1 wurden 63 % 4-(Dimethoxymethyl)phenylessigsäuremethylester isoliert (Selektivität 72 %). Daneben wurden nur höhersiedende Produkte gefunden.
Die Elektrolyse wurde mit 2,5 F/mol 4-Methylbenzylmethylether durchgeführt.
Claims (4)
- Verfahren zur Herstellung von Benzaldehydacetalen der allgemeinen Formel I
- Verfahren nach Anspruch 1, dadurch gekennzeichnet, daß man die elektrochemische Oxidation in ungeteilten Durchflußzellen durchführt.
- Verfahren nach Anspruch 1, dadurch gekennzeichnet, daß man die elektrochemische Oxidation an Graphitelektroden durchführt.
- Verfahren nach Anspruch 1, dadurch gekennzeichnet, daß man als Alkanol R¹-OH Methanol oder Ethanol verwendet.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| DE4201544 | 1992-01-22 | ||
| DE4201544A DE4201544A1 (de) | 1992-01-22 | 1992-01-22 | Verfahren zur herstellung von benzaldehydacetalen |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| EP0554564A1 true EP0554564A1 (de) | 1993-08-11 |
Family
ID=6449963
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| EP92121990A Withdrawn EP0554564A1 (de) | 1992-01-22 | 1992-12-24 | Verfahren zur Herstellung von Benzaldehydacetalen |
Country Status (2)
| Country | Link |
|---|---|
| EP (1) | EP0554564A1 (de) |
| DE (1) | DE4201544A1 (de) |
Cited By (4)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009059944A1 (de) * | 2007-11-06 | 2009-05-14 | Basf Se | Elektrochemisches verfahren zur herstellung von benzaldehyddimethylacetalen |
| WO2010108874A1 (de) | 2009-03-27 | 2010-09-30 | Basf Se | Elektrochemisches verfahern zur herstellung von 3-tert.-butylbenzaldehyd-dimethylacetal |
| WO2011098432A2 (de) | 2010-02-12 | 2011-08-18 | Basf Se | Verfahren zur herstellung von 4-isopropylcyclohexylmethanol |
| US8889920B2 (en) | 2010-02-12 | 2014-11-18 | Basf Se | Process for preparing 4-isopropylcyclohexylmethanol |
Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2351932A1 (fr) * | 1976-05-21 | 1977-12-16 | Rhone Poulenc Ind | Procede d'oxydation anodique de methylbenzenes |
| EP0012240A2 (de) * | 1978-11-30 | 1980-06-25 | Bayer Ag | Verfahren zur Herstellung von gegebenenfalls substituierten Benzaldehyd-dialkylacetalen |
| DE2912058A1 (de) * | 1979-03-27 | 1980-10-09 | Bayer Ag | Verfahren zur herstellung von gegebenenfalls substituierten benzaldehyd- dialkylacetalen |
| EP0129795A2 (de) * | 1983-06-22 | 1985-01-02 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Benzaldehyddialkylacetalen |
| EP0152801A2 (de) * | 1984-02-03 | 1985-08-28 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Benzaldehyddialkylacetalen |
| EP0164705A2 (de) * | 1984-06-14 | 1985-12-18 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Phthalaldehydacetalen |
| EP0275489A1 (de) * | 1986-12-23 | 1988-07-27 | BASF Aktiengesellschaft | Neue Benzaldehydderivate, ihre Herstellung und Verwendung |
| EP0287954A2 (de) * | 1987-04-24 | 1988-10-26 | BASF Aktiengesellschaft | Neue Benzaldehyddialkylacetale, ihre Herstellung und Verwendung |
| EP0393668A2 (de) * | 1989-04-21 | 1990-10-24 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Benzaldehyddialkylacetalen und neue Benzaldehyddialkylacetale |
| EP0502372A1 (de) * | 1991-03-02 | 1992-09-09 | BASF Aktiengesellschaft | 4-tert-Alkyl-2-Methylbenzaldehyddialkylacetale |
-
1992
- 1992-01-22 DE DE4201544A patent/DE4201544A1/de not_active Withdrawn
- 1992-12-24 EP EP92121990A patent/EP0554564A1/de not_active Withdrawn
Patent Citations (10)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| FR2351932A1 (fr) * | 1976-05-21 | 1977-12-16 | Rhone Poulenc Ind | Procede d'oxydation anodique de methylbenzenes |
| EP0012240A2 (de) * | 1978-11-30 | 1980-06-25 | Bayer Ag | Verfahren zur Herstellung von gegebenenfalls substituierten Benzaldehyd-dialkylacetalen |
| DE2912058A1 (de) * | 1979-03-27 | 1980-10-09 | Bayer Ag | Verfahren zur herstellung von gegebenenfalls substituierten benzaldehyd- dialkylacetalen |
| EP0129795A2 (de) * | 1983-06-22 | 1985-01-02 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Benzaldehyddialkylacetalen |
| EP0152801A2 (de) * | 1984-02-03 | 1985-08-28 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Benzaldehyddialkylacetalen |
| EP0164705A2 (de) * | 1984-06-14 | 1985-12-18 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Phthalaldehydacetalen |
| EP0275489A1 (de) * | 1986-12-23 | 1988-07-27 | BASF Aktiengesellschaft | Neue Benzaldehydderivate, ihre Herstellung und Verwendung |
| EP0287954A2 (de) * | 1987-04-24 | 1988-10-26 | BASF Aktiengesellschaft | Neue Benzaldehyddialkylacetale, ihre Herstellung und Verwendung |
| EP0393668A2 (de) * | 1989-04-21 | 1990-10-24 | BASF Aktiengesellschaft | Verfahren zur Herstellung von Benzaldehyddialkylacetalen und neue Benzaldehyddialkylacetale |
| EP0502372A1 (de) * | 1991-03-02 | 1992-09-09 | BASF Aktiengesellschaft | 4-tert-Alkyl-2-Methylbenzaldehyddialkylacetale |
Cited By (6)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2009059944A1 (de) * | 2007-11-06 | 2009-05-14 | Basf Se | Elektrochemisches verfahren zur herstellung von benzaldehyddimethylacetalen |
| WO2010108874A1 (de) | 2009-03-27 | 2010-09-30 | Basf Se | Elektrochemisches verfahern zur herstellung von 3-tert.-butylbenzaldehyd-dimethylacetal |
| US8629304B2 (en) | 2009-03-27 | 2014-01-14 | Basf Se | Electrochemical method for producing 3-tert-butylbenzaldehyde dimethyl acetal |
| WO2011098432A2 (de) | 2010-02-12 | 2011-08-18 | Basf Se | Verfahren zur herstellung von 4-isopropylcyclohexylmethanol |
| CN102762774A (zh) * | 2010-02-12 | 2012-10-31 | 巴斯夫欧洲公司 | 生产4-异丙基环己基甲醇的方法 |
| US8889920B2 (en) | 2010-02-12 | 2014-11-18 | Basf Se | Process for preparing 4-isopropylcyclohexylmethanol |
Also Published As
| Publication number | Publication date |
|---|---|
| DE4201544A1 (de) | 1993-07-29 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| EP0072914B1 (de) | Verfahren zur Herstellung von alkylsubstituierten Benzaldehyden | |
| EP0129795B1 (de) | Verfahren zur Herstellung von Benzaldehyddialkylacetalen | |
| EP2411564A1 (de) | Elektrochemisches verfahern zur herstellung von 3-tert.-butylbenzaldehyd-dimethylacetal | |
| EP0554564A1 (de) | Verfahren zur Herstellung von Benzaldehydacetalen | |
| EP0522312A1 (de) | o-Phthaldialdehydtetraalkylacetale, ihre Herstellung und ihre Verwendung als Depotverbindung | |
| EP0638665B1 (de) | Verfahren zur Herstellung von Bezaldehyddialkylacetalen | |
| DE2855508A1 (de) | Verfahren zur herstellung von benzaldehyden | |
| EP0029995B1 (de) | Verfahren zur Herstellung von 4-tert. Butylbenzaldehyd | |
| EP1619273B1 (de) | Verfahren zur Herstellung von 2-Alkin-1-acetalen | |
| EP0502372B1 (de) | 4-tert-Alkyl-2-Methylbenzaldehyddialkylacetale | |
| EP0164705B1 (de) | Verfahren zur Herstellung von Phthalaldehydacetalen | |
| DE10043789A1 (de) | Verfahren zur Herstellung von Orthocarbonsäuretrialkylestern | |
| EP0525351B1 (de) | 2-Aryl-2,2-dialkoxyessigsäurealkylester, Verfahren zu ihrer Herstellung und ihre Verwendung zur Herstellung von Arylglyoxylsäureestern | |
| EP0581181B1 (de) | Verfahren zur Herstellung von 4-Dialkoxymethylpyrazolen | |
| EP0513577B1 (de) | Verfahren zur Herstellung von 1-Alkoxyisochromanen | |
| DE4407986A1 (de) | Verfahren zur Herstellung von o-Phthalaldehydtetraalkylacetalen | |
| EP0100498B1 (de) | Verfahren zur Herstellung von Dichlormilchsäure oder dem Nitril oder Amid der Dichlormilchsäure | |
| EP0179377B1 (de) | Verfahren zur Herstellung von 1-Alkoxyisochromanen und neue 1-Alkoxy-alkylisochromane | |
| DE68906589T2 (de) | Elektrochemische Synthese von 2-Aryl-Hydrochinonen. | |
| DE10146566A1 (de) | Verfahren zur Herstellung von Orthocarbonsäuretrialkylestern | |
| WO2003020679A1 (de) | Verfahren zur herstellung von oxo-cyclohexyl- oder oxo-cyclohexylenderivaten | |
| DE1961364A1 (de) | Verfahren zur Herstellung von substituierten Hydrazinen | |
| EP0621352A2 (de) | Verfahren zur Herstellung von Terephthalaldehydtetraalkylacetalen | |
| DE10143161A1 (de) | Verfahren zur Herstellung von Oxo-cyclohexyl-oder Oxo-cyclohexylenderivaten | |
| DE2923531A1 (de) | Verfahren zur herstellung von gegebenenfalls substituierten benzaldehyd- dialkylacetalen |
Legal Events
| Date | Code | Title | Description |
|---|---|---|---|
| PUAI | Public reference made under article 153(3) epc to a published international application that has entered the european phase |
Free format text: ORIGINAL CODE: 0009012 |
|
| AK | Designated contracting states |
Kind code of ref document: A1 Designated state(s): BE CH DE ES FR GB LI NL |
|
| 17P | Request for examination filed |
Effective date: 19930625 |
|
| 17Q | First examination report despatched |
Effective date: 19940531 |
|
| STAA | Information on the status of an ep patent application or granted ep patent |
Free format text: STATUS: THE APPLICATION HAS BEEN WITHDRAWN |
|
| 18W | Application withdrawn |
Withdrawal date: 19941217 |