ES2768718T3 - Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1 - Google Patents
Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1 Download PDFInfo
- Publication number
- ES2768718T3 ES2768718T3 ES15731260T ES15731260T ES2768718T3 ES 2768718 T3 ES2768718 T3 ES 2768718T3 ES 15731260 T ES15731260 T ES 15731260T ES 15731260 T ES15731260 T ES 15731260T ES 2768718 T3 ES2768718 T3 ES 2768718T3
- Authority
- ES
- Spain
- Prior art keywords
- compound
- formula
- group
- meoh
- gpbar1
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 102100025353 G-protein coupled bile acid receptor 1 Human genes 0.000 title claims description 58
- 101000857733 Homo sapiens G-protein coupled bile acid receptor 1 Proteins 0.000 title claims description 58
- IGRCWJPBLWGNPX-UHFFFAOYSA-N 3-(2-chlorophenyl)-n-(4-chlorophenyl)-n,5-dimethyl-1,2-oxazole-4-carboxamide Chemical compound C=1C=C(Cl)C=CC=1N(C)C(=O)C1=C(C)ON=C1C1=CC=CC=C1Cl IGRCWJPBLWGNPX-UHFFFAOYSA-N 0.000 title claims description 25
- 238000011282 treatment Methods 0.000 title claims description 25
- 230000001404 mediated effect Effects 0.000 title description 7
- 230000006806 disease prevention Effects 0.000 title description 3
- 150000001875 compounds Chemical class 0.000 claims abstract description 85
- OKKJLVBELUTLKV-UHFFFAOYSA-N Methanol Chemical compound OC OKKJLVBELUTLKV-UHFFFAOYSA-N 0.000 claims description 171
- 239000012448 Lithium borohydride Substances 0.000 claims description 20
- 238000000034 method Methods 0.000 claims description 18
- 230000009467 reduction Effects 0.000 claims description 15
- -1 alkyl lithium Chemical compound 0.000 claims description 13
- 239000000203 mixture Substances 0.000 claims description 12
- WQDUMFSSJAZKTM-UHFFFAOYSA-N Sodium methoxide Chemical compound [Na+].[O-]C WQDUMFSSJAZKTM-UHFFFAOYSA-N 0.000 claims description 9
- 125000002887 hydroxy group Chemical group [H]O* 0.000 claims description 9
- MZRVEZGGRBJDDB-UHFFFAOYSA-N N-Butyllithium Chemical compound [Li]CCCC MZRVEZGGRBJDDB-UHFFFAOYSA-N 0.000 claims description 8
- DQBAHTQWQZRMFH-CRPAWOMZSA-N (3R,5S,6S,7S,8S,9S,10S,13R,14S,17R)-6-ethyl-17-[(2R)-5-hydroxypentan-2-yl]-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthrene-3,7-diol Chemical compound CC[C@@H]1[C@H](O)[C@H]2[C@@H]3CC[C@H]([C@H](C)CCCO)[C@@]3(C)CC[C@@H]2[C@@]4(C)CC[C@@H](O)C[C@@H]14 DQBAHTQWQZRMFH-CRPAWOMZSA-N 0.000 claims description 7
- 239000012279 sodium borohydride Substances 0.000 claims description 7
- 229910000033 sodium borohydride Inorganic materials 0.000 claims description 7
- IKHGUXGNUITLKF-XPULMUKRSA-N acetaldehyde Chemical compound [14CH]([14CH3])=O IKHGUXGNUITLKF-XPULMUKRSA-N 0.000 claims description 6
- 208000030159 metabolic disease Diseases 0.000 claims description 6
- 206010028980 Neoplasm Diseases 0.000 claims description 5
- 201000011510 cancer Diseases 0.000 claims description 5
- 125000002915 carbonyl group Chemical group [*:2]C([*:1])=O 0.000 claims description 5
- 239000003814 drug Substances 0.000 claims description 5
- 208000017169 kidney disease Diseases 0.000 claims description 5
- 208000019423 liver disease Diseases 0.000 claims description 5
- 201000001320 Atherosclerosis Diseases 0.000 claims description 4
- 208000024172 Cardiovascular disease Diseases 0.000 claims description 4
- 208000018522 Gastrointestinal disease Diseases 0.000 claims description 4
- 238000006345 epimerization reaction Methods 0.000 claims description 4
- 208000027866 inflammatory disease Diseases 0.000 claims description 4
- 230000002265 prevention Effects 0.000 claims description 4
- 230000008569 process Effects 0.000 claims description 4
- 208000035473 Communicable disease Diseases 0.000 claims description 3
- 208000012902 Nervous system disease Diseases 0.000 claims description 3
- 208000025966 Neurological disease Diseases 0.000 claims description 3
- 238000005882 aldol condensation reaction Methods 0.000 claims description 3
- 238000009903 catalytic hydrogenation reaction Methods 0.000 claims description 3
- 230000007062 hydrolysis Effects 0.000 claims description 3
- 238000006460 hydrolysis reaction Methods 0.000 claims description 3
- 201000006370 kidney failure Diseases 0.000 claims description 3
- 125000003668 acetyloxy group Chemical group [H]C([H])([H])C(=O)O[*] 0.000 claims description 2
- 230000002757 inflammatory effect Effects 0.000 claims description 2
- 229910052744 lithium Inorganic materials 0.000 claims description 2
- 229910052698 phosphorus Inorganic materials 0.000 claims description 2
- 125000004492 methyl ester group Chemical group 0.000 claims 2
- 239000004615 ingredient Substances 0.000 claims 1
- 125000000896 monocarboxylic acid group Chemical group 0.000 claims 1
- 239000008194 pharmaceutical composition Substances 0.000 claims 1
- OKKJLVBELUTLKV-MZCSYVLQSA-N Deuterated methanol Chemical compound [2H]OC([2H])([2H])[2H] OKKJLVBELUTLKV-MZCSYVLQSA-N 0.000 description 62
- 239000002904 solvent Substances 0.000 description 42
- 229940030980 inova Drugs 0.000 description 39
- 239000000243 solution Substances 0.000 description 30
- ZMANZCXQSJIPKH-UHFFFAOYSA-N Triethylamine Chemical compound CCN(CC)CC ZMANZCXQSJIPKH-UHFFFAOYSA-N 0.000 description 28
- 102100038495 Bile acid receptor Human genes 0.000 description 27
- 101000603876 Homo sapiens Bile acid receptor Proteins 0.000 description 27
- 238000002360 preparation method Methods 0.000 description 27
- YMWUJEATGCHHMB-UHFFFAOYSA-N Dichloromethane Chemical compound ClCCl YMWUJEATGCHHMB-UHFFFAOYSA-N 0.000 description 25
- XEKOWRVHYACXOJ-UHFFFAOYSA-N Ethyl acetate Chemical compound CCOC(C)=O XEKOWRVHYACXOJ-UHFFFAOYSA-N 0.000 description 23
- 238000005481 NMR spectroscopy Methods 0.000 description 22
- 238000000746 purification Methods 0.000 description 20
- 238000001644 13C nuclear magnetic resonance spectroscopy Methods 0.000 description 19
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 description 19
- 230000000694 effects Effects 0.000 description 16
- HYCMOIGNYNCMRH-APIYUPOTSA-N (3R,5S,6R,7R,8S,9S,10S,13R,14S,17R)-6-ethyl-17-[(2R)-4-hydroxybutan-2-yl]-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1H-cyclopenta[a]phenanthrene-3,7-diol Chemical compound CC[C@H]1[C@@H](O)[C@H]2[C@@H]3CC[C@H]([C@H](C)CCO)[C@@]3(C)CC[C@@H]2[C@@]4(C)CC[C@@H](O)C[C@@H]14 HYCMOIGNYNCMRH-APIYUPOTSA-N 0.000 description 15
- 210000004027 cell Anatomy 0.000 description 15
- 150000004702 methyl esters Chemical group 0.000 description 15
- VLKZOEOYAKHREP-UHFFFAOYSA-N n-Hexane Chemical compound CCCCCC VLKZOEOYAKHREP-UHFFFAOYSA-N 0.000 description 14
- 239000003613 bile acid Substances 0.000 description 13
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Substances O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 description 13
- JUJWROOIHBZHMG-UHFFFAOYSA-N Pyridine Chemical compound C1=CC=NC=C1 JUJWROOIHBZHMG-UHFFFAOYSA-N 0.000 description 12
- 230000015572 biosynthetic process Effects 0.000 description 12
- 229910052938 sodium sulfate Inorganic materials 0.000 description 12
- RUDATBOHQWOJDD-UHFFFAOYSA-N (3beta,5beta,7alpha)-3,7-Dihydroxycholan-24-oic acid Natural products OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)CC2 RUDATBOHQWOJDD-UHFFFAOYSA-N 0.000 description 11
- 238000004128 high performance liquid chromatography Methods 0.000 description 11
- 238000003786 synthesis reaction Methods 0.000 description 11
- 239000003480 eluent Substances 0.000 description 10
- QAEDZJGFFMLHHQ-UHFFFAOYSA-N trifluoroacetic anhydride Chemical compound FC(F)(F)C(=O)OC(=O)C(F)(F)F QAEDZJGFFMLHHQ-UHFFFAOYSA-N 0.000 description 10
- OCKGFTQIICXDQW-ZEQRLZLVSA-N 5-[(1r)-1-hydroxy-2-[4-[(2r)-2-hydroxy-2-(4-methyl-1-oxo-3h-2-benzofuran-5-yl)ethyl]piperazin-1-yl]ethyl]-4-methyl-3h-2-benzofuran-1-one Chemical compound C1=C2C(=O)OCC2=C(C)C([C@@H](O)CN2CCN(CC2)C[C@H](O)C2=CC=C3C(=O)OCC3=C2C)=C1 OCKGFTQIICXDQW-ZEQRLZLVSA-N 0.000 description 9
- WFDIJRYMOXRFFG-UHFFFAOYSA-N Acetic anhydride Chemical compound CC(=O)OC(C)=O WFDIJRYMOXRFFG-UHFFFAOYSA-N 0.000 description 9
- 241000699670 Mus sp. Species 0.000 description 9
- 208000003251 Pruritus Diseases 0.000 description 9
- VYPSYNLAJGMNEJ-UHFFFAOYSA-N Silicium dioxide Chemical compound O=[Si]=O VYPSYNLAJGMNEJ-UHFFFAOYSA-N 0.000 description 9
- KXGVEGMKQFWNSR-UHFFFAOYSA-N deoxycholic acid Natural products C1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)C(O)C2 KXGVEGMKQFWNSR-UHFFFAOYSA-N 0.000 description 9
- 239000000543 intermediate Substances 0.000 description 9
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical compound [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 description 8
- ZMXDDKWLCZADIW-UHFFFAOYSA-N N,N-Dimethylformamide Chemical compound CN(C)C=O ZMXDDKWLCZADIW-UHFFFAOYSA-N 0.000 description 8
- 239000007832 Na2SO4 Substances 0.000 description 8
- PMZURENOXWZQFD-UHFFFAOYSA-L Sodium Sulfate Chemical compound [Na+].[Na+].[O-]S([O-])(=O)=O PMZURENOXWZQFD-UHFFFAOYSA-L 0.000 description 8
- UIIMBOGNXHQVGW-UHFFFAOYSA-M Sodium bicarbonate Chemical class [Na+].OC([O-])=O UIIMBOGNXHQVGW-UHFFFAOYSA-M 0.000 description 8
- RUDATBOHQWOJDD-BSWAIDMHSA-N chenodeoxycholic acid Chemical compound C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)CC1 RUDATBOHQWOJDD-BSWAIDMHSA-N 0.000 description 8
- 229960001091 chenodeoxycholic acid Drugs 0.000 description 8
- IAZDPXIOMUYVGZ-UHFFFAOYSA-N dimethyl sulfoxide Natural products CS(C)=O IAZDPXIOMUYVGZ-UHFFFAOYSA-N 0.000 description 8
- 239000000741 silica gel Substances 0.000 description 8
- 229910002027 silica gel Inorganic materials 0.000 description 8
- 235000011152 sodium sulphate Nutrition 0.000 description 8
- 241001465754 Metazoa Species 0.000 description 7
- KXGVEGMKQFWNSR-LLQZFEROSA-N deoxycholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 KXGVEGMKQFWNSR-LLQZFEROSA-N 0.000 description 7
- 229960003964 deoxycholic acid Drugs 0.000 description 7
- 235000019439 ethyl acetate Nutrition 0.000 description 7
- 230000007803 itching Effects 0.000 description 7
- QBYUNVOYXHFVKC-GBURMNQMSA-N taurolithocholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(=O)NCCS(O)(=O)=O)C)[C@@]2(C)CC1 QBYUNVOYXHFVKC-GBURMNQMSA-N 0.000 description 7
- OISVCGZHLKNMSJ-UHFFFAOYSA-N 2,6-dimethylpyridine Chemical compound CC1=CC=CC(C)=N1 OISVCGZHLKNMSJ-UHFFFAOYSA-N 0.000 description 6
- 206010008635 Cholestasis Diseases 0.000 description 6
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 description 6
- 238000006243 chemical reaction Methods 0.000 description 6
- 239000003795 chemical substances by application Substances 0.000 description 6
- 230000007870 cholestasis Effects 0.000 description 6
- 231100000359 cholestasis Toxicity 0.000 description 6
- 208000037265 diseases, disorders, signs and symptoms Diseases 0.000 description 6
- 210000004185 liver Anatomy 0.000 description 6
- UMJSCPRVCHMLSP-UHFFFAOYSA-N pyridine Natural products COC1=CC=CN=C1 UMJSCPRVCHMLSP-UHFFFAOYSA-N 0.000 description 6
- LPXPTNMVRIOKMN-UHFFFAOYSA-M sodium nitrite Chemical compound [Na+].[O-]N=O LPXPTNMVRIOKMN-UHFFFAOYSA-M 0.000 description 6
- HSINOMROUCMIEA-FGVHQWLLSA-N (2s,4r)-4-[(3r,5s,6r,7r,8s,9s,10s,13r,14s,17r)-6-ethyl-3,7-dihydroxy-10,13-dimethyl-2,3,4,5,6,7,8,9,11,12,14,15,16,17-tetradecahydro-1h-cyclopenta[a]phenanthren-17-yl]-2-methylpentanoic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)C[C@H](C)C(O)=O)CC[C@H]21 HSINOMROUCMIEA-FGVHQWLLSA-N 0.000 description 5
- JBDOSUUXMYMWQH-UHFFFAOYSA-N 1-naphthyl isothiocyanate Chemical compound C1=CC=C2C(N=C=S)=CC=CC2=C1 JBDOSUUXMYMWQH-UHFFFAOYSA-N 0.000 description 5
- GNFTZDOKVXKIBK-UHFFFAOYSA-N 3-(2-methoxyethoxy)benzohydrazide Chemical compound COCCOC1=CC=CC(C(=O)NN)=C1 GNFTZDOKVXKIBK-UHFFFAOYSA-N 0.000 description 5
- 208000008439 Biliary Liver Cirrhosis Diseases 0.000 description 5
- 208000033222 Biliary cirrhosis primary Diseases 0.000 description 5
- 0 C[C@](CCCO)[C@@](CC1)[C@]2(C)C1C1[C@@](*)C[C@@](C[C@](*)CC3)[C@@]3(C)C1CC2 Chemical compound C[C@](CCCO)[C@@](CC1)[C@]2(C)C1C1[C@@](*)C[C@@](C[C@](*)CC3)[C@@]3(C)C1CC2 0.000 description 5
- BDAGIHXWWSANSR-UHFFFAOYSA-N Formic acid Chemical compound OC=O BDAGIHXWWSANSR-UHFFFAOYSA-N 0.000 description 5
- 208000012654 Primary biliary cholangitis Diseases 0.000 description 5
- 230000001476 alcoholic effect Effects 0.000 description 5
- 239000012267 brine Substances 0.000 description 5
- IJOOHPMOJXWVHK-UHFFFAOYSA-N chlorotrimethylsilane Chemical compound C[Si](C)(C)Cl IJOOHPMOJXWVHK-UHFFFAOYSA-N 0.000 description 5
- 230000001684 chronic effect Effects 0.000 description 5
- 229940121360 farnesoid X receptor (fxr) agonists Drugs 0.000 description 5
- 235000019253 formic acid Nutrition 0.000 description 5
- 230000006870 function Effects 0.000 description 5
- SMEROWZSTRWXGI-HVATVPOCSA-N lithocholic acid Chemical compound C([C@H]1CC2)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)CC1 SMEROWZSTRWXGI-HVATVPOCSA-N 0.000 description 5
- 238000004519 manufacturing process Methods 0.000 description 5
- 238000006748 scratching Methods 0.000 description 5
- 230000002393 scratching effect Effects 0.000 description 5
- HPALAKNZSZLMCH-UHFFFAOYSA-M sodium;chloride;hydrate Chemical compound O.[Na+].[Cl-] HPALAKNZSZLMCH-UHFFFAOYSA-M 0.000 description 5
- 239000007787 solid Substances 0.000 description 5
- JOXIMZWYDAKGHI-UHFFFAOYSA-N toluene-4-sulfonic acid Chemical compound CC1=CC=C(S(O)(=O)=O)C=C1 JOXIMZWYDAKGHI-UHFFFAOYSA-N 0.000 description 5
- 239000013598 vector Substances 0.000 description 5
- YYROPELSRYBVMQ-UHFFFAOYSA-N 4-toluenesulfonyl chloride Chemical compound CC1=CC=C(S(Cl)(=O)=O)C=C1 YYROPELSRYBVMQ-UHFFFAOYSA-N 0.000 description 4
- 108091003079 Bovine Serum Albumin Proteins 0.000 description 4
- FGUUSXIOTUKUDN-IBGZPJMESA-N C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 Chemical compound C1(=CC=CC=C1)N1C2=C(NC([C@H](C1)NC=1OC(=NN=1)C1=CC=CC=C1)=O)C=CC=C2 FGUUSXIOTUKUDN-IBGZPJMESA-N 0.000 description 4
- 102100032373 Coiled-coil domain-containing protein 85B Human genes 0.000 description 4
- 206010010356 Congenital anomaly Diseases 0.000 description 4
- 101000868814 Homo sapiens Coiled-coil domain-containing protein 85B Proteins 0.000 description 4
- CSNNHWWHGAXBCP-UHFFFAOYSA-L Magnesium sulfate Chemical compound [Mg+2].[O-][S+2]([O-])([O-])[O-] CSNNHWWHGAXBCP-UHFFFAOYSA-L 0.000 description 4
- 239000000556 agonist Substances 0.000 description 4
- 230000001587 cholestatic effect Effects 0.000 description 4
- 230000008878 coupling Effects 0.000 description 4
- 238000010168 coupling process Methods 0.000 description 4
- 238000005859 coupling reaction Methods 0.000 description 4
- LVTYICIALWPMFW-UHFFFAOYSA-N diisopropanolamine Chemical compound CC(O)CNCC(C)O LVTYICIALWPMFW-UHFFFAOYSA-N 0.000 description 4
- 201000010099 disease Diseases 0.000 description 4
- 238000001704 evaporation Methods 0.000 description 4
- 230000008020 evaporation Effects 0.000 description 4
- 238000002474 experimental method Methods 0.000 description 4
- 239000012091 fetal bovine serum Substances 0.000 description 4
- 238000005984 hydrogenation reaction Methods 0.000 description 4
- 239000003446 ligand Substances 0.000 description 4
- AMXOYNBUYSYVKV-UHFFFAOYSA-M lithium bromide Chemical compound [Li+].[Br-] AMXOYNBUYSYVKV-UHFFFAOYSA-M 0.000 description 4
- DLEDOFVPSDKWEF-UHFFFAOYSA-N lithium butane Chemical compound [Li+].CCC[CH2-] DLEDOFVPSDKWEF-UHFFFAOYSA-N 0.000 description 4
- 238000002156 mixing Methods 0.000 description 4
- 208000008338 non-alcoholic fatty liver disease Diseases 0.000 description 4
- 239000012074 organic phase Substances 0.000 description 4
- CTSLXHKWHWQRSH-UHFFFAOYSA-N oxalyl chloride Chemical compound ClC(=O)C(Cl)=O CTSLXHKWHWQRSH-UHFFFAOYSA-N 0.000 description 4
- 230000023603 positive regulation of transcription initiation, DNA-dependent Effects 0.000 description 4
- 238000001228 spectrum Methods 0.000 description 4
- UCSJYZPVAKXKNQ-HZYVHMACSA-N streptomycin Chemical compound CN[C@H]1[C@H](O)[C@@H](O)[C@H](CO)O[C@H]1O[C@@H]1[C@](C=O)(O)[C@H](C)O[C@H]1O[C@@H]1[C@@H](NC(N)=N)[C@H](O)[C@@H](NC(N)=N)[C@H](O)[C@H]1O UCSJYZPVAKXKNQ-HZYVHMACSA-N 0.000 description 4
- RUDATBOHQWOJDD-UZVSRGJWSA-N ursodeoxycholic acid Chemical compound C([C@H]1C[C@@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)CC1 RUDATBOHQWOJDD-UZVSRGJWSA-N 0.000 description 4
- 102000002260 Alkaline Phosphatase Human genes 0.000 description 3
- 108020004774 Alkaline Phosphatase Proteins 0.000 description 3
- ZHGNHOOVYPHPNJ-UHFFFAOYSA-N Amigdalin Chemical compound FC(F)(F)C(=O)OCC1OC(OCC2OC(OC(C#N)C3=CC=CC=C3)C(OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C2OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C(OC(=O)C(F)(F)F)C1OC(=O)C(F)(F)F ZHGNHOOVYPHPNJ-UHFFFAOYSA-N 0.000 description 3
- OJRUSAPKCPIVBY-KQYNXXCUSA-N C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N Chemical compound C1=NC2=C(N=C(N=C2N1[C@H]3[C@@H]([C@@H]([C@H](O3)COP(=O)(CP(=O)(O)O)O)O)O)I)N OJRUSAPKCPIVBY-KQYNXXCUSA-N 0.000 description 3
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 3
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 description 3
- BFPYWIDHMRZLRN-SLHNCBLASA-N Ethinyl estradiol Chemical compound OC1=CC=C2[C@H]3CC[C@](C)([C@](CC4)(O)C#C)[C@@H]4[C@@H]3CCC2=C1 BFPYWIDHMRZLRN-SLHNCBLASA-N 0.000 description 3
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 3
- 206010020772 Hypertension Diseases 0.000 description 3
- 108060001084 Luciferase Proteins 0.000 description 3
- 239000005089 Luciferase Substances 0.000 description 3
- 208000030831 Peripheral arterial occlusive disease Diseases 0.000 description 3
- 241000242739 Renilla Species 0.000 description 3
- 208000006011 Stroke Diseases 0.000 description 3
- 230000004913 activation Effects 0.000 description 3
- 239000000538 analytical sample Substances 0.000 description 3
- 238000003556 assay Methods 0.000 description 3
- 229940125758 compound 15 Drugs 0.000 description 3
- 238000010511 deprotection reaction Methods 0.000 description 3
- UAOMVDZJSHZZME-UHFFFAOYSA-N diisopropylamine Chemical compound CC(C)NC(C)C UAOMVDZJSHZZME-UHFFFAOYSA-N 0.000 description 3
- 230000009977 dual effect Effects 0.000 description 3
- OAYLNYINCPYISS-UHFFFAOYSA-N ethyl acetate;hexane Chemical compound CCCCCC.CCOC(C)=O OAYLNYINCPYISS-UHFFFAOYSA-N 0.000 description 3
- 238000003818 flash chromatography Methods 0.000 description 3
- CBOIHMRHGLHBPB-UHFFFAOYSA-N hydroxymethyl Chemical group O[CH2] CBOIHMRHGLHBPB-UHFFFAOYSA-N 0.000 description 3
- 208000015181 infectious disease Diseases 0.000 description 3
- 210000000936 intestine Anatomy 0.000 description 3
- ZXERDUOLZKYMJM-ZWECCWDJSA-N obeticholic acid Chemical compound C([C@@]12C)C[C@@H](O)C[C@H]1[C@@H](CC)[C@@H](O)[C@@H]1[C@@H]2CC[C@]2(C)[C@@H]([C@H](C)CCC(O)=O)CC[C@H]21 ZXERDUOLZKYMJM-ZWECCWDJSA-N 0.000 description 3
- VLTRZXGMWDSKGL-UHFFFAOYSA-N perchloric acid Chemical compound OCl(=O)(=O)=O VLTRZXGMWDSKGL-UHFFFAOYSA-N 0.000 description 3
- 108090000623 proteins and genes Proteins 0.000 description 3
- 230000002829 reductive effect Effects 0.000 description 3
- 238000010992 reflux Methods 0.000 description 3
- 235000010288 sodium nitrite Nutrition 0.000 description 3
- 239000007858 starting material Substances 0.000 description 3
- 230000019635 sulfation Effects 0.000 description 3
- 238000005670 sulfation reaction Methods 0.000 description 3
- 238000012360 testing method Methods 0.000 description 3
- DTQVDTLACAAQTR-UHFFFAOYSA-N trifluoroacetic acid Substances OC(=O)C(F)(F)F DTQVDTLACAAQTR-UHFFFAOYSA-N 0.000 description 3
- GHYOCDFICYLMRF-UTIIJYGPSA-N (2S,3R)-N-[(2S)-3-(cyclopenten-1-yl)-1-[(2R)-2-methyloxiran-2-yl]-1-oxopropan-2-yl]-3-hydroxy-3-(4-methoxyphenyl)-2-[[(2S)-2-[(2-morpholin-4-ylacetyl)amino]propanoyl]amino]propanamide Chemical compound C1(=CCCC1)C[C@@H](C(=O)[C@@]1(OC1)C)NC([C@H]([C@@H](C1=CC=C(C=C1)OC)O)NC([C@H](C)NC(CN1CCOCC1)=O)=O)=O GHYOCDFICYLMRF-UTIIJYGPSA-N 0.000 description 2
- QFLWZFQWSBQYPS-AWRAUJHKSA-N (3S)-3-[[(2S)-2-[[(2S)-2-[5-[(3aS,6aR)-2-oxo-1,3,3a,4,6,6a-hexahydrothieno[3,4-d]imidazol-4-yl]pentanoylamino]-3-methylbutanoyl]amino]-3-(4-hydroxyphenyl)propanoyl]amino]-4-[1-bis(4-chlorophenoxy)phosphorylbutylamino]-4-oxobutanoic acid Chemical compound CCCC(NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](Cc1ccc(O)cc1)NC(=O)[C@@H](NC(=O)CCCCC1SC[C@@H]2NC(=O)N[C@H]12)C(C)C)P(=O)(Oc1ccc(Cl)cc1)Oc1ccc(Cl)cc1 QFLWZFQWSBQYPS-AWRAUJHKSA-N 0.000 description 2
- BHQCQFFYRZLCQQ-UHFFFAOYSA-N (3alpha,5alpha,7alpha,12alpha)-3,7,12-trihydroxy-cholan-24-oic acid Natural products OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(O)=O)C)C1(C)C(O)C2 BHQCQFFYRZLCQQ-UHFFFAOYSA-N 0.000 description 2
- UNILWMWFPHPYOR-KXEYIPSPSA-M 1-[6-[2-[3-[3-[3-[2-[2-[3-[[2-[2-[[(2r)-1-[[2-[[(2r)-1-[3-[2-[2-[3-[[2-(2-amino-2-oxoethoxy)acetyl]amino]propoxy]ethoxy]ethoxy]propylamino]-3-hydroxy-1-oxopropan-2-yl]amino]-2-oxoethyl]amino]-3-[(2r)-2,3-di(hexadecanoyloxy)propyl]sulfanyl-1-oxopropan-2-yl Chemical compound O=C1C(SCCC(=O)NCCCOCCOCCOCCCNC(=O)COCC(=O)N[C@@H](CSC[C@@H](COC(=O)CCCCCCCCCCCCCCC)OC(=O)CCCCCCCCCCCCCCC)C(=O)NCC(=O)N[C@H](CO)C(=O)NCCCOCCOCCOCCCNC(=O)COCC(N)=O)CC(=O)N1CCNC(=O)CCCCCN\1C2=CC=C(S([O-])(=O)=O)C=C2CC/1=C/C=C/C=C/C1=[N+](CC)C2=CC=C(S([O-])(=O)=O)C=C2C1 UNILWMWFPHPYOR-KXEYIPSPSA-M 0.000 description 2
- XWKFPIODWVPXLX-UHFFFAOYSA-N 2-methyl-5-methylpyridine Natural products CC1=CC=C(C)N=C1 XWKFPIODWVPXLX-UHFFFAOYSA-N 0.000 description 2
- HSJKGGMUJITCBW-UHFFFAOYSA-N 3-hydroxybutanal Chemical compound CC(O)CC=O HSJKGGMUJITCBW-UHFFFAOYSA-N 0.000 description 2
- IKHGUXGNUITLKF-UHFFFAOYSA-N Acetaldehyde Chemical compound CC=O IKHGUXGNUITLKF-UHFFFAOYSA-N 0.000 description 2
- 102000004625 Aspartate Aminotransferases Human genes 0.000 description 2
- 108010003415 Aspartate Aminotransferases Proteins 0.000 description 2
- IJGRMHOSHXDMSA-UHFFFAOYSA-N Atomic nitrogen Chemical compound N#N IJGRMHOSHXDMSA-UHFFFAOYSA-N 0.000 description 2
- BPYKTIZUTYGOLE-IFADSCNNSA-N Bilirubin Chemical compound N1C(=O)C(C)=C(C=C)\C1=C\C1=C(C)C(CCC(O)=O)=C(CC2=C(C(C)=C(\C=C/3C(=C(C=C)C(=O)N\3)C)N2)CCC(O)=O)N1 BPYKTIZUTYGOLE-IFADSCNNSA-N 0.000 description 2
- 101100101413 Caenorhabditis elegans ubh-4 gene Proteins 0.000 description 2
- 102000000844 Cell Surface Receptors Human genes 0.000 description 2
- 108010001857 Cell Surface Receptors Proteins 0.000 description 2
- 239000004380 Cholic acid Substances 0.000 description 2
- DHMQDGOQFOQNFH-UHFFFAOYSA-N Glycine Chemical compound NCC(O)=O DHMQDGOQFOQNFH-UHFFFAOYSA-N 0.000 description 2
- 208000022559 Inflammatory bowel disease Diseases 0.000 description 2
- ZDXPYRJPNDTMRX-VKHMYHEASA-N L-glutamine Chemical compound OC(=O)[C@@H](N)CCC(N)=O ZDXPYRJPNDTMRX-VKHMYHEASA-N 0.000 description 2
- 229930182816 L-glutamine Natural products 0.000 description 2
- WMFOQBRAJBCJND-UHFFFAOYSA-M Lithium hydroxide Chemical compound [Li+].[OH-] WMFOQBRAJBCJND-UHFFFAOYSA-M 0.000 description 2
- 108020005497 Nuclear hormone receptor Proteins 0.000 description 2
- 208000012868 Overgrowth Diseases 0.000 description 2
- 229930182555 Penicillin Natural products 0.000 description 2
- JGSARLDLIJGVTE-MBNYWOFBSA-N Penicillin G Chemical compound N([C@H]1[C@H]2SC([C@@H](N2C1=O)C(O)=O)(C)C)C(=O)CC1=CC=CC=C1 JGSARLDLIJGVTE-MBNYWOFBSA-N 0.000 description 2
- 208000005764 Peripheral Arterial Disease Diseases 0.000 description 2
- 208000018262 Peripheral vascular disease Diseases 0.000 description 2
- 241000251745 Petromyzon marinus Species 0.000 description 2
- 108700008625 Reporter Genes Proteins 0.000 description 2
- 108091027981 Response element Proteins 0.000 description 2
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical class [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 description 2
- 102100036325 Sterol 26-hydroxylase, mitochondrial Human genes 0.000 description 2
- 241000700605 Viruses Species 0.000 description 2
- WLLIXJBWWFGEHT-UHFFFAOYSA-N [tert-butyl(dimethyl)silyl] trifluoromethanesulfonate Chemical compound CC(C)(C)[Si](C)(C)OS(=O)(=O)C(F)(F)F WLLIXJBWWFGEHT-UHFFFAOYSA-N 0.000 description 2
- 230000021736 acetylation Effects 0.000 description 2
- 238000006640 acetylation reaction Methods 0.000 description 2
- 239000002253 acid Substances 0.000 description 2
- 210000000577 adipose tissue Anatomy 0.000 description 2
- 210000004404 adrenal cortex Anatomy 0.000 description 2
- 238000006668 aldol addition reaction Methods 0.000 description 2
- 230000029936 alkylation Effects 0.000 description 2
- 238000005804 alkylation reaction Methods 0.000 description 2
- 150000003863 ammonium salts Chemical class 0.000 description 2
- 239000005557 antagonist Substances 0.000 description 2
- 239000008346 aqueous phase Substances 0.000 description 2
- 230000001580 bacterial effect Effects 0.000 description 2
- 125000003178 carboxy group Chemical group [H]OC(*)=O 0.000 description 2
- 230000015556 catabolic process Effects 0.000 description 2
- 239000003054 catalyst Substances 0.000 description 2
- 208000001088 cerebrotendinous xanthomatosis Diseases 0.000 description 2
- 229920001429 chelating resin Polymers 0.000 description 2
- HVYWMOMLDIMFJA-DPAQBDIFSA-N cholesterol Chemical group C1C=C2C[C@@H](O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCCC(C)C)[C@@]1(C)CC2 HVYWMOMLDIMFJA-DPAQBDIFSA-N 0.000 description 2
- BHQCQFFYRZLCQQ-OELDTZBJSA-N cholic acid Chemical compound C([C@H]1C[C@H]2O)[C@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@@H](CCC(O)=O)C)[C@@]2(C)[C@@H](O)C1 BHQCQFFYRZLCQQ-OELDTZBJSA-N 0.000 description 2
- 229960002471 cholic acid Drugs 0.000 description 2
- 235000019416 cholic acid Nutrition 0.000 description 2
- 239000012230 colorless oil Substances 0.000 description 2
- 229940125797 compound 12 Drugs 0.000 description 2
- 229940126214 compound 3 Drugs 0.000 description 2
- 238000006731 degradation reaction Methods 0.000 description 2
- 208000035475 disorder Diseases 0.000 description 2
- 229940079593 drug Drugs 0.000 description 2
- 229940011871 estrogen Drugs 0.000 description 2
- 239000000262 estrogen Substances 0.000 description 2
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 description 2
- 230000001939 inductive effect Effects 0.000 description 2
- 238000002347 injection Methods 0.000 description 2
- 239000007924 injection Substances 0.000 description 2
- 230000003834 intracellular effect Effects 0.000 description 2
- 208000002551 irritable bowel syndrome Diseases 0.000 description 2
- 150000002632 lipids Chemical class 0.000 description 2
- XGZVUEUWXADBQD-UHFFFAOYSA-L lithium carbonate Chemical compound [Li+].[Li+].[O-]C([O-])=O XGZVUEUWXADBQD-UHFFFAOYSA-L 0.000 description 2
- 229910052808 lithium carbonate Inorganic materials 0.000 description 2
- 229910052943 magnesium sulfate Inorganic materials 0.000 description 2
- 235000019341 magnesium sulphate Nutrition 0.000 description 2
- 210000003205 muscle Anatomy 0.000 description 2
- YYHPEVZFVMVUNJ-UHFFFAOYSA-N n,n-diethylethanamine;sulfur trioxide Chemical compound O=S(=O)=O.CCN(CC)CC YYHPEVZFVMVUNJ-UHFFFAOYSA-N 0.000 description 2
- 206010053219 non-alcoholic steatohepatitis Diseases 0.000 description 2
- 102000006255 nuclear receptors Human genes 0.000 description 2
- 108020004017 nuclear receptors Proteins 0.000 description 2
- 229960001601 obeticholic acid Drugs 0.000 description 2
- 239000004006 olive oil Substances 0.000 description 2
- 235000008390 olive oil Nutrition 0.000 description 2
- 239000012044 organic layer Substances 0.000 description 2
- 229940049954 penicillin Drugs 0.000 description 2
- 229920001223 polyethylene glycol Polymers 0.000 description 2
- 239000000047 product Substances 0.000 description 2
- 125000006239 protecting group Chemical group 0.000 description 2
- 239000011541 reaction mixture Substances 0.000 description 2
- 102000005962 receptors Human genes 0.000 description 2
- 108020003175 receptors Proteins 0.000 description 2
- 229920006395 saturated elastomer Polymers 0.000 description 2
- 210000002966 serum Anatomy 0.000 description 2
- 235000017557 sodium bicarbonate Nutrition 0.000 description 2
- 229910000030 sodium bicarbonate Inorganic materials 0.000 description 2
- 159000000000 sodium salts Chemical class 0.000 description 2
- 230000002269 spontaneous effect Effects 0.000 description 2
- 150000003431 steroids Chemical class 0.000 description 2
- 229960005322 streptomycin Drugs 0.000 description 2
- XOAAWQZATWQOTB-UHFFFAOYSA-N taurine Chemical compound NCCS(O)(=O)=O XOAAWQZATWQOTB-UHFFFAOYSA-N 0.000 description 2
- 238000001890 transfection Methods 0.000 description 2
- 230000009466 transformation Effects 0.000 description 2
- 208000001072 type 2 diabetes mellitus Diseases 0.000 description 2
- ONBQEOIKXPHGMB-VBSBHUPXSA-N 1-[2-[(2s,3r,4s,5r)-3,4-dihydroxy-5-(hydroxymethyl)oxolan-2-yl]oxy-4,6-dihydroxyphenyl]-3-(4-hydroxyphenyl)propan-1-one Chemical compound O[C@@H]1[C@H](O)[C@@H](CO)O[C@H]1OC1=CC(O)=CC(O)=C1C(=O)CCC1=CC=C(O)C=C1 ONBQEOIKXPHGMB-VBSBHUPXSA-N 0.000 description 1
- QGJZLNKBHJESQX-UHFFFAOYSA-N 3-Epi-Betulin-Saeure Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C(=C)C)C5C4CCC3C21C QGJZLNKBHJESQX-UHFFFAOYSA-N 0.000 description 1
- CLOUCVRNYSHRCF-UHFFFAOYSA-N 3beta-Hydroxy-20(29)-Lupen-3,27-oic acid Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C(O)=O)CCC5(C)CCC(C(=C)C)C5C4CCC3C21C CLOUCVRNYSHRCF-UHFFFAOYSA-N 0.000 description 1
- MIJYXULNPSFWEK-GTOFXWBISA-N 3beta-hydroxyolean-12-en-28-oic acid Chemical compound C1C[C@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C(O)=O)CCC(C)(C)C[C@H]5C4=CC[C@@H]3[C@]21C MIJYXULNPSFWEK-GTOFXWBISA-N 0.000 description 1
- QSHQKIURKJITMZ-OBUPQJQESA-N 5β-cholane Chemical compound C([C@H]1CC2)CCC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@H]([C@H](C)CCC)[C@@]2(C)CC1 QSHQKIURKJITMZ-OBUPQJQESA-N 0.000 description 1
- 102100033350 ATP-dependent translocase ABCB1 Human genes 0.000 description 1
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 1
- 208000022309 Alcoholic Liver disease Diseases 0.000 description 1
- 206010002388 Angina unstable Diseases 0.000 description 1
- 206010003827 Autoimmune hepatitis Diseases 0.000 description 1
- 208000027496 Behcet disease Diseases 0.000 description 1
- 208000009137 Behcet syndrome Diseases 0.000 description 1
- DIZWSDNSTNAYHK-XGWVBXMLSA-N Betulinic acid Natural products CC(=C)[C@@H]1C[C@H]([C@H]2CC[C@]3(C)[C@H](CC[C@@H]4[C@@]5(C)CC[C@H](O)C(C)(C)[C@@H]5CC[C@@]34C)[C@@H]12)C(=O)O DIZWSDNSTNAYHK-XGWVBXMLSA-N 0.000 description 1
- 206010004593 Bile duct cancer Diseases 0.000 description 1
- 102100028282 Bile salt export pump Human genes 0.000 description 1
- KZMGYPLQYOPHEL-UHFFFAOYSA-N Boron trifluoride etherate Chemical compound FB(F)F.CCOCC KZMGYPLQYOPHEL-UHFFFAOYSA-N 0.000 description 1
- 206010006187 Breast cancer Diseases 0.000 description 1
- 208000026310 Breast neoplasm Diseases 0.000 description 1
- DQBAHTQWQZRMFH-UOVQWRRNSA-N CC[C@@H]([C@H](C[C@@H](CC1)O)[C@@]1(C)C(CC1)C2C(CC3)[C@@]1(C)[C@H]3[C@H](C)CCCO)[C@H]2O Chemical compound CC[C@@H]([C@H](C[C@@H](CC1)O)[C@@]1(C)C(CC1)C2C(CC3)[C@@]1(C)[C@H]3[C@H](C)CCCO)[C@H]2O DQBAHTQWQZRMFH-UOVQWRRNSA-N 0.000 description 1
- MVCNVEOJSIFSOO-ZRCHPSMRSA-N CC[C@@H]([C@H](C[C@@H](CC1)OC(C)=O)[C@@]1(C)C(CC1)C2C(CC3)[C@@]1(C)[C@H]3[C@H](C)CCC(OC)=O)C2=O Chemical compound CC[C@@H]([C@H](C[C@@H](CC1)OC(C)=O)[C@@]1(C)C(CC1)C2C(CC3)[C@@]1(C)[C@H]3[C@H](C)CCC(OC)=O)C2=O MVCNVEOJSIFSOO-ZRCHPSMRSA-N 0.000 description 1
- BPOATSVWPBTFPF-COCBOFATSA-N CC[C@@](CCC1[C@@](C)(CC[C@H](CC=N)O)CC2)([C@H](CC3)[C@H](C)CCC(OC)=O)C3C1C2O Chemical compound CC[C@@](CCC1[C@@](C)(CC[C@H](CC=N)O)CC2)([C@H](CC3)[C@H](C)CCC(OC)=O)C3C1C2O BPOATSVWPBTFPF-COCBOFATSA-N 0.000 description 1
- IOBLILNCUSICGD-NXHNBZDPSA-N C[C@H](CCC(OC)=O)[C@@H](CC1)[C@@](C)(CCC2C(C)(CC[C@H](C3)OC(C)=O)C3C3)C1C2C3=O Chemical compound C[C@H](CCC(OC)=O)[C@@H](CC1)[C@@](C)(CCC2C(C)(CC[C@H](C3)OC(C)=O)C3C3)C1C2C3=O IOBLILNCUSICGD-NXHNBZDPSA-N 0.000 description 1
- PYHISIRPLRPHGM-QXRYKYLUSA-N C[C@H](CCC(OC)=O)[C@@H](CC1)[C@@](C)(CCC2[C@@](C)(CCCC3)[C@@H]3C3)C1C2C3=O Chemical compound C[C@H](CCC(OC)=O)[C@@H](CC1)[C@@](C)(CCC2[C@@](C)(CCCC3)[C@@H]3C3)C1C2C3=O PYHISIRPLRPHGM-QXRYKYLUSA-N 0.000 description 1
- GRQROVWZGGDYSW-KONPATMESA-N C[C@H](CCC(OC)=O)[C@@H](CC1)[C@@](C)(CCC2[C@@](C)(CC[C@H](C3)O)[C@@H]3C3)C1C2C3O Chemical compound C[C@H](CCC(OC)=O)[C@@H](CC1)[C@@](C)(CCC2[C@@](C)(CC[C@H](C3)O)[C@@H]3C3)C1C2C3O GRQROVWZGGDYSW-KONPATMESA-N 0.000 description 1
- YNHXRKRNVRYHAX-SEJMHNBNSA-N C[C@H](CCCCCO)[C@@H](CC1)[C@@](C)(CCC2[C@@](C)(CCCC3)C3C3)C1C2[C@H]3O Chemical compound C[C@H](CCCCCO)[C@@H](CC1)[C@@](C)(CCC2[C@@](C)(CCCC3)C3C3)C1C2[C@H]3O YNHXRKRNVRYHAX-SEJMHNBNSA-N 0.000 description 1
- UXVMQQNJUSDDNG-UHFFFAOYSA-L Calcium chloride Chemical compound [Cl-].[Cl-].[Ca+2] UXVMQQNJUSDDNG-UHFFFAOYSA-L 0.000 description 1
- 206010063209 Chronic allograft nephropathy Diseases 0.000 description 1
- 206010009900 Colitis ulcerative Diseases 0.000 description 1
- 206010009944 Colon cancer Diseases 0.000 description 1
- 208000001333 Colorectal Neoplasms Diseases 0.000 description 1
- 201000006306 Cor pulmonale Diseases 0.000 description 1
- 208000011231 Crohn disease Diseases 0.000 description 1
- 208000007342 Diabetic Nephropathies Diseases 0.000 description 1
- 208000032928 Dyslipidaemia Diseases 0.000 description 1
- JKLISIRFYWXLQG-UHFFFAOYSA-N Epioleonolsaeure Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C)(C)CC5C4CCC3C21C JKLISIRFYWXLQG-UHFFFAOYSA-N 0.000 description 1
- 208000001640 Fibromyalgia Diseases 0.000 description 1
- 102000003688 G-Protein-Coupled Receptors Human genes 0.000 description 1
- 108090000045 G-Protein-Coupled Receptors Proteins 0.000 description 1
- 101150021752 GPBAR1 gene Proteins 0.000 description 1
- 208000022461 Glomerular disease Diseases 0.000 description 1
- 206010018367 Glomerulonephritis chronic Diseases 0.000 description 1
- 102000051325 Glucagon Human genes 0.000 description 1
- 108060003199 Glucagon Proteins 0.000 description 1
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 description 1
- 239000004471 Glycine Substances 0.000 description 1
- 208000009329 Graft vs Host Disease Diseases 0.000 description 1
- 208000024815 Granulomatous liver disease Diseases 0.000 description 1
- 102000005623 HSP27 Heat-Shock Proteins Human genes 0.000 description 1
- 108010045100 HSP27 Heat-Shock Proteins Proteins 0.000 description 1
- 208000018565 Hemochromatosis Diseases 0.000 description 1
- 206010019799 Hepatitis viral Diseases 0.000 description 1
- 208000002972 Hepatolenticular Degeneration Diseases 0.000 description 1
- 101000978937 Homo sapiens Nuclear receptor subfamily 0 group B member 2 Proteins 0.000 description 1
- 101000610640 Homo sapiens U4/U6 small nuclear ribonucleoprotein Prp3 Proteins 0.000 description 1
- 241000725303 Human immunodeficiency virus Species 0.000 description 1
- 208000035150 Hypercholesterolemia Diseases 0.000 description 1
- 208000013016 Hypoglycemia Diseases 0.000 description 1
- 206010022489 Insulin Resistance Diseases 0.000 description 1
- 208000032382 Ischaemic stroke Diseases 0.000 description 1
- 229910010084 LiAlH4 Inorganic materials 0.000 description 1
- 208000017170 Lipid metabolism disease Diseases 0.000 description 1
- 206010067125 Liver injury Diseases 0.000 description 1
- 206010025476 Malabsorption Diseases 0.000 description 1
- 208000004155 Malabsorption Syndromes Diseases 0.000 description 1
- 108010047230 Member 1 Subfamily B ATP Binding Cassette Transporter Proteins 0.000 description 1
- 108010093662 Member 11 Subfamily B ATP Binding Cassette Transporter Proteins 0.000 description 1
- 208000001145 Metabolic Syndrome Diseases 0.000 description 1
- 241000699666 Mus <mouse, genus> Species 0.000 description 1
- 208000009525 Myocarditis Diseases 0.000 description 1
- 102100023172 Nuclear receptor subfamily 0 group B member 2 Human genes 0.000 description 1
- 208000008589 Obesity Diseases 0.000 description 1
- YBRJHZPWOMJYKQ-UHFFFAOYSA-N Oleanolic acid Natural products CC1(C)CC2C3=CCC4C5(C)CCC(O)C(C)(C)C5CCC4(C)C3(C)CCC2(C1)C(=O)O YBRJHZPWOMJYKQ-UHFFFAOYSA-N 0.000 description 1
- MIJYXULNPSFWEK-UHFFFAOYSA-N Oleanolinsaeure Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C)(C)CC5C4=CCC3C21C MIJYXULNPSFWEK-UHFFFAOYSA-N 0.000 description 1
- 206010033128 Ovarian cancer Diseases 0.000 description 1
- 206010061535 Ovarian neoplasm Diseases 0.000 description 1
- 206010061902 Pancreatic neoplasm Diseases 0.000 description 1
- 206010033645 Pancreatitis Diseases 0.000 description 1
- 206010033647 Pancreatitis acute Diseases 0.000 description 1
- QGMRQYFBGABWDR-UHFFFAOYSA-M Pentobarbital sodium Chemical compound [Na+].CCCC(C)C1(CC)C(=O)NC(=O)[N-]C1=O QGMRQYFBGABWDR-UHFFFAOYSA-M 0.000 description 1
- 208000004186 Pulmonary Heart Disease Diseases 0.000 description 1
- 101001110823 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-A Proteins 0.000 description 1
- 101000712176 Saccharomyces cerevisiae (strain ATCC 204508 / S288c) 60S ribosomal protein L6-B Proteins 0.000 description 1
- 206010039710 Scleroderma Diseases 0.000 description 1
- 206010040047 Sepsis Diseases 0.000 description 1
- 208000021386 Sjogren Syndrome Diseases 0.000 description 1
- 208000007718 Stable Angina Diseases 0.000 description 1
- 208000005718 Stomach Neoplasms Diseases 0.000 description 1
- 101001082043 Sulfolobus acidocaldarius (strain ATCC 33909 / DSM 639 / JCM 8929 / NBRC 15157 / NCIMB 11770) Translation initiation factor 5A Proteins 0.000 description 1
- 238000006859 Swern oxidation reaction Methods 0.000 description 1
- WBWWGRHZICKQGZ-UHFFFAOYSA-N Taurocholic acid Natural products OC1CC2CC(O)CCC2(C)C2C1C1CCC(C(CCC(=O)NCCS(O)(=O)=O)C)C1(C)C(O)C2 WBWWGRHZICKQGZ-UHFFFAOYSA-N 0.000 description 1
- 238000008050 Total Bilirubin Reagent Methods 0.000 description 1
- 229920004890 Triton X-100 Polymers 0.000 description 1
- 239000013504 Triton X-100 Substances 0.000 description 1
- 206010067584 Type 1 diabetes mellitus Diseases 0.000 description 1
- 102100040374 U4/U6 small nuclear ribonucleoprotein Prp3 Human genes 0.000 description 1
- 201000006704 Ulcerative Colitis Diseases 0.000 description 1
- 208000007814 Unstable Angina Diseases 0.000 description 1
- 206010047115 Vasculitis Diseases 0.000 description 1
- 208000018839 Wilson disease Diseases 0.000 description 1
- YTAHJIFKAKIKAV-XNMGPUDCSA-N [(1R)-3-morpholin-4-yl-1-phenylpropyl] N-[(3S)-2-oxo-5-phenyl-1,3-dihydro-1,4-benzodiazepin-3-yl]carbamate Chemical compound O=C1[C@H](N=C(C2=C(N1)C=CC=C2)C1=CC=CC=C1)NC(O[C@H](CCN1CCOCC1)C1=CC=CC=C1)=O YTAHJIFKAKIKAV-XNMGPUDCSA-N 0.000 description 1
- 201000000690 abdominal obesity-metabolic syndrome Diseases 0.000 description 1
- 238000009825 accumulation Methods 0.000 description 1
- 239000012190 activator Substances 0.000 description 1
- 201000003229 acute pancreatitis Diseases 0.000 description 1
- 210000002171 adipose macrophage Anatomy 0.000 description 1
- 230000008484 agonism Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 150000001299 aldehydes Chemical class 0.000 description 1
- 208000006682 alpha 1-Antitrypsin Deficiency Diseases 0.000 description 1
- 230000008485 antagonism Effects 0.000 description 1
- 230000001093 anti-cancer Effects 0.000 description 1
- 230000003510 anti-fibrotic effect Effects 0.000 description 1
- 230000003110 anti-inflammatory effect Effects 0.000 description 1
- 235000019789 appetite Nutrition 0.000 description 1
- 230000036528 appetite Effects 0.000 description 1
- 239000012300 argon atmosphere Substances 0.000 description 1
- 210000001367 artery Anatomy 0.000 description 1
- 238000007681 bariatric surgery Methods 0.000 description 1
- 230000006399 behavior Effects 0.000 description 1
- 230000008901 benefit Effects 0.000 description 1
- QGJZLNKBHJESQX-FZFNOLFKSA-N betulinic acid Chemical compound C1C[C@H](O)C(C)(C)[C@@H]2CC[C@@]3(C)[C@]4(C)CC[C@@]5(C(O)=O)CC[C@@H](C(=C)C)[C@@H]5[C@H]4CC[C@@H]3[C@]21C QGJZLNKBHJESQX-FZFNOLFKSA-N 0.000 description 1
- 210000000941 bile Anatomy 0.000 description 1
- 239000003858 bile acid conjugate Substances 0.000 description 1
- 208000026900 bile duct neoplasm Diseases 0.000 description 1
- 230000004071 biological effect Effects 0.000 description 1
- 238000012925 biological evaluation Methods 0.000 description 1
- 210000004369 blood Anatomy 0.000 description 1
- 239000008280 blood Substances 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 210000004556 brain Anatomy 0.000 description 1
- 239000001110 calcium chloride Substances 0.000 description 1
- 235000011148 calcium chloride Nutrition 0.000 description 1
- 229910001628 calcium chloride Inorganic materials 0.000 description 1
- 229910052799 carbon Inorganic materials 0.000 description 1
- 150000001728 carbonyl compounds Chemical class 0.000 description 1
- 239000013592 cell lysate Substances 0.000 description 1
- 208000026106 cerebrovascular disease Diseases 0.000 description 1
- 239000007795 chemical reaction product Substances 0.000 description 1
- 238000002512 chemotherapy Methods 0.000 description 1
- QSHQKIURKJITMZ-BRPMRXRMSA-N cholane Chemical group C1CC2CCCC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H]([C@H](C)CCC)[C@@]1(C)CC2 QSHQKIURKJITMZ-BRPMRXRMSA-N 0.000 description 1
- 208000006990 cholangiocarcinoma Diseases 0.000 description 1
- 235000012000 cholesterol Nutrition 0.000 description 1
- 208000019425 cirrhosis of liver Diseases 0.000 description 1
- 206010009887 colitis Diseases 0.000 description 1
- 229940125904 compound 1 Drugs 0.000 description 1
- 229940125773 compound 10 Drugs 0.000 description 1
- 229940126142 compound 16 Drugs 0.000 description 1
- 238000001816 cooling Methods 0.000 description 1
- 230000006196 deacetylation Effects 0.000 description 1
- 238000003381 deacetylation reaction Methods 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 238000013461 design Methods 0.000 description 1
- 238000011161 development Methods 0.000 description 1
- 230000018109 developmental process Effects 0.000 description 1
- 208000033679 diabetic kidney disease Diseases 0.000 description 1
- 208000010643 digestive system disease Diseases 0.000 description 1
- PZXJOHSZQAEJFE-UHFFFAOYSA-N dihydrobetulinic acid Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C(O)=O)CCC(C(C)C)C5C4CCC3C21C PZXJOHSZQAEJFE-UHFFFAOYSA-N 0.000 description 1
- 229940043279 diisopropylamine Drugs 0.000 description 1
- 208000016097 disease of metabolism Diseases 0.000 description 1
- KPUWHANPEXNPJT-UHFFFAOYSA-N disiloxane Chemical class [SiH3]O[SiH3] KPUWHANPEXNPJT-UHFFFAOYSA-N 0.000 description 1
- 238000001035 drying Methods 0.000 description 1
- 230000008030 elimination Effects 0.000 description 1
- 238000003379 elimination reaction Methods 0.000 description 1
- 206010014665 endocarditis Diseases 0.000 description 1
- 239000006274 endogenous ligand Substances 0.000 description 1
- 210000002889 endothelial cell Anatomy 0.000 description 1
- 238000011156 evaluation Methods 0.000 description 1
- 239000000706 filtrate Substances 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- 210000000232 gallbladder Anatomy 0.000 description 1
- 206010017758 gastric cancer Diseases 0.000 description 1
- 230000005176 gastrointestinal motility Effects 0.000 description 1
- 208000018685 gastrointestinal system disease Diseases 0.000 description 1
- 239000011521 glass Substances 0.000 description 1
- 231100000852 glomerular disease Toxicity 0.000 description 1
- MASNOZXLGMXCHN-ZLPAWPGGSA-N glucagon Chemical compound C([C@@H](C(=O)N[C@H](C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)O)C(O)=O)C(C)C)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](C)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CO)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CCCCN)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](N)CC=1NC=NC=1)[C@@H](C)O)[C@@H](C)O)C1=CC=CC=C1 MASNOZXLGMXCHN-ZLPAWPGGSA-N 0.000 description 1
- 229960004666 glucagon Drugs 0.000 description 1
- 239000008103 glucose Substances 0.000 description 1
- 230000014101 glucose homeostasis Effects 0.000 description 1
- 208000024908 graft versus host disease Diseases 0.000 description 1
- 208000035474 group of disease Diseases 0.000 description 1
- 208000019622 heart disease Diseases 0.000 description 1
- 230000009716 hepatic expression Effects 0.000 description 1
- 231100000753 hepatic injury Toxicity 0.000 description 1
- 230000013632 homeostatic process Effects 0.000 description 1
- 238000011905 homologation Methods 0.000 description 1
- 239000001257 hydrogen Substances 0.000 description 1
- 229910052739 hydrogen Inorganic materials 0.000 description 1
- 150000002431 hydrogen Chemical class 0.000 description 1
- 230000001631 hypertensive effect Effects 0.000 description 1
- 208000006575 hypertriglyceridemia Diseases 0.000 description 1
- 230000002218 hypoglycaemic effect Effects 0.000 description 1
- 238000000338 in vitro Methods 0.000 description 1
- 238000011065 in-situ storage Methods 0.000 description 1
- MGXWVYUBJRZYPE-YUGYIWNOSA-N incretin Chemical class C([C@@H](C(=O)N[C@@H](CO)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](C)C(=O)N[C@@H](CCSC)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C=CC=CC=1)C(=O)N[C@@H](C(C)C)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](C)C(=O)N[C@@H](CCC(N)=O)C(=O)N[C@@H](CCCCN)C(=O)NCC(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H](CC(O)=O)C(=O)N[C@@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CCCCN)C(=O)N[C@@H](CC=1NC=NC=1)C(=O)N[C@@H](CC(N)=O)C(=O)N[C@@H]([C@@H](C)CC)C(=O)N[C@@H]([C@@H](C)O)C(=O)N[C@@H](CCC(N)=O)C(O)=O)NC(=O)[C@H](CC(O)=O)NC(=O)[C@H](CO)NC(=O)[C@@H](NC(=O)[C@H](CC=1C=CC=CC=1)NC(=O)[C@@H](NC(=O)CNC(=O)[C@H](CCC(O)=O)NC(=O)[C@H](C)NC(=O)[C@@H](N)CC=1C=CC(O)=CC=1)[C@@H](C)O)[C@@H](C)CC)C1=CC=C(O)C=C1 MGXWVYUBJRZYPE-YUGYIWNOSA-N 0.000 description 1
- 239000000859 incretin Substances 0.000 description 1
- 230000002401 inhibitory effect Effects 0.000 description 1
- 238000009434 installation Methods 0.000 description 1
- 230000003914 insulin secretion Effects 0.000 description 1
- 201000004332 intermediate coronary syndrome Diseases 0.000 description 1
- 230000000968 intestinal effect Effects 0.000 description 1
- 201000002161 intrahepatic cholestasis of pregnancy Diseases 0.000 description 1
- ZLVXBBHTMQJRSX-VMGNSXQWSA-N jdtic Chemical compound C1([C@]2(C)CCN(C[C@@H]2C)C[C@H](C(C)C)NC(=O)[C@@H]2NCC3=CC(O)=CC=C3C2)=CC=CC(O)=C1 ZLVXBBHTMQJRSX-VMGNSXQWSA-N 0.000 description 1
- NLYAJNPCOHFWQQ-UHFFFAOYSA-N kaolin Chemical compound O.O.O=[Al]O[Si](=O)O[Si](=O)O[Al]=O NLYAJNPCOHFWQQ-UHFFFAOYSA-N 0.000 description 1
- 150000002576 ketones Chemical class 0.000 description 1
- 210000003734 kidney Anatomy 0.000 description 1
- 230000004322 lipid homeostasis Effects 0.000 description 1
- 239000012280 lithium aluminium hydride Substances 0.000 description 1
- 201000007270 liver cancer Diseases 0.000 description 1
- 208000014018 liver neoplasm Diseases 0.000 description 1
- 238000003670 luciferase enzyme activity assay Methods 0.000 description 1
- 238000004020 luminiscence type Methods 0.000 description 1
- 239000012139 lysis buffer Substances 0.000 description 1
- 230000036210 malignancy Effects 0.000 description 1
- 208000015486 malignant pancreatic neoplasm Diseases 0.000 description 1
- 230000037353 metabolic pathway Effects 0.000 description 1
- 230000011987 methylation Effects 0.000 description 1
- 238000007069 methylation reaction Methods 0.000 description 1
- 208000008275 microscopic colitis Diseases 0.000 description 1
- 208000010125 myocardial infarction Diseases 0.000 description 1
- 208000031225 myocardial ischemia Diseases 0.000 description 1
- MQYXUWHLBZFQQO-UHFFFAOYSA-N nepehinol Natural products C1CC(O)C(C)(C)C2CCC3(C)C4(C)CCC5(C)CCC(C(=C)C)C5C4CCC3C21C MQYXUWHLBZFQQO-UHFFFAOYSA-N 0.000 description 1
- 150000002825 nitriles Chemical class 0.000 description 1
- 229910052757 nitrogen Inorganic materials 0.000 description 1
- 238000005935 nucleophilic addition reaction Methods 0.000 description 1
- 235000020824 obesity Nutrition 0.000 description 1
- 230000000414 obstructive effect Effects 0.000 description 1
- 229940100243 oleanolic acid Drugs 0.000 description 1
- 230000036284 oxygen consumption Effects 0.000 description 1
- 210000000496 pancreas Anatomy 0.000 description 1
- 201000002528 pancreatic cancer Diseases 0.000 description 1
- 208000008443 pancreatic carcinoma Diseases 0.000 description 1
- 235000016236 parenteral nutrition Nutrition 0.000 description 1
- 229960001412 pentobarbital Drugs 0.000 description 1
- 230000002093 peripheral effect Effects 0.000 description 1
- 230000003389 potentiating effect Effects 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- HZLWUYJLOIAQFC-UHFFFAOYSA-N prosapogenin PS-A Natural products C12CC(C)(C)CCC2(C(O)=O)CCC(C2(CCC3C4(C)C)C)(C)C1=CCC2C3(C)CCC4OC1OCC(O)C(O)C1O HZLWUYJLOIAQFC-UHFFFAOYSA-N 0.000 description 1
- 230000009993 protective function Effects 0.000 description 1
- 208000002815 pulmonary hypertension Diseases 0.000 description 1
- 230000005855 radiation Effects 0.000 description 1
- 230000008929 regeneration Effects 0.000 description 1
- 238000011069 regeneration method Methods 0.000 description 1
- 230000001105 regulatory effect Effects 0.000 description 1
- 230000004044 response Effects 0.000 description 1
- 206010039073 rheumatoid arthritis Diseases 0.000 description 1
- 150000003839 salts Chemical class 0.000 description 1
- 208000010157 sclerosing cholangitis Diseases 0.000 description 1
- 230000028327 secretion Effects 0.000 description 1
- 230000019491 signal transduction Effects 0.000 description 1
- 230000011664 signaling Effects 0.000 description 1
- 238000010898 silica gel chromatography Methods 0.000 description 1
- 101150101156 slc51a gene Proteins 0.000 description 1
- 201000011549 stomach cancer Diseases 0.000 description 1
- 238000010254 subcutaneous injection Methods 0.000 description 1
- 239000007929 subcutaneous injection Substances 0.000 description 1
- 239000000126 substance Substances 0.000 description 1
- 230000004083 survival effect Effects 0.000 description 1
- 208000011580 syndromic disease Diseases 0.000 description 1
- 201000000596 systemic lupus erythematosus Diseases 0.000 description 1
- 235000020679 tap water Nutrition 0.000 description 1
- 239000008399 tap water Substances 0.000 description 1
- 229960003080 taurine Drugs 0.000 description 1
- WBWWGRHZICKQGZ-GIHLXUJPSA-N taurocholic acid Chemical compound C([C@@H]1C[C@H]2O)[C@@H](O)CC[C@]1(C)[C@@H]1[C@@H]2[C@@H]2CC[C@@H]([C@@H](CCC(=O)NCCS(O)(=O)=O)C)[C@@]2(C)[C@H](O)C1 WBWWGRHZICKQGZ-GIHLXUJPSA-N 0.000 description 1
- 210000001519 tissue Anatomy 0.000 description 1
- 238000007070 tosylation reaction Methods 0.000 description 1
- 238000013518 transcription Methods 0.000 description 1
- 230000035897 transcription Effects 0.000 description 1
- 230000032258 transport Effects 0.000 description 1
- 239000005051 trimethylchlorosilane Substances 0.000 description 1
- IYKMDRMCUIFHRA-UHFFFAOYSA-H tripotassium;trisodium;2-hydroxypropane-1,2,3-tricarboxylate;hydrate Chemical compound O.[Na+].[Na+].[Na+].[K+].[K+].[K+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O.[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O IYKMDRMCUIFHRA-UHFFFAOYSA-H 0.000 description 1
- JLEXUIVKURIPFI-UHFFFAOYSA-N tris phosphate Chemical compound OP(O)(O)=O.OCC(N)(CO)CO JLEXUIVKURIPFI-UHFFFAOYSA-N 0.000 description 1
- 208000025086 undetermined colitis Diseases 0.000 description 1
- 229960001661 ursodiol Drugs 0.000 description 1
- 208000019553 vascular disease Diseases 0.000 description 1
- 201000001862 viral hepatitis Diseases 0.000 description 1
- 239000013585 weight reducing agent Substances 0.000 description 1
- 238000011816 wild-type C57Bl6 mouse Methods 0.000 description 1
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J31/00—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring
- C07J31/006—Normal steroids containing one or more sulfur atoms not belonging to a hetero ring not covered by C07J31/003
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/56—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids
- A61K31/575—Compounds containing cyclopenta[a]hydrophenanthrene ring systems; Derivatives thereof, e.g. steroids substituted in position 17 beta by a chain of three or more carbon atoms, e.g. cholane, cholestane, ergosterol, sitosterol
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/04—Drugs for disorders of the alimentary tract or the digestive system for ulcers, gastritis or reflux esophagitis, e.g. antacids, inhibitors of acid secretion, mucosal protectants
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P1/00—Drugs for disorders of the alimentary tract or the digestive system
- A61P1/16—Drugs for disorders of the alimentary tract or the digestive system for liver or gallbladder disorders, e.g. hepatoprotective agents, cholagogues, litholytics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P13/00—Drugs for disorders of the urinary system
- A61P13/12—Drugs for disorders of the urinary system of the kidneys
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P17/00—Drugs for dermatological disorders
- A61P17/02—Drugs for dermatological disorders for treating wounds, ulcers, burns, scars, keloids, or the like
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P19/00—Drugs for skeletal disorders
- A61P19/02—Drugs for skeletal disorders for joint disorders, e.g. arthritis, arthrosis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P21/00—Drugs for disorders of the muscular or neuromuscular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P25/00—Drugs for disorders of the nervous system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P29/00—Non-central analgesic, antipyretic or antiinflammatory agents, e.g. antirheumatic agents; Non-steroidal antiinflammatory drugs [NSAID]
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/04—Anorexiants; Antiobesity agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/06—Antihyperlipidemics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P3/00—Drugs for disorders of the metabolism
- A61P3/08—Drugs for disorders of the metabolism for glucose homeostasis
- A61P3/10—Drugs for disorders of the metabolism for glucose homeostasis for hyperglycaemia, e.g. antidiabetics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/14—Antivirals for RNA viruses
- A61P31/18—Antivirals for RNA viruses for HIV
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P31/00—Antiinfectives, i.e. antibiotics, antiseptics, chemotherapeutics
- A61P31/12—Antivirals
- A61P31/20—Antivirals for DNA viruses
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P37/00—Drugs for immunological or allergic disorders
- A61P37/02—Immunomodulators
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P43/00—Drugs for specific purposes, not provided for in groups A61P1/00-A61P41/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/38—Drugs for disorders of the endocrine system of the suprarenal hormones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/48—Drugs for disorders of the endocrine system of the pancreatic hormones
- A61P5/50—Drugs for disorders of the endocrine system of the pancreatic hormones for increasing or potentiating the activity of insulin
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P9/00—Drugs for disorders of the cardiovascular system
- A61P9/10—Drugs for disorders of the cardiovascular system for treating ischaemic or atherosclerotic diseases, e.g. antianginal drugs, coronary vasodilators, drugs for myocardial infarction, retinopathy, cerebrovascula insufficiency, renal arteriosclerosis
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J11/00—Normal steroids containing carbon, hydrogen, halogen or oxygen, not substituted in position 3
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J41/00—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring
- C07J41/0033—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring not covered by C07J41/0005
- C07J41/0094—Normal steroids containing one or more nitrogen atoms not belonging to a hetero ring not covered by C07J41/0005 containing nitrile radicals, including thiocyanide radicals
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J9/00—Normal steroids containing carbon, hydrogen, halogen or oxygen substituted in position 17 beta by a chain of more than two carbon atoms, e.g. cholane, cholestane, coprostane
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07J—STEROIDS
- C07J9/00—Normal steroids containing carbon, hydrogen, halogen or oxygen substituted in position 17 beta by a chain of more than two carbon atoms, e.g. cholane, cholestane, coprostane
- C07J9/005—Normal steroids containing carbon, hydrogen, halogen or oxygen substituted in position 17 beta by a chain of more than two carbon atoms, e.g. cholane, cholestane, coprostane containing a carboxylic function directly attached or attached by a chain containing only carbon atoms to the cyclopenta[a]hydrophenanthrene skeleton
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- General Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Veterinary Medicine (AREA)
- Public Health (AREA)
- Animal Behavior & Ethology (AREA)
- Pharmacology & Pharmacy (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Diabetes (AREA)
- Virology (AREA)
- Toxicology (AREA)
- Hematology (AREA)
- Obesity (AREA)
- Oncology (AREA)
- Communicable Diseases (AREA)
- Molecular Biology (AREA)
- Endocrinology (AREA)
- Immunology (AREA)
- Neurology (AREA)
- Urology & Nephrology (AREA)
- Heart & Thoracic Surgery (AREA)
- Orthopedic Medicine & Surgery (AREA)
- Physical Education & Sports Medicine (AREA)
- Rheumatology (AREA)
- Cardiology (AREA)
- Epidemiology (AREA)
- Dermatology (AREA)
- Child & Adolescent Psychology (AREA)
- AIDS & HIV (AREA)
- Gastroenterology & Hepatology (AREA)
- Emergency Medicine (AREA)
- Vascular Medicine (AREA)
- Pain & Pain Management (AREA)
Abstract
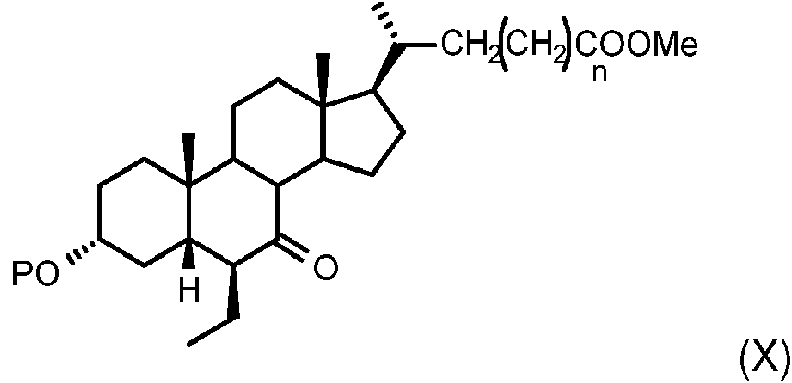
Un compuesto seleccionado del grupo que consiste en:**Fórmula**
Description
DESCRIPCIÓN
Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1
Campo de la invención
La presente invención se refiere a compuestos que tienen armazones de colano, dichos compuestos para su uso en el tratamiento y/o la prevención de enfermedades mediadas por FXR y TGR5/GPBAR1.
Estado de la técnica
Los ácidos biliares (BA) son moléculas de señalización que interactúan con dos tipos de receptores celulares dedicados, los receptores nucleares intracelulares y los receptores de la superficie celular. Los receptores nucleares incluyen el receptor farnesoide X (FXR), identificado como el sensor de ácido biliar endógeno (Makishima et al. Science, 1999, 284, 1362; Parks et al. Science 1999, 284, 1365).
Altamente expresado en tejidos enterohepáticos (hígado e intestino), el FXR regula la homeostasis de los ácidos biliares, incluyendo también las vías metabólicas la homeostasis de los lípidos y la glucosa (Zhang et al. Proc. Natl. Acad. Sci. USA 2006, 103, 1006). Además, los agonistas de FXR proporcionan efectos antiinflamatorios y antifibróticos y anticancerígenos (Renga et al. FASEB J. 2012, 26, 3021-3031).
El receptor de la superficie celular de los ácidos biliares (GPBAR1, M-BAR1, GP-BAR1, TGR5) pertenece a la superfamilia similar a la rodopsina de los receptores acoplados a la proteína G (Takeda et al. FEBS Lett. 2002, 520, 97; Kawamata et al. J. Biol. Chem. 2003, 278, 9435).
La unión del ligando a TGR5/GPBAR1 da como resultado la elevación de los niveles de AMPc intracelular con la consiguiente activación de una cascada de señalización. GPBAR1 es altamente expresado en el hígado y en el intestino, pero también en los músculos, el cerebro, el tejido adiposo, los macrófagosy las células endoteliales. En el tejido adiposo muscular y pardo, TGR5/GPBAR1 aumenta el gasto de energía y el consumo de oxígeno (Watanabe et al. Nature 2006, 439, 484) en las células L enteroendocrinas, la activación de TGR5/GPBAR1 estimula la secreción de péptido similar al glucagón (GLP)-1, una incretina que mejora la liberación de insulina en el páncreas, regulando así los niveles de glucosa en sangre, la motilidad gastrointestinal y el apetito (Thomas et al. Cell. Metab.
2009, 10, 167).
Químicamente, los BA son derivados de la cadena lateral de colesterol truncados. Su repertorio molecular se genera en primer lugar en el hígado con la producción de ácidos biliares primarios, ácido cólico (CA) y ácido quenodesoxicólico (CDCA). La transformación por microbios en el intestino genera ácidos biliares secundarios, ácido desoxicólico (DCA) y ácido litocólico (LCA). En el cuerpo humano, los ácidos biliares se conjugan con glicina y taurina. La actividad hacia los dos receptores de BA depende de la estructura, siendo CDCA, el activador de FXR endógeno más potente, y LCA y TLCA, los agonistas naturales más fuertes de TGR5/GPBAR1.
Se ha observado prurito colestásico como un efecto secundario grave asociado con el uso de agonistas de FXR en PBC y un estudio reciente indicó que TGR5/GPBAR1 es la diana molecular involucrada en el desarrollo de este efecto secundario (Alemi et al. J. Clin. Invest. 2013, 123, 1513-1530).
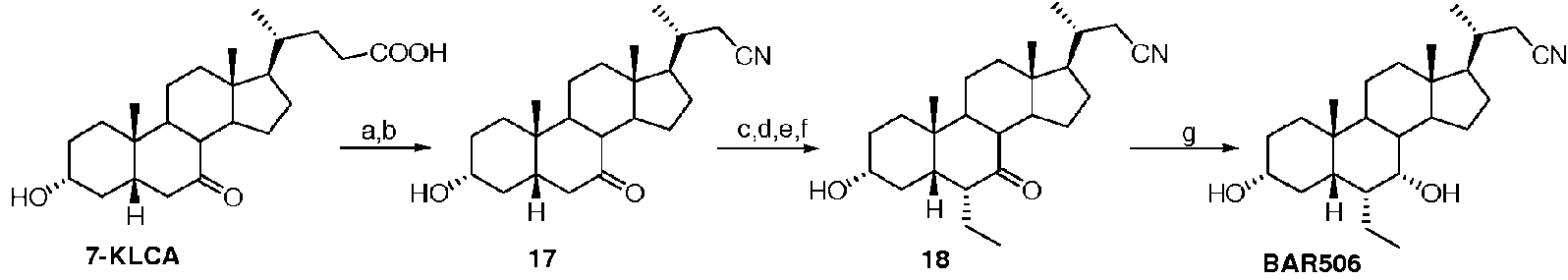
El documento WO2013192097 describe el ácido 6-alfa-etil-quenodesoxicólico (6-ECDCA), un potente y selectivo agonista de FXR dotado de efecto anticolostático. El documento WO2008002573 describe derivados de ácidos biliares como ligandos FXR para la prevención o el tratamiento de enfermedades o afecciones mediadas por FXR. El documento WO2010014836 y Sato H. (J Med Chem. 2008, 51,4849) describen los moduladores de TGR5.
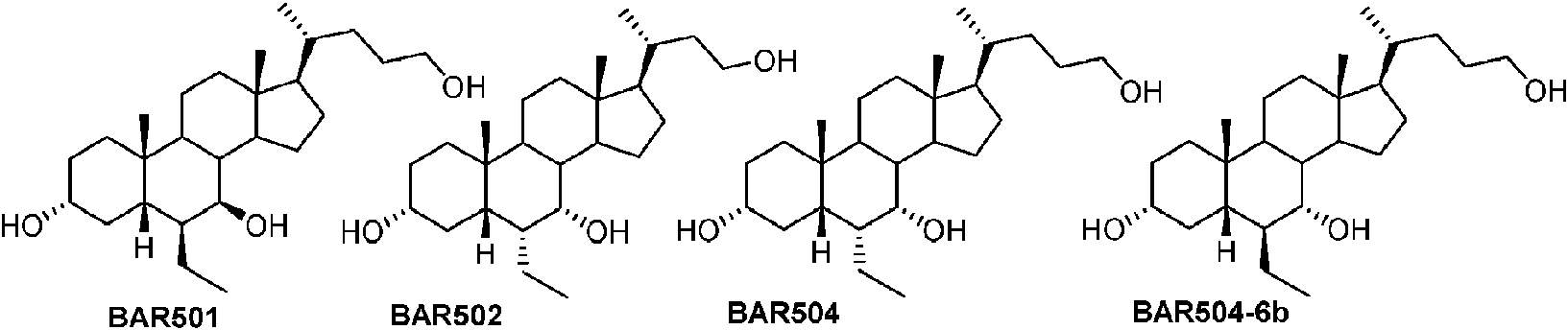
D'Amore C. et al. (J. Med. Chem. 2014, 57, 937) describen el diseño, la síntesis y la evaluación biológica de los
agonistas duales de GP-BAR1/FXR. D'Amore et al. describen los compuestos BAR502 y BAR504 como intermedios de síntesis.
Iguchi Y. et al. (J Lipid Res. 2010, 51, 1432) describen la función de los alcoholes biliares como ligandos de TGR5. Kihira K. et al. (Steroids 1992, 57(4), 193-198) describen los compuestos BAR107 como intermedios de la síntesis. Swaan P. W.et al. (J. Comp. Aid. Mol. Des. 1997, 11, 581-588), en un modelo molecular del portador de ácido biliar intestinal analizaron el ursocolato (el compuesto 15 allí, BARn406 en la presente memoria) entre un conjunto de productos conjugados de ácido biliar. BARn406 resultó tener una capacidad indetectable para inhibir el transporte de ácido taurocólico en células CaCo-2.
Burns et al. (Steroids 2011, 76(3), 291-300) describen la síntesis y la actividad olfativa de derivados de ácidos biliares sulfatados en la posición 5 no naturales en la lamprea marina (Petromyzon marinus). El compuesto 9e descrito en ese documento (compuesto BAR407 en la presente memoria) no provocó una respuesta olfativa.
Festa et al. (J. Med. Chem. 2014, 57, 8477) describen la síntesis de moduladores selectivos de FXR o GPBAR1. El objetivo de la presente invención es la identificación de nuevos compuestos que contengan el armazón químico del colano y que modulen FXR y/o TGR5/GPBAR1.
Compendio de la invención
El objeto de la presente invención es un compuesto de fórmula
Se ha encontrado que los compuestos descritos anteriormente son moduladores de FXR o/y TGR5/GPBAR1 y, por lo tanto, son útiles para el tratamiento de enfermedades mediadas por FXR y TGR5/GPBAR1.
Por lo tanto, para un aspecto, la presente invención se refiere a un compuesto para su uso como medicamento, dicho compuesto de fórmula
Para un aspecto adicional, la presente invención se refiere a compuestos de fórmula
para su uso en la prevención y/o el tratamiento de trastornos gastrointestinales, enfermedades hepáticas, enfermedades cardiovasculares, aterosclerosis, enfermedades metabólicas, enfermedades infecciosas, cáncer, trastornos renales, trastornos inflamatorios y trastornos neurológicos (tales como accidente cerebrovascular).
La presente invención también se refiere a un procedimiento para preparar un compuesto como se describió anteriormente.
Descripción detallada de la invención
Se ha encontrado que los compuestos de acuerdo con la invención son moduladores de FXR o TGR5/GPBAR1 altamente selectivos o moduladores duales de FXR y TGR5/GPBAR1 y, por lo tanto, son útiles como medicamentos en particular para su uso en la prevención y/o el tratamiento de trastornos gastrointestinales, enfermedades hepáticas, enfermedades cardiovasculares, aterosclerosis, enfermedades metabólicas, trastornos metabólicos, enfermedades infecciosas, cáncer, trastornos renales, trastornos inflamatorios y trastornos neurológicos tales como el accidente cerebrovascular.
En ciertas realizaciones, la enfermedad hepática se selecciona del grupo que consiste en enfermedades hepáticas crónicas que incluyen cirrosis biliar primaria (PBC), xantomatosis cerebrotendinosa (CTX), colangitis esclerosante primaria (PSC), colestasis inducida por fármacos, colestasis intrahepática del embarazo, colestasis asociada a la nutrición parenteral, sobrecrecimiento bacteriano y colestasis asociada a sepsis, hepatitis autoinmunitaria, hepatitis viral crónica, enfermedad hepática alcohólica, enfermedad del hígado graso no alcohólico (NAFLD), esteatohepatitis no alcohólica (NASH), enfermedad de injerto contra anfitrión asociada al trasplante de hígado, trasplante de donante vivo, regeneración del hígado, fibrosis hepática congénita, enfermedad hepática granulomatosa, neoplasia maligna intra- o extrahepática, enfermedad de Wilson, hemocromatosis y deficiencia de alfa 1 -antitripsina.
En ciertas realizaciones, la enfermedad gastrointestinal se selecciona del grupo que consiste en enfermedad inflamatoria intestinal (EII) (incluida la enfermedad de Crohn, la colitis ulcerosa y la colitis indeterminada), síndrome del intestino irritable (SII), sobrecrecimiento bacteriano, pancreatitis aguda y crónica, malabsorción, colitis post radiación y colitis microscópica.
En ciertas realizaciones, la enfermedad renal se selecciona del grupo que consiste en nefropatía diabética, nefropatía hipertensiva, enfermedad glomerular crónica, que incluye glomerulonefritis crónica y glomerulopatía de trasplante crónica, enfermedades tubulointersticiales crónicas y trastornos vasculares del riñón.
En ciertas realizaciones, la enfermedad cardiovascular se selecciona del grupo que consiste en aterosclerosis, dislipidemia, hipercolesterolemia, hipertrigliceridemia, hipertensión también conocida como hipertensión arterial, cardiopatía inflamatoria que incluye miocarditis y endocarditis, angina estable por cardiopatía isquémica, angina inestable, infarto de miocardio, enfermedad cerebrovascular incluyendo accidente cerebrovascular isquémico, enfermedad cardíaca pulmonar incluyendo hipertensión pulmonar, enfermedad arterial periférica (EAP), también conocida como enfermedad vascular periférica (PVD), enfermedad oclusiva de la arteria periférica y arteriopatía obliterante periférica.
En ciertas realizaciones, la enfermedad metabólica se selecciona del grupo que consiste en resistencia a la insulina, síndrome metabólico, diabetes tipo I y tipo II, hipoglucemia, trastornos de la corteza suprarrenal, incluyendo la insuficiencia de la corteza suprarrenal.
En ciertas realizaciones, el trastorno metabólico se selecciona del grupo que consiste en obesidad y afecciones asociadas a la cirugía bariátrica.
En ciertas realizaciones, el cáncer se selecciona del grupo de cáncer de hígado, cáncer de conducto biliar, cáncer de páncreas, cáncer gástrico, cáncer colorrectal, cáncer de mama, cáncer de ovario y afecciones asociadas con la resistencia a la quimioterapia.
En ciertas realizaciones, el trastorno infeccioso se selecciona del grupo de enfermedades asociadas con la infección por el virus de la inmunodeficiencia humana (SIDA) y trastornos relacionados, infección por virus B y virus C.
En ciertas realizaciones, el trastorno inflamatorio se selecciona del grupo de artritis reumatoide, fibromialgia, síndrome de Sjogren, esclerodermia, síndrome de Behcet, vasculitis y lupus eritematoso sistémico.
Los datos sobre la actividad de ciertos compuestos de la invención sobre FXR y TGR5/GPBAR1 se describen en la siguiente tabla. En esta tabla, las actividades para los compuestos de la invención sobre FXR y GPBAR1 se compararon con las de los compuestos de referencia: es decir, CDCA para FXR y TLCA para TGR5/GPBAR1. Cada compuesto se probó a una concentración 10 microM y la actividad de transactivación de CDCA sobre FXR y de TLCA sobre CRE (es decir, TGR5/GPBAR1) se consideró igual a 100%.
Tabla 1
Para un aspecto, la presente invención se refiere a los compuestos mencionados anteriormente en donde los compuestos son agonistas duales de FXR y TGR5/GPBAR1. Un ejemplo seleccionado en este grupo es BAR502. Sorprendentemente, BAR502 no induce picazón cuando se administra a animales colestáticos mediante la administración de ANIT o Estrógeno. En los síndromes colestáticos, se cree que la acumulación de ácidos biliares en el organismo causa picazón. Recientemente, se demostró que TGR5/GPBAR1 mediaba en la picazón causada por la administración intradérmica de DCA y LCA (Alemi et al. J. Clin. Invest. 2013, 123, 1513-1530). En ensayos clínicos, la administración a pacientes que padecen cirrosis biliar primaria (PBC) de ácido obeticólico ha provocado picazón severa en aproximadamente 80% de los pacientes. Una ventaja específica y sorprendente de BAR502 es que este agente no induce picazón cuando se administra a animales que se vuelven colestáticos mediante la administración de a-naftil-isotiocianato (ANIT) o 17a-etinilestradiol (dos modelos validados de colestasis). En estos entornos experimentales, la administración de BAR502 aumenta la supervivencia, atenúa los niveles de fosfatasa alcalina en suero y modula de forma sólida la expresión hepática de genes diana de FXR canónicos, incluyendo OSTa, BSEP, SHP y MDR1, sin inducir prurito. En el modelo de 17a-etinilestradiol, BAR502 atenúa la colestasis y da forma al conjunto de ácidos biliares sin inducir picazón, lo que demuestra que en los modelos de colestasis no obstructiva, BAR502 atenúa la lesión hepática sin causar picazón.
En un aspecto, la presente invención se refiere a compuestos que son agonistas de FXR altamente selectivos sin efectos sobre GPBAR1 cuando se administran solos pero eficaces para inhibir la activación de GPBAR1 causada por TLCA (10 ^M), comportándose así como antagonistas de GPBAR1. En un aspecto, la presente invención se refiere a compuestos de fórmula (I) en donde los compuestos son agonistas de GpBAR1 altamente selectivos sin efectos sobre FXR. En un aspecto, la presente invención se refiere a compuestos de fórmula (I) en donde los compuestos son antagonistas de GPBAR1 altamente selectivos sin efectos sobre FXR.
La presente invención se refiere también a procedimientos para preparar un compuesto como se describió anteriormente.
Para un aspecto, la presente descripción se refiere a un procedimiento para preparar un compuesto de fórmula (I) como se describió anteriormente en donde n = 0, comprendiendo dicho procedimiento poner en contacto un compuesto de fórmula (XII)
con HCOOH y HClO4 y posteriormente poner en contacto el compuesto resultante con TFA, anhídrido trifluoroacético y NaNO2 para obtener un compuesto de fórmula (VII)
Las transformaciones químicas simples y bien conocidas pueden pasar a continuación de un compuesto de fórmula (VII) a un compuesto de fórmula (I) como se describió anteriormente, de modo que el grupo -CN puede hidrolizarse a COOH, así como el grupo OCHO puede hidrolizarse a un grupo hidroxilo o el grupo =O puede reducirse a grupo hidroxilo.
Para un aspecto, la presente invención se refiere a un procedimiento para preparar un compuesto descrito anteriormente, comprendiendo dicho procedimiento someter un compuesto de fórmula (VIII) a una condensación aldólica, poniendo en contacto de ese modo un compuesto de fórmula (VIII)
en donde n = 0,1, P es una función protectora alcohólica, preferiblemente OAc, con alquil litio, tal como nBuLi, y posteriormente con acetaldehído, preferiblemente en presencia también de BF3(OEt)2, para obtener un compuesto de fórmula (IX)
en donde n y P se describen como anteriormente.
Una condensación aldólica es una reacción de adición de aldol, que podría implicar la adición nucleófila de un enolato de cetona a un aldehído, en donde una vez formado, el producto aldólico pierde una molécula de agua para formar un compuesto de carbonilo a,p-insaturado.
Sometiendo un compuesto de fórmula (IX) a una hidrogenación catalítica, preferiblemente con H2 en presencia de Pd (OH)2/C, se puede obtener un compuesto de fórmula (X)
Para un aspecto, la presente invención se refiere a un procedimiento para preparar un compuesto de fórmula
comprendiendo dicho procedimiento poner en contacto un compuesto de fórmula (XIV)
en donde n es 0, R8 es OAc;
con MeONa/MeOH para obtener la epimerización del estereocentro C6 obteniendo de ese modo un compuesto de fórmula (XI)
en donde n es 0, R8 se describe como anteriormente. En caso de que R8 sea OAc, el tratamiento con MeONa/MeOH proporciona simultáneamente la hidrólisis del grupo acetoxi C3, obteniendo de ese modo un compuesto de fórmula (XI) en donde R8 es OH.
La reducción del carbonilo en C7 se puede obtener poniendo en contacto un compuesto de fórmula (X) con NaBH4 o Ca(BH4)2 para obtener una mezcla de beta-OH (hasta 70% en el caso del compuesto BAR501) y alfa-OH en C7. El tratamiento posterior con LiBH4 reduce, si está presente, la función éster metílico en la cadena lateral a
-CH2OH y el grupo protector OAc en c 3 a OH.
La reducción de carbonilo en C7 se puede obtener poniendo en contacto un compuesto de fórmula (XI) o el compuesto correspondiente que tiene COOH en la cadena lateral, con UBH4 obteniendo casi exclusivamente alfa-OH en C7. Simultáneamente el tratamiento con LiBH4 reduce, si está presente, la función éster metílico en la cadena lateral a -CH2OH y el grupo protector OAc en C3 a OH. Sometiendo un compuesto de fórmula (IX) a una reducción de NaBH4 seguida de tratamiento con LiBH4, se produjo la reducción en C7 y en la cadena lateral con desprotección simultánea, en particular desacetilación, en C3, para obtener un compuesto en donde R1 es alfa-OH, R2 es = CH-CH3, R3 es beta-OH, n = 0,1 y R es CH2OH.
Sometiendo el compuesto anterior en donde R1 es alfa-OH, R2 es = CH-CH3, R3 es beta-OH, n = 0,1 y R es CH2OH a una hidrogenación catalítica, preferiblemente con H2 y Pd(OH)2/C, se puede obtener un compuesto de fórmula (I) en donde R1 es alfa-OH, R2 es alfa-Et, R3 es beta-OH, n = 0,1 y R es CH2OH.
La presente invención se podría comprender mejor a la luz de los ejemplos y la sección experimental a continuación. Sección experimental
Química
Ejemplo 1. Preparación de compuestos de fórmula (I) en donde R2= H (no forma parte de la invención)
Ejemplo 1A. Síntesis de derivados de bis-homo-ursodesoxicolano
Una secuencia de reacción de cuatro etapas en 1, que incluye la protección de las funciones alcohólicas en C3 y C7, la reducción del éster metílico de la cadena lateral y la posterior oxidación de Swern de recipiente único/homologación de Wittig C2 proporcionó el éster metílico protegido de A24,25-bis-homoUDCA. La hidrogenación del doble enlace de la cadena lateral y la desprotección de la función alcohólica proporcionaron éster metílico de bis-homoUDCA 4, que se utilizó como material de partida en la preparación de BAR305 y su correspondiente alcohol, BAR304, mediante tratamiento con LiOH y LiBH4, respectivamente.
a) 2,6-lutidina, trifluorometanosulfonato de t-butildimetilsililo, CH2Cl2, 0°C; b) LiBH4, MeOH seco, THF, 0°C, rendimiento cuantitativo a lo largo de dos etapas; c) DMSO, cloruro de oxalilo, TEA seco, CH2Cl2, -78°C a continuación (trifenilfosforaniliden)acetato de metilo, 76%; d) H2, Pd(OH)2/C tipo Degussa, THF/MeOH 1:1, rendimiento cuantitativo; e) HCl 37%, MeOH, rendimiento cuantitativo; f) NaOH 5% en MeOH/H2O 1:1 v/v, 60%; g) LiBH4, MeOH seco, THF, 0°C, 77%.
Etapa a, b) Preparación de 3a,7p-di(fe/'c-butildimetilsililoxi)-5p-colan-24-ol (2)
El Compuesto 1 (1,2 g, 3 mmoles) se protegió en las dos funciones alcohólicas siguiendo el mismo procedimiento sintético descrito en J. Med. Chem. 2014, 57, 937 para obtener 1,9 g de 3a,7p-di(fe/'c-butildimetilsililoxi)-5|3-colan-24-oato de metilo (rendimiento cuantitativo) en forma de agujas incoloras, que se sometió a la siguiente etapa sin ninguna purificación.
Se añadieron metanol (850 ^L, 21 mmoles) y L¡BH4 (10,5 mL, 2 M en THF, 21 mmoles) a una solución de éster metílico (1,9 g, 3 mmoles) en THF seco (30 mL) a 0°C siguiendo el mismo procedimiento sintético descrito en J. Med. Chem. 2014, 57, 937. La purificación por medio de gel de sílice (hexano/acetato de etilo 99:1 y TEA al 0,5%) proporcionó 2 en forma de un sólido de color blanco (1,8 g, rendimiento cuantitativo).
Etapa c) Preparación en recipiente único de 3a,7p-di(terc-butildimetilsililoxi)-25,26-bishomo-5p-col-24-en-26-oato de metilo (3).
Se añadió DMSO (2,1 mL, 30 mmoles) gota a gota durante 15 minutos a una solución de cloruro de oxalilo (7,5 mL, 15 mmoles) en diclorometano seco (30 mL) a -78°C en atmósfera de argón. Después de 30 minutos, se añadió mediante una cánula una solución de 2 (1,8 g, 3 mmoles) en CH2Cl2 seco y la mezcla se agitó a -78°C durante 30 min. Se añadió Et3N (2,5 mL, 18 mmoles) gota a gota. Después de 1 h, se añadió (trifenilfosforaniliden)- acetato de metilo (2,0 g, 6 mmoles) y la mezcla se dejó calentando a temperatura ambiente. Se añadió una solución saturada de NaCl y la fase acuosa se extrajo con éter dietílico (3x100 mL). Las fases orgánicas combinadas se lavaron con agua, se secaron (Na2SO4) y se concentró. La purificación por medio de gel de sílice (hexano-acetato de etilo 95:5 y TEA al 0,5%) proporcionó el compuesto 3 en forma de un aceite incoloro (1,5 g, 76%).
Etapa d) Preparación de 3a,7p-di(terc-butildimetilsililoxi)-25,26-bishomo-5p-colan-26-oato de metilo. Una solución del compuesto 3 (1,5 g, 2,3 mmoles) en THF seco/MeOH seco (25 mL/25 mL, v/v) se hidrogenó en presencia de Pd(OH)2 al 5% peso en carbón activado tipo Degussa (20 mg) siguiendo el mismo procedimiento sintético descrito en J. Med. Chem. 2014, 57, 937 proporcionando 3a,7p-di(terc-butildimetilsililoxi)-25,26-bishomo-5p-colan-26-oato de metilo (1,5 g, rendimiento cuantitativo) que se sometió a la etapa e) sin purificación.
Etapa e) Preparación de 3a,7p-dihidroxi-25,26-bishomo-5p-colan-26-oato de metilo (4)
Se disolvió 3a,7p-di(terc-butildimetilsililoxi)-25,26-bishomo-5p-colan-26-oato de metilo (1,5 g) en metanol (70 mL). A la solución, se le añadió HCl (2 mL, 37% v/v) siguiendo el mismo procedimiento sintético descrito en J. Med. Chem.
2014, 57, 937 proporcionando 4 en forma de un sólido amorfo incoloro (1,0 g, rendimiento cuantitativo).
Etapa f) Preparación de ácido 3a,7p-dihidroxi-25,26-bishomo-5p-colan-26-oico (BAR305). Una porción de compuesto 4 (430 mg, 1 mmol) se hidrolizó con NaOH (400 mg, 10 mmoles) en una solución de MeOH:
H2O 1:1 v/v (20 mL) durante 4 h a reflujo. Una muestra analítica se purificó por medio de HPLC en un Nucleodur 100-5 C18 (5 ^m; 4,6 mm d.i. x 250 mm) con MeOH/H2O (95:5) como eluyente (velocidad de flujo 1 mL/min) (tR= 5 min).
BAR305: C26H44O4
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,47 (2H, m, H-3 y H-7), 2,27 (2H, t, J = 7,2 Hz, H2-25), 0,96 (3H, s, H3-19), 0,94 (3H, d, J = 6,5 Hz, H3-21), 0,70 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 178,2, 72,1, 71,9, 57,6,
56,7, 44,8, 44,5, 44,0, 41,6, 40,7, 38,6, 38,0, 36,9, 36,8, 36,1, 35,3, 35,2, 30,9, 29,8, 27,9, 26,7, 26,6, 23,9 , 22,4, 19,3, 12,7.
Etapa g) 25,26-bishomo-5p-colan-3a,7p,26-triol (BAR304). El Compuesto 4 (500 mg, 1.2 mmoles) se redujo en las mismas condiciones operativa descritas en la etapa b). La purificación por medio de gel de sílice (CH2Cl2/metanol 9:1) proporcionó BAR304 en forma de un aceite incoloro (375 mg, 77%). Una muestra analítica se purificó por medio de HPLC en un Nucleodur 100-5 C18 (5 ^m; 4,6 mm d.i. x 250 mm) con MeOH/H2O (85:15) como eluyente (velocidad de flujo 1 mL/min) (tR = 9 min).
BAR 304: C26H46O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,53 (2H, t, J = 6,5 Hz, H2-26), 3,48 (2H, m, H-3 y H-7), 0,95 (3H, s, H3-19), 0,93 (3H, d, J =6,5 Hz, H3-21), 0,70 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 572,1, 71,9, 63,0, 57,5, 56,7, 44,7, 44,4, 44,0, 41,6, 40,7, 38,5, 37,9, 37,2, 37,0, 36,1, 35,2, 33,7, 30,9, 29,8, 27,9, 27,4, 27,1, 23,9, 22,4, 19,4, 12,7.
Ejemplo 1B. Síntesis de 3a,7p-dihidroxi-24-nor-5p-colan-23-il-23-sulfato de sodio (BAR106) y 3a,7p-dihidroxi-24-nor-5p-colan-23-ol (BAR107)
Se preparó BAR106 a partir de UDCA mediante una secuencia de reacción que comprendía la performilación en los grupos hidroxilo, la degradación de un carbono de Beckmann en C24 y la transformación del grupo carboxilo C23 en el correspondiente intermedio éster metílico. La protección en los grupos hidroxilo en C-3 y C-7 como silil éteres, la reducción a éster metílico en C23, la sulfatación en la función alcohólica primaria en C23 y finalmente la desprotección proporcionaron BAR106 bruto en forma de una sal de amonio. La purificación en Amberlite y a continuación por medio de HPLC proporcionó el BAR106 del título en forma de una sal de sodio.
a) HCOOH, HClÜ4 , 96%; b) TFA, anhídrido trifluoroacético, NaNÜ2 , 96%; c) KOH 30% en MeOH/hbO 1:1 v/v, 97%; d) p-TsOH, MeOH seco, 98%; e) 2,6-lutidina, trifluorometanosulfonato de t-butildimetilsililo, CH2Cl2, 0°C, 88%; f) LiBH4, MeOH seco, THF, 0°C, rendimiento cuantitativo; g) Et3N.SO3, DMF, 95°C; h) HCl 37%, MeOH, a continuación Amberlite CG-120, MeOH, 86% a lo largo de dos etapas; i) LiBH4, MeOH seco, THF, 0°C, rendimiento cuantitativo.
Etapas a, d) Preparación de 3a,7p-dihidroxi-24-nor-5p-colan-23-oato de metilo (6).
El ácido ursodesoxicólico (2,0 g, 5,1 mmoles) se transformó en 3a,7p-dihidroxi-24-nor-5p-colan-23-oato de metilo (6, 1,6 g, 87%) siguiendo el mismo procedimiento sintético descrito en J. Med. Chem. 2014, 57, 937.
Etapa e) Preparación de 3a,7p-di(terc-butildimetilsililoxi)-5p-colan-24-oato de metilo
El Compuesto 6 (1,2 g, 3,0 mmoles) se protegió en los grupos hidroxilo en la mismas condiciones operativas descritas en el ejemplo 1A, etapa a). La purificación por cromatografía instantánea sobre gel de sílice utilizando hexano/acetato de etilo 9:1 y trietilamina al 0,5% como eluyente, proporcionó éster metílico protegido (1,6 g, 88%). Etapa f) Preparación de 3a,7p-di(terc-butildimetilsililoxi)-5p-colan-24-ol (7)
El éster metílico de cadena lateral (818 mg, 1,3 mmoles) se redujo en la mismas condiciones operativas descritas en el ejemplo 1A, etapa b). La purificación por cromatografía instantánea sobre gel de sílice utilizando hexano/acetato de etilo 98:2 y tiretilamina al 0,5% como eluyente, proporcionó 7 (770 mg, rendimiento cuantitativo).
Etapas g, h) Preparación de sulfato de 3a,7p-dihidroxi-24-nor-5p-colan-23-il-23-sodio (BAR106)
El complejo de trietilamina-trióxido de azufre (2,0 g, 11 mmoles) se añadió a una solución de 7 (660 mg, 1,1 mmoles) en DMF seco (25 mL) siguiendo el mismo procedimiento sintético descrito en J. Med. Chem. 2014, 57, 937. La HPLC
en Nucleodur 100-5 C18 (5 ^m; 10 mm d.i. x 250 mm) con MeOH/H2O (65:35) como eluyente (velocidad de flujo 3 mL/min), proporcionó 442 mg (86% a lo largo de dos etapas) de BAR106 (tR= 8,4 min).
BAR 106: C2sHs9NaO6S
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 54,04 (2H, m, H2-23), 3,48 (2H, m, H-3 y H-7), 1,00 (3H, d, J = 6,5 Hz, H3-21), 0,97 (3H, s, H3-19), 0,72 (3H, s, H3-18).
Etapa i) Preparación de 3a,7p-dihidroxi-24-nor-5p-colan-23-ol (BAR107)
El Compuesto 6 se transformó en BAR107 en las mismas condiciones operativas descritas en la etapa f.
BAR107: C23H4üO3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,60 (1H, m, H-7), 3,51 (1H, m, H-3), 3,50 (2H, m, H2-23), 0,97 (3H, d, ovl, H3-21), 0,96 (3H, s, H3-19), 0,72 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 572,1, 71,9, 60,8, 57,5, 57,1, 44,8, 44,5, 44,0, 41,6, 40,7, 39,9, 38,6, 38,0, 36,1, 35,2, 34,1,31,0, 29,8, 27,9, 23,9, 22,4, 19,5, 12,6;
Ejemplo 1C. Síntesis de sulfato de 7a-hidroxi-5p-colan-24-il-24-sodio (BAR402)
La tosilación y eliminación en el grupo hidroxilo C-3 en el éster metílico 8 seguido de reducción del doble enlace, posterior tratamiento con LiBH4 y sulfatación regioselectiva en el grupo hidroxilo primario C-24 proporcionaron BAR402.
a) p-TsCl, piridina, rendimiento cuantitativo; b) LiBr, Li2CO3, DMF, reflujo, c) H2, Pd(OH)2, THF/MeOH 1:1, temperatura ambiente, rendimiento cuantitativo; d) LiBH4, MeOH seco, THF, 0°C, 79°C; e) Et3N.sO3, DMS, 95°C.
Etapas a-c) Preparación de 7-ceto-5p-colan-24-oato de metilo (9)
A una solución de 8 (965 mg, 2,5 mmoles) en piridina seca (100 mL), se le añadió cloruro de tosilo (4,7 g, 25,0 mmoles) y la mezcla se agitó a temperatura ambiente durante 4 h. Se vertió en agua fría (150 mL) y se extrajo con CH2Cl2 (3 x 150 mL). La capa orgánica combinada se lavó con solución saturada de NaHCO3 (150 mL) y agua (150 mL), y a continuación se secó sobre MgSO4 anhidro y se evaporó a vacío para proporcionar 1,4 g de 3a-tosiloxi-7-ceto-5p-colan-24-oato de metilo (rendimiento cuantitativo). Se añadieron bromuro de litio (434 mg, 5,0 mmoles) y carbonato de litio (370 mg, 5,0 mmoles) a una solución de 3a-tosiloxi-7-ceto-5p-colan-24-oato (1,4 g, 2,5 mmoles) en DMF seco (30 mL), y la mezcla se calentó a reflujo durante 2 h. Después de enfriar a temperatura ambiente, la mezcla se vertió lentamente en una solución de HCl al 10% (20 mL) y se extrajo con CH2Cl2 (3 x 50 mL). La capa orgánica combinada se lavó sucesivamente con agua, solución saturada de NaHCO3 y agua, y a continuación se secó sobre MgSO4 anhidro y se evaporó hasta sequedad para proporcionar 965 mg de residuo oleoso (rendimiento cuantitativo), que se sometió a la siguiente etapa sin ninguna purificación. La hidrogenación en Pd(OH)2 en la mismas condiciones operativas descritas en el ejemplo 1A, etapa d, proporcionó 975 mg de 9 (rendimiento cuantitativo), que se sometió a la siguiente etapa sin ninguna purificación.
Etapa d) Preparación de 5p-colan-7a, 24-diol
Tratamiento con LiBH4 en el compuesto 9 en la mismas condiciones operativas descritas en el ejemplo 1A, etapa b y la purificación por medio de gel de sílice (acetato de etilo-hexano, 85:15) proporcionó 5p-colan-7a, 24-diol en forma de un sólido de color blanco (714 mg, 79%).
Etapa e) Preparación de sulfato de 7a-hidroxi-5p-colan-24-il-24-sodio (BAR402). La sulfatación en C24 se realizó en las mismas condiciones operativas descritas en el ejemplo 1B, etapa g) para proporcionar BAR402 bruto en forma de una sal de amonio. RP18/HPLC en un Nucleodur 100-5 C18 (5 ^m; 10 mm d.i. x 250 mm) con MeOH/H2O (90:10) como eluyente (velocidad de flujo 3 mL/min) proporcionó BAR402 (tR= 6,6 min) en forma de una sal de sodio.
BAR402: C24H41NaO3S
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,96 (2H, t, J = 6,6 Hz, H2-24), 3,78 (1H, brs, H-7), 0,96 (3H, d, J = 6,5 Hz, H3-21), 0,92 (3H, s, H3-19), 0,69 (3H, s, H3-18);
El RMN C13 se registró en Varían Inova a 100 MHz, utilizando CD3OD como disolvente: 569,7, 69,4, 57,7, 51,6, 45,0, 43,8, 41,2, 41,0, 39,0, 37,1, 37,036,3, 34,2, 33,3, 31,7, 29,5, 29,0, 27,3, 24,8, 24,3, 22,7, 21,9, 19,2, 12,3 Ejemplo 2. Preparación de compuestos de fórmula (I) en donde R2 =Et o =CH-CH3
Ejemplo 2A. Síntesis de 6p-etil-3a,7p-dihidroxi-5p-colan-24-ol (BAR501)
La formación de éster metílico y la acetilación en el grupo hidroxilo C-3 en 7-KLCA facilitaron el compuesto intermedio a un 84% de rendimiento en dos etapas. La adición aldólica a un intermedio de silil enol éter generó 11 que se hidrogenó en el doble enlace exocíclico (H2 en Pd(OH)2) proporcionando 12 a un 80% de rendimiento en tres etapas. El tratamiento con NaBH4 en metanol seguido de la reducción con LiBH4 en el producto de reacción bruto proporcionaron una mezcla cuya purificación por HPLC (88% MeOH:H2O) proporcionó BAR501 puro con un rendimiento de 79% con respecto a su epímero C7, BAR504-6b.
a) p-TsOH, MeOH seco; b) anhídrido acético, piridina, rendimiento 84% a lo largo de dos etapas; c) DIPA, n-BuLi, TMSCl, TEA seco, THF seco -78°C; d) acetaldehído, BF3(OEt)2, CH2Cl2, -60°C, 80% a lo largo de dos etapas.
Etapas a-d). Preparación de 3a-acetoxi-6-etilideno-7-ceto-5p-colan-24-oato de metilo (11)
A una solución de ácido 7-cetolitocólico (5 g, 12,8 mmoles), disuelto en 100 mL de metanol seco, se le añadió ácido p-toluenosulfónico (11 g, 64,1 mmoles). La solución se dejó en reposo a temperatura ambiente durante 2 h. La mezcla se inactivó mediante la adición de una solución saturada de NaHCO3. Después de la evaporación del metanol, el residuo se extrajo con EtOAc (3x150 mL). El extracto combinado se lavó con salmuera, se secó con Na2SO4, y se evaporó para proporcionar el éster metílico en forma de un sólido amorfo (5,13 g, rendimiento cuantitativo).
En la solución del éster metílico (5,13 g, 12,7 mmoles) en piridina seca (100 mL), se añadió un exceso de anhídrido acético (8,4 mL, 89 mmoles). Cuando se completó la reacción, la piridina se concentró a vacío. El residuo se vertió en agua fría (100 mL) y se extrajo con AcOEt (3 x 150 mL). Las fases orgánicas combinadas se secaron (Na2SO4) y se concentraron para proporcionar un residuo que se purificó adicionalmente por cromatografía instantánea sobre gel de sílice utilizando hexano/acetato de etilo 8:2 y tiretilamina al 0,5% como eluyente (4,8 g de 10 en forma de un sólido de color blanco, 84% de rendimiento a lo largo de dos etapas).
A una solución de diisopropilamina (23 mL, 0,16 moles) en THF seco (50 mL) se le añadió gota a gota una solución de n-butil litio (60 mL, 2,5 M en hexano, 0,15 moles) a -78°C. Después de 30 minutos, se añadió trimetilclorosilano (27,1 mL, 0,21 moles). Después de 30 minutos adicionales, se añadió una solución de compuesto 10 (4,8 g, 10,7 mmoles) en THF seco (70 mL). La reacción se agitó a -78°C durante 45 minutos adicionales y a continuación se añadió trietilamina (54 mL, 0,38 moles). Después de 1 h, la mezcla de reacción se dejó calentar a
-20°C, se trató con solución acuosa saturada de NaHCO3 (100 mL) y se llevó a temperatura ambiente en 2 h. La fase acuosa se extrajo con acetato de etilo (3x50 mL). Las fases orgánicas combinadas se lavaron a continuación con solución saturada de NaHCO3, agua y salmuera. Después de secar sobre Na2SO4 anhidro, el residuo se evaporó a vacío para proporcionar 6 g de residuo de color amarillo, que se diluyó en CH2Cl2 seco (50 mL) y se enfrió a -78°C. En esta solución agitada, se le añadieron gota a gota acetaldehído (3 mL, 53 mmoles) y BF3- OEt2 (13,5 mL, 0,107 moles). La mezcla de reacción se agitó durante 2 ha -60°C y se dejó calentar a temperatura ambiente. La mezcla se sofocó con una solución acuosa saturada de NaHCO3 y se extrajo con CH2Cl2. Las fases orgánicas combinadas se lavaron con salmuera, se secaron sobre Na2SO4 anhidro y concentraron a vacío.
La purificación por medio de gel de sílice (hexano-acetato de etilo 9:1 y TEA al 0,5%) proporcionó el compuesto 11 (4,1 g, 80%). El análisis de RMN demostró una razón diastereomérica E/Z > 95%. La configuración E en el doble enlace exocíclico se estableció mediante el acoplamiento dipolar H3-26 (51,67)/H-5 (52,62) en espectro Noesy (400 MHz, tiempo de mezcla 400 ms).
(E)-3a-acetoxi-6-etiliden-7-ceto-5p-colan-24-oato (11): C29H44O5
El RMN H1 se registró en Varían Inova 400 MHz, utilizando CDCI3 como disolvente: 86,16 (1H, q, J = 7,0 Hz, H-25), 4,74 (1H, m, H-3), 3,64 (3H, s, COOCH3), 2,62 (1H, dd, J = 13,0, 3,6 Hz, H-5), 1,98 (3H, s, COCH3), 1,67 (3H, d, J = 7,0 Hz, H3-26), 1,00 (3H, s, H3-19), 0,92 (3H, d, J = 6,0 Hz, H3-21), 0,67 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CDCI3 como disolvente: 8204,5, 174,6, 170,7, 143,1, 130,2, 72,5, 54,5, 51,4, 50,7, 48,6, 45,2, 43,5, 39,1, 38,9, 35,1, 34,9, 34,1, 33,4, 31,0, 30,9, 28,4, 25,9 (2C) , 22,8, 21,4, 21,2, 18,4, 12,7, 12,2.
Etapas e) Preparación de 3a-acetoxi-6p-etil-7-ceto-5p-colan-24-oato de metilo (12).
Una solución de 11 (4,0 g, 8,5 mmoles) en THF seco/MeOH seco (100 mL, 1:1 v/v) se hidrogenó en presencia de Pd(OH)2 al 20% en peso sobre carbón activado (100 mg) tipo Degussa. La mezcla se transfirió a un aparato PARR convencional y se lavó con nitrógeno y a continuación con hidrógeno varias veces. El aparato fue sacudido bajo 344,738 Pa (50 psi) de H2. La reacción se agitó a temperatura ambiente durante 8 h.
El catalizador se filtró a través de Celite, y el producto filtrado recuperado se concentró a vacío para proporcionar 12 (4,0 g, rendimiento cuantitativo).
3a-Acetoxi-6p-etil-7-ceto-5p-colan-24-oato de metilo (12): C29H46O5
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 84,65 (1H, m, H-3), 3,66 (3H, s, COOCH3), 2,56 (1H, t, J = 11,5 Hz, H-8), 2,35 (1H, m, H-23a), 2,22 (1H, m, H-23b), 1,99 (3H, s, COCH3), 1,22 (3H, s, H3-19), 0,92 (3H, d, J = 6,3 Hz, H3-21), 0,83 (3H, t, J = 7,2 Hz, H3-26), 0,67 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 8214,7, 174,3, 170,2, 72,6, 61,7, 54,8, 51,3, 49,0, 48,5, 45,3, 42,7, 42,3 (2C), 38,6, 35,4, 35,1, 35,0, 31,0, 30,8, 28,0 (2C), 26,4, 25,7, 24,7, 21,3, 21,1, 18,2, 12,9, 11,9. La configuración p del grupo etilo en C-6 se determinó mediante acoplamientos dipolares H3-26 (80,83)/H3-19 (81,22) y H-8 (82,56)/H-25 (81,83) en espectro Noesy (400 MHz, tiempo de mezcla 400 ms). Etapas f, g) Preparación de 6p-etil-3a,7p-dihidroxi-5p-colan-24-ol (BAR501).
A una solución en metanol del compuesto 12 (1,18 g, 2,5 mmoles), se le añadió un gran exceso de NaBH4 a 0°C. La mezcla se dejó a temperatura ambiente durante 2 horas y a continuación se añadieron gota a gota agua y MeOH durante un período de 15 minutos a 0°C, observándose efervescencia. Después de la evaporación de los disolventes, el residuo se diluyó con agua y se extrajo con AcOEt (3x50 mL). El extracto combinado se lavó con salmuera, se secó con Na2SO4, y se evaporó para proporcionar 1,3 g de un residuo bruto que se sometió a la siguiente etapa sin purificación adicional. El residuo bruto se trató con LiBH4 (2 M en THF) en las mismas condiciones operativas descritas en el ejemplo 1A, etapa b). La purificación por HPLC en un Nucleodur 100-5 C18 (5 |jm; 10 mm d.i. x 250 mm) con MeOH/H2O (88:12) como eluyente (velocidad de flujo 3 mL/min), proporcionó 802 mg de BAR501 (79%, t„= 11 min).
Alternativamente, la etapa f se realizó con Ca(BH4)2, producido in situ.
A una solución de compuesto 12 (500 mg, 1,05 mmoles) y etanol absoluto (4 mL), a 0°C, se le añadió CaCl2 (466 mg, 4,2 mmoles). A la misma solución se le añadió una solución de NaBH4 (159 mg, 4,2 mmoles) en etanol absoluto (4 mL). Después de 4 h a -5°C, se añadió MeOH gota a gota. A continuación, después de la evaporación de los solventes, el residuo se diluyó con agua y se extrajo con AcOEt (3x50 mL). El extracto combinado se lavó con salmuera, se secó con Na2SO4 y se evaporó para proporcionar 500 mg de un residuo bruto que se sometió a la etapa g sin purificación adicional.
BAR501: C26H46O3
El RMN H1 se registró en Varian Inova 700 MHz, utilizando CD3OD como disolvente: 83,74 (1H, dd, J = 10,3, 6,0 Hz, H-7), 3,51 (1H, ovl, H-3), 3,49 (2H, ovl, H2-24), 1,00 (3H, s, H3-19), 0,97 (3H, d, J = 6,5 Hz, H3-21), 0,96 (3H, t, J = 7,6 Hz, H3-26), 0,72 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova 175 MHz, utilizando CD3OD como disolvente: 875,371,9, 63,6, 57,5, 56,5, 51.6, 45,7, 44,9, 42,1, 41,5, 40,4, 40,3, 37,1, 35,8, 32,4, 30,7, 30,3, 29,7, 29,6, 28,3, 26,2, 23,4, 22,1, 19,4, 14,8, 12.7.
Ejemplo 2B. Preparación de 6p-etil-3a,7a-dihidroxi-5p-colan-24-ol (BAR504-6b)
Se preparó BAR504-6b como se describe en el Ejemplo 2A (tR= 20,4 min).
BAR504-6b: C26H46O3
El RMN H1 se registró en Varían Inova 700 MHz, utilizando CD3OD como disolvente: 53,60 (1H, s, H-7), 3,51 (2H, m, H2-24), 3,35 (1H, ovl, H-3), 2,30 (1H, q, J =13,5 Hz, H-4a), 0,97 (3H, d, J =6,8 Hz, H-21), 0,95 (3H, t, J =7,3 Hz, H3-26), 0,94 (3H, s, Hs-19), 0,70 (3H, s, Hs-18).
El RMN C13 se registró en Varian Inova 175 MHz, utilizando CD3OD como disolvente: 571,9, 71,8, 62,7, 56,8, 51,7, 50,5, 46,7, 42,5, 41,4, 40,1, 36,6, 36,4, 36,2, 36,0, 33,2, 32,4, 30,1, 29,5, 28,8, 28,5, 25,3, 23,9, 20,7, 18,4, 13,7, 11,4.
Ejemplo 2C. Síntesis de 6a-etil-3a,7a-dihidroxi-24-nor-5p-colan-23-ol (BAR502), 6p-etil-3a,7p-dihidroxi-24-nor-5pcolan-23-ol (BARn501- no forma parte de la invención) y 6p-etil-3a,7a-dihidroxi-24-n/-5p-colan-23-ol (BARn504-6b) Se sometió 7-KLCA (1 g, 2,56 mmoles) a degradación de Beckmann en C24 y metilación en C-23 facilitando 13 con un rendimiento de 66%. La acetilación en C-3 y alquilación proporcionaron 14 que se hidrogenó proporcionando 15. El tratamiento con MeONa/MeOH proporcionó la hidrólisis concomitante en C-3 y la epimerización en C-6. La reducción simultánea en la función éster metílico de C-23 y en el grupo carbonilo C-7 proporcionó BAR502 con un rendimiento de 89%. El intermedio 15 (250 mg, 0,54 mmoles) también se utilizó como material de partida en la preparación de BARn501 y BARn504-6b.
a) HCOOH, HClO4; b) TFA, anhídrido trifluoroacético, NaNO2; c) KOH 30% en MeOH/H2O 1:1 v/v, 88% a lo largo de tres etapas; d) p-TsOH, MeOH seco; e) anhídrido acético, piridina; f) DIPA, n-BuLi, TMSCl, TEA seco, THF seco -78°C; g) acetaldehído, BF3(OEt)2, CH2Cl2, -60°C, 60% a lo largo de cuatro etapas; h) H2, Pd(OH)2, THF/MeOH 1:1, rendimiento cuantitativo; i) MeONa, MeOH; j) LiBH4, MeOH, THF seco, 0°C, 77% a lo largo de dos etapas.
Etapas a-d) Preparación de 7-ceto-24-nor-LCA de metilo (13)
El Compuesto 13 (660 mg, 1,69 mmoles, 66% a lo largo de cuatro etapas) se preparó a partir de 7-KLCA en las mismas condiciones operativas descritas en el ejemplo 1B, etapas a-d).
Etapas e-h) Preparación de 3a-acetoxi-6p-etil-7-ceto-24-nor-5p-colan-23-oato de metilo (15). El Compuesto 13 (660 mg, 1,69 mmoles) se sometió a las mismas condiciones operativas descritas en el ejemplo 2A, etapas b-d para obtener 603 mg de 14 (78% a lo largo de tres etapas). El análisis de RMN demostró una razón diastereomérica E/Z > 95%. La configuración E en el doble enlace exocíclico se estableció mediante el acoplamiento dipolar H3-25 (5 1,67)/H-5 (52,61) en espectro Noesy (400 MHz, tiempo de mezcla 400 ms).
(E)-3a-acetoxi-6-etiliden-7-ceto-24-nor-5p-colan-23-oato (14): C28H42O5 El RMN H1 se registró en Varian Inova 400 MHz, utilizando CDCls como disolvente: 56,17 (1H, q, J =7,2 Hz, H-24), 4,75 (1H, m, H-3), 3,64 (3H, s, COOCH3), 2,61 (1H, dd, J = 13,1, 4,0 Hz, H-5), 1,98 (3H, s, COCH3), 1,67 (3H, d, J =7,2 Hz, Hs-25), 1,00 (3H, s, Hs-19), 0,97 (3H,d, J = 6,8 Hz, H3-21), 0,67 (3H, s, H3-18).
El RMN C13 se registró en Varían Inova a 100 MHz, utilizando CDCI3 como disolvente: 5204,5, 174,2, 170,5, 143,0, 130,6, 72,5, 54,7, 51,4, 50,7, 48,6, 45,3, 43,7, 41,5, 39,1, 38,8, 34,6, 34,2, 33,6, 33,4, 28,5, 25,9 (2C), 22,8, 21,3 (2C), 19,7, 12,7, 12,1. La hidrogenación en Pd (OH)2 en las mismas condiciones operativas descritas en el ejemplo 2A, etapa e, proporcionó 600 mg de 15 (rendimiento cuantitativo).
La configuración p del grupo etilo en C-6 se determinó mediante acoplamientos dipolares H3-25 (5 0,83)/H3-19 (5 1,22) en espectro Noesy (400 MHz, tiempo de mezcla 400 ms).
3a-acetoxi-6p-etil-7-ceto-24-nor-5p-colan-23-oato (15): C28H44O5
El RMN H1 se registró en Varian Inova 400 MHz, utilizando CDCh como disolvente: 54,65 (1H, m, H-3), 3,67 (3H, s, COOCH3), 2,60 (1H, t, J = 11,2 Hz, H-8), 2,43 (1H, dd, J = 14,2, 2,6 Hz, H-22a), 1,98 (3H, s, COCH3), 1,88 (1H, m ovl, H-6), 1,22 (3H, s, H3-19), 0,98 (3H, d, J = 6,4 Hz, H3-21), 0,83 (3H, t, J = 7,0 Hz, H3-25), 0,70 (3H, s, H3-18). El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CDCh como disolvente: 5215,3, 174,0, 170,5, 72,8, 61,9, 55,0, 51,4, 49,2, 48,7, 45,5, 42,9, 42,6, 41,4, 38,7 (2C), 35,6, 35,3, 34,9, 28,3 (2C), 26,5, 25,9, 24,8, 21,4, 21,3, 19.6, 13,0, 12,1.
Etapas i, j) Preparación de 6a-etil-3a,7a-dihidroxi-24-nor-5p-colan-23-ol (BAR502)
A una solución de compuesto 15 (450 mg, 1,0 mmoles) y metanol seco (4 mL), se le añadió MeONa (20 mL, 0,5 M en MeOH, 10 mmoles). Después de 24 h, se añadió gota a gota H2O. A continuación, después de la evaporación de los solventes, el residuo se diluyó con agua y se extrajo con AcOEt (3x50 mL). El extracto combinado se lavó con agua, se secó con Na2SO4 y se evaporó para proporcionar 16 que se sometió a la etapa g sin más purificación. 6a-Etil-3a-hidroxi-7-ceto-24-nor-5p-colan-23-oato de metilo (16): C26H42O4
El RMN H1 se registró en Varian Inova 400 MHz, utilizando CDCh como disolvente: 53,64 (3H, s, COOCH3), 3,45 (1H, m, H-3), 2,83 (1H, q, J = 7,3 Hz, H-6), 2,51 (1H, t, J = 11,2 Hz, H-8), 2,45 (1H, dd, J =14,5, 3,2 Hz, H-22a), 1,26 (3H, s, H3-19), 0,98 (3H, d, J = 6,6 Hz, H3-21), 0,81 (3H, t, J = 7,0 Hz, H3-25), 0,73 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CDCh como disolvente: 5214,9, 175,4, 71,6, 56,2, 53,2, 52,0, 51,9, 51,0, 50,5, 45,2, 43,8, 42,2, 40,2, 36,7, 35,3, 34,8, 32,5, 30,5, 29,4, 25,6, 24,0, 22,9, 20,1, 20,0, 12.6, 12,4.
El Compuesto 16 se sometió a reducción con LiBH4 en las mismas condiciones operativas descritas en el ejemplo 1A, etapa g. La cromatografía en gel de sílice eluyendo con hexano/EtOAc 6:4 proporcionó BAR502 (274 mg, 70% en dos etapas). Se obtuvo una muestra analítica por HPLC en un Nucleodur 100-5 C18 (5 pm; 4,6 mm d.i. x 250 mm) con MeOH/H2O (88:12) como eluyente (velocidad de flujo 1 ml/min, tR= 10.8 min).
BAR502: C25H44O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,65 (1H, s, H-7), 3,61 (1H, m, H-23a), 3,53 (1H, m, H-23b) 3,31 (1H, m, H-3), 0,97 ( 3H, d, J = 6,6 Hz, H3-21), 0,92 (3H, s, H3-19), 0,91 (3H, t, J = 7,0 Hz, H3-25), 0,71 (3H, s, H3-18).
El RMN-C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 73,2, 71,1, 60,7, 57,7, 51,4, 46,9, 43,8, 42,9, 41,3, 40,9, 39,8, 36,7, 36,5, 34,6, 34,5, 34,2, 31,2, 29,4, 24,5, 23,7, 23,4, 21,8, 19,3, 12,1, 11,9.
Etapas k, l). Preparación de 6p-etil-3a,7p-dihidroxi-24-nor-5p-colan-23-ol (BARn501) y 6p-etil-3a,7a-dihidroxi-24-nor-5p-colan-23-ol (BARn504-6b). El Compuesto 15 (100 mg, 0,22 mmoles) se sometió a las mismas condiciones operativas descritas en el ejemplo 2A, etapas f-g. La purificación por HPLC en un Nucleodur 100-5 C18 (5 pm; 10 mm d.i. x 250 mm) con MeOH/H2O (86:14) como eluyente (velocidad de flujo 3 ml/min), proporcionó 47 mg de BARn501 (54%, tR= 11 min) y 20 mg de BARn504-6b (23%, tR= 15 min).
BARn501: C25H44O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,73 (1H, dd, J = 10,5, 5,5 Hz, H-7), 3,61 (1H, m, H-23a), 3,51 (1H, m, ovl, H-23b), 3,51 (1H, m, ovl, H-3), 0,98 ( 3H, d, ovl, H3-21), 0,97 (3H, s, H3-19), 0,96 (3H, t, ovl, H3-25), 0,70 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 75,2, 71,8, 60,8, 57,5, 56,6, 51,5, 45,5, 44,8, 42,0, 41,4, 40,7, 40,3, 39,9, 36,9, 36,0, 34,2, 30,5, 29,6, 28,3, 26,2, 23,4, 22,0, 19,4, 14,7,
12,9.
BARn504-6b: C25H44O3
El RMN H1 se registró en Varían Inova a 400 MHz, utilizando CD3OD como disolvente: 53,63 (1H, m, H-23a), 3,60 (1H, m, H-7), 3,55 (1H, m, H-23b), 3,37 (1H, m, H-3), 2,30 (1H, q, J = 12,5 Hz, H-4a), 0,97 (3H, d, J = 6,6 Hz, H3-21), 0,95 (3H, s, H3-19), 0,95 (3H, t, J =7,0 Hz, H3-25), 0,72 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 572,8, 72,7, 60,8, 57,9, 52,7, 51,4, 47,5, 43,7, 42,3, 41,0, 39,9, 37,5, 37,3, 36,7, 34,2, 33,3, 31,0, 29,6, 29,4, 26,2, 24,8, 21,6, 19,3 , 14,5, 12,1.
Ejemplo 2D. Síntesis de 6-etiliden-3a,7p-dihidroxi-5p-colan-24-ol (BAR503), 6a-etil-3a,7p-dihidroxi-5p-colan-24-ol (BAR501-6a - no forma parte de la invención), 6-etiliden-3a,7p-dihidroxi-24-nor-5p-colan-23-ol (BARn503 - no forma parte de la invención) y 6a-etil-3a,7p-dihidroxi-24-nor-5p-colan-23-ol (BARn501-6a - no forma parte de la invención) El intermedio 11 se sometió a reducción con NaBH4 seguida de tratamiento con UBH4. Alternativamente, se llevó a cabo de manera directa el tratamiento con LiAlH4, lo que permitió la reducción concomitante en C-24 y C-7. BAR503 también se utilizó como material de partida para BAR501-6a por hidrogenación sobre catalizador Pd(OH)2. El mismo protocolo sintético se realizó en el intermedio 14 produciendo los derivados en la posición 23 correspondientes, BARn503 y BARn501-6a.
a) NaBH4 , MeOH; b) UBH4 , MeOH seco, THF, 0°C, 85% a lo largo de dos etapas; c) H2 , Pd(OH)2 , THF:MeOH 1:1 v/v.
Etapas a, b). Preparación de 6-etiliden-3a,7p-dihidroxi-5p-colan-24-ol (BAR503) y 6-etiliden-3a,7p-dihidroxi-24-nor-5p-colan-23-ol (BARn503).
El Compuesto 11 (1 g, 2,11 mmoles) se sometió a las mismas condiciones operativas descritas en el ejemplo 2A, etapas f, g. La purificación por HPLC en un Nucleodur 100-5 C18 (5 ^m; 10 mm d.i. x 250 mm) con MeOH/H2O (88:12) como eluyente (velocidad de flujo de 3 ml/min), proporcionó 727 mg de BAR503 (85% en dos etapas, tR= 9,2 min). Alternativamente, el tratamiento con LiAIH4 en 11 proporcionó BAR503.
BAR503: C26H44O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 55,66 (1H, q, J = 6,9 Hz, H-25), 3,90 (1H, d, J = 9,8 Hz, H-7), 3,55 (1H, m, H-3), 3,50 (2H, m, H2-24), 2,50 (1H, dd, J = 4,0, 13,1 Hz, H-5), 1,62 (3H,d, J = 6,9 Hz, H3-26), 0,97 (3H, d, J = 6,8 Hz, H3-21), 0,81 (3H, s, H3-19), 0,70 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 142,7, 114,5, 73,4, 71,1, 63,6, 57,1, 56,1, 45,2, 44,9, 44,2, 40,7, 40,2, 36,3, 36,2, 35,9, 34,7, 32,4, 30,2, 29,5, 28,8, 27,4, 22,6, 21,5, 18,5, 11,8, 11,7.
El mismo protocolo sintético se realizó con el intermedio 14. La purificación por HPLC en un Nucleodur 100-5 C18 (5 ^m; 10 mm d.i. x 250 mm) con MeOH/H2O (86:14) como eluyente (velocidad de flujo 3 ml/min), proporcionó BARn503 (tR= 8 min).
BARn503: C25H42O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 55,66 (1H, q, J = 6,8 Hz, H-24), 3,92 (1H, d, J = 9,9 Hz, H-7), 3,60 (1H, m, H-23a), 3,56 (1H, m, H-3), 3,55 (1H, m, H-23b), 2,52 (1H, dd, J = 3,7, 13,2 Hz, H-5), 1,63 (3H, d, J = 6,8 Hz, H3-25), 0,98 (3H, d, J = 6,5 Hz, H3-21), 0,95 (3H, s, H3-19), 0,71 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 143,7, 115,4, 74,1, 71,8, 60,8, 58,0, 57,1, 46,1, 45,9, 45,1, 41,6, 41,1, 39,9, 37,0, 36,4, 35,8, 34,1, 30,9, 29,8, 28,1, 23,5, 22,5, 19,5, 12,7,
Etapa c). Preparación de 6a-etil-3a,7p-dihidroxi-5p-colan-24-ol (BAR501-6a) y 6a-etil-3a,7p-dihidroxi-24-nor-5pcolan-23-ol (BARn501-6a) Se sometió BAR503 (350 mg, 0,86 mmoles) a las mismas condiciones operativas descritas en el ejemplo 2A, etapa e, obteniendo BAR501-6a con rendimiento cuantitativo.
BAR501-6a: C26H46O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,50 (2H, t, J = 6,8 Hz, H3-24), 3,44 (1H, m, H-3), 3,07 (1H, t, J = 9,8 Hz, H-7), 0,96 (3H, d, J = 6,8 Hz, H3-2 I), 0,95 (3H, s, H3-19), 0,86 (3H, t, J = 7,4 Hz, H3-26), 0,71 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 76,5, 72,3, 63,6, 57,9, 57,3, 46,3, 45,0, 44,8, 41,8, 41,0, 39,9, 37,0, 36,4, 35,5, 33,3, 31,3, 31,0, 30,3, 29,8, 27,8, 24,3, 22,5, 22,0, 19,3, 12,8, 11,8.
Se sometió BARn503 a las mismas condiciones operativas descritas en el ejemplo 2A, etapa e, obteniendo BARn501-6a con rendimiento cuantitativo.
BARn501-6a: C25H44O3
El RMN H1 se registró en Varian Inova a 400 MHz, utilizando CD3OD como disolvente: 53,62 (1H, m, H-23a), 3,54 (1H, m, H-23b), 3,45 (1H, m, H-3), 3,08 (1H, t, J = 9,8 Hz, H-7), 0,97 (3H, d, J = 6,5 Hz, H3-21), 0,95 (3H, s, H3-19), 0,86 (3H, t, J =7,4 Hz, H3-25), 0,73 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova a 100 MHz, utilizando CD3OD como disolvente: 5 76,4, 72,5, 60,8, 57,9, 57,2, 46,2, 45,1, 44,7, 41,8, 41,2, 40,0, 39,8, 36,5, 35,6, 34,2, 31,2, 30,9, 29,9, 27,9, 24,1, 22,7, 22,0, 19,5, 12,7, 11,7.
Ejemplo 2E Síntesis de 6a-etil-3a,7a-dihidroxi-24-nor-5p-colan-23-nitrilo (BAR506 - no forma parte de la invención) Se transformó 7-KLCA en nitrilo 17 siguiendo el mismo procedimiento sintético descrito en el Ejemplo 1B, etapas ab. La alquilación seguida de reducción del doble enlace y epimerización en C-6 en las mismas condiciones operativas descritas en el ejemplo 2A, etapas c-d y en el ejemplo 2C, etapa i, respectivamente proporcionaron 18. El tratamiento con LiBH4 como en el ejemplo 2C, etapa j, proporcionó el grupo hidroxilo 7a deseado en BAR506.
a) HCOOH, HCIO4; b) TFA, trifluoroacetic anhydride, NaNO:; c) DIPA, n-BuLi, TMSC1, TEA dry, THF dry
-78 °C; d) acetaldehyde, BF3(OEt)2, CH2C12, -60 °C; e) H; Pd(OH)2, THF/MeOH 1:1; f) MeONa, MeOH; g) FiBH4, MeOH, THF dry, 0 °C
a) HCOOH, HClO4; b) TFA, anhídrido trifluoroacético, NaNO2; c) DIPA, n-BuLi, TMSCl, TEA seco, THF seco -78°C; d) acetaldehído, BF3 (OEt)2 , CH2O 2 , -60°C; e) H2 , Pd(OH)2 , TMF/MeOH 1:1; f) MeONa, MeOH; g) LiBH4, MeOH, THF seco, 0°C
BAR506: C25H41NO2
El RMN H1 se registró en Varian Inova 700 MHz, utilizando CD3OD como disolvente: 53,66 (1H, br s, H-7), 3,31 (1H, ovl, H-3), 2,46 (1H, dd, J = 3,8, 16,9 Hz, H-22a), 2,34 (1H, dd, J = 7,4, 16,9 Hz, H-22b), 1,16 (3H, d, J = 6,5 Hz, H3-21), 0,91 (3H, t, J =7,5 Hz, H3-25), 0,92 (3H, s, H3-19), 0,73 (3H, s, H3-18).
El RMN C13 se registró en Varian Inova 175 MHz, utilizando CD3OD como disolvente: 5120,3, 72,9, 70,9, 56,1, 51,5, 46,7, 43,4, 42,9, 41,4, 40,2, 36,5, 36,2, 34,3 (2C), 34,2, 30,7, 29,2, 24,9, 24,4, 23,4, 23,3, 21,9, 18,5, 12,1, 11,6. Actividades biológicas. La actividad de los compuestos seleccionados se probó in vitro utilizando un modelo de células completas transfectadas con genes informadores para establecer la selectividad de los compuestos que se muestran en la tabla 1 hacia FXR y TGR5/GPBAR1 en comparación con el ácido quenodesoxicólico (CDCA) y el TLCA. CDCA es un ácido biliar primario que funciona como un ligando endógeno para FXR, mientras que TlCa es un ligando fisiológico para TGR5/GPBAR1. En este ensayo, se cultivaron células HepG2 (una línea celular derivada de hígado) a 37°C en medio esencial mínimo con sales de Earl que contenía 10% de suero fetal bovino (FBS), 1% de L-glutamina y 1% de penicilina/estreptomicina. Las células HEK-293T se cultivaron a 37°C en D-MEM que contenía 10% de suero fetal bovino (FBS), 1% de L-glutamina y 1% de penicilina/estreptomicina. Los experimentos
de transfección se realizaron utilizando Fugene HD de acuerdo con las especificaciones del fabricante. Las células se sembraron en una placa de 24 pocillos a 5 x 104 células/pocillo. Para la transactivación mediada por FXR, las células HepG2 se transfectaron con 100 ng de pSG5-FXR, 100 ng de pSG5-RXR, 100 ng de pGL4.70, un vector que codifica el gen Renilla humano y 250 ng del vector informador p(hsp27)-TK-LUC que contenía el elemento de respuesta a FXR IR1 clonado del promotor de la proteína de choque térmico 27 (hsp27).
Para la transactivación mediada por GPBAR1, las células HEK-293T se transfectaron con 200 ng de pGL4.29, un vector informador que contenía un elemento de respuesta a AMPc (CRE) que impulsa la transcripción del gen informador luciferasa luc2P, con 100 ng de pCMVSPORT6-GPBAR1 humano, y con 100 ng de pGL4.70, un vector que codifica el gen Renilla humano. En los experimentos de control, las células HEK-293T se transfectaron solo con los vectores pGL4.29 y pGL4.70 para excluir cualquier posibilidad de que los compuestos pudieran activar el CRE de una manera independiente de GPBAR1. A las 24 h de la transfección, las células se estimularon durante 18 h con TLCA 10 |jM como agente de control o agonistas putativos de GPBAR1 a la misma concentración. Después de los tratamientos, las células se lisaron en 100 j L de tampón de lisis (Tris-fosfato 25 mM, pH 7,8; DTT 2 mM; 10% de glicerol; 1% de Triton X-100), y se sometieron a ensayo 20 j L de producto lisado celular para determinar la actividad luciferasa utilizando el sistema de ensayo de luciferasa. La luminiscencia se midió utilizando un luminómetro Glomax 20/20. Las actividades luciferasa se normalizaron frente a las actividades de Renilla. El antagonismo contra FXR de GPBAR1/TGR5 se midió como porcentaje de actividad en el ensayo de transactivación que demanda TLCA como ejemplo de agonismo.
Animales y protocolos. Se alojaron ratones con el gen GPBAR1 inactivado (“null”) (GPBAR1-B6 = ratones GPBAR12/2, generados directamente en un fondo C57BL/6NCrl) y compañeros de camada congénicos en C57BL/6NCrl a temperaturas (22°C) y fotoperiodos (12:12 horas de ciclo de luz/oscuridad) controlados, permitiendo el acceso sin restricciones a comida convencional para ratones y agua del grifo y se aclimataron a estas condiciones durante al menos 5 días antes de su inclusión en un experimento.
Prueba de rascado. Se utilizaron ratones macho GPBAR1-/" y sus compañeros de camada congénicos (de 8 a 12 semanas de edad) para estos estudios. El pelo en la base del cuello se afeitó y los ratones se colocaron en cilindros individuales en un estante de vidrio. Se dibujó una circunferencia de aprox. 0,5 cm de diámetro en el cuello y se inyectaron agentes de prueba en esta zona. Los ratones se aclimataron a la sala experimental, el aparato de retención y los investigadores durante períodos de 2 horas durante 2 días sucesivos antes de los experimentos. El comportamiento de rascado fue cuantificado por 2 observadores que desconocían los agentes o los genotipos probados. Un rasguño se definió como el levantamiento de la extremidad posterior al sitio de inyección y a continuación la colocación de la pata en el suelo, independientemente del número de golpes. Si los recuentos diferían en más de 5 rasguños durante un período de 30 minutos, ambos observadores reevaluaban los registros. Los resultados se expresaron como el número de eventos de rascado durante 30 o 60 minutos de observación. Los agentes probados fueron: DCA (25 jg), TLCA (25 jg), UDCA (25 jg ) y BAR502 (25 jg), o con ácido betulínico (50 jg), ácido oleanólico (50 jg). LCA y DCA se disolvieron en DMSO y los otros agentes en NaCl al 0,9% (10 j L). En otro entorno experimental a los ratones GPBAR1-/" y sus compañeros de camada congénicos se les administró alfanaftilisotiocianato (ANIT) (25 mg/kg, per os) disuelto en aceite de oliva o aceite de oliva solo (ratones de control) o con la combinación de ANIT más BAR502 (15 mg/kg una vez al día, por os) durante 10 días. El día 5 se evaluó el rascado espontáneo durante 60 minutos y después de la inyección subcutánea de 25 jg de DCA. Los niveles séricos de bilirrubina total, aspartato aminotransferasa (AST) y fosfatasa alcalina se midieron mediante pruebas de química clínica de rutina realizadas en un analizador automático Hitachi 717. Para el modelo de estrógenos, a los ratones C57BL6 de tipo salvaje se les administraron 10 mg/kg i.p. con 17a-Etinilestradiol (17aE2) disuelto en PEG o PEG solo (ratones de control) o la combinación de 17aE2 y BAR502 (15 mg/kg al día, por os) durante 8 días. Al final del estudio, se registraron el rascado espontáneo y el rascado inducido por la inyección s.c. de 25 jg de DCA. También se midieron el peso de la vesícula biliar y los niveles séricos de bilirrubina y fosfatasa alcalina. A lo largo de los estudios, los investigadores fueron evaluados visualmente por lo menos dos veces al día de lunes a viernes y una vez al día durante el fin de semana por investigadores y por personal altamente capacitado de la instalación de animales, incluido el veterinario de la instalación de animales. Los animales se pesaron diariamente y se sacrificaron en los puntos de tiempo indicados o cuando sus condiciones clínicas se volvían críticas según lo evaluado mediante una reducción de peso corporal superior al 25% del peso basal en 7 días. Además, los animales fueron sacrificados cuando en la evaluación diaria demostraron incapacidad para elevarse o deambular. Los ratones fueron sacrificados por una sobredosis de pentobarbital sódico (> 100 mg/kg i.p.).
Claims (10)
2. El compuesto de acuerdo con la reivindicación 1, siendo dicho compuesto 6p-etil-3a,7p-dihidroxi-5p-colan-24-ol.
4. Un compuesto para su uso como medicamento, de acuerdo con la reivindicación 3, seleccionándose dicho compuesto del grupo que consiste en 6p-etil-3a,7p-dihidroxi-5p-colan-24-ol y 6a-etil-3a,7a-dihidroxi-24-nor-5p-colan-23-ol.
5. Un compuesto para su uso, como modulador de FXR y/o TGR5/GPBAR1, en la prevención y/o el tratamiento de trastornos gastrointestinales, enfermedades hepáticas, enfermedades cardiovasculares, aterosclerosis, enfermedades metabólicas, enfermedades infecciosas, cáncer, trastornos renales, trastornos inflamatorios y trastornos neurológicos, seleccionándose dicho compuesto del grupo que consiste en
6. Una composición farmacéutica que comprende un compuesto seleccionado del grupo que consiste en BAR501, BAR503 y BAR504-6b como se define en la reivindicación 1 y al menos otro ingrediente farmacéutico.
7. Un procedimiento para preparar un compuesto seleccionado del grupo que consiste en
comprendiendo dicho procedimiento someter un compuesto de fórmula (VIII) a una condensación aldólica poniendo en contacto de ese modo un compuesto de fórmula (VIII)
en donde n es 0 o 1, P es un grupo protector de hidroxilo, con alquil litio, tal como nBuLi, y posteriormente con acetaldehído, preferiblemente también en presencia de BF3(OEt)2, para obtener un compuesto de fórmula (IX)
en donde n y P se describen como anteriormente y sometiendo a continuación el compuesto de fórmula (IX) a una hidrogenación catalítica, para obtener un compuesto de fórmula (X)
8. El procedimiento de acuerdo con la reivindicación 7, para preparar un compuesto seleccionado del grupo que consiste en
en donde el compuesto de fórmula (X) se somete a reducción de carbonilo en C7 poniendo en contacto el compuesto de fórmula (X) con NaBH4 o Ca(BH4)2 para obtener una mezcla de alfa-OH y beta-OH en C7; y posteriormente se somete a un tratamiento con LiBH4 que reduce completamente la función éster metílico en la cadena lateral a -CH2OH.
9. Un procedimiento para preparar un compuesto de fórmula
comprendiendo dicho procedimiento poner en contacto con MeONa/MeOH un compuesto de fórmula (XIV)
en donde n es 0, R8 es OAc para obtener la epimerización del estereocentro C6 obteniendo así un compuesto de fórmula (XI)
en donde el tratamiento con MeONa/MeOH proporciona simultáneamente la hidrólisis del grupo acetoxi C3.
10. El procedimiento de acuerdo con la reivindicación 9, en donde se obtiene una reducción de carbonilo en C7 poniendo en contacto un compuesto de fórmula (XI) o el compuesto correspondiente que tiene COOH en la cadena lateral, con LiBH4 obteniendo casi exclusivamente alfa-OH en C7; en donde el tratamiento con LiBH4 reduce simultáneamente, si está presente, la función éster metílico en la cadena lateral a -CH2OH y desprotege OAc, si está presente en C3.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| ITFI20140130 | 2014-05-29 | ||
| PCT/EP2015/061802 WO2015181275A1 (en) | 2014-05-29 | 2015-05-28 | Cholane derivatives for use in the treatment and/or prevention of fxr and tgr5/gpbar1 mediated diseases |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2768718T3 true ES2768718T3 (es) | 2020-06-23 |
Family
ID=51454763
Family Applications (2)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19204247T Active ES2938874T3 (es) | 2014-05-29 | 2015-05-28 | Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1 |
| ES15731260T Active ES2768718T3 (es) | 2014-05-29 | 2015-05-28 | Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1 |
Family Applications Before (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES19204247T Active ES2938874T3 (es) | 2014-05-29 | 2015-05-28 | Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1 |
Country Status (25)
| Country | Link |
|---|---|
| US (2) | US10407462B2 (es) |
| EP (2) | EP3626725B1 (es) |
| JP (1) | JP6820253B2 (es) |
| KR (1) | KR102491556B1 (es) |
| CN (2) | CN106661079B (es) |
| AU (1) | AU2015265893B2 (es) |
| CA (1) | CA2948585C (es) |
| CY (1) | CY1122631T1 (es) |
| DK (2) | DK3149019T3 (es) |
| EA (1) | EA032820B1 (es) |
| ES (2) | ES2938874T3 (es) |
| FI (1) | FI3626725T3 (es) |
| HR (2) | HRP20200225T1 (es) |
| HU (2) | HUE048351T2 (es) |
| LT (2) | LT3626725T (es) |
| MA (1) | MA39881B1 (es) |
| MX (2) | MX388957B (es) |
| PH (1) | PH12016502327A1 (es) |
| PL (2) | PL3626725T3 (es) |
| PT (2) | PT3149019T (es) |
| RS (2) | RS59910B1 (es) |
| SG (2) | SG11201609403UA (es) |
| SI (2) | SI3626725T1 (es) |
| SM (2) | SMT202000070T1 (es) |
| WO (1) | WO2015181275A1 (es) |
Families Citing this family (52)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| EP2545964A1 (en) | 2011-07-13 | 2013-01-16 | Phenex Pharmaceuticals AG | Novel FXR (NR1H4) binding and activity modulating compounds |
| SMT202000070T1 (it) * | 2014-05-29 | 2020-03-13 | Bar Pharmaceuticals S R L | Derivati del colano per l'uso del trattamento e/o la prevenzione di malattie mediate da fxr e tgr5/gpbar1 |
| CN106459136B (zh) * | 2014-09-28 | 2018-06-26 | 江苏盛迪医药有限公司 | 一种奥贝胆酸的制备方法 |
| SG11201703717SA (en) | 2014-11-06 | 2017-06-29 | Enanta Pharm Inc | Bile acid analogs an fxr/tgr5 agonists and methods of use thereof |
| CN111944006B (zh) * | 2014-11-17 | 2021-12-17 | 正大天晴药业集团股份有限公司 | 新的7-酮-6β-烷基胆烷酸衍生物在制备奥贝胆酸以及其在医药领域的用途 |
| KR102546748B1 (ko) | 2014-11-19 | 2023-06-22 | 엔제트피 유케이 리미티드 | 스테로이드 FXR 조절인자를 제조하기 위한 중간체로서의 6α-알킬-3,7-다이온 스테로이드 |
| EA033445B1 (ru) | 2014-11-19 | 2019-10-31 | Nzp Uk Ltd | 5-бета-6-алкил-7-гидрокси-3-оновые стероиды в качестве промежуточных соединений для получения стероидных модуляторов fxr |
| KR102527821B1 (ko) | 2014-11-19 | 2023-05-02 | 엔제트피 유케이 리미티드 | 스테로이드 FXR 조절인자를 제조하기 위한 중간체로서의 6α-알킬-6,7-다이온 스테로이드 |
| CN107207559B (zh) | 2014-11-19 | 2019-10-25 | Nzp英国有限公司 | 作为制备类固醇fxr调节剂的中间体的6-烷基-7-羟基-4-烯-3-酮类固醇 |
| US11578097B2 (en) | 2014-11-26 | 2023-02-14 | Enanta Pharmaceuticals, Inc. | Tetrazole derivatives of bile acids as FXR/TGR5 agonists and methods of use thereof |
| US10208081B2 (en) | 2014-11-26 | 2019-02-19 | Enanta Pharmaceuticals, Inc. | Bile acid derivatives as FXR/TGR5 agonists and methods of use thereof |
| EP3223823A4 (en) | 2014-11-26 | 2018-10-17 | Enanta Pharmaceuticals, Inc. | Bile acid analogs as fxr/tgr5 agonists and methods of use thereof |
| EP3256134A4 (en) | 2015-02-11 | 2018-10-03 | Enanta Pharmaceuticals, Inc. | Bile acid analogs as fxr/tgr5 agonists and methods of use thereof |
| WO2016161003A1 (en) | 2015-03-31 | 2016-10-06 | Enanta Phamraceuticals, Inc. | Bile acid derivatives as fxr/tgr5 agonists and methods of use thereof |
| US10800807B2 (en) | 2015-06-19 | 2020-10-13 | Intercept Pharmaceuticals, Inc. | TGR5 modulators and methods of use thereof |
| AU2016325619A1 (en) | 2015-09-24 | 2018-04-12 | Intercept Pharmaceuticals, Inc. | Methods and intermediates for the preparation bile acid derivatives |
| WO2017147159A1 (en) * | 2016-02-23 | 2017-08-31 | Enanta Pharmaceuticals, Inc. | Deuterated bile acid derivatives as fxr/tgr5 agonists and methods of use thereof |
| WO2017147174A1 (en) * | 2016-02-23 | 2017-08-31 | Enanta Pharmaceuticals, Inc. | Heteroaryl containing bile acid analogs as fxr/tgr5 agonists and methods of use thereof |
| US10323060B2 (en) | 2016-02-23 | 2019-06-18 | Enanta Pharmaceuticals, Inc. | Benzoic acid derivatives of bile acid as FXR/TGR5 agonists and methods of use thereof |
| ES2874682T3 (es) * | 2016-03-11 | 2021-11-05 | Intercept Pharmaceuticals Inc | Derivados de 3-desoxi y composiciones farmacéuticas de los mismos |
| CN105859817A (zh) * | 2016-05-09 | 2016-08-17 | 成都宇西医药技术有限公司 | 一种制备3α-羟基-6-乙烯基-7-酮基-5β-胆烷酸的方法 |
| GB201608777D0 (en) | 2016-05-18 | 2016-06-29 | Dextra Lab Ltd | Compounds |
| WO2017207648A1 (en) | 2016-05-31 | 2017-12-07 | Bionice, S.L.U | Process and intermediates for the preparation of obeticholic acid and derivatives thereof |
| EP3464316A4 (en) * | 2016-06-01 | 2020-02-19 | Dr. Reddy's Laboratories Ltd. | PROCESS FOR THE PREPARATION OF OBETICHOLIC ACID |
| CA3252823A1 (en) | 2016-06-13 | 2025-02-25 | Gilead Sciences, Inc. | Substituted tert-butyl-3-(2-chloro-phenyl)-3-hydroxyazetidine-1-carboxylate compounds |
| MX385718B (es) | 2016-06-13 | 2025-03-18 | Gilead Sciences Inc | Compuestos moduladores de fxr (nr1h4). |
| IT201600068742A1 (it) * | 2016-07-01 | 2018-01-01 | Bar Pharmaceuticals Soc A Responsabilita Limitata | Derivati dell'acido iodesossicolico e loro uso |
| CN110121347A (zh) | 2016-11-29 | 2019-08-13 | 英安塔制药有限公司 | 制备磺酰脲胆汁酸衍生物的方法 |
| US10472386B2 (en) | 2017-02-14 | 2019-11-12 | Enanta Pharmaceuticals, Inc. | Bile acid derivatives as FXR agonists and methods of use thereof |
| PT3600309T (pt) | 2017-03-28 | 2022-10-03 | Gilead Sciences Inc | Combinações terapêuticas para o tratamento de doenças hepáticas |
| BR112019020780A2 (pt) * | 2017-04-07 | 2020-04-28 | Enanta Pharm Inc | processo para preparação de derivados de ácido biliar de carbamato de sulfonila |
| CN109021056B (zh) * | 2017-06-09 | 2021-03-09 | 博瑞生物医药(苏州)股份有限公司 | 法尼酯x受体激动剂 |
| CN109021055B (zh) * | 2017-06-09 | 2021-04-09 | 博瑞生物医药(苏州)股份有限公司 | Fxr激动剂 |
| CN109021054B (zh) * | 2017-06-09 | 2021-04-09 | 博瑞生物医药(苏州)股份有限公司 | 一种fxr激动剂 |
| WO2019020067A1 (zh) * | 2017-07-26 | 2019-01-31 | 正大天晴药业集团股份有限公司 | 甾体类衍生物fxr激动剂的制备方法 |
| CN111247160B (zh) * | 2017-11-02 | 2021-09-28 | 正大天晴药业集团股份有限公司 | 一种胆酸类化合物的制备方法 |
| EP3911647B1 (en) | 2019-01-15 | 2023-12-13 | Gilead Sciences, Inc. | Isoxazole compound as fxr agonist and pharmaceutical compositions comprising same |
| CA3233305A1 (en) | 2019-02-19 | 2020-08-27 | Gilead Sciences, Inc. | Solid forms of fxr agonists |
| JP2022552655A (ja) | 2019-10-07 | 2022-12-19 | キャリーオペ,インク. | Gpr119アゴニスト |
| CN112824425B (zh) * | 2019-11-21 | 2023-10-03 | 成都西岭源药业有限公司 | 一种6-位烯基取代胆酸化合物及其制备方法和应用 |
| IL295825A (en) | 2020-02-28 | 2022-10-01 | Kallyope Inc | gpr40 agonists |
| IT202000008515A1 (it) | 2020-04-21 | 2021-10-21 | Bar Pharmaceuticals Soc A Responsabilita Limitata | Metodo per la sintesi di un derivato del colano |
| WO2021236617A1 (en) | 2020-05-19 | 2021-11-25 | Kallyope, Inc. | Ampk activators |
| CA3183575A1 (en) | 2020-06-26 | 2021-12-30 | Iyassu Sebhat | Ampk activators |
| TW202333741A (zh) * | 2021-11-15 | 2023-09-01 | 大陸商海湃泰克(北京)生物醫藥科技有限公司 | 多環化合物及其方法 |
| IT202200011705A1 (it) * | 2022-06-01 | 2023-12-01 | Prec Bio Therapeutics S R L | Derivati del colesterolo e loro usi |
| WO2024006537A1 (en) * | 2022-07-01 | 2024-01-04 | Intercept Pharmaceuticals, Inc. | Methods for ameliorating cognitive impairment using bile acid derivatives |
| IT202200018669A1 (it) | 2022-09-13 | 2024-03-13 | Bar Pharmaceuticals Soc A Responsabilita Limitata | Combinazioni farmaceutiche comprendenti derivati del colano e loro usi |
| EP4611888A1 (en) * | 2022-10-31 | 2025-09-10 | Intercept Pharmaceuticals, Inc. | Uses of farnesoid x receptor agonists |
| WO2024195903A1 (ko) * | 2023-03-21 | 2024-09-26 | 경희대학교 산학협력단 | 신규한 콜린산 유도체 및 이의 용도 |
| GB202314563D0 (en) * | 2023-09-22 | 2023-11-08 | Nzp Uk Ltd | Compounds |
| WO2025202883A1 (en) * | 2024-03-25 | 2025-10-02 | Bar Pharmaceuticals Societa' A Responsabilita' Limitata | Cholane derivatives for the treatment and the prevention of fxr and tgr5gp-bar1 receptors mediated diseases |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| DE69940958D1 (de) * | 1998-12-23 | 2009-07-16 | Glaxo Group Ltd | Bestimmungsmethode fur liganden der nuklearen rezeptoren |
| ES2248581T3 (es) * | 2001-03-12 | 2006-03-16 | Intercept Pharmaceuticals, Inc. | Esteroides como agonistas de fxr. |
| EP1568706A1 (en) * | 2004-02-26 | 2005-08-31 | Intercept Pharmaceuticals, Inc. | Novel steroid agonist for FXR |
| PL1734970T3 (pl) * | 2004-03-12 | 2015-05-29 | Intercept Pharmaceuticals Inc | Leczenie zwłóknienia z zastosowaniem ligandów FXR |
| ITMI20050912A1 (it) * | 2005-05-19 | 2006-11-20 | Erregierre Spa | Processo di preparazione di acidi 3-a-ya(b)-diidrossi-6-a(b)-alchil-5b-colanici |
| US7932244B2 (en) * | 2006-06-27 | 2011-04-26 | Intercept Pharmaceuticals, Inc. | Bile acid derivatives as FXR ligands for the prevention or treatment of FXR-mediated diseases or conditions |
| US8940719B2 (en) | 2006-07-03 | 2015-01-27 | Academia Sinica | Lithocholic acid analogues that inhibit sialyltransferase |
| FR2908310B1 (fr) * | 2006-11-14 | 2009-07-10 | Phytodia | Produits agonistes de tgr5 et leurs applications |
| EP1947108A1 (en) * | 2007-01-19 | 2008-07-23 | Intercept Pharmaceuticals, Inc. | TGR5 modulators and methods of use thereof |
| KR101555716B1 (ko) * | 2007-01-19 | 2015-09-25 | 인터셉트 파마슈티컬즈, 인크. | Tgr5 조절제로서의 23-치환 담즙산 및 이의 사용 방법 |
| WO2010014836A2 (en) | 2008-07-30 | 2010-02-04 | Intercept Pharmaceuticals, Inc. | Tgr5 modulators and methods of use thereof |
| DK2698375T3 (en) * | 2008-11-19 | 2018-05-28 | Intercept Pharmaceuticals Inc | TGR5 modulators and methods for using them |
| ES2774368T3 (es) * | 2008-11-19 | 2020-07-20 | Intercept Pharmaceuticals Inc | Moduladores de TGR5 y métodos de uso de los mismos |
| EP2575821B1 (en) * | 2010-05-26 | 2015-08-12 | Satiogen Pharmaceuticals, Inc. | Bile acid recycling inhibitors and satiogens for treatment of diabetes, obesity, and inflammatory gastrointestinal conditions |
| WO2012047495A2 (en) * | 2010-09-27 | 2012-04-12 | Kythera Biopharmaceuticals, Inc. | Methods for preparing synthetic bile acids and compositions comprising the same |
| CA2842707A1 (en) * | 2011-08-04 | 2013-02-07 | Lumena Pharmaceuticals, Inc. | Bile acid recycling inhibitors for treatment of pancreatitis |
| SI3336097T1 (sl) * | 2012-06-19 | 2021-07-30 | Intercept Pharmaceuticals, Inc. | Priprava nekristalinične oblike obetiholne kisline |
| SG11201503247UA (en) * | 2012-10-26 | 2015-06-29 | Intercept Pharmaceuticals Inc | Process for preparing bile acid derivatives |
| US20140206657A1 (en) * | 2013-01-18 | 2014-07-24 | City Of Hope | Bile acid analog tgr5 agonists |
| CN103143021A (zh) * | 2013-03-21 | 2013-06-12 | 中国药科大学 | PPARα-UGT通路抑制剂在治疗炎性肠疾病中的应用 |
| TN2015000497A1 (en) * | 2013-05-14 | 2017-04-06 | Intercept Pharmaceuticals Inc | 11-hydroxyl-derivatives of bile acids and amino acid conjugates thereof as farnesoid x receptor modulators |
| BR112016002268B1 (pt) * | 2013-08-01 | 2022-11-01 | The Penn State Research Foundation | Uso de inibidores do receptor x farnesoide |
| US10166246B2 (en) * | 2014-05-27 | 2019-01-01 | City Of Hope | TGR5 agonist complexes for treating diabetes and cancer |
| SMT202000070T1 (it) * | 2014-05-29 | 2020-03-13 | Bar Pharmaceuticals S R L | Derivati del colano per l'uso del trattamento e/o la prevenzione di malattie mediate da fxr e tgr5/gpbar1 |
| US20170233431A1 (en) * | 2016-02-17 | 2017-08-17 | City Of Hope | Bile acid derivatives and methods for synthesis and use |
-
2015
- 2015-05-28 SM SM20200070T patent/SMT202000070T1/it unknown
- 2015-05-28 EP EP19204247.1A patent/EP3626725B1/en active Active
- 2015-05-28 PL PL19204247.1T patent/PL3626725T3/pl unknown
- 2015-05-28 PL PL15731260T patent/PL3149019T3/pl unknown
- 2015-05-28 PT PT157312604T patent/PT3149019T/pt unknown
- 2015-05-28 SI SI201531924T patent/SI3626725T1/sl unknown
- 2015-05-28 US US15/314,771 patent/US10407462B2/en active Active
- 2015-05-28 SG SG11201609403UA patent/SG11201609403UA/en unknown
- 2015-05-28 SI SI201531091T patent/SI3149019T1/sl unknown
- 2015-05-28 PT PT192042471T patent/PT3626725T/pt unknown
- 2015-05-28 HR HRP20200225TT patent/HRP20200225T1/hr unknown
- 2015-05-28 SG SG10201809362RA patent/SG10201809362RA/en unknown
- 2015-05-28 EA EA201692316A patent/EA032820B1/ru unknown
- 2015-05-28 CN CN201580028528.2A patent/CN106661079B/zh active Active
- 2015-05-28 FI FIEP19204247.1T patent/FI3626725T3/fi active
- 2015-05-28 HU HUE15731260A patent/HUE048351T2/hu unknown
- 2015-05-28 JP JP2017514960A patent/JP6820253B2/ja active Active
- 2015-05-28 MX MX2020004024A patent/MX388957B/es unknown
- 2015-05-28 CA CA2948585A patent/CA2948585C/en active Active
- 2015-05-28 SM SM20230057T patent/SMT202300057T1/it unknown
- 2015-05-28 HU HUE19204247A patent/HUE061506T2/hu unknown
- 2015-05-28 DK DK15731260.4T patent/DK3149019T3/da active
- 2015-05-28 AU AU2015265893A patent/AU2015265893B2/en active Active
- 2015-05-28 LT LTEP19204247.1T patent/LT3626725T/lt unknown
- 2015-05-28 LT LTEP15731260.4T patent/LT3149019T/lt unknown
- 2015-05-28 RS RS20200163A patent/RS59910B1/sr unknown
- 2015-05-28 EP EP15731260.4A patent/EP3149019B1/en active Active
- 2015-05-28 KR KR1020167034084A patent/KR102491556B1/ko active Active
- 2015-05-28 DK DK19204247.1T patent/DK3626725T3/da active
- 2015-05-28 HR HRP20230170TT patent/HRP20230170T1/hr unknown
- 2015-05-28 WO PCT/EP2015/061802 patent/WO2015181275A1/en not_active Ceased
- 2015-05-28 RS RS20230132A patent/RS64050B1/sr unknown
- 2015-05-28 ES ES19204247T patent/ES2938874T3/es active Active
- 2015-05-28 MA MA39881A patent/MA39881B1/fr unknown
- 2015-05-28 CN CN201910107511.6A patent/CN110003301B/zh active Active
- 2015-05-28 MX MX2016015724A patent/MX373721B/es active IP Right Grant
- 2015-05-28 ES ES15731260T patent/ES2768718T3/es active Active
-
2016
- 2016-11-22 PH PH12016502327A patent/PH12016502327A1/en unknown
-
2019
- 2019-08-01 US US16/529,571 patent/US11117926B2/en active Active
-
2020
- 2020-02-12 CY CY20201100131T patent/CY1122631T1/el unknown
Also Published As
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2768718T3 (es) | Derivados de colano para su uso en el tratamiento y/o prevención de enfermedades mediadas por FXR y TGR5/GPBAR1 | |
| CA3067219A1 (en) | Methods and intermediates for the preparation of bile acid derivatives | |
| CN106999551A (zh) | 作为fxr/tgr5激动剂的胆汁酸类似物和其使用方法 | |
| JP2020512994A (ja) | スルホニルカルバマート胆汁酸誘導体の調製のためのプロセス | |
| CA2993540A1 (en) | Methods for preparation of bile acids and derivatives thereof | |
| US9745338B2 (en) | Pro-drug forming compounds | |
| EP2221313A1 (en) | Process for the preparation of ursodeoxycholic acid disodium 3,7-disulfate | |
| EP4519281B1 (en) | Process for the preparation of cholic acid derivatives | |
| BR112016028085B1 (pt) | Derivados de colano para uso no tratamento e/ou na prevenção de doenças mediadas por fxr e tgr5/gpbar1 | |
| RU2616974C1 (ru) | Способ получения ω-(бис(пиридин-2-илметил)амино)алифатических кислот - прекурсоров с хелатными центрами для связывания металлов | |
| WO2019020067A1 (zh) | 甾体类衍生物fxr激动剂的制备方法 | |
| EP3655419B1 (en) | Process and intermediates for the synthesis of obeticholic acid and derivatives thereof | |
| RU2791682C2 (ru) | Способ получения сульфонилкарбаматных производных желчных кислот | |
| CN114907437A (zh) | 具有抗肿瘤活性的雄诺龙衍生物及其制备方法与应用 | |
| CN103044518A (zh) | 3-氧代-7-肟基-4-氮杂-A-homo-鹅脱氧胆酸甲酯和3-O-苄肟基-7-氮杂-7a-氧代-B-homo-鹅脱氧胆酸甲酯及其在制备抗肿瘤药物中的应用 | |
| Masullo | Identification of new synthetic and semi-synthetic derivatives for the treatment of entero-hepatic disorders | |
| HK1234067A1 (en) | Tgr5 modulators and methods of use thereof | |
| HK1100776B (zh) | 地舍平的半合成方法 | |
| HK1164887A (en) | Tgr5 modulators and methods of use thereof |