ES2786399T3 - Preparación transdérmica que contiene donepezilo como principio activo - Google Patents
Preparación transdérmica que contiene donepezilo como principio activo Download PDFInfo
- Publication number
- ES2786399T3 ES2786399T3 ES15870365T ES15870365T ES2786399T3 ES 2786399 T3 ES2786399 T3 ES 2786399T3 ES 15870365 T ES15870365 T ES 15870365T ES 15870365 T ES15870365 T ES 15870365T ES 2786399 T3 ES2786399 T3 ES 2786399T3
- Authority
- ES
- Spain
- Prior art keywords
- weight
- pyrrolidone
- derivative
- transdermal composition
- matrix layer
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/44—Non condensed pyridines; Hydrogenated derivatives thereof
- A61K31/445—Non condensed piperidines, e.g. piperocaine
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/12—Carboxylic acids; Salts or anhydrides thereof
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/08—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite containing oxygen, e.g. ethers, acetals, ketones, quinones, aldehydes, peroxides
- A61K47/14—Esters of carboxylic acids, e.g. fatty acid monoglycerides, medium-chain triglycerides, parabens or PEG fatty acid esters
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/06—Organic compounds, e.g. natural or synthetic hydrocarbons, polyolefins, mineral oil, petrolatum or ozokerite
- A61K47/22—Heterocyclic compounds, e.g. ascorbic acid, tocopherol or pyrrolidones
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K47/00—Medicinal preparations characterised by the non-active ingredients used, e.g. carriers or inert additives; Targeting or modifying agents chemically bound to the active ingredient
- A61K47/30—Macromolecular organic or inorganic compounds, e.g. inorganic polyphosphates
- A61K47/32—Macromolecular compounds obtained by reactions only involving carbon-to-carbon unsaturated bonds, e.g. carbomers, poly(meth)acrylates, or polyvinyl pyrrolidone
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7038—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer
- A61K9/7046—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds
- A61K9/7053—Transdermal patches of the drug-in-adhesive type, i.e. comprising drug in the skin-adhesive layer the adhesive comprising macromolecular compounds obtained by reactions only involving carbon to carbon unsaturated bonds, e.g. polyvinyl, polyisobutylene, polystyrene
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K9/00—Medicinal preparations characterised by special physical form
- A61K9/70—Web, sheet or filament bases ; Films; Fibres of the matrix type containing drug
- A61K9/7023—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms
- A61K9/703—Transdermal patches and similar drug-containing composite devices, e.g. cataplasms characterised by shape or structure; Details concerning release liner or backing; Refillable patches; User-activated patches
- A61K9/7084—Transdermal patches having a drug layer or reservoir, and one or more separate drug-free skin-adhesive layers, e.g. between drug reservoir and skin, or surrounding the drug reservoir; Liquid-filled reservoir patches
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/40—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having five-membered rings with one nitrogen as the only ring hetero atom, e.g. sulpiride, succinimide, tolmetin, buflomedil
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- General Health & Medical Sciences (AREA)
- Veterinary Medicine (AREA)
- Pharmacology & Pharmacy (AREA)
- Epidemiology (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- Engineering & Computer Science (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Dermatology (AREA)
- Chemical Kinetics & Catalysis (AREA)
- General Chemical & Material Sciences (AREA)
- Oil, Petroleum & Natural Gas (AREA)
- Inorganic Chemistry (AREA)
- Medicinal Preparation (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
Abstract
Composición transdérmica que contiene donepezilo como principio activo, comprendiendo la composición transdérmica: (a) una capa de soporte; (b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco, (b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo, (b-2) 25-70% en peso de un adhesivo a base de EVA, (b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y (b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico, (c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico, en el que el adhesivo acrílico no contiene un grupo funcional; y (d) una capa de liberación.
Description
DESCRIPCIÓN
Preparación transdérmica que contiene donepezilo como principio activo
Campo técnico
La presente invención se refiere a una composición transdérmica que comprende donepezilo como principio activo y, más específicamente, a una composición transdérmica que comprende donepezilo como principio activo, conteniendo la composición transdérmica: (a) una capa de soporte; (b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco, (b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo, (b-2) 25-70% en peso de un adhesivo a base de EVA, (b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y (b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico, (c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; y (d) una capa de liberación.
Técnica anterior
La demencia se refiere a un síndrome de deterioro cognitivo complejo caracterizado por amnesia, degeneración de la inteligencia, cambios en la personalidad, anomalías de comportamiento y similares. Estos síntomas, que son los de la enfermedad degenerativa del nervio cerebral asociada con el cerebro que forma parte del sistema nervioso central, causan una disfunción irreversible en la red neuronal debido a la lenta apoptosis de las células nerviosas, lo que causa enfermedades degenerativas del sistema nervioso central, lo que finalmente conduce a la pérdida permanente de las funciones corporales correspondientes. La característica común de las enfermedades degenerativas del nervio cerebral es la apoptosis de células generales o específicas. Dado que las células nerviosas diferenciadas no poseen potenciales regenerativos, la apoptosis de las células nerviosas causa la pérdida irreversible de las funciones cerebrales.
No se ha establecido completamente cómo se produce la demencia, y no ha habido ningún fármaco para la demencia capaz de administrarse eficazmente solo, ya que la demencia tiene varios factores patológicos y fisiopatológicos. Sin embargo, se sabe indirectamente que la colina acetiltransferasa (ChAT), que participa en la síntesis de acetilcolina (ACh), se reduce en aproximadamente un 20-30% en el cerebro de los pacientes con demencia en comparación con el cerebro de las personas normales. También se sabe que la concentración de acetilcolina como neurotransmisor se reduce en aproximadamente un 16-30%. Por lo tanto, se han realizado investigaciones sobre el uso de agentes inhibidores que suprimen la colinesterasa (ChE), que es una enzima que hidroliza la acetilcolina como neurotransmisor, a través de un procedimiento terapéutico indirecto. La colinesterasa tiene dos formas: acetilcolinesterasa (AChE) y butilcolinesterasa (BuChE). La acetilcolinesterasa mencionada anteriormente es una enzima que hidroliza la acetilcolina, que es uno de los neurotransmisores que median la actividad de los nervios parasimpáticos en el cuerpo, en colina y acetato. La acetilcolinesterasa se forma en las membranas del retículo endoplásmico y se mueve a las membranas celulares para realizar sus funciones. La enzima es la más ampliamente distribuida en los nervios colinérgicos y sus alrededores, especialmente en las uniones músculo-nerviosas, a la vez que es una enzima importante que se encuentra en el plasma, el hígado y otros tejidos. Por lo tanto, la mayoría de los agentes terapéuticos utilizados actualmente para la demencia de Alzheimer son inhibidores de la acetilcolinesterasa, que es una enzima de degradación de la acetilcolina. Estos incluyen donepezilo (nombre comercial: Aricept), tacrina (nombre comercial: Cognex), rivastigmina (nombre comercial: Exelon) y galantamina (nombre comercial: Reminyl).
El donepezilo, que es un inhibidor de la acetilcolinesterasa (AChE), se usa para el tratamiento de la demencia, tal como la enfermedad de Alzheimer con un grado de leve a grave o superior. En la enfermedad de Alzheimer, en asociación con la cual se han descrito trastornos del sistema nervioso colinérgico en el cerebro, los inhibidores de la AChE, tales como donepezilo, aumentan la acetilcolina en el cerebro para activar los nervios colinérgicos en el cerebro. Una composición de donepezilo, que actualmente se usa comúnmente, está en forma de comprimido y se prescribe a pacientes con enfermedad de Alzheimer en forma de preparación oral.
Sin embargo, en general, el inhibidor de la acetilcolinesterasa como una composición oral tiene efectos secundarios graves y, en particular, se describe que causa problemas, tales como la disfunción o trastorno hepático o digestivo. La causa del efecto secundario es que una composición oral generalmente no puede evitar el efecto del paso primario hacia el hígado y, como resultado, la composición oral afecta fácilmente las funciones hepáticas. Además, la composición oral tiene una alta concentración en el tracto digestivo y, por lo tanto, es probable que se produzcan efectos secundarios en el tracto digestivo. Además, con respecto a un cambio en la concentración de fármaco en sangre después de la administración de una composición oral, la proporción de la concentración máxima de fármaco en sangre alcanzada después de la administración con respecto a la concentración en sangre 24 horas después (es decir, en el momento de una administración posterior) es alta y, por lo tanto, no es fácil mantener un efecto terapéutico durante un largo período de tiempo, mientras que la concentración en sangre no alcanza una concentración en la que se producen los efectos secundarios.
Por lo tanto, la publicación de solicitud de patente japonesa abierta a inspección pública No. 1999-315016 da a conocer que una administración oral puede ser difícil cuando las condiciones de la demencia están significativamente avanzadas, y por lo tanto, se ha propuesto un supositorio para administración rectal y una pomada para resolver el problema. Sin embargo, estas formas de dosificación son problemáticas, ya que no son prácticas para la administración continua de principios activos durante un largo período de tiempo.
Además, la solicitud de patente de Estados Unidos abierta a inspección pública No. 20040258741 y la solicitud de Patente Coreana abierta a inspección pública No. 2005-0037405 propusieron una composición transdérmica usando polímeros a base de caucho sintético de bases SIS y PIB. Sin embargo, dado que su velocidad de permeación es insuficiente, y una composición transdérmica que tiene un área de 50 cm2 o más debe aplicarse durante uno o dos días a la vez, una administración a largo plazo de la misma impone una carga pesada sobre la piel. Además, la composición transdérmica tiene una dificultad para contener una alta concentración de un fármaco en una matriz significativamente hidrófoba, y genera cristales a una concentración del 8% o más, causando una disminución de la fuerza adhesiva, falta de uniformidad de la velocidad de permeación de la piel, y problemas de almacenamiento. Además, para permitir que una matriz contenga un fármaco que tenga la cantidad necesaria para satisfacer la dosis requerida, el grosor de la matriz debe aumentarse proporcionalmente a la cantidad del fármaco y, por lo tanto, la velocidad de permeación del fármaco no cambia mucho al principio, pero se reduce con el tiempo.
Paralelamente, los presentes inventores han presentado una solicitud de patente (Solicitud de Patente Coreana Abierta a Inspección Pública No. 2009-0101667) para una composición transdérmica de donepezilo de una sola capa capaz de minimizar los efectos secundarios del fármaco mientras facilita la complacencia por un paciente con demencia en comparación con una composición oral. Sin embargo, la composición transdérmica en la solicitud anterior tiene desventajas indeseables para la adhesión (y la dosificación) en un período prolongado de sustancialmente más de un día, ya que dicha composición transdérmica contiene un fármaco en una concentración demasiado baja para administrarse durante un período de tiempo prolongado; un parche que contiene el fármaco es grueso; y un adhesivo de EVA que constituye la capa que contiene el fármaco posee una fuerza adhesiva baja a pesar de que la composición transdérmica se administra como un sistema en el que la capa que contiene el fármaco está en contacto directo con la piel.
Además, muchos parches convencionales se proporcionan en una forma en la que un fármaco deseado se incorpora en una capa en contacto directo con la piel con el fin de aumentar la cantidad de permeación de la piel de un fármaco. Sin embargo, en este caso, los cristales se forman en dicha capa a lo largo del tiempo y, por lo tanto, dicho parche reduce la fuerza adhesiva y cambia las propiedades físicas, y se libera poco de una película de liberación. Ha habido intentos de aumentar la fuerza adhesiva colocando una capa que contiene fármaco y una capa adhesiva separada. Sin embargo, cuando se coloca una capa adhesiva separada, existen varios problemas, tal como garantizar que la cantidad de permeación de la piel del fármaco sea suficiente para lograr un efecto de dosificación deseado y cambios en las propiedades físicas de la capa adhesiva debido al fármaco difundido en la capa de fármaco, y por lo tanto, de manera similar, el intento no es satisfactorio para proporcionar una composición transdérmica de liberación sostenida a largo plazo. La solicitud de patente US-20090291127 describe una composición de absorción transdérmica para el tratamiento de la demencia que comprende una capa de soporte, la capa matriz que contiene fármaco, la capa adhesiva y la capa de liberación, la capa de matriz que contiene fármaco comprende de 1 a 25% en peso de donepezilo y copolímeros de EVA (VA es 4-50%), 5-20 % de potenciadores de absorción percutánea como derivado de pirrolidona, como monooleato de glicerol (OMG), monolaurato de sorbitán (SML), monooleato de sorbitán (SMO), derivados de pirrolidona.
Las solicitudes de patente WO-2009120002 y KR-1020090101667 describen una composición de absorción percutánea para el tratamiento de la demencia que comprende una capa de soporte protectora del fármaco, la capa de matriz que contiene el fármaco y la capa de liberación, la capa de matriz que contiene el fármaco comprende de 2,0 a 25% en peso de donepezilo, de 50 a 80% de adhesivo sensible a la presión de EVA, de 10 a 25% de potenciadores de la penetración de la piel como derivados de pirrolidona, derivado alifático C8-18 y cualquiera de dos o más seleccionados de triacetina y citrato de trietilo.
Además, los adhesivos sensibles a la presión utilizados generalmente en parches requieren que muestren adhesividad a la piel, compatibilidad con los fármacos y otros excipientes, y similares. Un adhesivo acrílico, tal como TRS (Sekisui Chemical Co., Osaka, Japón) o Duro-Tak (Henkel, EE. UU.), se usa convencionalmente como un adhesivo que tiene las características anteriores. Sin embargo, cuando dicho adhesivo acrílico se usa como matriz adhesiva para una composición transdérmica, la difusión del fármaco en la capa adhesiva se ralentiza debido a la interacción entre el fármaco y los polímeros acrílicos en la capa adhesiva, y también disminuye la migración del fármaco desde la capa adhesiva a la piel, lo que dificulta la liberación de una cantidad requerida del fármaco.
Descripción detallada de la invención
Problema técnico
Por lo tanto, los presentes inventores han preparado una composición transdérmica que tiene un sistema de doble capa permeable al fármaco especial. Los presentes inventores han verificado que dicha composición transdérmica logra una reducción en el tamaño y el grosor del parche, lo que conduce a una menor irritación de la piel cuando se
une a la piel durante un largo período de tiempo, contiene una alta concentración de fármaco en una matriz hidrófoba para permitir una administración a largo plazo y tiene una velocidad de permeación de la piel significativamente mejorada en comparación con los parches de donepezilo existentes. Como tal, los presentes inventores han verificado que dicha composición transdérmica puede mantener una eficacia terapéutica válida durante un largo período de tiempo y, por lo tanto, han completado la presente invención.
Por lo tanto, un aspecto de la presente invención es proporcionar una composición transdérmica que contiene donepezilo como principio activo, comprendiendo la composición transdérmica:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico,
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; en la que el adhesivo acrílico no contiene un grupo funcional y
(d) una capa de liberación.
Otro aspecto de la presente invención es proporcionar una composición transdérmica para usar en un procedimiento para administrar donepezilo en un sujeto, comprendiendo el procedimiento:
(1) unir, a la piel de un sujeto, una composición transdérmica que comprende donepezilo como principio activo, en la que la composición transdérmica comprende
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico;
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; en la que el adhesivo acrílico no contiene un grupo funcional y
(d) una capa de liberación; y
(2) mantener la composición transdérmica unida a la piel del sujeto durante un tiempo suficiente para suministrar el donepezilo al sujeto.
Todavía otro aspecto de la presente invención es proporcionar un kit que comprende una composición transdérmica, en la que la composición transdérmica comprende:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico;
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; en la que el adhesivo acrílico no contiene un grupo funcional y
(d) una capa de liberación.
Solución técnica
De acuerdo con un aspecto de la presente invención, se proporciona una composición transdérmica que contiene donepezilo como principio activo, comprendiendo la composición transdérmica:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico,
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; en la que el adhesivo acrílico no contiene un grupo funcional, y
(d) una capa de liberación.
De acuerdo con otro aspecto de la presente invención, se proporciona una composición transdérmica para usar en un procedimiento para administrar donepezilo en un sujeto, comprendiendo el procedimiento:
(1) unir, a la piel de un sujeto, una composición transdérmica que comprende donepezilo como principio activo, en la que la composición transdérmica comprende
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico;
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; en la que el adhesivo acrílico no contiene un grupo funcional y
(d) una capa de liberación; y
(2) mantener la composición transdérmica unida a la piel del sujeto durante un tiempo suficiente para suministrar donepezilo al sujeto.
De acuerdo con todavía otro aspecto de la presente invención, se proporciona un kit que comprende una composición transdérmica, en la que la composición transdérmica comprende:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico;
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; en la que el adhesivo acrílico no contiene un grupo funcional y
(d) una capa de liberación.
En lo sucesivo, la presente invención se describirá en detalle.
La composición transdérmica de acuerdo con la presente invención tiene una capa de soporte, que está dispuesta en una superficie de una capa de matriz que contiene el fármaco y se compone de un material base que soporta la capa de matriz que contiene el fármaco, con el fin de evitar la pérdida de donepezilo de la composición mientras está unida a la piel o almacenado. Como material base que constituye la capa de soporte, se puede usar un material base conocido usado en un parche o similar. El material base usado en la capa de soporte de la presente invención es preferiblemente un material (material base) que es delgado y flexible, no tiene reactividad con la capa de matriz que contiene el fármaco, no causa reacción alérgica debido a la ausencia de reacción con la piel, y no conduce a la absorción o difusión de un fármaco en la capa de soporte. Específicamente, para la capa de soporte de acuerdo con la presente invención, se puede usar una película de plástico utilizada comúnmente en una composición transdérmica, tal como polietileno, polipropileno, copolímero de etileno y acetato de vinilo, vinilon, poliéster, poliuretano, nylon, poliacrilonitrilo, tereftalato de polietileno, poliolefina y similares; para evitar la separación de la composición transdérmica por la humedad que se evapora del cuerpo humano, una tela no tejida, tal como rayón o poliéster, que tiene capacidad de absorción de agua; una tela tejida, tal como poliéster, acrílico, seda o algodón; o se puede usar un material híbrido laminado del mismo, mientras que se puede usar cualquier material protector de fármaco (material base) usado en una composición transdérmica convencional. Preferiblemente, el material base que constituye la capa de soporte de la presente invención puede ser poliéster.
El grosor de la capa de soporte de acuerdo con la presente invención puede ser 8-100 pm, preferiblemente 10-60 mm.
En la composición transdérmica de la presente invención, la capa de matriz que contiene el fármaco está dispuesta en una superficie de la capa de soporte, y contiene donepezilo como principio activo. El donepezilo es un inhibidor de la acetilcolina esterasa, y en la presente invención, el donepezilo puede usarse en cualquier forma de una base libre de donepezilo o una sal farmacéuticamente aceptable del mismo. La base libre de donepezilo está
representada por la fórmula química C24H29NO3, y su nombre IUPAC es (±)-2,3-dihidro-5,6-dimetoxi-2-[[1-(fen¡lmet¡l)-4-p¡per¡d¡n¡l]met¡l]-1H-inden-1-ona. La base libre de donepezilo puede tener, preferiblemente, la estructura de la Fórmula Química 1 a continuación.
<Fórmula 1>
Una sal de adición de ácido formada por un ácido libre farmacéuticamente aceptable es útil como sal farmacéuticamente aceptable de donepezilo. Se puede obtener una sal de adición de ácido a partir de ácidos inorgánicos, tales como ácido clorhídrico, ácido nítrico, ácido fosfórico, ácido sulfúrico, ácido bromhídrico, ácido yodhídrico, ácido nitroso y ácido fosforoso; y ácidos orgánicos no tóxicos, tales como monocarboxilatos y dicarboxilatos alifáticos, alcanoatos sustituidos con fenilo, hidroxialcanoatos y alcanodioatos, ácidos aromáticos, ácidos sulfónicos alifáticos y aromáticos. Las sales farmacéuticamente no tóxicas incluyen sulfato, pirosulfato, bisulfato, sulfito, bisulfito, nitrato, fosfato, monohidrógeno fosfato, dihidrógeno fosfato, metafosfato, pirofosfato, cloruro, bromuro, yoduro, fluoruro, acetato, propionato, decanoato, caprilato, acrilato, formiato, isobutilato, caprato, heptanoato, propiolato, oxalato, malonato, succinato, suberato, cabacato, fumarato, maleato, butino-1,4-dioato, hexano-1,6-dioato, benzoato, clorobenzoato, metilbenzoato, dinitrobenzoato, hidroxibenzoato, metoxibenzoato, ftalato, tereftalato, bencenosulfonato, toluenosulfonato, clorobencenosulfonato, xilenosulfonato, fenilacetato, fenilpropionato, fenilbutilato, citrato, lactato, p-hidroxibutilato, glicolato, malato, tartrato, metanosulfonato, propanosulfonato, naftaleno-1-sulfonato, naftaletano-2-sulfonato y mandelato. Preferiblemente, el donepezilo contenido en la capa de matriz que contiene fármaco de la presente invención puede caracterizarse por estar en forma de su base libre.
Además, el donepezilo se dispersa uniformemente en una capa de matriz que contiene el fármaco, y puede estar contenido en una cantidad de 15-55% en peso en base al peso total de la capa de matriz que contiene el fármaco. Es decir, el donepezilo puede estar contenido en una cantidad de 15-50% en peso, 15-45% en peso, 15-40% en peso, 15-35% en peso, 15-30% en peso, 15-25% en peso, 15-20% en peso, 20-55% en peso, 20-50% en peso, 20-45% en peso, 20-40% en peso, 20-35% en peso, 20-30% en peso, 20-25% en peso, 25-55% en peso, 25 50% en peso, 25-45% en peso, 25-40% en peso, 25-35% en peso, 25-30% en peso, 30-55% en peso, 30-50% en peso, 30-45% en peso, 30-40% en peso, 30-35% en peso, 35-55% en peso, 35-50% en peso, 35-45% en peso, 35-40% en peso, 40-55% en peso, 40-50% en peso, 40- 45% en peso, 45-55% en peso, 45-50% en peso, o 50-55% en peso, preferiblemente 26-55% en peso, y lo más preferiblemente 30-50% en peso.
Si el contenido de donepezilo o una sal farmacéuticamente aceptable del mismo es inferior al 15% en peso, su efecto de fármaco es insuficiente, mientras que, si el contenido del mismo es superior al 55% en peso, el contenido de un material base de polímero es pequeño en la composición, no logrando suficiente dureza. Por lo tanto, dicho contenido de donepezilo o una sal farmacéuticamente aceptable del mismo puede no ser deseable en la preparación de una composición transdérmica. En la composición transdérmica de la presente invención, el donepezilo está contenido en un estado sobresaturado en la capa de matriz que contiene fármaco, y los microcristales de donepezilo de tamaño uniforme se distribuyen en una densidad uniforme en toda la capa de matriz que contiene fármaco.
La capa de matriz que contiene el fármaco de la presente invención se caracteriza por el uso de un material base de polímero, junto con un adhesivo de EVA como un adhesivo sensible a la presión. Un copolímero de polietileno y acetato de vinilo, que es una materia prima principal del adhesivo de eVa , tiene varias aplicaciones según el contenido de acetato de vinilo; tiene excelente resistencia a la intemperie, estabilidad al envejecimiento, resistencia al desgarro, resistencia al estrés y resistencia al ozono; y es una resina elástica termoplástica no tóxica que es más transparente que el caucho. En la presente invención, para poseer una fuerza adhesiva preferible, el contenido de acetato de vinilo (VA) del polietileno-acetato de vinilo (EVA) usado en el adhesivo de EVA puede estar contenido en un contenido de 4-50% en peso, y preferiblemente 35-45% en peso.
El contenido del adhesivo de EVA como material base polímero que constituye la capa de matriz que contiene el fármaco puede estar contenido en una cantidad de 25-70% en peso en base al peso total de la capa de matriz que contiene el fármaco. Es decir, el contenido del adhesivo de EVA puede estar contenido en una cantidad de 25-70% en peso, 25-65% en peso, 25-60% en peso, 25-55% en peso, 25-50% en peso, 25-45% en peso, 25-40% en peso, 25-35% en peso, 25-30% en peso, 30-70% en peso, 30-65% en peso, 30-60% en peso, 30-55% en peso, 30-50% en peso, 30-45% en peso, 30-40% en peso, 30-35% en peso, 35-70% en peso, 35-65% en peso, 35-60% en peso, 35-55% en peso, 35-50% en peso, 35- 45% en peso, 35-40% en peso, 40-70% en peso, 40-65% en peso, 40-60% en peso, 40-55% en peso, 40-50% en peso, 40-45% en peso, 45-70% en peso, 45-65% en peso, 45-60% en peso, 45 55% en peso, 45-50% en peso, 50-70% en peso, 50-65% en peso, 50-60% en peso, 50-55% en peso, 55-70% en peso, 55-65% en peso, 55-60% en peso, 60-70% en peso, 60-65% en peso, o 65-70% en peso, y preferiblemente
30-60% en peso. Si el contenido del adhesivo de EVA está fuera del intervalo de contenido indicado anteriormente, dicho contenido puede causar desventajas en términos de aplicabilidad a la piel y compatibilidad con un fármaco y otros excipientes.
Para la mejora de la permeabilidad de la piel de un fármaco, se puede utilizar un derivado de pirrolidona, un derivado alifático C8-18, triacetina y un derivado de ácido cítrico como potenciador de la permeación de la piel en su combinación específica en la capa de matriz que contiene el fármaco de la presente invención.
Por lo tanto, la capa de matriz que contiene el fármaco de la presente invención contiene al menos un material seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18. Es decir, la capa de matriz que contiene fármaco de la presente invención contiene al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona, un derivado alifático C8-18 y una mezcla de los mismos.
El tipo del derivado de pirrolidona no está particularmente limitado con tal de que sea un derivado de pirrolidona conocido. Por ejemplo, el derivado de pirrolidona puede ser al menos uno seleccionado del grupo que consiste en N-ciclohexil-2-pirrolidona, 1 -butil-3-dodecil-2-pi rrolidona, 1,5-dimetil-2-pirrolidona, 1 -etil-2-pi rrolidona, 1-hexil-4-metiloxicarbonil-2-pirrolidona, 1 -hexil-2-pirrolidona, 1 -(2-hidroxietil)pirrolidona, 3-hidroxi-N-metil-2-pirrolidona, 1-lauril-4-metiloxicarbonil-2-pirrolidona, N-metil-2-pirrolidona, N-caprilil-2-pirrolidona y N-dodecil-2-pirrolidona. Preferiblemente, el derivado de pirrolidona puede ser N-dodecil-2-pirrolidona.
El tipo del derivado alifático C8-18 no está particularmente limitado con tal de que sea un derivado alifático C8-18 conocido. Por ejemplo, el derivado alifático C8-18 puede ser al menos uno seleccionado del grupo que consiste en alcohol laurílico, alcohol oleílico, lactato de laurilo, monolaurato de glicerol, monooleato de glicerol, miristato de isopropilo, monolaurato de sorbitán, monooleato de sorbitán, monolaurato de propilenglicol, monooleato de propilenglicol, glicérido de macrogol oleilo, ácido oleico, glicérido de macrogol lauroilo, glicérido de macrogol lineloilo, capilato/caprato de propilenglicol, monocaprilato de propilenglicol y monoestearato de sorbitán. Preferiblemente, el derivado alifático C8-18 puede ser monooleato de glicerol o miristato de isopropilo.
Al menos un material seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18 puede estar contenido en un contenido de 5-20% en peso en base al peso total de la capa de matriz que contiene el fármaco. Es decir, el material puede estar contenido en un contenido de 6-20% en peso, 6-19% en peso, 6-18% en peso, 6-17% en peso, 6-16% en peso, 6-15% en peso, 6- 14% en peso, 6-13% en peso, 7-20% en peso, 7-19% en peso, 7-18% en peso, 7-17% en peso, 7-16% en peso, 7-15% en peso, 7-14% en peso %, 7-13% en peso, 8-20% en peso, 8-19% en peso, 8-18% en peso, 8-17% en peso, 8-16% en peso, 8-15% en peso, 8-14% en peso, 8-13% en peso, 9-20% en peso, 9-19% en peso, 9-18% en peso, 9-17% en peso, 9-16% en peso, 9-15% en peso, 9-14% en peso, 9- 13% en peso, y preferiblemente 8-17% en peso. Es deseable minimizar un efecto secundario en la piel minimizando el uso de dicho material.
Además, la capa de matriz que contiene el fármaco de la presente invención contiene cualquier material seleccionado de entre triacetina o un derivado de ácido cítrico. Es decir, la triacetina y un derivado de ácido cítrico no están contenidos simultáneamente en una composición en la capa de matriz que contiene el fármaco de la presente invención.
El tipo del derivado de ácido cítrico no está particularmente limitado con tal de que sea un derivado de ácido cítrico conocido. Por ejemplo, el derivado de ácido cítrico puede ser al menos uno seleccionado del grupo que consiste en citrato de acetil trietilo, citrato de dietilo, citrato de tributilo, citrato de trietilo y citrato de acetil tributilo. Preferiblemente, el derivado de ácido cítrico puede ser citrato de trietilo.
Cualquier material de triacetina o un derivado de ácido cítrico puede estar contenido en una cantidad de 1-10% en peso en base al peso total de la capa de matriz que contiene el fármaco. Es decir, dicho material puede estar contenido en un contenido de 1-10% en peso, 1-9% en peso, 1-8% en peso, 1-7% en peso, 1-6% en peso, 2-10% en peso, 2 -9% en peso, 2-8% en peso, 2-7% en peso, 2-6% en peso, 3-10% en peso, 3-9% en peso, 3-8% en peso, 3-7% en peso, 3-6 % en peso, 4-10% en peso, 4-9% en peso, 4-8% en peso, 4-7% en peso, o 4-6% en peso, y preferiblemente 3-8% en peso.
Es decir, para la composición transdérmica de la presente invención, se pueden usar las siguientes combinaciones de ejemplo en la presente invención: una combinación de un derivado de pirrolidona y triacetina; una combinación de un derivado alifático Cs-18 y triacetina; una combinación de un derivado de pirrolidona y un derivado de ácido cítrico; una combinación de un derivado alifático Cs-18 y un derivado de ácido cítrico; una combinación de un derivado de pirrolidona, un derivado alifático C8-18 y triacetina; una combinación de un derivado de pirrolidona, un derivado alifático C8-18 y un derivado de ácido cítrico.
Preferiblemente, la capa de matriz que contiene el fármaco de la presente invención puede estar compuesto de (b-1) 15-55% en peso de donepezilo o una sal farmacéutica aceptable del mismo, (b-2) 25-70 [K1] % en peso de un adhesivo a base de EVA, (b-3) 5-20% en peso de un derivado de pirrolidona, y (b-4) 1-10% en peso de triacetina.
Además, la capa de matriz que contiene el fármaco de la presente invención se puede preparar en su grosor de 50 150 pm, y preferiblemente 70-120 pm.
La composición transdérmica de la presente invención tiene una capa de matriz adhesiva, que está dispuesta en la otra superficie de la capa de matriz que contiene el fármaco y pone la composición transdérmica en contacto continuo con la piel para facilitar la absorción de su principio activo. Tal como se usa en el presente documento, el término "capa de matriz adhesiva" se usa indistintamente con el término "capa adhesiva". En la presente invención, la capa de matriz adhesiva se caracteriza por sus funciones de controlar una liberación continua de fármaco y mejorar la adhesividad.
En la presente invención, la capa de matriz adhesiva se caracteriza por que contiene 60% en peso o más de un adhesivo acrílico. Por ejemplo, el adhesivo acrílico puede estar contenido en una cantidad de 60% en peso, 61% en peso, 62% en peso, 63% en peso, 64% en peso, 65% en peso, 66% en peso, 67% en peso, 68% en peso, 69 % en peso, 70% en peso, 71% en peso, 72% en peso, 73% en peso, 74% en peso, 75% en peso, 76% en peso, 77% en peso, 78% en peso, 79% en peso, 80% en peso, 81% en peso, 82% en peso, 83% en peso, 84% en peso, 85% en peso, 86% en peso, 87% en peso, 88% en peso, 89% en peso, 90% en peso, 91% en peso, 92% en peso, 93% en peso, 94 % en peso, 95% en peso, 96% en peso, 97% en peso, 98% en peso, 99% en peso, o 100% en peso. Preferiblemente, el adhesivo acrílico puede estar contenido en un contenido de 60-100% en peso en base al peso total de la capa de matriz adhesiva, y lo más preferiblemente, 80% en peso o más (es decir, 80-100% en peso).
El adhesivo acrílico contenido en la capa de matriz adhesiva de la presente invención es un adhesivo acrílico que no contiene ningún grupo funcional. El tipo de dicho grupo funcional no está particularmente limitado, mientras que, específicamente, un grupo funcional, tal como un grupo hidroxi, un grupo carboxilo, un grupo amino y un grupo sulfonilo puede no estar contenido en el adhesivo acrílico.
En particular, en cuanto al adhesivo acrílico que no contiene un grupo funcional de acuerdo con la presente invención, se puede utilizar un producto comercializado conocido, por ejemplo, Duro-Tak™ 87-9088, Duro-Tak™ 87-900A, Duro-Tak™ 87-901A, Duro-Tak™ 4098, Duro-Tak™ 5298 o Duro-Tak™ 87-9301, sin limitación.
La capa de matriz adhesiva puede contener además un potenciador de permeación de la piel. El tipo de potenciador de permeación de la piel no está particularmente limitado, mientras que, por ejemplo, se puede usar un derivado de pirrolidona, un derivado alifático Cs-18, triacetina, un derivado de ácido cítrico y similares. Dicho material es como se describe anteriormente. En la presente invención, el potenciador de permeación de la piel contenido en la capa de matriz adhesiva puede ser preferiblemente un derivado alifático Cs-18, y lo más preferiblemente puede ser miristato de isopropilo o monooleato de glicerol.
El potenciador de permeación de la piel contenido en la capa de matriz adhesiva puede estar contenido como una cantidad restante de la proporción adhesivo acrílico en base al peso total de la capa de matriz adhesiva. Por ejemplo, si el adhesivo acrílico está contenido en un contenido del 95% en peso en la capa de matriz adhesiva, el potenciador de permeación de la piel puede estar contenido en un contenido del 5% en peso. Si el adhesivo acrílico está contenido en un contenido del 100%, el potenciador de permeación de la piel no está realmente contenido. Preferiblemente, el potenciador de permeación de la piel puede estar contenido en un contenido de 1-40% en peso en base al peso total de la capa de matriz adhesiva. Es decir, el potenciador de permeación de la piel puede estar contenido en 1-40% en peso, 1-35% en peso, 1-30% en peso, 1-25% en peso, 1-20% en peso, 1-15% en peso, 1-10% en peso, 1-5% en peso, 5-40% en peso, 5-35% en peso, 5-30% en peso, 5-25% en peso, 5-20% en peso, 5-15% en peso, 5-10% en peso, 10-40% en peso, 10-35% en peso, 10-30% en peso, 10-25% en peso, 10-20% en peso, 10-15% en peso, 15-40% en peso, 15-35% en peso %, 15-30% en peso, 15-25% en peso, 15-20% en peso, 20-40% en peso, 20-35% en peso, 20-30% en peso, 20-25% en peso, 25-40% en peso, 25-35% en peso, 25-30% en peso, 30-40% en peso, 30-35% en peso o 35-40% en peso.
Según un ejemplo de la presente invención, la permeabilidad de la piel tiende a aumentar a medida que el contenido del potenciador de permeación de la piel aumentaba en la capa adhesiva. Cuando el contenido del potenciador de permeación de la piel era bajo, el efecto de potenciar la permeación de la piel aumentaba linealmente. Sin embargo, cuando el contenido del potenciador de permeación de la piel excedía aproximadamente el 20% en peso, el efecto de mejorar dicha permeación de la piel aumentaba de forma no lineal. Paralelamente, si el contenido del potenciador de permeación de la piel contenido en la capa de matriz adhesiva excede el 40% en peso en base al peso total de la capa de matriz adhesiva, dicho contenido no es preferible, ya que influye en las propiedades físicas de la composición transdérmica, causando un problema en el que quedan materiales residuales cuando se unen a la piel.
La capa de matriz adhesiva de la presente invención no contiene donepezilo como principio activo.
La capa de matriz adhesiva puede prepararse para tener su grosor de 20-70 pm, y preferiblemente 30-60 pm.
La composición transdérmica de la presente invención comprende una capa de liberación, que está dispuesta en la otra superficie de la capa de matriz adhesiva y debe ser eliminada antes de aplicar la composición transdérmica sobre la piel. Como capa de liberación, se puede usar una película de liberación o material laminado de la misma
convencionalmente usados para una composición transdérmica. Por ejemplo, se puede usar una película de polietileno, poliéster, cloruro de polivinilo, cloruro de polivinilideno o similar, un papel o un material laminado del mismo, que está recubierto con una resina de silicona o una resina de flúor, sin limitarse a los mismos.
La composición transdérmica de la presente invención exhibe su efecto terapéutico a través de donepezilo como principio activo. Por lo tanto, el uso de la composición transdérmica de la presente invención no está particularmente limitado siempre que el uso de la composición transdérmica sea para cualquier enfermedad en la que el donepezilo muestre su eficacia terapéutica, sin limitación a la misma. Por ejemplo, la composición transdérmica de la presente invención tiene un uso terapéutico para la enfermedad cerebral degenerativa, y la enfermedad cerebral degenerativa incluye Alzheimer, demencia, daño de memoria y similares, pero no se limita a las mismas.
Además, la composición transdérmica de la presente invención es administrable durante 1-10 días, y puede mostrar un efecto terapéutico eficaz durante preferiblemente 3-7 días.
La composición transdérmica de la presente invención contiene, como principio activo, donepezilo a 1-6 mg/cm2 para el área de la misma (es decir, para el área de un parche), y preferiblemente 2-5 mg/cm2. Si el contenido del principio activo es inferior a 1 mg/cm2, el efecto del fármaco puede ser insuficiente. Si el contenido del principio activo es superior a 6 mg/cm2, el contenido del material base de polímero y el potenciador de permeación de la piel son pequeños y, por lo tanto, indeseables en la preparación de una composición transdérmica, ya que la composición transdérmica no presenta una dureza suficiente.
Con respecto a la composición transdérmica que contiene donepezilo como principio activo según la presente invención, el tamaño y el grosor del parche se reducen en comparación con los parches que contienen donepezilo existentes, a la vez que una alta concentración de fármaco está contenida en una matriz hidrófoba; un fármaco puede liberarse continuamente durante un largo período de tiempo debido a una adhesividad excelente de la composición transdérmica a la piel durante un largo período de tiempo; y la permeabilidad cutánea de un fármaco es excelente, de modo que la concentración en sangre del principio activo alcanza una concentración terapéutica de alto equilibrio dinámico durante el período de aplicación sin alcanzar una concentración en la que se producen efectos secundarios y, por lo tanto, la composición transdérmica puede usarse favorablemente como sustitución para una composición oral convencional para tratar la demencia.
Estas características se deben a un sistema de doble capa especial permeable al fármaco (capa de matriz que contiene el fármaco y la capa de matriz adhesiva) proporcionado por la presente invención, y el efecto de la dosificación a largo plazo del parche de la presente invención se muestra notablemente debido a la composición especial del material de la doble capa, que se describe por primera vez en la presente invención.
La presente invención proporciona una composición transdérmica para usar en un procedimiento para administrar donepezilo en un sujeto, comprendiendo el procedimiento:
(1) unir, a la piel de un sujeto, una composición transdérmica que comprende donepezilo como principio activo, en la que la composición transdérmica comprende:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico;
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico, en la que el adhesivo acrílico no contiene un grupo funcional; y
(d) una capa de liberación; y
(2) mantener la composición transdérmica unida a la piel del sujeto durante un tiempo suficiente para suministrar donepezilo al sujeto.
La etapa de unir a la piel puede conseguirse mediante la eliminación de una capa de liberación de la composición transdérmica y el contacto de la capa de matriz adhesiva con la piel. En la presente invención, la parte de la piel a la que está unida la composición transdérmica no está particularmente limitada, pero, preferiblemente, puede ser la espalda, el pecho, los brazos o similares.
En el presente documento, el término "tiempo suficiente para suministrar donepezilo a un sujeto" puede ser interpretado en el sentido de un tiempo suficiente para que el donepezilo alcance una concentración en sangre en el que se puede ejercer la eficacia del fármaco. En la presente invención, el tiempo suficiente para administrar donepezilo al sujeto puede ser de 1 a 10 días, preferiblemente de 2 a 7 días, y lo más preferiblemente de 3 a 4 días, pero no se limita a los mismos.
La presente invención proporciona un kit que comprende una composición transdérmica, en la que la composición transdérmica comprende:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico;
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; y
(d) una capa de liberación.
Efectos ventajosos
La composición transdérmica de la presente invención contiene una alta concentración de donepezilo en la matriz hidrófoba y tiene una excelente adhesividad a la piel durante un largo período de tiempo, de modo que un fármaco puede liberarse continuamente durante un largo período de tiempo y la velocidad de permeación de la piel mejora notablemente en comparación con los parches de donepezilo existentes. Por lo tanto, la composición transdérmica de la presente invención puede mantener continuamente un efecto terapéutico efectivo durante un largo período de tiempo.
Modo para llevar a cabo la invención
En lo sucesivo, la presente invención se describirá en detalle.
Sin embargo, los siguientes ejemplos son meramente para ilustrar la presente invención y no pretenden limitar el alcance de la presente invención.
<Ejemplos 1 a 8 y Ejemplos comparativos 1 a 4>
Preparación de la composición transdérmica que contiene donepezilo.
Ejemplo 1
Se añadió cloruro de metileno a 55% en peso de donepezilo, 5% en peso de triacetina, 10% en peso de N-dodecil-2-pirrolidona, y 30% en peso de un adhesivo de EVA para obtener un contenido de sólidos del 40%, que, a continuación, se disolvió por completo, preparando así la solución adhesiva que contiene el fármaco. La solución adhesiva que contiene el fármaco recubrió una película de liberación de poliéster tratada con silicona fijada en un aplicador, y se secó a 70°C durante 10 minutos a una velocidad del aire de 1300 rpm para preparar una lámina de una capa de matriz que contiene el fármaco con un grosor de 70 pm, que, a continuación, se unió a una película de soporte de poliéster (correspondiente a una capa de soporte), preparando así una capa de matriz que contiene el fármaco. Además, un adhesivo acrílico (Duro-Tak™ 87-9301) que tenía un contenido de sólidos de 35-42% recubrió una película de liberación de poliéster tratada con silicona y se secó a 100 °C durante 10 minutos a una velocidad del aire de 1300 rpm, preparando así una capa de matriz adhesiva con un grosor de 50 pm. Posteriormente, la película de liberación de la capa de matriz que contiene el fármaco se extrajo y, a continuación, se unió a la capa de matriz adhesiva. Después de la unión, el producto resultante se cortó en un tamaño de 50 cm2 para completar una composición transdérmica.
Ejemplos 2 a 9 y ejemplos comparativos 1 a 2
Los ejemplos 2 a 9 y los ejemplos comparativos 1 a 2 se prepararon mediante el mismo procedimiento que se describe en el ejemplo 1, excepto que se varió cada composición. La tabla 1 a continuación muestra las composiciones de los ejemplos 2 a 9 y los ejemplos comparativos 1 y 2.
Ejemplo comparativo 3
Se añadió tolueno a 13% en peso de donepezilo, 10% en peso de N-dodecil-2-pirrolidona, 5% en peso de triacetina y 72% en peso de un adhesivo de EVA para obtener un contenido de sólidos del 40%, que, a continuación, se disolvió completamente. Posteriormente, la solución adhesiva que contiene el fármaco recubrió una película de liberación de poliéster tratada con silicona fijada en el aplicador y se secó a 90°C durante 10 minutos a una velocidad del aire de 1300 rpm para preparar una lámina de capa adhesiva con un grosor de 85 pm, que, a continuación, se unió a una película de soporte de poliéster, seguido del corte con un tamaño de 50 cm2 para completar una composición transdérmica.
Ejemplo comparativo 4
El ejemplo comparativo 4 se preparó mediante el mismo procedimiento que el descrito en el Ejemplo comparativo 3, excepto que se cambió la composición. La Tabla 1 a continuación muestra la composición del Ejemplo Comparativo 4.
Ejemplo 10
En el Ejemplo 10, se preparó una capa de matriz que contiene el fármaco mediante la preparación de una solución adhesiva que contiene un fármaco, que tiene la misma composición que en el Ejemplo 4, y a continuación la realización de secado mediante el mismo procedimiento que se describe en el Ejemplo 1. Además, se añadió acetato de etilo a 95% en peso de un adhesivo acrílico (Duro-Tak™ 87-9301) que tenía un contenido de sólidos del 35-42% y 5% en peso de miristato de isopropilo para obtener un contenido de sólidos del 35%, que, a continuación, se disolvió completamente. Posteriormente, la solución recubrió una película de liberación de poliéster tratada con silicona y se secó a 100°C durante 10 minutos a una velocidad del aire de 1300 rpm, preparando así una capa de matriz adhesiva con un grosor de 50 mm. A continuación, se extrajo la película de liberación de la capa de matriz que contiene el fármaco y, a continuación, se unió a la capa de matriz adhesiva. Después de la unión, el producto resultante se cortó con un tamaño de 50 cm2 para completar una composición transdérmica.
Ejemplos 11 a 19 y ejemplos comparativos 5 a 12
Las composiciones transdérmicas de los Ejemplos 11 a 19 y los Ejemplos Comparativos 5 a 12 se prepararon mediante el mismo procedimiento descrito en el Ejemplo 10, excepto que se varió cada composición. La Tabla 2, a continuación, muestra las composiciones de capas adhesivas en los Ejemplos 11 a 19 y los Ejemplos Comparativos 5 a 12.
[Tabla 1]
Tabla de composición de los ejemplos 1 a 9 y ejemplos comparativos 1 a 4
M
Adhesivo de EVA: adhesivo de polietileno y acetato de vinilo; TA: triacetina; TC: citrato de trietilo; NP: N-dodecil-2-pirrolidona; IPM: miristato de isopropilo; GML: monolaurato de glicerilo; adhesivo acrílico: adhesivo de poliacrilato
[Tabla 2]
Tabla de composición de los ejemplos 10 a 19 y ejemplos comparativos 5 a 12
Ejemplo de ensayo 1: Evaluación de la permeación de fármacos a través de la piel de composiciones transdérmicas
Se llevó a cabo un ensayo de permeación a través de la piel de donepezilo en los parches preparados en los Ejemplos 1 a 9 y los Ejemplos Comparativos 1 a 4 de la siguiente manera.
Se preparó la fase acuosa de un dispositivo de difusión para un ensayo de permeación del fármaco (celda Franz) añadiendo 0,1% en peso de azida de sodio a un tampón de fosfato de pH 7,4 para evitar que la descomposición de la piel. La temperatura se mantuvo a 32 ± 0,5 cargando la fase acuosa en el dispositivo de ensayo de difusión (celda Franz), mientras se usaba la piel de cadáver humano. Los parches preparados en los ejemplos y ejemplos comparativos se cortaron de acuerdo con el tamaño de las células donantes y, a continuación, se aplicaron a la piel. A medida que transcurrió el tiempo, el tampón difundido con el fármaco se tomó a 500 ml cada hora para cuantificar la cantidad del fármaco que había permeado. Se utilizó HPLC (HPLC Agilent serie 1100) para el análisis. Para condiciones analíticas, se utilizó como fase móvil una mezcla líquida 40:60 (proporción en volumen) de acetonitrilo y una solución de mezcla de tampón de dihidrógeno fosfato de potasio, metanol y trietilamina (la solución de mezcla se prepara mezclando un tampón de dihidrógeno fosfato de potasio de 0,02 mol/l con metanol y trietilamina en una proporción de 50:50:1 (proporción en volumen); la cantidad de inyección de muestra fue de 20 ml; el caudal fue de 1,0 ml/min; la longitud de onda de detección fue de 268 nm; y la columna de fase inversa C18 se usó como columna. La Tabla 3 muestra la cantidad acumulada de permeación del fármaco y la velocidad de
permeación de la piel a los 3 días después de la permeación del fármaco en los parches preparados en los Ejemplos y Ejemplos comparativos.
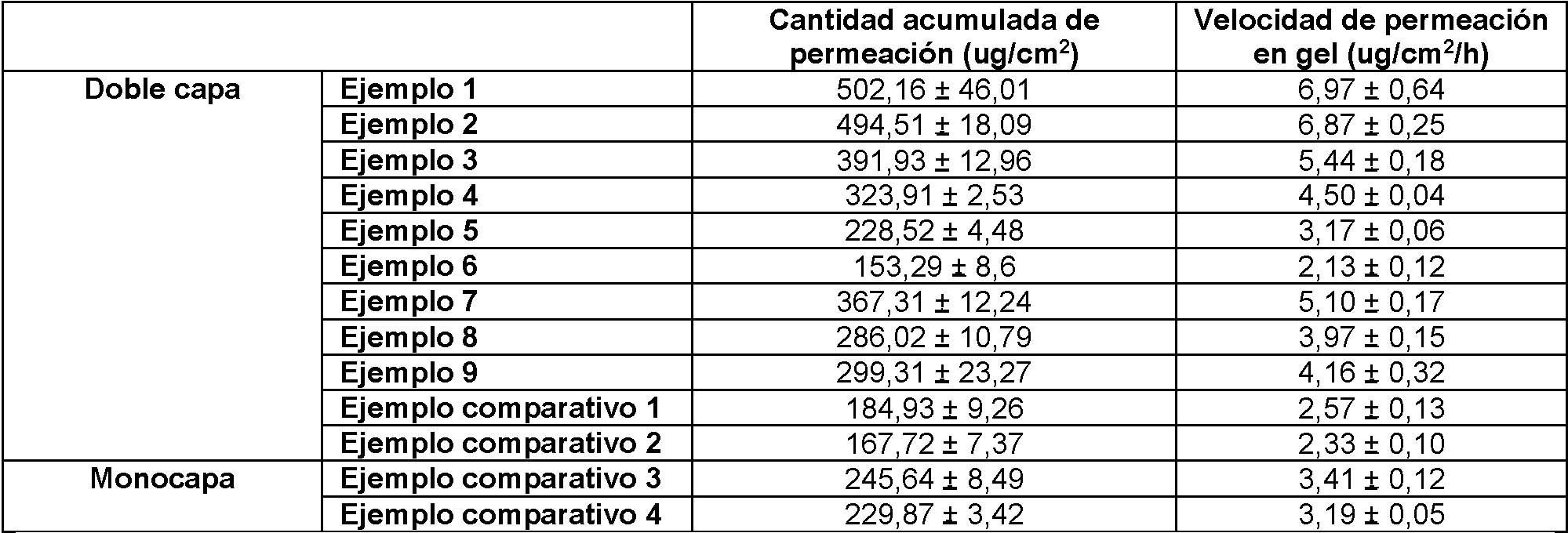
[Tabla 3]
Cantidad acumulada de permeación y velocidad de permeación a través de la piel de la preparación de absorción transdérmica (1)
A partir de la comparación entre los Ejemplos y Ejemplos comparativos 3 y 4 en la Tabla 3, se puede observar que los parches en monocapa de donepezilo mostraron una alta permeabilidad de la piel en consideración del contenido de fármaco. Esto se debe a que el fármaco penetra directamente a través de la capa adhesiva. Sin embargo, cuando se aplicó realmente a la piel, la composición en monocapa tiene una baja adhesividad y, por lo tanto, no es adecuada como parche de tipo de fijación a largo plazo. Sin embargo, las composiciones transdérmicas de la presente invención, tal como se muestra en los Ejemplos 1 a 8, fueron muy adecuadas como una composición transdérmica del tipo de liberación de fármaco a largo plazo debido a la excelente fuerza adhesiva de la capa de matriz adhesiva (capa adhesiva), incluso cuando se aplica a la piel real.
Además, a partir de la comparación entre los Ejemplos y los Ejemplos Comparativos 1 y 2 en la Tabla 3, se puede observar que el uso combinado de potenciadores de permeación de la piel en una combinación específica fue más eficaz que el uso singular de un potenciador de permeación de la piel. En particular, el uso combinado de triacetina y N-dodecil-2-pirrolidona, el uso combinado de triacetina y miristato de isopropilo, o el uso combinado de citrato de trietilo y N-dodecil-2-pirrolidona se encontraron efectivos.
Además, en el caso de 5 mg de una composición oral, la concentración en sangre máxima fue 9,8 ± 1,1 ng/ml cuando se administró por vía oral una vez. La composición oral alcanzó un estado estable dentro de los 15 días posteriores a la administración repetida, y en el estado estable, la concentración plasmática media fue de 26,5 ± 3,9 ng/ml y la depuración plasmática media fue constante a 0,13 l/h/kg. A través de los datos anteriores, se encontró que la velocidad de permeación de la piel requerida fue de aproximadamente 4,134 mg/cm2/h. Se puede observar que, cuando se comparan los Ejemplos en la Tabla 2, las velocidades de permeación de la piel se mantuvieron similares o ligeramente más altas que la velocidad de permeación de la piel requerida. Además, se puede observar que, en el ensayo de permeación de la piel de los Ejemplos, el fármaco se liberó continuamente durante el período de ensayo. Además, debido a las características del donepezilo, el fármaco tiene una vida media larga (58-90 h) y una alta biodisponibilidad (96-100%), y por lo tanto, el fármaco se acumula en el cuerpo para su administración durante un período largo de tiempo y alcanza una concentración terapéutica de un estado de equilibrio dinámico y, por lo tanto, exhibe persistencia del tratamiento. Por lo tanto, la composición transdérmica de la presente invención puede obtener un efecto terapéutico suficiente durante un largo período de tiempo incluso con una aplicación, y puede resolver los inconvenientes de la administración diaria requerida al paciente.
Ejemplo de ensayo 2: Evaluación de la eficacia de la composición transdérmica según el grupo funcional contenido en la capa adhesiva
Se prepararon composiciones transdérmicas que contienen donepezilo usando DURO-TAK 87-900A, DURO-TAK 87-9301 y DURO-TAK 87-4098 como adhesivos acrílicos sin un grupo funcional, DURO-TAK 87-2516 como adhesivo acrílico que contiene un grupo hidroxilo, DURO-TAK 87-503A y DURO-TAK 87-504A como adhesivos acrílicos que son híbridos acrilato y caucho, y DURO-TAK 87-2852 como adhesivo acrílico que contiene un grupo carboxilo. Todos los demás detalles (los tipos y el contenido de los componentes que constituyen la capa de soporte, la capa de matriz que contiene el fármaco y la capa de liberación, y el contenido del adhesivo acrílico contenido en la capa adhesiva), aparte del tipo de adhesivo acrílico, fueron idénticos a los del Ejemplo 3. Las composiciones
transdérmicas preparadas se midieron para determinar la cantidad de permeación de la piel mediante el mismo procedimiento que en el Ejemplo de ensayo 1.
Como resultado, se verificó, tal como se muestra en la figura 2, que las composiciones transdérmicas preparadas usando DURO-TAK 87-900A, DURO-TAK 87-9301 y DURO-TAK 87-4098, que son adhesivos acrílicos que no tienen grupo funcional, respectivamente, mostraron velocidades de permeación de fármaco significativamente elevadas. Ejemplo de ensayo 3: Evaluación de la eficacia de la composición transdérmica según el potenciador de permeación de la piel contenido en la capa adhesiva
Se prepararon composiciones transdérmicas usando capas adhesivas de acuerdo con las composiciones de la Tabla 2, mientras que todos los detalles (los tipos y el contenido de los ingredientes que constituyen la capa de soporte, la capa de matriz que contiene el fármaco y la capa de liberación) aparte de la capa adhesiva fueron idénticos a los del Ejemplo 4. Las composiciones transdérmicas preparadas se midieron para determinar la cantidad de permeación de la piel mediante el mismo procedimiento que en el Ejemplo de ensayo 1.
[Tabla 4]
Como resultado, se verificó, tal como se muestra en la Tabla 4, que, al comparar los Ejemplos 10 a 19 y los Ejemplos Comparativos 5 a 12, que son composiciones transdérmicas que contienen un potenciador de permeación de la piel en la capa adhesiva, con el Ejemplo 4 que es una composición transdérmica que no contiene un potenciador de permeación de la piel en la capa adhesiva, las velocidades de permeación del fármaco fueron notablemente altas cuando un potenciador de permeación de la piel estaba contenido en la capa adhesiva.
Además, como en el Ejemplo de ensayo 1, a medida que aumentaba el contenido del potenciador de permeación de la piel en la capa adhesiva, la permeabilidad de la piel tendía a aumentar. Sin embargo, cuando el contenido del potenciador de permeación de la piel era bajo, el efecto de mejora de la permeación de la piel aumentaba linealmente. Sin embargo, cuando la cantidad del potenciador de permeación de la piel excedió un contenido específico de aproximadamente el 20%, el efecto de mejora de la permeación de la piel aumentó de forma no lineal. Además, se produjo un problema en el que un mayor contenido del potenciador de permeación de la piel influía en las propiedades físicas de la composición transdérmica y, por lo tanto, quedaban residuos cuando la composición transdérmica se unía a la piel.
Además, todos los potenciadores de permeación de la piel utilizados en los Ejemplos Comparativos 5 a 12 presentaron un aumento de la permeabilidad de la piel, pero mostraron velocidades de permeación de fármacos más bajas o ejercían una mayor influencia sobre las propiedades físicas de la composición de permeación transdérmica, en comparación con los Ejemplos 10 a 19, y por lo tanto, quedaban más residuos cuando se unía a la piel que en los Ejemplos.
Aplicabilidad industrial
Como se ha expuesto anteriormente, la presente invención está dirigida a una composición transdérmica que contiene donepezilo como principio activo y, más específicamente, a una composición transdérmica que contiene
donepezilo como principio activo, comprendiendo la composición transdérmica: (a) una capa de soporte; (b) una capa de matriz que contiene fármaco que comprende, en base al peso total de una capa de matriz que contiene fármaco, (b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo, (b-2) 25-70% en peso de un adhesivo a base de EVA, (b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y (b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico, (c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico; y (d) una capa de liberación.
La composición transdérmica de la presente invención contiene una alta concentración de donepezilo en la matriz hidrófoba y tiene una excelente adhesividad a la piel durante un largo período de tiempo, por lo que un fármaco puede ser liberado continuamente durante un largo período de tiempo y la velocidad de permeación de la piel se puede mejorar notablemente en comparación con los parches de donepezilo existentes y, por lo tanto, la composición transdérmica de la presente invención puede mantener continuamente un efecto terapéutico eficaz durante un largo período de tiempo. Por consiguiente, la composición transdérmica de la presente invención es altamente industrialmente aplicable.
Claims (14)
1. Composición transdérmica que contiene donepezilo como principio activo, comprendiendo la composición transdérmica:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico,
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico, en el que el adhesivo acrílico no contiene un grupo funcional; y
(d) una capa de liberación.
2. Composición transdérmica, según la reivindicación 1, en la que el grupo funcional no tiene un grupo hidroxilo, un grupo carboxilo, un grupo amino y un grupo sulfonilo.
3. Composición transdérmica, según la reivindicación 1, en la que el donepezilo está en forma de una base libre, opcionalmente
en la que el donepezilo está contenido en una cantidad de 26-55% en peso en base al peso total de la capa de matriz que contiene el fármaco.
4. Composición transdérmica, según la reivindicación 1, en la que la capa de matriz adhesiva comprende, además, un potenciador de permeación de la piel.
5. Composición transdérmica, según la reivindicación 4, en la que el potenciador de permeación de la piel es al menos un material seleccionado del grupo que consiste en un derivado de pirrolidona, un derivado alifático C8-18, un derivado de ácido cítrico y triacetina.
6. Composición transdérmica, según las reivindicaciones 1 a 5, en la que el derivado de pirrolidona es al menos uno seleccionado del grupo que consiste en N-ciclohexil-2-pirrolidona, 1-butil-3-dodecil-2-pirrolidona, 1,5-dimetil-2-pirrolidona, 1 -etil-2-pirrolidona, 1-hexil-4-metiloxicarbonil-2-pirrolidona, 1 -hexil-2-pirrolidona, 1-(2-hidroxietil)pirrolidona, 3-hidroxi-N-metil-2-pirrolidona, 1 -lauril-4-metiloxicarbonil-2-pirrolidona, N-metil-2-pirrolidona, N-caprilil-2-pirrolidona y N-dodecil-2-pirrolidona, preferiblemente
en la que el derivado de pirrolidona es N-dodecil-2-pirrolidona.
7. Composición transdérmica, según la reivindicación 1 o 5, en la que el derivado alifático C8-18 es al menos uno seleccionado del grupo que consiste en alcohol laurílico, alcohol oleílico, lactato de laurilo, monolaurato de glicerol, monooleato de glicerol, miristato de isopropilo, monolaurato de sorbitán, monooleato de sorbitán, monolaurato de propilenglicol, monooleato de propilenglicol, glicérido de macrogol oleilo, ácido oleico, glicérido de macrogol lauroilo, glicérido de macrogol linoleoilo, caprilato/caprato de propilenglicol, monocaprilato de propilenglicol, y monoestearato de sorbitán, opcionalmente
en la que el derivado alifático es monooleato de glicerol o miristato de isopropilo.
8. Composición transdérmica, según la reivindicación 1 o 5, en la que el derivado de ácido cítrico es al menos uno seleccionado del grupo que consiste en citrato de acetil trietilo, citrato de dietilo, citrato de tributilo, citrato de trietilo y citrato de acetil tributilo.
9. Composición transdérmica, según la reivindicación 8, en la que el derivado de ácido cítrico es citrato de trietilo.
10. Composición transdérmica, según la reivindicación 1, en la que el contenido de acetato de vinilo (VA) en polietileno-acetato de vinilo (EVA) usado en el adhesivo de EVA es 4-50% en peso, opcionalmente
en la que el contenido de acetato de vinilo (VA) en polietileno-acetato de vinilo (EVA) usado en el adhesivo de EVA es del 35-45% en peso.
11. Composición transdérmica, según la reivindicación 1, en la que la capa de matriz adhesiva no contiene donepezilo.
12. Composición transdérmica para usar en un procedimiento para administrar donepezilo en un sujeto, comprendiendo el procedimiento:
(1) unir, a la piel de un sujeto, una composición transdérmica que comprende donepezilo como principio activo, en la que la composición transdérmica comprende:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico,
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico, en el que el adhesivo acrílico no contiene un grupo funcional; y
(d) una capa de liberación; y
(2) mantener la composición transdérmica unida a la piel del sujeto durante un tiempo suficiente para suministrar donepezilo al sujeto.
13. Composición transdérmica para usar, según la reivindicación 12, en la que el tiempo es de 1 a 10 días.
14. Kit que comprende una composición transdérmica, en el que la composición transdérmica comprende:
(a) una capa de soporte;
(b) una capa de matriz que contiene fármaco que comprende, en base al peso total de la capa de matriz que contiene fármaco,
(b-1) 15-55% en peso de donepezilo o una sal farmacéuticamente aceptable del mismo,
(b-2) 25-70% en peso de un adhesivo a base de EVA,
(b-3) 5-20% en peso de al menos uno seleccionado del grupo que consiste en un derivado de pirrolidona y un derivado alifático C8-18, y
(b-4) 1-10% en peso de triacetina o un derivado de ácido cítrico,
(c) una capa de matriz adhesiva de polímero que comprende, en base al peso total de la capa de matriz adhesiva de polímero, 60% en peso o más de un adhesivo acrílico, en el que el adhesivo acrílico no contiene un grupo funcional; y
(d) una capa de liberación.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| KR20140183446 | 2014-12-18 | ||
| PCT/KR2015/013940 WO2016099198A1 (ko) | 2014-12-18 | 2015-12-18 | 도네페질을 유효성분으로 함유하는 경피흡수제제 |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2786399T3 true ES2786399T3 (es) | 2020-10-09 |
Family
ID=56126987
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15870365T Active ES2786399T3 (es) | 2014-12-18 | 2015-12-18 | Preparación transdérmica que contiene donepezilo como principio activo |
Country Status (15)
| Country | Link |
|---|---|
| US (1) | US10888533B2 (es) |
| EP (1) | EP3235494B1 (es) |
| JP (1) | JP6793648B2 (es) |
| KR (1) | KR101796771B1 (es) |
| CN (2) | CN107106510A (es) |
| AU (1) | AU2015363883B2 (es) |
| CA (1) | CA2970276C (es) |
| DK (1) | DK3235494T3 (es) |
| ES (1) | ES2786399T3 (es) |
| HU (1) | HUE048569T2 (es) |
| MY (1) | MY181540A (es) |
| PL (1) | PL3235494T3 (es) |
| PT (1) | PT3235494T (es) |
| RU (1) | RU2713207C2 (es) |
| WO (1) | WO2016099198A1 (es) |
Families Citing this family (12)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| WO2017117554A1 (en) | 2015-12-30 | 2017-07-06 | Corium International, Inc. | Systems and methods for long term transdermal administration |
| AU2017281789B2 (en) | 2016-06-23 | 2023-04-13 | Corium, LLC. | Adhesive matrix with hydrophilic and hydrophobic domains and a therapeutic agent |
| EP3490559A1 (en) | 2016-07-27 | 2019-06-05 | Corium International, Inc. | Transdermal delivery systems with pharmacokinetics bioequivalent to oral delivery |
| US10300025B2 (en) | 2016-07-27 | 2019-05-28 | Corium, Inc. | Donepezil transdermal delivery system |
| WO2018022818A1 (en) | 2016-07-27 | 2018-02-01 | Corium International, Inc. | Memantine transdermal delivery systems |
| KR102033686B1 (ko) * | 2017-05-19 | 2019-10-18 | 보령제약 주식회사 | 도네페질을 함유하는 마이크로니들 경피 패치 |
| AU2018307792B2 (en) * | 2017-07-26 | 2024-08-08 | Corium, LLC. | Transdermal delivery system with a microporous membrane having solvent-filled pores |
| US11173132B2 (en) | 2017-12-20 | 2021-11-16 | Corium, Inc. | Transdermal adhesive composition comprising a volatile liquid therapeutic agent having low melting point |
| KR102024996B1 (ko) * | 2017-12-27 | 2019-09-25 | 동아에스티 주식회사 | 도네페질을 함유하는 치매 치료용 경피흡수제제 |
| KR102115102B1 (ko) * | 2018-12-21 | 2020-05-26 | 동아에스티 주식회사 | 안정화된 도네페질 함유 경피 흡수제제 |
| KR102709239B1 (ko) | 2021-10-20 | 2024-09-25 | 서울대학교병원 | 치매 약물의 부작용을 평가할 수 있는 치매 약물 패치 |
| KR20240146479A (ko) * | 2023-03-29 | 2024-10-08 | 아이큐어 주식회사 | 고용량 도네페질 약물탑재 지속방출 경피흡수제제 |
Family Cites Families (21)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US5985317A (en) * | 1996-09-06 | 1999-11-16 | Theratech, Inc. | Pressure sensitive adhesive matrix patches for transdermal delivery of salts of pharmaceutical agents |
| JP3987655B2 (ja) | 1998-03-03 | 2007-10-10 | エーザイ・アール・アンド・ディー・マネジメント株式会社 | 抗痴呆薬を含有した経皮適用製剤又は坐剤 |
| BR0207955A (pt) * | 2001-03-07 | 2004-02-25 | Hisamitsu Pharmaceutical Co | Agente de emplastro |
| KR20050037405A (ko) | 2001-10-17 | 2005-04-21 | 히사미쯔 제약 주식회사 | 경피 흡수형 제제 |
| US20100048628A1 (en) * | 2006-12-01 | 2010-02-25 | Sumiyo Nishi | Method for suppressing discoloration over time of adhesive preparation containing donepezil |
| KR101454362B1 (ko) * | 2008-03-24 | 2014-10-23 | 아이큐어 주식회사 | 도네페질을 유효성분으로 함유하는 치매 치료용경피흡수제제 |
| US20090291127A1 (en) * | 2008-05-21 | 2009-11-26 | Jianye Wen | Transdermal anti-dementia active agent formulations and methods for using the same |
| CA2733265A1 (en) * | 2008-09-30 | 2010-04-08 | Teikoku Pharma Usa, Inc. | Transdermal extended-delivery donepezil compositions and methods for using the same |
| US8456368B2 (en) * | 2009-01-27 | 2013-06-04 | Casio Computer Co., Ltd. | Antenna device and radio-wave receiver with such antenna device |
| US20100209484A1 (en) * | 2009-02-13 | 2010-08-19 | Hoo-Kyun Choi | Transdermal Triptan Delivery System |
| CN102630160B (zh) * | 2009-09-16 | 2014-05-07 | 株式会社三养生物制药 | 透皮递送系统、其制备方法以及使用所述系统的透皮递送方法 |
| JP2012236773A (ja) * | 2009-12-16 | 2012-12-06 | Goto Takeshi | 抗認知症薬物の経皮吸収製剤 |
| US20100178307A1 (en) * | 2010-01-13 | 2010-07-15 | Jianye Wen | Transdermal anti-dementia active agent formulations and methods for using the same |
| NZ605352A (en) * | 2010-06-30 | 2013-10-25 | Nal Pharmaceuticals Ltd | Process for producing glycosaminoglycans |
| TWI433904B (zh) * | 2011-01-12 | 2014-04-11 | Taiwan Biotech Co Ltd | 多奈哌齊經皮貼片 |
| KR101395557B1 (ko) * | 2011-08-25 | 2014-05-16 | 아이큐어 주식회사 | 경피 흡수 제제 및 그 제조방법 |
| KR101239150B1 (ko) * | 2012-02-28 | 2013-03-06 | 에스케이케미칼주식회사 | 도네페질-함유 경피흡수제제 및 그의 제조방법 |
| US9539201B2 (en) * | 2012-04-20 | 2017-01-10 | KAT Transdermals LLC | Selegiline transdermal system |
| CN102895217A (zh) * | 2012-11-13 | 2013-01-30 | 沈阳药科大学 | 长效多奈哌齐经皮吸收贴剂 |
| KR101770675B1 (ko) * | 2013-01-30 | 2017-08-23 | 에스케이케미칼주식회사 | 도네페질-함유 경피흡수제제 및 그의 제조방법 |
| CN108123793A (zh) * | 2017-12-19 | 2018-06-05 | 杭州中天微系统有限公司 | 基于apb总线的spi通信装置 |
-
2015
- 2015-12-18 JP JP2017533482A patent/JP6793648B2/ja active Active
- 2015-12-18 MY MYPI2017702165A patent/MY181540A/en unknown
- 2015-12-18 HU HUE15870365A patent/HUE048569T2/hu unknown
- 2015-12-18 WO PCT/KR2015/013940 patent/WO2016099198A1/ko not_active Ceased
- 2015-12-18 EP EP15870365.2A patent/EP3235494B1/en active Active
- 2015-12-18 AU AU2015363883A patent/AU2015363883B2/en active Active
- 2015-12-18 RU RU2017125361A patent/RU2713207C2/ru active
- 2015-12-18 CN CN201580069780.8A patent/CN107106510A/zh active Pending
- 2015-12-18 KR KR1020150181809A patent/KR101796771B1/ko active Active
- 2015-12-18 CA CA2970276A patent/CA2970276C/en active Active
- 2015-12-18 CN CN202111197382.8A patent/CN113797180A/zh active Pending
- 2015-12-18 PL PL15870365T patent/PL3235494T3/pl unknown
- 2015-12-18 PT PT158703652T patent/PT3235494T/pt unknown
- 2015-12-18 ES ES15870365T patent/ES2786399T3/es active Active
- 2015-12-18 DK DK15870365.2T patent/DK3235494T3/da active
-
2017
- 2017-06-16 US US15/625,054 patent/US10888533B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| EP3235494A4 (en) | 2018-08-15 |
| CN107106510A (zh) | 2017-08-29 |
| JP2017538771A (ja) | 2017-12-28 |
| BR112017012951A2 (pt) | 2018-03-06 |
| CA2970276C (en) | 2023-08-01 |
| PT3235494T (pt) | 2020-03-05 |
| EP3235494A1 (en) | 2017-10-25 |
| CN113797180A (zh) | 2021-12-17 |
| WO2016099198A1 (ko) | 2016-06-23 |
| EP3235494B1 (en) | 2019-11-27 |
| US20170290780A1 (en) | 2017-10-12 |
| RU2017125361A3 (es) | 2019-07-17 |
| JP6793648B2 (ja) | 2020-12-02 |
| RU2713207C2 (ru) | 2020-02-04 |
| KR101796771B1 (ko) | 2017-11-10 |
| AU2015363883A1 (en) | 2017-06-29 |
| AU2015363883B2 (en) | 2021-03-25 |
| KR20160074433A (ko) | 2016-06-28 |
| HUE048569T2 (hu) | 2020-07-28 |
| RU2017125361A (ru) | 2019-01-18 |
| PL3235494T3 (pl) | 2020-08-24 |
| CA2970276A1 (en) | 2016-06-23 |
| DK3235494T3 (da) | 2020-03-02 |
| US10888533B2 (en) | 2021-01-12 |
| MY181540A (en) | 2020-12-28 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2786399T3 (es) | Preparación transdérmica que contiene donepezilo como principio activo | |
| KR101454362B1 (ko) | 도네페질을 유효성분으로 함유하는 치매 치료용경피흡수제제 | |
| ES2652491T3 (es) | Preparación que contiene donepecilo de absorción transdérmica | |
| ES2286028T3 (es) | Parches para uso externo. | |
| ES2317138T3 (es) | Parche transdermico que comprende un agente de diminucion del punto de fusion. | |
| ES2657016T3 (es) | Parche cutáneo adhesivo que contiene ropinirol y producto envasado del mismo | |
| CN103313705B (zh) | 含有利凡斯的明的经皮吸收制剂 | |
| PT99749B (pt) | Processo de preparacao de uma composicao incrementadora da permeacao na pele | |
| US20090285877A1 (en) | Percutaneous absorption preparation containing palonosetron | |
| JP7071958B2 (ja) | メマンチン経皮送達システム | |
| ES2449042T3 (es) | Parche adhesivo | |
| JP4271869B2 (ja) | 経皮投与用抗嘔吐剤組成物およびこれを含む製剤 | |
| JP2002363070A (ja) | 経皮吸収貼付剤 | |
| ES2661911T3 (es) | Parche farmacéutico para la administración transdérmica de tapentadol | |
| US20130324950A1 (en) | Transdermal delivery system containing galantamine or salts thereof | |
| US8563031B2 (en) | Piroxicam-containing matrix patches and methods for the topical treatment of acute and chronic pain and inflammation therewith | |
| CN106361728A (zh) | 经皮吸收制剂及制备经皮吸收制剂的方法 | |
| BR112017012951B1 (pt) | Composição transdérmica contendo donepezila como ingrediente ativo e kit | |
| KR101669095B1 (ko) | 그라니세트론을 함유하는 매트릭스형 경피흡수패치 및 이를 이용한 구토의 치료 및 예방 방법 | |
| WO2024127805A1 (ja) | ドネペジル含有経皮吸収製剤 | |
| WO2018133010A1 (zh) | 经皮吸收制剂及制备经皮吸收制剂的方法 | |
| HK1117029A (en) | Transdermal method and patch for nausea |