ES2806624T3 - Derivados de podofilotoxina y su uso - Google Patents
Derivados de podofilotoxina y su uso Download PDFInfo
- Publication number
- ES2806624T3 ES2806624T3 ES15907433T ES15907433T ES2806624T3 ES 2806624 T3 ES2806624 T3 ES 2806624T3 ES 15907433 T ES15907433 T ES 15907433T ES 15907433 T ES15907433 T ES 15907433T ES 2806624 T3 ES2806624 T3 ES 2806624T3
- Authority
- ES
- Spain
- Prior art keywords
- compound
- cancer
- optionally substituted
- alkyl
- tumor
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 0 CCN(*)*C=C Chemical compound CCN(*)*C=C 0.000 description 2
Classifications
-
- C—CHEMISTRY; METALLURGY
- C07—ORGANIC CHEMISTRY
- C07D—HETEROCYCLIC COMPOUNDS
- C07D519/00—Heterocyclic compounds containing more than one system of two or more relevant hetero rings condensed among themselves or condensed with a common carbocyclic ring system not provided for in groups C07D453/00 or C07D455/00
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K31/00—Medicinal preparations containing organic active ingredients
- A61K31/33—Heterocyclic compounds
- A61K31/395—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins
- A61K31/435—Heterocyclic compounds having nitrogen as a ring hetero atom, e.g. guanethidine or rifamycins having six-membered rings with one nitrogen as the only ring hetero atom
- A61K31/47—Quinolines; Isoquinolines
- A61K31/4738—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems
- A61K31/4745—Quinolines; Isoquinolines ortho- or peri-condensed with heterocyclic ring systems condensed with ring systems having nitrogen as a ring hetero atom, e.g. phenantrolines
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P35/00—Antineoplastic agents
- A61P35/02—Antineoplastic agents specific for leukemia
Landscapes
- Health & Medical Sciences (AREA)
- Chemical & Material Sciences (AREA)
- Organic Chemistry (AREA)
- Life Sciences & Earth Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Animal Behavior & Ethology (AREA)
- General Health & Medical Sciences (AREA)
- Public Health (AREA)
- Veterinary Medicine (AREA)
- Medicinal Chemistry (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Oncology (AREA)
- Hematology (AREA)
- Epidemiology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Nitrogen Condensed Heterocyclic Rings (AREA)
- Heterocyclic Carbon Compounds Containing A Hetero Ring Having Oxygen Or Sulfur (AREA)
- Nitrogen And Oxygen Or Sulfur-Condensed Heterocyclic Ring Systems (AREA)
- Medicinal Preparation (AREA)
Abstract
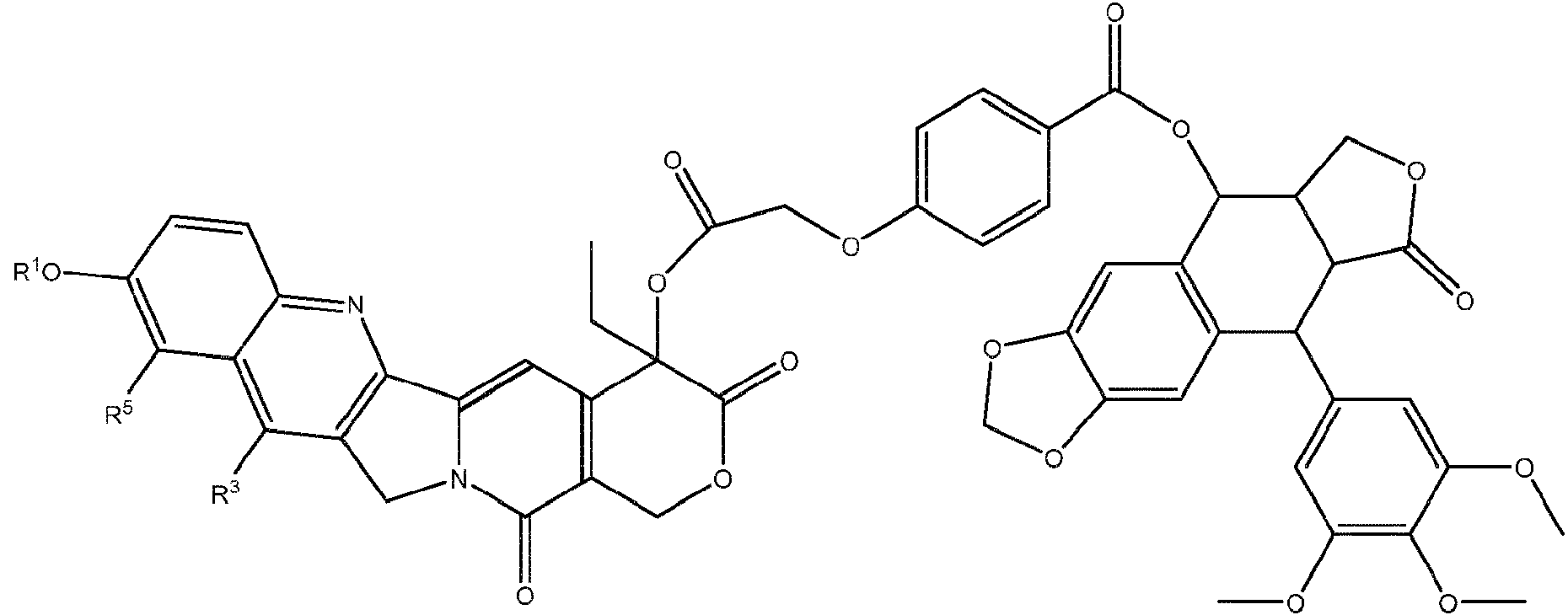
Un compuesto de fórmula (I): **(Ver fórmula)** o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores, en donde R1 es H o tiene una estructura de: **(Ver fórmula)** R3 es H, un alquilo C1-C8 opcionalmente sustituido, un cicloalquilo de 3-10 miembros opcionalmente sustituido, un heterociclilo de 3-10 miembros opcionalmente sustituido, un arilo de 6-10 miembros opcionalmente sustituido o un heteroarilo de 5-10 miembros opcionalmente sustituido; R5 es H o tiene una estructura de: **(Ver fórmula)** y R11 y R12 son independientemente un alquilo C1-C8 opcionalmente sustituido.
Description
DESCRIPCIÓN
Derivados de podofilotoxina y su uso
Campo
La presente divulgación se refiere a derivados de podofilotoxina, composiciones de los mismos, y su uso para tratar diversos tipos de cánceres en un sujeto y/o retrasar o reducir diversos tipos de crecimientos tumorales en un sujeto.
Estado de la técnica
Podofilotoxina es un compuesto conocido que tiene la fórmula:
El compuesto muestra actividad como antivírico y como agente antineoplásico. La presente divulgación se refiere a derivados de podofilotoxina que son útiles para tratar el cáncer.
El documento US2009/298870 A1 divulga ésteres 4-O de podofilotoxina y 4'-desmetilepipodofilotoxina. Los compuestos son ésteres 4-0 de un ácido alcanoico o ácido alcanoico sustituido y podofilotoxina y 4'-desmetilepipodofllotoxina. Se dice que los compuestos son útiles para tratar el cáncer.
Sumario
En un aspecto, se proporciona en el presente documento un compuesto de fórmula (I):
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores, en donde
R1 es H o tiene una estructura de:
R3 es H, un alquilo C1-C8 opcionalmente sustituido, un cicloalquilo de 3-10 miembros opcionalmente sustituido, un heterociclilo de 3-10 miembros opcionalmente sustituido, un arilo de 6-10 miembros opcionalmente sustituido o un heteroarilo de 5-10 miembros opcionalmente sustituido;
R5 es H o tiene una estructura de:
y
R11 y R12 son independientemente un alquilo C1-C8 opcionalmente sustituido.
En otro aspecto, se proporciona en el presente documento una composición farmacéutica que comprende un compuesto proporcionado en el presente documento, y al menos un excipiente farmacéuticamente aceptable.
En otro aspecto, se proporciona en el presente documento un método para tratar el cáncer en un sujeto que lo necesita que comprende administrar al sujeto una cantidad terapéuticamente eficaz de un compuesto proporcionado en el presente documento.
En otro aspecto, se proporciona en el presente documento un método para retrasar o reducir el crecimiento tumoral en un sujeto que lo necesita, que comprende administrar al sujeto una cantidad terapéuticamente eficaz de un compuesto proporcionado en el presente documento.
En otro aspecto, se proporciona en el presente documento un método para tratar el cáncer en un sujeto que lo necesita, que comprende administrar al sujeto una cantidad terapéuticamente eficaz de una composición farmacéutica proporcionada en el presente documento.
Breve descripción de los dibujos
La Fig. 1A muestra los espectros de resonancia magnética nuclear de 1H de N2. Las Figs. 1B y 1F muestran los espectros de resonancia magnética nuclear de 1H de los Compuestos diana 1 y 4, respectivamente. Las Figs 1C-1E muestran los espectros de resonancia magnética nuclear de 1H del Compuesto diana 3.
La Fig. 2 muestra el espectro de resonancia magnética nuclear de 13C de N2.
Las Figs. 3A-3D muestran los espectros de masas-cromatografía líquida de N2 y los Compuestos diana 1, 3, y 4, respectivamente.
La Fig. 4A muestra la actividad antitumoral del N2-HCl formulado (i.v.) en el tratamiento del Modelo de xenoinjerto de cáncer de colon humano COLO205. La Fig. 4B muestra la actividad antitumoral del N2-HCl (i.p.) en el tratamiento del modelo de xenoinjerto de cáncer de colon humano COLO205.
La Fig. 5A muestra la actividad antitumoral del N2 formulado (i.v.) en el tratamiento del modelo de xenoinjerto de cáncer de colon humano HCT116. La Fig. 5B muestra la actividad antitumoral del N2-HCl (i.p.) en el tratamiento del modelo de xenoinjerto de cáncer de colon humano HCT116.
La Fig. 6 muestra las curvas de crecimiento tumoral de diferentes grupos de ratones descritos en la Tabla 1.7. La Fig. 7 muestra la actividad antitumoral del N2 formulado e Imatinib en el tratamiento del modelo de xenoinjerto
K562.
Descripción detallada
Los compuestos de la divulgación son activos contra tumores en ratones y son generalmente bien tolerados o se considera que lo son. Son útiles para tratar diversos tipos de cánceres y se pueden formular para fabricar preparaciones farmacéuticas, por ejemplo, para administración oral, tópica o parenteral.
Salvo que se indique otra cosa, todos los números que expresan cantidades de ingredientes, condiciones de reacción y otros que se usan en la memoria descriptiva y las reivindicaciones deben considerarse como modificados en todos los casos por el término "aproximadamente". Por consiguiente, Salvo que se indique lo contrario, los parámetros numéricos que se definen en la siguiente memoria descriptiva y reivindicaciones adjuntas son aproximaciones. Cada parámetro numérico debe interpretarse al menos a la luz del número de dígitos significativos indicados y aplicando técnicas de redondeo habituales.
A lo largo de esta divulgación, el texto se refiere a diversas realizaciones de los presentes compuestos, composiciones y métodos. Las diversas realizaciones descritas pretenden proporcionar varios ejemplos ilustrativos y no deben interpretarse como descripciones de especies alternativas. En su lugar, debe señalarse que las descripciones de varias realizaciones proporcionadas en el presente documento pueden ser de alcance superpuesto. Las realizaciones descritas en el presente documento son meramente ilustrativas y no pretenden limitar el alcance de la presente invención.
Se debe indicar que, tal como se utiliza en el presente documento y en las reivindicaciones adjuntas, las formas en singular "un", "uno/a" y "el/la" incluyen referencias en plural salvo que el contexto indique claramente otra cosa. Por lo tanto, por ejemplo, la referencia a "un excipiente" incluye una pluralidad de excipientes.
Como se utiliza en el presente documento, se aplicarán las siguientes definiciones salvo que se indique otra cosa. Además, si algún término o símbolo usado en el presente documento no se define como se muestra a continuación, tendrá su significado ordinario en la técnica.
"Que comprende" pretende significar que las composiciones y los métodos incluyen los elementos citados, pero sin excluir otros. "Que consiste esencialmente de" cuando se usa para definir composiciones y métodos, significará excluir otros elementos de cualquier significado esencial para la combinación. Por ejemplo, una composición que consiste esencialmente de los elementos que se definen en el presente documento no excluiría otros elementos que no afecten materialmente las características básicas y novedosas de la invención reivindicada. "Consiste de" significa excluir más que los elementos traza de otros ingredientes y etapas del procedimiento sustanciales enumerados. Las realizaciones definidas por cada uno de estos términos de transición están dentro del alcance de la presente invención.
El término "alquilo" se refiere a un radical hidrocarburo alifático saturado monovalente que tiene el número indicado de átomos de carbono. Por ejemplo, un "alquilo C1-6" o un "alquilo de 1-6 átomos de carbono" o "Alq 1-6" se referirá a cualquier grupo alquilo que contiene de uno a seis átomos de carbono en la estructura. "Alquilo C1-20" se refiere a un grupo alquilo que tiene de uno a veinte átomos de carbono. Alquilo puede ser una cadena lineal (es decir lineal) o una cadera ramificada. Los ejemplos representativos de radicales alquilo inferior incluyen metilo, etilo, n-propilo, nbutilo, n-pentilo, n-hexilo, isopropilo, isobutilo, isopentilo, amilo, sec-butilo, terc-butilo, terc-pentilo, n-heptilo, n-octilo y similares, junto con sus variaciones ramificadas. El radical puede estar opcionalmente sustituido con sustituyentes en posiciones que no interfieren de forma significativa con la preparación de los compuestos que están comprendidos en el alcance de la presente invención y que no reducen de forma significativa la eficacia de los compuestos. El alquilo puede estar opcionalmente sustituido con de uno a cinco sustituyentes seleccionados independientemente entre el grupo que consiste en halo, alcoxi inferior, hidroxi, ciano, nitro o amino.
El término "alcoxi" se refiere a un radical monovalente de la fórmula RO-, donde R es un alquilo tal como se define en el presente documento. Alcoxi inferior se refiere a un alcoxi de 1-6 átomos de carbono, donde alcoxi superior es un alcoxi de siete o más átomos de carbono. Los radicales alcoxi inferiores representativos incluyen metoxi, etoxi, npropoxi, n-butoxi, n-pentiloxi, n-hexiloxi, isopropoxi, isobutoxi, isopentiloxi, amiloxi, sec-butoxi, terc-butoxi, terc-pentiloxi, y similares. Los radicales alcoxi superiores incluyen aquellos correspondientes a los radicales alquilo superiores que se definen en el presente documento. El radical puede estar opcionalmente sustituido con sustituyentes en posiciones que no interfieren de forma significativa con la preparación de los compuestos que están comprendidos en el alcance de la presente invención y que no reducen de forma significativa la eficacia de los compuestos. El radical puede estar opcionalmente sustituido con de uno a cinco sustituyentes seleccionados independientemente entre el grupo que consiste en halo, alquilo inferior, alcoxi inferior, hidroxi, ciano, nitro o amino.
El término "cicloalquilo" se refiere a un radical hidrocarburo saturado alicíclico monovalente que tiene tres o más átomos de carbono formando el anillo. Aunque los compuestos de cicloalquilo conocidos pueden tener hasta 30 o más átomos de carbono, generalmente habrá de tres a siete átomos de carbono en el anillo. Los últimos incluyen, por ejemplo, ciclopropilo, ciclobutilo, ciclopentilo, ciclohexilo y cicloheptilo. El radical puede estar opcionalmente sustituido con sustituyentes en posiciones que no interfieren de forma significativa con la preparación de los compuestos que
están comprendidos en el alcance de la presente invención y que no reducen de forma significativa la eficacia de los compuestos. El cicloalquilo está opcionalmente sustituido con de uno a cinco sustituyentes seleccionados independientemente entre el grupo que consiste en halo, alquilo inferior, alcoxi inferior, hidroxi, ciano, nitro, amino, alquilo inferior halogenado, alcoxi inferior halogenado, hidroxicarbonilo, alcoxicarbonilo inferior, alcoxicarbonilo inferior y alquilcarbonilamino inferior.
El término "hidroxicarbonilo" es un radical monovalente que tiene la fórmula -C(O)OH.
El término "alcoxicarbonilo inferior" es un radical monovalente que tiene la fórmula -C(O)OAlq, donde Alq es alquilo inferior.
El término "alquilcarboxiloxi inferior" es un radical monovalente que tiene la fórmula - OC(O)Alq, donde Alq es alquilo inferior.
el término "alquilcarbonilamino" inferior es un radical monovalente que tiene la fórmula -NHC(O)Alq, donde Alq es alquilo inferior.
El término "alquilamino" es un radical monovalente que tiene la fórmula -NR1 , R2 donde R1 es alquilo y R2 es hidrógeno o alquilo y el alquilo está opcionalmente sustituido.
"Amino" se refiere al grupo -NH2.
"Arilo" o "Ar" se refiere a un grupo carbocíclico aromático monovalente de 6 a 14 átomos de carbono que tiene un único anillo (por ejemplo, fenilo (Ph)) o múltiples anillo condensados (por ejemplo, naftilo o antrilo) cuyos anillos condensados pueden ser aromáticos o no (por ejemplo, 2-benzoxazolinona, 2H-1,4-benzoxazin-3(4H)-ona-7-ilo, y similares) con la condición que el punto de unión sea un átomo de carbono aromático. Los grupos arilo preferidos incluyen fenilo y naftilo.
"Arilo sustituido" se refiere a grupos arilo que están sustituidos con de 1 a 5, preferentemente de 1 a 3 o más preferentemente de 1 a 2 sustituyentes seleccionados entre el grupo que consiste de alquilo, alquilo sustituido, alquenilo, alquenilo sustituido, alquinilo, alquinilo sustituido, alcoxi, alcoxi sustituido, acilo, acilamino, aciloxi, amino, amino sustituido, aminocarbonilo, aminotiocarbonilo, aminocarbonilamino, aminotiocarbonilamino, aminocarboniloxi, aminosulfonilo, aminosulfoniloxi, aminosulfonilamino, amidino, arilo, arilo sustituido, ariloxi, ariloxi sustituido, ariltio, ariltio sustituido, carboxilo, éster de carboxilo, amino (éster de carboxilo), oxi (éster de carboxilo), ciano, cicloalquilo, cicloalquilo sustituido, cicloalquiloxi, cicloalquiloxi sustituido, cicloalquiltio, cicloalquiltio sustituido, guanidino, guanidino sustituido, halo, hidroxi, heteroarilo, heteroarilo sustituido, heteroariloxi, heteroariloxi sustituido, heteroariltio, heteroariltio sustituido, heterocíclico, heterocíclico sustituido, heterocicliloxi, heterocicliloxi sustituido, heterocicliltio, heterocicliltio sustituido, nitro, SO3H, sulfonilo sustituido, sulfoniloxi, tioacilo, tiol, alquiltio y alquiltio sustituido, en donde dichos sustituyentes se definen en el presente documento.
Un sustituyente "halo" es un radical halógeno monovalente seleccionado entre cloro, bromo, yodo y flúor. Un compuesto "halogenado" es un compuesto sustituido con uno o más sustituyentes halo.
"Heteroarilo" se refiere a un grupo aromático de 1 a 10 átomos de carbono y de 1 a 4 heteroátomos seleccionados entre el grupo que consiste en oxígeno, nitrógeno y azufre dentro del anillo. Dichos grupos heteroarilo pueden tener un único anillo (por ejemplo, piridilo o furilo) o múltiples anillos condensados (por ejemplo, indolizinilo o benzotienilo) en donde los anillos condensados pueden ser aromáticos o no y/o contienen un heteroátomo con la condición de que el punto de unión sea a través de un átomo del grupo heteroarilo aromático. En una realización, el átomo o átomos de anillo de nitrógeno y/o azufre del grupo heteroarilo se oxidan opcionalmente para proporcionar los restos N-óxido (N ^O ), sulfinilo o sulfonilo. Los heteroarilos preferidos incluyen heteroarilos de 5 o 6 miembros tales como piridinilo, pirrolilo, indolilo, tiofenilo y furanilo.
"Heteroarilo sustituido" se refiere a grupos heteroarilo que están sustituidos con de 1 a 5, preferentemente de 1 a 3 o más preferentemente de 1 a 2 sustituyentes seleccionados del grupo que consiste en el mismo grupo de sustituyentes definidos para arilo sustituido.
"Heterociclo" o "heterocíclico" o "heterocicloalquilo" o "heterociclilo" se refiere a un grupo saturado o parcialmente saturado, pero no aromático, que tiene de 1 a 10 átomos de carbono en el anillo y de 1 a 4 heteroátomos del anillo seleccionados entre el grupo que consiste en nitrógeno, azufre u oxígeno. Cicloalquilo Cx se refiere a un grupo heterocicloalquilo que tiene x número de átomos del anillo que incluyen los heteroátomos del anillo. Heterociclo abarca un único anillo o múltiples anillos condensados, incluyendo los sistemas de anillos condensados con puente y los sistemas de anillos espiro. En los sistemas de anillos condensados, uno o más de los anillos pueden ser cicloalquilo, arilo o heteroarilo con la condición de que el punto de unión sea a través del anillo no aromático. En una realización, el átomo o átomos de nitrógeno y/o azufre del grupo heterocíclico se oxidan opcionalmente para proporcionar los restos N-óxido, sulfinilo, sulfonilo.
"Heterocíclico sustituido" o "heterocicloalquilo sustituido" o "heterociclilo sustituido" se refiere a grupos heterociclilo que están sustituidos con de 1 a 5 o preferentemente de 1 a 3 de los mismos sustituyentes que se han definido para el cicloalquilo sustituido.
Los ejemplos de heterociclo y heteroarilo incluyen, aunque no de forma limitativa, azetidina, pirrol, imidazol, pirazol, piridina, pirazina, pirimidina, piridazina, indolizina, isoindol, indol, dihidroindol, indazol, purina, quinolizina, isoquinolina, quinolina, ftalazina, naftilpiridina, quinoxalina, quinazolina, cinolina, pteridina, carbazol, carbolina, fenantridina, acridina, fenantrolina, isotiazol, fenazina, isoxazol, fenoxazina, fenotiazina, imidazolidina, imidazolina, piperidina, piperazina, indolina, ftalimida, 1,2,3,4-tetrahidroisoquinolina, 4,5,6,7-tetrahidrobenzo[b]tiofeno, tiazol, tiazolidina, tiofeno, benzo[b]tiofeno, morfolinilo, tiomorfolinilo (también denominado tiamorfolinilo), 1,1-dioxotiomorfolinilo, piperidinilo, pirrolidina y tetrafuranilo.
Un "amino cíclico" es un radical monovalente de un anillo de amina cíclica de 5, 6 o 7 miembros que no tiene más de un heteroátomo adicional tal como nitrógeno, oxígeno o azufre. Los ejemplos representativos incluyen, por ejemplo, 1 -pirrolidino, 1 -piperidino, morfolino, piperazino, 3-bencilpiperidino y similares. Estos pueden estar sustituidos o no sustituidos. De estar sustituidos, generalmente no tendrán más de 2 sustituyentes seleccionados entre alquilo inferior, cicloalquilo inferior, hidroxialquilo inferior, fenilo (sustituido o no sustituido), bencilo (sustituido o no sustituido), aminocarbonilmetilo, alquilaminocarbonilmetilo inferior, amino, monoalquilamino o dialquilamino inferior, amino cíclico o un anillo heterocíclico de 5 o 6 miembros.
Otros términos químicos reciben su significado convencional como entiende un experto en la materia según las directrices encontradas en textos y diccionarios convencionales.
El término "MTD" es la abreviatura de la dosis máxima tolerada.
El término "nM" es la abreviatura de nanomolar.
El término "ip" es la abreviatura de intraperitoneal.
"Tratar" o "tratamiento" de una enfermedad en un paciente se refiere a 1) evitar que se produzca la enfermedad en un paciente que está predispuesto o no presenta todavía síntomas de la enfermedad; 2) inhibir la enfermedad o detener su desarrollo; o 3) mejorar o producir la regresión de la enfermedad
"Sujeto" se refiere a mamíferos e incluye seres humanos y mamíferos no humanos. Los ejemplos de pacientes incluyen, aunque no de forma limitativa, ratones, ratas, hámsteres, cobayas, cerdos, conejos, gatos, perros, cabras, ovejas, vacas y seres humanos. En algunas realizaciones, paciente se refiere a un ser humano.
La expresión "farmacéuticamente aceptable" se refiere a seguro y no tóxico para administración in vivo, preferentemente, para la administración a seres humanos.
"Sal farmacéuticamente aceptable" se refiere a una sal que es farmacéuticamente aceptable. Cualquier compuesto descrito en el presente documento puede administrarse como una sal farmacéuticamente aceptable.
"Sal" se refiere a un compuesto iónico formado entre un ácido y una base. Cuando el compuesto proporcionado en el presente documento contiene una funcionalidad ácida, dichas sales incluyen, aunque no de forma limitativa, sales de metales alcalinos, metales alcalinotérreos y amonio. Como se utiliza en el presente documento, las sales de amonio incluyen, sales que contienen bases nitrogenadas protonadas y bases nitrogenadas alquiladas. Los cationes ilustrativos y no limitantes útiles en las sales farmacéuticamente aceptables incluyen los cationes Na, K, Rb, Cs, NH4, Ca, Ba y amonio basados en aminoácidos de origen natural. Cuando los compuestos utilizados en el presente documento contienen una funcionalidad básica, dichas sales incluyen, aunque no de forma limitativa, sales de ácidos orgánicos, tales como ácidos carboxílicos y ácidos sulfónicos, y ácidos minerales, tales como haluros de hidrógeno, ácido sulfúrico, ácido fosfórico y similares. Los aniones ilustrativos y no limitantes útiles las sales farmacéuticamente aceptables incluyen oxalato, maleato, acetato, propionato, succinato, tartrato, cloruro, sulfato, bisulfato, fosfato monobásico, dibásico y tribásico, mesilato, tosilato y similares.
"Cantidad eficaz" o dosis de un compuesto o composición, se refiere a la cantidad del compuesto o la composición que proporciona un resultado previsto que se desea basado en la divulgación en el presente documento. Se pueden determinar cantidades eficaces mediante procedimientos farmacéuticos convencionales en cultivos celulares o animales experimentales, por ejemplo, y no de forma limitativa, por determinación de la DL50 (la dosis letal para el 50 % de la población) y la DE50 (la dosis terapéuticamente eficaz en el 50 % de la población). La relación de dosis entre los efectos tóxicos y terapéuticos es el índice terapéutico, que puede expresarse como el cociente DL50/DE50.
"Cantidad terapéuticamente eficaz" o dosis de un compuesto o una composición se refiere a la cantidad del compuesto o la composición que da como resultado la reducción o inhibición de los síntomas o una prolongación de la supervivencia en un paciente. Los resultados pueden requerir múltiples dosis del compuesto o la composición.
Los términos "opcional" u "opcionalmente", tal como se usan a lo largo de esta memoria descriptiva, significan que el evento o circunstancia que se describe posteriormente puede producirse, aunque no necesariamente, y que la descripción incluye casos en los que se produce el evento o la circunstancia y casos en los que no se produce. Por ejemplo, "el átomo de nitrógeno se oxida opcionalmente para proporcionar el resto N-óxido (N^-O)" significa que el átomo de nitrógeno no tiene que estar obligatoriamente oxidado, y la descripción incluye situaciones donde al átomo de nitrógeno no se oxida y situaciones donde al átomo de nitrógeno se oxida y situaciones donde el átomo de nitrógeno se oxida.
La expresión "opcionalmente sustituido" se refiere a un grupo sustituido o no sustituido. El grupo puede estar sustituido con uno o más sustituyentes., tales como, por ejemplo, 1,2, 3, 4 o 5 sustituyentes. Preferentemente, los sustituyentes se seleccionan entre los grupos funcionales proporcionados en el presente documento. En determinadas realizaciones más preferidas, los sustituyentes se seleccionan entre oxo, halo, -CN, NO2, -CO2R100, -OR100, -SR100, -SOR100, -SO2R100, -NR101R102, -CONR101R102, -SO2NR101R102, alquilo C1-C6, alcoxi Cr Ca, -CR100=C(R100)2, -CCR100, cicloalquilo C3-C10, heterociclilo C3-C10, -arilo C6-C12 y -heteroarilo C5-C12, en donde cada R100 es independientemente hidrógeno o alquilo C1-C8; cicloalquilo C3-C12; heterociclilo C3-C10; arilo C6-C12; o heteroarilo C2-C12; en donde cada alquilo, cicloalquilo, heterociclilo, arilo o heteroarilo está opcionalmente sustituido con 1-3 grupos halo, 1-3 grupos alquilo C1C6 , 1-3 grupos haloalquilo C1C6 o 1-3 grupos alcoxi C1C6. Más preferentemente, los sustituyentes se seleccionan entre el grupo que consiste de cloro, flúor, -OCH3, metilo, etilo, isopropilo, ciclopropilo, -OCF3 , -CF3 y -OCHF2.
r101 y r102 son independientemente hidrógeno; alquilo C1-C8 , opcionalmente sustituido con -CO2H o un éster del mismo, alcoxi C1-C6 , oxo, -CR103=C(R103)2, -CCR, cicloalquilo C3-C10, heterociclilo C3-C10, arilo C6-C12 o heteroarilo C2-C12, en donde cada R103 es independientemente hidrógeno o alquilo C1-C8 ; cicloalquilo C3-C12; heterociclilo C3-C10; arilo C6-C12; o heteroarilo C2-C12; en donde cada cicloalquilo, heterociclilo, arilo o heteroarilo está opcionalmente sustituido con 1-3 grupos alquilo o 1-3 grupos halo, o R101 y R102 junto con el átomo de nitrógeno al que están unidos forman un heterociclo de 5-7 miembros.
Salvo que se indique otra cosa, la nomenclatura de los sustituyentes que no se define explícitamente en el presente documento se consigue nombrando la parte final de la funcionalidad seguido por la funcionalidad adyacente en dirección al punto de unión. Por ejemplo, el sustituyente "alcoxicarbonilalquilo" se refiere al grupo (alcoxi)-alquilo-C(O)-(alquilo)-.
Se entiende que, en todos los grupos sustituidos definidos anteriormente, los polímeros que se obtienen definiendo sustituyentes con sustituyentes adicionales a sí mismos (por ejemplo, arilo sustituido que tiene un grupo arilo sustituido como sustituyente que está sustituido a su vez con un grupo arilo sustituido, etc.) no están previstos para su inclusión en el presente documento. En dichos casos, el número máximo de dichos sustituyentes es tres. Es decir, que cada una de las anteriores definiciones está restringida por una limitación en la que, por ejemplo, los grupos arilo sustituidos están limitados a -arilo sustituido-(arilo sustituido)-arilo sustituido.
Compuestos
En un aspecto, se proporciona en el presente documento un compuesto de fórmula (I):
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores, en donde
R1 es H o tiene una estructura de:
R3 es H, un alquilo C1-C8 opcionalmente sustituido, un cicloalquilo de 3-10 miembros opcionalmente sustituido, un heterociclilo de 3-10 miembros opcionalmente sustituido, un arilo de 6-10 miembros opcionalmente sustituido o un heteroarilo de 5-10 miembros opcionalmente sustituido;
R5 es H o tiene una estructura de:
y
R11 y R12 son independientemente un alquilo C1-C8 opcionalmente sustituido.
En una realización, R1 es H. En otra realización, R1 tiene una estructura de:
En una realización, R5 es H. En otra realización, R5 es:
En una realización, R11 es un alquilo C1C8 opcionalmente sustituido. En otra realización, R11 es alquilo C1-C8. En otra realización, R11 es metilo.
En una realización, R12 es un alquilo C1C8 opcionalmente sustituido. En otra realización, R12 es alquilo C1-C8. En otra realización, R12 es metilo.
En una realización, R3 es H. En una realización, R3 es un alquilo C1C8 opcionalmente sustituido. En otra realización, R3 es alquilo C1-C8. En otra realización, R3 es un cicloalquilo de 3-10 miembros opcionalmente sustituido. En otra realización, R3 es un heterociclilo de 3-10 miembros opcionalmente sustituido. En otra realización, R3 es un arilo de 6 10 miembros opcionalmente sustituido. En otra realización, R3 es un heteroarilo de 5-10 miembros opcionalmente sustituido. En otra realización, R3 es etilo.
En una realización, el compuesto de fórmula (I) tiene la estructura de:
En una realización, el compuesto de fórmula (I) es:
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores.
En una realización, el compuesto de fórmula (I) es:
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores.
En una realización, el compuesto de fórmula (I) es:
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores.
En una realización, el compuesto de fórmula (I) es:
o
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores.
En una realización, se proporcionan en el presente documento estereoisómeros individuales, tales como enantiómeros, de los compuestos proporcionados en el presente documento. En una realización, los compuestos proporcionados en el presente documento tienen una configuración estereoquímica como se muestra a continuación:
El técnico experto puede preparar derivados de podofilotoxina basándose en los métodos descritos en el presente documento y/o en el documento US 8.158.809, o adaptando dichos métodos.
Composición farmacéutica
En otro aspecto, se proporciona en el presente documento una composición farmacéutica que comprende un compuesto proporcionado en el presente documento, y al menos un excipiente farmacéuticamente aceptable.
En una realización, la composición farmacéutica es una forma sólida, forma líquida, forma inyectable o una formulación liposómica. En otra realización, la composición farmacéutica es una forma sólida. En otra realización, la composición farmacéutica es una forma líquida. En otra realización, la composición farmacéutica es una forma inyectable. En otra realización, la composición farmacéutica es una formulación liposómica. En otra realización, la composición farmacéutica es una formulación micelar.
Este aspecto de la divulgación es una composición farmacéutica útil para tratar el cáncer en un animal de sangre caliente, cuya composición comprende un compuesto de la divulgación como se define en el presente documento junto con un excipiente farmacéuticamente aceptable. La composición se prepara de acuerdo con técnicas de formulación conocidas para proporcionar una composición adecuada para la administración oral, tópica, transdérmica, rectal, mediante inhalación, parenteral (intravenosa, intramuscular, o intraperitoneal), y similares. Las directrices detalladas para preparar composiciones de la invención se encuentran por referencia en la 18a o 19a edición de Remington's Pharmaceutical Sciences, publicado por la Mack Publishing Co., Easton, PA 18040.
Se contemplan formas en dosis unitaria formas en dosis múltiples, ofreciendo cada una ventajas en determinados escenarios clínicos. La dosis unitaria contendría una cantidad predeterminada de principio activo calculada para producir el efecto o efectos deseados en el escenario para tratar el cáncer. La forma en dosis múltiple puede ser particularmente útil cuando se requieren múltiplos de dosis unitarias, o dosis fraccionadas, para conseguir los fines deseados. Cualquiera de estas formas farmacéuticas puede tener especificaciones que están dirigidas o son directamente dependientes de la única característica del compuesto particular, el efecto terapéutico particular a conseguir, y cualquiera de las limitaciones inherentes en la técnica de preparar el compuesto concreto para el tratamiento del cáncer.
Una dosis unitaria contendrá una cantidad terapéuticamente eficaz suficiente para tratar el cáncer en un sujeto y puede contener de aproximadamente 1,0 a 1000 mg del compuesto, por ejemplo, de aproximadamente 50 a 500 mg.
El compuesto se administrará preferentemente por vía oral en una formulación adecuada como un comprimido ingerible, un comprimido bucal, cápsula, comprimido alargado, elixir, suspensión, jarabe, pastilla soluble, oblea, gominola, y similares. Generalmente, la formulación más sencilla es un comprimido o cápsula (designado individualmente o en conjunto como una "unidad de dosificación oral"). Las formulaciones adecuadas se preparan de acuerdo con técnicas de formulación convencionales disponibles que emparejen las características del compuesto con los excipientes disponibles para formular una composición adecuada. Un comprimido o cápsula contendrá, preferentemente, de aproximadamente 50 a aproximadamente 500 mg de un compuesto de Fórmula (I).
La forma puede administrar un compuesto rápidamente o puede ser una preparación de liberación continua. El compuesto puede encerrarse en una cápsula dura o blanda, puede comprimirse en comprimidos, o puede incorporarse a bebidas, alimentos o de otra forma en la dieta. El porcentaje de las composiciones y preparaciones finales puede, por supuesto, variarse y puede variar convenientemente entre 1 y 90 % del peso de la forma final, por ejemplo, comprimido. La cantidad en dichas composiciones terapéuticamente útiles es tal que se obtendrá una dosificación adecuada. Las composiciones preferidas de acuerdo con la invención actual se preparan de tal manera que una forma unitaria de dosificación oral contiene de aproximadamente 5,0 a aproximadamente 50 % en peso (% en peso) en unidades de dosificación que pesan entre 5 y 1000 mg.
La formulación adecuada de una unidad de dosificación oral puede contener también: un aglutinante, tal como goma tragacanto, goma arábiga, almidón de maíz, gelatina; agentes edulcorantes tales como lactosa o sacarosa; agentes disgregantes tales como almidón de maíz, ácido algínico y similares; un lubricante, tal como estearato de magnesio; o un aromatizante tal como menta piperita, aceite de gaulteria o similar. Pueden estar presentes otros materiales diversos en forma de revestimientos o para modificar de otro modo la forma física de la unidad de dosificación oral. La unidad de dosificación oral puede revestirse con goma laca, un azúcar o ambas. Un jarabe o elixir pueden contener el compuesto, sacarosa como agente edulcorante, metil y propilparabenos como conservante, un colorante y un aromatizante. Cualquier material utilizado debe ser farmacéuticamente aceptable y sustancialmente no tóxico. Se pueden encontrar detalles de los tipos de excipientes útiles en la decimonovena edición de "Remington: The Science and Practice of Pharmacy", Mack Printing Company, Easton, PA. Véanse especialmente los capítulos 91-93 para un análisis más completo.
Se puede administrar un compuesto por vía parenteral, por ejemplo, por vía intravenosa, por vía intramuscular, por vía intravenosa, por vía subcutánea o por vía intraperitoneal. El transportador o excipiente o mezcla de excipientes puede ser un disolvente o medio de dispersión que contiene, por ejemplo, diversos disolventes polares o no polares, mezclas adecuadas de los mismos, o aceites. Como se usa en el presente documento, "transportador" o "excipiente" significa un transportador o excipiente farmacéuticamente aceptable e incluye cualquiera y todos los disolventes, agentes o medios dispersantes, revestimiento(s), agentes antimicrobianos, agentes iso/hipo/hipertónicos, agentes de adsorciónmodificación, y similares. Se conoce bien en la técnica el uso de dichas sustancias y los agentes para sustancias farmacéuticamente activas. Excepto en la medida en que cualquier medio o agente convencional sea incompatible con el principio activo, se contempla su uso en composiciones terapéuticas. Por otra parte, otros principios o principios activos suplementarios también se pueden incorporar en la composición final.
Se pueden preparar soluciones del compuesto en diluyentes adecuados tales como agua, etanol, glicerol, polietilenglicol(es) líquido(s), diversos aceites, y/o mezclas de los mismos, y otros conocidos por los expertos en la materia.
Las formas farmacéuticas adecuadas para uso inyectable incluyen soluciones, dispersiones o emulsiones acuosas estériles y polvos estériles. La forma final debe ser estable en condiciones de fabricación y almacenamiento. Asimismo, la forma farmacéutica final debe protegerse contra la contaminación y debe, por tanto, ser capaz de inhibir el crecimiento de los microorganismos tales como bacterias u hongos. Se puede administrar una única dosis intravenosa o intraperitoneal. Como alternativa, se puede utilizar una infusión lenta a largo plazo o infusiones diarias múltiples a corto plazo, durando normalmente de 1 a 8 días. Se pueden dosificar en días alternos o dosificar una vez cada varios días.
Se prepararon soluciones inyectables estériles incorporando un compuesto en la cantidad requerida en uno o más disolventes adecuados al que el resto de ingredientes, relacionados anteriormente o conocidos por los expertos en la materia, pueden añadirse según se requiera. Se prepararon soluciones inyectables estériles incorporando los compuestos la cantidad necesaria en el disolvente adecuado con otros diversos ingredientes según se requiera. Siguen a continuación procedimientos de esterilización, tales como filtración. Normalmente, se realizan dispersiones incorporando el compuesto en un vehículo estéril que contiene también el medio de dispersión y el resto de ingredientes requeridos como se indica anteriormente. En el caso de un polvo estéril, los métodos preferidos incluyen secado al vacío o criodesecación al que se añaden cualquiera de los ingredientes requeridos.
En una realización, las composiciones proporcionadas en este punto son para inyección, tales como soluciones para inyección. En una realización, los compuestos proporcionados en el presente documento pueden administrarse mediante una solución inyectable. En una realización, la solución inyectable comprende al menos un excipiente farmacéuticamente aceptable. En una realización, el excipiente farmacéuticamente aceptable es uno o más de D-manitol, ácido L-láctico, un agente de ajuste del pH y agua estéril. Un ejemplo no limitante de un agente de ajuste del pH es hidróxido de sodio. En una realización, el compuesto 801 HCl se administra como una solución inyectable (véase la Tabla A siguiente).
T l A
En todos los casos, la forma final, según se indica, debe ser estéril y debe poder pasar fácilmente a través de un dispositivo de inyección tal como una aguja hueca. Se puede conseguir la viscosidad adecuada y mantenerse para la selección adecuada de disolventes o excipientes. Por otra parte, se puede utilizar el uso de revestimientos moleculares o de partículas tales como lecitinas, la selección adecuada de tamaños de partículas en dispersiones, o el uso de materiales con propiedades tensioactivas.
Se puede conseguir la prevención o inhibición del crecimiento de microorganismos mediante la adición de uno o más agentes antimicrobianos tales como clorobutanol, ácido ascórbico, parabenos, termerosal, o similares. Puede ser también preferible incluir agentes que alteran la tonicidad tal como azúcares o sales.
Aunque los compuestos de esta divulgación tienden a ser solubles en agua, en algunos casos, por ejemplo, cuando un compuesto de la invención es menos soluble en agua, puede ser útil proporcionar la administración liposómica. el sistema restringe que se incorpore el compuesto de la invención, encapsulando, rodeando, o atrapando el compuesto de la invención en, sobre, o por vesículas lipídicas o liposomas, o por micelas.
Se han usado liposomas satisfactoriamente para administrar medicamentos a pacientes con cáncer, y se ha mostrado que son clínicamente útiles en la administración de fármacos anticancerosos tales como complejos de doxorrubicina, daunorrubicina, y cisplatino. Forssen, et al., Cancer Res. 1992, 52: 3255-3261; Perex-Soler, et al., Cancer Res. 1990,
50: 4260-4266; y, Khokhar, et al., J. Med. Chem. 1991, 34: 325-329.
De manera similar, se han usado también micelas para administrar medicaciones a pacientes, (Broden et al., Acta Pharm Suec. 19: 267-284 (1982)) y se han usados micelas como transportadores de fármacos y para dirigir la administración de fármacos, (D.D. Lasic, Nature 335:279-280 (1992); y, Supersaxo et al., Pharm Res. 8: 1280-1291 (1991)), incluyendo medicaciones contra el cáncer, (Fung et al., Biomater. Artif. Cells. Artif. Organs 16: 439 et seq. (1988); y Yokoyama et al., Cancer Res. 51: 3229-3236 (1991)).
Los liposomas y/o micelas que contienen el compuesto de la invención pueden administrarse a un paciente con cáncer, normalmente por vía intravenosa. La directriz adicional para preparar composiciones liposómicas útiles en la presente invención se puede encontrar en la patente de Estados Unidos n.° 6.096.336).
Métodos de tratamiento
En otro aspecto, se proporciona en el presente documento un método para tratar el cáncer en un sujeto que lo necesita que comprende administrar al sujeto una cantidad terapéuticamente eficaz de un compuesto proporcionado en el presente documento.
En una realización, la cantidad terapéuticamente eficaz del compuesto administrado es aproximadamente 15 mg/m2 a aproximadamente 1500 mg/m2. En otra realización, la cantidad terapéuticamente eficaz de un compuesto del compuesto administrado es aproximadamente 50 mg/m2 a aproximadamente 1000 mg/m2. En otra realización, la cantidad terapéuticamente eficaz del compuesto administrado es aproximadamente 100 mg/m2 a aproximadamente 750 mg/m2. En otra realización, la cantidad terapéuticamente eficaz del compuesto administrado es aproximadamente 250 mg/m2 a aproximadamente 500 mg/m2.
En una realización, el cáncer es cáncer de colon, cáncer de pulmón no microcítico, leucemia mieloide crónica, leucemia mieloide aguda, cáncer de pulmón microcítico, cáncer de cuello uterino, cáncer de estómago, cáncer de mama, cáncer de próstata, cáncer de piel, melanoma, linfoma, tumor cerebral, sarcoma, cáncer de testículo, cáncer de ovario, cáncer renal, cáncer de cabeza y cuello, cáncer de hígado, leucemia, leucemia linfoblásica aguda, leucemia linfoblástica crónica, tricoleucemia, leucemia prolinfocítica de linfocitos T, leucemia linfocítica granular de células grandes, leucemia de linfocitos T adultos, y un cáncer de la sangre.
En una realización, el cáncer comprende un tumor sólido.
En otro aspecto, se proporciona en el presente documento un método para retrasar o reducir el crecimiento tumoral en un sujeto que lo necesita, que comprende administrar al sujeto una cantidad terapéuticamente eficaz de un compuesto proporcionado en el presente documento.
En una realización, el crecimiento del tumor es un tumor sólido.
En una realización, el cáncer es cáncer de colon, cáncer de pulmón no microcítico, leucemia mieloide crónica, leucemia mieloide aguda, cáncer de pulmón microcítico, cáncer de cuello uterino, cáncer de estómago, cáncer de mama, cáncer de próstata, cáncer de piel, melanoma, linfoma, tumor cerebral, sarcoma, cáncer de testículo, cáncer de ovario, cáncer renal, cáncer de cabeza y cuello, cáncer de hígado, leucemia, leucemia linfoblásica aguda, leucemia linfoblástica crónica, tricoleucemia, leucemia prolinfocítica de linfocitos T, leucemia linfocítica granular de células grandes, leucemia de linfocitos T adultos, y un cáncer de la sangre.
En otro aspecto, se proporciona en el presente documento un método para tratar el cáncer en un sujeto que lo necesita, que comprende administrar al sujeto una cantidad terapéuticamente eficaz de una composición farmacéutica proporcionada en el presente documento.
En una realización, el cáncer es cáncer de colon, cáncer de pulmón no microcítico, leucemia mieloide crónica, leucemia mieloide aguda, cáncer de pulmón microcítico, cáncer de cuello uterino, cáncer de estómago, cáncer de mama, cáncer de próstata, cáncer de piel, melanoma, linfoma, tumor cerebral, sarcoma, cáncer de testículo, cáncer de ovario, cáncer renal, cáncer de cabeza y cuello, cáncer de hígado, leucemia, leucemia linfoblásica aguda, leucemia linfoblástica crónica, tricoleucemia, leucemia prolinfocítica de linfocitos T, leucemia linfocítica granular de células grandes, leucemia de linfocitos T adultos, y un cáncer de la sangre.
En una realización, el cáncer comprende un tumor sólido.
Un compuesto útil en esta divulgación se administra a un sujeto adecuado que necesita estos compuestos en una dosis terapéuticamente eficaz mediante una ruta de administración médicamente aceptable tal como por vía oral, por vía parenteral (por ejemplo, por vía intramuscular, por vía intravenosa, por vía subcutánea, por vía interperitoneal), por vía transdérmica, por vía rectal, mediante inhalación y similares.
El término cáncer debe considerarse en la definición general más amplia como una neoplasia maligna, una masa
anómala de tejido, cuyo crecimiento excede y está descoordinado con el de los tejidos normales y persiste de la misma manera excesiva tras el cese de los estímulos que evocan el cambio. Se podría agregar que la masa anómala no tiene propósito, se alimenta del hospedador y es virtualmente autónoma. Se puede considerar también un cáncer como un tumor maligno. Una descripción adicional de la neoplasia se encuentra en "Robbins Pathologic Basis of Disease", Sexta Edición, por R.S. Cotran, V. Kumar, y T. Collins, Capítulo 8 (W.B. Saunders Company). La siguiente Tabla B proporciona ejemplos de los tipos de cánceres, es decir, tumores o neoplasias malignas que se pueden tratar administrando un compuesto de la presente divulgación.
Tabla B
Tejido de origen maligno
Compuesto por un tipo de célula parenquimal
Tumores mesenquimales
Tejido conectivo y derivados Fibrosarcoma
Liposarcoma
Condrosarcoma
Sarcoma osteogénico
Tejidos endoteliales y relacionados
Vasos sanguíneos Angiosarcoma
Vasos linfáticos Linfangiosarcoma
Sinovio Sarcoma sinovial
Mesotelio Mesotelioma
Cubiertas del cerebro Meningioma invasivo
Células de la sangre y células relacionadas
Células hematopoyéticas Leucemias
Tejido linfoide Linfomas malignos
Músculo
liso Leiomiosarcoma
Tejido Estriado Rabdomiosarcoma
Tumores epiteliales
escamoso estratificado carcinoma de células escamosas o epidermoide Células basales de la piel o anejas Carcinoma de células basales Revestimiento epitelial
Glándulas o conductos Adenocarcinoma
Carcinoma papilar
cistadenocarcinoma
Vías respiratorias Carcinoma broncogénico
Adenomas bronquiales (carcinoides) Neuroectodermo Melanoma maligno
Epitelio renal Carcinoma de células renales
Células hepáticas Carcinoma hepatocelular
Epitelio del tracto urinario (transicional) Carcinoma de células transicionales
Epitelio placentario (trofoblasto) Coriocarcinoma
Epitelio testicular (células germinales) Seminoma
Carcinoma embrionario
Tejido de origen Maligno
Tejidos mixtos-más de una célula neoplásicas, usualmente
derivados de una capa germinal
Glándulas salivales Tumor mixto maligno de origen en las glándulas salivales
Mama Cistosarcoma phyllodes maligno
Primordio renal tumor de Wilms
Más de un tipo de célula neoplásica derivado de más de una
capa germinal-Teratógeno
Células totipotenciales en gónadas o en restos embriónicos Teratoma inmaduro,
teratocarcinoma
Los compuestos de la divulgación son por tanto útiles en el tratamiento de leucemias y tumores sólidos, tales como tumores de colon, colorrectales, de ovario, mamario, próstata, pulmón, riñón y también tumores de melanoma. El intervalo de dosificación adoptado dependerá de la ruta de administración y de la edad, peso y la dolencia del paciente a tratar. los compuestos pueden administrarse, por ejemplo, Por la ruta parenteral, por ejemplo, por vía intramuscular, intravenosa o por infusión en bolo.
Como se utiliza en el presente documento, una "cantidad terapéuticamente eficaz" de derivados de podofilotoxina de la presente invención se pretende que signifique que signifique que la cantidad del compuesto que inhibirá el crecimiento, o el retardo del cáncer, o las células malignas del kit, y produce la regresión y paliación de los tumores
malignos, es decir, reducir el volumen o el tamaño de dichos tumores o eliminar la totalidad del tumor.
Con mamíferos, incluyendo seres humanos, las cantidades eficaces se pueden administrar sobre la base del área superficial corporal. La interrelación de dosificaciones varía para animales de diversos tamaños y especies, y para seres humanos (basado en mg/m2 de superficie corporal) se describe en E. J. Freireichet al., Cancer Chemother. Rep., 50(4) 219 (1966). Se puede determinar aproximadamente el área de la superficie corporal a partir de la altura y el peso un individuo (véase, por ejemplo, Scientific Tables, Geigy Pharmaceuticals, Ardsley, N.Y. págs 537-538 (1970)). Un intervalo de dosis adecuado es de 1 a 1000 mg de equivalente por m2 de área superficial corporal de un compuesto de la invención, por ejemplo, de 50 a 500 mg/m2.
Para todas las rutas de administración, la temporalización exacta de la administración de las dosificaciones puede variarse para conseguir resultados óptimos. Generalmente, si se usa Intralipid 20 como el transportador para el derivado, la dosificación real del derivado que llega hasta el paciente será menor. Esto se debe a alguna pérdida del derivado en las paredes de las jeringuillas, agujas y recipientes de preparación, que es prevalente con la suspensión Intralipid 20. Cuando se usa un transportador, tal como un aceite de semillas de algodón, está pérdida anteriormente descrita no es tan prevalente porque el derivado no se adhiere lo mismo a la superficie de las jeringuillas, etc.
Otra característica importante del método proporcionado por la presente divulgación se refiere a la toxicidad general aparente relativamente baja de los derivados administrados de acuerdo con las enseñanzas en el presente documento. Se puede juzgar la toxicidad general usando diversos criterios. Por ejemplo, la pérdida de peso corporal en un sujeto de aproximadamente el 10% del peso corporal inicialmente registrado (es decir, antes del tratamiento) se puede considerar como un signo de toxicidad. Además, la pérdida de movilidad y actividad generales y signos de diarrea o cistitis en un sujeto se puede interpretar también como una evidencia de la toxicidad.
Ejemplos
Ejemplo 1: Síntesis de N2
Esquema 1.
ácido 4-carboxifenoxi acético (2). A una suspensión de ácido 4-hidroxibenzoico (50 g, 361,4 mmol) y K2CO3 (200 g, 1,45 mol) en acetona (720 ml) se añadió bromoacetato de etilo (140 ml, 1,27 mol). Después de agitar a temperatura ambiente durante 24 h, la mezcla se filtró y concentró (60 torr, 40 °C temperatura del baño). El aceite espeso restante se disolvió en MeOH (720 ml) y se añadió una solución de NaOH al 30% p/v en agua (108 g de NaOH en 360 ml de H2O). La mezcla se mantuvo a reflujo a 95 °C durante 17 h. La mezcla se enfrió a 0 °C y se añadió lentamente HCl concentrado (350 ml) agitando a la vez. Una vez que se completó la adición, se filtró la mezcla y se lavó el precipitado con agua (1x100 ml) y acetona (2x100 ml) seguido por secado a vacío elevado a 40 °C durante 4 días para dar como resultado 42,5 g de producto como un sólido de color blanco (60 %). ESIMS: calculado para C9H8O5 [M+H]+ 197,04, encontrado197,1.
Esquema 2.
piperidinopiperidinacarbamilo de acuerdo con las condiciones señaladas en la bibliografía (patente de Estados Unidos n.° 6.121.451. En resumen, A una solución de 4-piperidino-piperidina (35 g, 208 mmol) en DCM (2,6 l) a 0 °C se añadió una solución de trifosgeno (22,1 g, 83,2 mmol) en DCM (300 ml) lentamente. La mezcla se agitó de 0 °C a ta durante 17 h. Se añadió Celite y se filtró la solución. El filtrado se lavó con una solución de NaHCO3 al 7 % p/v y se secó con MgSO4 (100 g). La mezcla se filtró y se evaporó el disolvente. El residuo restante se disolvió en DCM anhidro (208 ml) para preparar una solución 1 M. La solución se usó como tal sin purificación adicional.
La 10-hidroxicamptotecina (25 g, 68.5 mmol) se disolvió en DCM/piridina 1:1 (1,37 l) y se añadió la solución de cloruro de 4-piperidinopiperidinacarbamilo preparada recientemente (208 ml). Tras agitar a ta durante 4 h, la mezcla de reacción se concentró y purificó mediante cromatografía en gel de sílice (600 g) con MeOH/DCM al 10 % (7l) para dar 38 g de producto como un sólido de color amarillo (100%). ESIMS: calculado para C31H34N4O6 [M+H]+ 559,25, encontrado 559,0.
Esquema 3
Ácido camptotecina-10-O-[4-piperidinopiperidina]carbamil]-20-O-[4-carboxifenoxi]acético. (5). Carbamato de camptotecina-10-0-[4-piperidinopiperidina] (4, 38 g, 68,5 mmol), EDC (61,4 g, 319,6 mmol), DMAP (4,85 g, 79,9 mmol) y ácido 4-carboxifenoxi acético (2, 39,2 g, 199,7 mmol) se disolvieron en 1:1 DCM/DMF (2,66 l). Tras agitar a ta durante 22 h, Se concentró la mezcla y el residuo restante se disolvió en DCM (3 l) y se lavó con una solución saturada de NaHCO3 (2 x 200 ml) seguido por agua (2 x 200 ml). La fase acuosa se combinó y se extrajo con DCM (2 x 200 ml). La capa orgánica y los extractos orgánicos se combinaron, se secaron con MgSO4 (100 g), se filtraron y se evaporó el disolvente. El residuo restante se purifico mediante cromatografía en gel de sílice (1 kg) con MeOH/DCM 10 % AcOH al 1 % (2 l), MeOH/DCM al 20 % AcOH al 2 %(5 l), y MeOH/DCM al 30 %+ AcOH al 3 %(4 l). Las fracciones que contenían el producto se combinaron y se evaporó el disolvente. El producto bruto se disolvió en MeOH/DCM al 10 % (100 ml) y la solución se añadió a MeOH (500 ml). La mezcla se agitó a ta durante 30 min y el precipitado resultante se recogió mediante filtración para dar 22,4 g de producto como un sólido de color amarillo claro (45 %). ESIMS: calculado para C40H40N4O10 [M+h ]+ 737,27, encontrado 737,0. Nota: esta etapa puede mejorarse adicionalmente y los inventores deben ser capaces de proporcionar un rendimiento de ~70 %.
Esquema 4.
N2. EDC (17,53 g, 91,3 mmol), DMAP (3,71 g, 30,4 mmol), 5 (22,4 g, 30,4 mmol) y podofilotoxina (25,2 g, 60,9 mmol) se disolvieron en 1:1 de DCM/DMF (1,52 l) y la mezcla se agitó a ta durante 24 h. La mezcla de reacción se diluyó con DCM (2 l), se lavó con una solución saturada de NaHCO3 (2 x 500 ml), agua (1x 500 ml), se secó con MgSO4 (100 g), se filtró y se evaporó el disolvente. El residuo restante se purificó mediante cromatografía en columna de gel de sílice (900 g) con MeOH/DCM al 5 % (2 l) y MeOH/DCM al 7,5 % (6 l). Se recogieron las fracciones que contenían el producto y se evaporó el disolvente. Se acidificó el producto puro disolviendo MeOH/DCM al 10 % (50 ml) seguido por la adición de HCl 4 m en dioxano (25 ml). Se añadió lentamente la mezcla al Et2O agitado (750 ml). El precipitado se filtró y se secó a vacío elevado durante la noche. Se recuperaron 17.5 g de sal de clorhidrato de N2 como un sólido de color amarillo (50 %). ESIMS: calculado para C62H60N4O17 [M+H]+ 1133,40, encontrado 1133,0.
Los espectros de RMN 1H y RMN 13C de N2 se muestran en las Figs. 1A y 2 respectivamente. El espectro de CL-EM de N2 se muestra en la Fig. 3A.
Ejemplo 2: Síntesis de la formulación de N2-HCI
Esquema 5.
Se preparó la formulación de N2 HCl mediante el proceso que se muestra en el Esquema 5. A una solución filtrada de base exenta de N2 (1 equiv) en diclorometano (Ac S) a 10 ± 5 °C se añadió HCl en éter (ACS, 1 M, 1,3 equiv). El disolvente se eliminó al vacío. Se añadió al residuo una solución de MPEG-2000-DSPE (cGMP, 2 equiv) en diclorometano. Se agitó la mezcla para obtener una solución transparente y a continuación se eliminó el disolvente al vacío. El residuo se disolvió en diclorometano, se concentró hasta sequedad, se secó al vacío a temperatura ambiente hasta que se determinó que el diclorometano NMT era de 600 ppm mediante GC, se micronizó con un mezclador y se cribó con un tamiz de 0,35 mm para dar como resultado la Formulación N2HCl, lote n.° 011000, 2,45 kg.
Ejemplo 3: Preparación de N2HCI para inyección
Se preparó una solución de ácido L-láctico (0,01 M, pH 3,5) combinando agua estéril para inyección (SWI, 18 ±0.5 kg) y ácido L-láctico (18,02 g), añadiendo hidróxido de sodio 0,5 N hasta que el pH de la solución es 3,5 ±0,1 y añadiendo suficiente SWI para llevar la cantidad total de la solución hasta 20,00 kg. Se ajustó el pH a 3,5± 0,1 mediante la adición de hidróxido de sodio 0,5 N.
Una mezcla de Formulación de N2HCl (697,7 g) y 0,01 M de solución de ácido L-láctico, pH 3,5 (17 ± 0,2 kg) se agitó hasta que se obtuvo la solución. Se añadió d-Manitol (168,0 g) con mezcla. El pH de la solución resultante se ajustó a 3.5 ± 0,1 mediante la adición de hidróxido de sodio 0,5 N. Se añadió suficiente solución de ácido L-láctico 0,01 M, pH 3.5 para llevar la cantidad total de la solución hasta 20.00 kg. Se ajustó el pH a 3,5± 0,1 mediante la adición de hidróxido de sodio 0,5 N. Se filtró la solución a través de un filtro estéril de 0,22 micrómetros de carboy estéril y a continuación se introdujo en viales de 10 ml estériles con 5,00 ± 0,10 g por vial. Se llevó a cabo la liofilización en condiciones estériles finalizando a 25 °C y 100 mTorr. El vacío se rompió con nitrógeno NF y se aplicaron cierres
estériles a los viales, que se almacenaron a que se almacenaron a 2-8 °C.
Ejemplo 4: Síntesis del compuesto diana 1
Esquema 6.
El compuesto diana 1 (denominado también en el presente documento como N1) se puede sintetizar siguiendo los procedimientos descritos anteriormente para el N2 con algunas modificaciones necesarias que serán evidentes al experto en la técnica (véase el Esquema 6). En las Figs 1B y 3B respectivamente, se muestran el espectro RMN 1H y el espectro CL-EM del Compuesto diana 1.
Ejemplo 5: Síntesis del compuesto diana 3
Esquema 7.
El Compuesto diana 3 (denominado también en el presente documento como N3) se puede sintetizar siguiendo los procedimientos descritos anteriormente para el N2 con algunas modificaciones necesarias que serán evidentes al técnico experto (véase el Esquema 7). En las Figs. 1C-1E y 3C respectivamente se muestran el espectro de RMN 1H y el espectro de CL-EM del Compuesto diana 3.
Ejemplo 6: Síntesis del compuesto diana 4
Esquema 8.
El compuesto diana 4 (denominado también en el presente documento como N4) se puede sintetizar siguiendo los procedimientos descritos anteriormente para el N2 con algunas modificaciones necesarias que serán evidentes al experto en la técnica (véase el Esquema 8). En las Figs. 1F y 3D respectivamente se muestran el espectro de RMN 1H y el espectro de CL-EM del Compuesto diana 4.
1.1. Antecedentes de los ensayos biológicos
Los estudios se realizaron usando N2 y los Compuestos diana 1, 3 y 4. Los estudios de eficacia in vitro demostraron que estos compuestos eran muy eficaces en destruir las células de cáncer de colon y de pulmón humanas, y las células de colon especialmente resistentes (que expresan en exceso el gen 1[MDR1] de resistencia a multifármacos). Para evaluar adicionalmente su eficacia preclínica, se han llevado a cabo estudios de eficacia in vivo sobre dos modelos de cáncer de colon y uno para el modelo de leucemia mieloide crónica (LMC). La toxicidad de cuatro compuestos principales fue notablemente baja en ratones. Entre ellos, N2 (denominado también en el presente documento 801) es un compuesto prometedor con toxicidad más baja y eficacia mayor contra xenoinjertos de cáncer humano. Los resultados mostraron que 801-HCI y la formulación de 801 son ambos eficaces en los modelos de xenoinjerto de cáncer de colon y LMC humanos.
1.2 Estudios de eficacia in vitro de análogos de podofilotoxina
1.2.1. Ensayo de formación de colonias
Se sembraron células cancerosas en placas Petri de 60 mm que contenían 2,7 ml de medio (medio 5a modificado de McCoy que contenía suero de feto bovino al 10 % y 100 unidades/ml de penicilina y 100 ug/ml de estreptomicina). Se incubaron las células en una estufa incubadora de CO2 a 37 grados centígrados durante 5 horas para la unión a la parte inferior de las placas de Petri. Los fármacos se prepararon nuevos en medio a diez veces la concentración final y a continuación se añadieron 0,3 ml de esta solución de depósito a los 2,7 ml de medio en la placa. A continuación,
se incubaron las células con fármacos durante 72 horas a 37 grados C. Al final de la incubación, se decantó el medio que contenía el fármaco, se enjuagaron las placas con 4 ml de solución salina equilibrada de Hank (HBSS), se añadieron 5 ml de medio nuevo y las placas se devolvieron a la estufa incubadora para la formación de colonias. Se contaron las colonias de células usando un contador de colonias tras incubación durante 7 días (línea de células HCT116), 14 días (línea de células VM46) y 15 días (línea de células H23). Se calculó la supervivencia celular (%) a partir de 3 placas repetidas para cada concentración de fármaco y se determinaron los valores medios de la CI50 (la concentración de fármaco que produce un 50 % de inhibición de la formación de colonias) para cada compuesto ensayado.
1.2.2. Efectos quimioterapéuticos sobre las células HCT116 de Cáncer de colon humano
Se tabularon a continuación los efectos quimioterapéuticos de los compuestos de podofilotoxina (N1-4) en células HCT116 de cáncer de colon humano.
1.2.3. Efectos quimioterapéuticos sobre las células VM46 de Cáncer de colon humano
Se tabularon a continuación los efectos quimioterapéuticos de los compuestos de podofilotoxina (N1-4) sobre células VM46 de cáncer de colon humano que expresan en exceso el Gen 1 de resistencia a multifármacos.
1.2.4. Efectos quimioterapéuticos sobre células H23 de Cáncer de pulmón no microcítico humano
Se tabularon a continuación los efectos quimioterapéuticos de los compuestos de podofilotoxina (N1-4) sobre células H23 de cáncer de pulmón de células no microcíticas humanas.
En resumen, N1, N2 (801), N3, N4 mostraron todas eficacia contra las tres líneas de células seleccionadas a concentraciones de nivel nM. N1 y N4 mostraron buena eficacia a una concentración muy baja. Entre las 3 líneas de células, las células VM46 de Cáncer de colon humano expresan en exceso el Gen 1 de resistencia a multifármacos (MDR1). Todos los compuestos superaron la resistencia al fármaco mediada por MDR1. N2 (801) demostró más eficacia contra el cáncer de pulmón de células no microcíticas que al cáncer de colon.
1.3. Estudios de toxicidad de los compuestos N1-4 en ratones normales
1.3.1. Método:
En los estudios de toxicidad, se dosificaron 2 ratones C3H normales con los compuestos N1-4 (N1, N2, N3, y N4) a dosis bajas y moderadas de 40 y 100 mg/kg. Como no se produjo toxicidad grave e irreversible a estas dosis, se inició una nueva pareja de animales a 120 mg/kg que era 1,2 veces mayor que 100 mg/kg. Las dosificaciones secuenciales (es decir, 2 ratones por cada dosis de fármaco) se aumentaron en un factor de 1,2-1,5 hasta que se observó una toxicidad irreversible (el animal se volvió demacrado; el animal experimentó una rápida pérdida de peso (caquexia) (20 %) que se produjo en varios (2-4) días (se requirió la eutanasia). A continuación, se inició otra pareja de animales en la dosificación no tóxica más elevada, y se aumentaron sucesivas dosificaciones en un factor de 1,15. Los resultados de este ejercicio fueron dos dosificaciones, una que era aparentemente no tóxica y la otra que demostró una toxicidad irreversible que requirió eutanasia, separada por un factor de 1,15. se dosificaron seis ratones para cada dosificación. Si no se produjo toxicidad irreversible en la dosificación inferior y al menos una con una toxicidad irreversible en la dosis superior, entonces, se consideró que la dosis inferior era la MYD. Se formularon sales de HCl de N1-4 en una solución de etanol:Cremophor EL: solución salina de NaAC 0,2 M (5:5:10:80) con un pH final de 5,0 5,5. Se formularon bases de N1-4 en una solución de etanol: Cremophor EL:solución salina (5:5:90). Se administraron
todos los compuestos a ratones C3H normales hembra mediante una única inyección i.p. en un volumen de 0,5 ml/20 g de ratón. Se evaluó la toxicidad del fármaco en ratones revisados diariamente durante 40 días. Los parámetros de toxicidad notificados fueron la MTD40. La MTD se definió como la dosis más alta que no producía toxicidad irreversible en un grupo de tratamiento, pero al menos un animal presentó toxicidad irreversible y se sometió a eutanasia en la siguiente dosis mayor. Al final del experimento, todos los ratones se sometieron a eutanasia.
1.3.2. Resultados:
Se ha completado la evaluación de los efectos tóxicos de N1, N2, N3 y N4 en ratones CH3 normales hembra. Como se muestra en la Tabla 1.3.1, los valores de MTD de todos los compuestos fueron significativamente mayores que muchos fármacos anticancerosos clínicamente disponibles. cuanto mayor es MTD, más baja es su toxicidad en ratones normales. Entre los cuatro compuestos, N2 fue el menos tóxico en ratones normales. Se señala que la MTD de su forma de base era igual que la de su forma de sal de HCl. El siguiente menos tóxico fue Neovia4. Su forma de base era menos tóxica en ratones que su forma de sal de HCl, sugiriendo que la menor solubilidad de su forma de base puede contribuir a esta diferencia.
Tabla 1.3.1. Los valores de MTD de los com uestos N1-4 en ratones^C3H.
1.4. Estudio preliminar de eficacia in vivo de cuatro análogos de podofilotoxina para la selección del fármaco candidato más prometedor
Para evaluar la eficacia in vivo de cuatro compuestos N1-4 sobre el cáncer de colon humano HCT116, se llevó a cabo el estudio de eficacia anticancerosa in vivo en ratones alotímicos (genotipo nu/nu) que soportaban xenoinjertos HCT116 de cáncer de colon humano.
1.4.1. Método
Se llevó a cabo el estudio de eficacia anticancerosa in vivo en ratones alotímicos (genotipo nu/nu) que soportaban xenoinjertos HCT116 de cáncer de colon humano. Estos tumores humanos crecieron exponencialmente tras el implante en los flancos de los ratones y alcanzaron un volumen tumoral promedio de 79,85 mm. cu. Se inició el tratamiento en este momento, designando el primer día de tratamiento como día 0 para todos los cálculos y gráficos. Se inyectaron los 6 ratones por vía i.p. con cada una de las cuatro soluciones del fármaco Neovia (alcohol al 5%, Cremophor EL al 5 % y solución salina al 90 %, 0,5 ml/20 g, inyección única). Las dosis del fármaco (i.p. dosis de MTD) fueron 120 mg/kg para Neovia-1, 300 mg/kg para Neovia-2, 120 mg/kg para Neovia-3, y 180 mg/kg para Neovia-4. El grupo de ratones del control se trató solo con vehículo. Después del tratamiento, Se midieron los tamaños de los tumores mediante calibre en días alternos. Se utilizó la medición de los diámetros del tumor (d1, d2) en dos direcciones ortogonales para calcular el volumen tumoral (volumen tumoral = n/6 {(d1+d2)/2}3) utilizando la aproximación de que los tumores son esféricos. Cada curva de crecimiento tumoral de cada ratón se representó gráficamente. Se calculó el tiempo (días) requerido para hacer crecer el tumor hasta el tamaño de 800 cu. mm tras diversos tratamientos como los índices de retraso del crecimiento tumoral para evaluar los efectos del tratamiento. Se observaron también los tiempos de supervivencia tras el tratamiento y se registraron.
1.4.2. Resultados
los cuatro compuestos N1-4 después de una única inyección i.p. demostraron ser muy eficaces en la inhibición del crecimiento de xenoinjertos HCT116 de cáncer de colon humano. Los resultados mostraron que N2 (801) sería el fármaco candidato más prometedor contra el cáncer de colon humano HCT116 entre los 4 compuestos.
1.5. Estudio de eficacia in vivo: 801 en el tratamiento del Modelo de xenoinjerto COLO205 de cáncer de colon humano.
1.5.1. Objetivo
Evaluar en preclínica la eficacia y la seguridad terapéutica in vivo del compuesto 801 en el tratamiento del modelo de xenoinjerto subcutáneo COLO205 de cáncer de colon humano y en comparación con el fármaco irinotecán de SOC.
1.5.2. Animales
1.5.3. Método
Cada ratón se inoculó por vía subcutánea con 5 x 106 COLO205 de células tumorales en 0,1 ml de PBS para el desarrollo del tumor. Se iniciaron los tratamientos cuando el volumen del tumor alcanzó 120 mm3. El criterio de valoración principal era observar si podría retrasarse o reducirse el crecimiento tumoral. El peso corporal y el volumen tumoral se midieron dos veces por semana. A continuación, se usó el volumen tumoral para los cálculos de ambos TC y los valores de inhibición del crecimiento tumoral (TGI).
1.5.4. Grupo y Tratamientos
1.5.5. Estadística
Las diferencias entre los valores medios del volumen natural para comparar grupos se analizaron para determinar la significancia usando el ensayo ANOVA unilateral. P <0,05 se consideró como estadísticamente significativo.
1.5.6. Resultados
Los resultados de mPEG-2000-DSPE i.v. que muestran la formulación de 801 a niveles de dosis de 125 mg/kg (q5d x 3) y 100 mg/kg (q3d x 3) produjeron una actividad antitumoral moderada con valores de TGI del 37% y 42%, respectivamente (p = 0,008 y p = 0,002 frente al control).
Los resultados muestran que 801-HCl i.p., a 125 mg/kg e irinotecán a 70 mg/kg produjeron una fuerte actividad antitumoral con valores de TGI del 70 % y 97 % en el día 29 (ambas p < 0,001 frente al control).
La Fig. 4A muestra la actividad antitumoral del N2-HCl formulado (i.v.) en el tratamiento del modelo de xenoinjerto COLO205 de cáncer de colon humano y la Fig. 4B muestra la actividad antitumoral del N2-HCl formulado (i.p.) en el tratamiento del modelo de xenoinjerto COLO205 de cáncer de colon humano.
Con respecto al perfil de seguridad, los ratones toleraron los tratamientos bien; no se observaron pérdidas de peso corporal graves u otras anomalías clínicas importantes durante el periodo de tratamiento.
1.5.7. Conclusión
801-HCI a 125 mg/kg (administración i.p.) demostró una fuerte actividad antitumoral con un buen perfil de seguridad. mPEG-2000-DSPE formulado 801(administración i.v.) produjo una eficacia moderada, que podría estar causada bien por las inyecciones divididas para cada dosificación i.v. debido a una limitación en el volumen de dosificación permitido para inyecciones i.v. en ratones.
1.6. Estudio de eficacia in vivo: 801 en el tratamiento del Modelo de xenoinjerto HCT116 de cáncer de colon humano
1.6.1. Objetivo
Evaluar en preclínica la eficacia y la seguridad terapéutica in vivo del compuesto 801 en el tratamiento del modelo de xenoinjerto subcutáneo HCT116 de cáncer de colon humano en ratones alotímicos.
1.6.2. Animales
1.6.3. Método
Cada ratón se inoculó por vía subcutánea con 5 x 106 HCT116 de células tumorales en 0,1 ml de PBS para el desarrollo del tumor. Se iniciaron los tratamientos cuando el volumen del tumor alcanzó 100 mm3 El criterio de valoración principal era observar si podría retrasarse o reducirse el crecimiento tumoral. El peso corporal y el volumen tumoral se midieron dos veces por semana. A continuación, se usó el volumen tumoral para los cálculos de ambos TC y los valores de inhibición del crecimiento tumoral (TGI).
1.6.4. Grupo y Tratamientos
1.6.5. Estadística
Las diferencias entre los valores medios del volumen natural para comparar grupos se analizaron para determinar la significancia usando el ensayo ANOVA unilateral. P <0,05 se consideró como estadísticamente significativo.
1.6.6. Resultados
Los resultados de la Fig. 5A que muestran mPEG-2000-DSPE i.v. formulado 801 a niveles de dosis de 125 mg/kg (q5d x 3) y 100 mg/kg (q3d x 3) produjeron una actividad antitumoral moderada con valores de TGI del 52 % y del 49 %, respectivamente (p = 0,002 y p = 0,001 frente al control).
los resultados de la Fig. 5B muestran que 801-HCI i.p.a 125 mg/kg e irinotecán a 70 mg/kg produjeron una actividad antitumoral similar y fuerte con valores de TGI del 93 % y 92 % en el día 29 (ambos p < 0,001 frente al control).
La Fig. 5A muestra la actividad antitumoral del N2 formulado (i.v.) en el tratamiento del modelo de xenoinjerto de cáncer de colon humano HCT116. La Fig. 5B muestra la actividad antitumoral del N2-HCl (i.p.) en el tratamiento del modelo de xenoinjerto de cáncer de colon humano HCT116.
Con respecto al perfil de seguridad, se observó una pérdida de peso corporal menor (4-6 %) para los animales tratados con 801-HCI y formulados con 801, mientras que irinotecán dio como resultado un 8 % de pérdida de peso corporal. no se observaron otras anomalías clínicas importantes durante el periodo de tratamiento.
1.6.7. Conclusión
801-HCI a 125 mg/kg (i.p.) demostró una fuerte actividad antitumoral con un buen perfil de seguridad. mPEG-2000-DSPE formulado 801 (i.v.) produjo una eficacia moderada, que puede producirse bien mediante inyecciones divididas
para la dosificación iv diaria debido a una limitación en el volumen permitido para la inyección iv en ratones.
1.7. Estudio de eficacia in vivo: 801 en el tratamiento del Modelo de xenoinjerto subcutáneo K562 de leucemia mieloide crónica humana.
1.7.1. Objetivos
Evaluar en preclínica la eficacia y la seguridad terapéutica in vivo del compuesto 801 en el tratamiento del modelo de xenoinjerto subcutáneo de leucemia mieloide crónica humana.
1.7.2. Animales
1.7.3. Método
Se irradiaron los ratones (2Gy) usando una fuente irradiadora de Co60. Después de 24 horas, se inoculó cada animal por vía subcutánea en el flanco derecho con células K562 (1 x 107/animal) en 0,1 ml de PBS para el desarrollo del tumor. Se dejó sin alterar el desarrollo del tumor hasta que el volumen medio alcanzó aproximadamente 150 mm3. El criterio de valoración principal era observar si podría retrasarse o reducirse el crecimiento tumoral. Se midieron el peso corporal y el volumen tumoral. A continuación, se usó el volumen tumoral para los cálculos de ambos TC y los valores de inhibición del crecimiento tumoral (TGI).
1.7.4. Grupo y Tratamientos
Tabla 1.7.
1.7.5. Estadística
Se analizaron las diferencias entre los valores tumorales medios para comparar grupos para determinar la significancia estadística usando el ensayo ANOVA unilateral. P <0,05 se consideró como estadísticamente significativo.
1.7.6. Resultados
Los animales del control se sometieron a eutanasia en el Día 25 para determinar la carga tumoral grande.
El vehículo mPEG-2000-DSPE fue tolerado bien por los animales del control. Sin embargo, el mPEG-2000-DSPE formulado 801 en la dosificación de ensayo de 60 mg/kg (iv, dosificación TID) produjo una grave toxicidad en los animales y solo se administró una dosificación TID; Se observó una drástica pérdida de peso corporal del 14,5 % el día siguiente después de la dosificación del Día 8, con 2 de 8 animales muertos en los Días 9 y 10. El agente de prueba 801-HCI fue bien tolerado por los animales cuando se administró i.p. e una dosificación de 300 mg/kg, con solo un máximo del 7,7 % de pérdida de peso el día siguiente después de la 2a dosificación. El fármaco positivo imatinib fue bien tolerado por los animales y se observó una pérdida de peso menor del 6,2 al final del tratamiento.
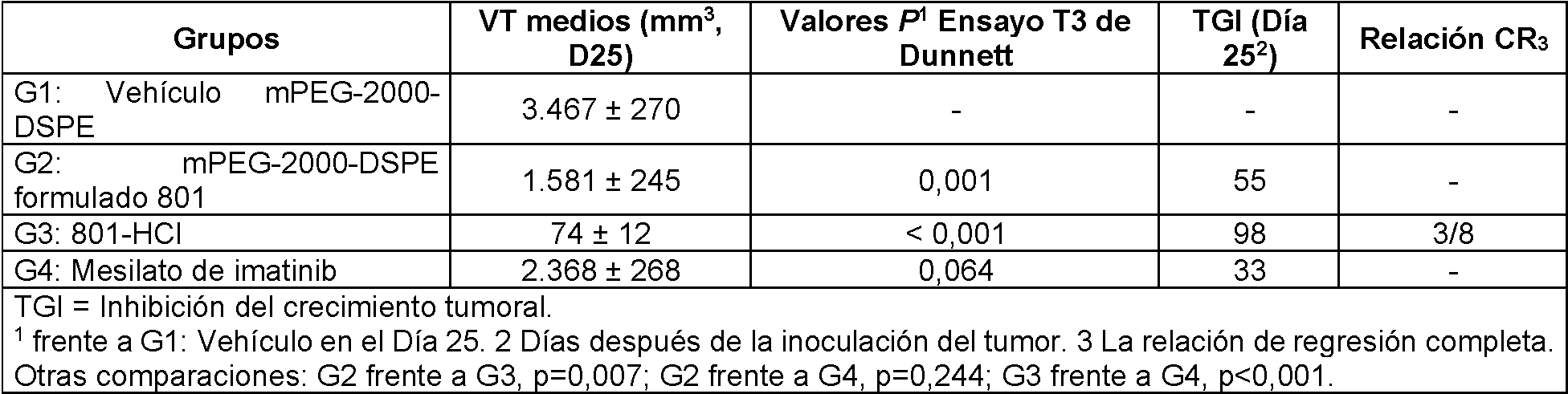
En la Tabla 1.7.1 se presentan los VT medios de diferentes grupos. En la Tabla 1.7.2 se muestran los valores TGI en el Día 25. En La Fig. 6 se presentan las curvas de crecimiento tumoral de los diferentes grupos de ratones tabulados en la Tabla 1.7.
Los VT medios de los animales del control alcanzaron 3.467 mm3 en el Día 25 tras la inoculación de células tumorales. El agente de prueba mPEG-2000-DSPE formulado 801 (60 mg/kg, iv, TID: total 180 mg/kg), que se administró solo
durante un día debido al problema de la tolerabilidad, produjo todavía una actividad antitumoral moderada con un valor de TGI del 55 % (p = 0,001 frente al control). El agente de prueba 801-HCl a 300 mg/kg (ip) presentó una actividad antitumoral drástica con un valor de TGI del 98 % (p < 0,001 frente al control). Para este grupo de tratamiento, 3 de 8 animales alcanzaron una remisión completa de los tumores en el Día 21 (7 días después de la última dosificación) sin recrecimiento tumoral adicional hasta el final del estudio. En comparación, imatinib a 75 mg/kg (por vía oral) presentó solo una actividad antitumoral menor con un valor de TGI del 33 %, que no es significativo a partil del control (p = 0,064 frente al control).
Tabla 1.7.1. Volúmenes tumorales medios.
Tabla 1.7.2. Actividad antitumoral de 801 en el tratamiento del modelo subcutáneo K562 de leucemia mieloide crónica humana.
1.7.7. Conclusión
801-HCI a 300 mg/kg (i.p.) presentó una fuerte actividad antitumoral con un buen perfil de seguridad. mPEG-2000-DSPE formulado 801 (60 mg/kg, iv, TID: total 180 mg/kg), administrado solo durante un día debido a la tolerabilidad en los ratones irradiados a 2Gy usando una fuente irradiadora de Co60, produjo todavía una actividad antitumoral moderada.
1.8. Estudio de eficacia in vivo: 801 en el tratamiento del Modelo de xenoinjerto subcutáneo K562 de leucemia mieloide crónica humana (2° estudio de K562).
1.8.1. Objetivos
El objetivo de este estudio era evaluar clínicamente la eficacia terapéutica in vivo y la tolerabilidad del artículo experimental, compuesto 801, en el tratamiento del xenoinjerto subcutáneo K562 de leucemia mieloide crónica humana en ratones NOD SCID, y en comparación con estos del fármaco imatinib de SOC.
1.8.2. Animales
1.8.3. Método
Se irradiaron los ratones (200 rad) usando una fuente irradiadora de Co60. Después de 24 horas, se inoculó cada animal por vía subcutánea en el flanco derecho con células K562 (1 x 107/animal) en 0,1 ml de PBS para el desarrollo del tumor. Se dejó sin alterar el desarrollo del tumor hasta que el volumen medio alcanzó aproximadamente 130 mm3. A continuación se aleatorizaron los animales en 6 grupos, Consistiendo cada grupo en 8 animales. Los artículos experimentales se administraron a los animales que soportaban el tumor de acuerdo con regímenes predeterminados como se muestra en la tabla de diseño experimental anterior.
1.8.4. Grupo y Tratamientos
Tabla 1.8
1.8.5. Estadística
Se analizaron las diferencias entre los valores tumorales medios para comparar grupos para determinar la significancia estadística usando el ensayo ANOVA unilateral. P <0,05 se consideró como estadísticamente significativo.
1.8.6. Resultados
a. 1.8.6.1 Volúmenes tumorales
En la Tabla 1.8.1 se muestran los tamaños de los tumores de los diferentes grupos.
___________________ Tabla 1.8.1. Tamaños de los tumores en los Grupos de tratamiento___________________
Volumen tumoral medio (mm3)1
Vehículo: Mesilato de
Días2 mPEG-2000- imatinib la formulación de la formulación de la formulación de la formulación de 801 150 mg/kg 801 100 mg/kg 801 50 mg/kg i.v. 801 25 mg/kg i.v. DSPE i.v. c3d 75 mg/kg p.o.
x 6 cd x 14 i.v. c3d x 2 i.v. c3d x 2 c3d x 8 c3d x 8
8 130 ± 9 129 ± 10 129 ± 10 128 ± 7 127 ± 9 129 ± 7
11 324 ± 29 206 ± 32 135 ± 14 138 ± 16 185 ± 16 192 ± 15
14 607 ± 71 423 ± 75 163 ± 15 221 ± 29 260 ± 29 354 ± 26
18 1.290 ±81 765 ± 121 338 ± 47 453 ± 58 474 ± 57 666 ± 48
21 1.643 ±95 1.094 ± 123 639 ± 81 826 ± 85 585 ± 59 936 ± 89 253 2.401 ± 167 1.504 ± 120 1.013 ± 105 1.222 ± 107 776 ± 69 1.305 ± 147 28 - 2.058 ± 168 1.514 ± 146 1.589 ± 109 1.007 ± 134 1.556 ± 180 32 - 2.676 ± 236 2.213 ±247 2.321 ± 193 1.435 ± 133 1.976 ±216 1Los valores se presentan como Media ± SEM
2 Días después de la inoculación del tumor.
3 El grupo del control se terminó en el Día 25 para determinar la carga tumoral grande.
b. 1.8.6.2 Inhibición del crecimiento tumoral
La inhibición del crecimiento tumoral se resumió en la Tabla 1.8.2. En la Fig. 7 se presentan las curvas de crecimiento tumoral de diferentes grupos de ratones tratados con la formulación de 801 e imatinib como se tabuló en la Tabla 1.8.
Tabla 1.8.2. Actividad antitumoral de la formulación de 801 e Imatinib en el tratamiento de modelo de ____________________ xenoinjerto K562 de leucemia mieloide crónica humana____________________ Tratamiento Tamaño del tumor (D25, mm3)1 TGI (%) valor P2 G1 Control con vehículo 2.401 ± 167 - -G2: Mesilato de imatinib 75 mg/kg 1.504 ± 120 37 < 0,001 G3: Formulación de 801 150 mg/kg 1.013 ± 105 62 < 0,001 G4: Formulación de 801 100 mg/kg 1.222 ± 107 51 < 0,001 G5: Formulación de 801 50 mg/kg 776 ± 69 70 < 0,001 G6: Formulación de 801 25 mg/kg 1.305 ± 147 45 < 0,001 1Los valores se presentan como Media ± SEM
2frente al control con vehículo;
valores P: G2 frente a G3 = 0,013; G2 frente a G4 = 0,144; G2 frente a G5< 0,001; G2 frente a G6 = 0,262; G3 frente a G4 = 0,305; G3 frente a G5 = 0,248; G3 frente a G6 = 0,130;
G4 frente a G5 = 0,033; G4 frente a G6 = 0,665; G5 frente a G6 = 0,008;
1.8.7 Conclusión
La formulación de 801 en la dosis de 50 mg/kg con la pauta de tratamiento q3d x 8 demostró una fuerte actividad antitumoral en el modelo de xenoinjerto K562 de leucemia mieloide crónica humana, pero bajo la toxicidad. La dosis de 50 mg/kg era significativamente más eficaz contra xenoinjertos K562 LMC que la dosis de 25 mg/kg utilizando la misma pauta de tratamiento, desvelando una relación de respuesta a la dosis. La formulación de 801 al nivel de dosis (50 mg/kg) mostró significativamente la actividad antitumoral más fuerte que la del imatinib (p < 0,001).
2.0 Estudios de seguridad
Los estudios de toxicidad en macacos normales mostraron que tras la dosificación con 801 HCl mediante infusión intravenosa dos veces al día con un intervalo de 5 horas, la MTD era de 60 mg/kg/día. Los resultados de un estudio de toxicidad con una dosis de repetición de 5 días de 801 HCl tras la infusión intravenosa en macacos presentaron que la MTD de 801 era de 30 mg/kg/día para la dosificación de repetición.
En el estudio MTD en ratas, Se dosificaron ratas Sprague-Dawley con 801 HCl a una concentración de 6 mg/ml mediante infusión intravenosa o inyección intravenosa lenta. La MTD de 801 en ratas normales era de 120 mg/kg/día. En el estudio de dosis de repetición de 7 días, Se administró a las ratas una inyección IV lenta de 891, dos veces al día durante 7 días. Los datos mostraron que la MTD de 801 era de 60 mg/kg/día para la dosificación de repetición.
Claims (15)
1. Un compuesto de fórmula (I):
o un N-óxido del mismo, o una sal farmacéuticamente aceptable de cada uno de los mismos, o un solvato farmacéuticamente aceptable de cada uno de los anteriores, en donde
R1 es H o tiene una estructura de:
R3 es H, un alquilo C1-C8 opcionalmente sustituido, un cicloalquilo de 3-10 miembros opcionalmente sustituido, un heterociclilo de 3-10 miembros opcionalmente sustituido, un arilo de 6-10 miembros opcionalmente sustituido o un heteroarilo de 5-10 miembros opcionalmente sustituido;
R5 es H o tiene una estructura de:
y
R ii y R12 son independientemente un alquilo C1-C8 opcionalmente sustituido.
2. El compuesto de la reivindicación 1, en donde R1 es H.
3. El compuesto de la reivindicación 1, en donde R 1 tiene la estructura de:
6. El compuesto de una cualquiera de las reivindicaciones 1-5, en donde R11 y R12 son independientemente alquilo C1-C8.
7. El compuesto de la reivindicación 6, en donde R11 es etilo y R12 es metilo.
8. El compuesto de una cualquiera de las reivindicaciones 1-4, en donde R5 es H.
9. El compuesto de una cualquiera de las reivindicaciones 1-3 y 5-8, en donde R3 es alquilo C1-C8.
10. El compuesto de una cualquiera de las reivindicaciones 1-3 y 5-8, en donde R3 es un etilo.
12. Una composición farmacéutica que comprende un compuesto de acuerdo con una cualquiera de las reivindicaciones 1-11 y al menos un excipiente farmacéuticamente aceptable.
13. La composición farmacéutica de la reivindicación 12, en donde la composición farmacéutica es una forma sólida, una forma líquida, una forma inyectable o una formulación liposómica.
14. El compuesto de una cualquiera de las reivindicaciones 1-11 o la composición farmacéutica de una cualquiera de las reivindicaciones 12-13 para su uso en el tratamiento del cáncer o retrasar o reducir el crecimiento del tumor en un sujeto que lo necesita.
15. El compuesto o la composición farmacéutica para el uso de la reivindicación 14, en donde el cáncer comprende un tumor sólido o el crecimiento del tumor es un tumor sólido.
Applications Claiming Priority (1)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| PCT/US2015/057645 WO2017074325A1 (en) | 2015-10-27 | 2015-10-27 | Podophyllotoxin derivatives and their use |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2806624T3 true ES2806624T3 (es) | 2021-02-18 |
Family
ID=58630785
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES15907433T Active ES2806624T3 (es) | 2015-10-27 | 2015-10-27 | Derivados de podofilotoxina y su uso |
Country Status (6)
| Country | Link |
|---|---|
| US (2) | US20190077813A1 (es) |
| EP (1) | EP3371192B1 (es) |
| JP (1) | JP6550538B2 (es) |
| CN (2) | CN106937529B (es) |
| ES (1) | ES2806624T3 (es) |
| WO (1) | WO2017074325A1 (es) |
Families Citing this family (3)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| CN109675053B (zh) * | 2018-11-01 | 2021-08-20 | 昆明理工大学 | 鬼臼毒素及其衍生物的靶向制剂及其制备方法 |
| CN113402527A (zh) * | 2021-06-22 | 2021-09-17 | 广东医科大学 | 一种鬼臼毒素结构修饰的衍生物及其制备方法 |
| CN114539292B (zh) * | 2022-01-28 | 2023-08-29 | 遵义医药高等专科学校 | 一种新型鬼臼毒素拼接抗肿瘤活性分子化合物及其制备方法及应用 |
Family Cites Families (25)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US2530037A (en) | 1947-06-09 | 1950-11-14 | Willis Paul | Envelope moistener and sealer |
| CH454169A (de) | 1964-08-12 | 1968-04-15 | Sandoz Ag | Verfahren zur Herstellung von neuen Podophyllotoxin-Derivaten |
| NL6613143A (es) | 1965-09-21 | 1967-03-22 | ||
| JPH01117885A (ja) | 1987-10-30 | 1989-05-10 | Dai Ichi Seiyaku Co Ltd | 新規ボドフィロトキシン誘導体及びその製造法 |
| JPH02300124A (ja) | 1989-02-28 | 1990-12-12 | Takeda Chem Ind Ltd | 骨粗鬆症予防治療剤 |
| US4965348A (en) | 1989-05-19 | 1990-10-23 | Bristol-Myers Company | Dimeric epipodophyllotoxin glucoside derivatives |
| US5614549A (en) | 1992-08-21 | 1997-03-25 | Enzon, Inc. | High molecular weight polymer-based prodrugs |
| US5840900A (en) | 1993-10-20 | 1998-11-24 | Enzon, Inc. | High molecular weight polymer-based prodrugs |
| US5880131A (en) | 1993-10-20 | 1999-03-09 | Enzon, Inc. | High molecular weight polymer-based prodrugs |
| US5534499A (en) | 1994-05-19 | 1996-07-09 | The University Of British Columbia | Lipophilic drug derivatives for use in liposomes |
| TW438775B (en) | 1995-04-07 | 2001-06-07 | Pharmacia & Upjohn Co Llc | Novel intermediates and process for the manufacture of camptothecin derivatives (CPT-11) and related compounds |
| US6096336A (en) * | 1996-01-30 | 2000-08-01 | The Stehlin Foundation For Cancer Research | Liposomal prodrugs comprising derivatives of camptothecin and methods of treating cancer using these prodrugs |
| FR2776550B1 (fr) * | 1998-03-26 | 2000-05-05 | Air Liquide | Procede de soudage ou de coupage plasma ou tig avec gaz non-oxydant a faible teneur en impuretes h2o et/ou o2 |
| US6251382B1 (en) | 1998-04-17 | 2001-06-26 | Enzon, Inc. | Biodegradable high molecular weight polymeric linkers and their conjugates |
| GB9814527D0 (en) | 1998-07-03 | 1998-09-02 | Cyclacel Ltd | Delivery system |
| IL142869A0 (en) | 1998-11-13 | 2002-03-10 | Cyclacel Ltd | Transport vectors |
| US6624317B1 (en) | 2000-09-25 | 2003-09-23 | The University Of North Carolina At Chapel Hill | Taxoid conjugates as antimitotic and antitumor agents |
| SE0102168D0 (sv) | 2001-06-19 | 2001-06-19 | Karolinska Innovations Ab | New use and new compounds |
| FR2837824B1 (fr) | 2002-03-28 | 2006-03-03 | Pierre Potier | Nouveaux derives de la podophyllotoxine, leur preparation et leur application en therapeutique |
| US6566393B1 (en) * | 2002-06-21 | 2003-05-20 | The University Of North Carolina At Chapel Hill | Etoposide analogs and methods of use thereof |
| US7342114B2 (en) * | 2003-07-01 | 2008-03-11 | California Pacific Medical Center | Podophyllotoxin derivatives |
| US7875602B2 (en) * | 2005-10-21 | 2011-01-25 | Sutter West Bay Hospitals | Camptothecin derivatives as chemoradiosensitizing agents |
| WO2012134446A1 (en) * | 2011-03-29 | 2012-10-04 | SUTTER WEST BAY HOSPITALS doing business as CALIFORNIA PACIFIC MEDICAL CENTER | Epiandrosterone and/or androsterone derivatives and method of use thereof |
| SI2900277T1 (sl) * | 2012-12-13 | 2022-05-31 | Immunomedics, Inc. | Odmerki imunokonjugatov protiteles in SN-38 za boljšo učinkovitost in zmanjšano toksičnost |
| US20160115192A1 (en) * | 2013-06-10 | 2016-04-28 | Cedars-Sinai Medical Center | Antioxidant, anti-inflammatory and anticancer derivatives of triptolide and nanospheres thereof |
-
2015
- 2015-10-27 JP JP2018521125A patent/JP6550538B2/ja active Active
- 2015-10-27 US US15/769,811 patent/US20190077813A1/en not_active Abandoned
- 2015-10-27 ES ES15907433T patent/ES2806624T3/es active Active
- 2015-10-27 CN CN201580005370.7A patent/CN106937529B/zh active Active
- 2015-10-27 CN CN202011599255.6A patent/CN112759603B/zh active Active
- 2015-10-27 WO PCT/US2015/057645 patent/WO2017074325A1/en not_active Ceased
- 2015-10-27 EP EP15907433.5A patent/EP3371192B1/en active Active
-
2020
- 2020-05-19 US US16/878,425 patent/US11186594B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| CN112759603A (zh) | 2021-05-07 |
| EP3371192B1 (en) | 2020-06-03 |
| CN106937529A (zh) | 2017-07-07 |
| CN112759603B (zh) | 2022-09-09 |
| WO2017074325A1 (en) | 2017-05-04 |
| JP6550538B2 (ja) | 2019-07-24 |
| US11186594B2 (en) | 2021-11-30 |
| EP3371192A1 (en) | 2018-09-12 |
| US20190077813A1 (en) | 2019-03-14 |
| JP2018531953A (ja) | 2018-11-01 |
| EP3371192A4 (en) | 2019-04-17 |
| CN106937529B (zh) | 2021-02-05 |
| US20200277310A1 (en) | 2020-09-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2629932T3 (es) | Inhibidor de PFKFB3 y métodos de uso como terapéutico contra el cáncer | |
| ES2928169T3 (es) | Derivados de 4-(3H-indol-5-il)-N-(piridin-2-il)pirimidin-2-amina como inhibidores de proteína cinasa, y método de preparación y uso médico de los mismos | |
| KR20220122662A (ko) | 스피로 고리를 함유하는 퀴나졸린 화합물 | |
| ES2660981T3 (es) | Imidazopiridazinas sustituidas con amino | |
| US20240317741A1 (en) | Naphthyridine derivative as atr inhibitor and method for preparing same | |
| ES2795950T3 (es) | Profármacos de oxabicicloheptano | |
| ES2806624T3 (es) | Derivados de podofilotoxina y su uso | |
| CN117940437A (zh) | Dna-pk选择性抑制剂及其制备方法和用途 | |
| KR20210070978A (ko) | 화합물 및 이의 용도 | |
| ES3042620T3 (en) | Antitumor-effect enhancer using pyrazolo[3,4-d]pyrimidine compound | |
| ES2879379T3 (es) | Derivados de colquicina para el tratamiento del cáncer | |
| BRPI0707089A2 (pt) | derivados de camptotecina e seus usos | |
| US10351586B2 (en) | Cytidine derivative dimers and applications thereof | |
| ES3053012T3 (en) | Condensed pyridine derivatives substitued by amide functions as acss2 inhibitors | |
| CN114736214A (zh) | 一种倍半萜衍生物、其药物组合物及其制备方法和用途 | |
| ES2940119T3 (es) | Derivados de alquino disustituidos | |
| WO2011154574A1 (es) | Derivados de camptotecina como agentes antitumorales | |
| US10087194B2 (en) | Podophyllotoxin derivatives and their use | |
| WO2023120696A1 (ja) | 二環性骨格を有する1h-ピラゾール-3-アミン誘導体 | |
| CN102532152B (zh) | 4′-去甲表鬼臼毒素类化合物及其作为抗癌剂的药物用途 | |
| EA049737B1 (ru) | Производное 1h-пиразол-3-амина, имеющее бициклическую основную цепь | |
| CA3209238A1 (en) | Heteroaromatic phosphonium salts and their use treating cancer | |
| WO2025214463A1 (zh) | 含有三并环结构的化合物 | |
| CN118434726A (zh) | 具有二环性骨架的1h-吡唑-3-胺衍生物 | |
| BR112021000103B1 (pt) | Composto de fórmula i, uso de um composto e composição farmacêutica compreendendo um composto |