ES2808409T3 - Método para sincronizar el tiempo de inseminación en cerdas primerizas - Google Patents
Método para sincronizar el tiempo de inseminación en cerdas primerizas Download PDFInfo
- Publication number
- ES2808409T3 ES2808409T3 ES13859305T ES13859305T ES2808409T3 ES 2808409 T3 ES2808409 T3 ES 2808409T3 ES 13859305 T ES13859305 T ES 13859305T ES 13859305 T ES13859305 T ES 13859305T ES 2808409 T3 ES2808409 T3 ES 2808409T3
- Authority
- ES
- Spain
- Prior art keywords
- hydrogen
- gonadotropin
- hormone
- releasing hormone
- hours
- Prior art date
- Legal status (The legal status is an assumption and is not a legal conclusion. Google has not performed a legal analysis and makes no representation as to the accuracy of the status listed.)
- Active
Links
- 238000000034 method Methods 0.000 title claims abstract description 238
- 230000009027 insemination Effects 0.000 title claims abstract description 104
- 101000857870 Squalus acanthias Gonadoliberin Proteins 0.000 claims abstract description 286
- XLXSAKCOAKORKW-AQJXLSMYSA-N gonadorelin Chemical compound C([C@@H](C(=O)NCC(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 XLXSAKCOAKORKW-AQJXLSMYSA-N 0.000 claims abstract description 277
- 229940035638 gonadotropin-releasing hormone Drugs 0.000 claims abstract description 277
- 239000000579 Gonadotropin-Releasing Hormone Substances 0.000 claims abstract description 275
- 230000012173 estrus Effects 0.000 claims abstract description 188
- 229940088597 hormone Drugs 0.000 claims abstract description 153
- 239000005556 hormone Substances 0.000 claims abstract description 153
- 230000001158 estrous effect Effects 0.000 claims abstract description 92
- 230000016087 ovulation Effects 0.000 claims abstract description 72
- 229910052739 hydrogen Inorganic materials 0.000 claims description 216
- 239000001257 hydrogen Substances 0.000 claims description 216
- 125000004435 hydrogen atom Chemical class [H]* 0.000 claims description 118
- 239000000203 mixture Substances 0.000 claims description 107
- VXKHXGOKWPXYNA-PGBVPBMZSA-N triptorelin Chemical group C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCNC(N)=N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 VXKHXGOKWPXYNA-PGBVPBMZSA-N 0.000 claims description 103
- 108010050144 Triptorelin Pamoate Proteins 0.000 claims description 97
- 229960004824 triptorelin Drugs 0.000 claims description 97
- OKTJSMMVPCPJKN-UHFFFAOYSA-N Carbon Chemical group [C] OKTJSMMVPCPJKN-UHFFFAOYSA-N 0.000 claims description 56
- KRKNYBCHXYNGOX-UHFFFAOYSA-N citric acid Chemical compound OC(=O)CC(O)(C(O)=O)CC(O)=O KRKNYBCHXYNGOX-UHFFFAOYSA-N 0.000 claims description 52
- 229910052799 carbon Inorganic materials 0.000 claims description 50
- -1 1H-indol-3-yl-methyl Chemical group 0.000 claims description 43
- 125000001495 ethyl group Chemical group [H]C([H])([H])C([H])([H])* 0.000 claims description 39
- 125000002496 methyl group Chemical group [H]C([H])([H])* 0.000 claims description 36
- FAPWRFPIFSIZLT-UHFFFAOYSA-M Sodium chloride Chemical compound [Na+].[Cl-] FAPWRFPIFSIZLT-UHFFFAOYSA-M 0.000 claims description 33
- 229920000609 methyl cellulose Polymers 0.000 claims description 28
- 239000001923 methylcellulose Substances 0.000 claims description 28
- LXCFILQKKLGQFO-UHFFFAOYSA-N methylparaben Chemical compound COC(=O)C1=CC=C(O)C=C1 LXCFILQKKLGQFO-UHFFFAOYSA-N 0.000 claims description 26
- QELSKZZBTMNZEB-UHFFFAOYSA-N propylparaben Chemical compound CCCOC(=O)C1=CC=C(O)C=C1 QELSKZZBTMNZEB-UHFFFAOYSA-N 0.000 claims description 26
- 229960004452 methionine Drugs 0.000 claims description 20
- QTBSBXVTEAMEQO-UHFFFAOYSA-N Acetic acid Chemical compound CC(O)=O QTBSBXVTEAMEQO-UHFFFAOYSA-N 0.000 claims description 19
- 125000000217 alkyl group Chemical group 0.000 claims description 19
- HEMHJVSKTPXQMS-UHFFFAOYSA-M Sodium hydroxide Chemical compound [OH-].[Na+] HEMHJVSKTPXQMS-UHFFFAOYSA-M 0.000 claims description 18
- 125000004404 heteroalkyl group Chemical group 0.000 claims description 18
- 239000000546 pharmaceutical excipient Substances 0.000 claims description 18
- NLJMYIDDQXHKNR-UHFFFAOYSA-K sodium citrate Chemical compound O.O.[Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O NLJMYIDDQXHKNR-UHFFFAOYSA-K 0.000 claims description 18
- VWAUPFMBXBWEQY-ANULTFPQSA-N Altrenogest Chemical group C1CC(=O)C=C2CC[C@@H]([C@H]3[C@@](C)([C@](CC3)(O)CC=C)C=C3)C3=C21 VWAUPFMBXBWEQY-ANULTFPQSA-N 0.000 claims description 17
- FFEARJCKVFRZRR-UHFFFAOYSA-N L-Methionine Natural products CSCCC(N)C(O)=O FFEARJCKVFRZRR-UHFFFAOYSA-N 0.000 claims description 17
- FFEARJCKVFRZRR-BYPYZUCNSA-N L-methionine Chemical compound CSCC[C@H](N)C(O)=O FFEARJCKVFRZRR-BYPYZUCNSA-N 0.000 claims description 17
- 229930195722 L-methionine Natural products 0.000 claims description 17
- 229960000971 altrenogest Drugs 0.000 claims description 17
- 239000001509 sodium citrate Substances 0.000 claims description 17
- 239000000872 buffer Substances 0.000 claims description 16
- 239000011780 sodium chloride Substances 0.000 claims description 16
- 235000010270 methyl p-hydroxybenzoate Nutrition 0.000 claims description 15
- 235000010232 propyl p-hydroxybenzoate Nutrition 0.000 claims description 15
- VEXZGXHMUGYJMC-UHFFFAOYSA-N Hydrochloric acid Chemical compound Cl VEXZGXHMUGYJMC-UHFFFAOYSA-N 0.000 claims description 13
- 238000002347 injection Methods 0.000 claims description 13
- 239000007924 injection Substances 0.000 claims description 13
- 239000004292 methyl p-hydroxybenzoate Substances 0.000 claims description 13
- 229960002216 methylparaben Drugs 0.000 claims description 13
- 239000004405 propyl p-hydroxybenzoate Substances 0.000 claims description 13
- 229960003415 propylparaben Drugs 0.000 claims description 13
- QGZKDVFQNNGYKY-UHFFFAOYSA-N Ammonia Chemical compound N QGZKDVFQNNGYKY-UHFFFAOYSA-N 0.000 claims description 12
- 125000000753 cycloalkyl group Chemical group 0.000 claims description 12
- 125000001188 haloalkyl group Chemical group 0.000 claims description 12
- 239000000243 solution Substances 0.000 claims description 12
- 230000008021 deposition Effects 0.000 claims description 11
- 239000006179 pH buffering agent Substances 0.000 claims description 11
- XLYOFNOQVPJJNP-UHFFFAOYSA-N water Chemical compound O XLYOFNOQVPJJNP-UHFFFAOYSA-N 0.000 claims description 11
- LYCAIKOWRPUZTN-UHFFFAOYSA-N Ethylene glycol Chemical compound OCCO LYCAIKOWRPUZTN-UHFFFAOYSA-N 0.000 claims description 10
- 150000001875 compounds Chemical class 0.000 claims description 9
- WQZGKKKJIJFFOK-GASJEMHNSA-N Glucose Natural products OC[C@H]1OC(O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-GASJEMHNSA-N 0.000 claims description 8
- 239000007979 citrate buffer Substances 0.000 claims description 8
- 125000003118 aryl group Chemical group 0.000 claims description 7
- 125000001797 benzyl group Chemical group [H]C1=C([H])C([H])=C(C([H])=C1[H])C([H])([H])* 0.000 claims description 7
- 150000002148 esters Chemical class 0.000 claims description 7
- 239000008103 glucose Substances 0.000 claims description 7
- 125000001072 heteroaryl group Chemical group 0.000 claims description 7
- 125000000959 isobutyl group Chemical group [H]C([H])([H])C([H])(C([H])([H])[H])C([H])([H])* 0.000 claims description 7
- 239000007788 liquid Substances 0.000 claims description 7
- 125000004042 4-aminobutyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])N([H])[H] 0.000 claims description 6
- BVKZGUZCCUSVTD-UHFFFAOYSA-M Bicarbonate Chemical compound OC([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-M 0.000 claims description 6
- BTBUEUYNUDRHOZ-UHFFFAOYSA-N Borate Chemical compound [O-]B([O-])[O-] BTBUEUYNUDRHOZ-UHFFFAOYSA-N 0.000 claims description 6
- BVKZGUZCCUSVTD-UHFFFAOYSA-L Carbonate Chemical compound [O-]C([O-])=O BVKZGUZCCUSVTD-UHFFFAOYSA-L 0.000 claims description 6
- LFQSCWFLJHTTHZ-UHFFFAOYSA-N Ethanol Chemical compound CCO LFQSCWFLJHTTHZ-UHFFFAOYSA-N 0.000 claims description 6
- 150000001408 amides Chemical class 0.000 claims description 6
- 229910021529 ammonia Inorganic materials 0.000 claims description 6
- 125000003710 aryl alkyl group Chemical group 0.000 claims description 6
- 239000007975 buffered saline Substances 0.000 claims description 6
- 229910021386 carbon form Inorganic materials 0.000 claims description 6
- BVKZGUZCCUSVTD-UHFFFAOYSA-N carbonic acid Chemical compound OC(O)=O BVKZGUZCCUSVTD-UHFFFAOYSA-N 0.000 claims description 6
- BNIILDVGGAEEIG-UHFFFAOYSA-L disodium hydrogen phosphate Chemical compound [Na+].[Na+].OP([O-])([O-])=O BNIILDVGGAEEIG-UHFFFAOYSA-L 0.000 claims description 6
- 125000004446 heteroarylalkyl group Chemical group 0.000 claims description 6
- 125000000623 heterocyclic group Chemical group 0.000 claims description 6
- 125000000592 heterocycloalkyl group Chemical group 0.000 claims description 6
- 239000000395 magnesium oxide Substances 0.000 claims description 6
- CPLXHLVBOLITMK-UHFFFAOYSA-N magnesium oxide Inorganic materials [Mg]=O CPLXHLVBOLITMK-UHFFFAOYSA-N 0.000 claims description 6
- AXZKOIWUVFPNLO-UHFFFAOYSA-N magnesium;oxygen(2-) Chemical compound [O-2].[Mg+2] AXZKOIWUVFPNLO-UHFFFAOYSA-N 0.000 claims description 6
- 229910000402 monopotassium phosphate Inorganic materials 0.000 claims description 6
- 235000019796 monopotassium phosphate Nutrition 0.000 claims description 6
- 239000008363 phosphate buffer Substances 0.000 claims description 6
- GNSKLFRGEWLPPA-UHFFFAOYSA-M potassium dihydrogen phosphate Chemical compound [K+].OP(O)([O-])=O GNSKLFRGEWLPPA-UHFFFAOYSA-M 0.000 claims description 6
- LWIHDJKSTIGBAC-UHFFFAOYSA-K potassium phosphate Substances [K+].[K+].[K+].[O-]P([O-])([O-])=O LWIHDJKSTIGBAC-UHFFFAOYSA-K 0.000 claims description 6
- 239000008223 sterile water Substances 0.000 claims description 6
- 102000006771 Gonadotropins Human genes 0.000 claims description 5
- 108010086677 Gonadotropins Proteins 0.000 claims description 5
- UFHFLCQGNIYNRP-UHFFFAOYSA-N Hydrogen Chemical compound [H][H] UFHFLCQGNIYNRP-UHFFFAOYSA-N 0.000 claims description 5
- 239000008351 acetate buffer Substances 0.000 claims description 5
- 239000002622 gonadotropin Substances 0.000 claims description 5
- WGCNASOHLSPBMP-UHFFFAOYSA-N hydroxyacetaldehyde Natural products OCC=O WGCNASOHLSPBMP-UHFFFAOYSA-N 0.000 claims description 5
- 125000000547 substituted alkyl group Chemical group 0.000 claims description 5
- HRXKRNGNAMMEHJ-UHFFFAOYSA-K trisodium citrate Chemical compound [Na+].[Na+].[Na+].[O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O HRXKRNGNAMMEHJ-UHFFFAOYSA-K 0.000 claims 1
- 238000011282 treatment Methods 0.000 description 127
- 239000011159 matrix material Substances 0.000 description 111
- 239000000499 gel Substances 0.000 description 107
- 150000002431 hydrogen Chemical class 0.000 description 93
- 235000002639 sodium chloride Nutrition 0.000 description 31
- 235000010981 methylcellulose Nutrition 0.000 description 27
- 229960002900 methylcellulose Drugs 0.000 description 27
- 239000003981 vehicle Substances 0.000 description 23
- 229920002678 cellulose Polymers 0.000 description 22
- 235000010980 cellulose Nutrition 0.000 description 21
- 210000002966 serum Anatomy 0.000 description 20
- 238000001514 detection method Methods 0.000 description 19
- 229920001282 polysaccharide Polymers 0.000 description 19
- 239000005017 polysaccharide Substances 0.000 description 19
- 150000004804 polysaccharides Chemical class 0.000 description 19
- 239000001913 cellulose Substances 0.000 description 17
- 239000003755 preservative agent Substances 0.000 description 17
- 239000003795 chemical substances by application Substances 0.000 description 16
- 239000003381 stabilizer Substances 0.000 description 16
- 238000012360 testing method Methods 0.000 description 16
- 229960004106 citric acid Drugs 0.000 description 15
- 230000035935 pregnancy Effects 0.000 description 15
- 150000003839 salts Chemical class 0.000 description 15
- 238000009472 formulation Methods 0.000 description 14
- QTBSBXVTEAMEQO-UHFFFAOYSA-M Acetate Chemical compound CC([O-])=O QTBSBXVTEAMEQO-UHFFFAOYSA-M 0.000 description 13
- 230000002335 preservative effect Effects 0.000 description 13
- NMJREATYWWNIKX-UHFFFAOYSA-N GnRH Chemical compound C1CCC(C(=O)NCC(N)=O)N1C(=O)C(CC(C)C)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)CNC(=O)C(NC(=O)C(CO)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C(CC=1NC=NC=1)NC(=O)C1NC(=O)CC1)CC1=CC=C(O)C=C1 NMJREATYWWNIKX-UHFFFAOYSA-N 0.000 description 12
- 102000009151 Luteinizing Hormone Human genes 0.000 description 12
- 108010073521 Luteinizing Hormone Proteins 0.000 description 12
- 229940040129 luteinizing hormone Drugs 0.000 description 12
- 241000282887 Suidae Species 0.000 description 11
- 230000001186 cumulative effect Effects 0.000 description 10
- 230000000694 effects Effects 0.000 description 10
- 238000004519 manufacturing process Methods 0.000 description 10
- 238000002156 mixing Methods 0.000 description 10
- 239000000126 substance Substances 0.000 description 10
- HPPONSCISKROOD-OYLNGHKZSA-N acetic acid;(2s)-n-[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2r)-1-[[(2s)-1-[[(2s)-1-[(2s)-2-[(2-amino-2-oxoethyl)carbamoyl]pyrrolidin-1-yl]-5-(diaminomethylideneamino)-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]amino]-3-(1h-indol-3-yl)-1-oxopropan-2-y Chemical compound CC(O)=O.C([C@@H](C(=O)N[C@H](CC=1C2=CC=CC=C2NC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 HPPONSCISKROOD-OYLNGHKZSA-N 0.000 description 9
- 229960000434 triptorelin acetate Drugs 0.000 description 9
- 229910052782 aluminium Inorganic materials 0.000 description 8
- XAGFODPZIPBFFR-UHFFFAOYSA-N aluminium Chemical compound [Al] XAGFODPZIPBFFR-UHFFFAOYSA-N 0.000 description 8
- 230000003993 interaction Effects 0.000 description 8
- 102000011022 Chorionic Gonadotropin Human genes 0.000 description 7
- 108010062540 Chorionic Gonadotropin Proteins 0.000 description 7
- 102000012673 Follicle Stimulating Hormone Human genes 0.000 description 7
- 108010079345 Follicle Stimulating Hormone Proteins 0.000 description 7
- 239000000556 agonist Substances 0.000 description 7
- 235000010443 alginic acid Nutrition 0.000 description 7
- 229920000615 alginic acid Polymers 0.000 description 7
- WQZGKKKJIJFFOK-VFUOTHLCSA-N beta-D-glucose Chemical compound OC[C@H]1O[C@@H](O)[C@H](O)[C@@H](O)[C@@H]1O WQZGKKKJIJFFOK-VFUOTHLCSA-N 0.000 description 7
- 229940084986 human chorionic gonadotropin Drugs 0.000 description 7
- 230000027758 ovulation cycle Effects 0.000 description 7
- CIWBSHSKHKDKBQ-JLAZNSOCSA-N Ascorbic acid Chemical compound OC[C@H](O)[C@H]1OC(=O)C(O)=C1O CIWBSHSKHKDKBQ-JLAZNSOCSA-N 0.000 description 6
- 241001465754 Metazoa Species 0.000 description 6
- 238000004458 analytical method Methods 0.000 description 6
- 229940028334 follicle stimulating hormone Drugs 0.000 description 6
- 230000000624 ovulatory effect Effects 0.000 description 6
- 230000001850 reproductive effect Effects 0.000 description 6
- 230000001568 sexual effect Effects 0.000 description 6
- KCXVZYZYPLLWCC-UHFFFAOYSA-N EDTA Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(O)=O)CC(O)=O KCXVZYZYPLLWCC-UHFFFAOYSA-N 0.000 description 5
- PEDCQBHIVMGVHV-UHFFFAOYSA-N Glycerine Chemical compound OCC(O)CO PEDCQBHIVMGVHV-UHFFFAOYSA-N 0.000 description 5
- 229920003091 Methocel™ Polymers 0.000 description 5
- 239000002253 acid Substances 0.000 description 5
- 239000005388 borosilicate glass Substances 0.000 description 5
- 229920005549 butyl rubber Polymers 0.000 description 5
- 210000003679 cervix uteri Anatomy 0.000 description 5
- 238000013461 design Methods 0.000 description 5
- 230000011514 reflex Effects 0.000 description 5
- 230000010076 replication Effects 0.000 description 5
- 239000012453 solvate Substances 0.000 description 5
- 238000007619 statistical method Methods 0.000 description 5
- 239000012929 tonicity agent Substances 0.000 description 5
- 238000002604 ultrasonography Methods 0.000 description 5
- 230000000007 visual effect Effects 0.000 description 5
- 229920002307 Dextran Polymers 0.000 description 4
- RTZKZFJDLAIYFH-UHFFFAOYSA-N Diethyl ether Chemical compound CCOCC RTZKZFJDLAIYFH-UHFFFAOYSA-N 0.000 description 4
- ZTHYODDOHIVTJV-UHFFFAOYSA-N Propyl gallate Chemical compound CCCOC(=O)C1=CC(O)=C(O)C(O)=C1 ZTHYODDOHIVTJV-UHFFFAOYSA-N 0.000 description 4
- 239000005557 antagonist Substances 0.000 description 4
- 239000004599 antimicrobial Substances 0.000 description 4
- 239000006172 buffering agent Substances 0.000 description 4
- 239000000969 carrier Substances 0.000 description 4
- 230000035558 fertility Effects 0.000 description 4
- 210000001672 ovary Anatomy 0.000 description 4
- 239000008194 pharmaceutical composition Substances 0.000 description 4
- 229920001223 polyethylene glycol Polymers 0.000 description 4
- 229920000642 polymer Polymers 0.000 description 4
- 210000000664 rectum Anatomy 0.000 description 4
- 230000004044 response Effects 0.000 description 4
- 229960002668 sodium chloride Drugs 0.000 description 4
- 229960001790 sodium citrate Drugs 0.000 description 4
- 235000011083 sodium citrates Nutrition 0.000 description 4
- 230000001360 synchronised effect Effects 0.000 description 4
- 210000001215 vagina Anatomy 0.000 description 4
- GVJHHUAWPYXKBD-UHFFFAOYSA-N (±)-α-Tocopherol Chemical compound OC1=C(C)C(C)=C2OC(CCCC(C)CCCC(C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-UHFFFAOYSA-N 0.000 description 3
- 125000000980 1H-indol-3-ylmethyl group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C(C([H])([H])[*])C2=C1[H] 0.000 description 3
- FJKROLUGYXJWQN-UHFFFAOYSA-N 4-hydroxybenzoic acid Chemical compound OC(=O)C1=CC=C(O)C=C1 FJKROLUGYXJWQN-UHFFFAOYSA-N 0.000 description 3
- 241000207199 Citrus Species 0.000 description 3
- 108010010803 Gelatin Proteins 0.000 description 3
- 125000000393 L-methionino group Chemical group [H]OC(=O)[C@@]([H])(N([H])[*])C([H])([H])C(SC([H])([H])[H])([H])[H] 0.000 description 3
- DNIAPMSPPWPWGF-UHFFFAOYSA-N Propylene glycol Chemical compound CC(O)CO DNIAPMSPPWPWGF-UHFFFAOYSA-N 0.000 description 3
- 229920002472 Starch Polymers 0.000 description 3
- 238000000540 analysis of variance Methods 0.000 description 3
- 230000000845 anti-microbial effect Effects 0.000 description 3
- 229940121375 antifungal agent Drugs 0.000 description 3
- 239000003963 antioxidant agent Substances 0.000 description 3
- 235000006708 antioxidants Nutrition 0.000 description 3
- 210000004369 blood Anatomy 0.000 description 3
- 239000008280 blood Substances 0.000 description 3
- 239000002738 chelating agent Substances 0.000 description 3
- 235000020971 citrus fruits Nutrition 0.000 description 3
- 239000002552 dosage form Substances 0.000 description 3
- 238000001647 drug administration Methods 0.000 description 3
- 239000008273 gelatin Substances 0.000 description 3
- 229920000159 gelatin Polymers 0.000 description 3
- 235000019322 gelatine Nutrition 0.000 description 3
- 235000011852 gelatine desserts Nutrition 0.000 description 3
- 239000000314 lubricant Substances 0.000 description 3
- 238000007726 management method Methods 0.000 description 3
- 229930182817 methionine Natural products 0.000 description 3
- 230000008569 process Effects 0.000 description 3
- 239000000583 progesterone congener Substances 0.000 description 3
- 239000008213 purified water Substances 0.000 description 3
- 235000019698 starch Nutrition 0.000 description 3
- LNAZSHAWQACDHT-XIYTZBAFSA-N (2r,3r,4s,5r,6s)-4,5-dimethoxy-2-(methoxymethyl)-3-[(2s,3r,4s,5r,6r)-3,4,5-trimethoxy-6-(methoxymethyl)oxan-2-yl]oxy-6-[(2r,3r,4s,5r,6r)-4,5,6-trimethoxy-2-(methoxymethyl)oxan-3-yl]oxyoxane Chemical compound CO[C@@H]1[C@@H](OC)[C@H](OC)[C@@H](COC)O[C@H]1O[C@H]1[C@H](OC)[C@@H](OC)[C@H](O[C@H]2[C@@H]([C@@H](OC)[C@H](OC)O[C@@H]2COC)OC)O[C@@H]1COC LNAZSHAWQACDHT-XIYTZBAFSA-N 0.000 description 2
- ZNQVEEAIQZEUHB-UHFFFAOYSA-N 2-ethoxyethanol Chemical compound CCOCCO ZNQVEEAIQZEUHB-UHFFFAOYSA-N 0.000 description 2
- WRMNZCZEMHIOCP-UHFFFAOYSA-N 2-phenylethanol Chemical compound OCCC1=CC=CC=C1 WRMNZCZEMHIOCP-UHFFFAOYSA-N 0.000 description 2
- LVDKZNITIUWNER-UHFFFAOYSA-N Bronopol Chemical compound OCC(Br)(CO)[N+]([O-])=O LVDKZNITIUWNER-UHFFFAOYSA-N 0.000 description 2
- 108010037003 Buserelin Proteins 0.000 description 2
- NLZUEZXRPGMBCV-UHFFFAOYSA-N Butylhydroxytoluene Chemical compound CC1=CC(C(C)(C)C)=C(O)C(C(C)(C)C)=C1 NLZUEZXRPGMBCV-UHFFFAOYSA-N 0.000 description 2
- OYPRJOBELJOOCE-UHFFFAOYSA-N Calcium Chemical compound [Ca] OYPRJOBELJOOCE-UHFFFAOYSA-N 0.000 description 2
- VTYYLEPIZMXCLO-UHFFFAOYSA-L Calcium carbonate Chemical compound [Ca+2].[O-]C([O-])=O VTYYLEPIZMXCLO-UHFFFAOYSA-L 0.000 description 2
- ZAMOUSCENKQFHK-UHFFFAOYSA-N Chlorine atom Chemical compound [Cl] ZAMOUSCENKQFHK-UHFFFAOYSA-N 0.000 description 2
- 239000004375 Dextrin Substances 0.000 description 2
- 229920001353 Dextrin Polymers 0.000 description 2
- 229920002153 Hydroxypropyl cellulose Polymers 0.000 description 2
- QPCDCPDFJACHGM-UHFFFAOYSA-N N,N-bis{2-[bis(carboxymethyl)amino]ethyl}glycine Chemical compound OC(=O)CN(CC(O)=O)CCN(CC(=O)O)CCN(CC(O)=O)CC(O)=O QPCDCPDFJACHGM-UHFFFAOYSA-N 0.000 description 2
- SEQKRHFRPICQDD-UHFFFAOYSA-N N-tris(hydroxymethyl)methylglycine Chemical compound OCC(CO)(CO)[NH2+]CC([O-])=O SEQKRHFRPICQDD-UHFFFAOYSA-N 0.000 description 2
- 229910019142 PO4 Inorganic materials 0.000 description 2
- WCUXLLCKKVVCTQ-UHFFFAOYSA-M Potassium chloride Chemical compound [Cl-].[K+] WCUXLLCKKVVCTQ-UHFFFAOYSA-M 0.000 description 2
- RJKFOVLPORLFTN-LEKSSAKUSA-N Progesterone Chemical class C1CC2=CC(=O)CC[C@]2(C)[C@@H]2[C@@H]1[C@@H]1CC[C@H](C(=O)C)[C@@]1(C)CC2 RJKFOVLPORLFTN-LEKSSAKUSA-N 0.000 description 2
- INVGWHRKADIJHF-UHFFFAOYSA-N Sanguinarin Chemical compound C1=C2OCOC2=CC2=C3[N+](C)=CC4=C(OCO5)C5=CC=C4C3=CC=C21 INVGWHRKADIJHF-UHFFFAOYSA-N 0.000 description 2
- 229920002125 Sokalan® Polymers 0.000 description 2
- CZMRCDWAGMRECN-UGDNZRGBSA-N Sucrose Chemical compound O[C@H]1[C@H](O)[C@@H](CO)O[C@@]1(CO)O[C@@H]1[C@H](O)[C@@H](O)[C@H](O)[C@@H](CO)O1 CZMRCDWAGMRECN-UGDNZRGBSA-N 0.000 description 2
- 229930006000 Sucrose Natural products 0.000 description 2
- MUMGGOZAMZWBJJ-DYKIIFRCSA-N Testostosterone Chemical compound O=C1CC[C@]2(C)[C@H]3CC[C@](C)([C@H](CC4)O)[C@@H]4[C@@H]3CCC2=C1 MUMGGOZAMZWBJJ-DYKIIFRCSA-N 0.000 description 2
- 229920001615 Tragacanth Polymers 0.000 description 2
- 208000027418 Wounds and injury Diseases 0.000 description 2
- 150000004781 alginic acids Chemical class 0.000 description 2
- 239000003429 antifungal agent Substances 0.000 description 2
- 235000010323 ascorbic acid Nutrition 0.000 description 2
- 239000011668 ascorbic acid Substances 0.000 description 2
- 229960000686 benzalkonium chloride Drugs 0.000 description 2
- CADWTSSKOVRVJC-UHFFFAOYSA-N benzyl(dimethyl)azanium;chloride Chemical compound [Cl-].C[NH+](C)CC1=CC=CC=C1 CADWTSSKOVRVJC-UHFFFAOYSA-N 0.000 description 2
- CUWODFFVMXJOKD-UVLQAERKSA-N buserelin Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](COC(C)(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 CUWODFFVMXJOKD-UVLQAERKSA-N 0.000 description 2
- 229960002719 buserelin Drugs 0.000 description 2
- CZBZUDVBLSSABA-UHFFFAOYSA-N butylated hydroxyanisole Chemical compound COC1=CC=C(O)C(C(C)(C)C)=C1.COC1=CC=C(O)C=C1C(C)(C)C CZBZUDVBLSSABA-UHFFFAOYSA-N 0.000 description 2
- 239000011575 calcium Substances 0.000 description 2
- 229910052791 calcium Inorganic materials 0.000 description 2
- 239000001506 calcium phosphate Substances 0.000 description 2
- OSGAYBCDTDRGGQ-UHFFFAOYSA-L calcium sulfate Chemical compound [Ca+2].[O-]S([O-])(=O)=O OSGAYBCDTDRGGQ-UHFFFAOYSA-L 0.000 description 2
- 239000003153 chemical reaction reagent Substances 0.000 description 2
- 239000000460 chlorine Substances 0.000 description 2
- 229910052801 chlorine Inorganic materials 0.000 description 2
- OSASVXMJTNOKOY-UHFFFAOYSA-N chlorobutanol Chemical compound CC(C)(O)C(Cl)(Cl)Cl OSASVXMJTNOKOY-UHFFFAOYSA-N 0.000 description 2
- 239000006071 cream Substances 0.000 description 2
- 230000006378 damage Effects 0.000 description 2
- 230000003247 decreasing effect Effects 0.000 description 2
- 235000019425 dextrin Nutrition 0.000 description 2
- 235000005911 diet Nutrition 0.000 description 2
- 230000037213 diet Effects 0.000 description 2
- XBDQKXXYIPTUBI-UHFFFAOYSA-N dimethylselenoniopropionate Natural products CCC(O)=O XBDQKXXYIPTUBI-UHFFFAOYSA-N 0.000 description 2
- 239000002270 dispersing agent Substances 0.000 description 2
- 229960001484 edetic acid Drugs 0.000 description 2
- 239000011521 glass Substances 0.000 description 2
- 235000011187 glycerol Nutrition 0.000 description 2
- 239000003688 hormone derivative Substances 0.000 description 2
- 239000000017 hydrogel Substances 0.000 description 2
- 235000010977 hydroxypropyl cellulose Nutrition 0.000 description 2
- 239000001863 hydroxypropyl cellulose Substances 0.000 description 2
- 235000010979 hydroxypropyl methyl cellulose Nutrition 0.000 description 2
- 229920003088 hydroxypropyl methyl cellulose Polymers 0.000 description 2
- 239000001866 hydroxypropyl methyl cellulose Substances 0.000 description 2
- UFVKGYZPFZQRLF-UHFFFAOYSA-N hydroxypropyl methyl cellulose Chemical compound OC1C(O)C(OC)OC(CO)C1OC1C(O)C(O)C(OC2C(C(O)C(OC3C(C(O)C(O)C(CO)O3)O)C(CO)O2)O)C(CO)O1 UFVKGYZPFZQRLF-UHFFFAOYSA-N 0.000 description 2
- 210000003016 hypothalamus Anatomy 0.000 description 2
- 230000000977 initiatory effect Effects 0.000 description 2
- 208000014674 injury Diseases 0.000 description 2
- 238000003780 insertion Methods 0.000 description 2
- 230000037431 insertion Effects 0.000 description 2
- 239000000463 material Substances 0.000 description 2
- 230000008774 maternal effect Effects 0.000 description 2
- 238000012986 modification Methods 0.000 description 2
- 230000004048 modification Effects 0.000 description 2
- 239000002674 ointment Substances 0.000 description 2
- 210000002394 ovarian follicle Anatomy 0.000 description 2
- 238000007911 parenteral administration Methods 0.000 description 2
- 239000006072 paste Substances 0.000 description 2
- 229960003330 pentetic acid Drugs 0.000 description 2
- 150000002989 phenols Chemical class 0.000 description 2
- 239000010452 phosphate Substances 0.000 description 2
- NBIIXXVUZAFLBC-UHFFFAOYSA-K phosphate Chemical compound [O-]P([O-])([O-])=O NBIIXXVUZAFLBC-UHFFFAOYSA-K 0.000 description 2
- 238000002360 preparation method Methods 0.000 description 2
- 239000000473 propyl gallate Substances 0.000 description 2
- 235000010388 propyl gallate Nutrition 0.000 description 2
- 229940075579 propyl gallate Drugs 0.000 description 2
- 125000001436 propyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])[H] 0.000 description 2
- 239000006077 pvc stabilizer Substances 0.000 description 2
- 230000028327 secretion Effects 0.000 description 2
- PESXGULMKCKJCC-UHFFFAOYSA-M sodium;4-methoxycarbonylphenolate Chemical compound [Na+].COC(=O)C1=CC=C([O-])C=C1 PESXGULMKCKJCC-UHFFFAOYSA-M 0.000 description 2
- IXMINYBUNCWGER-UHFFFAOYSA-M sodium;4-propoxycarbonylphenolate Chemical compound [Na+].CCCOC(=O)C1=CC=C([O-])C=C1 IXMINYBUNCWGER-UHFFFAOYSA-M 0.000 description 2
- 239000002904 solvent Substances 0.000 description 2
- 241000894007 species Species 0.000 description 2
- 238000006467 substitution reaction Methods 0.000 description 2
- 239000005720 sucrose Substances 0.000 description 2
- 235000000346 sugar Nutrition 0.000 description 2
- 150000008163 sugars Chemical class 0.000 description 2
- VZCYOOQTPOCHFL-UHFFFAOYSA-N trans-butenedioic acid Natural products OC(=O)C=CC(O)=O VZCYOOQTPOCHFL-UHFFFAOYSA-N 0.000 description 2
- 229920001285 xanthan gum Polymers 0.000 description 2
- KIUKXJAPPMFGSW-DNGZLQJQSA-N (2S,3S,4S,5R,6R)-6-[(2S,3R,4R,5S,6R)-3-Acetamido-2-[(2S,3S,4R,5R,6R)-6-[(2R,3R,4R,5S,6R)-3-acetamido-2,5-dihydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-2-carboxy-4,5-dihydroxyoxan-3-yl]oxy-5-hydroxy-6-(hydroxymethyl)oxan-4-yl]oxy-3,4,5-trihydroxyoxane-2-carboxylic acid Chemical compound CC(=O)N[C@H]1[C@H](O)O[C@H](CO)[C@@H](O)[C@@H]1O[C@H]1[C@H](O)[C@@H](O)[C@H](O[C@H]2[C@@H]([C@@H](O[C@H]3[C@@H]([C@@H](O)[C@H](O)[C@H](O3)C(O)=O)O)[C@H](O)[C@@H](CO)O2)NC(C)=O)[C@@H](C(O)=O)O1 KIUKXJAPPMFGSW-DNGZLQJQSA-N 0.000 description 1
- YGGIRYYNWQICCP-LDRBRYNMSA-N (2s)-n-[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2s)-1-[[(2r)-1-[[(2s)-1-[[(2s)-5-(diaminomethylideneamino)-1-[(2s)-2-(ethylcarbamoyl)pyrrolidin-1-yl]-1-oxopentan-2-yl]amino]-4-methyl-1-oxopentan-2-yl]-methylamino]-3-(1h-indol-3-yl)-1-oxopropan-2-yl]amino]-3-(4-hydrox Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)N(C)C(=O)[C@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CNC2=CC=CC=C12 YGGIRYYNWQICCP-LDRBRYNMSA-N 0.000 description 1
- SGKRLCUYIXIAHR-AKNGSSGZSA-N (4s,4ar,5s,5ar,6r,12ar)-4-(dimethylamino)-1,5,10,11,12a-pentahydroxy-6-methyl-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1=CC=C2[C@H](C)[C@@H]([C@H](O)[C@@H]3[C@](C(O)=C(C(N)=O)C(=O)[C@H]3N(C)C)(O)C3=O)C3=C(O)C2=C1O SGKRLCUYIXIAHR-AKNGSSGZSA-N 0.000 description 1
- FFTVPQUHLQBXQZ-KVUCHLLUSA-N (4s,4as,5ar,12ar)-4,7-bis(dimethylamino)-1,10,11,12a-tetrahydroxy-3,12-dioxo-4a,5,5a,6-tetrahydro-4h-tetracene-2-carboxamide Chemical compound C1C2=C(N(C)C)C=CC(O)=C2C(O)=C2[C@@H]1C[C@H]1[C@H](N(C)C)C(=O)C(C(N)=O)=C(O)[C@@]1(O)C2=O FFTVPQUHLQBXQZ-KVUCHLLUSA-N 0.000 description 1
- DTOUUUZOYKYHEP-UHFFFAOYSA-N 1,3-bis(2-ethylhexyl)-5-methyl-1,3-diazinan-5-amine Chemical compound CCCCC(CC)CN1CN(CC(CC)CCCC)CC(C)(N)C1 DTOUUUZOYKYHEP-UHFFFAOYSA-N 0.000 description 1
- IXPNQXFRVYWDDI-UHFFFAOYSA-N 1-methyl-2,4-dioxo-1,3-diazinane-5-carboximidamide Chemical compound CN1CC(C(N)=N)C(=O)NC1=O IXPNQXFRVYWDDI-UHFFFAOYSA-N 0.000 description 1
- YFVBASFBIJFBAI-UHFFFAOYSA-M 1-tetradecylpyridin-1-ium;chloride Chemical compound [Cl-].CCCCCCCCCCCCCC[N+]1=CC=CC=C1 YFVBASFBIJFBAI-UHFFFAOYSA-M 0.000 description 1
- FPIPGXGPPPQFEQ-UHFFFAOYSA-N 13-cis retinol Natural products OCC=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-UHFFFAOYSA-N 0.000 description 1
- IHPYMWDTONKSCO-UHFFFAOYSA-N 2,2'-piperazine-1,4-diylbisethanesulfonic acid Chemical compound OS(=O)(=O)CCN1CCN(CCS(O)(=O)=O)CC1 IHPYMWDTONKSCO-UHFFFAOYSA-N 0.000 description 1
- HGUFODBRKLSHSI-UHFFFAOYSA-N 2,3,7,8-tetrachloro-dibenzo-p-dioxin Chemical compound O1C2=CC(Cl)=C(Cl)C=C2OC2=C1C=C(Cl)C(Cl)=C2 HGUFODBRKLSHSI-UHFFFAOYSA-N 0.000 description 1
- JKMHFZQWWAIEOD-UHFFFAOYSA-N 2-[4-(2-hydroxyethyl)piperazin-1-yl]ethanesulfonic acid Chemical compound OCC[NH+]1CCN(CCS([O-])(=O)=O)CC1 JKMHFZQWWAIEOD-UHFFFAOYSA-N 0.000 description 1
- RWMSXNCJNSILON-UHFFFAOYSA-N 2-[4-(2-propylpentyl)piperidin-1-yl]ethanol Chemical compound CCCC(CCC)CC1CCN(CCO)CC1 RWMSXNCJNSILON-UHFFFAOYSA-N 0.000 description 1
- DVLFYONBTKHTER-UHFFFAOYSA-N 3-(N-morpholino)propanesulfonic acid Chemical compound OS(=O)(=O)CCCN1CCOCC1 DVLFYONBTKHTER-UHFFFAOYSA-N 0.000 description 1
- WPDXAMRGYMDTOV-UHFFFAOYSA-N 3-bromo-2-methylphenol Chemical class CC1=C(O)C=CC=C1Br WPDXAMRGYMDTOV-UHFFFAOYSA-N 0.000 description 1
- ANAAMBRRWOGKGU-UHFFFAOYSA-M 4-ethyl-1-tetradecylpyridin-1-ium;chloride Chemical compound [Cl-].CCCCCCCCCCCCCC[N+]1=CC=C(CC)C=C1 ANAAMBRRWOGKGU-UHFFFAOYSA-M 0.000 description 1
- 229940090248 4-hydroxybenzoic acid Drugs 0.000 description 1
- 125000004203 4-hydroxyphenyl group Chemical group [H]OC1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- SODWJACROGQSMM-UHFFFAOYSA-N 5,6,7,8-tetrahydronaphthalen-1-amine Chemical compound C1CCCC2=C1C=CC=C2N SODWJACROGQSMM-UHFFFAOYSA-N 0.000 description 1
- FHVDTGUDJYJELY-UHFFFAOYSA-N 6-{[2-carboxy-4,5-dihydroxy-6-(phosphanyloxy)oxan-3-yl]oxy}-4,5-dihydroxy-3-phosphanyloxane-2-carboxylic acid Chemical compound O1C(C(O)=O)C(P)C(O)C(O)C1OC1C(C(O)=O)OC(OP)C(O)C1O FHVDTGUDJYJELY-UHFFFAOYSA-N 0.000 description 1
- 239000005725 8-Hydroxyquinoline Substances 0.000 description 1
- GJCOSYZMQJWQCA-UHFFFAOYSA-N 9H-xanthene Chemical compound C1=CC=C2CC3=CC=CC=C3OC2=C1 GJCOSYZMQJWQCA-UHFFFAOYSA-N 0.000 description 1
- NIXOWILDQLNWCW-UHFFFAOYSA-N Acrylic acid Chemical compound OC(=O)C=C NIXOWILDQLNWCW-UHFFFAOYSA-N 0.000 description 1
- 229920001817 Agar Polymers 0.000 description 1
- 229920000945 Amylopectin Polymers 0.000 description 1
- 229920000856 Amylose Polymers 0.000 description 1
- 241000416162 Astragalus gummifer Species 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-M Bromide Chemical compound [Br-] CPELXLSAUQHCOX-UHFFFAOYSA-M 0.000 description 1
- 239000004255 Butylated hydroxyanisole Substances 0.000 description 1
- 239000004322 Butylated hydroxytoluene Substances 0.000 description 1
- 0 CC(C)C[C@@](C(N[C@@](*CCN=C(N)N)C(N(CCC1)[C@]1C(N*)=O)=O)=O)N(*)C(C(*)(*)NC([C@](Cc(cc1)ccc1O)NC(C(C1)([C@]1O)NC([C@](Cc1c[n]c2ccccc12)NC([C@](Cc1cnc[n]1)NC([C@](CC1)NC1=O)=O)=O)=O)=O)=O)=O Chemical compound CC(C)C[C@@](C(N[C@@](*CCN=C(N)N)C(N(CCC1)[C@]1C(N*)=O)=O)=O)N(*)C(C(*)(*)NC([C@](Cc(cc1)ccc1O)NC(C(C1)([C@]1O)NC([C@](Cc1c[n]c2ccccc12)NC([C@](Cc1cnc[n]1)NC([C@](CC1)NC1=O)=O)=O)=O)=O)=O)=O 0.000 description 1
- 229920002134 Carboxymethyl cellulose Polymers 0.000 description 1
- 229920002101 Chitin Polymers 0.000 description 1
- 229920001661 Chitosan Polymers 0.000 description 1
- GHXZTYHSJHQHIJ-UHFFFAOYSA-N Chlorhexidine Chemical compound C=1C=C(Cl)C=CC=1NC(N)=NC(N)=NCCCCCCN=C(N)N=C(N)NC1=CC=C(Cl)C=C1 GHXZTYHSJHQHIJ-UHFFFAOYSA-N 0.000 description 1
- VEXZGXHMUGYJMC-UHFFFAOYSA-M Chloride anion Chemical compound [Cl-] VEXZGXHMUGYJMC-UHFFFAOYSA-M 0.000 description 1
- KRKNYBCHXYNGOX-UHFFFAOYSA-K Citrate Chemical compound [O-]C(=O)CC(O)(CC([O-])=O)C([O-])=O KRKNYBCHXYNGOX-UHFFFAOYSA-K 0.000 description 1
- HZZVJAQRINQKSD-UHFFFAOYSA-N Clavulanic acid Natural products OC(=O)C1C(=CCO)OC2CC(=O)N21 HZZVJAQRINQKSD-UHFFFAOYSA-N 0.000 description 1
- QCDFBFJGMNKBDO-UHFFFAOYSA-N Clioquinol Chemical compound C1=CN=C2C(O)=C(I)C=C(Cl)C2=C1 QCDFBFJGMNKBDO-UHFFFAOYSA-N 0.000 description 1
- RYGMFSIKBFXOCR-UHFFFAOYSA-N Copper Chemical compound [Cu] RYGMFSIKBFXOCR-UHFFFAOYSA-N 0.000 description 1
- 244000303965 Cyamopsis psoralioides Species 0.000 description 1
- FBPFZTCFMRRESA-FSIIMWSLSA-N D-Glucitol Natural products OC[C@H](O)[C@H](O)[C@@H](O)[C@H](O)CO FBPFZTCFMRRESA-FSIIMWSLSA-N 0.000 description 1
- FBPFZTCFMRRESA-KVTDHHQDSA-N D-Mannitol Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-KVTDHHQDSA-N 0.000 description 1
- ZZZCUOFIHGPKAK-UHFFFAOYSA-N D-erythro-ascorbic acid Natural products OCC1OC(=O)C(O)=C1O ZZZCUOFIHGPKAK-UHFFFAOYSA-N 0.000 description 1
- FBPFZTCFMRRESA-JGWLITMVSA-N D-glucitol Chemical compound OC[C@H](O)[C@@H](O)[C@H](O)[C@H](O)CO FBPFZTCFMRRESA-JGWLITMVSA-N 0.000 description 1
- RGHNJXZEOKUKBD-SQOUGZDYSA-M D-gluconate Chemical compound OC[C@@H](O)[C@@H](O)[C@H](O)[C@@H](O)C([O-])=O RGHNJXZEOKUKBD-SQOUGZDYSA-M 0.000 description 1
- GJKXGJCSJWBJEZ-XRSSZCMZSA-N Deslorelin Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCN=C(N)N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CNC2=CC=CC=C12 GJKXGJCSJWBJEZ-XRSSZCMZSA-N 0.000 description 1
- FEWJPZIEWOKRBE-JCYAYHJZSA-N Dextrotartaric acid Chemical compound OC(=O)[C@H](O)[C@@H](O)C(O)=O FEWJPZIEWOKRBE-JCYAYHJZSA-N 0.000 description 1
- 235000019739 Dicalciumphosphate Nutrition 0.000 description 1
- PHMNXPYGVPEQSJ-UHFFFAOYSA-N Dimethoxane Chemical compound CC1CC(OC(C)=O)OC(C)O1 PHMNXPYGVPEQSJ-UHFFFAOYSA-N 0.000 description 1
- 239000004386 Erythritol Substances 0.000 description 1
- UNXHWFMMPAWVPI-UHFFFAOYSA-N Erythritol Natural products OCC(O)C(O)CO UNXHWFMMPAWVPI-UHFFFAOYSA-N 0.000 description 1
- FCEXWTOTHXCQCQ-UHFFFAOYSA-N Ethoxydihydrosanguinarine Natural products C12=CC=C3OCOC3=C2C(OCC)N(C)C(C2=C3)=C1C=CC2=CC1=C3OCO1 FCEXWTOTHXCQCQ-UHFFFAOYSA-N 0.000 description 1
- 239000004258 Ethoxyquin Substances 0.000 description 1
- 239000001856 Ethyl cellulose Substances 0.000 description 1
- ZZSNKZQZMQGXPY-UHFFFAOYSA-N Ethyl cellulose Chemical compound CCOCC1OC(OC)C(OCC)C(OCC)C1OC1C(O)C(O)C(OC)C(CO)O1 ZZSNKZQZMQGXPY-UHFFFAOYSA-N 0.000 description 1
- VZCYOOQTPOCHFL-OWOJBTEDSA-N Fumaric acid Chemical compound OC(=O)\C=C\C(O)=O VZCYOOQTPOCHFL-OWOJBTEDSA-N 0.000 description 1
- 108700012941 GNRH1 Proteins 0.000 description 1
- 229920002148 Gellan gum Polymers 0.000 description 1
- 229920002527 Glycogen Polymers 0.000 description 1
- BLCLNMBMMGCOAS-URPVMXJPSA-N Goserelin Chemical compound C([C@@H](C(=O)N[C@H](COC(C)(C)C)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NNC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 BLCLNMBMMGCOAS-URPVMXJPSA-N 0.000 description 1
- 108010069236 Goserelin Proteins 0.000 description 1
- 229920002907 Guar gum Polymers 0.000 description 1
- 239000007995 HEPES buffer Substances 0.000 description 1
- 101000904173 Homo sapiens Progonadoliberin-1 Proteins 0.000 description 1
- CPELXLSAUQHCOX-UHFFFAOYSA-N Hydrogen bromide Chemical compound Br CPELXLSAUQHCOX-UHFFFAOYSA-N 0.000 description 1
- 229920000663 Hydroxyethyl cellulose Polymers 0.000 description 1
- 239000004354 Hydroxyethyl cellulose Substances 0.000 description 1
- 229920001479 Hydroxyethyl methyl cellulose Polymers 0.000 description 1
- 206010062767 Hypophysitis Diseases 0.000 description 1
- DGAQECJNVWCQMB-PUAWFVPOSA-M Ilexoside XXIX Chemical compound C[C@@H]1CC[C@@]2(CC[C@@]3(C(=CC[C@H]4[C@]3(CC[C@@H]5[C@@]4(CC[C@@H](C5(C)C)OS(=O)(=O)[O-])C)C)[C@@H]2[C@]1(C)O)C)C(=O)O[C@H]6[C@@H]([C@H]([C@@H]([C@H](O6)CO)O)O)O.[Na+] DGAQECJNVWCQMB-PUAWFVPOSA-M 0.000 description 1
- 150000008575 L-amino acids Chemical class 0.000 description 1
- GUBGYTABKSRVRQ-QKKXKWKRSA-N Lactose Natural products OC[C@H]1O[C@@H](O[C@H]2[C@H](O)[C@@H](O)C(O)O[C@@H]2CO)[C@H](O)[C@@H](O)[C@H]1O GUBGYTABKSRVRQ-QKKXKWKRSA-N 0.000 description 1
- 235000010643 Leucaena leucocephala Nutrition 0.000 description 1
- 240000007472 Leucaena leucocephala Species 0.000 description 1
- 108010000817 Leuprolide Proteins 0.000 description 1
- NNJVILVZKWQKPM-UHFFFAOYSA-N Lidocaine Chemical compound CCN(CC)CC(=O)NC1=C(C)C=CC=C1C NNJVILVZKWQKPM-UHFFFAOYSA-N 0.000 description 1
- 208000035752 Live birth Diseases 0.000 description 1
- 239000007993 MOPS buffer Substances 0.000 description 1
- FYYHWMGAXLPEAU-UHFFFAOYSA-N Magnesium Chemical compound [Mg] FYYHWMGAXLPEAU-UHFFFAOYSA-N 0.000 description 1
- 229930195725 Mannitol Natural products 0.000 description 1
- YJPIGAIKUZMOQA-UHFFFAOYSA-N Melatonin Natural products COC1=CC=C2N(C(C)=O)C=C(CCN)C2=C1 YJPIGAIKUZMOQA-UHFFFAOYSA-N 0.000 description 1
- BYBLEWFAAKGYCD-UHFFFAOYSA-N Miconazole Chemical compound ClC1=CC(Cl)=CC=C1COC(C=1C(=CC(Cl)=CC=1)Cl)CN1C=NC=C1 BYBLEWFAAKGYCD-UHFFFAOYSA-N 0.000 description 1
- 229920000881 Modified starch Polymers 0.000 description 1
- FSVCELGFZIQNCK-UHFFFAOYSA-N N,N-bis(2-hydroxyethyl)glycine Chemical compound OCCN(CCO)CC(O)=O FSVCELGFZIQNCK-UHFFFAOYSA-N 0.000 description 1
- JOCBASBOOFNAJA-UHFFFAOYSA-N N-tris(hydroxymethyl)methyl-2-aminoethanesulfonic acid Chemical compound OCC(CO)(CO)NCCS(O)(=O)=O JOCBASBOOFNAJA-UHFFFAOYSA-N 0.000 description 1
- 229910002651 NO3 Inorganic materials 0.000 description 1
- 108010021717 Nafarelin Proteins 0.000 description 1
- 229930193140 Neomycin Natural products 0.000 description 1
- NHNBFGGVMKEFGY-UHFFFAOYSA-N Nitrate Chemical compound [O-][N+]([O-])=O NHNBFGGVMKEFGY-UHFFFAOYSA-N 0.000 description 1
- MUBZPKHOEPUJKR-UHFFFAOYSA-N Oxalic acid Chemical compound OC(=O)C(O)=O MUBZPKHOEPUJKR-UHFFFAOYSA-N 0.000 description 1
- 239000007990 PIPES buffer Substances 0.000 description 1
- 229920003171 Poly (ethylene oxide) Polymers 0.000 description 1
- 239000002202 Polyethylene glycol Substances 0.000 description 1
- 239000004372 Polyvinyl alcohol Substances 0.000 description 1
- 102100024028 Progonadoliberin-1 Human genes 0.000 description 1
- QAOWNCQODCNURD-UHFFFAOYSA-L Sulfate Chemical compound [O-]S([O-])(=O)=O QAOWNCQODCNURD-UHFFFAOYSA-L 0.000 description 1
- 101000996723 Sus scrofa Gonadotropin-releasing hormone receptor Proteins 0.000 description 1
- UZMAPBJVXOGOFT-UHFFFAOYSA-N Syringetin Natural products COC1=C(O)C(OC)=CC(C2=C(C(=O)C3=C(O)C=C(O)C=C3O2)O)=C1 UZMAPBJVXOGOFT-UHFFFAOYSA-N 0.000 description 1
- 239000007994 TES buffer Substances 0.000 description 1
- 229920002253 Tannate Polymers 0.000 description 1
- BGNXCDMCOKJUMV-UHFFFAOYSA-N Tert-Butylhydroquinone Chemical compound CC(C)(C)C1=CC(O)=CC=C1O BGNXCDMCOKJUMV-UHFFFAOYSA-N 0.000 description 1
- 239000004098 Tetracycline Substances 0.000 description 1
- 239000007997 Tricine buffer Substances 0.000 description 1
- XEFQLINVKFYRCS-UHFFFAOYSA-N Triclosan Chemical compound OC1=CC(Cl)=CC=C1OC1=CC=C(Cl)C=C1Cl XEFQLINVKFYRCS-UHFFFAOYSA-N 0.000 description 1
- 239000007983 Tris buffer Substances 0.000 description 1
- 208000034953 Twin anemia-polycythemia sequence Diseases 0.000 description 1
- LEHOTFFKMJEONL-UHFFFAOYSA-N Uric Acid Chemical compound N1C(=O)NC(=O)C2=C1NC(=O)N2 LEHOTFFKMJEONL-UHFFFAOYSA-N 0.000 description 1
- TVWHNULVHGKJHS-UHFFFAOYSA-N Uric acid Natural products N1C(=O)NC(=O)C2NC(=O)NC21 TVWHNULVHGKJHS-UHFFFAOYSA-N 0.000 description 1
- 241000251539 Vertebrata <Metazoa> Species 0.000 description 1
- FPIPGXGPPPQFEQ-BOOMUCAASA-N Vitamin A Natural products OC/C=C(/C)\C=C\C=C(\C)/C=C/C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-BOOMUCAASA-N 0.000 description 1
- 229930003268 Vitamin C Natural products 0.000 description 1
- 229930003427 Vitamin E Natural products 0.000 description 1
- HCHKCACWOHOZIP-UHFFFAOYSA-N Zinc Chemical compound [Zn] HCHKCACWOHOZIP-UHFFFAOYSA-N 0.000 description 1
- 229940022663 acetate Drugs 0.000 description 1
- 239000008186 active pharmaceutical agent Substances 0.000 description 1
- 239000000654 additive Substances 0.000 description 1
- 230000000996 additive effect Effects 0.000 description 1
- 239000002671 adjuvant Substances 0.000 description 1
- 239000008272 agar Substances 0.000 description 1
- 235000010419 agar Nutrition 0.000 description 1
- 238000005054 agglomeration Methods 0.000 description 1
- 230000002776 aggregation Effects 0.000 description 1
- 150000001298 alcohols Chemical class 0.000 description 1
- 229950010221 alexidine Drugs 0.000 description 1
- LFVVNPBBFUSSHL-UHFFFAOYSA-N alexidine Chemical compound CCCCC(CC)CNC(=N)NC(=N)NCCCCCCNC(=N)NC(=N)NCC(CC)CCCC LFVVNPBBFUSSHL-UHFFFAOYSA-N 0.000 description 1
- 229940072056 alginate Drugs 0.000 description 1
- 239000000783 alginic acid Substances 0.000 description 1
- 229960001126 alginic acid Drugs 0.000 description 1
- 229910052783 alkali metal Inorganic materials 0.000 description 1
- OENHQHLEOONYIE-UKMVMLAPSA-N all-trans beta-carotene Natural products CC=1CCCC(C)(C)C=1/C=C/C(/C)=C/C=C/C(/C)=C/C=C/C=C(C)C=CC=C(C)C=CC1=C(C)CCCC1(C)C OENHQHLEOONYIE-UKMVMLAPSA-N 0.000 description 1
- FPIPGXGPPPQFEQ-OVSJKPMPSA-N all-trans-retinol Chemical compound OC\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C FPIPGXGPPPQFEQ-OVSJKPMPSA-N 0.000 description 1
- SNAAJJQQZSMGQD-UHFFFAOYSA-N aluminum magnesium Chemical compound [Mg].[Al] SNAAJJQQZSMGQD-UHFFFAOYSA-N 0.000 description 1
- 150000001413 amino acids Chemical group 0.000 description 1
- LSQZJLSUYDQPKJ-NJBDSQKTSA-N amoxicillin Chemical compound C1([C@@H](N)C(=O)N[C@H]2[C@H]3SC([C@@H](N3C2=O)C(O)=O)(C)C)=CC=C(O)C=C1 LSQZJLSUYDQPKJ-NJBDSQKTSA-N 0.000 description 1
- 229960003022 amoxicillin Drugs 0.000 description 1
- 239000003098 androgen Substances 0.000 description 1
- 229940030486 androgens Drugs 0.000 description 1
- 229960004543 anhydrous citric acid Drugs 0.000 description 1
- 230000000843 anti-fungal effect Effects 0.000 description 1
- 229940027983 antiseptic and disinfectant quaternary ammonium compound Drugs 0.000 description 1
- 229940027991 antiseptic and disinfectant quinoline derivative Drugs 0.000 description 1
- 239000007864 aqueous solution Substances 0.000 description 1
- 229940072107 ascorbate Drugs 0.000 description 1
- 229960005070 ascorbic acid Drugs 0.000 description 1
- 239000000305 astragalus gummifer gum Substances 0.000 description 1
- 229940098164 augmentin Drugs 0.000 description 1
- 239000003855 balanced salt solution Substances 0.000 description 1
- 229910052788 barium Inorganic materials 0.000 description 1
- DSAJWYNOEDNPEQ-UHFFFAOYSA-N barium atom Chemical compound [Ba] DSAJWYNOEDNPEQ-UHFFFAOYSA-N 0.000 description 1
- 230000009286 beneficial effect Effects 0.000 description 1
- 125000003785 benzimidazolyl group Chemical group N1=C(NC2=C1C=CC=C2)* 0.000 description 1
- 229940050390 benzoate Drugs 0.000 description 1
- WPYMKLBDIGXBTP-UHFFFAOYSA-N benzoic acid Chemical compound OC(=O)C1=CC=CC=C1 WPYMKLBDIGXBTP-UHFFFAOYSA-N 0.000 description 1
- 235000013734 beta-carotene Nutrition 0.000 description 1
- 239000011648 beta-carotene Substances 0.000 description 1
- TUPZEYHYWIEDIH-WAIFQNFQSA-N beta-carotene Natural products CC(=C/C=C/C=C(C)/C=C/C=C(C)/C=C/C1=C(C)CCCC1(C)C)C=CC=C(/C)C=CC2=CCCCC2(C)C TUPZEYHYWIEDIH-WAIFQNFQSA-N 0.000 description 1
- 229960002747 betacarotene Drugs 0.000 description 1
- 239000007998 bicine buffer Substances 0.000 description 1
- 239000011230 binding agent Substances 0.000 description 1
- 230000003115 biocidal effect Effects 0.000 description 1
- 239000006177 biological buffer Substances 0.000 description 1
- 230000033228 biological regulation Effects 0.000 description 1
- 150000004287 bisbiguanides Chemical class 0.000 description 1
- 238000010241 blood sampling Methods 0.000 description 1
- 230000036760 body temperature Effects 0.000 description 1
- 230000037396 body weight Effects 0.000 description 1
- 229910021538 borax Inorganic materials 0.000 description 1
- KGBXLFKZBHKPEV-UHFFFAOYSA-N boric acid Chemical compound OB(O)O KGBXLFKZBHKPEV-UHFFFAOYSA-N 0.000 description 1
- 239000004327 boric acid Substances 0.000 description 1
- 230000001488 breeding effect Effects 0.000 description 1
- 229960003168 bronopol Drugs 0.000 description 1
- 125000000484 butyl group Chemical group [H]C([*])([H])C([H])([H])C([H])([H])C([H])([H])[H] 0.000 description 1
- 235000019282 butylated hydroxyanisole Nutrition 0.000 description 1
- 229940043253 butylated hydroxyanisole Drugs 0.000 description 1
- 235000010354 butylated hydroxytoluene Nutrition 0.000 description 1
- 229940095259 butylated hydroxytoluene Drugs 0.000 description 1
- 229910000019 calcium carbonate Inorganic materials 0.000 description 1
- 229910000389 calcium phosphate Inorganic materials 0.000 description 1
- 235000011010 calcium phosphates Nutrition 0.000 description 1
- 235000011132 calcium sulphate Nutrition 0.000 description 1
- 239000002775 capsule Substances 0.000 description 1
- 229960001631 carbomer Drugs 0.000 description 1
- 235000010948 carboxy methyl cellulose Nutrition 0.000 description 1
- 239000001768 carboxy methyl cellulose Substances 0.000 description 1
- 125000002057 carboxymethyl group Chemical group [H]OC(=O)C([H])([H])[*] 0.000 description 1
- 239000008112 carboxymethyl-cellulose Substances 0.000 description 1
- 235000021466 carotenoid Nutrition 0.000 description 1
- 150000001747 carotenoids Chemical class 0.000 description 1
- 229920003086 cellulose ether Polymers 0.000 description 1
- 229960001927 cetylpyridinium chloride Drugs 0.000 description 1
- YMKDRGPMQRFJGP-UHFFFAOYSA-M cetylpyridinium chloride Chemical compound [Cl-].CCCCCCCCCCCCCCCC[N+]1=CC=CC=C1 YMKDRGPMQRFJGP-UHFFFAOYSA-M 0.000 description 1
- 229960003260 chlorhexidine Drugs 0.000 description 1
- 229960004926 chlorobutanol Drugs 0.000 description 1
- 229960002227 clindamycin Drugs 0.000 description 1
- KDLRVYVGXIQJDK-AWPVFWJPSA-N clindamycin Chemical compound CN1C[C@H](CCC)C[C@H]1C(=O)N[C@H]([C@H](C)Cl)[C@@H]1[C@H](O)[C@H](O)[C@@H](O)[C@@H](SC)O1 KDLRVYVGXIQJDK-AWPVFWJPSA-N 0.000 description 1
- 229960004022 clotrimazole Drugs 0.000 description 1
- VNFPBHJOKIVQEB-UHFFFAOYSA-N clotrimazole Chemical compound ClC1=CC=CC=C1C(N1C=NC=C1)(C=1C=CC=CC=1)C1=CC=CC=C1 VNFPBHJOKIVQEB-UHFFFAOYSA-N 0.000 description 1
- 229940110456 cocoa butter Drugs 0.000 description 1
- 235000019868 cocoa butter Nutrition 0.000 description 1
- 229910052802 copper Inorganic materials 0.000 description 1
- 239000010949 copper Substances 0.000 description 1
- 210000004246 corpus luteum Anatomy 0.000 description 1
- 238000007405 data analysis Methods 0.000 description 1
- 230000003111 delayed effect Effects 0.000 description 1
- QSFOWAYMMZCQNF-UHFFFAOYSA-N delmopinol Chemical compound CCCC(CCC)CCCC1COCCN1CCO QSFOWAYMMZCQNF-UHFFFAOYSA-N 0.000 description 1
- 229960003854 delmopinol Drugs 0.000 description 1
- 230000001419 dependent effect Effects 0.000 description 1
- 229960005408 deslorelin Drugs 0.000 description 1
- 108700025485 deslorelin Proteins 0.000 description 1
- 239000008121 dextrose Substances 0.000 description 1
- NEFBYIFKOOEVPA-UHFFFAOYSA-K dicalcium phosphate Chemical compound [Ca+2].[Ca+2].[O-]P([O-])([O-])=O NEFBYIFKOOEVPA-UHFFFAOYSA-K 0.000 description 1
- 229910000390 dicalcium phosphate Inorganic materials 0.000 description 1
- 229940038472 dicalcium phosphate Drugs 0.000 description 1
- KCFYHBSOLOXZIF-UHFFFAOYSA-N dihydrochrysin Natural products COC1=C(O)C(OC)=CC(C2OC3=CC(O)=CC(O)=C3C(=O)C2)=C1 KCFYHBSOLOXZIF-UHFFFAOYSA-N 0.000 description 1
- 238000007865 diluting Methods 0.000 description 1
- 239000003085 diluting agent Substances 0.000 description 1
- OGGXGZAMXPVRFZ-UHFFFAOYSA-M dimethylarsinate Chemical compound C[As](C)([O-])=O OGGXGZAMXPVRFZ-UHFFFAOYSA-M 0.000 description 1
- 150000002009 diols Chemical class 0.000 description 1
- 239000007884 disintegrant Substances 0.000 description 1
- 238000004090 dissolution Methods 0.000 description 1
- 231100000673 dose–response relationship Toxicity 0.000 description 1
- 229960003722 doxycycline Drugs 0.000 description 1
- 229960003645 econazole nitrate Drugs 0.000 description 1
- 229920001971 elastomer Polymers 0.000 description 1
- 239000003995 emulsifying agent Substances 0.000 description 1
- 229940046085 endocrine therapy drug gonadotropin releasing hormone analogues Drugs 0.000 description 1
- 230000007613 environmental effect Effects 0.000 description 1
- UNXHWFMMPAWVPI-ZXZARUISSA-N erythritol Chemical compound OC[C@H](O)[C@H](O)CO UNXHWFMMPAWVPI-ZXZARUISSA-N 0.000 description 1
- 235000019414 erythritol Nutrition 0.000 description 1
- 229940009714 erythritol Drugs 0.000 description 1
- 150000002159 estradiols Chemical class 0.000 description 1
- 229940011871 estrogen Drugs 0.000 description 1
- 239000000262 estrogen Substances 0.000 description 1
- BEFDCLMNVWHSGT-UHFFFAOYSA-N ethenylcyclopentane Chemical compound C=CC1CCCC1 BEFDCLMNVWHSGT-UHFFFAOYSA-N 0.000 description 1
- DECIPOUIJURFOJ-UHFFFAOYSA-N ethoxyquin Chemical compound N1C(C)(C)C=C(C)C2=CC(OCC)=CC=C21 DECIPOUIJURFOJ-UHFFFAOYSA-N 0.000 description 1
- 235000019285 ethoxyquin Nutrition 0.000 description 1
- 229940093500 ethoxyquin Drugs 0.000 description 1
- 235000019325 ethyl cellulose Nutrition 0.000 description 1
- 229920001249 ethyl cellulose Polymers 0.000 description 1
- 238000000605 extraction Methods 0.000 description 1
- 229930003935 flavonoid Natural products 0.000 description 1
- 150000002215 flavonoids Chemical class 0.000 description 1
- 235000017173 flavonoids Nutrition 0.000 description 1
- XRECTZIEBJDKEO-UHFFFAOYSA-N flucytosine Chemical compound NC1=NC(=O)NC=C1F XRECTZIEBJDKEO-UHFFFAOYSA-N 0.000 description 1
- 229960004413 flucytosine Drugs 0.000 description 1
- 230000003325 follicular Effects 0.000 description 1
- 235000013305 food Nutrition 0.000 description 1
- WIGCFUFOHFEKBI-UHFFFAOYSA-N gamma-tocopherol Natural products CC(C)CCCC(C)CCCC(C)CCCC1CCC2C(C)C(O)C(C)C(C)C2O1 WIGCFUFOHFEKBI-UHFFFAOYSA-N 0.000 description 1
- 235000010492 gellan gum Nutrition 0.000 description 1
- 239000000216 gellan gum Substances 0.000 description 1
- 239000003349 gelling agent Substances 0.000 description 1
- 229940050410 gluconate Drugs 0.000 description 1
- 125000005456 glyceride group Chemical group 0.000 description 1
- 150000002334 glycols Chemical class 0.000 description 1
- 210000002149 gonad Anatomy 0.000 description 1
- XLXSAKCOAKORKW-UHFFFAOYSA-N gonadorelin Chemical compound C1CCC(C(=O)NCC(N)=O)N1C(=O)C(CCCN=C(N)N)NC(=O)C(CC(C)C)NC(=O)CNC(=O)C(NC(=O)C(CO)NC(=O)C(CC=1C2=CC=CC=C2NC=1)NC(=O)C(CC=1NC=NC=1)NC(=O)C1NC(=O)CC1)CC1=CC=C(O)C=C1 XLXSAKCOAKORKW-UHFFFAOYSA-N 0.000 description 1
- 229960002913 goserelin Drugs 0.000 description 1
- 239000008187 granular material Substances 0.000 description 1
- 238000000227 grinding Methods 0.000 description 1
- 239000000665 guar gum Substances 0.000 description 1
- ACGUYXCXAPNIKK-UHFFFAOYSA-N hexachlorophene Chemical compound OC1=C(Cl)C=C(Cl)C(Cl)=C1CC1=C(O)C(Cl)=CC(Cl)=C1Cl ACGUYXCXAPNIKK-UHFFFAOYSA-N 0.000 description 1
- 229960004068 hexachlorophene Drugs 0.000 description 1
- 229960004867 hexetidine Drugs 0.000 description 1
- HHXHVIJIIXKSOE-QILQGKCVSA-N histrelin Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@H](NC(=O)[C@H](CC=1C=CC(O)=CC=1)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC(N=C1)=CN1CC1=CC=CC=C1 HHXHVIJIIXKSOE-QILQGKCVSA-N 0.000 description 1
- 108700020746 histrelin Proteins 0.000 description 1
- 229960002193 histrelin Drugs 0.000 description 1
- 230000003054 hormonal effect Effects 0.000 description 1
- 239000003668 hormone analog Substances 0.000 description 1
- 229920002674 hyaluronan Polymers 0.000 description 1
- 229960003160 hyaluronic acid Drugs 0.000 description 1
- 229920001477 hydrophilic polymer Polymers 0.000 description 1
- 125000002768 hydroxyalkyl group Chemical group 0.000 description 1
- 235000019447 hydroxyethyl cellulose Nutrition 0.000 description 1
- 229920003132 hydroxypropyl methylcellulose phthalate Polymers 0.000 description 1
- 229940031704 hydroxypropyl methylcellulose phthalate Drugs 0.000 description 1
- 125000002883 imidazolyl group Chemical group 0.000 description 1
- 125000003453 indazolyl group Chemical group N1N=C(C2=C1C=CC=C2)* 0.000 description 1
- 125000000814 indol-3-yl group Chemical group [H]C1=C([H])C([H])=C2N([H])C([H])=C([*])C2=C1[H] 0.000 description 1
- 125000001041 indolyl group Chemical group 0.000 description 1
- 230000006698 induction Effects 0.000 description 1
- 238000001802 infusion Methods 0.000 description 1
- 239000004615 ingredient Substances 0.000 description 1
- QRYFGTULTGLGHU-NBERXCRTSA-N iturelix Chemical compound C([C@H](C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCCNC(C)C)C(=O)N1[C@@H](CCC1)C(=O)N[C@H](C)C(N)=O)NC(=O)[C@H](CCCCNC(=O)C=1C=NC=CC=1)NC(=O)[C@H](CO)NC(=O)[C@@H](CC=1C=NC=CC=1)NC(=O)[C@@H](CC=1C=CC(Cl)=CC=1)NC(=O)[C@@H](CC=1C=C2C=CC=CC2=CC=1)NC(C)=O)CCCNC(=O)C1=CC=CN=C1 QRYFGTULTGLGHU-NBERXCRTSA-N 0.000 description 1
- 108010083551 iturelix Proteins 0.000 description 1
- 210000004731 jugular vein Anatomy 0.000 description 1
- 229960000318 kanamycin Drugs 0.000 description 1
- 229930027917 kanamycin Natural products 0.000 description 1
- SBUJHOSQTJFQJX-NOAMYHISSA-N kanamycin Chemical compound O[C@@H]1[C@@H](O)[C@H](O)[C@@H](CN)O[C@@H]1O[C@H]1[C@H](O)[C@@H](O[C@@H]2[C@@H]([C@@H](N)[C@H](O)[C@@H](CO)O2)O)[C@H](N)C[C@@H]1N SBUJHOSQTJFQJX-NOAMYHISSA-N 0.000 description 1
- 229930182823 kanamycin A Natural products 0.000 description 1
- 239000008101 lactose Substances 0.000 description 1
- GFIJNRVAKGFPGQ-LIJARHBVSA-N leuprolide Chemical compound CCNC(=O)[C@@H]1CCCN1C(=O)[C@H](CCCNC(N)=N)NC(=O)[C@H](CC(C)C)NC(=O)[C@@H](CC(C)C)NC(=O)[C@@H](NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1N=CNC=1)NC(=O)[C@H]1NC(=O)CC1)CC1=CC=C(O)C=C1 GFIJNRVAKGFPGQ-LIJARHBVSA-N 0.000 description 1
- 229960004338 leuprorelin Drugs 0.000 description 1
- 229960004194 lidocaine Drugs 0.000 description 1
- 239000003589 local anesthetic agent Substances 0.000 description 1
- 229960005015 local anesthetics Drugs 0.000 description 1
- 239000006210 lotion Substances 0.000 description 1
- 239000007937 lozenge Substances 0.000 description 1
- 229960003822 lutrelin Drugs 0.000 description 1
- 239000011777 magnesium Substances 0.000 description 1
- 229910052749 magnesium Inorganic materials 0.000 description 1
- 238000012423 maintenance Methods 0.000 description 1
- 229940049920 malate Drugs 0.000 description 1
- VZCYOOQTPOCHFL-UPHRSURJSA-N maleic acid Chemical compound OC(=O)\C=C/C(O)=O VZCYOOQTPOCHFL-UPHRSURJSA-N 0.000 description 1
- BJEPYKJPYRNKOW-UHFFFAOYSA-N malic acid Chemical compound OC(=O)C(O)CC(O)=O BJEPYKJPYRNKOW-UHFFFAOYSA-N 0.000 description 1
- 235000010355 mannitol Nutrition 0.000 description 1
- 239000000594 mannitol Substances 0.000 description 1
- 230000013011 mating Effects 0.000 description 1
- 230000035800 maturation Effects 0.000 description 1
- DRLFMBDRBRZALE-UHFFFAOYSA-N melatonin Chemical compound COC1=CC=C2NC=C(CCNC(C)=O)C2=C1 DRLFMBDRBRZALE-UHFFFAOYSA-N 0.000 description 1
- 229960003987 melatonin Drugs 0.000 description 1
- 229910052751 metal Inorganic materials 0.000 description 1
- 239000002184 metal Substances 0.000 description 1
- 150000002739 metals Chemical class 0.000 description 1
- 235000006109 methionine Nutrition 0.000 description 1
- KRCMKUNIILUXPF-UHFFFAOYSA-N methyl 4-hydroxybenzoate;sodium Chemical compound [Na].COC(=O)C1=CC=C(O)C=C1 KRCMKUNIILUXPF-UHFFFAOYSA-N 0.000 description 1
- 229960000282 metronidazole Drugs 0.000 description 1
- VAOCPAMSLUNLGC-UHFFFAOYSA-N metronidazole Chemical compound CC1=NC=C([N+]([O-])=O)N1CCO VAOCPAMSLUNLGC-UHFFFAOYSA-N 0.000 description 1
- 229960002509 miconazole Drugs 0.000 description 1
- 230000000813 microbial effect Effects 0.000 description 1
- 229960004023 minocycline Drugs 0.000 description 1
- 235000019426 modified starch Nutrition 0.000 description 1
- 229960002333 nafarelin Drugs 0.000 description 1
- RWHUEXWOYVBUCI-ITQXDASVSA-N nafarelin Chemical compound C([C@@H](C(=O)N[C@H](CC=1C=C2C=CC=CC2=CC=1)C(=O)N[C@@H](CC(C)C)C(=O)N[C@@H](CCCN=C(N)N)C(=O)N1[C@@H](CCC1)C(=O)NCC(N)=O)NC(=O)[C@H](CO)NC(=O)[C@H](CC=1C2=CC=CC=C2NC=1)NC(=O)[C@H](CC=1NC=NC=1)NC(=O)[C@H]1NC(=O)CC1)C1=CC=C(O)C=C1 RWHUEXWOYVBUCI-ITQXDASVSA-N 0.000 description 1
- 229960004927 neomycin Drugs 0.000 description 1
- 210000002569 neuron Anatomy 0.000 description 1
- MGFYIUFZLHCRTH-UHFFFAOYSA-N nitrilotriacetic acid Chemical compound OC(=O)CN(CC(O)=O)CC(O)=O MGFYIUFZLHCRTH-UHFFFAOYSA-N 0.000 description 1
- 231100000252 nontoxic Toxicity 0.000 description 1
- 230000003000 nontoxic effect Effects 0.000 description 1
- 229960000988 nystatin Drugs 0.000 description 1
- VQOXZBDYSJBXMA-NQTDYLQESA-N nystatin A1 Chemical compound O[C@H]1[C@@H](N)[C@H](O)[C@@H](C)O[C@H]1O[C@H]1/C=C/C=C/C=C/C=C/CC/C=C/C=C/[C@H](C)[C@@H](O)[C@@H](C)[C@H](C)OC(=O)C[C@H](O)C[C@H](O)C[C@H](O)CC[C@@H](O)[C@H](O)C[C@](O)(C[C@H](O)[C@H]2C(O)=O)O[C@H]2C1 VQOXZBDYSJBXMA-NQTDYLQESA-N 0.000 description 1
- 229950002404 octapinol Drugs 0.000 description 1
- 229960001774 octenidine Drugs 0.000 description 1
- SMGTYJPMKXNQFY-UHFFFAOYSA-N octenidine dihydrochloride Chemical compound Cl.Cl.C1=CC(=NCCCCCCCC)C=CN1CCCCCCCCCCN1C=CC(=NCCCCCCCC)C=C1 SMGTYJPMKXNQFY-UHFFFAOYSA-N 0.000 description 1
- 239000006186 oral dosage form Substances 0.000 description 1
- 229960003540 oxyquinoline Drugs 0.000 description 1
- 229940094443 oxytocics prostaglandins Drugs 0.000 description 1
- LSQZJLSUYDQPKJ-UHFFFAOYSA-N p-Hydroxyampicillin Natural products O=C1N2C(C(O)=O)C(C)(C)SC2C1NC(=O)C(N)C1=CC=C(O)C=C1 LSQZJLSUYDQPKJ-UHFFFAOYSA-N 0.000 description 1
- 239000006201 parenteral dosage form Substances 0.000 description 1
- 230000032696 parturition Effects 0.000 description 1
- 230000035515 penetration Effects 0.000 description 1
- 125000001997 phenyl group Chemical group [H]C1=C([H])C([H])=C(*)C([H])=C1[H] 0.000 description 1
- WVDDGKGOMKODPV-ZQBYOMGUSA-N phenyl(114C)methanol Chemical compound O[14CH2]C1=CC=CC=C1 WVDDGKGOMKODPV-ZQBYOMGUSA-N 0.000 description 1
- 229940067107 phenylethyl alcohol Drugs 0.000 description 1
- 150000003053 piperidines Chemical class 0.000 description 1
- 210000003635 pituitary gland Anatomy 0.000 description 1
- 239000004033 plastic Substances 0.000 description 1
- 229920003023 plastic Polymers 0.000 description 1
- 229920002503 polyoxyethylene-polyoxypropylene Polymers 0.000 description 1
- 229920002451 polyvinyl alcohol Polymers 0.000 description 1
- 239000001103 potassium chloride Substances 0.000 description 1
- 235000011164 potassium chloride Nutrition 0.000 description 1
- 159000000001 potassium salts Chemical class 0.000 description 1
- 239000000843 powder Substances 0.000 description 1
- 108090000765 processed proteins & peptides Proteins 0.000 description 1
- 239000000186 progesterone Substances 0.000 description 1
- 229940077150 progesterone and estrogen Drugs 0.000 description 1
- 150000003146 progesterones Chemical class 0.000 description 1
- 229940095055 progestogen systemic hormonal contraceptives Drugs 0.000 description 1
- 235000019260 propionic acid Nutrition 0.000 description 1
- WXSLOYPZKHFWII-UHFFFAOYSA-N propyl 4-hydroxybenzoate;sodium Chemical compound [Na].CCCOC(=O)C1=CC=C(O)C=C1 WXSLOYPZKHFWII-UHFFFAOYSA-N 0.000 description 1
- 150000003180 prostaglandins Chemical class 0.000 description 1
- 230000000541 pulsatile effect Effects 0.000 description 1
- 125000003226 pyrazolyl group Chemical group 0.000 description 1
- 125000004076 pyridyl group Chemical group 0.000 description 1
- 125000000714 pyrimidinyl group Chemical group 0.000 description 1
- 125000000168 pyrrolyl group Chemical group 0.000 description 1
- 150000003856 quaternary ammonium compounds Chemical class 0.000 description 1
- IUVKMZGDUIUOCP-BTNSXGMBSA-N quinbolone Chemical compound O([C@H]1CC[C@H]2[C@H]3[C@@H]([C@]4(C=CC(=O)C=C4CC3)C)CC[C@@]21C)C1=CCCC1 IUVKMZGDUIUOCP-BTNSXGMBSA-N 0.000 description 1
- MCJGNVYPOGVAJF-UHFFFAOYSA-N quinolin-8-ol Chemical compound C1=CN=C2C(O)=CC=CC2=C1 MCJGNVYPOGVAJF-UHFFFAOYSA-N 0.000 description 1
- 150000003248 quinolines Chemical class 0.000 description 1
- 125000002943 quinolinyl group Chemical group N1=C(C=CC2=CC=CC=C12)* 0.000 description 1
- 230000007115 recruitment Effects 0.000 description 1
- 239000003488 releasing hormone Substances 0.000 description 1
- 230000003362 replicative effect Effects 0.000 description 1
- 229920005989 resin Polymers 0.000 description 1
- 239000011347 resin Substances 0.000 description 1
- 229950000975 salicylanilide Drugs 0.000 description 1
- WKEDVNSFRWHDNR-UHFFFAOYSA-N salicylanilide Chemical compound OC1=CC=CC=C1C(=O)NC1=CC=CC=C1 WKEDVNSFRWHDNR-UHFFFAOYSA-N 0.000 description 1
- 229940084560 sanguinarine Drugs 0.000 description 1
- YZRQUTZNTDAYPJ-UHFFFAOYSA-N sanguinarine pseudobase Natural products C1=C2OCOC2=CC2=C3N(C)C(O)C4=C(OCO5)C5=CC=C4C3=CC=C21 YZRQUTZNTDAYPJ-UHFFFAOYSA-N 0.000 description 1
- 238000009517 secondary packaging Methods 0.000 description 1
- 239000011734 sodium Substances 0.000 description 1
- 229940083542 sodium Drugs 0.000 description 1
- 229910052708 sodium Inorganic materials 0.000 description 1
- 235000010413 sodium alginate Nutrition 0.000 description 1
- 239000000661 sodium alginate Substances 0.000 description 1
- 229940005550 sodium alginate Drugs 0.000 description 1
- WXMKPNITSTVMEF-UHFFFAOYSA-M sodium benzoate Chemical compound [Na+].[O-]C(=O)C1=CC=CC=C1 WXMKPNITSTVMEF-UHFFFAOYSA-M 0.000 description 1
- 235000010234 sodium benzoate Nutrition 0.000 description 1
- 239000004299 sodium benzoate Substances 0.000 description 1
- 229960003885 sodium benzoate Drugs 0.000 description 1
- HRZFUMHJMZEROT-UHFFFAOYSA-L sodium disulfite Chemical compound [Na+].[Na+].[O-]S(=O)S([O-])(=O)=O HRZFUMHJMZEROT-UHFFFAOYSA-L 0.000 description 1
- 229940001584 sodium metabisulfite Drugs 0.000 description 1
- 235000010262 sodium metabisulphite Nutrition 0.000 description 1
- 235000010268 sodium methyl p-hydroxybenzoate Nutrition 0.000 description 1
- 159000000000 sodium salts Chemical class 0.000 description 1
- 239000004328 sodium tetraborate Substances 0.000 description 1
- 235000010339 sodium tetraborate Nutrition 0.000 description 1
- 239000008279 sol Substances 0.000 description 1
- 239000007787 solid Substances 0.000 description 1
- 235000010199 sorbic acid Nutrition 0.000 description 1
- 239000004334 sorbic acid Substances 0.000 description 1
- 229940075582 sorbic acid Drugs 0.000 description 1
- 239000000600 sorbitol Substances 0.000 description 1
- 230000021595 spermatogenesis Effects 0.000 description 1
- 238000010561 standard procedure Methods 0.000 description 1
- 239000008107 starch Substances 0.000 description 1
- 238000003756 stirring Methods 0.000 description 1
- 229940086735 succinate Drugs 0.000 description 1
- KDYFGRWQOYBRFD-UHFFFAOYSA-L succinate(2-) Chemical compound [O-]C(=O)CCC([O-])=O KDYFGRWQOYBRFD-UHFFFAOYSA-L 0.000 description 1
- 229940124530 sulfonamide Drugs 0.000 description 1
- 239000000829 suppository Substances 0.000 description 1
- 239000002511 suppository base Substances 0.000 description 1
- 230000002459 sustained effect Effects 0.000 description 1
- 229940095064 tartrate Drugs 0.000 description 1
- 239000004250 tert-Butylhydroquinone Substances 0.000 description 1
- 235000019281 tert-butylhydroquinone Nutrition 0.000 description 1
- 210000001550 testis Anatomy 0.000 description 1
- 229960003604 testosterone Drugs 0.000 description 1
- 150000003515 testosterones Chemical class 0.000 description 1
- 229960002180 tetracycline Drugs 0.000 description 1
- 229930101283 tetracycline Natural products 0.000 description 1
- 235000019364 tetracycline Nutrition 0.000 description 1
- 150000003522 tetracyclines Chemical class 0.000 description 1
- 125000000335 thiazolyl group Chemical group 0.000 description 1
- 239000002562 thickening agent Substances 0.000 description 1
- 235000010384 tocopherol Nutrition 0.000 description 1
- 239000011732 tocopherol Substances 0.000 description 1
- 229930003799 tocopherol Natural products 0.000 description 1
- 229960001295 tocopherol Drugs 0.000 description 1
- 230000000699 topical effect Effects 0.000 description 1
- 238000012384 transportation and delivery Methods 0.000 description 1
- QORWJWZARLRLPR-UHFFFAOYSA-H tricalcium bis(phosphate) Chemical compound [Ca+2].[Ca+2].[Ca+2].[O-]P([O-])([O-])=O.[O-]P([O-])([O-])=O QORWJWZARLRLPR-UHFFFAOYSA-H 0.000 description 1
- LENZDBCJOHFCAS-UHFFFAOYSA-N tris Chemical compound OCC(N)(CO)CO LENZDBCJOHFCAS-UHFFFAOYSA-N 0.000 description 1
- 229940116269 uric acid Drugs 0.000 description 1
- 239000006213 vaginal ring Substances 0.000 description 1
- 239000000003 vaginal tablet Substances 0.000 description 1
- 235000019155 vitamin A Nutrition 0.000 description 1
- 239000011719 vitamin A Substances 0.000 description 1
- 235000019154 vitamin C Nutrition 0.000 description 1
- 239000011718 vitamin C Substances 0.000 description 1
- 235000019165 vitamin E Nutrition 0.000 description 1
- 239000011709 vitamin E Substances 0.000 description 1
- 229940046009 vitamin E Drugs 0.000 description 1
- 229940045997 vitamin a Drugs 0.000 description 1
- 229920003169 water-soluble polymer Polymers 0.000 description 1
- 239000000080 wetting agent Substances 0.000 description 1
- 235000010493 xanthan gum Nutrition 0.000 description 1
- 239000000230 xanthan gum Substances 0.000 description 1
- 229940082509 xanthan gum Drugs 0.000 description 1
- 229910052725 zinc Inorganic materials 0.000 description 1
- 239000011701 zinc Substances 0.000 description 1
- GVJHHUAWPYXKBD-IEOSBIPESA-N α-tocopherol Chemical compound OC1=C(C)C(C)=C2O[C@@](CCC[C@H](C)CCC[C@H](C)CCCC(C)C)(C)CCC2=C1C GVJHHUAWPYXKBD-IEOSBIPESA-N 0.000 description 1
- OENHQHLEOONYIE-JLTXGRSLSA-N β-Carotene Chemical compound CC=1CCCC(C)(C)C=1\C=C\C(\C)=C\C=C\C(\C)=C\C=C\C=C(/C)\C=C\C=C(/C)\C=C\C1=C(C)CCCC1(C)C OENHQHLEOONYIE-JLTXGRSLSA-N 0.000 description 1
Classifications
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61K—PREPARATIONS FOR MEDICAL, DENTAL OR TOILETRY PURPOSES
- A61K38/00—Medicinal preparations containing peptides
- A61K38/04—Peptides having up to 20 amino acids in a fully defined sequence; Derivatives thereof
- A61K38/08—Peptides having 5 to 11 amino acids
- A61K38/09—Luteinising hormone-releasing hormone [LHRH], i.e. Gonadotropin-releasing hormone [GnRH]; Related peptides
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P15/00—Drugs for genital or sexual disorders; Contraceptives
- A61P15/08—Drugs for genital or sexual disorders; Contraceptives for gonadal disorders or for enhancing fertility, e.g. inducers of ovulation or of spermatogenesis
-
- A—HUMAN NECESSITIES
- A61—MEDICAL OR VETERINARY SCIENCE; HYGIENE
- A61P—SPECIFIC THERAPEUTIC ACTIVITY OF CHEMICAL COMPOUNDS OR MEDICINAL PREPARATIONS
- A61P5/00—Drugs for disorders of the endocrine system
- A61P5/02—Drugs for disorders of the endocrine system of the hypothalamic hormones, e.g. TRH, GnRH, CRH, GRH, somatostatin
-
- A—HUMAN NECESSITIES
- A01—AGRICULTURE; FORESTRY; ANIMAL HUSBANDRY; HUNTING; TRAPPING; FISHING
- A01K—ANIMAL HUSBANDRY; AVICULTURE; APICULTURE; PISCICULTURE; FISHING; REARING OR BREEDING ANIMALS, NOT OTHERWISE PROVIDED FOR; NEW BREEDS OF ANIMALS
- A01K2227/00—Animals characterised by species
- A01K2227/10—Mammal
- A01K2227/108—Swine
Landscapes
- Health & Medical Sciences (AREA)
- Life Sciences & Earth Sciences (AREA)
- Animal Behavior & Ethology (AREA)
- Veterinary Medicine (AREA)
- Reproductive Health (AREA)
- Chemical & Material Sciences (AREA)
- Endocrinology (AREA)
- Engineering & Computer Science (AREA)
- Medicinal Chemistry (AREA)
- Public Health (AREA)
- General Health & Medical Sciences (AREA)
- Pharmacology & Pharmacy (AREA)
- Bioinformatics & Cheminformatics (AREA)
- Organic Chemistry (AREA)
- Nuclear Medicine, Radiotherapy & Molecular Imaging (AREA)
- General Chemical & Material Sciences (AREA)
- Chemical Kinetics & Catalysis (AREA)
- Epidemiology (AREA)
- Proteomics, Peptides & Aminoacids (AREA)
- Immunology (AREA)
- Gastroenterology & Hepatology (AREA)
- Gynecology & Obstetrics (AREA)
- Diabetes (AREA)
- Pregnancy & Childbirth (AREA)
- Medicines That Contain Protein Lipid Enzymes And Other Medicines (AREA)
- Peptides Or Proteins (AREA)
- Environmental Sciences (AREA)
- Medicinal Preparation (AREA)
- Zoology (AREA)
- Animal Husbandry (AREA)
- Biodiversity & Conservation Biology (AREA)
- Pharmaceuticals Containing Other Organic And Inorganic Compounds (AREA)
- Fodder In General (AREA)
- Synchronisation In Digital Transmission Systems (AREA)
Abstract
Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de: administrar a la cerda primeriza una hormona de sincronización del estro; administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; e inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
Description
DESCRIPCIÓN
Método para sincronizar el tiempo de inseminación en cerdas primerizas
Campo de la invención
La invención se refiere a un método para sincronizar el tiempo de inseminación en cerdas primerizas. De manera más particular, la invención se refiere a un método para sincronizar el tiempo de inseminación en cerdas primerizas utilizando una hormona liberadora de gonadotropina y una hormona de sincronización del estro.
Antecedentes de la invención
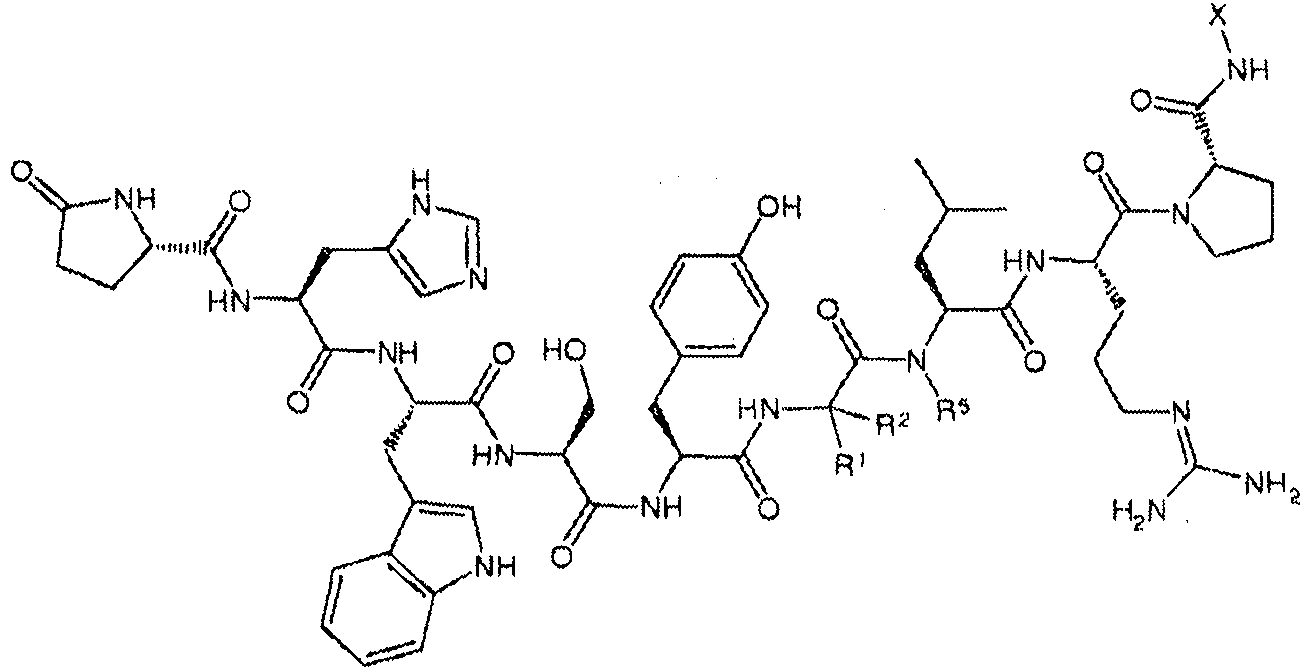
La hormona liberadora de gonadotropina es un péptido de 10 aminoácidos y también se conoce como hormona liberadora de hormona luteinizante (luteinizing-hormone releasing hormone, LHRH). La hormona liberadora de gonadotropina se produce en el hipotálamo y es responsable de la liberación de la hormona folículoestimulante (folitropina u hormona estimulante de los folículos) y de la hormona luteinizante de la glándula pituitaria. La hormona liberadora de gonadotropina se libera de las neuronas en el hipotálamo y juega un papel en la regulación compleja de la liberación de la hormona foliculoestimulante y de la hormona luteinizante. Las hormona foliculoestimulante y la hormona luteinizante, en combinación, regulan el funcionamiento de las gónadas para producir testosterona en los testículos y progesterona y estrógeno en los ovarios, y regulan la producción y maduración de los gametos. Por ejemplo, la hormona foliculoestimulante estimula el crecimiento y el reclutamiento de folículos ováricos inmaduros en el ovario, y la hormona luteinizante desencadena la ovulación.
Entre machos y hembras existen diferencias en cuanto a la secreción de la hormona liberadora de gonadotropina. En los machos, la hormona liberadora de gonadotropina se secreta en pulsos a una frecuencia constante, pero en las hembras, la frecuencia de los pulsos varía durante el ciclo estral y justo antes de la ovulación hay un gran aumento de hormona liberadora de gonadotropina. La secreción de hormona liberadora de gonadotropina es pulsátil en todos los vertebrados, y es necesaria para una correcta función reproductora. Por tanto, la hormona liberadora de gonadotropina controla un proceso de crecimiento folicular complejo, la ovulación y el mantenimiento del cuerpo lúteo en las hembras y la espermatogénesis en los machos.
La hormona liberadora de gonadotropina se ha aislado y caracterizado como un decapéptido. Se dispone de formas sintéticas de la hormona liberadora de gonadotropina y las modificaciones de la estructura decapeptídica de la hormona liberadora de gonadotropina han llevado a múltiples análogos de la hormona liberadora de gonadotropina que estimulan o suprimen la liberación de las gonadotropinas, tales como la hormona luteinizante y la hormona foliculoestimulante.
Es importante que la producción porcina comercial maximice la eficiencia reproductiva para que la producción porcina sea más rentable. Actualmente se requieren métodos laboriosos, tales como controles diarios del estro, para aumentar la probabilidad de éxito con la inseminación artificial en el ganado porcino, tal como en cerdas primerizas y cerdas adultas. Actualmente es necesario dedicar tiempo, mano de obra y costes de materiales para comprobar diariamente la detección del estro porque es difícil predecir el momento del esto (es decir, predecir el mejor momento para la inseminación) sin utilizar métodos que requieran la detección diaria del estro. En consecuencia, se necesitan métodos más sencillos, menos laboriosos, pero igualmente eficaces para optimizar el éxito de la inseminación del ganado porcino, incluyendo cerdas primerizas y cerdas adultas, para reducir los costes salariales y materiales y aumentar la rentabilidad de la producción porcina.
Las altas tasas de reposición de cerdas adultas ejercen presiones significativas sobre la gestión de la reposición de cerdas primerizas para mantener un flujo de producción porcino constante. La variación asociada al proceso de ovulación en las cerdas primerizas es uno de los problemas cruciales relacionados con la optimización del rendimiento reproductor. Por lo tanto, se necesitan tratamientos eficaces para controlar con mayor precisión la ovulación para que todas las cerdas primerizas de un grupo puedan inseminarse sin tener que controlar diariamente el estro.
MARTINAT -BOTTE F AL, THERIOGENOLOGY, 2010, 332-342 desvela la inducción y sincronización de la ovulación de cerdas nulíparas y multíparas con una inyección de agonista de la hormona liberadora de gonadotropina (Receptal)
En el documento US 2012/046519 (WEBEL, ET AL} se desvela un método para sincronizar el tiempo de inseminación en la cerda primeriza.
Sumario de la invención
Los solicitantes han descubierto tratamientos eficaces para controlar con mayor precisión la ovulación en las cerdas primerizas, de modo que las cerdas primerizas de un grupo puedan inseminarse sin tener que controlar diariamente el estro. El método descrito en el presente documento es mucho más sencillo que la detección diaria del estro, pero,
sorprendentemente, es tan eficaz como un régimen diario de control del estro, en la optimización del rendimiento reproductor de las cerdas primerizas, incluyendo, pero sin limitación, el tamaño de la camada y el total de lechones nacidos vivos.
Las realizaciones de la invención son
1. Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de:
administrar a la cerda primeriza una hormona de sincronización del estro;
administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; e
inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
2. El método según la realización 1, en donde la hormona liberadora de gonadotropina tiene la fórmula
o un solvato, un hidrato, o una sal farmacéuticamente aceptable del mismo, en donde
R1 y R2 son independientemente en cada caso hidrógeno, o se seleccionan independientemente del grupo que consiste en alquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, haloalquilo, arilo, heteroarilo, arilalquilo y heteroarilalquilo, cada uno de los cuales está opcionalmente sustituido, o R1 y R2 y el carbono unido forman un carbociclo o heterociclo;
R5 es hidrógeno o alquilo; y
X es hidrógeno, o X se selecciona del grupo que consiste en alquilo, cicloalquilo, heteroalquilo, alquilenocarboxamida opcionalmente sustituida y HNC(O)NR3R4, donde R3 y R4 en cada caso se seleccionan independientemente del grupo que consiste en hidrógeno, alquilo, heteroalquilo y haloalquilo.
3. El método según la realización 2, en donde la hormona liberadora de gonadotropina se selecciona del grupo que consiste en compuestos de la fórmula de la reivindicación 2 en donde
a) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
b) R1 es hidrógeno, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
c) R1 es 1H-1-bencil-imidazol-4-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
d) R1 es 2-metilpropilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
e) R1 es 2-naftilmetilo, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
f) R1 es t-butoximetilo, R2 es hidrógeno, X es etilo; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
g) R1 es bencilo, R2 es hidrógeno, X es CH2(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
h) R1 es t-butoximetilo, R2 es hidrógeno, X es HN(CO)NH2; y R5 es hidrógeno;
i) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
j) R1 es metilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
k) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; R5 es metilo; y la configuración del carbono al que está unido R1 es R;
l) R1 es metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
m) R1 es 4-aminobutilo, R2 es hidrógeno, X es HN(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
n) R1 es metilo, R2 es metilo, X es HN(CO)NH2 ; y R5 es hidrógeno; y
o) R1 es etilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
4. El método según una cualquiera de las realizaciones 1 a 3, en donde la inseminación es una inseminación artificial.
5. El método según una cualquiera de las realizaciones 1 a 4, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 200 |jg.
6. El método según una cualquiera de las realizaciones 1 a 5, en donde la dosis de la hormona liberadora de gonadotropina se administra utilizando un método seleccionado del grupo que consiste en el uso de un catéter de deposición, administración manual e inyección
7. El método de la realización 6, en donde la hormona liberadora de gonadotropina se administra utilizando un catéter de deposición.
8. El método de la realización 6, en donde la hormona liberadora de gonadotropina se administra por inyección. 9. El método según una cualquiera de las realizaciones 2 a 8, en donde en la fórmula X es H2CC(O)NH2 , R1 es hidrógeno y R2 es
10. El método de una cualquiera de las realizaciones 1 a 9, en donde la hormona liberadora de gonadotropina es triptorelina.
11. El método de una cualquiera de las realizaciones 1 a 10, en donde la hormona que sincroniza el estro es altrenogest.
12. El método de una cualquiera de las realizaciones 1 a 11, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende metilparabeno en una cantidad de 0,09 % en peso por volumen, propilparabeno en una cantidad de 0,01 % en peso por volumen, cloruro de sodio en una cantidad de 0,91 % en peso por volumen, citrato de sodio en una cantidad de 0,186 % en peso por volumen, L-metionina en una cantidad de 0,1 % en peso por volumen, ácido cítrico en una cantidad de 0,07 % en peso por volumen, triptorelina en una cantidad de 0,01 % en peso por volumen, y metilcelulosa en una cantidad que proporciona una viscosidad de 250 cP a 400 cP.
13. El método según una cualquiera de las realizaciones 1 a 11, en donde la hormona liberadora de gonadotropina está en un excipiente seleccionado del grupo que consiste en solución salina tamponada, un alcohol líquido, un glicol, una solución de glucosa, un éster, una amida y agua estéril y en donde el excipiente comprende además un agente tamponador de pH seleccionado del grupo que consiste en un tampón de acetato, un tampón de borato, un tampón de carbonato, un tampón de citrato, un tampón de fosfato, ácido clorhídrico, hidróxido de sodio, oxido de magnesio, fosfato monopotásico, bicarbonato, amoniaco, ácido carbónico, citrato de sodio, ácido cítrico, ácido acético e hidrogenofosfato disódico.
14. El método de una cualquiera de las realizaciones 1 a 13, en donde la hormona liberadora de gonadotropina se administra de 125 a 133 horas o de 126 a 130 horas después de la última administración diaria de la hormona de sincronización del estro.
15. El método de una cualquiera de las realizaciones 1 a 14, en donde la hormona liberadora de gonadotropina se administra 126 horas después de la última administración diaria de la hormona de sincronización del estro.
16. El método de una cualquiera de las realizaciones 1 a 15, en donde la cerda primeriza se insemina de 24 a 28 horas después de la administración de la hormona liberadora de gonadotropina.
17. El método de una cualquiera de las realizaciones 1 a 15, en donde la cerda primeriza se insemina de 20 a 24 horas después de la administración de la hormona liberadora de gonadotropina.
Breve descripción de los dibujos
La FIGURA 1 muestra el porcentaje acumulativo de cerdas primerizas, que ovularon 96 horas después de la administración de gel vehículo (VG 96) o de gel de triptorelina (TG 96), que contenía 200 |jg de triptorelina, 120 horas (TG 120) o 144 horas (TG 144) después de la última alimentación con MATRIX® en la réplica 1.
La FIGURA 2 muestra el porcentaje acumulativo de cerdas primerizas, que ovularon 96 horas después de la administración de gel vehículo (VG 96) o de gel de triptorelina (TG 96), que contenía 200 jg de triptorelina, 120 horas (TG 120) o 144 horas (TG 144) después de la última alimentación con MATRIX® en la réplica 2.
La FIGURA 3 muestra el porcentaje acumulativo de cerdas primerizas, que ovularon 96 horas después de la administración de gel vehículo (VG 96) o de gel de triptorelina (TG 96), que contenía 200 jg de triptorelina, 120 horas (TG 120) o 144 horas (Tg 144) después de la última alimentación con MATRIX® en las réplicas 1 y 2 combinadas.
La FIGURA 4 muestra el porcentaje medio acumulativo de cerdas primerizas, que ovularon después de la administración de gel vehículo o gel de triptorelina, que contenía 100, 200 o 400 mcg de triptorelina, 120 horas después de la última alimentación con MATRIX®.
Descripción detallada de las realizaciones ilustrativas
Los solicitantes han descubierto que el método descrito en el presente documento proporciona tratamientos eficaces para controlar con mayor precisión la ovulación en las cerdas primerizas, de manera que las cerdas primerizas de un grupo puedan inseminarse sin tener que controlar diariamente el estro. El método descrito en el presente documento es mucho más sencillo que la detección diaria del estro, pero, sorprendentemente, es tan eficaz para optimizar el rendimiento reproductor como lo es un régimen diario de control del estro, incluyendo, pero sin limitación, el tamaño de la camada y el total de lechones nacidos vivos.
En una realización, se proporciona un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza:
Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de:
administrar a la cerda primeriza una hormona de sincronización del estro;
administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; y
inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
Por ejemplo, las realizaciones descritas en las siguientes cláusulas, o cualquier combinación de las mismas, se contemplan para su uso en los métodos y composiciones de la invención.
1. Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de:
administrar a la cerda primeriza una hormona de sincronización del estro;
administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; y
inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
2. El método según la cláusula 1, en donde la hormona liberadora de gonadotropina tiene la fórmula
o un solvato, un hidrato, o una sal farmacéuticamente aceptable del mismo, en donde
R1 y R2 son independientemente en cada caso hidrógeno, o se seleccionan independientemente del grupo que consiste en alquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, haloalquilo, arilo, heteroarilo, arilalquilo y heteroarilalquilo, cada uno de los cuales está opcionalmente sustituido, o R1 y R2 y el carbono unido forman un carbociclo o heterociclo;
R5 es hidrógeno o alquilo; y
X es hidrógeno, o X se selecciona del grupo que consiste en alquilo, cicloalquilo, heteroalquilo, alquilenocarboxamida opcionalmente sustituida y HNC(O)NR3R4, donde R3 y R4 en cada caso se seleccionan independientemente del grupo que consiste en hidrógeno, alquilo, heteroalquilo y haloalquilo.
3. El método según la cláusula 2, en donde la hormona liberadora de gonadotropina se selecciona del grupo que consiste en compuestos de la fórmula de la reivindicación 2 en donde
a) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
b) R1 es hidrógeno, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
c) R1 es 1H-1-bencil-imidazol-4-il-metilo, R es hidrógeno, X es etilo; y R5 es hidrógeno;
d) R1 es 2-metilpropilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
e) R1 es 2-naftilmetilo, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
f) R1 es t-butoximetilo, R2 es hidrógeno, X es etilo; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
g) R1 es bencilo, R2 es hidrógeno, X es CH2(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
h) R1 es t-butoximetilo, R2 es hidrógeno, X es HN(CO)NH2; y R5 es hidrógeno;
i) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
j) R1 es metilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
k) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; R5 es metilo; y la configuración del carbono al que está unido R1 es R;
l) R1 es metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
m) R1 es 4-aminobutilo, R2 es hidrógeno, X es HN(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
n) R1 es metilo, R2 es metilo, X es HN(CO)NH2 ; y R5 es hidrógeno; y
o) R1 es etilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
4. El método según una cualquiera de las cláusulas 1 a 3, en donde la inseminación es una inseminación artificial.
5. El método según una cualquiera de las cláusulas 1 a 4, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 1 |jg a aproximadamente 500 |jg.
6. El método según una cualquiera de las cláusulas 1 a 5, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 100 jg a aproximadamente 300 jg.
7. El método según una cualquiera de las cláusulas 1 a 6, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 200 jg.
8. El método según una cualquiera de las cláusulas 1 a 7, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 50 jg/ml a aproximadamente 200 jg/ml.
9. El método según una cualquiera de las cláusulas 1 a 8, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 50 jg/ml a aproximadamente 150 jg/ml.
10. El método de una cualquiera de las cláusulas 1 a 9, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 100 jg/ml.
11. El método según una cualquiera de las cláusulas 1 a 10, en donde que la dosis de la hormona liberadora de gonadotropina se administra utilizando un método seleccionado del grupo que consiste en el uso de un catéter de deposición, administración manual e inyección.
12. El método de la cláusula 11, en donde la hormona liberadora de gonadotropina se administra utilizando un catéter de deposición.
13. El método de la cláusula 11, en donde la hormona liberadora de gonadotropina se administra por inyección. 14. El método según una cualquiera de las cláusulas 1 a 13, en donde la hormona está en forma de acetato.
15. El método según una cualquiera de las cláusulas 1 a 12 o 14, en donde la hormona se administra en una composición que comprende un gel.
16. El método según la cláusula 15, en donde el gel es un polisacárido seleccionado del grupo que consiste en celulosas, dextranos y alginatos.
17. El método según la cláusula 16, en donde el polisacárido es una celulosa y la celulosa es metilcelulosa.
18. El método de la cláusula 17, en donde el gel comprende de aproximadamente 0,5% en peso a aproximadamente 4,0 % en peso de metilcelulosa.
19. El método de la cláusula 18, en donde el gel es metilcelulosa al 1,2 %.
20. El método según la cláusula 15, en donde el gel tiene una viscosidad de aproximadamente 200 cP a aproximadamente 5000 cP.
21. El método de una cualquiera de las cláusulas 1 a 12 o 14 a 20, en donde la hormona liberadora de gonadotropina se administra por vía intravaginal.
22. El método de la cláusula 21, en donde la hormona liberadora de gonadotropina se administra en la pared anterior de la vagina.
23. El método según una cualquiera de las cláusulas 1 a 22, en donde el método da como resultado la fertilidad de la cerda primeriza.
24. El método según una cualquiera de las cláusulas 2 a 23, en donde en la fórmula X es H2CC(O)NH2, R1 es hidrógeno y R2 es
25. El método de una cualquiera de las cláusulas 1 a 24, en donde la hormona liberadora de gonadotropina es triptorelina.
26. El método de cualquiera de las cláusulas 1 a 25, en donde la hormona que sincroniza el estro es altrenogest. 27. El método según una cualquiera de las cláusulas 1 a 12 o 14 a 26, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende además un estabilizador en donde el estabilizador es L-metionina.
28. El método de una cualquiera de las cláusulas 1 a 12 o 14 a 27, en donde la hormona liberadora de gonadotropina está en una composición con un pH de aproximadamente 5 a aproximadamente 6.
29. El método de una cualquiera de las cláusulas 1 a 12 o 14 a 28, en donde la hormona liberadora de gonadotropina está en una composición que comprende además un conservante.
30. El método de la cláusula 29, en donde el conservante se selecciona del grupo que consiste en metilparabeno y propilparabeno.
31. El método de una cualquiera de las cláusulas 1 a 12 o 14 a 30, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende metilparabeno, propilparabeno, cloruro de sodio, citrato de sodio, L-metionina, ácido cítrico, triptorelina y metilcelulosa.
32. El método de la cláusula 31, en donde la composición comprende metilparabeno en una cantidad de aproximadamente 0,09 % en peso por volumen, propilparabeno en una cantidad de aproximadamente 0,01 % en peso por volumen, cloruro de sodio en una cantidad de aproximadamente 0,91 % en peso por volumen, citrato de sodio en una cantidad de aproximadamente 0,186% en peso por volumen, L-metionina en una cantidad de aproximadamente 0,1 % en peso por volumen, ácido cítrico en una cantidad de aproximadamente 0,07% en peso por volumen, triptorelina en una cantidad de aproximadamente 0,01 % en peso por volumen, y metilcelulosa en una cantidad que proporciona una viscosidad de aproximadamente 250 cP a aproximadamente 400 cP.
33. El método según una cualquiera de las cláusulas 1 a 14 o 21 a 26, en donde la hormona liberadora de gonadotropina está en un excipiente seleccionado del grupo que consiste en solución salina tamponada, un alcohol líquido, un glicol, una solución de glucosa, un éster, una amida y agua estéril.
34. El método de la cláusula 33, en donde el excipiente comprende además un agente tamponador de pH seleccionado del grupo que consiste en un tampón de acetato, un tampón de borato, un tampón de carbonato, un tampón de citrato, un tampón de fosfato, ácido clorhídrico, hidróxido de sodio, oxido de magnesio, fosfato monopotásico, bicarbonato, amoniaco, ácido carbónico, citrato de sodio, ácido cítrico, ácido acético e
hidrogenofosfato disódico.
35. El método de una cualquiera de las cláusulas 1 a 34, que comprende además la etapa de exponer la cerda primeriza a un verraco.
36. El método de una cualquiera de las cláusulas 1 a 35, en donde la hormona de sincronización del estro se administra a través de la alimentación.
37. El método de una cualquiera de las cláusulas 1 a 36, en donde la hormona liberadora de gonadotropina se administra aproximadamente 118 a aproximadamente 124 horas después de la última administración diaria de la hormona de sincronización del estro.
38. El método de una cualquiera de las cláusulas 1 a 36, en donde la hormona liberadora de gonadotropina se administra aproximadamente 124 a aproximadamente 132 horas después de la última administración diaria de la hormona de sincronización del estro.
39. El método de una cualquiera de las cláusulas 1 a 38, en donde la cerda primeriza se insemina de aproximadamente 24 a aproximadamente 28 horas después de la administración de la hormona liberadora de gonadotropina.
40. Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de:
administrar a la cerda primeriza una hormona de sincronización del estro;
administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; y
inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
41. El método según la cláusula 40, en donde la hormona liberadora de gonadotropina tiene la fórmula
o un solvato, un hidrato, o una sal farmacéuticamente aceptable del mismo, en donde
R1 y R2 son independientemente en cada caso hidrógeno, o se seleccionan independientemente del grupo que consiste en alquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, haloalquilo, arilo, heteroarilo, arilalquilo y heteroarilalquilo, cada uno de los cuales está opcionalmente sustituido, o R1 y R2 y el carbono unido forman un carbociclo o heterociclo;
R5 es hidrógeno o alquilo; y
X es hidrógeno, o X se selecciona del grupo que consiste en alquilo, cicloalquilo, heteroalquilo, alquilenocarboxamida opcionalmente sustituida y HNC(O)NR3R4 donde R3 y R4 en cada caso se seleccionan independientemente del grupo que consiste en hidrógeno, alquilo, heteroalquilo y haloalquilo.
42. El método según la cláusula 41, en donde la hormona liberadora de gonadotropina se selecciona del grupo que
consiste en compuestos de la fórmula de la reivindicación 41 en donde
a) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
b) R1 es hidrógeno, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
c) R1 es 1H-1-bencil-imidazol-4-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
d) R1 es 2-metilpropilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
e) R1 es 2-naftilmetilo, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
f) R1 es t-butoximetilo, R2 es hidrógeno, X es etilo; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
g) R1 es bencilo, R2 es hidrógeno, X es CH2(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
h) R1 es t-butoximetilo, R2 es hidrógeno, X es HN(CO)NH2; y R5 es hidrógeno;
i) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
j) R1 es metilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
k) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; R5 es metilo; y la configuración del carbono al que está unido R1 es R;
l) R1 es metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
m) R1 es 4-aminobutilo, R2 es hidrógeno, X es HN(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
n) R1 es metilo, R2 es metilo, X es HN(CO)NH2 ; y R5 es hidrógeno; y
o) R1 es etilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
43. El método según una cualquiera de las cláusulas 40 a 42, en donde la inseminación es una inseminación artificial.
44. El método según una cualquiera de las cláusulas 40 a 43, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 1 |jg a aproximadamente 500 |jg.
45. El método según una cualquiera de las cláusulas 40 a 44, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 100 jg a aproximadamente 300 jg.
46. El método según una cualquiera de las cláusulas 40 a 45, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 200 jg.
47. El método según una cualquiera de las cláusulas 40 a 46, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 50 jg/ml a aproximadamente 200 jg/ml.
48. El método según una cualquiera de las cláusulas 40 a 47, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 50 jg/ml a aproximadamente 150 jg/ml.
49. El método de una cualquiera de las cláusulas 40 a 48, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 100 jg/ml.
50. El método según una cualquiera de las cláusulas 40 a 49, en donde la dosis de la hormona liberadora de gonadotropina se administra utilizando un método seleccionado del grupo que consiste en el uso de un catéter de
deposición, administración manual e inyección.
51. El método de la cláusula 50, en donde la hormona liberadora de gonadotropina se administra utilizando un catéter de deposición.
52. El método de la cláusula 50, en donde la hormona liberadora de gonadotropina se administra por inyección. 53. El método según una cualquiera de las cláusulas 40 a 52, en donde la hormona liberadora de gonadotropina está en forma de acetato.
54. El método según una cualquiera de las cláusulas 40 a 51 o 53, en donde la hormona liberadora de gonadotropina se administra en una composición que comprende un gel.
55. El método según la cláusula 54, en donde el gel es un polisacárido seleccionado del grupo que consiste en celulosas, dextranos y alginatos.
56. El método según la cláusula 55, en donde el polisacárido es una celulosa y la celulosa es metilcelulosa.
57. El método de la cláusula 56, en donde el gel comprende de aproximadamente 0,5 % en peso a aproximadamente 4,0 % en peso de metilcelulosa.
58. El método de la cláusula 57, en donde el gel es metilcelulosa al 1,2 %.
59. El método según la cláusula 54, en donde el gel tiene una viscosidad de aproximadamente 200 cP a aproximadamente 5000 cP.
60. El método de una cualquiera de las cláusulas 40 a 51 o 53 a 59, en donde la hormona liberadora de gonadotropina se administra por vía intravaginal.
61. El método de la cláusula 60, en donde la hormona liberadora de gonadotropina se administra en la pared anterior de la vagina.
62. El método según una cualquiera de las cláusulas 40 a 61, en donde el método da como resultado la fecundidad de la cerda primeriza.
63. El método según una cualquiera de las cláusulas 41 a 62, en donde en la fórmula X es H2CC(O)NH2 , R1 es hidrógeno y R2 es
64. El método de una cualquiera de las cláusulas 40 a 63, en donde la hormona liberadora de gonadotropina es triptorelina.
65. El método de una cualquiera de las cláusulas 40 a 64, en donde la hormona que sincroniza el estro es altrenogest.
66. El método según una cualquiera de las cláusulas 40 a 51 o 53 a 65, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende además un estabilizador en donde el estabilizador es L-metionina.
67. El método de una cualquiera de las cláusulas 40 a 51 o 53 a 66, en donde la hormona liberadora de gonadotropina está en una composición con un pH de aproximadamente 5 a aproximadamente 6.
68. El método de una cualquiera de las cláusulas 40 a 51 o 53 a 67, en donde la hormona liberadora de gonadotropina está en una composición que comprende además un conservante.
69. El método de la cláusula 68, en donde el conservante se selecciona del grupo que consiste en metilparabeno y propilparabeno.
70. El método de una cualquiera de las cláusulas 40 a 51 o 53 a 69, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende metilparabeno, propilparabeno, cloruro de sodio, citrato de sodio, L-metionina, ácido cítrico, triptorelina y metilcelulosa.
71. El método de la cláusula 70, en donde la composición comprende metilparabeno en una cantidad de aproximadamente 0,09 % en peso por volumen, propilparabeno en una cantidad de aproximadamente 0,01 % en peso por volumen, cloruro de sodio en una cantidad de aproximadamente 0,91 % en peso por volumen, citrato de sodio en una cantidad de aproximadamente 0,186% en peso por volumen, L-metionina en una cantidad de aproximadamente 0,1 % en peso por volumen, ácido cítrico en una cantidad de aproximadamente 0,07% en peso por volumen, triptorelina en una cantidad de aproximadamente 0,01 % en peso por volumen, y metilcelulosa en una cantidad que proporciona una viscosidad de aproximadamente 250 cP a aproximadamente 400 cP.
72. El método según una cualquiera de las cláusulas 40 a 53 o 60 a 65, en donde la hormona liberadora de gonadotropina está en un excipiente seleccionado del grupo que consiste en solución salina tamponada, un alcohol líquido, un glicol, una solución de glucosa, un éster, una amida y agua estéril.
73. El método de la cláusula 72, en donde el excipiente comprende además un agente tamponador de pH seleccionado del grupo que consiste en un tampón de acetato, un tampón de borato, un tampón de carbonato, un tampón de citrato, un tampón de fosfato, ácido clorhídrico, hidróxido de sodio, oxido de magnesio, fosfato monopotásico, bicarbonato, amoniaco, ácido carbónico, citrato de sodio, ácido cítrico, ácido acético e hidrogenofosfato disódico.
74. El método de una cualquiera de las cláusulas 40 a 73, que comprende además la etapa de exponer la cerda primeriza a un verraco.
75. El método de una cualquiera de las cláusulas 40 a 74, en donde la hormona de sincronización del estro se administra a través de la alimentación.
76. El método de una cualquiera de las cláusulas 40 a 75, en donde la hormona liberadora de gonadotropina se administra aproximadamente 118 a aproximadamente 124 horas después de la última administración diaria de la hormona de sincronización del estro.
77. El método de una cualquiera de las cláusulas 40 a 75, en donde la hormona liberadora de gonadotropina se administra aproximadamente 124 a aproximadamente 132 horas después de la última administración diaria de la hormona de sincronización del estro.
78. El método de una cualquiera de las cláusulas 40 a 77, en donde la cerda primeriza se insemina la primera vez al cabo de aproximadamente dos horas después de la administración de la hormona liberadora de gonadotropina, si la cerda primeriza está en estro el quinto día después de la última administración diaria de la hormona de sincronización del estro.
79. El método de una cualquiera de las cláusulas 40 a 78, en donde la cerda primeriza se insemina el sexto día de aproximadamente 24 a aproximadamente 28 horas después de la administración de la hormona liberadora de gonadotropina.
80. Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de:
administrar a la cerda primeriza una hormona de sincronización del estro;
administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; y
inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
81. El método según la cláusula 80, en donde la hormona liberadora de gonadotropina tiene la fórmula
o un solvato, un hidrato, o una sal farmacéuticamente aceptable del mismo, en donde
R1 y R2 son independientemente en cada caso hidrógeno, o se seleccionan independientemente del grupo que consiste en alquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, haloalquilo, arilo, heteroarilo, arilalquilo y heteroarilalquilo, cada uno de los cuales está opcionalmente sustituido, o R1 y R2 y el carbono unido forman un carbociclo o heterociclo;
R5 es hidrógeno o alquilo; y
X es hidrógeno, o X se selecciona del grupo que consiste en alquilo, cicloalquilo, heteroalquilo, alquilenocarboxamida opcionalmente sustituida y HNC(O)NR3R4, donde R3 y R4 en cada caso se seleccionan independientemente del grupo que consiste en hidrógeno, alquilo, heteroalquilo y haloalquilo.
82. El método según la cláusula 81, en donde la hormona liberadora de gonadotropina se selecciona del grupo que consiste en compuestos de la fórmula de la reivindicación 81 en donde
a) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
b) R1 es hidrógeno, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
c) R1 es 1H-1-bencil-imidazol-4-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
d) R1 es 2-metilpropilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
e) R1 es 2-naftilmetilo, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
f) R1 es t-butoximetilo, R2 es hidrógeno, X es etilo; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
g) R1 es bencilo, R2 es hidrógeno, X es CH2(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
h) R1 es t-butoximetilo, R2 es hidrógeno, X es HN(CO)NH2; y R5 es hidrógeno;
i) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
j) R1 es metilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
k) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; R5 es metilo; y la configuración del carbono al que está unido R1 es R;
l) R1 es metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
m) R1 es 4-aminobutilo, R2 es hidrógeno, X es HN(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
n) R1 es metilo, R2 es metilo, X es HN(CO)NH2 ; y R5 es hidrógeno; y
o) R1 es etilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
83. El método según una cualquiera de las cláusulas 80 a 82, en donde la inseminación es una inseminación artificial.
84. El método según una cualquiera de las cláusulas 80 a 83, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 1 |jg a aproximadamente 500 |jg.
85. El método según una cualquiera de las cláusulas 80 a 84, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 100 jg a aproximadamente 300 jg.
86. El método según una cualquiera de las cláusulas 80 a 85, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 200 jg.
87. El método según una cualquiera de las cláusulas 80 a 86, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 50 jg/ml a aproximadamente 200 jg/ml.
88. El método según una cualquiera de las cláusulas 80 a 87, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 50 jg/ml a aproximadamente 150 jg/ml.
89. El método de una cualquiera de las cláusulas 80 a 88, en donde la hormona liberadora de gonadotropina está a una concentración de aproximadamente 100 jg/ml.
90. El método según una cualquiera de las cláusulas 80 a 89, en donde la dosis de la hormona liberadora de gonadotropina se administra utilizando un método seleccionado del grupo que consiste en el uso de un catéter de deposición, administración manual e inyección.
91. El método de la cláusula 90, en donde la hormona liberadora de gonadotropina se administra utilizando un catéter de deposición.
92. El método de la cláusula 90, en donde la hormona liberadora de gonadotropina se administra por inyección. 93. El método según una cualquiera de las cláusulas 80 a 92, donde la hormona liberadora de gonadotropina está en forma de acetato.
94. El método según una cualquiera de las cláusulas 80 a 91 o 93, en donde la hormona liberadora de gonadotropina se administra en una composición que comprende un gel.
95. El método según la cláusula 94, en donde el gel es un polisacárido seleccionado del grupo que consiste en celulosas, dextranos y alginatos.
96. El método según la cláusula 95, en donde el polisacárido es una celulosa y la celulosa es metilcelulosa.
97. El método de la cláusula 96, en donde el gel comprende de aproximadamente 0,5 % en peso a aproximadamente 4,0 % en peso de metilcelulosa.
98. El método de la cláusula 97, en donde el gel es metilcelulosa al 1,2 %.
99. El método según la cláusula 94, en donde el gel tiene una viscosidad de aproximadamente 200 cP a aproximadamente 5000 cP.
100. El método de una cualquiera de las cláusulas 90 a 91 o 93 a 99, en donde la hormona liberadora de gonadotropina se administra por vía intravaginal.
101. El método de la cláusula 100, en donde la hormona liberadora de gonadotropina se administra en la pared anterior de la vagina.
102. El método según una cualquiera de las cláusulas 80 a 101, en donde el método da como resultado la fecundidad de la cerda primeriza.
103. El método según una cualquiera de las cláusulas 81 a 102, en donde en la fórmula X es H2CC(O)NH2 , Ri es hidrógeno y R2 es
104. El método de una cualquiera de las cláusulas 80 a 103, en donde la hormona liberadora de gonadotropina es triptorelina.
105. El método de una cualquiera de las cláusulas 80 a 104, en donde la hormona que sincroniza el estro es altrenogest.
106. El método según una cualquiera de las cláusulas 80 a 91 o 93 a 105, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende además un estabilizador en donde el estabilizador es L-metionina.
107. El método de una cualquiera de las cláusulas 80 a 91 o 93 a 106, en donde la hormona liberadora de gonadotropina está en una composición con un pH de aproximadamente 5 a aproximadamente 6.
108. El método de una cualquiera de las cláusulas 80 a 91 o 93 a 107, en donde la hormona liberadora de gonadotropina está en una composición que comprende además un conservante.
109. El método de la cláusula 108, en donde el conservante se selecciona del grupo que consiste en metilparabeno y propilparabeno.
110. El método de una cualquiera de las cláusulas 80 a 91 o 93 a 109, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende metilparabeno, propilparabeno, cloruro de sodio, citrato de sodio, L-metionina, ácido cítrico, triptorelina y metilcelulosa.
111. El método de la cláusula 110, en donde la composición comprende metilparabeno en una cantidad de aproximadamente 0,09 % en peso por volumen, propilparabeno en una cantidad de aproximadamente 0,01 % en peso por volumen, cloruro de sodio en una cantidad de aproximadamente 0,91 % en peso por volumen, citrato de sodio en una cantidad de aproximadamente 0,186% en peso por volumen, L-metionina en una cantidad de aproximadamente 0,1 % en peso por volumen, ácido cítrico en una cantidad de aproximadamente 0,07% en peso por volumen, triptorelina en una cantidad de aproximadamente 0,01 % en peso por volumen, y metilcelulosa en una cantidad que proporciona una viscosidad de aproximadamente 250 cP a aproximadamente 400 cP.
112. El método según una cualquiera de las cláusulas 80 a 93 o 100 a 105, en donde la hormona liberadora de gonadotropina está en un excipiente seleccionado del grupo que consiste en solución salina tamponada, un alcohol líquido, un glicol, una solución de glucosa, un éster, una amida y agua estéril.
113. El método de la cláusula 112, en donde el excipiente comprende además un agente tamponador de pH seleccionado del grupo que consiste en un tampón de acetato, un tampón de borato, un tampón de carbonato, un tampón de citrato, un tampón de fosfato, ácido clorhídrico, hidróxido de sodio, oxido de magnesio, fosfato monopotásico, bicarbonato, amoniaco, ácido carbónico, citrato de sodio, ácido cítrico, ácido acético e hidrogenofosfato disódico.
114. El método de una cualquiera de las cláusulas 80 a 113, que comprende además la etapa de exponer la cerda primeriza a un verraco.
115. El método de una cualquiera de las cláusulas 80 a 114, en donde la hormona de sincronización del estro se administra a través de la alimentación.
116. El método de una cualquiera de las cláusulas 80 a 115, en donde la hormona liberadora de gonadotropina se administra aproximadamente 118 a aproximadamente 124 horas después de la última administración diaria de la hormona de sincronización del estro.
117. El método de una cualquiera de las cláusulas 80 a 115, en donde la hormona liberadora de gonadotropina se administra aproximadamente 124 a aproximadamente 132 horas después de la última administración diaria de la hormona de sincronización del estro.
118. El método de una cualquiera de las cláusulas 80 a 117, en donde la cerda primeriza se insemina la primera vez
aproximadamente 2 a aproximadamente 4 horas después de la administración de la hormona liberadora de gonadotropina.
119. El método de una cualquiera de las cláusulas 80 a 118, en donde la cerda primeriza se insemina la segunda vez de aproximadamente 24 a aproximadamente 28 horas después de la administración de la hormona liberadora de gonadotropina.
120. El método de una cualquiera de las cláusulas 80 a 119, en donde la cerda primeriza se insemina la primera vez aproximadamente 2 a aproximadamente 3 horas después de la administración de la hormona liberadora de gonadotropina.
121. El método de una cualquiera de las cláusulas 1 a 120, en donde el tamaño de la camada de la cerda primeriza es similar al tamaño de la camada de las cerdas primerizas de control inseminadas basándose en la detección diaria del estro.
122. El método de una cualquiera de las cláusulas 1 a 121, en donde el total de lechones nacidos vivos de la cerda primeriza, es similar al total de lechones nacidos vivos de las cerdas primerizas de control basándose en la detección diaria del estro.
Como se usa en el presente documento, "cerdas primerizas de control inseminadas basándose en la detección diaria del estro" significa cerdas primerizas inseminadas basándose en procedimientos estándar utilizados en las granjas (es decir, un régimen diario para controlar el estro) donde el estro de las cerdas primerizas se controla durante dos a ocho días o más, para predecir el momento óptimo de la inseminación. Todas las realizaciones ilustrativas, modificaciones y formas alternativas descritas a continuación, pueden aplicarse a las realizaciones descritas en los párrafos anteriores [00139] a [00264] de esta sección de la Descripción Detallada de las Realizaciones Ilustrativas y en las realizaciones descritas en el Sumario de la Invención.
Los métodos para sincronizar el tiempo de inseminación en cerdas primerizas descritos en el presente documento, incluyen la etapa de administrar a la cerda primeriza, una dosis de una hormona liberadora de gonadotropina. Según una realización, la hormona se administra a cualquier especie porcina, por ejemplo, a cerdas adultas o primerizas (es decir, a hembras de cerdo antes del primer apareamiento), incluidas cerdas primerizas tanto púberes como sexualmente maduras (es decir, que han tenido al menos un ciclo estral) o que son sexualmente inmaduras (es decir, que no ha tenido ningún ciclo estral). Los métodos descritos en el presente documento pueden dar como resultado la fecundidad de la cerda primeriza. Normalmente, los métodos descritos en el presente documento son tan eficaces para optimizar el rendimiento reproductor de las cerdas primerizas como lo es un régimen diario para controlar el estro, incluyendo, pero sin limitación, el tamaño de la camada y el total de lechones nacidos vivos.
En una realización, se proporciona un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza. El método comprende las etapas de 1) administrar a la cerda primeriza una hormona de sincronización del estro, 2) administrar a la cerda primeriza una sola dosis de una hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona de sincronización del estro y 3) inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro. De manera ilustrativa, en la realización del párrafo [00267], las cerdas primerizas reciben generalmente una sola dosis de la hormona liberadora de gonadotropina, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, el quinto día después de la última administración diaria a la cerda primeriza de una hormona de sincronización del estro (por ejemplo, altrenogest). En esta realización, la hormona liberadora de gonadotropina puede administrase, por ejemplo, por ejemplo, el cuarto día después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En otra realización ilustrativa, la hormona liberadora de gonadotropina puede administrase el quinto día después de la última administración diaria a la cerda primeriza de una hormona de sincronización del estro, por ejemplo, aproximadamente 120 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. Como se usa en el presente documento, las frases "el cuarto día después de la última administración diaria de la hormona de sincronización del estro", "el quinto día después de la última administración diaria de la hormona de sincronización del estro" y "el sexto día después de la última administración diaria de la hormona de sincronización del estro", significan el día 4, día 5 o día 6, respectivamente, después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro, en donde la última administración diaria a la cerda primeriza de la hormona de sincronización del estro es el día 0.
En la realización del párrafo [00267], la hormona liberadora de gonadotropina puede administrarse de aproximadamente 105 a aproximadamente 120, de aproximadamente 105 a aproximadamente 136, de aproximadamente 116 a aproximadamente 126, de aproximadamente 117 a aproximadamente 125, de aproximadamente 117 a aproximadamente 124, de aproximadamente 118 a aproximadamente 122, de aproximadamente 119 a aproximadamente 121 o a aproximadamente 120 horas después de la última administración
diaria a la cerda primeriza de la hormona de sincronización del estro. En realizaciones alternativas, la hormona liberadora de gonadotropina puede administrarse aproximadamente 117, aproximadamente 118, aproximadamente 119, aproximadamente 120, aproximadamente 121, aproximadamente 122, aproximadamente 123 o aproximadamente 124 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En la realización del párrafo [00267], la hormona liberadora de gonadotropina puede administrarse de aproximadamente 124 a aproximadamente 134, de aproximadamente 125 a aproximadamente 133, de aproximadamente 125 a aproximadamente 132, de aproximadamente 126 a aproximadamente 130, de aproximadamente 127 a aproximadamente 129 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En realizaciones alternativas, la hormona liberadora de gonadotropina puede administrarse aproximadamente 125, aproximadamente 126, aproximadamente 127, aproximadamente 128, aproximadamente 129, aproximadamente 130, aproximadamente 131 o aproximadamente 132 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En la realización del párrafo [00267], las cerdas primerizas que reciben tratamiento con la hormona liberadora de gonadotropina generalmente se inseminan una sola vez a las 20 horas (o 20 horas ± 2 h), 22 horas (o 22 horas ± 2 h), 23 horas (o 23 horas ± 2 h), 24 horas (o 24 horas ± 2 h), 25 horas (o 25 horas ± 2 h), 26 horas (o 26 horas ± 2 h), 27 horas (o 27 horas ± 2 h), 28 horas (o 28 horas ± 2 h), 29 horas (o 29 horas ± 2 h) o 30 horas (o 30 horas ± 2 h) después de la administración de la hormona liberadora de gonadotropina.
En la realización del párrafo [00267], la cerda joven también puede inseminarse una vez, por ejemplo, de aproximadamente 24 a aproximadamente 28 horas después de la administración de la hormona liberadora de gonadotropina. En varias realizaciones ilustrativas adicionales, la cerda primeriza se insemina de aproximadamente 22 a aproximadamente 30 horas después de la administración de la hormona liberadora de gonadotropina, de aproximadamente 10 a aproximadamente 40 horas, de aproximadamente 23 a aproximadamente 29 horas, de aproximadamente 24 a aproximadamente 27 horas o de aproximadamente 23 a aproximadamente 30 horas después de la administración de la hormona liberadora de gonadotropina. En esta realización, la cerda primeriza se insemina sin controlar el estro. Como se usa en este documento, la frase "sin controlar el estro" significa que no se realizan las pruebas, bien conocidas en la técnica, para detectar si un animal está en estro.
Se ilustra un método para sincronizar el tiempo de inseminación en una cerda primeriza. El método comprende las etapas de 1) administrar a la cerda primeriza una hormona de sincronización del estro, 2) administrar a la cerda primeriza una sola dosis de una hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde la hormona liberadora de gonadotropina se administra a la cerda primeriza el quinto día después de la última administración diaria de la hormona de sincronización del estro. 3) controlar el estro el quinto día después de la última administración diaria de la hormona de sincronización del estro, 4) después inseminar a la cerda primeriza el quinto día después de la última administración diaria de la hormona de sincronización del estro, si la cerda primeriza está en estro, en donde la cerda primeriza se insemina en combinación con la administración de la hormona liberadora de gonadotropina, y 5) si la cerda primeriza está en estro o no está en estro el quinto día después de la última administración diaria de la hormona para sincronizar el estro, inseminar a la cerda primeriza el sexto día después de la última administración diaria de la hormona de sincronización del estro, en donde el estro no se controla el sexto día después de la última administración diaria de la hormona de sincronización del estro.
De manera ilustrativa, en el párrafo [00273], las cerdas primerizas generalmente reciben una sola dosis de la hormona liberadora de gonadotropina, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, después de la última administración diaria a la cerda primeriza de una hormona para sincronizar estro (por ejemplo, altrenogest). En esta realización, la hormona liberadora de gonadotropina puede administrase, por ejemplo, por ejemplo, el cuarto día después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En otra realización ilustrativa, la hormona liberadora de gonadotropina puede administrase el quinto día después de la última administración diaria a la cerda primeriza de una hormona de sincronización del estro, por ejemplo, aproximadamente 120 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En esta realización, las frases "el cuarto día después de la última administración diaria de la hormona de sincronización del estro", "el quinto día después de la última administración diaria de la hormona de sincronización del estro" y "el sexto día después de la última administración diaria de la hormona de sincronización del estro", significan día 4, día 5 o día 6, respectivamente, después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro, en donde la última administración diaria a la cerda primeriza de la hormona de sincronización del estro es el día 0.
En el párrafo [00273], la hormona liberadora de gonadotropina puede administrarse en esta realización a aproximadamente 105 a aproximadamente 120, de aproximadamente 105 a aproximadamente 136, de aproximadamente 116 a aproximadamente 126, de aproximadamente 117 a aproximadamente 125, de aproximadamente 117 a aproximadamente 124, de aproximadamente 118 a aproximadamente 122, de aproximadamente 119 a aproximadamente 121 o a aproximadamente 120 horas después de la última administración
diaria a la cerda primeriza de la hormona de sincronización del estro. En realizaciones alternativas, la hormona liberadora de gonadotropina puede administrarse aproximadamente 117, aproximadamente 118, aproximadamente 119, aproximadamente 120, aproximadamente 121, aproximadamente 122, aproximadamente 123 o aproximadamente 124 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En el párrafo [00273], la hormona liberadora de gonadotropina puede administrarse de aproximadamente 124 a aproximadamente 134, de aproximadamente 125 a aproximadamente 133, de aproximadamente 125 a aproximadamente 132, de aproximadamente 126 a aproximadamente 130, de aproximadamente 127 a aproximadamente 129 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En realizaciones alternativas, la hormona liberadora de gonadotropina puede administrarse aproximadamente 125, aproximadamente 126, aproximadamente 127, aproximadamente 128, aproximadamente 129, aproximadamente 130, aproximadamente 131 o aproximadamente 132 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En el párrafo [00273], las cerdas primerizas que reciben tratamiento con la hormona liberadora de gonadotropina se inseminan una o dos veces. Las cerdas primerizas pueden inseminarse en combinación con la administración de la hormona liberadora de gonadotropina, si la cerda primeriza está en estro el quinto día después de la última administración diaria de la hormona de sincronización del estro (por ejemplo, altrenogest). Como se usa en el presente documento, "en combinación con la administración de la hormona liberadora de gonadotropina" significa que la cerda primeriza se insemina el quinto día después de la última administración diaria de la hormona de sincronización del estro y que la hormona liberadora de gonadotropina se administra a la cerda primeriza el mismo día (es decir, el quinto día). La inseminación y la administración de la hormona liberadora de gonadotropina a la cerda primeriza pueden realizarse en cualquier orden. Por ejemplo, la cerda primeriza puede inseminarse la mañana del quinto día después de la última administración diaria de la hormona de sincronización del estro, y la hormona liberadora de gonadotropina puede administrarse a la cerda primeriza en cualquier momento a partir del quinto día. En esta realización, la hormona liberadora de gonadotropina se administra preferentemente a la cerda primeriza al menos dos horas después de su inseminación. En otra realización, la hormona liberadora de gonadotropina puede administrarse primero a la cerda primeriza, por ejemplo, la mañana del quinto día después de la última administración diaria de la hormona de sincronización del estro. Después, la cerda primeriza puede inseminarse en cualquier momento a partir del quinto día después de que se la haya inseminado la hormona liberadora de gonadotropina. En esta realización, la cerda primeriza se insemina preferentemente al menos dos horas después de que se la haya administrado la hormona liberadora de gonadotropina. En varias otras realizaciones, la cerda primeriza se insemina aproximadamente en las dos horas siguientes al momento en que se administra la hormona liberadora de gonadotropina. Por ejemplo, la inseminación puede realizarse aproximadamente en los 10 minutos, 20 minutos, 30 minutos, 45 minutos, 60 minutos, 75 minutos o 120 minutos siguientes al momento en que se administra la hormona liberadora de gonadotropina, independientemente del orden de inseminación de la cerda primeriza y de la administración de la hormona liberadora de gonadotropina a la cerda primeriza.
En consecuencia, en el párrafo [00273], la inseminación el quinto día puede realizarse de aproximadamente 108 a aproximadamente 120, de aproximadamente 108 a aproximadamente 132, de aproximadamente 116 a aproximadamente 126, de aproximadamente 117 a aproximadamente 125, de aproximadamente 117 a aproximadamente 124, de aproximadamente 118 a aproximadamente 122, de aproximadamente 119 a aproximadamente 121 o a aproximadamente 120 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En otras realizaciones ilustrativas, la inseminación el quinto día puede realizarse de aproximadamente 124 a aproximadamente 134, de aproximadamente 125 a aproximadamente 133, de aproximadamente 125 a aproximadamente 132, de aproximadamente 126 a aproximadamente 130, de aproximadamente 127 a aproximadamente 129 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En la realización del párrafo [00273], las cerdas primerizas se inseminan el sexto día 22 horas (o 22 horas ± 2 h), 23 horas (o 23 horas ± 2 h), 24 horas (o 24 horas ± 2 h), 25 horas (o 25 horas ± 2 h), 26 horas (o 26 horas ± 2 h), 27 horas (o 27 horas ± 2 h), 28 horas (o 28 horas ± 2 h), 29 horas (o 29 horas ± 2 h) o 30 horas (o 30 horas ± 2 h) después de la administración de la hormona liberadora de gonadotropina.
En el párrafo [00273], la cerda primeriza puede inseminarse el sexto día después de la última administración diaria de la hormona de sincronización del estro, por ejemplo, de aproximadamente 24 a aproximadamente 28 horas después de la administración de la hormona liberadora de gonadotropina. En varias realizaciones ilustrativas adicionales, la cerda primeriza se insemina el sexto día después de la última administración diaria de la hormona de sincronización del estro de aproximadamente 22 a aproximadamente 30 horas después de la administración de la hormona liberadora de gonadotropina, de aproximadamente 10 a aproximadamente 40 horas, de aproximadamente 23 a aproximadamente 29 horas, de aproximadamente 24 a aproximadamente 27 horas o de aproximadamente 23 a aproximadamente 30 horas después de la administración de la hormona liberadora de gonadotropina. En esta realización, si la cerda primeriza está en estro (es decir, el estro se controla el quinto día después de la última administración diaria de la hormona para sincronizar el estro) la cerda primeriza se insemina el quinto día después de la última administración diaria de la hormona de sincronización del estro. La cerda primeriza se insemina el sexto
día después de la última administración diaria de la hormona de sincronización del estro sin controlar el estro.
Se ilustra un método para sincronizar el tiempo de inseminación en una cerda primeriza. El método comprende las etapas de 1) administrar a la cerda primeriza una hormona de sincronización del estro, 2) administrar a la cerda primeriza una sola dosis de una hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro, 3) inseminar a la cerda primeriza por primera vez de aproximadamente 2 a aproximadamente 7 horas después de la administración de la hormona liberadora de gonadotropina y 4) inseminar a la cerda primeriza una segunda vez el sexto día después de la última administración diaria de la hormona de sincronización del estro, en donde la primera y la segunda inseminaciones se realizan sin controlar el estro.
De manera ilustrativa, en el párrafo [00281], las cerdas primerizas generalmente reciben una sola dosis de la hormona liberadora de gonadotropina, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, el quinto día después de la última administración diaria a la cerda primeriza de una hormona de sincronización del estro (por ejemplo, altrenogest). En esta realización, la hormona liberadora de gonadotropina puede administrase, por ejemplo, por ejemplo, el cuarto día después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En otra realización ilustrativa, la hormona liberadora de gonadotropina puede administrase el quinto día después de la última administración diaria a la cerda primeriza de una hormona de sincronización del estro, por ejemplo, aproximadamente 120 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En esta realización, las frases "el cuarto día después de la última administración diaria de la hormona de sincronización del estro", "el quinto día después de la última administración diaria de la hormona de sincronización del estro" y "el sexto día después de la última administración diaria de la hormona de sincronización del estro", significan día 4, día 5 o día 6, respectivamente, después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro, en donde la última administración diaria a la cerda primeriza de la hormona de sincronización del estro es el día 0.
En el párrafo [00281], la hormona liberadora de gonadotropina puede administrarse en esta realización a aproximadamente 105 a aproximadamente 120, de aproximadamente 105 a aproximadamente 136, de aproximadamente 116 a aproximadamente 126, de aproximadamente 117 a aproximadamente 125, de aproximadamente 117 a aproximadamente 124, de aproximadamente 118 a aproximadamente 122, de aproximadamente 119 a aproximadamente 121 o a aproximadamente 120 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En realizaciones alternativas, la hormona liberadora de gonadotropina puede administrarse aproximadamente 117, aproximadamente 118, aproximadamente 119, aproximadamente 120, aproximadamente 121, aproximadamente 122, aproximadamente 123 o aproximadamente 124 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En el párrafo [00281], la hormona liberadora de gonadotropina puede administrarse de aproximadamente 124 a aproximadamente 134, de aproximadamente 125 a aproximadamente 133, de aproximadamente 125 a aproximadamente 132, de aproximadamente 126 a aproximadamente 130, de aproximadamente 127 a aproximadamente 129 o aproximadamente 128 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro. En realizaciones alternativas, la hormona liberadora de gonadotropina puede administrarse aproximadamente 125, aproximadamente 126, aproximadamente 127, aproximadamente 128, aproximadamente 129, aproximadamente 130, aproximadamente 131 o aproximadamente 132 horas después de la última administración diaria a la cerda primeriza de la hormona de sincronización del estro.
En el párrafo [00281], las cerdas primerizas que reciben tratamiento con la hormona liberadora de gonadotropina normalmente se inseminan dos veces. Las cerdas primerizas se inseminan por primera vez aproximadamente de 2 horas a aproximadamente 8 horas después de la administración de la hormona liberadora de gonadotropina o aproximadamente de 2 horas a aproximadamente 14 horas después de la administración de la hormona liberadora de gonadotropina. En otras realizaciones, la primera inseminación puede realizarse de aproximadamente 2 horas a aproximadamente 7 horas, de aproximadamente 2 horas a aproximadamente 6 horas, de aproximadamente 2 horas a aproximadamente 5 horas o de aproximadamente 2 horas a aproximadamente 4 horas después de la administración de la hormona liberadora de gonadotropina.
En el párrafo [00281], las cerdas primerizas se inseminan una segunda vez a las 22 horas (o 22 horas ± 2 h), 23 horas (o 23 horas ± 2 h), 24 horas (o 24 horas ± 2 h), 25 horas (o 25 horas ± 2 h), 26 horas (o 26 horas ± 2 h), 27 horas (o 27 horas ± 2 h), 28 horas (o 28 horas ± 2 h), 29 horas (o 29 horas ± 2 h) o 30 horas (o 30 horas ± 2 h) después de la administración de la hormona liberadora de gonadotropina.
En el párrafo [00281], la cerda primeriza también puede inseminarse la segunda vez, por ejemplo, de aproximadamente 24 a aproximadamente 28 horas después de la administración de la hormona liberadora de gonadotropina. En varias realizaciones ilustrativas adicionales, la cerda primeriza se insemina la segunda vez aproximadamente de 22 a 30 horas después de la administración de la hormona liberadora de gonadotropina, de
aproximadamente 10 a aproximadamente 40 horas, de aproximadamente 23 a aproximadamente 29 horas, de aproximadamente 24 a aproximadamente 27 horas o de aproximadamente 23 a aproximadamente 30 horas después de la administración de la hormona liberadora de gonadotropina. En esta realización, la cerda primeriza se insemina la primera y segunda vez sin controlar el estro. Como se usa en el presente documento, la frase "sin controlar el estro" significa que no se realizan pruebas, bien conocidas en la técnica, para detectar si un animal está en estro. Cualquiera de las realizaciones descritas a continuación, son aplicables a cualquiera de las realizaciones descritas anteriormente. Cualquiera de las realizaciones descritas a continuación, incluyendo cualquiera de las realizaciones de la hormona liberadora de gonadotropina y cualquier método de administración (por ejemplo, inyección o administración intravaginal en una composición de gel descrita en el presente documento), también son aplicables a un método para sincronizar el tiempo de inseminación en una cerda adulta, excepto cuando las realizaciones se limiten específicamente a cerdas primerizas.
La reproducción del animal puede ser por cualquier medio, incluida la inseminación artificial (IA), o a través de reproducción natural. En cualquier realización descrita en el presente documento, puede realizarse una segunda reproducción o reproducciones posteriores (por ejemplo, inseminación artificial). En otra realización más, la cerda adulta se insemina artificialmente solo una vez. En otro aspecto ilustrativo, no hay detección del estro (es decir, control del estro). En otra realización ilustrativa, los métodos descritos en el presente documento pueden comprender además la etapa de exponer la cerda primeriza o la cerda adulta a un verraco durante el proceso de control del estro para establecer el momento de la inseminación artificial.
En cualquier realización descrita en el presente documento, las composiciones para sincronizar el tiempo de inseminación en un porcino comprenden: a) una hormona liberadora de gonadotropina; y b) un agente tamponador de pH farmacéuticamente aceptable, para proporcionar un pH en el intervalo de pH de aproximadamente 4 a aproximadamente 9. El pH de la composición descrita puede variar de aproximadamente 4 a aproximadamente 9. En otras realizaciones, el pH puede variar de aproximadamente 4 a aproximadamente 8, de aproximadamente 4 a aproximadamente 7, de aproximadamente 4,5 a aproximadamente 6,5, de aproximadamente 4,5 a aproximadamente 6 o de aproximadamente 5 a aproximadamente 6.
Además, las composiciones de la hormona liberadora de gonadotropina pueden producirse, según la forma farmacéutica, a través de un método habitual mezclando con, diluyendo con o disolviendo en, adecuadamente, un aditivo, tal como varios excipientes, disgregantes, aglutinantes, sales, lubricantes, anestésicos locales (por ejemplo, lidocaína), diluyentes, conservantes, agentes quelantes, tampones, agentes de tonicidad, agentes antisépticos, agentes humectantes, emulsionantes, dispersantes, estabilizantes, un adyuvante en solución, o combinaciones de los mismos.
De manera ilustrativa, las composiciones que comprenden la hormona liberadora de gonadotropina pueden estar en forma de un gel y la composición puede tener, por ejemplo, una viscosidad de aproximadamente 10 cP (centipoise) a aproximadamente 300000 cP. En varias realizaciones ilustrativas, la viscosidad de la composición puede ser de aproximadamente 100 cP a aproximadamente 100000 cP, de aproximadamente 250 cP a aproximadamente 400 cP, de aproximadamente 300 cP a aproximadamente 400 cP, de aproximadamente 500 cP a aproximadamente 100.000 cP, de aproximadamente 700 cP a aproximadamente 100.000 cP, de aproximadamente 200 cP a aproximadamente 20.000 cP, de aproximadamente 200 cP a aproximadamente 10.000 cP, de aproximadamente 200 cP a aproximadamente 5.000 cP, de aproximadamente 200 a aproximadamente 1000 cP, de aproximadamente 200 cP a aproximadamente 600 cP, de aproximadamente 100 cP a aproximadamente 600 cP, de aproximadamente 100 cP a aproximadamente 500 cP, de aproximadamente 200 cP a aproximadamente 500 cP, de aproximadamente 200 cP a aproximadamente 450 cP o de aproximadamente 100000 cP a aproximadamente 250000 cP. Según varias realizaciones descritas en el presente documento, la viscosidad de la composición puede ser de aproximadamente 200 cP, de aproximadamente 250 cP, de aproximadamente 300 cP, de aproximadamente 400 cP, de aproximadamente 500 cP, de aproximadamente 1000 cP, de aproximadamente 15000 cP, de aproximadamente 20 000 cP, de aproximadamente 30000 cP, de aproximadamente 40000 cP, de aproximadamente 50000 cP, de aproximadamente 75000 cP, de aproximadamente 100000 cP, de aproximadamente 200000 cP o de aproximadamente 300000 cP. La viscosidad de una solución puede medirse utilizando un viscosímetro, tal como un reómetro, basándose en técnicas bien conocidas en la materia. El término gel incluye soluciones viscosas que no están solidificadas.
Normalmente, los geles, como los descritos en el presente documento, comprenden de aproximadamente 0,001 a aproximadamente 3,0% en peso/peso (p/p) de la hormona liberadora de gonadotropina o de una sal de la misma, más normalmente de aproximadamente 0,5-5,0 % (p/p) o de aproximadamente 0,1-5,0% (p/p) de la hormona liberadora de gonadotropina o de una sal de la misma, un conservante, un gel (es decir, un agente modificador de la viscosidad tal como metilcelulosa), un tampón para mantener un pH entre aproximadamente 5 y aproximadamente 6, y un agente de tonicidad para mantener una tonicidad entre aproximadamente 200 y aproximadamente 400 mOsm/kg.
Según cualquier realización descrita en el presente documento, la composición es suficientemente viscosa de tal manera que la composición puede adherirse al tejido diana (por ejemplo, tejido vaginal) durante un tiempo suficiente
para suministrar una cantidad eficaz de la hormona liberadora de gonadotropina a la cerda primeriza o adulta. La viscosidad típica dependerá de factores tales como, por ejemplo, la tasa de penetración de la hormona liberadora de gonadotropina y de la cantidad de hormona liberadora de gonadotropina que se aplique. Los agentes moduladores de la viscosidad adecuados incluyen, pero sin limitación, polímeros hidrosolubles iónicos y no iónicos; polímeros de ácido acrílico reticulados; polímeros hidrófilos tales como óxidos de polietileno, copolímeros de polioxietilenopolioxipropileno y alcohol polivinílico; polímeros celulósicos y derivados de polímeros celulósicos tales como hidroxipropilcelulosa, hidroxietilcelulosa, hidroxipropilmetilcelulosa, ftalato de hidroxipropilmetilcelulosa, metilcelulosa, carboximetilcelulosa y celulosa eterificada; gomas tales como goma de tragacanto y xantana; alginato de sodio; gelatina, ácido hialurónico y sus sales, quitosano, goma gellan o cualquier combinación de los mismos.
El agente modulador de la viscosidad puede estar en forma de gel, pasta, crema, pomada y similares. En una realización, la composición comprende una hormona liberadora de gonadotropina y un gel (por ejemplo, para formar una solución viscosa), como agente modificador de la viscosidad, y la hormona liberadora de gonadotropina se administra en la composición que comprende el gel. En una realización, el gel es un hidrogel, un lipogel o un sol viscoso. En otra realización, el gel es un hidrogel. El gel puede prepararse utilizando cualquier método conocido en la técnica, tal como, por ejemplo, los métodos descritos en las patentes de Estados Unidos N°6908623 y 7456207.
En cualquier realización descrita en el presente documento, el gel (es decir, un agente modificador de la viscosidad) comprende un polisacárido. Según los métodos y las composiciones descritos en el presente documento, el polisacárido puede incluir, por ejemplo, alginatos y glucosa, tales como glucógenos, almidones (p. ej., amilosa y amilopectina), celulosas y dextranos. El polisacárido puede ser, por ejemplo, un éster de metil, etil o propil celulosa, éter, hidroxiéter, hidroxialquilo o hidroxiester. Para conseguir la viscosidad deseada, puede utilizarse una cantidad suficiente de uno o más polisacáridos. Normalmente, de aproximadamente 0,25 a aproximadamente 10% en peso de polisacárido (basándose en el peso total de la composición). En otra realización, el % en peso del polisacárido es de aproximadamente 0,25% en peso a aproximadamente 3,0% en peso, de aproximadamente 1,0% en peso a aproximadamente 7% en peso, de aproximadamente 1,0% en peso a aproximadamente 4,0% en peso o de aproximadamente 1,0% en peso a aproximadamente 2,0% en peso. En otras realizaciones, el % en peso del polisacárido es de aproximadamente 0,1 %, aproximadamente 0,5%, aproximadamente 0,75%, aproximadamente 0,8%, aproximadamente 0,9%, aproximadamente 1,0%, aproximadamente 1,1%, aproximadamente 1,2%, aproximadamente 1,4%, aproximadamente 1,8%, aproximadamente 2,0%, aproximadamente 5%, aproximadamente 8% o aproximadamente 10% (todo en peso/peso). Para aumentar la viscosidad de la composición, el polisacárido puede utilizarse junto con uno o más viscosificadores no polisacarídicos conocidos en la técnica. Los ejemplos de viscosificadores no polisacarídicos que se pueden utilizarse junto con uno o más polisacáridos incluyen goma xantana, ácidos algínicos y sus sales, silicato de aluminio y magnesio, dextrinas, sacarosa y sus derivados, y sus mezclas. La cantidad de viscosificador no polisacarídico, si está presente, puede ser de aproximadamente 0,1 % en peso a aproximadamente 10 % en peso, dependiendo de la viscosidad deseada.
En cualquier realización descrita en el presente documento, el gel puede comprender una celulosa. Las realizaciones ilustrativas de la celulosa, como se describe en el presente documento, incluyen metilcelulosa, etilcelulosa, hidroxipropilcelulosa, carbometilcelulosa, hidroxipropilmetilcelulosa e hidroxietilmetilcelulosa. La celulosa puede ser un derivado de celulosa, preferentemente un éster, éter, hidroxiéter o hidroxiéster de celulosa no iónico, o un derivado de almidón no iónico. Normalmente, es deseable de aproximadamente 0,25 % en peso a aproximadamente 10 % en peso de la celulosa (basándose en el peso total de la composición). En otra realización, el % en peso de la celulosa es de aproximadamente 0,25% en peso a aproximadamente 3,0% en peso, de aproximadamente 0,5 % en peso a aproximadamente 3,0 % en peso, de aproximadamente 0,5 % en peso a aproximadamente 4,0% en peso, de aproximadamente 1,0% en peso a aproximadamente 7% en peso, de aproximadamente 1,0% en peso a aproximadamente 4,0% en peso o de aproximadamente 1,0% en peso a aproximadamente 2,0 % en peso. En otras realizaciones, el % en peso de la celulosa es de aproximadamente 0,1 %, aproximadamente 0,5 %, aproximadamente 0,75 %, aproximadamente 0,8 %, aproximadamente 0,9 %, aproximadamente 1,0%, aproximadamente 1,1%, aproximadamente 1,2%, aproximadamente 1,4%, aproximadamente 1,8%, aproximadamente 2,0%, aproximadamente 5%, aproximadamente 8% o aproximadamente 10% (todo en peso/peso). Si se desea un gel uniforme, pueden añadirse agentes dispersantes tales como alcohol, sorbitol o glicerina, o el agente gelificante se puede dispersar por trituración, mezcla mecánica, o agitación, o combinaciones de los mismos.
Los estabilizadores aceptables para su uso en las composiciones para los métodos descritos en el presente documento incluyen, un L-aminoácido, tal como una L-metionina. En otras realizaciones, los estabilizadores que pueden utilizarse incluyen, pero sin limitación, polisacáridos tales como la goma arábiga, agar, ácido algínico, goma guar y tragacanto, gelatina y polímeros sintéticos y semisintéticos tales como resinas de carbómero, éteres de celulosa y carboximetil quitina. El estabilizador está generalmente en una cantidad de aproximadamente 0,05 a aproximadamente 10 %, de aproximadamente 0,05 a aproximadamente 5 %, de aproximadamente 0,05 a aproximadamente 2,0%, de aproximadamente 0,05 a aproximadamente 1,0%, de aproximadamente 0,05 a aproximadamente 0,5 %, de aproximadamente 0,05 a aproximadamente 0,2 %, de aproximadamente 0,1 a aproximadamente 5%, de aproximadamente 0,1 a aproximadamente 10%, de aproximadamente 0,1 a aproximadamente 20 %, de aproximadamente 1 a aproximadamente 5 %, de aproximadamente 1 a aproximadamente 10 %, de aproximadamente 1 a aproximadamente 20 % (todo en peso/volumen). En una
realización, en presencia de un estabilizador como se describe en el presente documento, el periodo de validez de la composición puede ser de al menos 12 meses, al menos 18 meses o al menos 24 meses. En otra realización, la composición puede conservarse a temperaturas que varían de aproximadamente 2° C a aproximadamente 8° C. También pueden incluirse transportadores inertes tales como lactosa, almidón, dextrina, fosfato dicálcico y sulfato de calcio. En una realización que incluye un estabilizador, la composición es químicamente estable y permanece al menos 97 %, al menos 98 %, al menos 99 % pura, al menos 99,5 % pura o al menos 99,7 % pura, durante al menos tres meses.
El agente de tonicidad puede ser no iónico o iónico. De manera ilustrativa, los agentes de tonicidad aceptables para su uso en las composiciones para los métodos descritos en el presente documento incluyen, por ejemplo, agentes iónicos tales como cloruro de sodio, cloruro de potasio, o una solución salina equilibrada. Según una realización, el agente de tonicidad está presente en una cantidad para conseguir una tonicidad de entre aproximadamente 200 400 mOsm/kg, aproximadamente 220-380 mOsm/kg o aproximadamente 250-340 mOsm/kg. Los agentes de tonicidad no iónicos incluyen dioles, tales como glicerol, manitol, eritritol, polietilenglicol, propilenglicol; y azúcares tales como sacarosa y dextrosa. El agente de tonicidad generalmente está en una cantidad de aproximadamente 0,05 a aproximadamente 10%, de aproximadamente 0,05 a aproximadamente 5%, de aproximadamente 0,05 a aproximadamente 2,0%, de aproximadamente 0,05 a aproximadamente 1,0%, de aproximadamente 0,05 a aproximadamente 0,5 %, de aproximadamente 0,05 a aproximadamente 0,2 %, de aproximadamente 0,1 a aproximadamente 5%, de aproximadamente 0,1 a aproximadamente 10%, de aproximadamente 0,1 a aproximadamente 20 %, de 0,5 a aproximadamente 2,0 %, de aproximadamente 0,6 a aproximadamente 2,0 %, de aproximadamente 0,5 a aproximadamente 1,8%, de aproximadamente 0,6 a aproximadamente 1,8%, de aproximadamente 1,0 a aproximadamente 5,0%, de aproximadamente 1,0 a aproximadamente 10% o de aproximadamente 1,0 a aproximadamente 20 % (todo en peso/volumen).
En cualquier realización descrita en el presente documento, los agentes tamponadores de pH para su uso en las composiciones de los métodos descritos en el presente documento, son aquellos agentes que los expertos en la materia saben que son agentes o composiciones tamponantes de pH e incluyen, por ejemplo, tampones de acetato, borato, carbonato, citrato y fosfato, así como varios tampones biológicos, por ejemplo, TAPS, Bicina, Tris, Tricina, HEPES, TES, MOPS, PIPES, Cacodilato y MES. Otros agentes tamponadores de pH incluyen ácido clorhídrico, hidróxido de sodio, oxido de magnesio, fosfato monopotásico, bicarbonato, amoniaco, ácido carbónico, citrato de sodio, ácido cítrico, ácido acético, hidrogenofosfato disódico, bórax, ácido bórico y similares. El agente tamponador generalmente está en una cantidad de aproximadamente 0,01 a aproximadamente 10 %, de aproximadamente 0,02 a aproximadamente 10%, de aproximadamente 0,02 a aproximadamente 5%, de aproximadamente 0,02 a aproximadamente 2,0%, de aproximadamente 0,02 a aproximadamente 1,0%, de aproximadamente 0,02 a aproximadamente 0,5%, de aproximadamente 0,05 a aproximadamente 10,0%, de aproximadamente 0,05 a aproximadamente 1,0%, de aproximadamente 0,05 a aproximadamente 0,5%, de aproximadamente 0,05 a aproximadamente 0,2%, de aproximadamente 0,1 a aproximadamente 5%, de aproximadamente 0,1 a aproximadamente 10%, de aproximadamente 0,1 a aproximadamente 20%, de aproximadamente 1 a aproximadamente 5 %, de aproximadamente 1 a aproximadamente 10 %, de aproximadamente 1 a aproximadamente 20 % (todo en peso/volumen).
El agente tamponador de pH utilizado en las formulaciones descritas en el presente documento puede usarse en cualquier concentración necesaria para obtener el intervalo de pH deseado. Por ejemplo, el agente tamponador puede utilizarse a una concentración de aproximadamente 0,001 M a aproximadamente 1 M, de aproximadamente 0,001 M a aproximadamente 2 M, de aproximadamente 0,001 M a aproximadamente 5 M, de aproximadamente 0,05 M a aproximadamente 0,1 M, de aproximadamente 0,05 M a aproximadamente 0,2 M, de aproximadamente 0,05 M a aproximadamente 1 M, de 0,05 M a aproximadamente 2 M, de aproximadamente 0,05 a aproximadamente 5 M, de aproximadamente 0,1 M a aproximadamente 1 M, de aproximadamente 0,1 M a aproximadamente 2 M, de aproximadamente 0,1 M a aproximadamente 5 M. En las formulaciones descritas en el presente documento puede utilizarse cualquier cantidad de agente tamponador necesaria para obtener el intervalo de pH deseado. Normalmente, el agente tamponador de pH farmacéuticamente aceptable puede utilizarse para proporcionar un pH en el intervalo de aproximadamente 4 a aproximadamente 9. El pH de la composición descrita en el presente documento puede variar de aproximadamente 3 a aproximadamente 10 o de aproximadamente 4 a aproximadamente 9. En cualquier realización descrita en el presente documento, el pH puede variar de aproximadamente 4 a aproximadamente 8, de aproximadamente 4 a aproximadamente 7, de aproximadamente 4,5 a aproximadamente 6,5, de aproximadamente 4,5 a aproximadamente 6, de aproximadamente 5 a aproximadamente 6, de aproximadamente 5 a aproximadamente 5,5, de aproximadamente 4 a aproximadamente 6 o de aproximadamente 4,5 a aproximadamente 5,5.
En cualquier realización, la composición descrita en el presente documento puede comprender uno o más conservantes farmacéuticamente aceptables. Como se usa en el presente documento, el término "conservante" incluye un agente o una combinación de agentes que ayuda a estabilizar la composición, inhibiendo el crecimiento microbiano, o ambas cosas. Los ejemplos de conservantes adecuados incluyen parabenos (por ejemplo, ésteres de metilo, etilo, propilo y butilo del ácido parahidroxibenzoico), galato de propilo, ácido sórbico y sus sales de sodio y potasio, ácido propiónico y sus sales de calcio y sodio, "Dioxina" (6-acetoxi-2,4-dimetil-m-dioxano), "Bronopol" (2-bromo-2-nitropropan-1,3-diol) y salicilanilidas tales como disbromosalicilanilida, tribromosalicilamidas, "Cinaryl" 100 y
200 o "Dowicil" 100 y 200 (isómero Cis de cloruro de 1-(3-cloroalil-3,5,7-triaza-1-azanidadamantano), hexaclorofeno, benzoato de sodio, ácido cítrico, ácido etilendiaminotetraacético y sus sales metálicas alcalinas y alcalinotérreas, butil hidroxianisol, butil hidroxitolueno, compuestos fenólicos tales como cloro y bromocresoles y cloro y bromooxilenoles, compuestos de amonio cuaternario como el cloruro de benzalconio, alcoholes aromáticos tales como alcohol feniletílico, alcohol bencílico, etc., clorobutanol, derivados de quinolina tales como yodoclorohidroxiquinolina y similares. La cantidad total de conservante, cuando está presente, es de aproximadamente 0,005% en peso a aproximadamente 2% en peso, de aproximadamente 0,001 % en peso a 1,0% en peso, de aproximadamente 0,005 % en peso a aproximadamente 0,25 % en peso o de aproximadamente 0,05 % en peso a aproximadamente 0,2% en peso, normalmente de aproximadamente 0,01 % en peso a aproximadamente 0,1 % en peso (todo en peso/peso).
En cualquier realización, la composición farmacéutica para el método descrito en el presente documento puede contener un agente quelante, tal como los conocidos por los expertos en la materia, por ejemplo, ácido etilendiaminotetraacético (EDTA), ácido dietilentriaminopentaacético (DTPA) y N,N-bis(carboximetil)glicina (NTA) o sus sales. La composición puede contener de aproximadamente 0,003% en peso a aproximadamente 1,0% en peso, de aproximadamente 0,02 % en peso a aproximadamente 0,2 % en peso, de aproximadamente 0,01 % en peso a aproximadamente 1,0 % en peso o de aproximadamente 0,02 % en peso a aproximadamente 0,5 % en peso (todo en peso/volumen) del agente quelante.
En cualquier realización descrita en el presente documento, en las composiciones para los métodos descritos en el presente documento pueden incluirse agentes antimicrobianos. Dichos agentes pueden incluir, pero sin limitación, 5-cloro-2-(2,4-diclorofenoxi)-fenol, 8-hidroxiquinolina, compuestos de cobre II, ácido Itálico, clorhexidina, alexidina, hexetidina, sanguinarina, cloruro de benzalconio, salicilanilida, bromuro de domifeno, cloruro de cetilpiridinio, cloruro de tetradecilpiridinio, cloruro de N-tetradecil-4-etilpiridinio, octenidina, yodo, sulfonamidas, bisbiguanidas, compuestos fenólicos, delmopinol, octapinol y otros derivados de piperidino y preparaciones de nicina, cualquier antibiótico adecuado tal como augmentin, amoxicilina, tetraciclina, doxiciclina, minociclina, metronidazol, neomicina, kanamicina y clindamicina, y cualquier sal de cualquiera de estos compuestos cuando corresponda, y cualquier combinación de estos compuestos. En otra realización más, pueden incluirse compuestos antifúngicos, solos o en combinación con cualquiera de los agentes antimicrobianos descritos anteriormente. Los agentes antifúngicos que son adecuados para su uso en las composiciones descritas en el presente documento incluyen, pero sin limitación, nistatina, miconazol, nitrato de econazol, clotrimazol y flucitosina. Los agentes antimicrobianos o antifúngicos pueden añadirse a las formulaciones descritas en el presente documento en una cantidad de aproximadamente 0,01 a aproximadamente 10%, de aproximadamente 0,01 a aproximadamente 5%, de aproximadamente 0,01 a aproximadamente 2,0%, de aproximadamente 0,01 a aproximadamente 1,0%, de aproximadamente 0,01 a aproximadamente 0,5 %, de aproximadamente 0,01 a aproximadamente 0,2 %, de 0,05 a aproximadamente el 10 %, de aproximadamente 0,05 a aproximadamente 5 %, de aproximadamente 0,05 a aproximadamente 2,0 %, de aproximadamente 0,05 a aproximadamente 1,0%, de aproximadamente 0,05 a aproximadamente 0,5%, de aproximadamente 0,05 a aproximadamente 0,2%, de aproximadamente 0,1 a aproximadamente 5%, de aproximadamente 0,1 a aproximadamente 10%, de aproximadamente 0,1 a aproximadamente 20%, de aproximadamente 1 a aproximadamente 5 %, de aproximadamente 1 a aproximadamente 10 %, de aproximadamente 1 a aproximadamente 20 % (todo en peso/volumen).
En cualquier realización de las composiciones del método descrito en el presente documento, también pueden añadirse antioxidantes. Por ejemplo, los antioxidantes utilizados en el presente documento pueden incluir betacaroteno, vitamina E, vitamina C, vitamina A, tocoferol, hidroxitolueno butilado, hidroxianisol butilado, butilhidroquinona terciaria, galato de propilo, ácido ascórbico, metabisulfito de sodio, ácido úrico, carotenoides, flavonoides, melatonina y etoxiquina. Los antioxidantes pueden añadirse a las formulaciones descritas en el presente documento en una cantidad de aproximadamente 0,01 a aproximadamente 10%, de aproximadamente 0,01 a aproximadamente 5 %, de aproximadamente 0,01 a aproximadamente 2,0 %, de aproximadamente 0,01 a aproximadamente 1,0%, de aproximadamente 0,01 a aproximadamente 0,5%, de aproximadamente 0,01 a aproximadamente 0,2 %, de 0,05 a aproximadamente el 10 %, de aproximadamente 0,05 a aproximadamente 5 %, de aproximadamente 0,05 a aproximadamente 2,0%, de aproximadamente 0,05 a aproximadamente 1,0%, de aproximadamente 0,05 a aproximadamente 0,5%, de aproximadamente 0,05 a aproximadamente 0,2%, de aproximadamente 0,1 a aproximadamente 5%, de aproximadamente 0,1 a aproximadamente 10%, de aproximadamente 0,1 a aproximadamente 20%, de aproximadamente 1 a aproximadamente 5%, de aproximadamente 1 a aproximadamente 10 %, de aproximadamente 1 a aproximadamente 20 % (todo en peso/volumen).
En una realización, la hormona liberadora de gonadotropina para su uso en el método descrito en el presente documento, está en una composición y la composición comprende metilparabeno, propilparabeno, cloruro de sodio, citrato de sodio, L-metionina, ácido cítrico, triptorelina y metilcelulosa. En otro aspecto, la composición comprende metilparabeno en una cantidad de aproximadamente 0,09 % en peso por volumen, propilparabeno en una cantidad de aproximadamente 0,01 % en peso por volumen, cloruro de sodio en una cantidad de aproximadamente 0,91 % en peso por volumen, citrato de sodio en una cantidad de aproximadamente 0,186 % en peso por volumen, L-metionina en una cantidad de aproximadamente 0,1 % en peso por volumen, ácido cítrico en una cantidad de aproximadamente 0,07 % en peso por volumen, triptorelina en una cantidad de aproximadamente 0,01 % en peso
por volumen, y metilcelulosa en una cantidad de aproximadamente 1,2% en peso por volumen (o con una viscosidad de aproximadamente 250 cP a aproximadamente 400 cP).
La composición de hormona liberadora de gonadotropina para el método descrito en el presente documento, contiene una hormona liberadora de gonadotropina en una cantidad eficaz para sincronizar el tiempo de inseminación en una cerda primeriza cuando se utiliza en el método descrito en el presente documento, Como se usa en el presente documento, "hormona liberadora de gonadotropina" se refiere a cualquier hormona liberadora de gonadotropina, incluyendo análogos y derivados de la hormona liberadora de gonadotropina, y agonistas y antagonistas de la hormona liberadora de gonadotropina. En otras realizaciones, en lugar de la hormona liberadora de gonadotropina, o en combinación con ella, puede utilizarse hormona luteinizante o gonadotropina coriónica humana, o derivados o análogos de las mismas y sus combinaciones. Como se usa en el presente documento, "hormona luteinizante" se refiere a cualquier hormona luteinizante, incluidos análogos y derivados de la hormona luteinizante, y agonistas y antagonistas de la hormona luteinizante. En una realización, la hormona luteinizante puede ser sintética. En otra realización, la hormona luteinizante puede ser HL (véase, por ejemplo, la patente de Estados Unidos N.°5444 167). Como se usa en el presente documento, "gonadotropina coriónica humana" se refiere a cualquier gonadotropina coriónica humana, incluyendo análogos y derivados de gonadotropina coriónica humana, y agonistas y antagonistas de gonadotropina coriónica humana. En una realización, la gonadotropina coriónica humana puede ser sintética. En otra realización, la gonadotropina coriónica humana puede ser GCh (véanse, por ejemplo, las patentes de Estados Unidos N.°6469139, 4400316 y 4804626. En otra realización más, en el método descrito en el presente documento no se utiliza GCe, GCh ni HL.
En una realización, la hormona liberadora de gonadotropina puede ser sintética. En otra realización, la hormona liberadora de gonadotropina puede estar en forma de acetato. En otra realización, la hormona liberadora de gonadotropina puede ser GnRH (pGlu-His-Trp-Ser-Tyr-Gly-Leu-Arg-Pro-GlyNH2) (véase, por ejemplo, la patente de Estados Unidos N.° 5688506) o triptorelina (pGlu-His-Trp-Ser-Tyr-D-Trp-Leu-Arg-Pro-Gly-NH2).
Como ejemplos de agonistas de la hormona liberadora de gonadotropina para su uso en el presente documento se incluyen, pero sin limitación, leuprolida, nafarelina, buserelina, [DAla6, des Gly-NH210]GnRH, [DLys6]GnRH, [DAla6] GnRH, [2-Me-Ala6]GnRH, [D-a-aminobutirol]6, des-GlyNH210]GnRH, triptorelina, lutrelina, goserelina, deslorelina e histrelina. En general, los agonistas de la hormona liberadora de gonadotropina se modelan a partir del decapéptido de la hormona liberadora de gonadotropina natural con sustituciones de aminoácidos específicas normalmente en las posiciones 6 y 10. La triptorelina es un ejemplo de un agonista de la hormona liberadora de gonadotropina con solo una única sustitución en la posición 6.
Como ejemplos de antagonistas de la hormona liberadora de gonadotropina se incluyen Antide (un decapéptido representado por la fórmula D-Ac-D-2-Nal1-DpClPhe2-D-3-Pal3-Ser4-NiLys5-D-NicLys6-Leu7-ILys8 -Pro9-D-Ala10), [Ac-D4ClDPhe1, D4ClDPhe2, DTrp3, DArg6, DAla10 ]GnRH, [Ac-4ClDPhe2, D3Pal3, Arg5, D2Nal6, DAla10 ]GnRH, [Ac-D2-Na1l, 4ClDPhe2, DTrp3, DArg6, DAla10 ]GnRH, [Ac-D2 Nal1, 4FDPhe2, DTrp3, DArg6 ]GnRH, [Ac-D2Nal1, 4ClDPhe2, DTrp3, DhArg(Et2)6, DAla10]GnRH y [Ac-Na11, DME4ClPhe2, DPal3, Ser4, Tyr5, DArg6, Le7, ILys8, Pro9, DAla10 ]GnRH. En cualquier realización descrita en el presente documento, se puede utilizar una hormona liberadora de gonadotropina de fórmula (I)
o un solvato, un hidrato, o una sal farmacéuticamente aceptable del mismo, en donde
R1 y R2 son independientemente en cada caso hidrógeno, o se seleccionan independientemente del grupo que
consiste en alquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, haloalquilo, arilo, heteroarilo, arilalquilo y heteroarilalquilo, cada uno de los cuales está opcionalmente sustituido, o R1 y R2 y el carbono unido forman un carbociclo o heterociclo;
R5 es hidrógeno o alquilo; y
X es hidrógeno, o X se selecciona del grupo que consiste en alquilo, cicloalquilo, heteroalquilo, alquilenocarboxamida opcionalmente sustituida y HNC(O)NR3R4, donde R3 y R4 en cada caso se seleccionan independientemente del grupo que consiste en hidrógeno, alquilo, heteroalquilo y haloalquilo.
En otra realización, R1 es un metilen-arilo. En otra realización, el arilo es fenilo o 4-hidroxifenilo. En otra realización, R1 es un metilen-heteroarilo. En otra realización más, el heteroarilo se selecciona del grupo que consiste en piridilo, tiazolilo, piridazolilo, pirimidinilo, quinolinilo, pirazolilo, imidazolilo, pirrolilo, indolilo, benzopirazolilo y bencimidazolilo; y R es hidrógeno o metilo. En varias otras realizaciones, R1 es 2-metilpropilo, R1 es 2-naftilmetilo, R1 es tbutoximetilo, R1 es metilo, R1 es 4-aminobutilo, R1 es etilo, R1 y R2 son metilo, R1 es 1H-indol-3-il-metilo, R1 es 1H-1-bencil-imidazol-4-il-metilo o R1 es bencilo.
En realizaciones adicionales, R2 es hidrógeno, R2 es hidrógeno y la hormona liberadora de gonadotropina tiene la configuración R en el carbono al que se une R1, R2 es hidrógeno y la hormona liberadora de gonadotropina tiene la configuración S en el carbono al que se une R1 o R2 es hidrógeno y la hormona liberadora de gonadotropina es una mezcla de hormonas liberadoras de gonadotropina que tienen la configuración R en el carbono al que se une R1 y la configuración S en el carbono al que se une R1.
En otras realizaciones adicionales, X es CH2(CO)NH2, X es HN(CO)NH2 , X es etilo, X es hidrógeno, R5 es hidrógeno o R5 es metilo.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es 1H-indol-3-ilmetilo, R2 es hidrógeno, X es CH2(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es hidrógeno, R2 es hidrógeno, X es CH2(CO)NH2 ; y R5 es hidrógeno.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es 1H-1 -bencilimidazol-4-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es 2-metilpropilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno.
En otra realización más, se proporciona una cualquiera de las realizaciones descritas anteriormente en donde X es CH2C(O)NH2.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es 2-naftlimetilo, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es t-butoximetilo, R2 es hidrógeno, X es etilo; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es bencilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es t-butoximetilo, R2 es hidrógeno, X es HN(CO)NH2; y R5 es hidrógeno.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es 1H-indol-3-ilmetilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es metilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es 1H-indol-3-ilmetilo, R2 es hidrógeno, X es etilo; R5 es metilo; y la configuración del carbono al que está unido R1 es R.
En otra realización, la hormona liberadora de gonadotropina es una hormona de fórmula I donde R1 es metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
Las hormonas liberadoras de gonadotropina, tales como las descritas en la fórmula anterior, utilizadas en el presente documento, pueden administrarse en forma de sales o complejos no tóxicos farmacéuticamente aceptables. Las sales incluyen sales de adición de ácido tales como, por ejemplo, clorhidrato, bromhidrato, sulfato, fosfato, nitrato, oxalato, fumarato, gluconato, tanato, maleato, acetato, benzoato, succinato, alginato, malato, ascorbato, tartrato y similares. Los complejos pueden ser con metales tales como, por ejemplo, zinc, bario, calcio, magnesio, aluminio y similares.
Como ejemplos adicionales de hormonas aceptables para su uso en los métodos descritos en el presente documento se incluyen, prostaglandinas, progestágenos, progesteronas, andrógenos, testosteronas, estrógenos y estradioles, derivados y análogos de los mismos, combinaciones de los mismos y similares. En los métodos descritos en el presente documento, la hormona utilizada para sincronizar el estro puede ser altrenogest (MATRIX® de Intervet, Inc. Summit, Nueva Jersey). La hormona utilizada para sincronizar el estro (por ejemplo, altrenogest o cualquier otra progestina adecuada) puede administrarse a la cerda primeriza a través de la alimentación, por ejemplo, mezclando la hormona con la alimentación de la cerda primeriza o aplicando la hormona a la alimentación de la cerda primeriza. En la técnica se conocen bien métodos para suministrar altrenogest a las cerdas primerizas. Por ejemplo, en una realización, se puede utilizar una solución de altrenogest al 0,22 % (o cualquier otra concentración adecuada) para administrar 15 mg de altrenogest por cerda primeriza una vez al día durante 14 días en la alimentación de la cerda primeriza. En otra realización, se puede utilizar una solución de altrenogest al 0,22 % (o cualquier otra concentración adecuada) para administrar 20 mg de altrenogest por cerda primeriza una vez al día durante 18 días en la alimentación de la cerda primeriza. Cualquier otro régimen adecuado para la administración de altrenogest u otra hormona para sincronizar el estro (por ejemplo, cualquier otra progestina adecuada) puede utilizarse según la invención. La hormona de sincronización del estro puede administrarse a la cerda primeriza mediante cualquier método adecuado conocido en la técnica, incluso a través de la alimentación.
La cantidad de hormona liberadora de gonadotropina eficaz para su uso según los métodos y composiciones descritos en el presente documento, depende de muchos parámetros, incluido el peso molecular de la hormona liberadora de gonadotropina, su vía de administración, y si está en su forma originaria. Como se describe en el presente documento, una "cantidad eficaz" de la hormona es una cantidad suficiente para sincronizar la ovulación o para sincronizar el tiempo de inseminación en una cerda primeriza o una cerda usando los métodos descritos en el presente documento.
La cantidad eficaz de la hormona liberadora de gonadotropina que se administrará a una cerda primeriza o a una cerda adulta puede variar de aproximadamente 100 ng a aproximadamente 2000 |jg, de aproximadamente 100 ng a aproximadamente 1000 jg, de aproximadamente 100 ng a aproximadamente 500 jg, de aproximadamente 1 jg a aproximadamente 2000 jg, de aproximadamente 1 jg a aproximadamente 500 jg, de aproximadamente 1 jg a aproximadamente 100 jg, de aproximadamente 1 jg a aproximadamente 50 jg, de aproximadamente 1 jg a aproximadamente 10 jg, de aproximadamente 10 jg a aproximadamente 2000 jg, de aproximadamente 10 jg a aproximadamente 1000 jg, de aproximadamente 10 jg a aproximadamente 500 jg, de aproximadamente 10 jg a aproximadamente 100 jg, de aproximadamente 10 jg a aproximadamente 50 jg, de aproximadamente 50 jg a aproximadamente 2000 jg, de aproximadamente 50 jg a aproximadamente 1000 jg, de aproximadamente 50 jg a aproximadamente 500 jg, de aproximadamente 50 jg a aproximadamente 300 jg, de aproximadamente 50 jg a aproximadamente 200 jg, de aproximadamente 100 jg a aproximadamente 200 jg, de aproximadamente 100 jg a aproximadamente 300 jg, de aproximadamente 100 jg a aproximadamente 500 jg, de aproximadamente 100 jg a aproximadamente 1000 jg, de aproximadamente 200 jg a aproximadamente 2000 jg o de aproximadamente 0,05 mg a aproximadamente 50 mg. En varios aspectos ilustrativos, la hormona liberadora de gonadotropina puede administrarse a una cerda primeriza o a una cerda adulta a una dosis de aproximadamente 1 jg, aproximadamente 2 jg, aproximadamente 5 jg, aproximadamente 10 jg, 20 jg, aproximadamente 50 jg, aproximadamente 75 jg, aproximadamente 100 jg, aproximadamente 150 jg, aproximadamente 180 jg, aproximadamente 200 jg, aproximadamente 225 jg, aproximadamente 250 jg, aproximadamente 300 jg, aproximadamente 400 jg, aproximadamente 500 jg, aproximadamente 750 jg, aproximadamente 1000 jg, aproximadamente 1500 jg o aproximadamente 2000 jg de la hormona liberadora de gonadotropina. La hormona liberadora de gonadotropina puede administrarse en una o más dosis. La hormona liberadora de gonadotropina se administra sin ninguna hormona adicional para sincronizar la ovulación.
La hormona liberadora de gonadotropina en la composición utilizada para los métodos descritos en el presente documento puede administrarse a una concentración de, por ejemplo, aproximadamente 0,1 jg/ml, aproximadamente 0,5 jg/ml, aproximadamente 1 jg/ml, aproximadamente 5 jg/ml, aproximadamente 10 jg/ml, de aproximadamente 50 jg/ml a aproximadamente 500 jg/ml, de aproximadamente 50 jg/ml a aproximadamente 400 jg/ml, de aproximadamente 50 jg/ml a aproximadamente 300 jg/ml, de aproximadamente 50 jg/ml a aproximadamente 200 jg/ml, de aproximadamente 50 jg/ml a aproximadamente 150 jg/ml, de aproximadamente 50 jg/ml a aproximadamente 250 jg/ml o de aproximadamente 100 jg/ml. En realizaciones ilustrativas, la composición puede administrarse en varios volúmenes que incluyen, por ejemplo, un volumen de dosificación de 0,1 ml, 0,5 ml, 1 ml, 2 ml, 3 ml, 4 ml o 5 ml. Para la administración al animal, puede utilizarse cualquier volumen adecuado, dependiendo, por ejemplo, de la vía de administración, del tamaño del animal al que se le va a administrar la hormona, de la especie del animal al que se le va a administrar la hormona y de otros factores conocidos por los expertos en la materia.
En cualquier realización descrita en el presente documento, la hormona liberadora de gonadotropina se administra en una cantidad eficaz para estimular la ovulación del folículo ovárico y sincronizar la ovulación según los métodos descritos en el presente documento. La dosis de la hormona liberadora de gonadotropina puede administrarse utilizando un método seleccionado del grupo que consiste en 1) el uso de un catéter de deposición, 2) la administración manual, 3) la inyección, o cualquier otro medio reconocido en la técnica para administrar una composición farmacéutica, por ejemplo, cualquier otro medio reconocido en la técnica para administrar por vía vaginal una composición farmacéutica, tal como una composición que contenga una hormona. En una realización, la hormona liberadora de gonadotropina puede administrarse a más de una cerda primeriza o adulta.
Aparte de la administración vaginal, como ejemplos de métodos para la administración eficaz de la hormona liberadora de gonadotropina a la cerda primeriza o adulta, se incluyen, la administración parenteral, por ejemplo, por vía subcutánea, intramuscular, intraperitoneal, intratecal o intravenosa, o en combinación con un transportador aceptable. Los medios adecuados para la administración parenteral incluyen inyectores de aguja (incluidas microagujas), inyectores sin aguja y técnicas de infusión. Las composiciones parenterales para su uso según esta invención, pueden estar en forma de un liofilizado reconstituible que comprende una o más dosis de la composición de hormona liberadora de gonadotropina. Como ejemplos de formas farmacéuticas parenterales se incluyen soluciones acuosas de la composición de la hormona liberadora de gonadotropina en transportadores líquidos aceptables bien conocidos, tales como alcoholes líquidos, glicoles (por ejemplo, polietilenglicoles), soluciones de glucosa (por ejemplo, al 5 %), ésteres, amidas, agua estéril, solución salina tamponada (incluidos tampones como fosfato o acetato; por ejemplo, solución salina isotónica).
En cualquier realización descrita en el presente documento, la composición de la hormona liberadora de gonadotropina para su uso en el método descrito en el presente documento, puede administrarse por vía local a la cerda primeriza o adulta. Como ejemplos del método de administración local para su uso en el presente documento se incluyen, la administración tópica, intravaginal e intrarrectal. Como ejemplos de formas farmacéuticas para su uso en esta realización se incluyen cremas, pomadas, geles, pastas, polvos, lociones, parches transdérmicos, dispositivos intrauterinos, anillos vaginales y comprimidos vaginales. En una realización ilustrativa, la composición de la hormona liberadora de gonadotropina se administra en la pared anterior de la vagina de la cerda primeriza o de la cerda adulta. Las hormonas liberadoras de gonadotropina también pueden formularse en composiciones vaginales o rectales tales como supositorios, por ejemplo, que contienen bases de supositorios convencionales tales como manteca de cacao, carboceras, polietilenglicoles u otros glicéridos, todo lo cual se funde a la temperatura corporal, aunque se solidifica a temperatura ambiente.
La hormona liberadora de gonadotropina puede administrarse a la cerda primeriza o adulta mediante cualquier procedimiento útil y puede utilizarse cualquier dosis y forma farmacéutica eficaz adecuada, incluyendo formas farmacéuticas orales conocidas en la técnica, tales como pastillas, gránulos o cápsulas, y las dosis eficaces pueden administrarse en formas farmacéuticas de liberación estándar o modificada. Las formulaciones farmacéuticas de liberación modificada incluyen formulaciones de liberación retardada, sostenida, pulsada, controlada, dirigida y programada.
Las composiciones de la hormona liberadora de gonadotropina también pueden comprender transportadores o excipientes adecuados en fase sólida o de gel. Como ejemplos de dichos transportadores o excipientes se incluyen, pero sin limitación, carbonato de calcio, fosfato de calcio, varios azúcares, almidones, derivados de celulosa, gelatina y polímeros tales como polietilenglicoles.
En otro aspecto ilustrativo, la hormona liberadora de gonadotropina para su uso en los métodos descritos en el presente documento puede estar en forma de un kit. El kit puede comprender una dosis o dosis múltiples de una hormona liberadora de gonadotropina como se describe en el presente documento. En esta realización, el kit puede comprender además un aplicador para administración manual, un catéter de deposición y/o una jeringa para la aplicación de la composición hormonal a la cerda primeriza o a la cerda adulta. En otra realización más, la hormona liberadora de gonadotropina está en una composición que comprende un gel como se describe en el presente documento. En una realización ilustrativa, el kit puede comprender la hormona liberadora de gonadotropina y el gel por separado para mezclarse antes de la administración a la cerda primeriza o adulta, o pueden estar juntos en una composición. En otra realización, el kit puede comprender la hormona liberadora de gonadotropina y el gel mezclados en un recipiente para la administración inmediata.
En otra realización más, el kit contiene instrucciones de uso. Las instrucciones pueden indicar que la inseminación debe realizarse a través de una o más inseminaciones artificiales. En las instrucciones también puede proporcionarse el momento para la administración de la hormona liberadora de gonadotropina y la hormona de sincronización del estro a la cerda primeriza, como se describe en el presente documento, y el momento para la inseminación artificial.
En otra realización más, se proporciona un artículo de fabricación. El artículo de fabricación puede comprender cualquiera de las composiciones de hormona liberadora de gonadotropina descritas en el presente documento para su uso en los métodos descritos en el presente documento. La composición de la hormona liberadora de
gonadotropina puede estar en un recipiente principal, por ejemplo, un vial de vidrio, tal como un vial de vidrio de ámbar con un tapón de goma y/o un sello de aluminio desprendible. En otra realización, el envase principal puede ser de plástico o aluminio y puede sellarse. En otra realización, el envase principal primario puede incluirse en un envase secundario para proteger aún más la composición de la luz. El envase secundario puede ser, por ejemplo, de cartón.
Cualquiera de estas realizaciones también se aplica a las realizaciones del kit descritas anteriormente, y cualquiera de las realizaciones de la composición de la hormona liberadora de gonadotropina descrita en el presente documento puede aplicarse al artículo de fabricación.
Ejemplos
EJEMPLO 1
Diseño del estudio y tratamientos
Todas las cerdas primerizas se alimentaron individualmente durante 14 días con MATRIX® aplicado sobre el pienso (top-dress) a la tasa recomendada de 15 mg/cerda/día. A las cerdas primerizas se las retiró la alimentación con MATRIX® (última alimentación aplicada sobre el pienso la mañana del día 0) y se las asignaron tratamientos. Los controles se trataron con una formulación en gel de metilcelulosa al 1,2 % sin triptorelina 96 horas después de retirar MATRIX® (última aplicación sobre el pienso). Las cerdas primerizas restantes recibieron 200 mcg (microgramos) de triptorelina, en forma de acetato, en una formulación en gel de metilcelulosa al 1,2% por vía intravaginal varias veces después de retirar MATRIX®. Los cuatro tratamientos fueron: 1) tratamiento con gel vehículo (VG, vehicle gel) 96 horas después de retirar MATRIX®, 2) tratamiento con gel de triptorelina (TG, triptorelin gel) 96 horas después de retirar MATRIX®, 3) tratamiento con TG 120 horas después de retirar MAt RiX® y 4) tratamiento con TG 144 horas después de retirar MATRIX®. Se controló el ciclo estral y el estado ovulatorio de todas las cerdas primerizas como se describe a continuación. Las cerdas primerizas incluidas en la réplica 1 se seleccionaron de cerdas primerizas de producción a escala comercial de la línea terminal ubicadas en establos de engorde/acabado. La madurez sexual, indicada por uno o más períodos estrales, no se verificó antes de comenzar la alimentación con MATRIX®. Las cerdas primerizas incluidas en la réplica 2 se seleccionaron de una población de cerdas primerizas de la línea materna. La madurez sexual se verificó mediante al menos un período estral, que se verificó y registró antes de comenzar la alimentación con MATRIX®.
Sustancia de ensayo
La triptorelina (pGlu-His-Trp-Ser-Tyr-D-Trp-Leu-Arg-Pro-Gly-NH2) se suministró en forma de acetato, de Bachem, Torrance, CA (artículo H-4075 calidad CGMP). El gel de triptorelina (200 pg/2 ml) se formuló en Argenta (Auckland, NZ), en un gel compuesto por Methocel Premium A4000 (Dow Chemical), tampón citrato (pH 5,5), NaCl, metionina y EDTA (como estabilizadores potenciales) y metil y propil parabenos (como conservantes). Se envasaron cincuenta y cuatro mililitros de gel de triptorelina (100 mcg de acetato de triptorelina/ml) en viales de suero de vidrio de borosilicato ámbar (610206-50) con un tapón de goma de butilo de color gris para viales de suero farmacéutico (73828A-SS) con un sello de aluminio estándar (SAS20NAT). El vehículo de gel de triptorelina contenía los mismos excipientes de formulación que los incluidos en el gel de triptorelina, excepto que no contenía triptorelina o los posibles estabilizadores, metionina y EDTA. MATRIX® se suministró como la forma disponible en el comercio de los Estados Unidos.
Observación del estro
Para la detección del estro posterior al tratamiento, las cerdas primerizas se instalaron en corrales individuales. Los verracos (cerdos macho) se instalaron en salas distintas y/o al menos a 12 m de distancia y a favor del viento. Para provocar señas de estro, un verraco maduro se paseaba lentamente por el callejón frente a los corrales de las cerdas primerizas, exponiendo cada cerda primeriza de ensayo, durante hasta 5 minutos, a señales visuales, auditivas y olfativas del verraco. Conforme a la práctica estándar en granjas comerciales, mientras que el verraco estaba cerca frente al corral de la cerda primeriza, un experto comprobaba el estro aplicando presión dorsal en la sección central de la cerda primeriza combinado con frotamiento lateral. El estro se confirmó cuando una cerda primeriza se mantuvo rígida a la presión dorsal, sin vocalización y con algún indicio de reflejo auditivo.
Para la réplica uno, la detección de estro se realizó en cerdas primerizas una vez al día desde el día 5 hasta el día 8. Para la réplica dos, la detección de estro se realizó en cerdas primerizas una vez al día desde el día 0 hasta el día 8. Control de la ovulación
El estado ovulatorio de todas las cerdas primerizas se controló mediante ecografía transrectal. Para la réplica uno, la ovulación se controló dos veces el día 5, después tres veces al día del día 6 al día 8. Para la réplica dos, la ovulación se controló tres veces al día del día 5 al día 8. Para ello, se utilizó un ecógrafo Aloka 500 con un transductor de matriz lineal de 7,5 MHz unido a una varilla estabilizadora de PVC de ángulo fijo para facilitar la inserción en el recto.
El transductor y la varilla de PVC se recubrieron con un lubricante ginecológico y se insertaron suavemente en el recto hasta que se visualizaron los ovarios, al mismo tiempo. En cada exploración, se registraron los diámetros de los tres folículos más grandes (con una precisión de 0,1 mm). Cuando el número de folículos grandes (> 6,5 mm) disminuyó a menos de 3, se confirmaba que una cerda primeriza había ovulado.
Administración
Con un catéter similar a los utilizados para la inseminación artificial, se depositó una sola dosis de 2 ml de gel de triptorelina o gel vehículo a una distancia de aproximadamente 1 a 2 cm posteriores al cuello uterino. La dosis se suministró utilizando un aplicador multidosis estándar conectado al catéter. Para cada cerda primeriza, se utilizaba una funda desechable nueva, que rodeaba el catéter.
Análisis estadístico
Los datos se analizaron utilizando los procedimientos de SAS para analizar Modelos Mixtos. Los modelos incluyeron efectos principales de tiempo de tratamiento después de la última alimentación con MATRIX®, réplicas y tratamiento por interacción de réplicas. Las diferencias entre los tratamientos se analizaron sobre estimaciones de medias mínimas cuadráticas utilizando la prueba T a P <0,05. Los datos para el análisis se analizaron en busca de suposiciones de normalidad de datos.
Resultados
Cinco cerdas primerizas en la réplica 1 y tres cerdas primerizas en la réplica 2, se retiraron del análisis de datos por razones no relacionadas con el tratamiento. Los resultados se presentan en las Figuras 1 y 2, presentándose los datos tabulares de las réplicas 1 y 2, en las Tablas 1 y 2, respectivamente. Después del tratamiento con MATRIX® se detectaron más cerdas primerizas en estro en la réplica 2 en comparación con la réplica 1.
La réplica 1 se realizó en un centro de investigación de acabado con hembras híbridas de la línea terminal PIC C-22 X línea 337 a un nivel inferior de madurez sexual en comparación con hembras de la línea materna PIC C-22, que eran más maduras sexualmente y estaban en un centro de reproducción ambiental sumamente mantenido en la réplica 2. Un porcentaje inferior de cerdas primerizas había mostrado su primer estro antes de la alimentación con MATRIX® en la réplica 1 en comparación con la réplica 2. La réplica 2 no solo se realizó en un lugar diferente al de la réplica 1, sino que la madurez sexual también fue mayor para las cerdas primerizas en la réplica 2, como lo demuestran los ciclos estrales documentados en todas las cerdas primerizas antes del inicio de la alimentación con MATRIX®. En la réplica 1, los ciclos estrales no pudieron documentarse de manera fidedigna en todas las cerdas primerizas antes del inicio de la alimentación con MATRIX®.
El intervalo desde la última alimentación con MATRIX® para la ovulación estaba influenciado por el tratamiento y la réplica. Se espera que el intervalo desde el tratamiento con gel de triptorelina y la ovulación alcance un pico después de 40-48 horas de tratamiento. Por lo tanto, se espera que el intervalo desde la alimentación con MATRIX® hasta la ovulación difiera cuando se administre el gel de triptorelina después de 96, 120 o 144 horas de la alimentación con MATRIX®. Esto se muestra en la Tabla 4 y se representa en la Figura 3. En cada grupo, el pico ovulatorio se produjo 48 horas después del tratamiento. Sin embargo, el pico se produjo 144, 168 y 192 horas después de la alimentación con MATRIX® para los grupos de tratamiento de 96, 120 y 140 horas, respectivamente. El grupo tratado con vehículo no mostró ningún pico ovulatorio sincronizado, sino más bien un aumento constante en el porcentaje de ovulación que nunca alcanzó el mismo nivel que el observado en cerdas primerizas tratadas con gel de triptorelina.
El efecto de replicar, o lo que es probablemente más importante, el impacto de la madurez sexual, se muestra comparando las Tablas 1 y 2. Se confirmó que las cerdas primerizas presentadas en la Tabla 2 eran sexualmente maduras, mientras que no lo eran las de la réplica o las de la Tabla 1. En las Figuras 1 y 2 pueden observarse las diferencias. Las cerdas primerizas sexualmente maduras (Figura 2) demostraron una respuesta ovulatoria más alta 48 horas después del tratamiento con gel de triptorelina durante cada uno de los tres tiempos de tratamiento. Por ejemplo, 90 % para la réplica 2 en comparación con 60 % para la réplica 1 en el tiempo de tratamiento de 120 horas con Tg (TG 120). Aunque el nivel de madurez sexual difería entre estos dos grupos de cerdas primerizas, cuando se compara la Figura 1 con la Figura 2 y los datos presentados en la Figura 3, se observan tendencias constantes. Las curvas del tiempo de ovulación para las cerdas de control tratadas con vehículo y las cerdas primerizas tratadas con gel de triptorelina a las 144 horas son casi idénticas, independientemente de si son inmaduras (Figura 1) o maduras (Figura 2) y la gráfica combinada en la Figura 3 sugiere que el tratamiento con gel de triptorelina a las 144 horas no sincronizó eficazmente la ovulación. El tiempo de tratamiento de 144 horas es aparentemente después de la liberación de HL endógena en muchas de las cerdas primerizas y, por tanto, demasiado tarde para inducir una ovulación sincronizada. Sin embargo, es interesante observar que el tratamiento a las 144 horas promovió y sincronizó la ovulación en las cerdas primerizas inmaduras (Figura 1) entre 40 y 48 horas después de la administración del gel de triptorelina, mientras que el 100 % de las cerdas primerizas ya habían ovulado en 40 horas en las cerdas primerizas sexualmente maduras (Figura 2). Estos datos sugieren que se puede recomendar un momento de tratamiento diferente para las cerdas primerizas sexualmente inmaduras en comparación con las sexualmente maduras.
El tratamiento con gel de triptorelina a las 96 o 120 horas, promovió y produjo una ovulación más sincronizada que la de las cerdas primerizas tratadas con control vehículo o las tratadas a las 144 horas. La proporción de cerdas primerizas ovulando en las 48 horas y la sincronía de la ovulación fue mayor en las cerdas primerizas tratadas a las 120 horas (72%) en comparación con las cerdas primerizas tratadas a las 96 horas (54,2%) (Tabla 4). Para las cerdas primerizas sexualmente maduras (Figura 2 y Tabla 2), la diferencia fue más pronunciada con un porcentaje de ovulación de 90,0 % y 77,8 % en 48 horas para TG 120 y TG 96, respectivamente. Estos datos demuestran que el momento más eficaz para el tratamiento es 120 horas después de la última alimentación con MATRIX®.
Tabla 1. Porcentaje acumulativo de cerdas primerizas que ovulan a varios intervalos de tiempo después de la última alimentación^ con MATRIX® tratamiento con VG o TG en la ré lica 1.
Tabla 2. Porcentaje acumulativo de cerdas primerizas que ovulan a varios intervalos de tiempo después de la última alimentación^ con MATRIX® tratamiento con VG o TG en la ré lica 2.
Tabla 3. Medias mínimas cuadráticas para las variables de respuesta medidas en cerdas primerizas después de alimentación con MATRIX® asignadas para recibir tratamiento con VG 96 horas después de retirar MATRIX® o con TG 96 120 o 144 horas des ués de la última alimentación con MATRIX® en ré licas 1 2 combinadas.
La réplica es significativa en todos estos, excepto MOV 136.
Tabla 4. Porcentaje acumulativo de cerdas primerizas que ovulan a varios intervalos de tiempo después de la última alimentación^ con MATRIX® tratamiento con VG o TG en las ré licas 1 2 combinadas.
EJEMPLO 2
Diseño del estudio y tratamientos
Doscientas noventa y siete (297) cerdas primerizas se alimentaron durante 14 días con MATRIX® aplicado sobre el pienso a la tasa recomendada de 15 mg/cerda/día. La última alimentación con MATRIX® fue a las 5:30 AM (Día 0). Aproximadamente cien cerdas se asignaron a cada uno de los siguientes tratamientos:
1. Grupo 1, Controles (n=100); tratadas con MATRIX®, pero no tratadas con OvuGel™, inseminadas diariamente durante el estro, como normalmente se practica (promedio de 1,9 inseminaciones por cerda primeriza).
2. Grupo (n=98); tratadas con OvuGel™ a las 6:30 am (+/- 1 h) el día 5 e inseminadas a las 2 a 11 horas después del tratamiento con OvuGel™ el día 5 si expresan estro. Todas las cerdas primerizas se inseminaron una vez el Día 6, 26 horas (+/- 2,5 horas) después del tratamiento con OvuGel™, independientemente del estado estral.
3. Grupo 3 (n=99); tratadas con OvuGel™ a las 6:30 a.m. (+/- 1 hora) el día 5 e inseminadas una vez a las 2,5 a 9,5 horas después del tratamiento con OvuGel™ el día 5 y nuevamente el día 6, 26,5 horas (+/- 3 horas) después del tratamiento con OvuGel™, independientemente del estro en cualquiera de los días.
Sustancia de ensayo
La triptorelina (pGlu-His-Trp-Ser-Tyr-D-Trp-Leu-Arg-Pro-Gly-NH2) se suministró en forma de acetato, de Bachem, Torrance, CA (artículo H-4075 calidad CGMP). El gel de triptorelina (200 mcg/2 ml) se formuló en DPT Laboratories (San Antonio, Tejas) en un gel compuesto por Methocel Premium A4000 (Dow Chemical) y otros excipientes de formulación inactivos. Se envasaron cincuenta y cuatro mililitros de gel de triptorelina (100 mcg de acetato de triptorelina/ml) en viales de suero de vidrio de borosilicato ámbar (610206-50) con un tapón de goma de butilo de color gris para viales de suero farmacéutico (73828A-SS) con un sello de aluminio estándar (SAS20NAT).
Observación del estro
Las cerdas primerizas se instalaron en corrales individuales. Los verracos se instalaron al menos a 12 m de distancia y a favor del viento. Para determinar la aparición y la duración del estro, diariamente se observó el estro de las cerdas primerizas desde 4 días hasta 8 días después de la última alimentación con MATRIX® o hasta que se confirmó el final del estro, lo que ocurriera primero. Para facilitar la detección del estro, un verraco maduro se paseaba lentamente por el callejón frente al corral de la cerda primeriza, exponiendo cada cerda primeriza, durante hasta 5 minutos, a señales visuales, auditivas y olfativas del verraco. Mientras que el verraco estaba cerca frente al corral de la cerda primeriza, un experto comprobaba el estro aplicando presión dorsal en la sección central de la cerda primeriza combinado con frotamiento lateral. El estro se confirmó cuando una cerda primeriza se mantuvo rígida a la presión dorsal, sin vocalización y con algún indicio de reflejo auditivo.
Administración de fármacos
Con un catéter similar a los utilizados para la inseminación artificial, se depositó una sola dosis de 2 ml de OvuGel™ a una distancia de aproximadamente 1 a 2 cm posteriores al cuello uterino. La dosis se suministró utilizando un aplicador multidosis estándar conectado al catéter. Para cada cerda primeriza, se utilizaba una funda desechable nueva, que rodeaba el catéter.
Análisis estadístico
Los datos se sometieron a análisis de varianza utilizando el procedimiento de SAS PROC MIX (versión 9,2) para determinar el efecto principal del tratamiento, réplicas y tratamiento por interacción de réplicas sobre el índice de partos y el tamaño de la camada. Las diferencias entre los tratamientos se analizaron sobre estimaciones de medias mínimas cuadráticas utilizando la prueba T a P <0,05.
Resultados
Doscientas noventa y siete (297) cerdas primerizas se asignaron a grupos de tratamiento (Grupo 1: 100, Grupo 2: 98, Grupo 3: 99). Una cerda primeriza de control se retiró del estudio debido a una lesión antes de que finalizara el estado estral después del destete el día 8 y, por lo tanto, se retiró del conjunto de datos final. Las tablas 5 a 8 presentan las medias mínimas cuadráticas y el análisis estadístico de todas las cerdas primerizas. Cuando las cerdas primerizas se inseminaron el día 5, hubo una diferencia temporal entre las réplicas. El día 5, las cerdas primerizas de la réplica 1, se inseminaron después de 7,5 a 11 horas del tratamiento con OvuGel™. Las cerdas primerizas inseminadas el día 5 en la réplica 2 se cruzaron después de 2,25 a 4,5 horas de la administración de OvuGel™. Debido a esta diferencia, las medias mínimas cuadráticas y el análisis estadístico de los datos de embarazos, partos y nacimientos vivos de las réplicas se presentan en la Tabla 9. No hubo tratamiento por interacciones de réplicas (P> 0,60) para ninguna de estas variables y solo una hubo una tendencia (P <0,09) para un efecto replicado para el índice de partos. En las Tablas 10 a 13, se muestran datos sin procesar y medias no ajustadas. Como se muestra en la Tabla 5, el porcentaje de cerdas primerizas preñadas 30 días después de la inseminación fue el mismo para todos los tratamientos (P>0,94), al igual que el porcentaje de cerdas primerizas que parieron (P>0,79). El total de lechones nacidos por camada (P>0,74) y de lechones nacidos vivos por camada (P> 0,44) no fue diferente entre los tratamientos. Tampoco hubo ninguna diferencia de tratamiento en el índice de lechones (P>0,80). La Tabla 6 presenta las medias mínimas cuadráticas para la expresión del estro después de alimentación con MATRIX®. No hubo diferencias debido al tratamiento en el porcentaje de cerdas primerizas que expresaron estro el día 5 (P>0,35) o el día 6 (P>0,15).
En la Tabla 7 se muestra el índice de gestación basado en cuándo las cerdas primerizas expresaban estro. Las cerdas primerizas de control y del tratamiento 2 que expresaron estro el día 5, tuvieron un mayor porcentaje de gestación a los 30 días que las cerdas primerizas del Tratamiento 3 (P <0,04). Hubo una tendencia (P = 0,10) a un mayor porcentaje de gestación entre las cerdas primerizas de Control que expresaron estro el día 6, en comparación con las cerdas primerizas en los Tratamientos 2 y 3. Sin embargo, al comparar el índice de gestación general de
todas las cerdas primerizas que expresaban estro, no hubo diferencias entre los tratamientos (P>0,94). La Tabla 8 muestra el índice de partos de cerdas primerizas en función de cuándo expresaban estro por primera vez. La única diferencia entre los tratamientos es para las cerdas primerizas que expresaron estro el día 5. En el Tratamiento 2, esas cerdas primerizas tuvieron un mayor índice de partos (P <0,03) que el de las cerdas primerizas de Control o Tratamiento 3 (94,1 % frente a 76,0 y 66,7 %, respectivamente).
Los resultados de este estudio demuestran que el índice de partos y el tamaño de la camada en cerdas primerizas inseminadas a un tiempo establecido después del tratamiento con MATRIX® y OvuGel™, no son diferentes de los de las cerdas primerizas inseminadas cuando se detecta el estro después del tratamiento con MATRIX®. Estos datos están también en consonancia con ensayos previos en cerdas destetadas en las que del 30 al 60 % de las cerdas maduras o cerdas primerizas que no expresaron estro, concibieron después de la inseminación a un tiempo establecido. El momento de inseminación los días 5 y 6 está en consonancia con el tiempo de los datos de ovulación observados en los ensayos del Ejemplo 1.
Este protocolo se realizó en dos lugares distintos con resultados diferentes. Todas las cerdas primerizas del primer lugar habían expresado estro un mínimo de tres veces y muchas de ellas habían pasado por 4 o 5 ciclos estrales antes de comenzar con MATRIX®. Las cerdas primerizas del segundo lugar solo tuvieron un estro confirmado antes de comenzar con MATRIX®. En el otro lugar, el índice de partos de las cerdas primerizas de control fue más alto que el de las cerdas primerizas tratadas con OvuGel™. La diferencia de edad de las cerdas primerizas podría haber contribuido a la diferencia en los resultados. Un promedio de 30,1 % de las cerdas primerizas más mayores en el primer lugar, expresó estro por primera vez el día 5 después de alimentación con MATRIX®. Solo el 7,4% de las cerdas primerizas más jóvenes en el segundo lugar mostró estro el día 5. El día 7 después de alimentación con MATRIX®, solo el 16,2 % de las cerdas primerizas de Control más mayores y el 2 % de las cerdas primerizas más mayores que recibieron OvuGel ™ expresaban estro por primera vez. En el segundo lugar, entre las cerdas primerizas más jóvenes aún había un 41,3% de las cerdas primerizas de Control y un 18,3% de las cerdas primerizas tratadas con OvuGel™ que expresaban estro por primera vez el Día 7.
Los resultados en el primer lugar, con cerdas primerizas sexualmente maduras, demuestran que OvuGel™ administrado a ~ 120 horas después de la última alimentación con MATRIX® y seguido de una inseminación condicional el día 5 junto con una inseminación a un tiempo establecido el día 6 o una doble inseminación a un tiempo establecido el día 5 y el día 6, da como resultado un índice de partos y un tamaño de camada similares en comparación con las cerdas primerizas inseminadas después de la detección del estro.
Tabla 5. Rendimiento de cerdas rimerizas
Tabla 6. Ex resión del estro des ués de alimentación con MATRIX®
Los controles de estro no fueron fiables en las cerdas primerizas que recibieron OvuGel™ (tratamientos 2 y 3) después del día 6. Los controles del estro continuaron en las cerdas de Control hasta que todas ellas expresaron el estro y se aparearon (9 a 32 días después de alimentación con MATRIX®).
T l Ín i i n n n l r rim riz x r n r
Las cerdas primerizas del Grupo 2 que expresaban estro el día 5 después de la alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
T l Ín i r n n l r rim riz x r n r
Las cerdas primerizas del Grupo 2 que expresaban estro el día 5 después de la alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
T l R n imi n r R li
Las cerdas primerizas del grupo 2 que expresaban estro el día 5 después de alimentación con MATRIX® recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro. Las cerdas primerizas de los Grupos 2 y 3 en la réplica 1 que se cruzaron el día 5, se inseminaron de 9,5 a 11 horas después del tratamiento con OvuGel™. Cerdas primerizas de la réplica 2 en los Grupos 2 y 3, se inseminaron el día 5, después de 2,25 a 4,5 horas de la administración de OvuGel™.
Tabla 10. Rendimiento - Medias no austadas
T l 11 Exr in l r l limn in n MATRIX - M i n
Los controles de estro no fueron fiables en las cerdas primerizas que recibieron OvuGel™ (tratamientos 2 y 3) después del día 6. Los controles del estro continuaron en las cerdas de Control hasta que todas ellas expresaron el estro y se aparearon (9 a 32 días después de alimentación con MATRIX®).
T l 12 Íni in n n l r rim riz xr n r - M i n
Las cerdas primerizas del Grupo 2 que expresaban estro el día 5 después de la alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
T l 1 Íni r n n l r rim riz xr n r - M i n
Las cerdas primerizas del Grupo 2 que expresaban estro el día 5 después de la alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
EJEMPLO 3
Diseño del estudio y tratamientos
Trescientas doce (312) cerdas primerizas se alimentaron durante 14 días con MATRIX® aplicado sobre el pienso a la tasa recomendada de 15 mg/cerda/día. La última alimentación con MATRIX® fue a las 6:30 AM (Día 0). Ciento cuatro cerdas primerizas se asignaron a cada uno de los siguientes tratamientos:
1. Grupo 1, Controles (n=104); tratadas con MATRIX®, pero no tratadas con OvuGel™, inseminadas diariamente durante el estro, como se practica normalmente en el sitio (promedio de 1,8 inseminaciones por cerda primeriza).
2. Grupo (n=104); tratadas con OvuGel™ a las 7:00 a.m. (+/-1,5 horas) el día 5 e inseminadas después de 2 a 4 horas del tratamiento con OvuGel™ el día 5 si expresan estro. Todas las cerdas primerizas se inseminaron una vez el Día 6, 26 horas (+/- 2 horas) después del tratamiento con OvuGel™, independientemente del estado estral.
3. Grupo 3 (n=104); tratadas con OvuGel™ a las 7:00 a.m. (+/- 1,5 horas) el Día 5 e inseminadas una vez después de 2 a 4 horas del tratamiento con OvuGel™ el Día 5 y nuevamente el Día 6, después de 26 horas (+/-2 horas) de tratamiento con OvuGel™, independientemente del estro en cualquiera de los días.
Sustancia de ensayo
La triptorelina (pGlu-His-Trp-Ser-Tyr-D-Trp-Leu-Arg-Pro-Gly-NH2) se suministró en forma de acetato, de Bachem, Torrance, CA (artículo H-4075 calidad CGMP). El gel de triptorelina (200 mcg/2 ml) se formuló en DPT Laboratories (San Antonio, Tejas) en un gel compuesto por Methocel Premium A4000 (Dow Chemical) y otros excipientes de formulación inactivos. Se envasaron cincuenta y cuatro mililitros de gel de triptorelina (100 mcg de acetato de triptorelina/ml) en viales de suero de vidrio de borosilicato ámbar (610206-50) con un tapón de goma de butilo de color gris para viales de suero farmacéutico (73828A-SS) con un sello de aluminio estándar (SAS20NAT).
Observación del estro
Las cerdas primerizas se instalaron en corrales individuales. Los verracos se instalaron al menos a 12 m de distancia y a favor del viento. Para determinar la aparición y la duración del estro, diariamente se observó el estro de las cerdas primerizas desde 4 días hasta 8 días después de la última alimentación con MATRIX® o hasta que se confirmó el final del estro, lo que ocurriera primero. Para facilitar la detección del estro, un verraco maduro se paseaba lentamente por el callejón frente al corral de la cerda primeriza, exponiendo cada cerda primeriza, durante hasta 5 minutos, a señales visuales, auditivas y olfativas del verraco. Mientras que el verraco estaba cerca frente al corral de la cerda primeriza, un experto comprobaba el estro aplicando presión dorsal en la sección central de la cerda primeriza combinado con frotamiento lateral. El estro se confirmó cuando una cerda primeriza se mantuvo rígida a la presión dorsal, sin vocalización y con algún indicio de reflejo auditivo.
Administración de fármacos
Con un catéter similar a los utilizados para la inseminación artificial, se depositó una sola dosis de 2 ml de OvuGel™ a una distancia de aproximadamente 1 a 2 cm posteriores al cuello uterino. La dosis se suministró utilizando un aplicador multidosis estándar conectado al catéter. Para cada cerda primeriza, se utilizaba una funda desechable nueva, que rodeaba el catéter.
Análisis estadístico
Los datos se sometieron a análisis de varianza utilizando el procedimiento de SAS PROC MIX (versión 9,2) para determinar el efecto principal del tratamiento, réplica, sitio, tratamiento por sitio, y tratamiento por interacción de réplicas sobre el índice de partos y el tamaño de la camada. Las diferencias entre los tratamientos se analizaron sobre estimaciones de medias mínimas cuadráticas utilizando la prueba T a P <0,05.
Resultados
Trescientas doce (312) cerdas primerizas se asignaron a grupos de tratamiento (Grupo 1: 104, Grupo 2: 104, Grupo 3: 104). Dado que dos equipos diferentes recogieron estos datos en dos sitios diferentes dentro de la granja, los datos de gestación, parto y tamaño de la camada, se analizaron para determinar el efecto del sitio y el sitio por interacciones de tratamiento. No hubo ningún efecto del sitio sobre el número de lechones nacidos vivos (P> 0,94), cerdas preñadas a los 30 días (P> 0,77) o índice de parto (P> 0,68). Tampoco hubo ningún tratamiento por interacción del sitio (P> 0,46) para ninguna de estas variables. Por tanto, los datos presentados en las Tablas 14 a 21 muestran los resultados combinados de ambos sitios. Las tablas 14 a 17 presentan las medias mínimas cuadráticas y el análisis estadístico de todas las cerdas primerizas. En las Tablas 18 a 21 se muestran datos sin procesar y medias no ajustadas.
El porcentaje de cerdas primerizas preñadas a los 30 días en la Tabla 14 fue mayor (P <0,02) para el grupo Control (91,3%) que para el Grupo 2 o 3 (76,9 y 82,7%, respectivamente). Las cerdas primerizas de Control también tuvieron mayor índice de partos (P <0,01) en comparación con el de las cerdas primerizas en los Grupos 2 y 3
(90,1 %, 72,8 % y 80,8 %, respectivamente). El número promedio de lechones nacidos vivos por camada (P> 0,22) y el total de lechones nacidos por camada (P> 0,28) no fue diferente entre los grupos. El índice de lechones fue mayor (P <0,02) para las cerdas primerizas en el grupo de Control (989) en comparación con el de las cerdas primerizas en el Grupo 2 (773) o el Grupo 3 (822).
La Tabla 15 presenta las medias mínimas cuadráticas para la expresión del estro después de alimentación con MATRIX®. No hubo diferencias entre los tratamientos en cuanto al porcentaje de cerdas primerizas que expresaron estro los días 5 y 6 después de la alimentación con MATRIX® (P> 0,53), aunque las cerdas primerizas de Control tuvieron un porcentaje más alto (P <0,0001) que expresaba estro por primera vez el Día 7 (41,3 %) que el de los Grupos 2 y 3 (16,3 y 20,2 %, respectivamente). Las cerdas primerizas tratadas con OvuGel™ (Grupos 2 y 3) tuvieron un mayor porcentaje (P <0,0001) de no expresión del estro el Día 8 después de la alimentación con MATRIX® (26,0 y 23,1 %, respectivamente) que el grupo de Control (2,9 %).
En la Tabla 16 se muestra el índice de gestación basado en cuándo las cerdas primerizas expresaban estro. No hubo diferencias en el índice de gestación entre los tratamientos en las cerdas primerizas que expresaron estro por primera vez los días 5 y 6 (P>0,16). Las cerdas primerizas de control que expresaron estro en el día 7, tuvieron un mayor porcentaje (P <0,003) de gestación a los 30 días (97,7 %) que las cerdas primerizas del Grupo 2 (64,7 %). La Tabla 17 muestra el índice de partos de cerdas primerizas en función de cuándo expresaban estro por primera vez. Las cerdas primerizas de control que expresaron estro el día 7, tuvieron un mayor porcentaje (P <0,003) de partos (97,7 %) que las cerdas primerizas del Grupo 2 (64,7 %). Las cerdas primerizas tratadas con OvuGel™ en los Grupos 2 y 3 que no expresaban estro, tuvieron un índice de partos de aproximadamente 78 % (40 cerdas las 51 que no expresaban estro, parieron).
Los resultados en esta granja, demuestran que OvuGel™ administrado a ~ 120 horas después de la última alimentación con MATRIX® (Día 0) y seguido de una inseminación condicional dependiente del estro el día 5 junto con una inseminación a un tiempo establecido el día 6 o una doble inseminación a un tiempo establecido el día 5 y el día 6, da como resultado un tamaño de camada similar en comparación con el de las cerdas primerizas inseminadas diariamente durante el estro.
Tabla 14. Rendimiento de hembras rimerizas
Incluye solo datos de gestación y parto de las cerdas primerizas cruzadas 8 días después de alimentación con MATRIX®.
Tabla 15. Ex resión del estro des ués de alimentación con MATRIX®
T l 1 Ín i i n n n l r rim riz x r n r
Las cerdas primerizas del Grupo 2 que expresaban estro el día 5 después de la alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
T l 1 Íni r n n l r rimriz xr n r
Las cerdas primerizas del grupo 2 que expresaban estro el d 5 después de alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
Tabla 18. Rendimiento - Medias no austadas
Incluye solo datos de gestación y parto de las cerdas primerizas cruzadas 8 días después de alimentación con MATRIX®.
T l 1 Exr in l r l limn in n MATRIX - M i n
T l 2 Ín i i n n n l r rim riz x r n r - M i n
Las cerdas primerizas del grupo 2 que expresaban estro el d 5 después de alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
T l 21 Ín i r n n l r rim riz x r n r - M i n
Las cerdas primerizas del grupo 2 que expresaban estro el d 5 después de alimentación con MATRIX®, recibieron 2 inseminaciones, el Día 5 y Día 6. Todas las demás cerdas primerizas del Grupo 2 recibieron solo una única inseminación el día 6. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 5 y el Día 6, independientemente de cuándo se expresaba el estro.
EJEMPLO 4
Diseño del estudio y tratamientos
Trescientas (300) cerdas primerizas se alimentaron durante 14 días con MATRIX® aplicado sobre el pienso a la tasa recomendada de 15 mg/cerda/día. La última alimentación con MATRIX® fue a las 7:00 AM (Día 0). Se asignaron cien cerdas primerizas a cada uno de los siguientes tratamientos:
1. Grupo 1, Controles (n=100); tratadas con MATRIX®, pero no tratadas con OvuGel™, inseminadas diariamente después de la detección de estro, como se practica normalmente en el sitio (número promedio de inseminaciones por cerda primeriza = 1,9).
2. Grupo (n=100); tratadas con OvuGel™ a las 8:00 a.m. (+/-1 h) el día 5 e inseminadas después de 4 a 6 horas de tratamiento con OvuGel™ el Día 5, independientemente del estado estral.
3. Grupo 3 (n=100); tratadas con OvuGel™ a las 8:00 a.m. (+/-1 hora) el Día 5 e inseminadas el día 6, después de 25 horas (+/-1 hora) de tratamiento con OvuGel™, sin tener en cuenta el estro.
Sustancia de ensayo
La triptorelina (pGlu-His-Trp-Ser-Tyr-D-Trp-Leu-Arg-Pro-Gly-NH2) se suministró en forma de acetato, de Bachem, Torrance, CA (artículo H-4075 calidad CGMP). El gel de triptorelina (200 mcg/2 ml) se formuló en DPT Laboratories (San Antonio, Tejas) en un gel compuesto por Methocel Premium A4000 (Dow Chemical) y otros excipientes de formulación inactivos. Se envasaron cincuenta y cuatro mililitros de gel de triptorelina (100 mcg de acetato de triptorelina/ml) en viales de suero de vidrio de borosilicato ámbar (610206-50) con un tapón de goma de butilo de color gris para viales de suero farmacéutico (73828A-SS) con un sello de aluminio estándar (SAS20NAT).
Observación del estro
Las cerdas primerizas se instalaron en corrales individuales. Los verracos se instalaron al menos a 12 m de distancia y a favor del viento. Para determinar la aparición y la duración del estro, diariamente se observaron cerdas
primerizas para detectar el estro desde 4 días hasta 8 días después de la última alimentación con MATRIX o hasta que se confirmó el final del estro, lo que ocurriera primero. Para facilitar la detección del estro, un verraco maduro se paseaba lentamente por el callejón frente al corral de la cerda primeriza, exponiendo cada cerda primeriza, durante hasta 5 minutos, a señales visuales, auditivas y olfativas del verraco. Mientras que el verraco estaba cerca frente al corral de la cerda primeriza, un experto comprobaba el estro aplicando presión dorsal en la sección central de la cerda primeriza combinado con frotamiento lateral. El estro se confirmó cuando una cerda primeriza se mantuvo rígida a la presión dorsal, sin vocalización y con algún indicio de reflejo auditivo.
Administración de fármacos
Con un catéter similar a los utilizados para la inseminación artificial, se depositó una sola dosis de 2 ml de OvuGel™ a una distancia de aproximadamente 1 a 2 cm posteriores al cuello uterino. La dosis se suministró utilizando un aplicador multidosis estándar conectado al catéter. Para cada cerda primeriza, se utilizaba una funda desechable nueva, que rodeaba el catéter.
Análisis estadístico
Los datos se sometieron a análisis de varianza utilizando el procedimiento de SAS PROC MIX (versión 9,2) para determinar el efecto principal del tratamiento, réplicas y tratamiento por interacción de réplicas sobre el índice de partos y el tamaño de la camada. Las diferencias entre los tratamientos se analizaron sobre estimaciones de medias mínimas cuadráticas utilizando la prueba T a P <0,05.
Resultados
Trescientas (300) cerdas se asignaron a grupos de tratamiento (Grupo 1: 100, Grupo 2: 100, Grupo 3: 100). Se retiraron dos cerdas primerizas de control del estudio debido a lesiones y se retiraron del conjunto de datos final. Las tablas 22 a 25 presentan las medias mínimas cuadráticas y el análisis estadístico de todas las primerizas. En las Tablas 26 a 29 se muestran datos sin procesar y medias no ajustadas.
Como se muestra en la Tabla 22, el porcentaje de cerdas primerizas, que expresaron estro el Día 8 después de la alimentación con MATRIX®, fue mayor (P <0,0001) para las cerdas primerizas de Control (90,8 %) en comparación con el de las cerdas de los Grupos 2 (72,0 %) y 3 (65,0 %). Las cerdas primerizas tratadas con OvuGel™ (Grupos 2 y 3) tuvieron un intervalo más corto (5,9 d) entre la alimentación con MATRIX® hasta el estro (P <0,01) en comparación con el de las cerdas primerizas de control (6,3 d). El porcentaje de cerdas primerizas preñadas 30 días después de la inseminación fue el mismo para todos los tratamientos (P>0,26). El porcentaje de cerdas primerizas que parieron no fue diferente (P> 0,16) entre los tratamientos, ni tampoco el índice de lechones (P>0,18), aunque las cerdas primerizas de Control tuvieron un índice de partos y un índice de lechones numéricamente más altos que los de los Grupos 2 y 3 (76,5 frente a 67,0 y 64,6 % y 888 frente a 727 y 789, respectivamente). Hubo una tendencia (P <0,09) de que las cerdas primerizas del Grupo 3 tuvieran más lechones nacidos vivos por camada que las cerdas primerizas de Control o del Grupo 2. El total de lechones nacidos por camada fue mayor (P <0,05) para las cerdas primerizas del Grupo 3 (13,5) que para las cerdas primerizas de Control (12,8) o las del Grupo 2 (11,9).
La Tabla 23 presenta las medias mínimas cuadráticas para la expresión del estro después de la alimentación con MATRIX®. Hubo más cerdas primerizas del Grupo 2 que expresaron estro el Día 5 (P <0,05, 23,0 %), pero no hubo diferencias debido al tratamiento el día 6 (P> 0,48). El día 7 después de la alimentación con MATRIX® hubo menos cerdas primerizas tratadas con OvuGel™ (Grupos 2 y 3) que expresaban estro por primera vez en comparación con las cerdas primerizas de Control (P <0,002). El porcentaje de cerdas primerizas que no expresan estro el día 9 después de la alimentación con MATRIX® fue mayor (P <0,0001) para los Grupos 2 y 3 en comparación con los Controles (24,0 %, 33,0 %, 8,2 %, respectivamente).
En la Tabla 24 se muestra el índice de gestación basado en cuándo las cerdas primerizas expresaban estro. Independientemente del tratamiento, las cerdas primerizas que expresaban estro los días 5, 6 y 7 tenían índices de gestación similares cada uno de los días (P> 0,73).
La Tabla 25 muestra el índice de partos de cerdas primerizas basado en cuándo expresaban estro por primera vez. Como se observa con los datos de gestación, las cerdas primerizas que expresaban estro los días 5, 6 o 7, independientemente del tratamiento, tuvieron índices de parto similares cada uno de los días. Las cerdas primerizas de los Grupos 2 y 3 que no expresaban estro, tenían un índice de partos de aproximadamente 49 %.
Los resultados indican que OvuGel™, administrado a ~ 120 horas después de la última alimentación con MATRIX®, y seguido de una sola inseminación el día 5 o de una sola inseminación el día 6, tiene índices de parto y tamaños de camada similares en comparación con las cerdas primerizas inseminadas después de la detección del estro.
T a b la 22. R e n d im ie n to de h e m b ra s rim eriza s
Incluye solo datos de gestación y parto de las cerdas primerizas cruzadas 8 días después de alimentación con MATRIX®.
Tabla 23. Exresión del estro desués de alimentación con MATRIX®
T l 24 Íni in n n l r rimriz xr n r
Todas las cerdas primerizas del Grupo 2 recibieron una inseminación el Día 5, independientemente de cuándo se expresaba el estro. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 6, independientemente de cuándo se expresaba el estro.
T l 2 Íni r n n l r rimriz xr n r
Todas las cerdas primerizas del Grupo 2 recibieron una inseminación el Día 5, independientemente de cuándo se expresaba el estro. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 6, independientemente de cuándo se expresaba el estro.
Tabla 26. Rendimiento - Medias no austadas
T l 2 Exr in l r l limn in n MATRIX - M i n
T l 2 Íni in n n l r rimriz xr n r - M i n
Todas las cerdas primerizas del Grupo 2 recibieron una inseminación el Día 5, independientemente de cuándo se expresaba el estro.
Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 6, independientemente de cuándo se expresaba el estro.
T l 2 Ín i r n n l r rim riz x r n r - M i n
Todas las cerdas primerizas del Grupo 2 recibieron una inseminación el Día 5, independientemente de cuándo se expresaba el estro. Todas las cerdas primerizas del Grupo 3 recibieron una inseminación el Día 6, independientemente de cuándo se expresaba el estro.
EJEMPLO 5
Diseño del estudio y tratamientos
Todas las cerdas primerizas se alimentaron individualmente durante 14 o 15 días con MATRIX® aplicado sobre el pienso a la tasa recomendada de 15 mg/cerda/día. A las cerdas primerizas se las retiró la alimentación con MATRIX® (dándose la última aplicación superficial la mañana del día 0) y se asignaron a cada uno de los siguientes tratamientos. Los controles se trataron con gel vehículo (gel vehículo sin triptorelina) 120 (+/- 2) horas después de retirar MATRIX® (última aplicación superficial). Las otras cerdas primerizas recibieron 100, 200 o 400 mcg de triptorelina en forma de acetato en una formulación en gel de metilcelulosa 120 (+/- 2) horas después retirar MATRIX®. Los cuatro tratamientos fueron:
1. Gel vehículo (VG, Vehicle Gel): gel vehículo sin triptorelina, 120 (+/- 2) horas después de retirar MATRIX®. 2. TG 100: 100 mcg (2 ml 50 mcg/ml) de gel de triptorelina, 120 (+/- 2) horas después de retirar MATRIX®.
3. TG 200: 200 mcg (2 ml 100 mcg/ml) de gel de triptorelina, 120 (+/- 2) horas después de retirar MATRIX®. 4. TG 400: 400 mcg (2 ml 200 mcg/ml) de gel de triptorelina, 120 (+/- 2) horas después de retirar MATRIX®. Sustancia de ensayo
La triptorelina (pGlu-His-Trp-Ser-Tyr-D-Trp-Leu-Arg-Pro-Gly-NH2) se suministró en forma de acetato, de Bachem, Torrance, CA (artículo H-4075 calidad CGMP). El gel de triptorelina (dosis de 100-400 mcg/2 ml) se formuló en Argenta (Auckland, NZ), en un gel compuesto por Methocel Premium A4000 (Dow Chemical), tampón citrato (pH 5,5), NaCl, metionina y metil y propil parabenos. Se envasaron cincuenta y cuatro mililitros de gel de triptorelina (100 mcg de acetato de triptorelina/ml) en viales de suero de vidrio de borosilicato ámbar (610206-50) con un tapón de goma de butilo de color gris para viales de suero farmacéutico (73828A-SS) con un sello de aluminio estándar (SAS20NAT). El vehículo de gel de triptorelina contenía los mismos excipientes de formulación que los incluidos en el gel de triptorelina, excepto que no contenía triptorelina. MATRIX® se suministró como la forma disponible en el comercio de los Estados Unidos.
Observación del estro
Para la detección del estro posterior al tratamiento, las cerdas primerizas se instalaron en corrales individuales. Los verracos (cerdos macho) se instalaron en salas distintas y/o al menos a 12 m de distancia y a favor del viento. Para provocar señas de estro, un verraco maduro se paseaba lentamente por el callejón frente a los corrales de las cerdas primerizas, exponiendo cada cerda primeriza de ensayo, durante hasta 5 minutos, a señales visuales, auditivas y olfativas del verraco. Conforme a la práctica estándar en granjas comerciales, mientras que el verraco estaba cerca frente al corral de la cerda primeriza, un experto comprobaba el estro aplicando presión dorsal en la sección central de la cerda primeriza combinado con frotamiento lateral. El estro se confirmó cuando una cerda primeriza se mantuvo rígida a la presión dorsal, sin vocalización y con algún indicio de reflejo auditivo. Las cerdas primerizas no estuvieron expuestas a los verracos durante los primeros tres días después de la retirada de MATRIX® (Día 0 al día 2). La detección del estro se realizó diariamente en todas las cerdas primerizas desde el día 3 hasta el día 7.
Control de la ovulación
La ovulación se controló dos veces el Día 5 (8 horas y 16 horas después del tratamiento) y cada 8 horas el Día 6 y el Día 7 o hasta que se confirmó la ovulación o 176 horas después de la última alimentación con MATRIX®. El estado ovulatorio de todas las cerdas primerizas se controló mediante ecografía transrectal. Para ello se utilizó un ecógrafo Aloka 500, con un transductor de matriz lineal de 7,5 MHz unido a una varilla estabilizadora de PVC de ángulo fijo para facilitar la inserción en el recto. El transductor y la varilla de PVC se recubren con un lubricante ginecológico y se insertan suavemente en el recto hasta que puedan visualizarse los ovarios, al mismo tiempo. En cada exploración, se registraron los diámetros de los tres folículos más grandes (con una precisión de 0,1 mm). Cuando el número de folículos grandes (> 6,5 mm) disminuyó a menos de 3, se confirmaba que una cerda primeriza había ovulado.
Extracción de sangre y análisis de HL
Se insertó un catéter de forma no quirúrgica en la vena yugular (Kraeling et al. 1982) de una subpoblación de cerdas primerizas de cada grupo de tratamiento (gel vehículo, n = 8; 100 mcg de triptorelina, n=6; 200 mcg de triptorelina, n=7 y 400 mcg de triptorelina, n=6). Se extrajeron muestras de sangre de diez ml cada 15 minutos durante una hora antes del tratamiento, inmediatamente después del tratamiento (0) y 0,5, 1, 2, 4, 6, 12, 18, 24, 36 y 48 horas después del tratamiento. Las muestras de sangre se conservaron a 4° C hasta que se centrifugaron a 800 x g durante 15 minutos, 12 horas después de la extracción. El suero resultante se conservó congelado hasta que se analizó la HL utilizando procedimientos validados para suero porcino (Kesner et al., 1987 y Kraeling et al., 1982). Se analizó la aparición, la duración y la magnitud del aumento de HL. Los datos de la HL se analizaron con el procedimiento de SAS de Modelos lineales generales. Las diferencias entre los tratamientos se analizaron sobre estimaciones de medias mínimas cuadráticas utilizando la prueba T a P <0,05. La aparición del aumento de HL es cuando la concentración de HL en suero es mayor o igual a dos desviaciones estándar de la media de las concentraciones de HL en suero previas al tratamiento. La duración del aumento de HL es el período entre la aparición y cuando la concentración de HL en suero es de nuevo menor o igual a dos desviaciones estándar de la media de las concentraciones de HL en suero previas al tratamiento. La magnitud del aumento de HL es la concentración máxima de HL en suero alcanzada durante el aumento de HL.
Administración
Con un catéter similar a los utilizados para la inseminación artificial, se depositó una sola dosis de 2 ml de gel de triptorelina o gel vehículo a una distancia de aproximadamente 1 a 2 cm posteriores al cuello uterino. La dosis se suministró utilizando un aplicador multidosis estándar conectado al catéter. Para cada cerda primeriza, se utilizaba una funda desechable nueva, que rodeaba el catéter.
Resultados
En este estudio, las cerdas primerizas tenían 171 ± 7 días de vida y un peso corporal de 130 ± 9 kg en la última alimentación con MATRIX®. El porcentaje de cerdas primerizas que expresaron estro después de la última alimentación con MATRIX® (97 %) y el intervalo desde la última alimentación con MATRIX® hasta el estro (146 ± 22 horas) no difirió entre los tratamientos. Se retiraron ocho cerdas primerizas del conjunto de datos final por razones no relacionadas con el tratamiento. No se detectaron interacciones de réplica por tratamiento en ninguno de los parámetros medidos y, por lo tanto, los datos se combinaron para las dos réplicas. Los resultados se presentan en la Figura 4 y las Tablas 30-32.
En general, el 94 % de las cerdas primerizas ovularon dentro del período experimental. En los grupos de tratamiento con gel de triptorelina (TG) en comparación con el gel vehículo (VG) 48 horas después del tratamiento o 168 horas después de la última alimentación con MATRIX®, ovularon más cerdas primerizas (P <0,01). El intervalo desde la última alimentación con MATRIX® hasta la ovulación no se vio afectado por el tratamiento y como promedio fue de 160 horas o 6,7 días. No hubo ningún efecto del tratamiento en el porcentaje acumulativo de cerdas primerizas, que ovularon entre 128 y 152 horas después de la última alimentación con MATRIX® (32 horas después del tratamiento). Sin embargo, hubo un efecto de tratamiento significativo sobre el porcentaje acumulativo de primerizas, que ovularon entre 160 y 176 horas después de la última alimentación con MATRIX® (40-56 horas después del tratamiento). Un porcentaje acumulativo más alto de cerdas primerizas ovularon en 168 horas (48 horas después del tratamiento) en los grupos tratados en comparación con el grupo tratado con gel vehículo (Tabla 30). En la Tabla 30 se muestra el momento en el que se detectó la ovulación y el porcentaje de cerdas primerizas que ovularon en cada observación ecográfica después del tratamiento con gel de triptorelina. No hubo diferencias significativas en la hora media en que se detectó la ovulación después del tratamiento con gel de triptorelina entre ningún grupo de tratamiento. El porcentaje de cerdas primerizas que ovularon 48 horas después del tratamiento con gel de triptorelina fue mayor para las cerdas primerizas que recibieron triptorelina en comparación con los controles, aunque no fue diferente entre los grupos de tratamiento con triptorelina (P> 0,05).
Los resultados demuestran que las dosis de gel de triptorelina entre 100-400 mcg de triptorelina promueven la ovulación en comparación con el vehículo, 168 horas después de la última alimentación con MATRIX®, sugiriendo que este intervalo de dosis de gel de triptorelina es eficaz en cerdas primerizas para sincronizar la ovulación después de la sincronización del ciclo estral con MATRIX®.
En un estudio previo, se demostró que 100 mcg de triptorelina en gel de triptorelina estimulaban la liberación de HL en cerdas primerizas ovariectomizadas sensibilizadas con estrógenos. En la Tabla 31 se muestra el número de cerdas primerizas que mostraron un aumento de HL, parámetros del aumento de HL, tiempo en que se detectó la ovulación y porcentaje de primerizas que ovularon 48 horas después del tratamiento con gel de triptorelina que contenía 0, 100, 200 o 400 mcg de acetato de triptorelina. No hubo diferencias significativas en la aparición media del aumento de HL, tiempo hasta la concentración máxima en suero de HL o la magnitud del aumento de HL entre los grupos de tratamiento. Sin embargo, la duración del aumento de HL fue mayor (P = 0,04) en el grupo de 0 mcg en comparación con las cerdas primerizas tratadas. En general, estos parámetros del aumento de HL fueron similares a los de nuestro estudio anterior en donde la administración intravaginal de triptorelina en gel de triptorelina estimuló la liberación del aumento de HL en cerdas primerizas ovariectomizadas sensibilizadas con estrógenos. Cuando se examinaron los datos de las cerdas primerizas individuales, parecía que esas cerdas, que no mostraron un aumento de HL durante el período de toma de muestras de sangre, estaban completando un aumento de HL en el momento del tratamiento con gel de triptorelina o pueden haber tenido ya un aumento de HL antes del tratamiento con gel de triptorelina. Aunque el análisis estadístico no reveló diferencias significativas entre los grupos de tratamiento durante la aparición del aumento de HL, tiempo hasta la concentración máxima de HL en suero o la magnitud del aumento de HL, las tres medias de estos parámetros sugieren que el aumento de HL se produjo antes en las cerdas primerizas tratadas con triptorelina que en las cerdas primerizas de control tratadas con 0 mcg. Además, la magnitud del aumento de HL pareció seguir un patrón de respuesta a la dosis. Similar a datos presentados para todas las cerdas primerizas en la Tabla 30, el porcentaje de cerdas primerizas, que ovularon 48 horas después del tratamiento con gel de triptorelina, fue mayor para las cerdas primerizas que recibieron triptorelina que para las de control.
En su conjunto, hubo un efecto beneficioso de los tratamientos con gel de triptorelina sobre la sincronía de la ovulación desde la última alimentación con MATRIX®. Los resultados también demuestran que las dosis de gel de triptorelina entre 100-400 mcg de triptorelina, administradas 120 horas después de la última alimentación con MATRIX®, promovió la ovulación en comparación con el vehículo 168 horas después de la última alimentación con MATRIX®, sugiriendo que este intervalo de dosis de gel de triptorelina es eficaz en cerdas primerizas para sincronizar la ovulación después de la sincronización del ciclo estral con MATRIX®. Los datos de HL en suero están en consonancia con estas conclusiones.
Tabla 30. Medias mínimas cuadráticas para las variables de respuesta medidas para cerdas primerizas después de la alimentación con MATRIX® asignadas para recibir vehículo, 100, 200 o 400 mcg de triptorelina como gel de tri torelina TG 120 horas des ués de retirar MATRIX®.
La réplica es significativa en el intervalo de Matrix a Estro, Intervalo de Matrix a OV, MOV 144 y MOV 152.
Tabla 31. Número de cerdas primerizas que muestran un aumento de HL, parámetros del aumento de HL, tiempo (horas) en que se detectó la ovulación y porcentaje de primerizas, que ovularon 48 horas después del tratamiento con tri torelina ue contenía 0 100 200 o 400 mc de tri torelina.
* Media Mínima Cuadrática ± DE
Tabla 32. Promedios sin procesar de las variables de respuesta medidas en cerdas primerizas después de la alimentación con MATRIX® asignadas para recibir un vehículo (V), 100, 200 o 400 mcg de triptorelina (T) 120 horas des ués de retirar MATRIX® inclu e la re 3 de PTK 1-07.
EJEMPLO 6
Preparación de la composición que contiene triptorelina
Se añadieron sal sódica de metilparabeno y sal sódica de propilparabeno al agua purificada con mezcla y la mezcla continuó durante 5-10 minutos. Después, se añadió cloruro de sodio USP con mezcla durante otros 10-15 minutos seguido de la adición de L-metionina con mezcla durante 10-15 minutos. Después, también se añadió citrato de sodio USP con mezcla durante otros 10-20 minutos.
En un mezclador distinto, se añadió ácido cítrico al agua purificada y se mezcló 5-10 minutos antes de la adición de acetato de triptorelina, y la mezcla continuó después durante 10-20 minutos. La composición que contenía parabeno se añadió después a la composición que contenía triptorelina y se mezcló durante 10-15 minutos. después, se añadió metilcelulosa lentamente para impedir la aglomeración y la mezcla continuó durante otros 30-60 minutos. Después, se verificó el pH de la mezcla y para ajustar el pH de la composición se añadió ácido cítrico en agua
purificada según fuera necesario.
EJEMPLO 7
EJEMPLOS DE FORMULACIONES
En las Tablas 33 y 34 se muestran ejemplos de formulaciones de la composición descrita en la presente solicitud.
Tabla 33
Ingrediente Función Peso (% en p/v) Metilparabeno, sal sódica (USNF) Conservante antimicrobiano 0,0900 Propilparabeno, sal sódica (USNF) Conservante antimicrobiano 0,0100 Cloruro de sodio, reactivo de laboratorio Agente de tonicidad 0,910 Citrato de sodio, dihidrato Agente tamponador 0,186 L-metionina, reactivo de laboratorio Agente estabilizante 0,100 Ácido cítrico, anhidro Tampón 0,0700 Acetato de triptorelina Principio farmacéutico activo (PFA) 0,0100 Agua (USNF) Solvente de disolución 98,4 Metilcelulosa (A4M Premium) (USP) Agente espesante 1,20 Tabla 34.
Componente Norma de calidad Función Cantidad por 100 mg % en p/p
Acetato de triptorelina Producción propia far S
m
u
a
s
c
ta
o
n
ló
c
g
ia
ica 11,0 mg 0,011 %* Agua purificada USP Disolvente 97,6 g 97,54 %* Metilparabeno, Sal Sódica** NF Conservante 89,0 mg 0,089%* Propilparabeno, Sal Sódica ** NF Conservante 10,0 mg 0,010* Cloruro de Sodio USP A
o
g
n
e
i
n
c
t
id
e
a
d
d e 90 t 1 mg 0,901 %* L-metionina USP Agente
estabilizante 99,0 mg 0,099%* Citrato de sodio USP Agente
tamponador 184 mg 0,184 %* Ácido cítrico USP Agente
tamponador 69,0 mg 0,069%* Metilcelulosa USP Modifi
o
c
s
a
i
d
d
o
a
r
d de 1,1 g visc 1,10 %* *Cantidad nominal
**Analizado para estándar farmacopéico
Claims (17)
1. Un método para sincronizar el tiempo de ovulación y el tiempo de inseminación en una cerda primeriza, comprendiendo el método las etapas de:
administrar a la cerda primeriza una hormona de sincronización del estro;
administrando a la cerda primeriza una sola dosis de hormona liberadora de gonadotropina para sincronizar la ovulación, sin tener que administrar ninguna otra hormona para sincronizar la ovulación, en donde para sincronizar el estro, la hormona liberadora de gonadotropina se administra el quinto día después de la última administración diaria de la hormona; e
inseminar a la cerda primeriza, sin controlar el estro, solo una vez el sexto día después de la última administración diaria de la hormona de sincronización del estro.
2. El método según la reivindicación 1, en donde la hormona liberadora de gonadotropina tiene la fórmula
R1 y R2 son independientemente en cada caso hidrógeno, o se seleccionan independientemente del grupo que consiste en alquilo, heteroalquilo, cicloalquilo, heterocicloalquilo, haloalquilo, arilo, heteroarilo, arilalquilo y heteroarilalquilo, cada uno de los cuales está opcionalmente sustituido, o R1 y R2 y el carbono unido forman un carbociclo o heterociclo;
R5 es hidrógeno o alquilo; y
X es hidrógeno, o X se selecciona del grupo que consiste en alquilo, cicloalquilo, heteroalquilo, alquilenocarboxamida opcionalmente sustituida y HNC(O)NR3R4, donde R3 y R4 en cada caso se seleccionan independientemente del grupo que consiste en hidrógeno, alquilo, heteroalquilo y haloalquilo.
3. El método según la reivindicación 2, en donde la hormona liberadora de gonadotropina se selecciona del grupo que consiste en compuestos de la fórmula de la reivindicación 2, en donde
a) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
b) R1 es hidrógeno, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
c) R1 es 1H-1-bencil-imidazol-4-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
d) R1 es 2-metilpropilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
e) R1 es 2-naftilmetilo, R2 es hidrógeno, X es CH2(CO)NH2; y R5 es hidrógeno;
f) R1 es t-butoximetilo, R2 es hidrógeno, X es etilo; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
g) R1 es bencilo, R2 es hidrógeno, X es CH2(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
h) R1 es t-butoximetilo, R2 es hidrógeno, X es HN(CO)NH2; y R5 es hidrógeno;
i) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; y R5 es hidrógeno;
j) R1 es metilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
k) R1 es 1H-indol-3-il-metilo, R2 es hidrógeno, X es etilo; R5 es metilo; y la configuración del carbono al que está unido R1 es R;
l) R1 es metilo, R2 es hidrógeno, X es CH2(CO)NH2 ; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
m) R1 es 4-aminobutilo, R2 es hidrógeno, X es HN(CO)NH2; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R;
n) R1 es metilo, R2 es metilo, X es HN(CO)NH2 ; y R5 es hidrógeno; y
o) R1 es etilo, R2 es hidrógeno, X es hidrógeno; R5 es hidrógeno; y la configuración del carbono al que está unido R1 es R.
4. El método según una cualquiera de las reivindicaciones 1 a 3, en donde la inseminación es una inseminación artificial.
5. El método según una cualquiera de las reivindicaciones 1 a 4, en donde la hormona liberadora de gonadotropina se administra en una cantidad eficaz y la cantidad eficaz de la hormona liberadora de gonadotropina es de aproximadamente 200 |jg.
6. El método según una cualquiera de las reivindicaciones 1 a 5, en donde la dosis de la hormona liberadora de gonadotropina se administra utilizando un método seleccionado del grupo que consiste en el uso de un catéter de deposición, administración manual e inyección.
7. El método de la reivindicación 6, en donde la hormona liberadora de gonadotropina se administra utilizando un catéter de deposición.
8. El método de la reivindicación 6, en donde la hormona liberadora de gonadotropina se administra por inyección.
10. El método de una cualquiera de las reivindicaciones 1 a 9, en donde la hormona liberadora de gonadotropina es triptorelina.
11. El método de una cualquiera de las reivindicaciones 1 a 10, en donde la hormona que sincroniza el estro es altrenogest.
12. El método de una cualquiera de las reivindicaciones 1 a 11, en donde la hormona liberadora de gonadotropina está en una composición y la composición comprende metilparabeno en una cantidad de 0,09% en peso por volumen, propilparabeno en una cantidad de 0,01 % en peso por volumen, cloruro de sodio en una cantidad de 0,91 % en peso por volumen, citrato de sodio en una cantidad de 0,186 % en peso por volumen, L-metionina en una cantidad de 0,1 % en peso por volumen, ácido cítrico en una cantidad de 0,07 % en peso por volumen, triptorelina en una cantidad de 0,01 % en peso por volumen, y metilcelulosa en una cantidad que proporciona una viscosidad de 250 cP a 400 cP.
13. El método según una cualquiera de las reivindicaciones 1 a 11, en donde la hormona liberadora de
gonadotropina está en un excipiente seleccionado del grupo que consiste en solución salina tamponada, un alcohol líquido, un glicol, una solución de glucosa, un éster, una amida y agua estéril y en donde el excipiente comprende además un agente tamponador de pH seleccionado del grupo que consiste en un tampón de acetato, un tampón de borato, un tampón de carbonato, un tampón de citrato, un tampón de fosfato, ácido clorhídrico, hidróxido de sodio, oxido de magnesio, fosfato monopotásico, bicarbonato, amoniaco, ácido carbónico, citrato de sodio, ácido cítrico, ácido acético e hidrogenofosfato disódico.
14. El método de una cualquiera de las reivindicaciones 1 a 13, en donde la hormona liberadora de gonadotropina se administra de 125 a 133 horas o de 126 a 130 horas después de la última administración diaria de la hormona de sincronización del estro.
15. El método de una cualquiera de las reivindicaciones 1 a 14, en donde la hormona liberadora de gonadotropina se administra 126 horas después de la última administración diaria de la hormona de sincronización del estro.
16. El método de una cualquiera de las reivindicaciones 1 a 15, en donde la cerda primeriza se insemina de 24 a 28 horas después de la administración de la hormona liberadora de gonadotropina.
17. El método de una cualquiera de las reivindicaciones 1 a 15, en donde la cerda primeriza se insemina de 20 a 24 horas después de la administración de la hormona liberadora de gonadotropina.
Applications Claiming Priority (2)
| Application Number | Priority Date | Filing Date | Title |
|---|---|---|---|
| US201261730763P | 2012-11-28 | 2012-11-28 | |
| PCT/US2013/072359 WO2014085674A1 (en) | 2012-11-28 | 2013-11-27 | Method for synchronizing time of insemination in gilts |
Publications (1)
| Publication Number | Publication Date |
|---|---|
| ES2808409T3 true ES2808409T3 (es) | 2021-02-26 |
Family
ID=50828486
Family Applications (1)
| Application Number | Title | Priority Date | Filing Date |
|---|---|---|---|
| ES13859305T Active ES2808409T3 (es) | 2012-11-28 | 2013-11-27 | Método para sincronizar el tiempo de inseminación en cerdas primerizas |
Country Status (17)
| Country | Link |
|---|---|
| US (2) | US9724380B2 (es) |
| EP (1) | EP2925339B1 (es) |
| JP (1) | JP2016508030A (es) |
| KR (1) | KR20150095715A (es) |
| CN (2) | CN113398243A (es) |
| AU (1) | AU2013352054A1 (es) |
| BR (1) | BR112015012453A8 (es) |
| CA (1) | CA2892762C (es) |
| CL (1) | CL2015001448A1 (es) |
| CR (1) | CR20150282A (es) |
| DK (1) | DK2925339T3 (es) |
| ES (1) | ES2808409T3 (es) |
| MX (1) | MX367876B (es) |
| PH (1) | PH12015501187A1 (es) |
| RU (1) | RU2015125549A (es) |
| WO (1) | WO2014085674A1 (es) |
| ZA (1) | ZA201504552B (es) |
Families Citing this family (9)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| ES2555681T3 (es) | 2003-10-03 | 2016-01-07 | Thorn Bioscience, Llc | Procedimiento para la sincronización de la ovulación para la fecundación programada sin detección del celo |
| EP2421545B1 (en) | 2009-04-23 | 2017-12-06 | JBS United Animal Health II LLC | Method and composition for synchronizing time of insemination |
| ES2808409T3 (es) | 2012-11-28 | 2021-02-26 | United Ah Ii Llc | Método para sincronizar el tiempo de inseminación en cerdas primerizas |
| WO2015081157A1 (en) * | 2013-11-27 | 2015-06-04 | Jbs United Animal Health Ii Llc | Method and composition for synchronizing time of insemination in gilts |
| CN107173329A (zh) * | 2017-07-07 | 2017-09-19 | 宣汉县蜀宣花牛养殖专业合作社 | 一种蜀宣花牛母牛繁殖方法 |
| CN108853484B (zh) * | 2018-07-23 | 2021-08-17 | 东北农业大学 | 一种诱导后备母猪同期发情的方法 |
| CN115192693B (zh) * | 2021-08-20 | 2025-08-01 | 北京市农林科学院 | 一种诱导母猪同期发情的方法 |
| CN117981715B (zh) | 2024-04-07 | 2024-07-09 | 中国农业大学 | 一种促进后备母猪初情期启动和改善发情障碍的后备母猪批次化养殖方法 |
| WO2026048957A1 (ja) * | 2024-08-29 | 2026-03-05 | 国立大学法人静岡大学 | 家禽用飼料及び家禽の飼育方法 |
Family Cites Families (53)
| Publication number | Priority date | Publication date | Assignee | Title |
|---|---|---|---|---|
| US3860701A (en) | 1968-04-22 | 1975-01-14 | Searle & Co | Method for use and compositions of 11-lower alkyl steroids and drug delivery system for the controlled elution of 11-lower alkyl steroids |
| CS180644B2 (en) | 1973-09-29 | 1978-01-31 | Takeda Chemical Industries Ltd | Process for preparing nonapeptides |
| US4005063A (en) | 1973-10-11 | 1977-01-25 | Abbott Laboratories | [Des-gly]10 -GnRH nonapeptide anide analogs in position 6 having ovulation-inducing activity |
| US3991750A (en) | 1975-04-28 | 1976-11-16 | Syntex Corporation | Dromostanolone propionate implant pellet useful for producing weight gains in animals and suppressing estrus in female animals |
| SU573159A1 (ru) | 1976-03-17 | 1977-09-25 | Всесоюзный Ордена Трудового Красного Знамени Научно-Исследовательский Институт Животноводства | Способ синхронизации охоты и овул ции у свиноматок |
| US4732763A (en) | 1978-10-17 | 1988-03-22 | Stolle Research And Development Corporation | Active/passive immunization of the internal female reproductive organs |
| US4756907A (en) | 1978-10-17 | 1988-07-12 | Stolle Research & Development Corp. | Active/passive immunization of the internal female reproductive organs |
| JPS5781447A (en) | 1980-11-11 | 1982-05-21 | Toyo Jozo Co Ltd | Human chorionic gonadotropic hormone c-terminal fragment |
| GB8428201D0 (en) | 1984-11-08 | 1984-12-19 | Glaxo Group Ltd | Biological preparations |
| US4931279A (en) | 1985-08-16 | 1990-06-05 | Bausch & Lomb Incorporated | Sustained release formulation containing an ion-exchange resin |
| US4804626A (en) | 1986-10-22 | 1989-02-14 | The General Hospital Corporation | Immunometric assay for the detection of human chorionic gonadotropin |
| US4780451B1 (en) | 1987-01-23 | 1995-04-04 | Asua International Inc | Composition and method for producing superovulation in cattle |
| US5276022A (en) | 1987-09-24 | 1994-01-04 | Jencap Research Ltd. | Hormone preparation and method |
| ATE90570T1 (de) | 1988-01-29 | 1993-07-15 | Sumitomo Pharma | Verbesserte formulierungen mit kontrollierter abgabe. |
| US4975280A (en) | 1989-01-23 | 1990-12-04 | Ethyl Corporation | Bioerodable sustained release implants |
| FR2663223B1 (fr) | 1990-06-14 | 1994-12-02 | Af Aplicaciones Far Lab | Forme galenique parenterale. |
| US5180711A (en) | 1990-06-14 | 1993-01-19 | Applied Research Systems Ars Holding N.V. | Combined treatment with gnrh antagonist and gnrh to control gonadotropin levels in mammals |
| US5434136A (en) | 1990-12-14 | 1995-07-18 | Mathias; John R. | Treatment of motility disorders with a GNRH analog |
| IE62665B1 (en) | 1990-12-17 | 1995-02-22 | Akzo Nv | Contraceptive regimen |
| HU222501B1 (hu) | 1991-06-28 | 2003-07-28 | Endorecherche Inc. | MPA-t vagy MGA-t tartalmazó nyújtott hatóanyag-felszabadulású gyógyászati készítmény és eljárás előállítására |
| US5444167A (en) | 1993-07-07 | 1995-08-22 | Wallac Oy | Variant luteinizing hormone encoding DNA |
| ATE183926T1 (de) | 1993-09-29 | 1999-09-15 | Alza Corp | Hautpermeabilitaetserhöher bestehend aus monoglycerid/laktat estern |
| US5650173A (en) | 1993-11-19 | 1997-07-22 | Alkermes Controlled Therapeutics Inc. Ii | Preparation of biodegradable microparticles containing a biologically active agent |
| US5688506A (en) | 1994-01-27 | 1997-11-18 | Aphton Corp. | Immunogens against gonadotropin releasing hormone |
| FR2717688B1 (fr) | 1994-03-28 | 1996-07-05 | Lhd Lab Hygiene Dietetique | Système matriciel transdermique d'administration d'un oestrogène et/ou un progestatif à base d'EVA. |
| US5747058A (en) | 1995-06-07 | 1998-05-05 | Southern Biosystems, Inc. | High viscosity liquid controlled delivery system |
| US5589457A (en) | 1995-07-03 | 1996-12-31 | Ausa International, Inc. | Process for the synchronization of ovulation |
| GB9514816D0 (en) | 1995-07-19 | 1995-09-20 | Ucli Ltd | Substances and their medical use |
| US5985320A (en) | 1996-03-04 | 1999-11-16 | The Penn State Research Foundation | Materials and methods for enhancing cellular internalization |
| FR2747042B1 (fr) | 1996-04-05 | 1998-06-05 | Besins Iscovesco Lab | Medicament a base de progesterone et d'oestradiol |
| WO1997045113A1 (en) | 1996-05-30 | 1997-12-04 | Sepracor Inc. | Nsaids for regulating the reproductive cycle of domesticated animals |
| US6051558A (en) | 1997-05-28 | 2000-04-18 | Southern Biosystems, Inc. | Compositions suitable for controlled release of the hormone GnRH and its analogs |
| US6028057A (en) | 1998-02-19 | 2000-02-22 | Thorn Bioscience, Llc | Regulation of estrus and ovulation in gilts |
| FR2776520B1 (fr) | 1998-03-25 | 2000-05-05 | Sod Conseils Rech Applic | Nouvelles compositions pharmaceutiques destinees a la liberation prolongee de peptides et leur procede de preparation |
| AU5675099A (en) | 1998-08-17 | 2000-03-06 | William E. Trout | Use of zeranol to modulate reproductive cycles |
| IL142432A0 (en) | 1998-10-05 | 2002-03-10 | Penn State Res Found | Compositions and methods for enhancing receptor-mediated cellular internalization |
| WO2000078335A1 (en) | 1999-06-18 | 2000-12-28 | Southern Biosystems, Inc. | COMPOSITIONS FOR CONTROLLED RELEASE OF THE HORMONE GnRH AND ITS ANALOGS |
| GB0117057D0 (en) | 2001-07-12 | 2001-09-05 | Ferring Bv | Pharmaceutical composition |
| DE602004030546D1 (de) | 2003-03-04 | 2011-01-27 | Aspenbio Pharma Inc | LH zur Verwendung der Erhaltung einer oder mehreren Schwangerschaften durch Induktion der Bildung des sekundären Gelbkörpers. |
| MXPA05011299A (es) * | 2003-04-30 | 2006-01-24 | Debiopharm Sa | Metodos y composiciones utilizando la hormona liberadora de la hormona gonadotropina. |
| US7456207B2 (en) | 2003-09-25 | 2008-11-25 | Teva Pharmaceuticals Usa, Inc. | Vaginal pharmaceutical compositions and methods for preparing them |
| ES2555681T3 (es) | 2003-10-03 | 2016-01-07 | Thorn Bioscience, Llc | Procedimiento para la sincronización de la ovulación para la fecundación programada sin detección del celo |
| FR2865938B1 (fr) | 2004-02-05 | 2006-06-02 | Sod Conseils Rech Applic | Formulation retard solide comprenant de l'acetate de triptoreline |
| KR20090008175A (ko) | 2005-10-24 | 2009-01-21 | 마나와투 바이오텍 인베스트먼츠 엘티디. (엠비아이엘) | 배란 주기 모니터링 및 관리 |
| NZ595633A (en) | 2005-12-02 | 2013-05-31 | Parnell Lab Aust Pty Ltd | Increasing pregnancy rates |
| US20070197435A1 (en) | 2006-02-17 | 2007-08-23 | Webel Stephen K | Process for the synchronization of ovulation for timed breeding without heat detection |
| EP1891941A1 (en) | 2006-08-11 | 2008-02-27 | OctoPlus Technologies B.V. | Aqueous gels comprising microspheres |
| EP2065032A1 (en) | 2007-11-27 | 2009-06-03 | Galderma Research & Development | A method for producing adapalene gels |
| EP2421545B1 (en) | 2009-04-23 | 2017-12-06 | JBS United Animal Health II LLC | Method and composition for synchronizing time of insemination |
| EP2811986A1 (en) | 2012-02-08 | 2014-12-17 | Dow Corning Corporation | Silicone emulsions for delivery of healthcare actives |
| ES2808409T3 (es) | 2012-11-28 | 2021-02-26 | United Ah Ii Llc | Método para sincronizar el tiempo de inseminación en cerdas primerizas |
| WO2015081157A1 (en) | 2013-11-27 | 2015-06-04 | Jbs United Animal Health Ii Llc | Method and composition for synchronizing time of insemination in gilts |
| TW201625218A (zh) | 2014-04-18 | 2016-07-16 | Jbs聯合動物保健有限責任公司 | 製造含gnrh凝膠之方法 |
-
2013
- 2013-11-27 ES ES13859305T patent/ES2808409T3/es active Active
- 2013-11-27 CN CN202110694692.4A patent/CN113398243A/zh active Pending
- 2013-11-27 RU RU2015125549A patent/RU2015125549A/ru not_active Application Discontinuation
- 2013-11-27 DK DK13859305.8T patent/DK2925339T3/da active
- 2013-11-27 CA CA2892762A patent/CA2892762C/en active Active
- 2013-11-27 CN CN201380071570.3A patent/CN104994865A/zh active Pending
- 2013-11-27 EP EP13859305.8A patent/EP2925339B1/en active Active
- 2013-11-27 AU AU2013352054A patent/AU2013352054A1/en not_active Abandoned
- 2013-11-27 BR BR112015012453A patent/BR112015012453A8/pt not_active Application Discontinuation
- 2013-11-27 KR KR1020157017237A patent/KR20150095715A/ko not_active Withdrawn
- 2013-11-27 MX MX2015006618A patent/MX367876B/es active IP Right Grant
- 2013-11-27 WO PCT/US2013/072359 patent/WO2014085674A1/en not_active Ceased
- 2013-11-27 US US14/648,182 patent/US9724380B2/en active Active
- 2013-11-27 JP JP2015545461A patent/JP2016508030A/ja active Pending
-
2015
- 2015-05-27 CR CR20150282A patent/CR20150282A/es unknown
- 2015-05-27 PH PH12015501187A patent/PH12015501187A1/en unknown
- 2015-05-28 CL CL2015001448A patent/CL2015001448A1/es unknown
- 2015-06-24 ZA ZA2015/04552A patent/ZA201504552B/en unknown
-
2017
- 2017-07-26 US US15/660,638 patent/US10376558B2/en active Active
Also Published As
| Publication number | Publication date |
|---|---|
| BR112015012453A2 (pt) | 2017-07-11 |
| CN113398243A (zh) | 2021-09-17 |
| US9724380B2 (en) | 2017-08-08 |
| CL2015001448A1 (es) | 2016-01-04 |
| BR112015012453A8 (pt) | 2021-06-29 |
| KR20150095715A (ko) | 2015-08-21 |
| CA2892762C (en) | 2022-07-19 |
| CR20150282A (es) | 2015-09-01 |
| ZA201504552B (en) | 2017-11-29 |
| JP2016508030A (ja) | 2016-03-17 |
| RU2015125549A (ru) | 2017-01-11 |
| AU2013352054A1 (en) | 2015-06-04 |
| PH12015501187A1 (en) | 2015-08-10 |
| EP2925339B1 (en) | 2020-04-29 |
| CA2892762A1 (en) | 2014-06-05 |
| EP2925339A1 (en) | 2015-10-07 |
| MX2015006618A (es) | 2015-12-16 |
| WO2014085674A1 (en) | 2014-06-05 |
| US20180133283A1 (en) | 2018-05-17 |
| US20150306169A1 (en) | 2015-10-29 |
| CN104994865A (zh) | 2015-10-21 |
| US10376558B2 (en) | 2019-08-13 |
| DK2925339T3 (da) | 2020-07-20 |
| MX367876B (es) | 2019-09-10 |
| EP2925339A4 (en) | 2016-08-03 |
Similar Documents
| Publication | Publication Date | Title |
|---|---|---|
| ES2808409T3 (es) | Método para sincronizar el tiempo de inseminación en cerdas primerizas | |
| US10668127B2 (en) | Method and composition for synchronizing time of insemination | |
| US8937044B2 (en) | Process for the synchronization of ovulation for timed breeding without heat detection | |
| US20160375090A1 (en) | Method and composition for synchronizing time of insemination in gilts | |
| HK1173373B (en) | Method and composition for synchronizing time of insemination |